Замещённые бензазолы и их применение в качестве ингибиторов киназы raf
Номер патента: 7987
Опубликовано: 27.02.2007
Авторы: Рамуртхи Савитхри, Левайн Берри Хаскелл, Пун Дэниел Дж., Ренхауэ Пол А., Эмайри Пэйман, Субраманиан Шарадха, Сунг Леонард, Фэнтл Уэнди
Формула / Реферат
1. Соединение формулы (I)
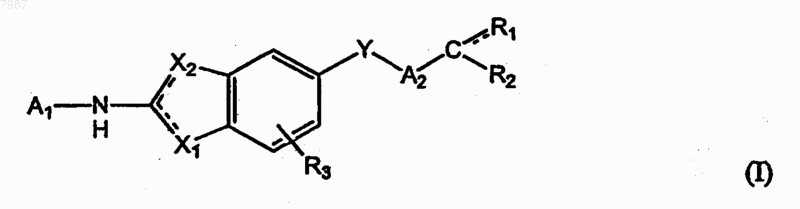
где X1 и Х2 независимо выбраны из =N-, -NR4-, -О- или -S- при условии, что если X1 представляет собой -NR4-, -О- или -S-, тогда Х2 представляет собой =N-, или если Х2 представляет -NR4-, -О- или -S-, тогда X1 представляет собой =N-, и как X1, так и Х2 не являются =N-; Y представляет О или S;
Y представляет О или S;
А1 представляет замещенный или незамещенный С1-С12алкил, С3-С8циклоалкил, С3-С8гетероциклоалкил, С5-С6арил, С9-С14полициклический арил, С9-С14полициклический арилС1-С12алкил, С5-С6гетероарил, С9-С14биарил, С5-С6гетероарилС5-С6арил, С5-С6гетероарилС5-С6гетероарил, С3-С8циклоалкилС1-С12алкил, С3-С8гетероциклоалкилС1-С12алкил, С5-С6арилС1-С12алкил, С5-С6гетероарилС1-С12алкил, С10-С12биарилС1-С12алкил или С5-С6гетероарилС5-С6арилС1-С12алкил;
А2 представляет замещенный или незамещенный С5-С6гетероарил;
R1 представляет О или Н, и
R2 представляет NR5R6 или гидроксил;
или R1, взятый вместе с R2, образуют замещенную или незамещенную С3-С8гетероциклоалкильную или C5-С6гетероарильную группу; где штрихпунктирная линия означает одинарную или двойную связь;
R3 представляет водород, галоген, C1-С6алкил или C1-С6алкокси;
R4 представляет водород, гидроксил, С1-С12алкиламино, C1-С12диалкиламино или С1-С12алкил;
R5 и R6 независимо выбраны из водорода и замещенного или незамещенного С1-С12алкила, С1-С12алкоксиС1-С12алкила, аминоС1-С12алкила, амидоС1-С12алкила, С1-С12ацила, С3-С8циклоалкила, С3-С8гетероциклоалкила, C5-С6арила, С5-С6гетероарила, С1-С12алкилокси, С1-С12алкилС3-С8гетероцикло и С5-С6гетероарилС1-С12алкила; или R5 и R6, взятые вместе, образуют замещенный или незамещенный С3-С8гетероцикло или C5-С6гетероарил; где замещенные группы замещенны одним или несколькими заместителями, выбранными из гидроксила, нитро, амино, имино, циано, галогена, тиогруппы, сульфонила, тиоамидо, амидино, имидино, оксо, оксамидино, метоксамидино, гуанидино, сульфонамидо, карбоксила, формила, C1-С6алкила, галогенC1-C6алкила, C1-Сбалкиламино, галогенС1-С6алкиламино, C1-С6алкокси, галогенС1-С6алкокси, C1-С6алкоксиалкила, С1-С12алкилкарбонила, аминокарбонила, С5-С6арилкарбонила, C5-C6арилС1-С12алкилкарбонила, C5-С6гетероарилкарбонила, C5-C6гетероарилС1-С12алкилкарбонила, C1-С12алкилтио, аминоС1-С12алкила, цианоС1-С12алкила и C5-С6арила;
и его фармацевтически приемлемые соли, сложные эфиры и их пролекарства.
2. Соединение формулы (II)
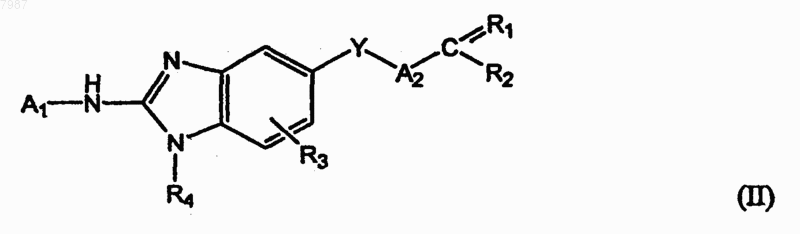
где и Y представляет О или S;
A1 представляет собой замещенный или незамещенный С1-С12алкил, С3-С8циклоалкил, С3-С8гетероциклоалкил, С5-С6арил, С9-С14полициклический арил, С9-С14полициклический арилС1-С12алкил, С5-С6гетероарил, С9-С14биарил, С5-С6гетероарилС5-С6арил, С5-С6гетероарилС5-С6гетероарил, С3-С8циклоалкилС1-С12алкил, С3-С8гетероциклоалкилС1-С12алкил, С5-С6арилС1-С12алкил, С5-С6гетероарилС1-С12алкил, С10-С12биарилС1-С12алкил, С5-С6гетероарил, С5-С6арилС1-С12алкил;
А2 представляет собой замещенный или незамещенный С5-С6гетероарил;
R1 представляет собой О и
R2 представляет собой NR5R6; или R1, взятый вместе с R2, образуют замещенную или незамещенную С3-С8гетероциклоалкильную или C5-C6гетероарильную группу; где штрихпунктирная линия означает одинарную или двойную связь;
R3 представляет собой водород, галоген, C1-C6алкил или C1-С6алкокси;
R4 представляет собой водород или C1-С6алкил;
R5 и R6 независимо выбраны из водорода и замещенного или незамещенного С1-С12алкила, С1-С12алкоксиС1-С12алкила, аминоС1-С12алкила, амидоС1-С12алкила, С1-С12ацила, С3-С8циклоалкила, С3-С8гетероциклоалкила, C5-С6арила, C5-С6гетероарила, С1-С12алкилоксиС1-С12алкилС3-С8гетероцикло и C5-C6гетероарилС1-С12алкила; или R5 и R6, взятые вместе, образуют замещенный или незамещенный С3-С8гетероцикло или C5-C6гетероарил; где замещенные группы замещенны одним или несколькими заместителями, выбранными из гидроксила, нитро, амино, имино, циано, галогена, тиогруппы, сульфонила, тиоамидо, амидино, имидино, оксо, оксамидино, метоксамидино, гуанидино, сульфонамидо, карбоксила, формила, C1-С6алкила, галогенС1-С6алкила, C1-С6алкиламино, галогенС1-С6алкиламино, C1-С6алкокси, галогенC1-C6алкокси, C1-С6алкоксиалкила, С1-С12алкилкарбонила, аминокарбонила, C5-С6арилкарбонила, C5-C6арилС1-С12алкилкарбонила, C5-С6гетероарилкарбонила, С5-С6гетероарилС1-С12алкилкарбонила, C1-С12алкилтио, аминоC1-С12алкила, цианоС5-С6алкила и C5-С6арила;
и его фармацевтически приемлемые соли, сложные эфиры и их пролекарства.
3. Соединение формулы (III)
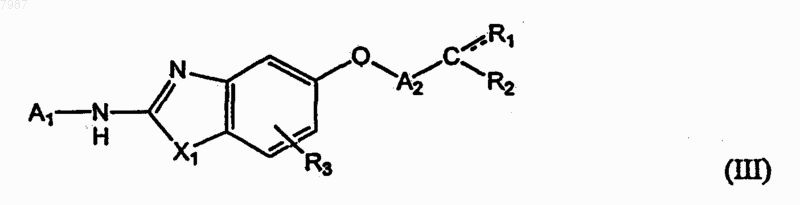
где X представляет NR4, О или S;
A1 представляет замещенный или незамещенный С1-С12алкил, С3-С8циклоалкил, С3-С8гетероциклоалкил, С5-С6арил, С9-С14полициклический арил, С9-С14полициклический арилС1-С12алкил, С5-С6гетероарил, С9-С14биарил, С5-С6гетероарилC5-C6арил, C5-C6гетероарилC5-C6гетероарил, C3-C8циклоалкилC1-C12алкил, C3-C8гетероциклоалкилC1-C12алкил, С5-C6арилC1-C12алкил, C5-C6гетероарилC1-C12алкил, C10-C12биарилC1-C12алкил, C5-C6гетероарил С5-C6арилC1-C12алкил;
A2 представляет замещенный или незамещенный C5-C6гетероарил;
R1 представляет О и
R2 представляет собой NR5R6; или R1, взятый вместе с R2, образуют замещенную или незамещенную C3-С8гетероциклоалкильную или C5-C6гетероарильную группу; где штрихпунктирная линия означает одинарную или двойную связь;
R3 представляет собой водород, галоген, C1-C6алкил или C1-C6алкокси;
R4 представляет собой водород или C1-C6алкил;
R5 и R6 независимо выбраны из водорода и замещенного или незамещенного C1-C12алкила, C1-C12алкоксиC1-C12алкила, аминоC1-С12алкила, амидоC1-C12алкила, C1-C12ацила, C3-C8циклоалкила, С3-C8гетероциклоалкила, C5-C6арила, C5-C6гетероарила, C1-C12алкилокси C1-C12алкилC3-C8гетероцикло и C5-C6гетероарилС1-С12алкила; или R5 и R6, взятые вместе, образуют замещенный или незамещенный C3-C8гетероцикло или C5-C6гетероарил; где замещенные группы замещены одним или несколькими заместителями, выбранными из гидроксила, нитро, амино, имино, циано, галогена, тиогруппы, сульфонила, тиоамидо, амидино, имидино, оксо, оксамидино, метоксамидино, гуанидино, сульфонамидо, карбоксила, формила, C1-С6алкила, галогенC1-C6алкила, C1-C6алкиламино, галогенC1-C6алкиламино, C1-C6алкокси, галогенC1-C6алкокси, C1-С6алкоксиалкила, C1-C12алкилкарбонила, аминокарбонила, С5-C6арилкарбонила, С5-C6арилC1-C12алкилкарбонила, C5-С6гетероарилкарбонила, С5-C6гетероарилC1-C12алкилкарбонила, C1-C12алкилтио, аминоC1-C12алкила, цианоC1-C12алкила и C5-C6арила;
и его фармацевтически приемлемые соли, сложные эфиры и их пролекарства.
4. Соединение по пп.1, 2 или 3, где А2 представляет собой замещенный или незамещенный пиридил.
5. Соединение по пп.1, 2 или 3, где R1 представляет O и штрихпунктирная линия означает одинарную или двойную связь.
6. Соединение формулы (IV)
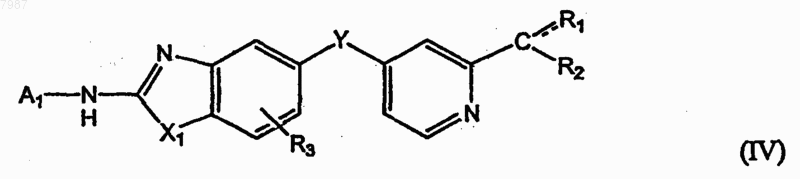
где X представляет NR4, О или S;
Y представляет О или S;
A1 представляет собой замещенный или незамещенный С3-C8циклоалкил, C3-C8гетероциклоалкил, C5-C6арил, C9-С14полициклический арил, С9-С14полициклический арил C1-C12алкил, С5-С6гетероарил, С9-С14биарил, C5-C6гетероарилC5-C6арил, С5-C6гетероарилС5-C6гетероарил, C3-C8циклоалкилC1-C12алкил, C3-C8гетероциклоалкилC1-C12алкил, С5-C6арилC1-C12алкил, С5-C6гетероарилС1-С12алкил, C10-C12биарилC1-C12алкил, C5-C6гетероарил С5-C6арилC1-C12алкил;
R1 представляет О и
R2 представляет собой NR5R6; или R1, взятый вместе с R2, образуют замещенную или незамещенную С3-C8гетероциклоалкильную или C5-C6гетероарильную группу; где штрихпунктирная линия означает одинарную или двойную связь;
R3 представляет собой водород, галоген, C1-C6алкил или C1-C6алкокси;
R4 представляет собой водород или C1-C6алкил;
R5 и R6 независимо выбраны из водорода и замещенного или незамещенного C1-C12алкила, C1-C12алкоксиC1-C12алкила, аминоC1-C12алкила, амидоC1-C12алкила, C1-C12ацила, C3-C8циклоалкила, С3-С8гетероциклоалкила, C5-C6арила, C5-C6гетероарила, C1-C12алкилоксиC1-C12алкилC3-C8гетероцикло и C5-C6гетероарилC1-C12алкила; или R5 и R6, взятые вместе, образуют замещенный или незамещенный С3-C8гетероцикло или С5-C8гетероарил; где замещенные группы замещены одним или несколькими заместителями, выбранными из гидроксила, нитро, амино, имино, циано, галогена, тиогруппы, сульфонила, тиоамидо, амидино, имидино, оксо, оксамидино, метоксамидино, гуанидино, сульфонамидо, карбоксила, формила, C1-C6алкила, галогенC1-C6алкила, C1-C6алкиламино, галогенC1-C6алкиламино, C1-C6алкокси, галогенC1-C6алкокси, C1-C6алкоксиалкила, C1-C12алкилкарбонила, аминокарбонила, C5-C6арилкарбонила, C5-C6арилС1-С12алкилкарбонила, С5-C6гетероарилкарбонила, C5-C6гетероарилС1-С12алкилкарбонила, C1-C12алкилтио, аминоC1-C12алкила, цианоС1-С12алкила и C5-C6арила;
и его фармацевтически приемлемые соли, сложные эфиры и их пролекарства.
7. Соединение по пп.1, 2, 6, где Y представляет собой О.
8. Соединение по п.6, где R1 представляет О и штрихпунктирная линия означает одинарную или двойную связь.
9. Соединение формулы (V)
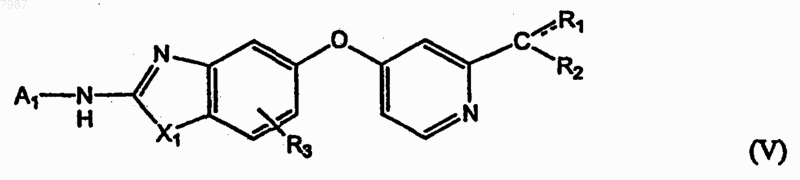
где X представляет NR4, О или S;
A1 представляет собой замещенный или незамещенный C3-C8циклоалкил, С3-С8гетероциклоалкил, С5-С6аршы, C9-С14полициклический арил, C9-C14полициклический арилС1-С12алкил, С5-C6гетероарил, C9-С14биарил, С5-C6гетероарилC5-C6арил, С5-C6гетероарилС5-C6гетероарил, C3-C8циклоалкилC1-C12алкил, С3-С8гетероциклоалкилС1-С12алкил, C5-C6арилС1-С12алкил, С5-C6гетероарилC1-C12алкил, C10-С12биарилC1-C12алкил, C5-C6гетероарил С5-С6арилC1-C12алкил;
R1 представляет О и R2 представляет собой NR5R6; или R1, взятый вместе с R2, образуют замещенную или незамещенную С3-C8гетероциклоалкильную или C5-C6гетероарильную группу; где штрих-пунктирная линия означает одинарную или двойную связь;
R3 представляет собой водород, галоген, C1-C6алкил или C1-C6алкокси;
R4 представляет собой водород или C1-С6алкил;
R5 и R6, независимо, выбраны из водорода и замещенного или незамещенного C1-C12алкила, С1-С12алкоксиС1-С12алкила, аминоC1-С12алкила, амидоC1-С12алкила, С1-С12ацила, C3-C8циклоалкила, С3-C8гетероциклоалкила, С5-С6арила, C5-C6гетероарила, С1-С12алкилоксиC1-C12алкилC3-C8гетероцикло и C5-C6гетероарилC1-C12алкила; или R5 и R6, взятые вместе, образуют замещенный или незамещенный C3-C8гетероцикло или C5-C8гетероарил; где замещенные группы замещенны одним или несколькими заместителями, выбранными из гидроксила, нитро, амино, имино, циано, галогена, тиогруппы, сульфонила, тиоамидо, амидино, имидино, оксо, оксамидино, метоксамидино, гуанидино, сульфонамидо, карбоксила, формила, C1-C6алкила, галогенC1-C6алкила, C1-C6алкиламино, галогенC1-C6алкиламино, C1-C6алкокси, галогенС1-C6алкокси, C1-C6алкоксиалкила, C1-C12алкилкарбонила, аминокарбонила, С5-C6арилкарбонила, C5-C6арилC1-C12алкилкарбонила, С5-C6гетероарилкарбонила, С5-C6гетероарилC1-C12алкилкарбонила, C1-С12алкилтио, аминоC1-C12алкила, цианоC1-C12алкила и C5-C6арила; и
его фармацевтически приемлемые соли, сложные эфиры и их пролекарства.
10. Соединение по пп.1, 3, 6, 9, где X представляет NR4.
11. Соединение по п.10, где R4 представляет водород.
12. Соединение по пп.1, 2, 3, 6, 9, где A1 выбран из группы, состоящей из замещенного или незамещенного фенила, пиридила, пиримидинила, фенилалкила, пиридилалкила, пиримидинилалкила, гетероциклилкарбонилфенила, гетероциклилфенила, гетероциклилалкилфенила, хлорфенила, фторфенила, бромфенила, иодфенила, дигалогенфенила, нитрофенила, 4-бромфенила, 4-хлорфенила, алкилбензоата, алкоксифенила, диалкоксифенила, диалкилфенила, триалкилфенила, тиофена, тиофен-2-карбоксилата, алкилтиофенила, трифторметилфенила, ацетилфенила, сульфамоилфенила, бифенила, циклогексилфенила, фенилоксифенила, диалкиламинофенила, алкилбромфенила, алкилхлорфенила, алкилфторфенила, трифторметилхлорфенила, трифторметилбромфенила, инденила, 2,3-дигидроинденила, тетралинила, трифторфенила, (трифторметил)тиофенила, алкоксибифенила, морфолинила, N-пиперазинила, N-морфолинилалкила, пиперазинилалкила, циклогексилалкила, индолила, 2,3-дигидроиндолила, 1-ацетил-2,3-дигидроиндолила, циклогептила, бицикло[2,2,1]гепт-2-ила, гидроксифенила, гидроксиалкилфенила, пирролидинила, пирролидин-1-ила, пирролидин-1-илалкила, 4-амино(имино)метилфенила, изоксазолила, индазолила, адамантила, бициклогексила, хинуклидинила, имидазолила, бензимидазолила, имидазолилфенила, фенилимидазолила, фталамидо, нафтила, бензофенона, анилинила, анизолила, хинолинила, хинолинонила, фенилсульфонила, фенилалкилсульфонила, 9Н-флоурен-1-ила, пиперидин-1-ила, пиперидин-1-илалкила, циклопропила, циклопропилалкила, пиримидин-5-илфенила, хинолидинилфенила, фуранила, фуранилфенила, N-метилпиперидин-4-ила, пирролидин-4-илпиридинила, 4-диазепан-1-ила, гидроксипирролидин-1-ила, диалкиламинопирролидин-1-ила, 1,4'-бипиперидин-1'-ила и (1,4'-бипиперидин-1'-илкарбонил)фенила.
13. Соединение по п.9, где R1 представляет О и штрихпунктирная линия означает одинарную или двойную связь.
14. Соединение по пп.1, 2, 3, 6, 9, где R2 представляет NR5R6, R5 представляет водород и R6 выбран из водорода и замещенного или незамещенного C1-C12алкила, C1-C12алкоксиC1-C12алкила, аминоС1-С12алкила, амидоC1-C12алкила, ацила, C3-C8циклоалкила, C3-С8гетероциклоалкила, C5-C6арила, C5-C6гетероарила, C1-С12алкилокси С1-С12алкилC3-C8гетероцикло и C5-C6гетероарилС1-С12алкила.
15. Соединение по пп.1, 2, 3, 6, 9, где R1, взятый вместе с R2, образуют замещенную или незамещенную C3-С8гетероциклоалкильную или C5-C6гетероарильную группу.
16. Соединение по пп.1, 2, 3, 6, 9, где R3 представляет собой C1-C6алкокси.
17. Соединение по п.16, где R3 представляет собой метокси.
18. Соединение по пп.1, 2, 3, 6, 9 или 18, где R4 представляет C1-C6алкил.
19. Соединение по пп.1, 2, 3, 6, 9, где R4 представляет собой метил.
20. Соединение по пп.1, 2, 3, 6, 9, где R1 представляет О, R2 представляет собой NR5R6, R5 представляет собой Н и R6 представляет собой метил.
21. Композиция, содержащая количество соединения по пп.1, 2, 3, 6 или 9, эффективное для ингибирования активности Raf у человека или животного, при введении его вместе с фармацевтически приемлемым носителем.
22. Композиция по п.21, которая дополнительно содержит по крайней мере одно дополнительное (лекарственное) средство для лечения рака.
23. Композиция по п.22, в которой по крайней мере одно дополнительное (лекарственное) средство для лечения рака выбрано из иринотекана, топотекана, гемцитабина, 5-флуороурацила, лейковорин карбоплатина, цисплатина, таксанов, тезацитабина, циклофосфамида, винка алкалоидов, иматиниба, антрациклинов, ритуксимаба и трастузумаба.
24. Способ ингибирования активности киназы Raf у человека или животного, включающий введение человеку или животному композиции, содержащей количество соединения по пп.1, 2, 3, 6 или 9, эффективное для ингибирования активности киназы Raf у человека или животного.
25. Способ лечения ракового расстройства, опосредованного Ras/митоген-активируемым протеинкиназным сигнальным путем, у человека или животного, включающий введение человеку или животному композиции, содержащей количество соединения по пп.1, 2, 3, 6 или 9, эффективное для ингибирования активности киназы Raf у человхър или животного.
26. Способ лечения гормонзависимого ракового расстройства, опосредованного Ras/митоген-активируемым протеинкиназным сигнальным путем, у человека или животного, включающий введение человеку или животному композиции, содержащей количество соединения по пп.1, 2, 3, 6 или 9, эффективное для ингибирования активности киназы Raf у человека или животного.
27. Способ по п.26, где гормонзависимый рак представляет собой рак молочной железы или рак простаты.
28. Способ лечения гематологического ракового расстройства, опосредованного Ras/митоген-активируемым протеинкиназным сигнальным путем, у человека или животного, включающий введение человеку или животному композиции, содержащей количество соединения по пп.1, 2, 3, 6 или 9, эффективное для ингибирования активности киназы Raf у человека или животного.
29. Способ по пп.25, 26, 28, который дополнительно включает введение человеку или животному по крайней мере одного дополнительного лекарственного средства для лечения рака.
30. Способ по пп.25, 26 или 29, в котором по крайней мере одно дополнительное средство для лечения рака выбирают из иринотекана, топотекана, гемцитабина, 5-флуороурацила, лейковорин карбоплатина, цисплатина, таксаноз, тезацитабина, циклофосфамида, винка алкалоидов, иматиниба, антрациклинов, ритуксимаба и трастузумаба.
31. Применение соединения по пп.1, 2, 3, 6 или 9 для лечения рака.
32. Применение соединения по пп.1, 2, 3, 6 или 9 для получения лекарственного средства для лечения рака.
Текст
007987 Данное изобретение относится к новым замещенным бензазолподобным соединениям и их фармацевтически приемлемым солям, сложным эфирам и к их пролекарствам, композициям новых соединений вместе с фармацевтически приемлемыми носителями и применениям новых соединений, либо самих по себе, либо в комбинации по крайней мере с одним дополнительным терапевтическим средством для профилактики или лечения рака.Raf серин/треониновые киназы представляют собой основные компоненты модуля передачи сигнала Ras/Митоген-активируемыми протеинкиназами (MAPK), который управляет комплексной программой транскрипции в ответ на внешние клеточные стимулы. Гены Raf кодируют высоко консервативные серин-треонинспецифические протеинкиназы, которые, как известно, связываются с онкогеном ras. Они являются частью пути сигнальной трансдукции, который, как полагают, состоит из рецепторных тирозинкиназ, р 21 ras, протеинкиназ Raf, киназ Mek1 (активатор ERK или MAPKK) и киназ ERK (MAPK),которые в конечном счете фосфорилируют факторы транскрипции. В этом пути киназы Raf активируются Ras и фосфорилируют и активируют две изоформы митоген-активированной протеинкиназной киназы(называемые Mek1 и Mek2), которые представляют собой треонин/тирозинкиназы двойной специфичности. Обе изоформы Mek активируют митоген-активируемые киназы 1 и 2 (MAPK, также называемой регулируемой внеклеточным лигандом киназой 1 и 2 или Erk1 и Erk2). MAPK фосфорилируют многие субстраты, включая факторы транскрипции, и при этом задают параметры их транскрипционной программы. Участие киназы Raf в Ras/MAPK пути оказывает воздействие и управляет многими клеточными функциями, такими как пролиферация, дифференцировка, выживание, онкогенная трансформация и апоптоз. Как существенная роль, так и позиция Raf во многих путях передачи сигнала были установлены в исследованиях, использующих клетки млекопитающих с мутациями гена Raf, приводящими к угнетению экспрессии этого гена и имеющими нерегулируемый доминантный характер, а также в исследованиях,использующих биохимические и генетические техники для моделирования процессов (протекающих) в организме. Во многих случаях активация Raf рецепторами, которые стимулируют клеточное фосфорилирование тирозина, зависит от активности Ras, что указывает на то, что Ras функционирует в обратном направлении Raf (против течения каскада передачи сигнала). После активации Raf-1 затем фосфорилирует и активирует Mek1, приводя к распространению сигнала в направлении эффекторов (по течению каскада передачи сигнала), таких как MAPK (митоген-активируемая протеинкиназа) (Crews et al. (1993) Cell 74:215). Предполагают, что Raf серин/треониновые киназы являются первичными эффекторами Ras, вовлеченными в пролиферацию клеток животных (Avruch et al. (1994) Trends Biochem. Sci. 19:279). Киназа Raf имеет три различные изоформы, Raf-1 (c-Raf), A-Raf и B-Raf, различающиеся по своей способности взаимодействовать с Ras, активировать MAPK киназный путь, тканевое распределение и субклеточную локализацию (Marias et al., Biochem. J. 351: 289-305, 2000; Weber et al., Oncogene 19:169176, 2000; Pritchard et al., Mol. Cell Biol. 15:6430-6442, 1995). Киназы Raf активируются Ras и фосфорилируют и активируют две изоформы митоген-активируемой протеинкиназной киназы (называемые Mek1 и Mek2), которые представляют собой треонин/тирозинкиназы двойной специфичности. Обе изоформыMek активируют митоген-активируемые киназы 1 и 2 (MAPK, также называемой регулируемой внеклеточным лигандом киназой 1 и 2 или Erk1 и Erk2). MAPK фосфорилируют многие субстраты, включая цитозолевые белки и семейство ETS факторов транскрипции. Участие киназы Raf в пути Ras/MAPK оказывает влияние и регулирует многие клеточные функции, такие как пролиферация, дифференцировка,выживание, развитие клеточного цикла и апоптоз. Активирование мутации одного из генов Ras можно наблюдать в 20% всех случаев опухолей и путь Raf/MEK/ERK активируется в 30% всех случаев опухолей (Bos et al., Cancer Res. 49:4682-4689,1989) (Hoshino et al., Oncogene 18:813-822, 1999). Последние исследования показали, что мутация B-Raf в кожных невусах (типа родимого пятна) является критической стадией в инициировании неоплазии меланоцитов (Pollock et al., Nature Genetics 25: 1-2, 2002). Кроме того, самые современные исследования показали, что активация мутации в домене киназы В-Raf происходит в 66% случаев меланом, 12% случаев карцином ободочной кишки и 14% случаев рака печени (Davies et al., Nature 417:949-954, 2002) (Yuen etal., Cancer Research 62:6451-6455, 2002) (Brose et al., Cancer Research 62:6997-7000, 2002). Ингибиторы пути Raf/MEK/ERK на уровне киназ Raf могут быть потенциально эффективными в качестве терапевтических средств против опухолей с гипер-экспрессируемыми или мутированными рецепторными тирозинкиназами, активированными внутриклеточными тирозинкиназами, опухолей с аберантно (отклонением от нормы) экспрессируемым Grb2 (адаптерный белок, который допускает стимуляцию Ras обменным фактором Sos), а также опухолей со скрытыми активирующими мутациями самихRaf. В ранних клинических испытаниях, ингибитор киназы Raf-1, который также ингибирует В-Raf, проявил себя перспективным в качестве терапевтических средств в терапии рака (Crump, Current Pharmaceutical Design 8: 2243-2248, 2002; Sebastien et al., Current Pharmaceutical Design 8: 2249-2253, 2002). Разрушение экспрессии Raf в клеточных линиях через применение метода антисмысловых РНК, как было установлено, подавляет как Ras, так и Raf-опосредованную онкогенность (Kolch et al., Nature 349:416-428, 1991; Monia et al., Nature Medicine 2(6):668-675, 1996). Было описано несколько ингибиторов киназ Raf, которые демонстрировали эффективность в инги-1 007987 бировании пролиферации опухолевых клеток in vitro и/или in vivo испытаниях (см., например, патенты США 6391636, 6358932, 6037136, 5717100, 6458813, 6204467 и 6268391). В других патентах и патентных заявках предлагается применение ингибиторов киназ Raf для лечения лейкоза (см., например, патенты США 6268391 и 6204467 и опубликованная заявка на патент США 20020137774; 20020082192; 20010016194 и 20010006975), или для лечения рака молочной железы (см., например, патенты США 6358932, 5717100, 6458813, 6268391 и 6204467, и опубликованная заявка на патент США 20010014679). Предлагаются новые соединения замещенных бензазолов и их фармацевтически приемлемые соли или сложные эфиры, содержащие участки, повышающие растворимость, или их пролекарства, представленные формулой (I) где X1 и Х 2 независимо выбраны из =N-, -NR4-, -О- или -S-, при условии, что когда X1 представляет собойY представляет О или S; А 1 представляет замещенный или незамещенный алкил, циклоалкил, гетероциклоалкил, арил, полициклический арил, полициклический арилалкил, гетероарил, биарил, гетероариларил, гетероарилгетероарил, циклоалкилалкил, гетероциклоалкилалкил, арилалкил, гетероарилалкил, биарилалкил или гетероариларилалкил; А 2 представляет замещенный или незамещенный гетероарил;R2 представляет NR5R6 или гидроксил; или R1, взятый вместе с R2, образуют замещенную или незамещенную гетероциклоалкильную или гетероарильную группу; где штрих-пунктирная линия означает одинарную или двойную связь;R3 представляет собой водород, галоген, низший алкил или низший алкокси;R5 и R6 независимо выбраны из группы, состоящей из водорода и замещенного или незамещенного алкила, алкоксиалкила, аминоалкила, амидоалкила, ацила, циклоалкила, гетероциклоалкила, арила, гетероарила, алкилоксиалкилгетероцикло и гетероарилалкила; или R5 и R6, взятые вместе, образуют замещенный или незамещенный гетероцикло или гетероарил; и их фармацевтически приемлемые соли, сложные эфиры и пролекарства. В других вариантах осуществления предлагаются новые замещенные соединения бензазола формулы (II) где и Y, A1, A2, R1, R2, R3 и R4 такие, как определено выше; и их фармацевтически приемлемые соли,сложные эфиры и пролекарства. В других вариантах осуществления предлагаются новые соединения замещенных бензазолов формулы (III) где X1, A1, A2, R1, R2 и R3 такие, как определено выше; и их фармацевтически приемлемые соли, сложные эфиры, таутомеры и их пролекарства. В других вариантах осуществления предлагаются новые соединения замещенных бензазолов формулы (IV)-2 007987 соли, сложные эфиры, таутомеры и их пролекарства. В следующих вариантах осуществления предлагаются новые соединения замещенных бензазолов,представленные формулой (V) где X1, A1, R1, R2 и R3 такие, как определено выше; и их фармацевтически приемлемые соли, сложные эфиры, таутомеры и их пролекарства. В других аспектах настоящее изобретение предлагает способы лечения расстройств, связанных сRaf, у человека или животного, при необходимости такого лечения, включающие введение указанному субъекту количества соединения формулы (I), (II), (III), (IV) или (V), эффективного для снижения или предотвращения роста опухоли у субъекта. В очередных аспектах настоящее изобретение предлагает способы лечения расстройств, связанных с Raf, у человеческого или животного субъекта, при необходимости такого лечения, включающие введение указанному субъекту количества соединения формулы (I), (II), (III), (IV) или (V), эффективного для снижения или предотвращения роста опухоли у субъекта, в комбинации по крайней мере с одним дополнительным средством для лечения рака. В очередных аспектах настоящее изобретение предлагает терапевтические композиции, содержащие по крайней мере одно соединение формулы (I), (II), (III), (IV) или (V) в комбинации с одним или несколькими дополнительными средствами для лечения рака, которые обычно используют при лечении рака. Соединения настоящего изобретения используют для лечения раков, включая карциномы (например, легких, поджелудочной железы, щитовидной железы, мочевого пузыря или толстой кишки), миелоидные нарушения (например, миелоидный лейкоз) и аденомы (например, ворсинчатая аденома толстой кишки). Кроме того, изобретение предлагает композиции, способы применения и способы получения, описанные в подробном описании изобретения. В соответствии с одним аспектом настоящего изобретения предлагаются новые соединения замещенных бензазолов и их фармацевтически приемлемые соли, сложные эфиры или их пролекарства, представленные формулой (I) где X1 и Х 2 независимо выбраны из =N-, -NR4-, -О- или -S-, при условии, что когда X1 представляет -NR4-,-О- или -S-, тогда Х 2 представляет =N-, или когда Х 2 представляет -NR4-, -О- или -S-, тогда Х 2 представляет =N-, и оба, X1 и Х 2, не являются =N-; Y представляет О или S;A1 представляет замещенный или незамещенный алкил, циклоалкил, гетероциклоалкил, арил, полициклический арил, полициклический арилалкил, гетероарил, биарил, гетероариларил, гетероарилгетероарил, циклоалкилалкил, гетероциклоалкилалкил, арилалкил, гетероарилалкил, биарилалкил или гетероариларилалкил; А 2 представляет замещенный или незамещенный гетероарил;R2 представляет NR5R6 или гидроксил; или R1, взятый вместе с R2, образуют замещенную или незамещенную гетероциклоалкильную или гетероарильную группу, где штрих-пунктирная линия означает одинарную или двойную связь;R3 представляет собой водород, галоген, низший алкил или низший алкокси;R5 и R6 независимо выбраны из водорода и замещенного или незамещенного алкила, алкоксиалкила, аминоалкила, амидоалкила, ацила, циклоалкила, гетероциклоалкила, арила, гетероарила, алкилоксиалкилгетероцикло и гетероарилалкила; или R5 и R6, взятые вместе, образуют замещенный или незамещенный гетероцикло или гетероарил; и их фармацевтически приемлемые соли, сложные эфиры и их пролекарства. В других вариантах осуществления предлагаются новые соединения замещенных бензазолов, представленные формулой (II) где и Y, A1, A2, R1, R2, R3 и R4 такие, как определено выше; и их фармацевтически приемлемые соли,сложные эфиры и пролекарства. В других вариантах осуществления предлагаются новые соединения замещенных бензазолов, представленные формулой (III) где X1, A1, A2, R1, R2 и R3 такие, как определено выше; и их фармацевтически приемлемые соли, сложные эфиры, таутомеры и их пролекарства. В других вариантах осуществления предлагаются новые соединения замещенных бензазолов, представленные формулой (IV) где X1, Y, A1, R1, R2 и R3 такие, как определено выше; и их фармацевтически приемлемые соли, сложные эфиры, таутомеры и их пролекарства. В очередных вариантах осуществления предлагаются новые соединения замещенных бензазолов,представленные формулой (V) где X1, A1, R1, R2 и R3 такие, как определено выше; и их фармацевтически приемлемые соли, сложные эфиры, таутомеры и их пролекарства. В другом аспекте настоящее изобретение предлагает способы лечения людей или животных, страдающих от расстройства, связанного с Raf, такого как рак. Таким образом, настоящее изобретение обеспечивает способы лечения человеческого или животного субъекта, при необходимости такого лечения,включающие введение субъекту терапевтически эффективного количества указанного выше соединения формулы I, II, III, IV или V, либо одного, либо в комбинации с другими противораковыми средствами. В других аспектах настоящее изобретение обеспечивает способы лечения связанных с Raf расстройств у человеческого или животного субъекта, при необходимости такого лечения, включающие введение указанному субъекту количества соединения формулы (I), (II), (III), (IV) или (V), эффективного для снижения или профилактики роста опухоли у субъекта. В следующих аспектах настоящее изобретение обеспечивает способы лечения связанных с Raf расстройств у человеческого или животного субъекта, при необходимости такого лечения, включающие введение указанному субъекту количества соединения формулы (I), (II), (III), (IV) или (V), эффективного для снижения или профилактики роста опухоли у субъекта, в комбинации по крайней мере с одним дополнительным средством для лечения рака. Ряд подходящих противораковых средств, которые используют в качестве комбинированных терапий для лечения рака, предполагаются для применения в способах настоящего изобретения. В самом деле, настоящее изобретение предусматривает, но не ограничивается ими, введение многочисленных противораковых средств, таких как средства, которые вызывают апоптоз; полинуклеотиды (например, рибозимы); полипептиды (например, ферменты); лекарственные средства; биологические миметики; алкалоиды; алкилирующие средства; противоопухолевые антибиотики; антиметаболиты; гормоны; соединения платины; моноклональные антитела, конъюгированные с противораковыми лекарственными средствами, токсинами и/или радиоактивными изотопами; модификаторы биологического ответа (например, интерфероны [например, IFN- и т.д.] и интерлейкины [например, IL-2 и т.д.] и т.д.); восприимчивые иммунотерапевтические средства; факторы гемопоэтического роста; средства, которые индуцируют дифференцировку опухолевых клеток (например, полностьютранс-ретиноевая кислота и т.д.); реагенты генотерапии; антисенсные терапевтические средства и нуклеотиды; опухолевые вакцины; ингибиторы ангиогенеза и т.п. Многочисленные другие примеры химиотерапевтических соединений и противораковых терапий, подходящих для совместного введения с заяв-4 007987 ляемыми соединениями формулы (I), (II), (III), (IV) или (V), известны специалистам в данной области. В предпочтительных вариантах осуществления противораковые средства, подлежащие использованию в комбинации с соединениями настоящего изобретения, включают средства, которые индуцируют или стимулируют апоптоз. Средства, которые вызывают апоптоз, включают, но не ограничиваясь ими,радиацию (например, W), ингибиторы киназ (например, ингибитор киназы рецепторов эпидермального фактора роста [EGFR], ингибитор киназы рецепторов фактора васкулярного роста [VGFR], ингибитор киназы рецепторов фактора роста фибробластов [FGFR], ингибитор киназы рецепторов I фактора тромбоцитарного роста [PGFR] и ингибиторы киназы Всr-Abl, такие как STI-571, Gleevec и Glivec); антисмысловые молекулы; антитела [например, Herceptin и Rituxan]; антиэстрогены [например, ралоксифен и тамоксифен]; антиандрогены [например, флутамид, бикалутамид, финастерид, аминоглутетамид, кетоконазол и сортикостероиды]; ингибиторы циклооксигеназы 2 (СОХ-2) [например, целококсиб, мелоксикам,NS-398, и нестероидные противовоспалительные лекарственные средства (NSAID)]; и раковые химиотерапевтические средства [например, иринотекан (Camptosar), СРТ-11, флударабин (Fludara), дакарбацин(DTIC), дексаметазон, митоксантрон, Милотарг, VP-16, цисплатина, 5-FU, Доксрубицин, Таксотер или таксол]; внутриклеточные молекулы, участвующие в передаче сигнала; церамиды и цитокины; и стауросприн и т.п. В других аспектах в настоящем изобретении предлагаются фармацевтические композиции, содержащие по крайней мере одно соединение формулы I, II, III, IV или V вместе с фармацевтически приемлемым носителем, подходящим для введения человеку или животному, либо как таковые, либо вместе с другими противораковыми средствами. В других аспектах в настоящем изобретении предлагаются способы получения соединений формулы I, II, III, IV или V, описываемых в данном описании. В очередных аспектах настоящее изобретение обеспечивает соединения, которые являются ингибиторами фермента киназы Raf. Поскольку фермент представляет нисходящий эффектор p21ras, настоящие ингибиторы полезны в фармацевтических композициях в медицине или ветеринарии в тех случаях, когда показано ингибирование пути киназы Raf, например, при лечении опухолей и/или роста злокачественных клеток, опосредованных киназой Raf. В частности, соединения полезны при лечении человека или животного, например, мышиного рака, поскольку прогрессирование этих раков зависит от каскада реакций,передающих сигнал белка ras и, поэтому, чувствительно к лечению путем прерывания каскада ингибированием активности киназы Raf. Следовательно, соединения данного изобретения полезны при лечении солидных злокачественных опухолей, таких как, например, карциномы (например, легких, поджелудочной железы, щитовидной железы, мочевого пузыря или толстой кишки), миелоидных нарушений (например, миелоидный лейкоз) или аденомы (например, ворсинчатая аденома толстой кишки). Используемый термин "ингибитор Raf" относится к соединению, которое демонстрирует IС 50 в отношении активности киназы Raf не более чем около 100 мкМ и более типично не более чем 50 мкМ, измеренную в фильтрационном анализе Raf/Mek, описанном, в общем, в настоящем описании ниже. Предпочтительные изоформы киназы Raf, по отношению к которым, как будет показано, соединения настоящего изобретения проявляют ингибирующее действие, включают A-Raf, B-Raf и C-Raf (Raf-1). "IC50" представляет собой концентрацию ингибитора, которая снижает активность фермента (например, киназыRaf) до половины максимального уровня. Репрезентативные соединения настоящего изобретения, как было установлено, демонстрируют ингибирующую активность по отношению к Raf. Соединения настоящего изобретения предпочтительно демонстрируют IC50 в отношении Raf не более чем около 10 мкМ, более предпочтительно не более чем около 5 мкМ, еще более предпочтительно не более чем около 1 мкМ и наиболее предпочтительно не более чем около 200 нМ, определенную в испытаниях киназы Raf,описанных ниже. Используемый в данном описании термин "бензазолы" включает бензимидазолы, бензотиазолы и бензоксазолы. Выражение "алкил" относится к алкильным группам, которые не содержат гетероатомы. Таким образом, выражение включает алкильные группы с прямой цепью, такие как метил, этил, пропил, бутил,пентил, гексил, гептил, октил, нонил, децил, ундецил, додецил и т.п. Кроме того, данное выражение включает изомеры разветвленных цепей алкильных групп с прямой цепью, включая, но ими не ограничиваясь, нижеследующие, которые представлены в качестве примера -СН(СН 3)2, -СН(СН 3)(СН 2 СН 3),-СН(СН 2 СН 3)2, -С(СН 3)3, -С(СН 2 СН 3)3, -СН 2 СН(СН 3)2, -СН 2 СН(СН 3)(СН 2 СН 3), -СН 2 СН(СН 2 СН 3)2,-СН 2 С(СН 3)3, -СН 2 С(СН 2 СН 3)3, -СН(СН 3)СН(СН 3)(СН 2 СН 3), -СН 2 СН 2 СН(СН 3)2,-СН 2 СН 2 СН(СН 3)(СН 2 СН 3), -СН 2 СН 2 СН(СН 2 СН 3)2, -СН 2 СН 2 С(СН 3)3, -СН 2 СН 2 С(СН 2 СН 3)3,-СН(СН 3)СН 2 СН(СН 3)2, -СН(СН 3)СН(СН 3)СН(СН 3)2, -СН(СН 2 СН 3)СН(СН 3)СН(СН 3)(СН 2 СН 3) и др. Кроме того, выражение включает циклоалкильные группы, такие как циклопропил, циклобутил, циклопентил, циклогексил, циклогептил и циклооктил и указанные циклы, замещенные алкильными группами с прямой и разветвленной цепью, определенными выше. Таким образом, выражение алкильные группы включает первичные алкильные группы, вторичные алкильные группы и третичные алкильные группы. Предпочтительные алкильные группы включают алкильные группы с прямой и разветвленной цепью и циклоалкильные группы, содержащие 1-12 атомов углерода.-5 007987 Используемый термин "низший алкил" включает замещенные или незамещенные алкильные группы с прямыми или разветвленными цепями, содержащие от 1 до 6 атомов углерода. Репрезентативные низшие алкильные группы включают, например, метил, этил, пропил, изопропил, н-бутил, трет-бутил,неопентил, трифторметил, пентафторэтил и т.п. Низшие алкильные группы могут быть замещены, как,например, галогеном, гидрокси, амино, нитро и/или цианогруппами и т.п. Репрезентативные галогензамещенные и гидроксизамещенные низшие алкилы включают хлорметил, трихлорметил, хлорэтил, гидроксиэтил и т.п. Другие подходящие замещенные низшие алкильные части включают, например, аралкил, аминоалкил, аминоаралкил, карбониламиноалкил, алкилкарбониламиноалкил, арилкарбониламиноалкил, аралкилкарбониламиноалкил, аминоалкоксиалкил и ариламиноалкил. Используемый термин "низший алкокси" относится к RO-, где R представляет низший алкил. Репрезентативные примеры низших алкоксигрупп включают метокси, этокси, т-бутокси, трифторметокси и т.п. Используемый термин "галоген" или "гало" относится к группам хлора, брома, фтора и иода. "Галогеналкил" относится к алкильному радикалу, замещенному одним или несколькими атомами галогена. Термин "галоген-низший алкил" относится к низшему алкильному радикалу, замещенному одним или несколькими атомами галогена. Термин "галогеналкокси" относится к алкоксирадикалу, замещенному одним или несколькими атомами галогена. Термин "галоген-низший алкокси" относится к низшему алкоксирадикалу, замещенному одним или несколькими атомами галогена. Термин "амино" относится к группе -NH2. Термин "алкиламино" относится к группе -NRR', где R иR', каждый, независимо выбран из водорода или низшего алкила. Термин "ариламино" относится к группе -NRR', где R представляет собой арил и R' представляет собой водород, низший алкил или арил. Термин "аралкиламино" относится к группе -NRR', где R представляет собой низший аралкил и R' представляет собой водород, низший алкил, арил или низший аралкил. Термин "алкоксиалкил" относится к группе -алк 1-O-алк 2, где алк 1 представляет собой алкил или алкенил и алк 2 представляет алкил или алкенил. Термин "низший алкоксиалкил" относится к алкоксиалкилу, где алк 1 представляет собой низший алкил или низший алкенил, и алк 2 представляет собой низший алкил или низший алкенил. Термин "арилоксиалкил" относится к группе -алкил-О-арил. Термин "аралкоксиалкил" относится к группе -алкиленил-О-аралкил, где аралкил представляет собой низший аралкил. Термин "алкоксиалкиламино" относится к группе -NR-(алкоксиалкил), где R представляет обычно водород, низший аралкил, или низший алкил. Термин "амино-низший алкоксиалкил" относится к аминоалкоксиалкилу, в котором алкоксиалкил представляет собой низший алкоксиалкил. Термин "аминокарбонил" относится к группе -C(O)-NH2. "Замещенный аминокарбонил" относится к группе -C(O)-NRR', где R представляет собой низший алкил и R' представляет собой водород или низший алкил. Термин "ариламинокарбонил" относится к группе -C(O)-NRR', где R представляет собой арил и R' представляет собой водород, низший алкил или арил. Термин "аралкиламинокарбонил" относится к группе -C(O)-NRR', где R представляет собой низший аралкил и R' представляет собой водород, низший алкил, арил или низший аралкил."Аминосульфонил" относится к группе -S(O)2-NH2. "Замещенный аминосульфонил" относится к группе -S(O)2-NRR', где R представляет собой низший алкил и R' представляет собой водород или низший алкил. Термин "аралкиламиносульфониларил" относится к группе -арил-S(О)2-NН-аралкил, где аралкил представляет низший аралкил."Карбонилокси" относится, как правило, к группе -С(О)-О. Указанные группы включают сложные эфиры, -C(O)-O-R, где R представляет собой низший алкил, циклоалкил, арил или низший аралкил. Термин "карбонилоксициклоалкил" относится обычно как к "карбонилоксикарбоциклоалкилу", так и к "карбонилоксигетероциклоалкилу", т.е, где R представляет собой карбоциклоалкил или гетероциклоалкил соответственно. Термин "арилкарбонилокси" относится к группе -С(О)-О-арил, где арил представляет моно- или полицикликлическую структуру, карбоциклоарил или гетероциклоарил. Термин "аралкилкарбонилокси" относится к группе -С(О)-О-аралкил, где аралкил представляет собой низший аралкил. Термин "сульфонил" относится к группе -SO2-."Алкилсульфонил" относится к замещенному сульфонилу структуры -SO2R-, в которой R представляет алкил. Алкилсульфонильные группы, используемые в настоящем изобретении, представляют обычно низший алкилсульфонильные группы, содержащие от 1 до 6 атомов углерода в своей основной структуре. Таким образом, типичные алкилсульфонильные группы в соединениях настоящего изобретения включают, например, метилсульфонил (т.е. где R представляет метил), этилсульфонил (т.е. где R представляет этил), пропилсульфонил (т.е. где R представляет пропил) и т.п. Термин "арилсульфонил" относится к группе -SO2-арил. Термин "аралкилсульфонил" относится к группе -SO2-аралкил, в которой аралкил представляет собой низший аралкил. Термин "сульфонамидо" относится к -SO2NH2. Используемый термин "карбониламино" относится к двухвалентной группе -NH-C(O)-, в которой атом водорода амидного азота карбониламиногруппы может быть заменен низшей алкильной, арильной или низшей аралкильной группой. Указанные группы включают части, такие как карбаматные сложные эфиры (-NH-C(O)-O-R) и амиды -NH-C(О)-O-R, где R представляет низший алкил с прямой или разветв-6 007987 ленной цепью, циклоалкил или арил или низший аралкил. Термин "низший алкилкарбониламино" относится к алкилкарбониламино, где R представляет низший алкил, содержащий от 1 до около 6 атомов углерода в своей основной структуре. Термин "арилкарбониламино" относится к группе -NH-C(O)-R, где R представляет арил. Аналогично, термин "аралкилкарбониламино" относится к карбониламино, где R представляет низший аралкил. Используемый термин "аминокарбонил" относится к двухвалентной группе -C(O)-NH-, где атом водорода амидного азота карбониламиногруппы может быть заменен низшей алкильной, арильной или низшей аралкильной группой, как описано выше. Используемый термин "гуанидино" или "гуанидил" относится к частям, производным от гуанидина,H2N-C(=NH)-NH2-. Указанные части включают части, присоединенные к атому азота, несущему формальную двойную связь (положение 2 гуанидина, например, диаминоэтиленамино, (H2N)2C=NH-) и части, присоединенные к любому из атомов азота, несущему формальную одинарную связь (положение 1 и/или 3 гуанидина, например, H2N-C(=NH)-NH-). Атомы водорода при любом из атомов азота могут быть заменены подходящим заместителем, таким как низший алкил, арил или низший аралкил. Используемый термин "амидино" относится к частям R-C(=N)-NR'- (при этом радикал находится при N1 азоте) и R(NR')C=N- (при этом радикал находится при N2 азоте), где R и R' могут быть водородом,низшим алкилом, арилом или низшим аралкилом."Циклоалкил" относится к моно- или полициклическому, гетероциклическому или карбоциклическому алкильному заместителю. Типичные циклоалкильные заместители содержат от 3 до 8 атомов в основной структуре (т.е. кольце), где каждый основной атом представляет собой либо углерод, либо гетероатом. Термин "гетероциклоалкил" относится к циклоалкильным заместителям, которые содержат от 1 до 5 и более предпочтительно от 1 до 4 гетероатомов в циклической структуре. Подходящими гетероатомами в соединениях настоящего изобретения являются азот, кислород и сера. Репрезентативные гетероциклоалкильные части включают, например, морфолино, пиперазинил, пиперадинил и т.п. Карбоциклоалкильные группы представляют собой циклоалкильные группы, в которых все атомы кольца являются углеродами. При использовании в связи с циклоалкильными заместителями, термин "полициклический" относится к конденсированным и неконденсированным алкилциклическим структурам. Термин "замещенный гетероцикл" или "гетероциклическая группа" или гетероцикл, используемый в данном описании, относится к любому 3- или 4-членному кольцу, содержащему гетероатом, выбранный из азота, кислорода и серы, или к 5- или 6-членному кольцу, содержащему от одного до трех гетероатомов, выбранных из группы, состоящей из азота, кислорода или серы; где 5-членное кольцо содержит 0-2 двойные связи и 6-членное кольцо содержит 0-3 двойные связи; где атомы азота и серы могут быть необязательно в окисленной форме; где гетероатомы азота и серы могут быть необязательно кватернизированы; и включая любую бициклическую группу, в которой любая из вышеуказанных гетероциклических структур конденсирована с бензольным кольцом или другой 5- или 6-членной гетероциклической структурой, независимо определенной выше. Таким образом, термин "гетероцикл" включает кольца, в которых азот является гетероатомом, а также частично и полностью насыщенные циклы. Предпочтительные гетероциклы включают, например: диазапинил, пиррил, пирролинил, пирролидинил, пиразолил, пиразолинил, пиразолидинил, имидазоил, имидазолинил, имидазолидинил, пиридил, пиперидинил, пиразинил, пиперазинил, N-метилпиперазинил, азетидинил, N-метилазетидинил, пиримидинил, пиридазинил, оксазолил, оксазолидинил, изоксазолил, изоазолидинил, морфолинил, тиазолил, тиазолидинил, изотиазолил, изотиазолидинил, индолил, хинолинил, изохинолинил, бензимидазолил, бензотиазолил, бензоксазолил, фурил, тиенил, триазолил и бензотиенил. Гетероциклические части могут быть незамещенными или монозамещены или дизамещены различными заместителями, независимо выбранными из гидрокси, галогена, оксо(С=O), алкиламино (RN=, гдеR представляет собой низшую алкильную или низшую алкоксигруппу), амино, алкиламино, диалкиламино, ациламиноалкила, алкокси, тиоалкокси, полиалкокси, низшего алкила, циклоалкила или галогеналкила. Гетероциклические группы могут быть присоединены в различных положениях, как это очевидно специалистам в области органической и медицинской химии из рассмотрения настоящего описания."Арил" относится к необязательно замещенным моноциклическим и полициклическим ароматическим группам, содержащим в основной структуре от 3 до 14 атомов углерода или гетероатомов, и включает как карбоциклические арильные группы, так и гетероциклические арильные группы. Карбоциклические арильные группы представляют собой арильные группы, в которых все атомы кольца в ароматическом кольце являются углеродами. Термин "гетероарил" относится к арильным группам, содержащим от 1 до 4 гетероатомов в качестве атомов кольца в ароматическом кольце, при этом остальные атомы кольца являются атомами углерода. При использовании в связи с арильными заместителями, термин "полициклический арил" относится к конденсированным и неконденсированным циклическим структурам, в которых по крайней мере одна циклическая структура является ароматической, такой как, например, бензодиоксозоло (который содержит гетероциклическую структуру, конденсированную с фенильной груп, нафтил и т.п. Иллюстративные арильные части в качестве заместителей в соединениях пой, т.е. настоящего изобретения включают фенил, пиридил, пиримидинил, тиазолил, индолил, имидазолил, оксадиазолил, тетразолил, пиразинил, триазолил, тиофенил, фуранил, хинолинил, пуринил, нафтил, бензотиазолил, бензопиридил и бензимидазолил и т.п."Аралкил" относится к алкильной группе, замещенной арильной группой. Обычно, аралкильные группы в соединениях настоящего изобретения содержат от 1 до 6 атомов углерода, включенных в состав алкильной части аралкильной группы. Подходящие аралкильные группы в соединениях настоящего изобретения включают, например, бензил, пиколил и т.п. Репрезентативные гетероарильные группы включают, например, группы, представленные ниже. Кроме того, эти гетероарильные группы могут быть замещены и могут быть присоединены в различных положениях, как это очевидно специалистам в области органической и медицинской химии из рассмотрения настоящего описания. Репрезентативные гетероарилы включают, например, имидазолил, пиридил, пиперазинил, азетидинил, тиазолил, триазолил, бензимидазолил, бензотиазолил и бензоксазолил. Термин "биарил" относится к группе или заместителю, в котором две арильные группы, будучи не конденсированными друг с другом, являются связанными. Иллюстративные примеры биарильных соединений включают, например, фенилбензол, дифенилдиазен, 4-метилтио-1-фенилбензол, феноксибензол, (2-фенилэтинил)бензол, дифенилкетон, (4-фенилбута-1,3-диинил)бензол, фенилбензиламин, (фенилметокси)бензол и т.п. Предпочтительные необязательно замещенные биарильные группы включают 2-(фениламино)-N-[4-(2-фенилэтинил)фенил]ацетамид,1,4-дифенилбензол,N-[4-(2-фенилэтинил)фенил]-2-[бензиламино]ацетамид,2-амино-N-[4-(2-фенилэтинил)фенил]пропанамид,2-амино-N-[4-(2-фенилэтинил)фенил]ацетамид,2-(циклопропиламино)-N-[4-(2-фенилэтинил)фенил]ацетамид,2-(этиламино)-N-[4-(2-фенилэтинил)фенил]ацетамид,2-[(2-метилпропил)амино]-N-[4-(2-фенилэтинил)фенил]ацетамид,5-фенил-2 Н-бензо[d]-1,3-диоксолен,2-хлор-1-метокси-4-фенилбензол,2-[(имидазолилметил)амино]-N-[4-(2-фенилэтинил)фенил]ацетамид,4-фенил-1-феноксибензол,N-(2-аминоэтил)-[4-(2-фенилэтинил)фенил]карбоксамид,2-[(4-фторфенил)метил]амино-N-[4-(2-фенилэтинил)фенил]ацетамид,2-[(4-метилфенил)метил]амино-N-[4-(2-фенилэтинил)фенил]ацетамид,4-фенил-1-(трифторметил)бензол,1-бутил-4-фенилбензол,2-(циклогексиламино)-N-[4-(2-фенилэтинил)фенил]ацетамид,2-(этилметиламино)-N-[4-(2-фенилэтинил)фенил]ацетамид,2-(бутиламино)-N-[4-(2-фенилэтинил)фенил]ацетамид,N-[4-(2-фенилэтинил)фенил]-2-(4-пиридиламино)ацетамид,N-[4-(2-фенилэтинил)фенил]-2-(хинуклидин-3-иламино)ацетамид,N-[4-(2-фенилэтинил)фенил]пирролидин-2-илкарбоксамид,2-амино-3-метил-N-[4-(2-фенилэтинил)фенил)бутанамид,4-(4-фенилбута-1,3-диинил)фениламин,2-(диметиламино)-N-[4-(4-фенилбута-1,3-диинил)фенил]ацетамид,2-(этиламино)-N-[4-(4-фенилбута-1,3-диинил)фенил]ацетамид,4-этил-1-фенилбензол,1-[4-(2-фенилэтинил)фенил]этан-1-он,N-(1-карбамоил-2-гидроксипропил)[4-(4-фенилбута-1,3-диинил)фенил]карбоксамид,N-[4-(2-фенилэтинил)фенил]пропанамид,-9 007987 4-метоксифенилфенилкетон,фенил-N-бензамид,(трет-бутокси)-N-[(4-фенилфенил)метил]карбоксамид,2-(3-фенилфенокси)этангидроксамовую кислоту,3-фенилфенилпропаноат,1-(4-этоксифенил)-4-метоксибензол и[4-(2-фенилэтинил)фенил]пиррол. Термин "гетероариларил" относится к биарильной группе, где одна из арильных групп представляет собой гетероарильную группу. Иллюстративные примеры гетероариларильных групп включают, например, 2-фенилпиридин, фенилпиррол, 3-(2-фенилэтинил)пиридин, фенилпиразол, 5-(2-фенилэтинил)-1,3 дигидропиримидин-2,4-дион, 4-фенил-1,2,3-тиадиазол, 2-(2-фенилэтинил)пиразин, 2-фенилтиофен, фенилимидазол, 3-(2-пиперазинилфенил)фуран, 3-(2,4-дихлорфенил)-4-метилпиррол и т.п. Предпочтительные необязательно замещенные гетероариларильные группы включают 5-(2-фенилэтинил)пиримидин-2-иламин,1-метокси-4-(2-тиенил)бензол,1-метокси-3-(2-тиенил) бензол,5-метил-2-фенилпиридин,5-метил-3-фенилизоксазол,2-[3-(трифторметил)фенил]фуран,3-фтор-5-(2-фурил)-2-метокси-1-проп-2-енилбензол,(гидроксиимино)(5-фенил(2-тиенилметан,5-[(4-метилпиперазинил)метил]-2-фенилтиофен,2-(4-этилфенил)тиофен,4-метилтио-1-(2-тиенил)бензол,2-(3-нитрофенил)тиофен,(трет-бутокси)-N-[(5-фенил(3-пиридилметил]карбоксамид,гидрокси-N-[(5-фенил(3-пиридилметил]амид,2-(фенилметилтио)пиридин и бензилимидазол. Термин "гетероарилгетероарил" относится к биарильной группе, где обе из арильных групп представляют собой гетероарильную группу. Иллюстративные гетероарилгетероарильные группы включают,например, 3-пиридилимидазол, 2-имидазолилпиразин и т.п. Предпочтительные необязательно замещенные гетероарилгетероарильные группы включают 2-(4-пиперазинил-3-пиридил)фуран, диэтил(3 пиразин-2-ил(4-пиридиламин и диметил 2-[2-(5-метилпиразин-2-ил)этинил](4-пиридил)амин."Необязательно замещенный" или "замещенный" относится к замене водорода одновалентным или двухвалентным радикалом. Подходящие замещающие группы включают, например, гидроксил, нитро,амино, имино, циано, галоген, тио, сульфонил, тиоамидо, амидино, имидино, оксо, оксамидино, метоксамидино, имидино, гуанидино, сульфонамидо, карбоксил, формил, низший алкил, галоген-низший алкил, низший алкиламино, галоген-низший алкиламино, низший алкокси, галоген-низший алкокси, низший алкоксиалкил, алкилкарбонил, аминокарбонил, арилкарбонил, аралкилкарбонил, гетероарилкарбонил, гетероаралкилкарбонил, алкилтио, аминоалкил, цианоалкил, арил и т.п. Группа-заместитель может сама по себе быть замещенной. Группой, замещающей на группузаместитель, может быть карбоксил, галоген; нитро, амино, циано, гидроксил, низший алкил, низший алкокси, аминокарбонил, -SR, тиоамидо, -SO3H, -SO2R или циклоалкил, где R представляет, как правило,водород, гидроксил или низший алкил. Когда замещенный заместитель включает группу с прямой цепью, замещение может происходить либо внутри цепи (например, 2-гидроксипропил, 2-аминобутил и т.п.), либо на конце цепи (например, 2 гидроксиэтил, 3-цианопропил и т.п.). Замещенные заместители могут иметь систему ковалентно связанных углеродных атомов или гетероатомов в пределах прямой цепи, разветвленной или циклической структуры. Используемый термин "карбоксизащитная группа" относится к карбонильной группе, которая этерифицирована одной из обычно используемых, защищающих карбоновую кислоту, сложноэфирных групп, применяемых для блокирования или защиты функции карбоновой кислоты, во время осуществления реакции с участием других функциональных групп соединения. Кроме того, карбоксизащитная группа может быть прикреплена к твердой подложке, посредством чего соединение остается связанным с твердой подложкой в виде карбоксилата до его отщепления гидролитическими методами для высвобождения соответствующей свободной кислоты. Иллюстративные карбоксизащитные группы включают,например, сложные низшие алкиловые эфиры, вторичные амиды и т.п. Используемый термин "фармацевтически приемлемые соли" относится к солям нетоксичных кислот или щелочно-земельных металлов соединений формулы I. Указанные соли можно получить in situ во время конечного выделения и очистки соединений формулы I или путем отдельного взаимодействия функций основания или кислоты с подходящей органической или неорганической кислотой или основанием соответственно. Репрезентативные соли включают, но не ограничиваясь ими, следующие: ацетат,- 10007987 адипат, альгинат, цитрат, аспартат, бензоат, бензолсульфонат, бисульфат, бутират, камфорат, камфорсульфонат, диглюконат, циклопентанпропионат, додецилсульфат, этансульфонат, глюкогептаноат, глицерофосфат, гемисульфат, гептаноат, гексаноат, фумарат, гидрохлорид, гидробромид, гидроиодид, 2 гидроксиэтансульфонат, лактат, малеат, метансульфонат, никотинат, 2-нафталинсульфонат, оксалат, памоат, пектинат, персульфат, 3-фенилпропионат, пикрат, пивалат, пропионат, сукцинат, сульфат, тартрат,тиоцианат, п-толуолсульфонат и ундеканоат. Кроме того, основные азотсодержащие группы могут быть кватернизированы такими средствами, как низшие алкилгалогениды, например метил-, этил-, пропил- и бутилхлоридами, бромидами и иодидами; диалкилсульфатами, подобными диметил-, диэтил-, дибутил- и диамилсульфатам, длинноцепочечными галогенидами, такими как децил-, лаурил-, миристил- и стеарилхлориды, бромиды и иодиды, аралкилгалогенидами, подобными бензил- и фенетилбромидам, и другими. Таким образом получают растворимые или диспергируемые в воде или масле продукты. Примеры кислот, которые могут быть использованы для получения фармацевтически приемлемых аддитивных солей кислоты, включают такие неорганические кислоты, как хлористо-водородная кислота,серная кислота и фосфорная кислота, и такие органические кислоты, как щавелевая кислота, малеиновая кислота, метансульфокислота, янтарная кислота и лимонная кислота. Аддитивные соли основания можно получить in situ во время конечного выделения и очистки соединений формулы (I) или отдельно взаимодействием частей карбоновой кислоты с подходящим основанием, таким как гидроксид, карбонат или бикарбонат фармацевтически приемлемого катиона-металла или с аммиаком, или органическим первичным, вторичным или третичным амином. Фармацевтически приемлемые соли включают, но не ограничиваясь ими, катионы на основе щелочных и щелочно-земельных металлов, такие как соли натрия, лития, калия, кальция, магния, алюминия и т.п., а также нетоксичные катионы аммония, кватернизированного аммония и аминов, включая, но не ограничиваясь ими, аммоний, тетраметиламмоний, тетраэтиламмоний, метиламин, диметиламин, триметиламин, триэтиламин, этиламин и т.п. Другие репрезентативные органические амины, используемые для образования аддитивных солей основания, включают диэтиламин, этилендиамин, этаноламин, диэтаноламин, пиперазин и т.п. Используемый термин "фармацевтически приемлемый сложный эфир" относится к сложным эфирам, которые гидролизуются in vivo и включают сложные эфиры, которые легко разрушаются в организме человека, высвобождая исходное соединение или его соль. Подходящие сложноэфирные группы включают, например, группы, полученные из фармацевтически приемлемых алифатических карбоновых кислот, в частности, алкановых, алкеновых, циклоалкановых и алкандиовых кислот, в которых каждая алкильная или алкенильная часть преимущественно содержит не более чем 6 углеродных атомов. Примеры конкретных сложных эфиров включают формиаты, ацетаты, пропионаты, бутираты, акрилаты и этилсукцинаты. Термин "фармацевтически приемлемые пролекарства", используемый в данном описании, относится к таким пролекарствам соединений настоящего изобретения, которые в пределах обоснованной медицинской оценки являются подходящими для использования для приведения в контакт с тканями людей и низших животных без проявления токсичности, раздражения, аллергической реакции и т.п., соизмеримых с разумным отношением польза/риск, и эффективными для их предполагаемого применения, а также цвиттер-ионным формам, когда они возможны, соединений данного изобретения. Термин "пролекарство" относится к соединениям, которые быстро трансформируются in vivo, с получением исходного соединения приведенной выше формулы, например, при гидролизе в крови. Исчерпывающее обсуждение вышеупомянутого представлено в Т. Higuchi and V. Stella, Pro-drugs as Novel Delivery Systems, vol. 14 ofPharmaceutical Association and Pergamon Press, 1987, содержание которых включено в настоящее описание в виде ссылки. Термин "рак" относится к раковым болезням, которые могут быть благоприятным образом подвергнуты лечению путем ингибирования киназы Raf, включая, например, солидные злокачественные образования, такие как карциномы (например, легких, поджелудочной железы, щитовидной железы, мочевого пузыря или толстой кишки), миелоидные расстройства (например, миелоидный лейкоз) и аденомы (например, ворсинчатая аденома толстой кишки). В иллюстративных вариантах осуществления настоящего изобретения A1 может представлять, например, фенил, который может быть замещен одним или несколькими заместителями, выбранными из группы, состоящей из гидроксила, нитро, циано, галогена, и замещенного или незамещенного амино,имино, тио, сульфонила, тиоамидо, амидино, имидино, оксо, оксамидино, метоксамидино, имидино, гуанидино, сульфонамидо, карбоксила, формила, низшего алкила, галоген-низшего алкила, низшего алкиламино, галоген-низшего алкиламино, низшего алкокси, галоген-низшего алкокси, низшего алкоксиалкила, алкилкарбонила, аминокарбонила, низшего алкиламинокарбонила, гетероциклоалкил-низший алкиламинокарбонила, карбокси-низший алкиламинокарбонила, арилкарбонила, аралкилкарбонила, гетероарилкарбонила, гетероаралкилкарбонила, алкилтио, аминоалкила, цианоалкила, арила и т.п. В других иллюстративных вариантах осуществления данного изобретения, A2 может представлять собой, например, пиридил, который может быть замещен одним или несколькими заместителями, выбранными из группы, состоящей из гидроксила, нитро, циано, галогена, и замещенного или незамещенного амино,- 11007987 имино, тио, сульфонила, тиоамидо, амидино, имидино, оксо, оксамидино, метоксамидино, имидино, гуанидино, сульфонамидо, карбоксила, формила, низшего алкила, галоген-низшего алкила, низшего алкиламино, галоген-низшего алкиламино, низшего алкокси, галоген-низшего алкокси, низшего алкоксиалкила, алкилкарбонила, аминокарбонила, низшего алкиламинокарбонила, гетероциклоалкил-низший алкиламинокарбонила, карбоксил-низший алкиламинокарбонила, арилкарбонила, аралкилкарбонила, гетероарилкарбонила, гетероаралкилкарбонила, алкилтио, аминоалкила, цианоалкила, арила и т.п. В репрезентативных вариантах осуществления изобретения, соединения изобретения включают,например,4-[(2-[4-хлор-3-(трифторметил)фенил]амино-1 Н-бензимидазол-6-ил)окси]-N-метилпиридин-2 карбоксамид,4-(2-[(3-хлорфенил)амино]-1 Н-бензимидазол-6-илокси)-N-метилпиридин-2-карбоксамид,4-(2-[(4-бромфенил)амино]-1 Н-бензимидазол-6-илокси)-N-метилпиридин-2-карбоксамид,4-(2-[(3-хлор-4-фторфенил)амино]-1 Н-бензимидазол-6-илокси)-N-метилпиридин-2-карбоксамид,N-метил-4-[2-(фениламино)-1 Н-бензимидазол-6-ил]оксипиридин-2-карбоксамид,4-[(2-[4-бром-2-(трифторметил)фенил]амино-1 Н-бензимидазол-6-ил)окси]-N-метилпиридин-2 карбоксамид,N-метил-4-(2-[(2-метилпропил)амино]-1 Н-бензимидазол-6-илокси)пиридин-2-карбоксамид,4-[(2-[4-(диметиламино)нафталин-1-ил]амино-1 Н-бензимидазол-6-ил)окси]-N-метилпиридин-2 карбоксамид,N-метил-4-(2-[(4-нитрофенил)амино]-1 Н-бензимидазол-6-илокси)пиридин-2-карбоксамид,N-метил-4-(2-[(фенилкарбонил)амино]-1 Н-бензимидазол-6-илокси)пиридин-2-карбоксамид,N-метил-4-(2-[(фенилметил)амино]-1 Н-бензимидазол-6-илокси)пиридин-2-карбоксамид,метил 4-[6-(2-[(метиламино)карбонил]пиридин-4-илокси)-1 Н-бензимидазол-2-ил]аминобензоат,4-(2-[(4-хлорфенил)амино]-1 Н-бензимидазол-6-илокси)-N-метилпиридин-2-карбоксамид,4-[(2-[2-(этилокси)фенил]амино-1 Н-бензимидазол-6-ил)окси]-N-метилпиридин-2-карбоксамид,N-метил-4-(2-[(2-морфолин-4-илэтил)амино]-1 Н-бензимидазол-6-илокси)пиридин-2-карбоксамид,4-(2-[(4-иодфенил)амино]-1 Н-бензимидазол-6-илокси)-N-метилпиридин-2-карбоксамид,N-метил-4-[(2-[4-(трифторметил)фенил]амино-1 Н-бензимидазол-6-ил)окси]пиридин-2-карбоксамид,4-(2-[(фуран-2-илметил)амино]-1 Н-бензимидазол-6-илокси)-N-метилпиридин-2-карбоксамид,4-(2-[(4-бром-3-метилфенил)амино]-1 Н-бензимидазол-6-илокси)-N-метилпиридин-2-карбоксамид,4-(2-[(4-ацетилфенил)амино]-1 Н-бензимидазол-6-илокси)-N-метилпиридин-2-карбоксамид,N-метил-4-(2-[(2,4,6-триметилфенил)амино]-1 Н-бензимидазол-6-илокси)пиридин-2-карбоксамид,4-[(2-[4-(1,1-диметилэтил)фенил]амино-1 Н-бензимидазол-6-ил)окси]-N-метилпиридин-2-кароксамид,4-(2-[(2-бромфенил)амино]-1 Н-бензимидазол-6-илокси)-N-метилпиридин-2-карбоксамид,4-(2-[(3-бромфенил)амино]-1 Н-бензимидазол-6-илокси)-N-метилпиридин-2-карбоксамид,4-(2-[(2-хлорфенил)амино]-1 Н-бензимидазол-6-илокси)-N-метилпиридин-2-карбоксамид,метил 3-[6-(2-[(метиламино)карбонил]пиридин-4-илокси)-1 Н-бензимидазол-2-ил]аминотиофен 2-карбоксилат,4-(2-[(4-бромфенил)амино]-1 Н-бензимидазол-6-илокси)-N-(3R,5R)-5-[(метилокси)метил] пирролидин-3-илпиридин-2-карбоксамид,4-(2-[(4-бромфенил)амино]-1-метил-1 Н-бензимидазол-5-илокси)-N-метилпиридин-2-карбоксамид,4-[(2-[4-хлор-3-(трифторметил)фенил]амино-1-метил-1 Н-бензимидазол-5-ил)окси]-N-метилпиридин-2-карбоксамид,N-метил-4-[(1-метил-2-[4-(трифторметил)фенил]амино-1 Н-бензимидазол-5-ил)окси]пиридин-2 карбоксамид,4-(2-[(4-бромфенил)амино]-1-метил-1 Н-бензимидазол-5-илокси)-N-этилпиридин-2-карбоксамид,4-(2-[(4-бромфенил)амино]-1-метил-1 Н-бензимидазол-5-илокси)-N-(2-гидроксиэтил)пиридин-2 карбоксамид,4-(2-[(4-бромфенил)амино]-1-метил-1 Н-бензимидазол-5-илокси)-N,N-диметилпиридин-2-карбоксамид,4-(2-[(4-бромфенил)амино]-1-метил-1 Н-бензимидазол-5-илокси)-N-(2,2,2-трифторэтил)пиридин 2-карбоксамид,N-(4-бромфенил)-1-метил-5-[2-(пирролидин-1-илкарбонил)пиридин-4-ил]окси-1 Н-бензимидазол 2-амин,этил (3R)-3-(метилокси)-4-[(4-[(2-[4-(трифторметил)фенил]амино-1 Н-бензимидазол-5-ил)окси] пиридин-2-илкарбонил)амино]пиперидин-1-карбоксилат,4-(2-[(4-бромфенил)амино]-1-метил-1 Н-бензимидазол-5-илокси)-N-[2-(диметиламино)этил]пиридин-2-карбоксамид,- 12007987 4-(2-[(4-бромфенил)амино]-1-метил-1 Н-бензимидазол-5-илокси)-N-(тетрагидрофуран-2-илметил) пиридин-2-карбоксамид,4-(2-[(4-бромфенил)амино]-1-метил-1 Н-бензимидазол-5-илокси)-N-(2-морфолин-4-илэтил)пиридин-2-карбоксамид,4-(2-[(4-бромфенил)амино]-1-метил-1 Н-бензимидазол-5-илокси)-N-(пиперидин-4-илметил) пиридин-2-карбоксамид,5-(2-[(3-аминопирролидин-1-ил)карбонил]пиридин-4-илокси)-N-(4-бромфенил)-1-метил-1 Нбензимидазол-2-амин,4-(2-[(4-бромфенил)амино]-1-метил-1 Н-бензимидазол-5-илокси)-N-[1-(дифенилметил)азетидин-3 ил]пиридин-2-карбоксамид,4-(2-[(4-бромфенил)амино]-1-метил-1 Н-бензимидазол-5-илокси)-N-пиперидин-3-илпиридин-2 карбоксамид,4-(2-[(4-бромфенил)амино]-1-метил-1 Н-бензимидазол-5-илокси)-N-(1,3-тиазол-2-ил)пиридин-2 карбоксамид,4-(2-[(4-бромфенил)амино]-1-метил-1 Н-бензимидазол-5-илокси)-N-[(1-этилпирролидин-2-ил) метил]пиридин-2-карбоксамид,(4-2-[(4-бромфенил)амино]бензотиазол-5-илокси(2-пиридил-N-метилкарбоксамид,(4-2-[(4-бромфенил)амино]бензоксазол-5-илокси(2-пиридил-N-метилкарбоксамид и другие репрезентативные соединения, представленные в примерах. В других аспектах настоящее изобретение относится к способам получения соединений формул I,II, III, IV и V и к синтетическим промежуточным продуктам, используемым в указанных способах. Соединения данного изобретения включают асимметрично замещенные атомы углерода. Такие асимметрично замещенные атомы углерода могут приводить к соединениям данного изобретения, представляющих собой смеси стереоизомеров, у которых имеется конкретный асимметрично замещенный атом углерода, или к отдельному стереоизомеру. В результате, рацемические смеси, смеси диастереомеров, а также отдельные диастереомеры соединений данного изобретения, все, входят в объем настоящего изобретения. Термины "S" и "R" конфигурация, используемые в данном описании, определены согласно(1976). Терминыииспользуют для положений кольца циклических соединений. -сторона плоскости отсчета является стороной, на которой расположен предпочтительный заместитель в положении низшей нумерации. Заместителям же, лежащим на противоположной стороне плоскости отсчета, приписывают дескриптор . Следует отметить, что это употребление отличается от употребления в случае циклических стереоисточников, в которыхозначает положение "под плоскостью" и означает абсолютную конфигурацию. Терминыиконфигурация, используемые в этом случае, являются такими, как они определены согласно CHEMICAL ABSTRACTS INDEX GUIDE-APPENDIX IV (1987) paragraph 203. Кроме того, настоящее изобретение относится к способам получения соединений изобретения и к синтетическим промежуточным продуктам, используемым в указанных способах, как это описано подробно ниже. Способы синтеза Соединения данного изобретения, содержащие ядро бензимидазола, можно получить, используя ряд способов, известных квалифицированному специалисту в данной области. В одном способе, надлежащим образом функционализированные диамины могут быть связаны с различными тиоизоцианатами с получением промежуточных продуктов, тиомочевин. Циклизация с образованием части бензимидазола может быть осуществлена в известных условиях, как, например, обработкой карбодиимидами или алкилгалогенидами, как это видно на следующих схемах. Схема Альтернативно, диамины могут быть подвергнуты взаимодействию, последовательно, с карбонилдиимидазолом и фосфорилхлоридом с последующим связыванием с соответствующим амином. Соединения, содержащие структуру оксазола, можно аналогично получить согласно приведенным выше способам или согласно другим известным общим методикам. Haviv et al. (J. Med. Chem. 1988,31:1719) описывает способ сборки ядер оксазола, где гидроксианилин обрабатывают этилксантогенатом калия. Затем полученный сульфурилбензоксазол может быть хлорирован и подвергнут связыванию с амином. Соединения, содержащие ядро бензотиазола, можно также получить известными способами. Ортогалогентиоизоцианат может быть подвергнут взаимодействию с амином с получением тиомочевины. Затем восстановление при помощи NaH дает возможность образования циклической структуры тиазола. Бензотиазолы могут быть обычно замещены в соответствии с настоящим изобретением, следуя, например, приведенному ниже пути синтеза: Бензоксазолы можно обычно синтезировать следующим путем: Соединения данного изобретения используют in vitro или in vivo для ингибирования роста раковых клеток. Соединения можно использовать как таковые или в композициях вместе с фармацевтически приемлемым носителем или эксципиентом. Подходящие фармацевтически приемлемые носители или эксципиенты включают, например, средства для (технологической) обработки и модификаторы для доставки лекарственных средств и энхансеры, такие как, например, фосфат кальция, стеарат магния, тальк, моносахариды, дисахариды, крахмал,желатин, целлюлоза, метилцеллюлоза, натрий карбоксиметилцеллюлоза, декстроза, гидроксипропил-циклодекстрин, поливинилпирролидин, низкоплавкие воски, ионообменные смолы (иониты) и т.п., а также комбинации из любых двух или большего числа из них. Другие подходящие фармацевтически приемлемые наполнители описаны в "Remington's Pharmaceutical Sciences," Mack Pub. Co., New Jersey(1991), включенный в настоящее описание в виде ссылки. Эффективные количества соединений данного изобретения, как правило, включают любое количество, достаточное для того, чтобы значимо ингибировать активность Raf согласно любому из описываемых в данном описании испытаний, согласно другим испытаниям активности киназы Raf, известным специалистам в данной области, или путем детектирования ингибирования или облегчения симптомов рака. Количество активного ингредиента, которое может быть объединено с веществами-носителями,чтобы получить разовую лекарственную форму, будет варьироваться в зависимости от хозяина, подлежащего лечению, и конкретного пути введения. Однако очевидно, что конкретный уровень дозы для любого отдельного пациента будет зависеть от ряда факторов, включая активность конкретного используемого соединения, возраста, массы тела, общего состояния здоровья, пола, диеты, времени введения, пути введения, скорости выделения, комбинации лекарственных средств и тяжести конкретной болезни, подвергающейся лечению. Терапевтически эффективное количество для данной ситуации может быть легко установлено повседневным экспериментированием и выбор его находится в пределах квалификации и оценки практикующего врача. Для целей настоящего изобретения, терапевтически эффективная доза, как правило, составляет общую суточную дозу, вводимую хозяину в разовой дозе или разделенных дозах, и эта доза может быть в количествах, например, от 0,001 до 1000 мг/кг массы тела ежедневно и более предпочтительно от 1,0 до 30 мг/кг массы тела ежедневно. Дозированные единичные композиции могут содержать такое количест- 15007987 во кратных единиц, которое составляет суточную дозу. Соединения настоящего изобретения могут вводиться перорально, парентерально, сублингвально,путем аэрозолизации или спрея для ингаляции, ректально или местно в составах лекарственных форм,содержащих обычные нетоксичные фармацевтически приемлемые носители, адъюванты и наполнители,как требуется. Кроме того, местное применение может включать использование трансдермального введения, такого как трансдермальные пластыри или устройства для ионофореза. Термин парентеральный,используемый в данном описании, включает подкожные инъекции, внутривенную, внутримышечную,внутригрудинную инъекцию или методы инфузии. Инъецируемые препараты, например, стерильные инъецируемые водные или маслянистые суспензии, могут быть формулированы в соответствии с известным в данной области использованием подходящих диспергирующих или увлажняющих средств и суспендирующих средств. Стерильный инъецируемый препарат может также представлять собой стерильный инъецируемый раствор или суспензию в нетоксичном, приемлемом для парентерального введения разбавителе или растворителе, например, в виде раствора в 1,3-пропандиоле. Среди приемлемых наполнителей и растворителей, которые могут быть использованы, вода, раствор Рингера и изотонический раствор хлорида натрия. Кроме того, в качестве растворителя или суспендирующей среды обычно используют стерильные, жирные масла. Для этой цели, может быть использовано любое легкое жирное масло, включая синтетические моно- или диглицериды. Кроме того, жирные кислоты, такие как олеиновая кислота, находят применение в приготовлении инъецируемых препаратов. Суппозитории для ректального введения лекарственного средства можно получить смешиванием лекарственного средства с подходящим, не вызывающим раздражение эксципиентом, таким как масло какао и полиэтиленгликоли, которые являются твердыми веществами при обычных температурах, но жидкими при ректальной температуре и поэтому будут плавиться в прямой кишке и высвобождать лекарственное средство. Твердые лекарственные формы для перорального введения могут включать капсулы, таблетки, пилюли, порошки и гранулы. В указанных твердых лекарственных формах активное соединение может быть смешано по крайней мере с одним инертным разбавителем, таким как сахароза, лактоза или крахмал. Указанные лекарственные формы могут также включать, и это нормальная практика, дополнительные вещества, другие, чем инертные разбавители, например, лубриканты, такие как стеарат магния. В случае капсул, таблеток и пилюль лекарственные формы могут также содержать буферирующие средства. Кроме того, таблетки и пилюли могут быть приготовлены с энтеросолюбильными покрытиями. Жидкие лекарственные формы для перорального введения могут включать фармацевтически приемлемые эмульсии, растворы, суспензии, сиропы и эликсиры, содержащие инертные разбавители, обычно используемые в данной области, такие как вода. Указанные композиции могут также содержать адъюванты, такие как увлажняющие средства, эмульгирующие и суспендирующие средства, циклодекстрины, и подслащивающие вещества, придающие вкус вещества и отдушки. Соединения настоящего изобретения могут быть также введены в форме липосом. Как известно в данной области, липосомы обычно получают из фосфолипидов или других липидных веществ. Липосомы могут быть представлены в виде моно- или многослойных гидратированных жидких кристаллов, которые диспергированы в водной среде. Можно использовать любой нетоксичный, физиологически приемлемый, метаболизируемый липид, способный образовывать липосомы. Предлагаемые композиции в липосомной форме могут содержать, помимо соединения настоящего изобретения, стабилизаторы, консерванты, эксципиенты и т.п. Предпочтительными липидами являются фосфолипиды и фосфатидилхолины (лецитины) как природного происхождения, так и полученные синтетическим путем. Способы получения липосом известны в данной области. См., например, Prescott, Ed., Methods in Cell Biology, vol.XIV, Academic Press, New York, N.W., p. 33 et seq. (1976). Хотя соединения данного изобретения могут быть введены в виде единственного активного фармацевтического средства, их также можно вводить в комбинации с одним или несколькими другими средствами, используемыми для лечения рака. Репрезентативные средства, используемые в комбинации с соединениями данного изобретения для лечения рака, включают, иринотекан, топотекан, демцитабин, 5 флуороурацил, лейковорин карбоплатин, цисплатин, таксаны, тезацитабин, циклофосфамид, винка алкалоиды, иматиниб (Gleevec), антрациклины, ритуксимаб, трастузумаб, а также другие раковые химиотерапевтические средства. Приведенные выше соединения, которые используют в комбинации с соединениями данного изобретения, обычно используют в терапевтических количествах, указанных в Physicians' Desk Reference(PDR) 47th Edition (1993), который включен в настоящее описание в виде ссылки, или их используют в таких терапевтических количествах, которые должны быть известны специалисту в данной области. Соединения данного изобретения и другие противораковые средства можно вводить в рекомендуемой максимальной клинической дозе или при более низких дозах. Уровни дозы активных соединений в композициях данного изобретения могут варьироваться с тем, чтобы получить желаемый терапевтический ответ в зависимости от пути введения, тяжести болезни и реакции пациента. Комбинация лекарственных средств может вводиться в виде раздельных композиций или в виде разовой лекарственной фор- 16007987 мы, содержащей оба средства. При введении в виде комбинации терапевтические средства могут быть сформулированы в виде раздельных композиций, которые дают в одно и то же время или в различное время, или терапевтические средства могут даваться в виде единой композиции. Антиэстрогены, такие как тамоксифен, ингибируют рост рака молочной железы посредством индуцирования подавления клеточного цикла, что требует действия p27Kip, ингибитора клеточного цикла. Недавно было установлено, что активация Ras-Raf-MAP киназного пути изменяет картину фосфорилирования p27Kip так, что его ингибирующая активность в подавлении клеточного цикла ослабляется, способствуя тем самым резистентности к антиэстрогену (Donovan et al., J. Biol. Chem. 276:40888, 2001). Как сообщалось Donovan и др., ингибирование передачи сигнала MAPK посредством обработки ингибитором МЕК изменяет картину фосфорилирования р 27 в раковых клеточных линиях молочной железы, реанимируя уровни гормона, и при этом восстанавливает чувствительность к гормону. Таким образом, в одном аспекте соединения формул (I), (II), (III), (IV) и (V) могут быть использованы для лечения гормонзависимых раков, таких как раки молочной железы и простаты, реверсируя гормонорезистентность,обычно наблюдаемую при приведенных выше раках при лечении обычными противораковыми средствами. В гематологических раках, таких как хронический миелоидный лейкоз (CML), транслокация хромосом ответственна за конститутивно активированную тирозинкиназу BCR-AB1. Пораженные болезнью пациенты чувствительны к Geevec, маленькой молекуле ингибитора тирозинкиназы, в результате ингибирования активности киназы Abl. Однако многие пациенты с прогрессируемой стадией болезни сначала реагируют на Gleevec, однако, затем позже переносят рецидив из-за возникновения мутаций в домене киназы Abl, обуславливающих резистентность. In vitro исследования показали, что BCR-Avl использует путь киназы Raf, чтобы выявить его действия. Кроме того, ингибирование более чем одной киназы в том же самом пути обеспечивает дополнительную защиту против возникновения мутаций, обуславливающих резистентность. Таким образом, в другом аспекте данного изобретения соединения формул (I), (II), (III),(IV) и (V) используют в комбинации по крайней мере с одним дополнительным средством, таким какGleevec, для лечения гематологических раков, таких как хронический миелоидный лейкоз (CML), чтобы реверсировать или предотвратить резистентность по крайней мере к одному дополнительному средству. Настоящее изобретение будет более доступным для понимания после его рассмотрения, ссылаясь на нижеcледующие примеры, которые приводятся в качестве иллюстрации и, как подразумевается, не являются ограничением настоящего изобретения. Репрезентативные боковые цепи для использования в соединениях нижеследующих примеров обычно можно получить в соответствии со следующими методиками. Пример 1. Синтез 4-[(2-[4-хлор-3-(трифторметил)фенил]амино-1 Н-бензимидазол-6-ил)окси]-Nметилпиридин-2-карбоксамида. Соединение 4-[(2-[4-хлор-3-(трифторметил)фенил]амино-1 Н-бензимидазол-6-ил)окси]-N-метилпиридин-2-карбоксамид синтезируют следующим образом: Стадия 1. Синтез 4-[(4-амино-3-нитрофенил)окси]-N-метилпиридин-2-карбоксамида. Смесь, содержащую 4-амино-3-нитрофенол (1 экв.) и бис(триметилсилил)амид калия (2 экв.), перемешивают в диметилформамиде в течение 2 ч при комнатной температуре. К смеси добавляют (4-хлор(2 пиридил-N-метилкарбоксамид (1 экв.) и карбонат калия (1,2 экв.) и перемешивают при 90 С в течение 3 дней. Затем реакционную смесь концентрируют и распределяют между этилацетатом и водой. Органический слой отделяют и промывают насыщенным раствором соли, сушат, фильтруют и концентрируют в вакууме, получая коричневое твердое вещество. Очистка на силикагеле (2% триэтиламин/50% этилацетат в гексане) дает 4-[(4-амино-3-нитрофенил)окси]-N-метилпиридин-2-карбоксамид в виде оранжевого твердого вещества. Продукт дает удовлетворительный ЯМР. ВЭЖХ, 3,39 мин; МС (MS): MH+=289. Стадия 2. Синтез 4-[(3,4-диаминофенил)окси]-N-метилпиридин-2-карбоксамида. Смесь, содержащую [4-(3-амино-4-нитрофенокси)(2-пиридил)]-N-карбоксамид в метаноле с каталитическим количеством 10%Pd/C, гидрируют до исчезновения желтой окраски, получая продукт - амин. ВЭЖХ, 2,5 мин; МС: МН+=259. Стадия 3. Синтез 4-[(2-[4-хлор-3-(трифторметил)фенил]амино-1 Н-бензимидазол-6-ил)окси]-Nметилпиридин-2-карбоксамида. Смесь, содержащую 4-[(3,4-диаминофенил)окси]-N-метилпиридин-2-карбоксамид (1 экв.) и 4-хлор 3-(трифторметил)бензолизотиоцианат (1 экв.) в тетрагидрофуране, перемешивают при комнатной температуре в течение 16 ч, получая соответствующую тиомочевину. К полученной смеси добавляют гидро- 17007987 хлорид 1-этил-3-(3-диметиламинопропил)карбодиимида (2 экв.) и смесь перемешивают в течение еще 10 ч. Смесь концентрируют и распределяют между этилацетатом и водой. Органический слой промывают насыщенным раствором соли и сушат. Очистка ВЭЖХ дает 4-[(2-[4-хлор-3-(трифторметил)фенил]амино-1 Н-бензимидазол-6-ил)окси]-N-метилпиридин-2-карбоксамид. МС: МН+=462. Примеры 2-108. Соединения, представленные в табл. 1 (примеры 2-108), получают, следуя методике, описанной в примере 1. Таблица 1- 29007987 Пример 109. Синтез (4-2-[(4-бромфенил)амино]бензотиазол-5-илокси(2-пиридил-N-метилкарбоксамида. Стадия 1. Синтез 2-бром-5-метоксибензотиазола. Раствор брома (3,6 экв.) в хлороформе (0,75 М) добавляют по каплям в течение периода 1 ч к перемешиваемой суспензии 5-метокси-2-меркаптобензотиазола (1 экв.) в хлороформе при 0 С. Смесь перемешивают в течение 30 мин, затем ее медленно добавляют к воде и перемешивают еще 20 мин. Смесь фильтруют, чтобы удалить твердое вещество кремового цвета. Органическую фазу сушат и упаривают до образования остатка в виде коричневого твердого вещества. Коричневое твердое вещество растворяют в простом эфире и фильтруют. Остаток промывают простым эфиром, фильтрат и промывные воды объединяют и упаривают, хроматографируют (гексаны и этилацетат 4:1), получая указанное в заголовке соединение в виде бледно-желтого твердого вещества. МС: МН+=244. Стадия 2. Синтез (4-бромфенил)(5-метоксибензотиазол-2-ил)амина. Смесь, содержащую 2-бром-5-метоксибензотиазол (1 экв.), 4-броманилин (2 экв.) и диизопропилэтиламин, подвергают микроволновой обработке в NMP при 220 С. Полученную смесь концентрируют и распределяют между этилацетатом и водой. Органический слой промывают насыщенным раствором соли и сушат. Очистка на силикагеле дает желаемый продукт. МС: МН+=335. Стадия 3. Синтез 2-[(4-бромфенил)амино]бензотиазол-5-ола. Смесь (4-бромфенил)(5-метоксибензотиазол-2-ил)амина и бромисто-водородной кислоты (48%) подвергают микроволновой обработке при 150 С в течение 6 мин, получая желаемый продукт. МС: МН+=321. Стадия 4. Синтез (4-2-[(4-бромфенил)амино]бензотиазол-5-илокси(2-пиридил-N-метилкарбоксамида. Смесь, содержащую 2-[(4-бромфенил)амино]бензотиазол-5-ол (1 экв.), бис(триметилсилил)амид калия (4 экв.), перемешивают в диметилформамиде в течение 30 мин при комнатной температуре. К смеси добавляют 4-хлор(2-пиридил)-N-метилкарбоксамид (1 экв.) и карбонат калия (1,2 экв.) и подвергают микроволновой обработке в течение 6 мин при 150 С. Затем реакционную смесь концентрируют и распределяют между этилацетатом и водой. Органический слой отделяют и промывают насыщенным раствором соли, сушат, фильтруют и концентрируют. Очистка методом препаративной ЖХ дает желаемый продукт. МС: МН+=455. Каждый из примеров 110-119, представленных в табл. 2, синтезируют по методике, описанной в примере 119. Таблица 2
МПК / Метки
МПК: C07D 401/12, C07D 401/14, A61K 31/41, C07D 405/14, C07D 413/12, C07D 417/12, C07D 407/14, C07D 413/14, C07D 417/14, C07D 409/14, C07D 471/08
Метки: бензазолы, киназы, замещённые, ингибиторов, применение, качестве
Код ссылки
<a href="https://eas.patents.su/30-7987-zameshhyonnye-benzazoly-i-ih-primenenie-v-kachestve-ingibitorov-kinazy-raf.html" rel="bookmark" title="База патентов Евразийского Союза">Замещённые бензазолы и их применение в качестве ингибиторов киназы raf</a>
Предыдущий патент: Применение липосом определенных размеров для лечения или предотвращения заболевания
Следующий патент: &zeta-зета форма периндоприл эрбумина