Производные имидазолидина в качестве ингибиторов глутаминилциклазы
Номер патента: 21150
Опубликовано: 30.04.2015
Авторы: Гэртнер Ульф-Торстен, Тремль Андреас, Альмштеттер Михаэль, Зоммер Роберт, Хаманн Антье, Демут Ханс-Ульрих, Хайзер Ульрих, Торманн Михаэль, Хоффманн Торстен
Формула / Реферат
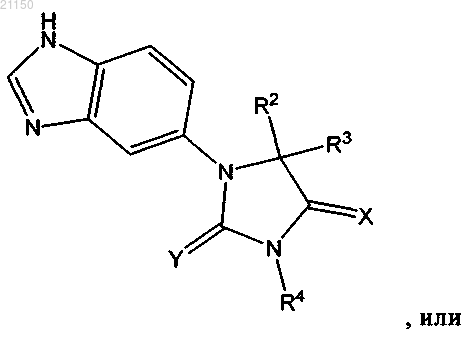
1. Соединение формулы (I)

или его стереоизомер, фармацевтически приемлемая соль или сольват,
где R1 обозначает 9-10-членную бициклическую гетероарильную группу, содержащую 1-3 гетероатома, выбранных из N, S или О, или -C2-C5-алкил-5-членный гетероарил, содержащий 1-3 атомов азота;
любые указанные выше гетероарильные группы необязательно могут быть замещены одной или несколькими группами, выбранными из C1-C6-алкила, C1-C6-алкокси и галогена;
R2 обозначает C6-C12-арил, 9-10-членную бициклическую гетероарильную группу, содержащую 1-3 гетероатома, выбранных из N, S или О, бифенил, фенил, конденсированный с 3-12-членной насыщенной или частично ненасыщенной гетероциклической группой, содержащей 1-3 гетероатома, выбранных из N, S или О; или
R2 и R3 вместе образуют C3-C12-карбоциклическое насыщенное или частично ненасыщенное кольцо, конденсированное с фенилом,
при этом указанные выше арильные, гетероарильные, фенильные, гетероциклические и карбоциклические группы необязательно могут быть замещены одной или более группами, выбранными из C1-C6-алкила, C1-C6-галогеналкила, C1-C6-алкоксигруппы, галогена и гидроксигруппы;
R3 обозначает Н;
R4 обозначает Н или метил;
X обозначает О или S и
Y обозначает О или S.
2. Соединение по п.1, где R1 обозначает 9-10-членную бициклическую гетероарильную группу, содержащую 1-3 гетероатома, выбранных из N, S или О.
3. Соединение по п.2, где R1 обозначает бензольное или пиридиновое кольцо, конденсированное с 5-членным кольцом, содержащим один или два атома азота.
4. Соединение по п.3, где указанные кольцевые системы присоединены к основной молекуле через бензольное или пиридиновое кольцо.
5. Соединение по п.4, где R1 обозначает
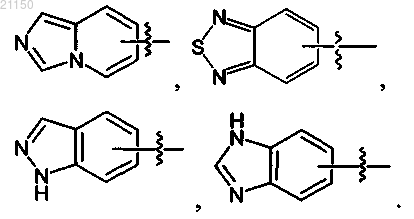
или имидазо[1,2-а]пиридин.
6. Соединение по п.5, где R1 обозначает
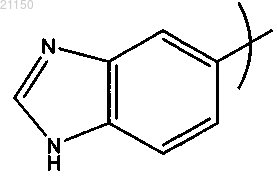
7. Соединение по п.1, где R1 обозначает -C2-C5-алкил-5-членный гетероарил, содержащий 1-3 атомов азота.
8. Соединение по п.7, где гетероарильная группа R1 обозначает 5-членное кольцо, содержащее от 1 до 3 атомов азота, которое необязательно замещено одним или более заместителями, выбранными из C1-C4-алкила, C1-C4-алкоксигруппы и галогена.
9. Соединение по п.8, где 5-членный гетероарил обозначает
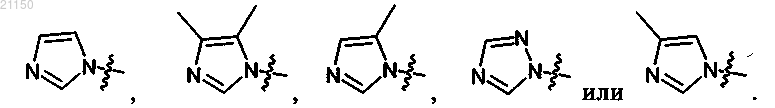
10. Соединение по п.1, где R1 обозначает
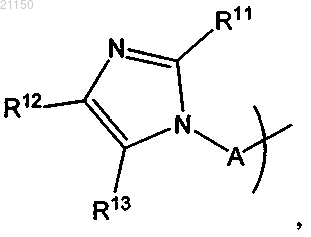
где А обозначает C2-C5-алкилен с прямой цепью или с разветвленной цепью и
R11, R12 и R13 независимо обозначают Н или C1-C2-алкил.
11. Соединение по любому из пп.1-10, представленное формулой
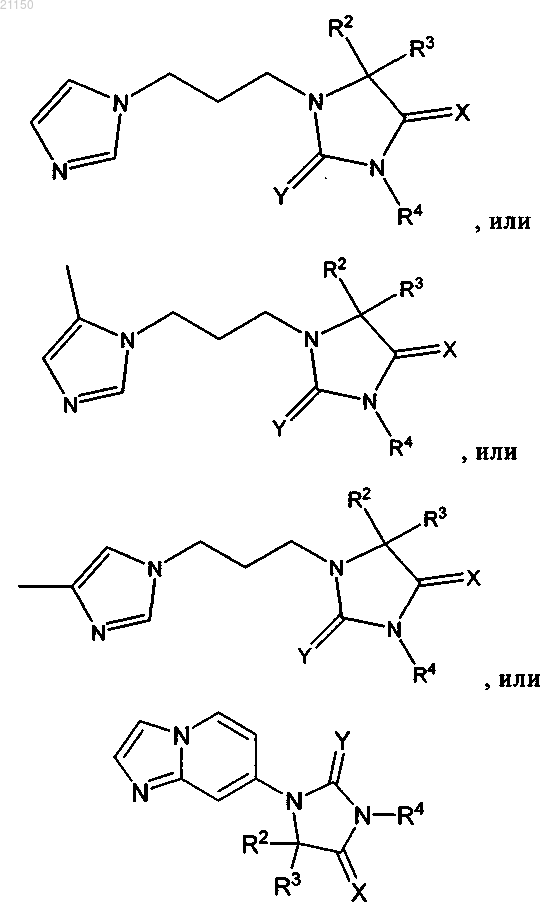
где R2, R3, R4, X и Y определены в п.1.
12. Соединение по любому из пп.1-11, где R2 обозначает бифенил, необязательно замещенный одним или более одинаковыми или различными заместителями, выбранными из галогена, OH, C1-C3-алкила, C1-C3-галогеналкила, C1-C3-алкоксигруппы.
13. Соединение по п.12, где R2 обозначает -бифенил-4-ил.
14. Соединение по любому из пп.1-11, где R2 обозначает фенил, необязательно замещенный одним, двумя или тремя одинаковыми или различными заместителями, выбранными из галогена, OH, C1-C3-алкила, C1-C3-галогеналкила, C1-C3-алкоксигруппы.
15. Соединение по п.14, где R2 обозначает фенил, замещенный н-пропилоксигруппой.
16. Соединение по любому из пп.1-15, где R3 обозначает Н.
17. Соединение по любому из пп.1-11, где R2 и R3 вместе образуют C3-C12-карбоциклическое насыщенное или частично ненасыщенное кольцо, конденсированное с фенилом.
18. Соединение по любому из пп.1-17, где R4 обозначает H.
19. Соединение по любому из пп.1-18, где X обозначает O.
20. Соединение по любому из пп.1-19, где Y обозначает O.
21. Соединение по любому из пп.1-19, где соединением формулы (I) являются следующие соединения:

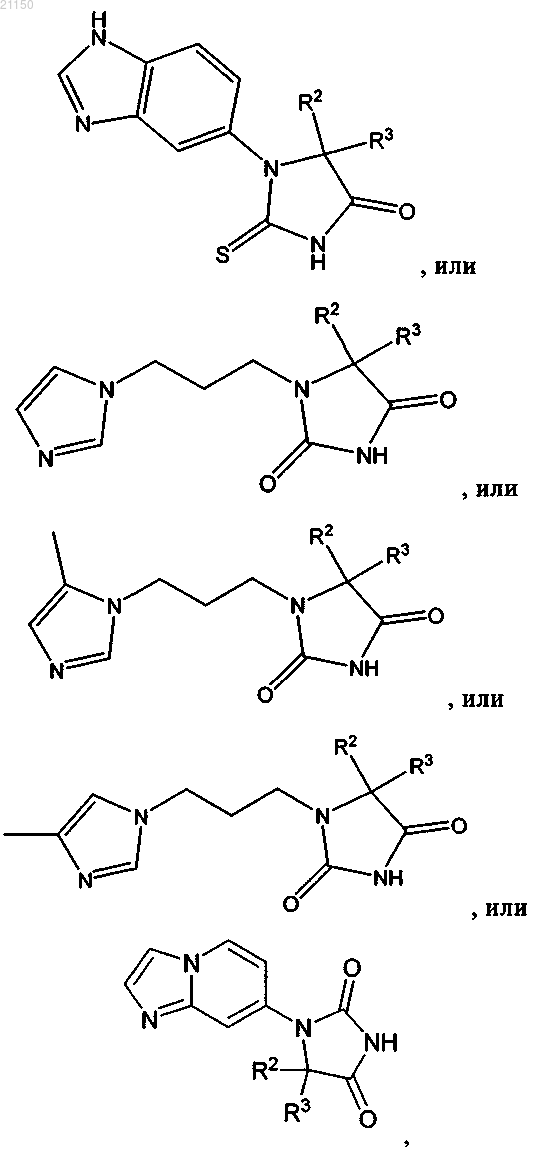
где значения R2 и R3 определены в п.1.
22. Соединение формулы (I), выбранное из следующих соединений:
5-(бензо[с][1,2,5]тиадиазол-6-ил)-1-(1Н-бензо[d]имидазол-5-ил)имидазолидин-2,4-дион;
1-(1Н-бензо[d]имидазол-5-ил)-5-фенилимидазолидин-2,4-дион;
1-(1Н-бензо[d]имидазол-5-ил)-5-(2-гидрокси-5-метилфенил)имидазолидин-2,4-дион;
1-(1Н-бензо[d]имидазол-5-ил)-5-(2-фтор-(5-трифторметил)фенил)имидазолидин-2,4-дион;
1-(1Н-бензо[d]имидазол-5-ил)-5-(2-бром-5-фторфенил)имидазолидин-2,4-дион;
1-(1Н-бензо[d]имидазол-5-ил)-5-(4-пропоксифенил)имидазолидин-2,4-дион;
1-(1Н-бензо[d]имидазол-5-ил)-5-(4-хлор-3-(трифторметил)фенил)имидазолидин-2,4-дион;
1-(1Н-бензо[d]имидазол-5-ил)-5-(3-фтор-4-(трифторметил)фенил)имидазолидин-2,4-дион;
1-(1Н-бензо[d]имидазол-5-ил)-5-(3-гидрокси-4-метоксифенил)имидазолидин-2,4-дион;
1-(1Н-бензо[d]имидазол-5-ил)-5-(2-гидрокси-3-метоксифенил)имидазолидин-2,4-дион;
1-(1Н-бензимидазол-5-ил)-5-(1,1'-бифенил-4-ил)имидазолидин-2,4-дион;
1-(1Н-бензо[d]имидазол-5-ил)-5-(3-хлорфенил)имидазолидин-2,4-дион;
1-(1Н-бензо[d]имидазол-5-ил)-5-(4-хлорфенил)имидазолидин-2,4-дион;
1-(1Н-бензо[d]имидазол-5-ил)-5-(2-хлорфенил)имидазолидин-2,4-дион;
1-(1Н-бензо[d]имидазол-5-ил)-5-(4-фторфенил)имидазолидин-2,4-дион;
1-(1Н-бензо[d]имидазол-5-ил)-5-(2,3-дигидробензо[b][1,4]диоксин-7-ил)имидазолидин-2,4-дион;
1-(3-(1Н-имидазол-1-ил)пропил)-5-фенилимидазолидин-2,4-дион;
1-(3-(1H-имидазол-1-ил)пропил)-5-(2-бром-4-фторфенил)имидазолидин-2,4-дион;
1-(3-(1Н-имидазол-1-ил)пропил)-5-(4-пропоксифенил)имидазолидин-2,4-дион;
1-(3-(1Н-имидазол-1-ил)пропил)-5-(3-фтор-4-(трифторметил)фенил)имидазолидин-2,4-дион;
1-[3-(1Н-имидазол-1-ил)пропил]-5-(4-бифенил)имидазолидин-2,4-дион;
1-(3-(1Н-имидазол-1-ил)пропил)-5-(3-хлорфенил)имидазолидин-2,4-дион;
1-(3-(1Н-имидазол-1-ил)пропил)-5-(2-хлорфенил)имидазолидин-2,4-дион;
1-(3-(5-метил-1Н-имидазол-1-ил)пропил)-5-фенилимидазолидин-2,4-дион;
5-(2-бром-5-фторфенил)-1-(3-(5-метил-1Н-имидазол-1-ил)пропил)имидазолидин-2,4-дион;
1-(3-(5-метил-1Н-имидазол-1-ил)пропил)-5-(4-пропоксифенил)имидазолидин-2,4-дион;
1-[3-(5-метил-1Н-имидазол-1-ил)пропил]-5-(4-фенилфенил)имидазолидин-2,4-дион;
5-(3-хлорфенил)-1-(3-(5-метил-1Н-имидазол-1-ил)пропил)имидазолидин-2,4-дион;
1-(3-(4-метил-1Н-имидазол-1-ил)пропил)-5-фенилимидазолидин-2,4-дион;
1-[3-(4-метил-1Н-имидазол-1-ил)пропил]-5-(4-бифенил)имидазолидин-2,4-дион;
5-(3-хлорфенил)-1-(3-(4-метил-1Н-имидазол-1-ил)пропил)имидазолидин-2,4-дион;
3-(1Н-бензимидазол-5-ил)-1',3'-дигидро-2Н,5Н-спиро[имидазолидин-4,2'-инден]-2,5-дион;
5-(бензо[с][1,2,5]тиадиазол-6-ил)-1-(1Н-бензо[d]имидазол-5-ил)-2-тиоксоимидазолидин-4-он;
1-(1Н-бензо[d]имидазол-5-ил)-5-фенил-2-тиоксоимидазолидин-4-он;
1-(1Н-бензимидазол-5-ил)-5-(1,1'-бифенил-4-ил)-2-тиоксоимидазолидин-4-он;
1-(1Н-бензо[d]имидазол-5-ил)-5-(3-гидрокси-4-метоксифенил)-2-тиоксоимидазолидин-4-он;
1-(1Н-бензо[d]имидазол-5-ил)-5-фенил-4-тиоксоимидазолидин-2-он;
1-(1Н-бензимидазол-5-ил)-5-(1,1'-бифенил-4-ил)-4-тиоксоимидазолидин-2-он;
3-(1Н-бензимидазол-5-ил)-5-тиоксо-1',3'-дигидро-2Н-спиро[имидазолидин-4,2'-инден]-2-он;
1-(1Н-бензо[d]имидазол-5-ил)-5-(4-хлорфенил)-4-тиоксоимидазолидин-2-он;
1-(1Н-бензо[d]имидазол-5-ил)-5-(2,3,4-трифторфенил)-4-тиоксоимидазолидин-2-он;
1-(1Н-бензо[d]имидазол-6-ил)-5-(4-бром-2-фторфенил)-4-тиоксоимидазолидин-2-он;
1-(1Н-бензо[d]имидазол-5-ил)-5-(2,3-дифтор-4-метилфенил)-4-тиоксоимидазолидин-2-он;
1-(1Н-бензо[d]имидазол-5-ил)-5-(4-хлор-3-метилфенил)-4-тиоксоимидазолидин-2-он;
1-(1Н-бензо[d]имидазол-5-ил)-3-метил-5-фенилимидазолидин-2,4-дион;
1-(Н-имидазо[1,2-а]пиридин-7-ил)-5-фенилимидазолидин-2,4-дион
или их стереоизомеров, фармацевтически приемлемых солей или сольватов.
23. 1-(1Н-Бензо[d]имидазол-5-ил)-5-(4-пропоксифенил)имидазолидин-2,4-дион формулы

или его стереоизомер, фармацевтически приемлемая соль или сольват.
24. Способ получения соединения формулы (I) по любому из пп.1-23, включающий:
а) гидролиз соединения формулы (II)

где значения R1, R2, R3 и Y определены в п.1 и
R обозначает C1-C6-алкил,
в водной среде в присутствии трифторуксусной кислоты с получением соединения формулы (I), где X обозначает О и R4 обозначает Н; или
б) взаимодействие соединения (II), указанного выше, с источником ионов сульфида, с получением соединения формулы (I), где X обозначает S, a R4 обозначает Н.
25. Способ получения соединения формулы (I) по любому из пп.1-23, включающий взаимодействие соединения формулы (VIII)
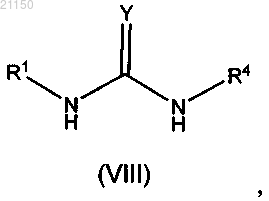
где значения R1 и R4 определены в п.1,
с соединением формулы (IX)
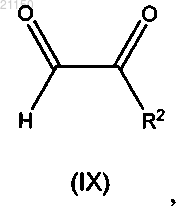
где значения R2 определены в п.1,
с получением соединения формулы (I), где значения R1, R2 и Y определены в п.1; R3 обозначает Н; R4 обозначает Н или метил и X обозначает О.
26. Способ получения соединения формулы (I) по любому из пп.1-23, включающий взаимодействие соединения формулы (XIII)

где значения R1, R2 и R3 определены в п.1,
с соединением формулы (XIV)

где либо J и K, оба, обозначают Н, либо J и K, оба, обозначают уходящие группы, где J и K, оба, обозначают имидазолил или J обозначает C1-C6-алкоксигруппу и K обозначает галоген,
с получением соединения формулы (I), где значения R1, R2, R3 и Y определены в п.1; X обозначает O и R4 обозначает Н.
27. Применение соединения по любому из пп.1-23 в качестве лекарственного средства, обладающего ингибирующей активностью в отношении глутаминилциклазы.
28. Фармацевтическая композиция для ингибирования глутаминилциклазы, содержащая соединение по любому из пп.1-23 в комбинации с одним или более фармацевтически приемлемым разбавителем или носителем.
29. Способ лечения или профилактики заболеваний, выбранных из группы, включающей нарушение когнитивной способности средней степени, болезнь Альцгеймера, семейную деменцию британского типа, семейную деменцию датского типа, нейродегенерацию при синдроме Дауна, болезнь Гентингтона, включающий введение пациенту, нуждающемуся в таком лечении, эффективного количества соединения по любому из пп.1-23.
30. Способ лечения или профилактики заболеваний, выбранных из группы, включающей ревматоидный артрит, атеросклероз, панкреатит и рестеноз, включающий введение пациенту, нуждающемуся в таком лечении, эффективного количества соединения по любому из пп.1-23.
31. Применение соединения по любому из пп.1-23 для получения лекарственного средства, предназначенного для лечения заболеваний, выбранных из группы, включающей нарушение когнитивной способности средней степени, болезнь Альцгеймера, семейную деменцию британского типа, семейную деменцию датского типа, нейродегенерацию при синдроме Дауна и болезнь Гентингтона.
32. Применение соединения по любому из пп.1-23 для получения лекарственного средства, предназначенного для лечения заболеваний, выбранных из группы, включающей ревматоидный артрит, атеросклероз, панкреатит и рестеноз.
Текст
В изобретении приведено описание соединений общей формулы (I) где R1, R2, R3, R4, X и Y определены в данном контексте, в качестве ингибиторов глутаминилциклазы и,следовательно, их применение для лечения состояний, которые можно лечить при модуляции активности глутаминилциклазы. Область изобретения Настоящее изобретение относится к новым производным имидазолидина в качестве ингибиторов глутаминилциклазы (ГЦ, ЕС 2.3.2.5). ГЦ катализирует внутримолекулярную циклизацию N-концевых остатков глутамина с образованием пироглутаминовой кислоты (5-оксопролил, pGlu) с выделением аммиака и межмолекулярную циклизацию N-концевых остатков глутамата с образованием пироглутаминовой кислоты и выделением воды. Предпосылки создания настоящего изобретения Глутаминилциклаза (ГЦ, ЕС 2.3.2.5) катализирует внутримолекулярную циклизацию N-концевых остатков глутамина с образованием пироглутаминовой кислоты (pGlu) и выделением аммиака. ГЦ впервые была выделена Мессером из млечного сока тропического растения Carica papaya в 1963 г.(Messer M., Nature, 4874, p. 1299 (1963. Через 24 года соответствующая ферментативная активность была обнаружена в гипофизе животных (Busby W.H.J. et al., J. Biol. Chem., 262, p. 8532-8536 (1987),Fischer W.H. и Spiess J., Proc. Natl. Acad. Sci. USA, 84, p. 3628-3632 (1987. В случае ГЦ млекопитающих превращение Gln в pGlu в присутствии ГЦ может наблюдаться для предшественников TRH и GnRHUSA, 84, p. 3628-3632 (1987. Кроме того, в ходе первоначальных экспериментов по локализации ГЦ была установлена совместная локализация ГЦ с предполагаемыми продуктами катализа в гипофизе крупного рогатого скота, что также подтвердило предполагаемое участие указанного фермента в синтезе пептидных гормонов (Bockers Т.М. et al., J. Neuroendocrinol. 7, p. 445-453 (1995. Напротив, физиологическая функция ГЦ практически не изучена. В случае фермента из С.papaya предлагают, что этот фермент защищает растения от патогенных микроорганизмов (El Moussaoui А. et al., Cell Mol. Life Sci. 58,p. 556-570 (2001. Недавно с использованием сравнения последовательностей были идентифицированы предполагаемые ферменты ГЦ из других растений (Dahl S.W. et al., Protein Expr. Purif. 20, p. 27-36(2000. Физиологическая функция указанных ферментов, однако, еще не определена. ГЦ из растений и животных характеризуются высокой специфичностью к L-глутамину вN-концевом положении субстратов, и их кинетический профиль подчиняется уравнению МихаэлисаМентен (Pohl Т. et al., Proc. Natl. Acad. Sci. USA, 88, p. 10059-10063 (1991), Consalvo A.P. et al., Anal.Biochem. 175, p. 131-138 (1988), Gololobov M.Y. et al., Biol. Chem. Hoppe Seyler, 377, p. 395-398 (1996. Сравнение первичной структуры ГЦ из растения С.papaya и первичной структуры высококонсервативного фермента ГЦ млекопитающих, однако, не выявило никакой гомологии в последовательности(Dahl S.W. et al., Protein. Expr. Purif. 20, p. 27-36 (2000. В то время как ферменты ГЦ из растений принадлежат к новому семейству ферментов (Dahl S.W. et al., Protein Expr. Purif. 20, 27-36 (2000, было установлено, что ГЦ млекопитающих характеризуются значительной гомологией последовательности с бактериальными аминопептидазами (Bateman R.С. et al., Biochemistry, 40, p. 11246-11250 (2001, что свидетельствует о различном эволюционном происхождении ферментов ГЦ растений и животных. Недавно было установлено, что рекомбинантная ГЦ человека, а также ГЦ из экстрактов мозга катализируют циклизацию как N-концевого глутамина, так и глутамата. Наиболее удивительным является тот факт, что наиболее эффективное катализируемое циклазой превращение Glu1 предпочтительно происходит при рН приблизительно 6,0, в то время как оптимальное превращение Gln1 в pGlu-производные происходит при рН приблизительно 8,0. Поскольку образование pGlu-A-родственных пептидов можно подавлять при ингибировании рекомбинантной циклазы ГЦ человека и ГЦ из экстрактов гипофиза свиньи, ГЦ является мишенью при разработке лекарственных средств для лечения болезни Альцгеймера. Ингибиторы ГЦ описаны в заявках WO 2004/098625, WO 2004/098591, WO 2005/039548,WO 2005/075436, WO 2008/055945, WO 2008/055947, WO 2008/055950 и WO2008/065141. В заявке ЕР 02011349.4 описаны полинуклеотиды, кодирующие глутаминилциклазу насекомых, а также кодируемые полипептиды и их применение для скрининга агентов, снижающих активность глутаминилциклазы. Указанные агенты можно использовать в качестве пестицидов. Определения Термины "ki" или "KI и "KD" обозначают константы связывания, которые описывают связывание ингибитора с ферментом и соответствующее высвобождение из фермента. Другой величиной является значение "IC50", которое обозначает концентрацию ингибитора, при которой при данной концентрации субстрата происходит снижение активности фермента на 50%. Термин "ингибитор ДПП IV", или "ингибитор дипептидилпептидазы IV", обычно известен специалистам в данной области техники и обозначает ингибиторы, которые ингибируют каталитическую активность ферментов ДПП IV или ДПП IV-подобных ферментов. Термин "активность ДПП IV" обозначает каталитическую активность дипептидилпептидазы IV(ДПП IV) и ДПП IV-подобных ферментов. Указанные ферменты являются сериновыми протеазами, которые расщепляют пептидную связь по остатку пролина (в меньшей степени по аланину, серину или глицину) и которые локализованы в различных тканях организма млекопитающих, включая почки, печень и кишечник, где они отщепляют дипептиды из N-концевых фрагментов биологически активных пептидов с высокой специфичностью, если в их последовательности остатки пролина или аланина расположены в соседнем положении к N-концевой аминокислоте. Термин "ингибитор ПЭП", или "ингибитор пролилэндопептидазы", обычно известен специалистам в данной области техники и обозначает ингибиторы, которые ингибируют каталитическую активность пролилэндопептидазы (ПЭП, пролилолигопептидазы, ПОП). Термин "активность ПЭП" обозначает каталитическую активность эндопротеазы, гидролизующей пептидные связи по остаткам пролина в пептидах или белках, в которых пролин расположен в положении 3 или более от N-концевого аминокислотного остатка в пептидном или белковом субстрате. Термин "ГЦ", использованный в данном контексте, обозначает глутаминилциклазу (ГЦ) и ГЦ-подобные ферменты. ГЦ и ГЦ-подобные ферменты характеризуются одинаковой или близкой ферментативной активностью (активностью ГЦ). При этом ГЦ-подобные ферменты могут значительно отличаться по своей молекулярной структуре от ГЦ. Примеры ГЦ-подобных ферментов включают глутаминилпептидциклотрансферазаподобные белки (QPCTL) человека (GenBank NM 017659), мыши(GenBank BC058181) и дикого быка Bos taurus (GenBank BT026254). Термин "активность ГЦ", использованный в данном контексте, обозначает внутримолекулярную циклизацию N-концевых остатков глутамина с образованием пироглутаминовой кислоты (pGlu) илиN-концевого L-гомоглутамина или Lгомоглутамина с образованием циклических пирогомоглутаминовых производных с выделением аммиака (см. схемы 1 и 2). Схема 1 Циклизация глутамина в присутствии ГЦ Термин "ЕС", использованный в данном контексте, обозначает действие ГЦ и ГЦ-подобных ферментов в качестве глутаматциклазы (ЕС), в дальнейшем обозначаемую как активность ЕС. Термин "активность ЕС", использованный в данном контексте, обозначает внутримолекулярную циклизацию N-концевых остатков глутамата с образованием пироглутаминовой кислоты (pGlu) в присутствии ГЦ (см. схему 3). Схема 3N-концевая циклизация незаряженных глутамилсодержащих пептидов в присутствии ГЦ (ЕС) Термины "ингибитор ГЦ" и "ингибитор глутаминилциклазы" известны специалистам в данной области техники и обозначают ингибиторы, ингибирующие каталитическую активность глутаминилциклазы (ГЦ) или активность глутаминилциклазы (ЕС). Эффективность ингибирования ГЦ. В связи с корреляцией с ингибированием циклазы ГЦ в предпочтительном варианте осуществления настоящего изобретения в основном способе и применении в медицине используют агент, характеризующийся значением IC50 ингибирования ГЦ 10 мкМ или менее, более предпочтительно 1 мкМ или менее, еще более предпочтительно 0,1 мкМ или менее или 0,01 мкМ или менее, наиболее предпочтительно 0,001 мкМ или менее. Действительно используют ингибиторы, характеризующиеся величиной Ki на уровне менее 1 мкМ, более предпочтительно менее 1 нМ, еще более предпочтительно менее 1 пМ. Таким образом, хотя активные агенты для удобства обозначены в данном контексте как "ингибиторы ГЦ", следует понимать, что такая номенклатура не ограничивает объем настоящего изобретения каким-либо конкретным механизмом действия. Молекулярная масса ингибиторов ГЦ. В общем случае ингибиторы ГЦ по настоящему изобретению представляют собой низкомолекулярные соединения, например, с молекулярной массой 500 г/моль или менее, 400 г/моль или менее, предпочтительно 350 г/моль или менее, более предпочтительно 300 г/моль или менее, наиболее предпочтительно 250 г/моль или менее. Термин "субъект", использованный в данном контексте, обозначает животное, предпочтительно млекопитающее, более предпочтительно человека, который является объектом лечения, наблюдения или эксперимента. Термин "терапевтически эффективное количество", использованный в данном контексте, обозначает количество активного соединения или фармацевтического агента, вызывающее биологическую или медицинскую ответную реакцию в культуре тканей, у животного или у человека, которые используются для испытаний, проводимых исследователем, ветеринаром, врачом или другим клиницистом, и указанная ответная реакция включает ослабление симптомов заболевания или состояния, подлежащего лечению. Термин "фармацевтически приемлемый", использованный в данном контексте, относится к применению в медицине и ветеринарии, например термин "фармацевтически приемлемый" относится к соединению, приемлемому в ветеринарии или для введения человеку и для лечения человека. В настоящем контексте термин "алкил", если не указано иное, обозначает C1-C12-алкил, предпочтительно C1-C8-алкил, например C1-C6-алкил, например C1-C4-алкил. Алкильная группа включает группы с прямой или разветвленной цепью. Пригодные алкильные группы включают, например, метил, этил, пропил (например, н-пропил и изопропил), бутил (например, н-бутил, изобутил, втор-бутил и трет-бутил),пентил (например, н-пентил), гексил (например, н-гексил), гептил (например, н-гептил) и октил (например, н-октил). Частица "алк", например, в терминах "алкоксигруппа", "галогеналкил" и "тиоалкил" относится к соответствующему определению "алкил". Примеры алкоксигрупп включают метоксигруппу, этоксигруппу,пропоксигруппу (например, н-пропоксигруппу), бутоксигруппу (например, н-бутоксигруппу), пентоксигруппу (например, н-пентоксигруппу), гексоксигруппу (например, н-гексоксигруппу), гептоксигруппу(например, н-гептоксигруппу) и октоксигруппу (например, н-октоксигруппу). Примеры тиоалкильных групп включают метилтиогруппу. Примеры галогеналкильных групп включают фторалкил, например CF3. Термин "алкенил", если не указано иное, обозначает C2-C12-алкенил, предпочтительноC2-C6-алкенил, например C2-C4-алкенил, содержащий по крайней мере одну двойную связь в любом положении и не содержащий тройную связь. Алкенил может содержать прямую или разветвленную цепи. Примеры алкенила, содержащего одну двойную связь, включают пропенил или бутенил. Примеры алкенила, содержащего две двойные связи, включают пентадиенил, например (1E,3 Е)-пентадиенил. Термин "алкинил", если не указано иное, обозначает C2-C12-алкинил, предпочтительноC2-C6-алкинил, например C2-C4-алкинил, который содержит по крайней мере одну тройную связь, расположенную в любом положении, и не содержит или содержит одну или более двойных связей. Алкинил может содержать прямую или разветвленную цепи. Типичные алкинилы включают пропинил и бутинил. Термин "алкилен" обозначает цепь формулы -(CH2)n-, где n равно целому числу, например 2-5, если не указано иное. Термин "циклоалкил" обозначает, если не указано иное, C3-C10-циклоалкил (т.е. содержащий от 3 до 10 атомов углерода в цикле), более предпочтительно C3-C8-циклоалкил, например C3-C6-циклоалкил. Типичные циклоалкилы включают циклопропил, циклобутил, циклопентил, циклогексил, циклогептил и циклооктил. Наиболее предпочтительно число атомов углерода в цикле равно от 3 до 6. Термин "циклоалкенил" обозначает, если не указано иное, C5-C10-циклоалкенил (т.е. содержащий от 5 до 10 атомов углерода в цикле), наиболее предпочтительно C5-C8-циклоалкенил, напримерC5-C6-циклоалкенил. Типичные циклоалкенилы включают циклопропенил, циклогексенил, циклогептенил и циклооктенил. Наиболее предпочтительно число атомов углерода равно от 5 до 6. Термин "карбоциклил" обозначает, если не указано иное, любую кольцевую систему, в которой все атомы в цикле представляют собой углерод и которая содержит от 3 до 12 атомов углерода в цикле,предпочтительно от 3 до 10 атомов углерода и наиболее предпочтительно от 3 до 8 атомов углерода. Карбоциклические группы могут включать насыщенные или частично ненасыщенные цепи, но они не содержат ароматические кольца. Примеры карбоциклических групп включают моноциклическую, бициклическую и трициклическую кольцевые системы, прежде всего моноциклическую и бициклическую кольцевые системы. Другие карбоциклические группы включают мостиковые системы (например, бицикло[2.2.1]гептенил). Специфический пример карбоциклической группы включает циклоалкильную группу. Другой пример карбоциклической группы включает циклоалкенильную группу. Термин "гетероциклил" обозначает, если не указано иное, карбоциклическую группу, где один или более (например, 1, 2 или 3) атомов кольца заменены на гетероатомы, выбранные из группы, включающей N, S и О. Специфический пример гетероциклической группы включает циклоалкильную группу (например, циклопентил или, прежде всего, циклогексил), где один или более (например, 1, 2 или 3, прежде всего 1 или 2, наиболее предпочтительно 1) атомов в цикле заменены на гетероатомы, выбранные из группы, включающей N, S и О. Примеры гетероциклических групп, содержащих один гетероатом, включают пирролидин, тетрагидрофуран и пиперидин, а пример гетероциклических групп, содержащих два гетероатома, включает морфолин и пиперазин. Другой специфический пример гетероциклической группы включает циклоалкенильную группу (например, циклогексенил), где один или более (например, 1, 2 или 3, прежде всего 1 или 2, наиболее предпочтительно 1) атомов в цикле заменены на гетероатомы, выбранные из группы, включающей N, S и О. Пример такой группы включает дигидропиранил (например,3,4-дигидро-2 Н-пиран-2-ил-). Термин "арил" обозначает, если не указано иное, C6-C12-арильную группу, предпочтительноC6-C10-арильную группу, наиболее предпочтительно C6-C8-арильную группу. Арильные группы содержат по крайней мере одно ароматическое кольцо (например, одно, два или три кольца). Пример типичной арильной группы, содержащей одно ароматическое кольцо, включает фенил. Пример типичной арильной группы, содержащей два ароматических кольца, включает нафтил. Термин "гетероарил" обозначает, если не указано иное, арильную группу, где один или более (например, 1, 2, 3 или 4, предпочтительно 1, 2 или 3) атомов в цикле заменены на гетероатомы, выбранные из группы, включающей N, S и О, или 5-членный ароматический цикл, содержащий один или более (например, 1, 2, 3 или 4, предпочтительно 1, 2 или 3) атомов в цикле, выбранных из группы, включающей N,S и О. Примеры моноциклических гетероарильных групп, содержащих один гетероатом, включают пиррол, фуран, тиофен и 6-членные циклы (например, пиридин, такие как пиридин-2-ил, пиридин-3-ил и пиридин-4-ил). Примеры моноциклических гетероарильных групп, содержащих два гетероатома, включают 5-членные циклы (например, пиразол, оксазол, изоксазол, тиазол, изотиазол, имидазол, такие как имидазол-1-ил, имидазол-2-ил, имидазол-4-ил), 6-членные циклы (например, пиридазин, пиримидин,пиразин). Примеры моноциклических гетероарильных групп, содержащих три гетероатома, включают 1,2,3-триазол и 1,2,4-триазол. Пример моноциклических гетероарильных групп, содержащих четыре гетероатома, включает тетразол. Примеры бициклических гетероарильных групп включают индол (например, индол-6-ил), бензофуран, бензотиофен, хинолин, изохинолин, индазол, бензимидазол, бензтиазол, хиназолин и пурин. Термин "-алкиларил" обозначает, если не указано иное, арильный остаток, который присоединен через алкиленовый остаток, например через C1-C4-алкиленовый остаток. Термин "-алкилгетероарил" обозначает, если не указано иное, гетероарильный остаток, который присоединен через алкиленовый остаток, например через C1-C4-алкиленовый остаток. Термин "галоген" включает фтор (F), хлор (Cl) и бром (Br). Термин "амино" относится к NH2 группе. Термин "фенил, замещенный фенилом" относится к бифенилу. Термин обозначает простую связь с неопределенной стереохимической конфигурацией. Если бензимидазол обозначен в виде бензимидазол-5-ила формулы то специалисту в данной области техники представляется очевидным, что бензимидазол-6-ил формулы является эквивалентной структурой. В данном описании две формы бензимидазолила включены в термин "бензимидазолил-5-ил". Стереоизомеры. Все возможные стереоизомеры заявленных соединений включены в настоящее изобретение. Если соединения по настоящему изобретению содержат по крайней мере один хиральный центр,они могут существовать в виде энантиомеров. Если соединения содержат два или более хиральных центров, они могут существовать также в виде диастереоизомеров. При этом следует понимать, что все такие изомеры и их смеси включены в объем настоящего изобретения. Получение и выделение стереоизомеров. Если способы получения соединений по настоящему изобретению сопровождаются образованием смеси стереоизомеров, то указанные стереоизомеры можно разделить с использованием стандартных методик, например, таких как препаративная хроматография. Соединения можно получать в виде рацематов или в виде индивидуальных энантиомеров, которые получают в ходе энантиоспецифического синтеза или разделения. Соединения, например, можно получить в виде отдельных энантиомеров с использованием стандартных методик, таких как получение пар диастереомеров при образовании их солей с использованием оптически активной кислоты, такой как (-)-ди-пара-толуоил-d-винной кислоты и/или(+)-ди-пара-толуоил-1-винной кислоты с последующей фракционной кристаллизацией и получением соединения в виде свободного основания. Соединения можно получать также при образовании сложных эфиров или амидов диастереомеров с последующим разделением хроматографией и удалением вспомогательного хирального компонента. В другом варианте соединения можно получать с использованием хиральной колонки для ЖХВР. Фармацевтически приемлемые соли. В связи с аналогичной структурой соединений в свободной форме и в форме их солей или сольватов, если в данном контексте упоминают указанное соединение, имеется в виду также соответствующая соль, сольват или полиморфная форма при условии, что образование указанной формы возможно в данных обстоятельствах. Пригодными для использования в медицине солями и сольватами соединений формулы (I) и их физиологически активными производными являются соли и сольваты, содержащие фармацевтически приемлемый противоион или связанный растворитель. Однако согласно настоящему изобретению соли и сольваты, содержащие фармацевтически непригодные противоионы или ассоциированные растворители,можно использовать, например, в качестве промежуточных соединений при получении других соединений и их фармацевтически приемлемых солей и сольватов. Согласно настоящему изобретению пригодные соли включают соли органических и неорганических кислот и оснований. Фармацевтически пригодные кислотно-аддитивные соли включают соли соляной, бромисто-водородной, серной, азотной, лимонной, винной, фосфорной, молочной, пировиноградной, уксусной, трифторуксусной, трифенилуксусной, сульфаминовой, сульфаниловой, янтарной, щавелевой, фумаровой, малеиновой, яблочной, миндальной, глютаминовой, аспарагиновой, щавелевоуксусной, метансульфоновой, этансульфоновой, арилсульфоновой (например, пара-толуолсульфоновой,бензолсульфоновой, нафталинсульфоновой или нафталиндисульфоновой), салициловой, глутаровой,глюконовой, трикарбаллиловой, коричной, замещенной коричной (например, фенил-, метил-, метоксиили галогензамещенной коричной, включая 4-метил- и 4-метоксикоричную кислоту), аскорбиновой, олеиновой, нафтойной, гидроксинафтойной (например, 1- или 3-гидрокси-2-нафтойной), нафталинакриловой (например, нафталин-2-акриловой), бензойной, 4-метоксибензойной, 2- или 4-гидроксибензойной,4-хлорбензойной, 4-фенилбензойной, бензолакриловой (например, 1,4-бензолдиакриловой), изэтиновых кислот, перхлорной, пропионовой, гликолевой, гидроксиэтансульфоновой, памовой, циклогексансульфаминовой, салициловой, сахариновой и трифторуксусной кислот. Фармацевтически приемлемые соли оснований включают соли аммония, соли щелочных металлов, таких как натрия и калия, соли щелочноземельных металлов, таких как кальций и магний, а также соли органических оснований, таких как дициклогексиламин и N-метил-D-глюкамин. Следует понимать, что в объем настоящего изобретения включены все фармацевтически приемлемые кислотно-аддитивные соли соединений по изобретению. Полиморфные кристаллические формы. Кроме того, некоторые соединения могут существовать в нескольких кристаллических формах, которые также включены в объем настоящего изобретения. Кроме того, некоторые соединения могут существовать в форме водных сольватов (т.е. гидратов) или стандартных органических растворителей, которые также включены в объем настоящего изобретения. Соединения, включая их соли, можно получать также в форме гидратов или могут включать другие растворители, используемые при их кристаллизации. Пролекарства. В объем настоящего изобретения включены также соединения по изобретению в форме пролекарств. Обычно указанными пролекарствами являются функционально активные производные соединений, которые легко превращаются in vivo в требуемое терапевтически активное соединение. Таким образом, в указанных случаях способы лечения по настоящему изобретению и термин "введение" включают лечение различных описанных нарушений с использованием вариантов пролекарств одного или более заявленных соединений, но которые превращаются в описанные выше конкретные соединения in vivo после введения субъекту. Стандартные методы выбора и получения пригодных пролекарств описаны,например, в книге "Design of Prodrugs", ed. Н. Bundgaard, Elsevier (1985). Защитные группы. При необходимости лабильные или реакционноспособные группы в составе любых молекул в ходе любого способа получения соединений по настоящему изобретению можно защищать защитными группами. С этой целью можно использовать стандартные защитные группы, например, описанные в книгеP.G.M. Wuts, Protective Groups in Organic Synthesis, John WileySons (1991), которые в полном объеме включены в настоящее описание в качестве ссылок. Защитные группы можно удалить на соответствующей стадии синтеза по стандартным методикам, известным специалисту в данной области техники. Термин "композиция", использованный в данном контексте, обозначает продукт, включающий заявленные соединения в терапевтически эффективном количестве, а также любой продукт, который можно получить непосредственно или косвенно из комбинаций заявленных соединений. Носители и добавки для галеновых составов. Таким образом, в случае жидких пероральных препаратов, например, таких как суспензии, эликсиры и растворы, пригодные носители и добавки включают воду, пригодные гликоли, масла, спирты, ароматизаторы, консерванты, красители и т.п., в случае твердых пероральных препаратов, например, таких как порошки, капсулы, гелевые капсулы и таблетки, пригодные носители и добавки включают крахмалы,сахара, разбавители, гранулирующие агенты, смазывающие вещества, связующие вещества, дезинтегрирующие агенты и т.п. Носители, которые можно добавлять в смеси, включают необходимые и инертные фармацевтические эксципиенты включая, но не ограничиваясь только ими, пригодные связующие агенты, суспендирующие агенты, смазывающие вещества, ароматизаторы, подсластители, консерванты, агенты для нанесения покрытий, дезинтегрирующие агенты, красители и пигменты. Растворимые полимеры, используемые в качестве носителей лекарственных средств, включают поливинилпирролидон,сополимер пирана,полигидроксипропилметакриламидофенол,полигидроксиэтиласпартамидфенол или полиэтиленоксидполилизин, замещенный остатками пальмитоила. Кроме того, соединения по настоящему изобретению можно присоединять к биодеградируемым полимерам, пригодным для получения препарата с контролируемым высвобождением лекарственного средства, например с полимолочной кислотой, поликапролактоном, полигидроксимасляной кислотой,сложными полиортоэфирами, полиацеталями, полидигидропиранами, полицианоакрилатами и сшитыми или амфифильными блок-сополимерными гидрогелями. Пригодные связующие агенты включают, но не ограничиваясь только ими, крахмал, желатин, природные сахара, такие как глюкоза или -лактоза, подсластители из кукурузы, природные и синтетические камеди, такие как аравийская, трагакантовая камедь или олеат натрия, стеарат натрия, стеарат магния,бензоат натрия, ацетат натрия, хлорид натрия и т.п. Дезинтегрирующие агенты включают, но не ограничиваясь только ими, крахмал, метилцеллюлозу,агар, бентонит, ксантановую камедь и т.п. Краткое описание сущности изобретения В настоящем изобретении предлагаются соединения формулы (I) или их фармацевтически приемлемые соли, сольваты или стереоизомеры,где R1 обозначает 9-10-членную бициклическую гетероарильную группу, содержащую 1-3 гетероатома, выбранных из N, S или О, или -C2-C5-алкил-5-членный гетероарил, содержащий 1-3 атомов азота,где любые указанные выше гетероарильные группы необязательно могут быть замещены одной или несколькими группами, выбранными из C1-C6-алкила, C1-C6-алкокси и галогена;R2 обозначает C6-C12-арил, 9-10-членную бициклическую гетероарильную группу, содержащую 1-3 гетероатома, выбранных из N, S или О, бифенил, фенил, конденсированный с 3-12-членной насыщенной или частично ненасыщенной гетероциклической группой, содержащей 1-3 гетероатома, выбранных из N,S или О; илиR2 и R3 вместе образуют C3-C12-карбоциклическое насыщенное или частично ненасыщенное кольцо,конденсированное с фенилом, при этом указанные выше арильные, гетероарильные, фенильные, гетероциклические и карбоциклические группы необязательно могут быть замещены одной или более группа-6 021150Y обозначает О или S. Соединения, подобные соединениям формулы (I), но которые не ингибируют активность ферментаWO 2008/076754 - ингибиторы каннабиноидов, в заявке WO 2008/028032 - соединения, пригодные для лечения гипертензии глаза, а в статье Werbel et al., J. Med. Chem., 20(12), 1569-1572 (1977) - соединения,предназначенные для лечения гельминтоза Schistosoma mansoni. Краткое описание фигур На фигуре представлена концентрация пептида pGlu-A3-42 в экстрактах муравьиной кислоты, полученных из организма трансгенных (ТГ) мышей, характеризующихся сверхэкспрессией AQ3-42. Мышам вводили в течение двух месяцев соединение (описанное в примере 6) или мыши получали только стандартный корм (плацебо). Лечение с использованием ингибитора QC привело к существенному снижению концентрации A, после лечения ингибитором QC концентрация указанного соединения (А) в стволе головного мозга снижалась ниже предела чувствительности метода анализа. А не обнаружен у мышей дикого типа, это подтверждает специфичность метода ИФА. Подробное описание изобретения Если карбоциклил и гетероциклил являются замещенными, то обычно они замещены 1 или 2 заместителями (например, 1 заместителем). Обычно заместителем является метил. Как правило, карбоциклил и гетероциклил являются не замещенными. Если арил и гетероарил являются замещенными, то обычно они замещены 1, 2 или 3 (например, 1 или 2) заместителями. Заместители для арила и гетероарила выбирают из C1-C6-алкила (например, метила), C1-C6-галогеналкила (например, фторметила, трифторметила), C1-C6-алкоксигруппы (например, метоксигруппы, этоксигруппы), -галогена (например, фтора, хлора, брома), гидроксильной группы. Как правило, заместители выбирают из C1-C6-алкила (например, метила), C1-C6-галогеналкила (например,C1-C6-фторалкила, например CF3), C1-C6-алкоксигруппы (например, ОМе), галогена и гидроксигруппы. В одном варианте осуществления настоящего изобретения R1 обозначает 9-10-членную бициклическую гетероарильную группу. Пригодные бициклические гетероарильные группы включают, например,9- или 10-членные, прежде всего 9-членные, гетероарильные группы. Указанные пригодные группы содержат атомы азота, например 1 или 2 атома азота. Наиболее пригодные бициклические гетероарильные кольца включают 9-членный гетероарильный цикл, содержащий 1 или 2 атома азота. В некоторых случаях гетероарильная группа необязательно содержит дополнительный гетероатом, выбранный из N, О илиS, прежде всего S. Пригодный 9-членный гетероарильный цикл включает бензольное или пиридиновое кольцо, конденсированное с 5-членным циклом, содержащим один или два атома азота. Наиболее пригодный цикл включает бензольное кольцо, конденсированное с 5-членным циклом, содержащим один или два атома азота. В некоторых случаях 5-членный цикл также может содержать дополнительный гетероатом, выбранный из N, О или S, прежде всего S, однако в наиболее пригодных соединениях гетероарильная группа не содержит атомов серы. В наиболее пригодных вариантах указанные конденсированные гетероарильные системы присоединены к основной молекуле через бензольное или пиридиновое кольцо. Описанные выше гетероарильные группы обычно являются незамещенными, но пригодными являются и группы, замещенные одним или более заместителями, например 1 или 2 заместителями, выбранными из алкила (например, C1-C4-алкила, такого как Me), алкоксигруппы (например,C1-C4-алкоксигруппы, такой как ОМе) и галогена (например, F). Конкретные примеры бициклических гетероарильных групп включают фенильную группу, конденсированную с 5-членным циклом, который может присутствовать в составе соединений общей формулы Указанные группы могут содержать заместители, описанные выше. Примеры наиболее пригодных бициклических гетероарильных групп включают имидазо[1,2-а]пиридин. В другом варианте R1 обозначает -C2-C5-алкил-5-членный гетероарил. В указанном варианте гетероарильной группой (в составе) R1 является бициклическая группа, например одна из групп, описанных выше. Однако более пригодными гетероарильными группами являются моноциклические, прежде всего 5- или 6-членные циклы, прежде всего 5-членные циклы. Обычно указанными группами являются гетероциклические группы, содержащие атом азота, прежде всего содержащие от 1 до 3 атомов азота. Предпочтительно гетероарильная группа не содержит атомов серы. Описанные выше гетероарильные группы являются незамещенными или замещены одним или более заместителями, предпочтительно 1 или 2 заместителями, выбранными из алкила (например, C1-C4-алкила,такого как Me), алкоксигруппы (например, C1-C4-алкоксигруппы, такой как ОМе) и галогена (например,F). Предпочтительные примеры пригодных моноциклических гетероарильных групп включают 5-членный цикл, содержащий 2 или 3 атома азота, который необязательно замещен (например, прежде всего одной или двумя группами, такими как метил), например: Прежде всего предпочтительной гетероарильной группой является имидазол-1-ил, необязательно замещенный, как описано выше, при этом наиболее пригодным заместителем является метил. Предпочтительными пригодными соединениями согласно данному варианту являются соединения,в которых R1 обозначает -C2-C5-алкил-5-членный гетероарил. Алкильная группа включает группы с прямой и разветвленной цепью, примеры указанной алкильной группы с разветвленной цепью включают группы: Наиболее пригодной алкильной группой является -(CH2)2- или -(CH2)3-, прежде всего -(CH2)3-. Наиболее пригодной -алкилгетероарильной группой является 3-имидазол-1-илпропил-. В одном варианте R1 обозначает где А обозначает C2-C5-алкилен с прямой цепью или с разветвленной цепью иR11, R12 и R13 независимо обозначают Н или C1-C2-алкил. Наиболее пригодными соединениями формулы (I) являются следующие соединения: Более предпочтительным соединением формулы (I) является соединение Если R2 необязательно обозначает замещенный арил, то арил обычно обозначает фенил. Примеры замещенных фенильных групп включают 2,4-дихлорфенил-, 2,4-дифторфенил-,2,4-диметоксифенил-,2,4-диметилфенил-,2,4-бис-(трифторметил)фенил-,2,4,6-трифторфенил-,2,4,6-триметилфенил-, 2,6-дихлорфенил-, 2,6-дифторфенил-, 2,6-диметоксифенил-, 2-изопропил-6 метилфенил-, 3-(циклопентилокси)-4-метоксифенил-, 3,4,5-триметоксифенил-, 3,4-диметоксифенил-,3,4-дихлорфенил-,3,4-диметилфенил-,3,4,5-трифторфенил-,3,5-бис-(трифторметил)фенил-,3,5-диметоксифенил-, 3-метоксифенил-, 4-(трифторметил)фенил-, 4-бром-2-(трифторметил)фенил-,4-бромфенил-, 4-хлор-3-(трифторметил)фенил-, 4-хлорфенил-, 4-цианофенил-, 4-этоксифенил-,4-этилфенил-, 4-фторфенил-, 4-изопропилфенил-, 4-метоксифенил-. В другом варианте R2 обозначает незамещенный фенил-. Другие примеры замещенных фенильных групп включают 2,3,4-трифторфенил,2,3-дифтор-4-метилфенил,2-бром-4-фторфенил-,2-бром-5-фторфенил-,2-хлорфенил-,2-фтор-5-(трифторметил)фенил-, 2-гидрокси-3-метоксифенил-, 2-гидрокси-5-метилфенил-, 3-хлорфенил-,3-фтор-4-(трифторметил)фенил-,3-гидрокси-4-метоксифенил-,4-бром-2-фторфенил,4-хлор-3-(трифторметил)фенил-, 4-хлор-3-метилфенил, 4-хлорфенил-, 4-фторфенил- и 4-пропоксифенил-. Если R2 необязательно обозначает замещенный арил, то арил обозначает нафтил, примеры указанной группы включают незамещенный нафтил (например, нафталин-1-ил, нафталин-2-ил, нафталин-3-ил),а также замещенный нафтил (например, 4-метилнафталин-2-ил-, 5-метилнафталин-3-ил-,7-метилнафталин-3-ил- и 4-фторнафталин-2-ил-). Если R2 необязательно обозначает замещенный гетероарил, примеры указанной группы включают бициклические кольца (например, 9- или 10-членные циклы), необязательно замещенные. В качестве заместителей можно использовать одну или более, например, 1, 2 или 3, групп, выбранных из галогена,гидроксильной группы, алкила (например, метила) и алкоксигруппы (например, метоксигруппы). Примеры замещенных 9-членных циклов включают 1H-индолил (например, 1 Н-индол-3-ил, 1 Н-индол-5-ил),бензотиофенил (например, бензо[b]тиофен-3-ил, прежде всего 2-бензо[b]тиофен-3-ил), бензо[1,2,5]оксадиазолил (например, бензо[1,2,5]оксадиазол-5-ил), бензо[1,2,5]тиадиазолил (например, бензо[1,2,5]тиадиазол-5-ил, бензо[1,2,5]тиадиазол-6-ил). Примеры 10-членных циклов включают хинолинил(например, хинолин-3-ил, хинолин-4-ил, хинолин-8-ил). В качестве заместителей можно использовать одну или более, например, 1, 2 или 3, различных групп, выбранных из галогена, гидроксильной группы,алкила (например, метила) и алкоксигруппы (например, метоксигруппы). Примеры замещенных 9-членных циклов включают 1-метил-1 Н-индол-3-ил, 2-метил-1 Н-индол-3-ил, 6-метил-1 Н-индол-3-ил. Примеры замещенных 10-членных циклов включают 2-хлорхинолин-3-ил, 8-гидроксихинолин-2-ил, оксохроменил (например, 4-оксо-4 Н-хромен-3-ил) и 6-метил-4-оксо-4 Н-хромен-3-ил. Если R2 обозначает фенил, замещенный фенилом, любые описанные выше фенильные группы необязательно замещены, примеры указанной группы включают -бифенил-4-ил. Если R2 обозначает необязательно замещенный фенил, конденсированный с необязательно замещенным гетероциклилом, примеры указанной группы включают бензо[1,3]диоксо-4-ил- и 2,3-дигидробензо[1,4]диоксин-4-ил-. В пригодных вариантах R2 обозначает арил, гетероарил, фенил, замещенный фенилом, фенил, конденсированный с гетероциклилом, или R2 и R3 вместе образуют карбоциклическое кольцо, которое конденсировано с фенилом, с указанными выше арильной, гетероарильной, фенильной, гетероциклической и карбоциклической группами, необязательно содержащими заместители. В более пригодных вариантах R2 обозначает арил, гетероарил, фенил, замещенный фенилом, или фенил, конденсированный с гетероциклилом, при этом указанные выше арил, гетероарил, фенил и гетероциклические группы необязательно являются замещенными. В одном варианте R2 обозначает необязательно замещенный гетероарил. Если R2 обозначает необязательно замещенный гетероарил, R2 предпочтительно обозначает бензо[с][1,2,5]тиадиазол-6-ил. В другом варианте R2 обозначает фенил, замещенный фенилом, где указанные выше фенильные группы необязательно являются замещенными, например, одним или более одинаковыми или различными заместителями,выбранными из галогена,OH,C1-C3-алкила,C1-C3-галогеналкила,C1-C3-алкоксигруппы, C1-C3-галогеналкоксигруппы. Если R2 обозначает фенил, замещенный фенилом, R2 предпочтительно обозначает -бифенил-4-ил.-9 021150 В еще одном варианте R2 обозначает необязательно замещенный фенил, конденсированный с необязательно замещенным гетероциклилом. Если R2 обозначает необязательно замещенный фенил, конденсированный с необязательно замещенным гетероциклилом, R2 предпочтительно обозначает 2,3-дигидробензо[1,4]диоксин-4-ил-. В одном варианте R2 обозначает необязательно замещенный арил, прежде всего необязательно замещенный фенил. В пригодных соединениях указанного типа R2 обозначает фенил, необязательно замещенный одним или более заместителями. Обычно, если R2 обозначает необязательно замещенный фенил,он является незамещенным или замещен одним, двумя или тремя одинаковыми или различными заместителями, выбранными из галогена, OH, C1-C3-алкила, C1-C3-галогеналкила, C1-C3-алкоксигруппы,C1-C3-галогеналкоксигруппы. Конкретные примеры указанных заместителей включают F, Cl, Br, OH,метил, трифторметил, этил, н-пропил, метоксигруппу, этоксигруппу и н-пропоксигруппу. Наиболее пригодной R2 группой является фенил, замещенный н-пропилоксигруппой, прежде всего 4-н-пропоксифенил. Если R2 и R3 вместе образуют карбоциклическое кольцо, необязательно замещенное одной или более C1-C2-алкильными группами, примеры включают циклоалкил (например, циклопропил, циклопентил и циклогексил) и циклоалкенил (например, циклогексенил). Если R2 и R3 вместе образуют карбоциклическое кольцо, конденсированное с фенилом, примеры включают инданил (например, индан-2-ил) и тетралинил. В пригодных вариантах R3 обозначает Н или R2 и R3 вместе образуют карбоциклическое кольцо,конденсированное с фенилом. В наиболее пригодных вариантах R3 обозначает Н. В наиболее пригодных вариантах R4 обозначает Н. В одном варианте X обозначает O. В другом варианте X обозначает S. В другом варианте Y обозначает O. В другом варианте Y обозначает S. В еще одном варианте X обозначает O, a Y обозначает S. В другом варианте X обозначает S, a Y обозначает О. В пригодных вариантах X и Y, оба, обозначают O. Наиболее предпочтительным соединением формулы (I) является соединение где значения R2 и R3 описаны выше. Наиболее пригодным соединением формулы (I) является соединение где значения R2 и R3 описаны выше. Соединения по настоящему изобретению характеризуются рядом преимуществ, их прежде всего можно использовать для лечения заболеваний ЦСН, связанных с ферментом QC, т.е. соединения по изобретению являются высокоэффективными ингибиторами фермента QC, характеризуются благоприятным коэффициентом распределения кровь/мозг (logBB), при этом достигается их высокая концентрация в мозге. Наиболее пригодные соединения общей формулы (I) выбирают из следующих соединений: 1) 5-(бензо[с][1,2,5]тиадиазол-6-ил)-1-(1 Н-бензо[d]имидазол-5-ил)имидазолидин-2,4-дион; 2) 1-(1 Н-бензо[d]имидазол-5-ил)-5-фенилимидазолидин-2,4-дион; 3) 1-(1H-бензо[d]имидазол-5-ил)-5-(2-гидрокси-5-метилфенил)имидазолидин-2,4-дион; 4) 1-(1 Н-бензо[d]имидазол-5-ил)-5-2-фтор-5-трифторметил)фенил)имидазолидин-2,4-дион; 5) 1-(1 Н-бензо[d]имидазол-5-ил)-5-(2-бром-5-фторфенил)имидазолидин-2,4-дион; 6) 1-(1 Н-бензо[d]имидазол-5-ил)-5-(4-пропоксифенил)имидазолидин-2,4-дион; 7) 1-(1 Н-бензо[d]имидазол-5-ил)-5-(4-хлор-3-(трифторметил)фенил)имидазолидин-2,4-дион; 8) 1-(1H-бензо[d]имидазол-5-ил)-5-(3-фтор-4-(трифторметил)фенил)имидазолидин-2,4-дион; 9) 1-(1 Н-бензо[d]имидазол-5-ил)-5-(3-гидрокси-4-метоксифенил)имидазолидин-2,4-дион; 10) 1-(1 Н-бензо[d]имидазол-5-ил)-5-(2-гидрокси-3-метоксифенил)имидазолидин-2,4-дион; 11) 1-(1H-бензимидазол-5-ил)-5-(1,1'-бифенил-4-ил)имидазолидин-2,4-дион; 12) 1-(1 Н-бензо[d]имидазол-5-ил)-5-(3-хлорфенил)имидазолидин-2,4-дион; 13) 1-(1 Н-бензо[d]имидазол-5-ил)-5-(4-хлорфенил)имидазолидин-2,4-дион; 14) 1-(1 Н-бензо[d]имидазол-5-ил)-5-(2-хлорфенил)имидазолидин-2,4-дион; 15) 1-(1 Н-бензо[d]имидазол-5-ил)-5-(4-фторфенил)имидазолидин-2,4-дион; 16) 1-(1 Н-бензо[d]имидазол-5-ил)-5-(2,3-дигидробензо[b][1,4]диоксин-7-ил)имидазолидин-2,4-дион; 17) 1-(3-(1 Н-имидазол-1-ил)пропил)-5-фенилимидазолидин-2,4-дион; 18) 1-(3-(1 Н-имидазол-1-ил)пропил)-5-(2-бром-4-фторфенил)имидазолидин-2,4-дион; 19) 1-(3-(1 Н-имидазол-1-ил)пропил)-5-(4-пропоксифенил)имидазолидин-2,4-дион; 20) 1-(3-(1 Н-имидазол-1-ил)пропил)-5-(3-фтор-4-(трифторметил)фенил)имидазолидин-2,4-дион; 21) 1-[3-(1 Н-имидазол-1-ил)пропил]-5-(4-бифенил)имидазолидин-2,4-дион; 22) 1-(3-(1 Н-имидазол-1-ил)пропил)-5-(3-хлорфенил)имидазолидин-2,4-дион; 23) 1-(3-(1 Н-имидазол-1-ил)пропил)-5-(2-хлорфенил)имидазолидин-2,4-дион; 24) 1-(3-(5-метил-1 Н-имидазол-1-ил)пропил)-5-фенилимидазолидин-2,4-дион; 25) 5-(2-бром-5-фторфенил)-1-(3-(5-метил-1 Н-имидазол-1-ил)пропил)имидазолидин-2,4-дион; 26) 1-(3-(5-метил-1 Н-имидазол-1-ил)пропил)-5-(4-пропоксифенил)имидазолидин-2,4-дион; 27) 1-[3-(5-метил-1 Н-имидазол-1-ил)пропил]-5-(4-фенилфенил)имидазолидин-2,4-дион; 28) 5-(3-хлорфенил)-1-(3-(5-метил-1 Н-имидазол-1-ил)пропил)имидазолидин-2,4-дион; 29) 1-(3-(4-метил-1 Н-имидазол-1-ил)пропил)-5-фенилимидазолидин-2,4-дион; 30) 1-[3-(4-метил-1 Н-имидазол-1-ил)пропил]-5-(4-бифенил)имидазолидин-2,4-дион; 31) 5-(3-хлорфенил)-1-(3-(4-метил-1 Н-имидазол-1-ил)пропил)имидазолидин-2,4-дион; 32) 3-(1 Н-бензимидазол-5-ил)-1',3'-дигидро-2 Н,5 Н-спиро[имидазолидин-4,2'-инден]-2,5-дион; 33) 5-(бензо[с][1,2,5]тиадиазол-6-ил)-1-(1 Н-бензо[d]имидазол-5-ил)-2-тиоксоимидазолидин-4-он; 34)1-(1 Н-бензо[d]имидазол-5-ил)-5-фенил-2-тиоксоимидазолидин-4-он; 35) 1-(1 Н-бензимидазол-5-ил)-5-(1,1'-бифенил-4-ил)-2-тиоксоимидазолидин-4-он; 36) 1-(1 Н-бензо[d]имидазол-5-ил)-5-(3-гидрокси-4-метоксифенил)-2-тиоксоимидазолидин-4-он; 37) 1-(1 Н-бензо[d]имидазол-5-ил)-5-фенил-4-тиоксоимидазолидин-2-он; 38) 1-(1 Н-бензимидазол-5-ил)-5-(1,1'-бифенил-4-ил)-4-тиоксоимидазолидин-2-он; 39) 3-(1 Н-бензимидазол-5-ил)-5-тиоксо-1',3'-дигидро-2 Н-спиро[имидазолидин-4,2'-инден]-2-он; 40) 1-(1 Н-бензо[d]имидазол-5-ил)-5-(4-хлорфенил)-4-тиоксоимидазолидин-2-он; 41) 1-(1 Н-бензо[d]имидазол-5-ил)-5-(2,3,4-трифторфенил)-4-тиоксоимидазолидин-2-он; 42) 1-(1 Н-бензо[d]имидазол-6-ил)-5-(4-бром-2-фторфенил)-4-тиоксоимидазолидин-2-он; 43) 1-(1 Н-бензо[d]имидазол-5-ил)-5-(2,3-дифтор-4-метилфенил)-4-тиоксоимидазолидин-2-он; 44) 1-(1 Н-бензо[d]имидазол-5-ил)-5-(4-хлор-3-метилфенил)-4-тиоксоимидазолидин-2-он; 45) 1-(1 Н-бензо[d]имидазол-5-ил)-3-метил-5-фенилимидазолидин-2,4-дион; 46) 1-(Н-имидазо[1,2-а]пиридин-7-ил)-5-фенилимидазолидин-2,4-дион или их фармацевтически приемлемых солей, сольватов или полиморфных форм, включая все таутомеры и стереоизомеры. В связи с этим наиболее пригодным соединением формулы (I) является соединение, описанное в примере 6, 1-(1 Н-бензо[d]имидазол-5-ил)-5-(4-пропоксифенил)имидазолидин-2,4-дион, характеризующийся следующей структурной формулой:R , и заявителями разработаны эффективные способы выделения каждого из энантиомеров соединений формулы (I). Например, в случае соединения, описанного в примере 6, заявителями были выделены иR4 обозначает Н,получают из соединения формулы (II) где R1, R2, R3 и Y имеют значения, описанные для соединения формулы (I);R обозначает алкил (например, бутил). Если X обозначает О, то превращение соединения (II) в соединение (I) включает превращение иминогруппы в карбонил в водной среде (например, в водном растворе трифторуксусной кислоты). Если X обозначает S, то получение указанного соединения включает реакцию соединения (II) с источником ионов сульфида, например сульфидом натрия. Реакцию предпочтительно проводят при повышенной температуре, предпочтительно в микроволновом реакторе. Реакцию обычно проводят в полярном протонном растворителе (например, в метаноле) в присутствии кислоты (например, соляной кислоты). Соединение формулы (II) получают из соединения формулы (III)- 12021150 где R1, R2 и R3 имеют значения, описанные выше для соединений формулы (I),по реакции с соединением формулы (IV) где Y имеет значения, описанные выше для соединений формулы (I); где R имеет значения, описанные выше для соединения формулы (II). Реакцию предпочтительно проводят в присутствии кислотного катализатора (например, гидрохлорида пиридиния). Реакцию обычно проводят в полярном протонном растворителе (например, в безводном этаноле). Соединение формулы (III) получают по реакции соединения формулы (VI) где R2 и R3 имеют значения, описанные выше для соединений формулы (I) с соединением формулы (VII) где R1 имеет значения, описанные выше для соединений формулы (I). Реакцию проводят в стандартных для получения иминов условиях, известных специалисту в данной области техники. Соединение формулы (I)X обозначает О,получают также по реакции соединения формулы (VIII) где R1 и R4 имеют значения, описанные выше для соединений общей формулы (I),с соединением формулы (IX) где R2 имеет значения, описные для соединений формулы (I). Реакцию обычно проводят в смеси HCl/AcOH (1:40 об./об.). Соединение формулы (VIII) получают по реакции соединения формулы (VII), описанного выше, с соединением формулы (X) где LG1 и LG2 независимо обозначают уходящие группы (например, LG1 и LG2, обе, обозначают имидазол-1-ил),и соединением формулы (XI) где R4 имеет значения, описанные для соединений формулы (I). Реакцию обычно проводят в полярном апротонном растворителе (например, в дихлорметане). В другом варианте соединение формулы (VIII) получают по реакции соединения формулы (VII),описанного выше, с соединением формулы (XII) где R4 имеет значения, описанные для соединения формулы (I). Реакцию обычно проводят в полярном апротонном растворителе (например, в тетрагидрофуране). Соединение формулы (I)X обозначает О,получают также по реакции соединения формулы (XIII) де R1, R2 и R3 имеют значения, описанные для соединений формулы (I),с соединением формулы (XIV) где J и K, оба, обозначают Н или J и K, оба, обозначают уходящие группы (например, J и K, оба,обозначают имидазолил или J обозначает алкоксигруппу (такую как этоксигруппа), а K обозначает галоген (например, хлор. Если J и K, оба, обозначают Н, реакцию обычно проводят при повышенной температуре. Если J и K, оба, обозначают уходящие группы, реакцию обычно проводят при повышенной температуре в присутствии основания (например, триэтиламина). Соединение формулы (XIII) получают при гидролизе соединения формулы (XV) где R1, R2 и R3 имеют значения, описанные для соединений формулы (I). Соединение формулы (XV) получают по реакции соединения формулы (VI) с соединением формулы (VII) в присутствии источника цианида (например, триметилсилилцианида). Соединение формулы (I)R4 обозначает -NH2, получают по реакции соединения формулы (I), где R4 обозначает Н,с соединением, источником ионов нитрита (например, нитрит натрия). Реакцию предпочтительно проводят в присутствии воды и кислоты (например, уксусной кислоты). Затем проводят реакцию восстановления (используя, например, цинковую пыль). Вторую стадию предпочтительно проводят в том же реакторе. Терапевтическое применение. Физиологическими субстратами фермента ГЦ (ЕС) млекопитающих являются, например, амилоид-пептиды (3-40), (3-42), (11-40) и (11-42), ABri, ADan, гастрин, нейротензин, FPP, CCL2, CCL7, CCL8,CCL16, CCL18, фракталкин, орексин A, [Gln3]-глюкагон(3-29), [Gln5]-соединение Р(5-11) и пептид QYNAD. Более подробная информация приведена в табл. 1. Соединения и/или комбинации по настоящему изобретению и фармацевтические композиции, содержащие по крайней мере один ингибитор ГЦ (ЕС),можно использовать для лечения состояний, которые поддаются лечению при модуляции активности ГЦ. Таблица 1 Аминокислотные последовательности физиологически активных пептидов,содержащих N-концевой остаток глутамина, который циклизуется с образованием pGlu В амилоидном -пептиде глутамат расположен в положениях 3, 11 и 22. Описан также мутант (замена глутаминовой кислоты (Е) на глутамин (Q) в положении 22) (соответствует амилоидному предшественнику белка АРР 693, Swiss-prot P05067), так называемая мутация, соответствующая цереброартериальному амилоидозу датского типа.-Амилоидные пептиды, содержащие остаток пироглутаминовой кислоты в положениях 3, 11 и/или 22, характеризуются более высокой цитотоксичностью и гидрофобностью по сравнению с амилоидными-пептидами 1-40 (42/43) (Saido Т.С., Medical Hypotheses, 54(3), p. 427-429 (2000. Множество вариантов пептидов с различными N-концевыми фрагментами, например A(3-40),A(3-42), A(11-40) и A(11-42), могут образовываться под действием -секретазы (фермента, расщепляющего амилоидный белок-предшественник по -участку (ВАСЕ) в различных фрагментах (Huse J.Т. et al., J.Biol. Chem., 277(18), p. 16278-16284 (2002, и/или под действием аминопептидазы или дипептидиламинопептидазы, осуществляющих процессинг полноразмерных пептидов A(1-40) и A(1-42). Во всех случаях циклизация N-концевого остатка глутаминовой кислоты катализируется ферментом ГЦ. Трансэпителиальные трансфектированные клетки, прежде всего гастрин-трансфектированные клетки (G), координируют секрецию желудочной кислоты при поступлении пищи в желудок. Недавно было установлено, что из предшественника гастрина образуется множество активных продуктов и что в биосинтезе гастрина существует множество контрольных точек. Биосинтетические предшественники и промежуточные соединения (прогастрин и Gly-гастрины) являются предполагаемыми факторами роста, их продукты, амидированные гастрины, регулируют пролиферацию эпителиальных клеток, дифференциацию париетальных клеток, продуцирующих кислоту, и секретирующих гистамин энтерохромаффиноподобных клеток (ECL), экспрессию генов, связанных с синтезом гистамина и его хранением в клеткахECL, а также острую стимуляцию секреции кислоты. Гастрин также стимулирует продуцирование членов семейства эпидермальных факторов роста (EGF), которые, в свою очередь, ингибируют функцию париетальных клеток, но стимулируют рост поверхностных эпителиальных клеток. Концентрация гастрина в плазме повышена у субъектов, у которых обнаружены бактерии Helicobacter pylori и у которых существует повышенный риск развития язвы двенадцатиперстной кишки и рака желудка (Dockray G.J., J.Physiol, 15, p. 315-324(1999. Известно, что пептидный гормон гастрин, высвобождающийся из антральных G клеток, стимулирует синтез и высвобождение гистамина из ECL клеток в слизистой оболочке желудка с участием рецепторов CCK-2. Активированный гистамин индуцирует секрецию кислоты при связывании с рецепторами Н(2), расположенными в париетальных клетках. Недавние исследования свидетельствуют о том, что гастрин как в полностью амидированной форме, так и в менее процессированных формах (прогастрин и глицинсодержащий гастрин) также является фактором роста желудочно-кишечного тракта. Установлено,что основное трофическое действие амидированный гастрин оказывает на париетальные клетки слизистой оболочки желудка, где гастрин вызывает увеличение пролиферации желудочных стволовых клеток и клеток ECL, что приводит к увеличению числа париетальных клеток и ECL клеток. С другой стороны,основной трофической мишенью в меньшей степени процессированного гастрина (например, глицинсодержащего гастрина) является слизистая оболочка ободочной кишки (Koh T.J., Chen D., Regul. Pept., p. 9337-9344 (2000. Нейротензин (НТ) является нейропептидом, принимающим участие в патофизиологии шизофрении,который специфически модулирует нейромедиаторную систему, разрегуляция которой, как было установлено ранее, наблюдается при этом заболевании. В ходе клинических испытаний определяли концентрацию НТ в спинномозговой жидкости и выявляли подгруппу пациентов с шизофренией, у которых наблюдался пониженный уровень НТ в спинномозговой жидкости, который восстанавливался при эффективном лечении с использованием нейролептических средств. Существуют также убедительные доказательства согласованного участия системы НТ в механизме действия нейролептических лекарственных средств. Поведенческие и биохимические действия НТ при центральном введении аналогичны действию нейролептических лекарственных средств при системном введении, при этом нейролептические лекарственные средства усиливают нейротрансмиссию НТ. Совокупность полученных данных позволяет предположить, что НТ действует как эндогенное нейролептическое средство. Более того, типичные и атипичные нейролептические средства изменяют нейротрансмиссию НТ по различным механизмам в нигростриальном и мезолимбическом концевых фрагментах допамина, и по интенсивности этих эффектов можно предположить возможные побочные действия и эффективность соответственно (Binder E.В. etal., Biol. Psychiatry, 50, p. 856-872 (2001. Пептид ускорения репродуктивной способности (FPP) является трипептидом, родственным тиротропин-рилизинг гормону (TRH), и присутствует в семенной плазме. Последние данные, полученные invitro и in vivo, свидетельствуют, что FPP играет важную роль в регуляции репродуктивной способности спермы. Прежде всего FPP стимулирует непродуктивные (неэффективные) сперматозоиды, т.е. "включает" их и быстро усиливает их репродуктивные свойства, а затем останавливает активацию, и, таким образом, не происходит потери акросомы, и, следовательно, сперматозоид не теряет репродуктивной способности. Эти ответные реакции являются имитацией и усиливаются в присутствии аденозина, который, как известно, является регулятором пути передачи сигнала аденилилциклазы (АЦ)/цАМФ. Установлено, что как FPP, так и аденозин не только стимулируют продуцирование цАМФ в непродуктивных клетках, но и ингибируют ее в репродуктивных клетках, при этом рецепторы FPP определенным образом взаимодействуют с аденозиновыми рецепторами и G белками, регулируя АЦ. Эти явления влияют на степень фосфорилирования различных белков, некоторые из которых играют важную роль в первоначальном "включении", а другие, возможно, принимают участие непосредственно в реакции акросом. Кальцитонин и ангиотензин II также присутствуют в семенной плазме и оказывают аналогичное действие in vitro на непродуктивные сперматозоиды, а также усиливают ответную реакцию на FPP. Указанные соединения оказывают аналогичное действие in vivo и влияют на репродуктивную способность, стимулируя и поддерживая ее потенциал. Снижение доступности FPP, аденозина, кальцитонина и ангиотензина II или нарушение структуры их рецепторов принимают участие в развитии мужского бесплодия (Fraser L.R., Adeoya-Osiguwa S.A., Vitam. Horm., 63, p. 1-28 (2001. Пептиды CCL2 (МСР-1), CCL7, CCL8, CCL16, CCL18 и фракталкин играют важную роль при патологических состояниях, таких как подавление пролиферации предшественников миелоидных клеток,неоплазия, воспалительная ответная реакция, рак, псориаз, ревматоидный артрит, атеросклероз, васкулит, гуморальный и клеточный иммунный ответ, процессы адгезии и миграции лейкоцитов в эндотелии,воспалительная болезнь кишечника, рестеноз, фиброз легких, легочная гипертензия, фиброз печени,цирроз печени, нефросклероз, ремоделирование желудочка, сердечная недостаточность, артериопатия после трансплантации органов и отторжение венозных трансплантатов. В некоторых исследованиях подчеркивается важная роль МСР-1 в развитии атеросклероза (Gu L. et(Wada Т. et al., J. Am. Soc. Nephrol., 15, p. 940-948 (2004 и отторжения трансплантатов (Saiura А. et al.,Arterioscler. Thromb. Vase. Biol., 24, p. 1886-1890 (2004. Более того, МСР-1 может принимать участие в развитии гестоза (Katabuchi Н. et al., Med. Electron Microsc., 36, p. 253-262 (2003, действовать в качестве паракринного фактора при развитии опухолей (Ohta М. et al., Int. J. Oncol., 22, p. 773-778 (2003), Li S. etUSA, (2005 и СПИД (Park I.W., Wang J.F. и Groopman J.E., Blood, 97, p. 352-358 (2001), Coll В. et al.,Cytokine, 34, p. 51-55 (2006. Уровень МСР-1 повышен в спинномозговой жидкости пациентов с болезнью Альцгеймера и у пациентов с когнитивными нарушениями средней степени (Galimberti D. et al., Arch. Neurol., 63, p. 538-543(2006. Более того, уровень МСР-1 повышен в сыворотке пациентов, страдающих когнитивными нарушениями средней степени и ранней формой болезни Альцгеймера (Clerici F. et al., Neurobiol. Aging., 27,p. 1763-1768 (2006. Недавно в ходе клинических испытаний были изучены некоторые пептидные вакцины против гепатита В, вируса иммунодефицита человека и меланомы, цитотоксичные в отношении T-лимфоцитов. Одним из перспективных компонентов вакцины против меланомы, в отдельности или в комбинации с другими противоопухолевыми агентами, является декапептид ELA. Указанные пептиды представляют собой антиген Melan-A/MART-1, аналог иммунодоминантного пептида, содержащий N-концевой остаток глутаминовой кислоты. Было установлено, что аминогруппа и -карбоксильная группа глутаминовой кислоты, а также аминогрупа и -карбоксильная группа глутамина быстро втупают в реакцию конденсации с образованием производных пироглутамина. Для решения проблемы стабильности были разработаны несколько представляющих интерес в фармацевтике пептидов, содержащих N-концевую пироглутаминовую кислоту вместо глутаминовой кислоты или глутамина, при этом пептиды сохраняют свои фармакологические свойства. К сожалению, по сравнению с ELA производные пироглутаминовой кислоты (PyrELA), а также защищенные ацетильными группами производные (AcELA) не проявляют цитотоксическую активность в отношении T-лимфоцитов (CTL). Несмотря на незначительную модификацию, эти два производных PyrELA и AcELA характеризуются более низкой аффинностью в отношении специфического комплекса гистосовместимости класса I по сравнению с ELA. Соответственно, для того чтобы сохранить полную активность ELA, следует исключить образование PyrELA (Beck А. et al., J. Pept. Res. 57(6), p. 528-538 (2001. Орексин A является нейропептидом, который играет важную роль в регуляции потребления пищи и циклов сон - бодрствование предположительно за счет координирования комплексных поведенческой и физиологической ответных реакций этих комплементарных гомеостатических функций. Он также играет роль в гомеостатической регуляции метаболизма энергии, функционировании вегетативной нервной системы, гормональном балансе и регуляции состава биологических жидкостей в организме. Недавно было установлено, что уровень пентапептида QYNAD в спинномозговой жидкости пациентов, страдающих рассеянным склерозом или синдромом Гиллиана-Барре, повышается по сравнению со здоровыми субъектами (Brinkmeier Н. et al., Nature Medicine, 6, p. 808-811 (2000. В литературе активно дискутируется вопрос о механизме действия пентапептида Gln-Tyr-Asn-Ala-Asp (QYNAD), прежде всего его эффективности при взаимодействии с блокаторами натриевых каналов, приводящем к усилению аксональной дисфункции, которая наблюдается при воспалительных аутоиммунных заболеваниях центральной нервной системы. Однако недавно было установлено, что не сам QYNAD, а его циклическая пироглутаматная форма, pEYNAD, является активной формой, блокирующей натриевые каналы, что приводит к усилению аксональной дисфункции. Натриевые каналы экспрессированы с высокой плотностью в миелиновых аксонах и играют важную роль в передаче биопотенциала в аксонах в головном и спинном мозге млекопитающих. Таким образом, предполагается, что они принимают участие на некоторых стадиях патофизиологии воспалительных аутоиммунных заболеваний, прежде всего при рассеянном склерозе, синдроме Гиллиана-Барре и хронической воспалительной демиелинизирующей полирадикулонейропатии. Более того, QYNAD является субстратом глутаминилциклазы (ГЦ, ЕС 2.3.2.5), которая локализована в мозге млекопитающих, прежде всего в мозге человека. Глутаминилциклаза эффективно катализирует образование pEYNAD из его предшественника QYNAD. Соответственно в настоящем изобретении предлагается применение соединений формулы (I) для получения лекарственного средства, предназначенного для профилактики, ослабления симптомов или лечения заболеваний, выбранных из группы, включающей нарушения когнитивной способности средней степени, болезнь Альцгеймера, семейную деменцию британского типа, семейную деменцию датского типа, нейродегенерацию при синдроме Дауна, болезнь Гентингтона, болезнь Кеннеди, язвенную болезнь,рак двенадцатиперстной кишки, сопровождающийся инфекцией Helicobacter pylori или без нее, колоректальный рак, синдром Золлигера-Эллисона, рак желудка, сопровождающийся инфекцией Helicobacterpylori или без нее, патогенные психотические состояния, шизофрению, бесплодие, неоплазию, воспалительную ответную реакцию хозяина, рак, злокачественное метастазирование, меланому, псориаз, ревма- 21021150 тоидный артрит, атеросклероз, панкреатит, рестеноз, нарушенный гуморальный и клеточный иммунный ответ, процессы адгезии и миграции лейкоцитов в эндотелии, нарушение потребления пищи, нарушение циклов сна - бодрствования, нарушенную гомеостатическую регуляцию метаболизма энергии, нарушенную вегетативную функцию, нарушенный гормональный баланс или нарушенную регуляцию состава жидкостей в организме, рассеянный склероз, синдром Гиллиана-Барре и хроническую воспалительную демиелинизирующую полирадикулонейропатию. Кроме того, при введении соединения по настоящему изобретению млекопитающему можно стимулировать пролиферацию предшественников миелоидных клеток. Введение ингибитора ГЦ по настоящему изобретению также может приводить к подавлению мужской репродуктивной способности. В одном варианте настоящего изобретения предлагается применение действия ингибиторов ГЦ(ЕС) в комбинации с другими агентами, прежде всего, для лечения нейрональных заболеваний, атеросклероза и рассеянного склероза. В настоящем изобретении также предлагается способ лечения упомянутых выше заболеваний,включающий введение терапевтически активного количества по крайне мере одного соединения формулы (I) млекопитающему, прежде всего человеку. Более предпочтительно указанный способ и соответствующие применения относятся к лечению заболевания, выбранного из группы, включающей нарушения когнитивной способности средней степени,болезнь Альцгеймера, семейную деменцию британского типа, семейную деменцию датского типа, нейродегенерацию при синдроме Дауна, болезнь Паркинсона и хорею Гентингтона, и указанный способ заключается во введении терапевтически активного количества по крайней мере одного соединения формулы (I) млекопитающему, прежде всего человеку. Еще более предпочтительно в настоящем изобретении предлагается способ лечения и соответствующие применения для лечения ревматоидного артрита, атеросклероза, панкреатита и рестеноза. Фармацевтические комбинации. В предпочтительном варианте настоящего изобретения предлагается композиция, предпочтительно фармацевтическая композиция, включающая по крайней мере один ингибитор ГЦ необязательно в комбинации по крайней мере с одним агентом, выбранным из группы, включающей ноотропные агенты,нейропротекторы, противопаркинсонические лекарственные средства, ингибиторы отложения амилоидных белков, ингибиторы синтеза -амилоидов, антидепрессанты, транквилизаторы, нейролептические средства и лекарственные препараты от рассеянного склероза. Наиболее предпочтительно указанные ингибиторы ГЦ являются соединениями формулы (I) по настоящему изобретению. Более конкретно, вышеперечисленный дополнительный агент выбран из группы, включающей-секретаз, ингибиторы аминопептидаз, прежде всего ингибиторы дипептидилпептидаз, наиболее предпочтительно ингибиторы ДПП IV, ингибиторы нейтральной эндопептидазы, ингибиторы фосфодиэстеразы-4 (ФДЭ-4), ингибиторы ФНО-, антагонисты мускаринового рецептора M1, антагонисты рецептора(натализумаб), неурелан (фампридин-SR), кампат (алемтузумаб), IR 208, NBI 5788/MSP 771 (типлимотид), паклитаксел, анергикс.MS (AG 284), SH636, дифферин (CD 271, адапален), BAY 361677 (интерлейкин-4), ингибиторы матричной металлопротеиназы (например, ВВ 76163), интерферон-тау (трофобластин) и SAIK-MS. Кроме того, другим агентом является, например, лекарственное средство, снижающее чувство тревоги, или антидепрессант, выбранное из группы, включающей:(б) селективные ингибиторы обратного захвата серотонина (SSRI), например циталопрам, флуоксетин, флувоксамин, эсциталопрам, сертралин, пароксетин;(е) ингибиторы обратного захвата серотонина-норэпинефрина, например венлафаксин, дулоксетин;(з) ингибиторы обратного захвата норэпинефрина, например ребоксетин;(м) лиганды NPY-рецептора: агонисты или антагонисты NPY-рецептора. В еще одном варианте настоящего изобретения другой агент, например, может представлять собой лекарственное средство от рассеянного склероза, выбранное из группы, включающей: а) ингибиторы дигидроортотатдегидрогеназы, например SC-12267, терифлуномид, MNA-715,HMR-1279 (или HMR-1715, MNA-279); б) аутоиммунный депрессант; в) паклитакесл; г) антитела, например AGT-1, моноклональные антитела против гранулоцит/макрофагеального колониестимулирующего фактора (GM-CSF), модуляторы рецептора Nogo, ABT-874, алемтузумаб(САМРАТН), антитела анти-ОХ 40, CNTO-1275, DN-1921, натализимаб (или AN-100226, антегрен,VLA-4 Mab), даклизумаб (или зенепакс, Ro-34-7375, SMART анти-Тас), J-695, приликсимаб (или Centara,CEN-000029, cM-T412), MRA, дантес, антитела анти-ил-12; д) препараты на основе пептидов нуклеиновой кислоты (ПНК), например ретикулоз; е) альфа-интерферон, например альфа-ферон, альфа-интерферон человека (или омниферон, альфалейкоферон),ж) -интерферон, например фрон, 1a-интерферон, такой как авонекс, бетрон (рефиб), аналоги-интерферона, гибридный белок -интерферонтрансферин, рекомбинантный интерферон -1b, например бетасерон; з) тау-интерферон; и) пептиды, например АТ-008, AnergiX.MS, иммуннокин (альфа-иммунокин-NNSO3), циклические пептиды, например ZD-7349; к) терапевтические ферменты, например растворимый CD8 (sCD8); л) плазмиду, кодирующую специфический аутоантиген в отношении рассеянного склероза, и плазмиду, кодирующую цитокин, например ВНТ-3009; м) ингибитор ФНО-альфа, например BLX-1002, талидомид, SH-636; н) антагонисты ФНО, например солимастат, ленерцепт (или RO-45-2081, тенефуз), онерцепт(sTNFR1), CC-1069; о) альфа-ФНО, например этанерцепт (или енбрел, TNR-001); п) антагонисты CD28, например абатисепт; р) ингибиторы тирозинкиназы Lck; с) ингибиторы катепсина K; т) антагонисты мембранного транспортного белка таурина, мишенью которого являются нейроны, и ингибитор калпаина растительного происхождения лейпептин, например неуродур; у) антагонист хемокинового рецептора-1 (CCR1), например ВХ-471; ф) антагонисты CCR2; х) антагонисты рецептора АМРА, например ER-167288-01 и ER-099487, Е-2007,талампанел; ц) блокаторы калиевых каналов, например фампридин; ч) низкомолекулярные антагонисты взаимодействия VLA-4/VCAM, содержащие тозилпролинфенилаланин, например ТВС-3342; ш) ингибиторы молекулы клеточной адгезии, например ТВС-772; э) антисмысловые олигонуклеотиды, например EN-101; ю) антагонисты связывания свободных легких цепей иммуноглобулина (IgLC) с рецепторами мастоцитов, например F-991; я) антигены, вызывающие апоптоз, например апоген Apogen MS; аа) агонист альфа-2 аденорецептора, например тизанидин (или занафлекс, тернелин, сирдалво, сирдалуд, мионидин); бб) сополимер L-тирозина, L-лизина, L-глутаминовой кислоты и L-аланина, например ацетат глатирамера (или копаксон, СОР-1, сополимер-1); вв) модуляторы топоизомеразы II, например гидрохлорид митоксантрона; гг) ингибитор аденозиндеаминазы, например кладрибин (или левстатин, милинакс, RWJ-26251); дд) интерлейкин-10, например илодекакин (или теновил, Sch-52000, CSIF); ее) антагонисты интерлейкина-12, например лизофиллин (или CT-1501R, LSF, лизофиллин); жж) этанаминум, например SRI-62-834 (или CRC-8605, NSC-614383); зз) иммуномодуляторы, например SAIK-MS, PNU-156804, пептид альфа-фетопротеин (AFP), IPDS; ии) агонисты ретиноидного рецептора, например адапален (или дифферин, CD-271); кк) TGF-бета, например GDF-1 (фактор роста и дифференциации 1); лл) TGF-бета-2, например BetaKine; мм) ингибиторы ММР, например гликомед; нн) ингибиторы фосфодиэстеразы 4 (ФДЭ 4), например RPR-122818; оо) ингибиторы опуриннуклеозидфосфорилазы, например, 9-(3-пиридилметил)-9-деазагуанин, пелдезин (или ВСХ-34, ТО-200);cc) цитокин-индуцирующие агенты, например нуклеозиды, ICN-17261; тт) ингибиторы цитокинов; уу) вакцины белков теплового шока, например HSPPC-96; фф) фактор роста неврегулина, например GGF-2 (или неврегулин, глиальный фактор роста 2); хх) ингибиторы катепсина S; цц) аналоги бропиримина, например PNU-56169, PNU-63693; чч) ингибиторы моноцитхемоатрактантного белка-1, например бензимидазолы, такие как ингибиторы МСР-1, LKS-1456, PD-064036, PD-064126, PD-084486, PD-172084, PD-172386. Кроме того, в настоящем изобретении предлагаются фармацевтические композиции, например, для парентального, энтерального или перорального введения, включающие по крайней мере один ингибитор ГЦ, необязательно в комбинации по крайней мере с одним из вышеупомянутых агентов. Указанные комбинации оказывают чрезвычайно благоприятное воздействие. Следовательно, такие комбинации являются эффективными и их можно использовать для лечения перечисленных выше заболеваний. Соответственно, в настоящем изобретении предлагается способ лечения указанных заболеваний. Способ включает совместное введение по крайней мере одного ингибитора ГЦ и по крайней мере одного другого агента или их последовательное введение. Совместное введение включает введение состава, который включает по крайней мере один ингибитор ГЦ и по крайней мере один другой агент или практически одновременное введение различных составов, содержащих каждый из указанных агентов. Антитела против бета-амилоидов и содержащие их композиции описаны, например, в заявкахWO 2006/137354, WO 2006/118959, WO 2006/103116, WO 2006/095041, WO 2006/081171,WO 2006/066233, WO 2006/066171, WO 2006/066089, WO 2006/066049, WO 2006/055178,WO 2006/046644, WO 2006/039470, WO 2006/036291, WO 2006/026408, WO 2006/016644,WO 2006/014638, WO 2006/014478, WO 2006/008661, WO 2005/123775, WO 2005/120571,WO 2005/105998, WO 2005/081872, WO 2005/080435, WO 2005/028511, WO 2005/025616,WO 2005/025516, WO 2005/023858, WO 2005/018424, WO 2005/011599, WO 2005/000193,WO 2004/108895, WO 2004/098631, WO 2004/080419, WO 2004/071408, WO 2004/069182,WO 2004/067561, WO 2004/044204, WO 2004/032868, WO 2004/031400, WO 2004/029630,WO 2004/029629, WO 2004/024770, WO 2004/024090, WO 2003/104437, WO 2003/089460,WO 2003/086310, WO 2003/077858, WO 2003/074081, WO 2003/070760, WO 2003/063760,WO 2003/055514, WO 2003/051374, WO 2003/048204, WO 2003/045128, WO 2003/040183,WO 2003/039467, WO 2003/016466, WO 2003/015691, WO 2003/014162, WO 2003/012141,WO 2002/088307, WO 2002/088306, WO 2002/074240, WO 2002/046237, WO 2002/046222,WO 2002/041842, WO 2001/062801, WO 2001/012598, WO 2000/077178, WO 2000/072880,WO 2000/063250, WO 1999/060024, WO 1999/027944, WO 1998/044955, WO 1996/025435,WO 1994/017197, WO 1990/014840, WO 1990/012871, WO 1990/012870, WO 1989/006242. Антитела против бета-амилоидов выбирают из группы, включающей, например, поликлональные,моноклональные, химерные или гуманизированные антитела. Кроме того, указанные антитела можно использовать для проведения активной и пассивной иммунной терапии, т.е. в качестве вакцин и моноклональных антител. Пригодные примеры антител против бета-амилоидов включают ACU-5A5, huC091 (Acumen/Merck),PF-4360365, RI-1014, RI-1219, RI-409, RN-1219 (Rinat Neuroscience Corp (Pfizer Inc, терапевтические нанотела Ablynx/Boehringer Ingelheim, специфические к бета-амилоидам гуманизированные моноклональные антитела Intellect Neurosciences/IBL, m266, m266.2 (Eli LillyCo.), AAB-02 (Elan), бапинеузумабMindset BioPharmaceuticals Inc. Прежде всего пригодными являются антитела, которые связываются с N-концевым фрагментом пептида А. Пригодными антителами, которые связываются с A-N-концевым фрагментом, являются,например, Acl-24 (АС Immune SA). Моноклональные антитела против бета-амилоидного пептида описано в заявке WO 2007/068412. Соответствующие химерные и гуманизированные антитела описаны в заявке WO 2008/011348. Способ получения вакцины для лечения амилоид-связанных заболеваний описан в заявке WO 2007/068411. Пригодными ингибиторами цистеинпротеазы являются ингибиторы катепсина В. Ингибиторы катепсина В и содержащие указанные ингибиторы композиции описаны, например, в заявках Примеры пригодных усилителей PIMT включают 10-аминоалифатилдибенз[b,f]оксепины, описанные в заявках WO 98/15647 и WO 03/057204 соответственно. Кроме того, в настоящем изобретении предлагаются модуляторы активности PIMT, описанные в заявке WO 2004/039773. Ингибиторы бета-секретазы и композиции, содержащие указанные ингибиторы, описаны, например, в заявках WO 2003/059346, WO 2006/099352, WO 2006/078576, WO 2006/060109, WO 2006/057983,WO 2006/057945, WO 2006/055434, WO 2006/044497, WO 2006/034296, WO 2006/034277,WO 2006/029850, WO 2006/026204, WO 2006/014944, WO 2006/014762, WO 2006/002004, US 7109217,WO 2005/113484, WO 2005/103043, WO 2005/103020, WO 2005/065195, WO 2005/051914,WO 2005/044830, WO 2005/032471, WO 2005/018545, WO 2005/004803, WO 2005/004802,WO 2004/062625, WO 2004/043916, WO 2004/013098, WO 03/099202, WO 03/043987, WO 03/039454,US 6562783, WO 2002/098849 и WO 2002/096897. Пригодные примеры ингибиторов бета-секретазы для применения по настоящему изобретению включают WY-25105 (Wyeth), посифен, (+)-фенсерин (TorreyPines/NIH), LSN-2434074, LY-2070275,LY-2070273, LY-2070102 (Eli LillyCo.), PNU-159775A, PNU-178025A, PNU-17820A, PNU-33312,PNU-38773, PNU-90530 (Elan/Pfizer), KMI-370, KMI-358, kmi-008 (Kyoto University), OM-99-2, OM-003Novo Pharmaceuticals Ltd.) и СТ-21166 (CoMentis Inc.). Ингибиторы гамма-секретазы и композиции, содержащие указанные ингибиторы, описаны, например, в заявках WO 2005/008250, WO 2006/004880, US 7122675, US 7030239, US 6992081, US 6982264,WO 2005/097768, WO 2005/028440, WO 2004/101562, US 6756511, US 6683091, WO 2003/066592,WO 2003/014075, WO 2003/013527, WO 2002/36555, WO 2001/53255, US 7109217, US 7101895,US 7049296, US 7034182, US 6984626, WO 2005/040126, WO 2005/030731, WO 2005/014553, US 6890956,EP 1334085, EP 1263774, WO 2004/101538, WO 2004/00958, WO 2004/089911, WO 2004/073630,WO 2004/069826, WO 2004/039370, WO 2004/031139, WO 2004/031137, US 6713276, US 6686449,WO 2003/091278, US 6649196, US 6448229, WO 2001/77144 и WO 2001/66564. Пригодные ингибиторы гамма-секретазы для применения по настоящему изобретению включаютWO 2006/068978. Пригодные ингибиторы ДПП IV по настоящему изобретению включают, например, ситаглиптин,дез-фтор-ситаглиптин (MerckCo.Inc), вилдаглиптин, ДПП-728, SDZ-272-070 (Novartis), ABT-279,ABT-341 (Abbott Laboratories), денаглиптин, ТА-6666 (GlaxoSmithKline plc.), SYR-322 (Takeda San DiegoNordisk A/S). Другие пригодные ингибиторы ДПП IV включают:(4) замещенные аминокетоны, описанные в заявке WO 2003/040174,(5) местные ингибиторы ДПП IV, описанные в заявке WO 2001/14318;(6) пролекарства, содержащие ингибиторы ДПП IV, описанные в заявках WO 1999/67278 и(7) глутаминилсодержащие ингибиторы ДПП IV, описанные в заявках WO 2003/072556 иWO 2004/099134. Пригодные ингибиторы синтеза бета-амилоидов по настоящему изобретению включают, например,биснорцимсерин (Axonyx Inc.), (R)-флурбипрофен (МСР-7869, Flurizan) (Myriad Genetics), нитрофлурбипрофен (NicOx), BGC-20-0406 (Sankyo Co. Ltd.) и BGC-20-0466 (BTG plc). Пригодные ингибиторы отложения амилоидных белков по настоящему изобретению включают, например, SP-233 (Samaritan Pharmaceuticals), AZD-103 (Ellipsis Neurotherapeutics Inc.), AAB-001(ArmaGen Technologies Inc.), TAK-070 (Takeda Pharmaceutical Co. Ltd.), CHF-5022, CHF-5074, CHF-5096 и CHF-5105 (Chiesi Farmaceutici SpA.). Пригодные ингибиторы ФДЭ-4 по настоящему изобретению включают, например, доксофиллинLaboratories Ltd.). Прежде всего предпочтительным ингибитором ФДЭ-4 является ролипрам. Ингибиторы МАО и композиции, содержащие указанные ингибиторы, описаны, например, в заявках WO 2006/091988, WO 2005/007614, WO 2004/089351, WO 2001/26656, WO 2001/12176,WO 1999/57120, WO 1999/57119, WO 1999/13878, WO 1998/40102, WO 1998/01157, WO 1996/20946,WO 1994/07890 и WO 1992/21333. Пригодные ингибиторы МАО по настоящему изобретению включают, например, линезолид(BASF AG), разагилин (Teva Pharmaceutical Industries Ltd.), ладостигил (Hebrew University of Jerusalem),сафинамид (Pfizer) и NW-1048 (Newron Pharmaceuticals SpA.). Пригодные антагонисты гистамина Н 3 по настоящему изобретению включают, например, АВТ-239,АВТ-834 (Abbott Laboratories), 3874-H1 (Aventis Pharma), UCL-2173 (Berlin Free University), UCL-1470JP 01042465, JP 03031298, JP 04208299, WO 00/71144, US 5847155, JP 09040693, JP 10077300,JP 05331072, JP 05015314, WO 1995/15310, WO 1993/00361, EP 0556482, JP 06234693, JP 01068396,EP 0709373, US 5965556, US 5756763, US 6121311, JP 63264454, JP 64000069, JP 63162672, EP 0268190,EP 0277588, EP 0275482, US 4977180, US 5091406, US 4983624, US 5112847, US 5100904, US 5254550,US 5262431, US 5340832, US 4956380, EP 0303434, JP 03056486, JP 01143897, JP 1226880, EP 0280956,US 4857537, EP 0461677, ЕР 0345428, JP 02275858, US 5506256, JP 06192298, ЕР 0618193, JP 03255080,ЕР 0468469, US 5118811, JP 05025125, WO 1993/13065, JP 05201970, WO 1994/12474, EP 0670309,EP 0451547, JP 06339390, US 5073549, US 4999349, EP 0268281, US 4743616, EP 0232849, EP 0224272,JP 62114978, JP 62114957, US 4757083, US 4810721, US 5198458, US 4826870, EP 0201742, EP 0201741,US 4873342, EP 0172458, JP 61037764, EP 0201743, US 4772587, EP 0372484, US 5028604, WO 91/18877,JP 04009367, JP 04235162, US 5407950, WO 1995/01352, JP 01250370, JP 02207070, US 5221752,EP 0468339, JP 04211648, WO 1999/46272, WO 2006/058720 и РСТ/ЕР 2006/061428. Пригодные ингибиторы пролилэндопептидаз по настоящему изобретению включают, например,Fmoc-Ala-Pyrr-CN, Z-Phe-Pro-бензотиазол (Probiodrug), Z-321 (Zeria Pharmaceutical Co Ltd.), ONO-1603(Ono Pharmaceutical Co Ltd), JTP-4819 (Japan Tobacco Inc.) и S-17092 (Servier). Другие пригодные соединения, которые можно использовать по настоящему изобретению в комбинации с ингибиторами ГЦ, включают NPY, миметик NPY, агонист или антагонист NPY или лиганд рецепторов NPY. Прежде всего предпочтительными соединениями по настоящему изобретению являются антагонисты рецепторов NPY. Пригодные лиганды или антагонисты рецепторовNPY включают производные 3 а,4,5,9b-тетрагидро-1h-бенз[е]индол-2-иламина, как описано в заявке WO 2000/68197. Антагонисты рецептора NPY включают соединения, описанные в патентах ЕР 0614911, ЕР 0747357,ЕР 0747356 и ЕР 0747378, в заявках WO 1994/17035, WO 1997/19911, WO 1997/19913, WO 1996/12489,WO 1997/19914, WO 1996/22305, WO 1996/40660, WO 1996/12490, WO 1997/09308, WO 1997/20820,WO 1997/20821, WO 1997/20822, WO 1997/20823, WO 1997/19682, WO 1997/25041, WO 1997/34843,WO 1997/46250, WO 1998/03492, WO 1998/03493, WO 1998/03494 и WO 1998/07420, WO 20000/30674,патентах US 5552411, 5663192, 5567714 и 6114336, JP 09157253, заявках WO 1994/00486,WO 1993/12139, WO 1995/00161 и WO 1999/15498, патенте US 5328899, патентах DE 3939797, ЕР 355794 и ЕР 355793, JP 06116284 и JP 07267988. Прежде всего пригодные антагонисты NPY включают соединения, описанные в указанных документах. Более предпочтительные соединения включают аминокислотные и непептидные антагонистыNPY. Указанные аминокислотные и непептидные антагонисты NPY включают описанные в патентах ЕР 0614911, ЕР 0747357, ЕР 0747356 и ЕР 0747378, в заявках WO 1994/17035, WO 1997/19911,WO 1997/19913, WO 1996/12489, WO 1997/19914, WO 1996/22305, WO 1996/40660, WO 1996/12490,WO 1997/09308, WO 1997/20820, WO 1997/20821, WO 1997/20822, WO 1997/20823, WO 1997/19682,WO 1997/25041, WO 1997/34843, WO 1997/46250, WO 1998/03492, WO 1998/03493, WO 1998/03494,WO 1998/07420 и WO 1999/15498, патентах US 5552411, 5663192, 5567714 и JP 09157253. Предпочтительные аминокислотные и непептидные антагонисты NPY включают соединения, описанные в указанных заявках. Прежде всего предпочтительные соединения включают аминокислотные антагонисты NPY. Указанные аминокислотные соединения описаны в заявках WO 1994/17035, WO 1997/19911, WO 1997/19913,WO 1997/19914 или WO 1999/15498. Предпочтительные аминокислотные антагонисты NPY включают описанные в указанных заявках соединения, например, BIBP3226 и, прежде всего, амид(R)-N2-(дифенилацетил)-(R)-N-[1-(4-гидроксифенил)этил]аргинина (пример 4, заявка WO 1999/15498). Агонисты рецептора M1 и композиции, содержащие указанные ингибиторы, описаны, например, в заявках WO 2004/087158 и WO 1991/10664. Пригодные антагонисты рецептора M1 по настоящему изобретению включают, например,CDD-0102 (Cognitive Pharmaceuticals), цевимелин (Evoxac) (Snow Brand Milk Products Co. Ltd.), NGX-267WO 1992/19238. Пригодные ингибиторы ацетилхолинэстеразы по настоящему изобретению включают, например,донепезил (Eisai Co. Ltd.), ривастигмин (Novartis AG), (-)-фенсерин (TorreyPines Therapeutics), ладостигилCo.), метрифонат (Bayer Corp.) и INM-176 (Whanln). Антагонисты рецептора NMDA и содержащие их композиции описаны, например, в заявкахWO 2006/094674, WO 2006/058236, WO 2006/058059, WO 2006/010965, WO 2005/000216,WO 2005/102390, WO 2005/079779, WO 2005/079756, WO 2005/072705, WO 2005/070429,WO 2005/055996, WO 2005/035522, WO 2005/009421, WO 2005/000216, WO 2004/092189,WO 2004/039371, WO 2004/028522, WO 2004/009062, WO 2003/010159, WO 2002/072542,WO 2002/34718, WO 2001/98262, WO 2001/94321, WO 2001/92204, WO 2001/81295, WO 2001/32640,WO 2001/10833, WO 2001/10831, WO 2000/56711, WO 2000/29023, WO 2000/00197, WO 1999/53922,WO 1999/48891, WO 1999/45963, WO 1999/01416, WO 1999/07413, WO 1999/01416, WO 1998/50075,WO 1998/50044, WO 1998/10757, WO 1998/05337, WO 1997/32873, WO 1997/23216, WO 1997/23215,WO 1997/23214, WO 1996/14318, WO 1996/08485, WO 1995/31986, WO 1995/26352, WO 1995/26350,WO 1995/26349, WO 1995/26342, WO 1995/12594, WO 1995/02602, WO 1995/02601, WO 1994/20109,WO 1994/13641, WO 1994/09016 и WO 1993/25534. Пригодные антагонисты рецептора NMDA по настоящему изобретению включают, например, мемантин (MerzCo. GmbH), топирамат (JohnsonJohnson), AVP-923 (невродекс) (Center for Neurologic(7-Cl-KYNA) (VistaGen), NPS-1407 (NPS Pharmaceuticals Inc.), YT-1006 (Yaupon Therapeutics Inc.),ED-1812 (Sosei RD Ltd.), гимантан (гидрохлорид N-2-(адамантил)гексаметиленимин) (RAMS), ланцицемин (AR-R-15896) (AstraZeneca), EVT-102, Ro-25-6981 и Ro-63-1908 (Hoffmann-La Roche AG/Evotec). Кроме того, предлагается комбинированная терапия для лечения атеросклероза, рестеноза или артрита при введении ингибитора ГЦ в комбинации с другим терапевтическим агентом, выбранным из группы, включающей ингибиторы ангиотензинконвертирующего фермента (АКФ), блокаторы рецептора ангиотензина II, диуретики, блокаторы кальциевых каналов, бета-блокаторы, ингибиторы агрегации тромбоцитов, модуляторы абсорбции холестерина, ингибиторы HMG-Co-A редуктазы, соединения, повышающие концентрацию липопротеинов высокой плотности (ЛПВП), ингибиторы ренина, ингибиторы ИЛ-6, противовоспалительные кортикостероиды, антипролиферативные агенты, доноры оксида азота,ингибиторы синтеза межклеточного матрикса, ингибиторы фактора роста или передачи сигнала цитокинов, антагонисты МСР-1 и ингибиторы тирозинкиназы, которые обеспечивают благоприятный или синергетический терапевтический эффект по сравнению с воздействием каждого компонента в отдельности. Блокаторы рецептора ангиотензина II являются активными агентами, которые связываются с подтипом рецепторов AT1 ангиотензина II, но не активируют указанный рецептор. В результате блокады рецептора ATI указанные агонисты можно, например, использовать в качестве антигипертензивных агентов. Пригодные блокаторы рецептора ангиотензина II, которые можно использовать в комбинации,включают антагонисты рецептора AT1, характеризующиеся различными структурными признаками,предпочтительно непептидной структурой. Например, можно упомянуть соединения, выбранные из группы, включающей валтасаран (ЕР 443983), лозартан (ЕР 253310), кандесартан (ЕР 459136), эпросартан (ЕР 403159), ирбесартан (ЕР 454511), олмесартан (ЕР 503785), тазосартан (ЕР 539086), телмисартан или в каждом случае их фармацевтически приемлемую соль. Предпочтительные антагонисты рецептора AT1 включают агенты, утвержденные органами здравоохранения и выпускающиеся фирмами, наиболее предпочтительно валтасаран или его фармацевтически приемлемую соль. Ингибирование ферментативной деградации ангиотензина до ангиотензина II под действием ингибиторов АКФ является эффективным вариантом регуляции кровяного давления и, таким образом, также представляет собой способ лечения гипертензии. Пригодными ингибиторами АКФ для применения в комбинации по настоящему изобретению являются, например, соединения, выбранные из группы, включающей алацеприл, беназеприл, беназеприлат, каптоприл, церонаприл, цилазаприл, делаприл, эналаприл, энаприлат, фозиноприл, имидаприл, лизиноприл, мовелтоприл, периндоприл, хинаприл, рамиприл, спираприл, темокаприл и трандолаприл или в каждом случае их фармацевтически приемлемую соль. Предпочтительные ингибиторы АКФ включают агенты, которые выпускаются фирмами, наиболее предпочтительно беназеприл и эналаприл. Диуретики включают, например, производные тиазидов, выбранные из группы, включающей хлортиазид, гидрохлортиазид, метилхлортиазид и хлорталидон. Наиболее предпочтительным диуретиком является гидрохлортиазол. Диуретик, кроме того, включает калий-сберегающий диуретик, такой как амилорид или триаметерин или их фармацевтически приемлемую соль. Блокаторы кальциевых каналов в основном включают дигидропиридины и недигидропиридины,например блокаторы типа дилтиазема и верапамила. Типичные блокаторы кальциевых каналов, используемые в указанной комбинации, представляют собой дигидропиридины, выбранные из группы, включающей амлодипин, фелодипин, риозидин, израдипин, ласидипин, никардипин, нифедипин, нигулдипин, нилудипин, нимодипин, низолдипин, нитрендипин и нивалдипин, типичные недигидропиридины выбраны из группы, включающей флунаризин, прениламин, дилтиазем, фендилин, галлопамил, мибефрадил, анипамил, тиапамил и верапамил и в каждом случае их фармацевтически приемлемую соль. Все указанные блокаторы кальциевых каналов используются в терапии, например, в качестве антигипертензивных средств, средств против стенокардии или противоаритмических лекарственных средств. Предпочтительные блокаторы кальциевых каналов включают амлодипин, дилтиазем, израдипин,никардипин, нифедипин, нимодипин, низолдипин, нитрендипин и верапамил или, например, в зависимости от конкретного блокатора кальциевого канала его фармацевтически приемлемую соль. Прежде всего предпочтительные дигидропиридины включают амлодипин или его фармацевтически приемелмую соль,прежде всего, безилат. Прежде всего предпочтительные недегидропиридины включают верапамил или его фармацевтически приемелмую соль, прежде всего, гидрохлорид. Бета-блокаторы, пригодные для применения по настоящему изобретению, включают бетаадренергические блокирующие агенты (бета-блокаторы), конкурирующие с эпинефрином за связывание с бета-адренергическими рецепторами и интерферирующие с действием эпинефрина. Соответственно,бета-блокаторы характеризуются селективностью в отношении бета-адренергического рецептора по сравнению с альфа-адренергическими рецепторами и, таким образом, не оказывают значительного альфа-блокирующего эффекта. Пригодные бета-блокаторы включают соединения, выбранные из группы,включающей ацебутолол, атенолол, бетаксолол, бизопролол, картеолол, карведилол, эсмолол, лабеталол,метопролол, надолол, окспренолол, пенбутолол, пиндолол, пропранолол, соталол и тимолол. Если бетаблокаторы представляют собой кислоту или основание или иным образом образуют фармацевтически приемлемые соли или пролекарства, то такие бета-блокаторы также включены в объем настоящего изобретения и следует понимать, что соединения можно вводить в свободной форме или в форме фармацевтически приемлемой соли или пролекарства, например, в форме приемлемого и гидролизуемого в физиологических условиях сложного эфира. Например, метопролол можно вводить в форме тартрата, пропранолол можно вводить в виде гидрохлорида и т.п.
МПК / Метки
МПК: C07D 405/14, A61K 31/433, A61P 29/00, C07D 403/04, A61K 31/437, C07D 401/14, A61K 31/4178, C07D 403/06, A61K 31/4184, C07D 417/04, C07D 403/14, C07D 409/14
Метки: качестве, глутаминилциклазы, имидазолидина, ингибиторов, производные
Код ссылки
<a href="https://eas.patents.su/30-21150-proizvodnye-imidazolidina-v-kachestve-ingibitorov-glutaminilciklazy.html" rel="bookmark" title="База патентов Евразийского Союза">Производные имидазолидина в качестве ингибиторов глутаминилциклазы</a>
Предыдущий патент: Косметические или дерматологические пенные составы, их применение и способы получения
Следующий патент: Аппарат для получения поглощающего изделия и способ получения поглощающего изделия
Случайный патент: Способ и установка для производства низкотемпературного кокса












