4-(n-фениламино)хиназолины/-хинолины в качестве ингибиторов тирозинкиназы
Формула / Реферат
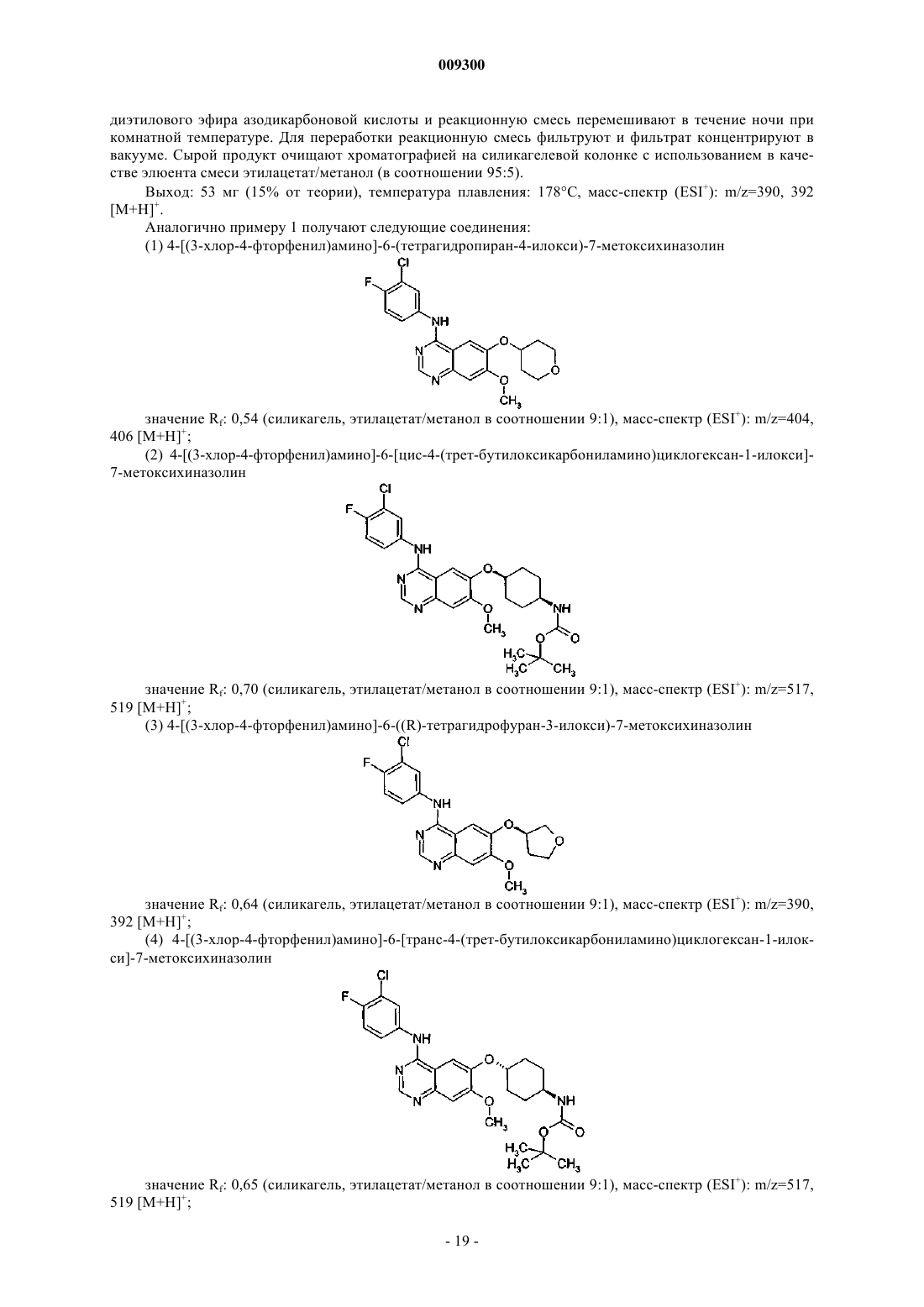
1. Бициклические гетероциклы общей формулы
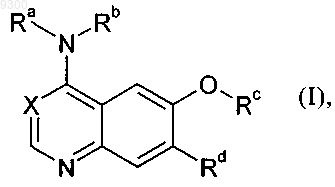
в которой
Ra обозначает атом водорода,
Rb обозначает фенил, в котором фенильное ядро замещено остатками R1-R3, где
R1 и R2 могут иметь идентичные или различные значения и обозначают атом водорода, фтора, хлора, брома или иода, C1-4алкильную группу, C1-4алкоксигруппу, С2-3алкинильную группу, арилметоксигруппу, гетероарилоксигруппу, гетероарилметоксигруппу и
R3 обозначает атом водорода,
Rc обозначает циклобутильную, циклопентильную или циклогексильную группу, каждая из которых замещена группой R4-N-R5, где
R4 обозначает атом водорода или C1-3алкильную группу, а
R5 обозначает атом водорода, C1-3алкильную группу, аминокарбонил-C1-3алкильную группу, пирролидин-1-илкарбонил-C1-3алкильную группу, пиперидин-1-илкарбонил-С1-3алкильную группу, морфолин-4-илкарбонил-C1-3алкильную группу, пиперазин-1-илкарбонил-С1-3алкильную группу, 4-C1-3алкилпиперазин-1-илкарбонил-C1-3алкильную группу, C1-4алкилоксикарбониламино-С2-4алкильную группу, амино-С2-4алкильную группу, C1-3алкиламино-С2-4алкильную группу, ди(C1-3алкил)амино-С2-4алкильную группу, C1-3алкилкарбониламино-С2-4алкильную группу, аминокарбониламино-С2-4алкильную группу, C1-3алкиламинокарбониламино-С2-4алкильную группу, ди(C1-3алкил)аминокарбониламино-С2-4алкильную группу, пирролидин-1-илкарбониламино-С2-4алкильную группу, пиперидин-1-илкарбониламино-С2-4алкильную группу, морфолин-4-илкарбониламино-С2-4алкильную группу, C1-3алкилсульфонил-С2-4алкильную группу, C1-3алкилсульфониламино-С2-4алкильную группу, (2-оксопирролидин-1-ил)-С2-4алкильную группу, (2-оксопиперидин-1-ил)-С2-4алкильную группу, (3-оксоморфолин-4-ил)-С2-4алкильную группу, (2-оксоимидазолидин-1-ил)-С2-4алкильную группу, (2-оксо-3-C1-3алкилимидазолидин-1-ил)-С2-4алкильную группу, (2-оксогексагидропиримидин-1-ил)-С2-4алкильную группу, (2-оксо-3-C1-3алкилгексагидропиримидин-1-ил)-С2-4алкильную группу, C1-4алкилсульфонильную группу, хлор-C1-4алкилсульфонильную группу, бром-С1-4алкилсульфонильную группу, амино-С1-4алкилсульфонильную группу, C1-3алкиламино-С1-4алкилсульфонильную группу, ди(C1-3алкил)амино-С1-4алкилсульфонильную группу, (пирролидин-1-ил)-С1-4
алкилсульфонильную группу, (пиперидин-1-ил)-С1-4алкилсульфонильную группу, (морфолин-4-ил)-С1-4
алкилсульфонильную группу, (пиперазин-1-ил)-С1-4алкилсульфонильную группу, (4-C1-3алкилпиперазин-1-ил)-С1-4алкилсульфонильную группу, С1-4алкилоксикарбонильную группу, C1-4алкилкарбонильную группу, C1-3алкилокси-С1-4алкилкарбонильную группу, тетрагидрофуранилкарбонильную группу, тетрагидропиранилкарбонильную группу, амино-C1-4алкилкарбонильную группу, C1-3алкиламино-С1-4алкилкарбонильную группу, ди(C1-3алкил)амино-С1-4алкилкарбонильную группу, пирролидин-1-ил-С1-4алкилкарбонильную группу, пиперидин-1-ил-C1-4алкилкарбонильную группу, морфолин-4-ил-C1-4алкилкарбонильную группу, (пиперазин-1-ил)-С1-4алкилкарбонильную группу, (4-C1-3алкилпиперазин-1-ил)-С1-4алкилкарбонильную группу, C1-3алкилсульфонил-C1-4алкилкарбонильную группу, цианогруппу, аминокарбонильную группу, C1-3алкиламинокарбонильную группу, ди(C1-3алкил)аминокарбонильную группу, (C1-3
алкилокси-С2-4алкил)аминокарбонильную группу, N-(C1-3алкил)-N-(C1-3алкилокси-С2-4алкил)аминокарбонильную группу, ариламинокарбонильную группу, пирролидин-1-илкарбонильную группу, пиперидин-1-илкарбонильную группу, морфолин-4-илкарбонильную группу, пиперазин-1-илкарбонильную группу, 4-C1-3алкилпиперазин-1-илкарбонильную группу, аминосульфонильную группу, C1-3алкиламиносульфонильную группу, ди(C1-3алкил)аминосульфонильную группу, пирролидин-1-ил-сульфонильную группу, пиперидин-1-илсульфонильную группу, морфолин-4-илсульфонильную группу, пиперазин-1-илсульфонильную группу, 4-C1-3алкилпиперазин-1-илсульфонильную группу,
Rd обозначает атом водорода, фтора, хлора или брома, гидроксигруппу, C1-4алкилоксигруппу, замещенную 1-3 атомами фтора метоксигруппу, замещенную 1-5 атомами фтора этилоксигруппу, С2-4алкилоксигруппу, которая замещена остатком R7, где
R7 обозначает гидроксигруппу, C1-3алкилоксигруппу, С3-6циклоалкилоксигруппу, аминогруппу, C1-3алкиламиногруппу, ди(C1-3алкил)аминогруппу, бис(2-метоксиэтил)аминогруппу, пирролидин-1-ильную группу, пиперидин-1-ильную группу, морфолин-4-ильную группу, пиперазин-1-ильную группу, 4-C1-3алкилпиперазин-1-ильную группу, формиламиногруппу, С1-4алкилкарбониламиногруппу, C1-3алкилокси-C1-3алкилкарбониламиногруппу, С1-4алкилоксикарбониламиногруппу, аминокарбониламиногруппу, C1-3алкиламинокарбониламиногруппу, ди(C1-3алкил)аминокарбониламиногруппу, пирролидин-1-илкарбониламиногруппу, пиперидин-1-илкарбониламиногруппу, пиперазин-1-илкарбониламиногруппу, 4-C1-3алкилпиперазин-1-илкарбониламиногруппу, морфолин-4-илкарбониламиногруппу или С1-4алкилсульфониламиногруппу, С3-7циклоалкилоксигруппу, С3-7циклоалкил-С1-4алкилоксигруппу, тетрагидрофуран-3-илоксигруппу, тетрагидропиран-3-илоксигруппу, тетрагидропиран-4-илоксигруппу, тетрагидрофуранил-С1-4алкилоксигруппу, тетрагидропиранил-С1-4алкилоксигруппу, С1-4алкоксигруппу, и
X обозначает атом азота,
при этом под упомянутыми в определениях указанных выше остатков арильными группами в каждом случае подразумевается фенильная группа, которая одно- или двузамещена остатком R9, где в случае двукратного замещения заместители могут иметь идентичные или различные значения и где
R9 обозначает атом водорода, фтора, хлора, брома или иода, C1-3алкильную группу, гидроксигруппу, C1-3алкилоксигруппу, дифторметильную группу, трифторметильную группу, дифторметоксигруппу, трифторметоксигруппу или цианогруппу,
под упомянутыми в определениях указанных выше остатков гетероарильными группами подразумевается пиридильная, пиридазинильная, пиримидинильная или пиразинильная группа, причем указанные выше гетероарильные группы в каждом случае одно- или двузамещены остатком R9, где в случае двукратного замещения заместители могут иметь идентичные или различные значения и где
R9 имеет указанные выше значения,
каждая из указанных выше пирролидинильных, пиперидинильных, пиперазинильных и морфолинильных групп может быть замещена одной или двумя С1-3алкильными группами и указанные выше алкильные группы, если не указано иное, могут иметь прямую или разветвленную цепь, за исключением 4-[(3-хлор-4-фторфенил)амино]-6-((S)-тетрагидрофуран-3-илокси)-7-гидроксихиназолина,
их таутомеры, их стереоизомеры, их смеси и их соли.
2. Бициклические гетероциклы общей формулы I по п.1, в которых
Ra обозначает атом водорода,
Rb обозначает замещенную остатками R1-R3 фенильную группу, где
R1 обозначает атом водорода, фтора, хлора шыш брома, метильную группу, этинильную группу, фенилметоксигруппу, где фенильный фрагмент вышеуказанных групп необязательно замещен атомом фтора или хлора, или пиридилокси- либо пиридинилметоксигруппу, где пиридинильный фрагмент вышеуказанных групп необязательно замещен метильной группой,
R2 обозначает атом водорода, фтора или хлора или метильную группу и
R3 обозначает атом водорода,
Rc обозначает циклопентильную группу, которая в положении 3 замещена группой R4-N-R5, где
R4 обозначает атом водорода или C1-3алкильную группу, а
R5 обозначает атом водорода, C1-3алкильную группу, аминокарбонил-C1-3алкильную группу, C1-3алкиламинокарбонил-C1-3алкильную группу, ди(C1-3алкил)аминокарбонил-C1-3алкильную группу, пирролидин-1-илкарбонил-С1-3алкильную группу, пиперидин-1-илкарбонил-C1-3алкильную группу, пиперазин-1-илкарбонил-С1-3алкильную группу, 4-C1-3алкилпиперазин-1-илкарбонил-С1-3алкильную группу, морфолин-4-илкарбонил-C1-3алкильную группу, гидрокси-С2-4алкильную группу, C1-3алкилокси-С2-4алкильную группу, C1-4алкилоксикарбониламино-С2-4алкильную группу, амино-С2-4алкильную группу, C1-3алкиламино-С2-4алкильную группу, ди(C1-3алкил)амино-С2-4алкильную группу, C1-3алкилкарбониламино-С2-4алкильную группу, аминокарбониламино-С2-4алкильную группу, C1-3алкиламинокарбониламино-С2-4алкильную группу, ди(C1-3алкил)аминокарбониламино-С2-4алкильную группу, морфолин-4-илкарбониламино-С2-4алкильную группу, C1-3алкилсульфонил-С2-4алкильную группу, C1-3алкилсульфониламино-С2-4алкильную группу, (2-оксопирролидин-1-ил)-С2-4алкильную группу, (2-оксопиперидин-1-ил)-С2-4алкильную группу, (3-оксоморфолин-4-ил)-С2-4алкильную группу, (2-оксоимидазолидин-1-ил)-С2-4алкильную группу, (2-оксо-3-метилимидазолидин-1-ил)-С2-4алкильную группу, (2-оксогексагидропиримидин-1-ил)-С2-4алкильную группу, (2-оксо-3-метилгексагидропиримидин-1-ил)-С2-4алкильную группу, C1-3алкилсульфонильную группу, хлор-С2-4алкилсульфонильную группу, бром-С2-4алкилсульфонильную группу, амино-С2-4алкилсульфонильную группу, С1-3алкиламино-С2-4алкилсульфонильную группу, ди(C1-3алкил)
амино-С2-4алкилсульфонильную группу, (пирролидин-1-ил)-С2-4алкилсульфонильную группу, (пиперидин-1-ил)-С2-4алкилсульфонильную группу, (морфолин-4-ил)-С2-4алкилсульфонильную группу, C1-4алкилоксикарбонильную группу, формильную группу, C1-3алкилкарбонильную группу, C1-3алкилокси-C1-3
алкилкарбонильную группу, тетрагидрофуранилкарбонильную группу, тетрагидропиранилкарбонильную группу, амино-C1-3алкилкарбонильную группу, C1-3алкиламино-C1-3алкилкарбонильную группу, ди(C1-3
алкил)амино-C1-3алкилкарбонильную группу, пирролидин-1-ил-C1-3алкилкарбонильную группу, пиперидин-1-ил-C1-3алкилкарбонильную группу, пиперазин-1-ил-C1-3алкилкарбонильную группу, 4-C1-3алкилпиперазин-1-ил-C1-3алкилкарбонильную группу, морфолин-4-ил-C1-3алкилкарбонильную группу, C1-3алкилсульфонил-C1-3алкилкарбонильную группу, цианогруппу, аминокарбонильную группу, C1-3алкиламинокарбонильную группу, ди(C1-3алкил)аминокарбонильную группу, (C1-3алкилокси-С2-4алкил)аминокарбонильную группу, N-(C1-3алкил)-N-(C1-3алкилокси-С2-4алкил)аминокарбонильную группу, фениламинокарбонильную группу, пирролидин-1-илкарбонильную группу, пиперидин-1-илкарбонил, морфолин-4-илкарбонильную группу, C1-3алкилморфолин-4-илкарбонильную группу, ди(C1-3алкил)морфолин-4-илкарбонильную группу, пиперазин-1-илкарбонильную группу, 4-(C1-3алкил)пиперазин-1-илкарбонильную группу, аминосульфонильную группу, C1-3алкиламиносульфонильную группу, ди(C1-3алкил)аминосульфонильную группу, пирролидин-1-илсульфонильную группу, пиперидин-1-илсульфонильную группу или морфолин-4-илсульфонильную группу,
Rd обозначает атом водорода, C1-3алкилоксигруппу, метоксигруппу, замещенную 1-3 атомами фтора, этилоксигруппу, которая в положении 2 замещена остатком R7, где
R7 обозначает гидроксигруппу, C1-3алкилоксигруппу, аминогруппу, C1-3алкиламиногруппу, ди(C1-3
алкил)аминогруппу, бис(2-метоксиэтил)аминогруппу, пирролидин-1-ильную группу, пиперидин-1-ильную группу, морфолин-4-ильную группу, пиперазин-1-ильную группу, 4-C1-3алкилпиперазин-1-ильную группу, формиламиногруппу, C1-4алкилкарбониламиногруппу, C1-3алкилокси-C1-3алкилкарбониламиногруппу, C1-4алкилоксикарбониламиногруппу, аминокарбониламиногруппу, C1-3алкиламинокарбониламиногруппу, ди(C1-3алкил)аминокарбониламиногруппу, пирролидин-1-илкарбониламиногруппу, пиперидин-1-илкарбониламиногруппу, пиперазин-1-илкарбониламиногруппу, 4-C1-3алкилпиперазин-1-илкарбониламиногруппу, морфолин-4-илкарбониламиногруппу или С1-4алкилсульфониламиногруппу,
при этом указанные выше алкильные группы, если не указано иное, могут иметь прямую или разветвленную цепь,
их таутомеры, их стереоизомеры, их смеси и их соли.
3. Бициклические гетероциклы общей формулы 1 по п.1, в которых
Ra обозначает атом водорода,
Rb обозначает 3-этинилфенильную группу, 3-бромфенильную группу, 3,4-дифторфенильную группу, 3-хлор-4-фторфенильную группу, 3-хлор-4-бензилоксифенильную группу, 3-хлор-4-[(3-фторбензил)
окси]фенильную группу, 4-(пиридин-3-илокси)фенильную группу, 4-[(6-метилпиридин-3-ил)окси]фенильную группу, 3-метил-4-(пиридин-3-илокси)фенильную группу, 3-метил-4-[(6-метилпиридин-3-ил)
окси]фенильную группу, 3-хлор-4-(пиридин-3-илокси)фенильную группу или 3-хлор-4-[(6-метилпиридин-3-ил)окси]фенильную группу,
Rc обозначает циклогексильную группу, которая в положении 3 или в положении 4 замещена группой R4-N-R5, где
R4 обозначает атом водорода, метильную группу или этильную группу, а
R5 обозначает атом водорода, метильную группу, аминокарбонилметильную группу, метиламинокарбонилметильную группу, диметиламинокарбонилметильную группу, пирролидин-1-илкарбонилметильную группу, пиперидин-1-илкарбонилметильную группу, пиперазин-1-илкарбонилметильную группу, 4-метилпиперазин-1-илкарбонилметильную группу, морфолин-4-илкарбонилметильную группу, 2-(морфолин-4-илкарбонил)этильную группу, 3-(морфолин-4-илкарбонил)пропильную группу, этильную группу, пропильную группу, 2-гидроксиэтильную группу, 3-гидроксипропильную группу, 2-метоксиэтильную группу, 3-метоксипропильную группу, 2-(бутилоксикарбониламино)этильную группу, 2-аминоэтильную группу, 3-аминопропильную группу, 2-(ацетиламино)этильную группу, 3-(ацетиламино)пропильную группу, 2-(этилкарбониламино)этильную группу, 3-(этилкарбониламино)пропильную группу, 2-(пропилкарбониламино)этильную группу, 3-(пропилкарбониламино)пропильную группу, 2-(этиламинокарбониламино)этильную группу, 3-(этиламинокарбониламино)пропильную группу, 2-(диметиламинокарбониламино)этильную группу, 3-(диметиламинокарбониламино)пропильную группу, 2-(морфолин-4-илкарбониламино)этильную группу, 3-(морфолин-4-илкарбониламино)пропильную группу, 2-(метилсульфонил)этильную группу, 3-(метилсульфонил)пропильную группу, 2-(метилсульфониламино)этильную группу, 3-(метилсульфониламино)пропильную группу, 2-(2-оксопирролидин-1-ил)этильную групяу, 2-(2-оксопиперидин-1-ил)этильную группу, 2-(3-оксоморфолин-4-ил)этильную группу, 2-(2-оксоимидазолидин-1-ил)этильную группу, 2-(2-оксо-3-метилимидазолидин-1-ил)этильную группу, 2-(2-оксогексагидропиримидин-1-ил)этильную группу, 2-(2-оксо-3-метилгексагидропиримидин-1-ил)этильную группу, 3-(2-оксопирролидин-1-ил)пропильную группу, 3-(2-оксопиперидин-1-ил)пропильную группу, 3-(3-оксоморфолин-4-ил)пропильную группу, 3-(2-оксоимидазолидин-1-ил)пропильную группу, 3-(2-оксо-3-метилимидазолидин-1-ил)пропильную группу, 3-(2-оксогексагидропиримидин-1-ил)пропильную группу, 3-(2-оксо-3-метилгексагидропиримидин-1-ил)пропильную группу, метилсульфонильную группу, этилсульфонильную группу, 3-хлорпропилсульфонильную группу, 2-(морфолин-4-ил)этилсульфонильную группу, 3-(морфолин-4-ил)пропилсульфонильную группу, пропилоксикарбонильную группу, бутилоксикарбонильную группу, формильную группу, ацетильную группу, этилкарбонильную группу, пропилкарбонильную группу, метоксиацетильную группу, (2-метоксиэтил)карбонильную группу, (3-метоксипропил)
карбонильную группу, тетрагидрофуран-2-илкарбонильную группу, тетрагидропиран-4-илкарбонильную группу, аминоацетильную группу, метиламиноацетильную группу, диметиламиноацетильную группу, морфолин-4-илацетильную группу, [2-(морфолин-4-ил)этил]карбонильную группу, [3-(морфолин-4-ил)
пропил]карбонильную группу, метилсульфонилацетильную группу, цианогруппу, аминокарбонильную группу, метиламинокарбонильную группу, диметиламинокарбонильную группу, этиламинокарбонильную группу, диэтиламинокарбонильную группу, пропиламинокарбонильную группу, (2-метоксиэтил)
аминокарбонильную группу, N-метил-N-(2-метоксиэтил)аминокарбонильную группу, (3-метоксипропил)
аминокарбонильную группу, N-метил-N-(3-метоксипропил)аминокарбонильную группу, фениламинокарбонильную группу, пирролидин-1-илкарбонильную группу, пиперидин-1-илкарбонильную группу, морфолин-4-илкарбонильную группу, 2-метилморфолин-4-илкарбонильную группу, 2,6-диметилморфо-лин-4-илкарбонильную группу, 4-метилпиперазин-1-илкарбонильную группу, аминосульфонильную группу, метиламиносульфонильную группу, диметиламиносульфонильную группу или морфолин-4-илсульфонильную группу,
Rd обозначает атом водорода, метоксигруппу, дифторметоксигруппу, этилоксигруппу, этилоксигруппу, которая в положении 2 замещена остатком R7, где
R7 обозначает гидроксигруппу, метоксигруппу, этоксигруппу, аминогруппу, диметиламиногруппу, диэтиламиногруппу, бис(2-метоксиэтил)аминогруппу, пирролидин-1-ильную группу, пиперидин-1-ильную группу, морфолин-4-ильную группу, 4-метилпиперазин-1-ильную группу, 4-этилпиперазин-1-ильную группу, ацетиламиногруппу, этилкарбониламиногруппу, пропилкарбониламиногруппу, бутилкарбониламиногруппу, метоксиацетиламиногруппу, бутилоксикарбониламиногруппу, этиламинокарбониламиногруппу, диметиламинокарбониламиногруппу, пирролидин-1-илкарбониламиногруппу, пиперидин-1-илкарбониламиногруппу, морфолин-4-илкарбониламиногруппу, метилсульфониламиногруппу, этилсульфониламиногруппу или бутилсульфониламиногруппу,
при этом указанные выше алкильные группы, если не указано иное, могут иметь прямую или разветвленную цепь,
их таутомеры, их стереоизомеры, их смеси и их соли.
4. Бициклические гетероциклы общей формулы I по п.1, в которых
Ra обозначает атом водорода,
Rb обозначает 3-бромфенильную группу, 3,4-дифторфенильную группу, 3-хлор-4-фторфенильную группу, 3-этинилфенильную группу, 3-хлор-4-бензилоксифенильную группу, 3-хлор-4-[(3-фторбензил)
окси]фенильную группу, 4-(пиридин-3-илокси)фенильную группу, 4-[(6-метилпиридин-3-ил)окси]фенильную группу, 3-метил-4-(пиридин-3-илокси)фенильную группу, 3-метил-4-[(6-метилпиридин-3-ил)
окси]фенильную группу, 3-хлор-4-(пиридин-3-илокси)фенильную группу или 3-хлор-4-[(6-метилпиридин-3-ил)окси]фенильную группу,
Rc обозначает циклогексильную группу, которая в положении 3 замещена амино-, ацетиламино-, трет-бутилоксикарбониламино- или метилсульфониламиногруппой, циклогексильную группу, которая в положении 4 замещена амино-, метиламино-, этиламино-, диметиламино-, аминокарбонилметиламино-, метиламинокарбонилметиламино-, диметиламинокарбонилметиламино-, морфолин-4-илкарбонилметиламино-, [3-(морфолин-4-илкарбонил)пропил]амино-, [2-(метилсульфонил)этил]амино-, [3-(метилсульфонил)пропил]амино- или [2-(метилсульфониламино)этил]аминогруппой, циклогексильную группу, которая в положении 4 замещена [2-(2-оксопирролидин-1-ил)этил]амино-, [2-(2-оксопиперидин-1-ил)этил]амино-, [2-(2-оксоимидазолидин-1-ил)этил]амино-, [2-(2-оксо-3-метилимидазолидин-1-ил)этил]амино-, [2-(2-оксогексагидропиримидин-1-ил)этил]амино- или [2-(2-оксо-3-метилгексагидропиримидин-1-ил)этил]аминогруппой, циклогексильную группу, которая в положении 4 замещена [3-(2-оксопирролидин-1-ил)пропил]
амино-, [3-(2-оксопиперидин-1-ил)пропил]амино-, [3-(2-оксоимидазолидин-1-ил)пропил]амино-, [3-(2-оксо-3-метилимидазолидин-1-ил)пропил]амино-, [3-(2-оксогексагидропиримидин-1-ил)пропил]амино- или [3-(2-оксо-3-метилгексагидропиримидин-1-ил)пропил]аминогруппой, циклогексильную группу, которая в положении 4 замещена ацетиламино-, N-(ацетил)метиламино-, аминометилкарбониламино-, метиламинометилкарбониламино-, диметиламинометилкарбониламино-, морфолин-4-илметилкарбониламино-, метоксиацетиламино-, N-(метоксиацетил)метиламино-, тетрагидропиран-4-илкарбониламино-, N-(тетрагидропиран-4-илкарбонил)метиламино-, трет-бутилоксикарбониламино-, N-(трет-бутилоксикарбонил)метиламино-, аминокарбониламино-, метиламинокарбониламино-, N-(этиламинокарбонил)метиламино-, диметиламинокарбониламино-, N-(диметиламинокарбонил)метиламино-, N-(пиперидин-1-илкарбонил)
метиламино-, морфолин-4-илкарбониламино-, N-(морфолин-4-илкарбонил)метиламино- или N-(4-метилпиперазин-1-илкарбонил)метиламиногруппой, циклогексильную группу, которая в положении 4 замещена 2-оксопирролидин-1-ильной, 2-оксопиперидин-1-ильной, 3-оксоморфолин-4-ильной, 2-оксоимидазолидин-1-ильной, 2-оксо-3-метилимидазолидин-1-ильной, 2-оксогексагидропиримидин-1-ильной или 2-оксо-3-метилгексагидропиримидин-1-ильной группой, циклогексильную группу, которая в положении 4 замещена метилсульфониламино-, N-(метилсульфонил)метиламино-, этилсульфониламино-, N-(этилсульфонил)метиламино-, диметиламиносульфониламино-, N-(диметиламиносульфонил)метиламино-, морфолин-4-илсульфониламино-, N-(морфолин-4-илсульфонил)метиламино-, 3-хлорпропилсульфониламино-, [2-(морфолин-4-ил)этил]сульфониламино- или [3-(морфолин-4-ил)пропил]сульфониламиногруппой, пирролидин-3-ильную группу, пирролидин-3-ильную группу, которая в положении 1 замещена метильной, ацетильной, метоксиацетильной, трет-бутилоксикарбонильной, морфолин-4-илкарбонильной или метилсульфонильной группой, пиперидин-3-ильную группу, пиперидин-3-ильную группу, которая в положении 1 замещена метильной, ацетильной, метоксиацетильной, трет-бутилоксикарбонильной, морфолин-4-илкарбонильной или метилсульфонильной группой, пиперидин-4-ильную группу, которая в положении 1 замещена метильной, этильной, пропильной, изопропильной, 2-гидроксиэтильной, 2-метоксиэтильной, 3-метоксипропильной, 2-(метилсульфонил)этильной, 3-(метилсульфонил)пропильной, 2-(трет-бутилоксикарбониламино)этильной, 2-аминоэтильной, 2-(ацетиламино)этильной, 2-(этилкарбониламино)
этильной, 2-(пропилкарбониламино)этильной, 2-(этиламинокарбониламино)этильной, 2-(диметиламинокарбониламино)этильной, 2-(морфолин-4-илкарбониламино)этильной, 3-(ацетиламино)пропильной, 3-(этилкарбониламино)пропильной, 3-(пропилкарбониламино)пропильной, 3-(этиламинокарбониламино)
пропильной, 3-(диметиламинокарбониламино)пропильной, 3-(морфолин-4-илкарбониламино)пропильной, 2-(метилсульфониламино)этильной, 3-(метилсульфониламино)пропильной, (аминокарбонил)метильной, (метиламинокарбонил)метильной, (диметиламинокарбонил)метильной, (пирролидин-1-илкарбонил)метильной, (морфолин-4-илкарбонил)метильной, 2-(морфолин-4-илкарбонил)этильной или 3-(морфолин-4-илкарбонил)пропильной группой, пиперидин-4-ильную группу, которая в положении 1 замещена 2-(2-оксопирролидин-1-ил)этильной, 2-(2-оксопиперидин-1-ил)этильной, 2-(3-оксоморфолин-4-ил)этильнющ, 2-(2-оксоимидазолидин-1-ил)этильной, 2-(2-оксо-3-метилимидазолидин-1-ил)этильной, 2-(2-оксогексагидропиримидин-1-ил)этильной или 2-(2-оксо-3-метилгексагидропиримидин-1-ил)этильной группой, пиперидин-4-ильную группу, которая в положении 1 замещена 3-(2-оксопирролидин-1-ил)пропильной, 3-(2-оксопиперидин-1-ил)пропильной, 3-(3-оксоморфолин-4-ил)пропильной, 3-(2-оксоимидазолидин-1-ил)пропильной, 3-(2-оксо-3-метилимидазолидин-1-ил)пропильной, 3-(2-оксогексагидропиримидин-1-ил)пропильной или 3-(2-оксо-3-метилгексагидропиримидин-1-ил)пропильной группой, пиперидин-4-ильную группу, которая в положении 1 замещена формильной, ацетильной, метоксиацетильной, (2-метоксиэтил)карбонильной, (3-метоксипропил)карбонильной, метилсульфонилацетильной, аминоацетильной, метиламиноацетильной, (диметиламино)ацетильной, (морфолин-4-ил)ацетильной, [2-(морфолин-4-ил)этил]карбонильной, [3-(морфолин-4-ил)пропил]карбонильной, тетрагидрофуран-2-илкарбонильной или тетрагидропиран-4-илкарбонильной группой, пиперидин-4-ильную группу, которая в положении 1 замещена цианогруппой, аминокарбонильной, метиламинокарбонильной, этиламинокарбонильной, (2-метоксиэтил)аминокарбонильной, N-метил-N-(2-метоксиэтил)аминокарбонильной, (3-метоксипропил)аминокарбонильной, N-метил-N-(3-метоксипропил)аминокарбонильной, изопропиламинокарбонильной, фениламинокарбонильной, диметиламинокарбонильной, диэтиламинокарбонильной, пирролидин-1-илкарбонильной, пиперидин-1-илкарбонильной, морфолин-4-илкарбонильной, 2-метилморфолин-4-илкарбонильной, 2,6-диметилморфолин-4-илкарбонильной, изопропилоксикарбонильной или трет-бутилоксикарбонильной группой, пиперидин-4-ильную группу, которая в положении 1 замещена метилсульфонильной, этилсульфонильной, [2-(морфолин-4-ил)этил]сульфонильной, [3-(морфолин-4-ил)пропил]сульфонильной, аминосульфонильной, метиламиносульфонильной, диметиламиносульфонильной или морфолин-4-илсульфонильной группой, тетрагидрофуран-3-ильную группу, тетрагидропиран-3-ильную группу или тетрагидропиран-4-ильную группу,
Rd обозначает атом водорода, метоксигруппу, дифторметоксигруппу, этилоксигруппу, 2-(морфолин-4-ил)этилоксигруппу, 3-(морфолин-4-ил)пропилоксигруппу, 4-(морфолин-4-ил)бутилоксигруппу, 3-(диметиламино)пропилоксигруппу, 3-(диэтиламино)пропилоксигруппу, 3-[бис(2-метоксиэтил)амино]
пропилоксигруппу, 3-(пиперазин-1-ил)пропилоксигруппу, 3-(4-метилпиперазин-1-ил)пропилоксигруппу, 3-(4-этилпиперазин-1-ил)пропилоксигруппу, 2-(2-оксопирролидин-1-ил)этилоксигруппу, 2-(2-оксопиперидин-1-ил)этилоксигруппу, 2-(3-оксоморфолин-4-ил)этилоксигруппу, 2-(2-оксоимидазолидин-1-ил)этилоксигруппу, 2-(2-оксо-3-метилимидазолидин-1-ил)этилоксигруппу, 2-(2-оксогексагидропиримидин-1-ил)
этилоксигруппу, 2-(2-оксо-3-метилгексагидропиримидин-1-ил)этилоксигруппу, 3-(2-оксопирролидин-1-ил)пропилоксигруппу, 3-(2-оксопиперидин-1-ил)пропилоксигруппу, 3-(3-оксоморфолин-4-ил)пропилоксигруппу, 3-(2-оксоимидазолидин-1-ил)пропилоксигруппу, 3-(2-оксо-3-метилимидазолидин-1-ил)пропилоксигруппу, 3-(2-оксогексагидропиримидин-1-ил)пропилоксигруппу, 3-(2-оксо-3-метилгексагидропиримидин-1-ил)пропилоксигруппу, 2-(метокси)этилоксигруппу, 2-(трет-бутилоксикарбониламино)этилоксигруппу, 2-(амино)этилоксигруппу, 2-(ацетиламино)этилоксигруппу, 2-(этилкарбониламино)этилоксигруппу, 2-(пропилкарбониламино)этилоксигруппу, 2-(изобутилкарбониламино)этилоксигруппу, 2-(метоксиацетиламино)этилоксигруппу, 2-(этиламинокарбониламино)этилоксигруппу, 2-(диметиламинокарбониламино)этилоксигруппу, 2-(пирролидин-1-илкарбониламино)этилоксигруппу, 2-(пиперидин-1-илкарбониламино)этилоксигруппу, 2-(морфолин-4-илкарбониламино)этилоксигруппу, 2-(метилсульфониламино)этилоксигруппу, 2-(этилсульфониламино)этилоксигруппу, 2-(бутилсульфониламино)этилоксигруппу, 3-(трет-бутилоксикарбониламино)пропилоксигруппу, 3-(амино)пропилоксигруппу, 3-(ацетиламино)пропилоксигруппу или 3-(метилсульфониламино)пропилоксигруппу и
их таутомеры, их стереоизомеры, их смеси и их соли.
5. Бициклические гетероциклы общей формулы I по п.1, в которых
Ra обозначает атом водорода,
Rb обозначает 3-хлор-4-фторфенильную группу или 3-этинилфенильную группу,
Rc обозначает циклогексильную группу, которая в положении 3 замещена амино-, ацетиламино-, трет-бутилоксикарбониламино- или метилсульфониламиногруппой, циклогексильную группу, которая в положении 4 замещена амино-, метиламино-, диметиламино-, ацетиламино-, N-(ацетил)метиламино-, метоксиацетиламино-, N-(метоксиацетил)метиламино-, тетрагидропиран-4-илкарбониламино-, N-(тетрагидропиран-4-илкарбонил)метиламино-, трет-бутилоксикарбониламино-, N-(трет-бутилоксикарбонил)
метиламино-, N-(этиламинокарбонил)метиламино-, диметиламинокарбониламино-, N-(диметиламинокарбонил)метиламино-, N-(пиперидин-1-илкарбонил)метиламино-, морфолин-4-илкарбониламино-, N-(морфолин-4-илкарбонил)метиламино-, N-(4-метилпиперазин-1-илкарбонил)метиламино-, метилсульфониламино, N-(метилсульфонил)метиламино-, этилсульфониламино-, N-(этилсульфонил)метиламино-, диметиламиносульфониламино-, N-(диметиламиносульфонил)метиламино-, морфолин-4-илсульфониламино-, N-(морфолин-4-илсульфонил)метиламино-, 3-хлорпропилсульфониламино- или [3-(морфолин-4-ил)
пропил]сульфониламиногруппой, пирролидин-3-ильную группу, пирролидин-3-ильную группу, которая в положении 1 замещена трет-бутилоксикарбонильной или метилсульфонильной группой, пиперидин-3-ильную группу, пиперидин-3-ильную группу, которая в положении 1 замещена трет-бутилоксикарбонильной или метилсульфонильной группой, пиперидин-4-ильную группу, пиперидин-4-ильную группу, которая в положении 1 замещена метильной, (аминокарбонил)метильной, (диметиламинокарбонил)метильной, (морфолин-4-илкарбонил)метильной, 2-(трет-бутилоксикарбониламино)этильной, 2-аминоэтильной, 2-(ацетиламино)этильной, 2-(метилсульфониламино)этильной группой, цианогруппой, ацетильной, метоксиацетильной, (диметиламино)ацетильной, (морфолин-4-ил)ацетильной, тетрагидропиран-4-илкарбонильной, этиламинокарбонильной, изопропиламинокарбонильной, фениламинокарбонильной, диметиламинокарбонильной, диэтиламинокарбонильной, пирролидин-1-илкарбонильной, пиперидин-1-илкарбонильной, морфолин-4-илкарбонильной, 2-метилморфолин-4-илкарбонильной, 2,6-диметилморфолин-4-илкарбонильной, 4-метилпиперазин-1-илкарбонильной, изопропилоксикарбонильной, трет-бутилоксикарбонильной, метилсульфонильной, диметиламиносульфонильной или морфолин-4-илсульфонильной группой, тетрагидрофуран-3-ильную группу, тетрагидропиран-3-ильную группу или тетрагидропиран-4-ильную группу,
Rd обозначает атом водорода, метоксигруппу, этилоксигруппу, 2-(морфолин-4-ил)этилоксигруппу, 3-(морфолин-4-ил)пропилоксигруппу, 4-(морфолин-4-ил)бутилоксигруппу, 2-(3-метил-2-оксогексагидропиримидин-1-ил)этилоксигруппу, 2-(метокси)этилоксигруппу, 2-(трет-бутилоксикарбониламино)этилоксигруппу, 2-аминоэтилоксигруппу, 2-(ацетиламино)этилоксигруппу, 2-(метилсульфониламино)этилоксигруппу, 3-(трет-бутилоксикарбониламино)пропилоксигруппу, 3-аминопропилоксигруппу, 3-(ацетиламино)пропилоксигруппу или 3-(метилсульфониламино)пропилоксигруппу и
X обозначает атом азота,
их таутомеры, их стереоизомеры, их смеси и их соли.
6. Соединения общей формулы I по п.1 из группы, включающей:
(а) 4-[(3-хлор-4-фторфенил)амино]-6-((S)-тетрагидрофуран-3-илокси)-7-метоксихиназолин,
(б) 4-[(3-хлор-4-фторфенил)амино]-6-(тетрагидропиран-4-илокси)-7-метоксихиназолин,
(в) 4-[(3-хлор-4-фторфенил)амино]-6-((R)-тетрагидрофуран-3-илокси)-7-метоксихиназолин,
(г) 4-[(3-хлор-4-фторфенил)амино]-6-(транс-4-аминоциклогексан-1-илокси)-7-метоксихиназолин,
(д) 4-[(3-хлор-4-фторфенил)амино]-6-(транс-4-метансульфониламиноциклогексан-1-илокси)-7-метоксихиназолин,
(е) 4-[(3-хлор-4-фторфенил)амино]-6-(пиперидин-4-илокси)-7-метоксихиназолин,
(ж) 4-[(3-хлор-4-фторфенил)амино]-6-(1-метансульфонилпиперидин-4-илокси)-7-метоксихиназолин,
(з) 4-[(3-хлор-4-фторфенил)амино]-6-(цис-4-{[3-(морфолин-4-ил)пропил]сульфониламино}циклогексан-1-илокси)-7-метоксихиназолин,
(и) 4-[(3-хлор-4-фторфенил)амино]-6-(тетрагидропиран-3-илокси)-7-метоксихиназолин,
(ъ) 4-[(3-хлор-4-фторфенил)амино]-6-(транс-4-{[3-(морфолин-4-ил)пропил]сульфониламино}циклогексан-1-илокси)-7-метоксихиназолин,
(л) 4-[(3-хлор-4-фторфенил)амино]-6-(1-метилпиперидин-4-илокси)-7-метоксихиназолин,
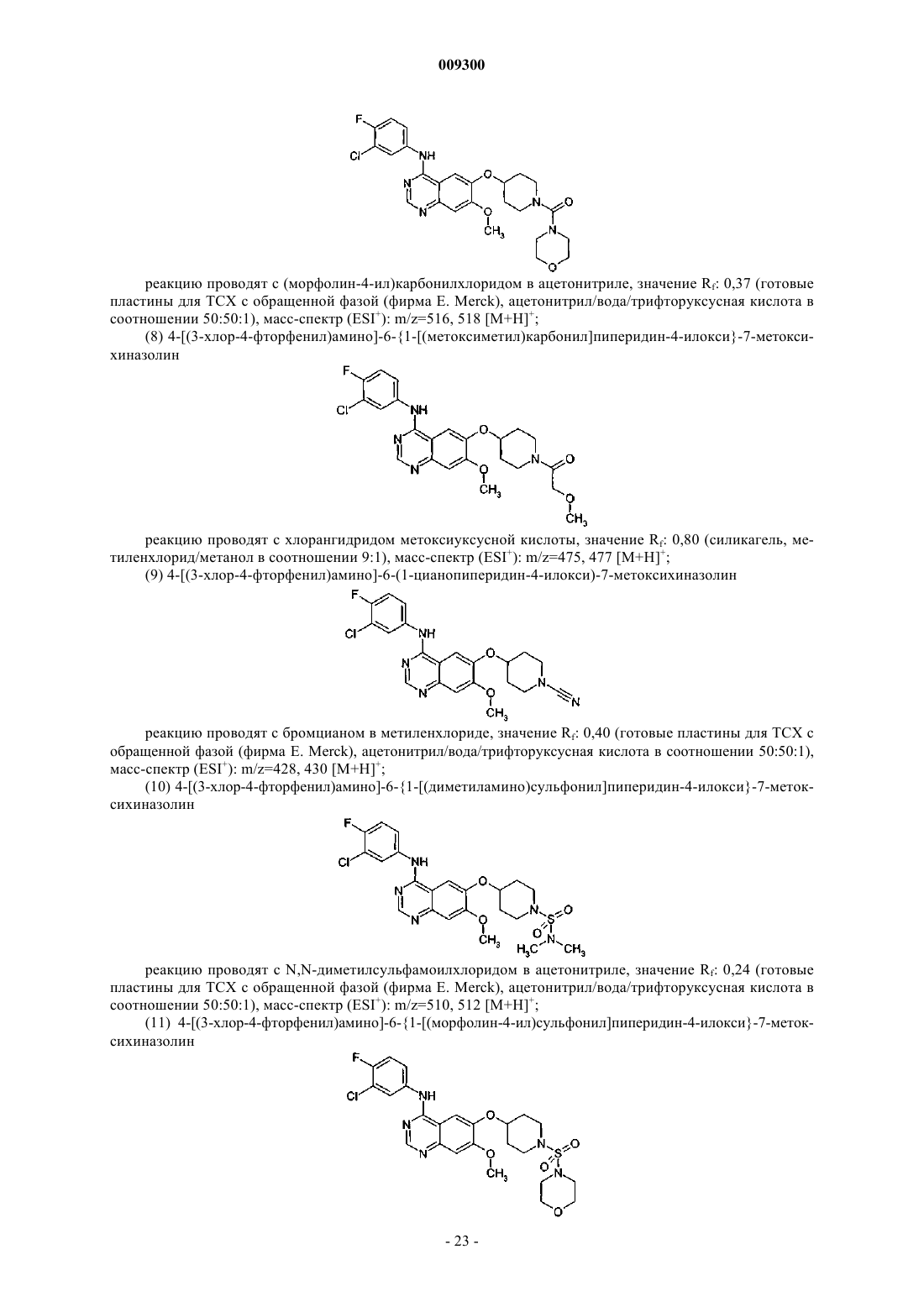
(м) 4-[(3-хлор-4-фторфенил)амино]-6-{1-[(морфолин-4-ил)карбонил]пиперидин-4-илокси}-7-метоксихиназолин,
(н) 4-[(3-хлор-4-фторфенил)амино]-6-{1-[(метоксиметил)карбонил]пиперидин-4-илокси}-7-метоксихиназолин,
(о) 4-[(3-хлор-4-фторфенил)амино]-6-(1-цианопиперидин-4-илокси)-7-метоксихиназолин,
(п) 4-[(3-хлор-4-фторфенил)амино]-6-{1-[(морфолин-4-ил)сульфонил]пиперидин-4-илокси}-7-метоксихиназолин,
(р) 4-[(3-хлор-4-фторфенил)амино]-6-[1-(2-ацетиламиноэтил)пиперидин-4-илокси]-7-метоксихиназолин,
(с) 4-[(3-хлор-4-фторфенил)амино]-6-{транс-4-[(диметиламино)сульфониламино]циклогексан-1-илокси}-7-метоксихиназолин,
(т) 4-[(3-хлор-4-фторфенил)амино]-6-{транс-4-[(морфолин-4-ил)карбониламино]циклогексан-1-илокси}-7-метоксихиназолин,
(у) 4-[(3-хлор-4-фторфенил)амино]-6-{транс-4-[(морфолин-4-ил)сульфониламино]циклогексан-1-илокси}-7-метоксихиназолин,
(ф) 4-[(3-хлор-4-фторфенил)амино]-6-(тетрагидропиран-4-илокси)-7-(2-ацетиламиноэтокси)хиназолин,
(х) 4-[(3-хлор-4-фторфенил)амино]-6-(тетрагидропиран-4-илокси)-7-(2-метансульфониламиноэтокси)хиназолин и
(ц) 4-[(3-хлор-4-фторфенил)амино]-6-(тетрагидропиран-4-илокси)-7-(2-метоксиэтокси)хиназолин,
а также их соли.
7. Физиологически совместимые соли соединений по одному из пп.1-6 с неорганическими или органическими кислотами или основаниями.
8. Способ получения соединений общей формулы I по одному из пп.1-6, отличающийся тем, что
а) соединение общей формулы
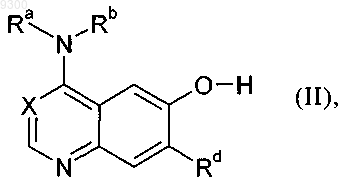
в которой
Ra, Rb, Rd и X имеют указанные в пп.1-6 значения,
подвергают взаимодействию с соединением общей формулы
![]()
в которой
Rc имеет указанные в пп.1-6 значения, a
Z1 обозначает уходящую группу, и
затем при необходимости полученное таким путем соединение общей формулы I, которое содержит амино-, алкиламино- или иминогруппу, переводят путем ацилирования, цианирования или сульфонилирования в соответствующее ацильное соединение, цианосоединение или сульфонильное соединение общей формулы I, и/или
полученное таким путем соединение общей формулы I, которое содержит амино-, алкиламино- или иминогруппу, переводят путем алкилирования или гидроалкилирования в соответствующее алкильное соединение общей формулы I, и/или
полученное таким путем соединение общей формулы I, которое содержит хлор-C1-4алкилсульфонильную или бром-С1-4алкилсульфонильную группу, переводят взаимодействием с амином в соответствующее амино-C1-4алкилсульфонильное соединение, и/или
полученное таким путем соединение общей формулы I, которое содержит трет-бутилоксикарбониламино-, N-алкил-N-(трет-бутилоксикарбонил)амино- или N-трет-бутилоксикарбонилиминогруппу, переводят обработкой кислотой в соответствующее амино-, алкиламино- или иминосоединение общей формулы I, и/или
при необходимости вновь отщепляют использовавшуюся при проведении указанных выше реакций защитную группу, и/или
при необходимости полученное таким путем соединение общей формулы I разделяют на его стереоизомеры, и/или
полученное таким путем соединение общей формулы I переводят в его соли, прежде всего в его пригодные для фармацевтического применения физиологически совместимые соли.
Текст
009300 Настоящее изобретение относится к бициклическим гетероциклам общей формулы их таутомерам, их стереоизомерам, их смесям и их солям, прежде всего их физиологически совместимым солям с неорганическими или органическими кислотами или основаниями, обладающим ценными фармакологическими свойствами, прежде всего ингибирующим действием на опосредуемую тирозинкиназами трансдукцию сигналов, к их применению для лечения различных заболеваний, прежде всего опухолевых заболеваний, а также доброкачественной гиперплазии простаты (ДГП), заболеваний легких и дыхательных путей, и к способу их получения. В приведенной выше общей формуле I заместители имеют следующие значения:Ra обозначает атом водорода или С 1-4 алкильную группу,Rb обозначает фенильную или 1-фенилэтильную группу, в каждой из которых фенильное ядро замещено остатками R1-R3, гдеR1 и R2 могут иметь идентичные или различные значения и обозначают атом водорода, фтора, хлора, брома или иода, С 1-4 алкильную группу, гидроксигруппу, С 1-4 алкоксигруппу, С 2-3 алкенильную группу,С 2-3 алкинильную группу, арильную группу, арилоксигруппу, арилметильную группу, арилметоксигруппу, гетероарильную группу, гетероарилоксигруппу, гетероарилметильную группу, гетероарилметоксигруппу, замещенную 1-3 атомами фтора метильную либо метоксигруппу или циано-, нитро- либо аминогруппу, иR3 обозначает атом водорода, фтора, хлора или брома, метильную или трифторметильную группу,Rc обозначает циклобутильную, циклопентильную или циклогексильную группу, каждая из которых замещена группой R4-N-R5, гдеR4 обозначает атом водорода или С 1-3 алкильную группу, аR5 обозначает атом водорода, С 1-3 алкильную группу, аминокарбонил-С 1-3 алкильную группу, С 1-3 алкиламинокарбонил-С 1-3 алкильную группу, ди(С 1-3 алкил)аминокарбонил-С 1-3 алкильную группу, пирролидин-1-илкарбонил-С 1-3 алкильную группу, пиперидин-1-илкарбонил-С 1-3 алкильную группу, гомопиперидин-1-илкарбонил-С 1-3 алкильную группу, морфолин-4-илкарбонил-С 1-3 алкильную группу, гомоморфолин-4-илкарбонил-С 1-3 алкильную группу, пиперазин-1-илкарбонил-С 1-3 алкильную группу, 4-С 1-3 алкилпиперазин-1-илкарбонил-С 1-3 алкильную группу, гомопиперазин-1-илкарбонил-С 1-3 алкильную группу, 4 С 1-3 алкилгомопиперазин-1-илкарбонил-С 1-3 алкильную группу, гидрокси-С 2-4 алкильную группу, С 1-3 алкилокси-С 2-4 алкильную группу, С 1-4 алкилоксикарбониламино-С 2-4 алкильную группу, амино-С 2-4 алкильную группу, С 1-3 алкиламино-С 2-4 алкильную группу, ди(С 1-3 алкил)амино-С 2-4 алкильную группу, С 1-3 алкилкарбониламино-С 2-4 алкильную группу, аминокарбониламино-С 2-4 алкильную группу, С 1-3 алкиламинокарбониламино-С 2-4 алкильную группу, ди(С 1-3 алкил)аминокарбониламино-С 2-4 алкильную группу, пирролидин-1-илкарбониламино-С 2-4 алкильную группу, пиперидин-1-илкарбониламино-С 2-4 алкильную группу,морфолин-4-илкарбониламино-С 2-4 алкильную группу, С 1-3 алкилсульфонил-С 2-4 алкильную группу, С 1-3 алкилсульфониламино-С 2-4 алкильную группу, (2-оксопирролидин-1-ил)-С 2-4 алкильную группу, (2-оксопиперидин-1-ил)-С 2-4 алкильную группу, (3-оксоморфолин-4-ил)-С 2-4 алкильную группу, (2-оксоимидазолидин-1-ил)-С 2-4 алкильную группу, (2-оксо-3-С 1-3 алкилимидазолидин-1-ил)-С 2-4 алкильную группу, (2-оксогексагидропиримидин-1-ил)-С 2-4 алкильную группу, (2-оксо-3-С 1-3 алкилгексагидропиримидин-1-ил)-С 2-4 алкильную группу, С 1-4 алкилсульфонильную группу, хлор-С 1-4 алкилсульфонильную группу, бром-С 1-4 алкилсульфонильную группу, амино-С 1-4 алкилсульфонильную группу, C1-3 алкиламино-С 1-4 алкилсульфонильную группу, ди(C1-3 алкил)амино-С 1-4 алкилсульфонильную группу, (пирролидин-1-ил)-С 1-4 алкилсульфонильную группу, (пиперидин-1-ил)-С 1-4 алкилсульфонильную группу, (гомопиперидин-1-ил)-С 1-4 алкилсульфонильную группу, (морфолин-4-ил)-C1-4 алкилсульфонильную группу, (гомоморфолин-4-ил)-C1-4 алкилсульфонильную группу, (пиперазин-1-ил)-C1-4 алкилсульфонильную группу, (4-C1-3 алкилпиперазин-1 ил)-С 1-4 алкилсульфонильную группу, (гомопиперазин-1-ил)-C1-4 алкилсульфонильную группу, (4-C1-3 алкилгомопиперазин-1-ил)-C1-4 алкилсульфонильную группу, С 1-4 алкилоксикарбонильную группу, формильную группу, С 1-4 алкилкарбонильную группу, C1-3 алкилокси-С 1-4 алкилкарбонильную группу, тетрагидрофуранилкарбонильную группу, тетрагидропиранилкарбонильную группу, амино-С 1-4 алкилкарбонильную группу, C1-3 алкиламино-C1-4 алкилкарбонильную группу, ди(C1-3 алкил)амино-С 1-4 алкилкарбонильную группу, пирролидин-1-ил-С 1-4 алкилкарбонильную группу, пиперидин-1-ил-C1-4 алкилкарбонильную группу,(гомопиперидин-1-ил)-C1-4 алкилкарбонильную группу, морфолин-4-ил-С 1-4 алкилкарбонильную группу,(гомоморфолин-4-ил)-С 1-4 алкилкарбонильную группу, (пиперазин-1-ил)-С 1-4 алкилкарбонильную группу,(4-C1-3 алкилпиперазин-1-ил)-С 1-4 алкилкарбонильную группу, (гомопиперазин-1-ил)-С 1-4 алкилкарбонильную группу, (4-C1-3 алкилгомопиперазин-1-ил)-C1-4 алкилкарбонильную группу, С 1-3 алкилсульфонил-С 1-4 алкилкарбонильную группу, цианогруппу, аминокарбонильную группу, C1-3 алкиламинокарбонильную группу,ди(C1-3 алкил)аминокарбонильную группу, (C1-3 алкилокси-С 2-4 алкил)аминокарбонильную группу, N-(C1-3 ал-1 009300 кил)-N-(C1-3 алкилокси-С 2-4 алкил)аминокарбонильную группу, ариламинокарбонильную группу, пирролидин-1-илкарбонильную группу, пиперидин-1-илкарбонильную группу, гомопиперидин-1-илкарбонильную группу, морфолин-4-илкарбонильную группу, гомоморфолин-4-илкарбонильную группу, 2-окса-5 азабицикло[2,2,1]гепт-5-илкарбонильную группу, 3-окса-8-азабицикло[3,2,1]окт-8-илкарбонильную группу,8-окса-3-азабицикло[3,2,1]окт-3-илкарбонильную группу, пиперазин-1-илкарбонильную группу, 4-C1-3 алкилпиперазин-1-илкарбонильную группу, гомопиперазин-1-илкарбонильную группу, 4-C1-3 алкилгомопиперазин-1-илкарбонильную группу, аминосульфонильную группу, C1-3 алкиламиносульфонильную группу, ди(C1-3 алкил)аминосульфонильную группу, пирролидин-1-илсульфонильную группу, пиперидин-1 илсульфонильную группу, гомопиперидин-1-илсульфонильную группу, морфолин-4-илсульфонильную группу, гомоморфолин-4-илсульфонильную группу, пиперазин-1-илсульфонильную группу, 4-C1-3 алкилпиперазин-1-илсульфонильную группу, гомопиперазин-1-илсульфонильную группу или 4-C1-3 алкилгомопиперазин-1-илсульфонильную группу, циклобутильную, циклопентильную или циклогексильную группу, каждая из которых замещена группой R6, гдеR6 обозначает 2-оксопирролидин-1-ильную группу, 2-оксопиперидин-1-ильную группу, 3-оксоморфолин-4-ильную группу, 2-оксоимидазолидин-1-ильную группу, 2-оксо-3-C1-3 алкилимидазолидин-1-ильную группу, 2-оксогексагидропиримидин-1-ильную группу или 2-оксо-3-C1-3 алкилгексагидропиримидин 1-ильную группу, азетидин-3-ильную группу, которая в положении 1 замещена остатком R5, где R5 имеет указанные выше значения, пирролидин-3-ильную группу, которая в положении 1 замещена остатком R5,где R5 имеет указанные выше значения, пиперидин-3-ильную группу, которая в положении 1 замещена остатком R5, где R5 имеет указанные выше значения, пиперидин-4-ильную группу, которая в положении 1 замещена остатком R5, где R5 имеет указанные выше значения, или тетрагидрофуран-3-ильную, тетрагидропиран-3-ильную либо тетрагидропиран-4-ильную группу,Rd обозначает атом водорода, фтора, хлора или брома, гидроксигруппу, C1-4 алкилоксигруппу, замещенную 1-3 атомами фтора метоксигруппу, замещенную 1-5 атомами фтора этилоксигруппу, С 2-4 алкилоксигруппу, которая замещена остатком R6 или R7, гдеR6 имеет указанные выше значения, а[3,2,1]окт-8-ильную группу, 8-окса-3-азабицикло[3,2,1]окт-3-ильную группу, пиперазин-1-ильную группу, 4C1-3 алкилпиперазин-1-ильную группу, гомопиперазин-1-ильную группу, C1-3 алкилгомопиперазин-1-ильную группу, формиламиногруппу, C1-4 алкилкарбониламиногруппу, C1-3 алкилокси-C1-3 алкилкарбониламиногруппу, С 1-4 алкилоксикарбониламиногруппу, аминокарбониламиногруппу, C1-3 алкиламинокарбониламиногруппу, ди(C1-3 алкил)аминокарбониламиногруппу, пирролидин-1-илкарбониламиногруппу, пиперидин-1-илкарбониламиногруппу, пиперазин-1-илкарбониламиногруппу, 4-C1-3 алкилпиперазин-1-илкарбониламиногруппу, морфолин-4-илкарбониламиногруппу или C1-4 алкилсульфониламиногруппу, С 3-7 циклоалкилоксигруппу, С 3-7 циклоалкил-С 1-4 алкилоксигруппу, тетрагидрофуран-3-илоксигруппу, тетрагидропиран-3-илоксигруппу, тетрагидропиран-4-илоксигруппу, тетрагидрофуранил-С 1-4 алкилоксигруппу, тетрагидропиранил-С 1-4 алкилоксигруппу, С 1-4 алкоксигруппу, которая замещена замещенной в положении 1 остатком R8 пирролидинильной, пиперидинильной или гомопиперидинильной группой, гдеR8 обозначает атом водорода, или C1-3 алкильную группу, или С 1-4 алкоксигруппу, которая замещена замещенной в положении 4 остатком R8 морфолинильной группой, где R8 имеет указанные выше значения, иX обозначает замещенную цианогруппой метиновую группу или атом азота, при этом под упомянутыми в определениях указанных выше остатков арильными группами в каждом случае подразумевается фенильная группа, которая одно- или двузамещена остатком R9, где в случае двукратного замещения заместители могут иметь идентичные или различные значения и гдеR9 обозначает атом водорода, фтора, хлора, брома или иода, C1-3 алкильную группу, гидроксигруппу, C1-3 алкилоксигруппу, дифторметильную группу, трифторметильную группу, дифторметоксигруппу,трифторметоксигруппу или цианогруппу, под упомянутыми в определениях указанных выше остатков гетероарильными группами подразумевается пиридильная, пиридазинильная, пиримидинильная или пиразинильная группа, причем указанные выше гетероарильные группы в каждом случае одно- или двузамещены остатком R9, где в случае двукратного замещения заместители могут иметь идентичные или различные значения и гдеR9 имеет указанные выше значения,каждая из указанных выше пирролидинильных, пиперидинильных, пиперазинильных и морфолинильных групп может быть замещена одной или двумя C1-3 алкильными группами и указанные выше алкильные группы, если не указано иное, могут иметь прямую или разветвленную цепь,за исключением 4-[(3-хлор-4-фторфенил)амино]-6-S)-тетрагидрофуран-3-илокси)-7-гидроксихиназолина. К предпочтительным соединениям приведенной выше общей формулы I относятся соединения, в которыхRa обозначает атом водорода,Rb обозначает замещенную остатками R1-R3 фенильную группу, гдеR1 обозначает атом водорода, фтора, хлора или брома, метильную группу, трифторметильную группу, этинильную группу, фенилоксигруппу либо фенилметоксигруппу, где фенильный фрагмент вышеуказанных групп необязательно замещен атомом фтора или хлора, или пиридилокси- либо пиридинилметоксигруппу, где пиридинильный фрагмент вышеуказанных групп необязательно замещен метильной или трифторметильной группой,R2 обозначает атом водорода, фтора или хлора или метильную группу иR4 обозначает атом водорода или C1-3 алкильную группу, аR6 обозначает 2-оксопирролидин-1-ильную группу, 2-оксопиперидин-1-ильную группу, 3-оксоморфолин-4-ильную группу, 2-оксоимидазолидин-1-ильную группу, 2-оксо-3-метилимидазолидин-1-ильную группу, 2-оксогексагидропиримидин-1-ильную группу или 2-оксо-3-метилгексагидропиримидин-1-ильную группу, циклогексильную группу, которая в положении 3 или в положении 4 замещена группой R4N-R5, где R4 и R5 имеют указанные выше значения, циклогексильную группу, которая в положении 3 или в положении 4 замещена группой R6, где R6 имеет указанные выше значения, пирролидин-3-ильную группу, которая в положении 1 замещена остатком R5, где R5 имеет указанные выше значения, пиперидин-3-ильную группу, которая в положении 1 замещена остатком R5, где R5 имеет указанные выше значения, пиперидин-4-ильную группу, которая в положении 1 замещена остатком R5, где R5 имеет указанные выше значения, или тетрагидрофуран-3-ильную, тетрагидропиран-3-ильную либо тетрагидропиран 4-ильную группу,Rd обозначает атом водорода, C1-3 алкилоксигруппу, метоксигруппу, замещенную 1-3 атомами фтора, этилоксигруппу, которая в положении 2 замещена остатком R6 или R7, гдеR6 имеет указанные выше значения, аR6 и R7 имеют указанные выше значения, или бутилоксигруппу, которая в положении 4 замещена остатком R6 или R7, где R6 и R7 имеют указанные выше значения, иX обозначает атом азота,при этом указанные выше алкильные группы, если не указано иное, могут иметь прямую или разветвленную цепь,их таутомеры, их стереоизомеры, их смеси и их соли. К более предпочтительным соединениям приведенной выше общей формулы I относятся соединения, в которыхR4 обозначает атом водорода, метильную группу или этильную группу, аR5 обозначает атом водорода, метильную группу, аминокарбонилметильную группу, метиламинокарбонилметильную группу, диметиламинокарбонилметильную группу, пирролидин-1-илкарбонилметильную группу, пиперидин-1-илкарбонилметильную группу, пиперазин-1-илкарбонилметильную группу, 4-метилпиперазин-1-илкарбонилметильную группу, морфолин-4-илкарбонилметильную группу, 2(морфолин-4-илкарбонил)этильную группу, 3-(морфолин-4-илкарбонил)пропильную группу, этильную группу, пропильную группу, 2-гидроксиэтильную группу, 3-гидроксипропильную группу, 2-метоксиэтильную группу, 3-метоксипропильную группу, 2-(бутилоксикарбониламино)этильную группу, 2-аминоэтильную группу, 3-аминопропильную группу, 2-(ацетиламино)этильную группу, 3-(ацетиламино)пропильную группу, 2-(этилкарбониламино)этильную группу, 3-(этилкарбониламино)пропильную группу,2-(пропилкарбониламино)этильную группу, 3-(пропилкарбониламино)пропильную группу, 2-(этиламинокарбониламино)этильную группу, 3-(этиламинокарбониламино)пропильную группу, 2-(диметиламинокарбониламино)этильную группу, 3-(диметиламинокарбониламино)пропильную группу, 2-(морфолин 4-илкарбониламино)этильную группу, 3-(морфолин-4-илкарбониламино)пропильную группу, 2-(метилсульфонил)этильную группу, 3-(метилсульфонил)пропильную группу, 2-(метилсульфониламино)этильную группу, 3-(метилсульфониламино)пропильную группу, 2-(2-оксопирролидин-1-ил)этильную группу,2-(2-оксопиперидин-1-ил)этильную группу, 2-(3-оксоморфолин-4-ил)этильную группу, 2-(2-оксоимидазолидин-1-ил)этильную группу, 2-(2-оксо-3-метилимидазолидин-1-ил)этильную группу, 2-(2-оксогексагидропиримидин-1-ил)этильную группу, 2-(2-оксо-3-метилгексагидропиримидин-1-ил)этильную группу,3-(2-оксопирролидин-1-ил)пропильную группу, 3-(2-оксопиперидин-1-ил)пропильную группу, 3-(3-оксоморфолин-4-ил)пропильную группу, 3-(2-оксоимидазолидин-1-ил)пропильную группу, 3-(2-оксо-3-метилимидазолидин-1-ил)пропильную группу, 3-(2-оксогексагидропиримидин-1-ил)пропильную группу, 3(2-оксо-3-метилгексагидропиримидин-1-ил)пропильную группу, метилсульфонильную группу, этилсульфонильную группу, 3-хлорпропилсульфонильную группу, 2-(морфолин-4-ил)этилсульфонильную группу, 3-(морфолин-4-ил)пропилсульфонильную группу, пропилоксикарбонильную группу, бутилоксикарбонильную группу, формильную группу, ацетильную группу, этилкарбонильную группу, пропилкарбонильную группу, метоксиацетильную группу, (2-метоксиэтил)карбонильную группу, (3-метоксипропил) карбонильную группу, тетрагидрофуран-2-илкарбонильную группу, тетрагидропиран-4-илкарбонильную группу, аминоацетильную группу, метиламиноацетильную группу, диметиламиноацетильную группу,морфолин-4-илацетильную группу, [2-(морфолин-4-ил)этил]карбонильную группу, [3-(морфолин-4-ил) пропил]карбонильную группу, метилсульфонилацетильную группу, цианогруппу, аминокарбонильную группу, метиламинокарбонильную группу, диметиламинокарбонильную группу, этиламинокарбонильную группу, диэтиламинокарбонильную группу, пропиламинокарбонильную группу, (2-метоксиэтил) аминокарбонильную группу, N-метил-N-(2-метоксиэтил)аминокарбонильную группу, (3-метоксипропил) аминокарбонильную группу, N-метил-N-(3-метоксипропил)аминокарбонильную группу, фениламино-4 009300 карбонильную группу, пирролидин-1-илкарбонильную группу, пиперидин-1-илкарбонильную группу,морфолин-4-илкарбонильную группу, 2-метилморфолин-4-илкарбонильную группу, 2,6-диметилморфолин-4-илкарбонильную группу, гомоморфолин-4-илкарбонильную группу, 2-окса-5-азабицикло[2,2,1] гепт-5-илкарбонильную группу, 3-окса-8-азабицикло[3,2,1]окт-8-илкарбонильную группу, 8-окса-3-азабицикло[3,2,1]окт-3-илкарбонильную группу, 4-метилпиперазин-1-илкарбонильную группу, аминосульфонильную группу, метиламиносульфонильную группу, диметиламиносульфонильную группу или морфолин-4-илсульфонильную группу, циклогексильную группу, которая в положении 3 или в положении 4 замещена группой R6, гдеR6 обозначает 2-оксопирролидин-1-ильную группу, 2-оксопиперидин-1-ильную группу, 3-оксоморфолин-4-ильную группу, 2-оксоимидазолидин-1-ильную группу, 2-оксо-3-метилимидазолидин-1-ильную группу, 2-оксогексагидропиримидин-1-ильную группу или 2-оксо-3-метилгексагидропиримидин-1-ильную группу, пирролидин-3-ильную группу, которая в положении 1 замещена остатком R5, где R5 имеет указанные выше значения, пиперидин-3-ильную группу, которая в положении 1 замещена остатком R5,где R5 имеет указанные выше значения, пиперидин-4-ильную группу, которая в положении 1 замещена остатком R5, где R5 имеет указанные выше значения, тетрагидрофуран-3-ильную группу, тетрагидропиран-3-ильную группу или тетрагидропиран-4-ильную группу,Rd обозначает атом водорода, метоксигруппу, дифторметоксигруппу, этилоксигруппу, этилоксигруппу, которая в положении 2 замещена остатком R6 или R7, гдеR6 имеет указанные выше значения, аR7 обозначает гидроксигруппу, метоксигруппу, этоксигруппу, аминогруппу, диметиламиногруппу,диэтиламиногруппу, бис(2-метоксиэтил)аминогруппу, пирролидин-1-ильную группу, пиперидин-1-ильную группу, морфолин-4-ильную группу, гомоморфолин-4-ильную группу, 2-окса-5-азабицикло[2,2,1] гепт-5-ильную группу, 3-окса-8-азабицикло[3,2,1]окт-8-ильную группу, 8-окса-3-азабицикло[3,2,1]окт-3 ильную группу, пиперазин-1-ильную группу, 4-метилпиперазин-1-ильную группу, 4-этилпиперазин-1 ильную группу, ацетиламиногруппу, этилкарбониламиногруппу, пропилкарбониламиногруппу, бутилкарбониламиногруппу, метоксиацетиламиногруппу, бутилоксикарбониламиногруппу, этиламинокарбониламиногруппу, диметиламинокарбониламиногруппу, пирролидин-1-илкарбониламиногруппу, пиперидин-1-илкарбониламиногруппу, морфолин-4-илкарбониламиногруппу, метилсульфониламиногруппу,этилсульфониламиногруппу или бутилсульфониламиногруппу, пропилоксигруппу, которая в положении 3 замещена остатком R6 или R7, где R6 и R7 имеют указанные выше значения, или бутилоксигруппу, которая в положении 4 замещена остатком R6 или R7, где R6 и R7 имеют указанные выше значения, иX обозначает атом азота,при этом указанные выше алкильные группы, если не указано иное, могут иметь прямую или разветвленную цепь,их таутомеры, их стереоизомеры, их смеси и их соли. К особо предпочтительным соединениям приведенной выше общей формулы I относятся соединения, в которыхX обозначает атом азота,их таутомеры, их стереоизомеры, их смеси и их соли. К наиболее предпочтительным соединениям общей формулы I относятся соединения, в которыхX обозначает атом азота,их таутомеры, их стереоизомеры, их смеси и их соли. Среди указанных выше бициклических гетероциклов общей формулы I, а также среди упомянутых выше как предпочтительные, более предпочтительные, особо предпочтительные и наиболее предпочтительные подгрупп соединений особо следует отметить те соединения, в которых(а) Rc обозначает замещенную в положении 4 циклогексильную группу,(б) Rc обозначает необязательно замещенную в положении 1 пирролидин-3-ильную группу,(в) Rc обозначает необязательно замещенную в положении 1 пиперидин-3-ильную группу,(г) Rc обозначает необязательно замещенную в положении 1 пиперидин-4-ильную группу,(д) Rc обозначает тетрагидрофуран-3-ильную группу,(е) Rc обозначает тетрагидропиран-3-ильную группу или(ж) Rc обозначает тетрагидропиран-4-ильную группу,a Ra, Rb, Rd и X в каждом случае имеют указанные выше значения. В качестве примера наиболее предпочтительных соединений общей формулы I можно назвать сле-7 009300 дующие:(22) 4-[(3-хлор-4-фторфенил)амино]-6-(тетрагидропиран-4-илокси)-7-(2-метоксиэтокси)хиназолин,а также их соли. Соединения общей формулы I можно получать, например, следующими методами. а) В этом варианте соединение общей формулы в которой Ra, Rb, Rd и X имеют указанные в начале описания значения, подвергают взаимодействию с соединением общей формулы в которой Rc имеет указанные в начале описания значения, a Z1 обозначает уходящую группу, такую как атом галогена, например атом хлора или брома, сульфонилоксигруппа, например метансульфонилоксиили n-толуолсульфонилоксигруппа, или гидроксигруппа. Взаимодействие с соединением общей формулы III, в которой Z1 обозначает гидроксигруппу, проводят в присутствии обезвоживающего агента, предпочтительно в присутствии фосфина и производного азодикарбоновой кислоты, например трифенилфосфина/диэтилового эфира азодикарбоновой кислоты,преимущественно в растворителе, например метиленхлориде, ацетонитриле, тетрагидрофуране, диоксане, толуоле или диэтиловом эфире этиленгликоля, при температуре от-50 до 150 С, предпочтительно,однако, при температуре от-20 до 80 С. б) В этом варианте для получения соединений общей формулы I, в которой Rd обозначает одну из указанных выше необязательно замещенных алкилоксигрупп, соединение общей формулы-8 009300 в которой Ra, Rb, Rc и X имеют указанные в начале описания значения, подвергают взаимодействию с соединением общей формулы в которой Rd' обозначает C1-4 алкильную группу, замещенную 1-3 атомами фтора метильную группу, замещенную 1-5 атомами фтора этильную группу, замещенную остатком R6 или R7 С 2-4 алкильную группу,где R6 и R7 имеют указанные в начале описания значения, C1-4 алкильную группу, которая замещена замещенной в положении 1 остатком R8 пирролидинильной, пиперидинильной или гомопиперидинильной группой, или C1-4 алкильную группу, которая замещена замещенной в положении 4 остатком R8 морфолинильной группой, гдеR8 в каждом случае имеет указанные в начале описания значения, a Z обозначает уходящую группу,например атом галогена, алкилсульфонилоксигруппу, арилсульфонилоксигруппу или гидроксигруппу. Если уходящая группа представляет собой атом галогена, например атом хлора, брома или иода,либо алкилсульфонилокси- или арилсульфонилоксигруппу, например метансульфонилокси- или n-толуолсульфонилоксигруппу, то реакцию предпочтительно проводят в присутствии органического или неорганического основания, например карбоната калия, гидрида натрия или N-этилдиизопропиламина. Если же уходящая группа представляет собой гидроксигруппу, то реакцию проводят в присутствии обезвоживающего агента, предпочтительно в присутствии фосфина и производного азодикарбоновой кислоты,например трифенилфосфина/диэтилового эфира азодикарбоновой кислоты. в) В этом варианте для получения соединений общей формулы I, в которой Rd обозначает одну из указанных в начале описания алкилоксигрупп, которая замещена необязательно замещенной амино-, алкиламино- или диалкиламиногруппой либо необязательно замещенной, присоединенной через атом азота иминогруппы гетероциклической группой, соединение общей формулы в которой Ra, Rb, Rc и X имеют указанные в начале описания значения, a Z3 обозначает уходящую группу,например атом галогена, в частности атом хлора или брома, или сульфонилоксигруппу, например метансульфонилокси- или n-толуолсульфонилоксигруппу, подвергают взаимодействию с аммиаком, соответствующим, необязательно замещенным алкиламином, диалкиламином или с иминосоединением либо их приемлемыми солями или производными, например морфолином. г) В этом варианте для получения соединений общей формулы I, в которой Rd обозначает гидроксигруппу, от соединения общей формулы в которой Ra, Rb, Rc и X имеют указанные в начале описания значения, a Rd обозначает переводимую в гидроксигруппу группу, например необязательно замещенную бензилоксигруппу, бензилетилсилилоксигруппу, ацетилоксигруппу, бензоилоксигруппу, метоксигруппу, этоксигруппу, трет-бутоксигруппу или тритилоксигруппу, отщепляют защитную группу. Защитную группу отщепляют, например, гидролитическим путем в водном растворителе, например в воде, изопропаноле/воде, уксусной кислоте/воде, тетрагидрофуране/воде или диоксане/воде, в присутствии кислоты, такой как трифторуксусная кислота, соляная кислота или серная кислота, или в присутствии основания щелочного металла, такого как гидроксид натрия или гидроксид калия, либо апротонным путем, например в присутствии иодтриметилсилана, при температуре от 0 до 120 С, предпочтительно при температуре от 10 до 100 С. Бензильную или метоксибензильную группу отщепляют, например, путем гидрогенолиза, в частности с использованием водорода в присутствии катализатора, такого как палладий на угле, в пригодном для этой цели растворителе, таком как метанол, этанол, этиловый эфир уксусной кислоты или ледяная уксусная кислота, необязательно с добавлением кислоты, такой как соляная кислота, при температуре от 0 до 100 С, предпочтительно, однако, при близких к комнатной температурах от 20 до 60 С, и при давлении водорода от 1 до 7 бар, предпочтительно от 3 до 5 бар. 2,4-Диметоксибензильную группу предпочтительно отщеплять, однако, в трифторуксусной кислоте в присутствии анизола. трет-Бутильную или бензильную группу отщепляют, например, обработкой кислотой, такой как трифторуксусная кислота, соляная кислота или бромисто-водородная кислота, или обработкой иодтриметилсиланом, необязательно с использованием растворителя, такого как метиленхлорид, диоксан, метанол или диэтиловый эфир.-9 009300 д) В этом варианте для получения соединений общей формулы I, в которой Rc обозначает группу-NH-, от соединения общей формулы в которой Ra, Rb, Rd и X имеют указанные в начале описания значения, a Rc' имеет указанные в начале описания для Rc значения, при условии, что Rc содержит защищенный атом азота, отщепляют защитную группу. В качестве примера обычных защитных групп для амино-, алкиламино- или иминогруппы можно назвать формильную группу, ацетильную группу, трифторацетильную группу, этоксикарбонильную группу, трет-бутоксикарбонильную группу, бензилоксикарбонильную группу, бензильную группу, метоксибензильную или 2,4-диметоксибензильную группу, а для аминогруппы дополнительно можно назвать фталильную группу. Защитную группу отщепляют, например, гидролитическим путем в водном растворителе, например в воде, изопропаноле/воде, уксусной кислоте/воде, тетрагидрофуране/воде или диоксане/воде, в присутствии кислоты, такой как трифторуксусная кислота, соляная кислота или серная кислота, или в присутствии основания щелочного металла, такого как гидроксид натрия или гидроксид калия, либо апротонным путем, например в присутствии иодтриметилсилана, при температуре от 0 до 120 С, предпочтительно при температуре от 10 до 100 С. Однако бензильную, метоксибензильную или бензилоксикарбонильную группу отщепляют, например, путем гидрогенолиза, в частности с использованием водорода в присутствии катализатора, такого как палладий на угле, в пригодном для этой цели растворителе, таком как метанол, этанол, этиловый эфир уксусной кислоты или ледяная уксусная кислота, необязательно с добавлением кислоты, такой как соляная кислота, при температуре от 0 до 100 С, предпочтительно, однако, при близких к комнатной температурах от 20 до 60 С, и при давлении водорода от 1 до 7 бар, но предпочтительно от 3 до 5 бар. 2,4-Диметоксибензильную группу предпочтительно отщеплять, однако, в трифторуксусной кислоте в присутствии анизола. трет-Бутильную или трет-бутилоксикарбонильную группу предпочтительно отщеплять обработкой кислотой, такой как трифторуксусная кислота или соляная кислота, или обработкой иодтриметилсиланом, необязательно с использованием растворителя, такого как метиленхлорид, диоксан, метанол или диэтиловый эфир. Трифторацетильную группу предпочтительно отщеплять обработкой кислотой, такой как соляная кислота, необязательно в присутствии растворителя, такого как уксусная кислота, при температуре от 50 до 120 С, либо обработкой едким натром, необязательно в присутствии растворителя, такого как тетрагидрофуран, при температуре от 0 до 50 С. Фталильную группу предпочтительно отщеплять в присутствии гидразина или первичного амина,такого как метиламин, этиламин или н-бутиламин, в растворителе, таком как метанол, этанол, изопропанол, толуол/вода или диоксан, при температуре от 20 до 50 С. е) В этом варианте для получения соединений общей формулы I, в которой Rc содержит замещенную необязательно замещенной амино-, алкиламино- или диалкиламиногруппой либо присоединенной через атом азота, необязательно замещенной гетероциклической группой алкильную группу, соединение общей формулы в которой Ra, Rb, Rd и X имеют указанные в начале описания значения, Z3 обозначает уходящую группу,например атом галогена, в частности атом хлора или брома, или сульфонилоксигруппу, например метансульфонилокси- или n-толуолсульфонилоксигруппу, a Rc при условии, что присоединенный к алифатическому атому углерода атом водорода заменен на группу Z3, имеет указанные в начале описания для Rc значения, подвергают взаимодействию с аммиаком, соответствующим, необязательно замещенным алкиламином, диалкиламином или с иминосоединением либо их приемлемыми солями или производными,например морфолином. При получении предлагаемым в изобретении способом соединения общей формулы I, которое содержит амино-, алкиламино- или иминогруппу, такое соединение можно путем ацилирования, цианирования или сульфонилирования перевести в соответствующее ацильное соединение, цианосоединение или сульфонильное соединение общей формулы I, используя в качестве агента ацилирования, например, изо- 10009300 цианаты, карбамоилхлориды, галогенангидриды карбоновых кислот, ангидриды карбоновых кислот и карбоновые кислоты совместно с активаторами, такими как N,N'-карбонилдиимидазол, N,N'-дициклогексилкарбодиимид или тетрафторборат O-(бензотриазол-1-ил)-N,N,N'N'-тетраметилурония, в качестве агента сульфонилирования - сульфонилгалогениды, а в качестве агента цианирования - хлор- или бромциан, и/или при получении соединения общей формулы I, которое содержит амино-, алкиламино- или иминогруппу, такое соединение можно путем алкилирования или гидроалкилирования перевести в соответствующее алкильное соединение общей формулы I, и/или при получении соединения общей формулыI, которое содержит хлор-C1-4 алкилсульфонильную группу или бром-C1-4 алкилсульфонильную группу,такое соединение можно взаимодействием с амином перевести в соответствующее амино-C1-4 алкилсульфонильное соединение, и/или при получении соединения общей формулы I, которое содержит третбутилоксикарбониламино-, N-алкил-N-(трет-бутилоксикарбонил)амино- или N-трет-бутилоксикарбонилиминогруппу, такое соединение можно обработкой кислотой, например соляной кислотой или трифторуксусной кислотой, перевести в соответствующее амино-, алкиламино- или иминосоединение общей формулы I. При проведении описанных выше реакций присутствующие при определенных условиях реакционноспособные группы, такие как гидрокси-, амино-, алкиламино- или иминогруппы, можно защищать на время протекания реакции обычными защитными группами и вновь отщеплять их по завершении реакции. В качестве примера защитной группы для гидроксигруппы можно назвать триметилсилильную,ацетильную, тритильную, бензильную или тетрагидропиранильную группу. В качестве примера защитной группы для амино-, алкиламино- или иминогруппы можно назвать формильную, ацетильную, трифторацетильную, этоксикарбонильную, трет-бутоксикарбонильную, бензилоксикарбонильную, бензильную, метоксибензильную или 2,4-диметоксибензильную группу. Использовавшуюся на время протекания реакции защитную группу в последующем при необходимости отщепляют, например, гидролитическим путем в водном растворителе, например в воде, изопропаноле/воде, уксусной кислоте/воде, тетрагидрофуране/воде или диоксане/воде, в присутствии кислоты,такой как трифторуксусная кислота, соляная кислота или серная кислота, или в присутствии основания щелочного металла, например гидроксида натрия или гидроксида калия, либо апротонным путем, например в присутствии иодтриметилсилана, при температуре от 0 до 120 С, предпочтительно при температуре от 10 до 100 С. Однако бензильную, метоксибензильную или бензилоксикарбонильную группу отщепляют, например, путем гидрогенолиза, в частности с использованием водорода в присутствии катализатора, такого как палладий на угле, в пригодном для этой цели растворителе, таком как метанол, этанол, этиловый эфир уксусной кислоты или ледяная уксусная кислота, необязательно с добавлением кислоты, такой как соляная кислота, при температуре от 0 до 100 С, предпочтительно, однако, при близких к комнатной температурах от 20 до 60 С и при давлении водорода от 1 до 7 бар, но предпочтительно от 3 до 5 бар. 2,4-Диметоксибензильную группу предпочтительно отщеплять, однако, в трифторуксусной кислоте в присутствии анизола. трет-Бутильную или трет-бутилоксикарбонильную группу предпочтительно отщеплять обработкой кислотой, такой как трифторуксусная кислота или соляная кислота, или обработкой иодтриметилсиланом, необязательно с использованием растворителя, такого как метиленхлорид, диоксан, метанол или диэтиловый эфир. Трифторацетильную группу предпочтительно отщеплять обработкой кислотой, такой как соляная кислота, необязательно в присутствии растворителя, такого как уксусная кислота, при температуре от 50 до 120 С, либо обработкой едким натром, необязательно в присутствии растворителя, такого как тетрагидрофуран или метанол, при температуре от 0 до 50C. Помимо этого полученные соединения общей формулы I можно разделять, как уже указывалось выше, на их энантиомеры и/или диастереомеры. Так, например, цис-/транс-смеси можно разделять на их отдельные цис- и транс-изомеры, а соединения по меньшей мере с 1 оптически активным атомом углерода можно разделять на их энантиомеры. Так, в частности, полученные цис-/транс-смеси можно разделять путем хроматографии на их отдельные цис- и транс-изомеры, полученные соединения общей формулы I, которые образуются в виде рацематов, можно разделять по известным методам (см. N.L. Allinger и E.L. Eliel, "Topics in Stereochemistry",изд-во Wiley Interscience, 1971, т. 6) на их оптические антиподы, а соединения общей формулы I по меньшей мере с 2 асимметрическими атомами углерода можно на основе различий их физико-химических свойств разделять по известным методам, например хроматографией и/или фракционной кристаллизацией, на их диастереомеры, которые при их образовании в рацемической форме в последующем можно разделять, как это описано выше, на энантиомеры. Разделение на энантиомеры предпочтительно осуществлять путем колоночного разделения на хиральных фазах либо путем перекристаллизации из оптически активного растворителя или взаимодействием с оптически активным веществом, которое с рацемическим соединением образует соли или производные, такие как сложные эфиры или амиды, прежде всего взаимодействием с кислотами и их активи- 11009300 рованными производными или спиртами, и разделением полученной в результате смеси диастереомерных солей или производных, например, на основе различий в их растворимости, при этом из чистых диастереомерных солей или производных можно высвобождать свободные антиподы воздействием пригодного для этой цели средства. В качестве примера наиболее часто используемых в вышеуказанных целях оптически активных кислот можно назвать D- и L-формы винной кислоты, дибензоилвинной кислоты,ди-о-толилвинной кислоты, яблочной кислоты, миндальной кислоты, камфорсульфоновой кислоты, глутаминовой кислоты, аспарагиновой кислоты или хинной кислоты. Примером оптически активного спирта служит (+)- или (-)-ментол, а в качестве примера оптически активного ацильного остатка в амидах можно назвать (+)- или (-)-ментилоксикарбонил. Полученные соединения формулы I можно, кроме того, переводить в их соли, прежде всего для фармацевтического применения в их физиологически совместимые соли, с неорганическими или органическими кислотами. В качестве примера пригодных для этой цели кислот можно назвать соляную кислоту, бромисто-водородную кислоту, серную кислоту, метансульфоновую кислоту, фосфорную кислоту,фумаровую кислоту, янтарную кислоту, молочную кислоту, лимонную кислоту, винную кислоту или малеиновую кислоту. Используемые в качестве исходных продуктов соединения общих формул II-IX частино известны из литературы, либо их можно получать по известным из литературы методам (см. примеры I-XXII) или по описанным выше методам, при необходимости с дополнительным введением защитных групп (см.,например, соединения формул IV, соответственно, VII и VIII). Предлагаемые в изобретении соединения общей формулы I и их физиологически совместимые соли обладают, как уже указывалось в начале описания, ценными фармакологическми свойствами, прежде всего ингибирующим действием на опосредуемую рецептором эпидермального фактора роста (EGF-R) трансдукцию сигналов, которая может быть вызвана, например, ингибированием связывания лигандов,димеризации рецепторов или самой тирозинкиназы. Помимо этого существует также возможность блокировать трансдукцию сигналов компонентам, расположенным на более глубоком уровне. Биологические свойства новых соединений исследовали по описанной ниже методике. Ингибирование человеческой EGF-рецепторной киназы определяли с помощью цитоплазматического домена тирозинкиназы (фрагмент от метионина в положении 664 до аланина в положении 1186 на основе последовательности, опубликованной в Nature 309, 1984, с. 418). С этой целью белок в виде слитого с GST (глутатион-S-трансфераза) белка экспрессировали в Sf9-клетках насекомых с использованием бакуловирусной системы экспрессии. Ферментативную активность определяли в присутствии или в отсутствие тестируемых соединений методом серийных разведений. В качестве субстрата использовали полимер pEY (4:1) фирмы SIGMA. В качестве меченого (индикаторного) субстрата добавляли биотинилированный полимер pEY (био-pEY). В каждых 100 мкл реакционного раствора содержалось 10 мкл ингибитора в 50%-ном ДМСО, 20 мкл раствора субстрата (200 мМ HEPES (N-2-гидроксиэтилпиперазин-N'-2-этансульфоновая кислота) с рН 7,4,50 мМ ацетат магния, 2,5 мг/мл полимера pEY, 5 мкг/мл био-pEY) и 20 мкл ферментативного препарата. Ферментативную реакцию инициировали добавлением 50 мкл 100-микромолярного раствора АТФ в 10 миллимолярном хлориде магния. Параметры процесса разведения ферментативного препарата подбирали с таким расчетом, чтобы встраивание фосфата в био-pEY происходило в линейной зависимости от времени и расхода фермента. Ферментативный препарат разводили в смеси из 20 мМ HEPES с рН 7,4, 1 мМ ЭДТК, 130 мМ поваренной соли, 0,05% тритона Х-100, 1 мМ дитиотреитола (ДТТ) и 10% глицерина. Опыты с ферментами проводили при комнатной температуре в течение 30 мин, прекращая реакцию добавлением 50 мкл стоп-раствора (250 мМ ЭДТК в 20 мМ HEPES с рН 7,4). Образец объемом 100 мкл переносили на покрытый стрептавидином титрационный микропланшет и инкубировали в течение 60 мин при комнатной температуре. После этого планшет промывали 200 мкл промывочного раствора (50 мМ трис, 0,05% твина 20). После добавления 100 мкл меченного пероксидазой хрена (HRPO) антитела к pPY(PY20H Anti-PTyr:HRP фирмы Transduction Laboratories, 250 нг/мл) инкубировали в течение 60 мин. После этого титрационный микропланшет трижды промывали промывочным раствором порциями по 200 мкл. Затем образцы смешивали с 100 мкл раствора ТМВ-пероксидазы (А:В=1:1, фирма Kirkegaard PerryLaboratories). Через 10 мин реакцию прекращали. Оптическую плотность ОП 450 нм измеряли с помощью планшет-ридера для ELISA-анализа. Все экспериментальные данные определяли в трех повторностях. Данные согласовывали путем итерационных вычислений с использованием программы анализа сигмоидальных кривых (программа Graph Pad Prism, версия 3.0) с переменным наклоном Хилла. Коэффициент корреляции у всех разрешенных данных, полученных итерацией, превышал 0,9, а верхние и нижние значения кривых проявляли расхождение с коэффициентом, равным по меньшей мере 5. На основе этих кривых определяли ту концентрацию действующего вещества, при которой активность EGF-рецепторной киназы ингибируется на 50% (IC50). При этом были получены следующие результаты. Из приведенных выше результатов следует, что предлагаемые в изобретении соединения общей формулы I ингибируют опосредуемую тирозинкиназами трансдукцию сигналов, как это проиллюстрировано на примере человеческого EGF-рецептора, и поэтому пригодны для лечения патофизиологических процессов, обусловленных гиперфункцией тирозинкиназ. В качестве примера подобных процессов можно назвать образование добро- и злокачественных опухолей, прежде всего опухолей эпителиального и нейроэпителиального происхождения, метастазирование, а также аномальную пролиферацию сосудистых эндотелиальных клеток (неоангиогенез). Предлагаемые в изобретении соединения пригодны также для профилактики и лечения заболеваний дыхательных путей и легких, связанных с избыточным или измененным слизеобразованием, обусловленным стимуляцией тирозинкиназ, например при воспалительных заболеваниях дыхательных путей,таких как хронический бронхит, хронический обструктивный бронхит, астма, бронхиэктазия, аллергический или неаллергический ринит или синусит, кистозном фиброзе, дефиците 1-антитрипсина или же при кашле, эмфиземе легких, фиброзе легких и повышенной реактивности дыхательных путей. Предлагаемые в изобретении соединения пригодны далее для лечения заболеваний желудочно-кишечного тракта, а также желчных протоков и желчного пузыря, связанных с нарушением активности тирозинкиназ, как это имеет место, например, при хронических воспалительных изменениях, таких как холецистит, болезнь Крона, язвенный колит и язвы в желудочно-кишечном тракте, или как это имеет место при заболеваниях желудочно-кишечного тракта, связанных с гиперсекрецией, таких как болезнь Менетрие, аденома секреторных желез и синдром потери белка. Соединения общей формулы I и их физиологически совместимые соли могут применяться, кроме того, для лечения иных заболеваний, обусловленных аберрантной функцией тирозинкиназ, таких, например, как эпидермальная гиперпролиферация (псориаз), доброкачественная гиперплазия простаты(ДГП), воспалительные процессы, заболевания иммунной системы, гиперпролиферация кроветворных клеток, а также для лечения полипов носа и т.д. Предлагаемые в изобретении соединения благодаря их биологическим свойствам могут применяться индивидуально или в сочетании с другими фармакологически активными соединениями, например,для терапевтического лечения опухолей при монотерапии либо в сочетании с другими противоопухолевыми лечебными средствами, например в сочетании с ингибиторами топоизомеразы (например, этопозидом), с антимитотическими средствами (например, винбластином), со взаимодействующими с нуклеиновыми кислотами соединениями (например, цис-платином, циклофосфамидом, адриамицином), с антагонистами гормонов (например, тамоксифеном), с ингибиторами метаболических процессов (например, 5FU и т.д.), с цитокинами (например, интерферонами), с антителами и т.д. Для лечения заболеваний дыха- 13009300 тельных путей эти соединения могут применяться индивидуально либо в сочетании с другими предназначенными для лечения дыхательных путей лекарственными средствами, такими, например, как вещества, обладающие отхаркивающим действием (в частности, амброксол, N-ацетилцистеин), бронхолитическим действием (в частности, тиотропий или ипратропий либо фенотерол, салметерол или салбутамол) и/или подавляющим воспалительный процесс действием (в частности, теофиллин или глюкокортикоиды). Для лечения заболеваний в области желудочно-кишечного тракта эти соединения также можно назначать индивидуально либо в сочетании с влияющими на перистальтику или секрецию веществами. В подобных сочетаниях действующие вещества можно вводить либо одновременно, либо последовательно. Предлагаемые в изобретении соединения индивидуально или в сочетании с другими действующими веществами можно вводить внутривенно, подкожно, внутримышечно, внутрибрюшинно, назально, путем ингаляции или чрескожно либо перорально, при этом для ингаляции пригодны, прежде всего, аэрозольные препараты. При фармацевтическом применении предлагаемые в изобретении соединения вводят, как правило,теплокровным позвоночным животным, прежде всего человеку, в дозах от 0,01 до 100 мг/кг веса тела,предпочтительно от 0,1 до 15 мг/кг. Для приготовления лекарственных препаратов такие соединения перерабатывают совместно с одним или несколькими обычными инертными носителями и/или разбавителями, например с кукурузным крахмалом, лактозой, тростниковым сахаром, микрокристаллической целлюлозой, стеаратом магния, поливинилпирролидоном, лимонной кислотой, винной кислотой, водой, водой/этанолом, водой/глицерином, водой/сорбитом, водой/полиэтиленгликолем, пропиленгликолем, стеариловым спиртом, карбоксиметилцеллюлозой или жиросодержащими веществами, такими как отвержденный жир, или их приемлемыми смесями, в обычные галеновы формы, такие как таблетки, драже,капсулы, порошки, суспензии, растворы, спреи или суппозитории. Ниже изобретение проиллюстрировано на примерах, не ограничивающих его объем. Получение исходных соединений Пример I. Гидрохлорид 4-[(3-хлор-4-фторфенил)амино]-6-(тетрагидропиран-4-илокси)-7-бензилоксихиназолина. Смесь из 10,84 г 4-хлор-6-(тетрагидропиран-4-илокси)-7-бензилоксихиназолина и 4,50 г 3-хлор-4 фторанилина в 300 мл изопропанола в течение 4 ч кипятят с обратным холодильником и затем оставляют стоять на ночь при комнатной температуре. Образовавшийся осадок отделяют вакуум-фильтрацией,промывают изопропанолом и смешивают с 150 мл метанола. Полученную суспензию перемешивают еще в течение получаса при комнатной температуре и затем подвергают вакуум-фильтрации. Осадок на фильтре несколько раз промывают метанолом и сушат. Выход: 9,07 г (60% от теории), значение Rf: 0,27 (силикагель, циклогексан/этилацетат в соотношении 1:1), масс-спектр (ESI-): m/z=478, 480 [М-Н]-. Аналогично примеру I получают следующие соединения:(2) гидрохлорид 4-[(3-хлор-4-фторфенил)амино]-6-(1-трифторацетилпиперидин-4-илокси)хиназолина: значение Rf: 0,17 (готовые пластины для ТСХ с обращенной фазой (фирма Е. Merck), ацетонитрил/вода/трифторуксусная кислота в соотношении 50:50:1), масс-спектр (ESI+): m/z=469, 471 [М+Н]+;(3) гидрохлорид 4-[(3-хлор-4-фторфенил)амино]-6-(1-трифторацетилпиперидин-4-илокси)-7-ацетоксихиназолина: значение Rf: 0,70 (силикагель, метиленхлорид/метанол/конц. водный раствор аммиака в соотношении 90:10:1), масс-спектр (ESI+): m/z=527, 529 [М+Н]+;(4) 4-[(3-этинилфенил)амино]-6-ацетокси-7-метоксихиназолин: значение Rf: 0,59 (силикагель, этилацетат), масс-спектр (ESI+): m/z=334 [M+H]+. Пример II. 4-Хлор-6-(тетрагидропиран-4-илокси)-7-бензилоксихиназолин. Указанное в заголовке соединение получают взаимодействием 6-(тетрагидропиран-4-илокси)-7 бензилокси-3 Н-хиназолин-4-она с тионилхлоридом в присутствии N,N-диметилформамида в ацетонитриле при кипячении с обратным холодильником. Значение Rf: 0,90 (силикагель, этилацетат/метанол в соотношении 9:1). Аналогично примеру II получают следующие соединения:(3) 4-хлор-6-(1-трифторацетилпиперидин-4-илокси)-7-ацетоксихиназолин. Пример III. 6-(Тетрагидропиран-4-илокси)-7-бензилокси-3H-хиназолин-4-он. Смесь из 15,08 г 2-амино-4-бензилокси-5-(тетрагидропиран-4-илокси)бензойной кислоты и 14,40 г формамидинацетата в 250 мл абсолютного этанола в течение ночи кипятят с обратным холодильником.- 14009300 Охлажденную реакционную смесь смешивают с 250 мл воды. Выпавший осадок отделяют вакуум-фильтрацией и сушат при 70C в сушильном шкафу. Выход: 10,00 г (65% от теории), значение Rf: 0,40 (готовые пластины для ТСХ с обращенной фазой(1) 6-S)-тетрагидрофуран-3-илокси)-7-бензилокси-3H-хиназолин-4-он: значение Rf: 0,60 (готовые пластины для ТСХ с обращенной фазой (фирма Е. Merck), ацетонитрил/вода/трифторуксусная кислота в соотношении 50:50:1), масс-спектр (ESI+): m/z=339 [М+Н]+;m/z=362 [М+Н]+. Пример IV. 2-Амино-4-бензилокси-5-(тетрагидропиран-4-илокси)бензойная кислота. 16,40 г 2-нитро-4-бензилокси-5-(тетрагидропиран-4-илокси)бензойной кислоты гидрируют в присутствии 1,64 г никеля Ренея в 800 мл метанола при 55C до поглощения расчетного количества водорода. После этого катализатор отфильтровывают и фильтрат концентрируют, что сопровождается выкристаллизовыванием целевого продукта. Выход: 15,08 г (100% от теории), значение Rf: 0,60 (готовые пластины для ТСХ с обращенной фазой(3) 2-амино-4-гидрокси-5-[1-(трет-бутилоксикарбонил)пиперидин-4-илокси]бензойная кислота: значение Rf: 0,23 (силикагель, метиленхлорид/метанол/уксусная кислота в соотношении 90:10:1). Пример V. 2-Нитро-4-бензилокси-5-(тетрагидропиран-4-илокси)бензойная кислота. Указанное в заголовке соединение получают омылением бензилового эфира 2-нитро-4-бензилокси 5-(тетрагидропиран-4-илокси)бензойной кислоты 1 н. едким натром в метаноле при комнатной температуре. Значение Rf: 0,20 (готовые пластины для ТСХ с обращенной фазой (фирма Е. Merck), ацетонитрил/вода/трифторуксусная кислота в соотношении 50:50:1), масс-спектр (ESI+): m/z=374 [М+Н]+. Пример VI. Бензиловый эфир 2-нитро-4-бензилокси-5-(тетрагидропиран-4-илокси)бензойной кислоты. К 38 мл тетрагидрофуран-4-ола в 228 мл N,N-диметилформамида при охлаждении на ледяной бане добавляют 42,60 г трет-бутанолята калия. Смесь в течение часа перемешивают при комнатной температуре, после чего добавляют 22,90 г 6-нитробензо[1,3]диоксол-5-карбоновой кислоты. По истечении 1,5 ч реакция по данным тонкослойной хроматографии завершается, и к смеси при охлаждении на ледяной бане по каплям добавляют 28,94 мл бензилбромида. Реакционную смесь перемешивают в течение ночи при комнатной температуре, смешивают с 100 мл 10%-ной лимонной кислоты и в течение последующего дня перемешивают при комнатной температуре. После этого реакционную смесь концентрируют в вакууме при 60C и ее объем добавлением смеси воды со льдом доводят до 800 мл. Водную фазу экстрагируют этилацетатом, после чего объединенные экстракты промывают водой и насыщенным раствором хлорида натрия, сушат над сульфатом магния и концентрируют. Остаток смешивают с диэтиловым эфиром, что сопровождается выкристаллизовыванием 2-нитро-4-бензилокси-5-(тетрагидропиран-4-илокси) бензойной кислоты в качестве побочного продукта. Эту кислоту отфильтровывают и фильтрат концентрируют. В качестве основного продукта остается бензиловый эфир 2-нитро-4-бензилокси-5-(тетрагидропиран-4-илокси)бензойной кислоты, который без дополнительной очистки омыляют до карбоновой кислоты (см. пример V). Аналогично примеру VI получают следующие соединения:(2) 2-нитро-4-гидрокси-5-[1-(трет-бутилоксикарбонил)пиперидин-4-илокси]бензойная кислота: без взаимодействия с бензилбромидом, значение Rf: 0,40 (силикагель, метиленхлорид/метанол/уксусная кислота в соотношении 90:10:1), масс-спектр (ESI-): m/z=381 [М-Н]-. Пример VII. 4-[(3-Хлор-4-фторфенил)амино]-6-1-[2-(трет-бутилоксикарбониламино)этил]пиперидин- 15009300 4-илокси-7-метоксихиназолин. Смесь из 410 мг дигидрохлорида 4-[(3-хлор-4-фторфенил)амино]-6-(пиперидин-4-илокси)-7-метоксихиназолина, 240 мг N-(трет-бутилоксикарбонил)-2-бромэтиламина и 360 мг карбоната калия в 5 млN,N-диметилформамида в течение ночи перемешивают при комнатной температуре. Далее вновь добавляют N-(трет-бутилоксикарбонил)-2-бромэтиламин порцией 80 мг и реакционную смесь перемешивают в течение последующих 4 ч при комнатной температуре. Для переработки реакционную смесь разбавляют водой и экстрагируют этилацетатом. Объединенные органические фазы промывают насыщенным раствором хлорида натрия, сушат над сульфатом магния и концентрируют. Остаток хроматографируют на силикагелевой колонке с использованием в качестве элюента смеси этилацетат/метанол (в соотношении,изменяющемся от 95:5 до 90:1). Выход: 370 мг (79% от теории), значение Rf: 0,33 (готовые пластины для ТСХ с обращенной фазой(1) 4-[(3-хлор-4-фторфенил)амино]-6-1-[2-(трет-бутилоксикарбониламино)этил]пиперидин-4-илоксихиназолин: значение Rf: 0,38 (готовые пластины для ТСХ с обращенной фазой (фирма Е. Merck), ацетонитрил/вода/трифторуксусная кислота в соотношении 50:50:1), масс-спектр (ESI+): m/z=516, 518 [M+H]+. Пример VIII. Дигидрохлорид 4-[(3-хлор-4-фторфенил)амино]-6-(пиперидин-4-илокси)-7-метоксихиназолина. Указанное в заголовке соединение получают обработкой 4-[(3-хлор-4-фторфенил)амино]-6-[1-(третбутилоксикарбонил)пиперидин-4-илокси]-7-метоксихиназолина концентрированной соляной кислотой в диоксане при комнатной температуре. Значение Rf: 0,53 (готовые пластины для ТСХ с обращенной фазой (фирма Е. Merck), ацетонитрил/вода/трифторуксусная кислота в соотношении 50:50:1), масс-спектр (ESI+): m/z=403, 405 [М+Н]+. Аналогично примеру VIII получают следующие соединения:(2) 6-(пиперидин-4-илокси)-7-гидрокси-3H-хиназолин-4-он: реакцию проводят с трифторуксусной кислотой в метиленхлориде, значение Rf: 0,60 (готовые пластины для ТСХ с обращенной фазой (фирма Е. Merck), ацетонитрил/вода/трифторуксусная кислота в соотношении 50:50:1), масс-спектр (ESI+): m/z=262 [М+Н]+. Пример IX. 4-[(3-Хлор-4-фторфенил)амино]-6-[1-(трет-бутилоксикарбонил)пиперидин-4-илокси]-7 метоксихиназолин. К смеси из 10,00 г 4-[(3-хлор-4-фторфенил)амино]-6-гидрокси-7-метоксихиназолина, 9,40 г 1-(третбутилоксикарбонил)-4-гидроксипиперидина и 12,40 г трифенилфосфина в 400 мл метиленхлорида при комнатной температуре по каплям добавляют раствор 7,80 мл диэтилового эфира азодикарбоновой кислоты в 100 мл метиленхлорида. Полученную суспензию перемешивают в течение 3 дней при комнатной температуре и затем подвергают вакуум-фильтрации. Фильтрат концентрируют и хроматографируют на силикагелевой колонке с использованием в качестве элюента смеси метиленхлорид/метанол (в соотношении, изменяющемся от 98:2 до 95:5). Полученный сырой продукт смешивают с диизопропиловым эфиром, в течение ночи перемешивают в нем, подвергают вакуум-фильтрации и сушат. Выход: 5,34 г (34% от теории), значение Rf: 0,46 (силикагель, этилацетат/метанол в соотношении 9:1), масс-спектр (ESI+): m/z=503, 505 [М+Н]+. Пример X. 4-[(3-Хлор-4-фторфенил)амино]-6-(тетрагидропиран-4-илокси)-7-(4-бромбутилокси)хиназолин. Смесь из 500 мг 4-[(3-хлор-4-фторфенил)амино]-6-(тетрагидропиран-4-илокси)-7-гидроксихиназолина, 165 мкл 1-бром-4-хлорпропана и 360 мг карбоната калия в 5 мл N,N-диметилформамида перемешивают в течение ночи при 80C. Для переработки реакционную смесь разбавляют водой и экстрагируют этилацетатом. Объединенные органические фазы промывают насыщенным раствором хлорида натрия, сушат над сульфатом магния и концентрируют. Сырой продукт без дополнительной очистки используют в последующей реакции. Выход: 650 мг (97% от теории). Аналогично примеру X получают следующие соединения:m/z=543, 545 [М+Н]+. Пример XI. 1-(2-Гидроксиэтил)-3-метилтетрагидропиримидин-2-он. Указанное в заголовке соединение получают расщеплением 1-(2-бензилоксиэтил)-3-метилтетрагидропиримидин-2-она путем гидрогенолиза в присутствии палладия на активированном угле в метаноле при комнатной температуре. Значение Rf: 0,23 (силикагель, этилацетат/метанол/конц. водный раствор аммиака в соотношении 90:10:1), масс-спектр (ESI+): m/z=159 [М+Н]+. Пример XII. 1-(2-Бензилоксиэтил )-3-метилтетрагидропиримидин-2-он. Указанное в заголовке соединение получают взаимодействием 1-(2-бензилоксиэтил)тетрагидропиримидин-2-она с метилиодидом в присутствии трет-бутанолята калия в N,N-диметилформамиде при комнатной температуре. Значение Rf: 0,62 (силикагель, этилацетат/метанол/конц. водный раствор аммиака в соотношении 90:10:1), масс-спектр (ESI+): m/z=249 [М+Н]+. Пример XIII. 1-(2-Бензилоксиэтил)тетрагидропиримидин-2-он. Указанное в заголовке соединение получают обработкой 1-(2-бензилоксиэтил)-3-(3-хлорпропил)мочевины трет-бутанолятом калия в N,N-диметилформамиде при комнатной температуре. Значение Rf: 0,42 (силикагель, этилацетат/метанол/конц. водный раствор аммиака в соотношении 90:10:1), масс-спектр (ESI+): m/z=235 [М+Н]+. Пример XIV. 1-(2-Бензилоксиэтил)-тетрагидропиримидин-2-он. Указанное в заголовке соединение получают взаимодействием 2-бензилоксиэтиламина с 3-хлорпропилизоцианатом в тетрагидрофуране. Значение Rf: 0,73 (силикагель, этилацетат/метанол/конц. водный раствор аммиака в соотношении 90:10:1), масс-спектр (ESI+): m/z=271, 273 [М+Н]+. Пример XV. 3-(трет-Бутилоксикарбониламино)циклогексанол. Указанное в заголовке соединение получают взаимодействием 3-аминоциклогексанола с ди-третбутиловым эфиром пироугольной кислоты в присутствии триэтиламина в смеси из диоксана/воды (в соотношении 2:1) при 50C. Значение Rf: 0,34 (силикагель, метиленхлорид/метанол/конц. водный раствор аммиака в соотношении 90:10:1), масс-спектр (ESI-): m/z=214 [М-Н]-. Аналогично примеру XV получают следующее соединение:m/z=230 [М+Н]+. Пример XVI. 6-(1-Трифторацетилпиперидин-4-илокси)-3H-хиназолин-4-он. Указанное в заголовке соединение получают взаимодействием 6-(пиперидин-4-илокси)-3H-хиназолин 4-она х 2 трифторуксусной кислоты с ангидридом трифторуксусной кислоты в присутствии триэтиламина в тетрагидрофуране. Значение Rf: 0,48 (силикагель, этилацетат/метанол в соотношении 9:1), масс-спектр (ESI+): m/z=342(1) 6-(1-трифторацетилпиперидин-4-илокси)-7-гидрокси-3H-хиназолин-4-он: реакцию проводят с метиловым эфиром трифторуксусной кислоты в присутствии основания Хюнига в метаноле, значение Rf: 0,80 (силикагель, метиленхлорид/метанол в соотношении 4:1), масс-спектр(ESI+): m/z=358 [М+Н]+. Пример XVII. 2-Нитро-5-[1-(трет-бутилоксикарбонил)пиперидин-4-илокси]бензойная кислота. К 25,14 г 1-(трет-бутилоксикарбонил)пиперидин-4-ола в 120 мл N,N-диметилформамида при охлаждении на ледяной бане порциями добавляют 21,00 г трет-бутанолята калия, поддерживая при этом температуру ниже 10C. Далее смесь перемешивают еще в течение 30 мин при охлаждении на ледяной бане,после чего добавляют 11,60 г 5-фтор-2-нитробензойной кислоты. По истечении последующих 3 ч реакционную смесь сливают в воду, значение рН с помощью концентрированной соляной кислоты устанавливают на 1 и экстрагируют этилацетатом. Объединенные органические фазы промывают разбавленным раствором лимонной кислоты, сушат над сульфатом магния и концентрируют. Остаток растирают с диэтиловым эфиром, подвергают вакуум-фильтрации и сушат. Из фильтрата при его длительном стоянии кристаллизуется дополнительное количество продукта, который также отделяют вакуум-фильтрацией и сушат. Выход: 9,58 г (42% от теории), значение Rf: 0,43 (силикагель, метиленхлорид/метанол/уксусная кислота в соотношении 90:10:1), масс-спектр (ESI+): m/z=367[М+Н]+. Пример XVIII. 4-[(3-Хлор-4-фторфенил)амино]-6-(1-бромацетилпиперидин-4-илокси)хиназолин и 4-[(3-хлор-4-фторфенил)амино]-6-(1-хлорацетилпиперидин-4-илокси)хиназолин. Указанные в заголовке соединения получают взаимодействием 4-[(3-хлор-4-фторфенил)амино]-6- 17009300(пиперидин-4-илокси)хиназолина с хлорангидридом бромуксусной кислоты в присутствии основания Хюнига в тетрагидрофуране при комнатной температуре. В результате образуется смесь из бром- и хлорзамещенного соединений. Значение Rf: 0,43 (силикагель, метиленхлорид/метанол в соотношении 9:1), масс-спектр (ESI+):(1) 4-[(3-хлор-4-фторфенил)амино]-6-(1-хлорацетилпиперидин-4-илокси)-7-метоксихиназолин: реакцию проводят с хлорацетилхлоридом, значение Rf: 0,59 (силикагель, этилацетат/метанол/конц. водный раствор аммиака в соотношении 90:10:1), масс-спектр (ESI-): m/z=477, 479, 481 [М-Н]-. Пример XIX. 1-Метил-3-[([1,4]оксазепан-4-ил)карбонил]-3H-имидазол-1-ийиодид. Указанное в заголовке соединение получают взаимодействием 3-[([1,4]оксазепан-4-ил)карбонил]3H-имидазола с метилиодидом в ацетонитриле при комнатной температуре. Сырой продукт без дополнительной очистки используют в последующей реакции. Аналогично примеру XIX получают следующие соединения:(1) 1-метил-3-[(цис-2,6-диметилморфолин-4-ил)карбонил]-3H-имидазол-1-ийиодид: значение Rf: 0,12 (силикагель, этилацетат/метанол/конц. водный раствор аммиака в соотношении 90:10:1);(2) 1-метил-3-[(2-метилморфолин-4-ил)карбонил]-3H-имидазол-1-ийиодид: значение Rf: 0,02 (силикагель, этилацетат/метанол/конц. водный раствор аммиака в соотношении 90:10:1). Пример XX. 3-[([1,4]Оксазепан-4-ил)карбонил]-3H-имидазол. Указанное в заголовке соединение получают взаимодействием [1,4]оксазепана с N,N'-карбонилдиимидазолом в присутствии триэтиламина в тетрагидрофуране при комнатной температуре. Значение Rf: 0,30 (силикагель, этилацетат/метанол/конц. водный раствор аммиака в соотношении 90:10:1), масс-спектр (ESI+): m/z=196 [М+Н]+. Аналогично примеру XX получают следующие соединения:(1) 3-[(цис-2,6-диметилморфолин-4-ил)карбонил]-3H-имидазол: значение Rf: 0,46 (силикагель, этилацетат/метанол/конц. водный раствор аммиака в соотношении 90:10:1);(2) 3-[(2-метилморфолин-4-ил)карбонил]-3H-имидазол: значение Rf: 0,43 (силикагель, этилацетат/метанол/конц. водный раствор аммиака в соотношении 90:10:1). Пример XXI. 4-[(3-хлор-4-фторфенил)амино]-6-(1-трифторацетилпиперидин-4-илокси)-7-гидроксихиназолин. Указанное в заголовке соединение получают обработкой гидрохлорида 4-[(3-хлор-4-фторфенил) амино]-6-(1-трифторацетилпиперидин-4-илокси)-7-ацетоксихиназолина насыщенным раствором гидрокарбоната натрия в метаноле при комнатной температуре. Наряду с целевым продуктом в качестве побочного продукта в небольшом количестве выделяют также 4-[(3-хлор-4-фторфенил)амино]-6-(пиперидин-4-илокси)-7-гидроксихиназолин. Значение Rf: 0,20 (силикагель, метиленхлорид/метанол=20:1), масс-спектр (ESI-): m/z=483, 485 [М-Н]-. Аналогично примеру XXI получают следующее соединение:(1) 4-[(3-этинилфенил)амино]-6-гидрокси-7-метоксихиназолин: реакцию проводят с 40%-ным едким натром в этаноле, значение Rf: 0,32 (силикагель, этилацетат),масс-спектр (ESI+): m/z=292 [М+Н]+. Пример XXII. 6-(1-Трифторацетилпиперидин-4-илокси)-7-ацетокси-3H-хиназолин-4-он. Указанное в заголовке соединение получают взаимодействием 6-(1-трифторацетилпиперидин-4 илокси)-7-гидрокси-3H-хиназолин-4-она с уксусным ангидридом в пиридине при 80C. Значение Rf: 0,60 (силикагель, метиленхлорид/метанол в соотношении 9:1), масс-спектр (ESI+):m/z=400 [М+Н]+. Получение конечных соединений Пример 1. 4-[(3-Хлор-4-фторфенил)амино]-6-S)-тетрагидрофуран-3-илокси)-7-метоксихиназолин. 300 мг 4-[(3-хлор-4-фторфенил)амино]-6-гидрокси-7-метоксихиназолина в 6 мл ацетонитрила смешивают с 114 мкл (R)-3-гидрокситетрагидрофурана и 370 мг трифенилфосфина. Далее добавляют 234 мкл- 18009300 диэтилового эфира азодикарбоновой кислоты и реакционную смесь перемешивают в течение ночи при комнатной температуре. Для переработки реакционную смесь фильтруют и фильтрат концентрируют в вакууме. Сырой продукт очищают хроматографией на силикагелевой колонке с использованием в качестве элюента смеси этилацетат/метанол (в соотношении 95:5). Выход: 53 мг (15% от теории), температура плавления: 178C, масс-спектр (ESI+): m/z=390, 392(8) 4-[(3-хлор-4-фторфенил)амино]-6-[(S)-1-(трет-бутилоксикарбонил)пирролидин-3-илокси]-7-метоксихиназолин: реакцию проводят с диизопропиловым эфиром азодикарбоновой кислоты в метиленхлориде, значение Rf: 0,51 (силикагель, метиленхлорид/метанол в соотношении 9:1), масс-спектр (ESI+): m/z=489, 491(9) 4-[(3-хлор-4-фторфенил)амино]-6-[1-(трет-бутилоксикарбонил)пиперидин-3-илокси]-7-метоксихиназолин: реакцию проводят с диизопропиловым эфиром азодикарбоновой кислоты в метиленхлориде, значение Rf: 0,56 (силикагель, метиленхлорид/метанол в соотношении 9:1), масс-спектр (ESI-): m/z=501, 503(10) 4-[(3-хлор-4-фторфенил)амино]-6-S)-тетрагидрофуран-3-илокси)-7-[2-(3-метил-2-оксогексагидропиримидин-1-ил)этокси]хиназолин: реакцию проводят с диизопропиловым эфиром азодикарбоновой кислоты в метиленхлориде, температура плавления: 235C, масс-спектр (ESI+): m/z=516, 518 [М+Н]+;(11) 4-[(3-хлор-4-фторфенил)амино]-6-[3-(трет-бутилоксикарбониламино)циклогексан-1-илокси]-7 метоксихиназолин: реакцию проводят с диизопропиловым эфиром азодикарбоновой кислоты в метиленхлориде, значение(12) 4-[(3-хлор-4-фторфенил)амино]-6-цис-4-[N-(трет-бутилоксикарбонил)-N-метиламино]циклогексан-1-илокси-7-метоксихиназолин: реакцию проводят с диизопропиловым эфиром азодикарбоновой кислоты в метиленхлориде, значение(13) 4-[(3-хлор-4-фторфенил)амино]-6-транс-4-[N-(трет-бутилоксикарбонил)-N-метиламино]циклогексан-1-илокси-7-метоксихиназолин: реакцию проводят с диизопропиловым эфиром азодикарбоновой кислоты в метиленхлориде, температура плавления: 231C, масс-спектр (ESI+): m/z=531, 533 [М+Н]+. Указанное в заголовке соединение получают обработкой 4-[(3-хлор-4-фторфенил)амино]-6-[цис-4(трет-бутилоксикарбониламино)циклогексан-1-илокси]-7-метоксихиназолина трифторуксусной кислотой в метиленхлориде при комнатной температуре. Температура плавления: 221C, масс-спектр (ESI+): m/z=417, 419 [М+Н]+. Аналогично примеру 2 получают следующие соединения: Указанное в заголовке соединение получают взаимодействием 4-[(3-хлор-4-фторфенил)амино]-6-(цис 4-аминоциклогексан-1-илокси)-7-метоксихиназолина х трифторуксусной кислоты с хлорангидридом метансульфоновой кислоты в присутствии основания Хюнига в тетрагидрофуране при комнатной температуре. Значение Rf: 0,77 (силикагель, этилацетат/метанол/конц. водный раствор аммиака в соотношении 40:10:1), масс-спектр (ESI+): m/z=495, 497 [М+Н]+. Аналогично примеру 3 получают следующие соединения: значение Rf: 0,59 (силикагель, этилацетат/метанол/конц. водный раствор аммиака в соотношении 90:10:1), масс-спектр (ESI+): m/z=481, 483 [М+Н]+; реакцию проводят с N,N-диметилкарбамоилхлоридом, значение Rf: 0,28 (готовые пластины для ТСХ с обращенной фазой (фирма Е. Merck), ацетонитрил/вода/трифторуксусная кислота в соотношении 50:50:1), масс-спектр (ESI+): m/z=474, 476 [М+Н]+; реакцию проводят с (морфолин-4-ил)карбонилхлоридом в ацетонитриле, значение Rf: 0,37 (готовые пластины для ТСХ с обращенной фазой (фирма Е. Merck), ацетонитрил/вода/трифторуксусная кислота в соотношении 50:50:1), масс-спектр (ESI+): m/z=516, 518 [М+Н]+; реакцию проводят с бромцианом в метиленхлориде, значение Rf: 0,40 (готовые пластины для ТСХ с обращенной фазой (фирма Е. Merck), ацетонитрил/вода/трифторуксусная кислота в соотношении 50:50:1),масс-спектр (ESI+): m/z=428, 430 [М+Н]+; реакцию проводят с N,N-диметилсульфамоилхлоридом в ацетонитриле, значение Rf: 0,24 (готовые пластины для ТСХ с обращенной фазой (фирма Е. Merck), ацетонитрил/вода/трифторуксусная кислота в соотношении 50:50:1), масс-спектр (ESI+): m/z=510, 512 [М+Н]+;- 23009300 реакцию проводят с (морфолин-4-ил)сульфонилхлоридом в ацетонитриле, значение Rf: 0,29 (готовые пластины для ТСХ с обращенной фазой (фирма Е. Merck), ацетонитрил/вода/трифторуксусная кислота в соотношении 50:50:1), масс-спектр (ESI+): m/z=552, 554 [М+Н]+;(12) 4-[(3-хлор-4-фторфенил)амино]-6-(1-метансульфонилпиперидин-3-илокси)-7-метоксихиназолин: значение Rf: 0,33 (готовые пластины для ТСХ с обращенной фазой (фирма Е. Merck), ацетонитрил/вода/трифторуксусная кислота в соотношении 50:50:1), масс-спектр (ESI+): m/z=481, 483 [М+Н]+;(14) 4-[(3-хлор-4-фторфенил)амино]-6-[1-(2-метансульфониламиноэтил)пиперидин-4-илокси]-7-метоксихиназолин: значение Rf: 0,49 (готовые пластины для ТСХ с обращенной фазой (фирма Е. Merck), ацетонитрил/вода/трифторуксусная кислота в соотношении 50:50:1), масс-спектр (ESI+): m/z=524, 526 [М+Н]+;(15) 4-[(3-хлор-4-фторфенил)амино]-6-[1-(2-ацетиламиноэтил)пиперидин-4-илокси]-7-метоксихиназолин: реакцию проводят с уксусным ангидридом, значение Rf: 0,51 (готовые пластины для ТСХ с обращенной фазой (фирма Е. Merck), ацетонитрил/вода/трифторуксусная кислота в соотношении 50:50:1),масс-спектр (ESI+): m/z=488, 490 [М+Н]+;(16) 4-[(3-хлор-4-фторфенил)амино]-6-транс-4-[(диметиламино)сульфониламино]циклогексан-1 илокси-7-метоксихиназолин: реакцию проводят с N,N-диметилсульфамоилхлоридом в ацетонитриле, значение Rf: 0,69 (силикагель, этилацетат/метанол/конц. водный раствор аммиака в соотношении 90:10:1), масс-спектр (ESI+): m/z=524, 526 [М+Н]+;(22) 4-[(3-хлор-4-фторфенил)амино]-6-(цис-3-ацетиламиноциклогексан-1-илокси)-7-метоксихиназолин: реакцию проводят с ацетилхлоридом в ацетонитриле, цис- и транс-изомеры разделяют хроматографией на силикагелевой колонке, значение Rf: 0,43 (силикагель, метиленхлорид/метанол/конц. водный раствор аммиака в соотношении 90:10:1), масс-спектр (ESI+): m/z=459, 461 [М+Н]+;(23) 4-[(3-хлор-4-фторфенил)амино]-6-(транс-3-ацетиламиноциклогексан-1-илокси)-7-метоксихиназолин: реакцию проводят с ацетилхлоридом в ацетонитриле, цис- и транс-изомеры разделяют хроматографией на силикагелевой колонке, значение Rf: 0,49 (силикагель, метиленхлорид/метанол/конц. водный раствор аммиака в соотношении 90:10:1), масс-спектр (ESI+): m/z=459, 461 [М+Н]+;(34) 4-[(3-хлор-4-фторфенил)амино]-6-(1-изопропилоксикарбонилпиперидин-4-илокси)-7-метоксихиназолин: реакцию проводят с изопропиловым эфиром хлормуравьиной кислоты, значение Rf: 0,67 (силикагель, этилацетат/метанол/конц. водный раствор аммиака в соотношении 98:2:1), масс-спектр (ESI+):(39) 4-[(3-хлор-4-фторфенил)амино]-6-1-[(диэтиламино)карбонил]пиперидин-4-илокси-7-метоксихиназолин: реакцию проводят с N,N-диэтилкарбамоилхлоридом, значение Rf: 0,40 (силикагель, этилацетат/метанол/конц. водный раствор аммиака в соотношении 95:5:1), масс-спектр (ESI+): m/z=502, 504 [М+Н]+;(40) 4-[(3-хлор-4-фторфенил)амино]-6-1-[(пиперидин-1-ил)карбонил]пиперидин-4-илокси-7-метоксихиназолин: реакцию проводят с (пиперидин-1-ил)карбонилхлоридом, значение Rf: 0,51 (силикагель, этилацетат/метанол/конц. водный раствор аммиака в соотношении 95:5:1), масс-спектр (ESI-): m/z=512, 514 [М-Н]-;(силикагель, метиленхлорид/метанол/конц. водный раствор аммиака в соотношении 90:10:1), массспектр (ESI-): m/z=527, 529 [N-Н]-;(48) 4-[(3-хлор-4-фторфенил)амино]-6-(цис-4-N-[(морфолин-4-ил)сульфонил]-N-метиламиноциклогексан-1-илокси)-7-метоксихиназолин: реакцию проводят с (морфолин-4-ил)сульфонилхлоридом в ацетонитриле, значение Rf: 0,24 (готовые пластины для ТСХ с обращенной фазой (фирма Е. Merck), ацетонитрил/вода/трифторуксусная кислота в соотношении 50:50:1), масс-спектр (ESI+): m/z=580, 582 [М+Н]+;(50) 4-[(3-хлор-4-фторфенил)амино]-6-(транс-4-этансульфониламиноциклогексан-1-илокси)-7-метоксихиназолин: реакцию проводят с хлорангидридом этансульфоновой кислоты в метиленхлориде, значение Rf: 0,41 (силикагель, этилацетат), масс-спектр (ESI+): m/z=509, 511 [М+Н]+;(61) 4-[(3-хлор-4-фторфенил)амино]-6-[цис-4-(N-этансульфонил-N-метиламино)циклогексан-1-илокси]7-метоксихиназолин: реакцию проводят с хлорангидридом этансульфоновой кислоты в метиленхлориде, значение Rf: 0,19 (готовые пластины для ТСХ с обращенной фазой (фирма Е. Merck), ацетонитрил/вода/трифторуксусная кислота в соотношении 50:50:1), масс-спектр (ESI+): m/z=523, 525 [М+Н]+;(62) 4-[(3-хлор-4-фторфенил)амино]-6-цис-4-[(морфолин-4-ил)карбониламино]циклогексан-1-илокси 7-метоксихиназолин: реакцию проводят с (морфолин-4-ил)карбонилхлоридом, значение Rf: 0,33 (готовые пластины для ТСХ с обращенной фазой (фирма Е. Merck), ацетонитрил/вода/трифторуксусная кислота в соотношении 50:50:1), масс-спектр (ESI+): m/z=530, 532 [М+Н]+;(64) 4-[(3-этинилфенил)амино]-6-(1-ацетилпиперидин-4-илокси)-7-метоксихиназолин: реакцию проводят с уксусным ангидридом, значение Rf: 0,30 (силикагель, этилацетат/метанол/конц. водный раствор аммиака в соотношении 90:10:1), масс-спектр (ESI+): m/z=417 [М+Н]+;(65) 4-[(3-этинилфенил)амино]-6-[1-(2-метоксиацетил)пиперидин-4-илокси]-7-метоксихиназолин: реакцию проводят с хлорангидридом метоксиуксусной кислоты, значение Rf: 0,37 (силикагель, метиленхлорид/метанол/конц. водный раствор аммиака в соотношении 90:10:1), масс-спектр (ESI+): m/z=447 [М+Н]+;(66) 4-[(3-этинилфенил)амино]-6-(1-метансульфонилпиперидин-4-илокси)-7-метоксихиназолин: значение Rf: 0,59 (силикагель, этилацетат/метанол/конц. водный раствор аммиака в соотношении 90:10:1), масс-спектр (ESI+): m/z=453 [М+Н]+;(67) 4-[(3-этинилфенил)амино]-6-1-[(морфолин-4-ил)карбонил]пиперидин-4-илокси-7-метоксихиназолин: реакцию проводят с (морфолин-4-ил)карбонилхлоридом, значение Rf: 0,43 (силикагель, этилацетат/метанол/конц. водный раствор аммиака в соотношении 90:10:1), масс-спектр (ESI+): m/z=488 [М+Н]+;. К 60 мг 4-[(3-хлор-4-фторфенил)амино]-6-цис-4-[(3-хлорпропил)сульфониламино]циклогексан-1-илокси-7-метоксихиназолина в 2 мл ацетонитрила добавляют 23 мкл морфолина и реакционную смесь в течение ночи кипятят с обратным холодильником. Для переработки смесь растворяют в этилацетате и промывают водой. Органическую фазу сушат над сульфатом магния и концентрируют. Сырой продукт очищают на силикагелевой колонке с использованием в качестве элюента смеси метиленхлорид/метанол (в соотношении 9:1). Выход: 18 мг (27% от теории), значение Rf: 0,36 (силикагель, метиленхлорид/метанол в соотношении 9:1), масс-спектр (ESI+): m/z=608, 610 [М+Н]+. Аналогично примеру 4 получают следующие соединения:- 27009300 значение Rf: 0,16 (силикагель, этилацетат/метанол/конц. водный раствор аммиака в соотношении 90:10:1), масс-спектр (ESI+): m/z=608, 610 [М+Н]+;(2) 4-[(3-хлор-4-фторфенил)амино]-6-(тетрагидропиран-4-илокси)-7-[4-(морфолин-4-ил)бутилокси] хиназолин: реакцию проводят в присутствии карбоната натрия и иодида натрия в N-метилпирролидоне при 100C, значение Rf: 0,18 (силикагель, этилацетат/метанол/конц. водный раствор аммиака в соотношении 40:10:0,5), масс-спектр (ESI+): m/z=531, 533 [М+Н]+;(3) 4-[(3-хлор-4-фторфенил)амино]-6-S)-тетрагидрофуран-3-илокси)-7-[4-(морфолин-4-ил)бутилокси] хиназолин: реакцию проводят в присутствии карбоната натрия и иодида натрия в N-метилпирролидоне при 100C, значение Rf: 0,32 (силикагель, этилацетат/метанол/конц. водный раствор аммиака в соотношении 80:20:1), масс-спектр (ESI+): m/z=517, 519 [М+Н]+;(4) 4-[(3-хлор-4-фторфенил)амино]-6-1-[(морфолин-4-ил)ацетил]пиперидин-4-илоксихиназолин: реакцию проводят в присутствии основания Хюнига в тетрагидрофуране при комнатной температуре, значение Rf: 0,30 (силикагель, метиленхлорид /метанол в соотношении 9:1), масс-спектр (ESI+):(5) 4-[(3-хлор-4-фторфенил)амино]-6-(1-диметиламиноацетилпиперидин-4-илокси)хиназолин: реакцию проводят в присутствии основания Хюнига в тетрагидрофуране при комнатной температуре, значение Rf: 0,11 (силикагель, метиленхлорид/метанол/конц. водный раствор аммиака в соотношении 90:10:1), масс-спектр (ESI+): m/z=458, 460 [М+Н]+;(6) 4-[(3-хлор-4-фторфенил)амино]-6-(1-диметиламиноацетилпиперидин-4-илокси)-7-метоксихиназолин: реакцию проводят в присутствии основания Хюнига в тетрагидрофуране при комнатной температуре, значение Rf: 0,19 (силикагель, этилацетат/метанол/конц. водный раствор аммиака в соотношении 90:10:1), масс-спектр (ESI+): m/z=488, 490 [М+Н]+;(7) 4-[(3-хлор-4-фторфенил)амино]-6-1-[(морфолин-4-ил)ацетил]пиперидин-4-илокси-7-метоксихиназолин: реакцию проводят в присутствии основания Хюнига в тетрагидрофуране при комнатной температуре, масс-спектр (ESI+): m/z=530, 532 [М+Н]+. Пример 5. Дигидрохлорид 4-[(3-хлор-4-фторфенил)амино]-6-S)-пирролидин-3-илокси)-7-метоксихиназолина. Раствор 370 мг 4-[(3-хлор-4-фторфенил)амино]-6-[(S)-1-(трет-бутилоксикарбонил)пирролидин-3-илокси]-7-метоксихиназолина в 5 мл диоксана смешивают с 0,32 мл концентрированной соляной кислоты и перемешивают в течение ночи при комнатной температуре. Выпавший осадок отделяют вакуум-фильтрацией и промывают большим количеством диоксана. Сырой продукт растворяют в небольшом количестве метанола и вновь осаждают добавлением такого же количества этилацетата. Полученное таким путем белое твердое вещество отделяют вакуум-фильтрацией и сушат. Выход: 200 мг (57% от теории), температура плавления: 281C, масс-спектр (ESI+): m/z=389, 391(4) дигидрохлорид 4-[(3-хлор-4-фторфенил)амино]-6-(тетрагидропиран-4-илокси)-7-(2-аминоэтокси)хиназолина: реакцию проводят с изопропанольным раствором соляной кислоты (5-6-молярным) в метиленхлориде, значение Rf: 0,58 (готовые пластины для ТСХ с обращенной фазой (фирма Е. Merck), ацетонитрил/вода/трифторуксусная кислота в соотношении 50:50:1), масс-спектр (ESI+): m/z=433, 435 [М+Н]+;(5) дигидрохлорид 4-[(3-хлор-4-фторфенил)амино]-6-(тетрагидропиран-4-илокси)-7-(3-аминопропилокси)хиназолина: реакцию проводят с изопропанольным раствором соляной кислоты (5-6-молярным) в метиленхлориде, значение Rf: 0,44 (готовые пластины для ТСХ с обращенной фазой (фирма Е. Merck), метанол/5%ный раствор хлорида натрия в соотношении 7:3), масс-спектр (ESI+): m/z=447, 449 [М+Н]+;(6) дигидрохлорид 4-[(3-хлор-4-фторфенил)амино]-6-[1-(2-аминоэтил)пиперидин-4-илокси]хиназолина: значение Rf: 0,50 (готовые пластины для ТСХ с обращенной фазой (фирма Е. Merck), ацетонитрил/вода/трифторуксусная кислота в соотношении 50:50:1), масс-спектр (ESI+): m/z=416, 418 [М+Н]+;(7) дигидрохлорид 4-[(3-хлор-4-фторфенил)амино]-6-(цис-4-метиламиноциклогексан-1-илокси)-7- 28009300 метоксихиназолина: реакцию проводят с изопропанольным раствором соляной кислоты (5-6-молярным) в метиленхлориде, значение Rf: 0,35 (готовые пластины для ТСХ с обращенной фазой (фирма Е. Merck), ацетонитрил/вода/трифторуксусная кислота в соотношении 50:50:1), масс-спектр (ESI+): m/z=431, 433 [М+Н]+;(8) дигидрохлорид 4-[(3-этинилфенил)амино]-6-(пиперидин-4-илокси)-7-метоксихиназолина: реакцию проводят с изопропанольным раствором соляной кислоты (5-6-молярным) в метиленхлориде, значение Rf: 0,50 (готовые пластины для ТСХ с обращенной фазой (фирма Е. Merck), ацетонитрил/вода/трифторуксусная кислота в соотношении 50:50:1), масс-спектр (ESI+): m/z=375 [М+Н]+;(9) дигидрохлорид 4-[(3-хлор-4-фторфенил)амино]-6-(транс-4-метиламиноциклогексан-1-илокси)-7 метоксихиназолина: температура плавления: 251C, масс-спектр (ESI+): m/z=431, 433 [М+Н]+. Пример 6. 4-[(3-Хлор-4-фторфенил)амино]-6-(тетрагидропиран-4-илокси)-7-гидроксихиназолин. Смесь из 9,00 г гидрохлорида 4-[(3-хлор-4-фторфенил)амино]-6-(тетрагидропиран-4-илокси)-7-бензилоксихиназолина и 50 мл трифторуксусной кислоты нагревают до 100C и выдерживают при этой температуре в течение 1,5 ч. Далее реакционную смесь концентрируют и остаток растворяют в 10 мл ацетонитрила. Этот раствор при интенсивном перемешивании по каплям добавляют к 100 мл насыщенного раствора гидрокарбоната натрия. По истечении 1,5 ч образовавшийся осадок отделяют вакуум-фильтрацией и несколько раз промывают водой. Сырой продукт смешивают с диэтиловым эфиром, подвергают вакуум-фильтрации и сушат. Выход: 5,90 г (87% от теории), значение Rf: 0,21 (силикагель, этилацетат), масс-спектр (ESI+):(1) 4-[(3-хлор-4-фторфенил)амино]-6-S)-тетрагидрофуран-3-илокси)-7-гидроксихиназолин: значение Rf: 0,44 (силикагель, этилацетат/метанол в соотношении 9:1), масс-спектр (ESI+): m/z=376,378 [М+Н]+. Пример 7. 4-[(3-Хлор-4-фторфенил)амино]-6-(тетрагидропиран-4-илокси)-7-[3-(морфолин-4-ил)пропилокси]хиназолин. Смесь из 300 мг 4-[(3-хлор-4-фторфенил)амино]-6-(тетрагидропиран-4-илокси)-7-гидроксихиназолина, 130 мг 3-(морфолин-4-ил)пропилхлорида и 530 мг карбоната калия в 5 мл N,N-диметилформамида перемешивают в течение ночи при 80C. Для переработки реакционную смесь разбавляют 25 мл воды и экстрагируют этилацетатом. Объединенные органические фазы промывают насыщенным раствором хлорида натрия, сушат над сульфатом магния и концентрируют. Остаток смешивают с диэтиловым эфиром,подвергают вакуум-фильтрации и сушат. Выход: 250 мг (63% от теории), температура плавления: 205C, масс-спектр (ESI+): m/z=517, 519 [M+H]+. Аналогично примеру 7 получают следующие соединения:(1) 4-[(3-хлор-4-фторфенил)амино]-6-(тетрагидропиран-4-илокси)-7-[2-(морфолин-4-ил)-этокси]хиназолин: значение Rf: 0,33 (силикагель, этилацетат/метанол/конц. водный раствор аммиака в соотношении 40:10:0,5), масс-спектр (ESI+): m/z=503, 505 [М+Н]+;(2) 4-[(3-хлор-4-фторфенил)амино]-6-(тетрагидропиран-4-илокси)-7-этоксихиназолин: значение Rf: 0,76 (силикагель, этилацетат/метанол/конц. водный раствор аммиака в соотношении 90:10:1), масс-спектр (ESI+): m/z=418, 420 [М+Н]+;(3) 4-[(3-хлор-4-фторфенил)амино]-6-S)-тетрагидрофуран-3-илокси)-7-[3-(морфолин-4-ил)пропилокси]хиназолин: значение Rf: 0,20 (силикагель, этилацетат/метанол/конц. водный раствор аммиака в соотношении 90:10:1), масс-спектр (ESI-): m/z=501, 503[M-Н]-;(4) 4-[(3-хлор-4-фторфенил)амино]-6-S)-тетрагидрофуран-3-илокси)-7-[2-(морфолин-4-ил)этокси] хиназолин: значение Rf: 0,19 (силикагель, этилацетат/метанол/конц. водный раствор аммиака в соотношении 90:10:1), масс-спектр (ESI+): m/z=489, 491 [М+Н]+;(6) 4-[(3-хлор-4-фторфенил)амино]-6-(тетрагидропиран-4-илокси)-7-[2-(трет-бутилоксикарбониламино) этокси]хиназолин: значение Rf: 0,64 (силикагель, этилацетат/метанол/конц. водный раствор аммиака в соотношении 95:5:0,1), масс-спектр (ESI+): m/z=533, 535 [М+Н]+;(7) 4-[(3-хлор-4-фторфенил)амино]-6-(тетрагидропиран-4-илокси)-7-[3-(трет-бутилоксикарбониламино) пропилокси]хиназолин: значение Rf: 0,74 (силикагель, этилацетат/метанол/конц. водный раствор аммиака в соотношении 95:5:0,1), масс-спектр (ESI+): m/z=547, 549 [М+Н]+. Пример 8. 4-[(3-Хлор-4-фторфенил)амино]-6-(пиперидин-4-илокси)хиназолин. Раствор 4,55 г гидрохлорида 4-[(3-хлор-4-фторфенил)амино]-6-(1-трифторацетилпиперидин-4-илок- 29009300 си)хиназолина в 35 мл метанола смешивают с 13 мл 3 н. едкого натра и в течение примерно получаса перемешивают при комнатной температуре. Для переработки реакционную смесь разбавляют водой и экстрагируют этилацетатом. Объединенные органические фазы промывают насыщенным раствором хлорида натрия, сушат над сульфатом магния и концентрируют. Остаток смешивают с диэтиловым эфиром, подвергают вакуум-фильтрации и сушат. Выход: 3,00 г (89% от теории), значение Rf: 0,48 (готовые пластины для ТСХ с обращенной фазой(1) 4-[(3-хлор-4-фторфенил)амино]-6-(пиперидин-4-илокси)-7-этоксихиназолин: значение Rf: 0,20 (силикагель, метиленхлорид/метанол/конц. водный раствор аммиака в соотношении 90:10:1), масс-спектр (ESI+): m/z=417, 419 [М+Н]+;(2) 4-[(3-хлор-4-фторфенил)амино]-6-(пиперидин-4-илокси)-7-(2-метоксиэтокси)хиназолин: значение Rf: 0,10 (силикагель, метиленхлорид/метанол/конц. водный раствор аммиака в соотношении 90:10:1), масс-спектр (ESI+): m/z=447, 449 [М+Н]+. Пример 9. 4-[(3-Хлор-4-фторфенил)амино]-6-1-[(этиламино)карбонил]пиперидин-4-илокси-7-метоксихиназолин. Указанное в заголовке соединение получают взаимодействием 4-[(3-хлор-4-фторфенил)амино]-6-(пиперидин-4-илокси)-7-метоксихиназолина с этилизоцианатом в тетрагидрофуране при комнатной температуре. Значение Rf: 0,53 (силикагель, этилацетат/метанол/конц. водный раствор аммиака в соотношении 90:10:1), масс-спектр (ESI+): m/z=474, 476 [М+Н]+. Аналогично примеру 9 получают следующие соединения:(2) 4-[(3-хлор-4-фторфенил)амино]-6-1-[(фениламино)карбонил]пиперидин-4-илокси-7-метоксихиназолин: значение Rf: 0,70 (силикагель, этилацетат/метанол/конц. водный раствор аммиака в соотношении 95:5:0,1), масс-спектр (ESI+): m/z=522, 524 [М+Н]+;m/z=502, 504 [М+Н]+. Пример 10. 4-[(3-Хлор-4-фторфенил)амино]-6-1-[(диметиламино)карбонилметил]пиперидин-4-илоксихиназолин. Указанное в заголовке соединение получают взаимодействием 4-[(3-хлор-4-фторфенил)амино]-6(пиперидин-4-илокси)хиназолина с 2-хлор-N,N-диметилацетамидом в присутствии карбоната калия в(1) 4-[(3-хлор-4-фторфенил)амино]-6-1-[(морфолин-4-ил)карбонилметил]пиперидин-4-илоксихиназолин: значение Rf: 0,42 (готовые пластины для ТСХ с обращенной фазой (фирма Е. Merck), ацетонитрил/вода/трифторуксусная кислота в соотношении 50:50:1), масс-спектр (ESI+): m/z=500, 502 [М+Н]+;(4) 4-[(3-хлор-4-фторфенил)амино]-6-1-[(морфолин-4-ил)карбонилметил]пиперидин-4-илокси-7 метоксихиназолин: температура плавления: 245C, масс-спектр (ESI+): m/z=530, 532 [М+Н]+. Пример 11. 4-[(3-Хлор-4-фторфенил)амино]-6-1-[(тетрагидропиран-4-ил)карбонил]пиперидин-4-илокси-7-метоксихиназолин. К смеси из 300 мг дигидрохлорида 4-[(3-хлор-4-фторфенил)амино]-6-(пиперидин-4-илокси)-7-метоксихиназолина, 82 мг тетрагидропиран-4-карбоновой кислоты и 0,54 мл основания Хюнига в 5 мл N,Nдиметилформамида добавляют 90 мг 1-гидрокси-1 Н-бензотриазола и 250 мг тетрафторбората 2-(1 Н-бензотриазол-1-ил)-1,1,3,3-тетраметилурония. Далее реакционную смесь перемешивают в течение ночи при комнатной температуре. Для переработки смесь смешивают с 25 мл этилацетата и промывают водой,10%-ным раствором карбоната калия и насыщенным раствором хлорида натрия. Органическую фазу су- 30
МПК / Метки
МПК: C07D 403/12, A61P 35/00, C07D 401/12, C07D 491/08, A61K 31/517, C07D 498/08, C07D 413/12, C07D 239/94, C07D 405/12
Метки: тирозинкиназы, качестве, ингибиторов
Код ссылки
<a href="https://eas.patents.su/30-9300-4-n-fenilaminohinazoliny-hinoliny-v-kachestve-ingibitorov-tirozinkinazy.html" rel="bookmark" title="База патентов Евразийского Союза">4-(n-фениламино)хиназолины/-хинолины в качестве ингибиторов тирозинкиназы</a>
Предыдущий патент: Стабилизатор приставной лестницы
Следующий патент: Способ получения производных тиоэфиров и его применение
Случайный патент: Способ и устройство для обеспечения кромки катодной основы диэлектрической накладкой