Производные бифениламидлактама в качестве ингибиторов 11-бета-гидроксистероиддегидрогеназы 1
Номер патента: 14718
Опубликовано: 28.02.2011
Авторы: Саеед Ашраф, Тот Джеймс Ли, Хинклин Рональд Джей, Хайт Гари Алан, Снайдер Нэнси Джун, Виннероски Джуниор Леонард Ларри, Маккауан Джефферсон Рэй, Йорк Джереми Шуленбург, Сюй Яньпин, Ли Жэньхуа, Красутский Алексей Павлович, Чэнь Чжаогэнь, Айкер Томас Дэниел, Уоллэйс Оуэн Брендан
Формула / Реферат
1. Соединение, структура которого представлена формулой
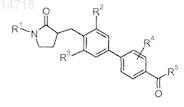
где R1представляет собой 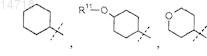 или
или ![]()
где пунктирной линией обозначено место присоединения в положение R1;
R2 представляет собой -Н, -галоген, -СН3(необязательно замещенный 1-3 атомами галогенов) или -О-СН3(необязательно замещенный 1-3 атомами галогенов);
R3 представляет собой -галоген, -СН3(необязательно замещенный 1-3 атомами галогенов) или -O-СН3 (необязательно замещенный 1-3 атомами галогенов);
R4 представляет собой -Н или -галоген;
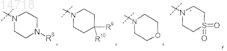
R5 представляет собой
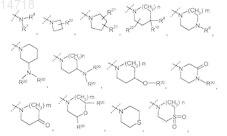
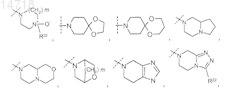
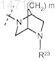 или
или 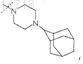
где пунктирной линией обозначено место присоединения в положение R5;
n имеет значения 0, 1 или 2 и если n равно 0, то (СН2)n представляет собой связь;
m имеет значения 1 или 2;
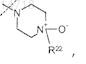
R6 представляет собой -Н, -(C1-С3)алкил (необязательно замещенный 1-3 атомами галогенов), -(C1-С3)алкил-O-R20, -(C1-С3)алкилпирролидинил, фенил, НЕТ1, -НЕТ2, -СН2-фенил, -СН2-НЕТ1, -СН2-НЕТ2, -(C1-С3)алкил-N(R20)(R20), -(C1-С3)алкил-N+(О-)(СН3)2, -(C1-С3)алкил-С(О)N(R41)(R41), -СН(С(О)ОН)(CH2OR20),
-СН(С(О)ОН)(CH2N(R20)(R20)), -(C1-С3)алкил-С(О)O-R20,
![]() или
или 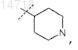
где пунктирной линией обозначено место присоединения в положение, обозначенное R6;
НЕТ1представляет собой
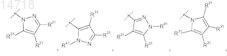
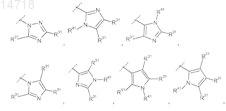
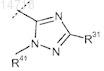 или
или 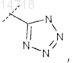
где пунктирной линией обозначено место присоединения в положение, обозначенное НЕТ1;
НЕТ2 представляет собой
![]() или
или ![]()
где пунктирной линией обозначено место присоединения в положение, обозначенное НЕТ2;
R7 представляет собой -Н, -(C1-С3)алкил (необязательно замещенный 1-3 атомами галогенов) или -(С1-С3)алкил-O-R20;
R8 представляет собой -Н, -ОН, -(C1-С6)алкил (необязательно замещенный 1-3 атомами галогенов), -(C1-С3)алкил-O-R20, -С(О)-(С1-С4)алкил (необязательно замещенный 1-3 атомами галогенов), -С(О)О-(C1-C4)алкил (необязательно замещенный 1-3 атомами галогенов) или -С(O)-N(R20)(R20);
R9 представляет собой -Н, -галоген, -СН3(необязательно замещенный 1-3 атомами галогенов) или -О-СН3(необязательно замещенный 1-3 атомами галогенов);
R10 в каждом случае независимо представляет собой -Н или -галоген;
R11 в каждом случае независимо представляет -Н, -СН3или -СН2-СН3;
R20 в каждом случае независимо представляет собой -Н или -(С1-С4)алкил (необязательно замещенный 1-3 атомами галогенов);
R21 в каждом случае независимо представляет собой -Н, -галоген или -(С1-С4)алкил (необязательно замещенный 1-3 атомами галогенов);
R22 в каждом случае независимо представляет собой -Н или -(C1-C6)алкил (необязательно замещенный 1-3 атомами галогенов);
R23 в каждом случае независимо представляет собой -Н, -(C1-С4)алкил или-С(О)О-(C1-C4)алкил;
R24 в каждом случае независимо представляет собой -Н, галоген или -(C1-С6)алкил (необязательно замещенный 1-3 атомами галогенов);
R31 в каждом случае независимо представляет собой -Н, галоген или -(C1-C6)алкил (необязательно замещенный 1-3 атомами галогенов) и
R41 в каждом случае независимо представляет собой -Н или -(C1-С6)алкил (необязательно замещенный 1-3 атомами галогенов);
при условии, что данное соединение не является {[3'-хлор-4'-(1-циклогексил-2-оксопирролидин-3-илметил)бифенил-4-карбонил]амино}уксусной кислотой, 4-{[3'-хлор-4'-(1-циклогексил-2-оксопирролидин-3-илметил)бифенил-4-карбонил]амино}масляной кислотой, 3'-хлор-4'-(1-циклогексил-2-оксопирролидин-3-илметил)бифенил-4-карбоновой кислоты пиперидин-4-иламидом или 3-[3-хлор-4'-(4-метилпиперазин-1-карбонил)бифенил-4-илметил-1-циклогексилпирролидин-2-оном;
или его фармацевтически приемлемая соль.
2. Соединение по п.1, где R1 представляет собой ![]()
![]() или
или ![]() или его фармацевтически приемлемая соль.
или его фармацевтически приемлемая соль.
3. Соединение по п.1 или 2, где R2 и R3представляют собой хлор, или его фармацевтически приемлемая соль.
4. Соединение по любому из пп.1-3, где R4 представляет собой водород, или его фармацевтически приемлемая соль.
5. Соединение по любому из пп.1-4, где R1 представляет собой ![]() или его фармацевтически приемлемая соль.
или его фармацевтически приемлемая соль.
6. Соединение по любому из пп.1-4, где R1 представляет собой ![]() или его фармацевтически приемлемая соль.
или его фармацевтически приемлемая соль.
7. Соединение по любому из пп.1-4, где R1 представляет собой ![]() или его фармацевтически приемлемая соль.
или его фармацевтически приемлемая соль.
8. Соединение по любому ил пп.1-7,
где R5 представляет собой
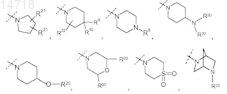
или
R8 представляет собой -Н, -(C1-C4)алкил (необязательно замещенный 1-3 атомами галогенов), -(С2-С3)алкил-O-R20, -С(O)-(С1-С4)алкил, -С(O)O-(C1-C4)алкил или -C(O)-N(R20)(R20);
R9 представляет собой -Н, -галоген, -СН3(необязательно замещенный 1-3 атомами галогенов) или -О-СН3(необязательно замещенный 1-3 атомами галогенов);
R10 в каждом случае независимо представляет собой -Н или -галоген;
R20 в каждом случае независимо представляет собой -Н или -(C1-С3)алкил (необязательно замещенный 1-3 атомами галогенов);
R21 в каждом случае независимо представляет собой -Н, галоген или -(C1-С3)алкил;
R22 в каждом случае независимо представляет собой -Н или -(C1-С3)алкил (необязательно замещенный 1-3 атомами галогенов) и
R23 в каждом случае независимо представляет собой -Н, -(C1-С3)алкил или -С(О)О-(С1-С4)алкил;
или его фармацевтически приемлемая соль.
9. Соединение по любому из пп.1-8, где R5 представляет собой
R8 представляет собой -(C1-C4)алкил (необязательно замещенный 1-3 атомами галогенов);
R9 представляет собой -Н, -галоген, -СН3(необязательно замещенный 1-3 атомами галогенов) и
R10 в каждом случае независимо представляет собой -Н или -галоген,
или его фармацевтически приемлемая соль.
10. Соединение по любому из пп.1-9, где R5 представляет собой
![]()
R8 представляет собой -(C1-С3)алкил (необязательно замещенный 1-3 атомами галогенов),
или его фармацевтически приемлемая соль.
11. Соединение по любому из пп.1-9, где R5 представляет собой ![]() или
или ![]() или его фармацевтически приемлемая соль.
или его фармацевтически приемлемая соль.
12. Соединение по любому из пп.1-9, где R5 представляет собой ![]() или его фармацевтически приемлемая соль.
или его фармацевтически приемлемая соль.
13. Соединение по любому из пп.1-9, где R5 представляет собой ![]() или его фармацевтически приемлемая соль.
или его фармацевтически приемлемая соль.
14. Соединение, которое представляет собой 1-циклогексил-3-{3,5-дихлор-4'-[4-(2-фторэтил)пиперазин-1-карбонил]бифенил-4-илметил}пирролидин-2-он, или его фармацевтически приемлемая соль.
15. Соединение, которое представляет собой (R)-3-[3,5-дихлор-4'-(4-трифторметилпиперидин-1-карбонил)бифенил-4-илметил]-1-(тетрагидропиран-4-ил)пирролидин-2-он, или его фармацевтически приемлемая соль.
16. Соединение по п.1, выбранное из группы, состоящей из
амида 3',5'-дихлор-4'-(1-циклогексил-2-оксопирролидин-3-илметил)-3-фторбифенил-4-карбоновой кислоты;
1-циклогексил-3-{3,5-дихлор-4'-[4-(2-гидроксиэтил)пиперазин-1-карбонил]бифенил-4-илметил}пирролидин-2-она;
1-циклогексил-3-[3,5-дихлор-4'-(пиперидин-1-карбонил)бифенил-4-илметил]пирролидин-2-она;
1-циклогексил-3-[3,5-дихлор-4'-(морфолин-4-карбонил)бифенил-4-илметил]пирролидин-2-она;
бис-(2-гидроксиэтил)амида 3',5'-дихлор-4'-(1-циклогексил-2-оксопирролидин-3-илметил)бифенил-4-карбоновой кислоты;
1-циклогексил-3-[3,5-дихлор-4'-(4-изопропилпиперазин-1-карбонил)бифенил-4-илметил]пирролидин-2-она;
(2-диметиламиноэтил)амида 3',5'-дихлор-4'-(1-циклогексил-2-оксопирролидин-3-илметил)бифенил-4-карбоновой кислоты;
(2-диметиламиноэтил)метиламида 3',5'-дихлор-4'-(1-циклогексил-2-оксопирролидин-3-илметил)бифенил-4-карбоновой кислоты;
1-циклогексил-3-[3,5-дихлор-4'-(4-трифторметилпиперидин-1-карбонил)бифенил-4-илметил]пирролидин-2-она;
1-циклогексил-3-[3,5-дихлор-4'-(4-гидроксипиперидин-1-карбонил)бифенил-4-илметил]пирролидин-2-она;
(2-гидроксиэтил)метиламида 3',5'-дихлор-4'-(1-циклогексил-2-оксопирролидин-3-илметил)бифенил-4-карбоновой кислоты;
1-циклогексил-3-[3,5-дихлор-4'-(тиоморфолин-4-карбонил)бифенил-4-илметил]пирролидин-2-она;
(2,2,2-трифторэтил)амида 3',5'-дихлор-4'-(1-циклогексил-2-оксопирролидин-3-илметил)бифенил-4-карбоновой кислоты;
1-циклогексил-3-{3,5-дихлор-4'-[4-(2-фторэтил)пиперазин-1-карбонилбифенил-4-илметил}пирролидин-2-она;
метиламида 3',5'-дихлор-4'-(1-циклогексил-2-оксопирролидин-3-илметил)бифенил-4-карбоновой кислоты;
диэтиламида 3',5'-дихлор-4'-(1-циклогексил-2-оксопирролидин-3-илметил)бифенил-4-карбоновой кислоты;
изопропиламида 3',5'-дихлор-4'-(1-циклогексил-2-оксопирролидин-3-илметил)бифенил-4-карбоновой кислоты;
этиламида 3',5'-дихлор-4'-(1-циклогексил-2-оксопирролидин-3-илметил)бифенил-4-карбоновой кислоты;
(пиридин-4-илметил)амида 3',5'-дихлор-4'-(1-циклогексил-2-оксопирролидин-3-илметил)бифенил-4-карбоновой кислоты;
циклопропиламида 3',5'-дихлор-4'-(1-циклогексил-2-оксопирролидин-3-илметил)бифенил-4-карбоновой кислоты;
циклобутиламида 3',5'-дихлор-4'-(1-циклогексил-2-оксопирролидин-3-илметил)бифенил-4-карбоновой кислоты;
3-[4'-(азетидин-1-карбонил)-3,5-дихлорбифенил-4-илметил]-1-циклогексилпирролидин-2-она;
бис-(2-гидроксиэтил)амида 3',5'-дихлор-4'-(1-циклогексил-2-оксопирролидин-3-илметил)бифенил-4-карбоновой кислоты;
1-[3',5'-дихлор-4'-(1-циклогексил-2-оксопирролидин-3-илметил)бифенил-4-карбонил]пиперидин-4-она;
(4-аминоциклогексил)амида 3',5'-дихлор-4'-(1-циклогексил-2-оксопирролидин-3-илметил)бифенил-4-карбоновой кислоты;
диметиламида 4-[3',5'-дихлор-4'-(1-циклогексил-2-оксопирролидин-3-илметил)бифенил-4-карбонил]пиперазин-1-карбоновой кислоты;
1-циклогексил-3-[3,5-дихлор-4'-(гексагидропирроло[1,2-а]пиразин-2-карбонил)бифенил-4-илметил]пирролидин-2-она;
1-циклогексил-3-[3,5-дихлор-4'-(гексагидропиразино[2,1-с][1,4]оксазин-8-карбонил)бифенил-4-илметил] пирролидин-2-она;
1-циклогексил-3-[3,5-дихлор-4'-(1,4,6,7-тетрагидроимидазо[4,5-с]пиридин-5-карбонил)бифенил-4-илметил]пирролидин-2-она;
1-циклогексил-3-[3,5-дихлор-4'-(гексагидропирроло[1,2-а]пиразин-2-карбонил)бифенил-4-илметил]пирролидин-2-она;
трет-бутилового эфира 5-[3',5'-дихлор-4'-(1-циклогексил-2-оксопирролидин-3-илметил)бифенил-4-карбонил]-2,5-диазабицикло[2.2.1]гептан-2-карбоновой кислоты;
1-циклогексил-3-[3,5-дихлор-4'-(пирролидин-1-карбонил)бифенил-4-илметил]пирролидин-2-она;
{[3',5'-дихлор-4'-(1-циклогексил-2-оксопирролидин-3-илметил)бифенил-4-карбонил]амино}уксусной кислоты;
(S)-2-{[3',5'-дихлор-4'-(1-циклогексил-2-оксопирролидин-3-илметил)бифенил-4-карбонил]амино}-3-гидроксипропионовой кислоты;
(R)-2-{[3',5'-дихлор-4'-(1-циклогексил-2-оксопирролидин-3-илметил)бифенил-4-карбонил]амино}-3-гидроксипропионовой кислоты;
2-{[3',5'-дихлор-4'-(1-циклогексил-2-оксопирролидин-3-илметил)бифенил-4-карбонил]амино}-3-диметиламинопропионовой кислоты;
метил-(1Н-тетразол-5-ил)амида 3',5'-дихлор-4'-(1-циклогексил-2-оксопирролидин-3-илметил)бифенил-4-карбоновой кислоты;
3-[4'-(4-трет-бутилпиперазин-1-карбонил)-3,5-дихлорбифенил-4-илметил]-1-циклогексилпирролидин-2-она;
1-циклогексил-3-[3,5-дихлор-4'-(3-трифторметил-5,6-дигидро-8Н-[1,2,4]триазоло[4,3-а]пиразин-7-карбонил)бифенил-4-илметил]пирролидин-2-она;
1-циклогексил-3-[3,5-дихлор-4'-(4-метилпиперазин-1-карбонил)бифенил-4-илметил]пирролидин-2-она;
азетидин-3-иламида 3',5'-дихлор-4'-(1-циклогексил-2-оксопирролидин-3-илметил)бифенил-4-карбоновой кислоты;
(3-аминоциклогексил)амида 3',5'-дихлор-4'-(1-циклогексил-2-оксопирролидин-3-илметил)бифенил-4-карбоновой кислоты;
1-циклогексил-3-[3,5-дихлор-4'-(пиперазин-1-карбонил)бифенил-4-илметил]пирролидин-2-она;
(4-аминоциклогексил)амида 3',5'-дихлор-4'-(1-циклогексил-2-оксопирролидин-3-илметил)бифенил-4-карбоновой кислоты;
(2-диметиламиноэтил)амид N-оксида 3',5'-дихлор-4'-(1-циклогексил-2-оксопирролидин-3-илметил)бифенил-4-карбоновой кислоты;
(1-окси-пиридин-4-илметил)амида 3',5'-дихлор-4'-(1-циклогексил-2-оксопирролидин-3-илметил)бифенил-4-карбоновой кислоты;
3-[4'-(4-ацетилпиперазин-1-карбонил)-3,5-дихлорбифенил-4-илметил]-1-циклогексилпирролидин-2-она;
амида 4-[3',5'-дихлор-4'-(1-циклогексил-2-оксопирролидин-3-илметил)бифенил-4-карбонил]пиперазин-1-карбоновой кислоты;
1-циклогексил-3-[3,5-дихлор-4'-(1,1-диоксо-1-l*6*-тиоморфолин-4-карбонил)бифенил-4-илметил]пирролидин-2-она;
(2-аминоэтил)амида 3',5'-дихлор-4'-(1-циклогексил-2-оксопирролидин-3-илметил)бифенил-4-карбоновой кислоты;
пиперидин-4-иламида 3',5'-дихлор-4'-(1-циклогексил-2-оксопирролидин-3-илметил)бифенил-4-карбоновой кислоты;
4-[3',5'-дихлор-4'-(1-циклогексил-2-оксопирролидин-3-илметил)бифенил-4-карбонил]-1-метилпиперазин-2-она;
1-циклогексил-3-[3,5-дихлор-4'-((1S,4S)-5-изопропил-2,5-диазабицикло[2.2.1]гептан-2-карбонил)бифенил-4-илметил]пирролидин-2-она;
1-циклогексил-3-{3,5-дихлор-4'-[4-(2-фторэтил)пиперазин-1-карбонил]бифенил-4-илметил}пирролидин-2-она;
1-циклогексил-3-[3,5-дихлор-4'-(морфолин-4-карбонил)бифенил-4-илметил]пирролидин-2-она;
1-циклогексил-3-[3,5-дихлор-4'-(4-метилпиперазин-1-карбонил)бифенил-4-илметил]пирролидин-2-она;
1-циклогексил-3-[3,5-дихлор-4'-(4-изопропилпиперазин-1-карбонил)бифенил-4-илметил]пирролидин-2-она;
1-циклогексил-3-[3,5-дихлор-4'-(4-метил-4-оксипиперазин-1-карбонил)бифенил-4-илметил]пирролидин-2-она;
1-циклогексил-3-[3,5-дихлор-4'-(4-метил-4-оксипиперазин-1-карбонил)бифенил-4-илметил]пирролидин-2-она;
1-циклогексил-3-[3,5-дихлор-4'-(4-изопропил-4-оксипиперазин-1-карбонил)бифенил-4-илметил]пирролидин-2-она;
1-циклогексил-3-{3,5-дихлор-4'-[4-(2,2,2-трифторэтил)пиперазин-1-карбонил]бифенил-4-илметил}пирролидин-2-она;
3-{3,5-дихлор-4'-[4-(2-фторэтил)пиперазин-1-карбонил]бифенил-4-илметил}-цис-1-(4-гидроксициклогексил)пирролидин-2-она;
3-[3,5-дихлор-4'-(1,1-диоксо-1-l*6*-тиоморфолин-4-карбонил)бифенил-4-илметил]-цис-1-(4-гидроксициклогексил)пирролидин-2-она;
(R)-3-[3,5-дихлор-4'-(морфолин-4-карбонил)бифенил-4-илметил]-цис-1-(4-гидроксициклогексил)пирролидин-2-она;
(R)-3-{3,5-дихлор-4'-[4-(2-фторэтил)пиперазин-1-карбонил]бифенил-4-илметил}-цис-1-(4-гидроксициклогексил)пирролидин-2-она;
(R)-3-[3,5-дихлор-4'-(4-трифторметилпиперидин-1-карбонил)бифенил-4-илметил]-цис-1-(4-гидроксициклогексил)пирролидин-2-она;
(R)-3-[4'-(4-трет-бутилпиперазин-1-карбонил)-3,5-дихлорбифенил-4-илметил]-цис-1-(4-гидроксициклогексил)пирролидин-2-она;
(R)-3-[3,5-дихлор-4'-([1,4]оксазепан-4-карбонил)бифенил-4-илметил]цис-1-(4-гидроксициклогексил) пирролидин-2-он;
(R)-3-[3,5-дихлор-4'-(4,4-дифторпиперидин-1-карбонил)бифенил-4-илметил]-цис-1-(4-гидроксициклогексил) пирролидин-2-она;
(R)-3-[3,5-дихлор-4'-(3,3-дифторпирролидин-1-карбонил)бифенил-4-илметил]-цис-1-(4-гидроксициклогексил)пирролидин-2-она;
(R)-3-[3,5-дихлор-4'-(4-метоксипиперидин-1-карбонил)бифенил-4-илметил]-цис-1-(4-гидроксициклогексил) пирролидин-2-она;
(R)-3-[3,5-дихлор-4'-(2,6-цис-диметилморфолин-4-карбонил)бифенил-4-илметил]-цис-1-(4-гидроксициклогексил)пирролидин-2-она;
(R)-3-[3,5-дихлор-4'-(пиперазин-1-карбонил)бифенил-4-илметил]-цис-1-(4-гидроксициклогексил) пирролидин-2-она;
(R)-3-{3,5-дихлор-4'-[4-(2,2,2-трифторэтил)пиперазин-1-карбонил]бифенил-4-илметил}-цис-1-(4-гидроксициклогексил)пирролидин-2-она;
(R)-3-[3,5-дихлор-4'-(2-окса-5-аза-бицикло[2.2.1]гептан-5-карбонил)бифенил-4-илметил]-цис-1-(4-гидроксициклогексил)пирролидин-2-она;
(R)-3-[3,5-дихлор-4'-(4-трифторметилпиперидин-1-карбонил)бифенил-4-илметил]-транс-1-(4-гидроксициклогексил)пирролидин-2-она;
(R)-3-{3,5-дихлор-4'-[4-(2,2,2-трифторэтил)пиперазин-1-карбонил]бифенил-4-илметил}-транс-1-(4-гидроксициклогексил)пирролидин-2-она;
(R)-3-[3,5-дихлор-4'-(морфолин-4-карбонил)бифенил-4-илметил]-транс-1-(4-гидроксициклогексил)пирролидин-2-она;
(R)-3-{3,5-дихлор-4'-[4-(2-фторэтил)пиперазин-1-карбонил]бифенил-4-илметил}-транс-1-(4-гидроксициклогексил)пирролидин-2-она;
(R)-3-[4'-(4-трет-бутилпиперазин-1-карбонил)-3,5-дихлорбифенил-4-илметил]-транс-1-(4-гидроксициклогексил)пирролидин-2-она;
(R)-1-циклогекс-3-енил-3-[3,5-дихлор-4'-(4-трифторметилпиперидин-1-карбонил)бифенил-4-илметил]пирролидин-2-она;
(R)-3-{3,5-дихлор-4'-[4-(2-фторэтил)-4-оксипиперазин-1-карбонил]бифенил-4-илметил}-цис-1-(4-гидроксициклогексил)пирролидин-2-она;
(R)-3-[3,5-дихлор-4'-(1,1-диоксо-1-l*6*-тиоморфолин-4-карбонил)бифенил-4-илметил]-транс-1-(4-гидроксициклогексил)пирролидин-2-она;
(R)-3-[3,5-дихлор-4'-(4-трифторметилпиперидин-1-карбонил)бифенил-4-илметил]-1-(тетрагидропиран-4-ил)пирролидин-2-она;
(R)-3-[3,5-дихлор-4'-(4-метилпиперазин-1-карбонил)бифенил-4-илметил]-1-(тетрагидропиран-4-ил)пирролидин-2-она;
(R)-3-[3,5-дихлор-4'-(4-изопропилпиперазин-1-карбонил)бифенил-4-илметил]-1-(тетрагидропиран-4-ил)пирролидин-2-она;
(R)-3-[3,5-дихлор-4'-(морфолин-4-карбонил)бифенил-4-илметил]-1-(тетрагидропиран-4-ил)пирролидин-2-она;
(R)-3-[3,5-дихлор-4'-(1,1-диоксо-1-l*6*-тиоморфолин-4-карбонил)бифенил-4-илметил]-1-(тетрагидропиран-4-ил)пирролидин-2-она;
(R)-3-{3,5-дихлор-4'-[4-(2-фторэтил)пиперазин-1-карбонил]бифенил-4-илметил}-1-(тетрагидропиран-4-ил)пирролидин-2-она;
(R)-3-{3,5-дихлор-4'-[4-(2,2,2-трифторэтил)пиперазин-1-карбонил]бифенил-4-илметил}-1-(тетрагидропиран-4-ил)пирролидин-2-она;
(R)-3-[4'-(4-адамантан-2-илпиперазин-1-карбонил)-3,5-дихлорбифенил-4-илметил]-1-(тетрагидропиран-4-ил)пирролидин-2-она;
(R)-3-[3,5-дихлор-4'-(4,4-дифторпиперидин-1-карбонил)бифенил-4-илметил]-1-(тетрагидропиран-4-ил)пирролидин-2-она;
(R)-3-[3,5-дихлор-4'-(4,4-дифторпиперидин-1-карбонил)бифенил-4-илметил]-транс-1-(4-гидроксициклогексил)пирролидин-2-она;
1-циклогексил-3-[4'-(4-метилпиперазин-1-карбонил)-3-трифторметоксибифенил-4-илметил]пирролидин-2-она;
1-циклогексил-3-[4'-(4-изопропилпиперазин-1-карбонил)-3-трифторметоксибифенил-4-илметил]пирролидин-2-она;
1-циклогексил-3-[4'-(морфолин-4-карбонил)-3-трифторметоксибифенил-4-илметил]пирролидин-2-она;
1-циклогексил-3-[3-трифторметокси-4'-(4-трифторметилпиперидин-1-карбонил)бифенил-4-илметил]пирролидин-2-она;
1-циклогексил-3-[4'-(1,1-диоксо-1-l*6*-тиоморфолин-4-карбонил)-3-трифторметоксибифенил-4-илметил]пирролидин-2-она;
3-[4'-(4-трет-бутилпиперазин-1-карбонил)-3-трифторметоксибифенил-4-илметил]-1-циклогексилпирролидин-2-она;
1-циклогексил-3-[4'-(4,4-дифторпиперидин-1-карбонил)-3-трифторметоксибифенил-4-илметил]пирролидин-2-она;
1-циклогексил-3-{4'-[4-(2-фторэтил)пиперазин-1-карбонил]-3-трифторметоксибифенил-4-илметил}пирролидин-2-она;
1-циклогексил-3-{4'-[4-(2,2,2-трифторэтил)пиперазин-1-карбонил]-3-трифторметоксибифенил-4-илметил} пирролидин-2-она;
3-[4'-(4-адамантан-2-илпиперазин-1-карбонил)-3-трифторметоксибифенил-4-илметил]-1-циклогексилпирролидин-2-она;
1-циклогексил-3-[4'-(1,1-диоксо-1-l*6*-тиоморфолин-4-карбонил)-3-трифторметилбифенил-4-илметил] пирролидин-2-она;
3-[4'-(4-трет-бутилпиперазин-1-карбонил)-3-трифторметилбифенил-4-илметил]-1-циклогексилпирролидин-2-она;
1-циклогексил-3-[4'-(пиперазин-1-карбонил)-3-трифторметилбифенил-4-илметил]пирролидин-2-она;
1-циклогексил-3-{4'-[4-(2-фторэтил)пиперазин-1-карбонил]-3-трифторметилбифенил-4-илметил} пирролидин-2-она;
1-циклогексил-3-[3-трифторметил-4'-(4-трифторметилпиперидин-1-карбонил)бифенил-4-илметил]пирролидин-2-она;
1-циклогексил-3-[4'-(4-метилпиперазин-1-карбонил)-3-трифторметил-бифенил-4-илметил]пирролидин-2-она;
метилкарбамоилметиламида 3',5'-дихлор-4'-[(R)-транс-1-(4-гидроксициклогексил)-2-оксопирролидин-3-илметил]бифенил-4-карбоновой кислоты;
(R)-3-[3,5-дихлор-4'-(4-метилпиперидин-1-карбонил)бифенил-4-илметил]транс-1-(4-гидроксициклогексил) пирролидин-2-она;
диметилкарбамоилметиламида 3',5'-дихлор-4'-[(R)-транс-1-(4-гидроксициклогексил)-2-оксопирролидин-3-илметил]бифенил-4-карбоновой кислоты;
карбамоилметиламида 3',5'-дихлор-4'-[(R)-транс-1-(4-гидроксициклогексил)-2-оксопирролидин-3-илметил]бифенил-4-карбоновой кислоты;
(R)-3-[3,5-дихлор-4'-(4-трифторметилпиперидин-1-карбонил)бифенил-4-илметил]-транс-1-(4-метоксицикл-огексил)пирролидин-2-она и
(R)-3-[3,5-дихлор-4'-(4,4-дифторпиперидин-1-карбонил)бифенил-4-илметил]-транс-1-(4-метоксициклогексил)пирролидин-2-она,
или его фармацевтически приемлемая соль.
17. Фармацевтическая композиция, которая содержит соединение по любому из пп.1-16 или его фармацевтически приемлемую соль и фармацевтически приемлемый носитель.
18. Применение соединения по любому из пп.1-16 или его фармацевтически приемлемой соли при получении лекарственного средства.
Текст
(CN), Хинклин Рональд Джей, Хайт Гари Алан, Красутский Алексей Павлович, Ли Жэньхуа, Маккауан Джефферсон Рэй, Саеед Ашраф, Снайдер Нэнси Джун, Тот Джеймс Ли,Уоллэйс Оуэн Брендан, Виннероски Джуниор Леонард Ларри, Сюй Яньпин, Йорк Джереми Шуленбург (US) Настоящее изобретение относится к новым соединениям формулы (I) обладающим антагонистической активностью по отношению к 11HSD 1 типа, а также способам получения таких соединений. В другом варианте реализации настоящее изобретение относится к фармацевтическим композициям, содержащим соединения формулы (I), а также способам применения этих соединений и композиций для лечения диабета, гипергликемии, ожирения,гипертензии, гиперлипидемии, метаболического синдрома, нарушений познавательной способности и других состояний, связанных с активностью 11HSD первого типа.(71)(73) Заявитель и патентовладелец: ЭЛИ ЛИЛЛИ ЭНД КОМПАНИ (US) 014718 Заявка на данный патент испрашивает приоритет согласно предварительной заявке на патент США 60/745311 от 21 апреля 2006 г. Настоящее изобретение относится к соединениям, представляющим собой ингибиторы 11-гидроксистероиддегидрогеназы 1 типа (11HSD1), к фармацевтическим композициям, содержащим такие соединения, и применению таких соединений и композиций для лечения организма человека или животного, а также к новым промежуточным соединениям, которые можно применять для получения ингибиторов. Настоящие соединения демонстрируют эффективное и селективное ингибирование 11-HSD1, в этом качестве их можно применять при лечении чувствительных к модуляции 11HSD1 нарушений, например диабета, метаболического синдрома, расстройства познавательной способности и т.п. Глюкокортикоиды, функционирующие в печени, жировой ткани и в мышцах, являются важными регуляторами метаболизма глюкозы, липидов и белков. Хронический избыток глюкокортикоидов связан с резистентностью к инсулину, висцеральным ожирением, гипертензией и дислипидемией, которые также представляют собой классические признаки метаболического синдрома. 11HSD1 катализирует преобразование неактивного кортизона в активный кортизол и, как полагают, вовлечен в развитие метаболического синдрома. Данные, полученные для грызунов и человека, свидетельствуют о связи 11-HSD1 с метаболическим синдромом. Данные позволяют предположить, что лекарственное средство,специфично ингибирующее 11HSD1 у пациентов с диабетом 2 типа, снижает уровень глюкозы в крови, замедляя глюконеогенез в печени, снижает центральное ожирение, улучшает атерогенный липопротеиновый фенотип, уменьшает кровяное давление и снижает резистентность к инсулину. Действие инсулина в мышцах должно усиливаться, и секреция инсулина бета-клетками островков также может возрастать. Данные, полученные при исследовании животных и человека, также свидетельствуют о том, что избыток глюкокортикоидов нарушает познавательную функцию. Недавние результаты указывают на то,что инактивация 11HSD1 усиливает функционирование памяти как у человека, так и у мышей. Было показано, что ингибитор 11HSD карбеноксолон улучшает познавательную функцию у здоровых пожилых людей и у людей, страдающих диабетом 2 типа, а инактивация гена 11HSD1 предотвращает обусловленные старением повреждения у мышей. Недавно было показано, что селективное ингибирование 11HSD1 фармацевтическим агентом улучшает сохранение информации в памяти у мышей. В последние годы появился ряд публикаций, сообщающих об агентах, ингибирующих 11HSD1. См. международную публикацию заявки WO 2004/056744, описывающую адамантилацетамиды в качестве ингибиторов 11HSD1, международную публикацию WO 2005/108360, в которой в качестве ингибиторов 11HSD описаны производные пирролидин-2-она и пиперидин-2-она, и международную публикацию WO 2005/108361, в которой в качестве ингибиторов 11HSD1 описаны производные адамантилпирролидин-2-она. Несмотря на существование ряда способов лечения заболеваний, в которые вовлечен 11HSD1, современные способы лечения имеют ряд недостатков, в том числе низкую или недостаточную эффективность, неприемлемые побочные эффекты, противопоказания для некоторых групп пациентов. Таким образом, сохраняется потребность в улучшении способов лечения с применением альтернативных или усовершенствованных фармацевтических агентов, которые ингибируют 11HSD1 и,таким образом, могут оказаться полезными при лечении заболеваний, при которых ингибирование 11-HSD1 может оказывать благоприятный эффект. Настоящее изобретение обеспечивает такой вклад в данную область техники благодаря тому, что был обнаружен новый класс соединений, оказывающих сильное и селективное ингибирующее действие на 11HSD1. Отличительной особенностью настоящего изобретения являются представленные конкретные структуры и их активность. Сохраняется потребность в новых способах лечения диабета, метаболического синдрома и расстройств познавательной способности, и задачей настоящего изобретения является удовлетворение данной и других потребностей. Настоящее изобретение относится к соединению, структура которого представлена формулой (I) или его фармацевтически приемлемой соли,где R1 представляет собой где пунктирной линией обозначено место присоединения к положению R1 в формуле (I); где пунктирной линией обозначено место присоединения к положению R5 в формуле (I);-СН(С(О)ОН)(CH2OR ), -СН(С(О)ОН)(CH2N(R )(R , -(C1-С 3)алкил-С(О)O-R20,или где пунктирной линией обозначено место присоединения к положению, обозначенному R6; НЕТ 1 представляет собой где пунктирной линией обозначено место присоединения к положению, обозначенному НЕТ 1; НЕТ 2 представляет собой или где пунктирной линией обозначено место присоединения к положению, обозначенному НЕТ 2;R10 в каждом случае независимо представляет собой -Н или -галоген;R11 в каждом случае независимо представляет собой -Н, -СН 3 или -СН 2-СН 3;R20 в каждом случае независимо представляет собой -Н или -(С 1-С 4)алкил (необязательно замещенный 1-3 атомами галогенов);R21 в каждом случае независимо представляет собой -Н, -галоген или -(C1-C4)алкил (необязательно замещенный 1-3 атомами галогенов);R22 в каждом случае независимо представляет собой -Н или -(C1-С 6)алкил (необязательно замещенный 1-3 атомами галогенов);R23 в каждом случае независимо представляет собой -Н, -(C1-С 4)алкил или -С(О)О-(C1-C4)алкил;R24 в каждом случае независимо представляет собой -Н, -галоген или -(C1-С 6)алкил (необязательно замещенный 1-3 атомами галогенов);R31 в каждом случае независимо представляет собой -Н, галоген или -(C1-С 6)алкил (необязательно замещенный 1-3 атомами галогенов) иR41 в каждом случае независимо представляет собой -Н или -(C1-С 6)алкил (необязательно замещенный 1-3 атомами галогенов); при условии, что данное соединение не является [3'-хлор-4'-(1-циклогексил-2-оксопирролидин-3 илметил)бифенил-4-карбонил]аминоуксусной кислотой,4-[3'-хлор-4'-(1-циклогексил-2 оксопирролидин-3-илметил)бифенил-4-карбонил]аминомасляной кислотой, пиперидин-4-иламидом 3'хлор-4'-(1-циклогексил-2-оксопирролидин-3-илметил)бифенил-4-карбоновой кислотой или 3-[3-хлор-4'(4-метилпиперазин-1-карбонил)бифенил-4-илметил]-1-циклогексилпирролидин-2-оном. Данное изобретение обеспечивает соединения формулы (I), которые пригодны для эффективного и селективного ингибирования 11HSD1. Кроме того, данное изобретение обеспечивает фармацевтическую композицию, которая содержит соединение формулы (I) или его фармацевтическую соль, и фармацевтически приемлемый носитель, разбавитель или эксципиент. Кроме того, данное изобретение обеспечивает способ лечения метаболического синдрома и связанных с ним расстройств, который включает введение пациенту, нуждающемуся в этом, эффективного количества соединения формулы (I) или его фармацевтически приемлемой соли. В одном из примеров реализации данное изобретение обеспечивает соединения формулы (I) или их фармацевтически приемлемую соль, как это подробно описано выше. В то время как все соединения по данному изобретению являются полезными, некоторые из этих соединений представляют особый интерес, и они являются предпочтительными. Последующий перечень представляет некоторые группы предпочтительных соединений. В другом примере реализации данное изобретение обеспечивает соединение, структура которого представлена формулой (I), или его фармацевтически приемлемую соль, где или где пунктирной линией обозначено место присоединения к положению R1 в формуле (I); где пунктирной линией обозначено место присоединения к положению R5 в формуле (I);-СН(С(O)ОН)(CH2OR ), -СН(С(О)ОН)(CH2N(R )(R , -(C1-С 3)алкил-С(О)O-R20, или где пунктирной линией обозначено место присоединения к положению, обозначенному R6; НЕТ 1 представляет собой-4 014718 где пунктирной линией обозначено место присоединения к положению, обозначенному НЕТ 1; НЕТ 2 представляет собой или где пунктирной линией обозначено место присоединения к положению, обозначенному НЕТ 2;R10 в каждом случае независимо представляет собой -Н или -галоген;R11 в каждом случае независимо представляет собой -Н, -СН 3 или -СН 2-СН 3;R20 в каждом случае независимо представляет собой -Н или -(С 1-С 4)алкил (необязательно замещенный 1-3 атомами галогенов);R21 в каждом случае независимо представляет собой -Н, -галоген или -(С 1-С 4)алкил (необязательно замещенный 1-3 атомами галогенов);R22 в каждом случае независимо представляет собой -Н или -(C1-С 6)алкил (необязательно замещенный 1-3 атомами галогенов);R23 в каждом случае независимо представляет собой -Н, -(C1-С 4)алкил или -С(О)О-(С 1-С 4)алкил;R24 в каждом случае независимо представляет собой -Н, -галоген или -(C1-С 6)алкил (необязательно замещенный 1-3 атомами галогенов);R31 в каждом случае независимо представляет собой -Н, -галоген или -(C1-С 6)алкил (необязательно замещенный 1-3 атомами галогенов) иR41 в каждом случае независимо представляет собой -Н или -(C1-С 6)алкил (необязательно замещенный 1-3 атомами галогенов). В другом примере реализации данное изобретение обеспечивает соединение, структура которого представлена формулой (I), или его фармацевтически приемлемую соль, где где пунктирной линией обозначено место присоединения к положению R1 в формуле (I); где пунктирной линией обозначено место присоединения к положению R5 в формуле (I);-СН(С(О)ОН)(CH2OR ), -СН(С(О)ОН)(CH2N(R )(R , -(C1-С 3)алкил-С(О)O-R20, или где пунктирной линией обозначено место присоединения к положению, обозначенному R6; НЕТ 1 представляет собой где пунктирной линией обозначено место присоединения к положению, обозначенному НЕТ 1; НЕТ 2 представляет собой или где пунктирной линией обозначено место присоединения к положению, обозначенному НЕТ 2;R10 в каждом случае независимо представляет собой -Н или -галоген;R11 в каждом случае независимо представляет собой -Н, -СН 3 или -СН 2-СН 3;R20 в каждом случае независимо представляет собой -Н или -(C1-С 3)алкил (необязательно замещенный 1-3 атомами галогенов);R21 в каждом случае независимо представляет собой -Н, -галоген или -(C1-С 3)алкил;R22 в каждом случае независимо представляет собой -Н или -(C1-С 3)алкил (необязательно замещенный 1-3 атомами галогенов);R23 в каждом случае независимо представляет собой -Н, -(C1-С 3)алкил или -С(О)О-(С 1-С 4)алкил;R24 в каждом случае независимо представляет собой -Н, -галоген или -(C1-С 3)алкил (необязательно замещенный 1-3 атомами галогенов);R31 в каждом случае независимо представляет собой -Н, -галоген или -(C1-С 3)алкил иR41 в каждом случае независимо представляет собой -Н или -СН 3. В другом примере реализации данное изобретение обеспечивает соединение, структура которого представлена формулой (I), или его фармацевтически приемлемую соль, где где пунктирной линией обозначено место присоединения к положению R1 в формуле (I); где пунктирной линией обозначено место присоединения к положению R5 в формуле (I);-СН(С(О)ОН)(CH2OR ), -СН(С(О)ОН)(CH2N(R )(R , -(C1-С 3)алкил-С(О)O-R20,или где пунктирной линией обозначено место присоединения к положению, обозначенному R6; НЕТ 1 представляет собой где пунктирной линией обозначено место присоединения к положению, обозначенному НЕТ 1; НЕТ 2 представляет собой или где пунктирной линией обозначено место присоединения к положению, обозначенному НЕТ 2;R10 в каждом случае независимо представляет собой -Н или -галоген;R11 в каждом случае независимо представляет собой -Н, -СН 3 или -СН 2-СН 3;R20 в каждом случае независимо представляет собой -Н или -(C1-С 3)алкил (необязательно замещенный 1-3 атомами галогенов);R21 в каждом случае независимо представляет собой -Н, -галоген или -(C1-С 3)алкил;R22 в каждом случае независимо представляет собой -Н или -(C1-С 3)алкил (необязательно замещенный 1-3 атомами галогенов);R23 в каждом случае независимо представляет собой -Н, -(C1-С 3)алкил или -С(О)О-(С 1-С 4)алкил;R24 в каждом случае независимо представляет собой -Н, -галоген или -(C1-С 3)алкил (необязательно замещенный 1-3 атомами галогенов);R31 в каждом случае независимо представляет собой -Н, галоген или -(C1-С 3)алкил иR41 в каждом случае независимо представляет собой -Н или -СН 3. В другом примере реализации данное изобретение обеспечивает соединение, структура которого представлена формулой (I), или его фармацевтически приемлемую соль, гдеR1 представляет собой где пунктирной линией обозначено место присоединения к положению R1 в формуле (I); где пунктирной линией обозначено место присоединения к положению R5 в формуле (I);-СН(С(О)ОН)(CH2OR ), -СН(С(О)ОН)(CH2N(R )(R , -(С 1-С 3)алкил-С(О)O-R20, или где пунктирной линией обозначено место присоединения к положению, обозначенному R6; НЕТ 1 представляет собой где пунктирной линией обозначено место присоединения к положению, обозначенному НЕТ 1; НЕТ 2 представляет собой или где пунктирной линией обозначено место присоединения к положению, обозначенному НЕТ 2;R10 в каждом случае независимо представляет собой -Н или -галоген;R20 в каждом случае независимо представляет собой -Н или -(С 1-С 3)алкил (необязательно замещенный 1-3 атомами галогенов);R21 в каждом случае независимо представляет собой -Н, -галоген или -(С 1-С 3)алкил;R22 в каждом случае независимо представляет собой -Н или -(C1-С 3)алкил (необязательно замещенный 1-3 атомами галогенов);R23 в каждом случае независимо представляет собой -Н, -(C1-С 3)алкил или -С(О)О-(C1-C4)алкил;R24 в каждом случае независимо представляет собой -Н, -галоген или -(C1-С 3)алкил (необязательно замещенный 1-3 атомами галогенов);R31 в каждом случае независимо представляет собой -Н, -галоген или -(C1-С 3)алкил иR41 в каждом случае независимо представляет собой -Н или -СН 3. В другом примере реализации данное изобретение обеспечивает соединение, структура которого-9 014718 представлена формулой (I), или его фармацевтически приемлемую соль, гдеR1 представляет собой где пунктирной линией обозначено место присоединения к положению R1 в формуле (I); где пунктирной линией обозначено место присоединения к положению R5 в формуле (I);-СН(С(О)ОН)(CH2OR ), -СН(С(О)ОН)(CH2N(R )(R , -(C1-С 3)алкил-С(О)O-R20, или где пунктирной линией обозначено место присоединения к положению, обозначенному R6; НЕТ 1 представляет собой где пунктирной линией обозначено место присоединения к положению, обозначенному НЕТ 1; НЕТ 2 представляет собой или где пунктирной линией обозначено место присоединения к положению, обозначенному НЕТ 2;R10 в каждом случае независимо представляет собой -Н или -галоген;R20 в каждом случае независимо представляет собой -Н или -(C1-С 3)алкил (необязательно замещенный 1-3 атомами галогенов);R21 в каждом случае независимо представляет собой -Н, -галоген или -(C1-С 3)алкил;R22 в каждом случае независимо представляет собой -Н или -(C1-С 3)алкил (необязательно замещенный 1-3 атомами галогенов);R23 в каждом случае независимо представляет собой -Н, -(С 1-С 3)алкил или -С(О)О-(С 1-С 4)алкил;R24 в каждом случае независимо представляет собой -Н, -галоген или -(С 1-С 3)алкил (необязательно замещенный 1-3 атомами галогенов);R31 в каждом случае независимо представляет собой -Н, -галоген или -(C1-С 3)алкил иR41 в каждом случае независимо представляет собой -Н или -СН 3. В другом примере реализации данное изобретение обеспечивает соединение, структура которого представлена формулой (I), или его фармацевтически приемлемую соль, гдеR1 представляет собой или где пунктирной линией обозначено место присоединения к положению R1 в формуле (I); где пунктирной линией обозначено место присоединения к положению R5 в формуле (I);-СН(С(О)ОН)(CH2OR ), -СН(С(О)ОН)(CH2N(R )(R , -(C1-С 3)алкил-С(О)O-R20, или где пунктирной линией обозначено место присоединения к положению, обозначенному R6; НЕТ 1 представляет собой где пунктирной линией обозначено место присоединения к положению, обозначенному НЕТ 1; НЕТ 2 представляет собой или где пунктирной линией обозначено место присоединения к положению, обозначенному НЕТ 2;R10 в каждом случае независимо представляет собой -Н или -галоген;R11 в каждом случае независимо представляет собой -Н или -СН 3;R20 в каждом случае независимо представляет собой -Н или -(С 1-С 3)алкил (необязательно замещенный 1-3 атомами галогенов);R21 в каждом случае независимо представляет собой -Н, -галоген или -(С 1-С 3)алкил;R22 в каждом случае независимо представляет собой -Н или -(C1-С 3)алкил (необязательно замещенный 1-3 атомами галогенов);R23 в каждом случае независимо представляет собой -Н, -(C1-С 3)алкил или -С(О)О-(С 1-С 4)алкил;R24 в каждом случае независимо представляет собой -Н;R31 в каждом случае независимо представляет собой -Н иR41 в каждом случае независимо представляет собой -Н. В другом примере реализации данное изобретение обеспечивает соединение, структура которого представлена формулой (I), или его фармацевтически приемлемую соль, где или где пунктирной линией обозначено место присоединения к положению R1 в формуле (I); где пунктирной линией обозначено место присоединения к положению R5 в формуле (I);R10 в каждом случае независимо представляет собой -Н или -галоген;R11 в каждом случае независимо представляет собой -Н;R20 в каждом случае независимо представляет собой -Н или -(C1-С 3)алкил (необязательно замещенный 1-3 атомами галогенов);R21 в каждом случае независимо представляет собой -Н, -галоген или -(C1-С 3)алкил;R22 в каждом случае независимо представляет собой -Н или -(C1-С 3)алкил (необязательно замещенный 1-3 атомами галогенов) иR23 в каждом случае независимо представляет собой -Н, -(С 1-С 3)алкил или -С(О)О-(С 1-С 4)алкил. В другом примере реализации данное изобретение обеспечивает соединение, структура которого представлена формулой (I), или его фармацевтически приемлемую соль, гдеR1 представляет собой или где пунктирной линией обозначено место присоединения к положению R1 в формуле (I); где пунктирной линией обозначено место присоединения к положению R5 в формуле (I);-СН(С(О)ОН)(CH2OR ), -СН(С(О)ОН)(CH2N(R )(R , -(C1-С 3)алкил-С(О)O-R20, или где пунктирной линией обозначено место присоединения к положению, обозначенному R6; НЕТ 1 представляет собой где пунктирной линией обозначено место присоединения к положению, обозначенному НЕТ 1; НЕТ 2 представляет собой или где пунктирной линией обозначено место присоединения к положению, обозначенному НЕТ 2;R11 в каждом случае независимо представляет собой -Н или -СН 3;R20 в каждом случае независимо представляет собой -Н или -(С 1-С 3)алкил (необязательно замещенный 1-3 атомами галогенов);R21 в каждом случае независимо представляет собой -Н, -галоген или -(C1-С 3)алкил;R22 в каждом случае независимо представляет собой -Н или -(C1-С 3)алкил (необязательно замещенный 1-3 атомами галогенов);R23 в каждом случае независимо представляет собой -Н, -(C1-С 3)алкил или -С(О)О-(С 1-С 4)алкил;R24 в каждом случае независимо представляет собой -Н;R31 в каждом случае независимо представляет собой -Н иR41 в каждом случае независимо представляет собой -Н. Обеспечены и другие примеры реализации данного изобретения, где каждый из описанных выше примеров реализации дополнительно ограничен, как это описано в последующих предпочтительных случаях. Конкретно, каждый из приведенных ниже предпочтительных случаев независимо объединен с каждым из вышеприведенных примеров реализации, и эта конкретная комбинация обеспечивает другой пример реализации, в котором переменные, указанные в предпочтительном случае, ограничены в соответствии с этим предпочтительным случаем. Предпочтительные примеры реализации данного изобретения структурно представлены формулой или Предпочтительно R1 представляет собой Предпочтительно R2 представляет собой -галоген, -СН 3 (необязательно замещенный 1-3 атомами галогенов) или -О-СН 3 (необязательно замещенный 1-3 атомами галогенов). Предпочтительно R2 представляет собой -галоген. Предпочтительно R2 представляет собой -СН 3 (необязательно замещенный 1-3 атомами галогенов). Предпочтительно R2 представляет собой -О-СН 3 (необязательно замещенный 1-3 атомами галогенов). Предпочтительно R2 представляет собой -хлор, -фтор или -бром. Предпочтительно Предпочтительно R5 представляет со Предпочтительно R5 представляет собой Предпочтительно R5 представляет собой представляет собой представляет собойR10 в каждом случае независимо представляет собой -Н или -галоген;R20 в каждом случае независимо представляет собой -Н или -(C1-С 3)алкил (необязательно замещенный 1-3 атомами галогенов);R21 в каждом случае независимо представляет собой -Н, -галоген или -(C1-С 3)алкил;R22 в каждом случае независимо представляет собой -Н или -(C1-С 3)алкил (необязательно замещенный 1-3 атомами галогенов) иR23 в каждом случае независимо представляет собой -Н, -(C1-С 3)алкил или -С(O)O-(C1-C4)алкил. Предпочтительно R5 представляет собойR10 в каждом случае независимо представляет собой -Н или -галоген. Предпочтительно R5 представляет собой где R8 представляет собой -(C1-С 3)алкил (необязательно замещенный 1-3 атомами галогенов). Предпочтительно R5 представляет собой Предпочтительно R5 представляет собой собой Предпочтительно R6 представляет собой -(C1-С 3)алкил (необязательно замещенный 1-3 атомами галогенов), -(C1-С 3)алкил-O-R20, -(C1-С 3)алкилпирролидинил, фенил, -НЕТ 1, -НЕТ 2, -СН 2-фенил, -СН 2 НЕТ 1, -СН 2-НЕТ 2, -(C1-С 3)алкил-N(R20)(R20), -(C1-С 3)алкил-N+(О-)(СН 3)2, -(C1-C3)алкил-C(O)N(R41)(R41),-СН(С(O)ОН)(CH2OR20), -СН(С(О)ОН)(CH2N(R20)(R20, -(C1-С 3)алкил-С(О)O-R20, или Предпочтительно R6 представляет собой -(C1-С 3)алкил (необязательно замещенный 1-3 атомами галогенов), -(C1-С 3)алкил-O-R20, -(C1-С 3)алкилпирролидинил, -(C1-С 3)алкил-N(R20)(R20), -(C1-С 3)алкилN+(O-)(СН 3)2, -(C1-С 3)алкил-С(O)N(R41)(R41), -СН(С(О)ОН)(CH2OR20), -СН(С(О)ОН)(CH2N(R20)(R20,-(C1-С 3)алкил-C(O)O-R20-СН 2-СН 3. В другом примере реализации данное изобретение обеспечивает соединение, структура которого представлена формулой (I), или его фармацевтически приемлемую соль, где или где пунктирной линией обозначено место присоединения к положению R1 в формуле (I); где пунктирной линией обозначено место присоединения к положению R5 в формуле (I);R6 представляет собой -Н, -СН 3, -СН 2-СН 3, -CH2-CF3, -С(СН 3)2, -СН 2-СН 2-ОН, -СН 2-СН 2-О-СН 3,-СН 2-СН 2-пирролидинил, -CH2-CH2-N(CH3)2, -CH2-CH2-NH2, -CH2-С(O)ОН, или где пунктирной линией обозначено место присоединения к положению, обозначенному R6;R20 в каждом случае независимо представляет собой -Н или -СН 3;R21 в каждом случае независимо представляет собой -Н или -фтор;R22 в каждом случае независимо представляет собой -Н, -СН 3 или -CF3 иR23 представляет собой -Н. Примеры реализации данного изобретения включают все стереоизомерные формы и конформационные формы соединений формулы (I) и более ограниченные примеры реализации, описанные выше. Предпочтительным вариантом реализации данного изобретения являются соединения, имеющие формулу 1-циклогексил-3-3,5-дихлор-4'-[4-(2-фторэтил)пиперазин-1-карбонил]бифенил-4 илметилпирролидин-2-он и (R)-3-[3,5-дихлор-4'-(4-трифторметилпиперидин-1-карбонил)бифенил-4 илметил]-1-(тетрагидропиран-4-ил)пирролидин-2-он. Еще один пример реализации настоящего изобретения относится к описанным в настоящем изобретении новым промежуточным соединениям, которые пригодны для получения ингибиторов 11HSD1 формулы (I) и описанных вариантов их реализации. Еще одним вариантом реализации данного изобретения являются описанные здесь новые промежуточные соединения, которые пригодны для получения 1-циклогексил-3-3,5-дихлор-4'-[4-(2 фторэтил)пиперазин-1-карбонил]бифенил-4-илметилпирролидин-2-она и(R)-3-[3,5-дихлор-4'-(4 трифторметилпиперидин-1-карбонил)бифенил-4-илметил]-1-(тетрагидропиран-4-ил)пирролидин-2-она или их фармацевтически приемлемой соли. У пациентов с диабетом 2 типа часто развивается "резистентность к инсулину", которая вызывает нарушение гомеостаза глюкозы и гипергликемию, что приводит к повышению процента смертности и преждевременным летальным исходам. Нарушение гомеостаза глюкозы связано с ожирением, гипертензией и с изменениями метаболизма липидов, липопротеинов и аполипопротеинов. У людей, страдающих диабетом 2 типа, имеется повышенный риск развития сердечно-сосудистых осложнений, например атеросклероза, коронарной болезни сердца, удара, заболевания периферических сосудов, гипертензии, нефропатии, невропатии и ретинопатии. Таким образом, терапевтический контроль гомеостаза глюкозы, метаболизма липидов, ожирения и гипертензии важен для ухода и лечения при сахарном диабете. Многие пациенты, у которых имеется резистентность к инсулину, но у которых не развился диабет 2 типа, также имеют риск развития "синдрома X" или "метаболического синдрома". Метаболический синдром характеризуется резистентностью к инсулину, наряду с брюшным ожирением, гиперинсулинемией, повышенным кровяным давлением, низким уровнем альфа-липопротеинов высокой плотности (ЛВП), высоким содержанием липопротеинов очень низкой плотности (ЛОНП), гипертензией, атеросклерозом, коронарной болезнью сердца и хронической почечной недостаточностью. У таких пациентов имеется повышенный риск развития сердечно-сосудистых осложнений, указанных выше, независимо от того, страдают ли они выраженным сахарным диабетом или нет. Благодаря способности соединений согласно настоящему изобретению ингибировать 11HSD1,они применимы для лечения широкого спектра патологических состояний и нарушений, при которых ингибирование 11HSD1 оказывает благоприятное действие. Такие нарушения и состояния в данном изобретении обозначены как "диабетические расстройства" и "нарушения, связанные с метаболическим синдромом". Специалист в данной области способен выявить "диабетические расстройства" и "нарушения, связанные с метаболическим синдромом" по вовлечению в патологический процесс активности 11-HSD1, либо в патофизиологию конкретного нарушения, либо в гомеостатический отклик на конкретное нарушение. Таким образом, соединения могут найти применение, например, для предотвращения,лечения или облегчения симптомов заболевания или патологического состояния или связанных с ним симптомов или осложнений "диабетических расстройств" и "нарушений, связанных с метаболическим синдромом."Диабетические расстройства" и "нарушения, связанные с метаболическим синдромом" включают,но не ограничены перечисленными, диабет 1 типа, диабет 2 типа, гипергликемию, гиперактивную инсулинемию, гамартию бета-клеток, усиление функции бета-клеток за счет возобновления первой фазы ответа, прандиальную гипергликемию, предотвращение апоптоза, нарушенную гликемию натощак (НГН),метаболический синдром, гипогликемию, гипер/гипокалиемию, стабилизацию уровня глюкагона, увеличение соотношения ЛНП/ЛВП, уменьшение аппетита, расстройства пищевого поведения, потерю веса,синдром поликистозных яичников (СКПЯ), ожирение вследствие диабета, латентный аутоиммунный диабет взрослых (LADA, latent autoimmune diabetes in adult), удар, трансплантацию островков, диабет детского возраста, гестационный диабет, поздние осложнения диабета, микро/макроальбуминурию, нефропатию, ретинопатию, невропатию, диабетические язвы стопы, снижение перистальтики кишечника вследствие введения глюкагона, синдром укороченной тонкой кишки, антидиарейное действие, усиление желудочной секреции, ослабление кровотока, эректильную дисфункцию, глаукому, постхирургический- 18014718 стресс, улучшение повреждений тканей органов, вызванных реперфузией кровотока после ишемической болезни, ишемическую болезнь сердца, сердечную недостаточность, застойную сердечную недостаточность, удар, инфаркт миокарда, аритмию, преждевременную смерть, антиапоптотическое действие, заживляемость ран, нарушение толерантности к глюкозе, синдромы инсулиновой резистентности, метаболический синдром, синдром X, гиперлипидемию, дислипидемию, гипертриглицеридемию, гиперлипопротеинемию, гиперхолестеролемию, артериосклероз, в том числе атеросклероз, глюкагоному, острый панкреатит, сердечно-сосудистые заболевания, гипертензию, сердечную гипертрофию, желудочнокишечные заболевания, ожирение, диабет, обусловленный ожирением, диабетическую дислипидемию и т.п. Таким образом, настоящее изобретение также обеспечивает способ лечения "диабетических нарушений" и "нарушений, связанных с метаболическим синдромом", который при этом уменьшает и/или устраняет один или более из нежелательных побочных эффектов, ассоциированных с существующими в настоящее время способами лечения. Кроме того, настоящее изобретение обеспечивает соединение формулы (I) или его фармацевтическую соль, фармацевтическую композицию, содержащую соединение формулы (I) или его фармацевтическую соль, и фармацевтически приемлемый носитель, растворитель или эксципиент: для применения для ингибирования активности 11HSD1; для применения для ингибирования обусловленных активностью 11HSD1 откликов клеток у млекопитающих; для применения для снижения уровня глюкозы у млекопитающего; для применения при лечении заболевания, вызванного избыточной активностью 11-HSD1; для применения при лечении диабетических и других связанных с метаболическим синдромом нарушений у млекопитающих и для применения при лечении диабета, метаболического синдрома, ожирения, гипергликемии, атеросклероза, ишемической болезни сердца, удара, невропатии и заживления ран. Таким образом, способы согласно настоящему изобретению охватывают профилактическое и терапевтическое введение соединения формулы (I). Настоящее изобретение, кроме того, обеспечивает применение соединения формулы (I) или его фармацевтической соли для производства лекарственного средства для ингибирования активности 11-HSD1; для производства лекарственного средства для ингибирования связанного с активностью 11-HSD1 откликов клеток у млекопитающих, для производства лекарственного средства для снижения уровня глюкозы у млекопитающих; для производства лекарственного средства для лечения заболевания,вызванного избыточной активностью 11HSD1; для производства лекарственного средства для лечения диабетических расстройств и других нарушений, связанных с метаболическим синдромом у млекопитающих; и для производства лекарственного средства для предотвращения или лечения диабета, метаболического синдрома, ожирения, гипергликемии, атеросклероза, ишемической болезни сердца, удара,невропатии и плохой заживляемости ран. Настоящее изобретение, кроме того, обеспечивает способ лечения у млекопитающих патологических состояний, обусловленных избыточной активностью 11HSD1; способ ингибирования активности 11HSD1 у млекопитающих; способ ингибирования клеточных откликов, связанных с активностью 11-HSD1 у млекопитающих; способ снижения уровня глюкозы у млекопитающих; способ лечения диабетических и других связанных с метаболическим синдромом нарушений у млекопитающих; способ предотвращения или лечения диабета, метаболического синдрома, ожирения, гипергликемии, атеросклероза,ишемической болезни сердца, удара, невропатии и плохой заживляемости ран; при этом вышеуказанные способы включают введение млекопитающему, нуждающемуся в таком лечении, количества соединения формулы (I) или его фармацевтически приемлемой соли; или фармацевтической композиции, содержащей соединение формулы (I) или его фармацевтическую соль и фармацевтически приемлемый носитель,растворитель или эксципиент, ингибирующего активность 11HSD1. Кроме того, настоящее изобретение обеспечивает фармацевтическую композицию, которая содержит соединение формулы (I) или его фармацевтическую соль и фармацевтически приемлемый носитель,растворитель или эксципиент, предназначенную для применения для ингибирования активности 11-HSD1; предназначенную для применения для ингибирования клеточных откликов, связанных с активностью 11HSD1; предназначенную для применения для снижения уровня глюкозы у млекопитающих; предназначенную для применения для лечения диабетических и других связанных с метаболическим синдромом нарушений у млекопитающих и предназначенную для применения для предотвращения или лечения диабета, метаболического синдрома, ожирения, гипергликемии, атеросклероза, ишемической болезни сердца, удара, невропатии и плохой заживляемости ран. В другом аспекте изобретения соединения по данному изобретению вводят в комбинации с одним или более дополнительным активным веществом в любых подходящих соотношениях. Такие дополнительные активные вещества могут быть выбраны, например, из антидиабетических средств, средств против ожирения, средств против повышенного давления, средств для лечения осложнений, вызванных диабетами или связанных с ними, и средств для лечения осложнений и нарушений, вызванных ожирением или связанных с ним. Ниже перечислены несколько групп комбинаций. Очевидно, что каждый из упомянутых агентов может быть объединен с другими упомянутыми агентами с получением дополнительных комбинаций.- 19014718 Таким образом, в дальнейших примерах реализации данного изобретения настоящие соединения можно вводить в комбинации с одним или более антидиабетических средств. Подходящие антидиабетические средства включают инсулин, аналоги и производные инсулина, например, описанные в ЕР 792290 (Novo Nordisk A/S), например NВ 29-тетрадеканоил дес (В 30) инсулин человека, ЕР 214826 и ЕР 705275 (Novo Nordisk A/S), например инсулин человека AspB28, US 5504188 (EliLilly), например инсулин человека LysB28 ProB29, ЕР 368187 (Aventis), например, Lantus, GLP-1 и производные GLP-1, например, описанные в WO 98/08871 (Novo Nordisk A/S), а также активные при пероральном введении соединения, понижающие уровень сахара в крови. Активные при пероральном введении соединения, понижающие уровень сахара в крови, предпочтительно включают имидазолины, сульфонилмочевины, бигуаниды, меглитиниды, оксадиазолидиндионы, тиазолидиндионы, сенсибилизаторы инсулина, средства, усиливающее секрецию инсулина, такие как глимепирид, ингибиторы -глюкозидазы, агенты, воздействующие на АТФ-зависимый калиевый канал-клеток, например деблокаторы калиевого канала, например, описанные в WO 97/26265,WO 99/03861 и WO 00/37474 (Novo Nordisk A/S), или митиглинид, или такие блокаторы калиевого канала, как BTS-67582, натеглинид, антагонисты глюкагона, например, такие как описаны в WO 99/01423 иWO 03/00262, WO 03/00267 и WO 03/15774 (AstraZeneca), ингибиторы GSK-3 (гликогенсинтазкиназы-3),соединения, модифицирующие метаболизм липидов, например противолипидемические агенты, такие как ингибиторы HMG СоА (статины), соединения, снижающие потребление пищи, лиганды PPAR (рецептора, активируемого пролифератором пероксисом), включая подтипы альфа-PPAR, гамма-PPAR и дельта-PPAR, и агонисты RXR (ретиноидного рецептора X), такие как ALRT-268, LG-1268 или LG-1069. В другом примере реализации соединения по данному изобретению вводят в комбинации с инсулином или аналогом или производным инсулина, например NВ 29-тетрадеканоил дез (В 30) инсулином человека, инсулином человека AspB28, инсулином человека LysB28 ProB29, Lantus, или смешанным препаратом, включающим одно или более из перечисленных средств. В другом примере реализации данного изобретения соединения вводят в комбинации с сульфонилмочевиной, например глибенкламидом, глипизидом, толбаутамидом, хлоропамидемом, толазамидом,глимепридом, гликазидом и глибуридом. В другом примере реализации данного изобретения соединения вводят в комбинации с бигунидом,например метформином. В еще одном примере реализации данного изобретения соединения вводят в комбинации с меглитинидом, например репаглинидом или натеглинидом. В еще одном примере реализации данного изобретения соединения вводят в комбинации с тиазолидиндионовым сенсибилизатором инсулина, например троглитазоном, циглитазоном, пиоглитазоном, розиглитазоном, изаглитазоном, дарглитазоном, энглитазоном, CS-011/CI-1037 или Т 174, или соединениями, описанными в WO 97/41097, WO 97/41119, WO 97/41120, WO 00/41121 и WO 98/45292 (Dr. Reddy'sResearch Foundation). В еще одном примере реализации данного изобретения соединения можно вводить в комбинации с сенсибилизатором инсулина, таким как, например, GI 262570, YM-440, МСС-555, JTT-501, AR-H039242,KRP-297, GW-409544, CRE-16336, AR-H049020, LY510929, МВХ-102, CLX-0940, GW-501516, или с соединениями, описанными в WO 99/19313, WO 00/50414, WO 00/63191, WO 00/63192, WO 00/63193, например рагаглитазаром (NN 622 или (-)DRF 2725) (Dr. Reddy's Research Foundation) и WO 00/23425,WO 00/23415, WO 00/23451, WO 00/23445, WO 00/23417, WO 00/23416, WO 00/63153, WO 00/63196,WO 00/63209, WO 00/63190 и WO 00/63189 (Novo Nordisk A/S). В дополнительном примере реализации данного изобретения данные соединения вводят в комбинации с ингибитором -глюкозидазы, например воглибозом, эмиглитатом, миглитолом или акарбозой. В другом примере реализации данного изобретения данные соединения вводят в комбинации с агентом, действующим на АТФ-зависимые калиевые каналы -клеток, например толбутамидом, глибенкламидом, глипизидом, гликазидом, BTS-67582 или репаглинидом. В еще одном примере реализации данного изобретения данные соединения вводят в комбинации с натеглинидом. В еще одном примере реализации данного изобретения данные соединения вводят в комбинации с противолипидемическим агентом или антигиперлипидемическим агентом, например холестирамином,колестиполом, клофибратом, гемфиброзилом, ловастатином, правастатином, симвастатином, питавастатином, розувастином, пробуколом, декстротироксином, фенофибратом или аторвастином. В еще одном примере реализации данного изобретения данные соединения вводят в комбинации с соединениями, уменьшающими потребление пищи.- 20014718 В другом примере реализации данного изобретения данные соединения вводят в комбинации более чем с одним из вышеуказанных соединений, например в комбинации с метформином и сульфонилмочевиной, например глибуридом; сульфонилмочевиной и акарбозой; натеглинидом и метформином; репаглинидом и метформином, акарбозой и метформином; сульфонилмочевиной, метформином и троглитазоном; инсулином и сульфонилмочевиной; инсулином и метформином; инсулином, метформином и сульфонилмочевиной; инсулином и троглитазоном; инсулином и ловастатином и т.п. Общие термины, используемые для описания соединений в данном патенте, имеют общепринятые значения. При использовании в данном изобретении термины "(C1-С 3)алкил", "(С 1-С 4)алкил" или "(C1C6)алкил" обозначают насыщенные алифатические группы с неразветвленной или разветвленной цепью,с указанным количеством атомов углерода, например метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил и т.п. Термин "(C1-C6)алкокси" обозначает группу С 1-С 6-алкила, присоединенную через кислород, и включает такие группы, как, например, метокси, этокси, н-пропокси, изопропокси и т.п. Термин "галоген" относится к фтору, хлору, брому и йоду. Термин "(С 3-C8)циклоалкил" относится к насыщенному или частично насыщенному карбоциклическому кольцу, включающему от 3 до 8 атомов углерода, как правило, от 3 до 7 атомов углерода. Примеры (С 3-C8)циклоалкилов включают, но не ограничены перечисленными, циклопропил, циклобутил, циклопентил, циклогексил, циклогептил и т.п. Термин "необязательно замещенный" или "необязательные заместители" при использовании в данном патенте означает, что описываемые группы либо не имеют заместителей, либо имеют один или более заместителей. Если описываемые группы имеют более чем один заместитель, заместители могут быть одинаковыми или различными. Кроме того, при использовании терминов "независимо," "независимо представляют собой" и "независимо выбраны из" подразумевается, что описываемые группы могут быть одинаковыми или различными. Некоторые из терминов, которым даны определения в данном изобретении, могут неоднократно встречаться в описании структурных формул и в таком случае каждый термин определяется независимо от другого. Следует понимать, что морские свинки, собаки, кошки, крысы, мыши, хомяки и приматы, включая человека, представляют собой примеры пациентов в пределах значения термина "пациент". Предпочтительным пациентом является человек. Термин "пациент" включает домашний скот. К домашнему скоту относятся животные, выращиваемые для продовольственных целей. Примерами домашнего скота являются жвачные животные или "жвачные", например коровы, быки, телки, волы, овцы, буйволы, бизоны,козлы и антилопы. Другие примеры домашнего скота включают свиней и птиц (домашняя птица), таких как цыплята,утки, индейки и гуси. Пациент, подлежащий лечению, предпочтительно представляет собой млекопитающее, в частности человека. Термины "лечение" и "лечить" при использовании в данном изобретении включают их общепринятые значения, т.е. наблюдение и уход за пациентом с целью предотвращения, уменьшения риска появления или развития данного патологического состояния или заболевания, запрещения, сдерживания, облегчения, улучшения, замедления, остановки, задержки или уменьшения прогрессирования или тяжести заболевания и удерживания под контролем и/или лечения существующих признаков болезни, нарушения или патологического состояния, описанного в данном изобретении, включая ослабление или облегчение симптомов или осложнений или лечение или устранение заболевания, нарушения или патологического состояния. Настоящий способ включает как медицинское терапевтическое, так и/или профилактическое лечение при необходимости. При использовании в данном изобретении термин "терапевтически эффективное количество" обозначает количество соединения по данному изобретению, которое способно облегчать симптомы описанных здесь различных патологических состояний. Конкретная доза вводимого соединения по данному изобретению, несомненно, определяется конкретными обстоятельствами, в том числе, например, вводимым соединением, способом введения, общим состоянием пациента и патологическим состоянием, подлежащим лечению."Композиция" обозначает фармацевтическую композицию и охватывает фармацевтический продукт, включающий активный компонент (компоненты), включающий соединение (соединения) формулы(I), и инертный компонент (компоненты), формирующий носитель. Таким образом, фармацевтические композиции настоящего изобретения охватывают любую композицию, полученную путем смешивания соединения настоящего изобретения и фармацевтически приемлемого носителя. Термин "по существу чистый" относится к чистой кристаллической форме соединения, включающей более чем примерно 90% желаемой кристаллической формы и предпочтительно более чем примерно 95% желаемой кристаллической формы. Термин "подходящий растворитель" относится к любому растворителю или смеси растворителей,инертных по отношению к протекающей реакции, который переводит в раствор активные вещества в достаточной степени для обеспечения среды, в которой осуществляется желаемая реакция. Термин "единичная дозированная форма" обозначает физически дискретные единицы, применимые в виде единичных дозировок для человека и других животных, помимо человека, содержащие заданное- 21014718 количество активного вещества, рассчитанное так, что в сочетании с подходящим фармацевтическим носителем оно вызывает желаемый терапевтический эффект. Соединения по данному изобретению могут иметь один или более хиральный центр и могут существовать в различных стереоизомерных конфигурациях. Вследствие наличия хиральных центров соединение по данному изобретению может быть представлено в виде рацемической смеси, в виде энантиомеров или смеси энантиомеров, а также в виде диастереомеров и смеси диастереомеров. Все рацемические смеси, энантиомеры, диастереомеры и смеси находятся в пределах объема настоящего изобретения, находятся ли они в чистом виде, в существенной степени чистом или в виде неочищенной смеси. В примерах, представленных в данном изобретении, в случае если представлена молекула, содержащая хиральный центр или центры с известной конфигурацией, ее стереохимическая структура обозначена в названии и в структурном изображении молекулы. Если стереохимическая структура молекулы не известна или не определена в названии и в структурном обозначении молекулы, стереохимическую структуру не указывают. Примеры реализации данного изобретения включают примеры, представленные в данном изобретении, и хотя представленные в примерах соединения (или их соли) могут иметь одну хиральную или конформационную форму, дополнительные варианты реализации изобретения включают все другие стереоизомеры и конформационные формы описанных в примерах соединений, а также их фармацевтически приемлемые соли. Такие примеры реализации включают любые изолированные энантиомеры, диастереомеры и/или конформационные варианты таких структур, а также любые смеси, содержащие более одной формы. Кроме того, если в молекуле присутствует двойная связь или полностью или частично насыщенная кольцевая система, или присутствует более одного центра асимметрии, или связь с ограниченным вращением, могут образовываться диастереомеры. Предполагают, что любые диастереомеры, в виде выделенных, очищенных или частично очищенных диастереомеров, или их смеси включены в объем данного изобретения. Кроме того, некоторые соединения по данному изобретению могут существовать в различных таутомерных формах, и предполагают, что любые таутомерные формы, которые могут образовывать соединения по данному изобретению, включены в объем настоящего изобретения. Термин "энантиомерное обогащение" при использовании в данном изобретении относится к увеличению количества одного энантиомера по сравнению с другим. Удобным методом выражения достигнутого энантиомерного обогащения является понятие энантиомерного избытка, или "ее" (enantiomeric excess), который определяют с использованием следующего уравнения: где Е 1 представляет собой количество первого энантиомера, а Е 2 представляет собой количество второго энантиомера. Таким образом, если исходное соотношение двух энантиомеров составляет 50:50,как, например, в рацемической смеси, и получают энантиомерное обогащение, достаточное для получения конечного соотношения 70:30, то "ее" относительно первого энантиомера составляет 40%. При этом,если конечное соотношение составляет 90:10, "ее" в отношении первого энантиомера составляет 80%. Значение "ее" более 90% является предпочтительным, более предпочтительным является "ее" более 95% и особенно предпочтительным является "ее" более 99%. Энантиомерное обогащение может быть легко определено специалистом в данной области с использованием стандартных способов и процедур, например газовой хроматографии или высокоэффективной жидкостной хроматографии с хиральной колонкой. Выбор подходящей хиральной колонки, элюента и условий, необходимых для осуществления разделения энантиомерных пар, находится в пределах компетенции специалиста в данной области. Кроме того, некоторые стереоизомеры и энантиомеры соединений формулы (I) могут быть получены специалистом в данной области с использованием хорошо известных методик и способов, например, таких как описаны вS.H. Wilen, "Stereochemistry of Organic Compounds" (Wiley-Interscience 1994), и европейской заявке на патентEP-А-838448, опубликованной 29 апреля 1998 г. Примеры способов разделения включают методы перекристаллизации или хиральную хроматографию. Соединения формулы (I) могут быть получены специалистом в данной области на основании ряда процедур, некоторые из которых проиллюстрированы в изложенных ниже способах и схемах. Конкретный порядок стадий, необходимых для получения соединения формулы (I), зависит от конкретного синтезируемого соединения, исходного вещества и относительной лабильности замещенных групп. Реагенты или исходные вещества доступны для специалиста в данной области, и в тех случаях, когда они не являются коммерчески доступными, они могут быть легко синтезированы специалистом в данной области на основании стандартных процедур, обычно применяемых в данной области, наряду с различными способами и схемами, изложенными ниже. Следующие схемы, препараты, примеры и способы представлены для лучшего объяснения практической стороны данного изобретения, и они никоим образом не ограничивают объем изобретения. Как ясно специалисту в данной области, возможны различные модификации, не выходящие за пределы сущности и объема изобретения. Все публикации, упомянутые в описании, свидетельствуют об уровне спе- 22014718 циалистов в области, к которой относится изобретение. Оптимальное время проведения реакций, представленных в схемах, примерах, описаниях получения препаратов и способах, можно определить путем наблюдения за протеканием реакции с помощью стандартных хроматографических методов. Кроме того, предпочтительно проведение реакций по данному изобретению в инертной атмосфере, такой как, например, аргоновой, азотной. Выбор растворителя,как правило, не является критичным при условии, что используемый растворитель является инертным по отношению к протекающей реакции и в достаточной степени переводит реагенты в раствор, чтобы могла проходить желаемая реакции. Соединения предпочтительно выделяют и очищают перед их применением в последующих реакциях. Некоторые соединения могут быть выкристаллизованы из реакционного раствора и затем собраны путем фильтрации или реакционный растворитель может быть удален путем экстракции, выпаривания или декантацией. Промежуточные и конечные продукты формулы (I) могут быть дополнительно очищены, если необходимо, с применением стандартных способов, например перекристаллизации или хроматографии на твердых носителях, таких как силикагель или оксид алюминия. Специалисту в данной области понятно, что не все заместители совместимы со всеми условиями реакции. Такие соединения могут быть защищены или модифицированы на подходящем этапе синтеза способами, хорошо известными в данной области. Термины и сокращения, используемые в настоящих схемах, описаниях получения соединений,примерах и способах, имеют общепринятые значения, если это не определено иначе. Например, при использовании в данном изобретении следующие термины имеют указанное значение: "экв." означает эквиваленты; "фунтов/кв.дюйм" ("psi") означает фунты на квадратный дюйм; "мин" обозначает минуты;"ч" обозначает часы; "ТСХ" обозначает тонкослойную хроматографию; "ВЭЖХ" относится к высокоэффективной жидкостной хроматографии; "Rf" относится к фактору удерживания; "Rt" относится к времени удерживания; относится к химическом сдвигу в миллионных долях (м.д.) по традиционной для ЯМР шкале относительно тетраметилсилана; "МС" обозначает масс-спектрометрию, наблюдаемую массу обозначают как [М+Н], если не указано иначе; "MS (FD)" относится к описанию области массспектрометрии; "MS (IS)" относится к масс-спектрометрии с ионным распылением; "Масс-спектр (ионное распыление)" относится к способу ионизации посредством ионного распыления; "MS (FIA)" относится к масс-спектрометрическому анализу с введением потока; "MS (FAB)"относится к массспектрометрии с бомбардировкой быстрыми атомами; "MS (EI)" относится к масс-спектрометрии с электронным ударом; "MS (ES)" относится к масс-спектрометрии с распылением электронов; "MS (EI+)" относится к масс-спектрометрии с электронным ударом при ионизации электрораспылением; "MS (ES+)" относится к масс-спектрометрии с ионизацией электрораспылением; "MS (APCi)" относится к массспектрометрии с химической ионизацией при атмосферном давлении; "УФ" относится к ультрафиолетовой спектрометрии; 1 Н ЯМР" относится к спектрометрии протонного ядерного магнитного резонанса;"LC-MS" относится к жидкостной хроматографии, завершающейся масс-спектрометрией; "GC/MS" относится к газовой хроматографии, завершающейся масс-спектрометрией; "ИК" относится к инфракрасной спектрометрии, для ИК-спектров приведены только максимумы поглощения, представляющие интерес, а не все наблюдаемые максимумы; "КТ" относится к комнатной температуре; "ТГФ (THF)" относится к тетрагидрофурану; "ЛАГ (LAH)" относится к алюмогидриду лития; "ЛДА (LDA)" обозначает диизопропиламид лития; "ДМСО (DMSO)" обозначает диметилсульфоксид; "ДМФ (DMF)" обозначает диметилформамид; "EtOAc" относится к этилацетату; "Pd-C" относится к палладию на углероде; "ДХМ (DCM)" имеет отношение к дихлорметану; "ДМАП (DMAP)" относится к диметиламинопиридину; "Li-ГМДС- 23014718 обозначает т-бутоксикарбонил; в структурных формулах "Ph" относится к фенилу; "Me" относится к метилу; "Et" обозначает этил; "Bn" обозначает бензил; "МеОН" обозначает метанол; "OTf" относится к трифторметансульфонат; "TIPSO" относится к триизопропилсиланилокси; "TBSO" обозначает третбутилдиметилсиланилокси. Примеры, представленные в данном патенте, иллюстрируют настоящее изобретение, но никоим образом не ограничивают объем настоящего изобретения. Названия промежуточных соединений и соединений из примеров получены с использованием программ AutoNom 2.2 в ChemDraw Ultra или AutoNom 2000 в MDL ISIS/Draw версии 2.5 SP1 от MDL Information Systems, Inc. или получены с помощью Chemical Abstracts Services. Для получения спектров 1 Н ЯМР с использованием указанных растворителей применяли спектрометр Varian INOVA 400 МГц. Прибор Agilent HP1100, оснащенный масс-спектрометром (Agilent MSDSL), применяли для LC-MS. Waters Xterra C18 (2,150 мм, 3,5 мкм) применяли в качестве стационарной фазы, стандартная методика включала использование элюента переменного состава 5-100% ацетонитрил/метанол (50:50) с 0,2% формиатом аммония в течение 3,5 мин, затем - 100% В в течение 0,5 мин при температуре колонки 50 С и скорости потока 1,0 мл/мин. Другой стандартный метод включал использование элюента переменного состава 5-100% ацетонитрил/метанол (50:50) с 0,2% формиатом аммония в течение 7,0 мин, затем - 100% В в течение 1,0 мин при температуре колонки 50 С и скорости потока 1,0 мл/мин. Дополнительный анализ методом МС с помощью Agilent MSD (замкнутая система) включал стандартный проточно-инжекционный анализ (ПИА) без применения колонки при скорости потока 0,5 мл/мин 80% МеОН с 6,5 мМ ацетатом аммония и времени пробега 30 с. Схема А В схеме А необязательно замещенный фенол 1 "защищают" (вводят защитную группу, например, с помощью TBSCl) с образованием соединения 2, затем соединение 2 преобразуют в альдегид 3. Соединение 3 реагирует с соединением, содержащим защитную группу (Pg) и уходящую группу (Lg) с образова- 24014718 нием эфирного соединения 4. Pg может представлять собой -СН 3 или -СН 2-фенил, a Lg может представлять собой мезилат или галоген. Предпочтительно соединение Lg-Pg представляет собой I-СН 3 или BrСН 2-фенил. Альдегид восстанавливают с образованием спирта 5, а затем преобразуют в соединение 6,подходящая форма которого может быть использована для взаимодействия с соединением 7. Предпочтительно соединение 5 галогенируют с помощью PBr3 с образованием 2-бром-метил-соединений. Проводят реакцию лактама 7 с основанием, например LDA, n-BuLi или трет-бутоксидом калия (предпочтительноLDA), а затем его алкилируют в апротонном растворителе (предпочтительно THF) соединением 6 с получением соединения 8. С соединения 8 снимают защиту подходящим способом, например используяBBr3 или водород с катализатором, с образованием фенола 9. Соединение 9 превращают в 10 путем проведения реакции с трифторметансульфоновым ангидридом и основанием, например, пиридином. С участием 10 проводят реакцию соединения, используя в качестве реагента фенилбороновую кислоту и катализатор, например тетракис-трифенилфосфин палладия. Фенилбороновая кислота может представлять собой п-карбоксифенилбороновую кислоту или пкарбоксиметилфенилбороновую кислоту. Если применяют п-карбоксифенилбороновую кислоту, получают соединение 12. Однако, если применяют п-карбоксиметилфенилбороновую кислоту, получают соединение 11. Таким образом, необходимо провести гидролиз метилового эфира с использованием соответствующего основания, например гидроксида калия. Амид Ia можно получить с использованием методики проведения реакции соединения, как это описано в методике проведения реакции соединения 1, 2, 3 или 4 в препаративных примерах и примерах. Введение и удаление защитных групп из соединений с образованием соединения формулы Ia и других хорошо известны специалистам в данной области и описаны в литературе (например, см. Greene and В схеме В амид Ib можно получить из соединения 10 путем проведения реакции с необязательно замещенной 4-цианофенилбороновой кислотой с образованием соединения 13. Соединение 13 затем окисляют с получением амида Ib. Схема С В схеме С соединение 10 можно превратить в Ic в одну стадию с применением катализатора (например, палладия), п-хлоркарбонилфенилбороновой кислоты, основания и амина в подходящем растворителе, например в диметоксиэтане. Препаративный пример 1. 2,6-Дихлор-4-гидроксибензальдегид. Растворяют 3,5-дихлорфенол (1 кг, 6,13 моль) в 3 л диметилформамида (ДМФ) и охлаждают до 0 С. Добавляют имидазол (918,74 г, 6,75 моль), а затем хлорид тетрабутилдиметилсилила (1017,13 г,6,75 моль). Нагревают смесь до комнатной температуры и перемешивают в течение 15 мин. Выливают в воду (6 л) и экстрагируют эфиром (4 л). Дважды промывают органический слой водой, затем 10% водным раствором хлорида лития и солевым раствором перед сушкой над сульфатом натрия. Фильтруют и концентрируют под вакуумом с получением трет-бутил(3,5-дихлорфенокси)диметилсилана (1700 г) в виде масла. Растворяют трет-бутил(3,5-дихлорфенокси)диметилсилан (425 г, 1,5 моль) в 4 л сухого тетрагидрофурана и охлаждают до -68 С. Медленно добавляют 1,1 эквивалент втор-бутиллития (103,1 г, 1,61 моль) при -68 С (1,75 ч). После завершения добавления перемешивают реакционную смесь при-70 С в тече- 25014718 ние 30 мин. Добавляют диметилформамид (168,5 г, 2,3 моль) и перемешивают реакционную смесь при 70 С в течение 1 ч. Добавляют 1 М соляную кислоту в воде (3,5 л) и дают реакционной смеси нагреться до комнатной температуры. Выливают реакционную смесь в эфир (5 л), промывают водой, затем солевым раствором. Сушат над сульфатом натрия и концентрируют под вакуумом до оранжевого твердого вещества. Растирают в порошок с холодным дихлорметаном и фильтруют с получением 250 г (80%) бледно-желтого твердого вещества. Препаративный пример 2. 2,6-Дихлор-4-метоксибензальдегид. Соединяют 2,6-дихлор-4-гидроксибензальдегид (120 г, 628,24 ммоль) и карбонат калия (173,65 г,1256,5 ммоль) в 900 мл диметилформамида и обрабатывают (107 г, 753,9 ммоль). Перемешивают реакционную смесь при комнатной температуре в течение 3 ч. Отфильтровывают твердое вещество и выливают в 6 л воды. Фильтруют твердое вещество, промывают несколько раз водой, сушат на воздухе и растворяют в этилацетате. Промывают водой, а затем солевым раствором, после чего сушат над сульфатом натрия. Фильтруют и концентрируют под вакуумом до объема 100 мл; в этот момент твердое вещество начинает разламываться. Затем отфильтровывают концентрат от фильтрата с получением второй партии. Промывают гексаном, объединяют все твердое вещество и сушат под вакуумом с получением 112,3 г грязно-белого твердого вещества. 1 Н ЯМР (400 МГц, CDCl3)10,41 (с, 1 Н), 6,90 (с, 2 Н), 3,87 (с, 3 Н). Препаративный пример 3. 2,6-Дихлор-4-бензилоксибензальдегид. Обрабатывают смесь 2,6-дихлор-4-гидроксибензальдегида (250 г, 1,3 моль) и карбоната калия(361,8 г, 2,62 моль) в 2 л диметилформамида бромистым бензилом (268,64 г, 1,57 моль). Перемешивают реакционную смесь при комнатной температуре в течение 1 ч. Отфильтровывают твердые вещества и выливают в 12 л воды. Отфильтровывают твердые вещества, промывают несколько раз водой, сушат на воздухе и растворяют в этилацетате. Сушат над сульфатом магния, фильтруют и концентрируют под вакуумом до 1,5 л. Дают осадиться в течение ночи и затем фильтруют. Промывают твердое вещество минимальным количеством гексана и сушат под вакуумом. Концентрируют фильтрат под вакуумом и растирают в порошок с гексаном с получением второй партии продукта, который при объединении с первой партией составляет 245 г белых кристаллов. Повторяют эти операции для получения третьей партии в 80 г в виде светло-красно-коричневого порошка (общий выход 88). 1 Н ЯМР (400 МГц, ДМСО-d6)10,26 (с, 1 Н), 7,43 (м, 5 Н), 7,28 (с, 2 Н), 5,25 (с, 2 Н). Препаративный пример 4.(2,6-Дихлор-4-метоксифенил)метанол. Суспендируют 2,6-дихлор-4-метоксибензальдегид (112 г, 546 ммоль) в 1500 мл этанола и охлаждают в ледяной бане до 7 С. Добавляют боргидрид натрия (20,67 г, 546 ммоль) порциями с получением раствора. Убирают ледяную баню и перемешивают в течение 2 ч. Осторожно добавляют реакционную смесь к насыщенному раствору хлорида аммония (4 л) и перемешивают до полного прекращения реакции. Экстрагируют дихлорметаном (31 л) и сушат объединенные органические экстракты над сульфатом натрия. Фильтруют и концентрируют под вакуумом с получением 113 г светло-красно-коричневого твердого вещества. 1 Н ЯМР (400 МГц, CDCl3)6,86 (с, 2 Н), 4,86 (с, 2 Н), 3,78 (с, 3 Н), 2,07 (с, 1 Н). Препаративный пример 5.(2,6-Дихлор-4-бензилоксифенил)метанол. Указанное соединение получают, по существу, так же, как получали препаративный пример 4. 1 Н ЯМР (ДМСО-d6)7,38 (м, 4 Н), 7,33 (м, 1 Н), 7,12 (с, 2 Н), 5,14 (с, 2 Н), 5,05 (т, 1 Н), 4,59 (д, 2 Н). Препаративный пример 6. 2-Бромметил-1,3-дихлор-5-метоксибензол. Растворяют (2,6-дихлор-4-метоксифенил)метанол (113 г, 545,76 ммоль) в 1200 мл сухого ТГФ и охлаждают до 0 С в атмосфере азота. Добавляют PBr3 (59,1 г, 218,3 ммоль) в атмосфере азота и перемешивают при 0 С в течение 30 мин. Выливают в насыщенный водный раствор NaHCO3 и экстрагируютEtOAc. Сушат и концентрируют под вакуумом с получением 129,4 г продукта в виде грязно-белого твердого вещества. ЯМР (CDCl3)6,88 (с, 2 Н), 4,73 (с, 2 Н), 3,79 (с, 3 Н). Препаративный пример 7. 2-Бромметил-1,3-дихлор-5-бензилоксибензол. Указанное соединение получают, по существу, так же, как получали препаративный пример 6, с выходом 89%. ES MS (m/z): 347 (М+1). Препаративный пример 8. 1-Циклогексил-3-(2,6-дихлор-4-метоксибензил)пирролидин-2-он. Растворяют имеющийся в продаже 1-циклогексилпирролидин-2-он (88,2 г, 527,9 ммоль) в 2500 мл- 26014718 тетрагидрофурана и охлаждают до -78 С. Добавляют 176 мл 2 М LDA и перемешивают в течение 5 мин. Добавляют 2-бромметил-1,3-дихлор-5-метоксибензол (95 г, 351,9 ммоль) и позволяют реакционной смеси нагреться до комнатной температуры. Выливают смесь в насыщенный раствор хлорида аммония и дважды экстрагируют дихлорметаном. Сушат над сульфатом натрия, фильтруют и концентрируют под вакуумом с получением красно-коричневого твердого вещества. Добавляют смесь гексанов и интенсивно перемешивают перед фильтрованием. Осадок на фильтре несколько раз промывают холодным гексаном с получением 86 г (69%) светло-красно-коричневого твердого вещества: MS (m/z): 356 (М+). Препаративный пример 9. 1-Циклогексил-3-(2,6-дихлор-4-гидроксибензил)пирролидин-2-он. Растворяют 1-циклогексил-3-(2,6-дихлор-4-метоксибензил)пирролидин-2-он (86 г, 241,4 ммоль) в 1300 мл дихлорметана, затем охлаждают до 0 С в атмосфере азота. К перемешиваемому холодному раствору медленно добавляют BBr3 (120,9 г, 482,75 ммоль), поддерживая внутреннюю температуру ниже 3,5 С. Перемешивают раствор в холодном состоянии в течение 2 ч, затем выливают в 4 л насыщенного раствора бикарбоната натрия и интенсивно перемешивают в течение 20 мин. Фильтруют и промывают твердое вещество водой, затем сушат на воздухе на воронке. Отделяют органическую часть фильтрата и промывают водой, а затем солевым раствором. Сушат над сульфатом натрия, фильтруют и концентрируют под вакуумом. Суспендируют полученный красно-коричневый осадок в дихлорметане, фильтруют,промывают твердое вещество дихлорметаном и сушат с получением 10,5 г грязно-белого твердого вещества. Объединяют все осадки и сушат в течение ночи в вакуумной печи при 45 С с получением 78,6 г(73,5 г,214,75 ммоль) в 1200 мл дихлорметана и охлаждают до 0 С. Добавляют пиридин (169,9 г, 2147,5 ммоль),а затем трифторметансульфоновый ангидрид (90,9 г, 322,12 ммоль). Выливают смесь в 2 л воды и разделяют слои. Промывают насыщенным раствором CuSO4 с получением эмульсии. Добавляют твердый NaCl с получением твердого синего осадка с эмульсией. Добавляют воду, чтобы сделать смесь жидкой, и отфильтровывают твердое вещество. Промывают твердое вещество водой, а затем дихлорметаном и отделяют синий водный слой от красного органического слоя. Сушат над сульфатом натрия, фильтруют и концентрируют под вакуумом с получением вязкого красного масла. Очищают с помощью хроматографии на силикагеле с использованием 2 кг силикагеля и 25% этилацетат/гексан с получением 78,4 г (77%) грязно-белого твердого вещества. 1 Н ЯМР (400 МГц, ДМСО-d6)7,8 (с, 2 Н), 3,7 (м, 1 Н), 3,3 (м, 2 Н), 3,15 (м, 1 Н), 2,85 (м, 1 Н), 2,67 (м,1 Н), 1,95 (м, 1 Н), 1,7 (м, 3 Н), 1,58 (м, 3 Н), 1,4-1,2 (м, 4 Н), 1,15 (м, 1 Н). Препаративный пример 11. Метиловый эфир 3',5'-дихлор-4'-(1-циклогексил-2-оксопирролидин-3-илметил)бифенил-4 карбоновой кислоты. Растворяют 3,5-дихлор-4-(1-циклогексил-2-оксопирролидин-3-илметил)фениловый эфир трифторметансульфоновой кислоты (5 г, 10,54 ммоль) в 50 мл толуола, добавляют 2 М водный раствор карбоната натрия и откачивают/продувают азотом 3 раза. Добавляют п-карбоксиметилфенилбороновую кислоту(2,85 г, 15,81 ммоль), снова дегазируют, затем добавляют Pd(PPh3)4 (1,22 г, 1,05 ммоль). Еще раз дегазируют/продувают, а затем кипятят с обратным холодильником в течение ночи. Разделяют слои, дважды промывают органический слой водой, а затем промывают солевым раствором. Сушат над сульфатом натрия, фильтруют и концентрируют под вакуумом с получением коричневой пены. Добавляют этилацетат с получением красно-коричневого твердого вещества и фильтруют его с получением 3,8 г продукта. Концентрируют фильтрат, чтобы извлечь еще 0,4 г продукта после очистки с помощью хроматографии на силикагеле с использованием 25% этилацетата: MS (m/z): 460 (М+). Препаративный пример 12. 3',5'-Дихлор-4'-(1-циклогексил-2-оксопирролидин-3-илметил)бифенил-4-карбоновая кислота. Помещают метиловый эфир 3',5'-дихлор-4'-(1-циклогексил-2-оксопирролидин-3-илметил)бифенил 4-карбоновой кислоты (45 г, 97,74 ммоль) в 2 л этанола и добавляют KOH (27,42 г, 488,7 ммоль). Нагревают смесь до 50 С в течение 4 ч. Фильтруют темную смесь через Celite, пока она еще горячая. Разбавляют 3 л воды и дают остыть до комнатной температуры. Подкисляют 1 н. хлористо-водородной кислотой до рН 2 при интенсивном перемешивании. Фильтруют, промывают водой и сушат под вакуумом до получения 42 г (96%) светло-красно-коричневого твердого вещества: MS (m/z): 446 (М+). Препаративный пример 13. Синтез 3',5'-дихлор-4'-(1-циклогексил-2-оксопирролидин-3-илметил)-3-фторбифенил-4 карбонитрила. Объединяют препаративный пример 10 (3,5-дихлор-4-(1-циклогексил-2-оксопирролидин-3 илметил)фениловый эфир трифторметансульфоновой кислоты) (1,85 г, 3,90 ммоль), ТГФ (40 мл), 4- 27014718 циано-3-фторфенилбороновую кислоту (0,77 г, 4,68 ммоль), карбонат натрия (1,24 г, 11,70 ммоль) и воду(10 мл) в круглодонной колбе. Перемешивают смесь 60 С в течение 5 мин, а затем добавляют тетракистрифенилфосфин палладия (0,225 г, 0,20 ммоль). Нагревают смесь при 80 С и перемешивают в течение 3 ч. Охлаждают и распределяют между этилацетатом и водным раствором хлористо-водородной кислоты(1 н.). Отделяют органическую фазу, промывают водой, а затем солевым раствором. Сушат жидкость над сульфатом натрия, фильтруют и концентрируют под вакуумом. Очищают силикагелем (25% этилацетат/гексан) с получением 1,07 г (62%) продукта: MS (m/z): 445,0 (М+). Схема D В схеме D лактам 15 получается при реакции лактона с цис- или транс-4-аминоциклогексанолом. Затем получают 4-(2-оксопирролидин-1-ил)циклогексиловый эфир нитробензойной кислоты 16 при реакции 15 с 4-нитробензойной кислотой. В этой реакции, если 15 представляет собой цисгидроксисоединение, то 16 представляет собой 4-(2-оксопирролидин-1-ил)циклогексиловый эфир транснитробензойной кислоты и 4-гидрокси в соединении Id представляет собой транс-. Если 15 представляет собой транс-гидроксисоединение, то 16 представляет собой 4-(2-оксопирролидин-1-ил)циклогексиловый эфир цис-нитробензойной кислоты, и 4-гидрокси в соединении Id представляет собой цис-. 4-Гидроксисоединение 17 соответствующим образом защищено (см. Greene), предпочтительно TBSCl, и защищенный лактам 18 алкилируют посредством 6 (см. схему А) с образованием соединения 19. С эфира 19 снимают защиту с образованием 20, и он реагирует с трифторметансульфоновым ангидридом с образованием 21. Карбоновую кислоту 22 получают за счет реакции соединения бороновой кислоты. Амид 23 получают, а затем снимают защиту с образованием соединения формулы Ic. Препаративный пример 14. 1-(транс-4-Гидроксициклогексил)пирролидин-2-он. Добавляют транс-4-аминоциклогексанол (230 г, 2,0 моль) к -бутиролактону (140 мл, 1,82 моль) в 1 л круглодонной колбе, снабженной большой магнитной мешалкой, термометром и холодильником/барботером для продувки азота. Нагревают смесь при 190 С в течение 68 ч. Охлаждают до температуры окружающей среды и смешивают с водой (1 л). Экстрагируют дихлорметаном (101,5 л). Сушат экстракты над сульфатом магния, фильтруют и выпаривают до коричневого твердого вещества. Растирают в порошок с диэтиловым эфиром с получением 144,7 г (43%) указанного соединения: MS (m/z): 184(M+1). Препаративный пример 15. 4-(2-Оксопирролидин-1-ил)циклогексиловый эфир цис-4-нитробензойной кислоты. Растворяют 1-(транс-4-гидроксициклогексил)пирролидин-2-он (144 г, 0,79 моль) в сухом тетрагидрофуране (5 л) и охлаждают до -5 С в атмосфере азота. Добавляют трифенилфосфин (310 г,- 28014718 1,185 моль) и 4-нитробензойную кислоту (198 г, 1,185 моль). По каплям добавляют диизопропил азодикарбоксилат (230 мл, 1,185 моль) и перемешивают при комнатной температуре в течение ночи. Добавляют насыщенный водный раствор бикарбоната натрия (1 л) и экстрагируют дихлорметаном (22,5 л) в 20 л разделительной воронке. Сушат объединенные органические слои над сульфатом магния, фильтруют и концентрируют. Очищают над силикагелем (изогексан/этилацетат 50-100%, затем 10% метанол в этилацетате) с получением 163 г (62%) указанного соединения. Препаративный пример 16. цис-1-(4-Гидроксициклогексил)пирролидин-2-он. Растворяют 4-(2-оксопирролидин-1-ил)циклогексиловый эфир цис-4-нитробензойной кислоты(87,9 г, 264 ммоль) в метаноле (1,35 л) и воде (150 мл) и обрабатывают карбонатом калия (109,5 г,800 ммоль). Перемешивают при комнатной температуре в течение ночи с образованием белого осадка. Выпаривают до сухого состояния. Удаляют избыток воды путем смешивания с этанолом и концентрирования до сухого состояния под вакуумом. Повторяют эту процедуру. Перемешивают в тетрагидрофуране(1 л) в течение 1 ч и затем фильтруют. Выпаривают фильтрат до (состояния) масла и кристаллизуют из диэтилового эфира (100 мл) с получением 40 г (83%) указанного соединения. Препаративный пример 17. цис-1-[4-(трет-Бутилдиметилсиланилокси)циклогексил]пирролидин-2-он. Растворяют цис-1-(4-гидроксициклогексил)пирролидин-2-он (40 г, 220 ммоль) в сухом дихлорметане (1 л). Добавляют имидазол (22,5 г, 330 ммоль), а затем трет-бутилдиметилсилил хлорид (50 г,330 ммоль). Перемешивают в атмосфере азота при комнатной температуре в течение ночи. Промывают водой (250 мл) и насыщенным раствором бикарбоната натрия (250 мл). Сушат над сульфатом магния,фильтруют и выпаривают до состояния масла. Пропускают через слой силикагеля посредством изогексана/этилацетата (0-50%) с получением 51 г (79%) указанного соединения в виде прозрачного бледножелтого масла: MS (m/z): 298 (M+1). Препаративный пример 18. 3-(4-Бензилокси-2,6-дихлорбензил)-цис-1-[4-(трет-бутилдиметилсиланилокси)циклогексил]пирролидин-2-он. Указанное соединение получают, по существу, способом для препаративного примера 8 (1 циклогексил-3-(2,6-дихлор-4-метоксибензилпирролидин-2-она с выходом 53%, исходя из 2-бромметил 1,3-дихлор-5-бензилоксибензола и цис-1-[4-(трет-бутилдиметилсиланилокси)циклогексил]пирролидин-2 она. Препаративный пример 19. цис-1-[4-(трет-Бутилдиметилсиланилокси)циклогексил]-3-(2,6-дихлор-4 гидроксибензил)пирролидин-2-он. Добавляют раствор 3-(4-бензилокси-2,6-дихлорбензил)-цис-1-[4-(трет-бутилдиметилсиланилокси)циклогексил]пирролидин-2-она (8,5 г, 15,1 ммоль) в 25 мл тетрагидрофурана к 0,5 г катализатораPearlman и гидрогенизируют полученную смесь, используя газообразный водород из баллона, в течение 2 ч. Фильтруют через Celite и концентрируют до достижения твердого состояния. Очищают с помощью хроматографии на силикагеле с использованием смеси гексаны/этилацетат с получением 4,4 г (61%) продукта. Препаративный пример 20. 4-цис-1-[4-(трет-Бутилдиметилсиланилокси)циклогексил]-2-оксопирролидин-3-илметил-3,5 дихлорфениловый эфир трифторметансульфоновой кислоты. Указанное соединение получают, по существу, способом для препаративного примера 10 с выходом 88%, исходя из цис-1-[4-(трет-бутилдиметилсиланилокси)циклогексил]-3-(2,6-дихлор-4-гидроксибензил)пирролидин-2-она. Препаративный пример 21. 4'-цис-1-[4-(трет-Бутилдиметилсиланилокси)циклогексил]-2-оксопирролидин-3-илметил-3',5'дихлорбифенил-4-карбоновая кислота. Указанное соединение получают, по существу, способом получения препаративного примера 11 с выходом 88%, исходя из 4-цис-1-[4-(трет-бутилдиметилсиланилокси)циклогексил]-2-оксопирролидин 3-илметил-3,5-дихлорфенилового эфира трифторметансульфоновой кислоты и 4-карбоксифенил бороновой кислоты.
МПК / Метки
МПК: C07D 491/08, C07D 417/10, C07D 207/12, C07D 403/10, C07D 401/12, C07D 401/10, C07D 487/04, C07D 487/08, C07D 471/04, C07D 413/10, C07D 417/14
Метки: производные, ингибиторов, бифениламидлактама, качестве, 11-бета-гидроксистероиддегидрогеназы
Код ссылки
<a href="https://eas.patents.su/30-14718-proizvodnye-bifenilamidlaktama-v-kachestve-ingibitorov-11-beta-gidroksisteroiddegidrogenazy-1.html" rel="bookmark" title="База патентов Евразийского Союза">Производные бифениламидлактама в качестве ингибиторов 11-бета-гидроксистероиддегидрогеназы 1</a>
Предыдущий патент: Производные лактама циклогексилимидазола в качестве ингибиторов 11-бета-гидроксистероид-дегидрогеназы 1
Следующий патент: Пиперидинилзамещённые пирролидиноны в качестве ингибиторов 11-бета-гидроксистероид дегидрогеназы 1
Случайный патент: Кнопочный переключатель с противозаклинивающим устройством












