Производные пиразоло [4,3-d]пиримидина
Номер патента: 4982
Опубликовано: 28.10.2004
Авторы: Девриз Кит Майкл, Стрит Стивен Дерек Алберт, Вуд Альберт Шо, Матайас Джон Пол, Баннейдж Марк Эдвард, Негри Джоанна Териза, Харрис Лоренс Джеймс, Леветт Филип Чарльз
Формула / Реферат
1. Соединение формулы I
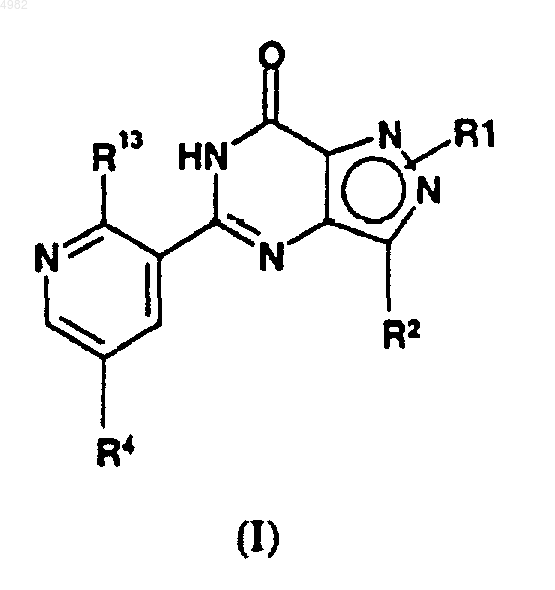
или его фармацевтически или ветеринарно приемлемая соль, или фармацевтически или ветеринарно приемлемый сольват, или пролекарство,
где R1 представляет собой C1-C6алкил или C3-C6алкенил, C3-C6циклоалкил или C4-C6циклоалкенил, где указанная алкильная группа может быть разветвленной или прямоцепочечной и где, когда R1 представляет собой C1-C3алкил, тогда указанная алкильная группа замещена,
и где когда R1 представляет собой C4-C6алкил, C3-C6алкенил или C3-C6циклоалкил, тогда указанная алкильная, алкенильная или циклоалкильная группа возможно замещена одним или более чем одним заместителем, выбранным из гидрокси; C1-C4алкокси; C3-C6циклоалкила; фенила, замещенного одним или более чем одним заместителем, выбранным из C1-C3алкила, C1-C4алкокси, C1-C4галогеноалкила, C1-C4галогеноалкокси, галогено, CN, NO2, NHR11, NHCOR12, NHSO2R12, SO2R12, SO2NHR11, COR11 или CO2R11, где указанные галогеноалкильные и галогеноалкоксигруппы содержат один или более чем один атом галогена; NR7R8, CONR7R8 или NR7COR11, где R7 и R8, каждый независимо, выбран из H, C1-C4алкила, C3-C4алкенила, CO2R9 или SO2R9, где указанные алкильные или алкенильные группы возможно замещены C1-C4галогеноалкилом или C1-C4галогеноалкокси; Het1; Het2 или Het3;
либо R1 представляет собой Het4 или фенил, где указанная фенильная группа возможно замещена одним или более чем одним заместителем, выбранным из C1-C4алкила, C3-C4алкенила, C1-C4алкокси, галогено, CN, CF3, OCF3, NO2, NHR11, NHCOR12, NHSO2R12, SO2R12, SO2NHR11, COR11, CO2R11;
R2 представляет собой C1-C6алкил, C3-C6алкенил или (CH2)n(C3-C6циклоалкил), где n равно 0, 1 или 2;
R13 представляет собой OR3 или NR5R6;
R3 представляет собой C1-C6алкил, возможно замещенный одним или двумя заместителями, выбранными из C3-C5циклоалкила, гидрокси, C1-C4алкокси, бензилокси, NR5R6, фенила, Het1, Het2, Het3 или Het4, где C1-C6алкильные и C1-C4алкоксигруппы возможно могут оканчиваться галогеноалкильной группой, такой как CF3, и где C3-C5циклоалкильная группа возможно может быть замещена C1-C4алкилом, гидрокси или галогено; C3-C6циклоалкил; Het1, Het2, Het3 или Het4;
R4 представляет собой пиперазин-1-илсульфонильную группу, имеющую заместитель R10 в положении 4 пиперазинильной группы, где указанная пиперазинильная группа возможно замещена одной или двумя C1-C4алкильными группами и возможно находится в форме 4-N-оксида;
R5 и R6, каждый независимо, выбран из H и C1-C4алкила, возможно замещенного C3-C5циклоалкилом или C1-C4алкокси, либо вместе с атомом азота, к которому они присоединены, образуют азетидинильную, пирролидинильную, пиперидинильную или морфолинильную группу;
R7 и R8, каждый независимо, выбран из H, C1-C4алкила, C3-C4алкенила, CO2R9 или SO2R9;
R9 представляет собой C1-C4алкил, возможно замещенный C1-C4галогеноалкилом, C1-C4галогеноалкокси или фенилом, где указанная фенильная группа возможно замещена одним или более чем одним заместителем, выбранным из C1-C4алкила, возможно замещенного C1-C4галогеноалкилом или C1-C4галогеноалкокси, C1-C4алкокси, галогено, CN, NO2, NHR11, NHCOR12, NHSO2R12, SO2R12, SO2NHR11, COR11 или CO2R11;
R10 представляет собой H; C1-C4алкил, возможно замещенный одним или двумя заместителями, выбранными из гидрокси, NR5R6, CONR5R6, фенила, возможно замещенного C1-C4алкилом или C1-C4алкокси; C3-C6алкенил или Het4;
R11 представляет собой H, C1-C4алкил, C3-C4алкенил, CO(C1-C4алкил) или C1-C4галогеноалкил;
R12 представляет собой C1-C4алкил, C3-C4алкенил, C1-C4галогеноалкил или C1-C4галогеноалкокси;
Het1 представляет собой N-связанную 4-, 5- или 6-членную азотсодержащую гетероциклическую группу, возможно содержащую один или более чем один дополнительный гетероатом, выбранный из S, N или O;
Het2 представляет собой C-связанную 5-членную гетероциклическую группу, содержащую гетероатом O, S или N, возможно содержащую один или более чем один гетероатом, выбранный из N, O или S;
Het3 представляет собой C-связанную 6-членную гетероциклическую группу, содержащую гетероатом O или S, возможно содержащую один или более чем один гетероатом, выбранный из O, S или N, либо Het3 представляет собой C-связанную 6-членную гетероциклическую группу, содержащую три гетероатома N;
Het4 представляет собой C-связанную 4-, 5- или 6-членную гетероциклическую группу, содержащую один, два или три гетероатома, выбранные из S, O или N; и
где любая из указанных гетероциклических групп Het1, Het2, Het3 или Het4 может быть насыщенной, частично ненасыщенной или ароматической, и где любая из указанных гетероциклических групп возможно может быть замещена одним или более чем одним заместителем, выбранным из C1-C4алкила, C3-C4алкенила, C1-C4алкокси, галогено, CF3, CO2R11, COR11, SO2R12, NHR11 или NHCOR12, и/или где любая из указанных гетероциклических групп является бензоконденсированной;
при условиях, что (а) когда R1 представляет собой C1-C3алкил, тогда Het1 не является морфолинилом или пиперидинилом, и (б) когда R1 представляет собой C1-C3алкил, замещенный фенилом, тогда указанная фенильная группа не замещена C1-C4алкокси, CN, галогено, CF3, OCF3 или C1-C4алкилом.
2. Соединение по п.1, где R1 представляет собой C1-C6алкил или C3-C6алкенил, где указанные алкильные или алкенильные группы могут быть разветвленными или прямоцепочечными, либо R1 представляет собой C3-C6циклоалкил или C4-C6циклоалкенил,
и где когда R1 представляет собой C1-C3алкил, тогда указанная алкильная группа замещена; и где когда R1 представляет собой C4-C6алкил, C3-C6алкенил, C3-C6циклоалкил или C4-C6циклоалкенил, тогда указанная алкильная, алкенильная, циклоалкильная или циклоалкенильная группа возможно замещена одним или более чем одним заместителем, выбранным из гидрокси; C1-C4алкокси; C3-C4циклоалкила; фенила, замещенного одним или более чем одним заместителем, выбранным из C1-C3алкила, C1-C4алкокси, C1-C4галогеноалкила или C1-C4галогеноалкокси, галогено, CN, NO2, NHR11, NHCOR12, NHSO2R12, SO2R12, SO2NHR11, COR11, CO2R11, где указанные галогеноалкильные и галогеноалкоксигруппы содержат один или более чем один атом галогена; NR7R8, CONR7R8 или NR7COR11; группы Het1, которая представляет собой N-связанную 4-членную N-содержащую гетероциклическую группу; группы Het2, которая представляет собой C-связанную 5-членную гетероциклическую группу, содержащую гетероатом O, S или N, возможно содержащую один или более чем один гетероатом, выбранный из N, O или S; группы Het3, которая представляет собой C-связанную 6-членную гетероциклическую группу, содержащую гетероатом O или S, возможно содержащую один или более чем один гетероатом, выбранный из O, S или N, либо группы Het3, которая представляет собой C-связанную 6-членную гетероциклическую группу, содержащую три гетероатома N;
где R7, R8, R11 и R12 являются такими, как определено здесь ранее,
либо R1 представляет собой группу Het4, которая представляет собой C-связанную 4- или 5-членную гетероциклическую группу, содержащую один гетероатом, выбранный из S, O или N; группу Het4, которая представляет собой C-связанную 6-членную гетероциклическую группу, содержащую один, два или три гетероатома, выбранные из S или O; группу Het4, которая представляет собой C-связанную 6-членную гетероциклическую группу, содержащую три гетероатома азота; группу Het4, которая представляет собой C-связанную 6-членную гетероциклическую группу, содержащую один или два гетероатома азота, которая замещена одним или более чем одним заместителем, выбранным из C1-C4алкила, C1-C4алкокси, CO2R11, SO2R12, COR11, NHR11 или NHCOR12, и которая возможно включает в себя дополнительный гетероатом, выбранный из S, O или N,
где любая из указанных гетероциклических групп Het1, Het2, Het3 или Het4 является насыщенной, частично ненасыщенной или ароматической, как подходит, и где любая из указанных гетероциклических групп возможно замещена одним или более чем одним заместителем, выбранным из C1-C4алкила, C3-C4алкенила, C1-C4алкокси, галогено, CO2R11, SO2R12, COR11 или NHR11, где R11 является таким, как определено выше, и/или где любая из указанных гетероциклических групп является бензоконденсированной;
либо R1 представляет собой фенил, замещенный одним или более чем одним заместителем, выбранным из CF3, OCF3, SO2R12 или CO2R12, где R12 представляет собой C1-C4алкил, который возможно замещен фенилом, C1-C4галогеноалкил или C1-C4галогеноалкокси, где указанные галогеноалкильные и галогеноалкоксигруппы содержат один или более чем один атом галогена;
R2 представляет собой C1-C6алкил;
R13 представляет собой OR3;
R3 представляет собой C1-C6алкил, возможно замещенный одним или двумя заместителями, выбранными из C3-C5циклоалкила, гидрокси, C1-C4алкокси, бензилокси, NR5R6, фенила, фуранила, тетрагидрофуранила или пиридинила, где указанные C1-C6алкильные и C1-C4алкоксигруппы возможно могут оканчиваться галогеноалкильной группой, такой как CF3; либо R3 представляет собой C3-C6циклоалкил, 1-(C1-C4алкил)пиперидинил, тетрагидрофуранил или тетрагидропиранил;
R4 представляет собой пиперазин-1-илсульфонильную группу, имеющую заместитель R10 в положении 4 пиперазинильной группы, где указанная пиперазинильная группа возможно замещена одной или двумя C1-C4алкильными группами и возможно находится в форме 4-N-оксида;
R5 и R6, каждый независимо, выбран из H и C1-C4алкила, возможно замещенного C3-C5циклоалкилом или C1-C4алкокси, либо вместе с атомом азота, к которому они присоединены, образуют азетидинильную, пирролидинильную, пиперидинильную или морфолинильную группу; и
R10 представляет собой H; C1-C4алкил, возможно замещенный одним или двумя заместителями, выбранными из гидрокси, NR5R6, CONR5R6, фенила, возможно замещенного C1-C4алкилом или C1-C4алкокси; C3-C6алкенил; Het4;
при условии, что когда R1 представляет собой C1-C3алкил, замещенный фенилом, тогда указанная фенильная группа не замещена C1-C4алкокси, CN, CF3, галогено, OCF3 или C1-C4алкилом.
3. Соединение по п.2, где R1 представляет собой C1-C6алкил, где указанный алкил может быть разветвленным или прямоцепочечным, либо R1 представляет собой C3-C6циклоалкил,
и где когда R1 представляет собой C1-C3алкил, тогда указанная алкильная группа замещена, и где когда R1 представляет собой C4-C6алкил или C3-C6циклоалкил, тогда указанная алкильная или циклоалкильная группа возможно замещена одним или более чем одним заместителем, выбранным из гидрокси; C1-C2алкокси; C3-C5циклоалкила; NR7R8, NR7COR11 или COR11, где R7 и R8 каждый независимо выбран из H, C1-C4алкила или CO2R9, где R9 и R11 являются такими, как определено здесь ранее; группы Het1, которая представляет собой N-связанную 4-членную N-содержащую гетероциклическую группу; группы Het3, которая представляет собой C-связанную 6-членную гетероциклическую группу, содержащую гетероатом O или S, возможно содержащую один или более чем один гетероатом, выбранный из O, S или N, либо группы Het3, которая представляет собой C-связанную 6-членную гетероциклическую группу, содержащую три гетероатома N;
либо R1 представляет собой группу Het4, которая представляет собой C-связанную 4-членную гетероциклическую группу, содержащую один гетероатом, выбранный из S, O или N, либо R1 представляет собой группу Het4, которая представляет сосющ C-связанную 6-членную гетероциклическую группу, содержащую один, два или три гетероатома, выбранные из S или O;
где любая из указанных гетероциклических групп Het1,Het2, Het3 или Het4 является насыщенной, частично ненасыщенной или ароматической и возможно замещена одним или более чем одним заместителем, выбранным из C1-C4алкила, C1-C4алкокси, -CO2R11, -SO2R12, -COR11 или NHR11, где R11 и R12 являются такими, как определено здесь выше, и/или где любая из указанных гетероциклических групп является бензоконденсированной;
либо R1 представляет собой фенил, замещенный одним или более чем одним заместителем, выбранным из CF3, -OCF3, -SO2R12, -COR11, -CO2R11, где R11 и R12 являются такими, как определено выше;
R2 представляет собой C1-C6алкил;
R13 представляет собой OR3;
R3 представляет собой метил, этил, н-пропил, изопропил, н-бутил, втор-бутил, изобутил или трет-бутил, возможно замещенный одним или двумя заместителями, выбранными из циклопропила, циклобутила, гидрокси, метокси, этокси, бензилокси, фенила, бензила, фуран-3-ила, тетрагидрофуран-2-илметила, тетрагидрофуран-3-илметила, пиридин-2-ила, пиридин-3-ила или NR5R6, где R5 и R6, каждый независимо, выбран из H и C1-C2алкила;
R4 представляет собой пиперазин-1-илсульфонильную группу, имеющую заместитель R10 в положении 4 пиперазинильной группы, где указанная пиперазинильная группа возможно замещена одной или двумя C1-C4алкильными группами и возможно находится в форме 4-N-оксида; и
R10 представляет собой H, C1-C3алкил, возможно замещенный одним или двумя заместителями, выбранными из гидрокси, NR5R6, CONR5R6, где R5 и R6, каждый независимо, выбран из H, C1-C4алкила и C3алкенила.
4. Соединение по п.3, где R1 представляет собой -(CH2)n(C3-C5)циклоалкил, где n равно 0, 1, 2 или 3; либо R1 представляет собой метил, этил, изопропил или н-пропил, замещенные одним или более чем одним заместителем C1-C4алкокси, где указанный заместитель алкокси может быть присоединен непосредственно к любому атому C в пределах этильной, изопропильной или н-пропильной групп; либо R1 представляет собой C4алкильную группу, выбранную из изо-, н-, втор- или трет-бутила, возможно замещенного одним или более чем одним заместителем, выбранным из C1-C4алкокси или C3-C4циклоалкила;
R2 представляет собой C1-C4алкил;
R13 представляет собой OR3, где R3 представляет собой C1-C4алкил, возможно замещенный одним или двумя заместителями C1-C4алкокси, где указанные C1-C4алкильные и C1-C4алкоксигруппы возможно могут оканчиваться галогеноалкильной группой, такой как CF3;
R4 представляет собой пиперазин-1-илсульфонильную группу, имеющую единственный заместитель R10 в положении 4 пиперазинильной группы и возможно находится в форме 4-N-оксида; и где R10 представляет собой метил или этил.
5. Соединение по п.4, имеющее общую формулу (IA) или (IB)
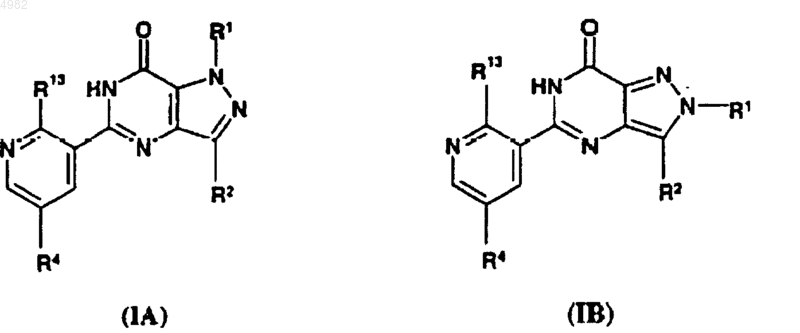
где R1 представляет собой -(CH2)n(C3-C4)циклоалкил, где n равно 1 или 2; либо R1 представляет собой -(CH2)n(C3-C5)циклоалкил, где n равно 0; либо R1 представляет собой -(CH2)n(C5)циклоалкил, где n равно 1; либо R1 представляет собой метил, этил, изопропил или н-пропил, замещенные метокси, этокси, н-пропокси или изопропокси, где указанный заместитель алкокси может быть присоединен непосредственно к любому атому C в пределах этильной, изопропильной или н-пропильной групп; либо R1 представляет собой изо-, н-, втор- или трет-бутил; R2 представляет собой C2-C4алкил; R13 представляет собой OR3, где алкильная группа R3 представляет собой метил, этил, н-пропил, изопропил, изобутил, н-бутил, втор-бутил или трет-бутил, возможно замещенные одним или двумя заместителями метокси, этокси, н-пропокси или изопропокси; и R4 представляет собой 4-метильную или 4-этилпиперазин-1-илсульфонильную группу.
6. Соединение по п.5, имеющее общую формулу (IB)
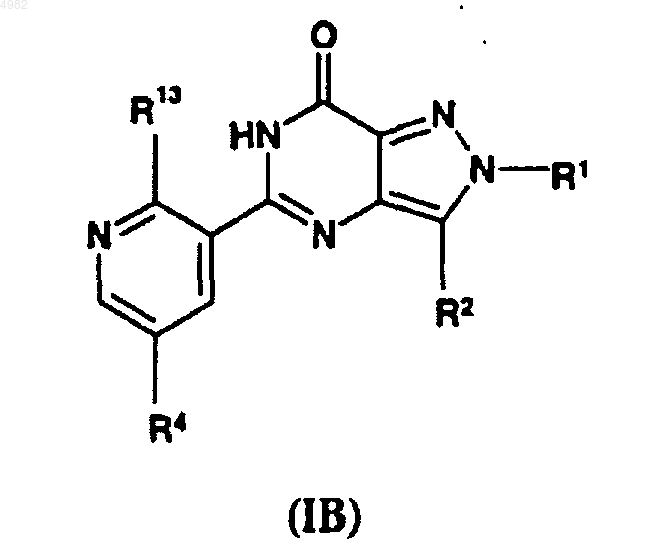
где R1 представляет собой -(CH2)n(C3-C4)циклоалкил, где n равно 1 или 2; либо R1 представляет собой -(CH2)n(C3-C5)циклоалкил, где n равно 0; либо R1 представляет собой -(CH2)n(C5)циклоалкил, где n равно 1; либо R1 представляет собой метил, этил, изопропил или н-пропил, замещенные метокси, этокси, н-пропокси или изопропокси, где указанный заместитель алкокси может быть присоединен непосредственно к любому атому C в пределах этильной, изо-пропильной или н-пропильной группы; либо R1 представляет собой изо-, н-, втор- или трет-бутил; R2 представляет собой C2-C4алкил; R13 представляет собой OR3, где алкильная группа R3 представляет собой метил, этил, н-пропил, изопропил, изобутил, н-бутил, втор-бутил или трет-бутил, возможно замещенные одним или двумя заместителями метокси, этокси, н-пропокси или изопропокси; и R4 представляет собой 4-метильную или 4-этилпиперазин-1-илсульфонильную группу.
7. Соединение по любому из пп.1-4, выбранное из
5-[2-этокси-5-(4-метилпиперазин-1-илсульфонил)пиридин-3-ил]-2-[2-метоксиэтил]-3-н-пропил-2,6-дигидро-7H-пиразоло[4,3-d]пиримидин-7-она,
5-[2-этокси-5-(4-метилпиперазин-1-илсульфонил)пиридин-3-ил]-3-этил-2-[2-метоксиэтил]-2,6-дигидро-7H-пиразоло[4,3-d]пиримидин-7-она,
5-[2-этокси-5-(4-этилпиперазин-1-илсульфонил)пиридин-3-ил]-2-[2-метоксиэтил]-3-н-пропил-2,6-дигидро-7H-пиразоло[4,3-d]пиримидин-7-она,
2-(втор-бутил)-5-[2-этокси-5-(4-этилпиперазин-1-илсульфонил)пиридин-3-ил]-3-этил-2,6-дигидро-7H-пиразоло[4,3-d]пиримидин-7-она,
2-(изобутил)-5-[2-этокси-5-(4-этилпиперазин-1-илсульфонил)пиридин-3-ил]-3-этил-2,6-дигидро-7H-пиразоло[4,3-d]пиримидин-7-она,
2-(циклопропилметил)-5-[2-этокси-5-(4-этилпиперазин-1-илсульфонил)пиридин-3-ил]-3-этил-2,6-дигидро-7H-пиразоло[4,3-d]пиримидин-7-она,
2-(циклобутилметил)-5-[2-этокси-5-(4-этилпиперазин-1-илсульфонил)пиридин-3-ил]-3-этил-2,6-дигидро-7H-пиразоло[4,3-d]пиримидин-7-она,
5-[2-этокси-5-(4-этилпиперазин-1-илсульфонил)пиридин-3-ил]-3-этил-2-[2-метоксиэтил]-2,6-дигидро-7H-пиразоло[4,3-d]пиримидин-7-она,
5-[2-этокси-5-(4-этилпиперазин-1-илсульфонил)пиридин-3-ил]-3-этил-2-[2-метокси-1-метилэтил]-2,6-дигидро-7H-пиразоло[4,3-d]пиримидин-7-она,
5-[2-этокси-5-(4-этилпиперазин-1-илсульфонил)пиридин-3-ил]-3-этил-2-[2-(метиламино)этил]-2,6-дигидро-7H-пиразоло[4,3-d]пиримидин-7-она,
2-(2-диметиламиноэтил)-5-[2-этокси-5-(4-этилпиперазин-1-илсульфонил)пиридин-3-ил]-3-этил-2,6-дигидро-7H-пиразоло[4,3-d]пиримидин-7-она,
5-[2-этокси-5-(4-этилпиперазин-1-илсульфонил)пиридин-3-ил]-3-этил-2-(1-метилазетидин-3-ил)-2,6-дигидро-7H-пиразоло[4,3-d]пиримидин-7-она,
5-[2-н-бутокси-5-(4-этилпиперазин-1-илсульфонил)пиридин-3-ил]-2-диметиламиноэтил-3-этил-2,6-дигидро-7H-пиразоло[4,3-d]пиримидин-7-она,
5-[2-этокси-5-(4-этилпиперазин-1-илсульфонил)пиридин-3-ил]-3-этил-2-(1-этилазетидин-3-ил)-2,6-дигидро-7H-пиразоло[4,3-d]пиримидин-7-она,
2-{2-[ацетил(метил)амино]этил}-5-[5-(4-этилпиперазин-1-илсульфонил)-2-н-пропоксипиридин-3-ил]-3-этил-2,6-дигидро-7H-пиразоло[4,3-d]пиримидин-7-она,
2-(1-ацетилазетидин-3-ил)-5-[2-н-бутокси-5-(4-этилпиперазин-1-илсульфонил)пиридин-3-ил]-3-этил-2,6-дигидро-7H-пиразоло[4,3-d]пиримидин-7-она,
5-[2-изобутокси-5-(4-этилпиперазин-1-илсульфонил)пиридин-3-ил]-2-(2-метоксиэтил)-3-н-пропил-2,6-дигидро-7H-пиразоло[4,3-d]пиримидин-7-она,
5-[2-н-бутокси-5-(4-этилпиперазин-1-илсульфонил)пиридин-3-ил]-3-этил-2-(2-метоксиэтил)-2,6-дигидро-7H-пиразоло[4,3-d]пиримидин-7-она,
3-этил-5-[5-(4-этилпиперазин-1-илсульфонил)-2-(2-метоксиэтокси)пиридин-3-ил]-2-(2-метоксиэтил)-2,6-дигидро-7H-пиразоло[4,3-d]пиримидин-7-она,
5-[2-н-бутокси-5-(4-этилпиперазин-1-илсульфонил)пиридин-3-ил]-3-этил-2-(1-метилазетидин-3-ил)-2,6-дигидро-7H-пиразоло[4,3-d]пиримидин-7-она,
5-[2-н-бутокси-5-(4-этилпиперазин-1-илсульфонил)пиридин-3-ил]-3-этил-2-(1-этилазетидин-3-ил)-2,6-дигидро-7H-пиразоло[4,3-d]пиримидин-7-она,
5-[2-бензилокси-5-(4-этилпиперазин-1-илсульфонил)пиридин-3-ил]-3-этил-2-(1-этилазетидин-3-ил)-2,6-дигидро-7H-пиразоло[4,3-d]пиримидин-7-она,
5-[2-изобутокси-5-(4-метилпиперазин-1-илсульфонил)пиридин-3-ил]-3-этил-2-(2-метоксиэтанол)-2,6-дигидро-7H-пиразоло[4,3-d]пиримидин-7-она,
3-этил-5-[5-(4-этилпиперазин-1-илсульфонил)-2-н-пропоксипиридин-3-ил]-2-(2-метоксиэтил)-2,6-дигидро-7H-пиразоло[4,3-d]пиримидин-7-она,
5-[2-н-бутокси-5-(4-этилпиперазин-1-илсульфонил)пиридин-3-ил]-3-этил-2-(2-метоксиэтанол)-2,6-дигидро-7H-пиразоло[4,3-d]пиримидин-7-она,
3-этил-5-[5-(4-этилпиперазин-1-илсульфонил)-2-изопропоксипиридин-3-ил]-2-(2-метоксиэтил)-2,6-дигидро-7H-пиразоло[4,3-d]пиримидин-7-она,
5-[(S)-2-втор-бутокси-5-(4-этилпиперазин-1-илсульфонил)пиридин-3-ил]-3-этил-2-(2-метоксиэтанол)-2,6-дигидро-7H-пиразоло[4,3-d]пиримидин-7-она,
5-[(R)-2-втор-бутокси-5-(4-этилпиперазин-1-илсульфонил)пиридин-3-ил]-3-этил-2-(2-метоксиэтанол)-2,6-дигидро-7H-пиразоло[4,3-d]пиримидин-7-она,
3-этил-5-[5-(4-этилпиперазин-1-илсульфонил)-2-{(пиридин-2-ил)метил}пиридин-3-ил]-2-(2-метоксиэтил)-2,6-дигидро-7H-пиразоло[4,3-d]пиримидин-7-она,
2-втор-бутил-3-этил-5-[5-(4-этилпиперазин-1-илсульфонил)-2-(2-метоксиэтокси)пиридин-3-ил]-2,6-дигидро-7H-пиразоло[4,3-d]пиримидин-7-она,
2-циклобутилметил-3-этил-5-[5-(4-этилпиперазин-1-илсульфонил)-2-(2-метоксиэтокси)пиридин-3-ил]-2,6-дигидро-7H-пиразоло[4,3-d]пиримидин-7-она,
3-этил-5-[5-(4-этилпиперазин-1-илсульфонил)-2-(S)-(2-метокси-1-метилэтокси)пиридин-3-ил]-2-(2-метоксиэтил)-2,6-дигидро-7H-пиразоло[4,3-d]пиримидин-7-она,
3-этил-5-[5-(4-этилпиперазин-1-илсульфонил)-2-(R)-(2-метокси-1-метилэтокси)пиридин-3-ил]-2-(2-метоксиэтил)-2,6-дигидро-7H-пиразоло[4,3-d]пиримидин-7-она,
5-[5-(4-этилпиперазин-1-илсульфонил)-2-(S)-(2-метокси-1-метилэтокси)пиридин-3-ил]-2-(2-метоксиэтил)-3-н-пропил-2,6-дигидро-7H-пиразоло[4,3-d]пиримидин-7-она,
5-[5-(4-этилпиперазин-1-илсульфонил)-2-(R)-(2-метокси-1-метилэтокси)пиридин-3-ил]-2-(2-метоксиэтил)-3-н-пропил-2,6-дигидро-7H-пиразоло[4,3-d]пиримидин-7-она,
5-[2-этокси-5-(4-этилпиперазин-1-илсульфонил)пиридин-3-ил]-3-этил-2-(2-гидроксиэтил)-2,6-дигидро-7H-пиразоло[4,3-d]пиримидин-7-она,
2-(2-диметиламиноэтил)-5-[2-этокси-5-(4-этилпиперазин-1-илсульфонил)пиридин-3-ил]-3-этил-2,6-дигидро-7H-пиразоло[4,3-d]пиримидин-7-она,
2-изобутил-3-этил-5-[2-(2-метоксиэтокси)-5-(4-метилпиперазин-1-илсульфонил)пиридин-3-ил]-2,6-дигидро-7H-пиразоло[4,3-d]пиримидин-7-она,
2-изобутил-3-этил-5-[5-(4-этилпиперазин-1-илсульфонил)-2-(2-метоксиэтокси)пиридин-3-ил]-2,6-дигидро-7H-пиразоло[4,3-d]пиримидин-7-она,
2-циклобутилметил-3-этил-5-[2-(2-метоксиэтокси)-5-(4-метилпиперазин-1-илсульфонил)пиридин-3-ил]-2,6-дигидро-7H-пиразоло[4,3-d]пиримидин-7-она,
5-[2-н-бутокси-5-(4-этилпиперазин-1-илсульфонил)пиридин-3-ил]-2-[2-(диметиламино)-2-оксоэтил]-3-этил-2,6-дигидро-7H-пиразоло[4,3-d]пиримидин-7-она,
5-[2-н-бутокси-5-(4-этилпиперазин-1-илсульфонил)пиридин-3-ил]-3-этил-2-{2-[метил(метилсульфонил)амино]этил}-2,6-дигидро-7H-пиразоло[4,3-d]пиримидин-7-она,
2-циклобутилпропилметил-3-этил-5-[2-(2-метоксиэтокси)-5-(4-метилпиперазин-1-илсульфонил)пиридин-3-ил]-2,6-дигидро-7H-пиразоло[4,3-d]пиримидин-7-она,
2-н-бутил-3-этил-5-[2-(2-метоксиэтокси)-5-(4-метилпиперазин-1-илсульфонил)пиридин-3-ил]-2,6-дигидро-7H-пиразоло[4,3-d]пиримидин-7-она,
5-[2-н-бутокси-5-(4-метилпиперазин-1-илсульфонил)пиридин-3-ил]-3-этил-2-(2-метоксиэтил)-2,6-дигидро-7H-пиразоло[4,3-d]пиримидин-7-она,
2-(2-этоксиэтил)-3-этил-5-[5-(4-этилпиперазин-1-илсульфонил)-2-(2-метоксиэтокси)пиридин-3-ил]-2,6-дигидро-7H-пиразоло[4,3-d]пиримидин-7-она,
5-[2-этокси-5-(4-этилпиперазин-1-илсульфонил)пиридин-3-ил]-3-этил-2-(3-метоксипропил)-2,6-дигидро-7H-пиразоло[4,3-d]пиримидин-7-она,
5-[2-этокси-5-(4-этилпиперазин-1-илсульфонил)пиридин-3-ил]-3-этил-2-(S)-(2-метоксипропил)-2,6-дигидро-7H-пиразоло[4,3-d]пиримидин-7-она,
5-[2-этокси-5-(4-этилпиперазин-1-илсульфонил)пиридин-3-ил]-3-этил-2-(R)-(2-метоксипропил)-2,6-дигидро-7H-пиразоло[4,3-d]пиримидин-7-она,
2-(S)-втор-бутил-3-этил-5-[5-(4-этилпиперазин-1-илсульфонил)-2-(2-метоксиэтокси)пиридин-3-ил]-2,6-дигидро-7H-пиразоло[4,3-d]пиримидин-7-она,
5-[2-этокси-5-(4-этилпиперазин-1-илсульфонил)пиридин-3-ил]-3-этил-1-(2-метоксиэтил)-1,6-дигидро-7H-пиразоло[4,3-d]пиримидин-7-она или
2-(R)-втор-бутил-3-этил-5-[5-(4-этилпиперазин-1-илсульфонил)-2-(2-метоксиэтокси)пиридин-3-ил]-2,6-дигидро-7H-пиразоло[4,3-d]пиримидин-7-она
и их фармацевтически приемлемых солей или полиморфов.
8. Соединение по п.1, выбранное из 1-{6-этокси-5-[3-этил-6,7-дигидро-2-(2-метоксиэтил)-7-оксо-2H-пиразоло[4,3-d]пиримидин-5-ил]-3-пиридилсульфонил}-4-этилпиперазина и его солей и полиморфов.
9. Соединение по п.1, выбранное из п-толуолсульфоната, бензолсульфоната, камфорсульфоната и этансульфоната 1-{6-этокси-5-[3-этил-6,7-дигидро-2-(2-метоксиэтил)-7-оксо-2H-пиразоло[4,3-d]пиримидин-5-ил]-3-пиридилсульфонил}-4-этилпиперазина.
10. Соединение по п.1, представляющее собой 1-{6-этокси-5-[3-этил-6,7-дигидро-2-(2-метоксиэтил)-7-оксо-2H-пиразоло[4,3-d]пиримидин-5-ил]-3-пиридилсульфонил}-4-этилпиперазин.
11. Фармацевтическая композиция, содержащая соединение формулы (I), (IA) или (IB), как определено в любом из пп.1-10, либо его фармацевтически приемлемые соль или полиморф, либо их фармацевтически приемлемые сольват или пролекарство по любому из пп.1-10 вместе с фармацевтически приемлемыми разбавителем или носителем.
12. Ветеринарный препарат, содержащий соединение формулы (I), (IA) или (IB) по любому из пп.1-10, либо его ветеринарно приемлемые соль или полиморф, либо их ветеринарно приемлемые сольват или пролекарство по любому из пп.1-10 вместе с ветеринарно приемлемыми разбавителем или носителем.
13. Применение соединения формулы (I), (IA) или (IB), либо его фармацевтически приемлемой соли или полиморфа, либо их фармацевтически приемлемого сольвата или пролекарства по любому из пп.1-10 в качестве лекарства для человека.
14. Применение соединения формулы (I), (IA) или (IB), либо его ветеринарно приемлемой соли или полиморфа, либо их ветеринарно приемлемого сольвата или пролекарства по любому из пп.1-10 в качестве лекарства для животного.
15. Применение фармацевтической композиции по п.11 в качестве лекарства для человека.
16. Применение ветеринарного препарата по п.12 в качестве лекарства для животного.
17. Применение соединения формулы (I), (IA) или (IB), либо его фармацевтически приемлемых соли или полиморфа, либо их фармацевтически приемлемых сольвата или пролекарства по любому из пп.1-10 для производства лекарства для человека для куративного или профилактического лечения медицинского состояния, фыя которого показан ингибитор цГМФ-ФДЭ5.
18. Применение соединения формулы (I), (IA) или (IB), либо его ветеринарно приемлемых соли или полиморфа, либо их ветеринарно приемлемых сольвата или пролекарства по любому из пп.1-10 для производства лекарства для животного для куративного, паллиативного или профилактического лечения медицинского состояния, для которого показан ингибитор цГМФ-ФДЭ5.
19. Применение соединения формулы (I), (IA) или (IB), либо его фармацевтически приемлемых соли или полиморфа, либо их фармацевтически приемлемых сольвата или пролекарства по любому из пп.1-10 для производства лекарства для человека для куративного, паллиативного или профилактического лечения мужской эректильной дисфункции (MED, male erectile dysfunction), импотенции, женской половой дисфункции (FSD, female sexual dysfunction), клиторальной дисфункции, женского расстройства, представляющего собой гипоактивное половое желание, женского расстройства полового возбуждения, женского полового болевого расстройства или женской половой оргазмической дисфункции (FSOD, female sexual orgasmic dysfunction).
20. Применение соединения формулы (I), (IA) или (IB), либо его ветеринарно приемлемых соли или полиморфа, либо их ветеринарно приемлемых сольвата или пролекарства по любому из пп.1-10 для производства лекарства для животного для куративного, паллиативного или профилактического лечения эректильной дисфункции у самца (MED), импотенции, половой дисфункции самки (FSD), клиторальной дисфункции, расстройства, представляющего собой гипоактивное половое желание у самки, расстройства полового возбуждения самки, полового болевого расстройства у самки или половой оргазмической дисфункции у самки (FSOD).
21. Способ лечения или предупреждения медицинского состояния, для которого показан ингибитор цГМФ-ФДЭ5, у млекопитающего (включая человека), при котором указанному млекопитающему вводят терапевтически эффективное количество соединения общей формулы (I), (IA) или (IB), либо его фармацевтически или ветеринарно приемлемых соли или полиморфа, либо их фармацевтически или ветеринарно приемлемых сольвата или пролекарства по любому из пп.1-10, либо фармацевтической композиции по п.11 или ветеринарного препарата по п.12, содержащих любое из вышеуказанного.
22. Способ лечения или предупреждения эректильной дисфункции у самца (MED), импотенции, половой дисфункции самки (FSD), клиторальной дисфункции, расстройства, представляющего собой гипоактивное половое желание у самки, расстройства полового возбуждения самки, полового болевого расстройства у самки или половой оргазмической дисфункции у самки (FSOD), у млекопитающего (включая человека), при котором указанному млекопитающему вводят терапевтически эффективное количество соединения общей формулы (I), (IA) или (IB), либо его фармацевтически или ветеринарно приемлемых соли или полиморфа, либо их фармацевтически или ветеринарно приемлемых сольвата или пролекарства по любому из пп.1-10, либо фармацевтической композиции по п.11 или ветеринарного препарата по п.12, содержащих любое из вышеуказанного.
23. Соединение формулы (IX)
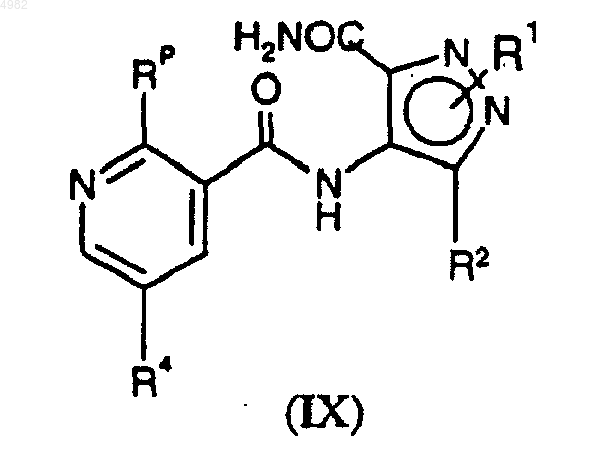
где Rp представляет собой R13, как определено в п.1, либо Rp представляет собой X, который является уходящей группой.
24. Способ получения соединения формулы (I)
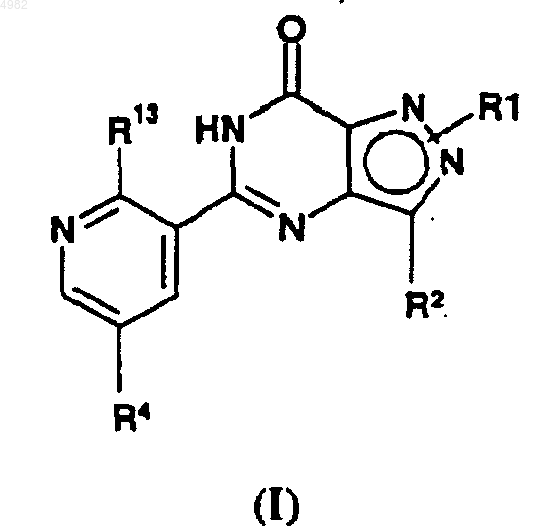
где R1, R2, R13 и R4 являются такими, как определено в п.1, при котором соединение формулы (IX)
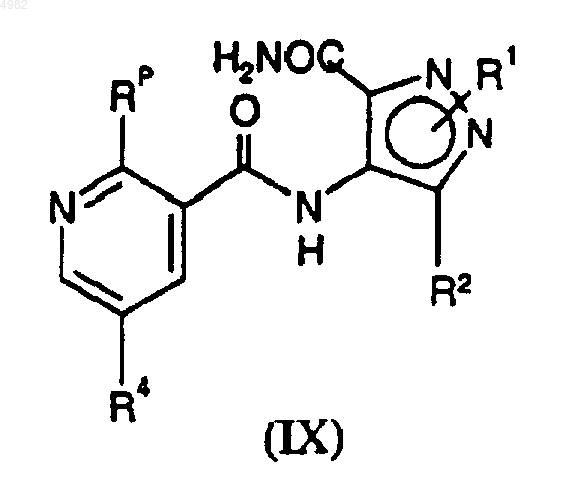
где Rp представляет собой R13, либо Rp представляет собой X, который является уходящей группой, а R1, R2, R4 и R13 являются такими, как определено в п.1, подвергают циклизации, причем после указанной реакции циклизации возможно осуществляют образование фармацевтически или ветеринарно приемлемой соли требуемого продукта, либо фармацевтически или ветеринарно приемлемых сольвата или пролекарства требуемого продукта.
25. Способ по п.24, где реакцию циклизации опосредуют основанием, используя соль щелочного металла стерически затрудненного спирта или амина.
26. Способ получения соединений общей формулы (IX) через реакцию сочетания между соединениями общей формулы (VII)
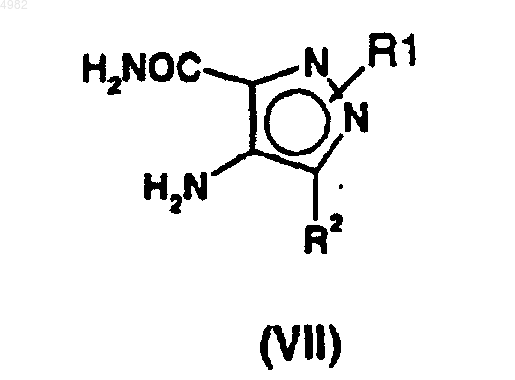
где R1 и R2 являются такими, как определено для соединений формулы (I) в п.1, и соединениями формулы (X)
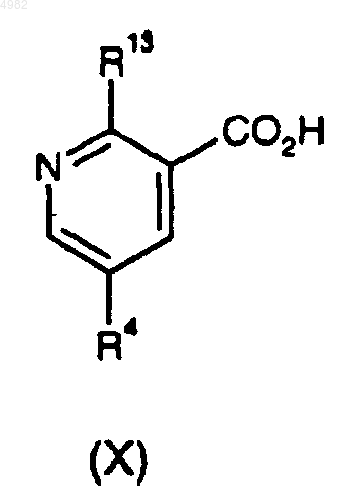
где R13 и R4 являются такими, как определено ранее для формулы (I) в п.1.
27. Способ по п.26, где реакцию сочетания проводят, используя общепринятые методики образования амидной связи.
28. Соединения общей формулы (VII)

где R1 и R2 являются такими, как определено для соединений формулы (I) в п.1.
29. Соединения общей формулы (VIIB)
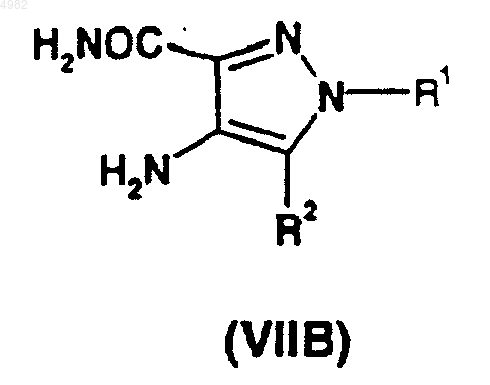
где R1 представляет собой метоксиэтил, а R2 представляет собой этил.
30. Соединения общей формулы (X)
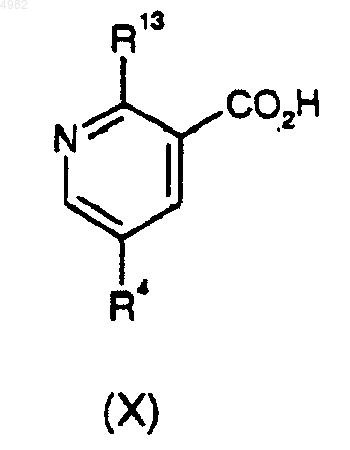
где R13 представляет собой OR3, где R3 представляет собой этил и где R4 представляет собой этилпиперазин-1-илсульфонил.
31. Способ получения соединения формулы (XB)
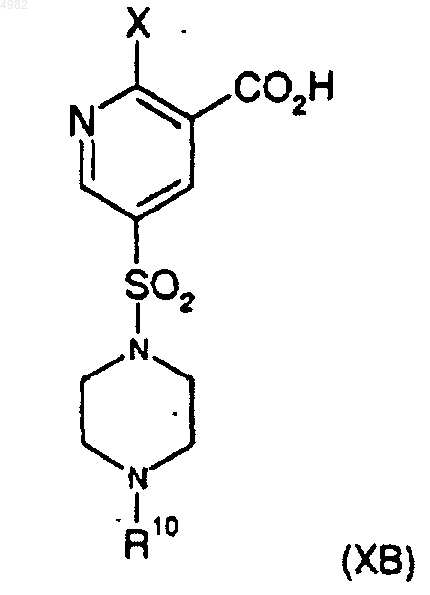
где X представляет собой арилсульфонилокси, C1-C4алкилсульфонилокси, C1-C4перфторалкилсульфонилокси, арилокси, C1-C4перфторалканоилокси, C1-C4алканоилокси, четвертичный аммонийC1-C4 алкилсульфонилокси или галогеносульфонилокси, или его соли, при котором соединение формулы (XIV)
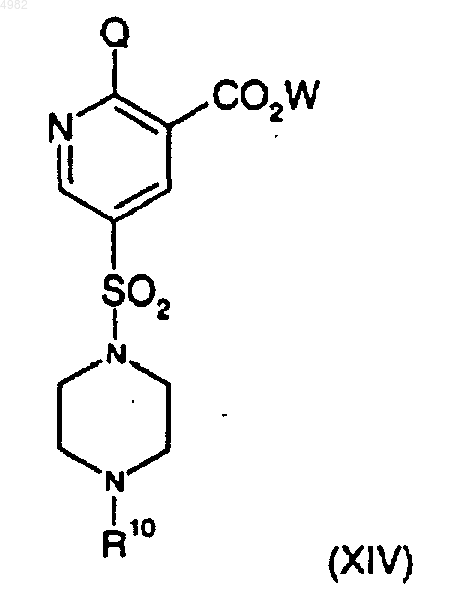
где Q и W представляют собой OH, подвергают реакции в присутствии подходящего для X сульфонилирующего, арилирующего или ацилирующего агента.
32. Способ получения соединения формулы (XB), показанной в п.31, где X представляет собой Cl, или его соли, при котором соединение формулы (XIV), показанной в п.31, где Q представляет собой Cl, W представляет собой P, а P представляет собой защитную группу, подвергают взаимодействию с агентом, удаляющим защиту.
33. Способ получения соединения формулы (XB), показанной в п.31, где X представляет собой диазоний, или его соли, при котором соединение формулы (XIV), показанной в п.31, где Q представляет собой NH2, W представляет собой OH, подвергают взаимодействию с азотистой кислотой.
34. Способ получения соединения формулы (XB), показанной в п.31, где X представляет собой (диарилсульфонил)амино, или его соли, при котором соединение формулы (XIV), показанной в п.31, где Q=NH2, а W=OH, подвергают реакции в присутствии подходящего для X сульфонилирующего агента.
35. Способ получения соединения формулы (XB), показанной в п.31, где X представляет собой OR3, где OR3 представляет собой C1-C6алкоксигруппу, или его соли, при котором соединение формулы (XIV), показанной в п.31, где W представляет собой P, где P представляет собой защитную группу, а Q представляет собой первичную или вторичную C1-C6алкоксигруппу, подвергают взаимодействию с агентом, удаляющим защиту.
36. Способ получения соединений формулы (XIV), показанной в п.31, где Q представляет собой OH и W представляет собой OH, при котором соединение формулы (XV)
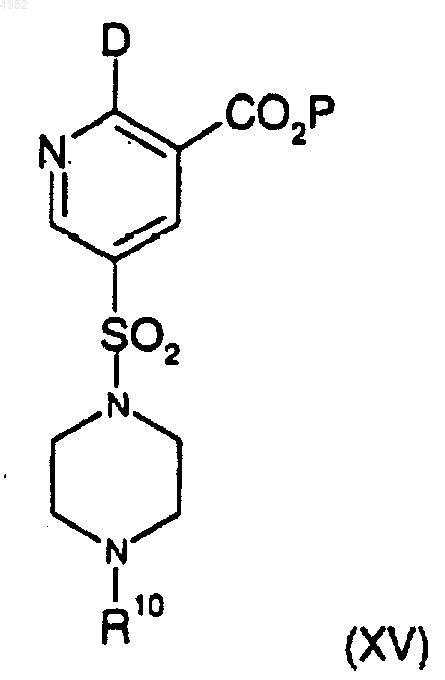
где D представляет собой Cl или Br, а P представляет собой защитную группу, подвергают взаимодействию с гидролизующим агентом и возможно с дополнительным агентом, удаляющим защиту, если защитная группа P не удаляется гидролизующим агентом.
37. Способ получения соединений формулы (XIV), показанной в п.31, где Q представляет собой NH2, а W представляет собой OH, при котором соединение формулы (XV), определенной в п.36, подвергают взаимодействию с аммонирующим агентом с образованием промежуточного соединения формулы (XIV), где Q представляет собой NH2, а W представляет собой P (защитную группу), и указанное промежуточное соединение (XIV) подвергают взаимодействию с агентом, удаляющим защиту.
38. Способ получения соединений формулы (XIV), показанной в п.31, где Q представляет собой OR3, который представляет собой C1-6алкокси, а W представляет собой P, при котором соединение формулы (XV), определенной в п.36, подвергают реакции в присутствии -OR3.
39. Способ получения соединения формулы (XV) по пп.36-38, при котором соединения формулы (XVI)

где D и P являются такими, как определено в п.36, подвергают реакции в присутствии N-R10 пиперазин-1-илсульфонила, где R10 является таким, как определено в п.1.
40. Способ получения соединения формулы (XVI) по п.39, при котором соединение формулы (XX)
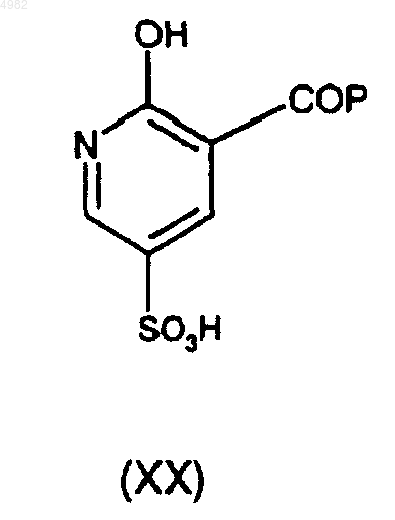
где P является таким, как определено в п.36, подвергают взаимодействию с хлорирующим или бромирующим агентом.
41. Способ по п. 40 получения соединения формулы (XX), при котором соединение формулы (XVII)
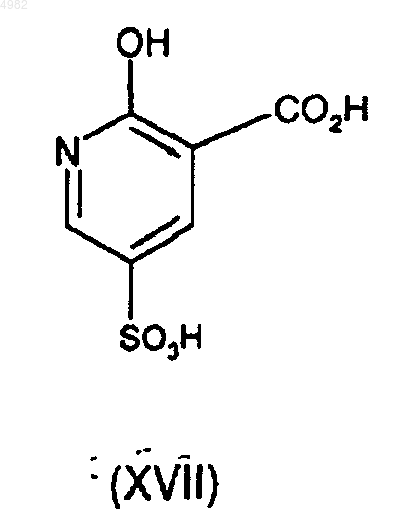
подвергают реакции в присутствии агента, который будет образовывать защитную группу (P) на карбоновой кислоте.
42. Способ по п.41 получения соединения формулы (XVII), при котором 2-гидроксиникотиновую кислоту или ее соль подвергают реакции в присутствии SO3 в растворителе.
43. Способ по п.42, где SO3 находится в органическом растворителе, в апротонном растворителе, в минеральной кислоте или в жидкой карбоновой кислоте.
44. Способ по любому из пп.35, 38-43, где соединения формул (XB), (XIV) и (XV) представляют собой соответственно:
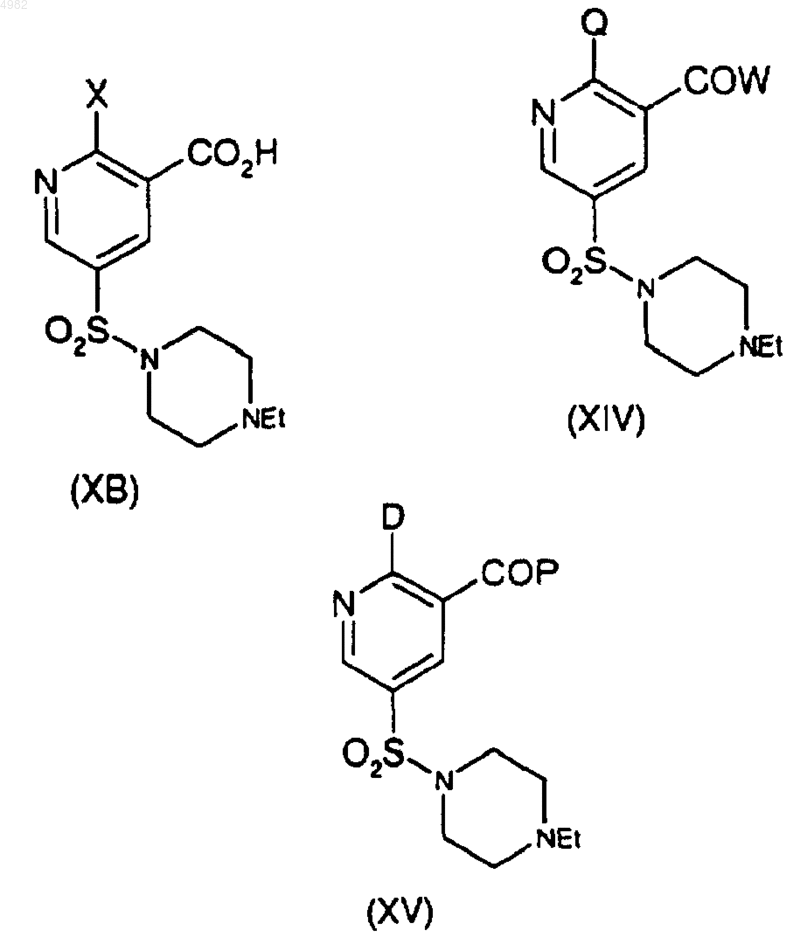
где X представляет собой C1-6алкоксигруппу, Q и W являются такими, как определено в пп.35 и 38, и соединения (XB) и (XIV) образованы согласно способам пп.35 и 38 соответственно, а соединение (XV) образовано согласно способу п.39 взаимодействием соединения (XVI) с N-этилпиперазином или его солью.
45. Способ по п.44, где X представляет собой OEt и соединение (XB) образовано взаимодействием соединения (XIV) с агентом, удаляющим защиту, а соединение (XIV) образовано реакцией соединения (XV) в присутствии OEt.
46. Способ по п.44 или 45, где соединение (XX) образовано взаимодействием соединения (XVII) или его соли с этанолом до образования защитной группы OEt.
47. Способ получения соединения формулы (I)
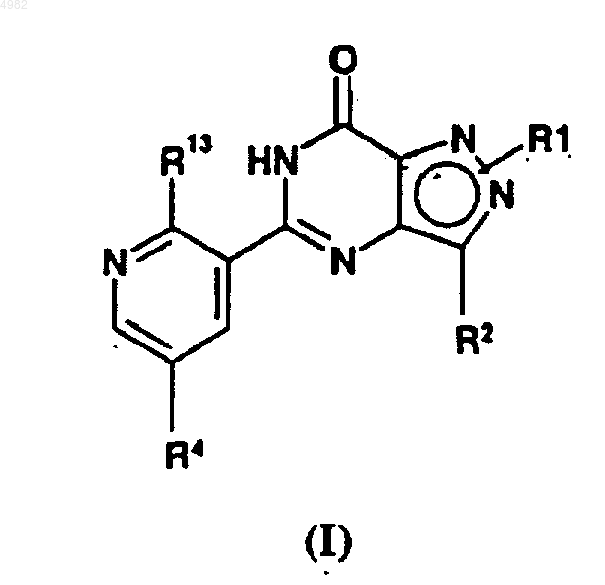
где R1, R2 и R4 являются такими, как определено в п.1, а R13 представляет собой OR3, как определено в п.1, при котором соединение формулы (XXX)
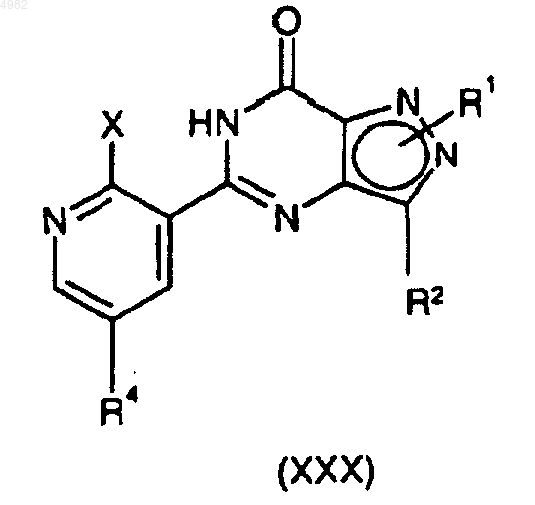
где X представляет собой уходящую группу, а R1, R2 и R4 являются такими, как определено в п.1, подвергают превращению, и после указанной реакции превращения возможно осуществляют образование фармацевтически или ветеринарно приемлемой соли требуемого продукта, либо фармацевтически или ветеринарно приемлемых сольвата или пролекарства требуемого продукта.
48. Соединение общей формулы (XXX)
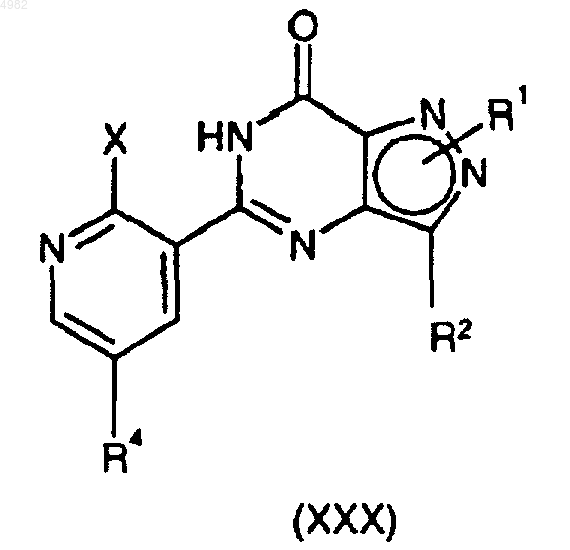
где R1, R2 и R4 являются такими, как определено в п.1, а X представляет собой уходящую группу.
49. Способ по п.24, где R13 представляет собой OR3, а Rp представляет собой X, при котором осуществляют циклизацию (IX) с последующим замещением уходящей группы на OR3.
50. Способ по п.49, где X представляет собой OR3a, где OR3a представляет собой алкоксигруппу, которая отличается от желаемой группы OR3 и способна к замещению на эту группу на конечных соединениях общей формулы (I), и где R3a выбран из C1-C6алкила, возможно замещенного.
51. Способ по п.24, где R13 представляет собой OR3, а Rp представляет собой X, при котором осуществляют замещение уходящей группы на OR3 с последующей циклизацией (IX).
52. Способ по п.51, где X представляет собой OR3a, где OR3a представляет собой алкоксигруппу, которая отличается от желаемой группы OR3 и способна к замещению на эту группу на конечных соединениях общей формулы (I), и где R3a выбран из C1-C6алкила, возможно замещенного.
53. Способ по п.24, где R13 представляет собой OR3, а Rp представляет собой X, при котором осуществляют прямую циклизацию (IX) с замещением уходящей группы на OR3.
Текст
1 Данное изобретение относится к серии пиразоло[4,3-d]пиримидин-7-онов, которые ингибируют фосфодиэстеразы циклического гуанозин-3',5'-монофосфата (цГМФ-ФДЭ). Особо примечательно, что соединения по изобретению являются сильнодействующими и избирательными ингибиторами фосфодиэстеразы циклического гуанозин-3',5'-монофосфата типа 5(цГМФ-ФДЭ 5) и поэтому полезны в ряде терапевтических областей. Соединения по изобретению имеют ценность для куративного или профилактического лечения половых расстройств у млекопитающих. В частности, эти соединения имеют ценность при лечении половых дисфункций у млекопитающих, например мужской эректильной дисфункции (МЭД), импотенции, женской половой дисфункции (ЖПД), клиторальной дисфункции, женского расстройства, представляющего собой гипоактивное половое желание,женского расстройства полового возбуждения,женского полового болевого расстройства или женской половой оргазмической дисфункции(ЖПОД), а также половой дисфункции вследствие повреждения спинного мозга или половой дисфункции, индуцированной избирательным ингибитором обратного захвата серотонина(ИОЗС). Однако ясно, что они также будут полезны для лечения других медицинских состояний, для которых показан сильнодействующий и избирательный ингибитор цГМФ-ФДЭ 5. Такие состояния включают преждевременные роды, дисменорею, доброкачественную гиперплазию простаты (ДГП), синдром инфравезикальной обструкции, недержание, стабильную, нестабильную и вариантную (Принцметала) стенокардию, гипертензию, легочную гипертензию, хроническую обструктивную болезнь легких, коронарную артериальную болезнь, застойную сердечную недостаточность, атеросклероз, состояния пониженной проходимости кровеносных сосудов, например, после чрескожной транслюминальной коронаропластики(post-PTCA), заболевание периферических сосудов, удар, нитрат-индуцированную толерантность, бронхит, аллергическую астму, хроническую астму, аллергический ринит, заболевания и состояния глаза, такие как глаукома, оптическая невропатия, дегенерация желтого пятна,повышенное внутриглазное давление, ретинальная или артериальная окклюзия и заболевания,характеризующиеся расстройствами перистальтики кишечника, например синдром раздраженного кишечника (СРК). Дополнительные медицинские состояния,для которых показан сильнодействующий и избирательный ингибитор цГМФ-ФДЭ 5 и для которых полезным может быть лечение соединениями по изобретению, включают преэклампсию, синдром Кавасаки, толерантность к нитратам, рассеянный склероз, диабетическую нефропатию, невропатию, включая автономную 2 и периферическую невропатию и, в частности,диабетическую невропатию и ее симптомы, например парез желудка, периферическую диабетическую невропатию, болезнь Альцгеймера,острую респираторную недостаточность, псориаз, некроз кожи, рак, метастазирование, облысение, "щелкающий" пищевод, трещину заднего прохода, геморрой, гипоксическую вазоконстрикцию, а также стабилизацию кровяного давления во время гемодиализа. Особенно предпочтительные состояния включают в себя МЭД и ЖПД. Заявка PCT/IB 99/00519 относится к ряду пиразоло[4,3-d]пиримидин-7-онов, которые ингибируют фосфодиэстеразы циклического гуанозин-3',5'-монофосфата (цГМФ-ФДЭ). Соответственно, согласно настоящему изобретению предложены соединения формулы или их фармацевтически или ветеринарно приемлемые соли, или фармацевтически или ветеринарно приемлемые сольваты любого из вышеуказанного,где R1 представляет собой С 1-С 6 алкил или С 3 С 6 алкенил, С 3-С 6 циклоалкил или С 4-С 6 циклоалкенил, где указанная алкильная группа может быть разветвленной или прямоцепочечной,и где, когда R1 представляет собой С 1-С 3 алкил,тогда указанная алкильная группа замещена, и где, когда R1 представляет собой С 4-С 6 алкил,С 3-С 6 алкенил или С 3-С 6 циклоалкил, тогда указанная алкильная, алкенильная или циклоалкильная группа возможно замещена одним или более чем одним заместителем, выбранным из гидрокси; С 1-С 4 алкокси; С 3-С 6 циклоалкила; фенила, замещенного одним или более чем одним заместителем, выбранным из С 1-С 3 алкила, С 1 С 4 алкокси,С 1-С 4 галогеноалкила,С 1-С 4 галогеноалкокси, галогено, CN, NO2, NHR11,NHCOR12, NHSO2R12, SO2R12, SO2NHR11, COR11 или CO2R11, где указанные галогеноалкильные и галогеноалкоксигруппы содержат один или более чем один атом галогена; NR7R8, CONR7R8 или NR7COR11,где R7 и R8, каждый независимо, выбран из Н,С 1-С 4 алкила, С 3-С 4 алкенила, CO2R9 или SO2R9,где указанные алкильные или алкенильные группы возможно замещены С 1-С 4 галогеноалкилом или С 1-С 4 галогеноалкокси; Het1; Het2 или Het3; либо R1 представляет собой Het4 или фенил, где указанная фенильная группа возможно 3 замещена одним или более чем одним заместителем, выбранным из С 1-С 4 алкила, С 3-С 4 алкенила, С 1-С 4 алкокси, галогено, CN, CF3, OCF3, NO2,NHR11, NHCOR12, NHSO2R12, SO2R12, SO2NHR11,COR11, CO2R11;R3 представляет собой С 1-С 6 алкил, возможно замещенный одним или двумя заместителями, выбранными из С 3-С 5 циклоалкила, гидрокси, С 1-С 4 алкокси, бензилокси, NR5R6, фенила, Het1, Het2, Het3 или Het4, где С 1-С 6 алкильные и С 1-С 4 алкоксигруппы возможно могут оканчиваться галогеноалкильной группой, такой какCF3, и где С 3-С 5 циклоалкильная группа возможно может быть замещена С 1-С 4 алкилом, гидрокси или галогено; С 3-С 6 циклоалкил; Het1, Het2,Het3 или Het4;R10 в положении 4 пиперазинильной группы, где указанная пиперазинильная группа возможно замещена одной группой или двумя С 1-С 4 алкильными группами и возможно находится в форме 4-N-оксида;R9 представляет собой С 1-С 4 алкил, возможно замещенный С 1-С 4 галогеноалкилом, С 1 С 4 галогеноалкокси или фенилом, где указанная фенильная группа возможно замещена одним или более чем одним заместителем, выбранным из С 1-С 4 алкила, возможно замещенного С 1-С 4 галогеноалкилом или С 1-С 4 галогеноалкокси, С 1-С 4 алкокси, галогено, CN, NO2, NHR11, NHCOR12,NHSO2R12, SO2R12, SO2NHR11, COR11 илиR10 представляет собой Н; С 1-С 4 алкил,возможно замещенный одним или двумя заместителями, выбранными из гидрокси, NR5R6,CONR5R6, фенила, возможно замещенного С 1 С 4 алкилом или С 1-С 4 алкокси; С 3-С 6 алкенил или 4 или более чем один дополнительный гетероатом, выбранный из S, N или О;Het2 представляет собой С-связанную 5 членную гетероциклическую группу, содержащую гетероатом О, S или N, возможно содержащую один или более чем один гетероатом,выбранный из N, О или S;Het3 представляет собой С-связанную 6 членную гетероциклическую группу, содержащую гетероатом О или S, возможно содержащую один или более чем один гетероатом, выбранный из О, S или N, либо Het3 представляет собой С-связанную 6-членную гетероциклическую группу, содержащую три гетероатома N;Het4 представляет собой С-связанную 4-, 5 или 6-членную гетероциклическую группу, содержащую один, два или три гетероатома, выбранных из S, О или N; и где любая из указанных гетероциклических групп Het1, Het2, Het3 или Het4 может быть насыщенной, частично ненасыщенной или ароматической, и где любая из указанных гетероциклических групп возможно может быть замещена одним или более чем одним заместителем, выбранным из С 1-С 4 алкила, С 3-С 4 алкенила,С 1-С 4 алкокси, галогено, CF3, CO2R11, COR11,SO2R12, NHR11 или NHCOR12, и/или где любая из указанных гетероциклических групп является бензоконденсированной; при условиях, что (а) когда R1 представляет собой С 1-С 3 алкил, тогда Het1 не является морфолинилом или пиперидинилом, и (б) когдаR1 представляет собой С 1-С 3 алкил, замещенный фенилом, тогда указанная фенильная группа не замещена С 1-С 4 алкокси, галогено, CN, CF3,OCF3 или С 1-С 4 алкилом. Как будет понятно специалисту-химику,общая формула (I) может быть представлена региоизомерными общими формулами (IA) и(IB). Соответственно, согласно настоящему изобретению предложены соединения формул (IA) и (IB) где R1, R2, R4 и R13 являются такими, как определено здесь выше. В приведенных выше определениях, если не указано иное, алкильные, алкокси и алкенильные группы, имеющие три или более чем три атома углерода, и алканоильные группы,имеющие четыре или более чем четыре атома углерода, могут быть прямоцепочечными или разветвленными. Например,заместитель С 4 алкил может находиться в форме нормального бутила (н-бутила), изобутила (изобутила),вторичного бутила (втор-бутила) или третично 5 го бутила (трет-бутила). Термин атом галогена включает в себя Cl, Br, F или I. Галогеноалкил и галогеноалкокси предпочтительно представляют собой -CF3 и -OCF3 соответственно. Термин"ароматический", как определено здесь, означает полностью ненасыщенную систему. Соединение формулы (I) содержит один или более чем один асимметрический атом углерода и, следовательно, существует в двух или более чем двух стереоизомерных формах. Если соединение формулы (I) содержит алкенильную или алкениленовую группу, то может иметь место также цис (Е) или транс (Z) изомерия. Настоящее изобретение охватывает индивидуальные стереоизомеры соединений формулы (I) и,если это свойственно, их индивидуальные таутомерные формы, и их смеси. Разделение диастереоизомеров или цис и транс изомеров может быть выполнено стандартными методами,например фракционной кристаллизацией, хроматографией или ВЭЖХ смеси стереоизомеров соединения формулы (I) или его подходящей соли или производного. Индивидуальный энантиомер соединения формулы (I) может быть получен также из соответствующего оптически чистого промежуточного соединения либо разделением, например ВЭЖХ, соответствующего рацемата с использование подходящей хиральной фазы, либо фракционной кристаллизацией диастереоизомерных солей, образованных путем взаимодействия соответствующего рацемата с подходящей оптически активной кислотой или основанием, где как подходит. Все стереоизомеры входят в объем изобретения. Соединения формул (IA) и (IB) могут также существовать в таутомерных формах, и данное изобретение охватывает как их смеси, так и индивидуальные таутомеры. В объем изобретения также входят меченные радиоактивными изотопами производные соединений формул (I), (IA) и (IB), которые пригодны для биологических исследований. Фармацевтически или ветеринарно приемлемые соли соединений по изобретению, которые содержат основной центр, представляют собой, например, нетоксичные соли присоединения кислоты, образованные с неорганическими кислотами, такими как соляная, бромоводородная, йодоводородная, серная и фосфорная кислоты, с карбоновыми кислотами или с органосульфоновыми кислотами. Примеры включают соли HCl, HBr, HI, сульфат или бисульфат,нитрат, фосфат или гидрофосфат, ацетат, бензоат, сукцинат, сахарат, фумарат, малеат, лактат,цитрат, тартрат, глюконат, камсилат, метансульфонат, этансульфонат, бензолсульфонат, птолуолсульфонат и памоат. Соединения по изобретению могут также образовывать с основаниями фармацевтически или ветеринарно приемлемые соли металлов, в частности нетоксичные соли щелочных или щелочно-земельных 6 металлов. Примеры включают соли натрия, калия, алюминия, кальция, магния, цинка и диэтаноламинные соли. Подходящие фармацевтические соли рассмотрены в Berge et al., J. Pharm.Sci., 66, 1-19, 1977. Фармацевтически приемлемые сольваты соединений по изобретению включают их гидраты. В объем соединения и различных солей по изобретению включены также их полиморфы. Предпочтительную группу соединений формул (I), (IA) и (IB) составляют соединения,где R1 представляет собой С 1-С 6 алкил или С 3 С 6 алкенил, где указанные алкильные или алкенильные группы могут быть разветвленными или прямоцепочечными, либо R1 представляет собой С 3-С 6 циклоалкил или С 4-С 6 циклоалкенил,и где, когда R1 представляет собой С 1-С 3 алкил,тогда указанная алкильная группа замещена; и где, когда R1 представляет собой С 4-С 6 алкил,С 3-С 6 алкенил,С 3-С 6 циклоалкил или С 4 С 6 циклоалкенил, тогда указанная алкильная,алкенильная, циклоалкильная или циклоалкенильная группа возможно замещена одним или более чем одним заместителем, выбранным из гидрокси; С 1-С 4 алкокси; С 3-С 4 циклоалкила; фенила, замещенного одним или более чем одним заместителем, выбранным из С 1-С 3 алкила, С 1 С 4 алкокси, С 1-С 4 галогеноалкила или С 1 С 4 галогеноалкокси, галогено, CN, NO2, NHR11,NHCOR12, NHSO2R12, SO2R12, SO2NHR11, COR11,CO2R11, где указанные галогеноалкильные и галогеноалкокси группы содержат один или более чем один атом галогена; NR7R8, CONR7R8 или NR7COR11; группы Het1, которая представляет собой N-связанную 4-членную Nсодержащую гетероциклическую группу; группы Het2, которая представляет собой Ссвязанную 5-членную гетероциклическую группу, содержащую гетероатом О, S или N, возможно содержащую один или более чем один гетероатом, выбранный из N, О или S; группыHet3, которая представляет собой С-связанную 6-членную гетероциклическую группу, содержащую гетероатом О или S, возможно содержащую один или более чем один гетероатом,выбранный из О, S или N, либо группы Het3,которая представляет собой С-связанную 6 членную гетероциклическую группу, содержащую три гетероатома N; где R7, R8, R11 и R12 являются такими, как определено здесь ранее,либо R1 представляет собой группу Het4,которая представляет собой С-связанную 4- или 5-членную гетероциклическую группу, содержащую один гетероатом, выбранный из S, О илиN; группу Het4, которая представляет собой Ссвязанную 6-членную гетероциклическую группу, содержащую один, два или три гетероатома,выбранных из S или О; группу Het4, которая представляет собой С-связанную 6-членную гетероциклическую группу, содержащую три 7 гетероатома азота; группу Het4, которая представляет собой С-связанную 6-членную гетероциклическую группу, содержащую один или два гетероатома азота, которая замещена одним или более чем одним заместителем, выбранным из С 1-С 4 алкила, С 1-С 4 алкокси, CO2R11, SO2R12,COR11, NHR11 или NHCOR12, и которая возможно включает в себя дополнительный гетероатом,выбранный из S, О или N,где любая из указанных гетероциклических групп Het1, Het2, Het3 или Het4 является насыщенной, частично ненасыщенной или ароматической, как подходит, и где любая из указанных гетероциклических групп возможно замещена одним или более чем одним заместителем, выбранным из С 1-С 4 алкила, С 3-С 4 алкенила,С 1-С 4 алкокси, галогено, CO2R11, SO2R12, COR11 или NHR11, где R11 является таким, как определено здесь выше, и/или где любая из указанных гетероциклических групп является бензоконденсированной; либо R1 представляет собой фенил, замещенный одним или более чем одним заместителем, выбранным из СF3, OCF3, SO2R12 илиCO2R12, где R12 представляет собой С 1-С 4 алкил,который возможно замещен фенилом, С 1-С 4 галогеноалкил или С 1-С 4 галогеноалкокси, причем указанные галогеноалкильные и галогеноалкокси группы содержат один или более чем один атом галогена;R3 представляет собой С 1-С 6 алкил, возможно замещенный одним или двумя заместителями, выбранными из С 3-С 5 циклоалкила, гидрокси, С 1-С 4 алкокси, бензилокси, NR5R6, фенила, фуранила, тетрагидрофуранила или пиридинила, где указанные С 1-С 6 алкильные и С 1-С 4 алкоксигруппы возможно могут оканчиваться галогеноалкильной группой, такой как CF3; либо R3 представляет собой С 3-С 6 циклоалкил, 1(С 1-С 4 алкил)пиперидинил, тетрагидрофуранил или тетрагидропиранил;R4 представляет собой пиперазин-1 илсульфонильную группу, имеющую заместитель R10 в положении 4 пиперазинильной группы, где указанная пиперазинильная группа возможно замещена одной или двумя С 1-С 4 алкильными группами и возможно находится в форме 4-N-оксида;R10 представляет собой Н; С 1-С 4 алкил,возможно замещенный одним или двумя заместителями, выбранными из гидрокси, NR5R6,CONR5R6, фенила, возможно замещенного С 1 004982Het4; при условии, что когда R1 представляет собой С 1-С 3 алкил, замещенный фенилом, тогда указанная фенильная группа не замещена С 1 С 4 алкокси, CN, галогено, CF3, OCF3 или С 1 С 4 алкилом. Следующую предпочтительную группу соединений формул (I), (IA) и (IB) составляют соединения, где R1 представляет собой С 1 С 6 алкил, где указанный алкил может быть разветвленным или прямоцепочечным, либо R1 представляет собой С 3-С 6 циклоалкил,и где, когда R1 представляет собой С 1 С 3 алкил, тогда указанная алкильная группа замещена, и где, когда R1 представляет собой С 4 С 6 алкил или С 3-С 6 циклоалкил, тогда указанная алкильная или циклоалкильная группа возможно замещена одним или более чем одним заместителем, выбранным из гидрокси; С 1-С 2 алкокси; С 3-С 5 циклоалкила; NR7R8, NR7COR11 илиCOR11, где R7 и R8 каждый независимо выбран из Н, С 1-С 4 алкила или CO2R9, где R9 и R11 являются такими, как определено здесь ранее; группы Het1, которая представляет собой Nсвязанную 4-членную N-содержащую гетероциклическую группу; группы Het3, которая представляет собой С-связанную 6-членную гетероциклическую группу, содержащую гетероатом О или S, возможно содержащую один или более чем один гетероатом, выбранный из О, S или N, либо группы Het3, которая представляет собой С-связанную 6-членную гетероциклическую группу, содержащую три гетероатомаN; либо R1 представляет собой группу Het4,которая представляет собой С-связанную 4 членную гетероциклическую группу, содержащую один гетероатом, выбранный из S, О илиN, либо R1 представляет собой группу Het4, которая представляет собой С-связанную 6 членную гетероциклическую группу, содержащую один, два или три гетероатома, выбранных из S или О; где любая из указанных гетероциклических групп Het1, Het2, Het3 или Het4 является насыщенной, частично ненасыщенной или ароматической и возможно замещена одним или более чем одним заместителем, выбранным из С 1-С 4 алкила, С 1-С 4 алкокси, -CO2R11, -SO2R12,-COR11 или NHR11, где R11 и R12 являются такими, как определено здесь выше, и/или где любая из указанных гетероциклических групп является бензоконденсированной; либо R1 представляет собой фенил, замещенный одним или более чем одним заместителем, выбранным из CF3, -OCF3, -SO2R12, -COR11,-CO2R11, где R11 и R12 являются такими, как определено здесь выше;R3 представляет собой метил, этил, нпропил, изопропил, н-бутил, втор-бутил, изобутил или трет-бутил, возможно замещенный одним или двумя заместителями, выбранными из циклопропила, циклобутила, гидрокси, метокси,этокси, бензилокси, фенила, бензила, фуран-3 ила, тетрагидрофуран-2-илметила, тетрагидрофуран-3-илметила, пиридин-2-ила, пиридин-3 ила или NR5R6, где R5 и R6 каждый независимо выбран из Н и С 1-С 2 алкила;R4 представляет собой пиперазин-1 илсульфонильную группу, имеющую заместитель R10 в положении 4 пиперазинильной группы, где указанная пиперазинильная группа возможно замещена одной или двумя С 1 С 4 алкильными группами и возможно находится в форме 4-N-оксида; иR10 представляет собой Н, С 1-С 3 алкил,возможно замещенный одним или двумя заместителями, выбранными из гидрокси, NR5R6,CONR5R6, где R5 и R6 каждый независимо выбран из Н, С 1-С 4 алкила и С 3 алкенила. Предпочтительные соединения по настоящему изобретению включают 5-[2-этокси-5-(4-метилпиперазин-1-илсульфонил)пиридин-3-ил]-2-[2-метоксиэтил]-3-нпропил-2,6-дигидро-7H-пиразоло[4,3-d]пиримидин-7-он,5-[2-этокси-5-(4-метилпиперазин-1-илсульфонил)пиридин-3-ил]-3-этил-2-[2-метоксиэтил]2,6-дигидро-7H-пиразоло[4,3-d]пиримидин-7 он,5-[2-этокси-5-(4-этилпиперазин-1-илсульфонил)пиридин-3-ил]-2-[2-метоксиэтил]-3-нпропил-2,6-дигидро-7 Н-пиразоло[4,3-d]пиримидин-7-он,2-(втор-бутил)-5-[2-этокси-5-(4-этилпиперазин-1-илсульфонил)пиридин-3-ил]-3-этил-2,6 дигидро-7H-пиразоло[4,3-d]пиримидин-7-он,2-(изо-бутил)-5-[2-этокси-5-(4-этилпиперазин-1-илсульфонил)пиридин-3-ил]-3-этил-2,6 дигидро-7H-пиразоло[4,3-d]пиримидин-7-он,2-(циклопропилметил)-5-[2-этокси-5-(4 этилпиперазин-1-илсульфонил)пиридин-3-ил]-3 этил-2,6-дигидро-7H-пиразоло[4,3-d]пиримидин-7-он,2-(циклобутилметил)-5-[2-этокси-5-(4-этилпиперазин-1-илсульфонил)пиридин-3-ил]-3-этил 2,6-дигидро-7 Н-пиразоло[4,3-d]пиримидин-7-он,5-[2-этокси-5-(4-этилпиперазин-1-илсульфонил)пиридин-3-ил]-3-этил-2-[2-метоксиэтил]-2,6 дигидро-7 Н-пиразоло[4,3-d]пиримидин-7-он,5-[2-этокси-5-(4-этилпиперазин-1-илсульфонил)пиридин-3-ил]-3-этил-2-[2-метокси 1-метилэтил]-2,6-дигидро-7H-пиразоло[4,3-d] пиримидин-7-он,5-[2-этокси-5-(4-этилпиперазин-1-илсульфонил)пиридин-3-ил]-3-этил-2-[2-(метиламино)этил]-2,6-дигидро-7 Н-пиразоло[4,3-d]пиримидин-7-он,2-(2-диметиламиноэтил)-5-[2-этокси-5-(4 этилпиперазин-1-илсульфонил)пиридин-3-ил]-3 004982[4,3-d]пиримидинон,2-циклобутилметил-3-этил-5-[5-(4-этилпиперазин-1-илсульфонил)-2-(тетрагидро-2-фуранилметокси)пиридин-3-ил]-2,6-дигидро-7H-пиразоло[4,3-d]пиримидинон,3-этил-5-[5-(4-этилпиперазин-1-илсульфонил)-2-(2-метоксиэтокси)пиридин-3-ил]-2-(2-метоксиэтокси)-2,6-дигидро-7H-пиразоло[4,3-d] пиримидинон,5-[2-этокси-5-(4-изо-пропилпиперазин-1 илсульфонил)пиридин-3-ил]-3-этил-2-(2-метоксиэтил)-2,6-дигидро-7 Н-пиразоло[4,3-d]пиримидинон и 5-[2-этокси-5-(4-н-пропилпиперазин-1 илсульфонил)пиридин-3-ил]-3-этил-2-(2-метоксиэтил)-2,6-дигидро-7H-пиразоло[4,3-d]пиримидинон. Еще одну предпочтительную группу соединений формул (I), (IA) и (IB) составляют соединения, гдеR1 представляет собой метил, этил, изопропил или н-пропил, замещенные одним или более чем одним заместителем С 1-С 4 алкокси,где указанный заместитель алкокси может быть присоединен непосредственно к любому атому С в пределах этильной, изопропильной или н 004982R1 представляет собой С 4 алкильную группу, выбранную из изо-, н-, втор- или третбутила, возможно замещенного одним или более чем одним заместителем, выбранным из С 1 С 4 алкокси или С 3-С 4 циклоалкила;R13 представляет собой OR3, где R3 представляет собой С 1-С 4 алкил, возможно замещенный одним или двумя заместителями С 1 С 4 алкокси, где указанные С 1-С 4 алкильные и С 1 С 4 алкоксигруппы возможно могут оканчиваться галогеноалкильной группой, такой как CF3;R4 представляет собой пиперазин-1 илсульфонильную группу, имеющую единственный заместитель R10 в положении 4 пиперазинильной группы и возможно находится в форме 4-N-оксида; и R10 представляет собой метил, этил, нпропил или изопропил. Особо предпочтительную группу соединений формул (I), (IA) и (IB) составляют соединения, гдеR1 представляет собой метил, этил, изопропил или н-пропил, которые замещены метокси,этокси, н-пропокси или изопропокси, где указанный заместитель алкокси может быть непосредственно присоединен к любому атому С в пределах этильной, изопропильной или нпропильной групп, кроме атома С, непосредственно связанного с пиразольным кольцом; либоR13 представляет собой OR3, где алкильная группа R3 представляет собой метил, этил, нпропил, изопропил, изобутил, н-бутил, вторбутил или трет-бутил, возможно замещенные одним или двумя заместителями метокси, этокси, н-пропокси или изопропокси; иR4 представляет собой 4-метильную, 4 этильную, 4-н-пропильную или 4-изопропилпиперазин-1-илсульфонильную группу. В очень предпочтительном воплощении настоящего изобретения предложено соединение формулы (IB), гдеR1 представляет собой метил, этил, изопропил или н-пропил, которые замещены метокси,этокси, н-пропокси или изопропокси, где ука 15 занный заместитель алкокси может быть непосредственно присоединен к любому атому С в пределах этильной, изопропильной или нпропильной групп, кроме атома С, непосредственно связанного с пиразольным кольцом; либоR13 представляет собой OR3, где алкильная группа R3 представляет собой метил, этил, нпропил, изопропил, изобутил, н-бутил, вторбутил или трет-бутил; иR4 представляет собой 4-метильную или 4 этилпиперазин-1-илсульфонильную группу. Очень предпочтительные соединения согласно настоящему изобретению включают 1-6 этокси-5-[3-этил-6,7-дигидро-2-(2-метоксиэтил)-7 оксо-2 Н-пиразоло[4,3-d]пиримидин-5-ил]-3-пиридилсульфонил-4-этилпиперазин и его соли и полиморфы. Предпочтительными солями 1-6-этокси-5-[3-этил-6,7-дигидро-2-(2-метоксиэтил)-7-оксо 2 Н-пиразоло[4,3-d]пиримидин-5-ил]-3-пиридилсульфонил-4-этилпиперазина являются соли сульфоновой кислоты, более предпочтительно птолуолсульфонат, бензолсульфонат, камфорсульфонат и этансульфонат соответственно, и особенно бензолсульфонат. Согласно следующему аспекту настоящего изобретения предложены соединения общей формулы I или их фармацевтически или ветеринарно приемлемые соли, либо фармацевтически или ветеринарно приемлемые сольваты любого из вышеуказанного, гдеR1 представляет собой С 1-С 6 алкил или С 3 С 6 алкенил, С 3-С 6 циклоалкил или С 3-С 6 циклоалкенил, где указанная алкильная группа может быть разветвленной или прямоцепочечной,и где когда R1 представляет собой С 1 С 3 алкильную группу, тогда указанная алкильная группа замещена, и где когда R1 представляет собой С 4-С 6 алкил, С 3-С 6 алкенил или С 3 С 6 циклоалкил, тогда указанная алкильная, алкенильная или циклоалкильная группа возможно замещена одним или более чем одним заместителем, выбранным из гидрокси; С 1-С 4 алкокси; С 3-С 6 циклоалкила; фенила, замещенного одним или более чем одним заместителем, выбранным из С 1-С 3 алкила, С 1-С 4 алкокси, С 1-С 4 галогеноалкила или С 1-С 4 галогеноалкокси, где указанные галогеноалкильные и галогеноалкокси группы содержат один или более чем один атомNR7R8, CONR7R8 или NR7COR11, где R7 и R8,каждый независимо, выбран из Н, С 1-С 4 алкила,С 2-С 4 алкенила, С 1-С 4 алкокси, CO2R9, SO2R9, где указанные алкильные, алкенильные или алкоксигруппы возможно замещены С 1 С 4 галогеноалкилом или С 1-С 4 галогеноалкокси, и где R9 представляет собой С 1-С 4 алкил, который возможно замещен фенилом, где указанная фенильная группа возможно замещена одним или более чем одним заместителем, выбранным из С 1-С 4 алкила, возможно замещенного С 1 С 4 галогеноалкилом или С 1-С 4 галогеноалкокси,С 1-С 4 алкокси, галогено, CN, NO2, NHR11,NHSO2R12, SO2R12, SO2NHR11, COR11 илиCO2R11; Het1; Het2 или Het3; либо R1 представляет собой Het4 или фенил, где указанная фенильная группа возможно замещена одним или более чем одним заместителем, выбранным из С 1-С 4 алкила, С 2-С 4 алкенила, С 1-С 4 алкокси, галогено, CN, CF3, OCF3,NO2, NHR11, NHSO2R12, SO2R12, SO2NHR11,COR11, CO2R11;R3 представляет собой С 1-С 6 алкил, возможно замещенный одним или двумя заместителями, выбранными из С 3-С 5 циклоалкила, гидрокси, С 1-С 4 алкокси, бензилокси, NR5R6, фенила, Het1, Het2, Het3 или Het4, где С 1-С 6 алкильные и С 1-С 4 алкокси группы возможно могут оканчиваться галогеноалкильной группой, такой какR4 представляет собой пиперазин-1 илсульфонильную группу, имеющую заместитель R10 в положении 4 пиперазинильной группы, причем указанная пиперазинильная группа возможно замещена одной или двумя С 1-С 4 алкильными группами и возможно находится в форме 4-N-оксида;R10 представляет собой Н; С 1-С 4 алкил,возможно замещенный одним или двумя заместителями, выбранными из гидрокси, NR5R6,CONR5R6, фенила, возможно замещенного С 1-С 4 алкилом или С 1-С 4 алкокси; С 2-С 6 алкенил илиHet1 представляет собой N-связанную 4-,5- или 6-членную азотсодержащую гетероциклическую группу, возможно содержащую один или более чем один дополнительный гетероатом, выбранный из S, N или О;Het2 представляет собой С-связанную 5 членную гетероциклическую группу, содержащую гетероатом О, S или N, возможно содержащую один или более чем один гетероатом,выбранный из О или S;Het3 представляет собой С-связанную 6 членную гетероциклическую группу, содержащую гетероатом О или S, возможно содержащую один или более чем один гетероатом, выбранный из О, S или N, либо Het3 представляет собой С-связанную 6-членную гетероциклическую группу, содержащую три гетероатома N;Het4 представляет собой С-связанную 4-, 5 или 6-членную гетероциклическую группу, содержащую один, два или три гетероатома, выбранные из S, О или N; и где любая из указанных гетероциклических групп Het1, Het2, Het3 или Het4 может быть насыщенной, частично ненасыщенной или ароматической, и где любая из указанных гетероциклических групп возможно может быть замещена одним или более чем одним заместителем, выбранным из С 1-С 4 алкила, С 2-С 4 алкенила,С 1-С 4 алкокси, галогено, CO2R11, COR11, SO2R12 или NHR11, и/или где любая из указанных гетероциклических групп является бензоконденсированной; при условиях, что (а) когда R1 представляет собой С 1-С 3 алкил, тогда Het1 не является морфолинилом или пиперидинилом, и (б) когдаR1 представляет собой С 1-С 3 алкил, замещенный фенилом, тогда указанная фенильная группа не замещена С 1-С 4 алкокси, галогено, CN, CF3,OCF3 или С 1-С 4 алкилом. Согласно следующему аспекту изобретения предложены способы получения соединений формул (I), (IA) и (IB), их фармацевтически и ветеринарно приемлемых солей и фармацевтически и ветеринарно приемлемых сольватов любого из вышеуказанного, как проиллюстрировано ниже. Специалистам в данной области техники должно быть понятно, что в пределах некоторых из описанных способов порядок используемых стадий синтеза можно варьировать,и он будет зависеть, среди прочего, от таких факторов, как природа других функциональных групп, присутствующих в конкретном субстрате, доступность ключевых промежуточных соединений и выбранная стратегия защитных групп (если она есть). Ясно, что такие факторы будут также влиять на выбор реагентов для использования на указанных стадиях синтеза. Иллюстрацией стратегии защитных групп является путь до азетидиновых аналогов (примеры 18, 19 и 20), предшественник которых (подготовительные примеры 63, 66 и 61 соответственно) 18 содержит трет-бутоксикарбонил (Вос) в качестве защитной группы для азота. Очевидно также, что различные стандартные взаимные превращения и трансформации заместителей или функциональных групп в пределах определенных соединений формул (I),(IA) или (IB) будут давать другие соединения формул (I), (IA) или (IB). Примерами являются алкоксидный обмен по положению 2 заместителя 5-(пиридин-3-ил) (см. превращения соединения примера 3 в соединения примера 27, соединения примера 8 в соединения примеров 28 и 29, соединения примера 21 в соединения примеров 32 и 33, соединения примера 4 в соединения примера 41, соединения примера 9 в соединение примера 43 и соединения примера 66 в соединение примера 75), аминный обмен по положению 2 заместителя 5-(пиридин-3-ил) (см. превращения соединения примера 7 в соединения примера 78), реакции по заместителю, содержащему атом азота, такие как восстановительное алкилирование (соединение примера 18 в соединение примера 21), образование ацетамида (соединения примеров 18 и 20 в соединения примеров 22 и 24 соответственно) или образование сульфонамида (соединения подготовительных примеров 68 и 67 в соединения примеров 25 и 62 соответственно) и восстановление функциональной нитрогруппы с получением аминогруппы (соединение примера 63 в соединение примера 64). Удаления защиты и трансформации,описанные здесь и проиллюстрированные в разделах Примеры и Подготовительные примеры,могут быть осуществлены по методике "в одном реакторе" (см., например, превращение соединения подготовительного примера 65 в соединение примера 26). Следующие способы являются иллюстрацией общих способов синтеза, которые могут быть использованы с целью получения соединений по изобретению. 1. Соединение формулы (I) где формула (I) может в равной степени быть представленной общими формулами (IA) и (IB) и где R1, R2, R4 и R13 являются такими, как определено здесь ранее, можно получить из соединения общей формулы (IX)NR5R6) или X, где R13, R3, R5 и R6 являются такими, как определено выше, а X представляет собой уходящую группу, и где общая формула(IX) может быть представлена формулами пример, инертный растворитель, например ДМФ (диметилформамид) или NHR5R6 или их смеси, при температуре дефлегмации реакционной смеси, возможно в присутствии примерно 1 молярного эквивалента этилацетата или этилпивалата, либо эта реакция возможно может быть проведена в запаянном сосуде при температуре примерно 100-130 С, возможно в присутствии примерно 1 молярного эквивалента этилацетата или этилпивалата. 1.2 Общий путь синтеза соединений (I) через соединения (IXB) проиллюстрирован на схеме 1, где указанные промежуточные соединения (IXB) имеют общую формулу где R1, R2, R3, R4, R5 и R6 являются такими, как определено здесь ранее, и где X представляет собой уходящую группу и может представлять собой любую группу, которая способна к замещению на аминогруппу формулы -NR5R6 или алкоксигруппу, и где промежуточные соединения общих формул (IXA) и (IXB) могут быть представлены их региоизомерными общими формулами, как ранее проиллюстрировано для соединений, имеющих общие формулы (I). Здесь подходящие уходящие группы X включают галоген, алкокси, амино, тозилат и другие группы, детализированные ниже. 1.1 Соединение формулы (I), гдеR13=NR5R6, можно получить циклизацией соединения общей формулы (IXA) где R1, R2 и R4 являются такими, как определено здесь ранее для соединений формулы (I), (IA) и(IB) и где X представляет собой уходящую группу, как она определена здесь выше, реакцией в присутствии -OR3 и агента, захватывающего гидроксид. Превращение (IXB) в (I) может быть предпринято либо постадийно, либо "в одном реакторе". Реально выполнимым является ряд постадийных превращений, некоторые из которых являются подмножеством других. Они включают 1) циклизацию (IXB до XXX) с последующим замещением (XXX до I); 2) циклизацию (IXCa до XXX) с последующим замещением (XXX до I); 3) замещение (IXB до IXC) с последующей циклизацией (IXC до I) и 4) замещение (IXCa до IXC) с последующей циклизацией (IXC до I), где соединения где R , R , R , R и R являются такими, как определено здесь ранее для соединений формулы(I), (IA) или (IB). Предпочтительно, эту циклизацию опосредуют основанием, используя соль щелочного металла стерически затрудненного спирта или амина. Например, требуемая циклизация может быть осуществлена с использованием примерно 1-5-кратного, предпочтительно 1,2-3,5-кратного избытка трет-бутоксида калия,бис(триметилсилил)амида калия или карбоната цезия, возможно в присутствии молекулярных сит, в подходящем растворителе, таком как, на где R1, R2, R4 и X являются такими, как определено здесь выше, a OR3a представляет собой алкоксигруппу, которая отличается от желаемойOR3 группы и замещается на эту OR3 группу на конечных соединениях общей формулы (I), и где R3a выбран из С 1-С 6 алкила, возможно замещенного одним или двумя заместителями, выбранными из С 3-С 5 циклоалкила, гидрокси, С 1-С 4 алкокси, бензилокси, NR5R6, фенила, Het1, Het2,Het3 или Het4, где С 1-С 6 алкильные и С 1-С 4 алкоксигруппы возможно могут оканчиваться галогеноалкильной группой, такой как CF3, и где С 3-С 5 циклоалкильная группа возможно можетHet4. Предпочтительно, R3a представляет собой С 1-С 6 алкил. Для осуществления исходного замещения без значительной одновременной циклизации замещение на группу -OR3 (в (3) или (4 предпочтительно проводить при температуре в пределах от примерно 80 до примерно 90 С с получением соединения общей формулы (IXC). Последующую циклизацию до соединения общей формулы (I) в общем случае проводят при температуре выше примерно 115 С. Для осуществления исходной циклизации без значительного одновременного замещения на -OR3 в R3aOH, для (IXCa) до (XXX) (в (II,реакцию предпочтительно проводить при температуре выше примерно 110 С. Последующее замещение до соединения общей формулы (I) в общем случае проводят с -OR3 в R3aOH при температуре в пределах от примерно 80 до примерно 90 С. Для превращения (IXB) в (I) (то есть (1) выше) предпочтительным может быть получение соединения общей формулы (I) непосредственно из соединений общей формулы (IXB),поскольку оба компонента данного взаимодействия, как циклизацию, так и замещение, можно проводить "в одном реакторе". Такой способ "в одном реакторе" может быть выполнен при более низких давлениях (то есть ближе к давлению окружающей среды), чем постадийный процесс циклизации и замещения (то есть (2) выше), если точка кипения R3OH выше, чем точка кипения R3aOH, и если точка кипенияR3aOH составляет менее примерно 115 С (то есть слишком низкая, чтобы осуществлять циклизацию при давлении окружающей среды). Следует отметить, что все же может возникнуть необходимость осуществлять такие способы при температурах, более высоких, чем точка кипения HOR3, то есть при более высоком давлении. В случае соединений общей формулы(IXC), как они подробно описаны здесь ниже,где X представляет собой OR3, соединения общей формулы (I) можно получить прямой циклизацией посредством реакции в присутствии вспомогательного основания, агента, захватывающего гидроксид, и соответствующего растворителя R3OH, или инертного растворителя,или их комбинации. Температура реакции соединений общей формулы (IXB) до соединений общей формулы(I) (такой как соответствующее образование соединений (IA) и (IB предпочтительно составляет по меньшей мере примерно 80 С, более предпочтительно от примерно 80 до примерно 130 С, еще более предпочтительно от примерно 100 до примерно 130 С и наиболее предпочтительно от примерно 115 до примерно 125 С. Эти температуры также подходят для превращения соединений (XXX) в (I), хотя в 22 этом случае температура, вероятно, могла бы быть более низкой (например примерно 60 С),поскольку циклизация не происходит. Предпочтительно, соединения формулыR1 представляет собой метил, этил, изопропил или н-пропил, замещенные метокси, этокси,н-пропокси или изопропокси, где указанный заместитель алкокси может быть непосредственно присоединен к любому атому С в пределах этильной, изопропильной или н-пропильной групп, кроме атома С, непосредственно связанного с пиразольным кольцом; либоR3 представляет собой метил, этил, н-пропил,изопропил, изобутил, н-бутил, втор-бутил или трет-бутил, возможно замещенные одним или двумя заместителями метокси, этокси, нпропокси или изопропокси; и R4 представляет собой 4-метильную, 4-этильную, 4-н-пропильную или 4-изопропилпиперазин-1-илсульфонильную группу,получают из соединений общей формулы (IXB),где X представляет собой OR3 (то есть соединений общей формулы (IXC), как подробно описано здесь выше и ниже). Соответственно, согласно следующему аспекту настоящего изобретения предложен еще один способ получения соединения общей формулы (I) или соединения общей формулы (IA) илиR1 представляет собой метил, этил, изопропил или н-пропил, замещенные метокси, этокси,н-пропокси или изопропокси, причем указанный заместитель алкокси может быть непосредственно присоединен к любому атому С в пределах этильной, изопропильной или н-пропильнойR3 представляет собой метил, этил, н-пропил,изопропил, изобутил, н-бутил, втор-бутил или трет-бутил, возможно замещенные одним или двумя заместителями метокси, этокси, нпропокси или изопропокси; и R4 представляет собой 4-метильную, 4-этильную, 4-н-пропильную или 4-изопропилпиперазин-1-илсульфонильную группу, при котором соединения общей формулы (IXC) где R1, R2, R3 и R4 являются такими, как определено здесь ранее, подвергают реакции, причем указанную реакцию проводят в присутствии-OR3 и агента, захватывающего гидроксид, или,альтернативно, подвергают реакции в присутствии агента, захватывающего гидроксид, и вспомогательного основания. Промежуточные соединения общей формулы (IXC) и, более конкретно, (IXCA) и (IXCB) составляют следующие аспекты изобретения. Особое преимущество от использования агента, захватывающего гидроксид, состоит в том, что можно получить более высокий выход конечного продукта (соединений общей формулы (I), (IA) или (IB, чем при той же реакции,где захватывающий агент не присутствует. Предпочтительно, агент, захватывающий гидроксид, представляет собой сложный эфир. Более предпочтительно, указанный агент, захватывающий гидроксид, представляет собой сложный эфир формулы где ОТ представляет собой OR3 или остаток объемистого спирта или не нуклеофильного спирта, либо ТОН представляет собой спирт,который может быть азеотропно удален в процессе реакции; и C(O)V представляет собой остаток карбоновой кислоты. Например, если OR3 представляет собой OEt в соединении (IXC),агентом, захватывающим гидроксид (TOC(O)V), 004982 24 может быть, например, этилацетат или этилпивалат. Предпочтительно, V представляет собой С 1-С 4 алкильную группу. Предпочтительно, X выбран из группы,состоящей из -OR3, галогено, возможно замещенной арилсульфонилоксигруппы, предпочтительно фенилсульфонилоксигруппы, более предпочтительно паразамещенный арил (фенил), например замещенный С 1-С 4 алкильной группой, например п-толуолсульфонилоксигруппы; С 1-С 4 алкилсульфонилоксигруппы, например метансульфонилоксигруппы; бензолсульфонилоксигруппы, которая замещена нитро или галогено, предпочтительно паразамещенной, например п-бромбензолсульфонилоксигруппы или п-нитробензолсульфонилоксигруппы; С 1-С 4 перфторалкилсульфонилоксигруппы, например трифторметилсульфонилоксигруппы; возможно замещенной ароилоксигруппы, такой как бензоилокси; С 1-С 4 перфторалканоилоксигруппы, такой как трифторацетилокси; С 1-С 4 алканоилоксигруппы, такой как ацетилокси; диазония; четвертичный аммонийС 1-С 4 алкилсульфонилоксигруппы; галогеносульфонилоксигруппы, например фторсульфонилокси и другие фторированные уходящие группы; и диарилсульфониламиногруппы, например дитозил (NTs2). Более предпочтительно, X представляет собой первичную или вторичную С 1-С 6 алкоксигруппу и особенно С 1-С 4 алкоксигруппу, такую как этокси или метокси.(чтобы замещать уходящую группу нуклеофильным замещением), и как основание (чтобы вызывать циклизацию).OR3 может образовываться в растворе из,например, соли ZOR3 (где Z представляет собой катион), такой как металлическая соль. Более конкретно, соль щелочного металла (такого как натрий или калий) или щелочно-земельного металла -OR3 в подходящем растворителе будет образовывать -OR3 в растворе. В другом воплощении -OR3 образуется in situ из R3OH плюс вспомогательное основание (то есть основание,иное чем -OR3). Однако в другой системе ZOR3 можно использовать в реакционной системе со вспомогательным основанием. Понятно, что растворитель, в котором эта реакция протекает, может представлять собойR3OH или инертный растворитель (либо смесь обоих). Под инертным растворителем авторы изобретения подразумевают растворитель, который не будет образовывать нуклеофил в реакционных условиях, или если нуклеофил образуется, то он является в достаточной степени стерически затрудненным или нереактивным, так что, в сущности, не конкурирует в реакции замещения. Если в качестве источника -OR3 используют R3OH, то отдельный растворитель по существу не требуется, но (вспомогательный) инертный растворитель (то есть растворитель, 25 иной чем R3OH) можно использовать в качестве сорастворителя в этой реакции. Подходящими растворителями являются следующие растворители: R3OH, вторичный или третичный С 4-С 12 алканол, С 3-С 12 циклоалканол,третичный С 4-С 12 циклоалканол, вторичный или третичный (С 3-С 7 циклоалкил)С 2-С 6 алканол, С 3 С 9 алканон, 1,2-диметоксиэтан, 1,2-диэтоксиэтан, диглим, тетрагидрофуран, 1,4-диоксан,толуол, ксилол, хлорбензол, 1,2-дихлорбензол,ацетонитрил, диметилсульфоксид, сульфолан,диметилформамид, N-метилпирролидин-2-он,пиридин и их смеси. Более предпочтительно, растворитель представляет собой R3OH, третичный С 4-С 12 алканол, третичный С 4-С 12 циклоалканол, третичный (С 3-С 7 циклоалкил)С 2-С 6 алканол, С 3-С 9 алканон, 1,2-диметоксиэтан, 1,2-диэтоксиэтан,диглим, тетрагидрофуран, 1,4-диоксан, толуол,ксилол, хлорбензол, 1,2-дихлорбензол, ацетонитрил, диметилсульфоксид, сульфолан, диметилформамид, N-метилпирролидин-2-он, пиридин и их смеси. Наиболее предпочтительно, растворитель представляет собой R3OH, что означает, чтоOR3 образуется in situ, например в присутствии вспомогательного основания. В способе по изобретению можно использовать широкий ряд вспомогательных оснований. Типично, эти основания практически не должны конкурировать с -OR3 в нуклеофильном замещении X (то есть, они не должны быть нуклеофильными), если они являются соответственно стерически затрудненными. Предпочтительно, вспомогательное основание выбирают из группы, состоящей из стерически затрудненного основания, гидрида металла, оксида металла, карбоната металла и бикарбоната металла. Стерически затрудненное основание предпочтительно представляет собой металлическую соль стерически затрудненного спирта или амина. Более предпочтительно, вспомогательные основания в соответствии с изобретением выбирают из группы, состоящей из металлических солей стерически затрудненного спирта или амина, такого как вторичный или третичный С 4 С 12 алканол, С 3-С 12 циклоалканол и вторичный или третичный (С 3-С 8 циклоалкил)С 1-С 6 алканол,N-(вторичный или третичный С 3-С 6 алкил)-N(первичный, вторичный или третичный С 3 С 6 алкил)амин, N-(С 3-С 8 циклоалкил)-N-(первичный, вторичный или третичный С 3-С 6 алкил) амин, ди-(С 3-С 8 циклоалкил)амин или гексаметилдисилазан; 1,5-диазабицикло[4,3,0]нон-5-ен и 1,8-диазабицикло[5,4,0]ундец-7-ен; гидрида,оксида, карбоната и бикарбоната металла. Еще более предпочтительно, вспомогательные основания в соответствии с изобретением выбирают из группы, состоящей из металлических солей стерически затрудненного спир 004982 26 та или амина, такого как третичный С 4-С 12 алканол, С 3-С 12 циклоалканол и третичный (С 3 С 8 циклоалкил)С 1-С 6 алканол, N-(вторичный или третичный С 3-С 6 алкил)-N-(первичный, вторичный или третичный С 3-С 6 алкил)амин, N-(С 3 С 8 циклоалкил)-N-(первичный, вторичный или третичный С 3-С 6 алкил)амин, ди-(С 3-С 8 циклоалкил)амин или гексаметилдисилазан; 1,5-диазабицикло[4,3,0]нон-5-ен и 1,8-диазабицикло[5,4,0]ундец-7-ен; гидрида, оксида, карбоната и бикарбоната металла. Еще более предпочтительно, вспомогательное основание выбирают из стерически затрудненных оснований предыдущего параграфа(то есть всех из них, за исключением гидрида,оксида, карбоната и бикарбоната металла). Наиболее предпочтительно, вспомогательное основание представляет собой металлическую соль третичного С 4-С 6 спирта, такую как соли щелочных или щелочно-земельных металлов (например Na/K) трет-бутанола или третамилового спирта, либо это основание представляет собой KHMDS (гексаметилдисилазан калия, или бис(триметилсилил)амид калия). Наиболее предпочтительно, вспомогательное основание представляет собой соль щелочного металла трет-бутанола (например третбутоксид калия). Металл соли ZOR3 и вспомогательного основания независимо может быть выбран из щелочных металлов (литий, натрий, калий, рубидий, цезий) или щелочно-земельных металлов(бериллий, магний, кальций, стронций, барий). Предпочтительно, металл представляет собой натрий, калий, литий или магний. Более предпочтительно, металл представляет собой натрий или калий. Когда X представляет собой любую группу, определенную здесь выше, за исключением-OR3, для максимизации выходов предпочтительно также использовать по меньшей мере примерно 1 молекулярный эквивалент вспомогательного основания и -OR3. Если -OR3 функционирует также как основание (то есть вспомогательное основание не присутствует), то предпочтительно присутствует по меньшей мере примерно 2 эквивалента -OR3. Соответственно,присутствует по меньшей мере 1 эквивалент захватывающего агента (предпочтительно по меньшей мере примерно 2 эквивалента). В случае если X=OR3 (то есть исходным соединением является (IXC), а не (IXB, то теоретически требуется по меньшей мере 1 эквивалент основания, причем указанное основание может представлять собой -OR3 или вспомогательное основание. Температура реакции соединений общей формулы (IXC) до соединений общей формулы(I) (например соответствующее образование соединений (IA) и (IB предпочтительно составляет по меньшей мере примерно 80 С, более предпочтительно от примерно 80 до при 27 мерно 130 С, еще более предпочтительно от примерно 100 до примерно 130 С и наиболее предпочтительно от примерно 115 до примерно 125 С. Температура реакции, достигаемая для осуществления превращения соединений общих формул (IXB), (IXC) или (XXX) в соединения общей формулы (I), зависит от растворителя,природы -OR3 и X. Когда X представляет собойOR3a (причем OR3a и OR3 не являются одинаковыми), т.е. соединение формулы (IXCa), и растворителем является R3OH, тогда предпочтительно удалять ХН (такой как С 1-С 6 спирт) азеотропной перегонкой (разумеется, реакционный сосуд должен быть изготовлен с расчетом на перегонку азеотропной смеси) с R3OH, проводя реакцию при температуре азеотропной смеси ХН и R3OH. Таким путем можно повысить выход и качество конечного продукта. Например,(в случае, когда X представляет собой алкокси,предпочтительно этанол) превращение соединения (XXX), (IXB) или (IXC) в (I) предпочтительно проводят при температуре азеотропной смеси спирта (то есть ХН (предпочтительно этанола с R3OH. Когда X=OR3, а растворитель представляет собой R3OH, нет необходимости отгонять R3OH азеотропной перегонкой. Соответственно, в предпочтительном воплощении настоящего изобретения предложен способ синтеза соединений общей формулы (I),(IA) или (IB) и, в частности, соединений общей формулы (I), (IA) или (IB), где R1 представляет собой (СН 2)n(С 3-С 4)циклоалкил, где n равно 1 или 2; либо R1 представляет собой (СН 2)n(С 3-С 6) циклоалкил, где n равно 0; либо R1 представляет собой (СН 2)n(С 5)циклоалкил, где n равно 1; либоR1 представляет собой метил, этил, изопропил или н-пропил, которые замещены метокси,этокси, н-пропокси или изопропокси, где указанный заместитель алкокси может быть присоединен непосредственно к любому атому С в пределах этильной, изопропильной или нпропильной групп; либо R1 представляет собой изо-, н-, втор- или трет-бутил; R2 представляет собой С 2-С 4 алкил; R13 представляет собой OR3,где алкильная группа R3 представляет собой метил, этил, н-пропил, изопропил, изобутил, нбутил, втор-бутил или трет-бутил, возможно замещенные одним или двумя метокси, этокси,н-пропокси или изопропокси; и R4 представляет собой 4-метильную, 4-этильную, 4-н-пропильную или 4-изопропилпиперазин-1-илсульфонильную группу, при котором соединение общей формулы (IXB), (IXC) или (XID) соответственно подвергают взаимодействию а) с R3OH и вспомогательным основанием в инертном растворителе и в присутствии указанного захватывающего агента; или б) с ZOR3 и вспомогательным основанием 3 в R OH либо в инертном растворителе, либо в обоих в присутствии указанного захватывающего агента; или 28 в) с ZOR3 и R3OH либо в инертном растворителе, либо в обоих в присутствии указанного захватывающего агента; или г) со вспомогательным основанием в инертном растворителе, либо в R3OH, либо в их комбинации и с агентом, захватывающим гидроксид, для соединений общей формулы (IXC). 1.3 Для соединений общей формулы (IXB),где X представляет собой OR3, а в качестве растворителя выбран спирт, соединение формулы(I) можно получить циклизацией соединения общей формулы (IXC) где R1, R2, R3 и R4 являются такими, как определено здесь ранее для соединений формулы (I),(IA) и (IB). В указанной реакции в качестве растворителя следует использовать соответствующий спирт формулы R3OH, чтобы избежать потенциальных проблем, связанных с алкоксидным обменом по положению 2 пиридинового кольца, либо инертный растворитель, либо смесь этих двух растворителей. Соответствующий спирт, как определено здесь, означает, что спирт-растворитель должен иметь такую же длину алкильной цепи, как и заместитель алкокси (-OR3); например, если -OR3 представляет собой этокси, соответствующим спиртом является этанол. Предпочтительно, указанную циклизацию опосредуют основанием, причем используют соль щелочного металла стерически затрудненного спирта или амина. Например,требуемая циклизация может быть осуществлена с использованием примерно 1-8-кратного,предпочтительно примерно 1-5-кратного, более предпочтительно 1,2-3,5-кратного избытка третбутоксида калия или бис(триметилсилил)амида калия, возможно в подходящих условиях сушки,то есть в присутствии молекулярных сит или в условиях азеотропной перегонки, в подходящем растворителе, как описано выше, при температуре дефлегмации реакционной смеси, возможно в присутствии примерно 1-2 молярных эквивалентов агента, захватывающего гидроксид,такого как этилацетат или этилпивалат, либо эта реакция возможно может быть проведена в запаянном сосуде при температуре примерно 100130 С, возможно в присутствии примерно 1-2 молярных эквивалентов агента, захватывающего гидроксид, такого как этилацетат или этилпивалат. Альтернативными реакционными условиями для реакций циклизации соединений(IXC), где X представляет собой OR3, являются проведение этой реакции примерно с 1,2-4,5 молекулярными эквивалентами стерически затрудненного основания, такого как третбутоксид калия или KHMDS, возможно в запа 29 янном сосуде при температуре от примерно 100 до примерно 150 С, с использованием в качестве растворителя стерически затрудненного спирта, например 3-метилпентан-3-ола, а не спирта формулы R3OH, возможно в присутствии примерно 1-2 молярных эквивалентов этилацетата или этилпивалата. Соединение формулы (IXA) или соединение общей формулы (IXB), где X представляет собой OR3 (то есть соединение общей формулы(IXC, можно получить реакцией сочетания между соединением формулы (VII) где R1 и R2 являются такими, как определено здесь ранее для формул (IXA), (IXB) или (IXC),и соединением формулы (ХА), (ХВ) или (ХС) соответственно где R3, R4, R5, R6 и X также являются такими,как определено здесь ранее для формул (IXA),(IXB) или (IXC). Когда любой из R5 и/или R6 в группе -NR5R6 соединения формулы (ХА) представляет собой Н, тогда предпочтительно использовать подходящую стратегию N-защитных групп. Можно использовать любую известную подходящую стратегию защитных групп. Реакцию сочетания можно проводить, используя общепринятые методики образования амидной связи, то есть через ацилхлоридное производное соединения (ХА) или (ХВ) в присутствии вплоть до примерно пятикратного избытка третичного амина, такого как триэтиламин или пиридин, который действует в качестве соединения, связывающего кислотный побочный продукт (HY) для его удаления, возможно в присутствии катализатора, такого как 4 диметиламинопиридин, в подходящем растворителе, таком как дихлорметан, при температуре от примерно 0 С до примерно комнатной температуры. Для удобства, пиридин можно также использовать в качестве растворителя. В частности, можно использовать любой из множества вариантов аминокислотного сочетания. Например, кислоту формулы (ХА), (ХВ) или (ХС) или ее подходящую соль (например натриевую соль) можно активировать, используя карбодиимид, такой как 1,3-дициклогексилкарбодиимид или 1-этил-3-(3-диметиламинопроп-1-ил)карбодиимид, возможно в присутствии 1-гидроксибензотриазола гидрата и/или 30 катализатора, такого как 4-диметиламинопиридин, либо используя галогенотрисаминофосфониевую соль, такую как бромтрис(пирролидино) фосфония гексафторфосфат, либо используя подходящую пиридиниевую соль, такую как 2 хлор-1-метилпиридиния йодид. Сочетание любого типа проводят в подходящем растворителе,таком как дихлорметан, тетрагидрофуран илиN,N-диметилформамид, возможно в присутствии третичного амина, такого как триэтиламин или N-этилдиизопропиламин (например, когда либо соединение формулы (VII), либо активирующий реагент присутствует в форме соли присоединения кислоты), при температуре от примерно 0 С до примерно комнатной температуры. Предпочтительно используют от 1 до 2 молекулярных эквивалентов активирующего реагента и от 1 до 3 молекулярных эквивалентов любого присутствующего третичного амина. В еще одном варианте карбоновокислотную функциональную группу соединения (ХА),(ХВ) или (ХС) можно сначала активировать,используя вплоть до примерно 5% избыток реагента, такого как N,N-карбонилдиимидазол, в подходящем растворителе, например в этилацетате или бутан-2-оне, при температуре от примерно комнатной температуры до примерно 80 С с последующим взаимодействием промежуточного имидазолида с соединением (VII) при температуре от примерно 20 до примерно 90 С. Понятно, что общая формула (VII) может быть также представлена региоизомерными формулами (VIIA) и (VIIB) где R1 и R2 являются такими, как определено здесь ранее. 4-Аминопиразол-5-карбоксамидные соединения, имеющие общие формулы (VII),(VIIA) или (VIIB), можно получить из пиразольных соединений общей формулы (XIII) где Rq выбран из ОН, С 1-С 6 алкокси или NR5R6,где R5 и R6 являются такими, как определено здесь выше, согласно методикам, подробно описанным здесь в разделе Подготовительные примеры и, в частности, описанным в подготовительных примерах 96(а)-96(з).(ХА) или (ХС), можно получить из карбоновых кислот общих формул (VIIIA), (VIIB) или где R3, R5 и R6 являются такими, как определено для соединений общих формул (I), (IA) и (IB),путем взаимодействия с 4-R10-пиперизинильным соединением, таким как, например, 4 метилпиперизин. Такое взаимодействие может быть проведено при температуре от примерно 0 С до примерно комнатной температуры,предпочтительно в присутствии соответствующего растворителя, такого как C1-C3 алканол или дихлорметан, возможно в присутствии подходящего основания, такого как триэтиламин, для удаления побочного кислотного продукта (HY). В случаях, когда либо R5, либо R6 представляет собой Н, можно использовать подходящую стратегию защиты аминогруппы, как подробно описано здесь выше. Соединения общих формул (VIIIA),(VIIIB) или (VIIIC) можно получить из соединений общих формул (XIA), (XIB) или (XIC) соответственно где R3, R5, R6 и X также являются такими, как определено для соединений общих формул (I),(IA) или (IB), применяя известные методы превращения аминогруппы в группу SO2Y, где Y представляет собой галогено, предпочтительно хлоро. Например, когда Y представляет собой хлоро, действуют примерно двукратным избытком нитрита натрия в смеси концентрированной соляной кислоты и ледяной уксусной кислоты при температуре от примерно -25 С до примерно 0 С с последующей обработкой избытком жидкого диоксида серы и раствором примерно трехкратного избытка хлорида меди в водной уксусной кислоте при температуре от примерно-15 С до примерно комнатной температуры. Когда R13 содержит первичную или вторичную аминогруппу, как правило, предпочтительной будет защита указанной аминогруппы кислотостойкой группой, такой как ацетил или бензил. Соединения общей формулы (XIA), (XIB) и (XIC) можно получить восстановлением соединений общих формул (XIIA), (XIIB) и (ХIIС) соответственно где R3, R5, R6 и X являются такими, как определено ранее. Такого превращения соединений общих формул (XIIA), (XIIB) и (ХIIС) в соединения общих формул (XIA), (XIB) и (XIC) можно достичь общепринятыми способами каталитического гидрирования или гидрирования путем каталитического переноса водорода. В типичном случае, гидрирование осуществляют,используя катализатор никель Ренея (RTM) или палладиевый катализатор, такой как 10% Pd на углероде, в подходящем растворителе, таком как этанол, при давлении водорода от примерно 345 кПа (50 фунт/кв. дюйм) до примерно 414 кПа (60 фунт/кв. дюйм) при температуре от примерно комнатной температуры до примерно 60 С, предпочтительно от примерно 40 до примерно 50 С. Промежуточные соединения общей формулы (IXC), как описано здесь выше в 1.2 и 1.3,можно получить реакцией сочетания между соединением общей формулы (ХВ) и соединением общей формулы (VII), где указанного сочетания можно достичь любым из способов, описанных здесь выше. Соединения общей формулы (ХВ) можно получить путем, изображенным на схеме 2. В соответствии со схемой 2 промежуточное соединение формулы (ХВ) образуется из соединения формулы (XIV), причем конкретный способ зависит от уходящей группы X. Для соединений формулы (ХВ), где X = арилсульфонилокси, С 1-С 4 алкилсульфонилокси,С 1-С 4 перфторалкилсульфонилокси,арилокси,С 1-С 4 перфторалканоилокси, С 1-С 4 алканоилокси,четвертичный аммонийС 1-С 4 алкилсульфонилокси или галогеносульфонилокси, соединение(ХВ) может быть образовано из соединений(XIV) (где Q=OH и W=OH) и соответствующего дериватизирующего агента, более конкретно соответствующего сульфонилирующего агента,такого как арилсульфонилгалогенид, С 1-С 4 алкилсульфонилгалогенид,С 1-С 4 перфторалкилсульфонилгалогенид, арилгалогенид, С 1-С 4 перфторалканоилгалгенид,С 1-С 4 алканоилгалогенид, четвертичный аммонийС 1-С 4 алкилсульфонилгалогенид или галогеносульфонилгалогенид, либо соответствующего арилирующего агента, такого как арилгалогенид, либо соответствующего ацилирующего агента, такого как С 1 С 4 перфторалканоилгалогенид или С 1-С 4 алканоилгалогенид соответственно (предпочтительно заместитель галогенид вышеуказанных соединений представляет собой хлорид), в подходящем растворителе. Соединения формулы(XIV) (где Q=OH и W=OH) могут быть образо 33 ваны из соединений (XV) (где Р представляет собой способную гидролизоваться группу) с использованием гидролизующего агента, предпочтительно гидроксидного основания (идеально 2 молярных эквивалента), более предпочтительно гидроксида металла, такого как гидроксид натрия, в подходящем растворителе, таком как вода. Металл этого гидроксидного основания может быть таким, как определено здесь выше для Z (в ZOR). Это основание также используется для других реакций, приведенных ниже на схемах 2 и 3, где используется гидроксидное основание/гидролизующий агент. Если Р представляет собой группу, которая не способна гидролизоваться под действием гидроксида, то следует использовать подходящую стратегию удаления защиты согласно стандартной литературной практике. Соединения формулы (ХВ), где X = хлоро,могут быть образованы из (XIV), где Q = Cl иW = Р (такой как OEt) (то есть соединения формулы XV), и гидроксидного основания (идеально 1 молярный эквивалент), такого как гидроксид натрия, предпочтительно в подходящем растворителе, таком как вода, и агента, удаляющего защиту. Предпочтительно агент, удаляющий защиту, используемый здесь, в соответствии с изобретением представляет собой гидролизующий агент, более предпочтительно гидроксидный нуклеофил, предпочтительно гидроксидное основание (идеально 1 молярный эквивалент),такое как гидроксид натрия, предпочтительно в подходящем растворителе, таком как вода. Соединения формулы (ХВ), где X = диазоний, может быть образовано из соединения(XIV) (где Q = NH2, W = ОН) и азотной кислоты. Соединения формулы (XIV) (где Q = NH2,W = ОН) могут быть образованы из соединений формулы (XIV) (где Q = NH2, W = Р, напримерOEt) и агента, удаляющего защиту, такого как гидроксидное основание, например гидроксид натрия, в подходящем растворителе, таком как вода. Промежуточное соединение (XIV) (гдеQ = NH2, W = Р, например OEt) образуется из соединения (XV) и аммонирующего агента, такого как аммиак, в подходящем растворителе,таком как вода. Соединения формулы (ХВ), где X = диарилсульфониламино, могут быть образованы из соединения (XIV) (где Q=NH2, W=OH) и подходящего дериватизирующего агента, предпочтительно соответствующего сульфонилирующего агента, такого как арилсульфонилгалогенид,предпочтительно арилсульфонилхлорид (идеально по меньшей мере 2 молярных эквивалента), и предпочтительно в присутствии основания(идеально его 2 молярных эквивалента), такого как триэтиламин, в подходящем растворителе. Соединения формулы (ХВ), где X = предпочтительно первичная или вторичная С 1-С 6 34 быть образовано из соединения (XIV), (где Q = первичная или вторичная С 1-С 6 (предпочтительно С 1-С 4) алкоксигруппа, и W = Р, такой какOEt), предпочтительно гидроксидного основания, такого как гидроксид натрия, в подходящем растворителе, таком как вода. Соединения формулы (XIV), (где Q = первичная или вторичная С 1-С 6 (предпочтительно С 1-С 4) алкоксигруппа, иW = Р, например OEt) может быть образовано из соединения (XV) и подходящего алкоксида, OR-,где R представляет собой С 1-С 6 алкил, более предпочтительно С 1-С 4 первичный или вторичный алкил, такого как этоксид натрия, в подходящем растворителе, таком как толуол. Наиболее предпочтительно Р = X (где X представляет собой алкокси), поскольку это позволяет избежать трансэтерификации. Соединения формулы (XV) могут быть образованы из соединений формулы (XVI) путем взаимодействия с моно-N-замещенной пиперазиновой группой, где монозаместитель R10 является таким, как определено здесь выше, возможно в присутствии добавочного основания(которое не взаимодействует необратимо с сульфонилхлоридной группировкой), такого как триэтиламин, предпочтительно в подходящем растворителе, таком как толуол. D в соединениях (XV) и (XVI) представляет собой Cl илиBr. Монозамещенная пиперазиновая группа может также представлять собой основание, где присутствует более чем один эквивалент монозамещенного пиперазина. Предпочтительно используют 2 эквивалента. Если используют дополнительное основание, оно либо не взаимодействует с сульфонилхлоридной группировкой (например оксид, карбонат или бикарбонат металла), либо взаимодействует с сульфонилхлоридной группировкой таким образом, чтобы сохранять ее активированной для нуклеофильной атаки (например третичный амин, такой как триэтиламин). АминNH(R3)(R4) может также действовать в качестве основания, причем в этом случае предпочтительно присутствие более чем одного эквивалента, более предпочтительно примерно 2 эквивалентов (или более). Соединения формулы (XVI) могут быть образованы из соединений формулы (XX) в присутствии хлорирующего или бромирующего агента, такого как тионилхлорид или тионилбромид, более предпочтительно в присутствии катализатора галогенирования, еще более предпочтительно тионилхлорида или тионилбромида в присутствии диметилформамида. Тионилхлоро/бромо может также действовать как растворитель, но более предпочтительно эта реакция протекает в другом подходящем растворителе,таком как толуол. В этом случае потребуются только стехиометрические количества тионилхлорида/бромида, предпочтительно по меньшей мере 2 молярных эквивалента, более предпочти 35 тельно по меньшей мере 5 молярных эквивалентов. Четвертую стадию превращения соединения (XX) в соединение (ХВ) можно выполнять в одну телескопическую стадию без выделения промежуточного продукта, используя один и тот же растворитель на протяжении всей стадии(группу -OR3), то стадии превращения (XX) в(ХВ) можно складывать, используя единый растворитель, такой как не смешиваемый с водой инертный органический растворитель. Более предпочтительно использовать углеводородный растворитель (такой как толуол, ксилол, анизол,хлорбензол, гексан, гептан, октан, нонан, декан,циклогексан, метилциклогексан), или простые эфиры (такие как дибутиловый эфир, дифениловый эфир), или кетоны (такие как метилизобутилкетон, метилэтилкетон), или сложные эфиры(такие как этилацетат, бутилацетат), или диметилформамид. Еще более предпочтительно использовать углеводородный растворитель (такой как толуол, ксилол, анизол, хлорбензол,октан, нонан, декан, метилциклогексан), или простые эфиры (такие как дибутиловый эфир,дифениловый эфир), или сложные эфиры (такие как этилацетат, бутилацетат). Еще более предпочтительным телескопическим растворителем является толуол. Промежуточное соединение формулы(XX) образуется из соединения формулы (XVII) в присутствии агента, который образует защитную группу (Р) для карбоновой кислоты (то есть образует группу -СОР). Предпочтительно, указанный агент представляет собой агент этерификации для образования сложного эфира карбоновой кислоты (где, например, Р будет представлять собой алкокси, а агент, образующий защиту, будет представлять собой спирт), такой как С 1-С 6 эфир карбоновой кислоты, который будет проходить по реакционной схеме и подвергаться гидролизу в основных условиях до образования карбоновокислотной функциональной группы соединения (ХВ). Наиболее предпочтительно, этот агент этерификации представляет собой этанол. Дополнительный растворитель, такой как толуол, может быть уместным. Промежуточное соединение формулы(XVII) образуется из 2-гидроксиникотиновой кислоты или ее соли в присутствии сульфонилирующего агента, более предпочтительно агента, содержащего SO3 (идеально по меньшей мере 1 молекулярный эквивалент SО 3), например с использованием SО 3 в органическом растворителе (например в ТГФ, диоксане или гептане), либо в апротонном растворителе (например в нитробензоле, нитрометане, 1,4-диоксане,дихлорметане), либо в минеральной кислоте в качестве растворителя (например в серной кислоте), либо в жидкой карбоновой кислоте в 36 качестве растворителя (например в уксусной кислоте), либо в ТГФ, либо в гептане. Еще более предпочтительно сульфонилирующий агент представляет собой олеум (SО 3 в серной кислоте), такой как примерно 20-30% олеум. Соединения общей формулы (IXB) образуется в результате взаимодействия промежуточных соединений общей формулы (ХВ) с соединениями общей формулы (VII), как подробно описано здесь выше, в присутствии агента сочетания, такого как N,N-карбонилдиимидазол, и подходящего растворителя, такого как этилацетат. Способы получения соединений общей формулы (VII) описаны ниже. В предпочтительном воплощении способа схемы 2 X представляет собой алкоксигруппу-OR3, и поэтому Q в соединении (XIV) представляет собой OR3. Предпочтительно OR3 представляет собой С 1-С 6 алкоксигруппу, более предпочтительно первичную или вторичную С 1 С 4 алкоксигруппу и особенно этоксигруппу. Однако для других уходящих групп можно применять общий способ для схемы 2. Данное предпочтительное воплощение способа схемы 2 проиллюстрировано на схеме 3. На схеме 3 промежуточное соединение формулы (ХВ) образуется из соединения формулы(XIV) удалением защитной группы Р с помощью агента, удаляющего защиту, предпочтительно омылением в присутствии гидроксидного основания, такого как гидроксид натрия,предпочтительно в подходящем растворителе,таком как вода и толуол. Промежуточное соединение формулы(XIV) образуется из соединения формулы (XV) в присутствии подходящего С 1-С 6 алкоксидного нуклеофила (-OR3) (такого как первичный или вторичный алкоксид), предпочтительно алкоксида металла формулы ZOR3, где металл (Z) является таким, как определено здесь выше дляZOR, такого как этоксид натрия, предпочтительно в подходящем растворителе, таком как толуол или R3OH, где R3OH является таким, как определено выше, и предпочтительно представляет собой этокси. D в соединениях формул(XV) образуется из соединения формулы (XVI) в результате взаимодействия с N-R10 пиперазином, предпочтительно в присутствии основания,такого как триэтиламин, или избытка N-R10 пиперазина, предпочтительно в подходящем растворителе, таком как толуол. Промежуточное соединение формулы(XVI) образуется из соединения формулы (XX) в присутствии хлорирующего или бромирующего агента, как определено для такой же стадии на схеме 2, такого как тионилхлорид или бромид, предпочтительно тионилхлорид или бромид/диметилформамид. Первый может также 37 действовать как растворитель, но более предпочтительно эта реакция протекает в другом подходящем растворителе, таком как толуол. В этом случае потребуются только стехиометрические количества тионилхлорида/бромида,предпочтительно по меньшей мере 2 молярных эквивалента, более предпочтительно по меньшей мере 5 молярных эквивалентов. Промежуточное соединение формулы(XX) образуется из соединения формулы (XVII) в присутствии агента, который будет образовывать защитную группу (Р) для карбоновой кислоты (то есть образовывать группу -СОР), как определено выше. Предпочтительно, указанный агент представляет собой агент этерификации для образования сложного эфира карбоновой кислоты, такой как С 1-С 6 эфир карбоновой кислоты, который будет проходить по реакционной схеме и подвергаться гидролизу в основных условиях до карбоновокислотной функциональной группы соединения (ХВ). Наиболее предпочтительно этот агент этерификации представляет собой этанол. Можно использовать дополнительный растворитель, такой как толуол, если это уместно. Промежуточное соединение формулы(XVII) образуется из 2-гидроксиникотиновой кислоты с сульфонилирующим агентом, таким как 30% олеум. Опять же, возможно осуществление четвертой стадии превращения соединения (XX) в соединение (ХВ) в одну совмещенную стадию(как изложено выше) в одном реакторе без выделения промежуточного продукта, используя один и тот же растворитель на всем протяжении(здесь "телескопический растворитель"). Перечень растворителей, описанных в отношении схемы 2, применим непосредственно здесь. Наиболее предпочтительно, этот растворитель представляет собой толуол. Например, после образования соединения(XVI) избыток хлорирующего/бромирующего агента можно удалить азеотропной перегонкой при температуре азеотропной смеси указанного агента и телескопического растворителя. После образования соединения (XV) НВr/HCl соли (то есть HD), которые образуются, можно отмыть (в водном растворе) или отфильтровать из реакционного сосуда, а остаток водного растворителя(если его использовали) можно удалить азеотропной перегонкой с некоторым количеством телескопического растворителя. При образовании соединения (XIV), если алкоксид, используемый для введения OR3, растворяют в растворителе (таком как этанол), то этот растворитель снова можно удалить азеотропной перегонкой с некоторым количеством телескопического растворителя. Если используют твердый алкоксид,то эта последняя стадия азеотропной перегонки не требуется. Более предпочтительным телескопическим растворителем для любых телескопических стадий схемы 3 является толуол. 38 Понятно, что соли соединений из схем 1-3 можно образовать в соответствии с изобретением путем превращения соответствующего соединения в его соль (либо in situ, либо на отдельной стадии). Соль присоединения кислоты соединения формулы (I) также можно образовать в соответствии с изобретением. 1.4. Ясно, что для некоторых соединений формул (I), (IA) или (IB), где R13 представляет собой OR3, используя методологию циклизации и алкоксидного обмена, описанную в разделах 1.2 и 2.1, можно, что чрезвычайно предпочтительно, образовать соединение формулы (I), (IA) или (IB) из соединения общей формулы (IXCa),где 2-алкоксигруппа заместителя 5-(пиридин-3 ил) в первом отличается от таковой в последнем, прямо "в одном реакторе". Чтобы достичь этого, следует использовать альтернативный спирт (R3OH), где алкильная цепь группы -R3 этого спирта отличается от алкильной цепи группы -R3a исходного соединения общей формулы (IXCa). В том случае, когда спирт, который должен давать альтернативную 2 алкоксигруппу (-OR3), является слишком дефицитным или дорогостоящим, чтобы применять его в качестве растворителя в реакционной смеси, более целесообразно использовать подходящую альтернативу, такую как 1,4-диоксан, в качестве растворителя с требуемым спиртом(R3aOH), присутствующим в количестве, достаточном для осуществления желаемого превращения, в типичном случае от примерно 1 до примерно 2 молекулярных эквивалентов. (IXCa) и R3a являются такими, как определено выше. 2. При еще одном обычно применяемом способе соединения общей формулы (I), (IA) или (IB) можно получить из альтернативных соединений общей формулы (I), (IA) или (IB),причем при указанном способе либо подвергают взаимному превращению различные группы-OR3, либо подвергают взаимному превращению группы X и -OR3, либо подвергают взаимному превращению группы -OR3 и -NR5R6, гдеX, R3 и NR5R6 являются такими, как определено выше. 2.1. Как упомянуто ранее, некоторые соединения формул (I), (IA) и (IB) могут быть подвергнуты взаимному превращению путем индуцирования алкоксидного обмена или замещения по положению 2 заместителя 5-(пиридин 3-ил). Этого можно достичь путем обработки соответствующего спирта формулы R3aOH, где алкильная группа R3a является такой, как определено выше, и отличается от группы R3 в исходном веществе формулы (I), (IA) или (IB) тем,что является солью щелочного металла стерически затрудненного спирта или амина, чтобы образовать необходимый алкоксидный анион,который затем взаимодействует с субстратом. В типичном случае, по двухстадийной методике смесь от примерно 1 до примерно 8, более предпочтительно от примерно 5 до примерно 8, и 39 особенно от примерно 4 до примерно 8 молекулярных эквивалентов бис(триметилсилил)амида калия и требуемого спирта (формулы R3aOH) в качестве растворителя нагревают при температуре от примерно 80 до примерно 100 С в течение от примерно 25 мин до примерно 1 ч с последующим добавлением соединения формулы(IA) или (IB) и нагреванием этой реакционной смеси при температуре от примерно 100 до примерно 130 С в течение от примерно 6 до примерно 24 ч. Альтернативно, по одностадийной методике субстрат можно прямо обработать в требуемом спирте как растворителе например бис(триметилсилил) амидом калия, третбутоксидом калия или карбонатом цезия в количестве от примерно 1,2 до примерно 6, предпочтительно от примерно 4 до примерно 6 молекулярных эквивалентов при температуре от примерно 80 до примерно 130 С. В такие реакции алкоксидного обмена возможно можно включать агент, захватывающий гидроксид. 2.2. Альтернативно, некоторые соединения общей формулы (I), (IA) или (IB), где R13 представляет собой -OR3, можно получить из соединений общей формулы (XXX) где R1, R2, R4 являются такими, как определено здесь ранее, и где X представляет собой любую группу, кроме -OR3, реакцией в присутствии-OR3-, возможно в присутствии агента, захватывающего гидроксид, как определено здесь выше. 2.3. При еще одном альтернативном синтезе соединения общей формулы (I), (IA) или (IB),где R13 представляет собой NR5R6, можно образовать непосредственно из соединения общей формулы (I), где R13 = OR3. Когда R13 представляет собой OR3, субстрат можно обработать избытком R5R6NH или его подходящей солью присоединения кислоты в присутствии избытка не нуклеофильного основания, такого как стерически затрудненный амин или подходящее неорганическое основание, в подходящем растворителе. Типично, R5R6NH используют в виде свободного основания в примерно 3-кратном избытке (по отношению к субстрату) бис(триметилсилил)амида калия (KHMDS) в диметилформамиде (ДМФ) в качестве растворителя при примерно 100 С. Альтернативно, в качестве растворителя можно использовать избыток R5R6NH и проводить эту реакцию в присутствии примерно 50% избытка сульфата меди(II) при температуре вплоть до температуры дефлегмации реакционной среды. Если желаемый заместитель амино на соединении формулы(I), (IA) или (IB) представляет собой -NR5R6 и один из либо R5, либо R6 представляет собой Н,то реакцию обмена можно проводить при кипячении с обратным холодильником соответствующего амина и сульфата меди(II) пента- или гептагидрата или безводного сульфата меди(II) или KHMDS в ДМФ. Типично, для обмена группы OR3 на альтернативные амины формулыNHR5R6, такие как соединения, где R5 или R6 выбраны из алифатических или циклических аминов, возможно включающих в себя атом кислорода (например морфолин), эту реакцию предпочтительно проводят путем обработки соответствующим амином и примерно 3 эквивалентами бис(триметилсилил)амида калия в ДМФ в течение примерно 18 ч при 100 С. 3. При еще одном альтернативном способе соединение общей формулы (I) можно получить из соединения общей формулы (IIА) или (IIС) соответственно где Y представляет собой галогено, предпочтительно хлоро, a R1, R2, R3, R5 и R6 являются такими, как определено ранее для формул (IXA) и(IXC),путем взаимодействия с 4R10 пиперазинильным соединением, как описано для получения соединений формулы (ХА) и(ХВ) из соединений формулы (VIIA) и (VIIB) соответственно. Альтернативно, соединение общей формулы (I), (IA) или (IB) можно получить из соединения общей формулы (IIВ) где R1, R2, R4 и X являются такими, как определено ранее, путем взаимодействия с 4R10 пиперазинильным соединением с последующей возможной реакцией замещения в присутствии агента, захватывающего гидроксид, и -OR3-, как подробно описано здесь выше для получения соединения (I) из соединения (IXB) или (XXX). 3.1 Соединение общей формулы (IIА), или(IIВ), или (IIС) можно получить из соединения общей формулы (IVA), или (IVB), или (IVC) соответственно 42 где R1, R2, R3, R5, R6 и X являются такими, как определено ранее для соединений общих формул VA, VB и VC, общепринятыми методами каталитического гидрирования или гидрирования с каталитическим переносом водорода, как подробно описано ранее для получения соединений общих формул (XIA) или (XIB) из соединений общих формул (ХIIА) или (ХIIВ) соответственно. Соединение формулы (VIA), (VIB) или(VIC) можно получить путем взаимодействия соединения формулы (VII), как оно определено здесь ранее, с соединением формулы (ХIIА),или (ХIIВ), или (ХIIС) соответственно где R1, R2, R3, R5, R6 и Х являются такими, как определено здесь ранее, применяя известные способы превращения аминогруппы в группуSO2Y, где Y также является таким, как определено ранее для формул (IIА), (IIВ) и (IIС). Такие реакции описаны ранее для получения соединений общих формул (VIIIA) и (VIIIB) из соединений общих формул (XIA) и (XIB) соответственно. Соединение общей формулы (IVA), или(IVB), или (IVC) можно получить циклизацией соединения общей формулы (VA), или (VB),или (VC) соответственно где R3, R5, R6 и X являются такими, как определено ранее для соединений общих формул(VIA), или (VIB), или (VIC). И опять, как подробно описано ранее, предпочтительной является общепринятая стратегия защиты амина защитной группой для (ХIIА), когда NR5R6 представляет собой первичную или вторичную аминогруппу. Эта реакция сочетания аналогична реакциям соединения (VII) с соединениями общих формул (ХА), или (ХВ), или (ХС), уже описанным здесь. 3.2. Соединение общих формул (IIА), или(IIВ), или (IIС) можно получить из соединения формулы (IVA), или (IVB), или (IVC) соответственно, как описано здесь выше, причем указанное соединение общей формулы (IVA), или(IVB), или (IVC) можно получить прямой циклизацией соединения общей формулы (VIA),или (VIB), или (VIC) соответственно где R1, R2, R3, R5, R6 и Х являются такими, как определено здесь ранее, и где условия циклизации аналогичны условиям, описанным ранее для циклизации соединений общих формул (IXA),(IXB) или (IXC). Соединение формулы (VA), или (VB), или(VC) можно получить восстановлением соединения формулы (VIA), или (VIB), или (VIC) соответственно где R1, R2, R3, R5, R6 и Х являются такими, как определено здесь ранее, и где условия указанной прямой циклизации аналогичны условиям,описанным ранее для циклизации соединений общих формул (IXA), или (IXB), или(IХС), и причем за указанной циклизацией следует восстановление полученных промежуточных соединений согласно способам, подробно описанным здесь ранее для получения соединений об 43 щих формул (IVA), или (IVB), или (IVC) из соединений общих формул (VA), или (VB), или(VC). Соединения общей формулы (ХIIС), где X представляет собой Cl, можно получить из 2 гидроксиникотиновой кислоты нитрованием с последующей этерификацией, а затем хлорированием соответственно защищенной никотиновой кислоты и последующим гидролизом сложного эфира. Соединения общей формулы (XIIIC) (то есть соединения общей формулы (XIIIВ), где X представляет собой -OR3) можно получить способами, аналогичными способам, подробно описанным здесь ранее. 4. Следующий общеприменимый путь синтеза соединений общей формулы (I), (IA) или(IB) включает в себя введение заместителя R1 на конечной стадии синтеза. Так, соединение общей формулы (I), (IA) или (IB) можно получить алкилированием соединения формулы (Ia), (IAa) или (IBa), где R1 представляет собой водород, aR2, R13 и R4 являются такими, как определено ранее для формул (I), (IA) и (IB), с использованием одного или более чем одного из множества общеизвестных способов, таких как(1) взаимодействие с соединением формулы R1J, где R1 является таким, как определено ранее для соединений общих формул (I), (IA) и(IB), a J представляет собой подходящую уходящую группу, например галогено (предпочтительно хлоро, бромо или йодо), С 1-С 4 алкансульфонилокси, трифторметансульфонилокси или арилсульфонилокси (например бензолсульфонилокси или п-толуолсульфонилокси), в присутствии соответствующего основания, возможно в присутствии йодида натрия или йодида калия, при температуре от примерно -70 до примерно 100 С. Предпочтительно, алкилирование проводят при температуре от примерно комнатной температуры до примерно 120 С. Подходящие комбинации основание - растворитель могут быть выбраны из а) карбоната натрия, калия или цезия, бикарбоната натрия или калия, или третичного амина, такого как триэтиламин или пиридин,вместе с С 1-С 4 алканолом, 1,2-диметоксиэтаном,тетрагидрофураном, 1,4-диоксаном, ацетонитрилом, пиридином, N,N-диметилформамидом или N,N-диметилацетамидом; б) гидроксида натрия или калия или С 1-С 4 алкоксида натрия или калия вместе с С 1-С 4 алканолом, водой или их смесями; в) гидрида лития, натрия или калия, или бис(триметилсилил)амида лития, натрия или калия, диизопропиламида лития или бутиллития вместе с толуолом, эфиром, 1,2-диметоксиэтаном, тетрагидрофураном или 1,4-диоксаном; или д) в условиях катализа фазового переноса,галогенида или гидроксида тетраалкиламмония вместе со смесью водного раствора гидроксида 44 натрия или калия и дихлорметана, 1,2 дихлорэтана или хлороформа. Типично, либо примерно 10% избыток гидрида натрия добавляют к раствору субстрата в подходящем растворителе, например в безводном тетрагидрофуране, либо используют карбонат цезия в диметилформамиде (ДМФ) и полученный в результате анион обрабатывают примерно 10% избытком требуемого R1J;(2) взаимодействие с соединением формулы R1OH, где R1 является таким, как определено ранее для соединений общих формул (I), (IA) и(IB), с использованием классической методики Мицунобу. Типичные реакционные условия включают в себя обработку субстрата алканолом в присутствии триарилфосфина и ди(С 1 С 4)алкилазодикарбоксилата в подходящем растворителе, таком как тетрагидрофуран или 1,4 диоксан, при температуре от примерно -5 С до примерно комнатной температуры;(3) взаимодействие с соединением формулы R1M, где R1 представляет собой возможно замещенный фенил, Het2, Het3 или Het4, причем указанные Het группы являются либо ароматическими, либо частично ненасыщенными по атому С, который присоединен к М, где М представляет собой возможно замещенную группу металла или бора, причем указанная группа металла или бора пригодна для реакций кросссочетания (соединений металла или бора), например дигидроксиборан, в присутствии подходящей каталитической системы (например ацетата меди(II, или в так называемых условиях Голдберга. Такое кросс-сочетание предпочтительно проводят в присутствии подходящего основания (например пиридина) и высушивающего агента, обычно молекулярных сит 4, в подходящем растворителе, таком как дихлорметан или N-метилпирролидин, и возможно в условиях облучения микроволновым излучением;(4) взаимодействие с соединением формулы R1E, где Е представляет собой галогено,предпочтительно бромо, в условиях, подходящих для кросс-сочетания галогенированных соединений, где R1 является таким, как определено в (3). Такое взаимодействие обычно проводят в присутствии подходящей каталитической системы (например палладиевого катализатора) в присутствии подходящего основания, такого как, например, трет-бутоксид калия, в подходящем растворителе, таком как толуол, при нагревании, типично при температуре примерно 70 С. 4.1. Соответственно, соединение общей формулы (Ia), (IAa) или (IBa), где R1 представляет собой водород, a R2, R13 и R4 являются такими, как определено ранее для соединений общих формул (I), (IA) и (IB), можно получить из соединения формулы (IXAa), или (IXBa), или(IXCa) соответственно, где R1 представляет собой водород, a R2, R3, R5, R6, R4 и X являются такими, как определено ранее для формул(IXA), (IXB) или (IXC), в условиях, таких же,как условия, используемые для превращения соединения общей формулы (IXA), (IXB) или(IXC) в соединение общей формулы (I), (IA) или(IB) соответственно, когда R является иным,чем водород, с последующим подкислением реакционной смеси до рН примерно 6. 4.2. В еще одной альтернативе общеприменимого пути синтеза соединения по настоящему изобретению можно получить циклизацией соединений общих формул (IXA), (IXB) или(IXC), где указанные соединения общих формул(IXA), (IXB) или (IXC) получены из соединений общих формул (IXAa), (IXBa) или (IXCa), где R1 представляет собой водород, a R2, R3, R5, R6 и R4 являются такими, как определено здесь ранее, с использованием одного или более чем одного из множества общеизвестных способов, таких как способы, подробно описанные здесь выше для превращения соединений общих формул (Ia),(IAa) и (IBa) в соединения общих формул (I),(IA) и (IB). Можно использовать любой из способов, подробно описанных ранее для такого общего превращения. Предпочтительными условиями такого превращения являются использование либо от примерно 1,0 до 1,3 эквивалентов гидрида натрия в тетрагидрофуране в качестве растворителя при температуре от примерно-78 С до примерно комнатной температуры и использование от примерно 1,3 до примерно 2,3 эквивалентов алкилирующего агента при температуре от примерно 60 до примерно 70 С, либо примерно 2,2 эквивалентов карбоната цезия в качестве основания в диметилформамиде в качестве растворителя и примерно 1,1 эквивалента алкилирующего агента при температуре примерно 60 С. 5. При еще одном альтернативном синтезе соединения общей формулы (I), (IA) или (IB) можно получить из соединений общей формулы(I), где R10 представляет собой Н, путем подходящей реакции алкилирования, такой как, например, с использованием алкилгалогенида и подходящего основания, например карбоната цезия и метилхлорида. При предпочтительном способе получения соединений по настоящему изобретению соединения общей формулы (VIIB) получают из соединений общей формулы (XIIIB) согласно способу, подробно описанному в подготовительных примерах 96(а)-(з). Эти соединения общей формулы (VIIB) подвергают сочетанию с соединениями общей формулы (ХС) согласно способу,подробно описанному в подготовительных примерах 29 и 96(и) с получением соединения общей формулы (IXC), причем указанное соединение общей формулы (IXC) получают согласно способу, подробно описанному в подготовительном примере 95. Соединение общей формулы (IXC) затем предпочтительно подвергают циклизации в основных условиях согласно способу, подробно описанному в примерах 8 и 102, 004982 46 с образованием соединений общей формулы(IB), где R13 представляет собой OR3. 4-Аминопиразол-5-карбоксамиды общих формул (VII), (VIIA) и (VIIB), пиразолы общей формулы (XIII), карбоновые кислоты формул(ХА), (ХВ), (ХIIА), (ХIIВ), (ХIIС), (VIIA),(VIIB), (VIIC) и (X) или соединения общей формулы R1J и R1E, когда они не являются ни коммерчески доступными, ни впоследствии описанными, могут быть получены либо по аналогии со способами, описанными в разделе подготовительные примеры, либо общепринятыми способами в соответствии со стандартными руководствами по органической химии или литературным прецедентом из легко доступных исходных веществ с использованием соответствующих реагентов и условий реакций. Более того, специалисты в данной области техники должны знать варианты и альтернативы способов, описанных здесь ниже в разделах Примеры и Подготовительные примеры, которые дают возможность получить соединения,охарактеризованные формулами (I), (IA) или(IB). Фармацевтически приемлемые соли присоединения кислоты соединений формул (I),(IA) или (IB), которые содержат основной центр, также можно получить общепринятым способом. В качестве иллюстрации, соли присоединения кислоты соединений формулы (I)(более конкретно IA и IB) могут быть образованы путем взаимодействия соединения формулы(I) с эквимолярным или избыточным количеством соответствующей кислоты, либо в чистом виде, либо в подходящем растворителе. Эту соль затем можно осадить из раствора или выделить фильтрованием, либо растворитель реакции можно удалить обычными способами, такими как выпаривание в вакууме. Типичные соли, которые можно использовать в схемах 1-3,приведены в PCT/IB 99/00519. Примерами солей соединений IA и IB являются п-толуолсульфонат, бензолсульфонат, камфорсульфонат и этансульфонат соответственно. Фармацевтически приемлемые соли присоединения основания могут быть получены аналогичным образом путем обработки раствора соединения формулы (I), (IA) или (IB) соответствующим основанием. Оба типа соли можно образовать или взаимно превратить, используя методики на основе ионообменных смол. Настоящее изобретение также охватывает все подходящие изотопные варианты соединения формулы (I) или его фармацевтически приемлемой соли. Изотопный вариант соединения формулы (I) или его фармацевтически приемлемой соли характеризуется как вариант, в котором по меньшей мере один атом заменен атомом, имеющим тот же атомный номер, но имеющий атомную массу, отличающуюся от атомной массы, обычно обнаруживаемой в природе. Примеры изотопов, которые могут быть 47 введены в соединения формулы (I) и их фармацевтически приемлемые соли, включают изотопы водорода, углерода, азота, кислорода, фосфора, серы, фтора и хлора, такие как 2 Н, 3 Н, 13 С,14 С, 15N, 17O, 18O, 31 Р, 32 Р, 35S, 18F и 36Cl соответственно. Некоторые изотопные варианты соединений формулы (I) и их фармацевтически приемлемых солей, например те, в которые введен радиоактивный изотоп, такой как 3 Н или 14 С,полезны в исследованиях на распределение лекарственного средства и/или субстрата в ткани. Изотопы тритий, то есть 3 Н, и углерод-14, то есть 14 С, особенно предпочтительны в связи с простотой их получения и обнаружения. Кроме того, замещение изотопами, такими как дейтерий, то есть 2 Н, может дать некоторые терапевтические преимущества за счет их большей метаболической стабильности, например увеличенного периода полураспада in vivo, или снижения требований к дозировке, и, следовательно, может быть предпочтительным при некоторых обстоятельствах. Изотопные варианты соединений формулы (I) и их фармацевтически приемлемых солей по данному изобретению,как правило, можно получить с помощью общепринятых методик, как например, проиллюстрированными способами или способами получения, описанными в примерах и подготовительных примерах здесь ниже, с использованием соответствующих изотопных вариантов подходящих реагентов. Специалистам в данной области техники будет также понятно, что некоторые защищенные производные соединений формул (I), (IA) или (IB), которые могут быть получены до конечной стадии удаления защиты, сами по себе могут не обладать фармакологической активностью, но в некоторых случаях их можно вводить перорально или парентерально, и после этого они претерпевают метаболизм в организме с образованием соединений по изобретению, которые являются фармакологически активными. Такие производные, следовательно, могут быть определены как "пролекарства". К тому же, некоторые соединения формул (I), (IA) или (IB) могут действовать как пролекарства других соединений формул (I), (IA) или (IB). Все защищенные производные и пролекарства соединений общих формул (I), (IA) или (IB) входят в объем изобретения. Подходящие защитные группы для использования в соответствии с изобретением можно найти в ProtectingYork, 1994 -см., в частности, главу 4, с. 118-154,в отношении защитных групп для карбокси; иProtective Groups in Organic Synthesis 2nd edition, T.W. GreeneP.G.M. Wutz, WileyInterscience (1991) - см., в частности, главу 5 в отношении защитных групп для карбокси. Примеры подходящих пролекарств для соединений по настоящему изобретению описаны в Drugs ofToday, Volume 19, Number 9, 1983, pp. 499-538 и в Topics in Chemistry, Chapter 31, pp. 306-316. Биологическую активность соединений по настоящему изобретению определяли следующими тест-методами. Ингибиторная активность в отношении фосфодиэстеразы (ФДЭ) Соединения по настоящему изобретению являются сильнодействующими и избирательными ингибиторами цГМФ-ФДЭ 5. In vitro ФДЭ-ингибиторную активность против фосфодиэстераз циклического гуанозин-3',5'-монофосфата (цГМФ) и циклического аденозин-3',5'монофосфата (цАМФ) определяли измерением их значений IC50 (концентрация соединения,необходимая для 50% ингибирования ферментативной активности). Необходимые ферменты ФДЭ выделяли из ряда источников, включая пещеристое тело человека, тромбоциты человека и кролика, желудочек сердца человека, скелетную мышцу человека и сетчатку быка, по существу по методуW.J. Thompson and M.M. Appleman (Biochem.,1971, 10, 311). В частности, цГМФспецифичную ФДЭ (ФДЭ 5) и цГМФингибируемую ФДЭ цАМФ (ФДЭ 3) получали из ткани пещеристого тела человека, тромбоцитов человека или тромбоцитов кролика; цГМФстимулируемую ФДЭ (ФДЭ 2) получали из пещеристого тела человека; кальций/кальмодулин(Са/САМ)-зависимую ФДЭ (ФДЭ 1) получали из желудочка сердца человека; цАМФспецифичную ФДЭ (ФДЭ 4) получали из скелетной мышцы человека и фоторецепторную ФДЭ(ФДЭ 6) получали из сетчатки быка. Фосфодиэстеразы 7-11 были получены из полноразмерных человеческих рекомбинантных клонов, которыми трансфецировали клетки SF9. Анализы проводили, используя либо модификацию метода групповой обработки по W.J. Thompson et al. (Biochem., 1979, 18, 5228),либо сцинтилляционный анализ приближений для прямого обнаружения АМФ/ГМФ с использованием модификации протокола, описанногоTRKQ7090/7100. В кратком изложении, воздействие ингибиторов ФДЭ исследовали анализом фиксированного количества фермента в присутствии варьирующих концентраций ингибитора и небольшого количества субстрата (цГМФ или цАМФ в соотношении [3 Н]-немеченого к [3 Н]меченому 3:1 в концентрации 1/3 Km), так что[20 мМ Трис-HCl рН 7,4, 5 мМ МgCl2, 1 мг/мл бычьего сывороточного альбумина]. Реакции инициировали ферментом, инкубировали в течение 30-60 мин при 30 С с получением 30% обмена субстрата и останавливали 50 мкл SPA гранул силиката иттрия (содержащих 3 мМ соответствующего немеченого циклического нуклеотида для ФДЭ 9 и 11). Планшеты повторно 49 запаивали и встряхивали в течение 20 мин, после чего гранулам давали возможность осесть в течение 30 мин в темноте, а затем считали на считывающем устройстве для планшетов TopCount (Packard, Meriden, CT). Единицы радиоактивности переводили в % активности не ингибированного контроля (100%), наносили на график против концентрации ингибитора и получали значения IC50 ингибитора, используя расширение 'Fit Curve' Microsoft Excel. Результаты этих тестов показывают, что соединения по настоящему изобретению являются сильнодействующими и избирательными ингибиторами цГМФ-специфичной ФДЭ 5. Предпочтительные соединения по настоящему изобретению, такие как соединения примеров 3-12, 14-17, 19, 21-30, 32, 33, 35-46, 48-59,61, 62, 65-75, 77, 79-102 имеют значения IC50 менее примерно 10 нМ для фермента ФДЭ 5. Более предпочтительные соединения, такие как соединения примеров 3-12, 14, 15, 17, 23-30, 32,33, 35-46, 48, 50-59, 61, 62, 65, 69-74, 79-102 имеют значения IC50 менее 5 нМ для фермента ФДЭ 5. Особенно предпочтительные соединения, такие как соединения примеров 4-10, 15,17, 23-28, 30, 32, 33, 35-42, 44, 45, 46, 50, 52-56,58, 59, 61, 62, 65, 69-74, 79-93, 96, 98-102 имеют значения IC50 менее примерно 2 нМ для фермента ФДЭ 5. Особенно предпочтительными являются соединения, которые имеют значение IC50 менее примерно 10, более предпочтительно менее примерно 5 и наиболее предпочтительно менее примерно 2 нМ для фермента ФДЭ 5 в сочетании с более чем 10-кратной избирательностью, более предпочтительно с более чем 50-кратной,более предпочтительно более чем 100-кратной и особенно более чем 200-кратной избирательностью для фермента ФДЭ 5 по сравнению с ферментом ФДЭ 6. Функциональная активность Данную активность оценивали in vitro определением способности соединения по изобретению усиливать индуцированную нитропруссидом натрия релаксацию предварительно сокращенных полосок ткани пещеристого тела кролика, как описано S. A. Ballard et al. (Brit. J.Pharmacol., 1996, 118 (suppl.), abstract 153P). Активность in vivo Скрининг соединений проводили на анестезированных собаках, чтобы определить их способность после внутривенного (в.в.) введения усиливать повышение давления в пещеристом теле пениса, индуцированное внутрикавернозной инъекцией нитропруссида натрия,используя способ, основанный на способе, описанном Trigo-Rocha et al. (Neurourol. And Urodyn., 1994, 13, 71). Соединения формул (I), (IA) или (IB), их фармацевтически приемлемые соли и фармацевтически приемлемые сольваты любого из них можно вводить сами по себе, но при тера 004982 50 пии человека их будут, как правило, вводить в смеси с подходящим фармацевтическим эксципиентом, разбавителем или носителем, выбранным с учетом назначенного пути введения и стандартной фармацевтической практики. Например, соединения формул (I), (IA) или (IB),либо их соли или сольваты можно вводить перорально, трансбуккально или сублингвально в форме таблеток, капсул (включая мягкие желатиновые капсулы), овулей, эликсиров, растворов или суспензий, которые могут содержать корригирующие или красящие агенты, для применений немедленного, замедленного, модифицируемого или регулируемого высвобождения,например пролонгированной, дуальной или импульсной доставки. Соединения по изобретению можно также вводить внутрикавернозной инъекцией. Соединения по изобретению можно также вводить посредством быстродиспергируемых или быстрорастворимых лекарственных форм, либо в форме высокоэнергичной дисперсии, либо в виде частиц, покрытых оболочкой. Подходящие фармацевтические препараты соединений по изобретению могут быть в форме,покрытой или не покрытой оболочкой, по желанию. Такие таблетки могут содержать эксципиенты, такие как микрокристаллическая целлюлоза, лактоза, цитрат натрия, карбонат кальция,двухосновный фосфат кальция, глицин и крахмал (предпочтительно кукурузный, картофельный или тапиоковый крахмал), разрыхлители,такие как крахмальный гликолят натрия, натриевая кроскармелоза и некоторые комплексные силикаты, и гранулирующие связывающие агенты, такие как поливинилпирролидон, гидроксипропилметилцеллюлоза (ГПМЦ), гидроксипропилцеллюлоза (ГПЦ), сахароза, желатин и аравийская камедь. Дополнительно, в состав могут быть включены смазывающие агенты,такие как стеарат магния, стеариновая кислота,глицерилбегенат и тальк. Твердые композиции подобного типа можно также использовать в качестве наполнителей в желатиновых капсулах. Предпочтительные эксципиенты в этом отношении включают лактозу, крахмал, целлюлозу, молочный сахар или высокомолекулярные полиэтиленгликоли. Для водных суспензий и/или эликсиров соединения формулы (I), (IA) или (IB) можно объединять с различными подсластителями или корригентами, красящим веществом или красителями,с эмульгирующими и/или суспендирующими агентами и с разбавителями, такими как вода,этанол, пропиленгликоль и глицерин, и их комбинациями. Лекарственные формы модифицированного высвобождения и импульсного высвобождения могут содержать эксципиенты, такие как те,которые подробно описаны для лекарственных форм немедленного высвобождения, вместе с дополнительными эксципиентами, которые дей 51 ствуют в качестве модификаторов скорости высвобождения, причем устройство ими покрыто и/или они находятся внутри устройства. Модификаторы скорости высвобождения включают,но не ограничены исключительно ими, гидроксипропилметилцеллюлозу, метилцеллюлозу,натриевую карбоксиметилцеллюлозу, этил целлюлозу, ацетат целлюлозы, полиэтиленоксид,смолу Xanthan, Carbomer, сополимер аммониометакрилат, гидрогенированное касторовое масло, карнаубский воск, парафиновый воск,фталат ацетата целлюлозы, фталат гидроксипропилметилцеллюлозы, сополимер метакриловой кислоты и их смеси. Лекарственные формы модифицированного высвобождения и импульсного высвобождения могут содержать один эксципиент, модифицирующий скорость высвобождения, или комбинацию таких эксципиентов. Эксципиенты, модифицирующие скорость высвобождения, могут находиться как внутри лекарственной формы, то есть внутри матрицы, так и/или на лекарственной форме, то есть на поверхности или покрытии. Быстродиспергируемые или быстрорастворимые лекарственные препараты (БДРЛП) могут содержать следующие ингредиенты: аспартам, ацесульфам калия, лимонную кислоту,натриевую кроскармелозу, кросповидон, диаскорбиновую кислоту, этилакрилат, этилцеллюлозу, желатин, гидроксипропилметилцеллюлозу, стеарат магния, маннит, метилметакрилат,мятный корригент, полиэтиленгликоль, белую сажу, диоксид кремния, крахмальный гликолят натрия, стеарилфумарат натрия, сорбит, ксилит. Термины "диспергируемые" или "растворимые" используют здесь для описания БДРЛП в зависимости от растворимости применяемого лекарственного вещества; то есть, если лекарственное вещество является нерастворимым, можно получить быстродиспергируемую лекарственную форму, а если лекарственное вещество является растворимым, можно получить быстрорастворимую лекарственную форму. Соединения по изобретению можно также вводить парентерально, например внутрикавернозно, внутривенно, внутриартериально, внутрибрюшинно, внутриоболочечно, интравентрикулярно, интрауретрально, интрастернально,интракраниально, внутримышечно или подкожно, либо их можно вводить инфузией или безыгольной инъекцией. Для такого парентерального введения их лучше всего использовать в форме стерильного водного раствора, который может содержать другие вещества, например достаточное количество солей или глюкозы, чтобы сделать этот раствор изотоническим с кровью. Если необходимо, водные растворы следует соответственно забуферить (предпочтительно до рН от 3 до 9). Приготовление подходящих парентеральных препаратов в стерильных условиях легко осуществить по стандартным фарма 004982 52 цевтическим методикам, общеизвестным специалистам в данной области техники. Для перорального и парентерального введения пациентам-людям суточный уровень дозировки соединений формулы (I), (IA) или (IB) либо их солей или сольватов будет обычно составлять от 10 до 500 мг (в однократной дозе или в разделенных дозах). Так, например, таблетки или капсулы соединений формул (I), (IA) или (IB) либо их солей или сольватов могут содержать от 5 мг до 250 мг активного соединения для введения по одной, по две или более одновременно, как целесообразно. Врач в любом случае будет определять фактическую дозировку, которая будет наиболее подходящей для любого индивидуального пациента, и она будет варьировать в зависимости от возраста, массы и реакции конкретного пациента. Вышеуказанные дозировки являются примерными для среднего случая. Разумеется, могут быть отдельные случаи, когда более высокие или более низкие диапазоны дозировки заслуживают внимания, и такие случаи входят в объем данного изобретения. Специалисту в данной области техники будет также понятно, что при лечении некоторых состояний (в том числе МЭД и ЖПД) соединения по изобретению можно принимать в однократной дозе на основе "по потребности" (то есть, как необходимо или желательно). Пример препарата Таблетки 10 мг Ингредиент мас.% Бесилатная соль соединения примера 103 13,038 Лактоза 62,222 Крахмал 20,740 Натриевая кроскармелоза 3,000 Стеарат магния 1,000 Количество, регулируемое в соответствии с активностью лекарственного средства. Такие таблетки могут быть изготовлены стандартными способами, например прямым прессованием или способом влажного или сухого гранулирования. Ядра таблеток можно покрыть подходящими оболочками. Соединения по изобретению можно также вводить интраназально или путем ингаляции, и их удобно доставлять в форме сухого порошкового ингалятора или аэрозольного спрея из контейнера под давлением, насоса, распылителя или небулайзера с применением подходящего пропеллента, например дихлордифторметана,трихлорфторметана,дихлортетрафторэтана,гидрофторалкана, такого как 1,1,1,2-тетрафторэтан (HFA 134A [товарный знак]) или 1,1,1,2,3,3,3-гептафторпропан (HFA 227EA [товарный знак]), диоксида углерода или другого подходящего газа. В случае аэрозоля под давлением дозировочную единицу можно определять,установив клапан для доставки отмеренного 53 количества. Контейнер под давлением, насос,распылитель или небулайзер может содержать раствор или суспензию активного соединения,причем используют, например, смесь этанола и пропеллента в качестве растворителя, которая может дополнительно содержать смазывающий агент, например сорбитана триолеат. Могут быть изготовлены капсулы и картриджи (например из желатина) для использования в ингаляторе или инсуффляторе, которые содержат порошковую смесь соединения формулы (I),(IA) или (IB) и подходящую порошковую основу, такую как лактоза или крахмал. Аэрозоль или сухие порошкообразные препараты предпочтительно готовят так, чтобы каждая отмеренная доза, или "пшик", содержала от 1 до 50 мг соединения формулы (I), (IA) или(IB) для доставки пациенту. Общая суточная доза с аэрозолем будет в пределах от 1 до 50 мг,и ее можно вводить в однократной дозе или,более обычно, в разделенных дозах в течение суток. Соединения по изобретению можно также включать в состав препаратов для доставки посредством пульверизатора. Препараты для пульверизаторов могут содержать следующие ингредиенты в качестве солюбилизаторов,эмульгаторов или суспендирующих агентов: воду, этанол, глицерин, низкомолекулярные полиэтиленгликоли, хлорид натрия, фторуглероды, полиэтиленгликолевые эфиры, сорбитана триолеат, олеиновую кислоту. Альтернативно, соединения формул (I),(IA) или (IB) либо их соли или сольваты можно вводить в форме суппозитория или пессария,либо их можно применять местно в форме геля,гидрогеля, лосьона, раствора, крема, мази или присыпки. Соединения формул (I), (IA) или (IB) либо их соли или сольваты можно также вводить дермально. Соединения формул (I), (IA) или (IB) либо их соли или сольваты можно также вводить трансдермально, например с использованием кожного пластыря. Их также можно вводить глазным, легочным или ректальным путями. Для глазного применения соединения можно включать в состав препаратов в виде микронизированных суспензий в изотоническом стерильном физиологическом растворе с заданным рН или, предпочтительно, в виде растворов в изотоническом стерильном физиологическом растворе с заданным рН, возможно в комбинации с консервантом, таким как бензилалкония хлорид. Альтернативно, их можно включать в состав препарата в виде мази, такой как вазелин. Для местного нанесения на кожу соединения формул (I), (IA) или (IB) либо их соли или сольваты можно включать в состав препаратов в виде подходящей мази, содержащей активное соединение, суспендированное или растворенное в, например, смеси с одним или более чем одним из следующего: минеральное масло, 004982 54 жидкий вазелин, белый вазелин, пропиленгликоль,полиоксиэтиленполиоксипропиленовое соединение, эмульгирующий воск и вода. Альтернативно, их можно включать в состав препаратов в виде подходящего лосьона или крема суспендированными или растворенными в, например, смеси одного или более чем одного из следующего: минеральное масло, сорбитана моностеарат, полиэтиленгликоль, жидкий парафин, полисорбат 60, цетилэфирный воск, цетеариловый спирт, 2-октилдодеканол, бензиловый спирт и вода. Соединения формул (I), (IA) или (IB) можно также применять в комбинации с циклодекстрином. Известно, что циклодекстрины образуют комплексы включения и не включения с молекулами лекарственного средства. Образование комплекса лекарственное средствоциклодекстрин может модифицировать растворимость, скорость растворения, биодоступность и/или стабильность молекулы лекарственного средства. Комплексы лекарственное средствоциклодекстрин, как правило, полезны для большинства лекарственных форм и путей введения. В качестве альтернативы прямому комплексообразованию с лекарственным средством циклодекстрин можно использовать в качестве вспомогательной добавки, например в качестве носителя, разбавителя или солюбилизатора. Наиболее широко используют альфа-, бета- и гамма-циклодекстрины, и подходящие примеры описаны в WO-А-91/11172, WO-A-94/02518 иWO-A-98/55148. Как правило, у людей пероральное введение соединений по изобретению является предпочтительным путем, поскольку он является наиболее удобным и, например, при МЭД позволяет избежать общеизвестных недостатков,связанных с внутрикавернозным (в.к.) введением. Предпочтительный режим перорального дозирования при МЭД для типичного мужчины составляет от 25 до 250 мг соединения по потребности. В обстоятельствах, когда реципиент страдает расстройством глотания или нарушением всасывания лекарственного средства после перорального введения, лекарственное средство можно вводить парентерально, сублингвально или буккально. Для ветеринарного применения соединение формулы (I), (IA) или (IB), либо его ветеринарно приемлемую соль, либо их ветеринарно приемлемые сольват или пролекарство вводят в виде подходящего приемлемого препарата в соответствии с обычной ветеринарной практикой, и ветеринарный врач будет определять режим дозирования и путь введения, который будет наиболее подходящим для конкретного животного. Следует иметь в виду, что здесь все ссылки на лечение включают куративное, паллиативное и профилактическое лечение. 55 Соответственно, согласно изобретению предложена фармацевтическая композиция, содержащая соединение формулы (I), (IA) или(IB), либо его фармацевтически приемлемую соль, либо их фармацевтически приемлемые сольват или пролекарство вместе с фармацевтически приемлемыми разбавителем или носителем. Предложен также ветеринарный препарат,содержащий соединение формулы (I), (IA) или(IB), либо его ветеринарно приемлемую соль,либо их ветеринарно приемлемые сольват или пролекарство, вместе с ветеринарно приемлемыми разбавителем или носителем. Согласно изобретению также предложено соединение формулы (I), (IA) или (IB), либо его фармацевтически приемлемая соль, либо их фармацевтически приемлемые сольват или пролекарство, либо фармацевтическая композиция,содержащая любое из вышеуказанного, для применения в качестве лекарства для человека. Кроме того, предложено соединение формулы (I), (IA) или (IB), либо его ветеринарно приемлемая соль, либо их ветеринарно приемлемые сольват или пролекарство, либо ветеринарный препарат, содержащий любое из вышеуказанного, для применения в качестве лекарства для животного. В еще одном аспекте изобретения предложено применение соединения формулы (I), (IA) или (IB), либо его фармацевтически приемлемой соли, либо их фармацевтически приемлемых сольвата или пролекарства для производства лекарства для человека для куративного, паллиативного или профилактического лечения медицинского состояния, для которого показан ингибитор цГМФ-ФДЭ 5. Предложено также применение соединения формулы (I), (IA) или(IB), либо его фармацевтически приемлемой соли, либо их фармацевтически приемлемых сольвата или пролекарства для производства лекарства для лечения медицинского состояния,для которого желательно ингибирование цГМФФДЭ 5. Также предложено применение соединения формулы (I), (IA) или (IB), либо его ветеринарно приемлемой соли, либо их ветеринарно приемлемых сольвата или пролекарства для производства лекарства для животного для куративного, паллиативного или профилактического лечения медицинского состояния, для которого показан ингибитор цГМФ-ФДЭ 5. Далее, согласно изобретению предложено применение соединения формулы (I), (IA) или(IB), либо его фармацевтически приемлемой соли, либо их фармацевтически приемлемых сольвата или пролекарства для производства лекарства для человека для куративного, паллиативного или профилактического лечения мужской эректильной дисфункции (МЭД), импотенции, женской половой дисфункции 56 расстройства, представляющего собой гипоактивное половое желание, женского расстройства полового возбуждения, женского полового болевого расстройства, женской половой оргазмической дисфункции (ЖПОД), половой дисфункции вследствие повреждения спинного мозга,половой дисфункции, индуцированной избирательным ингибитором обратного захвата серотонина (ИОЗС), преждевременных родов, дисменореи, доброкачественной гиперплазии простаты (ДГП), синдрома инфравезикальной обструкции, недержания, стабильной, нестабильной и вариантной (Принцметала) стенокардии,гипертензии, легочной гипертензии, хронической обструктивной болезни легких, коронарной артериальной болезни, застойной сердечной недостаточности, атеросклероза, состояний пониженной проходимости кровеносных сосудов,заболевания периферических сосудов, удара,нитрат-индуцированной толерантности, бронхита, аллергической астмы, хронической астмы,аллергического ринита, заболеваний и состояний глаза, заболеваний, характеризующихся расстройствами перистальтики кишечника, преэклампсии, синдрома Кавасаки, толерантности к нитратам, рассеянного склероза, диабетической нефропатии, невропатии, включая автономную и периферическую невропатию и, в частности,диабетическую невропатию и ее симптомы, например парез желудка, болезни Альцгеймера,острой респираторной недостаточности, псориаза, некроза кожи, рака, метастазирования, облысения, "щелкающего" пищевода, трещины заднего прохода, геморроя, гипоксической вазоконстрикции или стабилизации кровяного давления во время гемодиализа. Особенно предпочтительные состояния включают в себя МЭД и ЖПД. Предложено также применение соединения формулы (I), (IA) или (IB), либо его ветеринарно приемлемой соли, либо их ветеринарно приемлемых сольвата или пролекарства для производства лекарства для животного для куративного, паллиативного или профилактического лечения мужской эректильной дисфункции (МЭД), импотенции, женской половой дисфункции (ЖПД), литоральной дисфункции,женского расстройства, представляющего собой гипоактивное половое желание, женского расстройства полового возбуждения, женского полового болевого расстройства, женской половой оргазмической дисфункции (ЖПОД), половой дисфункции вследствие повреждения спинного мозга, половой дисфункции, индуцированной избирательным ингибитором обратного захвата серотонина (ИОЗС), преждевременных родов,дисменореи, доброкачественной гиперплазии простаты (ДГП), синдрома инфравезикальной обструкции, недержания, стабильной, нестабильной и вариантной (Принцметала) стенокардии, гипертензии, легочной гипертензии, хронической обструктивной болезни легких, коро 57 нарной артериальной болезни, застойной сердечной недостаточности, атеросклероза, состояний пониженной проходимости кровеносных сосудов, заболевания периферических сосудов,удара, нитрат-индуцированной толерантности,бронхита, аллергической астмы, хронической астмы, аллергического ринита, заболеваний и состояний глаза, заболеваний, характеризующихся расстройствами перистальтики кишечника, преэклампсии, синдрома Кавасаки, толерантности к нитратам, рассеянного склероза,диабетической нефропатии, невропатии, включая автономную и периферическую невропатию и, в частности, диабетическую невропатию и ее симптомы, например парез желудка, болезни Альцгеймера, острой респираторной недостаточности, псориаза, некроза кожи, рака, метастазирования, облысения, "щелкающего" пищевода, трещины заднего прохода, геморроя, гипоксической вазоконстрикции или стабилизации кровяного давления во время гемодиализа. Особенно предпочтительные состояния включают в себя МЭД и ЖПД. Дополнительно, согласно изобретению предложен способ лечения или предупреждения медицинского состояния, для которого показан ингибитор цГМФ-ФДЭ 5, у млекопитающего(включая человека), при котором указанному млекопитающему вводят терапевтически эффективное количество соединения формулы (I),(IA) или (IB), либо его фармацевтически или ветеринарно приемлемой соли, либо их фармацевтически или ветеринарно приемлемых сольвата или пролекарства, либо фармацевтической композиции или ветеринарного препарата, содержащих любое из вышеуказанного. Кроме того, согласно изобретению предложен способ лечения или предупреждения мужской эректильной дисфункции (МЭД), импотенции, женской половой дисфункции(ЖПД), клиторальной дисфункции, женского расстройства, представляющего собой гипоактивное половое желание, женского расстройства полового возбуждения, женского полового болевого расстройства, женской половой оргазмической дисфункции (ЖПОД), половой дисфункции вследствие повреждения спинного мозга,половой дисфункции, индуцированной избирательным ингибитором обратного захвата серотонина (ИОЗС), преждевременных родов, дисменореи, доброкачественной гиперплазии простаты (ДГП), синдрома инфравезикальной обструкции, недержания, стабильной, нестабильной и вариантной (Принцметала) стенокардии,гипертензии, легочной гипертензии, хронической обструктивной болезни легких, коронарной артериальной болезни, застойной сердечной недостаточности, атеросклероза, состояний пониженной проходимости кровеносных сосудов,заболевания периферических сосудов, удара,нитрат-индуцированной толерантности, бронхита, аллергической астмы, хронической астмы, 004982 58 аллергического ринита, заболеваний и состояний глаза, заболеваний, характеризующихся расстройствами перистальтики кишечника, преэклампсии, синдрома Кавасаки, толерантности к нитратам, рассеянного склероза, диабетической нефропатии, невропатии, включая автономную и периферическую невропатию и, в частности,диабетическую невропатию и ее симптомы, например парез желудка, болезни Альцгеймера,острой респираторной недостаточности, псориаза, некроза кожи, рака, метастазирования, облысения, "щелкающего" пищевода, трещины заднего прохода, геморроя, гипоксической вазоконстрикции или стабилизации кровяного давления во время гемодиализа у млекопитающего(включая человека), при котором указанному млекопитающему вводят терапевтически эффективное количество соединения формулы (I),(IA) или (IB), либо его фармацевтически или ветеринарно приемлемой соли, либо их фармацевтически или ветеринарно приемлемых сольвата или пролекарства, либо фармацевтической композиции или ветеринарного препарата, содержащего любое из вышеуказанного. В еще одном дополнительном аспекте настоящего изобретения предложена комбинация соединений общей формулы (I), (IA) или (IB) с дополнительными соединениями, полезными в ингибировании ФДЭ 5, причем указанная комбинация пригодна для лечения или предупреждения мужской эректильной дисфункции(МЭД), импотенции, женской половой дисфункции (ЖПД), клиторальной дисфункции,женского расстройства, представляющего собой гипоактивное половое желание, женского расстройства полового возбуждения, женского полового болевого расстройства, женской половой оргазмической дисфункции (ЖПОД), половой дисфункции вследствие повреждения спинного мозга, половой дисфункции, индуцированной избирательным ингибитором обратного захвата серотонина (ИОЗС), преждевременных родов,дисменореи, доброкачественной гиперплазии простаты (ДГП), синдрома инфравезикальной обструкции, недержания, стабильной, нестабильной и вариантной (Принцметала) стенокардии, гипертензии, легочной гипертензии, хронической обструктивной болезни легких, коронарной артериальной болезни, застойной сердечной недостаточности, атеросклероза, состояний пониженной проходимости кровеносных сосудов, заболевания периферических сосудов,удара, нитрат-индуцированной толерантности,бронхита, аллергической астмы, хронической астмы, аллергического ринита, заболеваний и состояний глаза, заболеваний, характеризующихся расстройствами перистальтики кишечника, преэклампсии, синдрома Кавасаки, толерантности к нитратам, рассеянного склероза,диабетической нефропатии, невропатии, включая автономную и периферическую невропатию и, в частности, диабетическую невропатию и ее 59 симптомы, например парез желудка, болезни Альцгеймера, острой респираторной недостаточности, псориаза, некроза кожи, рака, метастазирования, облысения, "щелкающего" пищевода, трещины заднего прохода, геморроя, гипоксической вазоконстрикции или стабилизации кровяного давления во время гемодиализа у млекопитающего (включая человека). Изобретение также охватывает любые новые промежуточные соединения, описанные здесь, например соединения формул (IXA),(IXB), (VIIA), (VIIB), (VIII), (VIIIA) и (X). В объем настоящего изобретения дополнительно включено совместное введение ингибитора цГМФ-ФДЭ 5 общей формулы (I), причем указанное совместное введение может быть в форме одновременного, последовательного или объединенного введения с(а) одним или более чем одним из встречающихся в природе или синтетических простагландинов или их сложных эфиров; подходящие простагландины для применения здесь включают такие соединения, как альпростадил,простагландин Е 1, простагландин Е 0, 13,14 дигидропростагландин Е 1, простагландин Е 2,эпростинол, природные, синтетические и полусинтетические простагландины и их производные, в том числе те, которые описаны в US 6037346, выданном 14 марта 2000 года и включенном сюда ссылкой, ПГЕ 0, ПГЕ 1, ПГА 1, ПГВ 1,ПГF1, ,19-гидрокси-ПГА 1, 19-гидрокси-ПГВ 1,ПГЕ 2, ПГВ 2, 19-гидрокси-ПГА 2, 19-гидроксиПГЕ 3,карбопрост-трометаминПГВ 2,динопрост, трометамин, динопростон, липопрост, гемепрост, метенопрост, сульпростан,тиапрост и моксизилат; и/или(б) одним или более соединениямиантагонистами -адренергических рецепторов,также известных как -адреноцепторы, или рецепторы, или -блокаторы; подходящие соединения для применения здесь включают: адренергические рецепторы, как они описаны в заявке РСТ WO99/30697, опубликованной 14 июня 1998 года, описание которой относится к-адренергическим рецепторам, которая включена сюда ссылкой, и включают избирательные 1-адреноцепторы или 2-адреноцепторы и неизбирательные адреноцепторы, причем подходящие 1-адреноцепторы включают: фентоламин, фентоламина мезилат, тразодон, альфузозин, индорамин, нафтопидил, тамсулозин, дапипразол, феноксибензамин, идазоксан, эфараксан, йохимбин, алкалоиды раувольфии, Recordati 15/2739, SNAP 1069, SNAP 5089, RS 17053,SL 89.0591, доксазозин, теразозин, абанохил и празозин; 2-блокаторы из US 6037346 [14 марта 2000] дибенамин, толазолин, тримазозин и дибенамин; -адренергические рецепторы, описанные в патентах США 4188390, 4026894,3511836, 4315007, 3527761, 3997666, 2503059,4703063, 3381009, 4252721 и 2599000, каждый 60 из которых включен сюда ссылкой; 2 адреноцепторы включают: клонидин, папаверин, папаверина гидрохлорид, возможно в присутствии кардиотонического агента, такого как пирксамин; и/или(в) одним или более чем одним соединением-NО-донором (NO-агонистом); подходящие соединения-NО-доноры для применения здесь включают органические нитраты, такие как моно-, ди- или тринитраты или органические нитратные сложные эфиры, в том числе глицерилбинитрат (также известный как нитроглицерин),изосорбида 5-мононитрат, изосорбида динитрат,пентаэритрола тетранитрат, эритритила тетранитрат, нитропруссид натрия (SNP), 3 морфолинозиднонимина молзидомин,Sнитрозо-N-ацетилпенициллиамин (SNAP), Sнитрозо-N-глутатион (SNO-GLU), N-гидроксиL-аргинин, амилнитрат, линзидомин, линзидомина хлоргидрат, (SIN-1) S-нитрозо-N-цистеин,диазения диолаты(NONOаты),1,5 пентандинитрат, L-аргинен, женьшень, плоды ююбы (китайского финика), молзидомин, Re2047, нитрозилированные производные максисилита, такие как NMI-678-11 и NMI-937, как описано в опубликованной заявке РСТ WO 0012075; и/или(г) одним или более чем одним открывателем калиевого канала; подходящие открыватели калиевого канала для применения здесь включают никорандил, кромокалим, левкромакалим,лемакалим, пинацидил, клиазоксид, миноксидил, харибдотоксин, глибурид, 4-аминипиридин, ВаСl2; и/или(д) одним или более чем одним дофаминергическим агентом; подходящие дофаминергические соединения для применения здесь включают D2-агонисты, такие как прамипексол,апоморфин; и/или(е) одним или более чем одним вазодилататором; подходящие вазодилататоры для применения здесь включают нимодепин, пинацидил, цикланделат, изоксуприн, хлорпрумазин,галоперидол, Rec 15/2739, тразодон, пентоксифиллин; и/или(ж) одним или более чем одним агонистом тромбоксана А 2; и/или(з) одним или более чем одним ЦНСактивным агентом; и/или(и) одним или более чем одним алкалоидом спорыньи; подходящие алкалоиды спорыньи описаны в патенте США 6037346, опубликованном 14 марта 2000 года, и включают ацетергамин, бразерголин, бромергурид, цианерголин, делорготрил, дисулергин, эргоновина малеат, эрготамина тартрат, этисулергин, лерготрил,лизергид, мезулергин, метерголин, метерготамин, ницерголин, перголид, пропизергид, протергурид, тергурид; и/или(к) одним или более чем одним соединением, которое модулирует действие предсердного натруретического фактора (также известного
МПК / Метки
МПК: A61P 15/10, A61K 31/519, C07D 487/04
Метки: 4,3-d]пиримидина, пиразоло, производные
Код ссылки
<a href="https://eas.patents.su/30-4982-proizvodnye-pirazolo-43-dpirimidina.html" rel="bookmark" title="База патентов Евразийского Союза">Производные пиразоло [4,3-d]пиримидина</a>
Предыдущий патент: Бициклические гетероциклы, содержащие эти соединения лекарственные средства, их применение и способ их получения
Следующий патент: Производные 2-аминокарбонил-9h-пурина
Случайный патент: Промывочный буровой раствор, содержащий гидрофобин












