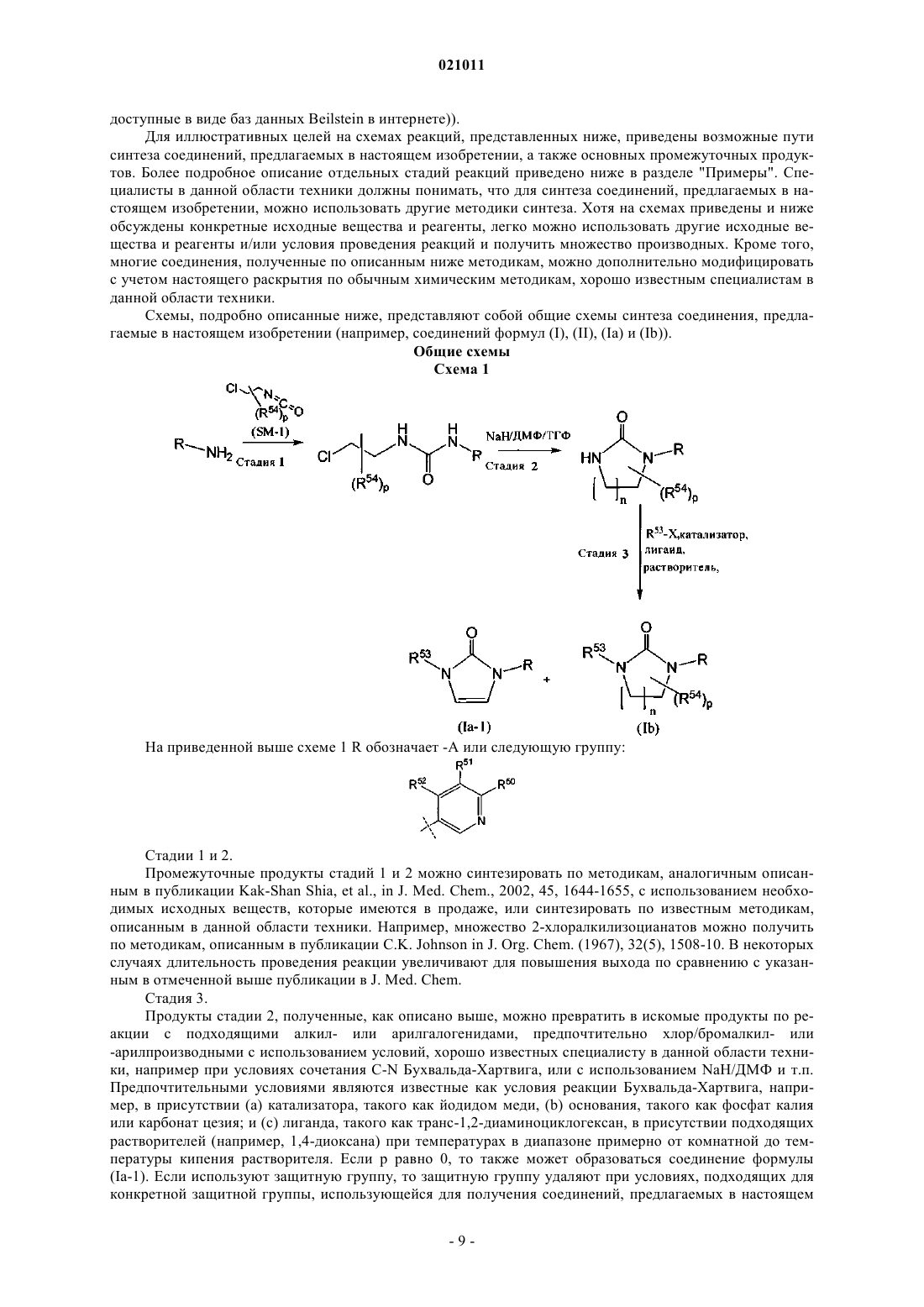
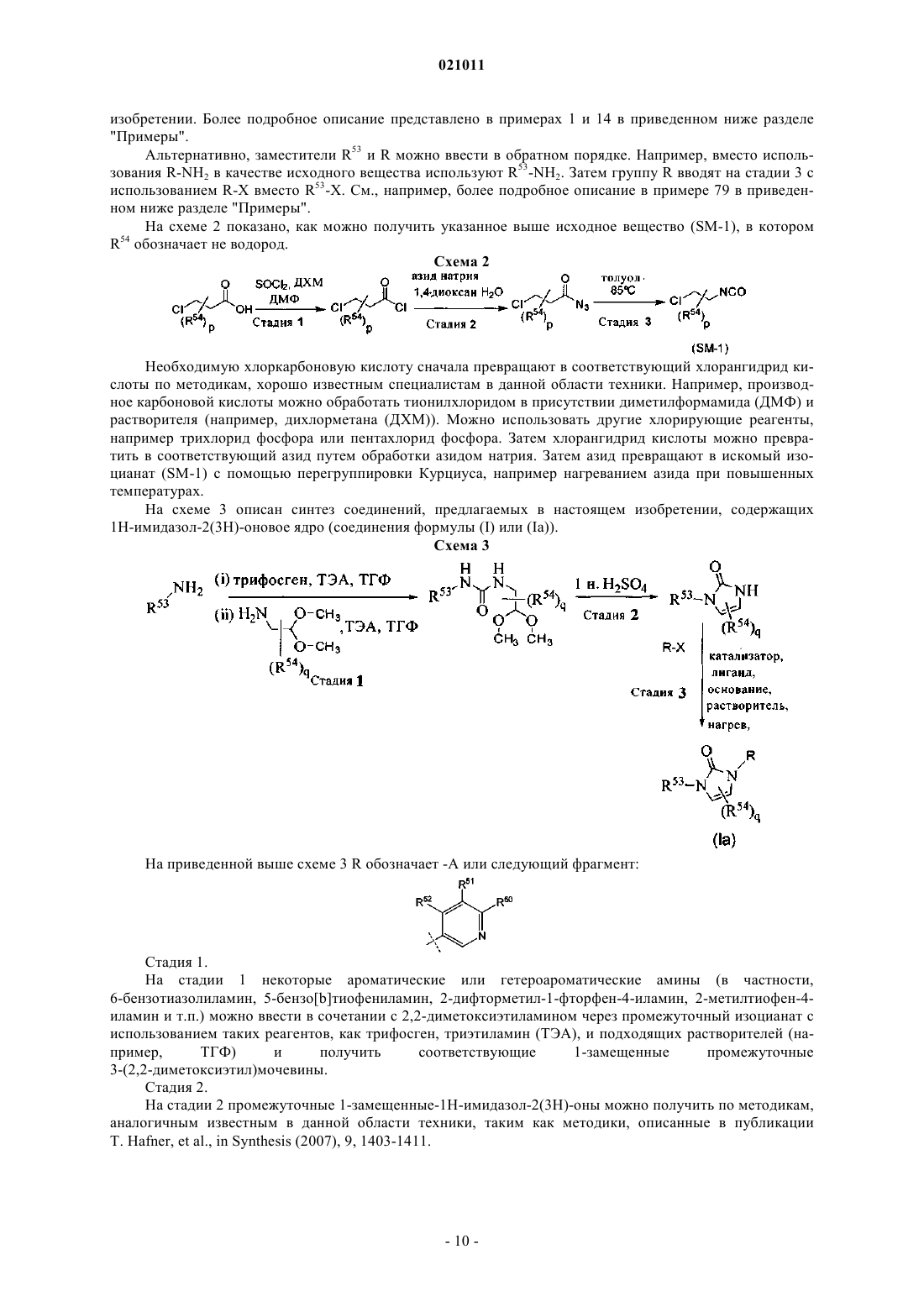
1,3-дизамещенные производные имидазолидин-2-она в качестве ингибиторов cyp 17
Номер патента: 21011
Опубликовано: 31.03.2015
Авторы: Сенгупта Саумитра, Гауль Кристоф, Гуммади Венкатешвар Рао, Бок Марк Г.
Формула / Реферат
1. Соединение формулы (Ia) или (Ib):
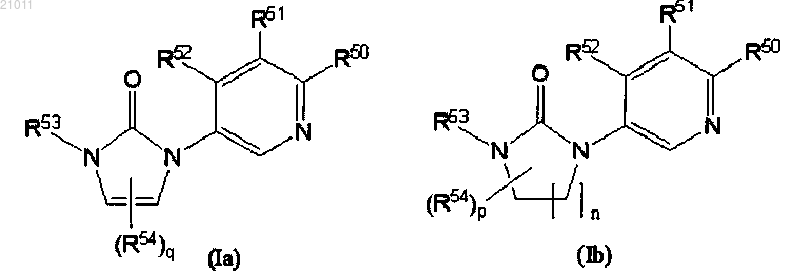
где n равно 1, 2 или 3;
R53 обозначает:
(i) фенил, необязательно содержащий от 1 до 2 заместителей, каждый из которых независимо выбран из группы, включающей фтор, хлор, метил, метоксигруппу, трифторметил, дифторметил или цианогруппу;
(ii) бифенил;
(iii) конденсированный фенил, выбранный из группы, включающей нафталин-2-ил, хинолин-6-ил, 3,4-дигидро-2-оксохинолин-6-ил, бензо[b]тиофен-5-ил, бензо[d]изоксазол-5-ил, 1Н-индазол-6-ил, 1Н-индазол-5-ил, бензотиазол-6-ил, 1,2-дигидро-3-оксоиндазол-6-ил, индан-5-ил, 1Н-бензотриазол-5-ил, бензофуран-5-ил, 2,3-дигидробензо[1,4]диоксин-6-ил, 2,3-дигидробензофуран-5-ил или бензо[1,3]диоксол-5-ил, где указанный конденсированный фенил необязательно содержит от 1 до 2 заместителей, каждый из которых независимо выбран из группы, включающей хлор, фтор, метил, этил, дифторметил, трифторметил, циклопропил, цианогруппу или аминогруппу;
(iv) 5-6-членный гетероарил, выбранный из группы, включающей изотиазол-4-ил, тиофен-2-ил, тиофен-3-ил или пиридин-4-ил, где указанный изотиазол-4-ил, указанный тиофен-2-ил, указанный тиофен-3-ил и указанный пиридин-4-ил необязательно содержат следующие заместители: фтор, хлор, метил, трифторметил, дифторметил или метоксигруппу; или
(v) конденсированный гетероарил, выбранный из группы, включающей тиено[3,2-с]пиридин-2-ил, тиено[3,2-с]пиридин-3-ил, тиено[3,2-с]пиридин-2-ил, имидазо[1,2-а]пиридин-7-ил или бензо[b]тиофен-2-ил, где указанный конденсированный гетероарил необязательно содержит от 1 до 2 заместителей, каждый из которых независимо выбран из группы, включающей фтор, хлор, метил, дифторметил, трифторметил, циклопропил или аминогруппу;
R54 обозначает (C1-C4)алкил, галогензамещенный (C1-C4)алкил или -CH2OH;
р равно 0, 1, 2 или 3;
q равно 0, 1 или 2;
R50, R51 и R52, каждый независимо, означают Н, галоген, -ОН, -CN, (C1-C4)алкил, глогензамещенный (C1-C4)алкил, гидроксизамещенный (C1-C4)алкил, -(CH2)r-O(C1-C4)алкил, -(CH2)r-CH(O(C1-C4)алкил)2, -NH2,
-NH(C1-C4)алкил, -N((C1-C4)алкил)2, -NHC(O)-(C1-C4)алкил, -C(O)NH2, -C(O)-NH(C1-C4)алкил, -C(O)-N((C1-C4)алкил)2 или -C(O)-O(C1-С4)алкил;
r равно 0, 1 или 2;
при условии, что когда R50, R51 и R52 означают Н и R53 означает фенил, то R53 не является незамещенным или замещенным галогеном или CF3,
или его фармацевтически приемлемая соль.
2. Соединение по п.1, которое представляет собой соединение формулы (Ia), или его фармацевтически приемлемая соль.
3. Соединение по п.2, в котором q равно 0, или его фармацевтически приемлемая соль.
4. Соединение по п.1, которое представляет собой соединение формулы (Ib), или его фармацевтически приемлемая соль.
5. Соединение по п.4, в котором R54 обозначает -CH3 или CF3, или его фармацевтически приемлемая соль.
6. Соединение по п.4 или 5, в котором n равно 1, или его фармацевтически приемлемая соль.
7. Соединение по пп.1-5 или 6, в котором R50 обозначает Н или метил; R51 обозначает Н, галоген, метил, трифторметил, метоксигруппу или -C(O)OCH3 и R52 обозначает галоген, -CN, метил, этил, метоксигруппу, гидроксиметил, 1-гидроксиэтил, 2-гидроксипропан-2-ил, дифторметил, трифторметил, диметоксиметил,
-NH2 или -NHC(O)CH3, или его фармацевтически приемлемая соль.
8. Соединение по пп.1-6 или 7, в котором R53 обозначает фенил, 4-хлор-3-фторфенил, м-толил, 3-метоксифенил, 3-хлор-4-фторфенил, 4-фтор-3-метилфенил, 3-трифторметилфенил, 3-хлорфенил, 4-фтор-3-трифторметилфенил, 3-дифторметил-4-фторфенил, 3-циано-4-фторфенил, 3-цианофенил, 3-хлор-4-цианофенил, 3,4-дифторфенил, 4-трифторметилфенил, или его фармацевтически приемлемая соль.
9. Соединение по пп.1-6 или 7, в котором R53 обозначает нафталин-2-ил, бензо[b]тиофен-5-ил, 3-метилбензо[d]изоксазол-5-ил, 1Н-индазол-5-ил, 1-метил-1Н-индазол-5-ил, 3-амино-1Н-индазол-5-ил, 1Н-индазол-6-ил, 3-амино-1Н-индазол-6-ил, 3-метил-1H-индазол-6-ил, 3-трифторметил-1Н-индазол-6-ил, бензотиазол-6-ил, 1,2-дигидро-3-оксоиндазол-6-ил, индан-5-ил, 1Н-бензотриазол-5-ил, 3-метилбензофуран-5-ил, 2,3-дигидробензо[1,4]диоксин-6-ил, 2,3-дигидробензофуран-5-ил или 2,2-дифторбензо[1,3]диоксол-5-ил, или его фармацевтически приемлемая соль.
10. Соединение по п.9, в котором R53 обозначает бензотиазол-6-ил, 3-метилбензофуран-5-ил, 1Н-индазол-6-ил, 3-метил-1Н-индазол-6-ил или 3-трифторметил-1Н-индазол-6-ил, или его фармацевтически приемлемая соль.
11. Соединение по пп.1-6 или 7, в котором R53 обозначает 5-метилтиофен-2-ил, 5-хлортиофен-2-ил, 5-трифторметилтиофен-2-ил, 5-дифторметилтиофен-3-ил, 5-метилтиофен-3-ил, 2-метилпиридин-4-ил, 2-трифторметилпиридин-4-ил, 2-хлорпиридин-4-ил или 2-метоксипиридин-4-ил, или его фармацевтически приемлемая соль.
12. Соединение по пп.1-6 или 7, в котором R53 обозначает 4-хлортиено[3,2-с]пиридин-2-ил, 4-хлортиено[3,2-с]пиридин-3-ил, тиено[3,2-с]пиридин-2-ил, 3-хлоримидазо[1,2-а]пиридин-7-ил, бензо[b]тиофен-2-ил или 4-метилтиено[3,2-с]пиридин-2-ил, или его фармацевтически приемлемая соль.
13. Соединение по п.1, выбранное из группы, включающей
1-бензотиазол-6-ил-3-(4-метилпиридин-3-ил)имидазолидин-2-он;
1-(2-хлорпиридин-4-ил)-3-(4-метилпиридин-3-ил)имидазолидин-2-он;
1-(4-хлортиено[3,2-с]пиридин-2-ил)-3-(4-метилпиридин-3-ил)имидазолидин-2-он;
1-(1Н-индазол-6-ил)-3-(4-метилпиридин-3-ил)имидазолидин-2-он;
1-(3-дифторметил-4-фторфенил)-3-(4-метилпиридин-3-ил)-1,3-дигидроимидазол-2-он;
1-(4-метилпиридин-3-ил)-3-(5-метилтиофен-3-ил)-1,3-дигидроимидазол-2-он;
1-(3-метил-1Н-индазол-6-ил)-3-(4-метилпиридин-3-ил)имидазолидин-2-он;
1-бензотиазол-6-ил-4-метил-3-(4-метилпиридин-3-ил)имидазолидин-2-он;
1-бензо[b]тиофен-5-ил-3-(4-метилпиридин-3-ил)-1,3-дигидроимидазол-2-он и
1-бензотиазол-6-ил-3-(4-метилпиридин-3-ил)-1,3-дигидроимидазол-2-он,
или его фармацевтически приемлемая соль.
14. Соединение по п.1, выбранное из группы, включающей
1-нафталин-2-ил-3-пиридин-3-илимидазолидин-2-он;
1-бензо[b]тиофен-5-ил-3-пиридин-3-илимидазолидин-2-он;
1-(4-метилпиридин-3-ил)-3-нафталин-2-илимидазолидин-2-он;
1-(4-метилпиридин-3-ил)-3-(5-метилтиофен-2-ил)имидазолидин-2-он;
1-бензотиазол-6-ил-3-(4-метилпиридин-3-ил)имидазолидин-2-он;
1-бензо[b]тиофен-5-ил-3-(4-метилпиридин-3-ил)имидазолидин-2-он;
1-(1H-индазол-5-ил)-3-(4-метилпиридин-3-ил)имидазолидин-2-он;
1-(3-метилбензофуран-5-ил)-3-(4-метилпиридин-3-ил)имидазолидин-2-он;
1-(5-хлортиофен-2-ил)-3-(4-метилпиридин-3-ил)имидазолидин-2-он;
1-(3,4-дифторфенил)-3-(4-метилпиридин-3-ил)имидазолидин-2-он;
1-(3-хлор-4-фторфенил)-3-(4-метилпиридин-3-ил)имидазолидин-2-он;
1-(2,3-дигидробензо[1,4]диоксин-6-ил)-3-(4-метилпиридин-3-ил)имидазолидин-2-он;
1-(2,3-дигидробензофуран-5-ил)-3-(4-метилпиридин-3-ил)имидазолидин-2-он;
1-(4-хлор-3-фторфенил)-3-(4-метилпиридин-3-ил)имидазолидин-2-он;
1-(4-метилпиридин-3-ил)-3-м-толилимидазолидин-2-он;
1-(3-метоксифенил)-3-(4-метилпиридин-3-ил)имидазолидин-2-он;
1-(2-хлорпиридин-4-ил)-3-(4-метилпиридин-3-ил)имидазолидин-2-он;
1-(4-фтор-3-метилфенил)-3-(4-метилпиридин-3-ил)имидазолидин-2-он;
1-(2,2-дифторбензо[1,3]диоксол-5-ил)-3-(4-метилпиридин-3-ил)имидазолидин-2-он;
1-(4-метилпиридин-3-ил)-3-фенилимидазолидин-2-он;
1-(4-метилпиридин-3-ил)-3-(3-трифторметилфенил)имидазолидин-2-он;
1-(2-метоксипиридин-4-ил)-3-(4-метилпиридин-3-ил)имидазолидин-2-он;
1-(5-дифторметилтиофен-3-ил)-3-(4-метилпиридин-3-ил)имидазолидин-2-он;
1-(3-хлорфенил)-3-(4-метилпиридин-3-ил)имидазолидин-2-он;
1-(4-фтор-3-трифторметилфенил)-3-(4-метилпиридин-3-ил)имидазолидин-2-он;
1-(3-дифторметил-4-фторфенил)-3-(4-метилпиридин-3-ил)имидазолидин-2-он;
1-(4-метилпиридин-3-ил)-3-(5-метилтиофен-3-ил)имидазолидин-2-он;
1-(4-хлортиено[3,2-с]пиридин-2-ил)-3-(4-метилпиридин-3-ил)имидазолидин-2-он;
1-(4-хлортиено[3,2-с]пиридин-3-ил)-3-(4-метилпиридин-3-ил)имидазолидин-2-он;
1-(4-метилпиридин-3-ил)-3-(2-метилпиридин-4-ил)имидазолидин-2-он;
1-(3-метилбензо[d]изоксазол-5-ил)-3-(4-метилпиридин-3-ил)имидазолидин-2-он;
1-(3-метил-1Н-индазол-6-ил)-3-(4-метилпиридин-3-ил)имидазолидин-2-он;
2-фтор-5-[3-(4-метилпиридин-3-ил)-2-оксоимидазолидин-1-ил]бензонитрил;
3-[3-(4-метилпиридин-3-ил)-2-оксоимидазолидин-1-ил]бензонитрил;
2-хлор-4-[3-(4-метилпиридин-3-ил)-2-оксоимидазолидин-1-ил]бензонитрил;
1-(1-метил-1H-индазол-5-ил)-3-(4-метилпиридин-3-ил)имидазолидин-2-он;
1-(3-амино-1Н-индазол-5-ил)-3-(4-метилпиридин-3-ил)имидазолидин-2-он;
1-(4-метилпиридин-3-ил)-3-тиено[3,2-с]пиридин-2-илимидазолидин-2-он;
1-(1H-индазол-6-ил)-3-(4-метилпиридин-3-ил)имидазолидин-2-он;
1-(3-амино-1Н-индазол-6-ил)-3-(4-метилпиридин-3-ил)имидазолидин-2-он;
1-бензотиазол-6-ил-3-(4-метоксипиридин-3-ил)имидазолидин-2-он;
1-бензотиазол-6-ил-3-(4-дифторметилпиридин-3-ил)имидазолидин-2-он;
1-бензотиазол-6-ил-3-(4-гидроксиметилпиридин-3-ил)имидазолидин-2-он;
1-бензотиазол-6-ил-3-(4-трифторметилпиридин-3-ил)имидазолидин-2-он;
1-индан-5-ил-3-(4-метилпиридин-3-ил)имидазолидин-2-он;
1-(1Н-бензотриазол-5-ил)-3-(4-метилпиридин-3-ил)имидазолидин-2-он;
1-(3-хлоримидазо[1,2-а]пиридин-7-ил)-3-(4-метилпиридин-3-ил)имидазолидин-2-он;
1-(4-метилпиридин-3-ил)-3-(2-трифторметилпиридин-4-ил)имидазолидин-2-он;
1-бензотиазол-6-ил-3-(4-диметоксиметилпиридин-3-ил)имидазолидин-2-он;
1-бензотиазол-6-ил-3-(5-хлор-4-метилпиридин-3-ил)имидазолидин-2-он;
1-(4-метилпиридин-3-ил)-3-(5-(трифторметил)тиофен-2-ил)имидазолидин-2-он;
1-(4-метилпиридин-3-ил)-3-(4-метилтиено[3,2-с]пиридин-2-ил)имидазолидин-2-он;
1-(бензо[d]тиазол-6-ил)-3-(4-(1-гидроксиэтил)пиридин-3-ил)имидазолидин-2-он;
1-(бензо[d]тиазол-6-ил)-3-(4-этилпиридин-3-ил)имидазолидин-2-он;
1-(4-метилпиридин-3-ил)-3-(3-(трифторметил)-1Н-индазол-6-ил)имидазолидин-2-он;
1-бензотиазол-6-ил-4-метил-3-(4-метилпиридин-3-ил)имидазолидин-2-он;
1-бензотиазол-6-ил-4-этил-3-(4-метилпиридин-3-ил)-1,3-дигидроимидазол-2-он;
1-бензотиазол-6-ил-4-этил-3-пиридин-3-ил-1,3-дигидроимидазол-2-он;
1-бензотиазол-6-ил-3-пиридин-3-ил-4-трифторметилимидазолидин-2-он;
1-бензотиазол-6-ил-3-(4-метилпиридин-3-ил)-1,3-дигидробензимидазол-2-он;
1-бензотиазол-6-ил-4-метил-3-(4-метилпиридин-3-ил)имидазолидин-2-он;
3-бензотиазол-6-ил-1-пиридин-3-ил-4-трифторметилимидазолидин-2-он;
1-бензотиазол-6-ил-3-(4-метилпиридин-3-ил)-4-трифторметилимидазолидин-2-он;
1-бензотиазол-6-ил-4,5-диметил-3-(4-метилпиридин-3-ил)имидазолидин-2-он;
1-бензотиазол-6-ил-3-(6-фтор-4-метилпиридин-3-ил)имидазолидин-2-он;
3-(3-бензотиазол-6-ил-2-оксоимидазолидин-1-ил)изоникотинамид;
1-бензотиазол-6-ил-3-(4-метил-5-трифторметилпиридин-3-ил)имидазолидин-2-он;
1-изотиазол-4-ил-3-(4-метилпиридин-3-ил)имидазолидин-2-он;
1-(4-метилпиридин-3-ил)-3-(5-трифторметилтиофен-2-ил)имидазолидин-2-он;
1-бензотиазол-6-ил-3-[4-(1-гидрокси-1-метилэтил)пиридин-3-ил]имидазолидин-2-он;
1-(4-метилпиридин-3-ил)-3-(4-метилтиено[3,2-с]пиридин-2-ил)имидазолидин-2-он;
1-бензотиазол-6-ил-3-[4-(1-гидроксиэтил)пиридин-3-ил]имидазолидин-2-он;
1-бензотиазол-6-ил-3-(4-этилпиридин-3-ил)имидазолидин-2-он;
1-(4-метилпиридин-3-ил)-3-(3-трифторметил-1Н-индазол-6-ил)имидазолидин-2-он;
1-(3-циклопропил-1H-индазол-6-ил)-3-(4-метилпиридин-3-ил)имидазолидин-2-он;
3-бензотиазол-6-ил-4,4-диметил-1-(4-метилпиридин-3-ил)имидазолидин-2-он;
1-бензотиазол-6-ил-4,4-диметил-3-пиридин-3-илимидазолидин-2-он;
1-бензотиазол-6-ил-4,4-диметил-3-(4-метилпиридин-3-ил)имидазолидин-2-он;
3-бензотиазол-6-ил-4-метил-1-(4-метилпиридин-3-ил)имидазолидин-2-он;
1-бензотиазол-6-ил-4-метил-3-(4-метилпиридин-3-ил)имидазолидин-2-он;
1-бензотиазол-6-ил-4,5-диметил-3-(4-метилпиридин-3-ил)имидазолидин-2-он;
1-бензотиазол-6-ил-4,4-диметил-3-пиридин-3-илимидазолидин-2-он и
3-бензотиазол-6-ил-4-метил-1-(4-метилпиридин-3-ил)имидазолидин-2-он,
или его фармацевтически приемлемая соль.
15. Соединение по п.1, которое представляет собой 1-(2-хлорпиридин-4-ил)-3-(4-метилпиридин-3-ил)имидазолидин-2-она (58А):
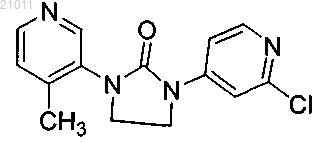
или его фармацевтически приемлемая соль.
16. Фармацевтическая композиция, предназначенная для лечения заболевания, нарушения или синдрома, опосредуемого ингибированием Cyp 17, содержащая соединение по любому из пп.1-15 или его фармацевтически приемлемую соль и фармацевтически приемлемый носитель или инертный наполнитель.
17. Применение соединения по любому из пп.1-15 или его фармацевтически приемлемой соли для получения лекарственного средства для лечения заболевания, нарушения или синдрома, опосредуемого ингибированием Cyp 17.
18. Применение по п.17, где заболевание, нарушение или синдром, опосредуемый ингибированием Cyp 17, представляют собой воспаление или рак.
19. Применение по п.18, где рак представляет собой рак простаты.
20. Применение соединения по любому из пп.1-15 для лечения заболевания, нарушения или синдрома, опосредуемого ингибированием Cyp 17.
21. Применение по п.20, где заболевание, нарушение или синдром, опосредуемый ингибированием Cyp 17, представляют собой воспаление или рак.
22. Применение по п.21, где рак представляет собой рак простаты.
Текст
В изобретении приведено описание соединений формул (Iа) и (Ib) или их фармацевтически приемлемых солей Область техники, к которой относится изобретение Настоящее изобретение относится к циклическим производным мочевины и их применению для лечения различных патологических состояний, опосредуемых регулированием 17-гидроксилазы/С 17,20 лиазы. Уровень техники Количество людей во всем мире, у которых диагностирован рак, значительно возросло и продолжает увеличиваться с вызывающей тревогу скоростью. Рак характеризуется увеличением количества аномальных клеток, образовавшихся из данной нормальной ткани, инвазией этих аномальных клеток в соседние ткани или распространением по лимфатической системе или с кровью злокачественных клеток в региональные лимфатические узлы и на удаленные участки (т.е. метастазированием). Особый интерес представляют индивидуумы, у которых диагностированы андрогензависимые нарушения, такие как рак предстательной железы, и эстрогензависимые нарушения, такие как рак молочной железы, матки и яичников. В настоящее время рак предстательной железы является самым распространенным раковым заболеванием, не являющимся заболеванием кожи, и второй по распространенности основной причиной вызванной раком смерти у мужчин после рака легких. Первичным курсом лечения пациентов, у которых диагностирован ограниченный органом рак предстательной железы, обычно является удаление предстательной железы или лучевая терапия. Эти методики лечения рака предстательной и молочной железы являются сильно инвазивными и характеризуются нежелательными и тяжелыми побочными эффектами. Кроме того, значительная доля индивидуумов, для которых использовали локализованные методики лечения, такие как оперативное вмешательство и лучевая терапия, могут страдать от рецидива рака и распространенных метастазов. Как и в случае оперативного вмешательства и лучевой терапии, имеются серьезные недостатки и у химиотерапии, включая тот факт, что почти все химиотерапевтические средства являются токсичными и химиотерапия приводит к тяжелым и часто опасным побочным эффектам, таким как сильная тошнота, подавление деятельности костного мозга и подавление иммунитета. Кроме того,многие опухолевые клетки могут стать или являются резистентными к химиотерапевтическим средствам вследствие множественной лекарственной резистентности. Методики лечения, такие как гормональная терапия, являются другим вариантом для индивидуумов, у которых диагностированы гормонозависимые, отвечающие на воздействие гормонов или чувствительные к гормонам типы рака, такие как рак предстательной или молочной железы. Однако у некоторых индивидуумов, для которых использовали современные методики гормональной терапии, может не проявляться существенный ответ на такое лечение и у некоторых может наблюдаться рецидив рака. В настоящее время для пациентов, страдающих резистентным по отношению к химиотерапевтическим средствам и по отношению к гормонам раком, существует очень мало методик лечения и сохраняется потребность в более эффективных путях лечения рака, такого как, но не ограничиваясь только ими,рак предстательной железы и рак молочной железы. Данные публикации Huggins and Hodges C.V. (Cancer Res., 1941, 1, 293) and Huggins et al. in Arch.Surg., 1941, 43, 209 привели к тому, что в качестве возможной методики лечения стали рассматривать абляцию андрогеном. Было показано, что при удалении яичка или введении аналогов GnRH (гонадотропный рилизинг-гормон) уменьшается содержание тестостерона. Аналоги GnRH могут приводить к побочным эффектам, таким как сердечно-сосудистая дегенерация и остеопороз, которые являются двумя потенциально самыми тяжелыми патологическими состояниям, вызывающимися постоянным наличием аналогов GnRH. Кроме того, эти методики лечения прекращают выработку тестостерона только яичками,но не надпочечниками. В надпочечниках каскад биосинтеза также приводит к образованию глюко- и минералокортикоидов. Поскольку андроген и эстроген являются гормонами, обладающими разнообразной физиологической активностью, такой как влияние на дифференциацию и пролиферацию клеток и т.п., полагают, что активные и специфические соединения, которые подавляют синтез андрогена в яичках, надпочечниках и других тканях, могут быть более эффективными для лечения рака предстательной железы (Njar, V.С.О.;prostate cancer", Current Pharm. Design, 1999, 5: 163-180). Для исключения нежелательных побочных эффектов ингибиторы биосинтеза андрогена должны быть достаточно специфичными, чтобы не влиять на биосинтез кортикостероидов. Перспективной новой стратегией лечения рака предстательной железы является получение активных и селективных ингибиторов Cyp 17, поскольку это приведет к полному и исключительному прекращению биосинтеза андрогена,как это предположено в публикации Current Medicinal Chemistry, 2005, 12, 1623-1629. Соединения стероидного типа и соединения нестероидного типа уже известны как ингибиторы стероид C17,20-лиазы. Соединения стероидного типа раскрыты, например, в WO 92/15404, WO 93/20097,ЕР-А-288053, ЕР-А-413270 и т.п. Соединения нестероидного типа описаны, например, в WO 94/27989,WO 96/14090 и WO 97/00257, производные азола описаны в WO 95/09157, производные-1 021011 1 Н-бензимидазола описаны в US 5491161, производные дигидронафталина описаны в WO 99/18075 и производные нафталина указаны в WO 99/54309. Описано большое количество активных стероидных и нестероидных ингибиторов Cyp17 и с помощью моделей на грызунах показано, что некоторые из них являются активными ингибиторами выработки тестостерона (Njar and Brodie, выше). Jarman с сотрудниками описали влияние на гормоны своего наиболее активного ингибитора Cyp17, абиратерона, у пациентов, страдающих раком предстательной железы (O'Donnell et al., "Hormonal impact of the 17-hydroxylase/C17,20-lyase inhibitors abiraterone acetate(CB7630) in patients with prostate cancer", Br. J. Cancer, 2004, 90:2317-2325). Абиратерон рассмотрен в патентах, таких как WO 2009/00132, WO 2008/024485, WO 2006/021776, WO 09/509178, WO 09/320097. Нестероидные малые молекулы-ингибиторы описаны, например, в ВМС 2004, 12 (4313), YM116, 2(1 Н-имидазол-4-илметил)-9 Н-карбазол, и их влияние на уменьшение синтеза андрогена надпочечниками путем ингибирования активности C17-20-лиазы в клетках NCI-H295 адренокортикальной карциномы человека описано в публикации Ideyama Y., Kudoh M., Tanimoto K., Susaki Y., Nanya T., Nakahara T.,Ishikawa H., Fujikura T., Akaza H., Shikama H. in "Jpn. J. Pharmacol., 1999, 79, No. 2 (213-20)". Новый нестероидный ингибитор цитохрома Р 450 (17-альфа-гидроксилаза/C17-20-лиаза), YM116 и его влияние на уменьшение массы предстательной железы путем уменьшения концентрации тестостерона и андрогенов надпочечников у крыс описаны в публикации Ideyama Y., Kudoh M., Tanimoto K., Susaki Y., Nanya T.,Nakahara T., Ishikawa H., Yoden T., Okada M., Fujikura T., Shikama H. Proc. Am. Assoc. Cancer Res., 1998,39:89 Meet. (384). Синтез и биологическое исследование новых нестероидных ингибиторов стероид-17,20-лиазы описаны в публикации Yoden T., Okada M., Kawaminami E., Kinoyama I., Ideyama Y., Isomura Y. in Abstr. Pap.Am. Chem. Soc., 1997, 213 Meet.: Pt. 2 (MEDI206). Другими иллюстрациями уровня техники для настоящего изобретения являются заявки на патенты,такие как US20080280864 A1 или WO 28154382 A1. Краткое изложение сущности изобретения Показано, что соединения, описанные в настоящем изобретении, являются ингибиторами 17-гидроксилазы/С 17,20-лиазы. В одном варианте осуществления настоящее изобретение относится к соединениям формулы (I) или(i) фенил, необязательно содержащий от 1 до 3 заместителей, выбранных из группы, включающей галоген, -CN, -ОН, (C1-C6)алкил, галогензамещенный (C1-C6)алкил, (C1-C6)алкоксигруппу, -NH2,-NH(C1-C4)алкил,-NC1-C4)алкил)2,-NHC(O)-(C1-C4)алкил,-C(O)NH2,-С(О)-NH(C1-C4)алкил,-C(O)-NC1-C4)алкил)2, или 5-6-членный гетероцикл,(ii) бифенил, необязательно содержащий от 1 до 3 заместителей, выбранных из группы, включающей (C1-C4)алкил или галоген,(iii) фенил, сконденсированный с дополнительным фенилом, 5-6-членный гетероарил, 5-6-членный частично или полностью насыщенный циклоалкил или 5-6-членный частично или полностью насыщенный гетероцикл, где указанный конденсированный фенил необязательно содержит от 1 до 4 заместителей, каждый из которых независимо выбран из группы, включающей галоген, -CN, (C1-C6)алкил,(C1-C6)алкоксигруппу, гидроксизамещенный (C1-C4)алкил, галогензамещенный (C1-C4)алкил, циклопропил, оксогруппу, -NH2, -NH(C1-С 4)алкил, -NC1-C4)алкил)2, -NHC(O-(С 1-С 4)алкил или =N-OH,(iv) 5-6-членный гетероарил, необязательно содержащий от 1 до 3 заместителей, выбранных из группы, включающей галоген, -CN, -ОН, (C1-C6)алкил, галогензамещенный (C1-C6)алкил,(C1-C6)алкоксигруппу, -NH2, -NH(C1-С 4)алкил, -NC1-C4)алкил)2, -NHC(O)-(C1-C4)алкил, -C(O)NH2,-C(O)-NH(C1-С 4)алкил, -С(О)-NC1-C4)алкил)2, или 5-6-членный гетероцикл,(v) 5-6-членный гетероарил, сконденсированный с другим 5-6-членным гетероарилом, фенилом,5-6-членным частично или полностью насыщенным циклоалкилом или 5-6-членным частично или полностью насыщенным гетероциклом, где указанный конденсированный гетероарил необязательно содержит от 1 до 4 заместителей, каждый из которых независимо выбран из группы, включающей галоген,-CN, (C1-C6)алкил, (C1-C6)алкоксигруппу, гидроксизамещенный (C1-C4)алкил, галогензамещенный-2 021011 вместе с атомом (атомами) углерода, к которому они присоединены, образуют 3-6-членное полностью или частично насыщенное карбоциклическое кольцо, или два R54, присоединенные к соседним атомам углерода, взятые вместе с атомами углерода, к которым они присоединены, образуют конденсированный фенил; р равно 0, 1, 2 или 3;q равно 0, 1 или 2; А обозначает 5-10-членный гетероарил, содержащий один или большее количество атомов азота, где указанный гетероарил необязательно содержит от 1 до 3 заместителей, каждый из которых независимо выбран из группы, включающей галоген, -ОН, -CN, (C1-C4)алкил, галогензамещенный-(CH2)sNH(С 1-С 4)алкил необязательно замещены 4-6-членным частично или полностью насыщенным гетероциклом или гетероарилом, содержащим от 1 до 3 гетероатомов, каждый из которых независимо выбран из группы, включающей О, S или N, где указанный гетероцикл и указанный гетероарил необязательно замещены 1-3 (C1-C4)алкильными группами;s равно 1 или 2; или их фармацевтически приемлемой соли; при условии что, если:(i) А представляет собой незамещенный пиридин и R53 обозначает фенил, R53 не является незамещенным или монозамещенным галогеном, CH3, NH2, -NHC(O)CH3 или CF3;(iii) указанное соединение не представляет собой 1-(3,4-дихлорфенил)-3-[6-(2-пиперидин-1-илэтокси)пиридин-3-ил]имидазолидин-2-он,1-(3,5-дихлорпиридин-2-ил)-3-фенилтетрагидропиримидин-2(1 Н)-он,1,3-бис-(6-хлорпиридин-2-ил)тетрагидропиримидин-2(1H)-он,1,3-бис-(4-метилпиридин-2-ил)имидазолидин-2-он,1-(5-хлор-1 Н-бензо[d]имидазол-2-ил)-3-фенилимидазолидин-2-он или 2-(2-оксо-3-фенилимидазолидин-1-ил)-1 Н-бензо[d]имидазол-5-карбонитрил. В предпочтительном варианте осуществления А обозначает 5-членный гетероарил, содержащий от 1 до 2 атомов азота, где указанный гетероарил необязательно замещен (С 1-С 4)алкилом или галогензамещенным (C1-С 4)алкилом; или его фармацевтически приемлемую соль. В другом предпочтительном варианте осуществления А обозначает 6-членный гетероарил, содержащий от 1 до 2 атомов азота, где указанный гетероарил необязательно замещен (C1-C4)алкилом или галогензамещенным (C1-С 4)алкилом; или его фармацевтически приемлемую соль. В другом предпочтительном варианте осуществления А обозначает пиридин, где указанный пиридин необязательно содержит от 1 до 3 заместителей, каждый из которых независимо выбран из группы, включающей галоген, -CN, (C1-C4)алкил, галогензамещенный (С 1-С 4)алкил, гидроксизамещенный(C1-C4)алкил,-(CH2)rO(C1-C4)алкил,-(CH2)rCH(O(C1-С 4)алкил)2,-(CH2)rNH(C1-C4)алкил,-(CH2)rNС 1-С 4)алкил)2, -(CH2)rNH(C3-С 6)циклоалкил, -NH2, -NHC(O)-(C1-C4)алкил, -C(O)NH2,-C(O)-NH(C1-С 4)алкил, -С(О)-NС 1-С 4)алкил)2 или -С(О)-O(С 1-С 4)алкил, где указанный (C1-C4)алкил,указанный -(CH2)rO(C1-C4)алкил и указанный -(CH2)rNH(C1-C4)алкил необязательно замещены 5-6-членным частично или полностью насыщенным гетероциклом или гетероарилом, содержащим от 1 до 2 гетероатомов, каждый из которых независимо выбран из группы, включающей О, S или N, где указанный гетероцикл и указанный гетероарил необязательно замещены 1-3 (C1-С 4)алкильными группами иr равно 1 или 2; или его фармацевтически приемлемую соль. Предпочтительно, если А обозначает необязательно замещенный пиридин-3-ил, предпочтительно пиридин-3-ил, замещенный трифторметилом, или(C1-C4)алкил, замещенный 5-6-членным частично или полностью насыщенным гетероциклом (предпочтительно, если гетероцикл присоединен к алкильной группе через кольцевой атом азота, например пирролидин-1-илметил). В еще одном предпочтительном варианте осуществления соединением формулы (I) или (II) является соединение формулы (Ia) или (Ib):-3 021011 где n, R50, R51, R52, R53, R54 и q являются такими, как определено выше; или его фармацевтически приемлемая соль. В предпочтительном варианте осуществления соединения формулы (Ib) R52 обозначает CF3 или(C1-C4)алкил, замещенный 5-6-членным частично или полностью насыщенным гетероциклом (предпочтительно, если гетероцикл присоединен к алкильной группе через кольцевой атом азота, например пирролидин-1-илметил). В другом предпочтительном варианте осуществления соединения формулы (Ib)n равно 1 и р равно 0. В другом варианте осуществления настоящее изобретение относится к соединениям формулы (Ia) или (Ib):(i) фенил, необязательно содержащий от 1 до 3 заместителей, выбранных из группы,включающей галоген, -CN, -ОН, (C1-C6)алкил, галогензамещенный (C1-С 6)алкил, (C1-C6)алкоксигруппу,-NH2, -NH(С 1-С 4)алкил, -NC1-C4)алкил)2, -NHC(O-(C1-C4)алкил, -C(O)NH2, -С(О)-NH(С 1-С 4)алкил,-C(O)-NC1-С 4)алкил)2, или 5-6-членный гетероцикл,(ii) бифенил, необязательно содержащий от 1 до 3 заместителей, выбранных из группы, включающей (C1-C4)алкил или галоген,(iii) фенил, сконденсированный с дополнительным фенилом, 5-6-членный гетероарил, 5-6-членный частично или полностью насыщенный циклоалкил или 5-6-членный частично или полностью насыщенный гетероцикл, где указанный конденсированный фенил необязательно содержит от 1 до 4 заместителей, каждый из которых независимо выбран из группы, включающей галоген, -CN, (C1-C6)алкил,(C1-C6)алкоксигруппу, гидроксизамещенный (C1-C4)алкил, галогензамещенный (C1-C4)алкил, циклопропил, оксогруппу, -NH2, -NH(C1-С 4)алкил, -NС 1-С 4)алкил)2, -NHC(O-(C1-C4)алкил или =N-OH,(iv) 5-6-членный гетероарил, необязательно содержащий от 1 до 3 заместителей, выбранных из группы, включающей галоген, -CN, -ОН, (C1-C6)алкил, галогензамещенный (C1-C6)алкил,(C1-C6)алкоксигруппу, -NH2, -NH(C1-C4)алкил, -NC1-C4)алкил)2, -NHC(O-(C1-C4)алкил, -C(O)NH2,-С(О)-NH(C1-C4)алкил, -С(О)-NC1-C4)алкил)2, или 5-6-членный гетероцикл,(v) 5-6-членный гетероарил, сконденсированный с другим 5-6-членным гетероарилом, фенилом,5-6-членным частично или полностью насыщенным циклоалкилом или 5-6-членным частично или полностью насыщенным гетероциклом, где указанный конденсированный гетероарил необязательно содержит от 1 до 4 заместителей, каждый из которых независимо выбран из группы, включающей галоген,-CN, (C1-C6)алкил, (C1-C6)алкоксигруппу, гидроксизамещенный (C1-C4)алкил, галогензамещенныйR54 обозначает (C1-C4)алкил (например, -CH3), галогензамещенный (C1-C4)алкил (например, -CF3) или -CH2OH или два R54, взятые вместе с атомом (атомами) углерода, к которому они присоединены,образуют 3-6-членное полностью или частично насыщенное карбоциклическое кольцо (например, для соединения формулы (Ia), если q равно 2, то два R54 у соседних атомов углерода могут образовать конденсированное циклоалкенильное кольцо; и в соединениях формулы (Ib), если р равно 2 или 3, то два R54 у соседних атомов углерода могут образовать конденсированное полностью или частично насыщенное циклоалкильное кольцо или два R54 у одного атома углерода могут образовать спирановое кольцо); р равно 0, 1, 2 или 3;R50, R51 и R52 все независимо обозначают Н, галоген, -ОН, -CN, (C1-C4)алкил, галогензамещенныйr равно 0, 1 или 2; при условии что, если R50, R51 и R52 обозначают Н и R53 обозначает фенил, R53 не является незамещенным или замещенным галогеном или CF3; или их фармацевтически приемлемой соли. Один вариант осуществления относится к соединению формулы (Ia), описывающемуся приведенными выше определениями.-4 021011 Другой вариант осуществления относится к соединению формулы (Ib), описывающемуся приведенными выше определениями. Еще один вариант осуществления относится к соединениям формулы (Ib), в которой n равно 1. Предпочтительно, если R50 обозначает Н или метил (более предпочтительно, если R50 обозначает Н), R51 обозначает Н, галоген, метил, трифторметил, метоксигруппу или -C(O)OCH3 и R52 обозначает галоген, -CN, метил, этил, метоксигруппу, гидроксиметил, 1-гидроксиэтил, 2-гидроксипропан-2-ил, дифторметил, трифторметил, диметоксиметил, -NH2 или -NHC(OCH3. Предпочтительно (для соединения формулы (I), (II), (Ia) и (Ib, если R53 обозначает:(i) фенил, необязательно содержащий от 1 до 2 заместителей, каждый из которых независимо выбран из группы, включающей фтор, хлор, цианогруппу, метил, дифторметил, трифторметил,метоксигруппу или -C(O)NHCH3;(iii) конденсированный фенил, выбранный из группы, включающей нафталин-2-ил, нафталин-1-ил,1 Н-индол-5-ил, 1H-индол-6-ил, бензотиазол-5-ил, бензотиазол-6-ил, 1,2,3,4-тетрагидрохинолин-6-ил,бензо[b]тиофен-5-ил,хинолин-6-ил,хинолин-7-ил,индан-5-ил,1,2-дигидрохинолин-6-ил,1 Н-индазол-5-ил,1 Н-индазол-6-ил,бензофуран-5-ил,2,3-дигидробензо[1,4]диоксин-6-ил,2,3-дигидробензофуран-5-ил, бензо[1,3]диоксол-5-ил, 1,2,3,4-тетрагидрохинолин-7-ил, хиноксалин-6-ил,бензооксазол-5-ил, бензо[d]изоксазол-5-ил, бензо[d]изоксазол-6-ил, 1 Н-бензимидазол-5-ил, 2,3-дигидро 1 Н-индазол-5-ил, 2,3-дигидро-1 Н-индазол-6-ил, индолин-5-ил или 1H-бензотриазол-5-ил, где указанный конденсированный фенил необязательно содержит от 1 до 3 заместителей, каждый из которых независимо выбран из группы, включающей фтор, хлор, метил, этил, трифторметил, метоксигруппу, оксогруппу,-NH2, =N-OH или циклопропил;(iv) 5-6-членный гетероарил, выбранный из группы, включающей тиофен-2-ил, тиофен-3-ил, пиридин-3-ил, пиридин-4-ил, пиримидин-5-ил, 1 Н-пиразол-4-ил, тиазол-2-ил или изотиазол-4-ил, где указанный 5-6-членный гетероарил необязательно содержит от 1 до 3 заместителей, каждый из которых независимо выбран из группы, включающей фтор, хлор, метил, этил, изопропил, гидроксигруппу, дифторметил, трифторметил, метоксигруппу, -NH2, -NHC(O)CH3, -C(O)NHCH3, или пирролидин-1-ил; или(v) конденсированный гетероарил, выбранный из группы, включающей бензо[b]тиофен-2-ил,бензо[b]тиофен-3-ил,хинолин-2-ил,хинолин-3-ил,бензооксазол-2-ил,бензотиазол-2-ил,4,5,6,7-тетрагидротиено[2,3-с]пиридин-2-ил, имидазо[1,2-а]пиридин-3-ил, имидазо[1,2-а]пиридин-6-ил,имидазо[1,2-а]пиридин-7-ил,3 Н-имидазо[4,5-b]пиридин-6-ил,тиено[3,2-с]пиридин-2-ил,тиено[3,2-с]пиридин-3-ил или 1 Н-индол-3-ил, где указанный конденсированный гетероарил необязательно содержит от 1 до 4 заместителей, каждый из которых независимо выбран из группы, включающей фтор, хлор, цианогруппу, метил или метоксигруппу; или его фармацевтически приемлемую соль. Более предпочтительно, если R53 обозначает:(i) фенил, необязательно содержащий от 1 до 2 заместителей, каждый из которых независимо выбран из группы, включающей фтор, хлор, метил, метоксигруппу, трифторметил, дифторметил или цианогруппу;(iii) конденсированный фенил, выбранный из группы, включающей нафталин-2-ил, хинолин-6-ил,3,4-дигидро-2-оксохинолин-6-ил, бензо[b]тиофен-5-ил, бензо[d]изоксазол-5-ил, 1H-индазол-6-ил,1 Н-индазол-5-ил, бензотиазол-6-ил, 1,2-дигидро-3-оксоиндазол-6-ил, индан-5-ил, 1 Н-бензотриазол-5-ил,бензофуран-5-ил,2,3-дигидробензо[1,4]диоксин-6-ил,2,3-дигидробензофуран-5-ил или бензо[1,3]диоксол-5-ил, где указанный конденсированный фенил необязательно содержит от 1 до 2 заместителей, каждый из которых независимо выбран из группы, включающей хлор, фтор, метил, этил,дифторметил, трифторметил, циклопропил, цианогруппу или аминогруппу;(iv) 5-6-членный гетероарил, выбранный из группы, включающей изотиазол-4-ил, тиофен-2-ил,тиофен-3-ил или пиридин-4-ил, где указанный изотиазол-4-ил, указанный тиофен-2-ил, указанный тиофен-3-ил и указанный пиридин-4-ил необязательно содержат следующие заместители: фтор, хлор,метил, трифторметил, дифторметил или метоксигруппу; или(v) конденсированный гетероарил, выбранный из группы, включающей тиено[3,2-с]пиридин-2-ил,тиено[3,2-с]пиридин-3-ил, тиено[3,2-с]пиридин-2-ил, имидазо[1,2-а]пиридин-7-ил или бензо[b]тиофен-2 ил, где указанный конденсированный гетероарил необязательно содержит от 1 до 2 заместителей, каждый из которых независимо выбран из группы, включающей фтор, хлор, метил, дифторметил, трифторметил, циклопропил или аминогруппу; или его фармацевтически приемлемую соль. В одном предпочтительном варианте осуществления R53 обозначает фенил, 4-хлор-3-фторфенил,м-толил,3-метоксифенил,3-хлор-4-фторфенил,4-фтор-3-метилфенил,3-трифторметилфенил,3-хлорфенил, 4-фтор-3-трифторметилфенил, 3-дифторметил-4-фторфенил, 3-циано-4-фторфенил,3-цианофенил, 3-хлор-4-цианофенил, 3,4-дифторфенил, 4-трифторметилфенил; или его фармацевтически приемлемую соль. В другом предпочтительном варианте осуществления R53 обозначает нафталин-2-ил, бензо[b]тиофен-5-ил, 3-метилбензо[d]изоксазол-5-ил, 1 Н-индазол-5-ил, 1-метил-1 Н-индазол-5-ил, 3-амино-5 021011 1 Н-индазол-5-ил,1 Н-индазол-6-ил,3-амино-1 Н-индазол-6-ил,3-метил-1 Н-индазол-6-ил,3-трифторметил-1 Н-индазол-6-ил, бензотиазол-6-ил, 1,2-дигидро-3-оксоиндазол-6-ил, индан-5-ил,1H-бензотриазол-5-ил,3-метилбензофуран-5-ил,2,3-дигидробензо[1,4]диоксин-6-ил,2,3-дигидробензофуран-5-ил или 2,2-дифторбензо[1,3]диоксол-5-ил; или его фармацевтически приемлемую соль. Более предпочтительно R53 обозначает бензотиазол-6-ил, 3-метилбензофуран-5-ил,1 Н-индазол-6-ил, 3-метил-1 Н-индазол-6-ил или 3-трифторметил-1 Н-индазол-6-ил; или его фармацевтически приемлемую соль. В еще одном предпочтительном варианте осуществления R53 обозначает 5-метилтиофен-2-ил,5-хлортиофен-2-ил, 5-трифторметилтиофен-2-ил, 5-дифторметилтиофен-3-ил, 5-метилтиофен-3-ил,2-метилпиридин-4-ил, 2-трифторметилпиридин-4-ил, 2-хлорпиридин-4-ил или 2-метоксипиридин-4-ил; или его фармацевтически приемлемую соль. В еще одном предпочтительном варианте осуществления R53 обозначает 4-хлортиено[3,2-с]пиридин-2-ил, 4-хлортиено[3,2-с]пиридин-3-ил, тиено[3,2-с]пиридин-2-ил, 3-хлоримидазо[1,2-а]пиридин-7-ил, бензо[b]тиофен-2-ил или 4-метилтиено[3,2-с]пиридин-2-ил; или его фармацевтически приемлемую соль. В другом варианте осуществления соединений формулы (I), (II), (Ia) или (Ib) R54 обозначает -CH3 или CF3. Предпочтительные соединения включают: 1-бензотиазол-6-ил-3-(4-метилпиридин-3-ил)имидазолидин-2-он; 1-(2-хлорпиридин-4-ил)-3-(4-метилпиридин-3-ил)имидазолидин-2-он; 1-(4-хлортиено[3,2-с]пиридин-2-ил)-3-(4-метилпиридин-3-ил)имидазолидин-2-он; 1-(1 Н-индазол-6-ил)-3-(4-метилпиридин-3-ил)имидазолидин-2-он; 1-(3-дифторметил-4-фторфенил)-3-(4-метилпиридин-3-ил)-1,3-дигидроимидазол-2-он; 1-(4-метилпиридин-3-ил)-3-(5-метилтиофен-3-ил)-1,3-дигидроимидазол-2-он; 1-(3-метил-1H-индазол-6-ил)-3-(4-метилпиридин-3-ил)имидазолидин-2-он; 1-бензотиазол-6-ил-4-метил-3-(4-метилпиридин-3-ил)имидазолидин-2-он; 1-бензо[b]тиофен-5-ил-3-(4-метилпиридин-3-ил)-1,3-дигидроимидазол-2-он и 1-бензотиазол-6-ил-3-(4-метилпиридин-3-ил)-1,3-дигидроимидазол-2-он или их фармацевтически приемлемую соль. Другие соединения включают описанные ниже в разделе "Примеры", предпочтительно соединения,характеризующиеся значением IC50, равным менее 1 мкМ (или 1 нМ), предпочтительно менее 500 нМ,более предпочтительно менее 100 нМ. Другим объектом настоящего изобретения является фармацевтическая композиция, которая содержит соединение формулы (I), (II), (Ia) или (Ib) или его фармацевтически приемлемую соль и фармацевтически приемлемый носитель или инертный наполнитель. Фармацевтическая композиция необязательно содержит по меньшей мере одно дополнительное фармацевтическое средство (подходящие фармацевтические средства описаны ниже в настоящем изобретении). Еще одним объектом настоящего изобретения является способ лечения заболевания, нарушения или синдрома, опосредуемого ингибированием Cyp 17, способ включает введение нуждающемуся в нем субъекту соединения формул (I), (II), (Ia) или (Ib) или фармацевтической композиции, содержащей соединение формул (I), (II), (Ia) или (Ib) и фармацевтически приемлемые инертные наполнители. Другим объектом настоящего изобретения является соединение формул (I), (II), (Ia) или (Ib), предназначенное для применения для лечения (например, применение соединения формулы (Ia) или (Ib) для лечения заболевания, нарушения или синдрома, опосредуемого ингибированием Cyp 17). Еще одним объектом настоящего изобретения является способ лечения заболевания, нарушения или синдрома, опосредуемого ингибированием Cyp 17, включающий стадию введения:(i) первой композиции, содержащей соединение по пп.1-21 формулы изобретения или его фармацевтически приемлемую соль и фармацевтически приемлемый носитель или инертный наполнитель; и(ii) второй композиции, содержащей по меньшей мере одно дополнительное фармацевтическое средство и фармацевтически приемлемый носитель или инертный наполнитель; где указанное по меньшей мере одно дополнительное фармацевтическое средство представляет собой противораковое средство, химиотерапевтическое средство или антипролиферативное соединение. Первую или вторую композицию можно вводить одновременно или последовательно в любом порядке. В одном предпочтительном варианте осуществления каждого из способов и применение, описанных выше, заболевание, нарушение или синдром выбрано из группы, включающей рак (в частности, рак предстательной железы) и воспаление. Определения При использовании в настоящем изобретении термин "алкил" означает углеводородный радикал общей формулы CnH2n+1. Алкановый радикал может быть линейным или разветвленным. Например, термин "(C1-C6)алкил" означает одновалентную линейную или разветвленную алифатическую группу, содержащую от 1 до 6 атомов углерода (например, метил, этил, н-пропил, изопропил, н-бутил, изобутил,сим-бутил, трет-бутил, н-пентил, 1-метилбутил, 2-метилбутил, 3-метилбутил, неопентил,3,3-диметилпропил, гексил, 2-метилпентил и т.п.). Аналогичным образом, алкильная часть (т.е. алкильный фрагмент) алкоксигруппы, ацила (например, алканоила), алкиламиногруппы, диалкиламиногруппы и алкилтиогруппы обладает таким же определением, как указанное выше."Галогензамещенный алкил" означает алкильную группу, определенную выше, замещенную по меньшей мере одним атомом галогена. Например, если атомом галогена является фтор, обычные галогеналкильные группы включают фторметил, дифторметил, трифторметил, 2,2,2-трифторэтил,2,2,2,1,1-пентафторэтил и т.п. Также включены смешанные галогенидные заместители (например, хлорфторметил). Термин "алкенил" означает одновалентную группу, образованную из углеводорода, содержащего по меньшей мере одну углерод-углеродную двойную связь. Термин "C2-C6-алкенил" означает одновалентную группу, образованную из углеводорода, содержащего от 2 до 6 атомов углерода и содержащего по меньшей мере одну углерод-углеродную двойную связь. Алкенильная группа может быть неразветвленной или разветвленной. Типичные примеры алкенила включают винил, 1-пропенил, 2-пропенил,1-метил-1-пропенил, 1-метил-2-пропенил, 2-метил-1-пропенил, 2-метил-2-пропенил, 1-бутенил,2-бутенил, 3-бутенил и т.п. Термин "алкинил" означает одновалентную группу, образованную из углеводорода, содержащего по меньшей мере одну углерод-углеродную тройную связь. Термин "C2-C6-алкинил" означает одновалентную группу, образованную из углеводорода, содержащего от 2 до 6 атомов углерода и содержащего по меньшей мере одну углерод-углеродную тройную связь. Алкинильная группа может быть неразветвленной или разветвленной. Типичные примеры включают этинил, пропинил, бутин-1-ил, бутин-2-ил и т.д. Термин "гидроксизамещенный алкил" означает алкильную группу, определенную выше, замещенную одной или большим количеством гидроксигрупп (-ОН) (например, -CH2OH, -CH(ОН)2,-CH(OH)-CH2OH, -CH(ОН)-CH3 и т.д.). Предпочтительно, если алкильная группа содержит от 1 до 2 замещающих гидроксигрупп, более предпочтительно 1 гидроксигруппу."Галоген" может представлять собой фтор, хлор, бром или йод (предпочтительными галогенами в качестве заместителей являются фтор и хлор). Термин "оксогруппа" или -С(О)- означает карбонильную группу. Например, кетонную, альдегидную или часть карбоксильной, сложноэфирной, амидной, лактонной или лактамной группы. Термин "частично или полностью насыщенное карбоциклическое кольцо" (также называющееся"частично или полностью насыщенным циклоалкилом") означает неароматические кольца, которые частично или полностью гидрированы и могут представлять собой одно кольцо, бициклическое кольцо или спирановое кольцо, если не указано иное, карбоциклическое кольцо обычно представляет собой 3-8-членное кольцо. Например, частично или полностью насыщенные карбоциклические кольца (или циклоалкил) включают такие группы, как циклопропил, циклопропенил, циклобутил, циклобутенил,циклопентил, циклопентенил, циклопентадиенил, циклогексил, циклогексенил, циклогексадиенил, норборнил (бицикло[2.2.1]гептил), норборненил, бицикло[2.2.2]октил и т.п. Термин "частично или полностью насыщенное гетероциклическое кольцо" (также называющееся"частично или полностью насыщенным гетероциклом") означает неароматические кольца, которые частично или полностью гидрированы и могут представлять собой одно кольцо, бициклическое кольцо или спирановое кольцо, если не указано иное, гетероциклическое кольцо обычно представляет собой 3-6-членное кольцо, содержащее от 1 до 3 гетероатомов (предпочтительно 1 или 2 гетероатома), каждый из которых независимо выбран из группы, включающей серу, кислород и/или азот. Частично насыщенные или полностью насыщенные гетероциклические кольца включают такие группы, как эпоксигруппу,азиридинил,тетрагидрофуранил,дигидрофуранил,дигидропиридинил,пирролидинил,N-метилпирролидинил, имидазолидинил, имидазолинил, пиперидинил, пиперазинил, пиразолидинил,2 Н-пиранил, 4 Н-пиранил, 2 Н-хроменил, оксазинил, морфолиновую группу, тиоморфолиновую группу,тетрагидротиенил, тетрагидротиенил 1,1-диоксид и т.п., если не указано иное, гетероциклическое кольцо может быть присоединено через любой элемент кольца. Термин "конденсированный фенил" означает фенильную группу, сконденсированную с другим кольцом, таким как другой фенил (т.е. нафталин (например, нафталин-2-ил, нафталин-1-ил), частично или полностью насыщенный циклоалкил (например, индан-5-ил, 2,3-дигидро-1H-инденил или тетрагидронафталинил и т.п.), гетероарил (например, 1 Н-индол-5-ил, 1 Н-индол-6-ил, бензотиазол-5-ил, бензотиазол-6-ил, бензо[b]тиофен-5-ил, хинолин-6-ил, хинолин-7-ил, изохинолин-5-ил, изохинолин-6-ил, изохинолин-7-ил, изохинолин-8-ил, индазол-4-ил, индазол-5-ил, индазол-6-ил, индазол-7-ил, бензофуран-4-ил,бензофуран-5-ил, бензофуран-6-ил, бензофуран-7-ил, бензимидазол-4-ил или хиноксалин-6-ил,-7 021011 бензооксазол-5-ил,бензо[d]изоксазол-5-ил,бензо[d]изоксазол-6-ил,1 Н-бензимидазол-4-ил,1 Н-бензимидазол-5-ил, 1H-бензимидазол-6-ил, 1 Н-бензимидазол-7-ил, 1 Н-бензотриазол-5-ил и т.п.) или частично насыщенный или полностью насыщенный гетероцикл (например, индолин-4-ил, индолин-5-ил,индолин-6-ил,индолин-7-ил,1,2-дигидрохинолин-6-ил,1,2,3,4-тетрагидрохинолин-6-ил,1,2,3,4-тетрагидрохинолин-7-ил,2,3-дигидро-1H-бензо[d]имидазолил,2,3-дигидро-1 Н-индазолил,2,3-дигидробензо[d]оксазолил, 2,3-дигидробензо[1,4]диоксин-6-ил, 2,3-дигидробензофуран-5-ил, бензо[1,3]диоксол-5-ил, 2,3-дигидро-1H-индазол-5-ил, 2,3-дигидро-1 Н-индазол-6-ил и т.п.), где группа присоединена через один из фенильных атомов углерода. Будучи замещенным, конденсированный фенил может быть замещен по любому из атомов конденсированной системы. Например, бензофуранильная группа может быть замещена по фенильному или фуранильному фрагменту бензофуранильной группы. Термин "гетероарил" или "гетероароматическое кольцо" означает ароматические фрагменты, содержащие по меньшей мере один гетероатом (например, кислород, серу, азот или их комбинацию) в 5-6-членной ароматической кольцевой системе (например, пирролил, пиридил, пиразолил, тиенил, фуранил, оксазолил, имидазолил, тетразолил, триазинил, пиримидил, пиразинил, тиазолил, изотиазолил и т.п.). Типичное одиночное гетероарильное кольцо обычно представляет собой 5-6-членное кольцо, содержащее от 1 до 3 гетероатомов, независимо выбранных из группы, включающей кислород, серу и азот. Термин "конденсированный гетероарил" означает гетероарильную группу, сконденсированную с другим кольцом, таким как другой гетероарил (например, пуринил, тиено[3,2-с]пиридинил(например, тиено[3,2-с]пиридин-2-ил и тиено[3,2-с]пиридин-3-ил), имидазо[1,2-а]пиридинил (например,имидазо[1,2-а]пиридин-3-ил,имидазо[1,2-а]пиридин-6-ил,имидазо[1,2-а]пиридин-7-ил и 3 Н-имидазо[4,5-b]пиридин-6-ил) или бензо[b]тиофенил и т.п.), фенил (например, бензо[b]тиофен-2-ил,бензо[b]тиофен-3-ил, хинолин-2-ил, хинолин-3-ил, бензооксазол-2-ил, бензотиазол-2-ил, 1 Н-индол-2-ил,1 Н-индол-3-ил, изохинолин-1-ил, изохинолин-3-ил, изохинолин-4-ил, бензофуран-2-ил, бензофуран-3-ил,индазол-3-ил, бензимидазол-2-ил и т.п.), частично или полностью насыщенный циклоалкил (например,4,5,6,7-тетрагидробензо[d]оксазолил,4,5,6,7-тетрагидро-1 Н-индолил,5,6,7,8-тетрагидрохинолинил,5,6,7,8-тетрагидроизохинолинил, 4,5,6,7-тетрагидробензо[b]тиофенил, 4,5,6,7-тетрагидробензофуранил,4,5,6,7-тетрагидро-1 Н-индазолил,4,5,6,7-тетрагидро-1H-бензо[d]имидазолил или 4,5,6,7-тетрагидробензо[d]оксазолил и т.п.) или частично насыщенный или полностью насыщенный гетероцикл(например,8,9-дигидро-7 Н-пуринил,2,3-дигидротиено[3,2-с]пиридинил,4,5,6,7-тетрагидротиено[2,3-с]пиридин-2-ил,4,5,6,7-тетрагидротиено[3,2-с]пиридинил или 5,6,7,8-тетрагидроимидазо[1,2-а]пиридинил и т.п.), где гетероарильная группа присоединена через один из кольцевых атомов гетероарила. Будучи замещенным, конденсированный гетероарил может быть замещен по любому из атомов конденсированной системы. Например, имидазо[1,2-а]пиридинильная группа может быть замещена по имидазольному или пиридиновому фрагменту конденсированной системы. Выражение "терапевтически эффективное количество" означает количество соединения, предлагаемого в настоящем изобретении, которое (i) лечит или предупреждает конкретное заболевание, патологическое состояние или нарушение, (ii) ослабляет, смягчает или устраняет один или большее количество симптомов конкретного заболевания, патологического состояния или нарушения или (iii) предупреждает или задерживает возникновение одного или большего количества симптомов конкретного заболевания,патологического состояния или нарушения, описанных в настоящем изобретении. Термин "животное" означает людей (мужчин или женщин), домашних животных (например, собак, кошек и лошадей), животных в зоопарках, морских животных, птиц и других видов животных. Выражение "фармацевтически приемлемое" указывает, что вещество или композиция должны быть химически и/или токсикологически совместимы с другими ингредиентами, образующими композицию,и/или с млекопитающим, подвергающимся лечению с его помощью. Термины "лечение", "лечить" или "подвергать лечению" включают и предупредительное, т.е. профилактическое, и паллиативное лечение. Термин "соединения, предлагаемые в настоящем изобретении" (если специально не указано иное) означает соединения формул (I), (II), (Ia) и (Ib), их пролекарства, фармацевтически приемлемые соли соединений и/или пролекарств и гидраты или сольваты соединений, солей и/или пролекарств, а также все стереоизомеры (включая диастереоизомеры и энантиомеры), таутомеры и изотопно-меченые соединения. Подробное описание изобретения Настоящее изобретение относится к соединениям и фармацевтическим композициям, которые применимы для лечения заболеваний, патологических состояний и/или нарушений, модулируемых ингибированием 17-гидроксилазы/C17,20-лиазы. Соединения, предлагаемые в настоящем изобретении, можно синтезировать путями, которые включают методики, аналогичные хорошо известным в химической науке, в частности, с учетом описания,приведенного в настоящем изобретении. Исходные вещества обычно можно приобрести у таких фирм,как Aldrich Chemicals (Milwaukee, Wis.), или легко получить по методикам, хорошо известным специалистам в данной области техники (например, получить по методикам, описанным в публикациях Louis F.-8 021011 доступные в виде баз данных Beilstein в интернете. Для иллюстративных целей на схемах реакций, представленных ниже, приведены возможные пути синтеза соединений, предлагаемых в настоящем изобретении, а также основных промежуточных продуктов. Более подробное описание отдельных стадий реакций приведено ниже в разделе "Примеры". Специалисты в данной области техники должны понимать, что для синтеза соединений, предлагаемых в настоящем изобретении, можно использовать другие методики синтеза. Хотя на схемах приведены и ниже обсуждены конкретные исходные вещества и реагенты, легко можно использовать другие исходные вещества и реагенты и/или условия проведения реакций и получить множество производных. Кроме того,многие соединения, полученные по описанным ниже методикам, можно дополнительно модифицировать с учетом настоящего раскрытия по обычным химическим методикам, хорошо известным специалистам в данной области техники. Схемы, подробно описанные ниже, представляют собой общие схемы синтеза соединения, предлагаемые в настоящем изобретении (например, соединений формул (I), (II), (Ia) и (Ib. Общие схемы Схема 1 На приведенной выше схеме 1 R обозначает -А или следующую группу: Стадии 1 и 2. Промежуточные продукты стадий 1 и 2 можно синтезировать по методикам, аналогичным описанным в публикации Kak-Shan Shia, et al., in J. Med. Chem., 2002, 45, 1644-1655, с использованием необходимых исходных веществ, которые имеются в продаже, или синтезировать по известным методикам,описанным в данной области техники. Например, множество 2-хлоралкилизоцианатов можно получить по методикам, описанным в публикации С.K. Johnson in J. Org. Chem. (1967), 32(5), 1508-10. В некоторых случаях длительность проведения реакции увеличивают для повышения выхода по сравнению с указанным в отмеченной выше публикации в J. Med. Chem. Стадия 3. Продукты стадии 2, полученные, как описано выше, можно превратить в искомые продукты по реакции с подходящими алкил- или арилгалогенидами, предпочтительно хлор/бромалкил- или-арилпроизводными с использованием условий, хорошо известных специалисту в данной области техники, например при условиях сочетания C-N Бухвальда-Хартвига, или с использованием NaH/ДМФ и т.п. Предпочтительными условиями являются известные как условия реакции Бухвальда-Хартвига, например, в присутствии (а) катализатора, такого как йодидом меди, (b) основания, такого как фосфат калия или карбонат цезия; и (с) лиганда, такого как транс-1,2-диаминоциклогексан, в присутствии подходящих растворителей (например, 1,4-диоксана) при температурах в диапазоне примерно от комнатной до температуры кипения растворителя. Если р равно 0, то также может образоваться соединение формулы(Ia-1). Если используют защитную группу, то защитную группу удаляют при условиях, подходящих для конкретной защитной группы, использующейся для получения соединений, предлагаемых в настоящем-9 021011 изобретении. Более подробное описание представлено в примерах 1 и 14 в приведенном ниже разделе"Примеры". Альтернативно, заместители R53 и R можно ввести в обратном порядке. Например, вместо использования R-NH2 в качестве исходного вещества используют R53-NH2. Затем группу R вводят на стадии 3 с использованием R-X вместо R53-X. См., например, более подробное описание в примере 79 в приведенном ниже разделе "Примеры". На схеме 2 показано, как можно получить указанное выше исходное вещество (SM-1), в котором Необходимую хлоркарбоновую кислоту сначала превращают в соответствующий хлорангидрид кислоты по методикам, хорошо известным специалистам в данной области техники. Например, производное карбоновой кислоты можно обработать тионилхлоридом в присутствии диметилформамида (ДМФ) и растворителя (например, дихлорметана (ДХМ. Можно использовать другие хлорирующие реагенты,например трихлорид фосфора или пентахлорид фосфора. Затем хлорангидрид кислоты можно превратить в соответствующий азид путем обработки азидом натрия. Затем азид превращают в искомый изоцианат (SM-1) с помощью перегруппировки Курциуса, например нагреванием азида при повышенных температурах. На схеме 3 описан синтез соединений, предлагаемых в настоящем изобретении, содержащих 1 Н-имидазол-2(3 Н)-оновое ядро (соединения формулы (I) или (Ia. Схема 3 На приведенной выше схеме 3 R обозначает -А или следующий фрагмент: Стадия 1. На стадии 1 некоторые ароматические или гетероароматические амины (в частности,6-бензотиазолиламин, 5-бензо[b]тиофениламин, 2-дифторметил-1-фторфен-4-иламин, 2-метилтиофен-4 иламин и т.п.) можно ввести в сочетании с 2,2-диметоксиэтиламином через промежуточный изоцианат с использованием таких реагентов, как трифосген, триэтиламин (ТЭА), и подходящих растворителей (например,ТГФ) и получить соответствующие 1-замещенные промежуточные 3-(2,2-диметоксиэтил)мочевины. Стадия 2. На стадии 2 промежуточные 1-замещенные-1 Н-имидазол-2(3 Н)-оны можно получить по методикам,аналогичным известным в данной области техники, таким как методики, описанные в публикации Т. Hafner, et al., in Synthesis (2007), 9, 1403-1411.- 10021011 Стадия 3. Продукты стадии 2, полученные, как описано выше, можно превратить в искомые продукты по реакции с соответствующими арилгалогенидами, предпочтительно йод- или бромарилпроизводными с использованием условий, таких как условия сочетания C-N Бухвальда-Хартвига, как это описано на приведенной выше схеме 1. Альтернативно, продукт можно получить с помощью катализируемого медьюN-арилирования промежуточного 1-замещенного-1 Н-имидазол-2(3 Н)-она с помощью обычного нагревания (например, R53-X, (CuOTf)2-C6H6, Cu:лиганд:дибензилиденацетон (dba) = 1:5:1, в диоксане примерно при 150 С). См. публикацию Hafner, et al., Synthesis (2007), 9, 1403-1411. Более подробное описание см. в примере 142 в приведенном ниже разделе "Примеры". На схеме 4 описан альтернативный путь синтеза соединений формулы (II) или (Ib). Схема 4 Необходимую группу R53 можно присоединить к соответствующему аминокарбоксилату при условиях сочетания C-N Бухвальда-Хартвига или с использованием NaH/ДМФ и т.п. Затем циклическую мочевину получают по методикам, аналогичным описанным в публикации Kak-Shan Shia, et al., in J. Med.Chem., 2002, 45, 1644-1655. Затем производное пиридина можно ввести в реакцию сочетания с имидазолином по описанной выше реакции сочетания C-N Бухвальда-Хартвига. Альтернативно, несимметричные дизамещенные-1 Н-имидазолин-2(3 Н)-оны можно получить по другим методикам, рассмотренных в публикациях Т. Hafner, et al., in Synthesis (2007), 9, 1403-1411 (например, Brazier, S.A., et al., J. Chem. Soc. (1912), 101, 2352 и Schonherr, H.J., et al., Chem. Ber. (1970), 103,1037). На схеме 5 описан другой альтернативный путь синтеза соединений формулы (II) или (Ib). Схема 5 На приведенной выше схеме 5 R обозначает -А или следующую группу: Промежуточный продукт (I-5 а) можно получить путем присоединения по Михаэлю соответствующего амина (R53-NH2) к соответствующей акриловой кислоте по методикам, хорошо известным специалистам в данной области техники. Например, амин и акриловую кислоту в подходящем растворителе(например, толуоле) нагревают при повышенной температуре (например, от примерно 70 до примерно 100 С) в инертной атмосфере. Затем промежуточную аминокислоту (I-5 а) можно циклизовать и получить промежуточную циклическую мочевину (I-5b). Например, промежуточную циклическую мочевину (I-5b) можно получить путем обработки промежуточной аминокислоты (I-5 а) активирующим реагентом (например, дифенилфосфорилазидом (ДФФА в присутствии амина (например, триэтиламина) и подходящего растворителя (например, толуола) при повышенных температурах. Необходимую группу А можно ввести в реакцию сочетания с промежуточной циклической мочевиной (I-5b) при стандартных условиях сочетания, описанных выше для получения соединения формулы (II) или (Ib). В представленном ниже разделе "Примеры" приведено более подробное описание схем синтеза, а также других альтернативных методик получения соединений, предлагаемых в настоящем изобретении,которые специалисты в данной области техники легко могут модифицировать (например, использовать другие исходные вещества). Соединения и промежуточные продукты, описанные в настоящем изобретении, можно выделить и использовать в качестве самих соединений или их солей. Многие из соединений, описывающихся формулами (I), (II), (Ia) и (Ib), могут образовывать соли присоединения с кислотами, предпочтительно фармацевтически приемлемые соли присоединения с кислотами. Фармацевтически приемлемые соли присоединения с кислотами соединения формул (I), (II), (Ia) и (Ib) включают соли с неорганическими кислотами, например галогенводородными кислотами, такими как хлористо-водородная, бромисто-водородная или йодисто-водородная кислоты, азотная, серная, фосфорная кислоты, и органическими кислотами, например алифатическими монокарбоновыми кислотами, такими как муравьиная, уксусная, пропионовая и масляная кислоты, алифатическими гидроксикислотами, такими как молочная, лимонная, винная или яблочная кислоты, дикарбоновыми кислотами, такими как малеиновая или янтарная кислота, ароматическими карбоновыми кислотами, такими как бензойная, п-хлорбензойная, дифенилуксусная или трифенилуксусная кислоты, ароматическими гидроксикислотами, такими как о-гидроксибензойная,п-гидроксибензойная, 1-гидроксинафталин-2-карбоновая или 3-гидроксинафталин-2-карбоновая кислоты, и сульфоновыми кислотами, такими как метансульфоновая или бензолсульфоновая кислота. Эти соли можно получить из соединений формул (I), (II), (Ia) или (Ib) по известным методикам получения солей. Соединения, предлагаемые в настоящем изобретении, которые содержат кислотные, например, карбоксигруппы, также могут образовывать соли с основаниями, предпочтительно с фармацевтически приемлемыми основаниями, такими как хорошо известные в данной области техники; такие подходящие соли включают соли металла, предпочтительно соли щелочного металла или щелочно-земельного металла, такие как соли натрия, калия, магния или кальция, или соли с аммиаком или фармацевтически приемлемыми органическими аминами или гетероциклическими основаниями, такими как этаноламины, бензиламины или пиридин. Эти соли можно получить из соединений формул (I), (II), (Ia) и (Ib) по известным методикам получения солей. В тех соединениях, в которых имеется асимметрический атом углерода, соединение существует в виде отдельных оптически активных изомерных форм или в виде их смесей, например в виде рацемических смесей или смесей диастереоизомеров. Настоящее изобретение включает отдельные оптически активные R- и S-изомеры, а также их смеси, например рацемические смеси или смеси диастереоизомеров. Настоящее изобретение включает все фармацевтически приемлемые изотопно-меченые соединения,предлагаемые в настоящем изобретении, в которых один или большее количество атомов заменены на атомы, обладающие таким же атомным номером, но атомной массой или массовым числом, отличающимся от атомной массы или массового числа, обычно обнаруживающихся в природе. Примеры изотопов, подходящих для включения в соединения, предлагаемые в настоящем изобретении, включают изотопы водорода, например 2 Н и 3 Н, углерода, например 11 С, 13C и 14 С, хлора, например 36Cl, фтора, например 18F, йода, например 123I и 125I, азота, например 13N и 15N, кислорода, например 15 О, 17 О и 18 О, фосфора, например 32 Р, и серы, например 35S. Замещение более тяжелыми изотопами, такими как дейтерий, т.е. 2 Н, может обеспечить некоторые терапевтические преимущества, обусловленные их более высокой метаболической стабильностью, например увеличенной длительностью полувыведения in vivo или возможностью использования меньших доз, и поэтому при некоторых обстоятельствах они могут быть предпочтительными.- 12021011 Изотопно-меченые соединения, предлагаемые в настоящем изобретении, обычно можно получить по стандартным методикам, известным специалистам в данной области техники, или по методикам, аналогичным описанным в приведенных ниже примерах и в разделе, посвященном синтезу, с использованием подходящего изотопно-меченого реагента вместо использовавшегося ранее не содержащего изотопа реагента. Соединения, предлагаемые в настоящем изобретении, могут существовать в несольватированной, а также в сольватированных формах с фармацевтически приемлемыми растворителями, такими как вода,этанол и т.п., и подразумевается, что в объем настоящего изобретения входят сольватированные и несольватированные формы. Для задач настоящего изобретения сольваты (включая гидраты) считаются фармацевтическими композициями, например соединение формул (I), (II), (Ia) или (Ib) (или его фармацевтически приемлемая соль) в комбинации с инертным наполнителем, где инертным наполнителем является растворитель. Соединения, предлагаемые в настоящем изобретении, применимы для лечения заболеваний, патологических состояний и нарушений, опосредуемых регулированием 17-гидроксилазы/С 17,20-лиазы (например, рака (в частности, рака предстательной железы) или воспаления); следовательно, соединения,предлагаемые в настоящем изобретении (включая композиции и способы их применения), можно использовать для приготовления лекарственного средства, предназначенного для применений в терапии,описанных в настоящем изобретении. Поэтому в другом варианте осуществления настоящее изобретение относится к фармацевтической композиции, содержащей соединение, предлагаемое в настоящем изобретении, в терапевтически эффективном количестве, и фармацевтически приемлемый инертный наполнитель, разбавитель или носитель. Типичный препарат получают смешиванием соединения, предлагаемого в настоящем изобретении,и носителя, разбавителя или инертного наполнителя. Подходящие носители, разбавители и инертные наполнители хорошо известны специалистам в данной области техники и включают такие материалы,как углеводы, воски, растворимые и/или набухающие в воде полимеры, гидрофильные или гидрофобные материалы, желатин, масла, растворители, воду и т.п. То, какой конкретный носитель, разбавитель или инертный наполнитель используют, зависит от путей и назначения применения соединения, предлагаемого в настоящем изобретении. Растворители для введения млекопитающему обычно выбирают из числа растворителей, известных специалистам в данной области техники, как безопасные. Обычно безопасными растворителями являются нетоксичные водные растворители, такие как вода, и другие нетоксичные растворители, которые растворимы в воде или смешиваются с водой. Подходящие водные растворители включают воду, этанол, пропиленгликоль, полиэтиленгликоли (например, PEG400, PEG300) и т.п. и их смеси. Препараты также могут включать один или большее количество буферов, стабилизирующих агентов, поверхностно-активных веществ, смачивающих агентов, смазывающих агентов, эмульгаторов, суспендирующих агентов, консервантов, антиоксидантов, замутняющих агентов, агентов, придающих скользкость, технологических добавок, красителей, подсластителей, отдушек, вкусовых агентов и других известных добавок, что обеспечивает превосходный внешний вид лекарственного препарата (т.е. соединения, предлагаемого в настоящем изобретении, или содержащей его фармацевтической композиции) или облегчает приготовление фармацевтического продукта (т.е. лекарственного препарата). Препараты можно приготовить по обычным методикам растворения и смешивания. Например, объемное лекарственное вещество (т.е. соединение, предлагаемое в настоящем изобретении, или стабилизированная форма соединения (например, комплекс с производным циклодекстрина или другим известным комплексообразующим агентом растворяют в подходящем растворителе в присутствии одного или большего количества инертных наполнителей. Соединение, предлагаемое в настоящем изобретении,обычно готовят в виде фармацевтических дозированных форм для обеспечения легко контролируемой дозировки лекарственного средства для предоставления пациенту обладающего превосходным внешним видом и удобного в использовании продукта. Фармацевтическую композицию (или препарат), предназначенную для использования, в зависимости от методики, использующейся для введения лекарственного средства, можно упаковать по-разному. Обычно продукт, предназначенный для распространения, включает контейнер, содержащий помещенный в него фармацевтический препарат в соответствующей форме. Подходящие контейнеры хорошо известны специалистам в данной области техники и включают такие материалы, как флаконы (пластмассовые и стеклянные), пакеты, ампулы, пластмассовые мешки, металлические цилиндры и т.п. Контейнер также может включать защищающее от неумелого обращения устройство, предназначенное для предупреждения непреднамеренного доступа к содержимому упаковки. Кроме того, на контейнер нанесена этикетка, на которой описано содержимое контейнера. На этикетке также могут находиться соответствующие предупреждающие сообщения. Ингибитор Cyp 17, предлагаемый в настоящем изобретении, может быть полезно объединить по меньшей мере с одним дополнительным фармакологически активным соединением, предпочтительно предназначенным для лечения рака. Например, соединение, предлагаемое в настоящем изобретении, определенное выше, можно вводить одновременно, последовательно или по отдельности в комбинации с одним или большим количеством средств, выбранных из группы, включающей химиотерапевтические- 13021011 средства, например ингибиторы митоза, такие как таксан (например, паклитаксел или доцетаксел), алкалоид барвинка (например, винкристин, винбластин, винорелбин или винфлунин), или другие противораковые средства, например цисплатин, 5-фторурацил или 5-фтор-2-4(1H,3 Н)пиримидиндион (5FU), флутамид или гемцитабин. такие комбинации могут обеспечивать значительные преимущества при лечении,включая синергетическую активность. Соединение, предлагаемое в настоящем изобретении, также можно применять в комбинации с другими антипролиферативными соединениями. Такие антипролиферативные соединения включают, но не ограничиваются только ими, ингибиторы ароматазы; антиэстрогены; ингибиторы топоизомеразы I; ингибиторы топоизомеразы II; средства, активные по отношению к микротрубочкам; алкилирующие соединения; соединения, которые индуцируют процессы дифференциации клеток; ингибиторы циклооксигеназы; ингибиторы ММР; ингибиторы mTOR; противоопухолевые антиметаболиты; соединения платины; соединения, предназначенные для избирательного воздействия/уменьшения активности протеин- или липидкиназы, и другие антиангиогенные соединения; соединения, которые предназначены для избирательного воздействия/уменьшения или ингибирования активности протеин- или липидфосфатазы; агонисты гонадорелина; антиандрогены; ингибиторы метионинаминопептидазы; бисфосфонаты; модификаторы биологического ответа; антипролиферативные антитела; ингибиторы гепараназы; ингибиторы онкогенных изоформ Ras; ингибиторы теломеразы; ингибиторы протеосомы; соединения, применяющиеся при лечении злокачественных заболеваний крови, которые предназначены для избирательного воздействия, уменьшения или ингибирования активности Flt-3; ингибиторы Hsp90, такие как 17-AAGTherapeutics; темозоломид (ТЕМОДАЛ); ингибиторы кинезинового белка веретена, такие как SB715992 или SB743921, выпускающиеся фирмой GlaxoSmithKline, или пентамидин/хлорпромазин, выпускающиеся фирмой CombinatoRx; ингибиторы PI3K; ингибиторы RAF, такие как RAF265; средства, связывающиеS-аденозилметиониндекарбоксилазы, антипролиферативные антитела или другие химиотерапевтические соединения. Кроме того, альтернативно или в дополнение, их можно применять в комбинации с другими методиками борьбы с опухолями, включая хирургию, применение ионизирующего излучения, фотодинамическую терапию, имплантаты, например совместно с кортикостероидами, гормонами, или их можно применять в качестве радиосенсибилизаторов. Кроме того, в противовоспалительное и/или антипролиферативное лечение включают комбинации с противовоспалительными лекарственными веществами. Также возможна комбинация с антигистаминными лекарственными веществами, бронхорасширяющими лекарственными средствами, НСПВС (нестероидные противовоспалительные лекарственные средства) или антагонистами хемокиновых рецепторов. Термин "ингибитор ароматазы" при использовании в настоящем изобретении означает соединение,которое ингибирует продуцирование эстрогена, т.е. превращение субстратов андростендиона и тестостерона в эстрон и эстрадиол соответственно. Термин включает, но не ограничивается только ими, стероиды, предпочтительно атаместан, экземестан и форместан, и предпочтительно нестероидные соединения,предпочтительно аминоглютетимид, роглетимид, пироглютетимид, трилостан, тестолактон, кетоконазол,ворозол, фадрозол, анастрозол и летрозол. Экземестан можно вводить, например, в той форме, в которой он продается, например, под торговым названием АРОМАЗИН. Форместан можно вводить, например, в той форме, в которой он продается, например, под торговым названием ЛЕНТАРОН. Фадрозол можно вводить, например, в той форме, в которой он продается, например, под торговым названием АФЕМА. Анастрозол можно вводить, например, в той форме, в которой он продается, например, под торговым названием АРИМИДЕКС. Летрозол можно вводить, например, в той форме, в которой он продается, например, под торговым названием ФЕМАРА или ФЕМАР. Аминоглютетимид можно вводить, например,в той форме, в которой он продается, например, под торговым названием ОРИМЕТЕН. Комбинация,предлагаемая в настоящем изобретении, включающая химиотерапевтическое средство, которое представляет собой ингибитор ароматазы, является особенно подходящей для лечения гормональнорецептороположительных опухолей, например опухолей молочной железы. Термин "антиэстроген" при использовании в настоящем изобретении относится к соединению, которое противодействует воздействию эстрогена на уровне эстрогенного рецептора. Термин включает, но не ограничивается только ими, тамоксифен, фулвестрант, ралоксифен и ралоксифенгидрохлорид. Тамоксифен можно вводить, например, в той форме, в которой он продается, например, под торговым названием НОЛВАДЕКС. Ралкосифенгидрохлорид можно вводить, например, в той форме, в которой он продается, например, под торговым названием ЭВИСТА. Фулвестрант можно приготовить так, как это раскрыто в US 4659516, или его можно вводить, например, в той форме, в которой он продается, например,под торговым названием ФАСЛОДЕКС. Комбинация, предлагаемая в настоящем изобретении, включающая химиотерапевтическое средство, которое представляет собой антиэстроген, является особенно полезной для лечения эстрогенных рецептороположительных опухолей, например опухолей молочной железы.- 14021011 Термин "антиандроген" при использовании в настоящем изобретении относится к любому соединению, которое может ингибировать биологические воздействия андрогенных гормонов, и включает, но не ограничивается только им, бикалутамид (КАСОДЕКС), который можно приготовить, например, так, как это раскрыто в US 4636505. Термин "агонист гонадорелина" при использовании в настоящем изобретении включает, но не ограничивается только ими, абареликс, госерелин и госерелинацетат. Госерелин раскрыт в US 4100274, и его можно вводить, например, в той форме, в которой он продается, например, под торговым названием ЗОЛАДЕКС. Абареликс можно приготовить, например, так, как это раскрыто в US 5843901. Термин "ингибитор топоизомеразы I" при использовании в настоящем изобретении включает, но не ограничивается только ими, топотекан, гиматекан, иринотекан, камптотецин и его аналоги,9-нитрокамптотецин и макромолекулярный конъюгат камптотецина PNU-166148 (соединение А 1 вWO 99/17804). Иринотекан можно вводить, например, в той форме, в которой он продается, например,под торговым названием КАПМТОСАР. Топотекан можно вводить, например, в той форме, в которой он продается, например, под торговым названием ГИКАМТИН. Термин "ингибитор топоизомеразы II" при использовании в настоящем изобретении включает, но не ограничивается только ими, антрациклины, такие как доксорубицин (включая липосомную композицию, например КАЕЛИКС), даунорубицин, эпирубицин, идарубицин, неморубицин, антрахиноны митоксантрон и лозоксантрон и подофиллотоксины этопозид и тенипозид. Этопозид можно вводить, например, в той форме, в которой он продается, например, под торговым названием ЭТОПОФОС. Тенипозид можно вводить, например, в той форме, в которой он продается, например, под торговым названиемVM 26-БРИСТОЛ. Доксорубицин можно вводить, например, в той форме, в которой он продается, например, под торговым названием АДРИБЛАСТИН или АДРИАМИЦИН. Эпирубицин можно вводить,например, в той форме, в которой он продается, например, под торговым названием ФАРМОРУБИЦИН. Идарубицин можно вводить, например, в той форме, в которой он продается, например, под торговым названием ЗАВЕДОС. Митоксантрон можно вводить, например, в той форме, в которой он продается,например, под торговым названием НОВАНТРОН. Термин "соединение, активное по отношению к микротрубочкам" относится к стабилизирующим микротрубочкам, дестабилизирующим микротрубочки соединениям и ингибиторам полимеризации микротубулина и включает, но не ограничивается только ими, таксаны, например паклитаксел и доцетаксел,алкалоиды барвинка, например винбластин, предпочтительно винбластинсульфат, винкристин, предпочтительно винкристинсульфат и винорелбин, дискодермолиды, колхицин и эпотилоны и их производные,например эпотилон В или D или его производные. Паклитаксел можно вводить, например, в той форме, в которой он продается, например, под торговым названием ТАКСОЛ. Доцетаксел можно вводить, например, в той форме, в которой он продается, например, под торговым названием ТАКСОТЕР. Винбластинсульфат можно вводить, например, в той форме, в которой он продается, например, под торговым названием ВИНБЛАСТИН R.P. Винкристинсульфат можно вводить, например, в той форме, в которой он продается, например, под торговым названием ФАРМИСТИН. Дискодермолид можно получить, например, так, как это раскрыто в US 5010099. Также включены производные эпотилона, которые раскрыты вWO 00/31247. Особенно предпочтительными являются эпотилон А и/или В. Термин "алкилирующее соединение" при использовании в настоящем изобретении включает, но не ограничивается только ими, циклофосфамид, ифосфамид, мелфалан и нитрозомочевину (BCNU или глиадел). Циклофосфамид можно вводить, например, в той форме, в которой он продается, например,под торговым названием ЦИКЛОСТИН. Ифосфамид можно вводить, например, в той форме, в которой он продается, например, под торговым названием ГОЛОКСАН. Термин "противоопухолевый антиметаболит" включает, но не ограничивается только ими,5-фторурацил, или 5-FU, капецитабин, гемцитабин, деметилирующие ДНК соединения, такие как 5-азацитидин и децитабин, метотрексат и эдатрексат, и антагонисты фолиевой кислоты, такие как пеметрексед. Капецитабин можно вводить, например, в той форме, в которой он продается, например, под торговым названием КСЕЛОДА. Гемцитабин можно вводить, например, в той форме, в которой он продается, например, под торговым названием ГЕМЗАР. Термин "соединение платины" при использовании в настоящем изобретении включает, но не ограничивается только ими, карбоплатин, цисплатин, цисплатинум и оксалиплатин. Карбоплатин можно вводить, например, в той форме, в которой он продается, например, под торговым названием КАРБОПЛАТ. Оксалиплатин можно вводить, например, в той форме, в которой он продается, например, под торговым названием ЭЛОКСАТИН. Термин "соединения, избирательно действующие/уменьшающие активность протеин- или липидкиназы"; или "активности протеин- или липидфосфатазы"; или "другие антиангиогенные соединения" при использовании в настоящем изобретении включает, но не ограничивается только ими, ингибиторы протеинтирозинкиназы и/или серии- и/или треонинкиназы или липидкиназы, например: а) соединения, избирательно действующие, уменьшающие или ингибирующие активность рецепторов тромбоцитарного фактора роста (PDGFR), такие как соединения, которые избирательно действуют,- 15021011 уменьшают или ингибируют активность PDGFR, предпочтительно соединения, которые ингибируют рецептор PDGF, например производное N-фенил-2-пиримидинамина, например иматиниб, SU101,SU6668 и GFB-111;b) соединения, избирательно действующие, уменьшающие или ингибирующие активность рецепторов фактора роста фибробластов (FGFR); с) соединения, избирательно действующие, уменьшающие или ингибирующие активность рецептора инсулиноподобного фактора роста I (IGF-IR), такие как соединения, которые избирательно действуют,уменьшают или ингибируют активность IGF-IR, предпочтительно соединения, которые ингибируют активность киназы рецептора IGF-I, такие как соединения, раскрытые в WO 02/092599, или антитела, которые избирательно действуют на внеклеточный домен рецептора IGF-I или его факторы роста;d) соединения, избирательно действующие, уменьшающие или ингибирующие активность семейства тирозинкиназ рецептора Trk, или ингибиторы эфрина В 4; е) соединения, избирательно действующие, уменьшающие или ингибирующие активность семейства тирозинкиназ рецептора Axl;f) соединения, избирательно действующие, уменьшающие или ингибирующие активность тирозинкиназы рецептора Ret;g) соединения, избирательно действующие, уменьшающие или ингибирующие активность тирозинкиназы рецептора Kit/SCFR, т.е. тирозинкиназ рецептора с-Kit (часть семейства PDGFR), такие как соединения, которые избирательно действуют, уменьшают или ингибируют активность семейства тирозинкиназ рецептора c-Kit, предпочтительно соединения, которые ингибируют рецептор с-Kit, например,иматиниб;h) соединения, избирательно действующие, уменьшающие или ингибирующие активность представителей семейства c-Abl, продуктов их слияния с генами (например, BCR-Abl киназы) и мутантов, такие как соединения, которые избирательно действуют, уменьшают или ингибируют активность представителей семейства с-Abl и продуктов их слияния с генами, например производное N-фенил-2 пиримидинамина, например иматиниб или нилотиниб (AMN107); PD180970; AG957; NSC 680410;i) соединения, избирательно действующие, уменьшающие или ингибирующие активность представителей семейства протеинкиназ С (PKC) и семейства Raf серин/треонинкиназ, представителей семействMEK, SRC, JAK, FAK, PDK1, PKB/Akt и Ras/MAPK и/или представителей семейства циклинзависимых киназ (CDK) и в особенности производные стауроспорина, раскрытые в US 5093330, например мидостаурин; примеры других соединений включают, например, UCN-01, сафингол, BAY 43-9006, бриостатин 1; перифосин; илмофосин; RO 318220 и RO 320432; GO 6976; Isis 3521; LY333531/LY379196; изохинолиновые соединения, такие как раскрытые в WO 00/09495; FTIs; PD184352 или QAN697 (ингибитор Р 13K) или АТ 7519 (ингибитор CDK);j) соединения, избирательно действующие, уменьшающие или ингибирующие активность ингибиторов протеинтирозинкиназы, включая иматинибмезилат (ГЛЕЕВЕК) и тирфостин. Тирфостин предпочтительно представляет собой соединение с низкой молекулярной массой (Mw1500) или его фармацевтически приемлемую соль, предпочтительно соединение, выбранное из группы, включающей класс бензилиденмалонитрилов, или класс S-арилбензолмалонитрилов, или класс бисубстратных хинолинов, более предпочтительно любое соединение, выбранное из группы, включающей тирфостин A23/RG-50810;k) соединения, избирательно действующие, уменьшающие или ингибирующие активность семейства тирозинкиназ рецептора эпидермального фактора роста (EGFR, ErbB2, ErbB3, ErbB4 в виде гомо- или гетеродимеров) и их мутантов, такие как соединения, которые избирательно действуют, уменьшают или ингибируют активность семейства рецепторов эпидермального фактора роста, предпочтительно соединения, белки или антитела, которые ингибируют представителей семейства тирозинкиназ рецептораEGF, например рецептора EGF, ErbB2, ErbB3 и ErbB4, или связываются с относящимися к EGF или EGF лигандами и предпочтительно являются такими соединениями, белками или моноклональными антителами, которые в общем и конкретно раскрыты в WO 97/02266, например соединение примера 39, или в ЕР 0564409, WO 99/03854, ЕР 0520722, ЕР 0566226, ЕР 0787722, ЕР 0837063, US 5747498, WO 98/10767,WO 97/30034, WO 97/49688, WO 97/38983 и в особенности в WO 96/30347 (например, соединение, известное как СР 358774), WO 96/33980 (например, соединение ZD 1839) и WO 95/03283 (например, соединение ZM105180); например, трастузумаб (герцептин), цетуксимаб (эрбутукс), пресса, тарцева,OSI-774, CI-1033, EKB-569, GW-2016, Е 1.1, Е 2.4, Е 2.5, Е 6.2, Е 6.4, Е 2.11, Е 6.3 или Е 7.6.3 и производные 7H-пирроло[2,3-d]пиримидина, которые раскрыты в WO 03/013541; иl) соединения, избирательно действующие, уменьшающие или ингибирующие активность рецептора c-Met, такие как соединения, которые избирательно действуют, уменьшают или ингибируют активность рецептора c-Met, предпочтительно соединения, которые ингибируют киназную активность рецептора c-Met, или антитела, которые избирательно действуют на внеклеточный домен c-Met или связыва- 16021011 ются с HGF. Другие антиангиогенные соединения включают соединения, характеризующиеся другим механизмом своей активности, например, не относящейся к ингибированию протеин- или липидкиназы, например талидомид (ТАЛОМИД) и TNP-470. Соединения, которые избирательно действуют, уменьшают или ингибируют активность протеинили липидфосфатазы, представляют собой, например, ингибиторы фосфатазы 1, фосфатазы 2 А илиCDC25, например окадаевая кислота или ее производное. Соединения, которые индуцируют процессы дифференциации клеток, представляют собой, например, ретиноевую кислоту, или токоферол, или токотриенол. Термин "ингибитор циклооксигеназы" при использовании в настоящем изобретении включает, но не ограничивается только ими,например,ингибиторы Сох-2,5-алкилзамещенную 2-ариламинофенилуксусную кислоту и производные, такие как целекоксиб (ЦЕЛЕБРЕКС), рофекоксиб(ВИОКС), эторикоксиб, валдекоксиб или 5-алкил-2-ариламинофенилуксусная кислота, например 5-метил-2-(2'-хлор-6'-фторанилино)фенилуксусная кислота, лумиракоксиб. Термин "бисфосфонаты" при использовании в настоящем изобретении включает, но не ограничивается только ими, этридоновую, клодроновую, тилудроновую, памидроновую, алендроновую, ибандроновую, риседроновую и золедроновую кислоту. "Этридроновую кислоту" можно вводить, например, в той форме, в которой она продается, например, под торговым названием ДИДРОНЕЛ. "Клодроновую кислоту" можно вводить, например, в той форме, в которой она продается, например, под торговым названием БОНЭФОС. "Тилудроновую кислоту" можно вводить, например, в той форме, в которой она продается,например, под торговым названием СКЕЛИД. "Памидроновую кислоту" можно вводить, например, в той форме, в которой она продается, например, под торговым названием АРЕДИА. "Алендроновую кислоту" можно вводить, например, в той форме, в которой она продается, например, под торговым названием ФОСАМАКС. "Ибандроновую кислоту" можно вводить, например, в той форме, в которой она продается, например, под торговым названием БОНДРАНАТ. "Риседроновую кислоту" можно вводить, например, в той форме, в которой она продается, например, под торговым названием АКТОНЕЛ. "Золедроновую кислоту" можно вводить, например, в той форме, в которой она продается, например, под торговым названием ЗОМЕТА. Термин "ингибиторы mTOR" относится к соединениям, которые ингибируют мишень воздействия рапамицина у млекопитающих (mTOR) и которые обладают антипролиферативной активностью, такие как сиролимус (рапамун), эверолимус (цертикан), CCI-779 и АВТ 578. Термин "ингибитор гепариназы" при использовании в настоящем изобретении означает соединения, которые избирательно действуют, уменьшают или ингибируют разложение гепаринсульфата. Термин включает, но не ограничивается только им, PI-88. Термин "модификатор биологического ответа" при использовании в настоящем изобретении означает лимфокин или интерфероны, например интерферон. Термин "ингибитор онкогенных изоформ Ras", например H-Ras, K-Ras или N-Ras, при использовании в настоящем изобретении означает соединения, которые избирательно действуют, уменьшают или ингибируют онкогенную активность Ras, например "ингибитор фарнезилтрансферазы", напримерL-744832, DK8G557 или R115777 (зарнестра). Термин "ингибитор теломеразы" при использовании в настоящем изобретении означает соединения, которые избирательно действуют, уменьшают или ингибируют активность теломеразы. Соединения,которые избирательно действуют, уменьшают или ингибируют активность теломеразы, предпочтительно представляют собой соединения, которые ингибируют рецептор теломеразы, например теломестатин. Термин "ингибитор метионинаминопептидазы" при использовании в настоящем изобретении означает соединения, которые избирательно действуют, уменьшают или ингибируют активность метионинаминопептидазы. Соединения, которые избирательно действуют, уменьшают или ингибируют активность метионинаминопептидазы, представляют собой, например, бенгамид или его производное. Термин "ингибитор протеосомы" при использовании в настоящем изобретении означает соединения, которые избирательно действуют, уменьшают или ингибируют активность протеосомы. Соединения, которые избирательно действуют, уменьшают или ингибируют активность протеосомы, включают,например, бортезомид (велкаде) и MLN 341. Термин "ингибитор матричной металлопротеиназы" или "ингибитор ММР" при использовании в настоящем изобретении включает, но не ограничивается только ими, пептидомиметические и непептидомиметические ингибиторы коллагена, производные тетрациклина, например пептидомиметический ингибитор гидроксамата - батимастат и его обладающий пероральной биологической доступностью аналог маримастат (ВВ-2516), приномастат (AG3340), метастат (NSC 683551) BMS-279251, BAY 12-9566,TAA211, MMI270B или AAJ996. Термин "соединения, применяющиеся при лечении злокачественных заболеваний крови" при использовании в настоящем изобретении включает, но не ограничивается только ими, FMS-подобные ингибиторы тирозинкиназы, например соединения, избирательно действующие, уменьшающие или ингибирующие активность рецепторов(Flt-3R); интерферон,- 17021011 1-b-D-арабинофурансилцитозин (ara-c) и бисульфан; и ингибиторы ALK, например соединения, которые избирательно действуют, уменьшают или ингибируют киназу анапластической лимфомы. Соединения, которые избирательно действуют, уменьшают или ингибируют активность рецепторовFMS-подобной тирозинкиназы (Flt-3R), предпочтительно представляют собой соединения, белки или антитела, которые ингибируют представителей семейства тирозинкиназ рецептора Flt-3R, напримерPKC412, мидостаурин, производное стауроспорина, SU11248 и MLN518. Термин "ингибиторы Hsp90" при использовании в настоящем изобретении включает, но не ограничивается только ими, соединения, которые избирательно действуют, уменьшают или ингибируют специфическую АТФазную активность Hsp90; разрушают, избирательно действуют, уменьшают или ингибируют клиентные белки Hsp90 по убиквитиновому пути протеосомы. Соединения, избирательно действующие, уменьшающие или ингибирующие специфическую АТФазную активность Hsp90, предпочтительно представляют собой соединения, белки или антитела, которые ингибируют специфическую АТФазную активность Hsp90, например 17-аллиламино,17-деметоксигелданамицин (17AAG), производное гелданамицина, другие родственные гелданамицину соединения и радицикол. Примером ингибитораHsp90 является AUY922. Термин "антипролиферативные антитела" при использовании в настоящем изобретении включает,но не ограничивается только ими, трастузумаб (герцептин), трастузумаб-DM1, эрбутукс, бевацизумаб(авастин), ритуксимаб (ритуксан), PRO64553 (анти-CD40) и 2 С 4 антитела. Под антителами понимаются,например, интактные моноклональные антитела, поликлональные антитела, поливалентные антитела,сформированные по меньшей мере из двух интактных антител, и фрагменты антител, если они обладают необходимой биологической активностью. Для лечения острого миелолейкоза (ОМЛ) соединения формулы (I) можно использовать в комбинации со стандартными противолейкозными препаратами, предпочтительно в комбинации с препаратами,применяющимися для лечения ОМЛ. В частности, соединения формулы (I) можно вводить в комбинации, например, с ингибиторами фарнезилтрансферазы и/или другими лекарственными препаратами,применяющимися для лечения ОМЛ, такими как даунорубицин, адриамицин, Ara-C, VP-16, тенипозид,митоксантрон, идарубицин, карбоплатин и PKC412. Термин "противолейкозные соединения" включает, например, Ara-С, аналог пиримидина, который представляет собой 2-альфа-гидроксирибозное (арабинозид) производное дезоксицитидина. Также включен пуриновый аналог гипоксантина, 6-меркаптопурин (6-МР) и флударабинфосфат."Антагонисты соматостатинового рецептора" при использовании в настоящем изобретении означают соединения, которые избирательно действуют, уменьшают или ингибируют соматостатиновый рецептор, такие как октреотид и SOM230 (пасиреотид). Методики повреждения опухолевых клеток представляют собой такие, как использующие ионизирующее излучение. Термин "ионизирующее излучение", использованный выше и ниже в настоящем изобретении, означает ионизирующее излучение, представляющее собой электромагнитное излучение (такое как рентгеновское излучение и гамма-излучение) или частицы (такие как альфа- и бета-частицы). Ионизирующее излучение применяется в лучевой терапии, но не ограничивается только ею, и известно в данной области техники. См. публикацию Hellman, Principles of Radiation Therapy, Cancer, in Principlesand Practice of Oncology, Devita et al., Eds., 4th Edition, Vol. 1, p. 248-275 (1993). Термин "средства, связывающие EDG" при использовании в настоящем изобретении означает класс иммуносупрессивных средств, которые модулируют рециркуляцию лимфоцитов, такие как FTY720. Термин "ингибиторы рибонуклеотидредуктазы" означает аналоги пиримидиновых или пуриновых нуклеозидов, включая, но не ограничиваясь только ими, флударабин и/или цитозинарабинозид (ara-C),6-тиогуанин, 5-фторурацил, кладрибин, 6-меркаптопурин (предпочтительно в комбинации с ara-C противALL) и/или пентостатин. Ингибиторами рибонуклеотидредуктазы предпочтительно являются гидроксимочевина или производные 2-гидрокси-1H-изоиндол-1,3-диона, такие как PL-1, PL-2, PL-3, PL-4, PL-5,PL-6, PL-7 или PL-8, указанные в публикации Nandy et al., Acta Oncologica, Vol. 33, No. 8, p. 953-961(1994). Термин "ингибиторы S-аденозинметиониндекрабоксилазы" при использовании в настоящем изобретении включает, но не ограничивается только ими, соединения, раскрытые в US 5461076. Также включены, в частности, соединения, белки или моноклональные антитела к VEGF, раскрытые в WO 98/35958, например 1-(4-хлоранилино)-4-(4-пиридилметил)фталазин или его фармацевтически приемлемая соль, например сукцинат, или в WO 00/09495, WO 00/27820, WO 00/59509, WO 98/11223,WO 00/27819 и ЕР 0769947; описанные в публикациях Prewett et al., Cancer Res., Vol. 59, p. 5209-5218VEGF, или антитела к рецептору VEGF, например rhuMAb и RHUFab, аптамер VEGF, например макугон; ингибиторы FLT-4, ингибиторы FLT-3, антитела к VEGFR-2 IgG1, ангиозим (RPI 4610) и бева- 18021011 цизумаб (авастин). Фотодинамическая терапия при использовании в настоящем изобретении означает терапию, в которой используются некоторые вещества, известные как фотосенсибилизирующие соединения, применяющиеся для лечения или предупреждения рака. Примеры фотодинамической терапии включают лечение такими соединениями, как, например, ВИЗУДИН и порфимер натрия. Ангиостатические стероиды при использовании в настоящем изобретении означают соединения,которые блокируют или ингибируют ангиогенез, такие как, например, анекортав, триамцинолон, гидрокортизон, 11-эпигидрокортизол, кортексолон, 17-гидроксипрогестерон, кортикостерон, дезоксикортикостерон, тестостерон, эстрон и дексаметазон. Имплантаты, содержащие кортикостероиды, означают такие соединения, как, например, флуоцинолон, дексаметазон."Другие химиотерапевтические соединения" включают, но не ограничиваются только ими, растительные алкалоиды, гормональные соединения и антагонисты; модификаторы биологического ответа,предпочтительно лимфокины или интерфероны; антисмысловые олигонуклеотиды или производные олигонуклеотидов; sh-РНК или si-РНК или разные соединения, или соединения, обладающие другим или неизвестным механизмом действия. Структура активных соединений, у которых имеются кодовые номера, родовые или торговые названия, приведена в последнем издании справочника "The Merck Index" и в базах данных, например Patents International (например, IMS World Publications). Примеры Следующие аббревиатуры, использующиеся в приведенных ниже примерах, обладают указанными значениями. Стадия 1. Получение промежуточного продукта 1-(2-хлорэтил)-3-пиридин-3-илмочевины (I-1 а):- 19021011 1-Хлор-2-изоцианатоэтан (560 мг, 5,31 ммоль) при перемешивании по каплям добавляли к раствору пиридин-3-иламина (500 мг, 5,31 ммоль) в толуоле (10 мл) в течение 30 мин при 0 С. Температуру реакционной смеси поддерживали равной комнатной в течение 5 ч. За протеканием реакции следили с помощью ТСХ (100% этилацетат). Реакционную смесь фильтровали, промывали толуолом и сушили при пониженном давлении и получали 1,0 г (выход 98%) 1-(2-хлорэтил)-3-пиридин-3-илмочевины. 1 Н ЯМР (ДМСО-d6, 300 МГц):8,9 (br s, 1H), 8,55 (br s, 1H), 8,1 (d, 1H), 7,9 (m, 1H), 7,3 (m, 1H), 6,5(t, 1H), 3,65 (t, 2H), 3,45 (q, 2H). Чистота по данным ЖХМС: 99,75%, m/z=200,2 (M+1). Стадия 2. Получение промежуточного продукта 1-пиридин-3-илимидазолидин-2-она (I-1b): 1-(2-Хлорэтил)-3-пиридин-3-илмочевину (I-1a: 1000 мг, 5,0 ммоль) в сухом ДМФ (10 мл) при перемешивании добавляли к раствору гидрида натрия (216 мг, 9,0 ммоль) в ТГФ (10 мл) при 0 С. Температуру реакционной смеси поддерживали равной комнатной в течение 30 мин. За протеканием реакции следили с помощью ТСХ (100% этилацетат). Реакцию останавливали с помощью MeOH (5 мл) при 0 С. Реакционную смесь концентрировали при пониженном давлении и подвергали распределению между водой со льдом и хлороформом. Органический слой сушили над Na2SO4 и концентрировали при пониженном давлении и получали 800 мг (выход 97%) 1-пиридин-3-илимидазолидин-2-она. 1(m, 2 Н), 3,45 (m, 2 Н). Чистота по данным ЖХМС: m/z=164,2 (M+1). Заключительная стадия. Получение 1-нафталин-2-ил-3-пиридин-3-илимидазолидин-2-она (1A). Йодид меди (10,0 мг, 0,113 ммоль), транс-1,2-диаминоциклогексан (10,0 мг, 0,091 ммоль) и карбонат калия (169 мг, 1,22 ммоль) добавляли к раствору 1,4-диоксана (5 мл), предварительно продутому аргоном (10 мин). Реакционную смесь продували аргоном в течение 10 мин, затем добавляли 1-пиридин-3-илимидазолидин-2-он (I-1b: 100 мг, 0,61 ммоль) и 2-бромнафталин (126 мг, 0,61 ммоль). Реакционную смесь кипятили с обратным холодильником при 110 С в течение 15 ч. За протеканием реакции следили с помощью ТСХ (10% MeOH в хлороформе). Реакционную смесь фильтровали через слой целита и слой промывали хлороформом. Органический слой концентрировали и очистка с помощью колоночной хроматографии (с использованием силикагеля с частицами размером 60-120 меш, 20% этилацетата в гексане в качестве элюента) давала 48 мг (выход 28%) 1-нафталин-2-ил-3-пиридин-3 илимидазолидин-2-она. 1 Н ЯМР (ДМСО-d6, 300 МГц):8,9 (d, 1H), 8,3 (d, 1H), 8,15-8,05 (m, 2H), 7,95-7,85 (m, 4 Н), 7,55-7,4(m, 3 Н), 4,2-4,0 (m, 4 Н). Чистота по данным ЖХМС: 98,57%; m/z=290,0 (M+1). ВЭЖХ: 96,05%. Пример 2. Получение 1-(1-этил-1 Н-индол-5-ил)-3-пиридин-3-илимидазолидин-2-она (2 А): При таких же условиях проведения реакции, как в примере 1, 1-пиридин-3-илимидазолидин-2-он(20,99 мг, 1,839 ммоль) и карбонатом калия (338 мг, 2,452 ммоль) и получали неочищенный продукт. Очистка с помощью колоночной хроматографии на силикагеле (30% этилацетата в гексане) давала 185 мг продукта (выход 49,33%). 1 Н ЯМР (ДМСО-d6, 300 МГц):8,85-8,8 (br s, 1H), 8,2 (d, 1H), 8,1-8,05 (m, 1H), 7,65 (s, 1H), 7,5 (s,2H), 7,4-7,35 (m, 2H), 6,4 (d, 1H), 4,5 (q, 2H), 4,1-4,0 (m, 4H), 1,4 (t, 3H). Чистота по данным ЖХМС: 96,97%, m/z=307,0 (М+1). ВЭЖХ: 98,74%. При таких же условиях проведения реакции, как в примере 1, 1-пиридин-3-илимидазолидин-2-он(I-1b: 68,7 мг, 0,4217 ммоль) вводили в реакцию с 2-бром-6-метоксинафталином (100 мг, 0,4217 ммоль),1,4-диоксаном (5 мл), йодидом меди (8,0 мг, 0,04217 ммоль), транс-1,2-диаминоциклогексаном (7 мг,0,0632 ммоль) и карбонатом калия (116 мг, 0,8432 ммоль) и получали неочищенный продукт. Очистка с помощью колоночной хроматографии на силикагеле (50% этилацетата в гексане) давала 72 мг продукта(d, 1H), 7,15 (dd, 1H), 4,2-4,0 (m, 4H), 3,85 (s, 3H). Чистота по данным ЖХМС: 96,72%, m/z=320,0 (M+1). ВЭЖХ: 97,84%. Пример 4. Получение 1-бензотиазол-6-ил-3-пиридин-3-илимидазолидин-2-она (4 А): При таких же условиях проведения реакции, как в примере 1, 1-пиридин-3-илимидазолидин-2-он(I-1b: 62 мг, 0,3831 ммоль) вводили в реакцию с 6-йодбензотиазолом (100 мг, 0,3831 ммоль),1,4-диоксаном (10 мл), йодидом меди (7 мг, 0,03831 ммоль), транс-1,2-диаминоциклогексаном (6 мг,0,5747 ммоль) и карбонатом калия (105 мг, 0,7662 ммоль) и получали неочищенный продукт. Очистка с помощью колоночной хроматографии на силикагеле (1% MeOH в хлороформе) давала 52 мг продуктаH ЯМР (ДМСО-d6, 300 МГц):9,3 (s, 1H), 8,9 (d, 1H), 8,35-8,25 (m, 2H), 8,1-8,0 (m, 2H), 7,95 (dd,1H), 7,45-7,4 (m, 1H), 4,2-4,0 (m, 4H). Чистота по данным ЖХМС: 93,45%, m/z=297,3 (М+1). ВЭЖХ: 95,65%. Пример 5. Получение 1-этил-6-(2-оксо-3-пиридин-3-илимидазолидин-1-ил)-3,4-дигидро-1 Н-хинолин-2-она При таких же условиях проведения реакции, как в примере 1, 1-пиридин-3-илимидазолидин-2-он(11 мг,0,05882 ммоль),транс-1,2-диаминоциклогексаном (10 мг, 0,08823 ммоль) и карбонатом калия (162 мг, 1,1764 ммоль) и получали неочищенный продукт. Очистка с помощью колоночной хроматографии на силикагеле (1%(m, 1H), 7,15 (d, 1H), 4,0 (s, 4H), 3,9 (q, 2 Н), 2,85 (t, 2H), 2,55-2,5 (m, 2 Н), 1,1 (t, 3 Н). Чистота по данным ЖХМС: 99,16%, m/z=337,3 (М+1). ВЭЖХ: 95,77%. Пример 6. Получение 1-(5-фтор-3-метилбензо[b]тиофен-2-ил)-3-пиридин-3-илимидазолидин-2-она (6 А): При таких же условиях проведения реакции, как в примере 1, 1-пиридин-3-илимидазолидин-2-он(7 мг, 0,0675 ммоль) и карбонатом калия (124 мг, 0,9 ммоль) и получали неочищенный продукт. Очистка с помощью колоночной хроматографии на силикагеле (1% MeOH в хлороформе) давала 90 мг продуктаH ЯМР (ДМСО-d6, 300 МГц):8,9 (d, 1H), 8,3 (dd, 1H), 8,15-8,05 (m, 1 Н), 7,95-7,7 (m, 1 Н), 7,6 (dd,1H), 7,45-7,4 (m, 1H), 7,3-7,2 (m, 1H), 4,15-4,0 (m, 4 Н), 2,3 (s, 3 Н). Чистота по данным ЖХМС: 98,04%, m/z=327,9 (М+1). ВЭЖХ: 95,05%. Пример 7. Получение 1-бензо[b]тиофен-5-ил-3-пиридин-3-илимидазолидин-2-она (7 А): При таких же условиях проведения реакции, как в примере 1, 1-пиридин-3-илимидазолидин-2-он(I-1b: 93,6 мг, 0,5747 ммоль) вводили в реакцию с 5-йодбензо[b]тиофеном (150 мг, 0,5747 ммоль),1,4-диоксаном (5 мл), йодидом меди (10 мг, 0,05747 ммоль), транс-1,2-диаминоциклогексаном (9 мг,0,0862 ммоль) и карбонатом калия (158,9 мг, 1,149 ммоль) и получали неочищенный продукт. Очистка с помощью колоночной хроматографии на силикагеле (1% MeOH в хлороформе) давала 70 мг продукта(m, 2 Н), 4,1-4,0 (m, 4 Н). Чистота по данным ЖХМС: 97,11%, m/z=296,3 (М+1). ВЭЖХ: 97,46%. Пример 8. Получение 1-пиридин-3-ил-3-хинолин-6-илимидазолидин-2-она (8 А): При таких же условиях проведения реакции, как в примере 1, 1-пиридин-3-илимидазолидин-2-он(I-1b: 117 мг, 0,7215 ммоль) вводили в реакцию с 6-бромхинолином (150 мг, 0,7215 ммоль),1,4-диоксаном (5 мл), йодидом меди (13 мг, 0,07215 ммоль), транс-1,2-диаминоциклогексаном (24,78 мг,0,21645 ммоль) и карбонатом калия (199,49 мг, 1,1443 ммоль) и получали неочищенный продукт. Очистка с помощью колоночной хроматографии на силикагеле (1% MeOH в хлороформе) давала 125 мг продукта (выход 60,09%). 1H ЯМР (ДМСО-d6, 300 МГц):8,9 (d, 1H), 8,8 (dd, 1H), 8,4-8,25 (m, 3H), 8,15-8,0 (m, 2H), 7,9 (d,1H), 7,55-7,4 (m, 2 Н), 4,2-4,0 (m, 4 Н). Чистота по данным ЖХМС: 98,99%, m/z=291,1 (М+1). ВЭЖХ: 98,55%. Пример 9. Получение 1-бензотиазол-5-ил-3-пиридин-3-илимидазолидин-2-она (9 А): При таких же условиях проведения реакции, как в примере 1, 1-пиридин-3-илимидазолидин-2-он(19,65 мг, 0,1724 ммоль) и карбонатом калия (159 мг, 1,1494 ммоль) и получали неочищенный продукт. Очистка с помощью колоночной хроматографии на силикагеле (1% MeOH в хлороформе) давала 105 мг продукта (выход 61,76%). 1(dd, 1 Н), 7,45-7,4 (m, 1 Н), 4,2-4,0 (m, 4 Н). Чистота по данным ЖХМС: 98,09%, m/z=296,9 (М+1). ВЭЖХ: 95,27%. Стадия 1. Получение промежуточного продукта 1-(3-хлорпропил)-3-пиридин-3-илмочевины 1-Хлор-3-изоцианатопропан (1,897 г, 15,873 ммоль) в течение 30 мин при 0 С при перемешивании по каплям добавляли к раствору пиридин-3-иламина (1 г, 10,582 ммоль) в толуоле (15 мл). Температуру реакционной смеси поддерживали равной комнатной в течение 6 ч. За протеканием реакции следили с помощью ТСХ (100% этилацетат). Реакционную смесь фильтровали, промывали толуолом и сушили при пониженном давлении и получали 2,1 г (выход 95,45%) 1-(3-хлорпропил)-3-пиридин-3-илмочевины. 1 1-(3-Хлорпропил)-3-пиридин-3-илмочевину (1-10 а: 2,1 г, 9,859 ммоль) в сухом ДМФ (10 мл) добавляли к раствору гидрида натрия (487 мг, 10,154 ммоль) в ТГФ (2 мл) при 0 С. Температуру реакционной смеси поддерживали равной комнатной в течение 30 мин. За протеканием реакции следили с помощью ТСХ (100% этилацетат). Реакцию останавливали с помощью MeOH (5 мл) при 0 С, концентрировали при пониженном давлении и подвергали распределению между охлажденной льдом водой и хлороформом. Органический слой сушили над Na2SO4 и концентрировали при пониженном давлении и получали 1,7 г(10 А). При таких же условиях проведения реакции, как в примере 1, 1-пиридин-3-илтетрагидропиримидин-2-он (1-10b: 118 мг, 0,724 ммоль) вводили в реакцию с 2-бромнафталином (150 мг,0,724 ммоль),1,4-диоксаном(13,79 мг,0,0724 ммоль),транс-1,2-диаминоциклогексаном (24,865 мг, 0,2172 ммоль) и карбонатом калия (200 мг, 1,448 ммоль) и получали неочищенный продукт. Очистка с помощью колоночной хроматографии на силикагеле (1%H ЯМР (ДМСО-d6, 300 МГц):8,65 (d, 1H), 8,35-8,3 (m, 1H), 7,95-7,75 (m, 5H), 7,6-7,4 (m, 4H),3,95-3,8 (m, 4H), 2,3-2,2 (m, 2H). Чистота по данным ЖХМС: 98,98%, m/z=304,0 (M+1). ВЭЖХ: 99,14%. Пример 11. Получение 1-(2-хлор-4-метилхинолин-6-ил)-3-пиридин-3-илимидазолидин-2-она (11A): При таких же условиях проведения реакции, как в примере 1, 1-пиридин-3-илимидазолидин-2-он(I-1b: 95,8 мг, 0,5882 ммоль) вводили в реакцию с 6-бром-2-хлор-4-метилхинолином (150 мг,0,5882 ммоль), 1,4-диоксаном (5 мл), йодидом меди (11,2 мг, 0,05882 ммоль),транс-1,2-диаминоциклогексаном (20,20 мг, 0,1764 ммоль) и карбонатом калия (162,6 мг, 1,1764 ммоль) и получали неочищенный продукт. Очистка с помощью колоночной хроматографии на силикагеле (1%H ЯМР (ДМСО-d6, 300 МГц):8,85 (d, 1H), 8,4-8,3 (m, 2H), 8,15-7,95 (m, 3 Н), 7,5-7,4 (m, 2H), 4,34,0 (m, 4H), 2,6 (s, 3 Н). Чистота по данным ЖХМС: 89,47%, m/z=339,0 (М+1). ВЭЖХ: 97,08%. Пример 12. Получение 1-(1-гидроксиминоиндан-5-ил)-3-пиридин-3-илимидазолидин-2-она (12 А): При таких же условиях проведения реакции, как в примере 1, 1-пиридин-3-илимидазолидин-2-он(56,976 мг, 0,4976 ммоль) и карбонатом калия (458,63 мг, 3,3174 ммоль) и получали неочищенный продукт. Очистка с помощью колоночной хроматографии на силикагеле (1% MeOH в хлороформе) давала 300 мг 1-(1-оксоиндан-5-ил)-3-пиридин-3-илимидазолидин-2-она (выход 61,72%). Гидроксиламингидрохлорид (141 мг, 2,044 ммоль) и ацетат натрия (167,6 мг, 2,044 ммоль) в 5 мл воды добавляли к раствору 1-(3-оксоиндан-5-ил)-3-пиридин-3-илимидазолидин-2-она (200 мг,0,6814 ммоль) в этаноле (7 мл). Реакционную смесь нагревали до 90 С и эту температуру поддерживали в течение 6 ч. Затем реакционную смесь охлаждали до комнатной температуры и растворитель отгоняли из реакционной смеси. Полученный осадок собирали, промывали хлороформом и сушили при пониженном давлении и получали 200 мг продукта (выход 90%). 1H ЯМР (ДМСО-d6, 300 МГц):10,5 (s, 1H), 8,9 (s, 1H), 8,35-8,25 (br s, 1H), 8,1 (d, 1H), 7,7-7,4 (m,4H), 4,0 (s, 4 Н), 3,05-3,0 (m, 2H), 2,85-2,7 (m, 2H). Чистота по данным ЖХМС: 98,13%, m/z=309,2 (М+1). ВЭЖХ: 83,39%. Пример 13. Получение 1-бензо[b]тиофен-5-ил-3-пиридин-3-илтетрагидропиримидин-2-она (13 А): При таких же условиях проведения реакции, как в примере 1, 1-пиридин-3-илтетрагидропиримидин-2-он (1-10b: 67,8 мг, 0,3831 ммоль) вводили в реакцию с 5-йодбензо[b]тиофеном (100 мг,0,3831 ммоль), 1,4-диоксаном (5 мл), йодидом меди (7,29 мг, 0,03831 ммоль),транс-1,2-диаминоциклогексаном (13,15 мг, 0,1149 ммоль) и карбонатом калия (106,1 мг, 0,7662 ммоль) и получали 15 мг продукта (выход 17,5%). 1H ЯМР (ДМСО-d6, 300 МГц):8,7-8,5 (br s, 1H), 8,4-8,3 (br s, 1H), 7,95 (d, 1H), 7,85-7,75 (m, 3H),7,45-7,35 (m, 3H), 3,9 (q, 4H), 2,35-2,25 (m, 2H). Чистота по данным ЖХМС: 99,84%, m/z=309,9 (М+1). ВЭЖХ: 94,28%. Пример 14. Получение 1-(4-метилпиридин-3-ил)-3-нафталин-2-илимидазолидин-2-она (14 А): Стадия 1. Получение промежуточного продукта 1-(2-хлорэтил)-3-(4-метилпиридин-3-ил)мочевины 1-Хлор-2-изоцианатоэтан (5,91 мл, 69,35 ммоль) при перемешивании по каплям добавляли к раствору 4-метилпиридин-3-иламина (5 г, 46,23 ммоль) в толуоле (180 мл) при 0 С. Температуру реакционной смеси поддерживали равной комнатной в течение 5 ч. За протеканием реакции следили с помощью ТСХ (5% MeOH в хлороформе). Реакционную смесь фильтровали, промывали толуолом и сушили приH ЯМР (ДМСО-d6, 300 МГц):8,95 (s, 1H), 8,1 (m, 2H), 7,25 (d, 1H), 6,95 (t, 1H), 3,7 (t, 2H), 3,45 (q,2H), 2,2 (s, 3 Н). ЖХМС: m/z=214,1 (М+1). Стадия 2. Получение промежуточного продукта 1-(4-метилпиридин-3-ил)имидазолидин-2-она 1-(2-Хлорэтил)-3-(4-метилпиридин-3-ил)мочевину (I-14 а: 8,5 г, 39,96 ммоль) в сухом ДМФ (150 мл) при перемешивании добавляли к смеси гидрида натрия (2,87 г, 59,94 ммоль) в ТГФ (150 мл) при 0 С. Температуру реакционной смеси поддерживали равной комнатной в течение 30 мин. За протеканием реакции следили с помощью ТСХ. Реакцию останавливали с помощью MeOH при 0 С, концентрировали при пониженном давлении и подвергали распределению между водой со льдом и хлороформом. Органический слой сушили над Na2SO4 и концентрировали при пониженном давлении и получали 6,5 г (выход 91%) 1-(4-метилпиридин-3-ил)имидазолидин-2-она. 1 Н ЯМР (ДМСО-d6, 300 МГц):8,4 (s, 1H), 8,3 (m, 1H), 7,3 (d, 1H), 6,85 (br s, 1H), 3,8 (t, 2 Н), 3,45 (t,2H), 2,25 (s, 3 Н). Чистота по данным ЖХМС: 100%, m/z=178,3 (М+1). Заключительная стадия. Получение 1-(4-метилпиридин-3-ил)-3-нафталин-2-илимидазолидин-2-она(10 мин). Реакционную смесь продували аргоном в течение еще 10 мин, затем добавляли 1-(4-метилпиридин-3-ил)имидазолидин-2-он (I-14b: 200 мг, 1,13 ммоль) и 2-бромнафталин (234 мг,1,13 ммоль). Полученную смесь кипятили с обратным холодильником при 110 С в течение 15 ч. За протеканием реакции следили с помощью ТСХ (10% MeOH в хлороформе). Реакционную смесь фильтровали через целит и слой промывали хлороформом. Органический слой сушили над Na2SO4 и концентрировали. Очистка с помощью колоночной хроматографии (с использованием силикагеля с частицами размером 60-120 меш, 1% MeOH в хлороформе в качестве элюента) давала 250 мг (выход 73%) 1-(4-метилпиридин-3-ил)-3-нафталин-2-илимидазолидин-2-она. 1(m, 3 Н), 4,4-4,25 (m, 2 Н), 3,95-4,1 (m, 2 Н), 2,35 (s, 3 Н). Чистота по данным ЖХМС: 98,31%, m/z=304,1 (М+1). ВЭЖХ: 97,55%. Пример 15. Получение 1-(4-метилпиридин-3-ил)-3-(5-метилтиофен-2-ил)имидазолидин-2-она (15A):(10 мин). Реакционную смесь продували аргоном в течение еще 10 мин, затем добавляли 1-(4-метилпиридин-3-ил)имидазолидин-2-он (I-14b: 150 мг, 0,84 ммоль) и 2-бром-5-метилтиофен (150 мг,0,84 ммоль). Полученную смесь кипятили с обратным холодильником при 110 С в течение 4 ч. За протеканием реакции следили с помощью ТСХ (10% MeOH в хлороформе). Реакционную смесь фильтровали через целит и слой целита промывали хлороформом. Органический слой сушили над Na2SO4 и концентрировали. Концентрат охлаждали льдом, полученный осадок собирали, сушили и получали 170 мг (выход 74%) 1-(4-метилпиридин-3-ил)-3-(5-метилтиофен-2-ил)имидазолидин-2-она. 1H ЯМР (ДМСО-d6, 300 МГц):8,5 (s, 1 Н), 8,4 (d, 1H), 7,35 (d, 1H), 6,55 (d, 1H), 6,25 (d, 1H), 4,0 (s,4H), 2,35 (s, 3 Н), 2,25 (s, 3 Н). Чистота по данным ЖХМС: 98,84%, m/z=274,0 (М+1). ВЭЖХ: 97,43%. При таких же условиях проведения реакции, как в примере 14, 1-(4-метилпиридин-3 ил)имидазолидин-2-он (I-14b: 150 мг, 0,847 ммоль) вводили в реакцию с 6-йодбензотиазолом (200,93 мг,0,847 ммоль), 1,4-диоксаном (20 мл), йодидом меди (16,135 мг, 0,0847 ммоль),транс-1,2-диаминоциклогексаном (0,03 мл, 0,254 ммоль) и карбонатом калия (233,97 мг, 1,694 ммоль) и получали неочищенный продукт. Очистка с помощью колоночной хроматографии на силикагеле (1%H ЯМР (ДМСО-d6, 300 МГц):9,26 (s, 1H), 8,56 (s, 1H), 8,4 (d, 1H), 8,3 (d, 1H), 8,1-8,06 (m, 1 Н),7,96 (dd, 1 Н), 7,38 (d, 1 Н), 4,2-4,1 (m, 2 Н), 4,0-3,92 (m, 2 Н), 2,3 (s, 3 Н). Чистота по данным ЖХМС: 97,79%, m/z=310,9 (М+1). ВЭЖХ: 96,64%. Пример 17. Получение 1-этил-6-[3-(4-метилпиридин-3-ил)-2-оксоимидазолидин-1-ил]-3,4-дигидро-1 Н-хинолин 2-она (17 А): При таких же условиях проведения реакции, как в примере 14, 1-(4-метилпиридин-3 ил)имидазолидин-2-он (I-14b: 150 мг, 0,847 ммоль) вводили в реакцию с 6-бром-1-этил-3,4-дигидро-1 Нхинолин-2-оном (215,15 мг, 0,847 ммоль), 1,4-диоксаном (0,03 мл, 0,254 ммоль), йодидом меди (16,13 мг,0,0847 ммоль), транс-1,2-диаминоциклогексаном (0,03 мл, 0,254 ммоль) и карбонатом калия (233,97 мг,1,694 ммоль) и получали неочищенный продукт. Очистка с помощью колоночной хроматографии на силикагеле (1% MeOH в хлороформе) давала 95 мг продукта (выход 31,99%). 1H ЯМР (ДМСО-d6, 300 МГц):8,56-8,5 (br s, 1H), 8,42-8,38 (br s, 1H), 7,52-7,46 (m, 2H), 7,35 (d,1H), 7,13 (d, 1H), 4,1-3,85 (m, 6H), 3,35-3,25 (m, 2H), 2,85 (t, 2H), 2,25 (s, 3H), 1,1 (t, 3H). Чистота по данным ЖХМС: 96,43%, m/z=351,0 (M+1). ВЭЖХ: 96,26%. Пример 18. Получение 1-(4-фторфенил)-3-(4-метилпиридин-3-ил)имидазолидин-2-она (18A): При таких же условиях проведения реакции, как в примере 14, 1-(4-метилпиридин-3 ил)имидазолидин-2-он (I-14b: 150 мг, 0,8465 ммоль) вводили в реакцию с 1-бром-4-фторбензолом(148,1 мг, 0,8465 ммоль), 1,4-диоксаном (25 мл), йодидом меди (16 мг, 0,08465 ммоль),транс-1,2-диаминоциклогексаном (29 мг, 0,2539 ммоль) и карбонатом калия (468 мг, 3,3860 ммоль) и получали неочищенный продукт. Очистка с помощью колоночной хроматографии на силикагеле (2%(m, 4H), 2,3 (s, 3 Н). Чистота по данным ЖХМС: 99,85%, m/z=272,0 (М+1). ВЭЖХ: 96,49%. При таких же условиях проведения реакции, как в примере 14, 1-(4-метилпиридин-3 ил)имидазолидин-2-он (I-14b: 150 мг, 0,8465 ммоль) вводили в реакцию с 4-бромбифенилом (197,3 мг,0,8465 ммоль),1,4-диоксаном(16 мг,0,08465 ммоль),транс-1,2-диаминоциклогексаном (29 мг, 0,2539 ммоль) и карбонатом калия (468 мг, 3,3860 ммоль) и получали неочищенный продукт. Очистка с помощью колоночной хроматографии на силикагеле (2%MeOH в хлороформе) давала 147 мг продукта (выход 52%). 1 Н ЯМР (ДМСО-d6, 300 МГц):8,6 (s, 1H), 8,4 (d, 1H), 7,8-7,6 (m, 6H), 7,45 (t, 2H), 7,35 (t, 2H), 4,1 (t,2H), 4,0 (t, 2H), 2,3 (s, 3 Н). Чистота по данным ЖХМС: 85,37%, m/z=330,1 (М+1). ВЭЖХ: 96,0%. Пример 20. Получение 1-этил-4-метил-6-[3-(4-метилпиридин-3-ил)-2-оксоимидазолидин-1-ил]-1 Н-хинолин-2 она (20 А): При таких же условиях проведения реакции, как в примере 14, 1-(4-метилпиридин-3 ил)имидазолидин-2-он (I-14b: 99 мг, 0,5597 ммоль) вводили в реакцию с 6-бром-1-этил-4-метил-1 Нхинолин-2-оном (150 мг, 0,5597 ммоль), 1,4-диоксаном (5 мл), йодидом меди (10,66 мг, 0,05597 ммоль),транс-1,2-диаминоциклогексаном (19,22 мг, 0,1679 ммоль) и карбонатом калия (77,37 мг, 1,1194 ммоль) и получали неочищенный продукт. Очистка с помощью колоночной хроматографии на силикагеле (1%H ЯМР (ДМСО-d6, 300 МГц):8,55 (s, 1H), 8,4 (d, 1 Н), 8,0-7,85 (m, 2H), 7,6 (d, 1H), 7,35 (d, 1H),6,55 (s, 1H), 4,25 (q, 2H), 4,2-4,1 (m, 2H), 4,0-3,9 (m, 2H), 2,4 (s, 3 Н), 2,3 (s, 3 Н), 1,15 (t, 3 Н). Чистота по данным ЖХМС: 99,36%, m/z=362,9 (М+1). ВЭЖХ: 97,77%. Пример 21. Получение 1-(2-хлор-4-метилхинолин-6-ил)-3-(4-метилпиридин-3-ил)имидазолидин-2-она (21 А): При таких же условиях проведения реакции, как в примере 14, 1-(4-метилпиридин-3 ил)имидазолидин-2-он (I-14b: 275,4 мг, 1,5564 ммоль) вводили в реакцию с 6-бром-2-хлор-4 метилхинолином (400 мг, 1,5564 ммоль), 1,4-диоксаном (10 мл), йодидом меди (29,649 мг,0,15564 ммоль), транс-1,2-диаминоциклогексаном (53,448 мг, 0,4668 ммоль) и карбонатом калия (430 мг,3,112 ммоль) и получали неочищенный продукт. Очистка с помощью колоночной хроматографии на силикагеле (1% MeOH в хлороформе) давала 256 мг продукта (выход 46,54%). 1(d, 1H), 4,25-4,15 (m, 2H), 4,05-3,95 (m, 2H), 2,65 (s, 3 Н), 2,3 (s, 3 Н). Чистота по данным ЖХМС: 96,22%, m/z=352,9 (М+1). ВЭЖХ: 98,78%.(5 мл) добавляли к 1-(2-хлор-4-метилхинолин-6-ил)-3-(4-метилпиридин-3 ил)имидазолидин-2-ону (21 А: 50 мг, 0,1418 ммоль). Реакционную смесь перемешивали при 120 С в течение ночи. Реакционную массу охлаждали до 0 С, водный раствор NaHCO3 добавляли до установления рН, равного примерно 8. Реакционную смесь экстрагировали хлороформом. Органический слой сушили над Na2SO4, концентрировали и получали 38 мг продукта (выход 80,85%). 1 Н ЯМР (ДМСО-d6, 300 МГц):11,5 (s, 1H), 8,55 (s, 1H), 8,4 (d, 1H), 7,85-7,8 (m, 2H), 7,4-7,3 (m,2H), 6,5-6,4 (br s, 1H), 4,15-4,05 (m, 2H), 4,0-3,9 (m, 2 Н), 2,4 (s, 3 Н), 2,3 (s, 3 Н). Чистота по данным ЖХМС: 98,45%, m/z=334,9 (М+1). ВЭЖХ: 93,73%. Пример 23. Получение 1-(4-метилпиридин-3-ил)-3-хинолин-2-илимидазолидин-2-она (23 А): При таких же условиях проведения реакции, как в примере 14, 1-(4-метилпиридин-3 ил)имидазолидин-2-он (I-14b: 150 мг, 0,84650 ммоль) вводили в реакцию с 2-хлорхинолином (138,4 мг,0,84650 ммоль), 1,4-диоксаном (30 мл), йодидом меди (16 мг, 0,08465 ммоль),транс-1,2-диаминоциклогексаном (29 мг, 0,2539 ммоль) и карбонатом калия (468 мг, 3,3860 ммоль) и получали неочищенный продукт. Очистка с помощью колоночной хроматографии на силикагеле (2%H ЯМР (ДМСО-d6, 300 МГц):8,6 (s, 1H), 8,5 (d, 1H), 8,4 (d, 1H), 8,3 (d, 1H), 7,9-7,8 (m, 2H), 7,757,65 (m, 1H), 7,5-7,45 (m, 1H), 7,4 (d, 1H), 4,3 (t, 2H), 4,0 (t, 2H), 2,3 (s, 3 Н). Чистота по данным ЖХМС: 97,22%, m/z=305,1 (М+1). ВЭЖХ: 96,07%. Пример 24. Получение 1-(4-метилпиридин-3-ил)-3-хинолин-3-илимидазолидин-2-она (24 А): При таких же условиях проведения реакции, как в примере 14, 1-(4-метилпиридин-3 ил)имидазолидин-2-он (I-14b: 150 мг, 0,847 ммоль) вводили в реакцию с 3-бромхинолином (176,13 мг,0,847 ммоль), 1,4-диоксаном (15 мл), йодидом меди (16,13 мг, 0,0847 ммоль),транс-1,2-диаминоциклогексаном (0,03 мл, 0,254 ммоль) и карбонатом калия (233,97 мг, 1,694 ммоль) и получали неочищенный продукт. Очистка с помощью колоночной хроматографии на силикагеле (1%H ЯМР (ДМСО-d6, 300 МГц):9,5 (d, 1H), 8,6 (s, 1H), 8,42 (d, 1H), 8,35 (d, 1H), 8,02-7,92 (m, 2H),7,7-7,58 (m, 2H), 7,4 (d, 1H), 4,25-4,15 (m, 2H), 4,05-3,9 (m, 2H), 2,35 (s, 3H). Чистота по данным ЖХМС: 98,34%, m/z=305,2 (М+1). ВЭЖХ: 95,64%. Пример 25. Получение 1-(6-метоксинафталин-2-ил)-3-(4-метилпиридин-3-ил)имидазолидин-2-она (25 А):- 28021011 При таких же условиях проведения реакции, как в примере 14, 1-(4-метилпиридин-3 ил)имидазолидин-2-он (I-14b: 150 мг, 0,847 ммоль) вводили в реакцию с 2-бром-6-метоксинафталином(200,74 мг, 0,847 ммоль), 1,4-диоксаном (15 мл), йодидом меди (16,13 мг, 0,0847 ммоль),транс-1,2-диаминоциклогексаном (0,03 мл, 0,254 ммоль) и карбонатом калия (233,97 мг, 1,694 ммоль) и получали неочищенный продукт. Очистка с помощью колоночной хроматографии на силикагеле (1%H ЯМР (ДМСО-d6, 300 МГц):8,62-8,58 (br s, 1H), 8,44-8,4 (br s, 1H), 8,28 (dd, 1H), 7,86-7,76 (m,3H), 7,4 (d, 1H), 7,28 (d, 1H), 7,16 (dd, 1H), 4,18-4,1 (m, 2 Н), 4,02-3,96 (m, 2 Н), 3,86 (s, 3 Н), 2,33 (s, 3 Н). Чистота по данным ЖХМС: 95,49%, m/z=334,1 (М+1). ВЭЖХ: 93,56%. Пример 26. Получение 1-бензо[b]тиофен-2-ил-3-(4-метилпиридин-3-ил)имидазолидин-2-она (26 А): При таких же условиях проведения реакции, как в примере 14, 1-(4-метилпиридин-3 ил)имидазолидин-2-он (I-14b: 109,25 мг, 0,6171 ммоль) вводили в реакцию с 2-бромбензо[b]тиофеном(150 мг, 0,6171 ммоль), 1,4-диоксаном (5 мл), йодидом меди (11,75 мг, 0,06171 ммоль),транс-1,2-диаминоциклогексаном (21,19 мг, 0,1851 ммоль) и карбонатом калия (170,62 мг, 1,2342 ммоль) и получали неочищенный продукт. Очистка с помощью колоночной хроматографии на силикагеле (1%(m, 1H), 7,2 (t, 1H), 6,75 (s, 1 Н), 4,25-4,1 (m, 2 Н), 4,1-4,0 (m, 2H), 2,3 (s, 3 Н). Чистота по данным ЖХМС: 97,09%, m/z=310,1 (М+1). ВЭЖХ: 92,27%. Пример 27. Получение 1-бензо[b]тиофен-5-ил-3-(4-метилпиридин-3-ил)имидазолидин-2-она (27 А): При таких же условиях проведения реакции, как в примере 14, 1-(4-метилпиридин-3 ил)имидазолидин-2-он (I-14b: 150 мг, 0,847 ммоль) вводили в реакцию с 5-бромбензо[b]тиофеном(180,5 мг, 0,847 ммоль), 1,4-диоксаном (15 мл), йодидом меди (16,13 мг, 0,0847 ммоль),транс-1,2-диаминоциклогексаном (0,03 мл, 0,254 ммоль) и карбонатом калия (233,97 мг, 1,694 ммоль) и получали неочищенный продукт. Очистка с помощью колоночной хроматографии на силикагеле (1%(d, 1 Н), 7,45 (d, 1 Н), 4,2-4,1 (m, 2 Н), 4,05-3,95 (m, 2 Н), 2,4 (s, 3 Н). Чистота по данным ЖХМС: 91,88%, m/z=309,9 (М+1). ВЭЖХ: 97,97%. Пример 28. Получение 1-(1H-индазол-5-ил)-3-(4-метилпиридин-3-ил)имидазолидин-2-она (28 А): При таких же условиях проведения реакции, как в примере 14, 1-(4-метилпиридин-3 ил)имидазолидин-2-он(10 мл), йодидом меди (0,011 г, 0,000051 моль), транс-1,2-диаминоциклогексаном (0,018 г, 0,00016 моль) и карбонатом калия (0,134 г, 0,00106 ммоль) и получали неочищенный продукт. Очистка с помощью колоночной хроматографии на силикагеле (1% MeOH в хлороформе) давала 0,24 г 1-(4-метилпиридин-3 ил)-3-[1-(2-триметилсиланилэтоксиметил)-1 Н-индазол-5-ил]имидазолидин-2-она (выход 97,5%). ТФК
МПК / Метки
МПК: C07D 409/14, A61K 31/4178, C07D 403/14, A61P 35/00, C07D 417/14, C07D 403/04, C07D 407/14
Метки: производные, качестве, ингибиторов, 1,3-дизамещенные, имидазолидин-2-она
Код ссылки
<a href="https://eas.patents.su/30-21011-13-dizameshhennye-proizvodnye-imidazolidin-2-ona-v-kachestve-ingibitorov-cyp-17.html" rel="bookmark" title="База патентов Евразийского Союза">1,3-дизамещенные производные имидазолидин-2-она в качестве ингибиторов cyp 17</a>
Предыдущий патент: Способ и устройство для удаления твердых частиц и смоляного компонента из газообразного монооксида углерода
Следующий патент: Устройство для ультразвукового соединения и устройство для изготовления абсорбирующего изделия
Случайный патент: Проточный сепаратор и способ проточного разделения