Бензотиазолы, обладающие антагонистической активностью по отношению к h3-рецептору гистамина, и фармацевтические композиции, включающие эти соединения
Номер патента: 15569
Опубликовано: 31.10.2011
Авторы: Лундбекк Яне Мари, Кристенсен Инге Тогер, Хольвег Рольф, Дервальд Флоренсио Сарагоса, Андерсен Кнуд Эрик
Формула / Реферат
1. Соединение общей формулы I
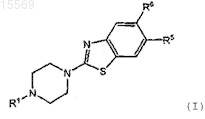
где R1означает циклопентил, циклопропил или изопропил;
R5 и R6независимо означают водород, галоген, циано, C1-6-алкокси или группу общей формулы -(СН2)s-(C=O)r-NR7R8, при условии, что R5 и R6 не могут одновременно означать водород;
r означает 0 или 1;
s означает 0 или 1 и
R7 и R8независимо означают водород, C1-6-алкил или С3-8-циклоалкил; или R7и R8 могут вместе с присоединенным атомом азота образовывать пирролидин-1-ил, морфолин-4-ил или пиперидин-1-ил;
или его диастереомер, или энантиомер, или таутомерная форма, или его фармацевтически приемлемая соль.
2. Соединение по п.1, которое представляет собой соединение, выбранное из группы, состоящей из
6-хлор-2-(4-циклопентилпиперазин-1-ил)бензотиазола,
2-(4-изопропилпиперазин-1-ил)-6-метоксибензотиазола,
2-(4-циклопропилпиперазин-1-ил)-6-метоксибензотиазола,
2-(4-изопропилпиперазин-1-ил)бензотиазол-6-карбонитрила,
[2-(4-изопропилпиперазин-1-ил)бензотиазол-6-ил]пиперидин-1-илметанона,
диметиламида 2-(4-изопропилпиперазин-1-ил)бензотиазол-6-карбоновой кислоты,
[2-(4-изопропилпиперазин-1-ил)бензотиазол-6-ил]морфолин-4-илметанона,
2-(4-изопропилпиперазин-1-ил)-6-пиперидин-1-илметилбензотиазола,
2-(4-изопропилпиперазин-1-ил)-6-(морфолин-4-илметил)бензотиазола,
[2-(4-изопропилпиперазин-1-ил)бензотиазол-6-илметил]диметиламина,
2-(4-циклопентилпиперазин-1-ил)бензотиазол-6-карбонитрила,
[2-(4-циклопропилпиперазин-1-ил)бензотиазол-6-илметил]диметиламина,
2-(4-циклопропилпиперазин-1-ил)-6-(пирролидин-1-илметил)бензотиазола,
2-(4-циклопропилпиперазин-1-ил)-6-(морфолин-4-илметил)бензотиазола,
2-(4-циклопропилпиперазин-1-ил)-6-(пиперидин-1-илметил)бензотиазола,
циклопропил-[2-(4-циклопропилпиперазин-1-ил)бензотиазол-6-илметил]амина,
2-(4-изопропилпиперазин-1-ил)бензотиазол-5-карбонитрила,
2-(4-изопропилпиперазин-1-ил)-5-пирролидин-1-илметилбензотиазола,
[2-(4-изопропилпиперазин-1-ил)бензотиазол-5-илметил]диметиламин и
[2-(4-изопропилпиперазин-1-ил)бензотиазол-5-ил]пирролидин-1-илметанона,
или его диастереомер, или энантиомер, или таутомерная форма, или его фармацевтически приемлемая соль.
3. Соединение по п.1, которое представляет собой 2-(4-циклопропилпиперазин-1-ил)-6-(пирролидин-1-илметил)бензотиазол или его фармацевтически приемлемую соль.
4. Соединение по п.1, которое представляет собой циклопропил-[2-(4-циклопропилпиперазин-1-ил)бензотиазол-6-илметил]амин или его фармацевтически приемлемую соль.
5. Соединение по п.1, которое представляет собой 2-(4-изопропилпиперазин-1-ил)-5-пирролидин-1-илметилбензотиазол или его фармацевтически приемлемую соль.
6. Фармацевтическая композиция, содержащая соединение по любому из пп.1-5 вместе с одним или несколькими фармацевтически приемлемыми носителями или эксципиентами.
Текст
Дата публикации и выдачи патента Номер заявки Дервальд Флоренсио Сарагоса,Андерсен Кнуд Эрик, Хольвег Рольф,Кристенсен Инге Тогер, Лундбекк Яне Мари (DK) Медведев В.Н. (RU) Некоторые новые бензотиазолы и бензоксазолы, например 2-(пиперазин-1-ил)бензотиазолы и 2(пиперазин-1-ил)бензоксазолы, необязательно замещенные в положениях 3 и/или 4 пиперазинового цикла, обладающие антагонистической активностью по отношению к Н 3-рецептору гистамина,которые могут быть использованы в фармацевтических композициях. БЕНЗОТИАЗОЛЫ, ОБЛАДАЮЩИЕ АНТАГОНИСТИЧЕСКОЙ АКТИВНОСТЬЮ ПО ОТНОШЕНИЮ К H3-РЕЦЕПТОРУ ГИСТАМИНА, И ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ, ВКЛЮЧАЮЩИЕ ЭТИ СОЕДИНЕНИЯ 015569 Область техники, к которой относится изобретение Настоящее изобретение относится к новым бензотиазолам и бензоксазолам, обладающим антагонистической активностью по отношению к Н 3-рецептору гистамина, применению этих соединений в фармацевтических композициях, включающим эти соединения фармацевтическим композициям и способам лечения при использовании этих соединений или композиций. Соединения согласно настоящему изобретению проявляют высокую и селективную в отношении связывания аффинность к Н 3-рецептору гистамина, означающую антагонистическую, обратную агонистическую или агонистическую активность по отношению к Н 3-рецептору гистамина. В результате, соединения являются пригодными для лечения заболеваний или нарушений, связанных с Н 3-рецептором гистамина. Предпосылки создания настоящего изобретения Существование Н 3-рецептора гистамина известно в течение нескольких лет и рецептор является актуальным в отношении получения новых лекарственных средств (см., например, Drugs Fut., 21, 507-520(1996); Progress in Drug Research, 45, 107-165 (1995. Недавно был клонирован человеческий Н 3 рецептор гистамина; см. Molecular Pharmacology, 55, 1101-1107 (1999). Н 3-Рецептор гистамина представляет собой пресинаптический авторецептор, локализованный как в центральной, так и в периферической нервной системе, коже и органах, таких как легкое, кишечник, вероятно, селезенка и желудочнокишечный тракт. Недавно полученные данные наводят на мысль, что Н 3-рецептор обладает внутренней конститутивной активностью in vitro, а также in vivo (то есть он является активным в отсутствие агониста; см, например, Nature, 408, 860-864 (2000. Соединения, действующие как обратные агонисты, могут ингибировать эту активность. Н 3-Рецептор гистамина участвует в регуляции выделения гистамина и также других нейротрансмиттеров, таких как серотонин и ацетилхолин. Поэтому предполагают, что антагонист или обратный агонист Н 3-рецептора гистамина должен повышать выделение этих нейротрансмиттеров в головном мозге. Агонист Н 3-рецептора гистамина, наоборот, приводит к ингибированию биосинтеза гистамина и ингибированию выделения гистамина и также других нейротрансмиттеров, таких как серотонин и ацетилхолин. Эти полученные данные наводят на мысль, что агонисты, обратные агонисты и антагонисты Н 3-рецептора гистамина могут быть важными медиаторами нейронной активности. Поэтому Н 3-рецептор гистамина является важной мишенью для новой клинической медицины. В некоторых публикациях раскрывается получение и применение агонистов и антагонистов Н 3 рецептора гистамина. Некоторыми из них являются производные имидазола (см., например, Drugs Fut.,21, 507-520 (1996); Expert Opinion on Therapeutic Patents, 10, 1045-1055 (2000. Однако также описано множество не содержащих имидазол лигандов Н 3-рецептора гистамина (см., например, Arch. Pharm.Chem., 331, 395-404 (1998); Il Farmaco, 54, 684-694 (1999); WO 99/42458; EP 0978512; WO 97/17345; US 6316475; WO 01/66534; WO 01/74810; WO 01/44191; WO 01/74815; WO 01/74773; WO 01/74813; WO 01/74814 и WO 02/12190). Уровень техники также рассматривается в Drug Discovery Today, 10, 1613-1617(2005); Nat. Rev. Drug Discov., 4, 107 (2005). Принимая во внимание интерес в области техники к агонистам, обратным агонистам и антагонистам Н 3-рецептора гистамина, новые соединения, которые взаимодействуют с Н 3-рецептором гистамина, должны быть очень желательным вкладом в уровень техники. Согласно настоящему изобретению предусматривается такой вклад в уровень техники на основании обнаружения того, что новый класс замещенных бензотиазолов и бензоксазолов обладает высокой и специфической аффинностью и эффективностью по отношению к Н 3-рецептору гистамина. Вследствие их взаимодействия с Н 3-рецептором гистамина, соединения согласно настоящему изобретению пригодны для лечения широкого ряда состояний и нарушений, в случае которых взаимодействие с Н 3-рецептором гистамина оказывает благоприятное воздействие. Таким образом, соединения могут находить применение, например, при лечении заболеваний центральной нервной системы, периферической нервной системы, сердечно-сосудистой системы, легочной системы, желудочно-кишечной системы и эндокринной системы. В патенте США 6130217, колонка 120, пример 85 указывается промежуточный продукт 2-(4 метилпиперазин-1-ил)бензотиазол-7-ол. Никакие фармакологические свойства для этого соединения не указываются. В патенте Японии 11199573 указываются следующие соединения: 2-(пиперазин-1-ил)-6 хлорбензотиазолфумарат; 2-(пиперазин-1-ил)-5-хлорбензотиазолфумарат; 2-(4-метилпиперазин-1-ил)-5 метилбензотиазолфумарат; 2-(пиперазин-1-ил)-5-метилбензотиазолфумарат; 2-(4-метилпиперазин-1-ил)6-хлорбензотиазолфумарат и 2-(4-метилпиперазин-1-ил)-5-хлорбензотиазолдигидрохлорид. В патенте Японии 2869561 указываются следующие соединения: 2-(пиперазин-1-ил)-6 хлорбензотиазол и 2-(пиперазин-1-ил)-6-(о-хлорбензиламино)бензотиазолгидрохлорид. Установлено, что соединения являются ингибиторами адгезии тромбоцитов. В патенте Японии 4316565 указываются следующие соединения: 2-(4-метилпиперазин-1-ил)-6 метоксибензотиазол и 2-(4-метилпиперазин-1-ил)-6-гидроксибензотиазол. Никакие фармакологические свойства для этих соединений не указываются. Объектом настоящего изобретения является преодоление или улучшение в отношении уменьшения по меньшей мере одного из недостатков известного уровня техники или обеспечение пригодной альтер-1 015569 нативы. Определения В структурных формулах, приведенных согласно данному описанию и на протяжении всего настоящего описания, следующие термины имеют указанное значение. Термин гидрокси означает радикал -ОН, термин окси означает радикал -О-, термин оксо означает радикал =O, термин карбонил означает радикал -С(=O)-, термин сульфинил означает радикал-(S=O)-, термин сульфонил означает радикал -S(=O)2, термин карбокси означает радикал -(C=O)O- и-С(=О)ОН, термин амино означает радикал -NH2, термин нитро означает радикал -NO2, и термин циано означает радикал -CN. Термин С 2-6-алкенил, как используется в данном описании, означает углеводородную группу с разветвленной или линейной цепью, имеющую 2-6 атомов углерода и по меньшей мере одну двойную связь, например С 2-6-алкенил, С 3-6-алкенил и т.п. Типичными примерами являются этенил (или винил),пропенил (например, проп-1-енил и проп-2-енил), бутадиенил (например, бута-1,3-диенил), бутенил (например, бут-1-ен-1-ил и бут-2-ен-1-ил), пентенил (например, пент-1-ен-1-ил и пент-2-ен-2-ил), гексенил(например, гекс-1-ен-2-ил и гекс-2-ен-1-ил), 1-этилпроп-2-енил, 1,1-(диметил)проп-2-енил, 1-этилбут-3 енил, 1,1-(диметил)бут-2-енил и т.п. Термин C1-6-алкокси, как используется в данном описании, относится к радикалу C1-6-алкил-О-. Типичными примерами являются метокси, этокси, пропокси (например, 1-пропокси и 2-пропокси), бутокси (например, 1-бутокси, 2-бутокси и 2-метил-2-пропокси), пентокси (1-пентокси и 2-пентокси), гексокси (1-гексокси и 3-гексокси) и т.п. Термин С 1-6-алкокси-С 1-6-алкил, как используется в данном описании, относится к C1-6-алкилу,замещенному C1-6-алкокси по любому атому углерода. Типичными примерами являются метоксиметил,этоксиметил, 2-метоксиэтил, 2-этоксиэтил, 3-метоксипроп-1-ил и т.п. Термин C1-6-алкоксикарбонил, как используется в данном описании, относится к радикалу C1-6 алкокси-C(=O)-. Типичными примерами являются метоксикарбонил, этоксикарбонил, 1 пропоксикарбонил,2-пропоксикарбонил,1-бутоксикарбонил,2-бутоксикарбонил,2-метил-2 пропоксикарбонил, 3-метилбутоксикарбонил, 1-гексоксикарбонил и т.п. Термин C1-6-алкил, как используется в данном описании, означает насыщенную углеводородную группу с разветвленной или линейной цепью, имеющую 1-6 атомов углерода, например C1-3-алкил, C1-4 алкил, С 2-6-алкил, С 3-6-алкил и т.п. Типичными примерами являются метил, этил, пропил (например,проп-1-ил и проп-2-ил (или изопропил, бутил (например, 2-метилпроп-2-ил (или трет-бутил), бут-1-ил и бут-2-ил), пентил (например, пент-1-ил, пент-2-ил и пент-3-ил), 2-метилбут-1-ил, 3-метилбут-1-ил, гексил (например, гекс-1-ил), гептил (например, гепт-1-ил) и т.п. Аналогично, термин C1-3-алкил, как используется в данном описании, означает насыщенную углеводородную группу с разветвленной или линейной цепью, имеющую 1-3 атома углерода. Типичными примерами являются метил, этил, пропил (например, проп-1-ил и проп-2-ил (или изопропил и т.п. Термин C1-6-алкилкарбонил, как используется в данном описании, относится к радикалу C1-6 алкил-С(=O)-. Типичными примерами являются ацетил (например, метилкарбонил), пропионил (например, этилкарбонил), бутаноил (например, проп-1-илкарбонил и проп-2-илкарбонил) и т.п. Термин C1-6-алкилкарбониламино, как используется в данном описании, относится к радикалуC1-6-алкил-C(=O)-NH-. Типичными примерами являются ацетиламино, пропиониламино, пивалоиламино,валероиламино и т.п. Термин С 1-6-алкилкарбониламино-С 1-6-алкил, как используется в данном описании, относится кC1-6-алкилу, замещенному C1-6-алкилкарбониламино по любому атому углерода. Типичными примерами являются ацетиламинометил, 1-(ацетиламино)этил, пропиониламинометил и т.п. Термин C1-6-алкилкарбокси, как используется в данном описании, относится к радикалу C1-6 алкил-C(=O)O-. Типичными примерами являются метилкарбокси, этилкарбокси, пропилкарбокси (например, проп-1-илкарбокси, проп-2-илкарбокси) и т.п. Термин C1-6-алкилен, как используется в данном описании, относится к углеводородной группе с разветвленной или линейной цепью, имеющей 1-6 атомов углерода и две свободные связи. Типичными примерами являются метилен, этилен, пропилены, например 1,3-пропилен, и бутилены, например 1,4 бутилен (1,4-бутандиил) и т.п. Аналогично, термин C1-4-алкилен относится к углеводородной группе с разветвленной или линейной цепью, имеющей 1-4 атома углерода и две свободные связи. Термин C1-6-алкилсульфанил, как используется в данном описании, относится к радикалу С 1-6 алкил-S-. Типичными примерами являются метилтио, этилтио, пропилтио (например, 1-пропилтио, 2 пропилтио и 3-пропилтио), битилтио, пентилтио, гексилтио и т.п. Термин C1-6-алкилсульфинил, как используется в данном описании, относится к радикалу С 1-6 алкил-S(=O)-. Типичными примерами являются метилсульфинил, этилсульфинил, пропилсульфинил,бутилсульфинил, пентилсульфинил, гексилсульфинил и т.п.-2 015569 Термин С 1-6-алкилсульфонил, как используется в данном описании, относится к радикалу С 1-6 алкил-S(=O)2-. Типичными примерами являются метилсульфонил, этилсульфонил, пропилсульфонил,бутилсульфонил, пентилсульфонил, гексилсульфонил и т.п. Термин С 2-8-алкинил, как используется в данном описании, означает углеводородную группу с разветвленной или линейной цепью, имеющую 2-8 атомов углерода, и по меньшей мере одну тройную связь. Типичными примерами являются этинил, пропинил (например, проп-1-инил и проп-2-инил), бутинил (например, бут-1-инил и бут-2-инил), пентинил (например, пент-1-инил и пент-2-инил), гексинил(например, гекс-1-инил и гекс-2-инил), 1-этилпроп-2-инил, 1,1-(диметил)проп-2-инил, 1-этилбут-3-инил,1,1-(диметил)бут-2-инил и т.п. Подразумевается, что термин арил, как используется в данном описании, включает моноциклические, бициклические или полициклические карбоциклические ароматические циклы. Типичными примерами являются фенил, нафтил (например, нафт-1-ил и нафт-2-ил), антрил (например, антр-1-ил и антр-9 ил), фенантрил (например, фенантр-1-ил и фенантр-9-ил) и т.п. Также подразумевается, что термин арил включает моноциклические, бициклические или полициклические карбоциклические ароматические циклы, замещенные карбоциклическими ароматическими циклами. Типичными примерами являются бифенил (например, бифенил-2-ил, бифенил-3-ил и бифенил-4-ил), фенилнафтил (например, 1 фенилнафт-2-ил и 2-фенилнафт-1-ил) и т.п. Также подразумевается, что термин арил включает частично насыщенные бициклические или полициклические карбоциклы по меньшей мере с одним ненасыщенным остатком (например, бензогруппа). Типичными примерами являются инданил (например, индан 1-ил, индан-5-ил), инденил (например, инден-1-ил и инден-5-ил), 1,2,3,4-тетрагидронафтил (например,1,2,3,4-тетрагидронафт-1-ил,1,2,3,4-тетрагидронафт-2-ил и 1,2,3,4-тетрагидронафт-6-ил),1,2 дигидронафтил (например, 1,2-дигидронафт-1-ил, 1,2-дигидронафт-4-ил и 1,2-дигидронафт-6-ил), флуоренил (например, флуорен-1-ил, флуорен-4-ил и флуорен-9-ил) и т.п. Также подразумевается, что термин арил включает частично насыщенные бициклические или полициклические ароматические карбоциклы, содержащие одну или две мостиковые связи. Типичными примерами являются бензонорборнил (например, бензонорборн-3-ил и бензонорборн-6-ил), 1,4-этано-1,2,3,4-тетрагидронафтил (например, 1,4 этано-1,2,3,4-тетрагидронафт-2-ил и 1,4-этано-1,2,3,4-тетрагидронафт-10-ил) и т.п. Также подразумевает,что термин арил включает частично насыщенные бициклические или полициклические ароматические карбоциклы, содержащие один или несколько спироатомов. Типичными примерами являются спиро[циклопентан-1,1'-индан]-4-ил, спиро[циклопентан-1,1'-инден]-4-ил, спиро[пиперидин-4,1'-индан]-1 ил, спиро[пиперидин-3,2'-индан]-1-ил, спиро[пиперидин-4,2'-индан]-1-ил, спиро[пиперидин-4,1'-индан]3'-ил, спиро[пирролидин-3,2'-индан]-1-ил, спиро[пирролидин-3,1'-(3',4'-дигидронафталин)]-1-ил, спиро[пиперидин-3,1'-(3',4'-дигидронафталин)]-1-ил,спиро[пиперидин-4,1'-(3',4'-дигидронафталин)]-1-ил,спиро[имидазолидин-4,2'-индан]-1-ил, спиро[пиперидин-4,1'-инден]-1-ил и т.п. Термин арилкарбонил, как используется в данном описании, относится к радикалу арил-С(=О)-. Типичными примерами являются бензоил, нафтилкарбонил, 4-фенилбензоил, антрилкарбонил, фенантрилкарбонил и т.п. Термин арилкарбониламино, как используется в данном описании, относится к радикалу арилС(=O)-NH-. Типичными примерами являются бензоиламино, нафтилкарбониламино, 4-фенилбензоиламино и т.п. Термин арилкарбониламино-С 1-6-алкил, как используется в данном описании, относится к С 1-6 алкилу, замещенному арилкарбониламино по любому атому углерода. Типичными примерами являются бензоиламинометил, нафтилкарбониламинометил, 2-(4-фенилбензоиламино)этил и т.п. Термин циано-С 1-6-алкил, как используется в данном описании, относится к C1-6-алкилу, замещенному циано по любому(ым) атому(ам) углерода. Типичными примерами являются цианометил, 2 цианоэтил и т.п. Термин С 5-8-циклоалкенил, как используется в данном описании, означает частично насыщенный моноциклический карбоцикл, имеющий 5-8 атомов углерода, и по меньшей мере одну двойную связь. Типичными примерами являются циклопентенил, циклогексенил, циклогептенил, циклооктенил, циклогекс-1,3-диенил и т.п. Очевидно, что термин С 5-8-циклоалкенил-С 2-6-алкенил является комбинацией C5-8-циклоалкенила и С 2-6-алкенила, как указано в данном описании. Очевидно, что термин С 5-8-циклоалкенил-С 1-6-алкил является комбинацией С 5-8-циклоалкенила иC1-6-алкила, как указано в данном описании. Очевидно, что термин С 5-8-циклоалкенил-С 2-6-алкинил является комбинацией C5-8-циклоалкенила и С 2-6-алкинила, как указано в данном описании. Термин С 3-8-циклоалкил, как используется в данном описании, означает насыщенный моноциклический карбоцикл, имеющий 3-8 атомов углерода, например С 3-6-алкил и т.п. Типичными примерами являются циклопропил, циклобутил, циклопентил, циклогексил, циклогептил, циклооктил и т.п. Подразумевается, что термин С 3-8-циклоалкил также означает насыщенный бициклический карбоцикл,имеющий 4-8 атомов углерода. Типичными примерами являются декагидронафталенил, бицик-3 015569 ло[3.3.0]октанил и т.п. Также подразумевается, что термин С 3-8-циклоалкил означает насыщенный карбоцикл, имеющий 3-8 атомов углерода и содержащий одну или две углеродные мостиковые связи. Типичными примерами являются адамантил, норборнанил, нортрициклил, бицикло[3.2.1]октанил, бицикло[2.2.2]октанил, трицикло[5.2.1.0/2,6]деканил, бицикло[2.2.1]гептил и т.п. Также подразумевается, что термин С 3-8-циклоалкил означает насыщенный карбоцикл, имеющий 3-8 атомов углерода и содержащий один или несколько спироатомов. Типичными примерами являются спиро[2.5]октанил, спиро[4.5]деканил и т.п. Очевидно, что термин С 3-8-циклоалкил-С 2-6-алкенил является комбинацией С 3-8-циклоалкила и С 2-6-алкенила, как указано в данном описании. Очевидно, что термин С 3-8-циклоалкил-С 1-6-алкил является комбинацией С 3-8-циклоалкила и C1-6 алкила. Типичными примерами являются циклопропилметил, 2-циклогексилэтил, 3-циклопентилпроп-1 ил, 1-циклогексилэтил, адамантилметил и т.п. В случае этого заместителя нециклическая алкильная группа предпочтительно имеет не более чем 3 атома углерода. Очевидно, что термин С 3-8-циклоалкил-С 2-6-алкинил является комбинацией С 3-8-циклоалкила и С 2-6-алкинила, как указано в данном описании. Очевидно, что термин ди(С 3-8-циклоалкил)-C1-6-алкил является комбинацией двух С 3-8 циклоалкильных групп и одной C1-6-алкильной группы, как указано в данном описании. Термин галоген-С 1-6-алкил, как используется в данном описании, относится к C1-6-алкилу, замещенному один или более раз любым атомом галогена по любому(ым) атому(ам) углерода. Типичными примерами являются трифторметил, 2,2,2-трифторэтил и т.п. Термин галоген-С 1-6-алкокси, как используется в данном описании, относится к C1-6-алкокси, замещенному один или более раз любым атомом галогена по любому(ым) атому(ам) углерода. Типичными примерами являются трифторметокси и 2,2,2-трифторэтокси и т.п. Термин галоген или гало означает фтор, хлор, бром или иод. Подразумевается, что термин гетероарил, как используется в данном описании, включает моноциклические гетероциклические ароматические циклы, содержащие один или несколько гетероатомов,выбираемых из группы, состоящей из азота, кислорода, серы, SO и S(=O)2. Типичными примерами являются пирролил (например, пиррол-1-ил, пиррол-2-ил и пиррол-3-ил), фуранил (например, фуран-2-ил и фуран-3-ил), тиенил (например, тиен-2-ил и тиен-3-ил), оксазолил (например, оксазол-2-ил, оксазол-4-ил и оксазол-5-ил), тиазолил (например, тиазол-2-ил, тиазол-4-ил и тиазол-5-ил), имидазолил (например,имидазол-2-ил, имидазол-4-ил и имидазол-5-ил), пиразолил (например, пиразол-1-ил, пиразол-3-ил и пиразол-5-ил), изоксазолил (например, изоксазол-3-ил, изоксазол-4-ил и изоксазол-5-ил), изотиазолил (например, изотиазол-3-ил, изотиазол-4-ил и изотиазол-5-ил), 1,2,3-триазолил (например, 1,2,3-триазол-1-ил,1,2,3-триазол-4-ил и 1,2,3-триазол-5-ил), 1,2,4-триазолил (например, 1,2,4-триазол-1-ил, 1,2,4-триазол-3 ил и 1,2,4-триазол-5-ил), 1,2,3-оксадиазолил (например, 1,2,3-оксадиазол-4-ил и 1,2,3-оксадиазол-5-ил),1,2,4-оксадиазолил (например, 1,2,4-оксадиазол-3-ил и 1,2,4-оксадиазол-5-ил), 1,2,5-оксадиазолил (например, 1,2,5-оксадиазол-3-ил и 1,2,5-оксадиазол-4-ил), 1,3,4-оксадиазолил (например, 1,3,4-оксадиазол 2-ил и 1,3,4-оксадиазол-5-ил), 1,2,3-тиадиазолил (например, 1,2,3-тиадиазол-4-ил и 1,2,3-тиадиазол-5-ил),1,2,4-тиадиазолил (например, 1,2,4-тиадиазол-3-ил и 1,2,4-тиадиазол-5-ил), 1,2,5-тиадиазолил (например,1,2,5-тиадиазол-3-ил и 1,2,5-тиадиазол-4-ил), 1,3,4-тиадиазолил (например, 1,3,4-тиадиазол-2-ил и 1,3,4 тиадиазол-5-ил), тетразолил (например, тетразол-1-ил и тетразол-5-ил), пиранил (например, пиран-2-ил),пиридинил (например, пиридин-2-ил, пиридин-3-ил и пиридин-4-ил), пиридазинил (например, пиридазин-2-ил и пиридазин-3-ил), пиримидинил (например, пиримидин-2-ил, пиримидин-4-ил и пиримидин-5 ил), пиразинил, 1,2,3-триазинил, 1,2,4-триазинил, 1,3,5-триазинил, тиадиазинил, азепинил, азецинил и т.п. Также подразумевается, что термин гетероарил включает бициклические гетероциклические ароматические циклы, содержащие один или несколько гетероатомов, выбираемых из группы, состоящей из азота, кислорода, серы, S(=O) и S(=O)2. Типичными примерами являются индолил (например, индол-1 ил, индол-2-ил, индол-3-ил и индол-5-ил), изоиндолил, бензофуранил (например, бензо[b]фуран-2-ил,бензо[b]фуран-3-ил, бензо[b]фуран-5-ил, бензо[с]фуран-2-ил, бензо[с]фуран-3-ил и бензо[с]фуран-5-ил),бензотиенил (например, бензо[b]тиен-2-ил, бензо[b]тиен-3-ил, бензо[b]тиен-5-ил, бензо[с]тиен-2-ил, бензо[с]тиен-3-ил и бензо[с]тиен-5-ил), индазолил (например, индазол-1-ил, индазол-3-ил и индазол-5-ил),индолизинил (например, индолизин-1-ил и индолизин-3-ил), бензопиранил (например, бензо[b]пиран-3 ил, бензо[b]пиран-6-ил, бензо[с]пиран-1-ил и бензо[с]пиран-7-ил), бензимидазолил (например, бензимидазол-1-ил, бензимидазол-2-ил и бензимидазол-5-ил), бензотиазолил (например, бензотиазол-2-ил и бензотиазол-5-ил), бензизотиазолил, бензоксазолил, бензизоксазолил, бензоксазинил, бензотриазолил, нафтиридинил (например, 1,8-нафтиридин-2-ил, 1,7-нафтиридин-2-ил и 1,6-нафтиридин-2-ил), фталазинил[2,3-b]пиридинил, фуро[2,3-с]пиридинил и фуро[3,2-c]пиридинил), тиенопиридинил (например, тиено[2,3-b]пиридинил, тиено[2,3-c]пиридинил и тиено[3,2-с]пиридинил), имидазопиридинил (например,имидазо[4,5-b]пиридинил, имидазо[4,5-c]пиридинил, имидазо[1,5-а]пиридинил и имидазо[1,2 а]пиридинил), имидазопиримидинил (например, имидазо[1,2-а]пиримидинил и имидазо[3,4-а]пиримидинил), пиразолопиридинил (например, пиразоло[3,4-b]пиридинил, пиразоло[3,4-c]пиридинил и пиразоло[1,5-а]пиридинил), пиразолопиримидинил (например, пиразоло[1,5-а]пиримидинил и пиразоло[3,4d]пиримидинил), тиазолопиридинил (например, тиазоло[3,2-d]пиридинил), тиазолопиримидинил (например, тиазоло[5,4-d]пиримидинил), имидазотиазолил (например, имидазо[2,1-b]тиазолил), триазолопиридинил (например, триазоло[4,5-b]пиридинил), триазолопиримидинил (например, 8-азапуринил) и т.п. Также подразумевается, что термин гетероарил включает полициклические гетероциклические ароматические циклы, содержащие один или несколько гетероатомов, выбираемых из группы, состоящей из азота, кислорода, серы, S(=O) и S(=O)2. Типичными примерами являются карбазолил (например, карбазол-2-ил, карбазол-3-ил, карбазол-9-ил), феноксазинил (например, феноксазин-10-ил), феназинил (например, феназин-5-ил), акридинил (например, акридин-9-ил и акридин-10-ил), фенолтиазинил (например, фенотиазин-10-ил), карболинил (например, пиридо[3,4-b]индол-1-ил, пиридо[3,4-b]индол-3-ил), фенантролинил (например, фенантролин-5-ил) и т.п. Также подразумевается, что термин гетероарил включает частично насыщенные моноциклические, бициклические или полициклических гетероциклы,содержащие один или несколько гетероатомов, выбираемых из группы, состоящей из азота, кислорода,серы, S(=O) и S(=O)2. Типичными примерами являются пирролинил, пиразолинил, имидазолинил (например, 4,5-дигидроимидазол-2-ил и 4,5-дигидроимидазол-1-ил), индолинил (например, 2,3-дигидроиндол-1-ил и 2,3-дигидроиндол-5-ил), дигидробензофуранил (например, 2,3-дигидробензо[b]фуран-2-ил и 2,3-дигидробензо[b]фуран-4-ил), дигидробензотиенил (например, 2,3-дигидробензо[b]тиен-2-ил и 2,3 дигидробензо[b]тиен-5-ил), 4,5,6,7-тетрагидробензо[b]фуран-5-ил), дигидробензопиранил (например, 3,4 дигидробензо[b]пиран-3-ил, 3,4-дигидробензо[b]пиран-6-ил, 3,4-дигидробензо[с]пиран-1-ил и дигидробензо[с]пиран-7-ил), 2,3-дигидробензо[1,4]диоксин-6-ил, 2,3-дигидробензо[1,4]диоксин-5-ил, 2,3 дигидробензо[1,4]диоксин-2-ил, бензо[1,3]диоксол-4-ил, бензо[1,3]диоксол-5-ил, бензо[1,3]диоксол-2-ил; 3,4-дигидро-2H-бензо[1,4]оксазин-7-ил, 4-метил-3,4-дигидро-2H-бензо[1,4]оксазин-7-ил, оксазолинил(например, 1,2,3,4-тетрагидрохиноксалинил и 5,6,7,8-тетрагидрохиноксалинил) и т.п. Также подразумевается, что термин гетероарил включает частично насыщенные бициклические или полициклические гетероциклы, содержащие один или несколько спироатомов. Типичными примерами являются спиро[изохинолин-3,1'-циклогексан]-1-ил, спиро[пиперидин-4,1'-бензо[с]тиофен]-1-ил, спиро[пиперидин 4,1'-бензо[с]фуран]-1-ил, спиро[пиперидин-4,3'-бензо[b]фуран]-1-ил, спиро[пиперидин-4,3'-кумарин]-1 ил и т.п. Термин гетероарилкарбонил, как используется в данном описании, относится к радикалу гетероарил-C(=O)-. Типичными примерами являются пиридинилкарбонил (например, пиридин-2-илкарбонил и пиридин-4-илкарбонил), хинолинилкарбонил (например, 2-(хинолин-2-ил)карбонил и 1-(хинолин-2 ил)карбонил), имидазолилкарбонил (например, имидазол-2-илкарбонил и имидазол-5-илкарбонил) и т.п. Термин гетероарилкарбониламино, как используется в данном описании, относится к радикалу гетероарил-C(=O)-NH-. Типичными примерами являются пиридинилкарбониламино (например, пиридин-2-илкарбониламино и пиридин-4-илкарбониламино), хинолинилкарбониламино (например, 2(хинолин-2-ил)карбониламино и 1-(хинолин-2-ил)карбониламино) и т.п. Термин гетероарилкарбониламино-С 1-6-алкил, как используется в данном описании, относится кC1-6-алкилу, замещенному гетероарилкарбониламино по любому атому углерода. Типичными примерами являются пиридинилкарбониламинометил (например, пиридин-2-илкарбониламинометил и пиридин-4 илкарбониламинометил), 2-(хинолинилкарбониламино)этил (например, 2-(2-(хинолин-2-ил)карбониламино)этил и 2-(1-(хинолин-2-ил)карбониламино)этил) и т.п. Термин гетероциклил, как используется в данном описании, означает насыщенный 3-8-членный моноцикл, содержащий один или несколько гетероатомов, выбираемых из группы, состоящей из азота,кислорода, серы, S(=O) и S(=O)2. Типичными примерами являются азиридинил (например, азиридин-1 ил), азетидинил (например, азетидин-1-ил и азетидин-3-ил), оксетанил, пирролидинил (например, пирролидин-1-ил, пирролидин-2-ил и пирролидин-3-ил), имидазолидинил (например, имидазолидин-1-ил,имидазолидин-2-ил и имидазолидин-4-ил), оксазолидинил (например, оксазолидин-2-ил, оксазолидин-3-5 015569 ил и оксазолидин-4-ил), тиазолидинил (например, тиазолидин-2-ил, тиазолидин-3-ил и тиазолидин-4-ил),изотиазолидинил, 1,1-диоксоизотиазолидин-2-ил, пиперидинил (например, пиперидин-1-ил, пиперидин 2-ил, пиперидин-3-ил и пиперидин-4-ил), гомопиперидинил (например, гомопиперидин-1-ил, гомопиперидин-2-ил, гомопиперидин-3-ил и гомопиперидин-4-ил), пиперазинил (например, пиперазин-1-ил и пиперазин-2-ил), морфолинил (например, морфолин-2-ил, морфолин-3-ил и морфолин-4-ил), тиоморфолинил (например, тиоморфолин-2-ил, тиоморфолин-3-ил и тиоморфолин-4-ил), 1-оксотиоморфолинил, 1,1 диоксотиоморфолинил, тетрагидрофуранил (например, тетрагидрофуран-2-ил и тетрагидрофуран-3-ил),тетрагидротиенил, тетрагидро-1,1-диоксотиенил, тетрагидропиранил (например, 2-тетрагидропиранил),тетрагидротиопиранил (например, 2-тетрагидротиопиранил), 1,4-диоксанил, 1,3-диоксанил и т.п. Также подразумевается, что термин гетероциклил означает насыщенный 6-12-членный бицикл, содержащий один или несколько гетероатомов, выбираемых из группы, состоящей из азота, кислорода, серы, S(=O) иS(=O)2. Типичными примерами являются октагидроиндолил (например, октагидроиндол-1-ил, октагидроиндол-2-ил, октагидроиндол-3-ил и октагидроиндол-5-ил), декагидрохинолинил (например, декагидрохинолин-1-ил, декагидрохинолин-2-ил, декагидрохинолин-3-ил, декагидрохинолин-4-ил и декагидрохинолин-6-ил), декагидрохиноксалинил (например, декагидрохиноксалин-1-ил, декагидрохиноксалин-2 ил и декагидрохиноксалин-6-ил) и т.п. Также подразумевается, что термин гетероциклил означает насыщенный 6-12-членный цикл, содержащий один или несколько гетероатомов, выбираемых из группы,состоящей из азота, кислорода, серы, S(=O) и S(=O)2 и имеющий одну или две мостиковые связи. Типичными примерами являются 3-азабицикло[3.2.2]нонил,2-азабицикло[2.2.1]гептил,3-азабицикло[3.1.0]гексил, 2,5-диазабицикло[2.2.1]гептил, атропинил, тропинил, хинуклидинил, 1,4 диазабицикло[2.2.2]октанил и т.п. Также подразумевается, что термин гетероциклил означает насыщенный 6-12-членному цикл, содержащий один или несколько гетероатомов, выбираемых из группы,состоящей из азота, кислорода, серы, S(=O) и S(=O)2 и содержащий один или несколько спироатомов. Типичными примерами являются 1,4-диоксаспиро[4.5]деканил (например, 1,4-диоксаспиро[4.5]декан-2 ил и 1,4-диоксаспиро[4.5]декан-7-ил), 1,4-диокса-8-азаспиро[4.5]деканил (например, 1,4-диокса-8 азаспиро[4.5]декан-2-ил и 1,4-диокса-8-азаспиро[4.5]декан-8-ил), 8-азаспиро[4.5]деканил (например, 8 азаспиро[4.5]декан-1-ил и 8-азаслиро[4.5]декан-8-ил), 2-азаспиро[5.5]ундеканил (например, 2 азаспиро[5.5]ундекан-2-ил), 2,8-диазаспиро[4.5]деканил (например, 2,8-диазаспиро[4.5]декан-2-ил и 2,8 диазаспиро[4.5]декан-8-ил), 2,8-диазаспиро[5.5]ундеканил (например, 2,8-диазаспиро[5.5]ундекан-2-ил),1,3,8-триазаспиро[4.5]деканил (например, 1,3,8-триазаспиро[4.5]декан-1-ил и 1,3,8-триазаспиро[4.5]декан-3-ил, 1,3,8-триазаспиро[4.5]декан-8-ил) и т.п. Термин гетероциклил-С 1-6-алкокси, как используется в данном описании, относится к радикалу гетероциклил-С 1-6-алкокси. Типичными примерами являются пиперидин-1-илметокси, 2-(пиперидин-1 ил)этокси, 3-(пиперидин-1-ил)проп-3-окси, пиперазин-1-илметокси, 2-(пиперазин-1-ил)этокси, 3(пиперазин-1-ил)проп-3-окси, морфолин-1-илметокси, 2-(морфолин-1-ил)этокси, 3-(морфолин-1 ил)проп-3-окси и т.п. Термин гетероциклил-С 1-6-алкил, как используется в данном описании, относится к радикалу гетероциклил-С 1-6-алкилу. Типичными примерами являются пиперидин-1-илметил, 2-(пиперидин-1-ил) этил, 3-гидрокси-3-(пиперидин-1-ил)пропил, пиперазин-1-илметил, 2-(пиперазин-1-ил)этил, 3-гидрокси 3-(пиперазин-1-ил)пропил, морфолин-1-илметил, 2-(морфолин-1-ил)этил, 3-гидрокси-3-(морфолин-1 ил)пропил и т.п. Термин гетероциклилкарбонил, как используется в данном описании, относится к радикалу гетероциклил-C(=O)-. Типичными примерами являются пиперидинилкарбонил (например, пиперидин-2 илкарбонил, пиперидин-3-илкарбонил и пиперидин-4-илкарбонил), пиперазинилкарбонил (например,пиперазин-1-илкарбонил и пиперазин-2-илкарбонил) и т.п. Термин гидрокси-С 1-6-алкил, как используется в данном описании, относится к C1-6-алкилу, замещенному один или более раз гидроксилом по любому(ым) атому(ам) углерода. Типичными примерами являются гидроксиметил, гидроксиэтил (например, 1-гидроксиэтил и 2-гидроксиэтил) и т.п. Термин мостиковая связь, как используется в данном описании, означает связь в насыщенном или частично насыщенном цикле между двумя атомами такого цикла, которые не являются соседними, через цепь из 1-4 атомов, выбираемых из углерода, азота, кислорода и серы. Типичными примерами таких связывающих цепей являются -СН 2-, -СН 2 СН 2-, -CH2NHCH2-, -СН 2 СН 2 СН 2-, -СН 2 ОСН 2- и т.п. Термин спироатом, как используется в данном описании, означает атом углерода в насыщенном или частично насыщенном цикле, который связывает оба конца цепи из 3-8 атомов, выбираемых из углерода, азота, кислорода и серы. Типичными примерами являются -(СН 2)5-, -(СН 2)3-, -(СН 2)4-,-CH2NHCH2CH2-, -CH2CH2NHCH2CH2-, -CH2NHCH2CH2CH2-, -СН 2 СН 2 ОСН 2-, -ОСН 2 СН 2 О- и т.п. Термин необязательно замещенный, как используется в данном описании, означает, что рассматриваемые группы являются или незамещенными, или замещенными одним или несколькими определенными заместителями. Когда рассматриваемая(ые) группа(ы) замещены более чем одним заместителем,заместители могут быть одинаковыми или различными. Некоторые из указанных терминов могут встречаться более чем один раз в структурых формулах, и-6 015569 в этих случаях каждый термин может быть определен независимо от другого. Некоторые из указанных терминов могут встречаться в сочетаниях, и должно быть понятно, что первый указанный радикал является заместителем у указанного впоследствии радикала, где место замещения, т.е. место присоединения к другой части молекулы, находится у указанного последним из радикалов. Термин сольват, как используется в данном описании, представляет собой комплекс определенной стехиометрии, образующийся из растворенного вещества (в данном случае, соединение согласно настоящему изобретению) и растворителя. Растворители являются таковыми, обычно используемыми в области фармации, как, например, вода, этанол, уксусная кислота и т.п. Термин гидрат относится к комплексу, где молекулой растворителя является вода. Термин лечение, как используется в данном описании, означает оказание помощи и уход за пациентом в целях борьбы с заболеванием, нарушением или состоянием. Подразумевается, что термин включает замедление прогрессирования заболевания, нарушения или состояния, облегчение или ослабление симптомов и осложнений заболевания, и/или курс лечения или ликвидацию заболевания, нарушения или состояния. Подвергаемым лечению пациентом является предпочтительно млекопитающее, в частности человек. Термины заболевание, состояние и нарушение, как используется в данном описании, используют взаимозаменяемо для указания состояния пациента, которое не является нормальным физиологическим состоянием человека. Термин лекарственное средство, как используется в данном описании, означает фармацевтическую композицию, пригодную для введения фармацевтически активного соединения пациенту. Термин пролекарство, как используется в данном описании, включает биогидролизуемые амиды и биогидролизуемые сложные эфиры и также включает а) соединения, в случае которых биогидролизуемая функциональная группа в таком пролекарстве включена в соединение согласно настоящему изобретению, и b) соединения, которые могут быть биологически окислены или восстановлены по данной функциональной группе с получением лекарственных веществ согласно настоящему изобретению. Примеры таких функциональных групп включают 1,4-дигидропиридин, N-алкилкарбонил-1,4-дигидропиридин,1,4-циклогексадиен, трет-бутил и т.п. Термин биогидролизуемый сложный эфир, как используется в данном описании, означает сложный эфир лекарственного вещества (согласно данному изобретению соединения формулы (I, который или а) не интерферирует с биологической активностью исходного вещества, а придает этому веществу предпочтительные свойства in vivo, такие как длительность действия, начало действия и т.п., или b) является биологически неактивным, но легко превращается in vivo у субъекта в биологически активное действующее начало. Преимуществом является, например, то, что биогидролизуемый сложный эфир,введенный перорально, абсорбируется из пищеварительного канала и превращается в соединение (I) в плазме. Многочисленные примеры таких сложных эфиров известны в уровне техники и включают, например, низшие алкильные сложные эфиры (например, C1-4-алкильные сложные эфиры), низшие ацилоксиалкильные сложные эфиры, низшие алкоксиацилоксиалкильные сложные эфиры, сложные алкоксиацилоксиэфиры, алкилациламиноалкильные сложные эфиры и сложные эфиры холина. Термин биогидролизуемый амид, как используется в данном описании, означает амид лекарственного вещества (согласно данному изобретению, соединения общей формулы (I, который или а) не интерферирует с биологической активностью исходного вещества, а придает этому веществу предпочтительные свойства in vivo, такие как длительность действия, начало действия и т.п., или b) является биологически неактивным, но легко превращается in vivo у субъекта в биологически активное действующее начало. Преимуществом является, например, то, что биогидролизуемый амид, введенный перорально,абсорбируется из пищеварительного канала и превращается в соединение (I) в плазме. Многочисленные примеры таких амидов известны в уровне техники и включают, например, низшие алкиламиды, амиды-аминокислот, алкоксиациламиды и алкиламиноалкилкарбониламиды. Термин фармацевтически приемлемый, как используется в данном описании, означает пригодный для обычных фармацевтических применений, то есть не дающий увеличения неблагоприятных результатов для пациента, и т.д. Термин эффективное количество, как используется в данном описании, означает дозу, которая является достаточной, чтобы быть эффективной в случае лечения пациента, по сравнению с отсутствием лечения. Термин терапевтически эффективное количество соединения, как используется в данном описании, означает количество, достаточное для курса лечения, облегчения или частичного подавления клинических проявлений данного заболевания и его осложнений. Адекватное для достижения этого количество определяют как терапевтически эффективное количество. Эффективные количества для каждой цели зависят от тяжести заболевания или повреждения, а также от веса тела и общего состояния субъекта. Должно быть понятно, что определение соответствующей дозировки может быть достигнуто, используя рутинное экспериментирование, путем конструирования матрицы значений и тестирования различных точек матрицы, что полностью находится в компетенции дипломированного врача или ветеринара.-7 015569 Термин метаболит, как используется в данном описании, является любым промежуточным продуктом или продуктом, получаемым в результате метаболизма. Термин метаболизм, как используется в данном описании, относится к биопревращению лекарственного вещества (согласно данному изобретению соединения общей формулы I), вводимого пациенту. Типичные примеры, указанные выше, являются конкретными воплощениями данного изобретения. Краткое изложение сущности изобретения Данное изобретение относится к соединениям общей формулы (I) Соединения согласно данному изобретению структурно отличаются от известных соединений. Данное изобретение также относится к применению вышеуказанных соединений в терапии и, в особенности, к фармацевтическим композициям, включающим вышеуказанные соединения. В другом воплощении данное изобретение относится к способам лечения, способу, включающему введение субъекту, нуждающемуся в этом, эффективного количества одного или нескольких соединений формулы (I). В еще одном дальнейшем воплощении данное изобретение относится к применению соединений формулы (I) для получения лекарственных средств. Описание предпочтительных воплощений Вследствие их взаимодействия с Н 3-рецептором гистамина, соединения согласно данному изобретению, как описывается в нижеприведенной формуле изобретения и где-либо еще в данном описании,пригодны для лечения широкого ряда состояний и нарушений, при которых взаимодействие с Н 3 рецептором гистамина оказывает благоприятное воздействие. Таким образом, соединения могут находить применение, например, при лечении заболеваний центральной нервной системы, периферической нервной системы, сердечно-сосудистой системы, системы легких, желудочно-кишечной системы и эндокринной системы. В дальнейшем указываются различные индивидуальные воплощения и признаки данного изобретения, и эти отдельные воплощения и признаки могут быть комбинированы любым соответствующим образом и/илиa) R1 означает циклопентил, циклопропил или изопропил,с) R2 означает водород,f) R3 означает водород,h) R4 означает водород,j) R5 означает хлор, циано, N,N-диметиламинокарбонил, N,N-диметиламинометил, метокси,k) R5 означает галоген, циано, C1-6-алкокси или группу общей формулы -Y-(CH2)s-(C=O)r-NR7R8, где 7 8R , R , r, s и Y, каждый, имеет значение, указанное в данном описании,m) R5 означает водород,n) R5 не означает водород,о) R6 означает хлор, циано, N,N-диметиламинокарбонил, N,N-диметиламинометил, метокси,р) R6 означает галоген, циано, C1-6-алкокси или группу общей формулы -Y-(CH2)s-(C=O)r-NR7R8, где 7 8R , R , r, s и Y, каждый, имеет значение, указанное в данном описании,r) R6 означает водород,s) R6 не означает водород,t) по меньшей мере два из символов R3, R4, R5 и R6 являются отличными от водорода,u) R7 означает метил,v) R7 означает С 1-6-алкил,w) R8 означает метил,х) R8 означает C1-6-алкил,cc) m означает 1,ее) r означает 0 или 1,ff) s означает 0 или 1. Комбинирование вышеуказанных индивидуальных воплощений приводит к дальнейшим воплощениям, и настоящее изобретение относится ко всем возможным комбинациям вышеуказанных индивидуальных воплощений и ко всем возможным комбинациям с нижеприведенными индивидуальными притязаниями. Для квалифицированного специалиста в данной области очевидно, какие из этих воплощений не могут быть комбинированы.-8 015569 Примерами конкретных соединений формулы (I) являются 6-хлор-2-(4-циклопентилпиперазин-1-ил)бензотиазол,2-(4-изопропилпиперазин-1-ил)-6-метоксибензотиазол,2-(4-циклопропилпиперазин-1-ил)-6-метоксибензотиазол,2-(4-изопропилпиперазин-1-ил)бензотиазол-6-карбонитрил,[2-(4-изопропилпиперазин-1-ил)бензотиазол-6-ил]пиперидин-1-илметанон,диметиламида 2-(4-изопропилпиперазин-1-ил)бензотиазол-6-карбоновая кислота,[2-(4-изопропилпиперазин-1-ил)бензотиазол-6-ил]морфолин-4-илметанон,2-(4-изопропилпиперазин-1-ил)-6-пиперидин-1-илметилбензотиазол,2-(4-изопропилпиперазин-1-ил)-6-(морфолин-4-илметил)бензотиазол,[2-(4-изопропилпиперазин-1-ил)бензотиазол-6-илметил]диметиламин,2-(4-циклопентилпиперазин-1-ил)бензотиазол-6-карбонитрил,[2-(4-циклопропилпиперазин-1-ил)бензотиазол-6-илметил]диметиламин,2-(4-циклопропилпиперазин-1-ил)-6-(пирролидин-1-илметил)бензотиазол,2-(4-циклопропилпиперазин-1-ил)-6-(морфолин-4-илметил)бензотиазол,2-(4-циклопропилпиперазин-1-ил)-6-(пиперидин-1-илметил)бензотиазол,циклопропил-[2-(4-циклопропилпиперазин-1-ил)бензотиазол-6-илметил]амин,2-(4-изопропилпиперазин-1-ил)бензотиазол-5-карбонитрил,2-(4-изопропилпиперазин-1-ил)-5-пирролидин-1-илметилбензотиазол,[2-(4-изопропилпиперазин-1-ил)бензотиазол-5-илметил]диметиламин и[2-(4-изопропилпиперазин-1-ил)бензотиазол-5-ил]пирролидин-1-ил-метанон. В одном аспекте данное изобретение конкретно относится к каждому из этих соединений отдельно. В другом аспекте данное изобретение конкретно относится к фармацевтически приемлемой соли каждого из этих соединений отдельно, более конкретно к конкретным солям, указанным в конкретных примерах, приводимых ниже. В одном воплощении данного изобретения все, за исключением 4, предпочтительно все, за исключением 3, более предпочтительно все, за исключением 2, и наиболее предпочтительно все, за исключением 1, из символов, указанных в п.1 ниже, являются символами групп или остатков, присутствующих в соединении формулы (I), указываемом индивидуально в каком-либо одном из нижеприводимых примеров, и остающийся(щиеся) символ или символы является(ются) символами, указанными в любом из индивидуальных воплощений от а) до w) включительно. Соединения согласно настоящему изобретению взаимодействуют с Н 3-рецептором гистамина и,соответственно, особенно пригодны для лечения различных заболеваний или состояний, при которых взаимодействие с Н 3-рецептором гистамина оказывает благоприятное воздействие. В одном аспекте данное изобретение относится к применению соединения формулы (I) в фармацевтической композиции. Фармацевтическая композиция согласно другому аспекту данного изобретения может содержать в качестве активного ингредиента по меньшей мере одно соединение формулы (I) вместе с одним или несколькими фармацевтически приемлемыми носителями или эксципиентами. В другом аспекте данное изобретение относится к такой фармацевтической композиции в единичной дозируемой форме, содержащей от примерно 0,05 до примерно 1000 мг, например от примерно 0,1 до примерно 500 мг, как, например, от примерно 0,5 до примерно 200 мг соединения формулы (I). В другом аспекте данное изобретение относится к применению соединения формулы (I), как описано выше, для получения фармацевтической композиции для лечения заболеваний и нарушений, при которых ингибирование Н 3-рецептора гистамина оказывает полезное действие. В другом аспекте данное изобретение относится к применению соединения формулы (I) для получения фармацевтической композиции, обладающей антагонистической активностью по отношению к Н 3 рецептору гистамина или обратной агонистической активностью по отношению к Н 3-рецептору гистамина. В другом аспекте данное изобретение относится к применению соединения формулы I для получения фармацевтической композиции для снижения массы тела. В другом аспекте данное изобретение относится к применению соединения формулы I для получения фармацевтической композиции для лечения избыточной массы тела или ожирения. В другом аспекте данное изобретение относится к применению соединения формулы I для получения фармацевтической композиции для подавления аппетита или индукции насыщения. В другом аспекте данное изобретение относится к применению соединения формулы (I) для получения фармацевтической композиции для предупреждения и/или лечения нарушений и заболеваний, связанных с избыточной массой тела или ожирением, таких как дислипидемия, коронарная болезнь сердца,заболевание желчного пузыря, остеоартрит и различные виды раковых заболеваний, такие как рак эндометрия, рак молочной железы, рак предстательной железы и рак ободочной кишки. В другом аспекте данное изобретение относится к применению соединения формулы (I) для получения фармацевтической композиции для предупреждения и/или лечения нарушений аппетита, таких как булимия или нарушения после обильного стола.-9 015569 В другом аспекте данное изобретение относится к применению соединения формулы I для получения фармацевтической композиции для лечения IGT (пониженная толерантность к глюкозе). В другом аспекте данное изобретение относится к применению соединения формулы I для получения фармацевтической композиции для лечения диабета типа 2. В другом аспекте данное изобретение относится к применению соединения формулы I для получения фармацевтической композиции для замедления или предупреждения прогрессирования от IGT к диабету типа 2. В другом аспекте данное изобретение относится к применению соединения формулы I для получения фармацевтической композиции для замедления или предупреждения прогрессирования от инсулиннезависимого диабета типа 2 к инсулинзависимому диабету типа 2. В другом аспекте данное изобретение относится к применению соединения формулы I для получения фармацевтической композиции для лечения заболеваний и нарушений, при которых стимулирование Н 3-рецептора гистамина оказывает благоприятное воздействие. В другом аспекте данное изобретение относится к применению соединения формулы I для получения фармацевтической композиции, обладающей агонистической активностью по отношению к Н 3 рецептору гистамина. В другом аспекте данное изобретение относится к применению соединения формулы I для получения фармацевтической композиции для лечения аллергического ринита, язвы или анорексии. В другом аспекте данное изобретение относится к применению соединения формулы I для получения фармацевтической композиции для лечения болезни Альцгеймера, нарколепсии, нарушений, связанных с дефицитом внимания, или пониженной инсомнии, или для регуляции сна. В другом аспекте данное изобретение относится к применению соединения формулы I для получения фармацевтической композиции для лечения нарушений дыхательных путей, таких как астма, для регуляции секреции желудочной кислоты или для лечения диареи. В другом аспекте данное изобретение относится к способу лечения нарушений или заболеваний,связанных с Н 3-рецептором гистамина, способу, включающему введение субъекту, нуждающемуся в этом, эффективного количества соединения общей формулы I, как описано выше, или фармацевтической композиции, содержащей такое соединение. В другом аспекте данное изобретение относится к способу, как описано выше, где эффективное количество соединения общей формулы I, как описано выше, находится в диапазоне от примерно 0,05 до примерно 2000 мг, предпочтительно от примерно 0,1 до примерно 1000 мг и более предпочтительно от примерно 0,5 до примерно 500 мг в сутки. В одном аспекте данное изобретение относится к соединениям, которые проявляют антагонистическую или обратную агонистическую активность по отношению к Н 3-рецептору гистамина, и которые могут быть, соответственно, пригодны для лечения широкого ряда состояний и нарушений, при которых блокада Н 3-рецептора гистамина оказывает благоприятное воздействие. В другом аспекте данное изобретение относится к способу снижения массы тела, способу, включающему введение субъекту, нуждающемуся в этом, эффективного количества соединения формулы (I),как описано выше. В другом аспекте данное изобретение относится к способу лечения избыточной массы тела или ожирения, способу, включающему введение субъекту, нуждающемуся в этом, эффективного количества соединения формулы (I). В другом аспекте данное изобретение относится к способу подавления аппетита или индукции насыщения, способу, включающему введение субъекту, нуждающемуся в этом, эффективного количества соединения формулы (I). В другом аспекте данное изобретение относится к способу предупреждения и/или лечения нарушений или заболеваний, связанных с избыточной массой тела или ожирением, таких как дислипидемия,коронарная болезнь сердца, заболевание желчного пузыря, остеоартрит и различные виды раковых заболеваний, например рак эндометрия, рак молочной железы, рак предстательной железы и рак ободочной кишки, способу, включающему введение субъекту, нуждающемуся в этом, эффективного количества соединения формулы (I). В другом аспекте данное изобретение относится к способу предупреждения и/или лечения нарушений аппетита, таких как булимия и нарушения после обильного стола, способу, включающему введение субъекту, нуждающемуся в этом, эффективного количества соединения формулы (I). В другом аспекте данное изобретение относится к способу лечения IGT (пониженная толерантность к глюкозе), способу, включающему введение субъекту, нуждающемуся в этом, эффективного количества соединения формулы (I). В другом аспекте данное изобретение относится к способу лечения диабета типа 2, способу, включающему введение субъекту, нуждающемуся в этом, эффективного количества соединения формулы (I). В другом аспекте данное изобретение относится к способу замедления или предупреждения прогрессирования от IGT к диабету типа 2, способу, включающему введение субъекту, нуждающемуся в этом, эффективного количества соединения формулы (I).- 10015569 В другом аспекте данное изобретение относится к способу замедления или предупреждения прогрессирования от инсулиннезависимого диабета типа 2 к инсулинзависимому диабету типа 2, способу,включающему введение субъекту, нуждающемуся в этом, эффективного количества соединения формулы (I). В другом аспекте данное изобретение относится к соединениям, которые проявляют агонистическую активность по отношению к Н 3-рецептору гистамина и которые могут быть, соответственно, пригодны для лечения широкого ряда состояний и нарушений, при которых активирование Н 3-рецептора гистамина оказывает благоприятное воздействие. Соединения согласно настоящему изобретению также можно применять для лечения нарушений дыхательных путей (таких как астма), в качестве противодиарейных средств и для модуляции секреции желудочной кислоты. Кроме того, соединения согласно настоящему изобретению можно применять для лечения заболеваний, связанных с регуляцией сна и инсомнии, и для лечения нарколепсии и нарушений, связанных с дефицитом внимания. Кроме того, соединения согласно данному изобретению могут быть использованы в качестве стимуляторов центральной нервной системы или в качестве седативных средств. Соединения согласно настоящему изобретению также могут быть использованы для лечения состояний, связанных с эпилепсией. Сверх того, соединения согласно данному изобретению могут быть использованы для лечения морской болезни и головокружения. Кроме того, они могут быть пригодны в качестве регуляторов гипоталамо-гипофизарной секреции, в качестве антидепрессантов, в качестве модуляторов мозгового кровообращения и при лечении синдрома раздраженной толстой кишки. Далее, соединения согласно настоящему изобретению могут быть использованы для лечения деменции и болезни Альцгеймера. Соединения согласно настоящему изобретению также могут быть пригодны для лечения аллергического ринита, язвы или анорексии. Соединения согласно настоящему изобретению, кроме того, могут быть пригодны для лечения мигрени [см., например, The Journal of Pharmacology and Experimental Therapeutics, 287, 43-50 (1998)] и для лечения инфаркта миокарда [см. Expert Opinion on Investigational Drugs, % 2537-2542 (2000)]. В дальнейшем аспекте данного изобретения, лечение пациента соединением согласно настоящему изобретению комбинируют с диетой и/или физической нагрузкой. В следующем аспекте изобретения одно или несколько соединений согласно настоящему изобретению вводят в комбинации с одним или несколькими другими активными веществами в любом подходящем(щих) соотношении(ниях). Такие другие активные агенты могут быть выбраны, например, из средств против ожирения, антидиабетических средств, антидислипидемических агентов, антигипертензивных агентов, средств для лечения осложнений, возникающих в результате диабета или связанных с ним, и средств для лечения осложнений и нарушений, возникающих в результате ожирения или связанных с ним. Таким образом, в дальнейшем аспекте изобретения, одно или несколько соединений согласно настоящему изобретению могут быть введены в комбинации с одним или несколькими средствами против ожирения или средствами для регуляции аппетита. Такие средства могут быть, например, выбраны из группы, состоящей из агонистов CART (регулируемый кокаин-амфетамином транскрипт), антагонистовNPY (нейропептид Y), агонистов MC4 (меланокортин-4), агонистов МС 3 (меланокортин-3), антагонистов орексина, агонистов TNF (фактор некроза опухоли), агонистов CRF (кортикотропинвысвобождающий фактор), антагонистов CRF BP (белок, связывающий кортикотропинвысвобождающий фактор), агонистов урокортина, 3-адренергических агонистов, таких как CL-316243, AJ-9677, GW-0604, LY362884,LY377267 или AZ-40140; агонистов MSH (меланоцитстимулирующий гормон), антагонистов МСН (меланоцитконцентрирующий гормон), агонистов CCK (холецистокинин); ингибиторов повторного поглощения серотонина, таких как флуоксетин, сероксат или циталопрам; ингибиторов повторного поглощения серотонина и норадреналина, смешанных серотонин- и норадренергических соединений, агонистов 5 НТ (серотонин), агонистов бомбезина, антагонистов галанина, гормона роста, факторов роста, таких как пролактин или плацентарный лактоген, высвобождающих гормон роста соединений, агонистов TRH (тиреотропинвысвобождающий гормон), модуляторов UCP 2 или 3 (несвязывающий белок 2 или 3), агонистов лептина, агонистов DA (бромокриптин, допрексин), ингибиторов липазы/амилазы, модуляторовPPAR (рецептор, активируемый агентами, стимулирующими рост пероксисом), модуляторов RXR (ретиноидный Х-рецептор), агонистов TR, ингибиторов AGRP (родственный агути белок), опиоидных антагонистов (как, например, налтрексон), эксендина-4, GLP-1 и цилиарного нейротрофического фактора. В одном воплощении изобретения средством против ожирения, вводимым в комбинации с одним или несколькими соединениями согласно настоящему изобретению, является лептин. В другом воплощении таким средством против ожирения является дексамфетамин или амфетамин. В другом воплощении таким средством против ожирения является фенфлурамин или дексфенфлурамин.- 11015569 В еще одном другом воплощении таким средством против ожирения является сибутрамин. В дальнейшем воплощении таким средством против ожирения является орлистат. В другом воплощении таким средством против ожирения является мазиндол или фентермин. В еще одном другом воплощении таким средством против ожирения является фендиметразин, дизтилпропион, флуоксетин, бупропион, топирамат или экопипам. В еще одном другом аспекте изобретения одно или несколько соединений согласно настоящему изобретению могут быть введены в комбинации с одним или несколькими антидиабетическими средствами. Подходящие антидиабетические средства включают инсулин, аналоги и производные инсулина,такие как раскрытые в ЕР 0792290 (Novo Nordisk A/S), например человеческий NB29-тетрадеканоилdes(B30) инсулин, в ЕР 0214826 и ЕР 0705275 (Novo Nordisk A/S), например человеческий AspB28 инсулин, в US 5504188 (Eli Lilly), например человеческий LysB28ProB29-инсулин, в ЕР 0368187 (Aventis),например Lantus, все из которых включены в данное описание путем ссылки, производные GLP-1, такие как раскрытые в WO 98/08871 (Novo Nordisk A/S), включенной в данное описание путем ссылки, а также перорально активные гипогликемические средства. Перорально активные гипогликемические средства предпочтительно включают имидазолины,сульфонилмочевины, бигуаниды, меглитиниды, оксадиазолидиндионы, тиазолидиндионы, сенсибилизаторы инсулина, ингибиторы -глюкозидазы, агенты, воздействующие на АТФ-зависимый калиевый канал -клеток, например открыватели калиевого канала, такие как раскрытые в WO 97/26265, WO 99/03861 и WO 00/37474 (Novo Nordisk A/S), которые включены в данное описание путем ссылки, или митиглинид, или блокатор калиевого канала, такой как BTS-67582, натеглинид, антагонисты глюкагона,такие как один из раскрытых в WO 99/01423 и WO 00/39088 (Novo Nordisk A/S и Agouron Pharmaceuticals, Inc.), обе из которых включены в данное описание путем ссылки; агонисты GLP-1, такие как раскрытые в WO 00/42026 (Novo Nordisk A/S и Agouron Pharmaceuticals, Inc.), включенной в данное описание путем ссылки; ингибиторы DPP-IV (дипептидилпептидаза-IV), ингибиторы РТРазы (протеинтирозинфосфатаза), ингибиторы ферментов печени, которые принимают активное участие в стимуляции глюконеогенеза и/или гликогенолиза, модуляторы поглощения глюкозы, ингибиторы GSK-3 (гликогенсинтазокиназа-3), соединения, модифицирующие липидный метаболизм, такие как антилипидемические агенты, соединения, снижающие потребление пищи, агонисты PPAR (рецептор, активируемый агентами,стимулирующими рост пероксисом) и RXR (ретиноидный Х-рецептор) , как, например, ALRT-268, LG1268 или LG-1069. В одном воплощении изобретения одно или несколько соединений согласно настоящему изобретению могут быть введены в комбинации с инсулином или аналогом или производным инсулина, такими как человеческий NВ 29-тетрадеканоил des(B30) инсулин, человеческий AspB28-инсулин, человеческийLysB28ProB29-инсулин, Lantus, или смешанный препарат, включающий один или несколько из них. В дальнейшем воплощении изобретения одно или несколько соединений согласно настоящему изобретению могут быть введены в комбинации с сульфонилмочевиной, как, например, толбутамидом,хлорпропамидом, толазамидом, глибенкламидом, глипизидом, глимепиридом, гликазидом или глибуридом. В другом воплощении изобретения одно или несколько соединений согласно настоящему изобретению могут быть введены в комбинации с бигуанидом, как, например, метформином. В еще одном другом воплощении изобретения одно или несколько соединений согласно настоящему изобретению могут быть введены в комбинации с меглитинидом, как, например, репаглинидом или натеглинидом. В еще одном другом воплощении изобретения одно или несколько соединений согласно настоящему изобретению могут быть введены в комбинации с тиазолидиндионом, сенсибилизатором инсулина,например, такие как троглитазон, циглитазон, пиоглитазон, розиглитазон, изаглитазон, дарглитазон, энглитазон, CS-011/CI-1037 или Т 174, или соединение, раскрытое в WO 97/41097, WO 97/41119, WO 97/41120, WO 00/41121 и WO 98/45292, все из которых включены в данное описание путем ссылки. В еще одном другом воплощении изобретения одно или несколько соединений согласно настоящему изобретению могут быть введены в комбинации с сенсибилизатором инсулина, таким, например, какGI-262570, YM-440, MCC-555, JTT-501, AR-H039242, KRP-297, GW-409544, CRE-16336, AR-H049020,LY-510929, МВХ-102, CLX-0940, GW-501516, или соединение, раскрытое в WO 99/19313, WO 00/50414,WO 00/63191, WO 00/63192 или WO 00/63193 или в WO 00/23425, WO 00/23415, WO 00/23451, WO 00/23445, WO 00/23417, WO 00/23416, WO 00/63153, W0 00/63196, WO 00/63209, WO 00/63190 или WO 00/63189 (Novo Nordisk A/S), все из которых включены в данное описание путем ссылки. В дальнейшем воплощении изобретения одно или несколько соединений согласно настоящему изобретению могут быть введены в комбинации с ингибитором -глюкозидазы, как, например, воглибозом,эмиглитатом, миглитотом или акарбозом. В другом воплощении изобретения одно или несколько соединений согласно настоящему изобретению могут быть введены в комбинации с агентом, воздействующим на АТФ-зависимый калиевый канал-клеток, как, например, толбутамидом, глибенкламидом, глипизидом, гликазидом, BTS-67582 или ре- 12015569 паглинидом. В еще одном другом воплощении изобретения одно или несколько соединений согласно настоящему изобретению могут быть введены в комбинации с натеглинидом. В еще одном другом воплощении изобретения одно или несколько соединений согласно настоящему изобретению могут быть введены в комбинации с антигиперлипидемическим агентом или антилипидемическим агентом, как, например, холестирамином, колестиполом, клофибратом, гемфиброзилом, ловастатином, правастатином, симвастатином, пробуколом или декстротироксином. В другом аспекте изобретения одно или несколько соединений согласно настоящему изобретению могут быть введены в комбинации с более чем одним из вышеуказанных соединений, например, в комбинации с метформином и сульфонилмочевиной, как, например, глибуридом; сульфонилмочевиной и акарбозом; натеглинидом и метформином; акарбозом и метформином; сульфонилмочевиной, метформином и троглитазоном; инсулином и сульфонилмочевиной; инсулином и метформином; инсулином, метформином и сульфонилмочевиной; инсулином и троглитазоном; инсулином и ловастатином и т.д. Кроме того, одно или несколько соединений согласно настоящему изобретению могут быть введены в комбинации с одним или несколькими антигипертензивными агентами. Примерами антигипертензивных агентов являются -блокаторы, такие как алпреналол, атенолол, тимолол, пиндолол, пропранолол и метопролол; ингибиторы АСЕ (ангиотензинконвертирующий фермент), такие как беназеприл, каптоприл, эналаприл, фозиноприл, лизиноприл, квинаприл и рамиприл; блокаторы кальциевого канала, такие как нифедипин, фелодипин, никардипин, исрадипин, нимодипин, дитиазем и верапамил; и -блокаторы,такие как доксазозин, урапидил, празозин и теразозин. Дальнейшая ссылка может быть сделана на Remington The Science and Practice of Pharmacy, 19-e издание, под ред. Gennaro, Mack Publishing Co., Eastin,PA, 1995. Должно быть понятно, что любую подходящую комбинацию соединений согласно данному изобретению с диетой и/или физической нагрузкой, одним или несколькими из вышеуказанных соединений и необязательно одним или несколькими другими активными веществами рассматривают как входящую в рамки настоящего изобретения. Соединения согласно настоящему изобретению могут быть хиральными, и подразумевается, что любые энантиомеры, как разделенные, чистые или частично очищенные энантиомеры или их рацемические смеси, входят в рамки настоящего изобретения. Кроме того, когда в молекуле присутствует двойная связь или полностью или частично насыщенная циклическая система или более чем один центр асимметрии или связь с ограниченной вращаемостью,могут быть получены диастереомеры. Подразумевается, что любые диастереомеры, как разделенные,чистые или частично очищенные диастереомеры или их смеси, входят в рамки данного изобретения. Кроме того, некоторые из соединений согласно настоящему изобретению могут существовать в различных таутомерных формах, и подразумевается, что любые таутомерные формы, которые способны образовывать соединения, входят в рамки настоящего изобретения. Настоящее изобретение также относится к фармацевтически приемлемым солям соединений согласно настоящему изобретению. Такие соли включают фармацевтические приемлемые кислотноаддитивные соли, фармацевтические приемлемые соли металлов, соли аммония и алкилированного аммония. Кислотно-аддитивные соли включают соли неорганических кислот, а также органических кислот. Типичные примеры подходящих неорганических кислот включают соляную, бромоводородную, иодоводородную, фосфорную, серную, азотную кислоты и т.п. Типичные примеры подходящих органических кислот включают муравьиную, уксусную, трихлоруксусную, трифторуксусную, пропионовую, бензойную, коричную, лимонную, фумаровую, гликолевую, молочную, малеиновую, яблочную, малоновую,миндальную, щевелевую, пикриновую, пирувиновую, салициловую, янтарную, метансульфоновую, этансульфоновую, винную, аскорбиновую, памовую, бисметиленсалициловую, этандисульфоновую, глюконовую, цитраконовую, аспарагиновую, стеариновую, пальмитиновую, этилендиаминтетрауксусную, гликолевую, п-аминобензойную, глутаминовую, бензолсульфоновую, п-толуолсульфоновую кислоты и т.п. Дальнейшие примеры фармацевтически приемлемых кислотно-аддитивных солей неорганических или органических кислот включают фармацевтические приемлемые соли, перечисленные в публикации J.Pharm. Sci., 66, 2 (1977), которая включена в данное описание путем ссылки. Примеры солей металлов включают соли лития, натрия, калия, магния и т.п. Примеры солей аммония и алкилированного аммония включают соли аммония, метиламмония, диметиламмония, триметиламмония, этиламмония, гидроксиэтиламмония, диэтиламмония, бутиламмония, тетраметиламмония и т.п. Также подразумевается, что фармацевтически приемлемыми кислотно-аддитивными солями являются гидраты, которые могут образовывать соединения согласно настоящему изобретению. Кислотно-аддитивные соли могут быть получены в качестве прямых продуктов синтеза соединения. Альтернативно, свободное основание может быть растворено в подходящем растворителе, содержащем соответствующую кислоту, и соль может быть выделена путем выпаривания растворителя или иным образом разделения соли и растворителя. Соединения согласно настоящему изобретению могут образовывать сольваты с обычными низко- 13015569 молекулярными растворителями, используя способы, хорошо известные специалисту в данной области. Подразумевается, что такие сольваты также входят в рамки настоящего изобретения. Настоящее изобретение также относится к пролекарствам соединений согласно настоящему изобретению, которые после введения подвергаются химическому превращению за счет метаболических процессов до образования фармакологически активных веществ. В целом, такие пролекарства являются функциональными производными соединений согласно настоящему изобретению, которые легко превращаются in vivo в необходимое соединение формулы (I). Стандартные способы в отношении подбора и получения подходящих пролекарственных производных описываются, например, в Design of Prodrugs,под ред. Н. Bundgaard, Elsevier, 1985. Настоящее изобретение также относится к активным метаболитам соединений согласно настоящему изобретению. Комбинирование одного или нескольких индивидуальных воплощений, описываемых здесь, необязательно также с одним или более нижеприведенными индивидуальными притязаниями, приводит к дальнейшим воплощениям, и настоящее изобретение относится ко всем возможным комбинациям вышеуказанных воплощений и притязаний. В одном воплощении настоящее изобретение относится к соединениям формулы (I) с указанными в данном описании определениями, при условии, что, когда R1 означает водород, C1-6-алкил, С 2-6-алкенил,С 3-8-циклоалкил или С 3-8-циклоалкил-С 1-6-алкил, R2 означает водород или C1-6-алкил; или R1 и R2 вместе с атомами, с которыми они связаны, образуют азотсодержащий цикл, необязательно другую гетероциклильную группу; m означает 0, 1 или 2; один из четырех заместителей R3, R4, R5 и R6 является любым из галогена, гидрокси, циано или С 1-6-алкила и три из четырех заместителей R3, R4, R5 и R6 являются водородом, тогда X является отличным от -S-, и в другом воплощении настоящее изобретение относится к применению таких соединений в качестве лекарственного средства и, в еще одном дальнейшем воплощении настоящее изобретение относится к применению таких соединений для лечения любого конкретного заболевания, указанного в данном описании, или любого конкретного состояния, указанного в данном описании. Фармацевтические композиции Соединения согласно настоящему изобретению могут быть введены индивидуально или в комбинации с фармацевтически приемлемыми носителями или эксципиентами, или в виде однократной дозы,или в виде многократных доз. Фармацевтические композиции согласно настоящему изобретению могут быть получены при использовании фармацевтически приемлемых носителей или разбавителей, а также любых других известных добавок и эксципиентов в соответствии с обычными способами, такими как раскрытые в Remigton The Science and Practice of Pharmacy, 19-e издание, под ред. Gennaro, Mack Publishing Co., Easton, PA, 1995. Фармацевтические композиции могут быть конкретно приготовлены для введения любым подходящим путем, таким как пероральный, ректальный, назальный, легочный, локальный (включая буккальный и сублингвальный), чрескожный, интрацистернальный, интраперитонеальный,вагинальный или парентеральный (включая подкожный, внутримышечный, интратекальный, внутривенный и интрадермальный) путь, причем пероральный путь введения является предпочтительным. Должно быть очевидно, что предпочтительный путь зависит от общего состояния и возраста субъекта, подвергаемого лечению, природы состояния, подвергаемого лечению, и выбора активного ингредиента. Фармацевтические композиции для перорального введения включают твердые дозированные формы, такие как капсулы, таблетки, драже, пилюли, лепешки, порошки игранулы. При необходимости, они могут быть получены с нанесенными покрытиями, такими как энтеросолюбильные покрытия, или они могут быть получены с контролируемым высвобождением активного ингредиента, таким как непрерывное или пролонгированное высвобождение, согласно способам, хорошо известным в уровне техники. Жидкие дозированные формы для перорального введения включают растворы, эмульсии, суспензии, сиропы и эликсиры. Фармацевтические композиции для парентерального введения включают стерильные водные и неводные инъецируемые растворы, дисперсии, суспензии или эмульсии, а также стерильные порошки, реконструируемые перед использованием в инъецируемые стерильные растворы или дисперсии. Должно быть понятно, что депо-инъецируемые готовые лекарственные формы также входят в рамки настоящего изобретения. Другие подходящие для введения формы включают суппозитории, спреи, мази, кремы, гели, лекарственные формы для ингаляции, кожные пластыри, имплантаты и т.д. Типичная пероральная доза находится в диапазоне от примерно 0,001 до примерно 100 мг/кг массы тела в сутки, предпочтительно от примерно 0,01 до примерно 50 мг/кг массы тела в сутки и более предпочтительно от примерно 0,05 до примерно 10 мг/кг массы тела в сутки, вводимая в виде одной или нескольких доз, как, например, от 1 до 3 доз. Точная дозировка зависит от частоты и способа введения, пола, возраста, массы тела и общего состояния подвергаемого лечению субъекта, природы и тяжести излечиваемого состояния и каких-либо сопутствующих заболеваний, подвергаемых лечению, и других факторов, очевидных квалифицированному специалисту в данной области.- 14015569 Готовые лекарственные формы можно без труда получать в единичной дозируемой форме способами, известными квалифицированному специалисту в данной области. Типичная единичная дозируемая форма для перорального введения один или несколько раз в сутки, как, например, от 1 до 3 раз в сутки,может содержать от 0,05 до примерно 1000 мг, предпочтительно от примерно 0,1 до примерно 500 мг и более предпочтительно от примерно 0,5 до примерно 200 мг соединения согласно данному изобретению(или его соли, или другого производного, как изложено выше). Для парентеральных путей введения, таких как внутривенный, интратекальный, внутримышечный и аналогичный, типичные дозы составляют примерно половину дозы, используемой для перорального введения. Соединения согласно данному изобретению обычно используют в виде свободного вещества или в виде его фармацевтически приемлемой соли. Одним примером является кислотно-аддитивная соль соединения, имеющего свободную основную функциональную группу. Когда соединение формулы (I) содержит свободную основную функциональную группу, такие соли получают обычным способом путем обработки раствора или суспензии свободной основной формы соединения формулы (I) с помощью химического эквивалента (эквивалент кислота-основание) фармацевтически приемлемой кислоты. Типичные примеры подходящих неорганических и органических кислот указаны выше. Физиологически приемлемые соли соединения согласно данному изобретению, имеющего гидроксильную группу, включают анион вышеуказанного соединения в комбинации с пригодным катионом, таким как ион натрия или ион аммония. Для парентерального введения можно применять растворы новых соединений формулы (I) в стерильном водном растворе, водном растворе пропиленгликоля или кунжутном или арахисовом масле. Такие водные растворы должны быть подходящим образом забуферены, если необходимо, и жидкий разбавитель сначала делают изотоническим с помощью достаточного количества насыщенного солевого раствора или глюкозы. Водные растворы особенно пригодны для внутривенного, внутримышечного, подкожного и интраперитонеального введения. Используемые стерильные водные среды все являются легкодоступными за счет стандартных способов, известных квалифицированному специалисту в данной области. Пригодные фармацевтические носители включают твердые инертные разбавители или наполнители, стерильный водный раствор и различные органические растворители. Примерами твердых носителей является лактоза, каолин, сахароза, циклодекстрин, тальк, желатин, агар, пектин, гуммиарабик, стеарат магния, стеариновая кислота или простые низшие алкиловые эфиры целлюлозы. Примерами жидких носителей являются сироп, арахисовое масло, оливковое масло, фосфолипиды, жирные кислоты, амины жирных кислот, полиоксиэтилены или вода. Подобным образом носитель или разбавитель может включать любое вещество для пролонгированного высвобождения, известное в уровне техники, такое как глицерилмоностеарат или глицерилдистеарат, индивидуально или в смеси с воском. Фармацевтические композиции, образованные путем комбинирования новых соединений формулы (I) и фармацевтически приемлемых носителей, затем без труда вводят в множестве дозированных форм, пригодных для описанных путей введения. Готовые лекарственные формы пригодным образом можно получать в единичной дозируемой форме способами, известными в области фармации. Готовые лекарственные формы согласно настоящему изобретению, пригодные для перорального введения, можно получать в виде дискретных единиц, таких как капсулы или таблетки, каждая из которых содержит заранее определенное количество активного ингредиента и которые могут включать пригодный эксципиент. Эти готовые лекарственные формы могут находиться в виде порошка или гранул, в виде раствора или суспензии в водной или неводной жидкости или в виде жидкой эмульсии масло-в-воде или вода-в-масле. Если твердый носитель используют для перорального введения, препарат можно таблетировать,помещать в твердую желатиновую капсулу в виде порошка или в виде шариков, или он может быть в виде пастилки или лепешки. Количество твердого носителя можно широко варьировать, но обычно оно составляет от примерно 25 мг до примерно 1 г. Если используют жидкий носитель, препарат может быть в виде сиропа, эмульсии, мягкой желатиновой капсулы или инъецируемой стерильной жидкости, как,например, водная или неводная жидкая суспензия или раствор. Типичная таблетка, которую можно получать стандартными способами таблетирования, может в сердцевине содержать 5,0 мг соединения согласно данному изобретению, 67,8 мг лактозы (Ph. Eur.), 31,4 мг микрокристаллической целлюлозы (Avicel), 1,0 мг Amberlite IRP88 (т.е. Polacrillin potassium NF, дезинтегрирующее средство таблетки, Rohm and Haas) и стеарат магния (Ph. Eur.) в достаточном количестве с нанесенным покрытием из приблизительно 9 мг гидроксипропилметилцеллюлозы и приблизительно 0,9 мг Mywacett 9-40 Т (представляющий собой ацилированный моноглицерид, используемый как пластификатор для пленочного покрытия). Если желательно, фармацевтическая композиция согласно данному изобретению может содержать соединение формулы (I) в комбинации с одним или несколькими другими фармакологически активными веществами, например веществами, выбираемыми среди описанных выше. Вкратце, соединения согласно данному изобретению можно получать способом, per se известным- 15015569 или аналогичным известным способам. Все ссылки, включая публикации, заявки на патенты и патенты, цитируемые в данном описании,настоящим включены путем ссылки во всей их полноте и в том же самом объеме, как если бы каждая ссылка отдельно и конкретно была указана как включенная путем ссылки и изложена во всей полноте в данном описании (до максимального объема, разрешенного законом). Все заголовки и подзаголовки используют в данном описании только для удобства, и они не могут быть истолкованы как ограничивающие данное изобретение каким-либо образом. Использование любого и всех примеров или касающегося конкретных примеров выражения (например, такой как), предусмотренного в данном описании, предназначено только для лучшего пояснения данного изобретения и не представляет собой ограничение рамок данного изобретения, за исключением иначе заявленного. Отсутствие касающегося конкретных примеров выражения в описании не должно быть истолковано как указывающее на какой-либо незаявленный элемент в качестве существенного для практики данного изобретения. Цитирование и включение патентных документов в случае данного описания сделано только для удобства и не отражает какого-либо представления об обоснованности, патентоспособности и/или обеспеченности правовой санкцией таких патентных документов. Упоминание в данном описании ссылок не является признанием, что они составляют известный уровень техники. В данном описании слово включать должно быть интерпретировано в широком смысле значений включать, содержать или охватывать (Европейское патентное ведомство, руководящие указания, С 4.13). Данное изобретение включает все модификации и эквиваленты предмета данного изобретения, перечисленные в прилагаемой изобретения, в качестве разрешенных применяемым законодательством. Следующие примеры предлагаются в качестве иллюстрации, но не в виде ограничения объема изобретения. Примеры Типичные примеры, указанные выше, являются конкретными воплощениями данного изобретения. Подразумевается, что в нижеприведенных примерах следующие термины имеют следующие общие значения: д означает день(дни), г означает грамм(ы), ч означает час(ы), Гц означает Герц, кДа означает килодальтон(ы), л означает литр(ы), М означает молярный (М), мбар означает миллибар, мг означает миллиграмм(ы), мин означает минуты, мл означает миллилитр(ы), мМ означает миллимолярный, ммоль означает миллимоль(и), моль означает моль(и), н означает нормальный, м.д. означает миллионные доли,psi означает фунт на кв.дюйм, APCI означает химическую ионизацию при атмосферном давлении, ESI означает ионизацию электронным распылением, I.v. означает внутривенный, m/z означает отношение массы к заряду, т.пл. означает температуру плавления, МС означает масс-спектрометрию, ВЭЖХ означает высокоэффективную жидкостную хроматографию, RP означает обращенную фазу, HPLC-MS означает высокоэффективную жидкостную хроматографию с масс-спектрометрией, ЯМР означает ядерную магнитную резонансную спектроскопию, р.о. означает пероральный, Rf означает относительную мобильность при ТСХ, rt означает комнатную температуру, s.c. означает подкожный, ТСХ означает тонкослойную хроматографию, tr означает время удерживания, ВОР означает (1-бензотриазолилокси)трис(диметиламино)фосфоний-гексафторфосфат, CDI означает карбонилдиимидазол, ДХМ означает дихлорметан, CH2Cl2 означает метиленхлорид, DBU означает 1,8-диазабицикло-[5.4.0]ундец-7-ен, DEAD означает диэтилазодикарбоксилат, DIC означает 1,3-диизопропилкарбодиимид, DIPEA означает N,Nдиизопропилэтиламин, DMA означает N,N-диметилацетамид, ДМФА означает N,N-диметилформамид,DMPU означает N,N'-диметилпропиленмочевину, 1,3-диметил-2-оксогексагидропиримидин, ДМСО означает диметилсульфоксид, EDAC означает 1-этил-3-(3-диметиламинопропил)карбодиимидгидрохлорид,Et2O означает диэтиловый эфир, EtOAc означает этилацетат, НМРА означает триамид гексаметилфосфорной кислоты, HOAt означает 1-гидрокси-7-азабензотриазол, HOBt означает 1-гидроксибензотриазол,LAH означает литийалюминийгидрид (LiAlH4), LDA означает литийдиизопропиламид, MeCN означает ацетонитрил, МеОН означает метанол, NMM означает N-метилморфолин (4-метилморфолин), NMP означает N-метилпирролидин-2-он, TEA означает триэтиламин, TFA означает трифторуксусную кислоту,ТГФ означает тетрагидрофуран, ТНР означает тетрагидропиранил, TTFH означает фтор-N,N,N',N'тетраметилформамидинийгексафторфосфат, CDCl3 означает дейтерохлороформ, CD3OD означает тетрадейтериометанол и ДМСО-d6 означает гексадейтериодиметилсульфоксид. Вкратце, соединения согласно данному изобретению можно получать способом, per se известным или аналогичным известным способам. Общие экспериментальные методики ЯМР-спектры регистрируют на спектрометре Bruker 300 или 400 МГц. Сдвигивыражают в миллионных долях (ppm; м.д.) в сторону нижнего поля от тетраметилсилана в качестве внутреннего ссылочного стандарта. ВЭЖХ, способ А.RP-анализы выполняют на приборе Shimadzu LC-20, используя YMC-ODS, 5,0 мкм, 4,650 мм, гра- 16015569 диент элюирования 0-30% растворителя В (0,1% TFA в ацетонитриле) в растворителе А (0,1% TFA в воде) в течение 6 мин, и затем выдерживают в течение 2 мин, 2,5 мл/мин, детектирование при 220 нм, при температуре 30 С. ВЭЖХ, способ В.RP-анализы выполняют на приборе Shimadzu LC-20, используя YMC-ODS, 5,0 мкм, 4,650 мм, градиент элюирования 0-60% растворителя В (0,1% TFA в ацетонитриле) в растворителе А (0,1% TFA в воде) в течение 8 мин, и затем выдерживают в течение 2 мин, 2,5 мл/мин, детектирование при 220 нм, при температуре 30 С. Примеры, приводимые ниже, и общие методики, описанные здесь, относятся к промежуточным соединениям и конечным продуктам общей формулы (I), идентифицированным в данном описании и на схемах синтеза. Получение соединений общей формулы (I) согласно настоящему изобретению описано подробно, используя следующие примеры. Иногда реакция не может быть осуществлена, как описано для каждого соединения, включенного в раскрытые рамки данного изобретения. Соединения, для которых это имеет место, без труда распознает квалифицированный специалист в данной области. В этих случаях реакции могут быть успешно осуществлены путем стандартных модификаций, известных квалифицированному специалисту в данной области, путем соответствующей защиты интерферирующих групп, путем замены другими обычными реагентами или путем рутинной модификации реакционных условий. Альтернативно, другие реакции, указанные в данном описании или иным образом общепринятые, должны быть пригодны для получения соответствующих соединений согласно данному изобретению. В случае всех препаративных методик все исходные вещества известны или могут быть получены квалифицированным специалистом в данной области по аналогии с получением подобных известных соединений или путем общих методик A-G, описанных здесь. Следующие примеры предлагаются в качестве иллюстрации, но не в виде ограничения объема изобретения. Общая методика А. Соединения формулы I, где X, R1, R2, R3, R4, R5, R6 и m имеют значения, как описано в случае формулы (I) (соединения, которые здесь обозначены формулой (Ia, могут быть получены, как показано ниже Амин формулы А-1, где R1, R2 и m имеют значения, как указано в данном описании, может быть введен во взаимодействие с замещенным бензотиазолом формулы А-2, где R3, R4, R5 и R6, каждый, имеет значение, как указано в данном описании, a Lg представляет собой удаляемую группу, такую как метилтио, хлор, бром или иод, с получением соединения формулы (Ia). Это взаимодействие можно осуществлять в подходящем растворителе, подобном, например, диметилсульфоксиду, при температуре вплоть до температуры кипения с обратным холодильником. Соединения формулы А-2 можно получать, например,из соответствующих 2-амино- или 2-меркаптозамещенных гетероциклов, в соответствии с известными методиками. Общая методика В. Соединения формулы (I), где X, R1, R2, R3, R4, R5, R6 и m имеют значения, как описано в случае формулы (I) (соединения, которые здесь обозначены формулой (Ib, могут быть получены, как показано ниже Амин формулы В-1, где X, R1, R2, R3, R4, R5, R6 и m, каждый, имеет значение, как указано в данном описании, может быть введен во взаимодействие с алифатическим галогенидом, с получением соединения формулы (Ib). Это взаимодействие может быть осуществлено в подходящем растворителе, подобном, например, диметилформамиду, диметилсульфоксиду, ацетонитрилу или 2-бутанону, при температуре вплоть до температуры кипения с обратным холодильником. Это взаимодействие можно осуществ- 17015569 лять в присутствии основания, такого как, например, гидрид натрия, карбонат калия или N,Nдиизопропилэтиламин, и катализатора, подобного, например, иодиду калия. Соединения формулы В-1 можно получать в соответствии с другой(ими) общей(ими) методикой(ами), описанной здесь. Общая методика С. Соединения формулы I, где X, R1, R2, R3, R4, R5, R6 и m имеют значения, как описано в случае формулы (I) (соединения, которые здесь обозначены формулой (Ic, могут быть получены, как показано ниже Амин формулы С-1, где X, R1, R2, R3, R4, R5, R6 и m, каждый, имеет значение, как указано в данном описании, может быть введен во взаимодействие с кетоном или альдегидом, в присутствии восстановителя, с получением соединения формулы (Ic). Это взаимодействие можно осуществлять в подходящем растворителе, подобном, например, тетрагидрофурану или 1,2-дихлорэтану, при температуре вплоть до температуры кипения с обратным холодильником. Восстановитель может представлять собой, например,NaCNBH3 или NaBH(OAc)3, в конце концов, в присутствии кислотного катализатора, подобного, например, уксусной кислоте. Соединения формулы С-1 могут быть получены в соответствии с другой(ими) общей(ими) методикой(ами), описанной здесь. Общая методика D. Соединения формулы I, где один из R3, R4, R5 или R6 означает -(С=O)-NR7R8 и R7 и R8 имеют значения, как описано в случае формулы I (соединения, которые здесь обозначены формулой (Id, могут быть получены, как показано ниже Карбоновая кислота формулы D-2 может быть введена во взаимодействие с амином формулыR7R8NH, с получением амида формулы (Id). Это взаимодействие можно осуществлять путем активирования карбоновой кислоты, например, с помощью HOBt/EDAC, в подходящем растворителе, подобном,например, ТГФ, и при температуре вплоть до температуры кипения с обратным холодильником. Карбоновую кислоту формулы D-2 можно получать путем гидролиза нитрила формулы D-1. Это взаимодействие можно осуществлять в сильно кислых условиях, например в 6 н. соляной кислоте, при температуре вплоть до температуры кипения с обратным холодильником. Соединения формулы D-1 могут быть получены в соответствии с другой(ими) общей(ими) методикой(ами), описанной здесь. Общая методика Е. Соединения формулы I, где один из R3, R4, R5 или R6 означает -CH2-NR7R8 и R7 и R8 имеют значения, как описано в случае формулы (I) (соединения, которые здесь обозначены формулой (Ie, могут быть получены, как показано ниже Карбоксальдегид формулы Е-2 может быть введен во взаимодействие с амином формулы R7R8NH в условиях восстановления, с получением амина формулы (Ie). Это взаимодействие можно осуществлять в подходящем растворителе, подобном, например, тетрагидрофурану или 1,2-дихлорэтану, при температуре вплоть до температуры кипения с обратным холодильником. Восстановителем может быть, например,NaCNBH3 или NaBH(OAc)3, в конце концов, в присутствии кислотного катализатора, подобного, например, уксусной кислоте. Карбоксальдегид формулы Е-2 можно получать путем восстановления нитрила формулы Е-1. Это взаимодействие можно осуществлять в подходящем растворителе, подобном, например, тетрагидрофурану или 1,2-дихлорэтану, при температуре вплоть до температуры кипения с обратным холодильником. Восстановителем может быть, например, DIBAH. Соединения формулы Е-1 могут быть получены в соответствии с другой(ими) общей(ими) методикой(ами), описанной здесь. Общая методика F. Соединения формулы I, где один из R3, R4, R5 или R6 означает замещенный 1,2,4-оксадиазол-3-ил,как описано в случае формулы I (соединения, которые здесь обозначены формулой (If, могут быть получены, как показано ниже Гидроксиамидин формулы F-2 может быть введен во взаимодействие с хлорангидридом или ангидридом карбоновой кислоты формулы F-3, с получением соединения формулы (Id). Это взаимодействие можно осуществлять в подходящем растворителе, подобном, например, N,N-диметилацетамиду или уксусной кислоте, при температуре вплоть до температуры кипения с обратным холодильником. Соединения формулы F-2 могут быть получены путем введения во взаимодействие нитрила формулы F-1 с гидроксиламином. Это взаимодействие можно осуществлять в подходящем растворителе, подобном, например, этанолу и воде, при температуре вплоть до температуры кипения с обратным холодильником, в присутствии основания, подобного, например, карбонату калия. Соединения формулы F-1 могут быть получены в соответствии с другой(ими) общей(ими) методикой(ами), описанной здесь. Общая методика G. Соединения формулы I, где один из R3, R4, R5 или R6 означает циано (соединения, которые здесь обозначены формулой (Ig, могут быть получены, как показано ниже Бромид формулы G-1 может быть введен во взаимодействие с цианидом меди(I), в присутствии катализатора, подобного, например, иодиду меди(I), с получением нитрила формулы (Ie). Это взаимодействие можно осуществлять в подходящем растворителе, подобном, например, N-метилпирролидону, при температуре вплоть до температуры кипения с обратным холодильником. Соединения формулы G-1 могут быть получены в соответствии с другой(ими) общей(ими) методикой(ами), описанной здесь. Общая методика Н. Соединения формулы I, где один из R3, R4, R5 или R6 означает -NH(C=O)-R (соединения, которые здесь обозначены формулой (Ih, могут быть получены, как показано ниже Бромид формулы Н-1 может быть введен во взаимодействие с карбоксамидом формулы Н-2, в присутствии катализатора, подобного, например, Pd(OAc)2, с получением ацилированного амина формулы(Ih). Это взаимодействие можно осуществлять в подходящем растворителе, подобном, например, 1,4 диоксану, в присутствии основания, подобного, например, Cs2CO3, при температуре вплоть до температуры кипения с обратным холодильником. Соединения формулы Н-1 могут быть получены в соответствии с другой(ими) общей(ими) методикой(ами), описанной здесь. Общая методика I. Соединения формулы I, где один из R3, R4, R5 или R6 означает А' (соединения, которые здесь обозначены формулой (Ii, могут быть получены, как показано ниже Соединение формулы I-1, где Hal означает хлор, бром или иод, может быть введено во взаимодействие с (гетеро)ароматическим производным бороновой кислоты формулы 1-2 или с соответствующим сложноэфирным производным бороновой кислоты, с получением соединения формулы (Ii). Это взаимодействие можно осуществлять в подходящем растворителе, подобном, например, ацетонитрил/вода, при температуре вплоть до 150 С, в присутствии подходящего катализатора, подобного, например, бистрифенилфосфинпалладий(II)дихлориду и карбонату натрия. Это взаимодействие также можно осуществлять другим путем, исходя из реагентов, где галоген и остатки бороновой кислоты взаимообменены. Это взаимодействие можно осуществлять в подобных условиях, как описано выше. Соединения формулы I-1 могут быть получены в соответствии с другой(ими) общей(ими) методикой(ами), описанной здесь. Общая методика N. Соединения формулы I, где R3, R4, R5 или R6 означают циклический сульфонамид, и где р означает 1-4, как описано в случае формулы (I), соединения, которые здесь обозначены формулой (In), могут быть Ароматический амин формулы N-1 может быть введен во взаимодействие с активированной сульфоновой кислотой формулы N-2, где р означает 1-4, и LG1 и LG2 представляют собой подходящие удаляемые группы, такие как, например, галоген, с получением соединения формулы N-3. Это взаимодействие можно осуществлять в подходящем растворителе, подобном, например, ДМФА, при температуре вплоть до температуры кипения с обратным холодильником и в присутствии основания, подобного, например, TEA. Соединение формулы N-3 может быть циклизовано с получением соединения формулы(In). Это взаимодействие можно осуществлять в подходящем растворителе, подобном, например, ДМФА,при температуре вплоть до температуры кипения с обратным холодильником и в присутствии основания,подобного, например, NaH. Соединения формулы N-1 могут быть получены в соответствии с другой(ими) общей(ими) методикой(ами), описанной здесь. Общая методика О. Соединения формулы I, где один из R3, R4, R5 или R6 означает -CH2-NR7R8 и R7 и R8 имеют значения, как описано в случае формулы (I) (соединения, которые здесь обозначены формулой (Io, могут быть получены, как показано ниже Карбоксальдегид формулы O-2 может быть введен во взаимодействие с амином формулы R7R8NH в условиях восстановления, с получением амина формулы (Io). Это взаимодействие можно осуществлять в подходящем растворителе, подобном, например, тетрагидрофурану или 1,2-дихлорэтану, при температуре вплоть до температуры кипения с обратным холодильником. Восстановителем может быть, например,NaCNBH3 или NaBH(OAc)3, в конце концов, в присутствии кислотного катализатора, подобного, например, уксусной кислоте. Карбоксальдегид формулы 0-2 можно получать из галогенида формулы 0-1 путем введения его во взаимодействие с сильным основанием, подобным, например, н-бутиллитию, с последующим добавлением формилирующего агента, подобного, например, ДМФА. Это взаимодействие можно осуществлять в подходящем растворителе, подобном, например, тетрагидрофурану, при температуре ниже -78 С. Соединения формулы 0-1 могут быть получены в соответствии с другой(ими) общей(ими)методикой(ами),описанной здесь. Пример 1 (общая методика А). 6-Хлор-2-(4-циклопентилпиперазин-1-ил)бензотиазолгидрохлорид. Смесь 2,6-дихлорбензотиазола (0,39 г, 1,9 ммоль), 1-циклопентилпиперазина (0,22 г, 1,4 ммоль) и диметилсульфоксида (2,0 мл) перемешивают при температуре 130 С в течение 23 ч. Реакционную смесь оставляют охлаждаться и добавляют воду (50 мл) и карбонат калия (1 г). Реакционную смесь экстрагируют смесью этилацетата и дихлорметана и отфильтровывают. Фильтрат разделяют и органический экстракт промывают насыщенным солевым раствором (2 раза) и сушат (MgSO4). Летучие вещества выпаривают, получая твердый остаток, который растворяют в смеси этанола (30 мл) и 1 н. раствора соляной кислоты (2,5 мл). Добавляют толуол и смесь концентрируют. Добавляют этанол и толуол и смесь концентрируют снова. Таким образом получают твердое вещество, которое обрабатывают этанолом (50 мл) и нагревают до температуры кипения с обратным холодильником. Полученную смесь оставляют в течение ночи для кристаллизации. Таким образом, после фильтрации и высушивани получают 0,35 г (выход 69%) 6-хлор-2-(4-циклопентилпиперазин-1-ил)бензотиазолгидрохлорида. Пример 2 (общая методика А). 2-(4-Изопропилпиперазин-1-ил)-6-метоксибензотиазолгидрохлорид. Смесь 2-хлор-6-метоксибензотиазола (0,20 г, 1,0 ммоль) и 1-изопропилпиперазина (0,26 г, 2,0 ммоль) перемешивают при температуре 120 С в течение 2 ч. Реакционную смесь оставляют охлаждаться- 20015569 и подвергают экстракции этилацетатом. Органический экстракт промывают раствором NaHCO3 и водой(3 раза). Органическую фазу экстрагируют 0,25 М раствором соляной кислоты (10 мл). Кислый водный экстракт концентрируют и повторно выпаривают с этанолом. Остаток кристаллизуют из смеси этанола и этилацетата, получая 260 мг (выход 80%) 2-(4-изопропилпиперазин-1-ил)-6-метоксибензотиазолгидрохлорида. 1 Н-ЯМР (400 МГц, ДМСО-d6)11,7 (ушир.с, 1 Н), 7,52 (д, 1 Н), 7,49 (д, 1 Н), 6,97 (дд, 1 Н), 4,23-4,15 Смесь 2-хлор-6-метоксибензотиазола (0,20 г, 1,0 ммоль) и 1-циклопропилпиперазина (0,25 г, 2,0 ммоль) перемешивают при температуре 120 С в течение ночи. Реакционную смесь оставляют охлаждаться и растворяют в смеси этилацетата и раствора NaHCO3. Фазы разделяют и органическую фазу промывают водой (3 раза) и затем экстрагируют 0,25 М раствором соляной кислоты (20 мл). Кислый водный экстракт концентрируют и повторно выпаривают с этанолом. Остаток кристаллизуют из смеси этанола и этилацетата, получая 60 мг (выход 18%) 2-(4-циклопропилпиперазин-1-ил)-6 метоксибензотиазолгидрохлорида. 1 Н-ЯМР (400 МГц, ДМСО-d6)11,3 (ушир.с, 1 Н), 7,48 (д, 1 Н), 7,45 (д, 1 Н), 6,93 (дд, 1 Н), 4,18-4,06 Смесь 2-хлор-6-метоксибензотиазола (0,17 г, 1,0 ммоль), октагидропиридо[1,2-а]пиразина (0,21 г,1,0 ммоль), DIPEA (0,51 мл) и диметилсульфоксида (1 мл) перемешивают при температуре 115 С в течение ночи. Реакционную смесь оставляют охлаждаться и растворяют в смеси этилацетата и раствораNaHCO3. Фазы разделяют и органическую фазу промывают водой (3 раза) и затем экстрагируют 0,25 М раствором соляной кислоты (20 мл). Кислый водный экстракт концентрируют и повторно выпаривают с этанолом. Остаток кристаллизуют из смеси этанола и этилацетата, получая 193 мг (выход 57%) 2-(6 метоксибензотиазол-2-ил)октагидропиридо[ 1,2-а]пиразингидрохлорида. 1 Н-ЯМР (400 МГц, ДМСО-d6)11,2 (ушир.с, 1 Н), 7,48 (д, 1 Н), 7,44 (д, 1 Н), 6,93 (дд, 1 Н), 4,15-4,08 К смеси 4-аминобензонитрила (23,6 г, 0,2 моль) и роданата аммония (30,4 г, 0,4 моль) добавляют ледяную уксусную кислоту (600 мл) и полученный раствор охлаждают до температуры 13,5 С на ледяной бане. Медленно и по каплям добавляют смесь брома и ледяной уксусной кислоты. Полученную смесь перемешивают в течение 1 ч при температуре 13,5 С и отфильтровывают. Фильтровальный осадок промывают ледяной уксусной кислотой (6 раз по 100 мл) и вносят в горячую воду (1000 мл) при перемешивании. Смесь отфильтровывают и рН фильтрата устанавливают равным 7 с помощью насыщенного раствора карбоната натрия. Осадок выделяют и высушивают, получая 19,5 г (выход 56%) 2 аминобензотиазол-6-карбонитрила. Смесь концентрированной соляной кислоты (113 мл) и воды (52 мл) нагревают при температуре 90 С во время добавления 2-аминобензотиазол-6-карбонитрила (19 г, 0,108 моль). Эту смесь охлаждают до температуры -5 С на ледяной бане и по каплям добавляют раствор нитрита натрия (7,72 г, 0,112 моль) в воде (20 мл), поддерживая температуру ниже 0 С. После завершения добавления смесь перемешивают в течение 0,5 ч и по каплям добавляют раствор CuCl2 (16 г) в воде (108- 21015569 мл). После завершения добавления смесь перемешивают в течение 10 мин и ледяную баню отставляют. Перемешивание продолжают в течение 2 ч и смесь охлаждают до комнатной температуры. Смесь отфильтровывают и твердое вещество промывают до нейтральной реакции водой и высушивают. Получают 12,8 г (выход 61%) 2-хлорбензотиазол-6-карбонитрила. 1H-ЯМР, : 8,14 (с, 1 Н), 8,03 (д, 1 Н), 7,75 (д, 1 Н). Стадия В. Раствор 2-хлорбензотиазол-6-карбонитрила (14,9 г, 0,077 моль) в ДМФА (250 мл) по каплям добавляют при температуре 10 С к смеси безводного пиперазина (60 г, 0,698 моль) и ДМФА (300 мл). Затем смесь перемешивают в течение 2 ч. Добавляют воду (1,550 мл) и смесь экстрагируют дихлорметаном (5 раз по 500 мл). Объединенные органические экстракты промывают водой (6 раз по 500 мл), сушат(Na2SO4), отфильтровывают и выпаривают, получая остаток, который перекристаллизовывают из этилацетата. Таким образом получают 10,5 г (выход 56%) 2-(пиперазин-1-ил)бензотиазол-6-карбонитрила. Смесь этого производного пиперазина (19,4 г, 0,08 моль), иодида натрия (1,94 г), триэтиламина (9,6 г,0,095 моль) и ДМФА (80 мл) нагревают при перемешивании, получая жидкость красного цвета. По каплям добавляют раствор 2-бромпропана (14,7 г, 0,12 моль) в ДМФА (80 мл) при температуре 117 С в течение 1 ч. Реакционную смесь перемешивают при температуре 110-117 С в течение следующих 3 ч и затем оставляют охлаждаться до комнатной температуры. Добавляют воду (110 мл) и смесь отфильтровывают. Фильтровальный осадок промывают до тех пор, пока фильтрат не станет бесцветным, и затем высушивают. Твердое вещество растворяют в ДМФА (250 мл) и отфильтровывают для удаления твердого остатка. К фильтрату добавляют воду (1000 мл) при перемешивании, получая осадок. Это твердое вещество выделяют, промывают водой и высушивают, получая 9,4 г (выход 41%) 2-(4 изопропилпиперазин-1-ил)бензотиазол-6-карбонитрила. 1 Н-ЯМР 8,25 (с, 1 Н), 7,61 (д, 1 Н), 7,45 (д, 1 Н), 3,55 (т, 4 Н), 2,68 (м, 1 Н), 2,51 (м, 4 Н), 0,93 (д, 6 Н). Пример 6 (общая методика D). К раствору 2-(4-изопропилпиперазин-1-ил)бензотиазол-6-карбоновой кислоты (800 мг, 2,1 ммоль) в ТГФ (14 мл) добавляют HOBt (342 мг, 2,5 ммоль), EDAC (807 мг, 4,2 ммоль), триэтиламин (1,7 г, 17 ммоль) и пиперидин (718 мг, 8,5 ммоль) при комнатной температуре. Реакционную смесь перемешивают при температуре 40-50 С в течение 12 ч в атмосфере азота. Эту смесь концентрируют в вакууме и остаток очищают с помощью колоночной хроматографии на силикагеле, элюируя градиентом CH2Cl2/MeOH(100:150:1), получая сырой продукт, который затем очищают с помощью препаративной ВЭЖХ, получая 167 мг К раствору 2-(4-изопропилпиперазин-1-ил)бензотиазол-6-карбоновой кислоты (800 мг, 2,1 ммоль) в ТГФ (14 мл) добавляют HOBt (342 мг, 2,5 ммоль), EDAC (807 мг, 4,2 ммоль), триэтиламин (1,7 г, 17 ммоль) и диметиламингидрохлорид (689 мг, 8,5 ммоль) при комнатной температуре. Реакционную смесь перемешивают при температуре 40-50 С в течение 12 ч в атмосфере азота. Эту смесь концентрируют в вакууме и остаток очищают с помощью колоночной хроматографии на силикагеле с градиентомCH2Cl2/MeOH (100:150:1) в качестве элюента, получая сырой продукт, который затем очищают с помощью препаративной ВЭЖХ, получая 178 мг (выход 25%) трифторацетата диметиламида 2-(4 изопропилпиперазин-1-ил)бензотиазол-6-карбоновой кислоты. 1 Н ЯМР (300 МГц, D2O)7,66 (д, 1 Н), 7,42 (д, 2 Н), 7,32 (дд, 1 Н), 4,08-4,22 (м, 2 Н), 3,42-3,65 (м, 5 Н),3,11-3,28 (м, 2 Н), 2,92 (с, 3 Н), 2,83 (с, 3 Н), 1,21 (д, 6 Н). Пример 8 (общая методика D). К раствору 2-(4-изопропилпиперазин-1-ил)бензотиазол-6-карбоновой кислоты (800 мг, 2,1 ммоль) в ТГФ (14 мл) добавляют HOBt (342 мг, 2,5 ммоль), EDAC (807 мг, 4,2 ммоль), триэтиламин (1,7 г, 17 ммоль) и морфолин (735 мг, 8,4 ммоль) при комнатной температуре. Реакционную смесь перемешивают при температуре 40-50 С в течение 12 ч в атмосфере азота. Эту смесь концентрируют в вакууме и остаток очищают с помощью колоночной хроматографии на силикагеле с градиентом CH2Cl2/MeOH (100:1 50:1) в качестве элюента, получая сырой продукт, который затем очищают с помощью препаративной ВЭЖХ, получая 224 мг (выход 28%) [2-(4-изопропилпиперазин-1-ил)бензотиазол-6-ил]морфолин-4 илметанонтрифторацетата. 1 ЯМР (300 МГц, D2O)7,64 (с, 1 Н), 7,40 (д, 2 Н), 7,29 (дд, 1 Н), 4,02-4,23 (м, 2 Н), 3,49-3,69 (м, 11 Н),3,35-3,49 (м, 2 Н), 3,07-3,28 (м, 2 Н), 1,19 (с, 6 Н). Пример 9 (общая методика Е). 2-(4-Изопропилпиперазин-1-ил)-6-пиперидин-1-илметилбензотиазол.(150 мл) при температуре -78 С по каплям добавляют DIBAL-H (175 мл, 0,0175 моль). После добавления смесь оставляют нагреваться до температуры -40 С и перемешивают в течение 1 ч при этой температуре. По каплям добавляют смесь Н 2 О/ТГФ (1:4, 250 мл). Смесь оставляют нагреваться до комнатной температуры и затем отфильтровывают. Летучие вещества выпаривают из фильтрата. Остаток очищают с помощью колоночной хроматографии на силикагеле, элюируя смесью CH2Cl2/MeOH (20:1), получая 2,5 г (выход 49%) 2-(4-изопропилпиперазин-1-ил)бензотиазол-6-карбоксальдегида. 1H ЯМР (300 МГц, CDCl3)1,10 (д, 6 Н), 2,69 (т, 4 Н), 2,81-2,85 (М, 1 Н), 3,74 (т, 4 Н), 7,58 (д, 1 Н),7,79 (дд, 1 Н), 8,12 (д, 1 Н), 9,92 (с, 1 Н). Стадия В. К раствору 2-(4-изопропилпиперазин-1-ил)бензотиазол-6-карбоксальдегида (0,5 г, 1,73 ммоль) и АсОН (11 мг, 0,173 ммоль) в ТГФ (5 мл) по очереди добавляют пиперазин (0,34 мл, 3,46 ммоль) иNaCNBH3 (132 мг, 2,08 ммоль). Реакционную смесь нагревают при температуре 63 С в течение 12 ч. Растворитель удаляют и смесь экстрагируют этилацетатом, промывают водой и насыщенным солевым раствором и сушат (MgSO4). Летучие вещества выпаривают и остаток очищают с помощью колоночной хроматографии на силикагеле, элюируя смесью этилацетата и метанола (10:1), получая 160 мг (выход 26%) 2-(4-изопропилпиперазин-1-ил)-6-пиперидин-1-илметилбензотиазола. 1 Н ЯМР (300 МГц, CD3OD)1,10 (д, 6 Н), 1,59 (м, 2 Н), 1,72-1,76 (м, 4 Н), 2,70 (т, 4 Н), 2,72-2,79 (м,1 Н), 2,92 (ушир.с, 4 Н), 3,65 (т, 4 Н), 4,03 (с, 2 Н), 7,35 (дд, 1 Н), 7,49 (д, 1 Н), 7,75 (с, 1 Н). Пример 10 (общая методика Е). 2-(4-Изопропилпиперазин-1-ил)-6-(морфолин-4-илметил)бензотиазолтрифторацетат. К раствору 2-(4-изопропилпиперазин-1-ил)бензотиазол-6-карбоксальдегида (0,5 г, 1,73 ммоль) и АсОН (11 мг, 0,173 ммоль) в ТГФ (5 мл) по очереди добавляют морфолин (0,31 мл, 3,4 6 ммоль) иNaCNBH3 (132 мг, 2,08 ммоль). Реакционную смесь нагревают при температуре 63 С в течение 12 ч. Растворитель удаляют и смесь экстрагируют этилацетатом, промывают водой и насыщенным солевым раствором и сушат (MgSO4). Летучие вещества выпаривают и остаток очищают с помощью препаративной ВЭЖХ, получая 130 мг (выход 21%) 2-(4-изопропилпиперазин-1-ил)-6-(морфолин-4-илметил)бензотиазолтрифторацетата. 1 Н ЯМР (300 МГц, D2O)1,25 (д, 6 Н), 3,07-3,32 (м, 6 Н), 3,49-3,66 (м, 7 Н), 3,96 (д, 2 Н), 4,20 (д, 2 Н),4,31 (с, 2 Н), 7,37 (дд, 1 Н), 7,49 (д, 1 Н), 7,75 (с, 1 Н). Пример 11 (общая методика Е). К раствору 2-(4-изопропилпиперазин-1-ил)бензотиазол-6-карбоксальдегида (0,7 г, 2,42 ммоль) и АсОН (291 мг, 4,84 ммоль) в ТГФ по очереди добавляют диметиламингидрохлорид (3 97 мг, 4,84 ммоль) и NaCNBH3 (245 мг, 3,88 ммоль). Реакционную смесь нагревают при температуре 63 С в течение 12 ч. Растворитель удаляют и смесь экстрагируют этилацетатом, промывают водой и насыщенным солевым раствором и сушат (MgSO4). Летучие вещества выпаривают и остаток очищают с помощью препаративной ВЭЖХ, получая 250 мг (выход 32%) [2-(4-изопропилпиперазин-1-ил)бензотиазол-6 илметил]диметиламинтрифторацетата. 1(50 мл) добавляют гидроксиламингидрохлорид (3,6 г, 52,4 ммоль), воду (8 мл) и карбонат калия (7,2 г,52,4 ммоль). Реакционную смесь кипятят в течение ночи с обратным холодильником. Эту смесь оставляют охлаждаться и затем концентрируют в вакууме. Остаток растворяют в ТГФ (30 мл) и затем отфильтровывают. Фильтрат концентрируют в вакууме, получая 4 г сырого N-гидрокси-2-(4 изопропилпиперазин-1-ил)бензотиазол-6-карбоксамидина. 1H ЯМР (300 МГц, ДМСО-d6):9,50 (с, 1 Н), 7,98 (с, 1 Н), 7,55 (д, 1 Н), 7,36 (д, 1 Н), 5,73 (с, 2 Н), 3,473,52 (м, 4 Н), 2,61-2,72 (м, 1 Н), 2,49-2,59 (м, 4 Н), 0,94 (д, 6 Н). Стадия В. Раствор N-гидрокси-2-(4-изопропилпиперазин-1-ил)бензотиазол-6-карбоксамидина (700 мг, 2,19 ммоль) в уксусном ангидриде (20 мл) нагревают при температуре 130 С в течение 6 ч. Растворитель удаляют при пониженном давлении и остаток очищают с помощью препаративной ВЭЖХ, получая 125 мг К раствору N-гидрокси-2-(4-изопропилпиперазин-1-ил)бензотиазол-6-карбоксамидина (650 мг, 2,04 ммоль) в уксусной кислоте (40 мл) добавляют бензоилхлорид (3 мл). Реакционную смесь перемешивают в течение ночи при комнатной температуре и затем кипятят с обратным холодильником в течение 2 ч. Реакционную смесь концентрируют в вакууме и остаток растворяют в 0,5 н. растворе соляной кислоты(30 мл). Водный раствор экстрагируют диэтиловым эфиром (3 раза по 15 мл). Органический слой удаляют и водную фазу подщелачивают до рН 13 4 н. раствором гидроксида натрия и затем экстрагируют этилацетатом (4 раза по 10 мл). Объединенные органические экстракты выпаривают и остаток три раза перекристаллизовывают из смеси CH2Cl2 и МеОН, получая 189 мг (выход 26%) 2-(4-изопропилпиперазин-1 ил)-6-(5-фенил-[1,2,4]оксадиазол-3-ил)бензотиазола. 1 К раствору N-гидрокси-2-(4-изопропилпиперазин-1-ил)бензотиазол-6-карбоксамидина (1,30 г, 4,07 ммоль) в уксусной кислоте (50 мл) добавляют изоникотиноилхлорид (1,42 г, 10,0 ммоль). Реакционную смесь перемешивают в течение ночи при комнатной температуре и затем кипятят с обратным холодильником в течение 8 ч. Реакционную смесь концентрируют в вакууме и остаток растворяют в 0,5 н. растворе соляной кислоты (40 мл). Водный раствор экстрагируют диэтиловым эфиром (3 раза по 15 мл). Органические экстракты удаляют и водную фазу подщелачивают до рН 13 4 н. раствором гидроксида натрия и затем экстрагируют этилацетатом (4 раза по 10 мл). Объединенные органические экстракты выпаривают и остаток перекристаллизовывают из смеси CH2Cl2 и МеОН, получая 175 мг (выход 11%) 2-(4 изопропилпиперазин-1-ил)-6-(5-пиридин-4-ил-[1,2,4]оксадиазол-3-ил)бензотиазола. 1(5,04 мл, 36,3 ммоль) и 1-циклопентилпиперазин (1,86 г, 12,1 ммоль). Реакционную смесь кипятят с обратным холодильником в течение 16 ч и затем концентрируют при пониженном давлении. Остаток экстрагируют этилацетатом и объединенные органические экстракты промывают насыщенным солевым раствором, сушат (Na2SO4) и концентрируют при пониженном давлении, получая 4,3 г (выход 99%) 6-бром 2-(4-циклопентилпиперазин-1-ил)бензотиазола. Стадия В. К раствору 6-бром-2-(4-циклопентилпиперазин-1-ил)бензотиазола (0,54 г, 1,50 ммоль) в Nметилпирролидин-2-оне (100 мл) добавляют иодид меди(I) (344 мг, 1,80 ммоль) и цианид меди(I) (270 мг,3,0 ммоль). Эту смесь нагревают при температуре 160 С в течение 4 ч, затем оставляют охлаждаться до комнатной температуры и отфильтровывают. Фильтровальный осадок промывают этилацетатом и фильтрат экстрагируют этилацетатом. Объединенные органические экстракты промывают насыщенным солевым раствором, сушат (Na2SO4) и концентрируют при пониженном давлении. Остаток очищают с помощью препаративной ВЭЖХ, получая 140 мг (выход 30%) 2-(4-циклопентилпиперазин-1 ил)бензотиазол-6-карбонитрила. 1 К раствору 2-(4-циклопропилпиперазин-1-ил)бензотиазол-6-карбоксальдегида (500 мг, 1,7 ммоль) в метаноле (14 мл) и ТГФ (28 мл) добавляют диметиламингидрохлорид (277 мг, 3,4 ммоль), уксусную кислоту (22 мг, 0,4 ммоль) и NaCNBH3 (158 мг, 2,7 ммоль). Смесь перемешивают при температуре 63 С в течение ночи. Затем полученную смесь концентрируют при пониженном давлении и остаток разбавляют дихлорметаном (15 мл). Смесь промывают насыщенным солевым раствором и органическую фазу сушат(MgSO4) и концентрируют при пониженном давлении. Остаток очищают с помощью препаративной ВЭЖХ, получая 367 мг (выход 32%) [2-(4-циклопропилпиперазин-1-ил)бензотиазол-6-илметил]диметиламинтрифторацетата. 1- 25015569 К раствору 2-(4-циклопропилпиперазин-1-ил)бензотиазол-6-карбоксальдегида (500 мг, 1,7 ммоль) в МеОН (14 мл) и ТГФ (28 мл) добавляют пирролидин (242 мг, 3,4 ммоль), уксусную кислоту (22 мг, 0,4 ммоль) и NaCNBH3 (158 мг, 2,7 ммоль). Эту смесь перемешивают при температуре 63 С в течение ночи. Затем смесь концентрируют при пониженном давлении и добавляют дихлорметан (15 мл). Смесь промывают насыщенным солевым раствором и органическую фазу сушат (MgSO4) и концентрируют при пониженном давлении. Остаток очищают с помощью препаративной ВЭЖХ, получая 318 мг (выход 27%) 2(4-циклопропилпиперазин-1-ил)-6-(пирролидин-1-илметил)бензотиазолтрифторацетата. 1 Н ЯМР (400 МГц, D2O)7,80 (с, 1 Н), 7,53 (д, 1 Н), 7,42 (д, 1 Н), 4,34 (с, 2 Н), 4,30-3,48 (м, 8 Н), 3,483,35 (м, 2 Н), 3,19-3,05 (м, 2 Н), 2,90-2,80 (м, 1 Н), 2,15-1,97 (м, 2 Н), 1,97-1,80 (м, 2 Н), 1,05-0,88 (м, 4 Н). ВЭЖХ (метод В): tr = 2,02 мин (97,9%). Пример 18 (общая методика Е). 2-(4-Циклопропилпиперазин-1-ил)-6-(морфолин-4-илметил)бензотиазолтрифторацетат. К раствору 2-(4-циклопропилпиперазин-1-ил)бензотиазол-6-карбоксальдегида (500 мг, 1,7 ммоль) в МеОН (14 мл) и ТГФ (28 мл) добавляют морфолин (296 мг, 3,4 ммоль), уксусную кислоту (22 мг, 0,4 ммоль) и NaCNBH3 (158 мг, 2,7 ммоль). Эту смесь перемешивают при температуре 63 С в течение ночи. Затем полученную смесь концентрируют при пониженном давлении и остаток разбавляют дихлорметаном (15 мл). Смесь промывают насыщенным солевым раствором, сушат (MgSO4) и концентрируют при пониженном давлении. Остаток очищают с помощью препаративной ВЭЖХ, получая 306 мг (выход 31%) 2-(4-циклопропилпиперазин-1-ил)-6-(морфолин-4-илметил)бензотиазолтрифторацетата. 1 Суспензию 2-хлорбензотиазол-6-карбонитрила (3,5 г, 18 ммоль), 1-циклопропилпиперазина (3,63 г,28,8 ммоль) и хлорида аммония (0,96 г, 18 ммоль) в бутан-1-оле (112 мл) кипятят с обратным холодильником в течение 48 ч. Растворитель удаляют при пониженном давлении и остаток разбавляют водой (30 мл). Эту смесь подщелачивают карбонатом калия и экстрагируют CH2Cl2 (3 раза по 20 мл). Объединенные органические экстракты концентрируют, получая остаток, который очищают с помощью колоночной хроматографии на силикагеле (20% этилацетата в петролейном эфире), получая 2,2 г (выход 43%) 2(4-циклопропилпиперазин-1-ил)бензотиазол-6-карбонитрила. Стадия В. 2-(4-Циклопропилпиперазин-1-ил)бензотиазол-6-карбальдегид. К раствору 2-(4-циклопропилпиперазин-1-ил)бензотиазол-6-карбонитрила (2 г, 7 ммоль) в толуоле по каплям добавляют DIBAH (15,5 мл, 15,5 ммоль, 1 М раствор в толуоле) при комнатной температуре и продолжают перемешивать в течение 1 ч при комнатной температуре. Реакционную смесь гасят H2SO4(5%-ный раствор в воде). Смесь отфильтровывают и фильтрат экстрагируют этилацетатом (3 раза по 20 мл). Объединенные органические экстракты концентрируют, получая 1,7 г (выход 85%) 2-(4 циклопропилпиперазин-1-ил)бензотиазол-6-карбоксальдегида. 1H ЯМР (300 МГц, CDCl3)9,92 (с, 1 Н), 8,12 (д, 1 Н), 7,79 (дд, 1 Н), 7,57 (д, 1 Н), 3,66 (т, 4 Н), 2,75 (т,4 Н), 1,75-1,65 (м, 1 Н), 0,55-0,40 (м, 4 Н). Стадия С. К раствору 2-(4-циклопропилпиперазин-1-ил)бензотиазол-6-карбоксальдегида (500 мг, 1,7 ммоль) в МеОН (14 мл) и ТГФ (28 мл) добавляют пиперидин (290 мг, 3,4 ммоль), уксусную кислоту (22 мг, 0,4 ммоль) и NaCNBH3 (158 мг, 2,7 ммоль). Смесь перемешивают при температуре 63C в течение ночи. Реакционную смесь концентрируют при пониженном давлении и к остатку добавляют CH2Cl2 (15 мл). Смесь промывают насыщенным солевым раствором, сушат (MgSO4) и концентрируют при пониженном давлении. Остаток очищают с помощью препаративной ВЭЖХ, получая 332 мг (выход 28%) 2-(4 циклопропилпиперазин-1-ил)-6-(пиперидин-1-илметил)бензотиазолтрифторацетата. 1 К раствору 6-бром-2-хлорбензотиазола (8,2 г, 33 ммоль) в EtOH (115 мл) добавляют Et3N (16,7 г,165 ммоль), затем 1-циклопропилпиперазин (5 г, 39,6 ммоль). Смесь кипятят с обратным холодильником в течение 12 ч. Затем смесь выпаривают для удаления EtOH. К остатку добавляют воду (120 мл) и смесь экстрагируют CH2Cl2 (3 раза по 50 мл). Объединенные органические экстракты промывают насыщенным солевым раствором, сушат (Na2SO4) и концентрируют с получением остатка, который очищают с помощью колоночной хроматографии на силикагеле, элюируя смесью EtOAc/петролейный эфир (1:10, с добавлением 0,1% NH4OH), с получением 3,46 г (выход 31%) 6-бром-2-(4-циклопропилпиперазин-1 ил)бензотиазола. 1 Н ЯМР (300 МГц, CDCl3):7,70 (т, 1 Н), 7,38 (дд, 2 Н), 3,60 (д, 4 Н), 2,80 (д, 4 Н), 1,68 (д, 1 Н), 0,500,39 (м, 4 Н). Стадия В. Смесь 6-бром-2-(4-циклопропилпиперазин-1-ил)бензотиазола (480 мг, 1,42 ммоль), ацетамида (251 мг, 4,26 ммоль), Pd(OAc)2 (15,9 мг, 0,071 ммоль), Cs2CO3 (694 мг, 2,13 ммоль) и ксантфоса (62 мг, 0,107 ммоль) в 1,4-диоксане (10 мл) кипятят с обратным холодильником в течение 12 ч. Добавляют воду (5 мл) и смесь отфильтровывают. Фильтрат экстрагируют EtOAc (3 раза по 5 мл). Объединенные органические экстракты промывают насыщенным солевым раствором, сушат (Na2SO4) и концентрируют с получением остатка, который очищают с помощью препаративной ВЭЖХ, получая 108 мг (выход 24%) N-[2-(4 циклопропилпиперазин-1-ил)бензотиазол-6-ил]ацетамидтрифторацетата. 1 Смесь 2-(4-циклопропилпиперазин-1-ил)бензотиазол-6-карбонитрила (500 мг, 1,7 ммоль) и концентрированной HCl (5 мл) кипятят с обратным холодильником в течение ночи. Растворитель удаляют при пониженном давлении, получая сырую 2-(4-циклопропилпиперазин-1-ил)бензотиазол-6-карбоновую кислоту. Стадия В. К суспензии 2-(4-циклопропилпиперазин-1-ил)бензотиазол-6-карбоновой кислоты (530 мг, 1,76 ммоль), 1-метилпиперазина (350 мг, 3,54 ммоль) и DIEA (0,92 мл, 5,28 ммоль) в ДМФА добавляют РуВор(1,8 г, 3,52 ммоль). Полученный раствор перемешивают в течение ночи при комнатной температуре. Растворитель удаляют при пониженном давлении и остаток разбавляют водой и дихлорметаном. Фазы разделяют и органическую фазу сушат (Na2SO4) и концентрируют с получением сырого продукта, который очищают с помощью препаративной ВЭЖХ. Получают 296 мг (выход 20%) [2-(4 циклопропилпиперазин-1-ил)бензотиазол-6-ил]-(4-метилпиперазин-1-ил)метанонтрифторацетата. 1Pd2(dba)3 (240 мг, 0,148 ммоль), затем P(t-Bu)3BF4 (86 мг, 0,296 ммоль) и K3PO4-H2O (1,97 г, 7,4 ммоль). Смесь нагревают при температуре 60 С в течение 3 ч. Смесь отфильтровывают и фильтрат выпаривают. Остаток разбавляют водой (5 мл) и экстрагируют CH2Cl2 (3 раза по 5 мл). Объединенные органические экстракты сушат (Na2SO4) и концентрируют с получением сырого продукта, который очищают с помощью колоночной хроматографии на силикагеле, элюируя смесью CH2Cl2/MeOH (1:50). Получают 258 мгPd2(dba)3 (191 мг, 0,118 ммоль), затем P(t-Bu)3BF4 (68 мг, 0,236 ммоль) и K3PO4H2O (1,57 г, 5,9 ммоль). Смесь нагревают при температуре 60 С в течение 3 ч. Эту смесь отфильтровывают и фильтрат выпаривают. Остаток разбавляют водой (5 мл) и экстрагируют CH2Cl2 (3 раза по 5 мл). Объединенные органические экстракты сушат (Na2SO4) и концентрируют с получением сырого продукта, который очищают с помощью колоночной хроматографии на силикагеле, элюируя смесью CH2Cl2/MeOH (1:50). Получают 253 мг (выход 58%) 2-(4-циклопропилпиперазин-1-ил)-6-(6-метоксипиридин-3-ил)бензотиазола. 1 Н ЯМР (300 МГц, CDCl3):8,38 (д, 1H), 7,80 (дд, 1H), 7,74 (д, 1 Н), 7,59 (д, 1 Н), 7,46 (д, 1 Н), 6,81(108 мг, 0,148 ммоль), затем CH3COOK (581 мг, 5,92 ммоль). Смесь нагревают при температуре 80 С в течение 2 ч, отфильтровывают и летучие вещества выпаривают. Добавляют воду (5 мл) и смесь экстрагируют CH2Cl2 (3 раза по 5 мл). Объединенные органические экстракты сушат (Na2SO4) и концентрируют. Остаток очищают с помощью препаративной ВЭЖХ, получая 35 мг (выход 6%) 6-(5-хлор-2 метоксипиридин-4-ил)-2-(4-циклопропилпиперазин-1-ил)-бензотиазолтрифторацетата. 1 Н ЯМР (300 МГц, D2O):7,99 (с, 1 Н), 7,61 (с, 1 Н), 7,37 (д, 2 Н), 6,58 (с, 1 Н), 4,00-3,40 (м, 11 Н),2,82-2,67 (м, 1 Н), 1,03-0,83 (м, 4 Н). ВЭЖХ (метод В): tr = 4,83 мин (98,5%). Пример 25 (общая методика Е). 2-(6-Пиперидин-1-илметилбензотиазол-2-ил)октагидропиридо[1,2-а]пиразинтрифторацетат.Pd2(dba)3 (240 мг, 0,148 ммоль), затем P(t-Bu)3BF4 (86 мг, 0,296 ммоль) и K3PO4H2O (1,97 г, 7,4 ммоль). Смесь нагревают при температуре 60 С в течение 3 ч, отфильтровывают и летучие вещества выпаривают. Добавляют воду (5 мл) и смесь экстрагируют CH2Cl2 (3 раза по 20 мл). Объединенные органические экстракты сушат (Na2SO4) и концентрируют. Остаток очищают с помощью препаративной ВЭЖХ, получая 42 мг (выход 7%) N-4-[2-(4-циклопропилпиперазин-1-ил)бензотиазол-6-ил]фенилацетамидтрифторацетата. 1 К раствору 2-(4-циклопропилпиперазин-1-ил)бензотиазол-6-карбальдегида (400 мг, 1,39 ммоль) и циклопропиламина (159 мг, 2,78 ммоль) в смеси СН 3 ОН и ТГФ (40 мл, 1:3) добавляют АсОН (417 мг,6,95 ммоль), затем NaCNBH3 (140 мг, 2,22 ммоль). Смесь кипятят с обратным холодильником в течение 12 ч и затем летучие вещества выпаривают. Добавляют воду (10 мл) и смесь экстрагируют CH2Cl2 (3 раза по 15 мл). Объединенные органические экстракты сушат (Na2SO4) и концентрируют. Остаток очищают с помощью препаративной ВЭЖХ, получая 362 мг (выход 79%) циклопропил[2-(4-циклопропилпиперазин 1-ил)бензотиазол-6-илметил]аминтрифторацетата. 1 Н ЯМР (300 МГц, CD3OD):7,87 (д, 1 Н), 7,60 (д, 1 Н), 7,46 (дд, 1 Н), 4,38 (с, 2 Н), 4,10-3,85 (м, 4 Н),3,65-3,55 (м, 4 Н), 2,95-2,85 (м, 1 Н), 2,85-2,72 (м, 1 Н), 1,15-0,80 (м, 8 Н). ВЭЖХ (метод В): tr = 2,63 мин (99,8%). Пример 28 (общая методика N). 2-(4-Циклопропилпиперазин-1-ил)-6-(1,1-диоксо-16-изотиазолидин-2-илметил)бензотиазол. К раствору 2-(4-циклопропилпиперазин-1-ил)бензотиазол-6-карбонитрила (1 г, 3,52 ммоль) в смеси МеОН-ТГФ (120 мл, 5:3) добавляют NH4OH (15 мл) и никель Ренея (200 мг). Смесь перемешивают в течение 12 ч при комнатной температуре, при давлении в 50 фунт/кв.дюйм, в атмосфере водорода. После фильтрации смесь концентрируют, получая 6-аминометил-2-(4-циклопропилпиперазин-1-ил)бензотиазол(500 мг, выход 49,3%), который используют на следующей стадии без дальнейшей очистки. Стадия В. [2-(4-Циклопропилпиперазин-1-ил)бензотиазол-6-илметил]амид 3-хлорпропан-1 сульфоновой кислоты.CH2Cl2 (15 мл) добавляют триэтиламин (879 мг, 8,2 ммоль). Смесь перемешивают при температуре 0 С в течение 5 мин и затем по каплям добавляют 3-хлорпропан-1-сульфонилхлорид (308 мг, 1,74 ммоль). Смесь перемешивают при температуре 0 С в течение 1 ч и затем оставляют постепенно достигать комнатной температуры. Затем смесь перемешивают в течение следующего часа при комнатной температуре. Летучие вещества выпаривают и остаток экстрагируют CH2Cl2. Получают сырой продукт, который очищают с помощью колоночной хроматографии на силикагеле (элюент: 5% CH2Cl2 в метаноле), полу- 29
МПК / Метки
МПК: C07D 263/58, C07D 277/82, C07D 413/04, C07D 471/04, A61P 25/00, A61K 31/496, A61K 31/4985, A61P 9/00, C07D 417/06, C07D 417/04
Метки: отношению, фармацевтические, гистамина, бензотиазолы, антагонистической, h3-рецептору, включающие, активностью, обладающие, эти, композиции, соединения
Код ссылки
<a href="https://eas.patents.su/30-15569-benzotiazoly-obladayushhie-antagonisticheskojj-aktivnostyu-po-otnosheniyu-k-h3-receptoru-gistamina-i-farmacevticheskie-kompozicii-vklyuchayushhie-eti-soedineniya.html" rel="bookmark" title="База патентов Евразийского Союза">Бензотиазолы, обладающие антагонистической активностью по отношению к h3-рецептору гистамина, и фармацевтические композиции, включающие эти соединения</a>
Предыдущий патент: Привитой сополимер крахмал-( мет)акрилата, набухаемые в масле или в масле и воде материалы и изготовленные из них изделия
Следующий патент: Фармацевтическая композиция
Случайный патент: Композиция, обладающая ноотропными свойствами, и способ ее получения


































