Спиро[1,3]оксазины и спиро[1,4]оксазепины в качестве ингибиторов bace1 и(или) bace2
Номер патента: 24286
Опубликовано: 30.09.2016
Авторы: Востль Вольфганг, Наркизан Робер, Пинар Эмманьюэль
Формула / Реферат
1. Соединение формулы I
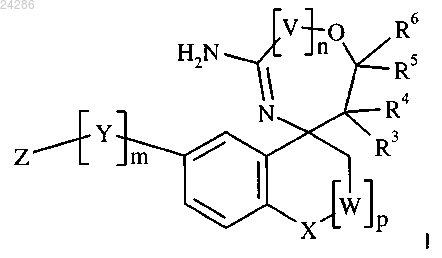
где V представляет собой -CR7aR7b-;
W представляет собой -CR2aR2b-;
X представляет собой -CR1aR1b-, -О-, -S- или -SO2-;
Y представляет собой -NH-C=O-;
Z выбран из группы, состоящей из следующего:
i) 6-членный гетероарил, содержащий 2 гетероатома N;
ii) 5-6-членный гетероарил, содержащий 1-2 гетероатома N, замещенный 1-2 заместителями, независимо выбранными из R8;
iii) фенил, замещенный 1-2 заместителями, независимо выбранными из R8;
R1a выбран из группы, состоящей из следующего:
i) водород;
ii) галоген;
iii) C1-6алкил;
R1b выбран из группы, состоящей из следующего:
i) водород;
ii) галоген;
iii) C1-6алкил;
R2a выбран из группы, состоящей из следующего:
i) водород;
ii) C1-6алкил;
R2b выбран из группы, состоящей из следующего:
i) водород;
ii) фенил;
iii) С1-6алкил;
или R2a и R2b вместе с атомом углерода, к которому они присоединены, образуют 6-членный гетероциклил, содержащий 1 гетероатом О;
R3 выбран из группы, состоящей из галогена;
R4 выбран из группы, состоящей из галогена;
R5 выбран из группы, состоящей из водорода;
R6 выбран из группы, состоящей из водорода;
R7a выбран из группы, состоящей из водорода;
R7b выбран из группы, состоящей из водорода;
R8 выбран из группы, состоящей из следующего:
i) циано;
ii) галоген;
iii) галоген-С1-6алкил, С1-6алкокси;
n представляет собой 0 или 1;
m представляет собой 0 или 1;
р представляет собой 0 или 1,
или его фармацевтически приемлемые соли.
2. Соединение по п.1, где
V представляет собой -CR7aR7b-;
W представляет собой -CR2aR2b-;
X представляет собой -CR1aR1b-, -О-, -S- или -SO2-;
Y представляет собой -NH-C=O-;
Z выбран из группы, состоящей из следующего:
i) 6-членный гетероарил, содержащий 2 гетероатома N;
ii) 5-6-членный гетероарил, содержащий 1-2 гетероатома N, замещенный 1-2 заместителями, независимо выбранными из R8;
iii) фенил, замещенный 1-2 заместителями, независимо выбранными из R8;
R1a выбран из группы, состоящей из следующего:
i) водород;
ii) галоген;
iii) C1-6алкил;
R1b выбран из группы, состоящей из следующего:
i) водород;
ii) галоген;
iii) C1-6алкил;
R2a выбран из группы, состоящей из следующего:
i) водород;
ii) C1-6алкил;
R2b выбран из группы, состоящей из следующего:
i) водород;
ii) фенил;
iii) C1-6алкил;
или R2a и R2b вместе с атомом углерода, к которому они присоединены, образуют тетрагидропиранил;
R3 представляет собой галоген;
R4 представляет собой галоген;
R5 представляет собой водород;
R6 представляет собой водород;
R7a представляет собой водород;
R7b представляет собой водород;
R8 выбран из группы, состоящей из следующего:
i) циано;
ii) галоген;
iii) галоген-C1-6алкил;
iv) C1-6алкокси;
n представляет собой 0 или 1;
m представляет собой 0 или 1;
р представляет собой 0 или 1,
или его фармацевтически приемлемые соли.
3. Соединение по любому из пп.1, 2, где n представляет собой 0.
4. Соединение по любому из пп.1-3, где X представляет собой -CR1aR1b- и оба R1a и R1b являются водородом.
5. Соединение по любому из пп.1-4, где р представляет собой 0.
6. Соединение по любому из пп.1-3, где X представляет собой -О-.
7. Соединение по пп.1-2 и 6, где р представляет собой 1; W представляет собой -CR2aR2b- и оба R2a и R2b являются водородом.
8. Соединение по любому из пп.1-7, где R3 представляет собой F.
9. Соединение по любому из пп.1-8, где R4 представляет собой F.
10. Соединение по любому из пп.1-9, где m представляет собой 0.
11. Соединение по любому из пп.1-9, где m представляет собой 1.
12. Соединение по любому из пп.1-11, где Z представляет собой 5-6-членный гетероарил, содержащий 1-2 гетероатома N, замещенный галогеном или циано.
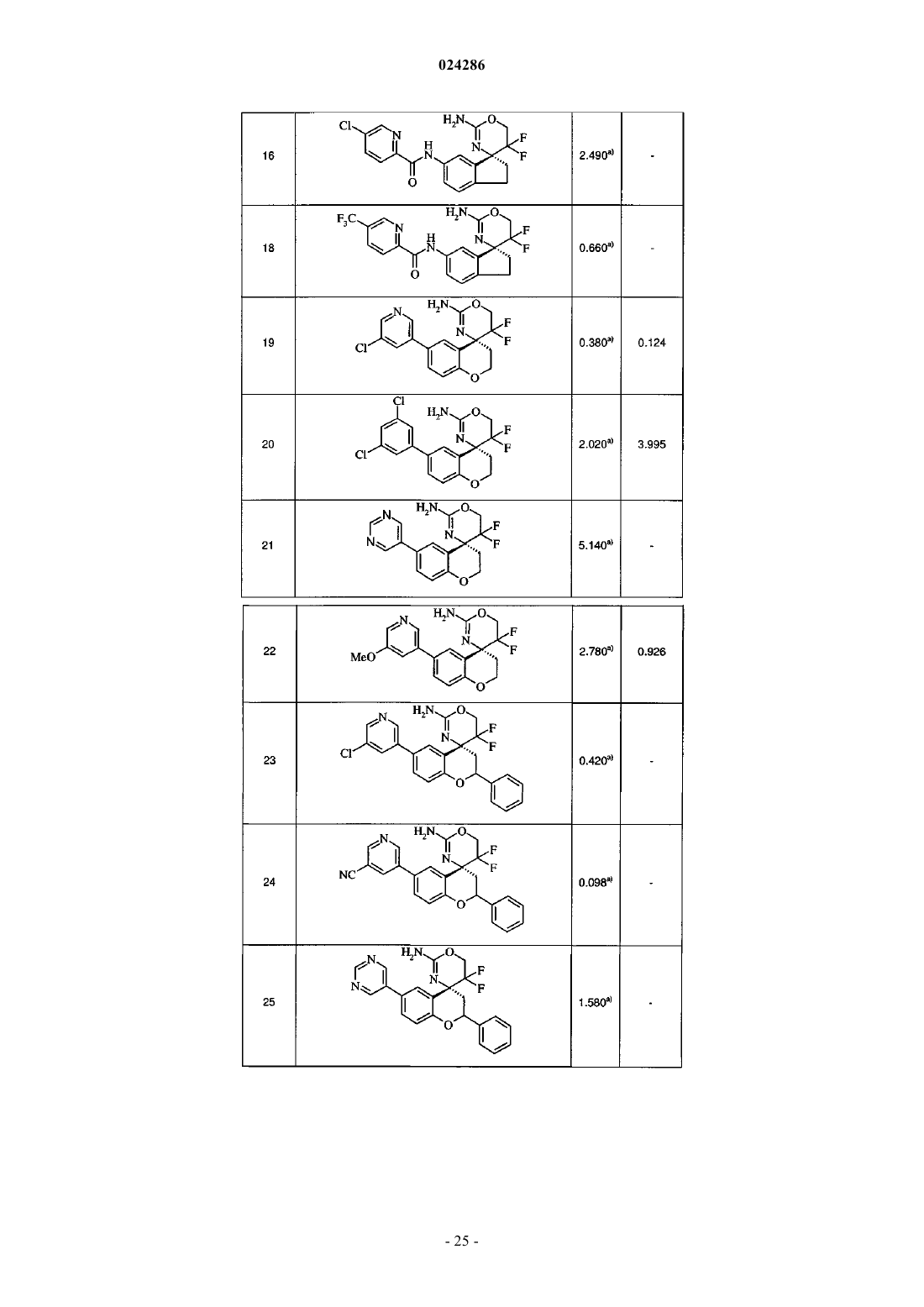
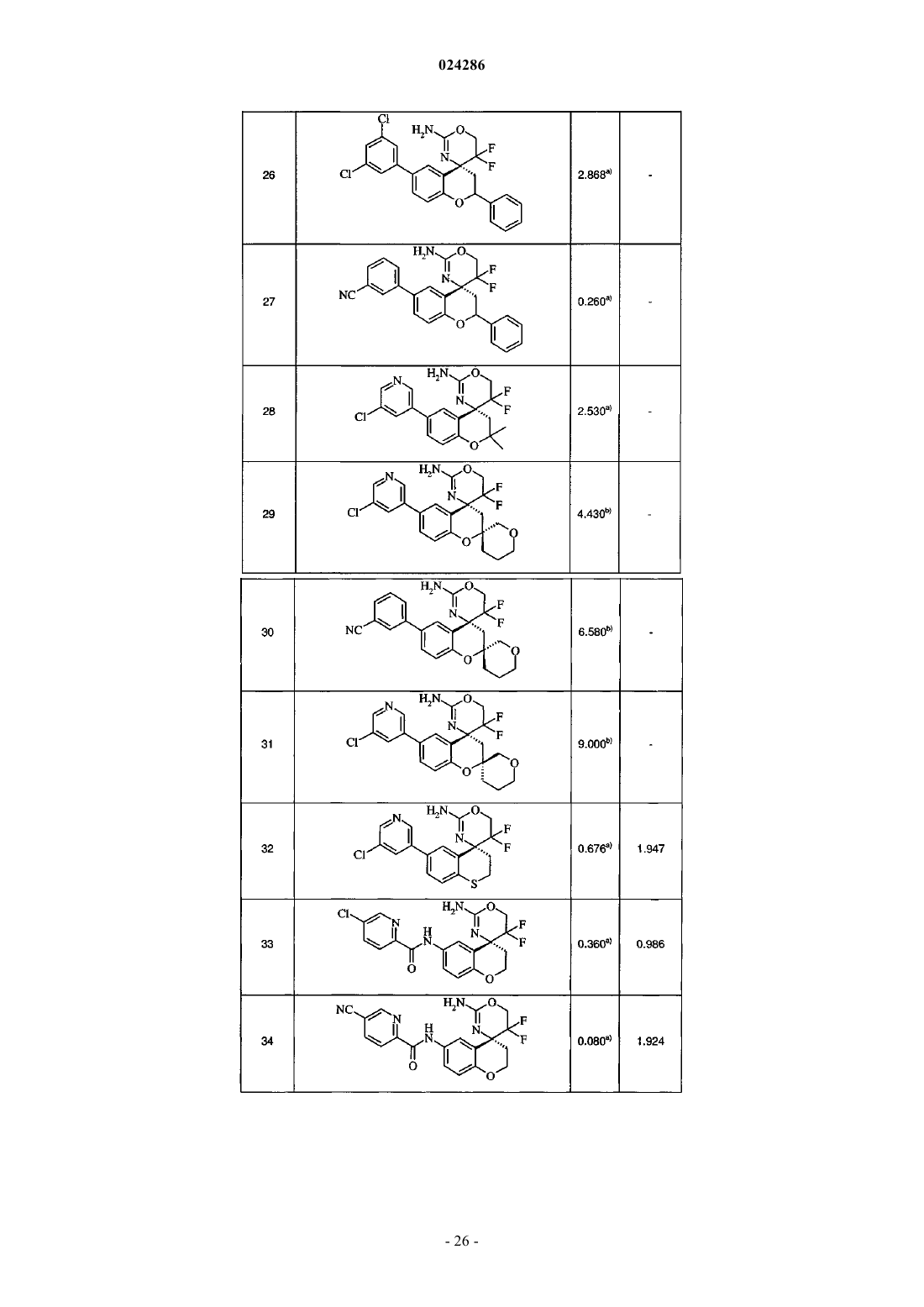
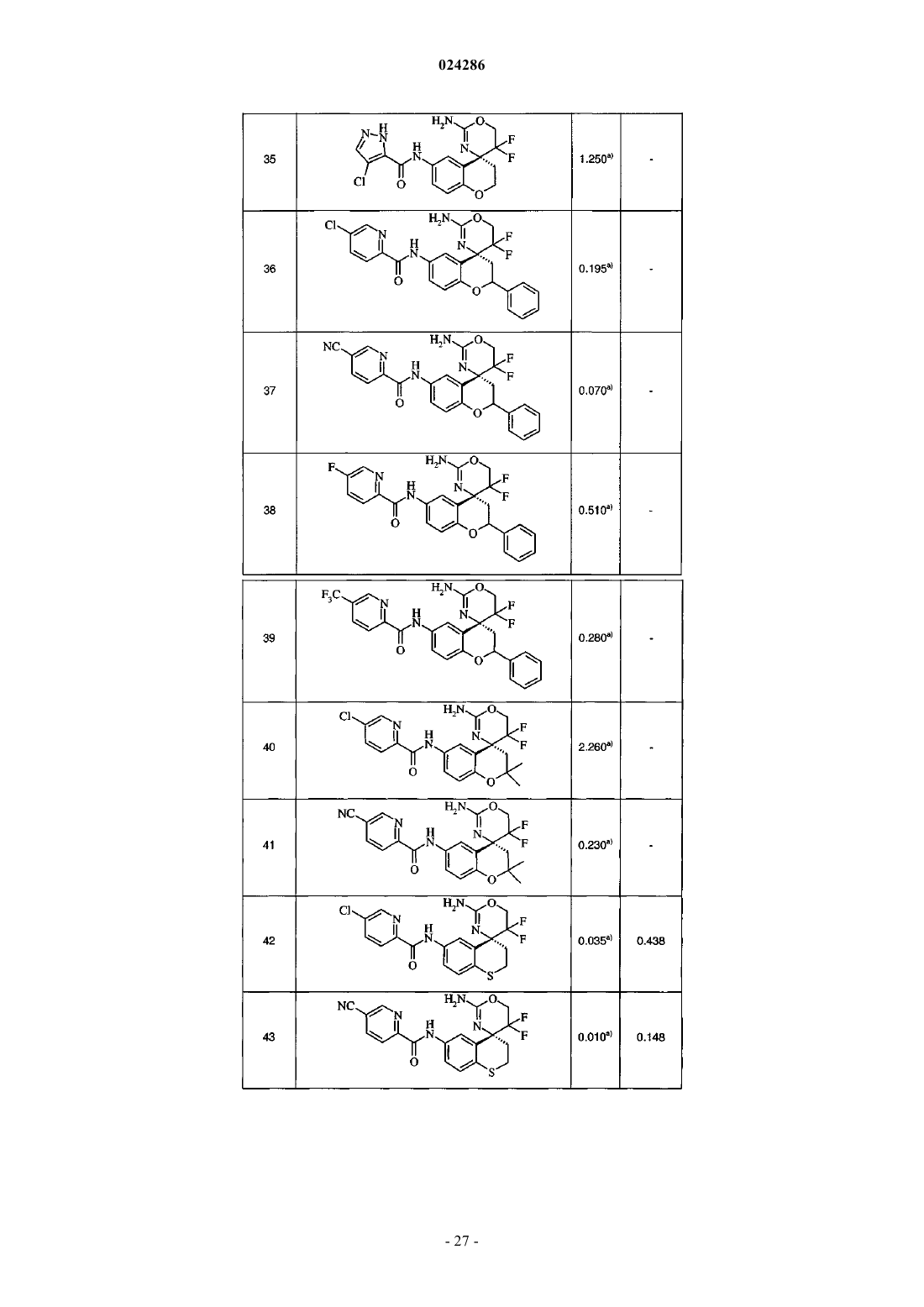
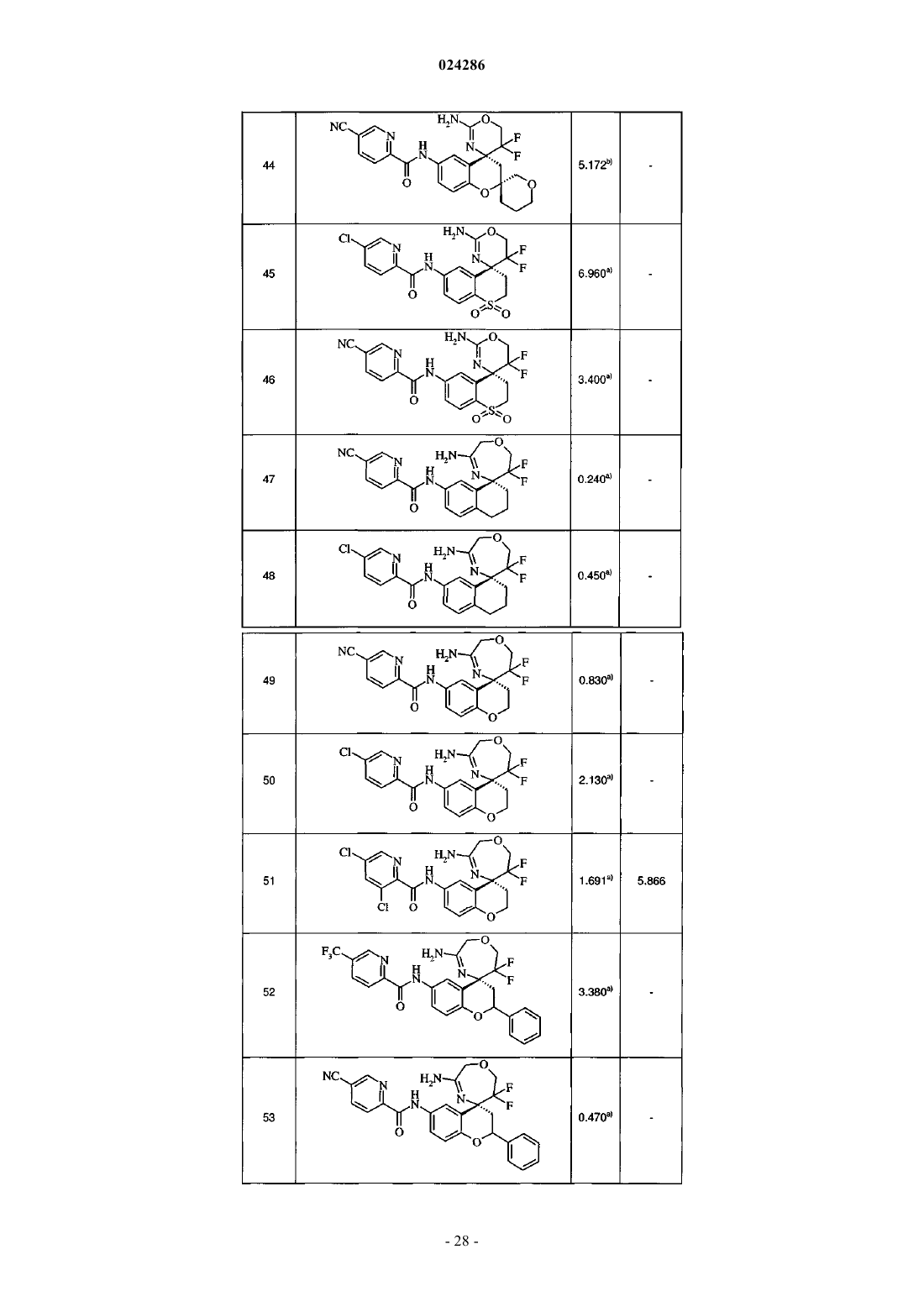
13. Соединение по любому из пп.1-12, выбранное из группы, состоящей из
(R)-7-(5-хлорпиридин-3-ил)-5',5'-дифтор-3,4,5',6'-тетрагидро-2Н-спиро[нафтален-1,4'-[1,3]оксазин]-2'-амина,
(2'R,4R)-6'-(5-хлорпиридин-3-ил)-5,5-дифтор-5,5",6,6"-тетрагидро-4"Н-диспиро[1,3-оксазин-4,4'-хромен-2',3"-пиран]-2-амина формиата,
(2RS,4R)-5',5'-дифтор-2-фенил-6-(пиримидин-5-ил)-5',6'-дигидроспиро[хроман-4,4'-[1,3]оксазин]-2'-амина,
(2RS,4R)-6-(3,5-дихлорфенил)-5',5'-дифтор-2-фенил-5',6'-дигидроспиро[хроман-4,4'-[1,3]оксазин]-2'-амина,
(2RS,4R)-6-(3,5-дихлорфенил)-6',6'-дифтор-2-фенил-6',7'-дигидро-2'H-спиро[хроман-4,5'-[1,4]оксазепин]-3'-амина,
(2RS,4R)-6-(5-хлорпиридин-3-ил)-5',5'-дифтор-2-фенил-5',6'-дигидроспиро[хроман-4,4'-[1,3]оксазин]-2'-амина,
(2RS,4R)-6-(5-хлорпиридин-3-ил)-6',6'-дифтор-2-фенил-6',7'-дигидро-2'Н-спиро[хроман-4,5'-[1,4]оксазепин]-3'-амина,
(2RS,4R)-6',6'-дифтор-2-фенил-6-(пиримидин-5-ил)-6',7'-дигидро-2'Н-спиро[хроман-4,5'-[1,4]оксазепин]-3'-амина,
(2'S,4R)-6'-(5-хлорпиридин-3-ил)-5,5-дифтор-5,5",6,6"-тетрагидро-4"Н-диспиро[1,3-оксазин-4,4'-хромен-2',3"-пиран]-2-амина формиата,
(R)-3-(2'-амино-5',5'-дифтор-2,3,5',6'-тетрагидроспиро[инден-1,4'-[1,3]оксазин]-6-ил)бензонитрила,
(R)-4,4,5',5'-тетрафтор-7-(5-фторпиридин-3-ил)-3,4,5',6'-тетрагидро-2Н-спиро[нафтален-1,4'-[1,3]оксазин]-2'-амина,
(R)-5-(2'-амино-4,4,5',5'-тетрафтор-3,4,5',6'-тетрагидро-2Н-спиро[нафтален-1,4'-[1,3]оксазин]-7-ил)никотинонитрила,
(R)-5-(2'-амино-5',5'-дифтор-2,3,5',6'-тетрагидроспиро[инден-1,4-[1,3]оксазин]-6-ил)никотинонитрила,
(R)-5-(2'-амино-5',5'-дифтор-3,4,5',6'-тетрагидро-2Н-спиро[нафтален-1,4'-[1,3]оксазин]-7-ил)никотинонитрила,
(R)-5',5'-дифтор-6-(5-метоксипиридин-3-ил)-5',6'-дигидроспиро[хроман-4,4'-[1,3]оксазин]-2'-амина,
(R)-5',5'-дифтор-6-(пиримидин-5-ил)-2,3,5',6'-тетрагидроспиро[инден-1,4'-[1,3]оксазин]-2'-амина,
(R)-5',5'-дифтор-6-(пиримидин-5-ил)-5',6'-дигидроспиро[хроман-4,4'-[1,3]оксазин]-2'-амина,
(R)-6-(2-хлорпиридин-4-ил)-5',5'-дифтор-2,3,5',6'-тетрагидроспиро[инден-1,4'-[1,3]оксазин]-2'-амина,
(R)-6-(3,5-дихлорфенил)-5',5'-дифтор-2,3,5',6'-тетрагидроспиро[инден-1,4'-[1,3]оксазин]-2'-амина,
(R)-6-(3,5-дихлорфенил)-5',5'-дифтор-5',6'-дигидроспиро[хроман-4,4'-[1,3]оксазин]-2'-амина,
(R)-6-(3,5-дихлорфенил)-6',6'-дифтор-6',7'-дигидро-2'Н-спиро[хроман-4,5'-[1,4]оксазепин]-3'-амина,
(R)-6-(5-хлорпиридин-3-ил)-5',5'-дифтор-2,2-диметил-5',6'-дигидроспиро[хроман-4,4'-[1,3]оксазин]-2'-амина,
(R)-6-(5-хлорпиридин-3-ил)-5',5'-дифтор-2,3,5',6'-тетрагидроспиро[инден-1,4'-[1,3]оксазин]-2'-амина,
(R)-6'-(5-хлорпиридин-3-ил)-5,5-дифтор-5,6-дигидроспиро[[1,3]оксазин-4,4'-тиохроман]-2-амина,
(R)-6-(5-хлорпиридин-3-ил)-5',5'-дифтор-5',6'-дигидроспиро[хроман-4,4'-[1,3]оксазин]-2'-амина,
(R)-6-(5-хлорпиридин-3-ил)-6',6'-дифтор-6',7'-дигидро-2'Н-спиро[хроман-4,5'-[1,4]оксазепин]-3'-амина,
(R)-7-(5-хлорпиридин-3-ил)-4,4,5',5'-тетрафтор-3,4,5',6'-тетрагидро-2Н-спиро[нафтален-1,4'-[1,3]оксазин]-2'-амина,
(R)-N-(2'-амино-5',5'-дифтор-2,2-диметил-5',6'-дигидроспиро[хроман-4,4'-[1,3]оксазин]-6-ил)-5-хлорпиколинамида,
(R)-N-(2'-амино-5',5'-дифтор-2,2-диметил-5',6'-дигидроспиро[хроман-4,4'-[1,3]оксазин]-6-ил)-5-цианопиколинамида,
(R)-N-(2'-амино-5',5'-дифтор-2,3,5',6'-тетрагидроспиро[инден-1,4'-[1,3]оксазин]-6-ил)-5-цианопиколинамида,
(R)-N-(2'-амино-5',5'-дифтор-2,3,5',6'-тетрагидроспиро[инден-1,4'-[1,3]оксазин]-6-ил)-5-хлорпиколинамида,
(R)-N-(2'-амино-5',5'-дифтор-2,3,5',6'-тетрагидроспиро[инден-1,4'-[1,3]оксазин]-6-ил)-5-фторпиколинамида,
(R)-N-(2'-амино-5',5'-дифтор-2,3,5',6'-тетрагидроспиро[инден-1,4'-[1,3]оксазин]-6-ил)-5-(трифторметил)пиколинамида,
(R)-N-(2'-амино-5',5'-дифтор-3,4,5',6'-тетрагидро-2Н-спиро[нафтапен-1,4'-[1,3]оксазин]-7-ил)-5-хлорпиколинамида,
(R)-N-(2'-амино-5',5'-дифтор-3,4,5',6'-тетрагидро-2Н-спиро[нафтален-1,4'-[1,3]оксазин]-7-ил)-5-цианопиколинамида,
(R)-N-(2'-амино-5',5'-дифтор-4,4-диметил-3,4,5',6'-тетрагидро-2Н-спиро[нафтален-1,4'-[1,3]оксазин]-7-ил)-5-цианопиколинамида,
(R)-N-(2-амино-5,5-дифтор-5,6-дигидроспиро[[1,3]оксазин-4,4'-тиохроман]-6'-ил)-5-хлорпиколинамида,
(R)-N-(2-амино-5,5-дифтор-5,6-дигидроспиро[[1,3]оксазин-4,4'-тиохроман]-6'-ил)-5-цианопиколинамида,
(R)-N-(2'-амино-5',5'-дифтор-5',6'-дигидроспиро[хроман-4,4'-[1,3]оксазин]-6-ил)-5-хлорпиколинамида,
(R)-N-(2'-амино-5',5'-дифтор-5',6'-дигидроспиро[хроман-4,4'-[1,3]оксазин]-6-ил)-5-цианопиколинамида,
(R)-N-(2'-амино-5',5'-дифтор-5',6'-дигидроспиро[хроман-4,4'-[1,3]оксазин]-6-ил)-4-хлор-1Н-пиразол-5-карбоксамида,
(R)-N-(3'-амино-6',6'-дифтор-3,4,6',7'-тетрагидро-2Н,2'Н-спиро[нафтален-1,5'-[1,4]оксазепин]-7-ил)-5-цианопиколинамида,
(R)-N-(3'-амино-6',6'-дифтор-3,4,6',7'-тетрагидро-2Н,2'Н-спиро[нафтален-1,5'-[1,4]оксазепин]-7-ил)-5-хлорпиколинамида,
(R)-N-(3'-амино-6',6'-дифтор-6',7'-дигидро-2'Н-спиро[хроман-4,5'-[1,4]оксазепин]-6-ил)-5-цианопиколинамида,
(R)-N-(3'-амино-6',6'-дифтор-6',7'-дигидро-2'Н-спиро[хроман-4,5'-[1,4]оксазепин]-6-ил)-5-хлорпиколинамида,
(R)-N-(3'-амино-6',6'-дифтор-6',7'-дигидро-2'Н-спиро[хроман-4,5'-[1,4]оксазепин]-6-ил)-3,5-дихлорпиколинамида,
3-((2RS,4R)-2'-амино-5',5'-дифтор-2-фенил-5',6'-дигидроспиро[хроман-4,4'-[1,3]оксазин]-6-ил)бензонитрила,
3-((2RS,4R)-3'-амино-6',6'-дифтор-2-фенил-6',7'-дигидро-2'Н-спиро[хроман-4,5'-[1,4]оксазепин]-6-ил)бензонитрила,
3-[(2'R,4R)-2-амино-5,5-дифтор-5,5",6,6"-тетрагидро-4"Н-диспиро[1,3-оксазин-4,4'-хромен-2',3"-пиран]-6'-ил]бензонитрила формиата,
5-((2RS,4R)-2'-амино-5',5'-дифтор-2-фенил-5',6'-дигидроспиро[хроман-4,4'-[1,3]оксазин]-6-ил)никотинонитрила,
5-(2RS,4R)-3'-амино-6',6'-дифтор-2-фенил-6',7'-дигидро-2'H-спиро[хроман-4,5'-[1,4]оксазепин]-6-ил)никотинонитрила,
N-((2R или 2S,4R)-2'-амино-5',5'-дифтор-2-фенил-5',6'-дигидроспиро[хроман-4,4'-[1,3]оксазин]-6-ил)-5-хлорпиколинамида,
N-((2R или 2S,4R)-2'-амино-5',5'-дифтор-2-фенил-5',6'-дигидроспиро[хроман-4,4'-[1,3]оксазин]-6-ил)-5-цианопиколинамида,
N-((2R или 2S,4R)-2'-амино-5',5'-дифтор-2-фенил-5',6'-дигидроспиро[хроман-4,4'-[1,3]оксазин]-6-ил)-5-фторпиколинамида,
N-((2R или 2S,4R)-2'-амино-5',5'-дифтор-2-фенил-5',6'-дигидроспиро[хроман-4,4'-[1,3]оксазин]-6-ил)-5-(трифторметил)пиколинамида,
N-(2RS,4R)-3'-амино-6',6'-дифтор-2-фенил-6',7'-дигидро-2'H-спиро[хроман-4,5'-[1,4]оксазепин]-6-ил)-5-(трифторметил)пиколинамида,
N-(2RS,4R)-3'-амино-6',6'-дифтор-2-фенил-6',7'-дигидро-2'Н-спиро[хроман-4,5'-[1,4]оксазепин]-6-ил)-5-цианопиколинамида,
N-[(2'R,4R)-2-амино-5,5-дифтор-5,5",6,6"-тетрагидро-4"Н-диспиро[1,3-оксазин-4,4'-хромен-2',3"-пиран]-6'-ил]-5-цианопиридин-2-карбоксамида,
N-[(4R)-2-амино-5,5-дифтор-1',1'-диоксидо-2',3',5,6-тетрагидроспиро[1,3-оксазин-4,4'-тиохромен]-6'-ил]-5-хлорпиридин-2-карбоксамида,
N-[(4R)-2-амино-5,5-дифтор-1',1'-диоксидо-2',3',5,6-тетрагидроспиро[1,3-оксазин-4,4'-тиохромен]-6'-ил]-5-цианопиридин-2-карбоксамида,
или его фармацевтически приемлемые соли.
14. Соединение по любому из пп.1-13, выбранное из группы, состоящей из
(R)-N-(2'-амино-5',5'-дифтор-2,3,5',6'-тетрагидроспиро[инден-1,4'-[1,3]оксазин]-6-ил)-5-цианопиколинамида,
(R)-6-(5-хлорпиридин-3-ил)-5',5'-дифтор-5',6'-дигидроспиро[хроман-4,4'-[1,3]оксазин]-2'-амина,
(R)-N-(2'-амино-5',5'-дифтор-2,3,5',6'-тетрагидроспиро[инден-1,4'-[1,3]оксазин]-6-ил)-5-хлорпиколинамида,
(R)-N-(2'-амино-5',5'-дифтор-2,3,5',6'-тетрагидроспиро[инден-1,4'-[1,3]оксазин]-6-ил)-5-фторпиколинамида,
или его фармацевтически приемлемые соли.
15. Применение соединения формулы I по любому из пп.1-14 в качестве ингибитора ВАСЕ1 и/или ВАСЕ2.
16. Применение соединения формулы I по любому из пп.1-14 в качестве терапевтически активного вещества при терапевтическом и/или профилактическом лечении заболеваний и нарушений, характеризующихся повышенными уровнями β-амилоида и/или олигомеров β-амилоида и/или β-амилоидных бляшек и дальнейших отложений или болезни Альцгеймера.
17. Применение соединения формулы I по любому из пп.1-14 в качестве терапевтически активного вещества при терапевтическом и/или профилактическом лечении диабета или диабета 2 типа.
18. Фармацевтическая композиция, проявляющая ингибирующую активность в отношении ВАСЕ1 и/или ВАСЕ2, содержащая соединение формулы I по любому из пп.1-14 и фармацевтически приемлемый носитель и/или фармацевтически приемлемое вспомогательное вещество.
19. Применение соединения формулы I по любому из пп.1-14 при изготовлении лекарственного средства для терапевтического или профилактического лечения болезни Альцгеймера.
20. Применение соединения формулы I по любому из пп.1-14 при изготовлении лекарственного средства для терапевтического или профилактического лечения диабета.
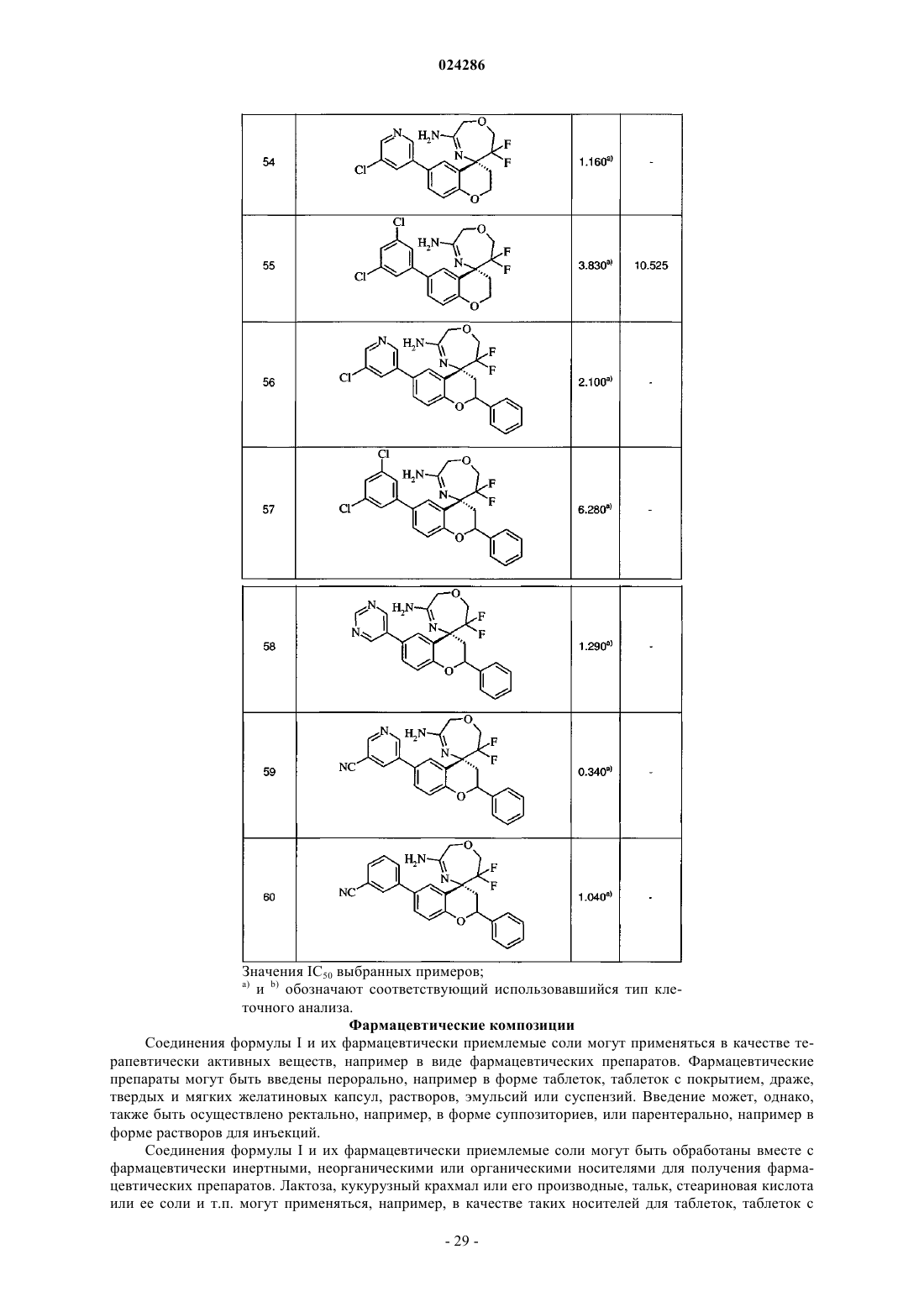
Текст
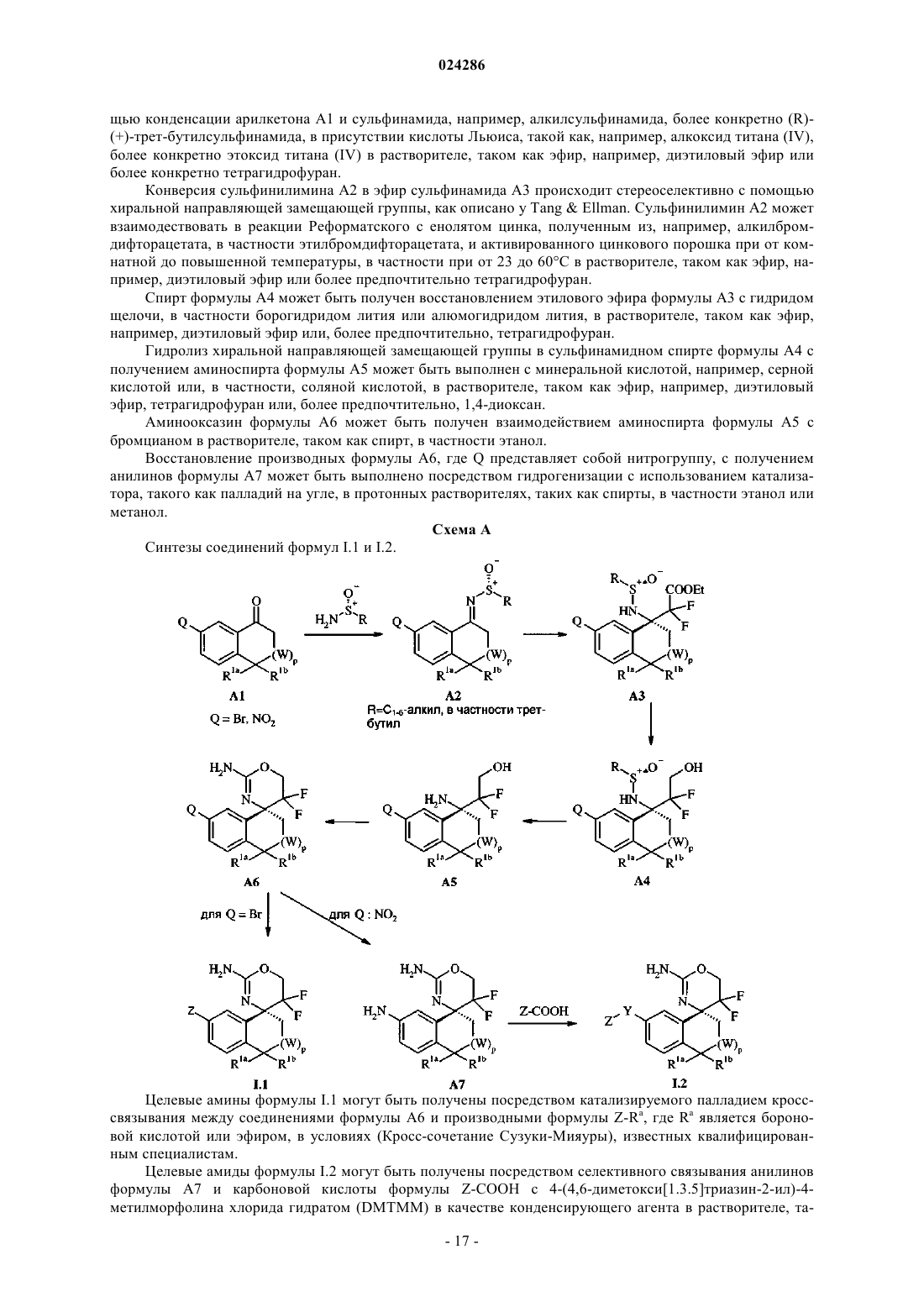
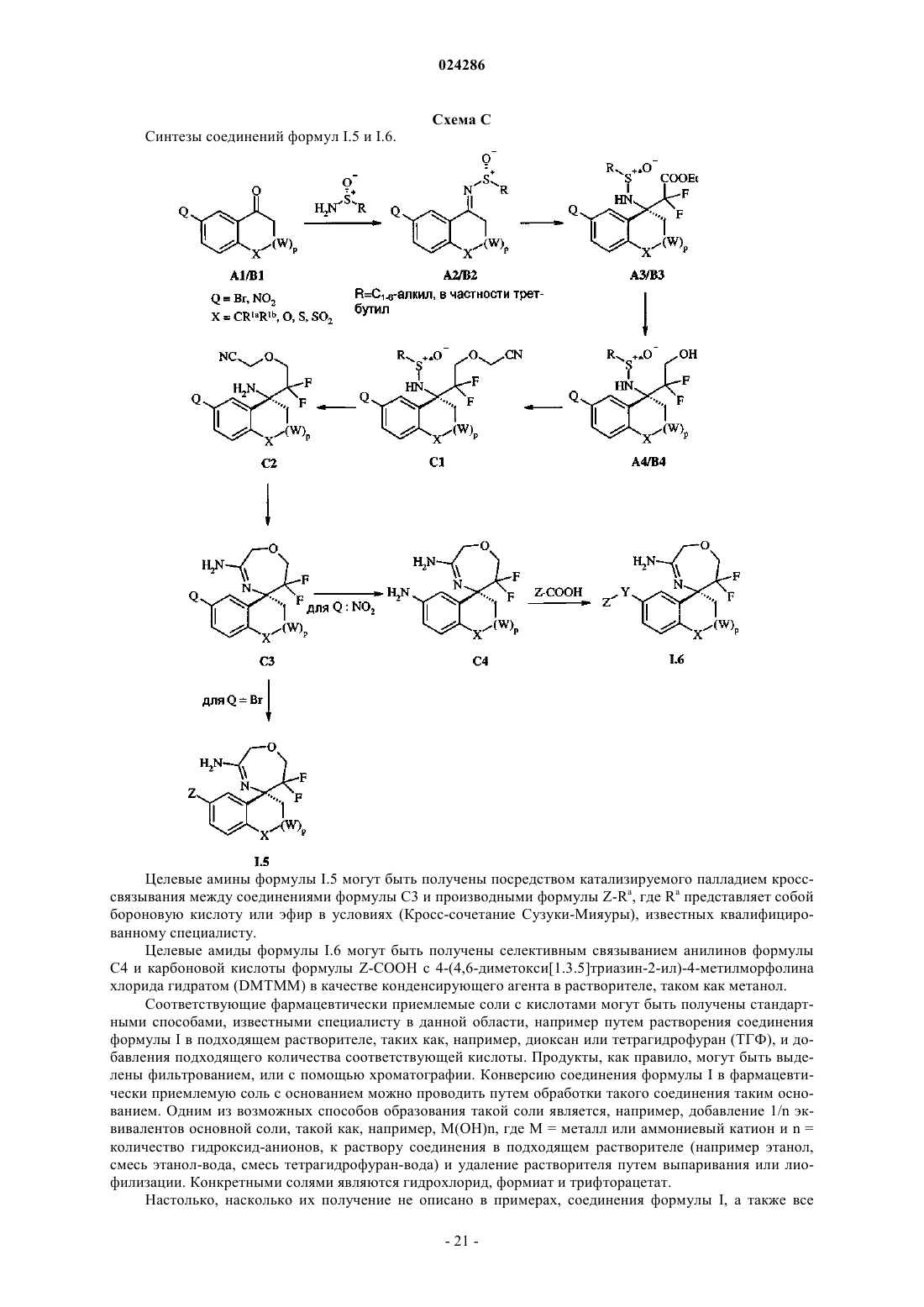
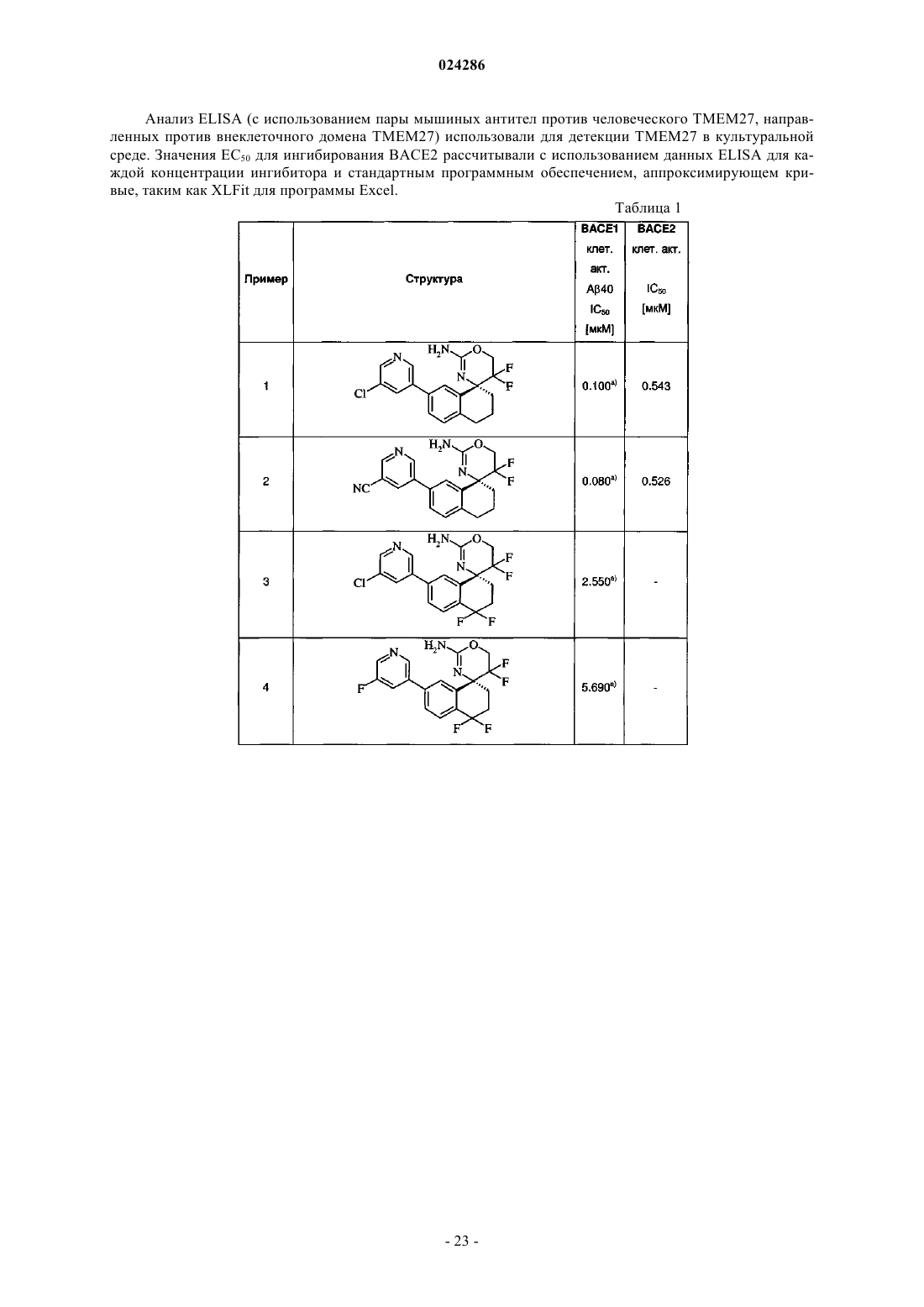
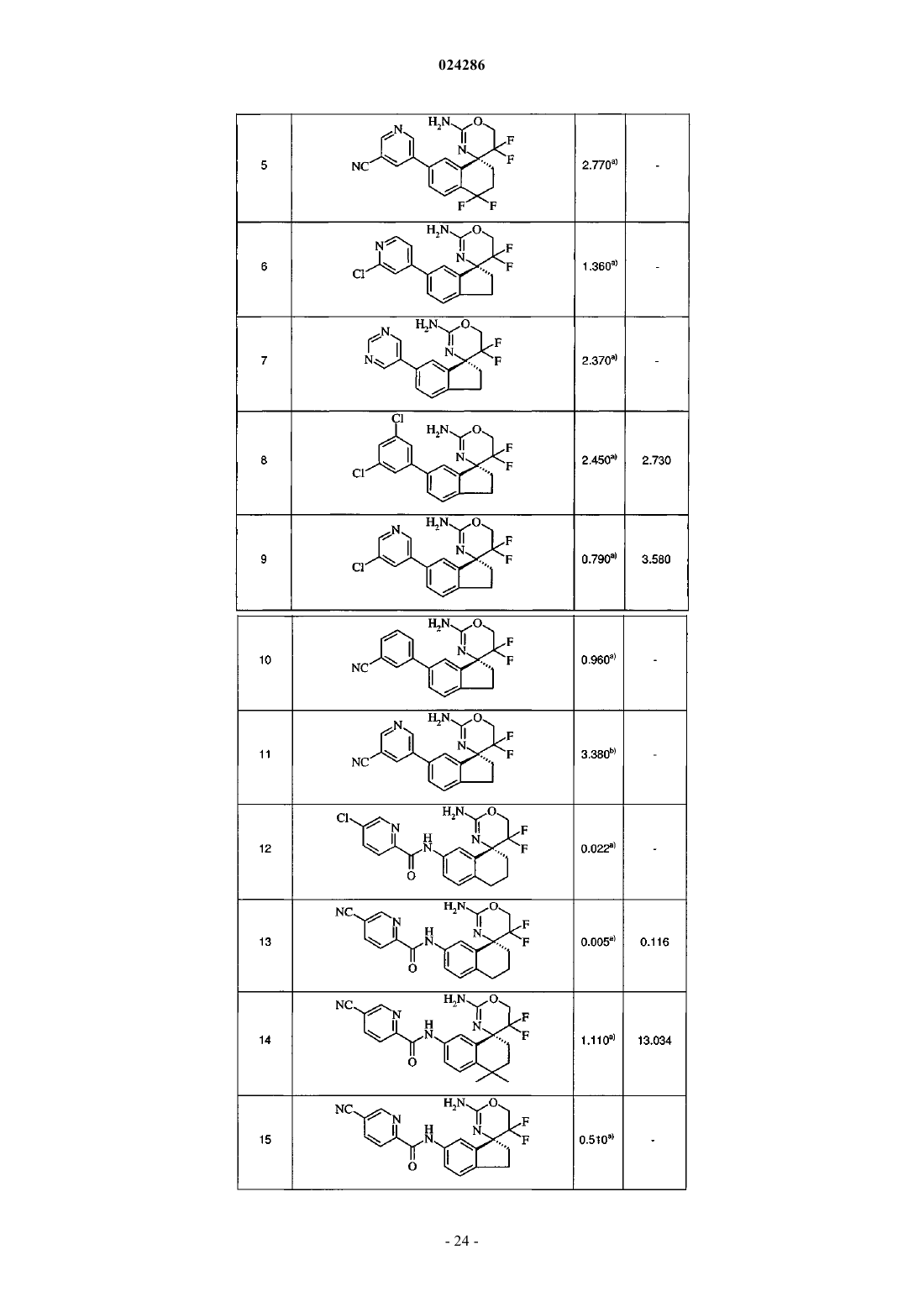
В настоящем изобретении предложены спиро[1,3]оксазины и спиро[1,4]оксазепины формулы I обладающие ингибиторной активностью в отношении ВАСЕ 1 и/или ВАСЕ 2, их изготовление,фармацевтические композиции, их содержащие, и их применение в качестве терапевтически активных веществ. Активные соединения настоящего изобретения полезны при терапевтическом или профилактическом лечении, например, болезни Альцгеймера и сахарного диабета 2 типа. Уровень техники Болезнь Альцгеймера (БА) представляет собой нейродегенеративное заболевание центральной нервной системы и является ведущей причиной прогрессивного слабоумия у пожилого населения. Ее клиническими симптомами являются ухудшение памяти, когнитивной деятельности, временной и локальной ориентации, суждений и рассуждений, а также тяжелые эмоциональные нарушения. В настоящее время нет способов лечения, которые могут предотвратить заболевание или его прогрессирование или стабильно обратить его клинические симптомы. БА стала серьезной проблемой здравоохранения во всех обществах с высокой продолжительностью жизни, а также значительным экономическим бременем для систем здравоохранения. БА характеризуется 2 основными патологиями в центральной нервной системе (ЦНС), образование амилоидных бляшек и нейрофибриллярных клубков (Hardy и соавт., The amyloid hypothesis of Alzheimer'sbiology of the amyloid beta-protein precursor и the mechanism of Alzheimer's disease, Annu Rev Cell Biol. 1994; 10:373-403). Обе патологии также часто наблюдаются у пациентов с синдромом Дауна (трисомия 21 хромосомы), при котором в более раннем возрасте также развиваются симптомы, похожие на БА. Нейрофибриллярные клубки представляют собой внутриклеточные агрегаты связанного с микротрубочками тау белка (МАРТ). Амилоидные бляшки образуются в межклеточном пространстве; их главным компонентом являются А-пептиды. Они представляют собой группу протеолитических фрагментов,полученных из предшественника белка -амилоида (АРР) в результате серии стадий протеолитического расщепления. Некоторые формы АРР были идентифицированы, из которых наиболее часто встречающимися являются белки длиной 695, 751 и 770 аминокислот. Все они происходят из одного гена посредством различного сплайсинга. А-пептиды получают из одного домена белка АРР, но они различаются на их N- и С-концах, длина основных разновидностей составляет 40 и 42 аминокислоты. Существует несколько доказательств, явно подтверждающих, что агрегированные А-пептиды являются существенными молекулами в патогенезе БА: 1) амилоидные бляшки, образованные из А-пептидов, являются неизменной составляющей патологии БА; 2) А-пептиды токсичны для нейронов; 3) при наследственной болезни Альцгеймера (FAD) мутации в генах, связанных с заболеванием, АРР, PSN1, PSN2 приводят к увеличенному уровню А-пептидов и раннему амилоидозу головного мозга; 4) у трансгенных мышей, экспрессирующих такие FAD гены, развивается патология, которая имеет много сходств с заболеванием человека. А-пептиды образуются из АРР посредством последовательного действия двух протеолитических ферментов, называемых - и -секретазами. -секретаза сначала расщепляет внеклеточный домен АРР приблизительно в районе 28 аминокислоты за пределами трансмембранного домена (ТМ) с получением С-концевого фрагмента АРР, содержащего ТМ- и цитоплазматический домен (CTF). CTF является субстратом для -секретазы, которая расщепляет в нескольких смежных позициях внутри ТМ-домена с получением А пептидом и цитоплазматического фрагмента, -секретаза представляет собой комплекс из по меньшей мере 4 различных белков, е каталитическая субъединица очень похожа на белок пресенилин (PSEN1, PSEN2). -секретаза (ВАСЕ 1, Asp2; ВАСЕ участки для -сайт АРР-расщепляющего фермента) представляет собой аспартил протеазу, которая закреплена в мембране с помощью трансмембранного домена (Vassar и соавт., Beta-secretase cleavage of Alzheimer's amyloid precursor protein by thetransmembrane aspartic protease BACE, Science. 1999 Oct 22; 286(5440):735). Она экспрессируется во множестве тканей человеческого организма, однако е уровень особенно высок в ЦНС. Генетическое удаление гена ВАСЕ 1 у мышей ясно показывает, что е активность является существенной для процессинга АРР, который приводит к образованию А-пептидов, при отсутствии ВАСЕ 1 А-пептиды не продуцируются (Luo и соавт., Mice deficient in BACE1, the Alzheimer's beta-secretase, have normal phenotype и abolished beta-amyloid generation, Nat Neurosci. 2001 Mar; 4(3):231-2, Roberds и соавт., ВАСЕ knockout mice arehealthy despite lacking the primary beta-secretase activity in brain: implications for Alzheimer's disease therapeutics, Hum Mol Genet. 2001 Jun 1; 10(12):1317-24). Генетически модифицированные мыши, которые экспрессируют человеческий ген АРР и обильно формируют амилоидные бляшки и патологии, аналогичные заболеванию БА при старении, теряют такую способность при снижении активности -секретазы посредством удаления одной из аллелей гена ВАСЕ 1 (McConlogue и соавт., Partial reduction of BACE1 hasdramatic effects on Alzheimer plaque и synaptic pathology in APP Transgenic Mice. J Biol Chem. 2007 Sep 7; 282(36):26326). Это, таким образом, допускает, что ингибиторы активности ВАСЕ 1 могут быть полезным средством для лечения болезни Альцгеймера (AD). Диабет 2 типа (T2D) является результатом резистентности к инсулину и анормальной секреции инсулина -клетками поджелудочной железы, приводя к сниженному контролю уровня глюкозы в крови и гипергликемии (М. PrentkiC.J. Nolan, "Islet beta-cell failure in type 2 diabetes." J. Clin. Investig. 2006,116(7), 1802-1812). Пациенты с T2D обладают повышенным риском микро- и макрососудистых заболеваний и рядом связанных осложнений, включая диабетическую нейропатию, ретинопатию и сердечнососудистые заболевания. В 2000, по оценкам, 171 млн человек страдали от такого состояния с предположительным удвоением этой цифры к 2030 (S. Wild, G. Roglic, A. Green, R. SicreeН. King, "Global prevalence of diabetes", Diabetes Care 2004, 27(5), 1047-1053), делая это заболевание главной проблемой здра-1 024286 воохранения. Рост распространенности сахарного диабета 2 типа связан с сидячим образом жизни и потреблением высококалорийной пищи населением мира (Р. Zimmet, KGMM AlbertJ. Shaw, "Global иsocietal implications of the diabetes epidemic" Nature 2001, 414, 782-787). Отказ -клеток и последующее резкое снижение секреции инсулина и гипергликемия означают начало T2D. Большинство современных способов лечения не предотвращают потерю массы -клеток, характеризующую явный T2D. Однако недавняя разработка GLP-1 аналогов, гастрина и других агентов показывают, что можно добиться сохранения и пролиферации -клеток, что приводит к улучшению толерантности к глюкозе и более медленному прогрессированию к явному T2D (LL BaggioDJ Drucker,"Therapeutic approaches to preserve islet mass in type 2 diabetes", Annu. Rev. Med. 2006, 57, 265-281).Tmem27 был идентифицирован как белок, способствующий пролиферации бета-клеток (Р. Akpinar,S. Kuwajima, J. Krtzfeldt, M. Stoffel, "Tmem27: A cleaved и shed plasma membrane protein that stimulatesCao, N. Takahashi и соавт., "The HNF-1 target Collectrin controls insulin exocytosis by SNARE complex formation", Cell Metab. 2005, 2, 373-384). Tmem27 является 42 кДа мембранным гликопротеином, который постоянно отсоединяется от поверхности -клеток, в результате деградации полноразмерного клеточногоTmem27. Сверхэкспрессия Tmem27 у трансгенных мышей увеличивает массу -клеток и улучшает толерантность к глюкозе у DIO модели диабета с вызванным диетой ожирением. Кроме того, миРНК нокаутTmem27 в анализе пролиферации -клеток грызунов (например, с помощью INS1e клеток) уменьшает скорость пролиферации, указывая на роль Tmem27 в контролировании массы -клеток. В том же анализе пролиферации, ингибиторы ВАСЕ 2 также увеличивали пролиферацию. Тем не менее, ингибирование ВАСЕ 2 в сочетании с Tmem27 миРНК нокдауном приводило к низкой скорости пролиферирования. Таким образом, можно сделать вывод, что ВАСЕ 2 является протеаза чувствительным для деградации Tmem27. Кроме того, in vitro, BACE2 расщепляет пептид на основе последовательностиTmem27. Тесно связанная протеаза ВАСЕ 1 не расщепляет этот пептид и селективное ингибирование одной только ВАСЕ 1 не дает увеличения пролиферации -клеток. Близкий гомолог ВАСЕ 2 является мембраносвязанной аспартилпротеазой и колокализуется сTmem27 в -клетках поджелудочной железы человека (G. Finzi, F. Franzi, С. Placidi, F. Acquati и соавт.,"ВАСЕ 2 is stored in secretory granules of mouse и rat pancreatic beta cells", Ultrastruct Pathol. 2008, 32(6),246-251). Известно также, что она способна разлагать АРР (I. Hussain, D. Powell, D. Howlett, G. Chapman и соавт., "ASP1 (BACE2) cleaves the amyloid precursor protein at the -secretase site" Mol Cell Neurosci. 2000, 16, 609-619), IL-1R2 (P. Kuhn, E. Marjaux, A. Imhof, В. De Strooper и соавт., "Regulated intramembrane proteolysis of the interleukin-1 receptor II by alpha-, beta-, и gamma-secretase" J. Biol. Chem. 2007,282(16), 11982-11995) и АСЕ 2. Способность к деградации АСЕ 2 указывает на возможную роль ВАСЕ 2 в контроле гипертензии. Поэтому ингибирование ВАСЕ 2 предлагается для лечения сахарного диабета 2 типа с потенциалом сохранения и восстановления массы -клеток и стимулирования секреции инсулина в предиабетическом состоянии и у больных сахарным диабетом. Соответственно, задачей настоящего изобретения является создание селективных ингибиторов ВАСЕ 2. Такие соединения являются полезными в качестве терапевтически активных веществ, в частности при лечении и/или профилактике заболеваний, которые связаны с ингибированием ВАСЕ 2. Кроме того, образование или образование и отложение -амилоидных пептидов в, на или вокруг неврологической ткани (например, мозга) ингибируются соединениями по настоящему изобретению, т.е. ингибируется А-продукция из АРР или фрагмента АРР. В настоящем изобретении предложены новые соединения формулы I, их изготовление, лекарственные средства на основе соединения в соответствии с настоящим изобретением и их получение, а также применение соединений формулы I при лечении или профилактике заболеваний, таких как болезнь Альцгеймера и сахарный диабет 2 типа. Новые соединения формулы I обладают улучшенными фармакологическими свойствами. Область, к которой относится изобретение В настоящем изобретении предложены спиро[1,3]оксазины и спиро[1,4]оксазепины, обладающие свойствами ингибиторов ВАСЕ 1 и/или ВАСЕ 2, их изготовление, фармацевтические композиции, их содержащие, и их применение в качестве терапевтически активных веществ. Краткое описание изобретения В настоящем изобретении предложены соединения формулы I где заместители и переменные являются такими, как описано ниже и в формуле изобретения,или их фармацевтически активные соли. Соединения настоящего изобретения обладают ингибиторной активностью в отношении Asp2 (секретаза, ВАСЕ 1 или Мемапсин-2) и, таким образом, могут применяться при лечении и/или профилактике заболеваний и нарушений, характеризующихся повышенными уровнями -амилоида и/или олигомеров -амилоидов и/или -амилоидных бляшек и дополнительных отложений, в частности болезни Альцгеймера. И/или соединения по настоящему изобретению обладают ингибиторной активностью в отношении ВАСЕ 2 и могут, таким образом, применяться в профилактическом и/или терапевтическом лечении заболеваний и нарушений, таких как диабет 2-го типа и других расстройств метаболизма. Подробное описание изобретения В настоящем изобретении предложены соединения формулы I и их фармацевтически приемлемые соли, получение вышеуказанных соединений, лекарственные средства, их содержащие, и их изготовление, а также применение вышеуказанных соединений I при терапевтическом и/или профилактическом лечении заболеваний и нарушений, которые связаны с ингибированием активности ВАСЕ 1 и/или ВАСЕ 2, таких как болезнь Альцгеймера и сахарный диабет 2 типа. Кроме того, образование или образование и отложение -амилоидных бляшек в, на или вокруг неврологической ткани (например, мозга) ингибируются соединениями по настоящему изобретению посредством ингибирования продукции А из АРР или фрагмента АРР. Следующие определения общих терминов, используемых в настоящем описании, применимы независимо от того, появляются ли термины, о которых идет речь, по отдельности или в комбинации с другими группами. Если не указано иное, следующие термины, используемые в данном изобретении, имеют значения,приведенные ниже. Следует отметить, что, как использовано в описании и прилагаемой формуле изобретения, формы единственного числа включают ссылки на множественное число, если из контекста явно не следует иное. Термин "C1-6 алкил", самостоятельно или в комбинации с другими группами, обозначает углеводородный радикал, который может быть линейным или разветвленным, с одной ли несколькими точками ветвления, где алкильная группа в основном содержит от 1 до 6 атомов углерода, например, метил (Me),этил (Et), пропил, изопропил (i-пропил), н-бутил, изо-бутил (изобутил), 2-бутил (втор-бутил), т-бутил(трет-бутил), изопентил, 2-этил-пропил, 1,2-диметил-пропил и т.п. Термин "C1-3 алкил", самостоятельно или в комбинации с другими группами, обозначает углеводородный радикал, который может быть линейным или разветвленным, где алкильная группа содержит от 1 до 3 атомов углерода. Конкретными примерами "C1-6 алкилов" являются "C1-3 алкилы". Конкретные примеры представляют собой метил и этил, наиболее конкретно - метил. Термин "циано-C1-6 алкил", самостоятельно или в комбинации с другими группами, обозначаетC1-6 алкил как здесь определено, который замещен одной или несколькими циано, в частности 1-5 циано,более конкретно 1 циано. Примерами являются циано-метил и т.п. Термин "галоген-C1-6 алкил", самостоятельно или в комбинации с другими группами, относится к С 1-6 алкилу, как определено здесь, который замещен одним или несколькими галогенами, в частности 1-5 галогенами, более конкретно 1-3 галогенами, ещ более конкретно 1 галогеном или 3 галогенами. Термин "галоген-C1-3 алкил", самостоятельно или в комбинации с другими группами, относится к С 1-3 алкилу,как определено здесь, который замещен одним или несколькими галогенами, в частности 1-5 галогенами,более конкретно 1-3 галогенами, ещ более конкретно 1 галогеном или 3 галогенами. Конкретный галоген представляет собой фтор. Конкретный "галоген-С 1-6 алкил" обозначает фтор-С 1-6 алкил, и конкретный"галоген-С 1-3 алкил" обозначает фтор-С 1-3 алкил. Примерами являются дифторметил, хлорметил, фторметил и т.п. Конкретным примером является трифторметил. Термин "C1-6 алкокси-C1-6 алкил", самостоятельно или в комбинации с другими группами, относится к С 1-6 алкилу, который замещен одним или несколькими C1-6 алкокси, как здесь определено. Примерами являются МеО-Ме, 1MeO-Et, 2MeO-Et, 1 МеО-2EtO-пропил и т.п. Термин "циано", самостоятельно или в комбинации с другими группами, относится к NC-(CN). Термин "галоген", самостоятельно или в комбинации с другими группами, обозначает хлор (Cl),йод (I), фтор (F) и бром (Br). Конкретными "галогенами" являются Cl и F. Конкретным "галогеном" явля-3 024286 ется F. Термин "гетероарил", самостоятельно или в комбинации с другими группами, относится к ароматической карбоциклической группе, имеющей одно 4-8-членное кольцо или несколько конденсированных колец, содержащих от 6 до 14, в частности от 6 до 10 кольцевых атомов и содержащие 1, 2 или 3 гетероатома, независимо выбранные из N, O и S, в частности N и О, в которых по меньшей мере одно гетероциклическое кольцо является ароматическим. Примеры "гетероарила" включают бензофурил, бензимидазолил, 1 Н-бензимидазолил, бензооксазинил, бензоксазолил, бензотиазинил, бензотиазолил, бензотиенил, бензотриазолил, фурил, имидазолил, индазолил, 1 Н-индазолил, индолил, изохинолинил, изотиазолил, изоксазолил, оксазолил, пиразинил, пиразолил (пиразил), 1 Н-пиразолил, пиразоло[1,5-а]пиридинил,пиридазинил, пиридинил, пиримидинил, пирролил, хинолинил, тетразолил, тиазолил, тиенил, триазолил,6,7-дигидро-5 Н-[1]пиридинил и т.п. Конкретными "гетероарилами" являются пиридинил, пиримидинил и 1 Н-пиразолил. Конкретными группами являются пиридин-2-ил, пиридин-3-ил, пиридин-4-ил, пиримидин-5-ил и 1 Н-пиразол-ил. Термин "арил" означает одновалентную ароматическую карбоциклическую моно- или бициклическую кольцевую систему, содержащую от 6 до 10 кольцевых атомов углерода. Примеры арильных групп включают фенил и нафтил. Конкретным "арилом" является фенил. Термин "гетероциклил", самостоятельно или в комбинации с другими группами, означает одновалентную насыщенную или частично ненасыщенную моно- или бициклическую кольцевую систему из 4-9 кольцевых атомов, содержащую 1, 2 или 3 кольцевых гетероатома, выбранных из N, О и S, остальные кольцевые атомы представляют собой углерод. Бициклический означает состоящий из двух циклов,имеющих два общих кольцевых атома, т.е. мостик, разделяющий два кольца, представляет собой или одинарную связь, или цепочку из одного или двух кольцевых атомов. Примерами моноциклического насыщенного гетероциклила являются азетидинил, пирролидинил, тетрагидрофуранил, тетрагидротиенил, пиразолидинил, имидазолидинил, оксазолидинил, изоксазолидинил, тиазолидинил, пиперидинил, тетрагидропиранил, тетрагидротиопиранил, пиперазинил, морфолинил, тиоморфолинил, 1,1-диоксотиоморфолин-4-ил, азепанил, диазепанил, гомопиперазинил или оксазепанил. Примерами бициклического насыщенного гетероциклила являются 8-азабицикло[3.2.1]октил, хинуклидинил, 8-окса-3 азабицикло[3.2.1]октил, 9-азабицикло[3.3.1]нонил, 3-окса-9-азабицикло[3.3.1]нонил или 3-тиа-9 азабицикло[3.3.1]нонил. Примерами частично ненасыщенного гетероциклила являются дигидрофурил,имидазолинил, дигидрооксазолил, тетрагидропиридинил или дигидропиранил. Конкретным "гетероциклилом" является тетрагидрофуранил. Термин "C1-6 алкокси", самостоятельно или в комбинации с другими группами, означает-O-C1-6 алкил, который может быть линейным или разветвленным, с одной или несколькими точками ветвления, где алкильная группа в основном содержит от 1 до 6 атомов углерода, например метокси"С 1-6 алкокси" являются группы с от 1 до 4 атомами углерода. Конкретными примерами являются метокси и этокси. Термин "галоген-С 1-6 алкокси", самостоятельно или в комбинации с другими группами, относится кC1-6 алкокси, как определено здесь, который замещен одним или несколькими галогенами, в частности фтором. Конкретной "галоген-С 1-6 алкокси" является фтор-С 1-6 алкокси. Конкретными группами являются дифторметокси и трифторметокси. Термин "С 2-6 алкинил", самостоятельно или в комбинации с другими группами, означает одновалентную линейную или разветвленную насыщенную углеводородную группу из 2-6 атомов углерода, в частности 2-4 атомов углерода, и содержащую одну, две или три тройные связи. Примеры С 2-6 алкинила включают этинил, пропинил и н-бутинил. Конкретными примерами являются этинил и пропинил. Термин "фармацевтически приемлемые соли" относится к солям, которые являются подходящими для использования при контакте с тканями человека и животных. Примеры подходящих солей с неорганическими и органическими кислотами являются, но не ограничиваются ими, уксусная кислота, лимонная кислота, муравьиная кислота, фумаровая кислота, соляная кислота, молочная кислота, малеиновая кислота, яблочная кислота, метансульфоновая кислота, азотная кислота, фосфорная кислота, птолуолсульфоновая кислота, янтарная кислота, серная кислота, серная кислота, винная кислота, трифторуксусная кислота и т.п. Конкретными примерами являются муравьиная кислота, трифторуксусная кислота и соляная кислота. В частности соляная кислота, трифторуксусная кислота и фумаровая кислота. Термины "фармацевтически приемлемый носитель" и "фармацевтически приемлемые вспомогательные вещества" относятся к носителям и вспомогательным веществам, таким как разбавители или наполнители, которые совместимы с другими ингредиентами композиции. Термин "фармацевтическая композиция" охватывает продукт, содержащий определенные ингредиенты в заранее определенных количествах или пропорциях, а также любой продукт, который прямо или косвенно приводит, из комбинации указанных ингредиентов в указанных количествах. В частности, он охватывает продукт, содержащий один или более активных ингредиентов и возможно носитель, содержащий инертные ингредиенты, а также любой продукт, который прямо или косвенно получается, в ре-4 024286 зультате комбинации, комплексообразования или агрегации любых двух или более ингредиентов или в результате диссоциации одного или нескольких ингредиентов, или в результате других типов реакций или взаимодействий одного или нескольких ингредиентов. Термин "ингибитор" означает соединение, которое конкурирует с, снижает или предотвращает связывание конкретного лиганда с конкретным рецептором или которое снижает или предотвращает ингибирование функции конкретного белка. Термин "половина максимальной ингибирующей концентрации" (IC50) обозначает концентрацию конкретного соединения, необходимую для получения 50%-ного ингибирования биологического процесса in vitro. Значения IC50 могут быть преобразованы в логарифмические значения pIC50 (-log IC50), для которых более высокие значения указывают экспоненциально большую эффективность. Значение IC50 не является абсолютным, но зависит от условий эксперимента, например использованных концентраций. Значение IC50 может быть преобразовано в абсолютную константу ингибирования (Ki) по уравнению Ченга-Прусова (Biochem. Pharmacol. (1973), 22:3099). Термин "константа ингибирования" (Ki) обозначает абсолютное сродство связывания конкретного ингибитора с рецептором. Она измеряется с помощью анализа конкурентного связывания и равна концентрации, при которой конкретный ингибитор будет занимать 50% рецепторов при отсутствии конкурирующего лиганда (например, радиоактивного лиганда). Значения Ki могут быть преобразованы логарифмически в значения pKI (-log Ki), для которых более высокие значения указывают экспоненциально большую эффективность."Терапевтически эффективное количество" означает количество соединения, которое, при введении субъекту для лечения болезненного состояния, достаточно для осуществления такого лечения болезненного состояния. "Терапевтически эффективное количество" будет варьироваться в зависимости от соединения, состояния заболевания, которое лечат, тяжести или заболевания для лечения, возраста и относительного состояния здоровья субъекта, способа и формы введения, мнения лечащего врача или ветеринара и других факторов. Термин "как определено здесь" и "как описано здесь", при ссылке на переменную, включает посредством ссылки широкое определение переменной, а также предпочтительные, более предпочтительные и наиболее предпочтительные определения, если таковые имеются. Термины "лечение", "контактирование" и "взаимодействие" в отношении химической реакции, означают добавление или смешивание двух или более реагентов при соответствующих условиях для получения указанного и/или желаемого продукта. Следует понимать, что реакция, которая приводит к указанному и/или желательному продукту, не обязательно приводит непосредственно из комбинации двух реагентов, которые были добавлены первоначально, т.е. может быть один или несколько промежуточных соединений, которые образуются в смеси, которые в конечном счете приводят к образованию указанного и/или желаемого продукта. Термин "защитная группа" обозначает группу, которая селективно блокирует реакционноспособный участок в многофункциональном соединении таким образом, что химическая реакция может быть проведена селективно в другом незащищенном реакционноспособном участке, в значении обычно связанным с ним в синтетической химии. Защитные группы могут быть удалены на соответствующей стадии. Типичные защитные группы представляют собой аминозащитные группы, карбоксизащитные группы или гидроксизащитные группы. Термин "аминозащитные группы" (здесь также Р 1) обозначает группы, предназначенные для защиты аминогруппы и включает бензил, бензилоксикарбонил (карбобензилокси,CBZ),9-флуоренилметилоксикарбонил(MMTr), 4,4-диметокситритил (DMTr), 4,4',4"-триметокситритил и трифторацетил. Другие примеры таких групп можно найти у TW Greene и PGM Wuts, "Protective Groups in Organic Synthesis", 2nd ed, JohnG. W. McOmie, Ed., Plenum Press, New York, NY, 1973, Chapter 5, и T.W. Greene, "Protective Groups in Organic Synthesis", John Wiley и Sons, New York, NY, 1981. Термин "защищенная аминогруппа " относится к аминогруппе, замещенной с помощью амино-защитной группы. Конкретными аминозащитными группами являются трет-бутоксикарбонильная группа и диметокситритил. Термин "уходящая группа" обозначает группу со значением, обычно связанным с ним в синтетической органической химии, т.е. атом или группа, замещаемые в условиях реакции замещения. Примеры уходящих групп включают галоген, в частности бром, алкан- или ариленсульфонилокси, такие как метансульфонилокси, этансульфонилокси, тиометил, бензолсульфонилокси, тозилокси и тиенилокси, дигалофосфиноилокси, возможно замещенный бензилокси, изопропилокси и ацилокси. Термин "ароматический" означает обычное понимание ароматичности, как определено в литературе, в частности в IUPAC - Compendium of Chemical Terminology, 2nd, A. D. McNaughtA. Wilkinson(Eds). Blackwell Scientific Publications, Oxford (1997). Термин "фармацевтически приемлемый эксципиент" означает любой ингредиент, не имеющий терапевтической активности и не являющийся токсичным, такой как разрыхлители, связующие вещества,наполнители, растворители, буферы, тонизирующие агенты, стабилизаторы, антиоксиданты, поверхностно-активные вещества или лубриканты, используемые при разработке фармацевтических продуктов. Всякий раз, когда в химической структуре присутствует хиральный атом углерода, предполагается,что все стереоизомеры, связанные с этим хиральным атомом углерода, охватываются структурами. Изобретение также относится к фармацевтическим композициям, способам применения и способам получения вышеуказанных соединений. Все отдельные варианты осуществления могут быть комбинированы. Одним из воплощений изобретения является соединение формулы Iii) 5-6-членный гетероарил, содержащий 1-2 гетероатома N, замещенный 1-2 заместителями, независимо выбранными из R8;iii) фенил, замещенный 1-2 заместителями, независимо выбранными из R8;m представляет собой 0 или 1; р представляет собой 0 или 1,или его фармацевтически приемлемые соли. Одним из воплощений является соединение, как здесь описано, гдеii) 5-6-членный гетероарил, содержащий 1-2 гетероатома N, замещенный 1-2 заместителями, независимо выбранными из R8;iii) фенил, замещенный 1-2 заместителями, независимо выбранными из R8;m представляет собой 0 или 1; р представляет собой 0 или 1,или его фармацевтически приемлемые соли. Одним из воплощений является соединение, как здесь описано, гдеii) 5-6-членный гетероарил, содержащий 1-2 гетероатома N, замещенный 1-2 заместителями, независимо выбранными из R8;iii) фенил, замещенный 1-2 заместителями, независимо выбранными из R8;m представляет собой 0 или 1; р представляет собой 0 или 1,или его фармацевтически приемлемые соли. Одним из воплощений является соединение, как здесь описано, гдеm представляет собой 1; р представляет собой 0,или его фармацевтически приемлемые соли. Одним из воплощений является соединение, как здесь описано, где n представляет собой 0. Одним из воплощений является соединение, как здесь описано, где n представляет собой 1. Одним из воплощений является соединение, как здесь описано, где m представляет собой 0. Одним из воплощений является соединение, как здесь описано, где m представляет собой 1. Одним из воплощений является соединение, как здесь описано, где р представляет собой 0. Одним из воплощений является соединение, как здесь описано, где р представляет собой 1. Одним из воплощений является соединение, как здесь описано, где X представляет собой -CR1aR1b-,1aa R и R1b оба являются водородом. Одним из воплощений является соединение, как здесь описано, где X представляет собой -CR1aR1b-. Одним из воплощений является соединение, как здесь описано, где R1a представляет собой водород. Одним из воплощений является соединение, как здесь описано, где R1a представляет собой галоген. Одним из воплощений является соединение, как здесь описано, где R1a представляет собой F. Одним из воплощений является соединение, как здесь описано, где R1a представляет собой С 1-6 алкил. Одним из воплощений является соединение, как здесь описано, где R1a представляет собой метил. Одним из воплощений является соединение, как здесь описано, где R1b представляет собой водород. Одним из воплощений является соединение, как здесь описано, где R1b представляет собой галоген. Одним из воплощений является соединение, как здесь описано, где R1b представляет собой F. Одним из воплощений является соединение, как здесь описано, где R1b представляет собойC1-6 алкил. Одним из воплощений является соединение, как здесь описано, где R1b представляет собой метил. Одним из воплощений является соединение, как здесь описано, где R2a представляет собойC1-6 алкил. Одним из воплощений является соединение, как здесь описано, где R2a представляет собой метил. Одним из воплощений является соединение, как здесь описано, где R2a представляет собой водород. Одним из воплощений является соединение, как здесь описано, где R2b представляет собойC1-6 алкил. Одним из воплощений является соединение, как здесь описано, где R2b представляет собой метил. Одним из воплощений является соединение, как здесь описано, где R2b представляет собой водород. Одним из воплощений является соединение, как здесь описано, где R2b представляет собой фенил. Одним из воплощений является соединение, как здесь описано, где R2a и R2b вместе с атомом угле-8 024286 рода, к которому они присоединены, образуют 6-членный гетероциклил, содержащий 1 гетероатом О. Одним из воплощений является соединение, как здесь описано, где R2a и R2b вместе с атомом углерода, к которому они присоединены, образуют тетрагидропиранил. Одним из воплощений является соединение, как здесь описано, где X представляет собой -О-. Одним из воплощений является соединение, как здесь описано, где X представляет собой -S-. Одним из воплощений является соединение, как здесь описано, где X представляет собой -SO2-. Одним из воплощений является соединение, как здесь описано, где р представляет собой 1, W представляет собой -CR2aR2b-, a R2a и R2b оба являются водородом. Одним из воплощений является соединение, как здесь описано, где V представляет собой -CR7aR7b-,7aa R и R7b оба являются водородом. Одним из воплощений является соединение, как здесь описано, где V представляет собой -CR7aR7b-. Одним из воплощений является соединение, как здесь описано, где R7a представляет собой водород. Одним из воплощений является соединение, как здесь описано, где R7b представляет собой водород. Одним из воплощений является соединение, как здесь описано, где W представляет собой -CR2aR2b-. Одним из воплощений является соединение, как здесь описано, где R3 представляет собой галоген. Одним из воплощений является соединение, как здесь описано, где R3 представляет собой F. Одним из воплощений является соединение, как здесь описано, где R4 представляет собой галоген. Одним из воплощений является соединение, как здесь описано, где R4 представляет собой F. Одним из воплощений является соединение, как здесь описано, где R5 представляет собой водород. Одним из воплощений является соединение, как здесь описано, где R6 представляет собой водород. Одним из воплощений является соединение, как здесь описано, где Y является -NH-C=O-. Одним из воплощений является соединение, как здесь описано, где Z представляет собой 5-6 членный гетероарил, содержащий 1-2 гетероатома N, замещенный галогеном или циано. Одним из воплощений является соединение, как здесь описано, где Z представляет собой 2 хлорпиридинил, 3,5-дихлорфенил, 3,5-дихлорпиридинил, 3-циано-фенил, 4-хлор-1 Н-пиразолил, 5 хлорпиридинил, 5-хлорпиридинил, 5-цианопиридинил, 5-цианопиридинил, 5-фторпиридинил, 5 фторпиридинил, 5-метоксипиридинил, 5-трифторметилпиридинил или пиримидинил. Одним из воплощений является соединение, как здесь описано, где Z представляет собой 2 хлорпиридин-4-ил, 3,5-дихлорфенил, 3,5-дихлорпиридин-2-ил, 3-циано-фенил, 4-хлор-1 Н-пиразол-5-ил,5-хлорпиридин-2-ил, 5-хлорпиридин-3-ил, 5-цианопиридин-2-ил, 5-цианопиридин-3-ил, 5-фторпиридин 2-ил, 5-фторпиридин-3-ил, 5-метоксипиридин-3-ил, 5-трифторметилпиридин-2-ил или пиримидин-5-ил. Одним из воплощений является соединение, как здесь описано, где Z представляет собой 5 цианопиридин-2-ил, 5-хлорпиридин-2-ил, 5-хлорпиридин-3-ил или 5-фторпиридин-2-ил. Одним из воплощений является соединение, как здесь описано, где Z представляет собой 6 членный гетероарил, содержащий 2 гетероатома N. Одним из воплощений является соединение, как здесь описано, где Z представляет собой пиримидинил. Одним из воплощений является соединение, как здесь описано, где Z представляет собой 5-6 членный гетероарил, содержащий 1-2 гетероатома N, замещенный 1-2 заместителями, независимо выбранными из R8. Одним из воплощений является соединение, как здесь описано, где Z представляет собой 1 Нпиразолил, пиридинил или пиримидинил. Одним из воплощений является соединение, как здесь описано, где Z представляет собой 1 Нпиразол-5-ил, пиридин-2-ил, пиридин-3-ил, пиридин-4-ил или пиримидин-5-ил. Одним из воплощений является соединение, как здесь описано, где Z представляет собой фенил,замещенный 1-2 заместителями, независимо выбранными из R8. Одним из воплощений является соединение, как здесь описано, где Z представляет собой фенил,замещенный 1-2 заместителями, независимо выбранными из хлора и циано. Одним из воплощений является соединение, как здесь описано, где R8 представляет собой циано. Одним из воплощений является соединение, как здесь описано, где R8 представляет собой галоген. Одним из воплощений является соединение, как здесь описано, где R8 представляет собой хлор. Одним из воплощений является соединение, как здесь описано, где R8 представляет собой фтор. Одним из воплощений является соединение, как здесь описано, где R8 представляет собой галогенС 1-6 алкил. Одним из воплощений является соединение, как здесь описано, где R8 представляет собой трифторметил. Одним из воплощений является соединение, как здесь описано, где R8 представляет собойC1-6 алкокси. Одним из воплощений является соединение, как здесь описано, где R8 представляет собой метокси Одним из воплощений является соединение, как здесь описано, выбранное из группы, состоящей из или его фармацевтически приемлемые соли. Одним из воплощений является соединение, как здесь описано, выбранное из группы, состоящей из или его фармацевтически приемлемые соли. В одном из воплощений настоящего изобретения предложен способ, описанный ниже где V, W, Y, Z, n, р, R1, R2, R3, R4, R5 и R6 являются такими, как здесь описано, и m представляет собой 1. В одном из воплощений настоящего изобретения предложено соединение формулы I, как здесь описано, полученное способом, как определено выше. В одном из воплощений настоящего изобретения предложено соединение формулы I, как здесь описано для применения в качестве терапевтически активного вещества. В одном из воплощений настоящего изобретения предложено соединение формулы I, как здесь описано для применения в качестве ингибитора активности ВАСЕ 1 и/или ВАСЕ 2. В одном из воплощений настоящего изобретения предложено соединение формулы I, как здесь описано для применения в качестве ингибитора активности ВАСЕ 1. В одном из воплощений настоящего изобретения предложено соединение формулы I, как здесь описано для применения в качестве ингибитора активности ВАСЕ 2. В одном из воплощений настоящего изобретения предложено соединение формулы I, как здесь описано для применения в качестве ингибитора активности ВАСЕ 1 и ВАСЕ 2. В одном из воплощений настоящего изобретения предложено соединение формулы I, как здесь описано для применения в качестве терапевтически активного вещества при терапевтическом и/или профилактическом лечении заболеваний и нарушений, характеризующихся повышенными уровнями амилоида и/или олигомеров -амилоида и/или -амилоидных бляшек и дальнейших отложений или болезни Альцгеймера. В одном из воплощений настоящего изобретения предложено соединение формулы I, как здесь описано для применения в качестве терапевтически активного вещества при терапевтическом и/или профилактическом лечении болезни Альцгеймера. В одном из воплощений настоящего изобретения предложено соединение формулы I, как здесь описано для применения в качестве терапевтически активного вещества при терапевтическом и/или профилактическом лечении диабета или диабета 2 типа. В одном из воплощений настоящего изобретения предложено соединение формулы I, как здесь описано для применения в качестве терапевтически активного вещества при терапевтическом и/или профилактическом лечении диабета. В одном из воплощений настоящего изобретения предложено соединение формулы I, как здесь описано для применения в качестве терапевтически активного вещества при терапевтическом и/или профилактическом лечении диабета или диабета 2 типа. В одном из воплощений настоящего изобретения предложено соединение формулы I, как здесь описано для применения в качестве терапевтически активного вещества при терапевтическом и/или профилактическом лечении болезни Альцгеймера, диабета или диабета 2 типа. В одном из воплощений настоящего изобретения предложена фармацевтическая композиция, содержащая соединение формулы I, как здесь описано, и фармацевтически приемлемый носитель и/или фармацевтически приемлемое вспомогательное вещество. В одном из воплощений настоящего изобретения предложено применение соединения формулы I,как здесь описано, при изготовлении лекарственного средства для применения при ингибировании активности ВАСЕ 1 и/или ВАСЕ 2. В одном из воплощений настоящего изобретения предложено применение соединения формулы I,как здесь описано, при изготовлении лекарственного средства для применения при ингибировании активности ВАСЕ 1. В одном из воплощений настоящего изобретения предложено применение соединения формулы I,как здесь описано, при изготовлении лекарственного средства для применения при ингибировании активности ВАСЕ 2. В одном из воплощений настоящего изобретения предложено применение соединения формулы I,как здесь описано, при изготовлении лекарственного средства для применения при ингибировании активности ВАСЕ 1 и ВАСЕ 2. В одном из воплощений настоящего изобретения предложено применение соединения формулы I,как здесь описано, при изготовлении лекарственного средства для терапевтического или профилактического лечения заболеваний и нарушений, характеризующихся повышенными уровнями -амилоида и/или-амилоидных олигомеров и/или -амилоидных бляшек и дальнейших отложений или болезни Альцгеймера. В одном из воплощений настоящего изобретения предложено применение соединения формулы I,как здесь описано, при изготовлении лекарственного средства для терапевтического или профилактического лечения болезни Альцгеймера. В одном из воплощений настоящего изобретения предложено применение соединения формулы I,как здесь описано, при изготовлении лекарственного средства для терапевтического или профилактического лечения диабета или диабета 2 типа. В одном из воплощений настоящего изобретения предложено применение соединения формулы I,как здесь описано, при изготовлении лекарственного средства для терапевтического или профилактического лечения диабета. В одном из воплощений настоящего изобретения предложено применение соединения формулы I,как здесь описано, при изготовлении лекарственного средства для терапевтического или профилактического лечения диабета или диабета 2 типа. В одном из воплощений настоящего изобретения предложено применение соединения формулы I,как здесь описано, при изготовлении лекарственного средства для терапевтического или профилактического лечения болезни Альцгеймера, диабета или диабета 2 типа. В одном из воплощений настоящего изобретения предложено применение соединения формулы I,как здесь описано, при изготовлении лекарственного средства для терапевтического или профилактического лечения болезни Альцгеймера. В одном из воплощений настоящего изобретения предложено применение соединения формулы I,как здесь описано, при изготовлении лекарственного средства для терапевтического или профилактического лечения диабета или диабета 2 типа. В одном из воплощений настоящего изобретения предложено применение соединения формулы I,как здесь описано при изготовлении лекарственного средства для терапевтического или профилактического лечения диабета. В одном из воплощений настоящего изобретения предложено применение соединения формулы I,как здесь описано при изготовлении лекарственного средства для терапевтического или профилактического лечения диабета 2 типа. В одном из воплощений настоящего изобретения предложено соединение формулы I, как здесь описано, для применения при ингибировании активности ВАСЕ 1 и/или ВАСЕ 2. В одном из воплощений настоящего изобретения предложено соединение формулы I, как здесь описано, для применения при ингибировании активности ВАСЕ 1. В одном из воплощений настоящего изобретения предложено соединение формулы I, как здесь описано, для применения при ингибировании активности ВАСЕ 2. В одном из воплощений настоящего изобретения предложено соединение формулы I, как здесь описано, для применения при ингибировании активности ВАСЕ 1 и ВАСЕ 2. В одном из воплощений настоящего изобретения предложено соединение формулы I, как здесь описано, для применения при терапевтическом и/или профилактическом лечении заболеваний и нарушений, характеризующихся повышенными уровнями -амилоида и/или -амилоидных олигомеров и/или амилоидных бляшек и дальнейших отложений или болезни Альцгеймера В одном из воплощений настоящего изобретения предложено соединение формулы I, как здесь описано, для применения при терапевтическом и/или профилактическом лечении болезни Альцгеймера. В одном из воплощений настоящего изобретения предложено соединение формулы I, как здесь описано, для применения при терапевтическом и/или профилактическом лечении диабета или диабета 2 типа. В одном из воплощений настоящего изобретения предложено соединение формулы I, как здесь описано, для применения при терапевтическом и/или профилактическом лечении диабета. В одном из воплощений настоящего изобретения предложено соединение формулы I, как здесь описано, для применения при терапевтическом и/или профилактическом лечении диабета или диабета 2 типа. В одном из воплощений настоящего изобретения предложено соединение формулы I, как здесь описано, для применения при терапевтическом и/или профилактическом лечении болезни Альцгеймера,диабета или диабета 2 типа. В одном из воплощений настоящего изобретения предложен способ для применения при ингибировании активности ВАСЕ 1 и/или ВАСЕ 2, в частности при терапевтическом или профилактическом лечении заболеваний и нарушений, характеризующихся повышенными уровнями -амилоида и/или амилоидных олигомеров и/или -амилоидных бляшек и дальнейших отложений, болезни Альцгеймера,диабета или диабета 2 типа, при этом способ включает введение соединения формулы I, как здесь описано, человеку или животному. В одном из воплощений настоящего изобретения предложен способ для применения при терапев- 15024286 тическом и/или профилактическом лечении болезни Альцгеймера, при этом способ включает введение соединения формулы I, как здесь описано, человеку или животному. В одном из воплощений настоящего изобретения предложен способ для применения при терапевтическом и/или профилактическом лечении диабета, при этом способ включает введение соединения формулы I, как здесь описано, человеку или животному. В одном из воплощений настоящего изобретения предложен способ для применения при терапевтическом и/или профилактическом лечении диабета 2 типа, при этом способ включает введение соединения формулы I, как здесь описано, человеку или животному. Кроме того, изобретение включает все оптические изомеры соединений формулы I, т.е. диастереоизомеры, диастереомерные смеси, рацемические смеси, все их соответствующие энантиомеры и/или таутомеры, а также их сольваты. Квалифицированный в уровне техники специалист понимает, что соединения формулы I могут существовать в таутомерной форме, например, в следующей таутомерной форме Все таутомерные формы включены в объем настоящего изобретения. Соединения формулы I могут содержать один или несколько асимметричных центров и, следовательно, могут существовать в виде рацематов, рацемических смесей, отдельных энантиомеров, диастереомерных смесей и индивидуальных диастереомеров. В зависимости от природы различных заместителей в молекуле могут присутствовать дополнительные асимметричные центры. Каждый такой асимметричный центр будет независимо давать два оптических изомера, и предполагается, что все возможные оптические изомеры и диастереомеры в смесях и в виде чистых или частично очищенных соединений включены в объем настоящего изобретения. Настоящее изобретение охватывает все такие изомерные формы этих соединений. Независимые синтезы этих диастереомеров или их хроматографическое разделение может быть достигнуто, как известно в данной области техники посредством соответствующей модификации методики, раскрытой в данном описании. Их абсолютная стереохимия может быть определена с помощью рентгеновской кристаллографии кристаллических продуктов или кристаллических промежуточных соединений, которые,если необходимо, подвергают дериватизации с реагентом, содержащим асимметрический центр известной абсолютной конфигурации. Если необходимо, рацемические смеси соединений могут быть разделены с выделением индивидуальных энантиомеров. Разделение может быть осуществлено способами, хорошо известными в данной области, такими как связывание рацемической смеси соединений с энантиомерно чистым соединением с образованием диастереомерной смеси, с последующим разделением индивидуальных диастереомеров стандартными способами, такими как фракционная кристаллизация или хроматография. Конкретным примером изомера соединения формулы I является соединение формулы Ia,где радикалы имеют значения, как описано в любом из вариантов осуществления В вариантах осуществления, где предложены оптически чистые энантиомеры, оптически чистый энантиомер означает, что соединение содержит 90% по массе желаемого изомера, в частности 95% желаемого изомера по массе или, более конкретно, 99% желаемого изомера по массе, указанный массовый процент основан на общем весе изомера(ов) соединения. Хирально чистые или хирально обогащенные соединения могут быть получены путем хирально селективного синтеза или путем разделения энантиомеров. Разделение энантиомеров может быть осуществлено из конечного продукта или, альтернативно, из подходящего промежуточного продукта. Соединения формулы I могут быть получены в соответствии со следующими схемами. Исходные вещества являются коммерчески доступными или могут быть получены в соответствии с известными способами. Любые ранее определенные радикалы и переменные будут и далее иметь ранее определенное значение, если не указано иного. Сульфинилимины общей формулы А 2, где X представляет собой -CR1aR1b (R1a, R1b являются водородом, низшим алкилом или фтором) и W представляет собой -CR2aR2b (с р = 1, R2a, R2b являются водородом), могут быть получены по аналогии с Т.P. TangJ.A. Ellman, J. Org. Chem. 1999, 64, 12, с помо- 16024286 щью конденсации арилкетона А 1 и сульфинамида, например, алкилсульфинамида, более конкретно (R)(+)-трет-бутилсульфинамида, в присутствии кислоты Льюиса, такой как, например, алкоксид титана (IV),более конкретно этоксид титана (IV) в растворителе, таком как эфир, например, диэтиловый эфир или более конкретно тетрагидрофуран. Конверсия сульфинилимина А 2 в эфир сульфинамида A3 происходит стереоселективно с помощью хиральной направляющей замещающей группы, как описано у TangEllman. Сульфинилимин А 2 может взаимодествовать в реакции Реформатского с енолятом цинка, полученным из, например, алкилбромдифторацетата, в частности этилбромдифторацетата, и активированного цинкового порошка при от комнатной до повышенной температуры, в частности при от 23 до 60 С в растворителе, таком как эфир, например, диэтиловый эфир или более предпочтительно тетрагидрофуран. Спирт формулы А 4 может быть получен восстановлением этилового эфира формулы A3 с гидридом щелочи, в частности борогидридом лития или алюмогидридом лития, в растворителе, таком как эфир,например, диэтиловый эфир или, более предпочтительно, тетрагидрофуран. Гидролиз хиральной направляющей замещающей группы в сульфинамидном спирте формулы А 4 с получением аминоспирта формулы А 5 может быть выполнен с минеральной кислотой, например, серной кислотой или, в частности, соляной кислотой, в растворителе, таком как эфир, например, диэтиловый эфир, тетрагидрофуран или, более предпочтительно, 1,4-диоксан. Аминооксазин формулы А 6 может быть получен взаимодействием аминоспирта формулы А 5 с бромцианом в растворителе, таком как спирт, в частности этанол. Восстановление производных формулы А 6, где Q представляет собой нитрогруппу, с получением анилинов формулы А 7 может быть выполнено посредством гидрогенизации с использованием катализатора, такого как палладий на угле, в протонных растворителях, таких как спирты, в частности этанол или метанол. Схема А Синтезы соединений формул I.1 и I.2. Целевые амины формулы I.1 могут быть получены посредством катализируемого палладием кросссвязывания между соединениями формулы А 6 и производными формулы Z-Ra, где Ra является бороновой кислотой или эфиром, в условиях (Кросс-сочетание Сузуки-Мияуры), известных квалифицированным специалистам. Целевые амиды формулы I.2 могут быть получены посредством селективного связывания анилинов формулы А 7 и карбоновой кислоты формулы Z-COOH с 4-(4,6-диметокси[1.3.5]триазин-2-ил)-4 метилморфолина хлорида гидратом (DMTMM) в качестве конденсирующего агента в растворителе, та- 17024286 ком как метанол. Другой обычный способ получения анилинов формулы А 7 через N-защищенные промежуточные соединения показан на схеме А.1. Защита аминогруппы в соединениях формулы А 6, где Q представляет собой бром, с получением арилбромидов формулы А 6.1 может быть выполнена с помощью триарилметилхлоридов, таких как трифенилметилхлорид(MMTr-Cl),ди(рметоксифенил)фенилметилхлорид (DMTr-Cl) или три(р-метоксифенил)метилхлорид (TMTr-Cl), в частности DMTr-Cl, в щелочных условиях, например, в присутствии амина, такого как триэтиламин или диизопропилэтиламин, в хлорированном растворителе, таком как дихлорметан или хлороформ, при температурах между 0 С и комнатной температурой. Арилбромиды формулы А 6.1 могут взаимодействовать с эквивалентами аммиака, такими как бензофенонимин, в присутствии подходящего катализатора на основе переходного металла, такого как бис(дибензилиденацетон)палладий(0) dba)2Pd) или трис-(дибензилиденацетон)дипалладий(0) [(dba)3Pd2], и подходящего лиганда, такого как рац-2,2'-бис-(дифенилфосфино)-1,1'-бинафтил (rac-BINAP), 2 бициклогексилфосфино-2',4',6'-триизопропилбифенил (X-PHOS) или 2-ди-трет-бутилфосфино-2',4',6'триизопропилбифенил (t-Bu X-PHOS), в присутствии основания, такого как трет-бутоксид натрия, фосфат калия или карбонат цезия, в подходящем растворителе, таком как толуол или 1,4-диоксан, в инертной атмосфере, такой как азотная или аргоновая, при температурах между 80 и 110 С, с получением соединений формулы А 6.2. Депротекция обеих аминогрупп в соединениях формулы А 6.2 может выполняться с помощью однореакторной процедуры посредством первоначального взаимодействия их с сильной органической кислотой, такой как трифторуксусная кислота, в хлорированных растворителях, таких как дихлорметан или хлороформ, в безводных условиях при температурах между 0 С и комнатной температурой для отщепления группы Р 1. Затем добавление воды для расщепления бензофенонимина и взаимодействие при комнатной температуре приводит к диаминам формулы А 7. Схема А.1 Альтернативный синтез промежуточных соединений анилинов формулы А 7. Сульфинилимины общей формулы В 2, где X представляет собой О или S, и W представляет собой CR2aR2b (с р = 1, R2a, R2b представляют собой водород, низший алкил, фенил или взятые вместе с атомом углерода, к которому они присоединены, образуют гетероциклил) могут образовывать гетероциклоалкил), могут быть получены по аналогии с Т.Р. TangJ.A. Ellman, J. Org. Chem. 1999, 64, 12, посредством конденсации арилкетона В 1 и сульфинамида, например, алкилсульфинамида, более конкретно (R)-(+)трет-бутилсульфинамида, в присутствии кислоты Льюиса, такой как, например, алкоксид титана(IV),более конкретно этоксид титана(IV) в растворителе, таком как эфир, например, диэтиловый эфир или,более предпочтительно, тетрагидрофуран. Конверсия сульфинилимина В 2 в сульфинамидный эфир В 3 проводится стереоселективно с использованием хиральной направляющей замещающей группы, как описано у TangEllman. Сульфинилимин В 2 может взаимодействовать в реакции Реформатского с енолятом цинка, полученным из, например,алкилбромдифторацетата, в частности этилбромдифторацетата, и активированного порошка цинка при от комнатной до повышенной температуры, в частности при от 23 до 60 С в растворителе, таком как эфир, например, диэтиловый эфир или более предпочтительно тетрагидрофуран. Спирт формулы В 4 может быть получен восстановлением этилового эфира формулы В 3 с гидридом щелочи, в частности борогидридом лития или алюмогидридом лития, в растворителе, таком как эфир,- 18024286 например диэтиловый эфир или более предпочтительно тетрагидрофуран. Гидролиз хиральной направляющей замещающей группы в сульфинамидном спирте формулы В 4 с получением аминоспирта формулы В 5 может быть выполнен с минеральной кислотой, например серной кислотой или, в частности, соляной кислотой, в растворителе, таком как эфир, например, диэтиловый эфир, тетрагидрофуран или более предпочтительно 1,4-диоксан. Аминооксазин формулы В 6 может быть получен взаимодействием аминоспирта формулы В 5 с бромцианом в растворителе, таком как спирт, в частности этанол. Восстановление производных формулы В 6, где Q представляет собой нитрогруппу, с получением анилинов формулы В 7 может быть проведено гидрированием с использованием катализатора, такого как палладий на угле, в протонных растворителях, таких как спирты, в частности этанол или метанол. Схема В Синтезы соединений формул I.3 и I.4. Целевые амины формулы I.3 могут быть получены посредством катализируемого палладием кросссвязывания между соединениями формулы В 6 и производными формулы Z-Ra, где Ra является бороновой кислотой или эфиром в условиях (Кросс-сочетание Сузуки-Мияуры), известных квалифицированному специалисту. Целевые амиды формулы I.4 могут быть получены селективным связыванием анилинов формулы В 7 и карбоновой кислоты формулы Z-COOH с 4-(4,6-диметокси[1.3.5]триазин-2-ил)-4-метилморфолина хлорида гидратом (DMTMM) в качестве конденсирующего агента в растворителе, таком как метанол. Целевые амиды формулы I.3 или I.4, где X представляет собой SO2, могут быть получены из соединений формулы I.3 или I.4, где X представляет собой S, посредством окисления в инертном растворителе при температурах между 0 С и комнатной температурой с использованием, например, пероксомоносульфата калия в качестве окислительного агента. Альтернативно, анилины формулы В 7 могут быть получены через N-защищенные промежуточные соединения как показано на схеме В.1. Защита аминогруппы в соединениях формулы А 6, где Q представляет собой бром, с получением арилбромидов формулы В 6.1 может быть выполнена с помощью триарилметилхлоридов, таких как трифенилметилхлорид(MMTr-Cl),ди(рметоксифенил)фенилметилхлорид (DMTr-Cl) или три(р-метоксифенил)метилхлорид (TMTr-Cl), в частности DMTr-Cl, в щелочных условиях, например, в присутствии амина, такого как триэтиламин или диизопропилэтиламин, в хлорированном растворителе, таком как дихлорметан или хлороформ, при температурах между 0 С и комнатной температурой. Арилбромиды формулы В 6.1 могут взаимодействовать с эквивалентами аммиака, такими как бензофенонимин, в присутствии подходящего катализатора на основе переходного металла, такого как бис(дибензилиденацетон)палладий(0) dba)2Pd) или трис-(дибензилиденацетон)дипалладий(0) [(dba)3Pd2], и подходящего лиганда, такого как рац-2,2'-бис-(дифенилфосфино)-1,1'-бинафтил (rac-BINAP), 2 бициклогексилфосфино-2',4',6'-триизопропилбифенил (X-PHOS) или 2-ди-трет-бутилфосфино-2',4',6'триизопропилбифенил (t-Bu X-PHOS), в присутствии основания, такого как трет-бутоксид натрия, фосфат калия или карбонат цезия, в подходящем растворителе, таком как толуол или 1,4-диоксан, в инертной атмосфере, такой как азотная или аргоновая, при температурах между 80 и 110 С, с получением соединений формулы В 6.2. Депротекция обеих аминогрупп в соединениях формулы В 6.2 может выполняться с помощью однореакторной процедуры посредством первоначального взаимодействия их с сильной органической кислотой, такой как трифторуксусная кислота, в хлорированных растворителях, таких как дихлорметан или хлороформ, в безводных условиях при температурах между 0 С и комнатной температурой для отщепления группы Р 1. Затем добавление воды для расщепления бензофенонимина и взаимодействие при комнатной температуре приводит к диаминам формулы В 7. Схема В.1 Альтернативный синтез промежуточных соединений анилинов формулы В 7. Алкилирование спиртов формулы А 4 или В 4 до нитрилов формулы С 1 может быть выполнено с подходящим слабым основанием, в частности оксидом серебра(1) в растворителе, таком как тетрагидрофуран или дихлорметан, более предпочтительно дихлорметан, в присутствии алкилирующего катализатора, такого как тетрабутиламмония йодид. Гидролиз хиральной направляющей замещающей группы в нитрилах формулы С 1 с получением аминонитрилов формулы С 2 может быть проведен с помощью минеральной кислоты, например серной кислоты и, в частности, соляной кислоты в растворителе, таком как эфир, например, диэтиловый эфир или более предпочтительно 1,4-диоксан. Аминооксазепины формулы С 3 могут быть получены взаимодействием аминонитрилов формулы С 2 и триметилалюминия в растворителе, таком как ксилон или толуол, в частности толуол. Восстановление производных формулы С 3, где Q представляет собой нитрогруппу, с получением анилинов формулы С 4 может быть проведено гидрогенизацией с использованием катализатора, такого как палладий на угле, в протонных растворителях, таких как спирты, в частности этанол или метанол. Схема С Синтезы соединений формул I.5 и I.6. Целевые амины формулы I.5 могут быть получены посредством катализируемого палладием кросссвязывания между соединениями формулы С 3 и производными формулы Z-Ra, где Ra представляет собой бороновую кислоту или эфир в условиях (Кросс-сочетание Сузуки-Мияуры), известных квалифицированному специалисту. Целевые амиды формулы I.6 могут быть получены селективным связыванием анилинов формулы С 4 и карбоновой кислоты формулы Z-COOH с 4-(4,6-диметокси[1.3.5]триазин-2-ил)-4-метилморфолина хлорида гидратом (DMTMM) в качестве конденсирующего агента в растворителе, таком как метанол. Соответствующие фармацевтически приемлемые соли с кислотами могут быть получены стандартными способами, известными специалисту в данной области, например путем растворения соединения формулы I в подходящем растворителе, таких как, например, диоксан или тетрагидрофуран (ТГФ), и добавления подходящего количества соответствующей кислоты. Продукты, как правило, могут быть выделены фильтрованием, или с помощью хроматографии. Конверсию соединения формулы I в фармацевтически приемлемую соль с основанием можно проводить путем обработки такого соединения таким основанием. Одним из возможных способов образования такой соли является, например, добавление 1/n эквивалентов основной соли, такой как, например, М(ОН)n, где М = металл или аммониевый катион и n = количество гидроксид-анионов, к раствору соединения в подходящем растворителе (например этанол,смесь этанол-вода, смесь тетрагидрофуран-вода) и удаление растворителя путем выпаривания или лиофилизации. Конкретными солями являются гидрохлорид, формиат и трифторацетат. Настолько, насколько их получение не описано в примерах, соединения формулы I, а также все промежуточные продукты могут быть получены в соответствии с аналогичными способами, или в соответствии со способами, изложенными в данном документе. Исходные материалы являются коммерчески доступными, известны в данной области или могут быть получены способами, известными в данной области, или по аналогии с ними. Следует понимать, что соединения общей формулы I по данному изобретению могут быть дериватизированы по функциональным группам с образованием производных, которые способны к обратному превращению в исходное соединение in vivo. Фармакологические тесты Соединения формулы I и их фармацевтически приемлемые соли обладают ценными фармакологическими свойствами. Было обнаружено, что соединения по настоящему изобретению ассоциированы с ингибированием активности ВАСЕ 1 и/или ВАСЕ 2. Соединения исследовали в соответствии с тестом,приведенным далее. Анализ клеточного снижения А.a) Клетки человека HEK293, которые были стабильно трасфицированы вектором, экспрессирующим cDNA гена АРР дикого типа человека (АРР 695), использовали для определения эффективности соединений в клеточном анализе. Клетки засеяли в 96-луночные микропланшеты в клеточную среду для культивирования (среда Искова, плюс 10% (об./об.) фетальной бычьей сыворотки, глутамин, пенициллин/стрептомицин) до приблизительно 80% конфлюэнтности и добавили соединения при 10 концентрации в 1/10 объема среды без FCS, содержащей 8% ДМСО (конечная концентрация ДМСО сохранилась при 0.8% об./об.). Через 18-20 ч инкубации при 37 С и 5% СО 2 в инкубаторе с влажностью культуральный супернатант собрали для определения концентрации А 40. 96-луночные ELISA планшеты (например, Nunc MaxiSorb) покрыли моноклональными антителами, которые специфично распознают С-конец пептида А 40 (Brockhaus и соавт., NeuroReport 9, 1481-1486; 1998). После блокирования сайтов неспецифического связывания с помощью, например, 1% БСА, и промывки, культуральные супернатанты в подходящем разведении добавили к антителам детекции А, связанным с пероксидазой хрена (например,антитело 4G8, Senetek, Maryland Heights, МО) и инкубировали в течение 5-7 ч. Впоследствии лунки микропланшет интенсивно промыли трис-буферизированным физраствором, содержащим 0.05% Tween 20 и анализ запустили тетраметилбензидин/Н 2 О 2 в буфере лимонной кислоты. После остановки реакции одним объемом 1 н. H2SO4 реакционную смесь измеряли на ELISA ридере при длине волны 450 нм. Концентрации А в культуральных супернатантах рассчитывали на основе стандартной кривой, полученной с использованием известных количеств чистого А пептида.b) Альтернативно, можно использовать А 40 AlphaLISA анализ. Клетки HEK293 АРР засеяли в 96 луночные микропланшеты в клеточную среду для культивирования (среда Искова, плюс 10% (об./об.) фетальной бычьей сыворотки, глутамин, пенициллин/стрептомицин) до приблизительно 80% конфлюэнтности и добавили соединения при 3 концентрации в 1/3 объема культуральной среды (конечная концентрация ДМСО сохранилась при 1% об./об.). Через 18-20 ч инкубации при 37 С и 5% СО 2 в инкубаторе с влажностью культуральный супернатант собрали для определения концентрации А 40 при помощи набора Perkin-Elmer Human Amyloid beta 1-40 (высокоспецифичный) (Cat AL275C). В планшеты Perkin-Elmer White Optiplate-384 (Cat 6007290), объединили 2 мкл культуральных супернатантов с 2 мкл смеси 10 Х AlphaLISA Anti-hAAcceptor шариков + биотинилированное антителоAnti-A 1-40 (50 мкг/мл/5 нМ). Через 1 ч инкубации при комнатной температуре добавили 16 мкл 1.25 X препарата Streptavidin (SA) Donor шариков (25 мкг/мл) и инкубировали 30 мин в темноте. Эмиссию света при 615 нм затем записывали с использованием ридера EnVision-Alpha Reader. Уровни А 40 в культуральных супернатантах рассчитывались как процент от максимального сигнала (клетки, обработанные 1% ДМСО без ингибитора). Значения IC50 рассчитывали с использованием программного обеспеченияExcel XLfit. Анализ ингибирования ВАСЕ посредством измерения расщепления клеточного ТМЕМ 27. Анализ использует принцип ингибирования расщепления ТМЕМ 27 человека эндогенным клеточным ВАСЕ 2 в клеточной линии Ins1e крысы и отделение от клеточной поверхности в культуральную среду, с последующей детекцией в анализе ELISA. Ингибирование ВАСЕ 2 предотвращает расщепление и отделение дозозависимым образом. Стабильная клеточная линия "INS-TMEM27" представляет полученную из INS1e клеточную линию с индуцируемой экспрессией (с использованием TetOn системы) полноразмерного hTMEM27 в доксициклинзависимой манере. Клетки в течение эксперимента культивировались в среде RPMI1640 + Glutamax (Invitrogen) Пенициллин/Стрептомицин, 10% фетальная бычья сыворотка, 100 мМ пируват, 5 мМ бета-меркаптоэтанол, 100 мкг/мл G418 и 100 мкг/мл гигромицина и росли в прикрепленной культуре при 37 С в обычном клеточном СО 2 инкубаторе. Клетки INS-TMEM27 засевали в 96-луночные планшеты. Через 2 дня культивирования добавляли ингибитор ВАСЕ 2 в диапазоне концентраций, необходимых для анализа и после дополнительных 2 ч добавили доксициклин до конечной концентрации 500 нг/мл. Клетки инкубировали в течение дополнительных 46 ч и собрали супернатант для детекции отделившегося ТМЕМ 27. Анализ ELISA (с использованием пары мышиных антител против человеческого ТМЕМ 27, направленных против внеклеточного домена ТМЕМ 27) использовали для детекции ТМЕМ 27 в культуральной среде. Значения ЕС 50 для ингибирования ВАСЕ 2 рассчитывали с использованием данных ELISA для каждой концентрации ингибитора и стандартным программным обеспечением, аппроксимирующем кривые, таким как XLFit для программы Excel. Таблица 1 Значения IC50 выбранных примеров; и b) обозначают соответствующий использовавшийся тип клеточного анализа. Фармацевтические композиции Соединения формулы I и их фармацевтически приемлемые соли могут применяться в качестве терапевтически активных веществ, например в виде фармацевтических препаратов. Фармацевтические препараты могут быть введены перорально, например в форме таблеток, таблеток с покрытием, драже,твердых и мягких желатиновых капсул, растворов, эмульсий или суспензий. Введение может, однако,также быть осуществлено ректально, например, в форме суппозиториев, или парентерально, например в форме растворов для инъекций. Соединения формулы I и их фармацевтически приемлемые соли могут быть обработаны вместе с фармацевтически инертными, неорганическими или органическими носителями для получения фармацевтических препаратов. Лактоза, кукурузный крахмал или его производные, тальк, стеариновая кислота или ее соли и т.п. могут применяться, например, в качестве таких носителей для таблеток, таблеток с
МПК / Метки
МПК: A61K 31/537, C07D 498/10, A61P 25/28
Метки: спиро[1,4]оксазепины, качестве, bace2, спиро[1,3]оксазины, и(или, bace1, ингибиторов
Код ссылки
<a href="https://eas.patents.su/30-24286-spiro13oksaziny-i-spiro14oksazepiny-v-kachestve-ingibitorov-bace1-iili-bace2.html" rel="bookmark" title="База патентов Евразийского Союза">Спиро[1,3]оксазины и спиро[1,4]оксазепины в качестве ингибиторов bace1 и(или) bace2</a>
Предыдущий патент: Способ улавливания металлов
Следующий патент: Измерительный модуль и устройство для измерения и оценки гибкости позвоночника с таким измерительным модулем (варианты)
Случайный патент: Способ количественной оценки предметов на ленте конвейера и конвейерный узел