Производные диаза-спиро-[4.4]нонана в качестве антагонистов нейрокинина (nk1)
Номер патента: 14239
Опубликовано: 29.10.2010
Авторы: Янссенс Франс Эдуард, Понселе Алан Филипп, Симонне Иван Рене Фердинан, Купа Софи, Схунтьес Брюно
Формула / Реферат
1. Соединение общей формулы (I)
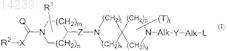
его фармацевтически приемлемые кислотно- или основно-аддитивные соли, стереохимические изомерные формы и N-оксиды, где
R2 обозначает Ar2;
X обозначает ковалентную связь;
Q обозначает О;
R1 выбран из группы, состоящей из Ar1-алкила и ди(Ar1)алкила;
n и m оба равны 1;
Z обозначает ковалентную связь;
j, k, р, q обозначают целые числа, независимо друг от друга равные нулю, 1, 2 или 3; при условии, что суммы (j+k) и (p+q) равны 3;
Т обозначает =O в альфа-положении по отношению к атому N, a t обозначает целое число, равное 0 или 1;
каждый Alk независимо обозначает ковалентную связь; бивалентный насыщенный углеводородный радикал, содержащий 1 атом углерода;
Y обозначает ковалентную связь или бивалентный радикал формулы -С(=O)-;
L выбран из группы, состоящей из водорода, алкила, Аг3 или Het2;
Ar1 обозначает фенил;
Ar2 обозначает фенил, необязательно замещенный 1 или 2 трифторметильными группами;
Ar3 обозначает фенил;
Het2 обозначает моноциклический гетероциклический радикал, выбранный из группы, состоящей из тетрагидрофуранила, фуранила, тиадиазолила, пиразинила и тиенила, где каждый моноциклический гетероциклический радикал может быть необязательно замещен по любому атому одним или несколькими радикалами, выбранными из алкила;
алкил обозначает линейный или разветвленный насыщенный углеводородный радикал, содержащий от 1 до 6 атомов углерода, или циклический насыщенный углеводородный радикал, содержащий от 3 до 6 атомов углерода.
2. Соединение по п.1, отличающееся тем, что спирофрагмент имеет формулу (f6) или (f8), в которой все переменные имеют такое же определение, как в формуле (I), а обозначает пиперидинильный фрагмент формулы (I), a b обозначает фрагмент Alk-Y-Alk-L формулы (I).
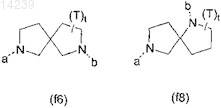
3. Соединение по любому из пп.1, 2, отличающееся тем, что R1обозначает бензил, присоединенный к 2 положению.
4. Соединение по любому из пп.1-3, отличающееся тем, что фрагмент R2-X-C(=Q)- обозначает 3,5-ди-(трифторметил)фенилкарбонил.
5. Соединение по любому из пп.1-4, отличающееся тем, что L выбран из группы, состоящей из водорода, трет-бутила, изопропила, тетрагидрофуранила, фуранила, тиенила, тиадиазолила, фенила и пиразинила.
6. Соединение по любому из пп.1-5, где
R1 обозначает бензил;
j, k, р, q обозначают целые числа, независимо равные нулю, 1, 2 или 3; при условии, что суммы (j+k) и (p+q) равны 3;
t обозначает целое число, равное 0;
Y обозначает ковалентную связь или бивалентный радикал формулы -С(=O)-;
L выбран из группы, состоящей из водорода, алкила, Ar3и Het2;
Ar3 обозначает фенил.
7. Соединение по п.1, выбранное из группы соединений

и
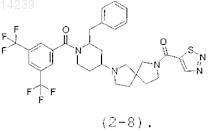
8. Применение соединения по любому из пп.1-7 в качестве лекарственного средства.
9. Применение соединения по любому из пп.1-7 в качестве лекарственного средства, активного при пероральном применении и способного проникать в центральную нервную систему.
10. Применение соединения по любому из пп.1-7 для получения лекарственного средства для лечения тахикининопосредованных состояний.
11. Применение соединения по пп.1-7 для получения лекарственного средства для лечения и/или профилактики шизофрении, рвоты, тревоги и депрессии, синдрома раздраженной кишки (IBS), нарушений циркодианного ритма, преэклампсии, ноцицепции, висцеральной и невропатической боли, панкреатита, нейрогенного воспаления, астмы, хронического обструктивного заболевания легких (COPD) и нарушений мочеиспускания, таких как недержание мочи.
12. Фармацевтическая композиция, содержащая фармацевтически приемлемый носитель и, в качестве активного ингредиента, терапевтически эффективное количество соединения по любому из пп.1-7.
13. Способ получения фармацевтической композиции по п.12, отличающийся тем, что фармацевтически приемлемый носитель однородно смешивают с терапевтически эффективным количеством соединения по любому из пп.1-7.
14. Способ получения соединения формулы (Ia), включающий восстановительное N-алкилирование промежуточного соединения формулы (II) промежуточным соединением формулы (III) с получением конечного соединения формулы (Ia), где все переменные имеют определение, указанное в п.1, в инертном растворителе и
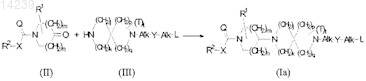
при необходимости, превращение соединения формулы (Ia) в терапевтически активную нетоксичную кислотно-аддитивную соль путем обработки кислотой, или в терапевтически активную нетоксичную основно-аддитивную соль путем обработки основанием, или, наоборот, превращение кислотно-аддитивной соли в свободное основание путем обработки щелочью, превращение основно-аддитивной соли в свободную кислоту путем обработки кислотой; и, при необходимости, получение стереохимических изомерных форм, N-оксидов и солей третичного аммония указанных соединений.
15. Способ по п.14, отличающийся тем, что фрагмент Alk-Y-Alk-L в соединениях формул (III) и (Ia) представляет собой бензил.
Текст
ПРОИЗВОДНЫЕ ДИАЗА-СПИРО-[4,4]НОНАНА В КАЧЕСТВЕ АНТАГОНИСТОВ НЕЙРОКИНИНА (NK1) Янссенс Франс Эдуард (BE), Купа Софи,Понселе Алан Филипп, Симонне Иван Рене Фердинан, Схунтьес Брюно (FR) Представитель: Данное изобретение относится к замещенному производному диаза-спиро-[4,4]нонана общей формулы (I) и его фармацевтически приемлемым кислотно- или основно-аддитивным солям,стереохимическим изомерным формам и N-оксидам, где все заместители имеют определения,указанные в п.1, обладающему антагонистической активностью по отношению к нейрокинину, в частности, антагонистической активностью по отношению к NK1, к способу получения данного производного, к композиции, содержащей указанное производное, и к его применению в качестве лекарственного средства, в особенности для лечения и/или профилактики шизофрении,рвоты, тревоги и депрессии, синдрома раздраженной кишки (IBS), нарушений циркодианного ритма, преэклампсии, ноцицепции, висцеральной и невропатической боли, панкреатита,нейрогенного воспаления, астмы, хронического обструктивного заболевания легких (COPD) и нарушений мочеиспускания, таких как недержание мочи. 014239 Область изобретения Данное изобретение относится к замещенным производным диаза-спиро-[4,4]нонана, обладающим антагонистической активностью по отношению к нейрокинину, в частности антагонистической активностью по отношению к NK1, к способам получения данных производных, к композициям, содержащим указанные производные, и к их применению в качестве лекарственных средств, в особенности для лечения и/или профилактики шизофрении, рвоты, тревоги и депрессии, синдрома раздраженной кишки (IBS),нарушений циркодианного ритма, преэклампсии, ноцицепции, боли, в частности висцеральной и невропатической боли, панкреатита, нейрогенного воспаления, астмы, хронического обструктивного заболевания легких (COPD) и нарушений мочеиспускания, таких как недержание мочи. Предшествующий уровень техники Тахикинины принадлежат к семейству коротких пептидов, которые широко распространены в центральной и периферической нервной системе млекопитающих (Bertrand and Geppetti, Trends Pharmacol.Sci. 17:255-259 (1996); Lundberg, Can. J. Physiol. Pharmacol. 73:908-914 (1995); Maggi, Gen. Pharmacol. 26:911-944 (1995); Regoli et al., Pharmacol. Rev. 46 (1994. Они имеют общую С-концевую последовательность Phe-Xaa-Gly-Leu-Met-NH2. Полагают, что тахикинины, высвобождающиеся из периферических сенсорных нервных окончаний, участвуют в нейрогенном воспалении. В спинном мозге/центральной нервной системе тахикинины могут участвовать в передаче/восприятии боли, а также в некоторых автономных и поведенческих рефлексах. Тремя основными тахикининами являются вещество Р (SP), нейрокинин А (NKA) и нейрокинин В (NKB), которые обладают избирательным сродством к трем разным подтипам рецепторов нейрокининов, обозначаемым NK1, NK2 и NK3, соответственно. Однако результаты функциональных исследований на клонированных рецепторах позволяют предположить, что существуют сильные функциональные перекрестные взаимодействия между тремя тахикининами и соответствующими рецепторами нейрокининов (Maggi and Schwartz, Trends Pharmacol. Sci. 18:351-355(1997. Видовые различия в структуре рецепторов NK1 обуславливают разную активность антагонистов(1994. Человеческий рецептор NK1 очень похож на рецептор NK1 морских свинок и песчанок, но сильно отличается от рецептора NK1 грызунов. На настоящий момент разработка антагонистов нейрокинина привела к получению ряда пептидных соединений, которые слишком активно метаболизируются, чтобы использоваться в качестве фармацевтически активных веществ (Longmore J. et al., DNP 8(1):5-23(1995. Тахикинины опосредуют шизофрению, депрессию (связанную со стрессом), состояния тревоги,рвоту, воспалительные ответы, сокращение гладкой мускулатуры и ощущение боли. На основе антагонистов нейрокининов разрабатываются лекарственные средства против рвоты, тревоги и депрессии, синдрома раздраженной кишки (IBS), нарушений циркодианного ритма, висцеральной боли, нейрогенного воспаления, астмы, нарушений мочеиспускания и ноцицепции. В частности, антагонисты NK1 имеют высокий терапевтический потенциал в отношении рвоты и депрессии, а антагонисты NK2 имеют высокий терапевтический потенциал в отношении астмы. Антагонисты NK3 могут участвовать в лечении боли/воспаления (Giardina, G. et al. Exp. Opin. Ther. Patents, 10(6):939-960 (2000 и шизофрении. Шизофрения Недавно было показано, что антагонист NK3 SR142801 (Sanofi) оказывает антипсихотическое действие на пациентов, страдающих шизофренией, не влияя на негативные симптомы (Arvantis, L. ACNPMeeting, December 2001). Активация рецепторов NK1 вызывает состояние тревоги, стрессогенные события приводят к повышению уровней вещества Р (SP) в плазме, а антагонисты NK1 по опубликованным данным обладают анксиолитическим действием на некоторые животные модели. Антагонист NK1 MK-869, полученный от Merck, оказывает антидепрессивное действие при глубокой депрессии, однако данные результаты не являются достоверными вследствие высокой частоты ответа на плацебо. Кроме того, показано, что антагонист NK1 (S)-GR205171 от Glaxo-Welcome повышает высвобождение допамина в лобной доле коры головного мозга, но не в стриатуме (Lejeune et al. Soc. Neurosci., November 2001). Следовательно, можно предположить, что антагонисты NK3 в сочетании с антагонистами NK1 оказывают благоприятное действие как на позитивные, так и на негативные симптомы шизофрении. Тревога и депрессия Депрессия является одним из наиболее распространенных аффективных расстройств в современном обществе с высокой и все увеличивающейся частотой заболеваний, особенно среди молодых членов популяции. В настоящее время частота заболевания глубокой депрессией (MDD, DSM-IV) составляет 1025% среди женщин и 5-12% среди мужчин, при этом приблизительно у 25% пациентов время жизниMDD является рецидивирующим, с отсутствием полного восстановления между приступами и с наложением на дистимическое расстройство. Существует высокая степень совместной заболеваемости депрессией и другими психическими нарушениями, в частности у молодого населения депрессия часто связана с зависимостью от наркотиков и алкоголя. Поскольку депрессия в основном поражает людей в возрасте от 18 до 44 лет, то есть наиболее трудоспособную часть населения, очевидно, что она является тяжелым-1 014239 бременем для отдельных людей, их семей и всего общества в целом. Среди всех терапевтических способов лечение антидепрессантами бесспорно является наиболее эффективным. В течение последних 40 лет разработано и поступило в продажу большое число антидепрессантов. Тем не менее, ни один из существующих антидепрессантов полностью не удовлетворяет всем критериям идеального лекарственного средства (высокая терапевтическая и профилактическая эффективность, быстродействие, полная кратковременная и долговременная безопасность, простые и удобные фармакокинетические параметры), в том числе отсутствие побочных эффектов, которые тем или иным способом ограничивают применение антидепрессантов во всех группах и подгруппах пациентов,страдающих от депрессии. Поскольку способы лечения причин депрессии в настоящее время отсутствуют и в ближайшем будущем их появление не предвидится и, кроме того, отсутствуют антидепрессанты, эффективные более чем для 60-70% пациентов, существует потребность в разработке новых антидепрессантов, которые позволили бы преодолеть недостатки, свойственные доступным лекарственным средствам. Некоторые данные указывают на участие SP в состояниях тревоги, связанных со стрессом. Введение SP в центральную нервную систему вызывает сердечно-сосудистый ответ, напоминающий классическую реакцию "борьбы или бегства", физиологически характеризующуюся расширением сосудов скелетных мышц и уменьшением мезентериального и почечного кровотока. Указанная сердечно-сосудистая реакция сопровождается поведенческим ответом, наблюдающимся у грызунов после воздействия вредного стимула или стресса (Culman and Unger, Can. J. Physiol. Pharmacol. 73:885-891 (1995. Агонисты и антагонисты NK1 после системного введения оказывают на мышей анксиогенное и анксиолитическое действие, соответственно (Teixeira et al., Eur. J. Pharmacol. 311:7-14 (1996. Способность антагонистовPharmacol. Sci. 17:255-259 (2001, согласуется с указанной антидепрессантной/анксиолитической активностью, поскольку у песчанок сердцебиение играет роль предупреждения об опасности или сигнала тревоги для животных того же вида. Рецептор NK1 можно обнаружить во всей лимбической системе и в участках мозга, отвечающих за формирование чувства страха, которые включают в себя мозжечковую миндалину, гиппокамп, перегородку, гипоталамус и околоводопроводный участок серого вещества. Кроме того, вещество Р высвобождается в центральной нервной системе в ответ на травматические или токсические стимулы, а опосредованная веществом Р передача нервного сигнала может вносить вклад или участвовать в формировании чувства тревоги, страха и эмоциональных нарушений, которые сопровождают аффективные расстройства, такие как депрессия и тревога. Данную точку зрения подтверждают изменения содержания вещества Р в отдельных участках мозга, происходящие в ответ на стрессогенные стимулы (Brodin et al., Neuropeptides 26:253-260 (1994. Введение миметиков вещества Р (агонистов) в центральную нервную систему индуцирует ряд защитных поведенческих и сердечно-сосудистых изменений, в том числе условную антипатию к месту(1998 и тревогу на приподнятом крестообразном лабиринте (Aguiar and Brandao, Physiol. Behav. 60:1183-1186 (1996. Данные соединения не влияют на двигательную активность и координацию движений на вращающемся аппарате или на способность передвигаться в клетке, приспособленной для активных движений. Понижающая регуляция биосинтеза вещества Р наблюдается в ответ на введение известных анксиолитических и антидепрессантных средств (Brodin et al., Neuropeptides 26:253-260 (1994); Shirayama et al., Brain. Res. 739:70-78 (1996. Подобным образом, голосовой ответ, индуцированный у морских свинок введением агониста NK1 в центральную нервную систему, может подавляться под действием антидепрессантов, таких как имипрамид и флуоксетин, а также L-733060, антагонист NK1. Результаты, полученные в проведенных исследованиях, позволяют предположить, что блокада рецепторов NK1 в центральной нервной системе приводит к подавлению психологического стресса по механизму, напоминающему механизм действия антидепрессантов и анксиолитиков (Rupniak and Kramer, Trends Pharmacol.Sci. 20:1-12 (1999, но при этом не имеет побочных эффектов, свойственных существующим в настоящее время лекарственным средствам. Рвота Тошнота и извержение рвотных масс являются наиболее неприятными побочными эффектами противораковой химиотерапии. Они снижают качество жизни и могут побуждать пациентов откладывать прием средств, которые могут им помочь, или совсем отказываться от их применения (Kris et al., J. Clin.Oncol, 3:1379-1384 (1985. Частота возникновения, интенсивность и характер рвоты определяются разными факторами, такими как тип, доза и способ введения химиотерапевтического средства. Как правило,ранняя или острая рвота начинается в пределах первых 4 ч после введения химиотерапевтического средства, достигает пика в интервале от 4 до 10 ч и уменьшается между 12 и 24 ч. Отсроченная рвота (развивающаяся после 24 ч и продолжающаяся в течение 3-5 дней после химиотерапии) наблюдается после введения большинства химиотерапевтических средств с интенсивным рвотным эффектом (уровень 4 и 5 в соответствии с Hesketh et al., J. Clin. Oncol. 15:103 (1997. Противораковые средства с интенсивным-2 014239 рвотным эффектом, включающие в себя цисплатин, вызывают острую рвоту более чем у 98% и отсроченную рвоту у 60-90% людей, страдающих от ракового заболевания. Животные модели химиотерапии, такие как индуцированная цисплатином рвота у хорьков (Ruddand Naylor, Neuropharmacology 33:1607-1608 (1994); Naylor and Rudd, Cancer. Surv. 21:117-135 (1996,позволяют успешно предсказывать клиническую эффективность антагонистов рецептора 5-НТ 3. Хотя данная модель помогает найти способ успешного лечения тошноты раковых пациентов, вызванной химиотерапией и облучением, антагонисты 5-НТ 3, такие как ондансетрон и гранисетрон (по отдельности или в сочетании с дексаметазоном), эффективно подавляют фазу острой рвоты (в течение первых 24 ч),но отсроченную рвоту (24 ч) они только уменьшают, причем с низкой эффективностью (De Mulder etal., Annuals of Internal Medicine 113:834-840 (1990); Roila, Oncology 50:163-167 (1993. Несмотря на то,что в настоящее время существуют эффективные способы предотвращения острой и отсроченной рвоты,50% пациентов все еще страдают от отсроченной рвоты и/или тошноты (Antiemetic Subcommittee, AnnalsOncol. 9:811-819 (1998. Показано, что в отличие от антагонистов 5-НТ 3, антагонисты NK1, такие как СР-99994 (Piedimonte(1999, ингибируют не только острую, но и отсроченную фазу цисплатин-индуцированной рвоты у животных (Rudd et al., Br. J. Pharmacol. 119:931-936 (1996); Tattersall et al., Neuropharmacology 39:652-663(2000. Также показано, что антагонисты NK1 уменьшают "отсроченную" рвоту у мужчин в отсутствие сопутствующей терапии (Cocquyt et al., Eur. J. Cancer 37:835-842 (2001); Navari et al., N. Engl. L. Med. 340:190-195 (1999. Более того, показано, что совместное введение антагонистов NK1 (таких как МК-869 и CJ-11974, также известный как эзлопитант) с дексаметазоном и антагонистами 5-НТ 3 дополнительно помогает предотвратить острую рвоту (Campos et al., J. Clin. Oncol. 19:1759-1767 (2001); Hesketh et al.,Clin. Oncol. 17:338-343 (1999. Рецепторы нейрокинина NK1 центральной нервной системы играют ключевую роль в регуляции рвоты. Антагонисты NK1 активно предотвращают рвоту, вызываемую широким рядом стимулов (Watsonal., J. Pharmacol. Exp. Ther. 302:696-709 (2002. Полагают, что действие данных соединений осуществляется путем блокады рецепторов NK1 в ядре центральной нервной системы. Следовательно, для проявления противорвотной активности данных соединений, помимо антагонистического действия по отношению к NK1, необходимым условием является их проникновение в ЦНС. Рвоту, индуцированную лоперамидом у хорьков, можно использовать в качестве быстрой и надежной модели для скрининга противорвотной активности антагонистов NK1. Кроме того, возможность применения данных соединений для лечения как острой, так и отсроченной фаз рвоты, индуцированной цисплатином, продемонстрирована на соответствующей модели хорьков (Rudd et al., Br. J. Pharmacol. 119:931-936 (1994. Данная модель позволяет исследовать как "острую", так и "отсроченную" рвоту после введения цисплатина и имеет подтвержденную чувствительность к антагонистам рецептора 5-НТ 3, глюкокортикоидам (Sam et al., Eur. J.Pharmacol. 417:231-237 (2001 и другим фармакологическим средствам. Если новое противорвотное средство не способно лечить и "острую", и "отсроченную" фазы рвоты, оно вряд ли найдет применение в клинике. Висцеральная боль и синдром раздраженной кишки (IBS) Висцеральное ощущение относится ко всей сенсорной информации, которая поступает от внутренних органов (сердце, легкие, ЖК тракт, гепатобилиарный тракт и мочеполовой тракт) в центральную нервную систему, где происходит осознавание ощущения. Первичные пути, по которым сенсорная информация передается от внутренних органов в ствол мозга и висцеросоматические участки коры головного мозга, включают в себя блуждающий нерв с нодозными ганглиями и первичные симпатические афферентные нервы с ганглиями задних корешков (DRG) и нейронами второго порядка из спинного рога. Висцеральная боль может быть вызвана опухолевыми процессами (например, раком поджелудочной железы), воспалением (например, холециститом, перитонитом), ишемией и механической закупоркой (например, камнем в мочеточнике). Медицинское лечение висцеральной боли, связанной с органическими нарушениями (в данном случае, с раком внутренних органов), по-прежнему основано на применении опиатов. Полученные в последнее время результаты позволяют предположить, что неорганические висцеральные нарушения, такие как синдром раздраженной кишки (IBS), экстракардиальная грудная боль (NCCP) и хроническая тазовая боль, могут возникать в результате состояния "висцеральной гиперальгезии". Данное состояние характеризуется тем, что физиологические, не причиняющие боль висцеральные стимулы (например, вздутие кишок) приводят к осознанию ощущения боли вследствие уменьшения болевого порога. Висцеральная гиперальгезия может отражать состояние продолжительного поствоспалительного восстановления порога деполяризации мембраны нейронных синапсов в висцеральных сенсорных путях. Изначально воспаление может возникать на периферии (например, инфекционный гастроэнтерит) или в участке интеграции висцеральной сенсорной информации (воспаление нервной ткани в спинном роге). Показано, что иSP, и пептид, кодируемый геном кальцитонина (CGRP), действуют как провоспалительные нейропепти-3 014239 ды в зоне воспаления нервной ткани. Висцеральная гиперальгезия, которая встречается у 15-25% западного населения, в настоящее время считается одной из основных мишеней лекарственных средств, разрабатываемых для лечения функциональных болезней кишечника. Она представляет собой серьезную социо-экономическую проблему, с точки зрения стоимости медицинского обслуживания, стоимости выписываемых лекарств и пропуска работы. Существующие в настоящее время способы лечения включают в себя, в числе прочих, применение спазмолитиков (IBS и NCCP), средств, улучшающих двигательные функции (например, тегасород при констипации-IBS), слабительных средств (констипация-IBS) и лоперамида (диарея-IBS). Показано,что ни один из этих способов не является очень эффективным, особенно при лечении боли. Для лечения висцеральной альгезии при болезненном IBS используют трициклические антидепрессанты в низких дозах и SSRI, однако соединения обоих указанных классов могут оказывать значительное влияние на прохождение толстой кишки. Проводимые в данной области исследования позволили идентифицировать значительное число молекулярных мишеней для разработки лекарственных средств против гиперальгезии. Данные мишени включают в себя рецепторы NK, рецептор CGRP, рецепторы 5-НТ 3, рецепторы глутамата и каппа-опиоидный рецептор. В идеале "висцеральный анальгетик" должен блокировать повышение сенсорной передачи от внутренних органов к ЦНС, не влияя на нормальный физиологический гомеостаз ЖК тракта, в том числе, обеспечение пропульсивного продвижения пищи, абсорбцию, секрецию и чувствительность. Существует очевидная связь тахикинина с висцеральным ноцицептивным сигнальным путем. Ряд доклинических публикаций по роли рецепторов NK1, NK2 и NK3 в формировании ощущения висцеральной боли и висцеральной гиперальгезии свидетельствует о том, что рецепторы NK1, NK2 и NK3 поразному участвуют в разных моделях воспалительной гиперчувствительности у грызунов. Недавно Kampet al., J. Pharmacol. Exp. Ther. 299:105-113 (2001) высказали предположение, что общий антагонист рецепторов нейрокининов может быть более активным, чем селективный антагонист рецептора нейрокинина. При клинических болевых состояниях, включающих в себя состояния висцеральной боли, повышены уровни вещества Р и рецепторов NK1, NK2 и NK3 (Lee et al., Gastroenterol. 118:A846 (2000. С учетом того, что проведенные в последнее время испытания антагонистов рецептора NK1 в качестве анальгетика потерпели неудачу (Goldstein et al., Clin. Pharm. Ther. 67:419-426 (2000, для получения значимого клинического эффекта может потребоваться применение сочетаний антагонистов. Антагонисты рецептора NK3 можно использовать в качестве средств против гиперальгезии (Julia et al., Gastroenterol. 116:11241131 (1999; J. Pharmacol. Exp. Ther. 299:105-113 (2001. В последнее время было показано, что участие рецепторов NK1 и NK3, но не рецепторов NK2, на уровне спинного мозга в висцеральной гиперчувствительности опосредуется ноцицептивными и не ноцицептивными афферентными стимулами (GaudreauPloudre, Neurosci. Lett. 351:59-62 (2003). Следовательно, интересной терапевтической мишенью для новых способов лечения висцеральной гиперальгезии является объединенная антагонистическая активность NK1-2-3. Существует несколько доклинических публикаций по роли рецепторов NK1 в формировании ощущения висцеральной боли. С использованием мышей с нокаутом гена рецептора NK1 и животных моделей, получающих антагонисты NK1, разные исследователи продемонстрировали, что рецептор NK1 играет важную роль в развитии гиперальгезии и висцеральной боли. Распределение рецепторов NK1 и вещества Р свидетельствует о том, что они скорее участвуют в формировании висцеральной боли, чем соматической. Действительно, вещество Р содержится более чем в 80% висцеральных первичных афферентных нервов и только в 25% кожных афферентных нервов. Рецепторы NK1 также участвуют в обеспечении двигательных функций желудочно-кишечного тракта (Tonini et al., Gastroenterol. 120:938-945 (2001);Okano et al., J. Pharmacol. Exp. Ther. 298:559-564 (2001. Поскольку антагонисты NK1 оказывают влияние и на двигательные функции желудочно-кишечного тракта, и на ноцицепцию, полагают, что они могут улучшать симптомы IBS. Недержание мочи Недержание мочи вызывается гиперрефлексией мочевого пузыря или детрузора ("чувствительный мочевой пузырь"). Такая гиперрефлексия связана с повышенной возбудимостью сенсорных афферентных С-волокон, передающих сигнал от мочевого пузыря в спинной мозг. Причиной повышенной возбудимости С-волокон могут быть разные факторы, например, она может возникать после инфекции мочевого пузыря и хронического растяжения стенки мочевого пузыря (например, при доброкачественной гипертрофии простаты, ВРН). Следовательно, лечение должно быть направлено на уменьшение повышенной возбудимости нервных клеток. Внутрипузырная инстилляция ваниллоидов (например, капсаицина) приводит к длительному улучшению гиперрефлексии детрузора, не поддающейся традиционному лечению антихолинергическими средствами. Как и у животных, у человека действие ваниллоидов опосредуется нейротоксическим эффектом на окончания сенсорных нервов. В мочевом пузыре человека субэндотелиальные сенсорные нервы содержат тахикинины, которые управляют повышенной возбудимостью детрузора. В данном процессе участвуют периферические рецепторы NK2 и, в меньшей степени, рецепторы NK1. Обнаружено, что последние участвуют в повышенной возбудимости мочевого пузыря на уровне спинного мозга. Следовательно, для лечения повышенной возбудимости детрузора предпочти-4 014239 тельно использовать антагонист действующего в центральной нервной системе NK1/действующего в периферической нервной системе NK2. Интересно, что активация рецепторов NK2 повышает активность ароматазы в клетках Сертоли. Антагонисты рецептора NK2 уменьшают уровни тестостерона в сыворотке мышей, что свидетельствует о возможности их применения для лечения ВРН. Предпосылки создания изобретения В WO 97/24324 (10 июля 1997), WO 97/24350 (10 июля 1997) и WO97/24356 (10 июля 1997), JanssenPharmaceutica N.V., описано применение соединений, содержащих пиперидинильный фрагмент, замещенных пиперидинильным или пирролидинильным фрагментом, в качестве антагонистов вещества Р(нейрокинина). В WO 01/94346 (13 декабря 2001), F. Hoffmann-La Roche AG, описано применение соединений, содержащих замещенный диаза-спиро[4.5]деканильный фрагмент, в качестве антагонистов рецептора нейрокинина. Соединения настоящего изобретения структурно отличаются от соединений предшествующего уровня техники тем, что все они содержат пиперидинильный фрагмент, замещенный диаза-спиро[4.4]нонильным фрагментом, а также тем, что они обладают повышенной антагонистической активностью по отношению к нейрокининам при пероральном и центральном введении и имеют терапевтический потенциал, особенно при лечении и/или профилактике шизофрении, рвоты, тревоги и депрессии,синдрома раздраженной кишки (IBS), нарушений циркодианного ритма, преэклампсии, ноцицепции, боли, в частности висцеральной и невропатической боли, панкреатита, нейрогенного воспаления, астмы,хронического обструктивного заболевания легких (COPD) и нарушений мочеиспускания, таких как недержание мочи. Описание изобретения Настоящее изобретение относится к новым производным замещенного диаза-спиро-[5,5]ундекана,соответствующим общей формуле (I) их фармацевтически приемлемым кислотно- или основно-аддитивным солям, стереохимическим изомерным формам и N-оксидам, гдеj, k, р, q обозначают целые числа, независимо друг от друга равные нулю, 1, 2 или 3; при условии, что суммы (j+k) и (p+q) равны 3; Т обозначает =O в альфа-положении по отношению к атому N, a t обозначает целое число, равное 0 или 1; каждый Alk независимо обозначает ковалентную связь; бивалентный насыщенный углеводородный радикал, содержащий 1 атом углерода;Y обозначает ковалентную связь или бивалентный радикал формулы -С(=O)-;Het2 обозначает моноциклический гетероциклический радикал, выбранный из группы, состоящей из тетрагидрофуранила, фуранила, тиадиазолила, пиразинила и тиенила, где каждый моноциклический гетероциклический радикал может быть необязательно замещен по любому атому одним или несколькими радикалами, выбранными из алкила; алкил обозначает линейный или разветвленный насыщенный углеводородный радикал, содержащий от 1 до 6 атомов углерода, или циклический насыщенный углеводородный радикал, содержащий от 3 до 6 атомов углерода. Данное изобретение также относится к соединению общей формулы (I), его фармацевтически приемлемым кислотно- или основно-аддитивным солям, стереохимическим изомерным формам и Nоксидам, используемым в качестве лекарственных средств. Далее, данное изобретение относится к композициям, содержащим соединение общей формулы (I),его фармацевтически приемлемые кислотно- или основно-аддитивные соли, стереохимические изомерные формы и N-оксиды, а также к способам получения соединений и композиций настоящего изобретения.-5 014239 Данное изобретение также относится к применению соединения общей формулы (I), его фармацевтически приемлемых кислотно- или основно-аддитивных солей и стереохимических изомерных форм для получения лекарственного средства для лечения тахикинин-опосредованных состояний, в частности для лечения и/или профилактики шизофрении, рвоты, тревоги и депрессии, синдрома раздраженной кишки (IBS), нарушений циркодианного ритма, преэклампсии, ноцицепции, боли, в частности висцеральной и невропатической боли, панкреатита, нейрогенного воспаления, астмы, хронического обструктивного заболевания легких (COPD) и нарушений мочеиспускания, таких как недержание мочи. Подробное описание изобретения Предпочтительно данное изобретение относится к соединению общей формулы (I), его фармацевтически приемлемым кислотно- или основно-аддитивным солям, стереохимическим изомерным формам и N-оксидам, где фрагмент спиро имеет одну из приведенных ниже структур, соответствующих любой из формул (f6) и (f8), в которых все переменные имеют такое же определение, как в формуле (I), "а" обозначает пиперидинильный фрагмент формулы (I), а "b" обозначает фрагмент Alk-Y-Alk-L формулы (I) Более предпочтительно данное изобретение относится к соединению общей формулы (I), его фармацевтически приемлемым кислотно- или основно-аддитивным солям, стереохимическим изомерным формам и N-оксидам, где R1 обозначает бензил и присоединен ко 2 положению, как показано в приведенной ниже формуле соединений формулы (I), в которых n и m равны 1. Более предпочтительно данное изобретение относится к соединению общей формулы (I), его фармацевтически приемлемым кислотно- или основно-аддитивным солям, стереохимическим изомерным формам и N-оксидам, где фрагмент R2-X-C(=Q)-обозначает 3,5-ди-(трифторметил)фенилкарбонил. Более предпочтительно данное изобретение относится к соединению общей формулы (I), его фармацевтически приемлемым кислотно- или основно-аддитивным солям, стереохимическим изомерным формам и N-оксидам, где Y обозначает ковалентную связь или -С(=O)-. Более предпочтительно данное изобретение относится к соединению общей формулы (I), его фармацевтически приемлемым кислотно- или основно-аддитивным солям, стереохимическим изомерным формам и N-оксидам, где каждый Alk независимо обозначает ковалентную связь. Более предпочтительно данное изобретение относится к соединению общей формулы (I), его фармацевтически приемлемым кислотно- или основно-аддитивным солям, стереохимическим изомерным формам и N-оксидам, где L выбран из группы, состоящей из водорода, трет-бутила, изопропила, тетрагидрофуранила, фуранила, тиенила, тиадиазолила и пиразинила. Предпочтительно L обозначает тетрагидрофуранил или тиадиазолил. Более предпочтительно данное изобретение относится к соединению общей формулы (I), его фармацевтически приемлемым кислотно- или основно-аддитивным солям, стереохимическим изомерным формам, N-оксидам, гдеt обозначает целое число, равное 0; каждый Alk независимо обозначает ковалентную связь или бивалентный линейный, насыщенный углеводородный радикал, содержащий 1 атом углерода;Y обозначает ковалентную связь или бивалентный радикал формулы -С(=O)-;Het2 обозначает моноциклический гетероциклический радикал, выбранный из группы, состоящей из тетрагидрофуранила, фуранила, тиенила, тиадиазолила и пиразинила; где каждый моноциклический гетероциклический радикал может быть необязательно замещен по любому атому одним или несколькими алкильными радикалами; и алкил обозначает линейный или разветвленный насыщенный углеводородный радикал, содержащий от 1 до 6 атомов углерода, или циклический насыщенный углеводородный радикал, содержащий от 3 до 6 атомов углерода. Более предпочтительно данное изобретение относится к соединению общей формулы (I), его фармацевтически приемлемым кислотно- или основно-аддитивным солям, стереохимическим изомерным формам, N-оксидам, где соединение представляет собой соединение, приведенное в таблицах данной заявки, например, в одной из таблиц 1-2, под номером 2-5 или 2-8. В контексте данной заявки алкил обозначает моновалентный линейный или разветвленный насыщенный углеводородный радикал, содержащий от 1 до 6 атомов углерода, и включает, например, метил,этил, пропил, бутил, 1-метилпропил, 1,1-диметилэтил, пентил, гексил; алкил также обозначает моновалентный циклический насыщенный углеводородный радикал, содержащий от 3 до 6 атомов углерода,например циклопропил, метилциклопропил, циклобутил, циклопентил и циклогексил. Определение алкила также включает алкильный радикал, необязательно замещенный по одному или нескольким атомам углерода одним или несколькими радикалами, выбранными из фенила, галогена, циано, оксо, гидрокси,формила и амино, например гидроксиалкил, такой как гидроксиметил и гидроксиэтил, и полигалогеналкил, такой как дифторметил и трифторметил. В контексте данной заявки галоген, как правило, относится к фтору, хлору, брому и иоду. В контексте данной заявки термин "соединения данного изобретения" относится к соединению общей формулы (I), его фармацевтически приемлемым кислотно- или основно-аддитивным солям, стереохимическим изомерным формам и N-оксидам. В контексте данной заявки, особенно в контексте фрагмента Alka-Y-Alkb формулы (I), ковалентная связь, обозначаемая двумя или более последовательными элементами, относится к одинарной ковалентной связи. Например, если Alka и Y оба обозначают ковалентную связь, а Alkb обозначает -СН 2-, то фрагмент Alka-Y-Alkb обозначает -СН 2-. Подобным образом, если каждый из Alka, Y и Alkb обозначает ковалентную связь, a L обозначает Н, то фрагмент Alka-Y-Alkb-L обозначает -Н. Фармацевтически приемлемые соли включают терапевтически активные нетоксичные кислотноаддитивные соли соединений формулы (I). Указанные соли можно получить путем обработки основной формы соединения формулы (I) подходящими кислотами, например неорганическими кислотами, такими как галогенводородные кислоты, в том числе хлористо-водородная кислота и бромисто-водородная кислота, серная кислота, азотная кислота и фосфорная кислота; органическими кислотами, такими как уксусная кислота, гидроксиуксусная кислота, пропановая кислота, молочная кислота, пировиноградная кислота, щавелевая кислота, малоновая кислота, янтарная кислота, малеиновая кислота, фумаровая кислота, яблочная кислота, винная кислота, лимонная кислота, метансульфоновая кислота, этансульфоновая кислота, бензолсульфоновая кислота, п-толуолсульфоновая кислота, цикламовая кислота, салициловая кислота, п-аминосалициловая кислота и памоевая кислота. Соединения формулы (I), содержащие кислые протоны, могут быть превращены в терапевтически активные нетоксичные соли добавления металлов или аминов путем обработки подходящими органическими и неорганическими основаниями. Подходящие основно-аддитивные соли включают в себя, например, соли аммония, соли щелочных и щелочно-земельных металлов, такие как соли лития, натрия,калия, магния и кальция, соли органических оснований, такие как соли бензатина, N-метил-Оглюкамина, гибрамина, и соли аминокислот, например аргинина и лизина. И наоборот, указанные солевые формы можно превратить в свободные формы путем обработки подходящим основанием или подходящей кислотой. Термин "аддитивная соль" в контексте данной заявки также включает в себя сольваты, образуемые соединениями формулы (I) и их солями. Примерами таких сольватов являются гидраты и алкоголяты.N-оксиды соединений формулы (I) включают в себя соединения формулы (I), в которых один или несколько атомов азота окислены до так называемого N-оксида, особенно соединения, в которых окислению подвергается один или несколько третичных атомов азота (например, радикал пиперазинила или пирролидинила). Указанные N-оксиды специалист в данной области может легко получить с помощью традиционных способов, и они, очевидно, являются альтернативой соединениям формулы (I), поскольку представляют собой метаболиты, образующиеся в организме человека в результате окисления. Широко известно, что окисление обычно является первой стадией метаболизма лекарственных средств (Textbookof Organic Medicinal and Pharmaceutical Chemistry, 1977, pages 70-75). Также известно, что метаболиты можно вводить человеку вместо самих соединений, и зачастую они оказывают такие же эффекты. Соединения данного изобретения обладают по меньшей мере двумя способными к окислению ато-7 014239 мами азота (фрагменты третичных аминов). Следовательно, существует высокая вероятность того, что Nоксиды образуются в результате метаболизма в организме человека. Соединения формулы (I) можно превратить в соответствующие N-оксиды с помощью известных в данной области способов превращения трехвалентного азота в N-оксидную форму. Указанную реакциюN-окисления, как правило, проводят путем взаимодействия исходного вещества формулы (I) с подходящим органическим или неорганическим пероксидом. Подходящие неорганические пероксиды включают в себя, например, пероксид водорода, пероксиды щелочных или щелочно-земельных металлов, такие как пероксид натрия и пероксид калия; подходящие органические пероксиды могут включать в себя пероксикислоты, такие как бензолкарбопероксикислота или галоген-замещенная бензолкарбопероксикислота,например 3-хлорбензолкарбопероксикислота, пероксоалкановые кислоты, например пероксоуксусная кислота, алкилгидропероксиды, например трет-бутилгидропероксид. Подходящими растворителями являются, например, вода, низшие алканолы, такие как этанол и т.п., углеводороды, такие как толуол, кетоны, например 2-бутанон, галогенированные углеводороды, например дихлорметан, а также смеси указанных растворителей. Термин "стереохимические изомерные формы" в данном описании относится ко всем возможным изомерным формам соединений формулы (I). Если не указано или не определено иначе, химическое наименование соединения включает в себя смесь всех возможных стереохимических изомерных форм,имеющих данное наименование, причем указанные смеси содержат все диастереомеры и энантиомеры основной молекулярной структуры. Более конкретно, стереогенные центры могут иметь R- или Sконфигурацию; заместители на бивалентных циклических (частично) насыщенных радикалах могут иметь либо цис-, либо транс-конфигурацию. Соединения, содержащие двойные связи, могут иметь Еили Z-стереохимию по указанным двойным связям. Очевидно, что стереохимические изомерные формы соединений формулы (I) входят в объем данного изобретения. Если в молекуле присутствует два стереогенных центра с известной абсолютной конфигурацией, то в соответствии с номенклатурой CAS хиральному центру с наименьшим номером, или центру отнесения,присваивается обозначение R или S (на основе правила Cahn-Ingold-Prelo). Каждый из R и S обозначает оптически чистые стереогенные центры с неопределенной абсолютной конфигурацией. Обозначения и используют следующим образом: положение заместителя наивысшего приоритета на асимметричном атоме углерода, имеющем минимальный номер, в циклической системе произвольно обозначают-положение по отношению к средней плоскости циклической системы. Положение заместителя наивысшего приоритета на другом асимметричном атоме углерода циклической системы (атом водорода в соединениях формулы (I по отношению к положению заместителя наивысшего приоритета на атоме отнесения обозначают , если оно располагается на той же стороне средней плоскости циклической системы, или "Р", если оно располагается на другой стороне средней плоскости циклической системы. Соединения формулы (I) и некоторые промежуточные соединения содержат по меньшей мере два стереогенных центра. С помощью описанных ниже способов соединения формулы (I) можно синтезировать в виде рацемических смесей энантиомеров, которые можно разделить с помощью известных в данной области методов. Рацемические соединения формулы (I) можно превратить в соответствующие диастереомерные соли путем взаимодействия с подходящей хиральной кислотой. Затем указанные диастереомерные соли можно разделить, например, путем селективной или фракционной кристаллизации с последующим высвобождением энантиомеров после обработки щелочью. Альтернативный способ разделения энантиомерных форм соединения формулы (I) включает в себя жидкостную хроматографию с использованием хиральной стационарной фазы. Указанные чистые стереохимические изомерные формы также можно получить путем использования в качестве исходных веществ соответствующих чистых стереохимических изомерных форм, при условии, что реакция протекает стереоспецифически. Если нужна конкретная стереоизомерная форма, указанное соединение предпочтительно синтезируют с помощью стереоспецифических методов получения. В данных способах в качестве исходных веществ используют чистые энантиомеры. Фармакология Вещество Р и другие тахикинины участвуют в осуществлении ряда биологических функций, таких как передача болевого ощущения (ноцицепция), воспаление нервных тканей, сокращение гладкой мускулатуры, экстравазация белков плазмы, расширение сосудов, секреция, дегрануляция тучных клеток, а также в активации иммунной системы. Полагают, что ряд заболеваний опосредуется активацией рецепторов нейрокининов, в частности рецептора NK1, в результате повышенного высвобождения вещества Р и других нейрокининов конкретными клетками, такими как клетки нейронной сети желудочнокишечного тракта, немиелинизированные первичные сенсорные афферентные нейроны, симпатические и парасимпатические нейроны, а также отличные от нейронов клетки (DNP 8(1):5-23 (1995) and Longmore J. et al., "Neurokinin Receptors" Pharmacological Reviews 46(4):551-599 (1994. Соединения настоящего изобретения являются эффективными ингибиторами нейрокининопосредованных эффектов, в частности эффектов, опосредованных рецептором NK1, и, следовательно,могут считаться антагонистами нейрокининов, особенно антагонистами вещества Р, что подтверждается-8 014239 путем подавления in vitro индуцированной веществом Р релаксации коронарных артерий свиней. Сродство связывания соединений настоящего изобретения с рецепторами нейрокининов человека, морских свинок и песчанок также можно определить in vitro путем анализа связывания рецептора с использованием 3 Н-вещества Р в качестве радиолиганда. Тестируемые соединения также демонстрируют антагонистическую активность по отношению к веществу Р in vivo, что подтверждается, например, подавлением индуцированной веществом Р экстравазации белков плазмы у морских свинок, или подавлением индуцированной лекарственными средствами рвоты у хорьков (Watson et al., Br. J. Pharmacol. 115:84-94 (1995. Благодаря их способности подавлять действие тахикининов путем блокирования рецепторов нейрокининов, в особенности рецептора NK1, соединения данного изобретения можно использовать в качестве лекарственного средства, например, для профилактики и лечения тахикинин-опосредованных состояний. В частности, для профилактики и лечения тахикинин-опосредованных состояний соединения данного изобретения можно использовать в качестве лекарственных средств, обладающих активностью при пероральном применении и способных проникать в центральную нервную систему. Следовательно, данное изобретение относится к применению соединения общей формулы (I), его фармацевтически приемлемых кислотно- или основно-аддитивных солей, стереохимических изомерных форм, N-оксидов, а также их пролекарств, в качестве лекарственного средства. Данное изобретение также относится к применению соединения общей формулы (I), его фармацевтически приемлемых кислотно- или основно-аддитивных солей, стереохимических изомерных форм, Nоксидов, а также их пролекарств, для получения лекарственного средства для профилактики и/или лечения тахикинин-опосредованных состояний. Соединения данного изобретения можно использовать для лечения нарушений ЦНС, таких как шизоаффективные расстройства; депрессия; тревожные расстройства; вызванные стрессом расстройства; нарушения сна; когнитивные расстройства; личностные расстройства; пищевые расстройства; нейродегенеративные заболевания; расстройства, связанные с зависимостью; расстройства настроения; половая дисфункция; висцеральная боль и другие состояния, связанные с нарушениями ЦНС; воспаления; аллергических нарушений; рвоты; желудочно-кишечных нарушений, таких как синдром раздраженной кишки(IBS); кожных заболеваний; вазоспастических заболеваний; фиброзных и коллагеновых болезней; нарушений, связанных с усилением или подавлением иммунитета; ревматических заболеваний; а также для регуляции массы тела. В частности, соединения данного изобретения можно использовать для лечения или профилактики шизоаффективных расстройств разной этиологии, включающих в себя шизоаффективные расстройства маниакального типа, депрессивного типа и смешанного типа; параноидальной, дезорганизующей, кататонической, недифференцированной и остаточной шизофрении; шизофреноподобного расстройства; галлюцинаторного расстройства; краткого психического расстройства; общего психического расстройства; психического расстройства, вызванного веществом; а также иных психических расстройств. В частности, соединения данного изобретения можно использовать для лечения или профилактики депрессии, включающей в себя, без ограничения, основные депрессивные нарушения, такие как биполярная депрессия; монополярная депрессия; одиночные или повторяющиеся приступы основной депрессии, иногда сопровождающейся психотическими признаками, кататоническими признаками, меланхолическими признаками, атипическими признаками или постнатальным появлением, причем повторяющиеся приступы могут носить сезонный характер. Другие психические нарушения, охватываемые термином"основное депрессивное нарушение", включают в себя дистимическое нарушение с ранним или поздним появлением, иногда сопровождающееся атипическими признаками; биполярное расстройство I; биполярное расстройство II; циклотимическое нарушение; рецидивирующее краткое депрессивное нарушение; смешанное аффективное нарушение; невротическую депрессию; нарушение, связанное с посттравматическим стрессом, и социофобию; ранняя или поздняя деменция Альцгеймеровского типа, сопровождающаяся депрессивным настроением; вызываемые веществами нарушения настроения, такие как нарушения настроения, вызываемые алкоголем, амфетаминами, кокаином, галлюциногенами, средствами для ингаляции, опиоидами, фенциклидином, седативными средствами, снотворными средствами, анксиолитиками и другими веществами; шизоаффективное нарушение депрессивного типа; и приспособленческое нарушение с депрессивным настроением. Основные депрессивные нарушения также могут возникать в результате общего медицинского состояния, включающего в себя, без ограничения, инфаркт миокарда,диабет, прерывание беременности или аборт и др. В частности, соединения данного изобретения можно использовать для лечения или профилактики тревожных расстройств, включающих в себя, без ограничения, приступ панического расстройства; агорафобию; паническое расстройство без агорафобии; агорафобию без панического расстройства; специфическую фобию; социофобию; обсессивно-компульсивное расстройство; нарушение, связанное с посттравматическим стрессом; связанное с острым стрессом; генерализованное тревожное расстройство; тревожное расстройство вследствие общего медицинского состояния; тревожное расстройство, индуцированное веществом; а также другие тревожные расстройства. В частности, соединения данного изобретения можно использовать для лечения или профилактики вызванных стрессом расстройств, связанных с депрессией и/или тревогой, включающих в себя, без огра-9 014239 ничения, острую стрессовую реакцию; расстройства приспособления, такие как краткая депрессивная реакция и длительная депрессивная реакция; смешанную тревожную и депрессивную реакции; нарушение приспособления с доминирующим нарушением других эмоций; нарушение приспособления с доминирующим нарушением поведения; нарушение приспособления со смешанным нарушением эмоций и поведения; нарушения приспособления с доминированием других симптомов; а также другие реакции на сильный стресс. В частности, соединения данного изобретения можно использовать для лечения или профилактики нарушений сна, включающих в себя, без ограничения, дисомнию и/или парасомнию как первичные нарушения сна; инсомнию; апноэ во сне/нарколепсию; нарушения циркодианного ритма; нарушения сна,связанные с другим психическим заболеванием; нарушение сна вследствие общего медицинского состояния; а также нарушение сна, индуцированное веществом. В частности, соединения данного изобретения можно использовать для лечения или профилактики когнитивных расстройств, включающих в себя, без ограничения, деменцию; амнестические расстройства и другие когнитивные расстройства, в особенности деменцию, вызываемую дегенеративными нарушениями, повреждениями, травмой, инфекциями, сосудистыми заболеваниями, токсинами, аноксией, дефицитом витаминов или эндокринными заболеваниями; раннюю или позднюю деменцию Альцгеймеровского типа, иногда с депрессивным настроением; связанную со СПИДом деменцию или амнестические нарушения, вызываемые алкоголем или другими причинами, включающими в себя дефицит тиамина,двустороннее повреждение височной доли вследствие герпетического энцефалита и других лимбических энцефалитов, уменьшение числа нейронов после аноксии/гипогликемии/тяжелых конвульсий и хирургии, дегенеративные нарушения, сосудистые нарушения или патологии в районе желудочка III. Кроме того, соединения данного изобретения также можно использовать в качестве средств, улучшающих память и/или познавательную способность у здоровых людей, не страдающих от дефицита познавательной способности и/или памяти. В частности, соединения данного изобретения можно использовать для лечения или профилактики личностных нарушений, включающих в себя, без ограничения, параноидальное личностное нарушение; шизоидное личностное нарушение; шизофреноподобное личностное нарушение; антисоциальное личностное нарушение; пограничное личностное нарушение; мимическое личностное нарушение; нарциссистическое личностное нарушение; личностное нарушение, связанное с замкнутым поведением; личностное нарушение, связанное с зависимостью; обсессивно-компульсивное личностное нарушение, а также другие личностные нарушения. В частности, соединения данного изобретения также можно использовать для лечения или профилактики пищевых нарушений, включающих в себя нервную анорексию; атипичную нервную анорексию; нейрогенную булимию; атипичную нейрогенную булимию; переедание, связанное с другими психологическими нарушениями; рвоту, связанную с другими психологическими нарушениями; и неспецифические пищевые нарушения. В частности, соединения данного изобретения также можно использовать для лечения или профилактики нейродегенеративных заболеваний, включающих в себя, без ограничения, болезнь Альцгеймера; хорею Гентингтона; болезнь Крейтцфельда-Якоба; болезнь Пика; демиелинизирующие заболевания, такие как рассеянный склероз и ALS; другие невропатии и невралгии; рассеянный склероз; боковой амиотрофический склероз; инсульт и травму головы. В частности, соединения данного изобретения также можно использовать для лечения или профилактики нарушений, связанных с зависимостью, включающих в себя, без ограничения, зависимость, иногда физиологическую, от веществ, или злоупотребление ими, особенно в тех случаях, когда вещество представляет собой алкоголь, амфетамины, амфетамин-подобные вещества, кафеин, кокаин, галлюциногены, средства для ингаляции, никотин, опиоиды (такие как каннабис, героин и морфин), фенциклидин,фенциклидин-подобные соединения, седативно-гипнотические средства, бензодиазепины и/или другие вещества, в особенности используемые для лечения абстиненции, возникающей при отмене вышеуказанных веществ, и делириозный синдром после отмены алкоголя. В частности, соединения данного изобретения также можно использовать для лечения или профилактики нарушений настроения, в особенности, вызванных алкоголем, амфетаминами, кафеином, каннабисом, кокаином, галлюциногенами, средствами для ингаляций, никотином, опиоидами, фенциклидином, седативными средствами, гипнотическими средствами, анксиолитиками и другими веществами. В частности, соединения данного изобретения также можно использовать для лечения или профилактики половой дисфункции, включающей в себя, без ограничения, нарушения полового влечения; нарушения полового возбуждения; оргазмические нарушения; сексуальные болевые нарушения; половую дисфункцию вследствие общего медицинского состояния; индуцированную веществом половую дисфункцию, а также другие половые дисфункции. В частности, соединения данного изобретения также можно использовать для лечения или профилактики боли, включающей в себя, без ограничения, травматическую боль, такую как послеоперационная боль; боль, связанную с травматическим разрывом, например плечевого сцепления; хроническую боль,такую как артритическая боль, например, встречающаяся при остеоревматоидном или псориатическом- 10014239 артрите; невропатическую боль, такую как постгерпетическая невралгия, невралгия тройничного нерва,сегментальная или межреберная невралгия, фибромиалгия, каузалгия, периферическая невропатия, диабетическая невропатия, невропатия, вызванная химиотерапией, невропатия, связанная со СПИДом, затылочная невралгия, невралгия при синдроме коленчатого ганглия, глоссофарингеальная невралгия, симпатическая рефлекторная дистрофия и фантомные боли; разные формы головной боли, такие как мигрень,острая или хроническая боль при повышенном давлении, височно-челюстная боль, боль в гайморовой полости и сильная приступообразная головная боль; одонталгию; раковую боль; висцеральную боль; желудочно-кишечную боль; боль при ущемлении нерва; боль при спортивных травмах; боль при дисменорее; менструальная боль; боль при менингите; боль при арахноидите; скелетно-мышечная боль; боль в нижней части спины, например при позвоночном стенозе, выпадающем диске, ишиасе, стенокардии, анкилозирующем спондилите; боль при подагре; боль при ожогах; боль в шрамах; зуд; а также таламическую боль, такую как таламическая боль после инсульта. В частности, соединения данного изобретения также можно использовать для лечения или профилактики других связанных с ЦНС состояний, таких как: акинезия, акинетические устойчивые синдромы,дискинезия и паркинсонизм, вызванный лекарственными средствами, синдром Gilles de la Tourette и его симптомы, тремор, хорея, миоклония, тик и дистония, нарушение, связанное с недостатком внимания/гиперактивностью (ADHD), болезнь Паркинсона, вызванный лекарственными средствами паркинсонизм, постэнцефалитный паркинсонизм, прогрессирующий супрануклеарный паралич, множественная атрофия, кортикобазальная дегенерация, комплексная деменция, связанная с паркинсонизмом-ALS, и кальцификация базальных ядер головного мозга, поведенческие нарушения и расстройства поведения при деменции и замедлении умственного развития, в том числе беспокойное состояние и тревожное возбуждение, нарушения экстрапирамидальных двигательных функций, синдром Дауна и акатизия. В частности, соединения данного изобретения также можно использовать для лечения или профилактики воспаления, включающего в себя, без ограничения, воспалительные состояния при астме, грипп,хронический бронхит и ревматоидный артрит; воспалительные состояния в желудочно-кишечном тракте,включающие в себя, без ограничения, болезнь Крона, язвенный колит, воспалительную болезнь кишечника и повреждение, вызванное нестероидным противовоспалительным средством; воспалительные состояния кожи, такие как герпес и экзема; воспалительные состояния мочевого пузыря, такие как цистит и неотложное недержание мочи; воспаление глаз и зубов и панкреатит, в том числе, хронический и острый панкреатит. В частности, соединения данного изобретения также можно использовать для лечения или профилактики аллергических заболеваний, включающих в себя, без ограничения, аллергические заболевания кожи, такие как крапивница; и аллергические заболевания дыхательных путей, такие как ринит. В частности, соединения данного изобретения также можно использовать для лечения или профилактики рвоты, т.е. тошноты, позыва на рвоту и извержения рвотных масс, включающей в себя без ограничения, острую рвоту, отсроченную рвоту и преждевременную рвоту; рвоту, вызываемую такими факторами, как лекарственные средства, включающие в себя противораковые химиотерапевтические средства, такие как алкилирующие средства, например циклофосфамид, кармустин, ломустин и хлорамбуцил; цитотоксические антибиотики, такие как дактиномицин, доксорубицин, митомицин-С и блеомицин; антиметаболиты, такие как цитарабин, метотрексат и 5-фторурацил; алкалоиды барвинка, такие как этопозид, винбластин и винкристин; а также другие лекарственные средства, такие как цисплатин, дакарбазин,прокарбазин и гидроксимочевина; а также их сочетания; лучевая болезнь; лучевая терапия, применяющаяся, например, для лечения рака; яды; токсины, такие как токсины, образующиеся при метаболических нарушениях или инфекциях, таких как гастрит, или высвобождающиеся в процессе бактериальной или вирусной желудочно-кишечной инфекции; беременность; вестибулярные нарушения, например укачивание, вертиго, головокружение и болезнь Меньера; послеоперационная тошнота; закупорка желудочно-кишечного тракта; уменьшение двигательной функции желудочно-кишечного тракта; висцеральная боль, например, при инфаркте миокарда или перитоните; мигрень; повышенное внутричерепное давление; пониженное внутричерепное давление (например, высотная болезнь); опиоидные анальгетики, такие как морфин; желудочно-пищеводный отток; изжога; чрезмерное потребление пищи или напитков; кислый желудок; кислая отрыжка; изжога/отрыжка; изжога, такая как эпизодическая изжога, ночная изжога и изжога, вызванная пищей; и диспепсия. В частности, соединения данного изобретения также можно использовать для лечения или профилактики желудочно-кишечных расстройств, включающих в себя, без ограничения, синдром раздраженной кишки (IBS), кожные заболевания, такие как псориаз, зуд и солнечный ожог; вазоспастические заболевания, такие как стенокардия, сосудистая головная боль и болезнь Рейно, церебральная ишемия, такая как церебральный вазоспазм после субарахноидального кровотечения; фиброзные и коллагеновые заболевания, такие как склеродермия и эозинофильный фасциолез; заболевания, связанные с усилением или подавлением иммунитета, такие как системная красная волчанка и ревматические заболевания, такие как фиброзит; кашель; а также нарушения регуляции массы тела, включающие в себя ожирение. Соединения данного изобретения также можно использовать для получения лекарственного средства для лечения и/или профилактики шизофрении, рвоты, тревоги и депрессии, синдрома раздраженной- 11014239 кишки (IBS), нарушений циркодианного ритма, преэклампсии, ноцицепции, боли, в частности висцеральной и невропатической боли, панкреатита, нейрогенного воспаления, астмы, хронического обструктивного заболевания легких (COPD) и нарушений мочеиспускания, таких как недержание мочи. Настоящее изобретение также относится к способу лечения и/или профилактики шизофрении, рвоты, тревоги и депрессии, синдрома раздраженной кишки (IBS), нарушений циркодианного ритма, преэклампсии, ноцицепции, боли, в частности, висцеральной и невропатической боли, панкреатита, нейрогенного воспаления, астмы, хронического обструктивного заболевания легких (COPD) и нарушений мочеиспускания, таких как недержание мочи, включающему в себя введение человеку, нуждающемуся в таком введении, эффективного количества соединения данного изобретения, в частности соединения формулы (I), его фармацевтически приемлемых кислотно- или основно-аддитивных солей, стереохимических изомерных форм, N-оксидов, а также их пролекарств. Данное изобретение также относится к фармацевтической композиции, содержащей фармацевтически приемлемый носитель и, в качестве активного ингредиента, терапевтически эффективное количество соединения данного изобретения, в частности соединения формулы (I), его фармацевтически приемлемых кислотно- или основно-аддитивных солей, стереохимических изомерных форм, N-оксидов и пролекарств. Соединения данного изобретения, в частности соединения формулы (I), их фармацевтически приемлемые кислотно- или основно-аддитивные соли, стереохимические изомерные формы, N-оксиды и пролекарства, или любое их сочетание, могут входить в состав разных фармацевтических форм, предназначенных для введения. В качестве подходящих композиций можно перечислить любые композиции,обычно используемые для системного введения лекарственных средств. Чтобы получить фармацевтические композиции данного изобретения, эффективное количество конкретного соединения, необязательно в виде аддитивной соли, в качестве активного ингредиента объединяют путем однородного смешивания с фармацевтически приемлемым носителем, который может иметь разные формы в зависимости от вида вводимого препарата. Желательно, чтобы данные фармацевтические композиции находились в виде разовых лекарственных форм, подходящих, например, для введения пероральным, ректальным, чрескожным способом, путем парентеральной инъекции или путем ингаляции. Например, для получения композиций в виде пероральной лекарственной формы можно использовать любые традиционные фармацевтические среды, такие как, например, вода, гликоли, масла, спирты и т.п. в случае жидких препаратов для перорального введения, таких как суспензии, сиропы, эликсиры, эмульсии и растворы; или твердые носители, такие как крахмалы, сахара, каолин, разбавители, смазывающие средства, связующие средства,дезынтегрирующие средства и т.п., в случае порошков, пилюль, капсул и таблеток. Благодаря простоте введения таблетки и капсулы являются наиболее предпочтительными стандартными лекарственными формами, для получения которых, естественно, используются твердые фармацевтические носители. В парентеральных композициях носитель обычно содержит стерильную воду, по меньшей мере, в основной части, хотя он может содержать и другие ингредиенты, например, повышающие растворимость лекарственных средств. Растворы для инъекций, например, в качестве носителя могут содержать физиологический раствор, раствор глюкозы или смесь физиологического раствора и раствора глюкозы. Суспензии для инъекций могут содержать подходящие жидкие носители, суспендирующие средства и т.п. В объем настоящего изобретения также входят твердые препараты, которые непосредственно перед применением нужно превращать в жидкие препараты. В композициях, подходящих для чрескожного введения, носитель необязательно содержит средство, повышающее проникание, и/или подходящее увлажняющее средство, необязательно в сочетании с подходящими добавками любой природы в минорных пропорциях, которые не оказывают существенного вредного воздействия на кожу. Указанные добавки могут облегчать введение в кожу и/или получение целевых композиций. Указанные композиции можно вводить разными способами, например с использованием чрескожного пластыря, точечного нанесения или мази. Особенно предпочтительно получать вышеуказанные фармацевтические композиции в виде стандартной лекарственной формы, обеспечивающей простоту введения и единообразие дозировки. Термин"стандартная лекарственная форма" в данном описании относится к физически дискретным единицам,которые можно использовать в качестве разовых доз, каждая из которых содержит определенное количество активного ингредиента, рассчитанное так, чтобы получить желательный терапевтический эффект, в сочетании с подходящим фармацевтическим носителем. Примерами таких стандартных лекарственных форм являются таблетки (в том числе таблетки с насечками или покрытые таблетки), капсулы, пилюли,пакетики с порошками, облатки, свечи, растворы или суспензии для инъекций и т.п., а также их раздельные части. Поскольку соединения данного изобретения представляют собой антагонисты NK, обладающие активностью, в основном в центральной нервной системе, после перорального введения, особенно предпочтительны фармацевтические композиции указанных соединений для перорального введения. Синтез Соединения данного изобретения, как правило, можно получить с использованием последовательности стадий, каждая из которых известна специалистам в данной области.- 12014239 Конечные соединения формулы (Ia) обычно получают путем восстановительного N-алкилирования промежуточного соединения формулы (II) промежуточным соединением формулы (III). Указанное восстановительное N-алкилирование можно проводить в инертном растворителе, таком как, например, дихлорметан, этанол или толуол, или их смесь, в присутствии подходящего восстанавливающего средства,такого как боргидрид, например боргидрид натрия, цианоборгидрид натрия или триацетоксиборгидрид. Если в качестве восстанавливающего средства применяется боргидрид, предпочтительно вместе с ним использовать комплексообразующий агент, такой как, например, изопропилат титана (IV), как описано вJ. Org. Chem, 1990, 55, 2552-2554. Применение указанного комплексообразующего агента может приводить к сдвигу цис/транс соотношения в сторону транс-изомера. В качестве восстанавливающего средства также можно использовать водород в сочетании с подходящим катализатором, таким как, например, палладий на угле или платина на угле. В случае использования водорода в качестве восстанавливающего средства к реакционной смеси можно добавить дегидратирующий агент, такой как, например, третбутоксид алюминия. Чтобы предотвратить нежелательное гидрирование некоторых функциональных групп реагентов и продуктов реакции, к реакционной смеси также можно добавить подходящий катализаторный яд, например тиофен или хинолин-серу. Скорость реакции можно увеличить путем перемешивания и необязательно путем применения повышенных температур и/или давления. В данном и последующих способах продукты реакции можно выделить из реакционной среды и,при необходимости, дополнительно очистить с помощью методов, хорошо известных в данной области,таких как, например, экстракция, кристаллизация, растирание и хроматография. Конечные соединения формулы (Ib) обычно получают путем восстановительного N-алкилирования промежуточного соединения формулы (IV) промежуточным соединением формулы (III). Указанное восстановительное N-алкилирование можно проводить в инертном растворителе, таком как, например, дихлорметан, этанол или толуол, или их смесь, в присутствии подходящего восстанавливающего средства,такого как боргидрид, например боргидрид натрия, цианоборгидрид натрия или триацетоксиборгидрид. Если в качестве восстанавливающего средства применяется боргидрид, предпочтительно вместе с ним использовать комплексообразующий агент, такой как, например, изопропилат титана(IV), как описано вJ. Org. Chem, 1990, 55, 2552-2554. В качестве восстанавливающего средства также можно использовать водород в сочетании с подходящим катализатором, таким как, например, палладий на угле или платина на угле. В случае использования водорода в качестве восстанавливающего средства к реакционной смеси можно добавить дегидратирующий агент, такой как, например, трет-бутоксид алюминия. Чтобы предотвратить нежелательное гидрирование некоторых функциональных групп реагентов и продуктов реакции,к реакционной смеси также можно добавить подходящий катализаторный яд, например тиофен или хинолин-серу. Скорость реакции можно увеличить путем перемешивания и необязательно путем применения повышенных температур и/или давления. Конечные соединения формулы (Ic) обычно получают путем взаимодействия соединения формулы(V) в виде карбоновой кислоты с промежуточным соединением формулы (III). Реакцию можно проводить в инертном растворителе, таком как хлорированный углеводород, например дихлорметан, в присутствии подходящего основания, такого как, например, карбонат натрия, гидрокарбонат натрия или триэтиламин, а также в присутствии активатора, такого как, например, DCC (дициклогексилкарбодиимид),CDI (карбонилдиимидазол) и EDCI (1-(3-диметиламинопропил)-3-этилкарбодиимидHCl). Скорость реакции можно увеличить путем перемешивания. Реакцию обычно проводят в интервале температур от комнатной до температуры кипения с обратным холодильником. В особенно предпочтительном способе получения конечного соединения любой из формул (Ia), (Ib) и (Ic), проводимом в соответствии с описанными выше схемами реакций, соединение формулы (II), (IV) или (V) взаимодействует с соединением формулы (III), в котором фрагмент Alk-Y-Alk-L представляет собой бензил (формула (XI, с образованием соединения, в котором фрагмент Alk-Y-Alk-L представляет собой бензил. Указанное конечное соединение является фармакологически активным и может быть превращено в конечное соединение формулы (I'), в котором фрагмент Alk-Y-Alk-L представляет собой водород, путем восстановительного гидрирования с использованием, например, водорода в качестве восстанавливающего средства в сочетании с подходящим катализатором, таким как, например, палладий на угле или платина на угле. Затем полученное конечное соединение данного изобретения можно превратить в другие соединения формулы (I) с помощью известных в данной области реакций, например ацилирования и алкилирования. В частности, конечные соединения формулы (Id) можно получить путем взаимодействия конечного соединения формулы (I') с промежуточным соединением формулы (VI), в котором W1 представляет собой подходящую уходящую группу, такую как галоген, например хлор или бром, или сульфонилоксильная уходящая группа, например метансульфонилокси или бензолсульфонилокси. Реакцию можно проводить в инертном растворителе, таком как хлорированный углеводород, например дихлорметан, или кетон, например метилизобутилкетон, в присутствии подходящего основания, такого как, например, карбонат натрия, гидрокарбонат натрия или триэтиламин. Скорость реакции можно увеличить путем перемешивания. Реакцию обычно проводят в интервале температур от комнатной до температуры кипения с обратным холодильником. Альтернативно, конечные соединения формулы (Id) можно получить путем взаимодействия конечного соединения формулы (I') с карбоновой кислотой формулы (VII). Реакцию можно проводить в инертном растворителе, таком как, например, хлорированный углеводород, например дихлорметан, в присутствии подходящего основания, такого как, например, карбонат натрия, гидрокарбонат натрия или триэтиламин, в присутствии активатора, такого как, например, DCC (дициклогексилкарбодиимид), CDI(карбонилдиимидазол) и EDCI (1-(3-диметиламинопропил)-3-этилкарбодиимидHCl). Скорость реакции можно увеличить путем перемешивания. Реакцию обычно проводят в интервале температур от комнатной до температуры кипения с обратным холодильником. Конечные соединения формулы (Ie) можно получить путем алкилирования конечного соединения формулы (I') соединением формулы (VIII), в котором W2 представляет собой подходящую уходящую группу, такую как, например, галоген, например хлор или бром, или сульфонилоксильную уходящую группу, например метансульфонилокси или бензолсульфонилокси. Реакцию можно проводить в инертном растворителе, таком как хлорированный углеводород, например дихлорметан, спирт, например этанол, или кетон, например метилизобутилкетон, в присутствии подходящего основания, такого как, например, карбонат натрия, гидрокарбонат натрия или триэтиламин. Скорость реакции можно увеличить- 14014239 путем перемешивания. Реакцию обычно проводят в интервале температур от комнатной до температуры кипения с обратным холодильником. Конечные соединения формулы (If) обычно получают путем восстановительного N-алкилирования промежуточного соединения формулы (I') промежуточным соединением формулы (IX). Указанное восстановительное N-алкилирование можно проводить в инертном растворителе, таком как, например, дихлорметан, этанол или толуол, или их смесь, в присутствии подходящего восстанавливающего средства,такого как боргидрид, например боргидрид натрия, цианоборгидрид натрия или триацетоксиборгидрид. Если в качестве восстанавливающего средства применяется боргидрид, предпочтительно вместе с ним использовать комплексообразующий агент, такой как, например, изопропилат титана (IV), как описано вJ. Org. Chem, 1990, 55, 2552-2554. В качестве восстанавливающего средства также можно использовать водород в сочетании с подходящим катализатором, таким как, например, палладий на угле или платина на угле. В случае использования водорода в качестве восстанавливающего средства к реакционной смеси можно добавить дегидратирующий агент, такой как, например, трет-бутоксид алюминия. Чтобы предотвратить нежелательное гидрирование некоторых функциональных групп реагентов и продуктов реакции,к реакционной смеси также можно добавить подходящий катализаторный яд, например тиофен или хинолин-серу. Скорость реакции можно увеличить путем перемешивания и необязательно путем применения повышенных температур и/или давления. Конечные соединения формулы (Ig) обычно получают путем бороновой реакции Манниха, описанной в Tetrahedron, 1997, 53, 16463-16470; J. Am. Chem. Soc. 1998, 120, 11798-11799 или Tetrahedron Letters, 2002, 43, 5965-5968, в которой участвуют промежуточное соединение формулы (I') и промежуточные соединения (X) и (XI), где Y в формуле (X) представляет собой бивалентный радикал формулы СН 2- или С(=O), a W3 в формуле (XI) представляет собой водород или алкильную цепь. Указанную бороновую реакцию Манниха можно проводить в одном сосуде в присутствии углевода или его димера формулы (X) и арилбороновой кислоты или эфира арилбороновой кислоты формулы (XI) в инертном растворителе, таком как, например, дихлорметан, этанол или 2,2,2-трифторэтанол, или их смесь. Скорость реакции можно увеличить путем перемешивания. Реакцию обычно проводят в интервале температур от комнатной до температуры кипения с обратным холодильником. Приведенные ниже примеры предназначаются для иллюстрации, но не для ограничения объема настоящего изобретения. Экспериментальная часть В данном описании "НОВТ" обозначает гидроксибензотриазол", "EDCI" обозначает гидрохлорид 1 этил-3-(3-диметиламинопропил)карбодиимида, a "PLDCC" обозначает полимер дициклогексилкарбодиимида. Получение промежуточных соединений Пример А 1. а. Получение промежуточного соединения 1Et3N (0,55 моль) добавляют при перемешивании к смеси 7-(фенилметил)-1,4-диокса-8 азаспиро[4,5]декана (0,5 моль) в толуоле (1500 мл). В течение 1 ч добавляют 3,5 бис(трифторметил)бензоилхлорид (0,5 моль) (экзотермическая реакция). Смесь перемешивают при комнатной температуре в течение 2 ч, затем оставляют стоять на выходные и промывают три раза водой (500 мл, 2250 мл). Органический слой отделяют, сушат, фильтруют и растворитель упаривают. Выход: 245 г(100%). После кристаллизации 2 г данной фракции из петролейного эфира получают 1 г промежуточного соединения 1 (50%).b. Получение промежуточного соединения 2 К смеси промежуточного соединения 1 (0,5 моль) в этаноле (300 мл) и Н 2 О (300 мл) добавляют HCl(300 мл). Реакционную смесь перемешивают при 60 С в течение 20 ч. Осадок отфильтровывают, размалывают, перемешивают в Н 2 О, снова отфильтровывают, промывают петролейным эфиром и сушат. Выход: 192 г промежуточного соединения 2 )-1-[3,5-бис(трифторметил)бензоил]-2-(фенилметил)-4 пиперидинона) (89,4%) (смесь R- и S-энантиомеров). с. Получение промежуточного соединения 3 и промежуточного соединения 4 Промежуточное соединение 2 разделяют на оптические изомеры с помощью хиральной колоночной хроматографии на колонке Chiralpak (CHIRALPAK AS 1000 20 мм (DAICEL); элюент: гексан/2 пропанол 70/30). Собирают две фракции продукта и упаривают все растворители. Выход для фракции 1: 32,6 г промежуточного соединения 3 (R), а для фракции 2: 30,4 г промежуточного соединения 4 (S). Пример А 2. а. Получение промежуточного соединения 5 Смесь [1-(фенилметил)-3-пирролидинилиден]уксусной кислоты этилового эфира (0,071 моль) (полученного по способу, описанному в европейском патенте ЕР 550025 А 1, содержание которого полностью включено в данное описание в качестве ссылки), CH3NO2 (170 мл) и N,N,N',N'тетраметилгуанидина (3 мл) перемешивают и нагревают с обратным холодильником в течение 18 ч. Добавляют H2O. Смесь экстрагируют, промывают CH2Cl2 и концентрируют, получая 15 г. Остаток очищают колоночной хроматографией на силикагеле (в качестве элюента используют градиент: CH2Cl2/МеOН от 100/0 до 99/1; 15-40 мкм). Собирают чистые фракции и упаривают растворитель. Выход: 4,7 г промежуточного соединения 5 (21%).b. Получение промежуточного соединения 6 Смесь промежуточного соединения 5 (полученного по способу примера А 2.а) (0,027 моль) и RaNi(8 г) в MeOH/NH3 (80 мл) гидрируют при комнатной температуре и давлении 3 бар в течение 18 ч. Смесь фильтруют через целит, промывают МеОН/CH2Cl2 и концентрируют. Остаток кристаллизуют из EtOAc,получая 2,4 г (38%) фракции 1. Маточный слой упаривают. Остаток (5,3 г) очищают колоночной хроматографией на силикагеле (элюент: CH2Cl2/МеОН 98/2; 20-45 мкм). Собирают чистые фракции и получают 1,3 г фракции 2. Фракцию 1 и фракцию 2 объединяют, получая 3,7 г промежуточного соединения 6(59%). с. Получение промежуточного соединения 7 Промежуточное соединение 6 (0,016 моль) добавляют порциями при 5 С к раствору LiAlH4 (0,032 моль) в THF (75 мл). Смесь перемешивают при комнатной температуре в течение 18 ч. При 5 С медленно добавляют H2O. Смесь фильтруют через целит, промывают EtOAc и CH2Cl2, сушат над MgSO4,фильтруют, сушат и концентрируют. Выход: 3,3 г промежуточного соединения 7 (95%). Получение конечных соединений Пример В 1. а. Получение конечного соединения 1-2 Смесь промежуточного соединения 3 (полученного по способу примера A1.c) (0,028 моль), 1(фенилметил)-1,7-диазаспиро[4.4]нонана (0,028 моль), Pd/C (1 г) и изопропилата титана (IV) (0,033 моль) в тиофене (1 мл) и СН 3 ОН (120 мл) гидрируют при 50 С в течение 18 ч, затем фильтруют через целит. Целит промывают СН 3 ОН. Фильтрат упаривают. Остаток растворяют в CH2Cl2. Добавляют 10% K2CO3. Смесь перемешивают при комнатной температуре в течение 30 мин, затем фильтруют через целит. Целит промывают CH2Cl2. Фильтрат экстрагируют CH2Cl2. Органический слой отделяют, сушат (MgSO4),фильтруют и растворитель упаривают. Остаток очищают колоночной хроматографией на силикагеле (в качестве элюента используют градиент: CH2Cl2/CH3OH/NH4OH от 98/2/0,2 до 97/3/0,2; 20-45 мкм). Чистые фракции собирают и растворитель упаривают, получая 4,9 г фракции 1 и 2,7 г фракции 2. Выход: 0,113 г конечного соединения 1-2.b. Получение конечного соединения 1-1 Смесь конечного соединения 1-2 (0,004 моль) и Pd/C (1 г) в СН 3 ОН (15 мл) гидрируют при 50 С в течение 18 ч под давлением 3 бар, после чего фильтруют через целит. Целит промывают CH2Cl2/CH3OH. Фильтрат упаривают. Выход: 2,3 г конечного соединения 1-1 (100%). Пример В 2. Получение конечного соединения 1-3EDCI (0,001 моль) добавляют при комнатной температуре к раствору конечного соединения 1-1(полученного по способу примера B1.b) (0,001 моль), циклопропанкарбоновой кислоты (0,001 моль),HOBt (0,001 моль) и Et3N (0,001 моль) в СН 2C12 (4 мл). Смесь перемешивают при комнатной температуре- 17014239 в течение 18 ч. Органический слой промывают 10% K2CO3, сушат (MgSO4), фильтруют и растворитель упаривают. Остаток (0,5 г) очищают колоночной хроматографией на силикагеле (в качестве элюента используют градиент: CH2Cl2/CH3OH от 99/1 до 80/20; 5 мкм). Чистые фракции собирают и растворитель упаривают. Выход: 0,22 г конечного соединения 1-3. Пример В 3 а. Получение конечного соединения 2-1 Смесь промежуточного соединения 3 (полученного по способу примера A1.c) (0,015 моль), промежуточного соединения 7 (полученного по способу примера А 2.с) (0,015 моль), изопропилата титана(IV)(0,023 моль), тиофена (0,6 мл) и Pd/C (0,6 г) в МеОН (60 мл) гидрируют при 50 С под давлением 3 бар в течение 18 ч. Смесь фильтруют через целит, промывают МеОН и концентрируют досуха. Остаток солюбилизируют в CH2Cl2, добавляют 10% K2CO3, смесь перемешивают при комнатной температуре в течение 30 минут, фильтруют через целит, промывают CH2Cl2. Фильтрат экстрагируют CH2Cl2, сушат надMgSO4, фильтруют и концентрируют. Остаток (8,7 г) очищают колоночной хроматографией на силикагеле (в качестве элюента используют градиент: CH2Cl2/MeOH/NH4OH от 98/2/0,2 до 95/5/0,2; 15-40 мкм). Выход: 0,9 г конечного соединения 2-1.b. Получение конечного соединения 2-2 Смесь конечного соединения 2-1 (полученного по способу примера В 3.а) (0,001 моль) и Pd/C (0,1 г) в МеОН (10 мл) гидрируют под давлением 3 бар в течение 18 часов при комнатной температуре. Смесь фильтруют через целит, промывают CH2Cl2/МеОН и концентрируют. Выход: 0,8 г конечного соединения 2-2 (100%). Пример В 4. Получение конечного соединения 2-4 Смесь конечного соединения 2-2 (полученного по способу примера В 3.b) циклопропанкарбоновой кислоты (1,2 эквивалента) и иммобилизованного на полимере циклогексилкарбодиимида (1,2 эквивалента) в CH2Cl2 перемешивают при комнатной температуре в течение 18 ч. Выход: 45% конечного соединения 2-4. Нижеследующие соединения получают по способу одного из приведенных выше примеров. Таблица 1cb: ковалентная связь С. Аналитические данные Некоторые соединения анализируют методами ЖХ-МС и ЯМР. С.1. Условия проведения ЖХ-МС Общий способ: Для проведения градиентной ВЭЖХ используют систему Alliance HT 2795 (Waters), состоящую из четвертичного насоса с дегазатором, автосэмплера и детектора DAD. Часть потока, выходящего из колонки, направляется в МС-детектор. МС-детекторы снабжены устройством для ионизации электрораспылением. Напряжение капиллярной иглы составляет 3 кВ, температуру источника поддерживают при 100 С. В качестве распыляющего газа используют азот. Данные получают с помощью системы WatersMicromass MassLynx-Openlynx. Способ 1. В добавление к общей процедуре: ВЭЖХ на обращенной фазе проводят на колонке Kromasil C18 (5 мкм, 4,6x150 мм) со скоростью потока 1 мл/мин. Две мобильные фазы (мобильная фаза А: 100% 6,5 мМ ацетат аммония + 0,2% муравьиной кислоты; мобильная фаза В: 100% ацетонитрил) используют для получения следующего градиента: от 60% А и 40% В в течение 1 мин, до 100% В в течение 4 мин, от 100% В в течение 5 мин, до 60% А и 40% В в течение 3 мин, с повторным уравновешиванием смесью 60% А и- 20014239 40% В в течение 3 мин. Объем впрыска составляет 5 мкл. Напряжение конуса составляет 20 В для режима положительной ионизации. Масс-спектр получают путем сканирования от 100 до 900 в течение 1 с с использованием времени выдержки 0,1 с. Способ 2. В добавление к общей процедуре: ВЭЖХ на обращенной фазе проводят на колонке Xterra-RP C18(5 мкм, 3,9150 мм) со скоростью потока 1,0 мл/мин. Две мобильные фазы (мобильная фаза А: 100% 7 мМ ацетат аммония; мобильная фаза В: 100% ацетонитрил) используют для получения следующего градиента: от 85% А, 5% В (в течение 3 мин) до 20% А, 80% В в течение 5 мин, 20% А и 80% В поддерживают в течение 6 мин и снова уравновешивают в исходных условиях в течение 3 мин. Объем впрыска составляет 20 мкл. Напряжение конуса составляет 20 В для режима положительной ионизации. Массспектр получают путем сканирования от 100 до 900 в течение 0,8 с с использованием времени задержки 0,08 с. Таблица 3. Результаты ЖХ-МС для отдельных соединений; основной пик и время удерживания С. 2. Условия проведения ЯМР Спектр протонного ЯМР записывают на спектрометрах Bruker Avance 400 (400 МГц) с использованием дейтерия в качестве внутреннего стандарта. Химические сдвиги приведены по отношению к внутреннему ДМСО ( 2,54) в ppm (частях на миллион), а константы взаимодействия (J) в Гц. Соединение 1-1: 1H ЯМР (DMSO-d6)1,2-2,05 (11 Н, м), 2,5-3,05 (8 Н, м), 3,2-5,1 (4 Н, м), 6,8-8,2D. Фармакологический пример Пример D1: Анализ связывания рецепторов h-NK1, h-NK2 и h-NK3 Взаимодействие соединений данного изобретения с рецепторами, участвующими в передаче нервного сигнала, ионными каналами и участками связывания транспортных белков анализируют методом радиолигандного связывания. Мембраны тканевых гомогенатов или клеток, экспрессирующих представляющий интерес рецептор или транспортный белок, инкубируют с радиомеченным веществом ([3 Н]- или[125I]-лиганд), взаимодействующим с конкретным рецептором. Специфическое связывание радиомеченного лиганда с рецептором отличают от неспецифического связывания с мембраной путем селективного- 21014239 ингибирования мечения рецептора немеченным веществом ("бланк"), которое, как известно, конкурирует с радиолигандом за связывание с рецептором. После инкубации меченные мембраны собирают, промывают избыточным количеством холодного буфера и удаляют несвязанную радиоактивную метку путем быстрой фильтрации под вакуумом. Мембраносвязанную радиоактивность считают с помощью сцинтилляционного счетчика и получают результаты в виде числа импульсов в минуту (cpm). Соединения растворяют в ДМСО, получая 10 разных концентраций в интервале от 10-10 до 10-5 М. Анализируют способность соединений данного изобретения замещать [3 Н]-вещество Р при связывании с клонированным человеческим рецептором h-NK1, экспрессированным в клетках СНО, замещать[3 Н]-SR-48968 при связывании с клонированным человеческим рецептором h-NK2, экспрессированным в клетках Sf9, и замещать [3 Н]-SR-142801 при связывании с клонированным человеческим рецептором hNK3, экспрессированным в клетках СНО. Значения, характеризующие связывание с рецептором (pIC50), в случае h-NK1 варьируют среди соединений данного изобретения от 10 до 6. Пример D2. Передача сигнала (ST) Данный тест позволяет оценить функциональную антагонистическую активность в отношении NK1in vitro. Чтобы измерить концентрацию внутриклеточного Са, клетки выращивают на 96-луночных(черные стенки/прозрачное дно) планшетах от Costar в течение 2 дней до достижения слияния. Затем клетки инкубируют с 2 мкм Fluo3 в DMEM, содержащей 0,1% БСА и 2,5 мМ пробенецид, в течение 1 ч при 37 С. После инкубации клетки промывают 3 буфером Кребса (140 мМ NaCl, 1 мМ MgCl26 Н 2 О, 5 мМ KCl, 10 мМ глюкоза, 5 мМ HEPES; 1,25 мМ CaCl2; рН 7,4), содержащим 2,5 мМ пробенецид и 0,1% БСА (Са-буфер). Клетки инкубируют с разными концентрациями антагонистов в течение 20 мин при комнатной температуре и затем измеряют Са-сигналы с помощью планшет-ридера Fluorescence Image(FLIPR от Molecular Devices, Crawley, England). Пик Са-переноса принимают за релевантный сигнал,средние значения от соответствующих лунок анализируют с помощью описанного ниже способа. Сигмоидальные кривые доза-ответ анализируют путем компьютерного подбора кривой с помощью программы GraphPad. Значение ЕС 50 представляет собой концентрацию, при которой эффект соединения составляет 50% от максимального. При получении усредненных кривых максимальный ответ на антагонист принимают за 100%. Антагонистические ответы оценивают по значениям IC50, рассчитанным по методу нелинейной регрессии. Данные pIC50 для некоторых соединений, полученные в анализе передачи сигнала, представлены в табл. 4. Последняя колонка указывает, без ограничения, наиболее подходящее применение для соединений.- 22014239 Таблица 4. Фармакологические результаты анализа передачи сигнала для некоторых соединений Е. Примеры композиций Термин "активный ингредиент" (A.I.) в данных примерах относится к соединению формулы (I), его фармацевтически приемлемым кислотно- или основно-аддитивным солям, стереохимическим изомерным формам, N-оксидам и их пролекарствам. Пример Е 1. Капли для перорального применения 500 г A.I. растворяют в 0,5 л 2-гидроксипропановой кислоты и 1,5 л полиэтиленгликоля при 6080 С. После охлаждения до 30-40 С добавляют 35 л полиэтиленгликоля и смесь тщательно перемешивают. Затем добавляют раствор 1750 г сахарина натрия в 2,5 л очищенной воды, при перемешивании добавляют 2,5 л ароматизатора какао и полиэтиленгликоль q.s. до 50 л, получая раствор для перорального применения, содержащий 10 мг/мл A.I. Полученный раствор наливают в подходящие контейнеры. Пример Е 2. Раствор для перорального применения 9 г метил 4-гидроксибензоата и 1 г пропил 4-гидроксибензоата растворяют в 4 л кипящей очищенной воды. В 3 л данного раствора растворяют вначале 10 г 2,3-дигидроксибутандикарбоновой кислоты и затем 20 г A.I. Последний раствор объединяют с оставшейся частью первого раствора и добавляют 12 л 1,2,3-пропандиола и 3 л 70% раствора сорбита. 40 граммов сахарина натрия растворяют в 0,5 л воды и добавляют 2 мл экстракта малины и 2 мл экстракта крыжовника. Последний раствор объединяют с первым, добавляют воду q.s. до 20 л, получая раствор для перорального применения, содержащий 5 мг активного ингредиента на чайную ложку (5 мл). Полученный раствор наливают в подходящие контейнеры. Пример Е 3. Таблетки с пленочным покрытием Получение основы таблетки Смесь 100 г A.I., 570 г лактозы и 200 г крахмала тщательно перемешивают, увлажняют раствором 5 г додецилсульфата натрия и 10 г поливинилпирролидона приблизительно в 200 мл воды. Влажную порошкообразную смесь просеивают, сушат и снова просеивают. Затем добавляют 100 г микрокристаллической целлюлозы и 15 г гидрированного растительного масла. Все вместе тщательно перемешивают и прессуют в таблетки, получая 10000 таблеток, каждая из которых содержит 10 мг активного ингредиента.- 23014239 Покрытие К раствору 10 г метилцеллюлозы в 75 мл денатурированного этанола добавляют раствор 5 г этилцеллюлозы в 150 мл дихлорметана. Затем добавляют 75 мл дихлорметана и 2,5 мл 1,2,3-пропантриола. 10 г полиэтиленгликоля расплавляют и растворяют в 75 мл дихлорметана. Последний раствор добавляют к первому и затем добавляют 2,5 г октадеканоата магния, 5 г поливинилпирролидона и 30 мл концентрированной суспензии красителя, после чего полученную смесь гомогенизируют. Основную часть таблеток покрывают полученной смесью в аппарате для нанесения покрытия. Пример Е 4. Раствор для инъекций 1,8 г метил 4-гидроксибензоата и 0,2 г пропил 4-гидроксибензоата растворяют приблизительно в 0,5 л кипящей воды для инъекций. После охлаждения примерно до 50 С при перемешивании добавляют 4 г молочной кислоты, 0,05 г пропиленгликоля и 4 г A.I. Раствор охлаждают до комнатной температуры и добавляют воду для инъекций q.s. до 1 л, получая раствор, содержащий 4 мг/мл A.I. Раствор стерилизуют фильтрацией и выливают в стерильные контейнеры. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Соединение общей формулы (I) его фармацевтически приемлемые кислотно- или основно-аддитивные соли, стереохимические изомерные формы и N-оксиды, гдеj, k, р, q обозначают целые числа, независимо друг от друга равные нулю, 1, 2 или 3; при условии,что суммы (j+k) и (p+q) равны 3; Т обозначает =O в альфа-положении по отношению к атому N, a t обозначает целое число, равное 0 или 1; каждый Alk независимо обозначает ковалентную связь; бивалентный насыщенный углеводородный радикал, содержащий 1 атом углерода;Y обозначает ковалентную связь или бивалентный радикал формулы -С(=O)-;Het2 обозначает моноциклический гетероциклический радикал, выбранный из группы, состоящей из тетрагидрофуранила, фуранила, тиадиазолила, пиразинила и тиенила, где каждый моноциклический гетероциклический радикал может быть необязательно замещен по любому атому одним или несколькими радикалами, выбранными из алкила; алкил обозначает линейный или разветвленный насыщенный углеводородный радикал, содержащий от 1 до 6 атомов углерода, или циклический насыщенный углеводородный радикал, содержащий от 3 до 6 атомов углерода. 2. Соединение по п.1, отличающееся тем, что спирофрагмент имеет формулу (f6) или (f8), в которой все переменные имеют такое же определение, как в формуле (I), "а" обозначает пиперидинильный фрагмент формулы (I), a "b" обозначает фрагмент Alk-Y-Alk-L формулы (I). 3. Соединение по любому из пп.1, 2, отличающееся тем, что R1 обозначает бензил, присоединенный ко 2 положению. 4. Соединение по любому из пп.1-3, отличающееся тем, что фрагмент R2-X-C(=Q)- обозначает 3,5- 24014239 ди-(трифторметил)фенилкарбонил. 5. Соединение по любому из пп.1-4, отличающееся тем, что L выбран из группы, состоящей из водорода, трет-бутила, изопропила, тетрагидрофуранила, фуранила, тиенила, тиадиазолила, фенила и пиразинила. 6. Соединение по любому из пп.1-5, гдеY обозначает ковалентную связь или бивалентный радикал формулы -С(=O)-;Ar3 обозначает фенил. 7. Соединение по п.1, выбранное из группы соединений 8. Применение соединения по любому из пп.1-7 в качестве лекарственного средства. 9. Применение соединения по любому из пп.1-7 в качестве лекарственного средства, активного при пероральном применении и способного проникать в центральную нервную систему. 10. Применение соединения по любому из пп.1-7 для получения лекарственного средства для лечения тахикинин-опосредованных состояний. 11. Применение соединения по пп.1-7 для получения лекарственного средства для лечения и/или профилактики шизофрении, рвоты, тревоги и депрессии, синдрома раздраженной кишки (IBS), нарушений циркодианного ритма, преэклампсии, ноцицепции, висцеральной и невропатической боли, панкреатита, нейрогенного воспаления, астмы, хронического обструктивного заболевания легких (COPD) и нарушений мочеиспускания, таких как недержание мочи. 12. Фармацевтическая композиция, содержащая фармацевтически приемлемый носитель и, в качестве активного ингредиента, терапевтически эффективное количество соединения по любому из пп.1-7. 13. Способ получения фармацевтической композиции по п.12, отличающийся тем, что фармацевтически приемлемый носитель однородно смешивают с терапевтически эффективным количеством соединения по любому из пп.1-7. 14. Способ получения соединения формулы (Ia), включающий восстановительное N-алкилирование промежуточного соединения формулы (II) промежуточным соединением формулы (III) с получением конечного соединения формулы (Ia), где все переменные имеют определение, указанное в п.1, в инертном растворителе и при необходимости, превращение соединения формулы (Ia) в терапевтически активную нетоксичную кислотно-аддитивную соль путем обработки кислотой, или в терапевтически активную нетоксичную основно-аддитивную соль путем обработки основанием, или, наоборот, превращение кислотноаддитивной соли в свободное основание путем обработки щелочью, превращение основно-аддитивной- 25014239 соли в свободную кислоту путем обработки кислотой; и, при необходимости, получение стереохимических изомерных форм, N-оксидов и солей третичного аммония указанных соединений. 15. Способ по п.14, отличающийся тем, что фрагмент Alk-Y-Alk-L в соединениях формул (III) и (Ia) представляет собой бензил.
МПК / Метки
МПК: A61K 31/435, C07D 487/08, A61P 25/00
Метки: качестве, антагонистов, диаза-спиро-[4.4]нонана, производные, нейрокинина-2, nk1
Код ссылки
<a href="https://eas.patents.su/27-14239-proizvodnye-diaza-spiro-44nonana-v-kachestve-antagonistov-nejjrokinina-nk1.html" rel="bookmark" title="База патентов Евразийского Союза">Производные диаза-спиро-[4.4]нонана в качестве антагонистов нейрокинина (nk1)</a>
Предыдущий патент: Производные n-гидроксиамида и их применение
Следующий патент: Анилиды тиазолкарбоновой кислоты
Случайный патент: Способ изготовления модифицированного активированного угля












