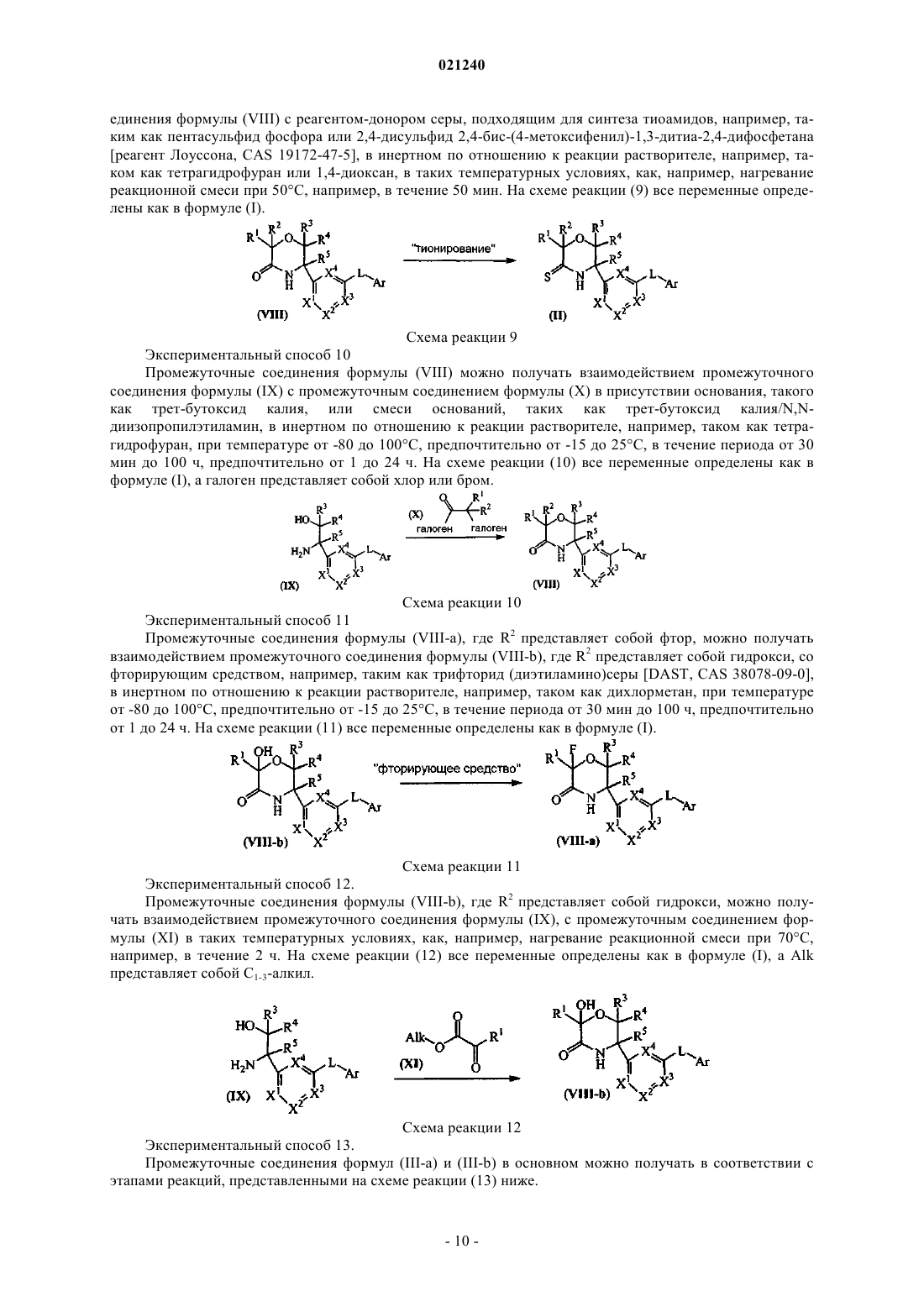
Производные 5,6-дигидро-2h-[1,4]оксазин-3-иламина в качестве ингибиторов бета-секретазы (bace)
Номер патента: 21240
Опубликовано: 29.05.2015
Авторы: Трабанко-Суарес Андрес Авелино, Гейсен Хенрикус Якобус Мария, Ван Гол Михиль Люк Мария, Мартинес Ламенка Каролина, Макдональд Грегор Джеймс, Тресадерн Гэри Джон, Ромбаутс Фредерик Ян Рита
Формула / Реферат
1. Соединение формулы (I)
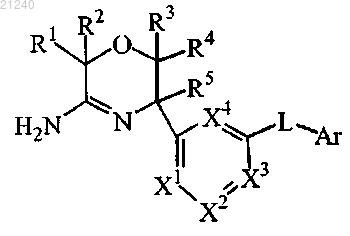
или его таутомерная или стереоизомерная форма, где
R1, R2 и R3 независимо выбраны из группы, состоящей из водорода и фтора;
R4 представляет собой фтор или трифторметил;
R5 выбран из группы, состоящей из C1-3-алкила и циклопропила;
X1, X2, X3, X4 независимо представляют собой C(R6);
каждый R6 выбран из группы, состоящей из водорода и галогена;
L представляет собой связь или -N(R7)CO-, где R7 представляет собой водород или C1-3-алкил;
Ar представляет собой гомоарил или гетероарил;
гомоарил представляет собой фенил или фенил, замещенный одним, двумя или тремя заместителями, выбранными из группы, состоящей из галогена, циано, C1-3-алкила, C1-3-алкилокси, моно- и полигалоген-C1-3-алкила, моно- и полигалоген-C1-3-алкилокси; гетероарил выбран из группы, состоящей из пиридила, пиримидила, пиразила, пиридазила, фуранила, тиенила, пирролила, пиразолила, имидазолила, триазолила, тетразолила, тиазолила, изотиазолила, тиадиазолила, оксазолила, изоксазолила и оксадиазолила, где каждый необязательно замещен одним, двумя или тремя заместителями, выбранными из группы, состоящей из галогена, циано, C1-3-алкила, C2-3-алкинила, C1-3-алкилокси, моно- и полигалоген-C1-3-алкила, моно- и полигалоген-C1-3-алкилокси и C1-3-алкилокси-C1-3-алкилокси; или
его соли присоединения или сольваты.
2. Соединение по п.1, где R1, R2 и R3 представляют собой водород, R4 представляет собой фтор и L представляет собой -N(R7)CO-, где R7 представляет собой водород.
3. Соединение по п.2, где R1, R2 и R3 представляют собой водород, R4 представляет собой фтор, L представляет собой -N(R7)CO-, где R7 представляет собой водород и R5 представляет собой метил, этил или циклопропил.
4. Соединение по п.2, где R1, R2 и R3 представляют собой водород, R4 представляет собой фтор, L представляет собой -N(R7)CO-, где R7 представляет собой водород, и R5 представляет собой метил, этил или циклопропил, X2, X3 и X4 представляют собой СН, и X1 представляет собой СН или CF.
5. Соединение по п.2, где R1, R2 и R3 представляют собой водород, R4 представляет собой фтор, L представляет собой -N(R7)CO-, где R7 представляет собой водород и R5 представляет собой метил, этил или циклопропил, и Ar представляет собой пиридил или пиразил, где каждый необязательно замещен одним или двумя заместителями, выбранными из галогена, циано, метокси, трифторэтокси и дифторметила.
6. Соединение по п.1, где R1, R2 и R3 представляют собой водород, R4 представляет собой трифторметил и L представляет собой -N(R7)CO-, где R7 представляет собой водород.
7. Соединение по п.6, где R1, R2 и R3 представляют собой водород, R4 представляет собой трифторметил, L представляет собой -N(R7)CO-, где R7 представляет собой водород и R5 представляет собой метил, этил или циклопропил.
8. Соединение по п.6, где R1, R2 и R3 представляют собой водород, R4 представляет собой трифторметил, L представляет собой -N(R7)CO-, где R7 представляет собой водород, R5 представляет собой метил, этил или циклопропил, X2, X3 и X4 представляют собой CH, и X1 представляет собой СН или CF.
9. Соединение по п.6, где R1, R2 и R3 представляют собой водород, R4 представляет собой трифторметил, L представляет собой -N(R7)CO-, где R7 представляет собой водород, R5 представляет собой метил, этил или циклопропил, и Ar представляет собой пиридил или пиразил, где каждый необязательно замещен одним или двумя заместителями, выбранными из галогена, циано, метокси, трифторэтокси и дифторметила.
10. Соединение по п.1, где R1 и R2 представляют собой водород, R3 представляет собой фтор, R4 представляет собой трифторметил и L представляет собой -N(R7)CO-, где R7 представляет собой водород.
11. Фармацевтическая композиция для лечения или предотвращения болезни Альцгеймера (AD), умеренного когнитивного нарушения, старости, деменции, деменции с тельцами Леви, синдрома Дауна, деменции, ассоциированной с инсультом, деменции, ассоциированной с болезнью Паркинсона, или деменции, ассоциированной с бета-амилоидом, содержащая терапевтически эффективное количество соединения по любому из пп.1-10 и фармацевтически приемлемый носитель.
12. Способ получения фармацевтической композиции по п.11, отличающийся тем, что фармацевтически приемлемый носитель тщательно смешивают с терапевтически эффективным количеством соединения по любому из пп.1-10.
13. Применение соединения по любому из пп.1-10 в лечении, предотвращении или профилактике болезни Альцгеймера (AD), умеренного когнитивного нарушения, старости, деменции, деменции с тельцами Леви, синдрома Дауна, деменции, ассоциированной с инсультом, деменции, ассоциированной с болезнью Паркинсона, или деменции, ассоциированной с бета-амилоидом.
14. Способ лечения нарушения, выбранного из группы, состоящей из болезни Альцгеймера, умеренного когнитивного нарушения, старости, деменции, деменции с тельцами Леви, синдрома Дауна, деменции, ассоциированной с инсультом, деменции, ассоциированной с болезнью Паркинсона, и деменции, ассоциированной с бета-амилоидом, включающий введение нуждающемуся в этом индивидууму терапевтически эффективного количества соединения по любому из пп.1-10.
15. Способ лечения нарушения, выбранного из группы, состоящей из болезни Альцгеймера, умеренного когнитивного нарушения, старости, деменции, деменции с тельцами Леви, синдрома Дауна, деменции, ассоциированной с инсультом, деменции, ассоциированной с болезнью Паркинсона, и деменции, ассоциированной с бета-амилоидом, включающий введение нуждающемуся в этом индивидууму терапевтически эффективного количества фармацевтической композиции по п.11.
Текст
Настоящее изобретение относится к новым производным 5,6-дигидро-2 Н-[1,4]оксазин-3-иламина в качестве ингибиторов бета-секретазы, также известной как фермент, расцепляющий амилоид в бета-участке, ВАСЕ, ВАСЕ 1, Asp2 или мемапсин 2. Изобретение также относится к фармацевтическим композициям, содержащим такие соединения, к способам получения таких соединений и композиций и к применению таких соединений и композиций для предотвращения и лечения нарушений, в которые вовлечена бета-секретаза, таких как болезнь Альцгеймера(ES), Ромбаутс Фредерик Ян Рита(BE), Тресадерн Гэри Джон, Ван Гол Михиль Люк Мария (ES),Макдональд Грегор Джеймс,Мартинес Ламенка Каролина, Гейсен Хенрикус Якобус Мария (BE) Медведев В.Н. (RU)(71)(73) Заявитель и патентовладелец: ЯНССЕН ФАРМАЦЕВТИКА НВ (BE) Область изобретения Настоящее изобретение относится к новым производным 5,6-дигидро-2H-[1,4]оксазин-3-иламина в качестве ингибиторов бета-секретазы, также известной как фермент, расщепляющий амилоид по бетаучастку, ВАСЕ, BACE1, Asp2 или мемапсин 2. Изобретение также относится к фармацевтическим композициям, содержащим такие соединения, к способам получения таких соединений и композиций и к применению таких соединений и композиций для предотвращения и лечения нарушений, в которые вовлечена бета-секретаза, таких как болезнь Альцгеймера (AD), умеренное когнитивное нарушение, старость, деменция, деменция с тельцами Леви, синдром Дауна, деменция, ассоциированная с инсультом,деменция, ассоциированная с болезнью Паркинсона, и деменция, ассоциированная с бета-амилоидом. Уровень техники, предшествующий изобретению Болезнь Альцгеймера (AD) представляет собой нейродегенеративное заболевание, ассоциированное со старением. Пациенты с AD страдают дефицитом когнитивных функций и потерей памяти, а также поведенческими проблемами, такими как тревожность. Более 90% из пораженных AD имеют спорадическую форму нарушения, тогда как менее 10% случаев являются семейными или наследуемыми. В Соединенных Штатах Америки приблизительно 1 из 10 человек в возрасте 65 лет страдает AD, тогда как в возрасте 85 лет AD поражен 1 из каждых двух индивидуумов. Средняя прогнозируемая продолжительность жизни от первичного диагноза составляет 7-10 лет, а пациенты с AD требуют интенсивного ухода или в домах престарелых, что является очень дорогостоящим, или членов семьи. Увеличивающееся количество пожилых людей в популяции AD, является растущей медицинской проблемой. Существующие в настоящее время способы лечения AD только лечат симптомы заболевания и включают ингибиторы ацетилхолинэстеразы для улучшения когнитивных свойств, а также анксиолитики и антипсихотические средства для контроля поведенческих проблем, ассоциированных с этим заболеванием. Характерными патологическими признаками в головном мозге пациентов с AD являются нейрофибриллярные клубки, образующиеся вследствие гиперфосфорилирования тау-белка, и амилоидные бляшки, формирующиеся при агрегации пептида бета-амилоида 1-42 (Абета 1-42). Абета 1-42 формирует олигомеры, а затем фибриллы и, наконец, амилоидные бляшки. Полагают, что олигомеры и фибриллы являются особенно нейротоксичными и могут вызывать большую часть неврологического повреждения,ассоциированного с AD. Средства, предотвращающие образование Абета 1-42, обладают потенциалом стать модифицирующими заболевание средствами для лечения AD. Абета 1-42 образуется из белкапредшественника амилоида (АРР), содержащего 770 аминокислот. N-конец Абета 1-42 отщепляется бета-секретазой (ВАСЕ), а затем гамма-секретаза отщепляет С-конец. Кроме Абета 1-42, гамма-секретаза также высвобождает Абета 1-40, являющийся преобладающим продуктом расщепления, а также Абета 138 и Абета 1-43. Эти формы Абета также могут агрегировать с формированием олигомеров и фибрилл. Таким образом, можно ожидать, что ингибиторы ВАСЕ будут предотвращать формирование Абета 1-42,а также Абета 1-40, Абета 1-38 и Абета 1-43 и могут являться потенциальными терапевтическими средствами для лечения AD. В WO-2011/009943 (Novartis) описаны незамещенные и 2-замещенные производные оксазина и их применение в качестве ингибиторов ВАСЕ для лечения неврологических нарушений. В WO-2011/020806(Hoffmann-LaRoche) описаны производные 2,6-незамещенного 3-амино-5-фенил-5,6-дигидро-2H[1,4]оксазина со свойствами ингибирования ВАСЕ 1 и/или ВАСЕ 2. Сущность изобретения Настоящее изобретение относится к производным 5,6-дигидро-2 Н-[1,4]оксазин-3-иламина формулыR1, R2, R3, R4 независимо выбраны из группы, состоящей из водорода, фтора, циано, C1-3-алкила,моно- и полигалоген-С 1-3-алкила и С 3-6-циклоалкила; илиX1, X2, X3, X4 независимо представляют собой C(R6) или N, при условии, что не более двух из них представляют собой N; каждый R6 выбран из группы, состоящей из водорода, галогена, C1-3-алкила, моно- и полигалоген-С 1-3-алкила, циано, С 1-3-алкилокси, моно- и полигалоген-С 1-3-алкилокси;L представляет собой связь или -N(R7)CO-, где R7 представляет собой водород или C1-3-алкил;Ar представляет собой гомоарил или гетероарил; где гомоарил представляет собой фенил или фенил, замещенный одним, двумя или тремя замести-1 021240 телями, выбранными из группы, состоящей из галогена, циано, C1-3-алкила, C1-3-алкилокси, моно- и полигалоген-С 1-3-алкила, моно- и полигалоген-C1-3-алкилокси; гетероарил выбран из группы, состоящей из пиридила, пиримидила, пиразила, пиридазила, фуранила, тиенила, пирролила, пиразолила, имидазолила, триазолила, тетразолила, тиазолила, изотиазолила,тиадиазолила, оксазолила, изоксазолила и оксадиазолила, где каждый необязательно замещен одним,двумя или тремя заместителями, выбранными из группы, состоящей из галогена, циано, C1-3-алкила, С 2-3 алкинила, C1-3-алкилокси, моно- и полигалоген-С 1-3-алкила, моно- и полигалоген-С 1-3-алкилокси и С 1-3 алкилокси-С 1-3-алкилокси; и их солям присоединения и сольватам. Иллюстрацией изобретения является фармацевтическая композиция, содержащая фармацевтически приемлемый носитель и любое из описанных выше соединений. Иллюстрацией изобретения является фармацевтическая композиция, получаемая посредством смешивания любого из описанных выше соединений и фармацевтически приемлемого носителя. Иллюстрацией изобретения является способ получения фармацевтической композиции, содержащей смесь любого из описанных выше соединений и фармацевтически приемлемого носителя. Примерами изобретения являются способы лечения нарушения, опосредуемого ферментом бетасекретазой, включающие введение нуждающемуся в этом индивидууму терапевтически эффективного количества любых описанных выше соединений или фармацевтических композиций. Дополнительными примерами изобретения являются способы ингибирования фермента бетасекретазы, включающие введение нуждающемуся в этом индивидууму терапевтически эффективного количества любых описанных выше соединений или фармацевтических композиций. Примером изобретения является способ лечения нарушения, выбранного из группы, состоящей из болезни Альцгеймера, умеренного когнитивного нарушения, старости, деменции, деменции с тельцами Леви, синдрома Дауна, деменции, ассоциированной с инсультом, деменции, ассоциированной с болезнью Паркинсона, и деменции, ассоциированной с бета-амилоидом, предпочтительно болезнью Альцгеймера, включающий введение нуждающемуся в этом индивидууму, терапевтически эффективного количества любых описанных выше соединений или фармацевтических композиций. Другим примером изобретения является любое из описанных выше соединений для применения при лечении у нуждающегося в этом индивидуума: (а) болезни Альцгеймера, (b) умеренного когнитивного нарушения, (с) старости, (d) деменции, (е) деменции с тельцами Леви, (f) синдрома Дауна, (g) деменции, ассоциированной с инсультом, (h) деменции, ассоциированной с болезнью Паркинсона, и (i) деменции, ассоциированной с бета-амилоидом. Подробное описание изобретения Настоящее изобретение относится к соединениям формулы (I), как определено ранее в настоящем документе, и к их фармацевтически приемлемым солям. Соединения формулы (I) представляют собой ингибиторы фермента бета-секретазы (также известной как фермент, расщепляющий участок бета, ВАСЕ, ВАСЕ 1, Asp2 или мемапсин 2) и пригодны при лечении болезни Альцгеймера, умеренного когнитивного нарушения, старости, деменции, деменции, ассоциированной с инсультом, деменции с тельцами Леви, синдрома Дауна, деменции, ассоциированной с болезнью Паркинсона, и деменции, ассоциированной с бета-амилоидом, предпочтительно болезни Альцгеймера, умеренного когнитивного нарушения или деменции, более предпочтительно болезни Альцгеймера. В частности настоящее изобретение относится к 6-замещенным производным 5,6-дигидро-2H[1,4]оксазин-3-иламина формулы (I)R1, R2 и R3 независимо выбраны из группы, состоящей из водорода, фтора, циано, C1-3-алкила, моно- и полигалоген-С 1-3-алкила и С 3-6-циклоалкила;R4 представляет собой фтор или трифторметил; илиX1, X2, X3, X4 независимо представляют собой C(R6) или N, при условии, что не более два из них представляют собой N; каждый R6 выбран из группы, состоящей из водорода, галогена, C1-3-алкила, моно- и полигалоген-С 1-3-алкила, циано, C1-3-алкилокси, моно- и полигалоген-С 1-3-алкилокси;L представляет собой связь или -N(R7)CO-, где R7 представляет собой водород или C1-3-алкил;Ar представляет собой гомоарил или гетероарил; где гомоарил представляет собой фенил или фенил, замещенный одним, двумя или тремя заместителями, выбранными из группы, состоящей из галогена, циано, C1-3-алкила, C1-3-алкилокси, моно- и полигалоген-С 1-3-алкила, моно- и полигалоген-C1-3-алкилокси; гетероарил выбран из группы, состоящей из пиридила, пиримидила, пиразила, пиридазила, фуранила, тиенила, пирролила, пиразолила, имидазолила, триазолила, тетразолила, тиазолила, изотиазолила,тиадиазолила, оксазолила, изоксазолила и оксадиазолила, где каждый необязательно замещен одним,двумя или тремя заместителями, выбранными из группы, состоящей из галогена, циано, C1-3-алкила, C2-3 алкинила, C1-3-алкилокси, моно-и полигалоген-C1-3-алкила, моно- и полигалоген-C1-3-алкилокси и C1-3 алкилокси-C1-3-алкилокси; и к их солям присоединения и сольватам. Соединения по изобретению, где R4 представляет собой электроотрицательную группу, такую как фтор или трифторметил, легче задерживаются в головном мозге, чем соединения на известном уровне техники с отсутствием таких электроотрицательных групп в 6 положении оксазина, так как они являются более слабыми субстратами для гликопротеина проницаемости (PGP), выкачивающего ксенобиотики из головного мозга. В одном из вариантов осуществления L представляет собой прямую связь. В одном из вариантов осуществления L представляет собой прямую связь, а Ar представляет собой фенил; фенил, замещенный одним или двумя заместителями, выбранными из группы галогена, циано, трифторметила, трифторметокси и C1-3-алкилокси; пиридинила; пиридинила, замещенного метилом, галогеном, метокси, этокси или циано; или пиримидинил. В одном из вариантов осуществления L представляет собой прямую связь, X1 представляет собой N,СН или CF, и X2, X3 и X4 представляют собой СН. В одном из вариантов осуществления L представляет собой прямую связь, X3 представляет собой N,1X представляет собой СН или CF, X2 и X4 представляют собой СН. В одном из вариантов осуществления L представляет собой прямую связь, R5 представляет собой метил. В одном из вариантов осуществления L представляет собой прямую связь, R5 представляет собой циклопропил. В одном из вариантов осуществления L представляет собой прямую связь, R5 представляет собой этил. В одном из вариантов осуществления изобретения R1, R2 и R3 представляют собой водород, R4 представляет собой фтор, и L представляет собой -N(R7)CO-, где R7 представляет собой водород. В одном из вариантов осуществления изобретения R1, R2 и R3 представляют собой водород, R4 представляет собой фтор, L представляет собой -N(R7)CO-, где R7 представляет собой водород, и R5 представляет собой метил, этил или циклопропил. В одном из вариантов осуществления изобретения R1, R2 и R3 представляют собой водород, R4 представляет собой фтор, L представляет собой -N(R7)CO-, где R7 представляет собой водород, R5 представляет собой метил, этил или циклопропил, X2, X3 и X4 представляют собой СН, и X1 представляет собой СН, CF или N. В одном из вариантов осуществления изобретения R1, R2 и R3 представляют собой водород, R4 представляет собой фтор, L представляет собой -N(R7)CO-, где R7 представляет собой водород, R5 представляет собой метил, этил или циклопропил, и Ar представляет собой пиридил или пиразил, где каждый необязательно замещен одним или двумя заместителями, выбранными из галогена, циано, метокси, трифторэтокси и дифторметила. В одном из вариантов осуществления изобретения R1, R2 и R3 представляют собой водород, R4 представляет собой фтор, L представляет собой -N(R7)CO-, где R7 представляет собой водород, R5 представляет собой метил, этил или циклопропил, и Ar представляет собой пиридил или пиразил, где каждый необязательно замещен одним или двумя заместителями, выбранными из галогена, циано, метокси, трифторэтокси и дифторметила, и оба положения 5 и 6 дигидро-2H-[1,4]оксазинового кольца находятся в Rконфигурации. В одном из вариантов осуществления изобретения R1, R2 и R3 представляют собой водород, R4 представляет собой фтор, L представляет собой -N(R7)CO-, где R7 представляет собой водород, R5 представляет собой метил или циклопропил, и Ar выбран из группы, состоящей из 5-метоксипиразила, 5 этоксипиразила, 5-(2,2,2-трифторэтокси)пиразила, 5-цианопиридин-2-ила, 5-хлорпиридин-2-ила, 3,5 дихлорпиридин-2-ила, 3-фтор-5-хлорпиридин-2-ила, 3-хлор-5-цианопиридин-2-ила и 5-цианопиридин-3 ила. В одном из вариантов осуществления изобретения R1, R2 и R3 представляют собой водород, R4 представляет собой трифторметил, и L представляет собой -N(R7)CO-, где R7 представляет собой водород. В одном из вариантов осуществления изобретения R1, R2 и R3 представляют собой водород, R4-3 021240 представляет собой трифторметил, L представляет собой -N(R7)CO-, где R7 представляет собой водород,и R5 представляет собой метил, этил или циклопропил. В одном из вариантов осуществления изобретения R1, R2 и R3 представляют собой водород, R4 представляет собой трифторметил, L представляет собой -N(R7)CO-, где R7 представляет собой водород,R5 представляет собой метил, этил или циклопропил, X2, X3 и X4 представляют собой СН, и X1 представляет собой СН, CF или N. В одном из вариантов осуществления изобретения R1, R2 и R3 представляют собой водород, R4 представляет собой трифторметил, L представляет собой -N(R7)CO-, где R7 представляет собой водород,R5 представляет собой метил, этил или циклопропил, и Ar представляет собой пиридил или пиразил, где каждый необязательно замещен одним или двумя заместителями, выбранными из галогена, циано, метокси, трифторэтокси и дифторметила, и оба положения 5 и 6 дигидро-2H-[1,4]оксазинового кольца находятся в R-конфигурации. В одном из вариантов осуществления изобретения R1, R2 и R3 представляют собой водород, R4 представляет собой трифторметил, L представляет собой -N(R7)CO-, где R7 представляет собой водород,R5 представляет собой метил или циклопропил, и Ar выбран из группы, состоящей из 4-пиримидила, 5 метоксипиразила, 5-этоксипиразила, 5-(2,2,2-трифторэтокси)пиразила, 5-цианопиридин-2-ила, 5 хлорпиридин-2-ила, 3,5-дихлорпиридин-2-ила, 3-фтор-5-хлорпиридин-2-ила, 3-хлор-5-цианопиридин-2 ила, 5-метоксипиридин-3-ила и 5-цианопиридин-3-ила. В одном из вариантов осуществления изобретения R1 и R2 представляют собой водород, R3 представляет собой фтор, R4 представляет собой трифторметил, и L представляет собой N(R7)CO-, где R7 представляет собой водород. В одном из вариантов осуществления изобретения R1 и R2 представляют собой водород, R3 представляет собой фтор, R4 представляет собой трифторметил, L представляет собой -N(R7)CO-, где R7 представляет собой водород, и R5 представляет собой метил, этил или циклопропил. В одном из вариантов осуществления изобретения R1 и R2 представляют собой водород, R3 представляет собой фтор, R4 представляет собой трифторметил, L представляет собой -N(R7)CO-, где R7 представляет собой водород, R5 представляет собой метил, этил или циклопропил, X2, X3 и X4 представляют собой СН, и X1 представляет собой СН, CF или N. В одном из вариантов осуществления изобретения R1 и R2 представляют собой водород, R3 представляет собой фтор, R4 представляет собой трифторметил, L представляет собой -N(R7)CO-, где R7 представляет собой водород, R5 представляет собой метил, этил или циклопропил, и Ar представляет собой пиридил или пиразил, где каждый необязательно замещен одним или двумя заместителями, выбранными из галогена, циано, метокси, трифторэтокси и дифторметила, и оба положения 5 и 6 дигидро-2H[1,4]оксазинового кольца находятся в R-конфигурации. В одном из вариантов осуществления изобретения R1 и R2 представляют собой водород, R3 представляет собой фтор, R4 представляет собой трифторметил, L представляет собой -N(R7)CO-, где R7 представляет собой водород, R5 представляет собой метил, этил или циклопропил, и Ar выбран из группы,состоящей из 4-пиримидила, 5-метоксипиразила, 5-этоксипиразила, 5-(2,2,2-трифторэтокси)пиразила, 5 цианопиридин-2-ила, 5-хлорпиридин-2-ила, 3,5-дихлорпиридин-2-ила, 3-фтор-5-хлорпиридин-2-ила, 3 хлор-5-цианопиридин-2-ила, 5-метоксипиридин-3-ила и 5-цианопиридин-3-ила. В одном из вариантов осуществления настоящего изобретения R1, R2, R3, R4 независимо выбраны из группы, состоящей из водорода, фтора, циано, C1-3-алкила, моно- и полигалоген-С 1-3-алкила и С 3-6 циклоалкила; илиX1, X2, X3, X4 независимо представляют собой C(R6) или N, при условии, что не более два из них представляют собой N; каждый R6 выбран из группы, состоящей из водорода, галогена, C1-3-алкила, моно- и полигалоген-C1-3-алкила, циано, C1-3-алкилокси, моно- и полигалоген-C1-3-алкилокси;L представляет собой связь или -N(R7)CO-, где R7 представляет собой водород или C1-3-алкил;Ar представляет собой гомоарил или гетероарил; гомоарил представляет собой фенил или фенил, замещенный одним, двумя или тремя заместителями, выбранными из группы, состоящей из галогена, циано, C1-3-алкила, C1-3-алкилокси, моно- и полигалоген-C1-3-алкила, моно- и полигалоген-C1-3-алкилокси; гетероарил выбран из группы, состоящей из пиридила, пиримидила, пиразила, пиридазила, фуранила, тиенила, пирролила, пиразолила, имидазолила, триазолила, тетразолила, тиазолила,изотиазолила, тиадиазолила, оксазолила, изоксазолила и оксадиазолила, каждого необязательно замещенного одним, двумя или тремя заместителями, выбранными из группы, состоящей из галогена, циано, C1-3-алкила, C1-3-алкилокси, моно- и полигалоген-C1-3-алкила; и их солей присоединения и сольватов. В одном из вариантов осуществления изобретения R1, R2, R3, R4 независимо выбраны из группы, со-4 021240 стоящей из водорода, фтора, циано и полигалоген-C1-3-алкила; или R1 и R2, взятые вместе с атомом углерода, с которым они связаны, могут образовывать С 3-6-циклоалкандиильное кольцо;X1, X2, X3, X4 независимо представляют собой С (R6), где каждый R6 выбран из водорода и галогена; также X1 может представлять собой N;L представляет собой связь или -N(R7)CO-, где R7 представляет собой водород;Ar представляет собой гомоарил или гетероарил; гомоарил представляет собой фенил или фенил, замещенный одним или двумя заместителями, выбранными из группы, состоящей из галогена, циано, C1-3-алкила и C1-3-алкилокси; гетероарил выбран из группы, состоящей из пиридила, пиримидила и пиразила, где каждый необязательно замещен одним или двумя заместителями, выбранными из группы, состоящей из галогена, циано, C1-3-алкила, C1-3-алкилокси, полигалоген-C1-3-алкила и полигалоген-C1-3-алкилокси или их солей присоединения или сольватов. В одном из вариантов осуществления настоящего изобретения R1, R2, R3, R4 независимо выбраны из группы, состоящей из водорода, фтора, циано и полигалоген-C1-3-алкила; илиX1, X2, X3, X4 независимо представляют собой С(R6), где каждый R6 выбран из водорода и галогена;L представляет собой связь или -N(R7)CO-, где R7 представляет собой водород;Ar представляет собой гомоарил или гетероарил; гомоарил представляет собой фенил или фенил, замещенный одним или двумя заместителями, выбранными из группы, состоящей из галогена, циано, C1-3-алкила и C1-3-алкилокси; гетероарил выбран из группы, состоящей из пиридила, пиримидила и пиразила, где каждый необязательно замещен одним или двумя заместителями, выбранными из группы, состоящей из галогена, циано, C1-3-алкила и C1-3-алкилокси; или их солей присоединения или сольватов. В другом варианте осуществления настоящего изобретения R1 и R2 независимо выбраны из группы,состоящей из водорода, фтора, циано и трифторметила; или R1 и R2, взятые вместе с атомом углерода, с которым они связаны, могут образовывать циклопропильное кольцо; оба, R3 и R4 представляют собой водород;X1 и X3 представляют собой СН или CF;L представляет собой связь или -N(R7)CO-, где R7 представляет собой водород;Ar представляет собой гомоарил или гетероарил; гомоарил представляет собой фенил или фенил, замещенный одним или двумя заместителями, выбранными из хлора и циано; гетероарил выбран из группы, состоящей из пиридила, пиримидила и пиразила, где каждый необязательно замещен одним или двумя заместителями, выбранными из группы, состоящей из хлора, фтора,циано, метила и метокси; или их солей присоединения или сольватов. В другом варианте осуществления настоящего изобретения R1 и R2 независимо выбраны из группы,состоящей из водорода, фтора, циано и трифторметила; или R1 и R2, взятые вместе с атомом углерода, с которым они связаны, могут образовывать циклопропильное кольцо;R3 и R4, оба представляют собой водород;L представляет собой связь или -N(R7)CO-, где R7 представляет собой водород;Ar представляет собой гомоарил или гетероарил; гомоарил представляет собой фенил или фенил, замещенный одним или двумя заместителями, выбранными из хлора и циано; гетероарил выбран из группы, состоящей из пиридила, пиримидила и пиразила, где каждый необязательно замещен одним или двумя заместителями, выбранными из группы, состоящей из хлора, фтора,циано, метила и метокси; или их солей присоединения или сольватов. В другом варианте осуществления настоящего изобретения R1 и R2, оба представляют собой водород; R3 и R4 независимо выбраны из группы, состоящей из водорода, фтора и трифторметил;X1 и X3 представляют собой СН или CF;L представляет собой связь или -N(R7)CO-, где R7 представляет собой водород;Ar представляет собой гомоарил или гетероарил; гомоарил представляет собой фенил или фенил, замещенный одним или двумя заместителями, выбранными из хлора и циано; гетероарил выбран из группы, состоящей из пиридила, пиримидила и пиразила, где каждый необязательно замещен одним или двумя заместителями, выбранными из группы, состоящей из хлора, фтора,циано, метила и метокси; или их солей присоединения или сольватов. Определения"Галоген" означает фтор, хлор и бром; "C1-3-алкил" означает неразветвленную или разветвленную насыщенную алкильную группу с 1, 2 или 3 атомами углерода, например, метил, этил, 1-пропил и 2 пропил; "C1-3-алкилокси" означает радикал простого эфира, где C1-3-алкил является таким, как определено ранее; "моно- и полигалоген-C1-3-алкил" означает C1-3-алкил, как определено ранее, замещенный 1, 2,3 или, когда возможно, большим количеством атомов галогенов, как определено ранее; "моно- и полигалоген-C1-3-алкилокси" означает радикал простого эфира, где моно- и полигалоген-C1-3-алкил является таким, как определено ранее; "С 3-6-циклоалкил" означает циклопропил, циклобутил, циклопентил и циклогексил; "С 3-6-циклоалкандиил" означает бивалентный радикал, такой как циклопропандиил, циклобутандиил, циклопентандиил и циклогександиил. Как применяют в настоящем документе, термин "индивидуум" относится к животному, предпочтительно млекопитающему, наиболее предпочтительно к человеку, который является или являлся объектом лечения, наблюдения или эксперимента. Как применяют в настоящем документе, термин "терапевтически эффективное количество" означает такое количество активного соединения или фармацевтического средства, которое вызывает в тканевой системе у животного или человека желаемый исследователем, ветеринаром, врачом или другим клиническим работником биологический или медицинский ответ, который включает облегчение симптомов подвергаемого лечению заболевания или нарушения. Как применяют в настоящем документе, термин "композиция" предназначен для включения продукта, содержащего указываемые ингредиенты в указываемых количествах, а также любой продукт, являющийся результатом непосредственных или косвенных комбинаций указываемых ингредиентов в указываемых количествах. Выше и далее в настоящем документе термин "соединение формулы (I)" предназначен для включения его солей присоединения, сольватов и стереоизомеров. Выше или далее в настоящем документе термины "стереоизомеры" или "стереохимически изомерные формы" используют взаимозаменяемо. Изобретение включает все стереоизомеры соединения формулы (I) в виде чистого стереоизомера или в виде смеси двух или более стереоизомеров. Энантиомеры представляют собой стереоизомеры, которые являются несовпадающими при наложении зеркальными отображениями друг друга. Смесь пары энантиомеров 1:1 представляет собой рацемат или рацемическую смесь. Диастереомеры (или диастереоизомеры) представляют собой стереоизомеры, которые не являются энантиомерами, т.е. они не связаны как зеркальные изображения. Если соединение содержит двойную связь, заместители могут находиться в Е- или Z-конфигурации. Если соединение содержит двузамещенную циклоалкильную группу, заместители могут находиться в цис- или трансконфигурации. Таким образом, изобретение включает энантиомеры, диастереомеры, рацематы, Еизомеры, Z-изомеры, цис-изомеры, транс-изомеры и их смеси. Абсолютная конфигурация указана по системе Кана-Ингольда-Прелога. Конфигурация у ассиметричного атома указана посредством R или S. Разделяемые соединения, абсолютная конфигурация которых неизвестна, можно обозначать (+) или (-) в зависимости от направления, в котором они вращают плоскополяризованный свет. Когда указан конкретный стереоизомер, это означает, что указанный стереоизомер является в значительной степени очищенным, т.е. ассоциирован менее чем с 50%, предпочтительно менее чем с 20%,более предпочтительно менее чем с 10%, даже более предпочтительно менее чем с 5%, в частности менее чем с 2%, а наиболее предпочтительно менее чем с 1% других изомеров. Таким образом, когда соединение формулы (I) указано, например как (R), это означает, что соединение в значительной степени очищено от (S)-изомера; когда соединение формулы (I) указано, например как Е, это означает, что соединение в значительно степени очищено от Z-изомера; когда соединение формулы (I) указано, например как цис,это означает, что соединение в значительной степени очищено от транс-изомера. Для применения в медицине соли соединений по настоящему изобретению относятся к нетоксическим "фармацевтически приемлемым солям". Однако другие соли могут подходить для получения соединений по настоящему изобретению или их фармацевтически приемлемых солей. Подходящие фармацевтически приемлемые соли соединений включают соли присоединения кислот, которые можно получать, например, смешивая раствор соединения с раствором фармацевтически приемлемой кислоты, такой как соляная кислота, серная кислота, фумаровая кислота, малеиновая кислота, янтарная кислота, уксусная кислота, бензойная кислота, лимонная кислота, винная кислота, угольная кислота или фосфорная кислота. Кроме того, когда соединения по изобретению несут кислотную группу, их подходящие фармацевтически приемлемые соли могут включать соли щелочных металлов, например, соли натрия или калия; соли щелочно-земельных металлов, например соли кальция или магния; и соли, формируемые с подходящими органическими лигандами, например четвертичные аммонийные соли. Типичные кислоты, которые можно использовать при получении фармацевтически приемлемых солей, в качестве неограничивающих примеров включают следующее: уксусную кислоту, 2,2 дихлоруксусную кислоту, ацилированные аминокислоты, адипиновую кислоту, альгиновую кислоту,аскорбиновую кислоту, L-аспарагиновую кислоту, бензолсульфоновую кислоту, бензойную кислоту, 4 ацетамидобензойную кислоту, (+)-камфорную кислоту, камфарсульфоновую кислоту, каприновую кислоту, капроевую кислоту, каприловую кислоту, коричную кислоту, лимонную кислоту, цикламовую кислоту, этан-1,2-дисульфоновую кислоту, этансульфоновую кислоту, 2-гидроксиэтансульфоновую кислоту, муравьиную кислоту, фумаровую кислоту, галактаровую кислоту, гентизиновую кислоту, глюкогептоновую кислоту, D-глюконовую кислоту, D-глюкуроновую кислоту, L-глутаминовую кислоту, бетаоксоглутаровую кислоту, гликолевую кислоту, гиппуровую кислоту, бромисто-водородную кислоту, соляную кислоту, (+)-L-молочную кислоту, -DL-молочную кислоту, лактобионовую кислоту, малеиновую кислоту, (-)-L-яблочную кислоту, малоновую кислоту, -DL-миндальную кислоту, метансульфоновую кислоту, нафталин-2-сульфоновую кислоту, нафталин-1,5-дисульфоновую кислоту, 1-гидрокси-2 нафтойную кислоту, никотиновую кислоту, азотную кислоту, олеиновую кислоту, оротовую кислоту,щавелевую кислоту, пальмитиновую кислоту, памовую кислоту, фосфорную кислоту, Lпироглутаминовую кислоту, салициловую кислоту, 4-аминосалициловую кислоту, себациновую кислоту,стеариновую кислоту, янтарную кислоту, серную кислоту, дубильную кислоту, (+)-L-винную кислоту,тиоциановую кислоту, п-толуолсульфоновую кислоту, трифторметилсульфоновую кислоту и ундеценовую кислоту. Типичные основания, которые можно использовать при получении фармацевтически приемлемых солей, в качестве неограничивающих примеров включают следующее: аммиак, L-аргинин, бенетамин, бензатин, гидроксид кальция, холин, диметилэтаноламин, диэтаноламин, диэтиламин, 2(диэтиламино)этанол, этаноламин, этилендиамин, N-метилглюкамин, гидрабамин, 1H-имидазол, Lлизин, гидроксид магния, 4-(2-гидроксиэтил)морфолин, пиперазин, гидроксид калия, 1-(2 гидроксиэтил)пирролидин, вторичный амин, гидроксид натрия, триэтаноламин, трометамин и гидроксид цинка. Химические наименования соединений по настоящему изобретению получали по правилам номенклатуры, принятой в Chemical Abstracts Service. Некоторые из соединений по формуле (I) также могут существовать в их таутомерной форме. Такие формы, хотя они явно не указаны в приведенной выше формуле, следует включать в объем настоящего изобретения. Получение соединений Экспериментальный способ 1. Конечные соединения формулы (I) можно получать взаимодействием промежуточного соединения формулы (II) с подходящим источником аммиака, например, таким как хлорид аммония или водный аммиак, по схеме реакции (1), реакцией, которую проводят в подходящем инертном по отношению к реакции растворителе, например, таком как вода или метанол, в таких температурных условиях, как, например, нагревание реакционной смеси при 60 С, например, в течение 6 ч. На схеме реакции (1) все переменные определены как в формуле (I). Схема реакции 1 Экспериментальный способ 2. Конечные соединения формулы (I-а), где L представляет собой -N(R7)CO-, можно получать взаимодействием промежуточного соединения формулы (III-а) с соединением формулы (IV) по схеме реакции(2), реакцией, которую проводят в подходящем инертном по отношению к реакции растворителе, например, таком как N,N-диметилформамид, в присутствии подходящего основания, например, такого какK3PO4, медного катализатора, например, такого как CuI, и диамина, например, такого как (1R,2R)-(-)-1,2 диаминоциклогексан, в таких температурных условиях, как, например, нагревание реакционной смеси при 180 С, например, в течение 135 мин, при микроволновом излучении. На схеме реакции (2) все переменные определены как в формуле (I), a W представляет собой галоген. Схема реакции 2 Экспериментальный способ 3. Кроме того, конечные соединения формулы (I-а) можно получать взаимодействием промежуточного соединения формулы (III-b) с соединением формулы (V) по схеме реакции (3), реакцией, которую проводят в подходящем инертном по отношению к реакции растворителе, например, таком как дихлорметан, в присутствии подходящего основания, например, такого как триэтиламин, в присутствии конденсирующего средства, например, такого как гексафторфосфат О-(7-азабензотриазол-1-ил)-N,N,N',N'тетраметилурония [HATU, CAS 148893-10-1], в таких температурных условиях, как, например, нагревание реакционной смеси при 25 С, например, в течение 2 ч. На схеме реакции (3) все переменные определены как в формуле (I). Схема реакции 3 Экспериментальный способ 4. Кроме того, конечные соединения формулы (I-а) можно получать взаимодействием промежуточного соединения формулы (III-b) с соединением формулы (VI) по схеме реакции (4), реакцией, которую проводят в подходящем инертном по отношению к реакции растворителе, например, таком как дихлорметан, в присутствии подходящего основания, например, такого как пиридин, при комнатной температуре в течение 2 ч. На схеме реакции (4) все переменные определены как в формуле (I), a Y представляет собой галоген. Схема реакции 4 Экспериментальный способ 5. Конечные соединения формулы (I-b), где L представляет собой связь, можно получать взаимодействием промежуточного соединения формулы (III-а) с соединением формулы (VII) по схеме реакции (5),реакцией, которую проводят в подходящем инертном по отношению к реакции растворителе, например,таком как этанол, или в смесях инертных растворителей, например, таких как 1,2 диметоксиэтан/вода/этанол, в присутствии подходящего основания, например, такого как водные K3PO4 катализатора комплекса[CAS 72287-26-4] или диацетат трансбисдициклогексиламин)палладия [DAPCy, CAS 628339-96-8], в таких температурных условиях, как, например, нагревание реакционной смеси при 80 С, например, в течение 20 ч, или например, нагревание реакционной смеси при 130 С, например, в течение 10 мин при микроволновом излучении. На схеме реакции (5) все переменные определены как в формуле (I), a W представляет собой галоген. R8 и R9 могут представлять собой водород или алкил, или, взятые вместе, могут образовывать, например, бивалентный радикал формул -СН 2 СН 2-, -СН 2 СН 2 СН 2- или -C(СН 3)2C(СН 3)2-. Экспериментальный способ 6. Промежуточные соединения формулы (I-c), где R3 представляет собой фтор, a R4 представляет собой трифторметил, формулы (I-d), где R3 представляет собой фтор, a R4 представляет собой водород, и формулы (I-е), где R3 представляет собой водород, a R4 представляет собой трифторметил, можно получать из соответствующих промежуточных соединений формул (XXIII-а) и (XXIII-b) по схеме реакции(6), реакцией, которую проводят в подходящем инертном по отношению к реакции растворителе, например, дихлорметане, в присутствии подходящей кислоты, например, трифторуксусной кислоты при комнатной температуре, например, в течение 2 ч. На схеме реакции (6) все переменные определены как в формуле (I). Схема реакции 6 Экспериментальный способ 7. Конечные соединения формулы (I-d), где R3 представляет собой фтор, a R4 представляет собой водород, и формулы (I-е), где R3 представляет собой водород, a R4 представляет собой трифторметил, можно получать из соответствующих промежуточных соединений формул (XXXII) и (XXVIII) с применением подходящего источника аммиака, например, такого как хлорид аммония или водный аммиак, по схеме реакции (7), реакцией, которую проводят в подходящем инертном по отношению к реакции растворителе, например, таком как вода или метанол, в таких температурных условиях, как, например, нагревание реакционной смеси при 60C, например, в течение 6 ч. На схеме реакции (7) все переменные определены как в формуле (I). Схема реакции 7 Экспериментальный способ 8. Конечные соединения формулы (I-f), где L представляет собой связь, можно получать взаимодействием промежуточного соединения формулы (XXV-b) с соединением формулы (VII) по схеме реакции (8),реакцией, которую проводят в подходящем инертном по отношению к реакции растворителе, например,таком как этанол, или в смесях инертных растворителей, например, таких как 1,2 диметоксиэтан/вода/этанол, в присутствии подходящего основания, например, такого как водные K3PO4 или[CAS 72287-26-4] или диацетат трансбисдициклогексиламин)палладия [DAPCy, CAS 628339-96-8], в таких температурных условиях, как, например, нагревание реакционной смеси при 80 С, например, в течение 20 ч, или например, нагревание реакционной смеси при 130C, например, в течение 10 мин при микроволновом излучении. На схеме реакции (8) все переменные определены как в формуле (I), a W представляет собой галоген. R8 и R9 могут представлять собой водород или алкил, или, взятые вместе, могут образовывать, например, бивалентный радикал формул -СН 2 СН 2-, -СН 2 СН 2 СН 2- или -С(СН 3)2 С(СН 3)2-. Схема реакции 8 Ряд промежуточных соединений и исходных веществ в указанных выше получениях представляет собой соединения, которые можно получить известными в данной области способами получения указанных или сходных соединений, а некоторые промежуточные соединения являются новыми. Ниже в настоящем документе более подробно описан ряд таких способов получения. Экспериментальный способ 9. Промежуточные соединения формулы (II) можно получать взаимодействием промежуточного со-9 021240 единения формулы (VIII) с реагентом-донором серы, подходящим для синтеза тиоамидов, например, таким как пентасульфид фосфора или 2,4-дисульфид 2,4-бис-(4-метоксифенил)-1,3-дитиа-2,4-дифосфетана[реагент Лоуссона, CAS 19172-47-5], в инертном по отношению к реакции растворителе, например, таком как тетрагидрофуран или 1,4-диоксан, в таких температурных условиях, как, например, нагревание реакционной смеси при 50 С, например, в течение 50 мин. На схеме реакции (9) все переменные определены как в формуле (I). Схема реакции 9 Экспериментальный способ 10 Промежуточные соединения формулы (VIII) можно получать взаимодействием промежуточного соединения формулы (IX) с промежуточным соединением формулы (X) в присутствии основания, такого как трет-бутоксид калия, или смеси оснований, таких как трет-бутоксид калия/N,Nдиизопропилэтиламин, в инертном по отношению к реакции растворителе, например, таком как тетрагидрофуран, при температуре от -80 до 100 С, предпочтительно от -15 до 25 С, в течение периода от 30 мин до 100 ч, предпочтительно от 1 до 24 ч. На схеме реакции (10) все переменные определены как в формуле (I), a галоген представляет собой хлор или бром. Схема реакции 10 Экспериментальный способ 11 Промежуточные соединения формулы (VIII-а), где R2 представляет собой фтор, можно получать взаимодействием промежуточного соединения формулы (VIII-b), где R2 представляет собой гидрокси, со фторирующим средством, например, таким как трифторид (диэтиламино)серы [DAST, CAS 38078-09-0],в инертном по отношению к реакции растворителе, например, таком как дихлорметан, при температуре от -80 до 100 С, предпочтительно от -15 до 25 С, в течение периода от 30 мин до 100 ч, предпочтительно от 1 до 24 ч. На схеме реакции (11) все переменные определены как в формуле (I). Схема реакции 11 Экспериментальный способ 12. Промежуточные соединения формулы (VIII-b), где R2 представляет собой гидрокси, можно получать взаимодействием промежуточного соединения формулы (IX), с промежуточным соединением формулы (XI) в таких температурных условиях, как, например, нагревание реакционной смеси при 70 С,например, в течение 2 ч. На схеме реакции (12) все переменные определены как в формуле (I), a Alk представляет собой C1-3-алкил. Схема реакции 12 Экспериментальный способ 13. Промежуточные соединения формул (III-а) и (III-b) в основном можно получать в соответствии с этапами реакций, представленными на схеме реакции (13) ниже.F: преобразование бромо в амин (когда R7 представляет собой Н) Амидиновые производные на приведенной выше схеме реакции можно подходящим способом получать из соответствующих тиоамидных производных известными в данной области способами преобразования тиоамидов в амидины (этап реакции А). Указанное преобразование можно подходящим способом проводить посредством обработки указанных тиоамидов источником аммиака, например, таким как хлорид аммония или водный аммиак, в подходящем инертном по отношению к реакции растворителе,например, таком как вода или метанол и т.п., в таких температурных условиях, как, например, нагревание реакционной смеси при 60 С, например, в течение 6 ч. Альтернативно, промежуточные соединения формулы (III-b), где R7 на приведенной выше схеме реакции (13) представляет собой водород, можно получать из соответствующего промежуточного соединения формулы (III-а) посредством катализируемого медью типа способа связывания (этап реакции F). Указанное связывание можно проводить посредством обработки указанных промежуточных соединений формулы (III-а) азидом натрия в подходящем инертном по отношению к реакции растворителе, например, таком как ДМСО, в присутствии смеси подходящих оснований, например, таких как диметилэтилендиамин и Na2CO3, и медного катализатора, такого как CuI, в таких температурных условиях, как, например, нагревание реакционной смеси при 110 С, до завершения реакции, например, 1 ч. Тиоамидные производные на приведенной выше схеме реакции (13) можно получать из амидных производных описанными ниже известными в данной области способами тионирования (этап реакции В). Указанное преобразование можно подходящим способом проводить посредством обработки указанных амидов тионирующим средством, например, таким как пентасульфид фосфора или 2,4-дисульфид 2,4-бис-(4-метоксифенил)-1,3-дитиа-2,4-дифосфетана [реагент Лоуссона, CAS 19172-47-5], в инертном по отношению к реакции растворителе, например, таком как тетрагидрофуран или 1,4-диоксан и т.п., в таких температурных условиях, как, например, нагревание реакционной смеси при 50 С, например, в тече- 11021240 ние 50 мин. Амидные производные на приведенной выше схеме реакции (13) можно получать из производных бета-аминоспиртов формулы (XV) и промежуточного соединения формулы (X) описанными ниже известными в данной области способами замыкания кольца (этап реакции С). Указанное замыкание кольца можно подходящим способом проводить посредством обработки указанных бета-аминоспиртов промежуточным соединением формулы (X) в присутствии основания, такого как трет-бутоксид калия, или смеси оснований, таких как трет-бутоксид калия/N,N-диизопропилэтиламин, в инертном по отношению к реакции растворителе, например, таком как тетрагидрофуран и т.п., при температуре от -80 до 100 С,предпочтительно от -15 до 25 С в течение периода от 30 мин до 100 ч предпочтительно от 1 до 24 ч. Кроме того, промежуточные соединения формул (XII-b) и (XIII-b) на приведенной выше схеме реакции (13) можно получать из соответствующих промежуточных соединений формул (XII-а) и (XIII-а) описанными ниже известными в данной области способами связывания типа Бухвальда-Хартвига (этап реакции D). Указанное связывание можно проводить посредством обработки промежуточных соединений формул (XII-а) и (XIII-а) промежуточным соединением формулы (XIV) в подходящем инертном по отношению к реакции растворителе, например, таком как этанол, или смеси инертных растворителей,например, таких как 1,2-диметоксиэтан/вода/этанол, в присутствии подходящего основания, например,такого как водные K3PO4 или Cs2CO3, катализатора комплекса Pd, например, такого как [1,1'бис(дифенилфосфино)ферроцен]дихлорпалладий(II)[CAS 72287-26-4] или диацетат трансбис(дициклогексиламин)палладия [DAPCy, CAS 628339-96-8], в таких температурных условиях, как,например, нагревание реакционной смеси при 80 С, например, в течение 20 ч, или, например, нагревание реакционной смеси при 130 С, например, в течение 10 мин при микроволновом излучении. Кроме того, промежуточные соединения формул (XII-b) и (XIII-b) на приведенной выше схеме реакции (13), где R7 представляет собой Н, можно получать из соответствующих промежуточных соединений формул (XII-с) и (XIII-с) описанными ниже известными в данной области способами восстановления нитро в амино (этап реакции Е). Указанное восстановление можно подходящим способом проводить описанными ниже известными в данной области способами каталитического гидрирования. Например,указанное восстановление можно проводить, перемешивая участвующие в реакции вещества в атмосфере водорода и в присутствии подходящего катализатора, например, такого как палладий на углероде,платина на углероде, никель Ренея и т.п. катализаторы. Подходящими растворителями являются, например, вода, алканолы, например, метанол, этанол и т.п., сложные эфиры, например, этилацетат и т.п. Для увеличения скорости указанной реакции восстановления предпочтительным может являться повышение температуры и/или давления в реакционной смеси. Нежелательное дополнительное гидрирование определенных функциональных групп в участвующих в реакции веществ и продуктах реакции можно предотвращать добавлением в реакционную смесь каталитического яда, например, такого как тиофен и т.п. Промежуточные соединения формул (IX), (XV-a), (XV-b) и (XV-c) в основном можно получать описанными ниже известными в данной области способами по типу реакции Штрекера, описанными в литературе, с последующими стандартными химическими преобразованиями цианогруппы. Экспериментальный способ 14. Промежуточные соединения формул (III-c) и (III-d), где R1 и R2 вместе с атомом углерода, с которым они связаны, объединены с формированием С 3-6-циклоалкандиильного кольца, в основном можно получать в соответствии с этапами реакций, представленными на схемах реакций (14) и (15) ниже. Индекс n на них может обозначать 1, 2, 3 или 4.D: связывание по типу Бухвальда-Хартвига (когда W представляет собой галоген) Е: восстановление нитро в амино (если R7 представляет собой Н)G: снятие защиты с амида Амидиновые производные на приведенной выше схеме реакции можно подходящим способом получать из соответствующих тиоамидных производных известными в данной области способами преобразование тиоамида в амидин (этап реакции А). Указанное преобразование можно подходящим способом проводить посредством обработки указанных тиоамидов источником аммиака, например, таким как хлорид аммония или водный аммиак, в подходящем инертном по отношению к реакции растворителе, например, таком как вода или метанол и т.п., в таких температурных условиях, как, например, нагревание реакционной смеси при 60 С, например, в течение 6 ч. Тиоамидные производные на приведенной выше схеме реакции (14) можно получать из амидных производных описанными ниже известными в данной области способами тионирования (этап реакции В). Указанное преобразование можно подходящим способом проводить посредством обработки указанных амидов тионирующим средством, например, таким как пентасульфид фосфора или 2,4-дисульфид 2,4-бис-(4-метоксифенил)-1,3-дитиа-2,4-дифосфетана [реагент Лоуссона, CAS 19172-47-5], в инертном по отношению к реакции растворителе, например, таком как тетрагидрофуран или 1,4-диоксан и т.п., в таких температурных условиях, как, например, нагревание реакционной смеси при 50 С, например, в течение 50 мин. Амидные производные на приведенной выше схеме реакции (14) можно получать из Nзащищенных амидных производных, где защитная группа амида может представлять собой, например, пметоксибензильную группу, описанными ниже известными в данной области способами снятия защиты сN-группы амидов (этап реакции G). Указанное преобразование можно подходящим способом проводить посредством обработки указанных N-замещенных амидов подходящим средством снятия защиты амидной функциональной группы, например, таким как аммоний нитрата церия (IV), в смеси инертных растворителей, например, таких как ацетонитрил/вода, при умеренно высокой температуре, например, такой как 25 С, например, в течение 4 ч. Кроме того, промежуточные соединения формул (XII-е), (XIII-е) и (XVI-b) на приведенной выше схеме реакции (14) можно получать из соответствующих промежуточных соединений формул (XII-d),(XIII-d) и (XVI-a) описанными ниже известными в данной области способами связывания типа Бухвальда-Хартвига, такими как способы, описанные на схеме реакции (13) (этап реакции D). Кроме того, промежуточные соединения формул (XII-е), (XIII-е) и (XVI-b) на приведенной выше схеме реакции (14), где R7 представляет собой Н, можно получать из соответствующих промежуточных соединений формул (XII-f), (XIII-f) и (XVI-с) описанными ниже известными в данной области способами восстановления нитро в амино, такими как способы, описанные на схеме реакции (13) (этап реакции Е).J: С-алкилирование Промежуточные соединения формул (XVI-a), (XVI-b) и (XVI-c) на приведенной выше схеме реакции (15) можно получать из соответствующих промежуточных соединений формул (XVII-а), (XVII-b) и(XVII-c) описанными ниже известными в данной области способами внутримолекулярного замыкания кольца (этап реакции Н). Указанное внутримолекулярное замыкание кольца можно подходящим способом проводить посредством обработки указанных промежуточных соединений формул (XVII-a), (XVII-b) и (XVII-c) в присутствии подходящего основания, например, такого как диизопропиламид лития, в инертном растворителе, например, таком как тетрагидрофуран, при низкой температуре, например, такой как 0 С, например, в течение 30 мин. Промежуточные соединения формул (XVII-a), (XVII-b) и (XVII-c) на приведенной выше схеме реакции (15) можно получать из соответствующих промежуточных соединений формул (XVIII-a), (XVIII-b) и (XVIII-c) описанными ниже известными в данной области способами сульфонилирования спиртов(этап реакции I). Указанное преобразование можно подходящим способом проводить посредством обработки указанных промежуточных соединений формул (XVIII-a), (XVIII-b) и (XVIII-c) промежуточным соединением формулы(XIX),таким как,например,метансульфонилхлорид или птолуолсульфонилхлорид, в присутствии подходящего основания, например, такого как N,Nдиизопропилэтиламин, в инертном растворителе, например, таком как дихлорметан, при низкой температуре, например, такой как 0 С, например, в течение 15 мин. Промежуточные соединения формул (XVIII-a), (XVIII-b) и (XVIII-c) на приведенной выше схеме реакции (15) можно получать из соответствующих промежуточных соединений формул (ХХ-а), (XX-b) и(ХХ-с) описанными ниже известными в данной области способами С-алкилирования (этап реакции J). Указанное преобразование можно подходящим способом проводить посредством обработки указанных промежуточных соединений формул (ХХ-а), (ХХ-b) и (ХХ-с) промежуточным соединением формулы(XXI), где Z2 представляет собой подходящую спиртовую защитную группу, например, такую как тетра- 14021240 гидропиранильная группа, a Y представляет собой галоген, в присутствии подходящего основания, например, такого как диизопропиламид лития, в инертном растворителе, например, таком как тетрагидрофуран, при низкой температуре, например, такой как 0 С, например, в течение 2 ч. Промежуточные соединения формул (ХХ-а), (ХХ-b) и (ХХ-с) на приведенной выше схеме реакции(15) можно получать из соответствующих промежуточных соединений формул (XXII-а), (XXII-b) и(XXII-c) описанными ниже известными в данной области способами замыкания кольца (этап реакции С). Указанное замыкание кольца можно подходящим способом проводить посредством обработки указанных промежуточных соединений формул (XXII-a), (XXII-b) и (XXII-c) промежуточным соединением формулы (X) в присутствии основания, такого как трет-бутоксид калия, или смеси оснований, таких как трет-бутоксид калия/N,N-диизопропилэтиламин, в инертном по отношению к реакции растворителе, например, таком как тетрагидрофуран и т.п., при температуре от -80 до 100 С, предпочтительно от -78 до 25 С, в течение периода от 30 мин до 100 ч, предпочтительно от 1 до 24 ч. Кроме того, промежуточные соединения формул (XVIII-b) и (ХХ-b) на схеме реакции (15) можно получать из соответствующих промежуточных соединений формул (XVIII-a) и (ХХ-а), где W представляет собой галоген, описанными ниже известными в данной области способами связывания типа Бухвальда-Хартвига, такими как способы, описанные на схеме реакции (13) (этап реакции D). Кроме того,промежуточные соединения формул (XVII-b), (XVIII-b) и (XX-b) на приведенной выше схеме реакции(15), где R7 представляет собой Н, можно получать из соответствующих промежуточных соединений формул (XVII-c), (XVIII-c) и (ХХ-с) описанными ниже известными в данной области способами восстановления нитро в амино, такими как способы, описанные на схеме реакции (13) (этап реакции Е). Промежуточные соединения формул (XXII-a), (XXII-b) и (XXII-c), где Z1 представляет собой подходящую защитную группу N-группы, например, такую как п-метоксибензильная группа, в основном можно получать описанными ниже известными в данной области способами по типу реакции Штрекера,описанными в литературе. Экспериментальный способ 16. Промежуточные соединения формул (XXIII-а), (XXIII-b) и (XXXII) в основном можно получать в соответствии с этапами реакций, представленными на схеме реакции (16) ниже.K: связывание по типу СузукиL: защита N-Boc Промежуточные соединения формулы (XXIII-а) на приведенной выше схеме реакции (16) можно получать взаимодействием промежуточного соединения формулы (XXIV-a) с подходящим арилборонатом или арилбороновой кислотой в реакции по типу Сузуки (этап реакции K). Таким образом, промежуточные соединения формулы (XXIV-a) могут вступать в реакцию в подходящем инертном по отношению к реакции растворителе, например, таком как 1,4-диоксан, этанол, или в смесях инертных растворителей,например, таких как 1,2-диметоксиэтан/вода/этанол, в присутствии подходящего основания, например,такого как водные K3PO4, Na2CO3 или Cs2CO3, катализатора комплекса Pd, например, такого как [1,1'бис(дифенилфосфино)ферроцен] дихлорпалладий(II) [CAS 72287-26-4] или диацетат трансбис(дициклогексиламин)палладия [DAPCy, CAS 628339-96-8], или тетракистрифенилфосфин)палладий[CAS 14221-01-3], в таких температурных условиях, как, например, нагревание реакционной смеси при 80 С, например, в течение периода времени от 2 до 20 ч, или, например, нагревание реакционной смеси при 130 С, например, в течение 10 мин при микроволновом излучении. Амидиновые производные на приведенной выше схеме реакции (16) можно защищать защитной группой N-Boc описанными ниже известными в данной области способами защиты N-группы (этап реакции L). Указанное преобразование можно подходящим способом проводить посредством обработки указанных промежуточных соединений формулы (XXV-a) ди-трет-бутилдикарбонатом, в присутствии основания, например, такого как диизопропилэтиламин, в смеси инертных растворителей, например, таких как 1,4-диоксан/вода, перемешивая реакционную смесь при подходящей температуре, например, такой как 25 С, в течение требуемого для расходования исходного вещества периода времени. Тиоамидные производные на приведенной выше схеме реакции (16) можно получать из амидных производных описанными ниже известными в данной области способами тионирования (этап реакции В). Указанное преобразование можно подходящим способом проводить посредством обработки указанных амидов тионирующим средством, например, таким как пентасульфид фосфора или 2,4-дисульфид 2,4-бис-(4-метоксифенил)-1,3-дитиа-2,4-дифосфетана [реагент Лоуссона, CAS 19172-47-5], в инертном по отношению к реакции растворителе, например, таком как тетрагидрофуран или 1,4-диоксан и т.п., в таких температурных условиях, как, например, нагревание реакционной смеси при температуре от 50 до 70 С, например, в течение 50-240 мин. Амидиновые производные на приведенной выше схеме реакции можно подходящим способом получать из соответствующих тиоамидных производных описанными ниже известными в данной области способами преобразования тиоамида в амидин (этап реакции А). Указанное преобразование можно подходящим способом проводить посредством обработки указанных тиоамидов источником аммиака, например, таким как хлорид аммония или водный аммиак, в подходящем инертном по отношению к реакции растворителе, например, таком как вода или метанол и т.п., в таких температурных условиях, как,например, нагревание реакционной смеси при температуре от 60 до 80 С, например, в течение 6-24 ч. Экспериментальный способ 17. Промежуточные соединения формулы (XXVIII) в основном можно получать в соответствии с этапами реакций, представленными на схеме реакции (17) ниже. Схема реакции 17 В: преобразование амида в тиоамид (тионирование) Л: связывание по типу Сузуки М: гидрирование Тиоамидные производные на приведенной выше схеме реакции (17) можно получать из амидных производных описанными ниже известными в данной области способами тионирования (этап реакции В). Указанное преобразование можно подходящим способом проводить посредством обработки указанных амидов тионирующим средством, например, таким как пентасульфид фосфора или 2,4-дисульфид 2,4-бис-(4-метоксифенил)-1,3-дитиа-2,4-дифосфетана [реагент Лоуссона, CAS 19172-47-5], в инертном по отношению к реакции растворителе, например, таком как тетрагидрофуран или 1,4-диоксан и т.п., в таких температурных условиях, как, например, нагревание реакционной смеси при температуре от 50 до 70 С, например, в течение 50-240 мин. Промежуточные соединения формулы (XXIX) можно получать из промежуточных соединений формулы (XXVII-c) описанными ниже известными в данной области способами гидрирования (этап реакции М). Указанное преобразование можно проводить посредством обработки промежуточного соединения формулы (XXX) водородом в присутствии ацетата калия, катализатора, например, такого как Pd-C(10%), в инертном по отношению к реакции растворителе, например, таком как метанол. Смесь перемешивают в атмосфере водорода при подходящей температуре, как правило, комнатной температуре, в течение периода времени, требуемого для завершения реакции, как правило, в течение 1 ч. Промежуточные соединения формулы (XXX) на приведенной выше схеме реакции (17) можно получать реакцией промежуточных соединений формулы (XXX) с подходящим арилборонатом или арилбороновой кислотой в реакции по типу Сузуки (этап реакции K). Таким образом, промежуточные соединения формулы (XXVII-c) могут взаимодействовать с арилборонатом или арилбороновой кислотой в подходящем инертном по отношению к реакции растворителе, например, таком как 1,4-диоксан, этанол,или в смеси инертных растворителей, например, таких как 1,2-диметоксиэтан/вода/этанол, в присутствии подходящего основания, например, такого как водные K3PO4, Na2CO3 или Cs2CO3, катализатора комплекса Pd, например, такого как [1,1'-бис(дифенилфосфино)ферроцен]дихлорпалладий(II) [CAS 7228726-4] или диацетат транс-бис(дициклогексиламин)палладия [DAPCy, CAS 628339-96-8], или тетракис(трифенилфосфин)палладий (0) [CAS 14221-01-3], в таких температурных условиях, как, например, нагревание реакционной смеси при 80 С, например, в течение периода времени от 2 до 20 ч, или например,нагревание реакционной смеси при 130 С, например, в течение 10 мин при микроволновом излучении. Экспериментальный способ 18. Промежуточные соединения формул (XXVII-a), (XXVII-b) и (XXVII-c) в основном можно получать в соответствии с этапами реакций, представленными на схеме реакции (18) ниже.R: замыкание кольца Промежуточные соединения формул (XXVII-a) и (XXVII-b) на приведенной выше схеме реакции(18) можно получать из промежуточных соединений формул (XXVIII-a) и (XXVIII-b) описанными ниже известными в данной области способами фторирования (этап реакции N). Указанное преобразование можно проводить посредством обработки промежуточных соединений формул (XXVIII-a) и (XXVIII-b) в присутствии фторирующего средства, например, такого как трифторид диэтиламиносеры (DAST) в подходящем инертном по отношению к реакции растворителе, например, таком как дихлорметан. Реакционную смесь перемешивают при подходящей температуре, например, 0 С, в течение периода времени, требуемого для завершения реакции, например, 20-40 мин. Промежуточное соединение формулы (XXVII-c) на приведенной выше схеме реакции (18) можно получать из промежуточных соединений формулы (XXVIII-a) описанными ниже известными в данной области способами хлорирования (этап реакции О). Указанное преобразование можно проводить посред- 17021240 ством обработки промежуточного соединения формулы (XXVII-а) подходящим хлорирующим средством, например, таким как тионилхлорид, в присутствии основания, например, такого как пиридин, в инертном по отношению к реакции растворителе, например, таком как дихлорметан. Реакционную смесь перемешивают при подходящей температуре, например, 0 С, в течение периода времени, требуемого для завершения реакции, например, 30-60 мин. Промежуточные соединения формулы (XXVIII-a) на приведенной выше схеме реакции (18) можно получать из промежуточных соединений формулы (XXXIII) описанными ниже известными в данной области способами трифторметилирования (этап реакции Р). Указанное преобразование можно проводить посредством обработки промежуточного соединения формулы (XXIII) в присутствии фторида тетрабутиламмония (TBAF), трифторметилирующим средством, например, таким как (трифторметил)триметилсилан, в подходящем инертном по отношению к реакции растворителе, например, таком как тетрагидрофуран. Реакционную смесь перемешивают при подходящей температуре, например, комнатной температуре, в течение периода времени, требуемого для завершения реакции, например, двух часов. Промежуточные соединения формулы (XXVIII-b) на приведенной выше схеме реакции (18) можно получать из промежуточных соединений формулы (XXXIII) описанными ниже известными в данной области способами восстановления (этап реакции Q). Указанное преобразование можно проводить посредством обработки промежуточного соединения формулы (XXXIII) восстановителем, например, таким как гидрид диизобутилалюминия, в подходящем инертном по отношению к реакции растворителе, например,таком как тетрагидрофуран. Реакционную смесь перемешивают при подходящей температуре, как правило, от -78 С до комнатной температуры, в течение периода времени, требуемого для завершения реакции, например, двух часов. Промежуточные соединения формулы (XXXIII) на приведенной выше схеме реакции (18) можно получать из промежуточных соединений формулы (XXXIV) описанными ниже известными в данной области способами двухэтапного замыкания кольца (этап реакции R). Указанное преобразование можно проводить сначала посредством обработки промежуточных соединений формулы (XXXIV) промежуточным соединением формулы (X) , например, таким как хлорацетилхлорид, в присутствии основания, например, такого как NaOH, в подходящей смеси инертных растворителей, например, таких как вода и 1,4 диоксан или вода и ТГФ. рН реакционной смеси доводят до подходящего значения рН, например, 10-11,добавляя подходящее основание, например, такое как NaOH. Реакционную смесь перемешивают при подходящей температуре, например, от 0 до 25 С, в течение периода времени, требуемого для завершения реакции, например, 1-4 ч. Затем полученный неочищенный осадок можно преобразовывать в цикл,получая промежуточное соединение (XXXIII), добавляя подходящее основание, например, такое какK2CO3, Cs2CO3, N,N-диизопропилэтиламин или NaHCO3, в подходящем инертном по отношению к реакции растворителе, например, таком как ацетонитрил или ДМФА. Реакционную смесь перемешивают в таких температурных условиях, как, например, нагревание реакционной смеси при температуре от 25 до 80 С в течение 2-24 ч или, например, нагревание реакционной смеси при 140 С в течение 15-30 мин при микроволновом излучении. Это преобразование также можно проводить в отсутствие основания в подходящем инертном по отношению к реакции растворителе, например, таком как ацетонитрил или ДМФА, при подходящей температуре, как правило, от 40 до 110 С, в течение периода, например, 24-48 ч. Экспериментальный способ 19.S: присоединение по Гриньяру с последующим восстановлением Промежуточное соединение формулы (XV-d) на приведенной выше схеме реакции (19), где R3 и R4 представляют собой Н, a R5 представляет собой C1-3-алкил или циклопропил, можно получать из промежуточных соединений формулы (XXXV), где R представляет собой C1-4-алкил, посредством присоединения по Гриньяру с последующим восстановлением карбоксильной группы до соответствующей спиртовой функциональной группы (этап реакции S). Указанное преобразование можно проводить посредством обработки промежуточного соединения формулы (XXXV) подходящим реактивом Гриньяра, например,таким как бромид метилмагния, в инертном по отношению к реакции растворителе, например, таком как ТГФ. Реакционную смесь перемешивают при подходящей температуре, например, -10 С, в течение периода времени, требуемого для расходования исходного вещества, например один час. Затем добавляют восстановитель, например, такой как гидрид алюминия лития, и реакционную смесь медленно нагревают до 0 С и перемешивают в течение периода времени, требуемого для завершения реакции восстановле- 18021240 ния, как правило, 1 ч. Промежуточные соединения формулы (XXXV) на приведенной выше схеме реакции (19) можно получать взаимодействием между промежуточным соединением формулы (XXXVI) и третбутилсульфинамидом (этап реакции Т) в подходящем инертном по отношению к реакции растворителе,например, таком как гептан, в присутствии тетраэтоксида титана в таких температурных условиях, как,например, нагревание реакционной смеси при 80 С, например, в течение периода 2 ч. На схеме реакции (19) R определен как C1-4-алкил, а все другие переменные определены, как в формуле (I), R3 и R4 представляют собой Н, R5 представляет собой C1-3-алкил или циклопропил, a W представляет собой галоген. Промежуточные соединения формулы (XXXVI) являются коммерчески доступными или их можно синтезировать известными в данной области реакционными способами. Экспериментальный способ 20.W: присоединение по Гриньяру Промежуточные соединения формулы (XV-e) на приведенной выше схеме реакции (20), где R3 и R4 представляют собой водород, a R5 представляет собой CF3, можно получать из промежуточных соединений формулы (XXXIX) известными в данной области реакциями гидролиза карбаматной функциональной группы (этап реакции U). Указанное преобразование можно проводить посредством обработки промежуточного соединения формулы (XXXIX) водным основанием, например, таким как гидроксид натрия(50% в воде), в инертном по отношению к реакции растворителе, например, таком как этанол, при подходящей температуре, как правило, при кипячении с обратным холодильником в течение периода времени, требуемого для завершения реакции, например, 24 ч. Промежуточные соединения формулы (XXXIX) на приведенной выше схеме реакции (20), где R5 представляет собой CF3, можно получать из промежуточного соединения формулы (XXXVIII) посредством восстановления эфира карбоновой кислоты с последующим замыканием кольца в основных условиях (этап реакции V). Указанное преобразование можно проводить посредством обработки промежуточного соединения формулы (XXXVIII) восстановителем, например, таким как гидрид алюминия лития, в инертном по отношению к реакции растворителе, например, таком как ТГФ. Реакционную смесь перемешивают при подходящей температуре, например, 0 С, в течение периода времени, требуемого для расходования исходного вещества, например, 24 ч. Затем после выделения продукта реакции неочищенное вещество повторно растворяют в инертном по отношению к реакции растворителе, например, таком как этанол, и гидролизуют водным неорганическим основанием, таким как гидроксид натрия, при подходящей температуре, как правило, при кипячении с обратным холодильником, в течение периода времени,требуемого для завершения реакции, как правило, в течение 1 ч. Промежуточные соединения формулы (XXXVIII) на приведенной выше схеме реакции (20) можно получать из промежуточных соединений формулы (XXXVII) известными в данной области реакциями присоединения Гриньяра (этап реакции W). Указанное преобразование можно проводить посредством обработки промежуточного соединения формулы (XXXVII) подходящим арильным реактивом Гриньяра,например, таким как бромид 3-хлорфенилмагния, в инертном по отношению к реакции растворителе,например, таком как тетрагидрофуран. Реакционную смесь перемешивают при подходящей температуре,как правило, от -78 С до комнатной температуры, в течение периода времени, требуемого для завершения реакции, например двух часов. На схеме реакции (20) все переменные определены как в формуле (I), R3 и R4 представляют собой 5 Н, R представляет собой CF3, a W представляет собой галоген. Промежуточные соединения формулы (XXXVII) являются коммерчески доступными (например,CAS 128970-26-3) или их можно синтезировать описанными ниже известными в данной области способами из литературы.X: гидролиз сложного эфира и удаление сульфинильной группыY: присоединение по Гриньяру Промежуточное соединение формулы (XXXIV) на приведенной выше схеме реакции (21), где R5 представляет собой C1-3-алкил или циклопропил, можно получать из промежуточных соединений формулы (ХХХХ), где R определен как C1-4-алкил, известными в данной области реакциями гидролиза функциональной группы эфира карбоновой кислоты, с последующим удалением сульфинильной группы (этап реакции X). Указанное преобразование можно проводить посредством обработки промежуточного соединения формулы (ХХХХ) водным основанием, например, таким как гидроксид натрия (1 М в воде), в инертном по отношению к реакции растворителе, например, таком как метанол, при подходящей температуре, как правило, при кипячении с обратным холодильником в течение периода времени, требуемого для завершения реакции, например, 4 ч. Затем проводят удаление сульфинильной группы посредством добавления подходящего инертного растворителя, например, такого как 1,4-диоксан, в присутствии подходящей кислоты, например, такой как соляная кислота, при комнатной температуре в течение периода времени, требуемого для завершения реакции, например, 30 мин. Промежуточное соединение формулы (ХХХХ) на приведенной выше схеме реакции (21), где R5 представляет собой C1-3-алкил или циклопропил, можно получать из промежуточных соединений формулы (XXXXI) посредством присоединения по Гриньяру (этап реакции Y). Указанное преобразование можно проводить посредством обработки промежуточного соединения формулы (XXXXI) подходящим реактивом Гриньяра, например, таким как бромид циклопропилмагния, в инертном по отношению к реакции растворителе, например, таком как дихлорметан. Реакционную смесь перемешивают при подходящей температуре, например, -40 С, в течение периода времени, требуемого для расходования исходного вещества, например одного часа. На схеме реакции (21) R определен как C1-4-алкил, а все другие переменные определены как в формуле (I), R5 представляет собой C1-3-алкил или циклопропил, a W представляет собой галоген. Промежуточные соединения формулы (XXXXI) можно синтезировать известными в данной области способами, такими как способы, описанные на схеме реакции (19) (этап реакции Т). Экспериментальный способ 22. Соединения формулы (I-b) в основном можно получать в соответствии с этапами реакций, представленными на схеме реакции (22) ниже.K: связывание по типу СузукиZ: преобразования галогенида в сложный боронатный эфир АА: защита амида Соединения формулы (I-b) можно получать из промежуточного соединения формулы (XXXXIV) способом с двумя этапами (этапы А и В), как описано в экспериментальных способах 9 (этап В) и 1 (этап А). Промежуточные соединения формулы (XXXXIV) на приведенной выше схеме реакции (22) можно получать из промежуточного соединения формулы (XXXXV), где Z1 представляет собой подходящую защитную группу амида, например, такую как п-метоксибензильная группа, описанными ниже известными в данной области способами снятия защиты с N-группы амидов такими, как способы, описанные на схеме реакции (14) (этап реакции G). Промежуточные соединения формулы (XXXXV) на приведенной выше схеме реакции (22) можно получать из промежуточного соединения формулы (XXXXVI) с использованием подходящего арилгалогенида описанными ниже известными в данной области способами связывания по типу Сузуки, такими как способы, описанные на схеме реакции (16) (этап реакции K). Промежуточные соединения формулы (XXXXVI) на приведенной выше схеме реакции (22) можно получать из промежуточного соединения формулы (XXXXVII) описанными ниже известными в данной области способами преобразования галогенида в сложный боронатный эфир (этап реакции Z). Указанное преобразование можно проводить посредством обработки промежуточного соединения формулы(XXXXVII), например, тетра(алкоксо)дибором, например, таким как бис(пинаколато)дибор [CAS 7318334-3], в подходящем инертном по отношению к реакции растворителе, например, таком как 1,4-диоксан,или в смеси инертных растворителей, например, такой как ДМФА и 1,4-диоксан, в присутствии подходящего основания, например, такого как КОАс, катализатора комплекса Pd, например, такого как [1,1'бис(дифенилфосфино)ферроцен]дихлорпалладий(II) [CAS 72287-26-4] в таких температурных условиях,как, например, нагревание реакционной смеси при 150 С, например, в течение 20 мин при микроволновом излучении. Промежуточные соединения формулы (XXXXVII) на приведенной выше схеме реакции (22), где Z1 представляет собой подходящую защитную группу амида, например, такую как п-метоксибензильная группа, можно получать из промежуточных соединений формул (ХIII-а), (XXXVII-a), (XXXVII-b) или(XXVII-c) описанными ниже известными в данной области способами защиты амида амидов (этап реакции АА). Указанное преобразование можно проводить посредством обработки промежуточного соединения формулы (XIII-а) защитной группой N-PMB, например, такой как 4-метоксибензилхлорид, в под- 21021240 ходящем инертном по отношению к реакции растворителе, например, таком как ДМФА, в присутствии подходящего основания, например, такого как гидрид натрия, при комнатной температуре в течение периода времени, требуемого для завершения реакции, например, 3 ч. На схеме реакции (22) все переменные определены, как в формуле (I), R5 представляет собой C1-3 алкил или циклопропил, а W представляет собой галоген. Экспериментальный способ 23. Промежуточное соединение формулы (XXXIII), где X2 и X4 представляют собой СН, и где один из 1X или X3 представляют собой N, а другой представляет собой СН, так называемое промежуточное соединение формулы (XXXXVII), в основном можно получать в соответствии с этапами реакций, представленными на схеме реакции (23) ниже.AD: алкилирование Промежуточное соединение формулы (XXXXVII) на приведенной выше схеме реакции (23) можно получать из промежуточного соединения формулы (XXXXVI) описанными ниже известными в данной области способами замыкания кольца (этап реакции АВ). Указанное преобразование можно проводить посредством обработки промежуточного соединения формулы (XXXXVI) подходящим конденсирующим средством, например, таким как гексафторфосфат О-(7-азабензотриазол-1-ил)-N,N,N',N'тетраметилурония [HATU, CAS 148893-10-1] или хлорид 4-(4,6-диметокси-1,3,5-триазин-2-ил)-4 метилморфолина [DMTMM, CAS 3945-69-5], в подходящем инертном по отношению к реакции растворителе, например, таком как диметилформамид, в присутствии подходящего основания, например, такого как диизопропилэтиламин, при подходящей температуре, как правило, при комнатной температуре, в течение периода времени, требуемого для завершения реакции, например 15-60 мин. Промежуточное соединение формулы (XXXXVI) на приведенной выше схеме реакции (23), где один из X1 или X3 представляет собой N, а другой представляет собой СН, можно получать из промежуточного соединения формулы (XXXXV), где R11 определен как алкильная или бензильная группа, например, такая как трет-бутильная группа, описанными ниже известными в данной области способами гидролиза сложноэфирной функциональной группы (этап реакции АС). Указанное преобразование можно проводить посредством обработки промежуточного соединения формулы (XXXXV) подходящей кислотой, например, такой как трифторуксусная кислота, в инертном по отношению к реакции растворителе, например, таком как дихлорметан, при подходящей температуре, как правило, при комнатной температуре, в течение периода времени, требуемого для завершения реакции, например, 15-60 мин. Промежуточное соединение формулы (XXXXV) на приведенной выше схеме реакции (23), где один из X1 или X3 представляет собой N, а другой представляет собой СН, можно получать из соответствующего промежуточного соединения формулы (XXXXIII) описанными ниже известными в данной области способами алкилирования кислотной функциональной группы (этап реакции AD). Указанное преобразование можно подходящим способом проводить посредством обработки промежуточного соединения формулы (XXXXIII) промежуточным соединением формулы (XXXXIV), например, таких как третбутилхлорацетат в присутствии основания, например, такого как K2CO3 или Cs2CO3, и подходящего инертного по отношению к реакции растворителя, например, такого как ацетонитрил или ДМФА. Реакционную смесь перемешивают при подходящей температуре, как правило, при комнатной температуре, в течение периода времени, требуемого для завершения реакции, например, 2-6 ч. На схеме реакции (23) все переменные определены как в формуле (I), и один из X1 или X3 представляет собой N, а другой представляет собой CH. R11 может представлять собой C1-6-алкил или бензил. Экспериментальный способ 24. Соединения формулы (LVI), где один из X1 или X3 представляет собой N, а другой представляет собой СН, в основном можно получать в соответствии с этапами реакций, представленными на схеме реакции (24) ниже.P: трифторметилирование О: хлорирование Соединения формулы (LVI) на приведенной выше схеме реакции (24) можно получать из промежуточного соединения формулы (LV), где Z1 представляет собой подходящую амидиновую защитную группу, например, такую как группа N-Boc, описанными ниже известными в данной области способами снятия защиты с N-группы (этап реакции АЕ). Указанное преобразование можно подходящим способом проводить посредством обработки промежуточного соединения формулы (LV) в присутствии подходящей кислоты, например, такой как трифторуксусная кислота, в подходящем инертном по отношению к реакции растворителе, например, дихлорметане, при комнатной температуре, например, в течение периода от 15 мин до 2 ч. Промежуточное соединение формулы (LV) на приведенной выше схеме реакции (24) можно получать из промежуточного соединения формулы (LIV), описанными ниже известными в данной области способами связывания (этап реакции AF). Указанное преобразование можно подходящим способом проводить взаимодействием промежуточного соединения формулы (LIV) с промежуточным соединением формулы (V) в подходящем инертном по отношению к реакции растворителе, например, таком как метанол, в присутствии конденсирующего средства, например, такого как хлорид 4-(4,6-диметокси-1,3,5 триазин-2-ил)-4-метилморфолина [DMTMM, CAS 3945-69-5], при подходящей температуре, например,такой как 25 С, в течение периода времени, требуемого для расходования исходного вещества, например, 2-6 ч. Промежуточное соединение формулы (LIV) на приведенной выше схеме реакции (24), где Z1 представляет собой подходящую амидиновую защитную группу, например, такую как группа N-Boc, можно получать из промежуточных соединений формулы (LIII) описанными ниже известными в данной области способами защиты N-группы (этап реакции L). Указанное преобразование можно подходящим способом проводить посредством обработки указанных промежуточных соединений формулы (LIII) подходящей защитной группы для N-группы, например, такой как ди-трет-бутилдикарбонат, в присутствии основания, например, такого как диизопропилэтиламин или триэтиламин, в подходящем инертном растворителе, таком как ТГФ, перемешивая реакционную смесь при подходящей температуре, например, такой как 25 С, в течение периода времени, требуемого для расходования исходного вещества. Промежуточное соединение формулы (LIII) на приведенной выше схеме реакции (24) можно получать из промежуточного соединения формулы (L), где W представляет собой галоген, трехэтапным (эта- 23021240 пы F, А и В) способом, как описано в экспериментальных способах 13 (этап F), 9 (этап В) и 1 (этап А). Промежуточное соединение формулы (L) на приведенной выше схеме реакции (24) можно получать из промежуточного соединения формулы (XXXXIX) описанными ниже известными в данной области способами восстановительного дегалогенирования (этап реакции AG). Указанное преобразование можно проводить посредством обработки промежуточного соединения формулы (XXXXIX) подходящим восстановителем, например, таких как цинковая пыль и уксусная кислота, при подходящей температуре,например, 80 С, в течение периода времени, требуемого для достижения завершения времени реакции,например 1-12 ч. Промежуточное соединение формулы (XXXXIX) на приведенной выше схеме реакции (24) можно получать из промежуточного соединения формулы (XXXXVII) двухэтапным (этапы Р и О) способом, как описано в экспериментальном способе 17 (этапы Р и О). На схеме реакции (24) все переменные определены как в формуле (I), и один из X1 или X3 представляет собой N, а другой представляет собой СН. Экспериментальный способ 25. Соединения формулы (LXIV), где один из X1 или X3 представляет собой N, а другой представляет собой СН, в основном можно получать в соответствии с этапами реакций, представленными на схеме реакции (25) ниже.Q: восстановление Соединения формулы (LXIV) на приведенной выше схеме реакции (25) можно получать из промежуточного соединения формулы (LXI) трехэтапным способом (этапы AD, АЕ и L), как описано в экспериментальном способе 24 (этапы АЕ, AF и L). Промежуточное соединение формулы (LXI) на приведенной выше схеме реакции (25) можно получать из промежуточного соединения формулы (LVIII), где W представляет собой галоген трехэтапным(этапы F, А и В) способом, как описано в экспериментальных способах 13 (этап F), 9 (этап В) и 1 (этап А). Промежуточное соединение формулы (LVIII) на приведенной выше схеме реакции (25) можно получать из промежуточного соединения формулы (XXXXVIII) двухэтапным (этапы N и Q) способом, как описано в экспериментальном способе 18 (этапы N и Q). На схеме реакции (25) все переменные определены как в формуле (I), и один из X1 или X3 представляет собой N, а другой представляет собой СН. Фармакология Соединения по настоящему изобретению и их фармацевтически приемлемые композиции ингиби- 24021240 руют ВАСЕ, и таким образом, они могут быть пригодными при лечении или предотвращении болезни Альцгеймера (AD), умеренного когнитивного нарушения (MCI), старости, деменции, деменции с тельцами Леви, церебральной амилоидной ангиопатии, мультиинфарктной деменции, синдрома Дауна, деменции, ассоциированной с болезнью Паркинсона, и деменции, ассоциированной с бета-амилоидом. Изобретение относится к соединению общей формулы (I), к форме его стереоизомера или к его фармацевтически приемлемым солям присоединения кислот или оснований или сольватам для применения в качестве лекарственного средства. Изобретение также относится к соединению общей формулы (I), к форме его стереоизомера или к его фармацевтически приемлемым солям присоединения кислот или оснований или сольватам для применения в лечении или предотвращении заболеваний или состояний, выбранных из группы, состоящей из AD, MCI, старости, деменции, деменции с тельцами Леви, церебральной амилоидной ангиопатии,мультиинфарктной деменции, синдрома Дауна, деменции, ассоциированной с болезнью Паркинсона, и деменции, ассоциированной с бета-амилоидом. Изобретение также относится к применению соединения общей формулы (I), формы его стереоизомера или фармацевтически приемлемых солей присоединения кислот или оснований или сольватов для получения лекарственного средства для лечения или предотвращения любого из болезненных состояний,указанных выше в настоящем документе. Принимая во внимание полезность соединения формулы (I), предоставлен способ лечения теплокровных животных, включая людей, страдающих любым из заболеваний, указанных выше в настоящем документе, или способ предотвращения у теплокровных животных, включая людей, заболевания любым из заболеваний, указанных выше в настоящем документе. Указанные способы включают введение, т.е. системное или местное введение, предпочтительно пероральное введение, эффективного количества соединения формулы (I), формы его стереоизомера, его фармацевтически приемлемых солей присоединения или сольватов, теплокровному животному, включая человека. Способ лечения также может включать введение активного ингредиента по схеме лечения от одного до четырех приемов в сутки. В этих способах лечения соединения по изобретению предпочтительно формулируют до введения. Как описано в настоящем документе ниже, подходящие фармацевтические составы получают известными способами с использованием хорошо известных и легкодоступных ингредиентов. Соединения по настоящему изобретению, которые могут подходить для лечения или предотвращения болезни Альцгеймера или ее симптомов, можно вводить отдельно или в комбинации с одним или несколькими дополнительными терапевтическими средствами. Комбинированное лечение включает введение одного фармацевтического лекарственного препарата, содержащего соединение формулы (I) и одного или нескольких дополнительных терапевтических средств, а также введение соединения формулы(I) и каждого из дополнительных терапевтических средств в его собственном отдельном фармацевтическом лекарственном препарате. Например, соединение формулы (I) и терапевтическое средство можно вводить пациенту вместе в одной пероральной композиции, такой как таблетка или капсула, или каждое средство можно вводить в отдельных пероральных лекарственных препаратах. Фармацевтические композиции Настоящее изобретение также относится к композиции для предотвращения или лечения заболеваний, при которых благоприятным является ингибирование бета-секретазы, таких как болезнь Альцгеймера (AD), умеренное когнитивное нарушение, старость, деменция, деменция с тельцами Леви, синдром Дауна, деменция, ассоциированная с инсультом, деменция, ассоциированная с болезнью Паркинсона, и деменция, ассоциированная с бета-амилоидом. Указанные композиции содержат терапевтически эффективное количество соединения формулы (I) и фармацевтически приемлемый носитель или разбавитель. Хотя активный ингредиент можно вводить отдельно, его предпочтительно предоставлять в виде фармацевтической композиции. Таким образом, настоящее изобретение дополнительно относится к фармацевтической композиции, содержащей соединение по настоящему изобретению вместе с фармацевтически приемлемым носителем или разбавителем. Носитель или разбавитель должен быть "приемлемым" в смысле совместимости с другими ингредиентами композиции и отсутствия вреда для его реципиентов. Фармацевтические композиции по настоящему изобретению можно получать любыми способами,хорошо известными в области фармации. Терапевтически эффективное количество конкретного соединения в форме основания или в форме соли присоединения в качестве активного ингредиента комбинируют в однородной смеси с фармацевтически приемлемым носителем, который может принимать широкое разнообразие форм в зависимости от формы препарата, желательной для введения. Эти фармацевтические композиции желательны в стандартной лекарственной форме, предпочтительно подходящей для системного введения, такого как пероральное, чрескожное или парентеральное введение; или местного введения, такого как посредством ингаляции, нозального спрея, глазных капель или посредством крема,геля, шампуня или т.п. Например, при получении композиции в пероральной лекарственной форме можно использовать любые из общепринятых фармацевтических сред, например, таких как вода, гликоли,- 25021240 масла, спирты и т.п. в случае жидких пероральных препаратов, таких как суспензии, сиропы, эликсиры и растворы; или твердых носителей, таких как крахмалы, сахара, каолин, смазочные средства, связывающие средства, дезинтегрирующие средства и т.п. в случае порошков, пилюль, капсул и таблеток. Вследствие простоты их введения, таблетки и капсулы представляют собой наиболее предпочтительную пероральную стандартную лекарственную форму, в случае чего, очевидно, используют твердые фармацевтические носители. Для парентеральных композиций, носитель, как правило, включает стерильную воду,по меньшей мере в большей части, хотя могут быть включены другие ингредиенты, например, для содействия растворимости. Например, можно получать инъецируемые растворы, в которых носитель содержит физиологический раствор, раствор глюкозы или смесь физиологического раствора и раствора глюкозы. Также можно получать инъецируемые суспензии, в случае чего можно использовать подходящие жидкие носители, суспендирующие средства и т.п. В композициях, подходящих для чрескожного введения, носитель необязательно содержит увеличивающее проницаемость средство и/или подходящее смачивающее средство, необязательно комбинируемые с подходящими добавками любой природы в незначительных пропорциях, которые не оказывают какого-либо значительного вредного воздействия на кожу. Указанные добавки могут облегчать введение в кожу и/или могут быть полезными для получения желаемых композиций. Эти композиции можно вводить различными способами, например, в виде трансдермального пластыря, в виде средства для точечного нанесения или в виде мази. Для простоты введения и единообразия дозирования особенно предпочтительно формулировать указанные выше фармацевтические композиции в стандартную лекарственную форму. Как применяют в описании и формуле изобретения настоящего документа, стандартная лекарственная форма относится к физически дискретным единицам, подходящим в качестве единичных доз, где каждая единица содержит предопределенное количество активного ингредиента, рассчитанного так, чтобы оказывать желаемое терапевтическое действие, в ассоциации с требуемым фармацевтическим носителем. Примерами таких стандартных лекарственных форм являются таблетки (включая таблетки с насечками или покрытые таблетки), капсулы, пилюли, пакеты с порошками, пластинки, инъецируемые растворы или суспензии, чайные ложки, столовые ложки и т.п., и их раздельные многократные дозы. Как хорошо известно специалистам в данной области, точная доза и частота введения зависит от конкретного используемого соединения формулы (I), конкретного состояния, подвергаемого лечению,тяжести состояния, подвергаемого лечению, возраста, массы, пола, степени нарушения и общего физического состояния конкретного пациента, а также другого лекарственного средства, которое может принимать индивидуум. Кроме того, очевидно, что указанное эффективное суточное количество можно уменьшать или увеличивать в зависимости от реакции подвергаемого лечению индивидуума и/или в зависимости от оценки лечащего врача, предписывающего соединения по настоящему изобретению. В зависимости от способа введения фармацевтические композиция содержат от 0,05 до 99 мас.%,предпочтительно от 0,1 до 70 мас.%, более предпочтительно от 0,1 до 50 мас.% активного ингредиента и от 1 до 99,95 мас.%, предпочтительно от 30 до 99,9 мас.%, более предпочтительно от 50 до 99,9 мас.% фармацевтически приемлемого носителя, где все проценты указаны от общей массы композиции. Соединения по настоящему изобретению можно использовать для системного введения, такого как пероральное, чрескожное или парентеральное введение; или местного введения, так как посредством ингаляции, назального спрея, глазных капель или посредством крема, геля, шампуня или т.п. Соединения предпочтительно вводить перорально. Как хорошо известно специалистам в данной области, точная доза и частота введения зависят от конкретного используемого соединения формулы (I), конкретного состояния, подвергаемого лечению, тяжести состояния, подвергаемого лечению, возраста, массы, пола, тяжести нарушения и общего физического состояния конкретного пациента, а также другого лекарственного средства, которое может принимать индивидуум. Кроме того, очевидно, что указанное эффективное суточное количество можно уменьшать или увеличивать в зависимости от реакции подвергаемого лечению индивидуума и/или в зависимости от оценки лечащего врача, предписывающего соединения по настоящему изобретению. Количество соединения формулы (I), которое можно комбинировать с веществом носителя для получения единичной лекарственной формы варьирует в зависимости от подвергаемого лечению заболевания, вида млекопитающего и конкретного способа введения. Однако в качестве общего руководства,подходящие стандартные дозы для соединений по настоящему изобретению, например, могут предпочтительно содержать от 0,1 до приблизительно 1000 мг активного соединения. Предпочтительная стандартная доза составляет от 1 до приблизительно 500 мг. Более предпочтительная стандартная доза составляет от 1 до приблизительно 300 мг. Еще более предпочтительная стандартная доза составляет от 1 до приблизительно 100 мг. Такие стандартные дозы можно вводить более одного раза в сутки, например,2, 3, 4, 5 или 6 раз в сутки, но предпочтительно 1 или 2 раза в сутки так, чтобы общая доза для взрослого массой 70 кг находилась в диапазоне от 0,001 до приблизительно 15 мг на кг массы индивидуума на введение. Предпочтительная доза составляет от 0,01 до приблизительно 1,5 мг на кг массы индивидуума на введение, и такое лечение можно продолжать в течение нескольких недель или месяцев, и в некоторых случаях, лет. Однако следует понимать, что указанный уровень дозирования для каждого конкретного пациента зависит от множества факторов, включая активность конкретного используемого соединения; возраст, массу тела, общее состояние здоровья, пол и диету индивидуума, подвергаемого лечению; времени и пути введения; скорости выведения; других лекарственных средств, которые вводили ранее; и тяжести конкретного заболевания, подвергаемого лечению, как хорошо понятно специалистам в данной области. Типичная доза может представлять собой таблетку от 1 до приблизительно 100 мг или от 1 до приблизительно 300 мг, принимаемую один раз в сутки или несколько раз в сутки, или одну капсулу или таблетку с задержанным высвобождением, принимаемые один раз в сутки и содержащие пропорционально более высокое количество активного ингредиента. Эффект задержанного высвобождения можно получать посредством веществ для капсул, которые растворяются при различных значениях рН, посредством капсул с медленным высвобождением вследствие осмотического давления, или посредством любых других известных средств контролируемого высвобождения. Как понимают специалисты в данной области, в некоторых случаях необходимым может являться использование доз вне этих диапазонов. Кроме того, следует отметить, что клиницист или лечащий врач должны знать как и когда начинать, прерывать, регулировать или прекращать лечение в зависимости от индивидуальной реакции пациента. Для композиций, способов и наборов, предоставленных выше, специалисту в данной области понятно, что предпочтительными соединениями для применения в каждой из них являются соединения,которые отмечены как предпочтительные выше. Дополнительными предпочтительными соединениями для композиций, способов и наборов являются соединения, предоставленные в неограничивающих примерах ниже. Экспериментальная часть Далее в настоящем документе термин "т.пл." означает температуру плавления, "водн." означает водный, "реакц. смесь" означает реакционную смесь, "комн. темп." означает комнатную температуру,"DIPEA" означает N,N-диизопропилэтиламин, "DIPE" означает диизопропиловый эфир, "ТГФ" означает тетрагидрофуран, "ДМФА" означает диметилформамид, "ДХМ" означает дихлорметан, "EtOH" означает этанол, "EtOAc" означает этилацетат, "АсОН" означает уксусную кислоту, "iPrOH" означает изопропанол, iPrNH2" означает изопропиламин, "MeCN" означает ацетонитрил, "МеОН" означает метанол,"Pd(OAc)2" означает диацетат палладия(II), "рац" означает рацемический, "насыщ." означает насыщенный, "SFC" означает хроматографию в суперкритической жидкости, "SFC/MC" означает хроматографию в суперкритической жидкости/масс-спектрометрию, "ЖХ/МС" означает жидкостную хроматографию/масс-спектрометрию, "ГХ/МС" означает газовую хроматографию/масс-спектрометрию, "ВЭЖХ" означает высокоэффективную жидкостную хроматографию, "RP" означает обратную фазу, "СЭЖХ" означает сверхэффективную жидкостную хроматографию, "Rt" означает время удержания (в минутах),"[М+Н]+" означает массу протонированного свободного основания соединения, "DAST" означает трифторид диэтиламиносеры, "DMTMM" означает хлорид 4-(4,6-диметокси-1,3,5-триазин-2-ил)-4 метилморфолина,"HATU" означает гексафторфосфатO-(7-азабензотриазол-1-ил)-N,N,N',N'тетраметилурония, "ксантфос" означает (9,9-диметил-9 Н-ксантен-4,5-диил)бис[дифенилфосфин],"ТВАТ" означает тетрабутиламмонийтрифенилдифторсиликат, "TFA" означает трифторуксусную кислоту, "Et2O" означает диэтиловый эфир, "ДМСО" означает диметилсульфоксид. Для ключевых промежуточных соединений, а также для некоторых конечных соединений, устанавливали абсолютную конфигурацию хиральных центров (указанную как R и/или S), сравнивая с образцами с известной конфигурацией или используя аналитические способы, подходящие для определения абсолютной конфигурации, таких как VCD (колебательный круговой дихроизм) или рентгеноструктурная кристаллография. А. Получение промежуточных соединений Пример А 1. Получение промежуточного соединения 1: рац-2-амино-2-(3-бромфенил)пропионитрилаNH3/MeOH (400 мл) добавляли триметилсилилцианид (20 г, 200 ммоль). Смесь перемешивали при комнатной температуре в течение 4 суток. Затем растворитель выпаривали в вакууме и остаток помещали вEtOAc (100 мл). Твердое вещество фильтровали и фильтрат выпаривали в вакууме с выходом промежуточного соединения 1 (20 г, выход 86%), которое использовали на следующем этапе без дополнительной очистки. Пример А 2. Получение промежуточного соединения 2: рац-(метилового эфира 2-амино-2-(3 бромфенил)пропионовой кислоты) Промежуточное соединение 1 (20 г, 88,9 ммоль) растворяли в НС 1/МеОН (500 мл) и смесь кипятили с обратным холодильником в течение 4 суток. После охлаждения до комнатной температуры добавляли EtOAc (100 мл) и воду (100 мл) и смесь экстрагировали EtOAc (2100 мл). Повышали основность объединенных водных слоев водным раствором аммиака до рН 8 и экстрагировали EtOAc (5100 мл). Объединенные органические слои сушили (Na2SO4), фильтровали и растворители выпаривали в вакууме с выходом рац-промежуточного соединения 2 (10,6 г, выход 46%) в виде масла. Пример A3. Получение промежуточного соединения 3: рац-2-амино-2-(3-бромфенил)пропан-1-ола К перемешиваемому раствору промежуточного соединения 2 (7,5 г, 29,1 ммоль) в ТГФ (200 мл) при-15 С по каплям добавляли гидрид алюминия лития (1M В ТГФ; 22 мл, 22 ммоль). Смесь оставляли медленно нагреваться до 0 С в течение 1 ч. Затем добавляли еще ТГФ (150 мл) и по каплям добавляли насыщенный Na2SO4 до прекращения выделения водорода. Затем добавляли безводный Na2SO4 и оставляли перемешиваться в течение ночи при комнатной температуре. Смесь фильтровали через диатомовую землю, промывали ТГФ и растворитель выпаривали в вакууме. Неочищенный продукт очищали посредством хроматографии на испарительной колонке (диоксид кремния; 7 М раствор аммиака в метаноле/ДХМ от 0/100 до 3/97). Желаемые фракции собирали и концентрировали в вакууме с выходом промежуточного соединения 3 (5,70 г, выход 85%) в виде масла. Пример А 4. Получение промежуточного соединения 4: (R)-2-амино-2-(3-бромфенил)пропан-1-ола Образец промежуточного соединения 3 (15,4 г) разделяли на соответствующие энантиомеры посредством препаративной SFC на (Chiralpak Daicel AD250 мм). В подвижной фазе (СО 2, МеОН с 0,2% iPrNH2) получали промежуточное соединение 4 (7,21 г, выход 40%).D: -14,9 (589 нм, конц. 0,2946 мас./об.%, МеОН, 20 С). Пример А 5. Получение промежуточного соединения 5: рац-5-(3-бромфенил)-5-метилморфолин-3-она К перемешиваемому раствору промежуточного соединения 3 (1,6 г, 6,95 ммоль) в ТГФ (60 мл) и диизопропилэтиламине (1,44 мл, 8,34 ммоль) при -78 С по каплям добавляли хлорацетилхлорид (0,55 мл,6,95 ммоль). Смесь перемешивали в течение 30 мин при -78 С. Затем добавляли трет-бутоксид калия(1,95 г, 17,38 ммоль) и смесь перемешивали при -15 С и оставляли нагреваться до 0 С в течение 90 мин. Смесь разбавляли насыщенным NH4Cl и экстрагировали ДХМ. Органический слой отделяли, сушили(Na2SO4), фильтровали и растворители выпаривали в вакууме. Неочищенный продукт растирали с Et2O,фильтровали и сушили с выходом промежуточного соединения 5 (1,65 г, выход 88%) в виде белого твердого вещества. Пример А 6. Получение промежуточного соединения 6: рац-5-[3-(5-метоксипиридин-3-ил)фенил]-5 метилморфолин-3-она К смеси промежуточного соединения 5 (0,5 г, 1,85 ммоль), 3-метокси-5-(4,4,5,5 тетраметил[1,3,2]диоксаборолан-2-ил)пиридина (0,87 г, 3,70 ммоль) и тетракис(трифенилфосфин)палладия (0,214 г, 0,185 ммоль) добавляли 1,4-диоксан (15 мл) и насыщенный водный Na2CO3 (5 мл). Смесь перемешивали и в течение нескольких минут продували N2, a затем нагревали при 80 С в течение 2 ч. После охлаждения смесь разбавляли водой и экстрагировали ДХМ. Органический слой отделяли, сушили (Na2SO4), фильтровали и растворители выпаривали в вакууме. Неочищенный продукт очищали посредством хроматографии на испарительной колонке (диоксид кремния; 7 М раствор аммиака в метаноле/ДХМ от 0/100 до 4/96). Желаемые фракции собирали и концентрировали в вакууме с выходом промежуточного соединения 6 (0,51 г, выход 92%) в виде грязно-белого твердого вещества. Пример А 7. Получение промежуточного соединения 7: рац-5-[3-(5-метоксипиридин-3-ил)фенил]-5 метилморфолин-3-тиона К смеси промежуточного соединения 6 (0,5 г, 1,56 ммоль) и пентасульфида фосфора (0,3 г, 1,35 ммоль) при комнатной температуре добавляли ТГФ (15 мл). Смесь перемешивали при 50 С в течение 60 мин. Смесь охлаждали до комнатной температуры и добавляли пиридин (10 мл). Смесь перемешивали при 80 С в течение 5 ч. Смесь охлаждали до комнатной температуры и фильтровали через хлопок, твердый остаток растирали со смесью ДХМ и МеОН и фильтровали через хлопок. Объединенные органические слои выпаривали в вакууме. Неочищенный продукт очищали посредством хроматографии на испарительной колонке (диоксид кремния; МеОН/ДХМ от 0/100 до 3/97). Желаемые фракции собирали и выпаривали в вакууме с выходом промежуточного соединения 7 (0,4 г, выход 82%) в виде твердого вещества. Пример А 8. Получение промежуточного соединения 8: рац-5-(3-бромфенил)-5-метилморфолин-3-тиона К смеси промежуточного соединения 5 (1,14 г, 3,92 ммоль) и пентасульфида фосфора (0,704 г, 3,17 ммоль) при комнатной температуре добавляли ТГФ (40 мл). Смесь перемешивали при 50 С в течение 50 мин. Затем смесь охлаждали до комнатной температуры и фильтровали через хлопок и выпаривали в вакууме. Неочищенный продукт очищали посредством хроматографии на испарительной колонке (диоксид кремния; ДХМ). Желаемые фракции собирали и выпаривали в вакууме с выходом промежуточного соединения 8 (1,05 г, выход 93%) в виде желтого твердого вещества. Пример А 9. Получение промежуточного соединения 9: трифторацетатной соли рац-5-(3-бромфенил)-5-метил 5,6-дигидро-2 Н-[1,4]оксазин-3-иламина Промежуточное соединение 8 (0,205 г, 0,716 ммоль) и 32% водный раствор аммиака (12 мл) пере- 29
МПК / Метки
МПК: C07D 413/04, C07D 265/30, A61P 25/28, A61K 31/5355, A61K 31/535, A61P 25/16
Метки: качестве, производные, bace, бета-секретазы, ингибиторов, 5,6-дигидро-2h-[1,4]оксазин-3-иламина
Код ссылки
<a href="https://eas.patents.su/30-21240-proizvodnye-56-digidro-2h-14oksazin-3-ilamina-v-kachestve-ingibitorov-beta-sekretazy-bace.html" rel="bookmark" title="База патентов Евразийского Союза">Производные 5,6-дигидро-2h-[1,4]оксазин-3-иламина в качестве ингибиторов бета-секретазы (bace)</a>
Предыдущий патент: Способ получения марбофлоксацина и его промежуточного соединения
Следующий патент: Оксазоло[5,4-b]пиридин-5-ильные соединения
Случайный патент: Пестициды на основе производных 5-(ациламино)пиразола