Замещенные производные триазола и имидазола в качестве модуляторов гамма-секретазы
Номер патента: 21047
Опубликовано: 31.03.2015
Авторы: Минн Гарретт Берлонд, Бертело Дидье Жан-Клод, Велтер Адриана Ингрид, Оельрих Дэниел, Бисхофф Франсуа Пол, Ван Брандт Свен Францискус Анна, Де Клейн Михел Анна Йозеф, Гейсен Хенрикус Якобус Мария, Ву Тонгфей, Суркин Михел, Питерс Серж Мария Алоисиус, Ромбаутс Фредерик Ян Рита
Формула / Реферат
1. Соединение формулы (I)
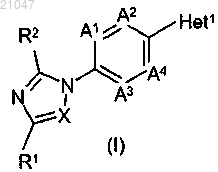
или его стереоизомерные формы, где
R1 представляет собой водород или С1-4алкил;
R2 представляет собой водород или С1-4алкил;
X представляет собой СН или N;
А1 представляет собой CR3a или N; где R3a представляет собой водород; галоген; циано; С1-4алкил или С1-4алкилокси, необязательно замещенный одним или несколькими галогеновыми заместителями;
А2 представляет собой CR3b или N, где R3b представляет собой водород, фтор или С1-4алкилокси;
каждый из А3 и А4 независимо представляет собой СН, CF или N;
при условии, что не более чем два из А1, А2, А3 и А4 представляют собой N;
Het1 представляет собой гетероцикл, имеющий формулу (а), (b) или (с)
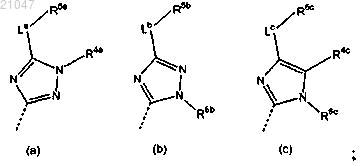
R4a представляет собой водород; тетрагидропиранил; тетрагидрофуранил; пиперидинил; морфолинил; пирролидинил; цикло-С3-7алкил; Ar1 или C1-6алкил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из группы, состоящей из галогена, гидроксила, циано, Ar1, цикло-С3-7алкила, С1-6алкилокси, С1-6алкилтио и О-Ar1;
R4c представляет собой Ar1 или С1-6алкил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена;
где в определениях R4a и R4c каждый Ar1 независимо представляет собой фенил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена;
R5a, R5b и R5c представляют собой водород; пиперидинил; морфолинил; пирролидинил; гексагидро-1H-1,4-диазепин-1-ил; 1,2,3,4-тетрагидро-2-хинолинил; 3,4-дигидро-2(1Н)-изохинолинил; 3,4-дигидро-1(2Н)-хинолинил; 2,2-дифтор-1,3-бензодиоксол-5-ил; 2,2-дифтор-1,3-бензодиоксол-4-ил; 1,6-дигидро-1-метил-6-оксо-3-пиридинил; 1,2-дигидро-1-метил-2-оксо-3-пиридинил; 2,3-дигидро-4Н-1,4-бензоксазин-4-ил; 3,4-дигидро-1,5-бензоксазепин-5(2Н)-ил; цикло-С3-7алкил; Ar2 или С1-6алкил;
где в определениях R5a, R5b и R5c пиперидинил, морфолинил, пирролидинил, гексагидро-1Н-1,4-диазепин-1-ил, 1,2,3,4-тетрагидро-2-хинолинил, 3,4-дигидро-2(1Н)-изохинолинил, 3,4-дигидро-1(2Н)-хинолинил и цикло-С3-7алкил могут быть замещены одним или несколькими заместителями, каждый из которых независимо выбран из группы, состоящей из С1-4ацила, галогена, С1-4алкилоксикарбонила, С1-4алкила, необязательно замещенного одним или несколькими галогеновыми заместителями, и
фенил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из группы, состоящей из С1-4алкила и трифторметила;
где в определениях R5a, R5b и R5c
Ar2 представляет собой фенил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из группы, состоящей из галогена, циано, NR7R8, (С=О)-NR7R8, С1-4ацила, С1-4алкилсульфонила, С1-4алкилсульфинила, тетрагидрофуранилокси, С1-4алкилокси, необязательно замещенного одним или несколькими заместителями, каждый из которых независимо выбран из группы, состоящей из галогена, гидроксила, С1-4алкилокси и циклопропила, и С1-4алкила, необязательно замещенного одним или несколькими заместителями, каждый из которых независимо выбран из группы, состоящей из галогена, гидроксила и С1-4алкилокси, необязательно замещенного одним или несколькими галогеновыми заместителями;
или Ar2 представляет собой 5- или 6-членный гетероарил, выбранный из группы, состоящей из пиразолила и пиридинила, где указанный 5- или 6-членный гетероарил необязательно замещен одним или несколькими заместителями, каждый из которых независимо выбран из группы, состоящей из галогена, C1-4алкилокси и С1-4алкила, необязательно замещенного одним или несколькими галогеновыми заместителями;
или Ar2 представляет собой хинолинил;
La, Lb и Lc представляют собой прямую связь; С2-6алкендиил; карбонил; О; S; S(=O)p; NR9; NR9-С1-4алкандиил; С1-4алкандиил-NR9; NR12-(С=O); (C=O)-NR12 или С1-6алкандиил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из группы, состоящей из галогена и гидрокси; два атома водорода, присоединенных к одному атому, в указанном С1-6алкандииле могут быть заменены С1-6алкандиилом;
R6b и R6c представляют собой водород или метил;
каждый R7 независимо представляет собой водород, С1-4ацил или С1-4алкил;
каждый R8 независимо представляет собой водород или C1-4алкил;
R9 представляет собой водород, С1-4ацил или С1-4алкил;
R12 представляет собой водород или метил;
или его фармацевтически приемлемая аддитивная соль или сольват;
при условии, что соединение не является 2-[4-(1Н-имидазол-1-ил)фенил]-4-(трифторметил)-1Н-имидазолом.
2. Соединение по п.1 или его стереоизомерная форма, где
А1 представляет собой CR3a или N, где R3a представляет собой водород, галоген или С1-4алкилокси;
А2 представляет собой CR3b или N, где R3b представляет собой водород или С1-4алкилокси;
каждый из А3 и А4 независимо представляет собой СН или N;
при условии, что не более чем два из А1, А2, А3 и А4 представляют собой N;
Het1 представляет собой гетероцикл, имеющий формулу (а), (b) или (с)

R4a представляет собой водород; цикло-С3-7алкил; Ar1 или C1-6алкил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из группы, состоящей из галогена, Ar1, цикло-С3-7алкила и С1-6алкилокси;
R4c представляет собой Ar1 или С1-6алкил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена;
где в определениях R4a и R4c каждый Ar1 независимо представляет собой фенил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из группы, состоящей из галогена и С1-4алкила;
R5a, R5b и R5c представляют собой водород; пиперидинил; морфолинил; пирролидинил; 1,6-дигидро-1-метил-6-оксо-3-пиридинил; 1,2-дигидро-1-метил-2-оксо-3-пиридинил; цикло-С3-7алкил; Ar2 или С1-6алкил;
где в определениях R5a, R5b и R5c пиперидинил, морфолинил, пирролидинил и цикло-С3-7алкил могут быть замещены одним или несколькими заместителями, каждый из которых независимо выбран из С1-4алкила;
где в определениях R5a, R5b и R5c
Ar2 представляет собой фенил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из группы, состоящей из галогена, С1-4алкилокси, циано, NR7R8 и С1-4алкила, необязательно замещенного одним или несколькими галогеновыми заместителями;
или Ar2 представляет собой 5- или 6-членный гетероарил, выбранный из группы, состоящей из пиразолила и пиридинила, где указанный 5- или 6-членный гетероарил необязательно замещен одним или несколькими заместителями, каждый из которых независимо выбран из группы, состоящей из галогена, С1-4алкилокси и С1-4алкила, необязательно замещенного одним или несколькими галогеновыми заместителями;
La, Lb и Lc представляют собой прямую связь; С2-6алкендиил; карбонил; О; S; NR9; NR9-C1-4алкандиил или С1-6алкандиил, необязательно замещенный одним или несколькими галогеновыми заместителями; или два атома водорода, присоединенных к одному атому, в указанном С1-6алкандииле могут быть заменены C1-6алкандиплом;
каждый R7 независимо представляет собой водород или С1-4алкил;
R9 представляет собой водород или С1-4алкил;
или его фармацевтически приемлемая аддитивная соль или сольват;
при условии, что соединение не является 2-[4-(1Н-имидазол-1-ил)фенил]-4-(трифторметил)-1Н-имидазолом.
3. Соединение по п.1 или его стереоизомерная форма, где
R2 представляет собой водород или С1-4алкил;
X представляет собой СН или N;
А1 представляет собой CR3a или N, где R3a представляет собой водород; галоген; циано; С1-4алкил или С1-4алкилокси, необязательно замещенный одним или несколькими галогеновыми заместителями;
А2 представляет собой CR3b или N, где R3b представляет собой водород, фтор или С1-4алкилокси;
каждый из А3 и А4 независимо представляет собой СН, CF или N;
при условии, что не более чем два из А1, А2, А3 и А4 представляют собой N;
Het1 представляет собой гетероцикл, имеющий формулу (a), (b) или (с);
R4a представляет собой водород; цикло-С3-7алкил; Ar1 или C1-6алкил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из группы, состоящей из галогена, гидроксила, циано, Ar1, цикло-С3-7алкила и C1-6алкилокси;
R4c представляет собой Ar1 или С1-6алкил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена;
где в определениях R4a и R4c каждый Ar1 независимо представляет собой фенил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из группы, состоящей из галогена и С1-4алкила, необязательно замещенного одним или несколькими галогеновыми заместителями;
R5a, R5b и R5c представляют собой водород; пиперидинил; морфолинил; пирролидинил; гексагидро-1H-1,4-диазепин-1-ил; 1,2,3,4-тетрагидро-2-хинолинил; 3,4-дигидро-2(1Н)-изохинолинил; 3,4-дигидро-1(2Н)-хинолинил; 2,2-дифтор-1,3-бензодиоксол-5-ил; 2,2-дифтор-1,3-бензодиоксол-4-ил; 1,6-дигидро-1-метил-6-оксо-3-пиридинил; 1,2-дигидро-1-метил-2-оксо-3-пиридинил; 2,3-дигидро-4Н-1,4-бензоксазин-4-ил; 3,4-дигидро-1,5-бензоксазепин-5(2Н)-ил; цикло-С3-7алкил; Ar2 или С1-6алкил;
где в определениях R5a, R5b и R5c пиперидинил, морфолинил, пирролидинил, гексагидро-1Н-1,4-диазепин-1-ил, 1,2,3,4-тетрагидро-2-хинолинил, 3,4-дигидро-2(1Н)-изохинолинил, 3,4-дигидро-1(2Н)-хинолинил и цикло-С3-7алкил могут быть замещены одним или несколькими заместителями, каждый из которых независимо выбран из группы, состоящей из С1-4ацила, С1-4алкила, необязательно замещенного одним или несколькими галогеновыми заместителями, и
фенил, необязательно замещенный одним или несколькими заместителями, выбранными из трифторметила;
где в определениях R5a, R5b и R5c
Ar2 представляет собой фенил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из группы, состоящей из галогена, циано, NR7R8, (C=O)-NR7R8, С1-4ацила, С1-4алкилсульфонила, C1-4алкилсульфинила, тетрагидрофуранилокси, С1-4алкилокси, необязательно замещенного одним или несколькими заместителями, каждый из которых независимо выбран из группы, состоящей из галогена, С1-4алкилокси и циклопропила, и С1-4алкила, необязательно замещенного одним или несколькими заместителями, каждый из которых независимо выбран из группы, состоящей из галогена, гидроксила и С1-4алкилокси;
или Ar2 представляет собой 5- или 6-членный гетероарил, выбранный из группы, состоящей из пиразолила и пиридинила, где указанный 5- или 6-членный гетероарил необязательно замещен одним или несколькими заместителями, каждый из которых независимо выбран из группы, состоящей из галогена, C1-4алкилокси и С1-4алкила, необязательно замещенного одним или несколькими галогеновыми заместителями;
или Ar2 представляет собой хинолинил;
La, Lb и Lc представляют собой прямую связь; С2-6алкендиил; карбонил; О; S; NR9; NR9-C1-4алкандиил; С1-4алкандиил-NR9; NR12-(С=O); (С=O)-NR12 или С1-6алкандиил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из группы, состоящей из галогена и гидрокси; два атома водорода, присоединенных к одному атому, в указанном С1-6алкандииле могут быть заменены С1-6алкандиилом;
каждый R7 независимо представляет собой С1-4ацил или C1-4алкил;
каждый R8 независимо представляет собой водород или C1-4алкил;
R9 представляет собой водород, С1-4ацил или С1-4алкил;
R12 представляет собой водород;
или его фармацевтически приемлемая аддитивная соль или сольват;
при условии, что соединение не является 2-[4-(1Н-имидазол-1-ил)фенил]-4-(трифторметил)-1Н-имидазолом.
4. Соединение по п.1 или его стереоизомерная форма, где
R1 представляет собой водород или С1-4алкил;
R2 представляет собой водород или С1-4алкил;
X представляет собой СН или N;
А1 представляет собой CR3a или N; где R3a представляет собой водород; циано; С1-4алкил или С1-4алкилокси;
А2 представляет собой CR3b или N, где R3b представляет собой водород, фтор или С1-4алкилокси;
А3 представляет собой СН или CF;
А4 представляет собой СН;
при условии, что когда А1 представляет собой N, то А2 представляет собой CR3b, и когда А2 представляет собой N, то А1 представляет собой CR3a;
Het1 представляет собой гетероцикл, имеющий формулу (а), (b) или (c);
R4a представляет собой водород; цикло-С3-7алкил; Ar1 или С1-6алкил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из группы, состоящей из галогена, гидроксила, циано, Ar1, цикло-С3-7алкила, С1-6алкилокси;
R4c представляет собой Ar1 или С1-6алкил;
где в определениях R4a и R4c каждый Ar1 независимо представляет собой фенил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из группы, состоящей из галогена и С1-4алкила, необязательно замещенного одним или несколькими галогеновыми заместителями;
R5a, R5b и R5c представляют собой водород; пиперидинил; морфолинил; пирролидинил; гексагидро-1H-1,4-диазепин-1-ил; 1,2,3,4-тетрагидро-2-хинолинил; 3,4-дигидро-2(1Н)-изохинолинил; 3,4-дигидро-1(2Н)-хинолинил; 2,2-дифтор-1,3-бензодиоксол-5-ил; 2,2-дифтор-1,3-бензодиоксол-4-ил; 1,6-дигидро-1-метил-6-оксо-3-пиридинил; 1,2-дигидро-1-метил-2-оксо-3-пиридинил; 2,3-дигидро-4Н-1,4-бензоксазин-4-ил; 3,4-дигидро-1,5-бензоксазепин-5(2Н)-ил; цикло-С3-7алкил; Ar2 или С1-6алкил;
где в определениях R5a, R5b и R5c пиперидинил, морфолинил, пирролидинил, гексагидро-1Н-1,4-диазепин-1-ил и цикло-С3-7алкил могут быть замещены одним или несколькими заместителями, каждый из которых независимо выбран из группы, состоящей из С1-4ацила, С1-4алкила, необязательно замещенного одним или несколькими галогеновыми заместителями, и фенила, необязательно замещенного одним или несколькими трифторметильными группами;
где в определениях R5a, R5b и R5c
Ar2 представляет собой фенил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из группы, состоящей из галогена, циано, NR7R8, (C=O)-NR7R8, С1-4ацила, С1-4алкилсульфонила, C1-4алкилсульфинила, тетрагидрофуранилокси, С1-4алкилокси, необязательно замещенного одним или несколькими заместителями, каждый из которых независимо выбран из группы, состоящей из галогена, гидроксила, С1-4алкилокси и циклопропила, и С1-4алкила, необязательно замещенного одним или несколькими заместителями, каждый из которых независимо выбран из группы, состоящей из галогена, гидроксила и С1-4алкилокси;
или Ar2 представляет собой 5- или 6-членный гетероарил, выбранный из группы, состоящей из пиридинила и пиразолила, где указанный 5- или 6-членный гетероарил необязательно замещен одним или несколькими заместителями, каждый из которых независимо выбран из группы, состоящей из галогена, С1-4алкилокси и С1-4алкила, необязательно замещенного одним или несколькими галогеновыми заместителями;
или Ar2 представляет собой хинолинил;
La, Lb и Lc представляют собой прямую связь; С2-6алкендиил; карбонил; О; S; NR9; NR9-С1-4алкандиил; С1-4алкандиил-NR9; (С=O)-NR12 или С1-6алкандиил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из группы, состоящей из галогена и гидрокси; два атома водорода, присоединенных к одному атому, в указанном C1-6алкандииле могут быть заменены С1-6алкандиилом;
R6b и R6c представляют собой водород или метил;
каждый R7 независимо представляет собой С1-4ацил или C1-4алкил;
каждый R8 независимо представляет собой водород или C1-4алкил;
R9 представляет собой водород, С1-4ацил или С1-4алкил;
R12 представляет собой водород;
или его фармацевтически приемлемая аддитивная соль или сольват.
5. Соединение по п.1, где La, Lb и Lc представляют собой NH.
6. Соединение по п.1, где А1 представляет собой С-О-СН3; А2 представляет собой СН или N.
7. Соединение по п.1, где Het1 представляет собой гетероцикл формулы (а) или (b).
8. Соединение по п.1, где Het1 представляет собой гетероцикл формулы (а).
9. Соединение по п.3, где
R1 представляет собой С1-4алкил;
R2 представляет собой водород;
X представляет собой СН;
А1 представляет собой CR3a, где R3a представляет собой C1-4алкилокси;
А2 представляет собой СН или N;
А3 и А4 представляют собой СН;
Het1 представляет собой гетероцикл формулы (а); где
R4a представляет собой C1-6алкил;
R5a представляет собой фенил, замещенный одним, двумя или тремя заместителями, каждый из которых независимо выбран из группы, состоящей из галогена, С1-4алкила, необязательно замещенного одним или несколькими галогеновыми заместителями, и С1-4алкилокси, необязательно замещенного одним или несколькими галогеновыми заместителями;
La представляет собой NH.
10. Соединение по п.1, где соединение представляет собой
N-[2-фтор-3-метокси-5-(трифторметил)фенил]-3-[6-метокси-5-(4-метил-1Н-имидазол-1-ил)-2-пиридинил]-1-метил-1Н-1,2,4-триазол-5-амин,
N-[2-фтор-3-метокси-5-(трифторметил)фенил]-3-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]-1-метил-1Н-1,2,4-триазол-5-амин,
3-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]-1-метил-N-(2-метилфенил)-1Н-1,2,4-триазол-5-амин,
N-[3-фтор-2-(трифторметил)фенил]-3-[6-метокси-5-(4-метил-1Н-имидазол-1-ил)-2-пиридинил]-1-метил-1Н-1,2,4-триазол-5-амин,
N-[2-фтор-3-(трифторметил)фенил]-3-[6-метокси-5-(4-метил-1Н-имидазол-1-ил)-2-пиридинил]-1-метил-1Н-1,2,4-триазол-5-амин,
N-[2-фтор-5-(трифторметокси)фенил]-3-[6-метокси-5-(4-метил-1Н-имидазол-1-ил)-2-пиридинил]-1-метил-1Н-1,2,4-триазол-5-амин,
3-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]-1-метил-N-[2-(трифторметил)фенил]-1Н-1,2,4-триазол-5-амин или
N-[2-фтор-5-(трифторметил)фенил]-3-[6-метокси-5-(4-метил-1Н-имидазол-1-ил)-2-пиридинил]-1-метил-1Н-1,2,4-триазол-5-амин,
или их фармацевтически приемлемую аддитивную соль или сольват.
11. Соединение по п.1, где соединение представляет собой 3-[3-метокси-4-(4-метил-1Н-имидазол-1-ил)фенил]-1-метил-N-(2-метилфенил)-1Н-1,2,4-триазол-5-амин.
12. Соединение по п.1, где соединение представляет собой N-[2-фтор-5-(трифторметил)фенил]-3-[6-метокси-5-(4-метил-1Н-имидазол-1-ил)-2-пиридинил]-1-метил-1Н-1,2,4-триазол-5-амин или его фармацевтически приемлемую аддитивную соль или сольват.
13. Соединение по п.12, где соединение представляет собой N-[2-фтор-5-(трифторметил)фенил]-3-[6-метокси-5-(4-метил-1Н-имидазол-1-ил)-2-пиридинил]-1-метил-1Н-1,2,4-триазол-5-амин.
14. Фармацевтическая композиция, содержащая в качестве активного ингредиента терапевтически эффективное количество соединения по любому из пп.1-13 и фармацевтически приемлемый носитель.
15. Применение соединения по любому из пп.1-13 в качестве лекарственного средства для лечения или профилактики заболеваний или состояний, выбранных из группы, состоящей из болезни Альцгеймера, травматического повреждения головного мозга, мягкого когнитивного нарушения, старческой деменции, деменции, деменции с тельцами Леви, церебральной амилоидной ангиопатии, мультиинфарктной деменции, синдрома Дауна, деменции, ассоциированной с болезнью Паркинсона, и деменции, ассоциированной с бета-амилоидом.
16. Применение по п.15, где соединение предназначено для лечения или профилактики болезни Альцгеймера.
Текст
ЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ ТРИАЗОЛА И ИМИДАЗОЛА В КАЧЕСТВЕ МОДУЛЯТОРОВ ГАММА-СЕКРЕТАЗЫ Настоящее изобретение относится к новым замещенным производным триазола и имидазола формулы (I), где R1, R2, А 1, А 2, А 3, А 4, X и Het1 имеют значения, определенные в формуле изобретения. Соединения согласно настоящему изобретению пригодны в качестве модуляторов гамма-секретазы. Кроме того, изобретение относится к фармацевтическим композициям,содержащим указанные соединения в качестве активного ингредиента, а также к применению указанных соединений в качестве лекарственного средства. Ву Тонгфей, Гейсен Хенрикус Якобус Мария, Ромбаутс Фредерик Ян Рита,Бишофф Франсуа Поль, Бертело Дидье Жан-Клод, Оельрих Дэниел,Де Клейн Михел Анна Йозеф, Питерс Серж Мария Алоисиус, Минн Гарретт Берлонд, Велтер Адриана Ингрид,Ван Брандт Свен Францискус Анна,Суркин Михел (BE) Медведев В.Н. (RU) Область техники, к которой относится изобретение Настоящее изобретение относится к новым замещенным производным триазола и имидазола, пригодным в качестве модуляторов гамма-секретазы. Кроме того, изобретение относится к фармацевтическим композициям, содержащим указанные соединения в качестве активного ингредиента, а также к применению указанных соединений в качестве лекарственного средства. Предшествующий уровень техники Болезнь Альцгеймера (AD) представляет собой прогрессирующее нейродегенеративное нарушение,для которого характерна потеря памяти, когнитивной способности и стабильности поведения. От AD страдают 6-10% популяции в возрасте старше 65 лет и вплоть до 50% в возрасте старше 85. Она является основной причиной деменции и третьей из основных причин смерти после сердечно-сосудистых заболеваний и злокачественных опухолей. В настоящее время не существует эффективного способа леченияAD. Суммарные затраты, связанные с AD, в США превышают 100 млрд долларов ежегодно. Этиология AD не является простой, однако она ассоциирована с определенными факторами риска,включающими (1) возраст, (2) семейный анамнез и (3) травму головы; другие факторы включают токсины окружающей среды и низкие уровни образования. Специфические невропатологические очаги повреждения в лимбической коре и коре головного мозга включают внутриклеточные нейрофибриллярные клубки, состоящие из гиперфосфорилированного тау-белка, и внеклеточное отложение фибриллярных агрегатов амилоидных бета-пептидов (амилоидных бляшек). Основным компонентом амилоидных бляшек являются пептиды амилоида-бета (А-бета, Abeta или АВ) различной длины. Полагают, что их вариант, который представляет собой пептид A1-42 (Abeta-42), является основным этиологическим фактором образования амилоида. Другим вариантом является пептид А 1-40 (Abeta-40). Амилоид-бета представляет собой протеолитический продукт белка-предшественника, бета-амилоидного белкапредшественника (бета-АРР или АРР). Семейные аутосомно-доминантные формы AD с ранним началом связывают с миссенс-мутациями в-АРР и в белках пресенилинах 1 и 2. У некоторых пациентов с формой AD с поздним началом была выявлена корреляция с конкретным аллелем гена аполипопротеина Е (АроЕ) и, позднее, с открытием мутации в альфа 2-макроглобулине, которая может быть связана по меньшей мере с 30% AD в популяции. Несмотря на эту гетерогенность, все формы AD проявляют сходные патологические признаки. Генетический анализ обеспечил наилучшие идеи для логического терапевтического подхода к AD. Все мутации,найденные к настоящему времени, влияют на количественную или качественную продукцию амилоидогенных пептидов, известных как Abeta-пептиды (A), в частности A42, и обеспечили существенную поддержку "гипотезе амилоидного каскада" AD (Tanzi and Bertram, 2005, Cell 120, 545). Вероятная связь между образованием А-пептидов и патологией AD усиливает необходимость в лучшем понимании механизмов продукции A и убедительно поддерживает терапевтический подход, связанный с модулированием уровней А. Высвобождение А-пептидов модулируется по меньшей мере двумя видами протеолитической активности, называемыми расщеплением - и -секретазой на N-конце (связь Met-Asp) и С-конце (остатки 37-42) пептида А соответственно. Существуют данные, что в секреторном каскаде сначала расщепление проводит -секретаза, что приводит к секреции s-APP (s) и удержанию 11-кДа связанного с мембраной С-концевого фрагмента (CTF). Полагают, что последний дает начало А-пептидам после расщепления секретазой. Количество более длинной изоформы, А 42, селективно увеличено у пациентов, несущих определенные мутации в конкретном белке (пресенилине), и была установлена корреляция этих мутаций с семейной AD с ранним началом. Таким образом, многие исследователи полагают, что А 42 является основным участником патогенеза AD. В настоящее время стало понятно, что активность -секретазы не может быть приписана одному белку, а в действительности она ассоциирована с системой различных белков. Активностью гамма-секретазы обладает мультибелковый комплекс, содержащий по меньшей мере четыре компонента: гетеродимер пресенилина (PS), никастрин, aph-1 и pen-2. Гетеродимер PS состоит из N- и С-концевых фрагментов PS, образованных эндопротеолизом белка-предшественника. В области контакта этого гетеродимера находятся два остатка аспартата. Недавно было предположено, что никастрин служит в качестве рецептора-субстрата -секретазы. Функции других членов у-секретазы неизвестны, однако они требуются для активности (Steiner, 2004. Curr. Alzheimer Research 1(3): 175-181). Таким образом, хотя молекулярный механизм второй стадии расщепления остается неясным до настоящего времени, -секретазный комплекс стал одной из основных мишеней при поиске соединений для лечения AD. Для нацеливания на -секретазу при AD были предложены различные стратегии, варьирующие от нацеливания непосредственно на каталитический центр до разработки субстрат-специфичных ингибиторов и модуляторов активности -секретазы (Marjaux et al., 2004. Drug Discovery Today: Therapeutic Strategies, Vol. 1, 1-6). Таким образом, описано множество соединений, мишенями которых являются секретазы (Larner, 2004. Secretases as therapeutics targets in AD: patents 2000-2004. Expert Opin. Ther. Patents 14,-1 021047 1403-1420). Действительно, это открытие подтверждено биохимическими исследованиями, в которых был показан эффект определенных нестероидных противовоспалительных лекарственных средств(NSAID) на -секретазу (US 2002/0128319; Eriksen (2003), J. Clin. Invest. 112, 440). Потенциальными ограничениями для применения NSAID для предупреждения или лечения AD являются их активность ингибирования ферментов циклооксигеназ (СОХ), которая может привести к нежелательным побочным эффектам, и их низкое проникновение в ЦНС (Peretto et al., 2005, J. Med. Chem. 48, 5705-5720). ПозднееNSAID R-флубипрофен - энантиомер, лишенный Сох-ингибиторной активности и связанной с ней желудочной токсичностью - оказался неуспешным в крупном испытании фазы III, поскольку это лекарственное средство не улучшило значимо способность к мышлению или способность пациентов к осуществлению повседневных действий, по сравнению с пациентами с плацебо.WO 2009/050227 относится к производным пиридазина для ингибирования укорочения бетаамилоидного пептида.WO 2004/110350 относится к производным тиазолила и их применению для модулирования амилоида-бета.US 20090062529 относится к полициклическим производным амида коричной кислоты, эффективным для лечения нейродегенеративного заболевания, вызываемого амилоидом-. В Journal of Organic Chemistry; vol. 51; no. 16; p. 3228-3231; Matthews, Donald P. et al., описаны способы синтеза для получения 4(5)-цианоимидазолов, включая 2-[4-(1 Н-имидазол-1-ил)фенил]-4(трифторметил)-1 Н-имидазол. Однако нет упоминаний о применении этих соединений. Существует высокая потребность в новых соединениях, которые модулируют активность секретазы, тем самым открывая новые направления для лечения AD. Задачей настоящего изобретения является преодоление или уменьшение по меньшей мере одного из недостатков уровня техники, или предоставление пригодной альтернативы. Таким образом, задачей настоящего изобретения является предоставление таких новых соединений. Описание изобретения Было открыто, что соединения по настоящему изобретению пригодны в качестве модуляторов секретазы. Соединения согласно изобретению и их фармацевтически приемлемые композиции могут быть пригодны для лечения или предупреждения AD. Настоящее изобретение относится к новым соединениям формулы (I)R1 представляет собой водород или С 1-4 алкил;R2 представляет собой водород или С 1-4 алкил;X представляет собой СН или N; А 1 представляет собой CR3a или N; где R3a представляет собой водород; галоген; циано; С 1-4 алкил или С 1-4 алкилокси, необязательно замещенный одним или несколькими галогеновыми заместителями; А 2 представляет собой CR3b или N, где R3b представляет собой водород, фтор или С 1-4 алкилокси; каждый из А 3 и А 4 независимо представляет собой СН, CF или N; при условии, что не более чем два из А 1, А 2, А 3 и А 4 представляют собой N;R4a представляет собой водород; тетрагидропиранил; тетрагидрофуранил; пиперидинил; морфолинил; пирролидинил; цикло-С 3-7 алкил; Ar1 или С 1-6 алкил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из группы, состоящей из галогена, гидроксила, циано, Ar1, цикло-С 3-7 алкила, С 1-6 алкилокси, С 1-6 алкилтио и О-Ar1;R4c представляет собой Ar1 или С 1-6 алкил, необязательно замещенный одним или несколькими за-2 021047 местителями, каждый из которых независимо выбран из галогена; где в определениях R4a и R4c каждый Ar1 независимо представляет собой фенил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена;R5a, R5b и R5c представляют собой водород; пиперидинил; морфолинил; пирролидинил; гексагидро 1 Н-1,4-диазепин-1-ил; 1,2,3,4-тетрагидро-2-хинолинил; 3,4-дигидро-2(1 Н)-изохинолинил; 3,4-дигидро 1(2 Н)-хинолинил; 2,2-дифтор-1,3-бензодиоксол-5-ил; 2,2-дифтор-1,3-бензодиоксол-4-ил; 1,6-дигидро-1 метил-6-оксо-3-пиридинил; 1,2-дигидро-1-метил-2-оксо-3-пиридинил; 2,3-дигидро-4 Н-1,4-бензоксазин-4 ил; 3,4-дигидро-1,5-бензоксазепин-5(2 Н)-ил; цикло-С 3-7 алкил; Ar2 или С 1-6 алкил; где в определениях R5a, R5b и R5c пиперидинил, морфолинил, пирролидинил, гексагидро-1 Н-1,4 диазепин-1-ил, 1,2,3,4-тетрагидро-2-хинолинил, 3,4-дигидро-2(1 Н)-изохинолинил, 3,4-дигидро-1(2 Н)хинолинил и цикло-С 3-7 алкил могут быть замещены одним или несколькими заместителями, каждый из которых независимо выбран из группы, состоящей из С 1-4 ацила, галогена, С 1-4 алкилоксикарбонила,С 1-4 алкила, необязательно замещенного одним или несколькими галогеновыми заместителями, и фенил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из группы, состоящей из С 1-4 алкила и трифторметила; где в определениях R5a, R5b и R5cAr2 представляет собой фенил, необязательно замещенный одним или несколькими заместителями,каждый из которых независимо выбран из группы, состоящей из галогена, циано, NR7R8, (C=O)-NR7R8,С 1-4 ацила, С 1-4 алкилсульфонила, C1-4 алкилсульфинила, тетрагидрофуранилокси, С 1-4 алкилокси, необязательно замещенного одним или несколькими заместителями, каждый из которых независимо выбран из группы, состоящей из галогена, гидроксила, С 1-4 алкилокси и циклопропила, и С 1-4 алкила, необязательно замещенного одним или несколькими заместителями, каждый из которых независимо выбран из группы,состоящей из галогена, гидроксила и С 1-4 алкилокси, необязательно замещенного одним или несколькими галогеновыми заместителями; или Ar2 представляет собой 5- или 6-членный гетероарил, выбранный из группы, состоящей из пиразолила и пиридинила, где указанный 5- или 6-членный гетероарил необязательно замещен одним или несколькими заместителями, каждый из которых независимо выбран из группы, состоящей из галогена,С 1-4 алкилокси и С 1-4 алкила, необязательно замещенного одним или несколькими галогеновыми заместителями; или Ar2 представляет собой хинолинил;La, Lb и Lc представляют собой прямую связь; С 2-6 алкендиил; карбонил; О; S; S(=O)p; NR9; 9NR -C1-4 алкандиил; С 1-4 алкандиил-NR9; NR12-(С=O); (С=О) -NR12 или C1-6 алкандиил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из группы,состоящей из галогена и гидрокси; два атома водорода, присоединенных к одному атому, в указанном С 1-6 алкандииле могут быть заменены С 1-6 алкандиилом;R6b и R6c представляют собой водород или метил; каждый R7 независимо представляет собой водород, С 1-4 ацил или С 1-4 алкил; каждый R8 независимо представляет собой водород или С 1-4 алкил;R12 представляет собой водород или метил; и их фармацевтически приемлемым аддитивным солям и сольватам,при условии, что соединение не является 2-[4-(1 Н-имидазол-1-ил)фенил]-4-(трифторметил)-1 Нимидазолом. Также настоящее изобретение относится к фармацевтическим композициям, содержащим соединения формулы (I). Неожиданно было открыто, что настоящие соединения модулируют активность -секретазы in vitro и in vivo и, таким образом, могут быть пригодны для лечения или профилактики болезни АльцгеймераAD, травматического повреждения головного мозга (TBI), мягкого когнитивного нарушения (MCI),старческой деменции, деменции, деменции с тельцами Леви, церебральной амилоидной ангиопатии,мультиинфарктной деменции, синдрома Дауна, деменции, ассоциированной с болезнью Паркинсона, и деменции, ассоциированной с бета-амилоидом, предпочтительно AD или других нарушений с бетаамилоидной патологией (например, глаукомы). Ввиду вышеупомянутой фармакологии соединений формулы (I) следует, что они могут быть пригодны для применения в качестве лекарственного средства для лечения или профилактики указанных заболеваний. Более конкретно, соединения могут быть пригодны для лечения или профилактики болезни Альцгеймера. Соединения общей формулы (I), его стереоизомерные формы и фармацевтически приемлемые кислотно- или основно-аддитивные соли и сольваты пригодны для модулирования активности -секретазы. Настоящее изобретение дополнительно описано далее. В следующих разделах подробно определены различные аспекты изобретения. Каждый аспект, определенный таким образом, может быть объеди-3 021047 нен с другим аспектом, если явно не указано иное. В частности, любой признак, указанный, как являющийся предпочтительным или преимущественным, можно объединить с любым другим признаком или признаками, указанными как являющиеся предпочтительными или преимущественными. Подробное описание изобретения При описании соединений по изобретению используемые термины следует истолковывать согласно следующим определениям, если контекст не указывает на иное. Когда используют термин "замещенный" в настоящем изобретении, подразумевают, если не указано иное или не очевидно из контекста, что он указывает на то, что один или более атомов водорода, в частности от 1 до 4 атомов водорода, предпочтительно от 1 до 3 атомов водорода, более предпочтительно 1 атом водорода на атоме или радикале, указанном в выражении с применением термина "замещенный", заменен группой, выбираемой из указанных групп, при условии, что обычная валентность не нарушается и что замещение приводит к химически стабильному соединению, т.е. к соединению, которое является достаточно устойчивым, чтобы выдерживать выделение до пригодной степени чистоты из реакционной смеси и изготовление в виде лекарственного средства. Термин "гало" или "галоген" в качестве группы или части группы является общим для фтора, хлора,брома, йода, если не указано или не ясно из контекста иное. Термин "С 1-6 алкил" в качестве группы или части группы относится к гидрокарбильному радикалу формулы CnH2n+1, где n представляет собой число в диапазоне от 1 до 6. С 1-6 алкильные группы включают от 1 до 6 атомов углерода, предпочтительно от 1 до 4 атомов углерода, более предпочтительно от 1 до 3 атомов углерода, еще более предпочтительно от 1 до 2 атомов углерода. Алкильные группы могут быть линейными или разветвленным и могут быть замещены, как указано в настоящем документе. Когда в настоящем документе после атома углерода используется подстрочный знак, подстрочный знак относится к количеству атомов углерода, которые может содержать названная группа. Таким образом, например,С 1-6 алкил включает все линейные или разветвленные алкильные группы с от 1 до 6 атомами углерода и,таким образом, включает группы, например, такие как метил, этил, н-пропил, изопропил, 2-метилэтил,бутил и его изомеры (например, н-бутил, изобутил и трет-бутил), пентил и его изомеры, гексил и его изомеры и т.п. Термин "С 1-4 алкил" в качестве группы или части группы относится к гидрокарбильному радикалу формулы CnH2n+1, где n представляет собой целое число в диапазоне от 1 до 4. C1-4 алкильные группы содержат от 1 до 4 атомов углерода, предпочтительно от 1 до 3 атомов углерода, более предпочтительно от 1 до 2 атомов углерода. С 1-4 алкил включает все линейные или разветвленный алкильные группы в диапазоне от 1 до 4 атомов углерода и, таким образом, включает группы, например, такие как метил, этил, нпропил, изопропил, 2-метилэтил, бутил и его изомеры (например, н-бутил, изобутил и трет-бутил) и т.п. Термин "С 1-4 ацил" отдельно или в комбинации относится к радикалу, содержащему от 1 до 4 атомов углерода, в котором карбонил связан с водородом или с прямым или разветвленным углеводородом,имеющим от 1 до 3 атомов углерода. Неограничивающие примеры пригодного С 1-4 ацила включают формил, ацетил, пропионил, бутирил и изобутирил. В частности, С 1-4 ацил представляет собой ацетил. Термин "С 1-6 алкилокси" в качестве группы или части группы относится к радикалу, имеющему формулу ORb, где Rb представляет собой С 1-6 алкил. Неограничивающие примеры пригодных алкилокси включают метилокси, этилокси, пропилокси, изопропилокси, бутилокси, изобутилокси, втор-бутилокси,трет-бутилокси, пентилокси и гексилокси. Термин "С 1-4 алкилокси в качестве группы или части группы относится к радикалу, имеющему формулу ORc, где Rc представляет собой С 1-4 алкил. Неограничивающие примеры пригодных С 1-4 алкилокси включают метилокси (также метокси), этилокси (также этокси), пропилокси, изопропилокси, бутилокси, изобутилокси, втор-бутилокси и трет-бутилокси. Термин "С 1-6 алкилтио" относится к неразветвленной или разветвленной алкилтиогруппе, имеющей от 1 до 6 атомов углерода, такой как метилтио, этилтио, пропилтио, изопропилтио, бутилтио, изобутилтио, втор-бутилтио, трет-бутилтио, пентилтио, неопентилтио, втор-пентилтио, н-пентилтио, изопентилтио, трет-пентилтио, гексилтио и т.п. Термин "С 1-4 алкилсульфонил" относится к неразветвленной или разветвленной алкилсульфонильной группе, имеющей от 1 до 4 атомов углерода, такой как метилсульфонил, этилсульфонил, пропилсульфонил, изопропилсульфонил, бутилсульфонил, изобутилсульфонил, втор-бутилсульфонил, третбутилсульфонил и т.п. Термин "С 1-4 алкилсульфинил" относится к неразветвленной или разветвленной алкилсульфинильной группе, имеющей от 1 до 4 атомов углерода, такой как метилсульфинил, этилсульфинил, изопропилсульфинил, бутилсульфинил, изобутилсульфинил, трет-бутилсульфинил и т.п. В рамках настоящего изобретения С 2-6 алкенил представляет собой прямой или разветвленный углеводородный радикал, имеющий от 2 до 6 атомов углерода, содержащих двойную связь, такой как этенил,пропенил, бутенил, пентенил, 1-пропен-2-ил, гексенил и т.п. Термин "цикло-С 3-7 алкил", отдельно или в комбинации, относится к циклическому насыщенному углеводородному радикалу, имеющему от 3 до 7 атомов углерода. Неограничивающие примеры пригодного цикло-С 3-7 алкила включают циклопропил, циклобутил, циклопентил, циклогексил и циклогептил. Термин "цикло-С 3-7 алкилокси", отдельно или в комбинации, относится к насыщенному цикло-С 3-7 алкилу-O, где цикло-С 3-7 алкил является таким, как определено выше. Неограничивающие примеры пригодного цикло-С 3-7 алкила включают циклопропилокси, циклобутилокси, циклопентилокси и циклогексилокси. В конкретном варианте осуществления цикло-С 3-7 алкил ограничен цикло-С 3-6 алкилом. В другом конкретном варианте осуществления цикло-С 3-7 алкилокси ограничен цикло-С 3-6 алкилокси. Термин "С 1-4 алкандиил" в качестве группы или части группы определяет двухвалентные прямые или разветвленные насыщенные углеводородные радикалы, имеющие от 1 до 4 атомов углерода, например, такие как метилен или метандиил, этан-1,2-диил, пропан-1,3-диил, пропан-1,2-диил, бутан-1,4-диил и т.п. Термин "С 1-6 алкандиил" в качестве группы или части группы определяет двухвалентные прямые или разветвленные насыщенные углеводородные радикалы, имеющие от 1 до 6 атомов углерода, например, такие как метилен или метандиил, этан-1,2-диил, этан-1,1-диил или этилиден, пропан-1,3-диил, пропан-1,2-диил, бутан-1,4-диил, пентан-1,5-диил, пентан-1,1-диил, гексан-1,6-диил, 2-метилбутан-1,4-диил,3-метилпентан-1,5-диил и т.п. Термин "С 2-6 алкандиил" в качестве группы или части группы определяет двухвалентные прямые или разветвленные насыщенные углеводородные радикалы, имеющие от 2 до 6 атомов углерода, например, такие как этан-1,2-диил, этан-1,1-диил или этилиден, пропан-1,3-диил, пропан-1,2-диил, бутан-1,4 диил, пентан-1,5-диил, пентан-1,1-диил, гексан-16-диил, 2-метилбутан-1,4-диил, 3-метилпентан-1,5-диил и т.п. В конкретном варианте осуществления С 2-6 алкандиил выбран из группы, состоящей из этан-1,2 диила, пропан-1,3-диила, бутан-1,4-диила, пентан-1,5-диила и гексан-1,6-диила. В конкретном варианте осуществления "С 1-4 алкандиил", "С 1-6 алкандиил" и "С 2-6 алкандиил" определяют двухвалентные неразветвленные насыщенные углеводородные радикалы. Термин "С 2-6 алкендиил" в качестве группы или части группы определяет двухвалентные прямые и разветвленные углеводородные радикалы, содержащие одну двойную связь и имеющие от 2 до 6 атомов углерода, например, такие как 1,2-этендиил, 2-пропендиил, 3-бутендиил, 2-пентендиил, 3-пентендиил, 3 метил-2-бутендиил и т.п. В конкретном варианте осуществления С 2-6 алкендиил определяет двухвалентные неразветвленные углеводородные радикалы, содержащие одну двойную связь и имеющие от 2 до 6 атомов углерода. Термин "тиофенил" эквивалентен термину "тиенил". Термин "оксопиридинил" определяет частично гидрогенизированные производные пиридинила, замещенные оксо, например, такие как 1,6-дигидро-6-оксо-3-пиридинил и 1,2-дигидро-2-оксо-3 пиридинил. Указанные частично гидрогенизированные производные пиридинила могут быть далее замещены заместителями, например, такими как метил, с образованием групп, например, таких как 1,6 дигидро-1-метил-6-оксо-3-пиридинил и 1,2-дигидро-1-метил-2-оксо-3-пиридинил. Когда La, Lb или Lc определен, например, как NR9-C1-4 алкандиил, это означает, что азот в NR9 связан с гетероциклическим кольцом (а), (b) или (с) соответственно и С 1-4 алкандиил связан с группой R5a, R5b или R5c соответственно. Когда La, Lb или Lc определен, например, как NR12-(С=O), это означает, что азот NR12 связан с гетероциклическим кольцом (а), (b) или (с) соответственно и (С=О) связан с группой R5a, R5b или R5c соответственно. Химические названия соединениям по настоящему изобретению давали согласно правилам номенклатуры, согласованным с Chemical Abstracts Service, с использованием программного обеспечения для номенклатуры Advanced Chemical Development, Inc., (ACD/Name product version 10.01; Build 15494, 1Dec 2006). В случае таутомерных форм должно быть понятно, что также в объем настоящего изобретения включена другая, не представленная таутомерная форма. Когда какая-либо переменная встречается более одного раза в каком-либо заместителе, каждое ее определение является независимым. Понятно, что некоторые из соединений формулы (I) и их фармацевтически приемлемые аддитивные соли и стереоизомерные формы могут содержать один или несколько центров хиральности и существовать в качестве стереоизомерных форм. Термин "стереоизомерные формы", как используют в настоящем документе выше, определяет все возможные изомерные формы, которыми могут обладать соединения формулы (I). Если не указано и не упоминается иное, химическое обозначение соединений обозначает смесь всех возможных стереохимически изомерных форм. Более конкретно, стереогенные центры могут иметь конфигурацию R или S; заместители на двухвалентных циклических (частично) насыщенных радикалах могут иметь либо цис-,либо транс-конфигурацию. Соединения, содержащие двойные связи, могут иметь Е- или Z-стереохимию по указанной двойной связи. Стереоизомерные формы соединений формулы (I) охватываются объемом этого изобретения. Когда указана конкретная стереоизомерная форма, это означает, что указанная форма является по существу свободной, т.е. ассоциирована менее чем с 50%, предпочтительно менее чем с 20%, более предпочтительно менее чем с 10%, еще более предпочтительно менее чем с 5%, более предпочтительно менее чем с 2% и наиболее предпочтительно менее чем с 1% другого изомера(ов). Для терапевтического применения соли соединений формулы (I) представляют собой соли, где противоион является фармацевтически приемлемым. Однако соли кислот и оснований, которые не являются фармацевтически приемлемыми, также применимы, например, для изготовления или очистки фармацевтически приемлемого соединения. Все соли, как фармацевтически приемлемые, так и не фармацевтически приемлемые, включены в объем настоящего изобретения. Подразумевают, что фармацевтически приемлемые кислотно- и основно-аддитивные соли, как упоминается в настоящем документе выше или ниже, включают терапевтически активные нетоксичные кислотно- и основно-аддитивную солевые формы, которые соединения формулы (I) способны образовывать. Фармацевтически приемлемые кислотно-аддитивные соли можно удобным образом получать путем обработки формы основания подходящей кислотой. Подходящие кислоты включают, например, неорганические кислоты, такие как галогенводородные кислоты, например хлористо-водородная или бромистоводородная кислота, серная, азотная, фосфорная и т.п. кислоты; или органические кислоты, например,такие как уксусная, пропановая, гидроксиуксусная, молочная, пировиноградная, щавелевая (т.е. этандиовая), малоновая, янтарная (т.е. бутандиовая кислота), малеиновая, фумаровая, яблочная, виннокаменная,лимонная, метансульфоновая, этансульфоновая, бензолсульфоновая, п-толуолсульфоновая, цикламовая,салициловая, п-аминосалициловая, памовая и т.п. кислоты. В противоположность этому, указанные солевые формы можно превращать путем обработки соответствующим основанием в форму свободного основания. Соединения формулы (I), содержащие кислотную часть, также можно превращать в их формы нетоксичных аддитивных солей металлов или аминов путем обработки подходящими органическими и неорганическими основаниями. Подходящие основные солевые формы включают, например, соли аммония, соли щелочных и щелочно-земельных металлов, например соли лития, натрия, калия, магния, кальция и т.п., соли с органическими основаниями, например первичными, вторичными и третичными алифатическими и ароматическими аминами, такие как соли метиламина, этиламина, пропиламина, изопропиламина, четырех изомеров бутиламина, диметиламина, диэтиламина, диэтаноламина, дипропиламина,диизопропиламина, ди-н-бутиламина, пирролидина, пиперидина, морфолина, триметиламина, триэтиламина, трипропиламина, хинукледина, пиридина, хинолина и изохинолина; бензатина, N-метил-Dглюкамина, гидрабамина, и соли с аминокислотами, например, такими как аргинин, лизин и т.п. В противоположность этому, форму соли можно превращать путем обработки кислотой в форму свободной кислоты. Термин "сольват" включает гидраты и аддитивные формы с растворителем, которые способны образовывать соединения формулы (I), а также их соли. Примерами таких форм являются, например, гидраты, алкоголяты и т.п. Соединения формулы (I), как их получают способами, описанными ниже, можно синтезировать в формерацемических смесей энантиомеров, которые можно отделять друг от друга известными в данной области способами разделения. Способ разделения энантиомерных форм соединений формулы (I) вовлекает жидкостную хроматографию с использованием хиральной неподвижной фазы. Указанные чистые стереохимически изомерные формы также можно получать из соответствующих чистых стереохимически изомерных форм соответствующих исходных материалов, при условии, что реакция протекает стереоспецифично. Предпочтительно, если является желательным конкретный стереоизомер, указанное соединение можно синтезировать стереоспецифическими способами получения. В этих способах преимущественно используют энантиомерно чистые исходные материалы. В рамках настоящего изобретения подразумевают, что соединение согласно изобретению по своему существу включает все изотопные комбинации его химических элементов. В рамках настоящего изобретения химический элемент, в частности, когда он упоминается применительно к соединению формулы(I), включает все изотопы и изотопные смеси этого элемента. Например, когда упоминается водород, понимают, что он относится к 1 Н, 2 Н, 3 Н и их смесям. Соединение согласно изобретению, таким образом, по своему существу включает соединение с одним или несколькими изотопами одного или нескольких элементов и их смесями, включая радиоактивное соединение, также называемое радиоактивно меченным соединением, где один или несколько нерадиоактивных атомов заменены одним из его радиоактивных изотопов. Под термином "радиоактивно меченное соединение" подразумевают любое соединение согласно формуле (I) или его фармацевтически приемлемую соль, которые содержат по меньшей мере один радиоактивный атом. Например, соединение может быть мечено позитрон- или гамма-излучающими радиоактивными изотопами. Для технологий связывания радиоактивного лиганда атом 3 Н или атом 125I представляет собой предпочтительный для выбора на замену атом. Для визуализации наиболее широко используемыми позитронно-активными(PET) радиоактивными изотопами являются 11 С, 18F, 15O и 13N, все из которых получают в ускорителе, и они имеют время полураспада 20, 100, 2 и 10 минут (мин) соответственно. Поскольку время полураспада для этих радиоактивных изотопов является слишком коротким, их возможно использовать только в уч-6 021047 реждениях, которые имеют местный ускоритель для их получения, что, таким образом, ограничивает их применение. Наиболее широко используемыми из них являются 18F, 99mTc, 201Tl и 123I. Обращение с этими радиоактивными изотопами, их получение, выделение и включение в молекулу известны специалисту в данной области. В частности, радиоактивный атом выбирают из группы из водорода, углерода, азота, серы, кислорода и галогена. В частности, радиоактивный изотоп выбирают из группы из 3 Н, 11 С, 18F, 122I, 123I, 125I, 131I,75Br, 76Br, 77Br и 82Br. Как используют в описании и прилагаемой формуле изобретения, форма единственного числа также включает форму множественного числа, если контекст явно не указывает на иное. Например, "соединение" означает 1 соединение или более одного соединения. Термины, описанные выше, и другие термины, используемые в описании, хорошо понятны специалистам в данной области. Предпочтительные признаки соединений по этому изобретению указаны далее. В одном варианте осуществления настоящее изобретение относится к новым соединениям формулы(I) и их стереоизомерным формам, где А 1 представляет собой CR3a или N, где R3a представляет собой водород, галоген или С 1-4 алкилокси; А 2 представляет собой CR3b или N, где R3b представляет собой водород или С 1-4 алкилокси; каждый из А 3 и А 4 независимо представляет собой СН или N; при условии, что не более чем два из А 1, А 2, А 3 и А 4 представляют собой N;R4a представляет собой водород; цикло-С 3-7 алкил; Ar1 или С 1-6 алкил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из группы, состоящей из галогена, Ar1, цикло-С 3-7 алкила и C1-6 алкилокси;R4c представляет собой Ar1 или С 1-6 алкил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена; где в определениях R4a и R4c каждый Ar1 независимо представляет собой фенил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из группы,состоящей из галогена и С 1-4 алкила;R5a, R5b и R5c представляют собой водород; пиперидинил; морфолинил; пирролидинил; 1,6-дигидро 1-метил-6-оксо-3-пиридинил; 1,2-дигидро-1-метил-2-оксо-3-пиридинил; цикло-С 3-7 алкил; Ar2 или С 1-6 алкил; где в определениях R5a, R5b и R5c пиперидинил, морфолинил, пирролидинил и цикло-С 3-7 алкил могут быть замещены одним или несколькими заместителями, каждый из которых независимо выбран из С 1-4 алкила; где в определениях R5a, R5b и R5cAr2 представляет собой фенил, необязательно замещенный одним или несколькими заместителями,каждый из которых независимо выбран из группы, состоящей из галогена, С 1-4 алкилокси, циано, NR7R8 и С 1-4 алкила, необязательно замещенного одним или несколькими галогеновыми заместителями; или Ar2 представляет собой 5- или 6-членный гетероарил, выбранный из группы, состоящей из пиразолила и пиридинила, где указанный 5- или 6-членный гетероарил необязательно замещен одним или несколькими заместителями, каждый из которых независимо выбран из группы, состоящей из галогена,С 1-4 алкилокси и С 1-4 алкила, необязательно замещенного одним или несколькими галогеновыми заместителями;La, Lb и Lc представляют собой прямую связь; С 2-6 алкендиил; карбонил; О; S; NR9; 9NR -C1-4 алкандиил или С 1-6 алкандиил, необязательно замещенный одним или несколькими галогеновыми заместителями; или два атома водорода, присоединенных к одному атому, в указанном С 1-6 алкандииле могут быть заменены C1-6 алкандиилом; каждый R7 независимо представляет собой водород или C1-4 алкил;R9 представляет собой водород или С 1-4 алкил; и их фармацевтически приемлемым аддитивным солям и сольватам; при условии, что соединение не является 2-[4-(1 Н-имидазол-1-ил)фенил]-4-(трифторметил)-1 Нимидазолом. В другом варианте осуществления настоящее изобретение относится к соединениям формулы (I)R2 представляет собой водород или С 1-4 алкил;X представляет собой СН или N; А 1 представляет собой CR3a или N; где R3a представляет собой водород; галоген; циано; С 1-4 алкил или С 1-4 алкилокси, необязательно замещенный одним или несколькими галогеновыми заместителями; А 2 представляет собой CR3b или N, где R3b представляет собой водород, фтор или С 1-4 алкилокси; каждый из А 3 и А 4 независимо представляет собой СН, CF или N; при условии, что не более чем два из А 1, А 2, А 3 и А 4 представляют собой N;R4a представляет собой водород; цикло-С 3-7 алкил; Ar1 или С 1-6 алкил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из группы, состоящей из галогена, гидроксила, циано, Ar1, цикло-С 3-7 алкила и С 1-6 алкилокси;R4c представляет собой Ar1 или С 1-6 алкил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из галогена; где в определениях R4a и R4c каждый Ar1 независимо представляет собой фенил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из группы,состоящей из галогена и С 1-4 алкила, необязательно замещенного одним или несколькими галогеновыми заместителями;R5a, R5b и R5c представляют собой водород; пиперидинил; морфолинил; пирролидинил; гексагидро 1 Н-1,4-диазепин-1-ил; 1,2,3,4-тетрагидро-2-хинолинил; 3,4-дигидро-2(1 Н)-изохинолинил; 3,4-дигидро 1(2 Н)-хинолинил; 2,2-дифтор-1,3-бензодиоксол-5-ил; 2,2-дифтор-1,3-бензодиоксол-4-ил; 1,6-дигидро-1 метил-6-оксо-3-пиридинил; 1,2-дигидро-1-метил-2-оксо-3-пиридинил; 2,3-дигидро-4 Н-1,4-бензоксазин-4 ил; 3,4-дигидро-1,5-бензоксазепин-5(2 Н)-ил; цикло-С 3-7 алкил; Ar2 или C1-6 алкил; где в определениях R5a, R5b и R5c пиперидинил, морфолинил, пирролидинил, гексагидро-1 Н-1,4 диазепин-1-ил, 1,2,3,4-тетрагидро-2-хинолинил, 3,4-дигидро-2(1 Н)-изохинолинил, 3,4-дигидро-1(2 Н)хинолинил и цикло-С 3-7 алкил могут быть замещены одним или несколькими заместителями, каждый из которых независимо выбран из группы, состоящей из C1-4 ацила, С 1-4 алкила, необязательно замещенного одним или несколькими галогеновыми заместителями, и фенил, необязательно замещенный одним или несколькими заместителями, выбранными из трифторметила; где в определениях R5a, R5b и R5cAr2 представляет собой фенил, необязательно замещенный одним или несколькими заместителями,каждый из которых независимо выбран из группы, состоящей из галогена, циано, NR7R8, (С=О)-NR7R8,C1-4 ацила, С 1-4 алкилсульфонила, С 1-4 алкилсульфинила, тетрагидрофуранилокси, С 1-4 алкилокси, необязательно замещенного одним или несколькими заместителями, каждый из которых независимо выбран из группы, состоящей из галогена, С 1-4 алкилокси и циклопропила, и С 1-4 алкила, необязательно замещенного одним или несколькими заместителями, каждый из которых независимо выбран из группы, состоящей из галогена, гидроксила и С 1-4 алкилокси; или Ar2 представляет собой 5- или 6-членный гетероарил, выбранный из группы, состоящей из пиразолила и пиридинила, где указанный 5- или 6-членный гетероарил необязательно замещен одним или несколькими заместителями, каждый из которых независимо выбран из группы, состоящей из галогена,C1-4 алкилокси и С 1-4 алкила, необязательно замещенного одним или несколькими галогеновыми заместителями; или Ar2 представляет собой хинолинил;La, Lb и Lc представляют собой прямую связь; С 2-6 алкендиил; карбонил; О; S; NR9; 9NR -С 1-4 алкандиил; С 1-4 алкандиил-NR9; NR12-(С=O); (C=O)-NR12 или С 1-6 алкандиил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из группы,состоящей из галогена и гидрокси; два атома водорода, присоединенных к одному атому, в указанном С 1-6 алкандииле могут быть заменены С 1-6 алкандиилом; каждый R7 независимо представляет собой С 1-4 ацил или C1-4 алкил; каждый R8 независимо представляет собой водород или С 1-4 алкил;R12 представляет собой водород; и их фармацевтически приемлемым аддитивным солям и сольватам; при условии, что соединение не является 2-[4-(1 Н-имидазол-1-ил)фенил]-4-(трифторметил)-1 Н-8 021047 имидазолом. Один вариант осуществления настоящего изобретения относится к соединениям формулы (I) и их стереоизомерным формам, гдеR1 представляет собой водород или С 1-4 алкил;R2 представляет собой водород или С 1-4 алкил;X представляет собой СН или N; А 1 представляет собой CR3a или N; где R3a представляет собой водород; циано; С 1-4 алкил или С 1-4 алкилокси; А 2 представляет собой CR3b или N, где R3b представляет собой водород, фтор или С 1-4 алкилокси; А 3 представляет собой СН или CF; А 4 представляет собой СН; при условии, что когда А 1 представляет собой N, то А 2 представляет собой CR3b, и когда А 2 представляет собой N, то А 1 представляет собой CR3a;R4a представляет собой водород; цикло-С 3-7 алкил; Ar1 или С 1-6 алкил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из группы, состоящей из галогена, гидроксила, циано, Ar1, цикло-С 3-7 алкила, С 1-6 алкилокси;R4c представляет собой Ar1 или С 1-6 алкил; где в определениях R4a и R4c каждый Ar1 независимо представляет собой фенил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из группы,состоящей из галогена и С 1-4 алкила, необязательно замещенного одним или несколькими галогеновыми заместителями;R5a, R5b и R5c представляют собой водород; пиперидинил; морфолинил; пирролидинил; гексагидро 1 Н-1,4-диазепин-1-ил; 1,2,3,4-тетрагидро-2-хинолинил; 3,4-дигидро-2(1 Н)-изохинолинил; 3,4-дигидро 1(2 Н)-хинолинил; 2,2-дифтор-1,3-бензодиоксол-5-ил; 2,2-дифтор-1,3-бензодиоксол-4-ил; 1,6-дигидро-1 метил-6-оксо-3-пиридинил; 1,2-дигидро-1-метил-2-оксо-3-пиридинил; 2,3-дигидро-4 Н-1,4-бензоксазин-4 ил; 3,4-дигидро-1,5-бензоксазепин-5(2 Н)-ил; цикло-С 3-7 алкил; Ar2 или С 1-6 алкил; где в определениях R5a, R5b и R5c пиперидинил, морфолинил, пирролидинил, гексагидро-1 Н-1,4 диазепин-1-ил и цикло-С 3-7 алкил могут быть замещены одним или несколькими заместителями, каждый из которых независимо выбран из группы, состоящей из С 1-4 ацила, С 1-4 алкила, необязательно замещенного одним или несколькими галогеновыми заместителями, и фенила, необязательно замещенного одним или несколькими трифторметильными группами; где в определениях R5a, R5b и R5cAr2 представляет собой фенил, необязательно замещенный одним или несколькими заместителями,каждый из которых независимо выбран из группы, состоящей из галогена, циано, NR7R8, (C=O) -NR7R8,С 1-4 ацила, С 1-4 алкилсульфонила, C1-4 алкилсульфинила, тетрагидрофуранилокси, С 1-4 алкилокси, необязательно замещенного одним или несколькими заместителями, каждый из которых независимо выбран из группы, состоящей из галогена, гидроксила, С 1-4 алкилокси и циклопропила, и С 1-4 алкила, необязательно замещенного одним или несколькими заместителями, каждый из которых независимо выбран из группы,состоящей из галогена, гидроксила и С 1-4 алкилокси; или Ar2 представляет собой 5- или 6-членный гетероарил, выбранный из группы, состоящей из пиридинила и пиразолила, где указанный 5- или 6-членный гетероарил необязательно замещен одним или несколькими заместителями, каждый из которых независимо выбран из группы, состоящей из галогена,С 1-4 алкилокси и С 1-4 алкила, необязательно замещенного одним или несколькими галогеновыми заместителями; или Ar2 представляет собой хинолинил;La, Lb и Lc представляют собой прямую связь; С 2-6 алкендиил; карбонил; О; S; NR9; 9NR -C1-4 алкандиил; C1-4 алкандиил-NR9; (С=О)-NR12 или C1-6 алкандиил, необязательно замещенный одним или несколькими заместителями, каждый из которых независимо выбран из группы, состоящей из галогена и гидрокси; два атома водорода, присоединенных к одному атому, в указанном С 1-6 алкандииле могут быть заменены С 1-6 алкандиилом;R6b и R6c представляют собой водород или метил; каждый R7 независимо представляет собой С 1-4 ацил или С 1-4 алкил; каждый R8 независимо представляет собой водород или C1-4 алкил;R12 представляет собой водород; и их фармацевтически приемлемым аддитивным солям и сольватам. В другом конкретном варианте осуществления La, Lb и Lc представляют собой NH. В следующем конкретном варианте осуществления А 1 представляет собой С-О-СН 3; А 2 представляет собой СН или N. В еще одном конкретном варианте осуществления Het1 представляет собой гетероцикл формулы (а) или (b). В следующем конкретном варианте осуществления изобретения Het1 представляет собой гетероцикл формулы (а). В другом варианте осуществления изобретенияX представляет собой СН; А 1 представляет собой CR3a, где R3a представляет собой С 1-4 алкилокси; А 2 представляет собой СН или N; А 3 и А 4 представляют собой СН;Het1 представляет собой гетероцикл формулы (а); гдеR5a представляет собой фенил, замещенный одним, двумя или тремя заместителями, каждый из которых независимо выбран из группы, состоящей из галогена, С 1-4 алкила, необязательно замещенного одним или несколькими галогеновыми заместителями, и С 1-4 алкилокси, необязательно замещенного одним или несколькими галогеновыми заместителями;La представляет собой NH. В одном варианте осуществления соединение формулы (I) представляет собойN-[2-фтор-5-(трифторметил)фенил]-3-[6-метокси-5-(4-метил-1 Н-имидазол-1-ил)-2-пиридинил]-1 метил-1 Н-1,2,4-триазол-5-амин,или их фармацевтически приемлемую аддитивную соль или сольват. Предпочтительно соединение формулы (I) представляет собой 3-[3-метокси-4-(4-метил-1 Нимидазол-1-ил)фенил]-1-метил-N-(2-метилфенил)-1 Н-1,2,4-триазол-5-амин. Также предпочтительно соединение формулы (I) представляет собой N-[2-фтор-5(трифторметил)фенил]-3-[6-метокси-5-(4-метил-1 Н-имидазол-1-ил)-2-пиридинил]-1-метил-1 Н-1,2,4 триазол-5-амин или его фармацевтически приемлемую аддитивную соль или сольват. Кроме того, предпочтительно соединение формулы (I) представляет собой N-[2-фтор-5(трифторметил)фенил]-3-[6-метокси-5-(4-метил-1 Н-имидазол-1-ил)-2-пиридинил]-1-метил-1 Н-1,2,4 триазол-5-амин. Все возможные комбинации указанных выше представляющих интерес вариантов осуществления считаются охватываемыми объемом этого изобретения. Соединения формулы (I) могут быть получены способами, раскрытыми далее. В описанных реакциях может быть необходимым защитить реакционноспособные функциональные группы, например гидрокси, амино или карбоксигруппу, где они желательны в конечном продукте, чтобы избежать их нежелательного участия в реакциях. Общепринятые защитные группы можно использовать в соответствии со стандартной практикой, например, см. Т. W. Greene and P.G.M. Wuts, "Protective Groups in OrganicChemistry", John Wiley and Sons, 1999. Соединения формулы (I) и их подгруппы можно получать с помощью последовательности стадий,как описано в настоящем документе ниже. Как правило, их получают из исходных материалов, которые либо являются коммерчески доступными, либо получают стандартными способами, известными специалистам в данной области. Соединения по настоящему изобретению также можно получать с использованием стандартных способов синтеза, широко используемых специалистами в области органической химии. Общие способы получения некоторых типичных примеров представлены ниже. Все переменные определены, как указано в настоящем документе выше, если нет иных указаний. LG определяет уходящую группу, например, такую как Cl, Br, I, тозилат, мезилат или трифлат, в частности F, Cl, Br или I, более конкретно Cl, Br или I, если нет иных указаний. Экспериментальная методика 1.R4a отличен от водорода; все другие переменные являются такими, как определено в настоящем документе выше; таким образом, соединения, названные соединениями формулы (III), можно получать замещением соединения формулы (II) соединением формулы R4a-LG, например, таким как арилгалогенид или алкилгалогенид (галогенид определяют как I, Cl, Br или F) согласно схеме 1. Реакцию можно проводить в присутствии основания, например, такого как NaH, в присутствии реакционно-инертных растворителей, таких как N,N-диметилформамид (DMF) или тетрагидрофуран (THF). Реакцию необязательно можно проводить в присутствии медного катализатора и/или лиганда, такого как N,N'-диметилэтилендиамин(DMEN), (1R,2R)-(-)-1,2-диаминоциклогексан или 1,10-пентантролин. Соли меди, например, такие как оксид меди(I), йодид меди(I) или бромид меди(I), можно использовать в каталитических или стехиометрических количествах. Повышенные температуры и/или давление могут увеличить скорость реакции. Как правило, получают смеси соединений формулы (III) и региоизомерных соединений формулы (IV). Когда алкилирующий реагент R6b-LG определен как CH3-LG, например, как в CH3I, получают региоизомерные соединения формулы (IV), которые представляют собой соединения формулы (I), где Het1 ограничен до (b), и где R6b представляет собой метил. Схема 1 Экспериментальная методика 2. Соединения формулы (III), где R4a отличен от водорода и где все другие переменные являются такими, как определено в экспериментальной методике 1, также можно получать реакцией конденсации между промежуточным соединением формулы (V-a) и промежуточным соединением формулы (VI), или реакцией конденсации между промежуточным соединением формулы (V-b) и промежуточным соединением формулы (VI) согласно схеме 2. Схема 2 Реакцию между промежуточными соединениями формулы (V-a) и (VI) можно проводить в присутствии источника аммония, такого как ацетат аммония (NH4+ -OAc), в растворителях, например, таких как уксусная кислота (АсОН), или в присутствии основания, например, такого как ацетат натрия (NaOAc), и в растворителе, например, таком как диоксан. Реакцию между промежуточными соединениями формулы(V-b) и (VI) проводят в присутствии пригодного основания, например, такого как K2CO3, и в растворителе, таком как н-бутанол. Перемешивание, повышенные температуры и/или давление могут увеличить скорость реакций, которые можно проводить при микроволновом нагревании или традиционном нагревании на масляной бане. В конкретном случае, где R4a представляет собой Н, получают соединения, где Het1 имеет формулу Соединения формулы (II), где все переменные определены так, как указано выше, также можно получать реакцией конденсации между промежуточным соединением формулы (VII) и промежуточным соединением формулы (VIII) или реакцией конденсации между промежуточным соединением формулы(VII) и промежуточным соединением формулы (VIIIa), согласно схеме 3. Схема 3 Реакцию, представленную на схеме 3, можно проводить в присутствии источника аммония, такого как NH4OAc, в растворителях, таких как АсОН, или в присутствии основания, такого как K2CO3 илиNaOAc, и в растворителе, таком как н-бутанол (n-BuOH) или диоксан. Перемешивание, повышенные температуры и/или давление могут увеличить скорость реакции, которую можно проводить при микроволновом или традиционном нагревании. Промежуточные соединения формулы (VIIIa) можно получать из промежуточного соединения формулы (VIII) с использованием способа, сходного со способом, описанным в экспериментальной методике 6. Экспериментальная методика 4. Соединения формулы (I) можно получать реакцией сочетания между промежуточными соединениями формулы (IX) и формулы (X), согласно схеме 4. Схема 4 На схеме 4 LG предпочтительно представляет собой Cl, Br или I. Реакцию можно проводить в присутствии галогенида металла, такого как CuI, и в присутствии основания, такого как Cs2CO3. Реакцию можно проводить в реакционно-инертном растворителе (например, DMF). Может присутствовать лиганд, такой как DMEN, (1R,2R)-(-)-1,2-диаминоциклогексан или 1,10-пентантролин. Экспериментальная методика 5. Соединение формулы (I) можно получать реакцией перекрестного сочетания Сузуки-Мияуры между промежуточными соединениями формулы (XI) и формулы (XII) согласно схеме 5. В формуле (XII) LG предпочтительно представляет собой Cl или Br, и в формуле (XI) B(OR)2 относится к бороновой кислоте В(ОН)2 или ее соответствующему боронатному сложному эфиру, такому как пинаколовый эфир. Реакция может катализироваться катализатором на основе Pd, таким как Pd(PPh3)4 или PdCl2(dppf). Реакцию проводят в присутствии основания, такого как K2CO3 или K3PO4, и в реакционно-инертном растворителе,таком как толуол, DMF или CH3CN, и она может включать H2O. Перемешивание, повышенные температуры (например, 50-120 С) и/или давление могут увеличить скорость реакции, которую можно проводить при микроволновом или традиционном нагревании. Схема 5 Альтернативно промежуточное соединение бороновую кислоту или промежуточное соединение боронатный сложный эфир также можно заменять соответствующим производным трифторборатом калия,которое можно легко получать с использованием типичных условий реакции, известных специалистам в данной области. Экспериментальная методика 6. Промежуточное соединение формулы (V-a), где все переменные определены так, как указано выше,можно получать реакцией нитрила (V-b) с этанолом (EtOH) в кислых условиях, например, таких как HCl,согласно схеме 6. Эту реакцию можно проводить в растворителях, например, таких как диэтиловый эфир Экспериментальная методика 7. Промежуточное соединение формулы (V-b), где все переменные определены так, как указано выше,можно получать нуклеофильным ароматическим замещением промежуточного соединения формулы(XIII) (не)замещенным имидазолом или триазолом формулы (IX) согласно схеме 7, где галоген определен как F, Cl или Br и где все другие переменные являются такими, как определено в настоящем документе выше. Реакцию можно проводить в защитной атмосфере, например, такой как атмосфера N2. Перемешивание, повышенные температуры (например, 70-170 С) и/или давление могут увеличить скорость реакции. Реакцию, как правило, проводят в органическом растворителе, например, таком как DMSO,DMF или N-метилпирролидинон (NMP), в присутствии основания, например, такого как K2CO3, Cs2CO3 или Et3N. Согласно схеме 7 реакцию можно проводить в присутствии медного катализатора. Соли меди, например, такие как оксид меди(I), йодид меди(I) или бромид меди(I), можно использовать в каталитических или стехиометрических количествах. Схема 7 Экспериментальная методика 8. Промежуточное соединение формулы (VII), где все переменные определены так, как указано выше,можно получать обработкой промежуточного соединения формулы (XIV-а) гидратом гидразина в растворителях, таких как EtOH, согласно схеме 8. Эту реакцию можно проводить в защитной атмосфере,например, такой как атмосфера N2. Эту реакцию, как правило, можно проводить в автоклаве при повышенных температурах (например, 120-130 С). Промежуточное соединение формулы (VII) также можно получать стандартной реакцией образования амидной связи с использованием гидразина в качестве источника амина и промежуточного соединения формулы (XIV-b) в качестве источника карбоновой кислоты. В качестве альтернативы гидразину для образования амидной связи можно использовать Bocзащищенный гидразин, после чего из полученного Boc-защищенного амида гидразида можно удалять защитную группу стандартными способами удаления Boc-защитной группы (такими как обработка TFA или HCl). Промежуточные соединения формулы (XIV-а) можно получать из промежуточного соединения формулы (XIV-b) реакцией этерификации с использованием типичных условий реакции, известных специалистам в данной области, например, путем обработки промежуточного соединения формулы (XIV-b) спиртовым растворителем, например, таким как МеОН или EtOH, в кислых условиях. В экспериментальной методике 8 гидразин также можно заменять замещенным гидразином формулы H2N-NH-R4a, где R4a является таким, как определено выше. Схема 8 Экспериментальная методика 9. Промежуточное соединение формулы (XIV-а или XIV-b), где все переменные определены так, как указано выше, можно получать катализируемой Pd реакцией встраивания СО в промежуточное соединение (XV) согласно схеме 9, где галоген определен как Br, Cl или I и где все другие переменные являются такими, как определено в настоящем документе выше. Перемешивание, повышенные температуры (например, 150 С) и/или давление могут увеличить скорость реакции. Реакцию осуществляют под газообразным СО и, как правило, проводят в органическом растворителе, например, таком как THF. В присутствии спиртовых растворителей, таких как метанол (MeOH), получают промежуточные соединения формулы (XIV-а). Реакция катализируется источником Pd, например, таким как Pd(OAc)2, Pd2(dba)3 или Экспериментальная методика 10. Промежуточное соединение формулы (XV), где все переменные определены так, как указано выше,можно получать преобразованием аминогруппы в промежуточном соединении (XVI) в группу галогена,известным как реакция Зандмейера. На схеме 10 галоген определен как I, Br или Cl, и все другие переменные являются такими, как определено в настоящем документе выше. Промежуточное соединение(XVI) сначала преобразуют в соответствующую соль диазония путем обработки NaNO2 в кислых условиях, а затем обрабатывают источником галогенида, например, таким как KI, CuBr или CuCl. Можно использовать типичные условия реакции, известные специалистам в данной области. Схема 10 Экспериментальная методика 11. Промежуточное соединение формулы (XVI), где все переменные определены так, как указано выше, можно получать восстановлением промежуточного соединения формулы (XVII) согласно схеме 11. Восстановление промежуточного соединения (XVII) до промежуточного соединения (XVI) можно проводить традиционным способом, например, таким как восстановительная гидрогенизация или восстановление металлом или солью металла и кислотой [например, металлом, таким как Fe, или солью металла,такой как SnCl2, и кислотой, такой как неорганическая кислота (HCl, H2SO4 сходные с ними) или органической кислотой (АсОН или сходные с ней)]. Альтернативно можно использовать другие хорошо известные способы преобразования нитрогруппы в соответствующий ей амин. Схема 11 Экспериментальная методика 12. Промежуточное соединение формулы (XVII), где все переменные определены так, как указано выше, можно получать нуклеофильным ароматическим замещением промежуточного соединения (XVIII)(не)замещенным имидазолом или триазолом формулы (IX) согласно схеме 12, где LG предпочтительно представляет собой F, Cl или Br и где все другие переменные являются такими, как определено в настоящем документе выше. Реакцию можно проводить в защитной атмосфере, например, такой как атмосфера N2. Перемешивание, повышенные температуры (например, 70-170 С) и/или давление могут увеличить скорость реакции. Реакцию, как правило, проводят в органическом растворителе, например, таком как DMSO, DMF или N-метилпирролидинон (NMP), в присутствии основания, например, такого какK2CO3, Cs2CO3 или Et3N. Реакцию можно проводить в присутствии медного катализатора. Соли меди,например, такие как оксид меди(I), йодид меди(I) или бромид меди(I), можно использовать в каталитических или стехиометрических количествах. Экспериментальная методика 13. Промежуточное соединение формулы (XV), где по меньшей мере один из А 1 или А 3 представляет собой N и где все другие переменные являются такими, как указано выше, таким образом, названное промежуточным соединением формулы (XV-a), можно получать нуклеофильным ароматическим замещением промежуточного соединения формулы (XIX), где по меньшей мере один из А 1 или А 3 представляет собой N, необязательно замещенным имидазолом или триазолом формулы (IX) согласно схеме 13,где LG предпочтительно представляет собой F, Cl или Br, где галоген определен как Br или I и где все другие заместители являются такими, как определено в настоящем документе выше. Реакцию можно проводить в сходных условиях, как описано для экспериментальной методики 12. Схема 13 Экспериментальная методика 14. Промежуточное соединение формулы (XV), где X представляет собой СН и где все другие переменные являются такими, как указано выше, таким образом, названное промежуточным соединением формулы (XV-b), также можно получать ацилированием промежуточного соединения (XX) с получением промежуточного соединения (XXI), в присутствии реакционно-инертного растворителя, например, такого как THF, и необязательно пригодного основания, такого как Et3N, согласно схеме 14. Промежуточное соединение формулы (XXIII) можно затем получать алкилированием промежуточного соединения формулы (XXI) промежуточным соединением формулы (XXII) в присутствии реакционно-инертного растворителя, например, такого как DMF, и пригодного основания, например, такого как Cs2CO3 или K2CO3, и необязательно в присутствии каталитического количества йодидной соли, например, такой как KI илиNaI. Затем реакция конденсации промежуточного соединения (XXIII) с источником аммиака, например,таким как NH4(OAc), приводит к соединению формулы (XV-b). На схеме 14 галоген определен как Cl, Br или I, LG предпочтительно представляет собой Cl или Br, и все другие переменные являются таким, как определено в настоящем документе выше. Схема 14 Экспериментальная методика 15. Промежуточное соединение формулы (X), где Het1 ограничен до гетероциклов формулы (а), где La определен, как в экспериментальной методике 1, и где все другие переменные определены как в соединениях формулы (I), таким образом, названное промежуточным соединением формулы (Х-а), можно получать 2-стадийной последовательностью реакций, начиная с реакции конденсации между промежуточным соединением формулы (XXIV) и промежуточным соединением формулы (VIII) с получением промежуточного соединения формулы (XXV), согласно схеме 15. Эту реакцию проводят в присутствии пригодного основания, например, такого как K2CO3, и в растворителе, таком как н-бутанол. Реакцию можно проводить при микроволновом нагревании или при традиционном нагревании на масляной бане. На второй стадии промежуточное соединение формулы (XXV) можно замещать R4-LG, например, таким как арилгалогенид или алкилгалогенид (галогенид представляет собой I, Cl, Br или F), с получением проме- 15021047 жуточного соединения формулы (Х-а). Реакцию можно проводить в присутствии основания, например,такого как NaH, в реакционно-инертных растворителях, таких как DMF или THF. Схема 15 Экспериментальная методика 16. Промежуточное соединение формулы (XXIV), где все переменные определены так, как указано выше, можно получать обработкой промежуточного соединения формулы (XXVI) гидратом гидразина в растворителе, например, таком как EtOH, согласно схеме 16. Эту реакцию можно проводить в защитной атмосфере, например, такой как атмосфера N2. Эту реакцию, как правило, проводят в автоклаве при повышенных температурах (например, 120-130 С). Схема 16 Аналогично гидразиды формулы (VI) можно получать из соответствующих алкиловых сложных эфиров карбоновых кислот и требуемых гидразинов. Экспериментальная методика 17. Промежуточное соединение формулы (XI), где все переменные определены так, как указано выше,можно получать реакцией перекрестного сочетания Сузуки-Мияуры между промежуточным соединением формулы (XV) и соединениями бора, такими как пинаколатдиборан, согласно схеме 17. На схеме 17 галоген определен как I, Br или Cl, и B(OR)2 относится к боронатному сложному эфиру или его соответствующей кислоте В(ОН)2. Эта реакция катализируется катализатором на основе Pd, например, таким какK2CO3 или K3PO4, и в реакционно-инертном растворителе, таком как DMF, MeCN или диоксан, и также может быть включена H2O. Перемешивание, повышенные температуры (например, 50-120 С) и/или давление могут увеличить скорость реакции, которую можно проводить при микроволновом или традиционном нагревании. Схема 17 Промежуточное соединение формулы (XI) также можно превращать в соответствующее производное калий с трифторборатом калия с использованием типичных условий реакции, известных специалистам в данной области, которые можно затем использовать в качестве альтернативы (XI) в реакциях сочетания Сузуки, таких как описаны в экспериментальной методике 5. Экспериментальная методика 18. Промежуточное соединение формулы (XII), где Het1 ограничен до гетероциклов формулы (а), где La представляет собой прямую связь и где все другие переменные определены, как в соединениях формулы(I), таким образом, названное промежуточным соединением формулы (XII-a), можно получать, начиная с замещения промежуточного соединения (XXVII) посредством R4a, например, алкилированием алкилгалогенидом, с последующей региоселективной реакцией перекрестного сочетания Сузуки-Мияуры между полученным промежуточным соединением формулы (XXVIII) и соединением бора (XXIX) согласно схеме 18. На схеме 18 LG предпочтительно представляет собой Cl или Br, галоген определен как I, Br или Cl и B(OR)2 относится к бороновой кислоте В(ОН)2 или ее соответствующему боронатному сложному эфиру. Реакция перекрестного сочетания Сузуки-Мияуры катализируется катализатором на основе Pd, например, таким как Pd(PPh3)4 или PdCl2(dppf), и ее проводят в присутствии пригодного основания, например, такого как K2CO3 или K3PO4, и в реакционно-инертном растворителе, таком как DMF, MeCN, и также может быть включена H2O. Эту реакцию, как правило, проводят при комнатной температуре (к.т.),однако повышенные температуры (например, 40-50 С) и/или давление могут увеличить скорость реакции. Схема 18 Экспериментальная методика 19. Как правило, соединения формулы (I), где Het1 ограничен до (с), R6c представляет собой водород и где все другие переменные являются такими, как определено в настоящем документе выше, таким образом, названные соединениями формулы (XXX), можно получать конденсацией промежуточного соединения формулы (XXXI) с промежуточным соединением формулы (XXXII) в присутствии источника аммиака, такого как NH4OAc, согласно схеме 19. Реакцию можно проводить в кислотном растворителе,таком как АсОН, с использованием повышенных температур (например, 100-180 С), которые могут быть достигнуты с помощью микроволнового или традиционного нагревания. Схема 19 Экспериментальная методика 20. Соединения формулы (I), где Het1 ограничен до (с), R6c представляет собой метил и где все другие переменные являются такими, как определено в настоящем документе выше, таким образом, названные соединениями формулы (XXXIII), можно получать алкилированием соединения (XXX) с помощью CH3I согласно схеме 20. Реакцию можно проводить в присутствии основания, например, такого как NaH, в реакционно-инертных растворителях, таких как DMF или THF. Схема 20 Экспериментальная методика 21 Промежуточное соединение формулы (XXXI), где все переменные определены так, как указано выше, можно получать нуклеофильным ароматическим замещением альдегидного промежуточного соединения (XXXIV) (не)замещенным имидазолом или триазолом формулы (IX) согласно схеме 21, где LG предпочтительно определен как F, Cl или Br и где все другие переменные являются такими, как определено в настоящем документе выше. Реакцию можно проводить в защитной атмосфере, например, такой как атмосфера N2. Перемешивание, повышенные температуры (например, 70-170 С) и/или давление могут увеличить скорость реакции. Реакцию, как правило, проводят в органическом растворителе, например, таком как DMSO, DMF или N-метилпирролидинон (NMP), в присутствии основания, например, такого как K2CO3, Cs2CO3 или Et3N. Реакцию можно проводить в присутствии медного катализатора. Соли меди, например, такие как оксид меди(I), йодид меди(I) или бромид меди(I), можно использовать в каталитических или стехиометрических количествах. Схема 21 Экспериментальная методика 22. В общем, соединения формулы (I), где Het1 ограничен до (а), и где La представляет собой NR9, и где все другие переменные являются такими, как определено в настоящем документе выше, таким образом,названные соединениями формулы (III-а), можно получать согласно схеме 22 путем превращения производного N-ацилкарбоимидотионовой кислоты в виде метилового сложного эфира общей формулы(XXXV) в 1,2,4-триазолы формулы (III-а) с использованием соответствующего гидразина (XXXVI) в известных в данной области условиях. Это превращение, как правило, проводят в протонном растворителе,таком как МеОН или высший спирт, и оно требует температуры между комнатной температурой и 150 С. В конкретном варианте осуществления высший спирт представляет собой третичный бутиловый спирт и температура реакции составляет от 70 до 120 С, наиболее предпочтительно 100 С. Для реакций,где гидразин (XXXVI) используют в качестве соли HCl, предпочтительным является добавление стехиометрического количества основания. Указанное основание может представлять собой неорганическое основание, такое как ацетат калия или карбонат калия, более предпочтительно, указанное основание представляет собой третичный амин, такой как диизопропилзтиламин или сходные с ним (схема 22). Как правило, получают смеси соединений формулы (III-а) и региоизомерных соединений формулы(IV-а). Соединения формулы (IV-a), где R6b определен как метил, представляют собой соединения формулы (I), где Het1 ограничен до (b), где L представляет собой NR9, и где R6 представляет собой метил. Схема 22 Соединения формулы (I), где Het1 ограничен до (а), где La представляет собой NR9-C1-4 алкандиил и где все другие переменные являются такими, как определено в настоящем документе выше, можно получать по аналогии со схемой 22. Экспериментальная методика 23. Промежуточное соединение формулы (XXXV), где все переменные определены так, как указано выше, можно получать с помощью протокола, который состоит из 3 синтетических превращений (схема 23), начиная с ацилхлорида формулы (XXXVII), который можно получать обработкой карбоновой кислоты (XIV-b) избытком оксалилхлорида или тионилхлорида, необязательно в присутствии DMF в качестве катализатора, при повышенной температуре, в частности, при температуре кипячения с обратным холодильником. Указанное превращение также можно проводить в присутствии органического растворителя,такого как дихлорметан или сходные с ним. На первой стадии агент ацилирования, такой как ацилхлорид(XXXVII), смешанный или симметричный ангидрид, ацилфторид и т.п., подвергают реакции с одновалентным катионом тиоцианата (MNCS на схеме 23), например, таким как тиоцианат калия или тиоцианат аммония, с получением соответствующего ацилизотиоцианата. Эту реакцию обычно проводят с использованием ацетона в качестве растворителя и при температуре от 0 до 70 С, предпочтительно при к.т. Промежуточное соединение ацилизотиоцианат не выделяют, а обрабатывают в той же реакционной среде соответствующим амином (XXXVIII) с получением N-ацилтиомочевины общей формулы (XXXIX). Эту реакцию превращения обычно проводят при температуре от 0 до 70 С, предпочтительно при к.т. На конечной стадии S-метилирование N-ацилтиомочевины (XXXIX) обеспечивает производное Nацилкарбоимидотионовой кислоты в виде метилового сложного эфира общей формулы (XXXV). Экспериментальная методика 24. Соединения формулы (III), где R4a не является водородом и где все другие переменные являются такими, как указано выше (см. экспериментальную методику 1), также можно получать ацилированием промежуточного соединения формулы (V-a) промежуточным соединением формулы (XL), представляющим собой кислый хлорид, с последующей реакцией конденсации с промежуточным соединением формулы (XXXVI), представляющим собой гидразин, согласно схеме 24. Схема 24 Реакцию между промежуточными соединениями формулы (V-a) и (XL) проводят в присутствии пригодного основания, например, такого как пиридин или Et3N, и в растворителе, таком как толуол, дихлорэтан, DCM, хлороформ. Эту реакцию, как правило, проводят при к.т., однако повышенные температуры (например, 40-120 С) могут увеличить скорость реакции. Как правило, (XXXVI) добавляют в неочищенную реакционную смесь (р.с), полученную после ацилирования. Стадию конденсации в (III) проводят при повышенных температурах (например, 40-120 С), необязательно в присутствии основания,например, такого как пиридин или Et3N. Как правило, также получают региоизомерные соединения формулы (IV), которые представляют собой соединения формулы (I), где Het1 ограничен до (b) и где R6 представляет собой метил. Экспериментальная методика 25. Соединения формулы (III-а), где R9 ограничен до водорода и где все переменные являются такими,как определено выше, таким образом, названные соединениями (XLI), также можно получать согласно схеме 25 реакцией конденсации между промежуточным соединением формулы (XLIII) и производным гидразина формулы (XXXVI), где R4a/6b ограничен до R4a и, таким образом, названным соединением формулы (XLII). Это превращение, как правило, проводят в протонном растворителе, таком как МеОН или высший спирт, и оно требует температуры между к.т. и 100 С. Схема 25 Экспериментальная методика 26. Промежуточное соединение формулы (XLIII), где все переменные определены так, как указано выше, можно получать реакцией промежуточного соединения формулы (V-a) с арилизотиоцианатом формулы (XLIV) согласно схеме 26. Эту реакцию, как правило, проводят в реакционно-инертном растворителе, таком как Et2O, THF, ацетон или CH3CN, и при температуре между к.т. и 70 С. Экспериментальная методика 27. Промежуточное соединение формулы (XII) можно получать превращением аминогруппы промежуточного соединения (XLV) в уходящую группу (LG) (реакция Зандмейера). На схеме 27 LG предпочтительно представляет собой Cl, Br или I. Промежуточное соединение (XLV) сначала превращают в соответствующую соль диазония посредством обработки NaNO2 или трет-бутилнитритом в реакционноинертном растворителе, таком как CH3CN, в нейтральных или кислых условиях, затем обрабатывают источником галогенида, например, таким как CuBr, CuBr2, CuCl или 1,2-дийодэтан. Это превращение требует температуры между к.т. и 80 С. Схема 27 Экспериментальная методика 28. Промежуточное соединение формулы (XLV), где Het1 ограничен до гетероциклов формулы (а), гдеL ограничен до NH и где все другие переменные являются такими, как определено для соединений формулы (I), таким образом, названное промежуточным соединением формулы (XLV-b), можно получать,согласно схеме 28, конденсацией промежуточного соединения формулы (XLVI) и производного гидразина (XLII). Эту трансформацию, как правило, проводят в протонном растворителе, таком как изопропанол, в условиях кипячения с обратным холодильником. Схема 28 Экспериментальная методика 29. Промежуточное соединение формулы (XLVI), где все переменные определены так, как указано выше, можно получать, согласно схеме 29, реакцией анилина формулы (XLVII) и дифенил-Nцианокарбоимидата (XLVIII). Эту реакцию, как правило, проводят либо в отсутствие основания в протонном растворителе, таком как изопропанол, и в условиях нагревания, либо в присутствии основания,например, такого как гексаметилдисилазид лития, в реакционно-инертном растворителе, таком как THF,и при к.т. Схема 29 Экспериментальная методика 30. Промежуточное соединение формулы (XII), где Het1 ограничен до гетероциклов формулы (а), где La ограничен до NH и где все другие переменные являются такими, как определено для соединений формулы (I), таким образом, названное промежуточным соединением формулы (XII-b), можно получать реакцией промежуточного аминосоединения формулы (XLVII) с промежуточным соединением формулы(XXVIII), где все переменные определены так, как указано выше, как на схеме 30. Эту реакцию, как правило, проводят в присутствии основания, например, такого как гексаметилдисилазид лития, в реакционно-инертном растворителе, таком как THF, и при температуре между к.т. и 70 С. Схема 30 Экспериментальная методика 31. Промежуточное соединение формулы (XLIX), где все переменные определены так, как указано выше, можно получать согласно схеме 31 реакцией между амином формулы (L) и промежуточным соединением формулы (XXVIII). Эту реакцию проводят в присутствии пригодного основания, например, такого как Na2CO3 или K2CO3, и в растворителе, например, таком как DMF, DMA или DMSO. Эту реакцию,как правило, проводят при повышенных температурах (например, 100-160 С). Перемешивание и условия микроволнового нагревания могут увеличить скорость реакции. Схема 31 Экспериментальная методика 32. Соединение формулы (XLI) также можно получать согласно схеме 32 реакцией между промежуточным соединением формулы (LI) и промежуточным соединением формулы (LII), где все переменные определены так, как указано выше. Эту реакцию проводят в присутствии пригодного основания, например, такого как Na2CO3, K2CO3 или Cs2CO3, и в растворителе, например, таком как DMF, DMA илиDMSO. Эту реакцию, как правило, можно проводить в присутствии медного катализатора, такого как йодид меди(I), и в присутствии лиганда, такого как диаминопроизводное, например DMEN, и при повышенных температурах, например, 100-200. Перемешивание и условия с использованием микроволнового облучения могут увеличить скорость реакции. Схема 32 Экспериментальная методика 33. Промежуточное соединение формулы (LI) можно получать согласно схеме 33 путем селективного удаления защитной группы (PG) промежуточного соединения формулы (LIII), где все переменные определены так, как указано выше. В типичном примере, когда PG представляет собой бензил, реакцию можно проводить в условиях гидрогенолиза, хорошо известных специалисту в данной области. Схема 33 Промежуточное соединение формулы (LIII) можно легко получать с помощью следующих экспериментальных методик, сходных с методиками 31 и 5, последовательно. Экспериментальная методика 34. Соединение формулы (I), где Het1 ограничен до (а), и где La представляет собой S, и где все другие переменные являются такими, как определено в настоящем документе выше, таким образом, названное соединением формулы (LIV), где все переменные определены так, как указано выше, можно получать согласно схеме 34 реакцией между промежуточным соединением формулы (LV) и промежуточным соединением формулы (LII). В формуле (LII) LG предпочтительно представляет собой Br или I. Эту реакцию проводят в присутствии пригодного основания, например, такого как Na2CO3, K2CO3 или Cs2CO3, и в растворителе, например, таком как DMF, DMA или диоксан. Эта реакция катализируется катализатором на основе Pd, таким как Pd2(dba)3, и в присутствии лиганда, например, такого как 9,9-диметил-4,5 бис-(дифенилфосфино)ксантен. Эту реакцию можно проводить при температуре от 70 до 120 С. Схема 34 Промежуточное соединение формулы (LV) можно получать в качестве побочного продукта, когда проводят экспериментальную методику 25. Экспериментальная методика 35. Промежуточное соединение формулы (XLIV), где R5a ограничен до Ar2, таким образом, названное соединением (XLIV-a) можно получать, как на схеме 35, путем реакции промежуточного соединения формулы (LVI) с реагентом переноса тиокарбонила, например, таким как 1,1'-тиокарбонил-2,2'-пиридон или тиофосген. Эту реакцию, как правило, проводят в реакционно-инертном растворителе, например,таком как DCM, при к.т. Схема 35 Экспериментальная методика 36. Промежуточное соединение формулы (V-b), где все переменные определены так, как указано выше,также можно получать цианированием промежуточного соединения формулы (XV), где галоген определен как Br, Cl или I, как представлено на схеме 36. Эту реакцию проводят в присутствии пригодного основания, например, такого как Na2CO3, K2CO3, и в растворителе, например, таком как DMF, DMA илиDMSO. Эту реакцию, как правило, проводят в присутствии источника цианида, например, такого как цианид цинка, и она катализируется катализатором на основе Pd, например, таким как Pd(PPh3)4. Перемешивание, повышенные температуры (например, 100-160 С) и/или давление могут увеличить скорость реакции, которую можно проводить при нагревании при микроволновом облучении или традиционном нагревании. Схема 36 Экспериментальная методика 37. Промежуточное соединение формулы (XLV), где Het1 ограничен до гетероциклов формулы (а), гдеL -R и R4a, взятые вместе, образуют двухвалентный радикал, как показано на схеме 37, причем n равно 0, 1 или 2, и где все другие переменные являются такими, как определено для соединений формулы (I),таким образом, названное промежуточным соединением формулы (XLV-c), можно получать реакцией конденсации между промежуточным соединением формулы (LVII), где галоген определен как Cl, Br, I, и аминогуанидиновым соединением (LVIII) согласно схеме 37. Перемешивание при повышенных температурах (например, 40-160 С) и/или давлении могут увеличить скорость реакции, которую можно проводить с использованием микроволнового излучения или традиционного нагревания. Как правило, можно использовать спиртовой растворитель, такой как 2-пропанол (iPrOH). Схема 37 Экспериментальная методика 38. Альтернативно промежуточное соединение формулы (XLV-c) можно получать через промежуточное соединение формулы (LIX), полученное реакцией замещения промежуточного соединения формулы(LVII) гидразином (стадия а), с последующей реакцией конденсации с амидином формулы (LX), несущим уходящую группу LG, такую как бензотриазол (стадия b, схема 38). Реакцию замещения проводят в присутствии пригодного основания, например, такого как NaH, и в реакционно-инертном растворителе,таком как DMF. Эту реакцию, как правило, проводят при низкой температуре или при к.т., однако повышенные температуры (например, 40-160 С) и/или давление могут увеличить скорость реакции, которую можно проводить с использованием микроволнового облучения или традиционного нагревания. Этот тип реакции, как правило, можно проводить в спиртовом растворителе, таком как iPrOH. Схема 38 Экспериментальная методика 39. Промежуточное соединение формулы (XLV), где Het1 ограничен до гетероциклов формулы (а), гдеL -R и R4a, взятые вместе, образуют двухвалентный радикал формулы СН=СН-СН=СН илиCH=CH-N=CH, таким образом, названное промежуточным соединением формулы (XLV-d) (Za представляет собой N, СН или С-С 1-4 алкил (например, С-СН 3, можно получать, начиная с реакции конденсации между промежуточным соединением формулы (LXI) и изотиоцианатным соединением формулы(LXII) в реакционно-инертном растворителе, таком как диоксан, при к.т., согласно схеме 39. Эту реакцию, как правило, проводят при низкой температуре или при к.т., однако повышенные температуры (например, 40-160 С) и/или давление могут увеличить скорость реакции, которую можно проводить с использованием микроволнового излучения или традиционного нагревания. Реакцию конденсации между промежуточным соединением формулы (LXIII) и источником амина, таким как гидроксиламин, с получением промежуточного соединения (XLV-d), как правило, можно проводить в подходящем спиртовом растворителе, таком как EtOH или МеОН, при к.т., однако повышенные температуры (например, 40160 С) при микроволновом излучении и/или под давлением могут увеличить скорость реакции. Схема 39 Аналогичной процедуре реакции можно следовать для получения промежуточных соединений формулы (XLV-d), где двухвалентный радикал La-R5a-L4a формулы СН=СН-СН=СН или CH=CHN=CH дополнительно замещен заместителями, как определено для соединений формулы (I). В этом случае, как правило, проводят опосредуемую Pd реакцию сочетания промежуточного соединения формулы (LXIV), например, с соответствующим соединениями амина, фенола, бороновой кислоты или сложного эфира, с получением промежуточного соединения формулы (LXI-a), которое можно далее подвергать реакции согласно схеме 39. Галоген определен как Br, Cl или I; Za определен, как упомянуто выше в настоящем документе. Это проиллюстрировано ниже на схеме 39 а. Схема 39 а Альтернативно промежуточные соединения формулы (XLV-d), где двухвалентный радикал La-R5aLформулы СН=СН-СН=СНили CH=CH-N=CH дополнительно замещен заместителями, как определено для соединений формулы (I), таким образом, названные промежуточными соединениями формулы (XLV-e), можно получать превращением промежуточного соединения, например, такого как промежуточное соединение формулы (LXIV), в промежуточное соединение формулы (XLV-f), следуя протоколу реакции, описанному на схеме 39. Затем промежуточное соединение формулы (XLV-f) можно превращать в промежуточное соединение формулы (XLV-e) в опосредуемой Pd реакции сочетания, например, с соответствующим соединением амина, фенола или бороновой кислоты или сложного эфира. Это проиллюстрировано ниже на схеме 39b. Все переменные являются такими, как указано для схемы 39 а. Схема 39b 4a В случае, когда заместитель в формуле (LXI-a) или (XLV-e) представляет собой Ar3, промежуточное соединение формулы (LXIV) или (XLV-f) соответственно, как правило, можно подвергать реакции с производным Ar3 и бороновой кислоты (Ar3-В(ОН)2) или сложного эфира (Ar3-B(OR)2). Эту реакцию сочетания можно проводить в пригодном растворителе, например, таком как диоксан, в присутствии катализатора на основе Pd, такого как Pd(PPh3), и основания, такого как NaHCO3, в присутствии H2O. Реакцию можно проводить с использованием микроволнового излучения или традиционного нагревания (например, 150 С). В случае, когда заместитель в формуле (LXI-a) или (XLV-e) представляет собой NR11-Ar3, промежуточное соединение формулы (LXIV) или (XLV-f) соответственно, как правило, можно подвергать реакции с производным Ar3 с амином (Ar3-NHR11). Эту реакцию сочетания можно проводить в пригодном растворителе, например, таком как t-BuOH, в присутствии катализатора на основе Pd, такого какPd2(dba)3, и основания, такого как Cs2CO3. Реакцию можно проводить в присутствии лиганда, например,такого как X-Phos. Как правило, реакцию можно проводить с использованием традиционного нагревания точное соединение формулы (LXIV) или (XLV-f) соответственно, как правило, можно подвергать реакции с фенольным производным (НО-Ar3) Ar3. Эту реакцию сочетания можно проводить в пригодном растворителе, таком как N,N-диметилацетамид (DMA), в присутствии медного катализатора. Используют соли меди, например, такие как Cu2O, CuI или CuBr. Обычно к р.с. добавляют основание, такое какK2CO3. Как правило, реакцию можно проводить с использованием традиционного нагревания (например,150-175 С). В случае, когда заместитель в формуле (LXI-a) или (XLV-e) представляет собой (С=O)-Ar3 или С 1-4 алкилкарбонил, промежуточное соединение формулы (LXIV) или (XLV-f) соответственно, как правило, можно подвергать реакции с соответствующим альдегидом Ar3 (Ar3-(С=О)Н) или С 1-4 алкилом(C1-4 алкил-(С=O)H). Эту реакцию сочетания, как правило, можно проводить в присутствии металлоорганического соединения, в частности, литийорганического реагента, такого как н-бутиллитий. Обычно реакцию можно проводить в пригодном растворителе, например, таком как THF. На конечной стадии гидроксильную группу можно окислять до соответствующего кетона с использованием условий реакции,известных специалистам в данной области. В случае, когда заместитель в формуле (LXI-a) или (XLV-e) представляет собой С 1-4 алкил, промежуточное соединение формулы (LXIV) или (XLV-f) соответственно, как правило, можно подвергать реакции с соответствующим альдегидом. Эту реакцию сочетания, как правило, можно проводить в присутствии металлоорганического соединения, в частности литийорганического реагента, такого как нбутиллитий. Обычно реакцию проводят в пригодном растворителе, например, таком как THF. Затем гидроксильную группу можно превращать в тозилат реакцией с тозилхлоридом в присутствии основания,например, такого как Et3N, в пригодном растворителе, как правило, таком как DCM. На конечной стадии тозилатную группу можно удалять восстановителем, например, таким как NaBH4, в присутствии спиртового растворителя, такого как МеОН. Реакцию можно проводить при к.т. или при повышенных температурах. Экспериментальная методика 40. Ароматические промежуточные соединения формулы (XLV-d), (XLV-e) и (XLV-f) можно восстанавливать до соответствующих восстановленных (тетрагидро) форм общепринятыми способами, например, такими как восстановительная гидрогенизация или восстановление металлом или солью металла и кислотой [например металлом, таким как Fe, или солью металла, такой как SnCl2, и кислотой, такой как неорганическая кислота (HCl, H2SO4 или сходные с ними) или органическая кислота (АсОН или сходные с ними)]. Альтернативно можно использовать другие хорошо известные способы превращения ароматического соединения в его соответствующую восстановленную форму. Аналогичный протокол реакции можно использовать для превращения соединений формулы (I), гдеR4a и -La-R5a, взятые вместе, образуют двухвалентный радикал формулы СН=СН-СН=СН илиCH=CH-N=CH, в их соответствующие восстановленные формы. Экспериментальная методика 41. Промежуточное соединение формулы (XII), где Het1 ограничен до гетероциклов формулы (а), гдеLG представляет собой Br, где La-R5a и R4a, взятые вместе, образуют двухвалентный радикал, как показано на схеме 41, где n равно 1 или 2 и где все другие переменные являются такими, как определено для соединений формулы (I), таким образом, названное промежуточным соединением формулы (LXV), можно получать, начиная с 3,5-дибром-1 Н-1,2,4-триазола (LXVI), согласно стадиям реакции, представленным на схеме 41. Алкилирование (LXVI) пригодным образом O-замещенным гидроксиэтилгалогенидом(n=1) или гидроксил-н-пропилгалогенидом (n=2) дает промежуточное соединение формулы (LXVII). Обмен литий-галоген в (LXVII), например, посредством обработки (LXVII) n-BuLi при температуре ниже -50 С с последующим добавлением требуемого Ar3-альдегида, дает промежуточное соединение формулы (LXVIII). Затем удаление защитной группы из (LXVIII) с получением (LXIX) с последующей реакцией дегидратации/циклизации, например, посредством обработки (LXIX) кислотой, такой как HCl, метилсульфоновая кислота или п-толуолсульфоновая кислота, в пригодном растворителе, таком как толуол или ксилол, при температурах кипячения с обратным холодильником (условия Дина-Старка), дают промежуточное соединение формулы (LXV). Защитная группа PG должна быть выбрана согласно уровню техники так, чтобы она выдерживала условия реакции на стадиях, ведущих к промежуточному соединению(LXVIII), например, тетрагидропиранильная группа. Условия удаления защитной группы для получения промежуточного соединения (LXIX) можно осуществлять согласно способам, известным в данной области. Экспериментальная методика 42. Соединение формулы (I), где Het1 ограничен до гетероциклов формулы (а), где La-R5a и R4a, взятые вместе, образуют двухвалентный радикал, как показано на схеме 42, где n равно 1 или 2, и А представляет собой прямую связь, О или CR', где R' представляет собой Н или С 1-4 алкил и где все другие переменные являются такими, как определено для соединений формулы (I), таким образом, названное соединением формулы (I-b1), можно получать реакцией конденсации промежуточного соединения формулы(VII) с промежуточным соединением формулы (LXX). В формуле (LXX) галоген определен как Cl, Br, I,предпочтительно Cl, Br. Схема 42 Реакцию, представленную на схеме 42, можно проводить в присутствии основания, такого как имидазол, триэтиламин (Et3N), K2CO3 или NaOAc, и в растворителе, таком как МеОН, EtOH, n-BuOH или диоксан. Перемешивание, повышенные температуры и/или давление могут увеличить скорость реакции,которую можно проводить при нагревании микроволновым излучением или при традиционном нагревании на масляной бане. Промежуточные соединения формулы (LXX) можно получать, начиная с промежуточного соединения формулы (LXXI), с использованием способов, известных в данной области, например, как описано в экспериментальной методике 6. Экспериментальная методика 43. Альтернативно соединение формулы (I-b1) можно получать реакцией конденсации промежуточного соединения формулы (LXXII) с промежуточным соединением формулы (V-a). В формуле (LXXII) галоген определен как Cl, Br, I, предпочтительно Cl, Br. Схема 43 Реакцию, представленную на схеме 43, можно проводить в присутствии основания, такого как имидазол, Et3N, K2CO3 или NaOAc, и в растворителе, таком как МеОН, EtOH, n-BuOH или диоксан. Перемешивание, повышенные температуры и/или давление могут увеличить скорость реакции, которую можно проводить при нагревании микроволновым излучением или традиционном нагревании на масляной бане. Промежуточные соединения формулы (LXXII) можно получать, начиная с промежуточного соединения формулы (LXXIII), с использованием способов, известных в данной области, например, как описано в экспериментальной методике 8. Экспериментальная методика 44. Соединение формулы (I), где Het1 ограничен до гетероциклов формулы (а), где La-R5a и R4a, взятые вместе, образуют двухвалентный радикал, как показано на схеме 44, где n равно 0, 1 или 2, А представляет собой СН или N и где все другие переменные являются такими, как определено для соединений формулы (I), таким образом, названное соединением формулы (I-b2), можно получать реакцией конден- 25021047 сации промежуточного соединения формулы (LXXIV) с промежуточным соединением формулы (V-a). Схема 44 Реакцию, представленную на схеме 44, можно проводить в присутствии основания, такого какK2CO3, имидазол, Et3N или NaOAc, и в растворителе, таком как МеОН, EtOH, n-BuOH или диоксан. Перемешивание, повышенные температуры и/или давление могут увеличить скорость реакции, которую можно проводить при нагревании микроволновым излучением или традиционном нагревании на масляной бане. Экспериментальная методика 45. Альтернативно соединение формулы (I-b2) можно получать реакцией образования амидной связи между промежуточным соединением формулы (XIV-b) или (XXXVII) и промежуточным соединением формулы (LXXIV) с получением промежуточного соединения формулы (LXXV), с последующей обработкой (LXXV) посредством POCl3 при повышенных температурах, находящихся в диапазоне от 80 С до температуры кипячения с обратным холодильником, и последующей реакцией в присутствии источника аммония, такого как NH4OAc, в растворителях, таких как АсОН. Для последней реакции, как правило,используют повышенные температуры, например, 130-160 С, и ее можно проводить при нагревании микроволновым излучением или традиционном нагревании на масляной бане. Схема 45 Экспериментальная методика 46. Соединение формулы (J), где Het1 ограничен до гетероциклов формулы (а), где La-R5a и R4a, взятые вместе, образуют двухвалентный радикал, как показано на схеме 46, причем п равно 1 или 2, и А представляет собой прямую связь, О или CR1, причем R1 представляет собой Н или С 1-4 алкил, где стереохимия указанного атома углерода имеет S-конфигурацию, где все другие переменные являются такими, как определено для соединений формулы (I), таким образом, названное соединением формулы (I-b3), можно получать путем хирального разделения соответствующего рацемического соединения формулы (I-b1) с использованием способов, известных в данной области. Например, можно использовать препаративнуюCO2 в комбинации с CH3CN или МеОН с 0,2% 2-пропиламином. Очевидно, также этим способом можно получать соответствующие R-энантиомеры. Предпочтительными являются S-энантиомеры. Схема 46 Промежуточные соединения формул (VI), (VIII), (IX), (XIII), (XVIII), (XIX), (XX), (XXII), (XXVI),(XXVIII), (XXXII), (XXXIV), (XXXVI), (XXXVIII), (XL), (XLII), (XLIV), (XLVII), (XLVIII), (L), (LII),(LVI), (LVII), (LIX), (LX), (LXI), (LXII), (LXIV), (LXVI), (LXXI), (LXXIII), (LXXIV) коммерчески доступны или могут быть легко получены специалистами в данной области. Где необходимо или желательно, можно проводить одну или несколько из следующих дополнительных стадий в любом порядке: Промежуточные соединения формулы (X), (XII) или (XLV) и соединения формулы (I), любую их подгруппу, аддитивные соли, сольваты и стереохимические изомерные формы можно превращать в другие промежуточные соединения и соединения согласно изобретению с использованием способов, известных в данной области. Специалистам в данной области будет понятно, что в способах, описанных выше, функциональные группы промежуточных соединений может быть необходимо блокировать защитными группами. В случае, когда функциональные группы промежуточных соединений блокировали защитными группами, защитную группу можно было удалить после стадии реакции. Фармакология. Было найдено, что соединения по настоящему изобретению модулируют активность -секретазы. Соединения согласно изобретению и их фармацевтически приемлемые композиции, таким образом, могут быть пригодны для лечения или профилактики AD, TBI, MCI, старческой деменции, деменции, деменции с тельцами Леви, церебральной амилоидной ангиопатии, мультиинфарктной деменции, синдрома Дауна, деменции, ассоциированной с болезнью Паркинсона, или деменции, ассоциированной с бетаамилоидом, предпочтительно AD. Соединения в соответствии с настоящим изобретением и их фармацевтически приемлемые композиции могут быть пригодны для лечения или профилактики заболевания или состояния, выбранного из группы, состоящей из AD, TBI, MCI, старческой деменции, деменции, деменции с тельцами Леви, церебральной амилоидной ангиопатии, мультиинфарктной деменции, синдрома Дауна, деменции, ассоциированной с болезнью Паркинсона, или деменции, ассоциированной с бета-амилоидом. Как используют в настоящем документе, термин "модулирование активности -секретазы" относится к эффекту на процессинг АРР -секретазным комплексом. Предпочтительно он относится к эффекту, в котором общая скорость процессинга АРР остается, по существу, такой, как без применения указанных соединений, но в котором изменяются относительные количества процессированных продуктов, более предпочтительно таким образом, что количество продуцированного А 42-пептида снижается. Например, могут образовываться различные типы А-бета (например, А-бета-38 или другие типы пептида Абета с более короткой аминокислотной последовательностью вместо А-бета-42) или относительные количества продуктов отличаются (например, изменяется отношение А-бета-40 к А-бета-42, предпочтительно увеличивается). Ранее было показано, что -секретазный комплекс также вовлечен в процессинг белка Notch. Notch представляет собой белок передачи сигнала, который играет важную роль в процессах развития (например, рассмотрено в Schweisguth F (2004), Curr. Biol. 14, R129). Что касается применения модуляторов усекретазы в терапии, кажется особенно преимущественным не вмешиваться в активность процессингаNotch -секретазы, чтобы избежать предполагаемых нежелательных побочных эффектов. В то время как ингибиторы -секретазы демонстрируют побочные эффекты вследствие одновременного ингибирования процессинга Notch, модуляторы -секретазы могут иметь преимущество селективного снижения продукции высоко агрегирующих и нейротоксичных форм А, т.е. А 42, без снижения продукции меньших,менее агрегирующих форм A, т.е. А 38, и без одновременного ингибирования процессинга Notch. Таким образом, являются предпочтительными соединения, которые не демонстрируют эффект на активность -секретазного комплекса в отношении процессинга Notch. Как используют в настоящем документе, термин "лечение" относится ко всем процессам, где может происходить замедление, прерывание, подавление или остановка прогрессирования заболевания, но он не обязательно указывает на полное устранение всех симптомов. Изобретение относится к соединению общей формулы (I), его стереоизомерным формам и их фармацевтически приемлемым кислотно- или основно-аддитивным солям и сольватам для применения в качестве лекарственного средства. Также изобретение относится к соединению согласно общей формуле (I), его стереоизомерным формам и фармацевтически приемлемым кислотно- или основно-аддитивным солям и сольватам, для применения в модулировании активности -секретазы. Также изобретение относится к соединению общей формулы (I), его стереоизомерным формам и его фармацевтически приемлемый кислотно- или основно-аддитивным солям и сольватам, для применения в лечении или предупреждении заболеваний или состояний, выбранных из группы, состоящей изAD, TBI, MCI, старческой деменции, деменции, деменции с тельцами Леви, церебральной амилоидной ангиопатии, мультиинфарктной деменции, синдрома Дауна, деменции, ассоциированной с болезнью Паркинсона, и деменции, ассоциированной с бета-амилоидом. В одном варианте осуществления указанное заболевание или состояние предпочтительно представляет собой AD. Также изобретение относится к соединению общей формулы (I), его стереоизомерным формам и фармацевтически приемлемым кислотно- или основно-аддитивным солям и сольватам для применения в лечении указанных заболеваний. Также изобретение относится к соединению общей формулы (I), его стереоизомерным формам и фармацевтически приемлемым кислотно- или основно-аддитивным солям и сольватам для лечения или профилактики указанных заболеваний. Также изобретение относится к соединению общей формулы (I), его стереоизомерным формам и фармацевтически приемлемым кислотно- или основно-аддитивным солям и сольватам для лечения или профилактики, в частности, лечения, опосредуемых -секретазой заболеваний или состояний. Также изобретение относится к применению соединения общей формулы (I), его стереоизомерных форм и фармацевтически приемлемых кислотно- или основно-аддитивных солей и сольватов для изготовления лекарственного средства. Также изобретение относится к применению соединения общей формулы (I), его стереоизомерных форм и фармацевтически приемлемых кислотно- или основно-аддитивных солей и сольватов, для изготовления лекарственного средства для модулирования активности -секретазы. Также изобретение относится к применению соединения общей формулы (I), его стереоизомерных форм и фармацевтически приемлемых кислотно- или основно-аддитивных солей и сольватов для изготовления лекарственного средства для лечения или профилактики любого из болезненных состояний,упомянутых в настоящем документе выше. Также изобретение относится к применению соединения общей формулы (I), его стереоизомерных форм и фармацевтически приемлемых кислотно- или основно-аддитивных солей и сольватов для изготовления лекарственного средства для лечения любого из болезненных состояний, упомянутых в настоящем документе выше. В изобретении конкретное предпочтение отдается соединениям формулы (I) или любой их подгруппе с величиной IC50 в отношении ингибирования продукции А 42-пептида менее чем 1000 нМ,предпочтительно менее чем 100 нМ, более предпочтительно менее чем 50 нМ, еще более предпочтительно менее чем 20 нМ при определении пригодным анализом, таким как анализ, используемый в примерах ниже. Соединения по настоящему изобретению можно вводить млекопитающим, предпочтительно человеку, для лечения или профилактики любого из заболеваний, упомянутых в настоящем документе выше. Ввиду применимости соединения формулы (I), предусмотрен способ лечения теплокровных животных, в том числе человека, страдающих от заболеваний, упомянутых в настоящем документе выше, или способ профилактики у теплокровных животных, в том числе человека, любого из заболеваний, упомянутых в настоящем документе выше. Указанные способы включают введение, т.е. системное или местное введение, предпочтительно пероральное введение, эффективного количества соединения формулы (I), его стереоизомерной формы и фармацевтически приемлемой аддитивной соли или сольвата теплокровным животным, в том числе человеку. Также настоящее изобретение относится к применению соединения формулы (I) для модулирования активности -секретазы, приводящего к снижению относительного количества продуцируемых А 42-пептидов. Преимуществом соединений или части соединений по настоящему изобретению может быть их увеличенное проникновение в ЦНС. Квалифицированные специалисты в области лечения таких заболеваний могут определить эффективное терапевтическое суточное количество из результатов тестирования, представленных в настоящем документе ниже. Эффективное терапевтическое суточное количество может составлять приблизительно от 0,005 до 50 мг/кг, в частности от 0,01 до 50 мг/кг массы тела, более конкретно от 0,01 до 25 мг/кг массы тела, предпочтительно от приблизительно 0,01 до приблизительно 15 мг/кг, более предпочтительно от приблизительно 0,01 до приблизительно 10 мг/кг, еще более предпочтительно от приблизительно 0,01 до приблизительно 1 мг/кг, наиболее предпочтительно от приблизительно 0,05 до приблизительно 1 мг/кг массы тела. Количество соединения в соответствии с настоящим изобретением, также называемого в настоящем документе активным ингредиентом, которое требуется для достижения терапевтического эффекта, безусловно, может варьировать от случая к случаю, например, в зависимости от конкретного соединения, пути введения, возраста и состояния реципиента и конкретного нарушения или заболевания,подвергаемого лечению. Способ лечения также может включать введение активного ингредиента в режиме от одного до четырех приемов в сутки. В этих способах лечения соединения по изобретению предпочтительно составляют в композиции перед введением. Как описано в настоящем документе ниже, пригодные фармацевтические композиции получают известными способами с использованием хорошо известных и широкодоступных ингредиентов. Соединения по настоящему изобретению, которые могут быть пригодны для лечения или профилактики AD или ее симптомов, можно вводить отдельно или в комбинации с одним или несколькими дополнительными лекарственными средствами. Комбинированная терапия включает введение одной фармацевтической дозированной композиции, которая содержит соединение формулы (I) и одно или несколько дополнительных лекарственных средств, а также введение соединения формулы (I) и каждого из дополнительных лекарственных средств в его собственной отдельной фармацевтической дозированной композиции. Например, соединение формулы (I) и лекарственное средство можно вводить пациенту вместе в одной пероральной дозированной композиции, такой как таблетка или капсула, или каждое средство можно вводить в отдельных пероральных дозированных композициях. Хотя возможно вводить активный ингредиент отдельно, предпочтительно, чтобы он был представ- 28021047 лен в качестве фармацевтической композиции. Таким образом, настоящее изобретение, кроме того, относится к фармацевтической композиции,содержащей фармацевтически приемлемый носитель и в качестве активного ингредиента - терапевтически эффективное количество соединения согласно формуле (I). Носитель или разбавитель должны быть "приемлемыми" в том смысле, что они должны быть совместимыми с другими ингредиентами композиции и не вредоносными для их реципиентов. Для простоты введения рассматриваемые соединения можно составлять в различные фармацевтические формы для целей введения. Соединения согласно изобретению, в частности соединения согласно формуле (I), их фармацевтически приемлемую кислотно- или основно-аддитивную соль, их стереохимически изомерную форму или любую их подгруппу или комбинацию, можно составлять в различные фармацевтические формы для целей введения. В качестве подходящих композиций могут быть перечислены все композиции, обычно используемые для системного введения лекарственных средств. Для получения фармацевтических композиций по этому изобретению эффективное количество конкретного соединения, необязательно в форме аддитивной соли, в качестве активного ингредиента,объединяют в однородную смесь с фармацевтически приемлемым носителем, который может принимать множество форм, в зависимости от формы препарата, желаемого для введения. Эти фармацевтические композиции являются желательными в единичных дозированных формах, пригодных, в частности, для введения перорально, ректально, подкожно, путем парентеральной инъекции или ингаляции. Например,при получении композиций в пероральной дозированной форме можно использовать любую из обычных фармацевтических сред, например, такую как вода, гликоли, масла, спирты и т.п., в случае пероральных жидких препаратов, таких как суспензии, сиропы, эликсиры, эмульсии и растворы; или твердые носители, такие как крахмалы, сахара, каолин, разбавители, лубриканты, связующие вещества, дезинтегрирующие вещества и т.п., в случае порошков, пилюль, капсул и таблеток. Вследствие простоты введения, таблетки и капсулы представляют собой наиболее преимущественные пероральные единичные дозированные формы, в случае которых обычно используют твердые фармацевтические носители. Для парентеральных композиций носитель обычно может содержать стерильную воду, по меньшей мере по большей части, хотя могут быть включены другие ингредиенты, например, для способствования растворимости. Можно получать, например, инъецируемые растворы, в которых носитель включает солевой раствор,раствор глюкозы или смесь солевого раствора и раствора глюкозы. Можно получать, например, инъецируемые растворы, в которых носитель включает солевой раствор, раствор глюкозы или смесь солевого раствора и раствора глюкозы. Инъецируемые растворы, содержащие соединения формулы (I), можно составлять в композиции в масле для пролонгированного действия. Подходящие масла для этой цели представляют собой, например, арахисовое масло, кунжутное масло, хлопковое масло, кукурузное масло,соевое масло, синтетические сложные эфиры глицерина и жирных кислот длинной цепи и смеси этих и других масел. Также можно получать инъецируемые суспензии, в случае которых можно использовать подходящие жидкие носители, суспендирующие вещества и т.п. Также включены препараты в твердой форме, которые предназначены для преобразования, непосредственно перед применением, в препараты в жидкой форме. В композициях, пригодных для чрескожного введения, носитель необязательно включает вещество, способствующее проникновению, и/или пригодное смачивающее вещество, необязательно в комбинации с пригодными добавками любой природы в небольших пропорциях, которые не оказывают существенного вредоносного эффекта на кожу. Указанные добавки могут способствовать нанесению на кожу и/или могут быть полезны для получения желаемых композиций. Эти композиции можно вводить различными путями, например, в качестве трансдермального пластыря, в качестве точечного нанесения,в качестве мази. Кислотно- или основно-аддитивные соли соединений формулы (I), вследствие их увеличенной растворимости в воде относительно соответствующей формы основания или кислоты, являются более пригодными для получения водных композиций. Особенно преимущественным является составление указанных выше фармацевтических композиций в единичной дозированной форме для простоты введения и единообразия дозировки. Единичная дозированная форма, как используют в настоящем документе, относится к физически дискретным единицам, пригодным в качестве однократных дозировок, причем каждая единица содержит заданное количество активного ингредиента, вычисленное для обеспечения желаемого терапевтического эффекта, вместе с требуемым фармацевтическим носителем. Примерами таких единичных дозированных форм являются таблетки (включая шероховатые или покрытые таблетки), капсулы, пилюли, пакеты с порошком, пластинки, суппозитории, инъецируемые растворы или суспензии и т.п. и их отдельные кратные единицы. Поскольку соединения по изобретению представляют собой сильнодействующие перорально вводимые соединения, особенно преимущественными являются фармацевтические композиции, содержащие указанные соединения, для перорального введения. Для увеличения растворимости и/или стабильности соединений формулы (I) в фармацевтических композициях может быть преимущественным использование -, - или -циклодекстринов или их производных, в частности гидроксиалкилзамещенных циклодекстринов, например 2-гидроксипропил-циклодекстрина или сульфобутилциклодекстрина. Также сорастворители, такие как спирты, могут
МПК / Метки
МПК: C07D 233/60, A61K 31/4178, C07D 405/14, C07D 471/04, C07D 401/14, A61K 31/4196, A61K 31/4439, C07D 498/04, C07D 403/10, A61P 25/28, C07D 487/04
Метки: качестве, gamma;-секретазы, производные, имидазола, замещенные, триазола, модуляторов
Код ссылки
<a href="https://eas.patents.su/30-21047-zameshhennye-proizvodnye-triazola-i-imidazola-v-kachestve-modulyatorov-gamma-sekretazy.html" rel="bookmark" title="База патентов Евразийского Союза">Замещенные производные триазола и имидазола в качестве модуляторов гамма-секретазы</a>
Предыдущий патент: Трубопрокатная установка
Следующий патент: Малеат 6-амино-2-{[(1s)-1-метилбутил]окси}-9-[5-(1-пиперидинил)пентил]-7,9-дигидро-8н-пурин-8-она
Случайный патент: Упаковочная машина


































