4-пиразолил-n-арилпиримидин-2-амины, 4-пиразолил-n-пиразолилпиримидин-2-амины и 4-пиразолил-n-пиридилпиримидин-2-амины в качестве ингибиторов киназ janus
Формула / Реферат
1. Соединение формулы IIa, IIb, IIc, IId, IIe, IIf или IIg
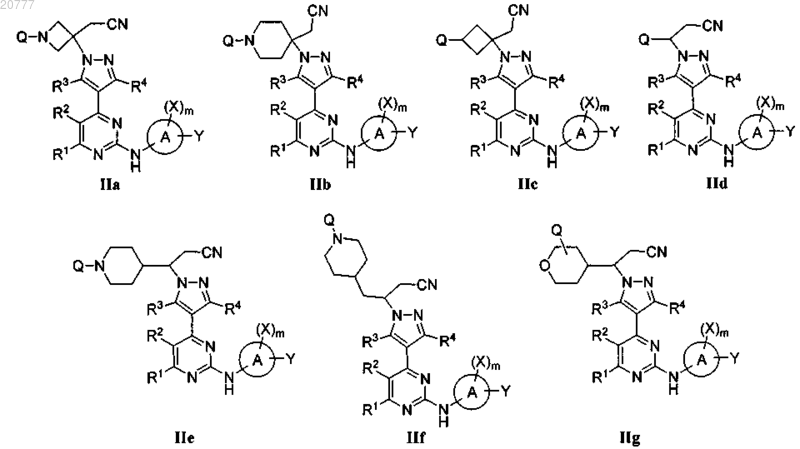
или его фармацевтически приемлемая соль, где
цикл А представляет собой C6-10арил, пиразолил или пиридил;
Q представляет собой Н, Су1, CN, C(O)Rb1 или S(O)2Rb1;
X представляет собой Н;
Y представляет собой Н, Су2, NO2, ORa1, C(O)Rb1, C(O)NRc1Rd1, C(O)ORa1, NRc1Rd1, NRc1C(O)Rb1, NRc1C(O)ORa1, S(O)2Rb1 или NRc1S(O)2Rb1;
R1, R2, R3 и R4 выбирают независимо из Н, C1-6-алкила, ORa и C(O)Rb;
Су1 и Су2 выбирают независимо из С6-10арила, C3-7циклоалкила, С3-10гетероарила и С3-5гетероциклоалкила, каждый из которых необязательно замещен 1 или 2 заместителями, независимо выбранными из галогена, C1-6-алкила и ORa1;
Ra и Rb выбирают независимо из Н, С1-6-алкила, С6-10арила, С3-10гетероарила и C3-5гетероциклоалкила, где указанный C1-6-алкил, C6-10арил, С3-10гетероарил и С3-5гетероциклоалкил необязательно замещен 1 или 2 заместителями, независимо выбранными из ОН, С1-6-алкила и С1-6-алкокси;
Ra1, Rb1, Rc1 и Rd1 выбирают независимо из Н, С1-6-алкила, С6-10арила, С3-7циклоалкила,
С3-10гетероарила, С3-5гетероциклоалкила, С3-10гетероарил-С1-4алкила, С3-7циклоалкил-C1-4алкила и
С3-5гетероциклоалкил-С1-4алкила, где указанный C1-6-алкил, С6-10арил, С3-7циклоалкил, С3-10гетероарил,
С3-5гетероциклоалкил, С3-10гетероарил-С1-4алкил, С3-7циклоалкил-С1-4алкил или С3-5гетероциклоалкил-С1-4алкил необязательно замещен 1 или 2 заместителями, независимо выбранными из С1-6-алкила, галогена, ORa2, C(O)NRc2Rd2, NRc2Rd2 и S(O)2Rb2; или
Rc1 и Rd1 вместе с атомом N, к которому они присоединены, образуют 4-, 5- или 6-членную гетероциклоалкильную группу, необязательно замещенную 1 или 2 заместителями, независимо выбранными из C1-6-алкила, CN, ORa2, C(O)Rb2, NRc2Rd2 и NRc2C(O)Rb2;
Ra2, Rb2, Rc2 и Rd2 выбирают независимо из H, С1-6-алкила, С3-7циклоалкила и С3-10гетероарила и
m равен 1,
где С3-10гетероарил относится к ароматическому гетероциклу по меньшей мере с одним гетероатомом членом цикла, выбранным из О, N или S;
С3-5гетероциклоалкил относится к моноциклическим и полициклическим неароматическим гетероциклам с одним или несколькими образующими цикл гетероатомами, выбранными из О, N или S.
2. Соединение по п.1 или его фармацевтически приемлемая соль, где А представляет собой С6-10арил.
3. Соединение по п.1 или его фармацевтически приемлемая соль, где А представляет собой фенил.
4. Соединение по п.1 или его фармацевтически приемлемая соль, где А представляет собой пиразолил.
5. Соединение по п.1 или его фармацевтически приемлемая соль, где А представляет собой пиридил.
6. Соединение по любому из пп.1-5 или его фармацевтически приемлемая соль, где Q представляет собой Н, Су1 или CN.
7. Соединение по любому из пп.1-5 или его фармацевтически приемлемая соль, где Q представляет собой Су1, C(O)Rb1, S(O)2Rb1 или ORa1.
8. Соединение по любому из пп.1-7 или его фармацевтически приемлемая соль, где Су1 представляет собой С6-10арил или С3-7циклоалкил.
9. Соединение по любому из пп.1-7 или его фармацевтически приемлемая соль, где Су1 представляет собой С3-10гетероарил или С3-5гетероциклоалкил.
10. Соединение по любому из пп.1-9 или его фармацевтически приемлемая соль, где R1 представляет собой Н.
11. Соединение по любому из пп.1-10 или его фармацевтически приемлемая соль, где R2 представляет собой Н.
12. Соединение по любому из пп.1-10 или его фармацевтически приемлемая соль, где R2 представляет собой C1-6-алкил.
13. Соединение по любому из пп.1-10 или его фармацевтически приемлемая соль, где R2 представляет собой метил.
14. Соединение по любому из пп.1-10 или его фармацевтически приемлемая соль, где R2 представляет собой C1-6-алкокси.
15. Соединение по любому из пп.1-10 или его фармацевтически приемлемая соль, где R2 представляет собой метокси.
16. Соединение по любому из пп.1-15 или его фармацевтически приемлемая соль, где R3 представляет собой Н.
17. Соединение по любому из пп.1-16 или его фармацевтически приемлемая соль, где R4 представляет собой Н.
18. Соединение по любому из пп.1-17 или его фармацевтически приемлемая соль, где Y представляет собой Н.
19. Соединение по любому из пп.1-18 или его фармацевтически приемлемая соль, где Су2 представляет собой С6-10арил или С3-7циклоалкил.
20. Соединение по любому из пп.1-18 или его фармацевтически приемлемая соль, где Су2 представляет собой С3-10гетероарил или С3-5гетероциклоалкил.
21. Соединение по п.1, выбранное из группы, в которую входят
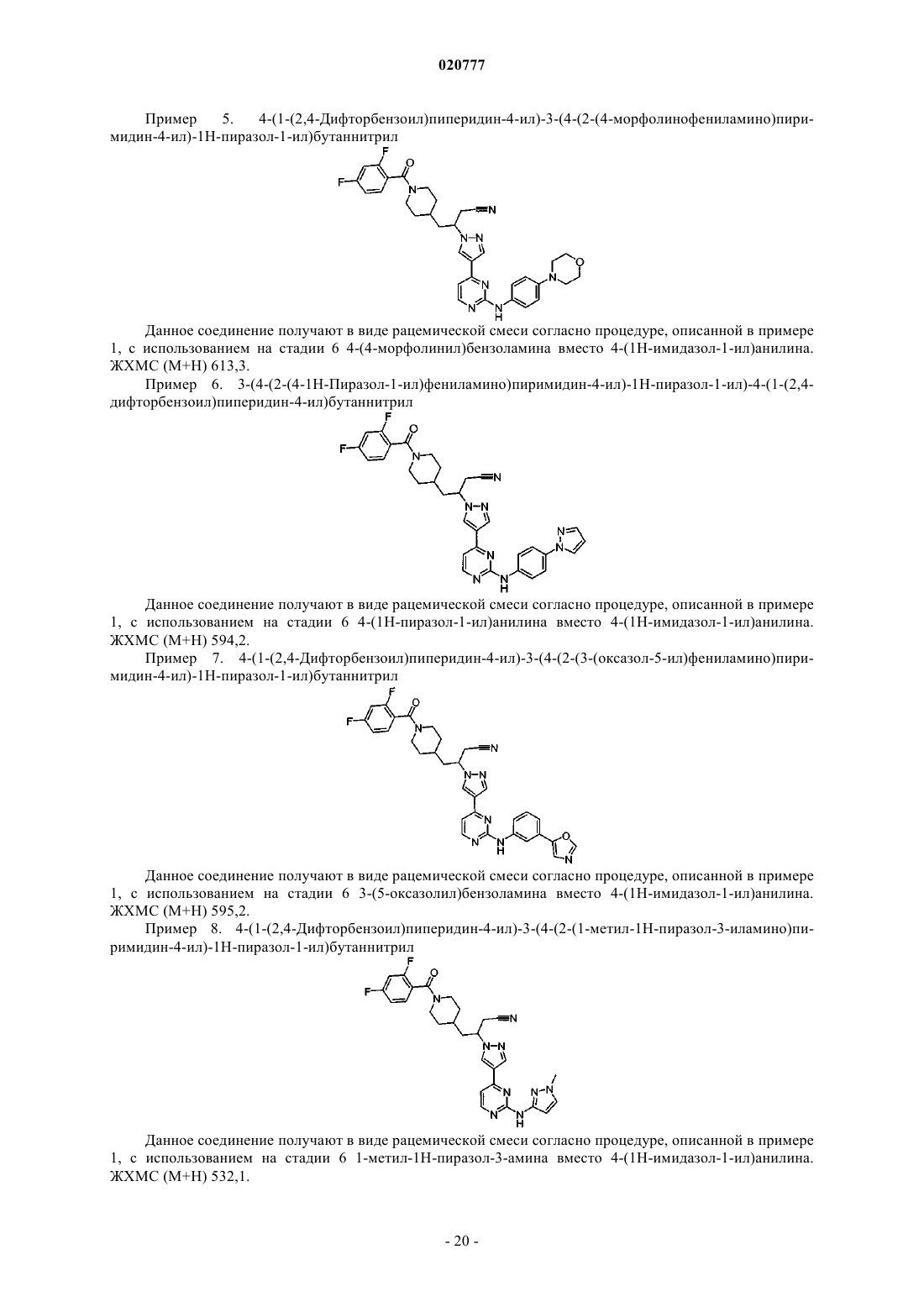
3-(4-(2-(4-(1Н-имидазол-1-ил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)-4-(1-(2,4-дифторбензоил)пиперидин-4-ил)бутаннитрил;
4-(1-(2,4-дифторбензоил)пиперидин-4-ил)-3-(4-(2-(4-пиперазин-1-ил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)бутаннитрил;
4-(1-(2,4-дифторбензоил)пиперидин-4-ил)-3-(4-(2-(4-метоксифениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)бутаннитрил;
4-(1-(2,4-дифторбензоил)пиперидин-4-ил)-3-(4-(2-(фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)бутаннитрил;
4-(1-(2,4-дифторбензоил)пиперидин-4-ил)-3-(4-(2-(4-морфолинофениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)бутаннитрил;
3-(4-(2-(4-(1Н-пиразол-1-ил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)-4-(1-(2,4-дифторбензоил)пиперидин-4-ил)бутаннитрил;
4-(1-(2,4-дифторбензоил)пиперидин-4-ил)-3-(4-(2-(3-(оксазол-5-ил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)бутаннитрил;
4-(1-(2,4-дифторбензоил)пиперидин-4-ил)-3-(4-(2-(1-метил-1Н-пиразол-3-иламино)пиримидин-4-ил)-1Н-пиразол-1-ил)бутаннитрил;
4-(1-(2,4-дифторбензоил)пиперидин-4-ил)-3-(4-(2-(4-феноксифениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)бутаннитрил;
2-(4-(4-(2-(4-(1Н-пиразол-1-ил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)-1-(изоксазол-5-карбонил)пиперидин-4-ил)ацетонитрил;
2-(1-(изоксазол-5-карбонил)-4-(4-(2-(3-(оксазол-5-ил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пиперидин-4-ил)ацетонитрил;
2-(4-(4-(2-(3-(1Н-тетразол-5-ил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)-1-(изоксазол-5-карбонил)пиперидин-4-ил)ацетонитрил;
2-(1-(изоксазол-5-карбонил)-4-(4-(2-(4-(морфолиносульфонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пиперидин-4-ил)ацетонитрил;
2-(1-(изоксазол-5-карбонил)-4-(4-(2-(6-метоксипиримидин-3-иламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пиперидин-4-ил)ацетонитрил;
2-(3-(4-(2-(4-(1Н-пиразол-1-ил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)-1-(циклопропилсульфонил)азетидин-3-ил)ацетонитрил;
2-(1-(циклопропилсульфонил)-3-(4-(2-(3-(оксазол-5-ил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)азетидин-3-ил)ацетонитрил;
N-(4-(4-(1-(3-(цианометил)-1-(циклопропилсульфонил)азетидин-3-ил)-1Н-пиразол-1-ил)пиримидин-2-иламино)фенил)ацетамид;
2-(1-(циклопропилсульфонил)-3-(4-(2-(3-(2-метилпиримидин-4-ил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)азетидин-3-ил)ацетонитрил;
2-(1-(циклопропилсульфонил)-3-(4-(2-(4-(оксазол-5-ил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)азетидин-3-ил)ацетонитрил;
3-(4-(2-(4-морфолинофениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)-3-(пиперидин-4-ил)пропаннитрил;
3-(1-(5-фторпиримидин-2-ил)(пиперидин-4-ил)-3-(4-(2-(4-морфолинофениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-(1-(метилсульфонил)пиперидин-4-ил)-3-(4-(2-(4-морфолинофениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-(4-(2-(4-морфолинофениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)-3-(1-(фенилсульфонил)пиперидин-4-ил)пропаннитрил;
3-(1-ацетилпиперидин-4-ил)-3-(4-(2-(4-морфолинофениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-(1-бензоилпиперидин-4-ил)-3-(4-(2-(4-морфолинофениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
2-(4-(4-(2-(4-(1Н-пиразол-1-ил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)-1-(циклопропилсульфонил)пиперидин-4-ил)ацетонитрил;
2-(1-(циклопропилсульфонил)-4-(4-(2-(4-морфолинофениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пиперидин-4-ил)ацетонитрил;
4-(4-(1-(4-(цианометил)-1-(циклопропилсульфонил)пиперидин-4-ил)-1Н-пиразол-4-ил)пиримидин-2-иламино)бензамид;
4-(4-(1-(4-(цианометил)-1-(циклопропилсульфонил)пиперидин-4-ил)-1Н-пиразол-4-ил)пиримидин-2-иламино)-N-(2-гидроксиэтил)бензамид;
4-(4-(1-(4-(цианометил)-1-(циклопропилсульфонил)пиперидин-4-ил)-1Н-пиразол-4-ил)пиримидин-2-иламино)-N,N-диметилбензамид;
4-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)бензамид;
3-(4-(2-(4-(1Н-пиразол-1-ил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)-3-циклопентилпропаннитрил;
3-циклопентил-3-(4-(2-(4-морфолинофениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-циклопентил-3-(4-(2-(фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-циклопентил-3-(4-(2-(3-(оксазол-5-ил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-циклопентил-3-(4-(2-(4-метоксифениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
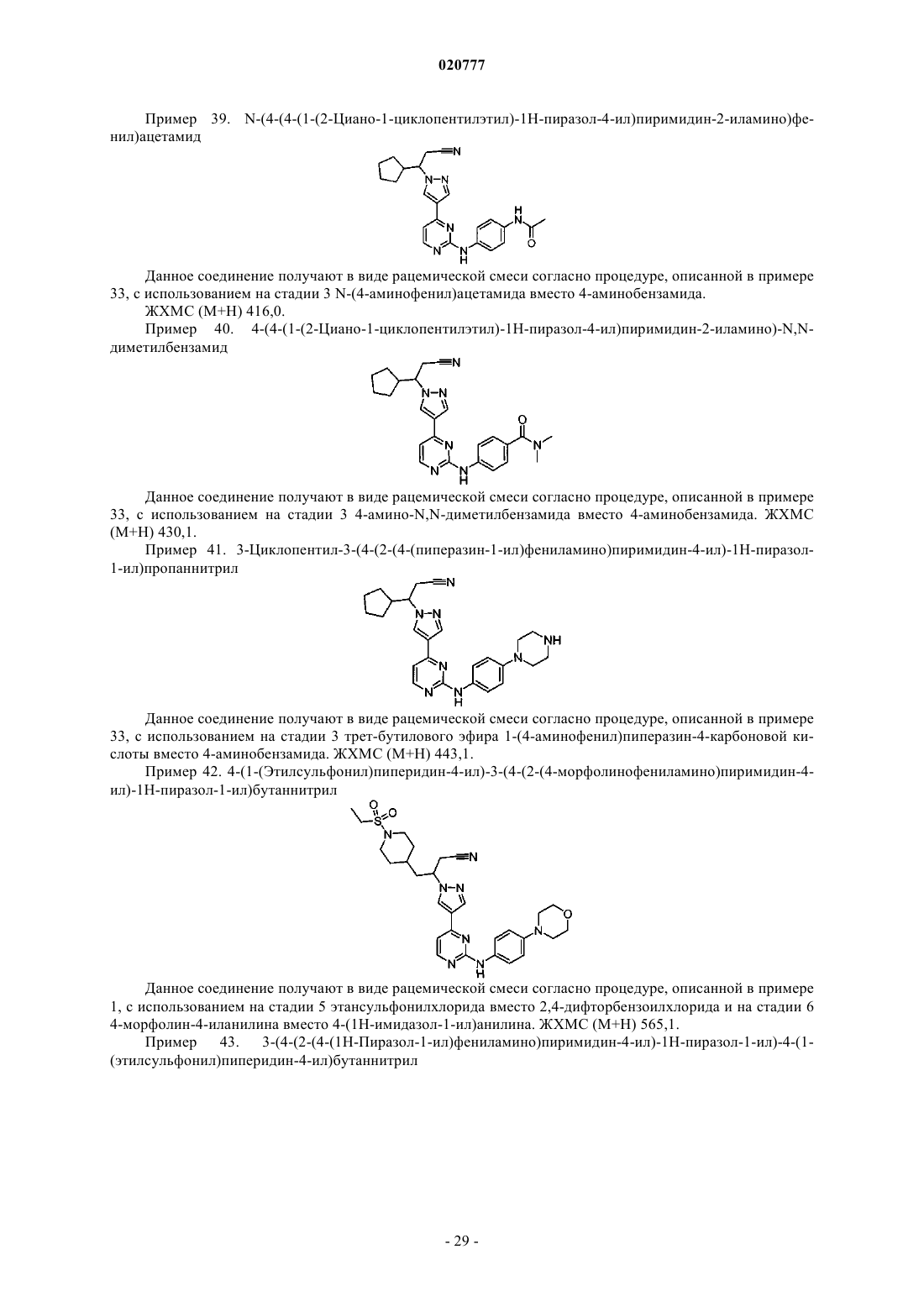
N-(4-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-1-ил)пиримидин-2-иламино)фенил)ацетамид;
4-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)-N,N-диметилбензамид;
3-циклопентил-(3-(4-(2-(4-пиперазин-1-ил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
4-(1-(этилсульфонил)пиперидин-4-ил)-3-(4-(2-(4-морфолинофениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)бутаннитрил;
3-(4-(2-(4-(1Н-пиразол-1-ил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)-4-(1-(этилсульфонил)пиперидин-4-ил)бутаннитрил;
4-(1-(этилсульфонил)пиперидин-4-ил)-3-(4-(2-(фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)бутаннитрил;
N-(4-(4-(1-(1-циано-3-(1-(1-метил-1Н-пиразол-3-илсульфонил)пиперидин-4-ил)пропан-2-ил)-1Н-пиразол-4-ил)пиримидин-2-иламино)фенил)ацетамид;
4-(4-(1-(1-циано-3-(1-(этилсульфонил)пиперидин-4-ил)пропан-2-ил)-1Н-пиразол-4-ил)пиримидин-2-иламино)-N,N-диметилбензамид;
4-(4-(1-(1-циано-3-(1-(1-метил-1Н-пиразол-3-илсульфонил)пиперидин-4-ил)пропан-2-ил)-1Н-пиразол-4-ил)пиримидин-2-иламино)бензамид;
4-(1-(этилсульфонил)пиперидин-4-ил)-3-(4-(5-метил-2-(4-морфолинофениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)бутаннитрил;
3-(4-(2-(4-(1Н-пиразол-1-ил)фениламино)-5-метилпиримидин-4-ил)-1Н-пиразол-1-ил)-4-(1-(этилсульфонил)пиперидин-4-ил)бутаннитрил;
4-(1-(этилсульфонил)пиперидин-4-ил)-3-(4-(5-метил-2-(фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)бутаннитрил;
N-(4-(4-(1-(1-циано-3-(1-(1-метил-1Н-пиразол-3-илсульфонил)пиперидин-4-ил)пропан-2-ил)-1Н-пиразол-4-ил)-5-метилпиримидин-2-иламино)фенил)ацетамид;
4-(4-(1-(1-циано-3-(1-(этилсульфонил)пиперидин-4-ил)пропан-2-ил)-1Н-пиразол-4-ил)-5-метилпиримидин-2-иламино)-N,N-диметилбензамид;
4-(4-(1-(1-циано-3-(1-(1-метил-1Н-пиразол-3-илсульфонил)пиперидин-4-ил)пропан-2-ил)-1Н-пиразол-4-ил)-5-метилпиримидин-2-иламино)бензамид;
3-циклопентил-3-(4-(2-(4-(4-(метилсульфонил)пиперазин-1-ил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
4-(1-(1-метил-1Н-пиразол-3-илсульфонил)пиперидин-4-ил)-3-(4-(2-(4-морфолинофениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)бутаннитрил;
3-(4-(2-(4-(1Н-пиразол-1-ил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)-4-(1-(1-метил-1Н-пиразол-3-илсульфонил)пиперидин-4-ил)бутаннитрил;
4-(1-(1-метил-1Н-пиразол-3-илсульфонил)пиперидин-4-ил)-3-(4-(2-(фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)бутаннитрил;
4-(4-(1-(1-циано-3-(1-(1-метил-1Н-пиразол-3-илсульфонил)пиперидин-4-ил)пропан-2-ил)-1Н-пиразол-4-ил)пиримидин-2-иламино)-N,N-диметилбензамид;
4-(4-(1-(1-циано-3-(1-(2,4-дифторбензоил)пиперидин-4-ил)пропан-2-ил)-1Н-пиразол-4-ил)пиримидин-2-иламино)-N,N-диметилбензамид;
N-(4-(4-(1-(1-циано-3-(1-(2,4-дифторбензоил)пиперидин-4-ил)пропан-2-ил)-1Н-пиразол-4-ил)пиримидин-2-иламино)фенил)ацетамид;
4-(1-(1-метил-1Н-пиразол-3-илсульфонил)пиперидин-4-ил)-3-(4-(5-метил-2-(4-морфолинофениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)бутаннитрил;
4-(1-(2,4-дифторбензоил)пиперидин-4-ил)-3-(4-(5-метил-2-(4-морфолинофениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)бутаннитрил;
3-(4-(2-(4-(1Н-пиразол-1-ил)фениламино)-5-метилпиримидин-4-ил)-1Н-пиразол-1-ил)-4-(1-(1-метил-1Н-пиразол-3-илсульфонил)пиперидин-4-ил)бутаннитрил;
3-(4-(2-(4-(1Н-пиразол-1-ил)фениламино)-5-метилпиримидин-4-ил)-1Н-пиразол-1-ил)-4-(1-(2,4-дифторбензоил)пиперидин-4-ил)бутаннитрил;
4-(1-(1-метил-1Н-пиразол-3-илсульфонил)пиперидин-4-ил)-3-(4-(5-метил-2-(фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)бутаннитрил;
4-(1-(2,4-дифторбензоил)пиперидин-4-ил)-3-(4-(5-метил-2-(фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)бутаннитрил;
4-(4-(1-(1-циано-3-(1-(1-метил-1Н-пиразол-3-илсульфонил)пиперидин-4-ил)пропан-2-ил)-1Н-пиразол-4-ил)-5-метилпиримидин-2-иламино)-N,N-диметилбензамид;
4-(4-(1-(1-циано-3-(1-(2,4-дифторбензоил)пиперидин-4-ил)пропан-2-ил)-1Н-пиразол-4-ил)-5-метилпиримидин-2-иламино)-N,N-диметилбензамид;
N-(4-(4-(1-(1-циано-3-(1-(2,4-дифторбензоил)пиперидин-4-ил)пропан-2-ил)-1Н-пиразол-4-ил)-5-метилпиримидин-2-иламино)фенил)ацетамид;
4-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)-5-метилпиримидин-2-иламино)бензамид;
3-(4-(2-(4-(1Н-пиразол-1-ил)фениламино)-5-метилпиримидин-4-ил)-1Н-пиразол-1-ил)-3-циклопентилпропаннитрил;
3-циклопентил-3-(4-(5-метил-2-(4-морфолинофениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-циклопентил-3-(4-(5-метил-2-(фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-циклопентил-3-(4-(5-метил-2-(4-(оксазол-5-ил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-циклопентил-3-(4-(2-(4-метоксифениламино)-5-метилпиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-циклопентил-3-(4-(5-метил-2-(4-(пиперазин-1-ил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-циклопентил-3-(4-(2-(4-(диэтиламино)фениламино)-5-метилпиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-циклопентил-3-(4-(2-(4-(этил(3-гидроксипропил)амино)фениламино)-5-метилпиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
4-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)-5-метилпиримидин-2-иламино)бензойная кислота;
3-циклопентил-3-(4-(5-метил-2-(4-нитрофениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
4-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)-5-метилпиримидин-2-иламино)-N-(2-гидроксиэтил)бензамид;
3-циклопентил-3-(4-(5-метил-2-(3-(оксазол-5-ил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-(4-(2-(4-аминофениламино)-5-метилпиримидин-4-ил)-1Н-пиразол-1-ил)-3-циклопентилпропаннитрил;
4-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)-5-метилпиримидин-2-иламино)-N-метилбензамид;
4-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)-5-метилпиримидин-2-иламино)-N-(1-метоксипропан-2-ил)бензамид;
3-циклопентил-3-(4-(2-(4-(4-гидроксипиперидин-1-карбонил)фениламино)-5-метилпиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
N-(4-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)-5-метилпиримидин-2-иламино)фенил)метансульфонамид;
метил-4-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)-5-метилпиримидин-2-иламино)фенилкарбамат;
N-(4-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)-5-метилпиримидин-2-иламино)фенил)-2-(пирролидин-1-ил)ацетамид;
3-(4-(2-(4-(3-оксоморфолино)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)-4-(пиперидин-4-ил)бутаннитрил;
2-(1-(циклопропилсульфонил)-3-(4-(2-(4-морфолинофениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)азетидин-3-ил)ацетонитрил;
2-(1-(изоксазол-5-карбонил)-4-(4-(2-(4-морфолинофениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пиперидин-4-ил) ацетонитрил;
4-(1-(метилсульфонил)пиперидин-4-ил)-3-(4-(2-(4-(3-оксоморфолино)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)бутаннитрил;
4-(1-(этилсульфонил)пиперидин-4-ил)-3-(4-(2-(4-(3-оксоморфолино)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)бутаннитрил;
4-(1-(циклопропилсульфонил)пиперидин-4-ил)-3-(4-(2-(4-(3-оксоморфолино)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)бутаннитрил;
3-циклопентил-3-(4-(2-(4-(3-оксоморфолино)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-циклопентил-3-(4-(2-(3-(2-метилпиримидин-4-ил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-((4-(1-(2-циано-1-циклопентилэтил)-1Н)пиразол-4-ил)пиримидин-2-иламино)бензойная кислота;
3-циклопентил-3-(4-(5-метокси-2-(4-морфолинофениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-(4-(2-(4-(1Н-пиразол-1-ил)фениламино)-5-метоксипиримидин-4-ил)-1Н-пиразол-1-ил)-3-циклопентилпропаннитрил;
N-(4-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)-5-метоксипиримидин-2-иламино)ацетамид;
4-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)-5-метоксипиримидин-2-иламино)-N,N-диметилбензамид;
3-циклопентил-3-(4-(2-(4-(2-оксопиперидин-1-ил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-циклопентил-3-(4-(2-(4-(2-оксо-1,3-оксазинан-3-ил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-циклопентил-3-(4-(2-(4-(2-оксооксазолидин-3-ил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-(4-(2-(3-аминофениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)-3-циклопентилпропаннитрил;
3-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)-N-метилбензамид;
3-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)-N,N-диметилбензамид;
3-циклопентил-3-(4-(2-(3-(4-гидроксипиперидин-1-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)-N-(2-гидроксиэтил)бензамид;
3-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)-N-(1-метоксипропан-2-ил)бензамид;
N-(3-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)фенил)этансульфонамид;
N-(3-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)фенил)метансульфонамид;
метил-3-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)фенилкарбамат;
N-(3-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)фенил)ацетамид;
N-(3-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)фенил)-2-(пирролидин-1-ил)ацетамид;
4-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)бензойная кислота;
3-циклопентил-3-(4-(2-(4-(4-метилпиперазин-1-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-циклопентил-3-(4-(2-(4-(4-(2-гидроксиэтил)пиперазин-1-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-циклопентил-3-(4-(2-(4-(пирролидин-1-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-циклопентил-3-(4-(2-(4-(3-оксопиперазин-1-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-циклопентил-3-(4-(2-(4-(4-гидроксипиперидин-1-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
4-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)-N-(циклопропилметил)-N-пропилбензамид;
4-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)-N-(циклопропилметил)бензамид;
3-циклопентил-3-(4-(2-(4-(3-гидроксипирролидин-1-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-(4-(2-(4-(азетидин-1-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)-3-циклопентилпропаннитрил;
3-циклопентил-3-(4-(2-(4-(2-оксопирролидин-1-ил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-циклопентил-3-(4-(5-метокси-2-(4-(2-оксопирролидин-1-ил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-циклопентил-3-(4-(5-метокси-2-(4-(оксазол-5-ил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-циклопентил-3-(4-(5-метокси-2-(3-(оксазол-5-ил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-циклопентил-3-(4-(5-метокси-2-(4-(3-оксоморфолино)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-циклопентил-3-(4-(5-метокси-2-(3-(2-метилпиримидин-4-ил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-циклопентил-3-(4-(5-метокси-2-(4-(2-оксопиперидин-1-ил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-циклопентил-3-(4-(5-метокси-2-(4-(2-оксооксазолидин-3-ил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-циклопентил-3-(4-(2-(3-(4-метилпиперазин-1-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-циклопентил-3-(4-(2-(3-(4-(2-гидроксиэтил)пиперазин-1-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-циклопентил-3-(4-(2-(3-(пирролидин-1-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-циклопентил-3-(4-(2-(3-(3-оксопиперазин-1-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-циклопентил-3-(4-(2-(3-(3-гидроксипиролидин-1-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-(4-(2-(3-азетидин-1-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)-3-циклопентилпропаннитрил;
3-(4-(2-(3-(4-ацетилпиперазин-1-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)-3-циклопентилпропаннитрил;
3-циклопентил-3-(4-(2-(3-(4-пиридин-3-илметил)пиперидин-1-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)-N-(1-(3-метоксифенил)этил)бензамид;
3-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)-N-(пиридин-3-илметил)бензамид;
3-циклопентил-3-(4-(2-(3-(морфолин-4-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)-N-((5-метилизоксазол-3-ил)метил)бензамид;
3-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)-N-(2-(1-метилпирролидин-2-ил)этил)бензамид;
3-циклопентил-3-(4-(2-(3-(4-гидрокси-4-фенилпиперидин-1-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-(4-(2-(3-(4-бензил-4-гидроксипиперидин-1-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)-3-циклопентилпропаннитрил;
3-циклопентил-3-(4-(2-(3-(3-пиридин-2-ил)пирролидин-1-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)-N-((тетрагидро-2Н-пиран-4-ил)метил)бензамид;
3-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)-N-(1-(метилпиперидин-4-ил)бензамид;
3-циклопентил-3-(4-(2-(3-(4-фенилпиперидин-1-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)-N-(1-(пиридин-2-ил)этил)бензамид;
3-циклопентил-3-(4-(2-(3-(3-(3-фторфенил)пирролидин-1-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
N-((3R)-1-(3-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)бензоил)пирролидин-3-ил)ацетамид;
3-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)-N-(2-(2-оксоимидазолидин-1-ил)этил)бензамид;
3-циклопентил-3-(4-(2-(3-(4-пиримидин-2-ил)пиперазин-1-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)-N-(2-(2-пиридин-3-ил)этил)бензамид;
3-циклопентил-3-(4-(2-(3-(2-(метоксиметил)пирролидин-1-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)-N-(2-метоксибензил)бензамид;
3-циклопентил-3-(4-(2-(3-(4-феноксипиперидин-1-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)-N-(1-(гидроксиметил)циклопентил)бензамид;
4-(4-(3-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)бензоил)пиперазин-1-ил)бензонитрил;
N-(1-бензилпирролидин-3-ил)-3-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)бензамид;
3-циклопентил-3-(4-(2-(3-(4-фенилпиперазин-1-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-циклопентил-3-(4-(2-(3-нитрофениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-циклопентил-3-(4-(2-(4-нитрофениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-циклобутил-3-(4-(2-(4-морфолинофениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-(4-(2-(4-аминофениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)-3-циклопентилпропаннитрил;
3-(4-(2-(4-(1Н-пиразол-1-ил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)-3-циклобутилпропаннитрил;
3-циклобутил-3-(4-(2-(4-(2-оксопиперидин-1-ил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-циклобутил-3-(4-(2-(4-(3-оксоморфолино)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-циклобутил-3-(4-(2-(3-(оксазол-5-ил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-циклопропил-3-(4-(2-(4-морфолинофениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-(4-(2-(4-(1Н-пиразол-1-ил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)-3-циклопропилпропаннитрил;
3-циклопропил-3-(4-(2-(4-(2-оксопиперидин-1-ил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-циклопропил-3-(4-(2-(4-(3-оксоморфолино)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-циклопропил-3-(4-(2-(3-(оксазол-5-ил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
N-(4-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)фенил)-2,6-(цис)-диметилморфолин-4-сульфонамид;
N-(4-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)фенил)бензамид;
N-(4-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)фенил)-1-(метилсульфонил)метансульфонамид;
N-(4-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)фенил)-3,5-дифторбензамид;
N'-(4-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)фенил)-N,N-диметилсульфамид;
N-(4-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)фенил)-5-метилизоксазол-3-карбоксамид;
N-(4-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)фенил)изоксазол-5-карбоксамид;
N-(4-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)фенил)-3,5-диметилизоксазол-4-карбоксамид;
N-(4-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)фенил)-1-метил-1Н-пиразол-3-сульфонамид;
N-(4-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)фенил)-2,5-дифторбензамид;
3-циклопентил-3-(4-(2-(4-(1,1-диоксидоизотиазолидин-2-ил)фенил)аминопиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
N-(4-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)фенил)-5-(2-метилтиазол-4-ил)тиофен-2-сульфонамид;
N-(4-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)фенил)-6-метилпиридин-2-сульфонамид;
N-(4-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)фенил)-5-(пиридин-2-ил)тиофен-2-сульфонамид;
5-хлор-N-(4-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)фенил)тиофен-2-сульфонамид;
N-(4-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)фенил)-6-морфолинопиридин-3-сульфонамид;
тетрагидрофуран-3-ил-4-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)фенилкарбамат;
тетрагидрофуран-3-ил-3-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)фенилкарбамат;
N-(3-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)фенил)-1-метил-1Н-пиразол-3-сульфонамид;
N'-(3-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)фенил)-N,N-диметилсульфамид;
N-(4-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)фенил)-2-(пирролидин-1-ил)ацетамид;
N-(4-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)фенил)-2-(3-гидроксипирролидин-1-ил)ацетамид;
N-(4-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)фенил)-2-(4-гидроксипиперидин-1-ил)ацетамид;
N-(4-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)фенил)-2-(3-оксопиперазин-1-ил)ацетамид;
N-(4-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)фенил)-2-морфолиноацетамид;
N-(4-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)фенил)-2-((тетрагидро-2Н-пиран-4-ил)метиламино)ацетамид;
N-(4-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)фенил)-2-((2-метоксиметил)пирролидин-1-ил)ацетамид;
N-(4-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)фенил)-2-(циклопропилметиламино)ацетамид;
N-(4-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)фенил)-2-(1-метоксипропан-2-иламино)ацетамид;
2-(4-(5-метилизоксазол-3-илокси)-1-(4-(2-(4-морфолинофениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)циклогексил)ацетонитрил;
3-циклопентил-(3-(4-(2-(4-морфолин-4-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
4-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)-N-((тетрагидро-2Н-пиран-4-ил)метил)бензамид;
3-циклопентил-3-(4-(2-(4-((3-эндо)-3-гидрокси-8-азабицикло[3.2.1]октан-8-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-циклопентил-3-(4-(2-(4-(2-окса-6-азатрицикло[3.3.1.1(3,7)]дец-6-илкарбонил)фенил)аминопиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
4-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)-N-(цис-4-гидроксициклогексил)-N-метилбензамид;
4-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)-N-метил-N-(тетрагидро-2Н-пиран-4-ил)бензамид;
3-циклопентил-3-(4-(2-(4-(S*)-(4,4-диметил-2-оксо-1-окса-3,7-диазаспиро[4.4]нонан-7-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-циклопентил-3-(4-(2-(4-(4,4-диметил-1-окса-7-азаспиро[4.4]нонан-7-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-циклопентил-3-(4-(2-(4-(4-метоксипиперидин-1-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
N-((3S)-1-(4-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)бензоил)пирролидин-3-ил)ацетамид;
4-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)-N-(цис-4-гидроксициклогексил)бензамид;
3-(4-(2-(4-(4-ацетилпиперазин-1-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)-3-циклопентилпропаннитрил;
(3S)-1-(4-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)бензоил)пирролидин-3-карбонитрил;
3-циклопентил-3-(4-(2-(4-(3-метоксипрролидин-1-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
4-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)-N-(1-метилпиперидин-4-ил)бензамид;
3-циклопентил-3-(4-(2-(4-(3-оксо-2,8-диазаспиро[4.5]декан-8-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-циклопентил-3-(4-(2-(4-(3-фторпирролидин-1-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-циклопентил-3-(4-(2-(4-(3-(диметиламино)пирролидин-1-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
этил-4-(4-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)бензамидо)пиперидин-1-карбоксилат;
4-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)-N-(1-(пиридин-2-ил)пирролидин-3-ил)бензамид;
3-циклопентил-3-(4-(2-(4-(3-(пиридин-2-илокси)пирролидин-1-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
1-(4-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)бензоил)-N,N-диметилпиперидин-4-карбоксамид;
4-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)-N-(1-(диметиламино)-1-оксобутан-2-ил)бензамид;
N-(3-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)фенил)-2-(4-метилпиперазин-1-ил)ацетамид;
N-(3-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)фенил)-2-(3-гидроксипирролидин-1-ил)ацетамид;
N-(3-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)фенил)-2-(3-оксопиперазин-1-ил)ацетамид;
N-(3-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)фенил)-2-(4-гидроксипиперазин-1-ил)ацетамид;
N-(3-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)фенил)-2-(4-(2-гидроксиэтил)пиперазин-1-ил)ацетамид;
N-(3-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)фенил)-2-(циклопропилметиламино)ацетамид;
N-(3-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)фенил)-2-морфолиноацетамид;
N-(3-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)фенил)-2-(этиламино)ацетамид;
2-(4-(5-метилизоксазол-3-илокси)-1-(4-(2-(4-(3-оксоморфолино)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)циклогексил)ацетонитрил;
2-(4-(5-метилизоксазол-3-илокси)-1-(4-(2-(4-(2-оксопиперидин-1-ил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)циклогексил)ацетонитрил;
2-(1-(4-(2-(4-(1Н-пиразол-1-ил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)-4-(5-метилизоксазол-3-илокси) циклогексил)ацетонитрил;
2-(4-(5-метилизоксазол-3-илокси)-1-(4-(2-(3-(оксазол-5-ил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)циклогексил)ацетонитрил;
3-(цианометил)-3-(4-(2-(4-морфолинофениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)циклобутанкарбонитрил;
4-(4-(1-(3-(цианометил)-1-(этилсульфонил)азетидин-3-ил)-1Н-пиразол-4-ил)пиримидин-2-иламино)бензойная кислота;
4-(4-(1-(2-циано-1-циклопропилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)бензойная кислота;
3-циклопропил-3-(4-(2-(4-(4-гидроксипиперидин-1-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-циклопропил-3-(4-(2-(4-((3-эндо)-3-гидрокси-8-азабицикло[3.2.1]октан-8-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-циклопропил-3-(4-(2-(4-(пирролидин-1-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
4-(4-(1-(2-циано-1-циклопропилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)-N-(1-тетрагидро-2Н-пиран-4-ил)бензамид;
2-(1-(этилсульфонил)-3-(4-(2-(4-(морфолин-4-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)азетедин-3-ил)ацетонитрил;
2-(1-(этилсульфонил)-3-(4-(2-(4-(4-гидроксипиперидин-1-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)азетедин-3-ил)ацетонитрил;
2-(1-(этилсульфонил)-3-(4-(2-(4-((3-эндо)-3-гидрокси-8-азабицикло[3.2.1]октан-8-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)азетедин-3-ил)ацетонитрил;
2-(1-(этилсульфонил)-3-(4-(2-(4-(пирролидин-1-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)азетедин-3-ил)ацетонитрил;
4-(4-(1-(3-цианометил)-1-(этилсульфонил)азетедин-3-ил)-1Н-пиразол-4-ил)пиримидин-2-иламино)-N-(тетрагидро-2Н-пиран-4-ил)бензамид;
3-циклопропил-3-(4-(2-(4-(морфолин-4-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-(4-(2-(4-(азетидин-1-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)-3-циклопропилпропаннитрил;
3-циклопропил-3-(4-(2-(4-(2-окса-6-азатрицикло[3.3.1.1(3,7)]дец-6-илкарбонил)фенил)аминопиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-циклопропил-3-(4-(2-(4-(4-метоксипиперидин-1-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
(3R)-1-(4-(4-(1-(2-циано-1-циклопропилэтил)-1Н-пиразол-4-ил)пиримидин-2-ил)амино)бензоил)пирролидин-3-карбонитрил;
3-циклопропил-3-(4-(2-(4-(3-метоксипирролидин-1-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-циклопропил-3-(4-(2-(4-(3-гидроксипирролидин-1-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-циклопропил-3-(4-(2-(4-(4-метилпиперазин-1-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
N-((3R)-1-(4-(4-(1-(2-циано-1-циклопропилэтил)-1Н-пиразол-4-ил)пиримидин-2-иламино)бензоил)пирролидин-3-ил)ацетамид;
3-(4-(2-(4-(4-ацетилпиперазин-1-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)-3-циклопропилпропаннитрил;
3-циклопропил-3-(4-(2-(4-(3-(диметиламино)пирролидин-1-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-циклопропил-3-(4-(2-(4-(3-фторпирролидин-1-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
этил-4-(4-(4-(1-(2-циано-1-циклопропилэтил)-1Н-пиразол-4-ил)пиримидин-2-ил)амино)бензоил)аминопиперидин-1-карбоксилат;
2-(3-(4-(2-(4-азетидин-1-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)-1-(этилсульфонил)азетидин-3-ил)ацетонитрил;
(1-(этилсульфонил)-3-(4-(2-(4-(2-окса-6-азатрицикло[3.3.1.1(3,7)]дец-6-илкарбонил)фенил)аминопиримидин-4-ил)-1Н-пиразол-1-ил)азетидин-3-ил)ацетонитрил;
(1-(этилсульфонил)-3-(4-(2-(4-((4-метоксипиперидин-1-ил)карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-илазетидин-3-ил)ацетонитрил;
1-(4-(4-(1-(3-(цианометил)-1-(этилсульфонил)азетидин-3-ил)-1Н-пиразол-4-ил)пиримидин-2-иламино)бензоил)пирролидин-3-карбонитрил;
2-(1-(этилсульфонил)-3-(4-(2-(4-(3-метоксипирролидин-1-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)азетидин-3-ил)ацетонитрил;
2-(1-(этилсульфонил)-3-(4-(2-(4-(3-гидроксипирролидин-1-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)азетидин-3-ил)ацетонитрил;
2-(1-(этилсульфонил)-3-(4-(2-(4-(4-метилпиперазин-1-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)азетидин-3-ил)ацетонитрил;
N-(1-(4-(4-(1-(3-цианометил)-1-(этилсульфонил)азетидин-3-ил)-1Н-пиразол-4-ил)пиримидин-2-иламино)бензоил)пирролидин-3-ил)ацетамид;
2-(3-(4-(2-(4-(4-ацетилпиперазин-1-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)-1-(этилсульфонил)азетидин-3-ил)ацетонитрил;
2-(3-(4-(2-(4-(3-(диметиламино)пирролидин-1-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)-1-(этилсульфонил)азетидин-3-ил)ацетонитрил;
2-(1-(этилсульфонил)-3-(4-(2-(4-(3-фторпирролидин-1-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)азетидин-3-ил)ацетонитрил;
этил-4-(4-(4-(1-(3-(цианометил)-1-(этилсульфонил)азетидин-3-ил)-1Н-пиразол-4-ил)пиримидин-2-иламино)бензамидо)пиперидин-1-карбоксилат;
4-(4-(1-(3-циано-1-(цианометил)циклобутил)-1Н-пиразол-4-ил)пиримидин-2-иламино)бензойная кислота;
4-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)-5-метоксипиримидин-2-иламино)бензойная кислота;
3-(цианометил)-3-(4-(2-(4-морфолин-4-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)циклобутанкарбонитрил;
3-(цианометил)-3-(4-(2-(4-(пирролидин-1-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)циклобутанкарбонитрил;
4-(4-(1-(3-циано-1-(цианометил)циклобутил)-1Н-пиразол-4-ил)пиримидин-2-иламино)-N-(тетрагидро-2Н-пиран-4-ил)бензамид;
3-(цианометил)-3-(4-(2-(4-(3-гидроксипирролидин-1-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)циклобутанкарбонитрил;
4-(4-(1-(3-циано-1-(цианометил)циклобутил)-1Н-пиразол-4-ил)пиримидин-2-иламино)-N-((5-метилизоксазол-3-ил)метил)бензамид;
3-(4-(2-(4-(азетидин-1-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)-3-(цианометил)циклобутанкарбонитрил;
3-(цианометил)-3-(4-(2-(4-(4-метилпиперазин-1-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)циклобутанкарбонитрил;
3-(цианометил)-3-(4-(2-(4-(3-фторпирролидин-1-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)циклобутанкарбонитрил;
3-(цианометил)-3-(4-(2-(4-(4-метоксипиперидин-1-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)циклобутанкарбонитрил;
3-(цианометил)-3-(4-(2-(4-(3-метоксипирролидин-1-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)циклобутанкарбонитрил;
1-(4-(4-(1-(3-циано-1-(цианометил)циклобутил)-1Н-пиразол-4-ил)пиримидин-2-иламино)бензоил)пирролидин-3-карбонитрил;
3-(4-(2-(4-(4-ацетилпиперазин-1-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)-3-(цианометил)циклобутанкарбонитрил;
N-(1-(4-(4-(1-(3-циано-1-(цианометил)циклобутил)-1Н-пиразол-4-ил)пиримидин-2-иламино)бензоил)пирролидин-3-ил)ацетамид;
3-(цианометил)-3-(4-(2-(4-((3-эндо)-3-гидрокси-8-азабицикло[3.2.1]октан-8-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)циклобутанкарбонитрил;
3-(цианометил)-3-(4-(2-(4-(4-гидроксипиперидин-1-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)циклобутанкарбонитрил;
3-циклопентил-3-(4-(5-метокси-2-(4-морфолин-4-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-циклопентил-3-(4-(5-метокси-2-(4-(пирролидин-1-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
3-циклопентил-3-(4-(5-метокси-2-(4-(4-метилпиперазин-1-карбонил)фениламино)пиримидин-4-ил)-1Н-пиразол-1-ил)пропаннитрил;
4-(4-(1-(2-циано-1-циклопентилэтил)-1Н-пиразол-4-ил)-5-метоксипиримидин-2-иламино)-N-(тетрагидро-2Н-пиран-4-ил)бензамид;
3-циклопентил-3-[4-(2-{[4-(2-пирролидин-1-илэтокси)фенил]амино}пиримидин-4-ил)-1Н-пиразол-1-ил]пропаннитрил;
3-(цианометил)-3-[4-(2-{[4-(2-пирролидин-1-илэтокси)фенил]амино}пиримидин-4-ил)-1Н-пиразол-1-ил]циклобутанкарбонитрил;
3-(4-{2-[(4-морфолин-4-илфенил)амино]пиримидин-4-ил}-1Н-пиразол-1-ил)-3-(тетрагидро-2Н-пиран-4-ил)пропаннитрил;
4-[(4-{1-[2-циано-1-(тетрагидро-2Н-пиран-4-ил)этил]-1Н-пиразол-4-ил}пиримидин-2-ил)амино]-N-(тетрагидро-2Н-пиран-4-ил)бензамид;
3-[4-(2-{[4-(пирролидин-1-илкарбонил)фенил]амино}пиримидин-4-ил)-1Н-пиразол-1-ил]-3-(тетрагидро-2Н-пиран-4-ил)пропаннитрил;
3-[4-(2-{[4-(морфолин-4-илкарбонил)фенил]амино}пиримидин-4-ил)-1Н-пиразол-1-ил]-3-(тетрагидро-2Н-пиран-4-ил)пропаннитрил;
3-{4-[2-({4-[(4-гидроксипиперидин-1-ил)карбонил]фенил}амино)пиримидин-4-ил]-1Н-пиразол-1-ил}-3-(тетрагидро-2Н-пиран-4-ил)пропаннитрил;
3-{4-[2-({4-[(4-метоксипиперидин-1-ил)карбонил]фенил}амино)пиримидин-4-ил]-1Н-пиразол-1-ил}-3-(тетрагидро-2Н-пиран-4-ил)пропаннитрил;
1-{4-[(4-{1-[2-циано-1-(тетрагидро-2Н-пиран-4-ил)этил]-1Н-пиразол-4-ил}пиримидин-2-ил)амино]бензоил}пиперидин-4-карбонитрил;
3-(4-{2-[(4-{[(3R)-3-гидроксипирролидин-1-ил]карбонил}фенил)амино]-5-пиримидин-4-ил}-1Н-пиразол-1-ил)-3-(тетрагидро-2Н-пиран-4-ил)пропаннитрил;
3-(4-{2-[(4-{[(3S)-3-метоксипирролидин-1-ил]карбонил}фенил)амино]пиримидин-4-ил}-1Н-пиразол-1-ил)-3-(тетрагидро-2Н-пиран-4-ил)пропаннитрил;
(3S)-1-{4-[(4-{1-[2-циано-1-(тетрагидро-2Н-пиран-4-ил)этил]-1Н-пиразол-4-ил}пиримидин-2-ил)амино]бензоил}пирролидин-3-карбонитрил;
1-[4-({4-[1-(2-циано-1-циклопропилэтил)-1Н-пиразол-4-ил]пиримидин-2-ил}амино)бензоил]пиперидин-4-карбонитрил;
1-{4-[(4-{1-[3-(цианометил)-1-(этилсульфонил)азетидин-3-ил]-1Н-пиразол-4-ил}пиримидин-2-ил)амино]бензоил}пиперидин-4-карбонитрил;
3-циклопропил-3-[4-(5-метокси-2-{[3-(1,3-оксазол-5-ил)фенил]амино}пиримидин-4-ил)-1Н-пиразол-1-ил]пропаннитрил;
3-циклопропил-3-(4-{5-метокси-2-[(3-нитрофенил)амино]пиримидин-4-ил}-1Н-пиразол-1-ил)пропаннитрил;
3-({4-[1-(2-циано-1-циклопропилэтил)-1Н-пиразол-4-ил]-5-метоксипиримидин-2-ил}амино)-N-(тетрагидро-2Н-пиран-4-ил)бензамид;
3-циклопропил-3-[4-(5-метокси-2-{[3-(пирролидин-1-илкарбонил)фенил]амино}пиримидин-4-ил)-1Н-пиразол-1-ил]пропаннитрил;
3-циклопропил-3-(4-{2-[(3-{[(3R)-3-гидроксипирролидин-1-ил]карбонил}фенил)амино]-5-метоксипиримидин-4-ил}-1Н-пиразол-1-ил)пропаннитрил;
3-циклопропил-3-(4-{5-метокси-2-[(3-{[(3S)-3-метоксипирролидин-1-ил]карбонил}фенил)амино]пиримидин-4-ил}-1Н-пиразол-1-ил)пропаннитрил;
(3S)-1-[3-({4-[1-(2-циано-1-циклопропилэтил)-1Н-пиразол-4-ил]-5-метоксипиримидин-2-ил}амино)бензоил]пирролидин-3-карбонитрил;
3-циклопропил-3-[4-(5-метокси-2-{[3-(морфолин-4-илкарбонил)фенил]амино}пиримидин-4-ил)-1Н-пиразол-1-ил]пропаннитрил;
3-циклопропил-3-{4-[2-({3-[(4-гидроксипиперидин-1-ил)карбонил]фенил}амино)-5-метоксипиримидин-4-ил)-1Н-пиразол-1-ил}пропаннитрил;
3-циклопропил-3-{4-[5-метокси-2-({3-[(4-метоксипиперидин-1-ил)карбонил]фенил}амино)пиримидин-4-ил)-1Н-пиразол-1-ил}пропаннитрил;
1-[3-({4-[1-(2-циано-1-циклопропилэтил)-1Н-пиразол-4-ил]-5-метоксипиримидин-2-ил}амино)бензоил]пиперидин-4-карбонитрил;
3-циклопропил-3-(4-{2-[(3-{[(3-эндо)-3-гидрокси-8-азабицикло[3.2.1]окт-8-ил]карбонил}фенил)амино]-5-метоксипиримидин-4-ил}-1Н-пиразол-1-ил)пропаннитрил;
3-({4-[1-(2-циано-1-циклопропилэтил)-1Н-пиразол-4-ил]-5-метоксипиримидин-2-ил}амино)-N-[(5-метилизоксазол-3-ил)метил]бензамид;
3-[4-(2-{[3-(азетидин-1-илкарбонил)фенил]амино}-5-метоксипиримидин-4-ил)-1Н-пиразол-1-ил]-3-циклопропилпропаннитрил;
3-(цианометил)-3-[4-(2-{[4-(2-оксопиперидин-1-ил)фенил]амино}пиримидин-4-ил)-1Н-пиразол-1-ил]циклобутанкарбонитрил;
3-(цианометил)-3-[4-(2-{[4-(2-оксо-1,3-оксазинан-3-ил)фенил]амино}пиримидин-4-ил)-1Н-пиразол-1-ил]циклобутанкарбонитрил;
3-(цианометил)-3-[4-(2-{[4-(3-оксоморфолин-4-ил)фенил]амино}пиримидин-4-ил)-1Н-пиразол-1-ил]циклобутанкарбонитрил;
3-(цианометил)-3-[4-(2-{[4-(2-оксо-1,3-оксазолидин-3-ил)фенил]амино}пиримидин-4-ил)-1Н-пиразол-1-ил]циклобутанкарбонитрил;
3-(цианометил)-3-[4-(2-{[4-(2-оксопирролидин-1-ил)фенил]амино}пиримидин-4-ил)-1Н-пиразол-1-ил]циклобутанкарбонитрил;
3-(цианометил)-3-[4-(2-{[4-(1Н-пиразол-1-ил)фенил]амино}пиримидин-4-ил)-1Н-пиразол-1-ил]циклобутанкарбонитрил;
3-(цианометил)-3-[4-(2-{[4-(1,3-оксазол-5-ил)фенил]амино}пиримидин-4-ил)-1Н-пиразол-1-ил]циклобутанкарбонитрил;
3-(цианометил)-3-[4-(2-{[3-(1,3-оксазол-5-ил)фенил]амино}пиримидин-4-ил)-1Н-пиразол-1-ил]циклобутанкарбонитрил;
3-(цианометил)-3-[4-(2-{[4-(морфолин-4-илсульфонил)фенил]амино}пиримидин-4-ил)-1Н-пиразол-1-ил]циклобутанкарбонитрил;
3-(4-{2-[(3-аминофенил)амино]-5-метоксипирмидин-4-ил}-1Н-пиразол-1-ил)-3-циклопропилпропаннитрил;
3-циклопропил-3-[4-(2-{[3-(1,1-диоксидоизотиазолидин-2-ил)фенил]амино}-5-метоксипиримидин-4-ил)-1Н-пиразол-1-ил]пропаннитрил;
4-[1-(2,4-дифторбензоил)пиперидин-4-ил]-3-{4-[5-метокси-2-(пиридин-3-иламино)пиримидин-4-ил]-1Н-пиразол-1-ил}бутаннитрил и
3-(цианометил)-3-[4-(2-{[3-(2-оксопирролидин-1-ил)фенил]амино}пиримидин-4-ил)-1Н-пиразол-1-ил]циклобутанкарбонитрил
или его фармацевтически приемлемая соль.
22. Фармацевтическая композиция, ингибирующая киназу JAK, включающая соединение по любому из пп.1-21 или его фармацевтически приемлемую соль и по меньшей мере один фармацевтически приемлемый носитель.
23. Способ модуляции активации одной или нескольких JAK киназ, включающий контактирование киназы с соединением по любому из пп.1-21.
24. Способ по п.23, где указанная JAK представляет собой JAK1, JAK2, JAK3 или TYK2.
25. Способ по п.23, где указанная JAK представляет собой JAK1 или JAK2.
26. Способ по п.23, где указанная JAK представляет собой JAK2.
27. Способ по п.23, где указанная JAK является мутантной.
28. Способ по п.27, где указанная мутантная JAK включает V617F, F537-K539delinsL, H538QK539L, K539L или N-542-E543del в мутациях в JAK2.
29. Способ по п.23, где указанная модуляция представляет собой ингибирование.
30. Способ по п.23, где указанное соединение является селективным ингибитором одной киназы относительно другой.
31. Способ по п.23, где указанное соединение является селективным ингибитором JAK2 относительно JAK1, JAK3 и TYK2.
32. Способ по п.23, где соединение ингибирует JAK2.
33. Способ по п.23, где для ингибирования активности одной киназы используют более одного соединения формулы I.
34. Способ по п.33, где киназа представляет собой JAK2.
35. Способ по п.23, где для ингибирования более одной киназы используют более одного соединения формулы I.
36. Способ по п.35, где по меньшей мере одна киназа представляет собой JAK2.
37. Способ по п.23, где для ингибирования активности одной киназы соединение используют в комбинации с другим ингибитором киназ.
38. Способ по п.37, где киназа представляет собой JAK2.
39. Способ по п.23, где для ингибирования активностей нескольких киназ соединение используют в комбинации с другим ингибитором киназ.
40. Способ по п.39, где по меньшей мере одна киназа представляет собой JAK2.
41. Способ по п.39, где по меньшей мере две киназы представляют собой ABL1 и JAK2.
42. Способ лечения заболевания у пациента, где указанное заболевание ассоциируется с анормальными активностями одной или нескольких JAK киназ, включающий введение указанному пациенту терапевтически эффективного количества соединения по любому из пп.1-21.
43. Способ по п.42, где соединение наносят местно.
44. Способ по п.42, где вводят более одного соединения формулы IIa-IIg.
45. Способ по п.42, где соединение вводят в комбинации с другим ингибитором киназ.
46. Способ по п.42, где указанное заболевание представляет собой отторжение аллотрансплантата или болезнь трансплантат против хозяина.
47. Способ по п.42, где указанное заболевание представляет собой аутоиммунное заболевание.
48. Способ по п.47, где указанное аутоиммунное заболевание представляет собой кожное расстройство, рассеяный склероз, ревматоидный артрит, ювенильный артрит, диабет типа I, волчанку, воспалительное заболевание кишечника, болезнь Крона, тяжелую псевдопаралитическую миастению, иммунноглобулиновые нефропатии, миокардит или аутоиммунное расстройство щитовидной железы.
49. Способ по п.47, где указанное аутоиммунное заболевание представляет собой буллезное кожное расстройство.
50. Способ по п.49, где указанное буллезное кожное расстройство представляет собой пузырчатку вульгарную (PV) или буллезный пемфигоид (ВР).
51. Способ по п.47, где указанное заболевание представляет собой кожное расстройство.
52. Способ по п.51, где указанное кожное расстройство представляет собой атопический дерматит, псориаз, сенсибилизацию кожи, раздражение кожи, покраснение кожи, контактный дерматит или аллергическую контактную сенсибилизацию.
53. Способ по п.47, где указанное заболевание представляет собой рак.
54. Способ по п.53, где указанный рак представляет собой солидную опухоль.
55. Способ по п.53, где указанный рак представляет собой рак предстательной железы, рак почек, рак печени, рак молочной железы, рак легких, рак щитовидной железы, саркому Капоши, болезнь Кастлемана или рак поджелудочной железы.
56. Способ по п.53, где указанный рак представляет собой рак предстательной железы.
57. Способ по п.53, где указанный рак представляет собой онкозаболевание кроветворной системы.
58. Способ по п.53, где указанный рак представляет собой лимфому, лейкоз или множественную миелому.
59. Способ по п.53, где указанный рак представляет собой острый лимфобластный лейкоз (ALL), хронический миелоидомоноцитарный лейкоз (CMML), хронический миелоидный лейкоз (CML), атипичный CML или атипичный CMML.
60. Способ по п.42, где указанный пациент является пациентом юношеского возраста.
61. Способ по п.53, где указанный рак представляет собой рак кожи.
62. Способ по п.61, где указанный рак кожи представляет собой кожную Т-клеточную лимфому или кожную В-клеточную лимфому.
63. Способ по п.53, где указанный рак представляет собой множественную миелому.
64. Способ по п.47, где указанное заболевание характеризуется мутантной JAK2.
65. Способ по п.64, где по меньшей мере одна мутация указанной мутантной JAK2 располагается в псевдокиназном домене указанной JAK2.
66. Способ по п.47, где указанное заболевание представляет собой миелоидопролиферативное расстройство.
67. Способ по п.66, где указанное миелоидопролиферативное расстройство (MPD) представляет собой истинную полицитемию (PV), эссенциальную тромбоцитемию (ЕТ), миелоидную метаплазию с миелофиброзом (МММ), хронический миелоидный лейкоз (CML), хронический миелоидомоноцитарный лейкоз (CMML), синдром гиперэозинофилии (HES), идиопатический миелофиброз (IMF) или системный мастоцитоз (SMCD).
68. Способ по п.47, где указанное заболевание представляет собой анорексию или кахексию, являющуюся результатом или ассоциированную с раком.
69. Способ лечения аутоиммунного заболевания, кожного расстройства, вирусного заболевания, рака или миелоидопролиферативного расстройства у пациента, включающий введение указанному пациенту терапевтически эффективного количества соединения по любому из пп.1-21.
70. Способ по п.69, где вводят более одного соединения формулы IIa-IIg.
71. Способ по п.69, где соединение формулы IIa-IIg вводят в комбинации с другим ингибитором киназ.
Текст
Настоящее изобретение относится к замещенным бициклическим гетероарильным соединениям формул IIа, IIb, IIc, IId, IIe, IIf и IIg, включая, например, 4-пиразолил-N-арилпиримидин-2 амины, 4-пиразолил-N-пиразолилпиримидин-2-амины и 4-пиразолил-N-пиридилпиримидин-2 амины, которые модулируют активность киназ и применимы при лечении заболеваний, связанных с активностью киназ, включая, например, болезни, связанные с иммунитетом, кожные расстройства,миелоиднопролиферативные расстройства, рак и другие заболевания. 4-ПИРАЗОЛИЛ-N-АРИЛПИРИМИДИН-2-АМИНЫ, 4-ПИРАЗОЛИЛN-ПИРАЗОЛИЛПИРИМИДИН-2-АМИНЫ И 4-ПИРАЗОЛИЛ-NПИРИДИЛПИРИМИДИН-2-АМИНЫ В КАЧЕСТВЕ ИНГИБИТОРОВ КИНАЗ JANUS Область техники, к которой относится изобретение Настоящее изобретение относится к замещенным бициклическим гетероарильным соединениям,включая, например, 4-пиразолил-N-арилпиримидин-2-амины и 4-пиразолил-N-гетероарилпиримидин-2 амины, которые модулируют активность киназ и применимы при лечении заболеваний, связанных с активностью киназ, в том числе, например, заболеваний, связанных с иммунитетом, кожных расстройств,миелоидных пролиферативных расстройств, рака, и других заболеваний. Предпосылки создания изобретения Протеинкиназы (РК) представляют собой группу ферментов, которые регулируют смешанные важные биологические процессы, в том числе, среди прочего, рост, продолжительность существования и дифференцировку клеток, формирование и морфогенез органов, образование новых сосудов, восстановление и регенерацию тканей. Протеинкиназы проявляют свои физиологические функции через катализ фосфорилирования белков (или субстратов) и модулирование, посредством этого, клеточной активности субстратов в различных биологических контекстах. Кроме функций в здоровых тканях/органах многие протеинкиназы также играют более специализированные роли в организме-носителе болезней человека,включая рак. Подгруппа протеинкиназ (также называемых онкогенными протеинкиназами) при разрегулировании может вызывать образование и рост опухоли и также вносит вклад в поддержание и развитие опухоли (Blume-Jensen P. et al., Nature, 2001, 411(6835): 355-365). До сих пор онкогенные протеинкиназы представляют собой одну из самых крупных и привлекающих внимание групп белков-мишеней для вмешательства при раке и разработке лекарственных средств. Протеинкиназы можно классифицировать как рецепторного типа и нерецепторного типа, и они могут показывать специфичность в отношении фосфорилирования или остатков Ser/Thr или остатка Tyr. Таким образом, киназу можно описать как Ser/Thr-киназу (например, рецепторную Ser/Thr-киназу или нерецепторную Ser/Thr-киназу) или Tyr-киназу (например, рецепторную Tyr-киназу или нерецепторнуюTyr-киназу). Рецепторы, которые связываются с лигандами из семейства TGF факторов роста, представляют собой Ser/Thr-киназы и называются TGFR. Примеры нерепторных Ser/Thr-киназ включают РКА, PKG, PKC, СаМ-киназу, киназу фосфорилазы, МАРК (ERK), МЕKK, Akt и mTOR. Рецепторные Tyr-киназы (RTK) имеют внеклеточную часть, трансмембранный домен и внутриклеточную часть, в то время как нерецепторные тирозинкиназы являются полностью внутриклеточными. Опосредуемая RTK сигнальная трансдукция типично инициируется внеклеточным взаимодействием со специфическим фактором роста (лигандом), с последующими, типично, димеризацией рецептора, стимуляцией присущей протеинтирозинкиназе активности и трансфосфорилированием. Посредством этого созадаются сайты связывания для молекул внутриклеточной сигнальной трансдукции, что приводит к образованию комплексов с рядом цитоплазматических молекул, передающих сигналы, что облегчает соответствующую клеточную реакцию, такую как деление клеток, дифференцировка, метаболические действия, и изменения во внеклеточной микросреде. В настоящее время идентифицированы по меньшей мере девятнадцать (19) различных подсемействRTK. Одно подсемейство RTK, названное подсемейством HER, включает EGFR, HER2, HER3 и HER4. Второе семейство RTK, названное инсулиновым подсемейством, включает INS-R, IGF-1R и IR-R. Третье семейство - подсемейство "PDGF" - включает альфа- и бета-рецепторы PDGF, CSFIR, c-kit и FLK-II. Еще одно подсемейство RTK, названное подсемейством FLK, охватывает киназу 1 Kinase insert DomainReceptor fetal liver (KDR/FLK-1), киназу 4 печени плода (FLK-4) и fms-подобную тирозинкиназу 1 (flt-1). Другие семейства RTK называются семейством рецептора FGF (FGFR1, FGFR2, FGFR3 и FGFR4) и подсемейством Met (c-Met, Ron и Sea). Другие RTK представляют собой VEGFR/Flt2, FLT4, семейство RTKEph (A1, А 2, A3, В 2, В 4) и Tie2. Подробное обсуждение протеинкиназ см., например, в Blume-Jensen P. etal., Nature, 2001, 411(6835): 355-365), и Manning G. et al., Science, 2002, 298(5600): 1912-1934. Обзор по семейству киназ TRK можно найти в статье в Cancer Letter, 169 (2001), 107-114, включенной в данное описание в качестве ссылки. Обзор по семейству киназ Eph можно найти в статье в GenesDevelopment,17: 1429-1450, включенной в данное описание в качестве ссылки. Сведения о киназе Tie2 можно найти вSociety. Нерецепторные Tyr-киназы можно разделить на ряд подсемейств, в том числе, Src, Btk, ABL, Fak иJAK. Каждое из таких подсемейств можно дополнительно подразделить на несколько членов, которых часто связывают с онкогенезом. Семейство ABL включает ABL1 и ARG (ABL2). Семейство JAK включает JAK1, JAK2, JAK3 и JAK4. Семейство Src является самым большим и включает, среди прочих, Src,Fyn, Lck и Fgr. Подробное обсуждение таких киназ см. в Bolen J.B., Nonreceptor tyrosine protein kinases,Oncogene, 1993, 8(8): 2025-31. Несоответствующая регуляция киназной активности может вносить вклад в болезненные состояния. Известно, что разрегулированная киназная активность имеет место в результате мутаций (т.е., слияний генов в результате хромосомных транслокаций, точечных мутаций, которые влияют на киназную активность) или изменений экспрессии гена киназы (т.е., повышенной экспрессии через амплификацию гена). Более 40 хромосомных транслокаций, ведущих к слияниям генов и дерегуляции 12 различных Tyr-1 020777 киназ, ассоциируются с различными гематологическими злокачественностями. Протеинтирозинкиназы,вовлеченные в гематологические злокачественности, включают ABL (ABL1), ARG (ABL2), PDGFR,PDGFR, JAK2, SYK, TRKC, FGFR1, FGFR3, FLT3 и FRK. Ряд заболеваний, ассоциированных с мутациями в таких киназах, включает миелопролиферативное расстройство MPD; хронический миелоидный лейкоз CML; острый миелоидный лейкоз AML; острый лимфобластный лейкоз ALL; хронический миеломоноцитарный лейкоз DMML/миелопролиферативный синдром 8 р 13 EMS; анапластическую крупноклеточную лимфому ALCL; воспалительную миелофибробластную опухоль IMF; периферическую Тклеточную лимфому PTL; истинную полицитемию PV и эссенциальную тромбоцитемию ЕТ (Y. Chalandon and J. Schwaller, Haematologica, 2005, 90(7): 949-968). Низкомолекулярные ингибиторы различных киназ успешно используют для лечения болезненных состояний. Низкомолекулярные ингибиторы протеинтирозинкиназ ABL, ALK, PDGFR, PDGFR, KIT, FLT3, FGFR1 и FGFR3 используют для лечения гематологических злокачественностей (Y. Chalandon and J. Schwaller, Haematologica, 2005, 90(7): 949968). Конкретно, несоответствующая активность нерецепторных Tyr-киназ ABL и JAK влечет за собой заболевание человека. Несоответствующая активность киназы ABL является признаком рака и может вносить вклад в миелопролиферативные расстройства и фиброзные состояния, такие как фиброз легкихJAK вносит вклад в рак, миелоидные пролиферативные расстройства и расстройства иммунной системы. Семейство ABL нерецепторных Tyr-киназ включает ABL1 и ARG (ABL2) (Kruh G. D. et al., PNAS,1990, Aug, 87(15), 5802-6). С этого времени семейство ABL будет называться просто ABL. ИсследованияABL1 показали вовлечение в несколько сигнальных путей, в том числе, в Ras-зависимый, Racзависимый, JNK-зависимый, Р 13K-зависимый, РКС-зависимый, mTOP и JAK/STAT. Такие сигнальные пути регулируют процессы, включающие развитие клеточного цикла, остановку клеточного цикла, рост клеток, дифференцировку клеток и апоптоз (M.G. Kharas and D.A. Fruman, Cancer Research, 65: 20472053; X. Zou and K. Calame, J. Biol. Chem., 274(26): 18141-18144). Дерегуляция активности киназы ABL связана с заболеванием и может иметь место благодаря амплификациям и мутациям генов. Например, слияния генов киназ ABL связаны с онкозаболеваниями крови, слияния ABL1 с TEL, NUP214, EMS и SFQ коррелируют с CML и ALL, и слияния ARG (ABL2) сBCR и TEL коррелируют с CML (Y. Chalandon and J. Schwaller, Haematologica, 2005, 90(7): 949-968). Повсеместно считается, что слитый ген BCR/ABL1, который является результатом хромосомной транслокации, образующей филадельфийскую хромосому (Ph), является причинным фактором при лейкозе: филадельфийская хромосома ассоциируется с 95% случаев CML и 10% случаев ALL (X. Zou and K. Calame,J. Biol. Chem., 274 (26) : 18141-18144). Низкомолекулярный ингибитор иматиниба мезилат (Gleevec) - низкомолекулярный ингибитор активности киназы ABL1 широко используется для лечения CML. Однако клиническая устойчивость к иматинибу является все возрастающей проблемой. Устойчивость имеет место в большинстве случаев благодаря клональной экспансии мутантов в киназном домене BCR/ABL1 (Corre M.E. et al., Science,293(5531): 876-80). Многочисленные мутации картированы из клинических изолятов, включая T315D,F359D, D276G, Е 255K, М 351 Т, G250E, H396R, Q252H, Y253H, E355G, F317L, G250E, Y253F, F359V,Q252R, L387M, M244V, M343T/F382L и V379I (Shan N. P. et al., Cancer Cell., 2: 117-25). Таким образом,необходимы низкомолекулярные ингибиторы для нацеливания на устойчивых к иматинибу мутантовABL1. Кроме того, ожидается, что комбинированная терапия с несколькими низкомолекулярными ингибиторами, имеющими мишенью ABL1, уменьшит вероятность устойчивости, возникающей в одной клетке благодаря мутации ABL1, и последующую клональную экспансию. Путь вовлечения протеинтирозинкиназ семейства киназ Janus (JAK) и клеток-трансдукторов сигнала и активаторов транскрипции (STAT) включается при передаче сигнала широким рядом цитокинов и факторов роста. Цитокины представляют собой низкомолекулярные полипептиды или гликопротеины,которые стимулируют биологические реакции фактически во всех типах клеток. Например, цитокины регулируют множество путей, вовлеченных в воспалительную реакцию организма-хозяина на сепсис. Цитокины влияют на дифференцировку, пролиферацию и активацию клеток, и они могут модулировать как провоспалительные, так и противовоспалительные реакции, что позволяет организму соответственно реагировать на патогены. Как правило, цитокиновые рецепторы не имеют собственной тирозинкиназной активности, и, таким образом, требуются рецепторассоциированные киназы для распространения каскада фосфорилирования. JAK выполняют такую функцию. Цитокины связываются со своими рецепторами,вызывая димеризацию рецепторов, и это позволяет JAK фосфорилировать друг друга, а также специфические тирозиновые мотивы в цитокиновых рецепторах. STAT, которые распознают такие фосфотирозиновые мотивы, собираются у рецептора и затем сами активируются событием JAK-зависимого фосфорилирования тирозина. После активации STAT диссоциируются от рецепторов, димеризуются и перемещаются к ядрам для связывания со специфическими сайтами ДНК и изменения транскрипции (Scott M. Семейство JAK играет некую роль в цитокинзависимой регуляции пролиферации и функции клеток, вовлеченных в иммунную реакцию. В настоящее время известны четыре члена семейства JAK млекопитающих: JAK1 (также известная как киназа-1 Janus), JAK2 (также известная как киназа-2 Janus),JAK3 (также известная как киназа Janus, лейкоцит; JAKL, L-JAK и киназа-3 Janus) и TYK2 (также известная как протеинтирозинкиназа 2). Белки JAK по размеру колеблются от 120 до 140 кД и включают семь консервативных доменов гомологии JAK (JH); один из них является функциональным каталитическим доменом киназы, и другой представляет собой домен псевдокиназы, обслуживающий, возможно,регуляторную функцию, и/или служащий в качестве сайта "причаливания" для STAT (Scott, Godshall etal., 2002, цит. выше). В то время как JAK1, JAK2 и TYK2 экспрессируются повсеместно, сообщается, чтоJAK3 экспрессируется преимущественно в лимфоцитах. Цитокинстимулированные иммунные и воспалительные реакции не только вносят вклад в нормальную защиту организма, но они также играют роль в патогенезе заболеваний: патологии, такие как тяжелый комбинированный иммунодефицит (SCID), появляются из гипоактивности и подавления иммунной системы, и гиперактивная или несоответствующая иммунная/воспалительная реакция вносит вклад в патологию аутоиммунных заболеваний, таких как ревматоидный и псориатический артрит, астма и системная красная волчанка, воспалительное заболевание кишечника, рассеяний склероз, сахарный диабет типа 1, тяжелая псевдопаралитическая миастения, тиреоидит, иммуноглобулиновые нефропатии, миокардит, а также такие болезни, как склеродерма и остеоартрит (Ortmann R. А., Т. Cheng et al. (2000), "Janus kinases and signal transducers and activators of transcription: their roles in cytokine signaling, developmentand immunoregulation", Arthritis Res., 2(1): 16-32). Более того, синдромы смешанной презентазии аутоиммунного заболевания и иммунодефицита являются вполне обычными (Candotti F., L. Notarangelo et al.(2002), "Molecular aspects of primary immunodeficiencies: lessons from cytokine and other signaling pathways", J. Clin. Invest., 109(10): 1261-9). Таким образом, терапевтические средства типично нацелены на усиление или подавление иммунных и воспалительных путей соответственно. Недостаточность экспрессии членов семейства JAK ассоциируется с болезненными состояниями. Мыши JAK1-/-, мелкие от рождения, не способны кормиться и погибают перинатально (Rodig S. J., M. A.in cytokine-induced biologic responses", Cell, 93(3): 373-83). Эмбрионы мышей JAK2-/- анемичны и погибают примерно на 12,5 день после коитуса из-за отсутствия доказательного эритропоэза. Фибробласты с дефицитом JAK2 не реагируют на IFN-гамма, хотя реакции на IFN-альфа/бета и IL-6 естественные. JAK2 функционирует в сигнальной трансдукции специфической группы цитокиновых рецепторов, требуемых в доказательном эритропоэзе (Neubauer H., A. Cumano et al. (1998), Cell, 93(3): 397-409; Parganas E., D.Wang et al. (1998), Cell, 93(3): 385-95). Оказывается, что JAK3 играет роль в нормальном развитии и функционировании В- и Т-лимфоцитов. Сообщается, что мутации JAK3 ответственны за аутосомнорецессивный тяжелый комбинированный иммунодефицит (SCID) у людей (Candotti F., S.A. Oakes et al.(1997), "Structural and functional basis for JAK3-deficient severe combined immunodeficiency", Blood, 90(10): 3996-4003). Полагают, что путь JAK/STAT, и в частности, все четыре члена семейства JAK, играют роль в патогенезе астматической реакции, хронической обструктивной болезни легких, бронхите и других реакциях,связанных с воспалением заболеваний нижних дыхательных путей. Например, несоответствующие иммунные реакции, которые характеризуют астму, сопровождаются субпопуляцией хелперных Т-клетокCD4+ , называемых Т-хелперными 2 клетками (Th2). Передача сигнала через цитокиновый рецептор IL-4 стимулирует JAK1 и JAK3 к активации STAT6, и передача сигнала через IL-12 стимулирует активациюJAK2 и TYK2 и последующее фосфорилирование STAT4. STAT4 и STAT6 регулируют несколько аспектов дифференцировки хелперных Т-клеток CD4+ (Pernis А.В. and P.В. Rothman (2002), "JAK-STAT signaling in astma", J. Clin. Invest., 109(10): 1279-83). Более того, обнаружено, что TYK2-дефицитные мыши имеют усиленное опосредуемое клетками Th2 аллергическое воспаление дыхательных путей (Seto Y., H.Nakajima et al. (2003), "Enhanced Th2 cell-mediated allergic inflammation in TYK2-deficient mice", J. Immunol., 170(2): 1077-83). Более того, многие цитокины, которые передают сигналы через киназы JAK, связаны с вопалительными заболеваниями или состояниями верхних дыхательных путей, такими как заболевания, поражающие нос и синус (т.е., ринит, синусит), классическими или неклассическими аллергическими реакциями. Также подразумевается, что путь JAK/STAT играет роль в воспалительных заболеваниях/состояниях глаз, включая, но не ограничиваясь перечисленным, ирит, увеит, склерит, конъюнктивит, а также хронические аллергические реакции. Следовательно, ингибирование киназ JAK может сыграть благоприятную роль в лекарственном лечении таких заболеваний. Путь JAK/STAT также вовлекается в онкозаболевания. Сообщается об активации STAT3 в случае эндометриальных и цервикальных онкозаболеваний (С.L. Chen et al. (2007), British Journal of Cancer, 96: 591-599). Кроме того, компоненты пути JAK/STAT, в частности, JAK3, играют роль в онкозаболеваниях иммунной системы. При Т-клеточном лейкозе/лимфоме взрослых (ATLL) Т-клетки CD4+ приобретают трансформированный фенотип - событие,которое коллерирует с обнаружением конститутивного фосфорилирования JAK и STAT. Более того, ас-3 020777 социация между JAK3 и STAT-1, STAT-3 и активация STAT-5 и развитие клеточного цикла показаны как окрашиванием иодидом пропидия, так и внедрением бромдезоксиуридина в клетки четырех проверенных больных ATLL. Такие результаты предполагают, что активация JAK/STAT ассоциируется с репликацией лейкозных клеток, и что терапевтические подходы, намеченные для ингибирования JAK/STAT, можно рассматривать как останавливающие рост неоплазмы (Takemoto S., J. С. Mulloy et al. (1997), "Proliferationof adult T cell leukemia/lymphoma cells is associated with the constitutive activation of JAK/STAT proteins",Proc. Natl. Acad. Sci. USA, 94(25): 13897-902). Блокада сигнальной трансдукции на уровне киназ JAK считается преспективной для разработки способов лечения онкозаболеваний человека. Цитокины семейства интерлейкина 6 (IL-6), которые активируют клетку-трансдуктор gp130, являются основными факторами выживания и роста для клеток множественной миеломы (ММ) человека. Полагают, что сигнальная трансдукция gp130 вовлекает JAK1,JAK2 и Tyk2 и последующие эффекторы STAT-3 и митогенактивированные пути протеинкиназ (МАРК). В клеточных линиях IL-6-зависимой ММ, обработанных ингибитором JAK2 тирфостином AG490, ингибируются активность киназы JAK2 и фосфорилирование ERK2 и STAT3. Более того, подавляется пролиферация клеток и индуцируется апоптоз (De Vos J., M. Jourdan et al. (2000), "JAK2 tyrosine kinase inhibitortyrphostin AG490 downregulates the mitogen-activated protein kinase (МАРК) and signal transducer and activator of transcription (STAT) pathways and induces apoptosis in myeloma cells", Br. J. Haematol., 109(4): 823-8). Однако в некоторых случаях AG490 может индуцировать состояние покоя у опухолевых клеток и затем фактически защищать их от гибели. Активация JAK/STAT при онкозаболеваниях может происходить по нескольким механизмам,включая стимуляцию цитокинами (например, IL-6 или GM-CSF), или путем уменьшения в эндогенных супрессорах передачи сигнала JAK, таких как SOCS (супрессор или передача сигнала цитокинами) илиPIAS (белковый ингибитор активированного STAT) (Boudny V. and Kovarik J., Neoplasm., 49: 349-355,2002). Важно, что активация передачи сигналов STAT, a также другие пути после JAK (например, Akt),коррелируют с плохим прогнозом при онкозаболеваниях многих типов (Bowman Т. et al., Oncogene, 19: 2474-2488, 2000). Более того, повышенные уровни циркулирующих цитокинов, которые передают сигналы через JAK/STAT, могут оказать вредное воздействие на здоровье пациента, так как полагают, что они играют причинную роль в кахексии и/или хронической усталости. Как таковое, ингибирование JAK может представлять терапевтическую ценность при лечении больных раком по причинам, которые распространяются за пределы противоопухолевой активности. Показание кахексии может получить дополнительную механистическую поддержку с пониманием, что фактор насыщения лептин передает сигналы через JAK. Фармакологическую нацеленность киназы Janus 3 (JAK3) успешно используют для регулирования отторжения аллотрансплантата и болезни трансплантат против хозяина (CVHD). Кроме вовлечения в передачу сигналов цитокиновых рецепторов JAK3 также участвует в пути передачи сигналов CD40 моноцитов периферической крови. Во время индуцируемого CD40 созревания миелоидных дендритных клеток (DC) индуцируется активность JAK3, и наблюдают усиление экспрессии молекул костимуляторов, выработки IL-12 и возможной аллогенной стимулирующей способности. Рационально созданный ингибитор JAK3 WHI-P-154 предупреждает такие эффекты, останавливая DC на уровне незрелости, причем предполагается, что иммуносупрессорная терапия, имеющая целью тирозинкиназу JAK3, также может поражать функцию миелоидных клеток (Saemann M. D., С. Diakos et al. (2003), "Prevention of CD40triggered dendritic cell maturation and induction of T-cell hyperactivity by targeting of Janus kinase 3", Am. J.Transplant., 3(11): 1341-9). В системе на мышиной модели также показано, что JAK3 является важной молекулярной мишенью для лечения аутоиммунного инсулинзависимого сахарного диабета (типа 1). Рационально созданный ингибитор JAK3 JANEX-1 обнаруживает сильную иммуномодулирующую активность и задерживает появление диабета у мышей NOD как модели аутоиммунного диабета типа 1type 1 diabetes in NOD mice", Clin. Immunol., 106(3): 213-25). Предполагается, что ингибирование тирозинкиназы JAK2 может быть благоприятным для пациентов с миелопролиферативным расстройством (Levine et al., Cancer Cell, Vol.7, 2005: 387-397). Миелопролиферативное расстройство (MPD) включает истинную полицитемию (PV), эссенциальную тромбоцитемию (ET), миелоидную метаплазию с миелофиброзом (МММ), хронический миелоидный лейкоз (CML),хронический миеломоноцитарный лейкоз (CMML), синдром гиперэозинофилии (HES) и системный мастоцитоз (SMCD). Хотя полагают, что миелопролиферативное расстройство (такое как PV, ЕТ и МММ) вызывается приобретенной соматической мутацией в гемопоэтических предшественниках, генетическая основа таких заболеваний неизвестна. Однако сообщается, что кроветворные клетки большинства больных PV и значительного числа больных ЕТ и МММ обладают повторной соматической активирующей мутацией в тирозинкиназе JAK2. Также сообщается, что ингибирование киназы JAK2V617F низкомолекулярным ингибитором ведет к ингибированию пролиферации кроветворных клеток, что наводит на мысль, что тирозинкиназа JAK2 является потенциальной мишенью для фармакологического ингибирования у больных PV, ЕТ и МММ. Также представляется, что ингибирование киназ JAK имеет терапевтическое благоприятное дейст-4 020777 вие у пациентов, страдающих от кожных иммунных расстройств, таких как псориаз, и кожной сенсибилизации. Как правило, признают, что при обыкновенном псориазе - наиболее обычной форме псориаза для поддержания заболевания и ассоциированных с ним псориатических бляшек важны активированные Т-лимфоциты (Gottlieb А. В. et al., Nat. Rev. Drug Disc, 4: 19-34). Псориатические бляшки содержат значительный иммунный инфильтрат, включающий лейкоциты и моноциты, а также несколько слоев эпидермиса с усиленной пролиферацией кератиноцитов. Хотя начальная активация иммуноцитов при псориазе происходит путем установленного механизма заболевания, полагают, что поддержание зависит от ряда цитокинов зоны воспаления в дополнение к различным цитокинам и факторам роста (JCI, 113: 16641675). Многие из них, в том числе, интерлейкины -2, -4, -6, -7, -12, -15, -18 и -23, а также GM-CSF и IFNg передают сигналы через киназы Janus (JAK) (Adv. Pharmacol., 2000, 47: 113-74). Как таковая, блокада сигнальной трансдукции на уровне киназ JAK может привести к благоприятным терапевтическим эффектам у пациентов, страдающих от псориаза или других иммунных расстройств кожи. Известно, что некоторые терапевтические средства могут вызывать у некоторых пациентов иммунные реакции, такие как накожное высыпание или диарея. Например, введение некоторых новых нацеленных противораковых средств, таких как иресса, эрбитукс и тарцева, вызывает у некоторых пациентов высыпание в форме акне. Другим примером является то, что некоторые терапевтические средства, применяемые местно, вызывают раздражение кожи, кожное высыпание, контактный дерматит или аллергическую контактную сенсибилизацию. Некоторых пациентов такие иммунные реакции могут беспокоить,но у других иммунные реакции, такие как сыпь или диарея, могут привести к невозможности продолжать лечение. Хотя движущая сила таких иммунных реакций в настоящее время полностью не выяснена, такие иммунные реакции вероятно связаны с иммунным инфильтратом. Ведется широкий поиск ингибиторов киназ Janus или родственных киназ, и в некоторых публикациях сообщается об эффективных классах соединений. Например, о некоторых ингибиторах сообщается в WO 99/65909, US 2004/0198737, WO 2004/099204, WO 2004/099205 и WO 01/42246. В WO 2004/72063 иWO 99/62908 сообщается о гетероарилзамещенных пирролах и других соединениях. Таким образом, новые или улучшенные средства, которые ингибируют киназы, снова и снова необходимы, в частности, для того, чтобы справиться с мутантами. Комбинированная терапия (с использованием вновь идентифицированных средств) может снизить случайности развития устойчивых к лекарственным средствам мутантов киназ, и необходимы новые средства для лечения существующих устойчивых к лекарственным средствам мутантов киназ (т.е., мутантов ABL1, которые устойчивы к иматинибу). Все время необходимы средства, которые ингибируют киназы JAK, которые действуют как иммунодепрессанты, для трансплантатов органов, а также средства для предупреждения и лечения аутоиммунных заболеваний (например, рассеяного склероза, ревматоидного артрита, астмы, диабета типа 1, воспалительного заболевания кишечника, болезни Крона, аутоиммунных расстройств щитовидной железы, болезни Альцгеймера), заболеваний, включающих гиперактивную воспалительную реакцию (например,экземы), аллергий, рака (например, рака предстательной железы, лейкоза, множественной миеломы) и некоторых иммунных реакций (например, высыпания акне или контактного дерматита или диареи), вызываемых другими терапевтическими средствами, немногие из которых названы. Соединения, композиции и способы, описанные в данном описании, относятся к таким потребностям и другим целям. Сущность изобретения Настоящее изобретение относится к соединениям формулы IIa, IIb, IIc, IId, IIe, IIf или IIg или их фармацевтически приемлемым солям, где в указанных формулах составляющие имеют значения, указанные ниже. Настоящее изобретение также относится к композициям, включающим соединение формулы IIa,IIb, IIc, IId, IIe, IIf или IIg или его фармацевтически приемлемую соль и по меньшей мере один фарма-5 020777 цевтически приемлемый носитель. Настоящее изобретение также относится к способам модуляции активности одной или несколькихJAK киназ, включающим контактирование киназы с соединением формулы IIa, IIb, IIc, IId, IIe, IIf или IIg или его фармацевтически приемлемой солью. Настоящее изобретение также относится к способам лечения заболевания у пациента, где указанное заболевание ассоциируется с анормальной активностью JAK, включающим введение пациенту терапевтически эффективного количества соединения формулы IIa, IIb, IIc, IId, IIe, IIf или IIg или его фармацевтически приемлемой соли. Подробное описание Настоящее изобретение относится, среди прочего, к соединениям, модулирующим активность одной или нескольких киназ JAK, и применимым, например, при лечении различных заболеваний, таких,какие ассоциируются с экспрессией или активностью JAK. Соединения по изобретению имеют формулу IIa, IIb, IIc, IId, IIe, IIf или IIg или его фармацевтически приемлемая соль, где цикл А представляет собой C6-10 арил, пиразолил или пиридил;R1, R2, R3 и R4 выбирают независимо из Н, C1-6-алкила, ORa и C(O)Rb; Су 1 и Су 2 выбирают независимо из С 6-10 арила, С 3-7 циклоалкила, C3-10 гетероарила и C35 гетероциклоалкила, каждый из которых необязательно замещен 1 или 2 заместителями, независимо выбранными из галогена, C1-6-алкила и ORa1;Ra и Rb выбирают независимо из Н, C1-6-алкила, С 6-10 арила, С 3-10 гетероарила и С 3-5 гетероциклоалкила, где указанный C1-6-алкил, С 6-10 арил, С 3-10 гетероарил и С 3-5 гетероциклоалкил необязательно замещен 1 или 2 заместителями, независимо выбранными из ОН, C1-6-алкила и C1-6-алкокси;Ra1, Rb1, Rc1 и Rd1 выбирают независимо из Н, C1-6-алкила, C6-10 арила, С 3-7 циклоалкила, С 3-10 гетероарила, С 3-5 гетероциклоалкила, С 3-10 гетероарил-С 1-4 алкила, С 3-7 циклоалкил-С 1-4 алкила и С 3-5 гетероциклоалкил-С 1-4 алкила, где указанный C1-6-алкил, С 6-10 арил, С 3-7 циклоалкил, С 3-10 гетероарил, С 3-5 гетероциклоалкил, С 3-10 гетероарил-С 1-4 алкил, С 3-7 циклоалкил-С 1-4 алкил или С 3-5 гетероциклоалкил-С 1-4 алкил необязательно замещен 1 или 2 заместителями, независимо выбранными из C1-6-алкила, галогена,ORa2, C(O)NRc2Rd2, NRc2Rd2 и S(O)2Rb2; или Rc1 и Rd1 вместе с атомом N, к которому они присоединены, образуют 4-, 5- или 6-членную гетероциклоалкильную группу, необязательно замещенную 1 или 2 заместителями, независимо выбранными из C1-6-алкила, CN, ORa2, C(O)Rb2, NRc2Rd2 и NRc2C(O)Rb2;Ra2, Rb2, Rc2 и Rd2 выбирают независимо из H, C1-6-алкила, С 3-7 циклоалкила и С 3-10 гетероарила иm равен 1. В некоторых воплощениях А представляет собой С 6-10 арил. В некоторых воплощениях А представляет собой фенил. В некоторых воплощениях А представляет собой пиразолил. В некоторых воплощениях А представляет собой пиридил. В некоторых воплощениях Q представляет собой Н, Су 1 или CN. В некоторых воплощениях Q представляет собой Су 1, C(O)Rb1, S(O)2Rb1 или ORa1. В некоторых воплощениях Су 1 представляет собой С 6-10 арил или С 3-7 циклоалкил. В некоторых воплощениях Су 1 представляет собой С 3-10 гетероарил или С 3-5 гетероциклоалкил. В некоторых воплощениях R1 представляет собой Н. В некоторых воплощениях R2 представляет собой Н. В некоторых воплощениях R2 представляет собой C1-6-алкил. В некоторых воплощениях R2 представляет собой метил. В некоторых воплощениях R2 представляет собой C1-6-алкокси. В некоторых воплощениях R2 представляет собой метокси. В некоторых воплощениях R3 представляет собой Н. В некоторых воплощениях R4 представляет собой Н. В некоторых воплощениях X представляет собой Н. В некоторых воплощениях Y представляет собой Н, Су 2, NO2, ORa1, C(O)Rb1, C(O)NRc1Rd1,C(O)ORa1, NRc1Rd1, NRc1C(O)Rb1, NRc1C(O)ORa1, S(O)2Rb1 или NRc1S(О)2Rb1. В некоторых воплощениях Y представляет собой Н. В некоторых воплощениях Су 2 представляет собой С 6-10 арил или С 3-7 циклоалкил. В некоторых воплощениях Су 2 представляет собой С 3-10 гетероарил или С 3-5 гетероциклоалкил. В различных местах настоящего описания заместители соединений по изобретению раскрываются в группах или в интервалах. Конкретно имеется в виду, что изобретение включает каждую и любую комбинацию членов таких групп и интервалов. Например, конкретно имеется в виду, что термин "C1-6-алкил" раскрывает по отдельности метил, этил, С 3-алкил, С 4-алкил, С 5-алкил и С 6-алкил. Также следует иметь в виду, что некоторые особенности изобретения, которые для ясности описаны в контексте отдельных воплощений, также могут быть представлены в комбинации в едином воплощении. Напротив, различные особенности изобретения, которые, для краткости, описаны в контексте единого воплощения, также могут быть представлены по отдельности или в любой подходящей комбинации. В различных местах настоящего описания описаны связующие заместители. Конкретно имеется в виду, что каждый связующий заместитель включает как прямую, так и обратную формы связующего заместителя. Например, -NR(CR'R")n- включает как -NR(CR'R")n-, так и - (CR'R")nNR-. Когда структура ясно требует связующей группы, следует иметь в виду, что связующими группами являются переменные Маркуша, перечисленные для такой группы. Например, если структура требует связующей группы, и определение группы Маркуша для такой группы указывает "алкил" или "арил", тогда подразумевается,что "алкил" или "арил" представляет собой связущую алкиленовую группу или ариленовую группу соответственно. Термин n-членный, где n равен целому числу, типично описывает число образующих цикл атомов в группе, где число образующих цикл атомов равно n. Например, пиперидинил является примером 6 членного гетероциклоалкильного цикла, и 1,2,3,4-тетрагидронафталин является примером 10-членной циклоалкильной группы. Используемый в данном описании термин "алкил" предназначен для обозначения насыщенной углеводородной группы, которая является линейной или разветвленной. Примеры алкильных групп включают метил (Me), этил (Et), пропил (например, н-пропил и изопропил), бутил (например, н-бутил, изобутил, втор-бутил, трет-бутил), пентил (например, н-пентил, изопентил, втор-пентил, неопентил) и т.п. Алкильная группа может содержать от 1 до примерно 20, от 2 до примерно 20, от 1 до примерно 10, от 1 до примерно 8, от 1 до примерно 6, от 1 до примерно 4 или от 1 до примерно 3 атомов углерода. Связующая алкильная группа в данном описании называется "алкилен". Используемый в данном описании термин "алкенил" относится к алкильной группе с одной или несколькими углерод-углеродными двойными связями. Примеры алкенильных групп включают этенил,пропенил, циклогексенил и т.п. Алкенильная группа может содержать от 2 до примерно 20, от 3 до примерно 15, от 2 до примерно 10, от 2 до примерно 8, от 2 до примерно 6, от 2 до примерно 4 или от 2 до примерно 3 атомов углерода. Связующая алкенильная группа в данном описании называется "алкенилен". Используемый в данном описании термин "алкинил" относится к алкильной группе с одной или несколькими углерод-углеродными тройными связями. Примеры алкинильных групп включают этинил,пропинил и т.п. Алкинильная группа может содержать от 2 до примерно 20, от 3 до примерно 15, от 2 до примерно 10, от 2 до примерно 8, от 2 до примерно 6, от 2 до примерно 4 или от 2 до примерно 3 атомов углерода. Связующая алкинильная группа в данном описании называется "алкинилен". Используемый в данном описании термин "галогеналкил" относится к алкильной группе с одним или несколькими галогеновыми заместителями. Примеры галогеналкильной группы включают CF3, C2F2,CHF2, CCl3, CHCl2, C2Cl5 и т.п. Используемый в данном описании термин "галогенсульфанил" относится к сульфогруппе с одним или несколькими галогеновыми заместителями. Примеры галогенсульфанильной группы включают пентагалогенсульфанильные группы, такие как SF5. Используемый в данном описании термин "арил" относится к моноциклическим или полициклическим (например, имеющим 2, 3 или 4 конденсированных цикла) ароматическим углеводородным группам, таким как, например, фенил, нафтил, антраценил, фенантренил, инданил, инденил и т.п. В некото-7 020777 рых воплощениях арильные группы содержат от 6 до примерно 20 атомов углерода, от 6 до примерно 15 атомов углерода или от 6 до примерно 10 атомов углерода. Связующая арильная группа в данном описании называется "арилен". Используемый в данном описании термин "циклоалкил" относится к неароматическим циклическим углеводородным группам, включая циклизованные алкильные, алкенильные и алкинильные группы. Циклоалкильные группы могут включать моно- или полициклические (например, имеющие 2, 3 или 4 конденсированных цикла) группы и спироциклы. Образующие цикл атомы углерода циклоалкильной группы могут быть, необязательно, замещены оксо или сульфидо. Циклоалкильные группы также включают циклоалкилидены. Примеры циклоалкильных групп включают циклопропил, циклобутил, циклопентил, циклогексил, циклогептил, циклопентенил, циклогексенил, циклогексадиенил, циклогептатриенил, норборнил, норпинил, норкарнил, адамантил и подобные группы. В определение циклоалкила также включены группы, которые имеют один или несколько ароматических циклов, конденсированных (т.е.,имеющих общую связь) с циклоалкильным циклом, например, бензо- или тиенильные производные циклопентана, циклопентена, циклогексена и т.п. Циклоалкильная группа, содержащая конденсированный ароматический цикл, может присоединяться через любой образующий цикл атом, включая образующий цикл атом конденсированного ароматического цикла. Циклоалкильная группа может содержать от 3 до примерно 20, от 3 до примерно 15, от 3 до примерно 10, от 3 до примерно 8, от 3 до примерно 7, от 3 до примерно 6 или от 4 до примерно 7 атомов углерода. Связующая циклоалкильная группа в данном описании называется "циклоалкилен". Используемый в данном описании термин "гетероарил" относится к ароматическому гетероциклу по меньшей мере с одним гетероатомом членом цикла, таким как атом серы, кислорода или азота. Гетероарильные группы включают моноциклические и полициклические (например, имеющие 2, 3 или 4 конденсированных цикла) системы. Примеры гетероарильных групп включают без ограничения пиридил, пиримидинил, пиразинил, пиридазинил, триазинил, фурил, хинолил, изохинолил, тиенил, имидазолил, тиазолил, индолил, пиррил, оксазолил, бензофурил, бензотиенил, бензтиазолил, изоксазолил, пиразолил, триазолил, тетразолил, индазолил, 1,2,4-тиадиазолил, изотиазолил, бензотиенил, пуринил, карбазолил, бензимидазолил, индолинил и подобные группы. В некоторых воплощениях любой образующий цикл N в гетероарильной группе может быть замещен оксо. В некоторых воплощениях гетероарильная группа содержит от 1 до примерно 20 атомов углерода, и в других воплощениях от примерно 3 до примерно 20 атомов углерода, от примерно 3 до примерно 10 атомов углерода, от примерно 3 до примерно 5 атомов углерода. В некоторых воплощениях гетероарильная группа содержит от 3 до примерно 14, от 4 до примерно 14, от 3 до примерно 7 или 5-6 атомов, образующих цикл. В некоторых воплощениях гетероарильная группа содержит от 1 до примерно 4, от 1 до примерно 3 или 1-2 гетероатома. Связующая гетероарильная группа в данном описании называется "гетероарилен". Используемый в данном описании термин "гетероциклоалкил" относится к неароматическим гетероциклам с одним или несколькими образующими цикл гетероатомами, такими как атом О, N или S. Гетероциклоалкильные группы включают моноциклические и полициклические (например, имеющие 2, 3 или 4 конденсированных цикла) системы, а также спироциклы. Примеры "гетероциклоалкильных" групп включают морфолино, тиоморфолино, пиперазинил, тетрагидрофуранил, тетрагидротиенил, 2,3 дигидробензофурил, 1,3-бензодиоксол, бензо-1,4-диоксан, пиперидинил, пирролидинил, изоксазолидинил, изотиазолидинил, пиразолидинил, оксазолидинил, тиазолидинил, имидазолидинил и подобные группы. Циклообразующие атомы углерода и гетероатомы гетероциклоалкильной группы могут быть,необязательно, замещены оксо или сульфидо. В определение гетероциклоалкила также включены группы, которые имеют один или несколько ароматических циклов, конденсированных (т.е., имеющих общую связь) с неароматическим гетероциклическим циклом, например фталаимидил, нафталимидил и бензопроизводные гетероциклов. Гетероциклоалкильная группа может присоединяться через образующий цикл атом углерода или образующий цикл гетероатом. Гетероциклоалкильная группа, содержащая конденсированный ароматический цикл, может присоединяться через любой образующий цикл атом,включая образующий цикл атом конденсированного ароматического цикла. В некоторых воплощениях гетероциклоалкильная группа может содержать от 1 до примерно 20 атомов углерода, и в других воплощениях от примерно 3 до примерно 20 атомов углерода. В некоторых воплощениях гетероциклоалкильная группа содержит от примерно 3 до примерно 14, от 4 до примерно 14, от 4 до примерно 7 или 5-6 атомов, образующих цикл. В некоторых воплощениях гетероциклоалкильная группа содержит от 1 до примерно 4, от 1 до примерно 3 или 1-2 гетероатома. Гетероциклоалкильная группа может содержать от 1 до примерно 20, от 1 до примерно 15, от 1 до примерно 10, от 1 до примерно 8, от 1 до примерно 7, от 1 до примерно 6 или от 1 до примерно 5 атомов углерода. В некоторых воплощениях гетероциклоалкильная группа содержит от 0 до 3 двойных или тройных связей. В некоторых воплощениях гетероциклоалкильная группа содержит от 0 до 2 двойных или тройных связей. Связующая гетероциклоалкильная группа в данном описании называется "гетероциклоалкилен". Используемый в данном описании термин "галоген" включает фтор, хлор, бром и иод. Используемый в данном описании термин "арилалкил" относится к алкилу, замещенному арилом, и является бензил. Используемый в данном описании термин "гетероарилалкил" относится к алкилу, замещенному гетероарилом, и "гетероциклоалкилалкил" относится к алкилу, замещенному гетероциклоалкилом. Используемый в данном описании термин "амино" относится к NH2. Используемый в данном описании термин "алкокси" относится к -О-алкильной группе. Примеры алкоксигрупп включают метокси, этокси, пропокси (например, н-пропокси и изопропокси), трет-бутокси и т.п. Используемый в данном описании термин "галогеналкокси" относится к -О-(галоген)алкильной группе. Соединения, описанные в данном описании, могут быть асимметричными (например, имеющими один или несколько стереоцентров). Подразумеваются все стереоизомеры, такие как энантиомеры и диастереомеры, если не указано иное. Соединения по настоящему изобретению, содержащие асимметрично замещенные атомы углерода, можно выделить в оптически активных или рацемических формах. Способы получения оптически активных форм из оптически неактивных исходных веществ известны в технике, как, например, расщепление рацемических смесей или стереоселективный синтез. Многие геометрические изомеры олефинов, двойных связей C=N и т.п. также могут присутствовать в соединениях, описанных в данном описании, и все такие устойчивые изомеры рассматриваются в настоящем изобретении. Геометрические цис- и транс-изомеры соединений по настоящему изобретению описаны и могут быть выделены в виде смеси изомеров или в виде отдельных изомерных форм. Расщепление рацемических смесей соединений можно осуществить многими способами, известными в технике. Примеры способов включают фракционную кристаллизацию с использованием хиральной расщепляющей кислоты, которая является оптически активной солеобразующей органической кислотой. Подходящими расщепляющими агентами для способов фракционной кристаллизации являются, например, оптически активные кислоты, такие как D- и L-формы винной кислоты, диацетилвинной кислоты,дибензоилвинной кислоты, миндальной кислоты, яблочной кислоты, молочной кислоты, или различные оптически активные камфорсульфоновые кислоты, такие как -камфорсульфоновая кислота. Другие расщепляющие агенты, подходящие для способов фракционной кристаллизации, включают стереоизомерно чистые формы -метилбензиламина (например, S- и R-формы или диастереомерно чистые формы), 2-фенилглицина, норэфедрина, эфедрина, N-метилэфедрина, циклогексилэтиламина, 1,2 диаминоциклогексана и т.п. Расщепление рацемических смесей также можно осуществить элюированием на колонке, заполненной оптически активным расщепляющим агентом (например, динитробензоилфенилглицином). Подходящий состав растворителя для элюирования может быть определен специалистом в данной области техники. Соединения по изобретению также включают таутомерные формы. Таутомерные формы являются результатом обмена простой связи с соседней двойной связью вместе с сопутствующей миграцией протона. Таутомерные формы включают прототропные таутомеры, которые являются изомерными состояниями протонирования, имеющими одну и ту же эмпирическую формулу и общий заряд. Примеры проторопных таутомеров включают пары кетон - енол, пары амид - имидокислота, пары лактам - лактим,пары амид - амидиолокислота, пары енамин - имин и кольцеобразные формы, где протон может занимать две или больше позиций гетероциклической системы, например, 1 Н- и 3H-имидазол, 1 Н-, 2 Н- и 4 Н-1,2,4 триазол, 1 Н- и 2 Н-изоиндол и 1 Н- и 2 Н-пиразол. Таутомерные формы могут находиться в равновесии или быть пространственно блокированы в одну форму посредством соответствующего замещения. Соединения по изобретению также включают гидраты и сольваты, а также безводные и несольватированные формы. Соединения по изобретению также могут включать все изотопы атомов, встречающихся в промежуточных или конечных соединениях. Изотопы включают атомы, имеющие одно и то же атомное число,но различные массовые числа. Например, изотопы водорода включают тритий и дейтерий. Термин "соединение", используемый в данном описании, предназначен для включения всех стереоизомеров, геометрических изомеров, таутомеров и изотопов изображенных структур. Все соединения и их фармацевтически приемлемые соли могут находиться вместе с другими веществами, такими как вода и растворители (т.е., как гидраты и сольваты), или могут быть выделены. В некоторых воплощениях соединения по изобретению и их соли, по существу, являются выделенными. Под "по существу, выделенное" подразумевается, что соединение, по меньшей мере, частично,или существенно отделено от среды, в которой оно образовалось или обнаружено. Частичное отделение может включать, например, композицию, обогащенную соединением по изобретению. Существенное отделение может включать композиции, содержащие по меньшей мере примерно 50 мас.%, по меньшей мере примерно 60 мас.%, по меньшей мере примерно 70 мас.%, по меньшей мере примерно 80 мас.%, по меньшей мере примерно 90 мас.%, по меньшей мере примерно 95 мас.%, по меньшей мере примерно 97 мас.% или по меньшей мере примерно 99 мас.% соединения по изобретению или его соли. Способы выделения соединений и их солей являются обычными в технике. Выражение "фармацевтически приемлемый" используется в данном описании как относящееся к таким соединениям, материалам, композициям и/или лекарственным формам, которые в объеме кажущегося здравого смысла в медицине подходят для применения в контакте с тканями человеческого организма и животных без излишней токсичности, раздражения, аллергической реакции или других проблем или осложнений, соразмерных с разумным соотношением польза/риск. Выражения "температура окружающей среды" и "комнатная температура", используемые в данном описании, известны в технике и относятся вообще к температуре, например, температуре реакционной смеси, которая примерно равна температуре помещения, в котором осуществляют реакцию, например температуре от примерно 20 до примерно 30 С. Настоящее изобретение также включает фармацевтически приемлемые соли соединений, описанных в данном описании. Используемое в данном описании определение фармацевтически приемлемые соли относится к производным раскрытых соединений, когда исходные соединения модифицируют посредством превращения имеющейся кислотной или основной группы в ее солевую форму. Примеры фармацевтически приемлемых солей включают, но не ограничиваются перечисленным, соли минеральных или органических кислот основных остатков, таких как амины; соли щелочей или органические соли кислотных остатков, таких как карбоновые кислоты и т.п. Фармацевтически приемлемые соли по настоящему изобретению включают обычные нетоксичные соли исходного соединения, образованные, например, с нетоксичными неорганическими или органическими кислотами. Фармацевтически приемлемые соли по настоящему изобретению можно получить обычными химическими методами из исходного соединения, которое содержит основную или кислотную группу. Как правило, такие соли можно получить взаимодействием форм свободных кислоты или основания указанных соединений со стехиометрическим количеством соответствующего основания или кислоты в воде или в органическом растворителе или в смеси указанных растворителей; как правило, предпочтительны неводные среды, такие как эфир,этилацетат, этанол, изопропанол или ацетонитрил (ACN). Перечни подходящих солей можно найти в работах Remington's Pharmaceutical Sciences, 17th ed., Mack Publishing Company, Easton, Pa., 1985, p.1418,и в Journal of Pharmaceutical Sciences, 66, 2 (1977), включенных в данное описание в качестве ссылок. Синтез Соединения по изобретению, включая их соли, можно получить с использованием известных методов органического синтеза и можно синтезировать согласно любому из возможных путей синтеза. Реакции получения соединений по изобретению можно осуществлять в подходящих растворителях,которые специалист в области органического синтеза легко выберет. Подходящие растворители могут быть, по существу, нереакционноспособны в отношении исходных материалов (реагентов), промежуточных соединений или продуктов реакции при температурах, при которых осуществляют взаимодействия,например, температурах, которые колеблются от температуры замерзания растворителя до температуры кипения растворителя. Данное взаимодействие может быть осуществлено в одном растворителе или в смеси нескольких растворителей. В зависимости от определенной стадии реакции, подходящие растворители для определенной стадии реакции могут быть выбраны специалистом. Получение соединений по изобретению может включать введение и удаление защитных групп для различных химических групп. Необходимость в введении и удалении защитных групп и выбор соответствующих защитных групп могут быть легко определены специалистом в данной области техники. С химией защитных групп можно ознакомиться, например, в труде Т. W. Greene and P. G. M. Wuts, Protective Groups in Organic Synthesis, 3rd Ed., WileySons, Inc., New York (1999), включенном в данное описание в качестве ссылки. Реакции можно контролировать согласно любому подходящему способу, известному в технике. Например, образование продукта можно контролировать средствами спектроскопии, такими как спектроскопия ядерного магнитного резонанса (например, 1 Н или 13 С), инфракрасная спектроскопия, спектрофотометрия (например, УФ-видимая), масс-спектрометрия, или хроматографическими способами,такими как высокоэффективная жидкостная хроматография (ВЭЖХ) или тонкослойная хроматография(ТСХ). Примеры способов синтеза для получения соединений по изобретению приводятся на схемах ниже. Например, соединения по изобретению можно получить общей синтетической процедурой, показанной на схеме 1. Эфиры пинакона и пиразол-4-бороновой кислоты формулы 1 вводят во взаимодействие с 5 замещенным 2,4-дихлорпиримидином в условиях сочетания по Судзуки, и получают 4 пиразолзамещенные 2-хлорпиримидины формулы 2. Последние можно подвергнуть катализируемой кислотой реакции замещения хлора с анилином формулы NH2-A-D-E-G с образованием соединений формулы 3. Когда NH2-A-D-E-G представляет собой амин, реакции замещения можно добиться непосредственно путем нагревания смеси 2 и амина в отсутствие катализатора. Как видно на схеме 2, эфиры пинакона и пиразол-4-бороновой кислоты 1 можно получить взаимодействием коммерчески доступных эфиров пиразол-4-бороновой кислоты с L-(Y)n-Z, где L представляет собой удаляемую группу, такую как галоген, трифлатная или подобная группа, в щелочной среде.N-Арилпиразол формулы 1 (где Y представляет собой ароматическую группу) можно получить взаимодействием эфиров пинакона и пиразол-4-бороновой кислоты с соответствующим образом замещенной арилбороновой кислотой в растворителе, таком как дихлорметан (DCM), в присутствии ацетата меди и пиридина. С другой стороны, N-арилпиразол формулы 1 (где Y представляет собой ароматическую группу) можно получить взаимодействием эфиров пинакона и пиразол-4-бороновой кислоты с соответствующим образом замещенным арилфторидом в растворителе, таком как ДМФА, при повышенной температуре. Замещенные пиразолы формулы 1 (где Z представляет собой такую группу, как нитрильная или сложноэфирная, и Y представляет собой по меньшей мере два атома углерода) также можно получить взаимодействием эфиров пинакона и пиразол-4-бороновой кислоты с соответствующим образом замещенным акрилатом, акрилонитрилом или другими акцепторами, подобными акцепторам по Михаэлю, в растворителе, таком как ацетнонитрил (ACN), в присутствии основания, такого как 1,8 диазабицикло[5.4.0]ундец-7-ен (DBU) или триэтиламин (TEA), и при температуре ниже температуры кипения растворителя. Схема 2 Следует отметить, что на всех схемах, описанных в данном описании, если в заместителе, таком какY, Z, R, R1, R5 и т.д., присутствуют функциональные группы, можно осуществлять дальнейшую модификацию, если это соответствует ситуации и желательно. Например, группу CN можно гидролизовать и получить амидную группу; карбоксильную группу можно превратить в эфирную, которую, в свою очередь, можно восстановить до спиртовой, которую, в свою очередь, можно модифицировать далее. В другом примере группу ОН можно превратить в группу, которая удаляется лучше, такую как мезилатная,которая, в свою очередь, подходит для нуклеофильного замещения, например, CN. Более того, группу ОН можно подвергнуть реакции с фенолом или гетероарильным спиртом в условиях по Мицунобу и получить ариловые или гетероариловые простые эфиры. Специалист в данной области техники будет представлять дальнейшие модификации. Также следует отметить, что последовательности реакций, описанные выше, можно изменять в соответствии с различными молекулами-мишенями. Например, эфиры пинакона и 4-пиразолбороновой кислоты можно ввести во взаимодействие с замещенным 1,4-дихлорпиримидином с образованием первого продукта реакции по Судзуки. Затем группу NH пиразола продукта реакции по Судзуки можно функционализировать далее, как описано на схеме 2. Способы Соединения по изобретению могут модулировать активность одной или нескольких различных киназ, включая, например, киназы Janus (JAK). Термин "модулировать" обозначает способность повышать или понижать активность киназы. Соответственно, соединения по изобретению можно использовать в способах модуляции киназ, таких как киназа JAK, посредством контактирования киназы с любым одним или несколькими соединениями или композициями, описанными в данном описании. В некоторых воплощениях соединения по настоящему изобретению могут действовать как ингибиторы одной или нескольких киназ. В других воплощениях соединения по изобретению можно использовать для модуляции активности киназы у индивидуума, нуждающегося в модуляции рецептора, посредством введения модулирующего количества соединения по изобретению. Исходя из того, что на рост и выживание раковых клеток могут оказать воздействие многие пути передачи сигналов, настоящее изобретение можно применить для лечения болезненных состояний, характеризующихся устойчивыми к лекарственным средствам мутантами киназ. Кроме того, можно использовать в сочетании различные ингибиторы киназ, проявляющие различные предпочтения к киназам,активность которых они модулируют. Такой подход мог бы обеспечить высокую эффективность при лечении болезненных состояний за счет нацеливания на многие пути передачи сигналов, уменьшения вероятности устойчивости к лекарственным средствам, возникающей в клетке, и уменьшения токсичности лечения заболевания. Киназы, с которыми связываются и/или которые модулируют соединения по настоящему изобретению, включают рецепторные и нерецепторные Ser/Thr киназы, такие как TGF-R, PKA, PKG, СаМкиназа, киназа фосфорилазы, MEKK, ERK, МАРК, Akt и mTOR; рецепторные Tyr-киназы, такие какEGFR, HER2, HER3, HER4, INS-R, IGF-1R, IR-R, PDGFR, PDGFR, CSFIR, KIT, FLK-II, KDR/FLK-1,FLK-4, fit-1, FGFR1, FGFR2, FGFR2, FGFR4, с-Met, Ron, Sea, TRKA, TRKB, TRKC, FLT3, VEGFR/Flt2,EphAl, EphA2, EphA3, EphB2, EphB4, Tie2; и нерецепторные Tyr-киназы, такие как Src, Fyn, Lck, Fgr,Btk, Fak, SYK, FRK, JAK или ABL. Некоторые JAK включают JAKl, JAK2, JAK3 или TYK2. В некоторых воплощениях JAK представляет собой JAKl или JAK2. В некоторых воплощениях JAK представляет собой JAK2. В некоторых воплощениях JAK представляет собой мутант. В некоторых воплощениях мутантная JAK содержит V617F, F537-K539delinsL, H538QK539L, K539L или N-542-E543del в мутацияхJAK2. В некоторых воплощениях нерецепторная Tyr-киназа представляет собой ABL, такую как ABL1 или ARG (ABL2). В некоторых воплощениях ABL является мутантом. В некоторых воплощениях мутантная ABL содержит мутацию E315I. В некоторых воплощениях мутантная ABL содержит мутациюT315D, F359D, D276G, Е 255 К, М 351 Т, G250E, H396R, Q252H, Y253H, E355G, F317L, G250E, Y253F,F259V, Q252R, L387M, M244V, M343T/F382L или V3791. В некоторых воплощениях модулируют киназные активности как JAK, так и ABL. В некоторых воплощениях киназа является результатом слияния нескольких генов, таких как, когда слияние происходит между двумя генами следующим образом:BCR/ABL1, TEL/ABL1, NUP214/ABL1, EMS/ABL1, SFQ/ABL1, BCR/ARG, TEL/ARG, TEL/PDGFR,HIP1/PDGFR, RAB5/PDGFR, H4/PDGFR, миомегалин/PDGFR, CEV14/PDGFR, NIN1/PDGFR,HCMOGT/PDGFR, KIAA1509/PDGFR, TP53BP1/PDGFR, FIIP1L1/PDGFR, BCR/PDGFR,BCR/JAK2, TEL/JAK2, PCM1/JAK2, TEL/SYK, TEL/TRKC, ZNF198/FGFR1, FOP/FGFR1, CEP110/FGFR1,HERVK/FGFR1, BCR/FGFR1, FGFR10P2/FGFR1, TIF1/FGFR1, TEL/FGFR3, TEL/FLT3, TEL/FRK,NPM/ALK, TPM3/ALK, TGF/ALK, ATIC/ALK, CLCT/ALK, MSN/ALK, TPM4/ALK, ALO17/ALK,RANBP2/ALK, MYH9/ALK, CARS/ALK. Киназы, с которыми связываются и/или которые модулируют соединения по настоящему изобретению, включают любой член семейства JAK. В некоторых воплощениях JAK представляет собой JAK1,JAK2, JAK3 или TYK2. В некоторых воплощениях JAK представляет собой JAK1 или JAK2. В некоторых воплощениях JAK представляет собой JAK3. В некоторых воплощениях для ингибирования активности одной киназы (например, JAK2) можно использовать более одного соединения по изобретению. В некоторых воплощениях для ингибирования активности более одной киназы (например, JAK2),например по меньшей мере двух киназ (ABL1 и JAK2), можно использовать более одного соединения по изобретению. В некоторых воплощениях для ингибирования активности одной киназы (например, JAK2) соединение можно использовать в комбинации с другим ингибитором киназ. В некоторых воплощениях для ингибирования активности более одной киназы (например, JAK2),например, по меньшей мере двух киназ, соединение можно использовать в комбинации с другим ингибитором киназ. Соединение по изобретению может быть селективным. Под "селективным" подразумевается, что соединение связывается с или ингибирует киназу с большей аффинностью или силой, соответственно, в сравнении по меньшей мере с одной другой киназой. В некоторых воплощениях соединения по изобретению являются селективными ингибиторами JAK1 или JAK2 по сравнению с JAK3 и/или TYK2. В некоторых воплощениях соединения по изобретению являются селективными ингибиторами JAK2 (например, по сравнению с JAK1, JAK3 и TYK2). Без связи к теорией, поскольку ингибиторы JAK3 могут привести к иммуносупрессивным эффектам, соединение, которое является селективным для JAK2 по сравнению с JAK3, и которое применимо при лечении рака (такого как множественная миелома, например),может предоставить дополнительное преимущество меньшего побочного иммуносупрессивного действия. Селективность может быть, по меньшей мере, примерно 5-кратной, по меньшей мере, примерно 10 кратной, по меньшей мере, примерно 20-кратной, по меньшей мере, примерно 50-кратной, по меньшей мере, примерно 100-кратной, по меньшей мере, примерно 200-кратной, по меньшей мере, примерно 500 кратной или, по меньшей мере, примерно 1000-кратной. Селективность можно измерить способами,обычными в технике. В некоторых воплощениях селективность можно проверить по Km концентрации АТФ каждого фермента. В некоторых воплощениях селективность соединений по изобретению в отношении JAK2 по сравнению с JAK3 можно определить клеточными анализами, ассоциированными с ак- 12020777 тивностью определенной киназы JAK. Другой аспект настоящего изобретения относится к способам лечения киназоассоциированного заболевания или расстройства у индивидуума (например, пациента) посредством введения индивидууму,нуждающемуся в таком лечении, терапевтически эффективного количества или дозы соединения по настоящему изобретению или его фармацевтической композиции. Киназоассоциированное заболевание может включать любое заболевание, расстройство или состояние, которое прямо или косвенно связано с экспрессией или активностью киназы, в том числе, сверхэксперссией и/или анормальными уровнями активности. Анормальные уровни активности можно определить путем сравнения уровня активности в нормальной здоровой ткани или клетках с уровнем активности в больных клетках. Киназоассоциированное заболевание также может включать любое заболевание, расстройство или состояние, которое можно предупредить, облегчить или излечить посредством модулирования киназной активности. В некоторых воплощениях заболевание характеризуется анормальной активностью JAK, ABL или тех и других. В некоторых воплощениях заболевание характеризуется мутантной JAK2, такой как с мутацией в псевдокиназном домене. В некоторых воплощениях заболевание характеризуется мутантной ABL, такой как с мутацией в киназном домене. Примеры киназоассоциированных заболеваний включают заболевания с участием иммунной системы, например, отторжение трансплантата органа (например, отторжение аллотрансплантата и болезнь трансплантат против хозяина). Другие примеры киназоассоциированных заболеваний включают аутоиммунные заболевания, такие как кожные расстройства, рассеяный склероз, ревматоидный артрит, ювенильный артрит, диабет типа 1,волчанка, псориаз, воспалительное заболевание кишечника, неспецифический язвенный колит, болезнь Крона, тяжелая псевдопаралитическая миастения, иммуноглобулиновые нефропатии, аутоиммунные расстройства щитовидной железы и т.п. В некоторых воплощениях аутоиммунное заболевание представляет собой буллезное кожное расстройство, такое как обыкновенная пузырчатка (PV) или буллезный пемфигоид (ВР). Другие примеры киназоассоциированных заболеваний включают аллергические состояния, такие как астма, пищевые аллергии, атопический дерматит и ринит. Другие примеры киназоассоциированных заболеваний включают вирусные заболевания, такие как из-за вируса Эпштейна-Барра (EBV), гепатит В,гепатит С, ВИЧ, HTLV 1, из-за вируса ветряной оспы (VZV) и вируса папилломы человека (HPV). Другие примеры киназоассоциированных заболеваний или состояний включают кожные рсстройства, такие как псориаз (например, псориаз обыкновенный), атопический дерматит, кожное высыпание,раздражение кожи, сенсибилизация кожи (например, контактный дерматит или аллергический контактный дерматит). Например, некоторые вещества, в том числе, фармацевтические препараты, при местном применении могут вызывать сенсибилизацию кожи. В некоторых воплощениях совместное введение или последовательное введение по меньшей мере одного ингибитора киназ по изобретению вместе со средством, вызывающим нежелательную сенсибилизацию, может быть полезным при лечении такой нежелательной сенсибилизации или дерматита. В некоторых воплощениях кожное расстройство можно лечить местным введением по меньшей мере одного ингибитора киназ по изобретению. В других воплощениях киназоассоциированное заболевание представляет собой рак, в том числе,характеризующийся солидными опухолями (например, рак предстательной железы, рак почек, рак печени, рак поджелудочной железы, рак желудка, рак молочной железы, рак легких, онкозаболевания головы и шеи, рак щитовидной железы, глиобластома, саркома Капоши, болезнь Кастлемана, меланома и т.д.),онкозаболевания кроветворной системы (например, лимфома, лейкоз, такой как острый лимфобластный лейкоз или множественная миелома) и рак кожи, такой как кожная Т-клеточная лимфома (CTCL) и кожная В-клеточная лимфома. Примеры кожной Т-клеточной лимфомы включают синдром Сезари и грибовидный микоз. В других воплощениях киназоассоциированное заболевание представляет собой эндометриальный и цервикальный рак. Киназоассоциированные заболевания также могут включать заболевания, характеризующиеся наличием мутации (генетической или эпигенетической), проявляющейся в усиленной передаче сигналов от киназ JAK. Такие заболевания включают заболевания с мутированными цитокином и рецепторами фактора роста (например, с мутантом EpoR или MPL). Далее, мутации после JAK, которые могут привести к общему повышению пути активации JAK (например, белков SOCS и PIAS), также следует рассматривать как киназоассоциированные. Киназоассоциированные заболевания также могут включать заболевания, характеризующиеся экспрессией мутантной киназы. Такие заболевания включают заболевания, характеризующиеся экспрессией мутантной JAK2, такие как заболевания с наличием по меньшей мере одной мутации в псевдокиназном домене (например, JAK2V617F) или вблизи псевдокиназного домена (экзон 12) (NEJM, 356: 459-468; 2007), и заболевания, характеризующиеся экспрессией мутантной ABL1 (например, BCR-ABL илиABL1T315I). Киназоассоциированные заболевания также могут включать миелопролиферативные расстройства(MPD), такие как истинная полицитемия (PV), эссенциальная тромбоцитемия (ЕТ), миелоидная метаплазия с миелофиброзом (МММ), хронический миелоидный лейкоз (CML), хронический миеломоноцитар- 13020777 ный лейкоз (CMML), синдром гиперэозинофилии (HES), системный мастоцитоз (SMCD) и т.п. Другие киназоассоциированные заболевания включают воспаление и воспалительные заболевания. Примеры воспалительных заболеваний включают воспалительные заболевания глаз (например, ирит,увеит, склерит, конъюнктивит или родственные заболевания), воспалительные заболевания дыхательных путей (например, верхних дыхательных путей, в том числе, носа и синуса, такие как ринит или синусит,или нижних дыхательных путей, в том числе, бронхит, хроническую обструктивную болезнь легких и т.п.), воспалительную миопатию, такую как миокардит, и другие воспалительные заболевания. Ингибиторы киназ, описанные в данном описании, также можно использовать для лечения ишемических реперфузионных повреждений или заболевания или состояния, родственного воспалительному ишемическому событию, такого как удар или остановка сердца. Ингибиторы киназ, описанные в данном описании, также можно использовать для лечения анорексии, кахексии или усталости, такой, какая является результатом или связана с раком. Ингибиторы киназ, описанные в данном описании, также можно использовать для лечения рестеноза, склеродермии или фиброза. Примерами фиброза являются почечный фиброгенез и фиброз легких. Ингибиторы киназ, описанные в данном описании, также можно использовать для лечения состояний, ассоциированных с гипоксией или астроглиозом, таких как, например, диабетическая ретинопатия, рак или нейродегенерация. См., например, Dudley А.С. et al., Biochem.J., 2005, 390 (Pt 2): 427-36; и Sriram K. et al., J. Biol. Chem., 2004, 279 (19): 19936-47, Epub 2004 Mar 2. Изобретение также относится к способам лечения аутоиммунного заболевания, кожного расстройства, вирусного заболевания, рака или миелопролиферативного расстройства у пациента посредством введения пациенту терапевтически эффективного количества соединения по изобретению (например,более одного соединения). В некоторых воплощениях соединение по изобретению можно вводить в комбинации с другим ингибитором киназ. Изобретение также относится к способам лечения подагры, синдрома системной воспалительной реакции (SIRS) и септического шока посредством введения соединения по изобретению. Настоящее изобретение также относится к способам лечения увеличения в размерах предстательной железы из-за, например, доброкачественной гипертрофии предстательной железы или доброкачественной простатической гиперплазии посредством введения соединения по изобретению. Используемый в данном описании термин "контактирование" относится к совместному внесению указанных частиц в систему in vitro или в систему in vivo. Например, "контактирование" киназы с соединением по изобретению включает введение соединения по настоящему изобретению индивидууму или пациенту, такому как человек, имеющему киназу, а также, например, введение соединения по изобретению в образец, содержащий клеточный или очищенный препарат, содержащий киназу. Используемые в данном описании термины "индивидуум" или "пациент", используемые как взаимозаменяемые, относятся к любому животному, включая млекопитающих, предпочтительно мышей,крыс, других грызунов, кроликов, собак, кошек, свиней, крупный рогатый скот, овец, лошадей или приматов, и наиболее предпочтительно, к людям. Используемый в данном описании термин "ювенильный" относится к больному человеку, у которого появление болезненного состояния или расстройства происходит до возраста 18 лет. Используемое в данном описании выражение "терапевтически эффективное количество" относится к количеству активного соединения или фармацевтического средства, которое выявляет биологическую или медицинскую реакцию в ткани, системе, у животного, индивидуума или человека, которой добивается исследователь, ветеринар, врач-терапевт или другой клиницист. Используемый в данном описании термин "лечение" относится к 1) предупреждению заболевания; например предупреждению заболевания, состояния или расстройства у индивидуума, который может быть предрасположен к заболеванию, состоянию или расстройству, но пока не испытывает или не отображает патологию или симптоматологию заболевания; 2) ингибированию заболевания; например, ингибированию заболевания, состояния или расстройства у индивидуума, который испытывает или отображает патологию или симптоматологию заболевания, состояния или расстройства (т.е., приостановку дальнейшего развития патологии и/или симптоматологии), или 3) облегчению заболевания; например,облегчению заболевания, состояния или расстройства у индивидуума, который испытывает или отображает патологию или симптоматологию заболевания, состояния или расстройства (т.е., реверсию патологии и/или симптоматологии). Комбинированная терапия Одно или несколько дополнительных фармацевтических средств, таких как, например, химиотерапевтические средства, противовоспалительные средства, иммунодепрессанты, а также ингибиторы киназBCR-ABL1, Flt-3, EGFR, HER2, с-МЕТ, VEGFR, PDGFR, cKit, IGF-1R, RAF и FAK, такие как, например,описанные в WO 2006/056399, или другие средства можно использовать в комбинации с соединениями по настоящему изобретению для лечения киназоассоциированных заболеваний, расстройств или состояний. Одно или несколько дополнительных фармацевтических средств можно вводить пациенту одновременно или последовательно. Терапевтические антитела можно использовать в комбинации с соединениями по настоящему изобретению для лечения киназоассоциированных заболеваний, расстройств или состояний. Примеры антител для применения в комбинированной терапии включают, но не ограничиваются перечисленным, трастузумаб (например, против HER2), ранибизумаб (например, против VEGF-A), бевацизумаб (торговое наименование авастин, например, против VEGF), панитумумаб (например, противEGFR), цетуксимаб (например, против EGFR) и антитела, направленные на с-МЕТ. Примеры химиотерапевтических средств включают ингибиторы протеосом (например, бортезомиб), талидомид, ревилимид и средства, повреждающие ДНК, такие как мелфалан, доксорубицин, циклофосфамид, винкристин, этопозид, кармустин и т.п. С соединениями по настоящему изобретению можно использовать в комбинации одно или несколько из следующих средств, перечисленных в виде списка, не являющегося ограничительным: цитостатическое средство, цисплатин, доксорубицин, таксотер, таксол, этопозид, иринотекан, каптостар, топотекан, паклитаксел, доцетаксел, эпотилоны, тамоксифен, 5-флуороурацил, метотрексат, темозоломид, циклофосфамид, SCH 66336, R115777, L778123, BMS 214662, иресса, тарцева, антитела к EGFR, гливек,интрон, ара-С, адриамицин, цитоксан, гемцитабин, урацилмустард, хлорметин, ифосфамид, мелфалан,хлорамбуцил, пипоброман, триэтиленмеламин, триэтилентиофосфорамин, бусульфан, кармустин, ломустин, стрептозоцин, дакарбазин, флоксуридин, цитарабин, 6-меркаптопурин, 6-тиогуанин, флударабина фосфат, оксалиплатин, лейковерин, элоксатин, пентостатин, винбластин, винкристин, виндезин, блеомицин, дактиномицин, даунорубицин, доксорубицин, эпирубицин, идарубицин, митрамицин, дезоксикоформицин, митомицин-С, L-аспарагиназа, тенипозид 17.альфа.-этинилэстрадиол, диэтилстилбестрол,тестостерон, преднизон, флуоксиместерон, дромостанолона пропионат, тестолактон, мегестролацетат,метилпреднизолон, метилтестостерон, преднизолон, триамцинолон, хлортрианизен, гидроксипрогестерон, аминоглутетимид, эстрамустин, медроксипрогестеронацетат, лейпролид, флутамид, торемифен, гозерелин, цисплатин, карбоплатин, гидроксимочевина, амсакрин, прокарбазин, митотан, митоксантрон,левамизол, навелбен, анастразол, летразол, капецитабин, релоксафин, дролоксафин, гексаметилмеламин,авастин, герцептин, бекссар, велкад, зевалин, тризенокс, кселода, винорелбин, порфимер, эрбитукс, липосомаль, тиотепа, альтретамин, трастузумаб, лерозол, фулвестрант, экземестан, ритуксимаб, С 225, кампат, клофарбин, кладрибин, афидиколон, ритуксан, сунтиниб, дазатиниб, тезацитабин, Sm11, флударабин, пентостатин, триапин, дидокс, тримидокс, амидокс, 3-АР и MDL-101731. Примеры стероидов включают кортикостероиды, такие как дексаметазон или преднизон. Примеры ингибиторов Bcr-ABL1 включают соединения и их фармацевтически приемлемые соли родов и видов, раскрытых в пат. США 5521184, WO 04/005281, ЕР 2005/009967, ЕР 2005/010408 и USper.60/578491. Примеры подходящих ингибиторов Flt-3 включают соединения и их фармацевтически приемлемые соли, раскрытые в WO 03/037347, WO 03/099771 и WO 04/046120. Примеры подходящих ингибиторов RAF включают соединения и их фармацевтически приемлемые соли, раскрытые в WO 00/09495 и WO 05/028444. Примеры подходящих ингибиторов FAK включают соединения и их фармацевтически приемлемые соли, раскрытые в WO 04/080980, WO 04/056786, WO 03/024967, WO 01/064655, WO 00/053595 и WO 01/014402. В некоторых воплощениях один или несколько ингибиторов киназ по изобретению можно использовать в комбинации с химиотерапевтическими средствами при лечении рака, и можно улучшить реакцию на лечение по сравнению с реакцией на одно химиотерапевтическое средство без обострения его токсического действия. Примеры дополнительных фармацевтических средств, используемых при лечении онкозаболеваний, таких как множественная миелома, например, могут включать, без ограничения,мелфалан, мелфалан плюс преднизон [МР], доксорубицин, дексаметазон и велкад (бортезомиб). Другие дополнительные средства, используемые при лечении множественной миеломы, включают ингибиторы киназ Bcr-ABL1, Flt-3, RAF и FAK. Аддитивное или синергическое действие является желательным результатом комбинирования ингибитора киназ по настоящему изобретению с другим средством. Более того, устойчивость раковых клеток (например, множественной миеломы, рака легких и т.д.) к терапевтическим средствам (например, дексаметазону, мелфалану, эрлотинибу/таркева, иматинибу, дазатинибу и т.д.) может быть обратимой после лечения ингибитором киназ по настоящему изобретению. Средства можно объединять с соединениями по изобретению в единой или непрерывной лекарственной форме,или средства можно вводить одновременно или последовательно в отдельных лекарственных формах. В некоторых воплощениях кортикостероид, такой как дексаметазон, вводят пациенту в комбинации по меньшей мере с одним ингибитором киназ, где дексаметазон или другое терапевтическое средство вводят периодически в противоположность непрерывному введению. В некоторых других воплощениях комбинации одного или нескольких ингибиторов киназ по изобретению с другими терапевтическими средствами можно вводить пациенту до, во время и/или после трансплантации костного мозга или трансплантации стволовых клеток. Фармацевтические композиции и лекарственные формы При использовании в качестве фармацевтических средств соединения по изобретению можно вводить в форме фармацевтических композиций. Такие композиции можно получить способом, известным в фармации, и можно вводить различными путями, в зависимости от того, желательно локальное или системное лечение, и от площади лечения. Введение может быть местным (включая трансдермальное, эпидермальное, офтальмическое, и в слизистые оболочки, включая интраназальную, вагинальную и ректальную доставку), пульмональным (например, ингаляцией или инсуффляцией порошков или аэрозолей,в том числе, небулайзером; интратрахеально или интраназально), пероральным или парентеральным. Парентеральное введение включает внутривенное, внутриартериальное, подкожное, интраперитонеальное, внутримышечное введение или инъекцию или инфузию; или интракраниальное, например, интратекальное или интравентрикулярное введение. Парентеральное введение может быть в форме одной болюсной дозы или может осуществляться, например, непрерывной перфузией насосом. Фармацевтические композициии и препараты для местного введения могут включать чрескожный пластырь, мази, лосьоны,кремы, гели, капли, суппозитории, спреи, жидкости и порошки. Могут быть необходимы или желательны обычные фармацевтические носители, водные, порошковые или масляные основы, загустители и т.п. Также можно применять кондомы, перчатки и т.п. Изобретение также включает фармацевтические композиции, которые содержат в качестве активного ингредиента одно или несколько соединений по изобретению, описанных выше, в комбинации с одним или несколькими фармацевтически приемлемыми носителями (эксципиентами). При получении композиций по изобретению активный ингредиент типично смешивают с эксципиентом, разбавляют эксципиентом или заключают в такой носитель в форме, например, капсулы, саше, бумажного пакетика или в другую емкость. Когда эксципиент служит в качестве разбавителя, он может представлять собой твердое, полутвердое или жидкое вещество, которое действует как наполнитель, носитель или среда для активного ингредиента. Таким образом, композиции могут находиться в форме таблеток, пилюль, порошков, лепешек, саше, крахмальных облаток, эликсиров, суспензий, эмульсий, растворов, сиропов, аэрозолей (в виде твердого вещества или в жидкой среде), мазей, содержащих, например, до 10 мас.% активного соединения, мягких или твердых желатиновых капсул, суппозиториев, стерильных растворов для инъекции и стерильно упакованных порошков. При получении препаратов активное соединение перед объединением с другими ингредиентами может быть измельчено для получения частиц соответствующего размера. Если активное соединение, по существу, нерастворимо, его можно измельчить до частиц размером менее 200 меш. Если активное соединение, по существу, растворимо в воде, размер частиц можно подогнать посредством измельчения для обеспечения, по существу, равномерного распределения в препарате, например, примерно до 40 меш. Соединения по изобретению можно измельчать с использованием известных процедур измельчения, таких как мокрое измельчение, для получения частиц размера, соответствующего формованию таблеток, и для препаратов других типов. Тонко измельченные (в форме наночастиц) препараты соединений по изобретению можно получить способами, известными в технике, см., например, патентную публ.WO 2002/000196. Некоторые примеры подходящих эксципиентов включают лактозу, декстрозу, сахарозу, сорбит,маннит, крахмалы, аравийскую камедь, фосфат кальция, альгинаты, трагакант, желатин, силикат кальция, микрокристаллическую целлюлозу, поливинилпирролидон, целлюлозу, воду, очищенную патоку и метилцеллюлозу. Композиции также могут включать смазывающие вещества, такие как тальк, стеарат магния и минеральное масло; смачивающие вещества; эмульгаторы и суспендирующие вещества; консерванты, такие как метил- и пропилгидроксибензоаты; подслащивающие вещества и корригенты. Композиции по изобретению с использованием процедур, известных в технике, можно составлять таким образом, чтобы после введения пациенту обеспечить быстрое, пролонгированное или отсроченное высвобождение активного ингредиента. Композиции можно получать в стандартной лекарственной форме, причем каждая дозировка содержит от примерно 5 до примерно 1000 мг (1 г), чаще от примерно 100 до примерно 500 мг активного ингредиента. Термин "стандартные лекарственные формы" относится к физически дискретным единицам, подходящим как единичные дозировки для людей и других млекопитающих, причем каждая единица содержит предварительно установленное количество активного материала, рассчитанное на получение нужного лечебного эффекта, в сочетании с подходящим фармацевтическим эксципиентом. Активное соединение может быть эффективным в широком интервале дозировок и, как правило,вводится в фармацевтически эффективном количестве. Однако, следует представлять, что количество соединения, вводимое фактически, как правило, будет определяться врачом согласно соответствующим обстоятельствам, включая состояние, от которого лечат, выбранный способ введения, фактическое вводимое соединение, возраст, массу и реакцию отдельного пациента, тяжесть симптомов у пациента и т.п. Для получения твердых композиций, таких как таблетки, основной активный ингредиент смешивают с фармацевтическим эксципиентом с образованием твердой предварительной композиции, содержащей однородную смесь с соединением по настоящему изобретению. Когда такие предварительные композиции называют однородными, активный ингредиент типично диспергирован равномерно в композиции, так что композицию можно легко разделить на равно эффективные стандартные лекарственные формы, такие как таблетки, пилюли и капсулы. Затем такую твердую предварительную композицию разделяют на стандартные лекарственные формы типов, описанных выше, содержащие от, например, при- 16020777 мерно 0,1 до примерно 1000 мг активного ингредиента по настоящему изобретению. На таблетки или пилюли по настоящему изобретению может быть нанесено покрытие, или они обработаны иначе для получения лекарственной формы, предоставляющей преимущество пролонгированного действия. Например, таблетка или пилюля может включать внутренний и наружный компонент лекарственной формы, причем последний находится в форме оболочки для первого. Два компонента могут быть разделены энтеросолюбильным слоем, который служит для предотвращения рассыпания в желудке и позволяет внутреннему компоненту пройти интактным в двенадцатиперстную кишку или высвобождаться замедленно. Различные материалы можно использовать для таких энтеросолюбильных слоев или покрытий, причем такие материалы включают ряд полимерных кислот и смеси полимерных кислот с такими материалами, как шеллак, цетиловый спирт и ацетат целлюлозы. Жидкие формы, в которые соединения и композиции по настоящему изобретению можно включать для введения перорально или посредством инъекции, включают водные растворы, сиропы с подходящими корригентами, водные или масляные суспензии и эмульсии с корригентами со съедобными маслами,такими как хлопковое масло, сезамовое масло, кокосовое масло или арахисовое масло, а также эликсиры и подобные фармацевтические носители. Композиции для ингаляции или инсуффляции включают растворы и суспензии в фармацевтически приемлемых водных или органических растворителях или их смесях и порошки. Жидкие или твердые композиции могут содержать фармацевтически приемлемые эксципиенты, описанные выше. В некоторых воплощениях композиции вводят путем вдыхания через рот или нос для местного или системного действия. Композиции могут распыляться с применением инертных газов. Распыляемые растворы можно вдыхать непосредственно из распыляющего устройства, или распыляющее устройство может быть присоединено к лицевой маске или дыхательному аппарату с переменным положительным давлением. Композиции в виде растворов, суспензий или порошков можно вводить перорально или назально из устройств, которые доставляют композицию соответствующим образом. Количество соединения или композиции, вводимое пациенту, будет изменяться в зависимости от того, что вводят, цели введения, такой как профилактика или лечение, состояния пациента, способа введения и т.п. При терапевтических применениях композиции можно вводить пациенту, уже страдающему от заболевания, в количестве, достаточном для лечения или, по меньшей мере, частичного угнетения симптомов заболевания и его осложнений. Эффективные дозы будут зависеть от болезненного состояния, от которого лечат, а также от решения лечащего врача, в зависимости от таких факторов, как тяжесть заболевания, возраст, масса и общее состояние пациента и т.п. Композиции, вводимые пациенту, могут находиться в форме фармацевтических композиций, описанных выше. Такие композиции можно стерилизовать обычными методами стерилизации или можно стерилизовать фильтрацией. Водные растворы могут быть упакованы для применения в том виде, как они есть, или лиофилизованы, причем перед введением лиофилизованный препарат объединяют со стерильным водным носителем. Типично рН сложных препаратов будет составлять от 3 до 11, предпочтительнее от 5 до 9, и наиболее предпочтительно от 7 до 8. Следует иметь в виду, что применение некоторых из вышеуказанных эксципиентов, носителей или стабилизаторов будет приводить к образованию фармацевтических солей. Терапевтическая дозировка соединений по настоящему изобретению может изменяться согласно,например, определенному применению для лечения, которое проводят, способу введения соединения,здоровью и состоянию пациента и мнению врача, назначающего лечение. Пропорция или концентрация соединения по изобретению в фармацевтической композиции может изменяться в зависимости от ряда факторов, включая дозировку, химические свойства (например, гидрофобность) и способ введения. Например, для парентерального введения соединения по изобретению могут предоставляться в водном физиологическом забуференном растворе, содержащем от примерно 0,1 до примерно 10%, мас./об., соединения. Некоторые типичные интервалы доз составляют от примерно 1 мкг/кг до примерно 1 г/кг массы тела в сутки. В некоторых воплощениях интервал доз составляет от примерно 0,01 до примерно 100 мг/кг массы тела в сутки. Дозировка вероятно зависит от таких переменных, как тип и степень развития заболевания или расстройства, общее состояние здоровья определенного пациента, относительная биологическая эффективность выбранного соединения, состава эксципиента и способа введения. Эффективные дозы можно экстраполировать из кривых зависимости реакции от дозы, полученных in vitro или на тестсистемах животных моделях. Композиции по изобретению также могут включать одно или несколько дополнительных фармацевтических средств, таких как химиотерапевтические средства, стероиды, противовоспалительные средства или иммунодепрессанты, примеры которых приводятся в данном описании выше. Изобретение будет описываться подробнее с помощью конкретных примеров. Приведенные далее примеры представлены с целью пояснения и не предназначены для ограничения изобретения каким-либо образом. Специалист в данной области техники легко распознает ряд некритических параметров, которые можно изменять или модифицировать и получать, по существу, одинаковые результаты. Обнаружено, что соединения примеров являются ингибиторами JAK согласно по меньшей мере одному анализу,описанному в данном описании. Примеры Как правило, соединения, полученные в примерах, очищают на колонке ВЭЖХ с обращенной фазой(ОФ-ВЭЖХ) Waters XBridge (C18, 19100 мм, 5 мкм), с объемом впрыска 2 мл и скоростью потока 30 мл/мин, с элюированием с градиентом смеси ацетонитрил/вода, содержащая 0,15% NH4OH. В случаях,когда обусловлена кислая среда препаративной ВЭЖХ, продукты элюируют с градиентом смеси ацетонитрил/вода, содержащая 0,01% трифторуксусной кислоты (ТФК). Аналитическую ЖХМС осуществляют на колонке ОФ-ВЭЖХ Waters SunFire (C18, 2,150 мм, 5 мкм) с объемом впрыска 2 мкл, скоростью потока 3 мл/мин, с элюированием с градиентом от 2 до 80% В за 3 мин (А = вода с 0,025% ТФК; В = ацетонитрил). Гидрохлорид Стадия 1. трет-Бутил-4-(2-оксоэтил)пиперидин-1-карбоксилат Диметилсульфоксид (7,43 мл, 0,105 моль) добавляют к оксалилхлориду (5,53 мл, 0,0654 моль) в метиленхлориде (244,2 мл) при -78 С. Через 10 мин добавляют трет-бутил-4-(2-гидроксиэтил)пиперидин-1 карбоксилат (10,0 г, 0,0436 моль) в метиленхлориде (488,4 мл) и полученную смесь перемешивают при -78 С в течение 30 мин. Затем добавляют триэтиламин (30,4 мл, 0,218 моль), и смесь перемешивают в течение 5 ч,позволяя температуре постепенно подниматься до комнатной температуры. После гашения реакции водой смесь экстрагируют метиленхлоридом. Органические слои объединяют, промывают рассолом, сушат надMgSO4, упаривают досуха, и остаток используют непосредственно на следующей стадии. ЖХМС (M+Na) 250,0. Стадия 2. трет-Бутил-4-(3-цианопроп-2-ен-1-ил)пиперидин-1-карбоксилат К 1,0 М раствору трет-бутоксида калия в тетрагидрофуране (45,8 мл) при 0 С добавляют по каплям раствор диэтилцианометилфосфоната (7,77 мл, 0,0480 моль) в тетрагидрофуране (58,39 мл). Реакционную смесь нагревают до комнатной температуры и затем снова охлаждают до 0 С. К реакционной смеси добавляют раствор трет-бутил-4-(2-оксоэтил)пиперидин-1-карбоксилата (9,91 г, 0,0436 моль) в тетрагидрофуране (11,7 мл). Реакционную смесь нагревают до комнатной температуры и перемешивают при комнатной температуре в течение ночи. После гашения реакции водой смесь экстрагируют EtOAc. Объединенные органические слои промывают рассолом, сушат и упаривают досуха. Сырую смесь очищают на силикагеле с элюированием смесями от 0-40% EtOAc в гексане и получают нужный продукт (8,22 г,75% за две стадии). ЖХМС (M+Na) 273,0. Стадия 3. трет-Бутил-4-(3-циано-2-(4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1 Н-пиразол-1 ил) пропил)пиперидин-1-карбоксилат К раствору 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1 Н-пиразола (1,28 г, 6,60 ммоль) в ацетонитриле (33,0 мл) добавляют трет-бутил-4-(3-цианопроп-2-ен-1-ил)пиперидин-1-карбоксилат (3,30 г,13,2 ммоль), а затем 1,8-диазабицикло[5.4.0]ундец-7-ен (0,987 мл, 6,60 ммоль). Полученную смесь перемешивают при комнатной температуре в течение ночи. После упаривания реакционной смеси досуха остаток очищают на силикагеле с элюированием смесями 0-50% EtOAc в гексане, и получают нужный продукт (2,35 г, 80%). ЖХМС (М+Н) 445,2. Стадия 4. трет-Бутил-4-(2-(4-(2-хлорпиримидин-4-ил)-1 Н-пиразол-1-ил)-3-цианопропил)пиперидин 1-карбоксилат Смесь 2,4-дихлорпиримидина (0,26 г, 1,7 ммоль), трет-бутил-4-3-циано-2-(4-(4,4,5,5-тетраметил 1,3,2-диоксаборолан-2-ил)-1 Н-пиразол-1-ил)пропилпиперидин-1-карбоксилата (0,76 г, 1,7 ммоль), тетракис(трифенилфосфин)палладия (0,1 г, 0,1 ммоль) и фосфата калия (1,1 г, 5,2 ммоль) в 1,4-диоксане (5 мл) и воде (0,5 мл) греют при 100 С в течение ночи. После охлаждения до комнатной температуры смесь разбавляют EtOAc, промывают водой и рассолом, сушат над MgSO4 и упаривают досуха. Остаток очищают на силикагеле с элюированием смесями 0-100% EtOAc в гексане, и получают нужный продукт (277 мг, 37%). ЖХМС (M+Na) 453,0. Стадия 5. 3-(4-(2-Хлорпиримидин-4-ил)-1 Н-пиразол-1-ил)-4-(1-(2,4-дифторбензоил)пиперидин-4 ил)бутаннитрил К смеси трет-бутил-4-2-(4-(2-хлорпиримидин-4-ил)-1 Н-пиразол-1-ил)-3-цианопропилпиперидин-1 карбоксилата (0,277 г, 0,643 ммоль) и 2 мл диоксана добавляют 4 мл 4 М раствора HCl в диоксане. Реакционную смесь перемешивают при комнатной температуре в течение 30 мин и затем упаривают досуха. К полученной сырой соли HCl в метиленхлориде (5,0 мл) добавляют триэтиламин (0,269 мл, 1,93 ммоль),а затем 2,4-дифторбензоилхлорид (0,0948 мл, 0,771 ммоль). Смесь перемешивают при комнатной температуре в течение 30 мин, промывают насыщенным раствором бикарбоната натрия, сушат и упаривают досуха. Полученный сырой продукт реакции используют непосредственно на следующей стадии (300 мг,99%). ЖХМС (М+Н) 471,0. Стадия 6. 3-(4-(2-(4-(1 Н-Имидазол-1-ил)фениламино)пиримидин-4-ил)-1 Н-пиразол-1-ил)-4-(1-(2,4 дифторбензоил)пиперидин-4-ил)бутаннитрил Смесь 3-(4-(2-хлорпиримидин-4-ил)-1 Н-пиразол-1-ил)-4-(1-(2,4-дифторбензоил)пиперидин-4 ил)бутаннитрила (30 мг, 0,06 ммоль), 4-(1 Н-имидазол-1-ил)анилина (15,2 мг, 0,0956 ммоль) и птолуолсульфоновой кислоты (9,3 мг, 0,054 ммоль) в сухом 1,4-диоксане (0,5 мл) кипятят с обратным холодильником в течение ночи. Смесь разбавляют ацетонитрилом и водой, очищают ОФ-ВЭЖХ, и получают нужный продукт в виде рацемической смеси (25 мг, 71%). ЖХМС (М+Н) 594,1. Пример 2. 4-(1-(2,4-Дифторбензоил)пиперидин-4-ил)-3-(4-(2-(4-(пиперазин-1-ил)фениламино)пиримидин-4-ил)-1 Н-пиразол-1-ил)бутаннитрил Данное соединение получают в виде рацемической смеси согласно процедуре, описанной в примере 1, заменяя на стадии 6 4-(1 Н-имидазол-1-ил)анилин на трет-бутиловый эфир 1-(4 аминофенил)пиперазин-4-карбоновой кислоты. ЖХМС (М+Н) 611,2. Пример 3. 4-(1-(2,4-Дифторбензоил)пиперидин-4-ил)-3-(4-(2-(4-метоксифениламино)пиримидин-4 ил)-1 Н-пиразол-1-ил)бутаннитрил Данное соединение получают в виде рацемической смеси согласно процедуре, описанной в примере 1, с использованием на стадии 6 п-метоксианилина вместо 4-(1 Н-имидазол-1-ил)анилина. ЖХМС (М+Н) 558,2. Пример 4. 4-(1-(2,4-Дифторбензоил)пиперидин-4-ил)-3-(4-(2-(фениламино)пиримидин-4-ил)-1 Нпиразол-1-ил)бутаннитрил Данное соединение получают в виде рацемической смеси согласно процедуре, описанной в примере 1, с использованием на стадии 6 анилина вместо 4-(1 Н-имидазол-1-ил)анилина. ЖХМС (М+Н) 528,1. Данное соединение получают в виде рацемической смеси согласно процедуре, описанной в примере 1, с использованием на стадии 6 4-(4-морфолинил)бензоламина вместо 4-(1 Н-имидазол-1-ил)анилина. ЖХМС (М+Н) 613,3. Пример 6. 3-(4-(2-(4-1 Н-Пиразол-1-ил)фениламино)пиримидин-4-ил)-1 Н-пиразол-1-ил)-4-(1-(2,4 дифторбензоил)пиперидин-4-ил)бутаннитрил Данное соединение получают в виде рацемической смеси согласно процедуре, описанной в примере 1, с использованием на стадии 6 4-(1 Н-пиразол-1-ил)анилина вместо 4-(1 Н-имидазол-1-ил)анилина. ЖХМС (М+Н) 594,2. Пример 7. 4-(1-(2,4-Дифторбензоил)пиперидин-4-ил)-3-(4-(2-(3-(оксазол-5-ил)фениламино)пиримидин-4-ил)-1 Н-пиразол-1-ил)бутаннитрил Данное соединение получают в виде рацемической смеси согласно процедуре, описанной в примере 1, с использованием на стадии 6 3-(5-оксазолил)бензоламина вместо 4-(1 Н-имидазол-1-ил)анилина. ЖХМС (М+Н) 595,2. Пример 8. 4-(1-(2,4-Дифторбензоил)пиперидин-4-ил)-3-(4-(2-(1-метил-1 Н-пиразол-3-иламино)пиримидин-4-ил)-1 Н-пиразол-1-ил)бутаннитрил Данное соединение получают в виде рацемической смеси согласно процедуре, описанной в примере 1, с использованием на стадии 6 1-метил-1 Н-пиразол-3-амина вместо 4-(1 Н-имидазол-1-ил)анилина. ЖХМС (М+Н) 532,1. Данное соединение получают в виде рацемической смеси согласно процедуре, описанной в примере 1, с использованием на стадии 6 п-феноксианилина вместо 4-(1 Н-имидазол-1-ил)анилина. ЖХМС (М+Н) 620,2. Пример 12. 2-(4-(4-(2-(4-(1 Н-пиразол-1-ил)фениламино)пиримидин-4-ил)-1 Н-пиразол-1-ил)-1(изоксазол-5-карбонил)пиперидин-4-ил)ацетонитрил Стадия 1. трет-Бутил-4-(цианометилен)пиперидин-1-карбоксилат К 1,0 М раствору трет-бутоксида калия в тетрагидрофуране (26,3 мл) при 0 С добавляют по каплям раствор диэтилцианометилфосфоната (4,47 мл, 0,0276 моль) в тетрагидрофуране (33,61 мл). Реакционную смесь нагревают до комнатной температуры и затем снова охлаждают до 0 С. К реакционной смеси добавляют раствор трет-бутил-4-оксо-1-пиперидинкарбоксилата (5,0 г, 0,025 моль) в тетрагидрофуране(6,72 мл). Реакционную смесь нагревают до комнатной температуры и перемешивают при комнатной температуре в течение ночи. После гашения реакции водой смесь экстрагируют EtOAc. Объединенные органические слои промывают рассолом, сушат и упаривают досуха. Сырую смесь очищают на силикагеле с элюированием смесями 0-60% EtOAc в гексане и получают нужный продукт (5,40 г, 97%). ЖХМС (M+Na) 244,9. Стадия 2. трет-Бутил-4-(цианометил)-4-(4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1 Нпиразол-1-ил)пиперидин-1-карбоксилат К раствору 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1 Н-пиразола (4,3 г, 0,022 моль) в ацетонитриле (50 мл) добавляют трет-бутил-4-(цианометилен)пиперидин-1-карбоксилат (4,9 г, 0,022 моль), а затем 1,8-диазабицикло[5.4.0]ундец-7-ен (3,3 мл, 0,022 моль). Полученную смесь перемешивают при комнатной температуре в течение ночи. После упаривания досуха остаток очищают на силикагеле с элюированием смесями 0-100% EtOAc в гексане и получают нужный продукт (5,62 г, 61%). ЖХМС (М+Н) 417,1. Стадия 3. трет-Бутил-4-(4-(2-хлорпиримидин-4-ил)-1 Н-пиразол-1-ил)-4- (цианометил)пиперидин-1 карбоксилат Смесь 2,4-дихлорпиримидина (1,00 г, 6,71 ммоль), трет-бутил-4-(цианометил)-4-(4-(4,4,5,5 тетраметил-1,3,2-диоксаборолан-2-ил)-1 Н-пиразол-1-ил)пиперидин-1-карбоксилата (2,8 г, 6,7 ммоль),тетракис(трифенилфосфин)палладия (0,5 г, 0,4 ммоль) и фосфата калия (4,3 г, 20 ммоль) в 1,4-диоксане(20 мл) и воде (2 мл) греют при 100 С в течение ночи. После охлаждения до комнатной температуры смесь разбавляют EtOAc, промывают водой и рассолом, сушат над MgSO4 и концентрируют. Остаток очищают на силикагеле с элюированием смесями 0-100% EtOAc в гексане, и получают нужный продукт(2,19 г, 82%). ЖХМС (М+Н) 403,0. Стадия 4. (4-(4-(2-Хлорпиримидин-4-ил)-1 Н-пиразол-1-ил)-1-(изоксазол-5-илкарбонил)пиперидин 4-ил)ацетонитрил К смеси трет-бутил-4-(4-(2-хлорпиримидин-4-ил)-1 Н-пиразол-1-ил)-4-(цианометил)пиперидин-1 карбоксилата (0,259 г, 0,643 ммоль) и 2 мл диоксана добавляют 4 М раствор HCl в диоксане (4 мл). Реакционную смесь перемешивают при комнатной температуре в течение 30 мин и затем упаривают досуха. К полученной сырой соли HCl в метиленхлориде (5,0 мл) добавляют триэтиламин (0,269 мл, 1,93 ммоль),а затем изоксазол-5-карбонилхлорид (0,0744 мл, 0,771 ммоль). Смесь перемешивают при комнатной температуре в течение 30 мин, промывают насыщенным раствором бикарбоната натрия, сушат и упаривают досуха. Остаток используют непосредственно на следующей стадии (233 мг, 91%). ЖХМС (М+Н) 398,0.(4-(4-(2-хлорпиримидин-4-ил)-1 Н-пиразол-1-ил)-1-(изоксазол-5-илкарбонил)пиперидин-4 ил)ацетонитрила (30 мг, 0,08 ммоль), 4-(1 Н-пиразол-1-ил)анилина (18,9 мг, 0,119 ммоль) и птолуолсульфоновой кислоты (12 мг, 0,067 ммоль) в сухом 1,4-диоксане (0,6 мл) кипятят с обратным холодильником в течение ночи. Смесь разбавляют ацетонитрилом и водой, очищают ОФ-ВЭЖХ, и получают нужный продукт в виде рацемической смеси (22 мг, 52%). ЖХМС (М+Н) 521,1. Пример 13. 2-(1-(Изоксазол-5-карбонил)-4-(4-(2-(3-(оксазол-5-ил)фениламино)пиримидин-4-ил)-1 Нпиразол-1-ил)пиперидин-4-ил)ацетонитрил Данное соединение получают в виде рацемической смеси согласно процедуре, описанной в примере 12, с использованием на стадии 5 3-(5-оксазолил)бензоламина вместо 4-(1 Н-пиразол-1-ил)анилина. ЖХМС (М+Н) 522,1. Пример 14. 2-(4-(4-(2-(3-(1 Н-Тетразол-5-ил)фениламино)пиримидин-4-ил)-1 Н-пиразол-1-ил)-1(изоксазол-5-карбонил)пиперидин-4-ил)ацетонитрил Данное соединение получают в виде рацемической смеси согласно процедуре, описанной в примере 12, с использованием на стадии 5 3-(2 Н-тетразол-5-ил)бензоламина вместо 4-(1 Н-пиразол-1-ил)анилина. ЖХМС (М+Н) 523,0. Пример 15. 2-(1-(Изоксазол-5-карбонил)-4-(4-(2-(4-(морфолиносульфонил)фениламино)пиримидин 4-ил)-1 Н-пиразол-1-ил)пиперидин-4-ил)ацетонитрил Данное соединение получают в виде рацемической смеси согласно процедуре, описанной в примере 12, с использованием на стадии 5 4-(4-морфолиносульфонил)бензоламина вместо 4-(1 Н-пиразол-1 ил)анилина. ЖХМС (М+Н) 604,2. Пример 16. 2-(1-(Изоксазол-5-карбонил)-4-(4-(2-(6-метоксипиридин-3-иламино)пиримидин-4-ил)1 Н-пиразол-1-ил)пиперидин-4-ил)ацетонитрил Данное соединение получают в виде рацемической смеси согласно процедуре, описанной в примере 12, с использованием на стадии 5 6-метокси-3-пиридинамина вместо 4-(1 Н-пиразол-1-ил)анилина. ЖХМС (М+Н) 486,1. Пример 17. 2-(3-(4-(2-(4-(1 Н-Пиразол-1-ил)фениламино)пиримидин-4-ил)-1 Н-пиразол-1-ил)-1(циклопропилсульфонил)азетидин-3-ил)ацетонитрил Стадия 1. трет-Бутил-3-(цианометилен)азетидин-1-карбоксилат К 1,0 М раствору трет-бутоксида калия в тетрагидрофуране (30,7 мл) при 0 С добавляют по каплям раствор диэтилцианометилфосфоната (5,20 мл, 0,0322 моль) в тетрагидрофуране (39,12 мл). Реакционную смесь нагревают до комнатной температуры и затем снова охлаждают до 0 С. К реакционной смеси добавляют раствор трет-бутил-3-оксоазетидин-1-карбоксилата (5,0 г, 0,029 моль) в тетрагидрофуране(7,82 мл). Реакционную смесь нагревают до комнатной температуры и перемешивают при комнатной температуре в течение ночи. После гашения реакции водой смесь экстрагируют EtOAc. Объединенные органические слои промывают рассолом, сушат и упаривают досуха. Сырую смесь очищают на силикагеле с элюированием смесями 0-70% EtOAc в гексане, и получают нужный продукт (5,40 г, 95%). ЖХМС(M+Na) 217,1. Стадия 2. трет-Бутил-3-(цианометил)-3-(4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1 Нпиразол-1-ил)азетидин-1-карбоксилат К раствору 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1 Н-пиразола (3,06 г, 0,0158 моль) в ацетонитриле (50 мл) добавляют трет-бутил-3-(цианометилен)азетидин-1-карбоксилат (3,06 г, 0,0158 моль), а затем 1,8-диазабицикло[5.4.0]ундец-7-ен (2,36 мл, 0,0158 моль). Полученную смесь перемешивают при комнатной температуре в течение ночи. После упаривания досуха остаток очищают на силикагеле с элюированием смесями 0-100% EtOAc в гексане и получают нужный продукт (5,40 г, 88%). ЖХМС (М+Н) 389,1. Стадия 3. трет-Бутил-3-(4-(2-хлорпиримидин-4-ил)-1 Н-пиразол-1-ил)-3-(цианометил)азетидин-1 карбоксилат Смесь 2,4-дихлорпиримидина (1,0 г, 6,7 ммоль), трет-бутил-3-(цианометил)-3-(4-(4,4,5,5 тетраметил-1,3,2-диоксаборолан-2-ил)-1 Н-пиразол-1-ил)азетидин-1-карбоксилата (2,6 г, 6,7 ммоль), тетракис(трифенилфосфин)палладия (0,5 г, 0,4 ммоль) и фосфата калия (4,3 г, 20 ммоль) в 1,4-диоксане (20 мл) и воде (2 мл) греют при 100 С в течение ночи. После охлаждения до комнатной температуры смесь разбавляют EtOAc, промывают водой и рассолом, сушат над MgSO4 и концентрируют. Остаток очищают на силикагеле с элюированием смесями 0-100% EtOAc в гексане, и получают нужный продукт (2,10 г,83%). ЖХМС (М+Н) 375,0. Стадия 4. (3-(4-(2-Хлорпиримидин-4-ил)-1 Н-пиразол-1-ил)-1-(циклопропилсульфонил)азетидин-3 ил)ацетонитрил К смеси трет-бутил-3-(4-(2-хлорпиримидин-4-ил)-1 Н-пиразол-1-ил)-3-(цианометил)азетидин-1 карбоксилата (0,241 г, 0,643 ммоль) и 2 мл диоксана добавляют 4 М раствор HCl в диоксане (4 мл). Реакционную смесь перемешивают при комнатной температуре в течение 30 мин и затем упаривают досуха. К полученной сырой соли HCl в метиленхлориде (5,0 мл) добавляют триэтиламин (0,269 мл, 1,93 ммоль),а затем циклопропансульфонилхлорид (0,0786 мл, 0,771 ммоль). Смесь перемешивают при комнатной температуре в течение 30 мин, промывают насыщенным раствором бикарбоната натрия, сушат и упаривают досуха. Остаток используют непосредственно на следующей стадии (229 мг, 94%). ЖХМС (М+Н) 379,0. Стадия 5. 1-(Циклопропилсульфонил)-3-(4-(2-(4-(1 Н-пиразол-1-ил)фенил)аминопиримидин-4-ил)1 Н-пиразол-1-ил)азетидин-3-илацетонитрил Смесь(3-(4-(2-хлорпиримидин-4-ил)-1 Н-пиразол-1-ил)-1-(циклопропилсульфонил)азетидин-3 ил)ацетонитрила (30 мг, 0,08 ммоль), 4-(1 Н-пиразол-1-ил)анилина (18,9 мг, 0,119 ммоль) и птолуолсульфоновой кислоты (12 мг, 0,067 ммоль) в сухом 1,4-диоксане (0,6 мл) кипятят с обратным холодильником в течение ночи. Смесь разбавляют ацетонитрилом и водой, очищают ОФ-ВЭЖХ и получают нужный продукт в виде рацемической смеси (17,6 мг, 44%). ЖХМС (М+Н) 502,0. Пример 18. 2-(1-(Циклопропилсульфонил)-3-(4-(2-(3-(оксазол-5-ил)фениламино)пиримидин-4-ил)1 Н-пиразол-1-ил)азетидин-3-ил)ацетонитрил Данное соединение получают согласно процедуре, описанной в примере 17, с использованием на Данное соединение получают согласно процедуре, описанной в примере 17, с использованием на стадии 5 N-(4-аминофенил)ацетамида вместо 4- (1 Н-пиразол-1-ил)анилина. ЖХМС (М+Н) 493,0. Пример 20. 2-(1-(Циклопропилсульфонил)-3-(4-(2-(3-(2-метилпиримидин-4-ил)фениламино)пиримидин-4-ил)-1 Н-пиразол-1-ил)азетидин-3-ил)ацетонитрил Данное соединение получают согласно процедуре, описанной в примере 17, с использованием на стадии 5 3-(2-метил-4-пиримидинил)бензоламина вместо 4-(1 Н-пиразол-1-ил)анилина. ЖХМС (М+Н) 528,2. Пример 21. 2-(1-(Циклопропилсульфонил)-3-(4-(2-(4-(оксазол-5-ил)фениламино)пиримидин-4-ил)1 Н-пиразол-1-ил)азетидин-3-ил)ацетонитрил Данное соединение получают согласно процедуре, описанной в примере 17, с использованием на стадии 5 4-(5-оксазолил)бензоламина вместо 4-(1 Н-пиразол-1-ил)анилина. ЖХМС (М+Н) 503,0. Пример 22. 3-(4-(2-(4-Морфолинофениламино)пиримидин-4-ил)-1 Н-пиразол-1-ил)-3-(пиперидин-4 ил)пропаннитрил Стадия 1. трет-Бутил-4-(2-циановинил)пиперидин-1-карбоксилат К 1,0 М раствору трет-бутоксида калия в тетрагидрофуране (24,6 мл) при 0 С добавляют по каплям раствор диэтилцианометилфосфоната (4,18 мл, 0,0258 моль) в тетрагидрофуране (31,40 мл). Реакционную смесь нагревают до комнатной температуры и затем снова охлаждают до 0 С. К реакционной смеси добавляют раствор трет-бутил-4-формилпиперидин-1-карбоксилата (5,0 г, 0,023 моль) в тетрагидрофуране (6,28 мл). Реакционную смесь нагревают до комнатной температуры и перемешивают при комнатной температуре в течение ночи. После гашения реакции водой смесь экстрагируют EtOAc. Объединенные органические слои промывают рассолом, сушат и упаривают досуха. Сырую смесь очищают на силикагеле с элюированием смесями 0-50% EtOAc в гексане, и получают нужный продукт (5,10 г, 92%). ЖХМС(M+Na) 259,0. Стадия 2. трет-Бутил-4-2-циано-1-(4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1 Н-пиразол-1 ил)этилпиперидин-1-карбоксилат К раствору 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1 Н-пиразола (4,11 г, 0,0212 моль) в ацетонитриле (70 мл) добавляют трет-бутил-4-(2-циановинил)пиперидин-1-карбоксилат (5,00 г, 0,0212 моль), а затем 1,8-диазабицикло[5.4.0]ундец-7-ен (3,16 мл, 0,0212 моль). Полученную смесь перемешивают при комнатной температуре в течение ночи. После упаривания досуха остаток очищают на силикагеле с элюированием смесями 0-100% EtOAc в гексане и получают нужный продукт (6,11 г, 67%). ЖХМС (М+Н) 431,2. Стадия 3. трет-Бутил-4-1-(4-(2-хлорпиримидин-4-ил)-1 Н-пиразол-1-ил)-2-цианоэтилпиперидин-1 карбоксилат Смесь 2,4-дихлорпиримидина (1,04 г, 6,98 ммоль), трет-бутил-4-2-циано-1-(4-(4,4,5,5-тетраметил 1,3,2-диоксаборолан-2-ил)-1 Н-пиразол-1-ил)этилпиперидин-1-карбоксилата (2,98 г, 6,93 ммоль), тетракис(трифенилфосфин)палладия (0,5 г, 0,4 ммоль) и фосфата калия (4,4 г, 0,021 моль) в 1,4-диоксане (20 мл) и воде (2 мл) греют при 100 С в течение ночи. После охлаждения до комнатной температуры смесь разбавляют EtOAc, промывают водой и рассолом, сушат над MgSO4 и концентрируют. Остаток очищают на силикагеле с элюированием смесями 0-100% EtOAc в гексане, и получают нужный продукт (2,23 г,77%). ЖХМС (М+Н) 417,1. Стадия 4. 3-(4-2-4-Морфолин-4-илфенил)амино)пиримидин-4-ил-1 Н-пиразол-1-ил)-3-пиперидин 4-илпропаннитрил Смесь трет-бутил-4-1-(4-(2-хлорпиримидин-4-ил)-1 Н-пиразол-1-ил)-2-цианоэтилпиперидин-1 карбоксилата (800 мг, 0,002 моль), 4-морфолин-4-иланилина (500 мг, 0,003 моль) и п-толуолсульфоновой кислоты (270 мг, 0,0016 моль) в сухом 1,4-диоксане (10 мл) кипятят с обратным холодильником в течение ночи. Смесь разбавляют водой, экстрагируют EtOAc и объединенные органические слои промывают рассолом, сушат и упаривают досуха. Остаток очищают на силикагеле с элюированием смесями 0-20% МеОН в дихлорметане, и получают нужный продукт в виде рацемической смеси (30 мг, 4%). ЖХМС Смесь 3-(4-2-4-морфолин-4-илфенил)амино)пиримидин-4-ил-1 Н-пиразол-1-ил)-3-пиперидин-4 илпропаннитрила (0,030 г, 0,065 ммоль), 2-хлор-5-фторпиримидина (0,013 г, 0,098 ммоль) и N,Nдиизопропилэтиламина (0,023 мл, 0,13 ммоль) в этаноле (0,5 мл) греют при 130 С в запаяной пробирке в течение 2 ч. После упаривания досуха остаток очищают ОФ-ВЭЖХ и получают нужный продукт в виде рацемической смеси (12 мг, 33%). ЖХМС (М+Н) 555,2. Пример 24. 3-(1-(Метилсульфонил)пиперидин-4-ил)-3-(4-(2-(4-морфолинофениламино)пиримидин 4-ил)-1 Н-пиразол-1-ил)пропаннитрил К смеси тригидрохлорида 3-(4-2-4-морфолин-4-илфенил)амино)пиримидин-4-ил-1 Н-пиразол-1 ил)-3-пиперидин-4-илпропаннитрила (30 мг, 0,05 ммоль) и 1,0 М раствора карбоната натрия в воде (0,25 мл) и тетрагидрофуране (0,25 мл) добавляют метансульфонилхлорид (6,1 мкл, 0,079 ммоль). Реакционную смесь встряхивают при комнатной температуре в течение 30 мин. Смесь разбавляют водой и ацетонитрилом, очищают ОФ-ВЭЖХ и получают нужный продукт в виде рацемической смеси (соль ТФК). ЖХМС (М+Н) 537,1. Пример 25. 3-(4-(2-(4-Морфолинофениламино)пиримидин-4-ил)-1 Н-пиразол-1-ил)-3-(1-(фенилсульфонил)пиперидин-4-ил)пропаннитрил Данное соединение получают в виде рацемической смеси согласно процедуре, описанной в примере 24, с использованием бензолсульфонилхлорида вместо метансульфонилхлорида. ЖХМС (М+Н) 599,1. Данное соединение получают в виде рацемической смеси согласно процедуре, описанной в примере 24, с использованием ацетилхлорида вместо метансульфонилхлорида. ЖХМС (М+Н) 501,2. Пример 27. 3-(1-Бензоилпиперидин-4-ил)-3-(4-(2-(4-морфолинофениламино)пиримидин-4-ил)-1 Нпиразол-1-ил)пропаннитрил Данное соединение получают в виде рацемической смеси согласно процедуре, описанной в примере 24, с использованием бензоилхлорида вместо метансульфонилхлорида. ЖХМС (М+Н) 563,2. Пример 28. 2-(4-(4-(2-(4-(1 Н-Пиразол-1-ил)фениламино)пиримидин-4-ил)-1 Н-пиразол-1-ил)-1(циклопропилсульфонил)пиперидин-4-ил)ацетонитрил Стадия 1. (4-(4-(2-Хлорпиримидин-4-ил)-1 Н-пиразол-1-ил)-1-(циклопропилсульфонил)пиперидин 4-ил)ацетонитрил К смеси трет-бутил-4-(4-(2-хлорпиримидин-4-ил)-1 Н-пиразол-1-ил)-4-(цианометил)пиперидин-1 карбоксилата (0,487 г, 1,21 ммоль) и 2 мл диоксана добавляют 4 М раствор HCl в диоксане (4,0 мл). Реакционную смесь перемешивают при комнатной температуре в течение 30 мин и затем упаривают досуха. К полученной сырой соли HCl в метиленхлориде (9,4 мл) добавляют триэтиламин (0,505 мл, 3,62 ммоль),а затем циклопропансульфонилхлорид (0,148 мл, 1,45 ммоль). Смесь перемешивают при комнатной температуре в течение 30 мин, промывают насыщенным раствором бикарбоната натрия, сушат и упаривают досуха. Остаток используют непосредственно на следующей стадии (402 мг, 82%). ЖХМС (М+Н) 407,0. Стадия 2. 1-(Циклопропилсульфонил)-4-(4-(2-(4-(1 Н-пиразол-1-ил)фенил)аминопиримидин-4-ил)1 Н-пиразол-1-ил)пиперидин-4-илацетонитрил Смесь(4-(4-(2-хлорпиримидин-4-ил)-1 Н-пиразол-1-ил)-1-(циклопропилсульфонил)пиперидин-4 ил)ацетонитрила (30 мг, 0,08 ммоль), 4-(1 Н-пиразол-1-ил)анилина (18,9 мг, 0,119 ммоль) и птолуолсульфоновой кислоты (12 мг, 0,067 ммоль) в сухом 1,4-диоксане (0,6 мл) кипятят с обратным холодильником в течение ночи. Смесь разбавляют ацетонитрилом и водой, очищают ОФ-ВЭЖХ при рН 10,и получают нужный продукт в виде свободного основания (30 мг, 72%). ЖХМС (М+Н) 530,1. Пример 29. 1-(Циклопропилсульфонил)-4-(4-(2-(4-морфолинофениламино)пиримидин-4-ил)-1 Нпиразол-1-ил)пиперидин-4-ил)ацетонитрил Данное соединение получают согласно процедуре, описанной в примере 28, с использованием на стадии 2 4-морфолин-4-иланилина вместо 4-(1 Н-пиразол-1-ил)анилина. ЖХМС (М+Н) 549,1. Данное соединение получают согласно процедуре, описанной в примере 28, с использованием на стадии 2 4-аминобензамида вместо 4-(1 Н-пиразол-1-ил)анилина. ЖХМС (М+Н) 507,0. Пример 31. 4-(4-(1-(4-(Цианометил)-1-(циклопропилсульфонил)пиперидин-4-ил)-1 Н-пиразол-4 ил)пиримидин-2-иламино)-N-(2-гидроксиэтил)бензамид Данное соединение получают согласно процедуре, описанной в примере 28, с использованием на стадии 2 4-амино-N-(2-гидроксиэтил)бензамида вместо 4-(1 Н-пиразол-1-ил)анилина. ЖХМС (М+Н) 551,0. Пример 32. 4-(4-(1-(4-(Цианометил)-1-(циклопропилсульфонил)пиперидин-4-ил)-1 Н-пиразол-4 ил)пиримидин-2-иламино)-N,N-диметилбензамид Данное соединение получают согласно процедуре, описанной в примере 28, с использованием на стадии 2 4-амино-N,N-диметилбензамида вместо 4-(1 Н-пиразол-1-ил)анилина. ЖХМС (М+Н) 535,2. Пример 33. 4-(4-(1-(2-(Циано-1-циклопентилэтил)-1 Н-пиразол-4-ил)пиримидин-2-иламино)бензамид Стадия 1. 3-Циклопентил-3-(4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1 Н-пиразол-1 ил)пропаннитрил К раствору 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1 Н-пиразола (2,00 г, 0,0103 моль) в ацетонитриле (30 мл) добавляют 3-циклопентилакрилонитрил (1,25 г, 0,0103 моль), а затем 1,8 диазабицикло[5.4.0]ундец-7-ен (1,54 мл, 0,0103 моль). Полученную смесь перемешивают при 60 С в течение ночи и затем упаривают досуха. Остаток очищают на силикагеле с элюированием смесями 0-50%EtOAc в гексане, и получают нужный продукт (2,36 г, 73%). ЖХМС (М+Н) 316,1. Стадия 2. 3-(4-(2-Хлорпиримидин-4-ил)-1 Н-пиразол-1-ил)-3-циклопентилпропаннитрил Смесь 2,4-дихлорпиримидина (0,28 г, 1,9 ммоль), 3-циклопентил-3-(4-(4,4,5,5-тетраметил-1,3,2 диоксаборолан-2-ил)-1 Н-пиразол-1-ил)пропаннитрила(0,500 г,1,59 ммоль),тетракис(трифенилфосфин)палладия (100 мг, 0,1 ммоль) и фосфата калия (1,0 г, 4,8 ммоль) в 1,4-диоксане (5 мл) и воде (0,5 мл) греют при 100 С в течение ночи. После охлаждения до комнатной температуры смесь разбавляют EtOAc, промывают водой и рассолом, сушат над MgSO4 и концентрируют. Остаток очищают на силикагеле с элюированием смесями 0-80% EtOAc в гексане, и получают нужный продукт (323 мг, 67%). ЖХМС (М+Н) 302,0. Стадия 3. 4-(4-(1-(2-(Циано-1-циклопентилэтил)-1 Н-пиразол-4-ил)пиримидин-2-иламино)бензамид Смесь 3-(4-(2-хлорпиримидин-4-ил)-1 Н-пиразол-1-ил)-3-циклопентилпропаннитрила (30 мг, 0,1 ммоль), 4-аминобензамида (20,3 мг, 0,149 ммоль) и п-толуолсульфоновой кислоты (14 мг, 0,084 ммоль) в сухом 1,4-диоксане (0,8 мл) кипятят с обратным холодильником в течение ночи. Смесь разбавляют аце- 27020777 тонитрилом и водой, очищают ОФ-ВЭЖХ при рН 1 и получают нужный продукт в виде рацемической смеси (соль ТФК, 38 мг, 75%). ЖХМС (М+Н) 402,1. Пример 34. 3-(4-(2-(4-(1 Н-Пиразол-1-ил)фениламино)пиримидин-4-ил)-1 Н-пиразол-1-ил)-3 циклопентилпропаннитрил Данное соединение получают в виде рацемической смеси согласно процедуре, описанной в примере 33, с использованием на стадии 3 4-(1 Н-пиразол-1-ил)анилина вместо 4-аминобензамида. ЖХМС (М+Н) 425,0. Пример 35. 3-Циклопентил-3-(4-(2-(4-морфолинофениламино)пиримидин-4-ил)-1 Н-пиразол-1 ил)пропаннитрил Данное соединение получают в виде рацемической смеси согласно процедуре, описанной в примере 33, с использованием на стадии 3 4-морфолин-4-иланилина вместо 4-аминобензамида. ЖХМС (М+Н) 444,1. Пример 36. 3-Циклопентил-3-(4-(2-(фениламино)пиримидин-4-ил)-1 Н-пиразол-1-ил)пропаннитрил Данное соединение получают в виде рацемической смеси согласно процедуре, описанной в примере 33, с использованием на стадии 3 анилина вместо 4-аминобензамида. ЖХМС (М+Н) 359,0. Пример 37. 3-Циклопентил-3-(4-(2-(3-(оксазол-5-ил)фениламино)пиримидин-4-ил)-1 Н-пиразол-1 ил)пропаннитрил Данное соединение получают в виде рацемической смеси согласно процедуре, описанной в примере 33, с использованием на стадии 3 3-(5-оксазолил)бензоламина вместо 4-аминобензамида. ЖХМС (М+Н) 426,0. Пример 38. 3-Циклопентил-3-(4-(2-(4-метоксифениламино)пиримидин-4-ил)-1 Н-пиразол-1 ил)пропаннитрил Данное соединение получают в виде рацемической смеси согласно процедуре, описанной в примере 33, с использованием на стадии 3 п-метоксианилина вместо 4-аминобензамида. ЖХМС (М+Н) 389,1. Данное соединение получают в виде рацемической смеси согласно процедуре, описанной в примере 33, с использованием на стадии 3 N-(4-аминофенил)ацетамида вместо 4-аминобензамида. ЖХМС (М+Н) 416,0. Пример 40. 4-(4-(1-(2-Циано-1-циклопентилэтил)-1 Н-пиразол-4-ил)пиримидин-2-иламино)-N,Nдиметилбензамид Данное соединение получают в виде рацемической смеси согласно процедуре, описанной в примере 33, с использованием на стадии 3 4-амино-N,N-диметилбензамида вместо 4-аминобензамида. ЖХМС Данное соединение получают в виде рацемической смеси согласно процедуре, описанной в примере 33, с использованием на стадии 3 трет-бутилового эфира 1-(4-аминофенил)пиперазин-4-карбоновой кислоты вместо 4-аминобензамида. ЖХМС (М+Н) 443,1. Пример 42. 4-(1-(Этилсульфонил)пиперидин-4-ил)-3-(4-(2-(4-морфолинофениламино)пиримидин-4 ил)-1 Н-пиразол-1-ил)бутаннитрил Данное соединение получают в виде рацемической смеси согласно процедуре, описанной в примере 1, с использованием на стадии 5 этансульфонилхлорида вместо 2,4-дифторбензоилхлорида и на стадии 6 4-морфолин-4-иланилина вместо 4-(1 Н-имидазол-1-ил)анилина. ЖХМС (М+Н) 565,1. Пример 43. 3-(4-(2-(4-(1 Н-Пиразол-1-ил)фениламино)пиримидин-4-ил)-1 Н-пиразол-1-ил)-4-(1(этилсульфонил)пиперидин-4-ил)бутаннитрил
МПК / Метки
МПК: A61K 31/506, C07D 417/14, C07D 401/14, C07D 409/14, A61P 35/00, C07D 491/107, C07D 403/14, C07D 405/14, C07D 491/16, C07D 451/06, C07D 413/14, C07D 498/10, C07D 471/10, C07D 403/04
Метки: janus, 4-пиразолил-n-арилпиримидин-2-амины, ингибиторов, качестве, 4-пиразолил-n-пиридилпиримидин-2-амины, 4-пиразолил-n-пиразолилпиримидин-2-амины, киназ
Код ссылки
<a href="https://eas.patents.su/30-20777-4-pirazolil-n-arilpirimidin-2-aminy-4-pirazolil-n-pirazolilpirimidin-2-aminy-i-4-pirazolil-n-piridilpirimidin-2-aminy-v-kachestve-ingibitorov-kinaz-janus.html" rel="bookmark" title="База патентов Евразийского Союза">4-пиразолил-n-арилпиримидин-2-амины, 4-пиразолил-n-пиразолилпиримидин-2-амины и 4-пиразолил-n-пиридилпиримидин-2-амины в качестве ингибиторов киназ janus</a>
Предыдущий патент: Способ лечения инсульта
Следующий патент: Система изоляции зданий снаружи
Случайный патент: Таблетка содержащая гранулированный пантопразол