N-содержащие бициклические производные для применения при лечении состояний, связанных с андрогенным рецептором
Номер патента: 17144
Опубликовано: 30.10.2012
Авторы: Хейлс Нил Джеймс, Брэдбери Роберт Хью, Рейбоу Алфред Артур
Формула / Реферат
1. Соединение формулы (Ic) или его фармацевтически приемлемая соль
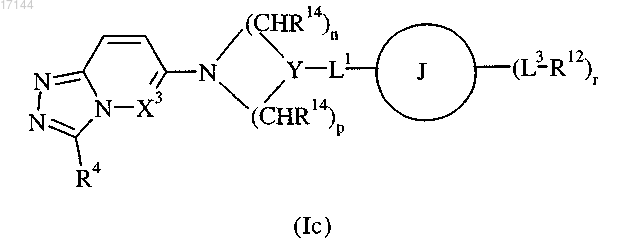
где X3 означает CH или N;
R4 означает галоС1-4алкил;
Y означает CH, COH или N;
R14, одинаково или по-разному в каждом случае, означает водород или метил;
n и p независимо означают 1 или 2;
L1 означает прямую связь, -(CR9R10)t-, -(CR9R10)v-O-(CR9R10)v-, -N(R11)-(CH2)q- или -S-, -S(O)- или -S(O)2-;
R9 и R10, одинаково или по-разному в каждом случае, означают водород или метил;
q, одинаково или по-разному в каждом случае, означает 0, 1, 2 или 3;
t означает 1, 2 или 3;
v, одинаково или по-разному в каждом случае, означает 0, 1 или 2;
J означает арил; полностью насыщенное моноциклическое 3-6-членное карбоциклическое кольцо; моноциклическое 4-, 5-, 6- или 7-членное гетероциклическое кольцо, которое включает 1, 2, 3 или 4 гетероатома, независимо выбранных из O, N или S; моноциклическое 5- или 6-членное гетероарильное кольцо, которое включает 1, 2, 3 или 4 гетероатома, независимо выбранных из O, N или S; или бициклическую 9- или 10-членную гетероарильную кольцевую систему, которая включает 1, 2, 3, 4 или 5 гетероатомов, независимо выбранных из O, N или S;
L3 означает прямую связь, -(CR9R10)t-, -C(O)N(R11)-(CH2)q-, -C(O)N(R11)-(CH2)q-S(O)2-, -NR11C(O)-(CH2)q-,
-C(O)-(CH2)q-, -O-(CH2)q-, -O-(CH2)q-NR11-(CH2)q-, -O-(CH2)q-C(O)NR11-(CH2)q-, -S-, -S(O)- или -S(O)2-;
R11 означает водород или метил;
R12 означает гало, C1-6алкил, C2-6алкенил, C2-6алкинил, карбокси, C1-6алкокси, циано, оксо, фторС1-6алкил, гидрокси, амино, N-C1-4алкиламино или N,N-ди-C1-4алкиламино;
арил, где арильное кольцо необязательно замещено 1, 2 или 3 заместителями, выбранными из R13;
моноциклическое 5- или 6-членное гетероарильное кольцо, которое включает 1, 2, 3 или 4 гетероатома, независимо выбранных из O, N или S, и которое является необязательно замещенным 1, 2 или 3 заместителями, выбранными из R13; или
моноциклическое 4-, 5-, 6- или 7-членное гетероциклическое кольцо, которое включает 1, 2, 3 или 4 гетероатома, независимо выбранных из O, N или S, и которое является необязательно замещенным 1, 2 или 3 заместителями, выбранными из R13;
R13 означает амино, гало, C1-6алкил, C2-6алкенил, C2-6алкинил, C1-6алкокси, С2-6алканоил, C1-6алкоксиС1-6алкил, карбокси, циано, оксо, фторС1-6алкил, гидрокси, гидроксиС1-6алкил, C1-6алкилсульфанил, C1-6алкилсульфинил, C1-6алкилсульфонил, N-C1-4алкиламино, N,N-ди-C1-4алкиламино или -C(O)NR14R15, где R14 и R15 независимо означают водород или метил; и
r означает 0, 1, 2 или 3.
2. Соединение формулы (Ic) или его фармацевтически приемлемая соль
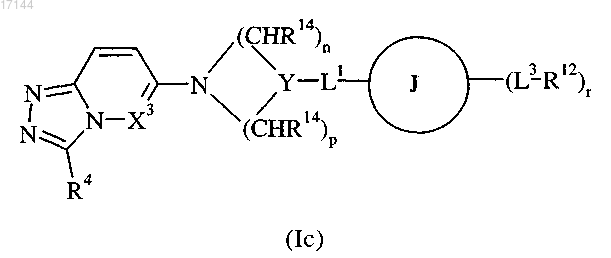
где X3 означает CH или N;
R4 означает галоС1-4алкил;
Y означает CH, COH или N;
R14, одинаково или по-разному в каждом случае, означает водород или метил;
n и p независимо означают 1 или 2;
L1 означает прямую связь, -(CR9R10)t-, -(CR9R10)v-O-(CR9R10)v-, -N(R11)-(CH2)q- или -S-, -S(O)- или -S(O)2-;
R9 и R10, одинаково или по-разному в каждом случае, означают водород или метил;
q, одинаково или по-разному в каждом случае, означает 0, 1, 2 или 3;
t означает 1, 2 или 3;
v, одинаково или по-разному в каждом случае, означает 0, 1 или 2;
J означает арил; полностью насыщенное моноциклическое 3-6-членное карбоциклическое кольцо; моноциклическое 4-, 5-, 6- или 7-членное гетероциклическое кольцо, которое включает 1, 2, 3 или 4 гетероатома, независимо выбранных из O, N или S; моноциклическое 5- или 6-членное гетероарильное кольцо, которое включает 1, 2, 3 или 4 гетероатома, независимо выбранных из O, N или S; или бициклическую 9- или 10-членную гетероарильную кольцевую систему, которая включает 1, 2, 3, 4 или 5 гетероатомов, независимо выбранных из O, N или S;
L3 означает прямую связь, -(CR9R10)t-, -C(O)N(R11)-(CH2)q-, -C(O)N(R11)-(CH2)q-S(O)2, -NR11C(O)-(CH2)q-,
-C(O)-(CH2)q-, -O-(CH2)q-, -O-(CH2)q-NR11-(CH2)q-, -O-(CH2)q-C(O)NR11-(CH2)q-, -S-, -S(O)- или -S(O)2-;
R11 означает водород или метил;
R12 означает гало, C1-6алкил, С2-6алкенил, C2-6алкинил, карбокси, C1-6алкокси, циано, оксо, фторС1-6алкил, гидрокси, амино, N-C1-4алкиламино или N,N-ди-C1-4алкиламино; арил, где арильное кольцо необязательно замещено 1, 2 или 3 заместителями, выбранными из R13;
моноциклическое 5- или 6-членное гетероарильное кольцо, которое включает 1, 2, 3 или 4 гетероатома, независимо выбранных из O, N или S, и которое является необязательно замещенным 1, 2 или 3 заместителями, выбранными из R13; или моноциклическое 4-, 5-, 6- или 7-членное гетероциклическое кольцо, которое включает 1, 2, 3 или 4 гетероатома, независимо выбранных из O, N или S, и которое является необязательно замещенным 1, 2 или 3 заместителями, выбранными из R13;
R13 означает амино, гало, C1-6алкил, C2-6алкенил, C2-6алкинил, C1-6алкокси, C2-6алканоил, C1-6алкоксиС1-6алкил, карбокси, циано, оксо, фторС1-6алкил, гидрокси, гидроксиС1-6алкил, C1-6алкилсульфанил, C1-6алкилсульфинил, C1-6алкилсульфонил, N-C1-4алкиламино, N,N-ди-C1-4алкиламино или -C(O)NR14R15, где R14 и R15 независимо означают водород или метил; и
r означает 0, 1, 2 или 3.
3. Соединение формулы (Ic) или его фармацевтически приемлемая соль
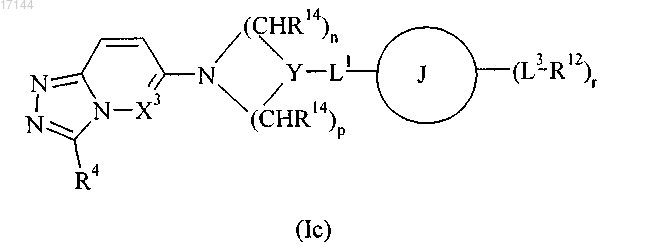
где X3 означает CH или N;
R4 означает галоС1-4алкил;
Y означает CH, COH или N;
R14, одинаково или по-разному в каждом случае, означает водород или метил;
n и p независимо означают 1 или 2;
L1 означает прямую связь, -(CR9R10)t-, -(CR9R10)v-O-(CR9R10)v-, -N(R11)-(CH2)q- или -S-, -S(O)- или -S(O)2-;
R9 и R10, одинаково или по-разному в каждом случае, означают водород или метил;
q, одинаково или по-разному в каждом случае, означает 0, 1, 2 или 3;
t означает 1, 2 или 3;
v, одинаково или по-разному в каждом случае, означает 0, 1 или 2;
J означает арил; полностью насыщенное моноциклическое 3-6-членное карбоциклическое кольцо; фуранил, имидазолил, изотиазолил, морфолинил, оксадиазолил, оксазолил, изоксазолил, оксетанил, тетрагидро-2H-пиранил, пиразолил, пиридазинил, пиридинил, пирролил или тиадиазолил; или бициклическую 9-членную гетероарильную кольцевую систему, которая включает 1 или 2 атома азота, 1 или 2 атома кислорода, 1 атом серы или 1 атом азота и 1 атом серы;
L3 означает прямую связь, -(CR9R10)t-, -C(O)N(R11)-(CH2)q-, -C(O)N(R11)-(CH2)q-S(O)2-, -NR11C(O)-(CH2)q-,
-C(O)-(CH2)q-, -O-(CH2)q-, -O-(CH2)q-NR11-(CH2)q-, -O-(CH2)q-C(O)NR11-(CH2)q-, -S-, -S(O)- или -S(O)2-;
R11 означает водород или метил;
R12 означает гало, C1-6алкил, C2-6алкенил, С2-6алкинил, карбокси, C1-6алкокси, циано, оксо, фторС1-6алкил, гидрокси, амино, N-C1-4алкиламино или N,N-ди-C1-4алкиламино; арил, где арильное кольцо необязательно замещено 1, 2 или 3 заместителями, выбранными из R13; моноциклическое 5- или 6-членное гетероарильное кольцо, которое включает 1, 2, 3 или 4 гетероатома, независимо выбранных из O, N или S, и которое является необязательно замещенным 1, 2 или 3 заместителями, выбранными из R13; или моноциклическое 4-, 5-, 6- или 7-членное гетероциклическое кольцо, которое включает 1, 2, 3 или 4 гетероатома, независимо выбранных из O, N или S, и которое является необязательно замещенным 1, 2 или 3 заместителями, выбранными из R13;
R13 означает амино, гало, C1-6алкил, С2-6алкенил, C2-6алкинил, C1-6алкокси, С2-6алканоил, C1-6алкоксиС1-6алкил, карбокси, циано, оксо, фторС1-6алкил, гидрокси, гидроксиС1-6алкил, C1-6алкилсульфанил, C1-6алкилсульфинил, C1-6алкилсульфонил, N-C1-4алкиламино, N,N-ди-C1-4алкиламино или -C(O)NR14R15, где R14 и R15 независимо означают водород или метил;
r означает 1, 2 или 3, когда J означает арил;
r означает 0, когда J означает полностью насыщенное моноциклическое 3-6-членное карбоциклическое кольцо; и
r означает 0, 1, 2 или 3, когда J означает фуранил, имидазолил, изотиазолил, морфолинил, оксадиазолил, оксазолил, изоксазолил, оксетанил, тетрагидро-2H-пиранил, пиразолил, пиридазинил, пиридинил, пирролил, тиадиазолил, или бициклическую 9-членную гетероарильную кольцевую систему, которая включает 1 или 2 атома азота, 1 или 2 атома кислорода, 1 атом серы или 1 атом азота и 1 атом серы;
при условии, что соединение формулы (Ic) не представляет собой
4-{4-[3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин-6-ил]пиперазин-1-ил}фенол;
6-[4-(пиридин-3-илметил)пиперазин-1-ил]-3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин;
6-[4-(2-фторбензил)пиперазин-1-ил]-3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин;
6-[4-(имидазо[1,2-a]пиридин-2-илметил)пиперазин-1-ил]-3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин;
6-[4-(3,4-диметоксибензил)пиперазин-1-ил]-3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин;
6-[4-(1H-индол-3-ил)пиперидин-1-ил]-3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин;
6-{4-[2-(3,5-диметоксифенил)этил]пиперидин-1-ил}-3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин;
6-[4-(4-метоксибензил)пиперазин-1-ил]-3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин;
6-[4-(3-хлорбензил)пиперазин-1-ил]-3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин;
6-[4-(4-хлорбензил)пиперазин-1-ил]-3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин;
6-[4-(2-метилбензил)пиперазин-1-ил]-3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин;
6-[4-(пиридин-4-илметил)пиперазин-1-ил]-3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин;
6-[4-(2,6-диметилфенил)пиперазин-1-ил]-3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин;
6-[4-(4-метоксифенил)пиперазин-1-ил]-3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин;
6-[4-(3-хлорфенил)пиперазин-1-ил]-3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин;
6-[4-(4-фторфенил)пиперазин-1-ил]-3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин или
6-{4-[(2,6-дифторфенил)сульфонил]пиперазин-1-ил}-3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин.
4. Соединение по п.3 или его фармацевтически приемлемая соль, где X3 означает N.
5. Соединение по п.3 или 4 или его фармацевтически приемлемая соль, где R4 означает дифторметил, трифторметил или хлор(дифтор)метил.
6. Соединение по п.3 или 4 или его фармацевтически приемлемая соль, где R4 означает трифторметил.
7. Соединение по любому из пп.3-6 или его фармацевтически приемлемая соль, где R14 означает водород.
8. Соединение по любому из пп.3-7 или его фармацевтически приемлемая соль, где n и p оба означают 2.
9. Соединение по любому из пп.3-8 или его фармацевтически приемлемая соль, где Y означает CH или СОН.
10. Соединение по любому из пп.3-9 или его фармацевтически приемлемая соль, где Y означает N.
11. Соединение по любому из пп.3-10 или его фармацевтически приемлемая соль, где L1 означает прямую связь.
12. Соединение по любому из пп.3-11 или его фармацевтически приемлемая соль, где J означает фенил, пиридинил, индолил, индазолил или пирролопиридинил.
13. Соединение по любому из пп.3-12 или его фармацевтически приемлемая соль, где L3 означает
-C(O)N(R11)-(CH2)q-, -NR11C(O)-(CH2)q-, -C(O)-(CH2)q- или -O-(CH2)q-.
14. Соединение по п.13 или его фармацевтически приемлемая соль, где R11 означает метил.
15. Соединение по любому из пп.3-14 или его фармацевтически приемлемая соль, где R12 означает фтор, хлор, метил, метокси, дифторметил, трифторметил, циано, гидрокси, метилсульфонил, диметиламино, пирролидинил, пиперидинил, пиперазинил, морфолинил или пиразолил.
16. Соединение по любому из пп.3-15 или его фармацевтически приемлемая соль, где R13 означает метил, оксо или гидрокси.
17. Соединение по любому из пп.3-16 или его фармацевтически приемлемая соль, где r означает 1.
18. Соединение по любому из пп.3-16 или его фармацевтически приемлемая соль, где J не означает арил и r означает 0.
19. Соединение по п.3, выбранное из
4-[[4-[3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин-6-ил]пиперазин-1-ил]метил]бензонитрила;
3-(трифторметил)-6-[4-[[3-(трифторметил)фенил]метил]пиперазин-1-ил][1,2,4]триазоло[4,3-b]пиридазина;
4-пиридин-3-ил-1-[3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин-6-ил]пиперидин-4-ола;
3-(дифторметил)-6-{4-[(1R)-1-(4-фторфенил)этил]пиперазин-1-ил}[1,2,4]триазоло[4,3-b]пиридазина;
4-(4-фторфенил)-1-[3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин-6-ил]пиперидин-4-ола;
N-(2-метоксиэтил)-N-метил-4-{1-[3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин-6-ил]пиперидин-4-ил}бензамида;
N-(2-гидроксиэтил)-N-метил-4-{1-[3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин-6-ил]пиперидин-4-ил}бензамида;
6-(4-{4-[(4-метилпиперазин-1-ил)карбонил]фенил}пиперидин-1-ил)-3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазина;
N-[2-(2-оксопирролидин-1-ил)этил]-4-{1-[3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин-6-ил]пиперидин-4-ил}бензамида;
6-[4-(1H-индазол-3-илметил)пиперазин-1-ил]-3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазина;
N-(2-метоксиэтил)-N-метил-3-({1-[3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин-6-ил]пиперидин-4-ил}окси)бензамида;
2-морфолин-4-ил-N-(4-{1-[3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин-6-ил]пиперидин-4-ил}фенил)ацетамида;
6-(4-{4-[2-(1-метил-1H-пиразол-5-ил)этокси]фенил}пиперидин-1-ил)-3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазина;
6-{4-[2-(дифторметил)-5-фторбензил]пиперазин-1-ил}-3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазина;
6-{4-[(6-метилпиридин-3-ил)метил]пиперазин-1-ил}-3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазина;
6-[4-(1H-пирроло[2,3-b]пиридин-3-ил)пиперидин-1-ил]-3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазина;
6-[4-(5-метокси-1H-индол-3-ил)пиперидин-1-ил]-3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазина;
1-[(4-{1-[3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин-6-ил]пиперидин-4-ил}фенил)карбонил]пиперидин-4-ола;
N-метил-N-[2-(метилсульфонил)этил]-4-{1-[3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин-6-ил]пиперидин-4-ил}бензамида;
6-[3-(4-метоксифенокси)азетидин-1-ил]-3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазина;
6-(4-{4-[2-(1-метил-1H-пиразол-5-ил)этокси]фенил}пиперазин-1-ил)-3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазина и
4-[4-[2-(1-метил-1H-пиразол-5-ил)этокси]фенил]-1-[3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин-6-ил]пиперидин-4-ола;
и его фармацевтически приемлемые соли.
20. Фармацевтическая композиция, которая включает соединение по любому из пп.3-19 или его фармацевтически приемлемую соль совместно с фармацевтически приемлемым разбавителем или носителем.
21. Способ получения соединений формулы (Ic), который включает введение в реакцию соединения формулы (IIa), где G означает галоген и R4 и X3 определены выше в отношении формулы (Ic), с амином формулы (IIIa), где J, Y, L1, L3, R12, R14, n, p и r определены выше в отношении формулы (Ic)
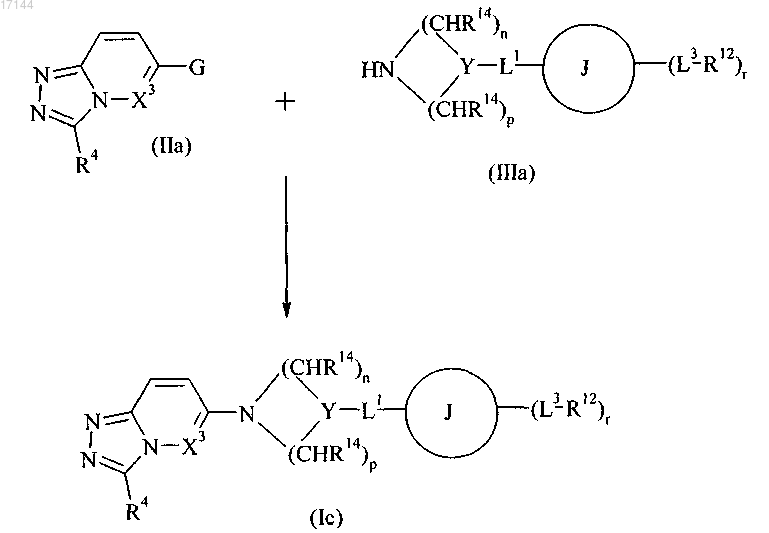
и затем, при необходимости:
(i) превращение функциональной группы одного из соединений изобретения в другую функциональную группу;
(ii) введение новой функциональной группы в одно из соединений изобретения;
(iii) удаление каких-либо защитных групп;
(iv) в случае соединений изобретения в форме отдельного энантиомера разделение рацемического соединения изобретения на отдельные энантиомеры;
(v) получение их фармацевтически приемлемой соли и/или
(vi) получение их кристаллической формы.
Текст
N-СОДЕРЖАЩИЕ БИЦИКЛИЧЕСКИЕ ПРОИЗВОДНЫЕ ДЛЯ ПРИМЕНЕНИЯ ПРИ ЛЕЧЕНИИ СОСТОЯНИЙ, СВЯЗАННЫХ С АНДРОГЕННЫМ РЕЦЕПТОРОМ Изобретение касается бициклических соединений формулы I Брэдбери Роберт Хью, Хейлс Нил Джеймс, Рейбоу Алфред Артур (GB) Веселицкая И.А., Пивницкая Н.Н.,Кузенкова Н.В., Веселицкий М.Б.,Каксис Р.А., Комарова О.М., Белоусов Ю.В. (RU) где переменные X1, X2, X3, кольцо A, R4, R5 и m определены в описании. Настоящее изобретение также относится к способам получения таких соединений, фармацевтическим композициям,содержащим их, и к их применению для изготовления лекарственного средства для применения для предотвращения или лечения состояний, связанных с андрогенным рецептором. 017144 Настоящее изобретение относится к новым бициклическим производным и, в частности, к бициклическим производным, которые выполняют функцию лигандов андрогенного рецептора (АР). Настоящее изобретение также относится к способам получения таких бициклических производных и новым промежуточным соединениям, используемым при их получении, к фармацевтическим композициям, содержащим такие бициклические производные, к применению таких бициклических производных при получении медикаментов и к применению таких бициклических производных для лечения состояний,связанных с андрогенным рецептором, таких как рак предстательной железы. Рак предстательной железы занимает второе место из самых распространенных причин смерти от рака среди мужчин в развитых странах. Четыре процента летальных исходов среди мужчин старше 55 лет могут быть приписаны раку предстательной железы. Хотя уровень смертности является относительно низким, в настоящее время наблюдается его ежегодный рост со скоростью около 14%. Доля мужчин,у которых можно будет ожидать диагностирование рака предстательной железы, в последние годы возросла на 30%, причем увеличение в значительной степени обусловлено лучшими диагностическими методами и общим увеличением возраста населения, а не каким-либо увеличением числа новых случаев заболевания (E.J. Small, D.M. Reese, Curr. Opinion. Oncology, 2000, 12, 265-272). Ранние стадии роста опухоли при раке предстательной железы являются андрогензависимыми. При условии, что опухоль ограничена непосредственно простатой, обычно можно использовать такие методы лечения, как удаление опухоли хирургическим путм, лучевая терапия и/или химиотерапия. В более запущенных случаях, в которых опухоль больше не ограничена простатой, а образует метастатические опухоли в других местах тела, опухоль можно лечить паллиативно, путем уменьшения уровней тестостерона в крови. Такого уменьшения уровней тестостерона в крови можно достичь с помощью хирургической кастрации (орхидэктомии) или медикаментозно путем лечения антиандрогенами (касодекс, ципротерон ацетат, флутамид), LH-RH-агонистами (золадекс, бусерелин), LH-RH-антагонистами (цетрореликс) или ингибиторами 5-редуктазы (финастерид). Поскольку хирургическая кастрация не оказывает влияния на надпочечный синтез андрогена, современные способы объединяют хирургическое и медикаментозное лечение. Такое лечение приносит только временный успех, так как после не более чем 2-летнего промежутка обычно наблюдается возобновление роста опухоли, и этот возобновлнный рост обычно не является гормонозависимым (L.J. Denis и K. Griffith, Seminars in Surg. Onc., 2000, 18, 52-74). Несмотря на обширное изучение этой темы в течение последних 50 лет, все еще нет ни одного эффективного способа лечения запущенных стадий рака предстательной железы. Для пациентов с запущенным раком предстательной железы 5-летняя выживаемость составляет ниже 15%. Есть доказательства, что андрогенный рецептор играет важную роль в развитии и росте раковой опухоли предстательной железы не только на ранних гормонозависимых стадиях, но также и на запущенных гормононезависимых стадиях. Андрогенный рецептор относится к семейству рецепторов стероидных гормонов, которые действуют в качестве факторов транскрипции. Присоединение андрогена к андрогенному рецептору приводит к стабилизации рецептора и его защите от протекания быстрого протеолитического расщепления. Комплекс андрогена и андрогенного рецептора транспортируется в ядра, где он регулирует экспрессию андроген-чувствительных генов путем присоединения к их андроген-ответным ДНК-элементам в промоторной области таких андроген-чувствительных генов (D.J. Lamb и др. Vitam. Horm. 2001, 62, 199-230). Исследование опухолей предстательной железы показывают, что в 30% запущенных случаях наблюдается амплификация локуса гена андрогенного рецептора; в других же случаях, в различных доменах андрогенного рецептора был найден ряд мутаций андрогенного рецептора, и это приводит к андрогенным рецепторам с измененными свойствами. Такие мутированные рецепторы могут иметь более высокое, чем нормальное, сродство к андрогенам, могут быть конститутивно активными, могут иметь измененное избирательное действие лиганда, приводящее к активации другими стероидными гормонами или даже антиандрогенами, могут активироваться путем взаимодействия с молекулами из других способствующих росту путей сигнальной трансдукции, могут изменять взаимодействие с другими кофакторами, или могут активировать другие целевые гены (J.P. Elo, Т. Visakorpi, Ann. Med. 2001, 33, 130141). Идентификация антиандрогенов, которые ингибировали бы не только исходную форму андрогенного рецептора, но также его мутированные формы, и посредством этого так изменили бы рецепторную молекулу, что она становилась нестабильной, будет очень полезной при лечении опухолей простаты на различных стадиях роста. Такие соединения могли бы ингибировать рецидив роста опухоли или, по крайней мере, удлинять временной промежуток до рецидива. В случае эстрогенных рецепторов такие лиганды, которые дестабилизируют рецептор и вызывают снижение содержания рецептора как in vitro,так и in vivo, уже были идентифицированы (S. Dauvois и др., Proc Natl. Acad. Sci. USA, 1992, 89, 4037-41;R.A. McClelland и др. Eur. J. Cancer, 1996, 32A, 413-416). Нестероидные антиандрогены были описаны в US 5411981 (фенилимидазолидиновые производные), в WO 97/00071 (в особенности замещенные фенилдиметилгидантоины и их имино- и тиопроизводные), в WO 00/37430 (фенилаланины, фенилгидантоины и фенилмочевины), в WO 01/58855 (аминопропанилиды) и в EP 1122242 (замещенные цианофенилпиперазины).-1 017144 В данной заявке описан ряд бициклических производных, способных индуцировать понижающую регуляцию андрогенного рецептора в клетках. Следовательно, в соответствии с первым аспектом настоящего изобретения обеспечивается применение соединения формулы (I) для лечения состояния, связанного с андрогенным рецепторомX3 выбирают из -N- и -C(R3)-; по меньшей мере один из X1, X2 и X3 не означает -N-; кольцо А выбирают из моно- или бициклического гетероциклического кольца и карбоциклического кольца;R1, R2 и R3 независимо выбирают из водорода, C1-6 алкила, C1-6 алкокси, C1-6 алкилтио, гало и циано,где алкильная цепь в R1, R2 и R3 необязательно замещена не более чем тремя галогенными группами;R4 выбирают из водорода, гидрокси, гало, циано, амино, N-C1-6 алкиламино, N,N-ди-C1-6 алкиламино,C1-6 алкила, C2-6 алкенила, C2-6 алкинила, C1-6 алкокси, C1-6 алкил-S(O)n-, где n означает целое число от 0 до 2, и C3-4 карбоциклического кольца, где алкильная, алкенильная или алкинильная цепь в пределах R4 может быть необязательно замещенной не более чем 5 группами, выбранными из циано, гало, амино, C1-6 алкокси, C1-4 алкоксиС 1-4 алкила и C1-6 алкилтио, и когда R4 включает алкильную цепь, эта цепь может быть перфторированной;R5 выбирают из оксо или группы -L1-J-L2-K,где L1 и L2 независимо выбирают из прямой связи, C1-6 алкилена, C2-6 алкенилена, C2-6 алкинилена, C1-6 алкилидена, где алкильная, алкенильная, алкинильная или алкилиденильная цепь в пределах L1 и L2 может быть необязательно замещенной не более чем 3 группами, выбранными из R7, и где L1 и L2 могут также быть выбраны из одной из следующих групп, или алкильной, алкенильной, алкинильной или алкилиденильной цепи, в которую введена одна из следующих групп, причем вышеупомянутые группы независимо выбраны из -O-, -C(O)-, -C(O)-O-, -O-C(O)-, -N(R6)-, -N(R6)-C(O)-; -C(O)-N(R6)-, -N(R6)-C(O)O-, -O-C(O)-N(R6)-, -C(O)-N(R6)-O-; -O-N(R6)-C(O)-, -N(R6)-C(O)-N(R6)-, -S(O)0-2-, -O-S(O2)-, S-(O2)-O-,-N(R6)-S(O)2- и -S(O)2-N(R6)-;J выбирают из прямой связи, C1-4 алкилена, арила, гетероциклила и гетероарила, где J необязательно замещен не более чем пятью группами, выбранными из R8;K выбирают из C1-6 алкила, C2-6 алкенила, C2-6 алкинила, карбоциклического кольца, арила, гетероциклила и гетероарила, где K необязательно замещен не более чем пятью группами, выбранными из R8;R6 выбирают из водорода и C1-6 алкила;R7 выбирают из гидрокси, карбокси, карбамоила, C1-6 алкила, C2-6 алкенила, C2-6 алкинила, C1-6 алкокси, C1-4 алкилоксиС 1-4 алкила, C1-6 алкоксикарбонила, C1-6 алкил-S(O)n-, где n означает целое число от 0 до 2, аминосульфонила, карбамоила, N-C1-4 алкиламино, N,N-ди-C1-4 алкиламино, N-C1-4 алкиламинокарбонила, N,N-ди-C1-4 алкиламинокарбонила, N-C1-4 алкиламиносульфонила, N,N-ди-C1-4 алкиламиносульфонила, оксо, C1-6 алкил(C1-6 алкокси)оксофосфинила, диС 1-6 алкилоксофосфинила, арила, карбоциклила, гетероциклила, гетероарила, где R7 необязательно замещена не более чем тремя группами, выбранными из гидрокси, гало, циано, C1-6 алкила, C1-6 алкокси и карбоциклического кольца, и N,N-ди-C1-4 алкиламиногруппа в пределах R7 необязательно циклизована с образованием кольца;R8 выбирают из гидрокси, оксо, циано, гало, нитро, гидрокси, карбокси, C1-6 алкила, C1-6 алкенила,C1-6 алкинила, C1-6 алкокси, C1-6 алкоксикарбонила, цианоС 1-6 алкокси, C1-6 алкенилокси, C1-6 алканоила, C1-4 алкоксикарбонила, C1-6 алкил-S(O)n-, где n означает целое число от 0 до 2, амино, C1-6 алкилсульфонилокси, карбамоила, аминосульфонила, N-C1-4 алкиламиносульфонила, N,N-ди-C1-4 алкиламиносульфонила, NC1-4 алкиламино, N,N-ди-C1-4 алкиламино, карбамоила, N-C1-4 алкиламинокарбонила, N,N-ди-C1-4 алкиламинокарбонила, арила, карбоциклила, гетероциклила и гетероарила, где алкильная цепь или кольцо в R8 необязательно замещена(о) не более чем пятью группами, выбранными из гало, амино, гидрокси, карбокси, C1-4 алкокси, N-C1-4 алкиламино, N,N-ди-C1-4 алкиламино, карбамоила, N-C1-4 алкиламинокарбонила,N,N-ди-C1-4 алкиламинокарбонила и оксо, и N,N-ди-C1-4 алкиламиногруппа в пределах R8 необязательно циклизована с образованием кольца; иm означает целое число от 1 до 4; или его фармацевтически приемлемой соли. В соответствии со вторым аспектом настоящего изобретения обеспечивается применение соединения формулы (Ia) в качестве лекарственного средства где X1, X2, X3, кольцо A, R1, R2, R3, R4 и R5 принимают значения, определенные выше для соединения формулы (I) при условии, что(i) когда m означает 1, тогда (R5)m не может означать гидрокси, оксо или C1-6 алкил, и когда m означает 2, тогда (R5)m не может означать дигидрокси;(ii) -L1-J-L2-K не может означать трифторфенилпиперидин-1-ил, когда пиперидиновая группа замещена с помощью амино или C1-4 алкилкарбониламино;(iii) когда кольцо А означает пирролидин-1-ил, m означает 2 и (R5)m означает замещенный пиперидин-1-илкарбонил и замещенный фенил или замещенный пиперидин-1-илкарбонил и замещенный пиридил, то фенильное или пиридильное кольцо не может быть замещенным с помощью фтора, хлора, циано,трифторметила или метокси;(iv) когда кольцо А означает индолин и m означает 1, то R5 не может означать незамещенный или замещенный пирролидинилкарбонил, или незамещенный или замещенный пиперидинилкарбонил,или его фармацевтически приемлемой соли. В соответствии с третьим аспектом настоящего изобретения обеспечивается соединение формулы (Ib) где X1, X2, X3, кольцо A, R1, R2, R3, R4 и R5 принимают значения, определенные выше для соединения формулы (I) при условии, что(i) когда m означает 1, тогда (R5)m не может означать гидрокси, C1-6 алкил, оксо, ацетил, карбамоил,этоксикарбонил, метилсульфонил, метилсульфониламино, изопропиламинокарбонилметил или изобутиламинокарбонилметил, и когда m означает 2, (R5)m не может означать дигидрокси и не может означать циано и амино;(ii) когда R4 означает трифторметил или метил и кольцо А означает пиперазин-1-ил, замещенный по 4 положению с помощью фенила, бензила, фенетила, фенилсульфонила, фенилкарбонила или анилинокарбонила, то фенильное кольцо не может быть незамещенным или замещенным с помощью 2-метила,2,3-диметила, 2,4-диметила, 2,6-диметила, 2-метокси, 4-метокси, 3-хлора, 4-хлора, 3-фтора, 4-фтора, 2,6 дифтора, 3-трифторметила, 2-нитро, 4-нитро или 2,3,5,6-тетрафтор-4-трифторметила;(iii) когда R4 означает трифторметил или метил и кольцо А означает пиперазинил, замещенный с помощью -L1-J-L2-K по 4 положению, и m означает 1, то -L1-J-L2-K не может означать незамещенный карбамоилбензил, -фенилбензил, незамещенный пирролидин-1-илкарбонил, незамещенный морфолинокарбонилметил, незамещенный тиен-3-илметил, незамещенный тиазол-2-ил, незамещенный пиридин 2-ил, незамещенный пиридин-4-илметил, незамещенный пиразин-2-ил, незамещенный пиримидин-2-ил,незамещенный тетразоло[1,5-b]пиридазин-6-ил, незамещенный хинолин-8-илметил, незамещенный 1,3 бензодиоксол-5-илметил, 2,6-дифторфенилсульфонил, 5-хлортиен-2-илсульфонил, 2-метилтиазол-4 илметил, 2-(4-метоксифенил)тиазол-4-илметил;(iv) -L1-J-L2-K не может означать трифторфенилпиперидин-1-ил, когда пиперидиновая группа замещена с помощью амино или C1-4 алкилкарбониламино; и(v) когда кольцо A означает пирролидин-1-ил, m означает 2 и (R5)m означает замещенный пиперидин-1-илкарбонил и замещенный фенил или замещенный пиперидин-1-илкарбонил и замещенный пиридил, то фенильное или пиридильное кольцо не может быть замещенным с помощью фтора, хлор, циано,трифторметила или метокси;(vi) когда кольцо A означает индолин и m означает 1, то R5 не может быть незамещенным или замещенным пирролидинилкарбонилом или незамещенным или замещенным пиперидинилкарбонилом;(vii) когда R означает трифторметил или метил и кольцо A означает пиперидинил, замещенный с помощью -L1-J-L2-K по 4 положению, и m означает 1, то -L1-J-L2-K не может быть моно- или дизамещенным карбамоилом;(viii) перечисленные ниже соединения исключены 6-[2-(2,4-диметоксифенил)-1-пирролидинил]-3-(трифторметил)-1,2,4-триазоло[4,3-b]пиридазин;N-циклопентил-N-метил-1-(3-метил-1,2,4-триазоло[4,3-b]пиридазин-6-ил)-4-пиперидинамин; 6-[4-(2-бензоксазол)-1-пиперидинил]-3-(трифторметил)-1,2,4-триазоло[4,3-b]пиридазин; 6-(3-фенилпиролидин-1-ил)-1,2,4-триазоло[4,3-b]пиридазин и 1-2,3-дигидро-1-(3-метил-1,2,4-триазоло[4,3-b]пиридазин-6-ил)-1H-индол-2-ил]карбонил]-3 метилпиперидин; или его соли. В то время как фармацевтически приемлемые соли соединений изобретения являются предпочтительными, другие соли соединений изобретения, не являющиеся фармацевтически приемлемыми, могут быть также полезными, например, при получении фармацевтически приемлемых солей соединений изобретения. Следует понимать, что поскольку некоторые из определенных выше соединений формулы (I) могут существовать в виде оптически активной или рацемической формы благодаря наличию одного или нескольких асимметричных атомов углерода, изобретение включает в свое определение любые такие оптически активные или рацемические формы, которые обладают вышеупомянутой активностью. Синтез оптически активных форм можно провести с помощью стандартных приемов органической химии, хорошо известных в уровне техники, например путем синтеза из оптически активных исходных веществ или путем разделения рацемической формы. Подобным образом вышеупомянутая активность может быть оценена с использованием стандартных лабораторных приемов, упомянутых ниже. Примеры пригодных способов разделения энантиомеров рацемического соединения включают хроматографию с использованием пригодной хиральной неподвижной фазы; или превращение рацемической смеси в диастереоизомерные производные, разделение смеси диастереоизомерных производных на два одиночных диастереомера и регенерацию отдельного одиночного энантиомера из каждого отдельного одиночного диастереоизомера. Примеры пригодных способов разделения смеси диастереомеров включают фракционную кристаллизацию, нормально-фазовую хроматографию или хроматографию с обращенной фазой. Следует понимать, что некоторые из определенных выше соединений формулы (I) могут демонстрировать явление таутомерии. В частности, таутомерия может затрагивать любые гетероциклические группы, которые несут 1 или 2 оксо-заместителя. Следует понимать, что настоящее изобретение включает в себя определения всех таких таутомерных форм или их смеси, которые обладают вышеупомянутой активностью и не ограничены только какой-либо одной таутомерной формой, использованной в рамках графических изображений формул или названой в примерах. Следует понимать, что некоторые из определенных выше соединений (I) могут существовать в несольватированных формах, так же как в сольватированных формах, таких как, например, гидратированные формы. Следует понимать, что настоящее изобретение охватывает все такие сольватированные формы, которые обладают лигандной активностью к андрогенному рецептору. Также следует понимать, что определенные соединения формулы (I) могут демонстрировать полиморфизм и что настоящее изобретение охватывает все такие формы, которые обладают лигандной активностью к андрогенному рецептору. В данном описании изобретения родовой термин "алкил", если специально не указано иное, включает алкильные группы и с неразветвленной, и с разветвленной цепью, такие как пропил, изопропил и трет-бутил. Однако указания на индивидуальные алкильные группы, такие как "пропил", являются специфическими исключительно для варианта с неразветвленной цепью, а указания на индивидуальные алкильные группы с разветвленной цепью, такие как "изопропил", являются специфическими исключительно для варианта с разветвленной цепью. Это же правило, если не указано иное, также применяют к родовым терминам "алкенил" и "алкинил". Под термином "фторС 1-6 алкил" следует понимать насыщенную углеродную цепь длиной 1-6 атомов углерода, которая может являться разветвленной или неразветвленной, где по меньшей мере один из атомов водорода замещен фтором. Например, фторС 1-6 алкил включает, но не ограничивается перечисленным, фторметил, фторэтил, фторпропил, фторизопропил, фторбутил, фторизобутил, фтор-трет-бутил,фторпентил, фторизопентил, фторгексил, фторизогексил, трифторметил, пентафторэтил, гептафторпропил, нонафторбутил, ундекафторпентил и тридекафторгексил. Термин "фторС 1-4 алкил" должен толковаться соответственно. Под термином "C1-6 алкокси" следует понимать насыщенную углеродную цепь длиной 1-6 атомов-4 017144 углерода, которая может являться разветвленной или неразветвленной, присоединенную к кислороду. Например, C1-6 алкокси включает, но не ограничивается перечисленным, метокси, этокси, пропокси, бутокси, пентокси и гексокси. Под термином "C2-6 алканоил" следует понимать насыщенную углеродную цепь длиной 1-5 атомов углерода, которая может являться разветвленной или неразветвленной, присоединенную к карбонилу. Например, C2-6 алканоил включает, но не ограничивается перечисленным, этаноил, пропаноил, бутаноил,пентаноил и гексаноил. Под термином "C1-6 алкоксиС 1-6 алкил" следует понимать насыщенную углеродную цепь длиной 1-6 атомов углерода, которая может являться разветвленной или неразветвленной, присоединенную через кислород к другой насыщенной углеродной цепи длиной 1-6 атомов углерода, которая может являться разветвленной или неразветвленной. Например, C1-6 алкоксиС 1-6 алкил включает, но не ограничивается перечисленным, метоксиэтил, метоксипропил, этоксипропил, пропоксиэтил и бутоксипропил. Под термином "гидроксиС 1-6 алкил" следует понимать насыщенную углеродную цепь длиной 1-6 атомов углерода, которая может являться разветвленной или неразветвленной, содержащую одну единственную гидроксильную группу. Например гидроксиС 1-6 алкил включает, но не ограничивается перечисленным, гидроксиметил, гидроксиэтил, 2-гидроксипропил, 3-гидроксипропил, 1-гидроксиизопропил, 4 гидроксибутил, гидроксипентил, гидроксигексил и гидроксиизогексил. Под термином "C1-6 алкилсульфанил" следует понимать насыщенную углеродную цепь длиной 1-6 атомов углерода, которая может являться разветвленной или неразветвленной, присоединенную к сере. Например, C1-6 алкилсульфанил включает, но не ограничивается перечисленным, метилсульфанил, этилсульфанил, пропилсульфанил, изопропилсульфанил, бутилсульфанил, изобутилсульфанил, третбутилсульфанил, пентилсульфанил и гексилсульфанил. Под термином "C1-6 алкилсульфинил" следует понимать насыщенную углеродную цепь длиной 1-6 атомов углерода, которая может являться разветвленной или неразветвленной, присоединенную к сульфоксиду. Например, C1-6 алкилсульфинил включает, но не ограничивается перечисленным, метилсульфинил, этилсульфинил, пропилсульфинил, изопропилсульфинил, бутилсульфинил, изобутилсульфинил,трет-бутилсульфинил, пентилсульфинил и гексилсульфинил. Под термином "C1-6 алкилсульфонил" следует понимать насыщенную углеродную цепь длиной 1-6 атомов углерода, которая может являться разветвленной или неразветвленной, присоединенную к диоксиду серы. Например, C1-6 алкилсульфонил включает, но не ограничивается перечисленным, метилсульфонил, этилсульфонил, пропилсульфонил, изопропилсульфонил, бутилсульфонил, изобутилсульфонил,трет-бутилсульфонил, пентилсульфонил и гексилсульфонил. Под термином "N-C1-4 алкиламино" следует понимать насыщенную углеродную цепь длиной 1-4 атомов углерода, которая может являться разветвленной или неразветвленной, присоединенную к вторичной аминогруппе. Например, N-C1-4 алкиламино включает, но не ограничивается перечисленным, метиламино, этиламино, пропиламино и бутиламино. Под термином "N,N-ди-C1-4 алкиламино" следует понимать насыщенную углеродную цепь длиной 1-4 атомов углерода, которая может являться разветвленной или неразветвленной, присоединенную к третичной аминогруппе, которая, в свою очередь, присоединена к дополнительной насыщенной углеродной цепи такой же длины. Например, "N,N-ди-C1-4 алкиламино" включает, но не ограничивается перечисленным, N,N-диметиламино, N,N-диэтиламино, N,N-дипропиламино и N,N-дибутиламино. Термин алкилиден используется для обозначения алкилиденовой цепи, которая может находиться в любой из двух ориентации в молекуле, так, например, если L1 означает пропилиден, то этот фрагмент покроется двумя следующими структурами: Термин "гало" используется здесь для обозначения фтора, хлора, брома и йода. Под термином "галоС 1-4 алкил" следует понимать насыщенную углеродную цепь длиной 1-4 атомов углерода, которая может являться разветвленной или неразветвленной, и где по меньшей мере один из атомов водорода замещен атомом галогена. Например, галоС 1-4 алкил включает, но не ограничивается перечисленным, дифторметил, трифторметил, хлор(дифтор)метил, дифторэтил и дифторпропил. Термин "арил" относится к фенилу или нафтилу. Термин "карбамоил" относится к группе -C(O)NH2. Если не определено иначе, термин "гетероарил" относится к 4-10-членному ароматическому моноили бициклическому кольцу, содержащему до 5 гетероатомов, независимо выбранных из азота, кислоро-5 017144 да или серы, присоединенному через атом углерода кольца или через атом азота кольца, если разрешена такая связь от азота, например не возможна связь к азоту пиридинового кольца, но возможна связь через 1-азот пиразольного кольца. В одном варианте осуществления термин "гетероарил" относится к 5-10 членному ароматическому моно- или бициклическому кольцу, содержащему до 5 гетероатомов, независимо выбранных из азота, кислорода или серы, присоединенному через атомы углерода кольца или атомы азота кольца, если разрешена такая связь от азота, например не возможна связь к азоту пиридинового кольца, но возможна связь через 1-азот пиразольного кольца. В другом варианте осуществления термин"гетероарил" относится к 5- или 6-членному ароматическому моноциклическому кольцу, содержащему до 4 гетероатомов, независимо выбранных из азота, кислорода или серы, присоединенному через атомы углерода кольца или атомы азота кольца, если разрешена такая связь от азота, например не возможна связь к азоту пиридинового кольца, но возможна связь через 1-азот пиразольного кольца. Примеры 5 или 6-членных гетероарильных колец включают пиррол, фуран, имидазол, триазол, тетразол, пиразин,пиразол, пиримидин, пиридазин, пиридин, пиррол, изоксазол, оксазол, 1,2,4-оксадиазол, изотиазол, тиазол, тиадиазол, 1,2,4-триазол и тиофен. Примеры 5/6 и 6/6 бициклических кольцевых систем включают бензофуран, бензимидазол, бензтиофен, бензтиазол, бензизотиазол, бензоксазол, бензизоксазол, 1,3 бензодиоксол, индол, пиридоимидазол, пиримидоимидазол, хинолин, изохинолин, хиноксалин, хиназолин, фталазин, циннолинин, нафтиридин. Это определение дополнительно включает серосодержащие кольца, где атом серы окислен до S(O)- или S(O2)-группы. Если не определено иначе, термин "гетероциклил" относится к 4-10-членному насыщенному или частично насыщенному моно- или бициклическому кольцу, содержащему до 5 гетероатомов, выбранных их азота, кислорода или серы, присоединенному через атомы углерода кольца или атомы азота кольца. Примеры гетероциклила включают тетрагидрофуранил, 2,3-дигидро-4H-пиранил, тетрагидро-2Hпиранил, пирролинил, пирролидинил, 1,3-тиазолидин, морфолинил, оксетанил, пиперидинил, пиперазинил, дигидропиридинил, дигидропиримидинил и азепан. Заслуживающие особого внимания примеры гетероциклила включают пирролинил, пирролидинил, морфолинил, пиперидинил, пиперазинил, дигидропиридинил и дигидропиримидинил. Это определение дополнительно включает серосодержащие кольца, где атом серы окислен до S(O)- или S(O2)-группы. Термин "карбоциклил" или "карбоциклическое кольцо" относится к полностью насыщенному или частично насыщенному моно-, бициклическому 3-10 членному углеродному кольцу. Примерами карбоциклических колец являются циклопропил, циклобутил, циклопентил, циклогексил, бицикло[4,2,0]октан или 2,3-дигидроинден. Заслуживающие особого внимания новые соединения изобретения включают, например, соединения формулы (I) или их фармацевтически приемлемые соли, где, если не указано иное, каждое из переменных R1, R2, R3, R4, R5, R6, R7,R8, A, J, K, L1, L2 и m принимает любое из значений, определенных выше или в пп.(1)-(56) ниже выбирают из одного из следующих:(7) в другом варианте осуществления кольцо A выбирают из тетрагидрофуранила, тетрагидропиранила и 5,6-дигидро-2H-пиранила;(11) кольцо А выбирают из пиперазинила и 3,3a,4,6,6a-гексагидропирроло[3,4-c]пирролила;(15) R1 выбирают из метила и этила;(16) R1 выбирают из водорода и метила;(17) R2 выбирают из водорода и метила;(18) R3 выбирают из водорода и метила;(20) R4 выбирают из гало, C1-6 алкила, необязательно замещенного не более чем 5 галогенными заместителями, C1-6 алкилS(O)n-, где n означает целое число от 0 до 2, и амино;(21) R4 выбирают из гало, C1-4 алкила, необязательно замещенного не более чем 5 галогенными заместителями, C1-4 алкилтио и амино;(28) L1 и L2 независимо выбирают из прямой связи, C1-6 алкилена, где алкильная цепь в пределах L1 2 и L может быть необязательно замещенной не более чем 3 группами, выбранными из R7, и где L1 и L2 могут также быть выбраны из одной из следующих групп или алкильной цепи, в которую введена одна из следующих групп, причем вышеупомянутые группы независимо выбраны из -O-, -C(O)-, -C(O)-O-, -OC(O)-, -N(R6)-, -N(R6)-C(O)-; -C(O)-N(R6)-, -N(R6)-C(O)-O, -O-C(O)-N(R6)-, -C(O)-N(R6)-O-; -O-N(R6)C(O)-, -N(R6)-C(O)-N(R6)-, -S(O)0-2-, -O-S(O2)-, S-(O2)-O-, -N(R6)-S(O)2- и -S(O)2-N(R6)-;(29) L1 и L2 независимо выбирают из прямой связи, C1-6 алкилена, где алкильная цепь в пределах L1 2 и L может быть необязательно замещенной не более чем 3 группами, выбранными из R7, и где L1 и L2 могут также быть выбраны из одной из следующих групп или алкильной цепи, в которую введена одна из следующих групп, причем вышеупомянутые группы независимо выбраны из -O-, -C(O)- и -S(O)0-2-;(30) L1 и L2 независимо выбирают из прямой связи, C1-4 алкилена, -O-, -C(O)-, -ОС(О)-, -C(O)О-,6-N(R )-, -N(R6)C(O)-, -C(O)N(R6)-, -N(R6)C(O)O-, -S(O)n-, где n означает целое число от 0 до 2, -OS(O)2-,-S(O)2N(R5)- и -N(R5)S(O)2-;(31) L1 и L2 независимо выбирают из прямой связи, C1-4 алкилена, -O-, -C(O)-, -C(O)О-, -N(R6)-,6(32) L1 и L2 независимо выбирают из прямой связи, C1-2 алкилена, -O-, -S(O)2N(R6)- и -N(R6)S(O)2-;(33) L1 независимо выбирают из прямой связи, C1-2 алкилена, -O-, -S(O)2N(R6)- и -N(R6)S(O)2-, и L2 означает прямую связь;(34) L1 выбирают из прямой связи, C1-4 алкилена, -C(O)-, -C(O)О-, -C(O)N(R6)-, -S(O)2- и -S(O)2N(R6)-;(35) L2 выбирают из прямой связи, -O-, -C(O)О-, -N(R6)-, -N(R6)C(O)-, -C(O)N(R6)-, -N(R6)C(O)O-,-S-, -S(O)2-, -OS(O)2-, -(R6)S(O)2-;(37) J выбирают из прямой связи, арильного и гетероарильного кольца, где J необязательно замещен не более чем пятью группами, выбранными из R8;(38) J выбирают из прямой связи, фенила, имидазолила и пиридила;(40) K выбирают из арильного и гетероарильного кольца, где K необязательно замещен не более чем пятью группами, выбранными из R8;(44) R6 выбирают из водорода и C1-4 алкила;(48) R8 выбирают из оксо, циано, гало, C1-6 алкила, C1-6 алкокси, C1-6 алкоксикарбонила, C1-6 алкилS(O)n-, где n означает целое число от 0 до 2, C1-6 алкилсульфонилокси, карбамоила, аминосульфонила, NC1-4 алкиламиносульфонила, N,N-ди-C1-4 алкиламиносульфонила, N-C1-4 алкиламинокарбонила, N,N-ди-C1-4 алкиламинокарбонила, арила, карбоциклила, гетероциклила и гетероарила, где алкильная цепь или кольцо в R8 необязательно замещена(о) не более чем пятью группами, выбранными из гало, карбокси, C1-4 алкокси, N,N-ди-C1-4 алкиламино, карбамоила, N-C1-4 алкиламинокарбонила, N,N-ди-C1-4 алкиламинокарбонила и оксо, и N,N-ди-C1-4 алкиламиногруппа в пределах R8 необязательно циклизована с образованием кольца;(49) R8 выбирают из C1-6 алкила, C1-6 алкенила, C1-6 алкинила, C1-6 алкокси, C1-6 алкоксикарбонила, гидрокси, карбамоила, циано, гало, нитро, амино, N-C1-4 алкиламино, N,N-диС 1-4 алкиламино и оксо, где алкильная цепь в R8 необязательно замещена не более чем 5 галогенными группами;(50) R8 выбирают из C1-6 алкила, C1-6 алкенила, C1-6 алкинила, C1-6 алкокси, C1-6 алкоксикарбонила, гидрокси, карбамоила, циано, гало, нитро, амино, N,N-диС 1-4 алкиламино и оксо, где алкильная цепь в R8 необязательно замещена не более чем 5 галогенными группами;(52) m означает целое число от 0 до 3;(56) m означает 4. Заслуживающие особого внимания новые соединения изобретения включают любое одно из следующих соединений: 6-[4-(4-нитрофенил)пиперазин-1-ил]-3-(трифторметил)-[1,2,4]триазоло[4,3-b]пиридазин,6-[4-[(3-бромфенил)метил]пиперазин-1-ил]-3-(трифторметил)-[1,2,4]триазоло[4,3-b]пиридазин,6-[4-(нафталин-1-илметил)пиперазин-1-ил]-3-(трифторметил)-[1,2,4]триазоло[4,3-b]пиридазин,6-[4-[(3-хлорфенил)метил]пиперазин-1-ил]-3-(трифторметил)-[1,2,4]триазоло[4,3-b]пиридазин,6-[4-[3-хлор-5-(трифторметил)пиридин-2-ил]-1,4-диазепан-1-ил]-3-(трифторметил)-[1,2,4]триазоло[4,3-b]пиридазин,6-(4-фенетилпиперазин-1-ил)-3-(трифторметил)-[1,2,4]триазоло[4,3-b]пиридазин,6-[4-(1-бензотиофен-3-илметил)пиперазин-1-ил]-3-(трифторметил)-[1,2,4]триазоло[4,3-b]пиридазин,3-(трифторметил)-6-[4-3-(трифторметил)фенил]метил]пиперазин-1-ил]-[1,2,4]триазоло[4,3-a]пиридин,6-[4-(3,5-дихлорпиридин-4-ил)пиперазин-1-ил]-3-(трифторметил)-[1,2,4]триазоло[4,3-b]пиридазин,4-5-[3-(трифторметил)-[1,2,4]триазоло[4,3-b]пиридазин-6-ил]-1,3,3a,4,6,6a-гексагидропирроло[3,4 с]пиррол-2-ил]метил]бензонитрил,3-(трифторметил)-6-[4-3-(трифторметил)фенил]метил]-1,4-диазепан-1-ил]-[1,2,4]триазоло[4,3-b] пиридазин,4-4-[3-(трифторметил)-[1,2,4]триазоло[4,3-b]пиридазин-6-ил]-1,4-диазепан-1-ил]метил]бензонитрил,6-[4-[(4-хлорфенил)метил]пиперазин-1-ил]-3-(трифторметил)-[1,2,4]триазоло[4,3-b]пиридазин,3-4-[3-(трифторметил)-[1,2,4]триазоло[4,3-b]пиридазин-6-ил]-1,4-диазепан-1-ил]метил]бензонитрил,6-[4-(тиофен-2-илметил)пиперазин-1-ил]-3-(трифторметил)-[1,2,4]триазоло[4,3-b]пиридазин,3-(трифторметил)-6-[4-3-(трифторметил)фенил]метил]пиперазин-1-ил]-[1,2,4]триазоло[4,3-b]пиридазин,6-[4-[(3-хлорфенил)метил]-1,4-диазепан-1-ил]-3-(трифторметил)-[1,2,4]триазоло[4,3-b]пиридазин,6-[4-[(2-хлорфенил)метил]-1,4-диазепан-1-ил]-3-(трифторметил)-[1,2,4]триазоло[4,3-b]пиридазин,6-[4-(1H-индол-6-илметил)пиперазин-1-ил]-3-(трифторметил)-[1,2,4]триазоло[4,3-b]пиридазин,6-[4-[(2,2-дифтор-1,3-бензодиоксол-4-ил)метил]пиперазин-1-ил]-3-(трифторметил)-[1,2,4]триазоло[4,3-b]пиридазин,6-[4-[(2-хлорфенил)метил]пиперазин-1-ил]-3-(трифторметил)-[1,2,4]триазоло[4,3-b]пиридазин,5-4-[3-(трифторметил)-[1,2,4]триазоло[4,3-b]пиридазин-6-ил]пиперазин-1-ил]метил]изохинолин,6-[4-[(4-нитрофенил)метил]пиперазин-1-ил]-3-(трифторметил)-[1,2,4]триазоло[4,3-b]пиридазин,6-[4-[(4-фторфенил)метил]-1,4-диазепан-1-ил]-3-(трифторметил)-[1,2,4]триазоло[4,3-b]пиридазин,6-[4-(2,6-диметилфенил)пиперазин-1-ил]-3-(трифторметил)-[1,2,4]триазоло[4,3-b]пиридазин,6-[4-[(4-хлорфенил)метил]пиперазин-1-ил]-3-(трифторметил)-[1,2,4]триазоло[4,3-a]пиридин,6-[4-[(3-фторфенил)метил]-1,4-диазепан-1-ил]-3-(трифторметил)-[1,2,4]триазоло[4,3-b]пиридазин,-8 017144 3-5-[3-(трифторметил)-[1,2,4]триазоло[4,3-b]пиридазин-6-ил]-1,3,3a,4,6,6a-гексагидропирроло[3,4c]пиррол-2-ил]метил]бензонитрил,6-[4-[(4-хлорфенил)метил]-1,4-диазепан-1-ил]-3-(трифторметил)-[1,2,4]триазоло[4,3-b]пиридазин,6-[4-[(3-фторфенил)метил]пиперазин-1-ил]-3-(трифторметил)-[1,2,4]триазоло[4,3-b]пиридазин,6-[4-[(3-метилфенил)метил]-1,4-диазепан-1-ил]-3-(трифторметил)-[1,2,4]триазоло[4,3-b]пиридазин,6-[4-[(2-фторфенил)метил]-1,4-диазепан-1-ил]-3-(трифторметил)-[1,2,4]триазоло[4,3-b]пиридазин,6-[4-(1H-индол-3-илметил)пиперазин-1-ил]-3-(трифторметил)-[1,2,4]триазоло[4,3-b]пиридазин,6-[4-[(4-метилсульфонилфенил)метил]-1,4-диазепан-1-ил]-3-(трифторметил)-[1,2,4]триазоло[4,3b]пиридазин,3-(трифторметил)-6-[4-[(2-(трифторметил)фенил]метил]-1,4-диазепан-1-ил]-[1,2,4]триазоло[4,3b]пиридазин,6-[4-(3-метилфенил)пиперазин-1-ил]-3-(трифторметил)-[1,2,4]триазоло[4,3-b]пиридазин,6-[4-[(4-метилсульфанилфенил)метил]пиперазин-1-ил]-3-(трифторметил)-[1,2,4]триазоло[4,3b]пиридазин,6-[4-3-(дифторметокси)фенил]метил]пиперазин-1-ил]-3-(трифторметил)-[1,2,4]триазоло[4,3b]пиридазин,6-[4-[(4,5-диметилфуран-2-ил)метил]пиперазин-1-ил]-3-(трифторметил)-[1,2,4]триазоло[4,3b]пиридазин,6-[4-[фенил-[4-(трифторметил)фенил]метил]пиперазин-1-ил]-3-(трифторметил)-[1,2,4]триазоло[4,3b]пиридазин,3-4-[3-(трифторметил)-[1,2,4]триазоло[4,3-b]пиридазин-6-ил]пиперазин-1-ил]метил]бензонитрил,3-(трифторметил)-6-[4-2-(трифторметил)фенил]метил]пиперазин-1-ил]-[1,2,4]триазоло[4,3b]пиридазин,6-[4-[(2-фторфенил)метил]пиперазин-1-ил]-3-(трифторметил)-[1,2,4]триазоло[4,3-b]пиридазин,4-4-[3-(трифторметил)-[1,2,4]триазоло[4,3-b]пиридазин-6-ил]пиперазин-1-ил]метил]бензонитрил,6-[4-[(4-метоксифенил)-фенилметил]пиперазин-1-ил]-3-(трифторметил)-[1,2,4]триазоло[4,3b]пиридазин,6-[4-[(3-фторфенил)метил]пиперазин-1-ил]-3-(трифторметил)-[1,2,4]триазоло[4,3-a]пиридин,3-(трифторметил)-6-[4-3-(трифторметилсульфанил)фенил]метил]пиперазин-1-ил][1,2,4]триазоло[4,3-b]пиридазин,6-[4-[(4-фторфенил)метил]пиперазин-1-ил]-3-(трифторметил)-[1,2,4]триазоло[4,3-b]пиридазин,6-[4-[4,4-бис(4-фторфенил)бутил]пиперазин-1-ил]-3-(трифторметил)-[1,2,4]триазоло[4,3b]пиридазин,6-[2-[(3-хлорфенил)метил]-1,3,3a,4,6,6a-гексагидропирроло[3,4-c]пиррол-5-ил]-3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин,или их фармацевтически приемлемых солей. В соответствии с четвертым аспектом настоящего изобретения обеспечивается соединение формулы (Ic) или его фармацевтически приемлемая соль для применения в качестве лекарственного средстваR14, одинаково или по-разному в каждом случае, означает водород или метил;R9 и R10 , одинаково или по-разному в каждом случае, означают водород или метил;J означает арил; полностью насыщенное моноциклическое 3-6-членное карбоциклическое кольцо; моноциклическое 4-, 5-, 6- или 7-членное гетероциклическое кольцо, которое включает 1, 2, 3 или 4 гетероатома, независимо выбранных из O, N или S; моноциклическое 5- или 6-членное гетероарильное кольцо, которое включает 1, 2, 3 или 4 гетероатома, независимо выбранных из O, N или S; или бициклическую 9- или 10-членную гетероарильную кольцевую систему, которая включает 1, 2, 3, 4 или 5 гетероатомов, независимо выбранных из O, N или S;R11 означает водород или метил;R12 означает гало, C1-6 алкил, C2-6 алкенил, C2-6 алкинил, карбокси, C1-6 алкокси, циано, оксо, фторС 1-6 алкил, гидрокси, амино, N-C1-4 алкиламино или N,N-ди-C1-4 алкиламино; арил, где арильное кольцо необязательно замещено 1, 2 или 3 заместителями, выбранными из R13; моноциклическое 5- или 6-членное гетероарильное кольцо, которое включает 1, 2, 3 или 4 гетероатома, независимо выбранных из O, N или S, и которое является необязательно замещенным 1, 2 или 3 заместителями, выбранными из R13; или моноциклическое 4-, 5-, 6- или 7-членное гетероциклическое кольцо, которое включает 1, 2, 3 или 4 гетероатома, независимо выбранных из O, N или S, и которое является необязательно замещенным 1, 2 или 3 заместителями, выбранными из R13;R14 и R15 независимо означают водород или метил; иr означает 0, 1, 2 или 3. В соответствии с пятым аспектом настоящего изобретения обеспечивается соединение формулы(Ic) или его фармацевтически приемлемая соль для применения при лечении рака предстательной железыR14, одинаково или по-разному в каждом случае, означает водород или метил;R9 и R10, одинаково или по-разному в каждом случае, означают водород или метил;J означает арил; полностью насыщенное моноциклическое 3-6-членное карбоциклическое кольцо; моноциклическое 4-, 5-, 6- или 7-членное гетероциклическое кольцо, которое включает 1, 2, 3 или 4 гетероатома, независимо выбранных из O, N или S; моноциклическое 5- или 6-членное гетероарильное кольцо, содержащее 1, 2, 3 или 4 гетероатома, независимо выбранных из O, N или S; или бициклическую 9 или 10-членную гетероарильную кольцевую систему, содержащую 1, 2, 3, 4 или 5 гетероатомов, независимо выбранных из O, N или S;R11 означает водород или метил;R12 означает гало, C1-4 алкил, C2-6 алкенил, C2-6 алкинил, карбокси, C1-6 алкокси, циано, оксо, фторС 1-6 алкил, гидрокси, амино, N-C1-4 алкиламино или N,N-ди-C1-4 алкиламино; арил, где арильное кольцо необязательно замещено 1, 2 или 3 заместителями, выбранными из R13; моноциклическое 5- или 6-членное гетероарильное кольцо, которое включает 1, 2, 3 или 4 гетероатома, независимо выбранных из O, N илиS, и которое является необязательно замещенным 1, 2 или 3 заместителями, выбранными из R13; или моноциклическое 4-, 5-, 6- или 7-членное гетероциклическое кольцо, которое включает 1, 2, 3 или 4 гетероатома, независимо выбранных из O, N или S, и которое является необязательно замещенным 1, 2 или 3 заместителями, выбранными из R13;R14 и R15 независимо означают водород или метил; иr означает 0, 1, 2 или 3. В соответствии с шестым аспектом настоящего изобретения обеспечивается соединение формулы(Ic) или его фармацевтически приемлемая сольR14, одинаково или по-разному в каждом случае, означает водород или метил;R9 и R10, одинаково или по-разному в каждом случае, означают водород или метил;J означает арил; полностью насыщенное моноциклическое 3-6-членное карбоциклическое кольцо; фуранил, имидазолил, изотиазолил, морфолинил, оксадиазолил, оксазолил, изоксазолил, оксетанил, тетрагидро-2H-пиранил, пиразолил, пиридазинил, пиридинил, пирролил или тиадиазолил; или бициклическую 9-членную гетероарильную кольцевую систему, которая включает 1 или 2 атома азота, 1 или 2 атома кислорода, 1 атом серы или 1 атом азота и 1 атом серы;R11 означает водород или метил;R12 означает гало, C1-6 алкил, C2-6 алкенил, C2-6 алкинил, карбокси, C1-6 алкокси, циано, оксо, фторС 1-6 алкил, гидрокси, амино, N-C1-4 алкиламино или N,N-ди-C1-4 алкиламино; арил, где арильное кольцо необязательно замещено 1, 2 или 3 заместителями, выбранными из R13; моноциклическое 5- или 6-членное гетероарильное кольцо, которое включает 1, 2, 3 или 4 гетероатома, независимо выбранных из O, N илиS, и которое является необязательно замещенным 1, 2 или 3 заместителями, выбранными из R13; или моноциклическое 4-, 5-, 6- или 7-членное гетероциклическое кольцо, которое включает 1, 2, 3 или 4 гетероатома, независимо выбранных из O, N или S, и которое является необязательно замещенным 1, 2 или 3 заместителями, выбранными из R13;R14 и R15 независимо означают водород или метил;r означает 0, когда J означает полностью насыщенное моноциклическое 3-6-членное карбоциклическое кольцо; иr означает 0, 1, 2 или 3, когда J означает фуранил, имидазолил, изотиазолил, морфолинил, оксадиазолил, оксазолил, изоксазолил, оксетанил, тетрагидро-2H-пиранил, пиразолил, пиридазинил, пиридинил,пирролил, тиадиазолил, или бициклическую 9-членную гетероарильную кольцевую систему, которая включает 1 или 2 атома азота, 1 или 2 атома кислорода, 1 атом серы или 1 атом азота и 1 атом серы; при условии, что соединение формулы (Ic) не представляет собой 4-4-[3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин-6-ил]пиперазин-1-илфенол; 6-[4-(пиридин-3-илметил)пиперазин-1-ил]-3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин; 6-[4-(2-фторбензил)пиперазин-1-ил]-3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин; 6-[4-(имидазо[1,2-a]пиридин-2-илметил)пиперазин-1-ил]-3-(трифторметил)[1,2,4]триазоло[4,3b]пиридазин; 6-[4-(3,4-диметоксибензил)пиперазин-1-ил]-3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин; 6-[4-(1H-индол-3-ил)пиперидин-1-ил]-3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин; 6-4-[2-(3,5-диметоксифенил)этил]пиперидин-1-ил-3-(трифторметил)[1,2,4]триазоло[4,3b]пиридазин; 6-[4-(4-метоксибензил)пиперазин-1-ил]-3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин; 6-[4-(3-хлорбензил)пиперазин-1-ил]-3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин; 6-[4-(4-хлорбензил)пиперазин-1-ил]-3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин; 6-[4-(2-метилбензил)пиперазин-1-ил]-3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин; 6-[4-(пиридин-4-илметил)пиперазин-1-ил]-3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин; 6-[4-(2,6-диметилфенил)пиперазин-1-ил]-3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин;- 11017144 6-[4-(4-метоксифенил)пиперазин-1-ил]-3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин; 6-[4-(3-хлорфенил)пиперазин-1-ил]-3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин; 6-[4-(4-фторфенил)пиперазин-1-ил]-3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин или 6-4-[(2,6-дифторфенил)сульфонил]пиперазин-1-ил-3-(трифторметил)[1,2,4]триазоло[4,3b]пиридазин. В соответствии с одним из вариантов осуществления шестого аспекта настоящего изобретения обеспечивается соединение формулы (Ic) или его фармацевтически приемлемая сольR14, одинаково или по-разному в каждом случае, означает водород или метил;R9 и R10, одинаково или по-разному в каждом случае, означают водород или метил;J означает арил; полностью насыщенное моноциклическое 3-6-членное карбоциклическое кольцо; имидазолил, изотиазолил, морфолинил, оксадиазолил, оксазолил, изоксазолил, оксетанил, тетрагидро 2H-пиранил, пиразолил, пиридазинил, пиридинил; или бициклическую 9-членную гетероарильную кольцевую систему, содержащую 1 или 2 атома азота или один единственный атом серы;R11 означает водород или метил;O, N или S, и которое является необязательно замещенным 1, 2 или 3 заместителями, выбранными из R13; или моноциклическое 4-, 5-, 6- или 7-членное гетероциклическое кольцо, которое включает 1, 2, 3 или 4 гетероатома, независимо выбранных из O, N или S, и которое является необязательно замещенным 1, 2 или 3 заместителями, выбранными из R13;R14 и R15 независимо означают водород или метил;r означает 0, когда J означает полностью насыщенное моноциклическое 3-6-членное карбоциклическое кольцо; иr означает 0, 1, 2 или 3, когда J означает имидазолил, изотиазолил, морфолинил, оксадиазолил, оксазолил, изоксазолил, оксетанил, тетрагидро-2H-пиранил, пиразолил, пиридазинил, пиридинил или бициклическую 9-членную гетероарильную кольцевую систему, содержащую 1 или 2 атома азота или один-единственный атом серы; при условии, что соединение формулы (Ic) не представляет собой 4-4-[3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин-6-ил]пиперазин-1-илфенол; 6-[4-(пиридин-3-илметил)пиперазин-1-ил]-3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин; 6-[4-(2-фторбензил)пиперазин-1-ил]-3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин; 6-[4-(имидазо[1,2-a]пиридин-2-илметил)пиперазин-1-ил]-3-(трифторметил)[1,2,4]триазоло[4,3b]пиридазин; 6-[4-(3,4-диметоксибензил)пиперазин-1-ил]-3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин; 6-[4-(1H-индол-3-ил)пиперидин-1-ил]-3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин; 6-4-[2-(3,5-диметоксифенил)этил]пиперидин-1-ил-3-(трифторметил)[1,2,4]триазоло[4,3b]пиридазин; 6-[4-(4-метоксибензил)пиперазин-1-ил]-3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин; 6-[4-(3-хлорбензил)пиперазин-1-ил]-3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин;- 12017144 6-[4-(4-хлорбензил)пиперазин-1-ил]-3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин; 6-[4-(2-метилбензил)пиперазин-1-ил]-3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин; 6-[4-(пиридин-4-илметил)пиперазин-1-ил]-3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин; 6-[4-(2,6-диметилфенил)пиперазин-1-ил]-3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин; 6-[4-(4-метоксифенил)пиперазин-1-ил]-3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин или 6-[4-(3-хлорфенил)пиперазин-1-ил]-3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин. В соответствии с дальнейшим вариантом осуществления шестого аспекта настоящего изобретения обеспечивается соединение формулы (If) или его фармацевтически приемлемая сольJ означает: арил; полностью насыщенное моноциклическое 3-6-членное карбоциклическое кольцо; фуранил, имидазолил, изотиазолил, морфолинил, оксадиазолил, оксазолил, изоксазолил, оксетанил, тетрагидро-2H-пиранил, пиразолил, пиридазинил, пиридинил, пирролил или тиадиазолил; или бициклическую 9-членную гетероарильную кольцевую систему, которая включает 1 или 2 атома азота, 1 или 2 атома кислорода, 1 атом серы или 1 атом азота и 1 атом серы;R9 и R10, одинаково или по-разному в каждом случае, означают водород или метил;R11 означает водород или метил;R12 означает гало, C1-6 алкил, C2-6 алкенил, С 2-6 алкинил, карбокси, C1-6 алкокси, фторС 1-6 алкил, гидрокси, амино, N-C1-4 алкиламино или N,N-ди-C1-4 алкиламино; арил, где арильное кольцо необязательно замещено 1, 2 или 3 заместителями, выбранными из R13; моноциклическое 5- или 6-членное гетероарильное кольцо, которое включает 1, 2, 3 или 4 гетероатома, независимо выбранных из O, N или S, и которое является необязательно замещенным 1, 2 или 3 заместителями, выбранными из R13; или моноциклическое 4-, 5-, 6- или 7-членное гетероциклическое кольцо, которое включает 1, 2, 3 или 4 гетероатома, независимо выбранных из O, N или S, и которое является необязательно замещенным 1, 2 или 3 заместителями, выбранными из R13;R14 и R15 независимо означают водород или метил;r означает 0, когда J означает полностью насыщенное моноциклическое 3-6-членное карбоциклическое кольцо; иr означает 0, 1, 2 или 3, когда J означает фуранил, имидазолил, изотиазолил, морфолинил, оксадиазолил, оксазолил, изоксазолил, оксетанил, тетрагидро-2H-пиранил, пиразолил, пиридазинил, пиридинил,пирролил, тиадиазолил, или бициклическую 9-членную гетероарильную кольцевую систему, которая включает 1 или 2 атома азота, 1 или 2 атома кислорода, 1 атом серы или 1 атом азота и 1 атом серы; при условии, что соединение формулы (If) не представляет собой 4-4-[3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин-6-ил]пиперазин-1-илфенол; 6-[4-(1H-индол-3-ил)пиперидин-1-ил]-3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин; 6-[4-(2,6-диметилфенил)пиперазин-1-ил]-3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин; 6-[4-(4-метоксифенил)пиперазин-1-ил]-3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин; 6-[4-(3-хлорфенил)пиперазин-1-ил]-3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин или 6-[4-(4-фторфенил)пиперазин-1-ил]-3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин. В соответствии с седьмым аспектом настоящего изобретения обеспечивается соединение формулы(Id) или его фармацевтически приемлемая сольR9 и R10, одинаково или по-разному в каждом случае, означают водород или метил;J означает арил; полностью насыщенное моноциклическое 3-6-членное карбоциклическое кольцо; моноциклическое 4-, 5-, 6- или 7-членное гетероциклическое кольцо, которое включает 1, 2, 3 или 4 гетероатома, независимо выбранных из O, N или S; моноциклическое 5- или 6-членное гетероарильное кольцо, которое включает 1, 2, 3 или 4 гетероатома, независимо выбранных из O, N или S; или бициклическую 9- или 10-членную гетероарильную кольцевую систему, которая включает 1, 2, 3, 4 или 5 гетероатомов, независимо выбранных из O, N или S;R11 означает водород или метил;R12 означает гало, C1-6 алкил, С 2-6 алкенил, C2-6 алкинил, карбокси, C1-6 алкокси, циано, оксо, фторС 1-6 алкил, гидрокси, амино, N-C1-4 алкиламино или N,N-ди-C1-4 алкиламино; арил, где арильное кольцо необязательно замещено 1, 2 или 3 заместителями, выбранными из R13; моноциклическое 5- или 6-членное гетероарильное кольцо, которое включает 1, 2, 3 или 4 гетероатома, независимо выбранных из O, N илиS, и которое является необязательно замещенным 1, 2 или 3 заместителями, выбранными из R13; или моноциклическое 4-, 5-, 6- или 7-членное гетероциклическое кольцо, которое включает 1, 2, 3 или 4 гетероатома, независимо выбранных из O, N или S, и которое является необязательно замещенным 1, 2 или 3 заместителями, выбранными из R13;R14 и R15 независимо означают водород или метил; иr означает 0, 1, 2 или 3. В соответствии с восьмым аспектом настоящего изобретения обеспечивается соединение формулы(Id) согласно вышеприведенному определению или его фармацевтически приемлемая соль для применения в качестве лекарственного средства. В соответствии с девятым аспектом настоящего изобретения обеспечивается соединение формулы(Id) согласно вышеприведенному определению или его фармацевтически приемлемая соль для применения при лечении рака предстательной железы. В соответствии с десятым аспектом настоящего изобретения обеспечивается соединение формулы(Ie) или его фармацевтически приемлемая сольR9 и R10, одинаково или по-разному в каждом случае, означают водород или метил;J означает арил; полностью насыщенное моноциклическое 3-6-членное карбоциклическое кольцо; моноциклическое 4-, 5-, 6- или 7-членное гетероциклическое кольцо, которое включает 1, 2, 3 или 4 гетероатома, независимо выбранных из O, N или S; моноциклическое 5- или 6-членное гетероарильное кольцо, которое включает 1, 2, 3 или 4 гетероатома, независимо выбранных из O, N или S; или бициклическую 9- или 10-членную гетероарильную кольцевую систему, которая включает 1, 2, 3, 4 или 5 гетероа- 14017144 томов, независимо выбранных из O, N или S;R11 означает водород или метил;R12 означает гало, C1-6 алкил, C2-6 алкенил, C2-6 алкинил, карбокси, C1-6 алкокси, циано, оксо, фторС 1-6 алкил, гидрокси, амино, N-C1-4 алкиламино или N,N-ди-C1-4 алкиламино; арил, где арильное кольцо необязательно замещено 1, 2 или 3 заместителями, выбранными из R13; моноциклическое 5- или 6-членное гетероарильное кольцо, которое включает 1, 2, 3 или 4 гетероатома, независимо выбранных из O, N илиS, и которое является необязательно замещенным 1, 2 или 3 заместителями, выбранными из R13; или моноциклическое 4-, 5-, 6- или 7-членное гетероциклическое кольцо, которое включает 1, 2, 3 или 4 гетероатома, независимо выбранных из O, N или S, и где гетероциклическое кольцо необязательно замещено 1, 2 или 3 заместителями, выбранными из R13;R14 и R15 независимо означают водород или метил; иr означает 0, 1, 2 или 3. В соответствии с одиннадцатым аспектом настоящего изобретения обеспечивается соединение формулы (Ie) согласно вышеприведенному определению или его фармацевтически приемлемая соль для применения в качестве лекарственного средства. В соответствии с двенадцатым аспектом настоящего изобретения обеспечивается соединение формулы (Ie) согласно вышеприведенному определению или его фармацевтически приемлемая соль для применения при лечении рака предстательной железы. В дальнейших вариантах осуществления четвертого, пятого, шестого, седьмого, восьмого, девятого,десятого, одиннадцатого и двеннадцатого аспектов настоящего изобретения каждое из следующих определений J, L1, L3, n, p, r, w, z, R4, R9, R10, R11, R12, R13, R14, X3 и Y в пп.(1)-(61) ниже могут использоваться индивидуально или в комбинации с одним или несколькими другими следующими определениями для ограничения наиболее широких определений формул (Ic), (Id), (Ie) или (If).(48) r означает 0 или 1, когда J означает имидазолил, изотиазолил, морфолинил, оксадиазолил, оксазолил, изоксазолил, оксетанил, тетрагидро-2H-пиранил, пиразолил, пиридазинил, пиридинил или бициклическую 9-членную гетероарильную кольцевую систему, содержащую 1 или 2 атома азота или одинединственный атом серы;(49) r означает 1, когда J означает имидазолил, изотиазолил, морфолинил, оксадиазолил, оксазолил,изоксазолил, оксетанил, тетрагидро-2H-пиранил, пиразолил, пиридазинил, пиридинил или бициклическую 9-членную гетероарильную кольцевую систему, содержащую 1 или 2 атома азота или одинединственный атом серы;(50) r означает 0, когда J означает имидазолил, изотиазолил, морфолинил, оксадиазолил, оксазолил,изоксазолил, оксетанил, тетрагидро-2H-пиранил, пиразолил, пиридазинил, пиридинил или бициклическую 9-членную гетероарильную кольцевую систему, содержащую 1 или 2 атома азота или одинединственный атом серы;(61) w и z оба означают 0. Заслуживающие особого внимания новые соединения формулы (Ic) включают, но не ограничиваются ими, перечисленные ниже соединения 4-4-[3-(трифторметил)-[1,2,4]триазоло[4,3-b]пиридазин-6-ил]пиперазин-1-ил]метил]бензонитрил; 3-(трифторметил)-6-[4-3-(трифторметил)фенил]метил]пиперазин-1-ил]-[1,2,4]триазоло[4,3b]пиридазин; 4-пиридин-3-ил-1-[3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин-6-ил]пиперидин-4-ол; 3-(дифторметил)-6-4-[(1R)-1-(4-фторфенил)этил]пиперазин-1-ил[1,2,4]триазоло[4,3-b]пиридазин; 4-(4-фторфенил)-1-[3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин-6-ил]пиперидин-4-ол;N-метил-N-[2-(метилсульфонил)этил]-4-1-[3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин-6 ил]пиперидин-4-илбензамид; 6-[3-(4-метоксифенокси)азетидин-1-ил]-3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин; 6-(4-4-[2-(1-метил-1H-пиразол-5-ил)этокси]фенилпиперазин-1-ил)-3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин и 4-[4-[2-(1-метил-1H-пиразол-5-ил)этокси]фенил]-1-[3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин-6-ил]пиперидин-4-ол и их фармацевтически приемлемые соли. Кристаллические формы заслуживающих особого внимания новых соединений формулы (Ic) и их солей также идентифицированы. Таким образом, в соответствии с настоящим изобретением обеспечивается кристаллическая форма безводной формыA 4-пиридин-3-ил-1-[3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин-6 ил]пиперидин-4-ола, которая имеет порошковую рентгенограмму по меньшей мере с одним характерным пиком при значениях 2 около 9,18, 15,51, 16,01, 18,94 или 24,59 при измерении с использованиемCuKa излучения, причем более предпочтительно указанные значения могут варьироваться в рамках 0,5 2. Таким образом, в соответствии с настоящим изобретением обеспечивается кристаллическая форма безводной формы A 4-пиридин-3-ил-1-[3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин-6-ил]пиперидин-4-ола, которая имеет порошковую рентгенограмму с характерными пиками при значениях 2 около 9,18, 15,51, 16,01, 18,94 и 24,59 при измерении с использованием CuKa излучения, причем более предпочтительно указанные значения могут варьироваться в рамках 0,5 2. Таким образом, в соответствии с настоящим изобретением обеспечивается кристаллическая форма безводной формы A 4-пиридин-3-ил-1-[3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин-6-ил]пиперидин-4-ола, которая имеет порошковую рентгенограмму с характерными пиками при значениях 2 8.30,9.18, 9.96, 10.41, 14.35, 15.02, 15.51, 16.01, 17.03, 18.46, 18.94, 19.18, 19.82, 20.35, 20.61, 21.80, 22.65,23.38, 24.15, 24.59, 25.43, 26.12, 26.35, 26.59, 27.43, 29.38, 31.83 и 37.33 при измерении с использованиемCuKa излучения, причем более предпочтительно указанные значения могут варьироваться в рамках 0,5 2. Таким образом, в соответствии с настоящим изобретением обеспечивается кристаллическая форма безводной формы A 4-пиридин-3-ил-1-[3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин-6-ил]пиперидин-4-ола, которая имеет порошковую рентгенограмму, по существу, тождественную порошковой рентгенограмме, показанной на фиг. 1 при измерении с использованием CuKa излучения. Таким образом, в соответствии с настоящим изобретением обеспечивается кристаллическая форма безводной формы A N-(2-метоксиэтил)-N-метил-4-[1-[3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин 6-ил]пиперидин-4-ил]бензамида, которая имеет порошковую рентгенограмму по меньшей мере с одним характерным пиком при значениях 2 около 12.34, 15.78, 20.42, 23.75 или 24.73 при измерении с использованием CuKa излучения, причем более предпочтительно указанные значения могут варьироваться в рамках 0,5 2. Таким образом, в соответствии с настоящим изобретением обеспечивается кристаллическая форма безводной формы A N-(2-метоксиэтил)-N-метил-4-[1-[3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин 6-ил]пиперидин-4-ил]бензамида, которая имеет порошковую рентгенограмму с характерными пиками при значениях 2 около 12.34, 15.78, 20.42, 23.75 и 24.73 при измерении с использованием CuKa излучения, причем более предпочтительно указанные значения могут варьироваться в рамках 0,5 2. Таким образом, в соответствии с настоящим изобретением обеспечивается кристаллическая форма безводной формы A N-(2-метоксиэтил)-N-метил-4-[1-[3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин 6-ил]пиперидин-4-ил]бензамида, которая имеет порошковую рентгенограмму с характерными пиками при значениях 2 6.28, 7.92, 9.65, 12.34, 12.69, 14.92, 15.78, 16.89, 18.78, 19.28, 20.42, 20.99, 21.57, 22.49,- 17017144 23.31, 23.75, 24.34, 24.73, 25.38, 26.93, 28.14, 29.08, 31.16, 31.86, 32.50, 33.14, 34.79, 36.34, 36.78, 38.01 и 38.64 при измерении с использованием CuKa излучения, причем более предпочтительно указанные значения могут варьироваться в рамках 0,5 2. Таким образом, в соответствии с настоящим изобретением обеспечивается кристаллическая форма безводной формы A N-(2-метоксиэтил)-N-метил-4-[1-[3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин 6-ил]пиперидин-4-ил]бензамида, которая имеет порошковую рентгенограмму, по существу, тождественную порошковой рентгенограмме, показанной на фиг. 2 при измерении с использованием CuKa излучения. Таким образом, в соответствии с настоящим изобретением обеспечивается кристаллическая форма безводной формы A 6-[4-[4-[2-(1-метил-1H-пиразол-5-ил)этокси]фенил]пиперидин-1-ил]-3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазина, которая имеет порошковую рентгенограмму по меньшей мере с одним характерным пиком при значениях 2 около 4.90, 13.47, 15.93, 16.64 или 22.83 при измерении с использованием CuKa излучения, причем более предпочтительно указанные значения могут варьироваться в рамках 0,5 2. Таким образом, в соответствии с настоящим изобретением обеспечивается кристаллическая форма безводной формыA 6-[4-[4-[2-(1-метил-1H-пиразол-5-ил)этокси]фенил]пиперидин-1-ил]-3(трифторметил)[1,2,4]триазоло[4,3-b]пиридазина, которая имеет порошковую рентгенограмму с характерными пиками при значениях 2 около 4.90, 13.47, 15.93, 16.64 и 22.83 при измерении с использованием CuKa излучения, причем более предпочтительно указанные значения могут варьироваться в рамках 0,5 2. Таким образом, в соответствии с настоящим изобретением обеспечивается кристаллическая форма безводной формы A 6-[4-[4-[2-(1-метил-1H-пиразол-5-ил)этокси]фенил]пиперидин-1-ил]-3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазина, которая имеет порошковую рентгенограмму с характерными пиками при значениях 2 4.90, 9.784, 11.50, 11.94, 12.97, 13.47, 14.72, 15.93, 16.64, 17.36, 18.32, 18.67,19.195, 19.67, 20.26, 20.58, 20.87, 21.33, 21.64, 22.83, 23.7, 24, 24.40, 25.99, 26.75, 27.15, 28.10, 28.55, 29.02,29.46, 29.74, 30.12, 30.65, 31.37, 31.85, 33.66, 34.28, 35.85, 36.42, 37.62 и 38.53 при измерении с использованием CuKa излучения, причем более предпочтительно указанные значения могут варьироваться в рамках 0,5 2. Таким образом, в соответствии с настоящим изобретением обеспечивается кристаллическая форма безводной формы A 6-[4-[4-[2-(1-метил-1H-пиразол-5-ил)этокси]фенил]пиперидин-1-ил]-3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазина, которая имеет порошковую рентгенограмму, по существу, тождественную порошковой рентгенограмме, показанной на фиг. 3 при измерении с использованием CuKa излучения. Таким образом, в соответствии с настоящим изобретением обеспечивается кристаллическая форма безводной формы A 6-[4-[4-[2-(1-метил-1H-пиразол-5-ил)этокси]фенил]пиперазин-1-ил]-3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазина, которая имеет порошковую рентгенограмму по меньшей мере с одним характерным пиком при значениях 2 около 6.90, 15.38, 21.55, 24.48 или 27.56 при измерении с использованием CuKa излучения, причем более предпочтительно указанные значения могут варьироваться в рамках 0,5 2. Таким образом, в соответствии с настоящим изобретением обеспечивается кристаллическая форма безводной формы A 6-[4-[4-[2-(1-метил-1H-пиразол-5-ил)этокси]фенил]пиперазин-1-ил]-3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазина, которая имеет порошковую рентгенограмму с характерными пиками при значениях 2 около 6.90, 15.38, 21.55, 24.48 и 27.56 при измерении с использованием CuKa излучения, причем более предпочтительно указанные значения могут варьироваться в рамках 0,5 2. Таким образом, в соответствии с настоящим изобретением обеспечивается кристаллическая форма безводной формы A 6-[4-[4-[2-(1-метил-1H-пиразол-5-ил)этокси]фенил]пиперазин-1-ил]-3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазина, которая имеет порошковую рентгенограмму с характерными пиками при значениях 2 6.90, 9.6, 10.78, 12.82, 13.16, 13.85, 14.44, 15.38, 16.44, 17.46, 18.25, 18.92, 19.27,20.18, 21.03, 21.55, 22.36, 22.63, 23.55, 23.76, 24.48, 25.2, 25.76, 26.47, 27.56, 27.83, 28.21, 29.10, 29.93,30.59, 31.20, 32.49, 33.33, 34.04, 34.62, 36.18, 36.54, 37.45, 38.17 и 39.32 при измерении с использованиемCuKa излучения, причем более предпочтительно указанные значения могут варьироваться в рамках 0,5 2. Таким образом, в соответствии с настоящим изобретением обеспечивается кристаллическая форма безводной формы A 6-[4-[4-[2-(1-метил-1H-пиразол-5-ил)этокси]фенил]пиперазин-1-ил]-3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазина, которая имеет порошковую рентгенограмму, по существу, тождественную порошковой рентгенограмме, показанной на фиг. 4 при измерении с использованием CuKa излучения. Таким образом, в соответствии с настоящим изобретением обеспечивается кристаллическая форма фумарата 6-[4-[4-[2-(1-метил-1H-пиразол-5-ил)этокси]фенил]пиперазин-1-ил]-3-(трифторметил)[1,2,4] триазоло[4,3-b]пиридазина, которая имеет порошковую рентгенограмму по меньшей мере с одним ха- 18017144 рактерным пиком при значениях 2 около 11.72, 16.46, 17.58 или 21.89 при измерении с использованием CuKa излучения, причем более предпочтительно указанные значения могут варьироваться в рамках 0,5 2. Таким образом, в соответствии с настоящим изобретением обеспечивается кристаллическая форма фумарата 6-[4-[4-[2-(1-метил-1H-пиразол-5-ил)этокси]фенил]пиперазин-1-ил]-3-(трифторметил)[1,2,4] триазоло[4,3-b]пиридазина, которая имеет порошковую рентгенограмму с характерными пиками при значениях 2 около 11.72, 16.46, 17.58 и 21.89 при измерении с использованием CuKa излучения,причем более предпочтительно указанные значения могут варьироваться в рамках 0,5 2. Таким образом, в соответствии с настоящим изобретением обеспечивается кристаллическая форма фумарата 6-[4-[4-[2-(1-метил-1H-пиразол-5-ил)этокси]фенил]пиперазин-1-ил]-3-(трифторметил)[1,2,4] триазоло[4,3-b]пиридазина, которая имеет порошковую рентгенограмму с характерными пиками при значениях 2 4.51, 5.90, 11.72, 12.22, 13.23, 16.46, 17.58, 19.74, 20.26, 21.18, 21.89, 23.86, 24.17, 25.83,26.75, 28.78, 30.54 и 31.51 при измерении с использованием CuKa излучения, причем более предпочтительно указанные значения могут варьироваться в рамках 0,5 2. Таким образом, в соответствии с настоящим изобретением обеспечивается кристаллическая форма фумарата 6-[4-[4-[2-(1-метил-1H-пиразол-5-ил)этокси]фенил]пиперазин-1-ил]-3-(трифторметил)[1,2,4] триазоло[4,3-b]пиридазина, которая имеет порошковую рентгенограмму, по существу, тождественную порошковой рентгенограмме, показанной на фиг. 5 при измерении с использованием CuKa излучения. Ссылку в данной заявке на соединение формулы (I) следует понимать как в равной степени относящуюся к соединению формулы (Ic), (Id), (Ie) и (If). Пригодными фармацевтически приемлемыми солями соединения формулы (I) являются, например,кислотно-аддитивная соль соединения формулы I, например кислотно-аддитивная соль с неорганической или органической кислотой, такой как соляная, бромисто-водородная, серная, трифторуксусная, лимонная или малеиновая кислота; или, например, соль соединения формулы I, которое является достаточно основным, например, с щелочным или щелочно-земельным металлом, такая как соль кальция или магния, или соль аммония, или соль с органическим основанием, таким как метиламин, диметиламин, триметиламин, пиперидин, морфолин или трис-(2-гидроксиэтил)амин. Дальнейшей пригодной фармацевтически приемлемой солью соединения формулы I является, например, соль, образованная внутри тела человека или животного после введения соединения формулы I. Пригодным фармацевтически приемлемым сольватом соединения формулы I является, например,гидрат, такой как полугидрат, моногидрат, дигидрат или тригидрат или их альтернативные количества. Соединения изобретения могут быть введены в виде пролекарства, которое представляет собой соединение, которое расщепляется в организме человека или животного с высвобождением соединения изобретения. Пролекарство можно использовать для изменения физических свойств и/или фармакокинетических свойств соединения изобретения. Пролекарство может образовываться, когда соединение изобретения содержит пригодную группу или заместитель, к которому может быть присоединена группа,модифицирующая свойства. Примеры пролекарств включают расщепляющиеся in vivo сложноэфирные производные, которые могут быть образованы по карбоксильной группе или гидроксильной группе в соединении формулы I, и расщепляющиеся in vivo амидные производные, которые могут быть образованы по карбоксильной группе или аминогруппе в соединении формулы I. Соответственно, настоящее изобретение включает те соединения формулы I согласно вышеприведенному определению, доступность которых достигается и путем органического синтеза, и в ходе расщепления его пролекарства внутри организма человека или животного. Соответственно, настоящее изобретение включает те соединения формулы I, которые получаются с помощью методов органического синтеза, а также те соединения, которые получаются в организме человека или животного в ходе метаболизма соединения-предшественника, то есть соединение формулы I может быть синтетически получающимся соединением или метаболически получающимся соединением. Пригодным фармацевтически приемлемым пролекарством соединения формулы I является то, которое на основе рациональной врачебной оценки признается пригодным для введения в организм человека или животного без нежелательных фармакологических проявлений и без чрезмерной токсичности. Различные формы пролекарства описаны, например, в следующих документах:h) E. Roche (редактор), "Bioreversible Carriers in Drug Design", Pergamon Press, 1987. Пригодным фармацевтически приемлемым пролекарством соединения формулы (I), которое имеет- 19017144 карбоксильную группу, является, например, расщепляющийся in vivo сложный эфир этого соединения. Расщепляющийся in vivo сложный эфир соединения формулы (I), содержащий карбоксильную группу,представляет собой, например, фармацевтически приемлемый сложный эфир, который расщепляется в организме человека или животного с получением исходной кислоты. Пригодные фармацевтически приемлемые сложные эфиры в случае карбоксильной группы включают C1-6 алкиловые сложные эфиры, такие как метиловый, этиловый и трет-бутиловый, C1-6 алкоксиметиловые сложные эфиры, такие как метоксиметиловый сложный эфир, C1-6 алканоилоксиметиловые сложные эфиры, такие как пивалоилоксиметиловые сложные эфиры, 3-фталидиловые сложные эфиры, C3-8 циклоалкилкарбонилокси-C1-6 алкиловые сложные эфиры, такие как циклопентилкарбонилоксиметиловый и 1-циклогексилкарбонилоксиэтиловый сложные эфиры, 2-оксо-1,3-диоксоленилметиловые сложные эфиры, такие как 5-метил-2 оксо-1,3-диоксолен-4-илметиловые сложные эфиры и C1-6 алкоксикарбонилокси-C1-6 алкиловые сложные эфиры, такие как метоксикарбонилоксиметиловые и 1-метоксикарбонилоксиэтиловые сложные эфиры. Пригодным фармацевтически приемлемым пролекарством соединения формулы (I), которое имеет гидроксильную группу, является, например, расщепляющийся in vivo сложный или простой эфир этого соединения. Расщепляющийся in vivo сложный или простой эфир соединения формулы (I), содержащий гидроксильную группу, представляет собой, например, фармацевтически приемлемый сложный или простой эфир, который расщепляется в организме человека или животного с получением исходного гидроксисоединения. Пригодные группы, образующие фармацевтически приемлемый сложный эфир в случае гидроксильной группы, включают неорганические сложные эфиры, такие как сложные эфиры фосфорной кислоты (в том числе фосфорамидные циклические сложные эфиры). Дальнейшие пригодные группы, образующие фармацевтически приемлемые сложные эфиры в случае гидроксильной группы, включают C1-10 алканоильные группы, такие как ацетильная, бензоильная, фенилацетильная и замещенные бензоильная и фенилацетильная группы, C1-10 алкоксикарбонильные группы, такие как этоксикарбонильная, N,N-[ди-C1-4 алкил]карбамоильная, 2-диалкиламиноацетильная и 2-карбоксиацетильная группы. Примеры заместителей кольца на фенилацетильной и бензоильной группах включают аминометил, Nалкиламинометил, N,N-диалкиламинометил, морфолинометил, пиперазин-1-илметил и 4-C1-4 алкилпиперазин-1-илметил. Пригодные группы, образующие фармацевтически приемлемый простой эфир в случае гидроксильной группы, включают -ацилоксиалкильные группы, такие как ацетоксиметильная и пивалоилоксиметильная группы. Пригодным фармацевтически приемлемым пролекарством соединения формулы (I), которое имеет карбоксильную группу, является, например, расщепляющийся in vivo амид этого соединения, например амид, образованный с амином, таким как аммиак, C1-4 алкиламином, таким как метиламин, ди-C1-4 алкиламином, таким как диметиламин, N-этил-N-метиламин или диэтиламин, C1-4 алкокси-С 2-4 алкиламином,таким как 2-метоксиэтиламин, фенил-C1-4 алкиламином, таким как бензиламин, и аминокислотами, такими как глицин, или их сложными эфирами. Пригодным фармацевтически приемлемым пролекарством соединения формулы (I), которое имеет аминогруппу, является, например, расщепляющееся in vivo амидное производное этого соединения. Пригодные фармацевтически приемлемые амиды, образованные из аминогруппы, включают, например,амид, образованный с C1-10 алканоильными группами, такими как ацетильная, бензоильная, фенилацетильная и замещенные бензоильная и фенилацетильная группы. Примеры заместителей кольца на фенилацетильной и бензоильной группах включают аминометил, N-алкиламинометил, N,N-диалкиламинометил, морфолинометил, пиперазин-1-илметил и 4-(C1-4)алкилпиперазин-1-илметил.In vivo действие соединения формулы (I) может быть частично вызвано посредством одного или нескольких метаболитов, которые образуются внутри организма человека или животного после введения соединения формулы (I). Как указано выше, in vivo действие соединения формулы (I) также может быть вызвано в ходе метаболизма соединения-предшественника (пролекарства). Примером метаболита соединения формулы (I) является 3-[4-гидрокси-1-[3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин-6-ил]пиперидин-4-ил]пиридин 1-оксид, который является метаболитом 4-пиридин-3-ил-1-[3-(трифторметил)[1,2,4]триазоло[4,3-b]пиридазин-6-ил]пиперидин-4-ола. Соединения формулы (I) могут быть получены с помощью способов, включающих стадии, выбранные из стадий (1)-(10), изложенных ниже, причем эти способы обеспечены в качестве дальнейшей особенности изобретения. Получение соединений формулы (I) 1. Способ получения соединений формулы (I) включает введение в реакцию соединения формулы(II), где G означает уходящую группу, такую как галоген, алкансульфонилокси или арилсульфонилокси,и R4, X1, X2 и X3 принимают определенные выше значения, с моноциклическим или бициклическим амином формулы (III), где R5 и m принимают определенные выше значения. Реакция может быть проведена путем объединения компонентов в инертном растворителе, таком как этанол, ксилол или N-метилпирролидон, при температурах между 25 и 250 С, предпочтительно между 50 и 150 С. Реакция преимущественно может быть катализирована с помощью оснований, таких как органические основания, например диизопропилэтиламин, или с помощью катализаторов на основе переходных металлов с низкой валентностью, таких как Pd(0), например бис(дибензилиденацетон)палладий(0). Реакционная смесь может быть нагрета с помощью обычного источника тепла, такого как масляная баня или нагревательное устройство, или с помощью микроволнового нагрева. В одном варианте осуществления изобретения обеспечивается способ получения соединений формулы (Ic), который включает введение в реакцию соединения формулы (IIa), где G означает пригодную уходящую группу, такую как галоген, например хлор, и R4 и X3 определены выше в отношении формулы(i) превращение функциональной группы одного из соединений изобретения в другую функциональную группу;(ii) введение новой функциональной группы в одно из соединений изобретения;(iv) в случае соединений изобретения в форме отдельного энантиомера, разделение рацемического соединения изобретения на отдельные энантиомеры;(v) получение их фармацевтически приемлемой соли и/или(vi) получение их кристаллической формы. В дополнительном варианте осуществления изобретения, обеспечивается способ получения соединений формулы (If), который включает введение в реакцию соединения формулы (IIb), где G означает галоген, с амином формулы (IIIb), где Y, J, L3, R12, k и r определены выше в отношении формулы (If)(i) превращение функциональной группы одного из соединений изобретения в другую функциональную группу;(ii) введение новой функциональной группы в одно из соединений изобретения;(iv) в случае соединений изобретения в форме отдельного энантиомера, разделение рацемического соединения изобретения на отдельные энантиомеры;(v) получение их фармацевтически приемлемой соли и/или(vi) получение их кристаллической формы. Упомянутые ранее реакции могут быть проведены путем объединения компонентов формулы (IIa) и (IIIa) или (IIb) и (IIIb) в пригодном растворителе, например диметилформамиде или диметилацетамиде,при пригодной температуре, например между 25 и 250C, более предпочтительно между 50 и 150C, в присутствии пригодного основания, например диизопропилэтиламина. Реакционная смесь может быть нагрета с помощью обычного источника тепла, такого как масляная баня или нагревательное устройство,или с помощью микроволнового нагрева. Соединения формулы (II), (IIa) или (IIb) могут быть получены с помощью способов, хорошо известных специалистам в данной области техники, включая способы в соответствии с таковыми или аналогичные таковым, описанным в химической литературе, например, как описано W.L. Mosby, Heterocyclic Compounds, т. 15, ч. 1 и 2, Systems with Bridgehead Nitrogen, Interscience, 1961; R.N. Castle, HeterocyclicCompounds, т. 27, Condensed Pyridazines, Wiley, 1973 и Heterocyclic Chemistry, т. 35, Condensed Pyrazines,G.W.H. Cheeseman и R.F. Cookson, Wiley, 1979, и присутствующих там ссылках. Амины формулы (III), (IIIa) или (IIIb) могут быть получены с помощью способов, хорошо известных специалистам в данной области техники, включая способы в соответствии с таковыми или аналогичные таковым, описанным в химической литературе, например J.R. Malpass, Aliphatic and CyclicI (1999) - т. Е 23 j Cyclic Compounds VI (2000) и присутствующих там ссылках, и, при необходимости,модифицированы путем преобразований функциональных групп, хорошо известным специалистам в данной области техники, включая способы в соответствии с таковыми или аналогичные таковым, описанным в химической литературе, например Comprehensive Functional Group Transformations, под ред.A.R. Katritzky, О. Meth-Cohn и C.W. Rees, Pergamon, 1995, и присутствующих там ссылках. 2. Способ получения соединений формулы (I) включает введение в реакцию соединения формулы(II), где G означает уходящую группу, такую как йодид, бромид, хлорид, алкансульфонилокси или арилсульфонилокси, и R4, X1, X2 и X3 принимают определенные выше значения, с моноциклическим или бициклическим металлоорганическим соединением, таким как цинкорганическое соединение формулы(IV), где R5 и m принимают определенные выше значения, и M означает пригодный металл, такой какZn-W, где W означает один инертный лиганд или несколько инертных лигандов, таких как бромид или йодид. Реакция преимущественно может быть катализирована с помощью катализаторов на основе переходных металлов с низкой валентностью,таких какPd(0),например дихлорид бис(дифенилфосфиноферроцен)палладия(II) (dppf). Реакция может быть проведена путем объединения компонентов в инертном растворителе, таком как ксилол или тетрагидрофуран, при температурах между 0 и 150C, предпочтительно между 25 и 100C. Реакционная смесь может быть нагрета с помощью обычного источника тепла, такого как масляная баня или нагревательное устройство, или с помощью микроволнового нагрева. Металлоорганические реактивы формулы (IV) могут быть получены с помощью способов, хорошо известных специалистам в данной области техники, включая способы в соответствии с таковыми или аналогичные таковым, описанным в химической литературе, например Е. Nakamura, Organozinc Chemistry с. 590 в Organometallics in Synthesis, M. Schlosser, изд. Wiley, 2002, и присутствующих там ссылках. 3. Способ получения соединений формулы (I) включает введение в реакцию соединения формулы(II), где G означает уходящую группу, такую как йодид, бромид, хлорид, алкансульфонилокси или арилсульфонилокси, и R4, X1, X2, и X3 принимают определенные выше значения, с моноциклическиим или бициклическим металлоорганическим соединением, таким как органоборановое соединение формулы(V), где M означает металлоорганический остаток, такой как B(OH)2, и где R5 и m принимают определенные выше значения Альтернативно, M означает уходящую группу, такую как йодид, бромид, хлорид, алкансульфонилокси или арилсульфонилокси, и R4, X1, X2, и X3 принимают определенные выше значения, и G означает металлоорганическое соединение, такое как органостаннан, и где R5 и m принимают определенные выше значения. Реакция преимущественно может быть катализирована с помощью катализаторов на основе переходных металлов с низкой валентностью, таких как Pd(0), например бис(дибензилиденацетон)палладий/трифениларсин. Реакция может быть проведена путем объединения компонентов в инертном растворителе, таком как ксилол, или тетрагидрофуран, или N-метилпирролидон, при температурах между 0 и 150C, предпочтительно между 25 и 100C. Реакционная смесь может быть нагрета с помощью обычного источника тепла, такого как масляная баня или нагревательное устройство, или с помощью микроволнового нагрева. Дополнительные сведения относительно таких реакций сочетания см., например, Organometallics inSynthesis, M. Schlosser, изд. Wiley, 2002 и присутствующих там ссылках. Металлоорганические реактивы формулы (V) могут быть получены с помощью способов, хорошо известных специалистам в данной области техники, включая способы в соответствии с таковыми или аналогичные таковым, описанным в химической литературе, например Comprehensive OrganometallicSchlosser изд. Wiley, 2002 и присутствующих там ссылках. 4. Способ получения соединений формулы (I) включает введение в реакцию соединения формулыVI с ацилирующим реагентом, таким как карбоновая кислота или ее реакционноспособное производное,где R4, Х 1, Х 2 и Х 3, R5 и m принимают определенные выше значения. Пригодными ацилирующими реактивами RC(Z)G являются, например, производные карбоновой кислоты, где G выбирают из Cl, OC(=O)R, O-алкила, S-алкила и Z выбирают из О, S, N-алкила или N-арила, или где Z и G, взятые вместе с атомом углерода, к которому они присоединены, образуют нитрил, или ортоэфир, или ортоамид. Реакция может быть проведена путем объединения компонентов при отсутствии растворителя или в инертном растворителе, таком как ортодихлорбензол, при температурах между 25 и 250C, предпочтительно между 50 и 150C. Реакционная смесь может быть нагрета с помощью обычного источника тепла, такого как масляная баня или нагревательное устройство, или с помощью микроволнового нагрева. Соединения формулы (VI) могут быть получены с помощью способов, хорошо известных специалистам в данной области техники, включая способы в соответствии с таковыми или аналогичные таковым, описанным в химической литературе, например как описано в W.L. Mosby, Heterocyclic Compounds,т. 15 ч. 1 и . 2, Systems with Bridgehead Nitrogen, Interscience, 1961; R.N. Castle, Heterocyclic Compounds, т. 27, Condensed Pyridazines, Wiley, 1973 и Heterocyclic Chemistry, т. 35, Condensed Pyrazines, G.W.H.Cheeseman и R.F. Cookson, Wiley, 1979, и присутствующих там ссылках. 5. Способ получения соединений формулы (I), где X1 и X2 означают C(R1) и C(R2) соответственно и 3X означает азот, включает введение в реакцию N-амино-1,2,4-триазола (VIII), где R4 принимает определенные выше значения, с ненасыщенным кетоном или ненасыщенным сложным эфиром (IX), где G означает уходящую группу, такую как алкокси или диалкиламино, и R1, R2, R5 и m принимают определенные выше значения. Реакция, как показано, может быть проведена в одну или две стадии, и последнюю стадию проводят в растворителе, таком как уксусная кислота, при температурах между 25 и 250C, предпочтительно между 50 и 150C, например в соответствии с методикой D.F. Lieberman и J.D. Albright, J. Het. Chem., 1988,827. Другие полезные и родственные способы получения соединений формулы (I) или получения исходных веществ для получения соединений формулы (I) раскрыты в литературе, например в W.L. Mosby,Heterocyclic Compounds, т. 15 ч. 1 и 2, Systems with Bridgehead Nitrogen, Interscience, 1961; R.N. Castle,Heterocyclic Compounds, т. 27, Condensed Pyridazines, Wiley, 1973 и Heterocyclic Chemistry, т. 35, Condensed Pyrazines, G.W.H. Cheeseman и R.F. Cookson, Wiley, 1979 и присутствующих там ссылках. 6. Способ получения соединений формулы (I) включает введение группы R5 путем введения в реакцию соединения формулы (X), где Z означает замещаемую группу, такую как водород первичного или вторичного амина, или Z означает уходящую группу, такую как галоген или алкил- или арилсульфонилокси, или Z означает противоион, такой как натрий(I) или магний(II), с соединением формулы (XI), гдеR5 принимает определенные выше значения и Q означает замещаемую группу, такую как водород первичного или вторичного амина, или Q означает уходящую группу, такую как галоген или алкил- или арилсульфонилокси, или Q означает противоион, такой как натрий(I) или магний(II). Примеры реакций этого типа включают алкилирование, ацилирование и сульфонилирование. Аль- 24017144 тернативно, если Z означает водород вторичного амина, предпочтительно циклического вторичного амина, и R5-Q означает альдегид, m-ная группа R5 может быть введена с помощью восстановительного аминирования, например путем восстановления смеси альдегида и вторичного амина цианоборогидридом натрия. 7. Способ получения соединений формулы (I) включает превращение функциональной группы одного из соединений изобретения в другую функциональную группу с использованием стандартных химических реакций, хорошо известных специалистам в данной области техники, с получением другого соединения изобретения. Такие способы описаны, например, в Comprehensive Organic Chemistry, т. 2, с. 3, под ред. D. Barton и D. Ollis, Pergamon, 1979, Comprehensive Functional Group Transformations, под ред.A.R. Katritzky, О. Meth-Cohn и C.W. Rees, Pergamon, 1995 и различными авторами в Houben-Weyl, Methods of Organic Chemistry, Verlag Chemie, в различные годы, и присутствующих там ссылках. 8. Способ получения соединений изобретения включает введение новой функциональной группы в одно из соединений изобретения с использованием стандартных химических реакций, хорошо известных специалистам в данной области техники, с получением другого соединения изобретения. Такие способы описаны, например, в Comprehensive Organic Chemistry, т. 2, с. 3, под ред. D. Barton и D. Ollis, Pergamon,1979, Comprehensive Functional Group Transformations, под ред. A.R. Katritzky, O. Meth-Cohn и C.W. Rees,Pergamon, 1995 и различными авторами в Houben-Weyl, Methods of Organic Chemistry, Verlag Chemie, в различные годы, и присутствующих там ссылках. 9. Способ получения соединений изобретения в виде одиночного энантиомера включает разделение рацемического соединения изобретения на отдельные энантиомеры. Примеры пригодных способов разделения энантиомеров рацемического соединения включают хроматографию с использованием пригодной хиральной неподвижной фазы; или превращение рацемической смеси в диастереоизомерные производные, разделение смеси диастереоизомерных производных на два одиночных диастереомера и регенерацию отдельных одиночных энантиомеров из каждого отдельного одиночного диастереоизомера или селективную химическую реакцию одного из энантиомеров рацемического соединения (кинетическое оптическое расщепление) с использованием диастереоселективной реакции, катализируемой микробиологическим агентом или ферментом. Примеры пригодных способов разделения смеси диастереомеров включают фракционную кристаллизацию, нормально-фазовую хроматографию или хроматографию с обращенной фазой. Примеры пригодных диастереоизомерных производных, где R5 включает гидрокси- или аминогруппу, включают сложные эфиры, образованные путем ацилирования R5 с использованием активированого производного одиночного энантиомера карбоновой кислоты. Примером пригодной карбоновой кислоты является камфановая кислота. Примеры пригодных диастереоизомерных производных, где R5 включает группу карбоновой кислоты, включают сложные эфиры или амиды, образованные путем ацилирования одиночного энантиомера спирта или амина с использованием активированного производного соединения формулы (I), где по меньшей мере один из R5 содержит группу карбоновой кислоты. Примером пригодного амина является 1-фенилэтиламин и примером пригодного спирта является ментол. Примеры пригодных агентов для проведения кинетического оптического расщепления рацемической смеси соединений изобретения включают эстеразу печени свиньи и пекарские дрожжи. 10. Способ получения соединения изобретения в форме одиночного энантиомера включает проведение одного из способов, описанных в предыдущих разделах, с использованием хиральных промежуточных соединений в разделенной форме. Специалист в данной области техники в полной мере поймет, что при проведении некоторых из способов/реакций, упомянутых здесь, может быть необходима/желательна защита каких-либо чувствительных групп в соединениях. Случаи, в которых необходима или желательна такая защита, и пригодные способы обеспечения такой защиты известны специалисту в данной области техники. Могут использоваться обычные защитные группы в соответствии с общепринятой практикой (например, см. P.G.M. Wuts и T.W. Green, Protective Groups in Organic Synthesis, 4-e изд., John Wiley and Sons, 2002). Таким образом,если реагенты включают группы, такие как амино, карбокси или гидрокси, может быть желательно осуществление защиты этих групп в некоторых из упомянутых здесь реакций. Какие-либо защитные группы, используемые в описанных здесь способах, могут в общем быть выбраны из любой из групп, описанных в литературе или известных квалифицированному химику в качестве подходящих для защиты конкретной группы, и могут быть введены с помощью обычных методов. Защитные группы можно удалять с помощью любых удобных методов, описанных в литературе или известных квалифицированному химику в качестве подходящих для удаления конкретной защитной группы, причем такие способы выбирают таким образом, чтобы осуществить удаления защитной группы с минимальным воздействием на группы, расположенные в других частях молекулы. Отдельные примеры защитных групп приведены с целью удобства ниже, причем в указанных группах термин "низший", как, например, в низшем алкиле, означает, что группа, к которой он относится,предпочтительно имеет 1-4 атома углерода. Следует понимать, что эти примеры не исчерпаны. В случае,когда ниже приведены отдельные примеры способовудаления защитных групп, они также не исчерпаны.- 25017144 Использование защитных групп и способов их снятия, не приведенное специально, также находится в рамках настоящего изобретения. Пригодной защитной группой для амино- или алкиламиногруппы является, например, ацильная группа, например алканоильная группа, такая как трифторацетильная, алкоксикарбонильная группа, например метоксикарбонильная, этоксикарбонильная или трет-бутоксикарбонильная группа, арилметоксикарбонильная группа, например бензилоксикарбонильная, или ароильная или гетероароильная группа,например пиколиноильная. Условия снятия защиты в случае упомянутых выше защитных групп непременно варьируются с выбором защитной группы. Так, например, ацильную группу, такую как алканоильная или алкоксикарбонильная группа или ароильная группа, можно удалить, например, путем гидролиза пригодной кислотой, такой как соляная, серная, или фосфорная кислота, или трифторуксусная кислота, или пригодным основанием, таким как гидроксид щелочного металла, например гидроксид лития или натрия. Альтернативно, ацильную группу, такую как трет-бутоксикарбонильная группа, можно удалить, например, путем обработки пригодной кислотой, такой как соляная, серная или фосфорная кислота,или трифторуксусная кислота, а арилметоксикарбонильную группу, такую как бензилоксикарбонильная группа, можно удалить, например, путем гидрирования над катализатором, таким как палладий-на-угле,или путем обработки кислотой Льюиса, например трис(трифторацетатом) бора. Пригодной альтернативной защитной группой для первичной аминогруппы является, например, фталоильная группа, которую можно удалить путем обработки алкиламином, например диметиламинопропиламином, или гидразином. Пригодной защитной группой для гидроксильной группы является, например, ацильная группа, например алканоильная группа, такая как ацетил, ароильная группа, например бензоильная, или арилметильная группа, например бензильная. Условия снятия защиты в случае упомянутых выше защитных групп непременно варьируются с выбором защитной группы. Так, например, ацильную группу, такую как алканоильная или ароильная группа, можно удалить, например, путем гидролиза пригодным основанием, таким как гидроксид щелочного металла, например гидроксид лития или натрия. Альтернативно,арилметильную группу, такую как бензильная группа, можно удалить, например, путем гидрирования над катализатором, таким как палладий-на-угле. Пригодной защитной группой для карбоксиьной группы является, например, этерифицирующая группа, например метильная или этильная группа, которую можно удалить, например, путем гидролиза основанием, таким как гидроксид натрия, или, например, трет-бутильная группа, которую можно удалить, например, путем обработки кислотой, например органической кислотой, такой как трифторуксусная кислота, или, например, бензильная группа, которую можно удалить, например, путем гидрирования на катализаторе, таком как палладий-на-угле. Защитные группы можно удалять на любой подходящей стадии синтеза, используя обычные приемы, хорошо известные в области химии. Биологические анализы Способность соединений уменьшать число андрогенных рецепторов (АР) оценивали в клеточном иммунофлюоресцентном анализе с использованием эпителиальной линии клеток предстательной железыa) LNCaP клеточный анализ на понижающую регуляцию андрогенного рецептора. Этот иммунофлуоресценсный конечно-точечный анализ позволяет измерять способность исследуемого соединения, понижающе регулировать и уменьшать измеряемые уровни АР в линии клеток карциномы предстательной железы LNCaP (LNCaP клон FGC (CRL-1740), полученных из американской коллекция типовых культур (American Type Culture Collection, ATCC. Клетки LNCaP выращивали в питательной среде (свободной от фенолового красного, Roswell Park(FBS в 5% CO2 воздушном инкубаторе при 37C. Клетки для анализа собирали из Т 175 колб с исходными растворами путем промывания один раз в PBS (фосфатно-солевой буферный раствор, pH 7.4) (Invitrogen код 14190-094) и собирали с использованием 5 мл 1 трипсина/этиламиндиаминтетрауксусной кислоты (ЭДТК) (10 трипсин-ЭДТК, 5,0 г/л трипсина, 2.0 г/л ЭДТК 4 Na и 8,5 г/л NaCl, без фенолового красного, Invitrogen код 15400-054), разбавленного в PBS растворе. Питательную среду объемом 5 мл добавляли к каждой колбе (как указано выше, за исключением того, что взамен 10% (об./об.) FBS включали 5% (об./об.) FBS, профильтрованной через древесный уголь (HyClone кодSH30068.03. Клетки спринцевали по крайней мере дважды с использованием стерильной 18G1,5" (1,240 мм) толстой иглы,и плотность клеток измеряли с использованием счетной камеры. Клетки далее разбавляли в питательной среде плюс 5% (об./об.) FBS, профильтрованной через древесный уголь, и высевали при плотности 6,5103 клеток на лунку (в 90 мкл) в прозрачные, чрные, 96-луночные планшеты для обработанной культуры ткани (Packard,6005182). Тестовые данные, представленные здесь, были получены с использованием двух различных спосо- 26017144 бов получения соединений и дозирования. В способе (1)10 мМ маточный раствор соединения в 100%(об./об.) ДМСО серийно разбавляли 4-кратными шагами в 100% (об./об.) ДМСО с использованиемThermo Scientific Matrix SerialMate. Разбавленные соединения затем дополнительно разбавляли 1 к 30 в среде для анализа с использованием Thermo Scientific Matrix PlateMate и 10 мкл аликвоту этого разбавления вручную дозировали к клеткам с использованием многоканальной пипетки. В способе (2) начинали с 10 мМ маточного раствора соединения, прибор Labcyte Echo 550 использовали для получения набора ответных концентраций соединения, разбавленных в 30 мкл среды для анализа. Echo 550 представляет собой устройство обработки жидкости, которое использует акустическую технологию для осуществления прямого микропланшет-микропланшетного переноса растворов соединений в ДМСО. Система может быть запрограммирована на перенос очень малых объемов, таких как 2,5 нл, с кратным увеличением между микропланшетами и тем самым позволяет создать серийное разбавление соединения, которое затем обратно наполняют для нормализации концентрации ДМСО по диапазону разбавления. Разбавленное соединение объемом 10 мкл затем дозируют к клеткам с использованием Thermo Scientific MatrixPlateMate. Планшеты инкубировали на протяжении ночи при 37C, 5% CO2. В лунки затем дозировали соединения, полученные одним из 2 упомянутых рванее способов, и дополнительно инкубировали в течение 20-22 ч при 37C, 5% CO2. Планшеты фиксировали путем добавления 20 мкл 10% (об./об.) раствора формальдегида (в PBS) к каждой лунке (конечная конц. формальдегида = 1,67% (об./об., и оставляли при комнатной температуре в течение 10 мин. Фиксирующий раствор удаляли и клетки промывали 250 мклPBS/0,05% (об./об.) Tween 20 (PBST) с использованием автоматической машины для мойки планшетов. Указанный способ затем повторяли ещ два раза. Иммуноокрашивание выполняли при комнатной температуре. Клетки пермеабилизовали путем добавления 35 мкл PBS, содержащей 0,5% Tween 20, и инкубировали в течение 1 ч при комнатной температуре. Пермеабилизационный раствор удаляли и клетки промывали 250 мкл PBST с использованием автоматической машины для мойки планшетов. Указанный способ затем повторяли ещ два раза. 35 мкл блокирующего раствора (PBST, содержащий 3% (мас./об.) сухого сепарированного молока "Marvel"(Nestle добавляли к каждой лунке и планшеты инкубировали при комнатной температуре в течение минимум 1 ч. Затем после удаления блокирующего раствора с помощью машины для мойки планшетов 35 мкл мышиного античеловеческого АР моноклонального антитела (клон АР 441) (иммуноген - синтетический пептид, соответствующий аминокислотам 229-315 человеческого АР, связанным с гемоцианином лимфы улитки, DAKO, кодМ 3562), разбавленного 1:500 в блокирующем растворе, добавляли к каждой лунке и инкубировали в течение 1 ч. Затем этот раствор первичного антитела удаляли из лунок и далее промывали 3100 мкл PBST с использованием машины для мойки планшетов. Затем 35 мкл AlexaFluor 488 козлиного антимышиного IgG вторичного антитела (Invitrogen, кодА-11001), разбавленного 1:500 в блокирующем растворе, добавляли к каждой лунке. С этого времени всегда, когда это возможно,планшеты защищали от световой экспозиции. Планшеты инкубировали в течение 1 ч и затем раствор вторичного антитела удаляли из лунок с последующим промыванием 3100 мкл PBST с использованием машины для мойки планшетов. Затем 50 мкл PBST добавляли к каждой лунке и планшеты закрывали черной крышкой и хранили при 4C перед считыванием. Платы считывали в течение 6 ч завершения иммуноокрашивания. Зеленый флюоресцентный АР-связанный сигнал в каждой лунке измеряли с использованием ридераAcumen Explorer HTS (TTP Labtech Ltd., Кембридж). АР-связанное испускание флуоресценции может быть обнаружено при 530 нм с последующим возбуждением при 488 нм. Прибор представлял собой лазер-сканирующий флуоресцентный микропланшетный цитометр, который анализирует лунку с регулярными интервалам и использует пороговые алгоритмы для идентифицирования всех интенсивностей люминесцентного излучения выше фона раствора без необходимости генерирования и анализа изображения. Эти флуоресцирующие объекты могут быть определены количественно, что, таким образом, обеспечивает измерение уровней АР в клетках. Флуоресцентные данные о зависимости между дозой и ответом, полученные с каждым соединением экспортировали в пригодный комплект программного обеспечения (такой как Origin) для осуществления анализа с подбором кривой. Понижающую регуляцию уровней АР представляли в виде значения IC50. Данное значение определяли путем вычисления концентрации соединения, которая необходима для достижения 50% снижения сигнала АР. Следующая таблица раскрывает биологические данные для соединений настоящего изобретения с использованием вышеупомянутого анализа на понижающую регуляцию.
МПК / Метки
МПК: A61K 31/4196, C07D 471/04, A61P 35/00, C07D 487/04, A61K 31/437, C07D 519/00, A61K 31/5025
Метки: состояний, связанных, бициклические, производные, андрогенным, n-содержащие, применения, рецептором, лечении
Код ссылки
<a href="https://eas.patents.su/30-17144-n-soderzhashhie-biciklicheskie-proizvodnye-dlya-primeneniya-pri-lechenii-sostoyanijj-svyazannyh-s-androgennym-receptorom.html" rel="bookmark" title="База патентов Евразийского Союза">N-содержащие бициклические производные для применения при лечении состояний, связанных с андрогенным рецептором</a>
Предыдущий патент: Система и способ получения нитробензола
Следующий патент: Способ превращения углеводородов в этанол
Случайный патент: Долгоживущий глюкагоноподобный пептид 2(glp-2, гпп-2) для лечения желудочно-кишечных заболеваний и расcтройств