Производные 5-тиа-5-диоксо-4b-азаиндено[2,1-a]индена, обладающие аффинностью к рецептору серотонина
Номер патента: 9367
Опубликовано: 28.12.2007
Авторы: Джасти Венкатесварлу, Рао Венката Сатья Веерабхадра Вадламуди, Ширсатх Викас Шрикришна, Камбхампати Рама Састри, Рамакришна Венката Сатья Нироги
Формула / Реферат
1. Соединение общей формулы (I)

где A может представлять собой -СН2- или - СН2-СН2-;
где R1, R3, R4, R6, R7, R8 и R9 могут быть одинаковыми или различными, и каждый означает водород, галоген, линейный или разветвленный (C1-C6)алкил, линейный или разветвленный (C1-C6)алкокси;
R2 означает водород, галоген, тио, линейный или разветвленный (C1-C6)алкил, линейный или разветвленный (C1-C6)алкокси; цикло(С3-С7)алкокси; арилокси, ар(C1-С3)алкилокси, гетероарил(C1-С3)алкилокси;
или R7 и R8, вместе с атомами углерода, к которым они присоединены, могут образовывать пяти- или шестичленное кольцо;
R14 и R15 могут быть одинаковыми или различными, и каждый означает водород или линейный или разветвленный (C1-C6)алкил;
R13, R16 и R17 могут быть одинаковыми или различными, и каждый означает водород или линейный или разветвленный (C1-С6)алкил;
необязательно R13 вместе с или R16, или R17 и двумя атомами азота может образовывать 5-7-членное гетероциклическое кольцо, которое может быть дополнительно замещено водородом, (C1-С3)алкилом, (C1-С3)алкокси, ацетилом, фенилом, гетероарилом, гетероциклилом, бензилом и бензоилом;
n равно целому числу от 1 до 3;
где термин "арил" сам по себе или как часть других групп означает фенил или нафтил;
термин "гетероциклил" означает 5-6-членный гетероциклил, содержащий 1-2 гетероатома О или N;
термин "гетероарил" означает 5-6-членный гетероарил, содержащий 1-2 гетероатома О или N.
2. Соединение по п.1, которое выбирают из группы, включающей
10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид;
1-бром-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид;
1-хлор-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид;
2-бром-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид;
хлористо-водородную соль 2-бром-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]
инден-5,5-диоксида;
2-метокси-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид;
2-метокси-12-(4-метилпиперазин-1-илметил)-5-тиа-4b-азабензо[4,5]пенталено[1,2-b]нафталин-5,5-диоксид;
2-этокси-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид;
2-этокси-8-метил-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид;
2-бензилокси-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид;
2-циклопентилокси-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид;
2-циклогексилокси-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид;
2-(фуран-2-илметокси)-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид;
1,2,3-трихлор-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид;
2,8-диметокси-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид;
2-бром-8-метокси-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид;
8-метокси-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид;
хлористо-водородную соль 2-метокси-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксида;
8-изопропокси-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид;
2-бром-8-метил-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид;
4-метил-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид;
(RS) 8-метил-10-[1-(4-метилпиперазин-1-ил)этил]-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид;
(RS) 2-метокси-10-[1-(4-метилпиперазин-1-ил)этил]-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид;
(RS) 2-бром-8-метокси-10-[1-(4-метилпиперазин-1-ил)этил]-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид;
(RS) 1-[4-(8-метокси-5,5-диоксо-5Н-5-тиа-4b-азаиндено[2,1-а]инден-10-илметил)-2-метилпиперазин-1-ил]
этанон;
10-(4-пиридин-2-ил-пиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид;
8-метокси-10-(4-пиридин-2-ил-пиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид;
2-изопропокси-10-(4-бензоилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид;
2-(фуран-2-илметокси)-10-(4-бензоилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид;
10-(4-бензилпиперазин-1-илметил)-8-метил-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид;
10-(4-бензилпиперазин-1-илметил)-8-метокси-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид;
2-метокси-10-пиперазин-1-илметил-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид;
2-изопропокси-10-пиперазин-1-илметил-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид;
2-(фуран-2-илметокси)-10-пиперазин-1-илметил-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид;
10-[1,4]диазепан-1-илметил-2-метокси-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид;
1-[4-(5,5-диоксо-5Н-тиа-4b-азаиндено[2,1-а]инден-10-илметил)-[1,4]диазепан-1-ил]фенилметанон;
10-(4-этил-[1,4]диазепан-1-илметил)-2-метокси-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид;
10-(4-изопропил-[1,4]диазепан-1-илметил)-2-метокси-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид;
2-фтор-10-(4-этилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид;
2-метилтио-10-(4-этилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]индено-5,5-диоксид;
2-метилтио-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид;
8-метил-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид;
8-метил-10-(4-этилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид;
2-метокси-8-метил-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид;
2-метокси-10-(4-этилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид;
(RS) 1-[4-(2-метокси-5,5-диоксо-5Н-тиа-4b-азаиндено[2,1-а]инден-10-илметил)-2-метилпиперазин-1-ил]этанон;
10-(4-этилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид;
1-хлор-10-(4-этилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид;
1-метокси-10-(4-этилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5, 5-диоксид;
их стереоизомер и их соли.
3. Способ получения соединения общей формулы (I)

где А может представлять собой -СН2- или - СН2-СН2-;
где R1, R3, R4, R6, R7, R8 и R9 могут быть одинаковыми или различными, и каждый означает водород, галоген, линейный или разветвленный (C1-C6)алкил, линейный или разветвленный (C1-C6) алкокси;
R2 означает водород, галоген, тио, линейный или разветвленный (C1-C6)алкил, линейный или разветвленный (C1-C6)алкокси; цикло(С3-С7)алкокси; арилокси, ар(C1-С3)алкилокси, гетероарил(C1-С3)алкилокси;
или R7 и R8, вместе с атомами углерода, к которым они присоединены, могут образовывать пяти- или шестичленное кольцо;
R14 и R15 могут быть одинаковыми или различными, и каждый означает водород или линейный или разветвленный (C1-C6)алкил;
R13, R16 и R17 могут быть одинаковыми или различными, ш каждый означает водород или линейный или разветвленный (C1-С6)алкил;
необязательно R13 вместе с или R16, или R17 и двумя атомами азота может образовывать 5-7-членное гетероциклическое кольцо, которое может быть дополнительно замещено водородом, (C1-С3)алкилом, (C1-С3)алкокси, ацетилом, фенилом, гетероарилом, гетероциклилом, бензилом и бензоилом;
n равно целому числу от 1 до 3;
где термин "арил" сам по себе или как часть других групп означает фенил или нафтил;
термин "гетероциклил" означает 5-6-членный гетероциклил, содержащий 1-2 гетероатома О или N;
термин "гетероарил" означает 5-6-членный гетероарил, содержащий 1-2 гетероатома О или N;
который включает взаимодействие соединения формулы (II), приведенной ниже
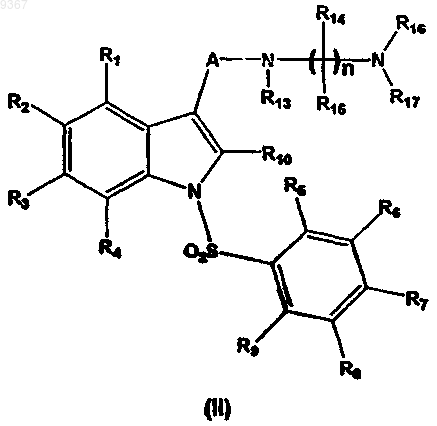
где R1, R2, R3, R4, R6, R7, R8, R9, R13, R14, R15, R16, R17 А и n определены выше, или его предшественника, где один из R5 или R10 означает атом галогена, такой как бром, хлор или иод, а второй означает водород; с производным тетракис(трифенилфосфин)палладия (0) или дихлор-бис(три-о-толилфосфин)палладия (II) в качестве катализатора.
4. Способ получения соединения общей формулы (I)
где А может представлять собой -СН2- или - СН2-СН2-;
где R1, R3, R4, R6, R7, R8 и R9 могут быть одинаковыми или различными, и каждый означает водород, галоген, линейный или разветвленный (C1-C6)алкил, линейный или разветвленный (C1-C6)алкокси;
R2 означает водород, галоген, тио, линейный или разветвленный (C1-C6)алкил, линейный или разветвленный (C1-C6)алкокси; цикло(С3-С7)алкокси; арилокси, ар(C1-С3)алкилокси, гетероарил(C1-С3)алкилокси;
или R7 и R8, вместе с атомами углерода, к которым они присоединены, могут образовывать пяти- или шестичленное кольцо;
R14 и R15 могут быть одинаковыми или различными, и каждый означает водород или линейный или разветвленный (C1-C6)алкил;
R13, R16 и R17 могут быть одинаковыми или различными, и каждый означает водород или линейный или разветвленный (C1-С6)алкил;
необязательно R13 вместе с или R16, или R17 и двумя атомами азота может образовывать 5-7-членное гетероциклическое кольцо, которое может быть дополнительно замещено водородом, (C1-С3)алкилом, (C1-С3)алкокси, ацетилом, фенилом, гетероарилом, гетероциклилом, бензилом и бензоилом;
n равно целому числу от 1 до 3;
где термин "арил" сам по себе или как часть других групп означает фенил или нафтил;
термин "гетероциклил" означает 5-6-членный гетероциклил, содержащий 1-2 гетероатома О или N;
термин "гетероарил" означает 5-6-членный гетероарил, содержащий 1-2 гетероатома О или N;
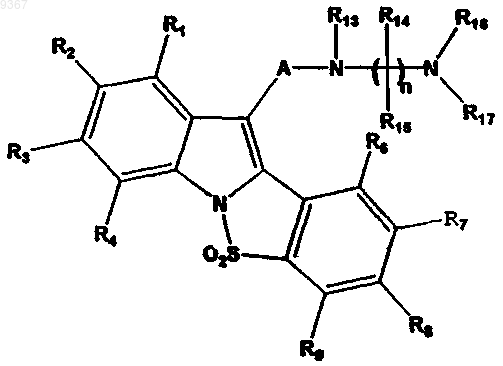
который включает взаимодействие соединения формулы (III), приведенной ниже
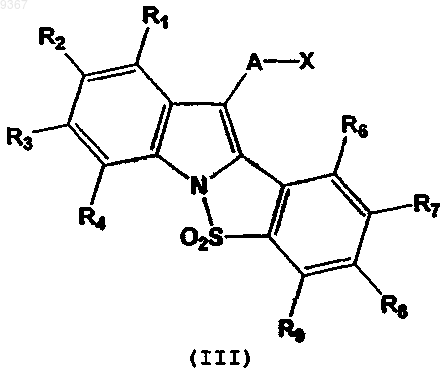
где все символы определены выше для соединения формулы, в которой A, R1, R2, R3, R4, R6, R7, R8 и R9 определены применительно к формуле (I), X означает водород или удаляемую группу, такую как гидрокси, мезил, тозил или галоген, например хлор, бром или иод, и т.п., с соединением формулы (IV) или его кислотно-аддитивной солью
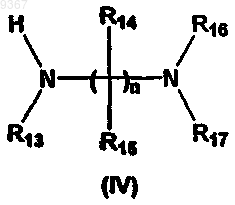
где все символы определены выше и X означает галоген, предпочтительно хлор, бром или иод.
5. Способ получения соединения общей формулы (I), где А означает -СН2-, который включает химическое или каталитическое восстановление соединений, в которых А означает СО, где все символы определены выше.
6. Способ по п.3 или 4, включающий осуществление одной или более из следующих необязательных стадий: i) удаление любой защитной группы; ii) разделение рацемической смеси на чистые энантиомеры в соответствии с известными методами и iii) получение фармацевтически приемлемой соли соединения формулы (I) и/или iv) получение его фармацевтически приемлемого пролекарства.
7. Фармацевтическая композиция, содержащая фармацевтически приемлемый носитель, разбавитель, эксципиент или сольват в сочетании с терапевтически эффективным количеством соединения по п.1, его стереоизомеров, его радиоактивных изотопов, его N-оксидов, его полиморфов, его фармацевтически приемлемых солей, его фармацевтически приемлемых сольватов, его полезных биоактивных метаболитов и любой приемлемой комбинации указанных веществ.
8. Фармацевтическая композиция по п.7 в форме таблетки, капсулы, порошка, сиропа, инъецируемой формы, раствора или суспензии.
9. Промежуточные соединения общей формулы (III)
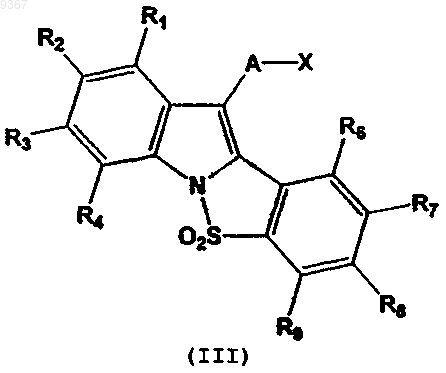
где А может означать -СН2-, -СН2-СН2-, -С=O или SO2;
X означает водород, удаляемую группу, такую как гидрокси, мезил, тозил или галоген, например хлор, бром или иод;
где R1, R3, R4, R6, R7, R8 и R9 могут быть одинаковыми или различными, и каждый означает водород, галоген, линейный или разветвленный (C1-C6)алкил, линейный или разветвленный (C1-C6)алкокси;
R2 означает водород, галоген, тио, линейный или разветвленный (C1-C6)алкил, линейный или разветвленный (C1-C6)алкокси; цикло(С3-С7)алкокси; арилокси, ap(C1-С3)алкилокси, гетероарил(C1-С3)алкилокси;
или R7 и R8, вместе с атомами углерода, к которым они присоединены, могут образовывать пяти- или шестичленное кольцо;
где термин "арил" сам по себе или как часть других групп означает фенил или нафтил;
термин "гетероарил" означает 5-6-членный гетероарил, содержащий 1-2 гетероатома О или N; и их стереоизомеры и их соли, при условии, что R1, R2, R3, R4, R6, R7, R8, R9 и X все не могут означать водород, так что 1Н-индол [1,2-b]бензо(d)изотиазол-10-метил-5,5'-диоксид формулы, приведенной ниже
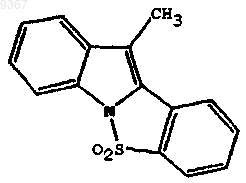
исключается из указанных соединений формулы (III).
10. Способ получения промежуточного соединения общей формулы (III) в соответствии с одним из вариантов, которые включают:
1) циклизацию соединения формулы (V), приведенной ниже
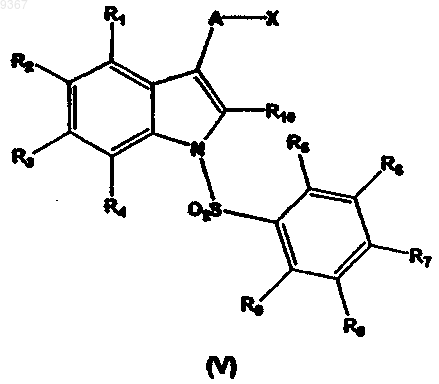
где X, A, R1, R2, R3, R4, R6, R7, R8 и R9 определены выше, и один из R10 и R5 означает атом галогена, например хлор, бром или иод и т.п., а другой означает водород; с использованием производного тетракис(трифенилфосфин)палладия(0) или дихлор-бис(три-о-толилфосфин)палладия(II) в качестве катализатора, и
2) превращение соединения формулы (VII), приведенной ниже
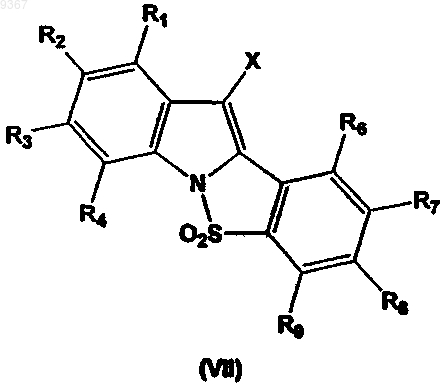
где X, R1, R2, R3, R4, R6, R7, R8 и R9 определены применительню ъ формуле (III), посредством металлизации и последующей реакции с газообразным SO2 и N-хлорсукцинимидом для получения соединения общей формулы (III), где А означает SO2.
11. Применение соединения общей формулы (I) по п.1 или его фармацевтической композиции по п.7 при получении лекарственных средств.
12. Применение соединения по п.1 при лечении и/или профилактике клинических состояний, таких как тревога, депрессия, судорожные расстройства, обсессивно-компульсивные расстройства, мигрень, головная боль, нарушение познавательной способности, ADHD (дефицит внимания/синдром гиперактивности), личностные расстройства, психоз, парафрения, психотическая депрессия, мания, шизофрения, шизофреноподобные расстройства, абстинентный синдром, приступы паники, хронобиологические аномалии, расстройства циркадного ритма, анксиолитическое расстройство, остеопороз, ишемический удар, риск развития синдрома внезапной смерти у младенцев, имеющих низкий эндогенный уровень мелатонина, проблемы репродуктивной сферы, глаукома, расстройства сна, а также расстройства, связанные с травмой спинного мозга и/или повреждением головы.
13. Применение соединения по п.1 при лечении умеренного ухудшения познавательной способности и/или других нейродегенеративных расстройств типа болезни Альцгеймера, паркинсонизма и хореи Хантингтона.
14. Применение соединения по п.1 при лечении некоторых расстройств ЖКТ (желудочно-кишечного тракта), таких как IBS (синдром раздраженного кишечника), или рвоты, вызванной химиотерапией.
15. Применение соединения по п.1 для лечения и профилактики заболеваний, связанных с избыточным весом.
16. Применение радиоактивно меченого соединения по п.1 в качестве диагностического инструмента для модуляции функции рецептора 5-НТ и/или мелатонина.
Текст
009367 Область техники, к которой относится изобретение Настоящее изобретение включает соединения, которые описываются общей формулой (I), их стереоизомеры, их радиоактивные изотопы, их N-оксиды, их полиморфы, их фармацевтически приемлемые соли, их фармацевтически приемлемые сольваты, их полезные биологически активные метаболиты и любую приемлемую комбинацию указанных выше веществ. Кроме того, настоящее изобретение включает также способы получения таких соединений общей формулы (I), их стереоизомеров, их радиоактивных изотопов, их N-оксидов, их полиморфов, их фармацевтически приемлемых солей, их фармацевтически приемлемых сольватов, их полезных биологически активных метаболитов, а также включает любую приемлемую комбинацию указанных выше веществ. Настоящее изобретение также описывает различные способы введения соединений, описываемых общей формулы (I), например фармацевтически приемлемых дозированных форм, и применение таких соединений и композиций либо в терапии, либо для диагностики. Соединения общей формулы (I) по настоящему изобретению являются лигандами 5-НТ (серотонина), то есть агонистами или антагонистами. Соединения общей формулы (I) по настоящему изобретению благодаря своим характерным химическим свойствам могут независимо или одновременно модулировать рецептор мелатонина, то есть либо указанные соединения являются мелатонергическими лигандами,например агонистами или антагонистами, либо могут взаимодействовать с рецепторами и 5-НТ, и/или мелатонина. Таким образом, соединения (I) по настоящему изобретению полезны для лечения заболеваний, таким образом, чтобы активность 5-НТ (серотонина) и/или мелатонина модулировалась с целью достижения желаемого терапевтического эффекта. В этой связи, соединения общей формулы (I) по настоящему изобретению могут быть полезны при лечении психотических, аффективных, вегетативных и психомоторных симптомов шизофрении и экстрапирамидальных двигательных побочных эффектов других антипсихотических средств; нейродегенеративных заболеваний, таких как болезнь Альцгеймера, болезнь Паркинсона и хорея Хантингтона, и рвоты,вызванной химиотерапией; а также при модуляции пищевого поведения, и в этой связи могут быть полезными в плане снижения уровней показателей заболеваемости и смертности, связанных с избыточным весом. Предпосылки создания изобретения Многие заболевания центральной нервной системы связаны с воздействием адренергических, допаминергических и серотонинергических нейротрансмиттерных систем. Серотонин участвует в развитии множества заболеваний и состояний, возникновение которых связано с центральной нервной системой. Перечень таких заболеваний включает заболевания и состояния, относящиеся ко сну, питанию, ощущению боли, регуляции температуры тела, регуляции давления крови, депрессии, тревоге, шизофрении и другим состояниям организма (ссылки: Fuller, R.W. Drugs Acting on Serotoninergic Neuronal Systems, inDeficiency, Wiley, Checester, 1978, pp. 1-340; Barchas J. et al., in "Serotonin and Behavior", Academic Press,NY (1973. Серотонин также играет важную роль в функционировании периферических систем, таких как желудочно-кишечная система, где было показано, что он опосредует множество сократительных,секреторных и электрофизиологических эффектов. В связи с широким распространением серотонина в организме проявляется огромный интерес, в том числе в плане применения, к лекарственным средствам, которые воздействуют на серотонинергические системы. В частности, предпочтительными являются те соединения, которые обладают рецепторспецифичным агонизмом и/или антагонизмом в случае лечения широкого перечня заболеваний, включая тревогу, депрессию, гипертензию, мигрень, ожирение, компульсивные расстройства, шизофрению, аутизм, некоторые нейродегенеративные заболевания типа болезни Альцгеймера, паркинсонизма, хореи Хантингтона, и рвоту, вызванную химиотерапией (ссылки: Gershon M.D. et al., 5-Hydroxytryptamine andOxford, 1989, p. 247-273; Saxena P.R. et al., Journal of Cardiovascular Pharmacology (1990), supplement 15, p. 17-34). Основные классы серотониновых рецепторов (5-HT1-7) содержат от 14 до 18 отдельных рецепторов,которые формально были классифицированы (ссылки: Glennon et al., Neuroscience and Behavioral Reviews(1990), 14, 35; and Hoyer D. et al., Pharmacol. Rev. (1994), 46, 157-203). Полученная в последнее время информация, касающаяся природы подтипов, их распределения, структуры и функций, позволяет предположить, что возможно идентифицировать новые средства, специфичные к тому или иному подтипу, обладающие улучшенными терапевтическими профилями и имеющие менее выраженные побочные эффекты. Рецептор 5-НТ 6 был идентифицирован в 1993 году (ссылки: Monsma et al., Mol. Pharmacol. (1993), 43,320-327; и Ruat M. et al., Biochem. Biophys. Res. Com. (1993), 193, 269-276). Некоторые антидепрессанты и нетипичные антипсихотические средства связываются с 5-НТ 6 с высокой аффинностью и такое связывание может представлять собой фактор, влияющий на профиль их активности (ссылки: Roth et al., J.Sleight et al., Brit. J. Pharmacol. (1998), 124, 556-562). Кроме того, рецептор 5-НТ 6 связан с генерализованным стрессом и состояниями тревоги (ссылки: Yoshioka et al., Life Sciences (1998), 17/18, 1473-1477). Указанные исследования и результаты наблюдений позволяют в совокупности предполагать, что соединение, которое является антагонистом рецепторов 5-НТ 6, будет полезным при лечении различных расстройств центральной нервной системы. Сообщается также, что антагонизм рецептора 5-НТ 6 может способствовать нейрональному росту в центральной нервной системе млекопитающих (WO 03/066056 A1). Имеются серьезные подтверждения того, что мелатонин важен для регуляции множества нервных и эндокринных функций, в особенности тех, для которых характерны циркадная и годичная ритмичность. В этой связи, огромный интерес проявляется к возможности получения клинически приемлемых аналогов мелатонина, которые были бы метаболически более стабильными, обладали агонистическими или антагонистическими характеристиками, и в отношении которых может ожидаться более выраженный терапевтический эффект в сравнении с самим гормоном. В патентной заявке РСТ приводится обширный перечень литературных данных, описывающих исследования по мелатонину и возможному терапевтическому применению различных лигандов, известных к настоящему времени. Указанные разнообразные эффекты проявляются через посредство мелатонин-специфичных рецепторов. Исследования по молекулярно-биологическим аспектам показали существование множества подтипов рецепторов, которые способны связывать данный гормон (Trends Pharmacol. Sci., 1995, 16, p. 50;WO 97 04094). Мелатонин воздействует на ЦНС, оказывая влияние на нервные механизмы через рецепторы, расположенные в мозге. Кроме того, ряд исследований указывает на наличие прямых эффектов мелатонина в периферических органах, осуществляемых через периферические рецепторы мелатонина. Мелатониновые рецепторы имеются в сердце, легких, предстательной железе, половых клетках, лейкоцитах, сетчатке, гипофизе, щитовидной железе, почке, кишечнике и кровеносных сосудах (Withyachumnamkul et al., Life Sci, 12 65, 1986). Три подтипа мелатониновых рецепторов были идентифицированы как МТ-1, МТ-2 и Mel-1 с (Barreft et al., Biol. Signals Recept., 1999, 8: 6-14). Имеются данные, позволяющие предполагать, что и агонисты, и антагонисты мелатонина могут найти терапевтическое применение в случае разного рода заболеваний и состояний. В РСТ заявке WO 00/72815 приводится подробное обсуждение возможностей практического внедрения и вариантов использования таких соединений, и их детали включены в настоящее описание посредством ссылки. Кроме того, в патенте США 6465660 и в публикации патентной заявки США 2003/0105087 обсуждаются некоторые трициклические индольные и трициклические азаиндольные производные, обладающие очень ценными фармакологическими свойствами в отношении мелатонинергических рецепторов. Патент США 4839377 и патент США 4855314 относятся к 5-замещенным 3 аминоалкилиндолам. Отмечается, что данные соединения будут полезны для лечения мигрени. Британский патент 2035310 относится к 3-аминоалкил-1 Н-индол-5-тиоамидам и к карбоксамидам. Отмечается, что указанные соединения полезны при лечении гипертензии, болезни Реймонда и мигрени. Публикация европейского патента 303506 относится к 3-полигидропиридил-5-замещенным 1 Ниндолам. Отмечается, что указанные соединения обладают агонистической активностью в отношении рецептора 5-HT1 и сосудосуживающей активностью, и полезны при лечении мигрени. Публикация европейского патента 354777 относится к производным N-пиперидинилиндолилэтилалкансульфонамида. Отмечается, что указанные соединения являются агонистами 5-HT1 рецептора, обладают сосудосуживающей активностью и полезны при лечении головной боли. Публикация европейского патента 438230 относится к индолзамещенным 5-членным гетероароматическим соединениям. Отмечается, что указанные соединения обладают агонистической активностью в отношении "5-НТ 1-подобного" рецептора и полезны при лечении мигрени и других расстройств, в отношении которых показано применение селективного агониста указанных рецепторов. Публикация европейского патента 313397 относится к производным 5-гетероциклического индола. Отмечается, что указанные соединения обладают исключительными свойствами в плане лечения и профилактики мигрени, очаговой головной боли и головной боли, связанной с сосудистыми расстрой-2 009367 ствами. Отмечается также, что указанные соединения обладают исключительным агонизмом в отношении "5-НТ 1-подобного" рецептора. Публикация международной патентной заявки WO 91/18897 относится к производным 5 гетероциклического индола. Отмечается, что указанные соединения обладают исключительными свойствами в плане лечения и профилактики мигрени, очаговой головной боли и головной боли, связанной с сосудистыми расстройствами. Отмечается также, что данные соединения обладают исключительным агонизмом в отношении"5-НТ 1-подобного" рецептора. Публикация европейского патента 457701 относится к производным арилоксиамина как обладающим высокой аффинностью в отношении серотониновых рецепторов 5-HT1D. Отмечается, что указанные соединения полезны для лечения заболеваний, связанных с дисфункцией рецептора серотонина, например мигрени. Публикация европейского патента 497512 A2 относится к классу производных имидазола, триазола и тетразола, которые являются селективными агонистами "5-НТ 1-подобных" рецепторов. Отмечается,что указанные соединения полезны для лечения мигрени и связанных с нею расстройств. В публикации международной патентной заявки WO 93/00086 описан ряд тетрагидрокарбазольных производных в качестве агонистов 5-НТ 1 рецептора, применяемых для лечения мигрени и родственных состояний. В публикации международной патентной заявки WO 93/23396 описаны производные конденсированных имидазолов и триазолов как агонисты 5-НТ 1 рецептора, применяемые для лечения мигрени и других расстройств.Schoeffter P. et al. описали метил-4-4-[4-(1,1,3-триоксо-2 Н-1,2-бензоизотиазол-2-ил)бутил]-1 пиперазанил-1 Н-индол-3-карбоксилат как селективный антагонист 5-HT1A рецептора, в работе, озаглавленной как "SDZ216-525, a selective and potent 5-HT1A receptor antagonist", European Journal of Pharmacology, 244, 251-257 (1993). Публикация международной патентной заявки WO 94/06769 относится к производным 2 замещенного 4-пиперазинбензотиофена, которые являются средствами, действующими в отношении серотонинового рецептора 5-HT1A и 5-HT1D, применяемыми при лечении тревоги, депрессии, мигрени, удара, стенокардии и гипертензии.(1997), 445-453) тетрациклическое индольное производное - 1 Н-индол[1,2-b]бензо(d)изотиазол-10-метил 5,5'-диоксид (структуру см. ниже, Benincori et al, соединение 9, в приведенной выше ссылке). Авторы синтезировали указанное соединение случайно, оно было получено в качестве примеси в ходе синтеза некоторых димерных индольных лигандов, в рамках разработок хиральных анизотропных бигетероароматических дифосфинов. Однако указанное выше соединение не было упомянуто авторами ни в одной из заявок. Краткое описание сущности изобретения Настоящее изобретение относится к соединениям общей формулы (I), их стереоизомерам, их радиоактивным изотопам, их N-оксиду, их полиморфам, их фармацевтически приемлемым солям, их фармацевтически приемлемым сольватам, их полезным биологически активным метаболитам и к любому приемлемому сочетанию указанных выше веществ. Соединения общей формулы (I) приведены ниже-3 009367 где А может представлять собой -CR11R12-, -C=O или -SO2-; где R1, R2, R3, R4, R6, R7, R8, R9, R11, R12, R13, R14 и R15 могут быть одинаковыми или различными, и каждый независимо означает водород, галоген, оксо, тио, пергалогеналкил, пергалогеналкокси, гидрокси,амино, нитро, циано, формил, амидино, гуанидино, замещенные или незамещенные группы, выбранные из линейного или разветвленного (C1-C12)алкила, (С 2-С 12)алкенила, (С 2-С 12)алкинила, (С 3-С 7)циклоалкила, (С 3-С 7)циклоалкенила, бициклоалкила, бициклоалкенила, (С 1-С 12)алкокси, цикло(С 3-С 7)алкокси,арила, арилокси, аралкила, аралкокси, гетероциклила, гетероарила, гетероциклилалкила, гетероаралкила,гетероарилокси, гетероаралкокси, гетероциклилалкилокси, ацила, ацилокси, ациламино, моноалкиламино, диалкиламино, ариламино, диариламино, аралкиламино, алкоксикарбонила, арилоксикарбонила,аралкоксиарбонила, гетероциклилалкоксикарбонила, гетероарилоксикарбонила, гидроксиалкила, аминоалкила, моноалкиламиноалкила, диалкиламиноалкила, алкоксиалкила, арилоксиалкила, аралкоксиалкила,алкилтио, тиоалкила, алкоксикарбониламино, арилоксиарбониламино, аралкилоксиарбониламино, аминокарбониламино, алкиламинокарбониламино, диалкиламинокарбониламино, алкиламидино, алкилгуанидино, диалкилгуанидино, гидразино, гидроксиламино, карбоновой кислоты и ее производных, сульфоновых кислот и их производных, фосфорной кислоты и ее производных; или смежные группы типа R1 иR2, или R2 и R3, или R3 и R4, или R6 и R7, или R7 и R8, или R8 и R9, вместе с атомами углерода, к которым они присоединены, могут образовывать пяти- или шестичленное кольцо, необязательно содержащее одну или более двойных связей и необязательно содержащее один или более гетероатомов, выбранных из кислорода, азота, серы или селена и сочетаний двойной связи и гетероатомов; или необязательно R11 иR12 вместе с атомами углерода, к которым они присоединены, могут образовывать трех-шестичленное кольцо, необязательно содержащее одну или более двойных связей и необязательно содержащее один или более гетероатомов, выбранных из кислорода, азота, серы или селена и сочетаний двойной связи и гетероатомов; или необязательно R11 или R12 могут образовывать связь с или R16, или R17 с получением 5-,6- или 7-членного гетероциклического кольца, которое может быть дополнительно замещено R14 и R15 и может содержать одну, две или три двойных связи;R13, R16 и R17 могут быть одинаковыми или различными, и каждый независимо означает водород,замещенные или незамещенные группы, выбранные из линейного или разветвленного (С 1-С 12)алкила,(С 2-С 12)алкенила, (С 2-С 12)алкинила, (С 3-С 7)циклоалкила, (С 3-С 7)циклоалкенила, бициклоалкила, бициклоалкенила, арила, аралкила, гетероарила, гетероциклилалкила; необязательно R13 вместе с или R16, илиR17 и двумя атомами азота может образовывать 5-, 6- или 7-членное гетероциклическое кольцо, которое может быть дополнительно замещено R14 и R15 и может содержать одну, две или три двойных связи; иn равно целому числу от 1 до 4, где углеродные цепи, для которых указывается параметр "n", могут быть линейными или разветвленными. Ниже приведен частичный перечень таких соединений общей формулы (I): 10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид; 1-бром-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид; 1-хлор-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид; 2-бром-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид; Хлористо-водородная соль 2-бром-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1 а]инден-5,5-диоксида; 2-метокси-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид; 2-метокси-12-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[4,5]пенталено[1,2-b]нафталин-5,5 диоксид; 2-этокси-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид; 2-этокси-8-метил-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид; 2-бензилокси-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид; 2-циклопентилокси-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид; 2-циклогексилокси-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид; 2-(фуран-2-илметокси)-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5 диоксид; 1,2,3-трихлор-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид; 2,8-диметокси-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид; 2-бром-8-метокси-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид; 8-метокси-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид; Хлористо-водородная соль 8-метокси-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1 а]инден-5,5-диоксида; 8-изопропокси-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид; 2-бром-8-метил-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид; 4-метил-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид;(RS) 1-[4-(8-метокси-5,5-диоксо-5 Н-5-тиа-4b-азаиндено[2,1-а]инден-10-илметил)-2-метилпиперазин-1-ил]этанон; 10-(4-пиридин-2-ил-пиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид; 8-метокси-10-(4-пиридин-2-илпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид; 2-изопропокси-10-(4-бензоилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид; 2-(фуран-2-илметокси)-10-(4-бензоилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5 диоксид; 10-(4-бензилпиперазин-1-илметил)-8-метил-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид; 10-(4-бензилпиперазин-1-илметил)-8-метокси-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид; 2-метокси-10-пиперазин-1-илметил-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид; 2-изопропокси-10-пиперазин-1-илметил-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид; 2-(фуран-2-илметокси)-10-пиперазин-1-илметил-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид; 10-[1,4]диазепан-1-илметил-2-метокси-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид; 1-[4-(5,5-диоксо-5 Н-5-тиа-4b-азаиндено[2,1-а]инден-10-илметил)-[1,4]диазепан-1-ил]фенилметанон; 10-(4-этил-[1,4]диазепан-1-илметил)-2-метокси-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид и 10-(4-изопропил-[1,4]диазепан-1-илметил)-2-метокси-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид; или их стереоизомер, полиморф, или любое приемлемое сочетание указанных выше соединений, оксид азота; пролекарство данного соединения или его оксида азота; фармацевтически приемлемая соль данного соединения, оксида азота или пролекарства; или сольват или гидрат данного соединения, оксида азота,пролекарства или фармацевтически приемлемой соли. Настоящее изобретение также относится к многочисленным способам получения соединений общей формулы (I), их стереоизомеров, их радиоактивных изотопов, их N-оксида, их полиморфов, их фармацевтически приемлемых солей, их фармацевтически приемлемых сольватов, их полезных биологически активных метаболитов и любой подходящей комбинации указанных выше соединений. В случае тех соединений общей формулы (I), где может иметь место таутомерия, настоящее изобретение относится ко всем возможным таутомерным формам и их возможным смесям. Настоящее изобретение также относится к стереоизомерам, которые, как правило, получают в виде рацематов, которые могут быть разделены на оптически активные изомеры известным как таковым способом. Настоящее изобретение также относится к радиоактивно меченым изотопам, которые идентичны соединениям, описываемым общей формулой (I), но в которых один или более атомов заменены атомом,имеющим атомную массу или массовое число, отличные от атомной массы или массового числа обычно встречающихся в природе. Примеры изотопов, которые могут быть включены в соединения по настоящему изобретению, включают изотопы водорода, углерода, азота, кислорода, фосфора, фтора, хлора,иода, брома и технеция, например 2 Н, 3 Н, 11C, 13 С, 14C, 13N, 15N, 15O, 18F, 99mTc, 31P, 33S, 123I и 125I. Те соединения общей формулы (I), описанные выше, которые содержат указанные выше изотопы и/или другие изотопы других атомов, входят в объем настоящего изобретения. В том случае, когда соединения общей формулы (I) обладают геометрической изомерией, настоящее изобретение относится ко всем таким геометрическим изомерам. Термин "оксид азота" или "N-оксид" относится к продукту окисления по меньшей мере одного из двух атомов азота в соединении общей формулы (I) (например, моно- или диоксид). Монооксиды азота могут существовать в виде одного позиционного изомера или в виде смеси 2 позиционных изомеров(например, смеси 1-N-оксида и 4-N-оксида пиперазина или смеси 1-N-оксида и 4-N-оксида пиперазинов). Подходящие фармацевтически приемлемые кислотно-аддитивные соли соединения общей формулы(I) могут быть получены из указанных выше основных соединений по настоящему изобретению, которые представляют собой соединения, образующие нетоксичные кислотно-аддитивные соли, и включают соли, содержащие фармакологически приемлемые анионы, такие как гидрохлорид, гидробромид, гидроиодид, нитрат, сульфат, бисульфат, фосфат, кислый фосфат, ацетат, лактат, цитрат, кислый цитрат, тартрат,битартрат, сукцинат, малеат, фумарат, глюконат, сахарат, бензоат, метансульфонат, этансульфонат, бензолсульфонат, п-толуолсульфонат, пальмоат и оксалат. Фармацевтически приемлемые соли, составляющие часть настоящего изобретения, приводятся с целью пояснения, но не для ограничения изобретения указанным выше перечнем. Подходящие фармацевтически приемлемые основно-аддитивные соли соединений общей формулы(I) могут быть получены из указанных выше кислых соединений по настоящему изобретению, которые образуют нетоксичные основно-аддитивные соли, и включают соли, содержащие фармацевтически приемлемые катионы, такие как литий, натрий, калий, кальций и магний, а также соли органических оснований, таких как лизин, аргинин, гуанидин, диэтаноламин, холин, трометамин и т.п.; соли аммония или замещенного аммония. Фармацевтически приемлемые соли, составляющие часть настоящего изобретения, приводятся с целью пояснения, но не для ограничения изобретения указанным выше перечнем. Кроме того, фармацевтически приемлемые соли соединения общей формулы (I) могут быть полу-5 009367 чены путем превращения производных, которые содержат третичные аминогруппы, в соответствующие четвертичные аммониевые соли по методам, описанным в литературе, при использовании кватернизирующих средств. Возможные кватернизирующие средства представляют собой, например, алкилгалогениды, такие как метилиодид, этилиодид и н-пропилхлорид, включая арилалкилгалогениды, такие как бензилхлорид или 2-фенилэтилбромид. В дополнение к фармацевтически приемлемым солям в объем настоящего изобретения также включены другие соли. Они могут служить в качестве промежуточных соединений при очистке соединений,при получении других солей или в методах идентификации и характеристики соединений или промежуточных соединений. Фармацевтически приемлемые соли соединений общей формулы (I) могут существовать в виде сольватов, таких как сольваты, образуемые с водой, метанолом, этанолом, диметилформамидом, этилацетатом и т.п. Могут быть также получены смеси таких сольватов. Источником образования такого сольвата может служить растворитель кристаллизации, который может представлять собой как исходный растворитель способа получения или процесса кристаллизации, так и дополнительный компонент, добавляемый к такому растворителю. Такие сольваты включены в объем настоящего изобретения. Настоящее изобретение также охватывает фармацевтически приемлемые пролекарства соединений общей формулы (I). Пролекарство представляет собой лекарство, которое было химически модифицировано, так что может стать биологически неактивным в сайте своего действия, но которое может быть далее подвергнуто разложению или модификации в ходе одного или более ферментативных или других процессов, протекающих in vivo, в исходную форму. Указанное пролекарство должно иметь иной фармакокинетический профиль, чем исходное соединение, что облегчает его всасывание через эпителий слизистой мембраны, оно должно легче образовывать соль или обладать лучшей растворимостью и/или улучшенной системной стабильностью (например, повышенным периодом полувыведения из плазмы). В типичном случае такие химические модификации включают следующие соединения: 1) сложноэфирные или амидные производные, которые могут расщепляться эстеразами или липазами; 2) пептиды, которые могут распознаваться специфическими или неспецифическими протеазами; или 3) производные, которые могут накапливаться в сайте своего действия за счет селективного прохождения через мембрану пролекарственной формы или модифицированной пролекарственной формы; или 4) любая комбинация производных 1-3 из числа указанных выше. Традиционные методики отбора и получения подходящих пролекарственных производных описаны, например, Н. Bundgard, в Design of prodrugs, (1985). Другой аспект настоящего изобретения включает фармацевтическую композицию, содержащую по меньшей мере одно из соединений общей формулы (I), их производных, их аналогов, производных таких аналогов, их стереоизомеров, их полиморфов, их фармацевтически приемлемых солей, их фармацевтически приемлемых сольватов в качестве активного ингредиента, вместе с фармацевтически применяемыми носителями, дополнительными компонентами и т.п. Эффективное количество соединения общей формулы (I) или его соли используют для получения лекарственных средств по настоящему изобретению вместе с традиционными фармацевтическими дополнительными компонентами, носителями и добавками. Настоящее изобретение также относится к фармацевтически приемлемым композициям, содержащим указанные соединения, и к применению таких соединений и композиций в медицине. Соединения общей формулы (I) по настоящему изобретению полезны при лечении и/или профилактике состояний, при которых желательна модуляция активности 5-НТ. Соединения общей формулы (I) по настоящему изобретению полезны при лечении и/или профилактике состояний, при которых желательна модуляция активности мелатонина. Соединения общей формулы (I) по настоящему изобретению полезны при лечении и/или профилактике состояний, при которых модуляция активности 5-НТ и мелатонина дает желаемый эффект. Настоящее изобретение относится к применению соединений общей формулы (I), описанной выше,при производстве лекарственных средств, которые могут применяться при лечении и/или профилактике некоторых заболеваний ЦНС, таких как психоз, парафрения, тревога, депрессия, мания, шизофрения,шизофреноподобные расстройства, мигрень, головная боль, лекарственная зависимость, судорожные расстройства, личностные расстройства, гипертензия, аутизм, посттравматический стресс-синдром, алкоголизм, приступы паники, обсессивно-компульсивные расстройства, хронобиологические аномалии и расстройства циркадного ритма, нарушения познавательной способности, такие как болезнь Альцгеймера и возрастное снижение познавательной способности, ADHD (расстройство, связанное с дефицитом внимания/синдром гиперактивности), абстинентный синдром, такой как в случае приема кокаина, этанола, никотина и бензодиазепинов, приступы паники, а также расстройства, связанные с травмой спинного мозга и/или повреждением головы, такие как гидроцефалия. В число других состояний с низким эндогенным уровнем мелатонина, при которых также можно достичь благоприятного эффекта, входят остеопороз, ишемический удар, риск развития синдрома внезапной смерти у младенцев, проблемы репродук-6 009367 тивной сферы, глаукома и расстройства сна. Ожидается, что соединения по настоящему изобретению могут быть полезны при лечении умеренного ухудшения познавательной способности и других нейродегенеративных расстройств типа болезни Альцгеймера, паркинсонизма и хореи Хантингтона. Ожидается, что соединения по настоящему изобретению могут применяться при лечении некоторых расстройств ЖКТ (желудочно-кишечного тракта), таких как IBS (синдром раздраженного кишечника), или рвоты, вызванной химиотерапией. Ожидается также, что соединения по настоящему изобретению могут применяться при модуляции пищевого поведения, а также указанные соединения могут использоваться для снижения уровня заболеваемости и смертности, связанных с избыточным весом. Настоящее изобретение относится к способу лечения человека или животного, страдающих от некоторых заболеваний ЦНС, таких как тревога, депрессия, судорожные расстройства, обсессивнокомпульсивные расстройства, мигрень, головная боль, нарушение познавательной способности, такое как болезнь Алыдгеймера и возрастное снижение познавательной способности, ADHD (гиперактивное расстройство, связанное с дефицитом внимания), личностные расстройства, психоз, парафрения, психотическая депрессия, мания, шизофрения, шизофреноподобные расстройства, абстинентный синдром,такой как в случае приема кокаина, этанола, никотина и бензодиазепинов, приступы паники, хронобиологические аномалии, расстройства циркадного ритма, анксиолитическое расстройство, остеопороз,ишемический удар, с целью снижения риска синдрома внезапной смерти у младенцев, имеющих низкий эндогенный уровень мелатонина, при лечении репродуктивной сферы, глаукомы, расстройств сна (включая нарушения циркадного ритма), а также расстройств, связанных с травмой спинного мозга и/или повреждением головы, таких как гидроцефалия. Ожидается, что соединения по настоящему изобретению полезны при лечении умеренного ухудшения познавательной способности, нейродегенеративных расстройств типа болезни Альцгеймера, паркинсонизма и хореи Хантингтона. Настоящее изобретение также относится к способу модуляции функции рецептора 5-НТ и/или мелатонина, желаемой в некоторых случаях. Соединения по настоящему изобретению могут вводиться в сочетании с другими фармацевтическими средствами, такими как ингибиторы аро-В/МТР, агонисты MCR-4, агонисты ССК-А, ингибиторы повторного поглощения моноамина, симпатомиметические средства, агонисты адренергического рецептора, агонисты допамина, аналоги рецептора меланоцит-стимулирующего гормона, антагонисты каннабиноидного рецептора 1, антагонисты меланин-концентрирующего гормона, лептины, аналоги лептинов,агонисты рецепторов лептина, антагонисты галанина, ингибиторы липазы, агонисты бомбезина, антагонисты нейропептида-Y, тиромиметические средства, дегидроэпиандростерон или его аналоги, агонисты или антагонисты глюкокортикоидного рецептора, антагонисты рецептора орексина, антагонисты урокортин-связывающего белка, агонисты рецептора глюкагон-подобного пептида-1, цилиарные нейротропные факторы, AGRP (агути-родственные белки человека), антагонисты рецептора грелина, антагонисты или обратные агонисты рецептора гистамина 3, агонисты рецептора нейромедина U и т.п., в терапевтически эффективном количестве, в виде подходящей фармацевтической композиции, для достижения желаемого эффекта у млекопитающих, в том числе у людей. Фраза "фармацевтически приемлемый" означает, что вещество или композиция должны быть совместимы химически и/или токсикологически с другими ингредиентами, входящими в состав композиции, и/или применительно к млекопитающему, подвергаемому лечению. Термины "лечение" или "терапия" охватывают все значения, такие как их превентивный, профилактический и паллиативный вариант. Термин "соединения по настоящему изобретению" (если особо не указано иное) относится к соединениям формулы (I), их оксидам азота, пролекарствам соединений или их оксидов азота, фармацевтически приемлемым солям соединений, оксидов азота и/или пролекарств и гидратам или сольватам соединений, их оксидов азота, солей и/или пролекарств, а также ко всем стереоизомерам (включая диастереоизомеры и энантиомеры), таутомерам и меченным изотопами соединениям. Настоящее изобретение также относится к новым промежуточным соединениям, описываемым общей формулой (III), их стереоизомерам, их радиоактивным изотопам, их N-оксиду, их солям, их сольватам и любому приемлемому сочетанию указанных выше веществ, используемым при получении соединений общей формулы (I), и к способу получения таких промежуточных соединений. Подробное описание изобретения Настоящее изобретение относится к соединениям общей формулы (I), их стереоизомерам, их радиоактивным изотопам, их N-оксидам, их полиморфам, их фармацевтически приемлемым солям, их фармацевтически приемлемым сольватам, их полезным биологически активным метаболитам и любому приемлемому сочетанию указанных выше веществ. Настоящее изобретение относится к соединениям общей формулы (I), описанным ниже где А может представлять собой -CR11R12-, -C=O или -SO2-; где R1, R2, R3, R4, R6, R7, R8, R9, R11, R12, R13, R14 и R15 могут быть одинаковыми или различными, и каждый означает водород, галоген, оксо, тио, пергалогеналкил, пергалогеналкокси, гидрокси, амино,нитро, циано, формил, амидино, гуанидино, замещенные или незамещенные группы, выбранные из линейного или разветвленного (С 1-С 12)алкила, (С 2-С 12)алкенила, (C2-C12)алкинила, (С 3-С 7)циклоалкила, (С 3 С 7)циклоалкенила, бициклоалкила, бициклоалкенила, (С 1-С 12)алкокси, цикло(С 3-С 7)алкокси, арила, арилокси, аралкила, аралкокси, гетероциклила, гетероарила, гетероциклилалкила, гетероаралкила, гетероарилокси, гетероаралкокси, гетероциклилалкилокси, ацила, ацилокси, ациламино, моноалкиламино, диалкиламино, ариламино, диариламино, аралкиламино, алкоксикарбонила, арилоксикарбонила, аралкоксиарбонила, гетероциклилалкоксикарбонила, гетероарилоксикарбонила, гидроксиалкила, аминоалкила,моноалкиламиноалкила, диалкиламиноалкила, алкоксиалкила, арилоксиалкила, аралкоксиалкила, алкилтио, тиоалкила, алкоксикарбониламино, арилоксикарбониламино, аралкилоксикарбониламино, аминокарбониламино, алкиламинокарбониламино, диалкиламинокарбониламино, алкиламидино, алкилгуанидино, диалкилгуанидино, гидразино, гидроксиламино, карбоновой кислоты и ее производных, сульфоновых кислот и их производных, фосфорной кислоты и ее производных; или смежные группы типа R1 и R2,или R2 и R3, или R3 и R4, или R6 и R7, или R7 и R8, или R8 и R9, вместе с атомами углерода, к которым они присоединены, могут образовывать пяти- или шестичленное кольцо, необязательно содержащее одну или более двойных связей и необязательно содержащее один или более гетероатомов, выбранных из кислорода, азота, серы или селена и сочетаний двойной связи и гетероатомов; или необязательно R11 и R12 вместе с атомами углерода, к которым они присоединены, могут образовывать трех-шестичленное кольцо, необязательно содержащее одну или более двойных связей и необязательно содержащее один или более гетероатомов, выбранных из кислорода, азота, серы или селена и сочетаний двойной связи и гетероатомов; или необязательно R11 или R12 могут образовывать связь с или R16, или R17 с получением 5-, 6 или 7-членного гетероциклического кольца, которое может быть дополнительно замещено R14 и R15 и может содержать одну, две или три двойных связи;R13, R16 и R17 могут быть одинаковыми или различными, и каждый независимо означает водород,замещенные или незамещенные группы, выбранные из линейного или разветвленного (С 1-С 12)алкила,(С 2-С 12)алкенила, (С 2-С 12)алкинила, (С 3-С 7)циклоалкила, (С 3-С 7)циклоалкенила, бициклоалкила, бициклоалкенила, арила, аралкила, гетероарила, гетероциклилалкила; необязательно R13 вместе с или R16, илиR17 и двумя атомами азота может образовывать 5-, 6- или 7-членное гетероциклическое кольцо, которое может быть дополнительно замещено R14 и R15 и может содержать одну, две или три двойных связи; иn равно целому числу от 1 до 4, где углеродные цепи, к которым относится n, могут быть линейными или разветвленными. Подходящие группы, обозначаемые R1, R2, R3, R4, R6, R7, R8, R9, R11, R12, R14 и R15, в соответствующем варианте могут быть выбраны из следующей группы атома галогена, такого как фтор, хлор, бром или иод; пергалогеналкила, в частности, пергалоген(C1-С 6)алкила, такого как фторметил, дифторметил,трифторметил, трифторэтил, фторэтил, дифторэтил и т.п.; пергалогеналкокси, в частности, пергалоген(C1-C6)алкокси, такого как фторметилокси, дифторметилокси, трифторметилокси и т.п.; замещенной или незамещенной (C1-C12)алкильной группы, в особенности линейной или разветвленной (C1C8)алкильной группы, такой как метил, этил, н-пропил, изопропил, н-бутил, изобутил, трет-бутил, нпентил, изопентил, гексил, изогексил, гептил, октил и т.п.; замещенной или незамещенной (С 2 С 12)алкенильной группы, такой как этилен, н-пропилен, пентенил, гексенил, гептинил, гептадиенил и т.п.; (С 2-С 12)алкинила, замещенной или незамещенной (С 2-С 12)алкинильной группы, такой как ацетилен и т.п.; цикло(С 3-С 7)алкильной группы, такой как циклопропил, циклобутил, циклопентил, циклогексил,циклогептил, где циклоалкильная группа может быть замещена; цикло(С 3-С 7)алкенильной группы, такой как циклопентенил, циклогексенил, циклогептинил, циклогептадиенил, циклогептатриенил и т.п., где циклоалкенильная группа может быть замещена; (C1-C12)алкокси, в особенности (C1-С 6)алкоксигруппы,такой как метокси, этокси, пропилокси, бутилокси, изопропилокси и т.п., которая может быть замещена;-8 009367 цикло(С 3-С 7)алкоксигруппы, такой как циклопропилокси, циклобутилокси, циклопентилокси, циклогексилокси, циклогептилокси и т.п., где циклоалкоксигруппа может быть замещена; арильной группы, такой как фенил или нафтил, где арильная группа может быть замещена; аралкильной группы, такой как бензил, фенетил, С 6 Н 5 СН 2 СН 2 СН 2, нафтилметил и т.п., где аралкильная группа может быть замещена, и замещенный аралкил представляет собой группу, такую как СН 3 С 6 Н 4 СН 2, Hal-C6H4CH2, СН 3 ОС 6 Н 4 СН 2,СН 3 ОС 6 Н 4 СН 2 СН 2 и т.п.; аралкоксигруппы, такой как бензилокси, фенетилокси, нафтилметилокси, фенилпропилокси и т.п., где аралкоксигруппа может быть замешена; гетероциклильных групп, таких как азиридинил, пирролидинил, морфолинил, пиперидинил, пиперазинил и т.п., где гетероциклильная группа может быть замещена; гетероарильной группы, такой как пиридил, тиенил, фурил, пирролил, оксазолил,имидазолил, оксадиазолил, тетразолил, бензопиранил, бензофуранил и т.п., где гетероарильная группа может быть замещена; гетероцикло(C1-С 6)алкила, такого как пирролидинилалкил, пиперидинилалкил,морфолинилалкил, тиоморфолиналкил, оксазолинилалкил и т.п., где гетероцикло(C1-С 6)алкильная группа может быть замещена; гетероаралкильной группы, такой как фуранилметил, пиридинилметил, оксазолилметил, оксазолилэтил и т.п., где гетероаралкильная группа может быть замещена; гетероарилокси,гетероаралкокси, гетероциклоалкокси, где гетероарильная, гетероаралкильная, гетероциклоалкильная и гетероциклилалкильная группы определены выше и могут быть замещены; таких как фуран-2 илметокси-; ацильных групп, таких как ацетил, пропионил или бензолил, где ацильная группа может быть замещена; ацилоксигруппы, такой как СН 3 СОО, СН 3 СН 2 СОО, С 6 Н 5 СОО и т.п., которая может быть необязательно замещена; ациламиногруппы, такой как CH3CONH, CH3CH2CONH, C3C7CONH,C6H5CONH, которая может быть замещена; (C1-C6)моноалкиламиногруппы, такой как CH3NH, C2H5NH,C3H7NH, C6H13NH и т.п., которая может быть замещена; (C1-C6)диалкиламиногруппы, такой как N(CH3)2,CH3(C2H5)N и т.п., которая может быть замещена; ариламиногруппы, такой как C6H5NH, CH3(C6H5)N,C6H4(CH3)NH, NH-C6H4-Hal и т.п., которая может быть замещена; арилалкиламиногруппы, такой какC6H5CH2NH, C6H5CH2CH2NH, C6H5CH2NCH3 и т.п., которая может быть замещена; гидрокси(C1C6)алкила, который может быть замещен; амино(C1-C6)алкила, который может быть замещен; моно(C1C6)алкиламино(C1-C6)алкильной, ди(C1-C6)алкиламино(C1-C6)алкильной групп, которые могут быть замещены; алкоксиалкильной группы, такой как метоксиметил, этоксиметил, метоксиэтил, этоксиэтил и т.п., которая может быть замещена; арилоксиалкильной группы, такой как С 6 Н 5 ОСН 2, С 6 Н 5 ОСН 2 СН 2,нафтилоксиметил и т.п., которая может быть замещена; аралкоксиалкильной группы, такой как С 6 Н 5 СН 2 ОСН 2, C6H5CH2OCH2CH2 и т.п., которая может быть замещена; (C1-C6)алкилтио, тио(C1C6)алкила, которые могут быть замещены, алкоксикарбониламиногруппы, такой как C2H5OCONH,CH3OCONH и т.п., которая может быть замещена; арилоксикарбониламиногруппы, такой какC6H5OCONH, C6H5OCONCH3, C6H5OCONC2H5, C6H4CH3OCONH, С 6 Н 4(ОСН 3)OCONCH3 и т.п., которая может быть замещена; аралкилоксиарбониламиногруппы,такой какC6H5CH2OCONH,C6H5CH2CH2OCONH,C6H5CH2OCON(CH3),C6H5CH2OCON(C2H5),C6H4CH3CH2OCONH,C6H4OCH3CH2OCONH и т.п., которая может быть замещена; аминокарбониламиногруппы; (C1 ди(C1-C6)алкиламинокарбониламиногруппы;(C1-C6)алкилC6)алкиламинокарбониламиногруппы,амидиногруппы, (C1-C6)алкилгуанидиногруппы, ди(C1-C6)алкилгуанидиногрупп, гидразино и гидроксиламиногрупп; карбоновой кислоты или ее производных, таких как амиды, типа CONH2, алкиламинокарбонил типа CH3NHCO, (CH3)2NCO, C2H5NHCO, (C2H5)2NCO, ариламинокарбонил типа PhNHCO,нафтилNHCO и т.п., аралкиламинокарбонил, такой как PhCH2NHCO, PhCH2CH2NHCO и т.п., гетероариламинокарбонильные и гетероаралкиламинокарбонильные группы, где гетероарильные группы определены выше, гетероциклиламинокарбонил, где гетероциклильная группа определена выше, производных карбоновой кислоты, таких как сложные эфиры, где сложноэфирные группы представляют собой алкоксикарбонильные группы, такие как незамещенный или замещенный феноксикарбонил, нафтилоксикарбонил и т.п.; аралкоксиарбонильной группы, такой как бензилоксикарбонил, фенетилоксикарбонил, нафтилметоксикарбонил и т.п., гетероарилоксикарбонила, гетероаралкоксикарбонила, где гетероарильная группа определена выше, гетероциклоксикарбонила, где гетероцикл определен выше и указанные производные карбоновой кислоты могут быть замещены; сульфоновой кислоты или ее производных, таких какSO2NH2, SO2NHCH3, SO2N(СН 3)2, SO2NHCF3, SO2NHCO(C1-C6)алкил, SO2NHCOарил, где арильная группа определена выше и где указанные производные сульфоновой кислоты могут быть замещены; фосфорной кислоты и ее производных, таких как P(O)(OH)2, Р(O)(ОС 1-С 6 алкил)2, Р(O)(O-арил)2 и т.п. Подходящие циклические структуры, образованные двумя смежными группами, такими как R1 и R2,или R2 и R3, или R3 и R4, или R6 и R7, или R7 и R8, или R8 и R9, или R11 и R12, или R14 и R15, вместе с атомами углерода, к которым они присоединены, могут содержать в кольце 5 или 6 атомов, и указанные кольца могут необязательно содержать один или более гетероатомов, выбранных из группы, состоящей из кислорода, азота или серы, а также одну или более двойных связей и другие сочетания двойной связи и гетероатомов, как указано выше. Примеры циклических структур, образованных таким образом, включают необязательно замещенные фенил, нафтил, пиридил, фуранил, тиенил, пирролил, имидазолил, пиримидинил, пиразинил и т.п. Подходящие заместители в циклических структурах, образованных R1 и R2,или R2 и R3, или R3 и R4, или R6 и R7, или R7 и R8, или R8 и R9, или R11 и R12, или R13 и R14, вместе со смежными атомами углерода, к которым они присоединены, включают оксогруппу, гидроксигруппу,-9 009367 атом галогена, такой как хлор, бром и иод; нитрогруппу, цианогруппу, аминогруппу, формильную, (C1C3) алкильную, (C1-C3)алкокси, тиоалкильную, алкилтио, фенильную или бензильную группы. Подходящие группы, описываемые R13, R16 и R17, включают водород, замещенный или незамещенный, линейный или нелинейный (C1-C12)алкил, такой как метил, этил, н-пропил, изопропил, н-бутил,изобутил, пентил, гексил, октил и т.п.; арильную группу, такую как фенил или нафтил, где арильная группа может быть замещена; цикло(С 3-С 7)алкильную группу, такую как циклопропил, циклобутил, циклопентил, циклогексил, циклогептил, где циклоалкильная группа может быть замещена; аралкильную группу, которая может быть замещена, и замещенный аралкил представляет собой группу, такую как СН 3 С 6 Н 4 СН 2, Hal-C6H4CH2, СН 3 ОС 6 Н 4 СН 2, СН 3 ОС 6 Н 4 СН 2 СН 2 и т.п.; (С 3-С 7)циклогетероалкил с гетероатомами типа кислорода, азота серы или селена, необязательно содержащий одну или две двойных или тройных связи. Подходящие гетероциклические кольца, образованные на основе R13 и либо R16, либо R17,могут быть выбраны из имидазолила, пиримидинила, пиразинила, пиперазинила, диазолинила и т.п., где гетероциклильная группа может быть замещена; гетероарильной группы, такой как пиридил, имидазолил, оксадиазолил, тетразолил и т.п., где гетероарильная группа может быть замещена; гетероцикло(C1C6)алкила, такого как пирролидиналкил, пиперидиналкил, морфолиналкил, тиоморфолиналкил, оксазолиналкил и т.п., где гетероцикло(C1-C6)алкильная группа может быть замещена; гетероаралкильной группы, такой как фуранметил, пиридинметил, оксазолметил, оксазолэтил и т.п., где гетероаралкильная группа может быть замещена; гетероарилокси, гетероаралкокси, гетероциклоалкокси, где гетероарильный, гетероаралкильный, гетероциклоалкильный и гетероциклилалкильный фрагменты определены выше и могут быть дополнительно замещены. Соединения по настоящему изобретению могут быть синтезированы с помощью способов синтеза,которые включают процессы, аналогичные известным в данной области химии, особенно на основании приведенного описания. Исходные вещества в основном доступны из коммерческих источников, таких как Aldrich Chemicals (Milwaukee, WI), или могут быть легко получены в соответствии с методами, известными специалистам в данной области (например, могут быть получены по методам, в основном описанным Louis F. Fieser and Mary Fieser, в Reagents for Organic Synthesis, v. 1-19, Wiley, New York (19671999 ed.) или Beilsteins Handbuch der organischen Chemie, 4, Auft. ed. Springer-Verlag, Berlin, включая приложения (также доступным из базы данных Beilstein, функционирующей в масштабе реального времени(он-лайн. Приведенные ниже с иллюстративной целью схемы реакции показывают возможные способы синтеза соединений по настоящему изобретению, а также их ключевых промежуточных соединений. Более подробное описание каждой отдельной стадии реакции приведено в разделе "Примеры". Специалистам в данной области будет очевидно, что могут быть использованы также другие пути синтеза для получения соединений по настоящему изобретению. Несмотря на то, что на схемах показаны и ниже обсуждаются конкретные исходные вещества и реагенты, они могут быть свободно заменены другими исходными материалами и реагентами, что определяет разнообразие производных и/или условий реакции. Кроме того,многие из соединений, полученных описанными ниже способами, могут быть далее модифицированы в свете приведенного описания с использованием методов традиционной химии, известных специалистам в данной области. Подходящими значениями для Lg являются, например, галоген, например хлор, бром, иод, или арильная или алкилсульфонилоксигруппа, например метансульфонилокси или толуол-4-сульфонилокси группа или трифторацетат. При получении соединений по настоящему изобретению может быть необходима защита некоторых функциональных групп (например, первичного или вторичного амина) в промежуточных продуктах. Потребность в такой защите варьирует в зависимости от природы такой функциональной группы и условий способов получения. Подходящие защитные группы для амина (NH-Pg) включают ацетил, трифторацетил, трет-бутоксикарбонил (ВОС), бензилоксикарбонил (CBz) и флуоренилметиленоксикарбонил(Fmoc). Потребность в такой защите легко может быть определена специалистом в данной области. С целью общего описания защитных групп и их применения см. T.W. Greene, Protective Groups in OrganicSynthesis, John WileySons, New York, 1991. Защитные группы могут быть удалены на последующей соответствующей удобной стадии с использованием методов, известных в данной области. Настоящее изобретение относится также к способам получения соединений общей формулы (I), определенной выше, их стереоизомеров, их полиморфов, их фармацевтически приемлемых солей, их фармацевтически приемлемых сольватов, и к новым промежуточным соединениям, участвующим в таких способах, которые будут описаны ниже. В описании и схемах реакций, которые приведены ниже, R1, R2, R3, R4, R6, R7, R8, R9, R11, R12, R13,R14, R15, R16, R17, A и n определены выше, a R5, R10, R и Х также определены в другой части данного описания. Получение соединений по настоящему изобретению Схема 1 Соединения общей формулы (I) могут быть получены путем циклизации соединения формулы (II),приведенной ниже где R1, R2, R3, R4, R6, R7, R8, R9, R13, R14, R15, R16, R17, А и n определены выше, или его предшественника,где один из R5 и R10 означает атом галогена, такой как бром, хлор или иод, а второй означает водород; с использованием производного Pd(0) или Pd (I) в качестве катализатора, например тетракистрифенилфосфинпалладия, (бис-три-о-толилфосфин)палладия и т.п.; и затем, при необходимости, с последующим проведением одной или более из указанных ниже стадий:i) превращение соединения формулы (I), имеющего реакционноспособную группу-заместитель, в другое соединение формулы (I);ii) удаление любой защитной группы илиiii) образование его фармацевтически приемлемой соли или пролекарства. Указанная реакция циклизации может быть осуществлена с использованием палладиевых катализаторов. Реакция может быть проведена в присутствии основания, такого как CH3COOK. Данная реакция может быть осуществлена в присутствии растворителей, таких как ТГФ, ДМФА, ДМСО, ДМА, ДМЭ,ацетон и т.п., и предпочтительно с использованием диметилацетамида. Инертная атмосфера может создаваться за счет использования инертных газов, таких как N2, Ar или He. Температура реакции может варьировать от 50 до 200 С в зависимости от природы выбранного растворителя и предпочтительно при температуре 160 С. Длительность реакции может варьировать от 10 до 24 ч, предпочтительно от 10 до 20 ч. Схема 2 Соединения общей формулы (I) могут быть получены взаимодействием соединения формулы (III),приведенной ниже где A, R1, R2, R3, R4, R6, R7, R8 и R9 определены выше применительно к формуле (I), X означает водород или удаляемую группу, такую как гидрокси, мезил, тозил или галоген, например хлор, бром или иод и т.п., с соединением формулы (IV) или его кислотно-аддитивной солью где R13, R14, R15, R16 и R17 определены выше применительно к формуле (I), или с его предшественником. В том случае, когда X означает галоген, данный способ применительно к реакции связывания пиперазина может быть осуществлен по методу 4 и 5, как показано ниже. Предпочтительно заместители, выбираемые для соединений формул (III) и (IV), являются инертными применительно к условиям данной реакции или чувствительными группами и подвергаются защи- 11009367 те с использованием подходящих защитных групп. В том случае, когда R означает подходящую защитную группу, требуется дополнительная стадия, описанная на схеме 2, для получения соединений формулы (I). Указанную реакцию предпочтительно проводят в растворителе, таком как ТГФ, ацетон, ксилол, толуол, метанол, этанол, пропанол и т.п., и предпочтительно с использованием ацетона или ДМФА. Инертная атмосфера может создаваться при использовании инертных газов, таких как N2, Ar или He. Реакционную смесь обычно нагревают при повышенной температуре или при температуре дефлегмации растворителя до завершения реакции. В данной реакции конденсации может использоваться широкий перечень основных агентов. Однако предпочтительные основные агенты включают карбонат натрия, бикарбонат натрия, карбонат калия, ацетат калия, алкоксиды натрия и т.п., при этом предпочтительным основным агентом является K2CO3. Обычно время реакции составляет от 30 мин до 72 ч. В конце реакции летучие компоненты удаляют при пониженном давлении. Реакционная смесь может быть необязательно подкислена перед дальнейшей обработкой. Продукт может быть выделен осаждением, далее промыт,высушен и очищен стандартными методами, такими как перекристаллизация, колоночная хроматография и т.п. Необязательные стадии (i), (ii) и (iii) могут осуществляться в соответствии с традиционными методами. Ниже приведены примеры, иллюстрирующие соответствующие реакции. Соединения, описываемые общей формулой (III), получают с помощью метода, приведенного в другой части данного описания. Соединения формулы (IV) являются коммерчески доступными или могут быть получены традиционными методами, или путем модификации с использованием известных способов, или при получении соединений формулы (IV) из коммерчески доступных источников. В ходе приведенной выше последовательности реакций синтеза может возникнуть потребность и/или необходимость в защите чувствительных, или реакционноспособных групп, расположенных на любых участвующих в процессе молекулах. Указанная цель может быть достигнута с помощью традиционных для применения защитных групп, таких как группы, описанные в Protective Groups in OrganicOrganic Synthesis, John WileySons, New York, 1991. Защитные группы могут быть удалены далее на соответствующей удобной стадии с использованием методов, известных в данной области. Стереоизомеры соединений общей формулы (I) могут быть получены с использованием одного или более способов, описанных ниже.(i) Один или более реагентов могут быть использованы в их оптически активной форме.(ii) В процессе восстановления могут быть использованы оптически чистые катализатор или хиральные лиганды в сочетании с металлическим катализатором. В процессе восстановления могут использоваться металлические катализаторы. Металлический катализатор может представлять собой родий,рутений, индий и т.п. Хиральные лиганды могут предпочтительно представлять собой хиральные фосфины (Principles of Asymmetric synthesis, J.E. Baldwin Ed., Tetrahedron series, 14, 311-316).(iii) Смесь стереоизомеров может быть разделена традиционными методами, такими как образование диастереомерных солей с хиральными кислотами или хиральными аминами, или хиральными аминоспиртами, или хиральными аминокислотами. Полученная смесь диастереомеров может быть далее разделена с использованием методов, таких как фракционная кристаллизация, хроматография и т.п., после чего следует дополнительная стадия выделения оптически активного продукта путем гидролиза производного (Jacques et al., "Enantiomers, Racemates and Resolution", Wiley Interscience, 1981).(iv) Смесь стереоизомеров может быть разделена традиционными методами, такими как микробное расщепление, разделение диастереомерных солей, образованных с хиральными кислотами или хиральными основаниями. Хиральные кислоты, которые могут использоваться, могут представлять собой винную кислоту,миндальную кислоту, молочную кислоту, камфорсульфоновую кислоту, аминокислоты и т.п. Хиральные основания, которые могут использоваться, могут представлять собой хинные алкалоиды, бруцин или соединения с основной аминогруппой, такие как лизин, аргинин и т.п. Меченные изотопами соединения по настоящему изобретению полезны с точки зрения изучения распределения по тканям лекарственного средства и/или субстрата и определения уровня достижения ткани-мишени. Так, меченные изотопами соединения нашли применение, в частности, в методах SPECT(однофотонная электронная компьютерная томография) и PET (эмиссионная позитронная томография). Фармацевтически приемлемые соли, представляющие собой часть настоящего изобретения, могут быть получены путем обработки соединения формулы (I) 1-6 экв. основания, такого как гидрид натрия,метоксид натрия, этоксид натрия, гидроксид натрия, трет-бутоксид калия, гидроксид кальция, ацетат кальция, хлорид кальция, гидроксид магния, хлорид магния и т.п. Могут использоваться растворители,такие как вода, ацетон, эфир, ТГФ, метанол, этанол, трет-бутанол, диоксан, изопропанол, изопропиловый эфир или их смеси. Могут использоваться органические основания, такие как лизин, аргинин, метилбензиламин, этаноламин, диэтаноламин, трометамин, холин, гуанидин и их производные. В приемлемых вариантах кислотно-аддитивные соли могут быть получены путем обработки кислотами, такими как винная кислота, миндальная кислота, фумаровая кислота, малеиновая кислота, молочная кислота, сали- 12009367 циловая кислота, лимонная кислота, аскорбиновая кислота, бензолсульфоновая кислота, п-толуолсульфоновая кислота, гидроксинафтоновая кислота, метансульфоновая кислота, яблочная кислота, уксусная кислота, бензойная кислота, янтарная кислота, пальмитиновая кислота, щавелевая кислота, хлористоводородная кислота, бромисто-водородная кислота, серная кислота, азотная кислота и т.п., в растворителях, таких как вода, спирты, эфиры, этилацетат, диоксан, ДМФА или низший алкилкетон, такой как ацетон, или их смеси. Различные полиморфы могут быть получены путем кристаллизации соединений общей формулы (I) в различных условиях, таких как различные применяемые для перекристаллизации растворители или смеси растворителей, в варьирующих пропорциях, с использованием различных методов кристаллизации, таких как медленное охлаждение, быстрое охлаждение или очень быстрое охлаждение или постепенное охлаждение в процессе кристаллизации. Также может быть использовано нагревание соединения,расплавление соединения и отверждение путем постепенного или быстрого охлаждения, нагревания или расплавления в вакууме или в инертной атмосфере и охлаждение в вакууме или в инертной атмосфере. Один или несколько методов, таких как дифференциальная сканирующая калориметрия, порошковая дифракция рентгеновских лучей, ИК-спектроскопия, ЯМР-спектроскопия твердой пробы и термомикроскопия, могут использоваться для идентификации различных полиморфов. Новые промежуточные соединения общей формулы (II) приведены нижеR1, R2, R3, R4, R6, R7, R8, R9, R11 и R12 могут быть одинаковыми или различными и каждый независимо означает водород, галоген, оксо, тио, пергалогеналкил, пергалогеналкокси, гидрокси, амино, нитро,циано, формил, амидино, гуанидино, замещенные или незамещенные группы, выбранные из линейного или разветвленного (С 1-С 12)алкила, (С 2-С 12)алкенила, (С 2-С 12)алкинила, (С 3-С 7)циклоалкила, (С 3 С 7)циклоалкенила, бициклоалкила, бициклоалкенила, (С 1-С 12)алкокси, цикло(С 3-С 7)алкокси, арила, арилокси, аралкила, аралкокси, гетероциклила, гетероарила, гетероциклилалкила, гетероаралкила, гетероарилокси, гетероаралкокси, гетероциклилалкилокси, ацила, ацилокси, ациламино, моноалкиламино, диалкиламино, ариламино, диариламино, аралкиламино, алкоксикарбонила, арилоксикарбонила, аралкоксикарбонила, гетероциклилалкоксикарбонила, гетероарилоксикарбонила, гидроксиалкила, аминоалкила,моноалкиламиноалкила, диалкиламиноалкила, алкоксиалкила, арилоксиалкила, аралкоксиалкила, алкилтио, тиоалкила, алкоксикарбониламино, арилоксикарбониламино, аралкилоксикарбониламино, аминокарбониламино, алкиламинокарбониламино, диалкиламинокарбониламико, алкиламидино, алкилгуанидино, диалкилгуанидино, гидразино, гидроксиламино, карбоновой кислоты и ее производных, сульфоновых кислот и их производных, фосфорной кислоты и ее производных; или смежные группы типа R1 и R2,или R2 и R3, или R3 и R4, или R6 и R7, или R7 и R8, или R8 и R9, вместе с атомами углерода, к которым они присоединены, могут образовывать пяти- или шестичленное кольцо, необязательно содержащее одну или более двойных связей и необязательно содержащее один или более гетероатомов, выбранных из кислорода, азота, серы или селена и сочетаний двойной связи и гетероатомов; или необязательно R11 и R12 вместе с атомами углерода, к которым они присоединены, могут образовывать трех-шестичленное кольцо, необязательно содержащее одну или более двойных связей и необязательно содержащее один или более гетероатомов, выбранных из кислорода, азота, серы или селена и сочетаний двойной связи и гетероатомов; или необязательно R11 или R12 представляют собой такие заместители, которые позволяют образовывать связь с или R16, или R17 с получением 5-, 6- или 7-членного гетероциклического кольца, а также включают их стереоизомеры и их соли. Способ 1. Соединения общей формулы (III) могут быть получены путем циклизации соединения формулы где A, R1, R2, R3, R4, R6, R7, R8 и R9 определены выше, X означает защищенную или удаляемую группу,такую как гидрокси, мезил, тозил или атом галогена, такой как хлор, бром или иод, один из R10 и R5 означает атом галогена, такой как хлор, бром или иод и т.п., а второй означает водород; с использованием производного Pd(0) или Pd(II) в качестве катализатора, например тетракистрифенилфосфинпалладия,(бис-три-о-толилфосфин)палладия и т.п.; и при осуществлении данного способа в соответствии с методикой, приведенной в другой части описания. Необязательные стадии (i) и (ii) могут быть проведены в соответствии с традиционными методами. Использование указанных методов зависит в каждом случае от конкретной природы заместителей на индоле. Способ 2. Соединения общей формулы (III) могут быть получены из других соединений формулы (III), в которых A заменен соответствующим образом другим типом заместителя, как показано на приведенной ниже схеме Стадия 1 представляет собой обычное окисление, тогда как стадия 2 представляет собой превращение кислоты в хлорангидрид. Альтернативно, при необходимости, кислота может быть подвержена соответствующей реакции с соединением формулы (IV) по стандартной методике сочетания пептидов, например, с использованием хлорангидрида бис(2-оксо-3-оксазолидинил)фосфорной кислоты (BOP-Cl) с последующим проведением восстановления. В соединениях, содержащих группу A, означающую -CO, последняя может быть восстановлена до-СН(ОН) или -СН 2 с использованием восстановителей, способных преобразовать амидогруппу в аминогруппу. Такие средства включают, например, литийалюмогидрид или другие комплексные гидриды алюминия. Реакции восстановления проводят в диэтиловом эфире или в тетрагидрофуране, или в стабильном диборановом комплексе, таком как боран-тетрагидрофуран или боран-диметилсульфид или другие средства (J. Org. Chem. 1982, 47, 1389) в соответствующем растворителе (например, в тетрагидрофуране). Специалистам в данной области известны многие другие восстановители, которые также могут использоваться (March, Advanced Organic Chemistry, Wiley Interscience Ed., 1992, 1212). Аналогично, если Х означает ОН, он может быть превращен в X, означающий галоген, в соответствии с методами, известными в данной области. Способ 3. Соединения общей формулы (III), в которой A означает SO2, могут быть получены посредством преобразования соединения формулы (VII), приведенной ниже где R1, R2, R3, R4, R6, R7, R8 и R9 определены применительно к формуле (I), X означает атом галогена,такой как хлор, бром или иод, путем металлизации, с использованием, например, трет-бутиллития, с последующим проведением реакции с газообразным SO2 и N-хлорсукцинимидом. При этом образуются соединения общей формулы (V), в которой А-Х означает SO2Cl. Фармацевтические композиции по настоящему изобретению могут быть получены традиционным способом с использованием одного или более фармацевтически приемлемых носителей. Так, активные соединения по настоящему изобретению могут быть введены в композицию для перорального, буккального, интраназального, парентерального (например, внутривенного, внутримышечного или подкожного) введения или ректального введения или имеющей форму, подходящую для введения ингаляцией или инсуффляцией. Термин "терапевтически эффективное количество" определен как количество соединения по настоящему изобретению, которое (i) позволяет лечить или предупредить развитие конкретного заболевания, состояния или расстройства, (ii) ослабляет, уменьшает или устраняет один или более симптомов конкретного заболевания, состояния или расстройства или (iii) предупреждает или задерживает начало развития одного или более симптомов конкретного заболевания, состояния или расстройства из числа приведенных в настоящем изобретении. Доза активных соединений может варьировать в зависимости от ряда факторов, таких как способ введения, возраст и вес пациента, природа и тяжесть заболевания, подлежащего лечению, и других аналогичных факторов. В этой связи, любая ссылка на фармакологически эффективное количество соединений общей формулы (I) дается с учетом указанных факторов. Доза активных соединений по настоящему изобретению, предлагаемая для перорального, парентерального, назального или буккального введения среднестатистическому взрослому человеку для лечения вышеуказанных состояний, составляет от 0,1 до 200 мг активного ингредиента на единичную дозу и указанная доза может вводиться, например, 1-4 раза в день. Для целей перорального введения фармацевтические композиции могут иметь форму, например,таблеток или капсул, полученных традиционными способами с использованием фармацевтически приемлемых эксципиентов, таких как связующие вещества (например, предварительно желированный кукурузный крахмал, поливинилпирролидон или гидроксипропилметилцеллюлоза); наполнители (например,лактоза, микрокристаллическая целлюлоза или фосфат кальция); лубриканты (например, стеарат магния,тальк или силикагель); дезинтегранты (например, картофельный крахмал или натрий-крахмал-гликолят); а также смачивающие вещества (например, лаурилсульфат натрия). На таблетку может быть нанесено покрытие с использованием известных в данной области методов. Жидкие препараты для перорального введения могут, например, иметь форму растворов, сиропов или суспензий, они также могут быть представлены в виде сухого продукта для восстановления водой или другим приемлемым носителем непосредственно перед употреблением. Такие жидкие препараты могут быть получены традиционными способами с использованием фармацевтически приемлемых добавок, таких как средства, способствующие суспендированию (например, сироп сорбита, метилцеллюлоза или гидрогенизированные пищевые жиры); эмульгаторы (например, лецитин или аравийская камедь); неводные носители (например, миндальное масло, сложные эфиры жирных кислот или этиловый спирт) и консерванты (например, метил- или пропил-п-гидроксибензоаты или сорбиновая кислота). Для целей буккального введения композиция может иметь формутаблеток или пастилок, изготовленных традиционным способом. Активные соединения по настоящему изобретению могут быть получены в виде, пригодном для парентерального введения путем инъекции, включая использование традиционных методов катетеризации и инфузии. Композиции для инъекция могут быть представлены в единичной дозированной форме, например, они могут иметь вид ампул или контейнеров с многократными дозами с добавленным в них консервантом. Композиции могут быть представлены в таких формах, как суспензии, растворы или эмульсии в масляных или водных носителях, и могут содержать средства, способствующие созданию композиции, такие как средства, способствующие суспендированию, стабилизаторы и/или средства, способствующие диспергированию. Альтернативно, активный ингредиент может быть представлен в порошковой- 15009367 форме, пригодной для последующего восстановления соответствующим носителем, например стерильной апирогенной водой, непосредственно перед употреблением. Активные соединения по настоящему изобретению могут быть также получены в виде ректальных композиций, таких как суппозитории или удерживаемые клизмы, например, содержащие традиционные для суппозиториев основания, такие как какао-масло или другие глицериды. Для целей интраназального введения или введения путем ингаляции активные соединения по настоящему изобретению могут удобно доставляться в виде аэрозольного спрея из контейнера, находящегося под давлением, или пульверизатора, или капсул с использованием ингалятора или инсуффлятора. В случае использования аэрозоля под давлением используют соответствующий газ-вытеснитель, например дихлордифторметан, трихлорфторметан, дихлортетрафторэтан, диоксид углерода или другой подходящий газ, и единица дозируемого количества может задаваться путем нажатия на клапан, контролирующий доставку отмеренного количества. Лекарственное средство, вводимое в контейнер под давлением,или пульверизатор может содержать раствор или суспензию активного соединения, тогда как в случае использования капсульной формы оно должно быть предпочтительно в виде порошка. Капсулы и картриджи (изготовленные, например, с использованием желатина), пригодные для использования в ингаляторе или инсуффляторе, могут быть получены с использованием порошковой смеси соединения по настоящему изобретению и соответствующей порошковой основы, такой как лактоза или крахмал.ii) Тест на 5-HT1B. Материалы и методы. Источник рецептора: мембраны полосатого тела крысы Радиолиганд: [125I]-иодцианопиндолол (2200 Ки/ммоль) Конечная концентрация лиганда: [0,15 нМ] Неспецифическая детерминанта: серотонин-[10 мкМ] Эталонное соединение: серотонин Положительный контроль: серотонин Условия инкубации. Реакции проводят в 50 мМ Трис-HCl (pH 7,4), содержащем 60 мкМ (-) изопротеренола при 37 С в течение 60 мин. Реакцию останавливают быстрым фильтрованием в вакууме через стекловолокнистые фильтры. Определяют количество задержанной на фильтре радиоактивности и сравнивают полученное значение с контрольными значениями для оценки наличия каких-либо взаимодействий исследуемого соединения с сайтом связывания 5-НТ 1 В. Цитированная литература.iii) Тест на 5-HT1D. Материалы и методы. Источник рецептора: кора головного мозга человека Радиолиганд: [3 Н]-5-карбоксамидотриптамин (20-70 Ки/ммоль) Конечная концентрация лиганда: [2,0 нМ] Неспецифическая детерминанта: 5-карбоксамидотриптамин (5-СТ)-[1,0 мкМ] Эталонное соединение: 5-карбоксамидотриптамин (5-СТ) Положительный контроль: 5-карбоксамидотриптамин (5-СТ) Условия инкубации. Реакцию проводят в 50 мМ Трис-HCl (pH 7,7), содержащем 4 мМ CaCl2, 100 нМ 8-OH-DPAT, 100 нМ мезулергина, 10 мкМ паргилина и 0,1% аскорбиновой кислоты, при 25 С в течение 60 мин. Реакцию останавливают быстрым фильтрованием в вакууме через стекловолокнистые фильтры. Определяют количество задержанной на фильтре радиоактивности и сравнивают полученное значение с контрольными значениями для оценки наличия каких-либо взаимодействий исследуемого соединения с сайтом связывания клонированного 5-HT1D. Цитированная литература.iv) Тест на 5-НТ 2 А. Материалы и методы. Источник рецептора: кора головного мозга человека Радиолиганд: [3 Н]-кетансерин (60-90 Ки/ммоль)- 16009367 Конечная концентрация лиганда: [2,0 нМ] Неспецифическая детерминанта: кетансерин [3,0 мкМ] Эталонное соединение: кетансерин Положительный контроль: кетансерин Условия инкубации. Реакцию проводят в 50 мМ Трис-HCl (pH 7,5) при комнатной температуре в течение 90 мин. Реакцию останавливают быстрым фильтрованием в вакууме на стекловолокнистых фильтрах. Определяют количество задержанной на фильтре радиоактивности и сравнивают полученное значение с контрольными значениями для оценки наличия каких-либо взаимодействий исследуемого соединения с сайтом связывания клонированного 5-НТ 2 А. Цитированная литература.v) Тест на 5-НТ 2 С. Материалы и методы. Источник рецептора: мембраны хориоидального сплетения свиньи Радиолиганд: [3 Н]-мезулергин (50-60 Ки/ммоль) Конечная концентрация лиганда: [1,0 нМ] Неспецифическая детерминанта: серотонин [100 мкМ] Эталонное соединение: миансерин Положительный контроль: миансерин Условия инкубации. Реакцию проводят в 50 мМ Трис-HCl (pH 7,7), содержащем 4 мМ CaCl2 и 0,1% аскорбиновой кислоты, при 37 С в течение 60 мин. Реакцию останавливают быстрым фильтрованием в вакууме через стекловолокнистые фильтры. Определяют количество задержанной на фильтре радиоактивности и сравнивают полученное количество с контрольными значениями для оценки наличия каких-либо взаимодействий исследуемого соединения с сайтом связывания 5-HT2C. Цитированная литература.vi) Тест на 5-НТ 3. Материалы и методы. Источник рецептора: клетки N1E-115 Радиолиганд: [3H]-GR 65630 (30-70 Ки/ммоль) Конечная концентрация лиганда: [0,35 нМ] Неспецифическая детерминанта: MDL-72222-[1,0 мкМ] Эталонное соединение: MDL-72222 Положительный контроль: MDL-72222 Условия инкубации. Реакцию проводят в 20 мМ HEPES (pH 7,4), содержащем 150 мМ NaCl, при 25 С в течение 60 мин. Реакцию останавливают быстрым фильтрованием в вакууме через стекловолокнистые фильтры. Определяют количество задержанной на фильтре радиоактивности и сравнивают полученное значение с контрольными значениями для оценки наличия каких-либо взаимодействий исследуемого соединения с сайтом связывания 5-НТ 3. Цитированная литература.vii) Тест на 5-НТ 4. Материалы и методы. Источник рецептора: мембраны полосатого тела морской свинки- 17009367 Радиолиганд: [3H]-GR 113808 (30-70 Ки/ммоль) Конечная концентрация лиганда: [0,2 нМ] Неспецифическая детерминанта: серотонин (5-НТ)-[30 мкМ] Эталонное соединение: серотонин (5-НТ) Положительный контроль: серотонин (5-НТ) Условия инкубации. Реакцию проводят в 50 мМ HEPES (pH 7,4) при 37 С в течение 60 мин. Реакцию останавливают быстрым фильтрованием в вакууме через стекловолокнистые фильтры. Определяют количество задержанной на фильтре радиоактивности и сравнивают полученное значение с контрольными значениями для оценки наличия каких-либо взаимодействий исследуемого соединения с сайтом связывания 5-НТ 4. Цитированная литература.viii) Тест на 5-НТ 5 А. Материалы и методы. Источник рецептора: человеческий рекомбинантный рецептор, экспрессируемый в клетках НЕК 293 Радиолиганд: [3H]-LSD (60-87 Ки/ммоль) Конечная концентрация лиганда: [1,0 нМ] Неспецифическая детерминанта: мезилат метиотепина-[1,0 мкМ] Эталонное соединение: мезилат метиотепина Положительный контроль: мезилат метиотепина Условия инкубации. Реакции проводят в 50 мМ Трис-HCl (pH 7,4), содержащем 10 мМ MgSO4 и 0,5 мМ EDTA, при 37 С в течение 60 мин. Реакцию останавливают быстрым фильтрованием в вакууме через стекловолокнистые фильтры. Определяют количество задержанной на фильтре радиоактивности и сравнивают полученное значение с контрольными значениями для оценки наличия каких-либо взаимодействий исследуемого соединения с сайтом связывания клонированного 5-HT5A. Цитированная литература.ix) Тест на 5-НТ 6. Материалы и методы. Источник рецептора: человеческий рекомбинантный рецептор, экспрессируемый в клетках НЕК 293 Радиолиганд: [3H]-LSD (60-80 Ки/ммоль) Конечная концентрация лиганда: [1,5 нМ] Неспецифическая детерминанта: мезилат метиотепина-[0,1 мкМ] Эталонное соединение: мезилат метиотепина Положительный контроль: мезилат метиотепина Условия инкубации. Реакции проводят в 50 мМ Трис-HCl (рН 7,4), содержащем 10 мМ MgCl2 и 0,5 мМ EDTA, при 37 С в течение 60 мин. Реакцию останавливают быстрым фильтрованием в вакууме через стекловолокнистые фильтры. Определяют количество задержанной на фильтре радиоактивности и сравнивают полученное значение с контрольными значениями для оценки наличия каких-либо взаимодействий исследуемого(ых) соединения(ий) с сайтом связывания клонированного серотонина-5-НТ 6. Цитированная литература.x) Тест на 5-НТ 7. Материалы и методы. Источник рецептора: человеческий рекомбинантный рецептор, экспрессируемый в клетках СНО Радиолиганд: [3H]-LSD (60-80 Ки/ммоль) Конечная концентрация лиганда: [2,5 нМ] Неспецифическая детерминанта: 5-карбоксамидотриптамин (5-СТ)-[0,1 мкМ] Эталонное соединение: 5-карбоксамидотриптамин Положительный контроль: 5-карбоксамидотриптамин Условия инкубации. Реакции проводят в 50 мМ Трис-HCl (рН 7,4), содержащем 10 мМ MgCl2 и 0,5 мМ EDTA, при 37 С в течение 60 мин. Реакцию останавливают быстрым фильтрованием в вакууме через стекловолокнистые фильтры. Определяют количество задержанной на фильтре радиоактивности и сравнивают полученное значение с контрольными значениями для оценки наличия каких-либо взаимодействий исследуемого(ых) соединения(ий) с сайтом связывания клонированного серотонина-5-НТ 7. Цитированная литература.hydroxytryptamine7 Serotonin Receptor Subtype. J. Biol. Chem. 268: 18200-18204. Представленное ниже описание поясняет способ получения различным образом замещенных соединений общей формулы (I) в соответствии с приведенными методами. Данное описание дано с целью иллюстрации и никоим образом не ограничивает объем настоящего изобретения. Коммерческие реактивы используют без дополнительной очистки. Термин комнатная температура относится к температуре 25-30 С. Точки плавления приводятся в некорректированном виде. ИКспектры получают с использованием KBr и в твердом состоянии. Если особо не оговорено иное, все масс-спектральные анализы проводят с использованием условий ESI (ионизация электрораспылением). Спектры 1 Н-ЯМР регистрируют при 200 МГц на приборе Bruker. В качестве растворителя используют дейтерированный хлороформ (99,8% D). В качестве внутреннего стандартного эталона используют ТМС. Значения химических сдвигов выражают в миллионных долях (м.д.) . Для описания множественности ЯМР сигналов используют следующие сокращения: с.=синглет, шс.=широкий синглет, д.=дублет,т.=триплет, к.=квартет, кви.=квинтет, г.=гептет, дд.=двойной дублет, дт.=двойной триплет, тт.=триплет триплетов, м.=мультиплет. Значение массы, получаемой методом ЯМР, корректируют с учетом фоновых пиков. Значения удельного вращения измеряют при комнатной температуре с использованием D-натрия(589 нм). Приведенные хроматографические данные относятся к колоночной хроматографии, которую осуществляют при использовании силикагеля с размером 60-120 меш и в условиях давления, созданного азотом (флэш-хроматография). Описание 1. 1-(2-Бромбензолсульфонил)-4-хлор-3-(4-метилпиперазин-1-илметил)-1 Н-индол (D1). 1-(2-Бромбензолсульфонил)-3-хлорметил-4-хлор-1 Н-индол (4,17 г, 0,01 моль) и триэтиламин (1,11 г, 0,011 моль) в дихлрметане (25 мл) перемешивают при 25 С. Реакционную смесь охлаждают и к указанной хорошо перемешиваемой реакционной смеси медленно добавляют N-метилпиперазин (1,1 г, 0,011 моль). Реакционную смесь перемешивают в течение 2-4 ч при 25 С и после завершения реакции (по данным ТСХ) данную смесь разбавляют еще 25 мл дихлорметана и органическую реакционную смесь промывают водой и насыщенным раствором соли. Дихлорметановый экстракт сушат над сульфатом натрия и летучие вещества удаляют при пониженном давлении с получением неочищенного промежуточного продукта. Полученный остаток очищают флэш-хроматографией (силикагель, EtOAc/гексаны, 2/8) с получением соединения, которое идентифицируют методами ИК, ЯМР и масс-спектрального анализа как указанное в заголовке соединение. Аналогично, используют [1,4]диазепан-1-илфенилметанон (2,05 г, 0,01 моль), [1,4]диазепан (1,10 г,0,011 моль) или 1-(2-метилпиперазин-1-ил)этанон (1,57 г, 0,01 моль) для получения других производных в соответствии с описанным выше методом. Перечень 1.(D7). 5-Метокси-3-(4-метилпиперазин-1-илметил)-1H-индол (2,59 г, 0,01 моль) в ДМФА (30 мл) медленно добавляют к суспензии гидрида натрия (0,26 г, 0,011 моль) в ДМФА (10 мл), поддерживая температуру ниже 10 С. Смесь перемешивают в течение 1 ч при температуре 25 С. Затем реакционную смесь охлаждают до 10 С и добавляют по каплям 2-бромбензолсульфонилхлорид (2,54 г, 0,01 моль). Далее реакционную смесь перемешивают в течение 1 ч при 25 С. После завершения реакции (по данным ТСХ) данную реакционную смесь выливают в смесь воды и льда и проводят экстракцию этилацетатом (20 мл 2). Объединенные органические экстракты промывают водой и насыщенным раствором соли и сушат над сульфатом натрия. Летучие примеси отгоняют при пониженном давлении с получением неочищенного остатка. Полученный остаток очищают флэш-хроматографией (силикагель, EtOAc/ТЭА, 9,9/0,1) с получением соединения, которое идентифицируют методами ИК, ЯМР и масс-спектрального анализа как указанное в заголовке соединение. Описание 14. 4-[1-(2-Бромбензолсульфонил)-1 Н-индол-3-илметил]пиперазин-1-ил)фенилметанон (D14). 1-(2-Бромбензолсульфонил)-3-хлорметил-1 Н-индол (3,83 г, 0,01 моль) отбирают в 20 мл дихлорэтана и к данному перемешиваемому раствору добавляют фенилпиперазин-1-илметанон (2,01 г, 0,011 моль). Далее реакционную смесь перемешивают в течение 3-5 ч до завершения реакции (по данным ТСХ). Реакционную смесь разбавляют дихлорметаном (20 мл), промывают водой, насыщенным раствором соли и насыщенным раствором бикарбоната натрия. Органический слой сушат над сульфатом натрия и органические растворители выпаривают в вакууме. Продукт очищают колоночной хроматографией с использованием в качестве стационарной фазы силикагеля G и в качестве подвижной фазы соответствующих сочетаний этилацетата и метанола в возрастающем градиенте концентраций. Аналогично, используют [1,4]диазепан-1-илфенилметанон (2,05 г, 0,01 моль), [1,4]диазепан (1,10 г,0,011 моль) или 1-(2-метилпиперазин-1-ил)этанон (1,57 г, 0,01 моль) для получения других производных в соответствии с описанным выше методом. Перечень 3.(1-(2-Бромбензолсульфонил)-1 Н-индол-3-ил)-(4-метилпиперазин-1-ил)метанон (0,03 г, 0,002 моль) в ТГФ (10 мл) медленно, в течение 2-5 ч обрабатывают холодной и перемешиваемой суспензией LAH (0,04 г, 0,01 моль) в ТГФ (10 мл) и реакционную смесь нагревают при температуре кипения с обратным холодильником в течение 2-4 ч. После завершения реакции реакционную смесь выливают на лед и проводят экстракцию этилацетатом. Полученный остаток очищают флэш-хроматографией (силикагель,EtOAc/гексаны, 2/6) с получением соединения, которое идентифицируют методами ИК, ЯМР и массспектрального анализа как указанное в заголовке соединение. Перечень 4. Описание 28. 1-(2-Бромбензолсульфонил)-1 Н-индол-3-карбоксальдегид (D28). Перемешиваемый раствор 1 Н-индол-3-карбоксальдегида (1 г, 6,89 моль) в ДМФА (25 мл) обрабатывают гидридом натрия (0,357 г, 60% в минеральном масле, 8,95 моль) в атмосфере азота при комнатной температуре, перемешивают в течение 30 мин, обрабатывают 2-бромбензолсульфонилхлоридом(1,18 мл, 8,25 ммоль) и перемешивают при комнатной температуре в течение 3-5 ч. После завершения реакции (по данным ТСХ) реакцию гасят добавлением 25 мл охлажденной льдом воды и разбавляют 25 мл этилацетата. Органическую фазу отделяют, промывают последовательно водой и насыщенным раствором соли, сушат над безводным MgSO4 и концентрируют в вакууме. Полученный остаток очищают флэш-хроматографией (силикагель, EtOAc/гексан, 2/8) с получением указанного в заголовке соединения в виде не совсем белой пены, которое идентифицируют методами ИК, ЯМР и масс-спектрального анализа. Перечень 5. Описание 31. 1-(2-Бромбензолсульфонил)-1 Н-индол-3-илметанол (D31). В трехгорлую круглодонную колбу, снабженную уравновешивающей давление воронкой, вносят 1(2-бромбензолсульфонил)-1 Н-индол-3-карбоксальдегид (D27, 3,63 г, 0,01 моль) и дихлорметан (8 мл). Добавляют медленно при комнатной температуре боргидрид натрия (0,005-0,01 моль) и реакционную смесь хорошо перемешивают в течение 3-4 ч. После завершения реакции (по данным ТСХ, 3-5 ч) продукт выделяют перегонкой при пониженном давлении. Остаток экстрагируют этилацетатом (25 мл). Объединенные органические экстракты промывают водой, затем насыщенным раствором соли и сушат над безводным сульфатом натрия. Органический слой выпаривают в вакууме. Остаток представляет собой в основном маслянистую жидкость, которую выделяют и очищают флэш-хроматографией (силикагель, EtOAc/гексан, 2/8) с получением указанного в заголовке соединения, которое идентифицируют методами ИК, ЯМР и масс-спектрального анализа. Перечень 6. Описание 34. 1-(2-Бромбензолсульфонил) -3-хлорметил-1 Н-индол (D34). В трехгорлую круглодонную колбу, снабженную уравновешивающей давление воронкой, вносят(8 мл). Медленно добавляют при комнатной температуре тионилхлорид (1,594 г, 0,012 моль) и реакционную смесь хорошо перемешивают в течение 1 ч. После завершения реакции (по данным ТСХ) продукт выделяют перегонкой при пониженном давлении. Остаток экстрагируют этилацетатом (225 мл). Объединенные органические экстракты промывают водой, затем насыщенным раствором соли и сушат над безводным сульфатом натрия. Органический слой выпаривают в вакууме. Полученный остаток затем растирают с н-гексаном, получая твердое вещество, которое идентифицируют методами ИК, ЯМР и масс-спектрального анализа как указанное в заголовке соединение. Перечень 7. Описание 37. 2-Хлор-10-хлорметил-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид (D37). В трехгорлую круглодонную колбу объемом 100 мл вносят 1-(2-бромбензолсульфонил)-3 хлорметил-1 Н-индол (0,286 моль), а также N,N-диметилацетамид (40 мл), ацетат калия (0,286 моль, 0,281 г) и дихлор-бис(три-о-толилфосфин)палладия (0,0143 моль, 0,0126 г). Реакционную смесь выдерживают в атмосфере азота и нагревают до температуры 160 С при перемешивании в течение 16 ч. После завершения реакции избыток диметилацетамида отгоняют при пониженном давлении и остаток очищают колоночной хроматографией на силикагеле с использованием в качестве элюента 20% метанола в этилацетате. Альтернативно, 1-бензолсульфонил-2-бром-1 Н-индол-3-карбальдегид может быть получен из 2 бром-1 Н-индол-3-карбальдегида и реакцию проводят аналогично указанной выше с получением тетрациклического соединения. Перечень 8. Пример 1. 10-(4-Метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид. В трехгорлую круглодонную колбу объемом 100 мл вносят 1-(2-бромбензолсульфонил)-3-(4 метилпиперазин-1-илметил)-1 Н-индол или 1-бензолсульфонил-2-бром-3-(4-метилпиперазин-1-илметил)1 Н-индол (0,286 моль), а также N,N-диметилацетамид (40 мл), ацетат калия (0,286 моль, 0,281 г) и дихлор-бис(три-о-толилфосфин)палладия (0,0143 моль, 0,0126 г). Реакционную смесь выдерживают в атмосфере азота и нагревают до температуры 160 С при перемешивании в течение 16 ч. После завершения реакции избыток диметилацетамида отгоняют при пониженном давлении и остаток очищают колоночной хроматографией на силикагеле с использованием в качестве элюента 20% метанола в этилацетате. Конечное желаемое соединение общей формулы (I) может быть затем подвергнуто очистке с получением его кислотно-аддитивной соли. Альтернативно, 10-хлорметил-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид (D37) может быть обработан N-метилпиперазином по методу, приведенному в рамках описания 1 с получением указанного выше соединения. Диапазон температур плавления (С): 121-125; ИК-спектр (см-1): 1180, 1289, 1336, 1439;H-ЯМР (м.д.): 2,42 (с, 3H), 2,73-2,83 (уш.с, 8 Н), 3,88 (с, 2 Н), 7,22-8,07 (м, 8 Н). Пример 2. 1-Бром-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид. С использованием, по существу, общей методики примера 1 и ряда непринципиальных изменений получают указанное выше производное. Масс-спектр (m/z): 446, 448 (М+Н)+. Пример 3. 1-Хлор-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид. С использованием, по существу. общей методики примера 1 и ряда непринципиальных изменений получают указанное выше производное. Масс-спектр (m/z): 402 (М+Н)+. Пример 4. 2-Бром-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид. С использованием, по существу, общей методики примера 1 и ряда непринципиальных изменений получают указанное выше производное. ИК-спектр (см-1): 1179, 1334, 1436, 1294; Масс-спектр (m/z): 446,448 (М+Н)+. 1H-ЯМР (м.д.): 2,08 (с, 3H), 2,32-2,76 (уш.с, 8 Н), 3,80 (с, 2 Н), 7,26-8,07 (м, 7 Н). Пример 5. Хлористо-водородная соль 2-бром-10-(4-метилпиперазин-1-илметил)-5-тиа-4bазаиндено[2,1-а]инден-5,5-диоксида. С использованием, по существу, общей методики примера 1 и ряда непринципиальных изменений получают указанное выше производное. ИК-спектр (см-1): 1181, 1336, 1438, 1290; Масс-спектр (m/z): 446(М+Н)+, 448 (М+2)+ (основание). Пример 6. 2-Метокси-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5 диоксид. С использованием, по существу, общей методики примера 1 и ряда непринципиальных изменений получают указанное выше производное. Диапазон температур плавления (С): 180-182; ИК-спектр (см-1): 1178, 1328, 1461, 1571; Масс-спектр (m/z): 398 (М+Н)+. 1H-ЯМР (м.д.): 2,28 (с, 3H), 2,40-2,45 (уш.с, 4 Н), 2,60-2,70 (уш.с, 4 Н), 3,79 (с, 2 Н), 3,87 (с, 3H), 6,978,09 (м, 7 Н). Пример 7. 2-Метокси-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5 диоксид. С использованием, по существу, общей методики примера 1 и ряда непринципиальных изменений получают указанное выше производное. Масс-спектр (m/z): 448 (М+Н)+. Пример 8. 2-Этокси-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид. С использованием, по существу, общей методики примера 1 и ряда непринципиальных изменений получают указанное выше производное. ИК-спектр (см-1): 1176, 1214, 1344, 1461; Масс-спектр (m/z): 412H-ЯМР (м.д.): 1,42-1,49 (т, 3H), 2,29 (с, 3H), 2,46-2,60 (уш.с, 8 Н), 3,79 (с, 2 Н), 4,04-4,14 (кв, 2 Н),6,97-8,10 (м, 7 Н). Пример 9. 2-Этокси-8-метил-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5 диоксид. С использованием, по существу, общей методики примера 1 и ряда непринципиальных изменений получают указанное выше производное. ИК-спектр (см-1): 1176, 1218, 1326, 1465; Масс-спектр (m/z): 426(кв, 2 Н), 6,97-7,92 (м, 6 Н). Пример 10. 2-Бензилокси-10-(4-метилпиперазин-1-илмешил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5 диоксид. С использованием, по существу, общей методики примера 1 и ряда непринципиальных изменений получают указанное выше производное. ИК-спектр (см-1): 1173, 1204, 1367, 1448; Масс-спектр (m/z.): 474(М+Н)+. 1 Н-ЯМР (м.д.): 2,29 (с, 3H), 2,46-2,59 (уш.с, 8 Н), 3,78 (с, 2 Н), 5,13 (с, 2 Н), 7,05-8,08 (м, 12 Н). Пример 11. 2-Циклопентилокси-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден 5,5-диоксид. С использованием, по существу, общей методики примера 1 и ряда непринципиальных изменений получают указанное выше производное. ИК-спектр (см-1): 1186, 1206, 1333, 1462; Масс-спектр (m/z): 452(М+Н)+. Пример 12. 2-Циклогексилокси-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден 5,5-диоксид. С использованием, по существу, общей методики примера 1 и ряда непринципиальных изменений получают указанное выше производное. ИК-спектр (см-1): 1178, 1200, 1372, 1462; Масс-спектр (m/z): 466(М+Н)+. Пример 13. 2-(Фуран-2-илметокси)-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1 а]инден-5,5-диоксид. С использованием, по существу, общей методики примера 1 и ряда непринципиальных изменений получают указанное выше производное. ИК-спектр (см-1): 1017, 1178, 1260, 1462; Масс-спектр (m/z): 494H-ЯМР (м.д.): 2,36 (с, 3H), 2,64-2,80 (уш.с, 8 Н), 3,81 (с, 2 Н), 5,06 (с, 2 Н), 6,40-8,01 (м, 10 Н). Пример 14. 1,2,3-Трихлор-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5 диоксид. С использованием, по существу, общей методики примера 1 и ряда непринципиальных изменений получают указанное выше производное. Масс-спектр (m/z): 470, 472, 474 (М+Н)+. Пример 15. 2,8-Диметокси-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5 диоксид. С использованием. по существу, общей методики примера 1 и ряда непринципиальных изменений получают указанное выше производное. Диапазон температур плавления (С): 172-177; ИК-спектр (см-1): 1173, 1331, 1384, 1477; Масс-спектр (m/z): 428 (М+Н)+. 1 Н-ЯМР (м.д.): 2,29 (с, 3H), 2,46-2,60 (уш.с, 8 Н), 3,77 (с, 2 Н), 3,87 (с, 3H), 3,94 (с, 3H), 6,92-7,37 (м,6 Н). Пример 16. 2-Бром-8-метокси-10-(4-метилпиперазин-1-илметил) -5-тиа-4b-азаиндено [2 ,1-а] инден 5,5-диоксид. С использованием, по существу, общей методики примера 1 и ряда непринципиальных изменений получают указанное выше производное. Масс-спектр (m/z): 476, 478 (М+Н)+. Пример 17. 8-Метокси-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5 диоксид. С использованием. по существу, общей методики примера 1 и ряда непринципиальных изменений получают указанное выше производное. ИК-спектр (см-1): 1177, 1244, 1331, 1438; Масс-спектр (m/z): 398(М+Н)+. Пример 18. Хлористо-водородная соль 2-метокси-10-(4-метилпиперазин-1-илметил)-5-тиа-4bазаиндено[2,1-а]инден-5,5-диоксида. С использованием, по существу, общей методики примера 1 и ряда непринципиальных изменений получают указанное выше производное. ИК-спектр (см-1): 1180, 1246, 1335, 1440; Масс-спектр (m/z): 398(М+Н)+. Пример 19. 8-Изопропокси-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5 диоксид. С использованием, по существу, общей методики примера 1 и ряда непринципиальных изменений получают указанное выше производное. Диапазон температур плавления (С): 153-156; ИК-спектр (см-1): 1178, 1287, 1341, 1462; Масс-спектр (m/z): 426 (М+Н)+. 1 Н-ЯМР (м.д.): 1,35-1,38 (д, 6 Н), 2,28 (с, 3H), 2,45-2,59 (уш.с, 8 Н), 3,78 (с, 2 Н), 4,54-4,60 (септ, 1 Н),6,96-8,09 (м, 7 Н). Пример 20. 2-Бром-8-метил-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5 диоксид. С использованием, по существу, общей методики примера 1 и ряда непринципиальных изменений получают указанное выше производное. Масс-спектр (m/z): 460, 462 (М+Н)+. Пример 21. 4-Метил-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5 диоксид. С использованием, по существу, общей методики примера 1 и ряда непринципиальных изменений получают указанное выше производное. ИК-спектр (см-1): 1176, 1261; 1333, 1465; Масс-спектр (m/z): 382(М+Н)+. Пример 22. (RS) 8-Метил-10-[1-(4-метилпиперазин-1-ил)этил]-5-тиа-4b-азаиндено[2,1-а]инден-5,5 диоксид. С использованием, по существу, общей методики примера 1 и ряда непринципиальных изменений получают указанное выше производное. Масс-спектр (m/z): 396 (М+Н)+. Пример 23. (RS) 2-Метокси-10-[1-(4-метилпиперазин-1-ил)зтил]-5-тиа-4b-азаиндено[2,1-а]инден 5,5-диоксид. С использованием, по существу, общей методики примера 1 и ряда непринципиальных изменений получают указанное выше производное. Масс-спектр (m/z): 412 (М+Н)+. Пример 24. (RS) 2-Бром-8-метокси-10-[1-(4-метилпиперазин-1-ил)этил]-5-тиа-4b-азаиндено[2,1 а]инден-5,5-диоксид. С использованием, по существу, общей методики примера 1 и ряда непринципиальных изменений получают указанное выше производное. Масс-спектр (m/z): 490, 492 (М+Н)+. Пример 25. (RS) 1-[4-(8-Метокси-5,5-диоксо-5 Н-5-тиа-4b-азаиндено[2,1-а]инден-10-илметил]-2 метилпиперазин-1-ил]этанон. С использованием, по существу, общей методики примера 1 и ряда непринципиальных изменений получают указанное выше производное. ИК-спектр (см-1): 1178, 1332, 1436, 1634; Масс-спектр (m/z): 440(М+Н)+. Пример 26. 10-(4-Пиридин-2-ил-пиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид. С использованием, по существу, общей методики примера 1 и ряда непринципиальных изменений- 24009367 получают указанное выше производное. ИК-спектр (см-1): 1181, 1338, 1437, 1592; Масс-спектр (m/z): 431(М+Н)+. 1 Н-ЯМР (м.д.): 2,69-2,71 (уш.с, 4 Н), 3,53-3,58 (уш.с, 4 Н), 3,89 (с, 2 Н), 6,59-8,20 (м, 11 Н). Пример 27. 8-Метокси-10-[4-(пиридин-2-ил)пиперазин-1-ил]метил-5-тиа-4b-азаиндено[2,1-а]инден 5,5-диоксид. С использованием, по существу, общей методики примера 1 и ряда непринципиальных изменений получают указанное выше производное. ИК-спектр (см-1): 1166, 1252, 1324, 1594; Масс-спектр (m/z): 461(М+Н)+. 1 Н-ЯМР (м.д.): 2,94 (уш.с, 4 Н), 3,59 (уш.с, 4 Н), 3,37 (с, 2 Н), 3,92 (с, 3H), 6,60-8,21 (м, 11 Н). Пример 28. 2-Изопропокси-10-(4-бензоилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден 5,5-диоксид. С использованием, по существу, общей методики примера 1 и ряда непринципиальных изменений получают указанное выше производное. ИК-спектр (см-1): 1176, 1279, 1333, 1632; Масс-спектр (m/z): 516(М+Н)+. Пример 29. 2-(Фуран-2-илметокси)-10-(4-бензоилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1 а]инден-5,5-диоксид. С использованием, по существу, общей методики примера 1 и ряда непринципиальных изменений получают указанное выше производное. ИК-спектр (см-1): 1178, 1335, 1445, 1633; Масс-спектр (m/z): 554(М+Н)+. Пример 30. 10-(4-Бензилпиперазин-1-илме'гил)-8-меатил-5-тиа-4b-азаиндено[2,1-а]инден-5,5 диоксид. С использованием, по существу, общей методики примера 1 и ряда непринципиальных изменений получают указанное выше производное. ИК-спектр (см-1): 1166, 1252, 1324, 1594; Масс-спектр (m/z): 458(М+Н)+. Пример 31. 10-(4-Бензилпиперазин-1-илметил)-8-метокси-5-тиа-4b-азаиндено[2,1-а]инден-5,5 диоксид. С использованием, по существу, общей методики примера 1 и ряда непринципиальных изменений получают указанное выше производное. ИК-спектр (см-1): 1159, 1218, 1346, 1453; Масс-спектр (m/z): 474(М+Н)+. 1 Н-ЯМР (м.д.): 2,50-2,60 (уш.с, 8 Н), 3,52 (с, 2 Н), 3,82 (с, 2 Н), 3,92 (с, 3H), 6,95-7,74 (м, 12 Н). Пример 32. 2-Метокси-10-пиперазин-1-илметил-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид. С использованием, по существу, общей методики примера 1 и ряда непринципиальных изменений получают указанное выше производное. ИК-спектр (см-1): 1177, 1227, 1333, 3411; Масс-спектр (m/z): 384(М+Н)+. 1 Н-ЯМР (м.д.): 2,58-2,69 (уш.с, 8 Н), 2,36 (с, 1 Н), 3,83 (с, 2 Н), 3,92 (с, 3H), 7,14-7,83 (м, 7 Н). Пример 33. 2-Изопропокси-10-пиперазин-1-илметил-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид. С использованием, по существу, общей методики примера 1 и ряда непринципиальных изменений получают указанное выше производное. ИК-спектр (см-1): 1119, 1278, 1372, 3430; Масс-спектр (m/z): 412(М+Н)+. Пример 34. 2-(Фуран-2-илметокси)-10-пиперазин-1-илметил-5-тиа-4b-азаиндено[2,1-а]инден-5,5 диоксид. С использованием, по существу, общей методики примера 1 и ряда непринципиальных изменений получают указанное выше производное. Масс-спектр (m/z): 450 (М+Н)+. Пример 35. 10-[1,4]Диазепан-1-илметил-2-метокси-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид. С использованием, по существу, общей методики примера 1 и ряда непринципиальных изменений получают указанное выше производное. Масс-спектр (m/z): 398 (М+Н)+. Пример 36. 1-[4-(5,5-Диоксо-5 Н-5-тиа-4b-азаиндено[2,1-а]инден-10-илметил)-[1,4]диазепан-1-ил] фенилметанон. С использованием, по существу, общей методики примера 1 и ряда непринципиальных изменений получают указанное выше производное. ИК-спектр (см-1): 1180, 1336, 1439, 1629; Масс-спектр (m/z): 472(М+Н)+. 1 Н-ЯМР (м.д.): 1,72 (уш.с, 2 Н), 2,68 (уш.с, 2 Н), 3,01 (д, 2 Н), 3,44-3,47 (с, 2 Н), 3,80-3,83 (уш.с, 2 Н),3,94-3,98 (д, 2 Н). 7,26-7,86 (м, 13 Н). Пример 37. 10-(4-Этил[1,4]диазепан-1-илметил)-2-метокси-5-тиа-4b-азаиндено[2,1-а]инден-5,5 диоксид. С использованием, по существу, общей методики примера 1 и ряда непринципиальных изменений получают указанное выше производное. Масс-спектр (m/z): 426 (М+Н)+. Пример 38. 10-(4-Изопропил[1,4]диазепан-1-илметил)-2-метокси-5-тиа-4b-азаиндено[2,1-а]инден 5,5-диоксид. С использованием, по существу, общей методики примера 1 и ряда непринципиальных изменений получают указанное выше производное. Масс-спектр (m/z): 426 (М+Н)+.- 25009367 ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Соединение общей формулы (I) где A может представлять собой -СН 2- или - СН 2-СН 2-; где R1, R3, R4, R6, R7, R8 и R9 могут быть одинаковыми или различными, и каждый означает водород, галоген, линейный или разветвленный (C1-C6)алкил, линейный или разветвленный (C1-C6)алкокси;R2 означает водород, галоген, тио, линейный или разветвленный (C1-C6)алкил, линейный или разветвленный (C1-C6)алкокси; цикло(С 3-С 7)алкокси; арилокси, ар(C1-С 3)алкилокси, гетероарил(C1 С 3)алкилокси; или R7 и R8, вместе с атомами углерода, к которым они присоединены, могут образовывать пятиили шестичленное кольцо;R14 и R15 могут быть одинаковыми или различными, и каждый означает водород или линейный или разветвленный (C1-C6)алкил;R13, R16 и R17 могут быть одинаковыми или различными, и каждый означает водород или линейный или разветвленный (C1-С 6)алкил; необязательно R13 вместе с или R16, или R17 и двумя атомами азота может образовывать 5-7-членное гетероциклическое кольцо, которое может быть дополнительно замещено водородом, (C1-С 3)алкилом,(C1-С 3)алкокси, ацетилом, фенилом, гетероарилом, гетероциклилом, бензилом и бензоилом;n равно целому числу от 1 до 3; где термин арил сам по себе или как часть других групп означает фенил или нафтил; термин гетероциклил означает 5-6-членный гетероциклил, содержащий 1-2 гетероатома О или N; термин гетероарил означает 5-6-членный гетероарил, содержащий 1-2 гетероатома О или N. 2. Соединение по п.1, которое выбирают из группы, включающей 10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид; 1-бром-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид; 1-хлор-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид; 2-бром-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид; хлористо-водородную соль 2-бром-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а] инден-5,5-диоксида; 2-метокси-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид; 2-метокси-12-(4-метилпиперазин-1-илметил)-5-тиа-4b-азабензо[4,5]пенталено[1,2-b]нафталин-5,5 диоксид; 2-этокси-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид; 2-этокси-8-метил-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид; 2-бензилокси-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид; 2-циклопентилокси-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид; 2-циклогексилокси-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид; 2-(фуран-2-илметокси)-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5 диоксид; 1,2,3-трихлор-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид; 2,8-диметокси-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид; 2-бром-8-метокси-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид; 8-метокси-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид; хлористо-водородную соль 2-метокси-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1 а]инден-5,5-диоксида; 8-изопропокси-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид; 2-бром-8-метил-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид; 4-метил-10-(4-метилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид;(RS) 1-[4-(2-метокси-5,5-диоксо-5 Н-тиа-4b-азаиндено[2,1-а]инден-10-илметил)-2-метилпиперазин 1-ил]этанон; 10-(4-этилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид; 1-хлор-10-(4-этилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5,5-диоксид; 1-метокси-10-(4-этилпиперазин-1-илметил)-5-тиа-4b-азаиндено[2,1-а]инден-5, 5-диоксид; их стереоизомер и их соли. 3. Способ получения соединения общей формулы (I) где А может представлять собой -СН 2- или - СН 2-СН 2-; где R1, R3, R4, R6, R7, R8 и R9 могут быть одинаковыми или различными, и каждый означает водород, галоген, линейный или разветвленный (C1-C6)алкил, линейный или разветвленный (C1-C6) алкокси;R2 означает водород, галоген, тио, линейный или разветвленный (C1-C6)алкил, линейный или разветвленный (C1-C6)алкокси; цикло(С 3-С 7)алкокси; арилокси, ар(C1-С 3)алкилокси, гетероарил(C1 С 3)алкилокси; или R7 и R8, вместе с атомами углерода, к которым они присоединены, могут образовывать пятиили шестичленное кольцо;R14 и R15 могут быть одинаковыми или различными, и каждый означает водород или линейный или разветвленный (C1-C6)алкил;R13, R16 и R17 могут быть одинаковыми или различными, и каждый означает водород или линейный или разветвленный (C1-С 6)алкил; необязательно R13 вместе с или R16, или R17 и двумя атомами азота может образовывать 5-7-членное гетероциклическое кольцо, которое может быть дополнительно замещено водородом, (C1-С 3)алкилом,(C1-С 3)алкокси, ацетилом, фенилом, гетероарилом, гетероциклилом, бензилом и бензоилом;n равно целому числу от 1 до 3; где термин арил сам по себе или как часть других групп означает фенил или нафтил; термин гетероциклил означает 5-6-членный гетероциклил, содержащий 1-2 гетероатома О или N; термин гетероарил означает 5-6-членный гетероарил, содержащий 1-2 гетероатома О или N;- 27009367 который включает взаимодействие соединения формулы (II), приведенной ниже(II) в качестве катализатора. 4. Способ получения соединения общей формулы (I) где А может представлять собой -СН 2- или - СН 2-СН 2-; где R1, R3, R4, R6, R7, R8 и R9 могут быть одинаковыми или различными, и каждый означает водород, галоген, линейный или разветвленный (C1-C6)алкил, линейный или разветвленный (C1-C6)алкокси;R2 означает водород, галоген, тио, линейный или разветвленный (C1-C6)алкил, линейный или разветвленный (C1-C6)алкокси; цикло(С 3-С 7)алкокси; арилокси, ар(C1-С 3)алкилокси, гетероарил(C1-С 3)алкилокси; или R7 и R8, вместе с атомами углерода, к которым они присоединены, могут образовывать пятиили шестичленное кольцо;R14 и R15 могут быть одинаковыми или различными, и каждый означает водород или линейный или разветвленный (C1-C6)алкил;R13, R16 и R17 могут быть одинаковыми или различными, и каждый означает водород или линейный или разветвленный (C1-С 6)алкил; необязательно R13 вместе с или R16, или R17 и двумя атомами азота может образовывать 5-7-членное гетероциклическое кольцо, которое может быть дополнительно замещено водородом, (C1-С 3)алкилом,(C1-С 3)алкокси, ацетилом, фенилом, гетероарилом, гетероциклилом, бензилом и бензоилом;n равно целому числу от 1 до 3; где термин арил сам по себе или как часть других групп означает фенил или нафтил; термин гетероциклил означает 5-6-членный гетероциклил, содержащий 1-2 гетероатома О или N; термин гетероарил означает 5-6-членный гетероарил, содержащий 1-2 гетероатома О или N; который включает взаимодействие соединения формулы (III), приведенной ниже- 28009367 где все символы определены выше для соединения формулы, в которой A, R1, R2, R3, R4, R6, R7, R8 и R9 определены применительно к формуле (I), X означает водород или удаляемую группу, такую как гидрокси, мезил, тозил или галоген, например хлор, бром или иод, и т.п., с соединением формулы (IV) или его кислотно-аддитивной солью где все символы определены выше и X означает галоген, предпочтительно хлор, бром или иод. 5. Способ получения соединения общей формулы (I), где А означает -СН 2-, который включает химическое или каталитическое восстановление соединений, в которых А означает СО, где все символы определены выше. 6. Способ по п.3 или 4, включающий осуществление одной или более из следующих необязательных стадий: i) удаление любой защитной группы; ii) разделение рацемической смеси на чистые энантиомеры в соответствии с известными методами и iii) получение фармацевтически приемлемой соли соединения формулы (I) и/или iv) получение его фармацевтически приемлемого пролекарства. 7. Фармацевтическая композиция, содержащая фармацевтически приемлемый носитель, разбавитель, эксципиент или сольват в сочетании с терапевтически эффективным количеством соединения по п.1, его стереоизомеров, его радиоактивных изотопов, его N-оксидов, его полиморфов, его фармацевтически приемлемых солей, его фармацевтически приемлемых сольватов, его полезных биоактивных метаболитов и любой приемлемой комбинации указанных веществ. 8. Фармацевтическая композиция по п.7 в форме таблетки, капсулы, порошка, сиропа, инъецируемой формы, раствора или суспензии. 9. Промежуточные соединения общей формулы (III)X означает водород, удаляемую группу, такую как гидрокси, мезил, тозил или галоген, например хлор, бром или иод; где R1, R3, R4, R6, R7, R8 и R9 могут быть одинаковыми или различными, и каждый означает водород, галоген, линейный или разветвленный (C1-C6)алкил, линейный или разветвленный (C1-C6)алкокси;R2 означает водород, галоген, тио, линейный или разветвленный (C1-C6)алкил, линейный или разветвленный (C1-C6)алкокси; цикло(С 3-С 7)алкокси; арилокси, ap(C1-С 3)алкилокси, гетероарил(C1 С 3)алкилокси; или R7 и R8, вместе с атомами углерода, к которым они присоединены, могут образовывать пятиили шестичленное кольцо; где термин арил сам по себе или как часть других групп означает фенил или нафтил; термин гетероарил означает 5-6-членный гетероарил, содержащий 1-2 гетероатома О или N; и их стереоизомеры и их соли, при условии, что R1, R2, R3, R4, R6, R7, R8, R9 и X все не могут означать водород, так что 1 Н-индол [1,2-b]бензо(d)изотиазол-10-метил-5,5'-диоксид формулы, приведенной ниже исключается из указанных соединений формулы (III). 10. Способ получения промежуточного соединения общей формулы (III) в соответствии с одним из вариантов, которые включают: 1) циклизацию соединения формулы (V), приведенной ниже где X, A, R1, R2, R3, R4, R6, R7, R8 и R9 определены выше, и один из R10 и R5 означает атом галогена, например хлор, бром или иод и т.п., а другой означает водород; с использованием производного тетракис(трифенилфосфин)палладия(0) или дихлор-бис(три-о-толилфосфин)палладия(II) в качестве катализатора, и 2) превращение соединения формулы (VII), приведенной ниже где X, R1, R2, R3, R4, R6, R7, R8 и R9 определены применительно к формуле (III), посредством металлизации и последующей реакции с газообразным SO2 и N-хлорсукцинимидом для получения соединения общей формулы (III), где А означает SO2. 11. Применение соединения общей формулы (I) по п.1 или его фармацевтической композиции по п.7 при получении лекарственных средств. 12. Применение соединения по п.1 при лечении и/или профилактике клинических состояний, таких как тревога, депрессия, судорожные расстройства, обсессивно-компульсивные расстройства, мигрень,головная боль, нарушение познавательной способности, ADHD (дефицит внимания/синдром гиперактивности), личностные расстройства, психоз, парафрения, психотическая депрессия, мания, шизофрения,шизофреноподобные расстройства, абстинентный синдром, приступы паники, хронобиологические аномалии, расстройства циркадного ритма, анксиолитическое расстройство, остеопороз, ишемический удар,риск развития синдрома внезапной смерти у младенцев, имеющих низкий эндогенный уровень мелатонина, проблемы репродуктивной сферы, глаукома, расстройства сна, а также расстройства, связанные с травмой спинного мозга и/или повреждением головы. 13. Применение соединения по п.1 при лечении умеренного ухудшения познавательной способности и/или других нейродегенеративных расстройств типа болезни Альцгеймера, паркинсонизма и хореи Хантингтона. 14. Применение соединения по п.1 при лечении некоторых расстройств ЖКТ (желудочнокишечного тракта), таких как IBS (синдром раздраженного кишечника), или рвоты, вызванной химиотерапией. 15. Применение соединения по п.1 для лечения и профилактики заболеваний, связанных с избыточным весом. 16. Применение радиоактивно меченого соединения по п.1 в качестве диагностического инструмента для модуляции функции рецептора 5-НТ и/или мелатонина.
МПК / Метки
МПК: A61K 31/425, C07D 209/00, C07D 275/00, A61P 25/00, C07D 513/04
Метки: 5-тиа-5-диоксо-4b-азаиндено[2,1-a]индена, обладающие, серотонина, производные, рецептору, аффинностью
Код ссылки
<a href="https://eas.patents.su/30-9367-proizvodnye-5-tia-5-diokso-4b-azaindeno21-aindena-obladayushhie-affinnostyu-k-receptoru-serotonina.html" rel="bookmark" title="База патентов Евразийского Союза">Производные 5-тиа-5-диоксо-4b-азаиндено[2,1-a]индена, обладающие аффинностью к рецептору серотонина</a>
Предыдущий патент: Связанные с полиэтиленгликолем соединения гпп-1
Следующий патент: Соединения-ингибиторы липазы поджелудочной железы, их синтез и применение
Случайный патент: Применение 3-(1н-имидазол-4-илметил)индан-5-ола при изготовлении лекарственного средства для интраспинального, подоболочечного или эпидурального введения












