Новые p2x7r антагонисты и их применение
Формула / Реферат
1. Соединение общей формулы
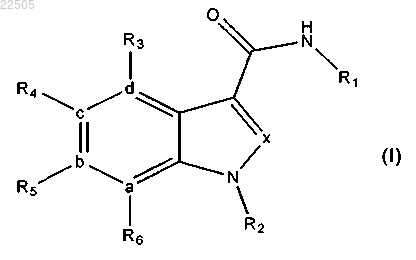
где R1 представляет собой моно- или бициклоалкилалкильную группу, выбранную из циклопентилметила, циклопентилэтила, циклогексилметила, циклогексилэтила, циклогептилметила, циклогептилэтила, бицикло[2.2.2]октан-1-илметила и бицикло[2.2.2]октан-1-илэтила;
R2 выбирают из неразветвленного или разветвленного С1-С5алкила, который необязательно может быть замещен -ОН, 2Н-тетразолилэтилом, метилкарбамоилом, диметилкарбамоилом или этилметилкарбамоилом;
R3, R4, R5 или R6, в каждом случае независимо, выбирают из водорода, галогена, метила, гидрокси, метокси, циано или трифторметила;
а, b, с, d, х, в каждом случае независимо, выбирают из углерода или азота;
или его фармацевтически приемлемая соль или сольват.
2. Соединение в соответствии с п.1, где R2 представляет собой С1-С5алкил или С2-С5гидроксиалкил.
3. Соединение в соответствии с п.1 или 2, где по меньшей мере два из R3, R4, R5 и R6 представляют собой водород.
4. Соединение в соответствии с любым из пп.1-3, где х представляет собой С.
5. Соединение в соответствии с любым из пп.1-3, где х представляет собой N.
6. Соединение в соответствии с любым из пп.1-5, где а, b, с и d представляют собой С.
7. Соединение в соответствии с любым из пп.1-5, где один из а, b, с и d представляет собой N.
8. Соединение в соответствии с любым из пп.1-7, выбранное из соединений
N-(циклопентилметил )-1-метил-1Н-индол-3-карбоксамид,
4-хлор-N-(циклопентилметил)-1-метил-1Н-индол-3-карбоксамид,
N-(циклопентилметил)-4-фтор-1-метил-1Н-индол-3-карбоксамид,
4-бром-N-(циклопентилметил)-1-метил-1Н-индол-3-карбоксамид,
N-(циклопентилметил)-1,4-диметил-1Н-индол-3-карбоксамид,
N-(циклопентилметил)-4-фтор-1-(2-гидроксиэтил)-1Н-индол-3-карбоксамид,
4-хлор-N-(циклопентилметил)-1-(2-гидроксиэтил)-1Н-индол-3-карбоксамид,
4-бром-N-(циклопентилметил)-1-(2-гидроксиэтил)-1Н-индол-3-карбоксамид,
N-(циклогексилметил)-1-метил-1Н-индол-3-карбоксамид,
4-хлор-N-(циклогексилметил)-1-метил-1Н-индол-3-карбоксамид,
N-(циклогексилметил)-4-фтор-1-метил-1Н-индол-3-карбоксамид,
4-бром-N-(циклогексилметил)-1-метил-1Н-индол-3-карбоксамид,
N-(циклогексилметил)-1,4-диметил-1Н-индол-3-карбоксамид,
N-(циклогексилметил)-4-фтор-1-(2-гидроксиэтил)-1Н-индол-3-карбоксамид,
4-хлор-N-(циклогексилметил)-1-(2-гидроксиэтил)-1Н-индол-3-карбоксамид,
4-бром-N-(циклогексилметил)-1-(2-гидроксиэтил)-1Н-индол-3-карбоксамид,
N-(циклогептилметил)-1-метил-1Н-индол-3-карбоксамид,
4-хлор-N-(циклогептилметил)-1-метил-1Н-индол-3-карбоксамид,
N-(циклогептилметил)-4-фтор-1-метил-1Н-индол-3-карбоксамид,
4-бром-N-(циклогептилметил)-1-метил-1Н-индол-3-карбоксамид,
N-(циклогептилметил)-1,4-диметил-1Н-индол-3-карбоксамид,
N-(циклогептилметил)-4-метокси-1-метил-1Н-индол-3-карбоксамид,
4-циано-N-(циклогептилметил)-1-метил-1Н-индол-3-карбоксамид,
N-(циклогептилметил)-1-метил-4-(трифторметил)-1Н-индол-3-карбоксамид,
N-(циклогептилметил)-1-этил-1Н-индол-3-карбоксамид,
N-(циклогептилметил)-1-этил-4-фтор-1Н-индол-3-карбоксамид,
4-хлор-N-(циклогептилметил)-1-этил-1Н-индол-3-карбоксамид,
4-бром-N-(циклогептилметил)-1-этил-1Н-индол-3-карбоксамид,
N-(циклогептилметил)-1-этил-4-метил-1Н-индол-3-карбоксамид,
N-(циклогептилметил)-1-этил-4-метокси-1Н-индол-3-карбоксамид,
4-циано-N-(циклогептилметил)-1-этил-1Н-индол-3-карбоксамид,
N-(циклогептилметил)-1-этил-4-(трифторметил)-1Н-индол-3-карбоксамид,
N-(циклогептилметил)-1-пропил-1Н-индол-3-карбоксамид,
N-(циклогептилметил)-4-фтор-1-пропил-1Н-индол-3-карбоксамид,
4-хлор-N-(циклогептилметил)-1-пропил-1Н-индол-3-карбоксамид,
4-бром-N-(циклогептилметил)-1-пропил-1Н-индол-3-карбоксамид,
N-(циклогептилметил)-4-метил-1-пропил-1Н-индол-3-карбоксамид,
N-(циклогептилметил)-4-метокси-1-пропил-1Н-индол-3-карбоксамид,
4-циано-N-(циклогептилметил)-1-пропил-1Н-индол-3-карбоксамид,
N-(циклогептилметил)-1-пропил-4-(трифторметил)-1Н-индол-3-карбоксамид,
4-хлор-N-(циклогептилметил)-1-изопропил-1Н-индол-3-карбоксамид,
4-бром-N-(циклогептилметил)-1-изопропил-1Н-индол-3-карбоксамид,
N-(циклогептилметил)-1-изопропил-4-метил-1Н-индол-3-карбоксамид,
4-хлор-N-(циклогептилметил)-1-изопропил-1Н-индол-3-карбоксамид,
4-бром-N-(циклогептилметил)-1-изопропил-1Н-индол-3-карбоксамид,
N-(циклогептилметил)-1-изопропил-4-метил-1Н-индол-3-карбоксамид,
4-хлор-N-(циклогептилметил)-1-изобутил-1Н-индол-3-карбоксамид,
4-бром-N-(циклогептилметил)-1-изобутил-1Н-индол-3-карбоксамид,
N-(циклогептилметил)-1-изобутил-4-метил-1Н-индол-3-карбоксамид,
N-(циклогептилметил)-1-(2-гидроксиэтил)-1Н-индол-3-карбоксамид,
N-(циклогептилметил)-4-фтор-1-(2-гидроксиэтил)-1Н-индол-3-карбоксамид,
4-хлор-N-(циклогептилметил)-1-(2-гидроксиэтил)-1Н-индол-3-карбоксамид,
4-бром-N-(циклогептилметил)-1-(2-гидроксиэтил)-1Н-индол-3-карбоксамид,
N-(циклогептилметил)-1-(2-гидроксиэтил)-4-метил-1Н-индол-3-карбоксамид,
N-(циклогептилметил)-1-(2-гидроксиэтил)-4-метокси-1Н-индол-3-карбоксамид,
4-циано-N-(циклогептилметил)-1-(2-гидроксиэтил)-1Н-индол-3-карбоксамид,
N-(циклогептилметил)-1-(2-гидроксиэтил)-4-(трифторметил)-1Н-индол-3-карбоксамид,
1-бутил-N-(циклогептилметил)-1Н-индол-3-карбоксамид,
1-бутил-N-(циклогептилметил)-4-фтор-1Н-индол-3-карбоксамид,
1-бутил-4-хлор-N-(циклогептилметил)-1Н-индол-3-карбоксамид,
4-бром-1-бутил-N-(циклогептилметил)-1Н-индол-3-карбоксамид,
1-бутил-N-(циклогептилметил)-4-метил-1Н-индол-3-карбоксамид,
N-(циклогептилметил)-4-фтор-1-(3-гидроксипропил)-1Н-индол-3-карбоксамид,
4-хлор-N-(циклогептилметил)-1-(3-гидроксипропил)-1Н-индол-3-карбоксамид,
4-бром-N-(циклогептилметил)-1-(3-гидроксипропил)-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-1-метил-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-4-хлор-1-метил-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-4-фтор-1-метил-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-4-бром-1-метил-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-1,4-диметил-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-4-метокси-1-метил-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-4-циано-1-метил-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-1-метил-4-(трифторметил)-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-1-этил-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-1-этил-4-фтор-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-4-хлор-1-этил-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-4-бром-1-этил-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-1-этил-4-метил-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-1-этил-4-метокси-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-4-циано-1-этил-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-1-этил-4-(трифторметил)-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-1-пропил-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-4-фтор-1-пропил-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-4-хлор-1-пропил-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-4-бром-1-пропил-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-4-метил-1-пропил-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-4-метокси-1-пропил-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-4-циано-1-пропил-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-1-пропил-4-(трифторметил)-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-1-изопропил-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-4-фтор-1-изопропил-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-4-хлор-1-изопропил-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-4-бром-1-изопропил-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-1-изопропил-4-метил-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-4-фтор-1-изобутил-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-4-хлор-1-изобутил-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-4-бром-1-изобутил-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-1-изобутил-4-метил-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-1-(2-гидроксиэтил)-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-4-фтор-1-(2-гидроксиэтил)-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-4-хлор-1-(2-гидроксиэтил)-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-4-бром-1-(2-гидроксиэтил)-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-1-(2-гидроксиэтил)-4-метил-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-1-(2-гидроксиэтил)-4-метокси-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-4-циано-1-(2-гидроксиэтил)-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-1-(2-гидроксиэтил)-4-(трифторметил)-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-1-бутил-4-фтор-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-1-бутил-4-хлор-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-4-бром-1-бутил-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-1-бутил-4-метил-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-4-фтор-1-(3-гидроксипропил)-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-4-хлор-1-(3-гидроксипропил)-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-4-бром-1-(3-гидроксипропил)-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-1-(3-гидроксипропил)-4-метил-1Н-индол-3-карбоксамид,
4-хлор-N-(2-циклогексилэтил)-1-метил-1Н-индол-3-карбоксамид,
N-(2-циклогексилэтил)-4-фтор-1-метил-1Н-индол-3-карбоксамид,
4-бром-N-(2-циклогексилэтил)-1-метил-1Н-индол-3-карбоксамид,
N-(2-циклогексилэтил)-1,4-диметил-1Н-индол-3-карбоксамид,
N-(2-циклогексилэтил)-1-этил-4-фтор-1Н-индол-3-карбоксамид,
4-хлор-N-(2-циклогексилэтил)-1-этил-1Н-индол-3-карбоксамид,
4-бром-N-(2-циклогексилэтил)-1-этил-1Н-индол-3-карбоксамид,
N-(2-циклогексилэтил)-1,4-диметил-1Н-индол-3-карбоксамид,
N-(2-циклогексилэтил)-1-этил-4-фтор-1Н-индол-3-карбоксамид,
4-хлор-N-(2-циклогексилэтил)-1-этил-1Н-индол-3-карбоксамид,
4-бром-N-(2-циклогексилэтил)-1-этил-1Н-индол-3-карбоксамид,
N-(2-циклогексилэтил)-1-этил-4-метил-1Н-индол-3-карбоксамид,
N-(2-циклогексилэтил)-4-фтор-1-(2-гидроксиэтил)-1Н-индол-3-карбоксамид,
4-хлор-N-(2-циклогексилэтил)-1-(2-гидроксиэтил)-1Н-индол-3-карбоксамид,
4-бром-N-(2-циклогексилэтил)-1-(2-гидроксиэтил)-1Н-индол-3-карбоксамид,
N-(2-циклогексилэтил)-1-(2-гидроксиэтил)-4-метил-1Н-индол-3-карбоксамид,
4-хлор-N-(2-циклогептилэтил)-1-метил-1Н-индол-3-карбоксамид,
4-бром-N-(2-циклогептилэтил)-1-метил-1Н-индол-3-карбоксамид,
N-(2-циклогептилэтил)-1,4-диметил-1Н-индол-3-карбоксамид,
4-хлор-N-(2-циклогептилэтил)-1-этил-1Н-индол-3-карбоксамид,
4-бром-N-(2-циклогептилэтил)-1-этил-1Н-индол-3-карбоксамид,
N-(2-циклогептилэтил)-1-этил-4-метил-1Н-индол-3-карбоксамид,
4-хлор-N-(2-циклогептилэтил)-1-(2-гидроксиэтил)-1Н-индол-3-карбоксамид,
4-бром-N-(2-циклогептилэтил)-1-(2-гидроксиэтил)-1Н-индол-3-карбоксамид,
N-(2-циклогептилэтил)-1-(2-гидроксиэтил)-4-метил-1Н-индол-3-карбоксамид,
5-хлор-N-(циклогептилметил)-1-метил-1Н-индол-3-карбоксамид,
5-бром-N-(циклогептилметил)-1-метил-1Н-индол-3-карбоксамид,
N-(циклогептилметил)-1,5-диметил-1Н-индол-3-карбоксамид,
5-хлор-N-(циклогептилметил)-1-этил-1Н-индол-3-карбоксамид,
5-бром-N-(циклогептилметил)-1-этил-1Н-индол-3-карбоксамид,
N-(циклогептилметил)-1-этил-5-метил-1Н-индол-3-карбоксамид,
5-хлор-N-(циклогептилметил)-1-(2-гидроксиэтил)-1Н-индол-3-карбоксамид,
5-бром-N-(циклогептилметил)-1-(2-гидроксиэтил)-1Н-индол-3-карбоксамид,
N-(циклогептилметил)-1-(2-гидроксиэтил)-5-метил-1Н-индол-3-карбоксамид,
6-хлор-N-(циклогептилметил)-1-метил-1Н-индол-3-карбоксамид,
6-бром-N-(циклогептилметил)-1-метил-1Н-индол-3-карбоксамид,
N-(циклогептилметил)-1,6-диметил-1Н-индол-3-карбоксамид,
6-хлор-N-(циклогептилметил)-1-этил-1Н-индол-3-карбоксамид,
6-бром-N-(циклогептилметил)-1-этил-1Н-индол-3-карбоксамид,
N-(циклогептилметил)-1-этил-6-метил-1Н-индол-3-карбоксамид,
6-хлор-N-(циклогептилметил)-1-(2-гидроксиэтил)-1Н-индол-3-карбоксамид,
6-бром-N-(циклогептилметил)-1-(2-гидроксиэтил)-1Н-индол-3-карбоксамид,
N-(циклогептилметил)-1-(2-гидроксиэтил)-6-метил-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-5-хлор-1-метил-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-5-бром-1-метил-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-1,5-диметил-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-5-хлор-1-этил-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-5-бром-1-этил-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-1-этил-5-метил-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-5-хлор-1-(2-гидроксиэтил)-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-5-бром-1-(2-гидроксиэтил)-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-1-(2-гидроксиэтил)-5-метил-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-6-хлор-1-метил-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-6-бром-1-метил-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-1,6-диметил-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-6-хлор-1-этил-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-6-бром-1-этил-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-1-этил-6-метил-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-6-хлор-1-(2-гидроксиэтил)-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-6-бром-1-(2-гидроксиэтил)-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-1-(2-гидроксиэтил)-6-метил-1Н-индол-3-карбоксамид,
4-хлор-N-(циклогептилметил)-6-фтор-1-метил-1Н-индол-3-карбоксамид,
4-бром-N-(циклогептилметил)-6-фтор-1-метил-1Н-индол-3-карбоксамид,
N-(циклогептилметил)-6-фтор-1,4-диметил-1Н-индол-3-карбоксамид,
4-хлор-N-(циклогептилметил)-1-этил-6-фтор-1Н-индол-3-карбоксамид,
4-бром-N-(циклогептилметил)-1-этил-6-фтор-1Н-индол-3-карбоксамид,
N-(циклогептилметил)-1-этил-6-фтор-4-метил-1Н-индол-3-карбоксамид,
4-хлор-N-(циклогептилметил)-6-фтор-1-изопропил-1Н-индол-3-карбоксамид,
4-бром-N-(циклогептилметил)-6-фтор-1-изопропил-1Н-индол-3-карбоксамид,
4-хлор-N-(циклогептилметил)-6-фтор-1-(2-гидроксиэтил)-1Н-индол-3-карбоксамид,
4-бром-N-(циклогептилметил)-6-фтор-1-(2-гидроксиэтил)-1Н-индол-3-карбоксамид,
N-(циклогептилметил)-6-фтор-1-(2-гидроксиэтил)-4-метил-1Н-индол-3-карбоксамид,
4,6-дихлор-N-(циклогептилметил)-1-метил-1Н-индол-3-карбоксамид,
6-хлор-N-(циклогептилметил)-4-фтор-1-метил-1Н-индол-3-карбоксамид,
4-бром-6-хлор-N-(циклогептилметил)-1-метил-1Н-индол-3-карбоксамид,
6-хлор-N-(циклогептилметил)-1,4-диметил-1Н-индол-3-карбоксамид,
6-хлор-N-(циклогептилметил)-1-этил-4-фтор-1Н-индол-3-карбоксамид,
4,6-дихлор-N-(циклогептилметил)-1-этил-1Н-индол-3-карбоксамид,
4-бром-6-хлор-N-(циклогептилметил)-1-этил-1Н-индол-3-карбоксамид,
6-хлор-N-(циклогептилметил)-1-этил-4-метил-1Н-индол-3-карбоксамид,
6-хлор-N-(циклогептилметил)-4-фтор-1-(2-гидроксиэтил)-1Н-индол-3-карбоксамид,
4,6-дихлор-N-(циклогептилметил)-1-(2-гидроксиэтил)-1Н-индол-3-карбоксамид,
4-бром-6-хлор-N-(циклогептилметил)-1-(2-гидроксиэтил)-1Н-индол-3-карбоксамид,
6-хлор-N-(циклогептилметил)-1-(2-гидроксиэтил)-4-метил-1Н-индол-3-карбоксамид,
6-бром-4-хлор-N-(циклогептилметил)-1-метил-1Н-индол-3-карбоксамид,
6-бром-N-(циклогептилметил)-4-фтор-1-метил-1Н-индол-3-карбоксамид,
4,6-дибром-N-(циклогептилметил)-1-метил-1Н-индол-3-карбоксамид,
6-бром-N-(циклогептилметил)-1,4-диметил-1Н-индол-3-карбоксамид,
6-бром-N-(циклогептилметил)-1-этил-4-фтор-1Н-индол-3-карбоксамид,
6-бром-4-хлор-N-(циклогептилметил)-1-этил-1Н-индол-3-карбоксамид,
4,6-дибром-N-(циклогептилметил)-1-этил-1Н-индол-3-карбоксамид,
6-бром-N-(циклогептилметил)-1-этил-4-метил-1Н-индол-3-карбоксамид,
6-бром-N-(циклогептилметил)-4-фтор-1-(2-гидроксиэтил)-1Н-индол-3-карбоксамид,
6-бром-4-хлор-N-(циклогептилметил)-1-(2-гидроксиэтил)-1Н-индол-3-карбоксамид),
4,6-дибром-N-(циклогептилметил)-1-(2-гидроксиэтил)-1Н-индол-3-карбоксамид,
6-бром-N-(циклогептилметил)-1-(2-гидроксиэтил)-4-метил-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-4-хлор-6-фтор-1-метил-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-4-бром-6-фтор-1-метил-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-6-фтор-1,4-диметил-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-4-хлор-1-этил-6-фтор-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-4-бром-1-этил-6-фтор-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-1-этил-6-фтор-4-метил-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-4-хлор-6-фтор-1-(2-гидроксиэтил)-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-4-бром-6-фтор-1-(2-гидроксиэтил)-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-6-фтор-1-(2-гидроксиэтил)-4-метил-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-4,6-дихлор-1-метил-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-6-хлор-4-фтор-1-метил-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-4-бром-6-хлор-1-метил-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-6-хлор-1,4-диметил-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-6-хлор-1-этил-4-фтор-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-4,6-дихлор-1-этил-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-4-бром-6-хлор-1-этил-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-6-хлор-1-этил-4-метил-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-6-хлор-4-фтор-1-(2-гидроксиэтил)-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-4,6-дихлор-1-(2-гидроксиэтил)-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-4-бром-6-хлор-1-(2-гидроксиэтил)-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-6-хлор-1-(2-гидроксиэтил)-4-метил-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-6-бром-4-хлор-1-метил-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-6-бром-4-фтор-1-метил-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-4,6-дибром-1-метил-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-6-бром-1,4-диметил-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-ил метил)-6-бром-1-этил-4-фтор-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-6-бром-4-хлор-1-этил-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-4,6-дибром-1-этил-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-6-бром-1-этил-4-метил-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-6-бром-4-фтор-1-(2-гидроксиэтил)-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-6-бром-4-хлор-1-(2-гидроксиэтил)-1Н-индол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-4,6-дибром-1-(2-гидроксиэтил)-1Н-индол-3-карбоксамид),
N-(бицикло[2.2.2]октан-1-илметил)-6-бром-1-(2-гидроксиэтил)-4-метил-1Н-индол-3-карбоксамид,
4-хлор-N-(циклогептилметил)-1-метил-1Н-индазол-3-карбоксамид,
4-бром-N-(циклогептилметил)-1-метил-1Н-индазол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-4-хлор-1-метил-1Н-индазол-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-4-бром-1-метил-1Н-индазол-3-карбоксамид,
4-хлор-N-(циклогептилметил)-1-метил-1Н-пирроло[2,3-b]пиридин-3-карбоксамид,
4-бром-N-(циклогептилметил)-1-метил-1Н-пирроло[2,3-b]пиридин-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-4-хлор-1-метил-1Н-пирроло[2,3-b]пиридин-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-4-бром-1-метил-1Н-пирроло[2,3-b]пиридин-3-карбоксамид,
4-хлор-N-(циклогептилметил)-1-метил-1Н-пирроло[3,2-с]пиридин-3-карбоксамид,
4-бром-N-(циклогептилметил)-1-метил-1Н-пирроло[3,2-с]пиридин-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-4-хлор-1-метил-1Н-пирроло[3,2-с]пиридин-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-4-бром-1-метил-1Н-пирроло[3,2-с]пиридин-3-карбоксамид,
4-хлор-N-(циклогептилметил)-1-метил-1Н-пирроло[2,3-с]пиридин-3-карбоксамид,
4-бром-N-(циклогептилметил)-1-метил-1Н-пирроло[2,3-с]пиридин-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-4-хлор-1-метил-1Н-пирроло[2,3-с]пиридин-3-карбоксамид,
N-(бицикло[2.2.2]октан-1-илметил)-4-бром-1-метил-1Н-пирроло[2,3-с]пиридин-3-карбоксамид,
1-(2-(2Н-тетразол-5-ил)этил)-4-хлор-N-(циклогептилметил)-1Н-индол-3-карбоксамид,
1-(2-(2Н-тетразол-5-ил)этил)-4-бром-N-(циклогептилметил)-1Н-индол-3-карбоксамид,
1-(2-(2Н-тетразол-5-ил)этил)-N-(циклогептилметил)-4-метил-1Н-индол-3-карбоксамид,
1-(2-(2Н-тетразол-5-ил)этил)-N-(бицикло[2.2.2]октан-1-илметил)-4-хлор-1Н-индол-3-карбоксамид,
1-(2-(2Н-тетразол-5-ил)этил)-N-(бицикло[2.2.2]октан-1-илметил)-4-бром-1Н-индол-3-карбоксамид,
1-(2-(2Н-тетразол-5-ил)этил)-N-(бицикло[2.2.2]октан-1-илметил)-4-метил-1Н-индол-3-карбоксамид,
4-хлор-N3-(циклогептилметил)-N1-метил-1Н-индол-1,3-дикарбоксамид,
4-бром-N3-(циклогептилметил)-N1-метил-1Н-индол-1,3-дикарбоксамид,
N3-(бицикло[2.2.2]октан-1-илметил)-4-хлор-N1-метил-1Н-индол-1,3-дикарбоксамид,
N3-(бицикло[2.2.2]октан-1-илметил)-4-бром-N1-метил-1Н-индол-1,3-дикарбоксамид,
4-хлор-N3-(циклогептилметил)-N1,N1-диметил-1Н-индол-1,3-дикарбоксамид,
4-бром-N3-(циклогептилметил)-N1,N1-диметил-1Н-индол-1,3-дикарбоксамид,
N3-(бицикло[2.2.2]октан-1-илметил)-4-хлор-N1,N1-диметил-1Н-индол-1,3-дикарбоксамид,
N3-(бицикло[2.2.2]октан-1-илметил)-4-бром-N1,N1-диметил-1Н-индол-1,3-дикарбоксамид,
4-хлор-N3-(циклогептилметил)-N1-этил-N1-метил-1Н-индол-1,3-дикарбоксамид,
4-бром-N3-(циклогептилметил)-N1-этил-N1-метил-1Н-индол-1,3-дикарбоксамид,
N3-бицикло[2.2.2]октан-1-илметил)-4-хлор-N1-этил-N1-метил-1Н-индол-1,3-дикарбоксамид и
N3-(бицикло[2.2.2]октан-1-илметил)-4-бром-N1-этил-N1-метил-1Н-индол-1,3-дикарбоксамид.
9. Фармацевтическая композиция для лечения аффективных расстройств, нейродегенеративных заболеваний и нарушений, заболеваний и нарушений, которые опосредованы или приводят к нейровоспалению, и центрально-опосредованных нервно-психиатрических заболеваний и нарушений, боли, воспалительных процессов и дегенеративных состояний, которая содержит соединение в соответствии с любым из пп.1-8 и фармацевтически приемлемые наполнители.
10. Фармацевтическая композиция в соответствии с п.9, где аффективное расстройство выбирают из депрессии, тревоги, биполярного расстройства и шизофрении.
11. Фармацевтическая композиция в соответствии с п.9, где воспалительный процесс выбирают из ревматоидного артрита, остеопороза и хронического обструктивного заболевания легких.
12. Фармацевтическая композиция в соответствии с п.9, где дегенеративное состояние выбирают из глаукомы, рассеянного склероза, бокового амиотрофического склероза, болезни Паркинсона и болезни Альцгеймера.
13. Фармацевтическая композиция в соответствии с п.9 для лечения невропатической боли.
Текст
Настоящее изобретение относится к новым антагонистам P2X7R, которые представляют собой индол-3-карбоксамидные или азаиндол-3-карбоксамидные соединения, фармацевтическим композициям, содержащим такие соединения, и их применению для профилактического или терапевтического лечения заболеваний, опосредованных активностью P2X7R. Настоящая заявка относится к новым антагонистам P2X7R, которые представляют собой индол-3 карбоксамидные и азаиндол-3-карбоксамидные соединения, фармацевтическим композициям, содержащим такие соединения, и их применению для профилактического или терапевтического лечения заболеваний, опосредованных активностью P2X7R. Предпосылки создания изобретенияP2X7R представляет собой АТР-управляемый ионный канал, который относится к семейству Р 2 Х ионотропных каналов. Ген изначально был выделен из головного мозга крыс (Surprenant и др. (1996) 272:735-738) и после этого из библиотеки моноцитов человека (Rassendren и др. (1997) J. Biol. Chem. 272:5482-5486; регистрационные номера Genbank NM002562, Y09561) в соответствии с гомологией его последовательности с другими членами Р 2 Х семейства. Позже было обнаружено, что P2X7R соответствует неидентифицированному P2Z рецептору, который опосредует действие АТР на проницаемость мембран на тучных клетках и макрофагах (Dahlqvist и Diamant (1974) Acta Physiol. Scand. 34:368-384;Steinberg и Silverstein (1987) J. Biol. Chem. 262:3118-3122; Gordon (1986) Biochem. J. 233:309-319). P2X7R имеет два гидрофобных домена, расположенных в мембране, внеклеточную петлю и образует трансмембранные ионные каналы. P2X7R имеет фармакологический профиль, существенно отличающийся от Р 2 Х гомо- или гетеромеров (North и Surprenant (2000) Annual Rev. Pharmacology Toxicology 40:563-580). ДляP2X7R необходимы уровни АТР свыше 1 мМ для осуществления активации, тогда как другие Р 2 Х рецепторы активируются при концентрациях АТР 100 мкМ (Steinberg и др. (1987) J. Biol. Chem. 262:88848888; Greenberg и др. (1988) J. Biol. Chem. 263:10337-10343). Несмотря на то, что все Р 2 Х рецепторы проявляют неселективные каналоподобные свойства после лигирования, каналы, образованные с помощьюP2X7R, могут превращаться в поры, через которые могут проходить молекулы размером вплоть до 900 Да (Virginio и др. (1999) J. Physiol. 519:335-346).P2X7R экспрессируется в гематопоэтических клетках, тучных клетках, лимфоцитах, эритроцитах,фибробластах, клетках Лангерганса и макрофагах (Surprenant и др., 1996, Science 272:3118-3122). В центральной нервной системе экспрессия P2X7R была обнаружена в глиальных клетках, шванновских клетках, астроцитах, а также в нейронах (Ferrari и др. (1996) J. Immunol 156:1531-1539; Collo и др. (1997) Neuropharmacology 36: 1277-1283; Anderson и Nedergaard (2006) Trends Neuroscien 29: 257-262).P2X7R вовлечен в регуляцию иммунной функции и воспалительной ответной реакции. Активация(1996) Blood 87:682-690), высвобождением цитокинов (Griffiths и др. (1995) J. Immol. 154:2821-2828) и образованием поликарионов макрофагов (Falzoni и др. (1995) J. Clin. Invest. 95:1207-1216). P2X7R вовлечен в процессинг и высвобождение активного интерлейкин-1 (IL-1) из провоспалительных клеток (Perregaux и Gabel (1998) J. Biol. Chem. 269:15195-15203; Ferrari и др., (2006) J. Immunol. 176: 3877-3883). Стимуляция P2X7R посредством ATP также может приводить к апоптозу и клеточной гибели путем запуска образования неселективных пор плазматической мембраны (Di Virgilio и др. (1998) Cell Death Differ. 5:191-199). Нарушение регуляции P2X7R наблюдается при ишемическом повреждении и некрозе, индуцированной окклюзией средней мозговой артерии в головном мозге крыс (Collo и др. (1997) Neuropharmacol. 36:1277-1283). В недавних исследованиях была показана роль P2X7R в образовании супероксида в микроглии и повышенная регуляция P2X7R была обнаружена вокруг амилоидных бляшек на модели трансгенных мышей для болезни Альцгеймера (Parvathenani и др. (2003) J. Biol. Chem. 278:13300-13317) и в очагах поражения при рассеянном склерозе из аутопсии срезов головного мозга (Narcisse и др. (2005)Glia, 49:245-258). При исследовании у мышей, у которых отсутствует P2X7R, было обнаружено отсутствие воспалительной и невропатической гиперчувствительности на механические и тепловые стимулы, что указывает на связь между P2X7R и воспалительной и невропатической болью (Chessell и др. (2005) Pain 114:386396). Антагонисты P2X7R существенно улучшают функциональное восстановление и снижают клеточную гибель при повреждении спинного мозга на моделях животных (Wang и др. (2004) Nature Med 10:B21-B27). Соединения, которые модулируют P2X7R, были описаны. Например, Brilliant Blue (Jiang и др., Mol.(WO 99/29660, WO 99/29661, WO 00/61569, WO 01/42194, WO 01/44170, WO 01/44213, WO 01/94338,WO 03/041707, WO 03/042190, WO 03/080579, WO 04/074224, WO 05/014529, WO 06/025783, WO 06/059945), соединения пиперидина и пиперазина (WO 01/44213, WO 01/46200, WO 08/005368), соединения бензамида и гетероариламида (WO 03/042191, WO 04/058731, WO 04/058270, WO 04/099146, WO 05/019182, WO 06/003500, WO 06/003513, WO 06/067444), замещенные тирозиновые производные (WO 00/71529, WO 03/047515, WO 03/059353), соединения имидазола (WO 05/014555), соединения аминотетразолов (WO 05/111003), цианоамидин (WO 06/017406), производные бициклогетероарила (WO 05/009968, WO 06/102588, WO 06/102610, WO 07/028022, WO 07/109154, WO 07/109160, WO 07/109172,-1 022505P2X7R, тогда как окисленный ATP (oATP) действует в качестве необратимого ингибитора рецептора(Chen и др., J. Biol. Chem., 268 (1993), 8199-8203). Следовательно, существуют убедительные доказательства того, что соединения, действующие наP2X7R, могут использоваться для лечения боли, воспалительных процессов и дегенеративных состояний,связанных с болезненными состояниями, такими как ревматоидный артрит, остеоартрит, псориаз, аллергический дерматит, астма, хроническое обструктивное заболевание легких, гиперреактивные ответные реакции дыхательных путей, септический шок, гломерулонефрит, синдром раздраженной толстой кишки, воспалительные заболевания кишечника, болезнь Крона, неспецифический язвенный колит, атеросклероз, рост и метастазирование злокачественных клеток, миобластный лейкоз, диабет, болезнь Альцгеймера, болезнь Паркинсона, рассеянный склероз, глаукома, депрессия, биполярное аффективное расстройство, тревога, менингит, травматическое повреждение головного мозга, острое повреждение спинного мозга, невропатическая боль, остеопороз, ожоговое поражение, ишемическая болезнь сердца, инфаркт миокарда, удар и варикозное расширение вен. Таким образом, объектом настоящего изобретения является обеспечение новых групп соединений,которые могут ингибировать активность P2X7R и могут использоваться для лечения вышеуказанных заболеваний. Подробное описание изобретения Настоящее изобретение относится к новым антагонистам P2X7R, которые представляют собой индол-3-карбоксамидные и азаиндол-3-карбоксамидные соединения, представленные общей формулой (I)R2 выбирают из неразветвленного или разветвленного C1-С 5 алкила, который необязательно может быть замещен -ОН, 2 Н-тетразолилэтилом, метилкарбамоилом, диметилкарбамоилом или этилметилкарбамоилом;R3, R4, R5 или R6, в каждом случае независимо, выбирают из водорода, галогена, метила, гидрокси,метокси, циано или трифторметила; а, b, с, d, х, в каждом случае независимо, выбирают из углерода или азота; или их фармацевтически приемлемую соль или сольват. Соединения, как описано выше, в которых R2 представляет собой С 1-С 5 алкил или С 2 С 5 гидроксиалкил, являются предпочтительными. Кроме того, является предпочтительным, когда по меньшей мере два из R3, R4, R5 и R6 представляют собой водород. Дополнительно является предпочтительным, когда а, b, с и d представляют собой С или один из а,b, с и d представляет собой N. Примеры новых индол-3-карбоксамидных и азаиндол-3-карбоксамидных соединений раскрыты в примерах 6-295. Изобретение также относится к соединению формулы (I) или его фармацевтически приемлемой соли или сольвату, которое представляет собой Настоящее изобретение также охватывает соединения, меченные радиоактивными изотопами, которые идентичны соединениям, указанным для формулы (I), но фактически отличаются тем, что один или несколько атомов заменены атомом, который имеет атомную массу или массовое число, отличающееся от атомной массы или массового числа, которые обычно существуют в природе. Примеры изотопов, которые могут быть инкорпорированы в соединения согласно изобретению, включают изотопы водорода, углерода, азота, кислорода, фосфора, фтора и хлора, такие как 2 Н, 3 Н, 13 С, 14 С, 15N, 18 О, 17 О, 31P,32P, 35S, 18F и 35Cl соответственно. Соединения согласно настоящему изобретению, их пролекарства и фармацевтически приемлемые соли указанных соединений или указанных пролекарств, которые содержат вышеуказанные изотопы и/или другие изотопы других атомов, подпадают под объем настоящего изобретения. Типичные меченные изотопом соединения согласно настоящему изобретению, например те, в которые инкорпорированы радиоактивные изотопы, такие как 3 Н и 14 С, пригодны в исследованиях распределения в тканях лекарственных средств и/или субстратов. Меченные тритием, то есть 3 Н, и углеродом-14, то есть 14 С, изотопы являются особенно предпочтительными в связи с простотой их приготовления и обнаружительной способностью. Дополнительно замещение более тяжелыми изотопами, такими как дейтерий, то есть 2 Н, может обеспечивать определенные терапевтические преимущества вследствие повышенной метаболической стабильности, например повышенному периоду полураспада in vivo или уменьшенной потребности во вводимой дозе и, следовательно, могут быть предпочтительными в определенных условиях. Меченные изотопами соединения формулы (I) согласно настоящему изобретению и их пролекарства обычно могут быть приготовлены путем осуществления методик, описанных в примерах ниже, путем замещения легко доступного меченного изотопом реагента на немеченный изотопом реагент. Фармацевтически приемлемые соли включают те соли, которые образованы с анионами, такими как анионы, имеющие происхождения из соляной, фосфорной, уксусной, щавелевой, винной кислот и т.д., и соли, образованные с катионами, такими как катионы, которые имеют происхождение из натрия, калия,аммония, кальция, окисей железа, изопропиламин, триэтиламин, 2-этиламиноэтанол, гистидин и прокаин. Другие фармацевтически приемлемые соли. В дальнейшем варианте осуществления настоящая заявка относится к фармацевтической композиции, которая содержит соединение формулы (I) согласно настоящему изобретению. Фармацевтическая композиция в соответствии с настоящим изобретением также может содержать дополнительное активное соединение в отдельной или единичной дозированной форме для одновременного или последовательного введения. Соединения формулы (I) или их фармацевтически приемлемая соль могут применяться для приготовления лекарственного средства для профилактического или терапевтического лечения любого болезненного состояния у человека, или другого млекопитающего, которое усугубляется или вызывается избыточной или нерегулируемой продукцией цитокинов такими клетками млекопитающих, например, но не ограничиваясь только ими, моноцитами и/или макрофагами. Настоящее изобретение также относится к лечению состояния, опосредованного IL-1 или цитокином. Как определено в настоящем изобретении, "состояние, опосредованное IL-1" и "состояние, опосредованное цитокином" включает, но не ограничиваясь только ими, заболевание или нарушение, выбранное из группы, включающей артрит (включая псориатический артрит, синдром Рейтера, ревматоидный артрит, подагру, травматический артрит, артрит, обусловленный краснухой, ревматоидный спондилит,остеоартрит, подагрический артрит и острый синовит), воспалительные заболевания кишечника, болезнь Крона, эмфизему, острый респираторный дистресс-синдром, респираторный дистресс-синдром у взрослых, астму, бронхит хроническое обструктивное заболевание легких, хроническое воспалительное заболевание легких, силикоз, легочный саркоидоз, аллергические реакции, аллергическую контактную гиперчувствительность, экзему, контактный дерматит, псориаз, солнечный ожог, злокачественное новообразование, изъязвление ткани, рестеноз, парадонтоз, врожденный буллезный эпидермолиз, остеопороз,резорбцию кости, расслаивание имплантатов искусственных суставов, атеросклероз, аневризму аорты,застойную сердечную недостаточность, инфаркт миокарда, удар, ишемию головного мозга, травму головы, нейротравму, повреждение спинного мозга, нейродегенеративные заболевания, болезнь Альцгеймера, болезнь Паркинсона, глаукому, мигрень, депрессию, периферическую нейропатию, боль, церебральную амилоидную ангиопатию, ноотропное или познавательное улучшение, боковой амиотрофический склероз, рассеянный склероз, развитие кровеносных сосудов в глазах, повреждение роговицы, дегенерацию желтого пятна, рубцевание роговицы, склерит, аномальное заживление ран, ожоги, аутоиммунные нарушения, болезнь Хантингтона, диабет, СНИД, кахексию, сепсис, септический шок, эндотоксический шок, конъюнктивальныйшок, бактериальный грамнегативный сепсис, синдром токсического шока, церебральную малярию, реперфузионное повреждение сердца и почек, тромбоз гломерулонефрит, реакцию трансплантат против хозяина, отторжение аллотрансплантата, токсичность трансплантированного органа, неспецифический язвенный колит или мышечную дегенерацию, у млекопитающего, включая человека, который включает введение указанному млекопитающему количества соединения формулы (I), эффективного для лечения такого состояния. Настоящее изобретение относится к фармацевтической композиции для лечения состояния, опосредованного IL-1, у млекопитающего, включая человека, которая содержит количество соединения формулы (I), эффективное для лечения такого состояния, и фармацевтически приемлемый носитель. Соединения согласно изобретению пригодны для лечения ревматоидного артрита, остеоартрита,псориаза, аллергического дерматита, астмы, хронического обструктивного заболевания легких (COPD),гиперчувствительности дыхательных путей, септического шока, гломерулонефрита, синдрома раздраженной толстой кишки, болезни Крона, неспецифического язвенного колита, атеросклероза, роста и метастазирования злокачественных клеток, миобластного лейкоза, диабета, болезни Альцгеймера, менингита, остеопороза, ожогового поражения, ишемической болезни сердца, удара и варикозного расширения вен. В другом аспекте изобретение также обеспечивает фармацевтическую композицию для лечения остеоартрита, которая содержит терапевтически эффективное количество соединения формулы (I) или его фармацевтически приемлемой соли или сольвата, как определено в настоящей заявке выше. Изобретение дополнительно обеспечивает фармацевтическую композицию для воздействия на иммуносупрессию (например, для лечения ревматоидного артрита, синдрома раздраженной толстой кишки,атеросклероза или псориаза), которая содержит терапевтически эффективное количество соединения формулы (I) или его фармацевтически приемлемой соли или сольвата, как определено в настоящей заявке выше. Изобретение также обеспечивает фармацевтическую композицию для лечения обструктивного заболевания дыхательных путей (например, астмы или COPD), которая содержит терапевтически эффективное количество соединения формулы (I), или его фармацевтически приемлемой соли или сольвата,как определено в настоящей заявке выше. Кроме того, изобретение обеспечивает фармацевтическую композицию для лечения млекопитающего, чувствительного к или страдающего от состояний, причины которых связаны с аномальной активностью Р 2 Х 7 рецептора, такие как нейродегенеративные заболевания и нарушения, включая, например,болезнь Паркинсона, рассеянный склероз, глаукому, заболевания и нарушения, которые опосредованы или приводят к нейровоспалению, такие как, например травматическое повреждение головного мозга и энцефалит; центрально-опосредованные нервно-психиатрические заболевания и нарушения, такие как,например, маниакальная депрессия, биполярное нарушение, тревога, шизофрения, расстройства пищеварения, нарушения сна и нарушения познавательной способности, эпилепсия и судорожные заболевания,которая содержат терапевтически эффективное количество соединения формулы (I) или его фармацевтически приемлемой соли или сольвата, как определено в настоящей заявке выше. В частном варианте осуществления фармацевтическая композиция в соответствии с настоящим изобретением может применяться для лечения аффективных расстройств. В предпочтительном варианте осуществления аффективное расстройство выбирают из депрессии, тревоги, биполярного расстройства и шизофрении. В альтернативном варианте осуществления фармацевтическая композиция в соответствии с настоящим изобретением пригодна для лечения нейродегенеративных заболеваний и нарушений, заболеваний и нарушений, которые опосредованы или приводят к нейровоспалению, и центральноопосредованных нервно-психиатрических заболеваний и нарушений. Кроме того, фармацевтическая композиция в соответствии с настоящим изобретением может быть особенно пригодной для лечения боли, воспалительных процессов и дегенеративных состояний. В более предпочтительном варианте осуществления воспалительный процесс выбирают из ревматоидного артрита, остеопороза и хронического обструктивного заболевания легких. Кроме того, фармацевтическая композиция в соответствии с настоящим изобретением может применяться для лечения невропатической боли. Дозировка, фармацевтический препарат и доставка соединения формулы (I) для применения в соответствии с настоящим изобретением может быть приготовлены общепринятым образом в соответствии с методами, известными в данной области, используя один или несколько физиологических носителей или наполнителей, см., например, Ansel и др. "Pharmaceutical Dosage Forms and Drug Delivery Systems", 7 ред.,Lippincott WilliamsWilkins Publishers, 1999. Таким образом, агент, модулирующий P2X7R, и его физиологически приемлемые соли и сольваты может быть приготовлен в виде лекарственного средства для введения путем ингаляции, инсуффляции (через рот либо через нос), перорального, буккального, парентерального или ректального введения. Для перорального введения, фармацевтическая композиция соединения формулы (I) может находиться в форме, например, таблеток или капсул, приготовленных общепринятым способом, с фармацевтически приемлемыми наполнителями, такими как связующие средства (например, прежелатинизированный кукурузный крахмал, поливинилпирролидон, гидроксипропилметилцеллюлоза), наполнители(например, стеарат магния, тальк, диоксид кремния), дезинтеграторы (например, картофельный крахмал,натриевая соль гликолята крахмала) или смачивающие средства (например, лаурилсульфат натрия). Фармацевтическая композиция может вводиться пациенту с физиологически приемлемым носителем,как описано в настоящей заявке. В специфическом варианте осуществления термин "фармацевтически приемлемый" обозначает разрешенный контрольным органом или другой общепризнанной фармакопеей для применения у животных и более предпочтительно у людей. Термин "носитель" относится к разбавителю, вспомогательному веществу, наполнителю или носителю, с которым вводится лекарственное вещество. Такими фармацевтическими носителями могут быть стерильные жидкости, такие как вода и масла, включая жидкости из нефтепродуктов, животного, растительного или синтетического происхождения, такие как арахисовое масло, соевое масло, минеральное масло, кунжутное масло и другие. Вода является предпочтительным носителем, если фармацевтическая композиция вводится внутривенно. В качестве жидких носителей также могут применяться солевые растворы и водные растворы декстрозы и глицерина, в особенности для инъекционных растворов. Подходящие фармацевтически приемлемые наполнители включают крахмал, глюкозу, лактозу, сахарозу, желатин, солод, рис, муку, мел, силикагель,стеарат натрия, глицерин моностеарат, тальк, ион натрия, сухое снятое молоко, глицерин, пропилен, гликоль, вода, этанол и другие. Композиция, при необходимости, также может содержать незначительные количества смачивающих или эмульгирующих средств или рН буферных средств. Эти композиции могут находиться в форме растворов, суспензий, эмульсий, таблеток, пилюль, капсул, порошков, препаратов с замедленным высвобождением и др. Композиция может быть приготовлена в виде суппозитория, с общепринятыми связующими и носителями, такими как триглицериды. Препараты для перорального введения могут включать стандартные носители, такие как фармацевтические классы маннита, лактозы,крахмала, стеарата магния, натрий сахарина, целлюлозы, карбоната магния и др. Примеры подходящих фармацевтических носителей описаны в "Remington's Pharmaceutical Sciences" под ред. E.W. Martin. Такие композиции будут содержать терапевтически эффективное количество вышеуказанных соединений,предпочтительно в очищенной форме, совместно с подходящим количество носителя, таким образом обеспечивая форму для надлежащего введения пациенту. Препарат должен соответствовать типу. Жидкие препараты для перорального введения могут находиться в виде, например, растворов, сиропов или суспензий или могут быть представлены в виде безводного продукта для восстановления водой или другим подходящим наполнителем перед использованием. Такие жидкие препараты могут быть приготовлены общепринятыми методами с фармацевтически приемлемыми вспомогательными веществами, такими как суспендирующие средства (например, сорбит, сироп, производные целлюлозы, гидрированные пищевые жиры), эмульгирующие средства (например, лецитин, гуммиарабик), неводные наполнители (например, миндальное масло, масляные сложные эфиры, этиловый спирт, фракционированные растительные масла), консерванты (например, метил или пропил-п-гидроксикарбонаты, сорбиновые кислоты). Препараты также могут содержать буферные соли, ароматизаторы, красители и подсластители,если это является подходящим. Препараты для перорального введения подходяще приготавливаются таким образом, чтобы обеспечить контролированное высвобождение соединения формулы (I). Для введения путем ингаляции соединение формулы (I) согласно настоящему изобретению подходяще доставляют в виде аэрозольного спрея, подаваемого из упаковки под давлением или распылителя, с использованием подходящего пропеллента (например, дихлордифторметан, трихлорфторметан, дихлортетрафторэтан, углекислый газ или другой подходящий газ). В случае аэрозоля под давлением единица дозирования может быть определена с помощью клапана для доставки определенного количества. Могут быть приготовлены капсулы и картриджи, например, из желатина для применения в ингаляторе или инсуффляторе, содержащие порошковую смесь соединения формулы (I), и подходящего порошкового основания, такого как лактоза или крахмал. Соединение формулы (I) согласно настоящему изобретению может быть приготовлено в виде препарата для парентерального введения путем инъекции, например путем болюсной инъекции или непрерывной инфузии. Участки для инъекций включают внутривенные, внутрибрюшинные или подкожные. Препараты для инъекций могут быть представлены в виде единичных дозированных форм (например, во флаконе, в контейнере для нескольких доз), и с добавлением консерванта. Соединение формулы (I) согласно настоящему изобретению могут быть представлены в таких формах, как суспензии, растворы или эмульсии в масляных или водных носителях, и могут содержать средства для приготовления препаратов, такие как суспендирующие, стабилизирующие или диспергирующие средства. Альтернативно, средство может быть представлено в порошковой форме для восстановления с помощью подходящего носителя (например, стерильной апирогенной воды) перед использованием. Обычно композиции для внутривенного введения представляют собой растворы в стерильном изотоничном водном буфере. При необходимости,композиция также может включать солюбилизирующее средство и анестезирующее средство местного действия, такое как лидокаин, для облегчения боли в участке инъекции. Обычно компоненты поставляются либо раздельно или смешанными вместе в единичной дозированной форме, например в виде высушенного лиофилизированного порошка или безводного концентрата в герметически запечатанном контейнере, таком как ампула или пакет-саше, с указанием количества активного компонента. Если композицию вводят путем инфузии, то она может диспергироваться из флакона для инъекций, содержащего стерильную воду фармакологической степени чистоты или солевой раствор. Если композицию вводят путем инъекции, то может обеспечиваться ампула со стерильной водой для инъекции или солевым раствором, таким образом, что компоненты можно смешивать перед введением. Соединение формулы (I) согласно настоящему изобретению может быть приготовлено в виде препарата для трансдермального введения. Трансдермальные композиции обычно приготавливают в виде мази или крема для местного применения, содержащей(го) активный(ые) компонент(ы) обычно в количестве в диапазоне от 0,01 до приблизительно 20 вес.%, предпочтительно от приблизительно 0,1 до приблизительно 20 вес.%, предпочтительно от приблизительно 0,1 до приблизительно 10 вес.% и более предпочтительно от предпочтительно 0,5 до предпочтительно 15 вес.%. Если приготовлен препарат в виде мази, то активные компоненты обычно объединяют с парафиновым или водорастворимым мазевым основанием. Альтернативно, активные компоненты могут быть приготовлены в виде крема, например, с кремовым основанием масло-в-воде. Такие трансдермальные препараты хорошо известны в данной области техники и обычно включают дополнительные компоненты для повышения проникновения через кожу стабильности активных компонентов или препарата. Все такие хорошо известные трансдермальные препараты и компоненты подпадают под объем настоящего изобретения. Соединения согласно настоящему изобретению также могут вводиться с помощью трансдермального устройства. Таким образом,трансдермальное введение может осуществляться, используя пластырь или резервуарного тип, или типа пористой мембраны, или разновидностью твердого матрикса. Фармацевтическая композиция согласно изобретению может быть приготовлена в виде нейтральных или солевых форм. Фармацевтически приемлемые соли включают те соли, которые образованы с анионами, такие как анионы, имеющие происхождение из соляной, фосфорной, уксусной, щавелевой,винной кислот и др., и те соли, которые образованы с катионами, такими как катионы, имеющие происхождение из натрия, калия, аммония, кальция, гидроксидов железа, изопропиламина, триэтиламина, 2 этиламиноэтанола, гистидина, прокаина и др. Соединение формулы (I) согласно настоящему изобретению, при необходимости, также может быть представлено в виде упаковки или диспергирующего устройства, которая(ое) может содержать одну или несколько единичных дозированных форм, содержащих указанное средство. Упаковка может содержать,например, металлическую или полимерную пленку, такую как блистерная упаковка. Упаковка или диспергирующее устройство может обеспечиваться инструкциями относительно введения. Соединение формулы (I) согласно настоящему изобретению может вводиться в виде единственного активного средства или может вводиться в комбинации с другими средствами. Такие средства включают нестероидные противовоспалительные средства (НСПВС), такие как целекоксиб, рофекоксиб, цимикоксиб, эторикоксиб, люмиракоксиб, вальдекоксиб, деракоксиб, N-(2-циклогексилоксинитрофенил)метан сульфонамид, СОХ 189, АВТ 963, JTE-522, GW-406381, LAS-34475, CS-706, РАС-10649, SVT-2016, GW644784, тенидап, ацетилсалициловая кислота (аспирин), амоксипин, бенорилат, холин салицилат магния,дифлунизал, файсламин, метил салицилат, салицилат магния, салицил салицилат (салсалат), диклофенак,ацеклофенак, ацеметацин, бромфенак, этодолак, индометацин, набуметон, сулиндак, толметин, ибупрофен, карпрофен, фунбуфен, фунопрофен, флурбипрофен, кетопрофен, кеторолак, локсопрофен, напрок- 20022505 сен, оксапрозин, тиапрофеновая кислота, супрофен, мефенамовая кислота, меклофенамовая кислота, фенилбутазон, азапропазон, метамизол, оксифенбутазон, сульфинпипазон, пироксикам, лорноксикам, мелоксикам, теноксикам, нимесулид, ликофелон, парацетамол. Соединение формулы (I) согласно настоящему изобретению может комбинироваться с такими средствами, как ингибиторы TNF-, такие как анти-TNF моноклональные антитела (такие как Remicade,CDP-870 и D2E7) и молекулы иммуноглобулинов рецептора TNF (такие как Enbrel), в низких дозах метотрексат, лефуномид; циклезинид; гидроксихлорхин, d-пеницилламин, ауронофин или парентеральное или пероральное золото. Соединение формулы (I) согласно настоящему изобретению также может вводиться в комбинации с ингибитором фермента проTNF конвертаза, (ТАСЕ), таким как 3-амино-N-гидрокси(2-метилпропил)-3-[4-[(2-метил-4-хинолинил)метокси]фенил]-2-оксо-1-пирролидинацетамид, 2(S),3(S)-пиперидиндикарбоксамид, N3-гидрокси-1-метил-N-2-[4-[(2-метил-4-хинолинил)метокси]фенил], 3-тиоморфолинкарбоксамид, 4-4-(2-бутинилокси)фенил]сульфонил]-N-гидрокси-2,2-диметил, 5-гексеновая кислота,3-[(гидроксиамино)карбонил]-2-(2-метилпропил)-6-фенил-,2-(2-метилпропил)-2-(метилсульфонил)гидразид,(2R,3S,5E)-2-пиперидинкарбоксамид,N,5-дигидрокси-1-4-(1-нафталенилметокси)фенил]сульфонил]-, (2R.5R)-пентанамид, 3-(формилгидроксиамино)-4-метил-2-(2-метилпропил)-N-[(1S,2S)-2-метил-1-[(2-пиридиниламино)карбонил]бутил]-, (2R,3S)-2-пропенамид, N-гидрокси-3[3-(4-метоксифенил)сульфонил](1-метилэтил)амино]фенил]-3-(3-пиридинил)-, (2 Е)-бензамид, N-(2,4 диоксо-1,3,7-триазаспиро[4,4]нон-9-ил)-4-[(2-метил-4-хинолинил)метокси], бензамид, N-[(1-ацетил-4 пиперидинил)(2,5-диоксо-4-имидахолидинил)метил]-4-[(2-метил-4-хинолинил)метокси] или 2,4-имидазолидиндион, 5-метил-5-4-[(2-метил-4-хинолинил)метокси]фенил]сульфонил]метил]. Другие примеры ингибиторов ТАСЕ описаны в WO 99/18074, WO 99/65867, патенте US6225311, WO 00/00465, WO 00/09485, WO 98/38179, WO 02/18326, WO 02/096426, WO 03/079986, WO 03/055856, WO 03/053941, WO 03/040103, WO 03/031431, WO 03/024899, WO 03/016248, WO 04/096206, WO 04/033632, WO 04/108086,WO 04/043349, WO 04/032846, WO 04/012663, WO 04/006925, WO 07/016597. Соединение формулы (I) согласно настоящему изобретению также могут вводиться в комбинации с кортикостероидом, таким как будесонид, кортикостерон, кортизол, кортизон ацетат, преднизон, преднизолон, метилпреднизолон, дексаметазон, бетаметазон, триамцинолон, беклобетазон, флудрокортизон ацетат, дезоксикортикостерон ацетат (doca), альдостерон. Соединение формулы (I) согласно настоящему изобретению дополнительно может вводиться в комбинации с агонистом 2-адренергического рецептора, таким как формотерол, сальбутамол (альбутерол), левалбутерол, тербуталин, пирбутерол, прокатерол, метапротеренол, фенотерол, битолтерол мезилат, сальметерол, бамбутерон, кленбутерол. Соединение формулы (I) согласно настоящему изобретению дополнительно может вводиться в комбинации с антидепрессантом, таким как сертралин, экциталопрам, флуоксетин, бупропион, пароксетин, венфлаксин, тразодон, амитриптилин, циталопрам, дулоксетин, миртазапин, нортриптилин, имипрамин, литий. Соединение формулы (I) согласно настоящему изобретению дополнительно может вводиться в комбинации с нейролептиком, таким как хлорпромазин, флуфеназин, перфеназин, прохлорперазин, тиоридазин, трифторперазин, мезоридазин, промазин, трифторпромазин, левомепромазин, прометазин,хлорпротиксен, флупетиксол, тиотиксен, зуклопентиксол, галоперидол, дроперидол, пимозид, мелперон,бенперидол, триперидол, клозапин, оланзапин, рисперидон, квитиапин, зипразидон, амисульприд, палиперидон, бифенпрунокс, арипапразол. Соединение формулы (I) согласно настоящему изобретению также может вводиться в комбинации с ингибитором биосинтеза лейкотриенов, ингибитором 5-липоксигеназы (5-LO) или антагонистом активирующего белка 5-липоксигеназы (FLAP), например зилеутон; АВТ-761; фенлеутон; тепоксалин; никаравен; VIA-2291; эталоциб; кетопрофен, Abt-79175; Abt-85761; N-(5-замещенные) тиофен-2 алкилсульфонамиды; TDT-070; ликофелон; РЕР-03; теноксикам; 2,6-ди-трет-бутилфенол гидразоны; метокситетрагидропираны, такие как Zeneca ZD-2138; соединение SB-210661; пиридинилзамещенные 2 цианонафталиновые соединения, такие как L-739-010; 2-цианохинолиновые соединения, такие как L-746530; индольные и хинолиновые соединения, такие как MK-591, MK-886, и BAY1005. Соединение формулы (I)согласно настоящему изобретению может вводиться в комбинации с антагонистами рецептора для лейкотриенов LTB4, LTC4, LTD4 и LTE, например, фенотиазин-3-оны, такие как L-651,392; амидино соединения, такие как CGS-25019c; бензоксаламины, такие как онтезоласт; бензолкарбоксимидамиды, такие как BIIL 284/260; и такие соединения, как зафирлукаст, аблукаст, монтелукаст, праниукаст, верлукаст (MK-679), RG-12525, Ro-245913 иралукаст (CGP 45715 А) и BAY7195; мазилукаст. Соединение формулы (I) согласно настоящему изобретению также может вводиться в комбинации с ингибитором PDE4, включая ингибиторы изоформы PDE4D. Соединение формулы (I) согласно настоящему изобретению также может вводиться в комбинации с антагонистами антигистаминового H1 рецептора, включая цетиризин, лоратадин, дезлоратадин, фексо- 21022505 фенадин, астемизол, азеластин и хлофенирамин. Соединение формулы (I) согласно настоящему изобретению дополнительно может вводиться в комбинации с антагонистом гастрозащитного Н 2 рецептора. Соединение формулы (I) согласно настоящему изобретению дополнительно может вводиться в комбинации с сосудосуживающим симпатомиметическим средством агонистом 1- и 2 адренорецептора, включая пропилгекседрин, фенилэфрин, фенилпропаноламин, псевдоэфедрин, нафазолин гидрохлорид, оксиметазолин гидрохлорид, тетрагидрозолин гидрохлорид, ксилометазолин гидрохлорид и этилнорэпинефрин гидрохлорид. Соединение формулы (I) согласно настоящему изобретению может вводиться в комбинации с антихолинергическим средством, включая ипратропий бромид; тиотропий бромид; окситропий бромид; пирензепин и телензепин. Настоящее изобретение также относится к комбинации соединения согласно изобретению совместно с агонистами 1-4-адренорецепторами, включая метапротеренол, изопротеренол, изопреналин, альбутерол, сальбутамол, формотерол, сальметерол, тербуталин, орципреналин, битолтерол мезилат и пирбутерол; или метилксантанины, включая теофиллин и аминофиллин; кромогликат натрия; или антагонист мускаринового рецептора (М 1, М 2 и М 3). Соединение формулы (I) согласно настоящему изобретению может вводиться в комбинации с миметиком инсулиноподобного фактора роста I типа (IGF-1). Соединение формулы (I) согласно настоящему изобретению может вводиться в комбинации с ингалируемым глюкокортикоидом с уменьшенными системными побочными действиями, включая, преднизон, преднизолон, флунизолид, триамцинолон ацетонид, беклометазон дипропионат, будесонид, флутиказон пропионат и мометазон фуроат. Соединение формулы (I) согласно настоящему изобретению может вводиться в комбинации с (а) ингибиторами триптазы; (b) антагонистами фактора, активирующего тромбициты (PAF); (с) ингибиторами интерлейкинпревращающего фермента (ICE); (d) ингибиторами IMPDH; (е) ингибиторами молекул адгезии, включая VLA-4 антагонисты; (f) катепсинами; (g) ингибиторами MAP киназы; (h) ингибиторы глюкозо-6-фосфат дегидрогеназы; (i) антагонистами кинин-B1- и В 2-рецептора; j) средствами против подагры, например колхицин; (k) ингибиторами ксантин-оксидазы, например аллопуринол; (l) средствами,способствующими выведению мочевой кислоты, например пробенецид, сульфинпиразон и бензбромарон; (m) средствами, усиливающими секрецию гормона роста; (n) трансформирующим фактором роста(TGFB); (о) фактором роста производных тромбоцитов (PDGF); (р) фактором роста фибробластов, например основным фактором роста фибробластов (bFGF); (q) фактором стимуляции колоний гранулоцитов-макрофагов (GM-CSF); (r) капсайциновым кремом; (s) антагонистами рецептора тахикинина NK1 иUT-77 и ZD-0892. Соединение формулы (I) согласно настоящему изобретению может вводиться в комбинации с ингибитором матриксных металлопротеаз (ММР), то есть стромелизины, коллагеназы и желатиназы, а также аггреканазы; в особенности коллагеназа-1 (ММР-1), коллагеназа-2 (ММР-8), коллагеназа-3 (ММР-13),стромелизин-1 (ММР-3), стромелизин-2 (ММР-10), и стромелизин-3 (ММР-11). Соединение формулы (I) согласно настоящему изобретению может вводиться в комбинации с противораковым лекарственным средством, таким как эндостатин и ангиостатин или цитотоксическими лекарственными средствами, такими как адриамицин, дауномицин, цис-платин, этопозид, таксол, таксотер и ингибиторы фарнезил-трансферазы, VEGF ингибиторы, СОХ- 2 ингибиторы и антиметаболиты, такие как метотрексат противоопухолевые средства, в особенности антимитотические средства, включая алкалоиды барвинка, такие как винбластин и винкристин. Соединение формулы (I) согласно настоящему изобретению может вводиться в комбинации с противовирусными средствами, такими как вирацепт, AZT, ацикловир и фамцикловир, и антисептическими соединениями, такими как валант. Соединение формулы (I) согласно настоящему изобретению может вводиться в комбинации с сердечно-сосудистыми средствами, такими как блокаторы кальциевых каналов, средства, снижающие уровни липидов, такие как статины, фибраты, -блокаторы, АСЕ ингибиторы, антагонисты рецептора ангиотензин-2 и ингибиторы агрегации тромбоцитов. Соединение формулы (I) согласно настоящему изобретению может вводиться в комбинации со средствами, действующими на ЦНС, такими как антидепрессанты (такие как сертралин), противопаркинсонические лекарственные средства (такие как депренил, L-допа, Requip, Mirapex, MAOB ингибиторы,такие как селегин и разагилин, comP ингибиторы, такие как Tasmar, А-2 ингибиторы, ингибиторы обратного захвата допамина, NMDA антагонисты, агонисты никотина, агонисты допамина и ингибиторы синтазы оксида азота нейронов) и средства для лечения болезни Альцгеймера, такие как донепезил, такрин,СОХ-2 ингибиторы, пропентофиллин или метрифонат. Соединение формулы (I) согласно настоящему изобретению может вводиться в комбинации с средствами для лечения остеопороза, такими как ролоксифен, дролоксифен, лазофоксифен или фозомакс, и иммунодепрессантами, такими как FK-506, рапамицин, циклоспорин, азатиоприн и метотрексат. Примеры Пример 1. Общая методика синтеза I. Общая методика для приготовления XInt01. Раствор производного индола X (1 экв.) в безводном диметилформамиде при 0 С добавляли к ангидриду трифторуксусной кислоты (1,5 экв.), перемешивали и медленно нагревали до комнатной температуры. После завершения реакции (1 ч) смесь обрабатывали ледяной водой для получения твердого вещества. Твердое вещество отделяли путем фильтрации и промывали водой и н-пентаном и высушивали в высоком вакууме, получая соединение XInt01 (80-94% выход). Общая методика для приготовления XY. Раствор XInt01 (1 экв.), K2CO3 (5 экв.) и алкилгалогенидов Y, таких как метилйодид, этилйодид, нпропилбромид, изопропилбромид, н-бутилбромид, изобутилбромид (1,5 экв., 1 ч.) или O-tбутилдиметилсилил-2-хлорэтанол (10 экв., 24 ч.) или O-t-бутилдиметилсилил-2-хлорпропанол в ацетоне перемешивали и нагревали в колбе с обратным холодильником. После завершения реакции (наблюдали с помощью тонкослойной хроматографии (ТСХ, смесь концентрировали в вакууме и остаток обрабатывали дихлорметаном. Нерастворимые примеси удаляли путем фильтрации и фильтрат концентрировали,получая соединение XY (60-95% выход). Общая методика для приготовления AFT20 XYZ. К смеси XY (1 экв.) и циклического производного Z (1,5 экв.), такого как циклопентилметиламин,циклопентилэтиламин, циклогексилметиламин, циклогексилэтиламин, циклогептилметиламин, циклогептилэтиламин, бицикло[2.2.2]октан-1-илметиламин или бицикло[2.2.2]октан-1-илэтиламин, в безводном ТГФ при -78 С добавляли гексаметилдисилазид лития (3,5 экв.). Бицикло[2.2.2]октан-1 илметиламин получали в соответствии с методиками, описанными в Unig и Kahanek (1957) Chem Ber 90:236, Delany и Berchtold (1988) J. Org. Chem. 53:3262-3265, Grob и др. (1958) Helv Chim Acta 41:11911197, Whitney и др. (1970) J. Med. Chem. 13:254-260. Полученный раствор нагревали до комнатной температуры и после этого нагревали в колбе с обратным холодильником в течение 16 ч. После завершения реакции (ТСХ), смесь концентрировали в вакууме. В случае несилилоксиэтильных производных остаток очищали либо путем растирания в порошок, колоночной хроматографии или препаративной ВЭЖХ, получая соединение XYZ (40-66% выход). В случае силилоксиэтильных соединений остаток использовали на стадии снятия защиты без дополнительной очистки. Общая методика для снятия зашиты трет-бутилдиметилсилильной группы. К раствору силилоксиэтильного соединения (1 экв.) в безводном тетрагидрофуране при 0 С добавляли фторид тетрабутиламмония (6 экв.) и перемешивали при комнатной температуре в течение 4 ч. Реакционную смесь концентрировали в вакууме и остаток очищали путем колоночной хроматографии, получая XYZ (50-60% выход). Реагенты, используемые для синтеза соединений согласно настоящему изобретению, доступны от коммерческих производителей, таких как Sigma-Aldrich, Alfa Aesar, и Sinova. Химические свойства оценивали путем жидкостной хроматографии-тандемной масс-спектрометрии (МС) и/или рассчитывали с помощью CS Chemdraw 8.0 (CambridgeSoft, USA). Общая методика синтеза II. Общая методика для приготовления XYInt01. К раствору азаиндольного производного X в гексаметилфосфорамиде (НМРА) при 0 С добавляли натрий водород (NaH; 1,2 экв.) и дополнительно перемешивали. Через 1 ч добавляли алкилгалогениды Y,такие как метилйодид, этилйодид, н-пропилбромид, изопропилбромид, н-бутилбромид, изобутилбромид(1,5 экв., 1 ч.), или O-t-бутилдиметилсилил-2-хлорэтанол (10 экв., 24 ч.), или O-t-бутилдиметилсилил-2 хлорпропанол (1,5 экв.) и перемешивали. После завершения реакции (наблюдали с помощью тонкослойной хроматографии (ТСХ реакцию закаливали с помощью ледяной воды и экстрагировали этилацетатом (EtOAc; 3). Органическую фазу высушивали над безводным Na2SO4 и концентрировали при пониженном давлении для получения остатка неочищенного продукта. Неочищенный продукт очищали путем колоночной хроматографии, получая XYInt01 (75-85% выход). Общая методика для приготовления XYInt02. К раствору безводного AlCl3 (5 экв.) в безводном диметилформамиде (ДМФА) при 0 С (20 мл) раствор XYInt01 в диметилформамиде и смесь дополнительно перемешивали. Через 1 ч добавляли трихлорацетилхлорид (5 экв.) и смеси позволяли нагреться до комнатной температуры. После завершения реакции (наблюдали с помощью ТСХ) реакцию закаливали ледяной водой и экстрагировали диметилформамидом (3). Органическую фазу высушивали над безводным Na2SO4 и концентрировали при пониженном давлении для получения остатка, который очищали путем колоночной хроматографии, получаяXYInt02 (60-70% выход). Общая методика для приготовления XYInt03. К раствору XYInt02 в ТГФ добавляли 5 н. NaOH и смесь перемешивали при комнатной температуре. После завершения реакции (наблюдали с помощью ТСХ) смесь концентрировали приблизительно до 1/4 исходного объема реакции и нейтрализовали с помощью разв. HCl. Образованный осадок фильтровали и высушивали в вакууме, получая XYInt03 (75-85% выход). Общая методика для приготовления XYZ. К раствору XYInt02 в безводном диметилформамиде добавляли 1-[3-(диметиламино)пропил]-3 этилкарбодиимидгидрохлорид (EDCIHCl; 1,5 экв.), 1-гидрокси-7-азабензотриазол (HOAt; 1,5 экв.),триэтаноламин (2 экв.) и Z (1,4 экв.), такой как циклопентилметиламин, циклопентилэтиламин, циклогексилметиламин, циклогексилэтиламин, циклогептилметиламин, циклогептилэтиламин, бицикло[2.2.2] октан-1-илметиламин или бицикло[2.2.2]октан-1-илэтиламин, и полученную реакционную смесь перемешивали при комнатной температуре. После завершения реакции (ТСХ) реакционную смесь обрабатывали водой и экстрагировали диметилформамидом (3). Органическую фазу высушивали над безводнымNa2SO4 и концентрировали при пониженном давлении для получения остатка, который очищали путем колоночной хроматографии, получая XYZ (40-55% выход). Общая методика для снятия защиты трет-бутилдиметилсилильной группы. К раствору силилоксиэтильного соединения (1 экв.) в безводном тетрагидрофуране при 0 С добавляли фторид тетрабутиламмония (6 экв.) и перемешивали при комнатной температуре в течение 4 ч. Реакционную смесь концентрировали в вакууме и остаток очищали путем колоночной хроматографии, получая XYZ (50-60% выход). Пример 3. Антагонизирующая активность индол-3-карбоксамидных и азаиндол-3-карбоксамидных соединений на P2X7R. Ингибирование P2X7R активности с помощью индол-3-карбоксамидных и азаиндол-3 карбоксамидных соединений согласно настоящему изобретению можно оценить путем измерения притока кальция в клетках HEK293 (ECACC85120602), которые стабильно трансфектировали кДНК дляP2X7R человека. Клетки HEK293 представляют собой клетки почек эмбриона человека, которые не экспрессируютP2X7R, получают с помощью трансфекции липофектамином кДНК P2X7R человека (рег. номер Genbank ВС 011913) под контролем предраннего промотора цитомегаловируса человека (CMV) и встраивали в вектор pcDNA3.1 (Invitrogen). Клетки культивировали при 37 С с 8,5% СО 2 в модифицированной по способу Дульбекко среде Игла (DMEM; GibcoBRL/lnvitrogen), дополненной инактивированной нагреванием фетальной телячьей сывороткой (10% v/v), 2 мМ L-глутамином, 100 ед./мл пенициллина, 0,1 мг/мл стрептомицина, и 750 мкг/мл генетицина G418 (GibcoBRL/lnvitrogen). Ингибирование Bz-ATP-стимулированного P2X7R с помощью тестируемых соединений наблюдали путем измерения притока кальция, используя Fluo-4-AM флуоресцентный краситель согласно инструкциям производителя (Molecular Devices Corporation, U.S.A.). Вкратце, HEK293 клетки, экспрессирующиеP2X7R, культивировали в планшетах на 96 лунок при конечной плотности около 10 тыс. клеток на лунку. В день эксперимента культуральную среду полностью удаляли из лунок и клетки промывали один раз в буфере для исследования (1 Х сбалансированный солевой раствор Хенкса (HBSS), содержащий 20 мМHepes буфера рН 7,4 и 250 мМ пробенецид; GibcoBRL/lnvitrogen). Клетки инкубировали в 50 мкл буфера для исследования, содержащего 100 мкМ Fluo-4 AM флуоресцентного красителя на лунку в течение 1 ч при комнатной температуре. После этого буфер для исследования, содержащий Fluo-4 AM флуоресцентный краситель, удаляли, клетки один раз промывали буфером для исследования (без Fluo-4 AM), после этого добавляли 100 мкл буфера для исследования (без Fluo-4 AM), содержащего тестируемые соединения, на лунку. После инкубирования в течение 15 мин добавляли 100 мкМ Bz-ATP и флуоресценцию измеряли на FlexStation II (Molecular Devices, U.S.A.) в соответствии со следующими параметрами: длина волны возбуждения 485 нм; длина волны испускания 525 нм; прерывание эмиссии 515 нм; высота пипетки 100 мкл; переносимый объем 25 мкл; 5-кратная концентрация соединения; 3 - коэффициент скорости добавления. Тестируемые соединения добавляли в концентрациях от 0,013 вплоть до 60 мкМ. Данные флуоресценции обрабатывали, используя время запаздывания 15 с, записывали 45 с, нулевую базовую линию калибровали, используя 2 точки, и коэффициент % базовой линии устанавливали равным 3. После этого рассчитывали площадь полученной кривой и определяли полумаксимальную ингибирующую концентрацию (IC50) для каждого тестируемого соединения, используя программное обеспечение SoftMaxPro (Molecular Devices, U.S.A.). Соединения согласно настоящему изобретению могут ингибировать активность P2X7R с IC50 в диапазоне от 1 до 0,001 мкМ. Например, IC50 соединения из примера 5 составляет около 0,134 мкМ. Пример 4. Индол-3-карбоксамидные и азаиндол-3-карбоксамидные соединения уменьшают секрецию интерлейкин-1. Влияния индол-3-карбоксамидных и азаиндол-3-карбоксамидных соединений согласно настоящему изобретению на секрецию IL-1 оценивали с помощью клеточной линии моноцитов человека ТНР-1 ( кат. АТСС 285-IF-100). Вкратце, ТНР-1 клетки помещали в планшеты на 96 лунок при концентрации 200 тыс. на лунки и позволяли дифференцироваться в RPMI-1640 среде ( кат. АТСС 30-2001), содержащей 10% FBS, 100 ед./мл пенициллина, 100 мкг/мл стрептомицина, 100 нМ РМА (форбол миристат ацетат) в течение 72 ч. В этих условиях ТНР-1 клетки дифференцировались в макрофаги, экспрессирующие эндогенный P2X7R. Соединения согласно настоящему изобретению добавляли к клеткам при различных концентрациях и после этого дифференцированные клетки стимулировали в течение 4 ч с помощью 1 мкг/мл LPS (липополисахарида) для активации транскрипции IL-1 (см. Humphreys и Dubyak (1998) J. Leukoc Biol. 64:26573). После этого процессинг и секрецию IL-1 стимулировали путем добавления 2 мМ АТР в течение 1 ч. После этого концентрацию IL-1 в супернатантах количественно определяли с помощью ELISA (RD система), используя специфические моноклональные античеловеческие IL-1 антитела в соответствии с инструкциями производителями. Более чем 90% детектируемого белка представлял собой биологически активный зрелый IL-1. Наблюдаемые результаты подтверждали статистически, используя односторонние ANOVA тесты. Примеры уменьшенной секреции IL-1 соединениями согласно настоящему изобретению иллюстрируются на фиг.1. Пример 5. Болеутоляющие и противовоспалительные действия. Этот пример иллюстрирует болеутоляющие и противовоспалительные преимущества соединений согласно настоящему изобретению, используя модель воспаления - индуцированный каррагенаном отек лапы. Отек у взрослых самцов крыс Sprague Dawley вызывали путем подкожной инъекции каррагенана(1% суспензия, 0,1 мл) в подошвенную поверхность правой задней лапы. Суспензию соединения в 0,5% метилцеллюлозе или наполнитель (0,5% метилцеллюлоза) вводили перорально через 1 ч после введения каррагенана. После этого лапу метили несмываемыми чернилами на уровне латеральной лодыжки таким образом, что лапу можно погрузить в плетизмометр, настроенный для этой метки. Плетизмометр позволяет определить небольшие изменения объема лапы. Через час после введения соединения или наполнителя (или 2 ч после введения каррагенана) осуществляли подошвенный тест с последующей записью объема лапы. Для подошвенного теста каждую крысу помещали на предварительно нагретую стеклянную подставку. Обе задние лапы животного стимулировали с помощью источника лучистого нагрева. Записывали латентный период отдергивания лапы от начала воздействия стимула. Повышение латентного периода ответной реакции отдергивания лапы толковали как болеутоляющую ответную реакцию. Для каждого животного проводили три пробы для получения среднего значения латентного периода отдергивания. Значения латентного периода отдергивания лапы (PWL) для тестируемой группы сравнивали с группой,получавшей наполнитель. Для теста отека лапы увеличение объема лапы для каждого животного рассчитывали путем вычитания объема задней левой лапы из объема задней правой лапы (разница объема лапы = объем правой задней лапы - объем левой задней лапы). Ингибирование повышения объема лапы толковали как противовоспалительную ответную реакцию. Наблюдаемые результаты подтверждали статистически, используяANOVA Tukey критерии множественного сравнения. Результаты представлены на фиг. 2. Соединение согласно настоящему изобретению оценивали относительно способности повышать латентный период отдергивания ланы в ответ на тепловой стимул, который указывает на обезболивающую ответную реакцию. Соединение согласно настоящему изобретению также оценивали относительно ингибирования отека лапы, индуцированной каррагенаном, который толковали как противовоспалительную ответную реакцию. Пример 6. N-(циклопентилметил)-1-метил-1 Н-индол-3-карбоксамид Синтезировали в соответствии с методикой, описанной в примере 1, где X представляет собой индол, Y представляет собой метилйодид и Z представляет собой циклопентилметиламин. Формула: Синтезировали в соответствии с методикой, описанной в примере 1, где X представляет собой 4 хлориндол, Y представляет собой метилйодид и Z представляет собой циклопентилметиламин. Формула: Синтезировали в соответствии с методикой, описанной в примере 1, где X представляет собой 4 фториндол, Y представляет собой метилйодид и Z представляет собой циклопентилметиламин. Формула: Синтезировали в соответствии с методикой, описанной в примере 1, где X представляет собой 4 броминдол, Y представляет собой метилйодид и Z представляет собой циклопентилметиламин. Формула: Синтезировали в соответствии с методикой, описанной в примере 1, где X представляет собой 4 метилиндол, Y представляет собой метилйодид и Z представляет собой циклопентилметиламин. Формула: C17H22N2O; молекулярный вес: 270,4; соотношение масса/заряд: 270,2 (100,0%), 271,2 (19,4%), 272,2 Синтезировали в соответствии с методикой, описанной в примере 1, где X представляет собой индол, Y представляет собой метилйодид и Z представляет собой циклогексилметиламин. Формула: Синтезировали в соответствии с методикой, описанной в примере 1, где X представляет собой 4 хлориндол, Y представляет собой метилйодид и Z представляет собой циклогексилметиламин. Формула: Синтезировали в соответствии с методикой, описанной в примере 1, где X представляет собой 4 фториндол, Y представляет собой метилйодид и Z представляет собой циклогексилметиламин. Формула: Синтезировали в соответствии с методикой, описанной в примере 1, где X представляет собой 4 броминдол, Y представляет собой метилйодид и Z представляет собой циклогексилметиламин. Формула: Синтезировали в соответствии с методикой, описанной в примере 1, где X представляет собой 4 метилиндол, Y представляет собой метилйодид и Z представляет собой циклогексилметиламин. Формула: C18H24N2O; молекулярный вес: 284,4; соотношение масса/заряд: 284,2 (100,0%), 285,2 (20,5%), 286,2
МПК / Метки
МПК: A61K 31/416, C07D 471/04, A61P 25/24, A61P 25/02, C07D 209/42, C07D 231/56, A61P 25/04, C07D 403/06, A61P 29/00, A61K 31/404, A61K 31/437, A61P 25/18
Метки: антагонисты, применение, новые, p2x7r
Код ссылки
<a href="https://eas.patents.su/30-22505-novye-p2x7r-antagonisty-i-ih-primenenie.html" rel="bookmark" title="База патентов Евразийского Союза">Новые p2x7r антагонисты и их применение</a>
Предыдущий патент: Способ получения растворимых в воде продуктов гидролиза целлюлозы
Следующий патент: Анализ частиц в акустическом цитометре
Случайный патент: Способ и композиция для улучшения сгорания топлива












