Новые антагонисты рецептора v1a и их применение в качестве лекарственного средства
Формула / Реферат
1. Соединение формулы I
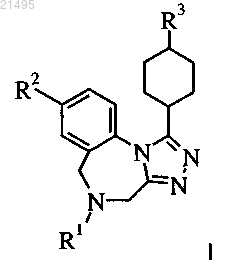
в которой R1 выбирают из группы, включающей:
i) Н,
ii) C1-6-алкил, незамещенный или содержащий от 1 до 5 заместителей, независимо выбранных из группы, состоящей из ОН-группы, галогена, цианогруппы и C1-6-алкоксигруппы,
iii) -S(О)2-C1-6-алкил, где C1-6-алкил является незамещенным или содержит от 1 до 5 заместителей, независимо выбранных из группы, состоящей из ОН-группы, галогена, цианогруппы и C1-6-алкоксигруппы,
iv) -С(О)-C1-6-алкил, где C1-6-алкил является незамещенным или содержит от 1 до 5 заместителей, независимо выбранных из группы, состоящей из ОН-группы, галогена, цианогруппы и C1-6-алкоксигруппы,
v) -С(О)O-C1-6-алкил, где C1-6-алкил является незамещенным или содержит от 1 до 5 заместителей, независимо выбранных из группы, состоящей из ОН-группы, галогена, цианогруппы и C1-6-алкоксигруппы;
vi) C3-6-циклоалкил, незамещенный или содержащий от 1 до 5 заместителей, независимо выбранных из группы, состоящей из ОН-группы, галогена, цианогруппы, C1-6-алкила и C1-6-алкоксигруппы,
vii) -S(O)2-(CH2)q-NRiRii, где q равно 0 или 1,
каждый из Ri и Rii независимо выбирают из группы, состоящей из Н и C1-6-алкила,
viii) -(CH2)r-NRiiiRiv, где r равно 1, 2 или 3,
каждый из Riii и Riv независимо выбирают из группы, состоящей из Н и C1-6-алкила, и
ix) -C(O)(CH2)s-NRvRvi, где s равно 1, 2 или 3,
каждый из Rv и Rvi независимо выбирают из группы, состоящей из Н и C1-6-алкила;
R2 представляет собой галоген;
R3 представляет собой 8-10-членный гетеробиарил, содержащий 2-3 гетероатома, выбранных из О, N и S, незамещенный или содержащий 1-5 заместителей, независимо выбранных из группы, состоящей из ОН-группы, галогена, цианогруппы, C1-6-алкила, C1-6-алкоксигруппы, галоген-C1-6-алкила, галоген-C1-6-алкоксигруппы и гидрокси-C1-6-алкила;
или его фармацевтически приемлемая соль.
2. Соединение по п.1, в котором R1 выбирают из группы, включающей:
i) Н,
ii) -C1-6-алкил,
iii) -S(O)2-C1-6-алкил,
iv) -C(O)O-C1-6-алкил,
v) C3-6-циклоалкил,
vi) -(CH2)r-NRiiiRiv, где r равно 1, 2 или 3,
каждый из Riii и Riv независимо выбирают из группы, состоящей из Н и C1-6-алкила, и
vii) -С(О)(СН2)s-NRvRvi, где s равно 1, 2 или 3,
каждый из Rv и Rvi независимо выбирают из группы, состоящей из Н и C1-6-алкила.
3. Соединение по любому из пп.1-2, в котором R1 выбирают из группы, включающей Н, метил, циклобутил, метил-2-этиламин, 1-оксоэтил, 1-оксо-2-(диметиламино)этил и метилсульфонил.
4. Соединение по любому из пп.1-2, в котором R1 выбирают из группы, включающей C1-6-алкил, C3-6-циклоалкил, -(СН2)2-N(C1-6-алкил)2 и -С(О)(СН2)-N(C1-6-алкил)2.
5. Соединение по любому из пп.1-4, в котором R1 выбирают из группы, включающей метил, циклобутил, метил-2-этиламин и 1-оксо-2-(диметиламино)этил.
6. Соединение по любому из пп.1-5, в котором R2 представляет собой атом хлора.
7. Соединение по любому из пп.1-6, в котором R3 представляет собой 8-10-членный гетеробиарил, содержащий 2-3 гетероатома, выбранных из О, N и S, незамещенный или содержащий в качестве заместителя 1-2 атома галогена.
8. Соединение по любому из пп.1-7, в котором R3 представляет собой бензо[d]изоксазолил, изоксазоло[4,5-b]пиридинил, изоксазоло[5,4-b]пиридинил, бензо[d]изотиазолил, изотиазоло[4,5-b]пиридинил или 4-изотиазоло[5,4-с]пиридинил, причем каждый из них является незамещенным или содержит в качестве заместителя 1-2 атома галогена.
9. Соединение по любому из пп.1-8, в котором R3 представляет собой бензо[d]изоксазол-3-ил, 6-фторбензо[d]изоксазол-3-ил, 5-фторбензо[d]изоксазол-3-ил, изоксазоло[4,5-b]пиридин-3-ил, изоксазоло[5,4-b]пиридин-3-ил, бензо[d]изотиазол-3-ил, изотиазоло[4,5-b]пиридин-3-ил или 4-изотиазоло[5,4-с]пиридин-3-ил.
10. Соединение по любому из пп.1-9, выбранное из группы, включающей



или его фармацевтически приемлемая соль.
11. Соединение по любому из пп.1-10, выбранное из группы, включающей



или его фармацевтически приемлемая соль.
12. Соединение по любому из пп.1-11, выбранное из группы, включающей

или его фармацевтически приемлемая соль.
13. Применение соединения формулы I по любому из пп.1-12 в качестве антагониста рецептора V1a.
14. Применение соединения формулы I по любому из пп.1-12 для профилактики или лечения дисменореи, мужской или женской половой дисфункции, гипертонии, хронической сердечной недостаточности, неадекватной секреции вазопрессина, цирроза печени, нефротического синдрома, тревожности, депрессивных расстройств, обcессивно-компульсивного расстройства, аутистических расстройств, шизофрении и агрессивного поведения.
15. Фармацевтическая композиция, обладающая антагонистической активностью в отношении V1a и включающая соединение формулы I по любому из пп.1-12.
16. Фармацевтическая композиция по п.15, которая полезна для профилактики или лечения дисменореи, мужской или женской половой дисфункции, гипертонии, хронической сердечной недостаточности, неадекватной секреции вазопрессина, цирроза печени, нефротического синдрома, тревожности, депрессивных расстройств, обcессивно-компульсивного расстройства, аутистических расстройств, шизофрении и агрессивного поведения.
17. Применение соединения формулы I по любому из пп.1-12 для изготовления лекарственного препарата для профилактики или лечения дисменореи, мужской или женской половой дисфункции, гипертонии, хронической сердечной недостаточности, неадекватной секреции вазопрессина, цирроза печени, нефротического синдрома, тревожности, депрессивных расстройств, обcессивно-компульсивного расстройства, аутистических расстройств, шизофрении и агрессивного поведения.
18. Способ терапевтического и/или профилактического лечения дисменореи, мужской или женской половой дисфункции, гипертонии, хронической сердечной недостаточности, неадекватной секреции вазопрессина, цирроза печени, нефротического синдрома, тревожности, депрессивных расстройств, обcессивно-компульсивного расстройства, аутистических расстройств, шизофрении и агрессивного поведения, включающий введение соединения по любому из пп.1-12 человеку или животному.
Текст
НОВЫЕ АНТАГОНИСТЫ РЕЦЕПТОРА V1a И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ЛЕКАРСТВЕННОГО СРЕДСТВА в которой R1, R2 и R3 таковы, как определено в настоящем описании. Предложены соединения по настоящему изобретению, действующие как модуляторы V1a рецептора, в частности как антагонисты V1a рецептора, а также их изготовление, содержащие их фармацевтические композиции и их применение в виде лекарственных препаратов. Действующие вещества по настоящему изобретению полезны как терапевтические средства, действующие на периферическом и центральном уровне при состояниях дисменореи, мужской или женской половой дисфункции,гипертонии, хронической сердечной недостаточности, неадекватной секреции вазопрессина,цирроза печени, нефротического синдрома, тревожности, депрессивных расстройств, обессивнокомпульсивного расстройства, аутистических расстройств, шизофрении и агрессивного поведения. Предшествующий уровень техники Вазопрессин представляет собой пептид, состоящий из 9 аминокислот, который главным образом синтезируется паравентрикулярным ядром гипоталамуса. В периферической нервной системе вазопрессин действует как нейрогормон и стимулирует вазоконстрикцию, гликогенолиз и антидиурез. Известны три рецептора вазопрессина, относящиеся к I классу рецепторов, сопряженных с Gбелком. Рецептор V1a экспрессируется в головном мозге, печени, гладкой мускулатуре сосудов, легких,матке и семенниках, рецептор V1b или V3 экспрессируется в головном мозге и питуитарной железе, рецептор V2 экспрессируется в почках, где он регулирует реабсорбцию воды и опосредует антидиуретические эффекты вазопрессина (Robben, et al. (2006). Am. J. Physiol. Renal. Physiol. 291, F257-70, "Cell biological aspects of the vasopressin type-2 receptor and aquaporin 2 water channel in nephrogenic diabetes insipidus"). Поэтому соединения, обладающие активностью рецептора V2, могут оказывать побочное действие на гомеостаз крови. Рецептор окситоцина относится к семейству рецепторов вазопрессина и опосредует эффекты нейрогормона окситоцина в головном мозге, а также в периферической нервной системе. Считают, что окситоцин оказывает анксиолитический эффект на центральную нервную систему (Neumann (2008). J. Neuroendocrinol. 20, 858-65, "Brain oxytocin: a key regulator of emotional and social behaviors in both females andmales"). Антагонизм рецептора окситоцина в центральной нервной системе может, таким образом, вызывать анксиогенные эффекты, что расценивается как нежелательное побочное действие. В головном мозге вазопрессин действует как нейромодулятор, и его уровень в мозжечковых миндалинах повышается во время стресса (Ebner, et al. (2002). Eur. J. Neurosci. 15, 384-8, "Forced swimming triggers vasopressin release within the amygdala to modulate stress-coping strategies in rats"). Известно, что жизнь в условиях стресса может инициировать тяжелую депрессию и тревожность (Kendler, et al. (2003). ArchGen Psychiatry. 60, 789-96, "Life Event Dimensions of Loss, Humiliation, Entrapment and Danger in the Prediction of Onsets of Major Depression and Generalized Anxiety"), причем эти расстройства обладают высокой коморбидностью, и тревожность часто предшествует тяжелой депрессии (Regier, et al. (1998). Br J.Psychiatry Suppl. 24-8, "Prevalence of anxiety disorders and their comorbidity with mood and addictive disorders"). Рецептор V1a активно экспрессируется в головном мозге и, особенно, в лимбических зонах, таких как мозжечковые миндалины, латеральная перегородка и гипоталамус, которые играют важную роль в регуляции тревожности. Действительно, V1a-нокаутированные мыши демонстрируют снижение поведенческой тревожности в тестах "приподнятый крестообразный лабиринт", "открытое поле" и "темносветлая камера" (Bielsky, et al. (2004). Neuropsychopharmacology. 29, 483-93, "Profound impairment in socialrecognition and reduction in anxiety-like behavior in vasopressin V1a receptor knockout mice"). Деактивация рецептора V1a путем инъекции антисмыслового олигонуклеотида в перегородку также вызывает снижение поведенческой тревожности (Landgraf, et al. (1995). Regul Pept. 59, 229-39, "V1 vasopressin receptorantisense oligodeoxynucleotide into septum reduces vasopressin binding, social discrimination abilities, and anxiety-related behavior in rats"). Вазопрессин или рецептор V1a имеют отношение также к другим нейрофизиологическим расстройствам: недавние генетические исследования выявили связь между полиморфизмом последовательности промотора человеческого рецептора V1a с аутистическими расстройствамиand autism in a family-based study: mediation by socialization skills"), было показано,что интраназальное введение вазопрессина влияет на агрессивность у мужчин (Thompson, et al. (2004). Psychoneuroendocrinology. 29, 35-48, "The effects of vasopressin on human facial responses related to social communication"), а также было обнаружено, что уровень вазопрессина повышается у пациентов с шизофренией (Raskind, etsecretion in obsessive-compulsive disorder"). Кроме того, рецептор V1 а опосредует эффекты вазопрессина на сердечно-сосудистую систему в головном мозге за счет регуляции центральной нервной системой кровяного давления и частоты сердечных сокращений в ядре одиночного пути (Michelini and Morris (1999). Ann N.Y. Acad Sci. 897, 198-211, "Endogenous vasopressin modulates the cardiovascular responses to exercise"). В периферической системе он индуцирует сокращение гладкой мускулатуры сосудов, и хроническое ингибирование рецептора V1a улучшает гемодинамические параметры у крыс с инфарктом миокарда (Van Kerckhoven, et al. (2002). Eur.in chronically infarcted rats"). Поэтому ожидается, что преимуществом будут обладать антагонисты V1a с улучшенной способностью проникать сквозь гематоэнцефалический барьер. Было показано, что антагонист V1a рецептора вазопрессина эффективно улучшает клиническую картину дисменореи (Brouard, et al. (2000). Bjog. 107, 614-9, "Effect of SR49059, an orally active V1a vasopressin receptor antagonist, in the prevention of dismenorrhea"). Кроме того, антагонизм V1a рецептора задействован при лечении женской половой дисфункции (Aughton, et al. (2008). Br. J. Pharmacol.smooth muscle in vitro"). Недавние исследования антагонистов V1a рецептора говорят об их терапевтиче-1 021495 ском действии как в отношении эректильной дисфункции, так и преждевременной эякуляции (Gupta, etal. (2008). Br. J. Pharmacol. 155, 118-26, "Oxytocin-induced contractions within rat and rabbit ejaculatory tissues are mediated by vasopressin V(1A) receptors and not oxytocin receptors"). Область техники Настоящее изобретение относится к гетеробиарил-циклогексил-тетраазабензо[е]азуленам, которые действуют как модуляторы V1a рецептора, и в частности как антагонисты V1a рецептора, их получению,содержащим их фармацевтическим композициям, а также их применению в качестве лекарственных средств. Сущность изобретения Настоящее изобретение предлагает соединения формулы I, полезные для оказания воздействия на периферическом и центральном уровне при состояниях дисменореи, мужской или женской половой дисфункции, гипертонии, хронической сердечной недостаточности, неадекватной секреции вазопрессина,цирроза печени, нефротического синдрома, тревожности, депрессивных расстройств, обсессивнокомпульсивного расстройства, аутистических расстройств, шизофрении и агрессивного поведения. В частности, настоящее изобретение относится к соединениям формулы I в которой R1, R2 и R3 таковы, как раскрыто в настоящем описании. Подробное описание изобретения Настоящее изобретение предлагает соединения, которые действуют как модуляторы V1a рецептора,и в частности как антагонисты V1a рецептора. Дополнительная цель настоящего изобретения - предложить селективные ингибиторы V1a рецептора, поскольку ожидается, что селективность приведет к снижению способности вызывать нежелательные нецелевые связанные побочные эффекты, подобные тем,которые обсуждались ранее. Такие V1a антагонисты эффективны в качестве терапевтических средств, действующих на периферическом или центральном уровне, при состояниях дисменореи, мужской или женской половой дисфункции, гипертонии, хронической сердечной недостаточности, неадекватной секреции вазопрессина,цирроза печени, нефротического синдрома, тревожности, депрессивных расстройств, обсессивнокомпульсивного расстройства, аутистических расстройств, шизофрении и агрессивного поведения. В частности, показаниями для лечения в отношении настоящего изобретения могут выступать тревожность, депрессивные расстройства, обсессивно-компульсивные расстройства, аутистические расстройства, шизофрения и агрессивное поведение. Активность V1a можно детектировать, как описано в экспериментальной части. Следующие определения общих терминов, используемые в настоящем описании, применяются независимо от того, встречаются ли обсуждаемые термины по отдельности или в комбинации. Используемый в данном тексте термин "C1-6-алкил", по отдельности или в комбинации с другими группами, обозначает углеводородный радикал, линейный или разветвленный, с одним или несколькими разветвлениями, в котором указанная алкильная группа содержит от 1 до 6 атомов углерода, например метил (Me), этил (Et), пропил, изопропил, н-бутил, изобутил, 2-бутил (втор-бутил), трет-бутил и т.п. В частности, алкильные группы представляют собой группы, содержащие от 1 до 4 атомов углерода. Например, они представляют собой метил, этил и трет-бутил. Термин "С 1-6-алкокси", по отдельности или в комбинации с другими группами, обозначает группу-O-R', в которой R' представляет собой C1-6-алкил, раскрытый ранее, например метокси-, этокси-, пропокси-, трет-бутоксигруппу и т.п. В частности, алкоксигруппы представляют собой группы, содержащие от 1 до 4 атомов углерода. В частности, такой группой является метоксигруппа. Термин "арил" относится к ароматической карбоциклической группе, содержащей от 6 до 14, в частности от 6 до 10 атомов углерода и содержащей по меньшей мере одно ароматическое кольцо или несколько конденсированных колец, среди которых по меньшей мере одно кольцо является ароматическим. Примерами являются фенил (Ph), бензил, нафтил, бифенил, антрил, азаленил или инданил. В частности, такой группой является фенил. Термин "гетероарил", по отдельности или в комбинации с другими группами, относится к циклической ароматической группе, содержащей единственное 5-6-членное кольцо и включающей 1, 2 или 3 гетероатома, в которой по меньшей мере одно гетероциклическое кольцо является ароматическим. Термин"6-членный гетероарил" относится к моноциклической ароматической группе, содержащей единственное 6-членное кольцо и включающий 1, 2 и 3 гетероатома, независимо выбранных из О, S и N. В частности,-2 021495 единственное 6-членное кольцо содержит 1 или 2 атома N. Примерами являются пиридинил, пиримидинил, пиразинил, пиридазинил, тиазинил, оксазинил и т.п. В частности, единственное 6-членное кольцо представляет собой пиридинил. В частности, "6-членные гетероарильные группы" присоединены через атом углерода к циклогексильной группе. В частности, такой группой является пиридин-3-ил. Термин "5 членный гетероарил" относится к моноциклической ароматической группе, содержащей единственное 5 членное кольцо и включающей 1, 2 или 3 гетероатома, независимо выбранных из О, S и N. В частности,единственное 5-членное кольцо содержит 2 атома N или же 1 атом О и 1 атом N. Примерами являются тиазолил, изоксазолил, изотиазолил, оксадиазолил, тиадиазолил и т.п. Например, такой группой является изоксазолил. В частности, "5-членная гетероарильная группа" присоединена через атом углерода к циклогексильному фрагменту. В частности, такой группой является изоксазол-3-ил. Термин "гетеробиарил", по отдельности или в комбинации с другими группами, относится к циклической группе, содержащей первое 4-8-членное ароматическое кольцо, предпочтительно 5-6-членное ароматическое кольцо, конденсированное со вторым 4-8-членным ароматическим кольцом, предпочтительно 5-6-членным ароматическим кольцом, при этом каждое кольцо по отдельности включает 1, 2 или 3 гетероатома, независимо выбранных из О, S и N. Примером является гетеробиарил, в котором одно кольцо представляет собой фенил или пиридинил. В частности, такой группой является гетеробиарил, в которой одно кольцо представляет собой фенил. Примерами гетеробиарила являются бензофурил, изобензофурил, индолил, изоиндолил, бензотиофенил, бензоимидазолил, пуринил, индазолил, бензоксазолил, бензоизоксазолил, бензотиазолил, бензотриазолил, 1,3-дигидро-2-индоксил, бензоизотиазолил, хинолинил, хиноксалинил, хиназолинил, циннолинил, 4,5,6,7-тетрагидробензоизоксазолил, изотиазоло[4,5b]пиридинил и т.п. Примерами также являются бензоизоксазолил, 4,5,6,7-тетрагидробензоизоксазолил,бензоизотиазолил, изотиазоло[5,4-b]пиридинил, изотиазоло[4,5-b]пиридинил и изотиазоло[4,5 с]пиридинил. В частности, "гетеробиарил" присоединен через атом углерода к циклогексильному фрагменту. В частности, примерами являются бензо[d]изоксазол-3-ил, изоксазоло[4,5-b]пиридин-3-ил, изоксазоло[5,4-b]пиридин-3-ил, бензо[d]изотиазол-3-ил, изотиазоло[4,5-b]пиридин-3-ил, 4-изотиазоло[5,4 с]пиридин-3-ил. Кроме того, примерами являются бензо[d]изоксазол-3-ил, изоксазоло[4,5-b]пиридин-3 ил, изотиазоло[4,5-b]пиридин-3-ил, 4-изотиазоло[5,4-с]пиридин-3-ил. Термин "циклоалкил" относится к углеродному кольцу, содержащему от 3 до 8 атомов, например циклопропил, циклобутил, циклопентил, циклогексил, циклофенил или циклооктил. В частности, такими группами являются циклоалкильные группы, содержащие 3-, 4-, 5- или 6-членное углеродное кольцо. В частности, такой группой является циклобутил. Термин "циано" обозначает группу -CN. Термин "гидрокси" обозначает группу -ОН. Термин "Boc" обозначает группу -С(О)О-трет-бутил (-С(О)ОС(СН 3)3). Термин "S(О)2-С 1-6-алкил" относится к "C1-6-алкилу", раскрытому в настоящем описании, присоединенному через группу -S(O)2-. Термин "C(O)-C1-6-алкил" относится к "C1-6-алкилу", раскрытому в настоящем описании, присоединенному через группу -С(=О)-. Термин "C(O)O-C1-6-алкил" относится к "C1-6-алкилу", раскрытому в настоящем описании, присоединенному через группу -С(=O)О-. Термин "галоген", по отдельности или в комбинации с другими группами, обозначает атом хлора(Cl), йода (I), фтора (F) и брома (Br). Например, галоген представляет собой атом F и Cl. В частности,галоген представляет собой атом Cl. Термин "галоген-C1-6-алкил" относится к C1-6-алкильной группе, замещенной одним или несколькими атомами галогена. В частности, такой группой являются фтор-C1-6 алкильные группы, например CF3,CHF2, CH2F, CH2CF3, CH2CH2CF3, CF2CHF2 и т.п. Термин "гидрокси-C1-6-алкил" обозначает C1-6-алкильную группу, содержащую в качестве заместителя одну или несколько гидроксигрупп, например следующие группы: гидроксиметил-, 2-гидроксиэтил-,2-гидрокси-1-метилэтил-, 2-гидроксипропил- и т.п. Термин "циано-C1-6-алкил" обозначает C1-6-алкильную группу, содержащую в качестве заместителя одну или несколько цианогрупп, например следующие группы: цианометил-, 2-цианоэтил-, 2-циано-1 метилэтил- или 2-цианопропил- и т.п. Термин "галоген-C1-6-алкокси" обозначает C1-6-алкоксигруппу, замещенную одним или несколькими атомами галогена, в частности атомами фтора, т.е. "фтор-C1-6 алкоксигруппы", например следующие группы: F-CH2-O-. Термин "гетероцикл" обозначает гетероциклическое кольцо, содержащее от 3 до 7 атомов, включающее по меньшей мере один гетероатом, например атом N, О или S, причем число атомов N равно 0, 1,2 или 3, а число каждого из атомов О и S равно 0, 1 или 2. Примерами гетероциклических групп являются пирролидинил, тетрагидрофурил, тетрагидротиенил, тетрагидропиридинил, тетрагидропирил, азетидинил, тиазолидинил, оксазолидинил, пиперидинил, морфолинил, тиоморфолинил, пиперазинил, азепанил, диазепанил, оксазепанил и т.п. Термин "возможно, содержащий в качестве заместителя" обозначает Ca-алкильную или Cb-3 021495 алкильную группу, которая может быть незамещенной или может содержать в качестве заместителя от 1 до 4 заместителей, независимо выбранных из группы, состоящей из ОН-группы, галогена, цианогруппы,галоген-C1-6-алкокси- и C1-6-алкоксигруппы; или циклоалкильную группу, которая может быть незамещенной или может содержать в качестве заместителя от 1 до 4 заместителей, независимо выбранных из группы, состоящей из ОН-группы, галогена, цианогруппы, C1-6-алкила, галоген-C1-6-алкила, галоген-C1-6 алкокси- и C1-6 -алкоксигруппы. Термин "фармацевтически приемлемые соли" относится к солям, которые подходят для применения в условиях контакта с тканями человека и животных без проявления нежелательной токсичности, раздражения, аллергической реакции и т.п. Примерами подходящих солей неорганических и органических кислот являются, без ограничения, соли хлороводородной кислоты, азотной кислоты, серной кислоты,фосфорной кислоты, лимонной кислоты, муравьиной кислоты, фумаровой кислоты, малеиновой кислоты, молочной кислоты, яблочной кислоты, уксусной кислоты, янтарной кислоты, виноградной кислоты,метансульфоновой кислоты, п-толуолсульфоновой кислоты, трифторуксусной кислоты и т.п. В частности, это соли хлороводородной кислоты. Термины "фармацевтически приемлемый носитель" и "фармацевтически приемлемое вспомогательное вещество" относятся к носителям и вспомогательным веществам, таким как разбавители или наполнители, которые совместимы с другими ингредиентами лекарственной формы. Термин "фармацевтическая композиция" охватывает продукт, включающий указанные компоненты в предварительно определенных количествах или соотношениях, равно как и любой продукт, который можно получить, прямо или косвенно, путем комбинирования указанных ингредиентов в указанных количествах. В частности, он охватывает продукт, включающий один или более активных ингредиентов и,возможно, носитель, включающий инертные ингредиенты, равно как и любой продукт, который можно получить, прямо или косвенно, за счет комбинирования, комплексообразования или агрегации любых двух или более ингредиентов, или за счет диссоциации одного или более ингредиентов, или посредством иных типов реакций или взаимодействий одного или более ингредиентов. Термин "ингибитор" обозначает соединение, которое конкурирует за, снижает или предотвращает связывание конкретного лиганда с конкретным рецептором, или которое снижает или предотвращает ингибирование функции конкретного белка. Термин "полумаксимальная ингибирующая концентрация" (IC50) обозначает концентрацию конкретного соединения, необходимую для достижения 50% ингибирования биологического процесса invitro. Значения IC50 можно логарифмически преобразовать в значения pIC50 (-log IC50), для которых более высокие значения соответствуют большей активности, по экспоненциальной зависимости. Величина IC50 не является абсолютной, но зависит от экспериментальных условий, т.е. используемых концентраций. Величину IC50 можно преобразовать в абсолютную константу ингибирования (Ki) по уравнению ЧенгаПрусоффа (Biochem. Pharmacol. (1973) 22:3099). Термин "константа ингибирования" (Ki) обозначает абсолютную связывающую способность конкретного ингибитора с рецептором. Ее измеряют с помощью конкурентных методов анализа, и она численно равна концентрации, при которой конкретный ингибитор связал бы 50% рецепторов, при отсутствии конкурирующего лиганда (например, радиолиганда). Значения Ki можно логарифмически преобразовать в величины pKi (-log Ki), для которых более высокие значения соответствуют большей активности, по экспоненциальной зависимости. Термины "как определено в данном описании" и "как раскрыто в данном описании", если они относятся к переменной величине, включают посредством ссылки широкое определение этой переменной величины, равно как и предпочтительные, более предпочтительные и самые предпочтительные определения, если таковые существуют. Термины "обработка", "введение в контакт" и "введение в реакцию" в тех случаях, когда они относятся к химической реакции, означают добавление или смешение двух или более реагентов в соответствующих условиях с получением указанного и/или целевого продукта. Следует понимать, что реакция, в ходе которой получают указанный и/или целевой продукт, не обязательно является прямым результатом сочетания двух изначально добавленных реагентов, т.е. возможно наличие одного или более промежуточных продуктов, которые образуются в смеси, что в конечном итоге приводит к образованию указанного и/или целевого продукта. Термин "ароматический" отражает общепринятое понятие ароматичности в том смысле, как оно определено в литературе, в частности в IUPAC - Compendium of Chemical Terminology, 2nd, A.D."Терапевтически эффективное количество" обозначает такое количество, которое эффективно предотвращает, смягчает или улучшает симптомы заболевания или продлевает срок жизни субъекта, который получает лечение. Далее перечислены сокращения, используемые в настоящем документе. Таблица 1 СокращенияK3PO4 - фосфат калия реагент Лавессона - 2,4-бис-(4-метоксифенил)-1,3,2,4-дитиадифосфетан-2,4-дисульфид МеОН - метанолRT-PCR - полимеразная цепная реакция с обратной транскриптазойZnBr2 - бромид цинка. Настоящее изобретение предлагает также фармацевтические композиции, способы применения и способы получения указанных выше соединений. Поскольку настоящее изобретение описано со ссылкой на конкретные варианты его осуществления,специалистам в данной области техники следует понимать, что можно внести различные изменения и заменить эквиваленты, не выходя за пределы сущности и объема настоящего изобретения. Кроме того,можно провести различные модификации, чтобы привести конкретную ситуацию, вещество, композицию веществ, способ, стадию или стадии способа в соответствие с объективной сущностью настоящего изобретения. Подразумевается, что все подобные модификации охвачены объемом и формулой изобретения, приложенной к настоящему описанию. Любые отдельные варианты осуществления можно комбинировать. Соединение формулы I может содержать асимметрический атом углерода. Таким образом, настоящее изобретение включает все стереоизомерные формы соединения формулы I, включая каждый из индивидуальных стереоизомеров и их смеси, т.е. их индивидуальные оптические изомеры и их смеси. Могут присутствовать дополнительные асимметрические центры в зависимости от природы различных заместителей в молекуле. Каждый такой асимметрический центр будет независимо давать два оптических изомера, и подразумевается, что все возможные оптические изомеры и диастереомеры в виде смесей и в виде чистых или частично очищенных соединений включены в объем настоящего изобретения. Подразумевается, что настоящее изобретение охватывает все подобные изомерные формы этих соединений. Независимые синтезы этих диастереомеров или их хроматографическое разделение можно осуществить способами, известными в данной области техники, путем соответствующей модификации методологии,раскрытой в настоящем описании. Их абсолютную стереохимию можно определить с помощью рентгеноструктурного анализа кристаллических продуктов или кристаллических интермедиатов, которые дериватизируют, если это необходимо, с помощью реагента, содержащего асимметрический центр с известной абсолютной конфигурацией. По желанию, рацемические смеси соединений можно разделить так,чтобы выделить индивидуальные энантиомеры. Разделение можно осуществлять способами, хорошо известными в данной области техники, например путем объединения рацемической смеси соединений с энантиомерно чистым соединением с образованием смеси диастереомеров, с последующим разделением индивидуальных диастереомеров стандартными способами, такими как дробная кристаллизация или хроматография. Это относится, в частности, к арильным концевым группам (HG) соединений формулы I, а именно в которой, по меньшей мере, атомы углерода 1 и 4 представляют собой асимметрический атом углерода и R3 может включать еще один асимметрический атом углерода. Следует понимать, что настоящее изобретение включает все индивидуальные стереоизомеры концевых групп и их смеси. В частности, такими концевыми HG-группами являются Кроме того, следует понимать, что все варианты осуществления настоящего изобретения, раскрытые в данном описании, можно комбинировать друг с другом. В частности, настоящее изобретение относится к соединению формулы Ii) H,ii) -С 1-6-алкил, незамещенный или содержащий от 1 до 5 заместителей, независимо выбранных из группы, состоящей из ОН-группы, галогена, цианогруппы и C1-6-алкоксигруппы,iii) -S(O)2-C1-6-алкил, где C1-6-алкил является незамещенным или содержит от 1 до 5 заместителей,независимо выбранных из группы, состоящей из ОН-группы, галогена, цианогруппы и C1-6 алкоксигруппы,iv) -С(О)-C1-6-алкил, где C1-6-алкил является незамещенным или содержит от 1 до 5 заместителей,независимо выбранных из группы, состоящей из ОН-группы, галогена, цианогруппы и C1-6 алкоксигруппы,v) -С(О)О-C1-6-алкил, где C1-6-алкил является незамещенным или содержит от 1 до 5 заместителей,независимо выбранных из группы, состоящей из ОН-группы, галогена, цианогруппы и C1-6 алкоксигруппы;vi) циклоалкил, незамещенный или содержащий от 1 до 5 заместителей, независимо выбранных из группы, состоящей из ОН-группы, галогена, цианогруппы, C1-6-алкила и C1-6-алкоксигруппы,vii) S(O)2-(CH2)q-NRiRii, где q равно 0 или 1,каждый из Ri и Rii независимо выбирают из группы, состоящей из Н и C1-6-алкила, или же Ri и Rii образуют совместно с атомом азота, к которому они присоединены, 3-7-членный гетероцикл, включающий один или два гетероатома, независимо выбранных из N, О и S, который является незамещенным или содержит от 1 до 5 заместителей, независимо выбранных из группы, состоящей из оксогруппы, галогена,-6 021495C1-6-алкила, C1-6-алкоксигруппы,viii) -(CH2)r-NRiiiRiv, где r равно 1, 2 или 3,каждый из Riii и Riv независимо выбирают из группы, состоящей из Н и C1-6-алкила, или же Riii и Riv образуют совместно с атомом азота, к которому они присоединены, 3-7-членный гетероцикл, включающий один или два гетероатома, независимо выбранных из N, О и S, причем указанный гетероцикл является незамещенным или содержит от 1 до 5 заместителей, независимо выбранных из группы, состоящей из оксогруппы, галогена, C1-6-алкила и C1-6-алкоксигруппы, иix) -C(O)(CH2)s-NRvRvi в которой s равно 1, 2 или 3,каждый из Rv и Rvi независимо выбирают из группы, состоящей из Н и C1-6 -алкила, или же Rv и Rvi образуют совместно с атомом азота, к которому они присоединены, 3-7-членный гетероцикл, включающий один или два гетероатома, независимо выбранных из N, О и S, причем указанный гетероцикл является незамещенным или содержит от 1 до 5 заместителей, независимо выбранных из группы, состоящей из оксогруппы, галогена, С 1-6-алкила и С 1-6-алкоксигруппы;R3 представляет собой гетеробиарил, незамещенный или содержащий в качестве заместителя 1-5 заместителей, независимо выбранных из группы, состоящей из ОН-группы, галогена, цианогруппы, С 1-6 алкила, C1-6-алкоксигруппы, галоген-С 1-6-алкила, галоген-С 1-6-алкоксигруппы и гидрокси-С 1-6-алкила; или к его фармацевтически приемлемой соли. Один из вариантов осуществления настоящего изобретения относится к соединению формулы Iai) Н,ii) C1-6-алкил, незамещенный или содержащий от 1 до 5 заместителей, независимо выбранных из группы, состоящей из ОН-группы, галогена, цианогруппы и C1-6-алкоксигруппы,iii) -S(О)2-C1-6-алкил, где C1-6-алкил является незамещенным или содержит от 1 до 5 заместителей,независимо выбранных из группы, состоящей из ОН-группы, галогена, цианогруппы и C1-6 алкоксигруппы,iv) -С(О)-C1-6-алкил, где C1-6-алкил является незамещенным или содержит от 1 до 5 заместителей,независимо выбранных из группы, состоящей из ОН-группы, галогена, цианогруппы и C1-6 алкоксигруппы,v) -С(О)О-C1-6-алкил, где C1-6-алкил является незамещенным или содержит от 1 до 5 заместителей,независимо выбранных из группы, состоящей из ОН-группы, галогена, цианогруппы и C1-6 алкоксигруппы;vi) циклоалкил, незамещенный или содержащий от 1 до 5 заместителей, независимо выбранных из группы, состоящей из ОН-группы, галогена, цианогруппы, C1-6-алкила и C1-6-алкоксигруппы,vii) S(O)2-(CH2)q-NRiRii, где q равно 0 или 1,каждый из Ri и Rii независимо выбирают из группы, состоящей из Н и C1-6-алкила, или же Ri и Rii образуют совместно с атомом азота, к которому они присоединены, 3-7-членный гетероцикл, включающий один или два гетероатома, независимо выбранных из N, О и S, причем указанный гетероцикл является незамещенным или содержит от 1 до 5 заместителей, независимо выбранных из группы, состоящей из оксогруппы, галогена, С 1-6-алкила и С 1-6-алкоксигруппы,viii) -(CH2)r-NRiiiRiv, где r равно 1, 2 или 3,каждый из Riii и Riv независимо выбирают из группы, состоящей из Н и C1-6-алкила, или же Riii и Riv образуют совместно с атомом азота, к которому они присоединены, 3-7-членный гетероцикл, включающий один или два гетероатома, независимо выбранных из N, О и S, причем указанный гетероцикл является незамещенным или содержит от 1 до 5 заместителей, независимо выбранных из группы, состоящей из оксогруппы, галогена, C1-6-алкила и C1-6-алкоксигруппы, иix) -C(O)(CH2)s-NRvRvi, где s равно 1, 2 или 3,каждый из Rv и Rvi независимо выбирают из группы, состоящей из Н и C1-6-алкила, или же Rv и Rvi образуют совместно с атомом азота, к которому они присоединены, 3-7-членный гетероцикл, включающий один или два гетероатома, независимо выбранных из N, О и S, причем гетероцикл является незамещенным или содержит от 1 до 5 заместителей, независимо выбранных из группы, состоящей из оксогруппы, галогена, C1-6-алкила и C1-6-алкоксигруппы;R3 представляет собой гетеробиарил, незамещенный или содержащий в качестве заместителя 1-5 заместителей, независимо выбранных из группы, включающей ОН-группу, галоген, цианогруппу, C1-6 алкил, C1-6-алкоксигруппу, галоген-С 1-6-алкил, галоген-C1-6-алкоксигруппу и гидрокси-C1-6-алкил; или к его фармацевтически приемлемой соли. Один из вариантов осуществления настоящего изобретения относится к соединению формулы I, в которойi) Н,ii) -С 1-6-алкил,iii) -S(О)2-C1-6-алкил,iv) -С(О)O-C1-6-алкил,v) циклоалкил,vi) -(CH2)r-NRiiiRiv, где r равно 1, 2 или 3,каждый из Riii и Riv независимо выбирают из группы, включающей Н и C1-6-алкил, иvii) -C(O)(CH2)s-NRvRvi, где s равно 1, 2 или 3,каждый из Rv и Rvi независимо выбирают из группы, включающей Н и C1-6-алкил. Один из вариантов осуществления настоящего изобретения относится к соединению формулы I, в которой R1 выбирают из группы, включающей Н, метил, циклобутил, метил-2-этиламин, 1-оксоэтил, 1 оксо-2-(диметиламино)этил и метилсульфонил. Один из вариантов осуществления настоящего изобретения относится к соединению формулы I, в которой R1 выбирают из группы, включающей -С 1-6-алкил, циклоалкил, -(СН 2)2-N(C1-6-алкил)2 и-С(О)(СН 2)-N(С 1-6-алкил)2. Один из вариантов осуществления настоящего изобретения относится к соединению формулы I, в которой R1 выбирают из группы, включающей метил, циклобутил, метил-2-этиламин и 1-оксо-2(диметиламино)этил. Один из вариантов осуществления настоящего изобретения относится к соединению формулы I, в которой R1 представляет собой Н. Один из вариантов осуществления настоящего изобретения относится к соединению формулы I, в которой R1 представляет собой C1-6-алкил. Один из вариантов осуществления настоящего изобретения относится к соединению формулы I, в которой R1 представляет собой метил. Один из вариантов осуществления настоящего изобретения относится к соединению формулы I, в которой R1 представляет собой -С(О)О-C1-6-алкил. Один из вариантов осуществления настоящего изобретения относится к соединению формулы I, в которой R1 представляет собой Boc. Один из вариантов осуществления настоящего изобретения относится к соединению формулы I, в которой R1 представляет собой циклоалкил. Один из вариантов осуществления настоящего изобретения относится к соединению формулы I, в которой R1 представляет собой циклобутил. Один из вариантов осуществления настоящего изобретения относится к соединению формулы I, в которой R1 представляет собой -(CH2)r-NRiiiRiv, в которой r равно 1, 2 или 3, а каждый из Riii и Riv независимо выбирают из группы, включающей Н и C1-6-алкил. Один из вариантов осуществления настоящего изобретения относится к соединению формулы I, в которой R1 представляет собой -(СН 2)2-N(C1-6-алкил)2. Один из вариантов осуществления настоящего изобретения относится к соединению формулы I, в которой R1 представляет собой метил-2-этиламин. Один из вариантов осуществления настоящего изобретения относится к соединению формулы I, в которой R1 представляет собой -С(О)-C1-6-алкил. Один из вариантов осуществления настоящего изобретения относится к соединению формулы I, в которой R1 представляет собой 1-оксоэтил. Один из вариантов осуществления настоящего изобретения относится к соединению формулы I, в которой R1 представляет собой -C(O)(CH2)s-NRvRvi, в которой s равно 1, 2 или 3, а каждый из Rv и Rvi независимо выбирают из группы, включающей Н и C1-6-алкил. Один из вариантов осуществления настоящего изобретения относится к соединению формулы I, в которой R1 представляет собой -C(O)(CH2)-N(C1-6-алкил)2. Один из вариантов осуществления настоящего изобретения относится к соединению формулы I, в которой R1 представляет собой 1-оксо-2-(диметиламино)этил. Один из вариантов осуществления настоящего изобретения относится к соединению формулы I, в которой R1 представляет собой -S(O)2-C1-6-алкил. Один из вариантов осуществления настоящего изобретения относится к соединению формулы I, в которой R1 представляет собой метилсульфонил. Один из вариантов осуществления настоящего изобретения относится к соединению формулы I, в которой R2 представляет собой атом хлора. Один из вариантов осуществления настоящего изобретения относится к соединению формулы I, в которой R3 представляет собой гетеробиарил, незамещенный или содержащий в качестве заместителя 1-2 атома галогена. Один из вариантов осуществления настоящего изобретения относится к соединению формулы I, в которой R3 представляет собой бензо[d]изоксазолил, изоксазоло[4,5-b]пиридинил, изоксазоло[5,4b]пиридинил, бензо[d]изотиазолил, изотиазоло[4,5-b]пиридинил или 4-изотиазоло[5,4-с]пиридинил, каждый из которых является незамещенным или содержит в качестве заместителя 1-2 атома галогена. Один из вариантов осуществления настоящего изобретения относится к соединению формулы I, в которой R3 представляет собой бензо[d]изоксазол-3-ил, 6-фторбензо[d]изоксазол-3-ил, 5-фторбензо[d]изоксазол-3-ил, изоксазоло[4,5-b]пиридин-3-ил, изоксазоло[5,4-b]пиридин-3-ил, бензо[d]изотиазол-3-ил, изотиазоло[4,5-b]пиридин-3-ил или 4-изотиазоло[5,4-с]пиридин-3-ил. Один из вариантов осуществления настоящего изобретения относится к соединению формулы I, в которой R3 представляет собой бензо[d]изоксазолил, 6-фторбензо[d]изоксазолил, 5-фторбензо[d]изоксазолил, изоксазоло[4,5-b]пиридинил, изоксазоло[5,4-b]пиридинил, бензо[d]изотиазолил,изотиазоло[4,5-b]пиридинил, 4-изотиазоло[5,4-с]пиридинил. Один из вариантов осуществления настоящего изобретения относится к соединению формулы I, в которой R3 представляет собой бензо[d]изоксазол-3-ил, 6-фторбензо[d]изоксазол-3-ил, 5-фторбензо[d]изоксазол-3-ил, изоксазоло[4,5-b]пиридин-3-ил, изоксазоло[5,4-b]пиридин-3-ил, бензо[d]изотиазол-3-ил, изотиазоло[4,5-b]пиридин-3-ил, 4-изотиазоло[5,4-с]пиридин-3-ил. Один из вариантов осуществления настоящего изобретения относится к соединению формулы I, в которой R3 представляет собой бензо[d]изоксазол-3-ил. Один из вариантов осуществления настоящего изобретения относится к соединению формулы I, в которой R3 представляет собой 6-фторбензо[d]изоксазол-3-ил. Один из вариантов осуществления настоящего изобретения относится к соединению формулы I, в которой R3 представляет собой 5-фторбензо[d]изоксазол-3-ил. Один из вариантов осуществления настоящего изобретения относится к соединению формулы I, в которой R3 представляет собой изоксазоло[4,5-b]пиридин-3-ил. Один из вариантов осуществления настоящего изобретения относится к соединению формулы I, в которой R3 представляет собой изоксазоло[5,4-b]пиридин-3-ил. Один из вариантов осуществления настоящего изобретения относится к соединению формулы I, в которой R3 представляет собой бензо[d]изотиазол-3-ил. Один из вариантов осуществления настоящего изобретения относится к соединению формулы I, в которой R3 представляет собой изотиазоло[4,5-b]пиридин-3-ил. Один из вариантов осуществления настоящего изобретения относится к соединению формулы I, в которой R3 представляет собой 4-изотиазоло[5,4-с]пиридин-3-ил. Примеры соединений по настоящему изобретению представлены в экспериментальной части и в нижеследующей таблице. Таблица 2 Структуры соединений, выбранных в качестве примеров Один из вариантов осуществления настоящего изобретения относится к соединению формулы I,выбранному из группы, включающей или их фармацевтически приемлемые соли. Один из вариантов осуществления настоящего изобретения относится к соединению формулы I,выбранному из группы, включающей или их фармацевтически приемлемые соли. Один из вариантов осуществления настоящего изобретения относится к соединению формулы I,выбранному из группы, включающей или их фармацевтически приемлемые соли. Один из вариантов осуществления настоящего изобретения относится к соединению формулы I,выбранному из группы, включающей или их фармацевтически приемлемые соли. Один из вариантов осуществления настоящего изобретения относится к соединению, описанному любым из вариантов осуществления, которое можно получить способом, раскрытым в данном описании. Один из вариантов осуществления настоящего изобретения относится к соединению, описанному любым из вариантов осуществления, во всех случаях, когда его можно получить способом, раскрытым в данном описании. Один из вариантов осуществления настоящего изобретения относится к соединению, описанному любым из вариантов осуществления, предназначенному для применения в качестве терапевтически активного вещества. Один из вариантов осуществления настоящего изобретения относится к соединению, описанному любым из вариантов осуществления, предназначенному для применения с целью профилактики или лечения дисменореи, мужской или женской половой дисфункции, гипертонии, хронической сердечной недостаточности, неадекватной секреции вазопрессина, цирроза печени, нефротического синдрома, тревожности, депрессивных расстройств, обсессивно-компульсивного расстройства, аутистических расстройств, шизофрении и агрессивного поведения. Один из вариантов осуществления настоящего изобретения относится к фармацевтической композиции, включающей соединение, описанное любым из вариантов осуществления. Один из вариантов осуществления настоящего изобретения относится к фармацевтической композиции, включающей соединение, описанное любым из вариантов осуществления, которая полезна для профилактики или лечения дисменореи, мужской или женской половой дисфункции, гипертонии, хронической сердечной недостаточности, неадекватной секреции вазопрессина, цирроза печени, нефротического синдрома, тревожности, депрессивных расстройств, обсессивно-компульсивного расстройства,аутистических расстройств, шизофрении и агрессивного поведения. Один из вариантов осуществления настоящего изобретения касается применения соединения, описанного любым из вариантов осуществления, для изготовления лекарственного препарата. Один из вариантов осуществления настоящего изобретения касается применения соединения, описанного любым из вариантов осуществления, для изготовления лекарственного препарата, который полезен для профилактики или лечения дисменореи, мужской или женской половой дисфункции, гипертонии,хронической сердечной недостаточности, неадекватной секреции вазопрессина, цирроза печени, нефротического синдрома, тревожности, депрессивных расстройств, обсессивно-компульсивного расстройства,аутистических расстройств, шизофрении и агрессивного поведения. Один из вариантов осуществления настоящего изобретения касается применения соединения, описанного любым из вариантов осуществления, для профилактики или лечения дисменореи, мужской или женской половой дисфункции, гипертонии, хронической сердечной недостаточности, неадекватной сек- 16021495 реции вазопрессина, цирроза печени, нефротического синдрома, тревожности, депрессивных расстройств, обсессивно-компульсивного расстройства, аутистических расстройств, шизофрении и агрессивного поведения. Один из вариантов осуществления настоящего изобретения касается способа терапевтического и/или профилактического лечения дисменореи, мужской или женской половой дисфункции, гипертонии,хронической сердечной недостаточности, неадекватной секреции вазопрессина, цирроза печени, нефротического синдрома, тревожности, депрессивных расстройств, обсессивно-компульсивного расстройства,аутистических расстройств, шизофрении и агрессивного поведения, включающий введение соединения,раскрытого в любом из вариантов осуществления, человеку или животному. В одном из вариантов осуществления соединение формулы I по настоящему изобретению можно изготовить способом, включающим стадию реакции соединения формулы II с получением соединения формулы I, в которой R1, R2 и R3 таковы, как раскрыто в настоящем описании выше для формулы I. Эти способы описаны более подробно с помощью нижеследующей схемы и методов A-F. Схема 1 Общая схема А Соединение формулы I можно получить путем термической конденсации гидразида формулы II и тиолактама формулы III. Синтез соединений формулы II показан в приведенных ниже общих схемах D-F. Соединение формулы III можно получить, следуя способам, описанным в общей схеме С, как раскрыто далее в настоящем описании. Общая схема А описана далее более подробно с помощью общего способа Соединение формулы I, в которой R1 отлично от Н, можно получить из соединения формулы I-2(соединение формулы I, в которой R1 представляет собой Н) способами, известными в данной области техники, например путем обработки соединения формулы I-2 неорганическим основанием, таким как карбонатная соль, или органическим основанием, таким как четвертичный амин, и электрофильным реагентом R1-LG (где LG представляет собой уходящую группу, например галоген или сульфонил), который либо коммерчески доступен, либо легко может быть получен с помощью способов и исходных веществ,хорошо известных в данной области техники. Как вариант, соединение формулы I можно получить с помощью восстановительного алкилирования путем последовательной обработки соединения формулы I-2 кетоном или альдегидом и подходящим восстанавливающим агентом, например производным борогидрида, таким как борогидрид натрия, цианоборогидрид натрия или триацетоксиборогидрид натрия. Как вариант, соединение формулы I, в которой R1 представляет собой ацильную группу, можно получить путем конденсации амина формулы I-2 с карбоновой кислотой. Для проведения конденсации с получением амида можно применять стандартные реагенты и протоколы, известные в данной области техники. Соединение формулы I-2 можно получить расщеплением заместителя R1 в соединении формулы I, применяя способы, известные в данной области техники. Соединение формулы I-2 обычно получают в виде соли или свободного основания после обработки водно-основным раствором в ходе реакции соединения формулы I-1 (соединение формулы I, в которой R1 представляет собой трет-бутоксикарбонил) с кислотой в подходящем растворителе, например с метансульфоновой кислотой в дихлорметане или тетрагирофуране, или же с хлороводородной кислотой в метаноле. Общая схема В представлена далее в общих процедурах IX и X. Схема 3 Общая схема С бутоксикарбонил) можно получить следующим образом. Превращение 2-нитробензилового спирта формулы в бензилхлорид формулы b можно осуществить с помощью хлорирующего агента, например тионилхлорида, в присутствии органического четвертичного аммониевого основания. Алкилирование соединения формулы b с помощью гидрохлорида глицилэтилового эфира в присутствии органического четвертичного аммониевого основания и проведение N-защиты полученного соединения формулы с с помощью ди-трет-бутилдикарбоната и каталитического количества 4-N,N-диметиламинопиридина дает соединение формулы d. Нитрогруппу можно селективно восстановить гидрированием над палладием или платиной на активированном угле, предварительно обработанными галогенидом цинка, например бромидом цинка, с образованием анилинового промежуточного продукта формулы е. Циклизацию до тиолактама формулы f проводят путем обработки соединения формулы е подходящим основанием, например трет-бутоксидом калия, в тетрагирофуране. Тиолактам формулы III-1 получают путем обработки соединения формулы f реагентом Лавессона или пентасульфидом фосфора при повышенной температуре. Схема 4 Общая схема D Промежуточный эфир 4-ароилциклогексанкарбоновой кислоты формулы VI можно получить путем конденсации моноэфира циклогексан-1,4-дикарбоновой кислоты формулы IV с арил- или гетероарилбороновой кислотой формулы g в присутствии ангидрида карбоновой кислоты, например триметилуксусного ангидрида, и подходящего палладиевого катализатора, например смеси ацетата палладия(II) и фосфинового лиганда, например трис(4-метоксифенил)фосфина, в тетрагирофуране, содержащем небольшое количество воды, при 60 С. Как вариант, промежуточный эфир 4-ароилциклогексанкарбоновой кислоты формулы VI можно синтезировать путем конденсации эфира 4-хлоркарбонилциклогексанкарбоновой кислоты формулы V, который можно получить из моноэфира циклогексан-1,4 дикарбоновой кислоты формулы IV способами, известными в данной области техники, позволяющими переводить карбоновые кислоты в хлориды карбоновых кислот, например, путем обработки с помощью тионилхлорида или оксалилхлорида и каталитического количества N,N-диметилформамида галогенида арил- или гетероарилцинка формулы h в присутствии подходящего палладиевого катализатора, например тетракис(трифенилфосфин)палладия(0) в тетрагирофуране при комнатной температуре. Обработка промежуточного эфира 4-ароилциклогексанкарбоновой кислоты формулы VI смесью гидроксиламина гидрохлорида и ацетата натрия в подходящем спирте при комнатной температуре приводит к оксиму промежуточного соединения формулы VII, который обычно получают в виде E/Z смеси. Оксим промежуточного соединения формулы VII можно циклизовать до арил- или гетероарил-изоксазольного промежуточного соединения формулы IX-1, путем обработки с помощью основания алкоксида калия в тетрагирофуране при комнатной температуре. Как вариант, обработка промежуточного эфира 4-ароилциклогексанкарбоновой кислоты формулы VI с бензилмеркаптаном и трет-бутоксидом калия в тетрагидрофуране при комнатной температуре приводит к бензиловому эфиру формулы VIII, который можно циклизовать до арил- или гетероарилизотиазольного промежуточного соединения формулы IX-2 через последовательное S-дебензилирование с помощью сульфурилхлорида в дихлорметане при комнатной температуре и обработки этанольным раствором аммиака в тетрагидрофуране при комнатной температуре. Общая схема D раскрыта далее более подробно в общих способах I-V. Схема 5 Общая схема Е Промежуточные цис/транс-смеси эфира 4-гетероарилциклогексанкарбоновой кислоты формулы IX в некоторых случаях можно разделить обычными способами, например с помощью колонки с силикагелем, или высокоэффективной жидкостной хроматографии, или кристаллизацией до чистых промежуточного эфира цис-4-гетероарилциклогексанкарбоновой кислоты формулы IX-а и промежуточного эфира транс-4-гетероарилциклогексанкарбоновой кислоты формулы IX-b, которые можно омылять до чистых промежуточной цис-4-гетероарилциклогексанкарбоновой кислоты формулы Х-а и промежуточной транс 4-гетероарилциклогексанкарбоновой кислоты формулы Х-b при стандартных условиях, например при перемешивании в смеси водного раствора гидроксида натрия и эфирного растворителя, такого как 1,4 диоксан, тетрагидрофуран или диэтиловый эфир, при комнатной температуре. Как вариант, промежуточную транс-4-гетероарилциклогексанкарбоновую кислоту формулы Х-b можно получить эпимеризацией цис-изомера цис/транс-смесей промежуточного эфира 4-гетероарилциклогексанкарбоновой кислоты формулы IX с помощью подходящего основания, например алкоксида щелочного металла, такого как метилат или этилат натрия или калия, в подходящем растворителе, таком как метанол, этанол или толуол, с обратным холодильником, с последующим омылением неочищенной реакционной смеси, которая может состоять из смеси промежуточной транс-4-гетероарилциклогексанкарбоновой кислоты формулы Х-b и промежуточного эфира транс-4-гетероарилциклогексанкарбоновой кислоты формулы IX-b, при стандартных условиях, например при перемешивании в смеси водного раствора гидроксида натрия и эфирного растворителя, такого как 1,4-диоксан, тетрагидрофуран или диэтиловый эфир, при комнатной температуре. В случае если реакцию эпимеризации проводят с использованием спирта в качестве растворителя, неочищенную реакционную смесь, возможно, подкисляют добавлением концентрированной серной кислоты и нагревают до температуры флегмы с получением промежуточного эфира транс-4 гетероарилциклогексанкарбоновой кислоты формулы IX-b. Промежуточный эфир 4-гетероарилциклогексанкарбоновой кислоты формулы IX можно превратить в гидразид формулы II нагреванием с гидратом гидразина. Как вариант, эфир формулы IX можно гидролизовать до карбоновой кислоты формулы X, используя двухфазную смесь водного раствора гидроксида натрия или калия и эфирного растворителя, такого как диоксан, тетрагидрофуран или диэтиловый эфир. Гидразид формулы II можно получить активацией промежуточной кислоты формулы X, например, с помощью этилхлорформиата, тионилхлорида, оксалилхлорида или пептид-связывающего реагента, и последующей конденсацией с гидразином. Общая схема F представлена далее в общих способах VI и VII. Соответствующие фармацевтически приемлемые соли с кислотами можно получить стандартными способами, известными специалисту в данной области техники, например путем растворения соединения формулы I в подходящем растворителе, таком как, например, диоксан или THF, и добавления нужного количества соответствующей кислоты. Эти продукты обычно можно выделить с помощью фильтрации или хроматографии. Переведение соединения формулы I в фармацевтически приемлемую соль с помощью основания можно осуществлять путем обработки такого соединения с помощью такого основания. Один из возможных методов получения такой соли заключается, например, в добавлении 1/n экв. основной соли, например М(ОН)n, в которой М представляет собой катион металла или аммония, a n - число гидроксидных анионов, к раствору соединения в подходящем растворителе (например, этанол, смесь этанол-вода, смесь тетрагидрофуран-вода) и удалении растворителя выпариванием или лиофилизацией. В случае если в примерах не описано получение соединения формулы I, это соединение, а также все промежуточные продукты, можно получить по аналогичным способам или способам, изложенным в данном описании. Исходные вещества коммерчески доступны или их можно получить способами, известными в данной области техники, или аналогичными им. Следует понимать, что соединение формулы I по настоящему изобретению можно дериватизировать по функциональным группам с получением производных, которые способны превращаться in vivo обратно в исходное соединение. Фармакологические тесты Соединения по настоящему изобретению проявляют активность V1a. Они являются селективными ингибиторами рецептора V1a и поэтому, скорее всего, обладают низкой способностью вызывать нежелательные нецелевые сопутствующие побочные эффекты. Активность V1a можно детектировать, как описано ниже. Человеческий V1a рецептор клонировали с помощью RT-PCR из тотальной человеческой печеночной РНК. Кодирующую последовательность субклонировали в вектор экспрессии после секвенирования с целью подтверждения идентичности амплифицированной последовательности. Для того чтобы продемонстрировать сродство соединений по настоящему изобретению к человеческому V1a рецептору, проводили исследования с помощью методов связывания. Клеточные мембраны получали из клетокHEK293, транзиентно трансфицированных с помощью вектора экспрессии и культивированных в 20 л биореакторе согласно следующей методике. 50 г клеток ресуспендировали в 30 мл свежеприготовленного охлажденного до 0 С лизирующего буфера (50 мМ HEPES, 1 мМ EDTA, 10 мМ дихлорид магния, доведенного до рН 7,4 + полная смесь ингибиторов протеаз (Roche Diagnostics. Гомогенизровали с помощью Polytron 1 мин и разрушали клетки ультразвуком на льду в течение 22 мин при интенсивности 80% (Vibracell sonicator). Препарат центрифугировали 20 мин при 500 g при 4C, осадок отбрасывали и супернатант цетрифугировали 1 ч при 43000 g при 4 С (19000 об/мин). Осадок ресуспендировали в 12,5 мл лизирующего буфера + 12,5 мл сахарозы 20% и гомогенизировали с помощью Polytron в течение 1-2 мин. Концентрацию белка определяли по методу Бредфорда и аликвоты хранили при -80 С до использования. Для исследования по методу свя- 21021495 зывания 60 мг гранул силиката иттрия SPA (Amersham) смешивали с аликвотой мембраны в связывающем буфере (50 мМ Tris, 120 мМ хлорид натрия, 5 мМ хлорид калия, 2 мМ дихлорид кальция, 10 мМ дихлорид магния) в течение 15 мин при перемешивании. Затем добавляли 50 мкл смеси гранулы/мембрана в каждую лунку 96-луночного планшета, а затем 50 мкл 4 нМ 3 Н-вазопрессина (AmericanRadiolabeled Chemicals). Для определения общего связывания добавляли 100 мкл связывающего буфера в соответствующие лунки, для определения неспецифического связывания - 100 мкл 8,4 мМ холодного вазопрессина, а для тестирования соединений - 100 мкл серийных разведений каждого соединения в 2% диметилсульфоксиде. Планшет инкубировали 1 ч при комнатной температуре, цетрифугировали 1 мин при 1000 g и проводили считывание с помощью Packard Top-Count. Величину неспецифического связывания вычитали из каждой лунки и нормализировали данные относительно максимального специфического связывания, которое принимали за 100%. Для расчета IC50 строили кривую с помощью нелинейной регрессионной модели (программа XLfit) и рассчитывали Ki по уравнению Ченга-Прусоффа. Нижеследующие репрезентативные данные демонстрируют антагонистическую активность по отношению к человеческому V1 а рецептору для соединений по настоящему изобретению. Таблица 3 Фармацевтические композиции. Соединение формулы I, равно как и их фармацевтически приемлемые соли, можно применять в качестве лекарственных средств, например, в форме фармацевтических препаратов. Фармацевтические препараты можно вводить орально, например в форме таблеток, таблеток, покрытых оболочкой, драже,твердых и мягких желатиновых капсул, растворов, эмульсий или суспензий. Тем не менее, введение можно осуществлять также ректально, например в форме суппозиториев, или парентерально, например в форме растворов для инъекций. Соединение формулы I и их фармацевтически приемлемые соли можно процессировать совместно с фармацевтически инертными, неорганическими или органическими вспомогательными веществами для изготовления таблеток, таблеток, покрытых оболочкой, драже и твердых желатиновых капсул. В качестве таких вспомогательных веществ можно применять лактозу, кукурузный крахмал или их производные,тальк, стеариновую кислоту или ее соли и т.д., например в случае таблеток, драже и твердых желатиновых капсул. Подходящими вспомогательными веществами для мягких желатиновых капсул являются,например, растительные масла, воски, жиры, полужидкие и жидкие полиолы и т.д. Подходящими вспомогательными веществами для изготовления растворов и сиропов являются, например, вода, полиолы, сахароза, инвертированный сахар, глюкоза и т.д. Подходящими вспомогательными веществами в случае растворов для инъекций являются, например, вода, спирты, полиолы, глицерин, растительные масла и т.д. Подходящими вспомогательными веществами для суппозиториев являются, например, натуральные или отвержденные масла, воски, жиры, полужидкие или жидкие полиолы и т.д. Кроме того, фармацевтические препараты могут содержать консерванты, солюбилизаторы, стабилизаторы, увлажняющие агенты, эмульгаторы, подсластители, красители, ароматизаторы, соли для варьирования осмотического давления, буферы, маскирующие агенты или антиоксиданты. Они могут также содержать и другие терапевтически полезные вещества. Дозировку можно варьировать в широких пределах и, разумеется, ее выбирают в соответствии с индивидуальными требованиями в каждом конкретном случае. В целом, в случае орального введения подходит суточная дозировка примерно от 10 до 1000 мг соединения формулы I на человека, однако вышеуказанный верхний предел можно превышать в случае необходимости. Примерами композиций по настоящему изобретению являются, без ограничения, следующие. Пример А. Таблетки нижеследующей композиции изготавливают обычным способом. Способ изготовления. 1. Смешать ингредиенты 1, 2, 3 и 4 и гранулировать с помощью очищенной воды. 2. Высушить гранулы при 50 С. 3. Пропустить гранулы через подходящее устройство для помола. 4. Добавить ингредиент 5 и смешать в течение минут; спрессовать с помощью подходящего пресса. Пример В-1. Изготовление капсул следующего состава. Таблица 5 Возможный ингредиентный состав капсулы Способ изготовления. 1. Смешать ингредиенты 1, 2 и 3 в подходящем смесителе в течение 30 мин. 2. Добавить ингредиенты 4 и 5 и смешивать в течение 3 мин. 3. Внести в подходящую капсулу. Соединение формулы I, лактозу и кукурузный крахмал сначала смешивают в смесителе, а затем в измельчителе. Эту смесь возвращают в смеситель, добавляют к ней тальк (и стеарат магния) и тщательно смешивают. С помощью устройства наполняют смесью подходящие капсулы, например твердые желатиновые капсулы. Пример В-2. Изготовление мягких желатиновых капсул следующего состава. Таблица 6 Возможный ингредиентный состав мягких желатиновых капсул Таблица 7 Возможный состав мягких желатиновых капсул Способ изготовления. Соединение формулы I растворяют в теплом расплаве других ингредиентов и наполняют смесью мягкие желатиновые капсулы подходящего размера. Заполненные мягкие желатиновые капсулы обрабатывают обычными способами. Пример С. Изготовление суппозиториев следующего состава. Таблица 8 Возможный состав суппозитория Способ изготовления. Массу суппозитория расплавляют в стеклянном или стальном сосуде, тщательно смешивают и охлаждают до 45C. Затем к ней добавляют тонкоизмельченное соединение формулы I и перемешивают до полного растворения. Смесь заливают в форму для суппозиториев подходящего размера, оставляют охладиться; затем суппозитории извлекают из формы и индивидуально упаковывают в парафинированную бумагу или металлическую фольгу. Пример D. Изготовление растворов для инъекции следующего состава. Таблица 9 Возможный состав раствора для инъекций Способ изготовления. Соединение формулы I растворяют в смеси полиэтиленгликоля 400 и воды для инъекций (частично). Доводят рН до 5,0 с помощью уксусной кислоты. Объем доводят до 1,0 мл добавлением оставшегося количества воды. Раствор фильтруют, разливают во флаконы в подходящем избыточном объеме и стерилизуют. Пример Е. Изготовление саше следующего состава. Способ изготовления. Соединение формулы I смешивают с лактозой, микрокристаллической целлюлозой и натрий карбоксиметилцеллюлозой и гранулируют со смесью поливинипирролидона в воде. Гранулят смешивают со стеаратом магния и вкусовыми добавками и помещают в саше. Примеры Нижеследующие примеры приведены в качестве наглядного представления настоящего изобретения. Их следует считать не ограничением объема настоящего изобретения, но лишь его иллюстрацией. Промежуточное соединение формулы (V). Метиловый эфир транс-4-хлоркарбонилциклогексанкарбоновой кислоты К раствору монометилэфира транс-1,4-циклогексанедикарбоновой кислоты (2,0 г, 11 ммоль) в дихлорметане (30 мл) добавляли оксалил хлорид (1,1 мл, 13 ммоль) и каталитическое количество N,Nдиметилформамида при 0-5C. Охлаждающую ванну убирали и реакционную смесь перемешивали в течение 24 ч при комнатной температуре. После выпаривания растворителя остаток растирали в н-гексане(100 мл). Преципитат удаляли фильтрацией. Фильтрат концентрировали в вакууме с образованием указанного в заголовке соединения (2,2 г, количественно) в виде бесцветного масла, которое использовали в следующей стадии без дополнительной очистки. Промежуточный эфир 4-ароилциклогексанкарбоновой кислоты формулы VI. Общий способ (I): конденсация Негиши. К раствору арил- или гетероарил бромида (1 экв.) в сухом тетрагидрофуране (0,2 М) добавляют 2 М раствор хлорида изопропилмагния в тетрагидрофуране (1,05 экв.) при 0-5 С. Охлаждающую ванну убирают и реакционную смесь перемешивают в течение 1 ч при комнатной температуре. К интермедиату Гриньяра добавляют раствор хлорида цинка (2 экв.), который предварительно сушат плавлением в вакууме с последующим охлаждением в атмосфере аргона в сухом тетрагидрофуране (1,0 М). Перемешивают в течение 1 ч, после чего добавляют метиловый эфир 4-хлоркарбонилциклогексанкарбоновой кислоты (1 экв.) и тетракис(трифенилфосфин)палладий(0) (0,05 экв.). Через 18-24 ч реакционную смесь гасят с помощью водного насыщенного раствора хлорида аммония и экстрагируют двумя или тремя порциями органического растворителя, такого как трет-бутилметиловый эфир или этилацетат. Объединенные органические слои высушивают над безводным сульфатом натрия и концентрируют досуха. В результате очистки с помощью флэш-хроматографии получают промежуточный эфир 4-ароилциклогексанкарбоновой кислоты формулы VI. Метиловый эфир 4-ароилциклогексанкарбоновой кислоты эфир 1. транс-4-(2-Фторбензоил)циклогексанкарбоновая кислота Указанное в заголовке соединение получали в виде бесцветной жидкости, выход 32%, из 1-бром-2 фторбензола по общему способу (I). MS m/e: 264 (М+). Эфир 4-ароилциклогексанкарбоновой кислоты 2. Раствор монометилового эфира цис/транс-1,4-циклогександикарбоновой кислоты (2,0 г, 11 ммоль),2-фторфенилбороновой кислоты (2,0 г, 14 ммоль), трис(4-метоксифенил)фосфина (0,76 г, 2,1 ммоль) и ацетата палладия(II) (0,24 г, 1,1 ммоль) в тетрагидрофуране (50 мл) и воде (0,48 мл, 27 ммоль) продували аргоном. Добавляли триметилуксусный ангидрид (3,3 мл, 16 ммоль) и перемешивали при 60C в течение 20 ч. После охлаждения до комнатной температуры осадок палладия удаляли фильтрацией с помощьюDecalite. Растворитель выпаривали. Остаток делили между слоями этилацетата (200 мл) и 1 М водного раствора карбоната натрия (100 мл). Слои разделяли. Органический слой промывали одной порцией 100 мл 2 М водного раствора карбоната натрия. Объединенные водные слои экстрагировали одной порцией 100 мл этилацетата. Объединенные органические слои высушивали над безводным сульфатом натрия и концентрировали досуха. В результате очистки с помощью флэш-хроматографии с использованием нгептана/этилацетата в качестве элюента получали указанное в заголовке соединение (0,52 г, 18%) в виде бесцветного масла. Эфир 4-ароилциклогексанкарбоновой кислоты 3. Метиловый эфир транс-4-(2,4-дифторбензоил)циклогексанкарбоновой кислоты Указанное в заголовке соединение получали в виде белого твердого вещества, выход 93%, из 1 бром-2,4-дифторбензола по общему способу (I). MS m/e: 282 (М+). Эфир 4-ароилциклогексанкарбоновой кислоты 4. Метиловый эфир транс-4-(2,5-дифторбензоил)циклогексанкарбоновой кислоты Указанное в заголовке соединение получали в виде бесцветного масла, выход 55%, из 1-бром-2,5 дифторбензол по общему способу (I). MS m/e: 282 (М+) Эфир 4-ароилциклогексанкарбоновой кислоты 5. Метиловый эфир транс-4-(3-фторпиридин-2-карбонил)циклогексанкарбоновой кислоты К раствору N,N,N',N'-тетраметилэтилендиамина (1,20 г, 10,3 ммоль) в диэтиловом эфире (50 мл) при -78C; добавляли 1,6 М раствор н-бутиллития в н-гексане (6,40 мл, 10,3 ммоль). Перемешивали в течение 1 ч при -20C, после чего добавляли 3-фторпиридин (1,00 г, 10,3 ммоль) при -78C. После перемешивания при (-60)-(-70)C в течение 3 ч добавляли по каплям раствор хлорида цинка (2,81 г, 20,6 ммоль),предварительно высушенного плавлением в вакууме с последующим охлаждением в атмосфере аргона, в диэтиловом эфире (20 мл) при максимальной температуре -60C. Реакционную смесь оставляли нагреться до комнатной температуры в течение 45 мин после окончания внесения. Добавляли тетракис(трифенилфосфин)палладий(0) (0,59 г, 0,51 ммоль) и метиловый эфир транс-4-хлоркарбонил- 26021495 циклогексанкарбоновой кислоты (2,10 г, 10,3 ммоль) и перемешивали в течение 16 ч. Реакционную смесь гасили с помощью водного насыщенного раствора хлорида аммония и экстрагировали смесь тремя порциями по 100 мл трет-бутилметилового эфира. Объединенные органические слои промывали одной порцией 50 мл 2 М водного раствора карбоната натрия и одной порцией 50 мл солевого раствора, высушивали над безводным сульфатом натрия и концентрировали досуха. При разделении с помощью флэшхроматографии с использованием н-гептана/этилацетата в качестве элюента получали метиловый эфир транс-4-(3-фторпиридин-2-карбонил)циклогексанкарбоновой кислоты (0,22 г, 7,9%) в виде желтого масла и метиловый эфир транс-4-(3-фторпиридин-4-карбонил)циклогексанкарбоновой кислоты (0,23 г, 8,4%) в виде желтого твердого вещества. Метиловый эфир транс-4-(3-фторпиридин-2-карбонил)циклогексанкарбоновой кислоты. MS m/e: 266 ([М+Н]+). Метиловый эфир транс-4-(3-фторпиридин-4-карбонил)циклогексанкарбоновой кислоты. MS m/e: 266 ([М+Н]+). Эфир 4-ароилциклогексанкарбоновой кислоты 7. Метиловый эфир транс-4-(2-хлорпиридин-3-карбонил)циклогексанкарбоновой кислоты К смеси хлорида лития (0,55 г, 13 ммоль) и стружек магния (0,63 г, 26 ммоль) в сухом тетрагидрофуране (34 мл) добавляли 1 М раствора гидрида диизобутилалюминия в тетрагидрофуране (0,10 мл, 0,10 ммоль) при комнатной температуре. После перемешивания в течение 5 мин добавляли раствор 3-бром-2 хлорпиридина (2,00 г, 10,4 ммоль) в сухом тетрагидрофуране (1 мл) при 0-5C. После перемешивания в течение 1 ч добавляли раствор хлорида цинка (1,42 г, 10,4 ммоль), предварительно высушенного плавлением в вакууме с последующим охлаждением в атмосфере аргона, в сухом тетрагидрофуране (10 мл). После перемешивания в течение 1 ч смесь декантировали в другую колбу путем канюляции в атмосфере аргона. После добавления тетракис(трифенилфосфин)палладия(0) (0,59 г, 0,51 ммоль) и метилового эфира транс-4-хлоркарбонилциклогексанкарбоновой кислоты (2,10 г, 10,3 ммоль) перемешивали при комнатной температуре в течение 18 ч. Смесь делили между слоями этилацетата (150 мл) и 0,1 М водного раствора хлороводорода (100 мл). Слои разделяли. Водный слой экстрагировали двумя порциями по 100 мл этилацетата. Объединенные органические слои высушивали над безводным сульфатом натрия и концентрировали досуха. При очистке с помощью флэш-хроматографии с н-гептаном/трет-бутилметиловым эфиром в качестве элюента получали указанное в заголовке соединение (1,3 г, 46%) в виде желтого твердого вещества. MS m/e: 282 ([М+Н]+). Промежуточный оксим формулы (VII). Общий способ (II): получение оксима. Смесь эфира 4-ароилциклогексанкарбоновой кислоты формулы VI (1 экв.), ацетата натрия (2,4 экв.) и гидрохлорида гидроксиламина (2,4 экв.) в спирте, например в метаноле или этаноле (0,1-0,2 М), перемешивают при комнатной температуре в течение 2-24 ч. Реакционную смесь, возможно, концентрируют досуха или сразу делят между слоями органического растворителя, такого как этилацетат или третбутилметиловый эфир, и 2 М водного раствора карбоната натрия. Слои разделяют. Водный слой экстрагируют одной или двумя порциями органического растворителя. Объединенные органические слои высушивают над безводным сульфатом натрия и концентрируют досуха. В результате очистки с помощью флэш-хроматографии получают промежуточный оксим формулы VII. Оксим 1 Метиловый эфир цис/транс-4-(2-фторфенил)-[(E/Z)-гидроксиимино]метилциклогексанкарбоновой кислоты Указанное в заголовке соединение получали в виде белого твердого вещества, выход 98%, из метилового эфира цис/транс-4-(2-фторбензоил)циклогексанкарбоновой кислоты (2:1) по общему способу (II). Указанное в заголовке соединение получали в виде грязно-белого твердого вещества, выход 97%,из метилового эфира транс-4-(2,4-дифторбензоил)циклогексанкарбоновой кислоты по общему способу Указанное в заголовке соединение получали в виде грязно-белого твердого вещества, выход 97%,из метилового эфира транс-4-(2,5-дифторбензоил)циклогексанкарбоновой кислоты по общему способу Указанное в заголовке соединение получали в виде грязно-белого твердого вещества, выход 97%,из метилового эфира транс-4-(3-фторпиридин-2-карбонил)циклогексанкарбоновой кислоты по общему способу (II). MS m/e: 281 ([М+Н]+). Оксим 5 Метиловый эфир транс-4-(2-хлорпиридин-3-ил)-[(E/Z)-гидроксиимино]метилциклогексанкарбоновой кислоты Указанное в заголовке соединение получали в виде оранжевого твердого вещества, выход 92%, из метилового эфира транс-4-(2-хлорпиридин-3-карбонил)циклогексанкарбоновой кислоты по общему способу (II). MS m/e: 297 ([М+Н]+). Промежуточный эфир 4-арилизоксазолциклогексанкарбоновой кислоты формулы (IX-1). Общий способ (III): получение арилизоксазола. К раствору промежуточного оксима соединения формулы VII (1 экв.) в тетрагидрофуране (0,1-0,2 М) добавляют трет-бутоксид калия (1,3 экв.) при 0C. Охлаждающую ванну убирают через 15 мин после окончания внесения и реакционную смесь перемешивают в течение 2-24 ч при комнатной температуре. Реакционную смесь делят между слоями органического растворителя, такого как этилацетат или третбутилметиловый эфир, и воды. Слои разделяют. Водный слой экстрагируют одной или двумя порциями органического растворителя. Объединенные органические слои высушивают над безводным сульфатом натрия и концентрируют досуха. В результате очистки с помощью флэш-хроматографии получают промежуточный эфир 4-арилизоксазолциклогексанкарбоновой кислоты формулы (IX-1). Эфир 4-арилизоксазолциклогексанкарбоновой кислоты 1. Метиловый эфир транс-4-(6-фторбензо[d]изоксазол-3-ил)циклогексанкарбоновой кислоты Указанное в заголовке соединение получали в виде светло-коричневого твердого вещества, выход количественный, из метилового эфира транс-4-(2,4-дифторфенил)-[(E/Z)-гидроксиимино]метилциклогексанкарбоновой кислоты по общему способу (III). MS m/e: 278 ([М+Н]+). Эфир 4-арилизоксазолциклогексанкарбоновой кислоты 2. Метиловый эфир транс-4-(5-фторбензо[d]изоксазол-3-ил)циклогексанкарбоновой кислоты Указанное в заголовке соединение получали в виде белого твердого вещества, выход 52%, из метилового эфира транс-4-(2,5-дифторфенил)-[(E/Z)-гидроксиимино]метилциклогексанкарбоновой кислоты по общему способу (III). MS m/e: 278 ([М+Н]+). Эфир 4-арилизоксазолциклогексанкарбоновой кислоты 3. Метиловый эфир транс-4-изоксазоло[4,5-b]пиридин-3-ил-циклогексанкарбоновой кислоты Указанное в заголовке соединение получали в виде грязно-белого твердого вещества, выход 71%,из метилового эфира транс-4-(3-фторпиридин-2-ил)-[(E/Z)-гидроксиимино]метилциклогексанкарбоновой кислоты по общему способу (III). MS m/e: 261 ([М+Н]+). Эфир 4-арилизоксазолциклогексанкарбоновой кислоты 4. Метиловый эфир транс-4-изоксазоло[5,4-b]пиридин-3-ил-циклогексанкарбоновой кислоты Указанное в заголовке соединение получали в виде белого твердого вещества, выход 46%, из метилового эфира транс-4(2-хлорпиридин-3-ил)-[(E/Z)-гидроксиимино]метилциклогексанкарбоновой кислоты по общему способу (III). MS m/e: 261 ([М+Н]+). Промежуточная 4-арилизоксазолциклогексанкарбоновая кислота формулы (Х-1). цис/транс-4-Бензо[d]изоксазол-3-ил-циклогексанкарбоновая кислота К раствору метилового эфира цис/транс-4-(2-фторфенил)-[(E/Z)-гидроксиимино]метилциклогексанкарбоновой кислоты (0,52 г, 1,9 ммоль) в сухом тетрагидрофуране (19 мл) добавляли метоксид натрия(0,13 г, 2,4 ммоль) при комнатной температуре. После перемешивания в течение 16 ч добавляли дополнительное количество метоксида натрия (0,13 г, 2,4 ммоль) и перемешивали в течение 1 ч при 60C. После охлаждения до комнатной температуры реакционную смесь делили между слоями трет-бутил- 29
МПК / Метки
МПК: A61P 13/12, A61K 31/5517, C07D 519/00, A61P 25/22, A61P 9/12, A61P 15/10, C07D 487/04, A61P 9/04, A61P 25/18, A61P 25/24, A61P 1/16, A61P 25/00
Метки: новые, качестве, применение, антагонисты, лекарственного, средства, рецептора
Код ссылки
<a href="https://eas.patents.su/30-21495-novye-antagonisty-receptora-v1a-i-ih-primenenie-v-kachestve-lekarstvennogo-sredstva.html" rel="bookmark" title="База патентов Евразийского Союза">Новые антагонисты рецептора v1a и их применение в качестве лекарственного средства</a>
Предыдущий патент: Диафрагма заданной пористости, способ ее изготовления и устройство для этого
Следующий патент: Лекарственный препарат, обладающий противовирусным и антибактериальным действием
Случайный патент: Пептид, стимулирующий регенерацию ткани печени, фармацевтическая композиция на его основе и способ ее применения












