Ингибиторы репликации вируса иммунодефицита человека
Номер патента: 19259
Опубликовано: 28.02.2014
Авторы: Фейдер Ли, Кавай Стивен, Карсон Ребека Дж., Ландри Серж, Лапланте Стивен, Халмос Тедди, Бейли Марри Д., Куломб Рене, Симоно Брюно, Билодо Франсуа, Паризьен Матьё, Морен Себастьен, Пупар Марк-Андре, Тсантризос Йюла С.
Формула / Реферат
1. Соединение формулы (I) и его атропоизомер, рацемат, энантиомер или диастереоизомер
в которой
R4 обозначает С6-10арил или Het, где каждый С6-10арил и Het необязательно содержит от 1 до 3 заместителей, каждый из которых независимо выбран из группы, включающей галоген, (С1-С6)алкил, (С1-С6)галогеналкил, (С3-С7)циклоалкил, -О(С1-С6)алкил, -S(С1-С6)алкил;
R6 и R7, каждый независимо, выбран из группы, включающей Н, галоген, (С1-С6)алкил; и
где Het обозначает 4-7-членный насыщенный, ненасыщенный или ароматический гетероцикл, содержащий от 1 до 4 гетероатомов, каждый из которых независимо выбран из О, N и S, или 7-14-членный насыщенный, ненасыщенный или ароматический гетерополицикл, содержащий, если это возможно, от 1 до 5 гетероатомов, каждый из которых независимо выбран из О, N и S;
или его фармацевтически приемлемая соль или сложный эфир, при условии, что упомянутое соединение не представляет собой соединения 1-7, где R4, R6 и R7 имеют следующие значения:
2. Соединение по п.1 или его фармацевтически приемлемая соль, в котором R4 обозначает Het, необязательно содержащий от 1 до 2 заместителей, каждый из которых независимо выбран из группы, включающей галоген, (C1-С3)алкил и O-(С1-С3)алкил.
3. Соединение по п.2 или его фармацевтически приемлемая соль, в котором R4 обозначает Het, необязательно содержащий от 1 до 2 заместителей, каждый из которых независимо выбран из группы, включающей Cl, F, CH3 и СН2СН3, где указанный Het обозначает 7-14-членный насыщенный, ненасыщенный или ароматический гетерополицикл, содержащий, если это возможно, от 1 до 2 гетероатомов, каждый из которых независимо выбран из группы, включающей О, N и S.
4. Соединение по п.1 или его фармацевтически приемлемая соль, в котором R4 выбран из группы, включающей
необязательно замещенный от 1 до 3 раз галогеном, (С1-С3)алкилом и О-(С1-С3)алкилом.
5. Соединение по п.4 или его фармацевтически приемлемая соль, в котором R4 выбран из группы, включающей
необязательно замещенный от 1 до 3 раз галогеном, (С1-С3)алкилом и О-(С1-С3)алкилом.
6. Соединение по любому из пп.1-5 или его фармацевтически приемлемая соль, в котором R6 обозначает Н, F, Cl или (С1-С2)алкил.
7. Соединение по п.6 или его фармацевтически приемлемая соль, в котором R6 обозначает Н или СН3.
8. Соединение по любому из пп.1-7 или его фармацевтически приемлемая соль, в котором R7 обозначает Н, F, Cl или СН3.
9. Соединение по п.8 или его фармацевтически приемлемая соль, в котором R7 обозначает Н или СН3.
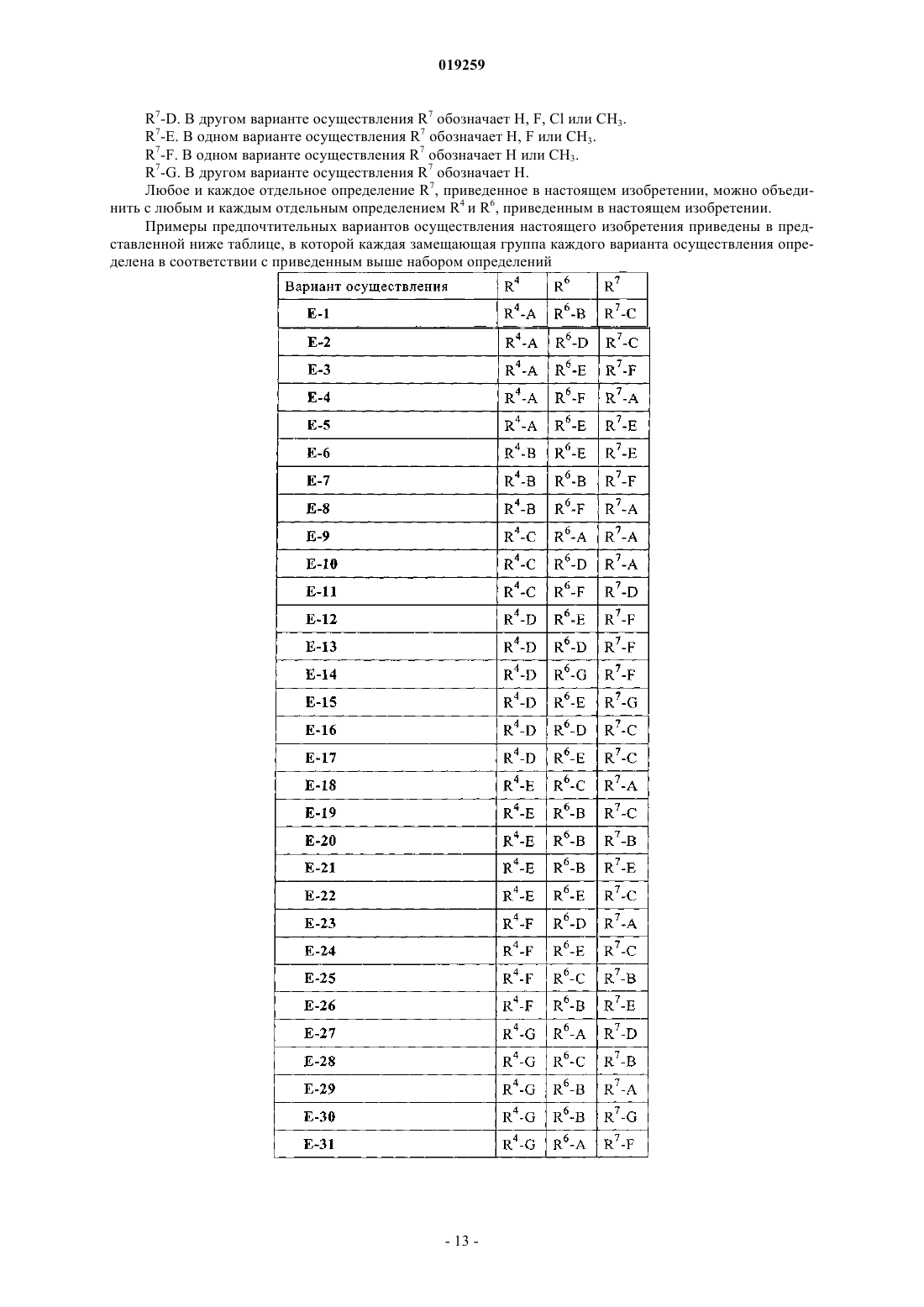
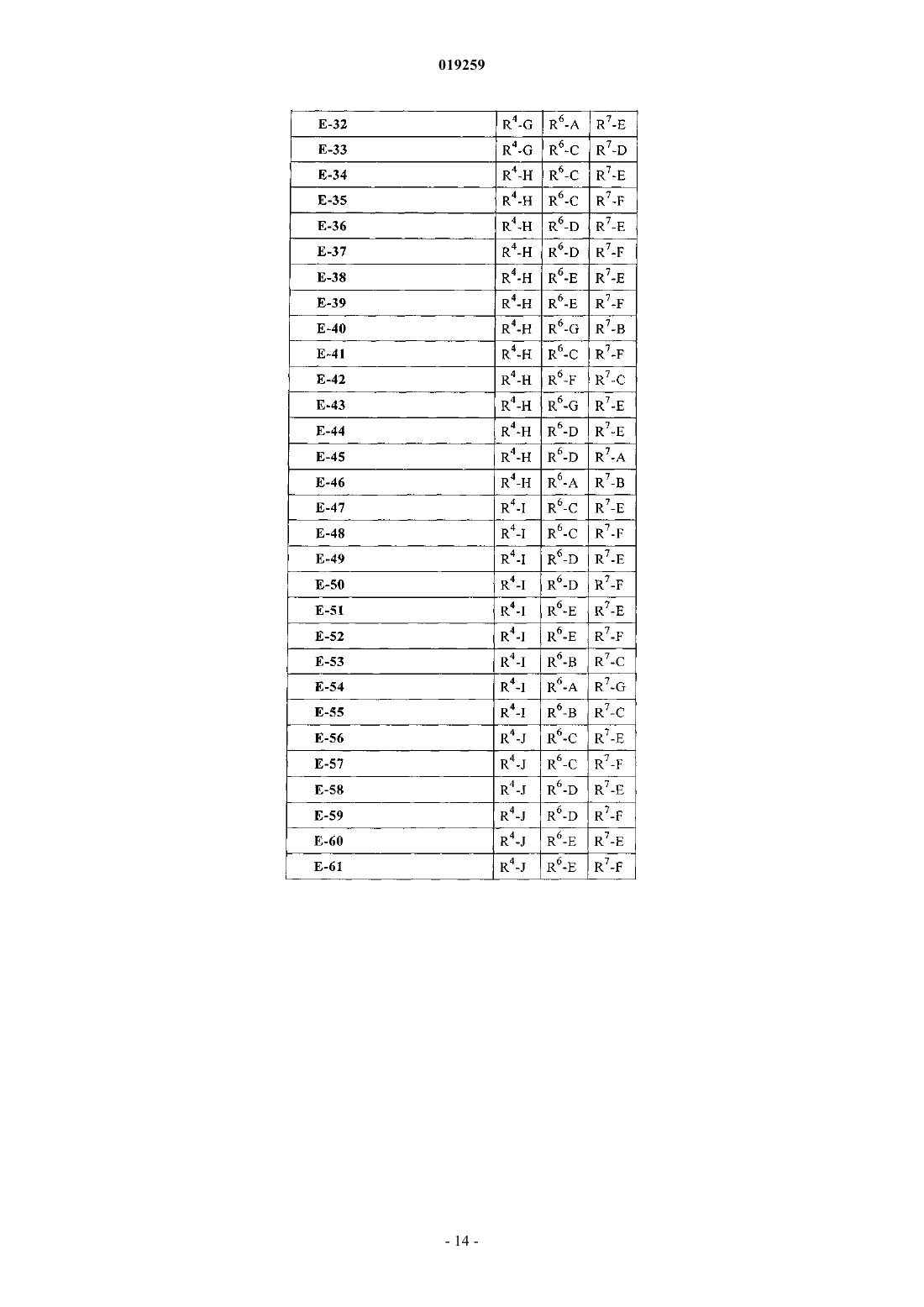
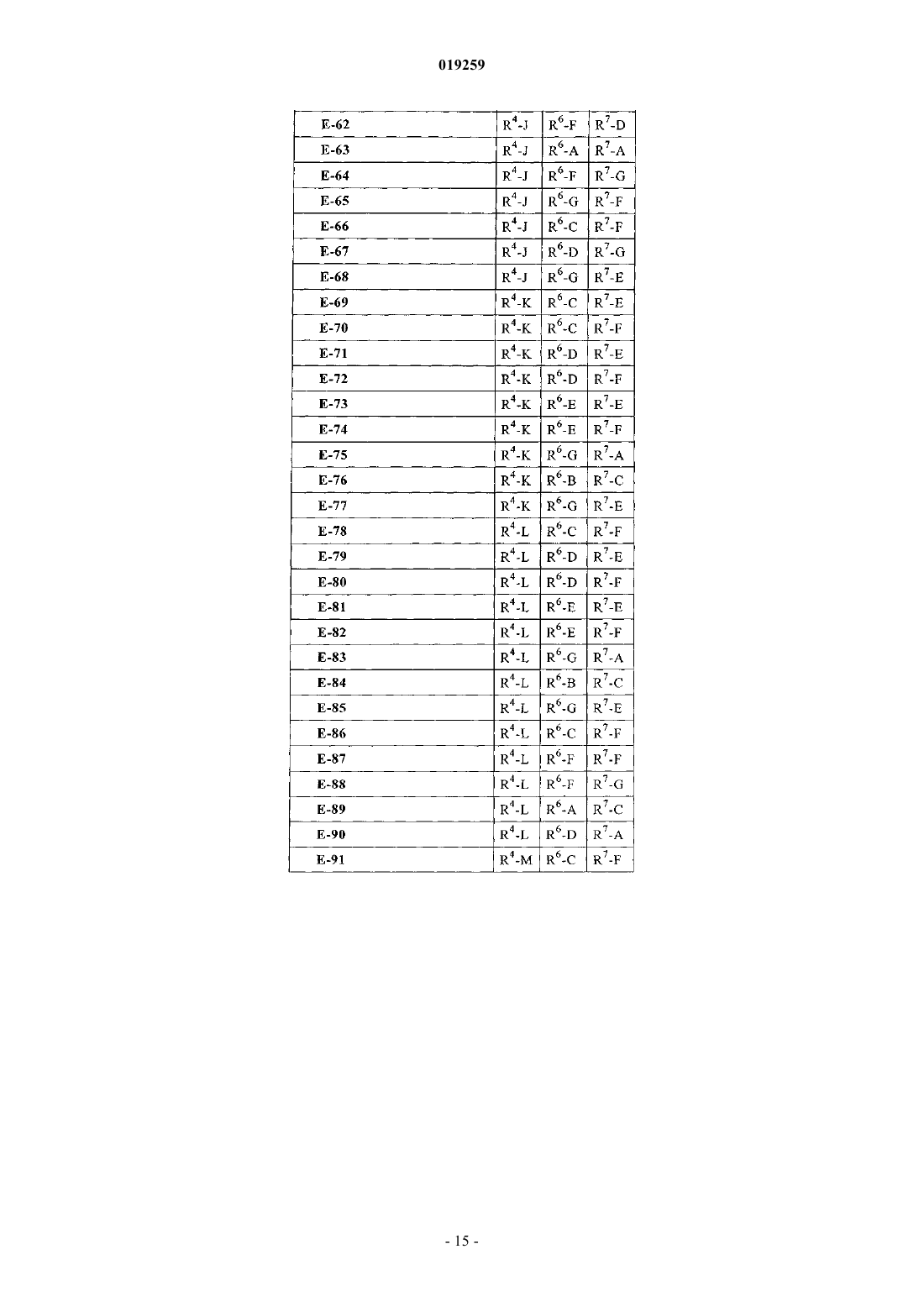
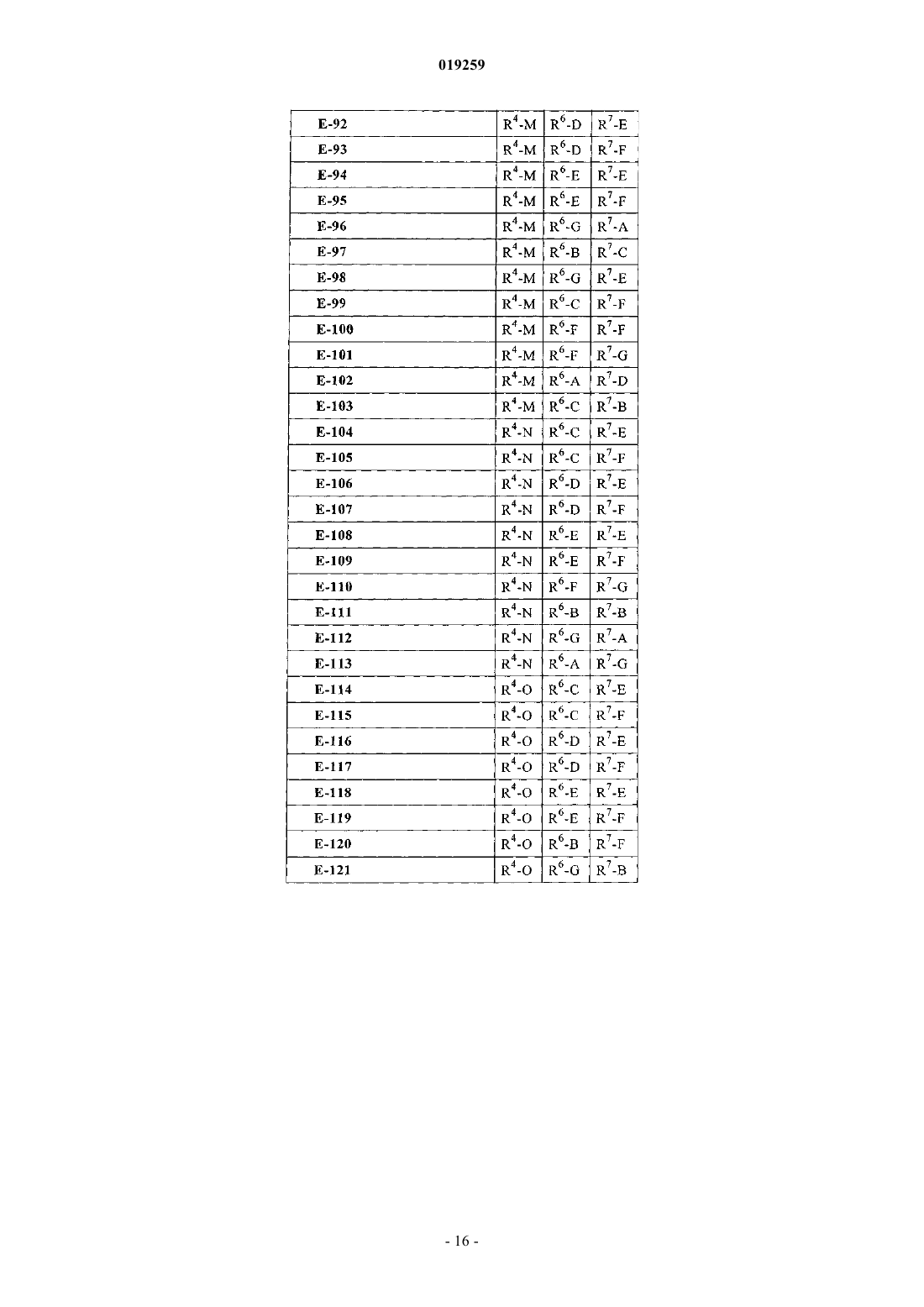
10. Соединение по п.1 формулы
в которой R4, R6 и R7 имеют следующие значения:
и его фармацевтически приемлемые соли или сложные эфиры.
11. Соединение по п.1 формулы
в которой R4, R6 и R7 имеют следующие значения:
и его фармацевтически приемлемые соли или сложные эфиры.
12. Соединение по п.1 формулы
в которой R4, R6 и R7 имеют следующие значения:
и его фармацевтически приемлемые соли или сложные эфиры.
13. Применение соединения формулы (I) по любому из пп.1-12 или его фармацевтически приемлемой соли или сложного эфира в качестве лекарственного средства.
14. Фармацевтическая композиция, включающая терапевтически эффективное количество соединения формулы (I) по любому из пп.1-12 или его фармацевтически приемлемую соль или сложный эфир и один или более фармацевтически приемлемых носителей.
15. Фармацевтическая композиция по п.14, дополнительно содержащая по меньшей мере одно другое противовирусное средство.
16. Применение соединения формулы (I) по любому из пп.1-12 или его фармацевтически приемлемой соли или сложного эфира для лечения и/или предупреждения ВИЧ-инфекции у млекопитающего.
Текст
ИНГИБИТОРЫ РЕПЛИКАЦИИ ВИРУСА ИММУНОДЕФИЦИТА ЧЕЛОВЕКА В изобретении описаны соединения формулы I в которой значения R4, R6 и R7 определены в настоящем изобретении, применимые в качестве ингибиторов репликации ВИЧ. Родственные заявки По настоящей заявке испрашивается приоритет по заявке U.S.60/988686, поданной 16 ноября 2007 г., которая включена в настоящее изобретение в качестве ссылки. Область техники, к которой относится изобретение Настоящее изобретение относится к соединениям, композициям и способам борьбы с инфицированием вирусом иммунодефицита человека (ВИЧ). В частности, настоящее изобретение относится к новым ингибиторам репликации ВИЧ, к фармацевтическим композициям, содержащим такие соединения, и способам применения этих соединений для лечения ВИЧ-инфекции. Точнее, настоящее изобретение относится к новым ингибиторам фермента ВИЧ-интегразы, к фармацевтическим композициям, содержащим такие соединения, и способам применения этих соединений для лечения ВИЧ-инфекции. Уровень техники Синдром приобретенного иммунодефицита (СПИД) вызывается вирусом иммунодефицита человека (ВИЧ), в частности штаммом ВИЧ-1. Большинство из утвержденных к применению современных средств лечения ВИЧ-инфекции воздействуют на ферменты вирусную ревертазу и протеазу. Имеется одно дополнительное утвержденное к применению лекарственное средство, воздействующее на gp41,подавляя проникновение вирусов. Затруднением является резистентность ВИЧ по отношению к имеющимся лекарственным средствам, входящим в группы ферментов ревертаз и протеаз. Поэтому важно обнаружить и использовать новые противоретровирусные соединения. Характерные генетические изменения самого ВИЧ привели к идентификации многих мутантов ВИЧ, обычно называющихся вариантами, у которых изменена восприимчивость к лекарственному средству. Для фермента интегразы установлено, что остатки 124 и 125 сильно изменчивы в вирусе ВИЧ-1 инфицированных пациентов в большинстве развитых и развивающихся стран. Для секвенированных вирусов, обнаруженных в основных развитых странах, содержащихся в базе данных Los Alamos(http://www.hiv.lanl.gov/content/hiv-db), основными преобладающими вариантами этой интегразы являются Thr124/Thr125 (44%), Ala124/Thr125 (17%), Ala124/Ala125 (16%), Thr124/Ala125 (10%), Asn124/Thr125(6%) и Asn124/Ala125 (1%). Эти варианты можно сгенерировать с помощью методик, известных в данной области техники, и общеизвестных полипептидных последовательностей для фермента интегразы,например из штамма NL4.3 интегразы ВИЧ-1 (SEQ ID NO: 1). Краткое изложение сущности изобретения Настоящее изобретение относится к новой группе соединений, обладающих способностью подавлять репликацию ВИЧ. Соединения, предлагаемые в настоящем изобретении, обладают сродством по отношению к ферменту ВИЧ-интегразе. Поэтому соединения, предлагаемые в настоящем изобретении,можно использовать для ингибирования активности ВИЧ-интегразы и можно использовать для ингибирования репликации ВИЧ. Соединения, предлагаемые в настоящем изобретении, обладают по меньшей мере одним из следующих неожиданных преимуществ: неожиданно высокой активностью по данным проводимого с использованием клеток анализа репликации ВИЧ-1 для четырех из главных вариантов интегразы по остаткам 124/125 (Thr124/Thr125,Ala124/Thr125, Ala124/Ala125 и Thr124/Ala125); и/или неожиданно высокой активностью по данным проводимого с использованием клеток анализа репликации ВИЧ-1 для всех шести главных вариантов интегразы по остаткам 124/125 (Thr124/Thr125,Ala124/Thr125, Ala124/Ala125, Thr124/Ala125, Asn124/Thr125 и Asn124/Ala125); и/или неожиданно хорошими фармакологическими характеристиками. Соединения, предлагаемые в настоящем изобретении, обладают неожиданно высокой активностью по отношению к четырем из главных вариантов интегразы по остаткам 124/125 (85% естественного содержания) и/или всем шести главным вариантам интегразы по остаткам 124/125. Значение этой неожиданно высокой наблюдающейся активности по отношению к указанным изменчивым остаткам 124/125 заключается в том, что для некоторых инфицированных посредством ВИЧ пациентов, у которых имеется вирус, содержащий варианты 124/125 остатков интегразы, и у которых наблюдается уже существующая резистентность по отношению к лекарственным средствам этого класса, можно ожидать наличие восприимчивости к соединениям, предлагаемым в настоящем изобретении. Другие объекты настоящего изобретения станут понятными для специалиста в данной области техники из последующего описания и примеров. Одним объектом настоящего изобретения является атропоизомер, рацемат, энантиомер или диастереоизомер соединений формулы (I)R4 обозначает С 6-10 арил или Het, где каждый С 6-10 арил и Het необязательно содержит от 1 до 3 заместителей, каждый из которых независимо выбран из группы, включающей галоген, (C1-C6)алкил, (C1C6)галогеналкил, (С 3-С 7)циклоалкил, -О(C1-C6)алкил, -S(C1-C6)алкил;R6 и R7, каждый независимо, выбран из группы, включающей Н, галоген, (C1-С 6)алкил; и где Het обозначает 4-7-членный насыщенный, ненасыщенный или ароматический гетероцикл, содержащий от 1 до 4 гетероатомов, каждый из которых независимо выбран из О, N и S, или 7-14-членный насыщенный, ненасыщенный или ароматический гетерополицикл, содержащий, если это возможно, от 1 до 5 гетероатомов, каждый из которых независимо выбран из О, N и S; или его фармацевтически приемлемая соль или сложный эфир. Другим объектом настоящего изобретения является соединение формулы (I) или его фармацевтически приемлемая соль или сложный эфир, обладающее по меньшей мере одним из следующих неожиданных преимуществ: неожиданно высокой активностью по данным проводимого с использованием клеток анализа репликации ВИЧ-1 для четырех из главных вариантов интегразы по остаткам 124/125 (Thr124/Thr125,Ala124/Thr125, Ala124/Ala125 и Thr124/Ala125); и/или неожиданно высокой активностью по данным проводимого с использованием клеток анализа репликации ВИЧ-1 для всех шести главных вариантов интегразы по остаткам 124/125 (Thr124/Thr125,Ala124/Thr125, Ala124/Ala125, Thr124/Ala125, Asn124/Thr125 и Asn124/Ala125); и/или неожиданно хорошими фармакологическими характеристиками. Другим объектом настоящего изобретения является применение соединения формулы (I) или его фармацевтически приемлемой соли или сложного эфира в качестве лекарственного средства. Еще одним объектом настоящего изобретения является фармацевтическая композиция, включающая в терапевтически эффективном количестве соединение формулы (I) или его фармацевтически приемлемую соль или сложный эфир; и один или более фармацевтически приемлемый носитель. В одном варианте осуществления этого объекта фармацевтическая композиция, предлагаемая в настоящем изобретении, дополнительно включает по меньшей мере одно другое противовирусное средство. В объем настоящего изобретения также входит применение соединения формулы (I), описанного в настоящем изобретении, или его фармацевтически приемлемой соли или сложного эфира для лечения ВИЧ-инфекции у млекопитающего. Подробное описание изобретения Определения При использовании в настоящем изобретении применяются приведенные ниже определения, если не указано иное. Термин "заместитель" при использовании в настоящем изобретении и, если не указано иное, означает атом, радикал или группу, которая может быть связана с атомом углерода, гетероатомом или любым другим атомом, который может быть частью молекулы или ее фрагмента и который в противном случае может быть связан по меньшей мере с одним атомом водорода. Заместители, находящиеся в конкретной молекуле или ее фрагменте, являются такими, которые приводят к химически стабильным соединениям,как это понимают специалисты в данной области техники. Термин "(C1-Cn)алкил" при использовании в настоящем изобретении, где n является целым числом,по отдельности или в комбинации с другим радикалом означает ациклические, обладающие линейной или разветвленной цепью алкильные радикалы, содержащие от 1 до n атомов углерода. "(C1-C6)алкил" включает, но не ограничивается только ими, метил, этил, пропил (н-пропил), бутил (н-бутил), 1 метилэтил (изопропил), 1-метилпропил (втор-бутил), 2-метилпропил (изобутил), 1,1-диметилэтил (третбутил), пентил и гексил. Аббревиатура Me означает метильную группу; Et означает этильную группу, Pr означает пропильную группу, iPr означает 1-метилэтильную группу, Bu означает бутильную группу иtBu означает 1,1-диметилэтильную группу. Термин "(C2-Cn)алкенил" при использовании в настоящем изобретении, где n является целым числом, по отдельности или в комбинации с другим радикалом означает ненасыщенный ациклический, обладающий линейной или разветвленной цепью радикал, содержащий от 2 до n атомов углерода, по меньшей мере два из которых связаны друг с другом двойной связью. Примеры таких радикалов включают, но не ограничиваются только ими, этинил (винил), 1-пропенил, 2-пропенил и 1-бутенил. Если не указано иное, термин (C2-Cn)алкенил" включает отдельные стереоизомеры, если это возможно, включая,но не ограничиваясь только ими, (Е) и (Z) изомеры и их смеси. Если (C2-Cn)алкенильная группа является замещенной, это означает, что она замещена по любому своему атому углерода, к которому в противном случае присоединен атом водорода, если не указано иное, так, чтобы замещение приводило к химически стабильному соединению, как это понимают специалисты в данной области техники. Термин "(C3-Cm)циклоалкил" при использовании в настоящем изобретении, где m является целым числом, по отдельности или в комбинации с другим радикалом означает циклоалкильный заместитель,содержащий от 3 до m атомов углерода и включает, но не ограничивается только ими, циклопропил,-2 019259 циклобутил, циклопентил, циклогексил и циклогептил. Термин "арил" при использовании в настоящем изобретении по отдельности или в комбинации с другим радикалом означает карбоциклическую ароматическую моноциклическую группу, содержащую 6 атомов углерода, которая может быть дополнительно сконденсирована со второй 5- или 6-членной карбоциклической группой, которая может быть ароматической, насыщенной или ненасыщенной. Арил включает, но не ограничивается только ими, фенил, инданил, инденил, 1-нафтил, 2-нафтил, тетрагидронафтил и дигидронафтил. Термин "карбоцикл" при использовании в настоящем изобретении по отдельности или в комбинации с другим радикалом означает циклическое соединение, ароматическое или неароматические, насыщенное или ненасыщенное, в котором все элементы кольца представляют собой атомы углерода. Карбоциклическая группа может содержать 5 или 6 атомов углерода и может быть дополнительно сконденсирована со второй 5- или 6-членной карбоциклической группой, которая может быть ароматической, насыщенной или ненасыщенной. Карбоцикл может быть замещенным. Если карбоцикл является замещенным, то заместители могут быть присоединены к любому атому углерода, к которому в противном случае присоединен атом водорода, если не указано иное, так, чтобы замещение приводило к химически стабильному соединению, как это понимают специалисты в данной области техники. Термин "Het" при использовании в настоящем изобретении по отдельности или в комбинации с другим радикалом означает 4-7-членный насыщенный, ненасыщенный или ароматический гетероцикл,содержащий от 1 до 4 гетероатомов, каждый из которых независимо выбран из О, N и S, или 7-14 членный насыщенный, ненасыщенный или ароматический гетерополицикл, содержащий, если это возможно, от 1 до 5 гетероатомов, каждый из которых независимо выбран из О, N и S, если не указано иное. Если группа Het является замещенной, это означает, что заместители могут быть присоединены к ее любому атому углерода или гетероатому, к которому в противном случае присоединен атом водорода, если не указано иное, так, чтобы замещение приводило к химически стабильному соединению, как это понимают специалисты в данной области техники. Термин "гетероатом" при использовании в настоящем изобретении означает О, S или N. Термин "гетероцикл" при использовании в настоящем изобретении и, если не указано иное, по отдельности или в комбинации с другим радикалом означает 3-7-членный насыщенный, ненасыщенный или ароматический гетероцикл, содержащий от 1 до 4 гетероатомов, каждый из которых независимо выбран из О, N и S; или одновалентный радикал, образованный из него путем удаления атома водорода. Примеры таких гетероциклов включают, но не ограничиваются только ими, азетидин, пирролидин, тетрагидрофуран, тетрагидротиофен, тиазолидин, оксазолидин, пиррол, тиофен, фуран, пиразол, имидазол,изоксазол, оксазол, изотиазол, тиазол, триазол, тетразол, пиперидин, пиперазин, азепин, диазепин, пиран,1,4-диоксан, 4-морфолин, 4-тиоморфолин, пиридин, пиридин-N-оксид, пиридазин, пиразин и пиримидин и их насыщенные, ненасыщенные и ароматические производные. Термин "гетерополицикл" при использовании в настоящем изобретении и, если не указано иное, по отдельности или в комбинации с другим радикалом означает гетероцикл, определенный выше, сконденсированный с одним или большим количеством других циклов, включая карбоцикл, гетероцикл или любой другой цикл; или одновалентный радикал, образованный из него путем удаления атома водорода. Примеры таких гетерополициклов включают, но не ограничиваются только ими, индол, изоиндол, бензимидазол, бензотиофен, бензофуран, бензопиран, бензодиоксол, бензодиоксан, бензотиазол, хинолин,изохинолин и нафтиридин и их насыщенные, ненасыщенные и ароматические производные. Термин "галоген" при использовании в настоящем изобретении означает галогенидный заместитель, выбранный из группы, включающей фтор, хлор, бром и йод. Термин "(C1-Cn)галогеналкил" при использовании в настоящем изобретении, где n является целым числом, по отдельности или в комбинации с другим радикалом означает алкильный радикал, содержащий от 1 до n атомов углерода, определенный выше, в котором один или большее количество атомов водорода содержат галогенидный заместитель. Примеры (C1-Cn)галогеналкила включают, но не ограничиваются только ими, хлорметил, хлорэтил, дихлорэтил, бромметил, бромэтил, дибромэтил, фторметил,дифторметил, трифторметил, фторэтил и дифторэтил. Термины "-О-(C1-Cn)алкил" или "(C1-Cn)алкоксигруппа" при использовании в настоящем изобретении, являющиеся взаимозаменяемыми, где n является целым числом, по отдельности или в комбинации с другим радикалом означают атом кислорода, дополнительно связанный с алкильным радикалом, содержащим от 1 до n атомов углерода, определенным выше. Примеры -О-(C1-Cn)алкила включают, но не ограничиваются только ими, метоксигруппу (CH3O-), этоксигруппу (СН 3 СН 2 О-), пропоксигруппу(трет-бутоксигруппу; (СН 3)3 С-О-). Если -O-(C1-Cn)алкильный радикал является замещенным, это означает, что он замещен по своему (C1-Cn)алкильному фрагменту так, чтобы замещение приводило к химически стабильному соединению, как это понимают специалисты в данной области техники. Термины "-S-(C1-Cn)алкил" или "(C1-Cn)алкилтиогруппа" при использовании в настоящем изобретении, являющиеся взаимозаменяемыми, где n является целым числом, по отдельности или в комбинации с другим радикалом означают атом серы, дополнительно связанный с алкильным радикалом, содержащим-3 019259 от 1 до n атомов углерода, определенным выше. Примеры -S-(C1-Cn)алкила включают, но не ограничиваются только ими, метилтиогруппу (CH3S-), этилтиогруппу (CH3CH2S-), пропилтиогруппу(трет-бутилтиогруппу; (СН 3)3 С-S-). Если -S-(C1-Cn)алкильный радикал или его окисленное производное,такое как -SO-(C1-Cn)алкильный радикал или -SO2-(C1-Cn)алкильный радикал, является замещенным, это означает, что он замещен по своему (C1-Cn)алкильному фрагменту так, чтобы замещение приводило к химически стабильному соединению, как это понимают специалисты в данной области техники. Термин "оксогруппа" при использовании в настоящем изобретении означает атом кислорода как заместитель, связанный с атомом углерода двойной связью (=O). Термин "цианогруппа" при использовании в настоящем изобретении означает атом углерода как заместитель, связанный с атомом азота тройной связью. Термин "эквивалентная функциональная группа" при использовании в настоящем изобретении означает атом или группу, которая может заменить другой атом или группу, которая обладает сходными электронными характеристиками, характеристиками гибридизации или связывания. Термин "защитная группа" при использовании в настоящем изобретении означает защитные группы, которые можно использовать при синтетических превращениях, включая, но не ограничиваясь только ими, примеры, которые приведены в публикации Greene, "Protective Groups in Organic Chemistry", JohnWileySons, New York (1981) и предыдущих ее изданиях, которая включена в настоящее изобретение в качестве ссылки. Следующее обозначение используется в субформулах для обозначения связи, которая образуется с оставшейся частью указанной молекулы в соответствии с определением. Термин "его соль" при использовании в настоящем изобретении означает любую соль присоединения с кислотой и/или с основанием соединения, предлагаемого в настоящем изобретении, включая, но не ограничиваясь только ею, его фармацевтически приемлемую соль. Термин "фармацевтически приемлемая соль" при использовании в настоящем изобретении означает соль соединения, предлагаемого в настоящем изобретении, которая по медицинским соображениям пригодна для применения с соприкосновением с тканями людей и низших животных без проявления нежелательной токсичности, раздражающего воздействия, аллергической реакции и т.п. при разумном соотношении преимущества/риск, обычно растворимую или диспергирующуюся в воде или масле и эффективную для применения по назначению. Термин включает фармацевтически приемлемые соли присоединения с кислотами и фармацевтически приемлемые соли присоединения с основаниями. Перечень подходящих солей приведен, например, в публикации S.M. Birge et al., J. Pharm. Sci., 1977, 66, pp. 1-19,которая включена в настоящее изобретение в качестве ссылки. Термин "фармацевтически приемлемая соль присоединения с кислотой" при использовании в настоящем изобретении означает такие соли, которые сохраняют биологическую эффективность и характеристики свободных оснований и которые не являются биологически или в другом отношении нежелательными, образующиеся с неорганическими кислотами, включая, но не ограничиваясь только ими, хлористо-водородную кислоту, бромисто-водородную кислоту, серную кислоту, сульфаминовую кислоту,азотную кислоту, фосфорную кислоту и т.п., и с органическими кислотами, включая, но не ограничиваясь только ими, уксусную кислоту, трифторуксусную кислоту, адипиновую кислоту, аскорбиновую кислоту, аспарагиновую кислоту, бензолсульфоновую кислоту, бензойную кислоту, масляную кислоту,камфорную кислоту, камфорсульфоновую кислоту, коричную кислоту, лимонную кислоту, диглюконовую кислоту, этансульфоновую кислоту, глутаминовую кислоту, гликолевую кислоту, глицерофосфорную кислоту, гемисульфиковую кислоту (hemisulfic acid), гексановую кислоту, муравьиную кислоту, фумаровую кислоту, 2-гидроксиэтансульфоновую кислоту (изетионовую кислоту), молочную кислоту, гидроксималеиновую кислоту, яблочную кислоту, малоновую кислоту, миндальную кислоту, мезитиленсульфоновую кислоту, метансульфоновую кислоту, нафталинсульфоновую кислоту, никотиновую кислоту, 2-нафталинсульфоновую кислоту, щавелевую кислоту, памоевую кислоту, пектиновую кислоту,фенилуксусную кислоту, 3-фенилпропионовую кислоту, триметилуксусную кислоту, пропионовую кислоту, пировиноградную кислоту, салициловую кислоту, стеариновую кислоту, янтарную кислоту, сульфаниловую кислоту, винную кислоту, п-толуолсульфоновую кислоту, ундекановую кислоту и т.п. Термин "фармацевтически приемлемая соль присоединения с основанием" при использовании в настоящем изобретении означает такие соли, которые сохраняют биологическую эффективность и характеристики свободных кислот и которые не являются биологически или в другом отношении нежелательными, образующиеся с неорганическими основаниями, включая, но не ограничиваясь только ими, аммиак или гидроксид, карбонат или бикарбонат аммония или катион металла, такого как натрий, калий, литий, кальций, магний, железо, цинк, медь, марганец, алюминий и т.п. Особенно предпочтительными являются соли аммония, калия, натрия, кальция и магния. Соли, образованные из фармацевтически приемлемых нетоксичных органических оснований, включают, но не ограничиваются только ими, соли первичных, вторичных и третичных аминов, четвертичные амины, замещенных аминов, включая природные замещенные амины, циклические амины и основные ионообменные смолы, такие как метиламин, диметиламин, триметиламин, этиламин, диэтиламин, триэтиламин, изопропиламин, трипропиламин, трибути-4 019259 ламин, этаноламин, диэтаноламин, 2-диметиламиноэтанол, 2-диэтиламиноэтанол, дихлоргексиламин,лизин, аргинин, гистидин, кофеин, гидрабамин, холин, бетаин, этилендиамин, глюкозамин, метилглюкамин, теобромин, пурины, пиперазин, пиперидин, N-этилпиперидин, тетраметиламмониевые соединения,тетраэтиламмониевые соединения, пиридин, N,N-диметиланилин, N-метилпиперидин, N-метилморфолин, дихлоргексиламин, дибензиламин, N,N-дибензилфенетиламин, 1-фенамин, N,N'-дибензилэтилендиамин, полиаминные смолы и т.п. Особенно предпочтительными органическими нетоксичными основаниями являются изопропиламин, диэтиламин, этаноламин, триметиламин, дихлоргексиламин, холин и кофеин. Термин "его сложный эфир" при использовании в настоящем изобретении означает сложный эфир соединения, предлагаемого в настоящем изобретении, в котором любой из заместителей -СООН в молекуле заменен на заместитель -COOR, в котором фрагментом R сложного эфира является любая углеродсодержащая группа, которая образует сложноэфирный фрагмент, включая, но не ограничиваясь только ими, алкил, алкенил, алкинил, циклоалкил, циклоалкилалкил, арил, арилалкил, гетероциклил, гетероциклилалкил, каждый из которых необязательно дополнительно замещен. Термин "его сложный эфир" включает, но не ограничивается только ими, его фармацевтически приемлемые сложные эфиры. Термин "фармацевтически приемлемый сложный эфир" при использовании в настоящем изобретении означает сложные эфиры соединения, предлагаемого в настоящем изобретении, в котором любой из заместителей -СООН в молекуле заменен на заместитель -COOR, в котором фрагмент R сложного эфира выбран из группы, включающей алкил (включая, но не ограничивается только ими, метил, этил, пропил,1-метилэтил, 1,1-диметилэтил, бутил); алкоксиалкил (включая, но не ограничивается только ими, метоксиметил); ацилоксиалкил (включая, но не ограничивается только ими, ацетоксиметил); арилалкил (включая, но не ограничивается только ими, бензил); арилоксиалкил (включая, но не ограничивается только ими, феноксиметил) и арил (включая, но не ограничивается только ими, фенил), необязательно замещенный галогеном, (C1-С 4)алкилом или (C1-C4)алкоксигруппой. Другие подходящие сложные эфиры приведены в публикации Design of Prodrugs, Bundgaard, H. Ed. Elsevier (1985), которая включена в настоящее изобретение в качестве ссылки. Такие фармацевтически приемлемые сложные эфиры обычно гидролизуются in vivo при инъекции млекопитающему и превращаются в кислотную форму соединения, предлагаемого в настоящем изобретении. В описанных выше сложных эфирах, если не указано иное, любой содержащийся алкильный фрагмент предпочтительно включает от 1 до 16 атомов углерода, более предпочтительно от 1 до 6 атомов углерода. Любой арильный фрагмент, содержащийся в таких сложных эфирах, предпочтительно включает фенильную группу. В частности, сложные эфиры могут представлять собой (C1-С 16)алкиловый сложный эфир, незамещенный бензиловый сложный эфир или бензиловый сложный эфир, замещенный по меньшей мере одним галогеном, (C1-С 6)алкилом, (C1-C6)алкоксигруппой,нитрогруппой или трифторметилом. Термин "млекопитающее" при использовании в настоящем изобретении означает людей, а также млекопитающих, не являющихся людьми, которые подвержены инфицированию ВИЧ. Млекопитающие,не являющиеся людьми, включают, но не ограничиваются только ими, домашних животных, таких как крупный рогатый скот, свиньи, лошади, кошки, кролики, крысы и мыши, и животных, не являющихся домашними. Термин "лечение" при использовании в настоящем изобретении означает введение соединения или композиции, предлагаемой в настоящем изобретении, для облегчения или устранения симптомов ВИЧинфекции и/или для уменьшения вирусной нагрузки пациента. Термин "лечение" также включает введение соединения или композиции, предлагаемой в настоящем изобретении, после воздействия вируса на индивидуума, но до появления симптомов заболевания и/или для предупреждения образования в крови обнаруживаемых концентраций вируса и введение соединения или композиции, предлагаемой в настоящем изобретении, для предупреждения перинатальной передачи ВИЧ от матери к младенцу путем введения матери до родов и младенцу в первые дни жизни. Термин "противовирусное средство" при использовании в настоящем изобретении означает средство, которое эффективно для ингибирования образования и/или репликации вируса у млекопитающего,включая, но не ограничиваясь только ими, средства, которые препятствуют действию механизмов хозяина или вируса, необходимых для образования и/или репликации вируса у млекопитающего. Термин "ингибитор репликации ВИЧ" при использовании в настоящем изобретении означает средство, способное уменьшать или устранять способность ВИЧ к репликации в клетках хозяина, in vitro, exvivo или in vivo. Термин "ВИЧ-интеграза" или "интеграза" используются в настоящем изобретении взаимозаменяемым образом и означают фермент интегразу, кодируемый вирусом иммунодефицита типа 1 человека. Термин "терапевтически эффективное количество" означает количество соединения, предлагаемого в настоящем изобретении, которое при введении нуждающемуся в нем пациенту является достаточным для лечения патологических состояний, заболеваний или нарушений, для которых применяются эти соединения. Такое количество должно быть достаточным для проявления биологической или медицинской реакции системы тканей или пациента, которых изучает исследователь или клиницист. Количество соединения, предлагаемого в настоящем изобретении, которое образует терапевтически эффективное ко-5 019259 личество, меняется в зависимости от таких факторов, как использующееся соединение и его биологическая активность, композиция, использующаяся для введения, время введения, путь введения, скорость выведения соединения, длительность лечения, тип подвергающегося лечению патологического состояния или нарушения и его тяжесть, лекарственные средства, использующиеся в комбинации с соединениями, предлагаемыми в настоящем изобретении, или совместно с ними, и возраст, масса тела, общее состояние здоровья, пол и диета пациента. Специалист с общей подготовкой в данной области техники может стандартным образом установить такое терапевтически эффективное количество на основе своей профессиональной подготовки, уровня техники и настоящего описания. Предпочтительные варианты осуществления В приведенных ниже предпочтительных вариантах осуществления подробно описаны группы и заместители соединений формулы (I)R4-А. В одном варианте осуществления R4 обозначает арил или Het, необязательно содержащий от 1 до 3 заместителей, каждый из которых независимо выбран из группы, включающей галоген, (С 1 С 6)алкил, (С 1-С 6)галогеналкил, (С 3-С 7)циклоалкил, -О(С 1-С 6)алкил, -S(С 1-С 6)алкил.R4-В. В другом варианте осуществления R4 обозначает Het, необязательно содержащий от 1 до 3 заместителей, каждый из которых независимо выбран из группы, включающей галоген, (C1-C6)алкил,(C1-C6)галогеналкил, (С 3-С 7)циклоалкил, -О(C1-C6)алкил, -S(C1-C6)алкил.R4-С. В другом варианте осуществления R4 обозначает нафтил или фенил, необязательно содержащий от 1 до 3 заместителей, каждый из которых независимо выбран из группы, включающей галоген,(C1-C4)алкил, (C1-С 4)галогеналкил, -О(C1-C4)алкил.R4-D. В другом варианте осуществления R4 обозначает фенил, необязательно содержащий от 1 до 3 заместителей, каждый из которых независимо выбран из группы, включающей галоген, (C1-C4)алкил,(C1-С 4)галогеналкил, -О(C1-C4)алкил.R4-Е. В одном варианте осуществления R4 обозначает Het, необязательно содержащий от 1 до 2 заместителей, каждый из которых независимо выбран из группы, включающей галоген, (C1-C3)алкил и О(C1-C3)алкил.R4-F. В одном варианте осуществления R4 обозначает Het, необязательно содержащий от 1 до 2 заместителей, каждый из которых независимо выбран из группы, включающей Cl, F, СН 3 и СН 2 СН 3, где указанный Het обозначает 7-14-членный насыщенный, ненасыщенный или ароматический гетерополицикл, содержащий, если это возможно, от 1 до 2 гетероатомов, каждый из которых независимо выбран из О, N и S.R4-G. В одном варианте осуществления R4 обозначает Het, необязательно содержащий от 1 до 2 заместителей, каждый из которых независимо выбран из группы, включающей галоген, (C1-C3)алкил и О(C1-C3)алкил, где указанный Het обозначает 9- или 10-членный насыщенный, ненасыщенный или ароматический гетерополицикл, содержащий, если это возможно, от 1 до 2 гетероатомов, каждый из которых независимо выбран из О, N и S.R4-Н. В другом варианте осуществления R4 обозначает фенил, необязательно содержащий от 1 до 3 заместителей, каждый из которых независимо выбран из группы, включающей галоген, (C1-C4)алкил,(C1-С 4)галогеналкил, -О(C1-C4)алкил, или R4 обозначает Het, необязательно содержащий от 1 до 3 заместителей, каждый из которых независимо выбран из группы, включающей галоген, (C1-C4)алкил и О-(C1C4)алкил, где указанный Het обозначает 7-14-членный насыщенный, ненасыщенный или ароматический гетерополицикл, содержащий, если это возможно, от 1 до 2 гетероатомов, каждый из которых независимо выбран из О, N и S.R4-I. В другом варианте осуществления R4 обозначает фенил, необязательно содержащий от 1 до 3 заместителей, каждый из которых независимо выбран из группы, включающей F, Cl, Br, -СН 3, -СН(СН 3)2,CH2F, -CH2CH2F, -ОСН 3, или R4 обозначает Het, необязательно содержащий от 1 до 3 заместителей, каждый из которых независимо выбран из группы, включающей Cl, F, СН 3, СН 2 СН 3 и ОСН 3, где указанныйHet обозначает 7- или 14-членный насыщенный, ненасыщенный или ароматический гетерополицикл,содержащий, если это возможно, от 1 до 3 гетероатомов, каждый из которых независимо выбран из О, N и S.R4-J. В другом варианте осуществления R4 выбран из группы, включающей необязательно замещенный от 1 до 3 раз галогеном, (C1-C3)алкилом и О-(C1-С 3)алкилом.R4-K. В другом варианте осуществления R4 выбран из группы, включающей необязательно замещенный от 1 до 2 раз галогеном, (C1-C3)алкилом и O-(C1-С 3)алкилом.R4-L. В другом варианте осуществления R4 выбран из группы, включающей необязательно замещенный от 1 до 2 раз галогеном, (C1-C3)алкилом и О-(C1-С 3)алкилом.R4-М. В другом варианте осуществления R4 выбран из группы, включающей необязательно замещенный от 1 до 2 раз галогеном, (C1-C3)алкилом и О-(С 1-С 3)алкилом.R4-N. В другом варианте осуществления R4 выбран из группы, включающейR4-О. В другом варианте осуществления R4 выбран из группы, включающей Специалист в данной области техники должен понимать, что, когда заместитель R4 замещен несимметрично относительно оси вращения связи, соединяющей R4 с ядром, возможны поворотные изомеры или атропоизомеры. Соединения, предлагаемые в настоящем изобретении, в которых заместитель R4 замещен несимметрично относительно оси вращения связи, соединяющей R3 с ядром, и в которых атом углерода, связанный с заместителями -СООН и R3, является хиральным, как это описано выше, будут содержать два хиральных центра, хиральный атом углерода содержит асимметричную ось вращения и поэтому атропоизомеры будут существовать в виде диастереоизомеров. Однако отдельные диастереоизомерные атропоизомеры могут быть или не быть обнаруживающимися и/или разделяющимися в зависимости от относительных количеств каждого атропоизомера, содержащегося при равновесии, и степени стерической заторможенности вращения вокруг хиральной оси С-4 и, таким образом, от скорости, с которой происходит вращение, приводящее к взаимопревращению этих атропоизомеров. После разделения отдельные атропоизомеры могут быстро или медленно превращаться друг в друга с образованием равновесной смеси атропоизомеров.R4-Р. В другом варианте осуществления R4 выбран из группы, включающейR4-Q. В другом варианте осуществления R4 выбран из группы, включающейR4-R. В другом варианте осуществления R4 обозначает арил или Het, где каждый из арилов и Het необязательно содержит от 1 до 3 заместителей, независимо выбранных из группы, включающей галоген, (C1-C6)алкил, (C1-С 6)галогеналкил, (С 3-С 7)циклоалкил, -О(C1-C6)алкил, -S(C1-C6)алкил; где арил не является монозамещенным в пара-положении. Любое и каждое отдельное определение R4, приведенное в настоящем изобретении, можно объединить с любым и каждым отдельным определением R6 и R7, приведенным в настоящем изобретении.R6-А. В одном варианте осуществления R6 обозначает Н, галоген, (С 1-С 6)алкил.R6-В. В другом варианте осуществления R6 обозначает Н, галоген или (С 1-С 3)алкил.R6-С. В другом варианте осуществления R6 обозначает Н, F, Cl или (C1-С 2)алкил.R6-D. В другом варианте осуществления R6 обозначает Н, F, Cl или СН 3.R6-Е. В другом варианте осуществления R6 обозначает Н, СН 3 или СН 2 СН 3.R6-F. В другом варианте осуществления R6 обозначает Н или СН 3.R6-G. В другом варианте осуществления R6 обозначает Н. Любое и каждое отдельное определение R6, приведенное в настоящем изобретении, можно объединить с любым и каждым отдельным определением R4 и R7, приведенным в настоящем изобретении.R7-А. В одном варианте осуществления R7 обозначает Н, галоген, (C1-С 6)алкил.R7-В. В другом варианте осуществления R7 обозначает Н, галоген или (C1-С 3)алкил.R7-С. В другом варианте осуществления R7 обозначает Н, F, Cl или (С 1-С 2)алкил.R7-D. В другом варианте осуществления R7 обозначает Н, F, Cl или СН 3.R7-Е. В одном варианте осуществления R7 обозначает Н, F или СН 3.R7-F. В одном варианте осуществления R7 обозначает Н или СН 3.R7-G. В другом варианте осуществления R7 обозначает Н. Любое и каждое отдельное определение R7, приведенное в настоящем изобретении, можно объединить с любым и каждым отдельным определением R4 и R6, приведенным в настоящем изобретении. Примеры предпочтительных вариантов осуществления настоящего изобретения приведены в представленной ниже таблице, в которой каждая замещающая группа каждого варианта осуществления определена в соответствии с приведенным выше набором определений Примерами наиболее предпочтительных соединений, предлагаемых в настоящем изобретении, являются все отдельные соединения, перечисленные в приведенной ниже табл. 1. Обычно подразумеваются все таутомерные и изомерные формы и их смеси, например отдельные таутомеры, геометрические изомеры, стереоизомеры, атропоизомеры, энантиомеры, диастереоизомеры,рацематы, рацемические и нерацемические смеси стереоизомеров, смеси диастереоизомеров или смеси любых из указанных выше форм химических структур или соединений, если в названии соединения или структуре специально не указана стереохимия или изомерная форма. В данной области техники хорошо известно, что биологическая и фармакологическая активность соединения сильно зависит от стереохимической конфигурации соединения. Так, например, энантиомеры часто обладают сильно различающейся биологической активностью, включая различия фармакокинетических характеристик, включая метаболизм, связывание с белком и т.п., и фармакологических характеристик, включая тип проявляющейся активности, степень активности, токсичность и т.п. Поэтому специалист в данной области техники должен понимать, что один энантиомер может быть более активным или может оказывать более благоприятное воздействие при содержании, превышающем содержание другого энантиомера, или когда он отделен от другого энантиомера. Кроме того, специалист в данной области техники на основании настоящего описания и подготовки в данной области техники должен понимать, как отделить, обогатить или селективно получить энантиомеры соединений, предлагаемых в настоящем изобретении. Получение чистых стереоизомеров, например энантиомеров и диастереоизомеров,или смесей с необходимым энантиомерным избытком (ЭИ) или энантиомерной чистотой проводят по одной или большему количеству следующих методик (а) выделения или разделения энантиомеров или- 17019259 комбинаций. Методики разделения обычно основаны на хиральном распознавании и включают, например, хроматографию с использованием хиральных стационарных фаз, энантиоселективного комплексообразования хозяин-гость, разделения или синтеза с использованием хиральных вспомогательных веществ, энантиоселективного синтеза, ферментативного и неферментативного кинетического разделения или самопроизвольной энантиоселективной кристаллизации. Такие методики в целом описаны в публикациях Chiral Separation Techniques: A Practical Approach (2nd Ed.), G. Subramanian (ed.), Wiley-VCH,2000; Т.Е. Beesley и R.P.W. Scott, Chiral Chromatography, John WileySons, 1999; and Satinder Ahuja,Chiral Separations by Chromatography, Am. Chem. Soc, 2000, включенных в настоящее изобретение в качестве ссылок. Кроме того, также существуют методики количественного определения энантиомерного избытка и чистоты, например ГХ (газовая хроматография), ВЭЖХ (высокоэффективная жидкостная хроматография), КЭ (капиллярный электрофорез) и ЯМР (спектроскопия ядерного магнитного резонанса), и определения абсолютной конфигурации и конформации, например КД (круговой дихроизм), ДОВ (дисперсия оптического вращения), рентгенография кристаллов и ЯМР. Фармацевтическая композиция Соединения, предлагаемые в настоящем изобретении, можно вводить млекопитающим, нуждающимся в лечении ВИЧ-инфекции, в виде фармацевтической композиции, включающей в терапевтически эффективном количестве соединение, предлагаемое в настоящем изобретении, или его фармацевтически приемлемую соль или сложный эфир; и один или более обычных нетоксичных фармацевтически приемлемых носителей, вспомогательных веществ или разбавителей. Конкретный состав композиции зависит от растворимости и химической природы соединения, выбранного пути введения и стандартной фармацевтической практики. Фармацевтическую композицию, предлагаемую в настоящем изобретении, можно вводить перорально или системно. Если один энантиомер хирально активного ингредиента обладает не такой биологической активностью, как другой, то подразумевается, что фармацевтическая композиция, предлагаемая в настоящем изобретении, может включать рацемическую смесь активного ингредиента, смесь, обогащенную одним энантиомером активного ингредиента, или чистый энантиомер активного ингредиента. Предполагается,что смесь, обогащенная одним энантиомером активного ингредиента, содержит от более 50 до примерно 100% одного энантиомера активного ингредиента и от примерно 0 до менее 50% другого энантиомера активного ингредиента. Предпочтительно, если композиция включает смесь, обогащенную одним энантиомером активного ингредиента, или чистый энантиомер активного ингредиента, так чтобы композиция включала от более 50 до примерно 100% физиологически более активного энантиомера и/или менее токсичного энантиомера. Хорошо известно, что один энантиомер активного ингредиента может быть физиологически более активным при одном терапевтическом показании, а другой энантиомер активного ингредиента может быть физиологически более активным при другом терапевтическом показании; поэтому предпочтительные энантиомерные составы фармацевтической композиции могут быть разными при использовании композиции при разных терапевтических показаниях. Для перорального введения соединение, или его фармацевтически приемлемую соль, или сложный эфир можно приготовить в виде любой перорально приемлемой дозированной формы, включая, но не ограничиваясь только ими, водные суспензии и растворы, капсулы, порошки, сиропы, эликсиры и таблетки. Для системного введения, включая, но не ограничиваясь только ими, подкожное, внутрикожное,внутривенное, внутримышечное, внутрисуставное, внутрисиновиальное, надчревное, внутриоболочечное и проводимое в пораженные ткани введения путем инъекции или вливания, предпочтительно использовать раствор соединения или его фармацевтически приемлемой соли или сложного эфира в фармацевтически приемлемом стерильном водном разбавителе. Фармацевтически приемлемые носители, вспомогательные вещества, разбавители, инертные наполнители и добавки, а также методики приготовления фармацевтических композиций, предназначенных для разных путей введения, хорошо известны специалистам в данной области техники и описаны в фармацевтических публикациях, таких как Remington: The Science and Practice of Pharmacy, 21st Edition,Lippincott WilliamsWilkins, 2005 и L.V. Allen, N.G. Popovish and H.C. Ansel, Pharmaceutical DosageForms and Drug Delivery Systems, 8th ed., Lippincott WilliamsWilkins, 2004, которые включены в настоящее изобретение в качестве ссылки. Вводимая доза зависит от известных факторов, включая, но не ограничиваясь только ими, активность и фармакодинамические характеристики конкретного использующегося соединения и режима,времени и пути введения; возраста, диеты, пола, массы тела и общего состояния здоровья реципиента; характера и тяжести симптомов; тяжести и протекания инфекции; типа сопутствующего лечения; частоты лечения; необходимого результата и решения лечащего врача. Обычно соединение наиболее предпочтительно вводить в дозе, которая обычно приводит к эффективному противовирусному воздействию без проявления каких-либо вредных побочных эффектов. Можно полагать, что суточная доза активного ингредиента составляет от примерно 0,001 до примерно 100 мг/(кг массы тела), а предпочтительная доза составляет от примерно 0,01 до примерно 50 мг/кг. Обычно фармацевтическую композицию, предлагаемую в настоящем изобретении, вводят от примерно 1 до примерно 5 раз в сутки или, альтернативно, в виде непрерывного вливания. Такое введение- 18019259 можно использовать в виде длительного или разового лечения. Количество активного ингредиента, которое можно комбинировать с носителями с получением разовой дозированной формы, меняется в зависимости от подвергающегося лечению реципиента и конкретного пути введения. Типичный препарат содержит от примерно 5 до примерно 95% активного соединения (мас./мас). Предпочтительно, если такие препараты содержат от примерно 20 до примерно 80% активного соединения. Поэтому в одном варианте осуществления фармацевтическая композиция, предлагаемая в настоящем изобретении, включает рацемическую смесь соединения формулы (I) или его фармацевтически приемлемой соли или сложного эфира. Альтернативный вариант осуществления относится к фармацевтической композиции, включающей смесь, обогащенную одним энантиомером соединения формулы (I) или его фармацевтически приемлемой соли или сложного эфира. Другой вариант осуществления относится к фармацевтической композиции, включающей чистый энантиомер соединения формулы (I) или его фармацевтически приемлемой соли или сложного эфира. Комбинированная терапия При комбинированной терапии соединение, предлагаемое в настоящем изобретении, или его фармацевтически приемлемую соль или сложный эфир вводят совместно по меньшей мере с одним дополнительным противовирусным средством. Дополнительные средства можно комбинировать с соединениями, предлагаемыми в настоящем изобретении, для приготовления разовой дозированной формы. Альтернативно, эти дополнительные средства можно вводить по отдельности, одновременно или последовательно в качестве части многокомпонентной дозированной формы. Если фармацевтическая композиция, предлагаемая в настоящем изобретении, включает комбинацию соединения, предлагаемого в настоящем изобретении, или его фармацевтически приемлемой соли или сложного эфира и одного или большего количества дополнительных противовирусных средств, то и соединение, и дополнительное средство должны содержаться в дозах, составляющих примерно от 10 до 100% и более предпочтительно примерно от 10 до 80% от дозы, обычно вводимой в режиме монотерапии. В случае синергетического взаимодействия между соединениями, предлагаемыми в настоящем изобретении, и дополнительным противовирусным средством или средствами, дозу любого перорального или всех активных средств, содержащихся в комбинации, можно уменьшить по сравнению с дозой,обычно вводимой в режиме монотерапии. Противовирусные средства, предназначенные для использования в такой комбинированной терапии, включают средства (соединения или биологические вещества), которые эффективно подавляют образование и/или репликацию вируса у млекопитающего, включая, но не ограничиваясь только ими, средства, которые оказывают мешающее воздействие на механизмы хозяина или вируса, необходимые для образования и/или репликации вируса у млекопитающего. Такие средства можно выбрать из группы,включающей ингибиторы NRTI (нуклеозидной или нуклеотидной ревертазы; включая, но не ограничиваясь только ими, зидовудин (AZT), диданозин (ddI), залцитабин (ddC), ставудин (d4T), ламивудин (3 ТС), эмтрицитабин, абакавирсукцинат, элвуцитабин, адефовирдипивоксил, лобукавир (BMS-180194), лоденосин(FddA) и тенофовир, включая тенофовирдизопроксил и тенофовирдизопроксилфумарат, Комбивир (содержит 3 ТС и AZT), Тризивир (содержит абакавир, 3 ТС и AZT), Трувада (содержит тенофовир и эмтрицитабин), Эпзиком (содержит абакавир и 3 ТС; ингибиторы NNRTI (ненуклеозидной ревертазы; включая, но не ограничиваясь только ими, невирапин, делавирадин, эфавиренц, этравирин и рилпивирин); ингибиторы протеазы (включая, но не ограничиваясь только ими, ритонавир, типранавир, саквинавир, нелфинавир, индинавир, ампренавир, фосампренавир, атазанавир, лопинавир, дарунавир (ТМС-114),ласинавир и бреканавир (VX-385; ингибиторы проникновения, включая, но не ограничиваясь только ими, антагонисты CCR5 (включая, но не ограничиваясь только ими, маравирок, викривирок, INCB9471 и TAK-652); антагонисты CXCR4 (включая но не ограничиваясь только ими, AMD-11070); ингибиторы слияния (включая, но не ограничиваясь только ими, энфувиртид (Т-20), TR1-1144 иTR1-999) и другие (включая, но не ограничиваясь только ими, BMS-488043); ингибиторы интегразы (включая, но не ограничиваясь только ими, ралтегравир (MK-0518), BMS707035 и элвитегравир (GS 9137; ингибиторы ТАТ; ингибиторы созревания (включая, но не ограничиваясь только ими, беривимат (РА-457; иммуномодулирующие средства (включая, но не ограничиваясь только ими, левамизол) и другие противовирусные средства (включая, но не ограничиваясь только ими, гидроксимочевину,рибаривин, IL-2, IL-12 и пензафузид). Кроме того, соединение, предлагаемое в настоящем изобретении, можно применять по меньшей мере с одним другим соединением, предлагаемым в настоящем изобретении, или с одним или большим- 19019259 количеством противогрибковых или антибактериальных средств (включая, но не ограничиваясь только ими, флуконазол). Поэтому в одном варианте осуществления фармацевтическая композиция, предлагаемая в настоящем изобретении, дополнительно включает одно или большее количество противовирусных средств. Другой вариант осуществления относится к фармацевтической композиции, предлагаемой в настоящем изобретении, в которой одно или более противовирусных средств включает по меньшей мере один NNRTI. В другом варианте осуществления фармацевтической композиции, предлагаемой в настоящем изобретении, одно или более противовирусных средств включает по меньшей мере один NRTI. В еще одном варианте осуществления фармацевтической композиции, предлагаемой в настоящем изобретении, одно или большее количество противовирусных средств включает по меньшей мере один ингибитор протеазы. В еще одном варианте осуществления фармацевтической композиции, предлагаемой в настоящем изобретении, одно или большее количество противовирусных средств включает по меньшей мере один ингибитор проникновения. В другом варианте осуществления фармацевтической композиции, предлагаемой в настоящем изобретении, одно или большее количество противовирусных средств включает по меньшей мере один ингибитор интегразы. Соединение, предлагаемое в настоящем изобретении, также можно использовать в качестве лабораторного реагента и реагента для научных исследований. Например, соединение, предлагаемое в настоящем изобретении, можно использовать в качестве положительного контроля для аттестации методик анализа, включая, но не ограничиваясь только ими, имитационные анализы с использованием клеток и исследования репликации вирусов in vitro или in vivo. Кроме того, соединение, предлагаемое в настоящем изобретении, можно использовать для борьбы с вирусным заражением материалов или его предупреждения и тем самым снижать опасность инфицирования вирусами персонала лаборатории и медицинского персонала или пациентов, соприкасающихся с такими материалами (например, кровью, тканями, хирургическими инструментами и одеждой, лабораторными приборами и одеждой и аппаратурой и материалами для сбора крови). Производные, включающие поддающуюся обнаружению метку. Производное соединения формулы (I) включает поддающуюся обнаружению метку. Такие метки обеспечивают распознавание, прямое или косвенное, производного, так что его можно обнаружить, исследовать и количественно определить. Поддающаяся обнаружению метка сама может поддаваться обнаружению, исследованию и количественному определению или она может взаимодействовать с одним или большим количеством других фрагментов, которые сами включают одну или большее количество поддающихся обнаружению меток, так что происходящее между ними взаимодействие позволяет обнаружить, исследовать и количественно определить производное. Такие соединения также можно использовать в качестве зондов при исследовании репликации ВИЧ, включая, но не ограничиваясь только ими, исследование механизма действия вирусных белков и белков хозяина, участвующих в репликации ВИЧ, исследование изменений конформации таких вирусных белков и белков хозяина при различных условиях и исследование взаимодействий с объектами, которые связываются с этими вирусными белками и белками хозяина или иным образом взаимодействуют с ними. Производные, предлагаемые в этом объекте настоящего изобретения, можно использовать при анализах для идентификации соединений, которые взаимодействуют с вирусными белками и белками хозяина, анализы включают, но не ограничиваются только ими, анализы вытеснения, при которых определяют степень замены производных вследствие взаимодействия с вирусными белками и белками хозяина. Такие производные также можно использовать для осуществления ковалентных и нековалентных взаимодействий с вирусными белками и белками хозяина или для идентификации остатков вирусных белков и белков хозяина, которые взаимодействуют с соединениями, предлагаемыми в настоящем изобретении. Поддающиеся обнаружению метки, предполагающиеся для применения с производными соединений, предлагаемых в настоящем изобретении, включают, но не ограничиваются только ими, флуоресцентные метки, хемолюминесцентные метки, хромофоры, антитела, ферментные маркеры, радиоактивные изотопы, метки сродства и фотохимически реакционноспособные группы. Флуоресцентная метка является меткой, которая флуоресцирует, испускает излучение одной длины волны после поглощения излучения другой длины волны. Флуоресцентные метки включают, но не ограничиваются только ими, флуоресцеин; Texas Red; аминометилкумарин; родаминовые красители, включая, но не ограничиваясь только ими, тетраметилродамин (TAMRA); красители Alexa, включая, но не ограничиваясь только ими, Alexa Fluor 555; цианиновые красители, включая, но не ограничиваясь только ими, Су 3; флуоресцирующие молекулы на основе европия или лантанидов и т.п. Хемолюминесцентная метка является меткой, которая может вступать в химическую реакцию с излучением света. Хемолюминесцентные метки включают, но не ограничиваются только ими, люминол,люциферин, люцигенин и т.п.- 20019259 Хромофор является меткой, которая селективно поглощает при некоторых длинах волн видимого света и пропускает или отражает при других, и поэтому соединения, которые содержат хромофор, выглядят цветными. Хромофоры включают, но не ограничиваются только ими, натуральные и синтетические красители. Антитело является белком, который образуется в иммунной системе в ответ на конкретный антиген, который специфически связывается с этим антигеном. Антитела, предполагающиеся для применения в качестве поддающихся обнаружению меток, предлагаемых в настоящем изобретении, включают, но не ограничиваются только ими, антитела против следующих объектов: полигистидиновые метки, глутатион-S-трансфераза (GST), гемагглютинин (ГА), эпитопные метки FLAG, метка Мус, связывающийся с мальтозой белок (СМБ), белок, обладающий зеленой флуоресценцией (БЗФ), и т.п. Ферментный маркер является ферментом, наличие которого можно определить с помощью методики анализа, специфичной для каталитической активности этого фермента. Ферментные маркеры, предполагающиеся для применения в качестве поддающихся обнаружению меток, предлагаемых в настоящем изобретении, включают, но не ограничиваются только ими, люциферазу, пероксидазу хрена (HRP), галактозидазу и т.п. Радиоактивный изотоп является изотопом атома, который при радиоактивном распаде испускает радиоактивное излучение. Радиоактивные изотопы включают, но не ограничиваются только ими, 14 С, 3 Н,31 Р, 121I, 125I и т.п. Метка сродства является меткой, которая обладает высоким сродством к другому фрагменту, обозначаемому в настоящем изобретении как компонент связывания. Такую метку сродства можно использовать для образования комплекса с компонентом связывания, так чтобы комплекс можно было селективно обнаружить или выделить из смеси. Метки сродства включают, но не ограничиваются только ими,биотин и его производное, полипептид гистидин, полиаргинин, фрагмент амилозного сахара или определенный эпитоп, распознаваемый специфическим антителом; подходящие эпитопы включают, но не ограничиваются только ими, глутатион-S-трансферазу (GST), гемагглютинин (ГА), эпитопные меткиFLAG, метку Мус, связывающийся с мальтозой белок (СМБ), белок, обладающий зеленой флуоресценцией, и т.п. Кроме того, соединения, предлагаемые в настоящем изобретении, использующиеся в качестве зондов, также можно снабдить использующейся в качестве метки фотохимически реакционноспособной группой, которая при активации светом преобразуется из инертной группы в реакционноспособную группу, такую как свободный радикал. Такие группы можно использовать для активации производного,так чтобы оно могло образовать ковалентную связь с одним или большим количеством остатков вирусного белка или белка хозяина. Фотохимически реакционноспособные группы включают, но не ограничиваются только ими, фотоаффинные метки, такие как бензофенон и азидные группы. Методология и синтез Синтез соединений формулы (I), предлагаемых в настоящем изобретении, предпочтительно проводить по описанной общей методике, представленной ниже на схемах, на которых R4, R6 и R7 являются такими, как определено в настоящем изобретении. Другие указания для специалиста в данной области техники приведены в конкретных примерах, представленных ниже в настоящем изобретении. Схема 1 Получение ингибиторов где R42, R43, R44, R45 и R46 могут являться заместителями фенильного фрагмента или (R42 и R43), (R43 иR44), (R44 и R45) или (R45 и R46) могут быть присоединены к фенильному фрагменту с образованием карбоцикла или гетероцикла, W обозначает йод, бром, хлор или OTf, Y обозначает В(ОН)2 или боронатные эфиры, такие как В(ОСН 3)2 и В(ОС(СН 3)2 С(СН 3)2 О), йод, SnR3, где R обозначает (C1-C6)алкил, ZnX, гдеX обозначает галоген, и Р обозначает защитную группу, такую как обычно использующиеся защитные группы для карбоновых кислот, включая, но не ограничиваясь только ими, метиловый или этиловый сложный эфир. Специалисты в данной области техники могут рассматривать несколько методик проведения реакций сочетания промежуточного продукта (I) (т.е. хинолинового ядра) и промежуточного продукта II (т.е. заместителя R4). Например, но не ограничиваясь только ими, реакция перекрестного сочетания Судзуки промежуточного производного бороновой кислоты или боронатного эфира II и промежуточного галоген- 21019259 или трифлатпроизводного I, катализируемая медью реакция перекрестного сочетания Ульмана промежуточных йодпроизводных I и II, реакция перекрестного сочетания Негиши промежуточного содержащего арилцинк реагента II и промежуточного йод- или трифлатпроизводного I и реакция перекрестного сочетания Стилле промежуточного содержащего арилолово реагента II и промежуточного бром- или йодпроизводного I, как показано выше, после омыления, могут приводить к образованию соединения формулы(I). Альтернативно, такие же методики проведения реакций перекрестного сочетания можно использовать при замене компонентов сочетания, как показано ниже. Например, реакции перекрестного сочетания типа Судзуки, Негиши и Стилле производного бороновой кислоты или боронатного эфира, содержащего арилцинк или арилолово производного промежуточного хинолина III и необходимого промежуточного йод-, бром-, хлор- или трифлатпроизводного IV после омыления, также могут приводить к образованию соединений формулы (I), предлагаемых в настоящем изобретенииR обозначает (C1-С 6)алкил, и ZnX, где X обозначает галоген. Кроме того, можно рассматривать последующую модификацию продукта, такую как превращение амина типа анилина в хлор- или бромзамещенное соединение по реакции Зандмайера, или алкилирование или дегалогенирование путем восстановления. Кроме того, как показано ниже, промежуточный продукт III можно использовать для реакций перекрестного сочетания биарила с декарбоксилированием, аналогичных описанным в публикации Forgione,Bilodeau and coworkers, J. Am. Chem. Soc. 2006, 128, 11350-11351, включенной в настоящее изобретение в качестве ссылки где W обозначает йод, бром, хлор или OTf, R может являться заместителем в кольце и Р является таким,как определено в настоящем изобретении. Существует целый ряд известных превращений, использующихся для получения хинолинового ядра. Как показано на схеме 1 А, можно использовать способ Фридландера, в котором соответствующим образом замещенный анилин вводят в реакцию конденсации с содержащим функциональную группу кетоном в безводной среде. Затем этот промежуточный продукт циклизуют при нагревании с последующим галогенированием полученного спирта. Как показано ниже, боковую цепь эфира уксусной кислоты можно окислить и ввести защитную группу с образованием фрагмента эфира -трет-бутоксиуксусной кислоты. Разделение энантиомеров можно провести с помощью образования диастереоизомеров путем добавления хирального вспомогательного вещества, такого как оксазолидинон, с последующим превращением в соответствующий сложный эфир по известным методикам. Альтернативно, как описано на схеме 2, для получения хинолинового ядра можно использовать модификацию этого способа. По этой методике соответствующим образом замещенное производное антраниловой кислоты можно ввести в реакцию конденсации в безводной среде с соответствующим кетоном с последующей циклизацией в присутствии смеси ДМАП (N,N-диметил-4-аминопиридин)/POCl3 и получить 4-хлорхинолин. Последующие превращения затем можно провести, как описано на схеме 1 А. Схема 2 Кроме того, альтернативно, хинолиновое ядро можно получить энантиоселективным способом, как описано на схеме 3. Схема 3- 23019259 Предшественник хинолина можно селективно бромировать в положении 3 с последующим превращением в хиральный диол по стандартным методикам, известным из литературы. В хиральный диол можно избирательно ввести защитную группу с образованием трет-бутилового эфира с последующим выделением первичного спирта. Затем этот спирт можно окислить с образованием соответствующей карбоновой кислоты с последующим введением защитной группы с образованием сложного метилового эфира и получить ключевой промежуточный хиральный 4-йодхинолин. Схема 4 Альтернативный синтез хинолинового ядра В альтернативном способе получения соединений общей формулы I известный альдегид VIa превращают во внутренний алкин VIb. Специалисты в данной области техники должны понимать, что существуют различные методики проведения этого превращения, такие как, но не ограничиваясь только ими,реакция Бестманна-Охира или реакция Кори-Фукса. Затем группу R4 присоединяют к алкину при условиях, хорошо известных специалистам в данной области техники, предпочтительно по реакции перекрестного сочетания Соногашира алкина и арилйодпроизводного R4, и получают внутренний алкин VIc. Другие методики могут включать реакцию Кастро-Стефенса или проводимую в присутствии серебра катализируемую палладием реакцию сочетания алкина VIb и производного бороновой кислоты или ее эфира R4,как описано в публикации Zou and coworkers (Tetrahedron Lett. 2003, 44, 8709-8711), с получением внутреннего алкина VIc. По этой методике соответствующим образом замещенный бензоилацетонитрил можно ввести в реакцию конденсации в присутствии серы с соответствующим кетоном или альдегидом по стандартным методикам, известным из литературы. Затем соединение VIc вводят в реакцию циклоконденсации с амидом VId и получают хинолин VIe. Специалисты в данной области техники должны понимать, что эта методика может включать активирование амида VId для облегчения полной конденсации. Активирование предпочтительно проводят путем обработки ангидридом трифторметансульфоновой кислоты и в присутствии 2-хлорпиридина, как описано в публикации Movassaghi (J. Am. Chem. Soc, 129(33), 10096-10097, 2007), но также можно проводить другими способами. Амиды VId обычно имеются в продаже, хотя специалисты в данной области техники должны понимать, что их также легко получить из имеющихся в продаже предшественников, анилина или нитроарена. Затем циклический дикеталь гидролизуют в кислой среде и получают диол VIf. Затем в концевой спирт вводят защитную группу и получают соединение VIg, где Р может являться одной из многих различных защитных групп, включая, но не ограничиваясь только ей, триметилацетильную группу. Затем вторичный спирт превращают в производное с трет-бутильной группой и получают соединение VIh. Специалисты в данной области техники должны понимать, что это превращение можно провести несколькими способами, включая реакцию SN1 или катализируемое кислотой присоединение к изобутилену. Затем защитную группу удаляют и получают первичный спирт VIj, который, в свою очередь, окисляют с образованием карбоновой кислоты VIk. Очевидно, что окисление соединения VIj с образованием соединения VIk можно провести по одно- или двустадийной реакции. В предпочтительной методике применяют окисление Десса-Мартина с образованием промежуточного альдегида с последующим окислением по Линдгрену.- 24019259 Схема 5 Альтернативный синтез хинолинового ядра В еще одном альтернативном способе получения соединений общей формулы I синтез промежуточного продукта VIh можно провести по схеме реакции, которая начинается с катализируемого кислотой гидролиза циклического дикеталя концевого алкина VIb с получением диола VIIa. Затем в концевой спирт вводят защитную группу и получают соединение VIIb, где Р может являться одной из многих различных защитных групп, включая, но не ограничиваясь только ей, триметилацетильную группу. Затем вторичный спирт превращают в производное с трет-бутильной группой и получают соединение VIIc. Специалисты в данной области техники должны понимать, что это превращение можно провести несколькими способами, включая реакцию SN1 или катализируемое кислотой присоединение к изобутилену. Затем к алкину присоединяют группу R4 при условиях, хорошо известных специалистам в данной области техники, предпочтительно по реакции перекрестного сочетания Соногашира алкина и арилйодпроизводного группы R4, и получают внутренний алкин VIId. Затем внутренний алкин VIId вводят в реакцию циклоконденсации с амидом VId и получают хинолин VIh, реакцию предпочтительно проводят путем обработки ангидридом трифторметансульфоновой кислоты и в присутствии 2-хлорпиридин, как описано на стадии 3 схемы 4. Затем из промежуточного продукта Vih по методикам, описанным на стадиях 7 и 8 схемы 4, проводят синтез соединений общей формулы I. Примеры Другие особенности настоящего изобретения станут понятными из приведенных ниже неограничивающих примеров, которые в качестве примеров иллюстрируют основные положения настоящего изобретения. Специалисту в данной области техники будет понятно, что приведенные ниже в качестве примеров методики с соответствующими изменениями можно использовать для получения других соединений, предлагаемых в настоящем изобретении, описанных в настоящем изобретении. Как хорошо известно специалисту в данной области техники, если нужно защитить компоненты реакции от воздействия воздуха или влаги, реакции проводят в инертной атмосфере (включая, но не ограничиваясь только ими, азот и аргон). Температуры приведены в градусах Цельсия (С). Если не указано иное, то выраженные в процентах содержания и отношения являются объемными. Флэш-хроматографию проводят на силикагеле (SiO2) по методике, описанной в публикации W.C. Still et al., J. Org. Chem.,(1978), 43, 2923. Macc-спектроскопические анализы проводят с помощью масс-спектрометрии с электрораспылением. Многие промежуточные продукты и конечные продукты очищают с использованием прибора CombiFlash Companion, приобретенного у фирмы Teledyne Isco Inc., с использованием предварительно заполненных картриджей с силикагелем и EtOAc и гексанов в качестве растворителей. Эти картриджи выпускаются фирмой Sililicycle Inc. (SiliaFlash, диоксид кремния 40-63 мкм) или фирмой Teledyne Isco (RediSep, диоксид кремния 40-63 мкм). Препаративную ВЭЖХ проводят при стандартных условиях на колонке с обращенной фазой SunFire Prep C18 OBD 5 мкм, 1950 мм, при элюировании в линейном градиентном режиме с использованием в качестве растворителей смесей 0,1% ТФК (трифторуксусная кислота)/ацетонитрил и 0,1% ТФК/вода. Соединения выделяют в виде солей с ТФК, если они применимы. Аналитическую ВЭЖХ проводят при стандартных условиях на колонке с обращенной фазой Combiscreen ODS-AQ С 18, YMC, 504,6 мм внутренний диаметр, 5 мкм, 120 при 220 нм, при элюировании в линейном градиентном режиме, как это описано в приведенной ниже таблице (растворителем А является 0,06% ТФК в Н 2 О; растворителем В является 0,06% ТФК в CH3CN)n-BuLi - н-бутиллитий; ЯМР - спектроскопия ядерного магнитного резонанса; ОП - оптическая плотность; ДОВ - дисперсия оптического вращения;Strep-EuK - меченый криптатом европия стрептавидин; трет-бутил или t-бутил - 1,1-диметилэтил; ТКЭФ - трис[2-карбоксиэтил]фосфин;Tf2O - ангидрид трифторметансульфоновой кислоты; ТФК - трифторуксусная кислота; ТГФ - тетрагидрофуран и ТСХ - тонкослойная хроматография. Пример 1. Синтез хинолинового ядра 1i Стадия 1. В 4-горлую круглодонную колбу объемом 500 мл, снабженную стержнем для магнитной мешалки,холодильником и ловушкой Дина-Штарка, добавляют диэтилацетилсукцинат (6 г, 0,026 моль), анилин 1 а(2,5 мл, 0,028 моль), Amberlyst 15 (0,08 г) и толуол (30 мл). Полученную смесь кипятят с обратным холодильником в течение примерно 3 дней, после этого ТСХ показывает наличие только следов ИВ. Реакционную смесь охлаждают до КТ и Amberlyst 15 удаляют фильтрованием. Фильтрат концентрируют в вакууме и получают суспензию твердого вещества в коричневой жидкости. Фильтрат разбавляют диэтиловым эфиром и охлаждают. Твердое вещество отфильтровывают и фильтрат концентрируют в вакууме и получают коричневое масло (7,8 г), которое содержит соединение 1b и небольшое количество циклизованного промежуточного продукта. Этот неочищенный промежуточный продукт используют на следующей стадии без дополнительной очистки. Стадия 2. 3-Горлую круглодонную колбу объемом 100 мл со смесью неочищенного промежуточного продукта 1b (7,8 г) и дифенилового эфира (50 мл) быстро нагревают в предварительно нагретом (250 С) нагревательном кожухе в течение 6 мин (внутренняя температура достигает 250 С), затем колбу удаляют из нагревательного кожуха и смесь перемешивают до тех пор, пока внутренняя температура не становится ниже 100 С. Затем реакционную смесь смешивают с гексаном (15 мл), при этом образуется светлокоричневое твердое вещество. Твердое вещество отфильтровывают и промывают гексаном (310 мл) и получают примерно 2,4 г циклизованного промежуточного продукта. Порцию этого образца (1,4 г, 5,87 ммоль) растворяют в оксихлориде фосфора (5 мл) и кипятят с обратным холодильником в течение 2,5 ч. Реакционную смесь охлаждают до КТ и концентрируют в вакууме. Остаток обрабатывают с помощью порошкообразного бикарбоната натрия, затем подвергают распределению между EtOAc и водой. Объединенный органический слой промывают рассолом, сушат над безводным Na2SO4, фильтруют, пропускают через слой силикагеля, концентрируют и получают соединение 1 с в виде неочищенного светлокоричневого твердого вещества (2,35 г). Стадия 3. Неочищенный хлорхинолин 1 с (1,36 г, 5,17 ммоль) растворяют в ТГФ (20 мл) и к этому раствору медленно добавляют раствор HCl в диоксане (4 М, 5,4 мл, 0,022 моль). Полученную реакционную смесь- 27019259 перемешивают при КТ в течение 40 мин. Затем растворитель удаляют в вакууме и остаток сушат в вакууме. Полученное твердое вещество и NaI (3,87 г) суспендируют в MeCN (20 мл) и полученную реакционную смесь кипятят с обратным холодильником в течение 16 ч. Реакционную смесь охлаждают до КТ и обрабатывают насыщенным водным раствором NaHCO3 (20 мл). Водный слой экстрагируют с помощью ДХМ и объединенный органический слой сушат над безводным MgSO4, фильтруют и концентрируют и получают коричневый сироп. Очистка с помощью хроматографии на силикагеле (30% EtOAc/гексаны) дает йодхинолин 1d в виде почти белого твердого вещества (1,72 г, выход 94%). Стадия 4. К раствору KHMDS (0,5 М раствор в толуоле, 3 мл, 1,5 ммоль) в ТГФ (8 мл) при -78 С добавляют раствор соединения 1d (0,35 г, 0,99 ммоль) в ТГФ (8 мл). После добавления сложного эфира раствор становится ярко-красным. Его перемешивают при -78 С в течение 30 мин, затем обрабатывают реагентом Дэвиса (0,39 г, 1,5 ммоль). После добавления окислительного реагента раствор становится бледножелтым и его перемешивают при -78 С в течение еще 30 мин. Реакцию останавливают насыщенным водным раствором NH4Cl (8 мл), смесь нагревают до КТ и разбавляют с помощью EtOAc. Смесь промывают рассолом и органическую фазу сушат (Na2SO4), фильтруют, концентрируют и получают твердое вещество. Очистка с помощью хроматографии на силикагеле (гексаны/EtOAc: 6/4) дает соединение 1 е в виде бежевого твердого вещества (0,50 г, выход 98%). Стадия 5. К суспензии йодзамещенного спирта 1 е (0,53 г, 1,4 ммоль) в трет-бутилацетате (12 мл) при КТ добавляют хлорную кислоту (0,66 мл, 4,6 ммоль). Реакционную смесь перемешивают при КТ в течение 2 ч(суспензия становится прозрачным раствором). Реакцию останавливают водой (12 мл) и смесь подкисляют твердым NaHCO3 до рН 6. Неочищенный продукт экстрагируют с помощью EtOAc (310 мл),промывают рассолом (10 мл), сушат над MgSO4, фильтруют, концентрируют и получают неочищенный продукт. Очистка с помощью хроматографии на силикагеле (гексаны/EtOAc: 85/15) дает соединение 1f в виде бледно-желтого масла (0,56 г, выход 91%). Стадия 6. Промежуточный продукт 1f (0,59 г, 1,4 ммоль) растворяют в 2 М водном растворе NaOH (7 мл, 0,014 моль) с этанолом (10 мл) и перемешивают при КТ в течение 4 ч. Затем этанол удаляют в вакууме. Полученный остаток разбавляют водой (3 мл) и подкисляют 2 М раствором HCl до рН 3-4. Затем остаток экстрагируют с помощью ДХМ (310 мл), сушат над Na2SO4, фильтруют, концентрируют, сушат в высоком вакууме и получают соединение 1g в виде вспененного твердого вещества (0,56 г, выход 98%). Стадия 7. К раствору кислоты 1g (0,39 г, 0,97 ммоль) и HBTU (0,48 г, 1,3 ммоль) в безводном ТГФ (5 мл) добавляют диизопропилэтиламин (0,5 мл, 2,9 ммоль). Смесь перемешивают при 30-35 С (внутренняя температура) в течение 5,5 ч, затем добавляют натриевую соль R-(+)-бензилоксазолидинона, который получают путем добавления гидрида натрия (60% дисперсия в минеральном масле, 78 мг, 1,95 ммоль) к раствору R-(+)-бензилоксазолидинона (0,35 г, 1,9 ммоль), в безводном ТГФ (5 мл). Затем полученный раствор перемешивают при КТ в течение 16 ч. Растворитель удаляют в вакууме и смесь подвергают распределению между водой и EtOAc. Затем водную фазу экстрагируют с помощью EtOAc и объединенные органические экстракты сушат над безводным Na2SO4, фильтруют, концентрируют в вакууме и получают бледно-желтое твердое вещество. Неочищенный продукт очищают с помощью хроматографии на силикагеле (10-30%EtOAc:гексаны) и получают искомый диастереоизомер 1h (190 мг, выход 35%, более полярный продукт,99% ЭИ (энантиомерный избыток) по данным хроматографии на хиральной колонке). Стадия 8. К раствору оксазолидинона 1h (190 мг, 0,34 ммоль) в смеси ТГФ/Н 2 О (2 мл/1 мл) при 0 С добавляют Н 2 О 2 (30%, 0,36 мл), затем моногидрат LiOH (17 мг, 0,41 ммоль), растворенный в воде (1 мл). Реакционную смесь перемешивают при 0 С в течение 30 мин, затем добавляют 10% раствор Na2SO3 (0,26 мл). Полученную смесь перемешивают в течение 10 мин и затем подкисляют 2 н. раствором HCl до рН 4-5. Затем продукт экстрагируют с помощью ДХМ (310 мл). Объединенные органические экстракты сушат над сульфатом натрия, концентрируют в вакууме и получают неочищенную промежуточную кислоту в виде белого вспененного вещества (0,13 г, выход 96%), которое используют на следующей стадии без дополнительной очистки. Кислоту (130 мг) суспендируют в диэтиловом эфире (3 мл) и обрабатывают диазометаном в диэтиловом эфире до полного израсходования исходной кислоты (по данным ТСХ). Реакцию останавливают небольшим количеством ледяной АсОН и затем смесь концентрируют в вакууме и получают почти белое твердое вещество. Неочищенный продукт, сложный эфир, очищают с помощью хроматографии на силикагеле (10-15% EtOAc/гексаны) и получают хинолиновый фрагмент 1i (120 мг,выход 89%), обладающий высокой энантиомерной чистотой (99% ЭИ по данным хиральной ВЭЖХ).K2CO3 (8,8 г, 64 ммоль) объединяют в МеОН (125 мл) и реакционную смесь перемешивают при КТ в течение ночи. Реакционную смесь выпаривают почти досуха и остаток подвергают распределению между Н 2 О (250 мл) и EtOAc (500 мл). Водный слой промывают с помощью EtOAc (2250 мл) и объединенные органические слои сушат над безводным Na2SO4, концентрируют и получают алкин 2 с (5,55 г, выход 97%). Стадия 2. Алкин 2 с (5,0 г, 25 ммоль) растворяют в ТФК (35 мл) и воде (3,6 мл) и раствор перемешивают при КТ. Через 30 мин реакционную смесь концентрируют при пониженном давлении и остаток очищают с помощью CombiFlash Companion и получают диол 2d (1,8 г, выход 84%). Стадия 3. Раствор диола 2d (1,2 г, 14 ммоль) и триэтиламина (1,7 мл, 12 ммоль) в ДХМ (80 мл) охлаждают до 0 С в атмосфере N2. По каплям добавляют триметилацетилхлорид и полученной смеси дают нагреться до КТ и ее перемешивают в течение ночи. Затем реакцию останавливают с помощью МеОН (100 мл) и перемешивание продолжают в течение 20 мин. Затем смесь концентрируют при пониженном давлении и остаток очищают с помощью CombiFlash Companion и получают желательный сложный моноэфир 2 е(550 мг, выход 40%), а также нежелательный региоизомерный сложный моноэфир (378 мг, выход 27%). Стадия 4. В герметизированной реакционной колбе раствор пропаргилового спирта 2 е (375 мг, 2,20 ммоль) и смолы Amberlyst H-15 (150 мг) в гексане (3 мл) охлаждают до -78 С. Затем через раствор пропускают изобутен до увеличения объема примерно в два раза. Затем колбу герметично закрывают, смесь нагревают до КТ и перемешивают в течение ночи. Затем колбу охлаждают до -78 С, открывают и повторно нагревают до КТ. Затем смесь фильтруют через слой SiO2 (промывая с помощью EtOAc), концентрируют при пониженном давлении и получают чистый трет-бутиловый эфир 2f (390 мг, выход 78%). Пример 3. Синтез алкина 3 а Стадия 1. Твердый Pd(PPh3)4 (444 мг, 0,385 ммоль) и CuI (146 мг, 0,769 ммоль) последовательно добавляют к раствору 6-йодхромана (10 г, 34 ммоль) и алкина 2 с (11 г, 55 ммоль) в ДМФ (23 мл) и диэтиламине (115 мл). Реакционную смесь перемешивают при КТ в течение ночи и затем концентрируют, разбавляют с помощью EtOAc (300 мл) и последовательно промывают рассолом, 1 н. водным раствором HCl и водой(по 300 мл каждого). Органический слой сушат над Na2SO4, остаток очищают с помощью CombiFlashCompanion и получают алкин 3 а (10,8 г, выход 84%). Пример 4. Синтез боронатного фрагмента 4f (используют для получения соединения 1086)
МПК / Метки
МПК: A61K 31/18, C07D 417/04, A61K 31/47, A61K 31/4709, C07D 215/14, C07D 413/04, A61K 31/538, C07D 401/04, C07D 409/04, C07D 405/04, C07D 491/06
Метки: ингибиторы, иммунодефицита, человека, вируса, репликации
Код ссылки
<a href="https://eas.patents.su/30-19259-ingibitory-replikacii-virusa-immunodeficita-cheloveka.html" rel="bookmark" title="База патентов Евразийского Союза">Ингибиторы репликации вируса иммунодефицита человека</a>
Предыдущий патент: Композиции, содержащие модуляторы фактора коагуляции viia, и их применение
Следующий патент: Способ сооружения защитной сетки против камнепада и тому подобного
Случайный патент: Механизм открытия и закрытия люка, преимущественно ниши шасси летательного аппарата