Энантиомерно чистые фосфоиндолы в качестве ингибиторов hiv
Номер патента: 16267
Опубликовано: 30.03.2012
Авторы: Мусса Адел М., Дуссон Кирил, Александр Франсуа-Рене, Бриджиз Эдвард, Сторер Ричард
Формула / Реферат
1. Соединение формулы (С) или его фармацевтически приемлемая соль
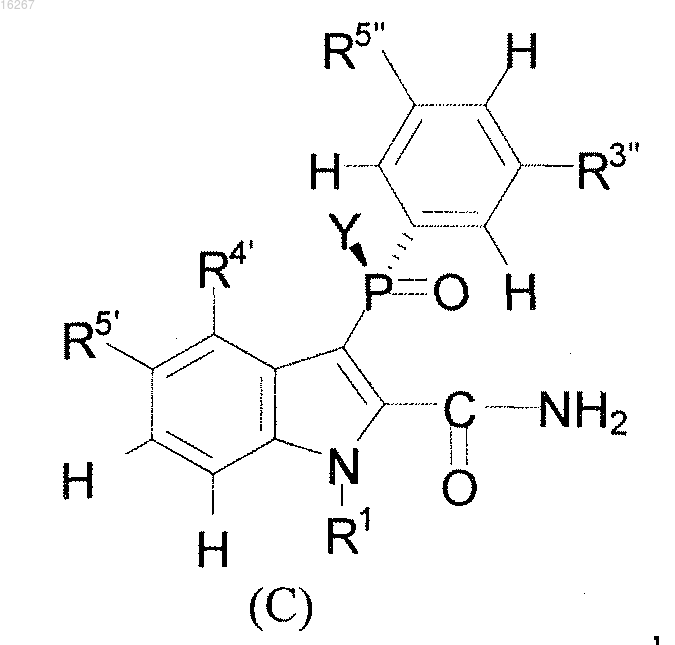
где R3¢¢ и R5¢¢ независимо представляют собой C1-6алкил или С2-6алкенил, каждый из которых может быть, возможно, независимо замещен CN или галогеном;
каждый из R4¢ и R5¢ независимо представляет собой водород или галоген;
R1 представляет собой водород, фенилсульфонил или 4-метоксибензил и
Y представляет собой О-С1-2алкил.
2. Соединение по п.1 формулы
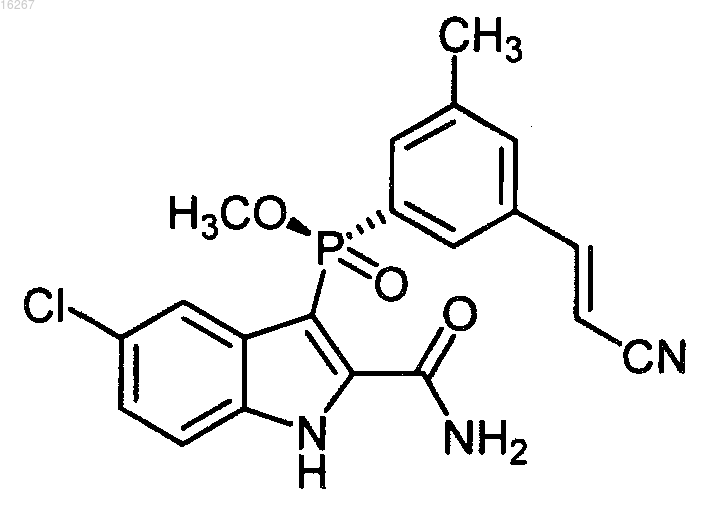
или его фармацевтически приемлемая соль.
3. Соединение по п.1 формулы
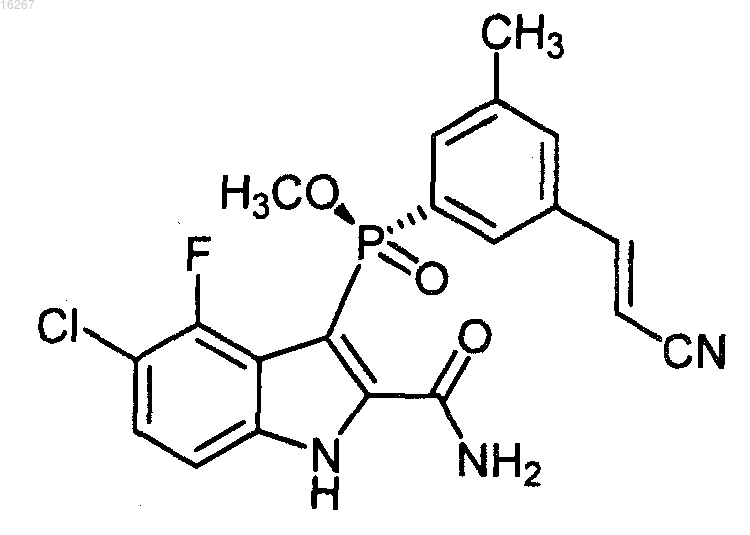
или его фармацевтически приемлемая соль.
4. Фармацевтически приемлемая соль соединения по любому из пп.1-3.
5. Фармацевтическая композиция, содержащая соединение по любому из пп.1-3 и фармацевтический носитель, эксципиент или разбавитель, где указанная композиция, по существу, не содержит противоположного энантиомера указанного соединения.
6. Фармацевтическая композиция, содержащая соединение по любому из пп.1-3 и второй агент против HIV (вирус иммунодефицита человека), где указанная композиция, по существу, не содержит противоположного энантиомера указанного соединения.
7. Фармацевтическая композиция по п.6, где второй агент против HIV представляет собой ингибитор протеазы или ингибитор интегразы.
8. Способ лечения инфекции HIV, включающий введение субъекту, нуждающемуся в этом, эффективного количества соединения по любому из пп.1-3.
9. Способ по п.8, дополнительно включающий введение субъекту соединения в комбинации или путем чередования, по меньшей мере, со вторым агентом против HIV.
10. Способ по п.9, где второй агент против HIV представляет собой ингибитор протеазы, нуклеозидный или нуклеотидный ингибитор обратной транскриптазы, ненуклеозидный ингибитор обратной транскриптазы, комбинацию с фиксированной дозой, ингибитор проникновения, антагонист корецептора CCR5, ингибитор созревания или ингибитор интегразы; где комбинацией с фиксированной дозой является комбинация нуклеозидных ингибиторов обратной транскриптазы с фиксированной дозой или комбинация нуклеозидного ингибитора обратной транскриптазы, нуклеотидного ингибитора обратной транскриптазы и, возможно, ненуклеозидного ингибитора обратной транскриптазы с фиксированной дозой.
11. Способ по п.8, где соединение вводят в комбинации или путем чередования с агентом против HBV (вируса гепатита В).
12. Способ по п.8, где соединение вводят перорально.
13. Способ по п.8, где соединение вводят в комбинации со вторым соединением, эффективным для лечения или предупреждения инфекции HCV (вирус гепатита С) у субъекта.
14. Применение соединения по любому из пп.1-3 в терапии.
15. Применение соединения по любому из пп.1-3 в изготовлении лекарственного средства для лечения, предупреждения, уменьшения симптомов или контроля над симптомами, ассоциированными с инфекцией HIV.
16. Фармацевтическая композиция по п.7, где второй агент против HIV представляет собой ампренавир, типранавир, индинавир, саквинавир, лопинавир, ритронавир, фосампренавир, дарунавир, атазанавир, нелфинавир, бреканивир, элвитегравир или ралтегравир.
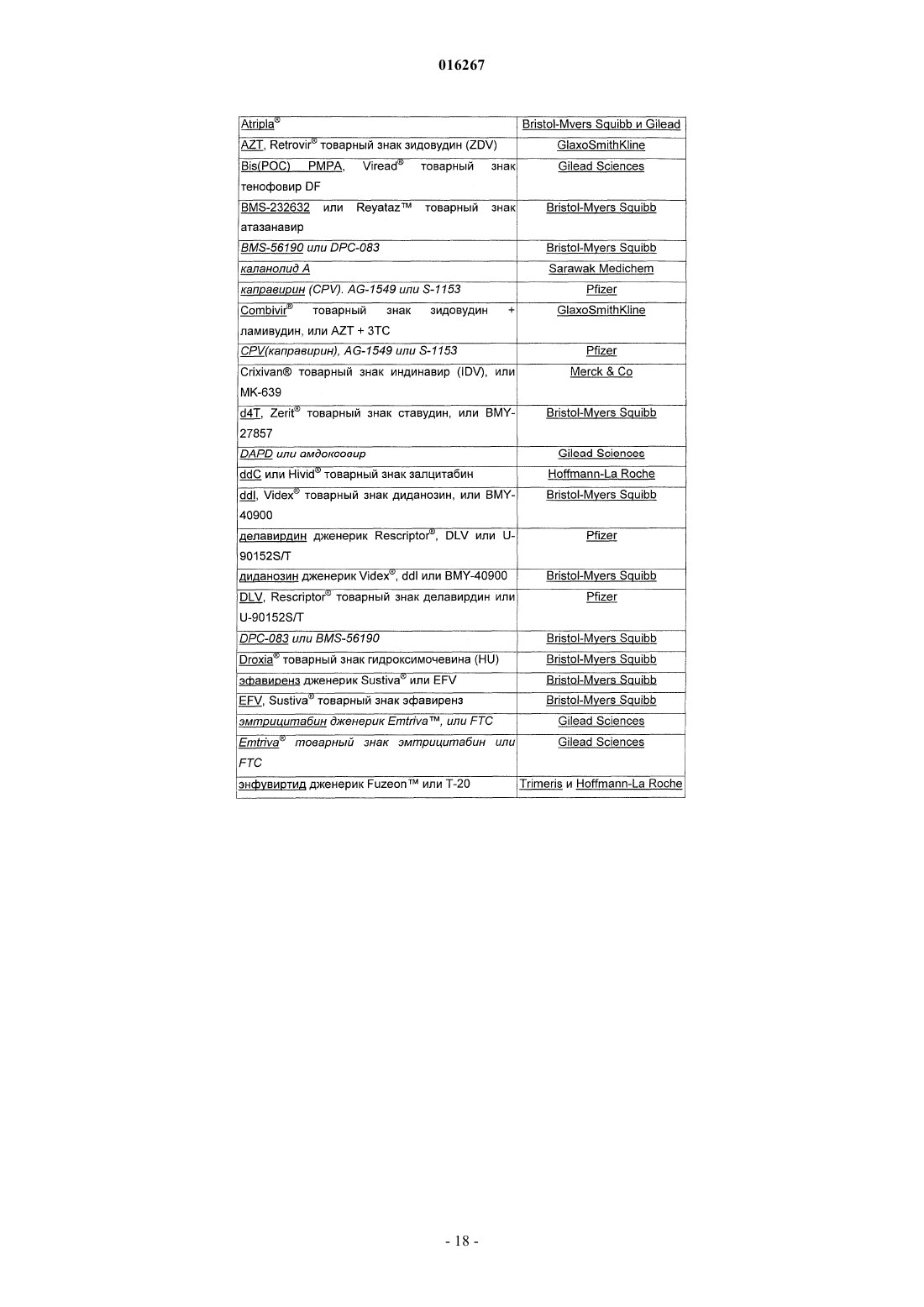
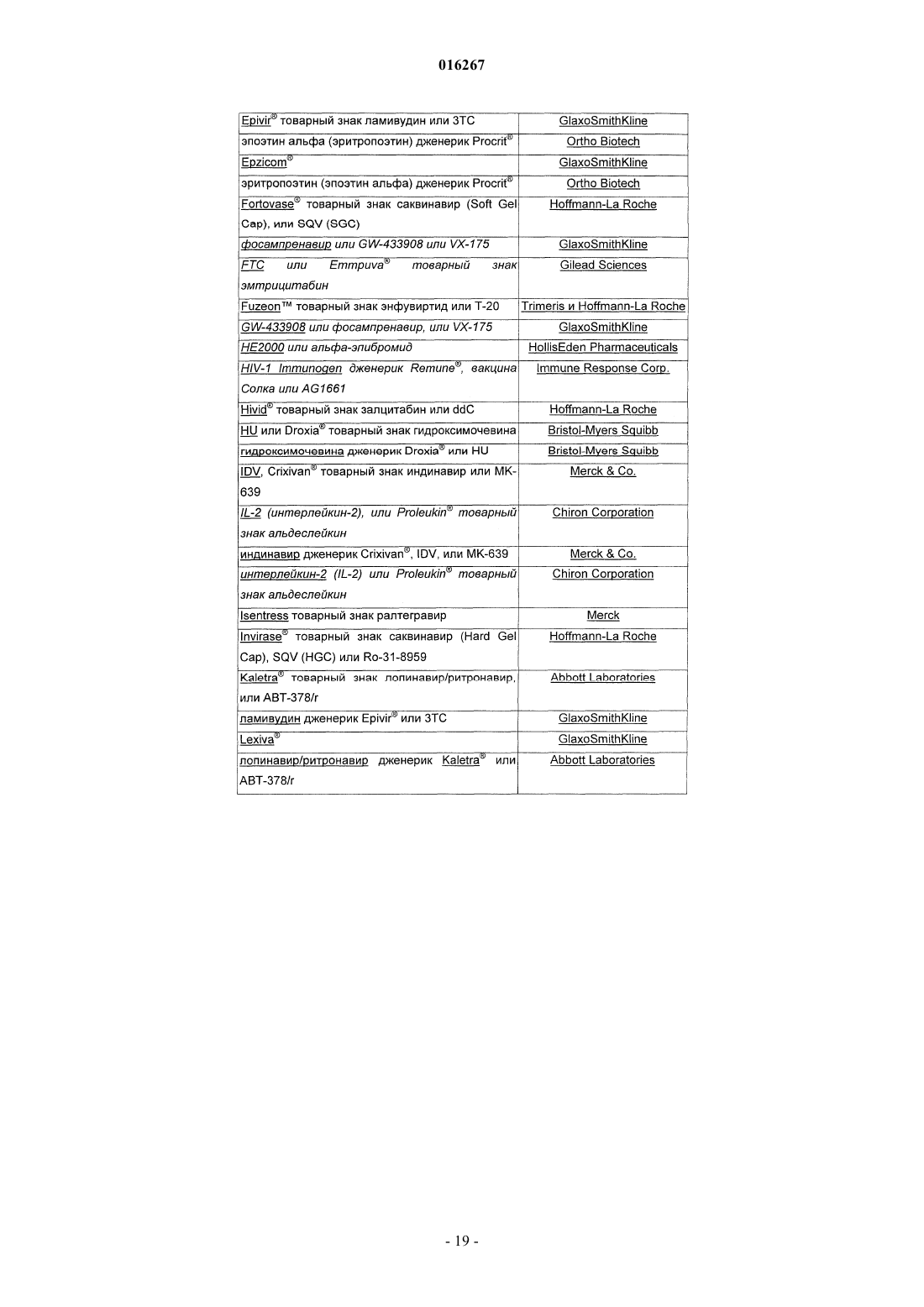
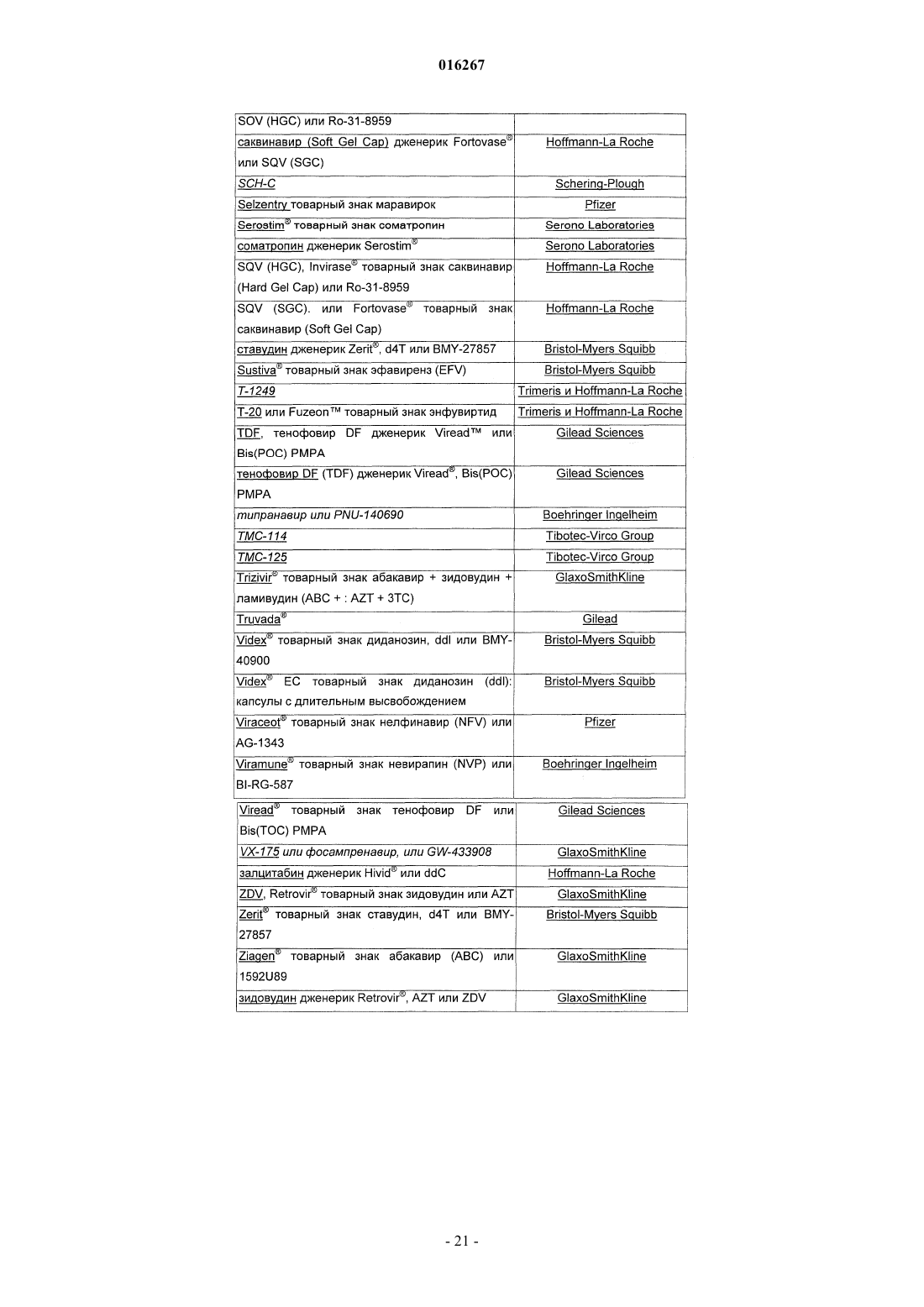
17. Способ по п.10, где второй агент против HIV представляет собой ампренавир, типранавир, индинавир, саквинавир, лопинавир, ритронавир, фосампренавир, дарунавир, атазанавир, нелфинавир, ламивудин, эмтрицитабин, абакавир, залцитабин, зидовудин, тенофовир, диданозин, ставудин, делавирдин, эфавиренз, невирапин, атриплу, комбивир, тризивир, труваду, маравирок, энфувиртид, бреканивир, амдоксовир, априцитабин, элвуцитабин, этравирин, рилпивирин, каланолид А, аплавирок, викривирок, бевиримат, элвитегравир или ралтегравир.
18. Способ по п.11, где агент против HBV представляет собой энтекавир, ламивудин, интерферон альфа-2b, пегинтерферон альфа-2а, адефовира дипивоксил, телбивудин, эмтрицитибин, клевудин, тенофовир, валторцитабин, амдоксовир, ремофовир или рацивир.
19. Фармацевтическая композиция, содержащая соединение по п.2 и фармацевтический носитель, эксципиент или разбавитель, где указанная композиция, по существу, не содержит противоположного энантиомера указанного соединения.
20. Фармацевтическая композиция по п.19, дополнительно содержащая второй агент против HIV.
21. Фармацевтическая композиция по п.20, где второй агент против HIV представляет собой ингибитор протеазы или ингибитор интегразы.
22. Фармацевтическая композиция по п.20, где второй агент против HIV представляет собой ампренавир, типранавир, индинавир, саквинавир, лопинавир, ритронавир, фосампренавир, дарунавир, атазанавир, нелфинавир, бреканивир, элвитегравир или ралтегравир.
23. Способ лечения инфекции HIV, включающий введение субъекту, нуждающемуся в этом, эффективного количества соединения по п.2.
24. Способ по п.23, дополнительно включающий введение субъекту соединения в комбинации или путем чередования, по меньшей мере, со вторым агентом против HIV.
25. Способ по п.24, где второй агент против HIV представляет собой ингибитор протеазы, нуклеозидный или нуклеотидный ингибитор обратной транскриптазы, ненуклеозидный ингибитор обратной транскриптазы, комбинацию с фиксированной дозой, ингибитор проникновения, антагонист корецептора CCR5, ингибитор созревания или ингибитор интегразы; где комбинацией с фиксированной дозой является комбинация нуклеозидных ингибиторов обратной транскриптазы с фиксированной дозой или комбинация нуклеозидного ингибитора обратной транскриптазы, нуклеотидного ингибитора обратной транскриптазы и, возможно, ненуклеозидного ингибитора обратной транскриптазы с фиксированной дозой.
26. Способ по п.24, где второй агент против HIV представляет собой ампренавир, типранавир, индинавир, саквинавир, лопинавир, ритронавир, фосампренавир, дарунавир, атазанавир, нелфинавир, ламивудин, эмтрицитабин, абакавир, залцитабин, зидовудин, тенофовир, диданозин, ставудин, делавирдин, эфавиренз, невирапин, атриплу, комбивир, тризивир, труваду, маравирок, энфувиртид, бреканивир, амдоксовир, априцитабин, элвуцитабин, этравирин, рилпивирин, каланолид А, аплавирок, викривирок, бевиримат, элвитегравир или ралтегравир.
27. Способ по п.23, дополнительно включающий введение субъекту соединения в комбинации или путем чередования с агентом против HBV.
28. Способ по п.27, где агент против HBV представляет собой энтекавир, ламивудин, интерферон альфа-2b, пегинтерферон альфа-2а, адефовира дипивоксил, телбивудин, эмтрицитибин, клевудин, тенофовир, валторцитабин, амдоксовир, ремофовир или рацивир.
29. Способ по п.23, где соединение вводят перорально.
30. Способ по п.23, где соединение вводят в комбинации со вторым соединением, эффективным для лечения или предупреждения инфекции HCV y субъекта.
Текст
ЭНАНТИОМЕРНО ЧИСТЫЕ ФОСФОИНДОЛЫ В КАЧЕСТВЕ ИНГИБИТОРОВ HIV В изобретении предложены 3-фосфоиндольные соединения, полезные для лечения инфекций,вызванных вирусами семейства Flaviviridae, и, в частности, инфекций HLV. Также предложены фармацевтические композиции, содержащие 3-фосфоиндольные соединения самостоятельно или в комбинации с одним или более чем одним другим противовирусным агентом, способы их получения и способы приготовления лекарственного средства, включающего эти соединения. 3 Фосфоиндольными соединениями являются соединения формулы (С) где R3 и R5 независимо представляют собой С 1-6 алкил или С 2-6 алкенил, каждый из которых может быть, возможно, независимо замещен CN или галогеном; каждый из R4 и R5 независимо представляет собой водород или галоген; R1 представляет собой водород, фенилсульфонил или 4 метоксибензил и Y представляет собой О-С 1-2 алкил, и их фармацевтически приемлемые соли. 016267 Область изобретения В изобретении предлагаются энантиомерно чистые фосфоиндольные соединения, полезные для ингибирования вирусной репликации. В некоторых воплощениях здесь предложены R-фосфоиндольные соединения, полезные для ингибирования вирусной репликации. Кроме того, предложены фармацевтически приемлемые соли соединений, фармацевтические композиции, содержащие соединения, способы применения соединений, например, при лечении или профилактики инфекции HIV (вируса иммунодефицита человека) и способы получения соединений. Предшествующий уровень техники Индолы, нуклеозиды и их аналоги известны в области техники как обладающие полезностью при лечении вирусных инфекций у млекопитающих, включая людей. Вирусы, которые инфицируют млекопитающих и которые можно лечить путем введения фармацевтических композиций, содержащих индолы, нуклеозиды или их аналоги или производные, включают гепацивирус, включающий HCV (вирус гепатита С), вирус иммунодефицита человека (HIV), пестивирусы, такие как вирус бычьей диареи (BVDV),вирус классической лихорадки свиней (CSFV, также известный как вирус холеры свиней), вирус пограничной болезни овец (BDV) и флавивирусы, такие как вирус геморрагической формы лихорадки денге(DHF или DENV), вирус жлтой лихорадки (YFV), вирус лихорадки Западного Нила (WNV), вирус токсического синдрома и вирус японского энцефалита, но не ограничиваются ими (Moennig et al., Adv. Vir.T.P. Monath, New Engl. J. Med., 1988, 319:641-3). Индолы Некоторые индольные аналоги и производные используют для лечения вируса иммунодефицита людей (HIV). Например, Williams et al. сообщает о замещенных индолах для лечения инфекции HIV в патенте США 5527819, выданном Merck. Соединения, раскрытые в патенте '819, содержат большой класс,представленный, в общем, виде следующей широкой структурной формулой (III): в которой переменные X, Y, Z, R и R6 широко определены таким образом, чтобы охватывать приблизительно одну сотню соединений. В большинстве представленных примеров Y представляет собойSO2, Z представляет собой -C(O)NH2 и R представляет собой возможно замещенный фенил. В патенте США 5124327, выданном Greenlee et al. и переуступленном MerckCo., раскрыт класс возможно замещенных сульфонилфенилиндольных соединений. Эти соединения предположительно активны в качестве ингибиторов обратной транскриптазы и, таким образом, полезны при лечении инфекции HIV и AIDS (синдрома приобретенного иммунодефицита человека). В патенте США 6710068, выданном Idenix Pharmaceuticals, Ltd., раскрыт класс фенилиндолов,замещенных по меньшей мере двумя группировками, отличающимися от водорода на фенильном кольце или бензильном кольце индольной функциональной группы либо на обоих кольцах. Заместители, как правило, располагаются в 3" и 5" позициях, если расположены на фенильном кольце, и в 4' и 5'; 5' и 6' или 5' и 7' позициях, если располагаются на бензильном кольце индольной группировки. Смотри также публикацию РСТ WO 02/083126. В публикации РСТ WO 2004/014364 от Idenix Pharmaceuticals раскрыт еще один класс фенилиндолов, демонстрирующих усиленную активность против HIV. Подобно своим предшественникам, эти соединения замещены по меньшей мере двумя группировками, отличающимися от водорода, на фенильном кольце или бензольном кольце индольной функциональной группировки, или на обоих кольцах. Дополнительно эти соединения включают множество заместителей, имеющих карбоксамидную функциональную группу в позиции 2 на индольной группе соединения, позиции, изображенной в формуле (III) выше как "Z".Idenix Pharmaceuticals раскрывает еще один класс фенилиндольных соединений, они представляют собой фосфофенилиндолы, полезные при лечении HIV и/или AIDS (US 2006/0074054 и WO 06/054182).Bristol Myers Squibb представляет собой патентообладатель многочисленных патентов, опубликованных заявок на патенты, и публикаций РСТ, раскрывающих различные, возможно, замещенные индолы, азаиндолы, пиперазины и пирролидины для лечения HIV и/или AIDS. Смотри публикацию US2004/0006090 от Kadow et al.; публикацию US2004/0063746 от Regueiro-Ren et al.; публикацию US2003/0096825 от Wang et al.; публикацию US2003/0236277 от Kadow et al. и WO 03/068221 от Kadowet al. В WO 01/02388 от SmithKline Beecham S.P.A раскрыты, возможно, замещенные фенилиндолы с карбамильным заместителем, полезные при лечении HIV, AIDS, остеопороза, рака и болезни Альцгеймера.ShinogiCo. раскрывает, возможно, замещенные индольные производные, представляющие собой ингибиторы вирусной интегразы, полезные в качестве лекарств против HIV (публикация US2002/0019434 от Fujishita et al.; патент США 6716605, выданный Fujishita et al.; и патент США 6506787, выданный Fujishita et al.) В патенте США 5945440, выданном Kleinschroth et al., раскрыт класс индолокарбазоламидов для лечения различных заболеваний, включая рак, вирусные заболевания (включая HIV), сердечные и сосудистые заболевания, бронхолегочные заболевания, воспалительные нарушения, дегенеративные заболевания центральной нервной системы и другие заболевания.Gunasekera et al. в патенте СШа 4866084 описывает некоторые бис-индолалкалоидные соединения, обладающие противовирусной и противоопухолевой активностью, включая HSV (вирус простого герпеса). Патент США 5935982, выданный Dykstra et al., сообщает о другом классе бис-индолов, обладающем специфической пользой против ретровирусных инфекций и в особенности HIV.Matsunaga et al. в патенте США 5852011 (December 22, 1998) раскрывает класс индольных производных, замещенных гетероарильной функциональной группой и амидной функциональной группой. Утверждают, что соединения, в общем, обладают противоопухолевыми, противовирусными и антимикробными свойствами.Dykstra et al. в патенте США 5935982 раскрывает класс бис-индолов и конкретно представляет их применение для лечения ретровирусных инфекций и в особенности инфекций HIV.Domagala et al. в патенте США 5929114 (27 июля 1999 года) раскрывает класс арилтио и битиобис-ариламидных соединений, включая индольные производные, которые, как сообщается, обладают антибактериальной и противовирусной активностью.Pevear et al. в патенте США 5830894 (3 ноября 1998 года) раскрывает класс триазиноиндольных производных, которые, как сообщается, обладают активностью против пестивирусов, в частности активностью против BVDV (вируса бычьей диареи). Индолы используют при лечении заболеваний, отличающихся от HIV. Патент США 5981525,выданный Farina et al., раскрывает комплексный ряд индолов для применения при лечении остеопороза,основанного на их способности ингибировать Н+-АТРазу остеокластов и, таким образом, уменьшать резорбцию кости. Патент США 6025390, также выданный Farina et al., описывает еще одну группу индольных производных, названных гетероароматические производные пентадиеновой кислоты, которые также полезны при лечении остеопороза. Патент США 5489685, выданный Houpis et al., раскрывает ряд соединений, представляющих собой сложные эфиры фуро(2,3-b)пиридинкарбоновой кислоты, которые полезны при лечении HIV. В свете того, что инфекции HIV по всему миру достигли эпидемических уровней и оказывают фатальное действие на инфицированного хозяина, сохраняется значительная потребность в получении новых и эффективных фармацевтических агентов для лечения этих вирусных инфекций, обладающих низкой токсичностью в отношении хозяина. Задача изобретения заключается в том, чтобы предложить соединения, способы применения и композиции для лечения хозяина, инфицированного HIV, или для лечения симптомов, связанных с AIDS. Краткое изложение сущности изобретения Соответственно здесь предложены энантиомерно чистые соединения, полезные для лечения или профилактики вирусной инфекции, например инфекции HIV, у нуждающегося в этом хозяина. Кроме того, предложены фармацевтические композиции, содержащие эти соединения, способы применения этих соединений для лечения или профилактики и способы получения этих соединений. Как представлено в приведенных ниже примерах, большая часть активности хиральных фосфоиндольных соединений свойственна одному энантиомеру или стереоизомеру. Кроме того, некоторые предложенные здесь соединения представляют собой сильные и избирательные ингибиторы HIV дикого типа и резистентных к ненуклеозидному ингибитору обратной транскриптазы (NNRTI) in vitro. Некоторые предложенные здесь соединения могут обеспечивать более высокий генетический барьер для развитияHIV резистентности по сравнению с имеющимися в настоящее время способами лечения, такими как эфавиренз. В одном из аспектов здесь предложены R-фосфоиндольные соединения и способы их применения для лечения или профилактики вирусной инфекции, такой как инфекции HIV, у хозяина, нуждающегося в этом. В одном из аспектов здесь предложены фосфоиндольные соединения формулы (С) или их фармацевтически приемлемые соли где R3 и R5 независимо представляют собой С 1-6 алкил или С 2-6 алкенил, каждый из которых может быть, возможно, независимо замещен CN или галогеном; каждый из R4 и R5 независимо представляет собой водород или галоген;Y представляет собой О-С 1-2 алкил. В одном из воплощений предложено соединение формулы (С), имеющее нижеследующую формулу, или его фармацевтически приемлемая соль: В другом воплощении предложено соединение формулы (С), имеющее нижеследующую формулу,или его фармацевтически приемлемая соль: В еще одном аспекте здесь предложены фармацевтически приемлемые соли предложенных здесь соединений. В еще одном аспекте предложена фармацевтическая композиция, содержащая предложенное здесь соединение и фармацевтический носитель, эксципиент или разбавитель, где указанная композиция, по существу, не содержит противоположного энантиомера указанного соединения. В еще одном аспекте предложена фармацевтическая композиция, содержащая предложенное здесь соединение и второй агент против HIV, где указанная композиция, по существу, не содержит противоположного энантиомера указанного соединения. Предпочтительно в указанной фармацевтической композиции второй агент против HIV представляет собой ингибитор протеазы или ингибитор интегразы. Более предпочтительно второй агент против HIV представляет собой ампренавир, типранавир, индинавир, саквинавир, лопинавир, ритронавир, фосампренавир, дарунавир, атазанавир, нелфинавир, бреканивир, элвитегравир или ралтегравир. В еще одном аспекте предложен способ лечения инфекции HIV, включающий введение субъекту,нуждающемуся в этом, эффективного количества предложенного здесь соединения. В одном из воплощений способ дополнительно включает введение субъекту соединения в комбинации или путем чередования по меньшей мере со вторым агентом против HIV. Предпочтительно второй агент против HIV представляет собой ингибитор протеазы, нуклеозидный или нуклеотидный ингибитор обратной транскриптазы, ненуклеозидный ингибитор обратной транскриптазы, комбинацию с фиксированной дозой, ингибитор проникновения, антагонист корецептора CCR5, ингибитор созревания или ингибитор интегразы. Более предпочтительно второй агент против HIV представляет собой ампренавир,типранавир, индинавир, саквинавир, лопинавир, ритронавир, фосампренавир, дарунавир, атазанавир,нелфинавир, ламивудин, эмтрицитабин, абакавир, залцитабин, зидовудин, тенофовир, диданозин, ставудин, делавирдин, эфавиренз, невирапин, атриплу, комбивир, тризивир, труваду, маравирок, энфувиртид,бреканивир, амдоксовир, априцитабин, элвуцитабин, этравирин, рилпивирин, каланолид А, аплавирок,викривирок, бевиримат, элвитегравир или ралтегравир. В другом воплощении способа соединение вводят в комбинации или путем чередования с агентом против HBV. Предочтительно агент против HBV представляет собой энтекавир, ламивудин, интерферон альфа-2b, пегинтерферон альфа-2 а, адефовира дипивоксил, телбивудин, эмтрицитибин, клевудин, тенофовир, валторцитабин, амдоксовир, ремофовир или рацивир.-3 016267 В еще одном воплощении способа соединение вводят перорально. В еще одном воплощении соединение вводят в комбинации со вторым соединением, эффективным для лечения или предупреждения инфекции HCV у субъекта. В еще одном аспекте предложено применение предложенного здесь соединения в терапии. В еще одном аспекте предложено применение предложенного здесь соединения в изготовлении лекарственного средства для лечения, предупреждения, уменьшения симптомов или контроля над симптомами, ассоциированными с инфекцией HIV. В еще одном аспекте предложена фармацевтическая композиция, содержащая соединение формулы и фармацевтический носитель, эксципиент или разбавитель, где указанная композиция, по существу, не содержит противоположного энантиомера указанного соединения. Предпочтительно фармацевтическая композиция дополнительно содержит второй агент против HIV. Более предпочтительно в указанной фармацевтической композиции второй агент против HIV представляет собой ингибитор протеазы или ингибитор интегразы. Наиболее предпочтительно, второй агент против HIV представляет собой ампренавир, типранавир, индинавир, саквинавир, лопинавир, ритронавир, фосампренавир, дарунавир, атазанавир, нелфинавир, бреканивир, элвитегравир или ралтегравир. В еще одном аспекте предложен способ лечения инфекции HIV, включающий введение субъекту,нуждающемуся в этом, эффективного количества соединения формулы (С), имеющего нижеследующую формулу: В одном из воплощений способ дополнительно включает введение субъекту соединения в комбинации или путем чередования по меньшей мере со вторым агентом против HIV. Предпочтительно второй агент против HIV представляет собой ингибитор протеазы, нуклеозидный или нуклеотидный ингибитор обратной транскриптазы, ненуклеозидный ингибитор обратной транскриптазы, комбинацию с фиксированной дозой, ингибитор проникновения, антагонист корецептора CCR5, ингибитор созревания или ингибитор интегразы. Более предпочтительно второй агент против HIV представляет собой ампренавир,типранавир, индинавир, саквинавир, лопинавир, ритронавир, фосампренавир, дарунавир, атазанавир,нелфинавир, ламивудин, эмтрицитабин, абакавир, залцитабин, зидовудин, тенофовир, диданозин, ставудин, делавирдин, эфавиренз, невирапин, атриплу, комбивир, тризивир, труваду, маравирок, энфувиртид,бреканивир, амдоксовир, априцитабин, элвуцитабин, этравирин, рилпивирин, каланолид А, аплавирок,викривирок, бевиримат, элвитегравир или ралтегравир. В другом воплощении способ дополнительно включает введение субъекту соединения в комбинации или путем чередования с агентом против HBV. Предпочтительно агент против HBV представляет собой энтекавир, ламивудин, интерферон альфа-2b, пегинтерферон альфа-2 а, адефовира дипивоксил,телбивудин, эмтрицитибин, клевудин, тенофовир, валторцитабин, амдоксовир, ремофовир или рацивир. В еще одном воплощении способа соединение вводят перорально. В еще одном воплощении соединение вводят в комбинации со вторым соединением, эффективным для лечения или предупреждения инфекции HCV у субъекта. Краткое описание чертежей Фиг. 1 А демонстрирует кристаллическую структуру обратной транскриптазы HIV K103N/Y181C с 3-фосфоиндольным соединением формулы I; фиг. 1 В - схему кристаллической структуры обратной транскриптазы HIV K103N/Y181C с 3 фосфоиндольным соединением формулы I; фиг. 2 А - кристаллическую структуру молекулы соединения (III); фиг. 2 В - кристаллическую структуру молекулы соединения (III). Подробное описание изобретения Предложены композиции вещества, способы применения и фармацевтические композиции для лечения вирусных инфекций, в частности инфекций HIV, у млекопитающих. В частности, предложены чистые 3-фосфоиндольные соединения, композиции, содержащие эти соединения, и способы применения-4 016267 соединений и композиций для лечения или профилактики инфекции, включая инфекцию HIV, у хозяина. Дополнительно здесь предложены способы получения чистых 3-фосфоиндолов. Определения В предложенных здесь композициях энантиомерно чистый фосфоиндол или его фармацевтически приемлемая соль могут присутствовать с другими активными или неактивными ингредиентами. Например, фармацевтическая композиция, содержащая (Р)-фосфоиндол, может содержать, например, приблизительно 90% эксципиента и приблизительно 10% (R)-фосфоиндола. В некоторых воплощениях активный ингредиент может быть приготовлен с небольшим количеством носителя, эксципиента или разбавителя, или без них. Независимо от упомянутого здесь диапазона, он включает независимо и по отдельности каждый член диапазона. В качестве неограничивающего объем изобретения примера считают, что термин "C1 С 10 алкил" включает независимо каждый член группы таким образом, что, например, C1-С 10 алкил включает прямоцепочечную, разветвленную и, когда подходит, циклическую C1, С 2, С 3, С 4, С 5, С 6, С 7, С 8, С 9 и С 10 алкильную функциональную группу. Аналогично, в качестве еще одного неограничивающего объем изобретения примера 1-10% включает независимо 1, 2, 3, 4, 5, 6, 7, 8, 9 и 10%, а также диапазоны между ними, такие как 1-2%, 2-3% и т.д. Использованный здесь термин "хиральный" включает соединение, обладающее свойством, которое заключается в том, что это соединение не налагается на свое зеркальное изображение. Термин "выделенный" включает композицию, которая включает по меньшей мере 85 или 90 мас.%,95, 98, 99 или 100 мас.% соединения. Если не указано иное, использованный здесь термин "алкил" включает насыщенный прямоцепочечный, разветвленный или циклический первичный, вторичный или третичный углеводород типично С 1-10,и конкретно включает метил, CF3, CCl3, CFCl2, CF2Cl, этил, CH2CF3, CF2CF3, пропил, изопропил, циклопропил, бутил, изобутил, втор-бутил, трет-бутил, пентил, циклопентил, изопентил, неопентил, гексил,изогексил, циклогексил, циклогексилметил, 3-метилпентил, 2,2-диметилбутил и 2,3-диметилбутил, но не ограничивается ими. Термин включает замещенные и незамещенные алкильные группы и, в частности,включает галогенированные алкильные группы и более конкретно фторированные алкильные группы. Неограничивающие объем изобретения примеры группировок, которыми алкильная группа может быть замещена, выбраны из группы, состоящей из галогена (фторо, хлоро, бромо или йодо), гидроксила, амино, алкиламино, ариламино, алкокси, арилокси, нитро, циано, сульфоновой кислоты, сульфата, фосфиновой кислоты, фосфата или фосфоната, незащищенного или защищенного при необходимости, как известно специалистам в данной области техники, например как изложено в Greene et al., Protected Groupsin Organic Synthesis, John Wiley and Sons, 2nd Ed., 1991. Если не указано иное, использованный здесь термин "низший алкил" относится к C1-6 насыщенной прямоцепочечной, разветвленной или, если подходит, циклической (например, циклопропильной) алкильной группе, включая замещенные и незамещенные группировки. Термины "алкиламино" или "ариламино" относятся к аминогруппе, имеющей один или два алкильных или арильных заместителя соответственно. Если специально не указано в данной заявке, когда алкил представляет собой подходящую группировку, то он представляет собой низший алкил, замещенный или незамещенный. Использованный здесь термин "нитро" обозначает -NO2; термин "сульфгидрил" обозначает -SH и термин "сульфонил" обозначает -SO2. Термины "алкенил" и "алкинил" включает алкильные группировки, включающие замещенные и незамещенные формы, где по меньшей мере одна насыщенная связь С-С замещена двойной или тройной связью. Таким образом, С 2-6 алкенил может представлять собой винил, аллил, 1-пропенил, 2-пропенил, 1 бутенил, 2-бутенил, 3-бутенил, 1-пентенил, 2-пентенил, 3-пентенил, 4-пентенил, 1-гексенил, 2-гексенил,3-гексенил, 4-гексенил или 5-гексенил. Аналогично, С 2-6 алкинил может представлять собой этинил, 1 пропинил, 2-пропинил, 1-бутинил, 2-бутинил, 3-бутинил, 1-пентинил, 2-пентинил, 3-пентинил, 4 пентинил, 1-гексинил, 2-гексинил, 3-гексинил, 4-гексинил или 5-гексинил. Термин "алкилен" включает насыщенный прямоцепочечный двухвалентный алкильный радикал формулы -(СН 2)n-, где "n" может представлять собой любое целое число от 1 до 10."Алкил", "алкокси", "алкенил", "алкинил" и т.д. включают прямоцепочечные и разветвленные группы. Тем не менее, ссылка на индивидуальный радикал, такой как "пропил", охватывает только прямоцепочечный радикал, тогда как изомер с разветвленной цепью, такой как "изопропил", назван специальным образом. Если не указано иное, использованный здесь термин "защищенный" относится к группе, добавляемой к атому кислорода, азота, серы или фосфора для предотвращения их дальнейшего взаимодействия или для других задач. Широкое разнообразие защитных групп кислорода, азота, серы или фосфора известно специалистам в области органического синтеза. Если не указано иное, использованный здесь термин "арил" относится к любому стабильному моноциклическому, бициклическому или трициклическому углеродному кольцу, имеющему до 8 членов в каждом кольце, где по меньшей мере одно кольцо является ароматическим, что определено правилом-5 016267 Хюккеля 4n+2, и в частности, фенил, бифенил или нафтил. Термин включает замещенные и незамещенные группировки. Арильная группа может быть замещена любой описанной группировкой, включающей одну или более чем одну группировку, выбранную из группы, состоящей из галогена (фторо, хлоро, бромо или йодо), гидроксила, амино, азидо, алкиламино, ариламино, алкокси, арилокси, нитро, циано, сульфоновой кислоты, сульфата, фосфоновой кислоты, фосфата или фосфоната, защищенной или незащищенной, как необходимо, но не ограничивающейся ими, как известно специалистам в данной области техники, например как изложено Greene et al., Protective Groups in Organic Synthesis, John WileySons,3rd Ed., 1999. Термины "алкарил" или "алкиларил" относятся к алкильной группе с арильным заместителем или алкильной группе, связанной с молекулой через определенную здесь арильную группу. Термины "аралкил" или "арилалкил" относятся к арильной группе, замещенной алкильным заместителем или связанной с молекулой через определенную здесь алкильную группу. Термин "циклоалкил" включает кольцо С 3-8, включая циклопропил, циклобутил, циклопентил, циклогексил, циклогептил и циклооктил, но не ограничиваясь ими. Термин "алкокси" обозначает прямоцепочечную или разветвленную алкильную группу, имеющую присоединенный кислородный радикал, алкильную группу, имеющую атомы углерода в указанном количестве или в любом количестве в пределах данного диапазона. Например, "-О-алкил", С 1-4 алкокси, метокси и т.д. Использованный здесь термин "галогено" относится к любому члену семейства галогенов. Специально включены фторо, хлоро, бромо и йодо. Термин "ацил" или "О-связанный сложный эфир" включает группу формулы C(O)R', где R' представляет собой прямоцепочечный, разветвленный или циклический алкил (включая низший алкил), карбоксилатный остаток аминокислоты, арил, включая фенил, гетероарил, алкарил, аралкил, включая бензил, алкоксиалкил, включая метоксиметил, арилоксиалкил, такой как феноксиметил; или замещенный алкил (включая низший алкил), арил, включая фенил, возможно, замещенный хлоро, бромо, фторо, йодо,С 1-С 4-алкил или С 1-С 4-алкокси, сульфонатные сложные эфиры, такие как алкил- или аралкилсульфонил,включая метансульфонил, моно-, ди- или трифосфатный эфир, тритил или монометокситритил, замещенный бензил, алкарил, аралкил, включая бензил, алкоксиалкил, включая метоксиметил, арилоксиалкил, такой как феноксиметил. Арильные группы в сложных эфирах оптимально содержат фенильную группу. В не ограничивающих объем изобретения воплощениях ацильные группы включают ацетил,трифторацетил, метилацетил, циклопропилацетил, циклопропилкарбокси, пропионил, бутирил, изобутирил, гексаноил, гептаноилоктаноил, нео-гептаноил, фенилацетил, 2-ацетокси-2-фенилацетил, дифенилацетил,-метокситрифторметилфенилацетил,бромацетил,2-нитробензолацетил,4-хлорбензолацетил, 2-хлор-2,2-дифенилацетил, 2-хлор-2-фенилацетил, триметилацетил, хлордифторацетил,фторацетил, бромдифторацетил, метоксиацетил, 2-тиофенацетил, хлорсульфонилацетил, 3 метоксифенилацетил, феноксиацетил, трет-бутилацетил, трихлорацетил, монохлорацетил, дихлорацетил,7 Н-додекафторгептаноил, перфторгептаноил, 7-хлордодекафторгептаноил, 7 Н-додекафторгептаноил,нонафтор-3,6-диоксагептаноил, метоксибензоил, метил 3-амино-5-фенилтиофен-2-карбоксил, 3,6 дихлор-2-метоксибензоил, 4-(1,1,2,2-тетрафторэтокси)бензоил, 2-бромопропионил, омега-аминокаприл,деканоил, н-пентадеканоил, стеарил, 3-циклопентилпропионил, 1-бензолкарбоксил, О-ацетилманделил,пивалоилацетил, 1-адамантанкарбоксил, циклогексанкарбоксил, 2,6-пиридиндикарбоксил, циклопропанкарбоксил, циклобутанкарбоксил, перфторциклогексил-карбоксил, 4-метилбензоил, хлорметилизоксазолилкарбонил, перфторциклогексилкарбоксил, кротонил, 1-метил-1 Н-индазол-3-карбонил, 2-пропенил,изовалерил, 1-пирролидинкарбонил, 4-фенилбензоил. Термин "ациламино" включает группу, имеющую структуру -N(R')-C(=O)-R', где каждый R' независимо является таким, как определено выше. Термин "карбонил" включает группу структуры "-C(=O)-X-R' " или "X-C(=O)-R' ", где X представляет собой О, S или связь и каждый R' независимо является таким, как определено выше. Термин "гетероатом" включает атом, отличающийся от углерода или водорода в структуре гетероциклического соединения, не ограничивающие объем изобретения примеры которого представляют собой азот, кислород, серу, фосфор или бор. За исключением того, где специально указано, использованные здесь термины "гетероцикл" или"гетероциклический" включают стабильное 5-7-членное моноциклическое или стабильное 8-11-членное бициклическое гетероциклическое кольцо, являющееся насыщенным или ненасыщенным, включая гетероарил, и которое состоит из атома(ов) углерода и от одного до четырех гетероатомов, включая О, S, N и Р, но не ограничивающихся ими; и где гетероатомы азота и серы могут быть, возможно, окислены и/или гетероатом азота кватернизирован, и включают любую бициклическую группу, в которой любое из идентифицированных выше гетероциклических колец конденсировано с бензольным кольцом. Гетероциклическое кольцо может быть присоединено к любому гетероатому или атому углерода, приводя в результате к образованию стабильной структуры. Гетероароматическое кольцо может быть частично или полностью гидрированным, если желательно. Например, дигидропиридин может быть использован вместо пиридина. Функциональные группы кислорода и азота на гетероариле могут быть, если необходимо или желательно, защищенными. Подходящие защитные группы для кислорода или азота включают триме-6 016267 тилсилильные, диметилгексилсилильные, трет-бутилдиметилсилильные, трет-бутилдифенилсилильные,тритильные, замещенные тритильные, алкильные, метансульфонильные, пара-толуолсульфонильные или ацильные группы, такие как ацетил и пропионил. Не ограничивающие объем изобретения примеры гетероарильных и гетероциклических групп включают фурил, пиридил, пиримидил, пиридазинил, пиразинил, пиперидинил, пиперазинил, тиенил,пирролил, пирролинил, пирролидинил, имидазолил, тетразолил, триазолил, триазинил, тиазинил, оксазолил, пуринил, карбазолил, хинолинил, пиразолил, морфолинил, бензимидазолил и т.п. Любая из гетероароматических и гетероциклических группировок может быть, возможно, замещена, как описано выше для арила, включая замещение(я) одним или более чем одним гидроксилом, амино, алкиламино, ариламино, алкокси, арилокси, алкил, гетероциклилом, галогено, карбокси, ацил, ацилокси, амидо, нитро, циано, сульфоновой кислоты, сульфатом, фосфиновой кислоты, фосфатом или фосфонатом, защищенным или незащищенным, если необходимо, как известно специалистам в данной области техники и как изложено, например, в Greene et al., Protective Groups in Organic Synthesis, John Wiley and Sons, Third Ed.,1999. Если не указано иное, использованный здесь термин "амино" включает группировку, представленную структурой "-NR2", и включает первичные, вторичные и третичные амины, возможно, замещенные алкильными, арильными, гетероциклильными и/или сульфонильными группами. Таким образом, R2 может представлять собой два атома водорода, две алкильные группировки или один водород и одну алкильную группировку. Термин "аминокислота" или "остаток аминокислоты" включает встречающиеся в природе и синтетические , ,илиаминокислоты и включает аминокислоты, обнаруживаемые в белках, т.е. глицин,аланин, валин, лейцин, изолейцин, метионин, фенилаланин, триптофан, пролин, серин, треонин, цистеин,тирозин, аспарагин, глутамин, аспартат, глутамат, лизин, аргинин и гистидин, но не ограничивается ими. В одном из воплощений аминокислота находится в L-конфигурации, но также может быть использована в D-конфигурации. Альтернативно, аминокислота может представлять собой производное аланила, валинила, лейцинила, изолейцинила, пролинила, фенилаланинила, триптофанила, метионинила, глицинила,серинила, треонинила, цистеинила, тирозинила, аспарагинила, глутаминила, аспартоила, глутароила, лизинила, аргининила, гистидинила, -аланила, -валинила, -лейцинила, -изолейцинила, -пролинила, фенилаланинила, -триптофанила, -метионинила, -глицинила, -серинила, -треонинила, цистеинила, -тирозинила, -аспарагинила, -глутаминила, -аспартоила, -глутароила, -лизинила, аргининила или -гистидинила. Когда используется термин аминокислота, предполагается, что он представляет собой специфическое и независимое описание каждого из сложных эфиров , ,илиглицина, аланина, валина, лейцина, изолейцина, метионина, фенилаланина, триптофана, пролина, серина, треонина, цистеина, тирозина, аспарагина, глутамина, аспартата, глутамата, лизина, аргинина и гистидина вD- и L-конфигурациях. Использованный здесь термин "амидо" включает аминозамещенный карбонил,тогда как термин "амидино" обозначает группу, имеющую структуру "-C(=NH)-NH2". Некоторые содержащие серу и фосфор термины имеют следующие структурные значения: "сульфонат" включает группу структуры -S(=O)(=O)-OR'; "сульфат" включает группу структуры О-S(=O)(=O)-OR'; "сульфонамид" включает группу структуры N(R')-S(=O)(=O)-R'; "сульфамоил" включает группу структуры -S(=O)(=O)N(R')(R'); "фосфорил" включает группу структуры -P(=O)-OR' и "фосфороамидат" включает группу структуры Q-P(NR1R2)(=O)-OR', где каждый R' независимо является таким, как определено выше. Использованный здесь термин "хозяин" относится к одноклеточному или многоклеточному организму, в котором вирус может реплицироваться, включая клеточные линии и животных, и, в некоторых случаях, человека. Альтернативно, хозяин может нести часть вирусного генома HIV, репликация или функция которого может быть изменена соединениями по настоящему изобретению. Термин хозяин конкретно относится к инфицированным клеткам, клеткам, трансфицированным целым геномом или частью генома HIV, и животным, в частности приматам (включая шимпанзе) и людям. Для большинства применений настоящего изобретения в отношении животных хозяин представляет собой пациентачеловека. Ветеринарные применения при некоторых показаниях, тем не менее, ясно охвачены воплощениями настоящего изобретения (такими как шимпанзе). Термин "замещенные" включает множественные степени замещения одним или более чем одним названным заместителем, таким как, например, галогено, гидроксил, тио, алкил, алкенил, алкинил, нитро, циано, азидо, амино, карбоксамидо и т.д. Когда существует множество возможных заместителей, соединение может быть замещенным одним или более чем одним, раскрытых или заявленных групп заместителей, независимо друг от друга, и взятых в единственном или множественном числе.-7 016267 Соединения В некоторых воплощениях здесь предложены соединения формулы (С) или их фармацевтически приемлемые соли где R3 и R5 независимо представляют собой С 1-6 алкил или С 2-6 алкенил, каждый из которых может быть, возможно, независимо замещен CN или галогеном; каждый из R4 и R5 независимо представляет собой водород или галоген;Y представляет собой О-С 1-2 алкил. В одном из воплощений предложено соединение или его фармацевтически приемлемые соли где абсолютная конфигурация по атому фосфора представляет собой R. Химическое название соединения I представляет собой метиловый эфир (2-карбамоил-5-хлор-4-фтор-1 Н-индол-3-ил)-[3-Е)-2 циановинил)-5-метилфенил]-(R)фосфиновой кислоты, и эмпирическая формула представляет собойC20H16ClFN3O3P с молекулярной массой 431,39. В одном из воплощений предложено соединение или его фармацевтически приемлемая соль где абсолютная конфигурация по атому фосфора представляет собой R. Химическое название соединения III представляет собой метиловый эфир (2-карбамоил-5-хлор-1 Н-индол-3-ил)-[3-Е)-2 циановинил)-5-метилфенил]-(R)фосфиновой кислоты, и эмпирическая формула представляет собойC20H17ClN3O3P с молекулярной массой 413,79. В одном из воплощений предложено соединение, выбранное из группы, состоящей из метилового эфира (2-карбамоил-5-хлор-1 Н-индол-3-ил)-[3-Е)-2-циановинил)-5-метилфенил](R)фосфиновой кислоты и метилового эфира(2-карбамоил-5-хлор-4-фтор-1 Н-индол-3-ил)-[3-Е)-2-циановинил)-5 метилфенил]-(R)фосфиновой кислоты,или его фармацевтически приемлемой соли. В одном из аспектов здесь раскрыты S-фосфоиндольные соединения и способы их применения для лечения или профилактики вирусной инфекции, такой как инфекция HIV, у хозяина, нуждающегося в этом. В настоящем изобретении раскрыто соединение или его фармацевтически приемлемая соль-8 016267 где абсолютная конфигурация по атому фосфора представляет собой S. Также в настоящем изобретении раскрыто соединение или его фармацевтически приемлемая соль где абсолютная конфигурация по атому фосфора представляет собой S. Кроме того, в настоящем изобретении раскрыто соединение, выбранное из группы, состоящей из метилового эфира (2-карбамоил-5-хлор-1 Н-индол-3-ил)-[3-Е)-2-циановинил)-5-метилфенил](S)фосфиновой кислоты и метилового эфира(2-карбамоил-5-хлор-4-фтор-1 Н-индол-3-ил)-[3-Е)-2-циановинил)-5 метилфенил]-(S)фосфиновой кислоты,или его фармацевтически приемлемой соли. Также предложены соединения, которые могут быть введены в виде соли, сложного эфира или пролекарства, которое после введения реципиенту приводит прямо или опосредованно к предложенному здесь соединению или которое само демонстрирует желаемую активность. Фармацевтически приемлемые соли, пролекарства, стереоизомеры и таутомеры Предложенное здесь соединение может быть введено в виде любой соли или пролекарства, которое после введения реципиенту способно прямо или опосредованно приводить к исходному соединению или которое само демонстрирует активность. Не ограничивающие объем изобретения примеры представляют собой фармацевтически или физиологически приемлемые соли. Фраза "фармацевтически или физиологически приемлемая соль или пролекарство" используется в описании для описания любой фармацевтически приемлемой формы (такой как сложный эфир, амид, соль сложного эфира, соль амида или родственная группа) соединения, которая после введения пациенту приводит к активному соединению по изобретению. Модификации, подобные этим, могут влиять на биологическую активность соединения, в некоторых случаях увеличивая активность относительно исходного соединения. Термин "фармацевтически приемлемая соль" относится к состоянию соединения, в котором соединение несет противоион, являющийся фармацевтически приемлемым, и где соль сохраняет желаемую биологическую активность идентифицированных здесь соединений, в то же время демонстрируя минимальные нежелательные токсические эффекты. Такие соли представляют собой нетоксичные терапевтически полезные формы соединений по настоящему изобретению. Любая соль, сохраняющая желаемую биологическую активность содержащихся здесь соединений и которая демонстрирует минимальные или отсутствие нежелательных или токсических действий, предполагается для включения в изобретение. Фармацевтически приемлемые соли включают соли, являющиеся производными фармацевтически приемлемых органических или неорганических кислот и оснований. Фармацевтически неприемлемые кислоты и основания также могут применяться здесь, например, при синтезе и/или очистке интересующих соединений. Таким образом, все "соли" предполагаются для включения в изобретение. Фармацевтически приемлемые соли включают соли, являющиеся производными фармацевтически приемлемых неорганических или органических оснований и кислот, и включают тозилат, метансульфонат, ацетат, цитрат, малонат, тартрат, сукцинат, бензоат, аскорбат, альфа-кетоглутарат, альфаглицерофосфат, формиат, фумарат, пропионат, гликолят, лактат, пируват, оксалат, малеат, салицилат,сульфат, сульфонат, нитрат, бикарбонат, гидробромат, гидробромид, гидройодид, карбонат и соли ортофосфорной кислоты. Конкретное воплощение представляет собой соль моно- или дигидрохлорид. Подходящие соли включают соли, являющиеся производными щелочных металлов, таких как калий и натрий, щелочно-земельных металлов, таких как кальций и магний, среди множества других кислот, хорошо известных в фармацевтической области. Фармацевтически приемлемые пролекарства относятся к соединению, которое подвергается метаболизму, например гидролизуется или окисляется в организме хозяина, с образованием соединения по настоящему изобретению. Типичные примеры пролекарств включают соединения, которые обладают биологически лабильными защитными группами на функциональной группировке активного соединения, включая группировку сложного эфира или ацильную группировку, но не ограничиваются ими. Пролекарства включают соединения, которые могут быть подвергнуты окислению, восстановлению, аминированию, дезаминированию, гидроксилированию, дегидроксилированию, гидролизу, дегидролизу, алкилированию, деалкилированию, ацилированию, деацилированию, фосфорилированию, дефосфорилированию с образованием активного соединения. Фармацевтически приемлемые соли могут быть получены с использованием стандартных способов,хорошо известных в области техники, например путем взаимодействия достаточно основного соединения, такого как амин, с подходящей кислотой, с образованием физиологически приемлемого аниона. Также могут быть получены соли карбоновых кислот с щелочным металлом (таким как калий, натрий-9 016267 или литий) или щелочно-земельным металлом (таким как кальций). Не ограничивающие объем изобретения примеры подходящих солей включают соли, являющиеся производными неорганических кислот, таких как, например, соляная кислота, бромисто-водородная кислота, серная кислота, ортофосфорная кислота, азотная кислота, гидрокарбоновая кислота, карбоновая кислота; и соли, образованные с органическими кислотами, такими как, например, муравьиная кислота,уксусная кислота, щавелевая кислота, винная кислота, янтарная кислота, яблочная кислота, малоновая кислота, аскорбиновая кислота, лимонная кислота, бензойная кислота, дубильная кислота, пальмовая кислота (palmoic acid), альгиновая кислота, полиглутаминовая кислота, тозиновая кислота, метансульфоновая кислота, нафталинсульфокислота, нафталиндисульфокислота, -кетоглутаровая кислота, глицерофосфорная кислота и полигалактуроновая кислота. Подходящие соли включают соли, являющиеся производными щелочных металлов, таких как литий, калий и натрий, щелочно-земельных металлов,таких как кальций и магний, а также других оснований, хорошо известных специалистам в фармацевтической области. Другие подходящие соли включают соли, являющиеся производными катионов металлов, таких как цинк, висмут, барий или алюминий, или катиона, образованного из амина, такого как аммоний, N,N-дибензилэтилендиамин, D-глюкозамин, тетраэтиламмоний или этилендиамин. Кроме того,подходящие соли включают соли, являющиеся производными комбинации кислот и оснований, такие как, например, соль танната цинка. Фармацевтически приемлемое пролекарство относится к соединению, которое метаболизирует (т.е.,например, гидролизуется или окисляется) в организме хозяина с образованием соединения по настоящему изобретению. Типичные примеры пролекарств включают соединения, обладающие биологически лабильными защитными группами на функциональной группировке активного соединения. Пролекарства включают соединения, которые могут быть окислены, восстановлены, аминированы, дезаминированы,гидроксилированы, дегидроксилированы, гидролизованы, дегидролизованы, алкилированы, деалкилированы, ацилированы, деацилированы, фосфорилированы и/или дефосфорилированы с образованием активного соединения. В одном из воплощений предложенные здесь соединения обладают антивирусной активностью против HIV или метаболизируют в соединение, которое демонстрирует такую активность. Способы лечения В одном из воплощений предложены способы лечения или профилактики инфекции HIV у хозяина,включающие введение эффективного против вируса количества описанного здесь соединения, включая соединение формулы (С), или его фармацевтически приемлемой соли. Соединения могут быть комбинированы с фармацевтически приемлемым носителем или разбавителем. В еще одном основном воплощении предложено применение раскрытого здесь соединения, включая соединение формулы (С), или его фармацевтически приемлемой соли при лечении или профилактике инфекции HIV у хозяина, возможно, в комбинации с фармацевтически приемлемым носителем или разбавителем. Также предложено применение описанного здесь соединения или его фармацевтически приемлемой соли в изготовлении лекарственного средства для лечения или профилактики инфекции HIV у хозяина,возможно, в комбинации с фармацевтически приемлемым носителем или разбавителем. В одном из воплощений предложен способ лечения или профилактики инфекции HIV у хозяина,включающий введение 3-фосфоиндольного соединения, по существу, в форме одного энантиомера, или его фармацевтически приемлемой соли, возможно, в комбинации с фармацевтически приемлемым носителем хозяину, нуждающемуся в этом. В одном из воплощений 3-фосфоиндол имеет формулу С. В одном из воплощений 3-фосфоиндол имеет формулу I, где абсолютная стереохимия по атому фосфора являетсяR. В еще одном воплощении 3-фосфоиндол может иметь формулу III с абсолютной стереохимией R. В других воплощениях у хозяина может быть поставлен диагноз путем измерения титра антитела против HIV в крови. В еще одном воплощении соединения вводят для уменьшения или предупреждения симптомов AIDS (синдром приобретенного иммунодефицита) у хозяина. В еще одном воплощении раскрытые здесь соединения вводят хозяину, имеющему риск инфицирования HIV. В еще одном воплощении активное соединение демонстрирует активность против резистентных к лекарствам формам HIV и таким образом демонстрирует уменьшенную перекрестную резистентность против принятых в настоящее время антивирусных терапий. Фраза "активность против резистентной к лекарству форме HIV" означает, что соединение (или его пролекарство, или фармацевтически приемлемая соль) активно против мутантного штамма с ЕС 50 (средней эффективной концентрацией), например меньше чем приблизительно 50, 25, 10 или 1 мкмоль. В одном из воплощений ненуклеозидный ингибитор обратной транскриптазы (NNRTI) демонстрирует ЕС 50 (в мольной концентрации) против мутантного штамма HIV меньше чем приблизительно 5, 2,5, 1 или 0,1 мкмоль. В одном из не ограничивающих объем изобретения воплощений мутантный штамм HIV имеет мутацию обратной транскриптазы по лизину 103 аспарагин и/или тирозин 181 цистеин. Предложенные здесь соединения могут быть оценены в отношении их способности ингибировать активность обратной транскриптазы in vitro в соответствии со стандартными способами скрининга.- 10016267 Спектр активности, демонстрируемой каким-либо конкретным соединением, определяют путем оценки соединения в анализах, описанных в этом описании или других подтверждающих анализах, известных специалистам в области соединений против HIV. Соединения могут демонстрировать ЕС 50 меньше чем 10-15 мкМ. В одном из воплощений эффективность 3-фосфоиндолов измеряют при помощи иммуноферментного анализа, специфического в отношении HIV, р 24 ELISA. Эффективность лекарства выражают в виде процентного ингибирования р 24 антигена HIV в этом быстром и чувствительном анализе. В родственном воплощении, полезном для конкретных экспериментов, эффективность соединения против HIV определяют при помощи "анализа уменьшения бляшек", в котором измеряют концентрацию соединения, необходимую для уменьшения количества бляшек вируса in vitro, в соответствии со способами, изложенными более конкретно далее, на 50% (т.е. ЕС 50 соединения). В некоторых воплощениях соединение демонстрирует ЕС 50 меньше чем 15 или меньше чем 10 мкмоль до наномольных количеств in vitro. В еще одном аспекте здесь предложены способы перорального введения соединения формулы (С) для терапии или для лечения. Как показано в приведенных ниже примерах, некоторые соединения формулы (С) обладают пероральной биодоступностью с благоприятной фармакокинетикой. В еще одном аспекте здесь предложены способы ингибирования цитохрома Р 450. Как показано в приведенных ниже примерах, некоторые описанные здесь соединения эффективны для ингибирования одного или более чем одного цитохрома Р 450, включая цитохром Р 450 3 А 4, цитохром Р 450 2 С 8 и цитохром Р 450 2 С 9. Соответственно здесь предложены способы применения предложенных здесь соединений для ингибирования цитохрома Р 450. Способы включают стадию приведения в контакт цитохрома Р 450 с количеством раскрытого здесь соединения, такого как соединение формулы (С), эффективным для ингибирования цитохрома Р 450. В еще одном аспекте здесь предложены способы модуляции фармакокинетики лекарства, метаболизируемого цитохромом Р 450. Способы включают стадию введения лекарства в комбинации или путем чередования с описанным здесь соединением. Лекарство может представлять собой любую фармацевтически приемлемую молекулу, известную специалистам в данной области техники как метаболизируемую цитохромом Р 450. В некоторых воплощениях цитохром Р 450 представляет собой цитохром Р 450 3 А 4,цитохром Р 450 2 С 8 или цитохром Р 450 2 С 9. Предложенные здесь соединения могут быть введены самостоятельно или в комбинации либо путем чередования с одним или более чем одним другим противовирусным агентом. Соединения или их композиции также могут быть использованы профилактически для предотвращения или замедления прогресса клинического заболевания индивидов, несущих антитело против HIV, являющихся положительными по HIV-антигену, или подвергшихся воздействию вируса HIV. В еще одном аспекте предложены композиции и способы лечения хозяина, коинфицированногоHIV и гепатитом В, включающие введение чистого раскрытого здесь соединения в комбинации с одним или более чем одним агентом, эффективным для лечения инфекции гепатитом В. В еще одном аспекте предложены композиции и способы лечения хозяина, коинфицированного HIV и гепатитом С, включающие введение чистого раскрытого здесь соединения в комбинации с одним или более чем одним агентом, эффективным для лечения инфекции гепатитом С. Комбинированная или чередующаяся терапия В некоторых воплощениях индольное соединение вводят в комбинации и/или путем чередования с одним или более чем одним другим агентом против HIV. В еще одном воплощении введение двух или более чем двух агентов против HIV приводит в результате к синергическому действию при ингибировании HIV. В еще одном воплощении действие от введения двух или более чем двух таких агентов в комбинации и/или путем чередования приводит к аддитивному действию при ингибировании репликацииHIV. В некоторых воплощениях индольное соединение вводят в комбинации и/или путем чередования с одним или более чем одним агентом против HBV или одним или более чем одним агентом против HCV. Например, в некоторых воплощениях индольное соединение может быть введено хозяину, коинфицированному HIV и HBV в комбинации с агентом, эффективным для лечения HBV. Агент, эффективный для лечения HBV, может представлять собой любой такой агент, известный специалистам в области техники. Здесь описаны примеры агентов. В некоторых воплощениях индольное соединение может быть введено хозяину, коинфицированному HIV и HCV, в комбинации с агентом, эффективным для лечения HCV. Агент, эффективный для лечения HCV, может представлять собой любой такой агент, известный специалистам в данной области техники. В некоторых воплощениях индольное соединение вводят в комбинации и/или путем чередования с одним или более чем одним агентом, который метаболизируется цитохром Р 450-монооксигеназой. Агент может представлять собой любой агент, который, как известно специалистам в данной в области техники, метаболизируется цитохром Р 450-монооксигеназой. Здесь описаны примеры агентов. В некоторых воплощениях цитохром Р 450 представляет собой цитохром Р 450 3 А 4,цитохром Р 450 2 С 8 или цитохром Р 450 2 С 9. В комбинированной терапии эффективные дозы двух или более чем двух агентов вводят вместе, тогда как при чередующейся терапии эффективную дозу каждого агента вводят последовательно. Дозы- 11016267 зависят от скоростей абсорбции, инактивации и экскреции лекарств, а также других факторов, известных специалистам в данной области техники. Дозы также варьируют в зависимости от тяжести состояния,которое облегчают. Для любого конкретного индивида специфические схемы и графики приема лекарственного средства должны быть скорректированы по времени для того, чтобы удовлетворять потребностям индивида, и в зависимости от профессионального решения лица, осуществляющего введение или наблюдающего за введением композиций. Лекарственная резистентность наиболее типично возникает при мутации гена, кодирующего фермент, используемый в цикле вирусной репликации. Продемонстрировано, что эффективность лекарства против HIV может быть продлена, увеличена или восстановлена путем введения соединения в комбинации или путем чередования со вторым и, возможно, третьим противовирусным соединением, вызывающим мутацию(и), отличающуюся(иеся) от выбранной(ых) для основного лекарства. Такие комбинации лекарств одновременно уменьшают возможность резистентности в отношении любого единичного лекарства и любые ассоциированные токсичные действия. Альтернативно, фармакокинетика, биологическое распределение или другие параметры лекарства могут быть изменены при помощи такой комбинированной или чередующейся терапии. Например, применение комбинации лекарств может дать возможность для введения индивидуального лекарства в комбинации в дозировке, меньшей чем дозировка, которая потребовалась бы при введении лекарства в виде монотерапии. Аналогично, когда объединяют лекарства, направленные против различных стадий жизненного цикла вируса, существует возможность усиления их действий. Кроме того, применение комбинаций лекарств может уменьшать или устранять неблагоприятные побочные действия применения одиночного лекарства, в то же время обеспечивая противовирусное действие. Как правило, комбинированная терапия обычно предпочтительна перед чередующейся терапией, поскольку она оказывает множественное одновременное воздействие на вирус. Агенты против HCV Интерфероны (IFN) для лечения хронического гепатита почти в течение десятилетия имеются в продаже и образуют основу имеющихся в настоящее время терапий против HCV. IFN представляют собой гликопротеины, продуцируемые иммунными клетками в ответ на вирусные инфекции. Они ингибируют репликацию множества вирусов, включая HCV, и при использовании в качестве самостоятельного лечения инфицирования гепатитом С IFN могут иногда подавлять РНК HCV в сыворотке крови до необнаруживаемых уровней. Кроме того, IFN могут нормализовать уровни аминотрансферазы в сыворотке крови. К сожалению, действие IFN является временным, и длительный ответ возникает только у 8-9% пациентов, хронически инфицированных HCV (Gary L. Davis, Gastroenterology, 2000, 118:S104-S114). Тем не менее, большинство пациентов тяжело переносят лечение интерфероном, который вызывает тяжелые симптомы, подобные симптомам гриппа, утрату массы тела и потерю энергии и сопротивляемости организма. Во множестве патентов раскрыты способы лечения Flaviviridae, включая HCV, при которых используются основанные на интерфероне терапии. Например, в патенте США 5980884, выданном Blattet al., раскрыты способы лечения пациентов, пораженных HCV, с использованием консенсусного интерферона. В патенте США 5942223, выданном Bazer et al., раскрыта терапия против HCV с использованием овечьего или бычьего интерферона тау. В патенте США 5928636, выданном Alber et al., раскрыта комбинированная терапия интерлейкином-12 и интерфероном-альфа для лечения инфекционных заболеваний, включая HCV. В патенте США 5849696, выданном Chretien et al., раскрыто применение тимозинов, самостоятельно или в комбинации с интерфероном для лечения HCV. В патенте США 5830455,выданном Valtuena et al., описана комбинированная терапия HCV, в которой используется интерферон и акцептор свободного радикала. В патенте США 5738845, выданном Imakawa, описано применение белков человеческого интерферона-тау для лечения HCV. Другие основанные на интерфероне способы лечения HCV приведены в патенте США 5676942, выданном Testa et al., и патенте США 5372808,выданном Blatt et al. Во множестве патентов также раскрыты пегилированные формы интерферонов и их применение, таких как, например, патенты США 5747646, 5792834 и 5834594, все из которых выданы Hoffmann-LaRoche, Inc.; PCT WO 99/32139 и WO 99/32140 от Enzon; WO 95/13090 и патенты США 5738846 и 5711944, выданные Schering Corporation; и патент США 5908621, выданный Glue et al. Интерферон альфа-2 а и интерферон альфа-2b в настоящее время приняты в качестве монотерапии для лечения HCV. ROFERON-A от Roche представляет собой рекомбинантную форму интерферона альфа-2 а. PEGASYS от Roche представляет собой пегилированную или модифицированную полиэтиленгликолем форму интерферона альфа-2 а. INTRON А от Schering Corporation представляет собой рекомбинантную форму интерферона альфа-2b, и PEG-INTRON от Schering Corporation представляет собой пегилированную форму интерферона альфа-2b. Другие формы интерферона альфа, а также интерферон бета, гамма, тау и омега в настоящее время разрабатываются для лечения HCV. Включенные здесь примеры представляют собой INFERGEN, интерферон альфакон-1, от InterMune; OMNIFERON, природный интерферон, от Viragen; ALBUFERON отHuman Genome Sciences; REBIF, интерферон бета-1 а, от Ares-Serono; омега интерферон от BioMedicine; интерферон альфа для перорального введения от Amarillo Biosciences и интерфероны гамма, тау и гамма- 12016267 1-b от InterMune. Рибавирин (1D-рибофуранозил-1-1,2,4-триазолил-3-карбоксамид) представляет собой синтетический, не индуцирующий интерферон нуклеозидный аналог широкого противовирусного спектра, продаваемый под товарным знаком Virazole (The Merck Index. 11th Ed., 1989, Editor: Budavari, S., MerckCo.,Inc., Rahway, NJ; p. 1304). Смотри патент США 3798209 и RE29835. Структурно рибавирин близок гуанозину и обладает активностью in vitro против нескольких ДНК и РНК вирусов, включающихFlaviviridae (Gary L. Davis, 2000, Gastroenterology, 118:S104-S114). Рибавирин уменьшает уровни аминотрансферазы в сыворотке крови до нормального у 40% пациентов, но не уменьшает уровни РНК HCV в сыворотке крови (Gary L. Davis, 2000, Gastroenterology,118:S104-S114). Таким образом, рибавирин самостоятельно не эффективен при уменьшении уровней вирусной РНК. Дополнительно рибавирин обладает значительной токсичностью и, как известно, вызывает анемию. Он не одобрен для монотерапии против HCV, но одобрен в комбинации с интерфероном альфа 2 а или интерфероном альфа-2b для лечения HCV. Существующий в настоящее время стандарт лечения хронического гепатита С представляет собой комбинированную терапию альфа интерфероном и рибавирином. Исследования продемонстрировали,что больше пациентов, страдающих от HCV, отвечают на комбинированную терапию пегилированным интерфероном-альфа/рибавирином по сравнению с комбинированной терапией непегилированным интерфероном альфа. Тем не менее, как с монотерапией во время комбинированной терапии развиваются значительные побочные действия, включающие гемолиз, симптомы, подобные симптомам гриппа, анемию и утомляемость (Gary L. Davis, 2000, Gastroenterology, 118: S104-S114). Комбинированная терапия капсулами PEG-INTRON (пегинтерферон альфа-2b) и REBETOLREBETOL от Schering Corporation также одобрен в комбинации с INTRON А (рекомбинантный интерферон альфа-2b от Schering Corporation). Roche's PEGASYS (пегилированный интерферон альфа 2 а) и COPEGUS (рибавирин) также одобрен для лечения инфекции HCV. В заявках РСТ WO 99/59621, WO 00/37110, WO 01/81359, WO 02/32414 и WO 03/024461, все отSchering Corporation, раскрыто применение комбинированной терапии пегилированным интерфероном альфа и рибавирином для лечения инфекции HCV. В заявках РСТ WO 99/15194, WO 99/64016 и WO 00/24355, все от Hoffmann-LaRoche, Inc., также раскрыто комбинированное применение пегилированного интерферона альфа и рибавирина для лечения инфекции HCV. Ведется разработка новых противовирусных агентов для лечения инфекций Flaviviridae, в особенности инфекций гепацивирусом HCV. Исследуют специфические ингибиторы HCV-производных ферментов, таких как протеаза, геликаза и полимераза. Также исследуются лекарства, которые ингибируют стадии репликации HCV, и включают лекарства,которые блокируют продукцию антигенов HCV из РНК (IRES ингибиторы), лекарства, которые предотвращают нормальный процессинг белков HCV (ингибиторы гликозилирования), лекарства, которые блокируют проникновение HCV в клетки, такое как путем блокирования их рецепторов, и неспецифические цитопротективные агенты, которые блокируют повреждение клеток, вызванное вирусной инфекцией. Кроме того, исследуются молекулярные подходы к лечению инфекции вирусом гепатита С. Например,проводятся исследования рибозимов, ферментов, которые разрушают специфические молекулы вирусной РНК, и антисмысловых олигонуклеотидов, которые представляют собой небольшие комплементарные сегменты ДНК, которые связываются и ингибируют вирусную РНК. Обзор способов лечения HCV можно найти в Bymock et al., Antiviral ChemistryChemotherapy, 2000,11:2 и De Francesco et al., AntiviralRes., 2003, 55:1-16. Другие классы лекарств, которые разрабатывают для лечения инфицирования Flaviviridae и инфицирования гепатитом С, в частности, включают: 1) ингибиторы протеазы: а) основанные на субстрате ингибиторы протеазы NS3 раскрыты Artwood et al. в WO 98/22496 и DE 19914474; в Attwood et al. Antiviral Chemistry and Chemotherapy, 1999, 70:259-273 и Tung et al. в WO 98/17679, которые включают альфакетоамиды и гидразиномочевины; б) ингибиторы субстрата, которые заканчиваются электрофилом, таким как бороновая кислота или фосфонат, представлены Llinas-Brunet et al. в WO 99/07734; в) не основанные на субстрате ингибиторы протеазы NS3, такие как 2,4,6-тригидрокси-3-нитробензамидные производные, RD3-4082 и RD3-4078 (первый замещен по амиду 14-углеродной цепью, а последний имеет пара-феноксифенильную группу), представлены Sudo et al. в Biochemical and Biophysical Res. Comm., 1997, 255:643-7 и в Antiviral Chemistry and Chemotherapy, 1998, 9:186; г) Sch 68631, фенантренхинон, раскрытый Chu et al. в Tetrahedron Letters, 1996, 57:7229-32 и Sch 351633, выделенный из гриба Penicillium griseofulvum, раскрытый Chu et al. в Bioorganic and MedicinalChem. Lett., 9:1949-52; д) Eglin с, макромолекула, выделенная из пиявок, которая демонстрирует наномольную активность ингибирования по сравнению с некоторыми сериновыми протеазами, такими как S. griseus протеазы А и В, -химотрипсин, химаза и субтилизин, как раскрыто Qasim et al., Biochemistry, 1997, 36:1598-1607;- 13016267 е) ингибиторы цистеиновых протеаз для ингибирования HCV эндопептидазы 2, как раскрыто в патенте США 6004933, выданном Spruce et al.; ж) синтетические ингибиторы NS3 протеазы вируса гепатита С или NS4A кофактора, представляющие собой подпоследовательности субстратов, используемых протеазой и/или кофактором, как показано в патенте США 5990276, выданном Zhang et al.; з) рестриктазы для лечения HCV, раскрытые в патенте США 5538865, выданном Reyes et al.; и) пептиды, такие как ингибиторы NS3 сериновой протеазы HCV, как представлено в WO 02/008251 от Corvas International, Inc. и в WO 02/08187 и WO 02/008256 от Schering Corporation; к) HCV трипептидные ингибиторы, раскрытые в патентах США 6534523; 6410531 и 6420380,выданных Boehringer Ingelheim и WO 02/060926 от Bristol Myers Squibb; л) диарильные пептиды, такие как ингибиторы сериновой протеазы HCV, изложенные Schering Corporation в WO 02/48172; м) имидазолидиноны, такие как ингибиторы NS3 сериновой протеазы HCV, раскрытые в WO 02/08198 от Schering Corporation и WO 02/48157 от Bristol Myers Squibb; и н) ингибиторы протеазы HCV, изложенные Vertex Pharmaceuticals в WO 98/17679 и Bristol MyersSquibb в WO 02/48116; 2) тиазолидиновые производные, демонстрирующие релевантное ингибирование в анализе путем обращенно-фазовой ВЭЖХ со слитым белком NS3/4A и субстратом NS5A/5B, что продемонстрировано вSudo et al., Antiviral Res., 1996, 52:9-18, в особенности соединения RD4 6205, RD4 6193 и RD-1-6250, которые имеют конденсированную циннамоильную группировку, замещенную длинной алкильной цепью; 3) тиазолидины и бензанилиды, раскрытые Kakiuchi et al., J. FEBS Letters, 421:217-220 и Takeshita etal., Analytical Biochemistry, 1997, 247:242-46; 4) ингибиторы геликазы, раскрытые Diana et al. в патенте США 5633358 и WO 97/36554; 5) нуклеотидные ингибиторы полимеразы и глиотоксин, представленные R. Ferrari et al., J. Virology,1999, 73:1649-54; 6) церуленин, природный продукт, представленный V. Lohmann et al., Virology, 1998, 249:108-118; 7) антисмысловые фосфоротиоатные олигодезоксинуклеотиды (S-ODN), комплементарные протяженным последовательностям в 5'-н кодирующей (NCR) последовательности вируса Flaviviridae, как продемонстрировано М. Alt et al., Hepatology, 1995, 22:707-717; 8) нуклеотиды 326-348, содержащие 3'-конец NCR, и нуклеотиды 371-388, располагающиеся в коровой кодирующей области РНК HCV, что продемонстрировано М. Alt et al., Archives of Virology, 1997,742:589-599; Galderisi et al., J. of Cellular Physiology, 1999, 757:251-257; 9) ингибиторы IRES-зависимой трансляции, раскрытой Ikeda et al., JP-08268890, и Y. Kai et al., JP10101591; 10) рибозимы, такие как резистентные к нуклеазе рибозимы, представленные D.D. Maccjak et al.,Hepatology, 1999, 50: abstract no. 995; Barber et al. в патенте США 6043077 и Draper et al. в патентах США 5869253 и 5610054; 11) нуклеозидные аналоги, включая применение разветвленных нуклеозидов при лечении флавивирусов, пестивирусов и гепацивируса, как представлено Idenix Pharmaceuticals в WO 01/92282, WO 01/90121, патентах США 6812219 и 6914054, где способ раскрыт для лечения инфекции гепатитом С,пестивирусом и/или флавивирусом у людей и других животных-хозяев, включающий введение эффективного количества биологически активного 1'-, 2'-, 3'- или 4'-разветвленных (-D или -L нуклеозидов или их фармацевтически приемлемой соли или производного, вводимых самостоятельно или в комбинации с другим противовирусным агентом, возможно, в фармацевтически приемлемом носителе. Нуклеозидные аналоги также можно найти в WO 01/32153 и WO 01/60315 от BioChem Pharma, Inc. (в настоящее время Shire Biochem, Inc.); WO 02/057425 и WO 02/057287, поданных MerckCo., Inc.; WO 02/18404 отRoche; WO 01/79246, WO 02/32920 и WO 02/48165 от Pharmasset, Ltd.; и WO 99/43691 от Emory University. На устных слушаниях V, посвященных вирусу гепатита С, Flaviviridae, 16 международной конференции по антивирусным исследованиям, 27 апреля, Саванна, Джоржия (Oral Session V, Hepatitis С Virus,Flaviviridae, 16th International Conference on Antiviral Research, April 27, 2003, Savannah, GA), 2'модифицированные нуклеозиды для ингибирования HCV описаны Eldrup et al.; нуклеозидные аналоги как возможные ингибиторы репликации РНК HCV изложены Bhar et al. (p. A75), где автор сообщает о том, что 2'-модифицированные нуклеозиды демонстрируют сильную ингибирующую активность в основанных на клетках анализах репликона; действие 2'-модифицированных нуклеозидов на репликацию РНК HCV сообщалось Olsen et al. (p. A76). 12) смешанные соединения, разработанные для лечения инфекций Flaviviridae и инфекций гепатитом С, в частности, включают 1-аминоалкилциклогексаны, описанные в патенте США 6034134, выданном Gold et al.; алкиллипиды, витамин Е и другие антиоксиданты в патенте США 5922757, выданном Chojkier et al.; сквален, амантадин и желчные кислоты, представленные в патенте США 5846964,выданном Ozeki et al.; N-(фосфоноацетил)-L-аспарагиновая кислота и пиперидины, представленные в патенте США 5830905, выданном Diana et al.; бензолдикарбоксамиды, раскрытые в патенте США 5633388, выданном Diana et al.; производные полиадениловой кислоты, описанные в патенте СШАal., и патенте США 5725859, выданном Omer et al.; 13) соединения, в настоящее время находящиеся в преклинической или клинической разработке для лечения вируса гепатита С, включая интерлейкин-10 от Schering Plough; IP-501 от Interneuron; меримебодиб (VX-497) от Vertex; AMANTADINE (Symmetrel) от Endo Labs Solvay; HEPTAZYME от RPI; IDN6556 от Idun Pharmaceuticals; XTL-002 от XTL; HCV/MF59 от Chiron; CIVACIR (иммуноглобулин против гепатита С) от NABI; LEVOVIRIN от ICN/Ribapharm; VIRAMIDINE от ICN/Ribapharm (Valeant);ZADAXIN (тимозин альфа-1) от Sci Clone; тимозин плюс ПЭГилированный интерферон от Sci Clone;Isis Pharmaceuticals/Elan; JTK 003 от AKROS Pharma; BILN-2061 от Boehringer Ingelheim; CellCept (микофенолата мофетил) от Roche; T67 (P-тубулиновый ингибитор) от Tularik; терапевтическую вакцину, направленную на Е 2, от Innogenetics; FK788 от Fujisawa Healthcare, Inc.; IdB 1016 (Siliphos, силибинфосфатидилхолиновая фитосома для перорального введения); ингибитор репликации РНК VP50406 отViroPharma/Wyeth; терапевтические вакцины от Intercell and Epimmune/Genencor; ингибитор IRES отBristol Myers Squibb/Axys и Corvas/Schering; ингибитор геликазы от Vertex; ингибитор слияния отTrimeris; Т-клеточную терапию от CellExSys; ингибитор полимеразы от Biocryst; нацеленное на РНК химическое соединение от РТС Therapeutics; дикатион от Immtech, International; ингибиторы протеаз отAgouron и Chiron/Medivir; антисмысловые способы терапии от AVI BioPharma и Hybridon; гемоочиститель от Aethlon Medical; терапевтическую вакцину от Merix; "Chron-VacC", терапевтическую вакцину, отTripep; UT 23IB от United Therapeutics; ингибиторы протеазы, геликазы и полимеразы от Genelabs Technologies; ингибиторы IRES от Immusol; R803 от Rigel Pharmaceuticals; INFERGEN (интерферон альфакон-1) от InterMune; OMNIFERON (природный интерферон) от Viragen; ALBUFERON от Human Genome Sciences; REBIF (интерферон бета-1 а) от Ares-Serono; омега интерферон от BioMedicine; интерферон альфа для перорального введения от Amariilo Biosciences; интерфероны гамма, тау и гамма-1b отInterMune; консенсусный интерферон от Valeant; нексавар от Onyx Pharmaceuticals; PI-88 от Progen Industries; трансгенный доксорубицин от Bio Alliance Pharma; JBK-122 от Jenken Biosciences; валопицитабин от Idenix; VGX-410C от VGX Pharmaceuticals; целгосивир от Migenix; сувус от Bioenvision; мультиферон от Viragen; омега интерферон от Intarcia; INNO0101 (Е 1) от Innogenetics; PF-03491390 от Pfizer; интерферон медузы от Flamel Technologies; IC41 от Intercell; SCH 503034 от Schering; G126270 от GlaxoSmithKline; GV1001 от Pharmexa; R1626 от Roche; Maxygen/Roche; R7128 от Pharmasset/Roche; белерофон отNautilus Biotech; алинию от Romark; бавитуксимаб от Peregrine; пероральный интерферон альфа от Amarillo Biosciences; NOV-205 от Novelos; CGI 5005 от GlobeImmune; HCV-796 от ViroPharma/Wyeth;DEBIO и UT-231B от United Therapeutics; 14) нуклеозидные пролекарства, описанные ранее для лечения других форм гепатита, включая 2'дезоксиL-нуклеозиды и их 3'-пролекарства для лечения HBV, раскрытые в WO 00/09531 и WO 01/96353, выданных Idenix Pharmaceuticals; и терапевтические сложные эфиры ацикловира, представленные в патенте США 4957924, выданном Beauchamp. Другие примеры противовирусных агентов, которые могут быть использованы в комбинации и/или при чередовании с раскрытыми здесь соединениями,включают агенты, такие как VX-950 и интерферон, но не ограничиваются ими. Интерфероны, которые могут быть использованы, включают альфа интерферон-2b от Schering-Plough, Intron А и PEG-Intron; и Co-Pegasus и PEGASYS (пегилированный интерферон альфа-2 а) от Hoffman La Roche. Агенты против гепатита В Агент против гепатита В может представлять собой любой агент, который известен специалистам в данной области техники как эффективный для лечения инфекции гепатитом В у нуждающегося в этом хозяина. В некоторых воплощениях агент против гепатита В представляет собой интерферон-альфа (Intron A, Schering-Plough), пегилированный интерферон (Pegasys, Roche), ламивудин (Epivir-HBV, Zeffix,или Heptodin, Glaxo-Smithkline), адефовир дипивоксил (Hepsera, Gilead), энтекавир (Baraclude, BristolMyers-Squibb), телбивудин (Tyzeka или Sebivo, Idenix) или иммуноглобулин против HBV (HyperHEP S/D,Talecris; Nabi-HBV, Nabi; Hepa Gam B, Cangene). В некоторых воплощениях агент против гепатита В представляет собой FTC (эмтрицитабин,Gilead), L-FMAU (клевудин, Pharmasset; Levovir, Bukwang), тенофовир (виреад, Gilead), monoval LdCeiRNA (HepX, Nucleonics), HepaVaxx В (Virexx), вакцину против корового антигена HBV (EmergentEurope) или SpecifEx-HepB (Chromos). Другие противовирусные агенты Любой из способов лечения от вируса, описанных здесь в разделе "Предшествующий уровень техники", может быть использован в комбинации или путем чередования с соединениями, описанными в этом описании. Не ограничивающие объем изобретения примеры включают а) ингибиторы протеазы; б) тиазолидиновые производные; в) ингибиторы геликазы; г) бензанилиды; д) фенантренхиноны; е) ингибиторы полимеразы и глиотоксин; ж) антисмысловые фосфоротиоатные олигодезоксинуклеотиды (S-ODN); з) ингибиторы IRES-зависимой трансляции; и) рибозимы; к) нуклеозидные аналоги; л) двузамещенные нуклеозидные аналоги, раскрытые Idenix Pharmaceuticals в WO 01/90121, WO 01/92282, WO 04/00300,WO 04/002999 и WO 04/002422; м) 2'-фторнуклеозидные аналоги; н) 1-NH2-алкилциклогексаны; о) алкиллипиды; п) витамин Е и другие антиоксиданты; р) сквален, амантадин и желчные кислоты; с) N(фосфоноацетил)-L-аспарагиновую кислоту; т) бензолдикарбоксамиды; у) производные полиадениловой кислоты; ф) бензимидазолы; х) 2',3'-дидезоксиинозин; ц) растительные экстракты; ч) пиперидины и ш) другие соединения, в настоящее время находящиеся в преклинической или клинической разработке для лечения пестивирусов, флавивирусов и/или гепацивируса, включая рибавирин и семейства интерферонов. Второй противовирусный агент для лечения HIV может представлять собой, например, ингибитор протеазы, ингибитор интегразы HIV, хемокиновый ингибитор или ингибитор обратной транскриптазы("RTI"), последний из которых может представлять собой синтетический нуклеозидный ингибитор обратной транскриптазы ("NRTI") или ненуклеозидный ингибитор обратной транскриптазы ("NNRTI"). В других воплощениях второе или третье соединение может представлять собой пирофосфатный аналог или связанный со слиянием ингибитор. Перечень обобщенных данных по резистентности, собранных invitro и in vivo для некоторых противовирусных соединений, можно найти в Schinazi et al. Mutations inretroviral genes associated with drug resistance, International Antiviral News, 1997, 5(8). В некоторых воплощениях индольное соединение вводят в комбинации и/или при чередовании с(Viread), D4T или AZT. Другие примеры противовирусных агентов, которые могут быть использованы в комбинации и/или при чередовании с раскрытыми здесь соединениями, включают фоскарнет; карбовир; ацикловир; интерферон; слитые ингибиторы, такие как энфувиртид; и -D-диоксолановые нуклеозиды, такие как -Dдиоксоланилгуанин (DXG), -D-диоксоланил-2,6-диаминопурин (DAPD), и -D-диоксоланил-6 хлорпурин (АСР), но не ограничиваются ими. Интерфероны, которые могут быть использованы, включают альфа интерферон-2b от Schering-Plough, Intron А и PEG-Intron; и Co-Pegasus и PEGASYS (пегилированный интерферон альфа-2 а) от Hoffman La Roche. Комбинации, с которыми могут быть введены 3-фосфоиндолы, включают эпзиком (АВС+3 ТС), тризивир (ABC + 3 ТС + AZT), трувада (FTC +Viread) и комбивир (AZT+3TC). Примеры ингибиторов протеаз, которые могут быть использованы в комбинации и/или при чередовании с раскрытыми здесь соединениями, включают индинавир (1(1S,2R),5(S)-2,3,5-тридезокси-N-(2,3 дигидро-2-гидрокси-1 Н-инден-1-ил)-5-[2-(1,1-диметилэтил)амино]карбонил]-4-(3-иридинилметил)-1 пиперазинил]-2-(фенилметил)-D-эритропентоамида сульфат; MerckCo., Inc.); нелфинавир (Agouron); ритронавир (Abbott Labs), саквинавир (Roche); ампренавир; атазанавир; фосампренавир; калетру и DMP450[4R-4(r-а,5-а,6-b,7-6)гексагидро-5,6-бис-(гидрокси)-1,3-бис-(3-амино)фенил]метил-4,7-бис(фенилметил)-2 Н-1,3-диазепин-2-он-бис-мезилат (Triangle Pharmaceuticals, Inc.), но не ограничиваются ими. Другие соединения, которые могут быть введены в комбинации или путем чередования с фосфоиндолом для усиления его противовирусных свойств, включают (1S,4R)-4-[2-амино-6-циклопропиламино 9 Н-пурин-9-ил]-2-циклопентен-1-метанола сукцинат (1592U89, аналог карбовира от GlaxoSmithKline);(аминодиольное производное ингибитор протеазы HIV-1) (Bristol-Myers Squibb); d4API (9-[2,5-дигидро 5-(фосфонометокси)-2-фуранил]аденин) (Gilead); HBY097 (S-4-изопропоксикарбонил-6-метокси-3[метилтиометил]-3,4-дигидрохиноксалин-2(1 Н)тион); НЕРТR)-9-(2 фосфонилметоксипропил)аденин) (Gilead); Ro 31-8959 (гидроксиэтиламиновое производное ингибитор протеазы HIV-1) (Roche); RPI-3121 (пептидильный ингибитор протеазы, 1-[(3S)-3-(н-альфабензилоксикарбонил)-1-аспаргинил)амино-2-гидрокси-4-фенилбутирил]-н-трет-бутил-1-пролина амид); 2720 (6-хлоро-3,3-диметил-4-(изопропенилоксикарбонил)-3,4-дигидрохиноксалин-2(1 Н)тион); SC-52151(гидроксиэтилмочевины изостерический ингибитор протеазы) (G.D. Searle); SC-55389A (гидроксиэтилмочевины изостерический ингибитор протеазы (G.D. Searle); TIBO R82150 +)-(5S)-4,5,6,7-тетрагидро-5 метил-6-(3-метил-2-бутенил)имидазо[4,5,1-jk]-[1,4]бензодиазепин-2(1 Н)тион) (Janssen Pharmaceuticals);Merck) и пенцикловир. В еще одном воплощении индольное соединение по изобретению вводят в комбинации с ингибитором протеазы LG 1350. Следующие лекарства могут быть использованы в комбинации и/или путем чередования с соединениями по настоящему изобретению- 21016267 Дополнительные лекарства, которые могут быть использованы в комбинации и/или путем чередования с 3-фосфоиндолами, включают Следующие лекарства могут быть использованы в комбинации и/или путем чередования с соединениями по настоящему изобретению Могут быть использованы продукты, которые разрешены к применению как Исследуемые новые лекарства (IND) в соответствии с FDA (Управление по контролю за продуктами питания и лекарственными средствами) для лечения осложнений инфекции HIV и AIDS. Следующие лекарства могут быть использованы в комбинации и/или путем чередования с соединениями по настоящему изобретению. Триметрексата глюкуронат для лечения пневмонии, вызванной Pneumocystis carinii, у пациентов,страдающих от AIDS, которые не могут переносить стандартные формы лечения. Ганцикловир для лечения ретинита, вызванного цитомегаловирусом, у пациентов, страдающих отAIDS. Аэрозольный пентамидин для профилактики пневмонии, вызванной Pneumocystis carinii, у пациентов, страдающих от AIDS. Эритропоэтин для лечения анемии, связанной с зидовудином. Атовахон для лечения пациентов, страдающих от AIDS, имеющих пневмонию, вызванную Pneumocystis carinii, не толерантных или не проявляющих ответ на триметоприм-сульфаметоксазол. Рифабутин для профилактики против бактериемии, вызванной комплексом Mycobacterium avium, у пациентов, страдающих от AIDS. Вистид внутривенный цидофовир для лиц, инфицированных HIV, с рецидивами цитомегаловируса(CMV), который прогрессирует, несмотря на лечение (Hoffmann-La Roche). Серостим, продуцируемый млекопитающими рекомбинантный человеческий гормон роста для лечения связанной с AIDS атрофии (Serono Laboratories). В конкретных воплощениях раскрытые здесь соединения могут быть введены в комбинации или путем чередования с одним, двумя или более чем двумя другими агентами против HIV. В одном из подвоплощений дополнительный агент выбран из ингибитора протеазы, возможно, выбранного из ампренавира, типранавира, индинавира, саквинавира (включающего саквинавира мезилат), лопинавира, ритронавира, фосампренавира, дарунавира, атазанавира (включающего соль сульфат) и нелфинавира (включающего соль мезилат); нуклеозидного или нуклеотидного ингибитора обратной транскриптазы, возможно, выбранного из ламивудина, эмтрицитабина, абакавира, залцитабина, зидовудина, тенофовира (включающего тенофовира дизопроксила фумарата), диданозина и ставудина; ненуклеозидного ингибитора обратной транскриптазы, возможно, выбранного из делавирдина, эфа- 24016267 виренза и невирапина; комбинации с фиксированной дозой, возможно, выбранной из атрипла, комбивира, тризивира и трувада; ингибитора проникновения (такого как ингибитор слияния или антагонист корецептора CCR5),возможно, выбранного из маравирока и энфувиртида; и ингибитора интегразы, такого как ралтегравир (MK-0518) или элвитегравир (GS-9137). Когда используют дополнительный агент против HIV, он может находиться в другой форме, такой как соль, сольват, гидрат, форма пролекарства, полиморф, энантиомер и т.п. Дополнительный агент против HIV также может быть выбран из нуклеозидного ингибитора обратной транскриптазы, возможно, выбранного из амдоксовира, априцитабина и элвуцитабина; ингибитора протеазы, который, возможно, представляет собой бреканивир или GS-8374; антагониста рецептора CCR5, возможно, выбранного из аплавирока, PRO2000 и викривирока; ненуклеозидного ингибитора обратной транскриптазы, который, возможно, представляет собой этравирин (ТМС-125), рилпивирин (ТМС-278) или каланолид А; ингибитора интегразы, который, возможно, представляет собой элвитегравир, GSK-364735 или ралтегравир; и ингибитора созревания, который, возможно, представляет собой бевиримат (РА 457); клеточного ингибитора, такого как гидроксимочевина; ингибитора проникновения, такого как викривирок или TNX-355; и иммунного ингибитора, такого как иммунитин (альфа-эпибромид), пролейкин (IL-2), ремун (HIV-1 иммуноген), BAY 50-4798 или IR103. Агенты, метаболизируемые цитохромом Р 450. В некоторых воплощениях предложенное здесь соединение может быть введено в комбинации или путем чередования с фармацевтически приемлемым агентом, метаболизируемым цитохром Р 450 моноксигеназой. Примеры полезных цитохром Р 450 моноксигеназ включают цитохром Р 450 2 С 8, цитохром Р 450 2 С 9 и цитохром Р 450 3 А 4. В некоторых воплощениях предложенные здесь чистые соединения могут ингибировать цитохром Р 450 моноксигеназу, таким образом улучшая фармакокинетику вводимого одновременно агента. В конкретных воплощениях ингибируемый изофермент Р 450 представляет собойCYP3A4. В конкретных воплощениях фосфоиндольное соединение вводят в комбинации со вторым соединением против HIV без необходимости сенсибилизации ритронавиром. В конкретных воплощениях фосфоиндольное соединение вводят в комбинации с одним или более чем одним из атазанавира, фосампренавира, дарунавира, индинавира, лопинавира, нелфинавира, саквинавира, типранавира или энфувиртида. В конкретных воплощениях фосфоиндольное соединение вводят в комбинированной терапии с одним или более чем одним нуклеозидным ингибитором обратной транскриптазы и/или одним или более чем одним ингибитором интегразы. Фармацевтически приемлемый агент, метаболизируемый цитохром Р 450 моноксигеназой, может представлять собой любой агент, известный или идентифицированный специалистом в области техники. Не ограничивающие объем изобретения примеры соединений, которые могут быть метаболизированы цитохром Р 450 моноксигеназой, включают паклитаксел, торсемид, амодиаквин, церивастатин и репаглинид (цитохром Р 450 2 С 8); некоторые NSAID (нестероидные противовоспалительные средства) (например, диклофенак, ибупрофен, лорноксикам, мелоксикам, S-напроксен, пироксикам, супрофен), некоторые вводимые перорально гипогликемические агенты (например, толбутамид, глипизид), некоторые блокаторы ангиотензина II (например, лосартан, ирбесартан), некоторые сульфонилмочевины (например,глибурид, глибенкламид, глипизид, глимепирид, толбутамид, амитриптилин), целекоксиб, флуоксетин,флувастатин глибурид, натеглинид, фенитоин, розиглитазон, тамоксифен, торсемид, S-варфарин (цитохром Р 450 2 С 9); некоторые макролидные антибиотики (например, кларитромицин, эритромицин, телитромицин), некоторые антиаритмические средства (например, хинидин), некоторые бензодиазепины (например, алпразолам, диазепам, мидазолам, триазолам), некоторые иммуномодуляторы (циклоспорин,такролимус), некоторые противовирусные средства против HIV (например, индинавир, нелфинавир, ритронавир, саквинавир), некоторые прокинетические агенты (например, цисаприд), некоторые антигистаминовые средства (например, астемизол, хлорфенирамин, терфенидин), некоторые блокаторы кальциевых каналов (например, амлодипин, дилтиазем, фелодипин, лерканидипин, нифедипин, низолдипин,нитрендипин, верапамил), некоторые ингибиторы HMG СоА редуктазы (например, аторвастатин, церивастатин, ловастатин, симвастатин), некоторые стероиды (эстрадиол, гидрокортизон, прогестерон, тестостерон), алфентанил, апрепитант, арипипразол, буспирон, кафергот, кафеин=TMU, цилостазол, кокаин,кодеин-N-деметилированный, дапсон, дексаметазон, декстрометорфан, доцетаксел, домперидон, эплеренон, фентанил, финастерид, глевек, галоперидол, иринотекан, LAAM, лидокаин, метадон, натеглинид,оданестрон, пимозид, пропранолол, кветиапин, хинин, рисперидон, NOT розувастатин, салметерол, силденафил, сиролимус, тамоксифен, таксол, терфенадин, тразодон, винкристин, залеплон, зипразидон, золпидем (цитохром Р 450 3 А 4), но не ограничиваются ими. В конкретных воплощениях здесь предложены- 25016267 способы в комбинации или путем чередования с противовирусными агентами против HIV, которые метаболизируются цитохромом Р 450 (например индинавиром, нелфинавиром, ритронавиром, саквинавиром). Дополнительные примеры соединений, которые могут метаболизироваться цитохром Р 450 моноксигеназой, включают ингибиторы CCR5 (например, PRO-140, вицивирок или SCH-417,690 и маравирок или UK-427857), ингибиторы интегразы (например, JTK-303/GS-9137, 6-(3-хлор-2-фторбензил)-1-[(2S)-1 гидрокси-3-метилбутан-2-ил]-7-метокси-4-оксо-1,4-дигидрохинолин-3-карбоновая кислота, MK-0518, 5(1,1-диоксидо-1,2-тиазинан-2-ил)-N-(4-фторбензил)-8-гидрокси-1,6-нафтиридин-7-карбоксамид, и описанные в патентах США 6924282, 6921759, 6919351, 6841558, 6541515, 6403347, 6395743, 6380249,6306891, 6271402, 6262055, 6245806, 6124327, 6110716, 5939414, 5858738, 5759842, 7176220 и 7112600,содержание которых включено здесь путем ссылки), ингибиторы протеаз (например, саквинавир, индинавир, ритронавир, нелфинавир, ампренавир, лопинавир, ритронавир, атазанавир, фосампренавир, типранавир, ампренавир и дарунавир), ингибиторы слияния (например, энфурвитид), ингибиторы созревания (например, бевиримат или РА-457) и нуклеозидные ингибиторы обратной транскриптазы (например,зидовудин, диданозин, залцитабин, ставудин, ламивудин, абакавир, энофовир, эмтрицитабин, комбивир,тризивир, трувада и эпзиком), но не ограничиваются ими. Дополнительные примеры соединений, которые могут быть метаболизированы цитохром Р 450 моноксигеназой, включают ритронавир, иммуносупрессанты циклоспорин, FK-506 и рапамицин, химиотерапевтические агенты таксол и таксотер, антибиотик кларитромицин и ингибиторы протеазы HIV А 77003, А-80987, MK-639, саквинавир, VX-478, AG1343, DMP-323, ХМ-450, BILA 2011 BS, BILA 1096BS, BILA 2185 BS, BMS 186,318, LB71262, SC-52151, SC-629 (N,N-диметилглицин-N-(2-гидрокси-3-4 метоксифенил)сульфонил)(2-метилпропил)амино)-1-(фенилметил)пропил)-3-метил-L-валинамид), KNI272, CGP 53437, CGP 57813 и U-103017, но не ограничиваются ими. В некоторых воплощениях предложены способы улучшения фармакокинетики ингибитора протеазы HIV (или его фармацевтически приемлемой соли), который метаболизируется цитохром Р 450 моноксигеназой. Способы включают введение ингибитора протеазы HIV в комбинации или путем чередования с описанным здесь соединением. Такая комбинация или чередование может быть полезно для ингибирования протеазы HIV у людей и также может быть полезно для ингибирования, лечения или профилактики инфекции HIV или AIDS у людей. Ингибитор протеазы HIV может представлять собой любой ингибитор протеазы HIV, известный специалистам в данной области техники. В некоторых воплощениях ингибитор протеазы HIV представляет собой ампренавир (агенераза, GlaxoSmithkline), типранавир (аптивус, Boehringer Ingelheim), индинавир (криксиван, Merck), саквинавир (фортоваза, Hoffmann-La Roche),саквинавира мезилат (инвираза, Hoffmann-La Roche), лопинавир и ритронавир (калетра, GlaxoSmithkline),ритронавир (норвир, Abort), дарунавир (презиста, Tibotec), атазанавира сульфат (Reyataz) или нелфинавира мезилат (вирацепт, Agouron) или их комбинацию. В конкретных подвоплощениях раскрытые здесь соединения могут быть введены в комбинации или путем чередования с одним, двумя или более чем двумя другими ингибиторами протеазы или ингибиторами интегразы - агентами против HIV, которые потенциально могут улучшать метаболизм второго агента. В одном из подвоплощений дополнительный агент выбран из ингибитора протеазы, возможно выбранного из ампренавира, типранавира, индинавира, саквинавира (включающего саквинавира мезилат), лопинавира, ритронавира, фосампренавира, дарунавира, атазанавира (включающего соль сульфат), нелфинавира (включающего соль мезилат), бреканавира или GS8374; ингибитора интегразы, такого как ралтегравир (MK-0518) или элвитегравир (GS-9137) или GSK364735. Как правило, при чередующейся терапии эффективную дозу каждого агента вводят последовательно. При комбинированной терапии эффективные дозы двух или более чем двух агентов вводят вместе. Вводимые дозы зависят от факторов, таких как скорости абсорбции, биораспределения, метаболизма и экскреции для каждого лекарства, а также других факторов, известных специалистам в данной области техники. Следует отметить, что количества доз варьируют в зависимости от тяжести состояния, которое облегчают, возраста, массы и общего физического состояния субъекта, принимающего лекарство. Также должно быть понятно, что для любого конкретного субъекта специфические схемы и графики приема лекарственного средства должны быть скорректированы по времени в соответствии с реакцией пациента на лекарство, потребностей субъекта и профессионального решения лица, осуществляющего введение или осуществляющего контроль за введением композиций. Примеры подходящих диапазонов доз для соединений, включающих нуклеозидные производные, такие как, например, D4T, DDI и 3 ТС, 2'разветвленный нуклеозиды или ингибиторы протеаз, такие как нелфинавир и индинавир, можно найти в научной литературе и настольных руководствах для лечащих врачей. Предложенные диапазоны эффективных доз соединений по настоящему изобретению представляют собой лишь руководство, и не предполагают, что они ограничивают объем или применение по изобретению. Раскрытая комбинированная и осуществляемая путем чередования схема приема может быть полезна при лечении и профилактике ретровирусных инфекций и других связанных состояний, таких как,- 26016267 например, комплекс, связанный со AIDS (ARC), персистирующая генерализованная лимфаденопатия(PGL), связанные со AIDS неврологические состояния, положение антител против HIV и HIVположительные состояния, саркома Капоши, пурпурная тромбоцитопения и оппортунистические инфекции. Кроме того, эти соединения или препараты могут применяться профилактически для предотвращения или замедления прогресса клинического заболевания у индивидов, являющихся положительными в отношении антител против HIV или антигена HIV либо которые подверглись воздействию HIV. Анализы. Предложенные здесь соединения могут быть проанализированы в отношении активности противHIV или инфекции HIV при помощи анализа, который, как полагает специалист в данной области, является подходящим. Примеры анализов включают анализы, описанные в этом разделе, и которые предложены в приведенных ниже примерах. Системы на основе культуры клеток для определения противовирусных активностей. Схемы обнаружения амплифицированного продукта. Гетерогенное обнаружение. Например, саузерн-блоттинг представляет собой способ гетерогенного обнаружения. При саузерн-блоттинге электрофорез используют для разделения продуктов амплификации по размеру и заряду. Фракционированные по размеру продукты переносят на мембрану или фильтр путем диффузии, вакуумирования или электроблоттинга. Меченые обнаруживающие зонды гибридизуют со связанными с мембраной мишенями в растворе, фильтры промывают для удаления любого негибридизованного зонда, и гибридизованный зонд на мембране обнаруживают при помощи любого из множества способов, известных специалистам в данной области техники. Другие типы гетерогенного обнаружения основаны на специфическом захвате продуктов амплификации при помощи иммуноферментных анализов (ИФА). Один из способов, используемых вместе с ПЦР(полимеразной цепной реакции), включает мечение одним праймером с гаптеном или лигандом, таким как биотин, и после амплификации захват антителом - или покрытым стрептавидином микропланшетом. Другой праймер метят репортером, таким как флуоресцеин, и обнаружение осуществляют путем добавления антитела против флуоресцеина, такого как конъюгат с пероксидазой хрена (HRP). Этот тип способа не так специфичен, как использование обнаруживающих зондов, которые гибридизуются с определенными интересующими продуктами амплификации. Система зондов LCx (Abbott Laboratories, Abbott Park, IL) и тест Amplicor HIV-1 (Roche MolecularSystems, Inc., Pleasanton, CA) представляют собой системы, в которых используются способы гетерогенного обнаружения. В системе LCx меченые гаптеном олигонуклеотидные зонды термоциклируют в лигазной цепной реакции. Захватываемый гаптен или обнаруживаемый гаптен ковалентно присоединяют с каждым из четырех праймерных олигонуклеотидов. После амплификации каждый амплифицированный продукт (ампликон) имеет один захватываемый гаптен и один обнаруживаемый гаптен. После завершения амплификации система LCx переносит реакционную среду в новую лунку, где связанные с антителами микрочастицы связываются с захватываемым гаптеном. Каждая микрочастица затем необратимо связывается с матрицей из стекловолокна. На стадии промывки удаляют микрочастицы слабым зондом,содержащим только обнаруживаемый гаптен. Аппарат LCx добавляет конъюгат щелочная фосфатаза(АР) - антитело, связывающийся с обнаруживаемым гаптеном. Флуорогенный субстрат для АР представляет собой 4-метилумбеллиферил. Дефосфорилирование 4-метилумбеллиферила АР превращает его в 4 метилумбеллиферон, который флуоресцирует. В тесте Amplicor HIV-1 используется формат ELiSA. После амплификации путем ПЦР ампликон химически денатурируют. Специфические в отношении ампликона олигонуклеотидные зонды захватывают денатурированные цепи на покрытом микропланшете. Оператор отмывает любые не включенные праймеры и не подвергшийся гибридизации материал на стадии промывки и затем добавляет в каждую лунку конъюгат авидин-HRP. Конъюгат связывается с меченым биотином ампликоном, захваченным на планшете. Оператор затем добавляет 3,3',5,5'-тетраметилбензидин (ТМВ), представляющий собой хромогенный субстрат HRP. В присутствии перекиси водорода HRP окисляет ТМВ. Сигнал обнаруживают колориметрически. Гомогенное обнаружение: поскольку гибридизуемые и негибридизуемые обнаруживаемые зонды физически не разделены в системах гомогенного обнаружения, эти способы требуют меньше стадий по сравнению с гетерогенными способами и, таким образом, менее подвержены контаминации. Такие имеющиеся в продаже наборы, в которых используется гомогенное обнаружение флуоресценции и хемилюминесцентные метки, представляют собой систему TaqMan (Applied Biosystems, Foster City, CA), система BDProbeTecET (Becton Dickinson, Franklin Lakes, NJ), система QPCR 5000 (Perkin-Elmer Corp., Norwalk, CT) и анализ гибридизации и защиты (Gen-Probe, Inc., San Diego, CA). Система TaqMan обнаруживает ампликон в режиме реального времени. Обнаруживаемый зонд, который гибридизуется с областью внутри ампликона, содержит донорный флуорозонд, такой как флуоресцеин, на своем 5'-конце и гасящую группировку, такую как родамин, на своем 3'-конце. Когда гаситель и флуорофор располагаются на одном и том же олигонуклеотиде, флуоресценция донора ингибируется. Во время амплификации зонд связывается с мишенью. Taq полимераза вытесняет и расщепляет обнаруживаемый зонд, поскольку она синтезирует замещающую цепь. Расщепление обнаруживаемого зон- 27016267 да приводит в результате к отделению флуорофора от гасителя, приводя к увеличению флуоресцентного сигнала донора. Во время каждого цикла амплификации процесс повторяется. Величина флуоресцентного сигнала увеличивается по мере увеличения числа ампликонов. В молекулярных маяках также используются гасители и флуорофоры. Маяки представляют собой зонды, комплементарные ампликонумишени, но содержат короткие участки (приблизительно из 5 нуклеотидов) комплементарных олигонуклеотидов по каждому концу. 5'- и 3'-концы маяков мечены флуорофором и гасителем соответственно. Когда маяк не гибридизован с мишенью, образуется структура шпильки, приводящая в контакт флуорофор и гаситель и приводящая в результате к гашению флуоресценции. Область петли содержит область,комплементарную ампликону. После гибридизации с мишенью структура шпильки раскрывается и гаситель и флуорофор разделяются, давая возможность для проявления флуоресцентного сигнала. Флуориметр измеряет сигнал в режиме реального времени. В системе BDProbeTecET используется способ обнаружения в режиме реального времени, комбинирующий аспекты TaqMan и молекулярных маяков. Зонд имеет структуру шпилька-петля и содержит флуоресцеиновые и родаминовые метки. Тем не менее, в этой системе область, комплементарная молекуле-мишени, находится не в петле, а скорее в области 3' относительно родаминовой метки. Вместо того чтобы содержать последовательность, комплементарную мишени, одноцепочечная петля содержит сайт рестрикции рестриктазы BsoBI. Одноцепочечная последовательность не представляет собой субстрат для фермента. Флуоресцеиновая и родаминовая метки перед амплификацией находятся рядом друг с другом,что гасит флуоресценцию флуоресцеина. Амплификация превращает зонд в двухцепочечную молекулу. Рестриктаза BsoBI может расщеплять молекулу, приводя в результате к отделению меток и увеличению флуоресцентного сигнала. В системе QPCR 5000 используется электрохемилюминесценция с рутениевыми метками. Используют биотинилированный праймер. После амплификации биотиновые продукты захватываются на покрытых стрептавидином парамагнитных шариках. Шарики переносят в электрохимическую проточную ячейку путем аспирации и магнитно удерживаются на поверхности электрода. После электрической стимуляции меченый рутением зонд испускает свет. Анализ гибридизации-защиты используется в анализах Gen-Probe's неамплифицированного РАСЕ, а также в анализах амплифицированных М. tuberculosis и С. trachomatis. Обнаруживаемые олигонуклеотидные зонды в НРА мечены хемилюминесцентным акридиниевым эфиром (АЕ) при помощи связывающей последовательности. Гибридизация протекает в течение 15 мин при 60 С в той же самой пробирке, в которой происходит амплификация. Отбирающий реагент, представляющий собой слегка основный буферный раствор, добавляемый после гибридизации, гидролизует АЕ на любом негибридизованном зонде, делая его нехемилюминесцентным. АЕ на гибридизованных зондах укладывается внутри небольшого желобка двойной спирали, таким образом защищаясь от гидролиза отбирающим реагентом. АЕ испускает хемилюминесцентный сигнал после гидролиза перекисью водорода с последующим добавлением гидроксида натрия. Люминометр регистрирует хемилюминесцентный сигнал в течение 2 с(период, названный "выключенный свет") и представляет количество испущенных фотонов, выраженное в относительных световых единицах (RLU). Дизайн обнаруживаемого зонда является критическим во всех способах, в которых используются зонды для обнаружения продуктов амплификации. Хорошо обнаруживаемые зонды гибридизуются только со специфическими продуктами амплификации и не гибридизуются с неспецифическими продуктами. Другой ключевой аспект при оптимизации способов обнаружения включает мечение зондов и максимизацию объема образца. Способы мечения и молекулы-репортеры. Обнаруживаемые зонды могут быть мечены несколькими различными путями. Ферментативное включение 32 Р или 35S в зонды представляет собой самый обычный способ изотопного мечения. После гибридизации и промывки сигнал обнаруживают на авторадиографической пленке. Для осуществления нерадиоактивного обнаружения зонды могут быть мечены ферментативно множеством молекул. Биотин может быть включен ферментативно и затем обнаружен с помощью конъюгированной со стрептавидином щелочной фосфатазы с использованием субстратов АР, таких как 5 бром-4-хлор-3-индолил фосфат (BCIP) и нитроголубой тетразолий (NBT). Хемилюминесцентные субстраты, такие как Lumi-Phos 530 или Lumi-Phos Plus (Lumigen, Southfield, MI), также могут быть использованы с АР. Дополнительно, дигоксегинин-11-dUTP может быть включен ферментативно в ДНК или РНК, и конъюгаты антител против дигоксигенина с АР могут быть использованы с колориметрическим или хемилюминесцентным обнаружением. Существует множество других типов молекул-репортеров, включающих хемилюминесцентные группировки, такие как акридиниевые сложные эфиры. Также существует множество флуоресцентных группировок. Также могут быть использованы электрохемилюминесцентные соединения, такие как трис(2,2'-бипиридин)рутений(II). Дополнительное обсуждение этих и похожих способов можно найти в Schiffet al. Semin. Liver Dis., 1999, 79:Suppl. 1:3-15. Анализ биодоступности у обезьян Cynomolgus. В течение 1 недели перед началом исследования обезьянам Cynomolgus хирургически имплантиру- 28016267 ют венозный катетер длительного использования и подкожный порт для доступа к вене (VAP) для облегчения отбора крови, и подвергают физической проверке, включающей гематологическую оценку и оценку сыворотки крови, и регистрировали массу организма. Каждая макака (всего шесть) получает каждую дозу активного соединения при уровне дозы 10 мг/кг с концентрацией дозы 5 мг/мл при помощи внутривенного болюса (3 макаки, IV (внутривенно или при помощи перорального зонда (3 макаки, РО (перорально. Каждый дозирующий шприц взвешивают перед введением дозы для гравиметрического определения количества вводимого препарата. Образцы мочи собирают при помощи поддона-ловушки в обозначенные интервалы времени (приблизительно 18-0 ч перед введением дозы, 0-4, 4-8 и 8-12 ч после введения дозы) и обрабатывают. Также собирают образцы крови (перед введением дозы, 0,25, 0,5, 1, 2, 3, 6,8, 12 и 24 ч после введения дозы) при помощи длительного венозного катетера и VAP или из периферического сосуда, если процедура с длительным венозным катетером невозможна. Образцы крови и мочи анализируют при помощи ЖХ/МС (жидкостной хроматографии/масс-спектрометрии) в отношении максимальной концентрации (Cmax), времени достижения максимальной концентрации (Tmax), площади под кривой (AUC), периода полувыведения дозы (Т 1/2), клиренса (CL), объема и распределения в спокойном состоянии (Vss) и биодоступности (F). Анализ токсичности в отношении костного мозга. Человеческие клетки костного мозга собирают у здоровых нормальных добровольцев, и мононуклеарную популяцию отбирают путем центрифугирования в градиенте Фиколла-Гипак, как описано ранее в Sommadossi J.-P., Carlisle R. "Toxicity of 3'-azido-3'-deoxythymidine and 9-(1,3-dihydroxy-2propoxymethyl)guanine for normal human hematopoietic progenitor cells in vitro", Antimicrobial Agents andcells" Biochemical Pharmacology 1992; 44:1921-1925. Культуральные анализы в отношении CFU-GM (гранулоцитарно-макрофагальной колониеобразующей единицы) и BFU-E (колониеобразующей эритроидной "взрывообразующей" единицы) осуществляют с использованием двухслойного мягкого агара или способа с метилцеллюлозой. Лекарства разбавляют в тканевой культуральной среде и фильтруют. Через 14-18 суток при 37 С в увлажненной атмосфере 5% СО 2 в воздухе колонии из более чем 50 клеток подсчитывают с использованием обращенной микроскопии. Результаты представлены в виде процентного ингибирования образования колоний в присутствии лекарства по сравнению с контрольными культурами, обработанными растворителем. Анализ цитотоксичности. Клетки высевают в количестве от 5103 до 5 104/лунку в 96-луночные планшеты в среде для роста в течение ночи при 37 С в увлажненной атмосфере CO2 (5%). Затем добавляют новую ростовую среду,содержащую серийные разведения лекарств. После инкубации в течение 4 суток культуры фиксируют в 50% ТХУ (трихлоруксусной кислоте) и окрашивают сульфородамином В. Оптическую плотность считывают при 550 нм. Цитотоксическую концентрацию выражают в виде концентрации, требуемой для уменьшения количества клеток на 50% (СС 50). Анализ клеточной защиты (СРА). Анализ осуществляют, по существу, как описано Baginski, S.G.; Pevear, D.С.; Seipel, М.; Sun, S.С.С.;NADL, АТСС) при множественности заражения (MOI) 0,02 бляшкообразующих единиц (PFU) на клетку,серийные разведения тестируемых соединений добавляют к инфицированным и неинфицированным клеткам в конечной концентрации 0,5% ДМСО в ростовой среде. Каждое разведение тестируют в четырех параллелях. Плотности клеток и вирусные инокуляты корректируют таким образом, чтобы обеспечивать непрерывный клеточный рост в течение эксперимента и достигать более чем 90% вызванную вирусом клеточную деструкцию в необрабатываемых контролях через четверо суток после инфицирования. Через четверо суток планшеты фиксируют при помощи 50% ТХУ и окрашивают сульфородамином В. Оптическую плотность в лунках считывают в аппарате для визуализации микропланшетов при 550 нм. Значения 50% эффективной концентрации (ЕС 50) определяют как концентрацию соединения, которая позволяет достичь 50% уменьшение цитопатического действия вируса. Анализ уменьшения бляшек. Для каждого соединения эффективную концентрацию определяют в двух 24-луночных планшетах при помощи анализов уменьшения бляшек. Клеточные монослои инфицируют 100 PFU (бляшкообразующих единиц) вируса/лунку. Затем серийные разведения тестируемых соединений в MEM дополняют 2% инактивированной сывороткой крови и к монослоям добавляют 0,75% метилцеллюлозу. Культуры дополнительно инкубируют при 37 С в течение 3 суток, затем фиксируют 50% этанолом и 0,8% кристаллическим фиолетовым, промывают и сушат на воздухе. Затем бляшки подсчитывают для определения концентрации, обеспечивающей 90% вирусную супрессию. Биологическая активность в отношении резистентных к лекарствам штаммов HIV.
МПК / Метки
МПК: A61P 31/18, A61K 31/675, C07F 9/572
Метки: качестве, чистые, ингибиторов, фосфоиндолы, энантиомерно
Код ссылки
<a href="https://eas.patents.su/30-16267-enantiomerno-chistye-fosfoindoly-v-kachestve-ingibitorov-hiv.html" rel="bookmark" title="База патентов Евразийского Союза">Энантиомерно чистые фосфоиндолы в качестве ингибиторов hiv</a>
Предыдущий патент: Полимерная смесь, моно- или многослойная пленка и способ изготовления пленки
Следующий патент: Способ получения антистафилококковой плазмы крови
Случайный патент: Система и способ получения нитробензола