Пиперазин с or-замещенной фенильной группой и его применение в качестве ингибиторов glyt1
Номер патента: 9986
Опубликовано: 28.04.2008
Авторы: Наркизян Робер, Джолидон Синесе, Шталдер Анри, Неттековен Маттиас Генрих, Норкросс Роджер Дейвид, Пинар Эмманьюэль
Формула / Реферат
1. Соединения общей формулы
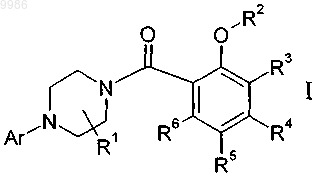
где Ar представляет собой незамещенный или замещенный арил или 6-членный гетероарил, содержащий 1, 2 или 3 атома азота, и где арильная и гетероарильная группы могут быть замещены одним или несколькими заместителями, выбранными из группы, состоящей из гидрокси, галогена, NO2, CN, (С1-С6)-алкила, (С1-С6)-алкила, замещенного галогеном, (C1-С6)-алкила, замещенного гидрокси, (СН2)n-(С1-С6)-алкокси, (С1-С6)-алкокси, замещенного галогеном, NR7R8, C(O)R9, SO2R10, -C(CH3)=NOR7 или 5-членным ароматическим гетероциклом, содержащим 1-4 гетероатома, выбранных из N и О, который необязательно замещен (С1-С6)-алкилом;
R1 представляет собой водород или (С1-С6)-алкил;
R2 представляет собой водород, (С1-С6)-алкил, (С2-С6)-алкенил, (С1-С6)-алкил, замещенный галогеном, (С1-С6)-алкил, замещенный гидрокси, (СН2)n-(С3-С7)-циклоалкил, необязательно замещенный (С1-С6)-алкокси или галогеном, или представляет собой СН(СН3)-(С3-С7)-циклоалкил, (CH2)n+1-C(O)-R9, (CH2)n+1-CN, бицикло[2,2,1]гептил, (СН2)n+1-О-(С1-С6)-алкил, (СН2)n-гетероциклоалкил, (СН2)n-арил или (СН2)n-5- или -6-членный гетероарил, содержащий 1, 2 или 3 гетероатома, выбранных из группы, состоящей из кислорода, серы или азота, где арил, гетероциклоалкил и гетероарил являются незамещенными или замещены одним или несколькими заместителями, выбранными из группы, состоящей из гидрокси, галогена, (С1-С6)-алкила или (С1-С6)-алкокси;
R3, R4 и R6 независимо друг от друга представляют собой водород, гидрокси, галоген, (С1-С6)-алкил, (С1-С6)-алкокси или О-(С3-С6)-циклоалкил;
R5 представляет собой NO2, CN, C(O)R9 или SO2R10;
R7 и R8 независимо друг от друга представляют собой водород или (C1-C6)-алкил;
R9 представляет собой водород, (С1-С6)-алкил, (С1-С6)-алкокси или NR7R8;
R10 представляет собой (С1-С6)-алкил, необязательно замещенный галогеном, (СН2)n-(С3-С6)-циклоалкил, (СН2)n-(С3-С6)-алкокси, (СН2)n-гетероциклоалкил или NR7R8;
n имеет значения 0, 1 или 2;
где "арил" обозначает моновалентный циклический ароматический углеводородный радикал, состоящий из одного или нескольких конденсированных колец, в котором по крайней мере одно кольцо является ароматическим, например фенил, бензил, нафтил, бифенил или инданил,
"гетероциклоалкил" обозначает неароматический углеводородный радикал, например оксетанил, тетрагидрофуранил, тетрагидропиранил, азетидинил, пирролидинил, пиперидинил, пиперазинил, морфолинил или тиоморфолинил,
и их фармацевтически приемлемые кислотные аддитивные соли,
при условии, что исключаются
1-[5-(аминосульфонил)-2-метоксибензоил]-4-(3-хлорфенил)пиперазин,
1-[5-(аминосульфонил)-2-метоксибензоил]-4-(4-фторфенил)пиперазин,
1-[5-(аминосульфонил)-2-метоксибензоил]-4-[3-(трифторметил)фенил]пиперазин,
4-(3-амино-4-нитрофенил)-1-[4-(диметиламино)-2-метокси-5-нитробензоил]-2-метилпиперазин,
1-[4-(диметиламино)-2-метокси-5-нитробензоил]-2-метил-4-(4-нитрофенил)пиперазин,
4-[4-(диметиламино)-2-метокси-5-нитробензоил]-2-метил-1-(4-нитрофенил)пиперазин,
1-(2-хлор-4-нитрофенил)-4-[4-(диметиламино)-2-метокси-5-нитробензоил]пиперазин,
1-[4-(диметиламино)-2-метокси-5-нитробензоил]-4-(2,4-динитрофенил)-2-метилпиперазин,
1-(4-хлор-2-нитрофенил)-4-[4-(диметиламино)-2-метокси-5-нитробензоил]пиперазин и
4-[4-(диметиламино)-2-метокси-5-нитробензоил]-1-(2,4-динитрофенил)-2-метилпиперазин.
2. Соединения формулы

где Ar представляет собой замещенный арил или незамещенный или замещенный 6-членный гетероарил, содержащий 1, 2 или 3 атома азота, и где арильная и гетероарильная группы являются замещенными одним или несколькими заместителями, выбранными из группы, состоящей из гидрокси, галогена, NO2, CN, (С1-С6)-алкила, (С1-С6)-алкила, замещенного галогеном, (С1-С6)-алкокси, (С1-С6)-алкокси, замещенного галогеном, NR7R8, C(O)R9 или SO2R10;
R1 представляет собой водород или (С1-С6)-алкил;
R2 представляет собой (С1-С6)-алкил, (С1-С6)-алкил, замещенный галогеном, (С3-С6)-циклоалкил, гетероциклоалкил, (С1-С6)-алкил-(С3-С6)-циклоалкил, (C1-С6)-алкилгетероциклоалкил, (С1-С6)-алкил-С(О)-R9, (C1-С6)-алкил-CN, (C2-C6)-алкил-O-R13, (C2-C6)-алкил-NR7R8, арил или 6-членный гетероарил, содержащий 1, 2 или 3 атома азота, (С1-С6)-алкиларил или (C1-С6)-алкил-5- или -6-членный гетероарил, содержащий 1, 2 или 3 гетероатома, выбранных из группы, состоящей из кислорода, серы или азота, где арил, гетероциклоалкил и гетероарил являются незамещенными или замещены одним или несколькими заместителями, выбранными из группы, состоящей из гидрокси, галогена, (С1-С6)-алкила или (C1-C6)-алкокси;
R3, R4 и R6 независимо друг от друга представляют собой водород, гидрокси, галоген, CN, (С1-С6)-алкил, (С1-С6)-алкокси или NR7R8;
R5 представляет собой NO2, CN, C(O)R9, SO2R10 или NR11R12;
R7 и R8 независимо друг от друга представляют собой водород или (С1-С6)-алкил;
R9 представляет собой гидрокси, (С1-С6)-алкил, (С3-С6)-циклоалкил, (C1-С6)-алкокси или NR7R8;
R10 представляет собой (С1-С6)-алкил, (С3-С6)-циклоалкил или NR7R8;
R11 и R12 независимо друг от друга представляют собой водород, С(О)-(С1-С6)-алкил, SO2-(С1-С6)-алкил или вместе с N-атомом образуют 5-членную гетероарильную группу, необязательно замещенную галогеном, (С1-С6)-алкилом, (C1-С6)-алкилом, замещенным галогеном или (С3-С6)-циклоалкилом;
R13 представляет собой гидрокси, (C1-С6)-алкил или (С3-С6)-циклоалкил;
где "арил" обозначает моновалентный циклический ароматический углеводородный радикал, состоящий из одного или нескольких конденсированных колец, в котором по крайней мере одно кольцо является ароматическим, например фенил, бензил, нафтил, бифенил шыш инданил,
"гетероциклоалкил" обозначает неароматический углеводородный радикал, например оксетанил, тетрагидрофуранил, тетрагидропиранил, азетидинил, пирролидинил, пиперидинил, пиперазинил, морфолинил или тиоморфолинил,
и их фармацевтически приемлемые кислотные аддитивные соли,
при условии, что исключаются
1-[5-(аминосульфонил)-2-метоксибензоил]-4-(3-хлорфенил)пиперазин,
1-[5-(аминосульфонил)-2-метоксибензоил]-4-(4-фторфенил)пиперазин,
1-[5-(аминосульфонил)-2-метоксибензоил]-4-[3-(трифторметил)фенил]пиперазин,
4-(3-амино-4-нитрофенил)-1-[4-(диметиламино)-2-метокси-5-нитробензоил]-2-метилпиперазин,
1-[4-(диметиламино)-2-метокси-5-нитробензоил]-2-метил-4-(4-нитрофенил)пиперазин,
4-[4-(диметиламино)-2-метокси-5-нитробензоил]-2-метил-1-(4-нитрофенил)пиперазин,
1-(2-хлор-4-нитрофенил)-4-[4-(диметиламино)-2-метокси-5-нитробензоил]пиперазин,
1-[4-(диметиламино)-2-метокси-5-нитробензоил]-4-(2,4-динитрофенил)-2-метилпиперазин,
1-(4-хлор-2-нитрофенил)-4-[4-(диметиламино)-2-метокси-5-нитробензоил]пиперазин и
4-[4-(диметиламино)-2-метокси-5-нитробензоил]-1-(2,4-динитрофенил)-2-метилпиперазин.
3. Соединения формулы I по п.1, где Ar представляет собой замещенный фенил, R2 представляет собой (C1-С6)-алкил и R5 представляет собой S(O)2CH3 или S(O)2CH2CH3.
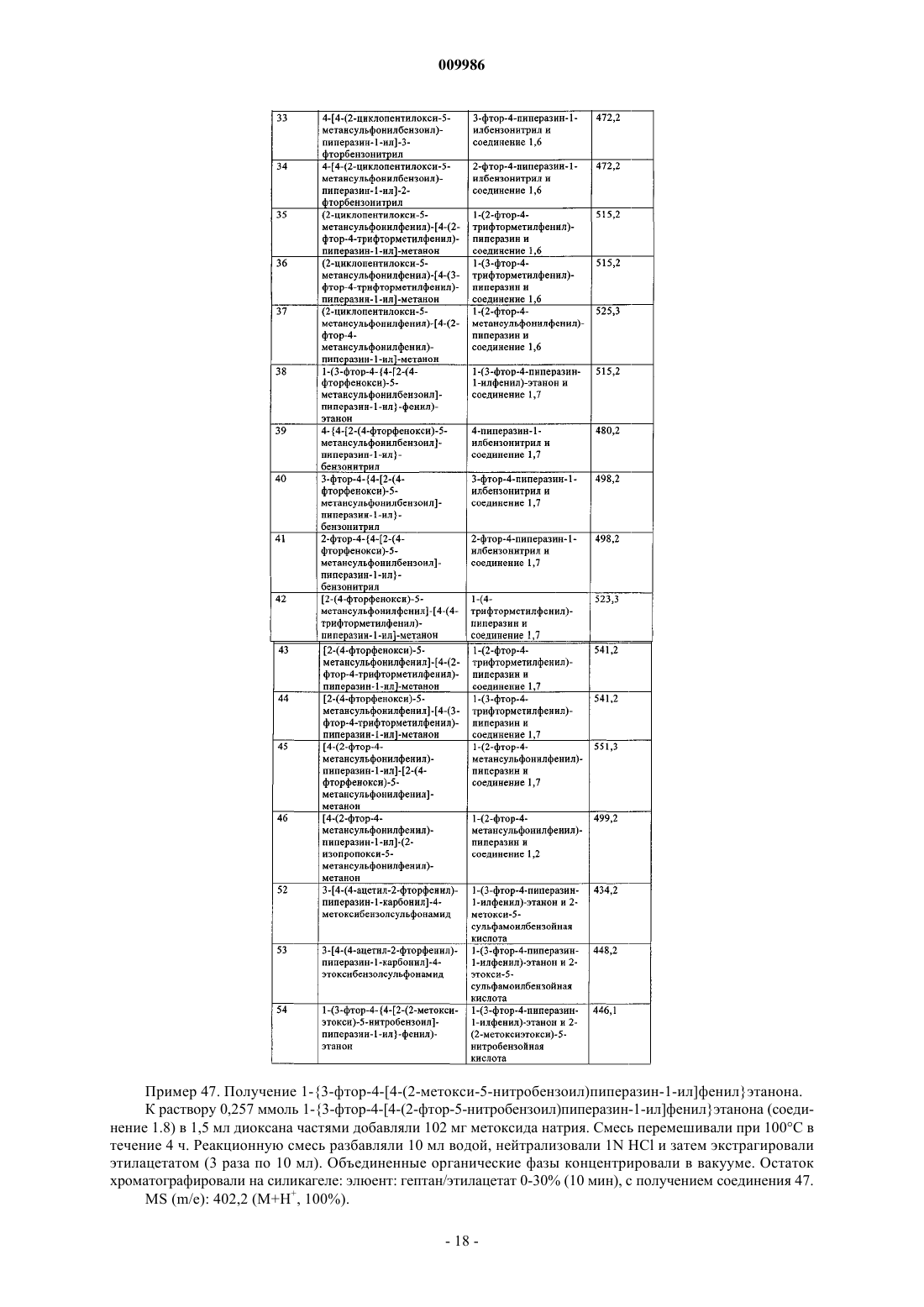
4. Соединения формулы I по п.3, где соединения представляют собой
1-{3-фтор-4-[4-(2-изопропокси-5-метансульфонилбензоил)пиперазин-1-ил]фенил}этанон,
3-фтор-4-[4-(2-изопропокси-5-метансульфонилбензоил)пиперазин-1-ил]бензонитрил,
2-фтор-4-[4-(2-изопропокси-5-метансульфонилбензоил)пиперазин-1-ил]бензонитрил,
[4-(2-фтор-4-трифторметилфенил)пиперазин-1-ил]-(2-изопропокси-5-метансульфонилфенил)метанон,
1-{3-фтор-4-[4-(2-изобутокси-5-метансульфонилбензоил)пиперазин-1-ил]фенил}этанон,
4-[4-(2-изобутокси-5-метансульфонилбензоил)пиперазин-1-ил]бензонитрил,
3-фтор-4-[4-(2-изобутокси-5-метансульфонилбензоил)пиперазин-1-ил]бензонитрил,
2-фтор-4-[4-(2-изобутокси-5-метансульфонилбензоил)пиперазин-1-ил]бензонитрил,
(2-изобутокси-5-метансульфонилфенил)-[4-(4-трифторметилфенил)пиперазин-1-ил]метанон,
[4-(2-фтор-4-трифторметилфенил)пиперазин-1-ил]-(2-изобутокси-5-метансульфонилфенил)метанон,
[4-(3-фтор-4-трифторметилфенил)пиперазин-1-ил]-(2-изобутокси-5-метансульфонилфенил)метанон,
[4-(2-фтор-4-метансульфонилфенил)пиперазин-1-ил]-(2-изобутокси-5-метансульфонилфенил)метанон,
[4-(2-фтор-4-метансульфонилфенил)пиперазин-1-ил]-(2-изопропокси-5-метансульфонилфенил)метанон,
2,3-дифтор-4-[4-(2-изопропокси-5-метансульфонилбензоил)пиперазин-1-ил]бензонитрил,
2,3-дифтор-4-[4-(2-изобутокси-5-метансульфонилбензоил)пиперазин-1-ил]бензонитрил,
2,5-дифтор-4-[4-(2-изобутокси-5-метансульфонилбензоил)пиперазин-1-ил]бензонитрил,
2,6-дифтор-4-[4-(2-изобутокси-5-метансульфонилбензоил)пиперазин-1-ил]бензонитрил,
3,5-дифтор-4-[4-(2-изобутокси-5-метансульфонилбензоил)пиперазин-1-ил]бензонитрил,
4-[4-(2-трет-бутокси-5-метансульфонилбензоил)пиперазин-1-ил]-2,3-дифторбензонитрил,
5-хлор-2-[4-(2-изопропокси-5-метансульфонилбензоил)пиперазин-1-ил]бензонитрил,
4-[4-(2-трет-бутокси-5-метансульфонилбензоил)пиперазин-1-ил]-2,5-дифторбензонитрил,
4-[4-(2-трет-бутокси-5-метансульфонилбензоил)пиперазин-1-ил]-3-фторбензонитрил,
(2-трет-бутокси-5-метансульфонилфенил)-[4-(2-фтор-4-трифторметилфенил)пиперазин-1-ил]метанон,
(2-трет-бутокси-5-метансульфонилфенил)-[4-(2,5-дифтор-4-метансульфонилфенил)пиперазин-1-ил]
метанон,
1-(4-{4-[2-(2,2-диметилпропокси)-5-метансульфонилбензоил]пиперазин-1-ил}-3-фторфенил)этанон,
4-{4-[2-(2,2-диметилпропокси)-5-метансульфонилбензоил]пиперазин-1-ил}бензонитрил,
4-{4-[2-(2,2-диметилпропокси)-5-метансульфонилбензоил]пиперазин-1-ил}-3-фторбензонитрил,
4-{4-[2-(2,2-диметилпропокси)-5-метансульфонилбензоил]пиперазин-1-ил}-2-фторбензонитрил,
[2-(2,2-диметилпропокси)-5-метансульфонилфенил]-[4-(4-трифторметилфенил)пиперазин-1-ил]метанон,
[2-(2,2-диметилпропокси)-5-метансульфонилфенил]-[4-(2-фтор-4-трифторметилфенил)пиперазин-1-ил]метанон,
[2-(2,2-диметилпропокси)-5-метансульфонилфенил]-[4-(3-фтор-4-трифторметилфенил)пиперазин-1-ил]метанон,
[2-(2,2-диметилпропокси)-5-метансульфонилфенил]-[4-(2-фтор-4-этансульфонилфенил)пиперазин-1-ил]метанон,
рац-1-{4-[4-(2-втор-бутокси-5-метансульфонилбензоил)пиперазин-1-ил]-3-фторфенил}этанон,
рац-4-[4-(2-втор-бутокси-5-метансульфонилбензоил)пиперазин-1-ил]-3-фторбензонитрил,
рац-4-[4-(2-втор-бутокси-5-метансульфонилбензоил)пиперазин-1-ил]-2-фторбензонитрил,
рац-(2-втор-бутокси-5-метансульфонилфенил)-[4-(2-фтор-4-трифторметилфенил)пиперазин-1-ил]метанон,
рац-(2-втор-бутокси-5-метансульфонилфенил)-[4-(3-фтор-4-трифторметилфенил)пиперазин-1-ил]метанон,
(2-изопропокси-5-метансульфонилфенил)-[4-(4-трифторметансульфонилфенил)пиперазин-1-ил]метанон,
(2-изобутокси-5-метансульфонилфенил)-[4-(4-трифторметансульфонилфенил)пиперазин-1-ил]метанон,
2-[4-(2-изопропокси-5-метансульфонилбензоил)пиперазин-1-ил]-5-трифторметилбензонитрил,
1-{2-фтор-4-[4-(2-изопропокси-5-метансульфонилбензоил)пиперазин-1-ил]фенил}этанон,
[4-(3-фтор-4-метансульфонилфенил)пиперазин-1-ил]-(2-изобутокси-5-метансульфонилфенил)метанон,
1-{2-фтор-4-[4-(2-изобутокси-5-метансульфонилбензоил)пиперазин-1-ил]фенил}этанон,
2-[4-(2-изобутокси-5-метансульфонилбензоил)пиперазин-1-ил]-5-трифторметилбензонитрил,
(5-этансульфонил-2-изопропоксифенил)-[4-(2-фтор-4-трифторметилфенил)пиперазин-1-ил]метанон,
[4-(4-дифторметил-2-фторфенил)пиперазин-1-ил]-(2-изопропокси-5-метансульфонилфенил)метанон,
[4-(3-хлор-5-трифторметилпиридин-2-ил)пиперазин-1-ил]-(2-изопропокси-5-метансульфонилфенил)
метанон,
3-фтор-4-[4-(2-изопропокси-5-метансульфонилбензоил)пиперазин-1-ил]бензальдегид,
[4-(4-этансульфонил-2-фторфенил)пиперазин-1-ил]-(2-изобутокси-5-метансульфонилфенил)метанон,
рац-(2-втор-бутокси-5-метансульфонилфенил)-[4-(4-этансульфонил-2-фторфенил)пиперазин-1-ил]
метанон,
[4-(4-циклобутансульфонил-2-фторфенил)пиперазин-1-ил]-(2-изопропокси-5-метансульфонилфенил)метанон,
[4-(4-циклопентансульфонил-2-фторфенил)пиперазин-1-ил]-(2-изопропокси-5-метансульфонилфенил)метанон,
[4-(4-циклопропансульфонил-2-фторфенил)пиперазин-1-ил]-(2-изобутокси-5-метансульфонилфенил)метанон и
[4-(4-циклопропансульфонил-2,5-дифторфенил)пиперазин-1-ил]-(2-изопропокси-5-метансульфонилфенил)метанон.
5. Соединения формулы I по п.1, где Ar представляет собой замещенный фенил, R2 представляет собой (СН2)n-(С3-С7)-циклоалкил и R5 представляет собой S(O)2CH3.
6. Соединения формулы I по п.5, где соединения представляют собой
1-{4-[4-(2-циклопропилметокси-5-метансульфонилбензоил)пиперазин-1-ил]-3-фторфенил}этанон,
4-[4-(2-циклопропилметокси-5-метансульфонилбензоил)пиперазин-1-ил]бензонитрил,
4-[4-(2-циклопропилметокси-5-метансульфонилбензоил)пиперазин-1-ил]-3-фторбензонитрил,
4-[4-(2-циклопропилметокси-5-метансульфонилбензоил)пиперазин-1-ил]-2-фторбензонитрил,
(2-циклопропилметокси-5-метансульфонилфенил)-[4-(4-трифторметилфенил)пиперазин-1-ил]метанон,
(2-циклопропилметокси-5-метансульфонилфенил)-[4-(2-фтор-4-трифторметилфенил)пиперазин-1-ил]метанон,
(2-циклопропилметокси-5-метансульфонилфенил)-[4-(3-фтор-4-трифторметилфенил)пиперазин-1-ил]метанон,
1-{4-[4-(2-циклопентилокси-5-метансульфонилбензоил)пиперазин-1-ил]-3-фторфенил}этанон,
4-[4-(2-циклопентилокси-5-метансульфонилбензоил)пиперазин-1-ил]бензонитрил,
4-[4-(2-циклопентилокси-5-метансульфонилбензоил)пиперазин-1-ил]-3-фторбензонитрил,
4-[4-(2-циклопентилокси-5-метансульфонилбензоил)пиперазин-1-ил]-2-фторбензонитрил,
(2-циклопентилокси-5-метансульфонилфенил)-[4-(2-фтор-4-трифторметилфенил)пиперазин-1-ил]метанон,
(2-циклопентилокси-5-метансульфонилфенил)-[4-(3-фтор-4-трифторметилфенил)пиперазин-1-ил]метанон,
(2-циклопентилокси-5-метансульфонилфенил)-[4-(4-трифторметилфенил)пиперазин-1-ил]метанон,
рац-[2-(1-циклопропилэтокси)-5-метансульфонилфенил]-[4-(4-трифторметилфенил)пиперазин-1-ил]
метанон,
4-[4-(2-циклопентилокси-5-метансульфонилбензоил)пиперазин-1-ил]-2,3-дифторбензонитрил,
4-[4-(2-циклопентилокси-5-метансульфонилбензоил)пиперазин-1-ил]-2,5-дифторбензонитрил,
4-[4-(2-циклобутилметокси-5-метансульфонилбензоил)пиперазин-1-ил]бензонитрил,
4-[4-(2-циклобутилметокси-5-метансульфонилбензоил)пиперазин-1-ил]-2-фторбензонитрил,
4-[4-(2-циклобутилметокси-5-метансульфонилбензоил)пиперазин-1-ил]-3-фторбензонитрил,
(2-циклобутилметокси-5-метансульфонилфенил)-[4-(4-трифторметилфенил)пиперазин-1-ил]метанон,
1-{4-[4-(2-циклобутилметокси-5-метансульфонилбензоил)пиперазин-1-ил]-3-фторфенил}этанон,
2-[4-(2-циклобутилметокси-5-метансульфонилбензоил)пиперазин-1-ил]-5-трифторметилбензонитрил,
4-[4-(2-циклобутилметокси-5-метансульфонилбензоил)пиперазин-1-ил]-2,3-дифторбензонитрил,
4-[4-(2-циклобутилметокси-5-метансульфонилбензоил)пиперазин-1-ил]-2,5-дифторбензонитрил,
4-[4-(2-циклобутилметокси-5-метансульфонилбензоил)пиперазин-1-ил]-3,5-дифторбензонитрил,
4-[4-(2-циклобутилметокси-5-метансульфонилбензоил)пиперазин-1-ил]-2,6-дифторбензонитрил,
4-[4-(2-циклопропилметокси-5-метансульфонилбензоил)пиперазин-1-ил]-3,5-дифторбензонитрил,
4-[4-(2-циклопентилокси-5-метансульфонилбензоил)пиперазин-1-ил]-3,5-дифторбензонитрил,
4-[4-(2-циклопропилметокси-5-метансульфонилбензоил)пиперазин-1-ил]-2,6-дифторбензонитрил,
4-[4-(2-циклопентилокси-5-метансульфонилбензоил)пиперазин-1-ил]-2,6-дифторбензонитрил,
5-хлор-2-[4-(2-циклопропилметокси-5-метансульфонилбензоил)пиперазин-1-ил]бензонитрил,
4-[4-(2-циклогексилокси-5-метансульфонилбензоил)пиперазин-1-ил]бензонитрил,
4-[4-(2-циклогексилокси-5-метансульфонилбензоил)пиперазин-1-ил]-3-фторбензонитрил,
4-[4-(2-циклогексилокси-5метансульфонилбензоил)пиперазин-1-ил]-2-фторбензонитрил,
(2-циклогексилокси-5-метансульфонилфенил)-[4-(4-трифторметилфенил)пиперазин-1-ил]метанон,
(2-циклогексилокси-5-метансульфонилфенил)-[4-(3-фтор-4-трифторметилфенил)пиперазин-1-ил]метанон,
(2-циклогексилокси-5-метансульфонилфенил)-[4-(2-фтор-4-метансульфонилфенил)пиперазин-1-ил]
метанон,
1-{4-[4-(2-циклобутокси-5-метансульфонилбензоил)пиперазин-1-ил]-3-фторфенил}этанон,
4-[4-(2-циклобутокси-5-метансульфонилбензоил)пиперазин-1-ил]-3-фторбензонитрил,
(2-циклобутокси-5-метансульфонилфенил)-[4-(3-фтор-4-трифторметилфенил)пиперазин-1-ил]метанон,
(2-циклопентилокси-5-метансульфонилфенил)-[4-(4-трифторметансульфонилфенил)пиперазин-1-ил]метанон,
1-{4-[4-(2-циклопропилметокси-5-метансульфонилбензоил)пиперазин-1-ил]-2-фторфенил}этанон,
2-[4-(2-циклопентилокси-5-метансульфонилбензоил)пиперазин-1-ил]-5-трифторметилбензонитрил,
(2-циклопропилметокси-5-метансульфонилфенил)-[4-(4-этансульфонил-2-фторфенил)пиперазин-1-ил]метанон,
(2-циклопентилокси-5-метансульфонилфенил)-[4-(4-этансульфонил-2-фторфенил)пиперазин-1-ил]
метанон,
(2-циклогексилокси-5-метансульфонилфенил)-[4-(4-этансульфонил-2-фторфенил)пиперазин-1-ил]метанон,
(2-циклопентилокси-5-метансульфонилфенил)-[4-(4-циклопропансульфонил-2-фторфенил)пиперазин-1-ил]метанон,
(2-циклогексилокси-5-метансульфонилфенил)-[4-(4-циклопропансульфонил-2-фторфенил)пиперазин-1-ил]метанон,
(2-циклобутокси-5-метансульфонилфенил)-[4-(4-циклопропансульфонил-2-фторфенил)пиперазин-1-ил]метанон.
7. Соединения формулы I по п.1, где Ar представляет собой замещенный фенил, R2 представляет собой (С1-С6)-алкил, замещенный галогеном, и R5 представляет собой S(O)2CH3.
8. Соединения формулы I по п.7, где соединения представляют собой
1-(3-фтор-4-{4-[5-метансульфонил-2-(2,2,2-трифторэтокси)бензоил]пиперазин-1-ил}фенил)этанон,
3-фтор-4-{4-[5-метансульфонил-2-(2,2,2-трифторэтокси)бензоил]пиперазин-1-ил}бензонитрил,
[4-(2-фтор-4-трифторметилфенил)пиперазин-1-ил]-[5-метансульфонил-2-(2,2,2-трифторэтокси)фенил]метанон,
[4-(3-фтор-4-трифторметилфенил)пиперазин-1-ил]-[5-метансульфонил-2-(2,2,2-трифторэтокси)фенил]метанон,
[4-(2-фтор-4-метансульфонилфенил)пиперазин-1-ил]-[5-метансульфонил-2-(2,2,2-трифторэтокси)фенил]метанон,
3-фтор-4-{4-[5-метансульфонил-2-(3,3,3-трифторпропокси)бензоил]пиперазин-1-ил}бензонитрил,
[4-(3-фтор-4-трифторметилфенил)пиперазин-1-ил]-[5-метансульфонил-2-(3,3,3-трифторпропокси)фенил]метанон,
[4-(2-фтор-4-трифторметилфенил)пиперазин-1-ил]-[5-метансульфонил-2-(3,3,3-трифторпропокси)фенил]метанон,
1-(3-фтор-4-{4-[5-метансульфонил-2-(3,3,3-трифторпропокси)бензоил]пиперазин-1-ил}фенил)этанон,
2,5-дифтор-4-[4-(5-метансульфонил-2-трифторметоксибензоил)пиперазин-1-ил]бензонитрил,
2,3-дифтор-4-{4-[2-(2-фтор-1-фторметилэтокси)-5-метансульфонилбензоил]пиперазин-1-ил}бензонитрил,
2-фтор-4-{4-[5-метансульфонил-2-(2,2,3,3,3-пентафторпропокси)бензоил]пиперазин-1-ил}бензонитрил,
[5-метансульфонил-2-(2,2,3,3,3-пентафторпропокси)фенил]-[4-(4-трифторметилфенил)пиперазин-1-ил]метанон,
2,3-дифтор-4-{4-[5-метансульфонил-2-(2,2,3,3,3-пентафторпропокси)бензоил]пиперазин-1-ил}бензонитрил,
3,5-дифтор-4-{4-[5-метансульфонил-2-(2,2,3,3,3-пентафторпропокси)бензоил]пиперазин-1-ил}бензонитрил,
2-{4-[2-(2-фтор-1-фторметилэтокси)-5-метансульфонилбензоил]пиперазин-1-ил}-5-трифторметилбензонитрил,
рац-2,3-дифтор-4-{4-[5-метансульфонил-2-(2,2,2-трифтор-1-метилэтокси)бензоил]пиперазин-1-ил}
бензонитрил,
2-фтор-4-{4-[5-метансульфонил-2-(2,2,3,3-тетрафторпропокси)бензоил]пиперазин-1-ил}бензонитрил,
3-фтор-4-{4-[5-метансульфонил-2-(2,2,3,3-тетрафторпропокси)бензоил]пиперазин-1-ил}бензонитрил,
[5-метансульфонил-2-(2,2,3,3-тетрафторпропокси)фенил]-[4-(4-трифторметилфенил)пиперазин-1-ил]метанон,
[4-(2-фтор-4-трифторметилфенил)пиперазин-1-ил]-[5-метансульфонил-2-(2,2,3,3-тетрафторпропокси)фенил]метанон,
2,3-дифтор-4-{4-[5-метансульфонил-2-(2,2,3,3-тетрафторпропокси)бензоил]пиперазин-1-ил}бензонитрил,
3,5-дифтор-4-{4-[5-метансульфонил-2-(2,2,3,3-тетрафторпропокси)бензоил]пиперазин-1-ил}бензонитрил,
[4-(3,4-дихлорфенил)пиперазин-1-ил]-[5-метансульфонил-2-(2,2,2-трифторэтокси)фенил]метанон,
рац-5-хлор-2-{4-[5-метансульфонил-2-(2,2,2-трифтор-1-метилэтокси)бензоил]пиперазин-1-ил}бензонитрил,
рац-3,5-дифтор-4-{4-[5-метансульфонил-2-(2,2,2-трифтор-1-метилэтокси)бензоил]пиперазин-1-ил}
бензонитрил,
рац-2,5-дифтор-4-{4-[5-метансульфонил-2-(2,2,2-трифтор-1-метилэтокси)бензоил]пиперазин-1-ил}
бензонитрил,
рац-2,6-дифтор-4-{4-[5-метансульфонил-2-(2,2,2-трифтор-1-метилэтокси)бензоил]пиперазин-1-ил}
бензонитрил,
рац-4-{4-[5-метансульфонил-2-(2,2,2-трифтор-1-метилэтокси)бензоил]пиперазин-1-ил}бензонитрил,
рац-3-фтор-4-{4-[5-метансульфонил-2-(2,2,2-трифтор-1-метилэтокси)бензоил]пиперазин-1-ил}бензонитрил,
рац-2-фтор-4-{4-[5-метансульфонил-2-(2,2,2-трифтор-1-метилэтокси)бензоил]пиперазин-1-ил}бензонитрил,
рац-5-метансульфонил-2-(2,2,2-трифтор-1-метилэтокси)фенил]-[4-(4-трифторметилфенил)пиперазин-1-ил]метанон,
рац-[4-(2-фтор-4-трифторметилфенил)пиперазин-1-ил]-[5-метансульфонил-2-(2,2,2-трифтор-1-метилэтокси)фенил]метанон,
рац-[4-(3-фтор-4-трифторметилфенил)пиперазин-1-ил]-[5-метансульфонил-2-(2,2,2-трифтор-1-метилэтокси)фенил]метанон,
[4-(2-фтор-4-трифторметилфенил)пиперазин-1-ил]-[5-метансульфонил-2-((S или R)-2,2,2-трифтор-1-метилэтокси)фенил]метанон,
[5-метансульфонил-2-((S или R)-2,2,2-трифтор-1-метилэтокси)фенил]-[4-(4-трифторметилфенил)пиперазин-1-ил]метанон и
[5-метансульфонил-2-((R или S)-2,2,2-трифтор-1-метилэтокси)фенил]-[4-(4-трифторметилфенил)пиперазин-1-ил]метанон.
9. Соединения формулы I по п.1, где Ar представляет собой замещенный фенил, R2 представляет собой (С1-С6)-алкил, (C1-С6)-алкил, замещенный галогеном, (СН2)n-(С3-С7)-циклоалкил, бицикло[2,2,1]
гептил, (СН2)n-О-(С1-С6)-алкил или (СН2)n-гетероциклоалкил и R5 представляет собой NO2.
10. Соединения формулы I по п.9, где соединения представляют собой
1-(3-фтор-4-{4-[2-(2-метоксиэтокси)-5-нитробензоил]пиперазин-1-ил}фенил)этанон,
(2-изопропокси-5-нитрофенил)-[4-(4-трифторметилфенил)пиперазин-1-ил]метанон,
(2-циклопропилметокси-5-нитрофенил)-[4-(4-трифторметилфенил)пиперазин-1-ил]метанон,
(2-циклобутилметокси-5-нитрофенил)-[4-(4-трифторметилфенил)пиперазин-1-ил]метанон,
(2-бутокси-5-нитрофенил)-[4-(4-трифторметилфенил)пиперазин-1-ил]метанон,
[2-(2,2-диметилпропокси)-5-нитрофенил]-[4-(4-трифторметилфенил)пиперазин-1-ил]метанон,
(2-изобутокси-5-нитрофенил)-[4-(4-трифторметилфенил)пиперазин-1-ил]метанон,
(2-циклопентилокси-5-нитрофенил)-[4-(4-трифторметилфенил)пиперазин-1-ил]метанон,
(5-нитро-2-пропоксифенил)-[4-(4-трифторметилфенил)пиперазин-1-ил]метанон,
(2-циклобутокси-5-нитрофенил)-[4-(4-трифторметилфенил)пиперазин-1-ил]метанон,
рац-(2-втор-бутокси-5-нитрофенил)-[4-(4-трифторметилфенил)пиперазин-1-ил]метанон,
[5-нитро-2-(2,2,3,3-тетрафторпропокси)фенил]-[4-(4-трифторметилфенил)пиперазин-1-ил]метанон,
[5-нитро-2-(2,2,2-трифторэтокси)фенил]-[4-(4-трифторметилфенил)пиперазин-1-ил]метанон,
[2-(бицикло[2,2,1]гепт-2-илокси)-5-нитрофенил]-[4-(4-трифторметилфенил)пиперазин-1-ил]метанон,
[2-(2-хлорэтокси)-5-нитрофенил]-[4-(4-трифторметилфенил)пиперазин-1-ил]метанон и
[5-нитро-2-(2,2,3,3,3-пентафторпропокси)фенил]-[4-(4-трифторметилфенил)пиперазин-1-ил]метанон.
11. Соединения формулы I по п.1, где Ar представляет собой замещенный фенил, R2 представляет собой (С1-С6)-алкил, (С1-С6)-алкил, замещенный галогеном, или (СН2)n-(С3-С7)-циклоалкил и R5 представляет собой S(O)2NHCH3.
12. Соединения формулы I по п.11, где соединения представляют собой
3-[4-(4-циано-3-фторфенил)пиперазин-1-карбонил]-N-метил-4-трифторметоксибензолсульфонамид,
3-[4-(4-циано-3-фторфенил)пиперазин-1-карбонил]-4-изобутокси-N-метилбензолсульфонамид,
3-[4-(4-циано-3-фторфенил)пиперазин-1-карбонил]-4-циклопентилокси-N-метилбензолсульфонамид,
3-[4-(4-циано-3-фторфенил)пиперазин-1-карбонил]-4-циклобутокси-N-метилбензолсульфонамид,
3-[4-(4-циано-3-фторфенил)пиперазин-1-карбонил]-4-циклобутилметокси-N-метилбензолсульфонамид,
3-[4-(4-цианофенил)пиперазин-1-карбонил]-4-изобутокси-N-метилбензолсульфонамид,
3-[4-(4-цианофенил)пиперазин-1-карбонил]-4-циклопентилокси-N-метилбензолсульфонамид,
3-[4-(4-цианофенил)пиперазин-1-карбонил]-4-циклобутилметокси-N-метилбензолсульфонамид,
3-[4-(4-циано-2-фторфенил)пиперазин-1-карбонил]-4-изобутокси-N-метилбензолсульфонамид,
3-[4-(4-циано-2-фторфенил)пиперазин-1-карбонил]-4-(2,2-диметилпропокси)-N-метилбензолсульфонамид,
3-[4-(4-циано-2-фторфенил)пиперазин-1-карбонил]-4-изопропокси-N-метилбензолсульфонамид,
3-[4-(4-циано-2-фторфенил)пиперазин-1-карбонил]-4-циклопентилокси-N-метилбензолсульфонамид,
3-[4-(4-циано-2-фторфенил)пиперазин-1-карбонил]-4-циклобутокси-N-метилбензолсульфонамид,
3-[4-(4-циано-2-фторфенил)пиперазин-1-карбонил]-4-циклопропилметокси-N-метилбензолсульфонамид,
3-[4-(4-циано-2-фторфенил)пиперазин-1-карбонил]-4-циклобутилметокси-N-метилбензолсульфонамид,
3-[4-(4-ацетил-2-фторфенил)пиперазин-1-карбонил]-4-изобутокси-N-метилбензолсульфонамид,
3-[4-(4-ацетил-2-фторфенил)пиперазин-1-карбонил]-4-(2,2-диметилпропокси)-N-метилбензолсульфонамид,
3-[4-(4-ацетил-2-фторфенил)пиперазин-1-карбонил]-4-циклопентилокси-N-метилбензолсульфонамид,
3-[4-(4-ацетил-2-фторфенил)пиперазин-1-карбонил]-4-циклобутокси-N-метилбензолсульфонамид,
3-[4-(4-ацетил-2-фторфенил)пиперазин-1-карбонил]-4-циклопропилметокси-N-метилбензолсульфонамид,
4-изобутокси-N-метил-3-[4-(4-трифторметилфенил)пиперазин-1-карбонил]бензолсульфонамид,
4-(2,2-диметилпропокси)-N-метил-3-[4-(4-трифторметилфенил)пиперазин-1-карбонил]бензолсульфонамид,
4-изопропокси-N-метил-3-[4-(4-трифторметилфенил)пиперазин-1-карбонил]бензолсульфонамид,
4-циклопентилокси-N-метил-3-[4-(4-трифторметилфенил)пиперазин-1-карбонил]бензолсульфонамид,
4-циклобутокси-N-метил-3-[4-(4-трифторметилфенил)пиперазин-1-карбонил]бензолсульфонамид,
4-циклопропилметокси-N-метил-3-[4-(4-трифторметилфенил)пиперазин-1-карбонил]бензолсульфонамид,
4-циклобутилметокси-N-метил-3-[4-(4-трифторметилфенил)пиперазин-1-карбонил]бензолсульфонамид,
N-метил-3-[4-(4-трифторметилфенил)пиперазин-1-карбонил]-4-(3,3,3-трифторпропокси)бензолсульфонамид,
3-[4-(4-циано-2-фторфенил)пиперазин-1-карбонил]-N-метил-4-(2,2,2-трифторэтокси)бензолсульфонамид,
N-метил-4-(2,2,2-трифторэтокси)-3-[4-(4-трифторметилфенил)пиперазин-1-карбонил]бензолсульфонамид,
рац-N-метил-4-(2,2,2-трифтор-1-метилэтокси)-3-[4-(4-трифторметилфенил)пиперазин-1-карбонил]
бензолсульфонамид,
рац-3-[4-(4-циано-2,5-дифторфенил)пиперазин-1-карбонил]-N-метил-4-(2,2,2-трифтор-1-метилэтокси)бензолсульфонамид и
рац-3-[4-(4-циано-2,3-дифторфенил)пиперазин-1-карбонил]-N-метил-4-(2,2,2-трифтор-1-метилэтокси)бензолсульфонамид.
13. Соединения формулы I по п.1, где Ar представляет собой замещенную 6-членную гетероарильную группу, содержащую 1, 2 или 3 атома азота, R2 представляет собой (С1-С6)-алкил или (СН2)n-(С3-С7)-циклоалкил и R5 представляет собой SO2CH3.
14. Соединения формулы I по п.13, где соединения представляют собой
[4-(3-хлор-5-трифторметилпиридин-2-ил)пиперазин-1-ил]-(2-циклопропилметокси-5-метансульфонилфенил)метанон,
6-[4-(2-циклопентилокси-5-метансульфонилбензоил)пиперазин-1-ил]никотинонитрил,
(2-циклопентилокси-5-метансульфонилфенил)-[4-(5-трифторметилпиридин-2-ил)пиперазин-1-ил]метанон,
[4-(3-хлор-5-трифторметилпиридин-2-ил)пиперазин-1-ил]-(2-циклопентилокси-5-метансульфонилфенил)метанон,
(2-циклопентилокси-5-метансульфонилфенил)-[4-(6-трифторметилпиридин-3-ил)пиперазин-1-ил]метанон,
[4-(3-фтор-5-трифторметилпиридин-2-ил)пиперазин-1-ил]-(2-изопропокси-5-метансульфонилфенил)метанон и
(2-циклопентилокси-5-метансульфонилфенил)-[4-(3-фтор-5-трифторметилпиридин-2-ил)пиперазин-1-ил]метанон.
15. Соединения формулы I по п.1, где, где Ar представляет собой замещенную 6-членную гетероарильную группу, содержащую 1, 2 или 3 атома азота, R2 представляет собой (С1-С6)-алкил, замещенный галогеном, и R5 представляет собой SO2CH3.
16. Соединения формулы I по п.15, где соединения представляют собой
рац-[4-(3-хлор-5-трифторметилпиридин-2-ил)пиперазин-1-ил]-[5-метансульфонил-2-(2,2,2-трифтор-1-метилэтокси)фенил]метанон,
рац-[5-метансульфонил-2-(2,2,2-трифтор-1-метилэтокси)фенил]-[4-(5-трифторметилпиридин-2-ил)
пиперазин-1-ил]метанон,
рац-[4-(5-бромпиридин-2-ил)пиперазин-1-ил]-[5-метансульфонил-2-(2,2,2-трифтор-1-метилэтокси)
фенил]метанон,
рац-[4-(3-фтор-5-трифторметилпиридин-2-ил)пиперазин-1-ил]-[5-метансульфонил-2-(2,2,2-трифтор-1-метилэтокси)фенил]метанон,
рац-[5-метансульфонил-2-(2,2,2-трифтор-1-метилэтокси)фенил]-[4-(6-трифторметилпиридин-2-ил)
пиперазин-1-ил]метанон,
[5-метансульфонил-2-((S или R)-2,2,2-трифтор-1-метилэтокси)фенил]-[4-(5-трифторметилпиридин-2-ил)пиперазин-1-ил]метанон,
[5-метансульфонил-2-((R или S)-2,2,2-трифтор-1-метилэтокси)фенил]-[4-(5-трифторметилпиридин-2-ил)пиперазин-1-ил]метанон,
[4-(3-фтор-5-трифторметилпиридин-2-ил)пиперазин-1-ил]-[5-метансульфонил-2-((S)-2,2,2-трифтор-1-метилэтокси)фенил]метанон и
[4-(3-фтор-5-трифторметилпиридин-2-ил)пиперазин-1-ил]-[5-метансульфонил-2-(2,2,2-трифтор-1,1-диметилэтокси)фенил]метанон.
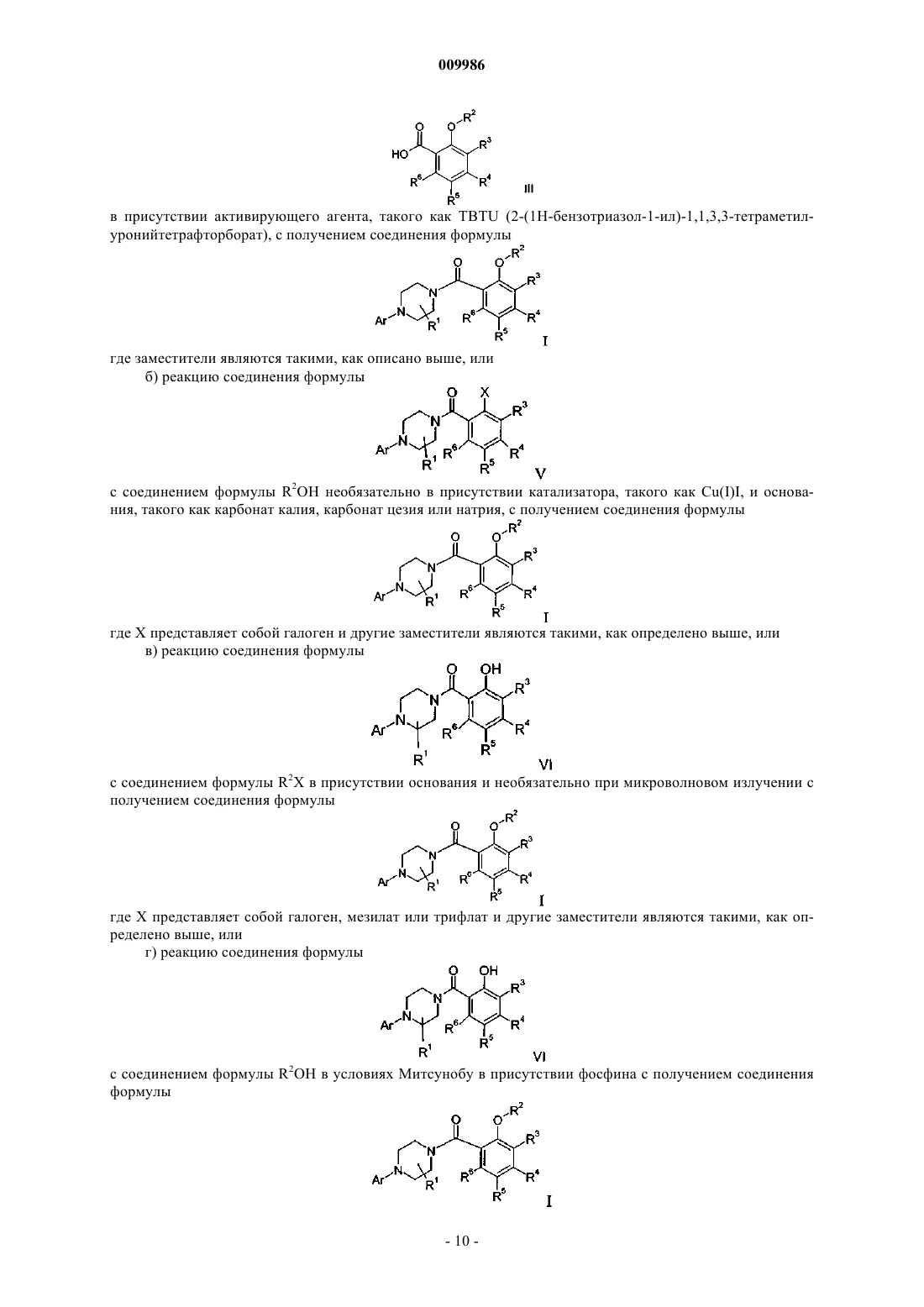
17. Способ получения соединения формулы I по п.1, который включает взаимодействие соединения формулы
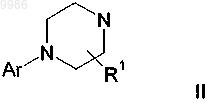
с соединением формулы
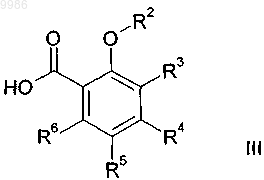
в присутствии активирующего агента, такого как TBTU (2-(1H-бензотриазол-1-ил)-1,1,3,3-тетраметилуронийтетрафторборат), с получением соединения формулы
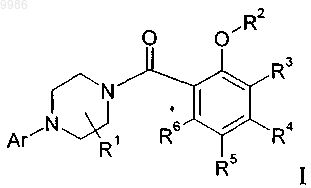
где заместители являются такими, как определено выше,
и, при необходимости, превращение полученных соединений в их фармацевтически приемлемые кислотные аддитивные соли.
18. Соединение по п.1, полученное способом, заявленным в п.17.
19. Лекарственное средство, содержащее одно или несколько соединений по п.1 или содержащее
4-(3-амино-4-нитрофенил)-1-[4-(диметиламино)-2-метокси-5-нитробензоил]-2-метилпиперазин,
1-[4-(диметиламино)-2-метокси-5-нитробензоил]-2-метил-4-(4-нитрофенил)пиперазин,
4-[4-(диметиламино)-2-метокси-5-нитробензоил]-2-метил-1-(4-нитрофенил)пиперазин,
1-(2-хлор-4-нитрофенил)-4-[4-(диметиламино)-2-метокси-5-нитробензоил]пиперазин,
1-[4-(диметиламино)-2-метокси-5-нитробензоил]-4-(2,4-динитрофенил)-2-метилпиперазин,
1-(4-хлор-2-нитрофенил)-4-[4-(диметиламино)-2-метокси-5-нитробензоил]пиперазин и
4-[4-(диметиламино)-2-метокси-5-нитробензоил]-1-(2,4-динитрофенил)-2-метилпиперазин
и фармацевтически приемлемые эксципиенты.
20. Лекарственное средство по п.19 для лечения заболеваний, в основе которых лежит ингибирование захвата глицина.
21. Лекарственное средство по п.20, где заболевание представляет собой психозы, боль, нарушение памяти и обучения, шизофрению, слабоумие и другие заболевания, в которых ослаблены когнитивные процессы, такие как рассеянное внимание или болезнь Альцгеймера.
22. Применение соединения по п.1 или
1-[5-(аминосульфонил)-2-метоксибензоил]-4-(3-хлорфенил)пиперазина,
1-[5-(аминосульфонил)-2-метоксибензоил]-4-(4-фторфенил)пиперазина,
1-[5-(аминосульфонил)-2-метоксибензоил]-4-[3-(трифторметил)фенил]пиперазина,
4-(3-амино-4-нитрофенил)-1-[4-(диметиламино)-2-метокси-5-нитробензоил]-2-метилпиперазина,
1-[4-(диметиламино)-2-метокси-5-нитробензоил]-2-метил-4-(4-нитрофенил)пиперазина,
4-[4-(диметиламино)-2-метокси-5-нитробензоил]-2-метил-1-(4-нитрофенил)пиперазина,
1-(2-хлор-4-нитрофенил)-4-[4-(диметиламино)-2-метокси-5-нитробензоил]пиперазина,
1-[4-(диметиламино)-2-метокси-5-нитробензоил]-4-(2,4-динитрофенил)-2-метилпиперазина,
1-(4-хлор-2-нитрофенил)-4-[4-(диметиламино)-2-метокси-5-нитробензоил]пиперазина и
4-[4-(диметиламино)-2-метокси-5-нитробензоил]-1-(2,4-динитрофенил)-2-метилпиперазина
для производства лекарственных средств для лечения психозов, боли, нейродегенеративных нарушений памяти и обучения, шизофрении, слабоумия и других заболеваний, в которых ослаблены когнитивные процессы, таких как рассеянное внимание или болезнь Альцгеймера.
Текст
009986 Настоящее изобретение относится к соединениям общей формулы I где Ar представляет собой незамещенный или замещенный арил или 6-членный гетероарил, содержащий 1, 2 или 3 атома азота, и где арильная и гетероарильная группы могут быть замещены одним или несколькими заместителями, выбранными из группы, состоящей из гидрокси, галогена, NO2, CN, (C1-С 6)алкила, (С 1-С 6)-алкила, замещенного галогеном, (C1-С 6)-алкила, замещенного гидрокси, (СН 2)n-(С 1-С 6)алкокси, (C1-С 6)-алкокси, замещенного галогеном, NR7R8, C(O)R9, SO2R10, -C(CH3)=NOR7 или 5-членным ароматическим гетероциклом, содержащим 1-4 гетероатома, выбранных из N и О, которые необязательно замещены (С 1-С 6)-алкилом;R1 представляет собой водород или (С 1-С 6)-алкил;R2 представляет собой водород, (С 1-С 6)-алкил, (С 2-С 6)-алкенил, (С 1-С 6)-алкил, замещенный галогеном, (C1-С 6)-алкил, замещенный гидрокси, (СН 2)n-(C3-С 7)-циклоалкил, необязательно замещенный (С 1 С 6)-алкокси или галогеном, или представляет собой СН(СН 3)-(С 3-С 7)-циклоалкил, (CH2)n+1-C(O)-R9,(CH2)n+1-CN, бицикло[2,2,1]гептил, (СН 2)n+1-О-(С 1-С 6)-алкил, (СН 2)n-гетероциклоалкил, (СН 2)n-арил или(СН 2)n-5- или 6-членный гетероарил, содержащий 1, 2 или 3 гетероатома, выбранных из группы, состоящей из кислорода, серы или азота, где арил, гетероциклоалкил и гетероарил являются незамещенными или замещены одним или несколькими заместителями, выбранными из группы, состоящей из гидрокси,галогена, (С 1-С 6)-алкила или (С 1-С 6)-алкокси;R3, R4 и R6 независимо друг от друга представляют собой водород, гидрокси, галоген, (C1-С 6)-алкил,(С 1-С 6)-алкокси или О-(С 3-С 6)-циклоалкил;R7 и R8 независимо друг от друга представляют собой водород или (C1-C6)-алкил;n имеет значение 0, 1 или 2; и к их фармацевтически приемлемым кислотным аддитивным солям,при условии, что исключаются соединения 1-[5-(аминосульфонил)-2-метоксибензоил]-4-(3-хлорфенил)пиперазин,1-[5-(аминосульфонил)-2-метоксибензоил]-4-(4-фторфенил)пиперазин,1-[5-(аминосульфонил)-2-метоксибензоил]-4-[3-(трифторметил)фенил]пиперазин,4-(3-амино-4-нитрофенил)-1-[4-(диметиламино)-2-метокси-5-нитробензоил]-2-метилпиперазин,1-[4-(диметиламино)-2-метокси-5-нитробензоил]-2-метил-4-(4-нитрофенил)пиперазин,4-[4-(диметиламино)-2-метокси-5-нитробензоил]-2-метил-1-(4-нитрофенил)пиперазин,1-(2-хлор-4-нитрофенил)-4-[4-(диметиламино)-2-метокси-5-нитробензоил]пиперазин,1-[4-(диметиламино)-2-метокси-5-нитробензоил]-4-(2,4-динитрофенил)-2-метилпиперазин,1-(4-хлор-2-нитрофенил)-4-[4-(диметиламино)-2-метокси-5-нитробензоил]пиперазин и 4-[4-(диметиламино)-2-метокси-5-нитробензоил]-1-(2,4-динитрофенил)-2-метилпиперазин. Соединения 1-[5-(аминосульфонил)-2-метоксибензоил]-4-(3-хлорфенил)пиперазин,1-[5-(аминосульфонил)-2-метоксибензоил]-4-(4-фторфенил)пиперазин и 1-[5-(аминосульфонил)-2-метоксибензоил]-4-[3-(трифторметил)фенил]пиперазин описаны в ЕР 0171636, обладают ингибирующей активностью в отношении карбоангидразы, которая играет определяющую роль во многих физиологических и патологических процессах. Другие исключенные соединения являются коммерчески доступными продуктами. Настоящее изобретение относится к соединениям общей формулы I, к фармацевтическим композициям, содержащим такие соединения, и к их применению для лечения неврологических и нейропсихиатрических заболеваний. Неожиданно было обнаружено, что соединения общей формулы I являются хорошими ингибиторами переносчика глицина 1 (GlyT-1) и что они обладают хорошей селективностью в отношении ингибиторов переносчика глицина 2 (GlyT-2). Шизофрения является прогрессирующим и разрушительным неврологическим заболеванием, характеризующимся эпизодическими положительными симптомами, такими как мании, галлюцинации,нарушениями умственной деятельности и психозы, и устойчивыми отрицательными симптомами, такими как затихающий аффект, рассеянное внимание, и социальная самоизоляция, и нарушения процессов познания (Lewis D.A. и Lieberman J.A., Neuron, 28: 325-33, 2000). В течение десятилетий исследования были направлены на гипотезу "допаминергической гиперактивности", которая привела к терапевтическим вмешательствам, включающим блокаду допаминергической системы (Vandenberg R.J. и Aubrey K.R., Exp.Opin. Ther. Targets, 5 (4): 507-518, 2001; Nakazato А. и Okuyama S. и др., Exp. Opin. Ther. Patents, 10 (1): 75-98, 2000). Этот фармакологический подход в незначительной степени направлен на отрицательные и познавательные симптомы, которые являются лучшими редикторами функционального проявления(Sharma Т., Br. J. Psychiatry, 174 (suppl. 28): 44-51, 1999). Комплементарная модель шизофрении была предложена в середине 1960-х годов и основывалась на психотомиметическом воздействии, вызванном блокадой глутаматной системы соединениями, подобными фенциклидину (РСР) и близкими ему агентами (кетамин), которые являются неконкурентными антагонистами рецептора NMDA. Интересно, что у здоровых волонтеров РСР-индуцированное психотомиметическое воздействие объединяет положительные и отрицательные симптомы, а также когнитивную дисфункцию, тем самым ярко напоминая шизофрению у пациентов (Javitt D.C. и др., Biol. Psychiatry, 45: 668679, 1999). Более того, трансгенные мыши, экспрессирующие пониженные уровни субъединиц NMDAR1,проявляют поведенческие отклонения, схожие с отклонениями, наблюдаемыми в фармакологически индуцированных моделях шизофрении, обеспечивая модель, в которой уменьшенная активность рецептораNMDA приводит к поведению, напоминающему шизофрению (Mohn A.R. и др., Cell, 98: 427-236, 1999). Нейротрамсмиссия глутамата, в частности активность рецептора NMDA, играет существенную роль в синаптической пластичности, обучении и памяти, и оказывается, что рецепторы, такие как NMDA, выступают в качестве градуированного переключателя для перехода через порог синаптической пластичности и образования памяти (Wiley, N.Y.; Bliss T.V. и Collingridge G.L., Nature, 361: 31-39, 1993). Трансгенные мыши, сверхэкспрессирующие субъединицу NR2B NMDA, показывают повышенную синаптическую пластичность и превосходную способность к обучению и запоминанию (Tang J.P. и др., Natur., 401-63-69, 1999). Таким образом, если дефицит глутамата связан с патофизиологией шизофрении, будет ожидаться повышенная трансмиссия глутамата, в частности, посредством активации рецептора NMDA с получением повешенного антипсихотического и когнитивного эффектов. Как известно, аминокислота глицин выполняет по меньшей мере две важные функции в ЦНС. Она выступает в качестве ингибирующей аминокислоты, связываясь с рецепторами глицина, чувствительными к стрихнину, и она также воздействует на активность возбуждения, выступая в качестве основного соагониста глутамата для функции рецептора N-метил-D-аспартата (NMDA). В то время как глутамат высвобождается в зависимости от его активности из синаптических терминалов, глицин, по-видимому, присутствует на более постоянном уровне и, как оказывается, модулирует/контролирует рецептор на его отклик на глутамат. Одним из самых эффективных способов контроля синаптических концентраций нейротрансмиттера является воздействие на их повторное поглощение в синапсах. Транспортеры нейротрансмиттера при удалении нейротрансмиттеров из внеклеточного пространства могут контролировать их внеклеточное время жизни и тем самым моделировать величину синаптической проводимости (Gainetdinov R.R. и др.,Trends in Pharm. Sci., 23 (8): 367-373, 2002). Транспортеры глицина, которые образуют часть натриевых и хлоридных семейств транспортеров нейротрансмиттера, играют важную роль в определении постсинаптических глицинергических воздействий и обеспечении низкой внеклеточной концентрации глицина путем повторного поглощения глицина в пресинаптических нервных терминалах и в сближении тонких глиальных процессов. Два различных гена транспортера глицина уже были клонированы (GlyT-1 и GlyT-2) из мозга млекопитающего, которые дали начали двум транспортерам 50% гомологичности последовательности аминокислот. GlyT-1 представляет четыре изоформы, берущие начало из альтернативного сплайсинга и использования альтернативного промотера (1a, 1b, 1 с и 1d). Только две из этих изоформ были обнаружены в мозге грызунов (GlyT-1a и GlyT-1b). GlyT-2 также имеет некоторую степень гетерогенности. Две изоформы GlyT-2 (2 а и 2b) были идентифицированы в мозге грызунов. Известно, что GlyT-1 располагается в ЦНС и в периферических тканях, тогда как GlyT-2 является специфическим по отношению к ЦНС.GlyT-1 имеет преимущественно глиальное распределение и обнаружен не только в зонах, соответствующих рецепторам глицина, чувствительных к стрихнину, но также и вне этих зон, где, как было установлено, он включается в модуляцию функции рецептора NMDA (Lopez-Corcuera В. и др., Mol. Mem. Biol.,18: 13-20, 2001). Таким образом, одна стратегия повышения активности рецептора NMDA состоит в том,чтобы поднять концентрацию глицина в локальном микроокружении синаптических рецепторов NMDA путем ингибирования транспортера GlyT-1 (Bergereon R. и др., Proc. Natl. Acad. Sci. USA, 95: 1573015734, 1998; Chen L. и др., J. Neurophysiol., 89 (2): 691-703, 2003). Ингибиторы транспортеров глицина пригодны для лечения неврологических и нейропсихиатрических заболеваний. Большинство приведенных выше заболеваний представляют собой психозы, шизофрению (Aimer R.E. и Miller D.J., Exp. Opin. Ther. Patents, 11 (4): 563-572, 2001), нарушения психического настроения, такие как тяжелое депрессивное расстройство, нарушения настроения, связанные с психическими расстройствами, такие как острая мания или депрессия, связанная с биполярными нарушениями, и нарушения настроения, связанные с шизофренией (Pralong E.T. и др., Prog. Neurobiol., 67: 173-202, 2002),аутические расстройства (Carlsson M.L., J. Neural. Trans,. 105: 525-535, 1998), когнитивные расстройства,такие как слабоумия, включая возрастное слабоумие и юношеское слабоумие типа Альцгеймера, расстройства памяти у млекопитающего, включая человека, нарушения, связанные с отсутствием внимания и боль (Armer R.E. и Miller D.J., Exp. Opin. Ther. Patents, 11 (4): 563-572, 2001).-2 009986 Таким образом, повышенная активация рецепторов NMDA посредством ингибирования GlyT-1 может приводить к получению агентов, которыми лечат психоз, шизофрению, слабоумие и другие заболевания, в которых ослаблены когнитивные процессы, такие как нарушения, связанные с отсутствием внимания, или болезнь Альцгеймера. Объектами настоящего изобретения являются соединения формулы I, применение соединений формулы I и их фармацевтически приемлемых солей для производства лекарственных средств для лечения заболеваний, связанных с активацией рецепторов NMDA посредством ингибирования GlyT-1, способ их получения, лекарственные средства на основе соединения в соответствии с изобретением и способ их получения, а также применение соединений формулы I для контроля или профилактики заболеваний, таких как психозы, нарушение памяти и обучения, шизофрения, слабоумие, и других заболеваний, в которых ослаблены когнитивные процессы, таких как недостаточная внимательность или болезнь Альцгеймера. Предпочтительными показаниями для соединений настоящего изобретения являются шизофрения,когнитивное нарушение и болезнь Альцгеймера. Кроме того, настоящее изобретение включает все рацемические смеси, все их соответствующие энантиомеры и/или оптические изомеры. Как здесь используется, термин "алкил" обозначает насыщенную линейную или разветвленную группу, содержащую от 1 до 6 атомов углерода, например метил, этил, пропил, изопропил, н-бутил, изобутил, 2-бутил, трет-бутил и им подобные. Предпочтительные алкильные группы представляют собой группы с 1-4 атомами углерода. Термин "галоген" обозначает хлор, йод, фтор и бром. Термин "арил" обозначает моновалентный циклический ароматический углеводородный радикал,состоящий из одного или нескольких конденсированных колец, в котором по крайней мере одно кольцо является ароматическим, например фенил, бензил, нафтил, бифенил или инданил. Термин "6-членный гетероарил, содержащий 1, 2 или 3 атома азота" обозначает моновалентный ароматический карбоциклический радикал, например пиридил, пиразинил, пиримидинил, пиридазинил или 1,3,5-триазинил. Термин "гетероциклоалкил" обозначает неароматический углеводородный радикал, например оксетанил, тетрагидрофуранил, тетрагидропиранил, азетидинил, пирролидинил, пиперидинил, пиперазинил,морфолинил или тиоморфолинил. Термин "5-членный ароматический гетероцикл, содержащий 1-4 гетероатома, выбранных из N и О" обозначает, например, 1,2,4-оксадиазолил, оксазолил, 1,3,4-оксадиазолил или тетразолил. Термин "5- или 6-членный гетероарил, содержащий 1, 2 или 3 гетероатома, выбранных из группы,состоящей из кислорода, серы или азота" обозначает моновалентный ароматический карбоциклический радикал, например пиридил, пиразинил, пиримидинил, пиридазинил, триазинил, тиазолил, тиенил, фурил, пирролил, имидазолил, пиразолил, изотиазолил или изоксазолил. Термин "алкил, замещенный галогеном" обозначает, например, следующие группы: CF3, CHF2,CH2F, CH2CF3, CH2CHF2, CH2CH2F, CH2CH2CF3, CH2CH2CH2CF3, CH2CH2Cl, CH2CF2CF3, CH2CF2CHF2,CF2CHFCF3, C(CH3)2CF3, CH(CH3)CF3 или CH(CH2F)CH2F. Термин "алкил, замещенный гидрокси" обозначает, например, следующие группы: СН(ОН)СН 3,СН 2 СН(ОН)СН 3, СН 2 СН(СН 3)СН 2 ОН, (СН 2)2 ОН, (СН 2)3 ОН или СН 2 С[(СН 3)]2-СН 2 ОН. Термин "фармацевтически приемлемые кислотные аддитивные соли" обозначает соли с неорганическими и органическими кислотами, такими как хлороводородная кислота, азотная кислота, серная кислота, фосфорная кислота, лимонная кислота, муравьиная кислота, фумаровая кислота, малеиновая кислота, уксусная кислота, янтарная кислота, винная кислота, метансульфоновая кислота, п-толуолсульфоновая кислота и им подобные. Одним вариантом осуществления настоящего изобретения являются соединения общей формулы где Ar представляет собой замещенный арил или незамещенный или замещенный 6-членный гетероарил,содержащий 1, 2 или 3 атома азота, и где арильная и гетероарильная группы являются замещенными одним или несколькими заместителями, выбранными из группы, состоящей из гидрокси, галогена, NO2,CN, (С 1-С 6)-алкила, (С 1-С 6)-алкила, замещенного галогеном, (С 1-С 6)-алкокси, (С 1-С 6)-алкокси, замещенного галогеном, NR7R8, C(O)R9 или SO2R10;R1 представляет собой водород или (С 1-С 6)-алкил;R2 представляет собой (С 1-С 6)-алкил, (С 1-С 6)-алкил, замещенный галогеном, (С 3-С 6)-циклоалкил, гетероциклоалкил, (С 1-С 6)-алкил-(С 3-С 6)-циклоалкил, (С 1-С 6)-алкилгетероциклоалкил, (С 1-С 6)-алкил-C(O)R9, (С 1-С 6)-алкил-CN, (С 2-С 6)-алкил-O-R13, (C2-C6)-алкил-NR7R8, арил или 6-членный гетероарил, содер-3 009986 жащий 1, 2 или 3 атома азота, (С 1-С 6)-алкиларил или (С 1-С 6)-алкил-5- или -6-членный гетероарил, содержащий 1, 2 или 3 гетероатома, выбранных из группы, состоящей из кислорода, серы или азота, где арил,гетероциклоалкил и гетероарил являются незамещенными или замещены одним или несколькими заместителями, выбранными из группы, состоящей из гидрокси, галогена, (С 1-С 6)-алкила или (C1-С 6)-алкокси;R3, R4 и R6 независимо друг от друга представляют собой водород, гидрокси, галоген, CN, (С 1-С 6)алкил, (С 1-С 6)-алкокси или NR7R8;R7 и R8 независимо друг от друга представляют собой водород или (С 1-С 6)-алкил;R11 и R12 независимо друг от друга представляют собой водород, С(О)-(С 1-С 6)-алкил, SO2-(С 1-С 6)алкил или вместе с N-атомом образуют 5-членную гетероарильную группу, необязательно замещенную галогеном, (C1-С 6)-алкилом, (С 1-С 6)-алкилом, замещенным галогеном или (С 3-С 6)-циклоалкилом;R13 представляет собой гидрокси, (С 1-С 6)-алкил или (С 3-С 6)-циклоалкил; и их фармацевтически приемлемые кислотные аддитивные соли,при условии, что исключаются 1-[5-(аминосульфонил)-2-метоксибензоил]-4-(3-хлорфенил)пиперазин,1-[5-(аминосульфонил)-2-метоксибензоил]-4-(4-фторфенил)пиперазин,1-[5-(аминосульфонил)-2-метоксибензоил]-4-[3-(трифторметил)фенил]пиперазин,4-(3-амино-4-нитрофенил)-1-[4-(диметиламино)-2-метокси-5-нитробензоил]-2-метилпиперазин,1-[4-(диметиламино)-2-метокси-5-нитробензоил]-2-метил-4-(4-нитрофенил)пиперазин,4-[4-(диметиламино)-2-метокси-5-нитробензоил]-2-метил-1-(4-нитрофенил)пиперазин,1-(2-хлор-4-нитрофенил)-4-[4-(диметиламино)-2-метокси-5-нитробензоил]пиперазин,1-[4-(диметиламино)-2-метокси-5-нитробензоил]-4-(2,4-динитрофенил)-2-метилпиперазин,1-(4-хлор-2-нитрофенил)-4-[4-(диметиламино)-2-метокси-5-нитробензоил]пиперазин и 4-[4-(диметиламино)-2-метокси-5-нитробензоил]-1-(2,4-динитрофенил)-2-метилпиперазин. Другим вариантом осуществления настоящего изобретения являются соединения формулы Ia где R представляет собой водород или галоген;R' представляет собой водород или галоген;R2 представляет собой (С 1-С 6)-алкил, (С 3-С 6)-циклоалкил, (С 1-С 6)-алкил-(С 3-С 6)-циклоалкил, (C1 С 6)-алкил, замещенный галогеном, -(СН 2)2O-(C1-С 6)-алкил, бензил или арил, необязательно замещенный галогеном; и их фармацевтически приемлемые кислотные аддитивные соли, за исключением 1-[5-(аминосульфонил)-2-метоксибензоил]-4-(3-хлорфенил)пиперазина и 1-[5-(аминосульфонил)-2-метоксибензоил]-4-[3-(трифторметил)фенил]пиперазина. Другим вариантом осуществления изобретения являются соединения формулы Ia, гдеR представляет собой водород или фтор;R' представляет собой водород или фтор;[4-(3-фтор-4-трифторметилфенил)пиперазин-1-ил]-(2-изобутокси-5-метансульфонилфенил)метанон. Другим вариантом осуществления настоящего изобретения являются соединения, где R5 представляет собой S(О)2-СН 3 и R2 представляет собой СН 2-циклопропил, например следующее соединение: 4-[4-(2-циклопропилметокси-5-метансульфонилбензоил)пиперазин-1-ил]-3-фторбензонитрил. Соединениями формулы Ia являются также соединения, где R5 представляет собой S(O)2-CH3 и R2 представляет собой CH2CF3, например следующие соединения:[4-(3-фтор-4-трифторметилфенил)пиперазин-1-ил]-[5-метансульфонил-2-(2,2,2-трифторэтокси)фенил]метанон. Соединениями формулы Ia являются также соединения, где R5 представляет собой S(O)2-CH3 и R2 представляет собой циклопентил, например следующие соединения: 4-[4-(2-циклопентилокси-5-метансульфонилбензоил)пиперазин-1-ил]-3-фторбензонитрил или 4-[4-(2-циклопентилокси-5-метансульфонилбензоил)пиперазин-1-ил]-2-фторбензонитрил. Предпочтительными соединениями формулы I настоящего изобретения являются соединения, гдеAr представляет собой замещенный фенил, R2 представляет собой (С 1-С 6)-алкил и R5 представляет собойS(О)2 СН 3 или S(O)2CH2CH3. Следующие конкретные соединения относятся к этой группе: 1-3-фтор-4-[4-(2-изопропокси-5-метансульфонилбензоил)пиперазин-1-ил]фенилэтанон,3-фтор-4-[4-(2-изопропокси-5-метансульфонилбензоил)пиперазин-1-ил]бензонитрил,2-фтор-4-[4-(2-изопропокси-5-метансульфонилбензоил)пиперазин-1-ил]бензонитрил,[4-(2-фтор-4-трифторметилфенил)пиперазин-1-ил]-(2-изопропокси-5-метансульфонилфенил)метанон,1-3-фтор-4-[4-(2-изобутокси-5-метансульфонилбензоил)пиперазин-1-ил]фенилэтанон,4-[4-(2-изобутокси-5-метансульфонилбензоил)пиперазин-1-ил]бензонитрил,3-фтор-4-[4-(2-изобутокси-5-метансульфонилбензоил)пиперазин-1-ил]бензонитрил,2-фтор-4-[4-(2-изобутокси-5-метансульфонилбензоил)пиперазин-1-ил]бензонитрил,(2-изобутокси-5-метансульфонилфенил)-[4-(4-трифторметилфенил)пиперазин-1-ил]метанон,[4-(2-фтор-4-трифторметилфенил)пиперазин-1-ил]-(2-изобутокси-5-метансульфонилфенил)метанон,[4-(3-фтор-4-трифторметилфенил)пиперазин-1-ил]-(2-изобутокси-5-метансульфонилфенил)метанон,[4-(2-фтор-4-метансульфонилфенил)пиперазин-1-ил]-(2-изобутокси-5-метансульфонилфенил)метанон,[4-(2-фтор-4-метансульфонилфенил)пиперазин-1-ил]-(2-изопропокси-5-метансульфонилфенил)метанон,2,3-дифтор-4-[4-(2-изопропокси-5-метансульфонилбензоил)пиперазин-1-ил]бензонитрил,2,3-дифтор-4-[4-(2-изобутокси-5-метансульфонилбензоил)пиперазин-1-ил]бензонитрил,2,5-дифтор-4-[4-(2-изобутокси-5-метансульфонилбензоил)пиперазин-1-ил]бензонитрил,2,6-дифтор-4-[4-(2-изобутокси-5-метансульфонилбензоил)пиперазин-1-ил]бензонитрил,3,5-дифтор-4-[4-(2-изобутокси-5-метансульфонилбензоил)пиперазин-1-ил]бензонитрил,4-[4-(2-трет-бутокси-5-метансульфонилбензоил)пиперазин-1-ил]-2,3-дифторбензонитрил,5-хлор-2-[4-(2-изопропокси-5-метансульфонилбензоил)пиперазин-1-ил]бензонитрил,4-[4-(2-трет-бутокси-5-метансульфонилбензоил)пиперазин-1-ил]-2,5-дифторбензонитрил,4-[4-(2-трет-бутокси-5-метансульфонилбензоил)пиперазин-1-ил]-3-фторбензонитрил,(2-трет-бутокси-5-метансульфонилфенил)-[4-(2-фтор-4-трифторметилфенил)пиперазин-1-ил]метанон,(2-трет-бутокси-5-метансульфонилфенил)-[4-(2,5-дифтор-4-метансульфонилфенил)пиперазин-1-ил]метанон,1-(4-4-[2-(2,2-диметилпроопкси)-5-метансульфонилбензоил]пиперазин-1-ил-3-фторфенил)этанон,4-4-[2-(2,2-диметилпропокси)-5-метансульфонилбензоил]пиперазин-1-илбензонитрил,4-4-[2-(2,2-диметилпропокси)-5-метансульфонилбензоил]пиперазин-1-ил-3-фторбензонитрил,4-4-[2-(2,2-диметилпропокси)-5-метансульфонилбензоил]пиперазин-1-ил-2-фторбензонитрил,[2-(2,2-диметилпропокси)-5-метансульфонилфенил]-[4-(4-трифторметилфенил)пиперазин-1-ил]метанон,[2-(2,2-диметилпропокси)-5-метансульфонилфенил]-[4-(2-фтор-4-трифторметилфенил)пиперазин-1 ил]метанон,[2-(2,2-диметилпропокси)-5-метансульфонилфенил]-[4-(3-фтор-4-трифторметилфенил)пиперазин-1 ил]метанон,[2-(2,2-диметилпропокси)-5-метансульфонилфенил]-[4-(2-фтор-4-этансульфонилфенил)пиперазин 1-ил]метанон,рац-1-4-[4-(2-втор-бутокси-5-метансульфонилбензоил)пиперазин-1-ил]-3-фторфенилэтанон,рац-4-[4-(2-втор-бутокси-5-метансульфонилбензоил)пиперазин-1-ил]-3-фторбензонитрил,рац-4-[4-(2-втор-бутокси-5-метансульфонилбензоил)пиперазин-1-ил]-2-фторбензонитрил,рац-(2-втор-бутокси-5-метансульфонилфенил)-[4-(2-фтор-4-трифторметилфенил)пиперазин-1-ил]метанон,рац-(2-втор-бутокси-5-метансульфонилфенил)-[4-(3-фтор-4-трифторметилфенил)пиперазин-1-ил]метанон,(2-изопропокси-5-метансульфонилфенил)-[4-(4-трифторметансульфонилфенил)пиперазин-1-ил]метанон,-5 009986[4-(4-циклопропансульфонил-2,5-дифторфенил)пиперазин-1-ил]-(2-изопропокси-5-метансульфонилфенил) метанон. Другой предпочтительной группой соединений формулы I являются соединения, где Ar представляет собой замещенный фенил, R2 представляет собой (СН 2)n-(С 3-С 7)-циклоалкил и R5 представляет собой S(O)2CH3, например следующие соединения: 1-4-[4-(2-циклопропилметокси-5-метансульфонилбензоил)пиперазин-1-ил]-3-фторфенилэтанон,4-[4-(2-циклопропилметокси-5-метансульфонилбензоил)пиперазин-1-ил]бензонитрил,4-[4-(2-циклопропилметокси-5-метансульфонилбензоил)пиперазин-1-ил]-3-фторбензонитрил,4-[4-(2-циклопропилметокси-5-метансульфонилбензоил)пиперазин-1-ил]-2-фторбензонитрил,(2-циклопропилметокси-5-метансульфонилфенил)-[4-(4-трифторметилфенил)пиперазин-1-ил]метанон,(2-циклопропилметокси-5-метансульфонилфенил)-[4-(2-фтор-4-трифторметилфенил)пиперазин-1 ил]метанон,(2-циклопропилметокси-5-метансульфонилфенил)-[4-(3-фтор-4-трифторметилфенил)пиперазин-1 ил]метанон,1-4-[4-(2-циклопентилокси-5-метансульфонилбензоил)пиперазин-1-ил]-3-фторфенилэтанон,4-[4-(2-циклопентилокси-5-метансульфонилбензоил)пиперазин-1-ил]бензонитрил,4-[4-(2-циклопентилокси-5-метансульфонилбензоил)пиперазин-1-ил]-3-фторбензонитрил,4-[4-(2-циклопентилокси-5-метансульфонилбензоил)пиперазин-1-ил]-2-фторбензонитрил,(2-циклопентилокси-5-метансульфонилфенил)-[4-(2-фтор-4-трифторметилфенил)пиперазин-1-ил]метанон,(2-циклопентилокси-5-метансульфонилфенил)-[4-(3-фтор-4-трифторметилфенил)пиперазин-1-ил]метанон,(2-циклопентилокси-5-метансульфонилфенил)-[4-(4-трифторметилфенил)пиперазин-1-ил]метанон,рац-[2-(1-циклопропилэтокси)-5-метансульфонилфенил]-[4-(4-трифторметилфенил)пиперазин-1-ил] метанон,4-[4-(2-циклопентилокси-5-метансульфонилбензоил)пиперазин-1-ил]-2,3-дифторбензонитрил,4-[4-(2-циклопентилокси-5-метансульфонилбензоил)пиперазин-1-ил]-2,5-дифторбензонитрил,4-[4-(2-циклобутилметокси-5-метансульфонилбензоил)пиперазин-1-ил]бензонитрил,4-[4-(2-циклобутилметокси-5-метансульфонилбензоил)пиперазин-1-ил]-2-фторбензонитрил,4-[4-(2-циклобутилметокси-5-метансульфонилбензоил)пиперазин-1-ил]-3-фторбензонитрил,(2-циклобутилметокси-5-метансульфонилфенил)-[4-(4-трифторметилфенил)пиперазин-1-ил]метанон,1-4-[4-(2-циклобутилметокси-5-метансульфонилбензоил)пиперазин-1-ил]-3-фторфенилэтанон,2-[4-(2-циклобутилметокси-5-метансульфонилбензоил)пиперазин-1-ил]-5-трифторметилбензонитрил,4-[4-(2-циклобутилметокси-5-метансульфонилбензоил)пиперазин-1-ил]-2,3-дифторбензонитрил,4-[4-(2-циклобутилметокси-5-метансульфонилбензоил)пиперазин-1-ил]-2,5-дифторбензонитрил,4-[4-(2-циклобутилметокси-5-метансульфонилбензоил)пиперазин-1-ил]-3,5-дифторбензонитрил,4-[4-(2-циклобутилметокси-5-метансульфонилбензоил)пиперазин-1-ил]-2,6-дифторбензонитрил,4-[4-(2-циклопропилметокси-5-метансульфонилбензоил)пиперазин-1-ил]-3,5-дифторбензонитрил,4-[4-(2-циклопентилокси-5-метансульфонилбензоил)пиперазин-1-ил]-3,5-дифторбензонитрил,4-[4-(2-циклопропилметокси-5-метансульфонилбензоил)пиперазин-1-ил]-2,6-дифторбензонитрил,4-[4-(2-циклопентилокси-5-метансульфонилбензоил)пиперазин-1-ил]-2,6-дифторбензонитрил,5-хлор-2-[4-(2-циклопропилметокси-5-метансульфонилбензоил)пиперазин-1-ил]бензонитрил,4-[4-(2-циклогексилокси-5-метансульфонилбензоил)пиперазин-1-ил]бензонитрил,4-[4-(2-циклогексилокси-5-метансульфонилбензоил)пиперазин-1-ил]-3-фторбензонитрил,4-[4-(2-циклогексилокси-5-метансульфонилбензоил)пиперазин-1-ил]-2-фторбензонитрил,(2-циклогексилокси-5-метансульфонилфенил)-[4-(4-трифторметилфенил)пиперазин-1-ил]метанон,-6 009986(2-циклогексилокси-5-метансульфонилфенил)-[4-(3-фтор-4-трифторметилфенил)пиперазин-1-ил] метанон,(2-циклогексилокси-5-метансульфонилфенил)-[4-(2-фтор-4-метансульфонилфенил)пиперазин-1-ил] метанон,1-4-[4-(2-циклобутокси-5-метансульфонилбензоил)пиперазин-1-ил]-3-фторфенилэтанон,4-[4-(2-циклобутокси-5-метансульфонилбензоил)пиперазин-1-ил]-3-фторбензонитрил,(2-циклобутокси-5-метансульфонилфенил)-[4-(3-фтор-4-трифторметилфенил)пиперазин-1-ил]метанон,(2-циклопентилокси-5-метансульфонилфенил)-[4-(4-трифторметансульфонилфенил)пиперазин-1 ил]метанон,1-4-[4-(2-циклопропилметокси-5-метансульфонилбензоил)пиперазин-1-ил]-2-фторфенилэтанон,2-[4-(2-циклопентилокси-5-метансульфонилбензоил)пиперазин-1-ил]-5-трифторметилбензонитрил,(2-циклопропилметокси-5-метансульфонилфенил)-[4-(4-этансульфонил-2-фторфенил)пиперазин-1 ил]метанон,(2-циклопентилокси-5-метансульфонилфенил)-[4-(4-этансульфонил-2-фторфенил)пиперазин-1-ил] метанон,(2-циклогексилокси-5-метансульфонилфенил)-[4-(4-этансульфонил-2-фторфенил)пиперазин-1-ил]метанон,(2-циклопентилокси-5-метансульфонилфенил)-[4-(4-циклопропансульфонил-2-фторфенил)пиперазин 1-ил]метанон,(2-циклогексилокси-5-метансульфонилфенил)-[4-(4-циклопропансульфонил-2-фторфенил)пиперазин 1-ил]метанон,(2-циклобутокси-5-метансульфонилфенил)-[4-(4-циклопропансульфонил-2-фторфенил)пиперазин 1-ил]метанон. Предпочтительными являются также соединения, где Ar представляет собой замещенный фенил, R2 представляет собой (С 1-С 6)-алкил, замещенный галогеном, и R5 представляет собой S(O)2CH3. Следующие соединения относятся к этой группе: 1-(3-фтор-4-4-[5-метансульфонил-2-(2,2,2-трифторэтокси)бензоил]пиперазин-1-илфенил)этанон,3-фтор-4-4-[5-метансульфонил-2-(2,2,2-трифторэтокси)бензоил]пиперазин-1-илбензонитрил,[4-(2-фтор-4-трифторметилфенил)пиперазин-1-ил]-[5-метансульфонил-2-(2,2,2-трифторэтокси)фенил] метанон,[4-(3-фтор-4-трифторметилфенил)пиперазин-1-ил]-[5-метансульфонил-2-(2,2,2-трифторэтокси)фенил] метанон,[4-(2-фтор-4-метансульфонилфенил)пиперазин-1-ил]-[5-метансульфонил-2-(2,2,2-трифторэтокси)фенил] метанон,3-фтор-4-4-[5-метансульфонил-2-(3,3,3-трифторпропокси)бензоил]пиперазин-1-илбензонитрил,[4-(3-фтор-4-трифторметилфенил)пиперазин-1-ил]-[5-метансульфонил-2-(3,3,3-трифторпропокси) фенил]метанон,[4-(2-фтор-4-трифторметилфенил)пиперазин-1-ил]-[5-метансульфонил-2-(3,3,3-трифторпропокси) фенил]метанон,1-(3-фтор-4-4-[5-метансульфонил-2-(3,3,3-трифторпропокси)бензоил]пиперазин-1-илфенил)этанон,2,5-дифтор-4-[4-(5-метансульфонил-2-трифторметоксибензоил)пиперазин-1-ил]бензонитрил,2,3-дифтор-4-4-[2-(2-фтор-1-фторметилэтокси)-5-метансульфонилбензоил]пиперазин-1-илбензонитрил,2-фтор-4-4-[5-метансульфонил-2-(2,2,3,3,3-пентафторпропокси)бензоил]пиперазин-1-илбензонитрил,[5-метансульфонил-2-(2,2,3,3,3-пентафторпропокси)фенил]-[4-(4-трифторметилфенил)пиперазин-1 ил]метанон,2,3-дифтор-4-4-[5-метансульфонил-2-(2,2,3,3,3-пентафторпропокси)бензоил]пиперазин-1-илбензонитрил,3,5-дифтор-4-4-[5-метансульфонил-2-(2,2,3,3,3-пентафторпропокси)бензоил]пиперазин-1-илбензонитрил,2-4-[2-(2-фтор-1-фторметилэтокси)-5-метансульфонилбензоил]пиперазин-1-ил-5-трифторметилбензонитрил,рац-2,3-дифтор-4-4-[5-метансульфонил-2-(2,2,2-трифтор-1-метилэтокси)бензоил]пиперазин-1-ил бензонитрил,2-фтор-4-4-[5-метансульфонил-2-(2,2,3,3-тетрафторпропокси)бензоил]пиперазин-1-илбензонитрил,3-фтор-4-4-[5-метансульфонил-2-(2,2,3,3-тетрафторпропокси)бензоил]пиперазин-1-илбензонитрил,[5-метансульфонил-2-(2,2,3,3-тетрафторпропокси)фенил]-[4-(4-трифторметилфенил)пиперазин-1 ил]метанон,[4-(2-фтор-4-трифторметилфенил)пиперазин-1-ил]-[5-метансульфонил-2-(2,2,3,3-тетрафторпропокси) фенил]метанон,2,3-дифтор-4-4-[5-метансульфонил-2-(2,2,3,3-тетрафторпропокси)бензоил]пиперазин-1-илбензонитрил,3,5-дифтор-4-4-[5-метансульфонил-2-(2,2,3,3-тетрафторпропокси)бензоил]пиперазин-1-илбензонитрил,[4-(3,4-дихлорфенил)пиперазин-1-ил]-[5-метансульфонил-2-(2,2,2-трифторэтокси)фенил]метанон,рац-5-хлор-2-4-[5-метансульфонил-2-(2,2,2-трифтор-1-метилэтокси)бензоил]пиперазин-1-илбензонитрил,рац-3,5-дифтор-4-4-[5-метансульфонил-2-(2,2,2-трифтор-1-метилэтокси)бензоил]пиперазин-1-ил бензонитрил,-7 009986 рац-2,5-дифтор-4-4-[5-метансульфонил-2-(2,2,2-трифтор-1-метилэтокси)бензоил]пиперазин-1-ил бензонитрил,рац-2,6-дифтор-4-4-[5-метансульфонил-2-(2,2,2-трифтор-1-метилэтокси)бензоил]пиперазин-1-ил бензонитрил,рац-4-4-[5-метансульфонил-2-(2,2,2-трифтор-1-метилэтокси)бензоил]пиперазин-1-илбензонитрил,рац-3-фтор-4-4-[5-метансульфонил-2-(2,2,2-трифтор-1-метилэтокси)бензоил]пиперазин-1-илбензонитрил,рац-2-фтор-4-4-[5-метансульфонил-2-(2,2,2-трифтор-1-метилэтокси)бензоил]пиперазин-1-илбензонитрил,рац-5-метансульфонил-2-(2,2,2-трифтор-1-метилэтокси)фенил]-[4-(4-трифторметилфенил)пиперазин 1-ил]метанон,рац-[4-(2-фтор-4-трифторметилфенил)пиперазин-1-ил]-[5-метансульфонил-2-(2,2,2-трифтор-1-метилэтокси)фенил]метанон,рац-[4-(3-фтор-4-трифторметилфенил)пиперазин-1-ил]-[5-метансульфонил-2-(2,2,2-трифтор-1-метилэтокси)фенил]метанон,[4-(2-фтор-4-трифторметилфенил)пиперазин-1-ил]-[5-метансульфонил-2-S или R)-2,2,2-трифтор-1 метилэтокси)фенил]метанон,[5-метансульфонил-2-S или R)-2,2,2-трифтор-1-метилэтокси)фенил]-[4-(4-трифторметилфенил)пиперазин-1-ил]метанон и[5-метансульфонил-2-R или S)-2,2,2-трифтор-1-метилэтокси)фенил]-[4-(4-трифторметилфенил)пиперазин-1-ил]метанон. Предпочтительными соединениями формулы I настоящего изобретения являются также соединения, где Ar представляет собой замещенный фенил, R2 представляет собой (С 1-С 6)-алкил, (С 1-С 6)-алкил,замещенный галогеном, (СН 2)n-(С 3-С 7)-циклоалкил, бицикло[2,2,1]гептил, (СН 2)n-О-(С 1-С 6)-алкил или[5-нитро-2-(2,2,3,3,3-пентафторпропокси)фенил]-[4-(4-трифторметилфенил)пиперазин-1-ил]метанон. Предпочтительными являются также соединения, где Ar представляет собой замещенный фенил, R2 представляет собой (С 1-С 6)-алкил, (С 1-С 6)-алкил, замещенный галогеном, или (СН 2)n-(С 3-С 7)-циклоалкил и R5 представляет собой S(O)2NHCH3. 3-[4-(4-Циано-3-фторфенил)пиперазин-1-карбонил]-N-метил-4-трифторметоксибензолсульфонамид,3-[4-(4-циано-3-фторфенил)пиперазин-1-карбонил]-4-изобутокси-N-метилбензолсульфонамид,3-[4-(4-циано-3-фторфенил)пиперазин-1-карбонил]-4-циклопентилокси-N-метилбензолсульфонамид,3-[4-(4-циано-3-фторфенил)пиперазин-1-карбонил]-4-циклобутокси-N-метилбензолсульфонамид,3-[4-(4-циано-3-фторфенил)пиперазин-1-карбонил]-4-циклобутилметокси-N-метилбензолсульфонамид,3-[4-(4-цианофенил)пиперазин-1-карбонил]-4-изобутокси-N-метилбензолсульфонамид,3-[4-(4-цианофенил)пиперазин-1-карбонил]-4-циклопентилокси-N-метилбензолсульфонамид,3-[4-(4-цианофенил)пиперазин-1-карбонил]-4-циклобутилметокси-N-метилбензолсульфонамид,3-[4-(4-циано-2-фторфенил)пиперазин-1-карбонил]-4-изобутокси-N-метилбензолсульфонамид,3-[4-(4-циано-2-фторфенил)пиперазин-1-карбонил]-4-(2,2-диметилпропокси)-N-метилбензолсульфонамид,3-[4-(4-циано-2-фторфенил)пиперазин-1-карбонил]-4-изопропокси-N-метилбензолсульфонамид,3-[4-(4-циано-2-фторфенил)пиперазин-1-карбонил]-4-циклопентилокси-N-метилбензолсульфонамид,3-[4-(4-циано-2-фторфенил)пиперазин-1-карбонил]-4-циклобутокси-N-метилбензолсульфонамид,3-[4-(4-циано-2-фторфенил)пиперазин-1-карбонил]-4-циклопропилметокси-N-метилбензолсульфонамид,3-[4-(4-циано-2-фторфенил)пиперазин-1-карбонил]-4-циклобутилметокси-N-метилбензолсульфонамид,3-[4-(4-ацетил-2-фторфенил)пиперазин-1-карбонил]-4-изобутокси-N-метилбензолсульфонамид,3-[4-(4-ацетил-2-фторфенил)пиперазин-1-карбонил]-4-(2,2-диметилпропокси)-N-метилбензолсульфонамид,3-[4-(4-ацетил-2-фторфенил)пиперазин-1-карбонил]-4-циклопентилокси-N-метилбензолсульфонамид,3-[4-(4-ацетил-2-фторфенил)пиперазин-1-карбонил]-4-циклобутокси-N-метилбензолсульфонамид,3-[4-(4-ацетил-2-фторфенил)пиперазин-1-карбонил]-4-циклопропилметокси-N-метилбензолсульфонамид,-8 009986 4-изобутокси-N-метил-3-[4-(4-трифторметилфенил)пиперазин-1-карбонил]бензолсульфонамид,4-(2,2-диметилпропокси)-N-метил-3-[4-(4-трифторметилфенил)пиперазин-1-карбонил]бензолсульфонамид,4-изопропокси-N-метил-3-[4-(4-трифторметилфенил)пиперазин-1-карбонил]бензолсульфонамид,4-циклопентилокси-N-метил-3-[4-(4-трифторметилфенил)пиперазин-1-карбонил]бензолсульфонамид,4-циклобутокси-N-метил-3-[4-(4-трифторметилфенил)пиперазин-1-карбонил]бензолсульфонамид,4-циклопропилметокси-N-метил-3-[4-(4-трифторметилфенил)пиперазин-1-карбонил]бензолсульфонамид,4-циклобутилметокси-N-метил-3-[4-(4-трифторметилфенил)пиперазин-1-карбонил]бензолсульфонамид,N-метил-3-[4-(4-трифторметилфенил)пиперазин-1-карбонил]-4-(3,3,3-трифторпропокси)бензолсульфонамид,3-[4-(4-циано-2-фторфенил)пиперазин-1-карбонил]-N-метил-4-(2,2,2-трифторэтокси)бензолсульфонамид,N-метил-4-(2,2,2-трифторэтокси)-3-[4-(4-трифторметилфенил)пиперазин-1-карбонил]бензолсульфонамид,рац-N-метил-4-(2,2,2-трифтор-1-метилэтокси)-3-[4-(4-трифторметилфенил)пиперазин-1-карбонил] бензолсульфонамид,рац-3-[4-(4-циано-2,5-дифторфенил)пиперазин-1-карбонил]-N-метил-4-(2,2,2-трифтор-1-метилэтокси) бензолсульфонамид и рац-3-[4-(4-циано-2,3-дифторфенил)пиперазин-1-карбонил]-N-метил-4-(2,2,2-трифтор-1-метилэтокси) бензолсульфонамид. Другой предпочтительной группой соединений формулы I является группа, где Ar представляет собой замещенную 6-членную гетероарильную группу, содержащую 1, 2 или 3 атома азота, R2 представляет собой (С 1-С 6)-алкил или (СН 2)n-(С 3-С 7)-циклоалкил и R5 представляет собой SO2CH3, например(2-циклопентилокси-5-метансульфонилфенил)-[4-(3-фтор-5-трифторметилпиридин-2-ил)пиперазин 1-ил]метанон. Другими предпочтительными соединениями являются соединения формулы I, где Ar представляет собой замещенную 6-членную гетероарильную группу, содержащую 1, 2 или 3 атома азота, R2 представляет собой (C1-С 6)-алкил, замещенный галогеном, и R5 представляет собой SO2CH3, например следующие соединения: рац-[4-(3-хлор-5-трифторметилпиридин-2-ил)пиперазин-1-ил]-[5-метансульфонил-2-(2,2,2-трифтор 1-метилэтокси)фенил]метанон,рац-[5-метансульфонил-2-(2,2,2-трифтор-1-метилэтокси)фенил]-[4-(5-трифторметилпиридин-2-ил) пиперазин-1-ил]метанон,рац-[4-(5-бромпиридин-2-ил)пиперазин-1-ил]-[5-метансульфонил-2-(2,2,2-трифтор-1-метилэтокси) фенил]метанон,рац-[4-(3-фтор-5-трифторметилпиридин-2-ил)пиперазин-1-ил]-[5-метансульфонил-2-(2,2,2-трифтор 1-метилэтокси)фенил]метанон,рац-[5-метансульфонил-2-(2,2,2-трифтор-1-метилэтокси)фенил]-[4-(6-трифторметилпиридин-2-ил) пиперазин-1-ил]метанон,[5-метансульфонил-2-S или R)-2,2,2-трифтор-1-метилэтокси)фенил]-[4-(5-трифторметилпиридин 2-ил)пиперазин-1-ил]метанон,[5-метансульфонил-2-R или S)-2,2,2-трифтор-1-метилэтокси)фенил]-[4-(5-трифторметилпиридин 2-ил)пиперазин-1-ил]метанон,[4-(3-фтор-5-трифторметилпиридин-2-ил)пиперазин-1-ил]-[5-метансульфонил-2-S)-2,2,2-трифтор 1-метилэтокси)фенил]метанон и[4-(3-фтор-5-трифторметилпиридин-2-ил)пиперазин-1-ил]-[5-метансульфонил-2-(2,2,2-трифтор-1,1 диметилэтокси)фенил]метанон. Настоящие соединения формулы I и их фармацевтически приемлемые соли могут быть получены известными способами, например способами, описанными далее, где способ включает: а) реакцию соединения формулы где заместители являются такими, как описано выше, или б) реакцию соединения формулы с соединением формулы R2OH необязательно в присутствии катализатора, такого как Cu(I)I, и основания, такого как карбонат калия, карбонат цезия или натрия, с получением соединения формулы где X представляет собой галоген и другие заместители являются такими, как определено выше, или в) реакцию соединения формулы с соединением формулы R2X в присутствии основания и необязательно при микроволновом излучении с получением соединения формулы где X представляет собой галоген, мезилат или трифлат и другие заместители являются такими, как определено выше, или г) реакцию соединения формулы- 10009986 где заместители являются такими, как определено выше, или д) реакцию соединения формулы где X представляет собой галоген и другие заместители являются такими, как определено выше, или е) реакцию соединения формулы с соответствующим амином или спиртом в присутствии активирующего агента с получением соединения формулы где R9 представляет собой (С 1-С 6)-алкил, (С 3-С 6)-циклоалкил, (C1-С 6)-алкокси или NR7R8 и другие заместители являются такими, как определено выше, или ж) реакцию соединения формулы где R представляет собой Н или алкил и другие заместители являются такими, как определено выше, или з) реакцию соединения формулы с восстанавливающим агентом, таким как боргидрид натрия (когда R представляет собой Н), или алкилирующим агентом, таким как алкиллитий (когда R представляет собой алкил), с получением соединения формулы где R представляет собой Н или алкил и другие заместители являются такими, как определено выше, и при необходимости, превращение полученных соединений в фармацевтически приемлемые кислотные аддитивные соли. Соединения формулы I могут быть получены в соответствии с вариантом способа а)-з) и по следующим схемам 1-8. Исходные реагенты являются коммерчески доступными или могут быть получены в соответствии с известными способами. Схема 1 Соединения общей формулы I могут быть получены реакцией производных пиперазина формулы II с соответствующей кислотой формулы III в присутствии активирующего агента, такого как TBTU (2-(1 Н-бензотриазол-1-ил)-1,1,3,3-тетраметилуронийтетрафторборат). Кислота формулы III может быть получена реакцией кислоты формулы IV со спиртом формулы R2OH, необязательно в присутствии соли меди, такой как Cu(I)Br. Производные пиперазина формулы II могут быть получены нагреванием соответствующего пиперазина сArX или реакцией N-защищенного пиперазина с ArX в присутствии палладиевого катализатора с последующим снятием защитной группы. Защитная группа обычно представляет собой трет-бутоксикарбонил (Boc). Схема 2 Альтернативно, соединения общей формулы I могут быть получены реакцией ацилпиперазина формулы V и спирта формулы R2OH, необязательно в присутствии соли меди, такой как Cu(I)I. Производные ацилпиперазина формулы V могут быть получены реакцией кислоты формулы IV с производными пиперазина формулы II в присутствии активирующего агента, такого как TBTU (2-(1 Н-бензотриазол- 12009986 1-ил)-1,1,3,3-тетраметилуронийтетрафторборат). Схема 3 Соединения общей формулы I могут быть получены реакцией соединения формулы VI с электрофильным реагентом формулы R2X в присутствии основания, такого как карбонат калия, и необязательно при микроволновом излучении, где X представляет собой галоген, мезилат или трифлат. Схема 4 Соединения общей формулы I могут быть получены реакцией фенола формулы VI со спиртом формулы R2OH в условиях реакции Митсунобу в присутствии фосфина, такого как трифенилфосфин или дифенил-2-пиридилфосфин, и диалкилазадикарбоксилата, такого как диэтилазадикарбоксилат или ди-третбутилазодикарбоксилат. Соединение формулы VI может быть получено снятием защиты (например, с помощью водорода) с фенола, защищенного бензиловым эфиром (I с R2: бензил). Альтернативно, соединение формулы VI может быть получено реакцией производных пиперазина формулы II с кислотой формулы VII в присутствии активирующего агента, такого как TBTU (2-(1 Н-бензотриазол-1-ил)-1,1,3,3-тетраметилуронийтетрафторборат). Схема 5 Соединения общей формулы I могут быть получены реакцией пиперазина формулы VIII с ArX. Схема 6 где R9 представляет собой (С 1-С 6)-алкокси или NR7R8. Соединения общей формулы Ib, где R9 является таким, как определено выше, могут быть получены- 13009986 реакцией кислоты формулы Ia с соответствующим амином или спиртом в присутствии активирующего агента, такого как карбонилдиимидазол. Схема 7 Соединения общей формулы Id могут быть получены в соответствии со схемой 7 реакцией соединения формулы Ic, имеющего карбонильную группу, с соединением формулы RONH2, где R представляет собой Н или алкил и R9 представляет собой (С 1-С 6)-алкил, (С 3-С 6)-циклоалкил, (С 1-С 6)-алкокси или NR7R8. Схема 8 Соединения общей формулы Ie, где R представляет собой Н или алкил и R9 представляет собой (С 1 С 6)-алкил или (С 3-С 6)-циклоалкил, могут быть получены реакцией соединения формулы Ic, имеющего карбонильную группу, с восстанавливающим агентом, таким как боргидрид натрия (когда R представляет собой Н) или алкилирующим агентом, таким как алкиллитий (когда R представляет собой алкил). Рацемические смеси хиральных соединений формулы I могут быть разделены с помощью хиральной ВЭЖХ. Кислотные аддитивные соли основных соединений формулы I могут быть превращены в соответствующие свободные основания обработкой, по крайней мере, стехиометрическим эквивалентом подходящего основания, такого как гидроксид натрия или калия, карбонат калия, бикарбонат натрия, аммиак и им подобные. Следующие 660 примеров иллюстрируют настоящее изобретение без его ограничения. Все температуры приведены в градусах Цельсия. В примерах использовались следующие сокращения:(a) трет-Бутиловый эфир 4-(2-фтор-4-трифторметилфенил)пиперазин-1-карбоновой кислоты. Смесь 20 ммоль 1-бром-2-фтор-4-трифторметилбензола, 24,7 ммоль н-Вос-пиперазина, 0,1 ммоль комплекса трис(дибензилиденацетон)дипалладия с хлороформом, 28,8 ммоль трет-бутоксида натрия и 0,4 ммоль 2-(дициклогексилфосфино)бифенила в 50 мл толуола нагревали в течение 16 ч при 80 С. После охлаждения до RT смесь обрабатывали 15 г Isolute HM-N и все летучие вещества удаляли в вакууме. Остаток очищали на силикагеле, элюируя градиентом гептан/EtOAc, с получением после упаривания указанного в заголовке соединения.(б) 1-(2-Фтор-4-трифторметилфенил)пиперазин. Смесь 9 ммоль трет-бутилового эфира 4-(2-фтор-4-трифторметилфенил)пиперазин-1-карбоновой кислоты в 20 мл диоксана обрабатывали 8,93 мл 4N HCl в диоксане в течение 2 ч при 80 С. Смесь концентрировали и обрабатывали 20 мл воды, 20 мл 2 М Na2CO3 и экстрагировали 50 мл EtOAc. Органическую фазу промывали 30 мл насыщенного NaCl. Все водные фазы объединяли и экстрагировали 50 млEtOAc. Объединенные органические фазы высушивали MgSO4 и упаривали с получением указанного в заголовке соединения 1.1. 1 Н-ЯМР (300 МГц, CDCl3):7,50 (d, J=13,3 Гц, 1 Н, Н-3), 7,45 (d, J=8,8 Гц, 1H, H-5), 7,16 (dd, J1=8,8 Гц,J2=8,8 Гц, 1H, H-6), 3,5-3,2 (s, br, 1H, NH), 3,04 (m, 4H, пиперазин), 2,87 (m, 4H, пиперазин).- 14009986 К 99 ммоль 2-хлор-5-(метилтио)бензойной кислоты в 400 мл метанола при 0 С добавляли 296 ммольoxone и смесь перемешивали при RT в течение 3,5 ч. Осадок отфильтровывали и фильтрат концентрировали при пониженном давлении. Остаток экстрагировали 3 раза 400 мл этилацетата и объединенные органические фазы промывали 2 раза 300 мл 1N HCl и 300 мл насыщенного водного раствора NaCl и высушивалиMgSO4. Упаривание при пониженном давлении приводило к получению указанного в заголовке соединения.(б) 2-Изопропокси-5-метансульфонилбензойная кислота. Смесь 2,13 ммоль 2-хлор-5-метансульфонилбензойной кислоты, 0,64 ммоль Cu(I)Br в 5 мл NEt3 и 25 мл изопропанола нагревали до 120 С в течение 16 ч в закрытой пробирке. Летучие вещества удаляли в вакууме и остаток переносили в 70 мл 1N HCl. Экстракция этилацетатом высушенных объединенных органических фракций и упаривание приводили к получению остатка, который очищали препаративной ВЭЖХ с обратной фазой, элюируя градиентом ацетонитрил/вода. Упаривание фракций продукта приводило к получению указанного в заголовке соединения 1,2.MS (m/e): 257,0 (МН-, 100%). Аналогично примеру 1.2(б) были получены соединения 1.3-1.7 в следующей таблице, исходя из 2 хлор-5-метансульфонилбензойной кислоты и соответствующего спирта.J. EN, 5: 3261-3272 (1999)] в 1 мл диоксана обрабатывали 0,522 ммоль триэтиламина и затем раствором 0,261 ммоль 1-(3-фтор-4-пиперазин-1-илфенил)этанона (CAS: 189763-57-3; WO 97/14,690) в 1 мл диоксана. Смесь перемешивали при RT в течение 30 мин. Растворитель удаляли в вакууме. Сырое масло переносили в воду. Водный слой экстрагировали 3 раза CH2Cl2. Объединенные экстракты высушивали Na2SO4,отфильтровывали и растворитель удаляли в вакууме. Сырое смолистое вещество очищали на силикагеле(а) 2-Амино-5-метансульфонилбензойная кислота. Смесь 4,26 ммоль 2-хлор-5-метансульфонилбензойной кислоты, 0,39 ммоль порошка меди и 10 мл 25% гидроксида аммония нагревали при 125-130 С при перемешивании в течение 18 ч. Смесь охлаждали до комнатной температуры и отфильтровывали. Твердое вещество промывали метанолом. Фильтрат концентрировали в вакууме. Остаток подкисляли 1N HCl до рН 2. Полученное твердое вещество промывали водой и высушивали (HV, 50 С, 1 ч) с получением указанного в заголовке соединения.(б) 2-Йод-5-метансульфонилбензойная кислота. К суспензии 3,0 ммоль 2-амино-5-метансульфонилбензойной кислоты в смеси 1,7 мл серной кислоты и 1,7 мл воды добавляли по каплям раствор 3,92 ммоль нитрита натрия в 1,7 мл воды с такой скоростью, чтобы температура не превышала 3 С. Смесь перемешивали при 0 С в течение 1 ч. По каплям при 0 С добавляли раствор 3,0 ммоль KI в 1,7 мл воды. Коричневую суспензию нагревали до RT и перемешивали в течение 30 мин. Избыток йода устраняли добавлением нескольких капель раствора гидросульфита натрия. Твердое вещество отфильтровывали, промывали водой и высушивали (HV, 50 С, 1 ч) с получением указанного в заголовке соединения.(в) (2-Йод-5-метансульфонилфенил)-[4-(4-трифторметилфенил)пиперазин-1-ил]метанон. К раствору 9,2 ммоль 2-йод-5-метансульфонилбензойной кислоты в 20 мл диметилформамида осторожно добавляли 11,5 ммоль TBTU, 46,0 ммоль N-этилдиизопропиламина и 11,0 ммоль 1-(4-трифторметилфенил)пиперазина (ABCR F07741NB, [30459-17-7]). Реакционную смесь затем перемешивали приRT в течение 2 ч, концентрировали в вакууме и очищали колоночной хроматографией (SiO2, 50 г,CH2Cl2/MeOH/NH3=от 100/0/0 до 95/4,5/0,5) с получением указанного в заголовке соединения 1.9.MS (m/e): 539,1 (М+Н+). Пример 5. Получение [4-(2-фтор-4-трифторметилфенил)пиперазин-1-ил]-(2-изопропокси-5-метансульфонилфенил)метанона. Смесь 0,05 ммоль 2-изопропокси-5-метансульфонилбензойной кислоты (соединение 1,2), 0,06 ммоль 1-(2-фтор-4-трифторметилфенил)пиперазина, 0,055 ммоль TBTU и 0,25 ммоль DIPEA в 1 мл ДМФА перемешивали при RT в течение 16 ч. Добавляли 0,5 мл МеОН/НСООН 1/1 и смесь подвергали разделению с помощью препаративной ВЭЖХ с обратной фазой, элюируя градиентом ацетонитрил/вода, с получением указанного в заголовке соединения.MS (m/e): 489,2 (МН+, 100%). Аналогично примеру 5 были получены соединения 1-4, 6-46 и 52-54 в следующей таблице, исходя из производных кислоты и производных пиперазина. Пример 47. Получение 1-3-фтор-4-[4-(2-метокси-5-нитробензоил)пиперазин-1-ил]фенилэтанона. К раствору 0,257 ммоль 1-3-фтор-4-[4-(2-фтор-5-нитробензоил)пиперазин-1-ил]фенилэтанона (соединение 1.8) в 1,5 мл диоксана частями добавляли 102 мг метоксида натрия. Смесь перемешивали при 100 С в течение 4 ч. Реакционную смесь разбавляли 10 мл водой, нейтрализовали 1N HCl и затем экстрагировали этилацетатом (3 раза по 10 мл). Объединенные органические фазы концентрировали в вакууме. Остаток хроматографировали на силикагеле: элюент: гептан/этилацетат 0-30% (10 мин), с получением соединения 47.(соединение 1.9), 0,037 ммоль CuI, 0,37 ммоль Cs2CO3, 0,074 ммоль 1,10-фенантролина и 0,4 мл бензилового спирта нагревали при 110 С в течение 16 ч. Смесь охлаждали до RT, разбавляли этилацетатом и отфильтровывали. Органический слой дважды промывали водой, высушивали Na2SO4, отфильтровывали и растворитель удаляли в вакууме. Сырое масло очищали на силикагеле, элюент: гептан/этилацетат 0-50% (25 мин), с получением соединения 48.MS (m/e): 519,2 (М+Н+, 100%). Аналогично примеру 48 были получены соединения 49-51 в следующей таблице из (2-йод-5-метансульфонилфенил)-[4-(4-трифторметилфенил)пиперазин-1-ил]метанона (соединение 1.9) и спиртов.(а) 2-Амино-5-метансульфонилбензойная кислота. Смесь 4,26 ммоль 2-хлор-5-метансульфонилбензойной кислоты (соединение 1,2 а), 0,39 ммоль порошка меди и 10 мл 25% гидроксида аммония нагревали при 125-130 С при перемешивании в течение 18 ч. Смесь охлаждали до комнатной температуры и отфильтровывали. Твердое вещество промывали метанолом. Фильтрат концентрировали в вакууме. Остаток подкисляли 1N HCl до рН 2. Полученное твердое вещество промывали водой и высушивали (HV, 50 С, 1 ч) с получением указанного в заголовке соединения.(б) 2-Йод-5-метансульфонилбензойная кислота. К суспензии 3,0 ммоль 2-амино-5-метансульфонилбензойной кислоты в смеси 1,7 мл серной кислоты и 1,7 мл воды по каплям добавляли раствор 3,92 ммоль нитрита натрия в 1,7 мл воды с такой скоростью, чтобы температура не поднималась выше 3 С. Смесь перемешивали при 0 С в течение 1 ч. По каплям добавляли раствор 3,0 ммоль KI в 1,7 мл воды при 0 С. Коричневую суспензию нагревали до RT и перемешивали в течение 30 мин. Избыток йода удаляли добавлением нескольких капель раствора гидросульфита натрия. Твердое вещество отфильтровывали, промывали водой и высушивали (HV, 50 С, 1 ч) с получением указанного в заголовке соединения.(в) 5-Метансульфонил-2-(2-метоксиэтокси)бензойная кислота. К раствору 1,6 ммоль 2-йод-5-метансульфонилбензойной кислоты в 30 мл 2-метоксиэтанола и 6 мл триэтиламина добавляли 79 мг бромида меди(I) и реакционную смесь нагревали при 120 С в течение 4 ч. Растворитель отгоняли и остаток растворяли в 90 мл 1N HCl. Водную фазу дважды экстрагировали этилацетатом и объединенные органические экстракты дважды промывали водой и 1 раз насыщенным раствором хлорида натрия. Органический слой высушивали Na2SO4, отфильтровывали и упаривали с получением указанного в заголовке соединения 1.10.(а) 2-Бром-5-цианобензойная кислота. К суспензии 7,1 ммоль бромида меди(II) в ацетонитриле (30 мл) по каплям добавляли 8,63 ммоль трет-бутилнитрита при 0 С в течение 2 мин. Частями добавляли 6,17 ммоль 2-амино-5-цианобензойной кислоты (CAS: 99767-45-0; WO9518097) в течение 10 мин при 0 С. Смесь перемешивали при 0 С в течение 2 ч и затем при комнатной температуре в течение ночи. Половину растворителя удаляли в вакууме. Остаток переносили в HCl 1N (15 мл) и этилацетат (30 мл). Органический слой экстрагировали NaOH 1N(310 мл). Водный слой подкисляли 2N HCl. Полученное твердое вещество отфильтровывали, промывали водой и высушивали (высокий вакуум, 50 С) с получением указанного в заголовке соединения.- 19009986 К раствору 0,16 ммоль 2-бром-5-цианобензойной кислоты в 6 мл 2-метоксиэтанола и 1,2 мл триэтиламина добавляли 23 мг бромида меди(I) и реакционную смесь нагревали при 120 С в течение 4 ч. Растворитель отгоняли и остаток растворяли в 20 мл 1N HCl. Водную фазу экстрагировали дважды этилацетатом и объединенные органические экстракты промывали дважды водой и 1 раз насыщенным раствором хлорида натрия. Органический слой высушивали Na2SO4, отфильтровывали и упаривали с получением указанного в заголовке соединения 1.11.MS (m/e): 220,4 (МН-, 100%). Пример 1.12. Получение 5-циано-2-(2,2,2-трифторэтокси)бензойной кислоты. Смесь 11,3 ммоль натрия в 66 ммоль 2,2,2-трифторэтанола нагревали при 100 С до растворения всего натрия (20 мин). Затем добавляли раствор 5,5 ммоль 5-циано-2-йодбензойной кислоты [CAS: 219841-92-6;WO9901455] в 2 мл N-метил-2-пирролидона и 0,5 ммоль бромида меди(I) и реакционную смесь нагревали при 120 С в течение 2 ч. Реакционную смесь выливали в воду, подкисляли до рН 2 с помощью конц. HCl и экстрагировали 3 раза этилацетатом. Объединенные органические экстракты промывали насыщенным раствором хлорида натрия, высушивали Na2SO4 и упаривали. Ускоренная хроматография на силикагеле с помощью смеси гептан/этилацетат приводила к получению указанного в заголовке соединения 1.12.MS (EI) (m/e): 245,1 (М+, 94%), 146,0 ([M-CF3CH2O]+, 100%). Аналогично примеру 1.12 были получены соединения 1.13-1.16 в следующей таблице из 5-циано-2 йодбензойной кислоты и соответствующего спирта. Аналогично примеру 5 были получены соединения 55-61 в следующей таблице из производных кислоты и производных пиперазина. Пример 2.1. Получение (2-гидрокси-5-нитрофенил)-[4-(4-трифторметилфенил)пиперазин-1-ил]метанона. Соединение 2.1 получали аналогично примеру 5 с помощью 2-гидрокси-5-нитробензойной кислотыMS (m/e): 394,0 (М-Н, 100%). Пример 2.2. Получение (2-гидрокси-5-метансульфонилфенил)-[4-(4-трифторметилфенил)пиперазин 1-ил]метанона. Соединение 2.2 получали аналогично примеру 5 с помощью 2-гидрокси-5-(метилсульфонил)бензойной кислоты [68029-77-6] и 1-(4-трифторметилфенил)пиперазина.- 20009986 Пример 66. Получение (2-бутокси-5-нитрофенил)-[4-(4-трифторметилфенил)пиперазин-1-ил]метанона. Раствор (2-гидрокси-5-нитрофенил)-[4-(4-трифторметилфенил)пиперазин-1-ил]метанона (50 мг),карбоната калия (87 мг) и 1-бромбутана (0,15 мл) в диметилацетамиде (0,3 мл) нагревали при 150 С в течение 15 мин в микроволновой печи. Реакционную смесь затем концентрировали и очищали колоночной хроматографией (SiO2) с получением указанного в заголовке соединения (55 мг). Аналогично примеру 66 были получены соединения 62-97 в следующей таблице из производных кислоты и производных пиперазина.(1 мл) перемешивали при 65 С в течение 16 ч. После этого реакционную смесь концентрировали в вакууме и очищали колоночной хроматографией (SiO2) с получением указанного в заголовке соединения (26 мг).MS (m/e): 446,0 (М+Н+, 100%). Пример 99. Получение 5-нитро-2-(2,2,3,3-тетрафторциклобутилметокси)фенил]-[4-(4-трифторметилфенил)пиперазин-1-ил]метанона. Пример 99 получали аналогично примеру 66 с помощью 1-(хлорметил)-2,2,3,3-тетрафторциклобутана [356-80-9].MS (m/e): 536,3 (М+Н+, 100%). Пример 100. Получение [5-нитро-2-(2,2,3,3,3-пентафторпропокси)фенил]-[4-(4-трифторметилфенил) пиперазин-1-ил]метанона. К перемешиваемому раствору 50 мг (2-гидрокси-5-нитрофенил)-[4-(4-трифторметилфенил)пиперазин-1 ил]метанона в ацетоне (2 мл), содержащему карбонат калия (35 мг), добавляли 2,2,3,3,3-пентафторпропилтрифторметансульфонат (54 мг) в течение 10 мин. Реакционную смесь кипятили с обратным холодилником в течение 20 ч перед концентрированием в вакууме и очищали колоночной хроматографией (SiO2, CH2Cl2/MeOH) с получением указанного в заголовке соединения в виде бесцветного твердого вещества (66 мг).(48 мг) кипятили с обратным холодильником в течение ночи, концентрировали в вакууме и очищали колоночной хроматографией (SiO2) с получением указанного в заголовке соединения в виде бесцветного твердого вещества (68 мг).MS (m/e): 474,1 (М+Н+, 100%). Аналогично примеру 48 были получены соединения 102-104 в следующей таблице из (2-йод-5-метансульфонилфенил)-[4-(4-трифторметилфенил)пиперазин-1-ил]метанона (соединение 1,9) и спирта.- 23009986 Пример 2.3. Получение (2-фтор-5-метансульфонилфенил)-[4-(5-трифторметилпиридин-2-ил)пиперазин-1-ил]метанона. Соединение 2.3 получали аналогично примеру 5 с помощью 2-фтор-5-(метилсульфонил)бензойной кислоты [247569-56-8] и 1-(5-трифторметил-2-пиридил)пиперазина [132834-58-3].(соединение 2.3, 20 мг), 2-трифторметил-2-пропанола (0,053 мл), карбоната калия или карбоната цезия (3 экв.) в диметилацетамиде нагревали при 150 С в течение 30 мин и затем при 180 С в течение 1 ч в микроволновой печи. После этого реакционную смесь концентрировали и очищали колоночной хроматографиейMS (m/e): 540,3 (М+Н+, 100%). Пример 2.4. Получение (2-изопропокси-5-метансульфонилфенил)пиперазин-1-ил-метанон трифторуксусной кислоты. Раствор 2-изопропокси-5-метансульфонилбензойной кислоты (соединение 1.2, 1,0 г), трет-бутил 1 пиперазинкарбоксилата (0,78 г), TBTU (1,4 г) и N-этилдиизопропиламина (4 мл) перемешивали при комнатной температуре в течение 2 ч. После этого реакционную смесь концентрировали в вакууме и очищали колоночной хроматографией (SiO2) с получением трет-бутилового эфира 4-(2-изопропокси-5-метансульфонилбензоил)пиперазин-1-карбоновой кислоты в виде бесцветной пены (1,6 г). Пену растворяли в дихлорметане (11 мл) и обрабатывали трифторуксусной кислотой (4,2 мл) в течение 30 мин. После этого реакционную смесь концентрировали в вакууме с получением указанного в заголовке соединения (1,6 г) в виде светло-желтого масла.MS (m/e): 327,1 (М+Н+, 100%). Пример 2.5. Получение 4-хлор-6-трифторметилпиримидина. 6-Трифторметилпиримидин-4-ол ([1546-78-7], 5 г) кипятили с обратным холодильником в оксихлориде фосфора (17 мл) в течение 2 ч. Реакционную смесь осторожно концентрировали в вакууме и остаток отгоняли (Кюгельрор) при пониженном давлении (tкип=30-55 С, 10 мбар) с получением указанного в заголовке соединения ([37552-81-1], 1,4 г).MS (EI): 182,0 (М). Пример 106. Получение (2-изопропокси-5-метансульфонилфенил)-[4-(5-нитропиридин-2-ил)пиперазин-1-ил]метанона. Раствор (2-изопропокси-5-метансульфонилфенил)пиперазин-1-ил-метанон трифторуксусной кислоты (соединение 2,4, 80 мг), 2-хлор-5-нитропиридина (29 мг), карбоната калия (50 мг) в 1-бутаноле (3 мл) перемешивали при 120 С в течение 20 ч. После этого раствор концентрировали в вакууме и очищали колоночной хроматографией (SiO2) с получением указанного в заголовке соединения в виде белой пеныMS (m/e): 449,1 (М+Н+, 100%). Пример 107. Получение (2-изопропокси-5-метансульфонилфенил)-[4-(6-трифторметилпиримидин 4-ил)пиперазин-1-ил]метанона. Соединение 107 получали аналогично примеру 106 с помощью 4-хлор-6-трифторметилпиримидинаMS (m/e): 473,1 (М+Н+, 100%). Пример 2.6. Получение 2-(4-фторфенокси)-5-нитробензойной кислоты. 2-(4-Фторфенокси)-5-нитробензойная кислота может быть получена аналогично способу, описанному в предшествующем уровне техники (например, WO9938845), реакцией этилового эфира 2-хлор-5 нитробензойной кислоты [16588-17-3] с 4-фторфенолом [371-35-7] c получением этилового эфира 2-(4 фторфенокси)-5-нитробензойной кислоты. Этиловый эфир 2-(4-фторфенокси)-5-нитробензойной кислоты затем может быть гидролизован, например, гидроксидом натрия с получением указанного в заголовке соединения.(а) трет-Бутиловый эфир 4-(4-циано-2,3-дифторфенил)пиперазин-1-карбоновой кислоты. К раствору N-Boc-пиперазина (0,65 г) в DMA (20 мл) медленно добавляли раствор 2,3,4-трифторбензонитрила (0,49 г) в DMA (10 мл). Реакционную смесь перемешивали в течение 2 ч при 80 С. После этого растворитель удаляли в вакууме и очищали колоночной хроматографией (SiO2) с получением указанного в заголовке соединения в виде белого твердого вещества (0,76 г).(0,72 г) в дихлорметане (5 мл) добавляли трифторуксусную кислоту и реакционную смесь перемешивали при комнатной температуре в течение 30 мин. После этого реакционную смесь концентрировали в вакууме с получением указанного в заголовке соединения (0,63 г).MS (m/e): 224,3 (М+Н+, 100%). Пример 2.8. Получение 2,5-дифтор-4-пиперазин-1-илбензонитрилтрифторуксусной кислоты. Пример 2.8 осуществляли аналогично примеру 2.7, используя 2,4,5-трифторбензонитрил.(а) 5-Хлорсульфонил-2-трифторметоксибензойная кислота. Раствор 2-трифторметоксибензойной кислоты [1979-29-9] (1,0 г) добавляли небольшими порциями к хлорсульфоновой кислоте (3,2 мл) при 0 С. После завершения добавления реакционную смесь перемешивали при 70 С в течение 4 ч, затем оставляли при комнатной температуре в течение ночи и нагревали при 75 С в течение 3 ч. После этого реакцию медленно выливали в лед и осадок затем отфильтровывали,промывали водой и высушивали с получением указанного в заголовке соединения в виде белого твердого вещества (1,2 г).(б) 5-Метилсульфамоил-2-трифторметоксибензойная кислота. К раствору 5-хлорсульфонил-2-трифторметоксибензойной кислоты (0,15 г) в дихлорметане (1,5 мл) добавляли раствор метиламина в метаноле (8 М, 0,31 мл) и реакционную смесь перемешивали в течение 2 мин после окончания осаждения. Реакционную смесь затем концентрировали в вакууме и остаток растворяли в 1N NaOH (2 мл) и экстрагировали диэтиловым эфиром. Водную фазу затем подкисляли с помощью 3N раствора хлороводородной кислоты (2 мл) и раствор экстрагировали дихлорметаном (210 мл). Объединенные органические фазы высушивали сульфатом натрия и концентрировали в вакууме с получением указанного в заголовке соединения в виде белого твердого вещества (0,12 г).(а) Метиловый эфир 5-метансульфонил-2-(3,3,3-трифторпропокси)бензойной кислоты. Раствор метил 5-(метансульфонил)салицилата [101371-44-2] (50 мг), трифенилфосфина (65 мг) 3,3,3-трифтор-1-пропанола и ди-трет-бутилазодикарбоксилата (55 мг) в ТГФ (3 мл) перемешивали при комнатной температуре в течение 1 ч. Реакционную смесь затем концентрировали в вакууме, очищали колоночной хроматографией (SiO2) с получением указанного в заголовке соединения в виде белого твердого вещества (65 мг).(б) 5-Метансульфонил-2-(3,3,3-трифторпропокси)бензойная кислота. К метиловому эфиру 5-метансульфонил-2-(3,3,3-трифторпропокси)бензойной кислоты (620 мг) в этаноле при 60 С добавляли 1N раствор NaOH (3,8 мл) и реакционную смесь перемешивали в течение 15 мин. После этого к реакционной смеси медленно добавляли 3,8 мл 1N HCl и этанол упаривали в вакууме. Осадок затем промывали водой несколько раз с получением указанного в заголовке соединения (497 мг).MS (m/e): 311,0 (М-Н+, 100%). Пример 2.11. Получение 5-метансульфонил-2-(тетрагидропиран-4-илокси)бензойной кислоты. Соединение 2.11 получали аналогично соединению 2.10, используя тетрагидро-2 Н-пиран-4-ол.MS (m/e): 299,4 (М-Н, 100%). Пример 2.12. Получение 2-циклобутилметокси-5-метансульфонилбензойной кислоты. Соединение 2.12 получали аналогично соединению 2.10, используя циклобутилметанол.MS (m/e): 299,4 (М-Н, 100%). Пример 2.13. Получение 3,5-дифтор-4-пиперазин-1-илбензонитрил трифторуксусной кислоты. Соединение 2.13 получали аналогично соединению 2.7, используя 3,4,5-трифторбензонитрил.MS (m/e): 224,1 (М+Н+, 100%). Пример 2.14. Получение 2,6-дифтор-4-пиперазин-1-илбензонитрил трифторуксусной кислоты. Соединение 2.14 получали аналогично соединению 2.7, используя 2,4,6-трифторбензонитрил.(а) 5-Сульфино-2-трифторметоксибензойная кислота. 5-Хлорсульфонил-2-трифторметоксибензойную кислоту (1,0 г, соединение 2.9 а) добавляли частями к раствору сульфита натрия (3,1 г) в 16 мл воды. Реакционную смесь подщелачивали добавлением соответствующего количества 20% NaOH и перемешивали при комнатной температуре в течение 45 мин. После этого реакционную смесь охлаждали в ледяной бане и затем подкисляли добавлением 20% раствора H2SO4 до значения рН 2. Раствор затем экстрагировали несколько раз диэтиловым эфиром и этилацетатом. Объединенные органические фазы высушивали (сульфат натрия) и концентрировали в вакууме с получением указанного в заголовке соединения в виде белого твердого вещества (0,88 г).(б) 5-Метансульфонил-2-трифторметоксибензойная кислота. К 5-сульфино-2-трифторметоксибензойной кислоте (0,82 г) в ДМФА (5 мл) добавляли 1,3 г карбоната калия и реакционную смесь перемешивали в течение 5 мин перед добавлением метилйодида (0,66 мл). Реакционную смесь затем перемешивали при комнатной температуре в течение 60 ч. После этого реакционную смесь концентрировали в вакууме и остаток обрабатывали 1N NaOH (10 мл) и ТГФ (4 мл). Ре- 25009986 акционную смесь перемешивали в течение 2 ч при комнатной температуре. После этого раствор подкисляли концентрированным раствором HCl. ТГФ затем удаляли в вакууме и осадок выделяли фильтрованием и промывали несколько раз водой с получением указанного в заголовке соединения.MS (m/e): 283,0 (М-Н, 100%). Пример 2.16. Получение 2,4-дифтор-6-пиперазин-1-илбензонитрил трифторуксусной кислоты. Соединение 2.16 получали аналогично соединению 2.7, используя 2,4,6-трифторбензонитрил.MS (m/e): 224,1 (М+Н+, 100%). Пример 2.17. Получение 2-(2-фтор-1-фторметилэтокси)-5-метансульфонилбензойной кислоты. Соединение 2.17 получали аналогично соединению 2.10, используя 1,3-дифтор-2-пропанол.(а) Метиловый эфир 5-метансульфонил-2-(2,2,3,3,3-пентафторпропокси)бензойной кислоты. Раствор метил 5-(метансульфонил)салицилата [101371-44-2] (0,50 г), 2,2,3,3,3-пентафторпропилового эфира трифторметансульфоновой кислоты (0,67 г) и карбоната калия (0,60 г) в ацетоне перемешивали при 60 С в течение 5 ч. Реакционную смесь затем концентрировали в вакууме и очищали колоночной хроматографией (SiO2) с получением указанного в заголовке соединения в виде белого твердого вещества (0,44 г).(б) 5-Метансульфонил-2-(2,2,3,3,3-пентафторпропокси)бензойная кислота. К метиловому эфиру 5-метансульфонил-2-(2,2,3,3,3-пентафторпропокси)бензойной кислоты (414 мг) в ТГФ (5 мл) добавляли раствор моногидрата гидроксида лития (72 мг) в воде (5 мл) и реакционную смесь перемешивали при комнатной температуре в течение 1 ч. После этого добавляли 1,72 мл 1N водного раствора хлороводородной кислоты. Реакционную смесь затем концентрировали в вакууме и полученный осадок затем промывали несколько раз водой с получением указанного в заголовке соединения в виде белого твердого вещества (367 мг).N,N-диметилформамид-ди-трет-бутилацеталя и реакционную смесь перемешивали при 80 С в течение 1 ч. После этого реакционную смесь концентрировали в вакууме и очищали колоночной хроматографией с получением указанного в заголовке соединения в виде бесцветного масла (258 мг).(б) 2-трет-Бутокси-5-метансульфонилбензойная кислота. К метиловому эфиру 2-трет-бутокси-5-метансульфонилбензойной кислоты (1,58 г) в ТГФ (25 мл) добавляли раствор моногидрата гидроксида лития (0,35 г) в воде (25 мл) и реакционную смесь перемешивали при комнатной температуре в течение 4 ч. После этого ТГФ удаляли в вакууме и к оставшемуся водному раствору добавляли 8 мл 1N раствора HCl, что приводило к осаждению соединения. Осадок отфильтровывали и промывали несколько раз водой с получением указанного в заголовке соединения (1,00 г) в виде белого твердого вещества.(а) 2,4,5-Трифторбензолсульфиновая кислота. 2,4,5-Трифторбензолсульфонилхлорид ([220227-21-4], 2,5 г) добавляли частями к раствору сульфита натрия (10,3 г) в 50 мл воды. Реакционную смесь подщелачивали добавлением соответствующего количества 20% NaOH и перемешивали при комнатной температуре в течение 1 ч. К реакционной смеси добавляли метанол и реакционную смесь перемешивали при комнатной температуре в течение часа. После этого реакционную смесь охлаждали в ледяной бане и затем подкисляли добавлением 20% раствораH2SO4 до значения рН 2. Водный раствор затем экстрагировали несколько раз диэтиловым эфиром и этилацетатом. Водный раствор затем экстрагировали этилацетатом с помощью аппарата Кучера-Штойделя (непрерывная экстракция). Объединенные органические фазы высушивали (сульфат натрия), затем концентрировали в вакууме с получением указанного в заголовке соединения в виде белого твердого вещества (2,1 г).(б) 1,2,4-Трифтор-5-метансульфонилбензол. К 2,4,5-трифторбензолсульфиновой кислоте (2,0 г) в ДМФА (17 мл) добавляли 4,3 г карбоната калия и реакционную смесь перемешивали в течение 5 мин перед добавлением метилйодида (2,2 мл). Реакционную смесь затем перемешивали при комнатной температуре в течение 60 ч. После этого в реакционную смесь выливали воду (30 мл) и реакционную смесь несколько раз экстрагировали диэтиловым эфиром. Объединенные органические фазы высушивали сульфатом натрия и оставшуюся смесь отгоняли с получением указанного в заголовке соединения в виде светло-желтого масла (2,1 г).(в) 1-(2,5-Дифтор-4-метансульфонилфенил)пиперазин трифторуксусная кислота. Указанное в заголовке соединение получали аналогично примеру 2.7, используя 1,2,4-трифтор-5 метансульфонилбензол.MS (m/e): 277,1 (М+Н+). Пример 2.21. Получение 1-(3,5-дифтор-4-метансульфонилфенил)пиперазин трифторуксусной кислоты. Соединение 2.21 получали аналогично соединению 2.20, используя 2,4,6-трифторбензолсульфонилхлорид [172326-59-9].MS (m/e): 277,1 (М+Н+). Пример 2.22. Получение 5-метансульфонил-2-(2,2,3,3-тетрафторпропокси)бензойной кислоты. Соединение 2.22 получали аналогично соединению 2.18, используя 2,2,3,3-тетрафтор-1-пропилтрифлат.MS (m/e): 329,1 (М-Н). Пример 2.23. Получение 1-(2,6-дифтор-4-метансульфонилфенил)пиперазин трифторуксусной кислоты. Соединение 2.23 получали аналогично соединению 2.20, используя 3,4,5-трифторбензолсульфонилхлорид [351003-43-5].MS (m/e): 277,1 (М+Н+). Пример 2.24. Получение 4-пиперазин-1-ил-6-трифторметилпиримидин трифторуксусной кислоты. Соединение 2.24 получали аналогично соединению 2.7, используя 4-хлор-6-трифторметилпиримидин [37552-81-1].(а) 2-(4-Бензилпиперазин-1-ил)-5-трифторметилпиримидин. К раствору хлорида (3-диметиламино-2-трифторметилаллилиден)диметиламмония ([176214-18-9],0,60 г) в ацетонитриле (10 мл) добавляли гидрохлорид 4-бензилпиперазин-1-карбоксамидина ([7773-69-5],0,66 г) и триэтиламин (0,87 мл) и реакционную смесь перемешивали в течение 3 ч при комнатной температуре. После этого реакционную смесь концентрировали в вакууме и очищали колоночной хроматографией с получением указанного в заголовке соединения в виде светло-желтого твердого вещества (0,79 г).(б) 2-Пиперазин-1-ил-5-трифторметилпиримидин. К раствору 2-(4-бензилпиперазин-1-ил)-5-трифторметилпиримидина (0,63 г) в метаноле добавляли палладий-С (Degussa E101N; 5%) и реакционную смесь нагревали при 60 С в атмосфере водорода. Реакционную смесь затем охлаждали до комнатной температуры, катализатор отфильтровывали и растворитель удаляли в вакууме с получением указанного в заголовке соединения в виде бесцветного твердого вещества (0,41 г).MS (m/e): 233,1 (М+Н+). Аналогично примеру 5 были получены соединения 108-280 в следующей таблице из производных кислоты и производных пиперазина.
МПК / Метки
МПК: A61K 31/497, C07D 295/192, A61P 25/28, C07D 213/74, A61K 31/495
Метки: glyt1, ингибиторов, группой, применение, фенильной, качестве, пиперазин, or-замещенной
Код ссылки
<a href="https://eas.patents.su/30-9986-piperazin-s-or-zameshhennojj-fenilnojj-gruppojj-i-ego-primenenie-v-kachestve-ingibitorov-glyt1.html" rel="bookmark" title="База патентов Евразийского Союза">Пиперазин с or-замещенной фенильной группой и его применение в качестве ингибиторов glyt1</a>
Предыдущий патент: Новый способ получения рофлумиласта
Следующий патент: Производные пробукола для лечения заболеваний, опосредованных vcam – 1
Случайный патент: Улучшение суспендирующих характеристик инвертных эмульсий