Производные циклопропила в качестве антагонистов рецептора nk3
Номер патента: 9477
Опубликовано: 28.02.2008
Авторы: Нергор Мортен Банг, Хансен Туре, Нильсен Серен Меллер, Келер Ян, Руланд Томас, Поульсен Андерс, Бьернхольм Берит
Формула / Реферат
1. Соединение формулы (I)
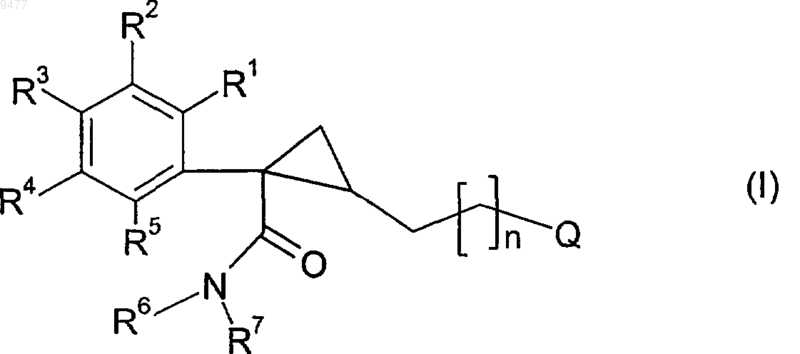
или его фармацевтически приемлемая соль;
где R1-R5 независимо выбирают из водорода и галогена;
R6 выбирают из водорода и C1-6алкила;
R7 является группой фенил-CR8R9-, R8 и R9 независимо выбирают из водорода и C1-6алкила;
n равно 0, 1 или 2;
Q выбирают из (ii), (iii), стрелки указывают на место присоединения:
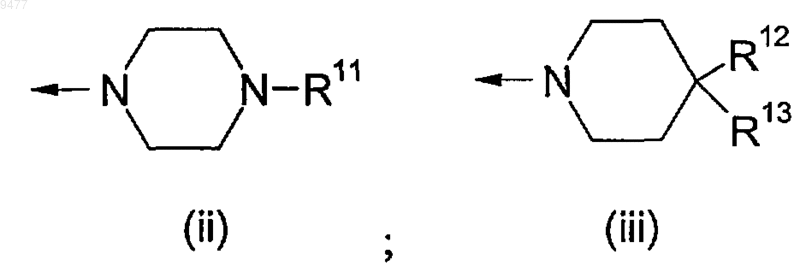
где R11 выбирают из фенила или бензила;
R12 является фенилом;
R13 является водородом, или гидрокси, или одной из следующих групп:
-NHC1-6алкил;
-N(C1-6алкил)2;
-NR14COR15, R14 является водородом или C1-6алкилом и R15 является C1-6алкилом;
-NR16COCONR17R18, R16 является водородом или C1-6алкилом и R17 и R18 независимо выбирают из водорода и С1-6алкила;
-NR19CONR20R21, R19 является водородом или С1-6алкилом и R20 и R21 независимо выбирают из водорода и C1-6алкила;
-NR22SO2R23, R22 является водородом или C1-6алкилом и R23 является амино или C1-6алкилом;
-COR24, R24 является C1-6алкилом;
-CONR25R26, R25 и R26 независимо выбирают из водорода, C1-6алкила или R25 и R26 вместе с атомом азота, к которому они присоединены, образуют пиперидинил, пиперазинил или морфолинил, где указанный пиперидинил, пиперазинил или морфолинил необязательно замещены C1-6алкилом;
-NHCOOR42, R42 является C1-6алкилом.
2. Соединение или соль по п.1, где R1-R5 являются водородом.
3. Соединение или соль по п.1, где R1-R5 независимо выбирают из водорода и хлора.
4. Соединение или соль по п.1, где R1-R5 независимо выбирают из водорода и фтора.
5. Соединение или соль по п.3, где R2 является хлором и R3 является водородом.
6. Соединение или соль по п.3, где R2 и R3 являются хлором.
7. Соединение или соль по п.4, где R2 является фтором и R3 является водородом.
8. Соединение или соль по п.4, где R2 и R3 являются фтором.
9. Соединение или соль по любому из пп.5-8, где R1, R4 и R5 являются водородом.
10. Соединение или соль по любому из пп.1-9, где R6 является водородом.
11. Соединение или соль по любому из пп.1-9, где R6 является C1-6алкилом.
12. Соединение или соль по п.11, где R6 является метилом.
13. Соединение или соль по п.1, где R8 и R9 независимо выбирают из водорода и метила.
14. Соединение или соль по п.1, где R8 и R9 являются водородом.
15. Соединение или соль по п.1, где R8 является водородом и R9 является метилом.
16. Соединение или соль по п.1, где указанный фенил в R7 не замещен.
17. Соединение или соль по п.1, где указанный фенил в R7 замещен одним или более заместителями.
18. Соединение или соль по п.17, где указанный фенил в R7 замещен одним или более заместителями, выбранными из галогена.
19. Соединение или соль по п.1, где R7 выбирают из бензила, 4-фторбензила или 2-хлорбензила.
20. Соединение или соль по любому из пп.1-19, где Q является (ii).
21. Соединение или соль по п.20, где R11 выбирают из необязательно замещенного фенила или необязательно замещенного бензила.
22. Соединение или соль по любому из пп.1-19, где Q является (iii).
23. Соединение или соль по п.22, где R12 является фенилом, замещенным одним или более заместителями.
24. Соединение или соль по п.23, где указанный фенил в R12 замещен одним или более заместителями, выбранными из галогена и трифторметила.
25. Соединение или соль по п.22, где R12 является 4-хлор-3-трифторметилфенилом.
26. Соединение или соль по любому из пп.22-25, где R13 является гидрокси.
27. Соединение или соль по п.26, где R12 такой, как определен в п.25.
28. Соединение или соль по любому из пп.22-25, где R13 является -NR14COR15.
29. Соединение или соль по п.28, где R14 является водородом или метилом.
30. Соединение или соль по любому из пп.28-29, где R15 является метилом.
31. Соединение или соль по п.30, где R14 является водородом и R15 является метилом или R14 и R15 являются метилом.
32. Соединение или соль по любому из пп.22-25, где R13 является -NR16COCONR17R18.
33. Соединение или соль по п.32, где
R16, R17 и R18 являются водородом;
R16 является C1-6алкилом и R17 и R18 являются водородом;
R16 и R17 являются водородом и R18 является C1-6алкилом;
R16 и R17 являются C1-6алкилом и R18 является водородом;
R16 является водородом и R17 и R18 являются C1-6алкилом или
R16, R17 и R18 являются C1-6алкилом.
34. Соединение или соль по любому из пп.22-25, где R13 является -NR19CONR20R21.
35. Соединение или соль по п.34, где
R19 является C1-6алкилом и R20 и R21 являются водородом;
R19 и R20 являются водородом и R21 является C1-6алкилом;
R19 и R20 независимо выбирают из C1-6алкила и R21 является H;
R19 является H и R20 и R21 независимо выбирают из C1-6алкила или
R19, R20 и R21 независимо выбирают из C1-6алкила.
36. Соединение или соль по п.34, где R19, R20 и R21 являются водородом.
37. Соединение или соль по любому из пп.34, 35, где R19 является H.
38. Соединение или соль по любому из пп.34, 35, где R20 и R21 независимо выбирают из группы, включающей водород, Me, Et, Bu и i-Pr.
39. Соединение или соль по п.38, где R19 является H.
40. Соединение или соль по любому из пп.22-25, где R13 является -NR22SO2R23.
41. Соединение или соль по п.40, где R22 является водородом и R23 является C1-6алкилом или R22 и R23 независимо выбирают из C1-6алкила.
42. Соединение или соль по п.40, где R22 является водородом.
43. Соединение или соль по любому из пп.40-42, где R23 является метилом.
44. Соединение или соль по любому из пп.40, 41, где R22 и R23 являются метилом.
45. Соединение или соль по любому из пп.40, 41, где R22 является водородом и R23 является метилом.
46. Соединение или соль по любому из пп.22-25, где R13 является -COR24.
47. Соединение или соль по п.46, где R24 является метилом.
48. Соединение или соль по любому из пп.22-25, где R13 является -CONR25R26.
49. Соединение или соль по п.48, где R25 и R26 независимо выбирают из водорода и метила.
50. Соединение или соль по п.48, где R25 и R26 вместе с атомом азота, к которому они присоединены, образуют пиперидинил, пиперазинил или морфолинил, где указанные пиперидинил, пиперазинил и морфолинил необязательно замещены C1-6алкилом.
51. Соединение или соль по п.48, где R25 и R26 вместе с атомом азота, к которому они присоединены, образуют пиперидинил, где указанный пиперидинил необязательно замещен C1-6алкилом.
52. Соединение или соль по п.1, где R1-5 такие, как определены в любом из пп.2-9, и R6 является метилом.
53. Соединение или соль по п.1, где R6 является метилом и R7 такой, как определен в п.19.
54. Соединение по любому из пп.1-53, где n=0.
55. Соединение или соль по любому из представленных выше пунктов, где соединение формулы (I) является (1S,2R)-изомером, т.е. указанное соединение имеет абсолютную конфигурацию, как показано в формуле IA
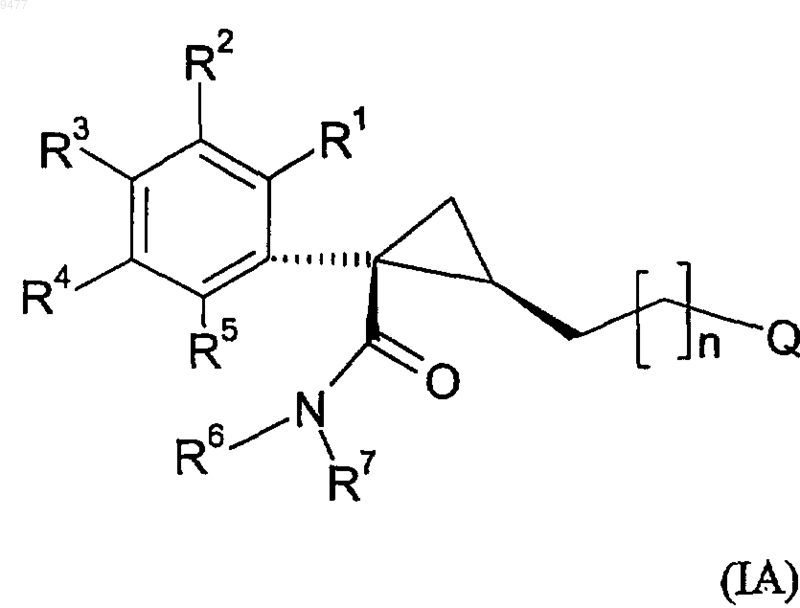
56. Соединение или соль по любому из пп.1-54, где указанное соединение формулы (I) является рацемической смесью, содержащей (1S,2R)-изомер по п.55.
57. Соединение или соль по любому из пп.1-54, где указанное соединение формулы (I) является смесью стереоизомеров указанного соединения, где смесь содержит (1S,2R)-изомер по п.55.
58. Соединение или соль по п.1, выбранное из группы, включающей:
(1a) (1S,2R)-2-(4-ацетиламино-4-фенилпиперидин-1-илметил)-1-(3,4-дихлорфенил)циклопропанкарбоновой кислоты бензилметиламид;
(2а) (1S,2R)-2-[4-(ацетилметиламино)-4-фенилпиперидин-1-илметил]-1-(3,4-дихлорфенил)циклопропанкарбоновой кислоты бензилметиламид;
(7а) (1S,2R)-1-фенил-2-[4-фенил-4-(пиперидин-1-карбонил)пиперидин-1-илметил]циклопропанкарбоновой кислоты бензилметиламид;
(9а) (1S,2R)-2-(4-ацетил-4-фенилпиперидин-1-илметил)-1-фенилциклопропанкарбоновой кислоты бензилметиламид;
(10а) (1S,2R)-2-[4-(4-хлор-3-трифторметилфенил)-4-гидроксипиперидин-1-илметил]-1-фенилциклопропанкарбоновой кислоты бензилметиламид;
(12а) (1S,2R)-2-(4-ацетиламино-4-фенилпиперидин-1-илметил)-1-(4-хлорфенил)циклопропанкарбоновой кислоты бензилметиламид;
(13а) (1S,2R)-1-(4-хлорфенил)-2-[4-фенил-4-(пиперидин-1-карбонил)пиперидин-1-илметил]циклопропанкарбоновой кислоты бензилметиламид;
(14а) (1S,2R)-2-[4-(ацетилметиламино)-4-фенилпиперидин-1-илметил]-1-(4-хлорфенил)циклопропанкарбоновой кислоты бензилметиламид;
(15а) (1S,2R)-2-(4-ацетил-4-фенилпиперидин-1-илметил)-1-(4-хлорфенил)циклопропанкарбоновой кислоты бензилметиламид;
(18а) (1S,2R)-2-(4-ацетиламино-4-фенилпиперидин-1-илметил)-1-(3,4-дифторфенил)циклопропанкарбоновой кислоты метил-(1-фенилэтил)амид;
(19а) (1S,2R)-2-[4-(ацетилметиламино)-4-фенилпиперидин-1-илметил]-1-(3,4-дифторфенил)циклопропанкарбоновой кислоты метил-([S]-1-фенилэтил)амид;
(21а) (1S,2R)-2-(4-ацетиламино-4-фенилпиперидин-1-илметил)-1-фенилциклопропанкарбоновой кислоты (4-фторбензил)метиламид;
(22a) (1S,2R)-2-[4-(ацетилметиламино)-4-фенилпиперидин-1-илметил]-1-фенилциклопропанкарбоновой кислоты (4-фторбензил)метиламид;
(24а) (1S,2R)-2-[4-(4-хлор-3-трифторметилфенил)-4-гидроксипиперидин-1-илметил]-1-фенилциклопропанкарбоновой кислоты (4-фторбензил)метиламид;
(26а) (1S,2R)-2-[4-(ацетилметиламино)-4-фенилпиперидин-1-илметил]-1-(4-хлорфенил)циклопропанкарбоновой кислоты (4-фторбензил)метиламид;
(28а) (1S,2R)-2-(4-ацетил-4-фенилпиперидин-1-илметил)-1-(4-хлорфенил)циклопропанкарбоновой кислоты (4-фторбензил)метиламид;
(31а) (1S,2R)-1-(4-фторфенил)-2-[4-фенил-4-(пиперидин-1-карбонил)пиперидин-1-илметил]циклопропанкарбоновой кислоты (4-фторбензил)метиламид;
(33а) (1S,2R)-1-(3,4-дифторфенил)-2-[4-фенил-4-(пиперидин-1-карбонил)пиперидин-1-илметил]циклопропанкарбоновой кислоты метиламид;
(36а) (1S,2R)-1-(3,4-дихлорфенил)-2-[4-фенил-4-(пиперидин-1-карбонил)пиперидин-1-илметил]циклопропанкарбоновой кислоты бензилметиламид;
(37а) (1S,2R)-2-(4-ацетил-4-фенилпиперидин-1-илметил)-1-(3,4-дихлорфенил)циклопропанкарбоновой кислоты бензилметиламид;
(39а) (1S,2R)-2-(4-ацетиламино-4-фенилпиперидин-1-илметил)-1-(3,4-дихлорфенил)циклопропанкарбоновой кислоты метил-(1-фенилэтил)амид;
(40а) (1S,2R)-1-(3,4-дихлорфенил)-2-[4-фенил-4-(пиперидин-1-карбонил)пиперидин-1-илметил]циклопропанкарбоновой кислоты метил-([S]-1-фенилэтил)амид;
(41а) (1S,2R)-2-[4-(ацетилметиламино)-4-фенилпиперидин-1-илметил]-1-(3,4-дихлорфенил)циклопропанкарбоновой кислоты метил-([S]-1-фенилэтил)амид;
(42а) (1S,2R)-1-фенил-2-[4-фенил-4-(пиперидин-1-карбонил)пиперидин-1-илметил]циклопропанкарбоновой кислоты (4-фторбензил)метиламид;
(43a) (1S,2R)-1-(4-хлорфенил)-2-[4-фенил-4-(пиперидин-1-карбонил)пиперидин-1-илметил]циклопропанкарбоновой кислоты (4-фторбензил)метиламид;
(44а) (1S,2R)-2-(4-ацетиламино-4-фенилпиперидин-1-илметил)-1-(4-хлорфенил)циклопропанкарбоновой кислоты (4-фторбензил)метиламид;
(45а) (1S,2R)-2-(4-ацетиламино-4-фенилпиперидин-1-илметил)-1-(4-хлорфенил)циклопропанкарбоновой кислоты (2-хлорбензил)метиламид;
(46а) (1S,2R)-1-(4-хлорфенил)-2-[4-фенил-4-(пиперидин-1-карбонил)пиперидин-1-илметил]циклопропанкарбоновой кислоты (2-хлорбензил)метиламид;
(47а) (1S,2R)-2-[4-(ацетилметиламино)-4-фенилпиперидин-1-илметил]-1-(4-хлорфенил)циклопропанкарбоновой кислоты (2-хлорбензил)метиламид;
(49а) (1S,2R)-2-[4-(ацетилметиламино)-4-фенилпиперидин-1-илметил]-1-(4-фторфенил)циклопропанкарбоновой кислоты (2-хлорбензил)метиламид;
(50а) (1S,2R)-2-[4-(ацетилметиламино)-4-фенилпиперидин-1-илметил]-1-(3,4-дифторфенил)циклопропанкарбоновой кислоты (2-хлорбензил)метиламид;
(51а) (1S,2R)-2-(4-ацетиламино-4-фенилпиперидин-1-илметил)-1-(3,4-дихлорфенил)циклопропанкарбоновой кислоты (2-хлорбензил)метиламид;
(52а) (1S,2R)-1-(3,4-дихлорфенил)-2-[4-фенил-4-(пиперидин-1-карбонил)пиперидин-1-илметил]циклопропанкарбоновой кислоты (2-хлорбензил)метиламид;
(53а) (1S,2R)-2-[4-(ацетилметиламино)-4-фенилпиперидин-1-илметил]-1-(3,4-дихлорфенил)циклопропанкарбоновой кислоты (2-хлорбензил)метиламид;
(55а) (1S,2R)-1-(3,4-дихлорфенил)-2-[4-фенилпиперидин-1-илметил]циклопропанкарбоновой кислоты бензилметиламид;
(56а) (1S,2R)-2-(4-ацетиламино-4-фенилпиперидин-1-илметил)-1-(3,4-дихлорфенил)циклопропанкарбоновой кислоты (1-метил-1-фенилэтил)амид;
(57а) (1S,2R)-2-(4-фенилпиперидин-1-илметил)-1-(3,4-дихлорфенил)циклопропанкарбоновой кислоты бензилэтиламид;
(58а) (1S,2R)-2-(4-ацетиламино-4-фенилпиперидин-1-илметил)-1-(3,4-дихлорфенил)циклопропанкарбоновой кислоты бензилметиламид-([R]-1-фенилэтил)амид;
(59а) (1R,2S)-2-(4-ацетиламино-4-фенилпиперидин-1-илметил)-1-(3,4-дихлорфенил)циклопропанкарбоновой кислоты бензилметиламид;
(60а) (1R,2R)-2-(4-ацетиламино-4-фенилпиперидин-1-илметил)-1-(3,4-дихлорфенил)циклопропанкарбоновой кислоты бензилметиламид;
(61а) (1S,2S)-2-(4-ацетиламино-4-фенилпиперидин-1-илметил)-1-(3,4-дихлорфенил)циклопропанкарбоновой кислоты бензилметиламид;
(62а) (1S,2R)-2-(4-ацетиламино-4-фенилпиперидин-1-илметил)-1-(3,4-дихлорфенил)циклопропанкарбоновой кислоты метил-([R]-1-фенилэтил)амид;
(63а) (1S,2R)-2-[4-(ацетилметиламино)-4-фенилпиперидин-1-илметил]-1-(3,4-дихлорфенил)циклопропанкарбоновой кислоты метил-([R]-1-фенилэтил)амид;
(66а) (1S,2R)-2-(4-ацетиламино-4-фенилпиперидин-1-илметил)-1-фенилциклопропанкарбоновой кислоты бензилметиламид;
(67а) (1S,2R)-1-(3,4-дихлорфенил)-2-[4-фенил-4-(пиперидин-1-карбонил)пиперидин-1-илметил]циклопропанкарбоновой кислоты метил-([S]-1-фенилэтил)амид;
(69а) (1S,2R)-1-фенил-2-[4-фенил-4-(пиперидин-1-карбонил)пиперидин-1-илметил]циклопропанкарбоновой кислоты (4-фторбензил)метиламид;
(70а) (1S,2R)-2-(4-ацетил-4-фенилпиперидин-1-илметил)-1-фенилциклопропанкарбонотющ кислоты (4-фторбензил)метиламид;
(71а) (1S,2R)-2-[1-метансульфонилспиро-2,3-дигидро-1Н-индол-3-ил-3,4'-пиперидин-1'-илметил]-1-(4-фторфенил)циклопропанкарбоновой кислоты (4-фторбензил)метиламид;
(72а) (1S,2R)-2-[4-(ацетилметиламино)-4-фенилпиперидин-1-илметил]-1-(4-фторфенил)циклопропанкарбоновой кислоты (4-фторбензил)метиламид;
(73а) (1S,2R)-2-(4-ацетил-4-фенилпиперидин-1-илметил)-1-(4-фторфенил)циклопропанкарбоновой кислоты (4-фторбензил)метиламид;
(75а) (1S,2R)-2-(4-ацетил-4-фенилпиперидин-1-илметил)-1-(3,4-дифторфенил)циклопропанкарбоновой кислоты (4-фторбензил)метиламид;
(77а) (1S,2R)-1-(4-фторфенил)-2-[4-фенил-4-(пиперидин-1-карбонил)пиперидин-1-илметил]циклопропанкарбоновой кислоты метил-([S]-1-фенилэтил)амид;
(78а) (1S,2R)-2-(4-ацетил-4-фенилпиперидин-1-илметил)-1-(4-хлорфенил)циклопропанкарбоновой кислоты (2-хлорбензил)метиламид;
(80а) (1S,2R)-2-(4-ацетиламино-4-фенилпиперидин-1-илметил)-1-(4-фторфенил)циклопропанкарбоновой кислоты (2-хлорбензил)метиламид;
(81а) (1S,2R)-1-(4-фторфенил)-2-[4-фенил-4-(пиперидин-1-карбонил)пиперидин-1-илметил]циклопропанкарбоновой кислоты (2-хлорбензил)метиламид;
(82а) (1S,2R)-2-(4-ацетиламино-4-фенилпиперидин-1-илметил)-1-(3,4-дифторфенил)циклопропанкарбоновой кислоты (2-хлорбензил)метиламид;
(83а) (1S,2R)-1-(3,4-дифторфенил)-2-[4-фенил-4-(пиперидин-1-карбонил)пиперидин-1-илметил]циклопропанкарбоновой кислоты (2-хлорбензил)метиламид;
(86а) (1S,2R)-1-(3,4-дихлорфенил)-2-(4-фенилпиперидин-1-илметил)циклопропанкарбоновой кислоты 3,4-дихлорбензиламид;
(87а) (1S,2R)-1-(3,4-дихлорфенил)-2-(4-фенилпиперидин-1-илметил)циклопропанкарбоновой кислоты 3,4-диметоксибензиламид;
(88а) (1S,2R)-2-(4-ацетиламино-4-фенилпиперидин-1-илметил)-1-(3,4-дихлорфенил)циклопропанкарбоновой кислоты фениламид;
(89а) (1S,2R)-2-(4-ацетиламино-4-фенилпиперидин-1-илметил)-1-(3,4-дихлорфенил)циклопропанкарбоновой кислоты (1-метил-1-фенилэтил)амид;
(90а) (1S,2R)-1-фенил-2-[4-(3-трифторметилфенил)пиперазин-1-илметил]циклопропанкарбоновой кислоты бензилметиламид;
(91а) (1S,2R)-2-(4-бензилпиперазин-1-илметил)-1-(4-хлорфенил)циклопропанкарбоновой кислоты (4-фторбензил)метиламид;
(92а) (1S,2R)-1-(4-хлорфенил)-2-[4-(3-трифторметилфенил)пиперазин-1-илметил]циклопропанкарбоновой кислоты N-фторбензилметиламид;
(93а) (1S,2R)-2-(4-бензилпиперазин-1-илметил)-1-(4-хлорфенил)циклопропанкарбоновой кислоты бензилметиламид;
(94а) (1S,2R)-2-(4-бензилпиперазин-1-илметил)-1-фенилциклопропанкарбоновой кислоты бензилметиламид;
(95а) (1S,2R)-1-(4-хлорфенил)-2-[4-(3-трифторметилфенил)пиперазин-1-илметил]циклопропанкарбоновой кислоты бензилметиламид;
(96а) (1S,2R)-1-фенил-2-[4-(3-трифторметилфенил)пиперазин-1-илметил]циклопропанкарбоновой кислоты 4-фторбензилметиламид;
(97а) (1S,2R)-2-(4-ацетиламино-4-фенилпиперидин-1-илметил)-1-(3,4-дихлорфенил)циклопропанкарбоновой кислоты бензиламид;
(99а) (1S,2R)-2-(4-ацетиламино-4-фенилпиперидин-1-илметил)-1-(3,4-дихлорфенил)циклопропанкарбоновой кислоты метил-[1-(4-метоксифенил)этил]амид;
(100а) (1S,2R)-2-(4-ацетиламино-4-фенилпиперидин-1-илметил)-1-(3,4-дихлорфенил)циклопропанкарбоновой кислоты (2-хлорбензил)амид;
(101а) (1S,2R)-2-(4-ацетиламино-4-фенилпиперидин-1-илметил)-1-(3,4-дихлорфенил)циклопропанкарбоновой кислоты (3,4-дихлорбензил)амид;
(102а) (1S,2R)-2-(4-ацетиламино-4-фенилпиперидин-1-илметил)-1-(3,4-дихлорфенил)циклопропанкарбоновой кислоты метилфениламид;
(103а) (1S,2R)-2-(4-ацетиламино-4-фенилпиперидин-1-илметил)-1-(4-метоксифенил)циклопропанкарбоновой кислоты (4-фторбензил)метиламид;
(104а) (1S,2R)-2-(4-ацетиламино-4-фенилпиперидин-1-илметил)-1-п-толилциклопропанкарбоновой кислоты (4-фторбензил)метиламид;
(105а) (1S,2R)-2-(4-ацетиламино-4-фенилпиперидин-1-илметил)-1-м-толилциклопропанкарбоновой кислоты бензилметиламид;
(106а) (1S,2R)-2-(4-ацетиламино-4-фенилпиперидин-1-илметил)-1-м-толилциклопропанкарбоновой кислоты (4-фторбензил)метиламид;
(107а) (1S,2R)-2-(4-ацетиламино-4-фенилпиперидин-1-илметил)-1-(3-метоксифенил)циклопропанкарбоновой кислоты (4-фторбензил)метиламид;
(108а) (1S,2R)-2-(4-ацетиламино-4-фенилпиперидин-1-илметил)-1-(4-метоксифенил)циклопропанкарбоновой кислоты бензилметиламид;
109а) (1S,2R)-2-(4-ацетиламино-4-фенилпиперидин-1-илметил)-1-п-толилциклопропанкарбоновой кислоты бензилметиламид;
(110а) (1S,2R)-2-(4-ацетиламино-4-фенилпиперидин-1-илметил)-1-(3-метоксифенил)циклопропанкарбоновой кислоты бензилметиламид;
(111a) (1S,2R)-1-фенил-2-(4-фенил-4-уреидопиперидин-1-илметил)циклопропанкарбоновой кислоты (4-фторбензил)метиламид;
(112а) (1S,2R)-1-(3,4-дихлорфенил)-2-(4-фенил-4-уреидопиперидин-1-илметил)циклопропанкарбоновой кислоты бензилметиламид;
(113а) (1S,2R)-1-фенил-2-[4-(3-метилуреидо)-4-фенилпиперидин-1-илметил]циклопропанкарбоновой кислоты (4-фторбензил)метиламид;
(114а) (1S,2R)-2-[4-(3-метилуреидо)-4-фенилпиперидин-1-илметил]-1-(3,4-дихлорфенил)циклопропанкарбоновой кислоты бензилметиламид;
(115а) (1S,2R)-N-(1-{2-[(4-фторбензил)метилкарбамоил]-2-фенилциклопропилметил}-4-фенилпиперидин-4-ил)оксаламид;
(116а) (1S,2R)-N-(1-{2-[бензилметилкарбамоил]-2-(3,4-дихлорфенил)циклопропилметил}-4-фенилпиперидин-4-ил)оксаламид;
(117а) (1S,2R)-1-фенил-2-(4-метансульфониламино-4-фенилпиперидин-1-илметил)циклопропанкарбоновой кислоты (4-фторбензил)метиламид;
(118а) (1S,2R)-2-(4-метансульфониламино-4-фенилпиперидин-1-илметил)-1-(3,4-дихлорфенил)циклопропанкарбоновой кислоты бензилметиламид;
(119а) (1S,2R)-{l-[2-((4-фторбензил)метилкарбамоил)-2-фенилциклопропилметил]-4-фенилпиперидин-4-ил}карбаминовой кислоты метиловый эфир;
(120а) (1S,2R)-(1-{2-[бензилметилкарбамоил]-2-(3,4-дихлорфенил)циклопропилметил}-4-фенилпиперидин-4-ил)карбаминовой кислоты метиловый эфир;
(121а) (1S,2R)-1-(3,4-дихлорфенил)-2-[4-(3,3-диметилуреидо)-4-фенилпиперидин-1-илметил]циклопропанкарбоновой кислоты бензилметиламид;
(122а) (1S,2R)-1-фенил-2-[4-(3,3-диметилуреидо)-4-фенилпиперидин-1-илметил]-циклопропанкарбоновой кислоты (4-фторбензил)метиламид;
(123а) (1S,2R)-2-[2-(4-ацетиламино-4-фенилпиперидин-1-ил)этил]-1-(3,4-дихлорфенил)циклопропанкарбоновой кислоты (4-фторбензил)метиламид;
(124а) (1S,2R)-2-[3-(4-ацетиламино-4-фенилпиперидин-1-ил)пропил]-1-(3,4-дихлорфенил)циклопропанкарбоновой кислоты (4-фторбензил)метиламид;
(125а) (1S,2R)-2-[4-(2-ацетиламино-5-фторфенил)пиперидин-1-илметил]-1-(3,4-дихлорфенил)циклопропанкарбоновой кислоты (4-фторбензил)метиламид;
(126а) (1S,2R)-2-(4-ацетиламино-4-фенилпиперидин-1-илметил)-1-(3,4-диметилфенил)циклопропанкарбоновой кислоты (4-фторбензил)метиламид;
(127а) (1S,2R)-2-(4-ацетиламино-4-фенилпиперидин-1-илметил)-1-(3,4-дихлорфенил)циклопропанкарбоновой кислоты (4-фторбензил)метиламид;
(128а) (1S,2R)-2-(4-ацетиламино-4-фенилпиперидин-1-илметил)-1-(3-хлорфенил)циклопропанкарбоновой кислоты (4-фторбензил)метиламид;
(129а) (1S,2R)-2-(4-ацетиламино-4-фенилпиперидин-1-илметил)-1-(3-фторфенил)циклопропанкарбоновой кислоты (4-фторбензил)метиламид;
(130а) (1S,2R)-1-(3,4-дихлорфенил)-2-(4-фенилпиперидин-1-илметил)циклопропанкарбоновой кислоты метилнафталин-1-илметиламид;
(131а) (1S,2R)-1-(3,4-дихлорфенил)-2-[1-ацетил-5-фторспиро-2,3-дигидро-1Н-индол-3-ил-3,4'-пиперидин-1'-илметил]циклопропанкарбоновой кислоты метилнафталин-1-илметиламид;
(132а) (1S,2R)-1-(3,4-дихлорфенил)-2-(4-ацетиламино-4-фенилпиперидин-1-илметил)циклопропанкарбоновой кислоты метилнафталин-1-илметиламид
или его соль.
59. Фармацевтическая композиция, содержащая соединение по любому из пп.1-58.
60. Применение соединения по любому из пп.1-58 или его фармацевтически приемлемой соли для получения лекарственного средства для лечения заболеваний, выбранных из группы, включающей психотические расстройства, шизофрению, депрессию, тревогу, болезнь Паркинсона, боль, судороги, кашель, астму, гиперчувствительность дыхательных путей, капиллярную гиперчувствительность, бронхостеноз, воспаление кишечника, воспалительное заболеваэшх пищеварительного тракта, гипертензию, дисбаланс гомеостаза воды и электролитов, ишемию, отек, экстравазацию плазмы и ожирение.
61. Применение соединения по любому из пп.1-58 или его соли для получения лекарственного средства для лечения шизофрении.
62. Применение по п.61 для лечения положительных симптомов шизофрении.
63. Применение соединения по любому из пп.1-58 или его соли для получения фармацевтического препарата для лечения расстройств центральной нервной системы.
64. Способ лечения заболеваний, выбранных из группы, включающей: шизофрению, психотические расстройства, депрессию, тревогу, болезнь Паркинсона, боль, судороги, кашель, астму, гиперчувствительность дыхательных путей, капиллярную гиперчувствительность, бронхостеноз, воспаление кишечника, воспалительное заболевание пищеварительного тракта, гипертензию, дисбаланс гомеостаза воды и электролитов, ишемию, отек, экстравазацию плазмы и ожирение, включающий введение терапевтически эффективного количества соединения по любому из пп.1-58 или его фармацевтически приемлемой соли.
65. Способ по предшествующему пункту, где заболеванием является шизофрения.
66. Способ лечения расстройства центральной нервной системы, включающий введение терапевтически эффективного количества соединения по любому из пп.1-58 или его соли.
Текст
009477 Область техники Данное изобретение относится к новым соединениям, которые являются антагонистами рецептораNK3 и, как таковые, применяются для лечения заболеваний, в которые вовлечен рецептор NK3. Уровень техники Три тахикинина, вещество P (SP), нейрокинин A (NKA) и нейрокинин В (NKB) широко распространены в центральной и периферийной нервной системе. Биологическое действие этих нейропептидов в первую очередь опосредовано связыванием и последующей активацией трех рецепторов нейрокинина,NK1, NK2 и NK3. Вещество P считается эндогенным лигандом для рецептора NK1, a NKA и NKB - для рецепторов NK2 и NK3 соответственно. Однако недавно полученные данные показали, что в системе тахикининов существует перекрестная реакционноспособность, которая может оказывать физиологическое воздействие, так как и NKA, и NKB потенциально способны связывать и активировать рецепторNK1 (см. Maggi, C.A. et al.: Trends Pharmacol. Sci. 1997, 18, p. 351-5). Три подтипа рецептора принадлежат к надсемейству сопряженных с G-белком рецепторов и были клонированы в разных видах, включая мышей, крыс и человека (Nakanishi S.: Annu Rev. Neurosci. 1991, 14, p. 123-36). Три рецептора тахикинина экспрессируются как в центральной, так и в периферийной нервной системе. Рецептор NK3 в основном экспрессируется в центральной нервной системе в областях,включающих кору головного мозга, стриатум, компактную черную субстанцию, брюшную тегментальную область, гипоталамус, миндалины и гиппокамп (Stroessl A.J. et al.: Brain. Res. 1990, 534, p. 1-7,Koutcherov Y. et al.: Neuroreport. 2000, 11, p. 3127-31). На периферии рецептор NK3 экспрессируется в областях, включающих толстую кишку, почки, легкие и мочевой пузырь (Regoli D. et al.: Trends Pharmacol. Sci. 1988 Aug.; 9(8): 290-5, Kamali F.: Curr. Opin. Investig. Drugs. 2001 July; 2(7): 950-6). B центральной нервной системе рецептор NK3 экспрессируется на холинергических (Chen L.W. et al.: Neuroscience. 2001; 103(2): 413-22), норадренергических (ссылки в Oury-Donat F. et al.: J. Pharmacol. Exp. Ther. 1995,274, p. 148-54) и допаминергических нейронах (Keegan K.D. et al.: Br. J. Pharmacol. 1992, 105, p. 3-5). Согласно полученным результатам активация рецептора NK3 вовлечена в регулирование различных моноаминовых трансмиттеров, например допамина и ацетилхолина (Marco N. et al.: Neuropeptides. 1998, 32,p. 481-8, Stoessl A.J. et al.: Brain Res. 1990, 517, p. 111-6), норадреналина (Jung M. et al.: Neuroscience,1996, 74, p. 403-14) и серотонина (Stoessl A.J. et al.: Brain Res. 1990, 517, p. 111-6). Опосредованное рецептором NK3 регулирование моноаминовых систем подтверждает, что рецептор NK3 вовлечен в различные функции, включая память, изучение, корковую обработку и контроль поведения (Yip J. et al.: Br. J. Pharmacol. 1997, 122, p. 715-25, Ding Y.Q. et al.: J. Comp. Neurol. 1996, 364,p. 290-310, Mileusnic D. et al.: Neurobiol Aging. 1999, 20, p. 19-35), и что он является мишенью для различных физиологических и неврологических расстройств (Emonds-Alt X. et al.: Can J. Physiol. Pharmacol. 2002, 80, p. 482-8, Kamali F., Curr. Opin. Investig. Drugs. 2001, 2, p. 950-6, Langlois X. et al.: J. Pharmacol.Exp. Ther. 2001, 299, p. 712-7). Действительно, было описано, что рецептор NK3 вовлечен в модулирование тревоги (Ribeiro S.J. et al.: Neuropeptides. 1999, 33, p. 181-8). Далее было описано, что антагонист рецептора NK3 SR142801 действует против шизофрении, в частности положительных симптомов. SR142801 описан, например, в EP 673928. Структура SR142801 представлена ниже (Kamali F.: Curr. Opin. Investig. Drugs. 2001 July; 2(7):950-6) Было описано, что in vivo центральная активация рецептора NK3 опосредует гипертензию и тахикардию (Nagashima A. et al.: Brain Res. 487, 1989, p. 392-396, Takano Y. et al.: Brain Res. 1990, 528, p. 2317, Picard P. et al.: Br. J. Pharmacol. 1994, 112, p. 240-9), в то время как периферийная активация рецептораNK3 опосредует пониженное кровяное давление и брадикардию (Couture R. et al.: Naunyn SchmiedebergsArch. Pharmacol. 1989, 340, p. 547-57). Дополнительные исследования in vivo показали, что активация рецептора NK3 снижает всасывание воды, соли и алкоголя (Massi M. et al.: Brain. Res. Bull. 1991, 26,p. 155-60, Massi M. et al.: Neurosci Lett. 1988, 92, p. 341-6 и Ciccocioppo R. et al.: Brain. Res. Bull. 1994, 33,p. 71-7), что вместе с локализацией рецептора NK3 в MCH нейронах подтверждает роль рецептора NK3 в регулировании потребления пищи (Griffond В. et al.: J. Chem. Neuroanat. 1997, 12, p. 183-9). Далее исследования in vivo показали, что рецептор NK3 вовлечен в почечный контроль гомеостаза воды и электролитов (Yuan Y.D.: Brit. J. Pharmacol. 1997, 120, p. 785-96). Было описано, что активация рецептора NK3 ингибирует выделение желудочной кислоты (Improta G. et al.: Peptides. 1991, 12, p. 1433-4), вызывает дискинезию рта (Liminga U. et al.: Pharmacol. Biochem. Behav. 1991, 38, p. 617-20) и отек (Inoue H. et al.:Inflamm. Res. 1996, 45, p. 316-23). Было описано, что активация NK3 in vitro способствует возникновению судорог (Maubach K.A. etal.: Neuroscience. 1998, 83, p. 1047-62) и гипервозбудимости при ишемическом повреждении (Stumm R. etal.: J. Neurosci. 2001, 21, p. 798-811). Было описано, что селективные непептидные антагонисты рецептора NK3 с высоким сродством являются антиноцицептиками (Fioramonti J. et al.: Neurogastroenterol. Motil. 2003, 15, p. 363-9, Couture R. etEuropean Journal of Pharmacology. 1998, 361, p. 175-184) и анальгетиками (Houghton A.K. et al.: Neuropharmacology. 2000, 39, p. 133-40). Кроме того, исследования продемонстрировали стойкое воздействие антагониста рецептора NK3 на внутреннюю боль, часто возникающую при запоре (Mayer E.A. et al.: Gastroenterology. 1999, 116, p. 1250-2, Julia V. et al.: Gastroenterology. 1999, 116, p. 1124-31). Установлено, что подобное ингибирование рецептора NK3 предотвращает воспаление кишечника, что еще раз подчеркивает действие против воспаления пищеварительного тракта (Mazelin L. et al.: Life Sci. 1998, 63, p. 293304), кашля, гиперчувствительность дыхательных путей, капиллярной гиперчувствительности и снижение бронхостеноза (Daoui S. et al.: Am. J. Respir. Crit. Care. Med. 1998, 158, p. 42-8, Rumsey W.L. et al.: J.Pharmacol. Exp. Ther. 2001, 298, p. 307-15, Daoui S. et al.: Pulm. Pharmacol. Ther. 1997, 10, p. 261-70). Ингибирование рецептора NK3 как часть терапевтического курса для болезни Паркинсона было подтверждено в нескольких работах (Arenas E.: J. Neurosci. 1991, 11, p. 2332-8, Kemel M.L. et al.: J. Neurosci. 2002, 22, p. 1929-36). Следовательно, доклинические, in vivo и in vitro исследования подтверждают, что антагонисты рецептора NK3 важны для лечения или предотвращения различных расстройств, включая шизофрению,депрессию, тревогу, болезнь Паркинсона, боль, судороги, кашель, астму, гиперчувствительность дыхательных путей, капиллярную гиперчувствительность, бронхостеноз, воспаление кишечника, воспалительное заболевание пищеварительного тракта, гипертензию, дисбаланс гомеостаза воды и электролитов,ишемию, отек и экстравазацию плазмы. Следовательно, существует необходимость в антагонистах рецептора NK3. Авторы данного изобретения обнаружили такие соединения с высоким сродством к рецептору NK3. Несколько заявок на патент относятся к соединениям, писанным как антагонисты рецептора NK3,например EP 474561, EP 512901 и WO 03/051869. В частности, некоторые заявки на патент относятся к соединениям, описанным как антагонисты рецептора NK3, например WO 9710211, US 5434158 иEP 673928. В US 5750549 описаны производные циклопентана в качестве антагонистов рецептора NK3. Все соединения в соответствии с данным изобретением являются производными циклопропила. Как описано далее, некоторые заявки на патент относятся к различным производным циклопентана. Однако ни одна из этих заявок на патент не относится к рецептору NK3 или другим рецепторам NK. В JP 03056415 описаны производные циклопропана формулы для лечения церебральной ишемии. В EP 68999 описаны производные циклопропана формулы для лечения депрессии. Сущность изобретения Объектом данного изобретения являются соединения, которые являются антагонистами рецептораNK3. Некоторые из этих соединений также могут иметь сродство к рецептору NK1 и/или NK2. Следовательно, в одном аспекте данное изобретение относится к соединению общей формулы где заместители такие, как описаны ниже,или его соли, в частности к его фармацевтически приемлемым кислотно-аддитивным солям. В частности, данное изобретение относится к (1S,2R)-изомерам таких соединений. Далее, в данном изобретении представлена фармацевтическая композиция, содержащая соединение формулы (I), такое как описано далее, или его фармацевтически приемлемую соль. Следовательно, в данном изобретении представлено соединение формулы (I), такое как представлено ниже, или его фармацевтически приемлемая соль для применения в медицине.-2 009477 В изобретении также представлено применение соединения формулы (I), такого как представлено ниже, или его фармацевтически приемлемой соли для получения лекарственного средства для лечения заболеваний, выбранных из группы, включающей шизофрению, психотические расстройства, депрессию,тревогу, болезнь Паркинсона, боль, судороги, кашель, астму, гиперчувствительность дыхательных путей,капиллярную гиперчувствительность, бронхостеноз, воспаление кишечника, воспалительное заболевание пищеварительного тракта, гипертензию, дисбаланс гомеостаза воды и электролитов, ишемию, отек и экстравазацию плазмы. Далее, данное изобретение относится к способу лечения заболеваний, выбранных из группы, включающей шизофрению, психотические расстройства, депрессию, тревогу, болезнь Паркинсона, боль, судороги, кашель, астму, гиперчувствительность дыхательных путей, капиллярную гиперчувствительность, бронхостеноз, воспаление кишечника, воспалительное заболевание пищеварительного тракта, гипертензию, дисбаланс гомеостаза воды и электролитов, ишемию, отек и экстравазацию плазмы, который включает введение терапевтически эффективного количества соединения формулы (I), такого, как описано ниже, или его фармацевтически приемлемой соли. Подробное описание изобретения Определения. Термин галоген означает фтор, хлор, бром или йод. Выражение C1-6 алк(ен/ин)ил означает C1-6 алкил, C2-6 алкенил или C2-6 алкинил. Термин C1-6 алкил относится к разветвленной или неразветвленной алкильной группе, имеющей от 1 до 6 атомов углерода включительно, содержащей, но не ограниченной ими, метил, этил, 1-пропил,2-пропил, 1-бутил, 2-бутил, 2-метил-2-пропил и 2-метил-1-пропил. Термин С 2-6 алкенил означает группы, имеющие от 2 до 6 атомов углерода, содержащие одну двойную связь, включающие, но не ограниченные ими, этенил, пропенил и бутенил. Термин C2-6 алкинил означает группы, имеющие от 2 до 6 атомов углерода, содержащие одну тройную связь, включающие, но не ограниченные ими, этинил, пропинил и бутинил. Выражение С 3-8 циклоалк(ен)ил означает С 3-8 циклоалкил или С 3-8 циклоалкенил. Термин С 3-8 циклоалкил означает моноциклический или бициклический карбоцикл, имеющий от 3 до 8 атомов углерода, включающий, но не ограниченный ими, циклопропил, циклопентил, циклогексил и т.д. Термин С 3-8 циклоалкенил означает моноциклический или бициклический карбоцикл, имеющий от 3 до 8 атомов углерода и одну двойную связь, включающий, но не ограниченный ими, циклопропенил,циклопентенил, циклогексенил и т.д. В выражении С 3-8 циклоалк(ен)ил-С 1-6 алк(ен/ин)ил термины С 3-8 циклоалк(ен)ил иC1-6 алк(ен/ин)иламино,галоген-C1-6 алк(ен/ин)ил, галоген-C1-6 алк(ен/ин)илсульфонил, галоген-C1-6 алк(ен/ин)илсульфанил,C1-6 алк(ен/ин)илсульфонил и C1-6 алк(ен/ин)илсульфанил и т.д., термины C1-6 алк(ен/ин)ил и гало такие, как определены выше. В данном описании термин ацил относится к формилу, C1-6 алк(ен/ин)илкарбонилу,арилкарбонилу,арил-C1-6 алк(ен/ин)илкарбонилу,С 3-8 циклоалк(ен)илкарбонилу или С 3-8 циклоалк(ен)ил-C1-6 алк(ен/ин)илкарбонилу, где C1-6 алк(ен/ин)ил и С 3-8 циклоалк(ен)ил такие, как определены выше, и арил такой, как определен ниже. Термин тиоацил означает соответствующую ацильную группу, в которой карбонильная группа замещена тиокарбонильной группой. Термин арил относится к карбоциклической ароматической группе, такой как фенил или нафтил,в частности фенил, и включает замещенную и незамещенную карбоциклические ароматические группы. Таким образом, арил необязательно замещен одним или более заместителями, выбранными из списка заместителей, представленного ниже. Следовательно, термин арил в данном описании означает необязательно замещенную карбоциклическую ароматическую группу, например фенил или нафтил, такую, что указанная ароматическая группа замещена одним или более заместителями, выбранными из списка заместителей, представленного ниже, например C1-6 алкила или галогена. Арил предпочтительно является моно- или бициклическим. Термин гетероарил относится к ароматической группе, содержащей по крайней мере один атом углерода и один или более гетероатомов, выбранных из О, S или N. В данном описании термин гетероарил относится к моно- или бициклической гетероциклической группе, включающей, но не ограниченной ими, индолил, тиенил, пиримидил, оксазолил, изоксазолил, тиазолил, изотиазолил, имидазолил, бензофуранил, бензотиенил, пиридил и фуранил, в частности пиримидил, индолил и тиенил. Термин гете-3 009477 роарил в данном описании включает замещенный и незамещенный гетероарил. Таким образом, арил необязательно замещен одним или более заместителями, выбранными из списка заместителей, представленного ниже, например C1-6 алкила или галогена. Термин моноциклический гетероарил в данном описании относится к 5-6-членной ароматической системе, содержащей от 1 до 5 атомов углерода и один или более гетероатом, выбранный из О, S или N. Следовательно, термин гетероарил относится к 5-членным моноциклическим кольцам, таким как, но не ограниченным ими, 1H-тетразолил, 3 Н-1,2,3-оксатиазолил, 3 Н-1,2,4-оксатиазолил,3H-1,2,5-оксатиазолил, 1,3,2-оксатиазолил, 1,3,4-оксатиазолил, 1,4,2-оксатиазолил, 3 Н-1,2,4-диоксазолил,1,3,2-диоксазолил, 1,4,2-диоксазолил, 3 Н-1,2,3-дитиазолил, 3 Н-1,2,4-дитиазолил, 1,3,2-дитиазолил,1,4,2-дитиазолил, 1,2,3-оксадиазолил, 1,2,4-оксадиазолил, 1,2,5-оксадиазолил, 1,3,4-оксадиазолил,1,2,3-тиадиазолил, 1,2,4-тиадиазолил, 1,2,5-тиадиазолил, 1,3,4-тиадиазолил, 1H-1,2,3-триазолил,1H-1,2,4-триазолил, изоксазолил, оксазолил, изотиазолил, тиазолил, 1 Н-имидазолил, 1 Н-пиразолил,1 Н-пирролил, фуранил, тиенил, 1 Н-пентазол. Далее, термин гетероарил относится к 6-членным моноциклическим кольцам, таким как, но не ограниченным ими, 1,2,3-оксатиазинил, 1,2,4-оксатиазинил, 1,2,5-оксатиазинил, 4H-1,3,5-оксатиазинил,1,4,2-оксатиазинил, 1,4,3-оксатиазинил, 1,2,3-диоксазинил, 1,2,4-диоксазинил, 4 Н-1,3,2-диоксазинил,4H-1,3,5-диоксазинил, 1,4,2-диоксазинил, 2 Н-1,5,2-диоксазинил, 1,2,3-дитиазинил, 1,2,4-дитиазинил,4 Н-1,3,2-дитиазинил,4H-1,3,5-дитиазинил,1,4,2-дитиазинил,2 Н-1,5,2-дитиазинил,2H-1,2,3-оксадиазинил,2 Н-1,2,4-оксадиазинил,2 Н-1,2,5-оксадиазинил,2 Н-1,2,6-оксадиазинил,2 Н-1,3,4-оксадиазинил,2H-1,3,5-оксадиазинил,2 Н-1,2,3-тиадиазинил,2 Н-1,2,4-тиадиазинил,2 Н-1,2,5-тиадиазинил,2 Н-1,2,6-тиадиазинил,2 Н-1,3,4-тиадиазинил,2 Н-1,3,5-тиадиазинил,1,2,3-триазинил,1,2,4-триазинил,1,3,5-триазинил,2 Н-1,2-оксазинил,2 Н-1,3-оксазинил,2 Н-1,4-оксазинил, 2 Н-1,2-тиазинил, 2 Н-1,3-тиазинил, 2 Н-1,4-тиазинил, пиразинил, пиридазинил,пиримидил, пиридил, 2H-пиранил, 2 Н-тиинил. Наконец, термин гетероарил также относится к бициклическим кольцам, таким как, но не ограниченным ими, 3H-1,2,3-бензоксатиазолил, 1,3,2-бензодиоксазолил, 3 Н-1,2,3-бензодитиазолил,1,3,2-бензодитиазолил,бензфуранил,1,2,3-бензоксадиазолил,1,2,3-бензотиадиазолил,2,1,3-бензотиадиазолил, 1 Н-бензотриазолил, 1,2-бензизоксазолил, 2,1-бензизоксазолил, бензоксазолил,1,2-бензизотиазолил, 2,1-бензизотиазолил, бензотиазолил, 1 Н-бензимидазолил, 1H-индазолил,3 Н-1,2-бензоксатиолил,1,3-бензоксатиолил,3 Н-2,1-бензоксатиолил,3 Н-1,2-бензодиоксолил,1,3-бензодиоксолил,3H-1,2-бензодитиолил,1,3-бензодитиолил,1H-индолил,2H-изоиндолил,бензофуранил,изобензофуранил,1-бензотиенил,2-бензотиенил,1 Н-2,1-бензоксазинил,1 Н-2,3-бензоксазинил,2H-1,2-бензоксазинил,2 Н-1,3-бензоксазинил,2 Н-1,4-бензоксазинил,2 Н-3,1-бензоксазинил,1 Н-2,1-бензотиазинил,1 Н-2,3-бензотиазинил,2 Н-1,2-бензотиазинил,2 Н-1,3-бензотиазинил, 2H-1,4-бензотиазинил, 2 Н-3,1-бензотиазинил, циннолинил, фталазинил,хиназолинил, хиноксалинил, изохинолил, хинолил, 1H-2-бензопиранил, 2 Н-1-бензопиранил,1 Н-2-бензотиопиранил или 2H-1-бензотиопиранил. Выражение список заместителей включает заместители, выбранные из группы, включающей галоген, циано, нитро, C1-6 алкил (например, метил), C1-6 алкиламино, ди(C1-6 алкил)амино,C1-6 алкилкарбонил, аминокарбонил, C1-6 алкиламинокарбонил, ди(C1-6 алкил)аминокарбонил, C1-6 алкокси,C1-6 алкилтио,алкилсульфонил,гидрокси,трифторметил,трифторметилсульфонил,C1-6 алкилкарбониламино и C1-6 алкилкарбонилC1-6 алкиламино. Термин лечение, применяемый в данном описании, в контексте заболевания или расстройства,включает также их предотвращение, если оно возможно. Соединения в соответствии с данным изобретением и их соли Данное изобретение относится к соединениям формулы (I), которые являются антагонистами рецептора NK3. Эти продукты могут применяться для лечения определенных заболеваний, таких как, например, шизофрения, психотические расстройства, депрессия, тревога или болезнь Паркинсона. В одном аспекте изобретение относится к соединению формулы или его соли, такой как фармацевтически приемлемая соль; где R1-R5 независимо выбирают из водорода, галогена, циано, нитро, C1-6 алк(ен/ин)ила (например,C1-6 алкила, С 2-6 алкенила или C2-6 алкинила; такого как метил), С 3-8 циклоалк(ен)ила (например,С 3-8 циклоалкила), С 3-8 циклоалк(ен)ил-C1-6 алк(ен/ин)ила (например, С 3-8 циклоалкил-C1-6 алкила), амино,C1-6 алк(ен/ин)иламиноR7 является арилом или гетероарилом или R7 является группой арил-CR8R9-, где R8 и R9 независимо выбирают из водорода, C1-6 алк(ен/ин)ила (например, C1-6 алкила, C2-6 алкенила или C2-6 алкинила, такого как метил), С 3-8 циклоалк(ен)ила (например, С 3-8 циклоалкила) и С 3-8 циклоалк(ен)ил-C1-6 алк(ен/ин)ила (например, С 3-8 циклоалкил-C1-6 алкила);Q выбирают из (i)-(vii), стрелки указывают на место присоединения: где R10 является необязательно замещенным арилом;R11 выбирают из необязательно замещенного арила или необязательно замещенного бензила,галоген-C1-6 алк(ен/ин)илсульфонилаR12 является необязательно замещенным арилом;R13 является водородом, гидрокси, циано или амино либо одной или более из следующих групп:-NR14COR15, где R14 является водородом или C1-6 алк(ен/ин)илом и R15 является C1-6 алк(ен/ин)илом или С 3-8 циклоалк(ен)илом;-NR16COCONR17R18, где R16 является водородом или C1-6 алк(ен/ин)илом и R17 и R18 независимо выбирают из водорода и C1-6 алк(ен/ин)ила (например, C1-6 алкила) или С 3-8 циклоалкила или R17 и R18 вместе с атомом азота, к которому они присоединены, образуют пиперидинил, пиперазинил или морфолинил,где указанный пиперидинил, пиперазинил или морфолинил необязательно замещены (например, не замещены или замещены) C1-6 алк(ен/ин)илом;-NR19CONR20R21, где R19 является водородом или C1-6 алк(ен/ин)илом и R20 и R21 независимо выбирают из водорода и C1-6 алк(ен/ин)ила или С 3-8 циклоалкила или R20 и R21 вместе с атомом азота, к которому они присоединены, образуют пиперидинил, пиперазинил или морфолинил, где указанный пиперидинил, пиперазинил или морфолинил необязательно замещены (например, не замещены или замещены)-NR22SO2R23, где R22 является водородом или C1-6 алк(ен/ин)илом или С 3-8 циклоалкилом и R23 является амино, C1-6 алк(ен/ин)илом или С 3-8 циклоалкилом;-CONR25R26, где R25 и R26 независимо выбирают из водорода, C1-6 алк(ен/ин)ила или С 3-8 циклоалкила или R25 и R26 вместе с атомом азота, к которому они присоединены, образуют пиперидинил, пиперазинил или морфолинил, где указанный пиперидинил, пиперазинил или морфолинил необязательно замещены (например, не замещены или замещены) C1-6 алк(ен/ин)илом, в частности C1-6 алкилом;X, Y и Z независимо выбирают из связи О; NR27; CR29R29 и S(O)m, m равно 0, 1 или 2;R27 является группой R31R32NCO- или R31R32NCS-, где R31 и R32 независимо выбирают из водорода,C1-6 алк(ен/ин)ила (например, C1-6 алкила, C2-6 алкенила или С 2-6 алкинила), С 3-8 циклоалкила и С 3-8 циклоалкил-C1-6 алкила и арила, где указанный арил необязательно замещен (т.е. не замещен или за-5 009477 мещен), например, одним или более заместителями, выбранными из C1-6 алкила или галогена; или R31 иR28 и R29 независимо выбирают из водорода, галогена, такого как фтор, C1-6 алк(ен/ин)ил (например,C1-6 алкил, C1-6 алкил, C2-6 алкенил или C2-6 алкинил), С 3-8 циклоалкил или С 3-8 циклоалкил-C1-6 алкил;R33-R36 независимо выбирают из водорода, галогена, циано, нитро, C1-6 алк(ен/ин)ила (например,C1-6 алкила, С 2-6 алкенила или С 2-6 алкинила), С 3-8 циклоалкила и С 3-8 циклоалкил-алкила, амино,C1-6 алкиламино, ди(C1-6 алкил)амино, C1-6 алкилкарбонила, аминокарбонила, C1-6 алкиламинокарбонила,ди(C1-6 алкил)аминокарбонила, C1-6 алкокси, C1-6 алкилтио, гидрокси, галоген-C1-6 алк(ен/ин)ила, предпочтительно трифторметила, трифторметилсульфонила и C1-6 алкилсульфонила;R37-R38 либо оба являются водородом, либо сконденсированы вместе в этиленовой цепи СН 2-СН 2- с образованием азабицикло[3.2.1]октан-ила;R39-R41 независимо выбирают из водорода и списка заместителей, такого как определен выше; при условии, что не более чем один из X, Y и Z может быть связью, и при условии, что две соседние группы X, Y или Z не могут одновременно быть выбраны из О или S. Для дальнейшей иллюстрации данного изобретения, без ограничений, следующие варианты R2-R5 включены в объем данного изобретения, в частности для соединений или их солей:R1-R5 независимо выбирают из водорода, галогена, циано, C1-6 алкила, С 3-8 циклоалкила,С 3-8 циклоалкил-C1-6 алкила, C1-6 алкилокси, C1-6 алкилтио и трифторметила;R1-R5 независимо выбирают из водорода и C1-6 алкила;R1-R5 независимо выбирают из водорода, Cl, F, циано, метила, метокси, метилтио и трифторметила;R1-R5 независимо выбирают из водорода и галогена;R1-R5 независимо выбирают из водорода, хлора и фтора;R1-R5 независимо выбирают из водорода и хлора;R1-R5 независимо выбирают из водорода и фтора;R2 является хлором и R3 является водородом, R2 и R3 являются хлором, R2 является фтором и R3 является водородом или R2 и R3 являются фтором, где остальные из R1-R5 могут быть, например, водородом, или они также могут быть заместителями из представленного выше списка; по крайней мере один из R1-R5 является F или Cl, такие как соединения в соответствии с данным изобретением, в которых R3 является F или Cl;R1-R5 независимо выбирают из H и циано;R1-R5 независимо выбирают из H и C1-6 алк(ен/ин)ила;R1-R5 независимо выбирают из H и C1-6 алкила, такого как метил или этил;R1-R5 независимо выбирают из H и C1-6 алк(ен/ин)илокси, предпочтительно, C1-6 алкокси, такого как метокси;R1-R5 независимо выбирают из H и C1-6 алкилтио, такого как метилтио;R1-R5 независимо выбирают из H и трифторметила; по крайней мере 3 из R1-R5 являются водородом, например 3, 4 или все R1-R5 являются водородом; один из R1-R5 замещен, например, в положениях R2 или R3, например, галогеном (например, F илиCl), C1-6 алкилом (например, метилом), C1-6 алкокси (например, метокси), в то время как остальные R1-R5 являются водородом; два из R1-R5 замещены, например, в положениях R2 или R3, например, заместителями, независимо выбранными из группы, включающей галоген (например, F или Cl), C1-6 алкил (например, метил),C1-6 алкокси (например, метокси), в то время как остальные R1-R5 являются водородом. Для дальнейшей иллюстрации данного изобретения, без ограничений, следующие варианты R6 включены в объем данного изобретения, в частности, для соединений или их солей:R6 выбирают из водорода и C1-6 алк(ен/ин)ила;R6 является этилом. Если R7 является арилом или гетероарилом, понятно, что арил и гетероарил такие, как определены далее, и могут быть выбраны из них. В одном аспекте данное изобретение относится к соединениям формулы (I), в которых R7 является арилом, таким как определен далее. Для дальнейшей иллюстрации данного изобретения, без ограничений, следующие варианты R7, где R7 является арилом, включены в объем данного изобретения, в частности, для соединений или их солей:R7 является фенилом, замещенным одним или более заместителями, например, моно- или дизаме-6 009477 щенным, где заместители независимо выбирают из списка заместителей, представленного выше, включая, например, галоген и C1-6 алкил;R7 является незамещенным фенилом и R6 является водородом;R7 является незамещенным фенилом и R6 является метилом. Для дальнейшей иллюстрации данного изобретения, без ограничений, следующие варианты R7, где 7R является группой арил-CR8R9-, включены в объем данного изобретения, в частности, для соединений или их солей:R8 и R9 независимо выбирают из водорода, C1-6 алкила, С 3-8 циклоалкила и С 3-8 циклоалкил-C1-6 алкила;R8 и R9 независимо выбирают из водорода и C1-6 алкила;R8 и R9 независимо выбирают из водорода и метила;R8 и R9 являются метилом. Понятно, что для R7, являющегося арил-CR8R9, арил из арил-CR8R9 такой, как определен далее,например, может иметь одну или более из следующих характеристик: арил является моноциклическим или бициклическим; арил незамещен; арил является фенилом; арил является нафталином, арил замещен одним или более заместителями, предпочтительно выбранными из группы, включающей галоген, циано, нитро, C1-6 алкилом, C2-6 алкенилом, С 2-6 алкинилом,С 3-8 циклоалкилом,С 3-8 циклоалкил-C1-6 алкилом,амино,C1-6 алкиламино,ди(C1-6 алкил)амино,C1-6 алкилкарбонилом, аминокарбонилом, C1-6 алкиламинокарбонилом, ди(C1-6 алкил)аминокарбонилом,C1-6 алкилкарбониламино, C1-6 алкилкарбонилC1-6 алкиламино, C1-6 алкокси (например, метокси),C1-6 алкилтио, гидрокси, трифторметилом, дифторметилом, фторметилом и трифторметилсульфонилом; арил, например фенил, является необязательно замещенным фенилом; арил, например фенил, является моно- или полизамещенным, например дизамещенным, например,галогеном, таким как фтор или хлор, и/или, например, C1-6 алкокси (например, метокси). В предпочтительном варианте R7 является арил-CR8R9-, выбранным из бензила или замещенного бензила, например бензила, замещенного галогеном, например 4-галобензила, такого как 4-фторбензил,или 2-галобензила, такого как 2-хлорбензил, или 3,4-дихлорбензиламида, 3,4-диметоксибензиламида,метил-1-фенилэтила, метил-1-(4-метоксифенил)этила или нафталин-1-илметила. Другие варианты данного изобретения относятся к соединениям формулы (I), в которых R6 является водородом или метилом. Другие аспекты данного изобретения относятся к соединениям формулы (I), в которых Q является(i). Один из аспектов данного изобретения относится к вариантам данного изобретения, в которых Q является (i) и арил из R10 выбирают из арилов, определенных далее. В других вариантах данное изобретение относится к соединению или соли в соответствии с данным изобретением, где Q является (ii), предпочтительно R11 выбирают из необязательно замещенного (т.е. замещенного или нет) арила или необязательно замещенного (т.е. замещенного или нет) бензила, трифторметилсульфонила, C1-6 алкилсульфонила, арилсульфонила, арилацила, C1-6 алкилкарбонила, аминокарбонила, C1-6 алкиламинокарбонила и ди(C1-6 алкил)аминокарбонила, где указанный арил выбирают из арилов, определенных далее. Бензил может быть замещен одним или более заместителями, выбранными из списка заместителей, представленного выше. В других вариантах данное изобретение относится к соединению или соли в соответствии с данным изобретением, в которых Q является (iii). Для дальнейшей иллюстрации данного изобретения, без ограничений, следующие варианты R12 включены в объем данного изобретения, в частности, для соединений или их солей:R12 является арилом, таким как определен далее;R12 является фенилом, замещенным одним или более заместителями, например моно- или дизамещенным, где заместители предпочтительно выбраны из списка заместителей, представленного выше; арил, например фенил, в R12 замещен одним или более, например одним или двумя, заместителями,выбранными из галогена и трифторметила; арил, например фенил, в R12 замещен по крайней мере одним хлором или по крайней мере одним фтором и по крайней мере одним трифторметилом; арил, например фенил, в R12 замещен одним Cl и одним трифторметилом;R12 является 4-хлор-3-трифторметилфенилом. Следующие варианты соединения в соответствии с данным изобретением, в котором Q являетсяR12 является арилом, замещенным одним или более заместителями, выбранными из галогена и аминоацила, и R13 является водородом;R12 является фенилом, замещенным одним или более заместителями, например моно- или дизаме-7 009477 щенным, где заместители выбраны из галогена и аминоацила, и R13 является водородом. В одном из вариантов, в которых Q является (iii), группа R13 является гидрокси. В предпочтительном варианте R12 является 4-хлор-3-трифторметилфенилом и R13 является гидрокси. В других вариантах (iii) R13 является -NR14COR15, где R14 и R15 такие, как определены далее. Для дальнейшей иллюстрации данного изобретения, без ограничений, следующие варианты R13 включены в объем данного изобретения, в частности, для соединений или их солей:R14 является водородом или C1-6 алкилом и R15 является C1-6 алкилом или С 3-8 циклоалкилом;R14 и R15 являются метилом. В других вариантах (iii) R13 является -NR16COCONR17R18, где R16, R17 и R18 такие, как определены далее. Для дальнейшей иллюстрации данного изобретения, без ограничений, следующие варианты R13 включены в объем данного изобретения, в частности, для соединений или их солей:R16 является водородом или C1-6 алкилом и где R17 и R18 независимо выбирают из водорода,C1-6 алкила и С 3-8 циклоалкила;R16 является водородом или C1-6 алкилом и где R17 и R18 вместе с атомом азота, к которому они присоединены, образуют пиперидинил, пиперазинил или морфолинил, где указанные пиперидинил, пиперазинил и морфолинил необязательно замещены C1-6 алкилом, например метилом;R16, R17 и R18 являются C1-6 алкилом (например, N',N'-ди(C1-6 алкил)-N-C1-6 алкилоксаламидом). В других вариантах (iii) R13 является -NR19CONR20R21, где R19, R20 и R21 такие, как определены далее. Для дальнейшей иллюстрации данного изобретения, без ограничений, следующие варианты R13 включены в объем данного изобретения, в частности, для соединений или их солей:R19, R20 и R21 независимо выбирают из водорода, C1-6 алкила и С 3-8 циклоалкила;R19, R20 и R21 независимо выбирают из водорода и C1-6 алкила;R19 и R20 независимо выбирают из C1-6 алкила и R21 является H;R19 является H и R20 и R21 независимо выбирают из C1-6 алкила или R19, R20 и R21 независимо выбирают из C1-6 алкила;R19 является H и R20 и R21 независимо выбирают из группы, включающей водород, Me, Et, Bu и i-Pr. В других вариантах (iii) R13 является -NR22SO2R23, где R22 и R23 такие, как определены далее. Для дальнейшей иллюстрации данного изобретения, без ограничений, следующие варианты R13 включены в объем данного изобретения, в частности, для соединений или их солей:R22 является водородом или C1-6 алкилом или С 3-8 циклоалкилом и R23 является амино, C1-6 алкилом или С 3-8 циклоалкилом;N-(C1-6 алкилсульфонамидом) или R22 и R23 независимо выбирают из C1-6 алкила, например метила, например N-C1-6 алкил(C1-6 алкилсульфонамида);R22 является водородом и R23 является метилом. В других вариантах (iii) R13 является -COR24, где R24 такой, как определен далее. Следующие варианты R13 также включены в объем данного изобретения без ограничений, в частности, для соединений или их солей:-8 009477 В других вариантах (iii) R13 является -CONR255R26, где R25 и R26 такие, как определены далее. Для дальнейшей иллюстрации данного изобретения, без ограничений, следующие варианты R13 включены в объем данного изобретения, в частности, для соединений или их солей:R25 и R26 независимо выбирают из водорода, C1-6 алкила и С 3-8 циклоалкила;R25 и R26 независимо выбирают из водорода и метила;R25 и R26 вместе с атомом азота, к которому они присоединены, образуют пиперидинил, где указанный пиперидинил необязательно замещен C1-6 алкилом, предпочтительно пиперидинил не замещен. В других вариантах данное изобретение относится к соединению или его соли в соответствии с данным изобретением, где Q является (vii) как описано выше Для дальнейшей иллюстрации данного изобретения, без ограничений, следующие варианты (vii) включены в объем данного изобретения:Y является связью и X и Z независимо выбирают из О, NR27 и CR28R29 и S(O)m при условии, что X иZ одновременно не могут быть выбраны из О и S;Y является связью и X и Z независимо выбирают из CR28R29 и NR27;R27 выбирают из группы R30SO2-, R30OCO- и R30SCO-;R33-R36 независимо выбирают из водорода и галогена, например хлора или фтора;R37-R38 сконденсированы вместе в этиленовой цепи СН 2-СН 2- с получением азабицикло[3.2.1]октанила, как показано на фигуре ниже В других вариантах соединения (I) Q является (iv). Для дальнейшей иллюстрации данного изобретения, без ограничений, следующие варианты (iv) включены в объем данного изобретения:R39 является водородом во всех положениях, т.е. соответствующая фенильная группа не замещена; соответствующая фенильная группа замещена только в одном или двух положениях заместителемR39, выбранным из списка заместителей, представленного выше, например галогена. В других вариантах соединения (I) Q является (v). Для дальнейшей иллюстрации данного изобретения, без ограничений, следующие варианты (v) включены в объем данного изобретения:R40 выбирают из группы, включающей водород или галоген;R40 является водородом во всех положениях, т.е. соответствующая фенильная группа не замещена; соответствующая фенильная группа замещена только в одном или двух положениях заместителемR40, выбранным из списка заместителей, представленного выше, например галогена. В других вариантах соединения (I) Q является (vi). Для дальнейшей иллюстрации данного изобретения, без ограничений, следующие варианты (vi) включены в объем данного изобретения:R41 выбирают из группы, включающей водород или галоген;R41 является водородом во всех положениях, т.е. соответствующая бензильная группа не замещена; соответствующая бензильная группа замещена только в одном или двух положениях заместителемR41, выбранным из списка заместителей, представленного выше, например галогена. Соединения в соответствии с данным изобретением могут иметь один или более центров асимметрии и подразумевается, что любой оптический изомер (например, энантиомеры или диастереомеры) при разделении, чистые или частично очищенные оптические изомеры и их смеси, включая рацемические смеси, например смеси стереоизомеров, включены в объем данного изобретения. Соединения формулы (I) существуют в виде оптических изомеров, которые также включены в данное изобретение. В частности, соединения в соответствии с данным изобретением, обладающие абсолютной стереохимией (1S,2R), также включены в объем данного изобретения либо в виде энантиомеров,либо в виде смесей, содержащих соединения в соответствии с данным изобретением, обладающие абсолютной стереохимией (1S,2R). Следовательно, важным аспектом данного изобретения является соединение или соль в соответствии с данным изобретением, как описано выше, где соединение формулы (I) является (1S,2R)-изомером,например соединение с абсолютной конфигурацией, как показано в формуле Соединение в соответствии с данным изобретением формулы (I) или его соль могут быть частью рацемических смесей, содержащих (1S,2R)-изомер, т.е. соединение, показанное в формуле IA, либо оно может присутствовать в виде энантиомера, т.е. без 3 других стереоизомеров. Данное изобретение в еще одном варианте относится к соединению формулы (I), где соединение является (1R,2R)-изомером. Данное изобретение в еще одном варианте относится к соединению формулы (I), где соединение является (1R,2S)-изомером. Данное изобретение в еще одном варианте относится к соединению формулы (I), где соединение является (1S,2S)-изомером. В данном контексте понятно, что при определении энантиомерной формы соединение предпочтительного варианта находится в энантиомерном избытке. Следовательно, один из вариантов данного изобретения относится к соединению в соответствии с данным изобретением, имеющему энантиомерный избыток по крайней мере 60% (60% энантиомерный избыток означает, что соотношение Va к его энантиомерам составляет 80:20 в интересующей смеси), по крайней мере 70%, по крайней мере 80%, по крайней мере 85%, по крайней мере 90%, по крайней мере 96%, предпочтительно по крайней мере 98%. Выражение смесь стереоизомеров, содержащая (1S,2R)-изомер формулы (I) означает, что в других вариантах соединение в соответствии с данным изобретением, т.е. продукт, может быть любой из следующих смесей стереоизомеров:(1S,2R)-изомер и (1R, 2R)-изомер формулы (I), т.е. состоять из 2, 3 или 4 соответствующих стереоизомеров. Рацемические формы могут быть разделены на оптические антиподы известными методами, например разделением диастереомерных солей с оптически активной кислотой и высвобождением оптически активного соединения амина обработкой основанием. Другие методы разделения рацематов на оптические антиподы основаны на хроматографии на оптически активной матрице. Рацемические соединения в соответствии с данным изобретением также могут быть разделены на их оптические антиподы, например, фракционной кристаллизацией. Соединения в соответствии с данным изобретением также могут быть разделены посредством образования диастереомерных производных. Могут применяться другие методы разделения оптических изомеров, известные специалистам в данной области техники. Такие ме- 10009477 тоды включают те, которые описаны у J. Jaques, A. Collet и S. Wilen в Enantiomers, Racemates, and Resolution, John Wiley and Sons, New York, 1981. Оптически активные соединения также могут быть получены из оптически активных исходных веществ. Далее, если в молекуле присутствует двойная связь или полностью или частично насыщенная кольцевая система, могут быть получены геометрические изомеры. Подразумевается, что любые геометрические изомеры, разделенные, полностью или частично очищенные геометрические изомеры или их смеси,включены в объем данного изобретения. Также молекулы, имеющие связь с ограниченным вращением,могут образовывать геометрические изомеры. Они также включены в объем данного изобретения. Далее, некоторые соединения в соответствии с данным изобретением могут существовать в различных таутомерных формах, подразумевается, что любая таутомерная форма, которую могут образовывать соединения в соответствии с данным изобретением, включена в объем данного изобретения. В других вариантах формулы (I) соединение в соответствии с данным изобретением представляет собой любое из следующих соединений:(132) 1-(3,4-дихлорфенил)-2-(4-ацетиламино-4-фенилпиперидин-1-илметил)циклопропанкарбоновой кислоты метилнафталин-1-илметиламид; или их солей, таких как фармацевтически приемлемые соли. В еще более предпочтительном варианте формулы (I) соединение является любым из представленных ниже соединений:(132 а) (1S,2R)-1-(3,4-дихлорфенил)-2-(4-ацетиламино-4-фенилпиперидин-1-илметил)циклопропанкарбоновой кислоты метилнафталин-1-илметиламид или их солей, таких как фармацевтически приемлемые соли. В других вариантах формулы (I) соединения в соответствии с данным изобретением включают любые из следующих соединений:(77b) 1-(4-фторфенил)-2-[4-фенил-4-(пиперидин-1-карбонил)пиперидин-1-илметил]циклопропанкарбоновой кислоты метил-(1-фенилэтил)амид или их солей, таких как фармацевтически приемлемые соли. В объем данного изобретения также включены соединения, выбранные из группы, включающей 5b,6b, 19b, 20b, 38b, 40b, 41b, 58b, 62b, 63b, 64b, 65b, 67b, 68b, 77b, которые являются (1S,2R)-изомерами,т.е. имеют абсолютную конфигурацию, показанную в формуле IA; или их соли, такие как фармацевтически приемлемые соли. Другие аспекты данного изобретения относятся к соединениям в соответствии с данным изобретением формулы (I), которые являются (1R,2R)-изомерами (т.е. отличаются от формулы (IA), которая является (1S,2R)-изомером). Другие аспекты данного изобретения относятся к соединениям в соответствии с данным изобретением формулы (I), которые являются (1S,2S)-изомерами (т.е. отличаются от формулы (IA), которая является (1S,2R)-изомером). Другие аспекты данного изобретения относятся к соединениям в соответствии с данным изобретением формулы (I), которые являются (1R,2S)-изомерами (т.е. отличаются от формулы (IA), которая является (1S,2R)-изомером). Данное изобретение также включает соли соединений в соответствии с данным изобретением,обычно фармацевтически приемлемые соли. Такие соли включают фармацевтически приемлемые кислотно-аддитивные соли, фармацевтически приемлемые соли металлов, аммония и алкилированные аммониевые соли. Кислотно-аддитивные соли включают соли с неорганическими кислотами, а также с органическими кислотами. Примеры подходящих неорганических солей включают соли с хлористо-водородной, бромистоводородной, йодисто-водородной, фосфорной, серной, сульфаминовой, азотной кислотами и т.п. Примеры подходящих органических кислот включают муравьиную, уксусную, трихлоруксусную,трифторуксусную, пропионовую, бензойную, коричную, лимонную, фумаровую, гликолевую, итаконовую, молочную, метансульфоновую, малеиновую, яблочную, малоновую, миндальную, щавелевую, пикриновую, пировиноградную, салициловую, янтарную, метановую, сульфоновую, этансульфоновую, винную, аскорбиновую, памовую, бисметиленовую салициловую, этандисульфоновую, глюконовую, цитраконовую, аспаргиновую, стеариновую, пальмитиновую, ЭДТК, гликолевую, п-аминобензойную, глутаминовую, бензолсульфоновую, п-толуолсульфоновую и теофиллинуксусные кислоты, а также 8 галогентеофиллины, например, 8-бромтеофиллин и т.п. Другие примеры фармацевтически приемлемых неорганических или органических кислотно-аддитивных солей включают фармацевтически приемлемые соли, перечисленные в J. Pharm. Sci. 1977, 66, 2, который включен сюда в качестве ссылки. Примеры солей металлов включают литиевые, натриевые, калиевые, магниевые соли и т.п. Примеры аммониевых и алкилированных аммониевых солей включают аммониевые, метил-, диметил-, триметил-, этил-, гидроксиэтил-, диэтил-, н-бутил-, втор-бутил-, трет-бутил-, тетраметиламмониевые соли и т.п. Также в качестве фармацевтически приемлемых кислотно-аддитивных солей рассматриваются гидраты, которые могут образовывать соединения в соответствии с данным изобретением. Далее, соединения в соответствии с данным изобретением могут существовать в несольватированной и в сольватированной формах с фармацевтически приемлемыми растворителями, такими как вода,этанол и т.п. В общем, сольватированные формы считаются эквивалентными несольватированным формам в целях данного изобретения. Изобретение также охватывает пролекарства соединений в соответствии с данным изобретением,которые при введении претерпевают химическое превращение вследствие метаболических процессов,- 20009477 прежде чем стать фармакологически активными веществами. В общем, такие пролекарства являются функциональными производными соединений общей формулы (I), которые легко превращаются in vivo в требуемые соединения формулы (I). Обычные методики выбора и получения подходящих производных пролекарств описаны, например, в Design of Prodrugs ed. H. Bundgaard, Elsevier, 1985. Данное изобретение также охватывает активные метаболиты соединений в соответствии с данным изобретением. Соединения (включая их соли) в соответствии с данным изобретением являются антагонистами рецептора NK3, имеющими сродство связывания с NK3 человека (Ki) 5 мкМ или менее, обычно 1 мкМ или менее и предпочтительно 200 нМ или менее, при измерении по методу, описанному в примере 20. Другим объектом данного изобретения являются соединения, включая их соли с активностью, при которой улучшаются один или более из следующих параметров: растворимость, метаболическая стабильность и биодоступность по сравнению с соединениями известного уровня техники. Фармацевтическое применение. Как указано выше, соединения в соответствии с данным изобретением являются антагонистами рецептора NK3 и, таким образом, могут применяться для лечения расстройств или заболеваний, в которые вовлечен рецептор NK3. Соединения в соответствии с данным изобретением и их соли могут применяться для лечения,включая предотвращение шизофрении, психотических расстройств, депрессии, тревоги, болезни Паркинсона, боли, судорог, кашля, астмы, гиперчувствительности дыхательных путей, капиллярной гиперчувствительности, бронхостеноза, воспаления кишечника, воспалительного заболевания пищеварительного тракта, гипертензии, дисбаланса гомеостаза воды и электролитов, ишемии, отека и экстравазации плазмы. В предпочтительном варианте соединения в соответствии с данным изобретением и их соли применяют в качестве антипсихотических средств. Таким образом, соединения в соответствии с данным изобретением могут применяться для лечения заболеваний или расстройств центральной нервной системы. В других вариантах соединения в соответствии с данным изобретением или их соли также могут оказывать некоторое воздействие на NK1 и/или NK2 в дополнение к воздействию на NK3, как описано выше. Следовательно, соединения в соответствии с данным изобретением и их соли также могут применяться для лечения, включая предотвращение заболеваний, в которые вовлечены рецептор NK1 и/или рецептор NK2, особенно рвоты, депрессии или тревоги. В другом аспекте данное изобретение относится к соединению в соответствии с данным изобретением или его соли для применения в качестве лекарственного средства. Данное изобретение также относится к фармацевтической композиции, включающей соединение в соответствии с данным изобретением или его соль и фармацевтически приемлемый носитель или разбавитель. Композиция может содержать любой из вариантов формулы (I), описанных выше. Данное изобретение также относится к применению соединения в соответствии с данным изобретением или его соли для получения лекарственного средства для лечения заболеваний или расстройств, в которых требуется антагонист рецептора NK, в частности антагонист рецептора NK3. Лекарственное средство может содержать любой из вариантов формулы (I), описанных выше. В частности, данное изобретение относится к применению соединения в соответствии с данным изобретением или его соли для получения лекарственного средства для лечения любого заболевания,указанного в данном описании, включая психотические расстройства, в частности шизофрению. В одном аспекте данное изобретение относится к применению соединения в соответствии с данным изобретением или его соли для лечения положительных симптомов шизофрении. Далее, данное изобретение также относится к применению соединения в соответствии с данным изобретением или его соли для получения лекарственного средства для лечения или предотвращения депрессии или тревоги. Данное изобретение также относится к применению соединения в соответствии с данным изобретением или его соли для получения лекарственного средства для лечения или предотвращения болезни Паркинсона. Далее, данное изобретение также относится к применению соединения в соответствии с данным изобретением или его соли для получения лекарственного средства для лечения или предотвращения судорог. В другом аспекте данное изобретение относится к способу лечения или предотвращения шизофрении, психотических расстройств, депрессии, тревоги, болезни Паркинсона, боли, судорог, кашля, астмы,гиперчувствительности дыхательных путей, капиллярной гиперчувствительности, бронхостеноза, воспаления кишечника, воспалительного заболевания пищеварительного тракта, гипертензии, дисбаланса гомеостаза воды и электролитов, ишемии, отека и экстравазации плазмы в организме животного, включая человека, включающему введение нуждающемуся в этом пациенту терапевтически эффективного количества соединения в соответствии с данным изобретением или его фармацевтически приемлемой кислотно-аддитивной соли. В общем, данное изобретение также относится к применению соединения в соответствии с данным изобретением или его соли для получения лекарственного средства для лечения или предотвращения указанных заболеваний/расстройств.- 21009477 Соединения в соответствии с данным изобретением или их соли могут вводиться в чистом виде или в сочетании с фармацевтически приемлемыми носителями или наполнителями, одной или несколькими дозами. Фармацевтические композиции в соответствии с данным изобретением могут быть соединены с фармацевтически приемлемыми носителями или разбавителями, а также любыми другими известными адъювантами и наполнителями в соответствии с обычными методиками, такими как описаны в Remington: The Science and Practice of Pharmacy, 19 Edition, Gennaro, Ed., Mack Publishing Co., Easton, PA, 1995. Фармацевтические композиции могут быть определенным образом сформированы для введения любым подходящим путем, таким как пероральный, ректальный, назальный, легочный, местный (включая щечный и подъязычный), чрескожный, интрацистернальный, внутрибрюшинный, вагинальный и парентеральный (включая подкожный, внутримышечный, интратекальный, внутривенный и внутрикожный) пути, где предпочтительным является пероральный путь. Понятно, что предпочтительный способ зависит от общего состояния и возраста пациента, подлежащего лечению, природы излечиваемого состояния и выбранного активного ингредиента. Фармацевтические композиции для перорального применения включают твердые дозированные формы, такие как капсулы, таблетки, драже, пилюли, пастилки, порошки и гранулы. Если применимо,они могут иметь оболочки, такие как энтеросолюбильные, или они могут быть составлены таким образом, чтобы обеспечивать контролируемое выделение активного ингредиента, такое как замедленное или пролонгированное выделение, с применением методов, известных в данной области техники. Жидкие дозированные формы для перорального введения включают растворы, эмульсии, суспензии, сиропы и эликсиры. Фармацевтические композиции для парентерального введения включают стерильные водные и не водные растворы, дисперсии, суспензии или эмульсии для инъекций, а также стерильные порошки, восстанавливаемые в виде стерильных растворов или дисперсий для инъекций непосредственно перед применением. Композиции для инъекций длительного хранения также включены в объем данного изобретения. Другие подходящие формы для введения включают суппозитории, спреи, мази, кремы, гели, средства для ингаляции, кожные пластыри, имплантаты и т.д. В одном из вариантов фармацевтических композиций соединение в соответствии с данным изобретением вводят в количестве от около 0,001 до около 100 мг/кг массы тела в день. Подходящим образом, соединения в соответствии с данным изобретением вводят в единичной дозированной форме, содержащей указанные соединения в количестве от около 0,01 до 100 мг. Общая суточная доза обычно составляет от около 0,05 до 500 мг. Обычная пероральная доза составляет от около 0,001 до около 100 мг/кг массы тела в день, предпочтительно от около 0,01 до около 50 мг/кг массы тела в день и более предпочтительно от около 0,05 до около 10 мг/кг массы тела в день при однократном или многократном введении, например 1-3 раза. Точная доза зависит от частоты и способа введения, пола, возраста, веса и общего состояния подлежащего лечению пациента, природы и тяжести излечиваемого состояния и каких-либо излечиваемых сопутствующих заболеваний, и других факторов, очевидных специалистам в данной области техники. Композиции могут быть подходящим образом сформированы в единичные дозированные формы методами, известными специалистам в данной области техники. Типовая единичная дозированная форма для перорального введения один или более раз в день, например 1-3 раза, может содержать от 0,01 до около 1000 мг, предпочтительно от около 0,05 до около 500 мг и более предпочтительно от около 0,5 до около 200 мг. Для парентерального введения, такого как внутривенный, интратекальный и подобные пути, типовые дозы составляют порядка половины от доз, применяемых для перорального введения. Соединения в соответствии с данным изобретением обычно применяют в виде свободных веществ или в виде их фармацевтически приемлемых солей. Одним из примеров является кислотно-аддитивная соль соединения, имеющего применение в виде свободного основания. Если соединение в соответствии с данным изобретением содержит свободное основание, такие соли получают обычным методом, обрабатывая раствор или суспензию свободного основания в соответствии с данным изобретением химическим эквивалентом фармацевтически приемлемой кислоты. Характерные примеры представлены выше. Для парентерального введения могут применяться растворы соединения в соответствии с данным изобретением в стерильном водном растворе, водном пропиленгликоле, водном витамине E или конопляном или арахисовом масле. Такие водные растворы могут, при необходимости, содержать подходящие буферы и жидкий разбавитель сначала делают изотоническим добавлением достаточного количества физиологического раствора или глюкозы. Водные растворы особенно подходят для внутривенного,внутримышечного, подкожного и внутрибрюшинного введения. Применяемая стерильная водная среда легко доступна стандартными методами, известными специалистам в данной области техники. Подходящие фармацевтические носители включают инертные твердые разбавители или наполнители, стерильные водные растворы и различные органические растворители. Примеры твердых носителей включают лактозу, белую трубочную глину, сахарозу, циклодекстрин, тальк, желатин, агар, пектин, аравийскую камедь, стеарат магния, стеариновую кислоту и низшие простые алкилэфиры целлюлозы. При- 22009477 меры жидких носителей включают сироп, арахисовое масло, оливковое масло, фосфолипиды, жирные кислоты, амины жирных кислот, полиоксиэтилен и воду. Также носитель или разбавитель может содержать любой материал замедленного выделения, известный в данной области техники, такой как глицерилмоностеарат или глицерилдистеарат, в чистом виде или в смеси с воском. Фармацевтические композиции, полученные объединением соединения в соответствии с данным изобретением и фармацевтически приемлемых носителей, легко вводятся в различных формах дозирования для описанных путей введения. Композиции могут быть представлены в единичных дозированных формах с применением методов, известных в области фармации. Композиции в соответствии с данным изобретением, подходящие для перорального введения, могут быть представлены в виде отдельных единиц, таких как капсулы или таблетки, каждая из которых содержит предварительно определенное количество активного ингредиента, и которые могут содержать подходящий наполнитель. Далее, композиции для перорального введения могут быть в виде порошков или гранул, раствора или суспензии в водной или не водной жидкости, или жидкой эмульсии масло-вводе или вода-в-масле. Если для перорального введения применяют твердый носитель, препаративная форма может быть в виде таблетки, помещенного в твердую желатиновую капсулу порошка или гранул, или она может быть в виде таблетки или пастилки. Количество твердого носителя может варьироваться в значительных пределах, но обычно составляет от около 25 мг до около 1 г. Если применяется жидкий носитель, композиция может быть в виде сиропа, эмульсии, мягких желатиновых капсул или стерильного раствора для инъекций, такого как водная или неводная жидкая суспензия или раствор. Фармацевтические композиции в соответствии с данным изобретением могут быть получены обычными методами, известными из уровня техники. Например, таблетки могут быть получены смешиванием активного ингредиента с обычными адъювантами и/или разбавителями с последующим прессованием смеси в обычной машине для получения таблеток. Примеры адъювантов или разбавителей включают кукурузный и картофельный крахмал, тальк,стеарат магния, желатин, лактозу, смолы и т.п. Любые другие адъюванты или добавки, обычно применяемые для этих целей, такие как красители, вкусовые добавки, консерванты и т.д., могут применяться при условии, что они совместимы с активными ингредиентами. Растворы для инъекций могут быть получены растворением активного ингредиента и возможных добавок в части растворителя для инъекций, предпочтительно, стерильной воде, доведением раствора до желаемого объема, стерилизацией раствора и помещением его в подходящие ампулы или флаконы. Могут быть добавлены любые подходящие добавки, обычно применяемые в данной области техники, такие как тонусные агенты, консерванты, антиокислители и т.д. Типовые примеры рецептов получения композиций в соответствии с данным изобретением представлены ниже. 1. Таблетки, содержащие 5,0 мг соединения в соответствии с данным изобретением, рассчитанного как свободное основание: Соединение 5,0 мг Лактоза 60 мг Кукурузный крахмал 30 мг Гидроксипропилцеллюлоза 2,4 мг Микрокристаллическая целлюлоза 19,2 мг Кросскармеллоза натрия тип A 2,4 мг Стеарат магния 0,84 мг 2. Таблетки, содержащие 0,5 мг соединения в соответствии с данным изобретением, рассчитанного как свободное основание: Соединение 0,5 мг Лактоза 46,9 мг Кукурузный крахмал 23,5 мг Повидон 1,8 мг Микрокристаллическая целлюлоза 14,4 мг Кросскармеллоза натрия тип А 1,8 мг Стеарат магния 0,63 мг 3. Сироп, содержащий на 1 мл: Соединение 25 мг Сорбит 500 мг Гидроксипропилцеллюлоза 15 мг Глицерин 50 мг Метилпарабен 1 мг Пропилпарабен 0,1 мг Этанол 0,005 мл- 23009477 Вкусовая добавка 0,05 мг Сахарин натрия 0,5 мг Вода до 1 мл 4. Раствор для инъекций, содержащий на 1 мл: Соединение 0,5 мг Сорбит 5,1 мг Уксусная кислота 0,05 мг Сахарин натрия 0,5 мг Вода до 1 мл Способы получения соединений в соответствии с данным изобретением Соединения в соответствии с данным изобретением могут быть получены следующим образом. Метод 1. Алкилирование амина формулы (III) алкилирующим производным формулы (II): где R1-R36, n и Q такие, как определены выше, и L является уходящей группой, такой как, например, галоген, мезилат или тозилат. Метод 2. Восстановительное алкилирование амина формулы (III) реагентом формулы (IV): где R3-R36, n и Q такие, как определены выше, и E является альдегидом или активированной карбоновой кислотой. Метод 3. Взаимодействие амина формулы (VI) с метиловым эфиром формулы (VI) с применением катализатора на основе кислоты Льюиса: где R1-R36, n и Q такие, как определены выше. Метод 4. Взаимодействие амина формулы (VI) с кислотой формулы (VIII) с применением активирующего реагента или конденсирующего реагента:- 24009477 Метод 5. Восстановление амина формулы (IX): где R1-R36, n и Q такие, как определены выше. Соединение формулы (I) выделяют в виде свободного основания или фармацевтически приемлемой кислотно-аддитивной соли. Алкилирование по методу 1 проводят в органическом растворителе, таком как спирт или кетон с подходящей температурой кипения, предпочтительно в присутствии органического или неорганического основания (карбонат калия, диизопропилэтиламин или триэтиламин) при температуре кипения с обратным холодильником. Альтернативно, алкилирование может быть проведено при фиксированной температуре, которая отличается от температуры кипения в одном из указанных выше растворителей или в диметилформамиде (ДМФ), диметилсульфоксиде (ДМСО) или N-метилпирролидин-2-оне (NMP), предпочтительно в присутствии основания. Алкилирующие производные формулы (II) с n=0 описаны в литературе и могут быть получены аналогичным методом, например Shuto et al. J. Org. Chem. 1996, 61,915 и Ronsisvalle et al. Biorg. Med. Chem. 2000, 8, 1503 и Bonnaud et al. J. Med. Chem. 1987, 30, 318. Алкилирующие производные формулы (II) с n=1 и n=2 могут быть получены из алкилирующих производных формулы (II) с n=0 стандартными методами удлинения цепи, например замещением бромида формулы (II) с n=0 цианидом с последующим гидролизом, восстановлением до спирта и превращением в уходящую группу L с получением алкилирующих производных формулы (II) с n=1. Соответственно, алкилирующие производные формулы (II) с n=2 могут быть получены замещением бромида формулы (II) сn=0 производным малонового эфира с последующим гидролизом, декарбоксилированием, восстановлением до спирта и превращением в уходящую группу L. Стандартные методы удлинения цепи описаны в литературе, например в Houben-Weyl, Methoden der organischen Chemie (Methods of Organic Chemistry),Georg-Thieme-Verlag, Stuttgart; или Organic Reactions, John WileySons, Inc. New York, а именно, проводятся в таких условиях реакции, которые известны и подходят для таких реакций. Амины формулы (III) являются либо коммерчески доступными, или могут быть получены методами, аналогичными тем, которые описаны в литературе, например в Marxer et al., J. Org. Chem. 1975, 40,1427, Parham et al. J. Org. Chem. 1976, 41, 2628 и Bauer et al. J. Med. Chem. 1976, 19, 1315, Maligres et al.Tetrahedron 1997, 53, 10983 и Cheng et al. Tet. Lett. 1997, 38, 1497, Chen, Meng-Hsin; Abraham, John A. Tetrahedron Lett. 1996, 37, 5233-5234 и Slade, P.D. et al. J. Med. Chem. 1998, 41, 1218-1235 или методами,описанными в примерах или аналогичными методами. Восстановительное алкилирование по методу 2 проводят методами, описанными в стандартной литературе. Альдегиды или кислоты формулы (IV) могут быть получены методами, аналогичными тем,которые описаны в Shuto et al. J. Org. Chem. 1996, 61, 915 и Shuto et al. J. Med. Chem. 1996, 38, 2964 иShuto et al. J. Chem. Soc., Perkin Trans 1, 2002, 1199 и Bonnaud et al. J. Med. Chem. 1987, 30, 318. Реакция может проводиться в две стадии, например, конденсацией аминов формулы (III) с реагентом формулы (IV) стандартными методами через хлорангидрид, активированные сложные эфиры карбоновой кислоты или с применением карбоновых кислот в сочетании со связующими реагентами, такими как,например, дициклогесилкарбодиимид, с последующим восстановлением полученного амида с алюмогидридом лития или аланом. Альтернативно, реакция может быть проведена в одну стадию восстановительным аминированием альдегида формулы (IV) с амином формулы (III) методами, описанными в стандартных трудах, таких как Houben-Weyl, Methoden der organischen Chemie (Methods of OrganicChemistry), Georg-Thieme-Verlag, Stuttgart; Organic Reactions, John WileySons, Inc. New York, а именно,в таких условиях реакции, которые известны и подходят для таких реакций. Ацилирование амина формулы (IV) в методе 3 сложным эфиром формулы (VII) может быть проведено методами, аналогичными тем, которые описаны в литературе, например, Lesimple et al. Synthesis 1991, 306. Амины формулы (VI) либо являются коммерчески доступными, либо могут быть получены методами, известными в литературе, методами, описанными в стандартных трудах, таких как HoubenWeyl, Methoden der organischen Chemie (Methods of Organic Chemistry), Georg-Thieme-Verlag, Stuttgart;Organic Reactions, John WileySons, Inc. New York, а именно, в таких условиях реакции, которые известны и подходят для таких реакций, и сложные эфиры формулы (VII) могут быть получены методами,аналогичными тем, которые описаны в литературе, например, Shuto et al. J. Org. Chem. 1996, 61, 915 иRonsisvalle et al. Biorg. Med. Chem. 2000, 8, 1503 и Bonnaud et al. J. Med. Chem. 1987, 30, 318. Ацилирование амина формулы (VI) в методе 4 кислотой формулы (VIII) может быть проведено стандартными методами через хлорангидрид, активированные сложные эфиры карбоновой кислоты или- 25009477 с применением карбоновых кислот в сочетании с конденсирующим реагентом, таким как дициклогексилкарбодиимид, карбонилдиимидазол или бензотриазол-1-илокситрис-(диметиламино)фосфония гексафторфосфат, как описано в стандартных трудах, например Bodanszky The practice of peptide synthesis,1994 Springer Verlag Berlin, ISBN 3-540-57505-7 и Houben-Weyl, Methoden der organischen ChemieNew York. Кислота формулы (VIII) может быть получена стандартным основным гидролизом сложного эфира, описанного в методе 3 и в примерах. Восстановление амина (IX) в методе 5 может проводиться стандартными методами, например, гидрированием в аппарате Парра (температура окружающей среды, 3 атм. Н 2) и добавлением катализатора,например, катализатора Крабтри ([(1,5-циклооктадиен)(пиридин)(трициклогексилфосфин)иридия(I) гексафторфосфат]), палладия или оксида платины. Амин формулы (IX) может быть получен по методике,описанной в методе 2, с применением оксоалкенильного соединения формулы (X), которое может быть получено реакцией Виттига между альдегидом формулы (IVa) и реагентом Виттига, полученным из Представленное здесь изобретение далее иллюстрировано не ограничивающими примерами. Примеры Общие методы. Температуры плавления определяют на аппарате Bchi SMP-20 и не корректируют. Аналитические данные ЖХ-МС определяют с помощью инструмента PE Sciex API 150EX, оборудованного источникомIonSpray и системой ЖХ Shimadzu LC-8A/SLC-10A. Условия ЖХ (С 18 колонка 4,630 мм с размером частиц 3,5 мкм) включают линейный градиент элюирования от вода/ацетонитрил/трифторуксусная кислота (90:10:0,05) до вода/ацетонитрил/трифторуксусная кислота (10:90:0,03) за 4 мин при 2 мл/мин. Чистоту определяют введением УФ-детекции (254 нм). Время удерживания Rt выражено в минутах. Масс-спектр получают методом переменного сканирования с получением информации о молекулярной массе. Молекулярный ион MH+ получают при низком напряжении на выходе (5-20 B) и фрагментации при высоком напряжении на выходе (100-200 В). Препаративное разделение ЖХ-МС проводят с применением того же оборудования. Условия ЖХ(C18 колонка 2050 мм с размером частиц 5 мкм) включают линейный градиент элюирования от вода/ацетонитрил/трифторуксусная кислота (80:20:0,05) до вода/ацетонитрил/трифторуксусная кислота(5:95:0,03) за 7 мин при 22,7 мл/мин. Сбор фракций проводят путем двухпоточного MC определения. 1H ЯМР спектр записывают при 500,13 МГц на приборе Bruker Avance DRX 500 или при 250,13 МГц на приборе Bruker AC 250. Дейтерированный хлороформ (99,8% D) или диметилсульфоксид(99,9% D) применяют в качестве растворителей. TMS применяют в качестве внутреннего стандарта. Значения химического сдвига выражают в частях на миллион (ч./млн). Следующие сокращения применяют для обозначения множеств ЯМР сигналов: с=синглет, д=дублет, т=триплет, кв.=квартет, кви=квинтет,г=гептет, дд=двойной дублет, дт=двойной триплет, т=триплет триплетов, м=мультиплет. ЯМР сигналы,соответствующие протонам кислоты, обычно пропускают. Для хроматографии на колонке применяют силикагель типа Kieselgel 60, 230-400 меш ASTM. Для ионообменной хроматографии применяют (SCX,1 г, Varian Mega Bond Elut, Chrompack кат.220776). Перед применением колонку SCX предварительно обрабатывают 10% раствором уксусной кислоты в метаноле (3 мл). Энантиомерную чистоту измеряют с помощью капиллярного электрофореза. Капиллярная длина 48,5 см 50 мкм В.Д. при 30 С с применением фиксированного тока 80 мкА. Применяемый буфер 25 мМ гидрофосфата натрия рН 3,0, содержащий 4% (мас./об.) сульфированного -циклодекстрина. Определение проводят с помощью УФ-спектрометра при 192 нм. Концентрация образца составляет 500 мкг/мл в метаноле и впрыскивание проводят под давлением 50 мбар в течение 5 с. Альтернативно, энантиомерную чистоту измеряют хиральной ВЭЖХ с применением системы хроматографии со сверхкритической жидкостью Gilson SF3, оборудованной колонками chiralcelOD(4,6 мм 25 см для аналитического и 10 мм 25 см для препаративного прогона). Размер частиц в колон- 26009477 ках составляет 10 мкм. Колонку элюируют двуокисью углерода - модификатором (75:25). Модификатором является 2-пропанол с диэтиламином (0,5%) и трифторуксусной кислотой (0,5%). Поток составляет 18,9 мл/мин при 30 МПа. Сбор фракций инициируется УФ-определением (210 нМ). Получение промежуточных соединений. Пример 1. Синтез рацемического 1-(3,4-дифторфенил)-3-окса-бицикло[3.1.0]гексан-2-она.(200 мл). Добавляют карбонат калия (61 г, 0,45 моль) и смесь перемешивают при комнатной температуре(кт) в течение 15 мин. Добавляют аллилбромид (47 г, 0,39 моль) и суспензию перемешивают при комнатной температуре в течение 20 ч. Смесь выливают в воду (250 мл) и экстрагируют диэтиловым эфиром(2300 мл). Объединенные органические фазы промывают водой (4100 мл), сушат (сульфат магния) и выпаривают в вакууме с получением 64 г (3,4-дифторфенил)уксусной кислоты аллилового эфира в виде прозрачного масла.(3,4-Дифторфенил)уксусной кислоты аллиловый эфир (64 г) растворяют в ацетонитриле (400 мл) и добавляют 4-ацетамидобензолсульфонилазид (p-ABSA, 87 г, 0,36 моль) и смесь перемешивают при комнатной температуре в течение 15 мин. Затем смесь охлаждают до температуры 0C и по каплям добавляют 1,8-диазабицикло[5.4.0]ундец-7-ен (DBU, 58,6 мл) при температуре 0C в течение 30 мин. Смесь нагревают до кт (комнатной температуры) и перемешивают при кт в течение 4-20 ч (до тех пор, покаTCX не покажет завершение реакции). Добавляют насыщенный хлорид аммония (500 мл) и органическую фазу отделяют от водной фазы. Водную фазу экстрагируют диэтиловым эфиром (3200 мл) и четыре объединенные органические фазы сушат (сульфат магния) и выпаривают в вакууме. Полученное твердое вещество экстрагируют 50:50 смесью диэтилового эфира/пентана (3200 мл). Объединенные эфирные фазы выпаривают в вакууме (сохраняя температуру ниже 40C) и очищают флэш-хроматографией на колонке (силикагель, элюент: 10:90 смесь диэтилового эфира/пентана). Желтые фракции объединяют и выпаривают в вакууме (сохраняя температуру ниже 40C) с получением 70 г диазо(3,4 дифторфенил)уксусной кислоты аллилового эфира. Диазо(3,4-дифторфенил)уксусной кислоты аллиловый эфир (70 г) растворяют в дихлорметане(1000 мл) и медленно добавляют в течение 36 ч через поршневой шприц (альтернативно, его добавляют по каплям через дополнительную воронку; 30 мл/ч) к кипящему с обратным холодильником раствору димера октаноата родия(II) (1,17 г, 1,5 ммоль) в дихлорметане (200 мл). После добавления всего диазосоединения смесь кипятят с обратным холодильником в течение еще 30 мин, затем выпаривают в вакууме и кристаллизуют добавлением циклогексана (200 мл). Это дает 30 г кристаллического вещества. Затем 15 г выделяют из маточной жидкости повторным выпариванием и кристаллизацией с получением всего 45 г 1-(3,4-дифторфенил)-3-окса-бицикло[3.1.0]гексан-2-она. Следующие соединения получают по той же методике: 1-(3,4-дихлорфенил)-3-окса-бицикло[3.1.0]гексан-2-он,1-(4-хлорфенил)-3-окса-бицикло[3.1.0]гексан-2-он,1-(4-фторфенил)-3-окса-бицикло[3.1.0]гексан-2-он,1-фенил-3-окса-бицикло[3.1.0]гексан-2-он. Пример 2. Синтез (1S,5R)-1-(3,4-дихлорфенил)-3-окса-бицикло[3.1.0]гексан-2-она. Раствор 3,4-дихлорфенилацетонитрила (62 г, 332 ммоль) в бензоле (250 мл) медленно добавляют к суспензии амида натрия (28,1 г, 720 ммоль) в бензоле (250 мл) при температуре 0C в атмосфере аргона и смесь перемешивают при комнатной температуре в течение 3 ч. К полученной смеси добавляют раствор(R)-эпихлоргидрина (30,1 г, 288 ммоль) в бензоле (250 мл) при температуре 0C в течение 45 мин и смесь перемешивают при комнатной температуре в течение 16 ч. После выпаривания растворителя к остатку добавляют EtOH (1250 мл) и 2N NaOH (500 мл), и смесь нагревают при температуре кипения с обратным холодильником в течение 15 ч, затем подкисляют 12 N HCl при температуре 0C (рН смеси около 1). Полученную смесь выпаривают и к остатку добавляют AcOEt (900 мл). Нерастворимые соли отфильтровывают и фильтрат промывают насыщенным раствором соли, сушат (Na2SO4) и выпаривают. Остаток очищают хроматографией на колонке (силикагель; AcOEt/гептан, 20:80) с получением продукта в виде оранжевых кристаллов (31,2 г, 39%).H-ЯМР (500 МГц, ДМСО-d6) 1,38 (1H, дд), 1,75 (1H, дд), 2,85 (1H, ддд), 4,25 (1H, д), 4,46 (1H, дд),7,45 (1H, д), 7,65 (1H, д), 7,75 (1H, с). Следующие соединения получают по той же методике:(200 мл) добавляют AlCl3 (16,0 г, 120 ммоль) и затем смесь охлаждают до температуры 0C и медленно добавляют бензилметиламин (240 ммоль, в виде 2,0M раствора бензилметиламина в ТГФ). Смесь перемешивают при комнатной температуре в течение 24 ч и затем реакционную смесь гасят насыщенным водным NH4Cl. После добавления CH2Cl2 и Н 2 О полученную смесь разделяют. Органический слой промывают 1N HCl и насыщенным раствором соли, сушат (Na2SO4), выпаривают и очищают хроматографией на колонке (силикагель; AcOEt/гексан, 1:4) с получением(1S,2R)-2-гидроксиметил-1-фенилциклопропанкарбоновой кислоты бензилметиламида. Следующие соединения получают по той же методике:(2-хлорбензил)метиламид; Пример 4. Сложные эфиры формулы (VII).HBr/ледяной уксусной кислоте и нагревают до температуры 80C в течение 5 ч, охлаждают до комнатной температуры и выливают в 1300 мл ледяной воды и перемешивают при комнатной температуре в течение 16 ч. Осажденную кислоту выделяют фильтрацией, повторно растворяют в толуоле (1000 мл), сушат над безводным сульфатом магния и выпаривают в вакууме с получением 30 г промежуточного соединения(1S,2R)-2-(Бромметил)-1-(3,4-дихлорфенил)циклопропанкарбоновую кислоту (30 г) растворяют в безводном толуоле (200 мл) и по каплям добавляют тионилхлорид (18 мл) в течение 15 мин, после чего смесь кипятят с обратным холодильником в течение 60 мин. Реакционную смесь охлаждают до температуры 5 С и добавляют метанол (200 мл), смесь нагревают да комнатной температуры и перемешивают- 28009477 при комнатной температуре в течение 2 ч. Смесь выпаривают в вакууме, повторно растворяют в диэтиловом эфире, промывают насыщенным водным гидрокарбонатом натрия (25 мл), насыщенным раствором соли (25 мл), сушат над безводным сульфатом магния и выпаривают в вакууме. Получают промежуточное соединение (1S,2R)-2-(бромметил)-1-(3,4-дихлорфенил)циклопропанкарбоновой кислоты метиловый эфир (27 г).(15 ммоль) растворяют в ацетонитриле (50 мл) и добавляют к смеси амина формулы (III) (15 ммоль) в смеси ацетонитрила (50 мл) и этилдиизопропиламина (30 ммоль). Смесь перемешивают при комнатной температуре в течение 16 ч, выпаривают в вакууме, помещают в этилацетат (200 мл) и последовательно промывают насыщенным водным гидрокарбонатом натрия (50 мл) и насыщенным раствором соли(50 мл), сушат над безводным сульфатом магния и выпаривают в вакууме с получением неочищенного продукта сложного эфира формулы (VII). Сложные эфиры формулы (VII) обычно очищают осаждением оксалата из ацетона. Другие сложные эфиры формулы (VII) могут быть получены по данной методике с применением соответствующим образом замещенного (1S,5R)-1-арил-3-окса-бицикло[3.1.0]гексан-2-она и амина формулы (III). Пример 5. Кислоты формулы (VIII). Оксалат(1S,2R)-2-(4-ацетиламино-4-фенилпиперидин-1-илметил)-1-(3,4-дихлорфенил)циклопропанкарбоновой кислоты метилового эфира (10 ммоль) растворяют в метаноле (80 мл) и воде (20 мл). Добавляют гидроксид лития (50 ммоль) и смесь нагревают до температуры кипения с обратным холодильником в течение 2 ч. Смесь охлаждают до комнатной температуры и подкисляют до рН 3 концентрированной хлористо-водородной кислотой и осажденный продукт (1S,2R)-2-(4-ацетиламино-4 фенилпиперидин-1-илметил)-1-(3,4-дихлорфенил)циклопропанкарбоновой кислоты гидрохлорид выделяют фильтрацией и сушат в вакууме. Другие кислоты формулы (VIII) получают по этой методике с применением соответствующим образом замещенных сложных эфиров формулы (VII). Пример 6. Пиперидины формулы (III). Спиропиперидиновые производные HQ формулы (vii), где X является кислородом, Z являетсяBauer et al. J. Med. Chem. 1976, 19, 1315. Следующие соединения получают по той же методике: 6-фторспиро[изобензофуран-1(3H),4'-пиперидин],6-трифторметилспиро[изобензофуран-1(3 Н),4'-пиперидин],6-фтор-3-метилспиро[изобензофуран-1(3 Н),4'-пиперидин],6-трифторметил-3-метилспиро[изобензофуран-1(3 Н),4'-пиперидин],5-метилспиро[изобензофуран-1(3 Н),4'-пиперидин],6-фтор-3-изобутилспиро[изобензофуран-1(3 Н),4'-пиперидин],6-фтор-3-циклогексилспиро[изобензофуран-1(3 Н),4'-пиперидин] и 6-фтор-3-(4-фторфенил)спиро[изобензофуран-1(3 Н),4'-пиперидин]. Спиропиперидиновые производные HQ формулы (vii), где X является CR27R28, Z является NR26, Y является связью, получают по методикам, описанным в Maligres et al. Tetrahedron 1997, 53, 10983 и Chenget al. Tet. Lett. 1997, 38, 1497. Следующие соединения получают по той же методике: 1-ацетил-5-фторспиро[2,3-дигидро-1 Н-индол-3,4'-пиперидин],1-ацетилспиро[2,3-дигидро-1 Н-индол-3,4'-пиперидин],1-метансульфонилспиро[2,3-дигидро-1 Н-индол-3,4'-пиперидин]. Спиропиперидиновые производные HQ формулы (vii), где X является CR27R28, Z является кислородом, Y является связью, например 2,3-дигидроспиро(бензофуран-3,4'-пиперидины), получают по методикам, описанным в Chen, Meng-Hsin; Abraham, John A. Tetrahedron Lett. 1996, 37, 5233-5234 и Slade, P.D. etal. J. Med. Chem. 1998, 41, 1218-1235. Следующие соединения получают по той же методике: 2,3-дигидро-5-фторспиро[бензофуран-3,4'-пиперидин] и 2,3-дигидро-5,6-дифторспиро[бензофуран-3,4'-пиперидин]. Заместители R33-R36 получают при применении подходящим образом замещенных исходных соединений по методикам, аналогичным представленным выше. Пример 7. 1-(трет-Бутоксикарбонил)-4-изоцианато-4-фенилпиперидин. Триэтиламин (5,02 мл, 36,1 ммоль) и дифенилфосфорилазид (4,24 мл, 19,7 ммоль) добавляют к раствору 1-(трет-бутоксикарбонил)-4-фенил-4-пиперидинкарбоновой кислоты (5,0 г, 16,4 ммоль) в сухом ДМФ (50 мл) в атмосфере азота при температуре окружающей среды. Смесь перемешивают при температуре окружающей среды в течение 2 ч и затем нагревают до температуры 60C в течение 3 ч. Смесь слегка охлаждают и концентрируют в вакууме. К остатку добавляют воду (75 мл) с последующим экст- 29009477 рагированием этилацетатом (275 мл). Объединенные органические фракции промывают насыщенным раствором соли (350 мл), сушат(MgSO4) и выпаривают досуха. Неочищенный продукт очищают хроматографией на колонке с силикагелем, элюируя этилацетатом-гептаном (1:4). Это дает 4,8 г (98%) целевого 1-(трет-бутоксикарбонил)-4 изоцианато-4-фенилпиперидина в виде прозрачного масла. ЖХ-МС (m/z) 203,2 (M-boc+H+); tR=3,64 мин. 1(дд, 1H), 7,39 (дт, 2H), 7,44 (дд, 2H). Пример 8. Пиперидины формулы (III), в которых Q является (iii) и R12 является фенилом и R13 является группой -NHCONR20R21. 1-(трет-Бутоксикарбонил)-4-изоцианато-4-фенилпиперидин (1 ммоль) растворяют в безводном ТГФ и добавляют амин HNR20R21 (1 ммоль), смесь перемешивают при комнатной температуре в течение 16 ч,выпаривают в вакууме и повторно растворяют в 50:50 смеси дихлорметана и трифторуксусной кислоты(10 мл) и перемешивают при комнатной температуре в течение 60 мин. Смесь выпаривают в вакууме с получением продукта пиперидина в виде соли трифторуксусной кислоты. Пример 9. Пиперидины формулы (III), в которых Q является (iii) и R12 является фенилом и R13 является H.N-(4-Фтор-2-пиперидин-4-илфенил)ацетамид гидрохлорид. 2-Бром-4-фторацетанилид (3,00 г, 12,9 ммоль) и пиридин-4-борную кислоту (1,60 г, 12,9 ммоль) растворяют в 1,2-диметоксиэтане (70 мл). Добавляют тетракис-(трифенилфосфин)палладий(0) (0,89 г, 0,77 ммоль) с последующим добавлением карбоната натрия (4,10 г, 38,7 ммоль), растворенного в воде (25 мл). Смесь нагревают при температуре кипения с обратным холодильником в течение 3 ч, затем перемешивают при температуре окружающей среды в течение ночи. Растворители выпаривают в вакууме, затем к остатку добавляют этилацетат (50 мл) и водный аммиак (разб.). Фазы разделяют и водный слой экстрагируют этилацетатом(250 мл). Объединенные органические фракции промывают насыщенным раствором соли, сушат(MgSO4), фильтруют и концентрируют выпариванием. Продукт очищают хроматографией на колонке с силикагелем,элюируя этилацетатом:гептаном:триэтиламиномN-(4-Фтор-2-пиридин-4-илфенил)ацетамид (2,37 г, 10,3 ммоль) растворяют в метаноле (40 мл), затем добавляют оксид платины (0,2 г, 0,88 ммоль) и ледяную уксусную кислоту (10 мл). Смесь гидрируют в аппарате Парра (температура окружающей среды, 3 атм. Н 2) в течение 24 ч. Катализатор удаляют фильтрацией через целит и смесь концентрируют в вакууме. Остаток растворяют в этилацетате (40 мл) и добавляют небольшое количество воды (10 мл). Водную фазу подщелачивают добавлением 2 М NaOH и слои разделяют. Водную фазу экстрагируют этилацетатом (230 мл), затем объединенные органические фракции промывают насыщенным раствором соли, сушат (MgSO4), фильтруют и концентрируют в вакууме. Гидрохлорид получают добавлением эфирного HCl к раствору неочищенного продукта в ацетоне. Осажденный продукт отфильтровывают и сушат в вакууме с получением 1,20 г (49%) указанного в заголовке соединения в виде белого кристаллического материала. ЖХ-МС (m/z) 237,0 (М+Н+). 1H-ЯМР (ДМСО-d6) 1,82 (м, 4H), 2,07 (с, 3H), 2,95 (м, 2H), 3,03 (м, 1H), 3,36 (м, 2H), 7,00 (дд, 1H),7,05 (дд, 1H), 7,28 (дд, 1H), 8,75-8, 91 (шир.д, 1H, NH, HCl), 9,48 (с, 1H, NH). Пример 10. (4-Фенилпиперидин-4-ил)пиперидин-1-илметанон. В потоке азота N,N'-карбонилдиимидазол (3,62 г, 22,3 ммоль), затем пиперидин (3,74 г, 43,9 ммоль) добавляют к раствору 1-(трет-бутоксикарбонил)-4-фенил-4-пиперидинкарбоновой кислоты (3,40 г,11,1 ммоль) в сухом ТГФ (50 мл). Смесь нагревают до температуры кипения с обратным холодильником в течение 18 ч, затем охлаждают до температуры окружающей среды и концентрируют выпариванием. Остаток повторно растворяют в этилацетате (150 мл) и последовательно промывают NaHCO3 (50 мл,водн., насыщ.), разбавляют HCl (50 мл) при рН 3, насыщенным раствором соли (50 мл), затем сушат(MgSO4) и выпаривают досуха. Это промежуточное соединение очищают хроматографией на колонке с силикагелем, элюируя этилацетатом-гептаном-триэтиламином (40:50:10) с получением 1,01 г (24%) 4-фенил-4-(пиперидин-1-карбонил)пиперидин-1-карбоновой кислоты трет-бутилового эфира в виде белого кристаллического твердого вещества. Вещество растворяют в смеси MeOH (10 мл) и ТГФ (10 мл),затем добавляют 2 М HCl в MeOH (5 мл) и смесь перемешивают при температуре окружающей среды в течение 2 ч. Добавляют воду (20 мл) и рН доводят до 12 добавлением 2 М NaOH. Органическую фазу отделяют и водную фазу экстрагируют этилацетатом (30 мл). Объединенные органические фракции сушат
МПК / Метки
МПК: C07D 211/32, C07D 211/58, C07D 211/52, C07D 471/20, A61K 31/495, C07D 211/64, A61P 25/00, C07D 211/14, A61K 31/435, C07D 471/10
Метки: качестве, циклопропила, антагонистов, рецептора, производные
Код ссылки
<a href="https://eas.patents.su/30-9477-proizvodnye-ciklopropila-v-kachestve-antagonistov-receptora-nk3.html" rel="bookmark" title="База патентов Евразийского Союза">Производные циклопропила в качестве антагонистов рецептора nk3</a>
Предыдущий патент: Фотоэлектрический элемент
Следующий патент: Ненуклеозидные ингибиторы обратной транскриптазы
Случайный патент: Корпус насоса


































