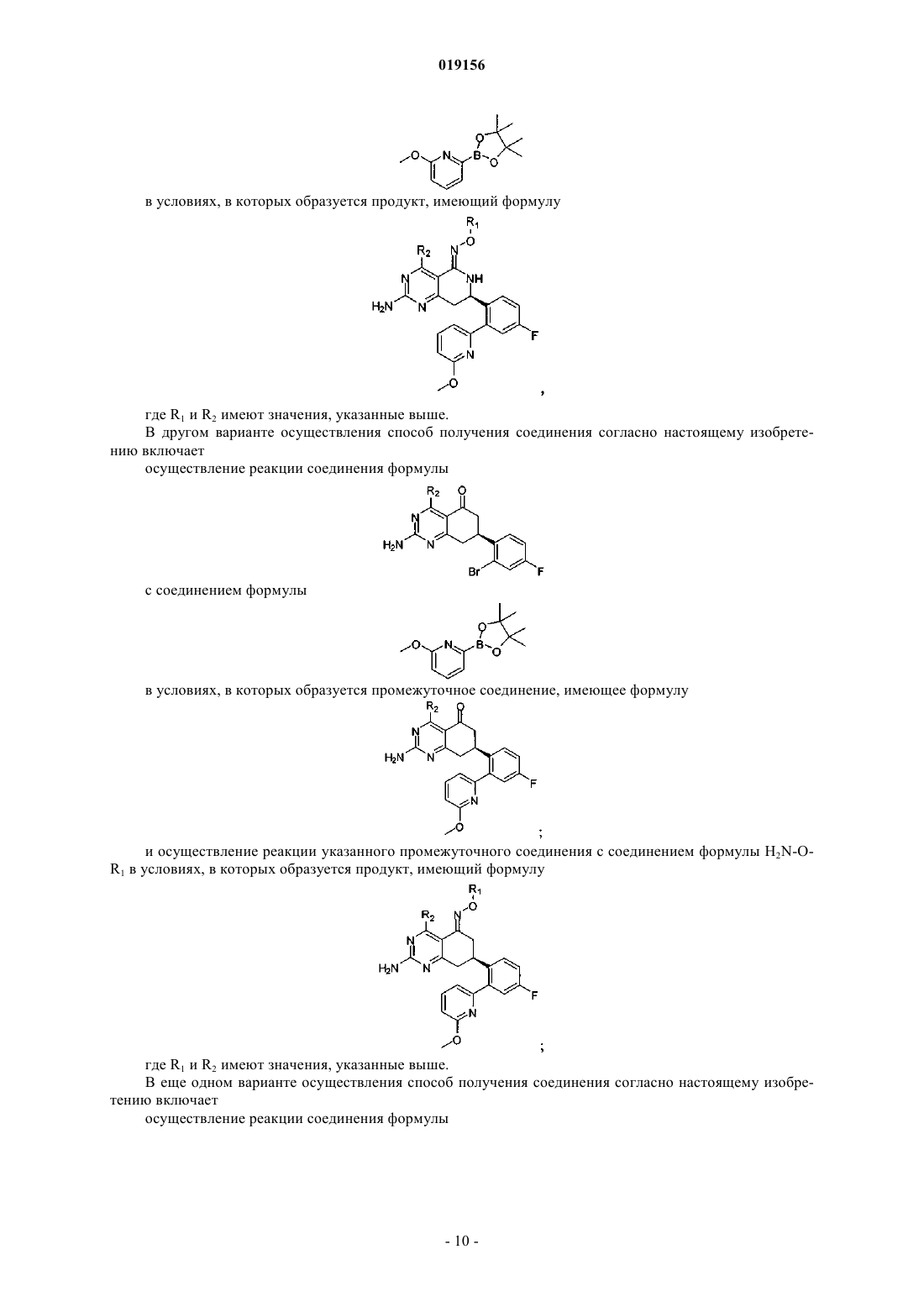
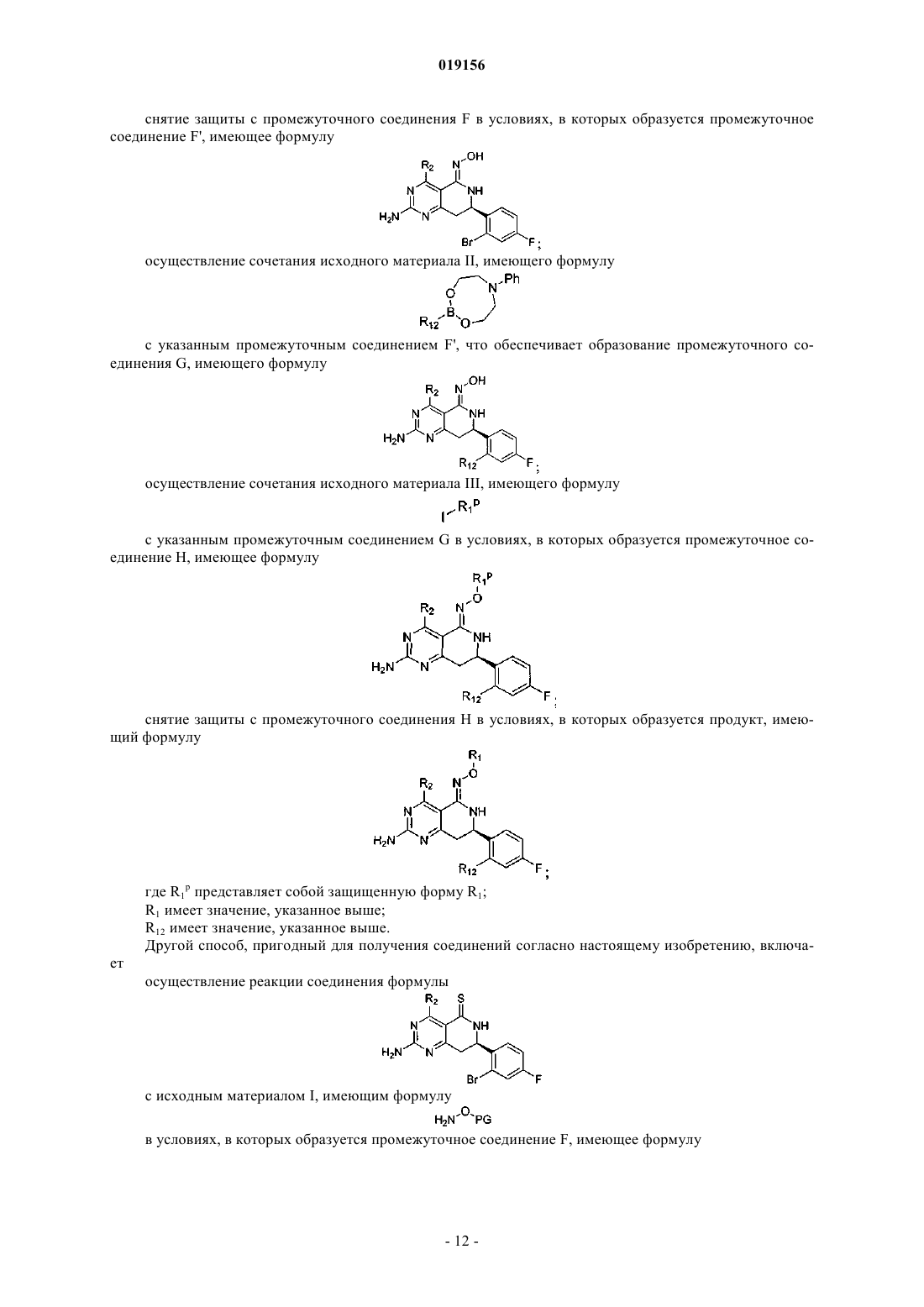
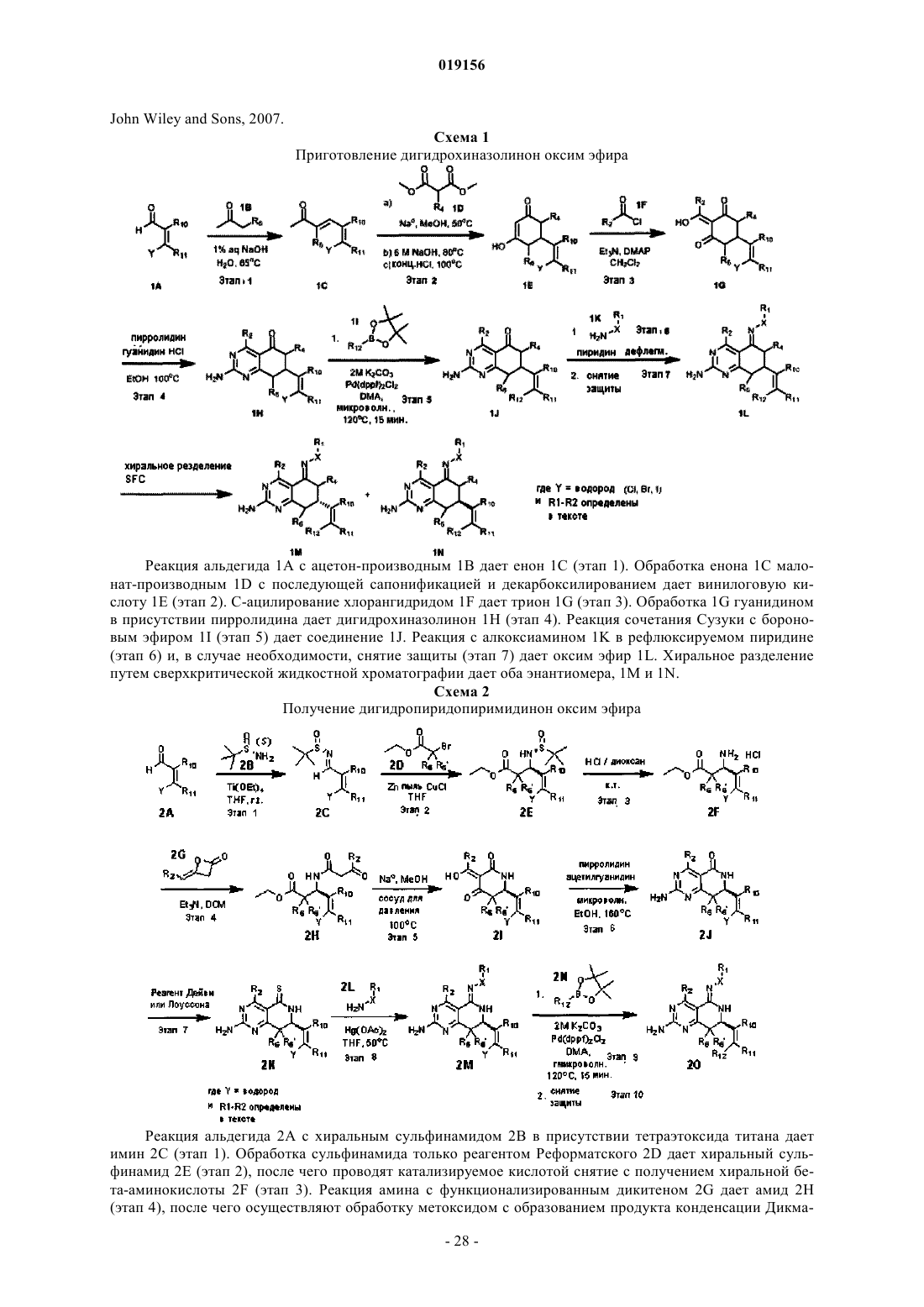
Производные оксима в качестве ингибиторов hsp90
Номер патента: 19156
Опубликовано: 30.01.2014
Авторы: Нотц Вольфганг Райнхард Людвиг, Чэнь Юн К., Ко Эрик Ван, Стаффорд Джеффри А., Гунтупалли Прасуна, Лосон Джон Дэвид, Тон-Ну Хуонг-Тху
Формула / Реферат
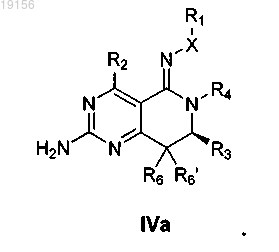
1. Соединение формулы
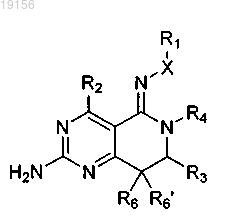
или его таутомер, стереоизомер или фармацевтически приемлемая соль, где
X представляет собой О;
R1 представляет собой -L-R45;
R2 выбран из группы, включающей водород и метил;
R3 выбран из группы, включающей
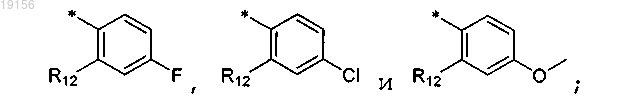
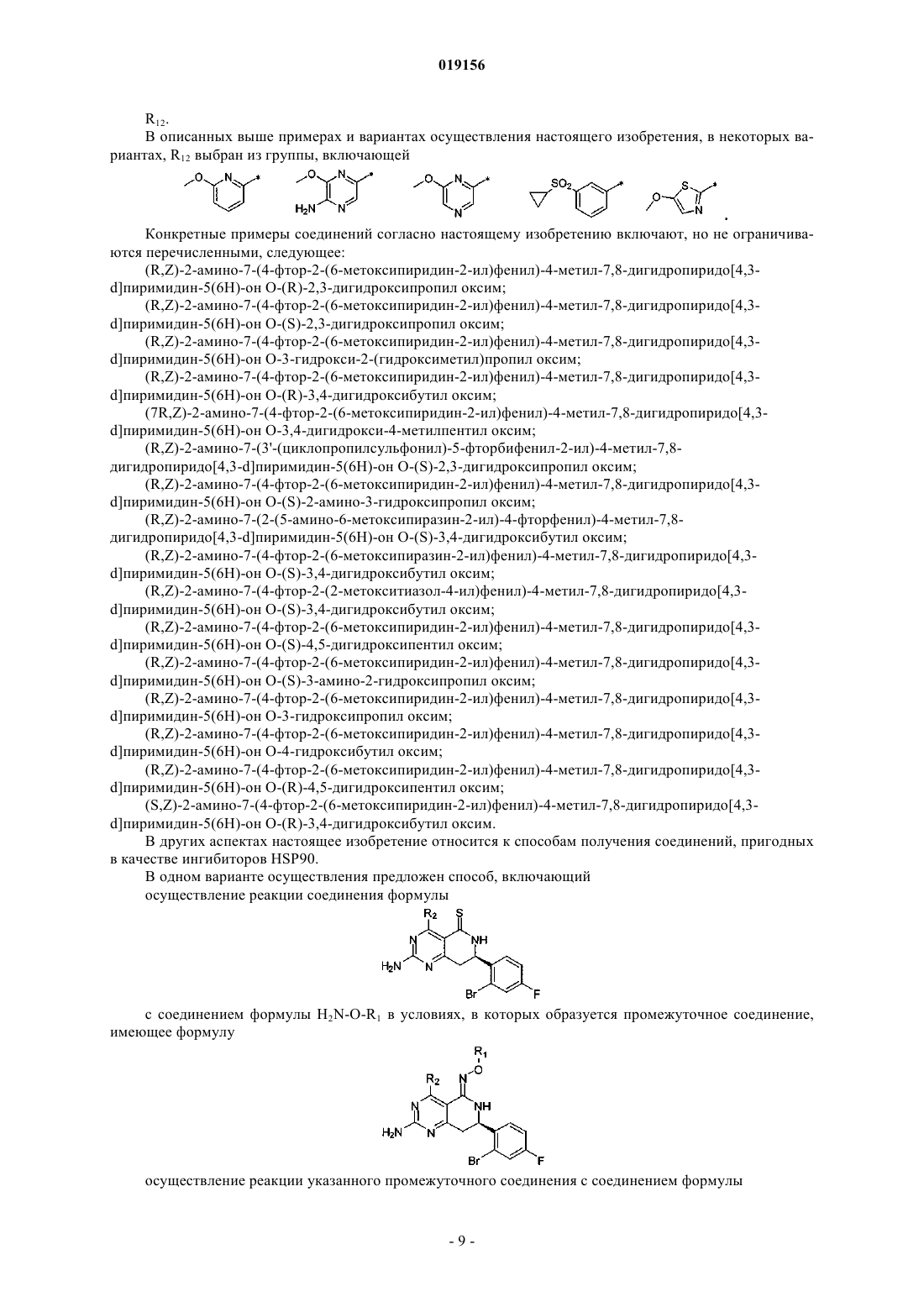
R12 выбран из группы, включающей
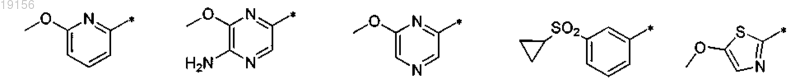
R4 представляет собой водород;
R6 и R6', оба, представляют собой водород;
R45 выбран из группы, включающей водород, амино и гидроксил;
L представляет собой (-CR46R47-)n;
n равно 1, 2, 3, 4 или 5;
R46 и R47, каждый независимо, выбраны из группы, включающей водород, гидроксил, амино, (С1-6)алкил и гидрокси(C1-6)алкил.
2. Соединение по п.1, имеющее формулу
3. Соединение по п.1 или 2, в котором L представляет собой (-CR46R47-)5.
4. Соединение по п.1 или 2, в котором L представляет собой (-CR46R47-)4.
5. Соединение по п.1 или 2, в котором L представляет собой (-CR46R47-)3.
6. Соединение по п.1 или 2, в котором L представляет собой (-CR46R47-)2.
7. Соединение по п.1 или 2, в котором L представляет собой -CR46R47-.
8. Соединение по п.1 или 2, в котором R2 представляет собой водород.
9. Соединение по п.1 или 2, в котором R2 представляет собой метил.
10. Соединение по п.1, выбранное из группы, включающей
(R,Z)-2-амино-7-(4-фтор-2-(6-метоксипиридин-2-ил)фенил)-4-метил-7,8-дигидропиридо[4,3-d]пиримидин-5(6H)-он О-(R)-2,3-дигидроксипропил оксим;
(R,Z)-2-амино-7-(4-фтор-2-(6-метоксипиридин-2-ил)фенил)-4-метил-7,8-дигидропиридо[4,3-d]пиримидин-5(6H)-он О-(S)-2,3-дигидроксипропил оксим;
(R,Z)-2-амино-7-(4-фтор-2-(6-метоксипиридин-2-ил)фенил)-4-метил-7,8-дигидропиридо[4,3-d]пиримидин-5(6H)-он О-3-гидрокси-2-(гидроксиметил)пропил оксим;
(R,Z)-2-амино-7-(4-фтор-2-(6-метоксипиридин-2-ил)фенил)-4-метил-7,8-дигидропиридо[4,3-d]пиримидин-5(6H)-он О-(R)-3,4-дигидроксибутил оксим;
(7R,Z)-2-амино-7-(4-фтор-2-(6-метоксипиридин-2-ил)фенил)-4-метил-7,8-дигидропиридо[4,3-d]пиримидин-5(6H)-он O-3,4-дигидрокси-4-метилпентил оксим;
(R,Z)-2-амино-7-(3'-(циклопропилсульфонил)-5-фторбифенил-2-ил)-4-метил-7,8-дигидропиридо[4,3-d]пиримидин-5(6H)-он О-(S)-2,3-дигидроксипропил оксим;
(R,Z)-2-амино-7-(4-фтор-2-(6-метоксипиридин-2-ил)фенил)-4-метил-7,8-дигидропиридо[4,3-d]пиримидин-5(6H)-он О-(R)-2-амино-3-гидроксипропил оксим;
(R,Z)-2-амино-7-(2-(5-амино-6-метоксипиразин-2-ил)-4-фторфенил)-4-метил-7,8-дигидропиридо[4,3-d]пиримидин-5(6H)-он O-(S)-3,4-дигидроксибутил оксим;
(R,Z)-2-амино-7-(4-фтор-2-(6-метоксипиразин-2-ил)фенил)-4-метил-7,8-дигидропиридо[4,3-d]пиримидин-5(6H)-он О-(S)-3,4-дигидроксибутил оксим;
(R,Z)-2-амино-7-(4-фтор-2-(2-метокситиазол-4-ил)фенил)-4-метил-7,8-дигидропиридо[4,3-d]пиримидин-5(6H)-он О-(S)-3,4-дигидроксибутил оксим;
(R,Z)-2-амино-7-(4-фтор-2-(6-метоксипиридин-2-ил)фенил)-4-метил-7,8-дигидропиридо[4,3-d]пиримидин-5(6H)-он О-(S)-4,5-дигидроксипентил оксим;
(R,Z)-2-амино-7-(4-фтор-2-(6-метоксипиридин-2-ил)фенил)-4-метил-7,8-дигидропиридо[4,3-d]пиримидин-5(6H)-он О-(S)-3-амино-2-гидроксипропил оксим;
(R,Z)-2-амино-7-(4-фтор-2-(6-метоксипиридин-2-ил)фенил)-4-метил-7,8-дигидропиридо[4,3-d]пиримидин-5(6H)-он O-3-гидроксипропил оксим;
(R,Z)-2-амино-7-(4-фтор-2-(6-метоксипиридин-2-ил)фенил)-4-метил-7,8-дигидропиридо[4,3-d]пиримидин-5(6H)-он O-4-гидроксибутил оксим;
(R,Z)-2-амино-7-(4-фтор-2-(6-метоксипиридин-2-ил)фенил)-4-метил-7,8-дигидропиридо[4,3-d]пиримидин-5(6H)-он О-(R)-4,5-дигидроксипентил оксим;
(S,Z)-2-амино-7-(4-фтор-2-(6-метоксипиридин-2-ил)фенил)-4-метил-7,8-дигидропиридо[4,3-d]пиримидин-5(6H)-он О-(R)-3,4-дигидроксибутил оксим.
11. Соединение по п.1, где соединение представляет собой (R,Z)-2-амино-7-(4-фтор-2-(6-метоксипиридин-2-ил)фенил)-4-метил-7,8-дигидропиридо[4,3-d]пиримидин-5(6H)-он О-(S)-3,4-дигидроксибутил оксим.
12. Соединение по п.1, где соединение представляет собой (R,Z)-2-амино-7-(4-фтор-2-(6-метоксипиридин-2-ил)фенил)-4-метил-7,8-дигидропиридо[4,3-d]пиримидин-5(6H)-он О-(R)-2,3-дигидроксипропил оксим.
13. Соединение по любому из пп.1-12, где соединение имеет форму фармацевтически приемлемой соли.
14. Соединение по любому из пп.1-13, где соединение присутствует в виде смеси стереоизомеров.
15. Соединение по любому из пп.1-13, где соединение представляет собой единственный стереоизомер.
16. Фармацевтическая композиция, содержащая в качестве активного ингредиента соединение по любому из пп.1-15 и фармацевтический наполнитель.
17. Применение соединения по любому из пп.1-15 в качестве лекарственного средства для ингибирования HSP90.
18. Применение соединения по любому из пп.1-15 для лечения рака, воспаления, воспалительного заболевания кишечника, псориаза, артрита и отторжения трансплантата.
Текст
Настоящее изобретение относится к соединениям, ингибирующим HSP90, имеющим формулу Чэнь Юн К., Ко Эрик Ван,Гунтупалли Прасуна, Лосон Джон Дэвид, Нотц Вольфганг Райнхард Людвиг, Стаффорд Джеффри А., ТонНу Хуонг-Тху (US)R4 представляет собой водород; R6 и R6', оба, представляют водород; R45 выбран из группы,включающей водород, амино и гидроксил; L представляет собой (-CR46R47-)n; n равно 1, 2, 3, 4 или 5; R46 и R47, каждый, независимо выбраны из группы, включающей водород, гидроксил, амино,(C1-6)алкил и гидрокси(C1-6)алкил. Настоящее изобретение также относится к фармацевтическим композициям и способам использования таких соединений.(71)(73) Заявитель и патентовладелец: ТАКЕДА ФАРМАСЬЮТИКАЛ КОМПАНИ ЛИМИТЕД (JP) Область техники Настоящее изобретение относится к соединениям, пригодным для ингибирования белка теплового шока 90 (HSP90), а также к композициям, наборам и изделиям, включающим такие соединения. Настоящее изобретение также относится к способам ингибирования HSP90 и способам лечения с использованием соединений согласно настоящему изобретению. Дополнительно, настоящее изобретение относится к способам получения соединений согласно настоящему изобретению, а также к промежуточным соединениям, которые можно применять в таких способах. В частности, настоящее изобретение относится к ингибиторам HSP90, композициям, наборам и изделиям, включающим такие соединения, способам ингибирования HSP90, а также способам и промежуточным соединениям для получения таких ингибиторов. Уровень техники Молекулярные шапероны поддерживают надлежащее свертывание и конформацию образующихся полипептидов. Данная активность критична для регуляции баланса между синтезом и разрушением белка. В случае повреждения белка молекулярные шапероны могут также способствовать повторному сворачиванию или, в случае необратимого повреждения белка, уничтожению такого белка клеточным механизмом разрушения белка 1. Белки теплового шока (HSP) первоначально определяли по повышенной экспрессии в ответ на воздействие различных повреждающих клетку факторов, таких как повышенная температура, а также воздействие тяжелых металлов и окислительный стресс 1. Большинство, но не все HSP представляют собой молекулярные шапероны, которые делят на семейства в соответствии с размером молекул и функцией,включая HSP100, HSP90, HSP70, HSP60, HSP40 и малые HSP. Быструю индукцию экспрессии гена HSP называют реакцией теплового шока (HSR), которая обеспечивает цитопротекцию при повторном воздействии повреждающего фактора, которое в противном случае вызвало бы летальное повреждение молекул. Цитопротекция является примером повышенной экспрессии молекулярного шаперона, связанной с функционированием нормальных клеток в организме. Однако абберантная экспрессия белков данного семейства может также быть связана с некоторыми болезненными состояниями. Существуют многочисленные свидетельства в пользу того, что молекулярные шапероны имеют значение для поддержания ракового фенотипа. Дополнительно, накапливающиеся свидетельства связи экспрессии молекулярных шаперонов с другими заболеваниями, включая, без ограничения, нейродегенеративные заболевания, включая болезнь Паркинсона, болезнь Альцгеймера, болезнь Хантингтона и прионные заболевания, воспаление и заболевания, связанные с воспалением, такие как боль, головные боли, лихорадка, артрит, астма, бронхит, тендинит, экзема, воспалительное заболевание кишечника и т.д., заболевания, зависящие от ангиогенеза, такие как рак, артрит, диабетическая ретинопатия, старческая дегенерация желтого пятна (AMD) и инфекционные заболевания, в частности грибковые инфекции,вирусные заболевания, включая, но не ограничиваясь перечисленными, заболевания, вызываемые вирусом гепатита В (HBV), вирусом гепатита С (HCV) и простым вирусом герпеса типа 1 (HSV-1), заболевания сердечно-сосудистой и центральной нервной системы 3, 4, 5, 6, 7.HSP90 представляет собой распространенный молекулярный шаперон, который составляет 1-2% общего белка клетки. Он осуществляет свою функцию шаперона, обеспечивая правильную конформацию, активность, локализацию внутри клетки и протеолитический оборот ряда белков, которые участвуют в росте, дифференцировке и выживании клеток 3, 5, 8. Поскольку было показано, что HSP90 ассоциирует с большим количеством важных сигнальных белков и способствует их стабилизации (такие белки обычно называют клиентами HSP90), существует логическое обоснование терапевтического применения ингибиторов HSP90 для лечения разнообразных заболеваний человека (как описано выше)9. АктивностьHSP90 необходима для стабилизации и функционирования многих онкогенных белков-клиентов, которые вносят свой вклад во все основные характеристики злокачественных процессов и соответственноHSP90 является широко признанной мишенью терапии при лечении рака 3, 4, 5, 8. Такие белки-клиенты включают, среди прочих, BCR-ABL, AKT/PKB, C-RAF, CDK4, рецепторы стероидных гормонов (эстрогена и андрогена), белки выживания, c-Met, HER-2 и теломеразы. Ингибирование функции HSP90 приводит к дестабилизации и разрушению белков-клиентов по убиквитин-протеасомному пути, что приводит к ослаблению сигналов, которые распространяются по онкогенным сигнальным путям и модулирования всех аспектов злокачественного фенотипа 3, 5, 8. Соответственно ингибиторы HSP90 обладают потенциалом для лечения рака, зависимого от разнообразных молекулярных аномалий и их совместное действие может также снижать способность к развитию устойчивости. Считают, что HSP90 осуществляет функцию шаперона в цикле, включающем координированные взаимодействия ряда белков, действующих совместно с шаперонами, которые вместе вовлечены в хорошо контролируемое, взаимно регулируемое взаимодействие с обменом АТФ/АДФ и гидролизом АТФ характерным и необходимым N-концевым АРФ-азным доменом. Кристаллографические исследования выявили, что некоторые ингибиторы HSP90 занимают N-концевой сайт связывания АТФ 10, что приводит к ингибированию АТФазной активности и функции HSP90. Вначале для 14-членного макроциклического антибиотика радицикола была продемонстрирована противоопухолевая активность in vitro, а также было показано, что он обращает злокачественный фенотип клеток, трансформированных v-SRC11. Впоследствии было с использованием рентгеновской кри-1 019156 сталлографии было показано, что радицикол связывается с N-концевым АТФ-связывающим карманомHSP90 с высокой аффинностью 10 и ингибирует АТФазную активность HSP90, что приводит к разрушению ряда сигнальных белков 12. Хотя радицикол подавляет рост опухолей in vitro, он не обладает активностью in vivo, наиболее вероятно, из-за наличия реактивной эпоксидной группы и других нежелательных химических особенностей, которые обуславливают нестабильность и возможную токсичность 8, 13. Бензохинон ансамицины являются вторым классом природных антибиотиков, для которых было продемонстрировано ингибирование активности HSP90. Первым примером является гелданамицин, который также конкурирует с АТФ за связывание с N-концевым сайтом связывания нуклеотидов HSP9014. Также как в случае с радициколом, несмотря на многообещающую противоопухолевую активность invitro (и in vivo), разработка средства для лечения людей на основе гелданамицина была прекращена из-за нестабильности и неприемлемой гепатотоксичности данного соединения в терапевтических дозах 15. С целью обнаружения средств с расширенными пределами безопасности для клинического применения,исследовали аналоги гелданамицина,включая производное 17-аллиламино-17 деметоксигелданамицин (17-AAG или танеспимицин)16. 17-AAG оказывает воздействием на клетки, подобное действию гелданамицина, включая разрушение белков-клиентов и блокирование клеточного цикла, но обладает повышенной метаболической стабильностью и более низкой токсичностью 5, 8. Доклинические исследования с использованием 17-AAG продемонстрировали высокую эффективность этого производного in vitro, а также его противоопухолевую активность в нетоксичных дозах в различных моделях с ксенографтами опухолей человека 17, 18. На основании биологической активности 17-AAG недавно прошел фазу I клинических испытаний с некоторыми обнадеживающими результатами 9, 19. В результате,к настоящему времени 17-AAG вступил во II фазу клинических испытаний в виде монотерапии для различных типов опухолей, включая меланому и рак груди. Существует несколько возможных факторов, которые могут снижать клиническую эффективность 17-AAG. Доклинические испытания показали, что метаболизм 17-AAG в печени под действием цитохрома Р 450 приводит к образованию 17-амино-17-деметоксигелданамицина (17-AG)17. Хотя 17-AG сохраняет ингибирующую активность, метаболизм под действием CYP3A4, вероятно, вызывает изменения в фармакокинетике. Кроме того, активность 17-AAG повышается в результате его перехода в форму гидрохинона, 17-AAGH2, под действием фермента-редуктазы NQO1 или DT-диафоразы 17, 20. Полиморфная экспрессия обоих указанных метаболических ферментов, возможно, накладывает ограничения на клиническое применение 17-AAG в популяции 5, 8, 17. Эффективность 17-AAG, возможно, также снижается его ассоциацией с белком множественной устойчивости к лекарствам MDR1 или Р-гликопротеином. Наконец, ограничения 17-AAG связаны с его низкой растворимостью, громоздкой и сложной конформацией и отсутствием биодоступности при пероральном введении. Попытки получить другую форму 17-AAG привели к началу клинических испытаний с CNF1010 и составом на основе кремафора (KOS-953), причем последний показал многообещающие результаты у пациентов с рецидивирующей рефрактерной миеломой. Национальный институт рака США и Kosan Biosciences также разработали более водорастворимый аналог 17-AAG, 17-диметиламиноэтиламино-17-деметоксигелданамицин (17-DMAG) или алвеспимицин (alvespimycin), который оценивали в доклинических и клинических испытаниях 9. 17-AAGH2,также известный как IPI-504, также вступил в клинические испытания в виде растворимого производного 17-AAG21. Недавно были описаны неприродные продукты, являющиеся ингибиторами HSP90. Один из таких продуктов содержит каркас 3,4-диарилпиразол резорцинола. Примерами таких молекул являются соединение ССТ 018159 и аналоги CCT0129397/VER-49009 и VER-50589. Обработка раковых клеток такими ингибиторами HSP90 вызвала индукцию HSP70, снижение количества белков-клиентов и апоптоз 22, 23, 24, 25.Chiosis et al.26 с использованием метода рациональной разработки лекарственных средств разработали новый класс ингибиторов HSP90 с пуриновым каркасом. Первое идентифицированное соединение из этого ряда, PU3, связывало HSP90 с умеренной аффинностью, вызывая клеточные эффекты, характерные для ингибиторов HSP90. Важным свойством PU3 является то, что он более растворим, чем 17-AAG; однако его эффективность в отношении клеток значительно ниже, чем у ансамицина 26. Дальнейшие усилия, направленные на повышение эффективности PU3, привели к идентификации PU24FCl27. Это соединение оказывало биологическое воздействие на клетку в диапазоне концентраций 2-6 мкМ 27 и также продемонстрировало в 10-50 раз более высокую аффинность к HSP90 из трансформированных клеток,чем к HSP90 из нормальных тканей 27. Применение PU24FCl в моделях с ксенографтами опухоли молочной железы человека обеспечило противоопухолевую активность без значительной токсичности 27. В более поздних исследованиях были идентифицированы производные PU 8-арилсульфанил, 8 арилсульфоксил и 8-арилсульфонил аденин, которые проявляли повышенную растворимость в воду и эффективность примерно 50 нМ в клеточных моделях, а также терапевтическую активность в моделях с ксенографтами опухолей человека 28. Также идентифицированы другие неприродные низкомолекулярные ингибиторы HSP90, включая соединения 2-амино-хиназолин-5-она (WO 2006113498 A2), 2-амино-7,8-дигидро-6 Н-пиридо[4,3d]пиримидин-5-она (WO 2007041362 A1) и производные хиназолин-оксима (WO 2008142720 A2), которые воздействуют на HSP90, обеспечивая профилактику или лечение заболеваний, связанных с пролифе-2 019156 рацией клеток. Эти молекулы обладают приемлемой эффективностью и лекарственными свойствами. Итоговые доклинические испытания обеспечили небольшие молекулы с приемлемыми лекарственными свойствами и в сочетании с итоговыми доклиническим исследованиями в рамках подхода ингибирования активности HSP90, достигаемого при использовании 17-AAG, вызвали значительный интерес в данной области к разработке дополнительных ингибиторов HSP90 с улучшенными лекарственными свойствами, которые обеспечили бы полезный терапевтический эффект для пациентов, страдающих от заболеваний, связанных с аномальной укладкой белка. В описании уровня техники содержатся ссылки на следующие публикации. 1. J.C. Young, V.R. Agashe, K. Siegers and F.U. Hartl, Pathways of chaperone-mediated protein folding inChem. 49 (2006), p. 381-390. Краткое изложение сущности изобретения Настоящее изобретение относится к соединениям, обладающим активностью в отношении ингибирования HSP90. Согласно настоящему изобретению также предложены композиции и наборы, включающие такие соединения. Дополнительно, настоящее изобретение относится к способам изготовления соединений согласно настоящему изобретению, а также промежуточным соединениям, которые можно использовать в указанных способах. Согласно одному аспекту настоящего изобретения предложено соединение формулы или его таутомер, стереоизомер или фармацевтически приемлемая соль, гдеR46 и R47, каждый, независимо выбраны из группы, включающей водород, гидроксил, амино,-4 019156(C1-6)алкил и гидрокси(C1-6)алкил. Другой аспект настоящего изобретения относится к фармацевтическим композициям, которые включают ингибитор HSP90 согласно настоящему изобретению в качестве активного ингредиента. Фармацевтические композиции согласно настоящему изобретению могут необязательно содержать 0.001100% одного или более ингибиторов согласно настоящему изобретению. Такие фармацевтические композиции можно вводить или вводить совместно различными путями, включая, например, пероральное,парентеральное, интраперитонеальное, внутривенное, внутриартериальное, чрескожное, сублингвальное,внутримышечное, ректальное, трансбуккальное, интраназальное введения, введение при помощи липосом, введение путем ингаляции, вагинальное введение, введение в глаз и местную доставку (например,при помощи катетера или стента), подкожное введение, введение в жировую ткань, введение в сустав или через трахею. Композиции также можно вводить или вводить совместно в формах с замедленным высвобождением. Один аспект настоящего изобретения относится к способам приготовления соединений, наборов и изделий согласно настоящему изобретению. Например, в настоящем описании приведено несколько схем синтеза для синтеза соединений согласно настоящему изобретению. Еще один аспект настоящего изобретения относится к способам применения соединений и композиций согласно настоящему изобретению. В одном варианте осуществления соединения и композиции применяют для ингибирования HSP90. В другом варианте осуществления соединения и композиции применяют для лечения болезненных состояний, в отношении которых HSP90 обладает активностью или участвует в патогенезе и/или развитии симптомов данного болезненного состояния. В другом варианте осуществления соединение вводят субъекту в случае, когда активность HSP90 в организме субъекта изменена, предпочтительно снижена. Относительно всех описанных выше вариантов реализации необходимо иметь в виду, что настоящее изобретение охватывает все фармацевтически приемлемые ионизированные формы (например, соли) и сольваты (например, гидраты) соединений, вне зависимости от того, указаны ли такая ионизированная форма или сольват, поскольку они хорошо известны в соответствующей области. Также следует отметить, что, если не указана конкретная стереохимическая структура, предполагается, что указание на соединение охватывает все возможные стереоизомеры (например, энантиомеры или диастереомеры, в зависимости от числа хиральных центров) вне зависимости от того, представлено ли данное соединение в виде отдельного изомера или смеси изомеров. Далее, если не указано другое, подразумевается, что указание на соединение охватывает все возможные резонансные формы и таутомеры. В формуле изобретения выражения "соединение, содержащее формулу", "соединение, соответствующее формуле" и "соединение формулы" охватывает данное соединение и все фармацевтически приемлемые ионизованные формы и сольваты, все возможные стереоизомеры и все возможные резонансные формы и таутомеры, если в конкретном пункте формулы явно не указано другое. Краткое описание графических материалов На фиг. 1 показаны SEQ ID NO: 1 и SEQ ID NO: 2, упоминаемые в настоящем описании. На фиг. 2 показана порошковая рентгеновская дифрактограмма (R,Z)-2-амино-7-(4-фтор-2-(6 метоксипиридин-2-ил)фенил)-4-метил-7,8-дигидропиридо[4,3-d]пиримидин-5(6H)-он О-(S)-3,4 дигидроксибутил оксим бензоата, форма А. На фиг. 3 показаны результаты дифференциальной сканирующей колориметрии и термогравиметрии(R,Z)-2-амино-7-(4-фтор-2-(6-метоксипиридин-2-ил)фенил)-4-метил-7,8-дигидропиридо[4,3d]пиримидин-5(6H)-он O-(S)-3,4-дигидроксибутил оксим бензоата, формы А. Определения Если не указано другое, приведенные ниже термины используются в данном описании в определенном ниже значении. Следует отметить, что в настоящем описании и формуле изобретения форма единственного числа включает и множество объектов, если из контекста явно не следует обратное. Кроме того, определения стандартных химических терминов можно найти в справочных изданиях, включая Carey and SundbergYork. Также, если не указано другое, используются стандартные методы масс-спектроскопии, ЯМР,ВЭЖХ, химии белка, биохимии, технологии рекомбинантных ДНК и фармакологии, находящиеся в пределах компетенции специалиста в данной области. в химической структуре, в частности в радикале, обозначает точку присоединения радикала."Алкил", представленный отдельно, представляет собой линейный или разветвленный, насыщенный или ненасыщенный, алифатический радикал, цепь которого состоит из атомов углерода. В обычно используемых обозначениях (CX)алкил и (CX-Y)алкил X и Y указывают число атомов углерода в цепи. Например, (C1-6)алкил включает алкилы, имеющие цепь, состоящую из 1-6 атомов углерода (например,метил, этил, пропил, изопропил, бутил, сек-бутил, изобутил, трет-бутил, винил, аллил, 1-пропенил, изопротенил, 1-бутенил, 2-бутенил, 3-бутенил, 2-метилаллил, этинил, 1-припинил, 2-пропинил и т.п.). Алкил совместно с другим радикалом (например, как в арилалкиле, гетероарилалкиле и т.п.) обозначает линей-5 019156 ный или разветвленный, насыщенный или ненасыщенный алифатический двухвалентный радикал, содержащий указанное число атомов, или, если число атомов не указано, обозначает связь (например,(C6-10)арил(C1-3)алкил включает бензил, фенэтил, 1-фенилэтил, 3-фенилпропил, 2-тиенилметил, 2 пиридинилметил и т.п.). В конкретных вариантах осуществления "алкил", отдельно или совместно с другим радикалом, может представлять собой (C1-20)алкил, (C1-15)алкил, (C1-10)алкил, (C1-5)алкил или(C1-3)алкил. В альтернативном варианте "алкил", отдельно или совместно с другим радикалом, может представлять собой (C1)алкил, или (C2)алкил, или (C3)алкил."Амино" обозначает азотсодержащую группу, содержащую два дополнительных заместителя, где,например, к азоту присоединен атом водорода или углерода. Например, типичные аминогруппы включают -NH2, -NHCH3, -N(CH3)2, -NHC1-10)алкил), -NC1-10)алкил)2, -NH(арил), -NH(гетероарил),-N(арил)2, -N(гетероарил)2 и т.п. Необязательно, указанные два заместителя вместе с атомом азота образуют цикл. Если не указано другое, соединения согласно настоящему изобретению, содержащие аминогруппы, могут включать их замещенные производные. Подходящие защитные группы для аминогрупп включают ацетил, трет-бутоксикарбонил, бензилоксикарбонил и т.п."Животное" включает людей и млекопитающих, не являющихся людьми (например, собаки, кошки,кролики, крупный рогатый скот, лошади, овцы, козы, свиньи, олени и т.д.), а также не млекопитающих"Заболевание" включает, в частности, нездоровое состояние животного или его части и включает нездоровые состояния, которые могут быть вызваны или присущи медицинским или ветеринарным средствам лечения, применяемым к животному, т.е. "побочные эффекты" такого лечения."ЕС 50" обозначает молярную концентрацию агониста, которая обеспечивает 50% максимального возможного эффекта такого агониста. Действие агониста может быть стимулирующим или ингибирующим."Изомеры" обозначают соединения, имеющие идентичные молекулярные формулы, но различающиеся по природе последовательности соединения атомов или по расположению атомов в пространстве. Изомеры, которые различаются расположением атомов в пространстве, называются "стереоизомерами." Стереоизомеры, которые являются зеркальным отражением друг друга, называются "диастереомерами",а стереомеры, которые на являются накладывающимися зеркальными отражениями, называются "энантиомерами" или иногда "оптическими изомерами", атом углерода, связанный с четырьмя неидентичными заместителями, называется "хиральным центром", соединение с одним хиральным центром имеет две энантиомерные формы противоположной хиральности. Смесь двух энантиомерных форм называется"рацемической смесью". Соединение с одним или более хиральными центрами имеет 2n-1 энантиомерных пар, где n - это число хиральных центров. Соединения с одним или более хиральными центрами могут существовать либо в форме отдельного диастереомера, либо в форме смеси диастереомеров, называемой"диастереомерной смесью". В случае присутствия одного хирального центра стереоизомер может характеризоваться абсолютной конфигурацией этого хирального центра. Абсолютная конфигурация относится к пространственному расположению заместителей, присоединенных к хиральному центру. Энантиомеры характеризуются абсолютной конфигурацией хиральных центров и описываются в соответствии с правилами последовательностей R- и S-, предложенными Cahn, Ingold и Prelog. Правила стереохимической номенклатуры, методы определения стереохимической структуры и разделения стереоизомеров хорошо известны в соответствующей литературе (например, см. "Advanced Organic Chemistry", 5th edition, March,Jerry, John WileySons, New York, 2001)."Уходящая группа" обозначает группу в смысле, принятом в синтетической органической химии,т.е. атом или группу, которая может быть удалены в условиях реакции (например, алкилирования). Примеры уходящих групп включают, но не ограничиваются перечисленными, галоген (например, F, Cl, Br и"Фармацевтически приемлемый" обозначает пригодный для приготовления фармацевтической композиции, которая в общем безопасна, не токсична и не обладает нежелательными с биологической или другой точки зрения свойствами, и включает объекты, приемлемые для использования в ветеринарии, а также для фармацевтического применения для людей."Фармацевтически приемлемые соли" обозначают соли соединений согласно настоящему изобретению, которые являются фармацевтически приемлемыми в определенном выше смысле и которые обладают желаемой фармакологической активностью. Такие соли включают соли присоединения, образованные с неорганическими кислотами, такими как хлористо-водородная кислота, бромисто-водородная кислота, серная кислота, азотная кислота, фосфорная кислота и т.п.; или органическими кислотами, такими как уксусная кислота, пропионовая кислота, гексаноевая кислота, гептаноевая кислота, циклопентанпропионовая кислота, гликолевая кислота, пировиноградная кислота, молочная кислота, малоновая кислота,-6 019156 янтарная кислота, яблочная кислота, малеиновая кислота, фумаровая кислота, винно-каменная кислота,лимонная кислота, бензойная кислота, o-(4-гидроксибензоил)бензойная кислота, коричная кислота, миндальная кислота, метансульфоновая кислота, этансульфоновая кислота, 1,2-этандисульфоновая кислота,2-гидроксиэтансульфоновая кислота, бензолсульфоновая кислота, p-хлоробензолсульфоновая кислота, 2 нафталинсульфоновая кислота, p-толуолсульфоновая кислота, камфорсульфоновая кислота, 4 метилбицикло[2.2.2]окс-2-ен-1-карбоновая кислота, глюкогептоновая кислота, 4,4'-метилен-бис-(3 гидрокси-2-ен-1-карбоновая кислота), 3-фенилпропионовая кислота, триметилуксусная кислота, третбутилуксусная кислота, лаурилсерная кислота, глюконовая кислота, глютаминовая кислота, гидроксинафтоевая кислота, салициловая кислота, стеариновая кислота, муконовая кислота и т.п. Фармацевтически приемлемые соли также включают соли присоединения основания, которые могут быть образованы, если присутствующие протоны кислоты способны взаимодействовать с неорганическими и органическими основаниями. Подходящие неорганические основания включают гидроксид натрия, карбонат натрия, гидроксид калия, гидроксид алюминия и гидроксид кальция. Приемлемые органические основания включают этаноламин, биэтаноламин, триэтаноламин, трометамин, Nметилглюкамин и т.п."Защищенные производные" обозначает производные, в которых реактивный сайт или сайты блокированы защитными группами. Защищенные производные пригодны для изготовления ингибиторов или могут сами обладать ингибирующей активностью. Подробный перечень защитных групп можно найти в P.G.M. Wuts and T.W. Greene, "Greene's Protecting Groups in Organic Synthesis, 4th edition, John"Субъект" и "пациент" включают людей и млекопитающих, не являющихся людьми (например, собаки, кошки, кролики, крупный рогатый скот, лошади, овцы, козы, свиньи, олени и т.д.), а также не млекопитающих (например, птица и т.п.)."Терапевтически эффективное количество" обозначает количество, которое при введении животному для лечения заболевания является достаточным для того, чтобы обеспечить такое лечение заболевания."Терапия" или "лечение" обозначает любое введение (применение) соединения согласно настоящему изобретению и включает:(1) предотвращение возникновения заболевания у животного, которое может быть предрасположено к такому заболеванию, но у которого оно еще не проявилось, или которое не демонстрирует патологической картины или симптомов такого заболевания,(2) подавление заболевания у животного, испытывающего или демонстрирующего патологическую картину или симптомы, характерные для больного (т.е. блокирование дальнейшего развития патологической картины или симптомов), или(3) снижение выраженности заболевания у животного, испытывающего или демонстрирующего патологическую картину или симптомы, характерные для больного (т.е. обращение патологической картины или симптомов). Относительно всех приведенных в настоящем описании определений следует отметить, что они являются открытыми в том смысле, что могут быть включены другие заместители, помимо указанных. Таким образом (C1)алкил указывает на то, что присутствует один атом углерода, но не указывает на то, какие существуют заместители при данном атоме углерода. Соответственно, (C1)алкил включает метил(т.е. -CH3), а также -CRR'R", где R, R' и R", каждый, независимо и необязательно могут представлять собой водород или дополнительный заместитель, в котором атом, связанный с данным атомом углерода,представляет собой гетероатом или циано. Следовательно, CF3, CH2OH и CH2CN, примерами являются все (C1)алкилы. Аналогично, такие термины, как "алкиламино" и т.п., включают диалкиламино и т.п. Кроме того, предполагается, что атомы, образующие настоящее соединение, включают все изотопы таких атомов. В настоящем описании изотопы включают все атомы, имеющие одинаковый атомный номер, но разные массовые числа. В качестве неограничивающего примера, изотопы водорода включают тритий и дейтерий, а изотопы углерода включают 13 С и 14 С. Подробное описание изобретения Настоящее изобретение относится к соединениям, которые можно применять для ингибированияHSP90. Настоящее изобретение также относится к фармацевтическим композициям, включающим такие соединения. Дополнительно, настоящее изобретение относится к способам и промежуточным соединениям, которые можно использовать для изготовления указанных соединений. Кроме того, настоящее изобретение относится к способам применения таких соединений. Следует отметить, что соединения согласно настоящему изобретению могут также обладать активностью в отношении других членов того же семейства белков и, таким образом, их можно применять в отношении болезненных состояний, связанных с указанными другими членами данного семейства. Следует отметить, что соединения согласно настоящему изобретению могут также обладать ингибирующей активностью в отношении других членов семейства HSP, и таким образом, их можно использовать при заболеваниях, связанных с этими другими членами данного семейства. Соединения согласно настоящему изобретению. Согласно одному из аспектов настоящего изобретения предложены соединения, которые можно применять в качестве ингибиторов HSP90. В одном варианте осуществления ингибитор HSP90 согласно настоящему изобретению имеет формулу или его таутомер, стереоизомер или фармацевтически приемлемая соль, гдеR46 и R47, каждый, независимо выбраны из группы, включающей водород, гидроксил, амино,(C1-6)алкил и гидрокси(C1-6)алкил.X. В одном варианте описанных выше примеров осуществления соединений согласно настоящему изобретению X представляет собой О.R1. В одном конкретном варианте указанных выше примеров осуществления соединений согласно настоящему изобретению R1 представляет собой -L-R45, где L представляет собой (-CR46R47-)n; n равно 1, 2,3, 4 или 5; R45 независимо выбран из группы, включающей водород, гидроксил, амино. В других вариантах L представляет собой (-CR46R47-)5. В других вариантах L представляет собой(-CR46R47-)n, R46 и R47, каждый, независимо выбраны из группы, включающей водород, гидрокси, амино,(C1-6)алкил и гидрокси(C1-6)алкил. В других вариантах R46 и R47, оба, представляют собой водород.R2. В другом варианте осуществления и вариантов соединений согласно настоящему изобретению R2 выбран из группы, включающей водород, метил.R3. В одном варианте указанных выше примеров осуществления соединений согласно настоящему изобретению R3 выбран из группы, включающейR12. В описанных выше примерах и вариантах осуществления настоящего изобретения, в некоторых вариантах, R12 выбран из группы, включающей Конкретные примеры соединений согласно настоящему изобретению включают, но не ограничиваются перечисленными, следующее:(S,Z)-2-амино-7-(4-фтор-2-(6-метоксипиридин-2-ил)фенил)-4-метил-7,8-дигидропиридо[4,3d]пиримидин-5(6 Н)-он О-(R)-3,4-дигидроксибутил оксим. В других аспектах настоящее изобретение относится к способам получения соединений, пригодных в качестве ингибиторов HSP90. В одном варианте осуществления предложен способ, включающий осуществление реакции соединения формулы с соединением формулы H2N-O-R1 в условиях, в которых образуется промежуточное соединение,имеющее формулу осуществление реакции указанного промежуточного соединения с соединением формулы где R1 и R2 имеют значения, указанные выше. В другом варианте осуществления способ получения соединения согласно настоящему изобретению включает осуществление реакции соединения формулы в условиях, в которых образуется промежуточное соединение, имеющее формулу и осуществление реакции указанного промежуточного соединения с соединением формулы H2N-OR1 в условиях, в которых образуется продукт, имеющий формулу где R1 и R2 имеют значения, указанные выше. В еще одном варианте осуществления способ получения соединения согласно настоящему изобретению включает осуществление реакции соединения формулы в условиях, в которых образуется промежуточное соединение F, имеющее формулу где PG представляет собой защитную группу, выбранную из группы, включающейR2 имеет значения, указанные выше. В описанных выше вариантах осуществления соединение может быть получено способом А, включающим осуществление сочетания исходного материала II, имеющего формулу с указанным промежуточным соединением F, что обеспечивает образование промежуточного соединения G, имеющего формулу осуществление сочетания исходного материала III, имеющего формулу с указанным промежуточным соединением G в условиях, в которых образуется промежуточное соединение H, имеющего формулу где R1p представляет собой защищенную форму R1;R12 имеет значения, указанные выше. В описанных выше вариантах осуществления соединение может быть получено способом В, включающим снятие защиты с промежуточного соединения F в условиях, в которых образуется промежуточное соединение F', имеющее формулу осуществление сочетания исходного материала II, имеющего формулу с указанным промежуточным соединением F', что обеспечивает образование промежуточного соединения G, имеющего формулу осуществление сочетания исходного материала III, имеющего формулу с указанным промежуточным соединением G в условиях, в которых образуется промежуточное соединение Н, имеющее формулу где R1p представляет собой защищенную форму R1;R12 имеет значение, указанное выше. Другой способ, пригодный для получения соединений согласно настоящему изобретению, включает осуществление реакции соединения формулы с исходным материалом I, имеющим формулу в условиях, в которых образуется промежуточное соединение F, имеющее формулу снятие защиты с промежуточного соединения F в условиях, в которых образуется промежуточное соединение F', имеющее формулу осуществление сочетания исходного материала III, имеющего формулу с промежуточным соединением F' в условиях, в которых образуется промежуточное соединение J,имеющее формулу снятие защиты, а затем осуществление сочетания исходного материала II, имеющего формулу где R1p представляет собой защищенную форму R1;R12 имеет значение, указанное выше. Во всех описанных выше вариантах осуществления способов в некоторых вариантах R1 представляет собой -L-R45,где L представляет собой (-CR46R47-)n, где n равно 1, 2, 3, 4 или 5; R46 и R47, каждый, независимо выбраны из группы, включающей водород, гидроксил, гидрокси(C1-6)алкил, амино, (C1-6)алкил;R45 независимо выбран из группы, включающей водород, гидроксил, амино. В некоторых вариантах способа согласно настоящему изобретению R2 выбран из группы, включающей водород, метил. В описанных выше вариантах осуществления способов согласно настоящему изобретению R12 выбран из группы, включающей Следует отметить, что соединения согласно настоящему изобретению могут иметь форму фармацевтически приемлемой соли, биоразлагаемого эфира, биогидролизуемого амида, биогидролизуемого карбамата, сольвата, гидрата или пролекарства. Например, соединение необязательно содержит заместитель, который in vivo может превратиться в другой заместитель, например водород. Далее следует отметить, что соединение может быть представлено в виде смеси стереоизомеров,либо соединение может быть представлено в виде единственного стереоизомера. Согласно другому аспекту предложена композиция, содержащая в качестве активного ингредиента соединение согласно любому из описанных выше вариантов воплощения или вариантов. В одном конкретном варианте композиция представляет собой твердую форму, пригодную для перорального введения. В другом конкретном варианте композиция представляет собой жидкую форму, пригодную для перорального введения. В еще одном конкретном варианте композиция представляет собой таблетку. В еще одном конкретном варианте композиция представляет собой жидкую лекарственную форму, пригодную для парентерального введения. Согласно настоящему изобретению также предложена фармацевтическая композиция, содержащая соединение согласно любому из описанных выше вариантов и примеров осуществления, причем указанная композиция пригодна для введения путем, выбранным из группы, включающей пероральное, парентеральное, интраперитонеальное, внутривенное, внутриартериальное, чрескожное, сублингвальное,внутримышечное, ректальное, трансбуккальное, интраназальное введения, введение при помощи липосом, введение путем ингаляции, вагинальное введение, введение в глаз и местную доставку (например,при помощи катетера или стента), подкожное введение, введение в жировую ткань, введение в сустав или через трахею. Согласно еще одному аспекту предложен способ лечения болезненного состояния, в отношении которого HSP90 обладает активностью, которая вносит вклад в патогенез и/или симптоматику данного болезненного состояния, причем указанный способ включает обеспечение присутствия соединения согласно любому из описанных выше вариантов и примеров осуществления в количестве, терапевтически эффективном для данного болезненного состояния. В каждом из указанных выше вариантов болезненное состояние выбрано из группы, включающей рак, воспаление, воспалительное заболевание кишечника, псориаз, артрит и отторжение трансплантата. В одном из вариантов каждого из описанных выше способов болезненное состояние представляет собой рак. Рак выбран из группы, включающей плоскоклеточную карциному, астроцитому, саркому Капоши, глиобластому, немелкоклеточный рак легких, рак мочевого пузыря, рак головы и шеи, меланому,рак яичника, рак предстательной железы, рак груди, мелкоклеточный рак легкого, глиому, рак прямой и ободочной кишки, рак мочеполовой системы, рак желудочно-кишечного тракта, рак почки, раковые заболевания крови, неходжкинскую лимфому, лимфому, множественную миелому, лейкемию (включая острую миелогенную лейкемию, хроническую миелогенную лейкемию, хроническую лимфоцитарную лейкемию), миелодиспластический синдром и мезотелиому. В одном из вариантов каждого из описанных выше способов HSP90 предоставляет HSP90. В другом варианте HSP90 представляет собой HSP90. Соли, гидраты и пролекарства ингибиторов HSP90. Следует понимать, что соединения согласно настоящему изобретению могут быть представлены и их можно необязательно вводить в форме солей, гидратов и пролекарств, которые in vivo превращаются в соединения согласно настоящему изобретению. Например, в объем настоящего изобретения входят превращение соединений согласно настоящему изобретению в и использование их в форме фармацевтически приемлемых солей, полученных из различных органических и неорганических кислот и оснований в соответствии с известными процедурами. В случае, когда у соединения согласно настоящему изобретению есть форма свободного основания,такие соединения можно приготовить в форме фармацевтически приемлемой соли присоединения кислоты с фармацевтически приемлемой неорганической или органической кислотой, например гидрогалидом,таким как гидрохлорид, гидробромид, гидроиодид; другие минеральные кислоты и соответствующие соли, такие как сульфат, нитрат, фосфат и т.д.; а также алкил- и моноарил и моноарилсульфонаты, такие как этансульфонат, толуолсульфонат и бензолсульфонат; а также другие органические кислоты и соответствующие соли, такие как ацетат, тартрат, малеат, сукцинат, цитра, бензоат, салицилат и аскорбат. Другие соли присоединения кислот согласно настоящему изобретению включают, но не ограничиваются перечисленными, адипат, альгинат, аргинат, аспартат, бисульфат, бисульфит, бромид, бутират, камформат, камфорсульфонат, каприлат, хлорид, хлорбензоат, циклопентанпропионат, диглюконат, дигидрофосфат, динитробензоат, додецилсульфат, фумарат, галактерат (из муциновой кислоты), галактуронат,глюкогептонат, глюконат, глютамат, глицерофосфат, гемисукцинат, гемисульфат, гептаноат, гексаноат,гиппурат, гидрохлорид, гидробромид, гидроиодид, 2-гидроксиэтансульфонат, иодид, изотионат, изобутират, лактат, лактобионат, малат, малонат, мандалат, метафосфат, метансульфонат, метилбензоат, моногидрофосфат, 2-нафталинсульфонат, никотинат, нитрат, оксалат, олеат, памоат, пектинат, персульфат,фенилацетат, 3-фенилпропионат, фосфат, фосфонат и фталат. Следует понимать, что формы свободных оснований обычно несколько отличаются от соответствующих солей по физическим свойствам, таким как растворимость в полярных растворителях, но в остальном соли эквивалентны соответствующим формам свободных оснований для целей настоящего изобретения. В случае, когда у соединений согласно настоящему изобретению есть форма свободной кислоты,- 14019156 могут быть получены фармацевтически приемлемые соли присоединения основания путем осуществления реакции соединения в форме свободного основания с фармацевтически приемлемым неорганическим или органическим основанием. Примерами таких оснований являются гидроксиды щелочных металлов, включая гидроксиды калия, натрия и лития; гидроксиды щелочно-земельных металлов, такие как гидроксиды бария и кальция; алкоксиды щелочных металлов, например этанолат калия и пропанолат натрия; и различные органические основания, такие как гидроксид аммония, пиперидин, диэтаноламин иN-метилглютамин. Также предусмотрены аммонийные соли соединений согласно настоящему изобретению. Другие соли оснований согласно настоящему изобретению включают, но не ограничиваются перечисленными, соли меди, соли двухвалентного и трехвалентного железа, соли лития, магния, соли двухвалентного и трехвалентного марганца, калия, натрия и цинка. Соли органических оснований включают,но не ограничиваются перечисленными, соли первичных, вторичных и третичных аминов, замещенные амины, включая природные замещенные амины, циклические амины и основные ионообменные смолы,например аргинин, бетаин, кафеин, хлорпрокаин, холин, N,N'-дибензилэтилендиамин (бензатин), дициклогексиламин, диэтаноламин, 2-диэтиламиноэтанол, 2-диметиламиноэтанол, этаноламин, этилендиамин,N-этилморфолин, N-этилпиперидин, глюкамин, глюкозамин, гистидин, гидрабрамин, изопропиламин,лидокаин, лизин, меглумин, N-метил-D-глютамин, морфолин, пиперазин, пиперидин, полиаминовые смолы, прокаин, пурины, теобромин, триэтаноламин, триэтиламин, триметиламин, трипропиламин и трис-(гидроксиметил)метиламин (трометанамин). Следует понимать, что формы свободных кислот обычно несколько отличаются от соответствующих солей по физическим свойствам, таким как растворимость в полярных растворителях, но в остальном соли эквивалентны соответствующим формам свободных оснований для целей настоящего изобретения. Соединения согласно настоящему изобретению, которые включают основные группы, содержащие азот, могут быть кватернизированы такими агентами, как (C1-4)алкилгалиды, например метил, этил, изопропил и трет-бутил хлориды, бромиды и иодиды; ди(C1-4)алкилсульфаты, например диметил, диэтил и диамил сульфаты; (C10-18)алкилгалиды, например децил-, додецил-, лаурил-, миристил- и стеарилхлориды, бромиды и иодиды; а также арил(С 1-4)алкилгалиды, например бензилхлорид и фенэтилбромид. Такие соли обеспечивают получение как водорастворимых, так и жирорастворимых соединений согласно настоящему изобретению. Также могут быть получены защищенные производные соединений согласно настоящему изобретению. Примеры методик, которые можно применять для получения защитных групп и их удаления, можно найти в P.G.M. Wuts and T.W. Greene in "Greene's Protective Groups in Organic Synthesis" 4th edition,John Wiley and Sons, 2007. Соединения согласно настоящему изобретению также могут быть легко получены или сформированы в процессе осуществления способов согласно настоящему изобретению в форме сольватов (например,гидратов). Гидраты соединений согласно настоящему изобретению могут быть легко получены путем рекристаллизации из смеси водного/органического растворителей, таких как диоксин, тетрагидрофуран или метанол. В настоящем описании "фармацевтически приемлемая соль" включает любое соединение согласно настоящему изобретению, которое применяют в форме соли, в частности, если соль обеспечивает улучшенную фармакокинетику соединения по сравнению со свободной формой соединения или другой солевой формой соединения. Форма фармацевтически приемлемой соли может также, в первую очередь,обеспечивать желаемые фармакокинетические свойства соединения, которыми оно ранее не обладало, и может даже положительно влиять на соединение в отношении его терапевтической активности в организме. Примером фармакокинетического свойства, на которое может быть оказано положительное влияние, является путь, которым данное соединение транспортируется через мембрану клетки, что, в свою очередь, может оказать прямое и положительное влияние на всасывание, распределение, биотрансформацию и выведение соединения. Хотя путь введения фармацевтической композиции имеет важное значение, и различные анатомические, физиологические и патологические факторы могут значительно снизить биодоступность, растворимость соединения обычно зависит от природы конкретной соли, которая используется. Для специалиста очевидно, что водный раствор соединения обеспечивает наиболее быстрое всасывание соединения в организме субъекта, которого лечат, а жировые растворы и суспензии, а также твердые лекарственные формы замедляют всасывание соединения. Применение соединений согласно настоящему изобретению. Одна группа симптомов, для лечения которых можно использовать ингибиторы HSP90 согласно настоящему изобретению, представляет собой симптомы, включающие нежелательную или неконтролируемую пролиферацию клеток. Такие симптомы включают доброкачественные опухоли, различные типа раковых заболеваний, такие как первичные опухоли и метастазы опухолей, рестеноз (например, поражение сердечных, сонных и церебральных сосудов), анормальная стимуляция клеток эндотелия (атеросклероз), повреждения тканей организма в результате хирургического вмешательства, анормального заживления ран, заболеваний, которые приводят к фиброзу тканей, травмы от повторяющихся движений, нарушения тканей, которые на являются высоковаскуляризированными, пролиферативные реакции, связанные с трансплантацией органов, нейродегенеративные заболевания, включая болезнь Паркинсона,- 15019156 болезнь Альцгеймера, болезнь Хантингтона и прионные заболевания, воспаление и заболевания, связанные с воспалением, такие как боль, головные боли, лихорадка, артрит, астма, бронхит, тендоинит, экзема, воспалительное заболевание кишечника и заболевания, зависимые от ангиогенеза, такие как рак, артрит, диабетическая ретинопатия, возрастная дегенерация желтого пятна (AMD) и инфекционные заболевания, в частности грибковые инфекции, вирусные заболевания, включая, но не ограничиваясь перечисленными, заболевания, вызванные вирусом гепатита В (HBV), вирусом гепатита С (HCV) и вирусом простого герпеса типа 1 (HSV-1), заболевания сердечно-сосудистой и центральной нервной систем 3, 4, 5, 6, 7. В целом, клетки в доброкачественных опухолях сохраняют свои дифференцированные признаки и не делятся полностью неконтролируемым образом. Доброкачественная опухоль обычно локализована и не образует метастазы. Конкретные типа доброкачественных опухолей, которые можно лечить ингибиторами HSP90 согласно настоящему изобретению, включают следующее: гемангиомы, гепатоцеллюлярные аденомы, кавернозные гемангиомы, фокальная нодулярная гиперплазия, нейромы слухового нерва,нейрофиброма, цистанома желчных протоков, фиброма, липомы, лейомиомы, мезотелиомы, тератомы,миксомы, нодулярная регенеративная гиперплазия, трахома и пирогенные гранулемы. В случае злокачественных опухолей клетки становятся недифференцированными, не отвечают на сигналы контроля роста со стороны организма и размножаются неконтролируемым образом. Злокачественные опухоли инвазивны и способны к распространению в отдаленные участки (метастазированию). Злокачественные опухоли обычно делят на две категории: первичные и вторичные. Первичные опухоли возникают непосредственно в ткани, где их обнаруживают. Вторичные опухоли или метастазы образуются в другом участке организма, но распространяются в отдаленные органы. Обычные пути метастазирования представляют собой прямое прорастание в прилежащие структуры, распространение по кровеносной или лимфатической системам и распространение вдоль пластов тканей и пустот организма (перетонеальная жидкость, цереброспинальная жидкость и т.д.). Конкретные типы раковых заболеваний или злокачественных опухолей, первичных или вторичных,которые можно лечить с использованием ингибиторов HSP90 согласно настоящему изобретению, включают, но не ограничиваются следующими, лейкемию, рак молочной железы, рак мочеполовой системы,рак кожи, рак кости, рак предстательной железы, рак печени, рак легкого, рак мозга, рак гортани, рак желчного пузыря, рак поджелудочной железы, рак прямой кишки, рак паращитовидной железы, рак щитовидной железы, надпочечников, нервной ткани, мочевого пузыря, головы и шеи, толстой кишки, желудка, рак прямой и толстой кишки, бронхов, почки, базальноклеточная карцинома, плоскоклеточная карцинома язвенного и папилларного типов, метастазирующая карцинома кожи, остеосаркома, саркома Эвинга, ретикулосаркома, миелома, гигантскоклеточная саркома, мелкоклеточная опухоль легкого, немелкоклеточная опухоль легкого, опухоль островковых клеток, первичная опухоль мозга, острые и хронические лимфоцитарные и гранулоцитарные опухоли, волосковоклеточные опухоли, аденома, гиперплазия, карцинома спинного мозга, феохромоцитома, mucosal neuronms, интестинальные ганглионейромы, гиперпластическая опухоль роговичного нерва, опухоль marfanoid habitus (марфаноидный внешний вид), опухоль Вильма, семинома, опухоль яичника, лейомиома, дисплазия и in situ карцинома шейки матки, нейробластома, ретинобластома, карцинома мягких тканей, злокачественный карциноид, местные поражения кожи, рак желудочно-кишечного тракта, злокачественные опухоли крови, миелодиспластический синдром, грибковые микозы, рабдомиосаркома, астроцитома, неходжкинская лимфома, саркома Капоши, остеогенная и другие саркомы, злокачественная гиперкальцемия, гипернефрома, истинная полицитемия, аденокарцинома, мультиформная глиобластома, глиома, лейкемия (включая острую миелогенную лейкемию, хроническую миелогенную лейкемию, хроническую лимфоцитарную лейкемию),лимфомы, злокачественные меланомы, плоскоклеточные карциномы и другие саркомы. Ингибиторы HSP90 согласно настоящему изобретению можно также использовать для лечения абнормальной пролиферации клеток вследствие повреждения тканей в ходе хирургического вмешательства. Такие повреждения могут возникать в результате разнообразных хирургических процедур, таких как операции на суставах, операции на кишечнике и образование келоидных рубцов. Заболевания, которые вызывают образование фиброзной ткани, включают эмфизему. Нарушения в результате повторяющихся движений, которые можно лечить согласно настоящему изобретению, включают синдром запястного туннеля. Пример нарушения, связанного с пролиферацией клеток, которое можно лечить согласно настоящему изобретению, включает рак кости. Пролиферативные реакции, связанные трансплантацией органов, которые можно лечить с использованием ингибиторов HSP90 согласно настоящему изобретению, включают пролиферативные ответы,которые вносят вклад в возможное отторжение органа или связанные с ним осложнения. В частности,такие пролиферативные реакции могут возникать в ходе трансплантации сердца, легкого, печени, почки и других органов или систем тела. Анормальный ангиогенез, который можно лечить с использованием настоящего изобретения,включает анормальный ангиогенез, сопровождающий ревматоидный артрит, ишемическиреперфузионный отек и повреждение мозга, ишемию коры, гиперплазию и гиперваскуляризацию яичников (синдром поликистозных яичников), эндометриоз, псориаз, диабетическую ретинопатию и другие ангиогенные заболевания глаз, такие как ретинопатия недоношенных (ретролентальная фиброплазия) дегенерация желтого пятна, отторжение трансплантата роговицы, неоваскулярная глаукома и синдром Остера-Вебера. Примеры связанных с неконтролируемым ангиогенезом заболеваний, которые можно лечить согласно настоящему изобретению, включают, но не ограничиваются перечисленными, неоваскуляризацию сетчатки/сосудистой оболочки и неоваскуляризацию роговицы. Примеры неоваскуляризации сетчатки/сосудистой оболочки включают, но не ограничиваются перечисленными, заболевания Бетца(Bests) миому, ямки диска зрительного нерва, болезнь Старгарта, Болезнь Педжета, окклюзию вен, окклюзию артерий, серповидно-клеточную анемию, саркоид, сифилис, эластическую псевдоксантому, каротидную обструкцию, хронический увеит, витрит, микобактериальные инфекции, болезнь Лайма, системную красную волчанку, ретинопатию недоношенных, болезнь Илза, диабетическую ретинопатию, дегенерацию желтого пятна, болезнь Бекета, инфекции, вызывающие ретинит или воспаление сосудистой оболочки глаза, возможно гистоплазмоз, промежуточный увеит (pars planitis), хроническое отслоение сетчатки, синдромы гипервязкости, травмы и осложнения после вмешательства с использованием лазера,заболевания, связанные с неоваскуляризацией угла глаза, и заболевания, вызванные анормальной пролиферацией сосудисто-волокнистой или фиброзной ткани, включая все формы витреоретинопатии. Примеры неоваскуляризации роговицы включают, но не ограничиваются перечисленными, эпидемический кератоконъюнктивит, дефицит витамина А, переутомление от контактных линз, аропический кератит,верхний лимбальный кератоконъюнктивит, сухой кератоконъюнктивит, синдром Сьергена, красные угри, фликтенулез, диабетическая ретинопатия, ретинопатия недоношенных, отторжение трансплантата роговицы, язва Мурена, краевая дегенерация Террьена, краевой кератолиз, полиартерит, саркоидоз Вегенара, воспаление склеры, пемфигоид, радиальная кератотомия, неоваскулярная глаукома и ректрорентальная фиброплазия, сифилис, инфекция микобактериями, жировое перерождение, химические ожоги,грибковые изъязвления, инфекция простым вирусом Герпеса, инфекция вирусом опоясывающего герпеса, инфекция, вызванная простейшими и саркома Капоши. Хронические воспалительные заболевания, связанные с неконтролируемым ангиогенезом, также можно лечить ингибиторами HSP90 согласно настоящему изобретению. Хроническое воспаление зависит от непрерывного прорастания капилляров, которое обеспечивает приток клеток воспаления. Приток и присутствие клеток воспаления обеспечивает образование гранулем и таким образом поддерживает состояние хронического воспаления. Подавление ангиогенеза при помощи ингибитора HSP90 или в комбинации с другими противовоспалительными агентами могут предотвратить образование гранулем и таким образом облегчат заболевание. Примеры хронических воспалительных заболеваний включают, но не ограничиваются перечисленными, воспалительные заболевания кишечники, такие как болезнь Крона и язвенный колит, псориаз, саркоидит и ревматоидный артрит. Воспалительные заболевания кишечника, такие как болезнь Крона и язвенный колит, характеризуются хроническим воспалением и ангиогенезом в различных отделах желудочно-кишечного тракта. Например, болезнь Крона возникает в форме трансмурального воспалительного заболевания, которое наиболее часто поражает дистальную подвздошную кишку и прямую кишку, но может возникать в любой части желудочно-кишечного тракта, от рта до ануса и прианальной области. Пациенты с болезнью Крона обычно страдают хронической диареей, ассоциированной с абдоминальной болью, лихорадкой, анорексией, потерей веса, а также вздутием живота. Язвенный колит также представляет собой хроническое,неспецифическое воспалительное и язвенное заболевание, возникающее в слизистой оболочки толстой кишки, и характеризуется кровавой диареей. Воспалительные заболевания кишечника обычно вызываются хроническим гранулематозным воспалением в желудочно-кишечном тракте, включающим образование новых сосудов, окруженных оболочкой из воспалительных клеток. Подавление ангиогенеза ингибиторами согласно настоящему изобретению, вероятно, обеспечит подавление образования новых капилляров и предотвращение образования гранулем. Воспалительные заболевания кишечника также имеют дополнительные кишечные проявления, такие как поражения кожи. Такие поражения характеризуются воспалением и ангиогенезом и могут возникать во многих участках вне желудочно-кишечного тракта. Ингибирование ангиогенеза ингибиторами HSP90 согласно настоящему изобретению может снизить приток клеток воспаления и предотвратить образование повреждений. Саркоидит, другое воспалительное заболевание, характеризуется как мультисистемное грануломатозное нарушение. Гранулемы при этом заболевании могут образовываться в любом участке тела. Соответственно, симптомы зависят от участка с гранулемами, от активности заболевания. Гранулемы образованы разрастаниями капилляров, которые обеспечивают постоянную доставку питания клеткам воспаления. Применение ингибиторов HSP90 согласно настоящему изобретению для подавления ангиогенеза может привести к подавлению образования таких гранулем. Псориаз, который также является хроническим воспалительным рецидивирующим заболеванием, характеризуются папулами и бляшками различного размера. Лечение с использованием таких ингибиторов отдельно или в комбинации с противовоспалительными агентами, вероятно, обеспечит предотвращение образование новых кровеносных сосудов,необходимых для поддержания характерных поражений и облегчение симптомов у пациента. Ревматоидный артрит (РА) также представляет собой хроническое воспалительное заболевание, характеризующееся неспецифическим воспалением периферических суставов, считают, что кровеносные сосуды в синовиальной выстилке также претерпевают ангиогенез. В дополнение к образованию новых сосудистых сетей, клетки эндотелия высвобождают факторы и активные молекулы кислорода, что приводит к росту паннуса и разрушению хряща. Факторы, вовлеченные в ангиогенез, могут активно участвовать и способствовать поддержанию состояния хронического воспаления при ревматоидном артрите. Лечение с использованием ингибиторов HSP90 согласно настоящему изобретению отдельно или в комбинации с антиревматоидными агентами, возможно, обеспечит предотвращение образования новых кровеносных сосудов, необходимых для поддержания хронического воспаления и обеспечат облегчение симптомов у пациента, страдающего РА. Комбинированная терапия. Разнообразные терапевтические агенты могут оказывать действие, аддитивное или синергетическое действию ингибиторов HSP90 согласно настоящему изобретению. Комбинированные средства терапии,которые включают один или более соединений согласно настоящему изобретению с одним или более другими терапевтическими агентами, можно использовать, например, для: 1) усиления терапевтического эффекта (эффектов) одного или более соединений согласно настоящему изобретению и/или указанных одного или более терапевтических агентов; 2) снижения побочных эффектов одного или более соединений согласно настоящему изобретению и/или указанных одного или более терапевтических агентов; и/или 3) снижения эффективной дозы одного или более соединений согласно настоящему изобретению и/или указанных одного или более терапевтических агентов. Следует отметить, что комбинированная терапия включает случай, когда агенты вводят до или после друг друга (последовательное введение), а также случай, когда агенты вводят одновременно. Примеры таких терапевтических агентов, которые можно использовать в комбинации с ингибиторами HSP90, включают, но не ограничиваются перечисленными, средства против пролиферации клеток,противораковые агенты, алкилирующие агенты, антибиотические агенты, гормональные агенты, агенты растительного происхождения и биологические агенты. Средства против пролиферации клеток (антипролиферативные агенты) - это агенты, которые подавляют нежелательную и неконтролируемую пролиферацию клеток. Примеры антипролиферативных агентов, которые можно использовать в комбинации с ингибиторами HSP90 согласно настоящему изобретению, включают, но не ограничиваются перечисленными, ретиноидную кислоту и ее производные,2-метоксиэстрадиол, белок ANGIOSTATIN, белок ENDOSTATIN, сурамин, скваламин, тканевый ингибитор металлопротеиназы-1, тканевый ингибитор металлопротеиназы-2, ингибитор активатора плазминогена-1, ингибитор активатора плазминогена-2, хрящевой ингибитор, паклитаксел, тромбоцитарный фактор 4, протамин сульфат (клупеин), сульфатированные производные хитина (полученные из панциря краба-стригуна), сульфатированный комплекс полисахарид-пептидогликан (sp-pg), стауроспорин, модуляторы метаболизма матрикса, включая, например, аналоги пролина (L-азетедин-2-карбоновая кислота(LACA, цисгидроксипролин, d,l-3,4-дегидропролин, тиапролин, бета-аминопропионитрил фумарат, 4 пропил-5-(4-пиридинил)-2(3H)-оксазолон, метотрексат, митоксантрон, гепарин, интерфероны, 2 макроглобулин-сыворотка, chimp-3, химостатин, бета-циклодекстрин тетрадекасульфат, эпонемицин; фумагиллин, золота натрий-тиомалат d-пеницилламин (CDPT), бета-1-антиколлагеназа-сыворотка альфа 2-антиплазмин, бисантрен, лобензарит динатрий, п-2-карбоксифенил-4-хлорантрониловой кислоты динатрий или "ССА", талидомид, ангостатический стероид, карбоксиаминоимидазол, ингибиторы металлопротеиназ, такие как ВВ 94. Другие антиангиогенные агенты, которые можно применять, включают антитела, предпочтительно моноклональные антитела к следующим ангиогенным факторам роста: bFGF,aFGF, FGF-5, изоформы VEGF, VEGF-C, HGF/SF и Ang-1/Ang-2. Ferrara N. and Alitalo, K. "Clinical application of angiogenic growth factors and their inhibitors" (1999), Nature Medicine, 5:1359-1364. Алкилирующие агенты представляют собой многофункциональные соединения, которые обладают способностью замещать ионы водорода алкильными группами. Примеры алкилирующих агентов включают, но не ограничиваются перечисленными, бисхлорэтиламины (азотсодержащие иприты, например хлорамбуцил, циклофосфамид, изосфамид, мехлорэтамин, мелфалан, уроиприт), азиридины (например,тиотепа), алкил алкон сульфонаты (например, бусульфан), нитрозомочевины (например, крамустин, ломустин, стрептозоцин), неклассические алкилирующие агенты (алтретамин, декарбазин и прокарбазин),соединения платины (карбопластин и циспластин). Указанные соединения реагируют с фосфат-, амино-,гидроксил-, сульфгидрильной, карбоксильной и имидазольной группами. В физиологических условиях указанные лекарственные средства ионизируются и образуют положительно заряженный ион, который присоединяется к чувствительным нуклеиновым кислотам и белкам, что приводит к блокированию клеточного цикла и/или гибели клеток. Комбинированные терапевтические средства, включающие ингибитор HSP90 и ингибирующий агент, возможно будут оказывать синергетическое действие на раковую опухоль и обеспечивать побочные эффекты, связанные с этими химиотерапевтическими агентами. Антибиотические агенты представляют собой группу лекарственных средств, получаемых аналогично антибиотикам путем модификации природных продуктов. Примеры антибиотических агентов включают, но не ограничиваются перечисленными, антрациклины (например, доксорубицин, даунорубицин, эпирубицин, идарубицин и антрацендион), митомицин С, блеомицин, дактиномицин, пликатомицин. Такие антибиотические агенты нарушают рост клеток путем направленного воздействия на различ- 18019156 ные компоненты клетки. Например, считается, что антрациклины воздействуют на активность ДКН топоизомеразы II в областях транскрипционно активной ДНК, что приводит к появлению разрывов в нитях ДНК. Считается, что блеомицин хелатирует железо и образует активированный комплекс, который затем связывается с основаниями ДНК, что приводит к разрывам нитей и гибели клеток. Комбинированная терапия, включающая ингибитор HSP90 и антибиотический агент, возможно будет оказывать синергетическое действие на раковую опухоль и снижать побочные эффекты, связанные с указанными химиотерапевтическими агентами. Антиметаболические агенты представляют собой группу лекарственных средств, которые воздействуют на метаболические процессы, жизненно важные для физиологии и пролиферации раковых клеток. Активно пролиферирующим клеткам необходим непрерывный синтез больших количеств нуклеиновых кислот, белков, жиров и других жизненно важных компонентов клетки. Многие антиметаболиты ингибируют синтез пуриновых или пиримидиновых нуклеозидов или ингибируют ферменты репликации ДНК. Некоторые антиметаболиты воздействуют на синтез нуклеозидов и РНК RNA и/или метаболизм аминокислот, а также синтез белков. Нарушая синтез жизненно необходимых компонентов клетки, антиметаболиты могут замедлить или блокировать рост раковых клеток. Примеры антиметаболических агентов включают, но не ограничиваются перечисленными, фторурацил (5-FU), флоксуридин (5-FUdR),метотрексат, лейковорин, гидроксимочевину, тиогуанин (6-TG), меркаптопурин (6-МР), цитрабин, пентостатин, флударабин фосфат, кладрибин (2-CDA), аспарагиназу и гемцитабин. Комбинированное терапевтическое средство, включающее ингибитор HSP90 и антиметаболический агент, может оказывать синергетическое воздействие на раковые опухоли и снижать побочные эффекты, связанные с указанными химиотерапевтическими агентами. Гормональные агенты представляют собой группу лекарственных средств, которые регулируют рост и развитие соответствующих органов-мишеней. Большинство гормональных агентов составляет группа из половых стероидов и их аналогов и производных, таких как эстрогены, андрогены и прогестины. Эти гормональные агенты могут служить антагонистами рецепторов половых гормонов и снижать экспрессию рецепторов и транскрипцию жизненно важных генов. Примерами таких гормональных агентов являются синтетические эстрогены (например, диэтилстибестрол), антиэстрогены (например, тамоксивен, торемифен, флуоксиместерол и ралоксифен), антиандрогены (бикалютамид, нилютамид и длютамид), ингибиторы ароматазы (например, аминоглютетимид, анастрозол и тетразол), каетоконазол, гозерелин ацетат, лейпролин, манэстрол ацетат и мифепрестон. Комбинированное терапевтическое средство,включающее ингибитор HSP90 и гормональный агент, может оказывать синергетическое воздействие на раковое заболевание и снижать побочные эффекты, связанные с указанными химиотерапевтическими агентами. Агенты растительного происхождения представляют собой группу лекарственных средств, которые получены из растений или модифицированы на основании молекулярной структуры таких агентов. Примеры агентов растительного происхождения включают, но не ограничиваются перечисленными, алкалоиды барвинка (например, винкристин, винбластин, виндезин, винзолидин и винорелбин), подофиллотоксины (например, этопозид (VP-16) и тенипозид (VM-26 и таксаны (например, паклитаксел и доцетаксел). Эти агенты растительного происхождения обычно действуют как антимитотические агенты, которые связывают тубулин и подавляют митоз. Считается, что подофиллотоксины, такие как этопозид,нарушают синтез ДНК путем взаимодействия с топоизомеразой II, что приводит к разрывам нити ДНК. Комбинированное терапевтическое средство, включающее ингибитор HSP90 и агент растительного происхождения, может оказывать синергетическое воздействие на рак и снижать побочные эффекты, связанные с указанными химиотерапевтическими агентами. Биологические агенты представляют собой группу агентов, которые вызывают обратное развитие ракового заболевания/опухоли при использовании отдельно или в комбинации с химиотерапией и/или радиотерапией. Примеры биологических агентов включают, но не ограничиваются перечисленными,иммуномодулирующие белки, такие как цитокины, моноклональные антитела к антигеном опухолей,гены-супрессоры опухолей и противораковые вакцины. Комбинированное терапевтическое средство,включающее ингибитор HSP90 и биологический агент, может оказывать синергетическое воздействие на рак, усиливать иммунные реакции пациента на туморогенные сигналы и снижать побочные эффекты,связанные с указанными химиотерапевтическими агентами. Цитокины обладают мощной иммуномодулирующей активностью. Некоторые цитокины, такие как интерлейкин-2 (IL-2, альдеслейкин) и интерферон, продемонстрировали противоопухолевую активность и были одобрены для лечения пациентов с метастазирующей карциномой почки и метастазирующей злокачественной меланомой. IL-2 представляет собой фактор роста Т-лимфоцитов, который играет центральную роль в опосредуемых Т-лимфоцитами иммунных ответах. Считается, что селективное действиеIL-2 на некоторых пациентов является результатом клеточного иммунного ответа, который отличает"свое" от "чужого". Примеры интерлейкинов, которые можно использовать в комбинации с ингибиторами HSP90, включают, но не ограничиваются перечисленными, интерлейкин-2 (IL-2), а также интерлейкин-4 (IL-4), интерлейкин-12 (IL-12). Интерферон включает более 23 родственных подтипов с перекрывающимися активностями, причем каждый из подтипов ИФН включен в объем настоящего изобретения. ИФН продемонстрировал активность в отношении солидных опухолей и злокачественных заболеваний крови, причем последние оказались особенно чувствительными. Другие цитокины, которые можно использовать в комбинации с ингибитором HSP90, включают цитокины, которые демонстрируют глубокое воздействие на гематопоэз и иммунные функции. Примеры таких цитокинов включают, но не ограничиваются перечисленными, эритропоэтин, гранулоцит-CSF(филграстин), колониестимулирующий фактор гранулоцитов и макрофагов (саргамостим). Эти цитокины можно использовать в комбинации с ингибитором HSP90 для снижения индуцированной химиотерапией миелопоэтической токсичности. Также в комбинации с ингибитором HSP90 можно использовать другие иммуномодулирующие агенты, не относящиеся к цитокинам. Примеры таких иммуномодулирующих агентов включают, но не ограничиваются перечисленными, бациллу Кльметта-Герена, левамизол и октреодит, октапептид продолжительного действия, который имитирует эффекты природного гормона соматостатина. Моноклональные антитела к антигенам опухолей - это антитела, вырабатывающиеся в ответ на антигены, экспрессируемые опухолями, предпочтительно опухоль-специфичные антигены. Например, моноклональное антитело HERCEPTIN (Траструцумаб, Trastruzumab) вырабатывается к рецептору 2 эпидермального фактора роста человека 2 (HER2), экспрессия которого повышены в некоторых опухолях молочной железы, включая метастазирующий рак молочной железы. Повышенная экспрессия белкаHER2 ассоциирована с более агрессивным заболеванием и более неблагоприятным клиническим прогнозом. HERCEPTIN используется в качестве агента монотерапии для лечения пациентов с метастазирующим раком молочной железы, при котором экспрессия белка HER2 опухолью повышена. Комбинированная терапия, включающая ингибитор HSP90 и HERCEPTIN, может оказывать синергетическое воздействие на опухоли, в частности на метастатические раковые опухоли. Другим примером моноклональных антител к антигенам опухоли является RITUXAN (ритуксимаб), которые вырабатывается в ответ на CD20 на клетках лимфомы и селективно снижает количество нормальных и злокачественных CD20+ пре-В и зрелых В-лимфоцитов. RITUXAN используют отдельно для лечения пациентов с рецидивирующей или рефрактерной низкодифференцированной или фолликулярной CD20+, В-клеточной неходжкинской лимфомой. Комбинированное терапевтическое средство,включающее ингибитор HSP90 и RITUXAN возможно будет оказывать синергетическое воздействие не только на лимфому, но также на другие виды и типы злокачественных опухолей. Гены-супрессоры опухолей представляют собой гены, которые подавляют рост клеток и циклы деления, предотвращая, таким образом, развитие новообразования. Мутации в генах-супрессорах опухолей приводят к тому, что клетки не реагируют на один или более компонентов сети ингибирующих сигналов,преодолевают контрольные точки клеточного цикла, что приводит к более интенсивному контролируемому росту клеток - раку. Примеры генов-супрессоров опухолей включают, но не ограничиваются перечисленными, DPC-4, NF-1, NF-2, RB, p53, WT1, BRCA1 и BRCA2. DPC-4 участвует в развитии рака поджелудочной железы и участвует в цитоплазматических механизмах подавления деления клеток. NF-1 кодирует булок, который подавляет Ras, ингибиторный белок цитоплазмы. NF-1 участвует в развитии нейрофибром и феохромацитом нервной системы, а также миелоидной лейкемии. NF-2 кодирует ядерный фактор, который участвует в развитии менингиомы, шванномы и эпендиомы нервной системы. RB кодирует белок pRB, ядерный фактор, который является основным ингибитором клеточного цикла. RB участвует в развитии ретинобластомы, а также рака кости, мочевого пузыря, мелкоклеточного рака легкого, а также рака молочной железы. р 53 кодирует белок р 53, который регулирует деление клеток и может вызвать апоптоз. Мутации и/или инактивация р 53 обнаруживаются в разнообразных раковых опухолях. WT1 участвует в развитии опухоли Вильмса (рак почки). BRCA1 участвует в развитии рака молочной железы и яичников, a BRCA2 участвует в развитии рака молочной железы. Гены-супрессоры опухолей могут быть перенесены в клетки опухолей, где они осуществляют свою функцию по подавлению опухоли. Комбинированное терапевтическое средство, включающее ингибитор HSP90 и супрессор опухоли, возможно, будет оказывать синергетические эффекты на пациентов с различными раковыми опухолями. Противораковые вакцины представляют собой группу агентов, которые вызывают специфический иммунный ответ организма на опухоли. Большинство исследуемых, разрабатываемых и проходящих клинические испытания противораковых вакцин представляют собой опухоль-ассоциированные антигены (ТАА). ТАА - это структуры (т.е. белки, ферменты или углеводы), которые присутствуют на опухолевых клетках или отсутствуют или присутствуют в меньших количествах на нормальных клетках. Благодаря тому что эти структуры являются достаточно уникальными для клеток опухоли, ТАА обеспечивают мишени, которые иммунная система может распознавать и разрушать. Примеры ТАА включают, но не ограничиваются перечисленными, ганглиозиды (GM2), простата-специфичный антиген (PSA), фетопротеин (AFP), онкофетальный антиген (СЕА) (продуцируемый опухолями толстой кишки и другими, например опухолями молочной железы, легкого, желудка и поджелудочной железы), антигены, ассоциированные с меланомой (MART-1, gp100, MAGE 1,3 тирозиназа), фрагменты Е 6 и Е 7 папилломавиру- 20019156 са, целые клетки или части/лизаты антологичных клеток опухоли и аллогенных клеток опухоли. Для усиления иммунного ответа на ТАА можно использовать адъювант. Примеры адъювантов включают, но не ограничиваются перечисленными, бациллу Кальметта-Герена (BCG), эндотоксинылипополисахариды, гемоцианин улитки (GKLH), интерлейкин-2 (IL-2), колониестимулирующий фактор гранулоцитов-макрофагов (GM-CSF) и цитоксан, химиотерапевтический агент, который в низких дозах,как считают, снижает индуцируемую опухолью иммуносупрессию. Композиции, включающие ингибиторы HSP90. В сочетании с соединениями согласно настоящему изобретению можно использовать разнообразные композиции и пути введения. Такие композиции могут включать в дополнение к соединению согласно настоящему изобретению обычные фармацевтические наполнители и другие фармацевтически неактивные агенты. Дополнительно, композиции могут включать активные агенты в дополнение к соединениям согласно настоящему изобретению. Такие дополнительные агенты могут включать дополнительные соединения согласно настоящему изобретению и/или один или более других фармацевтических агентов. Композиции могут иметь газообразную, жидкую, полужидкую или твердую форму и изготовлены таким образом, чтобы быть пригодными для выбранного пути введения. Для перорального введения обычно используют капсулы и таблетки. Для парентерального введения обычно используют восстановленные лиофилизированные порошки, приготовленные, как описано в настоящем патенте. Композиции, включающие соединения согласно настоящему изобретению, можно вводить или вводить совместно перорально, парентерально, интраперитонеально, внутривенно, внутриартериально,трансдермально, сублингвально, через слизистые, ректально, трансбуккально, интраназально, с использованием липосом, путем ингаляции, вагинально, в глаз, путем местной доставки (например, при помощи катетера или стента), подкожно, в жировую ткань, в сустав или в трахею. Соединения и/или композиции согласно настоящему изобретению можно также вводить или вводить совместно в лекарственных формах с замедленным высвобождением. Ингибиторы HSP90 и включающие их композиции можно вводить или вводить совместно в любой стандартной лекарственной форме. Совместное введение в контексте настоящего изобретения обозначает введение более одного терапевтических агентов, один из которых включает ингибитор HSP90, в ходе согласованного лечения для достижения улучшенного клинического результата. Такое совместное введение может быть одновременным, т.е. происходить в перекрывающиеся периоды времени. Растворы или суспензии, используемые для парентерального, внутрикожного, подкожного или топического введения, могут необязательно включать один или более из следующих компонентов: стерильный разбавитель, такой как вода для инъекций, солевой раствор, нелетучее масло, полиэтиленгликоль, глицерин, пропиленгликоль или другие синтетические растворители; антимикробные агенты, такие как бензиловый спирт и метилпарабены; антиоксиданты, такие как аскорбиновая кислота и бисульфит натрия; хелатирующие агенты, такие как этилендиаминтетрауксусная кислота (ЭДТА); буферы, такие как ацетаты, цитраты и фосфаты; средства для регулирования тоничности, такие как хлорид натрия или декстроза, и средства для регулирования кислотности и щелочности композиции, такие как щелочные или кислые агенты, например карбоната, бикарбоната, фосфаты, соляная кислота и органические кислоты, такие как уксусная кислота и лимонная кислота. Препараты для парентерального введения могут быть дополнительно заключены в ампулы, одноразовые шприцы или сосуды, содержащие одну или множество доз, выполненные из стекла, пластика или другого подходящего материала. В случае, когда соединения согласно настоящему изобретению недостаточно растворимы, можно использовать методы солюбилизации соединений. Такие методы известны специалистам и включают, но не ограничиваются перечисленными, использование сорастворителей, таких как диметилсульфоксид(ДМСО), использование поверхностно-активных веществ, таких как TWEEN, или растворение в водном бикарбонате натрия. Производные соединений, такие как пролекарства соединений, также можно использовать для изготовления эффективных фармацевтических композиций. После смешивания или добавления соединений согласно настоящему изобретению в композицию возможно образуется раствор, суспензия, эмульсия или нечто подобное. Форма полученной композиции будет зависеть от ряда факторов, включая предполагаемый путь введения и растворимость соединения в выбранном носителе или среде. Эффективная концентрация, необходимая для снижения выраженности заболевания, которое лечат, может быть определена эмпирическим путем. Композиции согласно настоящему изобретению могут быть необязательно представлены в виде лекарственных форм для введения человеку и животным, таких как таблетки, капсулы, пилюли, порошки,сухие порошки для ингаляторов, гранулы, стерильные растворы или суспензии для парентерального введения, растворы и суспензии для перорального введения, эмульсии вода-масло, содержащие подходящее количество соединений, в частности фармацевтически приемлемых солей соединений. Фармацевтически терапевтически активные соединения обычно изготавливают и вводят в виде лекарственных форм, содержащих одну дозу или множество доз. Лекарственные формы, содержащие одну дозу, в настоящем описании включают физически раздельные объекты, пригодные для введения животным и человеку и упакованные, как принято в данной области. Каждая единичная доза содержит заранее определенное количество терапевтически активного соединения, достаточное для того, чтобы обеспечить желаемый терапевтический эффект, в комбинации с необходимым фармацевтическим носителем, средой или разбавителем. Примеры лекарственных форм, содержащих одну дозу, включают ампулы и шприцы, отдельно упакованные таблетки и капсулы. Лекарственные формы, содержащие одну дозу, можно вводить частями или по несколько. Лекарственные формы, содержащие множество форм, представляют собой множество идентичных форм, содержащих одну дозу, упакованных в один контейнер для введения отдельных форм с одной дозой. Примеры лекарственных форм, содержащих множество доз, включают сосуды и бутылки таблеток или капсул или бутылок объемом пинта или галлон. Таким образом, лекарственная форма, содержащая множество доз, представляет собой множество лекарственных форм, содержащих одну дозу, которые не разделены в упаковке. В дополнение к одному или более соединениям согласно настоящему изобретению композиция может включать разбавитель, такой как лактоза, сахароза, дикальция фосфат или карбоксиметилцеллюлоза; смазывающее вещество, такое как стеарат магния, стеарат кальция и тальк; и связующее вещество,такое как крахмал, натуральные смолы, гуммиарабик, желатин, глюкоза, молассы, поливинилпирролидон, целлюлозы и их производные, повидон, кросповидоны и другие подобные связующие вещества,известные специалистам. Жидкие композиции для фармацевтического применения могут, например,быть приготовлены путем растворения, диспергирования или другого вида смешивания определенного выше активного соединения и необязательных фармацевтических вспомогательных веществ, таких как носители, например вода, физ. раствор, водный раствор декстрозы, гликоли, этанол и т.п., с образованием растворов или суспензий. При желании, фармацевтическая композиция для введения может содержать незначительные количества вспомогательных веществ, таких как смачивающие агенты или солюбилизирующие агенты, эмульгирующие агенты, рН-буферные агенты, такие как, например, ацетат, цитрат натрия, производные циклодекстрина, сорбитан монолаурат, триэтаноламин натрия ацетат, триэтаноламин олеат и другие подобные агенты. Актуальные способы получения таких лекарственных форм известны или будут очевидны для специалиста в соответствующей области; например, см. Remington:The Science and Practices of Pharmacy, Lippincott Williams, and Wilkins Publisher, 21st edition, 2005. Композиции и составы для введения будут в любом случае содержать количество ингибитора по настоящему изобретению, достаточное для снижения активности HSP90 in vivo, и, таким образом, обеспечения лечения болезненного состояния субъекта. Лекарственные формы или композиции могут необязательно включать одно или более соединений согласно настоящему изобретению в диапазоне от 0.005 до 100% (мас./мас.), а также дополнительные вещества, такие как вещества, указанные в настоящем описании. Для перорального применения фармацевтически приемлемая композиция может необязательно включать любой один или более используемых обычно наполнителей, таких как, например, маннитол, лактоза, крахмал, стеарат магния, тальк, производные целлюлозы, натрий-кроскармеллозу, глюкозу, сахарозу, карбонат магния, стеарин натрия,тальк фармацевтического качества. Такие композиции включают растворы, суспензии, таблетки, порошки, сухие порошки для ингаляторов и составы с замедленным высвобождением, такие как, но не ограничиваясь перечисленными, импланты и микроинкапсулированные системы доставки, биоразрушаемые и биосовместимые полимеры, такие как коллаген, этиленвинилацетат, полиангидриды, полигликолевая кислота, полиортоэфиры, полимолочная кислота и др. Способы приготовления таких составов известны специалистам в соответствующей области. Композиции могут необязательно включать 0.01-100%(мас./мас.) одного или более ингибиторов HSP90, возможно 0.1-95%, и возможно 1-95%. Соли, предпочтительно натриевые соли, могут быть приготовлены с носителями, носителей, которые защищают соединение от быстрого выведения из организма, например составы или оболочки с контролируемым высвобождением. Составы могут дополнительно включать другие активные соединения,что обеспечит желаемые комбинации свойств. А. Составы для перорального введения. Лекарственные формы для перорального введения могут быть твердыми, гелеобразными или жидкими. Примеры твердых лекарственных форм включают, но не ограничиваются перечисленными, таблетки, капсулы, гранулы и нерасфасованные порошки. Более конкретные примеры таблеток для перорального применения включают прессованные жевательные пастилки и таблетки, которые могут быть покрыты оболочкой, растворяющейся в кишечнике, сахаром или пленкой. Гранулы и порошки могут быть представлены в нешипучей и шипучей формах. Каждый из вышеперечисленных ингредиентов можно комбинировать с ингредиентами, известными в соответствующей области. В некоторых вариантах осуществления соединения согласно настоящему изобретению производятся в твердой лекарственной форме, предпочтительно в форме капсул или таблеток. Таблетки, пилюли,капсулы, пастилки и т.п. могут необязательно содержать один или более из следующих ингредиентов или соединений сходной природы: связующий компонент; разбавитель; дезинтегратор; лубрикант; вещество, улучшающее скольжение; подсластитель и вкусовую добавку. Примеры связующих компонентов, которые можно использовать, включают, но не ограничиваются перечисленными, следующее: микрокристаллическая целлюлоза, трагакантовая камедь, раствор глюкозы, растительная слизь акации, раствор желатина, сахарозы и крахмальный клейстер. Примеры лубрикантов, которые можно использовать, включают, но не ограничиваются перечисленными, следующее: тальк, крахмал, магния или кальция стеарат, ликоподиевая кислота и стеариновая кислота. Примеры разбавителей, которые можно использовать, включают, но не ограничиваются перечисленными, следующее: лактоза, сахароза, крахмал, каолин, соль, маннитол и дикальций фосфат. Примеры глидантов, которые можно использовать, включают, но не ограничиваются перечисленными, следующее: коллоидный диоксид кремния. Примеры улучшителей распадаемости, которые можно использовать, включают, но не ограничиваются перечисленными, следующее: кроскамеллоза натрия, карбоксиметилкрахмал натрия, альгиновая кислота, кукурузный крахмал, картофельный крахмал, бентонит, метилцеллюлоза, агар и карбоксиметилцеллюлоза. Примеры красящих добавок, которые можно использовать, включают, но не ограничиваются перечисленными, любые из красителей для пищевых и косметических продуктов, их смесей; и суспензия водорастворимых красителей классов FD и С в гидратированном оксиде алюминия. Примеры подсластителей, которые можно использовать, включают, но не ограничиваются перечисленными, следующее: сахароза, лактоза, маннитол и искусственные подсластители, такие как цикламат натрия и сахарин, и любое количество высушенных распылением вкусовых добавок. Примеры вкусовых добавок, которые можно использовать, включают, но не ограничиваются перечисленными, натуральные вкусовые добавки, экстрагированные из растений, таких как фрукты, и синтетические смеси, обладающие приятным вкусом, такие как, но не ограничивающиеся ими, перечная мята и метилсатицилат. Примеры смачивающих агентов, которые можно использовать, включают, но не ограничиваются перечисленными, пропиленгликоль моностеарат, сорбитан моноолеат, диэтиленгликоль монолаурат, полиоксиэтилен лаурил эфир. Примеры противорвотных покрытий, которые можно использовать, включают, но не ограничиваются перечисленными, жирные кислоты, жиры, мази, шеллак, насыщенный аммиаком шеллак и ацетатфталат целлюлозы. Примеры пленочных покрытий, которые можно использовать, включают, но не ограничиваются перечисленными, гидроксиэтилцеллюлозу, натрия карбоксиметилцеллюлозу, полиэтиленгликоль 4000 и ацетатфталат целлюлозы. Если желательно пероральное введение, соль данного соединения может быть необязательно получена в композиции, защищающей ее от воздействия кислой среды желудка. Например, композиция может быть произведена в кишечнорастворимой оболочке, которая поддерживает ее целостность в желудке и высвобождает активное соединение в кишечнике. Композиция также может быть получена в комбинации с антацидным или другим подобным ингредиентом. В случае если единицей лекарственной формы является капсула, она может необязательно дополнительно включать жидкий носитель, такой как жирное масло. В дополнение, единицы лекарственной формы могут необязательно дополнительно содержать различные другие материалы, которые изменяют физическую форму единицы лекарственной формы, например, покрытия из сахара или других энтеральных агентов. Соединения согласно настоящему изобретению также можно вводить в качестве компонента эликсира, суспензии, сиропа, облатки, разбрызгиваемой жидкости, жевательной резинки или других. Сироп может необязательно содержать, в дополнение к активным соединениям, сахарозу в качестве подсластителя и определенные консерванты, красители, красящие добавки и вкусовые добавки. Соединения согласно настоящему изобретению могут также быть перемешаны с другими активными материалами, которые не обладают нужным действием, или с материалами, которые дополняют нужное действие, такие как антациды, Н 2 блокаторы и диуретики. Например, если соединение используют для лечения астмы или гипертензии, оно может быть использовано с другими бронхорасширяющими и противогипертензивными средствами соответственно. Примеры фармацевтически приемлемых носителей, которые могут входить в состав таблеток, содержащих соединения согласно настоящему изобретению, включают, но не ограничиваются перечисленными, связующие компоненты, лубриканты, разбавители, дезинтеграторы, красящие добавки, вкусовые добавки и увлажнители. Таблетки, покрытые кишечнорастворимым покрытием, из-за кишечнорастворимого покрытия не подвержены воздействию кислот желудка и растворяются или распадаются в нейтральной или щелочной среде кишечника. Таблетки с сахарным покрытием могут быть прессованными таблетками, к которым присоединяют различные слои фармацевтически приемлемых веществ. Таблетки,покрытые пленкой, могут быть прессованными таблетками, покрытыми полимером или другим подходящим покрытием. Различные прессованные таблетки могут быть прессованными таблетками, полученными с помощью одного или более циклов компрессии, использующих фармацевтически приемлемые вещества, упомянутые ранее. Красящие вещества могут также применяться при производстве таблеток. Вкусовые добавки и подсластители могут применяться при производстве таблеток, и особенно полезны при производстве жевательных таблеток и пастилок. Примеры жидких пероральных лекарственных форм, которые можно использовать, включают, но не ограничиваются перечисленными, водные растворы, эмульсии, суспензии, растворы и/или суспензии,восстановленные из нешипучих гранул, и шипучие препараты, восстановленные из шипучих гранул. Примеры водных растворов, которые можно использовать, включают, но не ограничиваются перечисленными, эликсиры и сиропы. Здесь термин "эликсиры" относится к прозрачным, подслащенным,водно-спиртовым препаратам. Примеры фармацевтически приемлемых носителей, которые можно использовать в эликсирах, включают, но не ограничиваются перечисленными, сольвенты. Частные примеры сольвентов, которые можно использовать, включают глицерин, сорбитол, этиловый спирт и сироп. Здесь термин "сиропы" относится к концентрированным водным растворам сахара, например сахарозе. Сиропы могут необязательно также содержать консерванты. Термин "эмульсии" относится к двухфазным системам, в которых одна жидкость распределена в форме маленьких шариков в другой жидкости. Эмульсии могут необязательно быть эмульсиями типа"масло в воде" и типа "вода в масле". Примеры фармацевтически приемлемых носителей, которые можно использовать в эмульсиях, включают, но не ограничиваются перечисленными, не водные жидкости,эмульгирующие агенты и консерванты. Примеры фармацевтически приемлемых веществ, которые можно использовать в нешипучих гранулах, из которых восстанавливают жидкую оральную лекарственную форму, включают разбавители,подсластители и увлажнители. Примеры фармацевтически приемлемых веществ, которые можно использовать в шипучих гранулах, из которых восстанавливают жидкую оральную лекарственную форму, включают органические кислоты и источник двуокиси углерода. Подкрашивающие и вкусовые добавки могут необязательно использоваться во всех указанных выше лекарственных формах. Частные примеры консервантов, которые можно использовать, включают глицерин, метил и пропилпарабен, бензойную кислоту, бензоат натрия и спирт. Частные примеры не водных жидкостей, которые можно использовать в эмульсиях, включают минеральное масло и хлопковое масло. Частные примеры эмульгирующих агентов, которые можно использовать, включают желатин, акацию, трагакант, бентонит и поверхностно-активные вещества, такие как полиоксиэтилен сорбитан моноолеат. Частные примеры суспендирующих агентов, которые можно использовать, включают натрия карбоксиметилцеллюлозу, пектин, трагакант, вигум и акацию. Разбавители включают лактозу и сахарозу. Подсластители включают сахарозу, сиропы, глицерин и искусственные подсластители, такие как натрия цикламат и сахарин. Частные примеры увлажнителей, которые можно использовать, включают пропиленгликоль моностеарат, сорбитан моноолеат, диэтилен гликоль монолаурат и полиоксиэтилен лаурил эфир. Частные примеры органических кислот, которые можно использовать, включают лимонную кислоту и винную кислоту. Источники двуокиси углерода, которые можно использовать, в шипучих композициях включают натрия бикарбонат и натрия карбонат. Красящие агенты включают любые из красителей для пищевых и косметических продуктов и их смесей. Частные примеры вкусовых добавок, которые можно использовать, включают экстрагированные из растений, таких как фрукты, и синтетические смеси, обладающие приятным вкусом. Для твердой лекарственной формы, раствора или суспензии, например в пропиленкарбонате, растительном масле или триглицеридах, такую форму предпочтительно заключают в твердую или мягкую желатиновую капсулу. Такие растворы, препараты и их формы в капсулах раскрыты в патентах США 4328245; 4409239 и 4410545. Для жидкой лекарственной формы, раствора, например в полиэтиленгликоле, соединение может быть разбавлено достаточным количеством фармацевтически приемлемого жидкого носителя, например воды, чтобы обеспечить легкость дозирования для введения. В альтернативном варианте жидкие или полутвердые составы для перорального введения могут быть приготовлены путем растворения или диспергирования активного соединения в растительных маслах, гликолях, триглицеридах, эфирах пропиленгликоля (например, пропиленкарбонате) и других подобных носителях, а также путем заключения таких растворов или суспензий в твердые или мягкие желатиновые оболочки капсул. Другие подходящие формы включают формы, раскрытые в патентах США 28819 и 4358603. В. Инъецируемые составы, растворы и эмульсии. Настоящее изобретение также относится к композициям, предназначенным для введения соединения согласно настоящему изобретению парентеральным путем, обычно характеризующимся подкожными, внутримышечными или внутривенными инъекциями. Композиции для введения путем инъекций могут быть получены в любой обычной форме, например в форме жидкого раствора или суспензии, твердых форм, пригодных для растворения или суспендирования в жидкости перед введением путем инъекции, или в форме эмульсий. Примеры наполнителей, которые можно использовать в сочетании с композициями для введения путем инъекции согласно настоящему изобретению, включают, но не ограничиваются перечисленными,воду, физиологический раствор, декстрозу, глицерин и этанол. Композиции для введения путем инъекции могут необязательно включать небольшие количества нетоксичных вспомогательных веществ, таких как смачивающие или эмульгирующие агенты, рН-буферные вещества, солюбилизаторы, стабилизаторы,вещества, улучшающие растворимость и другие подобные агенты, такие как, например, ацетат натрия,сорбитан монолаурат, триэтаноламин олеат и циклодекстрины. Также в настоящем изобретении предусмотрена имплантация систем с медленным высвобождением или продолжительным высвобождением,которые обеспечивают поддержание постоянного уровня дозировки (см., например, патент США 3710795). Процентная доля активного соединения, содержащегося в таких композициях для парентерального введения, в большой степени зависит от природы композиции, а также от активности соединения и потребностей субъекта. Парентеральное введение составов включает внутривенное, подкожной и внутримышечное введение. Препараты для парентерального введения включают стерильные растворы, готовые для введения путем инъекции, стерильные сухие растворимые продукты, такие как описанные в настоящем патенте лиофилизированные порошки, готовые для смешивания с растворителем перед введением, включая подкожные таблетки, стерильные суспензии, готовые для введения путем инъекции, стерильные сухие нерастворимые продукты, готовые для смешивания со средой непосредственно перед введением, и стерильные эмульсии. Растворы могут быть либо водными, либо неводными. В случае внутривенного введения, примеры подходящих носителей включают, но не ограничиваются перечисленными, физиологический раствор или фосфатный буферной раствор (ФБР) и растворы,содержащие загустители и солюбилизирующие агенты, такие как глюкоза, полиэтиленгликоль и пропиленгликоль, а также их смеси. Примеры фармацевтически приемлемых носителей, которые можно использовать в препаратах для парентерального введения, включают, но не ограничиваются перечисленными, водные среды, неводные среды, антимикробные агенты, изотонические агенты, буферы, антиоксиданты, местные анастетики, суспендирующие и диспергирующие агенты, эмульгирующие агенты, секвестрирующие или хелатирующие агенты, а также другие фармацевтически приемлемые вещества. Примеры водных сред, которые можно использовать, включают раствор хлорид натрия для инъекций, раствор Рингера для инъекций, изотонический раствор декстрозы для инъекций, стерильную воду для инъекций, раствор Рингера для инъекций с лактатом и декстрозой. Примеры неводных сред для парентерального введения, которые можно использовать, включают нелетучие масла растительного происхождения, хлопковое масло, кукурузное масло, кунжутное масло и кокосовое масло. В парентеральные препараты можно добавлять антимикробные агенты в бактериостатических или фунгистатических концентрациях, в частности, в случаях, когда такие препараты упакованы в контейнеры, содержащие множество доз, и таким образом предназначены для хранения и извлечения множества аликвот. Примеры антимикробных агентов, которые можно использовать, включают фенолы или крезолы, ртутные препараты, хлорбутанол, метиловый и пропиловый эфиры p-гидроксибензойной кислоты,тимеросал, бензалкония хлорид и бензэтония хлорид. Примеры изотонических агентов, которые можно использовать, включают хлорид натрия и декстрозу. Примеры буферов, которые можно использовать, включают фосфат и цитрат. Примеры антиоксидантов, которые можно использовать, включают бисульфат натрия. Примеры местных анастетиков, которые можно использовать, включают прокаин гидрохлорид. Примеры суспендирующих и диспергирующих агентов, которые можно использовать, включают натрий-карбоксиметилцеллюлозу, гидроксипропил метилцеллюлозу и поливинилпирролидон. Примеры эмульгирующих агентов, которые можно использовать, включают Полисорбат 80 (TWEEN 80). Агенты, секвестрирующие или хелатирующие ионы металлов, включают ЭДТА. Фармацевтические носители могут также необязательно включать этиловый спирт, полиэтиленгликоль и пропиленгликоль для смешивающихся с водой сред и гидроксид натрия, серную кислоту, лимонную кислоту или молочную кислоту для контроля pH. Концентрацию ингибитора в составе для парентерального введения можно регулировать таким образом, чтобы инъекция обеспечивала введение фармацевтически эффективного количества, обеспечивающего желаемый фармакологический эффект. Точная концентрация ингибитора и/или доза в конечном счете зависеть от возраста, массы и состояния пациента или животного, как известно в соответствующей области. Препараты для парентерального введения, содержащие одну дозу, могут быть упакованы в ампулу,склянку или шприц с иглой. Все препараты для парентерального введения должны быть стерильными,как известно в данной области. Инъецируемые формы могут быть предназначены для местного или системного введения. Обычно терапевтически эффективная доза содержит концентрацию от по меньшей мере около 0.1 до около 90% мас./мас. или более предпочтительно более 1% мас./мас. ингибитора HSP90 в ткани (тканях), кото- 25019156 рые лечат. Ингибиторы можно вводить за один прием или разделить на несколько более мелких доз и вводить через некоторые промежутки времени. Очевидно, что точная доза и продолжительность лечения будут зависеть от участка, в которые композицию вводят парентерально, носителя и других факторов,которые могут быть определены экспериментально с использованием известных протоколов тестирования или путем экстраполяции экспериментальных данных in vivo или in vitro. Следует отметить, что значения дозировок и концентраций также могут варьировать в зависимости от возраста субъекта, которого лечат. Дополнительно следует понимать, что конкретные режимы дозирования со временем может быть необходимо скорректировать, чтобы он соответствовал индивидуальным потребностям конкретного субъекта и профессиональному мнению лица, которое вводит или руководит введением составов. Соответственно, следует понимать, что указанные в настоящем описании диапазоны концентраций приведены исключительно в качестве примера и не предполагают ограничения объема или осуществления заявленных составов. Ингибитор HSP90 может необязательно быть суспендирован в микронизированной или другой подходящей форме или может быть дериватизирован с получением более растворимого активного продукта или пролекарства. Форма полученной смеси зависит от ряда факторов, включая предполагаемые путь введения и растворимость соединения в выбранном носителе или среде. Эффективная концентрация является достаточной для облегчения симптомов болезненного состояния и может быть определена эмпирически.C. Лиофилизированные порошки. Соединения согласно настоящему изобретению могут также быть приготовлены в форме лиофилизированных порошков, которые могут быть восстановлены для введения в форме растворов, эмульсий и других смесей. Лиофилизированные порошки также могут быть изготовлены в твердой форме или в форме гелей. Стерильные лиофилизированные порошки могут быть приготовлены путем растворения соединения в натрий-фосфатном буферном растворе, содержащем декстрозу или другой подходящий наполнитель. Последующая стерильная фильтрация раствора, за которой следует лиофилизация в обычных условиях, известных специалистам в соответствующей области, обеспечивает получение желаемых растворов. Вкратце, лиофилизированный порошок может, но не обязательно, быть приготовлен путем растворения декстрозы, сорбита, фруктозы, кукурузной патоки, ксилитола, глицерина, глюкозы, сахарозы или других подходящих агентов в количестве примерно 1-20%, предпочтительно примерно от 5 до 15%, в подходящем буфере, таком как цитратный, натрий- или калий-фосфатный буфер или другие известные буферы, обычно приблизительно при примерно нейтральном рН. Затем к полученной смеси добавляют ингибитор HSP90, предпочтительно при температуре выше комнатной, предпочтительно приблизительно при 30-35C, и перемешивают до растворения. Полученную смесь разбавляют путем добавления дополнительного количества буфера до желаемой концентрации, полученную смесь подвергают стерильной фильтрации или обрабатывают для удаления твердых частиц, чтобы обеспечить стерильность, и распределяют в сосуды для лиофилизации. Каждый сосуд может содержать одну дозу или множество доз ингибитора.D. Составы для местного введения. Соединения согласно настоящему изобретению также можно вводить в форме смесей для топического применения. Смеси для местного применения могут включать смеси для местного и системного введения. Конечные смеси могут представлять собой раствор, суспензию, эмульсию и т.д. и могут иметь форму кремов, гелей, мазей, эмульсий, эликсиров, лосьонов, суспензий, настоев, паст, пен, аэрозолей,жидкостей для спринцевания, спреев, суппозиториев, бандажей, кожных пластырей или могут представлять собой другую форму для топического введения. Ингибиторы HSP90 могут быть изготовлены в форме аэрозолей для топического введения, например, путем ингаляции (см. патенты США 4044126, 4414209 и 4364923, в которых описаны аэрозоли для доставки стероидов, которые можно применять для лечения воспалительных заболеваний, в частности астмы). Такие состав для введения в дыхательные пути могут иметь форму аэрозоля или раствора для небулайзера, или представлять собой ультратонкий порошок для вдыхания, отдельно или в комбинации с инертным носителем, таким как лактоза. В таких случаях частицы лекарственной формы будут обычно иметь диаметр менее 50 мкм, предпочтительно менее 10 мкм. Ингибиторы также могут быть изготовлены в форме для местного или топического применения,например, для топического нанесения на кожу и слизистые оболочки, например, в глазу, в форме гелей,кремов и лосьонов для нанесения на глаз или для интрацестернального или интраспинального введения. Топическое введение предполагается для чрескожной доставки в глаза или слизистую оболочку, для ингаляционных средств терапии. Также можно использовать растворы ингибитора HSP90 отдельно или в комбинации с другими фармацевтическими наполнителями для назального введения. Е. Составы для других путей введения. В зависимости от болезненного состояния, которое лечат, можно использовать другие пути введения, такие как местное нанесение трансдермальные пластыри и ректальное введение. Например, лекарственные формы для ректального введения представляют собой ректальные суппозитории, капсулы и таб- 26019156 летки для системного действия. Ректальные суппозитории в настоящем описании обозначают твердые тела для введения в прямую кишку, которые плавятся или размягчаются при температуре тела с высвобождением одного или более фармацевтически или терапевтически активных ингредиентов. Фармацевтически приемлемые вещества, которые можно применять в ректальных суппозиториях, представляют собой основы или носители, или вещества, повышающие точку плавления. Примеры оснований включают какао-масло, глицерин-желатин, карбовакс (полиоксиэтиленгликоль) и подходящие смеси моно- и диглицеридожирных кислот. Можно использовать комбинации различных оснований. Средства, повышающие точку плавления, включают спермацет и воск. Ректальные суппозитории могут быть получены либо путем прессования, либо формованием. Обычно масса ректального суппозитория составляет примерно от 2 до 3 г. Таблетки и капсулы для ректального введения могут быть изготовлены с использованием тех же фармацевтически приемлемых веществ и теми же методами, что и в случаях составов для перорального введения.F. Примеры составов. Ниже приведены конкретные примеры составов для перорального, внутривенного введения и таблеток, которые необязательно можно использовать для соединений согласно настоящему изобретению. Следует отметить, что эти составы могут варьировать в зависимости от конкретного используемого соединения и показаний, при которых это соединение предполагают применять. Состав для перорального введения Соедининие согласно настоящему изобретению 10-100 мг Моногидрат лимонной кислоты 105 мг Гидроксид натрия 18 мг Ароматизатор Вода в достаточном количестве до 100 мл Составы для внутривенного введения Соедининие согласно настоящему изобретению 0.1-10 мг Декстроза моногидрат в достаточном количестве до получения изотонического раствора Моногидрат лимонной кислоты 1.05 мг Гидроксид натрия 0.18 мг Вода для инъекций в достаточном количестве до 1,0 мл Составы в форме таблеток Дозировка, хозяин и безопасность. Соединения согласно настоящему изобретению стабильны и их применение безопасно. В частности, соединения согласно настоящему изобретению можно применять в качестве ингибиторов HSP90 у разнообразных субъектов (например, людей, млекопитающих, не являющихся людьми и не являющихся млекопитающими). Оптимальная доза может варьировать в зависимости от таких событий, как, например, тип субъекта, масса тела субъекта, тяжесть состояния, путь введения и специфические свойства конкретного соединения, которое используют. Обычно, приемлемые и эффективные дозы представляют собой количество,достаточное для того, чтобы эффективно замедлять или устранять состояние, которое лечат. Обычно,ежедневная доза для перорального введения взрослому (масса тела около 60 кг) составляет приблизительно от 1 до 1000 мг, приблизительно от 3 от 300 мг или приблизительно от 10 до 200 мг. Очевидно,что ежедневную дозу можно вводить одной или несколькими (например, 2 или 3) порциями в день. Получение ингибиторов HSP90. Могут быть разработаны различные способы получения соединений согласно настоящему изобретению. Типичные способы синтеза таких соединений приведены в разделе "Примеры". Однако необходимо отметить, что соединения согласно настоящему изобретению могут также быть получены с использованием других способов синтеза, разработанными другими специалистами. Схемы синтеза соединений согласно настоящему изобретению. Соединения согласно настоящему изобретению могут быть получены с использованием приведенных ниже схем реакций. Специалист в соответствующе области сможет легко разработать другие схемы реакции. Также очевидно, что для оптимизации выходов данных реакций могут быть использованы различные растворители, температуры и другие условия реакций. В описанных ниже реакциях может быть необходимой защита реакционных функциональных групп, например, гидрокси, амино, имино, тио или карбоксигрупп, в случае, когда желательно их присутствие в конечном продукте, чтобы избежать их нежелательного участия в реакциях. Можно использовать стандартные защитные группы в соответствии со стандартными процедурами, которые описаны,например, в P.G.M. Wuts and T.W. Greene in "Greene's Protective Groups in Organic Synthesis", 4th edition,- 27019156John Wiley and Sons, 2007. Схема 1 Приготовление дигидрохиназолинон оксим эфира Реакция альдегида 1 А с ацетон-производным 1 В дает енон 1 С (этап 1). Обработка енона 1 С малонат-производным 1D с последующей сапонификацией и декарбоксилированием дает винилоговую кислоту 1E (этап 2). С-ацилирование хлорангидридом 1F дает трион 1G (этап 3). Обработка 1G гуанидином в присутствии пирролидина дает дигидрохиназолинон 1 Н (этап 4). Реакция сочетания Сузуки с бороновым эфиром 1I (этап 5) дает соединение 1J. Реакция с алкоксиамином 1K в рефлюксируемом пиридине(этап 6) и, в случае необходимости, снятие защиты (этап 7) дает оксим эфир 1L. Хиральное разделение путем сверхкритической жидкостной хроматографии дает оба энантиомера, 1 М и 1N. Схема 2 Получение дигидропиридопиримидинон оксим эфира Реакция альдегида 2 А с хиральным сульфинамидом 2 В в присутствии тетраэтоксида титана дает имин 2 С (этап 1). Обработка сульфинамида только реагентом Реформатского 2D дает хиральный сульфинамид 2 Е (этап 2), после чего проводят катализируемое кислотой снятие с получением хиральной бета-аминокислоты 2F (этап 3). Реакция амина с функционализированным дикитеном 2G дает амид 2 Н(этап 4), после чего осуществляют обработку метоксидом с образованием продукта конденсации Дикма- 28019156 на 2I (этап 5). Реакция винилоговой кислоты 2I с ацетилгуанидином дает продукт конденсации 2J (этап 6). Превращение лактама 2J в тиолактам 2K осуществляют с использованием реагента Леви или Лоуссона (этап 7). Превращение тиолактама 2K в амидин 2 М осуществляют путем обработки замещенным алкоксиамином 2L (этап 8). Наконец, реакция сочетания Сузуки с бороновым эфиром 2N (этап 9) и, в случае необходимости, удаление защиты (этап 10) дает конечный продукт 2 О. Схема 3 Получение дигидроизохинолинон оксим эфира Реакция альдегида 3 А с ацетон-производным 3 В дает енон 3 С (этап 1). Обработка енона 3 С малонат-производным 3D с последующей сапонификацией и декарбоксилированием дает винилоговую кислоту 3 Е (этап 2). С-ацилирование хлорангидридом 3F дает трион 3G (этап 3). Ацетилирование винилоговой кислоты дает 3 Н (этап 4), которое, в свою очередь, обрабатывают малононитрилом в основной среде с получением 3I (этап 5). Обработка биснитрила 3I аммиаком дает аминопиридин 3J (этап 6). Реакция сочетания Сузуки с бороновым эфиром 3K (этап 7) дает соединение 3L. Реакция с алкоксиамином 3 М в дефлегмируемом пиридине (этап 8) и, в случае необходимости, снятие защиты (этап 9) дает оксим эфир 3N. Хиральное разделение путем сверхкритической жидкостной хроматографии дает оба энантиомера, 3 О и 3 Р. Далее, 3L можно подвергнуть описанной ниже серии трансформаций с получением различных групп R7. Аминопиридин 3L защищают в форме ацетил-производного 3Q (этап 10). Обработка нитрила 3Q HCl дает кислоту 3R (этап 11). Перегруппировка Куртиса, стимулируемая дифенилфосфорилазидом(этап 12), дает анилин 3S. Наконец, анилин 3S может быть превращен в фенол 3 Т с использованием реагентов Зандмейера. Любое из промежуточных соединений 3Q, 3R, 3S и 3 Т может быть функционализировано, как показано в этапах 8 и 9 с получением соответствующих оксимэфиров, с последующим хиральным разделением путем сверхкритической жидкостной хроматографии.
МПК / Метки
МПК: A61P 35/00, A61K 31/519, A61K 31/517, C07D 487/04, C07D 239/84
Метки: ингибиторов, качестве, hsp90, оксима, производные
Код ссылки
<a href="https://eas.patents.su/30-19156-proizvodnye-oksima-v-kachestve-ingibitorov-hsp90.html" rel="bookmark" title="База патентов Евразийского Союза">Производные оксима в качестве ингибиторов hsp90</a>
Предыдущий патент: Способ получения биоэтанола из лигноцеллюлозного растительного исходного материала
Следующий патент: Пылевая камера
Случайный патент: Изготовление элементов с низким коэффициентом трения