Соединения и композиции в качестве ингибиторов протеинкиназы
Номер патента: 18484
Опубликовано: 30.08.2013
Авторы: Пэй Вэй, Ву Баогэнь, Цзян Тао, Мишелли Пьерр-Ив, Нгуйен Трук Нгок, Чжу Сюфэн
Формула / Реферат
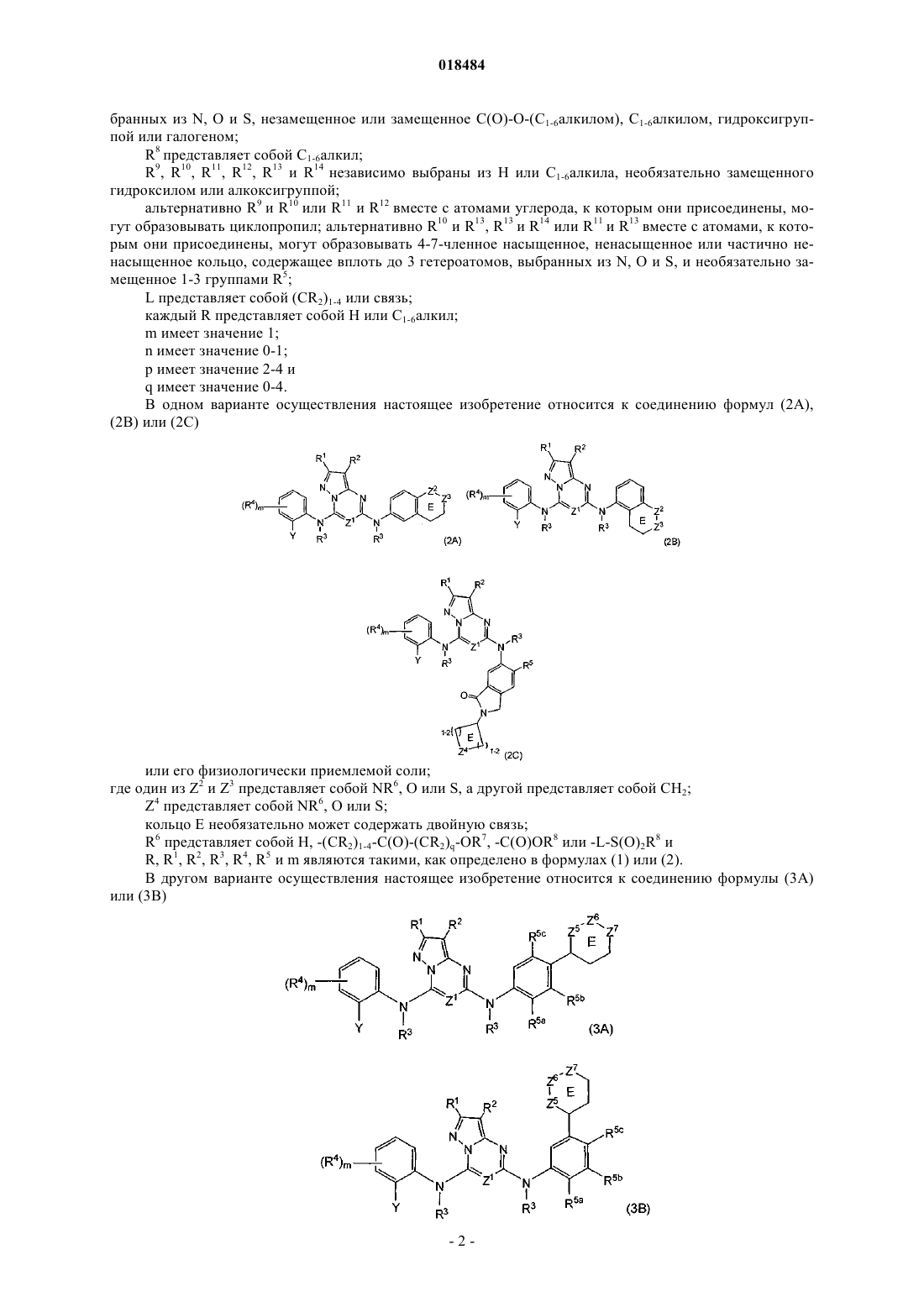
1. Соединение формул (1) или (2)
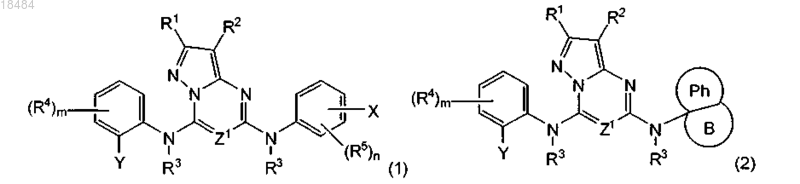
или его физиологически приемлемая соль;
где X представляет собой 5-6-членный гетероарил, замещенный C1-6алкилом; 6-членное гетероциклическое кольцо, содержащее NR6 или О; или (CR2)0-4CR(NRR7)(CO2R7);
Y представляет собой S(O)0-2R8;
Z1 представляет собой N или CH;
Ph представляет собой фенил и
В представляет собой 5-6-членное кольцо, необязательно содержащее NR6, О, =O или S;
R1, R2, R3 и R4 представляют собой H;
R5 представляет собой H, галоген, гидроксил, C1-6алкил или C1-6алкоксигруппу;
R6 представляет собой H, C1-6алкил, незамещенный или замещенный галогеном, аминогруппой или гидроксилом; -L-W, где W представляет собой циклопропил, тетрагидропиранил, тетрагидротиопиранол или пиразол, незамещенный или замещенный C1-6алкилом; -L-C(O)-R7; -L-C(O)-NRR7; -L-C(O)-CR(R7)-NRR7; -L-S(O)2R8 или радикал, выбранный из формул (а) или (b)
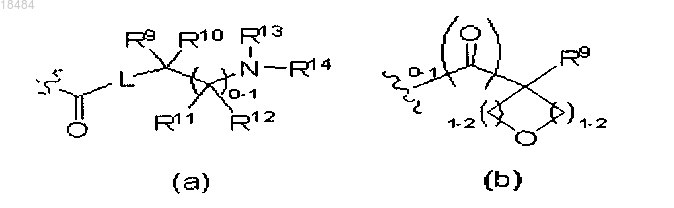
R7 представляет собой H; C1-6алкил, незамещенный или замещенный гидроксигруппой; или (CR2)q-W', где W' представляет собой 5-6-членное гетероциклическое кольцо, содержащее 1-3 гетероатома, выбранных из N, О и S, незамещенное или замещенное C(O)-O-(C1-6алкилом), C1-6алкилом, гидроксигруппой или галогеном;
R8 представляет собой C1-6алкил;
R9, R10, R11, R12, R13 и R14 независимо выбраны из Н или C1-6алкила, необязательно замещенного гидроксилом или алкоксигруппой; альтернативно R9 и R10 или R11 и R12 вместе с атомами углерода, к которым они присоединены, могут образовывать циклопропил; альтернативно R10 и R13, R13 и R14 или R11 и R13 вместе с атомами, к которым они присоединены, могут образовывать 4-7-членное насыщенное, ненасыщенное или частично ненасыщенное кольцо, содержащее вплоть до 3 гетероатомов, выбранных из N, О и S, и необязательно замещенное 1-3 группами R5;
L представляет собой (CR2)1-4 или связь;
каждый R представляет собой H или C1-6алкил;
m имеет значение 1;
n имеет значение 0-1;
р имеет значение 2-4 и
q имеет значение 0-4.
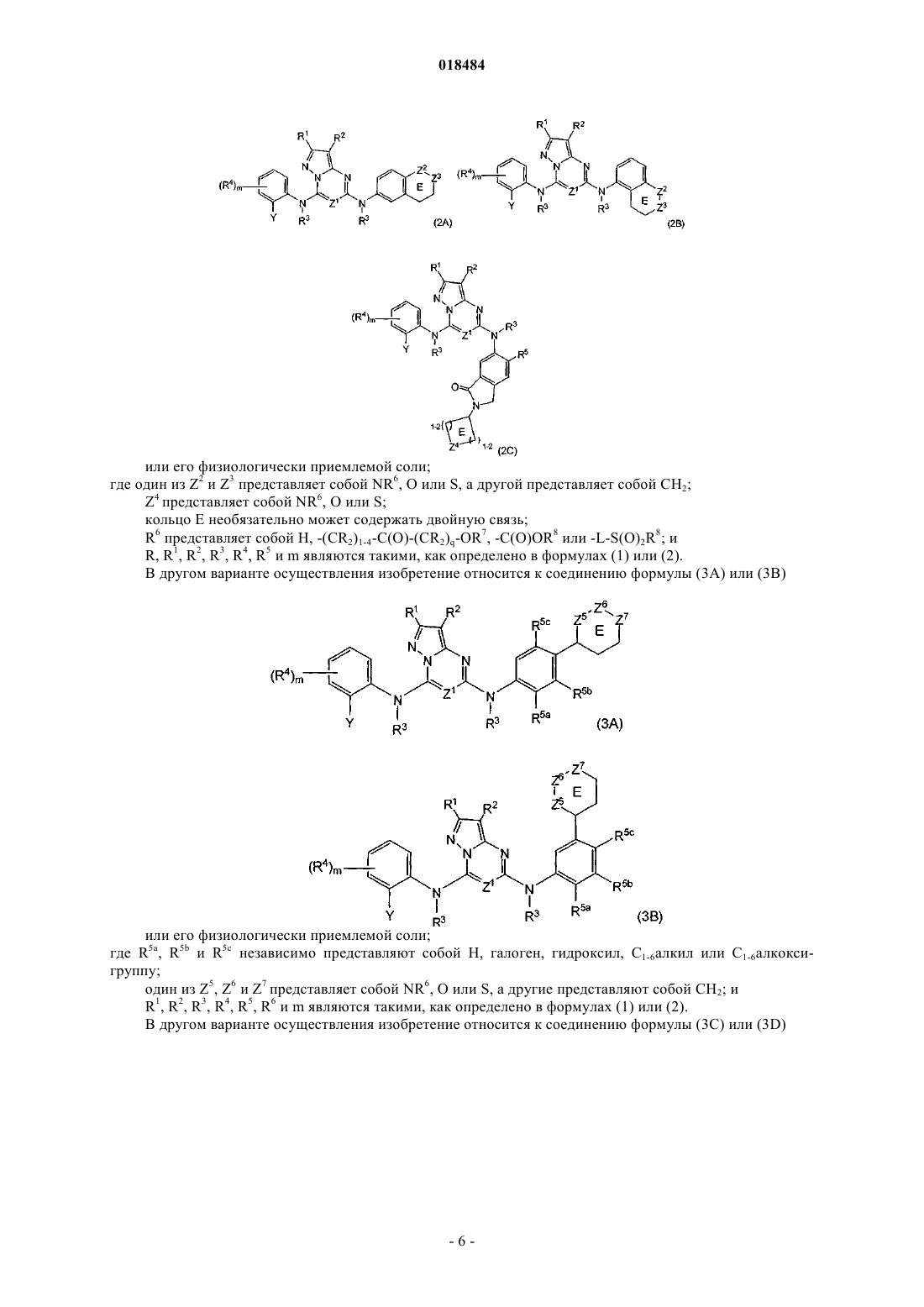
2. Соединение по п.1, где указанное соединение имеет формулы (2А), (2В) или (2С)
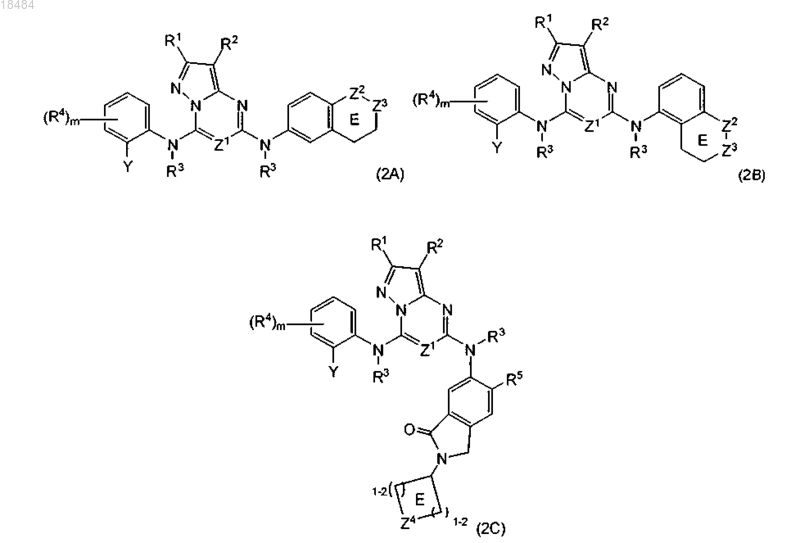
или его физиологически приемлемая соль;
где один из Z2 и Z3 представляет собой NR6, О или S, а другой представляет собой CH2;
Z4 представляет собой NR6, О или S;
кольцо Е необязательно может содержать двойную связь;
R6 представляет собой H, -(CR2)1-4-C(O)-(CR2)q-OR7, -C(O)OR8 или -L-S(O)2R8 и
R, R1, R2, R3, R4, R5 и m являются такими, как определено в п.1.
3. Соединение по п.1, где указанное соединение имеет формулы (3A) или (3B)
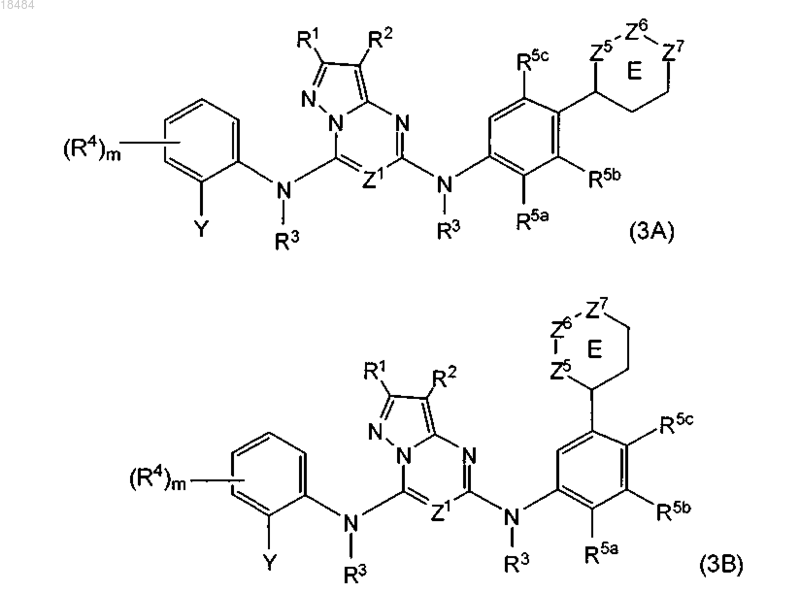
или его физиологически приемлемая соль;
где R5a, R5b и R5с независимо представляют собой H, галоген, гидроксил, C1-6алкил или C1-6алкоксигруппу;
один из Z5, Z6 и Z7 представляет собой NR6, О или S, а другие представляют собой CH2; и
R1, R2, R3, R4, R5, R6 и m являются такими, как определено в п.1.
4. Соединение по п.3, где Z7 представляет собой NR6 или О и Z5 и Z6 представляют собой CH2.
5. Соединение по п.3, где R5b представляет собой H и R5a и R5c независимо представляют собой галоген, гидроксил, C1-6алкил или C1-6алкоксигруппу.
6. Соединение по п.1, где указанное соединение имеет формулы (3C) или (3D)
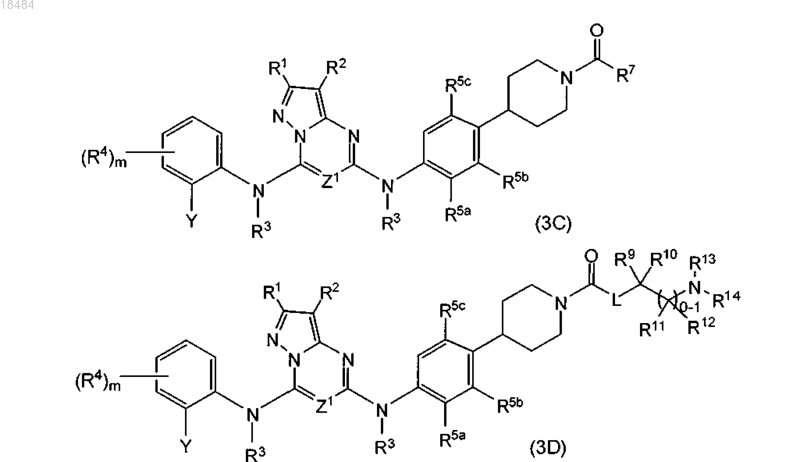
или его физиологически приемлемая соль.
7. Соединение по любому одному из пп.1-6, где Z1 представляет собой N.
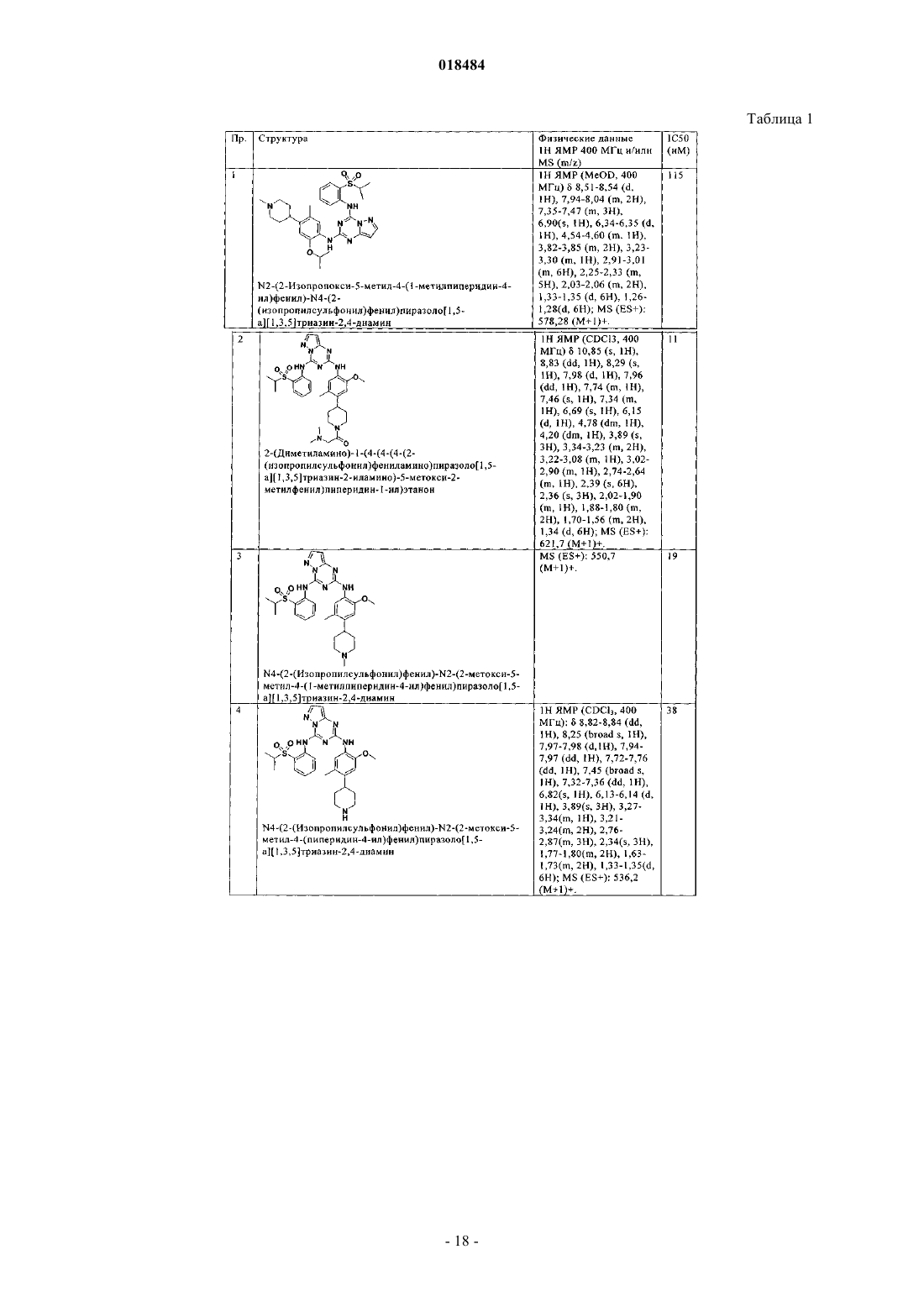
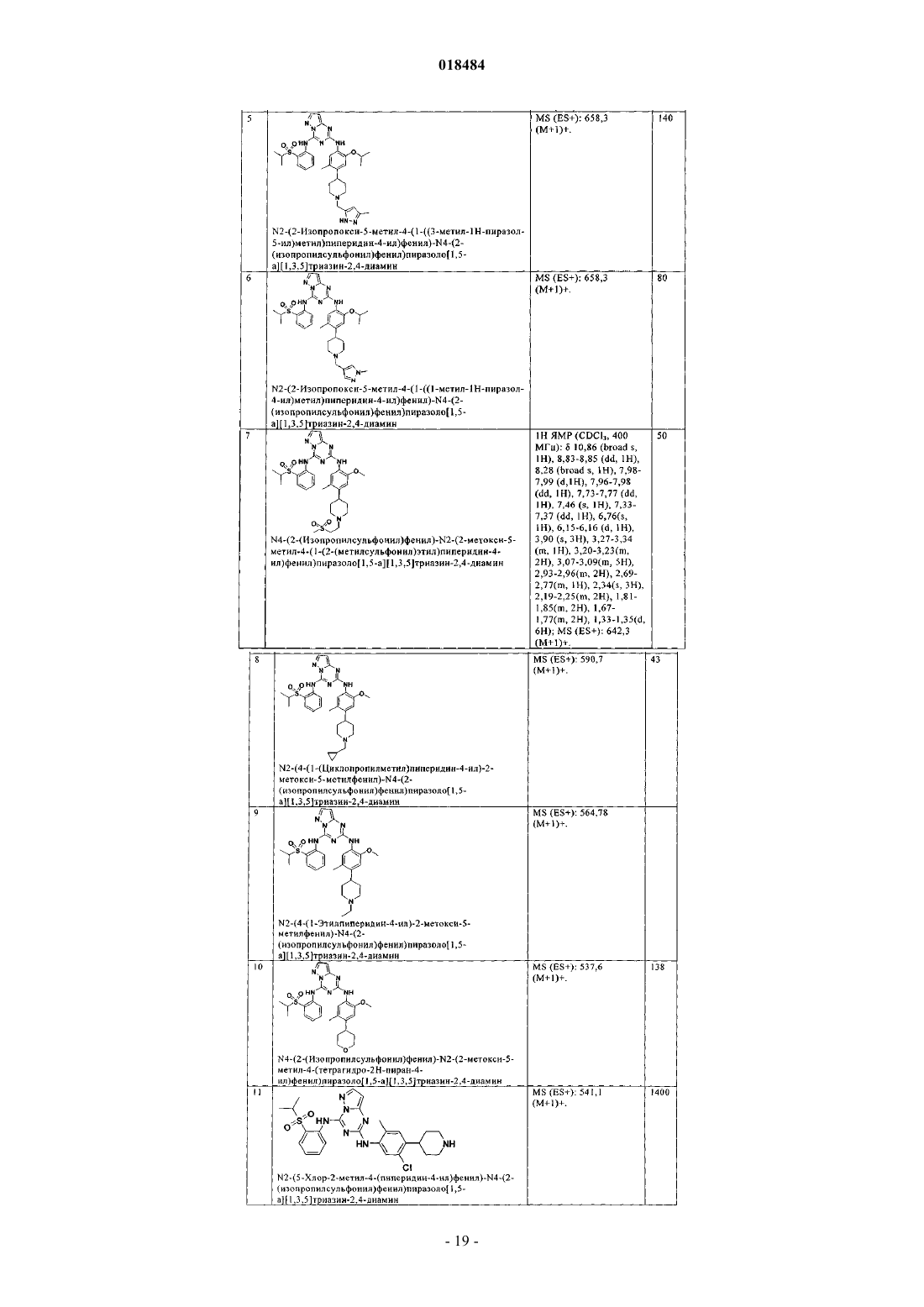
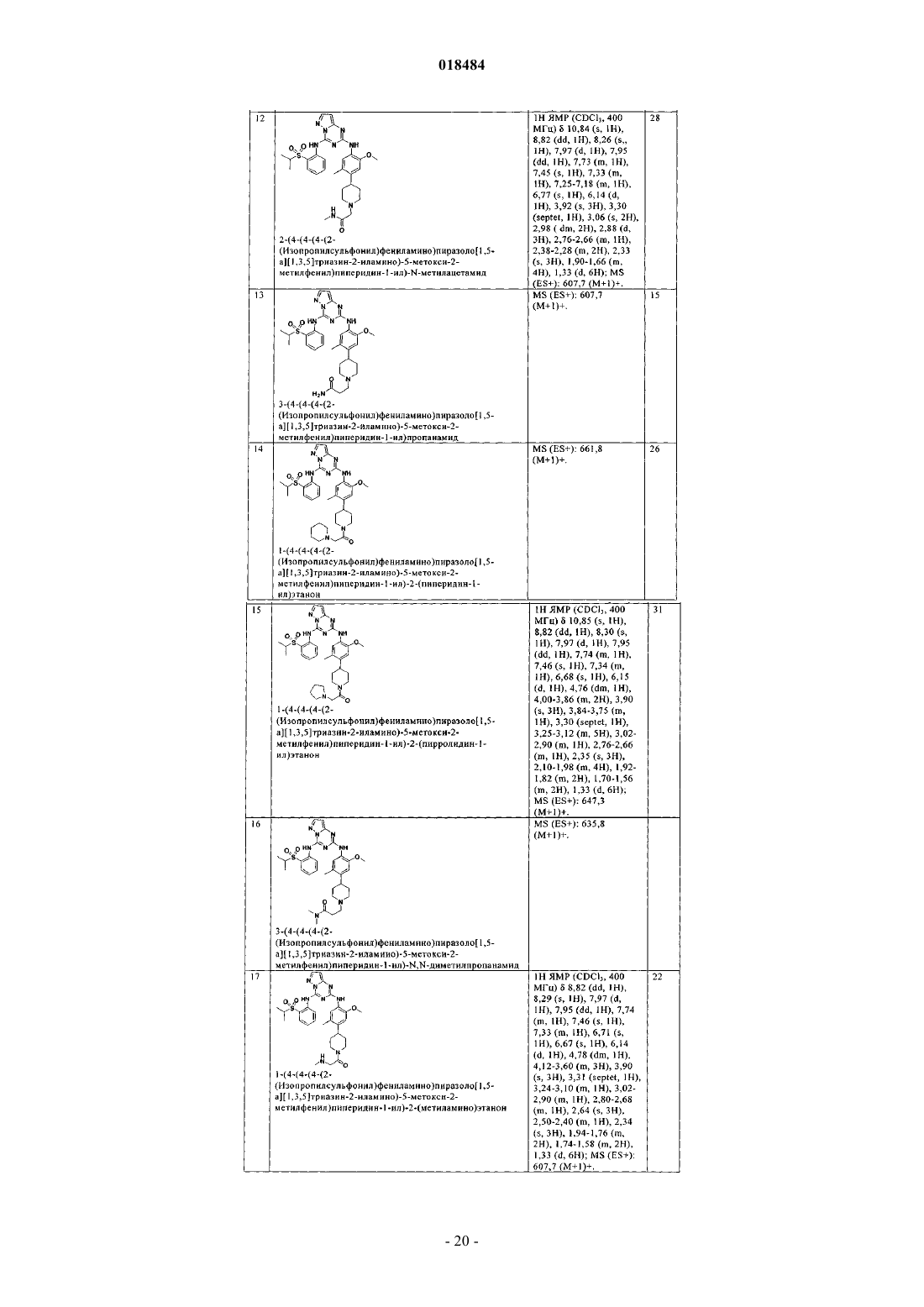
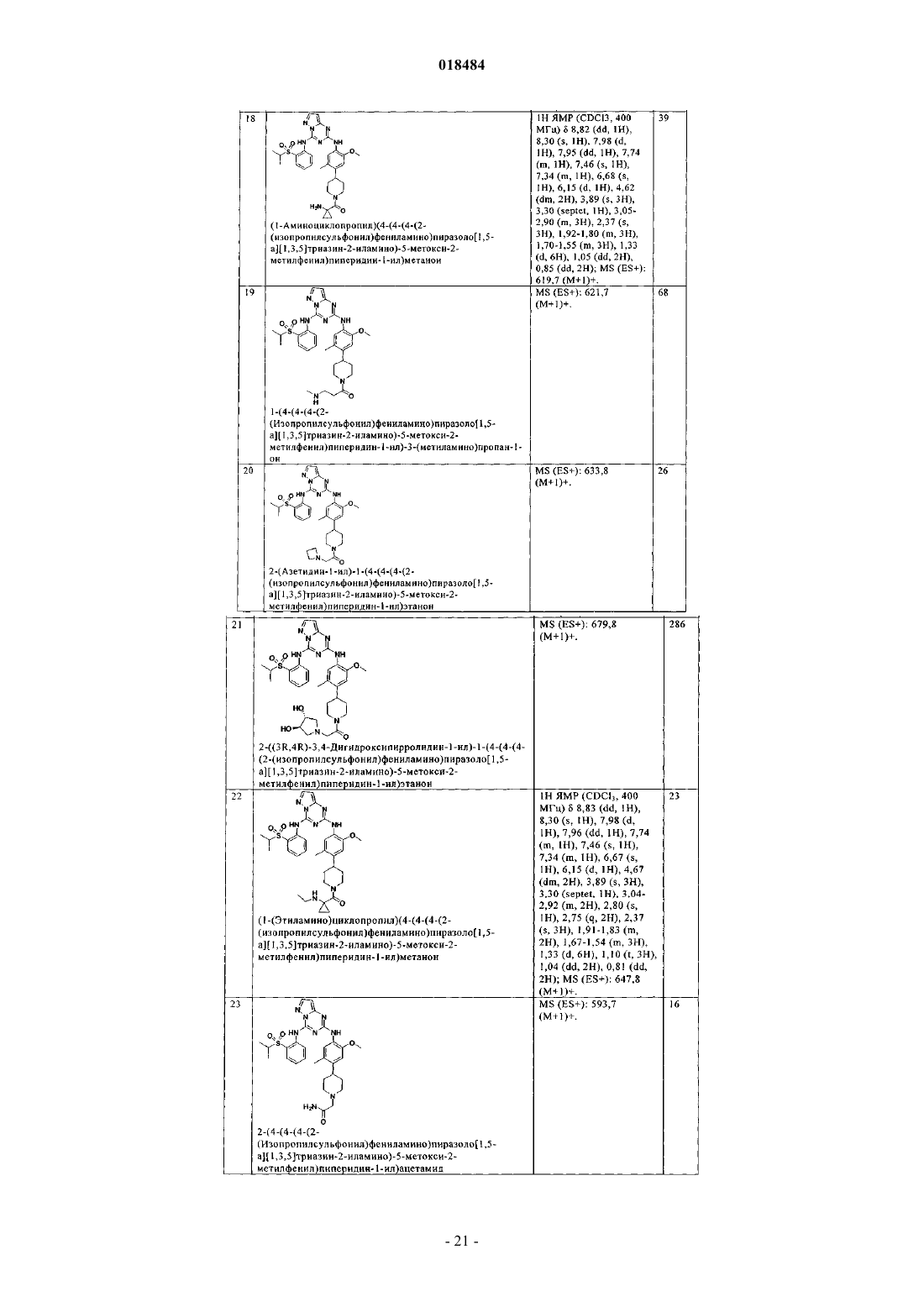
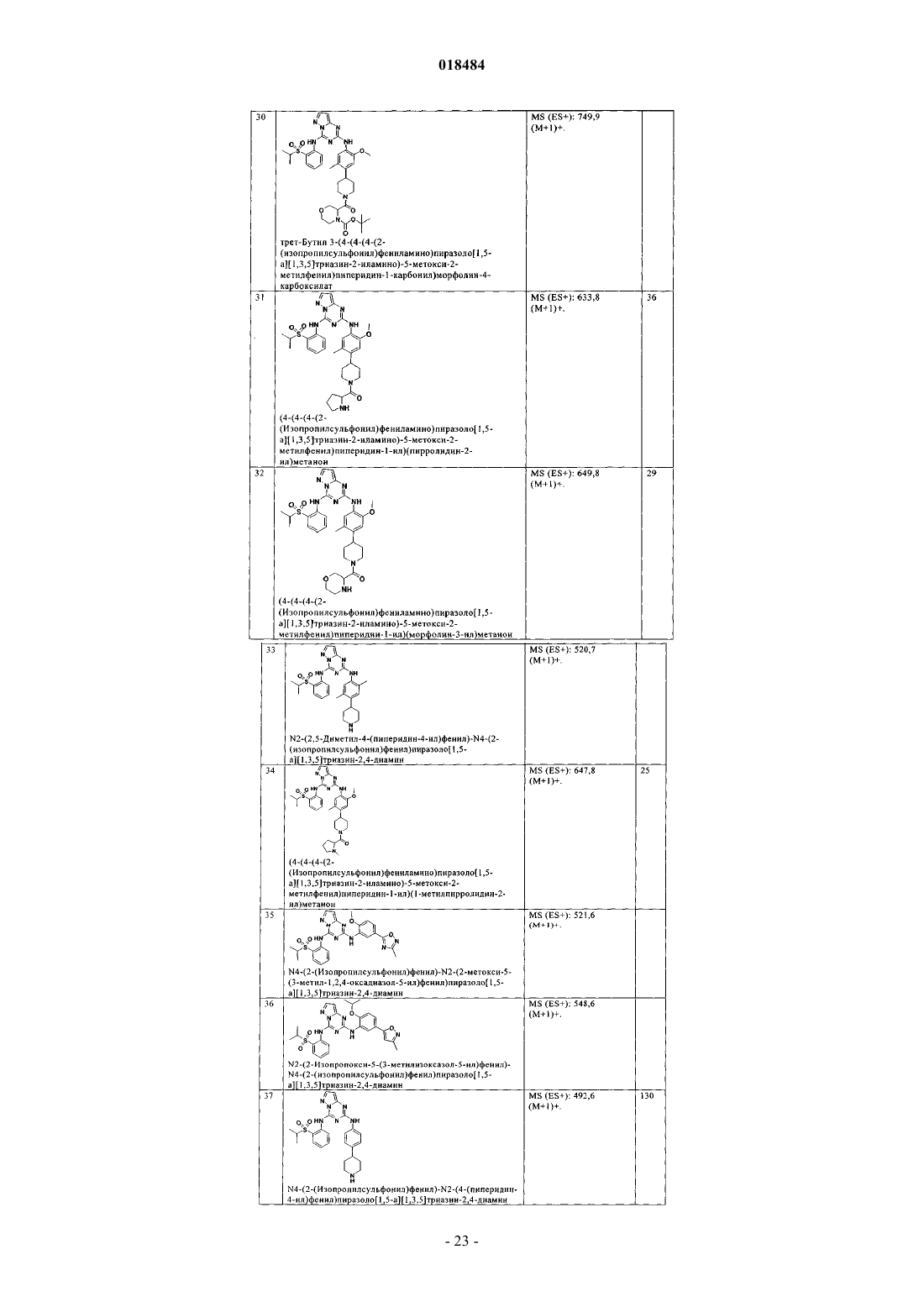
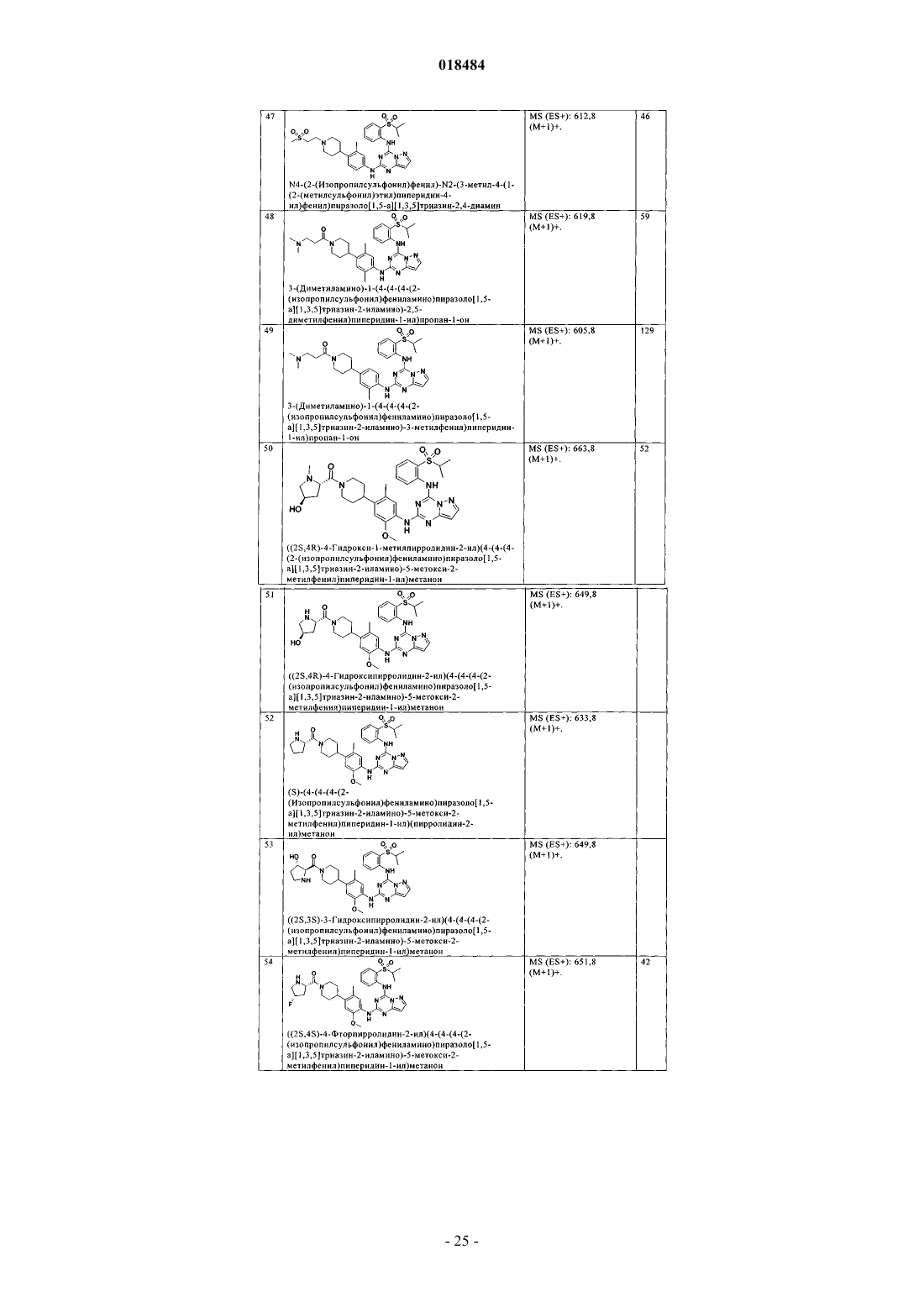
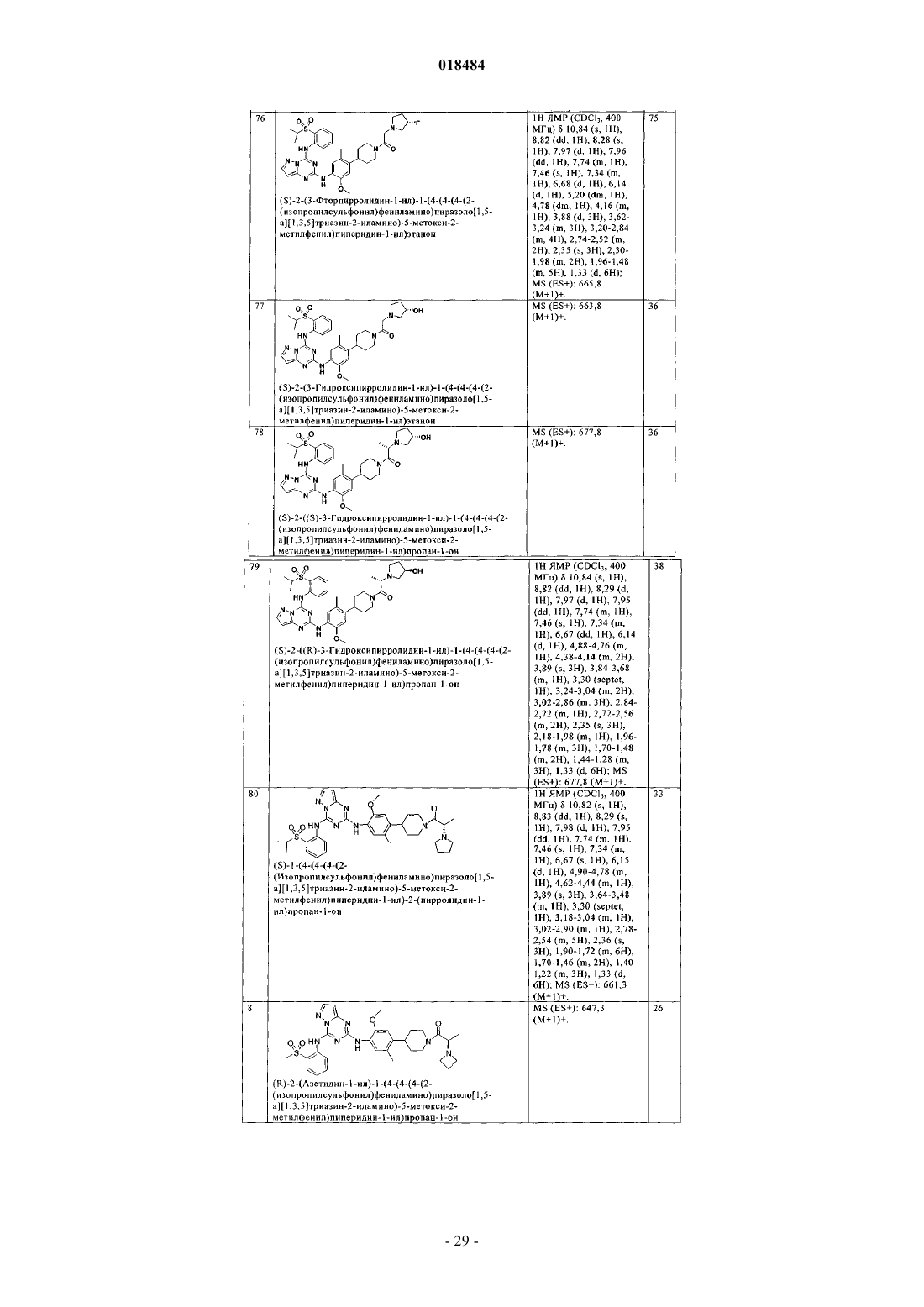
8. Соединение по п.1, где указанное соединение выбрано из группы, состоящей из следующих соединений:
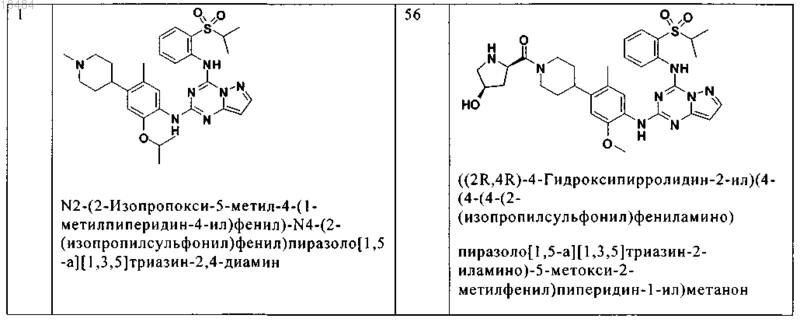
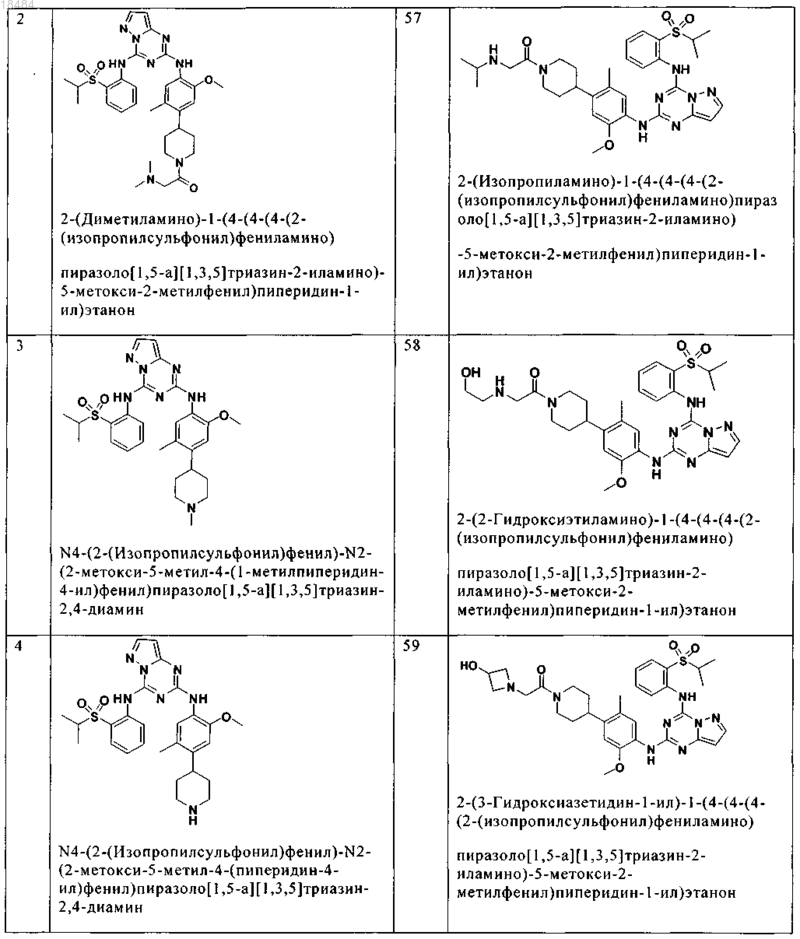
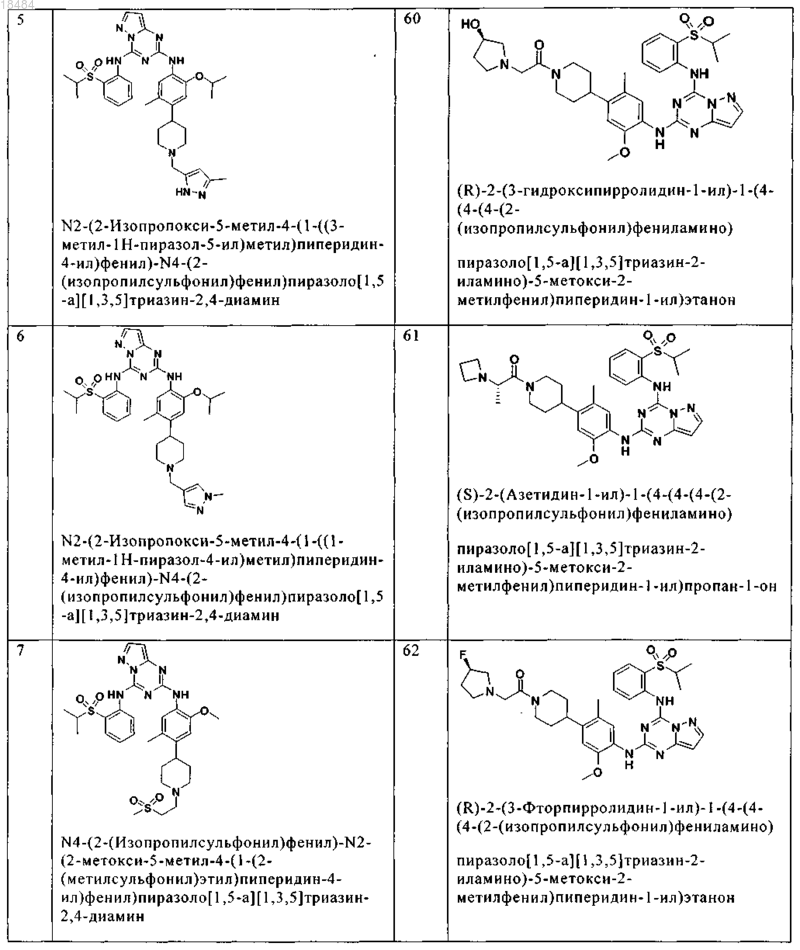
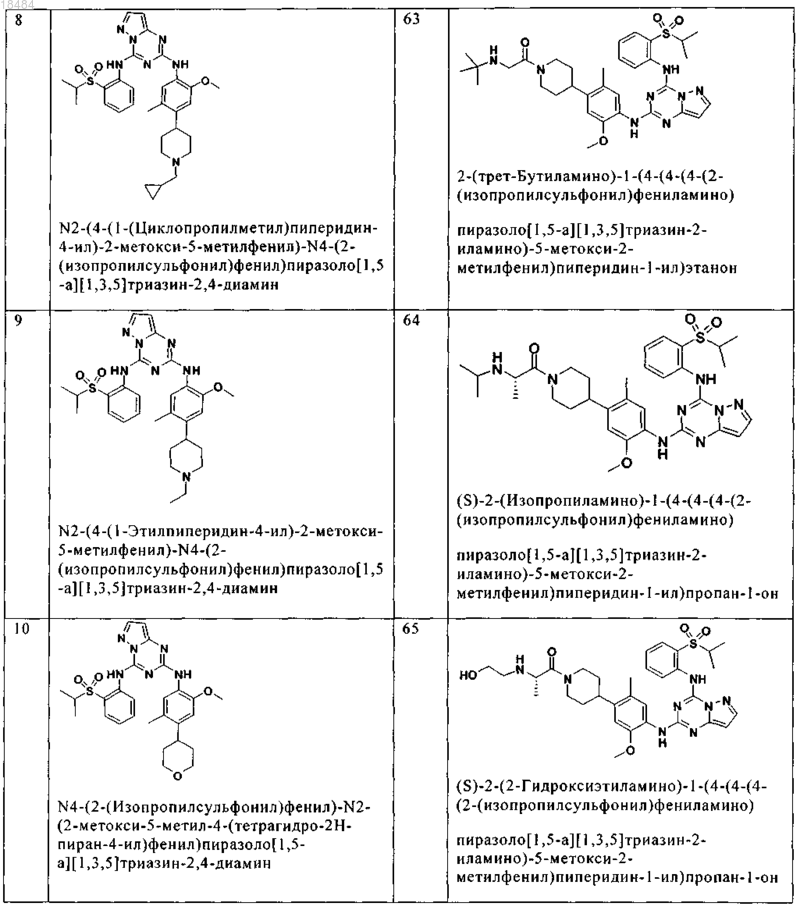
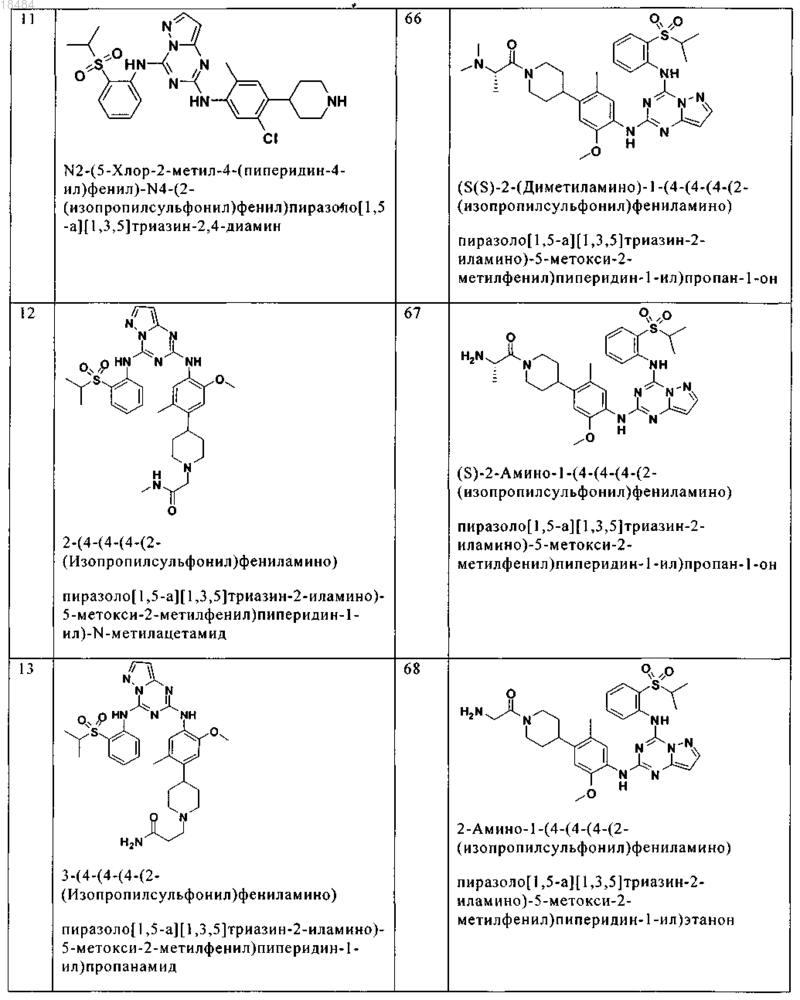

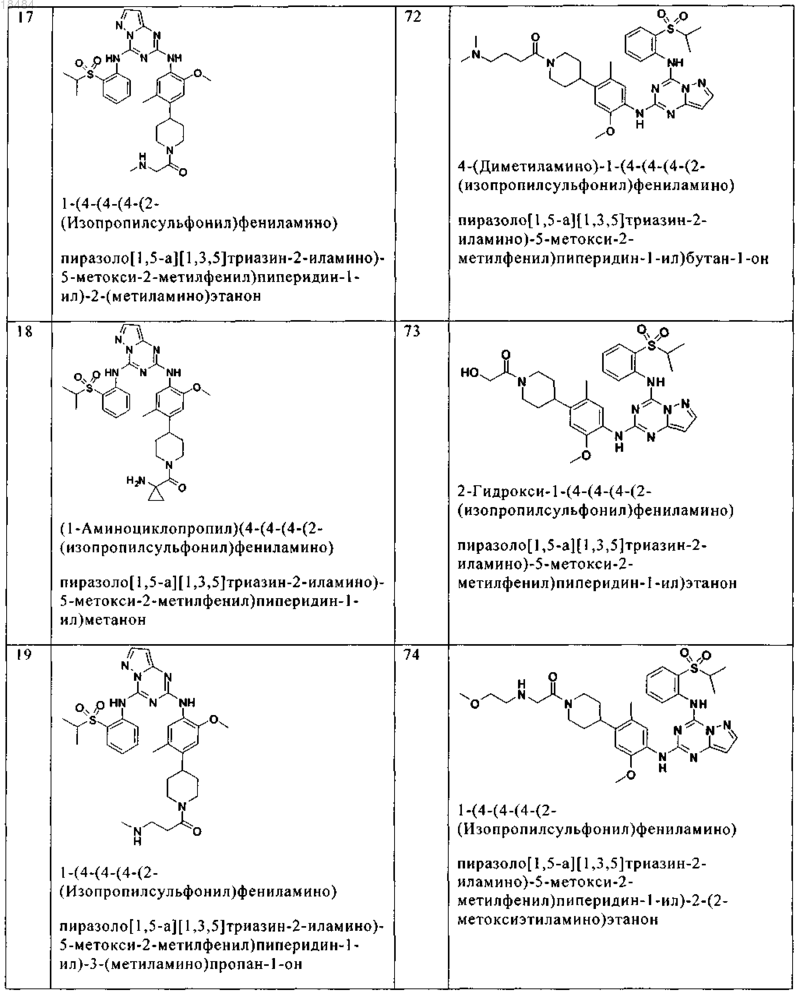
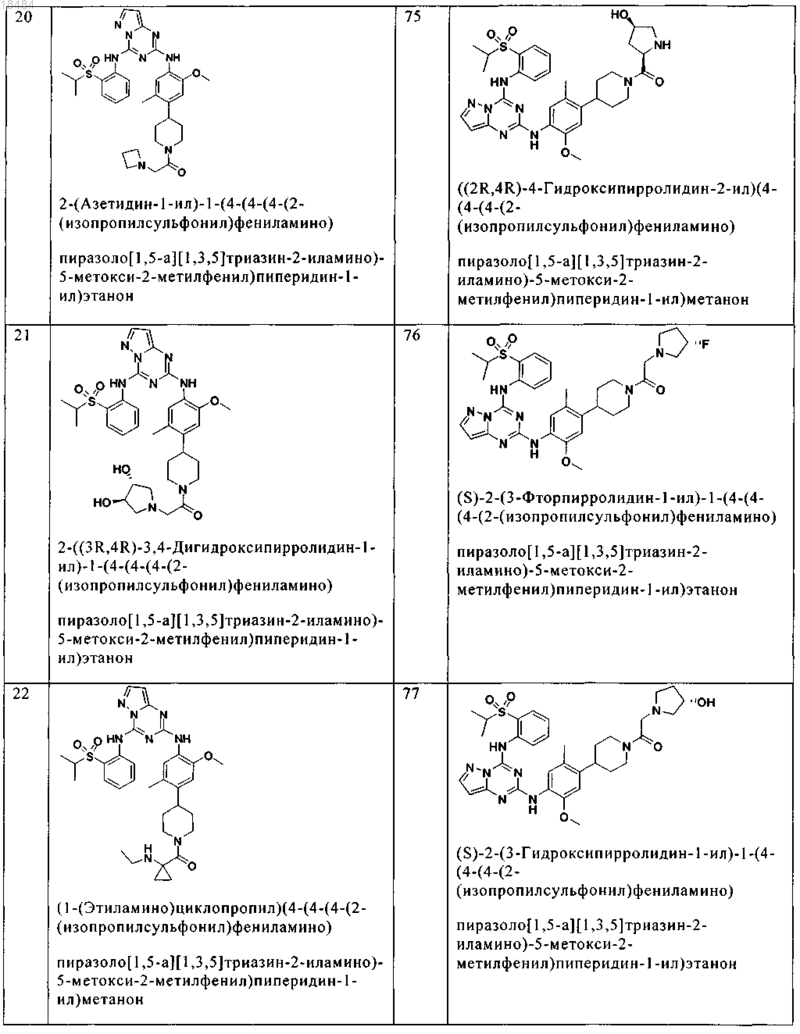

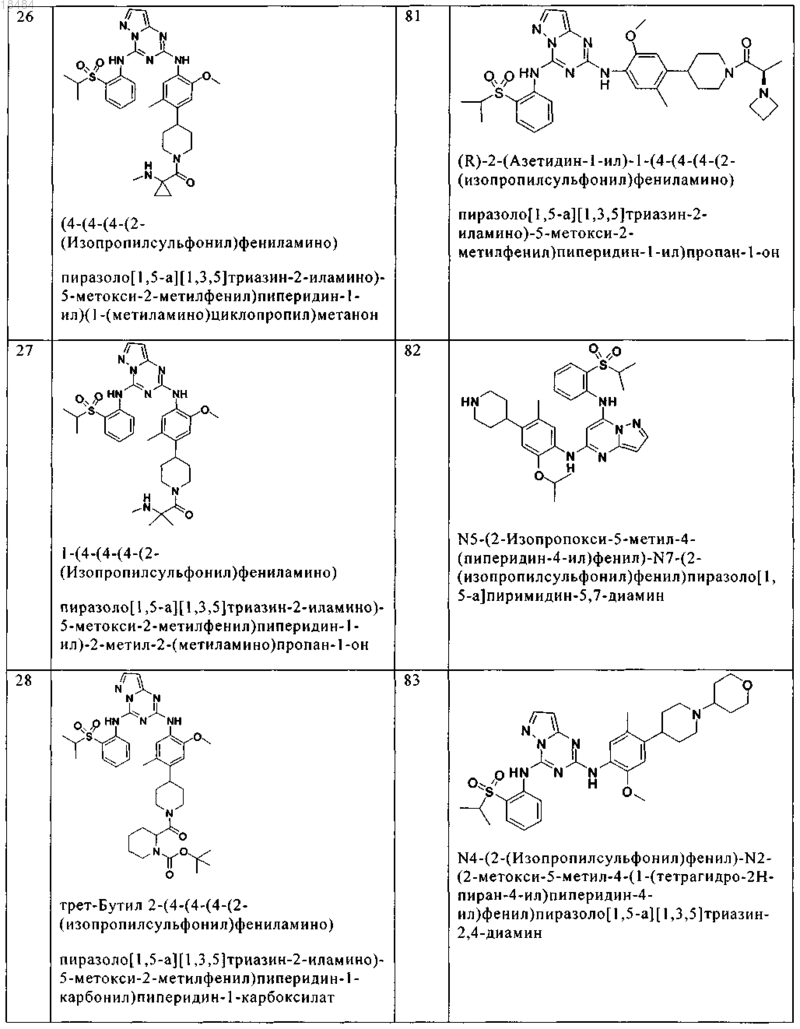
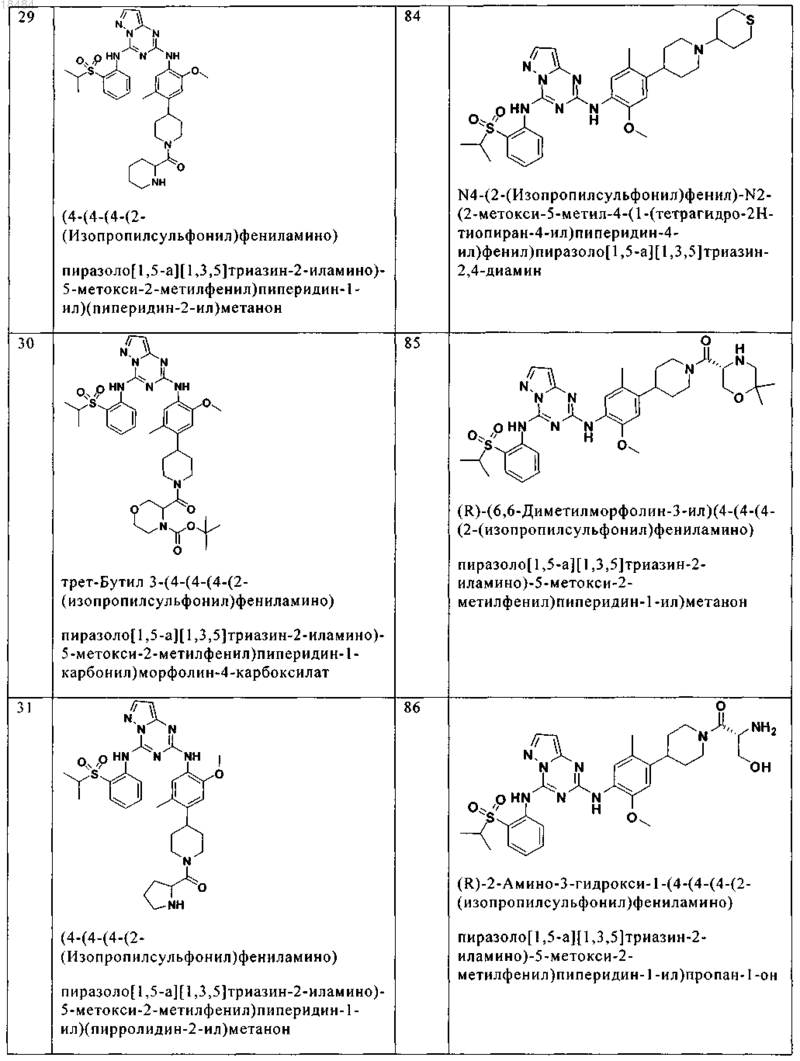
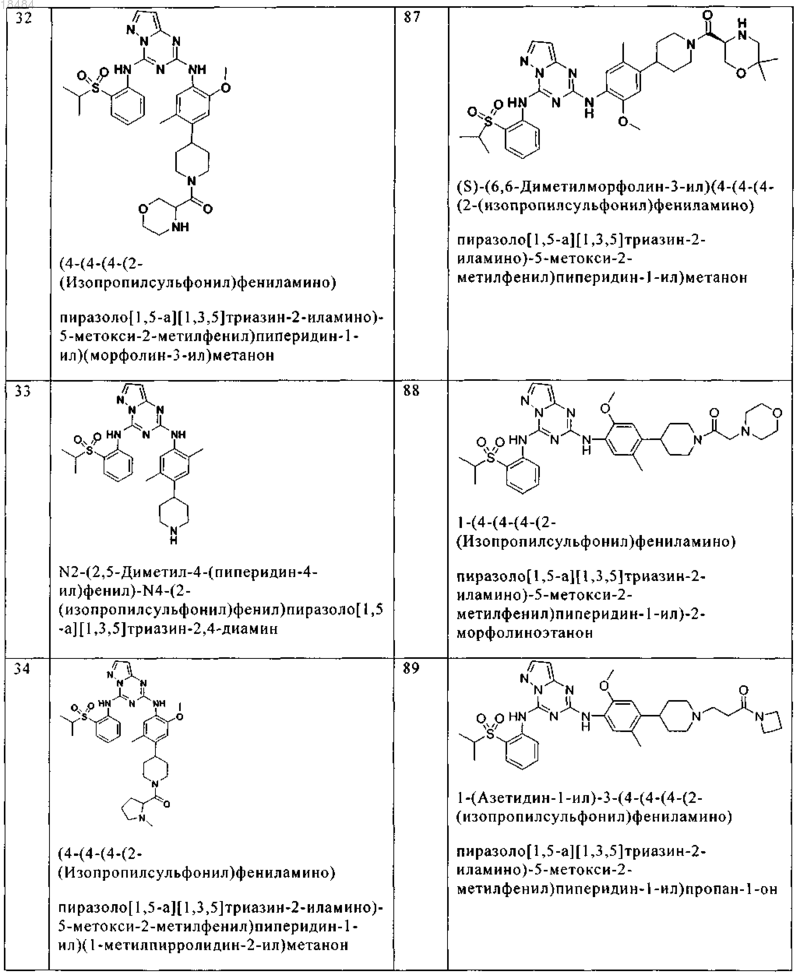
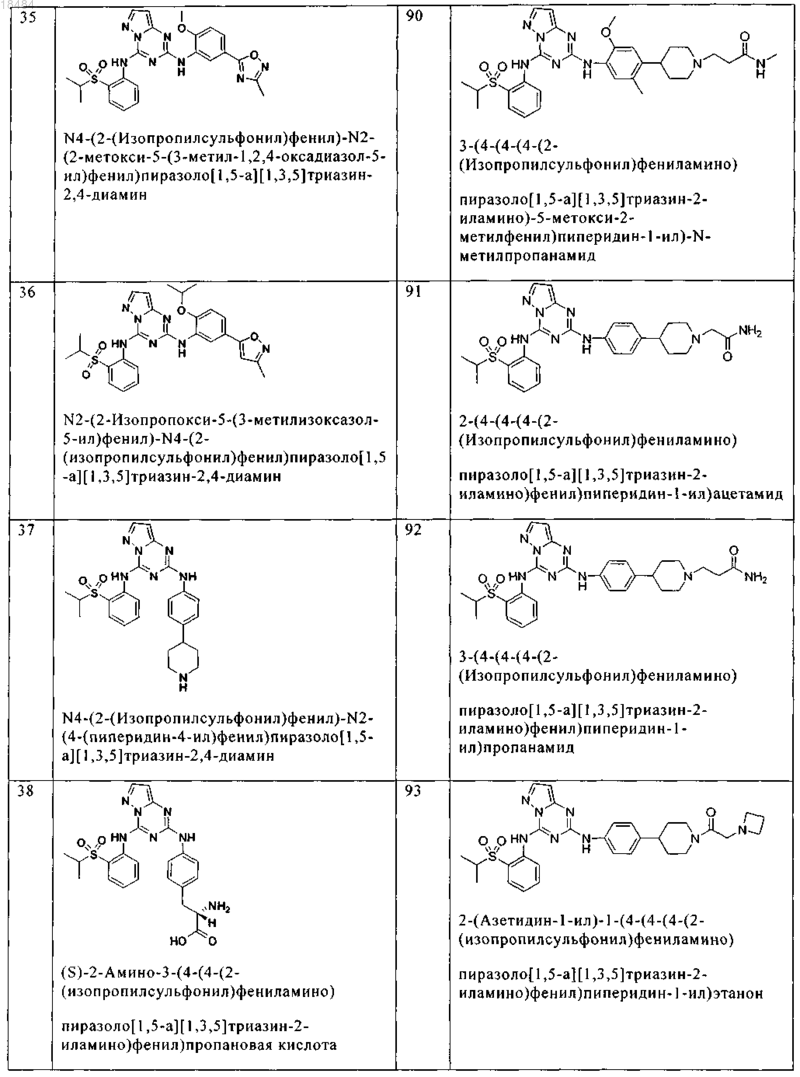
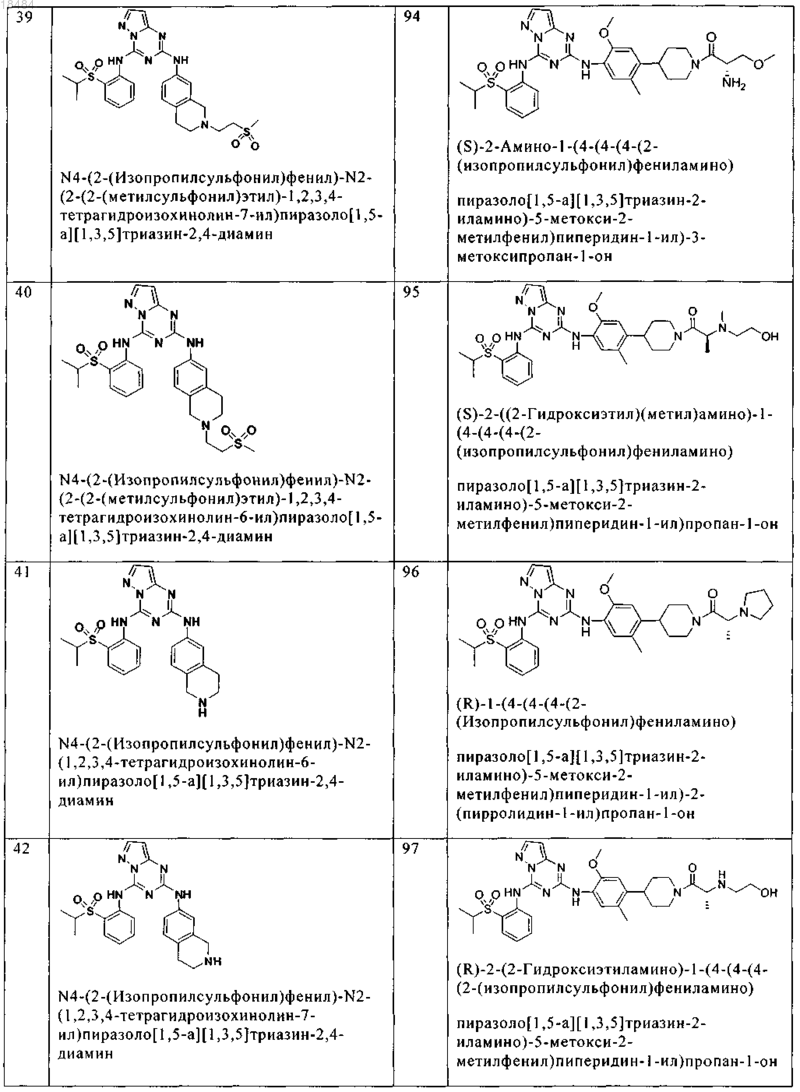
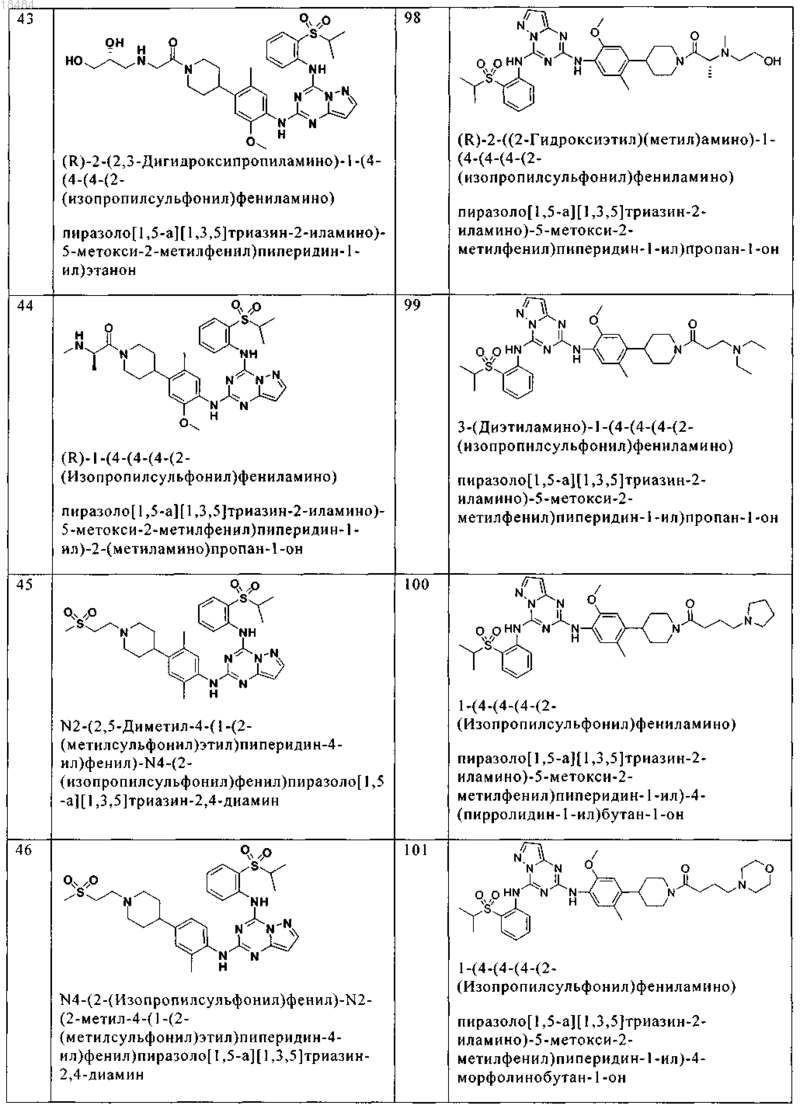
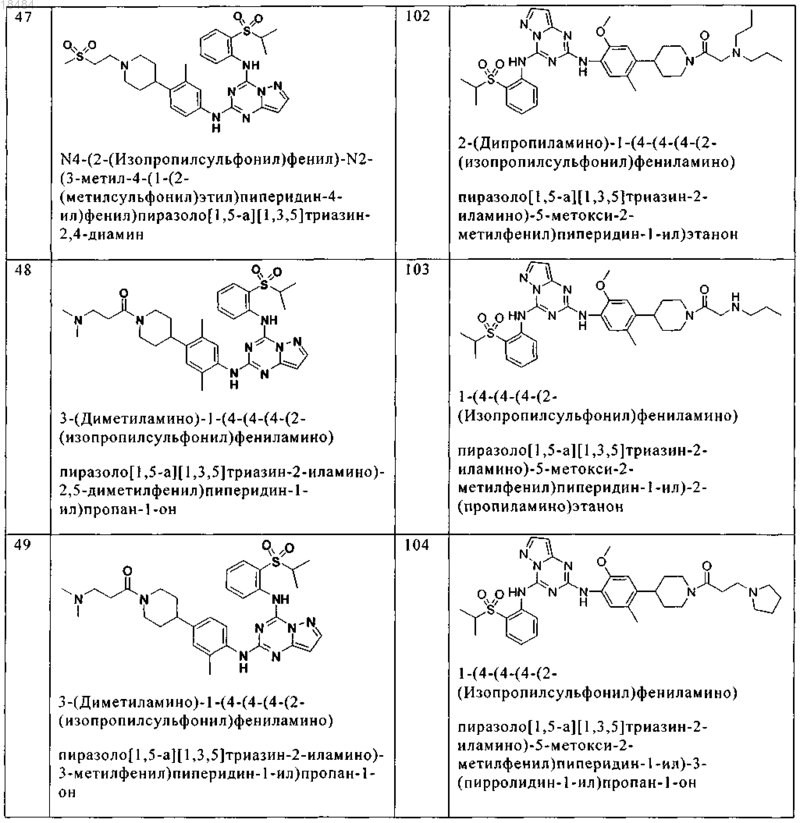
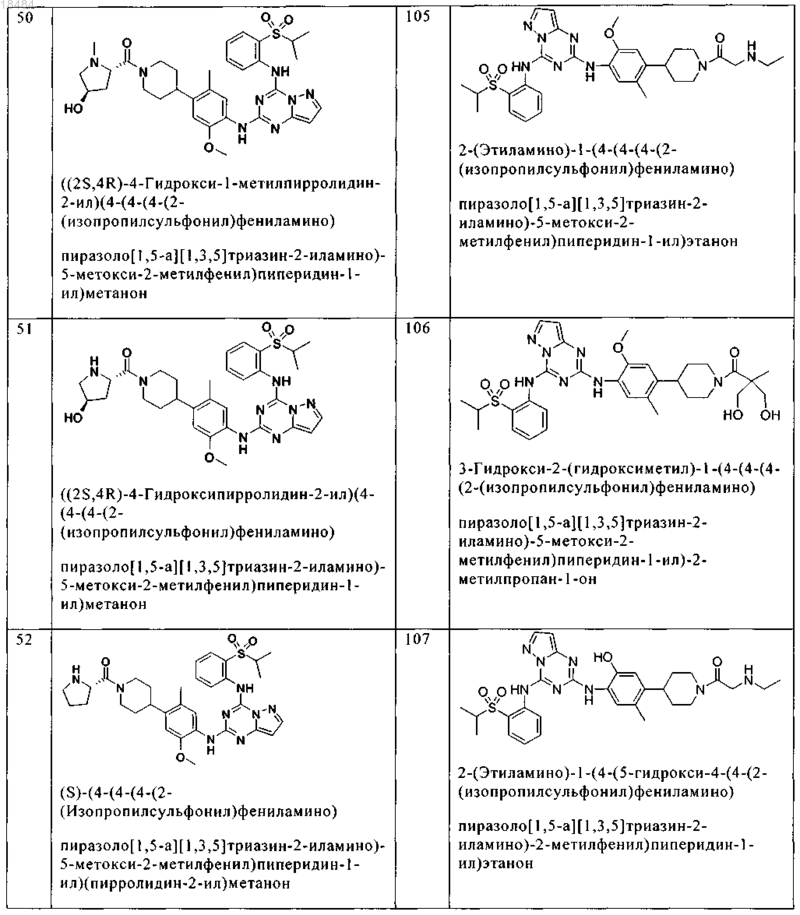
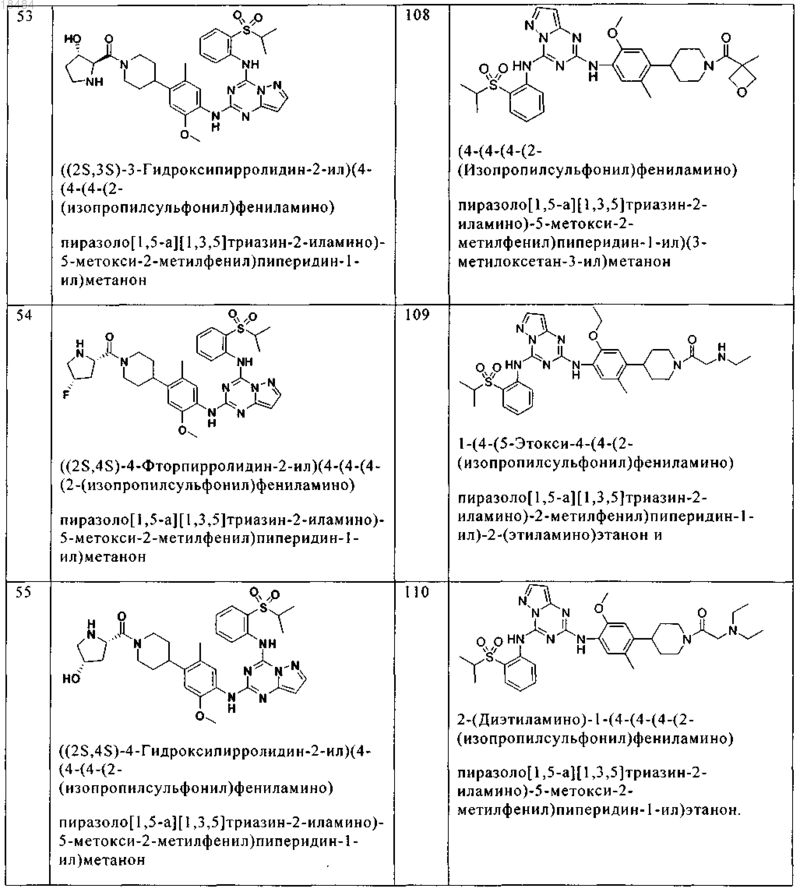
9. Фармацевтическая композиция, включающая терапевтически эффективное количество соединения по любому из пп.1-8 и физиологически приемлемый носитель необязательно в комбинации со вторым антигиперпролиферативным агентом.
10. Способ ингибирования анапластической лимфомной киназы в клетке, включающий контактирование клетки с эффективным количеством соединения по любому из пп.1-8 или его физиологически приемлемой соли и необязательно в комбинации со вторым химиотерапевтическим агентом.
11. Применение соединения по любому одному из пп.1-8 для изготовления лекарственного средства для лечения состояния, опосредованного анапластической лимфомной киназой (ALK), и необязательно в комбинации со вторым химиотерапевтическим агентом, где указанное состояние представляет собой аутоиммунное заболевание, заболевание, связанное с трансплантацией, инфекционное заболевание или клеточное пролиферативное нарушение.
12. Применение соединения по любому одному из пп.1-8 для изготовления лекарственного средства для лечения клеточного пролиферативного нарушения необязательно в комбинации со вторым химиотерапевтическим агентом, где указанное клеточное пролиферативное нарушение представляет собой множественную миелому, нейробластому, лимфому, лейкемию, меланому, саркому, остеосаркому, синовиальную саркому, саркому Эвинга, гепатому, желудочно-кишечную опухоль стромы или солидную опухоль груди, почек, простаты, прямой кишки, щитовидной железы, яичников, поджелудочной железы, легких, матки, дыхательного тракта, головного мозга, желудочно-кишечного тракта, мочевыводящих путей, глаз, печени, кожи, головы и шеи, щитовидной железы или паращитовидной железы.
Текст
Настоящее изобретение относится к новым производным триазина и пиримидина формул (1) или (2) и к способам применения таких соединений. Например, соединения по изобретению могут использоваться для лечения, облегчения или профилактики состояния, которое связано с ингибированием активности анапластической лимфомной киназы (ALK), онкогена c-ros (ROS),инсулиноподобного фактора роста (IGF-1R) и/или инсулинового рецептора (InsR) или их комбинации. Ссылки на заявки-аналоги Данная заявка имеет приоритет согласно заявкам на патент US 61/043111, поданной 7.04.2008, и US 61/095883, поданной 10.09.2008, каждая из которых включена здесь полностью в качестве ссылки. Область техники, к которой относится изобретение Настоящее изобретение относится к ингибиторам протеинкиназы и к способам применения таких соединений. Более конкретно, настоящее изобретение относится к ингибиторам Ros, IGF-1R, Ins и анапластической лимфомной киназы (ALK) и к их применениям в качестве терапевтических агентов. Уровень техники Рак представляет собой заболевание, вызванное нарушенным ростом ткани. Некоторые виды рака обладают потенциалом вторгаться в локальные ткани, а также метастазировать в различные органы. Это заболевание может развиваться в большом ряду различных органов, тканей и клеточных типов. Следовательно, термин "рак" относится к набору тысяч других заболеваний. Анапластическая лимфомная киназа (ALK), член суперсемейства инсулинового рецептора рецепторных тирозинкиназ, участвует в онкогенезе в гематопоэтических и негематопоэтических опухолях. Нарушенная экспрессия полноцепочечных белков рецептора ALK участвует в нейробластомах и глиобластомах; и слитые белки ALK встречаются при лимфоме анапластичных больших клеток. Исследование слитых белков ALK также повышает возможность новых терапевтических способов лечения пациентов сALK-положительными злокачественными образованиями (статья Pulford и др., Cell. Mol. Life Sci., 2004,61, cc. 2939-2953). Передача сигнала инсулиноподобного фактора роста (IGF-1) в большой степени встречается при раке с рецептором IGF-1 (IGF-1R) в качестве преобладающего фактора. IGR-1R является важным для трансформации опухоли и выживания злокачественных клеток, но только частично участвуют в нормальном клеточном росте. Связывание IGF-1R, как предполагается, является обещающим подходом для терапии рака (статья Larsson и др., Br. J. Cancer, 2005, 92, сс. 2097-2101).c-ros онкоген 1 (ROS1, также известный как ROS), член семейства гена инсулинового рецептора тирозинкиназы, высоко экспрессируется в различных опухолевых клеточных линиях. Несмотря на развитие уровня техники, остается потребность в противораковых терапиях и противораковых соединениях. Описание изобретения Настоящее изобретение относится к новым производным пиримидина и их фармацевтическим композициям и к их применению в качестве фармацевтических средств. В одном варианте осуществления настоящее изобретение относится к соединению формулы (1) или (2) или его физиологически приемлемой соли; где X представляет собой 5-6-членный гетероарил, замещенный C1-6 алкилом; 6-членное гетероциклическое кольцо, содержащее NR6 или O; или (CR2)0-4CR(NRR7)(CO2R7);Ph представляет собой фенил иR6 представляет собой H, C1-6 алкил, незамещенный или замещенный галогеном, аминогруппой или гидроксилом; -L-W, где W представляет собой циклопропил, тетрагидропиранил, тетрагидротиопиранол или пиразол, незамещенный или замещенный C1-6 алкилом; -L-C(O)-R7; -L-C(O)-NRR7; -L-C(O)-CR(R7)NRR7; -L-S(O)2R8 или радикал, выбранный из формул (а) или (b)R7 представляет собой H; C1-6 алкил, незамещенный или замещенный гидроксигруппой; или (CR2)qW', где W' представляет собой 5-6-членное гетероциклическое кольцо, содержащее 1-3 гетероатома, вы-1 018484 бранных из N, О и S, незамещенное или замещенное C(O)-O-(C1-6 алкилом), C1-6 алкилом, гидроксигруппой или галогеном;R9, R10, R11, R12, R13 и R14 независимо выбраны из H или C1-6 алкила, необязательно замещенного гидроксилом или алкоксигруппой; альтернативно R9 и R10 или R11 и R12 вместе с атомами углерода, к которым они присоединены, могут образовывать циклопропил; альтернативно R10 и R13, R13 и R14 или R11 и R13 вместе с атомами, к которым они присоединены, могут образовывать 4-7-членное насыщенное, ненасыщенное или частично ненасыщенное кольцо, содержащее вплоть до 3 гетероатомов, выбранных из N, О и S, и необязательно замещенное 1-3 группами R5;q имеет значение 0-4. В одном варианте осуществления настоящее изобретение относится к соединению формул (2 А),(2 В) или (2 С) или его физиологически приемлемой соли; где один из Z2 и Z3 представляет собой NR6, О или S, а другой представляет собой CH2;Z4 представляет собой NR6, О или S; кольцо Е необязательно может содержать двойную связь;R, R1, R2, R3, R4, R5 и m являются такими, как определено в формулах (1) или (2). В другом варианте осуществления настоящее изобретение относится к соединению формулы (3A) или (3B) или его физиологически приемлемой соли; где R5a, R5b и R5c независимо представляют собой H, галоген, гидроксил, C1-6 алкил или C1-6 алкоксигруппу; один из Z5, Z6 и Z7 представляет собой NR6, О или S, а другие представляют собой CH2; иR1, R2, R3, R4, R5, R6 и m являются такими, как определено в формулах (1) или (2). В некоторых примерах Z7 в описанной выше формуле (3A) или (3B) представляет собой NR6 или О; 5 и Z и Z6 представляют собой CH2. В другом варианте осуществления изобретение относится к соединению формулы (3C) или (3D) или его физиологически приемлемой соли; иR, R1, R2, R3, R4, R9, R10, R11, R12, R13, R14, L, q и m являются такими, как определено в формулах (1) или (2). В некоторых примерах приведенных выше формул (3A), (3B), (3C) или (3D), R5b представляет собой H; и R5a и R5c независимо представляют собой галоген, гидроксил, C1-6 алкил, C1-6 алкоксигруппу. В любом из описанных выше соединений Z1 представляет собой N. В другом варианте осуществления настоящее изобретение относится к фармацевтическим композициям, содержащим соединение формул (1), (2), (2 А), (2 В), (2 С), (3A), (3B), (3C) или (3D) и физиологически приемлемый эксципиент. В другом варианте осуществления изобретение относится к способам ингибирования киназы в клетке, включающим контактирование клеток с эффективным количеством соединения формул (1), (2),(2 А), (2 В), (2 С), (3A), (3B), (3C) или (3D) или его физиологически приемлемой соли, и необязательно в комбинации со вторым терапевтическим агентом. Изобретение также относится к применению соединения формул (1), (2), (2 А), (2 В), (2 С), (3A), (3B),(3C) или (3D) для изготовления лекарственного средства для лечения состояния, опосредованного анапластической лимфомной киназой (ALK). Соединения по изобретению могут использоваться отдельно или в комбинации со вторым терапевтическим агентом, таким как химиотерапевтический агент, где указанное состояние представляет собой аутоиммунное заболевание, заболевание, связанное с трансплантацией, инфекционное заболевание или клеточное пролиферативное нарушение. В конкретных вариантах осуществления изобретение относится к применению соединения формул(1), (2), (2 А), (2 В), (2 С), (3A), (3B), (3C) или (3D) для изготовления лекарственного средства для лечения клеточного пролиферативного нарушения. В конкретных примерах соединения по изобретению могут использоваться отдельно или в комбинации с химиотерапевтическим агентом для лечения клеточного пролиферативного нарушения, включая, но не ограничиваясь ими, множественную миелому, нейробластому, лимфому, лейкемию, меланому, саркому, остеосаркому, синовиальную саркому, саркому Эвинга,гепатому, желудочно-кишечную опухоль стромы или солидную опухоль груди, почек, простаты, прямой кишки, щитовидной железы, яичников, поджелудочной железы, легких, матки, дыхательного тракта, головного мозга, желудочно-кишечного тракта, мочевыводящих путей, глаз, печени, кожи, головы и шеи,щитовидной железы или паращитовидной железы. Определения."Алкил" обозначает группу и может быть структурным элементом других групп, например галогензамещенного алкила и алкоксигруппы, и может быть линейным или разветвленным. Необязательно замещенный алкил, алкенил или алкинил, как здесь используется, может быть необязательно галогенированным (например, CF3) или может иметь один или несколько атомов углерода, которые замещены или заменены на гетероатом, такой как NR, О или S (например, -OCH2CH2O-, алкилтиолы, тиоалкоксигруппа,алкиламины и т.д.)."Арил" обозначает моноциклическое или конденсированное бициклическое ароматическое кольцо,содержащее атомы углерода. "Арилен" обозначает двухвалентный радикал, полученный из арильной группы. Например, арильной группой может быть фенил, инденил, инданил, нафтил или 1,2,3,4 тетрагидронафталенил, который может быть необязательно замещен в орто-, мета- или пара-положении."Гетероарил", как здесь используется, обозначает арил, как описано выше, в котором один или несколько членов кольца являются гетероатомами. Примеры гетероарилов включают, но не ограничиваются ими, пиридил, пиразинил, индолил, индазолил, хиноксалинил, хинолинил, бензофуранил, бензопиранил, бензотиопиранил, бензо[1,3]диоксол, имидазолил, бензоимидазолил, пиримидинил, фуранил, оксазолил, изоксазолил, триазолил, бензотриазолил, тетразолил, пиразолил, тиенил, пирролил, изохинолинил,пуринил, тиазолил, тетразинил, бензотиазолил, оксадиазолил, бензоксадиазолил и т.д."Карбоциклическое кольцо", как здесь используется, обозначает насыщенное или частично ненасыщенное, моноциклическое, конденсированное бициклическое или мостиковое полициклическое кольцо, содержащее атомы углерода, которое необязательно может быть замещено, например, =O. Примеры карбоциклических колец включают, но не ограничиваются ими, циклопропил, циклобутил, циклопентил,циклогексил, циклопропилен, циклогексанон и т.д."Гетероциклическое кольцо", как здесь используется, является таким, как определено выше для карбоциклического кольца, где один или несколько атомов углерода в кольце являются гетероатомами. Например, гетероциклическое кольцо может содержать N, О, S, -N=, -S-, -S(O), -S(O)2- или -NR-, где R может представлять собой водород, C1-4 алкил или защитную группу. Примеры гетероциклических колец включают, но не ограничиваются ими, морфолино, пирролидинил, пирролидинил-2-он, пиперазинил,пиперидинил, пиперидинилон, 1,4-диокса-8-азаспиро[4.5]дец-8-ил, 1,2,3,4-тетрагидрохинолинил и т.д. Гетероциклические кольца, как здесь используется, могут включать бициклические амины и бициклические диамины. Как здесь используется, атом H в любых группах заместителя (например, CH2) включает все подходящие изотопные варианты, например H, 2H и 3H. Если не указано иное, когда заместитель обозначен как "необязательно замещенный", это обозначает, что заместитель представляет собой группу, которая может быть замещена одной или несколькими группами, отдельно и независимо выбранными, например, из необязательно галогенированного алкила,алкенила, алкинила, алкоксигруппы, алкиламина, алкилтиогруппы, алкинила, амида, аминогруппы,включая моно- и дизамещенные аминогруппы, арила, арилоксигруппы, арилтиогруппы, карбонила, карбоцикла, цианогруппы, циклоалкила, галогена, гетероалкила, гетероалкенила, гетероалкинила, гетероарила, гетероциклила, гидроксигруппы, изоцианатогруппы, изотиоцианатогруппы, меркаптогруппы, нитрогруппы, O-карбамила, N-карбамила, O-тиокарбамила, N-тиокарбамила, C-амидогруппы, Nамидогруппы, S-сульфонамидогруппы, N-сульфонамидогруппы, С-карбоксигруппы, О-карбоксигруппы,пергалогеналкила, перфторалкила, силила, сульфонила, тиокарбонила, тиоцианатогруппы, тригалогенметансульфонила и из защищенных соединений. Защитные группы, которые могут образовывать защищенные соединения описанных выше заместителей, известны специалисту в данной области техники и могут быть обнаружены в источниках, таких как Greene и Wuts, Protective Groups in Organic Synthesis, 3 е изд.,John WileySons, New York, NY, 1999 и Kocienski, Protective Groups, Thieme Verlag, New York, NY,1994, которые приведены здесь полностью в качестве ссылки. Термин "фармацевтическая комбинация", как здесь используется, обозначает продукт, который получают смешением или объединением более одного активного ингредиента и включает фиксированные и нефиксированные комбинации активных ингредиентов. Термин "фиксированная комбинация" обозначает, что активные ингредиенты, например соединение формулы (1) и совместно вводимый агент, оба вводятся пациенту одновременно в форме одного целого или одной дозировки. Термин "нефиксированная комбинация" обозначает, что активные ингредиенты, например соединение формулы (1) и совместно вводимый агент, оба вводятся пациенту раздельными частями совместно, одновременно или последовательно в неограниченном периоде времени, где такое введение обеспечивает терапевтически эффективные уровни двух соединений в организме пациента. Последнее также включает коктейльную терапию,например введение трех или более активных ингредиентов. Термин "терапевтически эффективное количество" обозначает количество конкретного соединения,которое вызывает биологический или медицинский отклик в клетке, такни, органе, системе, животном или человеке, которое определяется исследователем, ветеринаром, врачом или другим доктором."Субъект" обозначает людей и млекопитающих, включая домашних и сельскохозяйственных животных, и животных зоопарка, спортивных животных или домашних животных, таких как собаки, кошки, крупный рогатый скот, лошади, овцы, свиньи, козы, кролики и т.д. В некоторых вариантах осуществления субъектом является человек. Введение "в комбинации с" одним или несколькими другими терапевтическими агентами включает одновременное (конкурентное) и последовательное введение в любом порядке. Способы осуществления изобретения Настоящее изобретение относится к новым производным пиримидина и триазина и их фармацевтическим композициям и к способам применения таких соединений. В одном варианте осуществления изобретение относится к соединению формулы (1) или (2) или его физиологически приемлемой соли; гдеPh представляет собой фенил и В представляет собой 5-6-членное кольцо, необязательно содержащее NR6, О, =O или S;R6 представляет собой H, C1-6 алкил, незамещенный или замещенный галогеном, аминогруппой или гидроксилом; -L-W, где W представляет собой циклопропил, тетрагидропиранил, тетрагидротиопиранол или пиразол, незамещенный или замещенный C1-6 алкилом; -L-C(O)-R7; -L-C(O)-NRR7; -L-C(O)-CR(R7)NRR7; -L-S(O)2R8 или радикал, выбранный из формул (а) или (b)R7 представляет собой H; C1-6 алкил, незамещенный или замещенный гидроксигруппой; или (CR2)qW', где W' представляет собой 5-6-членное гетероциклическое кольцо, содержащее 1-3 гетероатома, выбранных из N, О и S, незамещенное или замещенное C(O)-O-(C1-6 алкилом), C1-6 алкилом, гидроксигруппой или галогеном;R9, R10, R11, R12, R13 и R14 независимо выбраны из H или C1-6 алкила, необязательно замещенного гидроксилом или алкоксигруппой; альтернативно R9 и R10 или R11 и R12 вместе с атомами углерода, к которым они присоединены, могут образовывать циклопропил; альтернативно R10 и R13, R13 и R14 или R11 и R13 вместе с атомами, к которым они присоединены, могут образовывать 4-7-членное насыщенное, ненасыщенное или частично ненасыщенное кольцо, содержащее вплоть до 3 гетероатомов, выбранных из N, О и S, и необязательно замещенное 1-3 группами R5;q имеет значение 0-4. В одном варианте осуществления изобретение относится к соединению формулы (2 А), (2 В) или или его физиологически приемлемой соли; где один из Z2 и Z3 представляет собой NR6, О или S, а другой представляет собой СН 2;Z4 представляет собой NR6, О или S; кольцо Е необязательно может содержать двойную связь;R, R1, R2, R3, R4, R5 и m являются такими, как определено в формулах (1) или (2). В другом варианте осуществления изобретение относится к соединению формулы (3A) или (3B) или его физиологически приемлемой соли; где R5a, R5b и R5c независимо представляют собой H, галоген, гидроксил, C1-6 алкил или C1-6 алкоксигруппу; один из Z5, Z6 и Z7 представляет собой NR6, О или S, а другие представляют собой CH2; иR1, R2, R3, R4, R5, R6 и m являются такими, как определено в формулах (1) или (2). В другом варианте осуществления изобретение относится к соединению формулы (3C) или (3D) или его физиологически приемлемой соли; иR, R1, R2, R3, R4, R9, R10, R11, R12, R13, R14, L, q и m являются такими, как определено в формулах (1) или (2). В каждой из описанных выше формул любые асимметричные атомы углерода могут присутствовать в (R)-, (S)- или (R,S)-конфигурации. Соединения, таким образом, могут присутствовать в виде смесей изомеров или в виде чистых изомеров, например в виде чистых энантиомеров или диастереомеров. Настоящее изобретение также включает возможные таутомеры соединений по изобретению. Настоящее изобретение также включает все подходящие изотопные варианты соединений по изобретению или их фармацевтически приемлемых солей. Изотопный вариант соединения по изобретению или его фармацевтически приемлемой соли определен как соединение, в котором по крайней мере один атом заменен атомом с тем же атомным номером, но атомная масса которого отличается от атомной массы, обычно обнаруженной в природе. Примеры изотопов, которые могут быть включены в соединения по изобретению и их фармацевтически приемлемые соли, включают, но не ограничиваются ими, изотопы водорода, углерода, азота и кислорода, такие как 2 Н, 3 Н, 11 С, 13 С, 14 С, 15N, 17 О, 18 О, 35S, 18F, 36Cl и 123I. Некоторые изотопные варианты соединений по изобретению и их фармацевтически приемлемых солей,например варианты, в которых присутствует радиоактивный изотоп, такой как 3 Н или 14 С, полезны для исследований тканевого распределения лекарственного вещества и/или субстрата. В конкретных примерах изотопы 2 Н, 3 Н и 14 С могут использоваться для получения и обнаружения. В других примерах замещение изотопами, такими как 2 Н, могут придавать некоторые терапевтические преимущества в результате большей метаболической стабильности, такой как повышенное время полувыведения in vivo или пониженная дозировка. Изотопные варианты соединений по изобретению или их фармацевтически приемлемые соли обычно могут быть получены обычными методиками, используя соответствующие изотопные варианты подходящих реагентов. Изотопные варианты также имеют потенциал изменения метаболической стабильности соединения и/или создания небольших изменений физических свойств, таких как гидроскопичность и им подобные. Изотопные варианты также имеют потенциал повышения эффективности и безопасности, повышения биодоступности и времени полувыведения,изменения связывания с белками, изменения биораспределения, повышение доли активных метаболитов и/или снижения образования реакционных или токсичных метаболитов. Фармакология и полезность Соединения по изобретению и их фармацевтически приемлемые соли обладают ценными фармакологическими свойствами при тестировании in vitro в бесклеточных анализах с киназой и в клеточных анализах и, следовательно, полезны в качестве фармацевтических средств. В одном варианте осуществления соединения формул (1), (2), (2 А-2 С) или (3A-3D) могут ингибировать активность тирозинкиназы анапластической лимфомной киназы (ALK) и слитого белка NPMALK. Этот белок тирозинкиназы является результатом слияния генов нуклеофозмина (NPM) и ALK, делая активность белка тирозинкиназы ALK лиганднезависимой. NPM-ALK играет ключевую роль в передаче сигнала ряда гематопоэтических и других клеток человека, что приводит к гематологическим и неоплатическим заболеваниям, например к анапластической лимфоме больших клеток (ALCL) и лимфоме не-Ходжкина (NHL), конкретно к ALK+NHL или Alkomas, в воспалительных миофибробластомных опухолях (IMT) и нейробластомах. (статья Duyster и др., 2001, Oncogene 20, cc. 5623-5637). В дополнение кNPM-ALK, другие слияния генов идентифицированы при гематологических и неопластических заболеваниях человека; например TPM3-ALK (слияние немышечного тропомиозина с ALK). Ингибирование активности тирозинкиназы ALK может быть показано, используя известные методы, например используя рекомбинантный киназный домен ALK в аналогии с киназным анализом VEGFR, описанным в статье J. Wood и др., Cancer Res., 2000, 60, cc. 2178-2189. Обычно ферментативные ана-7 018484 лизы in vitro с помощью белка тирозинкиназы GST-ALK осуществляли в 96-луночных планшетах в виде анализа со связыванием на фильтре в 20 мМ Tris HCl, pH 7,5, 3 мМ MgCl2, 10 мМ MnCl2, 1 мМ DTT, 0,1 мкCi/анализ (=30 мкл) [-33 Р]-АТФ, 2 мкМ АТФ, 3 мкг/мл поли(Glu,Tyr 4:1) Poly-EY (Sigma P-0275), 1% ДМСО, 25 нг фермента ALK. Анализы инкубировали в течение 10 мин при комнатной температуре. Реакции останавливали добавлением 50 мкл 125 мМ EDTA и реакционную смесь переносили в планшетуMAIP Multiscreen (Millipore, Bedford, MA, США), заранее смоченную метанолом и повторно смоченную через 5 мин H2O. После промывания (0,5% Н 3 РО 4) планшеты определяли количественно в жидкостном сцинтилляционном счетчике. Значения IC50 рассчитывали линейным регрессионным анализом процентного ингибирования. Соединения формул (1), (2), (2 А-2 С) или (3A-3D) могут потенциально ингибировать рост NPMALK человека, сверхэкспрессирующий клетки BaF3 мыши (DSMZ Deutsche Sammiung von Mikroorganismen und Zelikulturen GmbH, Германия). Экспрессия NPM-ALK может осуществляться трансфекцией клеточной линии BaF3 с помощью вектора экспрессии pClneo (Promega Corp., Madison WI, США), кодирующего NPM-ALK, и последующей селекции G418 резистентных клеток. НетрансфецированныеBaF3 клетки зависят от IL-3 в отношении клеточной выживаемости. Наоборот, NPM-ALK, экспрессирующие клетки BaF3 (называемые далее BaF3-NPM-ALK), могут пролиферировать в отсутствии IL-3 изза того, что они получают пролиферативный сигнал через киназу NPM-ALK. Предполагаемые ингибиторы киназы NPM-ALK, следовательно, устраняют сигнал роста и могут приводить к антипролиферативной активности. Антипролиферативная активность предполагаемых ингибиторов киназы NPM-ALK, однако, может подавляться добавлением IL-3, который обеспечивает сигналы роста через механизм, независимый от NPM-ALK. Аналогичная клеточная система, использующая киназу FLT3, также была описана (см. статью Е. Weisberg и др., Cancer Cell; 2002, 1, cc. 433-443). Ингибирующая активность соединений по изобретению может определяться следующим образом. Обычно клетки BaF3-NPM-ALK (15,000/микротитровальная планшета) переносили в 96-луночные микротитровальные планшеты. Тестируемые соединения, растворенные в диметилсульфоксиде (ДМСО),добавляли в ряду концентраций (серии разбавлений) таким образом, чтобы конечная концентрация ДМСО не превышала 1 об.%. После добавления планшеты инкубировали в течение двух суток, в это время контрольные культуры без тестируемого соединения способны подвергаться двум циклам клеточного деления. Рост клеток BaF3-NPM-ALK измеряли с помощью окрашивания YOPRO [статья Т. Idziorek и др., J. Immunol. Methods; 1995, 185, cc. 249-258]: 25 мкл буфера для лизиса, содержащего 20 мМ цитрата натрия, pH 4,0, 26,8 мМ хлорида натрия, 0,4% NP40, 20 мМ EDTA и 20 мМ добавляли в каждую лунку. Лизис клеток завершался через 60 мин при комнатной температуре, и общее количествоBiosystems) со следующими установками: возбуждение (нм) 485/20 и поглощение (нм) 530/25. Значения IC50 могут быть определены компьютерной системой, используя формулу(ABS = поглощение) Значение IC50 в этих экспериментах показывает ту концентрацию тестируемого соединения, которая приводит к количеству клеток, которое на 50% меньше количества, которое получают с помощью контроля без ингибитора. Соединения по изобретению в свободной форме или в форме фармацевтически приемлемой соли могут иметь ценные фармакологические свойства, например, как показано в тестах invitro, описанных в данной заявке. Обычно, соединения по изобретению имеют значения IC50 от 1 нМ до 10 мкМ. В некоторых примерах соединения по изобретению имеют значения IC50 от 1 нМ до 5 мкМ или более предпочтительно от 1 нМ до 1 мкМ. В других примерах соединения по изобретению имеют значения IC50 менее 1 нМ или более 10 мкМ. Соединения по изобретению могут проявлять процентное ингибирование более 50% или в других вариантах осуществления могут проявлять процентное ингибирование более 70% в отношении ALK при 10 мкМ. Антипролиферативное действие соединений по изобретению также может определяться на клеточной линии лимфомы KARPAS-299 человека (DSMZ Deutsche Sammiung von Mikroorganismen und Zelikulturen GmbH, Braunschweig, Германия, описанной в статье W.G. Dirks и др., Int. J. Cancer, 2002, 100, cc. 4956), используя ту же методику, описанную выше для клеточной линии BaF3-NPM-ALK. В некоторых вариантах осуществления соединения по изобретению могут проявлять ингибирующую активность со значениями IC50 в диапазоне от около 0,01 до 1 мкМ. Действие соединений по изобретению на автофосфорилирование ALK может определяться на клеточной линии лимфомы KARPAS-299 человека с помощью иммуноблота, как описано в статье W.G. Dirks и др., Int. J. Cancer, 2002, 100, cc. 49-56. Соединения по изобретению также могут ингибировать рецептор инсулиноподобного фактора роста 1 (IGF-1R) и могут использоваться для лечения опосредованных IGF-1R заболеваний. Примеры опосредованных IGF-1R заболеваний включают, но не ограничиваются ими, пролиферативные заболевания,такие как опухоли, например опухоли груди, почек, простаты, прямой и ободочной кишки, щитовидной железы, яичников, поджелудочной железы, нейронов, легких, матки и желудочно-кишечного тракта, а также остеосаркомы и меланомы. Эффективность соединений по изобретению в качестве ингибиторов активности тирозинкиназы IGF-1R может быть показана с помощью клеточного захвата ELISA. В этом анализе определяли активность соединений по изобретению в отношении (IGF-1)-индуцированного автофосфорилирования IGF-1R. Соединения по изобретению также могут быть полезны для лечения и/или профилактики острых или хронических воспалительных заболеваний или нарушений или аутоиммунных заболеваний, например ревматоидный артрит, остеоартрит, системная красная волчанки, тироидит Хашимото, рассеянный склероз, астенический бульбарный паралич, диабет (I и II типа) и связанные с ними нарушения, респираторные заболевания, такие как астма или воспалительное повреждение печени, воспалительное гломерулярное повреждение, кожные проявления иммунных нарушений или заболеваний, воспалительные и гиперпролиферативные кожные заболевания (такие как псориаз, атопический дерматит, аллергический контактный дерматит, раздражающий контактный дерматит и другие экзематозные дерматиты, себорейный дерматит), воспалительные глазные заболевания, например синдром Сьергена, кератоконъюнктивит или увеит, болезнь раздраженного кишечника, болезнь Крона или язвенный колит. В соответствии с вышеизложенным также предполагается:(1) соединение по изобретению для применения в качестве фармацевтического средства;(2) соединение по изобретению для применения в качестве ингибитора ALK, ингибитора Ros, ингибитора IGF-1R и/или InsR, например для применения в любом из описанных выше конкретных показаний;(3) фармацевтическая композиция, например, для применения в любом из описанных выше конкретных показаний, содержащая соединение по изобретению в качестве активного ингредиента вместе с одним или несколькими фармацевтически приемлемыми разбавителями или носителями;(4) способ лечения любого из описанных выше конкретных показаний у субъекта, нуждающегося в этом, включающий введение эффективного количества соединения по изобретению или содержащей его фармацевтической композиции;(5) применение соединения по изобретению для изготовления лекарственного средства для лечения или профилактики заболевания или состояния, при котором играет роль или участвует активация ALK,Ros, IGF-1R и/или InsR;(6) способ, как описано выше в разделе (4), включающий совместное введение, например одновременное или последовательное, терапевтически эффективного количества соединения по изобретению и одного или нескольких других лекарственных веществ, причем указанное другое лекарственное вещество полезно для любого из описанных выше конкретных показаний;(7) комбинация, содержащая терапевтически эффективное количество соединения по изобретению и одно или несколько других лекарственных веществ, причем указанное другое лекарственное вещество полезно для любого из описанных выше конкретных показаний;(8) применение соединения по изобретению для изготовления лекарственного средства для лечения или профилактики заболевания, которое чувствительно к ингибированию анапластической лимфомной киназы;(9) применение в соответствии с разделом (8), где излечиваемое заболевание выбрано из анапластической крупноклеточной лимфомы, лимфомы не-Ходжкина, воспалительных миофибробластомных опухолей, нейробласты и неопластических заболеваний;(10) применение в соответствии с разделами (8) или (9), где соединение или его фармацевтически приемлемая соль описаны в одном из примеров;(11) способ лечения заболевания, которое чувствительно к ингибированию анапластической лимфомной киназы, особенно заболевания, выбранного из анапластической крупноклеточной лимфомы,лимфомы не-Ходжкина, воспалительных миофибробластомных опухолей, нейробласты и неопластических заболеваний, включающий введение эффективного количества соединения по изобретению или его фармацевтически приемлемой соли. Введение и фармацевтические композиции Фармацевтическая композиция, как здесь используется, обозначает смесь соединения по изобретению с другими химическими компонентами, такими как носители, стабилизаторы, разбавители, диспергирующие агенты, суспендирующие агенты, загущающие агенты и/или эксципиенты. Фармацевтическая композиция облегчает введение соединения в организм. Фармацевтические композиции, содержащие соединение по изобретению, могут вводиться в терапевтически эффективных количествах в виде фармацевтических композиций в любой обычной форме и способом, известным из предшествующего уровня техники, включая, но не ограничиваясь ими, внутривенное, пероральное, ректальное, аэрозольное, парентеральное, офтальмическое, легочное, трансдермальное, вагинальное, ушное, назальное и местное введение. Можно ввести соединение локально, а не системно, например, инъекцией соединения непосредственно в орган, часто в базовом составе или составе длительного высвобождения. Кроме того, можно ввести фармацевтическую композицию, содержащую соединение по изобретению, в системе направленной доставки лекарственного препарата, например в липосоме, покрытой специфичным к органу антителом. Липосомы будут связываться и высвобождаться селективно в орган. Дополнительно фармацевтические композиции, содержащие соединение по изобретению, могут быть получены в форме состава быстрого высвобождения, в форме состава отсроченного высвобождения или в форме состава промежуточного высвобождения. Для перорального введения соединение по изобретению может быть легко получено объединением активных соединений с фармацевтически приемлемыми носителями или эксципиентами, хорошо известными из предшествующего уровня техники. Такие носители позволяют ввести описанные соединения в состав таблеток, порошков, пилюль, драже, капсул, жидкостей, гелей, сиропов, эликсиров, эмульсий,суспензий и им подобных для перорального приема пациентом. Фармацевтические препараты для перорального применения могут быть получены смешением одного или нескольких твердых эксципиентов с одним или несколькими описанными здесь соединениями,необязательно измельчением полученной смеси и формированием из смеси гранул, после добавления подходящих добавок, при необходимости, для получения таблеток или ядер драже. Подходящими эксципиентами являются, в частности, наполнители, такие как сахара, включая лактозу, сахарозу, маннит или сорбит; составы целлюлозы, такие как, например, кукурузный крахмал, пшеничный крахмал, рисовый крахмал, картофельный крахмал, желатин, смола трагаканта, метилцеллюлоза, микрокристаллическая целлюлоза, гидроксипропилметилцеллюлоза, натрийкарбоксиметилцеллюлоза; или другие вещества,такие как поливинилпирролидон (PVP или повидон) или фосфат кальция. При необходимости, могут добавляться разрыхляющие агенты, такие как поперечно-сшитая натрийкроскармелоза, поливинилпирролидон, агар или альгиновая кислота или ее соль, такая как альгинат натрия. Ядра драже могут быть покрыты подходящими оболочками. Для этих целей могут использоваться концентрированные растворы сахаров, которые необязательно могут содержать гуммиарабик, тальк, поливинилпирролидон, гель карбопол, полиэтиленгликоль и/или диоксид титана, лакирующие растворы и подходящие органические растворители или смеси растворителей. Красители или пигменты могут добавляться к покрытиям таблеток или драже для идентификации или характеристики различных комбинаций доз активного соединения. Фармацевтические препараты, которые могут использоваться перорально, включают наполненные капсулы из желатина, а также мягкие закрытые капсулы из желатина и пластификатора, такого как глицерин или сорбит. Наполненные капсулы могут содержать активные ингредиенты в смеси с наполнителем, таким как лактоза, связующими, такими как крахмалы, и/или лубрикантами, такими как тальк или стеарат магния, и необязательно стабилизаторами. В мягких капсулах активные соединения могут быть растворены или суспендированы в подходящих жидкостях, таких как жирные масла, жидкие парафины или жидкие полиэтиленгликоли. Кроме того, могут добавляться стабилизаторы. Для буккального или сублингвального введения композиции могут иметь форму таблеток, лепешек или гелей, составленных обычным способом. Парентеральные инъекции могут включать болюсную инъекцию или непрерывную инфузию. Фармацевтическая композиция соединения по изобретению может быть получена в форме, подходящей для парентеральной инъекции в виде стерильных суспензий, растворов или эмульсий в масле или водных носителях, и могут содержать составляющие агенты, такие как суспендирующие, стабилизирующие и/или диспергирующие агенты. Фармацевтические составы для парентерального введения включают водные растворы активных соединений в растворимой в воде форме. Дополнительно суспензии активных соединений могут быть получены в виде подходящих масляных инъекционных суспензий. Подходящие липофильные растворители или носители включают жирные масла, такие как кунжутное масло, или синтетические эфиры жирных кислот, такие как этилолеат или триглицериды, или липосомы. Водные инъекционные суспензии могут содержать вещества, которые повышают вязкость суспензии, такие как натрийкарбоксиметилцеллюлоза, сорбит или декстран. Необязательно, суспензия также может содержать подходящие стабилизаторы или агенты, которые повышают растворимость соединений для получения высококонцентрированных растворов. Альтернативно, активный ингредиент может находиться в форме порошка для соединения с подходящим носителем, например стерильной апирогенной водой, перед применением. Соединения по изобретению могут наноситься местно и могут быть введены в различные местно применимые композиции, такие как растворы, суспензии, лосьоны, гели, пасты, медицинские карандаши,бальзамы, кремы или мази. Такие фармацевтические соединения могут содержать солюбилизаторы, стабилизаторы, агенты для повышения тоничности, буферы и консерванты. Составы, подходящие для трансдермального введения, могут включать устройства для трансдермальной доставки и пластыри для трансдермальной доставки и могут представлять собой липофильные эмульсии или забуференные водные растворы, растворенные и/или диспергированные в полимере или связующем. Такие пластыри могут быть получены для длительной, пульсирующей доставки или доставки по требованию фармацевтических агентов. Далее трансдермальная доставка соединений по изобретению может осуществляться с помощью ионофорезных пластырей и им подобных. Дополнительно трансдермальные пластыри могут обеспечивать контролируемую доставку соединений по изобретению. Скорость абсорбции может быть замедлена с помощью контролирующих скорость мембран или захватом соединения полимерной матрицей или гелем. Наоборот, усилители абсорбции могут использоваться для повышения абсорбции. Усилитель абсорбции или носитель может включать абсорбируемые фармацев- 10018484 тически приемлемые растворители для облегчения прохождения через кожу. Например, трансдермальные устройства присутствуют в форме бандажа, включающего основу, емкость, содержащую соединение необязательно с носителями, необязательно барьер для контроля скорости для доставки соединения на кожу пациента с контролируемой и предварительно заданной скоростью в течение пролонгированного периода времени, и средства для удержания устройства на коже. Для введения ингаляцией соединения по изобретению могут присутствовать в форме аэрозоля,дымки или порошка. Фармацевтические композиции соединений по изобретению могут быть обычно получены в форме аэрозольного спрея из емкостей под давлением или небулайзера с применением подходящего газа-вытеснителя, например дихлордифторметана, трихлорфторметана, дихлортетрафторэтана,диоксида углерода или другого подходящего газа. В случае аэрозоля под давлением дозированная единица может быть определена нажатием клапана для доставки отмеренного количества. Могут быть получены капсулы и картриджи, такие как, например, желатиновые, для применения в ингаляторе или воздушном инжекторе, содержащие порошковую смесь соединения и подходящей порошковой основы, такой как лактоза или крахмал. Соединения по изобретению также могут быть введены в ректальные композиции, такие как клизмы, ректальные гели, ректальные пенки, ректальные аэрозоли, суппозитории, желейные суппозитории или удерживающие клизмы, содержащие обычные суппозиторные основы, такие как масло какао или другие глицериды, а также синтетические полимеры, такие как поливинилпирролидон, PEG и им подобные. В суппозиторных формах композиций сначала расплавляется низкоплавкий воск, такой как, но не ограничиваясь им, смесь триглицеридов жирной кислоты, необязательно, в комбинации с маслом какао. Фармацевтические композиции могут быть получены обычным способом, используя один или несколько физиологически приемлемых носителей, включающих эксципиенты и добавки, которые облегчают включение активных соединений в составы, которые могут использоваться фармацевтически. Нужный состав зависит от выбранного способа введения. Любая из известных методик, носителей и эксципиентов может использоваться в качестве подходящей и является известной из предшествующего уровня техники. Фармацевтические композиции, включающие соединение по изобретению, могут быть получены обычным способом, таким как, например, обычное смешение, растворение, гранулирование, получение драже, растирание, эмульгирование, инкапсулирование, захват или прессование. Фармацевтические композиции включают по крайней мере один фармацевтически приемлемый носитель, разбавитель или эксципиент и описанное соединение формул (1), (2 А-2 С) или (3A-3D) в качестве активного ингредиента в форме свободной кислоты, или свободного основания, или в форме фармацевтически приемлемой соли. Кроме того, описанные способы и фармацевтические композиции включают применение N-оксидов, кристаллических форм (также известных как полиморфы), а также активных метаболитов этих соединений, имеющих ту же активность. В некоторых случаях соединения могут существовать в виде таутомеров. Все таутомеры включены в объем представленных соединений. Дополнительно описанные соединения могут существовать в несольватированной, а также сольватированной формах с фармацевтически приемлемыми растворителями, такими как вода, этанол и им подобные. Сольватированные формы представленных соединений также здесь описаны. Кроме того, фармацевтические композиции могут включать другие медицинские или фармацевтические агенты, носители, адъюванты, такие как консервант, стабилизирующие, увлажняющие или эмульгирующие агенты, промотеры раствора, соли для регулирования осмотического давления и/или буферы. Кроме того, фармацевтические композиции также могут содержать другие терапевтически ценные вещества. Способы получения композиций, включающих описанные соединения, включают объединение соединений с одним или несколькими инертными, фармацевтически приемлемыми эксципиентами или носителями с образованием твердого, полутвердого или жидкого вещества. Твердые композиции включают, но не ограничиваются ими, порошки, таблетки, диспергируемые гранулы, капсулы, саше и суппозитории. Жидкие композиции включают растворы, в которых соединение растворено, эмульсии, содержащие соединение, или раствор, содержащий липосомы, мицеллы или наночастицы, включающие описанное соединение. Полутвердые композиции включают, но не ограничиваются ими, гели, суспензии и кремы. Композиции могут быть в форме жидких растворов или суспензий, твердых форм, подходящих для растворения или суспендирования в жидкости перед применением, или в виде эмульсий. Эти композиции также могут содержать минорные количества нетоксичных добавок, таких как увлажняющие или эмульгирующие агенты, pH буферные агенты и так далее. Обзор описанных фармацевтических композиций может быть обнаружен, например, в книгах Remington: The Science and Practice of Pharmacy, 19-oe изд. (Easton, Pa.: Mack Publishing Company, 1995); Hoover, John E., Remington's Pharmaceutical Sciences, Mack Publishing Co., Easton, Pennsylvania, 1975; под ред.Liberman, H.A. и Lachman, L., Pharmaceutical Dosage Forms, Marcel Decker, New York, N.Y., 1980; и Pharmaceutical Dosage Forms and Drug Delivery Systems, 17-ое изд. (Lippincott WilliamsWilkins 1999), включенных здесь в качестве ссылки. Способы введения и способы лечения Композиции, содержащие описанное соединение (соединения), могут вводиться для профилактического и/или терапевтического лечения. При терапевтических применениях композиции вводят пациенту,- 11018484 уже страдающему заболеванием или состоянием, в количестве, достаточном для излечения или, по крайней мере, частичной остановки симптомов заболевания или состояния. Специалист в данной области техники способен определить такие терапевтически эффективные количества проведением рутинных экспериментов (включая, но не ограничиваясь ими, дозозависимые клинические испытания). Соединения по изобретению могут вводиться в виде отдельного активного ингредиента или в комбинации со вторым терапевтическим агентом. Например, соединения по изобретению могут вводиться вместе с другими терапевтическими агентами в отношении неопластических заболеваний, с агентами,полезными при иммуномодулирующих режимах лечения или с фармацевтическими композициями, эффективными для различных заболеваний, как описано выше, например с циклофосфамидом, 5 фторурацилом, флударабином, гемцитабином, цисплатином, карбоплатином, винкристином, винбластином, этопозидом, иринотеканом, паклитакселем, доцетакселем, ритуксаном, доксорубицином, гефитинибом или иматинибом; или также с циклоспоринами, рапамицинами, аскомицинами или их иммунодепрессантными аналогами, например циклоспорином А, циклоспорином G, FK-506, сиролимусом или эверолимусом, кортикостероидами, например преднизоном, циклофосфамидом, азатиопреном, метотрексатом, солями золота, сульфазалазином, антималярийными средствами, брехинаром, лефлуномидом, мизорибином, микофенольной кислотой, микофенолятом, мофетилом, 15-дезоксиспергуалином, иммунодепрессорными моноклональными антителами, например, моноклональным антителом к лейкоцитным рецепторам, например МНС, CD2, CD3, CD4, CD7, CD25, CD28, I CD40, CD45, CD58, CD80, CD86, CD152,CD137, CD154, ICOS, LFA-1, VLA-4 или их лиганды, или другими иммуномодулирующими соединениями, например CTLA41g. Соединения по изобретению также могут использоваться в комбинации с химиотерапевтическим агентом для лечения клеточного пролиферативного нарушения, включая, но не ограничиваясь ими, лимфому, остеосаркому, меланому или опухоль груди, почек, простаты, толстой кишки, щитовидной железы, яичников, поджелудочной железы, нейронов, легких, матки или желудочно-кишечную опухоль. Примеры химиотерапевтических агентов, которые могут использоваться в композициях и способах по изобретению, включают но не ограничиваются ими, антрациклины, алкилирующие агенты (например,митомицин С), алкилсульфонаты, азиридины, этиленимины, метилмеламины, горчичный азот, нитрозомочевины, антибиотики, антиметаболиты, аналоги фолиевой кислоты (например, ингибиторы дигидрофолатредуктазы, такие как метотрексат), аналоги пурина, аналоги пиримидина, ферменты, подофиллотоксины, платинасодержащие агенты, интерфероны и интерлейкины. Конкретные примеры известных химиотерапевтических агентов, которые могут использоваться в композициях и способах по изобретению, включают, но не ограничиваются ими, бусульфан, импросульфан, пипосульфан, бензодепа, карбоквуон, метуредепа, уредепа, альтретамин, триэтиленмеламин, триэтиленфосфорамид, триэтилентиофосфорамид, триметилоломеламин, хлорамбуцил, хлорнафазин, циклофосфамид, эстрамустин, ифосфамид,мехлоретамин, гидрохлорид оксида мехлоретамина, мельфалан, новембицин, фенестерин, преднимустин,трофосфамид, горчичный урацил, кармустин, хлорозотоцин, фотемустин, ломустин, нимустин, ранимустин, дакарбазин, манномустин, митобронетол, митолактол, пипоброман, аклациномицины, актиномицинF(1), антрамицин, азасерин, блеомицин, кактиномицин, карубицин, карзинофилин, хромомицин, дактиномицин, даунорубицин, дауномицин, 6-диазо-5-оксо-1-норлейцин, доксорубицин, эпирубицин, митомицин С, микофенольную кислоту, ногаламицин, оливомицин, пепломицин, пликамицин, порфиромицин,пуромицин, стрептонигрин, стрептозоцин, туберцидин, убенимекс, зиностатин, зорубицин, деноптерин,метотрексат, птероптерин, триметрексат, флударабин, 6-меркаптопурин, тиамиприн, тиогуанин, анцитабин, азацитидин, 6-азауридин, кармофур, цитарабин, дидезоксиуридин, доксифлуридин, эноцитабин,флоксуридин, фторурацил, тегафур, L-аспарагиназу, пульмозим, ацеглатон, гликозид альдофосфамида,аминолевулиновую кислоту, амсакрин, бестрабуцил, бисантрен, карбоплатин, цисплатин, дефофамид,демеколцин, диазиквуон, эльфорнитин, ацетат эллиптиния, этоглуцид, этопозид, флутамид, нитрат галлия, гидроксимочевину, интерферон-альфа, интерферон-бета, интерферон-гамма, интерлейкин-2, лентинан, лонидамин, митогуазон, митоксантрон, мопидамол, нитракрин, пентостатин, фенамет, пирарубицин,подофиллиновую кислоту, 2-этилгидразид, прокарбазин, разоксан, сизофиран, спирогерманий, паклитаксель, тамоксифен, тенипозид, тенуазоновую кислоту, триазиквуон, 2,2',2"-трихлортриэтиламин, уретане,винбластин, винкристин и виндезин. Когда соединения по изобретению вводят в смеси с другими лекарственными средствами, дозировки совместно вводимых соединений сильно зависят от типа совместно используемого лекарственного препарата, от конкретного используемого лекарственного препарата, от излечиваемого заболевания или состояния и так далее. Кроме того, при совместном введении с одним или несколькими биологическими активными агентами, соединения по изобретению могут вводиться одновременно с биологически активным агентом (агентами) или последовательно. Введение соединения по изобретению в комбинации со вторым терапевтическим агентом может иметь аддитивный или синергетический эффект. Обычно соединения по изобретению вводят в терапевтически эффективных количествах любыми обычными и приемлемыми способами, известными из уровня техники, отдельно или в комбинации с одним или несколькими терапевтическими агентами. Терапевтически эффективное количество может широко варьироваться в зависимости от степени тяжести заболевания, возраста и относительного здоровья субъекта, активности используемого соединения и других факторов. Обычно удовлетворительные результаты получают при систематических суточных дозировках от около 0,03 до 2,5 мг/кг веса тела. Показанная суточная дозировка для большего млекопитающего, например человека, может находиться в диапазоне от около 0,5 до около 100 мг, которая обычно вводится, например, раздельными дозами вплоть до четырех раз в день или в замедленной форме. Подходящие единичные дозированные формы для перорального введения включают от около 1 до 50 мг активного ингредиента. Токсичность и терапевтическая эффективность таких терапевтических режимов может определяться стандартными фармацевтическими методиками на клеточных культурах или на экспериментальных животных, включая, но не ограничиваясь ими, для определения LD50 (доза, летальная для 50% популяции) и ED50 (доза, терапевтически эффективная для 50% популяции). Соотношение дозы токсичного и терапевтического действия представляет собой терапевтический индекс, и он может выражаться как соотношение LD50 и ED50. Данные, полученные из анализов с клеточными культурами и исследований с животными, могут использоваться при составлении диапазона дозировки для применения на человеке. Дозировка таких соединений предпочтительно находится в диапазоне циркулирующих концентраций,которые включают значения ED50 с минимальной токсичностью. Дозировка может изменяться в этом диапазоне в зависимости от используемой дозированной формы и используемого способа введения. Способы получения соединений по изобретению Общие методики получения соединений по изобретению описаны далее в примерах. В описанных реакциях реакционоспособные функциональные группы, например гидроксигруппа, аминогруппа, иминогруппа, тиогруппа или карбоксигруппа, где она необходима в конечном продукте, может быть защищена для устранения ее нежелательного участия в реакциях. Обычные защитные группы могут использоваться в соответствии со стандартной практикой (см., например, книгу T.W. Greene и P.G.M. Wuts,"Protective Groups in Organic Chemistry", John Wiley and Sons, 1991). В некоторых примерах соединения формулы (1) могут быть получены в соответствии с методикой синтеза, приведенной на схеме 1. Схема 1W = CH2 или NH; Z1 = N или СН Альтернативно, соединения формулы (1) могут быть получены синтетическими методиками, описанными на схеме 2. Схема 2Z1 = N или СН Соединения по изобретению, включая их соли, также получают в форме гидратов, или их кристаллы могут включать, например, растворитель, использующийся при кристаллизации (представлены как сольваты). Соли обычно могут превращаться в соединения в свободной форме, например, обработкой подходящими основными агентами, например карбонатами щелочных металлов, гидрокарбонатами щелочных металлов или гидроксидами щелочных металлов, такими как карбонат калия или гидроксид натрия. Соединение по изобретению в форме основной аддитивной соли может быть превращено в соответствующую свободную кислоту обработкой подходящей кислотой (например, хлористо-водородной кислотой и т.д.). Ввиду тесной связи новых соединений в свободной форме и соединений в форме их солей, включая соли, которые могут использоваться в качестве промежуточных соединений, например, для очистки или идентификации новых соединений, любая ссылка на свободные соединения должна пониматься как относящаяся также к соответствующим солям, если это возможно. Соли соединений по изобретению с солеобразующей группой могут быть получены известным способом. Кислотные аддитивные соли соединений формул (1), (2), (2 А-2 С) или (3A-3D), следовательно,могут быть получены обработкой кислотой или подходящим анионообменным реагентом. Фармацевтически приемлемые соли соединений по изобретению могут быть получены, например, в виде кислотных аддитивных солей, с органическими или неорганическими кислотами, из соединений формул (1), (2),(2 А-2 С) или (3A-3D), с основным атомом азота. Подходящие неорганические кислоты включают, но не ограничиваются ими, галогенсодержащие кислоты, такие как хлористо-водородная кислота, серная кислота или фосфорная кислота. Подходящие органические кислоты включают, но не ограничиваются ими, карбоновые, фосфорные, сульфоновые или сульфаминовые кислоты, например уксусная кислота, пропионовая кислота, октановая кислота, декановая кислота, додекановая кислота, гликолевая кислота, молочная кислота, фумаровая кислота, янтарная кислота, адипиновая кислота, пимелиновая кислота, субериновая кислота, азелаиновая кислота, яблочная кислота, винная кислота, лимонная кислота, аминокислоты, такие как глутаминовая кислота или аспарагиновая кислота, малеиновая кислота, гидроксималеиновая кислота, метилмалеиновая кислота, циклогексанкарбоновая кислота, адамантанкарбоновая кислота, бензойная кислота, салициловая кислота, 4 аминосалициловая кислота, фталевая кислота, фенилуксусная кислота, миндальная кислота, коричная кислота, метан- или этансульфоновая кислота, 2-гидроксиэтансульфоновая кислота, этан-1,2 дисульфоновая кислота, бензолсульфоновая кислота, 2-нафталенсульфоновая кислота, 1,5 нафталендисульфоновая кислота, 2-, 3- или 4-метилбензолсульфоновая кислота, метилсерная кислота,этилсерная кислота, додецилсерная кислота, N-циклогексилсульфаминовая кислота, N-метил-, N-этилили N-пропилсульфаминовая кислота или другие органические протонные кислоты, такие как аскорбиновая кислота. Для выделения или очистки также возможно использование фармацевтически неприемлемых солей, например пикратов или перхлоратов. Для терапевтического применения используются только фармацевтически приемлемые соли или свободные соединения (при необходимости в форме фармацевтических препаратов). Соединения по изобретению в неокисленной форме могут быть получены из N-оксидов соединений по изобретению обработкой восстанавливающим агентом (например, серой, диоксидом серы, трифенилфосфином, боргидридом лития, боргидридом натрия, трихлоридом фосфора, трибромидом или им подобными) в подходящем инертном органическом растворителе (например, ацетонитриле, этаноле, водном диоксане или им подобных) при температуре от 0 до 80C. Пролекарственные производные соединений по изобретению могут быть получены способами, известными специалисту в данной области техники (например, более подробно см. книгу Saulnier и др.,1994, Bioorganic and Medicinal Chemistry Letters, т. 4, с. 1985). Например, подходящие пролекарства могут быть получены реакцией нефункционализированного соединения по изобретению с подходящим карбамилирующим агентом (например, 1,1-ацилоксиалкилкарбанохлоридат, паранитрофенилкарбонат или им подобные). Защищенные производные соединений по изобретению могут быть получены методами, известными специалисту в данной области техники. Подробное описание методик, подходящих для создания защитных групп, и их удаление может быть обнаружено в книге Т.W. Greene, "Protecting Groups in OrganicChemistry", 3e изд., John Wiley and Sons, Inc., 1999. Соединения по изобретению могут быть получены в виде их отдельных стереоизомеров реакцией рацемической смеси соединения с оптически активным расщепляющим агентом с получением пары диастереоизомерных соединений, разделяя диастереомеры и восстанавливая оптически чистые энантиомеры. Расщепление энантиомеров может осуществляться с помощью ковалентных диастереомерных производных соединений по изобретению или с помощью диссоциируемых комплексов (например, кристаллические диастереомерные соли). Диастереомеры имеют различные физические свойства (например, температуры плавления, температуры кипения, растворимости, реакционноспособность и т.д.) и могут быть легко разделены на основании этих различий. Диастереомеры могут быть разделены фракционной кристаллизацией, хроматографией или методиками разделения/расщепления, основанными на различиях в растворимости. Оптически чистый энантиомер затем выделяют наряду с расщепляющим агентом любыми практическими методами, которые не приводят к рацемизации. Более подробное описание методик,подходящих для выделения стереоизомеров соединений из их рацемической смеси, может быть обнаружено в книге Jean Jacques, Andre Collet, Samuel H. Wilen, "Enantiomers, Racemates and Resolutions", JohnWiley And Sons, Inc., 1981. Итак, соединения по изобретению могут быть получены способом, описанным в примерах; и(а) необязательно превращением соединения по изобретению в фармацевтически приемлемую соль;(б) необязательно превращением формы соли соединения по изобретению в несолевую форму;(в) необязательно превращением неокисленной формы соединения по изобретению в фармацевти- 14018484(г) необязательно превращением N-оксидной формы соединения по изобретению в его неокисленную форму;(д) необязательно выделением индивидуального изомера соединения по изобретению из смеси изомеров;(е) необязательно превращением нефункционализированного соединения по изобретению в фармацевтически приемлемое пролекарственное производное и(ж) необязательно превращением пролекарственного производного соединения по изобретению в его нефункционализированную форму. Несмотря на то, что получение исходных материалов конкретно не описано, соединения являются известными или могут быть получены аналогично способам, известным из предшествующего уровня техники, или как описано далее в примерах. Специалисту в данной области техники ясно, что описанные выше превращения только иллюстрируют способы получения соединений настоящего изобретения и что другие хорошо известные способы аналогично могут использоваться. Настоящее изобретение далее представлено, но не ограничено, следующими примерами, которые иллюстрируют получение соединений по изобретению. Пример 1. N2-(2-Изопропокси-5-метил-4-(1-метилпиперидин-4-ил)фенил)-N4-(2-(изопропилсульфонил)фенил)пиразоло[1,5-a][1,3,5]триазин-2,4-диамин (1). 7 г 2-меркаптопиразоло[1,5-а][1,3,5]триазин-4-ола (полученного в соответствии с методикой, описанной в статье Chemische Berichte, 1971, 104, cc. 3039-47), растворяли в 5% водном растворе NaOH (100 мл). Раствор охлаждали до 5C (ледяная баня) и по каплям добавляли 6 г метилйодида. Через 15-20 мин добавляли уголь и смесь отфильтровывали, затем подкисляли уксусной кислотой. Осадок (2(метилтио)пиразоло[1,5-а][1,3,5]триазин-4-ола отфильтровывали, сушили и выделяли. Дальнейшая перекристаллизация изАсОН приводила к получению 2-(метилтио)пиразоло[1,5-а][1,3,5]триазин-4-ола. К смеси 10 мл оксихлорида фосфора и 1 мл N,N-диметиланилина добавляли 0,5 г 2(метилтио)пиразоло[1,5-а][1,3,5]триазин-4-ола (сырой с предыдущей стадии). Раствор кипятили с обратным холодильником в течение 30-60 мин до растворения твердого вещества. Избыток фосфора удаляли при пониженном давлении и мутный остаток выливали при интенсивном перемешивании в смесь льда и воды. Через 10 мин водный раствор экстрагировали диэтиловым эфиром. Эфирные слои собирали и промывали холодной водой, затем сушили безводным Na2SO4. Фильтрация и концентрирование при пониженном давлении приводили к получению целевого 4-хлор-2-(метилтио)пиразоло[1,5-а][1,3,5]триазина. фонил)анилина (10 ммоль) в 100 мл изопропанола перемешивали при кипении с обратным холодильником в течение 1 ч. После охлаждения до комнатной температуры в реакционную смесь добавляли Et3N(12 ммоль), затем раствор нагревали при кипении с обратным холодильником в течение 30 мин. После обработки остаток очищали ускоренной колоночной хроматографией на SiO2 (элюент: гексан/EtOAc 4:1) с получением целевого N-(2-(изопропилсульфонил)фенил)-2-(метилтио)пиразоло[1,5-а][1,3,5]триазин-4 амина.(1 ммоль) в 10 мл 1,2-дихлорэтана медленно добавляли МСРВА (метахлорпероксибензойная кислота) (3 ммоль) при 0C. Реакционную смесь постепенно нагревали до КТ и перемешивали в течение 1 ч. После обработки остаток очищали ускоренной колоночной хроматографией на SiO2 (элюент: CH2Cl2/МеОН 9:1) с получением N-(2-(изопропилсульфонил)фенил)-2-(метилсульфонил)пиразоло[1,5-а][1,3,5]триазин-4 амина. К суспензии N-(2-(изопропилсульфонил)фенил)-2-(метилсульфонил)пиразоло[1,5-а][1,3,5]триазин 4-амина (0,5 ммоль) в 1 мл изопропанола добавляли 2-изопропокси-5-метил-4-(1-метилпиперидин-4 ил)анилин (0,5 ммоль) и 4-метилбензолсульфоновую кислоту (1 ммоль). Суспензию перемешивали при 150C в течение 3 ч. После охлаждения до КТ и обработки остаток очищали препаративной ВЭЖХ с получением N2-(2-изопропокси-5-метил-4-(1-метилпиперидин-4-ил)фенил)-N4-(2-(изопропилсульфонил) фенил)пиразоло[1,5-а][1,3,5]триазин-2,4-диамина. 1 Н ЯМР (MeOD, 400 МГц)8,51-8,54 (d, 1H), 7,94-8,04 (m, 2H), 7,35-7,47 (m, 3H), 6,90 (s, 1H), 6,346,35 (d, 1H), 4,54-4,60 (m, 1H), 3,82-3,85 (m, 2H), 3,23-3,30 (m, 1H), 2,91-3,01 (m, 6H), 2,25-2,33 (m, 5H),2,03-2,06 (m, 2H), 1,33-1,35 (d, 6H), l,26-l,28 (d, 6H); К смеси N-(2-(изопропилсульфонил)фенил)-2-(метилсульфонил)пиразоло[1,5-а][1,3,5]триазин-4 амина (6,3 г, 15,9 ммоль) и соли трифторуксусной кислоты 2-метокси-5-метил-4-(пиперидин-4 ил)анилина (15,9 ммоль по свободному основанию) в 80 мл 2-пропанола в круглодонной колбе для повышенного давления объемом 350 мл добавляли трифторуксусную кислоту (ТФУК) (1,22 мл, 15,9 ммоль). Полученную смесь нагревали при 150C в течение 3 ч. После охлаждения до комнатной температуры осаждался продукт. Фильтрат промывали холодным 2-пропанолом и сушили на воздухе с получением[1,3,5]триазин-2,4-диамина в виде соли ТФУК. К смеси этой соли ТФУК (1,26 г, 2,0 ммоль), (R)-4-(трет-бутоксикарбонил)морфолин-3-карбоновой кислоты (0,504 г, 2,2 ммоль) и (2-(7-аза-1H-бензотриазол-1-ил)-1,1,3,3-тетраметилурониумгексафторфосфат) (HATU) (0,847 г, 2,2 ммоль) в 30 мл диметилфумарата (ДМФА) добавляли диизопропилэтиламин (DIPEA) (1,76 мл, 10 ммоль). Полученный раствор перемешивали при комнатной температуре в течение 30 мин и затем по каплям добавляли в 150 мл воды. Осадок собирали фильтрацией и сушили на воздухе с получением (R)-трет-бутил-3-(4-(4-(4-(2-(изопропилсульфонил)фениламино)пиразоло[1,5 а][1,3,5]триазин-2-иламино)-5-метокси-2-метилфенил)пиперидин-1-карбонил)морфолин-4-карбоксилата в виде белого твердого вещества. Этот карбоксилат (1,3 г, 1,7 ммоль) растворяли в 10 мл 4 М HCl в 1,4 диоксане и перемешивали в течение 30 мин при комнатной температуре. Растворитель удаляли упариванием и остаток разделяли между 100 мл CH2Cl2 и 100 мл насыщенного NaHCO3. Слои разделяли и водный слой экстрагировали CH2Cl2 (3100 мл). Объединенные органические слои сушили NaSO3, концентрировали и очищали хроматографией на силикагеле (от 0 до 8% МеОН в CH2Cl2 в качестве элюента) с получением указанного в заголовке соединения в виде белого твердого вещества. 1 Н ЯМР (CDCl3, 400 МГц):10,85 (broad s, 1 Н), 8,82-8,84 (dd, 1H), 8,30 (broad s, 1H), 7,98-7,99(1,0 ммоль) в 5 мл ДМФА осторожно добавляли NaH (24 мг). Полученную суспензию перемешивали при 50C в течение 2 ч. После охлаждения до КТ осторожно гасили (лед), добавляли воду и смесь экстрагировали EtOAc. Органические слои собирали, сушили (Na2SO4), отфильтровывали и концентрировали. Остаток очищали колоночной хроматографией на SiO2 (элюент: 9:1 гексан:EtOAc) с получением целевого 5-хлор-N-(2-(изопропилсульфонил)фенил)пиразоло[1,5-а]пиримидин-7-амина.N5-(2-Изопропокси-5-метил-4-(пиперидин-4-ил)фенил)-N7-(2-(изопропилсульфонил)фенил)пиразоло[1,5-а]пиримидин-5,7-диамин. К раствору 5-хлор-N-(2-(изопропилсульфонил)фенил)пиразоло[1,5-а]пиримидин-7-амина (0,1 ммоль) и 2-изопропокси-5-метил-4-(пиперидин-4-ил)анилина (0,1 ммоль) в 2 мл изопропанола добавляли 25 мклHCl в диоксане (2N). Суспензию перемешивали при 150C в течение 3 ч. После обработки и преп-ВЭЖХ получали продукт. 1MS (ES+): 563,28 (M+1)+. В табл. 1 описаны некоторые соединения по изобретению, их получали следующими методиками,описанными выше. Значения IC50 измеряли с помощью анализа NPM-ALK BaF3.
МПК / Метки
МПК: A61P 31/00, C07D 471/04, A61K 31/53, A61P 37/00, A61P 35/00, A61K 31/519
Метки: протеинкиназы, соединения, ингибиторов, качестве, композиции
Код ссылки
<a href="https://eas.patents.su/30-18484-soedineniya-i-kompozicii-v-kachestve-ingibitorov-proteinkinazy.html" rel="bookmark" title="База патентов Евразийского Союза">Соединения и композиции в качестве ингибиторов протеинкиназы</a>
Предыдущий патент: Способ получения амидов в присутствии перегретой воды
Следующий патент: Прекомпозиция серного цемента и способ приготовления такой прекомпозиции серного цемента
Случайный патент: Кристаллы циклопентенонового соединения &alpha-типа