Соединения и композиции в качестве ингибиторов катепсина
Формула / Реферат
1. Соединение формулы I
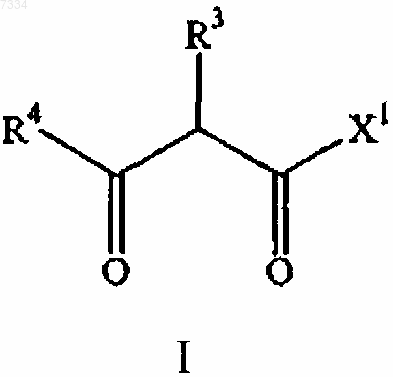
где X1 является -NHC(R1)(R2)2;
X2 является циано, -C(R7)(R8)X3; R7 и R8 вместе образуют оксогруппу;
X3 содержит гетеромоноциклическое кольцо, имеющее от 4 до 6 атомов, являющихся членами кольца или конденсированную гетеробициклическую кольцевую систему, содержащую от 8 до 14 атомов, являющихся членами кольца и любой карбоциклический кетон, иминокетон или его тиокетоновое производное;
R1 является водородом и R2 является водородом;
R3 является -C(R6)(R6)Х5, где R6 является водородом и X5 является выбранным из -Х4R12, -R14, -X4SR14, -X4S(O)2R14, где X4 является связью или (С1-6)алкилом; R12 при каждом появлении независимо является водородом или (С1-6)алкилом и R14 является (С3-10)циклоалкил(С0-6)алкилом, гетеро(С3-10)циклоалкил(С0-3)алкилом, (С6-10)арил(С0-6)алкилом, гетеро(С5-10)арил(С0-6)алкилом, (С9-10)бициклоарил(С0-6)алкилом или гетеро(С8-10)бициклоарил(С0-6)алкилом;
R4 является -NR6R6, -NR6R14, -NR6R15 или -NR6X5C(O)R14, где R6, X5 и R14 являются теми, которые описаны выше и R15 является водородом, -(С1-6)алкилом;
где в R3 и R4 любая алициклическая или ароматическая кольцевая система может быть дополнительно замещена нитро, -X4OR12, -X4C(O)NR12R12, -X4OR14, где R4, X12 и R14 являются теми, которые описаны выше, и в R3 и R4 любой алифатический остаток может быть замещен дополнительно циано; и
N-оксидные производные, производные пролекарств, защищенные производные, индивидуальные изомеры и смеси этих изомеров; и фармацевтически приемлемые соли и сольваты таких соединений и N-оксидные производные, производные пролекарств, защищенные производные, индивидуальные изомеры и смеси этих изомеров.
2. Соединение по п.1, где
X2 является циано, -С(O)Х3, -С(O)СF3;
R3 является -СН2Х5, где X3 и X5 являются теми, что указано выше.
3. Соединение по п.2, где
X2 является циано, -С(O)Х3, -СF3, -CF2CF3, (Е)-2-бензолсульфонилвинилом, 2-диметилкарбамоил-2,2-дифторацетилом, 1-бензилкарбамоилметаноилом, 1-бензилокси(оксалилом), 2-бензилоксиацетилом, 2-бензолсульфониламиноэтаноилом или 2-оксо-2-фенилэтаноилом;
X3 является 1H-бензоимидазол-2-илом, пиримидин-2-илом, бензооксазол-2-илом, бензотиазол-2-илом, пиридазин-3-илом, 3-фенил-[1,2,4]оксадиазол-5-илом, 3-этил-[1,2,4]оксадиазол-5-илом, 2-метил-4-оксотетрагидрофуран-3-илом, 2-этил-4-оксотетрагидрофуран-3-илом, 4-оксо-1-(1-фенилметаноил)пирролидин-3-илом или (S)-2-ацетокси-4-оксоазетидин-3-илом;
R1 является водородом или метилом и R2 представляет собой водород, метоксиметил, (С1-6)алкил, фенэтил, тиофен-2-ил или 5-метилфуран-2-ил или R1 и R2 вместе с атомом углерода, к которому они присоединены, образуют циклопропилен, тетрагидрофуран-4-илен или метилпиперидин-4-илен.
4. Соединение по п.3, где R3 выбрано из тиофен-2-сульфонилметила, 3-хлор-2-фтор-фенилметансульфонилметила, бензолсульфонилметила, фенилметансульфонилметила, 2-(1,1-дифторметокси)фенилметансульфонилметила, 2-бензолсульфонилэтила, 2-(пиридин-2-сульфонил)этила, 2-(пиридин-4-сульфонил)этила, 2-фенилметансульфонилэтила, оксипиридин-2-илметансульфонилметила, проп-2-ен-1-сульфонилметила, 4-метоксифенилметансульфонилметила, n-толилметансульфонилметила, 4-хлорфенилметансульфонилэтила, о-толилметансульфонилметила, 3,5-диметилфенилметансульфонилметила, 4-трифторметилфенилметансульфонилметила, 4-трифторметоксифенилметансульфонилметила, 2-бромфенилметансульфонилметила, пиридин-2-илметансульфонилметила, пиридин-3-илметансульфонилметила, пиридин-4-илметансульфонилметила, нафтален-2-илметансульфонилметила, 3-метилфенилметансульфонилметила, 3-трифторметилфенилметансульфонилметила, 3-трифторметоксифенилметансульфонилметила, 4-фтор-2-трифторметоксифенилметансульфонилметила, 2-фтор-6-трифторметилфенилметансульфонилметила, 3-хлорфенилметансульфонилметила, 2-фторфенилметансульфонилметила, 2-трифторфенилметансульфонилметила, 2-цианофенилметансульфонилметила, 4-трет-бутилфенилметансульфонилметила, 2-фтор-3-метилфенилметансульфонилметила, 3-фторфенилметансульфонилметила, 4-фторфенилметансульфонилметила, 2-хлорфенилметансульфонилметила, 2,5-дифторфенилметансульфонилметила, 2,6-дифторфенилметансульфонилметила, 2,5-дихлорфенилметансульфонилметила, 3,4-дихлорфенилметансульфонилметила, 2-(1,1-дифторметокси)фенилметансульфонилметила, 2-цианофенилметансульфонилметила, цианофенилметанесульфонилметила, 2-трифторметоксифенилметансульфонилметила, 2,3-дифторфенилметансульфонилметила, 2,5-дифторфенилметансульфонилметила, бифенил-2-илметансульфонилметила, циклогексилметила, 3-фторфенилметансульфонилметила, 3,4-дифторфенилметансульфонилметила, 2,4-дифторфенилметансульфонилметила, 2,4,6-трифторфенилметансульфонилметила, 2,4,5-трифторфенилметансульфонилметила, 2,3,4-трифторфенилметансульфонилметила, 2,3,5-трифторфенилметансульфонилметила, 2,5,6-трифторфенилметансульфонилметила, 2-хлор-5-трифторметилфенилметансульфонилметила, 2-метилпропан-1-сульфонила, 2-фтор-3-трифторметилфенилметансульфонилметила, 2-фтор-4-трифторметилфенилметансульфонилметила, 2-фтор-5-трифторметилфенилметансульфонилметила, 4-фтор-3-трифторметилфенилметансульфонилметила, 2-метоксифенилметансульфонилметила, 3,5-бис-трифторметилфенилметансульфонилметила, 4-дифторметоксифенилметансульфонилметила, 2-дифторметоксифенилметансульфонилметила, 3-дифторметоксифенилметансульфонилметила, 2,6-дихлорфенилметансульфонилметила, бифенил-4-илметансульфонилметила, 3,5-диметилизоксазол-4-илметансульфонилметила, 5-хлортиофен-2-илметансульфонилметила, 2-[4-(1,1-дифторметокси)бензолсульфонил]этила, 2-[2-(1,1-дифторметокси)бензолсульфонил]этила, 2-[3-(1,1-дифторметокси)бензолсульфонил]этила, 2-(4-трифторметоксибензолсульфонил)этила, 2-(3-трифторметоксибензолсульфонил)этила, 2-(2-трифторметоксибензолсульфонил)этила, (цианометилметилкарбамоил)метила, бутила, бифенил-3-илметила, 2-оксо-2-пирролидин-1-илэтила, 2-бензолсульфонилэтила, изобутилсульфанилметила, 2-фенилсульфанилэтила, циклогексилметансульфонилметила, 2-циклогексилэтансульфонила, бензила, нафтален-2-ила, бензилсульфанилметила, 2-трифторметилбензилсульфанилметила, 5-бромтиофен-2-илметила, фенилсульфанилэтила и циклопропилметансульфонилметила.
5. Соединение по п.4, где R4 выбрано из фениламино, бензиламино, 4-феноксифениламино, фенэтиламино, 3-фенилпропиламино, морфолин-4-ила, циклогексиламино, нафтален-1-илметиламино, пиридин-3-иламино, 6-метоксипиридин-3-иламино, диизобутиламино, 4-нитробензиламино, 2-тиофен-2-илэтиламино, 3-феноксифениламино, цианометиламино, (пиридин-3-илметил)амино, 5,6,7,8-тетрагидронафтален-1-иламино, 2-пиридин-2-илэтиламино, 2,3-дигидроиндол-1-ила, 3,4-дигидро-1Н-изохинолин-2-ила, циклогексилметиламино, 2-метоксибензиламино, 1-фенилэтиламино, (пиридин-4-илметил)амино, бензилметиламино, 3-нитробензиламино, 4-метоксифениламино, 3-карбамоилфениламино, 4-карбамоилфениламино, (тетрагидрофуран-2-илметил)амино, 3,4-дигидро-2Н-хинолин-1-ила, диметиламино, бутилметиламино, диизопропиламино, пропилметиламино, 1-(бензооксазол-2-карбонил)пропиламино и изобутилметиламино.
6. Соединение по п.5 выбрано из группы, включающей таъшх соединения, как 2-бутил-N-цианометил-N'-фенилмалонамид, N-цианометил-2-циклогексилэтил-N'-фенилмалонамид; N-цианометил-2-циклогексилметил-N'-фенэтилмалонамид; N-цианометил-2-циклогексилметил-N'-пиридин-4-илметилмалонамид; N-[1-(бензоксазол-2-карбонил)-3-фенилпропил]-N'-бензил-2-циклогексилметилмалонамид; N-цианометил-N'-циклогексил-2-циклогексилметилмалонамид; N-бензил-N'-цианометил-2-циклогексилметилмалонамид; N-цианометил-2-циклогексилметил-N'-(4-феноксифенил)малонамид; N-цианометил-2-циклогексилметил-N'-(3-фенилпропил)малонамид; N-цианометил-2-циклогексилметил-3-морфолин-4-ил-3-оксопропионамид; N-цианометил-2-циклогексилметил-N'-нафтален-1-илметилмалонамид; N-цианометил-2-циклогексилметил-N'-пиридин-3-илмалонамид; N-цианометил-2-циклогексилметил-N',N'-диизобутилмалонамид; N-цианометил-2-циклогексилметил-N',N'-диизопропилмалонамид; N-цианометил-2-циклогексилметил-N'-(6-метоксипиридин-3-ил)малонамид; N-цианометил-2-циклогексилметил-N'-(2-тиофен-2-ил-этил)малонамид; N-цианометил-2-циклогексилметил-N'-(3-феноксифенил)малонамид; N-цианометил-2-циклогексилметил-N'-(4-нитробензил)малонамид; N,N'-биc-циaнoмeтил-2-циклoгeкcилмeтилмaлoнaмид; N-цианометил-2-циклогексилметил-N'-(5,6,7,8-тетрагидронафтален-1-ил)малонамид; N-цианометил-2-циклогексилметил-N'-(2-пиридин-2-ил-этил)малонамид; N-цианометил-2-циклогексилметил-3-(2,3-дигидроиндол-1-ил)-3-оксопропионамид; N-цианометил-2-циклогексилметил-3-(3,4-дигидро-1Н-изохинолин-2-ил)-3-оксопропионамид; N-цианометил-2,N'-бис-циклогексилметилмалонамид; N-цианометил-2-циклогексилметил-N'-(2-метоксибензил)малонамид; N-цианометил-2-циклогексилметил-N'-(1-фенилэтил)малонамид; N-бензил-N-цианометил-2-циклогексилметил-N'-метилмалонамид; N-цианометил-2-циклогексилметил-N'-(3-нитробензил)малонамид; N-цианометил-2-циклoгeкcилмeтил-N'-(4-мeтoкcибeнзил)мaлoнaмид; N-(3-кapбaмoилфeнил)-N-цианометил-2-циклогексилэтилмалонамид; N-цианометил-2-циклогексилметил-N'-пиридин-3-илметилмалонамид; N-(4-карбамоилфенил)-N'-цианометил-2-циклогексилметилмалонамид; N-цианометил-2-циклогексилметил-N-тетрагидрофур-2-илметилмалонамид; N-цианометил-2-циклогексилметил-3-(3,4-дигидро-2H-хинолин-1-ил)-3-оксопропионамид; N-трет-бyтил-N'-циaнoмeтил-2-циклoreкcилмeтил-N-метилмалонамид; N-цианометил-2-циклогексилметил-N'-метил-N'-пропилмалонамид; N-бyтил-N'-циaнoмeтил-2-циклoгeкcилмeтил-N-мeтилмaлoнaмид; N-цианометил-2-циклогексилметил-N',N'-диметилмалонамид; N-бензил-N'-цианометил-2-(2-фенилсульфанилэтил)малонамид; 2-(2-фенилсульфонилэтил)-N-бензил-N'-цианометилмалонамид; 2-(2-бeнзoлcyльфонилэтил)-N-[(S)-1-(1-бeнзоокcaзoл-2-ил-метаноил)пентил]-N'-бензилмалонамид; N,N'-бис-[(S)-1-(1-бензооксазол-2-ил-метаноил)пропил]-2-циклогексилметилмалонамид; и N-оксидные производные, производные пролекарств, защищенные производные, индивидуальные изомеры и смеси этих изомеров;
и фармацевтически приемлемые соли и сольваты таких соединений и N-оксидные производные, производные пролекарств, защищенные производные, индивидуальные изомеры и смеси этих изомеров.
7. Фармацевтическая композиция, содержащая терапевтически эффективное количество соединения по п.1 в комбинация с фармацевтически приемлемым наполнителем.
8. Способ лечения заболевания животного, при котором ингибирование катепсина S может предотвращать, ингибировать или уменьшать патологию и/или симптомологию заболевания, включающий введение животному терапевтически эффективного количества соединения по п.1 или его N-оксидного производного или индивидуального изомера или смеси изомеров; или его фармацевтически приемлемой соли или сольвата таких соединений и N-оксидных производных, производных пролекарств, защищенны производных, индивидуальных изомеров и смеси этих изомеров.
9. Применение соединения по п.1 для получения лекарственного средства для лечения заболевания животного, при котором активность катепсина S оказывает влияние на патологию и/или симптомологию болезни.
10. Способ получения соединения формулы I:
(а) взаимодействием соединения формулы 2
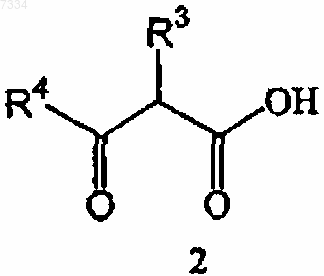
с соединением формулы NH2CR1R2X2, где R1, R2, R3, R4 и X2 являются теми, как определено в п.1; или
(b) взаимодействием соединения формулы 2 с соединением формулы NH2X3, где R3, R4 и X3 являются теми, как определено в п.1.
Текст
007334 Настоящее изобретение относится к соединениям и композициям для лечения заболеваний, связанных с активностью цистеиновой протеазы, особенно заболеваний, связанных с активностью Катепсина S. Область изобретения Цистеиновые протеазы представляют собой класс пептидаз, которые характеризуются присутствием цистеинового остатка на каталитическом сайте фермента. Цистеиновые протеазы ассоциируются с нормальным разложением и действием белков. Аберрантная активность цистеиновых протеаз, например,как результат повышенной экспрессии или усиления активации, однако, может вызывать патологические последствия. В этом отношении, некоторые цистеиновые протеазы связаны со множеством заболеваний,включая артрит, мышечную дистрофию, воспаление, инвазию опухоли, гломерулонефрит, малярию, периодонтальную болезнь, метахроматическую лейкодистрофию и другие. Повышение активности Катепсина С оказывает влияние на патологию и/или симптомалогию множества болезней. Соответственно,молекулы, которые ингибируют активность протеазы Катепсина С, полезны в качестве терапевтических агентов при лечении перечисленных заболеваний. Сущность изобретения Настоящее изобретение относится к соединениям формулы IR6 является водородом или (С 1-6)алкилом; R7 является водородом или (С 1-4)алкилом, и R8 является гидрокси или R7 и R8 вместе образуют оксогруппу; R9 является водородом, галогеном, (С 1-4)алкилом, (С 5-10) арил(С 0-6)алкилом или (С 5-10)гетероарил(С 0-6)алкилом;X3 содержит гетеромоноциклическое кольцо, включающее от 4 до 6 атомов, являющихся членами кольца или конденсированную гетероциклическую кольцевую систему, содержащую от 8 до 14 атомов,являющихся членами кольца и любой карбоциклический кетон, иминокетон или его тиокетоновое производное; где любая алициклическая или ароматическая кольцевая система в составе R5, X2 или X3 может быть замещена дополнительно 1-5 радикалами, независимо выбранными из (С 1-6)алкила, (С 1-6)алкилидена, циано, галогена, галогензамещенного(С 1-4)алкила, нитро, -X4NR12R2, -X4NR12C(O)R12,-X4NR12C(O)OR12, -X4NR12C(O)NR12R12, -X4NR12C(NR12)NR12R12, -X4OR12, -X4SR12, -X4C(O)OR12,-X4C(O)R12, -X4OC(O)R12, -X4C(O)NR12R12, -X4S(O)2NR12R12, -X4NR12S(O)2R12, -X4P(O)(OR12)OR12,-X4OP(O)(OR12)OR12, -X4NR12C(O)R13, -X4S(O)R13 и -X4S(O)2R13 и/или 1 радикалом, выбранным из -R14,-X4OR14, -X4SR14, -X4S(O)R14, -X4S(O)2R14, -X4C(O)R14, -X4C(O)OR14, -X4OC(O)R14, -X4NR14R2,-X4NR12C(O)OR14,-X4C(O)NR12R12,-X4S(O)2NR14R12,-X4NR12S(O)2R14,-X4NR12C(O)R14,4 12 14 12 4 12 12 14 12 4 12-X NR C(O)NR R и -X NR C(NR )NR R , где Х означает связь или (С 1-6)алкил; R каждый раз независимо является водородом, (С 1-6)алкилом или галогензамещенным(С 1-6)алкилом; R13 означает (С 1-6) алкил или галогензамещенный (С 1-6)алкил; и R14 означает (С 3-10)циклоалкил(С 0-6)алкил, гетеро(С 3-10)циклоалкил(С 0-3)алкил, (С 6-10)арил(С 0-6)алкил, гетеро(С 5-10)арил(С 0-6)алкил, (С 9-10)бициклоарил(С 0-6)алкил или гетеро(С 8-10)бициклоарил(С 0-6)алкил;R1 представляет собой водород, галоген или (С 1-6)алкил, и R2 выбирают из группы, состоящей из водорода, циано, галогена, -X4NR12R12, -X4NR12C(O)R12, -X4NR12C(O)OR12, -X4NR12C(O)NR12R12,-X4NR12C(NR12)NR12R12, -X4OR12, -X4SR12, -X4C(O)OR12, -X4C(O)R12, -X4OC(O)R12, -X4C(O)NR12R12,-X4S(O)2NR12R12, -X4NR12S(O)2R12, -X4P(O)(OR12)OR12, -X4OP(O)(OR12)OR12, -X4NR12C(O)R13, -X4S(O)R13,-X4S(O)2R13, -R14, -X4OR14, -X4SR14, -X4S(O)R14, -X4S(O)2R14, -X4C(O)R14, -X4C(O)OR14, -X4OC(O)R14,-X4NR14R12, -X4NR12C(O)R14, -X4NR12C(O)OR14, -X4C(O)NR12R12, -X4S(O)2NR14R12, -X4NR12S(O)2R14,-X4NR12C(O)NR14R12 и -X4NR12C(NR12)NR14R12, где X4, R12, R13 и R14 имеют значения определенные выше; или R1 и R2, взятые вместе с атомом углерода, к которому оба R1 и R2 присоединены, образуют (С 3-8) циклоалкилен или (С 3-8)гетероциклоалкилен; где любой гетероарил, арил, циклоалкил, гетероциклоалкил, циклоалкилен или гетероциклоалкилен в составе R2 является необязательно замещенным 1-3 радикалами, независимо выбранными из (С 1-6)алкила, (С 1-6)алкилидена, циано, галогена, галогензамещенного(С 1-4)алкила, нитро, -X4NR12R12, -X4NR12C(O)R12, -X4NR12C(O)OR12, -X4NR12C(O)NR12R12,-X4NR12C(NR12)NR12R12, -X4OR12, -X4SR12, -X4C(O)OR12, -X4C(O)R12, -X4OC(O)R12, -X4C(O)NR12R12,-X4S(O)2NR12R12, -X4NR12S(O)2R12, -X4P(O)(OR12)OR12, -X4OP(O)(OR12)OR12, -X4NR12C(O)R13, -X4S(O)R13,-X4S(O)2R13 и -X4C(O)R13, где X4, R12 и R13 имеют значения определенные выше;R3 представляет собой -C(R6)(R6)X5, где R6 имеет значения определенные выше, и X5 выбирают из-X NR C(O)NR R и -X NR C(NR )NR R , где X , R , R и R имеют значения определенные выше;R4 означает -NR6R6, -NR6R14, -NR6R15 или -NR5X5C(O)R14, где R6, X5 и R14 имеют значения, которые приведены выше, и R15 означает водород, -(С 1-6)алкил или -X5OR6, где X5 имеет значения определенные выше; или R6 и R15 вместе с атомом азота, к которому R6 и R15 присоединены, образуют гетеро(С 3-10) циклоалкил, гетеро(С 5-10)арил или гетеро(С 8-10)бициклоарил; где любая алициклическая или ароматическая кольцевая система в составе R3 и R4 может быть дополнительно замещена 1-5 радикалами, независимо выбранными из (С 1-6)алкила, (С 1-6)алкилидена, циано, галогена, галогензамещенного(С 1-4)алкила, нитро, -X4NR12R12, -X4NR12C(O)R12, -X4NR12C(O)OR12,-Х 4NR12C(O)NR12R2, -X4NR12C(NR12)NR12R12, -X4OR12, -X4SR12, -X4C(O)OR12, -X4C(O)R12, -X4OC(O)R12,-X4C(O)NR12R12,-X4S(O)2NR12R12,-X4NR12S(O)2R12,-X4P(O)(OR12)OR12,-X4OP(O)(OR12)OR12,4 12 13 4 13 4 13 4 13-X4NR12C(NR12)NR14R12; и любой алифатический остаток в составе R3 и R4 может быть замещен дополнительно 1-5 радикалами, независимо выбранными из циано, галогена, нитро, -NR12R12, -NR12C(O)R12,-NR12C(O)OR12, -NR12C(O)NR12R12, -NR12C(NR12)NR12R12, -OR12, -SR12, -C(O)OR12, -C(O)R12, -OC(O)R12,-C(O)NR12R12, -S(O)2NR12R12, -NR12S(O)2R12, -P(O)(OR12)OR12, -OP(O)(OR12)OR12, -NR12C(O)R13, -S(O)R13 и -S(O)2R13; где X4, R12, R13 и R14 имеют значения определенные выше; при условии, что только одна бициклическая кольцевая структура присутствует в R3 или R4; и Nоксидные производные, производные пролекарств, защищенные производные, индивидуальные изомеры и смеси этих изомеров; и фармацевтически приемлемые соли и сольваты (например, гидраты) таких соединений и их N-оксидные производные, производные пролекарств, защищенные производные, индивидуальные изомеры и смеси этих изомеров. Вторым аспектом изобретения является фармацевтическая композиция, которая содержит соединение формулы I или N-оксидное производное, индивидуальный изомер или смесь указанных изомеров или его фармацевтически приемлемую соль, в смеси с одним или более соответствующих наполнителей. Третьим аспектом изобретения является способ лечения заболеваний у животных, в котором ингибирование Катепсина S может предотвращать, ингибировать или уменьшать патологию и/или симптоматологию заболевания, который включает введение животному терапевтически эффективного количества соединения формулы I или N-оксидного производного, индивидуального изомера или смеси его изомеров; или его фармацевтически приемлемой соли. Четвертым аспектом изобретения являются способы получения соединений формулы I и Nоксидных производных, производных пролекарств, защищенных производных, индивидуальных изомеров и смесей этих изомеров; и их фармацевтически приемлемых солей. Подробное описание изобретения Определения Если не указано иное, следующие термины, использованные в описании и формуле изобретения,приведенные для их раскрытия, имеют указанные ниже значения. Термин "алициклический" означает остаток, характеризующийся расположением в нем атомов углерода в виде закрытых неароматических кольцевых структур, имеющих свойства, схожие со свойствами алифатических углеводородов, которые могут быть насыщенными или частично ненасыщенными с двумя или более двойными или тройными связями. Термин "алифатический" означает остаток, характеризующийся линейным или разветвленным цепочечным расположением входящих в него атомов углерода, и он может быть насыщенным или частично ненасыщенным с двумя или более двойными или тройными связями. Термин "алкил" представленный как таковой, означает линейный или разветвленный, насыщенный или ненасыщенный алифатический радикал, имеющий указанное число атомов углерода (например,(С 1-6)алкил включает метил, этил, пропил, изопропил, бутил, втор-бутил, изобутил, трет-бутил, винил,аллил, 1-пропенил, изопропенил, 1-бутенил, 2-бутенил, 3-бутенил, 2-метилаллил, этинил, 1-пропинил, 2 пропинил, и им подобные). Алкил, представленный вместе с другим радикалом (например, как в арилалкиле) означает линейный или разветвленный, насыщенный или ненасыщенный алифатический двухвалентный радикал, имеющий указанное число атомов или, когда нет указания на атомы, означает связь-2 007334 Термин "алкилен", если не указано иное, означает линейный или разветвленный, насыщенный или ненасыщенный, алифатический, двухвалентный радикал, имеющий указанное число атомов углеродаCН 2 СН 2-), пентаметилен (-CH2CH2CH2CH2CH2-) и им подобные). Термин "алкилиден" означает линейный или разветвленный, насыщенный или ненасыщенный алифатический двухвалентный радикал, имеющий указанное число атомов углерода (например, (С 1-6)алкилиден включает метилиден (=СН 2), этилиден (=СНСН 3), изопропилиден (=С(СН 3)2), пропилиден(=СНСН 2 СН 3), аллилиден (=СН-СН=СН 2), и им подобные). Термин "амино" означает радикал -NH2. Если не указано иное, соединения изобретения, содержащие остаток аминогруппы, включают их защищенные производные. Соответствующие защитные группы для остатков аминогруппы включают ацетил, трет-бутоксикарбонил, бензилоксикарбонил и им подобные. Определение "животное" включает людей, млекопитающих, помимо человека, (например, собак,кошек, кроликов, крупный рогатый скот, лошадей, овец, коз, свиней, оленей, и им подобных) и немлекопитающих (например, птиц, и им подобных). Термин "ароматический" означает остаток, в котором составляющие его атомы образуют ненасыщенную кольцевую систему, все атомы в кольцевой системе имеют sp2 гибридизацию и общее число к электронов равно 4n+2. Термин "арил" означает моноциклическую или конденсированную бициклическую кольцевую систему, содержащую общее указанное число атомов углерода в кольце, где каждое кольцо содержит 6 кольцевых атомов углерода и является ароматическим или в случае конденсации со вторым кольцом образует ароматическую кольцевую систему. Например, необязательно замещенный (С 6-10)арил, как использовано в настоящем изобретении, включает, но без ограничения, бифенил-2-ил, 2-бромфенил, 2 бромкарбонилфенил, 2-бром-5-фторфенил, 4-трет-бутилфенил, 4-карбамоилфенил, 4-карбокси-2-нитрофенил, 2-хлорфенил, 4-хлорфенил, 3-хлоркарбонилфенил, 4-хлоркарбонилфенил, 2-хлор-4-фторфенил, 2 хлор-6-фторфенил, 4-хлор-2-нитрофенил, 6-хлор-2-нитрофенил, 2,6-дибромфенил, 2,3-дихлорфенил, 2,5 дихлорфенил, 3,4-дихлорфенил, 2-дифторметоксифенил, 3,5-диметилфенил, 2-этоксикарбонилфенил, 2 фторфенил, 2-иодфенил, 4-изопропилфенил, 2-метоксифенил, 4-метоксифенил, 2-метилфенил, 3 метилфенил, 4-метилфенил, 5-метил-2-нитрофенил, 4-метилсульфонилфенил, нафт-2-ил, 2-нитрофенил,3-нитрофенил, 4-нитрофенил, 2,3,4,5,6-пентафторфенил, фенил, 2-трифторметоксифенил, 3-трифторметоксифенил, 4-трифторметоксифенил, 2-трифторметилфенил, 3-трифторметилфенил, 4-трифторметилфенил, 2-трифторметилсульфанилфенил, 4-трифторметилсульфанилфенил и им подобные. Необязательно замещенный (С 6-10)арил как использовано в настоящем изобретении, включает 3-ацетилфенил,3-трет-бутоксикарбониламинометилфенил, бифенил-4-ил, 3-гидроксифенил, 4-гидроксифенил, 3 метоксифенил, нафт-2-ил, 3-феноксифенил, фенил, и им подобные. Термин "бициклоарил" означает бициклическую кольцевую систему, содержащую указанное число атомов углерода в кольце, где кольца связаны друг с другом простой связью или сконденсированы и по крайней мере одно кольцо, составляющее систему, является ароматическим и любым карбоциклическим кетоном, тиокетоном или их иминокетоновым производным (например, (С 9-10)бициклоарил включает циклогексилфенил, 1,2-дигидронафтил, 2,4-диоксо-1,2,3,4-тетрагидронафтил, инданил, инденил, 1,2,3,4 тетрагидронафтил, и им подобные). Термин "карбамоил" означает радикал -C(O)NH2. Если не указано иное, соединения изобретения,содержащие карбамоильные остатки, включают их защищенные производные. Соответствующие защитные группы для карбамоильного остатка включают ацетил, трет-бутоксикарбонил, бензилоксикарбонил,и им подобные, и оба незащищенное и защищенное производные, находятся в рамках настоящего изобретения. Термин "производное карбоциклического кетона" означает производное, содержащее остаток -С(O)-. Термин "карбокси" означает радикал -С(O)ОН. Если не указано иное, соединения настоящего изобретения, содержащие карбоксильные остатки, включают их защищенные производные. Соответствующие защитные группы для карбоксильных остатков включают бензил, трет-бутил и им подобные. Термин "циклоалкил" означает насыщенную или частично ненасыщенную, моноциклическую, конденсированную бициклическую или мостиковую полициклическую кольцевую систему, содержащую указанное число атомов углерода в кольце и любой карбоциклический кетон, тиокетон или их иминокетоновое производное (например, (С 3-10)циклоалкил включает циклопропил, циклобутил, циклопентил,циклогексил, циклогексенил, 2,5-циклогексадиенил, бицикло[2,2,2]октил, адамантан-1-ил, декагидронафтил, оксоциклогексил, диоксоциклогексил, тиоциклогексил, 2-оксобицикло[2,2,1]гепт-1-ил и им подобные). Термин "циклоалкилен" означает двухвалентную насыщенную или частично ненасыщенную, моноциклическую кольцевую или мостиковую полициклическую кольцевую систему, содержащую определенное число атомов углерода в кольце и любой карбоциклический кетон, тиокетон или их иминокетоновое производное. Например, в случае, когда R1 и R2 вместе с атомом углерода, к которому оба R1 и R2 присоединены, образуют (С 3-8)циклоалкилен, включают, без ограничения, следующие соединения: Термин "заболевание", в частности, включает любое болезненное состояние животного или части его тела и болезненное состояние, которое может быть вызвано или случилось во время медицинской или ветеринарной терапии, примененной к такому животному, то есть "побочные эффекты" такой терапии. Термин "галоген" означает фтор, хлор, бром или иод. Термин "галогензамещенный алкил", в качестве отдельной группы или части большой группы, означает "алкил", замещенный с помощью одного или более атомов "галогена", как эти термины, определены в настоящем изобретеним. Галогензамещенный алкил включает галогеналкил, дигалогеналкил,тригалогеналкил, пергалогеналкил и им подобные (например, галогензамещенный (С 1-3)алкил включает хлорметил, дихлорметил, дифторметил, трифторметил, 2,2,2-трифторэтил, перфторэтил, 2,2,2-трифтор 1,1-дихлорэтил, и им подобные). Термин "гетероатомный остаток" включает -N=, -NR-, -О-, -S- или -S(O)2-, где R является водородом, (С 1-6)алкилом или защитной группой. Термин "гетероциклоалкилен" означает циклоалкилен, как он определен в настоящем изобретении,при условии, что один или более указанных атомов углерода в кольце, замещены на гетероатомный остаток, выбранный из -N=, -NR-, -О-, -S- или -S(O)2-, где R является водородом или (С 1-6)алкилом. Например, в случае, когда R1 и R2 вместе с атомом углерода, к которому оба R1 и R2 присоединены, образуют гетеро(С 3-8)циклоалкил, он включает, без ограничения, следующие соединения: где R является водородом, (С 1-6)алкилом или защитной группой. Термин "гетероарил" означает арил, как он определен в настоящем изобретении, при условии, что один или более указанных атомов углерода в кольце замещены на гетероатомный остаток, выбранный из-N=, -NR-, -О- или -S-, где R означает водород, (С 1-6)алкил, защитную группу или представляет собой свободную валентность, которая служит как место присоединения к атому азота в кольце и каждое кольцо содержит 5 или 6 атомов в кольце. Например, необязательно замещенный гетеро(С 5-10)арил, как использовано в настоящем изобретении, включает, но без ограничения, 4-амино-2-гидроксипиримидин-5 ил, бензотиазол-2-ил, 1H-бензоимидазол-2-ил, 2-бромпирид-5-ил, 5-бромпирид-2-ил, 4-карбамоилтиазол 2-ил, 3-карбоксипирид-4-ил, 5-карбокси-2,6-диметилпирид-3-ил, 3,5-диметилизоксазол-4-ил, 5-этокси 2,6-диметилпирид-3-ил, 5-фтор-6-гидроксипиримидин-4-ил, фур-2-ил, фур-3-ил, 5-гидрокси-4,6 диметилпирид-3-ил, 8-гидрокси-5,7-диметилхинолин-2-ил, 5-гидроксиметилизоксазол-3-ил, 3-гидрокси 6-метилпирид-2-ил, 3-гидроксипирид-2-ил, 1H-имидазол-2-ил, 1H-имидазол-4-ил, 1H-индол-3-ил, изотиазол-4-ил, изоксазол-4-ил, 2-метилфур-3-ил, 5-метилфур-2-ил, 1-метил-1H-имидазол-2-ил, 5-метил-3Hимидазол-4-ил, 5-метилизоксазол-3-ил, 5-метил-2H-пиразол-3-ил, 3-метилпирид-2-ил, 4-метилпирид-2 ил, 5-метилпирид-2-ил, 6-метилпирид-2-ил, 2-метилпирид-3-ил, 2-метилтиазол-4-ил, 5-нитропирид-2-ил,2H-пиразол-3-ил, 3 Н-пиразол-4-ил, пиридазин-3-ил, пирид-2-ил, пирид-3-ил, пирид-4-ил, 5-пирид-3-ил 2H-[1,2,4]триазол-3-ил, пиримидин-4-ил, пиримидин-5-ил, 1H-пиррол-3-ил, хинолин-2-ил, 1 Н-тетразол 5-ил, тиазол-2-ил, тиазол-5-ил, тиен-2-ил, тиен-3-ил, 2H-[1,2,4]триазол-3-ил, 3 Н-[1,2,3]триазол-4-ил, 5 трифторметилпирид-2-ил и им подобные. Подходящие защитные группы включают тpeтбутоксикарбонил, бензилоксикарбонил, бензил, 4-метоксибензил, 2-нитробензил и им подобные. Необязательно замещенный гетеро(С 5-10)арил, как использовано в настоящем изобретении для определения R4 включает бензофур-2-ил, фур-2-ил, фур-3-ил, пирид-3-ил, пирид-4-ил, хинол-2-ил, хинол-3-ил, тиен-2-ил,тиен-3-ил и им подобные. Термин "гетеробициклоарил" означает бициклоарил, как определено в настоящем изобретении, при условии, что один или более указанных атомов углерода в кольце замещены на гетероатомный остаток,выбранный из -N=, -NR-, -О- или -S-, где R является водородом, (С 1-6)алкилом, защитной группой или свободной валентностью, которая служит как место присоединения к атому азота в кольце и любой карбоциклический кетон, тиокетон или их иминокетоновое производное. Например, необязательно замещенный гетеро(С 8-10)бициклоарил, как использовано в настоящем изобретении, включает, без ограничения, 2-амино-4-оксо-3,4-дигидроптеридин-6-ил и им подобные. Вообще, термин гетеробициклоарил как использовано в настоящем изобретении, включает, например, бензо[1,3]диоксол-5-ил, 3,4-дигидро-2H[1,8]нафтиридинил, 3,4-дигидро-2H-хинолинил, 2,4-диоксо-3,4-дигидро-2H-хиназолинил, 1,2,3,4,5,6 гексагидро[2,2']бипиридинилил, 3-оксо-2,3-дигидробензо[1,4]оксазинил, 5,6,7,8-тетрагидрохинолинил и им подобные.-4 007334 Термин "гетероциклоалкил" означает циклоалкил, как определено в настоящем изобретении, при условии, что один или более указанных атомов углерода в кольце замещены на гетероатомный остаток,выбранный из -N=, -NR-, -О- или -S-, где R означает водород, (С 1-6)алкил, защитную группу или свободную валентность, которая служит как место присоединения к атому азота в кольце и любой карбоциклический кетон, тиокетон или их иминокетоновое производное (например, термин "гетеро(С 5-10)циклоалкил" включает имидазолидинил, морфолинил, пиперазинил, пиперидил, пирролидинил, пирролинил, хинуклидинил и им подобные). Подходящие защитные группы включают трет-бутоксикарбонил, бензилоксикарбонил, бензил, 4-метоксибензил, 2-нитробензил, и им подобные. Как незащищенное, так и защищенное производные входят в рамки изобретения. Термин "гидрокси" означает радикал -ОН. Если не указано иное, соединения настоящего изобретения, содержащие гидроксильные радикалы, включают их защищенные производные. Подходящие защитные группы для гидроксильного остатка включают бензил и им подобные. Термин "иминокетоновое производное" означает производное, содержащее остаток -C(NR)-, где R является водородом или (С 1-6)алкилом. Термин "изомеры" означает соединения формулы I, имеющие идентичную молекулярную формулу,но отличающиеся по природе или последовательности связывания их атомов или по расположению атомов в пространстве. Изомеры, которые отличны по расположению их атомов в пространстве, называются"стереоизомерами". Стереоизомеры, которые не являются зеркальными отображениями друг по отношению к другу, называются "диастереоизомерами" и стереоизомеры, которые являются точным зеркальным отображением, называются "энантиомерами" или иногда "оптическими изомерами". Атом углерода, связанный с четырьмя неидентичными заместителями называется "хиральным центром". Соединение с одним хиральным центром, имеющее две энантиомерных формы с противоположной хиральностью, называется "рацемической смесью". Соединение, которое имеет более, чем один хиральный центр, имеет 2n-1 энантиомерных пар, где n определяет число хиральных центров. Соединения с более чем одним хиральным центром могут существовать как в виде отдельных диастереоизомеров, так и в виде смеси диастереоизомеров, которая называется "диастереоизомерной смесью". Когда присутствует один хиральный центр, стереоизомер может быть охарактеризован с помощью абсолютной конфигурации этого хирального центра. Абсолютная конфигурация относится к расположению в пространстве заместителей, присоединенных к хиральному центру. Энантиомеры, характеризуются с помощью абсолютной конфигурации их хиральных центров, и они описываются с помощью R- и S- последовательностей, в соответствии с правилами, установленными Cahn, Ingold и Prelog. Определения для стереохимической номенклатуры,способы определения стереохимии и разделение стереоизомеров хорошо известны из уровня техники(например, см. "Advanced Organic Chemistry", 4th edition, March, Jerry, John WileySons, New York,1992). Ясно, что все названия соединений формулы I и их иллюстрации, приведенные в настоящем изобретении, включают все возможные стереоизомеры, которые охватываются изобретением. Так, например, название N-[1-(1-бензилкарбамоилметаноил)пропил]-4-морфолин-4-ил-4-оксо-2-фенилметансульфонилметилбутирамид означает, что он включает N-[(S)-1-(1-бензилкарбамоилметаноил)пропил]-4 морфолин-4-ил-4-оксо-2-фенилметансульфонилметилбутирамид иN-[(R)-1-(1-бензилкарбамоилметаноил)пропил]-4-морфолин-4-ил-4-оксо-2-фенилметансульфонилметилбутирамид и любую смесь, рацемическую или другую. Термин "производное кетона" означает, производное, содержащее остаток -С(O)-. Например, в настоящем изобретении X3 может быть 2-ацетоксиазетидин-3-илом. "Карбоциклическое производное кетона" указанного примера X3 может быть 2-ацетокси-4-оксоазетидин-3-илом (см. табл. 3, С 32). Термин "нитро" означает радикал -NO2. Термин "необязательный" или "необязательно" означает, что последовательно описанное событие или обстоятельство может произойти или не произойти, и, что описание включает ссылки, где событие или обстоятельство случается и ссылки, где это отсутствует. Например, фраза "где любая алициклическая или ароматическая кольцевая система в составе R3 и R4 может быть замещена дополнительно 1-5 радикалами" означает, что R3 и R4 могут быть замещены или не замещены, для того чтобы войти в рамки изобретения. Термин "оксоалкил" означает радикал алкил, как он определен выше, где один из общего числа атомов углерода, замещен на кислородную группу (-O-), например, оксо(С 2-6)алкил включает метоксиметил, и так далее. Термин "N-оксидные производные" означает производные соединения формулы I, в которых атомы азота находятся в окисленном состоянии (то есть O-N) и которые обладают желательной фармакологической активностью. Термин "патология" болезни означает сущность природы, причины и развитие болезни, так же как структурные и функциональные изменения, которые следуют из процессов, протекающих во время болезни. Термин "фармацевтически приемлемый" означает, что он является полезным при получении фармацевтической композиции, а именно, как правило, является безопасным, нетоксичным и биологически-5 007334 или как-нибудь иначе желательным и включает то, что является приемлемым для использования в ветеринарии и в фармацевтике для человека. Термин "фармацевтически приемлемые соли" означает соли соединений формулы I, которые являются фармацевтически приемлемыми, в том смысле как это определено выше, и которые обладают желательной фармакологической активностью. Такие соли включают кислотно-аддитивные соли, образованные с минеральными кислотами, такими как соляная кислота, бромисто-водородная кислота, серная кислота, азотная кислота, фосфорная кислота, и т.п.; или с органическими кислотами, такими как уксусная кислота, пропионовая кислота, капроновая кислотная, энантовая кислота, циклопентанпропионовая кислота, гликолевая кислота, пировиноградная кислота, молочная кислота, малоновая кислота, янтарная кислота, яблочная кислота, малеиновая кислота, фумаровая кислота, винная кислота, лимонная кислота,бензойная кислота, о-(4-гидроксибензоил)бензойная кислота, коричная кислота, маделевая кислота, метансульфоновая кислота, этансульфоновая кислота, 1,2-этандисульфоновая кислота, 2-гидроксиэтансульфоновая кислота, бензолсульфоновая кислота, p-хлорбензолсульфоновая кислота, 2 нафталинсульфоновая кислота, n-толуолсульфоновая кислота, камфорсульфоновая кислота, 4 метилбицикло [2,2,2]окт-2-ен-1-карбоновая кислота, глюкогептановая кислота, 4,4'-метиленбис(3 гидрокси-2-ен-1-карбоновая кислота), 3-фенилпропионовая кислота, триметилуксусная кислота, третбутилуксусная кислота, лаурилсерная кислота, глюконовая кислота, глутаминовая кислота, гидроксинафтойная кислота, салициловая кислота, стеариновая кислота, муконовая кислота и им подобные. Фармацевтически приемлемые соли также включают основно-аддитивные соли, которые могут быть образованы, когда имеющиеся кислотные протоны являются способными к взаимодействию с неорганическими или органическими основаниями. Приемлемые неорганические основания включают гидроксид натрия, карбонат натрия, гидроксид калия, гидроксид алюминия и гидроксид кальция. Приемлемые органические основания включают этаноламин, диэтаноламин, триэтаноламин, трометамин, Nметилглюкамин и им подобные. Термин "пролекарство" означает соединение, которое является способным к превращению in vivo за счет метаболизма, (например, с помощью гидролиза) в соединение формулы I. Например, эфир соединения формулы I, содержащий гидроксигруппу может быть преобразован путем гидролиза in vivo в исходную молекулу. Альтернативно, эфир соединения формулы I, содержащий карбоксильную группу,может быть преобразован путем гидролиза in vivo в исходную молекулу. Подходящими эфирами простые соединения формулы I, содержащими гидроксильную группу, являются, например, ацетаты, цитраты, лактаты, тартраты, малонаты, оксалаты, салицилаты, пропионаты, сукцинаты, фумараты, малеаты,метилен-бис-b-гидроксинафтоаты, гентизаты, изэтионаты, ди-n-толуолтартраты, метансульфонаты, этаносульфонаты, бензолсульфонаты, п-толуолсульфонаты, циклогексилсульфаматы и хинаты. Подходящими эфирами соединений формулы I, содержащими карбоксильную группу, являются например те,которые описаны у F.J. Leinweber, Drug Metab. Res., 1987, 18, р. 379. Особенно полезный класс эфиров соединений формулы I, содержащих гидроксильную группу, может быть образован из кислотных остатков, выбранных из тех, которые описаны у Bundgaard et al., J. Med. Chem., 1989, 32, p. 2503-2507, и включает замещенные (аминометил)бензоаты, например, диалкиламинометилбензоаты, где две алкильные группы могут быть объединены вместе и/или разделены с помощью атома кислорода или с помощью необязательно замещенного атома азота, например, алкилированного атома азота, главным образом(морфолинометил)бензоаты, например, 3-или 4-(морфолинометил)бензоаты и (4-алкилпиперазин-1 ил)бензоаты, например, 3- или 4-(4-алкилпиперазин-1-ил)бензоаты. Термин "защищенные производные" означает производные соединений формулы I, в которых реакционноспособная группа или группы блокированы защитными группами. Защищенные производные соединений формулы I являются полезными для получения соединений формулы I, или они сами могут быть активными ингибиторами Катепсина S. Полный список соответствующих защитных групп может быть найден в книге Т.W. Greene, Protecting Groups in Organic Synthesis, 3rd edition, John WileySons,Inc. 1999. Термин "терапевтически эффективное количество" означает, что количество, которое, вводят животному для лечения заболевания, является достаточным для воздействия на такое заболевание. Термин "тиокетоновое производное" означает производное, содержащее остаток -C(S)-. Термин "лечение" или "обработка" означает любое введение соединения настоящего изобретения и включает:(1) профилактику болезни от ее появления у животного, которое может быть предрасположено к болезни, но еще не испытывает ее, или демонстрирует патологию или симптоматологию заболевания,(2) ингибирование болезни у животного, которое испытывает или демонстрирует патологию или симптоматологию заболевания (то есть предотвращение дальнейшего развития патологии и/или симптоматологии), или(3) снижение признаков болезни у животного, которое испытывает или демонстрирует патологию или симптоматологию патологических изменений (то есть прекращение патологии и/или симптоматологии).-6 007334 Номенклатура Соединения формулы I, промежуточные соединения и исходные продукты, использованные для их получения, названы в соответствии с IUPAC требованиями по определению номенклатуры, в которой характеристические группы имеют сниженный приоритет для определения, по сравнению с основной группой, такой как: кислоты, сложные эфиры, амиды, и т.д. Альтернативно, соединения называют в соответствии с AutoNom 4.0 (Beilstein Information Systems, Inc.). Например, соединение формулы I, где X1 является -NHC(R1)(R2)X2 (R1 и R2 каждый является водородом), X2 является циано, R3 является циклогексилметилом, и R4 является фениламино; то есть соединение, имеющее следующую структуру: называют N-цианометил-2-циклогексилметил-N'-фенилмалонамид. Присутствующие предпочтительные воплощения В то время как самое широкое определение изобретения сформулировано в разделе Сущность изобретения, некоторые аспекты изобретения являются предпочтительными. Например, X1 означает-C(O)C(O)R5; где R5 и R6 имеют значения определенные выше; X3 содержит гетеромоноциклическое кольцо, содержащее от 4 до 6 атомов, являющихся членами кольца или конденсированную гетеробициклическую кольцевую систему, содержащую от 8 до 14 атомов в кольце и любой карбоциклический кетон,иминокетон или его тиокетоновое производное; где любая алициклическая или ароматическая кольцевая система в составе R5, X2 или X3 может быть замещена дополнительно 1-5 радикалами, независимо выбранными из (С 1-6)алкила или -X5OC(O)R12 и/или 1 радикалом, выбранным из -R14, -X4C(O)R14 или-X4OC(O)R14; где X4, R12 и R14 имеют значения, определенные выше; R1 означает водород или (С 1-6)алкил,и R2 означает водород, -X4OR12, (С 5-10)гетероарил(С 0-6)алкил, (С 5-10)арил(С 0-6)алкил, (С 5-10)циклоалкил(С 0-6)алкил, (С 5-10)гетероциклоалкил(С 0-6)алкил или (С 1-6)алкил; или R1 и R2, взятые вместе с атомом углерода, к которому оба R1 и R2 присоединены, образуют (С 3-8)циклоалкилен или (С 3-8)гетероциклоалкилен; где любой гетероарил, арил, циклоалкил, гетероциклоалкил, циклоалкилен или гетероциклоалкилен в составе R2 является необязательно замещенным 1-3 радикалами, независимо выбранными из (С 1-6)алкила и гидрокси; R3 является -СН 2 Х 5, где X5 в каждом случае независимо выбирают из -X4SR12,-X4C(O)NR12R12, -X4S(O)2R13, -X4C(O)R13, -X4SR14, -X4R12, -R14, -X4S(O)2R14, -X4C(O)R14, -X4C(O)NR14R12,где X4, R12, R13 и R14 имеют значения определенные выше; R4 означает -NR6R6, -NR6R14, -NR6R15 илиR6 и R15 присоединены, образуют гетеро(С 3-10)циклоалкил, гетеро(С 5-10)арил или гетеро(С 8-10)бициклоарил; где любая алициклическая или ароматическая кольцевая система в составе R3 и R4 может быть замещена дополнительно 1-5 радикалами, независимо выбранными из (С 1-6)алкила, циано, галогена, нитро,галогензамещенного(С 1-4)алкила, -X4OR12, -Х 4 С(O)ОR12, -Х 4C(O)R13, -X4C(O)NR12R12, -X4NR12S(O)2R12 и/или 1 радикалом, выбранным из -R14, -X4OR14 и -X4C(O)NR14R12; любой алифатический остаток в составе R3 и R4 может быть замещен дополнительно 1-5 радикалами, независимо выбранными из циано; гдеX4, R12, R13 и R14 имеют значения, указанные выше; при условии, что присутствует только одна бициклическая кольцевая структура в составе R3 или R4. В частности, X1 является -NHC(R1)(R2)X2 или -NHX3; X2 означает пиано, -С(O)Х 3, -СF3, -СF2 СF3,(Е)-2-бензолсульфонилвинил, 2-диметилкарбамоил-2,2-дифторацетил, 1-бензилкарбамоилметаноил, 1 бензилокси(оксалил), 2-бензилоксиацетил, 2-бензолсульфониламиноэтаноил или 2-оксо-2-фенилэтаноил;X3 означает 1H-бензоимидазол-2-ил, пиримидин-2-ил, бензооксазол-2-ил, бензотиазол-2-ил, пиридазин 3-ил, 3-фенил-[1,2,4]оксадиазол-5-ил, 3-этил-[1,2,4]оксадиазол-5-ил, 2-метил-4-оксотетрагидрофуран-3 ил, 2-этил-4-оксотетрагидрофуран-3-ил, 4-оксо-1-(1-фенилметаноил)пирролидин-3-ил или (S)-2aцетокси-4-оксоазетидин-3-ил; R1 означает водород или метил, и R2 означает водород, метоксиметил,(С 1-6)алкил, фенэтил, тиофен-2-ил или 5-метилфуран-2-ил, или (ii) R1 и R2, взятые вместе с атомом углерода, к которому оба R1 и R2 присоединены, образуют циклопропилен, тетрагидропиран-4-илен или метилпиперидин-4-илен. Более предпочтительно R3 означает тиофен-2-сульфонилметил, 3-хлор-2-фторфенилметансульфонилметил, бензолсульфонилметил, фенилметансульфонилметил, 2-(1,1-дифторметокси)фенилметансульфонилметил, 2-бензолсульфонилэтил, 2-(пиридин-2-сульфонил)этил, 2-(пиридин-4-сульфонил)этил, 2 фенилметансульфонилэтил, оксипиридин-2-илметансульфонилметил, проп-2-ен-1-сульфонилметил, 4 метоксифенилметансульфонилметил, n-толилметансульфонилметил, 4-хлорфенилметансульфонилэтил,о-толилметансульфонилметил, 3,5-диметилфенилметансульфонилметил, 4-трифторметилфенилметан-7 007334 сульфонилметил, 4-трифторметоксифенилметансульфонилметил, 2-бромфенилметансульфонилметил,пиридин-2-илметансульфонилметил, пиридин-3-илметансульфонилметил, пиридин-4-илметансульфонилметил, нафтален-2-илметансульфонилметил, 3-метилфенилметансульфонилметил, 3-трифторметилфенилметансульфонилметил, 3-трифторметоксифенилметансульфонилметил, 4-фтор-2-трифторметоксифенилметансульфонилметил, 2-фтор-6-трифторметилфенилметансульфонилметил, 3-хлорфенилметансульфонилметил, 2-фторфенилметансульфонилметил, 2-трифторфенилметансульфонилметил, 2-цианофенилметансульфонилметил, 4-трет-бутилфенилметансульфонилметил, 2-фтор-3-метилфенилметансульфонилметил, 3-фторфенилметансульфонилметил, 4-фторфенилметансульфонилметил, 2-хлорфенилметансульфонилметил, 2,5-дифторфенилметансульфонилметил, 2,6-дифторфенилметансульфонилметил,2,5-дихлорфенилметансульфонилметил, 3,4-дихлорфенилметансульфонилметил, 2-(1,1-дифторметокси) фенилметансульфонилметил, 2-цианофенилметансульфонилметил, 3-цианофенилметансульфонилметил,2-трифторметоксифенилметансульфонилметил, 2,3-дифторфенилметансульфонилметил, 2,5-дифторфенилметансульфонилметил, бифенил-2-илметансульфонилметил, циклогексилметил, 3-фторфенилметансульфонилметил, 3,4-дифторфенилметансульфонилметил, 2,4-дифторфенилметансульфонилметил,2,4,6-трифторфенилметансульфонилметил, 2,4,5-трифторфенилметансульфонилметил, 2,3,4-трифторфенилметансульфонилметил, 2,3,5-трифторфенилметансульфонилметил, 2,5,6-трифторфенилметансульфонилметил, 2-хлор-5-трифторметилфенилметансульфонилметил, 2-метилпропан-1-сульфонил, 2 фтор-3-трифторметилфенилметансульфонилметил, 2-фтор-4-трифторметилфенилметансульфонилметил,2-фтор-5-трифторметилфенилметансульфонилметил,4-фтор-3-трифторметилфенилметансульфонилметил, 2-метоксифенилметансульфонилметил, 3,5-бис-трифторметилфенилметансульфонилметил, 4 дифторметоксифенилметансульфонилметил, 2-дифторметоксифенилметансульфонилметил, 3-дифторметоксифенилметансульфонилметил, 2,6-дихлорфенилметансульфонилметил, бифенил-4-илметансульфонилметил,3,5-диметилизоксазол-4-илметансульфонилметил,5-хлортиофен-2-илметансульфонилметил,2-[4-(1,1-дифторметокси)бензолсульфонил]этил,2-[2-(1,1-дифторметокси)бензолсульфонил]этил, 2-[3-(1,1-дифторметокси)бензолсульфонил]этил, 2-(4-трифторметоксибензолсульфонил) этил, 2-(3-трифторметоксибензолсульфонил)этил, 2-(2-трифторметоксибензолсульфонил)этил, (цианометилметилкарбамоил)метил, бутил, бифенил-3-илметил, 2-оксо-2-пирролидин-1-ил-этил, 2-бензолсульфонилэтил, изобутилсульфанилметил, 2-фенилсульфанилэтил, циклогексилметансульфонилметил, 2 циклогексилэтансульфонил, бензил, нафтален-2-ил, бензилсульфанилметил, 2-трифторметилбензилсульфанилметил, 5-бромтиофен-2-илметил, фенилсульфанилэтил и циклопропилметансульфонилметил. Более предпочтительно R4 означает фениламино, бензиламино, 4-феноксифениламино, фенэтиламино, 3-фенилпропиламино, морфолин-4-ил, циклогексиламино, нафтален-1-илметиламино, пиридин-3 иламино, 6-метоксипиридин-3-иламино, диизобутиламино, 4-нитробензиламино, 2-тиофен-2-илэтиламино, 3-феноксифениламино, цианометиламино, (пиридин-3-илметил)амино, 5,6,7,8-тетрагидронафтален-1-иламино, 2-пиридин-2-илэтиламино, 2,3-дигидроиндол-1-ил, 3,4-дигидро-1H-изохинолин-2 ил, циклогексилметиламино, 2-метоксибензиламино, 1-фенилэтиламино, (пиридин-4-илметил)амино,бензилметиламино, 3-нитробензиламино, 4-метоксифениламино, 3-карбамоилфениламино, 4-карбамоилфениламино, (тетрагидрофуран-2-илметил)амино, 3,4-дигидро-2 Н-хинолин-1-ил, диметиламино, бутилметиламино, диизопропиламино, пропилметиламино, 1-(бензооксазол-2-карбонил)пропиламино и изобутилметиламино. Отсылка к предпочтительным воплощениям, приведенная выше, означает, что изобретение включает все комбинации частных и предпочтительных групп. Конкретные соединения изобретения выбраны из соединений, образованных путем связывания ацильного атома углерода (С) одного из фрагментов (от А 1 до 37), представленного в табл. 1, с метиновым атомом углерода (СН) одного из фрагментов (от В 1 до В 88), представленного в табл. 2, и присоединения метинового атома углерода (СН) одного из фрагментов (от В 1 до В 88), представленного в табл. 2 к ацильному атому углерода (С) одного из фрагментов (от С 1 до С 36), представленного в табл. 3. Следующие таблицы предназначены для обеспечения руководства для лучшего осуществления настоящего изобретения. Однако они не ограничивают область изобретения. Средние специалисты могут селективно синтезировать конкретные соединения, присоединяя один из фрагментов, показанных в табл. 1 к любому из фрагментов, показанных в табл. 2, а затем присоединяя фрагменты, показанные в табл. 2 к любому одному из фрагментов табл. 3. Так, например, в табл. 4 соединение, обозначенное как А 2-В 45-С 35 является комбинированным продуктом группы А 2 из табл. 1 и В 45 из табл. 2 и С 35 в табл. 3, и имеет название N-[1-(1-бензооксазол 2-ил-метаноил)-3-фенилпропил]-N'-бензил-2-циклогексилметилмалонамид Наиболее предпочтительными являются соединения формулы I, выбранные из группы, состоящей из 2-бутил-N-цианометил-N-фенилмалонамид (cоединение 1; обозначенное как А 1-В 88-С 1);N,N'-бис-[(S)-1-(1-бензооксазол-2-ил-метаноил)пропил]-2-циклогексилметилмалонамид (cоединение 42; обозначенное как А 37-В 45-С 13); и их N-оксидные производные, производные пролекарств, защищенные производные,отдельные стереоизомеры и смеси изомеров; а также фармацевтически приемлемые соли и сольваты (например, гидраты) таких соединений и их N-оксидные производные, производные пролекарств, защищенные производные, отдельные изомеры и смеси изомеров. Фармакология и применение Соединения по изобретению являются селективными ингибиторами Катепсина S и, как таковые,полезны для лечения заболеваний, в которых активность Катепсина S влияет на патологию и/или симптоматологию заболевания. Например, соединения по изобретению являются полезными для лечения аутоиммунных заболеваний, включая ювенильный начальный диабет, рассеянный склероз, пузырчатку,болезнь Грейва, миастению, системную красную волчанку, ревматоидный артрит и тироидит Хашимото,но не ограничиваясь перечисленными, а также для лечения аллергических заболеваний, включая астму, и аллогенные иммунные ответы, включая, но не ограничиваясь, пересадки органа или ткани. Катепсин S также участвует в заболеваниях, включающих излишний эластолиз, таких как хронические обструктивные заболевания легких (например, эмфизема), бронхиолит, излишний эластолиз дыхательных путей при астме и бронхите, пневмониях и сердечно-сосудистые заболевания, такие как разрывы бляшек и атерома. Катепсин S участвует в образовании фибрилл и, поэтому, ингибиторы КатепсиновS полезны для лечения системного амилоидоза.- 14007334 Ингибирующая активность цистеиновой протеазы для соединений по изобретению может быть определена способами, известными среднему специалисту в данной области техники. Известны соответствующие испытания in vitro для измерения протеазной активности и ее ингибирования тестируемыми соединениями. Как правило, в испытаниях измеряют гидролиз, вызванный протеазой, пептидного субстрата. Детали испытания для измерения ингибирующей активности протеазы приведены в примерах 6-9. Введение и фармацевтические композиции: Как правило, соединения формулы I вводят в терапевтически эффективных количествах любым из обычных и приемлемых способов, известным из уровня техники, отдельно или в комбинации с одним или более терапевтическими агентами. Терапевтически эффективное количество может широко изменяться в зависимости от серьезности заболевания, возраста и относительного здоровья пациента, активности используемого соединения и других факторов. Например, терапевтически эффективные количества соединения формулы I могут составлять приблизительно от 1 микрограмма на килограмм веса тела(мкг/кг) в день приблизительно до 1 миллиграмма на килограмм веса тела (мг/кг) в день, обычно приблизительно от 10 мкг/кг/день приблизительно до 0,1 мг/кг/день. Поэтому, терапевтически эффективное количество для 80-килограммового человека может колебаться приблизительно от 100 мкг/день до приблизительно 100 мг/день, обычно приблизительно от 1 мкг/день до приблизительно 10 мг/день. Как правило,любой средний специалист, обладающий соответствующими знаниями и действующий в соответствии с описанием данной заявки, способен установить терапевтически эффективное количество соединения формулы I для лечения установленного заболевания. Соединения формулы I могут вводиться в виде фармацевтических композиций одним из следующих способов: оральный, системный (например, трансдермальный, интраназальный или с помощью свечей) или парентеральный (например, внутримышечный, внутривенный или подкожный). Композиции могут иметь форму таблеток, пилюль, капсул, полутвердых веществ, порошков, составов с длительным высвобождением, растворов, суспензий, эликсиров, аэрозолей или любой другой соответствующей композиции и состоять в основном из соединения формулы I в комбинации по крайней мере с одним фармацевтически приемлемым наполнителем. Приемлемые наполнители являются нетоксичными, способствующими введению, и не имеют неблагоприятно действия на терапевтическую активность активного ингредиента. Таким наполнителем может быть любой твердый, жидкий, полутвердый или, в случае аэрозольных композиций, газообразный наполнитель, который является общедоступным специалисту в данной области техники. Твердые фармацевтические наполнители включают крахмал, целлюлозу, тальк, глюкозу, лактозу,сахарозу, желатин, солод, рис, муку, мел, силикагель, стеарат магния, стеарат натрия, моностеарат глицерина, хлорид натрия, высушенное цельное молоко и т.п. Жидкие и полутвердые наполнители могут быть выбраны из воды, этанола, глицерина, пропиленгликоля и различных масел, включая масла из нефти, животного, растительного или синтетического происхождения (например, арахисовое масло, соевое масло, минеральное масло, кунжутное масло и т.п.). Предпочтительные жидкие носители, особенно для растворов для инъекции, включают воду, соляной раствор, водную декстрозу и гликоли. Количество соединения формулы I в композиции может широко меняться в зависимости от типа состава, единичной дозы, вида наполнителей и других факторов, известных специалисту в области фармацевтики. Как правило, композиция соединения формулы I для лечения установленного заболевания будет включать от 0,01% по весу до 10% по весу, предпочтительно от 0,3% по весу до 1% по весу, активного компонента с остатком, являющимся наполнителем или наполнителями. Предпочтительно фармацевтическая композиция вводится в дозированной форме для непрерывного лечения или в дозированной форме ad libitum, когда специально требуется облегчение симптомов. Примерные фармацевтические составы, содержащие соединение формулы I, описаны в примере 10. Химия Способы получения соединений формулы I. Соединения по настоящему изобретению могут быть получены с помощью способов, раскрытых в описании или модификации известных способов, которые были использованы прежде или описаны в литературе, например, которые описаны у R.C. Larock в Comprehensive Organic Transformations, VCHpublishers, 1989. При проведении реакций, описанных в дальнейшем, может быть необходимо введение защиты реакционноспособных функциональных групп, например, гидроксильной, амино, имино, тио или карбоксильных групп, которые являются желательными в конечном продукте, чтобы избежать их нежелательного участия в реакциях. Обычно защитные группы могут быть использованы в соответствии с общепринятой практикой, например, см. у T.W. Greene and P. G. M. Wuts в "Protective Groups in OrganicChemistry" John Wiley and Sons, 1991. Соединения формулы I, где X1 является -NHC(R1)(R2)X2, могут быть получены с помощью способов, приведенных на следующей реакционной схеме 1: где X2, R1, R2, R3 и R4 имеют значения, определенные в разделе Сущность изобретения. Соединения формулы I могут быть получены путем конденсации кислоты формулы 2 с соединением формулы NH2CR1R2X2. Реакция конденсации может быть проведена в присутствии подходящего связывающего агента (например, гексафторфосфата бензотриазол-1-илокситриспирролидинофосфония (РуВОР), гидрохлорида 1-(3-диметиламинопропил)-3-этилкарбодиимида (EDCI), гексафторфосфата Обензотриазол-1-ил-N,N,N,N'-тетраметилурония (HBTU), 1,3-дициклогексилкарбодиимида (DCC) или им подобных) и необязательного подходящего катализатора (например, 1-гидроксибензотриазола (HOBt), 1 гидрокси-7-азабензотриазола (HOAt) или им подобных) и ненуклеофильного основания (например, Nметилморфолина, триэтиламина или им подобных или их любой подходящей комбинации) в подходящем растворителе (N-метилпирролидиноне или ему подобном) при температуре окружающей среды, что требует продолжительности от 3 до 10 ч, чтобы закончить реакцию. Подробное описание синтеза соединения формулы I с помощью процессов в соответствии с реакционной схемой 1 изложены в примерах,представленных ниже. Соединения формулы I, где X1 является -NHX3, могут быть получены с помощью способов, приведенных на следующей реакционной схеме 2. Реакционная схема 2 где X3, R3 и R4 имеют значения, определенные в разделе Раскрытие изобретения. Соединения формулы I могут быть получены путем конденсации кислоты формулы 2 с соединением формулы NH2X3. Реакция конденсации может быть проведена в присутствии подходящего связывающего агента (например, гексафторфосфата бензотриазол-1-илокситриспирролидинофосфония (РуВОР),гидрохлорида 1-(3-диметиламинопропил)-3-этилкарбодиимида (EDCI), гексафторфосфат О-бензотриазол-1-ил-N,N,N',N'-тетраметилурония (HBTU), 1,3-дициклогексилкарбодиимида (DCC), или им подобных) и необязательного подходящего катализатора (например, 1-гидроксибензотриазола (HOBt), 1 гидрокси-7-азабензотриазола (HOAt), или им подобных) и ненуклеофильного основания (например, Nметилморфолина, триэтиламина, или им подобного или их любой подходящей комбинации) в подходя- 16007334 щем растворителе (N-метилпирролидиноне, или ему подобном) при температуре окружающей среды и продолжительности процесса от 3 до 10 ч, чтобы завершить реакцию. Подробное описание синтеза соединения формулы I с помощью процессов в соответствии с реакционной схемой 2 изложены в примерах, представленных ниже. Дополнительные способы получения соединений формулы I: Соединение формулы I может быть получено в виде фармацевтически приемлемой кислотноаддитивной соли при взаимодействии соединения в форме свободного основания с фармацевтически приемлемой неорганической или органической кислотой. Альтернативно, фармацевтически приемлемая основно-аддитивная соль соединения формулы I может быть получена при взаимодействии соединения в форме свободной кислоты с фармацевтически приемлемым неорганическим или органическим основанием. Неорганические и органические кислоты и соответствующие основания для получения фармацевтически приемлемой соли соединения формулы I раскрыты в разделе "определения" настоящего описания. Альтернативно, соединения формулы I в форме солей могут быть получены при использовании солей исходных продуктов или промежуточных соединений. Соединения формулы I в виде свободной кислоты или свободного основания могут быть получены из соответствующей основно-аддитивной соли или из кислотно-аддитивной соли. Например, соединение формулы I в виде кислотно-аддитивной соли может быть превращено в соответствующее свободное основание обработкой соответствующим основанием (например, раствором гидроксида аммония, гидроксида натрия и им подобным). Соединение формулы I в виде основно-аддитивной соли может быть превращено в соответствующую свободную кислоту обработкой соответствующей кислотой (например, соляной кислотой, и так далее).N-оксиды соединения формулы I могут быть получены с помощью способов, известных средним специалистам в данной области. Например, N-оксиды могут быть получены путем обработки неокисленной формы соединения формулы I окислителем (например, трифторперуксусной кислотой, пермалеиновой кислотой, пербензойной кислотой, перуксусной кислотой, мета-хлорпероксибензойной кислотой,или им подобным) в подходящем инертном органическом растворителе (например, галогенированном углеводороде таком, как дихлорметан) при температуре близкой к 0 С. Альтернативно, N-оксиды соединения формулы I могут быть получены из N-оксида соответствующего исходного продукта. Соединения формулы I в неокисленной форме могут быть получены из N-оксидов соединений формулы I путем обработки их восстановителем (например, серой, диоксидом серы, трифенилфосфином,боргидридом лития, боргидридом натрия, трихлоридом фосфора, трибромидом, или им подобными) в подходящем инертном органическом растворителе (например, ацетонитриле, этаноле, водном растворе диоксана, или им подобном) при температуре от 0 до 80 С. Пролекарства соединения формулы I могут быть получены с помощью способов, известных средним специалистам в данной области (например, дополнительные детали см. у Saulnier et аl. (1994),Bioorganic and Medicinal Chemistry Letters, Vol. 4, p. 1985). Например, соответствующие пролекарства могут быть получены с помощью реакции немодифицированного соединения формулы I с подходящим карбамилирующим агентом (например, 1,1-ацилоксиалкилкарбонхлоридатом, пара-нитрофенилкарбонатом, или им подобным). Защищенные производные соединения формулы I могут быть получены с помощью способов, известных средним специалистам рассматриваемой области. Подробное описание подходящих технических приемов создания защитных групп и их удаления могут быть найдены у T.W. Greene, ProtectingGroups in Organic Synthesis, 3rd edition, John WileySons, Inc. 1999. Соединения по настоящему изобретению могут быть легко получены в соответствии со способами настоящего изобретения, в качестве сольватов (например, гидратов). Гидраты соединений настоящего изобретения могут быть легко получены путем перекристаллизации из смеси водного/органического растворителя, при использовании таких органических растворителей, как диоксан, тетрагидрофуран или метанол. Соединения формулы I могут быть получены в виде их индивидуальных стереоизомеров с помощью реакции рацемической смеси соединений с оптически активным разрешающим агентом, чтобы образовать пару диастереоизомерных соединений, разделения диастереоизомеров и выделения оптически чистого энантиомера. Разделение энантиомеров может быть выполнено при использовании ковалентных диастереоизомерных производных соединений формулы I, при этом диссоциируемые комплексы являются предпочтительными (например, кристаллические диастереоизомерные соли). Диастереоизомеры имеют различные физические свойства (например, температуру плавления, температуру кипения, растворимость, реакционную способность, и т.д.), и они могут быть легко разделены при использовании этих отличий. Диастереоизомеры могут быть разделены с помощью хроматографии или, предпочтительно, способами разделения/разрешения, основанными на различиях в их растворимости. Оптически чистый энатиомер затем выделяют, наряду с разрешающим агентом, с помощью любой методики, которая не должна приводить к рацемизации. Более детальное описание способов, применяемых для выделения стереоизомерных соединений из их рацемической смеси может быть найдено у Jean(А) взаимодействие соединения формулы 2: с соединением формулы NH2CR1R2X2, где R1, R2, R3, R4 и X2 имеют значения, определенные в разделе Сущность изобретения для соединений формулы I; или(B) взаимодействие соединения формулы 2 с соединением формулы NH2X3, где R3, R4 и X3 имеют значения, определенные в разделе Сущность изобретения для соединений формулы I; и(C) необязательное превращение соединения формулы I в фармацевтически приемлемую соль;(D) необязательное превращение соли соединения формулы I в несолевую форму;(Е) необязательное превращение неокисленной формы соединения формулы I в фармацевтически приемлемый N-оксид;(F) необязательное превращение соединения формулы I в форме N-оксида в его неокисленную форму;(G) необязательное выделение отдельного изомера соединения формулы I из смеси изомеров;(Н) необязательное превращение немодифицированного соединения формулы I в фармацевтически пригодное пролекарство; и(I) необязательное превращение производного пролекарства соединения формулы I в его немодифицированную форму. Примеры Настоящее изобретение далее иллюстрируется, без ограничения, с помощью следующих примеров,которые демонстрируют получение соединений формулы I (Примеры) и промежуточных соединений(Ссылки) в соответствии с настоящим изобретением. Ссылка 1. 2-Фенилкарбамоилгексановая кислота. Раствор анилина (5,47 мл, 60 ммоль) и триэтиламина (8.36 мл, 60 ммоль) в хлористом метилене (150 мл) охлаждают до -20 С и обрабатывают метилмалонилхлоридом (8,36 мл, 60 ммоль) в хлористом метилене (20 мл). Реакционной смеси дают возможность нагреться до температуры окружающей среды в течение 3 ч, а затем ее выливают в холодную 1N HCl. Органический слой отделяют и промывают водным раствором бикарбоната натрия, а затем рассолом, сушат над сульфатом магния и упаривают, что дает метил-2-фенилкарбамоилацетат. Смесь метил-2-фенилкарбамоилацетата (1,159 г, 6 ммоль) гидроксида лития (0,43 г, 18 ммоль) и 1 иодбутана (0,91 мл, 8 ммоль) в N-метилпирролидиноне (10 мл) перемешивают при температуре окружающей среды в течение 1,5 ч. Реакционную смесь выливают в ледяную воду, экстрагируют этилацетатом (дважды, по 50 мл каждый раз). Объединенные экстракты промывают рассолом, сушат над сульфатом магния и выпаривают. Остаток очищают с помощью флеш хроматографии на силикагеле, элюируя 20% смесью этилацетат/гексан, что дает метил-2-фенилкарбамоилгексаноат (0,715 г, 48% выход). Раствор метил-2-фенилкарбамоилгексаноата (0,98 г, 3,9 ммоль) в метаноле (10 мл) обрабатывают гидроксидом натрия (4 мл, 4 ммоль) при температуре окружающей среды в течение 17 ч. Метанол удаляют при пониженном давлении и остаток обрабатывают 1N HCl и экстрагируют этилацетатом (дважды,по 50 мл каждый раз). Органические слои промывают рассолом, сушат над сульфатом магния и выпаривают, что дает 2-фенилкарбамоилгексановую кислоту (0,68 г, 2,9 ммоль, 74% выход). Ссылка 2. 2-Циклoгeкcилмeтил-N-фeнилмaлoнaминoвaя кислота. Смесь метил-2-фенилкарбамоилацетата (полученного как в ссылке примера 1) (4,39 г, 22,7 ммоль),гидроксида лития (1,08 г, 45 ммоль) и бромметилциклогексана (3,76 мл, 27 ммоль) в Nметилпирролидиноне (25 мл) перемешивают при температуре окружающей среды в течение 17 ч. Реакционную смесь выливают в ледяную воду и экстрагируют эфиром (трижды, по 100 мл каждый раз). Экстракты промывают водой, затем рассолом, сушат над сульфатом магния и выпаривают. Остаток очищают с помощью флеш хроматографии на силикагеле, элюируя 10% этилацетатом (гексан), что дает метил 2-циклогексилметил-N-фенилмалонамат (1,89 г, 6,5 ммоль, 29% выход). Указанный выше водный слой охлаждают с помощью льда и подкисляют до значения рН 2 с помощью 1N HCl. Водный слой экстрагируют эфиром (3 раза, по 100 мл каждый раз) и экстракты промывают водой, затем рассолом, сушат над сульфатом магния и выпаривают, что дает 2-циклогексилметил-N-фенилмалонаминовую кислоту (1,12 г,18% выход). Ссылка 3. 2-Циклогексилметил-N-фенэтилмалонаминовая кислота. Натрий (6,9 г, 0,3 моль) растворяют в этаноле (300 мл), а затем добавляют диэтилмалонат (50,3 мл,0,3 моль). Добавляют бромметилциклогексан (46 мл, 0,33 моль) и реакционную смесь нагревают при температуре 70 С в течение 14 ч. Реакционную смесь охлаждают и этанол удаляют с помощью упаривания. Полученную массу растворяют в ледяной воде, а затем экстрагируют этилацетатом. Органические- 18007334 слои промывают водой, затем рассолом и сушат над сульфатом магния. Растворители удаляют при пониженном давлении, что дает диэтилциклогексилмалонат. Раствор диэтилциклогексилмалоната (12,8 г, 0,05 моль) в этаноле (100 мл) обрабатывают раствором гидроксида лития (1,2 г, 0,05 молей) в воде (50 мл), а затем перемешивают при температуре окружающей среды в течение 15 ч. Этанол удаляют при пониженном давлении и к остатку добавляют воду (50 мл). Реакционную смесь экстрагируют эфиром, охлаждают с помощью льда и подкисляют до значения рН 1,5 с помощью НСl. Водную фазу насыщают NaCl и экстрагируют этилацетатом (дважды, 150 мл каждый раз). Высушивают над сульфатом магния и упаривание растворителя дает этил-2-циклогексилмалонат(8,52 г, 37 ммоль, 74% выход). Этил-2-циклогексилмалонат (8,52 г, 37 ммоль) в этилацетате (80 мл) охлаждают до температуры 0 С и обрабатывают диметилформамидом (50 мкл), а затем оксалилхлоридом (3,93 мл, 45 ммоль). Температуру реакции поднимают до комнатной температуры и через 2 ч растворители удаляют при пониженном давлении, что дает этил-2-циклогексилмалонилхлорид. Малонилхлорид, указанный выше, разбавляют до объема 28 мл этилацетатом и 2 мл этого раствора добавляют к раствору фенэтиламина (0,376 мл, 3 ммоль) и N-метилморфолина (0,40 г, 4 ммоль) в этилацетате (4 мл) при температуре -20 С. Через 15 мин реакционной смеси дают возможность нагреться до температуры окружающей среды в течение ночи. Реакционную смесь разбавляют этилацетатом (5 мл) и ледяной водой (5 мл). Органический слой отделяют и промывают холодным 0,05N НСl, затем водным раствором NaHCO3, после чего рассолом, сушат над сульфатом магния и выпаривают при пониженном давлении. Остаток очищают с помощью радиальной хроматографии, что дает этил-2-циклогексилметилN-фенэтилмалонамат (0,366 г, 1,10 ммоль, 42% выход). Эфир, указанный выше (0,366 г, 1,10 ммоль), в этаноле (10 мл) обрабатывают при температуре окружающей среды водным раствором гидроксида натрия (1,3 мл 1N) в течение 2,5 ч. Реакционную смесь разбавляют водой (30 мл) и промывают эфиром (3 раза, 30 мл каждый раз). Водный слой охлаждают,подкисляют с помощью 1N HCl (2 мл) и экстрагируют этилацетатом (3 раза, по 30 мл каждый раз). Экстракты этилацетата промывают рассолом, сушат над сульфатом магния и выпаривают, что дает 2 циклогексилметил-N-феметилмалонаминовую кислоту (0,138 г, 0,46 ммоль, 42% выход). Ссылка 4. 2-Циклoгeкcилмeтил-N-пиpидин-4-илмeтилмaлoнaминoвaя кислота. Этил-2-циклогексилметилмалонилхлорид, полученный как описано в ссылке 3 (0,307 г, 1,25 ммоль), конденсируют с 4-аминометилпиридином, используя способ, описанный в ссылке 3, что дает этил-2-циклогексилметил-4-пирин-4-илметилмалонамат (0,237 г, 0,74 ммоль, 58% выход). Полученный эфир гидролизуют гидроксидом натрия, используя способ, описанный в ссылке 3, что дает 2-циклогексилметил-N-пиридин-4-илметилмалонаминовую кислоту (0,041 г, 0,14 ммоль, 19% выход). В соответствии с методикой получения соединений в выше упомянутых примерах, получают следующие соединения:(140 мг, 0,9 ммоль) и триэтиламином (600 мкл, 4,3 ммоль). Смесь перемешивают в течение 3 ч, а затем распределяют между слоем воды (20 мл) и этилацетата (50 мл). Органический слой отделяют и промывают 1 М насыщенным раствором гидрокарбоната натрия, 1 М раствором соляной кислоты и водой, сушат (MgSO4) и концентрируют. Продукт очищают от остатка с помощью флеш-хроматографии на колонке с силикагелем (60 ) с 50% этилацетатом в гексане, что дает 2-бутил-N-цианометил-N'фенилмалонамид (125 мг, 57% выход). 1 Н ЯМР: (ДМСО) 10,01 (с, 1 Н), 7,59 (д, J=8 Гц, 2 Н), 7,31 (т, J=7 Гц, 2 Н), 7,06 (т, J=7 Гц, 1 Н), 4,13 (д, J=6 Гц, 2 Н), 3,32 (т, J=8 Гц, 1 Н), 1,80 (м, 2 Н), 1,25 (м, 4 Н), 0,86 (т,J=7 Гц, 3 Н). MS: м/е 273,9. Пример 2. N-Цианометил-2-циклогексилметил-N'-фенилмалонамид (cоединение 2). Раствор, содержащий 2-циклогексилметил-N-фенилмалонаминовую кислоту (350 мг, 1,2 ммоль),полученную как описано в ссылке 2, EDCI (250 мг, 1,3 ммоль), HOBt гидрат (199 мг, 1,3 ммоль), бисульфат аминоацетонитрила (200 мг, 1,3 ммоль) и N-метилморфолин (0,30 мл, 2,7 ммоль) в N,Nдиметилпирролидиноне (5 мл) перемешивают при температуре окружающей среды в течение 15 ч. Реакционную смесь выливают в холодный 1N HCl и экстрагируют этилацетатом. Органическую фазу промывают водным раствором насыщенного гидрокарбоната натрия, а затем рассолом (50 мл каждый раз), сушат над сульфатом магния и выпаривают. Остаток очищают с помощью радиальной хроматографии, используя 50% смесь этилацетат/гексан в качестве элюента, что дает N-цианометил-2-циклогексилметилN'-фенилмалонамид (179 мг, 48% выход). 1 Н ЯМР: (ДМСО) 10,01 (с, 1 Н), 8,47 (т, J=5 Гц, 1 Н), 7,59 (д, J=7 Гц, 2 Н), 7,31 (т, J=8 Гц, 2 Н), 7,07 (т, J=7 Гц, 1 Н), 4,13 (д, J=5 Гц, 2 Н), 3,47 (т, J=7 Гц, 1 Н), 1,6 (м, 7 Н), 1,1 Раствор, содержащий 2-циклогексилметил-N-фенэтилмалоновую кислоту (138 мг, 0,46 ммоль), полученную как описано в ссылке 3, EDCI (115 мг, 0,60 ммоль), HOBt гидрат (92 мг, 0,60 ммоль), Nметилморфолин (115 мл, 1,38 ммоль) в N,N-диметилпирролидиноне (4 мл) перемешивают при температуре окружающей среды в течение 10 мин. Добавляют бисульфат аминоацетонитрила (106 мг, 0,69 ммоль). Реакционную смесь перемешивают при температуре окружающей среды в течение 2 ч, а затем выливают в холодный 1N HCl и экстрагируют дважды этилацетатом (50 мл каждый раз). Органическую фазу промывают водным раствором гидрокарбоната натрия, а затем рассолом (50 мл каждый раз), сушат над сульфатом магния и выпаривают. Остаток очищают с помощью радиальной хроматографии, используя 50% смесь этилацетат/гексан в качестве элюента, что дает N-цианометил-2-циклогексилметил-N'-фенэтилмалонамид (56 мг, 36% выход). 1 Н ЯМР: (ДМСО) 8,38 (т, J=5 Гц, 1 Н), 7,98 (т, J=6 Гц, 1 Н), 7,25 (м, 5 Н), 4,10 (д, J=6 Гц, 2 Н), 3,2 (м,3 Н), 2,71 (т, J=7 Гц, 2 Н), 1,6 (м, 7 Н), 1,1 (м, 4 Н), 0,85 (м, 2 Н). MS: м/е 342,10. Раствор, содержащий 2-циклогексилметил-N-пиридин-4-илметилмалоновую кислоту (41 мг, 0,14 ммоль), полученную как описано в ссылке 4, конденсируют с аминоацетонитрилом как описано в примере 3, что дает N-цианометил-2-циклогексилметил-N'-пирид-4-илметилмалонамид (13 мг, 28% выход). 1H ЯМР: (ДМСО) 8,5 (м, 4 Н), 7,20 (д, J=6 Гц, 2 Н), 4,3 (м, 2 Н), 4,13 (д, J=5 Гц, 2 Н), 3,3 (м, 1 Н), 1,6 (м, 7 Н), 1,1 Смесь N-бензил-2-циклогексилметилмалонаминовой кислоты (200 мг, 0,69 ммоль), HOBt (159 мг,1,04 ммоль), EDC (146 мг, 0,76 ммоль), 2-амино-1-бензооксазол-2-ил-4-фенилбутан-1-она (195 мг, 0,69 ммоль), дихлорметана (3 мл) и триэтиламина (106 мкл, 0,76 ммоль) перемешивают в течение 2 ч. Продукт экстрагируют этилацетатом (60 мл) и промывают двумя порциями по 15 мл 1N HCl, и двумя порциями по 15 мл насыщенного раствора NaHSO3, сушат над MgSO4 и концентрируют. Затем добавляют этилацетат (5 мл) и собирают выпавший осадок белого цвета, что дает N-[1-(1-бензооксазол-2-ил-1-гидроксиметил)-3-фенилпропил]-N'-бензил-2-циклогексилметил-малонамид (81 мг, 0,12 ммоль, 21% выход).Dess Martin периодинаном (107 мг, 0,253 ммоль). Смесь перемешивают в течение 2 ч, затем добавляют 8 мл 0,26 М NаS2 О 3 в насыщенном NaHSO3 и смесь экстрагируют двумя порциями по 15 мл этилацетата и промывают двумя порциями по 4 мл насыщенного раствора NaHSO3. Органический слой сушат надMgSO4 и концентрируют. Продукт повторно кристаллизуют из этилацетата и гексана, что дает N-[1-(1 бензооксазол-2-илметаноил)-3-фенилпропил]-N'-бензил-2-циклогексилметилмалонамид (40 мг, 0,072 ммоль, 57% выход); 1H ЯМР: (ДМСО) 7,88 (м, 1 Н), 7,68-7,40 (м, 3 Н), 7,35-7,10 (м, 10 Н), 6,90 (м, 1 Н), 5,65(м, 1 Н), 4,43 (д, J=5,7 Гц, 2 Н), 3,25 (м, 1 Н), 2,74 (т, J=8,0 Гц, 1 Н), 2,46 (м, 1 Н), 2,17 (м, 1 Н), 1,77 (т, J=7,4 Гц, 1 Н), 1,64 (м, 7 Н), 1,22 (м, 4 Н), 0,87 (м, 2 Н); MS: (М 1) 552,8; 551,68. Следующие соединения формулы I получены в соответствии с методикой, приведенной в указанных выше примерах:N,N'-бис-[(S)-1-(1-бензооксазол-2-илметаноил)пропил]-2-циклогексилметилмалонамид (cоединение 42); 1 Н ЯМР (ДМСО): 8,41 (д, J=6 Гц, 2 Н), 8,00 (д, J=8 Гц, 2 Н), 7,89 (д, J=8 Гц, 2 Н), 7,65 (т, J=7 Гц, 2 Н),7,53 (т, J=8 Гц, 2 Н), 5,19 (м, 2 Н), 3,42 (т, J=8 Гц, 1 Н), 1,98 (м, 2 Н), 1,74 (м, 2 Н), 1,52 (м, 7 Н), 0,94 (м, 10 Н),0,77 (м, 2 Н); MS (м/е)=572,26. Молекулярный вес 573,4. Пример 6. Опыт с Катепсином S. Растворы тестируемых соединений в различных концентрациях получают в 10 мкл диметилсульфоксида (ДМСО), а затем разбавляют в анализируемом буфере (40 мкл, содержащем: MES, 50 ммоль (рН 6,5); EDTA, 2,5 ммоль; и NaCl, 100 ммоль). Человеческий Катепсин S (0,158 мМ в 25 мкл анализируемого буфера) добавляют к растворам. Анализируемые растворы смешивают в течение 5-10 с на вибрационной пластинке, закрывают и выдерживают в течение 30 мин при температуре окружающей среды. К анализируемым растворам добавляют Z-Val-Val-Arg-AMC (9 нмолей в 25 мкл анализируемого буфера) и после гидролиза в течение 5 мин проводят спектрофотометрию при ( 460 нм). Соответствующие константы реального ингибирования (Ki) вычисляют, исходя из прогрессирующей кривой графика функции фермента, используя стандартные математические модели. Пример 7. Опыт с Катепсином В. Растворы тестируемых соединений в различных концентрациях получают в 10 мкл диметилсульфоксида (ДМСО), а затем разбавляют в анализируемом буфере (40 мкл, содержащем: N,N-бис(2 гидроксиэтил)-2-аминоэтансульфоновую кислоту (BES), 50 ммоль (рН 6); монолаурат полиоксиэтилен- 23007334 сорбитана, 0,05%; и дитиотреитол (DTT), 2,5 ммоль). К растворам добавляют человеческий Катепсин В(0,025 пмолей в 25 мкл анализируемого буфера). Анализируемые растворы перемешивают в течение 5-10 с на вибрационной пластинке, закрывают и выдерживают в течение 30 мин при температуре окружающей среды. К анализируемым растворам добавляют Z-FR-AMC (20 нмоль в 25 мкл анализируемого буфера) и после гидролиза в течение 5 мин проводят спектрофотометрию ( 460 нм). Соответствующие константы реального ингибирования (Ki) вычисляют, исходя из прогрессирующей кривой графика функции фермента, используя стандартные математические модели. Пример 8. Опыт с Катепсином К. Растворы тестируемых соединений в различных концентрациях получают в 10 мкл диметилсульфоксида (ДМСО), а затем разбавляют в анализируемом буфере (40 мкл, содержащем: MES, 50 ммоль (рН 5,5); EDTA, 2.5 ммоль; и DTT, 2,5 ммоль). К растворам добавляют человеческий Катепсин К (0,0906 пмоль в 25 мкл анализируемого буфера). Анализируемые растворы смешивают в течение 5-10 с на вибрационной пластинке, закрывают и выдерживают в течение 30 мин при температуре окружающей среды. К анализируемым растворам добавляют Z-Phe-Arg-AMC (4 нмоля в 25 мкл анализируемого буфера) и после гидролиза в течение 5 мин проводят спектрофотометрию ( 460 нм). Соответствующие константы ингибирования (Kj) вычисляют, исходя из прогрессирующей кривой графика функции фермента, используя стандартные математические модели. Пример 9. Опыт с Катепсином L. Растворы тестируемых соединений в различных концентрациях получают в 10 мкл диметилсульфоксида (ДМСО), а затем разбавляют в анализируемом буфере (40 мкл, содержащем: MES, 50 ммоль (рН 5,5); EDTA, 2,5 ммоль; и DTT, 2.5 ммоль). К растворам добавляют человеческий Катепсин L (0,05 пмолей в 25 мкл анализируемого буфера). Анализируемые растворы смешивают в течение 5-10 с на вибрационной пластинке, закрывают и выдерживают в течение 30 мин при температуре окружающей среды. К анализируемым растворам добавляют Z-Phe-Arg-AMC (1 нмоль в 25 мкл анализируемого буфера) и после гидролиза проводят в течение 5 мин спектрофотометрию ( 460 нм). Соответствующие константы реального ингибирования (Кi) вычисляют, исходя из прогрессирующей кривой графика функции фермента, используя стандартные математические модели. Соединения по настоящему изобретению тестируют в соответствии с описанными выше анализами на ингибирование протеазы и, как обнаружено, демонстрируют селективную ингибирующую активность по отношению к Катепсину S. Например, было найдено, что соединения по настоящему изобретению ингибируют активность Катепсина S протеазы при концентрациях, которые по меньшей мере в 50 раз меньше концентрации, которая требуется для эквиактивного ингибирования активности Катепсина К протеазы. Соответствующие константы ингибирования (Кi) для соединений изобретения по отношению к Катепсину S, составляют приблизительно от 10-10 М до приблизительно 10-7 М. Пример 10. Образцы фармацевтических составов, содержащих соединение формулы I. Оральный состав. Соединение формулы I 10-100 мг Моногидрат лимонной кислоты 105 мг Гидроксид натрия 18 мг Вкусовая или ароматизирующая добавка Вода до 100 мл Внутривенный состав. Соединение формулы I Моногидрат декстрозы Моногидрат лимонной кислоты Гидроксид натрия Вода для инъекцииq.c., чтобы сделать изотоническим 1,05 мг 0,18 мг до 1,0 мл Состав для таблетки. Соединение формулы I Микрокристаллы целлулезы Стеариновая кислота Коллоидный силикагельX3 содержит гетеромоноциклическое кольцо, имеющее от 4 до 6 атомов, являющихся членами кольца или конденсированную гетеробициклическую кольцевую систему, содержащую от 8 до 14 атомов, являющихся членами кольца и любой карбоциклический кетон, иминокетон или его тиокетоновое производное;R3 является -C(R6)(R6)Х 5, где R6 является водородом и X5 является выбранным из -Х 4R12, -R14,4-X SR14, -X4S(O)2R14, где X4 является связью или (С 1-6)алкилом; R12 при каждом появлении независимо является водородом или (С 1-6)алкилом и R14 является (С 3-10)циклоалкил(С 0-6)алкилом, гетеро(С 3(С 6-10)арил(С 0-6)алкилом,гетеро(С 5-10)арил(С 0-6)алкилом,(С 910)циклоалкил(С 0-3)алкилом,)бициклоарил(С 0-6)алкилом или гетеро(С 8-10)бициклоарил(С 0-6)алкилом; 10R4 является -NR6R6, -NR6R14, -NR6R15 или -NR6X5C(O)R14, где R6, X5 и R14 являются теми, которые описаны выше и R15 является водородом, -(С 1-6)алкилом; где в R3 и R4 любая алициклическая или ароматическая кольцевая система может быть дополнительно замещена нитро, -X4OR12, -X4C(O)NR12R12, -X4OR14, где R4, X12 и R14 являются теми, которые описаны выше, и в R3 и R4 любой алифатический остаток может быть замещен дополнительно циано; иN-оксидные производные, производные пролекарств, защищенные производные, индивидуальные изомеры и смеси этих изомеров; и фармацевтически приемлемые соли и сольваты таких соединений и Nоксидные производные, производные пролекарств, защищенные производные, индивидуальные изомеры и смеси этих изомеров. 2. Соединение по п.1, гдеR1 является водородом или метилом и R2 представляет собой водород, метоксиметил, (С 1-6)алкил,фенэтил, тиофен-2-ил или 5-метилфуран-2-ил или R1 и R2 вместе с атомом углерода, к которому они присоединены, образуют циклопропилен, тетрагидрофуран-4-илен или метилпиперидин-4-илен. 4. Соединение по п.3, где R3 выбрано из тиофен-2-сульфонилметила, 3-хлор-2-фторфенилметансульфонилметила, бензолсульфонилметила, фенилметансульфонилметила, 2-(1,1-дифторметокси)фенилметансульфонилметила, 2-бензолсульфонилэтила, 2-(пиридин-2-сульфонил)этила, 2-(пиридин-4-сульфонил)этила, 2-фенилметансульфонилэтила, оксипиридин-2-илметансульфонилметила, проп 2-ен-1-сульфонилметила, 4-метоксифенилметансульфонилметила, n-толилметансульфонилметила, 4 хлорфенилметансульфонилэтила, о-толилметансульфонилметила, 3,5-диметилфенилметансульфонилметила, 4-трифторметилфенилметансульфонилметила, 4-трифторметоксифенилметансульфонилметила,2-бромфенилметансульфонилметила, пиридин-2-илметансульфонилметила, пиридин-3-илметансульфонилметила, пиридин-4-илметансульфонилметила, нафтален-2-илметансульфонилметила, 3-метилфенилметансульфонилметила, 3-трифторметилфенилметансульфонилметила, 3-трифторметоксифенилметансульфонилметила, 4-фтор-2-трифторметоксифенилметансульфонилметила, 2-фтор-6-трифторметилфенилметансульфонилметила,3-хлорфенилметансульфонилметила,2-фторфенилметансульфонилметила, 2-трифторфенилметансульфонилметила, 2-цианофенилметансульфонилметила, 4-третбутилфенилметансульфонилметила, 2-фтор-3-метилфенилметансульфонилметила, 3-фторфенилметан- 25007334 сульфонилметила, 4-фторфенилметансульфонилметила, 2-хлорфенилметансульфонилметила, 2,5 дифторфенилметансульфонилметила, 2,6-дифторфенилметансульфонилметила, 2,5-дихлорфенилметансульфонилметила, 3,4-дихлорфенилметансульфонилметила, 2-(1,1-дифторметокси)фенилметансульфонилметила, 2-цианофенилметансульфонилметила, цианофенилметанесульфонилметила, 2-трифторметоксифенилметансульфонилметила,2,3-дифторфенилметансульфонилметила,2,5-дифторфенилметансульфонилметила, бифенил-2-илметансульфонилметила, циклогексилметила, 3-фторфенилметансульфонилметила,3,4-дифторфенилметансульфонилметила,2,4-дифторфенилметансульфонилметила, 2,4,6-трифторфенилметансульфонилметила, 2,4,5-трифторфенилметансульфонилметила,2,3,4-трифторфенилметансульфонилметила, 2,3,5-трифторфенилметансульфонилметила, 2,5,6-трифторфенилметансульфонилметила, 2-хлор-5-трифторметилфенилметансульфонилметила, 2-метилпропан-1 сульфонила,2-фтор-3-трифторметилфенилметансульфонилметила,2-фтор-4-трифторметилфенилметансульфонилметила, 2-фтор-5-трифторметилфенилметансульфонилметила, 4-фтор-3-трифторметилфенилметансульфонилметила, 2-метоксифенилметансульфонилметила, 3,5-бис-трифторметилфенилметансульфонилметила,4-дифторметоксифенилметансульфонилметила,2-дифторметоксифенилметансульфонилметила, 3-дифторметоксифенилметансульфонилметила, 2,6-дихлорфенилметансульфонилметила, бифенил-4-илметансульфонилметила, 3,5-диметилизоксазол-4-илметансульфонилметила,5-хлортиофен-2-илметансульфонилметила, 2-[4-(1,1-дифторметокси)бензолсульфонил]этила, 2-[2-(1,1 дифторметокси)бензолсульфонил]этила, 2-[3-(1,1-дифторметокси)бензолсульфонил]этила, 2-(4-трифторметоксибензолсульфонил)этила, 2-(3-трифторметоксибензолсульфонил)этила, 2-(2-трифторметоксибензолсульфонил)этила, (цианометилметилкарбамоил)метила, бутила, бифенил-3-илметила, 2-оксо-2 пирролидин-1-илэтила, 2-бензолсульфонилэтила, изобутилсульфанилметила, 2-фенилсульфанилэтила,циклогексилметансульфонилметила, 2-циклогексилэтансульфонила, бензила, нафтален-2-ила, бензилсульфанилметила, 2-трифторметилбензилсульфанилметила, 5-бромтиофен-2-илметила, фенилсульфанилэтила и циклопропилметансульфонилметила. 5. Соединение по п.4, где R4 выбрано из фениламино, бензиламино, 4-феноксифениламино, фенэтиламино, 3-фенилпропиламино, морфолин-4-ила, циклогексиламино, нафтален-1-илметиламино, пиридин 3-иламино, 6-метоксипиридин-3-иламино, диизобутиламино, 4-нитробензиламино, 2-тиофен-2-илэтиламино, 3-феноксифениламино, цианометиламино, (пиридин-3-илметил)амино, 5,6,7,8-тетрагидронафтален-1-иламино, 2-пиридин-2-илэтиламино, 2,3-дигидроиндол-1-ила, 3,4-дигидро-1 Н-изохинолин-2 ила, циклогексилметиламино, 2-метоксибензиламино, 1-фенилэтиламино, (пиридин-4-илметил)амино,бензилметиламино, 3-нитробензиламино, 4-метоксифениламино, 3-карбамоилфениламино, 4-карбамоилфениламино, (тетрагидрофуран-2-илметил)амино, 3,4-дигидро-2 Н-хинолин-1-ила, диметиламино, бутилметиламино, диизопропиламино, пропилметиламино, 1-(бензооксазол-2-карбонил)пропиламино и изобутилметиламино. 6. Соединение по п.5 выбрано из группы, включающей такие соединения, как 2-бутил-Nцианометил-N'-фенилмалонамид, N-цианометил-2-циклогексилэтил-N'-фенилмалонамид; N-цианометил 2-циклогексилметил-N'-фенэтилмалонамид; N-цианометил-2-циклогексилметил-N'-пиридин-4-илметилмалонамид; N-[1-(бензоксазол-2-карбонил)-3-фенилпропил]-N'-бензил-2-циклогексилметилмалонамид;cyльфонилэтил)-N-[(S)-1-(1-бeнзоокcaзoл-2-ил-метаноил)пентил]-N'-бензилмалонамид; N,N'-бис-[(S)-1(1-бензооксазол-2-ил-метаноил)пропил]-2-циклогексилметилмалонамид; и N-оксидные производные,производные пролекарств, защищенные производные, индивидуальные изомеры и смеси этих изомеров; и фармацевтически приемлемые соли и сольваты таких соединений и N-оксидные производные,производные пролекарств, защищенные производные, индивидуальные изомеры и смеси этих изомеров. 7. Фармацевтическая композиция, содержащая терапевтически эффективное количество соединения по п.1 в комбинация с фармацевтически приемлемым наполнителем. 8. Способ лечения заболевания животного, при котором ингибирование катепсина S может предотвращать, ингибировать или уменьшать патологию и/или симптомологию заболевания, включающий введение животному терапевтически эффективного количества соединения по п.1 или его N-оксидного производного или индивидуального изомера или смеси изомеров; или его фармацевтически приемлемой соли или сольвата таких соединений и N-оксидных производных, производных пролекарств, защищенны производных, индивидуальных изомеров и смеси этих изомеров. 9. Применение соединения по п.1 для получения лекарственного средства для лечения заболевания животного, при котором активность катепсина S оказывает влияние на патологию и/или симптомологию болезни. 10. Способ получения соединения формулы I:(а) взаимодействием соединения формулы 2(b) взаимодействием соединения формулы 2 с соединением формулы NH2X3, где R3, R4 и X3 являются теми, как определено в п.1.
МПК / Метки
МПК: C07C 255/42, A61K 31/277
Метки: соединения, катепсина, ингибиторов, качестве, композиции
Код ссылки
<a href="https://eas.patents.su/28-7334-soedineniya-i-kompozicii-v-kachestve-ingibitorov-katepsina.html" rel="bookmark" title="База патентов Евразийского Союза">Соединения и композиции в качестве ингибиторов катепсина</a>
Предыдущий патент: Фунгицидные смеси на базе дитианона
Следующий патент: Новые соединения и композиции как ингибиторы катепсина
Случайный патент: Способ и устройство для соединения слоев, образующих абсорбирующий лист












