Соединения и композиции в качестве ингибиторов активности каннабиноидного рецептора 1
Номер патента: 17696
Опубликовано: 28.02.2013
Авторы: Филлипс Дин, Хе Сяосюй, Лю Хон, Ван Син, Сиэ Юнпин, Нгуэн Трук Нгок, Ву Баогэнь, Ян Куньюн, Ло Томас, Чжу Сюэфэн
Формула / Реферат
1. Соединение формулы I
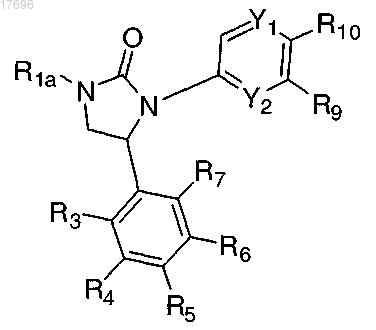
или его фармацевтически приемлемая соль, в которой
Y1 выбран из N и CR11;
Y2 выбран из N и CR8;
R1a выбран из циано, замещенного цианогруппой C1-6алкила, -X1R12, -X1NR13S(O)2R13, -X1OS(O)2R13,
-X1NR13X1OR13, -X1OR13, -X1C(O)OR13, -X1S(O)2R12, -X1S(O)2NR13C(O)R13, -X1S(O)2R13, -X1C(O)R12,
-X1R13R13, -X1S(O)2NR13R13, -X1OC(O)NR13R13, -X1C(O)NR12R13, -X1NR13X1C(O)R12, -X1NR13X1C(O)NR13R13,
-X1C(O)NR13X1C(O)OR13, -X1C(O)NR13X1NR13R13, -X1C(O)NR13X1OR13 и -X1C(O)NR13R13;
где R12 выбран из С6-10арила, С5-10гетероарила, С3-12циклоалкила и С3-10гетероциклоалкила; где указанный арил, гетероарил, циклоалкил или гетероциклоалкил в качестве R12 необязательно замещен 1-3 радикалами, независимо выбранными из галогена, гидрокси, бис-гидрокси-C1-6алкиламино, C1-6алкиламино, диэтиламино, C1-6алкила, C1-6алкокси, C1-6алкоксикарбонила, C1-6алкилсульфокси, C1-6алкилкарбокси, C1-6алкилсульфонила, аминосульфонила, замещенного галогеном C1-6алкила, замещенного галогеном C1-6алкокси, С3-12циклоалкила, С3-10гетероциклоалкила, С5-10гетероарила и С6-10арила, необязательно замещенного 1-3 радикалами галогена; где указанные циклоалкильные, гетероциклоалкильные, гетероарильные и арильные заместители R12 могут быть далее необязательно замещены 1-3 C1-6алкильными радикалами или метилсульфонилом, метоксикарбонилом и метокси;
каждый R13 независимо выбран из водорода, C1-6алкила, гидрокси-С1-6алкила, С6-10арила, С3-10гетероциклоалкила; где указанный арил или гетероциклоалкил в качестве R13 необязательно замещен группой, выбранной из C1-6алкила и C1-6алкокси;
каждый X1 независимо выбран из связи и C1-4алкилена;
R3, R5, R6 и R7, каждый независимо, выбран из водорода, галогена и амино;
R4 выбран из водорода, галогена, циано, диметиламинопропила, гидрокси, C1-6алкила, C1-6алкокси, замещенного галогеном C1-6алкила, замещенного галогеном C1-6алкокси, замещенного гидроксигруппой C1-6алкила, замещенного гидроксигруппой C1-6алкокси, замещенного цианогруппой C1-6алкила, замещенного цианогруппой C1-6алкокси и -OX5R4a;
где X5 выбран из связи и C1-4алкилена;
R4a выбран из C1-6алкила, С3-8циклоалкила, С6-10арила и С5-10гетероарила; где любой циклоалкил, арил или гетероарил в качестве R4a необязательно замещен 1-3 радикалами, независимо выбранными из галогена, циано, амино, C1-6алкила, C1-6алкокси, замещенного галогеном C1-6алкила, замещенного галогеном C1-6алкокси, замещенного гидроксигруппой C1-6алкила, замещенного гидроксигруппой C1-6алкокси, замещенного цианогруппой C1-6алкила и замещенного цианогруппой C1-6алкокси;
R8, R9 и R11, каждый независимо, выбран из водорода, галогена, C1-6алкила, C1-6алкокси, замещенного галогеном C1-6алкила и замещенного галогеном С1-6алкокси;
R10 выбран из галогена, циано, C1-6алкила, C1-6алкокси, замещенного галогеном C1-6алкила, замещенного галогеном C1-6алкокси, бензоила, -X4OR17, -X4S(O)0-2R17 и -X4R17;
где Х4 выбран из связи и C1-4алкилена; и
R17 выбран из С6-10арила и C5-10гетероарила; где R17 необязательно замещен 1-3 радикалами галогена.
2. Соединение по п.1, в котором R1a выбран из циано, метилкарбониламиносульфонилэтила, пирролидин-2-онилэтила, имидазолилэтила, оксазолидинонилэтила, 1-пиразолилэтила, цианометила, 4'-(4-хлорфенокси)фенила, 1,3-диоксанилэтила, фенила, пиразинила, пиперазинилсульфонилэтила, азетидинилсульфонилэтила, морфолиносульфонилэтила, пирролидинилсульфонилэтила, пирролидинилпропила, пирролидинилэтила, пиперазинилпропила, пиперидинилсульфонилэтила, пиридазинила, (5-(4-метоксифенил)-1,2,4-оксадиазол-3-ил)метила, пиперидинилкарбонилметила, 3-(N,N-бис(4-метоксифенил)сульфамоил)пропила, 2-оксо-2-(пиперидин-1-иламино)этила, пропиламинокарбонилметила, 2-(карбоксиметиламино)-2-оксоэтила, бис-гидроксиэтиламиносульфонилэтила, карбоксиметиламинокарбонилметила, аминокарбонилэтила, аминосульфонилэтила, аминосульфонилпропила, метиламиноэтила, пиперидинилэтила, пиперазинилэтила, метилсульфонилэтила, карбоксиметила, тетразолметила, бензила, 1,2,4-оксадиазолметила, 1,2,4-оксадиазолэтила, изоксазолметила, 2-(2-гидроксиэтиламино)-2-оксоэтила, диметиламиноэтиламинокарбонилметила, гидроксилэтила, метоксиэтила, гидроксилэтиламиноэтила, морфолиноэтила, метилпиперазинилэтила, 2-(карбамоилокси)этила, метилсульфонилоксиэтила, морфолинокарбонилметила, метилсульфонилпиперазинилэтила, 2-морфолиноэтила, аминоэтила, 2-(3,3-диметилуреидо)этила, морфолинокарбониламиноэтила, метилсульфониламиноэтила, пиридинилметила, гидроксилпропила, 2-(2,6-диметилморфолино)этила, 2-(2-метилморфолино)этила, метилсульфонилпропила и морфолинопропила;
где указанные кольцевые системы в качестве R1a необязательно замещены 1-3 радикалами, независимо выбранными из галогена, трифторметила, метила, бис-гидроксиэтиламино, трет-бутила, трет-бутоксикарбонила, гидрокси, метилсульфонила, аминосульфонила, диэтиламино, морфолино, циклогексила, пиридинила, пиперидинила, пирролидинила, пиперазинила, необязательно замещенного этилом или метилсульфонилом, метоксикарбонила и метокси.
3. Соединение по п.1 или 2, в котором R3, R5, R6 и R7, каждый независимо, представляет собой водород.
4. Соединение по любому из пп.1-3, в котором R4 выбран из водорода, трифторметила, галогена, гидрокси, цианометокси, диметиламинопропила, циано, циклопропилметокси, пиразинилокси, необязательно замещенного амино, пиридинилокси, пиримидинилокси; бензокси, фенокси, необязательно замещенного метилом или циано, этокси, тетразолилметокси, необязательно замещенного метилом, пиридазинилокси, пиразинилокси, гидроксиэтокси и метокси.
5. Соединение по любому из пп.1-4, в котором R8, R9 и R11, каждый независимо, выбран из водорода, галогена, трифторметила и метила.
6. Соединение по любому из пп.1-5, в котором R10 выбран из галогена, циано, метокси, трифторметила, пиридинилокси, бензоила, фенокси, бензила, пиридазинилокси, фенилсульфонила и пиримидинилокси; где указанный пиридинилокси, фенилсульфонил, фенокси, бензоил, бензил, пиридазинилокси и пиримидинилокси может быть необязательно замещен 1-3 радикалами галогена.
7. Соединение по п.1, выбранное из следующих соединений:
3-(4-(4-хлорфенокси)фенил)-1-тозил-4-(3-(трифторметил)фенил)имидазолидин-2-он;
этил-2-(3-(4-(4-хлорфенокси)фенил)-2-оксо-4-(3-(трифторметил)фенил)имидазолидин-1-ил)ацетат;
(S)-2-(3-(4-(4-хлорфенокси)фенил)-2-оксо-4-(3-(трифторметил)фенил)имидазолидин-1-ил)ацетонитрил;
3-(4-(4-хлорфенокси)фенил)-1-(4-(трифторметил)бензил)-4-(3-(трифторметил)фенил)имидазолидин-2-он;
3-[4-(4-хлорфенокси)фенил]-1-(3,5-диметилизоксазол-4-илметил)-4-(3-трифторметилфенил)имидазолидин-2-он;
(S)-3-(4-(4-хлорфенокси)фенил)-1-(4-метоксибензил)-4-(3-(трифторметил)фенил)имидазолидин-2-он;
(S)-3-[6-(4-хлорфенокси)пиридин-3-ил]-1-(4-метоксибензил)-4-(3-трифторметилфенил)имидазолидин-2-он;
(S)-3-[5-(4-хлорфенокси)пиразин-2-ил]-1-(4-метоксибензил)-4-(3-трифторметилфенил)имидазолидин-2-он;
(S)-2-(3-(5-(4-хлорфенокси)пиразин-2-ил)-2-оксо-4-(3-(трифторметил)фенил)имидазолидин-1-ил)этансульфонамид;
(S)-3-[4-(4-хлорфенокси)фенил]-1-(2-метансульфонилэтил)-4-(3-трифторметилфенил)имидазолидин-2-он;
(S)-2-(3-(4-(4-хлорфенокси)фенил)-2-оксо-4-(3-(трифторметил)фенил)имидазолидин-1-ил)этансульфонамид;
2-(3-(4-(4-хлорфенокси)фенил)-2-оксо-4-(3-(трифторметил)фенил)имидазолидин-1-ил)уксусная кислота;
1-((1Н-тетразол-5-ил)метил)-3-(4-(4-хлорфенокси)фенил)-4-(3-(трифторметил)фенил)имидазолидин-2-он;
2-(3-(4-(4-хлорфенокси)фенил)-2-оксо-4-(3-(трифторметил)фенил)имидазолидин-1-ил)-N-пропилацетамид;
2-(3-(4-(4-хлорфенокси)фенил)-2-оксо-4-(3-(трифторметил)фенил)имидазолидин-1-ил)-N-(пиперидин-1-ил)ацетамид;
2-(2-(3-(4-(4-хлорфенокси)фенил)-2-оксо-4-(3-(трифторметил)фенил)имидазолидин-1-ил)ацетамидо)уксусная кислота;
2-(3-(4-(4-хлорфенокси)фенил)-2-оксо-4-(3-(трифторметил)фенил)имидазолидин-1-ил)-N-(2-гидроксиэтил)ацетамид;
2-(3-(4-(4-хлорфенокси)фенил)-2-оксо-4-(3-(трифторметил)фенил)имидазолидин-1-ил)-N-(2-(диметиламино)этил)ацетамид;
3-(4-(4-хлорфенокси)фенил)-1-(2-гидроксиэтил)-4-(3-(трифторметил)фенил)имидазолидин-2-он;
2-(3-(4-(4-хлорфенокси)фенил)-2-оксо-4-(3-(трифторметил)фенил)имидазолидин-1-ил)этилметансульфонат;
3-(4-(4-хлорфенокси)фенил)-1-(2-метоксиэтил)-4-(3-(трифторметил)фенил)имидазолидин-2-он;
3-(4-(4-хлорфенокси)фенил)-1-(2-(2-гидроксиэтиламино)этил)-4-(3-(трифторметил)фенил)имидазолидин-2-он;
3-(4-(4-хлорфенокси)фенил)-1-(2-морфолиноэтил)-4-(3-(трифторметил)фенил)имидазолидин-2-он;
3-(4-(4-хлорфенокси)фенил)-1-(2-(4-метилпиперазин-1-ил)этил)-4-(3-(трифторметил)фенил)имидазолидин-2-он;
2-(3-(4-(4-хлорфенокси)фенил)-2-оксо-4-(3-(трифторметил)фенил)имидазолидин-1-ил)этилкарбамат;
3-(4-(4-хлорфенокси)фенил)-1-(2-(метиламино)этил)-4-(3-(трифторметил)фенил)имидазолидин-2-он;
3-(4-(4-хлорфенокси)фенил)-1-(2-(пиперидин-1-ил)этил)-4-(3-(трифторметил)фенил)имидазолидин-2-он;
3-(4-(4-хлорфенокси)фенил)-1-(2-(пиперазин-1-ил)этил)-4-(3-(трифторметил)фенил)имидазолидин-2-он;
1-(4-хлорбензил)-3-(4-(4-хлорфенокси)фенил)-4-(3-(трифторметил)фенил)имидазолидин-2-он;
1-бензил-3-(4-(4-хлорфенокси)фенил)-4-(3-(трифторметил)фенил)имидазолидин-2-он;
3-(4-(4-хлорфенокси)фенил)-1-(3-метоксибензил)-4-(3-(трифторметил)фенил)имидазолидин-2-он;
3-(4-(4-хлорфенокси)фенил)-1-(2-метоксибензил)-4-(3-(трифторметил)фенил)имидазолидин-2-он;
3-(4-(4-хлорфенокси)фенил)-1-(4-метоксифенил)-4-(3-(трифторметил)фенил)имидазолидин-2-он;
3-(4-(4-хлорфенокси)фенил)-1-(2-морфолино-2-оксоэтил)-4-(3-(трифторметил)фенил)имидазолидин-2-он;
3-(4-(4-хлорфенокси)фенил)-1-(2-(4-(метилсульфонил)пиперазин-1-ил)этил)-4-(3-(трифторметил)фенил)имидазолидин-2-он;
3-(4-(4-хлорфенокси)фенил)-1-(2-((2S,6R)-2,6-диметилморфолино)этил)-4-(3-(трифторметил)фенил)имидазолидин-2-он;
1-(2-аминоэтил)-3-(4-(4-хлорфенокси)фенил)-4-(3-(трифторметил)фенил)имидазолидин-2-он;
3-(2-(3-(4-(4-хлорфенокси)фенил)-2-оксо-4-(3-(трифторметил)фенил)имидазолидин-1-ил)этил)-1,1-диметилмочевина;
N-(2-(3-(4-(4-хлорфенокси)фенил)-2-оксо-4-(3-(трифторметил)фенил)имидазолидин-1-ил)этил)морфолин-4-карбоксамид;
N-(2-(3-(4-(4-хлорфенокси)фенил)-2-оксо-4-(3-(трифторметил)фенил)имидазолидин-1-ил)этил)метансульфонамид;
3-(4-(4-хлорфенокси)фенил)-1-(пиридин-2-илметил)-4-(3-(трифторметил)фенил)имидазолидин-2-он;
3-(4-(4-хлорфенокси)фенил)-1-(пиридин-3-илметил)-4-(3-(трифторметил)фенил)имидазолидин-2-он;
3-(4-(4-хлорфенокси)фенил)-1-(пиридин-4-илметил)-4-(3-(трифторметил)фенил)имидазолидин-2-он;
(S)-3-(4-(4-хлорфенокси)фенил)-1-(3-гидроксипропил)-4-(3-(трифторметил)фенил)имидазолидин-2-он;
3-(4-(4-хлорфенокси)фенил)-1-(2-((R)-2-метилморфолино)этил)-4-(3-(трифторметил)фенил)имидазолидин-2-он;
3-(4-(4-хлорфенокси)фенил)-1-(2-((S)-2-метилморфолино)этил)-4-(3-(трифторметил)фенил)имидазолидин-2-он;
(S)-3-(4-(4-хлорфенокси)фенил)-1-(3-(метилсульфонил)пропил)-4-(3-(трифторметил)фенил)имидазолидин-2-он;
3-(4-(4-хлорфенокси)фенил)-1-(3-морфолинопропил)-4-(3-(трифторметил)фенил)имидазолидин-2-он;
3-(4-(4-хлорфенокси)фенил)-4-(3-(бензилокси)фенил)-1-(2-(метилсульфонил)этил)имидазолидин-2-он;
3-(4-(4-хлорфенокси)фенил)-4-(3-гидроксифенил)-1-(2-(метилсульфонил)этил)имидазолидин-2-он;
3-(4-(4-хлорфенокси)фенил)-1-(2-(метилсульфонил)этил)-4-(3-(пиридин-2-илокси)фенил)имидазолидин-2-он;
3-(4-(4-хлорфенокси)фенил)-1-(2-(метилсульфонил)этил)-4-(3-(пиразин-2-илокси)фенил)имидазолидин-2-он;
4-(3-(2-цианофенокси)фенил)-3-(4-(4-хлорфенокси)фенил)-1-(2-(метилсульфонил)этил)имидазолидин-2-он;
4-(3-(бензилокси)фенил)-3-(4-хлорфенил)-1-(2-(метилсульфонил)этил)имидазолидин-2-он;
3-(4-хлорфенил)-4-(3-гидроксифенил)-1-(2-(метилсульфонил)этил)имидазолидин-2-он;
3-(4-хлорфенил)-1-(2-(метилсульфонил)этил)-4-(3-(пиразин-2-илокси)фенил)имидазолидин-2-он;
4-(3-(2-цианофенокси)фенил)-3-(4-хлорфенил)-1-(2-(метилсульфонил)этил)имидазолидин-2-он;
3-(4-хлорфенил)-1-(2-(метилсульфонил)этил)-4-(3-(пиримидин-2-илокси)фенил)имидазолидин-2-он;
3-(4-хлорфенил)-1-(2-(метилсульфонил)этил)-4-(3-(пиридин-2-илокси)фенил)имидазолидин-2-он;
3-(4-хлорфенил)-1-(2-(метилсульфонил)этил)-4-(3-(пиридин-3-илокси)фенил)имидазолидин-2-он;
3-(4-хлорфенил)-1-(2-(метилсульфонил)этил)-4-(3-(пиридин-4-илокси)фенил)имидазолидин-2-он;
3-(4-хлорфенил)-1-(2-(метилсульфонил)этил)-4-(3-(пиридазин-3-илокси)фенил)имидазолидин-2-он;
4-(3-(4-метоксифенокси)фенил)-3-(4-хлорфенил)-1-(2-(метилсульфонил)этил)имидазолидин-2-он;
4-(3-(5-аминопиразин-2-илокси)фенил)-3-(4-хлорфенил)-1-(2-(метилсульфонил)этил)имидазолидин-2-он;
3-(4-хлорфенил)-1-(2-(метилсульфонил)этил)-4-(3-(пиримидин-5-илокси)фенил)имидазолидин-2-он;
(S)-3-(4-(4-хлорфенокси)фенил)-4-(3-(трифторметил)фенил)-1-(пиразин-2-ил)имидазолидин-2-он;
(S)-3-(4-хлорфенил)-1-((5-(4-метоксифенил)-1,2,4-оксадиазол-3-ил)метил)-4-(3-(трифторметил)фенил)имидазолидин-2-он;
(S)-3-(4-хлорфенил)-1-(пиридин-3-илметил)-4-(3-(трифторметил)фенил)имидазолидин-2-он;
(S)-3-(4-хлорфенил)-1-(4-метоксибензил)-4-(3-(трифторметил)фенил)имидазолидин-2-он;
(S)-2-(3-(4-хлорфенил)-2-оксо-4-(3-(трифторметил)фенил)имидазолидин-1-ил)этансульфонамид;
(S)-3-(4-хлорфенил)-1-(2-гидроксиэтил)-4-(3-(трифторметил)фенил)имидазолидин-2-он;
(S)-3-(4-хлорфенил)-1-(3-гидроксипропил)-4-(3-(трифторметил)фенил)имидазолидин-2-он;
(S)-2-(3-(4-хлорфенил)-2-оксо-4-(3-(трифторметил)фенил)имидазолидин-1-ил)-N-пропилацетамид;
(S)-3-(4-хлорфенил)-1-(2-оксо-2-(пиперидин-1-ил)этил)-4-(3-(трифторметил)фенил)имидазолидин-2-он;
(S)-2-(3-(4-хлорфенил)-2-оксо-4-(3-(трифторметил)фенил)имидазолидин-1-ил)-N-(пиперидин-1-ил)ацетамид;
(S)-трет-бутил-4-(2-(3-(4-хлорфенил)-2-оксо-4-(3-(трифторметил)фенил)имидазолидин-1-ил)ацетил)пиперазин-1-карбоксилат;
(S)-3-(4-хлорфенил)-1-((5-(4-метоксифенил)-1,3,4-оксадиазол-2-ил)метил)-4-(3-(трифторметил)фенил)имидазолидин-2-он;
(S)-3-(4-хлорфенил)-1-((5-(4-хлорфенил)оксазол-2-ил)метил)-4-(3-(трифторметил)фенил)имидазолидин-2-он;
(S)-метил-3-((3-(4-хлорфенил)-2-оксо-4-(3-(трифторметил)фенил)имидазолидин-1-ил)метил)изоксазол-5-карбоксилат;
(S)-3-(4-хлорфенил)-1-(2-морфолиноэтил)-4-(3-(трифторметил)фенил)имидазолидин-2-он;
(S)-3-(4-хлорфенил)-1-(2-(4-гидроксипиперидин-1-ил)этил)-4-(3-(трифторметил)фенил)имидазолидин-2-он;
(S)-3-(4-хлорфенил)-1-(3-морфолинопропил)-4-(3-(трифторметил)фенил)имидазолидин-2-он;
(S)-3-(4-хлорфенил)-1-(2-(4-(метилсульфонил)пиперазин-1-ил)этил)-4-(3-(трифторметил)фенил)имидазолидин-2-он;
(S)-1-((5-трет-бутил-1,2,4-оксадиазол-3-ил)метил)-3-(4-хлорфенил)-4-(3-(трифторметил)фенил)имидазолидин-2-он;
(S)-3-(4-хлорфенил)-1-(2-(4-метилпиперазин-1-илсульфонил)этил)-4-(3-(трифторметил)фенил)имидазолидин-2-он;
(S)-3-(4-хлорфенил)-1-(2-(пиперидин-1-илсульфонил)этил)-4-(3-(трифторметил)фенил)имидазолидин-2-он;
(S)-3-(4-хлорфенил)-1-(2-(пирролидин-1-илсульфонил)этил)-4-(3-(трифторметил)фенил)имидазолидин-2-он;
(S)-3-(4-хлорфенил)-1-(2-(морфолиносульфонил)этил)-4-(3-(трифторметил)фенил)имидазолидин-2-он;
(S)-3-(3-(4-хлорфенил)-2-оксо-4-(3-(трифторметил)фенил)имидазолидин-1-ил)пропан-1-сульфонамид;
(S)-2-(3-(4-хлорфенил)-2-оксо-4-(3-(трифторметил)фенил)имидазолидин-1-ил)-N,N-бис(2-гидроксиэтил)этансульфонамид;
(S)-3-(4-хлорфенил)-1-((6-морфолинопиридин-3-ил)метил)-4-(3-(трифторметил)фенил)имидазолидин-2-он;
(S)-3-(4-хлорфенил)-1-((6-(4-этилпиперазин-1-ил)пиридин-3-ил)метил)-4-(3-(трифторметил)фенил)имидазолидин-2-он;
(S)-3-(4-хлорфенил)-1-((6-(пиперидин-1-ил)пиридин-3-ил)метил)-4-(3-(трифторметил)фенил)имидазолидин-2-он;
(S)-3-(4-хлорфенил)-1-((6-(пирролидин-1-ил)пиридин-3-ил)метил)-4-(3-(трифторметил)фенил)имидазолидин-2-он;
(S)-1-((6-(бис(2-гидроксиэтил)амино)пиридин-3-ил)метил)-3-(4-хлорфенил)-4-(3-(трифторметил)фенил)имидазолидин-2-он;
(S)-3-(4-хлорфенил)-1-((6-(4-(метилсульфонил)пиперазин-1-ил)пиридин-3-ил)метил)-4-(3-(трифторметил)фенил)имидазолидин-2-он;
(S)-3-(4-хлорфенил)-1-(3-(4-(метилсульфонил)пиперазин-1-ил)пропил)-4-(3-(трифторметил)фенил)имидазолидин-2-он;
(4S)-3-(4-хлорфенил)-1-(3-(3-(диэтиламино)пирролидин-1-ил)пропил)-4-(3-(трифторметил)фенил)имидазолидин-2-он;
(S)-3-(4-хлорфенил)-1-(2-(5-циклогексил-1,2,4-оксадиазол-3-ил)этил)-4-(3-(трифторметил)фенил)имидазолидин-2-он;
(S)-1-(2-(5-трет-бутил-1,2,4-оксадиазол-3-ил)этил)-3-(4-хлорфенил)-4-(3-(трифторметил)фенил)имидазолидин-2-он;
(S)-3-(4-хлорфенил)-1-(2-(5-(пиридин-3-ил)-1,2,4-оксадиазол-3-ил)этил)-4-(3-(трифторметил)фенил)имидазолидин-2-он;
(S)-3-(4-(4-хлорфенокси)фенил)-1-(2-(морфолиносульфонил)этил)-4-(3-(трифторметил)фенил)имидазолидин-2-он;
(S)-3-(3-(4-(4-хлорфенокси)фенил)-2-оксо-4-(3-(трифторметил)фенил)имидазолидин-1-ил)пропан-1-сульфонамид;
(S)-3-(4-(4-хлорфенокси)фенил)-1-(2-(4-метилпиперазин-1-илсульфонил)этил)-4-(3-(трифторметил)фенил)имидазолидин-2-он;
(S)-2-(3-(4-(4-хлорфенокси)фенил)-2-оксо-4-(3-(трифторметил)фенил)имидазолидин-1-ил)-N-(2-гидроксиэтил)этансульфонамид;
(S)-2-(3-(4-(4-хлорфенокси)фенил)-2-оксо-4-(3-(трифторметил)фенил)имидазолидин-1-ил)-N,N-бис-(2-гидроксиэтил)этансульфонамид;
(S)-2-(3-(4-(4-хлорфенокси)фенил)-4-(3-метоксифенил)-2-оксоимидазолидин-1-ил)этансульфонамид;
(S)-2-(3-(4-(4-хлорфенокси)фенил)-4-(3-(2-гидроксиэтокси)фенил)-2-оксоимидазолидин-1-ил)этансульфонамид;
(S)-N-(2-(3-(4-(4-хлорфенокси)фенил)-2-оксо-4-(3-(трифторметил)фенил)имидазолидин-1-ил)этилсульфонил)ацетамид;
(S)-3-(4-(4-хлорфенокси)фенил)-4-(3-(2-гидроксиэтокси)фенил)-1-(2-(метилсульфонил)этил)имидазолидин-2-он;
трет-бутил-4-((2-((S)-3-(4-(4-хлорфенокси)фенил)-4-(3-(трифторметил)фенил)-2-оксоимидазолидин-1-ил)этил)сульфонил)пиперазин-1-карбоксилат;
(S)-3-(4-(4-хлорфенокси)фенил)-4-(3-(трифторметил)фенил)-1-(2-((пиперазин-1-ил)сульфонил)этил)имидазолидин-2-он;
(S)-3-(4-хлорфенил)-1-(2-(морфолиносульфонил)этил)-4-(3-(пиридазин-3-илокси)фенил)имидазолидин-2-он;
(S)-3-(4-хлорфенил)-1-(2-(4-метилпиперазин-1-илсульфонил)этил)-4-(3-(пиридазин-3-илокси)фенил)имидазолидин-2-он;
(S)-3-(4-хлорфенил)-4-(3-(пиридазин-3-илокси)фенил)-1-(2-(пирролидин-1-илсульфонил)этил)имидазолидин-2-он;
(S)-2-(3-(4-хлорфенил)-2-оксо-4-(3-(пиридазин-3-илокси)фенил)имидазолидин-1-ил)этансульфонамид;
(S)-3-(4-хлорфенил)-4-(3-(2-гидроксиэтокси)фенил)-1-(2-(метилсульфонил)этил)имидазолидин-2-он;
(S)-3-(4-хлорфенил)-4-(3-(2-гидроксиэтокси)фенил)-1-(2-(морфолиносульфонил)этил)имидазолидин-2-он;
(S)-3-(4-хлорфенил)-4-(3-(2-гидроксиэтокси)фенил)-1-(2-(4-метилпиперазин-1-илсульфонил)этил)имидазолидин-2-он;
(S)-3-(4-хлорфенил)-4-(3-(2-гидроксиэтокси)фенил)-1-(2-(пирролидин-1-илсульфонил)этил)имидазолидин-2-он;
(S)-2-(3-(4-хлорфенил)-4-(3-(2-гидроксиэтокси)фенил)-2-оксоимидазолидин-1-ил)этансульфонамид;
(S)-3-(4-(4-хлорфенокси)фенил)-1-(2-(метилсульфонил)этил)-4-(3-(пиразин-2-илокси)фенил)имидазолидин-2-он;
(S)-2-(3-(4-(4-хлорфенокси)фенил)-2-оксо-4-(3-(пиразин-2-илокси)фенил)имидазолидин-1-ил)этансульфонамид;
(S)-3-(5-(4-хлорфенокси)пиразин-2-ил)-4-(3-метоксифенил)-1-(2-(метилсульфонил)этил)имидазолидин-2-он;
(S)-1-(2-(азетидин-1-илсульфонил)этил)-3-(4-(4-хлорфенокси)фенил)-4-(3-(трифторметил)фенил)имидазолидин-2-он;
(S)-1-(2-(азетидин-1-илсульфонил)этил)-3-(4-хлорфенил)-4-(3-(пиридазин-3-илокси)фенил)имидазолидин-2-он;
(S)-3-(4-(4-хлорфенокси)фенил)-1-(4-(метилсульфонил)фенил)-4-(3-(трифторметил)фенил)имидазолидин-2-он;
(S)-3-(4-хлорфенил)-1-(4-(метилсульфонил)фенил)-4-(3-(пиридазин-3-илокси)фенил)имидазолидин-2-он;
(S)-4-(3-(4-(4-хлорфенокси)фенил)-2-оксо-4-(3-(трифторметил)фенил)имидазолидин-1-ил)бензолсульфонамид;
(S)-4-(3-(4-хлорфенил)-2-оксо-4-(3-(пиридазин-3-илокси)фенил)имидазолидин-1-ил)бензолсульфонамид;
(S)-метил-3-(3-(4-(4-хлорфенокси)фенил)-2-оксо-4-(3-(трифторметил)фенил)имидазолидин-1-ил)пропаноат;
(S)-3-(4-хлорфенил)-1-(2-(метилсульфонил)этил)-4-(3-(трифторметил)фенил)имидазолидин-2-он;
(S)-3-(3-(4-(4-хлорфенокси)фенил)-2-оксо-4-(3-(трифторметил)фенил)имидазолидин-1-ил)пропанамид;
(S)-3-(4-хлорфенил)-1-(пиразин-2-ил)-4-(3-(пиразин-2-илокси)фенил)имидазолидин-2-он;
(S)-3-(4-хлорфенил)-1-(2-(метилсульфонил)этил)-4-(3-(пиридин-2-илокси)фенил)имидазолидин-2-он;
(4S)-3-(4-(4-хлорфенокси)фенил)-1-(2-(1-метилпирролидин-2-ил)этил)-4-(3-(трифторметил)фенил)имидазолидин-2-он;
(S)-1-(2-(1,3-диоксан-2-ил)этил)-3-(4-(4-хлорфенокси)фенил)-4-(3-(трифторметил)фенил)имидазолидин-2-он;
3-(4-(4-хлорфенокси)фенил)-1-(2-(2-оксопирролидин-1-ил)этил)-4-(3-(трифторметил)фенил)имидазолидин-2-он;
3-(2-(3-(4-(4-хлорфенокси)фенил)-2-оксо-4-(3-(трифторметил)фенил)имидазолидин-1-ил)этил)оксазолидин-2-он;
1-(2-(1H-пиразол-1-ил)этил)-3-(4-(4-хлорфенокси)фенил)-4-(3-(трифторметил)фенил)имидазолидин-2-он;
1-(2-(1H-имидазол-1-ил)этил)-3-(4-(4-хлорфенокси)фенил)-4-(3-(трифторметил)фенил)имидазолидин-2-он;
(S)-3-(4-хлорфенил)-1-(2-(метилсульфонил)этил)-4-(3-(пиразин-2-илокси)фенил)имидазолидин-2-он;
(S)-2-(3-(4-хлорфенил)-2-оксо-4-(3-(пиразин-2-илокси)фенил)имидазолидин-1-ил)этансульфонамид;
(S)-3-(4-хлорфенил)-4-(3-(пиразин-2-илокси)фенил)-1-(2-(пирролидин-1-илсульфонил)этил)имидазолидин-2-он;
(S)-3-(4-хлорфенил)-1-(2-(морфолиносульфонил)этил)-4-(3-(пиразин-2-илокси)фенил)имидазолидин-2-он;
(S)-3-(4-хлорфенил)-1-(2-(4-метилпиперазин-1-илсульфонил)этил)-4-(3-(пиразин-2-илокси)фенил)имидазолидин-2-он;
(S)-3-(4-хлорфенил)-1-(2-(пиперазин-1-илсульфонил)этил)-4-(3-(пиразин-2-илокси)фенил)имидазолидин-2-он;
(S)-1-(2-(1,3-диоксан-2-ил)этил)-3-(4-хлорфенил)-4-(3-(пиразин-2-илокси)фенил)имидазолидин-2-он;
(S)-3-(4-(4-хлорфенокси)фенил)-4-(3-метоксифенил)-1-(2-(метилсульфонил)этил)имидазолидин-2-он;
(S)-3-(3-(4-хлорфенил)-2-оксо-4-(3-(пиразин-2-илокси)фенил)имидазолидин-1-ил)пропанамид;
(S)-1-(2-(1H-1,2,4-триазол-3-ил)этил)-3-(4-хлорфенил)-4-(3-(пиразин-2-илокси)фенил)имидазолидин-2-он;
(S)-3-(3-(3-(4-хлорфенил)-1-(2-(метилсульфонил)этил)-2-оксоимидазолидин-4-ил)фенокси)пиразин-2-карбонитрил;
(S)-3-(4-хлорфенил)-4-(3-(3-этилпиразин-2-илокси)фенил)-1-(2-(метилсульфонил)этил)имидазолидин-2-он и
(S)-4-(3-(5-аминопиразин-2-илокси)фенил)-3-(4-хлорфенил)-1-(2-(метилсульфонил)этил)имидазолидин-2-он.
8. Способ лечения заболевания, опосредованного каннабиноидным рецептором 1, включающий введение пациенту, нуждающемуся в таком лечении, соединения по любому из пп.1-7 в терапевтически эффективном количестве.
9. Способ по п.8, в котором заболевание, опосредованное каннабиноидным рецептором 1, представляет собой нарушение приема пищи, связанное с избыточным потреблением пищи.
10. Способ по п.9, в котором нарушение приема пищи, связанное с избыточным потреблением пищи, выбрано из ожирения, нейрогенной булимии и принудительных нарушений приема пищи.
11. Способ по п.10, в котором нарушение приема пищи, связанное с избыточным потреблением пищи, представляет собой ожирение.
12. Способ профилактики ожирения у пациента с риском ожирения, включающий введение указанному пациенту от около 0,001 до около 100 мг на 1 кг соединения, выбранного из соединения по любому из пп.1-7.
13. Фармацевтическая композиция, включающая фармацевтически приемлемый носитель и соединение, выбранное из соединения по любому из пп.1-7.
14. Применение соединения для изготовления лекарственного средства, предназначенного для лечения заболевания, опосредованного каннабиноидным рецептором 1 человека, у пациента, нуждающегося в таком лечении, где указанное соединение выбрано из соединения по любому из пп.1-7.
15. Применение по п.14, в котором заболевание, опосредованное каннабиноидным рецептором 1, выбрано из метаболических нарушений, а также состояний, связанных с метаболическими нарушениями, включая ожирение, нейрогенную булимию, принудительные нарушения приема пищи, диабет, атеросклероз, гипертензию, остеопороз, поликистозное заболевание яичников, сердечно-сосудистое заболевание, остеоартрит, дерматологические нарушения, гипертензию, резистентность к инсулину, гиперхолестеринемию, гипертриглицеридемию, желчно-каменную болезнь и нарушения сна и гиперлипидемические состояния; или психических нарушений, таких как злоупотребление веществами, психоз, депрессия, беспокойство, стресс, эпилепсия, мания и шизофрения; или когнитивных нарушений, таких как слабоумие, включая болезнь Альцгеймера, слабая память, потеря краткосрочной памяти и нарушения дефицита внимания; или нейродегенеративных нарушений, таких как болезнь Паркинсона, церебральный паралич и черепно-мозговая травма, гипотензия, катаболизм вместе с легочной дисфункцией и недостаточностью вентиляции; или сердечной дисфункции, включая клапанное заболевание, инфаркт миокарда, гипертрофию сердца и острую сердечную недостаточность; или общего нарушения легочной функции, отторжения трансплантата, ревматоидного артрита, мигрени, невропатии, рассеянного склероза, синдрома Гийена-Барре, воспалительных последствий вирусного энцефалита, церебральных васкулярных травм, воспалительного заболевания кишечника, волчанки, заболевания "трансплантат против хозяина", Т-клеточного заболевания гиперчувствительности, псориаза, остеопороза, астмы, тироидита Хашимото, синдрома Гийена-Барре, рака, контактного дерматита, аллергического ринита, ишемической или реперфузионной травмы, травмы головы и нарушений движений.
16. Применение по п.15, в котором заболевание, опосредованное каннабиноидным рецептором 1, представляет собой нарушение приема пищи, связанное с избыточным потреблением пищи.
17. Применение по п.16, в котором нарушение приема пищи, связанное с избыточным потреблением пищи, выбрано из ожирения, нейрогенной булимии и принудительных нарушений приема пищи.
18. Применение по п.17, в котором нарушение приема пищи, связанное с избыточным потреблением пищи, представляет собой ожирение.
19. Применение соединения по любому из пп.1-7 для изготовления лекарственного средства для профилактики ожирения у пациента с риском ожирения.
Текст
СОЕДИНЕНИЯ И КОМПОЗИЦИИ В КАЧЕСТВЕ ИНГИБИТОРОВ АКТИВНОСТИ КАННАБИНОИДНОГО РЕЦЕПТОРА 1 Настоящее изобретение относится к соединениям, фармацевтическим композициям, содержащим такие соединения, и к способам применения таких соединений для лечения или профилактики заболеваний или нарушений, связанных с активностью каннабиноидного рецептора 1 (СВ 1). 017696 Ссылки на заявки-аналоги Данная заявка является продолжением заявки US 60/870339, поданной 15.12.2006, и заявки US 60/953595, поданной 02.08.2007. Полное описание этих заявок приведено здесь полностью и во всех целях в качестве ссылки. Область изобретения Изобретение относится к соединениям, фармацевтическим композициям, включающим такие соединения, и к способам применения таких соединений для лечения или профилактики заболеваний или нарушений, связанных с активностью каннабиноидного рецептора 1 (СВ 1). Уровень техники Каннабиноиды являются психоактивными ингредиентами марихуаны, в основном 9 тетрагидроканнабинол. Клонированы два каннабиноидных рецептора, СВ 1 и СВ 2. СВ 1 преимущественно экспрессируется в центральной нервной системе, тогда как СВ 2 экспрессируется в периферийных тканях, главным образом в иммунной системе. Оба рецептора являются членами класса, связанного с Gбелком, и их ингибирование связано с активностью аденилатциклазы. Новые соединения настоящего изобретения ингибируют активность СВ 1 и, следовательно, как предполагается, являются полезными для лечения заболеваний или нарушений, связанных с CB1, таких как, но не ограничиваясь ими, психоз, слабая память, когнитивные нарушения, мигрень, невропатия,нейровоспалительные нарушения, травмы сосудов головного мозга, травма головы, беспокойство, злоупотребление веществами (такими как курение), стресс, эпилепсия, болезнь Паркинсона, шизофрения,остеопороз, запор, хроническая кишечная псевдонепроходимость, цирроз печени, астма, ожирение и другие нарушения, связанные с избыточным потреблением пищи. Сущность изобретения В одном варианте осуществления настоящее изобретение относится к соединению формулы IR1a выбран из водорода, циано, C1-6 алкила, цианозамещенного C1-6 алкила, С 2-6 алкенила, -X1R12,-X1NR13S(O)2R13, -X1OS(O)2R13, -X1NR13X1OR13, -X1OR13, -X1C(O)OR13, -X1S(O)2R12, -X1S(O)2NR13C(O)R13,-X1S(O)2R13,-X1C(O)R12,-X1NR13R13,-X1S(O)2NR13R13,-X1OC(O)NR13R13,-X1C(O)NR12R13,-X1NR13X1C(O)NR12,-X1NR13X1C(O)NR13R13,-X1C(O)NR13X1C(O)OR13,-X1C(O)NR13X1NR13R13,-X1C(O)NR13X1OR13 и -X1C(O)NR13R13; где R12 выбран из С 6-10 арила, С 5-10 гетероарила, С 3-12 циклоалкила и С 3-10 гетероциклоалкила; где указанный арил, гетероарил, циклоалкил или гетероциклоалкил в R12 необязательно замещен 1-3 радикалами, независимо выбранными из гидрокси, бис-гидрокси-С 1-6 алкиламино,C1-6 алкиламино, С 1-6 алкила, С 1-6 алкокси, С 1-6 алкоксикарбонила, С 1-6 алкилсульфокси, С 1-6 алкилкарбокси,С 1-6 алкилсульфонила, галогензамещенного С 1-6 алкила, галогензамещенного С 1-6 алкокси, С 3-12 циклоалкила, С 3-10 гетероциклоалкила, C5-10 гетероарила и С 6-10 арила, необязательно замещенного 1-3 радикалами галогена; где указанные циклоалкильные, гетероциклоалкильные, гетероарильные и арильные заместители в R12 могут быть далее необязательно замещены 1-3 С 1-6 алкильными радикалами; где каждый R13 независимо выбран из водорода, С 1-6 алкила, гидрокси-С 1-6 алкила,С 6-10 арила, С 3-10 гетероциклоалкила; где указанный арил или гетероциклоалкил в R13 необязательно замещен группой, выбранной из С 1-6 алкила и С 1-6 алкокси; где каждый X1 независимо выбран из связи и С 1-4 алкилена; где любой алкил в R1 необязательно замещен циано;R2a выбран из водорода, С 1-6 алкила, галогензамещенного С 1-6 алкила, С 6-10 арила, -X2NR14X2NR14R14,-X2NR14C(O)X2NR14C(O)OR14,-X2NR14X2R15,-X2OC(O)NR14R14,-X2OC(O)NR14R15,-X2NR14R14,-X2NR14S(O)2R14, -X2NR14S(O)2R15, -X2S(O)0-2R15, -X2NR14C(O)R14, -X2NR14C(O)R15, -X2NR14C(O)X2NR14R14,-X2OSi(R14)3, -X2OC(O)NR14R15, -X2C(O)OR14, -X2OR14, -X2OX2R15, -X2R15 и -X2C(O)R15; где каждый R14 независимо выбран из водорода и С 1-6 алкила; R15 выбран из циано, С 6-10 арила, C5-10 гетероарила, С 3-12 циклоалкила и С 3-10 гетероциклоалкила; где указанный арил, гетероарил, циклоалкил или гетероциклоалкил вR15 необязательно замещен 1-3 радикалами, независимо выбранными из гидрокси, С 1-6 алкила, С 1-6 алкокси, С 1-6 алкилсульфокси, галогензамещенного С 1-6 алкила, галогензамещенного С 1-6 алкокси, -X3NR16R16,-X3ONR16R16, -X3OR16, -X3S(O)2R16, -X3NR16C(O)OR16, -X3NR16S(O)0-2R16, -X3R16, -X3C(O)OR16,-X3C(O)NR16R16, -X3OC(O)NR16R16, -X3S(O)0-2NR16R16, -X3C(O)R16, C6-10 арила и С 5-10 гетероарила; где указанные арильные и гетероарильные заместители в R15 необязательно замещены 1-3 радикалами галогена; каждый Х 2 и Х 3 независимо выбран из связи и С 1-4 алкилена; и каждый R16 независимо выбран из водорода, С 1-6 алкила, С 6-10 арила, С 5-10 гетероарила, С 3-8 циклоалкила и С 3-12 гетероциклоалкила; где любой арил,гетероарил, циклоалкил или гетероциклоалкил в R16 необязательно замещен 1-3 радикалами, независимо выбранными из галогена, циано, С 1-6 алкила, C1-6 алкилкарбониламино и С 1-6 алкокси;R2b выбран из водорода и С 1-6 алкила; или R2a и R2b вместе с атомом углерода, к которому R2a и R2b присоединены, образуют карбонил;R4 выбран из водорода, галогена, гидрокси, С 1-6 алкила, С 1-6 алкокси, галогензамещенного С 1-6 алкила,галогензамещенного С 1-6 алкокси, гидроксизамещенного С 1-6 алкила, гидроксизамещенного С 1-6 алкокси,цианозамещенного С 1-6 алкила, цианозамещенного С 1-6 алкокси, -OX5R4a и -OX5R4a; где Х 5 выбран из связи и С 1-4 алкилена; R4a выбран из С 1-6 алкила, С 3-8 циклоалкила, С 6-10 арила и С 6-10 гетероарила; где любой циклоалкил, арил или гетероарил в R4a необязательно замещен 1-3 радикалами, независимо выбранными из галогена, циано, амино, С 1-6 алкила, С 1-6 алкокси, галогензамещенного С 1-6 алкила, галогензамещенного С 1-6 алкокси, гидроксизамещенного С 1-6 алкила, гидроксизамещенного С 1-6 алкокси, цианозамещенного С 1-6 алкила и цианозамещенного С 1-6 алкокси;R10 выбран из галогена, циано, С 1-6 алкила, С 1-6 алкокси, галогензамещенного C1-6 алкила, галогензамещенного С 1-6 алкокси, -X4OR17, -X4S(O)0-2R17 и -X4R17; где X4 выбран из связи и С 1-4 алкилена; и R17 выбран из С 6-10 арила и С 5-10 гетероарила; где R17 необязательно замещен 1-3 радикалами галогена; и его фармацевтически приемлемым солям, гидратам, сольватам и изомерам. Во втором варианте осуществления настоящее изобретение относится к фармацевтической композиции, которая включает соединение формулы I или его N-оксидное производное, индивидуальные изомеры и смесь изомеров; или его фармацевтически приемлемую соль, в смеси с одним или несколькими подходящими эксципиентами. В третьем варианте осуществления настоящее изобретение относится к способу лечения заболевания у животного, в котором модулирование активности СВ 1 может предотвращать, ингибировать или улучшать патологию и/или симптоматику заболеваний, который включает введение животному терапевтически эффективного количества соединения формулы I или его N-оксидного производного, индивидуальных изомеров и смеси изомеров, или его фармацевтически приемлемой соли. В четвертом варианте осуществления настоящее изобретение относится к применению соединения формулы I для изготовления лекарственного средства для лечения заболевания у животного, в котором активность СВ 1 участвует в патологии и/или симптоматике заболевания. В пятом варианте осуществления настоящее изобретение относится к способу получения соединений формулы I и их N-оксидных производных, пролекарственных производных, защищенных производных, индивидуальных изомеров и смеси этих изомеров и их фармацевтически приемлемых солей. Подробное описание изобретения Определения"Алкил" как группа и в качестве структурного элемента других групп, например галогензамещенного алкила и алкокси, может быть линейным или разветвленным. С 1-6 алкокси включает метокси, этокси и им подобные. Галогензамещенный алкил включает трифторметил, пентафторэтил и им подобные."Арил" обозначает моноциклический или конденсированный бициклический ароматический кольцевой комплекс, содержащий от шести до десяти атомов углерода в кольце. Например, арил может представлять собой фенил или нафтил, предпочтительно фенил. "Арилен" обозначает двухвалентный радикал, полученный из арильной группы. "Гетероарил" является таким, как определено для арила, где один или несколько членов кольца являются гетероатомом, выбранным из -О-, -N=, -NR-, -С(О)-, -S-, -S(O)или -S(O)2-, где R представляет собой водород, С 1-4 алкил или защитную группу для азота. Например, С 1-10 гетероарил включает пиридил, индолил, индазолил, хиноксалинил, хинолинил, бензофуранил, бензопиранил, бензотиопиранил, бензо[1,3]диоксол, имидазолил, бензоимидазолил, пиримидинил, фуранил, оксазолил, изоксазолил, триазолил, тетразолил, пиразолил, тиенил, 1 Н-пиридин-2-онил, 6-оксо-1,6 дигидропиридин-3-ил и т.д. "С 6-10 арилС 0-4 алкил" обозначает арил, как описано выше, присоединенный через алкиленовую группу. Например, С 6-10 арилС 0-4 алкил включает фенэтил, бензил и т.д. Гетероарил также включает N-оксидные производные, например пиридин-N-оксидные производные следующей структуры:"Циклоалкил" обозначает насыщенный или частично ненасыщенный, моноциклический, конденсированный бициклический или мостиковый полициклический кольцевой комплекс, содержащий указанное количество атомов в кольце. Например, С 3-10 циклоалкил включает циклопропил, циклобутил, циклопентил, циклогексил и т.д. "Гетероциклоалкил" обозначает циклоалкил, как определено в настоящем описании, при условии, что один или несколько указанных атомов углерода в кольце замещены группой,выбранной из -О-, -N=, -NR-, -С(О)-, -S-, -S(O)- или -S(O)2-, где R представляет собой водород, С 1-4 алкил или защитную группу для атома азота. Например, С 3-8 гетероциклоалкил, как используется в настоящем описании для описания соединений по изобретению, включает морфолино, пирролидинил, пиперазинил,пиперидинил, пиперидинилон, 1,4-диокса-8-азаспиро[4.5]дец-8-ил, 2-оксопирролидин-1-ил, 2-оксопиперидин-1-ил и т.д."Галоген" (или гало) предпочтительно представляет собой хлор или фтор, но также может быть бром или йод."Лечить", "излечение" и "лечение" относятся к способу облегчения или ослабления заболевания и/или сопровождающих его симптомов. Описание предпочтительных вариантов осуществления Настоящее изобретение относится к соединениям, композициям и способам лечения заболеваний, в которых ингибирование активности СВ 1 может предотвращать, ингибировать или улучшать патологию и/или симптоматику заболеваний, которые включают введение животному терапевтически эффективного количества соединения формулы I. В одном варианте осуществления в отношении соединений формулы I, R1a выбран из циано, метилкарбониламиносульфонилэтила, пирролидин-2-онилэтила, имидазолилэтила, оксазолидин-2-онилэтила,1-пиразолилэтила, цианометила, 4'-(4-хлорфенокси)фенила, 1,3-диоксанилэтила, аллила, фенила, пиразинила, пиперазинилсульфонилэтила, азетидинилсульфонилэтила, морфолиносульфонилэтила, пирролидинилсульфонилэтила, пирролидинилпропила, пирролидинилэтила, пиперазинилпропила, пиперидинилсульфонилэтила, пиридазинила, (5-(4-метоксифенил)-1,2,4-оксадиазол-3-ил)метила, изоксазолила, пиперидинилкарбонилметила, 3-(N,N-бис-(4-метоксифенил)сульфамоил)пропила, метилфенилсульфонила,цианометила, 2-оксо-2-(пиперидин-1-иламино)этила, пропиламинокарбонилметила, 2-(карбоксиметиламино)-2-оксоэтила, бис-гидроксиэтиламиносульфонилэтила, карбоксиметиламинокарбонилметила, аминокарбонилэтила, аминосульфонилэтила, аминосульфонилпропила, метиламиноэтила, пиперидинилэтила, пиперазинилэтила, метилсульфонилэтила, карбоксиметила, тетразолметила, бензила, 1,2,4 оксадиазола, 1,2,4-оксадиазолметила, 1,2,4-оксадиазолэтила, изоксазолметила, 2-(2-гидроксиэтиламино)2-оксоэтила, диметиламиноэтиламинокарбонилметила, гидроксилэтила, метоксиэтила, гидроксилэтиламиноэтила, морфолиноэтила, метилпиперазинилэтила, 2-(карбамоилокси)этила, метилсульфонилоксиэтила, морфолинокарбонилметила, метилсульфонилпиперазинилэтила, 2-морфолиноэтила, аминоэтила,2-(3,3-диметилуреидо)этила, морфолинокарбониламиноэтила, метилсульфониламиноэтила, пиридинилметила, гидроксилпропила, 2-(2,6-диметилморфолино)этила, 2-(2-метилморфолино)этила, метилсульфонилпропила и морфолинопропила; где указанные кольцевые системы в R1a необязательно замещены 1-3 радикалами, независимо выбранными из галогена, трифторметила, метила, бис-гидроксиэтиламина, третбутила, трет-бутоксикарбонила, гидрокси, метилсульфонила, аминосульфонила, диэтиламино, морфолино, циклогексила, пиридинила, пиперидинила, пирролидинила, пиперазинила, необязательно замещенного этилом или метилсульфонилом, метоксикарбонила и метокси; и R1b выбран из водорода и аллила. В другом варианте осуществления R2a выбран из (4-(азепан-1-илметил)-1 Н-1,2,3-триазол-1 ил)метила, диэтиламинопирролидинилметила, N,N-метил-(трет-бутоксикарбонил)аминопирролидинилметила, (4-(5-цианопиридин-2-ил)пиперазин-1-ил)метила, 5-цианопиридинилоксиметила, (4-(6-метоксипиридин-3-ил)-3-оксопиперазин-1-ил)метила, (4-(6-метоксипиридин-2-ил)-3-оксопиперазин-1-ил)метила,(4-(6-метоксипиридин-2-ил)пиперазин-1-ил)метила, 4-трет-бутоксикарбонил-2-оксопиперазин-1-ил)метила, (4-(4-фторпиридин-2-ил)пиперазин-1-ил)метила, 5-(1-(трет-бутоксикарбонил)пиперидин-4-ил)-2 Нтетразол-2-илметила,5-(1-(трет-бутоксикарбонил)пиперидин-4-ил)-2 Н-тетразол-1-илметила,третбутоксикарбонилпиперидинилметила, 4-(4-цианофенил)-1 Н-1,2,3-триазол-1-ила, 4-(пиридин-3-ил)-1 Н 1,2,3-триазол-1-ила, 4-тетрагидрофуран-3-илокси)метил)-1 Н-1,2,3-триазол-1-ила, 5-фенил-2 Н-тетразол 2-ила, 4-оксадиазолилпиперидинилметила, 4-(бензилоксикарбонил)-2-оксопиперазин-1-ила, 4-(1-метил 1 Н-имидазол-5-ил)-1 Н-1,2,3-триазол-1-ила, 4-(3-метил-1,2,4-оксадиазол-5-ил)-1 Н-1,2,3-триазол-1-ила, 4 этокси-1 Н-1,2,3-триазол-1-ила, 4-(5-метил-1,3,4-оксадиазол-2-ил)-1 Н-1,2,3-триазол-1-ила, 5-(2-этокси-2 оксоэтил)-2 Н-тетразол-2-ила, 5-(гидроксиэтил)-2 Н-тетразол-2-ила, (4-(пиперидин-1-илкарбамоил)-1 Н 1,2,3-триазол-1-ил)метила, 1-тетрагидро-2 Н-пиран-4-ил)метил)-1 Н-1,2,3-триазол-4-ила, 5-(6-метоксипиридин-3-ил)-2 Н-тетразол-2-илметила, 5-(пиридин-3-ил)-2 Н-тетразол-2-илметила, (3-(тетрагидрофуран 3-ил)изоксазол-5-ил)метила,5-(морфолиноэтил)-2 Н-тетразол-2-ила,(4-(этоксикарбонил)-1 Н-1,2,3 триазол-1-ил)метила, этилсульфонилпиперазинилметила, (4-(этилсульфонилметил)-1 Н-1,2,3-триазол-1-3 017696 ил)метила, метила, метилпиперазинилметила, диметиламиноэтиламинометила, аминометила, метилсульфониламинометила, метоксикарбонила, этоксикарбонила, фенила, гидроксиметила, метоксиметила,морфолинометила, фенилсульфонилметила, диметиламинокарбонилпиперазинилметила, диметиламиносульфонилпиперазинилметила,пиперидинилметила,трет-бутилкарбамоилметила,трет-бутоксикарбониламинопиперидинилметила, фенилсульфониламинометила, (4-(тетрагидрофуран-2-карбонил) пиперазин-1-ил)метила, (4-тетрагидрофуран-2-ил)метил)пиперазин-1-ил)метила, хлорметила, морфолиноэтилпиперазинилметила, трет-бутоксикарбониламинопирролидинилметила, тиоморфолинометила,аминопирролидинилметила,пиперазинилметила,бензиламинометила,бензилоксиметила,4 фторбензилоксиметила,2,4-дифторбензилоксиметила,(4-(3,5-дифторфенил)-1 Н-1,2,3-триазол-1 ил)метила, диметиламинометила, морфолиноуреидометила, (4-метилсульфониламинометил-1 Н-1,2,3 триазол-1-ил)метила, морфолинокарбонила, пропаргиламинометила, фенилсульфанилметила, пиридинилметиламинометила, (4-(диметиламинометил)-1 Н-1,2,3-триазол-1-ил)метила, пиримидинилпиперазинилметила, фенилпиразонилметила, (2-(трет-бутоксикарбониламино)-3-метилбутанамидо)метила, (2 амино-3-метилбутанамидо)метила, (4-(3-фторфенил)-1H-1,2,3-триазол-1-ил)метила, (изопропилкарбамоилокси)метила, трет-бутил)(диметил)силокси)метила, имидазолилпропиламинометила, (3-(2 оксопирролидин-1-ил)пропиламино)метила, пирролидинилэтиламинометила, пирролидинилпропиламинометила, (циклогексилкарбамоилокси)метила, (бензо[d][1,3]диоксол-5-илкарбамоилокси)метила, (1,3 диоксоизоиндолин-2-ил)метила, метилкарбониламинометила, (3-этилуреидо)метила, (тетрагидро-2 Нпиран-2-илокси)метила, трет-бутоксикарбонилпиперазинилметила, пиридинилэтиламинометила, метилкарбонилпиперазинилметила, пиридинилпиперазинилметила, метоксикарбонилпиперазинилметила,этоксикарбонилпиперазинилметила,пиперидинилметил-2 Н-тетразол-2-ила,5-хлорпиридинил-2 оксиметила, 4-фенилпиперидинилметила, 4-(пиримидин-2-ил)пиперидинилметила, (5-(пиразин-2-ил)-2 Нтетразол-2-ил)метила, (5-(пиридин-2-ил)-2 Н-тетразол-2-ил)метила, (5-(пиридин-2-ил)-1 Н-тетразол-1 ил)метила,5-(6-метилпиридин-3-ил)-1 Н-тетразол-1-ил)метила,(5-(пиримидин-2-ил)-2 Н-тетразол-2 ил)метила, (4-(пиразин-2-ил)пиперазин-1-ил)метила, 4-(пиридин-2-ил)пиперидинилметила, 3-третбутоксикарбониламинопирролидинилметила, (5-(6-хлорпиридин-3-ил)-2 Н-тетразол-2-ил)метила, пиперидинилметил-1 Н-1,2,3-триазол-1-илметила, 4-метилпиперидинилметил-1 Н-1,2,3-триазол-1-илметила, 4 изопропиламинометил-1H-1,2,3-триазол-1-илметила, 4-фенил-1 Н-имидазол-1-ила, 1H-1,2,3-триазол-1 илметила, 5-(этоксикарбонил)-2 Н-тетразол-2-ила, (4-(3,5-диметилфенил)-3-оксопиперазин-1-ил)метила,(5-(имидазо[1,2-а]пиридин-6-ил)-2 Н-тетразол-2-ил)метила, 4-гидрокси-4-фенилпиперидинилметила, 4 гидрокси-4-(4-хлорфенил)пиперидинилметила, (5-метил-2-оксопиридин-1(2 Н)-ил)метила, 4-метилпиридинил-2-оксиметила,4-этокси-1 Н-1,2,3-триазол-1-илметила,морфолинометил-1 Н-1,2,3-триазол-1 илметила,диэтиламиноэтил-1 Н-1,2,3-триазол-1-илметила,пиперидинилэтил-1 Н-1,2,3-триазол-1 илметила,пиперидинилметил-1 Н-1,2,3-триазол-1-илметила,диэтиламиноэтил-1 Н-1,2,3-триазол-1 илметила, изопропилэтил-1 Н-1,2,3-триазол-1-илметила, (4-3-метил-1 Н-пиразол-1-ил)метил)-1 Н-1,2,3 триазол-1-ил)метила, (4-4-метил-1 Н-пиразол-1-ил)метил)-1 Н-1,2,3-триазол-1-ил)метила, ацетамидофенил-1 Н-1,2,3-триазол-1-илметила, ацетил-1 Н-1,2,3-триазол-1-илметила, циклогексилметил-1 Н-1,2,3 триазол-1-илметила, тиенил-1 Н-1,2,3-триазол-1-илметила, (2-оксо-4-(пиридин-2-ил)пиперазин-1-ил)метила, (4-(2-метоксифенил)-1 Н-1,2,3-триазол-1-ил)метила, (4-(3-фторфенил)-1 Н-1,2,3-триазол-1-ил)метила, (4-(трет-бутоксикарбонил)-1,4-диазепан-1-ил)метила, этоксикарбонилпиперидинилметила и изобутоксикарбонилпиперазинилметила; и R2b выбран из водорода и метила; или R2a и R2b вместе с атомом углерода, к которому R2a и R2b присоединены, образуют карбонил. В другом варианте осуществления R3, R5, R6 и R7, каждый независимо, выбран из водорода, галогена и амино. В другом вариант осуществления R4 выбран из водорода; трифторметила; галогена; гидрокси; цианометокси; диметиламинопропила; циано; циклопропилметокси; пиразинилокси, необязательно замещенного амино; пиридинилокси; пиримидинилокси; бензокси; фенокси, необязательно замещенного метилом или циано; этокси; тетразолилметокси, необязательно замещенного метилом; пиридазинилокси; пиразинилокси; гидроксиэтокси и метокси. В другом варианте осуществления R8, R9, R11 и R12a, каждый независимо, выбран из водорода, галогена, трифторметила и метила. В другом варианте осуществления R10 выбран из галогена, циано, метокси, трифторметила, пиридинилокси, бензоила, фенокси, бензила, пиридазинилокси, фенилсульфонила и пиримидинилокси; где указанный пиридинилокси, фенилсульфонил, фенокси, бензоил, бензил, пиридазинилокси и пиримидинилокси может быть необязательно замещен 1-3 радикалами галогена. В другом варианте осуществления описаны соединения, выбранные из следующих соединений: 1-[4-(4-хлорфенокси)фенил]-5-фенилпирролидин-2-он; 5-(4-амино-3-трифторметилфенил)-1-[4-(4-хлорфенокси)фенил]пирролидин-2-он; 1-[4-(4-хлорфенокси)фенил]-5-(3-трифторметилфенил)пирролидин-2-он;(S)-4-(3-(5-аминопиразин-2-илокси)фенил)-3-(4-хлорфенил)-1-(2-(метилсульфонил)этил)имидазолидин-2-он. Другой вариант осуществления относится к способу лечения заболевания, опосредованного каннабиноидным рецептором 1 (например, пищевое нарушение, связанное с избыточным приемом пищи, такие как ожирение, нейрогенная булимия и принудительные пищевые нарушения), включающему введение пациенту, нуждающемуся в таком лечении, терапевтически эффективного количества соединения,выбранного из раздела сущность изобретения (выше). Другой вариант осуществления относится к способу профилактики ожирения у пациента с риском ожирения, включающему введение указанному пациенту от около 0,001 до около 100 мг на 1 кг соединения, выбранного из раздела сущность изобретения (выше). Другие предпочтительные соединения по изобретению подробно описаны далее в примерах и таблице I. Фармакология и полезность Соединения по изобретению ингибируют активность СВ 1 и, таким образом, являются полезными для лечения заболеваний или нарушений, в которых активность СВ 1 участвует в патологии и/или симптоматике заболевания. Настоящее изобретение также относится к соединениям настоящего изобретения для применения при изготовлении лекарственных средств для лечения заболеваний или нарушений, в которых активность СВ 1 участвует в патологии и/или симптоматике заболевания. Заболевания или состояния, связанные с СВ 1, включают, но не ограничиваются ими, метаболические нарушения, а также состояния, связанные с метаболическими нарушениями, включая ожирение, нейрогенную булимию, принудительные нарушения приема пищи, диабет, атеросклероз, гипертензию, поликистозное заболевание яичников, остеопороз, сердечно-сосудистое заболевание, остеоартрит, дерматологические нарушения,гипертензию, инсулиновую резистентность, гиперхолестеринемию, гипертриглицеридемию, желчнокаменную болезнь и нарушения сна и гиперлипидемические состояния; или психические нарушения,такие как злоупотребление веществами, психоз, депрессия, беспокойство, стресс, эпилепсия, мания и шизофрения; или когнитивные нарушения, такие как слабоумие, включая болезнь Альцгеймера, недостаток памяти, потеря длительной памяти и нарушения дефицита внимания; или нейродегенеративные нарушения, такие как болезнь Паркинсона, церебральный паралич и черепно-мозговая травма, гипотензия,катаболизм вместе с легочной дисфункцией и недостаточностью вентиляции; или сердечная дисфункция,включая клапанное заболевание, инфаркт миокарды, гипертрофия сердца и острая сердечная недостаточность; или общее нарушение легочной функции, отторжение трансплантата, ревматоидный артрит,мигрень, невропатия, рассеянный склероз, синдром Гийена-Барре, воспалительные последствия вирусного энцефалита, церебральные васкулярные травмы, воспалительное заболевание кишечника, волчанка,- 18017696 заболевание "трансплантат против хозяина", Т-клеточное заболевание гиперчувствительности, псориаз,астма, тироидит Хашимото, синдром Гийена-Барре, рак, контактный дерматит, аллергический ринит,ишемическая или реперфузионная травма, травма головы и нарушения движения. Соединения также полезны для лечения нарушений, связанных со злоупотреблением веществами, особенно опиатами, спиртом, марихуаной и никотином, включая курение. Соединения также полезны для лечения нарушений приема пищи подавлением избыточного потребления пищи, и в результате ожирения и связанных с ним осложнений, включая гипертрофию левого желудочка. Соединения также полезны для лечения запора и хронической псевдонепроходимости кишечника, а также для лечения астмы, остеопороза и цирроза печени. Марихуана и ее производные использовались веками в медицинских и развлекательных целях. Было установлено, что основным активным ингредиентом в марихуане и гашише является 9 тетрагидроканнабинол (9-ТНС). Биологическое действие 9-ТНС и других членов каннабиноидного семейства осуществляется двумя рецепторами, связанными с G-белком, названными CB1 и СВ 2. Рецептор СВ 1 главным образом обнаружен в центральной и периферийной нервной системе и в меньшей степени в некоторых периферийных органах. Рецептор СВ 2 обнаружен главным образом в лимфоидных тканях и клетках. Были идентифицированы три эндогенных лиганда для каннабиноидных рецепторов, полученных из арахидоновой кислоты(анандамид, 2-арахидоноилглицерин и 2-арахидонильный эфир глицерина). Каждый является агонистом с активностями, аналогичными 9-ТНС, включая седацию, гипотермию, кишечную неподвижность, антиноцицепцию, аналгезию, каталепсию, противорвотное действие и стимуляцию аппетита. Гены для каждого из соответствующих каннабиноидных рецепторов были блокированы у мыши. Мыши с блокированным рецептором СВ 1 оказались нормальными и способными к размножению. Они являлись резистентными к действию 9-ТНС и демонстрировали сильное снижение укрепляющих свойств морфина и степени тяжести синдрома зависимости. Они также демонстрировали пониженную моторную активность и гипоалгезию. Мыши с блокированным рецептором СВ 2 также являлись здоровыми и способными к размножению. Они не являлись резистентными к опосредованным центральной нервной системой действиям вводимого 9-ТНС. Наблюдались некоторые действия на активацию иммунных клеток, усиление роли рецептора СВ 2 на функции иммунной системы. Избыточное воздействие на 9-ТНС может привести к перееданию, психозу, гипотермии, потери памяти и седации. Лечение астмы модуляторами рецептора СВ 1 (такими как обратные агонисты СВ 1) основано на обнаружении того, что пресинаптические каннабиноидные рецепторы СВ 1 медиируют ингибирование высвобождения норадреналина. Лечение цирроза печени модуляторами рецептора СВ 1 основано на обнаружении того, что модулятор рецептора СВ 1 меняет низкое кровяное давление, наблюдаемое у крыс с циррозом печени, вызванным тетрахлористым углеродом, и снижает повышенный брыжеечный поток крови и давление воротной вены. В соответствии с вышеизложенным настоящее изобретение также относится к способу профилактики или лечения любых описанных выше заболеваний или нарушений у субъекта, нуждающегося в таком лечении, который включает введение указанному субъекту терапевтически эффективного количества (см. раздел "Введение и фармацевтические композиции" далее) соединения формулы I или его фармацевтически приемлемой соли. Для любого из указанных выше применений, необходимая дозировка будет изменяться в зависимости от способа введения, конкретного излечиваемого состояния и желаемого эффекта. Введение и фармацевтические композиции Обычно соединения по изобретению вводят в терапевтически эффективных количествах любыми обычными и приемлемыми способами, известными из уровня техники, отдельно или в комбинации с одним или несколькими терапевтическими агентами. Терапевтически эффективное количество может широко варьироваться в зависимости от степени тяжести заболевания, возраста и относительного здоровья субъекта, активности используемого соединения и других факторов. Обычно удовлетворительные результаты получают при систематических суточных дозировках от около 0,03 до 2,5 мг/кг веса тела. Показанная суточная дозировка для большего млекопитающего, например для людей, находится в диапазоне от около 0,5 до около 100 мг, которая обычно вводится, например, раздельными дозами вплоть до четырех раз в день или в замедленной форме. Подходящие единичные дозированные формы для перорального введения включают от около 1 до 50 мг активного ингредиента. Соединения по изобретению могут вводиться в форме фармацевтических композиций любым обычным способом, в частности энтерально, например перорально, например в форме таблеток или капсул, или парентерально, например в форме инъекционных растворов или суспензий, местно, например в форме лосьонов, гелей, мазей или кремов, или в назальной или суппозитарной форме. Фармацевтические композиции, включающие соединение настоящего изобретения в свободной форме или в форме фармацевтически приемлемой соли вместе по крайней мере с одним фармацевтически приемлемым носителем- 19017696 или разбавителем, могут быть изготовлены обычными способами смешения, гранулирования или покрытия. Например, пероральными композициями могут быть таблетки или желатиновые капсулы, содержащие активный ингредиент вместе с а) разбавителями, например лактозой, декстрозой, сахарозой, маннитом, сорбитом, целлюлозой и/или глицином; б) лубрикантами, например оксидом кремния, тальком,стеариновой кислотой, ее солью магния или кальция и/или полиэтиленгликолем; для таблеток также в) связующими, например магнийалюмосиликатом, крахмальной пастой, желатином, трагакантом, метилцеллюлозой, натрийкарбоксиметилцеллюлозой и/или поливинилпирролидоном; при необходимости г) разрыхлителями, например крахмалами, агаром, альгиновой кислотой или ее натриевой солью, или смесями для сухого шипучего напитка; и/или д) абсорбентами, красителями, отдушками и подсластителями. Инъекционными композициями могут быть водные изотонические растворы или суспензии, и суппозитории могут быть получены из жирных эмульсий или суспензий. Композиции могут быть стерилизованы и/или содержать адъюванты, такие как консервирующие, стабилизирующие, увлажняющие или эмульгирующие агенты, промоторы раствора, соли для регулирования осмотического давления и/или буферы. Кроме того, они также могут содержать другие терапевтически активные вещества. Подходящие составы для трансдермальных применений включают эффективное количество соединения настоящего изобретения с носителем. Носитель может включать абсорбируемые фармакологически приемлемые растворители для обеспечения проникновения через кожу пациента. Например, трансдермальные устройства выполнены в форме бандажа, включающего подложку, емкость, содержащую соединение, необязательно с носителями, необязательно барьер для контроля скорости доставки соединения на кожу пациента с контролируемой и предварительно заданной скоростью в течение пролонгированного периода времени, и средства для удержания устройства на коже. Вязкие трансдермальные составы также могут использоваться. Подходящими составами для местного применения, например на кожу и в глаза, предпочтительно являются водные растворы, мази, кремы или гели, хорошо известные из предшествующего уровня техники. Они могут содержать солюбилизаторы, стабилизаторы, повышающие тоничность агенты, буферы и консерванты. Соединения по изобретению могут вводиться в терапевтически эффективных количествах в комбинации с одним или несколькими терапевтическими агентами (фармацевтические комбинации). Например, синергетические действия могут возникать с другими веществами, использующимися для лечения заболеваний или нарушений, таких как психоз, слабая память, когнитивные нарушения, мигрень, невропатия, нейровоспалительные нарушения, церебральные васкулярные травмы, травма головы, беспокойства, стресс, эпилепсия, болезнь Паркинсона, шизофрения, злоупотребление веществами, такое как курение, остеопороз, запор, хроническая псевдонепроходимость кишечника, цирроз печени, астма, ожирение и другие нарушения приема пищи, связанные с избыточным потреблением пищи, ожирение и т.д. (см. раздел "Фармакология и полезность" выше). Когда соединения по изобретению вводят в сочетании с другими лекарственными препаратами, дозировки совместно вводимых соединений, конечно, будут зависеть от вида совместно вводимого лекарственного препарата, от конкретного используемого лекарственного препарата, от излечиваемого состояния и прочих условий. Объединенный состав или фармацевтическая композиция может включать соединение по изобретению, как определено выше, или его фармацевтически приемлемую соль и по крайней мере один активный ингредиент, выбранный из а) антидиабетических агентов, таких как инсулин, производные и миметики инсулина; вещества,повышающие секрецию инсулина, такие как сульфонилмочевины, например глипизид, глибурид и амарил; лиганды инсулинотропного рецептора сульфонилмочевины, такие как меглитиниды, например натеглинид и репаглинид; вещества, повышающие чувствительность к инсулину, такие как ингибиторы протеинтирозинфосфатазы-1B (РТР-1B), такие как РТР-112; ингибиторы GSK3 (гликогенсинтазакиназа 3), такие как SB-517955, SB-4195052, SB-216763, NN-57-05441 и NN-57-05445; лиганды RXR, такие какGW-0791 и AGN-194204; ингибиторы натрийзависимых сотранспортеров глюкозы, такие как Т-1095; ингибиторы гликогенфосфорилазы А, такие как BAY R3401; бигуаниды, такие как метформин; ингибиторы -глюкозидазы, такие как акарбоза; GLP-1 (глюкагоноподобный пептид-1), аналоги GLP-1, такие как эксендин-4, и миметики GLP-1; ингибиторы ДПП IV (дипептидилпептидазы IV), такие как DPP728,LAF237 (вилдаглиптин - пример 1 WO 00/34241), MK-0431, саксаглиптин, GSK23A; разрушители AGE; производное тиазолидона (глитазон), такие как пиоглитазон, розиглитазон или (R)-1-4-[5-метил-2-(4 трифторметилфенил)оксазол-4-илметокси]бензолсульфонил-2,3-дигидро-1H-индол-2-карбоновая кислота, описанная в заявке WO 03/043985, как соединение 19 примера 4, -агонист неглитазонового типаPPAR, например GI-262570; ингибиторы диацилглицеринацетилтрансферазы (DGAT), такие как соединения, описанные в WO 2005044250, WO 2005013907, WO 2004094618 и WO 2004047755; б) гиполипидемических агентов, таких как ингибиторы 3-гидрокси-3-метилглутарилкоэнзим AUS 3983140, велостатин, флувастатин, далвастатин, аторвастатин, розувастатин и аналогичные соединения статина, описанные в US 5753675, ривастатин, пиразольные аналоги мевалонолактонных производных, как описано в US 4613610, инденовые аналоги мевалонолактонных производных, как описано в WO 86/03488, 6-[2-(замещенный-пиррол-1-ил)алкил)пиран-2-оны и их производные, как описано в US 4647576, Searle's SC-45355 (3-замещенное производное пентандионовой кислоты)дихлорацетат, имидазольные аналоги мевалонолактона, как описано в WO 86/07054, производные 3-карбокси-2 гидроксипропанфосфониевой кислоты, как описано в FR 2596393, производные 2,3-дизамещенного пиррола, фурана и тиофена, как описано в ЕР 0221025, нафтильные аналоги мевалонолактона, как описано вUS 4686237, октагидронафталены, такие как описано в US 4499289, кетоаналоги мевинолина (ловастатин), как описано в ЕР 0142146 А 2, и хинолиновые и пиридиновые производные, описанные в US 5506219 и 5691322. Кроме того, соединения фосфиновой кислоты, полезные для ингибирования HMG СоА редуктазы, подходящие для применения здесь, описаны в GB 2205837; ингибиторы скваленсинтазы; лиганды FXR (фарнезоидный X рецептор) и LXR (рецептор печени X); холестирамин; фибраты; никотиновая кислота и аспирин; в) агента против ожирения или агента, регулирующего аппетит, таких как агонисты рецептора меланокортина (MC4R), антагонисты меланин-концентрирующего гормонального рецептора (MCHR), антагонисты рецептора, повышающего секрецию гормона роста (GHSR), модуляторы рецептора галанина,антагонисты орексина, агонисты CCK, агонисты GLP-1 и другие пептиды из Pre-проглюкагона; антагонисты NPY1 или NPY5, модуляторы NPY2 и NPY4, агонисты кортикотропинвысвобождающего фактора,модуляторы рецептора гистамина-3 (Н 3), ингибиторы аР 2, модуляторы -PPAR, модуляторы -PPAR,ингибиторы ацетил-СоА карбоксилазы (АСС), ингибиторы 11HSD-1, модуляторы рецептора адинопектина; агонисты -3 адренергического рецептора, такие как AJ9677 (Takeda/Dainippon), L750355(Merck) или СР 331648 (Pfizer) или другие известные агонисты -3, как описано в US 5541204, 5770615,5491134, 5776983 и 5488064, модулятор -тироидного рецептора, такой как лиганд тироидного рецептора, как описано в WO 97/21993 (U. Cal SF), WO 99/00353 (KaroBio) и GB 98/284425 (KaroBio), ингибиторSCD-1, как описано в WO 2005011655, ингибитор липазы, такой как орлистат или ATL-962 (Alizyme),агонисты рецептора серотонина, (например, BVT-933 (Biovitrum, ингибиторы захвата моноамина или высвобождающие агенты, такие как фенфлурамин, дексфенфлурамин, флувоксамин, флуоксетин, пароксетин, сертралин, хлорфентермин, клофорекс, клортермин, пицилорекс, сибутрамин, дексамфетамин,фентермин, фенилпропаноламин или мазиндол, аноректические агенты, такие как топирамат (JohnsonJohnson), CNTF (цилиарный нейротропный фактор)/Axokine (Regeneron), BDNF (нейротропный фактор мозга), лептин и модуляторы рецептора лептина, фентермин, лептин, бромкриптин, дексамфетамин, амфетамин, фенфлурамин, дексфенфлурамин, сибутрамин, орлистат, дексфенфлурамин, мазиндол, фентермин, фендиметразин, диэтилпропион, флуоксетин, бупропион, топирамат, диэтилпропион, бензфетамин,фенилпропаноламин или экопипам, эфедрин, псевдоэфедрин; г) антигипертензивных агентов, таких как петлевые диуретики, такие как этакриновая кислота, фуросемид и торсемид; диуретики, такие как тиазидные производные, хлортиазид, гидрохлортиазид, амилорид; ингибиторы ангиотензинпревращающего фермента (АСЕ), такие как беназеприл, каптоприл, эналаприл, фозиноприл, лизиноприл, моексиприл, периндоприл, хинаприл, рамиприл и трандолаприл; ингибиторы Na-K-АТФазного мембранного насоса, такие как дигоксин; ингибиторы нейтралэндопептидазыACE/NEP, такие как омапатрилат, сампатрилат и фазидотрил; антагонисты ангиотензина II, такие как кандесартан, эпросартан, ирбесартан, лосартан, телмисартан и вальсартан, в частности валсартан; ингибиторы ренина, такие как алискирен, терлакирен, дитекирен, RO 66-1132, RO-66-1168; блокаторы адренергического рецептора, такие как ацебутолол, атенолол, бетаксолол, бисопролол, метопролол, надолол, пропранолол, соталол и тимолол; инотропные агенты, такие как дигоксин, добутамин и милринон; блокаторы кальциевого канала, такие как амлодипин, бепридил, дилтиазем, фелодипин, никардипин, нимодипин, нифедипин, низолдипин и верапамил; антагонисты альдостеронового рецептора; ингибиторы альдостеронсинтазы и двойные антагонисты ET/AII, такие, как описано в WO 00/01389; д) соединения, повышающего HDL; е) модулятора абсорбции холестерина, такого как Zetia и KT6-971; ж) аналогов и миметиков Аро-А 1; з) ингибиторов тромбина, таких как ксимелагатран; и) ингибиторов альдостерона, таких как анастразол, фадразол, эплеренон; к) ингибиторов агрегации тромбицитов, таких как аспирин, клопидогрел бисульфат; л) эстрогена, тестостерона, селективного модулятора эстрогенового рецептора, селективного модулятора андрогенового рецептора; м) химиотерапевтического агента, такого как ингибиторы ароматазы, например фемара, антиэстрогены, ингибиторы топоизомеразы I, ингибиторы топоизомеразы II, микротубулярные активные агенты,алкилирующие агенты, антинеопластические антиметаболиты, соединения платины, соединения, снижающие активность протеинкиназы, такие как ингибитор PDGF рецептора тирозинкиназы, предпочти- 21017696 тельно иматиниб (N-5-[4-(4-метилпиперазинометил)бензоиламидо]-2-метилфенил-4-(3-пиридил)-2 пиримидинамин), описанный в ЕР-А-0564409 в примере 21, или 4-метил-N-[3-(4-метилимидазол-1-ил)5-трифторметилфенил]-3-(4-пиридин-3-илпиримидин-2-иламино)бензамид, описанный в WO 04/005281 в примере 92; и н) агента, взаимодействующего с рецептором 5-НТ 3, и/или агента, взаимодействующего с рецептором 5-НТ 4, такого как тегасерод, описанный в US 5510353 в примере 13, гидромалеат тегасерода, цисаприд, цилансетрон; о) агента для лечения табакозависимости, например частичные агонисты никотинового рецептора,гипохлорид бупропиона (также известный под товарным знаком Zyban) и агенты никотинзамещающей терапии; п) агента для лечения эректильной дисфункции, например допаминергические агенты, такие как апоморфин), агенты ADD/ADHD (например, Ritalin, Strattera, Concerta и Adderall); р) агента для лечения алкоголизма, такого как опиоидные антагонисты (например, налтрексон (также известный под товарным знаком ReVia) и налмефен), дисульфирам (также известный под товарным знаком Antabuse) и акампросат (также известный под товарным знаком Campral. Кроме того, также могут вводиться совместно агенты для снижения симптомов алкогольной зависимости, такие как бензодиазепины, -блокаторы, клонидин, карбамазепин, прегабалин и габапентин (Neurontin); с) других агентов, которые являются полезными, включая противовоспалительные агенты (например, ингибиторы СОХ-2); антидепрессанты (например, гидрохлорид флуоксетина (Prozac; агенты,улучшающие когнитивное восприятие (например, гидрохлорид донепезила (Aircept) и другие ингибиторы ацетилхолинэстеразы); нейропротекторные агенты (например, мемантин); антипсихотические лекарственные средства (например, зипразидон (Geodon), рисперидон (Risperdal) и оланзапин (Zyprexa; или в каждом случае их фармацевтически приемлемые соли и необязательно фармацевтически приемлемый носитель. Изобретение также относится к фармацевтическим комбинациям, например набору, включающему а) первый агент, который представляет собой соединение по изобретению, как здесь описано, в свободной форме или в форме фармацевтически приемлемой соли, и б) по крайней мере один совместно вводимый агент. Набор может включать инструкции для его применения. Термины "совместное введение", или "объединенное введение", или им подобные используются здесь для обозначения введения выбранных терапевтических агентов отдельному пациенту и включают режимы лечения, в которых агенты необязательно вводятся одним и тем же путем введения или в одно и то же время. Термин "фармацевтическая комбинация", как здесь используется, обозначает продукт, который получают смешением или объединением более одного активного ингредиента, и включает фиксированные и нефиксированные комбинации активных ингредиентов. Термин "фиксированная комбинация" обозначает, что активные ингредиенты, например соединение формулы I и совместно вводимый агент, оба вводятся пациенту одновременно в форме одного целого или одной дозировки. Термин "нефиксированная комбинация" обозначает, что активные ингредиенты, например соединение формулы I и совместно вводимый агент, оба вводятся пациенту раздельными частями совместно, одновременно или последовательно в неограниченном периоде времени, где такое введение обеспечивает терапевтически эффективные уровни двух соединений в организме пациента. Последнее также включает коктейльную терапию, например введение трех или более активных ингредиентов. Способы получения соединений по изобретению Настоящее изобретение также включает способы получения соединений по изобретению. В описанных реакциях может быть необходимо защитить реакционные функциональные группы, например гидрокси, амино, имино, тио или карбоксигруппы, где они присутствуют в конечных продуктах, для устранения их нежелательного участия в реакциях. Обычные защитные группы могут использоваться в соответствии со стандартной практикой, например см. книгу T.W. Greene и P.G.M. Wuts, "Protective Groupsin Organic Chemistry", John Wiley and Sons, 1991. На следующих схемах приведены некоторые способы получения соединений настоящего изобретения. Специалисту в данной области техники ясно, что эти способы являются иллюстрирующими и никоим образом не исключают все способы получения соединений настоящего изобретения. Радикалы на схемах являются такими, как описано в разделе сущность изобретения (выше). В каждых схемах реакций ниже R1 представляет собой 4-хлорфенил. Иллюстрация синтеза соединений настоящего изобретения формулы I приведена ниже на схеме реакций. Иллюстрация синтеза соединений настоящего изобретения формулы I, в которых Z2=CH2 и Z1=O,приведена на схеме 1. Ангидрид янтарной кислоты (I-а, n=1) или ангидрид глутаровой кислоты (I-b, n=2) может быть превращен в соединение I-c кипячением с обратным холодильником с обозначенным анилином в толуоле с последующей циклизацией, которая опосредована тионилхлоридом. Восстановление соединения I-c с помощью DIBAL в CH2Cl2 при низкой температуре (предпочтительно при -78 С) приводит к получению соединения I-d, которое затем подвергают реакции Фриделя-Крафтца с подходящим ареном в кислотных условиях с получением соединения I-е. Схема 2 Иллюстрация синтеза соединений настоящего изобретения формулы I, в которых Z2=О и Z1=O,приведена на схеме 2. Оксазолидинон II-b может быть получен асимметричным аминогидроксилированием Шарплесса алкена II-а с последующей циклизацией в основных условиях (статья N. Barta и др., Org.Lett., 2000, 2, с. 2821). 3-Арилоксазолидиноны II-с затем могут быть получены катализируемым медьюN-арилированием соединения II-b. Для методик асимметричного аминогидроксилирования Шарплесса см. статьи Sharpless K.В. и др., 1996. N-Halocarbamate salts lead to more efficient catalytic asymmetric aminohydroxylation." Angew. Chem. Int. Ed. Engl., 35(23/24), cc. 2813-2816; Sharpless, K.В. и др., 1998. "Fromstyrols to enantiopure -arylglycines in two steps". J. Am. Chem. Soc, 120, cc. 1207-17. Для реакция карадизируемого медью N-арилирования см. статью: Buchwald S.L. и др., 2001. "A general and efficient copper Иллюстрация асимметричного синтеза 1,5-диарилимидазолидин-2-она приведена на схеме 3. Гидроксикарбамат III-b может быть получен стандартным способом аминогидроксилирования Шарплесса. Тозилирование спирта с последующим нуклеофильным замещением азидом натрия приводят к получению азида III-d, который затем может превращаться в соединение III-е последующими гидрированием,восстановительным аминированием с помощью n-метоксибензальдегида с последующей циклизацией insitu. Полученный имидазолидин-2-он III-е затем подвергают катализируемому медью N-арилированию с получением имидазолидин-2-она III-f, который затем после кислотного снятия защитных групп с nметоксибензильной группы приводит к получению соединения III-g. Альтернативный асимметричный синтез 1,5-диарилимидазолидин-2-она приведен на схеме 4. Стирол IV-a превращают в аминоспирт IV-c стандартной реакцией асимметричного аминогидроксилирования Шарплесса (АА) с последующим гидролизом для удаления защитной группы Cbz. Бистозилирование соединения IV-c с последующей циклизацией in situ приводит к получению тозилактивированного азиридина IV-d, который подвергают LilO4-катализируемой реакции с раскрытием кольца с обращением конфигурации с помощью анилина Ar1NH2 с получением промежуточного соединения IV-e (статьяYadav, J.S.; Reddy, В.V.S.; Jyothirmai, В.; Murty, M.S.R., Synlett, 2002, с. 53). Соединение IV-e легко циклизуется с помощью трифосгена с получением соединения IV-f. Магниевое восстановительное расщепление группы N-Ts в соединении IV-f приводит к получению целевого 1,5-диарилимидазолидин-2-онаIV-g. Синтез рацемической формы соединения IV-g осуществляют тем же способом с некоторыми упрощениями, в котором рацемический азиридин может быть получен непосредственно из стирола IV-a катализируемой йодом реакцией азиридирования, используя хлорамин-Т в качестве источника азота (статья Иллюстрация асимметричного синтеза 5-замещенных-4-арилоксазолидинонов приведена на схеме 5. Соединение V-b получают стандартным способом аминогидроксилирования Шарплесса (статья K.L.Reddy и K.В. Sharpless, J. Am. Chem. Soc, 1998, 120, с. 1207). С промежуточного карбамата затем снимали защитные группы в стандартных кислотных условиях, который затем после превращения в оксазолидинон V-c с помощью карбонилдиимидазола или подходящего эквивалента. Катализируемое медью Nарилирование приводит к получению соединения V-d. Карбоксилатный эфир затем восстанавливают натрийборгидридом с получением спирта V-e, который затем может быть превращен в соединение V-f нуклеофильным замещением соответствующего мезилата с подходящим нуклеофилом (например, амины,тиол и т.д.). Альтернативный синтез 5-замещенных 4-арилоксазолидинонов показан на схеме 6. Сложный эфир оксазолидинон-5-карбоновой кислоты VI-a обрабатывают боргидридом натрия с получением промежуточного спирта, который затем превращают в тетрагидропираниловый (ТНР) эфир VI-b. Катализируемое медью N-арилирование приводит к получению соединения VI-c, которое затем подвергают кислотному снятию защитных групп с группы ТНР, с последующим мезилированием и нуклеофильным замещением Иллюстрация асимметричного синтеза морфолинонов приведена на схеме 7. После асимметричного аминогидроксилирования стирола VII-а осуществляют конверсию в простой эфир VII-c. После снятия защитных групп трет-бутоксикарбаматной группы осуществляют катализируемую основанием циклизацию с получением морфолинона VII-d. Катализируемое медью N-арилирование приводит к получению морфолинона VII-e. Схема 8 Иллюстрация превращения оксазолидинона VIII-а в соответствующие 1,2,3-триазольные производные VIII-c приведена на схеме 8. Спирт VIII-а сначала превращают в нужный мезилат, который затем обрабатывают азидом натрия с получением азида VIII-b. Азид затем подвергают катализируемому медью наращиванию цикла с помощью алкина RCCH с получением триазола VIII-c. Для эффективного синтеза 1,2,3-триазолов из азида и алкина см. статью P. Wu, А.K. Feldman, А.K. Nugent, С.J. Hawker, A. Scheel, В.to Triazole Dendrimers via the Cu(I)-Catalyzed Ligation of Azides and Alkynes, Angew. Chem. Int. Ed., 2004,43, с 3928. Для эффективного синтеза тетразолов из азида и нитрила см. статьи: Z.P. Demko и K.В. Sharpless, An Intramolecular [2+3] Cycloaddition Route to Fused 5-Heterosubstituted Tetrazoles, Org. Lett., 2001, 3,с 4091; Z.P. Demko и K.В. Sharpless, Preparation of 5-Substituted-1H-Tetrazoles from Nitriles in Boga, J. Org.Chem., 2001, 66, с. 7945. Для обзора соответствующей химии лекарственных средств см. статьи Н.С. Kolb и K.В. Sharpless, The Growing Impact of Click Chemistry on Drug Discovery, Drug Discovery Today, 2003, 8,с. 1128; H.С Kolb, M.G. Finn и K.В. Sharpless, Click Chemistry: Diverse Chemical Function From a Few Good Альтернативный рацемический синтез 1,5-диарилимидазолидин-2-она приведен на схеме 9. СтиролIX-а превращают в азиридин IX-b катализируемой йодом реакции азиридинирования, используя хлорамин-Т в качестве источника азота (статья Ando, Т.; Kano, D.; Minakata, S.; Ryu, I.; Komatsu, M., Tedrahedron, 1998, 54, с. 13485). Азиридин IX-b подвергают региоселективной реакции наращивания цикла с помощью арилизоцианата OCN-Ar2 с получением соединения IX-с (статья Nadir, U.K.; Basu, N., Tedrahedron Lett., 1992, 33, с. 7949). Магниевое восстановительное расщепление группы Ts приводило к получению целевого 1,5-диарилимидазолидин-2-она IX-d. Схема 10 Иллюстрация синтеза 1,5-диарилимидазолидин-2,4-диона приведена на схеме 10. NАриламинокислоту Х-b получали из -аминокислоты Х-а и арилгалогенида катализируемой CuI реакцией конденсации, описанной в статье Ma, D.; Zhang, Y.; Yao, J.; Wu, S.; Tao, F.J., Am. Chem. Soc, 1998, 120,с. 12459. Соединение X-b циклизуют с помощью цианата калия в кислотной среде с получением 1,5 диарилимидазолидин-2,4-диона Х-с. Схема 11 Иллюстрация асимметричного синтеза 5-арилзамещенного пирролидин-2-она структуры XI-h приведена на схеме 11. N-Boc-защищенные -арилглицины XI-c легко получают стандартным двухстадийным методом Шарплесса из стиролов XI-а (статья K.L. Reddy и K.В. Sharpless, J. Am. Chem. Soc, 1998,120, с. 1207). Моноалкилатную кислоту Мельдрума XI-е получали из соединения XI-c конденсацией с кислотой Мельдрума с последующим окончательным восстановлением его кетогруппы (статьи М.Hin, P. Majer и Т. Tsukamoto, J. Org. Chem., 2002, 67, с. 7365). Соединение XI-е подвергают термическому раскрытию кольца до N-Вос-защищенного 3-карбоксипирролидин-2-она XI-f, который может быть далее превращен в 5-арилзамещенный пирролидин-2-он XI-g обработкой ТФУК. Катализируемое медью IVарилирование Бушвальда приводит к получению соединения XI-h с хорошим выходом. Альтернативный асимметричный синтез 5-арилзамещенного пирролидин-2-она структуры XII-g приведен на схеме 12. -Кетоэфир XII-с может быть получен с помощью Rh-катализируемого хелатного гидроацилирования ароматического альдегида XII-а с помощью метилакрилата XII-b (статья Eun-Ae Jo иChul-Ho Jum, Eur. J. Org. Chem., 2006, cc. 2504-2507). Асимметричное восстановление соединения XII-с,используя (-)-В-хлордиизопинокамфенилборан -)-DIP-хлорид), приводит к получению гидроксильного эфира XII-d, который затем превращают в соответствующий лактон XII-е (статья Р.V. Ramachandran, S.Pitre и Н.С. Brown, J. Org. Chem., 2002, 67, cc. 5315-5319). Амидирование Вейнреба и циклодегидратация Мицунобу приводит к получению 5-арилзамещенного пирролидин-2-она с хорошим выходом и энантиомерной чистотой (статья I.M. Bell, D.С. Beshore, S.N. Gallicchio и Т.М. Williams, Tetrahedron Lett., 2000,41, cc. 1141-1145). Недавно было описано несколько новых синтетических способов, которые обеспечивают более доступную катализируемую медью перекрестную конденсацию большинства азотсодержащих функциональных групп в sp2-галогениды (статья Ley и др., Angew. Chem. Int. Ed., 2003, 42, с. 5400). Большая часть этих новых способов осуществляется с различными объемными медными хелаторами, которые обеспечивают более легкую конструкцию связей sp2-углерод-гетероатом (Buchwald и др., J. Org. Chem.,2004, 59, с. 5578 и приведенные там ссылки). Несмотря на эти преимущества, относительно высокий нагрев (100 С) и длительное время реакции (24 ч) все еще затрудняют получить хорошие результаты. Следовательно, все еще существует потребность в способах с улучшенной реакционностью, более широким объемом реакции и субстратной толерантностью. Поскольку для большинства групп используют эффекты лиганда донора для улучшения перекрестной конденсации, не уделяется внимания другим важным компонентам реакции. Неочевидное замещение обычных оснований (K2CO3, K3PO4, Cs2CO3) более мягким фторидом цезия катализирует конденсацию ряда амидов, карбаматов и азотсодержащих гетероциклов с арилйодидами, во многих случаях при комнатной температуре. Кроме того, субстраты, которые несовместимы с катализируемой медью реакцией, требующей более сильных оснований, могут быть совместимы с CsF. Оптимизированные условия для субстратов, которые не совместимы с обычными условиями (CuI,диамин, K3PO4 или K2CO3, 100-110 С), заменяли более простыми субстратами. Более слабые основания,такие как KHCO3, KOAc или CsF, будут устранять нежелательные побочные реакции. Использование этих оснований приводит к эффективной конденсации оксазолидинона 1 с арилйодидом 2 с получением продукта 3 с хорошим выходом при 100 С (схема 1). С фторидом цезия требуется только 2 ч, тогда как сKHCO3 и KOAc требуется 18 ч. Когда те же реагенты обрабатывают CsF при 25 С в течение 18 ч, получают выход соединения 3 около количественного. Другие эксперименты показали, что ТГФ, ACN илиEtOAc (табл. 2) являются оптимальными растворителями для этой реакции и что необходимо минимум 2-2,5 экв. CsF. Поскольку CsF показывает улучшенную стабильность для обеспечения CuIкатализируемой реакции в этой модельной системе, исследовали его способность промотировать конденсацию других субстратов.- 27017696 Схема 13 Модифицированные конденсации Бушвальда со слабыми основаниями Ряд контрольных реакций осуществляли для того, чтобы показать, что эффект может быть обусловлен не только наличием цезия или фторида, но синергией между CsF и CuI. Когда CsF заменяют KF,K2CO3 или Cs2CO3, выход существенно снижается при 25 С (табл. 3, номер 5-7) и при 100 С (табл. 3,номер 5). Эти пониженные выходы могут быть обусловлены пониженной растворимостью этих солей при комнатной температуре в этилацетате по сравнению с растворимостью CsF. Однако когда KF иK2CO3 объединены с субстехиометрическим количеством CsF, наблюдается 3,5-10-кратное повышение выхода (табл. 3, номер 8, 9). Эти результаты предполагают, что существует некоторое синергетическое действие между CsF и CuI для заметного повышения выхода. Таблица 2 Обзор растворителя для реакции N-арилирования, используя CsF в качестве основанияа% выделенного выхода; в 100 С, 16 ч; г определено по данным LC-MS. б 017696 Реакции некоторых амидов, относящихся к заявленным соединениям, с различными арилйодидами подробно описаны в табл. 4. Эти реакции осуществляли в 1 ммол. масштабе с 2,5 экв. CsF, 5 мол.% CuI и 10 ммол.% N,N'-диметилэтилендиамина в ТГФ или EtOAc, обычно в течение 18-24 ч. Было обнаружено,что большинство амидов и карбаматов конденсируются очень эффективно с арилйодидами с п- или мзаместителями при 25 С, и только 4u требует нагрева при 60 С (табл. 4). Эффективность этих условий в 10 ммол. масштабе показана при 60 С в примере 4b, показывая, что эти условия могут быть масштабированы. Электронодефицитные и электронодонорные арилгалогениды конденсируются с почти равной эффективностью в этих условиях. Везде наблюдали отличную толерантность и селективность к субстрату. Пример 4i примечателен тем, что в нем не наблюдалось обмена галогенида в этих условиях. Слегка пониженный выход для 4n может объясняться стерическим затруднением метильной группы или, возможно, немного более высоким значением pKa для исходного амида по сравнению с его дезметилированным аналогом. Проксимальная сложноэфирная группа в примере 4 о вероятно помогает образованию Cu-координированного промежуточного соединения, приводя к почти количественному выходу. Кроме того, в этих условиях не наблюдали ни рацемизации, ни гидролиза, но были проблемы с обычными основаниями. Арилгалогениды с o-заместителями, как известно, подавляют N-арилирование большинства субстратов; это ограничение преодолевается конденсацией этих субстратов при 85-100 С Амидирование арилбромидов приведено в табл. 5. Арил- и гетероарилбромиды обычно требуют более высоких температур реакции и/или более длительного времени реакции по сравнению с соответствующими арийодидами. Даже если ряд новых лигандов вводить несколькими группами для понижения этих барьеров, до настоящего времени это не было совсем успешным. Когда арилбромиды подвергают нашим промотируемым CsF условиям, мы получали результаты от хороших до отличных в большинстве случаев, когда субстраты обрабатывали при 100 С (табл. 5).
МПК / Метки
МПК: C07D 233/52, C07D 207/40, C07D 233/32, C07D 403/14, C07D 233/12, C07D 233/42, C07D 233/46, C07D 285/06, C07D 263/22, C07D 233/16, C07D 233/50, C07D 413/04, C07D 403/06, C07D 403/04, C07D 265/32
Метки: соединения, каннабиноидного, ингибиторов, рецептора, композиции, качестве, активности
Код ссылки
<a href="https://eas.patents.su/30-17696-soedineniya-i-kompozicii-v-kachestve-ingibitorov-aktivnosti-kannabinoidnogo-receptora-1.html" rel="bookmark" title="База патентов Евразийского Союза">Соединения и композиции в качестве ингибиторов активности каннабиноидного рецептора 1</a>
Предыдущий патент: Остекление
Следующий патент: Реконструированные поверхностно-активные вещества, имеющие улучшенные свойства
Случайный патент: Ребро радиатора и радиатор отопления












