Производные 2-бензилпиридазинона в качестве ингибиторов мет киназы
Номер патента: 21362
Опубликовано: 30.06.2015
Авторы: Шадт Оливер, Блаукат Андрее, Штибер Франк, Дорш Дитер
Формула / Реферат
1. Соединение формулы I
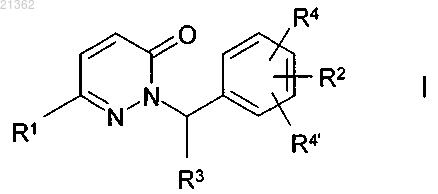
в которой
R1 означает Н или А,
R2 означает фурил, тиенил, пирролил, имидазолил, пиразолил, оксазолил, изоксазолил, тиазолил, изотиазолил, пиридил, пиримидинил, триазолил, тетразолил, оксадиазолил или тиадиазолил, каждый из которых является монозамещенным Hal, A, [C(R3)2]nN(R3)2, [C(R3)2]nHet, O[C(R3)2]nN(R3)2 или O[C(R3)2]nHet,
R3 означает Н, метил, этил или пропил,
R4, R4' означают Н,
Het означает пиперидинил, пиперазинил, пирролидинил, морфолинил, фурил, тиенил, пирролил, имидазолил, пиразолил, оксазолил, изоксазолил, тиазолил, изотиазолил, пиридил, пиримидинил, триазолил, тетразолил, оксадиазолил, тиадиазолил, пиридазинил или пиразинил, каждый из которых является монозамещенным А или [C(R3)2]nHet1,
Het1 означает пирролидин, пиперидин, пиперазин или морфолин, каждый из которых является незамещенным или моно- или дизамещенным А и/или =O (карбонильным кислородом),
А означает неразветвленный или разветвленный алкил, содержащий 1-8 атомов С, в котором 1-7 атомов Н может быть замещено F и/или Cl, или циклический алкил, содержащий 3-7 атомов С,
Hal означает F, Cl, Br или I,
n равно 0, 1, 2, 3 или 4,
и его фармацевтически пригодные соли, таутомеры и стереоизомеры, включая их смеси во всех соотношениях.
2. Соединение по п.1, выбранное из группы


и его фармацевтически пригодные соли, таутомеры и стереоизомеры, включая их смеси во всех соотношениях.
3. Способ получения соединения формулы I по пп.1-2 и его фармацевтически пригодных солей, таутомеров и стереоизомеров, характеризующийся тем, что соединение формулы II
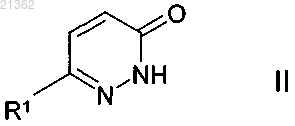
в которой R1 имеет значения, указанные в п.1, подвергают реакции с соединением формулы III
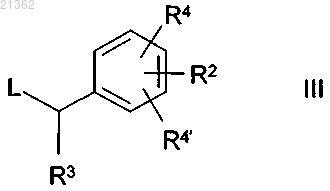
в которой R2, R3, R4 и R4' имеют значения, указанные в п.1, и L означает Cl, Br, I или свободную или реакционноспособную функционально-модифицированную ОН-группу,
где полученное соединение может быть выделено в свободном состоянии из одного из его функциональных производных путем обработки сольволизирующим или гидрогенолизирующим агентом и/или основание или кислота формулы I может быть превращена в одну из его(ее) солей.
4. Лекарственное средство, содержащее по меньшей мере одно соединение формулы I по пп.1-2 и/или его фармацевтически пригодные соли, таутомеры и стереоизомеры, включая их смеси во всех соотношениях, и необязательно наполнители и/или вспомогательные вещества.
5. Применение соединений по пп.1-2 и их фармацевтически пригодных солей, таутомеров и стереоизомеров, включая их смеси во всех соотношениях, для приготовления лекарственного средства для лечения заболеваний, на которые оказывает влияние ингибирование Met киназы соединениями по пп.1-2.
6. Применение по п.5, где заболевание, подвергаемое лечению, представляет собой солидную опухоль.
7. Применение по п.6, где солидная опухоль имеет происхождение из группы опухолей плоского эпителия, мочевого пузыря, желудка, почек, головы и шеи, пищевода, шейки матки, щитовидной железы, кишечника, печени, головного мозга, предстательной железы, мочеполового тракта, лимфатической системы, желудка, гортани и/или легкого.
8. Применение по п.6, где солидная опухоль имеет происхождение из группы моноцитарного лейкоза, аденокарциномы легкого, мелкоклеточного рака легкого, рака поджелудочной железы, глиобластом и рака молочной железы.
9. Применение по п.7, где солидная опухоль имеет происхождение из группы аденокарциномы легкого, мелкоклеточного рака легкого, рака поджелудочной железы, глиобластом, рака толстой кишки и рака молочной железы.
10. Применение по п.5, где заболевание, подвергаемое лечению, представляет собой опухоль крови и иммунной системы.
11. Применение по п.10, где опухоль имеет происхождение из группы острого миелоидного лейкоза, хронического миелоидного лейкоза, острого лимфолейкоза и/или хронического лимфолейкоза.
12. Лекарственное средство, содержащее по меньшей мере одно соединение формулы I по п.1 или 2 и/или его фармацевтически пригодные соли и стереоизомеры, включая их смеси во всех соотношениях, и по меньшей мере один дополнительный активный противораковый компонент лекарственного средства.
13. Комплект (набор), состоящий из отдельных пакетов:
(а) эффективного количества соединения формулы I по п.1 или 2 и/или его фармацевтически пригодных солей и стереоизомеров, включая их смеси во всех соотношениях, и
(б) эффективного количества дополнительного активного противоракового компонента лекарственного средства.
Текст
(71)(73) Заявитель и патентовладелец: МЕРК ПАТЕНТ ГМБХ (DE) Предпосылки создания изобретения Объектом изобретения является выявление новых соединений, обладающих ценными свойствами, в частности тех, которые могут применяться для приготовления лекарственных средств. Настоящее изобретение относится к соединениям и к применению соединений, которые принимают участие в ингибировании, регуляции и/или модуляции передачи сигналов с помощью киназ, в особенности тирозинкиназ и/или серин/треонинкиназ, а также к фармацевтическим композициям, которые содержат указанные соединения, и к применению соединений для лечения заболеваний, индуцированных киназой. В частности, настоящее изобретение относится к соединениям и к применению соединений, которые принимают участие в ингибировании, регуляции и/или модуляции передачи сигналов с помощьюMet киназы. Одним из основных механизмов, с помощью которого осуществляется клеточная регуляция, является передача внеклеточных сигналов через мембрану, что, в свою очередь, моделирует биохимические пути передачи сигналов в клетке. Фосфорилирование белков представляет собой один путь, с помощью которого внутриклеточные сигналы передаются от молекулы к молекуле, что в результате приводит к ответной реакции в клетке. Эти каскады передачи сигналов в высокой степени регулируются и часто перекрываются, очевидно, вследствие существования многих протеинкиназ, а также фосфатаз. Фосфорилирование белков преимущественно происходит в остатках серина, треонина или тирозина, поэтому протеинкиназы классифицируют по специфичности их участков фосфорилирования, т.е. серин/треониновые киназы и тирозинкиназы. Поскольку фосфорилирование представляет собой широко распространенный процесс в клетках, а фенотипы клеток значительно зависят от активности этих путей, то в настоящее время полагают, что многие болезненные состояния и/или заболевания могут быть вызваны или аберрантной активацией, или функциональными мутациями в молекулярных компонентах киназных каскадов. Следовательно, характеристике этих белков и соединений, способных модулировать их активность,уделяется пристальное внимание (для обзора см. Weinstein-Oppenheimer и др. Pharma.Therap., 2000,88, 229-279). Роль рецепторной тирозинкиназы Met в образовании и развитии опухолей у людей и возможность ингибирования HGF (фактор роста гепатоцитов)-зависимой активации Met описаны S. Berthou и др. вOncogene, т. 23,31, сс. 5387-5393 (2004). Ингибитор SU11274, раскрытый в этом источнике, пирролиндолиновое соединение, потенциально пригоден для борьбы со злокачественным новообразованием. Другой ингибитор Met киназы для лечения злокачественного новообразования описан J.G. Christensen и др. в Cancer Res. 2003, 63(21), 7345-55. Дальнейший ингибитор тирозинкиназы для борьбы со злокачественным новообразованием описан Н. Hov и др. в Clinical Cancer Research т. 10, 6686-6694 (2004). Соединение РНА-665752, производное индола, направлено против HGF рецептора c-Met. Кроме того, в этом документе описано, что HGF и Met оказывают существенное влияние на злокачественность различных видов рака, таких как, например,множественная миелома. Поэтому является желательным синтезировать небольшие соединения, которые специфически ингибируют, регулируют и/или модулируют передачу сигналов с помощью тирозинкиназ и/или серин/треонинкиназ, в частности Met киназы, и это составляет задачу настоящего изобретения. Было обнаружено, что соединения в соответствии с изобретением и их соли обладают чрезвычайно ценными фармакологическими свойствами, а также хорошей переносимостью. Более подробно, настоящее изобретение относится к соединениям формулы I, которые ингибируют,регулируют и/или модулируют передачу сигналов Met киназами, к композициям, которые содержат эти соединения, и к способам их применения для лечения заболеваний и состояний, индуцированных Met киназой, таких как ангиогенез, рак, образование, рост и распространение опухолей, артериосклероз, заболевания глаз, такие как дегенерация желтого пятна, связанная со старением, образование новых сосудов в хориоидальной оболочке и диабетическая ретинопатия, воспалительные заболевания, артрит,тромбоз, фиброз, гломерулонефрит, нейродегенерация, псориаз, рестеноз, заживление ран, отторжение трансплантата, нарушения обмена веществ и заболевания иммунной системы, а также аутоиммунные заболевания, цирроз, диабет и заболевания кровеносных сосудов, включая нестабильность и проницаемость и др., у млекопитающих. Солидные опухоли, в особенности быстрорастущие опухоли, можно подвергать лечению с применением ингибиторов Met киназы. Такие солидные опухоли включают моноцитарный лейкоз, рак головного мозга, мочеполового тракта, лимфатической системы, желудка, гортани и легкого, включая аденокарциному легкого и мелкоклеточный рак легкого. Настоящее изобретение относится к способам регуляции, модуляции или ингибирования Met киназы для предотвращения и/или лечения заболеваний, связанных с нерегулируемой или нарушенной активностью Met киназы. В частности, соединения формулы I также могут применяться для лечения определенных типов злокачественных новообразований. Кроме того, соединения формулы I могут применяться для обеспечения дополнительного или синергетического действий при определенных существующих химиотерапиях при лечении злокачественных новообразований и/или могут применяться для восстановления эффективности определенных существующих химиотерапии и лучевых терапий злока-1 021362 чественных новообразований. Соединения формулы I также могут применяться для выделения и исследования активности или экспрессии Met киназы. Дополнительно они чрезвычайно пригодны для применения в диагностических способах при заболеваниях, связанных с нерегулируемой или нарушенной активностью Met киназы. Может быть продемонстрировано, что соединения в соответствии с изобретением обладают антипролиферативным действием в условиях in vivo на модели ксенотрансплантированной опухоли. Соединения в соответствии с изобретением вводятся пациенту с гиперпролиферативным заболеванием, например, для ингибирования роста опухоли, для уменьшения воспаления, связанного с лимфопролиферативным заболеванием, для ингибирования отторжения трансплантата или неврологического повреждения в результате восстановления ткани и т.д. Эти соединения пригодны для профилактических или терапевтических целей. Как используется в настоящем изобретении, термин "лечение" применяется для обозначения как предотвращения заболеваний, так лечения ранее существующих состояний. Предотвращение пролиферации достигают путем введения соединений в соответствии с изобретением до явного развития заболевания, например, для предотвращения роста опухолей, предотвращения метастатического роста,уменьшения рестеноза, связанного с сердечно-сосудистой хирургией и т.д. Альтернативно, соединения применяются для лечения продолжающихся заболеваний путем стабилизации или улучшения клинических симптомов у пациента. Хозяин или пациент может принадлежать к любому виду млекопитающих, например, такому как приматы, предпочтительно человек; грызуны, включая мышей, крыс и хомячков, кролики; лошади, коровы, собаки, кошки и т.д. Животные модели представляют интерес для экспериментальных исследований,поскольку они обеспечивают модель для лечения заболевания человека. Чувствительность определенной клетки к лечению с помощью соединений в соответствии с изобретением может быть определена при исследованиях в условиях in vitro. В общем случае культуру клеток объединяют с соединением в соответствии с изобретением при различных концентрациях в течение периода времени, достаточного для того, чтобы позволить активным веществам индуцировать гибель клетки или ингибировать миграцию, обычно в интервале времени приблизительно от одного часа до одной недели. Для исследования в условиях in vitro можно использовать культивируемые клетки из образца биопсии. Затем подсчитывают жизнеспособные клетки, оставшиеся после обработки. Доза будет изменяться в зависимости от конкретного применяемого соединения, конкретного заболевания, состояния пациента и т.д. Обычно терапевтическая доза будет достаточной для существенного уменьшения нежелательной популяции клеток в ткани-мишени, при поддержании жизнеспособности пациента. Лечение в общем случае продолжают до тех пор, пока не будет достигнуто существенное уменьшение, например по меньшей мере приблизительно 50% уменьшение популяции клеток, представляющих интерес, при этом лечение можно продолжать до тех пор, пока, по существу, в организме не будут определяться нежелательные клетки. Для идентификации пути передачи сигналов и определения взаимодействий между различными сигнальными путями различными учеными были разработаны приемлемые модели или модельные системы, например модели на основе культур клеток (например, Khwaja и др., ЕМВО, 1997, 16, 2783-93) и модели трансгенных животных (например, White и др., Oncogene, 2001, 20, 7064-7072). С целью проверки определенных этапов каскада передачи сигналов можно использовать соединения, которые препятствуют этому процессу, для модуляции сигнала (например, Stephens и др., Biochemical J., 2000, 351, 95105). Соединения в соответствии с изобретением могут также быть полезными в качестве реагентов для тестирования зависимых от киназы путей передачи сигналов у животных и/или на моделях культур клеток, а также на любом из клинических расстройств, указанных в данной заявке. Измерение киназной активности представляет собой известный способ, который может осуществить любой специалист в данной области. Общие аналитические системы для определения киназной активности с субстратами, например гистоном (например, Alessi и др., FEBS Lett. 1996, 399, 3, стр. 333-338) или основным миелиновым белком, описаны в литературе (например, Campos-Gonzlez, R. и Glenney, Jr.,J.R. 1992 J. Biol. Chem. 267, стр. 14535). Для идентификации ингибиторов киназы доступными являются различные аналитические системы. В исследовании сцинтилляционной схожести (Sorg и др., J. of. Biomolecular Screening, 2002, 7, 11-19) и анализе флэш-планшетов измеряют радиоактивное фосфорилирование белка или пептида в качестве субстрата с АТФ. В присутствии ингибиторного соединения не выявляется никакого сигнала или выявляется снижение радиоактивного сигнала. Кроме того, в качестве аналитических способов являются полезными способы гомогенного переноса энергии флуоресцентного резонанса с разрешением во времени(HTR-FRET) и флуоресцентной поляризации (FP) (Sills и др., J. of Biomolecular Screening, 2002, 191-214). В других нерадиоактивных способах анализа на основе ELISA используются специфические фосфоантитела (фосфо-АВ). Фосфо-АВ связываются только с фосфорилированным субстратом. Это связывание может быть определено с использованием вторичного антиовечьего антитела, конъюгированного с пероксидазой, с помощью хемолюминисценции (Ross и др., 2002, Biochem. J.). Существует много заболеваний, связанных с нарушением регулирования пролиферации клеток и клеточной гибели (апоптоза). Состояния, которые представляют интерес, включают, но не ограничиваясь только ими, следующие состояния. Соединения в соответствии с изобретением являются полезными для лечения разнообразных состояний, при которых существует пролиферация и/или миграция клеток гладкой мускулатуры и/или воспалительных клеток в слой интимы сосудов, что приводит к ограниченному потоку крови через этот сосуд, например, в случае неоинтимальных окклюзивных повреждений. Окклюзивные заболевания трансплантированных сосудов, которые представляют интерес, включают атеросклероз, коронарное сосудистое заболевание после трансплантации, стеноз в результате пересадки вен,перианастомотический рестеноз в результате введения протеза, рестеноз после ангиопластики или внедрения стента и т.п. Уровень техники Другие производные пиридазина описываются в качестве ингибиторов Met киназы в WO 2007/065518. Тиадиазиноны описываются в DE 19604388, WO 2003/037349 WO 2007/057093 или WO 2007/057092. Дигидропиридазиноны для борьбы со злокачественным новообразованием описываются в WO 03/037349 А 1. Другие пиридазины для лечения заболеваний иммунной системы, ишемических и воспалительных заболеваний известны из ЕР 1043317 А 1 и ЕР 1061077 А 1. ЕР 0738716 А 2 и ЕР 0711759 В 1 описывают другие дигидропиридазиноны и пиридазиноны в качестве фунгицидов и инсектицидов. Другие пиридазиноны описываются в качестве кардиотонических средств в US 4397854.JP 57-95964 раскрывает другие пиридазиноны. Краткое изложение сущности изобретения Изобретение относится к соединениям формулы IR1 означает Н или А,R2 означает фурил, тиенил, пирролил, имидазолил, пиразолил, оксазолил, изоксазолил, тиазолил,изотиазолил, пиридил, пиримидинил, триазолил, тетразолил, оксадиазолил или тиадиазолил, каждый из которых является монозамещенным Hal, A, [C(R3)2]nN(R3)2, [C(R3)2]nHet, O[C(R3)2]nN(R3)2 илиO[C(R3)2]nHet,R3 означает Н, метил, этил или пропил,R4, R4' означают Н,Het означает пиперидинил, пиперазинил, пирролидинил, морфолинил, фурил, тиенил, пирролил,имидазолил, пиразолил, оксазолил, изоксазолил, тиазолил, изотиазолил, пиридил, пиримидинил, триазолил, тетразолил, оксадиазолил, тиадиазолил, пиридазинил или пиразинил, каждый из которых является монозамещенным А или [C(R3)2]nHet1,Het1 означает пирролидин, пиперидин, пиперазин или морфолин, каждый из которых является незамещенным или моно- или дизамещенным А и/или =O (карбонильным кислородом),А означает неразветвленный или разветвленный алкил, содержащий 1-8 атомов С, в котором 1-7 атомов Н может быть замещено F и/или Cl, или циклический алкил, содержащий 3-7 атомов С,Hal означает F, Cl, Br или I,n равно 0, 1, 2, 3 или 4,и их фармацевтически пригодным солям, таутомерам и стереоизомерам, включая их смеси во всех соотношениях. Под соединениями формулы I также подразумеваются их фармацевтически пригодные производные и сольваты. Изобретение также относится к оптически активным формам (стереоизомерам), энантиомерам, рацематам, диастереомерам, а также гидратам и сольватам указанных соединений. Под сольватами соединений подразумевают аддукты молекул инертного растворителя на соединениях, которые образуются благодаря их силе взаимного притяжения. Сольваты представляют собой, например, моно- или дигидраты или алкоголяты. Под фармацевтически пригодными производными подразумевают, например, соли соединений в соответствии с изобретением, а также так называемые пролекарственные соединения. Под производными пролекарств подразумевают соединения формулы I, которые являются модифицированными, например, алкильной или ацильной группами, сахарами или олигопептидами, и которые быстро расщепляются в организме с образованием активных соединений в соответствии с изобретением. Это понятие также включает производные биоразлагаемых полимеров соединений в соответствии с изобретением, как описано, например, в Int. J. Pharm. 115, 61-67(1995). Выражение "эффективное количество" обозначает количество лекарственного средства или фармацевтического активного компонента, которое вызывает в ткани, системе, животном или человеке биологическую или медицинскую ответную реакцию, которую предполагает или желает получить, например,исследователь или лечащий врач. Кроме того, выражение "терапевтически эффективное количество" обозначает то количество, которое имеет следующие последствия по сравнению с соответствующим субъектом, который не получал этого количества: улучшение лечения, излечение, предотвращение или элиминацию заболевания, синдрома, состояния, жалобы, расстройства или побочных действий, или также уменьшения прогрессирования заболевания, жалобы или расстройства. Выражение "терапевтически эффективное количество" также охватывает количества, которые эффективны для усиления нормальной физиологической функции. Изобретение также относится к применению смесей соединений формулы I, например, смесей двух диастереомеров, например, в соотношении 1:1, 1:2, 1:3, 1:4, 1:5, 1:10, 1:100 или 1:1000. Особенно предпочтительными являются смеси стереоизомерных соединений. Изобретение относится к соединениям формулы I и их солям и к способу получения соединений формулы I и их фармацевтически пригодных солей, таутомеров и стереоизомеров, который отличается тем, что соединение формулы IIL означает Cl, Br, I или свободную или реакционноспособную функционально-модифицированную ОН-группу, где полученное соединение может быть выделено в свободном состоянии из одного из его функциональных производных путем обработки сольволизирующим или гидрогенолизирующим агентом, и/или основание или кислота формулы I может быть превращена в одну из его(ее) солей. При указании выше и ниже радикалы R1, R2, R3, R4, R4' имеют значения, указанные для формулы I,если специально не указано иначе. А означает алкил, который является неразветвленным (линейным) или разветвленным и имеет 1, 2,3, 4, 5, 6, 7 или 8 атомов С. А предпочтительно означает метил, кроме того, этил, пропил, изопропил, бутил, изобутил, втор-бутил или трет-бутил, кроме того, также пентил, 1-, 2- или 3-метилбутил, 1,1-, 1,2 или 2,2-диметилпропил, 1-этилпропил, гексил, 1-, 2-, 3- или 4-метилпентил, 1,1-, 1,2-, 1,3-, 2,2-, 2,3- или 3,3-диметилбутил, 1- или 2-этилбутил, 1-этил-1-метилпропил, 1-этил-2-метилпропил, 1,1,2- или 1,2,2 триметилпропил, более предпочтительно, например, трифторметил. А наиболее предпочтительно означает алкил, содержащий 1, 2, 3, 4, 5 или 6 атомов С, предпочтительно метил, этил, пропил, изопропил,бутил, изобутил, втор-бутил, трет-бутил, пентил, гексил, трифторметил, пентафторэтил или 1,1,1 трифторэтил. Циклический алкил (циклоалкил) предпочтительно означает циклопропил, циклобутил, циклопентил, циклогексил или циклогептил. Независимо от дальнейших замещений, Het означает, например, 2- или 3-фурил, 2- или 3-тиенил, 1-,2- или 3-пирролил, 1-, 2, 4- или 5-имидазолил, 1-, 3-, 4- или 5-пиразолил, 2-, 4- или 5-оксазолил, 3-, 4- или 5-изоксазолил, 2-, 4- или 5-тиазолил, 3-, 4- или 5-изотиазолил, 2-, 3- или 4-пиридил, 2-, 4-, 5-или 6 пиримидинил, более предпочтительно 1,2,3-триазол-1-, -4- или -5-ил, 1,2,4-триазол-1-, -3- или 5-ил, 1 или 5-тетразолил, 1,2,3-оксадиазол-4- или -5-ил, 1,2,4-оксадиазол-3- или -5-ил, 1,3,4-тиадиазол-2- или -5 ил, 1,2,4-тиадиазол-3- или -5-ил, 1,2,3-тиадиазол-4- или -5-ил, 3- или 4-пиридазинил, пиразинил.Hal предпочтительно означает F, Cl или Br, но также и I, особенно предпочтительно F или Cl. Для всего изобретения все радикалы, которые встречаются более одного раза, могут быть одинаковыми или разными, то есть их значения являются независимыми друг от друга. Соединения формулы I могут иметь один или несколько хиральных центров и поэтому могут встречаться в разных стереоизомерных формах. Формула I охватывает все эти формы. Таким образом, изобретение относится, в частности, к соединениям формулы I, в которых по меньшей мере один из указанных радикалов имеет одно из предпочтительных значений, указанных выше. Соединения формулы I, а также исходные вещества для их получения могут, кроме того, быть получены при помощи методов, известных per se, как описано в литературе (например, в стандартных работах, таких как Houben-Weyl, Methoden der organischen Chemie [Методы органической химии], GeorgThieme-Verlag, Штутгарт), в соответствии с условиями реакций, которые известны и приемлемы для указанных реакций. Также при этом можно применять разнообразные модификации, которые известные perse, но о которых здесь подробно не упоминается. Исходные соединения формул II и III, как правило, известны. Однако если они являются новыми, то они могут быть получены методами, известными per se. Используемые пиридазиноны формулы II, если они не являются коммерчески доступными, обычно могут быть получены с помощью способа W.J. Coates, A. McKillop, Synthesis, 1993, 334-342. Соединения формулы I предпочтительно могут быть получены путем взаимодействия соединения формулы II с соединением формулы III. В соединениях формулы III, L предпочтительно представляет собой Cl, Br, I или свободную или реакционноспособную модифицированную ОН-группу, такую как,например, активированная сложноэфирная, имидазолидная группа или алкилсульфонилокси, содержащий 1-6 атомов углерода (предпочтительно метилсульфонилокси или трифторметилсульфонилокси) или арилсульфонилокси, содержащий 6-10 атомов углерода (предпочтительно фенил- или птолилсульфонилокси). Обычно реакцию осуществляют в присутствии вещества, связывающего кислоту, предпочтительно органического основания, такого как DIPEA, триэтиламин, диметиланилин, пиридин или хинолин. Прибавление гидроксида щелочного или щелочно-земельного металла, карбоната или бикарбоната или другой соли слабой кислоты щелочных или щелочно-земельных металлов, предпочтительно калия, натрия,кальция или цезия, также может являться благоприятным. В зависимости от применяемых условий продолжительность реакции находится в интервале от нескольких минут до 14 дней, температура реакции находится в интервале приблизительно от -30 до 140,обычно в интервале от -10 до 90, более предпочтительно от приблизительно 0 до приблизительно 70. Примерами подходящих инертных растворителей являются углеводороды, такие как гексан, петролейный эфир, бензол, толуол или ксилол; хлорированные углеводороды, такие как трихлорэтилен, 1,2 дихлорэтан, четыреххлористый углерод, хлороформ или дихлорметан; спирты, такие как метанол, этанол, изопропанол, н-пропанол, н-бутанол или трет-бутанол; простые эфиры, такие как диэтиловый эфир,диизопропиловый эфир, тетрагидрофуран (ТГФ) или диоксан; гликолевые эфиры, такие как этиленгликольмонометиловый или моноэтиловый эфир, этиленгликольдиметиловый эфир (диглим); кетоны, такие как ацетон или бутанон; амиды, такие как ацетамид, диметилацетамид или диметилформамид (ДМФА); нитрилы, такие как ацетонитрил; сульфоксиды, такие как диметилсульфоксид (ДМСО); сероуглерод, карбоновые кислоты, такие как муравьиная кислота или уксусная кислота, нитросоединения, такие как нитрометан или нитробензол; сложные эфиры, такие как этилацетат, или смеси указанных растворителей. Особенно предпочтительными являются ацетонитрил, дихлорметан и/или ДМФА. Реакцию соединения формулы II с соединением формулы III, в которой L представляет собой ОН,предпочтительно проводят в условиях реакции Мицунобу путем добавления, например, трифенилфосфина и диалкилазодикарбоксилата. В качестве растворителя является предпочтительным ТГФ. Соединения формулы I к тому же могут быть получены путем превращения радикала R2 в другой радикал R2 с помощью, например, арилирования гетероцикла в реакции Сузуки. Соединения формулы I также могут быть получены их выделением в свободном состоянии из их функциональных производных путем сольволиза, в частности гидролиза, или путем гидрогенолиза. Предпочтительными исходными веществами для сольволиза или гидрогенолиза являются те, которые содержат соответствующие защищенные амино- и/или гидроксильные группы вместо одной или нескольких свободных амино- и/или гидроксильных групп, предпочтительно те, которые несут аминозащитную группу вместо атома водорода, связанного с атомом азота, например те, которые соответствуют формуле I, но несут NHR' группу (в которой R' представляет собой аминозащитную группу, например ВОС или CBZ) вместо NH2 группы. Кроме того, предпочтительными являются исходные вещества, которые несут гидроксилзащитную группу вместо атома водорода гидроксильной группы, например те, которые соответствуют формуле I,но содержат R"O-фенильную группу (в которой R" представляет собой гидроксилзащитную группу) вместо гидроксифенильной группы. Также существует возможность присутствия в молекуле исходного вещества множества - одинаковых или различных - защищенных амино- и/или гидроксильных групп. Если присутствующие защитные группы отличаются друг от друга, то во многих случаях они могут быть отщеплены селективно. Понятие "аминозащитная группа" в общем известно и относится к группам, которые являются подходящими для защиты (блокирования) аминогруппы от химических реакций, но которые легко удаляются после того, как желательная химическая реакция была проведена в другой части молекулы. Типичными такими группами являются, в частности, незамещенная или замещенная ацильная группа, арильная группа, аралкоксиметильная группа или аралкильная группа. Так как аминозащитные группы удаляют после желательной реакции (или последовательности реакций), то их тип и размер не являются, кроме того, критическими; однако предпочтение отдается тем, которые имеют 1-20, в особенности 1-8 атомов углерода. Понятие "ацильная группа" следует понимать в самом широком смысле в связи с настоящим способом. Оно включает ацильные группы, производные от алифатических, аралифатических, ароматических или гетероциклических карбоновых кислот или сульфоновых кислот и, в частности, алкоксикарбонильные, арилоксикарбонильные и особенно аралкоксикарбонильные группы. Примерами таких ацильных групп являются алканоил, такой как ацетил, пропионил и бутирил; аралканоил, такой как фенилацетил; ароил, такой как бензоил и толил; арилоксиалканоил, такой как РОА; алкоксикарбонил, такой как метоксикарбонил, этоксикарбонил, 2.2.2-трихлорэтоксикарбонил, ВОС и 2-йодэтоксикарбонил; аралкоксикарбонил, такой как CBZ ("карбобензокси"), 4-метоксибензилоксикарбонил и FMOC; и арилсульфонил, такой как Mtr, Pbf и Pmc. Предпочтительными аминозащитными группами являются ВОС и Mtr,кроме того, CBZ, Fmoc, бензил и ацетил. Понятие "гидроксилзащитная группа" также в общем известно и относится к группам, которые являются подходящими для защиты гидроксильной группы от химических реакций, но которые легко удаляются после того, как желательная химическая реакция была проведена в другой части молекулы. Типичными такими группами являются указанные выше незамещенные или замещенные арильная, аралкильная или ацильная группы, кроме того, также алкильные группы. Природа и размер гидроксилзащитных групп не являются критическими, так как их удаляют после желательной химической реакции или последовательности реакций; предпочтение отдается группам, которые имеют 1-20, в особенности 110 атомов углерода. Примерами гидроксилзащитных групп являются, в числе других, третбутоксикарбонил, бензил, п-нитробензоил, п-толуолсульфонил, трет-бутил и ацетил, где бензил и третбутил являются особенно предпочтительными. Группы СООН в аспарагиновой кислоте и глутаминовой кислоте предпочтительно защищены в виде их трет-бутиловых эфиров (например, Asp(OBut. Соединения формулы I выделяют в свободном состоянии из их функциональных производных - в зависимости от используемых защитных групп - например, применяя сильные кислоты, преимущественно применяя ТФУ или перхлорную кислоту, но также используют другие сильные неорганические кислоты, такие как соляная кислота или серная кислота, сильные органические карбоновые кислоты, такие как трихлоруксусная кислота, или сульфоновые кислоты, такие как бензол- или п-толуолсульфоновая кислота. Присутствие дополнительного инертного растворителя допускается, но не всегда необходимо. Приемлемыми инертными растворителями предпочтительно являются органические, например карбоновые кислоты, такие как уксусная кислота, простые эфиры, такие как тетрагидрофуран или диоксан, амиды, такие как ДМФА, галогенированные углеводороды, такие как дихлорметан, кроме того, также спирты, такие как метанол, этанол или изопропанол, и вода. Также приемлемыми являются смеси указанных выше растворителей. ТФУ предпочтительно используют в избытке без добавления другого растворителя и перхлорную кислоту предпочтительно используют в виде смеси уксусной кислоты и 70% перхлорной кислоты в соотношении 9:1. Температура реакций для осуществления расщепления предпочтительно находится в интервале между приблизительно 0 и приблизительно 50, предпочтительно между 15 и 30(комнатная температура). ВОС, OBut, Pbf, Pmc и Mtr группы могут, например, предпочтительно быть отщеплены при использовании ТФУ в дихлорметане или используя приблизительно 3-5 н. HCl в диоксане при 15-30, и FMOC группа может быть отщеплена, используя приблизительно 5-50% раствор диметиламина, диэтиламина или пиперидина в ДМФА при 15-30. Тритильная группа применяется для защиты аминокислот гистидина, аспарагина, глутамина и цистеина. Их отщепляют, в зависимости от желательного конечного продукта, с помощью ТФУ/10% тиофенол, где тритильная группа отщепляется от всех указанных аминокислот; с помощью ТФУ/анизол или ТФУ/тиоанизол, отщепляется только тритильная группа от His, Asn и Gln, тогда как она остается на боковой цепи Cys. Pbf (пентаметилбензофуранил) группа используется для защиты Arg. Она отщепляется,например, с помощью ТФУ в дихлорметане. Защитные группы, которые могут быть удалены гидрогенолитически (например, CBZ или бензил),могут быть отщеплены, например, обработкой водородом в присутствии катализатора (например, катализатора на основе благородного металла, такого как палладий, предпочтительно на подложке, такой как уголь). При этом подходящими растворителями являются растворители, указанные выше, в частности,например, спирты, такие как метанол или этанол, или амиды, такие как ДМФА. Гидрогенолиз в основном проводится при температурах в интервале между приблизительно 0 и 100 и давлении между приблизительно 1 и 200 бар, предпочтительно при 20-30 и 1-10 бар. Гидрогенолиз CBZ группы происходит успешно, например, на 5-10% Pd/C в метаноле или при использовании формиата аммония (вместо водорода) на Pd/C в метаноле/ДМФА при 20-30. Фармацевтические соли и другие формы. Соединения, раскрытые в изобретении, могут использоваться в своей заключительной, несолевой форме. С другой стороны, настоящее изобретение также относится к применению таких соединений в форме их фармацевтически приемлемых солей, которые могут быть получены с помощью разнообраз-6 021362 ных органических и неорганических кислот и оснований в соответствии со способами, хорошо известными в данной области техники. Фармацевтически приемлемые формы солей соединений формулы I готовят, главным образом, при использовании традиционных способов. В случае, если соединение формулы I содержит карбоксильную группу, то его приемлемая соль может быть образована с помощью реакции соединения с приемлемым основанием для получения соответствующей соли присоединения основания. Примерами таких оснований являются гидроксиды щелочных металлов, включая гидроксид калия, гидроксид натрия и гидроксид лития; гидроксиды щелочно-земельных металлов, такие как гидроксид бария и гидроксид кальция; алкоксиды щелочных металлов, например этанолят калия и пропанолят натрия; а также различные органические основания, такие как пиперидин, диэтаноламин и Nметилглутамин. Сюда также включены соли алюминия соединений формулы I. Для некоторых соединений формулы I соли присоединения кислоты могут быть образованы путем обработки указанных соединений фармацевтически приемлемыми органическими и неорганическими кислотами, например галогеноводородами, такими как хлороводород, бромоводород или йодоводород; другими минеральными кислотами и их соответствующими солями, такими как, сульфат, нитрат или фосфат и др.; и алкил- и моноарилсульфонатами, такими как этансульфонат, толуолсульфонат и бензолсульфонат; и другими органическими кислотами их соответствующими солями, такими как ацетат, трифторацетат, тартрат, малеат,сукцинат, цитрат, бензоат, салицилат, аскорбат и др. Таким образом, фармацевтически приемлемые соли присоединения кислоты соединений формулы I включают следующие соли, но не ограничиваясь только ими, ацетат, адипат, альгинат, аргинат, аспартат, бензоат, бензолсульфонат (безилат), бисульфат, бисульфит, бромид, бутират, камфорат, камфорсульфонат, каприлат, хлорид, хлорбензоат, цитрат, циклопентанпропионат, диглюконат, дигидрофосфат, динитробензоат, додецилсульфат, этансульфонат, фумарат, галактерат (из слизевой кислоты), галактуронат, глюкогептаноат, глюконат, глутамат, глицерофосфат, гемисукцинат, гемисульфат, гептаноат, гексаноат, гиппурат, гидрохлорид, гидробромид, гидройодид, 2-гидроксиэтансульфонат, йодид, изотионат, изобутират, лактат, лактобионат, малат, малеат, малонат, манделат, метафосфат, метансульфонат, метилбензоат, моногидрофосфат, 2-нафталинсульфонат,никотинат, нитрат, оксалат, олеат, пальмоат, пектинат, персульфат, фенилацетат, 3-фенилпропионат,фосфат, фосфонат, фталат. Кроме того, основные соли соединений в соответствии с изобретением включают, но не ограничиваясь только ими, соли алюминия, аммония, кальция, меди, железа(III), железа(II), лития, магния, марганца(III), марганца(II), калия, натрия и цинка. Предпочтительными среди перечисленных выше солей являются аммонийные; соли щелочных металлов натрия и калия; и соли щелочно-земельных металлов кальция и магния. Соли соединений формулы I, которые имеют происхождение от фармацевтически приемлемых органических нетоксических оснований, включают, но не ограничиваясь только ими, соли первичных, вторичных и третичных аминов, замещенных аминов, также включая природные замещенные амины, циклические амины и основные ионообменные смолы, например аргинин, бетаин, кофеин,хлорпрокаин, холин, N,N'-дибензилэтилендиамин (бензатин), дициклогексиламин, диэтаноламин, диэтиламин, 2-диэтиламиноэтанол, 2-диметиламиноэтанол, этаноламин, этилендиамин, N-этилморфолин, Nэтилпиперидин, глюкамин, глюкозамин, гистидин, гидрабамин, изопропиламин, лидокаин, лизин, меглумин, N-метил-D-глюкамин, морфолин, пиперазин, пиперидин, полиаминные смолы, прокаин, пурины,теобромин,триэтаноламин,триэтиламин,триметиламин,трипропиламин и трис(гидроксиметил)метиламин (трометамин). Соединения в соответствии с настоящим изобретением, которые включают основные азотсодержащие группы, могут быть кватернизированы с помощью таких агентов, как С 1-С 4-алкилгалогениды, например метил-, этил-, изопропил- и трет-бутилхлориды, бромиды и йодиды; ди-С 1-С 4-алкилсульфаты,например диметил-, диэтил- и диамилсульфаты; С 10-С 18-алкилгалогениды, например децил-, додецил-,лаурил-, миристил- и стеарилхлориды, бромиды и йодиды; и арил-С 1-С 4-алкилгалогениды, например бензилхлорид и фенетилбромид. Указанные соли позволяют получать как растворимые в воде, так и растворимые в масле соединения в соответствии с изобретением. Предпочтительные фармацевтические соли, указанные выше, включают, но не ограничиваясь только ими, ацетат, трифторацетат, безилат, цитрат, фумарат, глюконат, гемисукцинат, гиппурат, гидрохлорид, гидробромид, изотионат, манделат, меглумин, нитрат, олеат, фосфонат, пивалат, фосфат натрия,стеарат, сульфат, сульфосалицилат, тартрат, тиомалат, тозилат и трометамин. Особенно предпочтительными являются гидрохлорид, дигидрохлорид, гидробромид, малеат, мезилат, фосфат, сульфат и сукцинат. Кислотно-аддитивные соли основных соединений формулы I получают путем приведения в контакт формы свободных оснований с достаточным количеством желаемой кислоты для получения соли традиционным способом. Свободное основание можно регенерировать путем приведения в контакт формы соли с основанием и выделения свободного основания традиционным способом. Формы свободного основания в некоторой степени отличаются от своих соответствующих форм солей своими определенными физическими свойствами, такими как растворимость в полярных растворителях, однако во всем остальном соли являются эквивалентными своим соответствующим формам свободных оснований для целей настоящего изобретения. Как было указано, фармацевтически приемлемые соли присоединения основания соединений формулы I образуются с металлами или аминами, такими как щелочные металлы и щелочно-земельные металлы или органические амины. Предпочтительные металлы представляют собой натрий, калий, магний и кальций. Предпочтительные органические амины представляют собой N,N'-дибензилэтилендиамин,хлорпрокаин, холин, диэтаноламин, этилендиамин, N-метил-D-глюкамин и прокаин. Соли присоединения основания кислых соединений в соответствии с изобретением получают путем приведения в контакт формы свободной кислоты с достаточным количеством желаемого основания для получения соли традиционным способом. Форма свободной кислоты может быть регенерирована путем приведения в контакт формы соли с кислотой и выделения формы свободной кислоты известным способом. Формы свободной кислоты в некоторой степени отличаются от своих соответствующих форм солей определенными физическими свойствами, такими как растворимость в полярных растворителях, однако во всем остальном соли являются эквивалентными своим соответствующим формам свободных кислот для целей настоящего изобретения. Если соединение в соответствии с изобретением включает более чем одну группу, которая способна к образованию фармацевтически приемлемых солей этого типа, то изобретение также охватывает сложные соли. Примеры типичных форм сложных солей включают, но не ограничиваясь только ими, битартрат, диацетат, дифумарат, димеглумин, дифосфат, динатрий и тригидрохлорид. В свете описанного выше можно увидеть, что выражение "фармацевтически приемлемая соль" в контексте данной заявки предназначено для обозначения активного компонента, который включает соединение формулы I в форме своей соли, особенно в том случае, если указанная форма соли обеспечивает указанному активному компоненту улучшенные фармакокинетические свойства по сравнению со свободной формой указанного активного компонента или другой солью указанного активного компонента,которые использовались ранее. Фармацевтически приемлемая форма соли активного компонента может также изначально обеспечивать желаемое фармакокинетическое свойство указанному активному компоненту, которым он ранее не обладал, а также может даже положительно влиять на фармакодинамику указанного активного компонента в отношении его терапевтической активности в организме. Изобретение, кроме того, относится к лекарственным средствам, содержащим по меньшей мере одно соединение формулы I и/или его фармацевтически пригодные производные, сольваты и стереоизомеры, включая их смеси во всех соотношениях, и, необязательно, наполнители и/или вспомогательные вещества. Лекарственные препараты могут вводиться в виде дозированных единиц, которые содержат заранее установленное количество активного компонента на дозированную единицу. Такая единица может включать, например, от 0,5 мг до 1 г, предпочтительно от 1 до 700 мг, более предпочтительно от 5 до 100 мг соединения в соответствии с изобретением в зависимости от состояния, подвергаемого лечению, способа введения, а также возраста, веса тела и состояния пациента, или фармацевтические композиции могут вводиться в виде дозированных единиц, которые содержат заранее установленное количество активного компонента на дозированную единицу. Предпочтительными дозированными единицами лекарственных препаратов являются те, которые содержат суточную дозу или часть суточной дозы, как указано выше, или соответствующую порцию их активного компонента. Лекарственные средства этого типа также могут быть получены способом, который хорошо известен в области фармацевтики. Лекарственные препараты могут адаптироваться для введения при помощи любого подходящего способа, например путем перорального (включая буккальное или подъязычное), ректального, назального,местного (включая буккальное, подъязычное или трансдермальное), вагинального или парентерального(включая подкожное, внутримышечное, внутривенное или внутрикожное) введения. Такие препараты могут быть приготовлены с помощью любого способа, известного в области фармацевтики, например путем объединения активного компонента с наполнителем(ями) или вспомогательным(и) веществом(ами). Лекарственные препараты, адаптированные для перорального введения, могут вводиться в виде отдельных единиц, таких как, например, капсулы или таблетки; порошки или гранулы; растворы или суспензии в водных или неводных жидкостях; пищевых пен или пенистых пищевых продуктов; или жидких эмульсий масло-в-воде или жидких эмульсий вода-в-масле. Так, например, в случае перорального введения в виде таблетки или капсулы активный компонент может быть объединен с пероральным, нетоксичным и фармацевтически приемлемым инертным наполнителем, таким как, например, этанол, глицерин, вода и т.п. Порошки получают путем измельчения соединения до подходящего небольшого размера и смешивания его с фармацевтическим наполнителем,измельченным аналогичным способом, таким как, например, пищевой углевод, такой как, например,крахмал или маннит. Также можно добавлять ароматизатор, консервант, диспергирующее вещество и краситель. Капсулы получают путем приготовления порошковой смеси, как описано выше, и заполняют ею желатиновые капсулы определенной формы. Перед заполнением капсул к порошковой смеси можно добавлять скользящие и смазывающие вещества, такие как, например, высокодисперсная кремниевая кислота, тальк, стеарат магния, стеарат кальция или полиэтиленгликоль в твердой форме. Для улучшения доступности лекарственного средства, заключенного в капсулу, также можно добавлять дезинтегрирующее вещество или солюбилизатор, такой как, например, агар-агар, карбонат кальция или карбонат натрия. Дополнительно, если это является желательным или необходимым, в смесь также можно добавлять подходящие связующие, смазывающие вещества, дезинтеграторы, а также красители. Подходящими связующими являются крахмал, желатин, природные сахара, такие как, например, глюкоза или -лактоза,подсластители, приготовленные из кукурузы, природных и синтетических каучуков, такие как, например, аравийская камедь, трагакантовая камедь или альгинат натрия, карбоксиметилцеллюлоза, полиэтиленгликоль, воски и т.п. Смазывающие вещества, которые могут применяться в таких дозированных формах, включают олеат натрия, стеарат натрия, стеарат магния, бензоат натрия, ацетат натрия, хлорид натрия и т.п. Дезинтеграторы включают, но не ограничиваясь только ими, крахмал, метилцеллюлозу,агар, бентонит, ксантановую камедь и т.п. Лекарственные средства в виде таблеток получают, например,путем приготовления порошковой смеси, гранулирования или сухого прессования смеси, добавления смазывающего вещества и дезинтегратора и прессования полученной смеси в таблетки. Порошковую смесь готовят путем смешивания соединения, измельченного подходящим образом, с разбавителем или основанием, как описано выше, и необязательно со связующим, таким как, например, карбоксиметилцеллюлоза, альгинат, желатин или поливинилпирролидон, замедлителем растворения, таким как, например, парафин, усилителем поглощения, таким как, например, четвертичная соль, и/или абсорбентом, таким как, например, бентонит, каолин или дикальцийфосфат. Порошковую смесь можно гранулировать путем смачивания со связующим, таким как, например, сироп, крахмальная паста, слизь акации или растворы целлюлозы или полимерных веществ и прессования ее через сито. В качестве альтернативы грануляции порошковую смесь можно пропускать через таблетировочную машину, получая куски неправильной формы, которые распадаются, образуя гранулы. Гранулы можно замасливать путем добавления стеариновой кислоты, стеарата, талька или минерального масла для предотвращения слипания в таблетировочной литейной форме. После этого смазанную смесь спрессовывают, получая таблетки. Соединения в соответствии с изобретением также можно объединять с сыпучим инертным наполнителем и затем подвергать прямому прессованию, получая таблетки без осуществления стадий грануляции или сухого прессования. Таблетки также можно покрывать прозрачным или светонепроницаемым защитным слоем, состоящим из шеллакового запечатывающего слоя, слоя сахара или полимерного вещества и глянцевого слоя воска. К этим покрытиям также можно добавлять красители для возможности различения между разными дозируемыми единицами. Жидкости для перорального введения, такие как, например, раствор, сиропы и эликсиры, могут быть приготовлены в виде дозируемых единиц таким образом, чтобы они содержали заранее установленное количество соединения. Сиропы могут быть получены путем растворения соединения в водном растворе с подходящим ароматизатором, тогда как эликсиры готовят с применением нетоксичного спиртового наполнителя. Суспензии могут быть приготовлены путем диспергирования соединения в нетоксичном наполнителе. Также можно добавлять солюбилизаторы и эмульсификаторы, такие как, например,этоксилированные изостеариловые спирты и полиоксиэтиленовые эфиры сорбита, консерванты, ароматические добавки, такие как, например, масло мяты перечной, или натуральные заменители сахара или сахарин, или другие искусственные заменители сахара и т.п. Лекарственные препараты для перорального введения в виде дозированных единиц могут быть инкапсулированы в микрокапсулы, если это является желательным. Также лекарственный препарат может быть приготовлен таким образом, чтобы пролонгировать или замедлить высвобождение, например, путем применения покрытий или заделывания требуемого вещества в полимеры, воск и т.п. Соединения формулы I и их соли, сольваты и физиологически функциональные производные также могут вводиться в виде липосомных систем доставки, таких как, например, небольшие однослойные пузырьки, большие однослойные пузырьки и многослойные пузырьки. Липосомы могут быть образованы с помощью различных фосфолипидов, таких как, например, холестерин, стеариламин или фосфатидилхолины. Соединения формулы I и их соли, сольваты и физиологически функциональные производные также могут доставляться с помощью моноклональных антител в качестве индивидуальных носителей, к которым присоединены молекулы соединения. Соединения также могут быть соединены с растворимыми полимерами в качестве нацеливающих носителей лекарственных средств. Такими полимерами могут являться поливинилпирролидон, сополимер пирана, полигидроксипропилметакриламидофенол, полигидроксиэтиласпартамидофенол или полиэтиленоксид полилизина, замещенный пальмитоиловыми радикалами. Кроме того, соединения можно связывать с биоразлагаемыми полимерами, которые пригодны для обеспечения контролируемого высвобождения лекарственного средства, например полимолочной кислотой, полиэпсилон-капролактоном, полигидроксимасляной кислотой, полиортоэфирами, полиацеталями, полидигидроксипиранами, полицианоакрилатами и перекрестно-сшитыми или амфипатическими блок-сополимерами гидрогелей. Лекарственные препараты, адаптированные для трансдермального введения, могут вводиться в виде независимых пластырей для удлиненного, тесного контакта с эпидермисом реципиента. Таким обра-9 021362 зом, например, активный компонент может доставляться из пластыря путем ионофореза, как, в общем,описано в Pharmaceutical Research, 3(6), 318 (1986). Фармацевтические композиции, адаптированные для местного введения, могут быть приготовлены в виде мазей, кремов, суспензий, лосьонов, порошков, растворов, паст, гелей, спреев, аэрозолей или масел. Для лечения глаз или других наружных тканей, например рта и кожи, предпочтительно применяются лекарственные препараты в виде местной мази или крема. Для приготовления лекарственного препарата в виде мази активный компонент может применяться с парафиновым или смешивающимся с водой мазевым основанием. Альтернативно, для получения крема активный компонент может быть приготовлен с основой для крема типа масло-в-воде или основой вода-в-масле. Лекарственные препараты, адаптированные для местного введения в глаза, включают глазные капли, в которых активный компонент растворен или суспендирован в подходящем носителе, предпочтительно в водном растворителе. Лекарственные препараты, адаптированные для местного введения в полость рта, включают лепешки, пастилки и жидкости для полоскания рта. Лекарственные препараты, адаптированные для ректального введения, могут вводиться в виде суппозиториев или клизм. Лекарственные препараты, адаптированные для интраназального введения, в которых носитель представляет собой твердое вещество, включают крупный порошок, имеющий размер частичек, например, в интервале 20-500 мкм, который вводится путем вдыхания, то есть путем быстрого вдоха через нос из контейнера, содержащего порошок, который придерживают возле носа. Подходящие лекарственные препараты для введения в виде интраназального аэрозоля или носовых капель с жидкостью в качестве носителя включают растворы активного вещества в воде или в масле. Лекарственные препараты, адаптированные для введения путем ингаляции, включают тонкоизмельченные частички в виде пыли или тумана, которые могут быть получены с помощью различных диспергирующих устройств под давлением с аэрозолями, распылителями или инсуффляторами. Лекарственные препараты, адаптированные для вагинального введения, могут вводиться в виде пессариев, тампонов, кремов, гелей, паст, пен или аэрозолей. Лекарственные препараты, адаптированные для парентерального введения, включают водные или неводные стерильные растворы для инъекций, содержащие антиоксиданты, буферы, бактериостатические вещества и растворенные вещества, с помощью которых лекарственное средство поддерживается изотоническим по отношению к крови реципиента, подвергаемого лечению; и водные или неводные стерильные суспензии, которые могут содержать суспензионную среду и загустители. Лекарственные препараты могут вводиться с помощью емкостей для однократного или многократного введения, например,запечатанных ампул и флаконов, и храниться в высушенном сублимацией (лиофилизированном) состоянии, при этом непосредственно перед введением необходимо только добавить стерильную жидкостьноситель, например воду для инъекций. Растворы и суспензии для инъекций, приготовленные согласно рецептуре, могут быть приготовлены из стерильных порошков, гранул и таблеток. Также является очевидным, что дополнительно к предпочтительным вышеописанным составляющим, лекарственные препараты также могут содержать другие вещества, которые используются в данной области для конкретных типов лекарственных средств; например лекарственные препараты, пригодные для перорального введения, могут содержать ароматизаторы. Терапевтически эффективное количество соединения формулы I зависит от многих факторов,включая, например, возраст и вес животного, определенное состояние, которое необходимо лечить, и его тяжесть, природу лекарственного средства и способ введения, и в конченом счете оно может быть определено лечащим врачом или ветеринаром. Тем не менее, эффективное количество соединения в соответствии с изобретением для лечения роста опухолей, например рака ободочной кишки или молочной железы, как правило, находится в интервале от 0,1 до 100 мг/кг веса тела реципиента (млекопитающего) в сутки и предпочтительно обычно находится в интервале от 1 до 10 мг/кг веса тела в сутки. Следовательно, действующее суточное количество для взрослого млекопитающего весом 70 кг обычно может составлять от 70 до 700 мг, причем это количество может вводиться в виде отдельной дозы один раз в день или обычно в виде циклов частичных доз (таких как, например, два, три, четыре, пять или шесть раз) в день,таким образом, что общая суточная доза является аналогичной. Эффективное количество его соли или сольвата или физиологически функционального производного может быть определено в виде доли эффективного количества соединения в соответствии с изобретением per se. Также можно предположить,что аналогичные дозы пригодны для лечения других состояний, описанных выше. Кроме того, изобретение относится к лекарственным средствам, содержащим по меньшей мере одно соединение формулы I и/или его фармацевтически пригодные соли и стереоизомеры, включая их смеси во всех соотношениях, и по меньшей мере один дополнительный активный противораковый компонент лекарственного средства. Изобретение также относится к комплекту (набору), состоящему из отдельных пакетов(а) эффективного количества соединения формулы I и/или его фармацевтически пригодных солей и стереоизомеров, включая их смеси во всех соотношениях, и(б) эффективного количества дополнительного активного противоракового компонента лекарственного средства. Комплект включает подходящие емкости, такие как коробки, индивидуальные бутылки, пакеты или ампулы. Комплект может включать, например, отдельные ампулы, каждая из которых содержит эффективное количество соединения формулы I и/или его фармацевтически пригодных производных, сольватов и стереоизомеров, включая их смеси во всех соотношениях, и эффективное количество дополнительного активного компонента лекарственного средства в растворенной или лиофиллизированной форме. Применение. Соединения согласно настоящему изобретению пригодны в качестве фармацевтически активных компонентов для млекопитающих, в особенности для людей, для лечения заболеваний, вызванных тирозинкиназой. Эти заболевания включают пролиферацию опухолевых клеток, патологическую неоваскуляризацию (или ангиогенез), которые вызывают рост солидных опухолей, неоваскуляризацию глаза (диабетическую ретинопатию, дегенерацию желтого пятна, связанную со старением и т.д.) и воспаление(псориаз, ревматоидный артрит и т.д.). Настоящее изобретение охватывает применение соединений формулы I и/или их физиологически приемлемых солей и сольватов для приготовления лекарственного средства для лечения или предотвращения злокачественного новообразования. Предпочтительные карциномы для лечения выбирают из группы рака головного мозга, рака мочеполового тракта, рака лимфатической системы, рака желудка,рака гортани и рака легкого. Дальнейшей группой предпочтительных типов рака являются моноцитарный лейкоз, аденокарцинома легкого, мелкоклеточный рак легкого, рак поджелудочной железы, глиобластомы и рак молочной железы. Также охватывается применение соединений согласно п.1 в соответствии с изобретением и/или их физиологически приемлемых солей и сольватов для приготовления лекарственного средства для лечения или предотвращения заболевания, в которое вовлечен ангиогенез. Такое заболевание, в которое вовлечен ангиогенез, представляет собой заболевание глаз, такое как васкуляризация сетчатки, диабетическая ретинопатия, дегенерация желтого пятна, связанная со старением, и т.п. Применение соединений формулы I и/или их физиологически приемлемых солей и сольватов для приготовления лекарственного средства для лечения или предотвращения воспалительных заболеваний также подпадает под объем настоящего изобретения. Примерами таких воспалительных заболеваний являются ревматоидный артрит, псориаз, контактный дерматит, аллергическая реакция замедленного типа и т.п. Также охватывается применение соединений формулы I и/или их физиологически приемлемых солей и сольватов для приготовления лекарственного средства для лечения или предотвращения заболевания,индуцированного тирозинкиназой, или состояния, индуцированного тирозинкиназой, у млекопитающего,при котором в этом способе терапевтически эффективное количество соединения в соответствии с изобретением вводят больному млекопитающему, нуждающемуся в таком лечении. Терапевтическое количество изменяется в зависимости от конкретного заболевания и легко может быть определено специалистом в данной области. Настоящее изобретение также охватывает применение соединений формулы I и/или их физиологически приемлемых солей и сольватов для приготовления лекарственного средства для лечения или предотвращения васкуляризации сетчатки. Способы лечения или предотвращения глазных заболеваний, такие как диабетическая ретинопатия и дегенерация желтого пятна, связанная со старением, также являются частью изобретения. Применение для лечения или предотвращения воспалительных заболеваний, таких как ревматоидный артрит, псориаз,контактный дерматит и аллергическая реакция замедленного типа, а также лечение или предотвращение патологий костей из группы, включающей остеосаркому, остеоартрит и рахит, также подпадает под объем настоящего изобретения. Выражение "заболевания или состояния, индуцированные тирозинкиназой" относится к патологическим состояниям, которые зависят от активности одной или несколько тирозикиназ. Тирозинкиназы непосредственно или опосредованно принимают участие в путях передачи сигналов различных активностей клеток, включая пролиферацию, адгезию, миграцию и дифференциацию. Заболевания, связанные с активностью тирозинкиназы, включают пролиферацию опухолевых клеток, патологическую неоваскуляризацию, которая стимулирует рост солидных опухолей, неоваскуляризацию глаза (диабетическую ретинопатию, дегенерацию желтого пятна, связанную со старением, и т.д.) и воспаление (псориаз, ревматоидный артрит и т.д.). Соединения формулы I могут вводиться пациентам для лечения злокачественного новообразования,в особенности быстрорастущих опухолей. Таким образом, изобретение относится к применению соединений формулы I и их фармацевтически пригодных солей и стереоизомеров, включая их смеси во всех соотношениях, для приготовления лекарственного средства для лечения заболеваний, при которых играет роль ингибирование, регуляция и/или модуляция передачи сигналов с помощью киназы. Предпочтение в настоящем изобретении отдается Met киназе. Предпочтение отдается применению соединений формулы I и их фармацевтически пригодных со- 11021362 лей и стереоизомеров, включая их смеси во всех соотношениях, для приготовления лекарственного средства для лечения заболеваний, на которые оказывает влияние ингибирование тирозинкиназ соединениями по п.1. Отдельное предпочтение отдается применению для приготовления лекарственного средства для лечения заболеваний, на которые оказывает влияние ингибирование Met киназы соединениями в соответствии с п.1. Особое предпочтение отдается применению для лечения заболевания, где заболевание представляет собой солидную опухоль. Солидную опухоль предпочтительно выбирают из группы опухолей легкого, плоского эпителия,мочевого пузыря, желудка, почек, головы и шеи, пищевода, шейки матки, щитовидной железы, кишечника, печени, головного мозга, предстательной железы, мочеполового тракта, лимфатической системы,желудка и/или гортани. Солидную опухоль также предпочтительно выбирают из группы, включающей аденокарциному легкого, мелкоклеточный рак легкого, рак поджелудочной железы, глиобластомы, рак толстой кишки и рак молочной железы. Кроме того, предпочтительным является применение для лечения опухоли крови и иммунной системы, предпочтительно для лечения опухоли, выбранной из группы, включающей острый миелоидный лейкоз, хронический миелоидный лейкоз, острый лимфолейкоз и/или хронический лимфолейкоз. Описанные соединения формулы I могут вводиться в комбинации с другими известными лекарственными средствами, включая противораковые средства. Как используется в настоящем изобретении,термин "противораковое средство" относится к любому средству, которое вводят пациенту со злокачественным новообразованием для лечения рака. Противоопухолевое лечение, описанное в изобретении, может применяться в виде монотерапии,или дополнительно к соединению по изобретению можно также применять обычные хирургические методы или радиотерапию или химиотерапию. Такая химиотерапия может включать один или несколько следующих классов противоопухолевых средств:(i) антипролиферативные/противоопухолевые/повреждающие ДНК лекарственные средства и их комбинации, которые применяются в медицинской онкологии, такие как алкилирующие средства (например, цисплатин, карбоплатин, циклофосфамид, азотный иприт, мельфалан, хлорамбуцил, бусульфан и нитрозомочевины); антиметаболиты (например, антифолаты, такие как фторпиримидины, такие как 5 фторурацил и тегафур, ралтитрексед, метотрексат, арабинозид цитозина, гидроксимочевина и гемцитабин); противоопухолевые антибиотики (например, антрациклины, такие как адриамицин, блеомицин,доксорубицин, дауномицин, эпирубицин, идарубицин, митомицин-С, дактиномицин и митрамицин); антимитотические средства (например, алкалоиды барвинка, такие как винкристин, винбластин, виндезин и винорелбин и таксоиды, такие как таксол и таксотер); ингибиторы топоизомеразы (например, эпиподофиллотоксины, такие как этопозид и тенипозид, амсакрин, топотекан, иринотекан и камптотецин); и цитодифференцирующие средства (например, ретиноевая кислота, полностью находящаяся в трансконфигурации, 13-цис-ретиноевая кислота и фенретинид);(ii) цитостатические средства, такие как антиэстрогены (например, тамоксифен, торемифен, ралоксифен, дролоксифен и йодоксифен), ингибиторы рецептора эстрогена (например, фульвестрант); антиандрогены (например, бикалутамид, флутамид, нилутамид и ципротерон ацетат), антагонисты LHRH или агонисты LHRH (например, гозерелин, лейпрорелин и бузерелин), прогестероны (например, мегестрол ацетат), ингибиторы ароматазы (например, анастрозол, летрозол, воразол и эксеместан) и ингибиторы 5-редуктазы, такие как финастерид;(iii) средства, которые ингибируют инвазию злокачественных клеток (например, ингибиторы металлопротеиназы, такие как маримастат, и ингибиторы функции рецептора урокиназного активатора плазминогена);(iv) ингибиторы действия фактора роста, например такие ингибиторы включают антитела к фактору роста, антитела к рецептору фактора роста (например, анти-erbb2 антитело трастузумаб [Herceptin] и анти-erbb1 антитело цетуксимаб [С 225]), ингибиторы фарнезилтрансферазы, ингибиторы тирозинкиназы и ингибиторы серин-треонинкиназы, например ингибиторы семейства фактора роста эпидермиса (например, ингибиторы EGFR семейства тирозинкиназ, такие как N-(3-хлор-4-фторфенил)-7-метокси-6-(3 морфолинопропокси)хиназолин-4-амин(гефитиниб,AZD1839),N-(3-этинилфенил)-6,7-бис(2 метоксиэтокси)хиназолин-4-амин (эрлотиниб, OSI-774) и 6-акриламидо-N-(3-хлор-4-фторфенил)-7-(3 морфолинопропокси)хиназолин-4-амин (CI 1033, например, ингибиторы семейства фактора роста производных тромбоцитов и, например, ингибиторы семейства фактора роста гепатоцитов;(v) антиангиогенные вещества, такие как те, которые ингибируют действие фактора роста эндотелия сосудов, (например, антитело к фактору роста клеток эндотелия сосудов бевацизумаб [Avastin],соединения, которые описаны в опубликованных международных заявках на патент WO 97/22596, WO 97/30035, WO 97/32856 и WO 98/13354) и соединения, которые действуют по другому механизму (например, линомид, ингибиторы действия интегрина 3 и ангиостатин);(vi) вещества, повреждающие сосуды, такие как комбретастатин А 4 и соединения, описанные в международных заявках на патент WO 99/02166, WO 00/40529, WO 00/41669, WO 01/92224, WO 02/04434 иWO 02/08213; (vii) антисмысловая терапия, например, такая, которая направлена на вышеперечисленные мишени, такая как ISIS 2503, антисмысловая терапия на основе гена ras;(viii) способы генной терапии, включая, например, способы замены аберрантных генов, такие как способы аберрации р 53 или аберрации BRCA1 или BRCA2, GDEPT (пролекарственная терапия, направленная на ген фермента), способы с использованием деаминазы цитозина, тимидинкиназы или бактериальной нитроредуктазы и способы повышения устойчивости пациента к химиотерапии или радиотерапии, такие как генная терапия резистентности ко многим лекарственным средствам; и(ix) способы иммунотерапии, включая, например, способы повышения иммуногенности опухолевых клеток пациента в условиях ex vivo и in vivo, такие как трансфекция цитокинами, такими как интерлейкин 2, интерлейкин 4 или фактор стимуляции колоний гранулоцитов-макрофагов, способы снижения активности Т-клеток, способы с использованием трансфектированных иммунных клеток, таких как цитокин-трансфектированные дендритные клетки, способы с использованием цитокин-трансфектированных линий опухолевых клеток и способы с использованием антиидиотипичных антител. Лекарственные средства, приведенные ниже в табл. 1, предпочтительно, но не исключительно, комбинируют с соединениями формулы I. Комбинированное лечение этого типа можно осуществлять с помощью одновременного, последовательного или отдельного дозирования отдельных компонентов для лечения. В комбинированных продуктах этого типа используют соединения в соответствии с изобретением. Исследования. Соединения формулы I, описанные в примерах, исследовались в анализах, описанных ниже, и было обнаружено, что они обладают ингибирующей активностью по отношению к киназе. Из литературы известны другие исследования, и они легко могут быть осуществлены специалистом в данной области (см.,например, Dhanabal и др., Cancer Res. 59:189-197; Xin и др., J. Biol. Chem. 274:9116-9121; Sheu и др., Anticancer Res. 18:4435-4441; Ausprunk и др., Dev. Biol. 38:237-248; Gimbrone и др., J. Natl. Cancer Inst. 52:413-427; Nicosia и др., In Vitro 18:538- 549). Измерение активности Met киназы. Согласно данным производителя (Met, активная, upstate,по каталогу 14-526), Met киназу экспрессируют для получения белка в клетках насекомых (Sf21; S. frugiperda) и затем очищают с помощью аффинной хроматографии в виде "N-концевого 6His-меченого" рекомбинантного белка человека в баку- 18021362 ловирусном экспрессионном векторе. Активность киназы может быть измерена с помощью различных доступных измерительных систем. В исследовании сцинтилляционной схожести (Sorg и др., J. of. Biomolecular Screening, 2002, 7, 11-19),анализе флэш-планшетов или тесте связывания на фильтре измеряют радиоактивное фосфорилирование белка или пептида в качестве субстрата с помощью радиоактивно меченного АТФ (32 Р-АТФ, 33 Р-АТФ). В присутствии ингибиторного соединения может быть обнаружено снижение радиоактивного сигнала или отсутствие сигналов. Кроме того, в качестве методов исследования являются полезными способы гомогенного переноса энергии флуоресцентного резонанса с разрешением во времени (HTR-FRET) и флуоресцентной поляризации (FP) (Sills и др., J. of Biomolecular Screening, 2002, 191-214). В других нерадиоактивных способах анализа на основе ELISA используются специфические фосфоантитела (фосфо-АВ). Фосфо-АВ связываются только с фосфорилированным субстратом. Это связывание может быть определено с использованием вторичного антитела, конъюгированного в пероксидазой, с помощью хемолюминисценции (Ross и др., 2002, Biochem. J.). Метод флэш-планшетов (Met киназа). Используемыми тестируемыми планшетами являются микротитровальные планшеты на 96 лунокFlashplateR от Perkin Elmer ( кат. SMP200). Компоненты киназной реакции, описанные ниже, питетируют в планшет для исследования. Met киназу и субстрат поли Ala-Glu-Lys-Tyr, (pAGLT, 6:2:5:1), инкубируют в течение 3 ч при комнатной температуре с радиоактивно меченным 33 Р-АТФ в присутствии и отсутствие тестируемых веществ в общем объеме 100 мкл. Реакцию останавливают с помощью 150 мкл 60 мМ раствора EDTA. После инкубирования дополнительно в течение 30 мин при комнатной температуре супернататы отфильтровывают с отсасыванием и лунки три раза промывают каждый раз 200 мкл 0,9% раствора NaCl. Связанную радиоактивность в крови измеряют с помощью прибора для измерения сцинтилляции (Topcount NXT, Perkin-Elmer). Используемое истинное значение представляет киназную реакцию без ингибитора. Это приблизительно должно находиться в интервале 6000-9000 имп. в минуту. Используемое значение фармакологического нуля представляет собой стауроспорин в конечной концентрации 0,1 мМ. Значения ингибирования (IC50) определяют с помощью RS1MTS программы. Условия киназной реакции на лунку: Тестирование в условиях in-vivo (фиг. 1/1). Экспериментальная методика: самки мышей Balb/C (от Charles River Wiga) получали в возрасте 5 недель. Их акклиматизировали, выдерживая в условиях в течение 7 дней. После этого каждой мыши подкожно вводили в тазовую область в количестве 4 млн TPR-Met/NIH3T3 клеток в 100 мкл PBS (без Са иMg). Через 5 дней животных рандомизировали на 3 группы, таким образом, чтобы каждая группа из 9 мышей имела средний размер опухоли 110 мкл (интервал: 55-165). 100 мкл наполнителя (0,25% метилцеллюлозы/100 мМ ацетатный буфер, рН 5,5) вводили ежедневно контрольной группе и 200 мг/кг "А 56" или "А 91", растворенного в наполнителе (объем приблизительно 100 мкл/животное), вводили ежедневно подопытным группам, в каждом случае с помощью желудочного зонда. Через 9 дней в контроле средний объем опухоли составлял 1530 мкл и опыт заканчивали. Измерения объема опухоли: длину (L) и ширину (В) измеряли с помощью штангенциркуля и объем опухоли рассчитывали согласно формуле LВВ/2. Условия содержаний: 4 или 5 животных в клетке, питание с помощью коммерчески доступного корма для мышей (Sniff). Соединения "А 18" и "А 22" обладают значительным противоопухолевым действием. Выше и ниже все температуры приводятся в градусах Цельсия, С. В последующих примерах"обычная обработка" обозначает, что при необходимости добавляют воду, рН устанавливают, при необходимости, на значение от 2 до 10 в зависимости от состава конечного продукта, смесь экстрагируют этилацетатом или дихлорметаном, фазы разделяют, органическую фазу высушивают над сульфатом натрия и выпаривают и остаток очищают при помощи хроматографии на силикагеле и/или кристаллизации. ВЭЖХ методы. ВЭЖХ/МС исследования проводят в 3 мм колонке Silica-Rod с 210-секундным градиентом от 20 до 100% вода/ацетонитрил/0,01% трифторуксусной кислоты, при скорости потока 2,2 мл/мин и детектировании при 220 нм. ВЭЖХ исследования (метод А).("А 1") и 6-циклопропил-2-(3-5-[1-(2-пирролидин-1-илэтил)-1 Н-пиразол-4-ил]пиримидин-2-илбензил)2 Н-пиридазин-3-она ("А 2") проводят аналогично следующей схемы: 1.1. Смесь 16,6 г (180 ммоль) моногидрата глиоксиловой кислоты и 50 мл (535 ммоль) циклопропилметилкетона нагревают при 120 С в течение 2 ч при перемешивании. Реакционную смесь охлаждают до 40 С и добавляют 70 мл воды и 14 мл 32% водного раствора аммиака. Эту смесь троекратно экстрагируют дихлорметаном. К водной фазе добавляют 8,7 мл (179 ммоль) гидроксида гидразиния и смесь нагревают с обратным холодильником в течение 1 ч. Реакционную смесь охлаждают до комнатной температуры. Образовавшийся осадок отфильтровывают с отсасыванием, промывают водой и сушат в вакууме: 6-циклопропил-2 Н-пиридазин-3-он в виде бесцветных кристаллов; ESI 137. 1.2. К раствору, находящемуся под азотом, 427 г (1,50 моль) 5-бром-2-йодпиримидина в 1,5 л толуола добавляют раствор 318 г (3,00 ммоль) карбоната натрия в 1,5 л воды. Эту смесь нагревают до 80 С и добавляют 34,7 г (30 ммоль) тетракис(трифенилфосфин)палладия и раствор 228 г (1,50 моль) 3(гидроксиметил)бензолбороновой кислоты в 3 л этанола. Реакционную смесь затем нагревают с обратным холодильником в течение 18 ч. Реакционную смесь охлаждают до комнатной температуры, фильтруют и распределяют между водой и трет-бутилметиловым эфиром. Органическую фазу сушат над сульфатом натрия и концентрируют до объема 1 л. Образовавшийся осадок отфильтровывают с отсасыванием и промывают толуолом: [3-(5-бромпиримидин-2-ил)фенил]метанол в виде бесцветных кристаллов;ESI 265, 267. 1.3. Раствор, находящийся под азотом, 2,23 г (8,41 ммоль) [3-(5-бромпиримидин-2 ил)фенил]метанола, 1,49 г (10,9 ммоль) 6-циклопропил-2 Н-пиридазин-3-она и 3,34 г (12,6 ммоль) трифенилфосфина в 80 мл ТГФ охлаждают на ледяной бане и медленно по каплям добавляют 2,61 мл (12,6 ммоль) диизопропилазодикарбоксилата (DIAD). Реакционную смесь перемешивают при комнатной температуре в течение 2 ч и упаривают. Остаток хроматографируют на силикагелевой колонке с дихлорметан/метанолом в качестве элюента. Фракции, содержащие продукт, объединяют, упаривают и перекристаллизовывают из изопропанола: 2-[3-(5-бромпиримидин-2-ил)бензил]-6-циклопропил-2 Н-пиридазин-3 он ("А 1") в виде бесцветных кристаллов; ESI 383, 385; 1 Н-ЯМР (ДМСО-d6):[м.д.] 0.80 (m, 2 Н), 0.93 (m, 2 Н), 1.96 (m, 1 Н), 5.26 (s, 2H), 6.91 (d, J = 9.5 Гц,- 21021362 1 Н), 7.29 (d, J = 9.5 Гц, 1 Н), 7.46 (dt, J1 = 7.5 Гц, J2 = 1 Гц, 1 Н), 7.51 (t, J = 7.5 Гц, 1 Н), 8.27 (dt, J1 = 7.5 Гц,J2 = 1 Гц, 1 Н), 8.30 (t, J = 1 Гц, 1 Н), 9.07 (s, 2H). 1.4. К раствору 8,58 г (43,3 ммоль) пинаколил пиразол-4-бороната в 86 мл ацетонитрила добавляют 15,0 г (86,7 ммоль) гидрохлорида N-(2-хлорэтил)пирролидина и 42,4 г (130 ммоль) карбоната цезия и образовавшуюся суспензию перемешивают при комнатной температуре в течение 18 ч. Реакционную смесь фильтруют и остаток промывают ацетонитрилом. Фильтрат упаривают и остаток распределяют между насыщенным раствором хлорида натрия и этилацетатом. Органическую фазу сушат над сульфатом натрия и упаривают: 10,9 г 1-(2-пирролидин-1-илэтил)-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2 ил)-1 Н-пиразола в виде желтого масла; ESI 292. 1.5. К раствору, находящемуся под азотом, 394 мг (1,00 ммоль) 2-[3-(5-бромпиримидин-2 ил)бензил]-6-циклопропил-2 Н-пиридазин-3-она и 337 мг (1,10 ммоль) 1-(2-пирролидин-1-илэтил)-4(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1 Н-пиразола в 10 мл 1,2-диметоксиэтана добавляют 425 мг (2,0 ммоль) тригидрата трикалий фосфата и 56,2 мг (0,08 ммоль) хлорида бис(трифенилфосфин)палладия и смесь перемешивают при 80 С в течение 18 ч. Реакционную смесь фильтруют через кизельгур и промывают дихлорметаном. Фильтрат упаривают и остаток хроматографируют на силикагелевой колонке с дихлорметан/метанолом в качестве элюента: 6-циклопропил-2-(3-5-[1-(2-пирролидин-1 илэтил)-1 Н-пиразол-4-ил]пиримидин-2-илбензил)-2 Н-пиридазин-3-он ("А 2") в виде бесцветного масла;(d, J = 7.5 Гц, 1 Н), 7.50 (t, J = 7.5 Гц, 1 Н), 8.11 (s, 1 Н), 8.31 (d, J = 7.5 Гц, 1 Н), 8.33 (bs, 1H), 8.45 (s, 1H),9.14 (s, 2H). Следующие соединения получают аналогично: 6-циклопропил-2-(3-5-[1-(2-морфолин-4-илэтил)-1 Н-пиразол-4-ил]пиримидин-2-илбензил)-2 Нпиридазин-3-он("А 4") проводят аналогично следующей схеме: 2.1. К суспензии 2,41 г (10,0 ммоль) метил 3-карбамимидоилбензоатацетата в 40 мл метанола добавляют 1,31 мл (11,0 ммоль) 3-этоксиметакролеина и 2,04 мл (11,0 ммоль) 30% раствора этилата натрия в метаноле и получающийся раствор перемешивают при 50 С в течение 18 ч. Реакционная смесь упаривают в вакууме и добавляют воду. Образовавшийся осадок отфильтровывают с отсасыванием, промывают водой и сушат в вакууме: метил 3-(5-метилпиримидин-2-ил)бензоат в виде бесцветных кристаллов;ESI 229. 2.2. К суспензии 400 мг (10,6 ммоль) борогидрида натрия в 20 мл ТГФ добавляют 600 мг (5,41 ммоль) порошкообразного хлорида кальция и смесь перемешивают при комнатной температуре в течение 1,5 ч. К этой суспензии по каплям при перемешивании добавляют раствор 751 мг (3,29 ммоль) метил 3-(5-метилпиримидин-2-ил)бензоата в 10 мл ТГФ и смесь перемешивают при комнатной температуре в течение 18 ч. К реакционной смеси добавляют 10 мл 1 н. NaOH, воду и дихлорметан и затем смесь фильтруют. Органическую фазу фильтрата отделяют, сушат над сульфатом натрия и упаривают. Остаток хроматографируют на силикагелевой колонке с дихлорметан/метанолом в качестве элюента: [3-(5 метилпиримидин-2-ил)фенил]метанол в виде бесцветного твердого вещества; ESI 201. 2.3. К раствору 68,1 мг (0,50 ммоль) 6-циклопропил-2 Н-пиридазин-3-она, 100 мг (0,50 ммоль) [3-(5 метилпиримидин-2-ил)фенил]метанола и 197 мг (0,75 ммоль) трифенилфосфина в 3 мл ТГФ по каплям добавляют 147 мкл (0,75 ммоль) диизопропил диазодикарбоксилата и получающийся раствор перемешивают при комнатной температуре в течение 18 ч. Реакционную смесь упаривают в вакууме и остаток хроматографируют на силикагелевой колонке с дихлорметан/метанолом в качестве элюента: 6 циклопропил-2-[3-(5-метилпиримидин-2-ил)бензил]-2 Н-пиридазин-3-он ("А 4") в виде бесцветного твердого вещества; ESI 319. Пример 3. Получение 6-циклопропил-2-3-[5-(1-пиперидин-4-ил-1 Н-пиразол-4-ил)пиримидин-2 ил]бензил-2 Н-пиридазин-3-она ("А 5") проводят аналогично следующей схеме: 3.1. К раствору, находящемуся под азотом, 599 мг (1,50 ммоль) 2-[3-(5-бромпиримидин-2 ил)бензил]-6-циклопропил-2 Н-пиридазин-3-она и 623 мг (1,65 ммоль) трет-бутил 4-[4-(4,4,5,5 тетраметил-1,3,2-диоксаборолан-2-ил)пиразол-1-ил]пиперидин-1-карбоксилата (полученного, как описано в WO 2007/066187) в 15 мл 1,2-диметоксиэтана добавляют 637 мг (3,0 ммоль) тригидрата трикалий фосфата и 84,2 мг (0,12 ммоль) хлорида бис(трифенилфосфин)палладия и смесь перемешивают при 80 С в течение 18 ч. Реакционную смесь фильтруют через кизельгур и промывают дихлорметаном. Фильтрат промывают водой. Органическую фазу сушат над сульфатом натрия и упаривают. Остаток хроматографируют на силикагелевой колонке с дихлорметан/метанолом в качестве элюента: трет-бутил 4-(4-2-[3(3-циклопропил-6-оксо-6 Н-пиридазин-1-илметил)фенил]пиримидин-5-илпиразол-1-ил)пиперидин-1 карбоксилат в виде желтоватого высоковязкого масла; ESI 554. 3.2. К суспензии 692 мг (1,24 ммоль) трет-бутил 4-(4-2-[3-(3-циклопропил-6-оксо-6 Н-пиридазин-1 илметил)фенил]пиримидин-5-илпиразол-1-ил)пиперидин-1-карбоксилата в 5 мл 4 н. HCl в диоксане добавляют 2 мл метанола и смесь нагревают при 80 С в течение 5 мин. Реакционную смесь упаривают и последовательно добавляют воду, дихлорметан и насыщенный раствор гидрокарбоната натрия. Органическую фазу отделяют, сушат над сульфатом натрия и упаривают. Остаток перекристаллизовывают из трет-бутилметилового эфира: 6-циклопропил-2-3-[5-(1-пиперидин-4-ил-1 Н-пиразол-4-ил)пиримидин-2 ил]бензил-2 Н-пиридазин-3-он ("А 5") в виде бесцветных кристаллов; ESI 454; 1 Н-ЯМР (ДМСО-d6):[м.д.] 0.81 (m, 2 Н), 0.94 (m, 2 Н), 1.80 (m, 2 Н), 1.99 (m, 3 Н), 2.60 (m, 2 Н), 3.05 получают аналогично. Пример 4. Получение 6-циклопропил-2-[3-(5-метил-1,2,4-оксадиазол-3-ил)бензил]-2 Н-пиридазин-3 она ("А 7") проводят аналогично следующей схеме: К раствору 68,1 мг (0,50 моль) 6-циклопропил-2 Н-пиридазин-3-она и 126,5 мг (0,50 ммоль) 3-(3 бромметилфенил)-5-метил-1,2,4-оксадиазола (полученного, как описано W.W.K.R. Mederski и др., Tetrahedron 55, 1999, 12757-12770) в 1 мл диметилформамида (ДМФА) добавляют 169 мг (1,0 ммоль) карбоната цезия и образовавшуюся суспензию перемешивают при комнатной температуре в течение 18 ч. К реакционной смеси добавляют воду и трет-бутилметиловый эфир. Органическую фазу отделяют, сушат над сульфатом натрия и упаривают. Остаток хроматографируют на силикагелевой колонке с дихлорметан/метанолом в качестве элюента: 6-циклопропил-2-[3-(5-метил-1,2,4-оксадиазол-3-ил)бензил]-2 Нпиридазин-3-он ("А 7") в виде бесцветных кристаллов; ESI 309. Пример 5. Получение 6-циклопропил-2-3-[5-(3-диметиламинопропокси)пиримидин-2-ил]бензил 2 Н-пиридазин-3-она ("А 8") проводят аналогично следующей схеме: 5.1. К суспензии, выдерживаемой при 30 С, 500 г (3,40 моль) 3-цианобензойной кислоты в 8 л метанола порциями при перемешивании добавляют 1382 г (10,0 моль) карбоната калия. Затем при внутренней температуре от 40 до 45 С небольшими порциями добавляют 695 г (10,0 моль) хлорида гидроксиламмония. Реакционную смесь нагревают до кипения в течение 15 ч. Реакционную смесь упаривают в вакууме, растворяют в воде и подкисляют с использованием 37% водной соляной кислоты. Образовавшийся осадок отфильтровывают с отсасыванием, промывают водой и сушат в вакууме: 3-(Nгидроксикарбамимидоил)бензойная кислота в виде бесцветных кристаллов; ESI 181. 5.2. Смесь 614 г (3,41 моль) 3-(N-гидроксикарбамимидоил)бензойной кислоты, 756 мл (8,0 моль) уксусного ангидрида и 2 л уксусной кислоты нагревают при температуре 118 С в течение 14 ч. Реакционную смесь охлаждают до 6 С и фильтруют с отсасыванием. Остаток переносят в 2 л воды, отфильтровывают с отсасыванием и хорошо промывают водой. Остаток перекристаллизовывают из этанола/воды: 3-(5-метил-1,2,4-оксадиазол-3-ил)бензойная кислота в виде бесцветных кристаллов; т.пл. 225 С; ESI 205. 5.3. К суспензии 30.0 г (147 ммоль) 3-(5-метил-1,2,4-оксадиазол-3-ил)бензойной кислоты в 150 мл метанола добавляют 7,83 мл (147 ммоль) концентрированной серной кислоты и смесь нагревают до кипения в течение 18 ч. Реакционную смесь охлаждают на ледяной бане, добавляют воду и продукт отфильтровывают с отсасыванием и хорошо промывают водой: метил 3-(5-метил-1,2,4-оксадиазол-3 ил)бензоат в виде бесцветных кристаллов; ESI 219. 5.4. К раствору 327 г (1,47 моль) метил 3-(5-метил-1,2,4-оксадиазол-3-ил)бензоата в 3 л метанола добавляют 150 мл уксусной кислоты, 150 мл воды и 50 г увлажненного водой никеля Ренея и смесь гидрируют при комнатной температуре и атмосферном давлении в течение 18 ч. Катализатор отфильтровывают и фильтрат упаривают. Остаток переносят в трет-бутилметиловый эфир, нагревают до кипения и отфильтровывают с отсасыванием. Остаток сушат в вакууме: ацетат 3-метоксикарбонилбензамидиния в виде бесцветных кристаллов; ESI 179. 5.5. К суспензии 259 г (1,09 моль) ацетата 3-метоксикарбонилбензамидиния и 528 г (1,08 моль) дигексафторфосфата (2-диметиламино-1-[диметилиммониометил]виниламинометилен)диметиламмония(полученного, как описано С.В. Dousson и др., Synthesis 2005, 1817) в 1 л метанола по каплям при перемешивании добавляют 2,2 л свежеприготовленного 1,5 М раствора метилата натрия. Реакционную смесь затем нагревают до 60 С в течение 40 мин и выдерживают при этой температуре в течение 30 мин. Реакционную смесь затем охлаждают до комнатной температуры, разбавляют 10 л дихлорметана и троекратно промывают 5 л воды каждый раз. Органическую фазу сушат над сульфатом натрия и упаривают. Остаток перекристаллизовывают из этилацетата: метил 3-[5-(диметиламинометиленамино)пиримидин-2 ил]бензоат в виде бежевых кристаллов; т.пл. 140 С, ESI 285. 5.6. К суспензии 103,5 г (364 ммоль) метил 3-[5-(диметиламинометиленамино)пиримидин-2 ил]бензоата в 1,3 л воды добавляют 160 мл (2,88 моль) концентрированной серной кислоты и смесь нагревают до кипения в течение 4 ч. Реакционную смесь охлаждают до комнатной температуры, разбавляют водой и фильтруют с отсасыванием. Остаток промывают водой и сушат в вакууме: 3-(5 гидроксипиримидин-2-ил)бензойная кислота в виде коричневатых кристаллов; ESI 217. 5.7. К суспензии 88,0 г (366 ммоль) 3-(5-гидроксипиримидин-2-ил)бензойной кислоты в 1,4 л метанола добавляют 32,7 мл (445 ммоль) тионилхлорида и смесь нагревают при 80 С в течение 2 ч. Затем добавляют 20 мл (276 ммоль) тионилхлорида и дополнительные 10 мл (138 ммоль) тионилхлорида. После каждого добавления реакционную смесь перемешивают при 80 С в течение 2 ч. Реакционную смесь концентрируют в вакууме до объема приблизительно 300 мл и образовавшийся осадок отфильтровывают и сушат в вакууме: метил 3-(5-гидроксипиримидин-2-ил)бензоат в виде коричневатых кристаллов; ESI 231. 5.8. Раствор, находящийся под азотом, 6,1 г (26,5 ммоль) метил (5-гидроксипиримидин-2 ил)бензоата, 10,5 г (39,8 ммоль) трифенилфосфина и 4,76 мл (39,8 ммоль) 3-(диметиламино)-1-пропанола в 200 мл ТГФ охлаждают на ледяной бане и медленно по каплям при перемешивании добавляют 8,21 мл(39,8 ммоль) диизопропил азодикарбоксилата. После перемешивания реакционной смеси при комнатной температуре в течение 2 ч ее упаривают в вакууме. Остаток распределяют между дихлорметаном и насыщенным водным раствором гидросульфата калия. Водную фазу отделяют, значение рН устанавливают на 12 с использованием насыщенного водного раствора гидроксида натрия и дважды экстрагируют дихлорметаном. Органическую фазу сушат над сульфатом натрия и упаривают. Остаток хроматографируют на силикагелевой колонке с дихлорметан/метанолом в качестве элюента: метил 3-[5-(3 диметиламинопропокси)пиримидин-2-ил]бензоат в виде бесцветных кристаллов; ESI 316. 5.9. К раствору, находящемуся под азотом, 12,6 г (40,0 ммоль) метил 3-[5-(3 диметиламинопропокси)пиримидин-2-ил]бензоата в 200 мл ТГФ по каплям при перемешивании добавляют 200 мл 1 М раствора диизобутилалюминий гидрида в ТГФ. После перемешивания смеси при комнатной температуре в течение 1 ч по каплям добавляют 10 мл насыщенного водного раствора сульфата натрия. Образовавшийся осадок отфильтровывают с отсасыванием и промывают дихлорметаном. Фильтрат сушат над сульфатом натрия и упаривают. Остаток переносят в смесь диэтилового эфира и петролейного эфира. Образовавшийся осадок отфильтровывают с отсасыванием, промывают петролейным эфиром и сушат в вакууме: 3-[5-(3-диметиламинопропокси)пиримидин-2-ил]фенилметанол в виде бесцветных кристаллов; т.пл. 95-97 С; ESI 288. 5.10. Суспензию 144 мг (0,50 ммоль) 3-[5-(3-диметиламинопропокси)пиримидин-2 ил]фенилметанола, 88,5 мг (0,65 ммоль) 6-циклопропил-2 Н-пиридазин-3-она и 199 мг (0,75 ммоль) трифенилфосфина в 1 мл ТГФ охлаждают на ледяной бане и медленно по каплям добавляют 160 мг (0,75 ммоль) диизопропил азодикарбоксилата. После перемешивания смеси при комнатной температуре в течение 1 ч добавляют этилацетат и 2 н. водную соляную кислоту. Водную фазу отделяют и троекратно промывают этилацетатом. Значение рН водной фазы устанавливают на 14 с использованием 2 н. раствора гидроксида натрия и дважды экстрагируют этилацетатом. Органическую фазу сушат над сульфатом натрия и упаривают. Остаток очищают с помощью препаративной ВЭЖХ. Фракции, содержащие продукт,упаривают, растворяют в 0,5 мл 1 н. водной соляной кислоты и небольшом количестве воды и лиофилизируют: гидрохлорид 6-циклопропил-2-3-[5-(3-диметиламинопропокси)пиримидин-2-ил]бензил-2 Нпиридазин-3-она ("А 8") в виде бесцветного стекла; ESI 406; 1 Н-ЯМР (ДМСО-d6):[м.д.] 0.80 (m, 2 Н), 0.93 (m, 2 Н), 1.96 (m, 1 Н), 2.21 (m, 2 Н), 2.78 (d, J = 5 Гц,6 Н), 3.22 (m, 2 Н), 4.31 (t, J = 6 Гц, 2 Н), 5.25 (s, 2H), 6.91 (d, J = 9.5 Гц, 1 Н), 7.29 (d, J = 9.5 Гц, 1 Н), 7.37 (d,J = 7.5 Гц, 1 Н), 7.46 (t, J = 7.5 Гц, 1 Н), 8.22 (d, J = 7.5 Гц, 1 Н), 8.25 (bs, 1H), 8.65 (s, 2H), 10.57 (bs, 1H). Следующие соединения получают аналогично: 6-циклопропил-2-3-[5-(1-метилпиперидин-4-илокси)пиримидин-2-ил]бензил-2 Н-пиридазин-3-он Пример 6. Получение 6-циклопропил-2-3-[5-(4-метилпиперазин-1-ил)пиримидин-2-ил]бензил-2 Нпиридазин-3-она ("А 12") проводят аналогично следующей схеме: 6.1. К раствору 23,3 г (82,1 ммоль) метил 3-[5-(диметиламинометиленамино)пиримидин-2 ил]бензоата в 300 мл диоксана добавляют раствор 30 г (215 ммоль) карбоната калия в 500 мл воды и смесь перемешивают при 100 С в течение 12 ч. Реакционную смесь охлаждают до комнатной температуры и значение рН устанавливают на 6-7 с использованием 35 мл 37% водной соляной кислоты. Раствор большей частью упаривают в вакууме и лиофилизируют (сырая 3-(5-аминопиримидин-2-ил)бензойная кислота; ESI 216). К остатку добавляют 400 мл метанола и к получающейся суспензии при охлаждении льдом добавляют по каплям 26 мл концентрированной серной кислоты. Реакционную смесь перемешивают при комнатной температуре в течение 6 ч, затем добавляют 500 мл воды и при охлаждении льдом добавляют 32% водный раствор гидроксида натрия до достижения основных значений рН. Смесь экстра- 27021362 гируют этилацетатом. Органическую фазу сушат над сульфатом натрия и упаривают: метил 3-(5 аминопиримидин-2-ил)бензоат в виде коричневого твердого вещества; ESI 230. 6.2. К раствору 2,50 г (10,9 ммоль) метил 3-(5-аминопиримидин-2-ил)бензоата в 10 мл 1-метил-2 пирролидона добавляют 2,59 г (1,7 ммоль) карбоната калия и 3,6 г (1,7 ммоль) хлорида бис(2 хлорэтил)метиламмония, и суспензию перемешивают под аргоном при 120 С в течение 18 ч и при 140 С в течение 6 ч. Реакционную смесь охлаждают до комнатной температуры, добавляют 150 мл воды и смесь фильтруют через кизельгур. Значение рН фильтрата устанавливают на 14 с использованием 32% раствора гидроксида натрия и дважды экстрагируют этилацетатом. Объединенные органические фазы сушат над сульфатом натрия и упаривают: метил 3-[5-(4-метилпиперазин-1-ил)пиримидин-2-ил]бензоат в виде коричневого масла; ESI 313. 6.3. К раствору, находящемуся подаргоном, 860 мг (2,75 ммоль) метил 3-[5-(4-метилпиперазин-1 ил)пиримидин-2-ил]бензоата в 16 мл ТГФ при комнатной температуре добавляют по каплям 13,8 мл 1 М раствора гидрида диизобутилалюминия в ТГФ. К реакционной смеси добавляют 3 мл насыщенного раствора сульфата натрия и дихлорметан. Образовавшийся осадок отфильтровывают с отсасыванием и промывают дихлорметаном. Фильтрат сушат над сульфатом натрия и упаривают: 3-[5-(4-метилпиперазин 1-ил)пиримидин-2-ил]фенилметанол в виде желтого твердого вещества; ESI 285. 6.4. К раствору, находящемуся под аргоном, 547 мг (0,402 ммоль) 6-циклопропил-2 Н-пиридазин-3 она и 114 мг (0,402 ммоль) 3-[5-(4-метилпиперазин-1-ил)пиримидин-2-ил]фенилметанола в 3 мл ТГФ и 1 мл ДМФА добавляют 402 мг (соответствует 1,2 ммоль) полимерсвязанного трифенилфосфина и 277 мг(1,20 ммоль) ди-трет-бутилазодикарбоксилата и смесь перемешивают при комнатной температуре в течение 3 ч. Реакционную смесь фильтруют через кизельгур с отсасыванием. Фильтрат упаривают и очищают с помощью препаративной ВЭЖХ: бистрифторацетат 6-циклопропил-2-3-[5-(4-метилпиперазин 1-ил)пиримидин-2-ил]бензил-2 Н-пиридазин-3-она ("А 12") в виде бесцветного масла; ESI 403. Пример 7. Получение 6-изопропил-2-(3-5-[1-(2-морфолин-4-илэтил)-1 Н-пиразол-4-ил]пиримидин 2-илбензил)-2 Н-пиридазин-3-она ("А 13") проводят аналогично следующей схеме: 7.1. Смесь 14,4 г (157 ммоль) моногидрата глиоксиловой кислоты и 50 мл (464 ммоль) изопропилметилкетона нагревают при 120 С при перемешивании в течение 2 ч. Реакционную смесь охлаждают до 40 С и добавляют 70 мл воды и 12 мл 32% водного раствора аммиака. Эту смесь троекратно экстрагируют дихлорметаном. К водной фазе добавляют 7,55 мл (155 ммоль) гидроксида гидразиния и смесь нагревают с обратным холодильником в течение 18 ч. Реакционную смесь охлаждают до комнатной температуры и экстрагируют дихлорметаном. Органическую фазу сушат над сульфатом натрия и упаривают. Остаток хроматографируют на силикагелевой колонке с помощью петролейного эфира/третбутилметилового эфира в качестве элюента с получением 4-гидрокси-5,5,6-триметил-4,5-дигидро-2 Нпиридазин-3-она в виде бесцветных кристаллов (ESI 157) и 6-изопропил-2 Н-пиридазин-3-она в виде бесцветных кристаллов (ESI 139). Следующее соединение было получено с помощью этого способа аналогично: 6-циклобутил-2 Нпиридазин-3-он. 7.2. К раствору, находящемуся под азотом, 2,65 г (10,0 моль) [3-(5-бромпиримидин-2- 28021362 ил)фенил]метанола и 3,38 г (11,0 ммоль) 4-2-[4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиразол-1 ил]этилморфолина в 50 мл 1,2-диметоксиэтана добавляют 4,25 г (20,0 ммоль) тригидрата трикалий фосфата и 842 мг (1,2 ммоль) хлорида бис(трифенилфосфин)палладия и смесь перемешивают при 80 С в течение 18 ч. Дихлорметан и воду добавляют к реакционной смеси, которую затем фильтруют через кизельгур, и остаток промывают дихлорметаном. Органическую фазу отделяют, сушат над сульфатом натрия и упаривают. Остаток перекристаллизовывают из 2-пропанола с получением (3-5-[1-(2-морфолин 4-илэтил)-1 Н-пиразол-4-ил]пиримидин-2-илфенил)метанола в виде желтоватых кристаллов; ESI 366. 7.3. Раствор, находящийся под азотом, 324 мг (0,70 ммоль) (3-5-[1-(2-морфолин-4-илэтил)-1 Нпиразол-4-ил]пиримидин-2-илфенил)метанола, 131 мг (0,91 ммоль) 6-изопропил-2 Н-пиридазин-3-она и 278 мг (1,05 ммоль) трифенилфосфина в 1,4 мл ТГФ охлаждают на ледяной бане и по каплям добавляют 217 мкл (1,056 ммоль) диизопропилазодикарбоксилата. После перемешивания реакционной смеси при комнатной температуре в течение 2 ч ее упаривают. Остаток хроматографируют на силикагелевой колонке с дихлорметан/метанолом в качестве элюента с получением 6-изопропил-2-(3-5-[1-(2-морфолин 4-илэтил)-1 Н-пиразол-4-ил]пиримидин-2-илбензил)-2 Н-пиридазин-3-она ("А 13") в виде желтоватых кристаллов; ESI 486; 1 Н-ЯМР (ДМСО-d6):[м.д.] 1.20 (d, J = 7 Гц, 6 Н), 2.44 (m, 4H), 2.77 (t, J = 6.5 Гц, 2 Н), 2.90 (септет, J = 7 Гц, 1 Н), 3.57 (m, 4 Н), 4.30 (t, J = 6.5 Гц, 2 Н), 5.31 (s, 2H), 6.97 (d, J = 9.3 Гц, 1 Н), 7.44 (d, J = 7.5 Гц, 1 Н),7.50 (t, J = 7.5 Гц, 1 Н), 7.51 (d, J = 9.3 Гц, 1 Н), 8.11 (s, 1 Н), 8.31 (d, J = 7.5 Гц, 1 Н), 8.36 (bs, 1H), 8.44 (s,1H), 9.13 (s, 2H). Следующее соединение получают аналогично: трифторацетат 2-(3-5-[1-(2-морфолин-4-илэтил)-1 Н-пиразол-4-ил]пиримидин-2-илбензил)-2 Нпиридазин-3-она ("А 14")("А 18") проводят аналогично следующей схеме. Отдельные стадии реакции проводят аналогично соответствующим реакциям примеров 5 и 6
МПК / Метки
МПК: C07D 401/14, A61K 31/501, C07D 403/10, C07D 403/14, A61P 35/00
Метки: производные, ингибиторов, киназы, качестве, мет, 2-бензилпиридазинона
Код ссылки
<a href="https://eas.patents.su/30-21362-proizvodnye-2-benzilpiridazinona-v-kachestve-ingibitorov-met-kinazy.html" rel="bookmark" title="База патентов Евразийского Союза">Производные 2-бензилпиридазинона в качестве ингибиторов мет киназы</a>
Предыдущий патент: Смесь для применения в автомобилях
Следующий патент: Пресс с переключаемой планетарной коробкой передач
Случайный патент: Способы обработки поверхностей ионными кремнийорганическими композициями












