Оксазолзамещенные индазолы в качестве ингибиторов pi3-киназ, содержащая их фармацевтическая композиция и их применение в лечении расстройств, опосредованных ненадлежащей активностью pi3-киназ
Номер патента: 21056
Опубликовано: 31.03.2015
Авторы: Хэмблин Джули Николь, Митчелл Шарлотт Джейн, Ли Джоэль, Килинг Сюзанн Элейн, Джоунс Пол Спенсер, Парр Найджел Джеймс
Формула / Реферат
1. Соединение формулы (I)
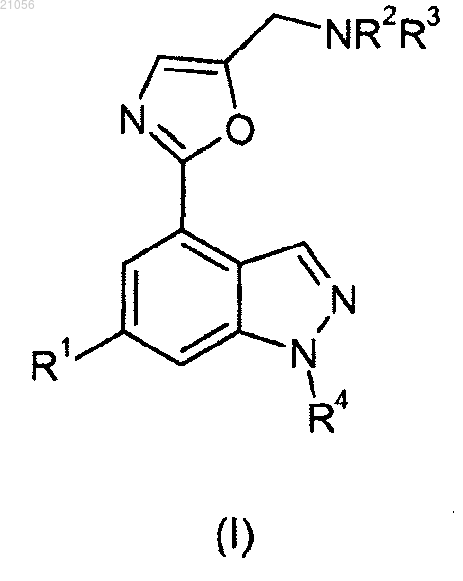
где R1 представляет собой 9-членный бициклический гетероарил, причем указанный 9-членный бициклический гетероарил содержит один или два атома азота, или пиридинил, возможно замещенный одним или двумя заместителями, независимо выбранными из -OR6 и -NHSO2R7;
R2 и R3 вместе с атомом азота, к которому они присоединены, связаны с образованием 6- или 7-членного гетероциклила, причем указанный 6- или 7-членный гетероциклил, возможно, содержит атом кислорода или дополнительный атом азота и, возможно, замещен одним или двумя заместителями, независимо выбранными из С1-6алкила;
R4 представляет собой водород или метил;
R6 представляет собой водород или С1-4алкил и
R7 представляет собой С1-6алкил или фенил, возможно замещенный одним или двумя заместителями, независимо выбранными из галогено,
или его соль.
2. Соединение по п.1 или его соль, где R1 представляет собой индолил.
3. Соединение по п.1 или его соль, где R1 представляет собой пиридинил, возможно замещенный одним или двумя заместителями, независимо выбранными из -OR6 и -NHSO2R7.
4. Соединение по любому из пп.1-3 или его соль, где R2 и R3 вместе с атомом азота, к которому они присоединены, связаны с образованием 6-членного гетероциклила, причем указанный 6-членный гетероциклил, возможно, содержит атом кислорода или дополнительный атом азота и, возможно, замещен одним или двумя заместителями, независимо выбранными из С1-6алкила.
5. Соединение по любому из пп.1-4 или его соль, где R2 и R3 вместе с атомом азота, к которому они присоединены, связаны с образованием 6-членного гетероциклила, причем указанный 6-членный гетероциклил содержит атом кислорода и, возможно, замещен одним или двумя заместителями, независимо выбранными из С1-4алкила.
6. Соединение по любому из пп.1-4 или его соль, где R2 и R3 вместе с атомом азота, к которому они присоединены, связаны с образованием 6-членного гетероциклила, причем указанный 6-членный гетероциклил содержит дополнительный атом азота и, возможно, замещен С1-4алкилом.
7. Соединение по любому из пп.1-6 или его соль, где R4 представляет собой водород.
8. Соединение, выбранное из группы, включающей
N-[5-[4-(5-{[(2R,6S)-2,6-диметил-4-морфолинил]метил}-1,3-оксазол-2-ил)-1H-индазол-6-ил]-2-(метилокси)-3-пиридинил]метансульфонамид;
N-[5-[4-(5-{[4-(1-метилэтил)-1-пиперазинил]метил}-1,3-оксазол-2-ил)-1Н-индазол-6-ил]-2-(метилокси)-3-пиридинил]метансульфонамид;
N-[5-[4-(5-{[(2R,6S)-2,6-диметил-4-морфолинил]метил}-1,3-оксазол-2-ил)-1Н-индазол-6-ил]-2-(метилокси)-3-пиридинил]-2,4-дифторбензолсульфонамид;
2,4-дифтор-N-[5-[4-(5-{[4-(1-метилэтил)-1-пиперазинил]метил}-1,3-оксазол-2-ил)-1H-индазол-6-ил]-2-(метилокси)-3-пиридинил]бензолсульфонамид;
4-(5-{[(2R,6S)-2,6-диметил-4-морфолинил]метил}-1,3-оксазол-2-ил)-6-(1Н-индол-4-ил)-1Н-индазол;
6-(1Н-индол-4-ил)-4-(5-{[4-(1-метилэтил)-1-пиперазинил]метил}-1,3-оксазол-2-ил)-1Н-индазол;
6-(1H-индол-4-ил)-4-[5-(4-морфолинилметил)-1,3-оксазол-2-ил]-1Н-индазол;
N-[5-[4-(5-{[(2R,6R)-2,6-диметил-4-морфолинил]метил}-1,3-оксазол-2-ил)-1Н-индазол-6-ил]-2-(метилокси)-3-пиридинил]метансульфонамид;
6-(1H-индол-4-ил)-4-[5-(1-пиперазинилметил)-1,3-оксазол-2-ил]-1H-индазол,
или его соль.
9. Соединение, которое представляет собой N-[5-[4-(5-{[(2R,6S)-2,6-диметил-4-морфолинил]метил}-1,3-оксазол-2-ил)-1Н-индазол-6-ил]-2-(метилокси)-3-пиридинил]метансульфонамид
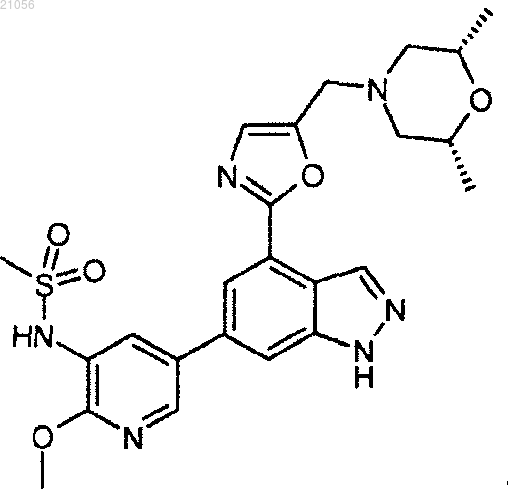
или его соль.
10. Соединение, которое представляет собой 6-(1Н-индол-4-ил)-4-(5-{[4-(1-метилэтил)-1-пиперазинил]метил}-1,3-оксазол-2-ил)-1Н-индазол

или его соль.
11. Соединение по любому из пп.1-10 в форме его фармацевтически приемлемой соли.
12. Соединение, которое представляет собой N-[5-[4-(5-{[(2R,6S)-2,6-диметил-4-морфолинил]метил}-1,3-оксазол-2-ил)-1H-индазол-6-ил]-2-(метилокси)-3-пиридинил]метансульфонамид
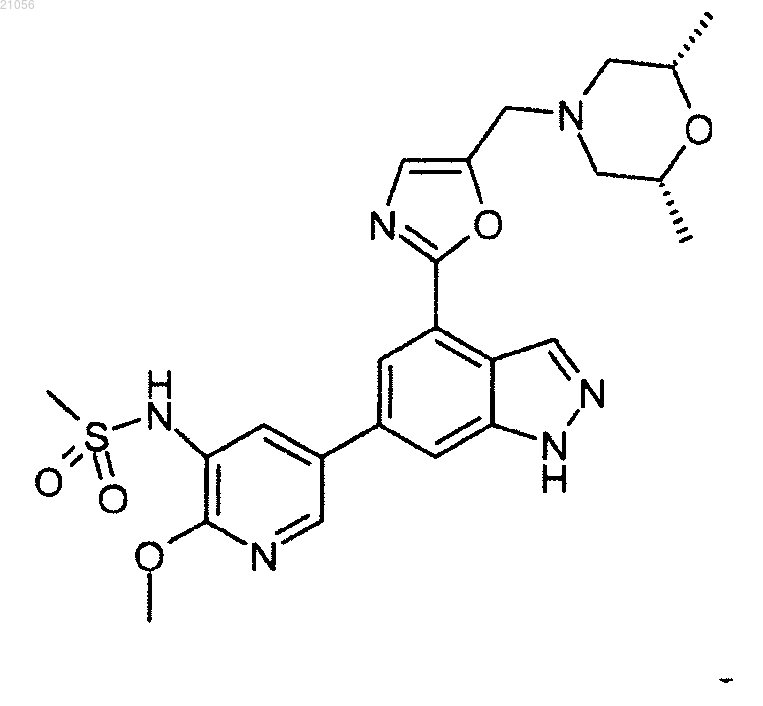
13. Соединение, которое представляет собой 6-(1Н-индол-4-ил)-4-(5-{[4-(1-метилэтил)-1-пиперазинил]метил}-1,3-оксазол-2-ил)-1Н-индазол
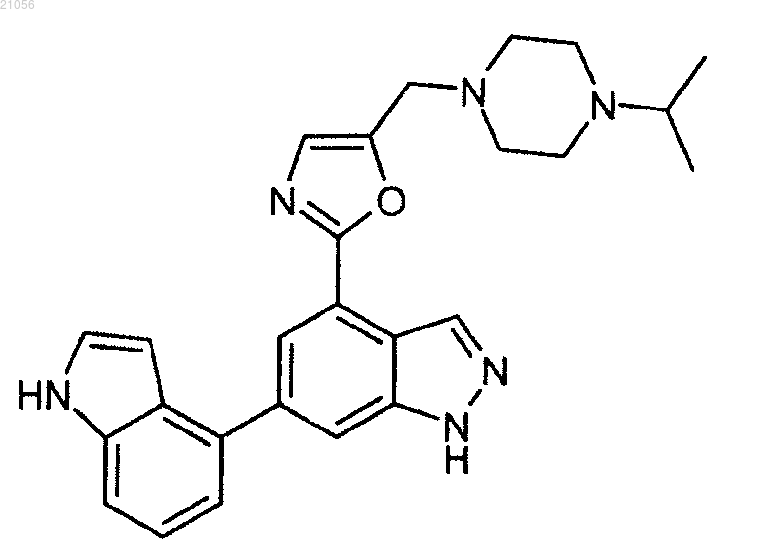
14. Фармацевтическая композиция, ингибирующая активность PI3-киназ, содержащая соединение по любому из пп.1-10 или его фармацевтически приемлемую соль и один или более фармацевтически приемлемых эксципиентов.
15. Фармацевтическая композиция, ингибирующая активность PI3-киназ, содержащая N-[5-[4-(5-{[(2R,6S)-2,6-диметил-4-морфолинил]метил}-1,3-оксазол-2-ил)-1H-индазол-6-ил]-2-(метилокси)-3-пиридинил]метансульфонамид или его фармацевтически приемлемую соль и один или более фармацевтически приемлемых эксципиентов.
16. Фармацевтическая композиция, ингибирующая активность PI3-киназ, содержащая 6-(1Н-индол-4-ил)-4-(5-{[4-(1-метилэтил)-1-пиперазинил]метил}-1,3-оксазол-2-ил)-1Н-индазол или его фармацевтически приемлемую соль и один или более фармацевтически приемлемых эксципиентов.
17. Применение соединения по любому из пп.1-10 или его фармацевтически приемлемой соли в качестве ингибитора активности PI3-киназ.
18. Применение N-[5-[4-(5-{[(2R,6S)-2,6-диметил-4-морфолинил]метил}-1,3-оксазол-2-ил)-1H-индазол-6-ил]-2-(метилокси)-3-пиридинил]метансульфонамида или его фармацевтически приемлемой соли в качестве ингибитора активности PI3-киназ.
19. Применение 6-(1Н-индол-4-ил)-4-(5-{[4-(1-метилэтил)-1-пиперазинил]метил}-1,3-оксазол-2-ил)-1Н-индазола или его фармацевтически приемлемой соли в качестве ингибитора активности PI3-киназ.
20. Применение соединения по любому из пп.1-10 или его фармацевтически приемлемой соли в лечении расстройства, опосредованного ненадлежащей активностью PI3-киназ.
21. Применение N-[5-[4-(5-{[(2R,6S)-2,6-диметил-4-морфолинил]метил}-1,3-оксазол-2-ил)-1H-индазол-6-ил]-2-(метилокси)-3-пиридинил]метансульфонамида или его фармацевтически приемлемой соли в лечении расстройства, опосредованного ненадлежащей активностью PI3-киназ.
22. Применение 6-(1H-индол-4-ил)-4-(5-{[4-(1-метилэтил)-1-пиперазинил]метил}-1,3-оксазол-2-ил)-1H-индазола или его фармацевтически приемлемой соли в лечении расстройства, опосредованного ненадлежащей активностью PI3-киназ.
23. Применение соединения по любому из пп.1-10 или его фармацевтически приемлемой соли в изготовлении лекарственного средства для лечения расстройства, опосредованного ненадлежащей активностью PI3-киназ.
24. Применение N-[5-[4-(5-{[(2R,6S)-2,6-диметил-4-морфолинил]метил}-1,3-оксазол-2-ил)-1H-индазол-6-ил]-2-(метилокси)-3-пиридинил]метансульфонамида или его фармацевтически приемлемой соли в изготовлении лекарственного средства для лечения расстройства, опосредованного ненадлежащей активностью PI3-киназ.
25. Применение 6-(1Н-индол-4-ил)-4-(5-{[4-(1-метилэтил)-1-пиперазинил]метил}-1,3-оксазол-2-ил)-1H-индазола или его фармацевтически приемлемой соли в изготовлении лекарственного средства для лечения расстройства, опосредованного ненадлежащей активностью PI3-киназ.
26. Применение по любому из пп.20-22, где расстройство, опосредованное ненадлежащей активностью PI3-киназ, представляет собой респираторное заболевание, вирусную инфекцию, невирусную респираторную инфекцию, аллергическое заболевание, аутоиммунное заболевание, воспалительное расстройство, сердечно-сосудистое заболевание, гематологическую злокачественность, нейродегенеративное заболевание, панкреатит, полиорганную недостаточность, почечное заболевание, агрегацию тромбоцитов, рак, подвижность сперматозоидов, отторжение трансплантата, отторжение имплантата, повреждение легких или боль.
27. Применение по любому из пп.20-22, где расстройство, опосредованное ненадлежащей активностью PI3-киназ, представляет собой астму, хроническое обструктивное заболевание легких (COPD), идиопатический фиброз легких (IPF), вирусные инфекции дыхательных путей, вирусное обострение респираторных заболеваний, аспергиллез, лейшманиоз, аллергический ринит, атопический дерматит, ревматоидный артрит, рассеянный склероз, воспалительное заболевание кишечника, тромбоз, атеросклероз, гематологическую злокачественность, нейродегенеративное заболевание, панкреатит, полиорганную недостаточность, почечное заболевание, агрегацию тромбоцитов, рак, подвижность сперматозоидов, отторжение трансплантата, отторжение имплантата, повреждение легких, боль, ассоциированную с ревматоидным артритом или остеоартритом, боль в спине, генерализованную воспалительную боль, пост-гепатическую невралгию, диабетическую невропатию, воспалительную невропатическую боль (травму), невралгию тройничного нерва или центральную боль.
28. Применение по п.27, где расстройство, опосредованное ненадлежащей активностью PI3-киназ, представляет собой астму.
29. Применение по п.27, где расстройство, опосредованное ненадлежащей активностью PI3-киназ, представляет собой COPD.
Текст
ОКСАЗОЛЗАМЕЩЕННЫЕ ИНДАЗОЛЫ В КАЧЕСТВЕ ИНГИБИТОРОВ PI3-КИНАЗ,СОДЕРЖАЩАЯ ИХ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И ИХ ПРИМЕНЕНИЕ В ЛЕЧЕНИИ РАССТРОЙСТВ, ОПОСРЕДОВАННЫХ НЕНАДЛЕЖАЩЕЙ АКТИВНОСТЬЮ PI3-КИНАЗ где заместители R1-R4 такие, как они определены в описании изобретения, и к их солям, которые являются ингибиторами активности PI3-киназ. Изобретение также относится к фармацевтическим композициям, содержащим такие соединения, и к применению соединений в лечении расстройств,опосредованных ненадлежащей активностью РI3-киназ, в частности астмы и хронического обструктивного заболевания легких.(71)(73) Заявитель и патентовладелец: ГЛАКСО ГРУП ЛИМИТЕД (GB) Область изобретения Настоящее изобретение относится к некоторым новым соединениям, которые являются ингибиторами активности киназ, к способам их получения, к фармацевтическим композициям, содержащим эти соединения, и к применению этих соединений или композиций в лечении различных расстройств. Более конкретно, соединения по изобретению являются ингибиторами активности или функции семейства фосфоинозитид-3'ОН-киназ (здесь далее PI3-киназы), например PI3K, PI3K, PI3K и/или PI3K. Соединения, которые являются ингибиторами активности или функции PI3-киназ, могут быть полезны в лечении расстройств, таких как респираторные заболевания, включая астму, хроническое обструктивное заболевание легких (COPD) и идиопатический фиброз легких (IPF); вирусные инфекции, включая вирусные инфекции дыхательных путей и вирусное обострение респираторных заболеваний, таких как астма иCOPD; невирусные респираторные инфекции, включая аспергиллез и лейшманиоз; аллергические заболевания, включая аллергический ринит и атопический дерматит; аутоиммунные заболевания, включая ревматоидный артрит и рассеянный склероз; воспалительные расстройства, включая воспалительное заболевание кишечника; сердечно-сосудистые заболевания, включая тромбоз и атеросклероз; гематологические злокачественности; нейродегенеративные заболевания; панкреатит; полиорганную недостаточность; почечные заболевания; агрегацию тромбоцитов; рак; подвижность сперматозоидов; отторжение трансплантата; отторжение имплантата; повреждения легких; боль, включая боль, ассоциированную с ревматоидным артритом или остеоартритом, боль в спине, генерализованную воспалительную боль,пост-гепатическую невралгию, диабетическую невропатию, воспалительную невропатическую боль(травму), невралгию тройничного нерва и центральную боль. Предшествующий уровень техники Клеточные мембраны предоставляют большое количество вторичных мессенджеров, которые могут быть вовлечены в целый ряд путей сигнальной трансдукции. Что касается функции и регуляции эффекторных ферментов в сигнальных путях фосфолипидов, PI3-киназы класса I (например, PI3K) генерируют вторичные мессенджеры из мембранных фосфолипидных пулов. PI3K-киназы класса I превращают мембранный фосфолипид PI(4,5)Р 2 в PI(3,4,5)Р 3, который функционирует как вторичный мессенджер. PI и PI(4)Р также являются субстратами PI3K и могут фосфорилироваться и превращаться в PI3P и PI(3,4)Р 2 соответственно. Кроме того, эти фосфоинозитиды могут превращаться в другие фосфоинозитиды 5'специфичными и 3'-специфичными фосфатазами. Таким образом, ферментативная активность PI3K приводит либо прямо, либо опосредованно к образованию двух подтипов 3'-фосфоинозитидов, которые функционируют как вторичные мессенджеры в путях внутриклеточной сигнальной трансдукции (Vanhaesebroeck et al., Trends Biochem. Sci. 22(7), p. 267-72 (1997); Leslie et al., Chem. Rev. 101(8), p. 2365-80(2001); Katso et al., Annu. Rev. Cell Dev. Biol. 17, p. 615-75 (2001) и Toker, Cell. Mol. Life Sci. 59(5), p. 76179 (2002. До настоящего времени идентифицировано восемь PI3K млекопитающих, которые разделены на три основных класса (I, II и III) на основе гомологии последовательностей, структуры, партнеров связывания, способа активации и предпочтения в отношении субстрата. In vitro PI3K класса I могут фосфорилировать фосфатидилинозитол (PI), фосфатидилинозитол-4-фосфат (PI4P) и фосфатидилинозитол-4,5 бисфосфат (PI(4,5)P2), продуцируя фосфатидилинозитол-3-фосфат (PI3P), фосфатидилинозитол-3,4 бисфосфат (PI(3,4)Р 2) и фосфатидилинозитол-3,4,5-трифосфат (PI(3,4,5)Р 3) соответственно. PI3K классаII могут фосфорилировать PI и PI4P. PI3K класса III могут фосфорилировать только фосфорилатный PIPI3K класса I представляет собой гетеродимер, состоящий из каталитической субъединицы р 110 и регуляторной субъединицы, и семейство этого класса дополнительно разделено на ферменты класса Ia и класса Ib на основе регуляторных партнеров и механизма регуляции. Ферменты класса Ia состоят из трех отдельных каталитических единиц (р 110, р 110 и р 110), которые димеризуются с пятью отдельными регуляторными субъединицами (р 85, р 55, р 50, р 85 и р 55), причем все каталитические субъединицы способны взаимодействовать со всеми регуляторными субъединицами с образованием различных гетеродимеров. PI3K класса Ia обычно активируются в ответ на стимуляцию рецепторных тирозинкиназ факторами роста, посредством взаимодействия доменов SH2 регуляторных субъединиц со специфическими фосфо-тирозиновыми остатками активированных рецепторных или адапторных белков, таких какIRS-1. Небольшие GTP-азы (гуанозинтрифосфатазы) (ras в качестве примера) также вовлечены в активацию PI3K в сочетании с активацией рецепторных тирозинкиназ. Обе р 110 и р 110 конститутивно экспрессируются во всех типах клеток, тогда как экспрессия р 110 в большей степени ограничена популяциями лейкоцитов и некоторыми эпителиальными клетками. Напротив, единственный фермент класса Ib состоит из каталитической субъединицы 110, которая взаимодействует с регуляторной субъединицей р 101. Кроме того, фермент класса Ib активируется в ответ на системы сопряженных с G-белком рецепторов (GPCR) и его экспрессия, по-видимому, ограничена лейкоцитами. Как проиллюстрировано на приведенной выше схеме А, фосфоинозитид-3-киназы (PI3K) фосфорилируют гидроксильную группу на атоме углерода в положении 3 инозитольного кольца. В результате фосфорилирования фосфоинозитидов с образованием PtdIns(3,4,5)P3, PtdIns(3,4)P2 и PtdIns(3)P продуцируются вторичные мессенджеры для различных путей сигнальной трансдукции, включая пути, необходимые для пролиферации клеток, клеточной дифференцировки, клеточного роста, размера клеток, жизнеспособности клеток, апоптоза, адгезии, подвижности клеток, миграции клеток, хемотаксиса, инвазии,реорганизации цитоскелета, изменений формы клеток, направленной миграции везикул, и пути метаболизма (Katso et al. (2001), см. Выше; Stein et al., Mol. Med. Today 6(9), p. 347-57 (2000. Активность PI3-киназ, ответственная за образование указанных фосфорилированных сигнальных продуктов, первоначально была идентифицирована как связанная с вирусными онкобелками и тирозинкиназами рецепторов факторов роста, которые фосфорилируют фосфатидилинозитол (PI) и его фосфорилированные производные по 3'-гидроксильной группе инозитольного кольца (Panayotou et al., Trends CellBiol. 2, p. 358-60 (1992. Однако более поздние биохимические исследования выявили, что PI3-киназы класса I (например, изоформа PI3K класса IA) являются двойственно-специфическими киназными ферментами, что означает, что они демонстрируют как липидкиназную (фосфорилирование фосфоинозитидов), так и протеинкиназную активность, которые, как было показано, способны фосфорилировать другой белок в качестве субстратов, включая аутофосфорилирование как внутримолекулярный регуляторный механизм (Vanhaesebroeck et al., EMBO J. 18(5), p. 1292-302 (1999. Клеточные процессы, в которыхPI3K играют важную роль, включают супрессию апоптоза, реорганизацию актинового скелета, рост сердечных миоцитов, стимуляцию гликогенсинтазы инсулином, опосредованное фактором некроза опухолей(TNF) примирование нуклеофилов и образование супероксидов, и миграцию лейкоцитов и адгезию к эндотелиальным клеткам. Полагают, что активация PI3-киназ вовлечена в широкий диапазон клеточных ответов, включая клеточный рост, дифференцировку и апоптоз (Parker, Current Biology 5(6), p. 577-79 (1995) и Yao et al.,Science 267(5206), p. 2003-06 (1995. Представляется, что PI3-киназы вовлечены в целый ряд аспектов активации лейкоцитов. Было показано, что р 85-ассоциированная PI3-киназа физически связывается с цитоплазматическим доменом CD28, который является важной ко-стимулирующей молекулой для активации Т-клеток в ответ на антиген (Pages et al., Nature 369, p. 327-29 (1994) и Rudd, Immunity 4, p. 527-34(1996. Активация Т-клеток через CD28 снижает порог для активации антигеном и повышает величину и продолжительность пролиферативного ответа. Эти эффекты связаны с увеличениями транскрипции целого ряда генов, включая интерлейкин-2 (IL-2), важный фактор роста Т-клеток (Fraseref et al., Science 251PI3K была идентифицирована как медиатор G зависимой регуляции активности JNK, и G являются субъединицами гетеротримерных G-белков (Lopez-Ilasaca et al., J. Biol. Chem. 273(5), p. 2505-8(1998. Позднее (Laffargue et al., Immunity 16(3), p. 441-51 (2002 стало известно, что PI3K передает воспалительные сигналы через различные рецепторы, сопряженные с G(i)-белком, и играет важную роль в отношении функции тучных клеток, стимулов в контексте лейкоцитов и иммунологии, включая цитокины, хемокины, аденозины, антитела, интегрины, факторы агрегации, факторы роста, вирусы или гормоны, например Lawlor et al., J. Cell Sci. 114 (Pt 16), p. 2903-10 (2001); Laffargue et al. (2002), см. выше;Stephens et al., Curr. Opinion Cell Biol. 14(2), p. 203-13 (2002). Специфические ингибиторы индивидуальных членов семейства ферментов предоставляют бесценные инструменты для понимания функций каждого фермента. Два соединения, LY294002 и вортманнин(см. ниже), широко применяются в качестве ингибиторов PI3-киназ. Эти соединения являются неспецифическими ингибиторами PI3K, так как они не делают различий между четырьмя членами PI3-киназ класса I. Например, значения IC50 вортманнина в отношении каждой из различных PI3-киназ класса I находятся в диапазоне 1-10 нМ. Подобным образом, значения IC50 для LY294002 в отношении каждой из этих PI3-киназ составляют примерно 15-20 мкМ (Fruman et al., Ann. Rev. Biochem. 67, p. 481-507 (1998,а также 5-10 мкМ в отношении CK2 протеинкиназы и проявляют некоторую ингибиторную активность в отношении фосфолипаз. Вортманнин представляет собой грибковый метаболит, который необратимо ингибирует активность PI3K в результате ковалентного связывания с каталитическим доменом этого фермента. Ингибирование активности PI3K вортманнином исключает последующий клеточный ответ на внеклеточный фактор. Например, нейтрофилы отвечают на хемокин fMet-Leu-Phe (fMLP) стимуляциейPI3K и синтезированием PtdIns(3,4,5)Р 3. Этот синтез коррелирует с активацией респираторного бурста,вовлеченного в нейтрофильную деструкцию инвазивных микроорганизмов. Обработка нейтрофилов вортманнином предотвращает fMLP-индуцированный респираторный бустерный ответ (Thelen et al.,Proc. Natl. Acad. Sci. USA 91, p. 4960-64 (1994. Фактически, эти эксперименты с вортманнином, а также другие экспериментальные данные показывают, что активность PI3K в клетках гематопоэтической клеточной линии, в частности в нейтрофилах, моноцитах и других типах лейкоцитов, вовлечена во многом в иммунный ответ, не требующий обращения к памяти, связанный с острым и хроническим воспалением. Имеется доказательство, основанное на исследованиях с использованием вортманнина, что функция PI3-киназ также требуется для некоторых аспектов лейкоцитарной передачи сигнала через рецепторы, сопряженные с G-белком (Thelen et al. (1994), см. выше). Более того, было показано, что вортманнин и LY294002 блокируют миграцию нейтрофилов и высвобождение супероксидов. В настоящее время уже совершенно ясно, что дерегуляция онкогенов и генов-супрессоров опухолей способствует образованию злокачественных опухолей, например, за счет увеличения роста и пролифирации клеток или повышения жизнеспособности клеток. Теперь также известно, что сигнальные пути,опосредованные семейством PI3K, играют центральную роль в ряде клеточных процессов, включая пролиферацию и выживание, и что дерегуляция этих путей является причинным фактором множества видов рака человека и других заболеваний (Katso et al., Annual Rev. Cell Dev. Biol. (2001) 17, p. 615-675 и Fosteret al., J. Cell Science (2003) 116(15), p. 3037-3040). Эффекторные белки PI3K инициируют сигнальные пути и цепи путем транслокации в плазматическую мембрану через консервативный плекстрингомологичный (РН) домен, который специфически взаимодействует с PtdIns(3,4,5)P3 (Vanhaesebroeck et(факторы гуанин-нуклеотидного обмена) и Arf GAP (белки активации GTP-азы). В В- и Т-клетках PI3K играют важную роль, активируя семейство Тес протеинтирозинкиназ, включающих тирозинкиназу Брутона (ВТК) в В-клетках и интерлейкин-2-индуцибельную Т-клеточную киназу (ITK) в Т-клетках. В результате PI3K-активации ВТК или ITK транслоцируются в плазматическую мембрану, где они впоследствии фосфорилируются Src-киназами. Одной из главных мишеней активированной ITK является фосфолипаза С- (PLC1), которая гидролизует PtdIns(4,5)P2 в Ins(3,4,5)P3 и инициирует внутриклеточное увеличение уровней кальция, и диацилглицерин (DAG), который может активировать протеинкиназы С в активированные Т-клетки. В отличие от р 110 и р 110 класса IA р 110 экспрессируется в ограниченных типах ткани. Ее высокий уровень экспрессии в лимфоцитах и лимфоидных тканях дает основание считать, что она играет роль в PI3K-опосредованной сигнализации в иммунной системе. Мыши, у которых отсутствует р 110,также жизнеспособны, и их фенотип ограничен дефектами в иммунной сигнализации (Okkenhaug et al.,Science (2002) 297, p. 1031-4). Эти трансгенные мыши дали представление о функции PI3K в В- и Тклеточной сигнализации. В частности, р 110 требуется для образования PtdIns(3,4,5)P3 по ходу CD28 и/или Т-клеточной рецепторной (TCR) сигнализации. Ключевым эффектом PI3K-сигнализации нижеTCR является активация Akt, которая фосфорилирует антиапоптические факторы, а также различные факторы транскрипции для продуцирования цитокинов. Как следствие, Т-клетки с неактивной р 110 имеют недостатки в пролифирации и секреции Th1- и Th2-цитокинов. Активация Т-клеток через CD28 снижает порог для активации TCR антигеном и повышает величину и продолжительность пролиферативного ответа. Эти эффекты опосредованы PI3K-зависимым увеличением транскрипции ряда генов,включая IL-2, важный Т-клеточный фактор роста. Таким образом, ожидается, что ингибиторы PI3K будут давать терапевтическую пользу путем модулирования опосредованных Т-клетками воспалительных ответов, связанных с респираторными заболеваниями, такими как астма, COPD и муковисцидоз. Кроме того, имеются данные, указывающие на то,что направленные на Т-клетки терапии могут обеспечивать кортикостероид-сберегающие свойства (Alexander et al., Lancet (1992) 339, p. 324-8), что дает основания предполагать, что можно обеспечивать полезную терапию, либо автономную, либо в комбинации с ингаляционными или пероральными глюкокортикостероидами, при респираторных заболеваниях. Ингибитор PI3K может быть также использован при астме вместе с другими традиционными терапевтическими средствами, такими как длительно действующий -агонист (LABA). В сосудистой сети PI3K экспрессируется эндотелиальными клетками и участвует в направленной миграции нейтрофилов путем модулирования проадгезивного состояния этих клеток в ответ на TNF(Puri et al., Blood (2004) 103(9), p. 3448-56). Роль PI3K в TNF-индуцированной сигнализации эндотелиальных клеток продемонстрирована путем фармакологического ингибирования фосфорилирования Akt и активности PDK1. Дополнительно, PI3K вовлечена в проницаемость сосудов и отек тканей дыхательных путей через VEGF-путь (Lee et al., J. Allergy Clin. Immunol. (2006) 118(2), p. 403-9). Эти наблюдения указывают на дополнительные преимущества ингибирования PI3K при астме за счет совместного снижения лейкоцитарной транссудации и проницаемости сосудов, ассоциированных с астмой. К тому же,активность PI3K требуется для функционирования тучных клеток как in vitro, так и in vivo (AN et al.,Nature (2004) 431, p. 1007-11; и Ali et al., J. Immunol. (2008) 180(4), p. 2538-44), что также позволяет предполагать, что ингибирование PI3K должно давать терапевтическую пользу при симптомах аллергических заболеваний, таких как астма, аллергический ринит и атопический дерматит. Роль PI3K в В-клеточной пролиферации, секреции антител, В-клеточной антигенной и IL-4 рецепторной сигнализации, В-клеточной антиген-презентирующей функции также установлена (Okkenhaug et al., (2002), см. выше; Al-Alwan et al., J. Immunol. (2007) 178(4), p. 2328-35 и Bilancio et al., Blood(2006) 107(2), p. 642-50) и указывает на участие в аутоиммунных заболеваниях, таких как ревматоидный артрит или системная красная волчанка. Следовательно, ингибиторы PI3K могут быть также полезны при симптомах этих заболеваний. Фармакологическое ингибирование PI3K ингибирует fMLP-зависимый хемотаксис нейтрофилов на ICAM (фактор межклеточной адгезии)-покрытой агарозной матричной интегрин-зависимой несимметричной системе (Sadhu et al., J. Immunol. (2003) 170(5), p. 2647-54). Ингибирование PI3K регулирует активацию, адгезию и миграцию нейтрофилов, не оказывая воздействия на опосредованный нейтрофилами фагоцитоз и бактериальную активность по отношению к Staphylococcus aureus (Sadhu et al., Biochem. Biophys. Res. Commun. (2003) 308(4), p. 764-9). В целом, эти данные указывают на то, что ингибирование PI3K не будет глобально ингибировать функции нейтрофилов, необходимые для врожденной иммунной защиты. Роль PI3K в нейтрофилах дает дополнительные возможности для лечения воспалительных заболеваний, в которые вовлечено ремоделирование ткани, таких как COPD или ревматоидный артрит. Дополнительно, имеется также доказательство того, что PI3K-ферменты класса Ia также вносят вклад в опухолегенез при множестве различных видов рака человека либо прямо, либо опосредованно(Vivanco and Sawyers, Nature Reviews Cancer (2002) 2(7), p. 489-501). Например, ингибирование PI3K может играть терапевтическую роль в лечении злокачественных гематологических расстройств, таких как острый миелоидный лейкоз (Billottet et al., Oncogene (2006) 25(50), p. 6648-59). Более того, активирующие мутации в р 110 (ген PIK3CA) связаны с различными другими опухолями, такими как опухоли ободочной кишки и опухоли молочной железы и легкого (Samuels et al., Science (2004) 304(5670), p. 554). Было также показано, что PI3K вовлечена в создание центральной сенситизации при болезненных воспалительных состояниях (Pezet et al., The J. of Neuroscience (2008) 28 (16), p. 4261-4270). Большое разнообразие ретровирусов и ДНК-содержащих вирусов активируют PI3K-путь как способ предотвращения гибели клеток-хозяев во время вирусной инфекции и в конечном счете использования механизма синтеза клеток-хозяев для его репликации (Vogt et al., Virology 344(1), p. 131-8 (2006) иBuchkovich et al., Nat. Rev. Microbiol. 6(4), p. 265-75 (2008. Таким образом, в дополнение к общепризнанным свойствам ингибиторы PI3K могут обладать противовирусными свойствами. Эти противовирусные эффекты представляют интерес с точки зрения перспектив при вызываемых вирусами воспалительных обострениях. Например, широко распространенный простудный риновирус человека (HRV) ответственен за более чем 50% инфекций дыхательных путей, но осложнения этих инфекций могут быть значительными в некоторых популяциях. В частности, они возникают при таких респираторных заболеваниях, как астма или хроническое обструктивное заболевание легких (COPD). Риновирусная инфекция эпителиальных клеток приводит к PI3K-зависимой секреции цитокинов и хемокинов (Newcomb et al., J.Biol. Chem. (2005) 280(44), p. 36952). Этот воспалительный ответ соотносится с ухудшением респиратор-4 021056 ных симптомов во время инфекции. Таким образом, ингибиторы PI3K могут гасить ненормально большой иммунный ответ на вирус, слабый в других обстоятельствах. Большинство штаммов HRV инфицируют бронхиальные эпителиальные клетки путем первоначального связывания с рецептором ICAM-1. Комплекс HRV-ICAM-1 затем дополнительно интернализируется в результате эндоцитоза, и было показано, что для этого события требуется активность PI3K (Lau et al., J. Immunol. (2008) 180(2), p. 870-880). Таким образом, ингибиторы PI3K могут также блокировать вирусные инфекции путем ингибирования проникновения вируса в клетки-хозяева. Ингибиторы PI3K могут быть полезны в ослаблении других типов респираторных инфекций, включая грибковый инфекционный аспергиллез (Bonifazi et al., Mucosal Immunol. (2010) 3(2), p. 193-205). Кроме того, мыши с дефицитом PI3K более устойчивы к инфицированию протозойным паразитомLeishmania major (Liu et al., J. Immunol. (2009) 183(3), p. 1921-1933). С учетом эффектов на вирусные инфекции эти сообщения свидетельствуют о том, что ингибиторы PI3K могут быть полезны для лечения множества различных инфекций. Было также показано, что ингибирование PI3K промотирует регуляторную Т-клеточную дифференцировку (Sauer et al., Proc. Natl. Acad. Sci. USA (2008) 105(22), p. 7797-7802), что свидетельствует о том,что ингибиторы PI3K могут быть полезны в терапевтических целях при аутоиммунных или аллергических заболеваниях путем индуцирования иммунотолерантности к аутоантигену или аллергену. Недавно была также установлена связь изоформы PI3K с индуцированной дымом глюкокортикоидной интенсивностью (Marwick et al., Am. J. Respir. Crit. Care Med. (2009) 179(7), p. 542-548). Это наблюдение свидетельствует о том, что пациенты с COPD, которые в иных обстоятельствах плохо реагируют на кортикостероиды, могут получать пользу от комбинации ингибитора PI3K с кортикостероидом.PI3K также вовлечена в другие респираторные состояния, такие как идиопатический фиброз легких(IPF). IPF представляет собой фиброзное заболевание с прогрессирующим ухудшением легочной функции и повышенной смертностью вследствие дыхательной недостаточности. При IPF циркулирующие фиброциты направленно поступают в легкое через хемокиновый рецептор CXCR4. PI3K необходим как для сигнализации, так и для экспрессии CXCR4 (Mehrad et al., Int. J. Biochem. и Cell Biol. (2009) 41, p. 1708-1718). Таким образом, снижая экспрессию CXCR4 и блокируя ее эффект или функции, ингибиторPI3K будет ингибировать рекрутинг фиброцитов в легкое и, следовательно, замедлять фибротический процесс, лежащий в основе IPF, заболевания с высокой неудовлетворенной потребностью лечения. Были предприняты попытки получить соединения, которые ингибируют активность PI3-киназ, и целый ряд таких соединений раскрыт в данной области. Однако с точки зрения патологических ответных реакций, которые опосредованы PI3-киназами, все еще остается потребность в ингибиторах PI3-киназ,которые могут быть использованы в лечении различных состояниях. Авторы настоящего изобретения открыли новые соединения, которые являются ингибиторами активности киназ, в частности активности PI3-киназ. Соединения, которые являются ингибиторами PI3 киназ, могут быть полезны в лечении расстройств, связанных с несоответствующей активностью киназ, в частности ненадлежаще активностью PI3-киназ, например, в лечении и предупреждении расстройств,опосредованных PI3-киназными механизмами. Такими расстройствами являются респираторные заболевания, включая астму, хроническое обструктивное заболевание легких (COPD) и идиопатический фиброз легких (IPF); вирусные инфекции, включая вирусные инфекции дыхательных путей и вирусные обострения респираторных заболеваний, таких как астма и COPD; невирусные респираторные инфекции, включая аспергиллез и лейшманиоз; аллергические заболевания, включая аллергический ринит и атопический дерматит; аутоиммунные заболевания, включая ревматоидный артрит и рассеянный склероз; воспалительные расстройства, включая воспалительное заболевание кишечника; сердечно-сосудистые заболевания, включая тромбоз и атеросклероз; гематологические злокачественности; нейродегенеративные заболевания; панкреатит; полиорганную недостаточность; почечные заболевания; агрегацию тромбоцитов; рак; подвижность сперматозоидов; отторжение трансплантата; отторжение имплантата; повреждения легких; боль, включая боль, ассоциированную с ревматоидным артритом или остеоартритом, боль в спине, генерализованную воспалительную боль, пост-гепатическую невралгию, диабетическую невропатию,воспалительную невропатическую боль (травму), невралгию тройничного нерва и центральную боль. В одном из воплощений соединения по изобретению могут проявлять избирательность в отношении PI3-киназ по сравнению с другими киназами. В другом воплощении соединения по изобретению могут быть сильнодействующими ингибиторамиPI3K. В еще одном воплощении соединения по изобретению могут проявлять избирательность в отношении PI3K по сравнению с другими PI3-киназами. Краткое изложение сущности изобретения Согласно настоящему изобретению предложено соединение формулы (I) где R1 представляет собой 9-членный бициклический гетероарил, причем указанный 9-членный бициклический гетероарил содержит один или два атома азота, или пиридинил, возможно замещенный одним или двумя заместителями, независимо выбранными из -OR6 и -NHSO2R7;R2 и R3 вместе с атомом азота, к которому они присоединены, связаны с образованием 6- или 7 членного гетероциклила, причем указанный 6- или 7-членный гетероциклил, возможно, содержит атом кислорода или дополнительный атом азота и, возможно, замещен одним или двумя заместителями, независимо выбранными из С 1-6 алкила;R4 представляет собой водород или метил;R6 представляет собой водород или С 1-4 алкил иR5 и R7, каждый независимо, представляют собой C1-6 алкил или фенил, возможно замещенный одним или двумя заместителями, независимо выбранными из галогено,или его соль. Предпочтительным является соединение по изобретению или его соль, где R1 представляет собой индолил или пиридинил, возможно замещенный одним или двумя заместителями, независимо выбранными из -OR6 и -NHSO2R7. Еще более предпочтительным является соединение по изобретению, как оно определено выше, или его соль, где R2 и R3 вместе с атомом азота, к которому они присоединены, связаны с образованием 6 членного гетероциклила, причем указанный 6-членный гетероциклил, возможно, содержит атом кислорода или дополнительный атом азота и, возможно, замещен одним или двумя заместителями, независимо выбранными из C1-6 алкила. Особенно предпочтительным является соединение по изобретению, как оно определено выше, или его соль, где R2 и R3 вместе с атомом азота, к которому они присоединены, связаны с образованием 6 членного гетероциклила, причем указанный 6-членный гетероциклил содержит атом кислорода и, возможно, замещен одним или двумя заместителями, независимо выбранными из С 1-4 алкила. Также особенно предпочтительным является соединение по изобретению, как оно определено выше, или его соль, где R2 и R3 вместе с атомом азота, к которому они присоединены, связаны с образованием 6-членного гетероциклила, причем указанный 6-членный гетероциклил содержит дополнительный атом азота и, возможно, замещен С 1-4 алкилом. Наиболее предпочтительным является соединение по изобретению, как оно определено выше, или его соль, где R4 представляет собой водород. В предпочтительном воплощении соединение по изобретению представляет собой соединение, выбранное из группы, включающей Согласно другому предпочтительному воплощению изобретения соединение по изобретению представляет собой N-[5-[4-(5-[(2R,6S)-2,6-диметил-4-морфолинил]метил-1,3-оксазол-2-ил)-1H-индазол-6 ил]-2-(метилокси)-3-пиридинил]метансульфонамид или его соль. Согласно еще одному предпочтительному воплощению изобретения соединение по изобретению представляет собой 6-(1 Н-индол-4-ил)-4-(5-[4-(1-метилэтил)-1-пиперазинил]метил-1,3-оксазол-2-ил)1 Н-индазол или его соль. В предпочтительном воплощении изобретения соединение находится в форме его фармацевтически приемлемой соли. В еще одном воплощении соединение по изобретению представляет собой N-[5-[4-(5-[(2R,6S)-2,6 диметил-4-морфолинил]метил-1,3-оксазол-2-ил)-1H-индазол-6-ил]-2-(метилокси)-3-пиридинил]метансульфонамид В еще одном воплощении соединение по изобретению представляет собой 6-(1 Н-индол-4-ил)-4-(5[4-(1-метилэтил)-1-пиперазинил]метил-1,3-оксазол-2-ил)-1 Н-индазол Согласно изобретению предложена фармацевтическая композиция, ингибирующая активность PI3 киназ, содержащая соединение по изобретению или его фармацевтически приемлемую соль и один или более фармацевтически приемлемых эксципиентов. В еще одном воплощении предложена фармацевтическая композиция, ингибирующая активностьPI3-киназ, содержащая N-[5-[4-(5-[(2R,6S)-2,6-диметил-4-морфолинил]метил-1,3-оксазол-2-ил)-1Hиндазол-6-ил]-2-(метилокси)-3-пиридинил]метансульфонамид или его фармацевтически приемлемую соль и один или более фармацевтически приемлемых эксципиентов. В еще одном воплощении предложена фармацевтическая композиция, ингибирующая активностьPI3-киназ, содержащая 6-(1 Н-индол-4-ил)-4-(5-[4-(1-метилэтил)-1-пиперазинил]метил-1,3-оксазол-2 ил)-1 Н-индазол или его фармацевтически приемлемую соль и один или более фармацевтически приемлемых эксципиентов. Согласно настоящему изобретению также предложено применение соединения по изобретению, как оно определено выше, или его фармацевтически приемлемой соли в качестве ингибитора активности PI3 киназ. В одном воплощении изобретения предложено применение N-[5-[4-(5-[(2R,6S)-2,6-диметил-4-7 021056 морфолинил]метил-1,3-оксазол-2-ил)-1 Н-индазол-6-ил]-2-(метилокси)-3-пиридинил]метансульфонамида или его фармацевтически приемлемой соли в качестве ингибитора активности PI3-киназ. В еще одном воплощении изобретения предложено применение 6-(1 Н-индол-4-ил)-4-(5-[4-(1 метилэтил)-1-пиперазинил]метил-1,3-оксазол-2-ил)-1 Н-индазола или его фармацевтически приемлемой соли в качестве ингибитора активности PI3-киназ. Согласно настоящему изобретению также предложено применение соединения по изобретению, как оно определено выше, или его фармацевтически приемлемой соли в лечении расстройства, опосредованного ненадлежащей активностью PI3-киназ. В одном воплощении изобретения предложено применение N-[5-[4-(5-[(2R,6S)-2,6-диметил-4 морфолинил]метил-1,3-оксазол-2-ил)-1H-индазол-6-ил]-2-(метилокси)-3-пиридинил]метансульфонамида или его фармацевтически приемлемой соли в лечении расстройства, опосредованного ненадлежащей активностью PI3-киназ. В еще одном воплощении изобретения предложено применение 6-(1 Н-индол-4-ил)-4-(5-[4-(1 метилэтил)-1-пиперазинил]метил-1,3-оксазол-2-ил)-1 Н-индазола или его фармацевтически приемлемой соли в лечении расстройства, опосредованного ненадлежащей активностью PI3-киназ. Согласно настоящему изобретению также предложено применение соединения по изобретению, как оно определено выше, или его фармацевтически приемлемой соли в изготовлении лекарственного средства для лечения расстройства, опосредованного ненадлежащей активностью PI3-киназ. В одном воплощении изобретения предложено применение N-[5-[4-(5-[(2R,6S)-2,6-диметил-4 морфолинил]метил-1,3-оксазол-2-ил)-1H-индазол-6-ил]-2-(метилокси)-3-пиридинил]метансульфонамида или его фармацевтически приемлемой соли в изготовлении лекарственного средства для лечения расстройства, опосредованного ненадлежащей активностью PI3-киназ. В еще одном воплощении изобретения предложено применение 6-(1 Н-индол-4-ил)-4-(5-[4-(1 метилэтил)-1-пиперазинил]метил-1,3-оксазол-2-ил)-1 Н-индазола или его фармацевтически приемлемой соли в изготовлении лекарственного средства для лечения расстройства, опосредованного ненадлежащей активностью PI3-киназ. Предпочтительно вышеуказанное расстройство, опосредованное ненадлежащей активностью PI3 киназ, представляет собой респираторное заболевание, вирусную инфекцию, невирусную респираторную инфекцию, аллергическое заболевание, аутоиммунное заболевание, воспалительное расстройство, сердечно-сосудистое заболевание, гематологическую злокачественность, нейродегенеративное заболевание,панкреатит, полиорганную недостаточность, почечное заболевание, агрегацию тромбоцитов, рак, подвижность сперматозоидов, отторжение трансплантата, отторжение имплантата, повреждение легких или боль. Более предпочтительно расстройство, опосредованное ненадлежащей активностью PI3-киназ, представляет собой астму, хроническое обструктивное заболевание легких (COPD), идиопатический фиброз легких (IPF), вирусные инфекции дыхательных путей, вирусное обострение респираторных заболеваний,аспергиллез, лейшманиоз, аллергический ринит, атопический дерматит, ревматоидный артрит, рассеянный склероз, воспалительное заболевание кишечника, тромбоз, атеросклероз, гематологическую злокачественность, нейродегенеративное заболевание, панкреатит, полиорганную недостаточность, почечное заболевание, агрегацию тромбоцитов, рак, подвижность сперматозоидов, отторжение трансплантата, отторжение имплантата, повреждение легких, боль, ассоциированную с ревматоидным артритом или остеоартритом, боль в спине, генерализованную воспалительную боль, пост-гепатическую невралгию, диабетическую невропатию, воспалительную невропатическую боль (травму), невралгию тройничного нерва или центральную боль. Наиболее предпочтительно расстройство, опосредованное ненадлежащей активностью PI3-киназ,представляет собой астму или COPD. Подробное описание изобретения Следует иметь в виду, что настоящее изобретение охватывает все комбинации групп-заместителей,описанных выше. Термины и определения"Алкил" относится к насыщенной углеводородной цепи с указанным количеством атомов-членов цепи. Например, C1-6 алкил относится к алкильной группе, имеющей от 1 до 6 атомов-членов цепи, например от 1 до 4 атомов-членов цепи. Алкильные группы могут быть прямыми или разветвленными. Репрезентативные разветвленные алкильные группы имеют одну, две или три ветвей. Алкил включает метил, этил, пропил (н-пропил и изопропил), бутил (н-бутил, изобутил и трет-бутил), пентил (н-пентил,изопентил и неопентил) и гексил."Циклоалкил" относится к насыщенному углеводородному кольцу, имеющему указанное количество атомов-членов кольца. Циклоалкильные группы представляют собой моноциклические кольцевые системы. Например, С 3-6 циклоалкил относится к циклоалкильной группе, имеющей от 3 до 6 атомовчленов кольца. В одном из воплощений циклоалкильные группы имеют 3 или 4 атома-члена кольца. В еще одном воплощении циклоалкильные группы имеют 5 или 6 атомов-членов кольца. Циклоалкил включает циклопропил, циклобутил, циклопентил и циклогексил."Энантиомерно обогащенный" относится к продуктам, чей энантиомерный избыток больше нуля. Например, "энантиомерно обогащенный" относится к продуктам, чей энантиомерный избыток составляет более 50, более 75 и более 90% ее."Энантиомерный избыток", или "ее", представляет собой избыток одного энантиомера по сравнению с другим энантиомером, выраженный в процентах. Таким образом, поскольку в рацемической смеси оба энантиомера присутствуют в равных количествах, энантиомерный избыток равен нулю (0% ее). Однако если один энантиомер обогащен таким образом, что он составляет 95% продукта, то энантиомерный избыток будет составлять 90% ее (количество обогащенного энантиомера, 95%, минус количество другого энантиомера, 5%)."Энантиомерно чистый" относится к продуктам, чей энантиомерный избыток равен 99% ее или больше."Период полувыведения" (или "периоды полувыведения") относится к периоду времени, необходимому для того, чтобы половина количества вещества превратилось in vitro или in vivo в другое, химически отличающееся вещество."Гетероарил", если не указано иное, относится к ароматической группе, содержащей от 1 до 3 гетероатомов в качестве атомов-членов кольца. Гетероарильные группы, содержащие более одного гетероатома, могут содержать разные гетероатомы. Гетероарильные группы, возможно, могут быть замещены,как определено в данном описании. Гетероарильные группы в данном описании представляют собой бициклические кольцевые системы. Бициклические гетероарильные кольца имеют 9 или 10 атомов-членов кольца. Бициклический гетероарил включает индолил, изоиндолил, индолизинил, бензофуранил, изобензофуранил, индазолил, бензимидазолил, пирролопиридинил, пиразолопиридинил, пирролопиримидинил,хинолил, изохинолинил, хиноксалинил, хиназолинил, циннолинил, бензопиранил, бензоксазолил, фуропиридинил и нафтиридинил."Гетероциклил", если не указано иное, относится к насыщенному или ненасыщенному кольцу, содержащему 1 или 2 гетероатома в качестве атомов-членов кольца. Однако гетероциклильные кольца не являются ароматическими. В некоторых воплощениях гетероциклил является насыщенным. В других воплощениях гетероциклил является ненасыщенным, но не ароматическим. Гетероциклильные группы,содержащие более одного гетероатома, могут содержать разные гетероатомы. Гетероциклильные группы, возможно, могут быть замещены одним или более заместителями, как определено в данном описании. Гетероциклильные группы в данном описании представляют собой моноциклические кольцевые системы, имеющие 6 или 7 атомов-членов кольца. Моноциклический гетероциклил включает пиперидинил, пиперазинил, морфолинил и гексагидро-1,4-оксазепинил."Атомы-члены" относятся к атому или атомам, которые образуют цепь или кольцо. В тех случаях,когда в цепи или в кольце присутствует более одного атома-члена, тогда каждый атом-член цепи или кольца ковалентно связан с соседним атомом-членом цепи или кольца. Атомы, которые составляют группу-заместитель на цепи или кольце, не являются атомами-членами цепи или кольца."Возможно замещенный" указывает на то, что группа, такая как гетероарил, может быть незамещенной или замещенной одним или более заместителями, как определено в данном описании."Замещенный" в отношении группы указывает на то, что атом водорода, присоединенный к атомучлену в группе, заменен. Следует иметь в виду, что термин "замещенный" охватывает не выраженное явным образом условие, что такое замещение находится в соответствии с допустимой валентностью замещенного атома и заместителя и что в результате замещения образуется стабильное соединение (т.е. соединение, которое самопроизвольно не подвергается трансформации, такой как перегруппировка, циклизация или элиминирование). В некоторых воплощениях единственный атом может быть замещен более чем одним заместителем, если такое замещение находится в соответствии с допустимой валентностью атома. Подходящие заместители определены в данном описании для каждой замещенной или возможно замещенной группы."Фармацевтически приемлемый" относится к тем соединениям, солям, веществам, композициям и лекарственным формам, которые в рамках обоснованного медицинского заключения являются подходящими для применения в контакте с тканями человеческих существ и животных без избыточной токсичности, раздражения или другой проблемы или осложнения, соизмеримыми с разумным соотношением польза/риск. Использованные в данном документе символы и условные обозначения в описании способов, на схемах и в примерах соответствуют тем символам и условным обозначениям, которые используются в современной научной литературе, например в Journal of the American Chemical Society или Journal of Biological Chemistry. Для обозначения аминокислотных остатков, которые, допустим, находятся в Lконфигурации, обычно, если не указано иное, использованы стандартные однобуквенные или трехбуквенные сокращения. Если не указано иное, все исходные вещества были приобретены у коммерческих поставщиков, и их использовали без дополнительной очистки. Конкретно, следующие сокращения могут быть использованы в примерах и по всему тексту данного описания: Все ссылки на рассол относятся к насыщенному водному раствору NaCl. Выражение "соединения по изобретению" охватывает все сольваты (включая гидраты), комплексы,полиморфы, пролекарства, меченные радиоактивными изотопами производные, стереоизомеры и оптические изомеры соединений формулы (I) и их солей. Соединения по изобретению могут существовать в твердой или жидкой форме. В твердом состоянии соединения по изобретению могут существовать в кристаллической или некристаллической форме или в виде их смеси. В отношении соединений по изобретению, которые находятся в кристаллической форме, специалисту будет очевидно, что могут быть образованы фармацевтически приемлемые сольваты, в которых молекулы растворителя включены в кристаллическую решетку при кристаллизации. Сольваты могут содержать неводные растворители, такие как этанол, изопропанол, DMSO, уксусная кислота,этаноламин и EtOAc, или они могут содержать в качестве растворителя воду, которая включена в кристаллическую решетку. Сольваты, в которых вода является растворителем, который включен в кристаллическую решетку, обычно называются "гидратами". Гидраты включают стехиометрические гидраты, а также структуры, содержащие вариабельные количества воды. Данное изобретение охватывает все такие сольваты. Специалисту также будет очевидно, что некоторые соединения по изобретению, которые существуют в кристаллической форме, включая их различные сольваты, могут проявлять полиморфизм (т.е. способность существовать в разных кристаллических формах). Эти разные кристаллические формы обычно известны как "полиморфы". Данное изобретение охватывает все такие полиморфы. Полиморфы имеют один и тот же химический состав, но отличаются упаковкой, геометрическим строением и другими дескриптивными свойствами кристаллического твердого состояния. Полиморфы, следовательно, могут иметь разные физические свойства, такие как форма, плотность, твердость, деформируемость, стабильность и растворимость. Полиморфы обычно демонстрируют разные точки плавления, ИК-спектры и картины дифракции рентгеновских лучей на порошке, которые могут быть использованы для идентификации. Специалисту очевидно, что разные полиморфы могут быть получены, например, в результате изменения или регулирования реакционных условий или реагентов, используемых при получении соединения. Например, изменения температуры, давления или растворителя могут привести к образованию полиморфов. Кроме того, в определенных условиях один полиморф может самопроизвольно превра- 10021056 щаться в другой полиморф. В одном аспекте настоящего изобретения предложен N-[5-[4-(5-[(2R,6S)-2,6-диметил-4 морфолинил]метил-1,3-оксазол-2-ил)-1 Н-индазол-6-ил]-2-(метилокси)-3-пиридинил]метансульфонамид или его соль в кристаллической форме. В одном из воплощений настоящего изобретения предложен N-[5-[4-(5-[(2R,6S)-2,6-диметил-4 морфолинил]метил-1,3-оксазол-2-ил)-1 Н-индазол-6-ил]-2-(метилокси)-3-пиридинил]метансульфонамид в кристаллической форме. В другом воплощении настоящего изобретения предложен кристаллический N-[5-[4-(5-[(2R,6S)2,6-диметил-4-морфолинил]метил-1,3-оксазол-2-ил)-1 Н-индазол-6-ил]-2-(метилокси)-3 пиридинил]метансульфонамид, характеризующийся тем, что он дает картину ДРЛП (дифракция рентгеновских лучей на порошке) с пиками (2) при примерно 4,5, примерно 11,7 и/или примерно 12,9. В другом воплощении настоящего изобретения предложен кристаллический N-[5-[4-(5-[(2R,6S)2,6-диметил-4-морфолинил]метил-1,3-оксазол-2-ил)-1H-индазол-6-ил]-2-(метилокси)-3 пиридинил]метансульфонамид, характеризующийся тем, что он дает картину ДРЛП, содержащую пики,по существу такие, как указано в табл. 2. В другом воплощении настоящего изобретения предложен кристаллический N-[5-[4-(5-[(2R,6S)2,6-диметил-4-морфолинил]метил-1,3-оксазол-2-ил)-1H-индазол-6-ил]-2-(метилокси)-3 пиридинил]метансульфонамид, характеризующийся тем, что он дает картину ДРЛП, по существу, в соответствии с фиг. 2. В следующем аспекте настоящего изобретения предложен 6-(1H-индол-4-ил)-4-(5-[4-(1 метилэтил)-1-пиперазинил]метил-1,3-оксазол-2-ил)-1 Н-индазол или его соль в кристаллической форме. В одном из воплощений настоящего изобретения предложен гидрохлорид 6-(1H-индол-4-ил)-4-(5[4-(1-метилэтил)-1-пиперазинил]метил-1,3-оксазол-2-ил)-1H-индазола в кристаллической форме. В другом воплощении настоящего изобретения предложен кристаллический гидрохлорид 6-(1Hиндол-4-ил)-4-(5-[4-(1-метилэтил)-1-пиперазинил]-метил-1,3-оксазол-2-ил)-1H-индазола,характеризующийся тем, что он дает картину ДРЛП с пиками (2) при примерно 5,2, примерно 10,3 и/или примерно 12,8. В другом воплощении настоящего изобретения предложен кристаллический гидрохлорид 6-(1 Ниндол-4-ил)-4-(5-[4-(1-метилэтил)-1-пиперазинил]-метил-1,3-оксазол-2-ил)-1 Н-индазола,характеризующийся тем, что он дает картину ДРЛП, содержащую пики, по существу такие, как указано в табл. 1. В еще одном воплощении настоящего изобретения предложен кристаллический гидрохлорид 6-(1Hиндол-4-ил)-4-(5-[4-(1-метилэтил)-1-пиперазинил]-метил-1,3-оксазол-2-ил)-1H-индазола,характеризующийся тем, что он дает картину ДРЛП, по существу, в соответствии с фиг. 1. Если в данном описании указано, что на картине ДРЛП имеется пик при данном значении, то это обычно означает, что этот пик находится в пределах указанного значения 0,2. Данное изобретение также охватывает соединения, меченные изотопом, которые идентичны соединениям формулы (I) и их солям, но фактически один или более атомов заменены атомом, имеющим атомную массу или массовое число, отличающиеся от атомной массы или массового числа, наиболее часто встречающихся в природе. Примеры изотопов, которые могут быть введены в соединения по изобретению, включают изотопы водорода, углерода, азота, кислорода и фтора, такие как 2 Н, 3 Н, 11 С, 14 С и 18F. Соединения формулы (I) могут содержать один или более асимметрических центров (называемых также хиральными центрами) и, следовательно, могут существовать в виде индивидуальных энантиомеров, диастереомеров либо других стереоизомерных форм или в виде их смесей. Хиральные центры, такие как хиральные атомы углерода, могут присутствовать также в заместителе, таком как алкильная группа. Если стереохимия хирального центра, присутствующего в формуле (I) или в любой химической структуре, проиллюстрированной в данном описании, конкретно не указана, то предполагается, что данная структура охватывает любой стереоизомер и все их смеси. Так, соединения формулы (I), содержащие один или более хиральных центров, могут быть использованы в виде рацемических смесей, энантиомерно обогащенных смесей или в виде энантиомерно чистых индивидуальных стереоизомеров. Индивидуальные стереоизомеры соединения формулы (I), которые содержат один или более асимметрических центров, могут быть разделены способами, известными специалистам в данной области техники. Например, такое разделение может быть осуществлено (1) путем образования диастереоизомерных солей, комплексов или других производных; (2) путем селективной реакции со стереоизомерспецифическим реагентом, например путем ферментативного окисления или восстановления; или (3) путем газово-жидкостной или жидкостной хроматографии в хиральной среде, например на хиральном носителе, таком как диоксид кремния со связанным хиральным лигандом, или в присутствии хирального растворителя. Специалисту очевидно, что если желаемый стереоизомер превращают в другое химическое вещество одним из способов разделения, описанных выше, то для выделения желаемой формы необходима дополнительная стадия. Альтернативно, конкретные стереоизомеры могут быть синтезированы в результате асимметрического синтеза с использованием оптически активных реагентов, подложек,- 11021056 катализаторов или растворителей или путем превращения одного энантиомера в другой энантиомер в результате асимметрической трансформации. Соединения формулы (I) могут также содержать центры геометрической асимметрии. Если стереохимия присутствующего центра геометрической асимметрии в формуле (I) или в химической структуре,проиллюстрированной в данном описании, конкретно не указана, то подразумевается, что данная структура охватывает транс-геометрический изомер, цис-геометрический изомер и все их смеси. Аналогично,все таутомерные формы также охвачены в формуле (I) независимо от того, существуют ли такие таутомеры в равновесии или существуют преимущественно в одной форме. Следует иметь в виду, что в данном описании ссылки на соединения формулы (I) и их соли охватывают соединения формулы (I) в форме свободной кислоты или свободного основания или в форме их солей, например в форме их фармацевтически приемлемых солей. Таким образом, в одном из воплощений данное изобретение относится к соединениям формулы (I) в форме свободной кислоты или свободного основания. В другом воплощении данное изобретение относится к соединениям формулы (I) и их солям. В еще одном воплощении изобретение относится к соединениям формулы (I) и их фармацевтически приемлемым солям. Специалисту должно быть ясно, что могут быть получены фармацевтически приемлемые соли соединений формулы (I). Фактически, в некоторых воплощениях данного изобретения фармацевтически приемлемые соли соединений формулы (I) могут быть предпочтительными по сравнению с соответствующим свободным основанием или соответствующей свободной кислотой, поскольку молекулы таких солей могут иметь более высокую стабильность или растворимость, что облегчает изготовление лекарственной формы. Соответственно данное изобретение также относится к соединениям формулы (I) и их фармацевтически приемлемым солям. Используемый в данном описании термин "фармацевтически приемлемые соли" относится к солям,которые сохраняют желаемую биологическую активность заявленного соединения и оказывают минимальные нежелательные токсикологические эффекты. Эти фармацевтически приемлемые соли могут быть получены in situ в процессе конечного выделения и очистки соединения или в результате отдельного взаимодействия очищенного соединения в форме свободной кислоты либо свободного основания или нефармацевтически приемлемой соли с подходящим основанием или подходящей кислотой соответственно. Соли и сольваты, имеющие нефармацевтически приемлемые противоионы или ассоциированные растворители, входят в объем настоящего изобретения и могут быть использованы, например, в качестве промежуточных соединений в получении других соединений формулы (I) и их фармацевтически приемлемых солей. Таким образом, одно из воплощений данного изобретения охватывает соединения формулы(I) и их соли. В некоторых воплощениях соединения формулы (I) могут содержать кислотную функциональную группу. Подходящие фармацевтически приемлемые соли включают соли соединений с такими кислотными функциональными группами. Репрезентативные соли включают фармацевтически приемлемые соли металлов, такие как натриевая, калиевая, литиевая, кальциевая, магниевая, алюминиевая и цинковая соли; карбонаты и бикарбонаты, образующиеся при взаимодействии с фармацевтически приемлемым катионом металла, такого как натрий, калий, литий, кальций, магний, алюминий и цинк; соли, образованные с фармацевтически приемлемыми органическими первичными, вторичными и третичными аминами, включая алифатические амины, ароматические амины, алифатические диамины и гидроксиалкиламины, такие как метиламин, этиламин, 2-гидроксиэтиламин, диэтиламин, TEA, этилендиамин, этаноламин, диэтаноламин и циклогексиламин. В некоторых воплощениях соединения формулы (I) могут содержать основные функциональные группы и они, следовательно, способны образовывать фармацевтически приемлемые соли присоединения кислоты в результате обработки подходящей кислотой. Подходящие кислоты включают фармацевтически приемлемые неорганические кислоты и фармацевтически приемлемые органические кислоты. Репрезентативные фармацевтически приемлемые соли присоединения кислоты включают гидрохлорид,гидробромид, нитрат, метилнитрат, сульфат, бисульфат, сульфамат, фосфат, ацетат, гидроксиацетат, фенилацетат, пропионат, бутират, изобутират, валерат, малеат, гидроксималеат, акрилат, фумарат, малат,тартрат, цитрат, салицилат, пара-аминосалицилат, гликолят, лактат, гептаноат, фталат, оксалат, сукцинат,бензоат, орто-ацетоксибензоат, хлорбензоат, метилбензоат, динитробензоат, гидроксибензоат, метоксибензоат, нафтоат, гидроксинафтоат, манделат, таннат, формиат, стеарат, аскорбат, пальмитат, олеат, пируват, памоат, малонат, лаурат, глутарат, глутамат, эстолат, метансульфонат (мезилат), этансульфонат(эзилат), 2-гидроксиэтанесульфонат, бензолсульфонат (безилат), пара-аминобензолсульфонат, паратолуолсульфонат (тозилат) и нафталин-2-сульфонат. В одном из воплощений фармацевтически приемлемая соль присоединения кислоты представляет собой гидрохлорид. В еще одном воплощении фармацевтически приемлемая соль присоединения кислоты представляет собой манделат, например (R)манделат. В одном из воплощений данного изобретения предложено соединение, которое представляет собой си)-3-пиридинил]метансульфонамид или его фармацевтически приемлемую соль. В другом воплощении данного изобретения предложено соединение, которое представляет собой 6(1H-индол-4-ил)-4-(5-[4-(1-метилэтил)-1-пиперазинил]метил-1,3-оксазол-2-ил)-1H-индазол или его фармацевтически приемлемую соль. Получение соединений Соединения по изобретению могут быть получены различными способами, включая стандартные химические способы. Любая определенная выше переменная и далее будет иметь ранее определенное значение, если не указано иное. Иллюстративные общие способы синтеза изложены ниже, и получение конкретных соединений по изобретению затем описано в разделе "Примеры". Способ А. Соединения формулы (I), где R1-R4 такие, как определено выше, или их соли могут быть получены из соединений формулы (II) где R2 и R3 такие, как определено выше, a R4a представляет собой метил или подходящую защитную группу, такую как бензолсульфонил, путем обработки подходящей бороновой кислотой или боронатным эфиром, таким как 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1 Н-индол (коммерчески доступный),в присутствии подходящего палладиевого катализатора, такого как хлор-[2'-(диметиламино)-2 бифенилил]палладий-(1R,4S)-бицикло[2.2.1]гепт-2-ил[(1S,4R)-бицикло[2.2.1]гепт-2-ил]фосфан, в подходящем растворителе, таком как смесь 1,4-диоксана и воды в подходящем соотношении, например в соотношении примерно 4:1, в присутствии подходящего основания, такого как бикарбонат натрия, и при подходящей температуре, такой как от примерно 80 до примерно 150 С, например при температуре примерно 120 С. Группа R1, введенная путем обработки бороновой кислотой или боронатным эфиром, может быть защищена подходящей защитной группой, например трет-бутилдиметилсилильной группой, и может потребоваться дополнительная стадия удаления защитной группы, например обработка подходящим фторидом, таким как тетра-н-бутиламмонийфторид, в подходящем растворителе, таком как тетрагидрофуран, и при подходящей температуре, такой как комнатная температура, например при температуре примерно 20 С. Если необходимо, в случае соединений формулы (II), где R4a представляет собой подходящую защитную группу, защитная группа, например бензолсульфонил, может быть впоследствии удалена путем обработки подходящим водным неорганическим основанием, таким как водный гидроксид натрия, в подходящем растворителе, таком как изопропанол, и при подходящей температуре, такой как комнатная температура, например при температуре примерно 20 С. Соединения формулы (II), где R2, R3 и R4a такие, как определено выше, могут быть получены из соединений формулы (III) где R4a такой, как определено выше, и X1 представляет собой подходящую уходящую группу, такую как Br, путем обработки амином формулы HNR2R3, где R2 и R3 такие, как определено выше, в подходящем растворителе, таком как дихлорметан, и при подходящей температуре, такой как комнатная температура, например при температуре примерно 20 С.- 13021056 Соединения формулы (III), где R4a такой, как определено выше, и X1 представляет собой Br, могут быть получены из соединений формулы (IV) где R4a такой, как определено выше, путем обработки подходящим бромирующим агентом, таким как тетрабромид углерода, и подходящим фосфином, таким как трифенилфосфин, в подходящем растворителе, таком как дихлорметан, и при подходящей температуре, такой как от примерно 0 до примерно 50 С, например при температуре примерно 0 С с нагреванием до примерно 20 С после добавления. Или, альтернативно, соединения формулы (III), где R4a такой, как определено выше, и X1 представляет собой Br, могут быть получены из соединений формулы (IV), где R4a такой, как определено выше,путем обработки подходящим бромирующим агентом, таким как трифенилфосфиндибромид, в подходящем растворителе, таком как дихлорметан, и при подходящей температуре, такой как от примерно 0 до примерно 50 С, например при температуре примерно 0 С. Соединения формулы (IV), где R4a такой, как определено выше, могут быть получены из соединений формулы (V) где R4a такой, как определено выше, путем обработки подходящим восстановителем, таким как гидрид диизобутилалюминия, в подходящем растворителе, таком как тетрагидрофуран, и при подходящей температуре, такой как от примерно -50 до примерно 0 С, например при температуре примерно 0 С. Соединения формулы (V), где R4a такой, как определено выше, могут быть получены из соединений формулы (VI) где R4a такой, как определено выше, путем обработки подходящим галогенидом, таким как этил-2 хлор-1,3-оксазол-5-карбоксилат (коммерчески доступный), в присутствии подходящего палладиевого катализатора, такого как тетракис(трифенилфосфин)палладий(0), в подходящем растворителе, таком какN,N-диметилформамид, в присутствии подходящего йодида, например йодида натрия, и под воздействием микроволнового излучения при подходящей температуре, такой как от примерно 80 до примерно 150 С, например при температуре примерно 100 С. Или, альтернативно, соединения формулы (V), где R4a такой, как определено выше, могут быть получены из соединений формулы (VII), как они определены ниже, путем обработки подходящим станнаном, таким как гексаметилдиолово, в присутствии подходящего палладиевого катализатора, такого как тетракис(трифенилфосфин)палладий(0), и подходящего основания, такого как триэтиламин, в подходящем растворителе, таком как толуол, и при подходящей температуре, такой как от примерно 100 до примерно 200 С, например при температуре примерно 120 С, и последующей обработки подходящим галогенидом, таким как метил-2-хлор-1,3-оксазол-5-карбоксилат (коммерчески доступный), в присутствии подходящего йодида, например йодида меди(I), и подходящего палладиевого катализатора, такого как тетракис(трифенилфосфин)палладий(0), в подходящем растворителе, таком как 1,3-диметил-3,4,5,6 тетрагидро-2(1 Н)-пиримидинон, и при подходящей температуре, такой как от примерно 50 до примерно 150 С, например при температуре примерно 85 С.- 14021056 Соединения формулы (VI), где R4a такой, как определено выше, могут быть получены из соединений формулы (VII) где R4a такой, как определено выше, путем обработки подходящим станнаном, таким как гексаметилдиолово, в присутствии подходящего палладиевого катализатора, такого как тетракис(трифенилфосфин)палладий(0), в подходящем растворителе, таком как ксилол, в присутствии подходящего основания, такого как триэтиламин, и при подходящей температуре, такой как от примерно 100 до примерно 200 С, например при температуре примерно 150 С. Соединения формулы (VII), где R4a представляет собой метил, могут быть получены, например, из соединения формулы (VIII) путем метилирования с использованием подходящего основания, такого как гидрид натрия, в подходящем растворителе, таком как тетрагидрофуран, и при подходящей температуре, такой как примерно 0 С, с последующим добавлением алкилирующего агента, такого как йодметан, и перемешиванием при подходящей температуре, такой как комнатная температура, например при температуре примерно 20 С. Соединение формулы (VIII) является коммерчески доступным. Соединения формулы (VII), где R4a представляет собой подходящую защитную группу, такую как бензолсульфонил, могут быть получены из соединения формулы (VIII), как оно определено выше, путем обработки подходящим основанием, таким как гидрид натрия, в подходящем растворителе, таком какN,N-диметилформамид, и при подходящей температуре, такой как от примерно 0 до примерно 20 С, например при температуре примерно 0 С, и последующей обработки подходящим сульфонилирующим агентом, таким как бензолсульфонилхлорид, при подходящей температуре, такой как от примерно 0 до примерно 50 С, например при температуре примерно 0 С с нагреванием до примерно 20 С после добавления. Или, альтернативно, соединения формулы (VII), где R4a представляет собой подходящую защитную группу, такую как бензолсульфонил, могут быть получены из соединения формулы (VIII), как оно определено выше, путем обработки подходящим основанием, таким как гидроксид натрия, и подходящим катализатором фазового переноса, таким как бисульфат тетра-н-бутиламмония, в подходящем растворителе, таком как тетрагидрофуран, и при подходящей температуре, такой как от примерно 0 до примерно 20 С, например при температуре примерно 20 С, с последующей обработкой подходящим сульфонилирующим агентом, таким как бензолсульфонилхлорид, при подходящей температуре, такой как от примерно 0 до примерно 50 С, например при температуре примерно 25 С. Способ Б. Соединения формулы (I), где R1-R3 такие, как определено выше, и R4 представляет собой водород,или их соли могут быть получены из соединений формулы (IX) где R1-R3 такие, как определено выше, и R4b представляет собой подходящую защитную группу, такую как бензолсульфонил, путем обработки подходящим водным неорганическим основанием, таким как водный гидроксид натрия, в подходящем растворителе, таком как 1,4-диоксан, и при подходящей температуре, такой как комнатная температура, например при температуре примерно 20 С.- 15021056 Соединения формулы (IX), где R1, R2, R3 и R4b такие, как определено выше, могут быть получены из соединений формулы (X) где R1 и R4b такие, как определено выше, и X2 представляет собой подходящую уходящую группу,такую как Br, путем обработки амином формулы HNR2R3, где R2 и R3 такие, как определено выше, в подходящем растворителе, таком как дихлорметан, и при подходящей температуре, такой как комнатная температура, например при температуре примерно 20 С. Соединения формулы (X), где R1 и R4b такие, как определено выше, и X2 представляет собой Br, могут быть получены из соединений формулы (XI) где R1 и R4b такие, как определено выше, путем обработки подходящим бромирующим агентом, таким как тетрабромид углерода, и подходящим фосфином, таким как трифенилфосфин, в подходящем растворителе, таком как дихлорметан, и при подходящей температуре, такой как от примерно 0 до примерно 50 С, например при температуре примерно 0 С с нагреванием до комнатной температуры после добавления. Соединения формулы (XI), где R1 и R4b такие, как определено выше, могут быть получены из соединений формулы (XII) где R1 и R4b такие, как определено выше, путем обработки подходящим восстановителем, таким как гидрид диизобутилалюминия, в подходящем растворителе, таком как дихлорметан, и при подходящей температуре, такой как от примерно -50 до примерно 0 С, например при примерно -20 С. Соединения формулы (XII), где R1 и R4b такие, как определено выше, могут быть получены из соединений формулы (XIII) где R4b такой, как определено выше, путем обработки подходящей бороновой кислотой или боронатным эфиром, таким как 1-[(1,1-диметилэтил)(диметил)силил]-1 Н-индол-4-илбороновая кислота(коммерчески доступная), в присутствии подходящего палладиевого катализатора, такого как хлор-[2'(диметиламино)-2-бифенилил]палладий-(1R,4S)-бицикло[2.2.1]гепт-2-ил[(1S,4R)-бицикло[2.2.1]гепт-2- 16021056 ил]фосфан, в подходящем растворителе, таком как смесь 1,4-диоксана и воды в подходящем соотношении, например в соотношении примерно 10:1, в присутствии подходящего основания, такого как трехосновный фосфат калия, и при подходящей температуре, такой как от примерно 80 до примерно 150 С,например при температуре примерно 100 С. Альтернативно, этот способ может быть осуществлен под воздействием микроволнового излучения и при подходящей температуре, такой как от примерно 80 до примерно 150 С, например при температуре примерно 120 С. Боронатные эфиры формулы (XIV) где R7 такой, как определено выше, R8 представляет собой C1-6 алкил, -OR6 или галогено, где R6 такой, как определено выше, и n=0 или 1, могут быть получены из соединений формулы (XV) где R8 такой, как определено выше, и n=0 или 1, путем обработки подходящим сульфонилхлоридом формулы R7SO2Cl, таким как метансульфонилхлорид, в подходящем растворителе, таком как пиридин, и при подходящей температуре, такой как комнатная температура, например при температуре примерно 20 С. Соединения формулы (XV), где R8 такой, как определено выше, и n=0 или 1, могут быть получены из соединений формулы (XVI) где R8 такой, как определено выше, для которых коммерчески доступны многие аналоги, путем обработки подходящим бороланом, таким как 4,4,4',4',5,5,5',5'-октаметил-2,2'-би-1,3,2-диоксаборолан, в присутствии подходящего палладиевого катализатора, такого как аддукт дихлор-[1,1'-бис(дифенилфосфино)ферроцен]палладия(II) с дихлорметаном, в присутствии подходящего основания, такого как ацетат калия, в подходящем растворителе, таком как 1,4-диоксан, и при подходящей температуре, такой как от примерно 50 до примерно 120 С, например при температуре примерно 80 С. Таким образом, в одном из воплощений данного изобретения предложен способ получения соединения по изобретению, включающий: а) взаимодействие соединения формулы (II) где R2 и R3 такие, как определено выше, и R4a представляет собой метил или подходящую защитную группу, с подходящей бороновой кислотой или боронатным эфиром, с последующим, при необходимости, удалением защитной группы; или- 17021056 б) для соединения формулы (I), где R1-R3 такие, как определено выше, и R4 представляет собой водород, взаимодействие соединения формулы (IX) где R1, R2, R3 и R4b такие, как определено выше, с подходящим водным неорганическим основанием. Способы применения Соединения по изобретению являются ингибиторами активности киназ, в частности активностиPI3-киназ. Соединения, которые являются ингибиторами PI3-киназ, могут быть полезны в лечении расстройств, в основе которых лежит патология, связанная (по меньшей мере, частично) с ненадлежащей активностью PI3-киназ, таких как астма и хроническое обструктивное заболевание легких (COPD). "Несоответствующая активность PI3-киназ" относится к любой активности PI3-киназ, которая отклоняется от нормальной активности PI3-киназ, ожидаемой у конкретного пациента. Ненадлежащая активностьPI3-киназ может принимать форму, например, аномального увеличения активности или отклонения от нормы в привязке ко времени и/или контролю активности PI3-киназ. Такая ненадлежащая активность может проявляться в результе, например, сверхэкспрессии или мутации протеинкиназы, приводящей к ненадлежащей или неконтролируемой активации. Соответственно в еще одном аспекте данного изобретения раскрыты способы лечения таких расстройств. Такие расстройства включают респираторные заболевания, включая астму, хроническое обструктивное заболевание легких (COPD) и идиопатический фиброз легких (IPF); вирусные инфекции, включая вирусные инфекции дыхательных путей и вирусные обострения респираторных заболеваний, таких как астма и COPD; невирусные респираторные инфекции, включая аспергиллез и лейшманиоз; аллергические заболевания, включая аллергический ринит и атопический дерматит; аутоиммунные заболевания,включая ревматоидный артрит и рассеянный склероз; воспалительные расстройства, включая воспалительное заболевание кишечника; сердечно-сосудистые заболевания, вклчая тромбоз и атеросклероз; гематологические злокачественности; нейродегенеративные заболевания; панкреатит; полиорганную недостаточность; почечные заболевания; агрегацию тромбоцитов; рак; подвижность сперматозоидов; отторжение трансплантата; отторжение имплантата; повреждения легких; боль, включая боль, ассоциированную с ревматоидным артритом или остеоартритом, боль в спине, генерализованную воспалительную боль, пост-гепатическую невралгию, диабетическую невропатию, воспалительную невропатическую боль (травму), невралгию тройничного нерва и центральную боль. В одном из воплощений такие расстройства включают респираторные заболевания, включая астму и хроническое обструктивное заболевание легких (COPD); аллергические заболевания, включая аллергический ринит и атопический дерматит; аутоиммунные заболевания, включая ревматоидный артрит и рассеянный склероз; воспалительные расстройства, включая воспалительное заболевание кишечника; сердечно-сосудистые заболевания, включая тромбоз и атеросклероз; гематологические злокачественности; нейродегенеративные заболевания; панкреатит; полиорганную недостаточность; почечные заболевания; агрегацию тромбоцитов; рак; подвижность сперматозоидов; отторжение трансплантата; отторжение имплантата; повреждения легких; боль,включая боль, ассоциированную с ревматоидным артритом или остеоартритом, боль в спине, генерализованную воспалительную боль, пост-гепатическую невралгию, диабетическую невропатию, воспалительную невропатическую боль (травму), невралгию тройничного нерва и центральную боль. Способы лечения по изобретению включают введение безопасного и эффективного количества соединения формулы (I) или его фармацевтически приемлемой соли пациенту, нуждающемуся в таком лечении. Отдельные аспекты данного изобретения раскрывают способы лечения любого из вышеупомянутых расстройств путем введения безопасного и эффективного количества соединения формулы (I) или его фармацевтически приемлемой соли пациенту, нуждающемуся в таком лечении. Используемый в данном описании термин "лечить" со ссылкой на расстройство означает (1) улучшать состояние или предупреждать расстройство или одно или более биологических проявлений этого расстройства; (2) препятствовать (а) одной или более точкам в биологическом каскаде, который приводит к расстройству или ответственен за расстройство, или (б) одному или более биологическим проявлениям заболевания; (3) ослаблять один или более симптомов или эффектов, ассоциированных с расстройством; или (4) замедлять прогрессирование расстройства или одного или более биологических проявлений расстройства. Как указано выше, "лечение" расстройства охватывает предупреждение расстройства. Специалисту должно быть ясно, что "предупреждение" не является абсолютным термином. В медицине "предупреж- 18021056 дение" относится к профилактическому введению лекарственного средства, по существу, для уменьшения вероятности или тяжести расстройства или его биологического проявления или для препятствования наступлению такого расстройства или его биологического проявления. Используемое в данном описании выражение "безопасное и эффективное количество" со ссылкой на соединение формулы (I) или его фармацевтически приемлемую соль или другой фармацевтически активный агент означает количество соединения, достаточное для лечения состояния пациента, но достаточно низкое, чтобы избежать серьезных побочных эффектов (при разумном соотношении польза/риск) в рамках обоснованного медицинского суждения. Безопасное и эффективное количество соединения будет варьировать в зависимости от выбранного конкретного соединения (например, с учетом силы действия,эффективности и периода полувыведения соединения), выбранного пути введения, расстройства, подлежащего лечению, тяжести расстройства, подлежащего лечению, возраста, размера, массы и физического состояния пациента, которого лечат, истории болезни пациента, которого лечат, продолжительности лечения, природы сопутствующей терапии, желательного терапевтического эффекта и подобных факторов,но, тем не менее, может быть в установленном порядке определено специалистом. Используемый в данном описании термин "пациент" относится к человеку (включая взрослых и детей) или другому животному. В одном из воплощений "пациент" относится к человеку. Соединения формулы (I) или их фармацевтически приемлемые соли можно вводить любым подходящим путем введения, включая системное введение и местное введение. Системное введение включает пероральное введение, парентеральное введение, трансдермальное введение и ректальное введение. Парентеральное введение относится к путям введения иным, чем энтеральное или трансдермальное, и обычно осуществляется инъекцией или инфузией. Парентеральное введение включает внутривенную,внутримышечную и подкожную инъекцию или инфузию. Местное введение включает нанесение на кожу, а также введение в глаз, введение в ухо, внутривагинальное введение, введение ингаляцией и интраназальное введение. Ингаляция относится к введению в легкие пациента вдыханием либо через рот, либо через носовые проходы. В одном из воплощений соединения формулы (I) или их фармацевтически приемлемые соли можно вводить перорально. В другом воплощении соединения формулы (I) или их фармацевтически приемлемые соли можно вводить ингаляцией. В еще одном воплощении соединения формулы (I) или их фармацевтически приемлемые соли можно вводить интраназально. Соединения формулы (I) или их фармацевтически приемлемые соли можно вводить однократно или в соответствии с режимом введения доз, когда несколько доз вводят через варьирующие интервалы времени в течение заданного периода времени. Например, дозы можно вводить один, два, три или четыре раза в сутки. В одном из воплощений дозу вводят один раз в сутки. В еще одном воплощении дозу вводят два раза в сутки. Дозы можно вводить до достижения желаемого терапевтического эффекта или в течение неограниченного периода для поддержания желаемого терапевтического эффекта. Подходящие режимы введения доз для соединения формулы (I) или его фармацевтически приемлемой соли зависят от фармакокинетических свойств этого соединения, таких как всасывание, распределение и период полувыведения, которые могут быть определены специалистом. Кроме того, подходящие режимы введения доз соединения формулы (I) или его фармацевтически приемлемой соли, включая длительность периода введения доз, зависят от расстройства, подлежащего лечению, тяжести расстройства, подлежащего лечению,возраста и физического состояния пациента, которого лечат, истории болезни пациента, которого лечат,природы сопутствующей терапии, желательного терапевтического эффекта и подобных факторов в рамках знаний и опыта специалиста. Специалисты понимают, что подходящие режимы введения доз могут потребовать корректировки с учетом ответной реакции индивидуального пациента на режим введения доз или со временем, когда потребуется изменить режим введения доз индивидуальному пациенту. Типичные суточные дозировки могут варьировать в зависимости от выбранного конкретного пути введения. Типичные суточные дозировки для перорального введения находятся в диапазоне от 0,001 до 50 мг на 1 кг общей массы тела, например от 1 до 10 мг на 1 кг общей массы тела. Например, суточные дозировки для перорального введения могут составлять от 0,5 мг до 2 г на пациента, например от 10 мг до 1 г на пациента. Дополнительно, соединения формулы (I) можно вводить в виде пролекарств. В данном описании"пролекарство" соединения формулы (I) представляет собой функциональное производное соединения,которое при введении пациенту в конечном счете высвобождает соединение формулы (I) in vivo. Введение соединения формулы (I) в виде пролекарства дает специалисту возможность осуществлять одно или более из следующих: (а) модифицировать наступление активности соединения in vivo; (б) модифицировать продолжительность действия соединения in vivo; (в) модифицировать транспорт или распределение соединения in vivo; (г) модифицировать растворимость соединения in vivo и (д) ослаблять побочный эффект или преодолевать другие трудности, с которыми сталкивается соединение. Типичные функциональные производные, используемые для получения пролекарств, включают модификации соединения,которые химически или ферментативно расщепляются in vivo. Такие модификации, которые включают получение фосфатов, амидов, эфиров, тиоэфиров, углеводов и карбаматов, известны специалистам в данной области техники. Таким образом, в одном аспекте изобретения раскрыт способ лечения расстройства, опосредован- 19021056 ного ненадлежащей активностью PI3-киназ, включающий введение безопасного и эффективного количества соединения формулы (I) или его фармацевтически приемлемой соли пациенту, нуждающемуся в таком лечении. В одном из воплощений изобретения раскрыт способ лечения расстройства, опосредованного ненадлежащей активностью PI3-киназ, включающий введение безопасного и эффективного количества N-[5-[4-(5-[(2R,6S)-2,6-диметил-4-морфолинил]метил-1,3-оксазол-2-ил)-1H-индазол-6-ил]-2(метилокси)-3-пиридинил]метансульфонамида или его фармацевтически приемлемой соли пациенту,нуждающемуся в таком лечении. В другом воплощении изобретения раскрыт способ лечения расстройства, опосредованного ненадлежащей активностью PI3-киназ, включающий введение безопасного и эффективного количества (R)-манделата N-[5-[4-(5-[(2R,6S)-2,6-диметил-4-морфолинил]метил-1,3 оксазол-2-ил)-1H-индазол-6-ил]-2-(метилокси)-3-пиридинил]метансульфонамида пациенту, нуждающемуся в таком лечении. В другом воплощении изобретения раскрыт способ лечения расстройства, опосредованного ненадлежащей активностью PI3-киназ, включающий введение безопасного и эффективного количества 6-(1 Н-индол-4-ил)-4-(5-[4-(1-метилэтил)-1-пиперазинил]метил-1,3-оксазол-2-ил)-1Hиндазола или его фармацевтически приемлемой соли пациенту, нуждающемуся в таком лечении. В еще одном воплощении изобретения раскрыт способ лечения расстройства, опосредованного ненадлежащей активностью PI3-киназ, включающий введение безопасного и эффективного количества гидрохлорида 6(1H-индол-4-ил)-4-(5-[4-(1-метилэтил)-1-пиперазинил]метил-1,3-оксазол-2-ил)-1H-индазола пациенту,нуждающемуся в таком лечении. В одном из воплощений расстройство, опосредованное ненадлежащей активностью PI3-киназ, выбрано из группы, состоящей из респираторных заболеваний (включая астму, хроническое обструктивное заболевание легких (COPD) и идиопатический фиброз легких (IPF; вирусных инфекций (включая вирусные инфекции дыхательных путей и вирусные обострения респираторных заболеваний, таких как астма и COPD); невирусных респираторных инфекций (включая аспергиллез и лейшманиоз); аллергических заболеваний (включая аллергический ринит и атопический дерматит); аутоиммунных заболеваний(включая ревматоидный артрит и рассеянный склероз); воспалительных расстройств (включая воспалительное заболевание кишечника); сердечно-сосудистых заболеваний (включая тромбоз и атеросклероз); гематологических злокачественностей; нейродегенеративных заболеваний; панкреатита; полиорганной недостаточности; почечных заболеваний; агрегации тромбоцитов; рака; подвижности сперматозоидов; отторжения трансплантата; отторжения имплантата; повреждений легких; боли (включая боль, ассоциированную с ревматоидным артритом или остеоартритом, боль в спине, генерализованную воспалительную боль, пост-гепатическую невралгию, диабетическую невропатию, воспалительную невропатическую боль (травму), невралгию тройничного нерва и центральную боль). В одном из воплощений расстройство, опосредованное ненадлежащей активностью PI3-киназ,представляет собой респираторное заболевание. В другом воплощении расстройство, опосредованное ненадлежащей активностью PI3-киназ, представляет собой астму. В другом воплощении расстройство,опосредованное ненадлежащей активностью PI3-киназ, представляет собой хроническое обструктивное заболевание легких (COPD). В еще одном воплощении расстройство, опосредованное ненадлежащей активностью PI3-киназ, представляет собой идиопатический фиброз легких (IPF). В одном из воплощений расстройство, опосредованное ненадлежащей активностью PI3-киназ,представляет собой боль. В одном из воплощений настоящего изобретения раскрыт способ лечения респираторного заболевания, включающий введение безопасного и эффективного количества N-[5-[4-(5-[(2R,6S)-2,6-диметил 4-морфолинил]метил-1,3-оксазол-2-ил)-1H-индазол-6-ил]-2-(метилокси)-3-пиридинил]метансульфонамида или его фармацевтически приемлемой соли пациенту, нуждающемуся в таком лечении. В другом воплощении настоящего изобретения раскрыт способ лечения астмы, включающий введение безопасного и эффективного количества N-[5-[4-(5-[(2R,6S)-2,6-диметил-4-морфолинил]метил 1,3-оксазол-2-ил)-1H-индазол-6-ил]-2-(метилокси)-3-пиридинил]метансульфонамида или его фармацевтически приемлемой соли пациенту, нуждающемуся в таком лечении. В другом воплощении настоящего изобретения раскрыт способ лечения респираторного заболевания, включающий введение безопасного и эффективного количества (R)-манделата N-[5-[4-(5-[(2R,6S)2,6-диметил-4-морфолинил]метил-1,3-оксазол-2-ил)-1 Н-индазол-6-ил]-2-(метилокси)-3 пиридинил]метансульфонамида пациенту, нуждающемуся в таком лечении. В другом воплощении настоящего изобретения раскрыт способ лечения астмы, включающий введение безопасного и эффективного количества (R)-манделата N-[5-[4-(5-[(2R,6S)-2,6-диметил-4 морфолинил]метил-1,3-оксазол-2-ил)-1H-индазол-6-ил]-2-(метилокси)-3-пиридинил]метансульфонамида пациенту, нуждающемуся в таком лечении. Композиции Перед тем как вводить пациенту соединения формулы (I) и их фармацевтически приемлемые соли обычно, но не обязательно, должны быть приготовлены в виде фармацевтических композиций. В одном аспекте данное изобретение относится к фармацевтическим композициям, содержащим от 0,05 до 1000 мг соединения формулы (I) или его фармацевтически приемлемой соли и от 0,1 до 2 г одного или более фармацевтически приемлемых эксципиентов. В еще одном аспекте данное изобретение относится к фармацевтической композиции для лечения или профилактики расстройства, опосредованного ненадлежащей активностью PI3-киназ, содержащей соединение формулы (I) или его фармацевтически приемлемую соль. В одном из воплощений настоящего изобретения предложена фармацевтическая композиция для лечения или профилактики расстройства, опосредованного ненадлежащей активностью PI3-киназ, содержащая N-[5-[4-(5-[(2R,6S)-2,6-диметил-4-морфолинил]метил-1,3-оксазол-2-ил)-1H-индазол-6-ил]-2(метилокси)-3-пиридинил]метансульфонамид или его фармацевтически приемлемую соль. В одном из воплощений настоящего изобретения предложена фармацевтическая композиция для лечения или профилактики расстройства, опосредованного ненадлежащей активностью PI3-киназ, содержащая (R)-манделат N-[5-[4-(5-[(2R,6S)-2,6-диметил-4-морфолинил]метил-1,3-оксазол-2-ил)-1 Ниндазол-6-ил]-2-(метилокси)-3-пиридинил]метансульфонамида. В одном из воплощений настоящего изобретения предложена фармацевтическая композиция для лечения или профилактики расстройства, опосредованного ненадлежащей активностью PI3-киназ, содержащая 6-(1 Н-индол-4-ил)-4-(5-[4-(1-метилэтил)-1-пиперазинил]метил-1,3-оксазол-2-ил)-1 Н-индазол или его фармацевтически приемлемую соль. В еще одном воплощении настоящего изобретения предложена фармацевтическая композиция для лечения или профилактики расстройства, опосредованного ненадлежащей активностью PI3-киназ, содержащая гидрохлорид 6-(1H-индол-4-ил)-4-(5-[4-(1-метилэтил)-1-пиперазинил]метил-1,3-оксазол-2 ил)-1 Н-индазола. Фармацевтические композиции по изобретению могут быть приготовлены и упакованы в нерасфасованной форме, из которой безопасное и эффективное количество соединения формулы (I) или его фармацевтически приемлемой соли может быть извлечено и затем введено пациенту, например, в виде порошка или сиропа. Альтернативно, фармацевтические композиции по изобретению могут быть приготовлены и упакованы в стандартной лекарственной форме, где каждая физически дискретная единица содержит соединение формулы (I) или его фармацевтически приемлемую соль. Фармацевтические композиции по изобретению, приготовленные в стандартной лекарственной форме, обычно могут содержать, например, от 0,5 мг до 1 г, или от 1 до 700 мг, или от 5 до 100 мг соединения формулы (I) или его фармацевтически приемлемой соли. Фармацевтические композиции по изобретению обычно содержат одно соединение формулы (I) или одну его фармацевтически приемлемую соль. Используемое в данном описании выражение "фармацевтически приемлемый эксципиент" означает фармацевтически приемлемое вещество, композицию или носитель, вводимые в предоставленной форме или консистенции в фармацевтические композиции. Каждый эксципиент должен быть совместимым с другими ингредиентами фармацевтических композиций при смешивании, чтобы избежать взаимодействий, которые могут существенно снизить эффективность соединения формулы (I) или его фармацевтически приемлемой соли при введении пациенту, и взаимодействий, которые могут привести к получению композиций, которые не являются фармацевтически приемлемыми. Кроме того, каждый эксципиент непременно должен быть фармацевтически приемлемым, например должен иметь достаточно высокую чистоту. Соединение формулы (I) или его фармацевтически приемлемая соль и фармацевтически приемлемый эксципиент или эксципиенты, как правило, будут готовить в лекарственной форме, адаптированной для введения пациенту желаемым путем введения. Например, лекарственные формы включают лекарственные формы, адаптированные (1) для перорального введения, такие как таблетки, капсулы, каплетки,пилюли, пастилки, порошки, сиропы, эликсиры, суспензии, растворы, эмульсии, саше и облатки; (2) для парентерального введения, такие как стерильные растворы, суспензии и порошки для разведения; (3) для трансдермального введения, такие как трансдермальные пластыри; (4) для ректального введения, такие как суппозитории; (5) для введения ингаляцией, такие как аэрозоли, растворы и сухие порошки; и (6) для местного введения, такие как кремы, мази, лосьоны, растворы, пасты, спреи, пены и гели. Подходящие фармацевтически приемлемые эксципиенты будут варьировать в зависимости от выбранной конкретной лекарственной формы. Кроме того, подходящие фармацевтически приемлемые эксципиенты могут быть выбраны с учетом конкретной функции, которую они могут выполнять в композиции. Например, некоторые фармацевтически приемлемые эксципиенты могут быть выбраны ввиду того,что они способны облегчать изготовление однородных лекарственных форм. Некоторые фармацевтически приемлемые эксципиенты могут быть выбраны ввиду того, что они способны облегчать изготовление стабильных лекарственных форм. Некоторые фармацевтически приемлемые эксципиенты могут быть выбраны ввиду того, что они способны облегчать перенос или транспорт соединения или соедине- 21021056 ний формулы (I) или их фармацевтически приемлемых солей сразу после введения пациенту из одного органа или участка тела в другой орган или участок тела. Некоторые фармацевтически приемлемые эксципиенты могут быть выбраны ввиду того, что они способны улучшать соблюдение пациентом режима и схемы лечения. Подходящие фармацевтически приемлемые эксципиенты включают следующие типы эксципиентов: разбавители, наполнители, связывающие вещества, разрыхлители, смазывающие вещества, глиданты, гранулирующие агенты, покровные агенты, увлажняющие агенты, растворители, со-растворители,суспендирующие агенты, эмульгаторы, подсластители, корригенты, агенты, маскирующие вкус, красители, антислеживатели, увлажнители, хелатирующие агенты, пластификаторы, агенты, повышающие вязкость, антиоксиданты, консерванты, стабилизаторы, поверхностно-активные вещества и буферные агенты. Для специалиста очевидно, что некоторые фармацевтически приемлемые эксципиенты могут выполнять более чем одну функцию имогут выполнять альтернативные функции в зависимости от того, насколько много эксципиента присутствует в композиции и какие другие эксципиенты присутствуют в композиции. Специалисты обладают необходимыми знаниями и способны выбрать подходящие фармацевтически приемлемые эксципиенты в соответствующих количествах для использования в данном изобретении. Кроме того, имеется большое количество доступных специалистам ресурсов, в которых описаны фармацевтически приемлемые эксципиенты и которые могут быть полезны в выборе подходящих фармацевтически приемлемых эксципиентов. Примеры включают Remington's Pharmaceutical Sciences (Mack Publishing Company), The Handbook of Pharmaceutical Additives (Gower Publishing Limited) и The Handbook ofPharmaceutical Excipients (the American Pharmaceutical Association и the Pharmaceutical Press). Фармацевтические композиции по изобретению готовят с использованием методов и способов, известных специалистам в данной области техники. Некоторые способы, обычно используемые в данной области, описаны в Remington's Pharmaceutical Sciences (Mack Publishing Company). Соответственно в еще одном аспекте данного изобретения раскрыт способ приготовления фармацевтической композиции, содержащей соединение формулы (I) или его фармацевтически приемлемую соль и один или более фармацевтически приемлемых эксципиентов, включающий смешивание ингредиентов. Фармацевтическая композиция, содержащая соединение формулы (I) или его фармацевтически приемлемую соль, может быть приготовлена, например, путем смешивания при температуре окружающей среды и атмосферном давлении. В одном из воплощений соединения формулы (I) или их фармацевтически приемлемые соли могут быть приготовлены в лекарственной форме для перорального введения. В другом воплощении соединения формулы (I) или их фармацевтически приемлемые соли могут быть приготовлены в лекарственной форме для введения ингаляцией. В еще одном воплощении соединения формулы (I) или их фармацевтически приемлемые соли могут быть приготовлены в лекарственной форме для интраназального введения. В одном из аспектов данное изобретение относится к твердой пероральной лекарственной форме,такой как таблетка или капсула, содержащей безопасное и эффективное количество соединения формулы(I) или его фармацевтически приемлемой соли и разбавитель или наполнитель. Подходящие разбавители и наполнители включают лактозу, сахарозу, декстрозу, маннит, сорбит, крахмал (например, кукурузный крахмал, картофельный крахмал и предварительно желатинизированный крахмал), целлюлозу и ее производные (например, микрокристаллическую целлюлозу), сульфат кальция и двухосновный фосфат кальция. Пероральная твердая лекарственная форма может дополнительно содержать связывающее вещество. Подходящие связывающие вещества включают крахмал (например, кукурузный крахмал, картофельный крахмал и предварительно желатинизированный крахмал), желатин, аравийскую камедь, альгинат натрия, альгиновую кислоту, трагакант, гуаровую камедь, повидон и целлюлозу и ее производные(например, микрокристаллическую целлюлозу). Пероральная твердая лекарственная форма может дополнительно содержать разрыхлитель. Подходящие разрыхлители включают кросповидон, крахмалгликолят натрия, кроскармелозу, альгиновую кислоту и натрий-карбоксиметилцеллюлозу. Пероральная твердая лекарственная форма может дополнительно содержать смазывающее вещество. Подходящие смазывающие вещества включают стеариновую кислоту, стеарат магния, стеарат кальция и тальк. В тех случаях, когда это целесообразно, композиции в стандартной лекарственной форме для перорального введения могут быть микроинкапсулированными. Композиция может также быть приготовлена для обеспечения пролонгированного или длительного высвобождения, например, путем нанесения покрытия или заключения дисперсного вещества в полимерах, воске или т.п. Соединения формулы (I) или их фармацевтически приемлемые соли могут быть также связаны с растворимыми полимерами в качестве носителя для направленной доставки лекарственного средства. Такие полимеры могут включать поливинилпирролидон, пирановый сополимер, полигидроксипропилметакриламид-фенол, полигидроксиэтиласпартамидфенол или полиэтиленоксидполилизин, замещенный пальмитоильными остатками. Кроме того, соединения формулы (I) или их фармацевтически приемлемые соли могут быть связаны с полимерами класса биоразлагаемых полимеров, полезными для достижения контролируемого высвобождения лекарственного средства, например с полимолочной кислотой, полиэпсилонкапролактоном, полигидроксимасляной кислотой, полиортоэфирами, полиацеталями, полидигид- 22021056 ропиранами, полицианоакрилатами и поперечно сшитыми или амфипатическими блок-сополимерами гидрогелей. В другом аспекте данное изобретение относится к жидкой пероральной лекарственной форме. Пероральные жидкости, такие как растворы, сиропы и эликсиры, могут быть приготовлены в стандартной лекарственной форме, заданное количество которой содержит предопределенное количество соединения формулы (I) или его фармацевтически приемлемой соли. Сиропы могут быть приготовлены путем растворения соединения формулы (I) или его фармацевтически приемлемой соли в соответствующим образом корригированном водном растворе, а эликсиры могут быть приготовлены с использованием нетоксичного спиртового носителя. Суспензии могут быть приготовлены путем диспергирования соединения формулы (I) или его фармацевтически приемлемой соли в нетоксичном носителе. Солюбилизаторы и эмульгаторы, такие как этоксилированные изостеариловые спирты и эфиры полиоксиэтиленсорбита,консерванты, корригирующая добавка, такая как масло перечной мяты или натуральные подсластители или сахарин или другие искусственные подсластители и т.п. также могут быть добавлены. В еще одном аспекте данное изобретение относится к лекарственной форме, адаптированной для введения пациенту ингаляцией, например, в виде сухого порошка, аэрозоля, суспензии или раствора. В одном из воплощений данное изобретение относится к лекарственной форме, адаптированной для введения пациенту ингаляцией в виде сухого порошка. В еще одном воплощении данное изобретение относится к лекарственной форме, адаптированной для введения пациенту ингаляцией при помощи небулайзера. Сухие порошковые композиции для доставки в легкое ингаляцией обычно содержат соединение формулы (I) или его фармацевтически приемлемую соль в виде тонкоизмельченного порошка вместе с одним или более фармацевтически приемлемыми эксципиентами в виде тонкоизмельченных порошков. Фармацевтически приемлемые эксципиенты, пригодные, в частности, для использования в сухих порошках, известны специалистам в данной области и включают лактозу, крахмал, маннит и моно-, ди- и полисахариды. Тонкоизмельченный порошок может быть получен, например, путем микронизации и измельчения. Как правило, измельченное соединение (например, микронизированное) может быть охарактеризовано значением D50 (средний диаметр частиц) примерно от 1 до примерно 10 мкм (измеренным, например, методом лазерной дифракции). Сухой порошок можно вводить пациенту при помощи резервуарного сухого порошкового ингалятора (RDPI), имеющего резервуар, пригодный для хранения многократных (недозированных) доз лекарственного средства в сухой порошковой форме. RDPI обычно включают в себя устройство для дозирования каждой дозы лекарственного средства из резервуара в положение доставки. Например, дозирующее устройство может содержать дозировочную чашку, перемещающуюся из первого положения, где чашка может заполняться лекарственным средством из резервуара, во второе положение, где отмеренная доза лекарственного средства предоставляется пациенту для ингаляции. Альтернативно, сухой порошок может находиться в капсулах (например, желатиновых или пластиковых), картриджах или блистерных упаковках для использования в многодозовом сухом порошковом ингаляторе (MDPI). MDPI являются ингаляторами, в которых лекарственное средство находится в многодозовой упаковке, содержащей (или, иначе, несущей) множество определенных доз (или их частей) лекарственного средства. Когда сухой порошок представлен в виде блистерной упаковки, тогда такая упаковка содержит множество блистеров, в которых находится лекарственное средство в форме сухого порошка. Блистеры обычно расположены в регулярном порядке с возможностью легкого высвобождения из них лекарственного средства. Например, блистеры могут быть расположены по окружности на блистерной упаковке в форме диска или блистеры могут иметь вытянутую форму, например форму полоски или ленты. Каждая(ый) капсула, картридж или блистер может содержать, например, от 20 мкг до 10 мг соединения формулы (I) или его фармацевтически приемлемой соли. Аэрозоли могут быть образованы путем суспендирования или растворения соединения формулы (I) или его фармацевтически приемлемой соли в сжиженном пропелленте. Подходящие пропелленты включают галогеноуглероды, углеводороды и другие сжиженные газы. Репрезентативные пропелленты включают трихлорфторметан (пропеллент 11), дихлорфторметан (пропеллент 12), дихлортетрафторэтан (пропеллент 114), тетрафторэтан (HFA-134 а), 1,1-дифторэтан (HFA-152a), дифторметан (HFA-32), пентафторэтан (HFA-12), гептафторпропан (HFA-227a), перфторпропан, перфторбутан, перфторпентан, бутан,изобутан и пентан. Аэрозоли, содержащие соединение формулы (I) или его фармацевтически приемлемую соль, в большинстве случаев могут быть введены пациенту с помощью дозирующего ингалятора(MDI). Такие устройства известны специалистам в данной области техники. Аэрозоль может содержать дополнительные фармацевтически приемлемые эксципиенты, обычно используемые с MDI, такие как поверхностно-активные вещества, смазывающие вещества, сорастворители и другие эксципиенты для повышения физической стабильности препарата, для улучшения работы клапана, для улучшения растворимости или для улучшения вкуса. Таким образом, в качестве еще одного аспекта данного изобретения предложена аэрозольная фармацевтическая композиция, содержащая соединение формулы (I) или его фармацевтически приемлемую соль и фторуглерод или водородсодержащий хлорфторуглерод в качестве пропеллента, возможно в ком- 23021056 бинации с поверхностно-активным веществом и/или со-растворителем. Согласно другому аспекту данного изобретения предложена аэрозольная фармацевтическая композиция, в которой пропеллент выбран из 1,1,1,2-тетрафторэтана, 1,1,1,2,3,3,3-гептафтор-н-пропана и их смесей. Композиции по изобретению могут быть забуферены путем добавления подходящих буферных агентов. Могут быть приготовлены капсулы и картриджи для использования в ингаляторе или инсуффляторе, например капсулы и картриджи из желатина, содержащие предназначенную для ингаляции порошковую смесь соединения формулы (I) или его фармацевтически приемлемой соли и подходящей порошковой основы, такой как лактоза или крахмал. Каждая(ый) капсула или картридж, как правило, может содержать от 20 мкг до 10 мг соединения формулы (I) или его фармацевтически приемлемой соли. Альтернативно, соединение формулы (I) или его фармацевтически приемлемая соль может присутствовать без эксципиентов, таких как лактоза. Доля активного соединения формулы (I) или его фармацевтически приемлемой соли в местных композициях согласно изобретению зависит от точного типа композиции, которую изготавливают, но будет составлять, как правило, от 0,001 до 10 мас.%. Как правило, для большинства типов композиций используемая доля будет составлять от 0,005 до 1%, например от 0,01 до 0,5%. Однако в порошках для ингаляции или инсуффляции используемая доля будет составлять от 0,1 до 5%. Аэрозольные композиции предпочтительно составлены таким образом, что каждая отмеренная доза или "пшик" аэрозоля содержит от 20 мкг до 10 мг, предпочтительно от 20 до 2000 мкг, более предпочтительно от примерно 20 до 500 мкг соединения формулы (I). Введение можно выполнять один раз в сутки или несколько раз в сутки, например 2, 3, 4 или 8 раз, с введением, например, 1, 2 или 3 доз каждый раз. Общая суточная доза, вводимая с аэрозолем, будет составлять от 100 мкг до 10 мг, предпочтительно от 200 до 2000 мкг. Общая суточная доза и отмеренная доза, доставляемая капсулами и картриджами, находящимися в ингаляторе или инсуффляторе, обычно будет в два раза больше дозы, доставляемой с аэрозольными композициями. В случае суспензионных аэрозольных композиций размер частиц дисперсного (например, микронизированного) лекарственного средства должен быть таким, чтобы обеспечивать вдыхание, по существу,всего лекарственного средства в легкие при введении аэрозольной композиции, и поэтому будет составлять менее 100 мкм, желательно менее 20 мкм и, в частности, в диапазоне от 1 до 10 мкм, например от 1 до 5 мкм, более предпочтительно от 2 до 3 мкм. Композиции по изобретению могут быть приготовлены путем диспергирования или растворения медикамента и соединения формулы (I) или его фармацевтически приемлемой соли в выбранном пропелленте в подходящем контейнере, например, с помощью обработки ультразвуком или с помощью смесителя с высокими сдвиговыми усилиями. Этот процесс желательно проводить в условиях с контролируемой влажностью. Химическая и физическая стабильность, а также фармацевтическая приемлемость аэрозольных композиций согласно изобретению могут быть определены методами, известными специалистам в данной области техники. Так, например, химическая стабильность компонентов может быть определена,например, ВЭЖХ-анализом после длительного хранения продукта. Данные по физической стабильности могут быть получены другими общепринятыми аналитическими методами, такими как, например, тестирование на утечку, анализ на производительность клапана (средняя масса выпускаемой дозы при срабатывании), анализ на воспроизводимость дозы (количество активного ингредиента при срабатывании) и анализ распределения распыляемой струи. Устойчивость суспензионных аэрозольных композиций согласно изобретению может быть определена общепринятыми методами, например путем определения распределения размеров флокуляции с использованием прибора для измерения светорассеяния в отраженном свете или путем определения распределения частиц по размерам в каскадном импакторе или аналитическим методом "двойной импинджер" ("twin impinger"). В данном описании ссылка на анализ "двойной импинджер" означает "Определение осаждения выпущенной дозы при ингаляциях под давлением с использованием аппарата А", как определено в Британской Фармакопее (British Pharmacopaeia 1988, p. A204-207, Appendix XVII С). Такие методы делают возможным расчет "вдыхаемой фракции" аэрозольных композиций. В одном методе"вдыхаемую фракцию" рассчитыают по тонкодисперсной фракции", которая представляет собой количество активного ингредиента, собранного в нижней камере импинджера при срабатывании, выраженное в процентах от общего количества активного ингредиента, доставленного при срабатывании, с использованием метода двойного импинджера, описанного выше. Термин "дозирующий ингалятор", или MDI, означает устройство, включающее баллончик, закрепленную на баллончике насадку и расположенный в насадке клапан, дозирующий композицию. MDIсистема включает в себя подходящее канальное устройство. Подходящие канальные устройства содержат, например, клапан-пускатель и цилиндрический или конусоподобный проход, через который лекарственное средство может доставляться из заполнененого баллончика посредством дозирующего клапана в нос или рот пациента, например мундштучный пускатель. Баллончики MDI обычно содержат контейнер, способный выдерживать давление паров используемого пропеллента, например пластмассовый или стеклянный сосуд с пластмассовым покрытием или предпочтительно металлический баллончик, например, из алюминия или из его сплава, возможно анодированный, покрытый лаком и/или с пластмассовым покрытием (например, как описано во включенной в данное описание посредством ссылки международной публикации WO 96/32099, где часть или вся внутренняя поверхность покрыта одним или более фторуглеродными полимерами, возможно в комбинации с одним или более полимерами, не являющимися фторуглеродными), и этот контейнер закрыт дозирующим клапаном. Насадка может быть закреплена на баллончике посредством ультразвуковой сварки, прикручивания или обжатия. MDI, упомянутые в данном описании, могут быть изготовлены способами, известными в данной области (см., например, Byron выше и WO 96/32099). Предпочтительно баллончик оснащен блоком-насадкой, где клапан, дозирующий лекарственное средство, расположен в насадке, и указанная насадка закреплена опрессовкой на своем месте. В одном из воплощений данного изобретения металлическая внутренняя поверхность баллончика покрыта фторполимером, более предпочтительно фторполимером, смешанным с полимером, не являющимся фторполимером. В другом воплощении данного изобретения металлическая внутренняя поверхность баллона покрыта полимерной смесью политетрафторэтилена (PTFE) и полиэфирсульфона (PES). В еще одном воплощении данного изобретения вся металлическая внутренняя поверхность баллончика покрыта полимерной смесью политетрафторэтилена (PTFE) и полиэфирсульфона (PES). Дозирующие клапаны предназначены для доставки отмеренного количества композиции при срабатывании и имеют герметизирующую прокладку для предотвращения утечки пропеллента через клапан. Прокладка может быть изготовлена из любого подходящего эластомерного материала, такого как, например, полиэтилен низкой плотности, хлорбутил, бромбутил, EPDM (этилен-пропилен-диеновый мономер), черные и белые бутадиен-акрилонитрильные каучуки, бутилкаучук и неопрен. Подходящие клапаны коммерчески доступны от производителей, известных в индустрии аэрозолей, например от Valois,France (например, DF10, DF30, DF60), Bespak pic, UK (например, BK300, ВК 357) и 3M-Neotechnic Ltd.,UK (например, Spraymiser). В различных воплощениях MDI могут быть также использованы совместно с другими системами,такими как, без ограничения, упаковки для хранения и содержания в них MDI, включая те из них, которые описаны в патентах США 6119853, 6179118, 6315112, 6352152, 6390291 и 6679374, а также счетчики доз, такие как, без ограничения, счетчики доз, описанные в патентах США 6360739 и 6431168. Для изготовления крупномасштабных партий в промышленном производстве заполненных баллонов могут быть использованы обычные способы и оборудование для массового производства, известные специалистам в области производства фармацевтических аэрозолей. Так, например, в одном способе массового изготовления суспензионных аэрозольных препаратов дозирующий клапан соединяют с алюминиевым контейнером опрессовкой с получением пустого баллончика. В загрузочный сосуд добавляют конкретное лекарственное средство и сжиженный пропеллент вместе с возможными эксципиентами под давлением подают через этот загрузочный сосуд в производственный сосуд. Суспензию лекарственного средства смешивают, затем осуществляют рециркуляцию в фасовочную машину и аликвоту суспензии лекарственного средства затем заливают через дозирующий клапан в баллон. В одном примере способа массового производственного изготовления аэрозольных препаратов в виде раствора дозирующий клапан закрепляют на алюминиевом контейнере опрессовкой с получением пустого баллончика. Сжиженный пропеллент вместе с возможными эксципиентами и растворенное лекарственное средство под давлением подают через загрузочный сосуд в производственный сосуд. В альтернативном способе аликвоту сжиженной композиции добавляют в открытый баллончик в условиях, достаточно холодных для того, чтобы композиция не испарялась, а затем дозирующий клапан закрепляют на баллоне опрессовкой. Обычно в партиях, изготовленных для фармацевтического применения, каждый заполненный баллончик взвешивают для контроля, снабжают кодом с номером партии, укладывают в лоток для хранения и затем проводят тестирование готовой продукции. Суспензии и растворы, содержащие соединение формулы (I) или его фармацевтически приемлемую соль, можно также вводить пациенту с помощью небулайзера. Растворитель или суспендирующий агент,используемый для небулизации, может представлять собой любую фармацевтически приемлемую жидкость, такую как вода, водный солевой раствор, спирты или гликоли, например этанол, изопропиловый спирт, глицерин, пропиленгликоль, полиэтиленгликоль и т.д. или их смеси. В солевых растворах используют соли, которые проявляют небольшую фармакологическую активность или не проявляют никакой фармакологической активности после введения. Для этой цели могут быть использованы неорганические соли, такие как соли щелочных металлов или аммонийгалогенидные соли, например хлорид натрия, хлорид калия, или органические соли, такие как калиевые, натриевые и аммониевые соли органических кислот, например аскорбиновой кислоты, лимонной кислоты, уксусной кислоты, винной кислоты и т.д. В суспензию или раствор могут быть добавлены другие фармацевтически приемлемые эксципиенты. Соединение формулы (I) или его фармацевтически приемлемая соль могут быть стабилизированы добавлением неорганической кислоты, например соляной кислоты, азотной кислоты, серной кислоты и/или фосфорной кислоты; органической кислоты, например аскорбиновой кислоты, лимонной кислоты,уксусной кислоты и винной кислоты и т.д., комплексообразующего агента, такого как EDTA (этилендиаминтетрауксусная кислота) или лимонная кислота и их соли; или антиоксиданта, такого как витамин Е или аскорбиновая кислота. Их можно использовать по отдельности или вместе для стабилизации соединения формулы (I) или его фармацевтически приемлемой соли. Могут быть добавлены консерванты,такие как хлорид бензалкония или бензойная кислота и их соли. Поверхностно-активное вещество может быть добавлено, в частности, для повышения физической стабильности суспензий. Поверхностноактивные вещества включают лецитин, динатрий-диоктилсульфосукцинат, олеиновую кислоту и сложные эфиры сорбитана. В дополнительном аспекте данное изобретение относится к лекарственной форме, адаптированной для интраназального введения. Композиции для введения в нос могут включать аэрозольные композиции под давлением и водные композиции, вводимые в нос с помощью нагнетательного насоса. Особый интерес представляют композиции, которые не находятся под давлением и адаптированы для местного введения в носовую полость. Подходящие для этой цели композиции содержат воду в качестве разбавителя или носителя. Водные композиции для введения в легкое или нос могут быть приготовлены с использованием традиционных эксципиентов, таких как буферные агенты, агенты, модифицирующие тоничность, и т.п. Водные композиции можно также вводить в нос небулизацией. Соединения формулы (I) или их фармацевтически приемлемые соли могут быть приготовлены в виде жидкой композиции для доставки из жидкостного дозирующего устройства, например жидкостного дозатора, имеющего дозирующее сопло или дозирующую насадку, через которое(ую) отмеренная доза жидкостной композиции распыляется, когда пользователь нажимает на насосный механизм жидкостного дозатора. Такие жидкостные дозаторы, как правило, снабжены резервуаром для множества отмериваемых доз жидкой композиции, причем эти дозы распыляются при последовательных срабатываниях насоса. Дозирующее сопло или насадка могут иметь конфигурацию, подходящую для введения в ноздри пользователя для впрыскивания жидкого препарата в носовую полость. Жидкостное дозирующее устройство вышеупомянутого типа описано и проиллюстрировано в публикации международной патентной заявки WO 05/044354, полное содержание которой включено в данное описание посредством ссылки. Дозирующее устройство имеет корпус, в котором находится выпускающее жидкость устройство с нагнетательным насосом, установленным на контейнере, в котором находится жидкая композиция. Корпус имеет по меньшей мере один приводимый в действие пальцами боковой рычаг, который двигается внутрь относительно корпуса, перемещая контейнер вверх в корпусе посредством эксцентрика, заставляя насос сжимать и нагнетать отмеренную дозу композиции из ствола насоса через назальное сопло корпуса. В одном воплощении жидкостное дозирующее устройство представляет собой дозатор общего типа,проиллюстрированный на фиг. 30-40 в WO 2005/044354. Фармацевтические композиции, адаптированные для интраназального введения, в которых носитель представляет собой твердое вещество, включают крупнозернистый порошок, имеющий размер частиц, например, в пределах от 20 до 500 мкм, который вводят быстрой ингаляцией через носовой проход из содержащего порошок контейнера, держа его вплотную к носу. Подходящие композиции, в которых носитель представляет собой жидкость, для введения в виде назального спрея или в виде назальных капель включают водные или масляные растворы соединения формулы (I) или его фармацевтически приемлемой соли. Фармацевтические композиции, адаптированные для трансдермального введения, могут быть представлены в виде отдельных пластырей, предназначенных для того, чтобы они находились в тесном контакте с эпидермисом пациента в течение длительного периода времени. Например, активный ингредиент может доставляться из пластыря в результате ионтофореза, как описано в Pharmaceutical Research, 3(6),318(1986). Фармацевтические композиции, адаптированные для местного введения, могут быть приготовлены в форме мазей, кремов, суспензий, лосьонов, порошков, растворов, паст, гелей, спреев, аэрозолей или масел. Мази, кремы и гели могут быть приготовлены, например, на водной или масляной основе с добавлением подходящего загустителя, и/или гелеобразующего агента, и/или растворителей. Такие основы могут включать, например, воду и/или масло, такое как вазелиновое масло или растительное масло, например арахисовое масло или касторовое масло, или растворитель, такой как полиэтиленгликоль. Загустители и гелеобразующие агенты, которые могут быть использованы в соответствии с природой основы,включают мягкий парафин, стеарат алюминия, цетостеариловый спирт, полиэтиленгликоли, ланолин,пчелиный воск, производные карбоксиполиметилена и целлюлозы, и/или глицерилмоностеарат, и/или неионные эмульгаторы. Лосьоны могут быть приготовлены на водной или масляной основе и будут, как правило, также содержать один или более эмульгаторов, стабилизаторов, диспергирующих агентов, суспендирующих агентов или загустителей. Порошки для наружного применения могут быть приготовлены с использованием любой подходя- 26021056 щей порошковой основы, например талька, лактозы или крахмала. Капли могут быть приготовлены на водной или неводной основе, содержащей также один или более диспергирующих агентов, солюбилизирующих агентов, суспендирующих агентов или консервантов. Препараты для местного применения можно вводить путем одного или более нанесений в сутки на пораженный участок, и на участках кожи преимущественно могут быть использованы окклюзионные повязки. Непрерывная или пролонгированная доставка может быть достигнута с использованием адгезивной резервуарной системы. Для лечения глаза или других наружных тканей, например ротовой полости и кожи, композиции можно наносить в виде мази или крема для местного применения. Для приготовления мази соединение формулы (I) или его фармацевтически приемлемая соль могут быть использованы либо с парафиновой,либо с водосмешиваемой мазевой основой. Альтернативно, соединение формулы (I) или его фармацевтически приемлемая соль могут быть приготовлены в виде крема с основой для крема типа масло-в-воде или вода-в-масле. Фармацевтические композиции, адаптированные для парентерального введения, включают водные и неводные стерильные инъекционные растворы, которые могут содержать антиоксиданты, буферы, бактериостаты и растворенные вещества, которые делают композицию изотоничной с кровью реципиента, и водные и неводные стерильные суспензии, которые могут содержать суспендирующие агенты и загустители. Композиции могут быть представлены в однодозовых или многодозовых контейнерах, например в запаянных ампулах и флаконах, и их можно хранить в высушенном сублимацией (лиофилизированном) состоянии, требующем только добавления стерильного жидкого носителя, например воды для инъекций,непосредственно перед применением. Инъекционные растворы и суспензии для немедленного введения могут быть получены из стерильных порошков, гранул и таблеток. Соединения и фармацевтические композиции по изобретению могут быть использованы в комбинации с одним или более другими терапевтическими агентами, например агентами, выбранными из противовоспалительных агентов, антихолинергических агентов (в частности, антагонист рецепторов М 1/М 2/М 3), агонистов (2-адренорецептора, противоинфекционных агентов, таких как антибиотики или противовирусные средства, или антигистаминных средств, или могут их содержать. Таким образом, в следующем аспекте данного изобретения предложена комбинация, содержащая соединение формулы (I) или его фармацевтически приемлемую соль вместе с одним или более другими терапевтически активными агентами, например агентами, выбранными из противовоспалительного агента, такого как кортикостероид или NSAID (нестероидное противовоспалительное лекарственное средство), антихолинергического агента, агониста 2-адренорецептора, противоинфекционного агента, такого как антибиотик или противовирусное средство, или антигистаминного средства. Одно воплощение изобретения охватывает комбинации, содержащие соединение формулы (I) или его фармацевтически приемлемую соль вместе с агонистом 2-адренорецептора, и/или антихолинергическим средством, и/или ингибитором PDE-4 (фосфодиэстераза-4), и/или антигистаминным средством. В одном из воплощений данное изобретение охватывает способ лечения расстройства, опосредованного ненадлежащей активностью PI3-киназ, включающий введение безопасного и эффективного количества комбинации, содержащей соединение формулы (I) или его фармацевтически приемлемую соль вместе с одним или более терапевтически активными агентами. Некоторые соединения по изобретению могут демонстрировать избирательность в отношенииPI3K по сравнению с другими PI3-киназами. Поэтому в еще одном аспекте данного изобретения предложена комбинация, содержащая соединение формулы (I) или его фармацевтически приемлемую соль,избирательное(ую) в отношении PI3K, вместе с соединением или его фармацевтически приемлемой солью, избирательным(ой) в отношении другой PI3-киназы, например PI3K. Одно из воплощений данного изобретения раскрывает комбинации, содержащие один или два других терапевтических агента. Специалисту в данной области будет ясно, что в тех случаях, когда это целесообразно, другой(ие) терапевтический(ие) ингредиент(ы) может быть использован в форме солей, например солей щелочных металлов, или аминных солей, или солей присоединения кислоты, или в виде пролекарств, или в виде эфиров, например низших алкиловых эфиров, или в виде сольватов, например гидратов, для оптимизации активности, и/или стабильности, и/или физических свойств, таких как растворимость, терапевтического ингредиента. Должно быть ясно также, что в тех случаях, когда это целесообразно, терапевтические ингредиенты могут быть использованы в оптически чистой форме. В одном из воплощений данное изобретение раскрывает комбинацию, содержащую соединение формулы (I) или его фармацевтически приемлемую соль вместе с агонистом 2-адренорецептора. Примеры агонистов 2-адренорецептора включают сальметерол (который может представлять собой рацемат или единственный энантиомер, например R-энантиомер), сальбутамол (который может представлять собой рацемат или единственный энантиомер, например R-энантиомер), формотерол (который может представлять собой рацемат или единственный диастереомер, например R,R-диастереомер),сальмефамол, фенотерол, кармотерол, этантерол, наминтерол, кленбутерол, пирбутерол, флербутерол,- 27021056 репротерол, бамбутерол, индакатерол, тербуталин и их соли, например соль ксинафоат (1-гидрокси-2 нафталинкарбоксилат) сальметерола, сульфатную соль или свободное основание сальбутамола или фумаратную соль формотерола. В одном из воплощений длительно действующие агонисты 2 адренорецептора, например соединения, которые обеспечивают эффективную бронходилатацию в течение примерно 12 ч или дольше, являются предпочтительными. Другие агонисты 2-адренорецептора включают те из них, которые описаны в WO 02/066422, WO 02/070490, WO 02/076933, WO 03/024439, WO 03/072539, WO 03/091204, WO 04/016578, WO 2004/022547, WO 2004/037807, WO 2004/037773, WO 2004/037768, WO 2004/039762, WO 2004/039766,WO 01/42193 и WO 03/042160. Примеры агонистов 2-адренорецептора включают 3-(4-[6-2R)-2-гидрокси-2-[4-гидрокси-3-(гидроксиметил)фенил]этиламино)гексил]оксибутил)бензолсульфонамид; 3-(3-[7-2R)-2-гидрокси-2-[4-гидрокси-3-гидроксиметил)фенил]этил-амино)гептил]оксипропил)бензолсульфонамид; 4-(1R)-2-[(6-2-[(2,6-дихлорбензил)окси]этоксигексил)амино]-1-гидроксиэтил-2-(гидроксиметил)фенол; 4-(1R)-2-[(6-4-[3-(циклопентилсульфонил)фенил]бутоксигексил)амино]-1-гидроксиэтил-2(гидроксиметил)фенол;N-2-2-[4-(3-фенил-4-метоксифенил)аминофенил]этил-2-гидрокси-2-(8-гидрокси-2(1 Н)-хинолинон-5-ил)этиламин и 5-[(R)-2-(2-4-[4-(2-амино-2-метилпропокси)фениламино]фенилэтиламино)-1-гидроксиэтил]-8 гидрокси-1 Н-хинолин-2-он. Агонист 2-адренорецептора может быть в форме соли, образованной с фармацевтически приемлемой кислотой, выбранной из серной, соляной, фумаровой, гидроксинафтойной (например, 1- или 3 гидрокси-2-нафтойной), коричной, замещенной коричной, трифенилуксусной, сульфаминовой, сульфаниловой, нафталинакриловой, бензойной, 4-метоксибензойной, 2- или 4-гидроксибензойной, 4 хлорбензойной и 4-фенилбензойной кислот. Подходящие противовоспалительные агенты включают кортикостероиды. Подходящими кортикостероидами, которые могут быть использованы в комбинации с соединением формулы (I) или его фармацевтически приемлемой солью, являются пероральные и ингалируемые кортикостероиды и их пролекарства, которые обладают противовоспалительной активностью. Примеры включают метилпреднизолон, преднизолон, дексаметазон, флутиказона пропионат, S-фторметиловый эфир 6,9-дифтор-11 гидрокси-16-метил-17-[(4-метил-1,3-тиазол-5-карбонил)окси]-3-оксо-андроста-1,4-диен-17-карботиокислоты, S-фторметиловый эфир 6,9-дифтор-17-[(2-фуранилкарбонил)окси]-11-гидрокси-16 метил-3-оксо-андроста-1,4-диен-17-карботиокислоты(флутиказона фуроат),S-(2-оксотетрагидрофуран-3S-иловый) эфир 6,9-дифтор-11-гидрокси-16-метил-3-оксо-17-пропионилоксиандроста-1,4-диен-17-карботиокислоты, S-цианометиловый эфир 6,9-дифтор-11-гидрокси-16 метил-3-оксо-17-(2,2,3,3-тетраметилциклопропил-карбонил)окси-андроста-1,4-диен-17-карботиокислоты и S-фторметиловый эфир 6,9-дифтор-11-гидрокси-16-метил-17-(1-метилциклопропилкарбонил)окси-3-оксо-андроста-1,4-диен-17-карботиокислоты, эфиры бекло-метазона (например, 17 пропионатный эфир или 17,21-дипропионатный эфир), будесонид, флунисолид, эфиры мометазона (например, мометазона фуроат), триамцинолона ацетонид, рофлепонид, циклесонид (16,17-(R)циклогексилметилен]-бис-(окси)]-11,21-дигидрокси-прегна-1,4-диен-3,20-дион), бутиксокорта пропионат, RPR-106541 и ST-126. Предпочтительные кортикостероиды включают флутиказона пропионат,S-фторметиловый эфир 6,9-дифтор-11-гидрокси-16-метил-17-[(4-метил-1,3-тиазол-5-карбонил)окси]-3-оксо-андроста-1,4-диен-17-карботиокислоты, S-фторметиловый эфир 6,9-дифтор-17[(2-фуранилкарбонил)окси]-11-гидрокси-16-метил-3-оксо-андроста-1,4-диен-17-карботиокислоты, Sцианометиловый эфир 6,9-дифтор-11-гидрокси-16-метил-3-оксо-17-(2,2,3,3-тетраметилциклопропилкарбонил)окси-андроста-1,4-диен-17-карботиокислоты и S-фторметиловый эфир 6,9-дифтор 11-гидрокси-16-метил-17-(1-метилциклопропилкарбонил)окси-3-оксо-андросга-1,4-диен-17-карботиокислоты. В одном из воплощений кортикостероид представляет собой S-фторметиловый эфир 6,9 дифтор-17-[(2-фуранилкарбонил)окси]-11-гидрокси-16-метил-3-оксо-андроста-1,4-диен-17-карботиокислоты. Примеры кортикостероидов могут включать кортикостероиды, которые описаны в WO 2002/088167, WO 2002/100879, WO 2002/12265, WO 2002/12266, WO 2005/005451, WO 2005/005452, WO 2006/072599 и WO 2006/072600. Нестероидные соединения с агонизмом глюкокортикоидов, которые проявляют избирательность в отношении трансрепрессии по сравнению с трансактивацией и которые могут быть полезны в комбини- 28021056 рованной терапии, включают соединения, охваченные в следующих патентных заявках: WO 03/082827,WO 98/54159, WO 04/005229, WO 04/009017, WO 04/018429, WO 03/104195, WO 03/082787, WO 03/082280, WO 03/059899, WO 03/101932, WO 02/02565, WO 01/16128, WO 00/66590, WO 03/086294, WO 04/026248, WO 03/061651 и WO 03/08277. Дополнительные нестероидные соединения охвачены в WO 2006/000401, WO 2006/000398 и WO 2006/015870. Примеры противовоспалительных агентов включают нестероидные противовоспалительные лекарственные средства (NSAID). Примеры NSAID включают кромгликат натрия, недокромил-натрий, ингибиторы фосфодиэстеразы(PDE) (например, теофиллин, ингибиторы PDE4 или смешанные ингибиторы PDE3/PDE4), антагонист лейкотриенов, ингибиторы синтеза лейкотриенов (например, монтелукаст), ингибиторы iNOS, ингибиторы триптазы и эластазы, антагонисты -2 интегрина и агонисты или антагонисты аденозиновых рецепторов (например, агонисты аденозина-2 а), антагонисты цитокинов (например, антагонисты хемокинов, такие как антагонист CCR3), или ингибиторы синтеза цитокинов, или ингибиторы 5-липоксигеназы. iNOS(ингибитор индуцибельной синтазы оксида азота) предпочтителен для перорального введения. Примеры ингибиторов iNOS включают ингибиторы iNOS, которые описаны в WO 93/13055, WO 98/30537, WO 02/50021, WO 95/34534 и WO 99/62875. Примеры ингибиторов CCR3 включают ингибиторы CCR3, которые описаны в WO 02/26722. В одном из воплощений данного изобретения раскрыто применение соединений формулы (I) в комбинации с ингибитором фосфодиэстеразы 4 (PDE4), особенно в случае композиции, адаптированной для ингаляции. PDE4-специфичный ингибитор, полезный в этом аспекте изобретения, может представлять собой любое соединение, о котором известно, что оно ингибирует фермент PDE4, или которое раскрыто как соединение, которое действует как ингибитор PDE4, и которое является ингибитором только PDE4, а не соединением, которое ингибирует другие члены семейства PDE, такие как PDE3 и PDE5, а такжеPDE4. Соединения включают цис-4-циано-4-(3-циклопентилокси-4-метоксифенил)циклогексан-1 карбоновую кислоту, 2-карбометокси-4-циано-4-(3-циклопропилметокси-4-дифторметоксифенил)циклогексан-1-он и цис-[4-циано-4-(3-циклопропилметокси-4-дифторметоксифенил)циклогексан-1-ол], а также цис-4-циано-4-[3-(циклопентилокси)-4-метоксифенил]циклогексан-1-карбоновую кислоту (также известную как циломиласт) и его соли, эфиры, пролекарства или физические формы, которые описаны в патенте США 5552438, выданном 03 сентября 1996 г. (полное содержание этого патента и соединения, которые в нем раскрыты, включены в данное описание посредством ссылки). Другие соединения включают AWD-12-281 от Elbion (Hofgen, N. et al. 15th EFMC Int. Symp. Med.Chem. (Sept 6-10, Edinburgh) 1998, Abst P.98; CAS ссылочный 247584020-9); производное 9 бензиладенина под наименованием NCS-613 (INSERM); D-4418 от Chiroscience и Schering-Plough; бензодиазепиновый ингибитор PDE4, идентифицированный как CI-1018 (PD-168787) и принадлежащий компании Pfizer; производное бензодиоксола, описанное Kyowa Hakko в WO 99/16766; K-34 от KyowaHakko; V-11294A от Napp (Landells, L.J. et al., Eur. Resp. J. [Annu. Cong. Eur. Resp. Soc. (Sept 19-23, Geneva) 1998] 1998, 12 (Suppl. 28): Abst P2393); рофлумиласт (CAS ссылочный 162401-32-3) и фталазинон (WO 99/47505, описание которой включено в данное описание посредством ссылки) от Byk-Gulden; пумафентрин,(-)-пара-[(4aR,10bS)-9-этокси-1,2,3,4,4a,10b-гексагидро-8-метокси-2-метилбензо[с][1,6]нафтиридин-6-ил]-N,N-диизопропилбензамид, являющийся ингибитором PDE3/PDE4, который получен и опубликован Byk-Gulden, в настоящее время Altana; арофиллин, разрабатываемый AlmirallProdesfarma; VM554/UM565 от Vernalis или Т-440 (Tanabe Seiyaku; Fuji, K. et al. J. Pharmacol. Exp. Then,1998, 284(1): 162) и Т 2585. Дополнительные соединения раскрыты в публикации международной патентной заявки WO 04/024728 (Glaxo Group Ltd), WO 04/056823 (Glaxo Group Ltd) и WO 04/103998 (Glaxo Group Ltd) (например, соединение примера 399 или соединение примера 544, раскрытые в этой заявке). Дополнительные соединения также раскрыты в WO 2005/058892, WO 2005/090348, WO 2005/090353 и WO 2005/090354, все от имени Glaxo Group Limited. Примерами антихолинергических агентов являются те соединения, которые действуют как антагонисты мускариновых рецепторов, в частности те соединения, которые являются антагонистами рецепторов M1 или М 3, двойственными антагонистами рецепторов M1/М 3 или М 2/М 3 или пан-антагонистами рецепторов М 1/М 2/М 3. Иллюстративные соединения для введения ингаляцией включают ипратропий (например, в форме бромида, CAS 22254-24-6, продаваемый под наименованием Atrovent), окситропий (например, в форме бромида, CAS 30286-75-0) и тиотропий (например, в форме бромида, CAS 136310-93-5,продаваемый под наименованием Spiriva). Интерес также представляют реватропат (например, в форме гидробромида, CAS 262586-79-8) и LAS-34273, который раскрыт в WO 01/04118. Иллюстративные соединения для перорального введения включают пирензепин (CAS 28797-61-7), дарифенацин (CAS 133099-04-4 или CAS 133099-07-7 для гидробромида, продаваемый под наименованием Enablex), оксибутинин (CAS 5633-20-5, продаваемый под наименованием Ditropan), теродилин (CAS 15793-40-5), толтеродин (CAS 124937-51-5, или CAS 124937-52-6 для тартрата, продаваемый под наименованием Detrol),отилоний (например, в форме бромида, CAS 26095-59-0, продаваемый под наименованием Spasmomen),- 29
МПК / Метки
МПК: A61P 31/12, A61P 35/00, A61P 37/00, A61P 11/00, C07D 413/14, A61K 31/422, A61K 31/4439
Метки: композиция, ненадлежащей, pi3-киназ, опосредованных, активностью, расстройств, оксазолзамещенные, качестве, индазолы, лечении, ингибиторов, применение, фармацевтическая, содержащая
Код ссылки
<a href="https://eas.patents.su/30-21056-oksazolzameshhennye-indazoly-v-kachestve-ingibitorov-pi3-kinaz-soderzhashhaya-ih-farmacevticheskaya-kompoziciya-i-ih-primenenie-v-lechenii-rasstrojjstv-oposredovannyh-nenadlezhashh.html" rel="bookmark" title="База патентов Евразийского Союза">Оксазолзамещенные индазолы в качестве ингибиторов pi3-киназ, содержащая их фармацевтическая композиция и их применение в лечении расстройств, опосредованных ненадлежащей активностью pi3-киназ</a>
Предыдущий патент: Способ увеличения скорости всасывания триптанов и способ лечения осложнений или симптомов мигрени
Следующий патент: Гетероциклические сульфонамиды, их применения и фармацевтические композиции
Случайный патент: 4-((феноксиалкил)тио)феноксиуксусные кислоты и аналоги












