Новые гетероциклические соединения в качестве положительных аллостерических модуляторов метаботропных глутаматных рецепторов
Номер патента: 14904
Опубликовано: 28.02.2011
Авторы: Гаглиарди Стефания, Фарина Марко, Рошер Джен-Филиппе, Ле Поул Эммануэль, Паломби Джиованни
Формула / Реферат
1. Соединение формулы I-B
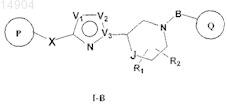
где V1и V2 представляют собой независимо атом кислорода или азота;
V3 представляет собой атом углерода или азота;
R1 и R2независимо друг от друга представляют собой водород;
Р представляет собой С6арил, возможно содержащий в качестве заместителя галоген;
Q представляет собой арильную или гетероарильную группу формулы

где R3, R4, R5, R6 и R7независимо друг от друга представляют собой водород, галоген, -(С1-С6)алкил или
-О(С1-С6)алкил;
R3', R4', R5' и R6' представляют собой независимо водород или галоген;
R3" и R4" представляют собой независимо водород;
R3'" и R4'" представляют собой независимо водород или -(С1-С6)алкил;
D и Н в Q независимо друг от друга представляют собой -С-;
Е и F в Q представляют собой независимо -С- или -N-;
G в Q представляет собой -NH- или -О-;
В представляет собой -С(=О)-;
X представляет собой -(С1-С6)алкил-, -(С1-С6)алкил(ОН), -(С1-С6)алкил(NH)-, -С=О-, -NH-, -О- или -S-;
J представляет собой -С-;
или фармацевтически приемлемая соль, гидрат, сольват или N-оксид указанного соединения.
2. Соединение по п.1, отличающееся тем, что
Р представляет собой незамещенный фенил или фенил, содержащий в качестве заместителя атом фтора;
Q представляет собой незамещенный фенил или фенил, содержащий в качестве заместителей один или два атома хлора или фтора, или Q представляет собой метилфенил или метоксифенил;
R3'" и R4'" представляют собой независимо водород или метил;
или фармацевтически приемлемая соль, гидрат, сольват или N-оксид указанного соединения.
3. Соединение по п.1, которое имеет формулу I-D

где Р представляет собой С6арил, возможно содержащий в качестве заместителя галоген;
Q представляет собой арильную или гетероарильную группу формулы
![]()
где R3, R4, R5, R6 и R7независимо друг от друга представляют собой водород, галоген, -(С1-С6)алкил или
-О(С1-С6)алкил;
R3', R4', R5' и R6' представляют собой независимо водород или галоген;
R3" и R4" представляют собой независимо водород;
R3'" и R4'" представляют собой независимо водород или -(С1-С6)алкил;
D и Н в Q независимо друг от друга представляют собой -С-;
Е и F в Q представляют собой независимо -С- или -N-;
G в Q представляет собой -NH- или -О-;
В представляет собой -С(=О)-;
X представляет собой -(С1-С6)алкил-, -(С1-C6)алкил(ОН), -(С1-С6)алкил(NH)-, -С=О-, -NH-, -О- или -S-;
J представляет собой -С-;
или фармацевтически приемлемая соль, гидрат, сольват или N-оксид указанного соединения.
4. Соединение по п.1, которое имеет формулу II-В
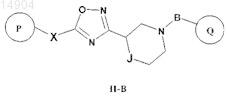
где Р представляет собой С6арил, возможно содержащий в качестве заместителя галоген;
Q представляет собой арильную или гетероарильную группу формулы
![]()
где R3, R4, R5, R6 и R7независимо друг от друга представляют собой водород, галоген, -(С1-С6)алкил или
-О(С1-С6)алкил;
R3', R4', R5' и R6' представляют собой независимо водород или галоген;
R3" и R4" представляют собой независимо водород;
R3'" и R4'" представляют собой независимо водород или -(С1-С6)алкил;
D и Н в Q независимо друг от друга представляют собой -С-;
Е и F в Q представляют собой независимо -С- или -N-;
G в Q представляет собой -NH- или -О-;
В представляет собой -С(=О)-;
X представляет собой -(С1-С6)алкил-, -(С1-С6)алкил(ОН), -(С1-С6)алкил(NH)-, -С=О-, -NH-, -О- или -S-;
J представляет собой -С-;
или фармацевтически приемлемая соль, гидрат, сольват или N-оксид указанного соединения.
5. Соединение по п.1, которое имеет формулу III-A
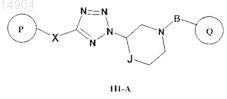
где Р представляет собой С6арил, возможно содержащий в качестве заместителя галоген;
Q представляет собой арильную или гетероарильную группу формулы
![]()
где R3, R4, R5, R6 и R7независимо друг от друга представляют собой водород, галоген, -(С1-С6)алкил или
-О(С1-С6)алкил;
R3', R4', R5' и R6' представляют собой независимо водород или галоген;
R3" и R4" представляют собой независимо водород;
R3'" и R4'" представляют собой независимо водород или -(С1-С6)алкил;
D и Н в Q независимо друг от друга представляют собой -С-;
Е и F в Q представляют собой независимо -С- или -N-;
G в Q представляет собой -NH- или -О-;
В представляет собой -С(=О)-;
X представляет собой -(С1-С6)алкил-, -(С1-С6)алкил(ОН), -(С1-С6)алкил(NH)-, -С=О-, -NH-, -О- или -S-;
J представляет собой -С-;
или фармацевтически приемлемая соль, гидрат, сольват или N-оксид указанного соединения.
6. Соединение по любому из пп.1-5, которое может существовать в виде оптических изомеров, отличающееся тем, что указанное соединение представляет собой либо рацемическую смесь, либо индивидуальный оптический изомер.
7. Соединение по любому из пп.1-5, отличающееся тем, что указанное соединение выбирают из
{(S)-3-[3-(4-фторбензил)-[1,2,4]оксадиазол-5-ил]-пиперидин-1-ил}-(4-фторфенил)метанона,
(3,4-дифторфенил)-{(S)-3-[3-(4-фторбензил)-[1,2,4]оксадиазол-5-ил]пиперидин-1-ил}метанона,
(3,4-дифторфенил)-{(S)-3-[5-(4-фторбензил)-[1,2,4]оксадиазол-3-ил]пиперидин-1-ил}метанона,
{(S)-3-[5-(4-фторбензил)-[1,2,4]оксадиазол-3-ил]пиперидин-1-ил}-(4-фторфенил)метанона,
(4-фторфенил)-{(S)-3-[5-((S)-1-фенилэтил)-[1,2,4]оксадиазол-3-ил]пиперидин-1-ил}метанона,
(4-фторфенил)-{(S)-3-[5-((R)-1-фенилэтил)-[1,2,4]оксадиазол-3-ил]пиперидин-1-ил}метанона,
[(S)-3-(5-бензил-[1,2,4]оксадиазол-3-ил)пиперидин-1-ил]-(4-фторфенил)метанона,
(4-фторфенил)-{(S)-3-[5-((S)-гидроксифенилметил)-[1,2,4]оксадиазол-3-ил]пиперидин-1-ил}метанона,
(4-фторфенил)-{(S)-3-[5-((R)-гидроксифенилметил)-[1,2,4]оксадиазол-3-ил]пиперидин-1-ил}метанона,
(4-фторфенил)-[(S)-3-(5-фенилэтил-[1,2,4]оксадиазол-3-ил)пиперидин-1-ил]метанона,
{3-[(S)-1-(4-фторбензоил)пиперидин-3-ил]-[1,2,4]оксадиазол-5-ил}фенилметанона,
(4-фторфенил)-[(S)-3-(5-фениламино-[1,2,4]оксадиазол-3-ил)пиперидин-1-ил]метанона,
{(S)-3-[5-(4-фторбензиламино)-[1,2,4]оксадиазол-3-ил]пиперидин-1-ил}-(4-фторфенил)метанона,
[(S)-3-(5-бензилтетразол-2-ил)пиперидин-1-ил]-(4-фторфенил)метанона,
{3-[3-(4-фторфенокси)-[1,2,4]оксадиазол-5-ил]пиперидин-1-ил}-(4-фторфенил)метанона,
(4-фторфенил)-[3-(3-фенокси-[1,2,4]оксадиазол-5-ил)пиперидин-1-ил]метанона,
(6-фторпиридин-3-ил)-[(S)-3-(3-фенокси-[1,2,4]оксадиазол-5-ил)пиперидин-1-ил]метанона,
{(S)-3-[3-(2-фторфенокси)-[1,2,4]оксадиазол-5-ил]пиперидин-1-ил}-(6-фторпиридин-3-ил)метанона,
{(S)-3-[3-(3-фторфенокси)-[1,2,4]оксадиазол-5-ил]пиперидин-1-ил}-(6-фторпиридин-3-ил)метанона,
(4-фторфенил)-[(S)-3-(3-фенилсульфанил-[1,2,4]оксадиазол-5-ил)пиперидин-1-ил]метанона,
{3-[3-(3-фторфенокси)-[1,2,4]оксадиазол-5-ил]пиперидин-1-ил}-(4-фторфенил)метанона,
(4-метилфенил)-[(S)-3-(3-фенокси-[1,2,4]оксадиазол-5-ил)пиперидин-1-ил]метанона,
(2-метоксифенил)-[(S)-3-(3-фенокси-[1,2,4]оксадиазол-5-ил)пиперидин-1-ил]метанона,
[(S)-3-(3-фенокси-[1,2,4]оксадиазол-5-ил)пиперидин-1-ил]пиридин-2-илметанона,
(2-фторпиридин-4-ил)-[(S)-3-(3-фенокси-[1,2,4]оксадиазол-5-ил)пиперидин-1-ил]метанона,
(3Н-имидазол-4-ил-[(S)-3-(3-фенокси-[1,2,4]оксадиазол-5-ил)пиперидин-1-ил]метанона,
(3,5-дифторфенил)-[(S)-3-(3-фенокси-[1,2,4]оксадиазол-5-ил)пиперидин-1-ил]метанона,
(5-метилизоксазол-4-ил)-[(S)-3-(3-фенокси-[1,2,4]оксадиазол-5-ил)пиперидин-1-ил]метанона,
[(S)-3-(3-фенокси-[1,2,4]оксадиазол-5-ил)пиперидин-1-ил]тиазол-5-илметанона,
[(S)-3-(3-фенокси-[1,2,4]оксадиазол-5-ил)пиперидин-1-ил]фенилметанона,
(4-хлорфенил)-[(S)-3-(3-фенокси-[1,2,4]оксадиазол-5-ил)пиперидин-1-ил]метанона,
(4-метоксифенил)-[(S)-3-(3-фенокси-[1,2,4]оксадиазол-5-ил)пиперидин-1-ил]метанона,
(3,4-дихлорфенил)-[(S)-3-(3-фенокси-[1,2,4]оксадиазол-5-ил)пиперидин-1-ил]метанона,
(3-метоксифенил)-[(S)-3-(3-фенокси-[1,2,4]оксадиазол-5-ил)пиперидин-1-ил]метанона,
(2-метилфенил)-[(S)-3-(3-фенокси-[1,2,4]оксадиазол-5-ил)пиперидин-1-ил]метанона,
(2-фторфенил)-[(S)-3-(3-фенокси-[1,2,4]оксадиазол-5-ил)пиперидин-1-ил]метанона,
(3-фторфенил)-[(S)-3-(3-фенокси-[1,2,4]оксадиазол-5-ил)пиперидин-1-ил]метанона,
[(S)-3-(3-фенокси-[1,2,4]оксадиазол-5-ил)пиперидин-1-ил]пиридин-3-илметанона,
[(S)-3-(3-фенокси-[1,2,4]оксадиазол-5-ил)пиперидин-1-ил]пиридин-4-илметанона,
(3,5-диметилизоксазол-4-ил)-[(S)-3-(3-фенокси-[1,2,4]оксадиазол-5-ил)пиперидин-1-ил]метанона,
(4-фторфенил)-[(S)-3-(3-фенокси-[1,2,4]оксадиазол-5-ил)пиперидин-1-ил]метанона,
{(S)-3-[3-(3-фторфенокси)-[1,2,4]оксадиазол-5-ил]пиперидин-1-ил}-(4-фторфенил)метанона,
{(S)-3-[3-(3-фторфенокси)-[1,2,4]оксадиазол-5-ил]пиперидин-1-ил}-п-толилметанона,
{(S)-3-[3-(3-фторфенокси)-[1,2,4]оксадиазол-5-ил]пиперидин-1-ил}-(2-метоксифенил)метанона,
{(S)-3-[3-(3-фторфенокси)-[1,2,4]оксадиазол-5-ил]пиперидин-1-ил}-(2-фторпиридин-4-ил)метанона,
{(S)-3-[3-(3-фторфенокси)-[1,2,4]оксадиазол-5-ил]пиперидин-1-ил}-(3Н-имидазол-4-ил)метанона,
(3,5-дифторфенил)-{(S)-3-[3-(3-фторфенокси)-[1,2,4]оксадиазол-5-ил]пиперидин-1-ил}метанона,
{(S)-3-[3-(3-фторфенокси)-[1,2,4]оксадиазол-5-ил]пиперидин-1-ил}-(5-метилизоксазол-4-ил)метанона,
{(S)-3-[3-(3-фторфенокси)-[1,2,4]оксадиазол-5-ил]пиперидин-1-ил}тиазол-5-илметанона,
{(S)-3-[3-(3-фторфенокси)-[1,2,4]оксадиазол-5-ил]пиперидин-1-ил}-(6-фторпиридин-3-ил)метанона,
{(S)-3-[3-(3-фторфенокси)-[1,2,4]оксадиазол-5-ил]пиперидин-1-ил}пиридин-2-илметанона,
{(S)-3-[3-(3-фторфенокси)-[1,2,4]оксадиазол-5-ил]пиперидин-1-ил}фенилметанона,
(4-хлорфенил)-{(S)-3-[3-(3-фторфенокси)-[1,2,4]оксадиазол-5-ил]пиперидин-1-ил}метанона,
{(S)-3-[3-(3-фторфенокси)-[1,2,4]оксадиазол-5-ил]пиперидин-1-ил}-(4-метоксифенил)метанона,
(3,4-дихлорфенил)-{(S)-3-[3-(3-фторфенокси)-[1,2,4]оксадиазол-5-ил]-пиперидин-1-ил}метанона,
{(S)-3-[3-(3-фторфенокси)-[1,2,4]оксадиазол-5-ил]пиперидин-1-ил}-(3-метоксифенил)метанона,
{(S)-3-[3-(3-фторфенокси)-[1,2,4]оксадиазол-5-ил]пиперидин-1-ил}-о-толилметанона,
{(S)-3-[3-(3-фторфенокси)-[1,2,4]оксадиазол-5-ил]пиперидин-1-ил}-(2-фторфенил)метанона,
{(S)-3-[3-(3-фторфенокси)-[1,2,4]оксадиазол-5-ил]пиперидин-1-ил}-(3-фторфенил)метанона,
{(S)-3-[3-(3-фторфенокси)-[1,2,4]оксадиазол-5-ил]пиперидин-1-ил}пиридин-3-илметанона,
{(S)-3-[3-(3-фторфенокси)-[1,2,4]оксадиазол-5-ил]пиперидин-1-ил}пиридин-4-илметанона,
{(S)-3-[3-(3-фторфенокси)-[1,2,4]оксадиазол-5-ил]пиперидин-1-ил}-(3,5-диметилизоксазол-4-ил)метанона,
и фармацевтически приемлемые соли, гидраты, сольваты или N-оксиды указанных соединений.
8. Соединение формулы I-B
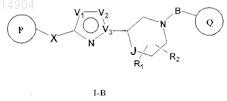
где V1и V2 представляют собой независимо атом кислорода или азота;
V3 представляет собой атом углерода или азота;
R1 и R2независимо друг от друга представляют собой водород;
Р представляет собой C6 арил, возможно содержащий в качестве заместителя галоген;
Q представляет собой арильную или гетероарильную группу формулы
![]()
где R3, R4, R5, R6 и R7независимо друг от друга представляют собой водород, галоген, -(С1-С6)алкил или
-О(С1-С6)алкил;
R3', R4', R5' и R6' представляют собой независимо водород или галоген;
R3" и R4" представляют собой независимо водород;
R3'" и R4'" представляют собой независимо водород или -(С1-С6)алкил;
D и Н в Q независимо друг от друга представляют собой -С-;
Е и F в Q представляют собой независимо -С- или -N-;
G в Q представляет собой -NH- или -О-;
В представляет собой -С(=О)-;
X представляет собой -(С1-С6)алкил-, -(С1-С6)алкил(ОН), -(С1-C6)алкил(NH)-, -С=О-, -NH-, -О- или -S-;
J представляет собой -С-;
или фармацевтически приемлемая соль, гидрат, сольват или N-оксид указанного соединения для лечения или предотвращения состояния у млекопитающего, включая человека, причем лечению или предотвращению указанного состояния способствует или на него оказывает влияние нейромодуляторное действие положительного аллостерического модулятора mGluR5, выступающего в роли усиливающего агента.
9. Соединение по п.8 для лечения или предотвращения расстройства центральной нервной системы, выбранного из группы, включающей тревожные расстройства: агорафобию, генерализованное тревожное расстройство (ГТР), обсессивно-компульсивное расстройство (ОКР), паническое расстройство, посттравматическое стрессовое расстройство (ПТСР), социофобию, другие фобии и тревожное расстройство, связанное с употреблением психоактивных веществ.
10. Соединение по п.8 для лечения или предотвращения расстройства центральной нервной системы, выбранного из группы, включающей расстройство у детей, такое как синдром дефицита внимания с гиперактивностью.
11. Соединение по п.8 для лечения или предотвращения расстройства центральной нервной системы, выбранного из группы, включающей расстройства пищевого поведения: нервную анорексию и нервную булимию.
12. Соединение по п.8 для лечения или предотвращения расстройства центральной нервной системы, выбранного из группы, включающей расстройства настроения: биполярные расстройства (I и II типа), циклотимическое расстройство, депрессию, дистимическое расстройство, большое депрессивное расстройство и расстройство настроения, связанное с употреблением психоактивных препаратов.
13. Соединение по п.8 для лечения или предотвращения расстройства центральной нервной системы, выбранного из группы, включающей психотические расстройства: шизофрению, бредовое расстройство, шизоаффективное расстройство, шизофреноформное расстройство и психотическое расстройство, связанное с употреблением психоактивных веществ.
14. Соединение по п.8 для лечения или предотвращения расстройства центральной нервной системы, выбранного из группы, включающей когнитивные расстройства: делирий, персистирующий делирий, связанный с употреблением психоактивных веществ, деменцию, деменцию, вызванную ВИЧ, деменцию, вызванную хореей Гентингтона, деменцию, вызванную болезнью Паркинсона, деменцию типа Альцгеймера, персистирующую деменцию, связанную с употреблением психоактивных веществ, и умеренное когнитивное расстройство.
15. Соединение по п.8 для лечения или предотвращения расстройства центральной нервной системы, выбранного из группы, включающей расстройства личности: обсессивно-компульсивное расстройство личности, шизоидное расстройство личности и шизотипальное расстройство личности.
16. Соединение по п.8 для лечения или предотвращения расстройства центральной нервной системы, выбранного из группы, включающей расстройства, связанные с употреблением психоактивных веществ: злоупотребление алкоголем, алкогольную зависимость, алкогольную абстиненцию, синдром отмены алкоголя с делирием, алкогольное психотическое расстройство, амфетаминовую зависимость, амфетаминовую абстиненцию, кокаиновую зависимость, кокаиновую абстиненцию, никотиновую зависимость, никотиновую абстиненцию, опиоидную зависимость и опиоидную абстиненцию.
17. Соединение по п.8 для лечения или предотвращения воспалительного заболевания центральной нервной системы, выбранного из форм рассеянного склероза, таких как доброкачественный рассеянный склероз, ремитирующий рассеянный склероз, вторично-прогрессирующий рассеянный склероз, первично-прогрессирующий рассеянный склероз и рецидивирующий рассеянный склероз.
18. Фармацевтическая композиция, которая содержит терапевтически эффективное количество соединения по любому из пп.1-17 и фармацевтически приемлемый носитель и/или наполнитель.
19. Способ лечения или предотвращения у млекопитающего, включая человека, состояния, на лечение или предотвращение которого оказывает действие или лечению или предотвращению которого способствует нейромодуляторное действие аллостерического модулятора mGluR5 (энхансера), который включает введение указанному млекопитающему, нуждающемуся в указанном лечении или предотвращении, эффективного количества соединения по любому из пп.1-17 и/или композиции по п.18.
20. Способ лечения или предотвращения у млекопитающего, включая человека, состояния, на лечение или предотвращение которого оказывает действие или лечению или предотвращению которого способствует нейромодуляторное действие положительного аллостерического модулятора mGluR5 (энхансера), который включает введение указанному млекопитающему, нуждающемуся в указанном лечении или предотвращении, эффективного количества соединения по любому из пп.1-17 и/или композиции по п.18.
21. Способ лечения или предотвращения расстройства центральной нервной системы, выбранного из группы, включающей тревожные расстройства: агорафобию, генерализованное тревожное расстройство (ГТР), обсессивно-компульсивное расстройство (ОКР), паническое расстройство, посттравматическое стрессовое расстройство (ПТСР), социофобию, другие фобии, тревожное расстройство, связанное с употреблением психоактивных веществ, включающий введение эффективного количества соединения по любому из пп.1-9 и/или композиции по п.18.
22. Способ лечения или предотвращения расстройства центральной нервной системы, выбранного из группы, включающей расстройства у детей: синдром дефицита внимания с гиперактивностью, включающий введение эффективного количества соединения по любому из пп.1-8 или 10 и/или композиции по п.18.
23. Способ лечения или предотвращения расстройства центральной нервной системы, выбранного из группы, включающей расстройства пищевого поведения: нервную анорексию, нервную булимию, включающий введение эффективного количества соединения по любому из пп.1-8 или 11 и/или композиции по п.18.
24. Способ лечения или предотвращения расстройства центральной нервной системы, выбранного из группы, включающей расстройства настроения: биполярные расстройства (I и II типа), циклотимическое расстройство, депрессию, дистимическое расстройство, большое депрессивное расстройство, расстройство настроения, связанное с употреблением психоактивных препаратов, включающий введение эффективного количества соединения по любому из пп.1-8 или 12 и/или композиции по п.18.
25. Способ лечения или предотвращения расстройства центральной нервной системы, выбранного из группы, включающей психотические расстройства: шизофрению, бредовое расстройство, шизоаффективное расстройство, шизофреноформное расстройство, психотическое расстройство, связанное с употреблением психоактивных веществ, включающий введение эффективного количества соединения по любому из пп.1-8 или 13 и/или композиции по п.18.
26. Способ лечения или предотвращения расстройства центральной нервной системы, выбранного из группы, включающей когнитивные расстройства: делирий, персистирующий делирий, связанный с употреблением психоактивных веществ, деменцию, деменцию, вызванную ВИЧ, деменцию, вызванную хореей Гентингтона, деменцию, вызванную болезнью Паркинсона, деменцию типа Альцгеймера, персистирующую деменцию, связанную с употреблением психоактивных веществ, умеренные когнитивные нарушения, включающий введение эффективного количества соединения по любому из пп.1-8 или 14 и/или композиции по п.18.
27. Способ лечения или предотвращения расстройства центральной нервной системы, выбранного из группы, включающей расстройства личности: обсессивно-компульсивное расстройство личности, шизоидное расстройство личности, шизотипальное расстройство личности, включающий введение эффективного количества соединения по любому из пп.1-8 или 15 и/или композиции по п.18.
28. Способ лечения или предотвращения расстройства центральной нервной системы, выбранного из группы, включающей расстройства, связанные с употреблением психоактивных веществ: злоупотребление алкоголем, алкогольную зависимость, алкогольную абстиненцию, синдром отмены алкоголя с делирием, алкогольное психотическое расстройство, амфетаминовую зависимость, амфетаминовую абстиненцию, кокаиновую зависимость, кокаиновую абстиненцию, никотиновую зависимость, никотиновую абстиненцию, опиоидную зависимость, опиоидную абстиненцию, включающий введение эффективного количества соединения по любому из пп.1-8 или 16 и/или композиции по п.18.
29. Способ лечения или предотвращения воспалительного заболевания центральной нервной системы, выбранного из форм рассеянного склероза, таких как доброкачественный рассеянный склероз, ремитирующий рассеянный склероз, вторично-прогрессирующий рассеянный склероз, первично-прогрессирующий рассеянный склероз, рецидивирующий рассеянный склероз, включающий введение эффективного количества соединения по любому из пп.1-8 или 17 и/или композиции по п.18.
30. Применение соединения по любому из пп.1-17 для приготовления лекарства для лечения или предотвращения заболевания или состояния, указанного в любом из пп.21-29.
31. Применение композиции по п.18 для приготовления лекарства для лечения или предотвращения заболевания или состояния, указанного в любом из пп.21-29.
32. Применение соединения по любому из пп.1-17 для приготовления метки для получения изображений метаботропных глутаматных рецепторов.
Текст
НОВЫЕ ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ В КАЧЕСТВЕ ПОЛОЖИТЕЛЬНЫХ АЛЛОСТЕРИЧЕСКИХ МОДУЛЯТОРОВ МЕТАБОТРОПНЫХ ГЛУТАМАТНЫХ РЕЦЕПТОРОВ Настоящее изобретение относится к новым соединениям, которые представляют собой гетероциклические производные формулы I, в которой А, В, Р, X, Y, Q, W, R1 и R2 определены в описании. Соединения согласно настоящему изобретению пригодны для лечения расстройств центральной или периферической нервной системы, а также других расстройств, в которые вовлечены рецепторы mGluR5, таких как снижение когнитивных функций, а также для лечения как позитивных, так и негативных симптомов шизофрении.(71)(73) Заявитель и патентовладелец: АДДЕКС ФАРМА СА (CH) Настоящее изобретение представляет новые соединения формулы I, которые представляют собой положительные аллостерические модуляторы метаботропных рецепторов - подтипа 5 ("mGluR5"),которые пригодны для лечения или предотвращения расстройств центральной нервной системы, таких как, например: снижение когнитивных функций, как позитивные, так и негативные симптомы шизофрении, а также различные другие расстройства центральной или периферической нервной системы, в которые вовлечены глутаматные метаботропные рецепторы подтипа mGluR5. Настоящее изобретение также направлено на фармацевтические соединения и композиции для предотвращения или лечения указанных заболеваний, в которые вовлечены mGluR5. Предпосылки изобретения Глутамат, основной аминокислотный трансмиттер в центральной нервной системе (ЦНС) млекопитающих, опосредует возбуждающую синаптическую нейротрансмиссию посредством активации рецепторных каналов ионотропных глутаматных рецепторов (iGluRs, а именно NMDA, АМРА и каинатных) и метаботропных глутаматных рецепторов (mGluRsiGluRs отвечают за быструю возбуждающую трансмиссию (Nakanishi S. et al., (1998) Brain Res. Rev., 26:230-235), тогда как mGluRs в большей степени играют модулирующую роль, что способствует тонкой настройке синаптической эффективности. Глутамат участвует в многочисленных физиологических функциях, таких как долговременное потенциирование (LTP), процесс, который, как полагают, лежит в основе обучения и памяти, а также сердечно-сосудистой регуляции, чувственного восприятия и развития синаптической пластичности. Кроме того, глутамат играет важную роль в патофизиологии различных неврологических и психиатрических заболеваний, особенно в тех случаях, когда наблюдают дисбаланс в глутаматэргической нейротрансмиссии.mGluRs представляют собой связанные с G-белками рецепторы, которые содержат семь трансмембранных доменов. Восемь членов семейства разделены на три группы (группы I, IIIII) в соответствии с гомологией их аминокислотных последовательностей и их фармакологическими свойствами (Schoepp D.D. et al. (1999) Neuropharmacology, 38:1431-1476). Активация mGluRs приводит к большому разнообразию внутриклеточных ответов и активации различных трансдукционных каскадов. Среди членов mGluR подтип mGluR5 представляет наибольший интерес для восстановления равновесия при недостатке или избытке нейропередачи при нейропсихиатрических заболеваниях. mGluR5 является членом группы I и его активация инициирует клеточные ответы при помощи опосредованных G-белком механизмов. mGluR5 связывается с фосфолипазой С и стимулирует фосфоинозитидный гидролиз и внутриклеточную мобилизацию кальция. Показано, что белки mGluR5 локализованы в постсинаптических элементах, граничащих с постсинаптическим уплотнением (Lujan R. et al. (1996) Eur. J. Neurosci., 8:1488-500; Lujan R. et al. (1997)J. Chem. Neuroanat, 13:219-41), и их редко наблюдают в пресинаптических элементах (Romano С. et al.(1995) J. Comp. Neural., 355:455-69). Рецепторы mGluR5 могут вследствие этого изменять постсинаптические отклики на нейротрансмиттер или регулировать высвобождение нейротрансмиттера. В ЦНС рецепторы mGluR5 широко распространены в основном в коре, гиппокампе, каудатопутамене (хвостатом ядре и скорлупе, вместе составляющих полосатое тело) и прилежащем ядре. Поскольку было показано, что указанные области головного мозга вовлечены в проявления эмоций,мотивационные процессы и многочисленные аспекты когнитивной функции прогнозируют, что модуляторы могут mGluR5 представлять большой терапевтический интерес. Предполагают, что создание модуляторов mGluR, селективных к подтипам рецептора, может оказаться полезным для множества потенциальных клинических показаний. Такие показания включают эпилепсию, нейропатическую и воспалительную боль, многочисленные психиатрические расстройстваUgolini A. (1999) Prog. Neurobiol., 59:55-79; Spooren W. et al. (2003) Behav. Pharmacol., 14:257-77). Предположение о том, что гипофункция глутаматэргической системы, которая выражается в гипофункции рецептора NMDA, может служить одной из причин шизофрении, получило в последние несколько лет возрастающую поддержку (Goff D.C. and Coyle J.T. (2001) Am. J. Psychiatry, 158:13671377; Carlsson A. et al. (2001) Annu. Rev. Pharmacol. Toxicol., 41:237-260 в качестве обзора). Указание на роль дисфункции глутаматэргической нейротрансмиссии также подтверждается тем фактом, что антагонисты глутаматных рецепторов подтипа NMDA могут вызывать полный спектр симптомов, а также психологических проявлений шизофрении, таких как гипофронтальность, нарушенное преимпульсное ингибирование и повышенное освобождение дофамина в подкорке. Кроме того,-1 014904 клинические исследования позволяют предположить, что частота аллелей mGluR5 связана с шизофренией в некоторых группах населения (Devon R.S. et al. (2001) Mol. Psychiatry., 6:311-4) и что увеличение передачи сигналов mGluR5 обнаружено в слоях пирамидальных клеток коры головного мозга больных шизофренией (Ohnuma T. et al. (1998) Brain Res. Mol. Brain Res., 56:207-17). Вовлечение mGluR5 в неврологические и психиатрические заболевания подтверждают данные,показывающие, что активация in vivo mGluRs группы I вызывает потенцирование функции рецепторовNMDA во многих областях головного мозга, главным образом за счет активации рецепторов mGluR5et al. (2001) Neuroscience, 106:579-87; Benquet P. et al. (2002) J. Neurosci., 22:9679-86). Роль глутамата в процессах памяти также твердо установлена в течение последнего десятилетияMem., 76:284-297). Эксперименты на мышах с нуль-мутацией по mGluR5 подтвердили роль mGluR5 в обучении и памяти. Указанные мыши показывают избирательную неспособность справиться с двумя заданиями на пространственное обучение и память и пониженное LTP в зоне СА 1 гиппокампа (Lu et al.Physiol. Behav., 73:793-802; Rodrigues et al. (2002) J. Neurosci., 22:5219-5229). Обнаружение того, что mGluR5 отвечает за потенцирование опосредованных рецепторами NMDA токов, может указывать на то, что агонисты указанных рецепторов могут оказаться полезными в качестве средств, улучшающих когнитивную функцию, а также в качестве новых антипсихотических средств,действующих посредством селективного усиления функции рецепторов NMDA. Активация NMDARs может потенцировать гипофункциональные NMDARs в цепях,задействованных в шизофрении. Последние данные in vivo указывают на то, что активация mGluR5 может представлять собой новый и эффективный подход к лечению снижения когнитивной функции и как позитивных, так и негативных симптомов шизофрении (Kinney G.G. et al. (2003) J. Pharmacol. Exp.Ther., 306(1):116-123). Поэтому рецептор mGluR5 рассматривают как потенциальную мишень для лекарственных средств для лечения психиатрических и неврологических расстройств, включая излечимые заболевания,которыми в данном контексте являются тревожные расстройства, нарушения внимания, пищевые нарушения, расстройства настроения, психотические расстройства, когнитивные расстройства,расстройства личности и расстройства смысловой сферы. Большинство существующих в настоящее время модуляторов функции mGluR5 были разработаны как структурные аналоги глутамата, квисквалата или фенилглицина (Schoepp D.D. et al. (1999)Neuropharmacology, 38:1431-1476) и крайне перспективно разработать in vivo активные и селективные модуляторы mGluR5, действующие на центр связывания глутамата. Новый путь разработки селективных модуляторов заключается в идентификации молекул, действующих по аллостерическим механизмам,модулируя рецептор посредством связывания с центром, отличным от высококонсервативного ортостерического центра связывания. Положительные аллостерические модуляторы mGluRs недавно были предложены в качестве новых лекарственных форм, обладающих указанными привлекательными свойствами. Указанный тип молекул был открыт для mGluR1, mGluR2, mGluR4 и mGluR5 (Knoflach F. et al. (2001) Proc. Natl. Acad. Sci. USA,98:13402-13407; O'Brien J.A. et al. (2003) Mol. Pharmacol., 64:731-40; Johnson K. et al. (2002)Trans., 32:881-7). DFB и родственные молекулы описаны в качестве положительных аллостерических модуляторов mGluR5 in vitro, однако они имеют низкую активность (O'Brien J.A. et al. (2003) Mol.Pharmacol., 64:731-40). Были запатентованы производные бензамида (WO 2004/087048; O'Brien J.A.(2004) J. Pharmacol. Exp. Ther., 309:568-77), а недавно в качестве положительных аллостерических модуляторов mGluR5 были описаны производные аминопиразола (Lindsley et al. (2004) J. Med. Chem.,47:5825-8; WO 2005/087048). Среди производных аминопиразола, CDPPB (3-циано-N-(1,3-дифенил-1Hпиразол-5-ил)бензамид) проявил при действии in vivo эффект, подобный антипсихотическому в моделях поведения крыс (Kinney G.G. et al. (2005) J. Pharmacol. Exp. Then., 313:199-206). Эти данные согласуются с гипотезой, что аллостерическое потенцирование mGluR5 может обеспечить новый подход к разработке антипсихотических средств. Недавно была описана новая серия положительных аллостерических модуляторов рецепторов mGluR5 (WO 2005/044797). Запатентованы производные арилоксадиазола(WO 04/014370); указанные соединения представляют собой отрицательные аллостерические модуляторы рецепторов mGluR5. Описаны несколько классов арил- и гетероарил- оксадиазольных соединений: WO 01/54507, 03/056823, 02/72570, GB 1164572, FR 6671). Опубликована информация о бензоилтриазолах, обладающих сродством к серотонинэргическим рецепторам (Caliendo G. et al. (1999)-2 014904 Никакие конкретные ранее описанные соединения структурно не связаны с соединениями согласно настоящему изобретению. Настоящее изобретение относится к способу лечения или предотвращения состояния у млекопитающего, включая человека, лечение или предотвращение которого обеспечивают или облегчают за счет нейромодуляторного действия положительного аллостерического модулятора mGluR5. Описание чертежа Чертеж показывает действие 10 мкМ вещества из примера 1 настоящего изобретения на культуру первичных кортикальных клеток, экспрессирующих mGluR5, в отсутствии или в присутствии 300 нМ глутамата. Подробное описание изобретения Согласно настоящему изобретению предложены новые соединения общей формулы I или фармацевтически приемлемые соли, гидраты или сольваты указанных соединений,где W представляет собой (С 5-С 7)циклоалкильное, (С 5-С 7)гетероциклоалкильное или (С 5-С 7)гетероциклоалкенильное кольцо;R1 и R2 независимо друг от друга представляют собой водород, -(С 1-С 6)алкил, -(С 2-С 6)алкенил, -(С 2 С 6)алкинил, арилалкил, гетероарилалкил, гидроксил, аминогруппу, аминоалкил, гидроксиалкил, -(С 1 С 6)алкоксил или R1 и R2 вместе могут образовывать (С 3-С 7)циклоалкильное кольцо, карбонильную связь С=О или углерод-углеродную двойную связь; Р и Q независимо друг от друга представляют собой циклоалкильную, гетероциклоалкильную,арильную или гетероарильную группу формулы где R3, R4, R5, R6 и R7 независимо друг от друга представляют собой водород, галоген, -CN, -NO2,-(С 1-С 6)алкил, -(С 3-С 6)циклоалкил, -(С 3-С 7)циклоалкилалкил, -(С 2-С 6)алкенил, -(С 2-С 6)алкинил, галоген(С 1-С 6)алкил, гетероарил, гетероарилалкил, арилалкил, арил, -OR8, -NR8R9, -C(=NR10)NR8R9,-N(=NR10)NR8R9, -NR8COR9, -NR8CO2R9, -NR8SO2R9, -NR10CONR8R9, -SR8, -S(=O)R8, -S(=O)2R8,-S(=O)2NR8R9, -C(=O)R8, -COOR8, -C(=O)NR8R9, -C(=NR8)R9 или -C(=NOR8)R9; при этом, возможно, два заместителя совместно с находящимися между ними атомами образуют бициклическое гетероциклоалкильное, арильное или гетероарильное кольцо; причем каждое кольцо, возможно,дополнительно несет замещение 1-5 группами, каждая из которых независимо представляет собой галоген, -CN, -(С 1-С 6)алкил, -О-(С 0-С 6)алкил, -О-(С 3-С 7)циклоалкилалкил, -О(арил), -О(гетероарил),-О-(С 1-С 3)алкиларил, -О-(С 1-С 3)алкилгетероарил, -N-С 0-С 6)алкил)С 0-С 3)алкиларил) или -NС 0 С 6)алкил)С 0-С 3)алкилгетероарил);R8, R9, R10 независимо друг от друга представляют собой водород, (С 1-С 6)алкил, (С 3-С 6)циклоалкил,(С 3-С 7)циклоалкилалкил, (С 2-С 6)алкенил, (С 2-С 6)алкинил, галоген-(С 1-С 6)алкил, гетероциклоалкил,гетероарил, гетероарилалкил, арилалкил или арил; любой из которых, возможно, несет замещение 1-5 группами, каждая из которых независимо представляет собой галоген, -CN, -(С 1-С 6)алкил, -О-(С 0 С 6)алкил, -О-(С 3-С 7)циклоалкилалкил, -О(арил), -О(гетероарил), -NC0-C6)алкил)2, -NС 0-С 6)алкил)С 3 С 7)циклоалкил) или -NС 0-С 6)алкил)(арил);D, E, F, G и Н в Р и Q независимо друг от друга представляют собой -C(R3)=, -C(R3)=C(R4)-,-C(=O)-, -C(=S)-, -О-, -N=, -N(R3)- или -S-; А представляет собой -N=N- в азогруппе, этил, этенил, этинил, -NR8C(=O)-, -NR8S(=O)2-,-C(=O)NR8-, -S-, -S(=O)-, -S(=O)2-, -S(=O)2NR8-, -C(=O)-O-, -O-C(=O)-, -C(=NR8)NR9-, -C(=NOR8)NR9-,-NR8C(=NOR9)-, =N-O-, -O-N=CH- или арильную либо гетероарильную группу формулы-3 014904 где R3, R4, R5 и R6 независимо друг от друга представляют собой группы, определенные выше;D, E, F, G и Н в А независимо друг от друга представляют собой углеродсодержащую группу,кислород, азот, серу или двойную связь; В представляет собой одинарную связь, -С(=О)-(С 0-С 2)алкил-, -С(=О)-(С 2-С 6)алкенил-, -С(=О)-(С 2 С 6)алкинил-, -С(=O)-O-, -С(=О)NR8-(С 0-С 2)алкил-, -С(=NR8)NR9-S(=О)-(С 0-С 2)алкил-, -S(=О)2-(С 0 С 2)алкил-,-S(=О)2NR8-(С 0-С 2)алкил-,C(=NR8)-(C0-С 2)алкил-,-С(=NOR8)-(С 0-С 2)алкилилиR8 и R9 независимо друг от друга представляют собой группы, определенные выше;X и Y независимо друг от друга выбирают из химической связи, -NR11C(=O)O-, возможно замещенного -(С 1-С 6)алкила-, -(С 2-С 6)алкинила-, -(С 2-С 6)алкенила-, -(С 3-С 7)циклоалкила-, -(С 3 С 8)циклоалкенила-, -(С 1-С 6)галогеналкила-, -(С 1-С 6)цианоалкила-, -(С 0-С 6)алкил-O-(С 0-С 6)алкила-, -(С 0 С 6)алкил-O-(С 2-С 6)алкинила-, -(С 0-С 6)алкил-O-(С 2-С 6)алкенила-, -(С 0-С 6)алкил-О-(С 3-С 7)циклоалкила-,-(С 0-С 6)алкил-O-(С 4-С 10)алкилциклоалкила-, -(С 0-С 6)алкил-С(=O)-(С 0-С 6)алкила-, -(С 0-С 6)алкил-С(=О)(С 2-С 6)алкинила-, -(С 0-С 6)алкил-С(=O)-(С 2-С 6)алкенила-, -(С 0-С 6)алкил-С(=О)-(С 3-С 7)алкилциклоалкила-,-(С 0-С 6)алкил-С(=О)-(С 4-С 10)циклоалкила-, -(С 0-С 6)алкил-С(=O)O-(С 0-С 6)алкила-, -(С 0-С 6)алкил-С(=О)О(С 2-С 6)алкинила-, -(С 0-С 6)алкил-С(=О)О-(С 2-С 6)алкенила-, -(С 0-С 6)алкил-С(=О)О-(С 3-С 7)циклоалкила-,-(С 0-С 6)алкил-С(=О)О-(С 4-С 10)алкилциклоалкила-, -(С 0-С 6)алкил-С(=О)NR11-(С 0-С 6)алкила-, -(С 0-С 6)алкил-С(=О)NR11-(С 2-С 6)алкинила-, -(С 0-С 6)алкил-С(=О)NR11-(С 2-С 6)алкенила-, -(С 0-С 6)алкил-С(=О)NR11(С 3-С 7)циклоалкила-, -(С 0-С 6)алкил-С(=O)NR11-(С 4-С 10)алкилциклоалкила-, -(С 0-С 6)алкил-S-(С 0-С 6)алкила-, -(С 0-С 6)алкил-S-(С 2-С 6)алкинила-, -(С 0-С 6)алкил-S-(С 2-С 6)алкенила-, -(С 0-С 6)алкил-S-(С 3-С 7)циклоалкила-, -(С 0-С 6)алкил-S-(С 4-С 10)алкилциклоалкила-, -(С 0-С 6)алкил-S(O)-(С 0-С 6)алкила-, -(С 0-С 6)алкил-О(С 2-С 6)алкинила-, -(С 0-С 6)алкил-S(О)-(С 2-С 6)алкенила-, -(С 0-С 6)алкил-S(О)-(С 3-С 7)циклоалкила-, -(С 0 С 6)алкил-S(О)-(С 4-С 10)алкилциклоалкила-, -(С 0-С 6)алкил-S(O)2-(С 0-С 6)алкила-, -(С 0-С 6)алкил-S(О)2-(С 2 С 6)алкинила-, -(С 0-С 6)алкил-S(О)2-(С 2-С 6)алкенила-, -(С 0-С 6)алкил-S(О)2-(С 3-С 7)циклоалкила-, -(С 0-С 6)алкил-S(О)2-(С 4-С 10)алкилциклоалкила-, -(С 0-С 6)алкил-S(О)2NR11-(С 0-С 6)алкила-, -(С 0-С 6)алкил-S(O)2NR11(С 2-С 6)алкинила-, -(С 0-С 6)алкил-S(O)2NR11-(С 2-С 6)алкенила-, -(С 0-С 6)алкил-S(О)2NR11-(С 3-С 7)циклоалкила-, -(С 0-С 6)алкил-S(O)2NR11-(С 4-С 10)алкилциклоалкила-, -(С 0-С 6)алкил-NR11-(С 0-С 6)алкила-, -(С 0 С 6)алкил-NR11-(С 2-С 6)алкинила-, -(С 0-С 6)алкил-NR11-(С 2-С 6)алкенила-, -(С 0-С 6)алкил-NR11-(С 3-С 7)циклоалкила-, -(С 0-С 6)алкил-NR11-(С 4-С 10)алкилциклоалкила-, -(С 0-С 6)алкил-NR11C(=O)-(C0-C6)алкила-, -(С 0 С 6)алкил-NR11C(=О)-(С 2-С 6)алкинила-,-(С 0-С 6)алкил-NR11C(=О)-(С 2-С 6)алкенила-,-(С 0-С 6)алкилNR11C(=О)-(С 3-С 7)циклоалкила-, -(С 0-С 6)алкил-NR11C(=О)-(С 4-С 10)алкилциклоалкила-, -(С 0-С 6)алкилNR12C(=O)NR11-(С 0-С 6)алкила-,-(С 0-С 6)алкил-NR12C(=O)NR11-(С 2-С 6)алкинила-,-(С 0-С 6)алкилNR12C(=О)NR11-(С 2-С 6)алкенила-, -(С 0-С 6)алкил-NR12C(=О)NR11-(С 3-С 7)циклоалкила-, -(C0-C6)алкилNR12C(=O)NR11-(С 4-С 10)алкилциклоалкила-,-(С 0-С 6)алкил-NR11S(O)2-(С 0-С 6)алкила-,-(С 0-С 6)алкилNR11S(O)2-(С 2-С 6)алкинила-, -(C0-C6)алкил-NR11S(O)2-(С 2-С 6)алкенила-, -(С 0-С 6)алкил-NR11S(O)2-(С 3 С 7)циклоалкила-, -(С 0-С 6)алкил-NR11S(O)2-(С 4-С 10)алкилциклоалкила-, -(С 0-С 6)алкил-NR12C(=S)NR11-(C0C6)алкила-, -(C0-C6)алкил-NR12C(=S)NR11-(C2-С 6)алкинила-, -(C0-C6)алкил-NR12C(=S)NR11-(C2-C6)алкенила-, -(С 0-C6)алкил-NR12C(=S)NR11-(С 3-С 7)циклоалкила-, -(С 0-С 6)алкил-NR12C(=S)NR11-(C4-C10)алкилциклоалкила-, -(С 0-С 6)алкил-ОС(=O)-(С 0-С 6)алкила-, -(С 0-С 6)алкил-ОС(=O)-(С 2-С 6)алкинила-, -(С 0 С 6)алкил-ОС(=О)-(С 2-С 6)алкенила-, -(С 0-С 6)алкил-ОС(=O)-(С 4-С 10)алкилциклоалкила-, -(С 0-С 6)алкилОС(=О)-(С 3-С 7)циклоалкила-, -(C0-C6)алкил-OC(=O)NR11-(C0-C6)алкила-, -(С 0-С 6)алкил-OC(=O)NR11-(C2 С 6)алкинила-, -(C0-C6)алкил-OC(=O)NR11-(C2-С 6)алкенила-, -(C0-C6)алкил-OC(=O)NR11-(С 4-С 10)алкилциклоалкила-, -(С 0-С 6)алкил-ОС(=O)NR11-(С 3-С 7)циклоалкила-, -(C0-C6)алкил-NR11C(=O)O-(C0-C6)алкила-, -(С 0-C6)алкил-NR11C(=O)O-(C2-C6)алкинила-, -(С 0-С 6)алкил-NR11C(=О)О-(С 2-С 6)алкенила-, -(C0C6)алкил-NR11C(=O)O-(C3-C7)циклоалкила- или -(C0-C6)алкил-NR11C(=O)O-(C4-C10)алкилциклоалкила-;X и Y не могут одновременно представлять собой химическую связь;R11 и R12 независимо друг от друга представляют собой водород, -(С 1-С 6)алкил, -(С 3-С 6)циклоалкил,-(С 3-С 7)циклоалкилалкил, -(С 2-С 6)алкенил, -(С 2-С 6)алкинил, галоген-(С 1-С 6)алкил, гетероциклоалкил,гетероарил, гетероарилалкил, арилалкил или арил; любой из которых, возможно, несет замещение 1-5 группами, каждая из которых независимо представляет собой галоген, -CN, -(С 1-С 6)алкил, -О(С 0 С 6)алкил, -О(С 3-С 7)циклоалкилалкил, -О(арил), -О(гетероарил), -NC0-С 6)алкил)С 0-С 6)алкил), -NС 0 С 6)алкил)С 3-С 7)циклоалкил) или -NС 0-С 6)алкил)(арил); любой N может представлять собой N-оксид. Настоящее изобретение охватывает оба возможных стереоизомера, а также включает как рацемические соединения, так и индивидуальные энантиомеры указанных соединений. В целях однозначности следует понимать, что в настоящем описании "(C1-С 6)" обозначает углеродную группу, содержащую 1, 2, 3, 4, 5 или 6 атомов углерода. "(С 0-С 6)" обозначает углеродную группу, содержащую 0, 1, 2, 3, 4, 5 или 6 атомов углерода. В настоящем описании "С" обозначает атом углерода. В приведенном выше определении термин "(С 1-С 6)алкил" включает такие группы, как метил, этил,пропил, изопропил, бутил, изобутил, втор-бутил, трет-бутил, пентил, изопентил, нео-пентил, третпентил, гексил или подобные им.-4 014904 Термин "(С 2-С 6)алкенил" включает такие группы, как этенил, 1-пропенил, аллил, изопропенил, 1 бутенил, 3-бутенил, 4-пентенил или подобные им. Термин "(С 2-С 6)алкинил" включает такие группы, как этинил, пропинил, бутинил, пентинил или подобные им. Термин "галоген" включает такие атомы, как фтор, хлор, бром и йод. Термин "циклоалкил" относится, возможно, к замещенному карбоциклу, не содержащему гетероатомов, включая моно-, би- и трициклические насыщенные карбоциклы, а также системы с конденсированными кольцами. Указанные системы с конденсированными кольцами могут включать полностью или частично ненасыщенное кольцо, такое как бензольное кольцо, с образованием систем с конденсированными кольцами, таких как карбоциклы, конденсированные с бензольным кольцом. Термин "циклоалкил" охватывает такие системы с конденсированными кольцами, как спироконденсированные кольцевые системы. Примеры циклоалкилов включают циклопропил, циклобутил,циклопентил, циклогексил, декагидронафталин, адамантан, индан, флуорен, 1,2,3,4-тетрагидронафталин или подобные им. Термин "гетероциклоалкил" относится, возможно, к замещенному карбоциклу, содержащему по меньшей мере один гетероатом, выбранный независимо из О, N, S. Этот термин включает моно-, би- и трициклические насыщенные карбоциклы, а также системы с конденсированными кольцами. Указанные системы с конденсированными кольцами могут содержать одно полностью или частично ненасыщенное кольцо, такое как бензольное кольцо, с образованием систем с конденсированными кольцами, таких как карбоциклы, конденсированные с бензольным кольцом. Примеры гетероциклоалкилов включают пиперидин, пиперазин, морфолин, тетрагидротиофен, индолин, изохинолин или подобные им. Термин "арил" включает (С 6-С 10)арильную группу, такую как фенил, 1-нафтил, 2-нафтил или подобные им. Термин "арилалкил" включает (С 6-С 10)арил-(С 1-С 3)алкильную группу, такую как бензильная группа, 1-фенилэтильная группа, 2-фенилэтильная группа, 1-фенилпропильная группа, 2-фенилпропильная группа, 3-фенилпропильная группа, 1-нафтилметильная группа, 2-нафтилметильная группа или подобные им. Термин "гетероарил" относится к 5-10-членной гетероциклической группе, содержащей от 1 до 4 гетероатомов, выбранных из кислорода, азота или серы, которая образует такое кольцо, как фурил(бензотиазольное кольцо), фуразанил (фуразановое кольцо) и тому подобное. Термин "гетероарилалкил" охватывает гетероарил-(С 1-С 3)алкильную группу, причем примеры гетероарила те же самые, что и приведенные в определении выше, такие как 2-фурилметильная группа,3-фурилметильная группа, 2-тиенилметильная группа, 3-тиенилметильная группа, 1-имидазолилметильная группа, 2-имидазолилметильная группа, 2-тиазолилметильная группа, 2-пиридилметильная группа, 3-пиридилметильная группа, 1-хинолилметильная группа или тому подобное. Термин "сольват" относится к комплексу непостоянной стехиометрии, образованному растворенным веществом (например, соединением формулы I) и растворителем. Растворитель представляет собой фармацевтически приемлемый растворитель, предпочтительно такой как вода; указанный растворитель не должен влиять на биологическую активность растворенного вещества. Термин "возможно" означает, что описанное после событие(я) может происходить или не происходить и включает оба случая, когда событие(я) происходит и когда событие(я) не происходит. Термин "замещенный" относится к замещению указанным заместителем или заместителями,множественные степени замещения допустимы, если не определено иначе. Предпочтительные соединения согласно настоящему изобретению представляют собой соединения формулы I-A, приведенной ниже или фармацевтически приемлемые соли, гидраты или сольваты указанных соединений,где R1 и R2 независимо друг от друга представляют собой водород, -(С 1-С 6)алкил, -(С 2-С 6)алкенил,-5 014904-(С 2-С 6)алкинил, арилалкил, гетероарилалкил, гидроксил, аминогруппу, аминоалкил, гидроксиалкил,-(С 1-С 6)алкоксил или R1 и R2 вместе могут образовывать (С 3-С 7)циклоалкильное кольцо, карбонильную связь С=О или углерод-углеродную двойную связь; Р и Q независимо друг от друга представляют собой циклоалкильную, гетероциклоалкильную,арильную или гетероарильную группу формулы где R3, R4, R5, R6 и R7 независимо друг от друга представляют собой водород, галоген, -CN, -NO2,-(С 1-С 6)алкил, -(С 3-С 6)циклоалкил, -(С 3-С 7)циклоалкилалкил, -(С 2-С 6)алкенил, -(С 2-С 6)алкинил, галоген(С 1-С 6)алкил, гетероарил, гетероарилалкил, арилалкил, арил, -OR8, -NR8R9, -C(=NR10)NR8R9,-N(=NR10)NR8R9, -NR8COR9, -NR8CO2R9, -NR8SO2R9, -NR10CONR8R9, -SR8, -S(=O)R8, -S(=O)2R8,-S(=O)2NR8R9, -C(=O)R8, -COOR8, -C(=O)NR8R9, -C(=NR8)R9 или -C(=NOR8)R9; при этом, возможно, два заместителя совместно с находящимися между ними атомами образуют бициклическое гетероциклоалкильное, арильное или гетероарильное кольцо; причем каждое кольцо, возможно,дополнительно несет замещение 1-5 группами, каждая из которых независимо представляет собой: галоген, -CN, -(С 1-С 6)алкил, -O-(С 0-С 6)алкил, -О-(С 3-С 7)циклоалкилалкил, -О(арил), -О(гетероарил),-O-(-C1-С 3)алкиларил, -О-(С 1-С 3)алкилгетероарил, -N-С 0-С 6)алкил)С 0-С 3)алкиларил) или -NС 0-С 6)алкил)С 0-С 3)алкилгетероарил);R8, R9, R10 независимо друг от друга представляют собой водород, (С 1-С 6)алкил, (С 3-С 6)циклоалкил,(С 3-С 7)циклоалкилалкил, (С 2-С 6)алкенил, (С 2-С 6)алкинил, галоген-(С 1-С 6)алкил, гетероциклоалкил,гетероарил, гетероарилалкил, арилалкил или арил; любой из которых, возможно, несет замещение 1-5 группами, каждая из которых независимо представляет собой галоген, -CN, -(С 1-С 6)алкил, -О-(С 0 С 6)алкил, -О-(С 3-С 7)циклоалкилалкил, -О(арил), -О(гетероарил), -NС 0-С 6)алкил)2, -NС 0-С 6)алкил)С 3 С 7)циклоалкил) или -NС 0-С 6)алкил)(арил);D, E, F, G и Н в Р и Q независимо друг от друга представляют собой -C(R3)=, -C(R3)=C(R4)-,-C(=O)-, -C(=S)-, -О-, -N=, -N(R3)- или -S-; А представляет собой -N=N- в азогруппе, этил, этенил, этинил, -NR8C(=O)-, -NR8S(=O)2-,-C(=O)NR8-, -S-, -S(=O)-, -S(=O)2-, -S(=O)2NR8-, -C(=O)-O-, -O-C(=O)-, -C(=NR8)NR9-, -C(=NOR8)NR9-,-NR8C(=NOR9)-, =N-O-, -O-N=CH- или арильную либо гетероарильную группу формулы где R3, R4, R5 и R6 независимо друг от друга представляют собой группы, определенные выше;D, E, F, G и Н в А независимо друг от друга представляют собой углеродсодержащую группу,кислород, азот, серу или двойную связь; В представляет собой одинарную связь, -С(=О)-(С 0-С 2)алкил-, -С(=О)-(С 2-С 6)алкенил-, -С(=O)-(С 2 С 6)алкинил-, -С(=O)-O-, -С(=О)NR8-(С 0-С 2)алкил-, -С(=NR8)NR9-S(=О)-(C0-С 2)алкил-, -S(=О)2-(С 0-С 2)алкил-, -S(=O)2NR8-(C0-C2)алкил-, C(=NR8)-(C0-С 2)алкил-, -C(=NOR8)-(C0-C2)алкил- или -C(=NOR8)NR9-(C0 С 2)алкил-;R8 и R9 независимо друг от друга представляют собой группы, определенные выше;X и Y независимо друг от друга выбирают из химической связи, -NR11C(=O)O-, возможно,замещенного -(С 1-С 6)алкила-, -(С 2-С 6)алкинила-, -(С 2-С 6)алкенила-, -(С 3-С 7)циклоалкила-, -(С 3-С 8)циклоалкенила-, -(С 1-С 6)галогеналкила-, -(С 1-С 6)цианоалкила-, -(С 0-С 6)алкил-O-(С 0-С 6)алкила-, -(С 0-С 6)алкилO-(С 2-С 6)алкинила-, -(С 0-С 6)алкил-O-(С 2-С 6)алкенила-, -(С 0-С 6)алкил-О-(С 3-С 7)циклоалкила-, -(С 0 С 6)алкил-O-(С 4-С 10)алкилциклоалкила-, -(С 0-С 6)алкил-С(=O)-(С 0-С 6)алкила-, -(С 0-С 6)алкил-С(=О)-(С 2 С 6)алкинила-, -(С 0-С 6)алкил-С(=O)-(С 2-С 6)алкенила-, -(С 0-С 6)алкил-С(=О)-(С 3-С 7)алкилциклоалкила-,-(С 0-С 6)алкил-С(=O)-(С 4-С 10)циклоалкила-, -(С 0-С 6)алкил-С(=O)O-(С 0-С 6)алкила-, -(С 0-С 6)алкил-С(=О)О(С 2-С 6)алкинила-, -(С 0-С 6)алкил-С(=О)О-(С 2-С 6)алкенила-, -(С 0-С 6)алкил-С(=О)О-(С 3-С 7)циклоалкила-,-(С 0-С 6)алкил-С(=О)О-(С 4-С 10)алкилциклоалкила-, -(С 0-С 6)алкил-C(=O)NR11-(C0-C6)алкила-, -(С 0-С 6)алкил-С(=О)NR11-(С 2-С 6)алкинила-, -(C0-C6)алкил-C(=O)NR11-(C2-C6)алкенила-, -(С 0-C6)алкил-C(=O)NR11(C3-C7)циклоалкила-, -(С 0-С 6)алкил-С(=O)NR11-(С 4-С 10)алкилциклоалкила-, -(С 0-С 6)алкил-S-(С 0-С 6)алкила-, -(С 0-С 6)алкил-S-(С 2-С 6)алкинила-, -(С 0-С 6)алкил-S-(С 2-С 6)алкенила-, -(С 0-С 6)алкил-S-(С 3-С 7)цикло-6 014904 алкила-, -(С 0-С 6)алкил-S-(С 4-С 10)алкилциклоалкила-, -(С 0-С 6)алкил-S(O)-(С 0-С 6)алкила-, -(С 0-С 6)алкил-О(С 2-С 6)алкинила-, -(С 0-С 6)алкил-S(О)-(С 2-С 6)алкенила-, -(С 0-С 6)алкил-S(O)-(С 3-С 7)циклоалкила-, -(С 0 С 6)алкил-S(O)-(С 4-С 10)алкилциклоалкила-, -(С 0-С 6)алкил-S(O)2-(С 0-С 6)алкила-, -(С 0-С 6)алкил-S(О)2-(C2 С 6)алкинила-, -(С 0-С 6)алкил-S(O)2-(С 2-С 6)алкенила-, -(С 0-С 6)алкил-S(O)2-(С 3-С 7)циклоалкила-, -(С 0 С 6)алкил-S(О)2-(С 4-С 10)алкилциклоалкила-,-(С 0-С 6)алкил-S(O)2NR11-(С 0-С 6)алкила-,-(C0-C6)алкилS(O)2NR11-(C2-С 6)алкинила-, -(С 0-С 6)алкил-S(O)2NR11-(С 2-С 6)алкенила-, -(С 0-С 6)алкил-S(О)2NR11-(С 3 С 7)циклоалкила-,-(С 0-С 6)алкил-S(O)2NR11-(С 4-С 10)алкилциклоалкила-,-(С 0-С 6)алкил-NR11-(С 0 С 6)алкила-, -(С 0-С 6)алкил-NR11-(С 2-С 6)алкинила-, -(C0-C6)алкил-NR11-(C2-С 6)алкенила-, -(С 0-С 6)алкилNR11-(С 3-С 7)циклоалкила-, -(С 0-С 6)алкил-NR11-(С 4-С 10)алкилциклоалкила-, -(С 0-С 6)алкил-NR11C(=O)-(С 0 С 6)алкила-, -(С 0-С 6)алкил-NR11C(=O)-(С 2-С 6)алкинила-, -(С 0-С 6)алкил-NR11C(=O)-(С 2-С 6)алкенила-, -(С 0 С 6)алкил-NR11C(=О)-(С 3-С 7)циклоалкила-, -(С 0-С 6)алкил-NR11C(=O)-(С 4-С 10)алкилциклоалкила-, -(C0C6)алкил-NR12C(=O)NR11-(C0-С 6)алкила-, -(С 0-С 6)алкил-NR12C(=O)NR11-(С 2-С 6)алкинила-, -(С 0-С 6)алкилNR12C(=О)NR11-(С 2-С 6)алкенила-, -(С 0-С 6)алкил-NR12C(=О)NR11-(С 3-С 7)циклоалкила-, -(C0-C6)алкилNR12C(=O)NR11-(С 4-С 10)алкилциклоалкила-,-(С 0-С 6)алкил-NR11S(O)2-(С 0-С 6)алкила-,-(С 0-С 6)алкилNR11S(O)2-(С 2-С 6)алкинила-, -(С 0-С 6)алкил-NR11S(O)2-(С 2-С 6)алкенила-, -(С 0-С 6)алкил-NR11S(O)2-(С 3 С 7)циклоалкила-, -(С 0-С 6)алкил-NR11S(O)2-(С 4-С 10)алкилциклоалкила-, -(С 0-С 6)алкил-NR12C(=S)NR11-(C0C6)алкила-, -(С 0-С 6)алкил-NR12C(=S)NR11-(С 2-С 6)алкинила-, -(С 0-С 6)алкил-NR12C(=S)NR11-(С 2-С 6)алкенила-, -(С 0-С 6)алкил-NR12C(=S)NR11-(С 3-С 7)циклоалкила-, -(С 0-С 6)алкил-NR12C(=S)NR11-(С 4-С 10)алкилциклоалкила-, -(С 0-С 6)алкил-ОС(=О)-(С 0-С 6)алкила-, -(С 0-С 6)алкил-ОС(=O)-(С 2-С 6)алкинила-, -(С 0-С 6)алкилОС(=О)-(С 2-С 6)алкенила-,-(С 0-С 6)алкил-ОС(=O)-(С 4-С 10)алкилциклоалкила-,-(С 0-С 6)алкил-ОС(=O)-(С 3 С 7)циклоалкила-, -(С 0-С 6)алкил-ОС(=O)NR11-(С 0-С 6)алкила-, -(С 0-С 6)алкил-ОС(=О)NR11-(С 2-С 6)алкинила-,-(С 0-С 6)алкил-ОС(=O)NR11-(С 2-С 6)алкенила-, -(С 0-С 6)алкил-ОС(=O)NR11-(С 4-С 10)алкилциклоалкила-, -(С 0 С 6)алкил-ОС(=O)NR11-(С 3-С 7)циклоалкила-, -(С 0-С 6)алкил-NR11C(=O)O-(С 0-С 6)алкила-, -(С 0-С 6)алкилNR11C(=О)О-(С 2-С 6)алкинила-, -(С 0-С 6)алкил-NR11C(=О)О-(С 2-С 6)алкенила-, -(С 0-С 6)алкил-NR11C(=O)O(С 3-С 7)циклоалкила- или -(С 0-С 6)алкил-NR11C(=O)O-(С 4-С 10)алкилциклоалкила-;X и Y не могут одновременно представлять собой химическую связь;R11 и R12 независимо друг от друга представляют собой водород, -(С 1-С 6)алкил, -(С 3-С 6)циклоалкил,-(С 3-С 7)циклоалкилалкил, -(С 2-С 6)алкенил, -(С 2-С 6)алкинил, галоген-(С 1-С 6)алкил, гетероциклоалкил,гетероарил, гетероарилалкил, арилалкил или арил; любой из которых, возможно, несет замещение 1-5 группами, каждая из которых независимо представляет собой галоген, -CN, -(С 1-С 6)алкил, -O(С 0 С 6)алкил, -О(С 3-С 7)циклоалкилалкил, -О(арил), -О(гетероарил), -NC0-С 6)алкил)С 0-С 6)алкил), -NС 0 С 6)алкил)С 3-С 7)циклоалкил) или -NС 0-С 6)алкил)(арил);J представляет собой одинарную связь, -C(R13)(R14)-, -O-, -N(R13)- или -S-;R13, R14 независимо друг от друга представляют собой водород, -(С 1-С 6)алкил, -(С 3-С 6)циклоалкил,-(С 3-С 7)циклоалкилалкил, -(С 2-С 6)алкенил, -(С 2-С 6)алкинил, галоген-(С 1-С 6)алкил, гетероарил,гетероарилалкил, арилалкил или арил; любой из которых, возможно, несет замещение 1-5 группами,каждая из которых независимо представляет собой галоген, -CN, -(С 1-С 6)алкил, -O(С 0-С 6)алкил, -О(С 3 С 7)циклоалкилалкил, -О(арил), -О(гетероарил), -NС 0-С 6)алкил)С 0-С 6)алкил), -NС 0-С 6)алкил)С 3 С 7)циклоалкил) или -NС 0-С 6)алкил)(арил); любой N может представлять собой N-оксид. Настоящее изобретение охватывает оба возможных стереоизомера, а также как рацемические соединения, так и индивидуальные энантиомеры указанных соединений. Особенно предпочтительные соединения согласно настоящему изобретению представляют собой соединения формулы I-В или фармацевтически приемлемые соли, гидраты или сольваты указанных соединений,где R1 и R2 независимо друг от друга представляют собой водород, -(C1-С 6)алкил, -(С 2-С 6)алкенил (С 2-С 6)алкинил, арилалкил, гетероарилалкил, гидроксил, аминогруппу, аминоалкил, гидроксиалкил, -(С 1 С 6)алкоксил или R1 и R2 вместе могут образовывать (С 3-С 7)циклоалкильное кольцо, карбонильную связь С=О или углерод-углеродную двойную связь;-7 014904 Р и Q независимо друг от друга представляют собой циклоалкильную, гетероциклоалкильную,арильную или гетероарильную группу формулы где R3, R4, R5, R6 и R7 независимо друг от друга представляют собой водород, галоген, -CN, -NO2,-(С 1-С 6)алкил, -(С 3-С 6)циклоалкил, -(С 3-С 7)циклоалкилалкил, -(С 2-С 6)алкенил, -(С 2-С 6)алкинил, галоген(С 1-С 6)алкил, гетероарил, гетероарилалкил, арилалкил, арил, -OR8, -NR8R9, -C(=NR10)NR8R9,-N(=NR10)NR8R9, -NR8COR9, -NR8CO2R9, -NR8SO2R9, -NR10CONR8R9, -SR8, -S(=O)R8, -S(=O)2R8,-S(=O)2NR8R9, -C(=O)R8, -COOR8, -C(=O)NR8R9, -C(=NR8)R9 или -C(=NOR8)R9; при этом, возможно, два заместителя совместно с находящимися между ними атомами образуют бициклическое гетероциклоалкильное, арильное или гетероарильное кольцо; причем каждое кольцо, возможно, дополнительно несет замещение 1-5 группами, каждая из которых независимо представляет собой галоген, -CN, -(С 1-С 6)алкил,-О-(С 0-С 6)алкил, -О-(С 3-С 7)циклоалкилалкил, -О(арил), -О(гетероарил), -O-(-C1-С 3)алкиларил, -О-(С 1 С 3)алкилгетероарил, -N-С 0-С 6)алкил)С 0-С 3)алкиларил) или -NС 0-С 6)алкил)С 0-С 3)алкилгетероарил);R8, R9, R10 независимо друг от друга представляют собой водород, (С 1-С 6)алкил, (С 3-С 6)циклоалкил,(С 3-С 7)циклоалкилалкил, (С 2-С 6)алкенил, (С 2-С 6)алкинил, галоген-(С 1-С 6)алкил, гетероциклоалкил,гетероарил, гетероарилалкил, арилалкил или арил; любой из которых, возможно, несет замещение 1-5 группами, каждая из которых независимо представляет собой галоген, -CN, -(С 1-С 6)алкил, -О-(С 0 С 6)алкил, -О-(С 3-С 7)циклоалкилалкил, -О(арил), -О(гетероарил), -NС 0-С 6)алкил)2, -NС 0-С 6)алкил)С 3 С 7)циклоалкил) или -NС 0-С 6)алкил)(арил);D, E, F, G и Н в Р и Q независимо друг от друга представляют собой -C(R3)=, -C(R3)=C(R4)-,-C(=O)-, -C(=S)-, -О-, -N=, -N(R3)- или -S-; В представляет собой одинарную связь, -С(=О)-(С 0-С 2)алкил-, -С(=О)-(С 2-С 6)алкенил-, -С(=О)-(С 2 С 6)алкинил-, -С(=О)-О-, -С(=О)NR8-(С 0-С 2)алкил-, -С(=NR8)NR9-S(=О)-(С 0-С 2)алкил-, -S(=О)2-(С 0 С 2)алкил-,-S(=О)2NR8-(С 0-С 2)алкил-,C(=NR8)-(C0-С 2)алкил-,-С(=NOR8)-(С 0-С 2)алкилилиR8 и R9 независимо друг от друга представляют собой группы, определенные выше;X и Y независимо друг от друга выбирают из химической связи, -NR11C(=O)O-, возможно,замещенного -(С 1-С 6)алкила-, -(С 2-С 6)алкинила-, -(С 2-С 6)алкенила-, -(С 3-С 7)циклоалкила-, -(С 3-С 8)циклоалкенила-, -(С 1-С 6)галогеналкила-, -(С 1-С 6)цианоалкила-, -(С 0-С 6)алкил-O-(С 0-С 6)алкила-, -(С 0-С 6)алкилO-(С 2-С 6)алкинила-, -(С 0-С 6)алкил-O-(С 2-С 6)алкенила-, -(С 0-С 6)алкил-O-(С 3-С 7)циклоалкила-, -(С 0-С 6)алкил-O-(С 4-С 10)алкилциклоалкила-, -(С 0-С 6)алкил-С(=O)-(С 0-С 6)алкила-, -(С 0-С 6)алкил-С(=О)-(С 2-С 6)алкинила-, -(С 0-С 6)алкил-С(=О)-(С 2-С 6)алкенила-, -(С 0-С 6)алкил-С(=О)-(С 3-С 7)алкилциклоалкила-, -(С 0-С 6)алкил-С(=O)-(С 4-С 10)циклоалкила-,-(С 0-С 6)алкил-С(=O)O-(С 0-С 6)алкила-,-(С 0-С 6)алкил-С(=О)О-(С 2 С 6)алкинила-, -(С 0-С 6)алкил-С(=O)O-(С 2-С 6)алкенила-, -(С 0-С 6)алкил-С(=O)O-(С 3-С 7)циклоалкила-, -(С 0 С 6)алкил-С(=О)О-(С 4-С 10)алкилциклоалкила-, -(С 0-С 6)алкил-C(=O)NR11-(C0-C6)алкила-, -(C0-C6)алкилC(=O)NR11-(C2-С 6)алкинила-, -(C0-C6)алкил-C(=O)NR11-(C2-C6)алкенила-, -(С 0-C6)алкил-C(=O)NR11-(C3C7)циклоалкила-, -(C0-C6)алкил-C(=O)NR11-(С 4-С 10)алкилциклоалкила-, -(С 0-С 6)алкил-S-(С 0-С 6)алкила-, -(С 0 С 6)алкил-S-(С 2-С 6)алкинила-, -(С 0-С 6)алкил-S-(С 2-С 6)алкенила-, -(С 0-С 6)алкил-S-(С 3-С 7)циклоалкила-, -(С 0 С 6)алкил-S-(С 4-С 10)алкилциклоалкила-, -(С 0-С 6)алкил-S(O)-(С 0-С 6)алкила-, -(С 0-С 6)алкил-О-(С 2-С 6)алкинила-, -(С 0-С 6)алкил-S(O)-(С 2-С 6)алкенила-, -(С 0-С 6)алкил-S(О)-(С 3-С 7)циклоалкила-, -(С 0-С 6)алкил-S(О)(С 4-С 10)алкилциклоалкила-, -(С 0-С 6)алкил-S(O)2-(С 0-С 6)алкила-, -(С 0-С 6)алкил-S(О)2-(С 2-С 6)алкинила-,-(С 0-С 6)алкил-S(О)2-(С 2-С 6)алкенила-, -(С 0-С 6)алкил-S(O)2-(С 3-С 7)циклоалкила-, -(С 0-С 6)алкил-S(O)2-(С 4 С 10)алкилциклоалкила-, -(С 0-С 6)алкил-S(О)2NR11-(С 0-С 6)алкила-, -(С 0-С 6)алкил-S(О)2NR11-(С 2-С 6)алкинила-, -(С 0-С 6)алкил-S(О)2NR11-(С 2-С 6)алкенила-, -(С 0-С 6)алкил-S(О)2NR11-(С 3-С 7)циклоалкила-, -(С 0 С 6)алкил-S(O)2NR11-(С 4-С 10)алкилциклоалкила-, -(С 0-С 6)алкил-NR11-(С 0-С 6)алкила-, -(С 0-С 6)алкил-NR11(С 2-С 6)алкинила-, -(С 0-С 6)алкил-NR11-(С 2-С 6)алкенила-, -(С 0-С 6)алкил-NR11-(С 3-С 7)циклоалкила-, -(С 0 С 6)алкил-NR11-(С 4-С 10)алкилциклоалкила-,-(С 0-С 6)алкил-NR11C(=O)-(С 0-С 6)алкила-,-(С 0-С 6)алкилNR11C(=O)-(С 2-С 6)алкинила-, -(С 0-С 6)алкил-NR11C(=O)-(С 2-С 6)алкенила-, -(С 0-С 6)алкил-NR11C(=О)-(С 3 С 7)циклоалкила-, -(С 0-С 6)алкил-NR11C(=O)-(С 4-С 10)алкилциклоалкила-, -(С 0-С 6)алкил-NR12C(=O)NR11(С 0-С 6)алкила-, -(C0-C6)алкил-NR12C(=O)NR11-(C2-C6)алкинила-, -(С 0-С 6)алкил-NR12C(=О)NR11-(С 2-С 6)алкенила-, -(С 0-С 6)алкил-NR12C(=О)NR11-(С 3-С 7)циклоалкила-, -(С 0-С 6)алкил-NR12C(=О)NR11-(С 4-С 10)алкилциклоалкила-, -(С 0-С 6)алкил-NR11S(O)2-(С 0-С 6)алкила-, -(С 0-С 6)алкил-NR11S(O)2-(С 2-С 6)алкинила-,-(С 0-С 6)алкил-NR11S(О)2-(С 2-С 6)алкенила-, -(С 0-С 6)алкил-NR11S(O)2-(С 3-С 7)циклоалкила-, -(С 0-С 6)алкилNR11S(O)2-(С 4-С 10)алкилциклоалкила-,-(С 0-С 6)алкил-NR12C(=S)NR11-(С 0-С 6)алкила-,-(С 0-С 6)алкилNR12C(=S)NR11-(С 2-С 6)алкинила-,-(С 0-С 6)алкил-NR12C(=S)NR11-(С 2-С 6)алкенила-,-(С 0-С 6)алкилNR12C(=S)NR11-(С 3-С 7)циклоалкила-,-(С 0-С 6)алкил-NR12C(=S)NR11-(С 4-С 10)алкилциклоалкила-,-(С 0 С 6)алкил-ОС(=О)-(С 0-С 6)алкила-,-(С 0-С 6)алкил-ОС(=O)-(С 2-С 6)алкинила-,-(С 0-С 6)алкил-ОС(=О)-(С 2 С 6)алкенила-, -(С 0-С 6)алкил-ОС(=О)-(С 4-С 10)алкилциклоалкила-, -(С 0-С 6)алкил-ОС(=O)-(С 3-С 7)циклоалкила-,-8 014904X и Y не могут одновременно представлять собой химическую связь;R11 и R12 независимо друг от друга представляют собой водород, -(С 1-С 6)алкил, -(С 3-С 6)циклоалкил,-(С 3-С 7)циклоалкилалкил, -(С 2-С 6)алкенил, -(С 2-С 6)алкинил, галоген-(С 1-С 6)алкил, гетероциклоалкил,гетероарил, гетероарилалкил, арилалкил или арил; любой из которых, возможно, несет замещение 1-5 группами, каждая из которых независимо представляет собой галоген, -CN, -(С 1-С 6)алкил, -О(С 0-С 6)алкил, -О(С 3-С 7)циклоалкилалкил, -О(арил), -О(гетероарил), -NC0-С 6)алкил)С 0-С 6)алкил), -NС 0 С 6)алкил)С 3-С 7)циклоалкил) или -NС 0-С 6)алкил)(арил);J представляет собой одинарную связь, -C(R13)(R14)-, -О-, -N(R13)- или -S-;R13, R14 независимо друг от друга представляют собой водород, -(С 1-С 6)алкил, -(С 3-С 6)циклоалкил,-(С 3-С 7)циклоалкилалкил, -(С 2-С 6)алкенил, -(С 2-С 6)алкинил, галоген-(С 1-С 6)алкил, гетероарил,гетероарилалкил, арилалкил или арил; любой из которых, возможно, несет замещение 1-5 группами,каждая из которых независимо представляет собой галоген, -CN, -(С 1-С 6)алкил, -O(С 0-С 6)алкил, -О(С 3 С 7)циклоалкилалкил, -О(арил), -О(гетероарил), -NC0-С 6)алкил)С 0-С 6)алкил), -NС 0-С 6)алкил)С 3 С 7)циклоалкил) или -NС 0-С 6)алкил)(арил); любой N может представлять собой N-оксид. Настоящее изобретение охватывает оба возможных стереоизомера, а также как рацемические соединения, так и индивидуальные энантиомеры. Кроме того, предпочтительные соединения согласно настоящему изобретению представляют собой соединения формулы I-C или фармацевтически приемлемые соли, гидраты или сольваты указанных соединений,где R1 и R2 независимо друг от друга представляют собой водород, -(C1-С 6)алкил, -(С 2-С 6)алкенил,-(С 2-С 6)алкинил, арилалкил, гетероарилалкил, гидроксил, аминогруппу, аминоалкил, гидроксиалкил, (С 1-С 6)алкоксил или R1 и R2 вместе могут образовывать (С 3-С 7)циклоалкильное кольцо, карбонильную связь С=О или углерод-углеродную двойную связь; Р и Q независимо друг от друга представляют собой циклоалкильную, гетероциклоалкильную,арильную или гетероарильную группу формулы где R3, R4, R5, R6 и R7 независимо друг от друга представляют собой водород, галоген, -CN, -NO2, (С 1-С 6)алкил, -(С 3-С 6)циклоалкил, -(С 3-С 7)циклоалкилалкил, -(С 2-С 6)алкенил, -(С 2-С 6)алкинил, галоген(С 1-С 6)алкил, гетероарил, гетероарилалкил, арилалкил, арил, -OR8, -NR8R9, -C(=NR10)NR8R9,-N(=NR10)NR8R9, -NR8COR9, -NR8CO2R9, -NR8SO2R9, -NR10CONR8R9, -SR8, -S(=O)R8, -S(=O)2R8,-S(=O)2NR8R9, -C(=O)R8, -COOR8, -C(=O)NR8R9, -C(=NR8)R9 или -C(=NOR8)R9; при этом, возможно, два заместителя совместно с находящимися между ними атомами образуют бициклическое гетероциклоалкильное, арильное или гетероарильное кольцо; причем каждое кольцо, возможно,дополнительно несет замещение 1-5 группами, каждая из которых независимо представляет собой: галоген, -CN, -(С 1-С 6)алкил, -O-(С 0-С 6)алкил, -О-(С 3-С 7)циклоалкилалкил, -О(арил), -О(гетероарил), -О(С 1-С 3)алкиларил, -О-(С 1-С 3)алкилгетероарил, -N-С 0-С 6)алкил)С 0-С 3)алкиларил) или -NС 0-С 6)алкил)С 0-С 3)алкилгетероарил);R8, R9, R10 независимо друг от друга представляют собой водород, (С 1-С 6)алкил, (С 3-С 6)циклоалкил,(С 3-С 7)циклоалкилалкил, (С 2-С 6)алкенил, (С 2-С 6)алкинил, галоген-(С 1-С 6)алкил, гетероциклоалкил,гетероарил, гетероарилалкил, арилалкил или арил; любой из которых, возможно, несет замещение 1-5 группами, каждая из которых независимо представляет собой галоген, -CN, -(С 1-С 6)алкил, -О-(С 0 С 6)алкил, -О-(С 3-С 7)циклоалкилалкил, -О(арил), -О(гетероарил), -NС 0-С 6)алкил)2, -NС 0-С 6)алкил)С 3 С 7)циклоалкил) или -NС 0-С 6)алкил)(арил);D, E, F, G и Н в Р и Q независимо друг от друга представляют собой -C(R3)=, -C(R3)=C(R4)-,-C(=O)-, -C(=S)-, -О-, -N=, -N(R3)- или -S-;-9 014904 В представляет собой одинарную связь, -С(=О)-(С 0-С 2)алкил-, -С(=О)-(С 2-С 6)алкенил-, -С(=О)-(С 2 С 6)алкинил-, -С(=О)-О-, -C(=O)NR8-(C0-C2)алкил-, -С(=NR8)NR9-S(=O)-(С 0-С 2)алкил-, -S(=О)2-(С 0 С 2)алкил-,-S(=O)2NR8-(C0-C2)алкил-,C(=NR8)-(C0-С 2)алкил-,-С(=NOR8)-(С 0-С 2)алкилилиR8 и R9 независимо друг от друга представляют собой группы, определенные выше;X и Y независимо друг от друга выбирают из химической связи, -NR11C(=O)O-, возможно,замещенного -(С 1-С 6)алкила-, -(С 2-С 6)алкинила-, -(С 2-С 6)алкенила-, -(С 3-С 7)циклоалкила-, -(С 3-С 8)циклоалкенила-, -(С 1-С 6)галогеналкила-, -(С 1-С 6)цианоалкила-, -(С 0-С 6)алкил-O-(С 0-С 6)алкила-, -(С 0-С 6)алкилO-(С 2-С 6)алкинила-, -(С 0-С 6)алкил-O-(С 2-С 6)алкенила-, -(С 0-С 6)алкил-О-(С 3-С 7)циклоалкила-, -(С 0 С 6)алкил-O-(С 4-С 10)алкилциклоалкила-, -(С 0-С 6)алкил-С(=O)-(С 0-С 6)алкила-, -(С 0-С 6)алкил-С(=О)-(С 2 С 6)алкинила-, -(С 0-С 6)алкил-С(=O)-(С 2-С 6)алкенила-, -(С 0-С 6)алкил-С(=О)-(С 3-С 7)алкилциклоалкила-,-(С 0-С 6)алкил-С(=O)-(С 4-С 10)циклоалкила-, -(С 0-С 6)алкил-С(=O)O-(С 0-С 6)алкила-, -(С 0-С 6)алкил-С(=О)О(С 2-С 6)алкинила-, -(С 0-С 6)алкил-С(=О)О-(С 2-С 6)алкенила-, -(С 0-С 6)алкил-С(=O)O-(С 3-С 7)циклоалкила-,-(С 0-С 6)алкил-С(=О)О-(С 4-С 10)алкилциклоалкила-, -(С 0-С 6)алкил-С(=O)NR11-(С 0-С 6)алкила-, -(C0-C6)алкил-C(=O)NR11-(C2-С 6)алкинила-, -(C0-C6)алкил-C(=O)NR11-(C2-C6)алкенила-, -(С 0-С 6)алкил-С(=О)NR11(С 3-С 7)циклоалкила-, -(C0-C6)алкил-C(=O)NR11-(С 4-С 10)алкилциклоалкила-, -(С 0-С 6)алкил-S-(С 0-С 6)алкила-, -(С 0-С 6)алкил-S-(С 2-С 6)алкинила-, -(С 0-С 6)алкил-S-(С 2-С 6)алкенила-, -(С 0-С 6)алкил-S-(С 3-С 7)циклоалкила-, -(С 0-С 6)алкил-S-(С 4-С 10)алкилциклоалкила-, -(С 0-С 6)алкил-S(O)-(С 0-С 6)алкила-, -(С 0-С 6)алкил-О(С 2-С 6)алкинила-, -(С 0-С 6)алкил-S(O)-(С 2-С 6)алкенила-, -(С 0-С 6)алкил-S(O)-(С 3-С 7)циклоалкила-, -(С 0 С 6)алкил-S(О)-(С 4-С 10)алкилциклоалкила-, -(С 0-С 6)алкил-S(O)2-(С 0-С 6)алкила-, -(С 0-С 6)алкил-S(О)2-(С 2 С 6)алкинила-, -(С 0-С 6)алкил-S(O)2-(С 2-С 6)алкенила-, -(С 0-С 6)алкил-S(O)2-(С 3-С 7)циклоалкила-, -(С 0-С 6)алкил-S(O)2-(С 4-С 10)алкилциклоалкила-, -(С 0-С 6)алкил-S(O)2NR11-(С 0-С 6)алкила-, -(С 0-С 6)алкил-S(O)2NR11(С 2-С 6)алкинила-, -(С 0-С 6)алкил-S(O)2NR11-(С 2-С 6)алкенила-, -(С 0-С 6)алкил-S(О)2NR11-(С 3-С 7)циклоалкила-, -(С 0-С 6)алкил-S(O)2NR11-(С 4-С 10)алкилциклоалкила-, -(С 0-С 6)алкил-NR11-(С 0-С 6)алкила-, -(С 0 С 6)алкил-NR11-(С 2-С 6)алкинила-, -(С 0-С 6)алкил-NR11-(С 2-С 6)алкенила-, -(С 0-С 6)алкил-NR11-(С 3-С 7)циклоалкила-, -(С 0-С 6)алкил-NR11-(С 4-С 10)алкилциклоалкила-, -(С 0-С 6)алкил-NR11C(=О)-(С 0-С 6)алкила-, -(С 0 С 6)алкил-NR11C(=О)-(С 2-С 6)алкинила-,-(С 0-С 6)алкил-NR11C(=О)-(С 2-С 6)алкенила-,-(С 0-С 6)алкилNR11C(=О)-(С 3-С 7)циклоалкила-, -(С 0-С 6)алкил-NR11C(=O)-(С 4-С 10)алкилциклоалкила-, -(С 0-С 6)алкилNR12C(=O)NR11-(С 0-С 6)алкила-,-(C0-C6)алкил-NR12C(=O)NR11-(C2-C6)алкинила-,-(С 0-С 6)алкилNR12C(=О)NR11-(С 2-С 6)алкенила-, -(С 0-С 6)алкил-NR12C(=О)NR11-(С 3-С 7)циклоалкила-, -(С 0-С 6)алкилNR12C(=O)NR11-(С 4-С 10)алкилциклоалкила-,-(C0-C6)алкил-NR11S(O)2-(C0-C6)алкила-,-(С 0-С 6)алкилNR11S(O)2-(С 2-С 6)алкинила-, -(С 0-С 6)алкил-NR11S(O)2-(С 2-С 6)алкенила-, -(С 0-С 6)алкил-NR11S(O)2-(С 3 С 7)циклоалкила-, -(С 0-С 6)алкил-NR11S(O)2-(С 4-С 10)алкилциклоалкила-, -(С 0-С 6)алкил-NR12C(=S)NR11-(С 0 С 6)алкила-, -(С 0-С 6)алкил-NR12C(=S)NR11-(С 2-С 6)алкинила-, -(С 0-С 6)алкил-NR12C(=S)NR11-(С 2-С 6)алкенила-, -(С 0-C6)алкил-NR12C(=S)NR11-(C3-C7)циклоалкила-, -(С 0-С 6)алкил-NR12C(=S)NR11-(С 4-С 10)алкилциклоалкила-, -(С 0-С 6)алкил-ОС(=О)-(С 0-С 6)алкила-, -(С 0-С 6)алкил-ОС(=O)-(С 2-С 6)алкинила-, -(С 0 С 6)алкил-ОС(=О)-(С 2-С 6)алкенила-, -(С 0-С 6)алкил-ОС(=O)-(С 4-С 10)алкилциклоалкила-, -(С 0-С 6)алкилОС(=О)-(С 3-С 7)циклоалкила-, -(С 0-С 6)алкил-ОС(=O)NR11-(С 0-С 6)алкила-, -(С 0-С 6)алкил-ОС(=О)NR11-(С 2 С 6)алкинила-, -(С 0-С 6)алкил-ОС(=О)NR11-(С 2-С 6)алкенила-, -(С 0-С 6)алкил-ОС(=O)NR11-(С 4-С 10)алкилциклоалкила-, -(С 0-С 6)алкил-ОС(=O)NR11-(С 3-С 7)циклоалкила-, -(С 0-С 6)алкил-NR11C(=O)O-(С 0-С 6)алкила-,-(С 0-С 6)алкил-NR11C(=О)О-(С 2-С 6)алкинила-, -(С 0-С 6)алкил-NR11C(=O)O-(С 2-С 6)алкенила-, -(С 0-С 6)алкилNR11C(=О)О-(С 3-С 7)циклоалкила- или -(С 0-С 6)алкил-NR11C(=O)O-(С 4-С 10)алкилциклоалкила-;X и Y не могут одновременно представлять собой химическую связь;R11 и R12 независимо друг от друга представляют собой водород, -(С 1-С 6)алкил, -(С 3-С 6)циклоалкил,-(С 3-С 7)циклоалкилалкил, -(С 2-С 6)алкенил, -(С 2-С 6)алкинил, галоген-(С 1-С 6)алкил, гетероциклоалкил,гетероарил, гетероарилалкил, арилалкил или арил; любой из которых, возможно, несет замещение 1-5 группами, каждая из которых независимо представляет собой галоген, -CN, -(С 1-С 6)алкил, -O(С 0 С 6)алкил, -O(С 3-С 7)циклоалкилалкил, -О(арил), -О(гетероарил), -NC0-С 6)алкил)С 0-С 6)алкил), -NС 0 С 6)алкил)С 3-С 7)циклоалкил) или -NС 0-С 6)алкил)(арил);J представляет собой одинарную связь, -C(R13)(R14)-, -О-, -N(R13)- или -S-;R13, R14 независимо друг от друга представляют собой водород, -(С 1-С 6)алкил, -(С 3-С 6)циклоалкил,-(С 3-С 7)циклоалкилалкил, -(С 2-С 6)алкенил, -(С 2-С 6)алкинил, галоген-(С 1-С 6)алкил, гетероарил,гетероарилалкил, арилалкил или арил; любой из которых, возможно, несет замещение 1-5 группами,каждая из которых независимо представляет собой галоген, -CN, -(С 1-С 6)алкил, -О(С 0-С 6)алкил, -О(С 3 С 7)циклоалкилалкил, -О(арил), -О(гетероарил), -NС 0-С 6)алкил)С 0-С 6)алкил), -NС 0-С 6)алкил)С 3 С 7)циклоалкил) или -NС 0-С 6)алкил)(арил); любой N может представлять собой N-оксид. Настоящее изобретение охватывает оба возможных стереоизомера, также как рацемические соединения и индивидуальные энантиомеры.- 10014904 Далее соединение согласно настоящему изобретению представляет собой соединение формулы или фармацевтически приемлемую соль, гидрат или сольват указанного соединения,где Р и Q независимо друг от друга представляют собой циклоалкильную, гетероциклоалкильную,арильную или гетероарильную группу формулы где R3, R4, R5, R6 и R7 независимо друг от друга представляют собой водород, галоген, -CN, -NO2,-(С 1-С 6)алкил, -(С 3-С 6)циклоалкил, -(С 3-С 7)циклоалкилалкил, -(С 2-С 6)алкенил, -(С 2-С 6)алкинил, галоген(С 1-С 6)алкил, гетероарил, гетероарилалкил, арилалкил, арил, -OR8, -NR8R9, -C(=NR10)NR8R9,-N(=NR10)NR8R9, -NR8COR9, -NR8CO2R9, -NR8SO2R9, -NR10CONR8R9, -SR8, -S(=O)R8, -S(=O)2R8,-S(=O)2NR8R9, -C(=O)R8, -COOR8, -C(=O)NR8R9, -C(=NR8)R9 или -C(=NOR8)R9; при этом, возможно, два заместителя совместно с находящимися между ними атомами образуют бициклическое гетероциклоалкильное, арильное или гетероарильное кольцо; причем каждое кольцо, возможно,дополнительно несет замещение 1-5 группами, каждая из которых независимо представляет собой галоген, -CN, -(С 1-С 6)алкил, -O-(С 0-С 6)алкил, -О-(С 3-С 7)циклоалкилалкил, -О(арил), -О(гетероарил), -О(С 1-С 3)алкиларил, -О-(С 1-С 3)алкилгетероарил, -N-С 0-С 6)алкил)С 0-С 3)алкиларил) или -NС 0-С 6)алкил)С 0-С 3)алкилгетероарил);R8, R9, R10 независимо друг от друга представляют собой водород, (С 1-С 6)алкил, (С 3-С 6)циклоалкил,(С 3-С 7)циклоалкилалкил, (С 2-С 6)алкенил, (С 2-С 6)алкинил, галоген-(С 1-С 6)алкил, гетероциклоалкил,гетероарил, гетероарилалкил, арилалкил или арил; любой из которых, возможно, несет замещение 1-5 группами, каждая из которых независимо представляет собой галоген, -CN, -(С 1-С 6)алкил, -О-(С 0 С 6)алкил, -О-(С 3-С 7)циклоалкилалкил, -О(арил), -О(гетероарил), -NС 0-С 6)алкил)2, -NС 0-С 6)алкил)С 3 С 7)циклоалкил) или -NС 0-С 6)алкил)(арил);D, E, F, G и Н в Р и Q независимо друг от друга представляют собой -C(R3)=, -C(R3)=C(R4)-,-C(=O)-, -C(=S)-, -O-, -N=, -N(R3)- или -S-; В представляет собой одинарную связь, -С(=О)-(С 0-С 2)алкил-, -С(=О)-(С 2-С 6)алкенил-, -С(=О)-(С 2 С 6)алкинил-, -С(=О)-О-, -C(=O)NR8-(C0-C2)алкил-, -C(=NR8)NR9-S(=O)-(C0-C2)алкил-, -S(=O)2-(С 0 С 2)алкил-,-S(=O)2NR8-(C0-C2)алкил-,C(=NR8)-(C0-С 2)алкил-,-C(=NOR8)-(C0-C2)алкилилиR8 и R9 независимо друг от друга представляют собой группы, определенные выше;R11 и R12 независимо друг от друга представляют собой водород, -(С 1-С 6)алкил, -(С 3-С 6)циклоалкил,-(С 3-С 7)циклоалкилалкил, -(С 2-С 6)алкенил, -(С 2-С 6)алкинил, галоген-(С 1-С 6)алкил, гетероциклоалкил,гетероарил, гетероарилалкил, арилалкил или арил; любой из которых, возможно, несет замещение 1-5 группами, каждая из которых независимо представляет собой галоген, -CN, -(С 1-С 6)алкил, -О(С 0 С 6)алкил, -О(С 3-С 7)циклоалкилалкил, -О(арил), -О(гетероарил), -NC0-С 6)алкил)С 0-С 6)алкил), -NС 0 С 6)алкил)С 3-С 7)циклоалкил) или -NС 0-С 6)алкил)(арил);J представляет собой одинарную связь, -C(R13)(R14)-, -О-, -N(R13)- или -S-;R13, R14 независимо друг от друга представляют собой водород, -(С 1-С 6)алкил, -(С 3-С 6)циклоалкил,-(С 3-С 7)циклоалкилалкил, -(С 2-С 6)алкенил, -(С 2-С 6)алкинил, галоген-(С 1-С 6)алкил, гетероарил, гетероарилалкил, арилалкил или арил; любой из которых, возможно, несет замещение 1-5 группами, каждая из которых независимо представляет собой галоген, -CN, -(С 1-С 6)алкил, -О(С 0-С 6)алкил, -О(С 3-С 7)циклоалкилалкил, -О(арил), -О(гетероарил), -NС 0-С 6)алкил)С 0-С 6)алкил), -NС 0-С 6)алкил)С 3-С 7)циклоалкил) или -NС 0-С 6)алкил)(арил); любой N может представлять собой N-оксид. Настоящее изобретение охватывает оба возможных стереоизомера, также как рацемические соединения и индивидуальные энантиомеры указанных соединений. Еще в одном варианте реализации соединение согласно настоящему изобретению представлено соединением формулы (I-D) или фармацевтически приемлемой солью, гидратом или сольватом указанного соединения,где X представляет собой, возможно, замещенный -(С 1-С 6)алкил-, -(С 2-С 6)алкинил-, -(С 2 С 6)алкенил-, -(С 3-С 7)циклоалкил-, -(С 3-С 8)циклоалкенил-, -(С 1-С 6)галогеналкил-, -(С 1-С 6)цианоалкил-,-(С 0-С 6)алкил-О-(С 0-С 6)алкил-, -(С 0-С 6)алкил-O-(С 2-С 6)алкинил-, -(С 0-С 6)алкил-О-(С 2-С 6)алкенил-, -(С 0 С 6)алкил-O-(С 3-С 7)циклоалкил-, -(С 0-С 6)алкил-O-(С 4-С 10)алкилциклоалкил-, -(С 0-С 6)алкил-С(=O)-(С 0 С 6)алкил-, -(С 0-С 6)алкил-С(=O)-(С 2-С 6)алкинил-, -(С 0-С 6)алкил-С(=О)-(С 2-С 6)алкенил-, -(С 0-С 6)алкил-С(=О)(С 3-С 7)алкилциклоалкил-, -(С 0-С 6)алкил-С(=O)-(С 4-С 10)циклоалкил-, -(С 0-С 6)алкил-S-(С 0-С 6)алкил-, -(С 0-С 6)алкил-S-(С 2-С 6)алкинил-, -(С 0-С 6)алкил-S-(С 2-С 6)алкенил-, -(С 0-С 6)алкил-S-(С 3-С 7)циклоалкил-, -(С 0-С 6)алкилS-(С 4-С 10)алкилциклоалкил-, -(С 0-С 6)алкил-S(О)-(С 0-С 6)алкил-, -(С 0-С 6)алкил-O-(С 2-С 6)алкинил-, -(С 0 С 6)алкил-S(O)-(С 2-С 6)алкенил-, -(С 0-С 6)алкил-S(O)-(С 3-С 7)циклоалкил-, -(С 0-С 6)алкил-S(O)-(С 4-С 10)алкилциклоалкил-, -(С 0-С 6)алкил-S(O)2-(С 0-С 6)алкил-, -(С 0-С 6)алкил-S(О)2-(С 2-С 6)алкинил-, -(С 0-С 6)алкилS(О)2-(С 2-С 6)алкенил-,-(С 0-С 6)алкил-S(O)2-(С 3-С 7)циклоалкил-,-(С 0-С 6)алкил-S(О)2-(С 4-С 10)алкилциклоалкил-, -(С 0-С 6)алкил-NR11-(С 0-С 6)алкил-, -(С 0-С 6)алкил-NR11-(С 2-С 6)алкинил-, -(С 0-С 6)алкил-NR11(С 2-С 6)алкенил-, -(С 0-С 6)алкил-NR11-(С 3-С 7)циклоалкил- или -(С 0-С 6)алкил-NR11-(С 4-С 10)алкилциклоалкил-;R11 представляет собой водород, -(С 1-С 6)алкил, -(С 3-С 6)циклоалкил, -(С 3-С 7)циклоалкилалкил, -(С 2 С 6)алкенил, -(С 2-С 6)алкинил, галоген-(С 1-С 6)алкил, гетероциклоалкил, гетероарил, гетероарилалкил,арилалкил или арил; любой из которых, возможно, несет замещение 1-5 группами, каждая из которых независимо представляет собой галоген, -CN, -(С 1-С 6)алкил, -О(С 0-С 6)алкил, -О(С 3-С 7)циклоалкилалкил,-О(арил), -О(гетероарил), -NС 0-С 6)алкил)С 0-С 6)алкил), -NС 0-С 6)алкил)С 3-С 7)циклоалкил) или-NС 0-С 6)алкил)(арил); любой N может представлять собой N-оксид. Настоящее изобретение охватывает оба возможных стереоизомера, а также как рацемические соединения, так и индивидуальные энантиомеры указанных соединений.- 12014904 В другом своем аспекте настоящее изобретение относится к соединениям формулы II-А или фармацевтически приемлемым солям, гидратам или сольватам указанных соединений,где R1 и R2 независимо друг от друга представляют собой водород, -(C1-С 6)алкил, -(С 2-С 6)алкенил,-(С 2-С 6)алкинил, арилалкил, гетероарилалкил, гидроксил, аминогруппу, аминоалкил, гидроксиалкил,-(С 1-С 6)алкоксил или R1 и R2 вместе могут образовывать (С 3-С 7)циклоалкильное кольцо, карбонильную связь С=О или углерод-углеродную двойную связь; Р и Q независимо друг от друга представляют собой циклоалкильную, гетероциклоалкильную,арильную или гетероарильную группу формулы где R3, R4, R5, R6 и R7 независимо друг от друга представляют собой водород, галоген, -CN, -NO2,-(С 1-С 6)алкил, -(С 3-С 6)циклоалкил, -(С 3-С 7)циклоалкилалкил, -(С 2-С 6)алкенил, -(С 2-С 6)алкинил, галоген(С 1-С 6)алкил, гетероарил, гетероарилалкил, арилалкил, арил, -OR8, -NR8R9, -C(=NR10)NR8R9,-N(=NR10)NR8R9, -NR8COR9, -NR8CO2R9, -NR8SO2R9, -NR10CONR8R9, -SR8, -S(=O)R8, -S(=O)2R8,-S(=O)2NR8R9, -C(=O)R8, -COOR8, -C(=O)NR8R9, -C(=NR8)R9 или -C(=NOR8)R9; при этом, возможно, два заместителя совместно с находящимися между ними атомами образуют бициклическое гетероциклоалкильное, арильное или гетероарильное кольцо; причем каждое кольцо, возможно,дополнительно несет замещение 1-5 группами, каждая из которых независимо представляет собой галоген, -CN, -(С 1-С 6)алкил, -О-(С 0-С 6)алкил, -О-(С 3-С 7)циклоалкилалкил, -О(арил), -О(гетероарил), -O-(C1-С 3)алкиларил, -О-(С 1-С 3)алкилгетероарил, -N-С 0-С 6)алкил)С 0-С 3)алкиларил) или -NС 0-С 6)алкил)С 0-С 3)алкилгетероарил);R8, R9, R10 независимо друг от друга представляют собой водород, (С 1-С 6)алкил, (С 3-С 6)циклоалкил,(С 3-С 7)циклоалкилалкил, (С 2-С 6)алкенил, (С 2-С 6)алкинил, галоген-(С 1-С 6)алкил, гетероциклоалкил,гетероарил, гетероарилалкил, арилалкил или арил; любой из которых, возможно, несет замещение 1-5 группами, каждая из которых независимо представляет собой галоген, -CN, -(С 1-С 6)алкил, -О-(С 0 С 6)алкил, -О-(С 3-С 7)циклоалкилалкил, -О(арил), -О(гетероарил), -NС 0-С 6)алкил)2, -NС 0-С 6)алкил)С 3 С 7)циклоалкил) или -NС 0-С 6)алкил)(арил);D, E, F, G и Н в Р и Q независимо друг от друга представляют собой -C(R3)=, -C(R3)=C(R4)-,-C(=O)-, -C(=S)-, -О-, -N=, -N(R3)- или -S-; В представляет собой одинарную связь, -С(=О)-(С 0-С 2)алкил-, -С(=О)-(С 2-С 6)алкенил-, -С(=О)-(С 2 С 6)алкинил-, -С(=О)-О-, -С(=О)NR8-(С 0-С 2)алкил-, -C(=NR8)NR9-S(=O)-(C0-C2)алкил-, -S(=О)2-(С 0 С 2)алкил-,-S(=O)2NR8-(С 0-С 2)алкил-,C(=NR8)-(C0-С 2)алкил-,-C(=NOR8)-(C0-C2)алкилилиR8 и R9 независимо друг от друга представляют собой группы, определенные выше;X и Y независимо друг от друга выбирают из химической связи, -NR11C(=O)O-, возможно,замещенного -(С 1-С 6)алкила-, -(С 2-С 6)алкинила-, -(С 2-С 6)алкенила-, -(С 3-С 7)циклоалкила-, -(С 3 С 8)циклоалкенила-, -(С 1-С 6)галогеналкила-, -(С 1-С 6)цианоалкила-, -(С 0-С 6)алкил-O-(С 0-С 6)алкила-, -(С 0 С 6)алкил-O-(С 2-С 6)алкинила-, -(С 0-С 6)алкил-О-(С 2-С 6)алкенила-, -(С 0-С 6)алкил-О-(С 3-С 7)циклоалкила-,-(С 0-С 6)алкил-O-(С 4-С 10)алкилциклоалкила-, -(С 0-С 6)алкил-С(=O)-(С 0-С 6)алкила-, -(С 0-С 6)алкил-С(=О)(С 2-С 6)алкинила-, -(С 0-С 6)алкил-С(=О)-(С 2-С 6)алкенила-, -(С 0-С 6)алкил-С(=О)-(С 3-С 7)алкилциклоалкила-,-(С 0-С 6)алкил-С(=О)-(С 4-С 10)циклоалкила-, -(С 0-С 6)алкил-С(=O)O-(С 0-С 6)алкила-, -(С 0-С 6)алкил-С(=О)О(С 2-С 6)алкинила-, -(С 0-С 6)алкил-С(=О)О-(С 2-С 6)алкенила-, -(С 0-С 6)алкил-С(=О)О-(С 3-С 7)циклоалкила-,-(С 0-С 6)алкил-С(=О)О-(С 4-С 10)алкилциклоалкила-, -(С 0-С 6)алкил-С(=O)NR11-(С 0-С 6)алкила-, -(С 0-С 6)алкил-С(=O)NR11-(С 2-С 6)алкинила-, -(С 0-С 6)алкил-С(=O)NR11-(С 2-С 6)алкенила-, -(С 0-С 6)алкил-С(=О)NR11(С 3-С 7)циклоалкила-, -(С 0-С 6)алкил-С(=O)NR11-(С 4-С 10)алкилциклоалкила-, -(С 0-С 6)алкил-S-(С 0-С 6)алкила-, -(С 0-С 6)алкил-S-(С 2-С 6)алкинила-, -(С 0-С 6)алкил-S-(С 2-С 6)алкенила-, -(С 0-С 6)алкил-S-(С 3-С 7)циклоалкила-, -(С 0-С 6)алкил-S-(С 4-С 10)алкилциклоалкила-, -(С 0-С 6)алкил-S(O)-(С 0-С 6)алкила-, -(С 0-С 6)алкил-О(С 2-С 6)алкинила-, -(С 0-С 6)алкил-S(О)-(С 2-С 6)алкенила-, -(С 0-С 6)алкил-S(O)-(С 3-С 7)циклоалкила-, -(С 0 С 6)алкил-S(О)-(С 4-С 10)алкилциклоалкила-, -(С 0-С 6)алкил-S(O)2-(С 0-С 6)алкила-, -(С 0-С 6)алкил-S(О)2-(С 2 С 6)алкинила-, -(С 0-С 6)алкил-S(О)2-(С 2-С 6)алкенила-, -(С 0-С 6)алкил-S(O)2-(С 3-С 7)циклоалкила-, -(С 0-С 6)алкилS(О)2-(С 4-С 10)алкилциклоалкила-,-(С 0-С 6)алкил-S(O)2NR11-(С 0-С 6)алкила-,-(С 0-С 6)алкил-S(O)2NR11-(С 2 С 6)алкинила-, -(С 0-С 6)алкил-S(O)2NR11-(С 2-С 6)алкенила-, -(С 0-С 6)алкил-S(О)2NR11-(С 3-С 7)циклоалкила-, -(С 0- 13014904 С 6)алкил-S(О)2NR11-(С 4-С 10)алкилциклоалкила-, -(С 0-С 6)алкил-NR11-(С 0-С 6)алкила-, -(С 0-С 6)алкил-NR11-(С 2 С 6)алкинила-, -(С 0-С 6)алкил-NR11-(С 2-С 6)алкенила-, -(С 0-С 6)алкил-NR11-(С 3-С 7)циклоалкила-, -(С 0 С 6)алкил-NR11-(С 4-С 10)алкилциклоалкила-,-(С 0-С 6)алкил-NR11C(=О)-(С 0-С 6)алкила-,-(С 0-С 6)алкилNR11C(=О)-(С 2-С 6)алкинила-, -(С 0-С 6)алкил-NR11C(=O)-(С 2-С 6)алкенила-, -(С 0-С 6)алкил-NR11C(=О)-(С 3 С 7)циклоалкила-, -(С 0-С 6)алкил-NR11C(=О)-(С 4-С 10)алкилциклоалкила-, -(C0-C6)алкил-NR12C(=O)NR11(C0-С 6)алкила-, -(C0-C6)алкил-NR12C(=O)NR11-(C2-C6)алкинила-, -(С 0-С 6)алкил-NR12C(=O)NR11-(С 2-С 6)алкенила-, -(С 0-С 6)алкил-NR12C(=О)NR11-(С 3-С 7)циклоалкила-, -(С 0-С 6)алкил-NR12C(=О)NR11-(С 4-С 10)алкилциклоалкила-, -(С 0-С 6)алкил-NR11S(O)2-(С 0-С 6)алкила-, -(С 0-С 6)алкил-NR11S(О)2-(С 2-С 6)алкинила-,-(C0-C6)алкил-NR11S(O)2-(С 2-С 6)алкенила-, -(С 0-С 6)алкил-NR11S(O)2-(С 3-С 7)циклоалкила-, -(С 0-С 6)алкилNR11S(O)2-(С 4-С 10)алкилциклоалкила-,-(С 0-С 6)алкил-NR12C(=S)NR11-(C0-C6)алкила-,-(C0-C6)алкилNR12C(=S)NR11-(C2-С 6)алкинила-,-(С 0-С 6)алкил-NR12C(=S)NR11-(С 2-С 6)алкенила-,-(С 0-С 6)алкилNR12C(=S)NR11-(С 3-С 7)циклоалкила-, -(С 0-С 6)алкил-NR12C(=S)NR11-(С 4-С 10)алкилциклоалкила-, -(С 0 С 6)алкил-ОС(=O)-(С 0-С 6)алкила-, -(С 0-С 6)алкил-ОС(=О)-(С 2-С 6)алкинила-, -(С 0-С 6)алкил-ОС(=О)-(С 2 С 6)алкенила-, -(С 0-С 6)алкил-ОС(=О)-(С 4-С 10)алкилциклоалкила-, -(С 0-С 6)алкил-ОС(=O)-(С 3-С 7)циклоалкила-, -(С 0-С 6)алкил-ОС(=О)NR11-(С 0-С 6)алкила-, -(С 0-С 6)алкил-ОС(=О)NR11-(С 2-С 6)алкинила-, -(С 0 С 6)алкил-ОС(=O)NR11-(С 2-С 6)алкенила-, -(С 0-С 6)алкил-ОС(=O)NR11-(С 4-С 10)алкилциклоалкила-, -(С 0 С 6)алкил-ОС(=O)NR11-(С 3-С 7)циклоалкила-, -(С 0-С 6)алкил-NR11C(=O)O-(С 0-С 6)алкила-, -(С 0-С 6)алкилNR11C(=О)О-(С 2-С 6)алкинила-, -(С 0-С 6)алкил-NR11C(=O)O-(С 2-С 6)алкенила-, -(C0-C6)алкил-NR11C(=O)O(C3-C7)циклоалкила- или -(С 0-С 6)алкил-NR11C(=O)O-(С 4-С 10)алкилциклоалкила-;X и Y не могут одновременно представлять собой химическую связь;R11 и R12 независимо друг от друга представляют собой водород, -(С 1-С 6)алкил, -(С 3-С 6)циклоалкил,-(С 3-С 7)циклоалкилалкил, -(С 2-С 6)алкенил, -(С 2-С 6)алкинил, галоген-(С 1-С 6)алкил, гетероциклоалкил,гетероарил, гетероарилалкил, арилалкил или арил; любой из которых, возможно, несет замещение 1-5 группами, каждая из которых независимо представляет собой галоген, -CN, -(С 1-С 6)алкил, -О(С 0 С 6)алкил, -О(С 3-С 7)циклоалкилалкил, -О(арил), -О(гетероарил), -NC0-С 6)алкил)С 0-С 6)алкил), -NС 0 С 6)алкил)С 3-С 7)циклоалкил) или -NС 0-С 6)алкил)(арил);J представляет собой одинарную связь, -C(R13)(R14)-, -О-, -N(R13)- или -S-;R13, R14 независимо друг от друга представляют собой водород, -(С 1-С 6)алкил, -(С 3-С 6)циклоалкил,-(С 3-С 7)циклоалкилалкил, -(С 2-С 6)алкенил, -(С 2-С 6)алкинил, галоген-(С 1-С 6)алкил, гетероарил, гетероарилалкил, арилалкил или арил; любой из которых, возможно, несет замещение 1-5 группами, каждая из которых независимо представляет собой галоген, -CN, -(С 1-С 6)алкил, -О(С 0-С 6)алкил, -О(С 3-С 7)циклоалкилалкил, -О(арил), -О(гетероарил), -NС 0-С 6)алкил)С 0-С 6)алкил), -NС 0-С 6)алкил)С 3-С 7)циклоалкил) или -NС 0-С 6)алкил)(арил); любой N может представлять собой N-оксид. Настоящее изобретение охватывает оба возможных стереоизомера, а также как рацемические соединения, так и индивидуальные энантиомеры указанных соединений. Еще один вариант реализации настоящего изобретения составляют соединения формулы II-В или фармацевтически приемлемые соли, гидраты или сольваты указанных соединений,где Р и Q независимо друг от друга представляют собой циклоалкильную, гетероциклоалкильную,арильную или гетероарильную группу формулы где R3, R4, R5, R6 и R7 независимо друг от друга представляют собой водород, галоген, -CN, -NO2,-(С 1-С 6)алкил, -(С 3-С 6)циклоалкил, -(С 3-С 7)циклоалкилалкил, -(С 2-С 6)алкенил, -(С 2-С 6)алкинил, галоген(С 1-С 6)алкил, гетероарил, гетероарилалкил, арилалкил, арил, -OR8, -NR8R9, -C(=NR10)NR8R9,-N(=NR10)NR8R9, -NR8COR9, -NR8CO2R9, -NR8SO2R9, -NR10CONR8R9, -SR8, -S(=O)R8, -S(=O)2R8,-S(=O)2NR8R9, -C(=O)R8, -COOR8, -C(=O)NR8R9, -C(=NR8)R9 или -C(=NOR8)R9; при этом, возможно, два заместителя совместно с находящимися между ними атомами образуют бициклическое гетероциклоалкильное, арильное или гетероарильное кольцо; причем каждое кольцо, возможно,дополнительно несет замещение 1-5 группами, каждая из которых независимо представляет собой галоген, -CN, -(С 1-С 6)алкил, -O-(С 0-С 6)алкил, -О-(С 3-С 7)циклоалкилалкил, -О(арил), -О(гетероарил), -О(С 1-С 3)алкиларил, -О-(С 1-С 3)алкилгетероарил, -N-С 0-С 6)алкил)С 0-С 3)алкиларил) или -NС 0-С 6)ал- 14014904 кил)С 0-С 3)алкилгетероарил);R8, R9, R10 независимо друг от друга представляют собой водород, (С 1-С 6)алкил, (С 3-С 6)циклоалкил,(С 3-С 7)циклоалкилалкил, (С 2-С 6)алкенил, (С 2-С 6)алкинил, галоген-(С 1-С 6)алкил, гетероциклоалкил,гетероарил, гетероарилалкил, арилалкил или арил; любой из которых, возможно, несет замещение 1-5 группами, каждая из которых независимо представляет собой галоген, -CN, -(С 1-С 6)алкил, -О-(С 0 С 6)алкил, -О-(С 3-С 7)циклоалкилалкил, -О(арил), -О(гетероарил), -NС 0-С 6)алкил)2, -NС 0-С 6)алкил)С 3 С 7)циклоалкил) или -NС 0-С 6)алкил)(арил);D, E, F, G и Н в Р и Q независимо друг от друга представляют собой -C(R3)=, -C(R3)=C(R4)-,-C(=O)-, -C(=S)-, -О-, -N=, -N(R3)- или -S-; В представляет собой одинарную связь, -С(=O)-(С 0-С 2)алкил-, -С(=О)-(С 2-С 6)алкенил-, -С(=О)-(С 2 С 6)алкинил-, -С(=О)-О-, -C(=O)NR8-(C0-C2)алкил-, -C(=NR8)NR9-S(=O)-(C0-C2)алкил-, -S(=O)2-(С 0 С 2)алкил-,-S(=O)2NR8-(С 0-С 2)алкил-,C(=NR8)-(C0-С 2)алкил-,-C(=NOR8)-(C0-C2)алкилилиR8 и R9 независимо друг от друга представляют собой группы, определенные выше;R11 и R12 независимо друг от друга представляют собой водород, -(С 1-С 6)алкил, -(С 3-С 6)циклоалкил,-(С 3-С 7)циклоалкилалкил, -(С 2-С 6)алкенил, -(С 2-С 6)алкинил, галоген-(С 1-С 6)алкил, гетероциклоалкил,гетероарил, гетероарилалкил, арилалкил или арил; любой из которых, возможно, несет замещение 1-5 группами, каждая из которых независимо представляет собой галоген, -CN, -(С 1-С 6)алкил, -O(С 0 С 6)алкил, -О(С 3-С 7)циклоалкилалкил, -О(арил), -О(гетероарил), -NC0-С 6)алкил)С 0-С 6)алкил), -NС 0 С 6)алкил)С 3-С 7)циклоалкил) или -NС 0-С 6)алкил)(арил);J представляет собой одинарную связь, -C(R13)(R14)-, -О-, -N(R13)- или -S-;R13, R14 независимо друг от друга представляют собой водород, -(С 1-С 6)алкил, -(С 3-С 6)циклоалкил,-(С 3-С 7)циклоалкилалкил, -(С 2-С 6)алкенил, -(С 2-С 6)алкинил, галоген-(С 1-С 6)алкил, гетероарил,гетероарилалкил, арилалкил или арил; любой из которых, возможно, несет замещение 1-5 группами,каждая из которых независимо представляет собой галоген, -CN, -(С 1-С 6)алкил, -O(С 0-С 6)алкил, -О(С 3 С 7)циклоалкилалкил, -О(арил), -О(гетероарил), -NС 0-С 6)алкил)С 0-С 6)алкил), -NС 0-С 6)алкил)С 3- 15014904 С 7)циклоалкил) или -NС 0-С 6)алкил)(арил); любой N может представлять собой N-оксид. Настоящее изобретение охватывает оба возможных стереоизомера, а также включает как рацемические соединения, так и индивидуальные энантиомеры указанных соединений. Другой вариант реализации настоящего изобретения охватывает соединения формулы II-B,где X представляет собой, возможно, замещенный -(С 1-С 6)алкил-, -(С 2-С 6)алкинил-, -(С 2 С 6)алкенил-, -(С 3-С 7)циклоалкил-, -(С 3-С 8)циклоалкенил-, -(С 1-С 6)галогеналкил-, -(С 1-С 6)цианоалкил-, (С 0-С 6)алкил-O-(С 0-С 6)алкил-, -(С 0-С 6)алкил-O-(С 2-С 6)алкинил-, -(С 0-С 6)алкил-О-(С 2-С 6)алкенил-, -(С 0 С 6)алкил-O-(С 3-С 7)циклоалкил-, -(С 0-С 6)алкил-O-(С 4-С 10)алкилциклоалкил-, -(С 0-С 6)алкил-С(=O)-(С 0 С 6)алкил-, -(С 0-С 6)алкил-С(=О)-(С 2-С 6)алкинил-, -(С 0-С 6)алкил-С(=О)-(С 2-С 6)алкенил-, -(С 0-С 6)алкилС(=O)-(С 3-С 7)алкилциклоалкил-, -(С 0-С 6)алкил-С(=O)-(С 4-С 10)циклоалкил-, -(С 0-С 6)алкил-S-(С 0-С 6)алкил-, (С 0-С 6)алкил-S-(С 2-С 6)алкинил-, -(С 0-С 6)алкил-S-(С 2-С 6)алкенил-, -(С 0-С 6)алкил-S-(С 3-С 7)циклоалкил-, -(С 0 С 6)алкил-S-(С 4-С 10)алкилциклоалкил-, -(С 0-С 6)алкил-S(O)-(С 0-С 6)алкил-, -(С 0-С 6)алкил-O-(С 2-С 6)алкинил-, (С 0-С 6)алкил-S(О)-(С 2-С 6)алкенил-,-(С 0-С 6)алкил-S(O)-(С 3-С 7)циклоалкил-,-(С 0-С 6)алкил-S(О)-(С 4 С 10)алкилциклоалкил-, -(С 0-С 6)алкил-S(O)2-(С 0-С 6)алкил-, -(С 0-С 6)алкил-S(O)2-(С 2-С 6)алкинил-, -(С 0 С 6)алкил-S(О)2-(С 2-С 6)алкенил-,-(С 0-С 6)алкил-S(О)2-(С 3-С 7)циклоалкил-,-(С 0-С 6)алкил-S(О)2-(С 4 С 10)алкилциклоалкил-, -(С 0-С 6)алкил-NR11-(С 0-С 6)алкил-, -(С 0-С 6)алкил-NR11-(С 2-С 6)алкинил-, -(С 0 С 6)алкил-NR11-(С 2-С 6)алкенил-, -(С 0-С 6)алкил-NR11-(С 3-С 7)циклоалкил- или -(С 0-С 6)алкил-NR11-(С 4 С 10)алкилциклоалкил-;R11 представляет собой водород, -(С 1-С 6)алкил, -(С 3-С 6)циклоалкил, -(С 3-С 7)циклоалкилалкил, -(С 2 С 6)алкенил, -(С 2-С 6)алкинил, галоген-(С 1-С 6)алкил, гетероциклоалкил, гетероарил, гетероарилалкил,арилалкил или арил; любой из которых, возможно, несет замещение 1-5 группами, каждая из которых независимо представляет собой галоген, -CN, -(С 1-С 6)алкил, -О(С 0-С 6)алкил, -О(С 3-С 7)циклоалкилалкил,-О(арил), -О(гетероарил), -NС 0-С 6)алкил)С 0-С 6)алкил), -NС 0-С 6)алкил)С 3-С 7)циклоалкил) или-NС 0-С 6)алкил)(арил); любой N может представлять собой N-оксид. Настоящее изобретение охватывает оба возможных стереоизомера, а также как рацемические соединения, так и индивидуальные энантиомеры указанных соединений. Еще один вариант реализации настоящего изобретения относится к соединениям формулы III-А или фармацевтически приемлемым солям, гидратам или сольватам указанных соединений,где Р и Q независимо друг от друга представляют собой циклоалкильную, гетероциклоалкильную,арильную или гетероарильную группу формулы где R3, R4, R5, R6 и R7 независимо друг от друга представляют собой водород, галоген, -CN, -NO2,-(С 1-С 6)алкил, -(С 3-С 6)циклоалкил, -(С 3-С 7)циклоалкилалкил, -(С 2-С 6)алкенил, -(С 2-С 6)алкинил, галоген(С 1-С 6)алкил, гетероарил, гетероарилалкил, арилалкил, арил, -OR8, -NR8R9, -C(=NR10)NR8R9,-N(=NR10)NR8R9, -NR8COR9, -NR8CO2R9, -NR8SO2R9, -NR10CONR8R9, -SR8, -S(=O)R8, -S(=O)2R8,-S(=O)2NR8R9, -C(=O)R8, -COOR8, -C(=O)NR8R9, -C(=NR8)R9 или -C(=NOR8)R9; при этом, возможно, два заместителя совместно с находящимися между ними атомами образуют бициклическое гетероциклоалкильное, арильное или гетероарильное кольцо; причем каждое кольцо, возможно,дополнительно несет замещение 1-5 группами, каждая из которых независимо представляет собой галоген, -CN, -(С 1-С 6)алкил, -О-(С 0-С 6)алкил, -О-(С 3-С 7)циклоалкилалкил, -О(арил), -О(гетероарил), -О(С 1-С 3)алкиларил, -О-(С 1-С 3)алкилгетероарил, -N-С 0-С 6)алкил)С 0-С 3)алкиларил) или -NС 0-С 6)алкил)С 0-С 3)алкилгетероарил);R8, R9, R10 независимо друг от друга представляют собой водород, (С 1-С 6)алкил, (С 3-С 6)циклоалкил,(С 3-С 7)циклоалкилалкил, (С 2-С 6)алкенил, (С 2-С 6)алкинил, галоген-(С 1-С 6)алкил, гетероциклоалкил,гетероарил, гетероарилалкил, арилалкил или арил; любой из которых, возможно, несет замещение 1-5 группами, каждая из которых независимо представляет собой галоген, -CN, -(С 1-С 6)алкил, -O-(С 0-С 6)алкил, -О-(С 3-С 7)циклоалкилалкил, -О(арил), -O(гетероарил), -NС 0-С 6)алкил)2, -NС 0-С 6)алкил)С 3 С 7)циклоалкил) или -NС 0-С 6)алкил)(арил);D, E, F, G и Н в Р и Q независимо друг от друга представляют собой -C(R3)=, -C(R3)=C(R4)-,- 16014904-С(=О)-, -C(=S)-, -О-, -N=, -N(R3)- или -S-; В представляет собой одинарную связь, -С(=О)-(С 0-С 2)алкил-, -С(=О)-(С 2-С 6)алкенил-, -С(=О)-(С 2 С 6)алкинил-, -С(=О)-О-, -C(=O)NR8-(C0-C2)алкил-, -C(=NR8)NR9-S(=O)-(C0-C2)алкил-, -S(=О)2-(С 0 С 2)алкил-,-S(=О)2NR8-(С 0-С 2)алкил-,C(=NR8)-(C0-С 2)алкил-,-С(=NOR8)-(С 0-С 2)алкилилиR8 и R9 независимо друг от друга представляют собой группы, определенные выше;R11 и R12 независимо друг от друга представляют собой водород, -(С 1-С 6)алкил, -(С 3-С 6)циклоалкил,-(С 3-С 7)циклоалкилалкил, -(С 2-С 6)алкенил, -(С 2-С 6)алкинил, галоген-(С 1-С 6)алкил, гетероциклоалкил,гетероарил, гетероарилалкил, арилалкил или арил; любой из которых, возможно, несет замещение 1-5 группами, каждая из которых независимо представляет собой галоген, -CN, -(С 1-С 6)алкил, -O(С 0 С 6)алкил, -O(С 3-С 7)циклоалкилалкил, -О(арил), -О(гетероарил), -NC0-С 6)алкил)С 0-С 6)алкил), -NС 0 С 6)алкил)С 3-С 7)циклоалкил) или -NС 0-С 6)алкил)(арил);J представляет собой одинарную связь, -C(R13)(R14)-, -О-, -N(R13)- или -S-;R13, R14 независимо друг от друга представляют собой водород, -(С 1-С 6)алкил, -(С 3-С 6)циклоалкил,-(С 3-С 7)циклоалкилалкил, -(С 2-С 6)алкенил, -(С 2-С 6)алкинил, галоген-(С 1-С 6)алкил, гетероарил,гетероарилалкил, арилалкил или арил; любой из которых, возможно, несет замещение 1-5 группами,каждая из которых независимо представляет собой галоген, -CN, -(С 1-С 6)алкил, -О(С 0-С 6)алкил, -О(С 3 С 7)циклоалкилалкил, -О(арил), -О(гетероарил), -NС 0-С 6)алкил)С 0-С 6)алкил), -NС 0-С 6)алкил)С 3 С 7)циклоалкил) или -NС 0-С 6)алкил)(арил); любой N может представлять собой N-оксид. Настоящее изобретение охватывает оба возможных стереоизомера, а также как рацемические соединения, так и индивидуальные энантиомеры. Еще один вариант реализации настоящего изобретения включает соединения формулы IV-A или фармацевтически приемлемые соли, гидраты или сольваты указанных соединений,где Р и Q независимо друг от друга представляют собой циклоалкильную, гетероциклоалкильную,арильную или гетероарильную группу формулы где R3, R4, R5, R6 и R7 независимо друг от друга представляют собой водород, галоген, -CN, -NO2,-(С 1-С 6)алкил, -(С 3-С 6)циклоалкил, -(С 3-С 7)циклоалкилалкил, -(С 2-С 6)алкенил, -(С 2-С 6)алкинил, галоген(С 1-С 6)алкил, гетероарил, гетероарилалкил, арилалкил, арил, -OR8, -NR8R9, -C(=NR10)NR8R9,-N(=NR10)NR8R9, -NR8COR9, -NR8CO2R9, -NR8SO2R9, -NR10CONR8R9, -SR8, -S(=O)R8, -S(=O)2R8,-S(=O)2NR8R9, -C(=O)R8, -COOR8, -C(=O)NR8R9, -C(=NR8)R9 или -C(=NOR8)R9; при этом, возможно, два заместителя совместно с находящимися между ними атомами образуют бициклическое гетероциклоалкильное, арильное или гетероарильное кольцо; причем каждое кольцо, возможно,дополнительно несет замещение 1-5 группами, каждая из которых независимо представляет собой галоген, -CN, -(С 1-С 6)алкил, -O-(С 0-С 6)алкил, -О-(С 3-С 7)циклоалкилалкил, -О(арил), -О(гетероарил), -О(С 1-С 3)алкиларил, -О-(С 1-С 3)алкилгетероарил, -N-С 0-С 6)алкил)С 0-С 3)алкиларил) или -NС 0-С 6)ал- 17014904 кил)С 0-С 3)алкилгетероарил);R8, R9, R10 независимо друг от друга представляют собой водород, (С 1-С 6)алкил, (С 3-С 6)циклоалкил,(С 3-С 7)циклоалкилалкил, (С 2-С 6)алкенил, (С 2-С 6)алкинил, галоген-(С 1-С 6)алкил, гетероциклоалкил,гетероарил, гетероарилалкил, арилалкил или арил; любой из которых, возможно, несет замещение 1-5 группами, каждая из которых независимо представляет собой галоген, -CN, -(С 1-С 6)алкил, -О-(С 0 С 6)алкил, -О-(С 3-С 7)циклоалкилалкил, -О(арил), -О(гетероарил), -NС 0-С 6)алкил)2, -NС 0-С 6)алкил)С 3 С 7)циклоалкил) или -NС 0-С 6)алкил)(арил);D, E, F, G и Н в Р и Q независимо друг от друга представляют собой -C(R3)=, -C(R3)=C(R4)-,-C(=O)-, -C(=S)-, -О-, -N=, -N(R3)- или -S-; В представляет собой одинарную связь, -С(=О)-(С 0-С 2)алкил-, -С(=О)-(С 2-С 6)алкенил-, -С(=О)-(С 2 С 6)алкинил-, -С(=О)-О-, -C(=O)NR8-(C0-C2)алкил-, -C(=NR8)NR9-S(=O)-(C0-C2)алкил-, -S(=О)2-(С 0 С 2)алкил-,-S(=O)2NR8-(C0-C2)алкил-,C(=NR8)-(C0-С 2)алкил-,-С(=NOR8)-(С 0-С 2)алкилилиR8 и R9 независимо друг от друга представляют собой группы, определенные выше;R11 и R12 независимо друг от друга представляют собой водород, -(С 1-C6)алкил, -(С 3-C6)циклоалкил,-(С 3-С 7)циклоалкилалкил, -(С 2-С 6)алкенил, -(С 2-С 6)алкинил, галоген-(С 1-С 6)алкил, гетероциклоалкил,гетероарил, гетероарилалкил, арилалкил или арил; любой из которых, возможно, несет замещение 1-5 группами, каждая из которых независимо представляет собой галоген, -CN, -(С 1-С 6)алкил, -О(С 0 С 6)алкил, -О(С 3-С 7)циклоалкилалкил, -О(арил), -О(гетероарил), -NC0-C6)алкил)С 0-C6)алкил), -NС 0C6)алкил)С 3-С 7)циклоалкил) или -NС 0-С 6)алкил)(арил);J представляет собой одинарную связь, -C(R13)(R14)-, -О-, -N(R13)- или -S-;R13, R14 независимо друг от друга представляют собой водород, -(С 1-C6)алкил, -(С 3-C6)циклоалкил,-(С 3-С 7)циклоалкилалкил, -(С 2-C6)алкенил, -(С 2-C6)алкинил, галоген-(С 1-С 6)алкил, гетероарил,гетероарилалкил, арилалкил или арил; любой из которых, возможно, несет замещение 1-5 группами,каждая из которых независимо представляет собой галоген, -CN, -(С 1-С 6)алкил, -О(С 0-С 6)алкил, -О(С 3 С 7)циклоалкилалкил, -О(арил), -О(гетероарил), -NС 0-С 6)алкил)С 0-С 6)алкил), -NС 0-C6)алкил)С 3- 18014904 С 7)циклоалкил) или -NС 0-C6)алкил)(арил);R15 представляет собой водород, -(С 1-С 6)алкил, -(С 3-С 6)циклоалкил, -(С 3-С 7)циклоалкилалкил, -(С 2 С 6)алкенил, -(С 2-С 6)алкинил, галоген-(С 1-C6)алкил, гетероциклоалкил, гетероарил, гетероарилалкил,арилалкил или арил; любой из которых, возможно, несет замещение 1-5 группами, каждая из которых независимо представляет собой галоген, -CN, -(С 1-C6)алкил, -О(С 0-C6)алкил, -О(С 3-С 7)циклоалкилалкил,-О(арил), -О(гетероарил), -NC0-C6)алкил)С 0-С 6)алкил), -NС 0-C6)алкил)С 3-С 7)циклоалкил) или-NС 0-C6)алкил)(арил); любой N может представлять собой N-оксид. Настоящее изобретение охватывает оба возможных стереоизомера, а также включает как рацемические соединения, так и индивидуальные энантиомеры указанных соединений. Особенно предпочтительными соединениями являются(S)-3-[3-(3-фторфенокси)-[1,2,4]оксадиазол-5-ил]пиперидин-1-илтиазол-5-илметанон,(S)-3-[3-(3-фторфенокси)-[1,2,4]оксадиазол-5-ил]пиперидин-1-ил-(6-фторпиридин-3-ил)метанон,(S)-3-[3-(3-фторфенокси)-[1,2,4]оксадиазол-5-ил]пиперидин-1-илпиридин-2-илметанон,(S)-3-[3-(3-фторфенокси)-[1,2,4]оксадиазол-5-ил]пиперидин-1-илфенилметанон,(4-хлорфенил)-(S)-3-[3-(3-фторфенокси)-[1,2,4]оксадиазол-5-ил]пиперидин-1-илметанон,(S)-3-[3-(3-фторфенокси)-[1,2,4]оксадиазол-5-ил]пиперидин-1-ил-(4-метоксифенил)метанон,(3,4-дихлорфенил)-(S)-3-[3-(3-фторфенокси)-[1,2,4]оксадиазол-5-ил]пиперидин-1-илметанон,(S)-3-[3-(3-фторфенокси)-[1,2,4]оксадиазол-5-ил]пиперидин-1-ил-(3-метоксифенил)метанон,(S)-3-[3-(3-фторфенокси)-[1,2,4]оксадиазол-5-ил]пиперидин-1-ил-о-толилметанон,(S)-3-[3-(3-фторфенокси)-[1,2,4]оксадиазол-5-ил]пиперидин-1-ил-(2-фторфенил)метанон,(S)-3-[3-(3-фторфенокси)-[1,2,4]оксадиазол-5-ил]пиперидин-1-ил-(3-фторфенил)метанон,(S)-3-[3-(3-фторфенокси)-[1,2,4]оксадиазол-5-ил]пиперидин-1-илпиридин-3-илметанон,(S)-3-[3-(3-фторфенокси)-[1,2,4]оксадиазол-5-ил]пиперидин-1-илпиридин-4-илметанон,(S)-3-[3-(3-фторфенокси)-[1,2,4]оксадиазол-5-ил]пиперидин-1-ил-(3,5-диметилизоксазол-4 ил)метанон. Настоящее изобретение относится к фармацевтически приемлемым солям, образованным присоединением кислот к соединениям формулы I или к фармацевтически приемлемым носителям или разбавителям. Настоящее изобретение относится к способу лечения или предотвращения состояния у млекопитающего, включая человека, лечение или предотвращение которого обеспечивают или облегчает посредством нейромодуляторного действия аллостерических модуляторов mGluR5 и, в частности,положительных аллостерических модуляторов. Настоящее изобретение относится к способу лечения или предотвращения различных расстройств периферической и центральной нервной системы, таких как толерантность или зависимость, тревога,депрессия, психиатрическое заболевание, такое как психоз, воспалительная или нейропатическая боль,ухудшение памяти, болезнь Альцгеймера, ишемия, злоупотребление и склонность к наркотикам, как описано в приложенной формуле изобретения. Настоящее изобретение относится к фармацевтическим композициям, которые обеспечивают от примерно 0,01 до 1000 мг активного компонента на отдельную дозу. Указанные композиции можно вводить любым подходящим способом. Например, перорально в форме капсул или таблеток,парентерально в форме растворов для инъекций, поверхностно в форме мазей или лосьонов, через глаза в форме глазной примочки, ректально в форме суппозиториев. Фармацевтические композиции согласно настоящему изобретению можно изготовить общепринятыми в данной области способами; тип применяемых фармацевтических композиций может зависеть от выбранного способа введения. Общая суточная доза обычно находится в пределах от примерно 0,05 до 2000 мг. Способы синтеза Соединения общей формулы I можно получить способами, известными в области органического синтеза, как это частично описано в следующих схемах синтеза. Во всех описанных ниже схемах следует понимать, что для чувствительных или реакционноспособных групп в случае необходимости применяют защитные группы в соответствии с общими принципами химии. На защитные группы воздействуют в соответствии со стандартными способами органического синтеза (Green T.W. and Wuts P.G.M. (1991)Protecting Groups in Organic Synthesis, John Wiley et Sons). Указанные группы удаляют на подходящей стадии синтеза соединения с применением способов, очевидных для специалистов в данной области. Выбор процесса, как и условий реакции и порядка их выполнения, должен соответствовать приготовлению соединений формулы I. Соединения формулы I могут быть представлены в виде смеси энантиомеров, которую можно разделить на индивидуальные чистые R- или S-энантиомеры. Если, например, желательно получить конкретный энантиомер соединения формулы I, его можно получить путем асимметрического синтеза или получением с применением хирального вспомогательного вещества, при этом разделяют полученную смесь диастереомеров и удаляют вспомогательную группу, чтобы получить требуемые энантиомеры в очищенном виде. Как вариант, если молекула содержит основную функциональную группу, такую как аминогруппа, или кислотную функциональную группу, такую как карбоксил,указанное разделение легко можно осуществить путем фракционной кристаллизации из различных растворителей солей соединений формулы I с оптически активными кислотами или другими известными в литературе способами, например хиральной колоночной хроматографией. Разделение конечного продукта и промежуточного или исходного вещества можно осуществлять любым подходящим способом, известным в данной области, как описано Eliel E.L., Wilen S.H. andMander L.N. (1984) Stereochemistry of Organic Compounds, Wiley-Interscience. Множество гетероциклических соединений формулы I можно получить, используя широко известные в данной области синтетические подходы (Katrizky A.R. and. Rees C.W. (1984) Comprehensive- 20014904 Продукт реакции можно выделить и очистить, применяя стандартные методики, такие как экстракция, хроматография, кристаллизация, перегонка или подобные им. Соединения формулы I-A, в которых W представляет собой 3-замещенное пиперидиновое кольцо,можно получить в соответствии с последовательностью синтеза, показанной на схемах 1-4. При этом Р и Q независимо друг от друга представляют собой арил или гетероарил, как описано выше;X представляет собой СН 2; В представляет собой -С(=О)-(С 0-С 2)алкил-;-S(=О)2-(С 0-С 2)алкил-. Исходное вещество амидоксим можно получить способами, известными в органическом синтезе,как это частично описывает следующая схема 1 синтеза. Схема 1 В свою очередь, проводят реакцию нитрильного производного (например, 4-фторбензонитрил) с гидроксиламином в нейтральной или щелочной среде, таким как триэтиламин, диизопропилэтиламин,карбонат натрия, гидроксид натрия, или аналогичным, в подходящем растворителе (например,метиловый спирт, этиловый спирт). Реакцию, как правило, проводят при медленном повышении температуры реакционной смеси от комнатной температуры до температуры в диапазоне от 70 до 80 С включительно за время в диапазоне от примерно 1 до 48 ч включительно (см., например, Lucca, GeorgeCommun.; EN; 28; 23; 1998; 4419-4430 и см. Sendzik, Martin; Hui, Hon C.; Tetrahedron Lett.; EN; 44; 2003; 8697-8700 и приведенные здесь ссылки на реакцию в нейтральной среде). Схема 2 Замещенное производное амидоксима (описанное на схеме 1) можно превратить в производное ациламидоксима с применением способа, приведенного на схеме 2. На схеме 2 PG1 представляет собой аминозащитную группу, такую как трет-бутилоксикарбонил, бензилоксикарбонил, этоксикарбонил,бензил, или аналогичную. Реакцию сочетания можно ускорить при помощи агентов сочетания,известных в области органического синтеза, таких как КДИ (1-(3-диметиламинопропил)-3 этилкарбодиимид), ДЦК (N,N'-дициклогексилкарбодиимид), в присутствии подходящего основания,такого как триэтиламин, диизопропилэтиламин, в подходящем растворителе (например,тетрагидрофуран, дихлорметан, N,N-диметилформамид, диоксан). Обычно в реакционной смеси может также присутствовать сокатализатор, такой как НОВТ (гидроксибензотриазол), НОАТ (1-гидрокси-7 азабензотриазол). Реакцию обычно проводят в температурном диапазоне от комнатной температуры до 60 С включительно на протяжении промежутка времени от примерно 2 до 12 ч, чтобы получить промежуточное соединение ациламидоксим. Реакцию циклизации можно вызвать термически в диапазоне температур от примерно 80 до примерно 150 С на протяжении интервала времени от примерно 2 до 18 ч (см., например, Suzuki, Takeshi; Iwaoka, Kiyoshi; Imanishi, Naoki; Nagakura, Yukinori;Miyata, Keiji; et al.; Chem. Pharm. Bull.; EN; 47; 1; 1999; 120-122). Продукт реакции можно выделить и очистить с применением стандартных методик, таких как экстракция, хроматография, кристаллизация,перегонка, или аналогичных. Конечную стадию можно осуществлять либо способом, описанным на схеме 3, либо способом,описанным на схеме 4. Схема 3 Как показано на схеме 3, защитные группы PG1 удаляют с применением стандартных способов. На схеме 3, где В определено выше, X представляет собой галоген, например, проводят реакцию- 21014904 производного пиперидина с арил- или гетероарилацилхлоридом с применением способа, легко понятного специалисту. Реакцию можно ускорить при помощи основания, такого как триэтиламин,диизопропиламин, пиридин, в подходящем растворителе (например, тетрагидрофуран, дихлорметан). Реакцию обычно проводят при медленном повышении температуры реакционной смеси от 0 С до комнатной температуры в течение промежутка времени от примерно 4 до 12 ч. Схема 4 Как показано на схеме 4, защитные группы PG1 удаляют с применением стандартных способов. Реакцию сочетания можно ускорить при помощи агентов сочетания, известных в области органического синтеза, таких как КДИ (1-(3-диметиламинопропил)-3-этилкарбодиимид), ДЦК (N,N'-дициклогексилкарбодиимид), или при помощи агентов сочетания на полимерном носителе, таких как карбодиимид на полимерном носителе (PS-DCC, ex Argonaut Technologies), в присутствии подходящего основания,такого как триэтиламин, диизопропилэтиламин, в подходящем растворителе (например,тетрагидрофуран, дихлорметан, N,N-диметилформамид, диоксан). Обычно в реакционной смеси может также присутствовать сокатализатор, такой как НОВТ (гидроксибензотриазол), НОАТ (1-гидрокси-7 азабензотриазол). Реакцию обычно проводят при комнатной температуре на протяжении интервала времени от примерно 2 до 12 ч. Соединения формулы II-B, в которых W представляет собой 3-замещенное пиперидиновое кольцо,можно получить в соответствии с последовательностью реакций синтеза, приведенной на схеме 5. При этом Р и Q независимо друг от друга представляют собой арил или гетероарил, как описано выше;X представляет собой СН 2, О, S; В представляет собой -С(=О)-С 0-С 2-алкил-. Оксадиазольное кольцо, описанное ниже, получают в соответствии с путями синтеза, хорошо известными в данной области (Katrizky A.R. and Rees W.C. (1984) Comprehensive Heterocyclic Chemistry,Pergamon Press). Схема 5 Проводят реакцию исходного нитрильного производного, полученного, как описано в Eur. J. Med.Chem., 1984, 19, 181-186, с гидроксиламином в нейтральной или щелочной среде, таким как триэтиламин, диизопропилэтиламин, карбонат натрия, гидроксид натрия, или аналогичным, в подходящем растворителе (например, таком как метиловый спирт или этиловый спирт). Как правило, в процессе реакции реакционную смесь медленно нагревают от комнатной температуры до температуры в диапазоне от 70 до 80 С включительно за промежуток времени в диапазоне от примерно 1 до 48 ч включительно (см., например, Lucca, George V. De; Kim, Ui Т.; Liang, Jing; Cordova, Beverly; Klabe,Ronald M.; et al.; J. Med. Chem.; EN; 41; 13; 1998; 2411-2423, Lila, Christine; Gloanec, Philippe; Cadet,Laurence; Herve, Yolande; Fournier, Jean et al.; Synth. Commun.; EN; 28; 23; 1998; 4419-4430 и см. Sendzik,Martin; Hui, Hon C.; Tetrahedron Lett.; EN; 44; 2003; 8697-8700 и ссылки здесь на реакцию в нейтральной среде). Замещенное производное амидоксима (описанное на схеме 5) можно превратить в производное ациламидоксима при помощи подхода, приведенного на схеме 1. На схеме 1 PG1 представляет собой аминозащитную группу, такую как трет-бутилоксикарбонил, бензилоксикарбонил, этоксикарбонил,бензил и тому подобное. Реакцию сочетания можно ускорить при помощи агентов сочетания, известных в органическом синтезе, таких как КДИ (1-(3-диметиламинопропил)-3-этилкарбодиимид), ДЦК (N,N'- 22014904 дициклогексилкарбодиимид), в присутствии подходящего основания, такого как триэтиламин,диизопропилэтиламин, в подходящем растворителе (например, тетрагидрофуран, дихлорметан, N,Nдиметилформамид, диоксан). Обычно в реакционной смеси может также присутствовать сокатализатор,такой как НОВТ (гидроксибензотриазол), НОАТ (1-гидрокси-7-азабензотриазол). Реакция, как правило,протекает в диапазоне значений температуры от комнатной температуры до 60 С включительно в течение промежутка времени от примерно 2 до 12 ч, чтобы получить промежуточное соединение ациламидоксим. Реакцию циклизации можно вызвать термически в диапазоне температур от примерно 80 до примерно 150 С в течение промежутка времени от примерно 2 до примерно 18 ч (см., например,Suzuki, Takeshi; Iwaoka, Kiyoshi; Imanishi, Naoki; Nagakura, Yukinori; Miyata, Keiji; et al., Chem. Pharm.Bull., EN, 47: 1, 1999, 120-122). Продукт реакции можно выделить и очистить с применением стандартных методик, таких как экстракция, хроматография, кристаллизация, перегонка, или подобных им. Затем защитные группы PG1 удаляют с применением стандартных способов. На схеме 5 В определено выше, X представляет собой галоген или гидроксил; например, проводят реакцию производного пиперидина с арил- или гетероарилацилхлоридом при помощи способов, легко понятных специалистам. Реакцию можно ускорить при помощи основания, такого как триэтиламин,диизопропиламин, пиридин, в подходящем растворителе (например, тетрагидрофуран, дихлорметан). Как правило, в процессе реакции реакционную смесь медленно нагревают от 0 С до комнатной температуры в течение от примерно 4 до 12 ч. Если X представляет собой ОН, реакцию сочетания можно ускорить при помощи известных в органическом синтезе агентов сочетания, таких как КДИ (1-(3-диметиламинопропил)-3 этилкарбодиимид), ДЦК (N,N'-дициклогексилкарбодиимид), или агентов сочетания на полимерном носителе, таких как карбодиимид на полимерном носителе (PS-DCC, ex Argonaut Technologies), в присутствии подходящего основания, такого как триэтиламин, диизопропилэтиламин, в подходящем растворителе (например, тетрагидрофуран, дихлорметан, N,N-диметилформамид, диоксан). Обычно в реакционной смеси может также присутствовать сокатализатор, такой как НОВТ (гидроксибензотриазол), НОАТ (1-гидрокси-7-азабензотриазол), или аналогичный. Реакция, как правило,протекает при комнатной температуре в течение промежутка времени от примерно 2 до 12 ч. Соединения формул III-A и IV-A, в которых W представляет собой 3-замещенное пиперидиновое кольцо, можно получить в соответствии с последовательностью синтеза, показанной на схеме 6. При этом Р и Q независимо друг от друга представляют собой арил или гетероарил, как описано выше;X представляет собой СН 2, О, S; В представляет собой -С(=О)-С 0-С 2-алкил-. Схема 6 Исходные производные арил-Х-тетразола получают в соответствии с путями синтеза, хорошо известными в данной области (Katrizky A.R. and Rees W.C. (1984) Comprehensive Heterocyclic Chemistry,Pergamon Press). Арил-Х-тетразол можно алкилировать под действием производного 3-гидроксипиперидина в условиях реакции Мицунобу, как описано в литературе (см., например, Synthetic Commun; 26; 14; 1996; 2687-2694). Соединения формулы I, имеющие основную природу, могут образовывать широкий спектр различных фармацевтически приемлемых солей с различными органическими и неорганическими кислотами. Указанные соли легко получить обработкой основных соединений, по существу,- 23014904 эквивалентным количеством выбранной минеральной или органической кислотой в подходящем органическом растворителе, таком как метанол, этанол или изопропанол (см. Stahl P.H., Wermuth C.G.,Handbook of Pharmaceuticals Salts, Properties, Selection and Use, Wiley, 2002). Следующие не ограничивающие примеры предназначены проиллюстрировать настоящее изобретение. Физические данные, приведенные для служащих примерами соединений, согласуются с установленной структурой указанных соединений. Примеры Если не оговорено иное, все исходные вещества получены от промышленных поставщиков и использованы без дальнейшей очистки. В частности, следующие сокращения могут быть использованы в примерах и на протяжении описания. Все ссылки на раствор соли относятся к насыщенному водному раствору NaCl. Если не указано иначе, все температуры выражены в С (градусы Цельсия). Все реакции проводят в инертной атмосфере при комнатной температуре, если не отмечено иное. 1 Н ЯМР спектры записывают на приборе Brucker 300 МГц. Химические сдвиги выражены в миллионных долях (м.д., единицы ). Константы взаимодействия выражены в герцах (Гц). Структуры расщепления описывают видимые мультиплетности и обозначены как с (синглет), д (дублет), т (триплет),кв (квадруплет), квинт (квинтуплет), м (мультиплет). Способ А). Прибор Waters Alliance 2795 НТ Micromass ZQ. Колонка Waters XTerra MS C18 (504,6 мм,2,5 мкм). Расход 1 мл/мин. Подвижная фаза: фаза А = вода/CH3CN 95/5 + 0,05% ТФУК, фаза В = вода/CH3CN = 5/95 + 0,05% ТФУК. 0-1 мин (А: 95%, В: 5%), 1-4 мин (А: 0%, В: 100%), 4-6 мин (А: 0%, В: 100%), 6-6,1 мин (А: 95%, В: 5%). Т = 35 С; УФ-детектирование: Waters Photodiode array 996, 200-400 нм. Способ В).+ 0,1% ТФУК, фаза В = вода/ацетонитрил 5/95 + 0,1% ТФУК. 0-1,0 мин (А: 98%, В: 2%), 1,0-5,0 мин (А: 0%, В: 100%), 5,0-9,0 мин (А: 0%, В: 100%), 9,1-12 мин (А: 98%, В: 2%); УФ-детектирование: длина волны 254 нм; объем закола: 5 мкл. Способ D). Прибор Waters Alliance 2795 НТ Micromass ZQ. Колонка Waters Symmetry C18 (754,6 мм,3,5 мкм). Расход 1,5 мл/мин. Подвижная фаза: фаза А = вода/CH3CN 95/5 + 0,05% ТФУК, фаза В = вода/CH3CN = 5/95 + 0,05% ТФУК. 0-2 мин (А: 95%, В: 5%), 6 мин (А: 0%, В: 100%), 6-8 мин (А: 0%, В: 100%), 8-8,1 мин (А: 95%, В: 5%). Т = 35 С; УФ-детектирование: Waters Photodiode array 996, 200-400 нм. Способ Е). Прибор Waters Alliance 2795 НТ Micromass ZQ. Колонка Waters Symmetry C18 (754,6 мм,3,5 мкм). Расход 1,5 мл/мин. Подвижная фаза: фаза А = вода/CH3CN 95/5 + 0,05% ТФУК, фаза В = вода/CH3CN = 5/95 + 0,05% ТФУК. 0-0,5 мин (А: 95%, В: 5%), 0,5-7 мин (А: 0%, В: 100%), 7-8 мин (А: 0%, В: 100%), 8-8,1 мин (А: 95%, В: 5%). Т = 35 С; УФ-детектирование: Waters Photodiode array 996,200-400 нм. Способ F). Система ВЭЖХ: Waters Acquity, MS детектор: Waters ZQ2000. Колонка: Acquity UPLC-BEH C18 502,1 мм 1,7 мкм; расход 0,4 мл/мин; подвижная фаза: фаза А = вода/ацетонитрил 95/5 + 0,1% ТФУК,фаза В = вода/ацетонитрил 5/95 + 0,1% ТФУК. 0-0,25 мин (А: 98%, В: 2%), 0,25-4,0 мин (А: 0%, В: 100%),4,0-5,0 мин (А: 0%, В: 100%), 5,1-6 мин (А: 98%, В: 2%); УФ-детектирование: длина волны 254 нм. Способ G). Система ВЭЖХ: Waters Acquity, MS детектор: Waters ZQ2000. Колонка: Acquity UPLC-BEH C18 502,1 мм 1,7 мкм; расход 0,6 мл/мин; подвижная фаза: фаза А = вода/ацетонитрил 95/5 + 0,1% ТФУК,фаза В = вода/ацетонитрил 5/95 + 0,1% ТФУК. 0 - 0,25 мин (А: 98%, В: 2%), 3,30 мин (А: 0%, В: 100%),3,3 - 4,0 мин (А: 0%, В: 100%), 4,1 мин (А: 98%, В: 2%); УФ-детектирование: длина волны 254 нм. Способ Н). Система ВЭЖХ: Waters Acquity, MS детектор: Waters ZQ2000. Колонка: Acquity UPLC-BEH C18 502,1 мм 1,7 мкм; расход 0,25 мл/мин; подвижная фаза: фаза А = вода/ацетонитрил 95/5 + 0,1% ТФУК, фаза В = вода/ацетонитрил 5/95 + 0,1% ТФУК. 0-1,0 мин (А: 98%, В: 2%), 1,0-5,0 мин (А: 0%, В: 100%), 5,0-9,0 мин (А: 0%, В: 100%), 9,1-12 мин (А: 98%, В: 2%); УФ-детектирование: длина волны 254 нм. Способ I). Прибор Waters Alliance 2795 НТ Micromass ZQ. Колонка Waters Symmetry C18 (754,6 мм,3,5 мкм). Расход 1,5 мл/мин. Подвижная фаза: фаза А = вода/CH3CN 95/5 + 0,05% ТФУК, фаза В = вода/CH3CN = 5/95 + 0,05% ТФУК. 0-0,1 мин (А: 95%, В: 5%), 6 мин (А: 0%, В: 100%), 6-8 мин (А: 0%, В: 100%), 8,1 мин (А: 95%, В: 5%). Т = 35 С; УФ-детектирование: Waters Photodiode array 996, 200-400 нм. Способ L). Прибор Waters Alliance 2795 НТ Micromass ZQ. Колонка Waters XTerra MS C18 (504,6 мм,2,5 мкм). Расход 1,2 мл/мин. Подвижная фаза: фаза А = вода/CH3CN 95/5 + 0,05% ТФУК, фаза В = вода/CH3CN = 5/95 + 0,05% ТФУК. 0-0,8 мин (А: 95%, В: 5%), 3,3 мин (А: 0%, В: 100%), 3,3-5 мин (А: 0%, В: 100%), 5,1 мин (А: 95%, В: 5%). Т = 35 С; УФ-детектирование: Waters Photodiode array 996,200-400 нм. Способ М). Система ВЭЖХ: Waters Acquity, MS детектор: Waters ZQ2000. Колонка: Acquity UPLC-BEH C18 502,1 мм 1,7 мкм; расход 0,5 мл/мин; подвижная фаза: фаза А = вода/ацетонитрил 95/5 + 0,1% ТФУК,фаза В = вода/ацетонитрил 5/95 + 0,1% ТФУК. 0-0,1 мин (А: 95%, В: 5%), 1,6 мин (А: 0%, В: 100%),1,6-1,9 мин (А: 0%, В: 100%), 2,4 мин (А: 95%, В: 5%); УФ-детектирование: длина волны 254 нм. Все масс-спектры сняты способами электрораспылительной ионизации (ESI). Используемая микроволновая печь представляет собой устройство фирмы Biotage (Optimizer),снабженное внутренним датчиком, который следит за температурой и давлением в реакции и поддерживает выбранную температуру при помощи компьютерного управления. За ходом большинства реакций наблюдали при помощи тонкослойной хроматографии на 0,25 мм пластинах силикагеля Macherey-Nagel (60F-2254), визуализация при помощи УФ-освещения. Высокоскоростную колоночную хроматографию (flash chromatography) выполняли на силикагеле(220-440 меш, Fluka). Определение температуры плавления выполняли на приборе Buchi B-540. 1(А). трет-Бутиловый эфир (S)-3-[3-(4-фторбензил)-[1,2,4]оксадиазол-5-ил]пиперидин-1-карбоновой кислоты. К раствору 4-фторфенилацетонитрила (0,37 мл, 3 ммоль) в EtOH (4 мл) добавляют при комнатной температуре гидроксиламин (50 вес.% водный раствор, 0,74 мл, 12 ммоль) и кипятят раствор с обратным холодильником при перемешивании в течение 1,5 ч. Удаляют растворитель при пониженном давлении,чтобы получить 2-(4-фторфенил)-N-гидроксиацетамидин, который немедленно используют на следующей стадии. Смесь 2-(4-фторфенил)-N-гидроксиацетамидина (3 ммоль), S-1-Вос-пиперидин-3-карбоновой кислоты (0,69 г, 3 ммоль), КДИ.HCl (0,86 г, 4,5 ммоль), НОВТ (0,46 г, 3 ммоль) и ТЭА (0,84 мл, 6 ммоль) в диоксане (10 мл) перемешивают в течение 24 ч при комнатной температуре в атмосфере азота, после чего реакционную смесь кипятят с обратным холодильником в течение 8 ч. Растворитель выпаривают при пониженном давлении. Полученный остаток разбавляют водой (50 мл) и этилацетатом (50 мл),разделяют фазы и промывают органический слой последовательно водой (50 мл 2 раза) и NaOH 1 N(50 мл 2 раза). Высушивают органический слой над Na2SO4 и концентрируют при пониженном давлении. Очистка чернового продукта при помощи высокоскоростной хроматографии (силикагель,элюент: ДХМ/MeOH/NH4OH 99,5/0,5/0,05) дает 0,74 г трет-бутилового эфира (S)-3-[3-(4-фторбензил)[1,2,4]оксадиазол-5-ил]пиперидин-1-карбоновой кислоты. Выход: 68%; ЖХ-МС (RT): 5,5 мин (способ А); МС (ES+) дает m/z: 362,1. 1 Н-ЯМР (ДМСО-d6, 363 K),(м.д.): 7,34 (дд, 2 Н); 7,09 (дд, 2 Н); 4,06 (с, 2 Н); 3,97 (м, 1 Н); 3,63 (м,1 Н); 3,34 (дд, 1 Н); 3,20-3,05 (м, 2 Н); 2,10 (м, 1 Н); 1,83 (м, 1 Н); 1,71 (м, 1 Н); 1,59-1,44 (м, 1 Н); 1,40 (с, 9 Н). 1(В). (S)-3-[3-(4-Фторбензил)-[1,2,4]оксадиазол-5-ил]пиперидина гидрохлорид. трет-Бутиловый эфир (S)-3-[3-(4-фторбензил)-[1,2,4]оксадиазол-5-ил]пиперидин-1-карбоновой кислоты (0,73 г, 2 ммоль) растворяют в диоксане (2 мл) и добавляют по каплям при 0 С 4 мл HCl 4 N(диоксановый раствор). Полученную смесь перемешивают при комнатной температуре в течение 1,5 ч. Выпаривают растворитель при пониженном давлении, чтобы получить 594 мг (выход: 100%) (S)-3-[3-(4 фторбензил)-[1,2,4]оксадиазол-5-ил]пиперидина гидрохлорида в виде белого твердого вещества. ЖХ-МС(RT): 3,67 мин (способ А); МС (ES+) дает m/z: 262,1. 1(С). (S)-3-[3-(4-Фторбензил)-[1,2,4]оксадиазол-5-ил]пиперидин-1-ил-(4-фторфенил)метанон. К суспензии (S)-3-[3-(4-фторбензил)-[1,2,4]оксадиазол-5-ил]пиперидина гидрохлорида (594 мг,2 ммоль) в сухом дихлорметане (15 мл) добавляют по каплям при 0 С триэтиламин (0,7 мл, 5 ммоль) и 4 фторбензоилхлорид (0,27 мл, 2,2 ммоль). Оставляют реакционную смесь нагреться до комнатной температуры и перемешивают в течение 24 ч в атмосфере азота. Полученный раствор обрабатываютNaOH 1 N (10 мл) и разделяют фазы. Органический слой промывают водой (5 мл) и раствором соли(5 мл), затем высушивают над Na2SO4 и выпаривают при пониженном давлении. Полученный неочищенный остаток очищают при помощи высокоскоростной хроматографии (силикагель, элюент: ДХМ/МеОН/NH4OH 99:1:0,1), чтобы получить 330 мг целевого соединения. Выход: 43% (бледно-коричневое масло); []D20 = +74,2 (с = 0,97, CHCl3); ЖХ-МС (RT): 7,29 мин Целевое соединение получают в соответствии с процедурой, описанной в примере 1(С), начиная с(S)-3-[3-(4-фторбензил)-[1,2,4]оксадиазол-5-ил]пиперидина гидрохлорида (полученного, как описано в примере 1(В и 3,4-дифторбензоилхлорида. Очистка при помощи высокоскоростной хроматографии(силикагель, элюент: ДХМ/МеОН/NH4OH 99,5:0,5:0,05) и последующего растирания с диэтиловым эфиром дает 80 мг (3,4-дифторфенил)-(S)-3-[3-(4-фторбензил)-[1,2,4]оксадиазол-5-ил]пиперидин-1 илметанона. Выход: 29% (белый порошок); []D20 = +64,22 (с = 0,86, МеОН); ЖХ-МС (RT): 6,76 мин (способ С); МС (ES+) дает m/z: 402,2 (МН+). 3(А). трет-Бутиловый эфир (S)-3-карбамоилпиперидин-1-карбоновая кислота. К раствору (S)-1-Вос-пиперидин-3-карбоновой кислоты (2 г, 8,72 ммоль) в хлороформе (40 мл) добавляют по каплям при 0 С триэтиламин (1,21 мл, 8,72 ммоль), а затем этилхлорформиат (0,8 мл,8,30 ммоль) в атмосфере азота. После перемешивания в течение 10 мин при 0 С в раствор пропускаютNH3 (газ) в течение 1 ч. Затем реакционную смесь перемешивают при комнатной температуре в течение 3 ч, добавляют 5% NaHCO3 (водн.) и разделяют фазы. Органический слой высушивают над сульфатом натрия и выпаривают при пониженном давлении, чтобы получить целевое соединение, которое используют на следующей стадии без дальнейшей очистки. Выход: количественный; ЖХ-МС (RT): 3,31 мин (способ А); MC (ES+) дает m/z: 229,0. 3(В). трет-Бутиловый эфир (S)-3-цианопиперидин-1-карбоновая кислота. Оксихлорид фосфора (812 мкл, 8,72 ммоль) добавляют по каплям при 0 С к раствору третбутилового эфира (S)-3-карбамоилпиперидин-1-карбоновой кислоты (2 г, 8,72 ммоль) в пиридине (20 мл) в атмосфере азота. После перемешивания на протяжении ночи при комнатной температуре, добавляют этилацетат и промывают полученный раствор 10% HCl (2 раза). Разделяют фазы, высушивают органический слой над сульфатом натрия и выпаривают досуха при пониженном давлении. Целевое соединение используют на следующей стадии без дальнейшей очистки. Выход: количественный; ЖХ-МС (RT): 4,48 мин (способ А); МС (ES+) дает m/z: 211,1. 3(С). трет-Бутиловый эфир (S)-3-(N-гидроксикарбамимидоил)пиперидин-1-карбоновая кислота. Раствор трет-бутилового эфира (S)-3-цианопиперидин-1-карбоновой кислоты (1,8 г, 8,72 ммоль) и водного гидроксиламина (50% в воде, 2,1 мл, 34,88 ммоль) в этаноле (20 мл) кипятят с обратным холодильником в течение 2 ч. Выпаривают растворитель при пониженном давлении, чтобы получить целевое соединение, которое используют на следующей стадии без дальнейшей очистки. Выход: количественный; ЖХ-МС (RT): 2,71 мин (способ А); МС (ES+) дает m/z: 244,0. 3(D). трет-Бутиловый эфир (S)-3-[5-(4-фторбензил)-[1,2,4]оксадиазол-3-ил]пиперидин-1-карбоновая кислота. Смесь трет-бутилового эфира (S)-3-(N-гидроксикарбамимидоил)пиперидин-1-карбоновой кислоты(360 мг, 1,48 ммоль), 4-фторфенилуксусной кислоты (0,230 г, 1,48 ммоль), НОВТ (0,2 г, 2,22 ммоль),КДИ.HCl (0,429 г, 1,48 ммоль) и сухого триэтиламина (0,41 мл, 2,96 ммоль) в сухом диоксане (10 мл) перемешивают при комнатной температуре в течение 12 ч в атмосфере азота. Затем реакционную смесь кипятят с обратным холодильником в течение 4 ч и выпаривают растворитель при пониженном давлении. Полученный остаток разбавляют водой (40 мл) и этилацетатом (40 мл), разделяют фазы и промывают органический слой последовательно 5% раствором лимонной кислоты (40 мл), водой (40 мл,дважды), Na2CO3 1 N (40 мл, дважды) и раствором соли. Органический слой высушивают над сульфатом натрия и удаляют растворитель в вакууме, чтобы получить остаток, который очищают при помощи высокоскоростной хроматографии (силикагель, элюент: гексан/этилацетат 85:15), чтобы получить чистое целевое соединение (105 мг). Выход: 20%; ЖХ-МС (RT): 5,5 мин (способ I); MC (ES+) дает m/z: 362,04. 3(Е). (S)-3-[5-(4-Фторбензил)-[1,2,4]оксадиазол-3-ил]пиперидина гидрохлорид. трет-Бутиловый эфир (S)-3-[5-(4-фторбензил)-[1,2,4]оксадиазол-3-ил]пиперидин-1-карбоновой кислоты (0,105 г, 0,29 ммоль) растворяют в диоксане (2 мл) и добавляют по каплям при 0 С 4 мл HCl 4 N(диоксановый раствор). Полученную смесь перемешивают при комнатной температуре в течение 1,5 ч. Выпаривают растворитель при пониженном давлении, чтобы получить 86 мг (выход: 100%) (S)-3-[5-(4 фторбензил)-[1,2,4]оксадиазол-3-ил]пиперидина гидрохлорида в виде белого твердого вещества. ЖХ-МС(RT): 3,9 мин (способ D); MC (ES+) дает m/z: 262,1. 3(F). (3,4-Дифторфенил)-(S)-3-[5-(4-фторбензил)-[1,2,4]оксадиазол-3-ил]пиперидин-1-илметанон. К суспензии (S)-3-[5-(4-фторбензил)-[1,2,4]оксадиазол-3-ил]пиперидина гидрохлорида (86 мг,0,29 ммоль) в дихлорметане (8 мл) добавляют по каплям при 0 С триэтиламин (0,1 мл, 0,73 ммоль) и 3,4-дифторбензоилхлорид (0,042 мл, 0,34 ммоль). Оставляют реакционную смесь согреться до комнатной температуры и перемешивают в течение 24 ч в атмосфере азота. Полученный раствор обрабатываютNaOH 1 N (10 мл) и разделяют фазы. Органический слой промывают водой (5 мл) и раствором соли(5 мл), затем высушивают над Na2SO4 и выпаривают при пониженном давлении. Полученный черновой неочищенный продукт очищают при помощи высокоскоростной хроматографии (силикагель, элюент: ДХМ/MeOH/NH4OH 99:1:0.1), чтобы получить 45 мг целевого соединения. Целевое соединение получают в соответствии с процедурой, описанной в примере 3(F), начиная с(S)-3-[5-(4-фторбензил)-[1,2,4]оксадиазол-3-ил]пиперидина гидрохлорида (полученного, как описано в примере 3(Е и 4-фторбензоилхлорида. Очистка при помощи высокоскоростной хроматографии 5(А). (S)-1-(4-Фторбензоил)пиперидин-3-карбонитрил. трет-Бутиловый эфир (S)-3-цианопиперидин-1-карбоновой кислоты (1,5 г, 7,14 ммоль),полученный, как описано в примере 3(В), растворяют в диоксане (15 мл) и добавляют по каплям при 0 С 10 мл HCl 4 N (диоксановый раствор). Полученную смесь перемешивают при комнатной температуре в течение 5 ч. Выпаривают растворитель при пониженном давлении, чтобы получить (S)-пиперидин-3 карбонитрила гидрохлорид в виде белого твердого вещества, которое используют на следующей стадии без дальнейшей очистки. К суспензии (S)-пиперидин-3-карбонитрила гидрохлорида (7,14 ммоль) в сухом дихлорметане (100 мл) добавляют по каплям при 0 С триэтиламин (3 мл, 21,4 ммоль) и 4-фторбензоилхлорид (930 мкл, 7,85 ммоль). Оставляют реакционную смесь нагреться до комнатной температуры и перемешивают в течение 3 ч в атмосфере азота. Полученный раствор обрабатывают 5% NaHCO3 (50 мл,дважды) и разделяют фазы. Органический слой промывают 1 N HCl (50 мл) и раствором соли (50 мл),затем высушивают над Na2SO4 и выпаривают при пониженном давлении. Полученный неочищенный продукт очищают при помощи высокоскоростной хроматографии (силикагель, градиент элюента: от петролейный эфир/этилацетат 7:3 до петролейный эфир/этилацетат 1:1), чтобы получить 1,01 г целевого соединения. Выход: 61% (желтое масло); ЖХ-МС (RT): 3,7 мин (способ Е); МС (ES+) дает m/z: 233,1. 5(В). (S)-1-(4-Фторбензоил)-N-гидроксипиперидин-3-карбоксамидин. Раствор (S)-1-(4-фторбензоил)пиперидин-3-карбонитрила (1,01 г, 4,35 ммоль) и водного гидроксиламина (50% в воде, 1,1 мл, 17,4 ммоль) в этаноле (10 мл) кипятят с обратным холодильником в течение 4 ч. Выпаривают растворитель при пониженном давлении, чтобы получить целевое соединение(1,15 г), которое используют на следующей стадии без дальнейшей очистки. Выход: количественный; 1 Н-ЯМР (ДМСО-d6, 343 K),(м.д.): 8,61 (с уш, 1H); 7,44 (дд, 2 Н); 7,22 (дд,2 Н); 5,12 (с уш, 2 Н); 4,00 (м, 2 Н); 3,17-2,82 (м, 3 Н); 2,23 (м, 1H); 1,98 (м, 1H); 1,78-1,55 (м, 2 Н). 5(С). (4-Фторфенил)-(S)-3-[5-S)-1-фенилэтил)-[1,2,4]оксадиазол-3-ил]пиперидин-1-илметанон. Смесь (S)-1-(4-фторбензоил)-N-гидроксипиперидин-3-карбоксамидина (200 мг, 0,75 ммоль), (S)-2 фенилпропионовой кислоты (0,12 мл, 0,83 ммоль), НОАТ (0,1 г, 0,75 ммоль), КДИ.HCl (0,22 г,1,13 ммоль) и сухого триэтиламина (0,21 мл, 1,51 ммоль) в сухом диоксане (10 мл) перемешивают при комнатной температуре в течение 24 ч в атмосфере азота. Затем реакционную смесь кипятят с обратным холодильником в течение 6 ч и выпаривают растворитель при пониженном давлении. Полученный остаток разбавляют водой (40 мл) и этилацетатом (40 мл), разделяют фазы и промывают органический слой последовательно 5% раствором лимонной кислоты (40 мл), водой (40 мл, дважды), Na2CO3 1 N(40 мл, дважды) и раствором соли. Органический слой высушивают над сульфатом натрия и удаляют растворитель в вакууме, чтобы получить остаток, который очищают при помощи высокоскоростной хроматографии (силикагель, элюент: ДХМ/МеОН/NH4OH 99,6:0,4:0,04), чтобы получить чистое целевое Целевое соединение получают в соответствии с процедурой, описанной в примере 5(С), начиная с(S)-1-(4-фторбензоил)-N-гидроксипиперидин-3-карбоксамидина (полученного, как описано в примере 5(В и (R)-2-фенилпропионовой кислоты. Очистка при помощи высокоскоростной хроматографии Целевое соединение получают в соответствии с процедурой, описанной в примере 5(С), начиная с(S)-1-(4-фторбензоил)-N-гидроксипиперидин-3-карбоксамидина (полученного, как описано в примере 5(В и фенилуксусной кислоты. Очистка при помощи высокоскоростной хроматографии (силикагель,элюент: петролейный эфир/ацетон 8:1) и последующей кристаллизацией из петролейного эфира/диэтилового эфира дает 56 мг [(S)-3-(5-бензил-[1,2,4]оксадиазол-3-ил)пиперидин-1-ил](4 фторфенил)метанона. Выход: 27% (белое твердое вещество); []D20 = +67,2 (с = 0,99, МеОН); т.пл. = 75 С; ЖХ-МС (RT): 6,82 мин (способ С); МС (ES+) дает m/z: 366,2 (МН+). 1 Н-ЯМР (ДМСО-d6, 343 K),(м.д.): 7,43 (дд, 2 Н); 7,38-7,26 (м, 5 Н); 7,21 (дд, 2 Н); 4,30 (с, 2 Н); 4,15 Целевое соединение получают в соответствии с процедурой, описанной в примере 5(С), начиная с(S)-1-(4-фторбензоил)-N-гидроксипиперидин-3-карбоксамидина (полученного, как описано в примере 5(В и (L)-миндальной кислоты. Очистка при помощи высокоскоростной хроматографии (силикагель,элюент: ДХМ/МеОН 96:4) и последующего растирания с этилацетатом/диэтиловым эфиром дает 22 мг
МПК / Метки
МПК: C07D 401/04, A61K 31/4439, C07D 413/04, C07D 413/14, A61P 25/18
Метки: положительных, аллостерических, соединения, глутаматных, новые, качестве, метаботропных, рецепторов, гетероциклические, модуляторов
Код ссылки
<a href="https://eas.patents.su/30-14904-novye-geterociklicheskie-soedineniya-v-kachestve-polozhitelnyh-allostericheskih-modulyatorov-metabotropnyh-glutamatnyh-receptorov.html" rel="bookmark" title="База патентов Евразийского Союза">Новые гетероциклические соединения в качестве положительных аллостерических модуляторов метаботропных глутаматных рецепторов</a>
Предыдущий патент: Способ изготовления графитового электрода
Следующий патент: Новый способ получения пиперазинильных производных бензамида
Случайный патент: Бортовое устройство летательных аппаратов для уменьшения эрозии грунта












