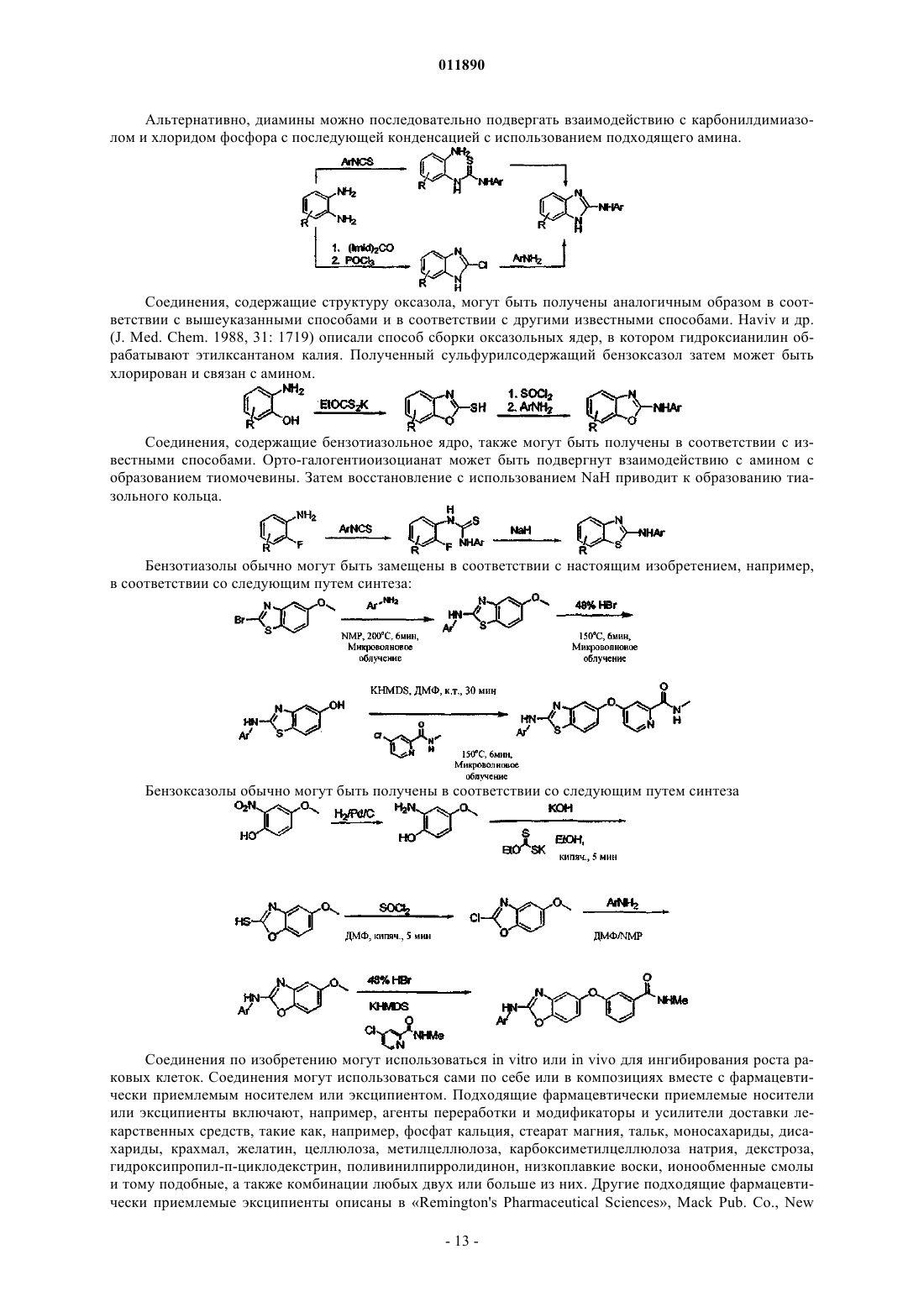
Замещённые бензазолы и их применение в качестве ингибиторов raf-киназы
Номер патента: 11890
Опубликовано: 30.06.2009
Авторы: Рамуртхи Савинтхри, Субраманиан Шарадха, Амири Пэйман, Ренхауэ Пол А., Сунг Леонард, Фантл Уэнди, Пун Дэниел Дж., Левайн Бэрри Хэскелл
Формула / Реферат
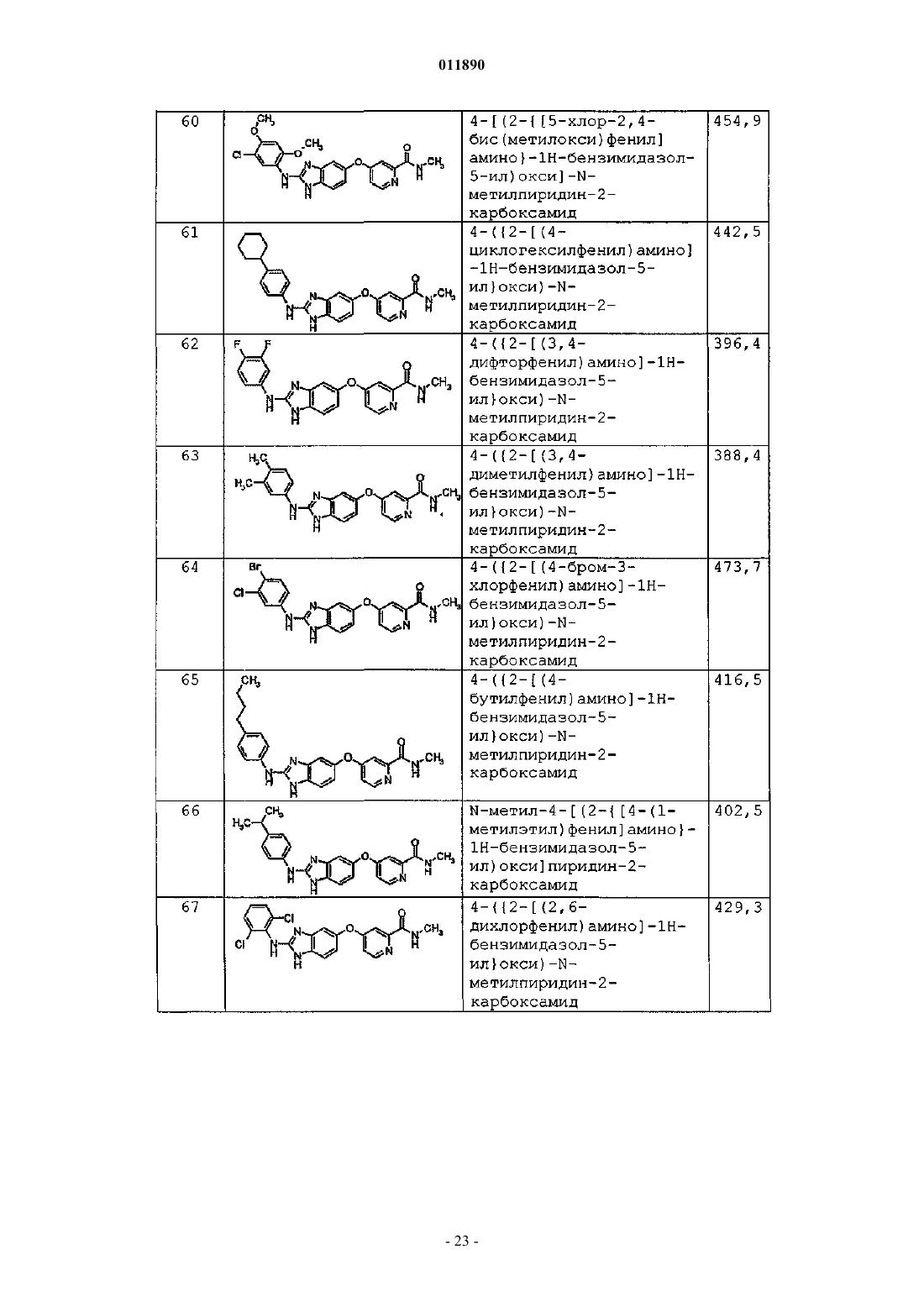
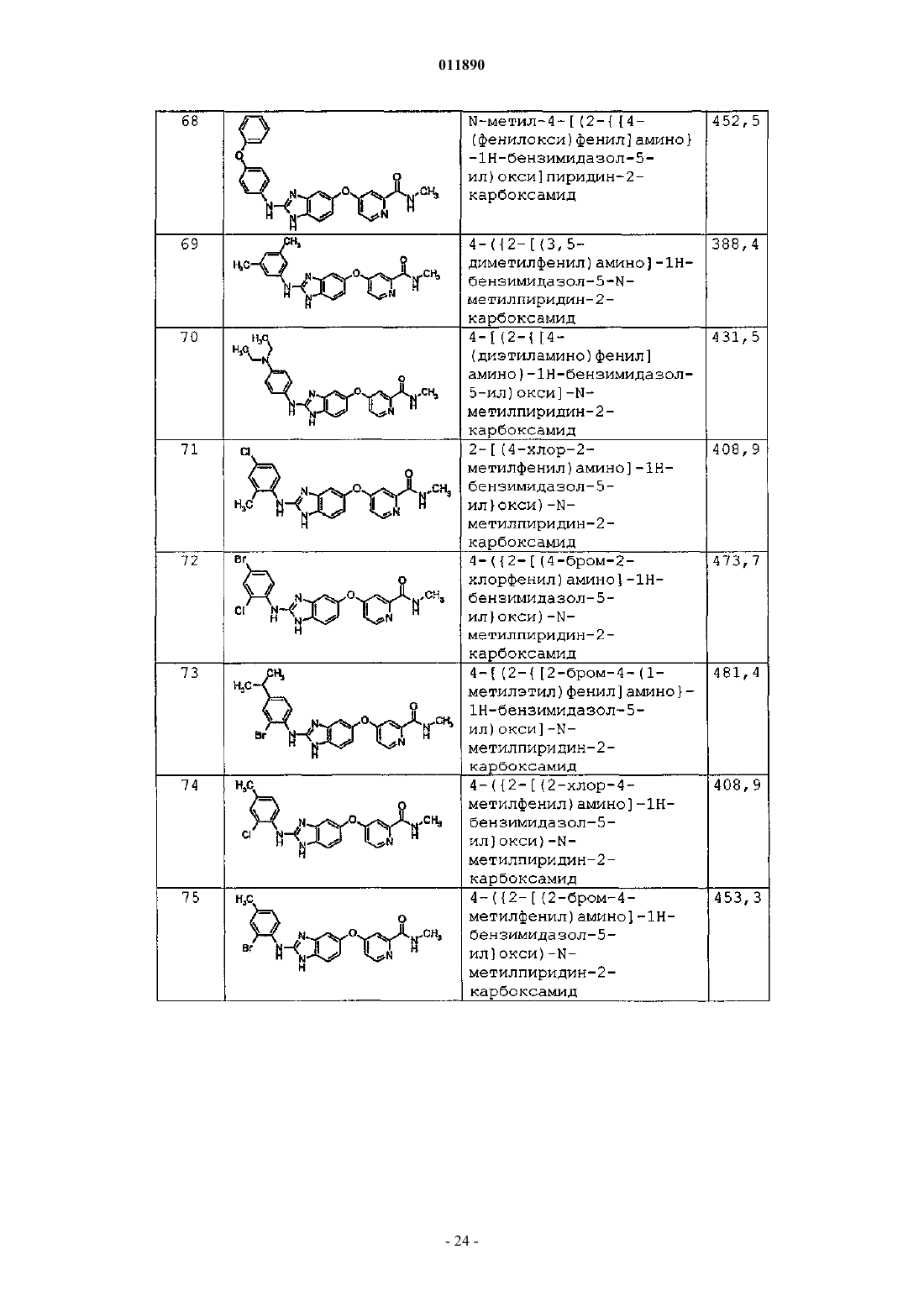
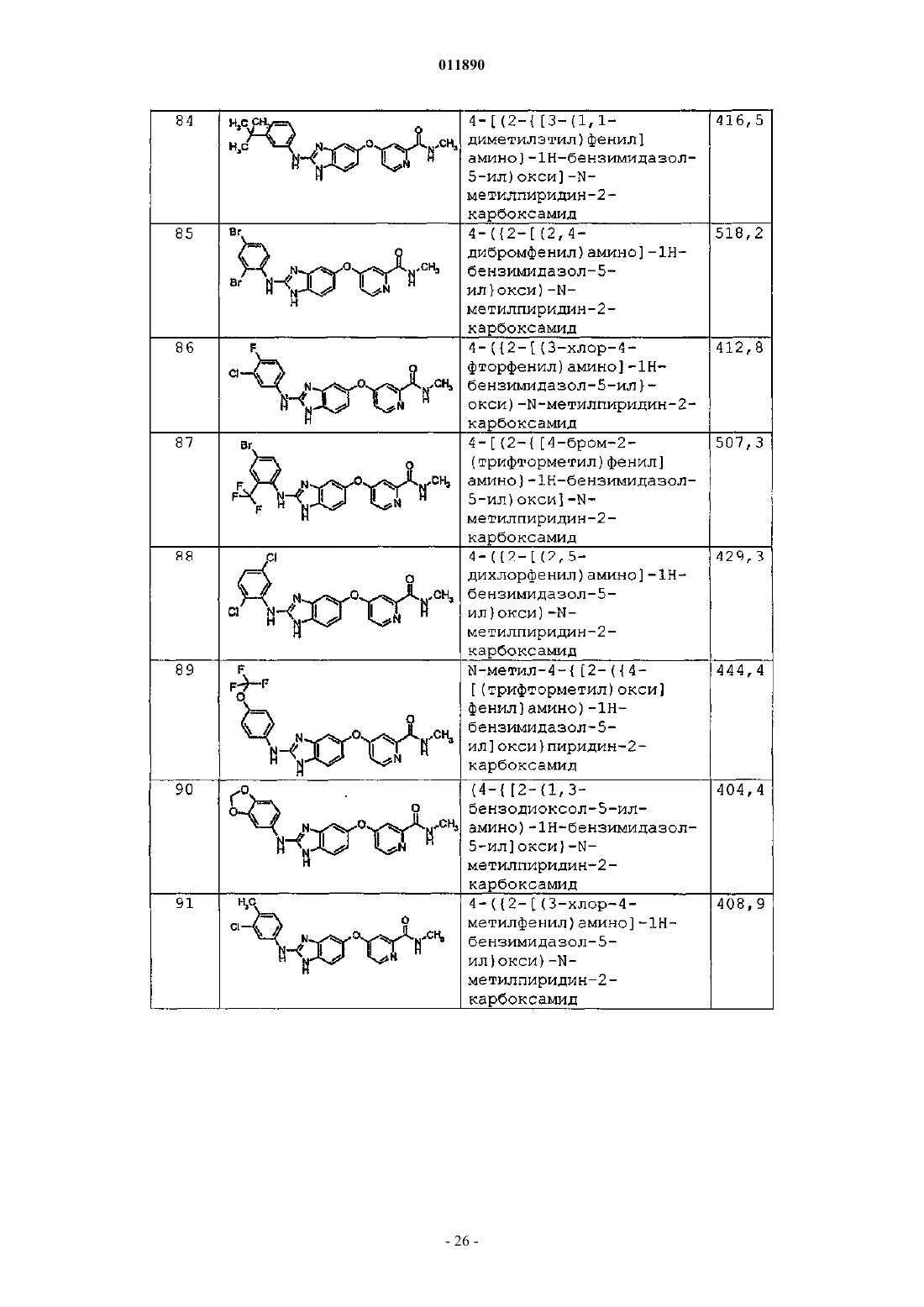
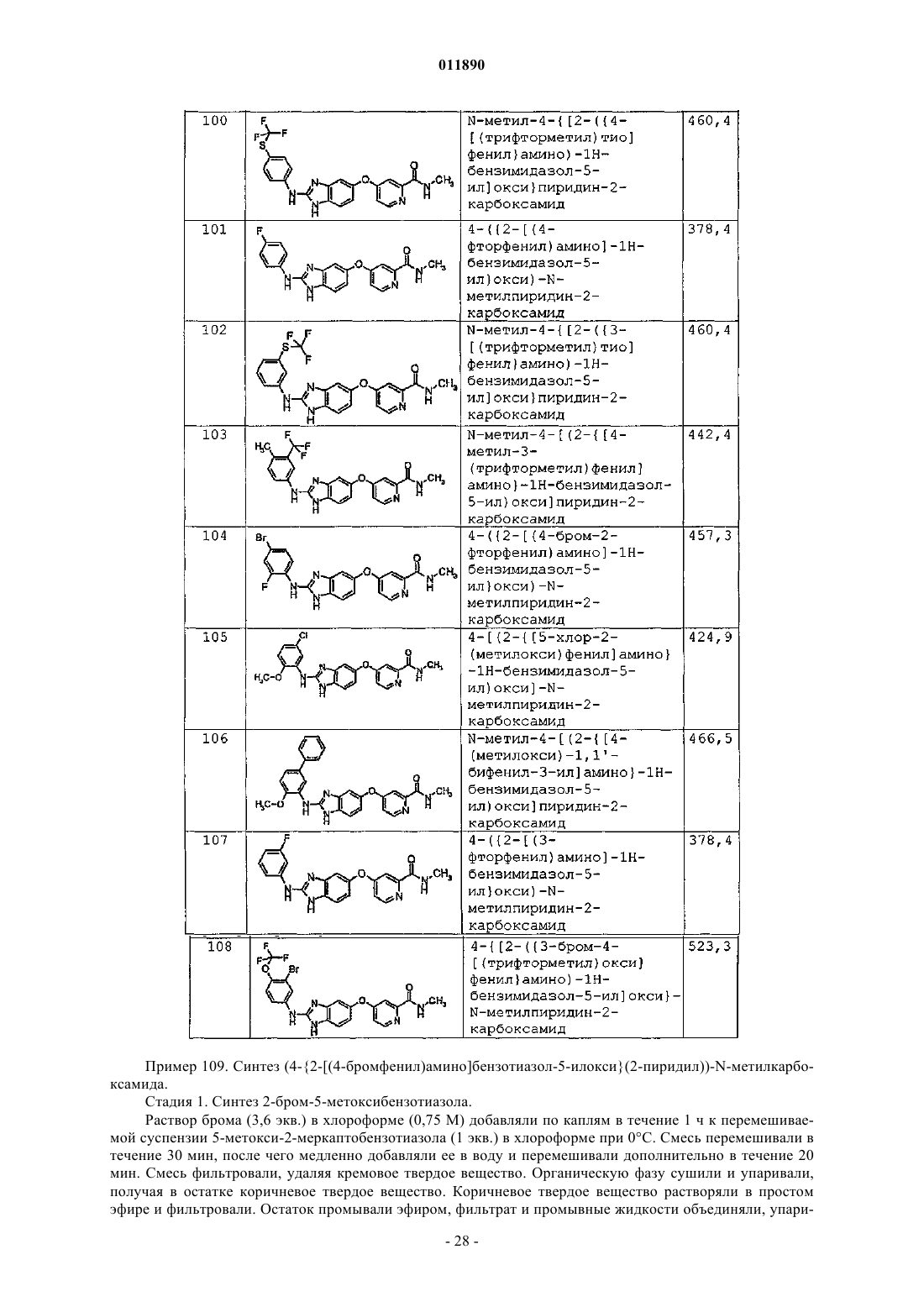
1. Соединение формулы (I)
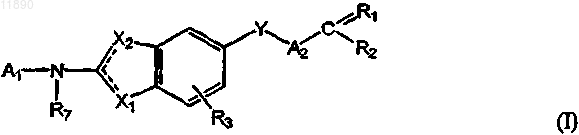
где пунктирная линия представляет собой простую или двойную связь;
X1 и Х2 независимо выбраны из =N-, -NR4-, -О- или -S- при условии, что если X1 представляет собой -NR4-, -О- или -S-, то Х2 представляет собой =N-, или если Х2 представляет собой -NR4-, -O- или -S-, то X1 представляет собой =N-, и оба X1 и Х2 не представляют собой =N-;
Y представляет собой O;
A1 представляет собой замещенный или незамещенный С3-С14арил;
А2 представляет собой замещенный или незамещенный пиридил;
R1 представляет собой O и R2 представляет собой NR5R6; или R1 вместе с R2 образуют замещенную или незамещенную С3-С8гетероциклоалкильную или С3-С14гетероарильную группу;
R3 представляет собой водород или С1-С6алкокси;
R4 представляет собой водород или С1-С12алкил;
R5 и R6 независимо выбраны из водорода и замещенного или незамещенного С1-С12алкила, С1-С12алкоксиС1-С12алкила, аминоС1-С12алкила, амидоС1-С12алкила, С1-С12ацила, С3-С8циклоалкила, С3-С8гетероциклоалкила, С3-С14арила, С3-С14гетероарила и С3-С14гетероарилС1-С12алкила; или
R5 и R6 вместе образуют замещенный или незамещенный С3-С8гетероцикл или С3-С14гетероарил;
где замещенные группы замещены одним или несколькими заместителями, выбранными из гидроксила, нитро, амино, имино, циано, галогена, тио, сульфонила, тиоамидо, амидино, имидино, оксо, оксамидино, метоксамидино, гуанидино, сульфонамидо, карбоксила, формила, С1-С6алкила, галогенС1-С6алкила, С1-С6алкиламино, галогенС1-С6алкиламино, С1-С6алкокси, галогенС1-С6алкокси, С1-С6алкоксиалкила, С1-С12алкилкарбонила, аминокарбонила, С3-С14арилкарбонила, С3-С14арилС1-С12алкилкарбонила, С3-С14гетероарилкарбонила, С3-С14гетероарилС1-С12алкилкарбонила, C1-С12алкилтио, аминоС1-С12алкила, цианоС1-С12алкила и С3-С14арила;
где гетероатомы, в случае присутствия, выбирают из N, О и S;
R7 представляет собой С1-С6алкил;
или его фармацевтически приемлемая соль, сложный эфир или пролекарство.
2. Соединение по п.1, где X1 представляет собой NR4, О или и S и Х2 представляет собой =N-; или его фармацевтически приемлемая соль, сложный эфир или пролекарство.
3. Соединение по п.1, где X1 представляет собой NR4.
4. Соединение по п.1, где Х2 представляет собой NR4.
5. Соединение по любому из пп.1-4, где R4 представляет собой водород.
6. Соединение по любому из пп.1-4, где R4 представляет собой метил.
7. Соединение по пп.1, 2, 3, 4, 5 или 6, где A1 выбирают из группы, состоящей из замещенного или незамещенного фенила, пиридила, пиримидинила, гетероциклокарбонилфенила, гетероциклофенила, гетероциклоалкилфенила, хлорфенила, фторфенила, бромфенила, йодфенила, дигалогенфенила, нитрофенила, 4-бромфенила, 4-хлорфенила, алкилбензоата, алкоксифенила, диалкоксифенила, диалкилфенила, триалкилфенила, тиофена, тиофен-2-карбоксилата, алкилтиофенила, трифторметилфенила, ацетилфенила, сульфамоилфенила, бифенила, циклогексилфенила, фенилоксифенила, диалкиламинофенила, алкилбромфенила, алкилхлорфенила, алкилфторфенила, трифторметилхлорфенила, трифторметилбромфенила, инденила, 2,3-дигидроинденила, тетралинила, трифторфенила, (трифторметил)тиофенила, алкоксибифенила, индолила, 2,3-дигидроиндолила, 1-ацетил-2,3-дигидроиндолила, гидроксифенила, гидроксиалкилфенила, 4-амино(имино)метилфенила, изоксазолила, индазолила, имидазолила, бензимидазолила, имидазолилфенила, фенилимидазолила, фталамидо, нафтила, бензофенона, анилинила, анизолила, хинолинила, хинолинонила, пиримидин-5-илфенила, хинолидинилфенила, фуранила, фуранилфенила, пирролидин-4-илпиридинила, 4-диазепан-1-ила и (1,4'-бипиперидин-1'-илкарбонил)фенила.
8. Соединение по любому из пп.1-7, где R5 представляет собой водород и R6 выбирают из водорода и замещенного или незамещенного С1-С12алкила, С1-С12алкоксиС1-С12алкила, аминоС1-С12алкила, амидоС1-С12алкила,ацила, С3-С6циклоалкила, С3-С8гетероциклоалкила, С3-С14арила, С3-С14гетероарила и С3-С14гетероарилС1-С12алкила.
9. Соединение по любому из пп.1-7, где R1 вместе с R2 образуют замещенную или незамещенную С3-С8гетероциклоалкильную или С3-С14гетероарильную группу.
10. Соединение по любому из пп.1-9, где R3 представляет собой водород.
11. Соединение по любому из пп.1-10, где R3 представляет собой C1-С6алкокси.
12. Соединение по п.11, где R3 представляет собой метокси.
13. Соединение по любому из пп.1-12, где R4 представляет собой С1-С6алкил.
14. Соединение по п.13, где R4 представляет собой метил.
15. Соединение по любому из пп.1-8, где R5 представляет собой Н и R6 представляет собой метил.
16. Фармацевтическая композиция, содержащая соединение по любому из пп.1-15 в количестве, эффективном для ингибирования активности Raf-киназы у человека или животного при введении вместе с фармацевтически приемлемым носителем.
17. Композиция по п.16, дополнительно содержащая по меньшей мере один дополнительный агент для лечения рака.
18. Композиция по п.17, в которой по меньшей мере один дополнительный агент для лечения рака выбран из иринотекана, топотекана, гемцитабина, 5-фторурацила, лейковорина, карбоплатина, цисплатина, таксанов, тезацитабина, циклофосфамида, алколоидов винка, иматиниба, антрациклинов, ритуксимаба и трастузумаба.
19. Способ ингибирования активности Raf-киназы у человека или животного, включающий введение человеку или животному композиции, содержащей соединение по любому из пп.1-15 в количестве, эффективном для ингибирования активности Raf-киназы у человека или животного.
20. Способ лечения ракового заболевания, опосредованного Ras/митоген-активируемым протеинкиназным сигнальным путем, у человека или животного, включающий введение человеку или животному композиции, содержащей соединение по любому из пп.1-15 в количестве, эффективном для ингибирования активности Raf-киназы у человека или животного.
21. Способ лечения гормонально зависимого ракового заболевания, опосредованного Ras/митоген-активируемым протеинкиназным сигнальным путем, у человека или животного, включающий введение человеку или животному композиции, содержащей соединение по любому из пп.1-15 в количестве, эффективном для ингибирования активности Raf-киназы у человека или животного.
22. Способ по п.21, где гормонально зависимый рак представляет собой рак молочной железы или рак предстательной железы.
23. Способ лечеэшя гематологического ракового заболевания, опосредованного Ras/митоген-активируемым протеинкиназным сигнальным путем, у человека или животного, включающий введение человеку или животному композиции, содержащей соединение по любому из пп.1-15 в количестве, эффективном для ингибирования активности Raf-киназы у человека или животного.
24. Способ по любому из пп.20-23, дополнительно включающий введение человеку или животному по меньшей мере одного дополнительного агента для лечения рака.
25. Способ по п.24, в котором по меньшей мере один дополнительный агент для лечения рака выбран из иринотекана, топотекана, гемцитабина, 5-фторурацила, лейковорина, карбоплатина, цисплатина, таксанов, тезацитабина, циклофосфамида, алколоидов винка, иматиниба, антрациклинов, ритуксимаба и трастузумаба.
26. Применение соединения по любому из пп.1-15 для лечения рака, опосредованного Ras/митоген-активируемым протеинкиназным сигнальным путем.
27. Применение соединения по любому из пп.1-15 для получения лекарственного средства для ингибирования активности Raf-киназы у человека или животного.
28. Применение соединения по любому из пп.1-15 для получения лекарственного средства для лечения рака, опосредованного Ras/митоген-активируемым протеинкиназным сигнальным путем, у человека или животного.
29. Применение по п.28, где лечение дополнительно включает введение человеку или животному по меньшей мере одного дополнительного агента для лечения рака.
30. Применение по п.29, в котором по меньшей мере один дополнительный агент для лечения рака выбран из иринотекана, топотекана, гемцитабина, 5-фторурацила, лейковорина, карбоплатина, цисплатина, таксанов, тезацитабина, циклофосфамида, алколоидов винка, иматиниба, антрациклинов, ритуксимаба и трастузумаба.
31. Применение по любому из пп.28-30, где рак представляет собой гормонально зависимое раковое заболевание.
32. Применение по п.31,где гормонально зависимый рак представляет собой рак молочной железы или рак предстательной железы.
33. Применение по любому из пп.28-30, где рак представляет собой гематологическое раковое заболевание.
Текст
011890 Данная заявка основывается на заявке на патент США, сер.10/405,945, поданной 31 марта 2003 г., которая базируется на предварительной заявке на патент США сер.60/369,066, поданной 29 марта 2002 г. Настоящее изобретение относится к новым замещенным соединениям бензазольного типа и их фармацевтически приемлемым солям, сложным эфирам или пролекарствам, композициям новых соединений вместе с фармацевтически приемлемыми носителями и применению новых соединений или по отдельности, или в комбинации по меньшей мере с одним дополнительным терапевтическим агентом для профилактики или лечения рака. Предпосылки создания изобретения Серин/треонин Raf-киназы являются неотъемлемыми компонентами сигнального модуляRas/митоген-активированная протеинкиназа (МАРК), который контролирует комплексную программу транскрипции в ответной реакции на внешние клеточные раздражители. Гены Raf кодируют высококонсервативные серин-треонин-специфические протеинакиназы, которые, как известно, связываются с онкогеном ras. Они представляют собой часть пути сигнальной трансдукции, который, как предполагается,состоит из рецепторных тирозинкиназ, р 21 ras, Raf-протеинкиназ, Mek1 (ERK активатор или MAPKK) киназ и ERK (MAPK) киназ, которые, в конечном счете, фосфорилируют факторы транскрипции. В таком пути Raf-киназы активируются с помощью Ras и фосфорилируют и активируют две изоформы митоген-активированной протеинкиназы (называемые Mek1 и Mek2), которые представляют собой треонин/тирозин киназы двойной специфичности. Обе изоформы Mek активируют митоген-активированные киназы 1 и 2 (MAPK, также называемые межклеточными лиганд-регулируемыми киназами 1 и 2 илиErk1 и Erk2). MAPK фосфорилируют многие субстраты, включая факторы транскрипции, и тем самым устанавливают их программу транскрипции. Участие Raf-киназы в пути Ras/MAPK оказывает влияние и регулирует многие клеточные функции, такие как пролиферация, дифференциация, выживание, онкогенные трансформации и апоптоз. Как существенная роль и положение Raf во многих сигнальных путях были продемонстрированы в исследованиях с использованием дерегулированных и доминантных ингибиторных мутантов Raf в клетках млекопитающих, а также в исследованиях с использованием биохимических и генетических методом моделирования организмов. Во многих случаях, активация Raf с использованием рецепторов, которые стимулируют клеточное тирозиновое фосфорилирование, зависит от активности Ras, указывая на то, чтоRas функционирует в 3'-5' направлении относительно Raf. При активации, Raf 1 затем фосфорилирует и активирует Mek1, приводя к распространению сигнала к ниже расположенным эффекторам, таким как МАРК (митоген-активированная протеинкиназа) (Crews и др. (1993) Cell 74: 215). Raf серин/треонин киназы рассматриваются как первичные эффекторы Ras, вовлеченные в пролиферацию клеток животныхRaf-киназа имеет три индивидуальные изоформы: Raf-1 (c-Raf), A-Raf и B-Raf, различающиеся по своей способности взаимодействовать с Ras, активировать путь МАРК киназы, распределению ткани и субклеточной локализации (Marias и др., Biochem. J. 351: 289-305, 2000; Weber и др., Oncogene 19: 169176,2000; Pritchard и др., Mol. Cell. Biol.15: 6430-6442,1995). Raf киназы активируются посредством Ras и фосфорилируют и активируют две изоформы митоген-активированной протеинкиназы (называемыеMek1 и Mek2), которые представляют собой треонин/тирозин киназы двойной специфичности. Обе изоформы Mek активируют митоген-активированные киназы 1 и 2 (МАРК, также называемые межклеточными лиганд-регулируемыми киназами 1 и 2 или Erk1 и Erk2). МАРК фосфорилируют многие субстраты,включая цитозольные белки и ETS семейство факторов транскрипции. Участие Raf киназы в путиRas/MAPK оказывает влияние и регулирует многие клеточные функции, такие как пролиферация, дифференциация, выживание, прогрессирование клеточного цикла и апоптоз. Активирующую мутацию одного из генов Ras можно видеть в примерно 20% всех опухолей, и путь(Hoshino и др., Oncogene 18: 813-822, 1999). Недавно проведенные исследования показали, что B-Raf мутация в родимых пятнах кожи представляет собой решающую стадию инициирования меланоцитной неоплазии (Pollock и др., Nature Genetics 25: 1-2, 2002). Кроме того, в еще более поздних исследованиях выявлено, что активирующая мутация в домене киназы B-Raf имеет место в примерно 66% меланом,12% карциномы толстой кишки и 14% рака печени (Davies и др., Nature 417: 949-954, 2002) (Yuen и др.,Cancer Research 62: 6451-6455, 2002) (Brose и др., Cancer Research 62: 6997-7000, 2002). Ингибиторы пути Raf/MEK/ERK на уровне Raf-киназ потенциально могут быть эффективными в качестве терапевтических агентов против опухолей со сверхэкспрессируемыми или мутированными рецепторными тирозинкиназами, активированными внутриклеточными тирозинкиназами, опухолей с аберрантно экспрессируемым Grb2 (адаптерный белок, дающий возможность стимуляции Ras посредствомSos фактора обмена), а также опухолей скрывающих активирующие мутации самой Raf. В ранних клинических исследованиях ингибитор киназы Raf-1, который также ингибирует B-Raf, оказался перспективным в качестве терапевтических агентов в терапии рака (Crump, Current Pharmaceutical Design 8: 2243-2248, 2002; Sebastien и др., Current Plaarmaceutical Design 8: 2249-2253, 2002). Было показано, что нарушение экспрессии Raf в клеточных линиях посредством применения РНК-1 011890 антисмысловой технологии подавляет как Ras-, так и Raf-опосредованную опухолегенность (Kolch и др.,Nature 349: 416-428, 1991; Monia и др., Nature Medicine 2 (6): 668-675, 1996). Описано несколько ингибиторов Raf-киназы, проявляющих эффективность при ингибировании пролиферации опухолевых клеток в анализах в vitro и/или in vivo (см., например, патенты US6391636, 6358932, 6037136, 5717100, 6458813, 6204467 и 6268391). В других патентах и патентных заявках предложено применение ингибиторов Raf-киназы для лечения лейкоза (см., например, патенты US6268391 и 6204467 и опубликованные заявки на патент US20020137774; 20020082192; 20010016194; и 20010006975) или для лечения рака молочной железы (см., например, патенты US6358932, 5717100, 6458813, 6268391 и 6204467, и опубликованную заявку US20010014679). Согласно изобретению предлагаются новые замещенные бензазолы и их фармацевтически приемлемые соли и сложные эфиры, содержащие повышающие растворимость фрагменты, или пролекарства формулы (I) где X1 и Х 2 независимо выбраны из =N-, -NR4-, -О- или -S-, при условии, что если X1 представляет собой -NR4-, -О- или -S-, то Х 2 представляет собой =N-, или если Х 2 представляет собой -NR4-, -О- или-S-, то Х 2 представляет собой =N-, и оба X1 и Х 2 не представляют собой =N-;A1 представляет собой замещенный или незамещенный алкил, циклоалкил, гетероциклоалкил, арил,полициклический арил, полициклический арилалкил, гетероарил, биарил, гетероариларил, гетероарилгетероарил, циклоалкилалкил, гетероциклоалкилалкил, арилалкил, гетероарилалкил, биарилалкил или гетероариларилалкил; А 2 представляет собой замещенный или незамещенный гетероарил;R1 представляет собой О или Н, и R2 представляет собой NR5R6 или гидроксил; или R1 вместе с R2 образуют замещенную или незамещенную гетероциклоалкильную или гетероарильную группы; где пунктирная линия представляет собой простую или двойную связь;R3 представляет собой водород, галоген, низший алкил или низший алкокси;R5 и R6 независимо выбраны из водорода и замещенного или незамещенного алкила, алкоксиалкила, аминоалкила, амидоалкила, ацила, циклоалкила, гетероциклоалкила, арила, гетероарила, алкилоксиалкилгетероцикла и гетероарилалкила; или R5 и R6 вместе образуют замещенный или незамещенный гетероцикл или гетероарил; иR7 представляет собой водород или низший алкил; или его фармацевтически приемлемая соль, сложный эфир или пролекарство. В других вариантах осуществления предлагаются новые замещенные бензазолы формулы (II) где Y, Ar1, Ar2, R1, R2, R3 и R4 являются такими, как определено выше; или их фармацевтически приемлемые соли, сложные эфиры или пролекарства. В других вариантах осуществления предлагаются новые замещенные бензазолы формулы (III) где X1, Ar1, Аr2, R1, R2 и R3 являются такими, как определено выше; и их фармацевтически приемлемые соли, сложные эфиры, таутомеры и пролекарства. В других вариантах осуществления предлагаются новые замещенные бензазолы формулы (IV) где X1, Y, Ar1, R1, R2 и R3 являются такими, как определено выше; и их фармацевтически приемлемые соли, сложные эфиры, таутомеры и пролекарства. Еще в других вариантах осуществления предлагаются новые замещенные бензазолы формулы (V)-2 011890 соли, сложные эфиры, таутомеры или пролекарства. В других аспектах настоящее изобретение относится к способам лечения связанных с Raf нарушений у субъекта, представляющего собой человека или животного и нуждающегося в таком лечении,включающим введение указанному субъекту количества соединения формулы (I), (II), (III), (IV) или (V),эффективного для уменьшения или предотвращения роста опухоли. В следующих аспектах настоящее изобретение относится к способам лечения связанных с Raf нарушений у субъекта, представляющего собой человека или животного, нуждающегося в таком лечении,включающим введение указанному субъекту количества соединения формулы (I), (II), (III), (IV) или (V),эффективного для уменьшения или предотвращения роста опухоли у субъекта, в сочетании по меньшей мере с одним дополнительным агентом для лечения рака. В других аспектах настоящее изобретение относится к терапевтическим композициям, включающим по меньшей мере одно соединение формулы (I), (II), (III), (IV) или (V) в сочетании с одним или несколькими дополнительными агентами для лечения рака, используемыми обычно для терапии рака. Соединения по изобретению могут использоваться при лечении разных видов рака, включая карциномы (например, легких, поджелудочной железы, щитовидной железы, мочевого пузыря или толстой кишки), миелоидных нарушений (например, миелоидного лейкозы) и аденом (например, волосатого полипа толстой кишки). Изобретение дополнительно относится к композициям, способам применения и способам получения, как описано в разделе Подробное описание изобретения. Подробное описание предпочтительных вариантов осуществления Одним аспектом настоящего изобретения являются новые замещенные бензазолы и их фармацевтически приемлемые соли, сложные эфиры или пролекарства формулы (I) где X1 и Х 2 независимо выбраны из =N-, -NR4-, -О- или -S-, при условии, что если X1 представляет собой -NR4-, -О- или -S-, то Х 2 представляет собой =N-, или если Х 2 представляет собой -NR4-, -О- или-S-, то Х 2 представляет собой =N-, и оба X1 и Х 2 не представляют собой =N-;A1 представляет собой замещенный или незамещенный алкил, циклоалкил, гетероциклоалкил, арил,полициклический арил, полициклический арилалкил, гетероарил, биарил, гетероариларил, гетероарилгетероарил, циклоалкилалкил, гетероциклоалкилалкил, арилалкил, гетероарилалкил, биарилалкил или гетероариларилалкил; А 2 представляет собой замещенный или незамещенный гетероарил;R1 представляет собой О или Н, и R2 представляет собой NR5R6 или гидроксил; или R1 вместе с R2 образуют замещенную или незамещенную гетероциклоалкильную или гетероарильную группу; где пунктирная линия представляет собой простую или двойную связь;R3 представляет собой водород, галоген, низший алкил или низший алкокси;R5 и R6 независимо выбраны из водорода и замещенного или незамещенного алкила, алкоксиалкила, аминоалкила, амидоалкила, ацила, циклоалкила, гетероциклоалкила, арила, гетероарила, алкилоксиалкилгетероцикла и гетероарилалкила; или R5 и R6 вместе образуют замещенный или незамещенный гетероцикл или гетероарил; иR7 представляет собой водород или низший алкил; или его фармацевтически приемлемая соль, сложный эфир или пролекарство. В другом варианте осуществления представлены новые замещенные бензазолы формулы (II) где Y, Ar1, Ar2, R1, R2, R3 и R4 являются такими, как определено выше; или их фармацевтически приемлемые соли, сложные эфиры или пролекарства. В другом варианте осуществления представлены новые замещенные бензазолы формулы (III) где X1, Ar1, Ar2, R1, R2 и R3 являются такими, как определено выше; и их фармацевтически приемлемые соли, сложные эфиры, таутомеры и пролекарства. В другом варианте осуществления представлены новые замещенные бензазолы формулы (IV) где X1, Y, Ar1, R1, R2 и R3 являются такими, как определено выше; и их фармацевтически приемлемые соли, сложные эфиры, таутомеры и пролекарства. Еще в другом варианте осуществления представлены новые замещенные бензазолы формулы (V) где X1, Ar1, R1, R2 и R3 являются такими, как определено выше; и их фармацевтически приемлемые соли, сложные эфиры, таутомеры или пролекарства. В следующем аспекте настоящее изобретение относится к способам лечения субъекта, представляющего собой человека или животного, страдающего от связанного с Raf нарушения, такого как рак. Таким образом, настоящее изобретение относится к способам лечения субъекта человека или животного,нуждающегося в таком лечении, включающим введение субъекту терапевтически эффективного количества соединения вышеуказанных формул I, II, III, IV или V, или по отдельности, или в сочетании с другими противораковыми агентами. В других аспектах, настоящее изобретение относится к способам лечения связанных с Raf нарушений у субъекта, представляющего собой человека или животного, нуждающегося в таком лечении, включающим введение субъекту количества соединения формулы (I), (II), (III), (IV) или (V), эффективного для уменьшения или предотвращения роста опухоли у субъекта. В следующих аспектах настоящее изобретение относится к способам лечения связанных с Raf нарушений у субъекта человека или животного, нуждающегося в таком лечении, включающим введение субъекту количества соединения формулы (I), (II), (III), (IV) или (V), эффективного для уменьшения или предотвращения роста опухоли у субъекта в сочетании по меньшей мере с одним дополнительным агентом для лечения рака. Для применения в способах по настоящему изобретению рассматривается ряд подходящих противораковых агентов для использования в качестве комбинируемых лекарственных средств. Действительно, настоящее изобретение предполагает, но не ограничивается указанным, введение многочисленных противораковых агентов, таких как агенты, которые индуцируют апоптоз; полинуклеотиды (например, рибозимы); полипептиды (например, ферменты); лекарственные средства; биологические миметики; алкалоиды; алкилирующие агенты; противоопухолевые антибиотики; гормоны; соединения платины; моноклональные антитела, конъюгированные с противораковыми лекарственными средствами; токсины и/или радионулиды; модификаторы биологического ответа (например, интерфероны [например, IFN-, и т.д.], и интерлейкины [например, IL-2, и т.д.]; адаптационные иммунотераппевтические агенты; гематопоэтические факторы роста; агенты, которые индуцируют дифференциацию клеток опухолей (например, все транс-ретиноевые кислоты и т.д.); реагенты для генной терапии; антисмысловые терапевтические реагенты и нуклеотиды; опухолевые вакцины; ингибиторы ангиогенеза и тому подобные. Многочисленные другие примеры химиотерапевтических соединений и противораковых терапевтических средств, подходящих для совместного введения с описанными соединениями формулы(I), (II), (III), (IV) или (V) известны специалистам в данной области. В предпочтительных вариантах осуществления противораковые агенты для использования в сочетании с соединениями по настоящему изобретению включают агенты, которые индуцируют или стимулируют апоптоз. Агенты, которые индуцируют апоптоз включают, но не ограничиваются указанным,лучевое облучение (например, W); ингибиторы киназы (например, ингибитор киназы рецептора эпидермального фактора роста [EGFR], ингибитор киназы рецептора фактора роста сосудов [VGFR], ингибитор киназы рецептора фактора роста фиброластов [FGFR], ингибитор киназы рецептора полученного из тромбоцитов фактора роста I [PGFR], и ингибиторы киназы Bcr-Abl, такие как STI-571, глиевек и гливек]), антисмысловые молекулы; антитела [например, герцептин и ритуксан]; антиэстрогены [например,ралоксифен и тамоксифен]; антиандрогены [например, флутамид, бикалутамид, финастерид, аминоглутетамид, кетоконазол и кортикостериоды]; ингибиторы циклооксигеназы 2 (СОХ-2) [например, целекоксиб, мелоксикам, NS-398, и нестероидные противовоспалительные лекарственные средства (НСПВС)]; и химиотерапевтические лекарственные средства против рака [например, иринотекан (Camptosar),СРТРЕТ-11, флударабин (Fludara), дакарбазин (DTIC), дексаметазон, митоксантрон, милотарг, VP-16,цисплатин, 5-FU, доксорубицин, таксотер или таксол]; клеточные сигнальные молекулы; керамиды и цитокины и стауросприн и тому подобные. В других аспектах настоящее изобретение относится к фармацевтическим композициям, включающим по меньшей мере одно соединение формулы I, II, III, IV или V вместе с фармацевтически приемлемым носителем, подходящим для введения субъекту человеку или животному или по отдельности или вместе с другими противораковыми агентами. В других аспектах настоящее изобретение относится к способам получения соединений формулы I,-4 011890II, III, IV или V, как описано в данном описании. В следующих аспектах настоящее изобретение относится к соединениям, которые ингибируют фермент raf-киназу. Поскольку фермент является расположенным в прямом (5'-3') направлении эффектором p21ras, настоящие ингибиторы могут использоваться в фармацевтических композициях для человека или ветеринарной практики, где требуется ингибирование пути raf-киназы, например, при лечении опухолей и/или роста раковых клеток, опосредованного raf-киназой. В частности, соединения могут использоваться для лечения человека или животного, например, мышиного рака, поскольку прогрессирование данного рака зависит от ras-белкового сигнального каскада трансдукции и следовательно восприимчивы к лечению при прерывании каскада путем ингибирования активности raf-киназы. Соответственно соединения по изобретению могут использоваться при лечении плотных опухолей, таких как, например, карциномы (например, легких, поджелудочной железы, щитовидной железы, мочевого пузыря или толстой кишки, миелоидных нарушений (например, миелоидной лейкемии) или аденом (например, ворсинчатого полипа толстой кишки. Термин ингибитор Raf используется в данном описании для упоминания соединения, которое проявляет IC50 в отношении активности Raf-киназы, составляющую не более примерно 100 мкМ и обычно не более примерно 50 мкМ, как измерено в фильтрационном анализе Raf/Mek, далее описанном в общем виде ниже. Предпочтительные изоформы Raf-киназы, которые, как будет показано, ингибируют соединения по настоящему изобретению, включают A-Raf, B-Raf и C-Raf (Raf-1). IC50 представляет собой концентрацию ингибитора, которая уменьшает активность фермента (например, Raf-киназы) до уровня, составляющего половину от максимального. Было установлено, что иллюстративные соединения по настоящему изобретению проявляют ингибирующую активность против Raf. Соединения по настоящему изобретению предпочтительно проявляют IC50 в отношении Raf не более чем примерно 10 мкМ,более предпочтительно не более чем примерно 5 мкМ, даже более предпочтительно не более сем примерно 1 мкМ и наиболее предпочтительно не более чем примерно 200 нМ, как измерено в описанных здесь анализах Raf-киназы. В данном описании термин бензазолы включает бензимидазолы, бензотиазолы и бензоксазолы. Термин алкил относится к алкильным группам, которые не содержат гетероатомов. Таким образом, термин включает линейные алкильные группы, такие как метил, этил, пропил, бутил, пентил, гексил, гептил, октил, нонил, децил, ундецил, додецил и тому подобные. Термин также включает изомеры линейных алкильных групп с разветвленной цепью, включая, но не ограничиваясь указанным, следующие группы, приведенные для примера: -СН(СН 3)2, -СН(СН 3)(СН 2 СН 3), -СН(СН 2 СН 3)2, -С(СН 3)3,-С(СН 2 СН 3)3, -СН 2 СН(СН 3)2, -СН 2 СН(СН 3)(СН 2 СН 3), -СН 2 СН(СН 2 СН 3)2, -СН 2 С(СН 3)3, -СН 2 С(СН 2 СН 3)3,-СН(СН 3)СН(СН 3)(СН 2 СН 3), -СН 2 СН 2 СН(СН 3)2, -СН 2 СН 2 СН(СН 3)(СН 2 СН 3), -СН 2 СН 2 СН(СН 2 СН 3)2,-СН 2 СН 2 С(СН 3)3,-СН 2 СН 2 С(СН 2 СН 3)3,-СН(СН 3)СН 2 СН(СН 3)2,-СН(СН 3)СН(СН 3)СН(СН 3)2,-СН(СН 2 СН 3)СН(СН 3)СН(СН 3)(СН 2 СН 3) и другие. Термин также включает циклические алкильные группы, такие как циклопропил, циклобутил, циклопентил, циклогексил, циклогептил и циклооктил, и такие кольца, замещенные линейными и разветвленными алкильными группами, как определено выше. Таким образом, термин алкильные группы включает первичные алкильные группы, вторичные алкильные группы и третичные алкильные группы. Предпочтительные алкильные группы включают линейные и разветвленные алкильные группы и циклические алкильные группы, имеющие от 1 до 12 атомов углерода. Согласно данному описанию термин низший алкил включает как замещенные, так и незамещенные линейные и разветвленные алкильные группы, имеющие от 1 до 6 атомов углерода. Иллюстративные низшие алкильные группы включают, например, метил, этил, пропил, изопропил, н-бутил, третбутил, неопентил, трифторметил, пентафторэтил и тому подобные. Низшие алкильные группы могут быть замещенными, например, галогеном, гидрокси, амино, нитро и/или циано группами и тому подобными. Иллюстративные галогензамещенные и гидроксизамещенные низшие алкилы включают хлорметил, трихлорметил, хлорэтил, гидроксиэтил и тому подобные. Другие подходящие замещенные низшие алкильные фрагменты включают, например, аралкил, аминоалкил, аминоаралкил, карбониламиноалкил,алкилкарбониламиноалкил, арилкарбониламиноалкил, аралкилкарбониламиноалкил, аминоалкоксиалкил и ариламиноалкил. Термин низший алкокси в данном описании относится к RO-, где R представляет собой низший алкил. Иллюстративные примеры низших алкоксильных групп включают метокси, этокси, трет-бутокси,трифторметокси и тому подобные. Согласно данному описанию термин галоген или галоид относится к группам хлора, брома,фтора и йода. Термин галогеналкил относится к алкильному радикалу, замещенному одним или несколькими атомами галогена. Термин низший галогеналкил относится к низшему алкильному радикалу, замещенному одним или несколькими атомами галогена. Термин галогеналкокси относится к алкоксильному радикалу, замещенному одним или несколькими атомами галогена. Термин низший галоген-алкокси относится к низшему алкоксильному радикалу, замещенному одним или несколькими атомами галогена. Термин амино относится в данном описании к группе -NH2.-5 011890 Термин алкиламино относится в данном описании к группе -NRR', где каждый из R и R' независимо выбран из водорода или низшего алкила. Термин ариламино относится в данном описании к группе -NRR', где R представляет собой арил, и R' представляет собой водород, низший алкил или арил. Термин аралкиламино относится в данном описании к группе -NRR', где R представляет собой низший аралкил, и R' представляет собой водород, низший алкил, арил или низший аралкил. Термин алкоксиалкил относится к группе-alk1-O-alk2, где alk1 представляет собой алкил или алкенил, и аlk2 представляет собой алкил или алкенил. Термин низший алкоксиалкил относится к алкоксиалкилу, где alk1 представляет собой низший алкил или низший алкенил, и alk2 представляет собой низший алкил или низший алкенил. Термин арилоксиалкил относится к группе -алкил-О-арил. Термин аралкоксиалкил относится к группе -алкиленил-О-аралкил, где аралкил представляет собой низший аралкил. Термин алкоксиалкиламино относится в данном описании к группе -NR-(алкоксиалкил), где R обычно представляет собой водород, низший аралкил или низший алкил. Термин амино-низший алкоксиалкил относится в данном описании к аминоалкоксиалкилу, в котором алкоксиалкил представляет собой низший алкоксиалкил. Термин аминокарбонил относится в данном описании к группе -C(O)-NH2. Термин замещенный аминокарбонил относится в данном описании к группе -C(O)-NRR', где R представляет собой низший алкил, и R' представляет собой водород или низший алкил. Термин ариламинокарбонил относится в данном описании к группе -C(O)-NRR', где R представляет собой арил, и R' представляет собой водород,низший алкил или арил. Термин аралкиламинокарбонил относится в данном описании к группе -C(O)NRR', где R представляет собой низший аралкил, и R' представляет собой водород, низший алкил, арил или низший аралкил. Термин аминосульфонил относится в данном описании к группе -S(O)2-NH2. Термин замещенный аминосульфонил относится в данном описании к группе -S(O)2-NRR', где R представляет собой низший алкил, и R' представляет собой водород или низший алкил. Термин аралкиламиносульфониларил относится в данном описании к группе -арил-S(О)2-NH-аралкил, где аралкил представляет собой низший аралкил. Термин карбонил относится к двухвалентной группе -С(О)-. Термин карбонилокси относится в общем к группе -С(О)-О. Такие группы включают сложные эфиры, -C(O)-O-R, где R представляет собой низший алкил, циклоалкил, арил или низший аралкил. Термин карбонилоксициклоалкил относится в данном описании в общем как к карбонилоксикарбоциклоалкилу, так и к карбонилоксигетероциклоалкилу, т.е. где R представляет собой карбоциклоалкил или гетероциклоалкил, соответственно. Термин арилкарбонилокси относится в данном описании к группе-С(О)-О-арил, где арил представляет собой моно- или полициклический карбоциклоарил или гетероциклоарил. Термин аралкилкарбонилокси относится в данном описании к группе -С(О)-О-аралкил, где аралкил представляет собой низший аралкил. Термин сульфонил относится в данном описании к группе -SO2-. Термин алкилсульфонил относится к замещенному сульфонилу структуры -SO2R-, в которой R представляет собой алкил. Алкилсульфонильные группы, используемые в соединениях по настоящему изобретению, обычно представляют собой низшие алкилсульфонильные группы, имеющие от 1 до 5 атомов углерода в структуре основной цепи. Таким образом, типичные алкилсульфонильные группы, используемые в соединениях по настоящему изобретению, включают, например, метилсульфонил (т.е., где R представляет собой метил),этилсульфонил (т.е., где R представляет собой этил), пропилсульфонил (т.е., где R представляет собой пропил) и тому подобные. Термин арилсульфонил относится в данном описании к группе -SO2-арил. Термин аралкилсульфонил относится в данном описании к группе -SO2-аралкил, в которой аралкил представляет собой низший аралкил. Термин сульфонамидо относится в данном описании к группе SO2NH2. В данном описании термин карбониламино относится к двухвалентной группе -NH-C(O)-, в которой атом водорода у амидного азота карбониламино-группы может быть заменен на низшую алкильную, арильную или низшую аралкильную группу. Такие группы включают такие фрагменты как карбаматные сложные эфиры (-NH-C(O)-O-R) и амиды -NH-C(О)-O-R, где R представляет собой линейный или разветвленный низший алкил, циклоалкил или арил, или низший аралкил. Термин низший алкилкарбониламино относится к алкилкарбониламино-группе, где R представляет собой низший алкил,имеющий от 1 до примерно 6 атомов углерода в основной структуре. Термин арилкарбониламино относится к группе -NH-C(O)-R, где R представляет собой арил. Аналогично, термин аралкилкарбониламино относится к карбониламино-группе, где R представляет собой низший аралкил. Как использовано в данном описании, термин аминокарбонил относится к двухвалентной группе -С(О)-NH-, в которой атом водорода у амидного азота в карбониламино группе может быть заменен на низшую алкильную,арильную или низшую аралкильную группу, как описано выше. В данном описании термин гуанидино или гуанидил относится к фрагментам, полученным из гуанидина, H2N-C(=NH)-NH2. Такие фрагменты включают те, которые связаны по атому азота, имеющему формальную двойную связь (положение 2-гуанидина, например, диаминометиленамино,-6 011890(H2N)2C=NH-), и связанные по любому атому азота, имеющему формальную одинарную связь (1 и/или 3-положения гуанидина, например, H2N-C(=NH)-NH-). Атомы водорода при любом из атомов азота могут быть замещены подходящими заместителями, такими как низший алкил, арил или низший аралкил. В данном описании термин амидино относится к фрагментам R-C(=N)-NR'- (радикал, находящийся при азоте N1) и R(NR')C=N- (радикал, находящийся при азоте N2), где R и R' могут представлять собой водород, низший алкил, арил или низший аралкил. Термин циклоалкил относится к моно- или полициклическому, гетероциклическому или карбоциклическому алькильному заместителю. Типичные циклоалкильные заместители содержат от 3 до 8 атомов основного фрагмента (т.е. кольца), в которых каждый атом фрагмента представляет собой или углерод или гетероатом. Термин гетероциклоалкил относится в данном описании к циклоалкильным заместителям, которые имеют от 1 до 5 и более обычно от 1 до 4 гетероатомов в кольцевой структуре. Подходящие гетероатомы, используемые в соединениях по настоящему изобретению, представляют собой азот, кислород и серу. Иллюстративные гетероциклоалкильные фрагменты включают, например,морфолино, пиперазинил, пиперадинил и тому подобные. Карбоциклоалкильные группы представляют собой циклоалкильные группы, в которых все кольцевые атомы представляют собой углерод. При использовании в связи с циклоалкильными заместителями, термин полициклический относится в данном описании к конденсированным и неконденсированным алкильным циклическим структурам. Термин замещенный гетероцикл или гетероциклическая группа или гетероцикл согласно данному описанию относится к любому 3- или 4-членному циклу, содержащему гетероатом, выбранный из азота, кислорода и серы, или 5- или 6-членному кольцу, содержащему от одного до трех гетероатомов,выбранных из группы, состоящей из азота, кислорода или серы; где 5-членное кольцо имеет 0-2 двойных связи, и 6-членное кольцо содержит 0-3 двойных связи; где атом азота и серы необязательно могут быть окислены; где гетероатомы азота и серы необязательно могут быть кватернизованы; и включает любую бициклическую группу, в которой любое из вышеуказанных гетероциклических колец конденсировано с бензольным кольцом или другим 5- или 6-членным гетероциклическим кольцом, независимо определенным выше. Термин гетероцикл таким образом включает кольца, в которых азот представляет собой гетероатом, а также частично и полностью насыщенные кольца. Предпочтительные гетероциклы включают, например диазапинил, пиррил, пирролинил, пирролидинил, пиразолил, пиразолинил, пиразолидинил, имидазоил, имидазолинил, имидазолидинил, пиридил, пиперидинил, пиразинил, пиперазинил, Nметилпиперазинил, азетидинил, N-метилазетидинил, пиримидинил, пиридазинил, оксазолил, оксазолидинил, изоксазолил, изоазолидинил, морфолинил, тиазолил, тиазолидинил, изотиазолил, изотиазолидинил, индолил, хинолинил, изохинолинил, бензимидазолил, бензотиазолил, бензоксазолил, фурил, тиенил,триазолил и бензотиенил. Гетероциклические фрагменты могут быть незамещенными или монозамещенными, или дизамещенными различными заместителями, независимо выбранными из гидроксила, гелогена, оксо (С=O),алкилимино (RN=, где R представляет собой низшую алкильную или низшую алкоксильную группу),амино, алкиламино, диалкиламино, ациламиноалкила, алкокси, тиоалкокси, полиалкокси, низшего алкила, циклоалкила или галогеналкила. Гетероциклические группы могут быть присоединены в различных положениях, как будет очевидно специалисту в области органической и медицинской химии в сочетании с настоящим описанием. где R представляет собой Н или гетероциклический заместитель, как указано в данном описании. Иллюстративные гетероциклы включают, например, имидазолил, пиридил, пиперазинил, азетидинил, тиазолил, фуранил, триазолил, бензимидазолил, бензотиазолил, бензоксазолил, хинолинил, изохинолинил, хиназолинил, хиноксалинил, фталазинил, индолил, нафтпиридинил, индазолил и хинолизинил. Термин арил относится к необязательно замещенным моноциклическим и полициклическим аро-7 011890 матическим группам, имеющим от 3 до 13 атомов углерода или гетероатомов, и включает как карбоциклические арильные группы, так и гетероциклические арильные группы. Карбоциклические арильные группы представляют собой арильные группы, в которых все кольцевые атомы в ароматическом кольце являются углеродами. Термин гетероарил относится в данном описании к арильным группам, имеющим от 1 до 4 гетероатомов в качестве кольцевых атомов ароматического кольца, тогда как оставшиеся кольцевые атомы представляют собой атомы углерода. При использовании в связи с арильными заместителями, термин полициклический арил относится в данном описании к конденсированным и неконденсированным циклическим структурам, где по меньшей мере одна циклическая структура является ароматической,таким как, например, бензодиоксозоло (который имеет гетероциклическую структуру, конденсирован), нафтил и тому подобные. Иллюстративные арильные фрагменную с фенильной группой, т.е.,ты, использованные в качестве заместителей в соединениях настоящего изобретения, включают фенил,пиридил, пиримидинил, тиазолил, индолил, имидазолил, оксадиазолил, тетразолил, пиразинил, триазолил, тиофенил, фуранил, хинолинил, пуринил, нафтил, бензотиазолил, бензопиридил и бензимидазолил,и тому подобные. Термин аралкил относится к алкильной группе, замещенной арильной группой. Обычно аралкильные группы, используемые в соединениях по настоящему изобретению, имеют от 1 до 6 атомов углерода, включенных в алкильную часть аралкильной группы. Подходящие аралкильные группы, используемые в соединениях по настоящему изобретению, включают, например, бензил, пиколил и тому подобные. Иллюстративные гетероарильные группы включают, например, те, которые представлены ниже. Данные гетероарильные группы могут быть дополнительно замещены и могут быть присоединены в различных положениях, как будет очевидно специалисту в области органической и медицинской химии в сочетании с настоящим описанием. Иллюстративные гетероарилы включают, например, имидазолил, пиридил, пиперазинил, азетидинил, тиазолил, триазолил, бензимидазолил, бензотиазолил и бензоксазолил. Термин биарил относится к группе или заместителю, с которым связаны две арильные группы, не сконденсированные друг с другом. Иллюстративные биарильные соединения включают, например, фенилбензол, дифенилдиазен, 4-метилтио-1-фенилбензол, феноксибензол, (2-фенилэтинил)бензол, дифенилкетон, (4-фенилбута-1,3-диинил)бензол, фенилбензиламин, (фенилметокси)бензол и тому подобные. Предпочтительные необязательно замещенные биарильные группы включают 2-(фениламино)-N-[4-(2 фенилэтинил)фенил]ацетамид, 1,4-дифенилбензол, N-[4-(2-фенилэтинил)фенил]-2-[бензиламино]ацетамид, 2-амино-М-[4-(2-фенилэтинил)фенил]пропанамид, 2-амино-N-[4-(2-фенилэтинил)фенил]ацетамид,2-(циклопропиламино)-N-[4-(2-фенилэтинил)фенил]ацетамид, 2-(этиламино)-N-[4-(2-фенилэтинил)фенил]ацетамид, 2-[(2-метилпропил)амино]-N-[4-(2-фенилэтинил)фенил]ацетамид, 5-фенил-2 Н-бензо[d] 1,3-диоксолен, 2-хлор-1-метокси-4-фенилбензол, 2-[(имидазолилметил)амино]-N-[4-(2-фенилэтинил) фенил]ацетамид, 4-фенил-1-феноксибензол, N-(2-аминоэтил)-[4-(2-фенилэтинил)фенил]карбоксамид, 2[(4-фторфенил)метил]амино-N-[4-(2-фенилэтинил)фенил]ацетамид, 2-[(4-метилфенил)метил]аминоN-[4-(2-фенилэтинил)фенил]ацетамид, 4-фенил-1-(трифторметил)бензол, 1-бутил-4-фенилбензол, 2(циклогексиламино)-N-[4-(2-фенилэтинил)фенил]ацетамид, 2-(этилметиламино)-N-[4-(2-фенилэтинил)-8 011890 фенил]ацетамид, 2-(бутиламино)-N-[4-(2-фенилэтинил)фенил]ацетамид, N-[4-(2-фенилэтинил)фенил]-2(4-пиридиламино)ацетамид, N-[4-(2-фенилэтинил)фенил]-2-(хинуклидин-3-иламино)ацетамид, N-[4-(2 фенилэтинил)фенил]пирролидин-2-илкарбоксамид, 2-амино-3-метил-N-[4-(2-фенилэтинил)фенил]бутанамид, 4-(4-фенилбута-1,3-диинил)фениламин, 2-(диметиламино)-N-[4-(4-фенилбута-1,3-диинил)фенил] ацетамид, 2-(этиламино)-N-[4-(4-фенилбута-1,3-диинил)фенил]ацетамид, 4-этил-1-фенилбензол, 1-[4-(2 фенилэтинил)фенил]этан-1-он,N-(1-карбамоил-2-гидроксипропил)[4-(4-фенилбута-1,3-диинил)фенил] карбоксамид, N-[4-(2-фенилэтинил)фенил]пропанамид, 4-метоксифенилфенилкетон, фенил-N-бензамид,(трет-бутокси)-N-[(4-фенилфенил)метил]карбоксамид, 2-(3-фенилфенокси)этангидроксамовую кислоту,3-фенилфенилпропаноат, 1-(4-этоксифенил)-4-метоксибензол и [4-(2-фенилэтинил)фенил]пиррол. Термин гетероариларил относится к биарильной группе, где одна из арильных групп представляет собой гетероарильную группу. Иллюстративные гетероариларильные группы включают, например, 2 фенилпиридин, фенилпиррол, 3-(2-фенилэтинил)пиридин, фенилпиразол, 5-(2-фенилэтинил)-1,3 дигидропиримидин-2,4-дион, 4-фенил-1,2,3-тиадиазол, 2-(2-фенилэтинил)пиразин, 2-фенилтиофен, фенилимидазол, 3-(2-пиперазинилфенил)фуран, 3-(2,4-дихлорфенил)-4-метилпиррол и тому подобные. Предпочтительные необязательно замещенные гетероариларильные группы включают 5-(2-фенилэтинил)пиримидин-2-иламин, 1-метокси-4-(2-тиенил)бензол, 1-метокси-3-(2-тиенил)бензол, 5-метил-2 фенилпиридин, 5-метил-3-фенилизоксазол, 2-[3-(трифторметил)фенил]фуран, 3-фтор-5-(2-фурил)-2 метокси-1-проп-2-енилбензол, (гидроксиимино)(5-фенил(2-тиенилметан, 5-[(4-метилпиперазинил)метил]-2-фенилтиофен, 2-(4-этилфенил)тиофен, 4-метилтио-1-(2-тиенил)бензол, 2-(3-нитрофенил) тиофен,(трет-бутокси)-N-[(5-фенил(3-пиридилметил]карбоксамид,гидрокси-N-[(5-фенил(3-пиридил метил]амид, 2-(фенилметилтио)пиридин и бензилимидазол. Термин гетероарилгетероарил относится к биарильной группе, где обе арильные группы представляют собой гетероарильную группу. Иллюстративные гетероарилгетероарильные группы включают,например, 3-пиридилимидазол, 2-имидазолилпиразин, и тому подобные. Предпочтительно необязательно замещенные гетероарилгетероарильные группы включают: 2-(4-пиперазинил-3-пиридил)фуран, диэтил(3-пиразин-2-ил (4-пиридил) ) амин и диметил 2-[2-(5-метилпиразин-2-ил)этинил](4-пиридил)амин. Термин необязательно замещенный или замещенный относится к замещению одного или нескольких атомов водорода на одновалентный или двухвалентный радикал. Подходящие замещающие группы включают, например, гидроксил, нитро, амино, имино, циано, галоген, тио, сульфонил, тиоамидо, амидино, имидино, оксо, оксамидино, метоксамидино, имидино, гуанидино, сульфонамидо, карбоксил, формил, низший алкил, низший галогеналкил, низший алкиламино, низший галогеналкиламино,низший алкокси, низший галогеналкокси, низший алкоксиалкил, алкилкарбонил, аминокарбонил, арилкарбонил, аралкилкарбонил, гетероарилкарбонил, гетероаралкилкарбонил, алкилтио, аминоалкил, цианоалкил, арил и тому подобные. Замещающая группа сама по себе может быть замещенной. Группа, находящаяся в качестве заместителя в замещающей группе, может представлять собой карбоксил, галоген, нитро, амино, циано, гидроксил, низший алкил, низший алкокси, аминокарбонил, -SR, тиоамидо, -SO3H, -SO2R или циклоалкил,где R обычно представляет собой водород, гидроксил или низший алкил. Когда замещенный заместитель включает линейную группу, замещение может происходить либо внутри цепи (например, 2-гидроксипропил, 2-аминобутил и тому подобные) или на конце цепи (например, 2-гидроксиэтил, 3-цианопропил и тому подобные). Подходящие заместители могут быть линейными, разветвленными или циклическими фрагментами, состоящими из ковалентно связанных атомов углерода или гетероатомов. В данном описании термин защитная группа карбоксила относится к карбонильной группе, которая была этерифицирована с использованием одной из обычно используемых защитных сложноэфирных групп для карбоновых кислот, применяемых для блокирования или защиты функции карбоновой кислоты во время проведения реакций, включающих другие функциональные группы соединения. Кроме того,защитная группа карбоксила может быть присоединена в твердой подложке, при этом соединения остаются связанными с твердой подложкой в виде карбоксилатов до проведения отщепления гидролитическими способами для высвобождения соответствующей свободной кислоты. Иллюстративные карбоксизащитные группы включают, например, низшие алкиловые сложные эфиры, вторичные амиды и тому подобное. В данном описании термин фармацевтически приемлемые соли относится к солям соединений формулы I с нетоксичными кислотами и щелочно-земельными металлами. Данные соли могут быть получены in situ во время конечного выделения и очистки соединений формулы I или при отдельном взаимодействии основных или кислотных функций соединения с подходящей органической или неорганической кислотой или основанием, соответственно. Иллюстративные соли включают, но не ограничиваются указанным: ацетат, адипат, альгинат, цитрат, аспартат, бензоат, бензолсульфонат, бисульфат, бутират,камфорат, камфорсульфонат, диглюконат, циклопентанпропионат, додецилсульфат, этансульфонат, глюкогептаноат, глицерофосфат, полусульфат, гептаноат, гексаноат, фумарат, гидрохлорид, гидробромид,гидроиодид, 2-гидроксиэтансульфонат, лактат, малеат, метансульфонат, никотинат, 2-нафталинсульфонат, оксалат, памоат, пектинат, персульфат, 3-фенилпропионат, пикрат, пивалат, пропионат, сук-9 011890 цинат, сульфат, тартрат, тиоцианат, п-толуолсульфонат и ундеканоат. Также основные азотсодержащие группы могут быть кватернизованы такими агентами, как низшие алкилгалогениды, такие как метил,этил, пропил и бутилхлориды, бромиды и иодиды; диалкилсульфаты, такие как диметил, диэтил, дибутил и диамилсульфаты, длинноцепочечными галогенидами, такими как децил, лаурил, миристил и стеарилхлориды, бромиды и иодиды, аралкилгалогенидами, такими как бензил и фенэтил бромиды и другими. Таким образом, получают растворимые или диспергируемые в воде или масле продукты. Примеры кислот, которые могут использоваться для образования фармацевтически приемлемых аддитивных солей, включают такие неорганические кислоты, как хлористо-водородная кислота, серная кислота и фосфорная кислота и такие органические кислоты, как щавелевая кислота, малеиновая кислота, метансульфоновая кислота, янтарная кислота и лимонная кислота. Основные аддитивные соли могут быть получены in situ во время конечного выделения и очистки соединений формулы (I) или отдельно,путем взаимодействия фрагментов карбоновых кислот с подходящими основаниями, такими как гидроксид, карбонат или бикарбонат фармацевтически приемлемого катиона металла, или с аммиаком, или органическим первичным, вторичным или третичным амином. Фармацевтически приемлемые соли включают, но не ограничиваются указанным, катионы на основе щелочных или щелочно-земельных металлов, такие как натрий, литий, калий, кальций, магний, соли алюминия и тому подобное, а также нетоксичные катионы аммония, четвертичного аммония и амина, включая, но не ограничиваясь указанным,аммоний, тетраметиламмоний, тетраэтиламмоний, метиламин, диметиламин, триметиламин, триэтиламин, этиламин и тому подобные. Другие иллюстративные органические амины, используемые при образовании основно-аддитивных солей, включают диэтиламин, этилендиамин, этаноламин, диэтаноламин,пиперазин и тому подобные. В данном описании термин фармацевтически приемлемый сложный эфир относится к сложным эфирам, которые гидролизуются in vivo, и которые легко расщепляются в организме человека с образованием исходного соединения или его соли. Подходящие сложноэфирные группы включают, например,полученные из фармацевтически приемлемых алифатических карбоновых кислот, в частности алкановых, алкеновых, циклоалкановых и алкандикарбоновых кислот, в которых каждый алкильный или алкенильный фрагмент преимущественно содержит не более 6 атомов углерода. Примеры конкретных сложных эфиров включают формиаты, ацетаты, пропионаты, бутираты, акрилаты и этилсукцинаты. Термин фармацевтически приемлемые пролекарства в данном описании относится к тем пролекарствам соединений по настоящему изобретению, которые в рамках тщательного медицинского подхода являются подходящими для применения в контакте с тканями человека и низших животных без проявления неспецифической токсичности, раздражения, аллергической ответной реакции и тому подобного, соответствуют разумному соотношению выигрыш/риск и эффективны для предназначенного применения, а также цвиттерионным формам, где это возможно, соединений по изобретению. Термин пролекарство относится к соединениям, которые легко трансформируются in vivo с образованием исходного соединения вышеуказанной формулы, например, посредством гидролиза в крови. Подробное обсуждение приведено в публикациях Т. Higuchi и V. Stella, Pro-drugs as Novel Delivery Systems, том 14, A.C.S. Symposium Series, и Edward B. Roche, ред., Bioreversible Carriers in Drug Design, American Pharmaceutical Association and Pergamon Press, 1987, обе из которых включены в данное описание путем ссылки. Термин рак относится к раковым заболеваниям, которые благоприятным образом поддаются лечению при ингибировании Raf-киназы, например, плотные опухоли, такие как карциномы (например,легких, поджелудочной железы, щитовидной железы, мочевого пузыря или прямой кишки), миелоидные нарушения (например, миелоидная лейкемия) и аденомы (например, волосатый полип толстой кишки). В иллюстративных вариантах осуществления изобретения А 1 может представлять собой, например,фенил, пиридил, пиримидинил, фенилалкил, пиридилалкил, пиримидинилалкил, гетероциклокарбонилфенил, гетероциклофенил, гетероциклоалкилфенил, хлорфенил, фторфенил, бромфенил, йодфенил, дигалогенфенил, нитрофенил, 4-бромфенил, 4-хлорфенил, алкилбензоат, алкоксифенил, диалкоксифенил,диалкилфенил, триалкилфенил, тиофен, тиофен-2-карбоксилат, алкилтиофенил, трифторметилфенил,ацетилфенил, сульфамоилфенил, бифенил, циклогексилфенил, фенилоксифенил, диалкиламинофенил,алкилбромфенил, алкилхлорфенил, алкилфторфенил, трифторметилхлорфенил, трифторметилбромфенил, инденил, 2,3-дигидроинденил, тетралинил, трифторфенил, (трифторметил)тиофенил, алкоксибифенил, морфолинил, N-пиперазинил, N-морфолинилалкил, пиперазинилалкил, циклогексилалкил, индолил,2,3-дигидроиндолил, 1-ацетил-2,3-дигидроиндолил, циклогептил, бицикло[2.2.1]гепт-2-ил, гидроксифенил,гидроксиалкилфенил,пирролидинил,пирролидин-1-ил,пирролидин-1-илалкил,4 амино(имино)метилфенил, изоксазолил, индазолил, адамантил, бициклогексил, хинуклидинил, имидазолил, бензимидазолил, имидазолилфенил, фенилимидазолил, фталамидо, нафтил, бензофенон, анилинил,анизолил, хинолинил, хинолинонил, фенилсульфонил, фенилалкилсульфонил, 9 Н-флуорен-1-ил, пиперидин-1-ил, пиперидин-1-илалкил, циклопропил, циклопропилалкил, пиримидин-5-илфенил, хинолидинилфенил, фуранил, фуранилфенил, N-метилпиперидин-4-ил, пирролидин-4-илпиридинил, 4-диазепан-1 ил, гидроксипирролидин-1-ил, диалкиламинопирролидин-1-ил, 1,4'-бипиперидин-1'-ил или (1,4'бипиперидин-1'-илкарбонил)фенил, которые могут быть замещены одним или несколькими заместителями, выбранными из группы, включающей гидроксил, нитро, циано, галоген и замещенный или неза- 10011890 мещенный амино, имино, тио, сульфонил, тиоамидо, амидино, имидино, оксо, оксамидино, метоксамидино, имидино, гуанидино, сульфонамидо, карбоксил, формил, низший алкил, галоген-низший алкил,низший алкиламино, галоген-низший алкиламино, низший алкокси, галоген-низший алкокси, низший алкоксиалкил, алкилкарбонил, аминокарбонил, низший алкиламинокарбонил, гетероциклоалкил-низший алкиламинокарбонил, карбоксил-низший алкиламинокарбонил, арилкарбонил, аралкилкарбонил, гетероарилкарбонил, гетероаралкилкарбонил, алкилтио, аминоалкил, цианоалкил, арил и тому подобные. В некоторых особенно предпочтительных вариантах осуществления A1 представляет собой замещенный или незамещенный фенил. В других иллюстративных вариантах осуществления изобретения, А 2 может представлять собой, например, пиридил, который может быть замещен одним или несколькими заместителями, выбранными из группы, включающей гидроксил, нитро, циано, галоген и замещенный или незамещенный амино, имино, тио, сульфонил, тиоамидо, амидино, имидино, оксо, оксамидино, метоксамидино, имидино, гуанидино, сульфонамидо, карбоксил, формил, низший алкил, галоген-низший алкил,низший алкиламино, галоген-низший алкиламино, низший алкокси, галоген-низший алкокси, низший алкоксиалкил, алкилкарбонил, аминокарбонил, низший алкиламинокарбонил, гетероциклоалкил-низший алкиламинокарбонил, карбоксил-низший алкиламинокарбонил, арилкарбонил, аралкилкарбонил, гетероарилкарбонил, гетероаралкилкарбонил, алкилтио, аминоалкил, цианоалкил, арил и тому подобные. В иллюстративных вариантах осуществления изобретения, соединения по изобретению включают, например,4-[(2-[4-хлор-3-(трифторметил)фенил]амино-1 Н-бензимидазол-6-ил)окси]-N-метилпиридин-2 карбоксамид, 4-(2-[(3-хлорфенил)амино]-1 Н-бензимидазол-6-илокси)-N-метилпиридин-2-карбоксамид, 4(2-[(4-бромфенил)амино]-1 Н-бензимидазол-6-илокси)-N-метилпиридин-2-карбоксамид,4-(2-[(3-хлор-4 фторфенил)амино]-1 Н-бензимидазол-6-илокси)-N-метилпиридин-2-карбоксамид, N-метил-4-[2-(фениламино)-1 Н-бензимидазол-6-ил]оксипиридин-2-карбоксамид, 4-[(2-[4-бром-2-(трифторметил)фенил]амино-1 Нбензимидазол-6-ил)окси]-N-метилпиридин-2-карбоксамид, N-метил-4-(2-[(2-метилпропил)амино]-1 Н-бензимидазол-6-илокси)пиридин-2-карбоксамид, 4-[(2-[4-(диметиламино)нафталин-1-ил]амино-1 Н-бензимидазол-6-ил)окси]-N-метилпиридин-2-карбоксамид, N-метил-4-(2-[(4-нитрофенил)амино]-1 Н-бензимидазол-6 илокси)пиридин-2-карбоксамид, N-метил-4-(2-[(фенилкарбонил) амино]-1 Н-бензимидазол-6-илокси)пиридин-2-карбоксамид, N-метил-4-(2-[(фенилметил)амино]-1 Н-бензимидазол-6-илокси)пиридин-2-карбоксамид, метил-4-[6-2-[(метиламино)карбонил]пиридин-4-илокси-1 Н-бензимидазол-2-ил]аминобензоат, 4(2-[(4-хлорфенил)амино]-1 Н-бензимидазол-6-илокси)-N-метилпиридин-2-карбоксамид, 4-[(2-[2-(этилокси) фенил]амино-1 Н-бензимидазол-6-ил)окси]-N-метилпиридин-2-карбоксамид, N-метил-4-(2-[(2-морфолин-4 илэтил)амино]-1 Н-бензимидазол-6-илокси) пиридин-2-карбоксамид, 4-(2-[(4-йодфенил)амино]-1 Н-бензимидазол-6-илокси)-N-метилпиридин-2-карбоксамид,N-метил-4-[(2-[4-(трифторметил)фенил]амино-1 Нбензимидазол-6-ил)окси]пиридин-2-карбоксамид,4-(2-[(фуран-2-илметил)амино]-1 Н-бензимидазол-6-ил окси)-N-метилпиридин-2-карбоксамид, 4-(2-[(4-бром-3-метилфенил)амино]-1 Н-бензимидазол-6-илокси)-Nметилпиридин-2-карбоксамид, 4-(2-[(4-ацетилфенил)амино]-1 Н-бензимидазол-6-илокси)-N-метилпиридин 2-карбоксамид, N-метил-4-(2-[(2,4,6-триметилфенил)амино]-1 Н-бензимидазол-6-илокси)пиридин-2-карбоксамид,4-[(2-[4-(1,1-диметилэтил)фенил]амино-1 Н-бензимидазол-6-ил)окси]-N-метилпиридин-2-карбоксамид, 4-(2-[(2-бромфенил)амино]-1 Н-бензимидазол-6-илокси)-N-метилпиридин-2-карбоксамид, 4-(2-[(3 бромфенил)амино]-1 Н-бензимидазол-6-илокси)-N-метилпиридин-2-карбоксамид, 4-(2-[(2-хлорфенил)амино]-1 Н-бензимидазол-6-илокси)-N-метилпиридин-2-карбоксамид, метил-3-[6-(2-[(метиламино)карбонил] пиридин-4-илокси)-1 Н-бензимидазол-2-ил]аминотиофен-2-карбоксилат, 4-(2-[(4-бромфенил)амино]-1 Нбензимидазол-6-илокси)-N-(3R,5R)-5-[(метилокси)метил]пирролидин-3-илпиридин-2-карбоксамид, 4-(2[(4-бромфенил)амино]-1-метил-1 Н-бензимидазол-5-илокси)-N-метилпиридин-2-карбоксамид, 4-[(2-[4-хлор 3-(трифторметил)фенил]амино-1-метил-1 Н-бензимидазол-5-ил)окси]-N-метилпиридин-2-карбоксамид,Nметил-4-[(1-метил-2-[4-(трифторметил)фенил]амино-1 Н-бензимидазол-5-ил)окси]пиридин-2-карбоксамид,4-(2-[(4-бромфенил)амино]-1-метил-1 Н-бензимидазол-5-илокси)-N-этилпиридин-2-карбоксамид, 4-(2-[(4 бромфенил)амино]-1-метил-1 Н-бензимидазол-5-илокси)-N-(2-гидроксиэтил)пиридин-2-карбоксамид, 4-(2[(4-бромфенил)амино]-1-метил-1 Н-бензимидазол-5-илокси)-N,N-диметилпиридин-2-карбоксамид, 4-(2-[(4 бромфенил)амино]-1-метил-1 Н-бензимидазол-5-илокси)-N-(2,2,2-трифторэтил)пиридин-2-карбоксамид, N(4-бромфенил)-1-метил-5-[2-(пирролидин-1-илкарбонил)пиридин-4-ил]окси-1 Н-бензимидазол-2-амин,этил-(3R)-3-(метилокси)-4-[(4-[(2-[4-(трифторметил)фенил]амино-1 Н-бензимидазол-5-ил)окси]пиридин-2 илкарбонил)амино]пиперидин-1-карбоксилат, 4-(2-[(4-бромфенил)амино]-1-метил-1 Н-бензимидазол-5-ил окси)-N-[2-(диметиламино)этил]пиридин-2-карбоксамид,4-(2-[(4-бромфенил)амино]-1-метил-1 Н-бензимидазол-5-илокси)-N-(тетрагидрофуран-2-илметил)пиридин-2-карбоксамид, 4-2-[(4-бромфенил)амино]-1 метил-1 Н-бензимидазол-5-илокси)-N-(2-морфолин-4-илэтил)пиридин-2-карбоксамид, 4-(2-[(4-бромфенил) амино]-1-метил-1 Н-бензимидазол-5-илокси)-N-(пиперидин-4-илметил)пиридин-2-карбоксамид,5-(2-[(3 аминопирролидин-1-ил)карбонил]пиридин-4-илокси)-N-(4-бромфенил)-1-метил-1 Н-бензимидазол-2-амин, 4(2-[(4-бромфенил)амино]-1-метил-1 Н-бензимидазол-5-илокси)-N-[1-(дифенилметил)азетидин-3-ил]пиридин-2-карбоксамид,4-(2-[(4-бромфенил)амино]-1-метил-1 Н-бензимидазол-5-илокси)-N-пиперидин-3-илпиридин-2-карбоксамид, 4-(2-[(4-бромфенил)амино]-1-метил-1 Н-бензимидазол-5-илокси)-N-(1,3-тиазол-2 ил)пиридин-2-карбоксамид и 4-(2-[(4-бромфенил)амино]-1-метил-1 Н-бензимидазол-5-илокси)-N-[(1-этилпирролидин-2-ил)метил]пиридин-2-карбоксамид, (4-2-[(4-бромфенил)амино]бензотиазол-5-илокси(2-пири- 11011890 дил-N-метилкарбоксамид, (4-2-[(4-бромфенил)амино]бензоксазол-5-илокси-(2-пиридил-N-метилкарбоксамид и другие иллюстративные соединения, указанные в примерах. В других аспектах, настоящее изобретение относится к способам получения соединений формул I,II, III, IV и V и промежуточным соединениям их синтеза, используемым в данных способах. Соединения по изобретению включают асимметрически замещенные атомы углерода. Такие асимметрически замещенные атомы углерода могут приводить к соединениям по изобретению, включающим смеси стереоизомеров за счет конкретного асимметрически замещенного атома углерода или единственный стероизомер. В результате настоящее изобретение включает рацемические смеси, смеси диастереомеров, а также отдельные диастереомеры соединений по изобретению. Термины S и R конфигурация, как они использованы в данном описании, определены правилами ИЮПАК 1974 г., "IUPAC RECOMMENDATIONS FOR SECTION E, FUNDAMENTAL STEREOCHEMISTRY, Pure Appl. Chem. 45: 1330 (1976). Терминыииспользуются для указания положений кольца в циклических соединений. Термин -сторона упоминаемой плоскости относится к стороне, на которой располагается предпочтительный заместитель, имеющий наименьшее пронумерованное положение. Те заместители, которые располагаются на противоположной стороне упоминаемой плоскости обозначены дескриптором . Следует отметить, что данное применение отличается от такового для циклических исходных стереосоединений,в которых обозначениеозначает ниже плоскости и указывает на абсолютную конфигурацию. Термины - и -конфигурации, как они использованы в данном описании, определены в параграфе 203, приложения IV (1987) Индексного указателя CHEMICAL ABSTRACTS [CHEMICAL ABSTRACTS INDEXGUIDE-APPENDIX IV (1987), параграф 203]. Настоящее изобретение также относится к способам получения соединений по изобретению и к синтетическим промежуточным соединениям, используемым в таких способах, как подробно описано ниже. Методы синтеза Соединения по изобретению, содержащие бензимидазольное ядро, могут быть получены с использованием ряда способов, известных специалистам в данной области. В одном способе, подходящим образом функционализированные диамины могут быть соединены с различными тиоизоцианатами с образованием промежуточных тиомочевин. Циклизация с образованием бензимидазольного фрагмента может быть осуществлена при известных условиях, например, при обработке карбодиимидами или алкилгалогенидами, как на следующих схемах.- 12011890 Альтернативно, диамины можно последовательно подвергать взаимодействию с карбонилдимиазолом и хлоридом фосфора с последующей конденсацией с использованием подходящего амина. Соединения, содержащие структуру оксазола, могут быть получены аналогичным образом в соответствии с вышеуказанными способами и в соответствии с другими известными способами. Haviv и др.(J. Med. Chem. 1988, 31: 1719) описали способ сборки оксазольных ядер, в котором гидроксианилин обрабатывают этилксантаном калия. Полученный сульфурилсодержащий бензоксазол затем может быть хлорирован и связан с амином. Соединения, содержащие бензотиазольное ядро, также могут быть получены в соответствии с известными способами. Орто-галогентиоизоцианат может быть подвергнут взаимодействию с амином с образованием тиомочевины. Затем восстановление с использованием NaH приводит к образованию тиазольного кольца. Бензотиазолы обычно могут быть замещены в соответствии с настоящим изобретением, например,в соответствии со следующим путем синтеза: Бензоксазолы обычно могут быть получены в соответствии со следующим путем синтеза Соединения по изобретению могут использоваться in vitro или in vivo для ингибирования роста раковых клеток. Соединения могут использоваться сами по себе или в композициях вместе с фармацевтически приемлемым носителем или эксципиентом. Подходящие фармацевтически приемлемые носители или эксципиенты включают, например, агенты переработки и модификаторы и усилители доставки лекарственных средств, такие как, например, фосфат кальция, стеарат магния, тальк, моносахариды, дисахариды, крахмал, желатин, целлюлоза, метилцеллюлоза, карбоксиметилцеллюлоза натрия, декстроза,гидроксипропил-п-циклодекстрин, поливинилпирролидинон, низкоплавкие воски, ионообменные смолы и тому подобные, а также комбинации любых двух или больше из них. Другие подходящие фармацевтически приемлемые эксципиенты описаны в Remington's Pharmaceutical Sciences, Mack Pub. Co., NewJersey (1991), включенной в данное описание путем ссылки. Эффективные количества соединений по изобретению обычно включают любое количество, достаточное для ингибирования активности Raf, обнаруживаемого с помощью любого из описанных в данном описании анализов, с помощью других анализов активности Raf-киназы, известными специалистам в данной области или путем обнаружения ингибирования или облегчения симптомов рака. Количество активного ингредиента, которое может быть объединено с материалами носителя для получения единичной препаративной лекарственной формы, будет изменяться в зависимости от подвергаемого лечению хозяина и конкретного пути введения. Однако следует понимать, что конкретный уровень дозировки для любого конкретного пациента будет зависеть от множества факторов, включая активность конкретных используемых соединений, возраста, веса тела, общего состояния здоровья, пола,питания, времени введения, пути введения, скорость выведения, комбинации лекарственных средств и серьезности конкретного заболевания, подвергаемого лечению. Терапевтически эффективное количество для данной ситуации легко может быть определено обычным экспериментом и находится в пределах компетенции обычного лечащего врача. В целях настоящего изобретения терапевтически эффективная доза обычно будет представлять собой общую дневную дозу, вводимую субъекту в виде разовой или разделенных доз, которые могут, например, составлять количества от 0,001 до 1000 мг/кг веса тела ежедневно и более предпочтительно от 1,0 до 30 мг/кг веса тела ежедневно. Композиции единичной дозировки могут содержать такие количества в виде их подмножеств для получения дневной дозы. Соединения по настоящему изобретению можно вводить орально, парентеально, сублингвально,путем аэрозольного или ингаляционного распыления, ректально или наружным образом в виде препаративных единичных лекарственных препаратов, содержащих обычные нетоксичные фармацевтически приемлемые носители, адьюванты и носители, по желанию. Применение наружных препаратов также может включать чрескожное введение в виде чрескожных пластырей или ионофорных устройств. Термин парентеральный, как он использован в данном описании, включает подкожные инъекции, внутривенные, внутримышечные, внутристволовые инъекции или методы инфузии. Инъекционные препараты, например, стерильные инъекционные водные и масляные суспензии, могут быть получены в соответствии с известными способами с использованием подходящих диспергирующих или смачивающих агентов и суспендирующих агентов. Стерильные инъекционные препараты также могут представлять собой стерильный инъекционный раствор или суспензию в нетоксичном парентерально приемлемом разбавителе или растворителе, например, в виде раствора в 1,3-пропандиоле. Приемлемые носители и растворители, которые можно использовать, включают воду, раствор Рингера и изотонический раствор хлорида натрия. Кроме того, стерильные нелетучие масла обычно используются в качестве растворителя или суспендирующей среды. С данной целью могут использоваться любые успокаивающие нелетучие масла, включая синтетические моно- и диглицериды. Кроме того, жирные кислоты, такие как олеиновая кислота, находят применение при получении инъекционных препаратов. Суппозитории для ректального введения лекарственного средства могут быть получены путем смешивания лекарственного средства с подходящим нераздражающим эксципиентом, таким как масло какао и полиэтиленгликоли, которые являются твердыми при обычной температуре, но жидкими при ректальной температуре, и, следовательно, расплавляются в прямой кишке и высвобождают лекарственное средство. Твердые препаративные лекарственные формы могут включать капсулы, таблетки, пилюли, порошки и гранулы. В таких твердых препаративных лекарственных формах активное соединение может быть смешано с по меньшей мере одним инертным разбавителем, таким как сахароза, лактоза или крахмал. Такие препаративные лекарственные формы также могут включать, как в обычной практике, дополнительные вещества, отличающиеся от инертных разбавителей, например, лубриканты, такие как стеарат магния. В случае капсул, таблеток и пилюль препаративные лекарственные формы могут также включать буферные агенты. Таблетки и пилюли дополнительно могут быть получены с покрытием, растворимым в кишечнике. Жидкие препаративные лекарственные формы для перорального введения могут включать фармацевтически приемлемые эмульсии, растворы, суспензии, сиропы и эликсиры, содержащие инертные разбавители, обычно используемые в данной области, такие как вода. Такие композиции могут также включать адьюванты, такие как смачивающие агенты, эмульгирующие и суспендирующие агенты, циклодекстрины и подсластители, придающие вкус агенты и ароматизаторы. Соединения по настоящему изобретению также можно вводить в виде липосом. Как известно в данной области, липосомы обычно получают в виде фосфолипидов или других липидных веществ. Липосомы образуются посредством моно- или многослойных гидратированных жидких кристаллов, которые диспергированы в водной среде. Можно использовать любой нетоксичный, физиологически приемлемый и метаболизируемый липид, способный образовывать липосомы. Настоящие композиции в виде липосом могут содержать, в дополнение к соединению по настоящему изобретению, стабилизаторы,консерванты, эксципиенты и тому подобное. Предпочтительными липидами являются фосфолипиды и фосфатидилхолины (лецитины), как природные, так и синтетические. Способы образования липосом- 14011890 известны в данной области. Смотри, например, Prescott, Ed., Methods in Cell Biology, Volume XIV, Academic Press, New York, N. W., p. 33 et seq. (1976). Хотя соединения по изобретению можно вводить в виде единственного фармацевтического агента,их также можно использовать в сочетании с одним или несколькими другими агентами, применяемыми при лечении рака. Иллюстративные агенты, используемые в сочетании с соединениями по изобретению для лечения рака, включают, например, иринотекан, топотекан, гемцитабин, 5-фторурацил, лейковорин,карбоплатин, цисплатин, таксаны, тезацитабин, циклофосфамид, алкалоиды винка, иматиниб (глиевек),антрациклины, ритуксимаб, трастузумаб, а также другие противораковые химиотерапевтические агенты. Вышеуказанные соединения для использования в комбинации с соединениями по изобретению будут использоваться в терапевтических количествах, как указано в Physicians' Desk Reference (PDR), 47 издание (1993), включенном в данное описание путем ссылки, или в таких терапевтически полезных количествах, которые известны обычному специалисту в данной области. Соединения по изобретению и другие противораковые агенты можно вводить в рекомендованных максимальных клинических дозах или в более низких дозах. Уровни дозировки активных соединений в композициях по изобретению могут изменяться таким образом, чтобы получать желаемую терапевтическую ответную реакцию в зависимости от пути введения, серьезности заболевания и ответной реакции пациента. Комбинация может вводиться в виде отдельных композиций или в единой препаративной лекарственной форме, содержащей оба агента. При введении в виде комбинации, терапевтические агенты могут быть введены в состав рецептур в виде отдельных композиций, которые вводят в одно и тоже время или в различные моменты времени, или терапевтические агенты можно вводить в виде единственной композиции. Антиэстрогены, такие как тамоксифен, ингибируют рост рака молочной железы, индуцируя остановку клеточного цикла, что требует действия ингибитора клеточного цикла p27Kip. Недавно было показано, что активация пути Ras-Raf-MAP киназы изменяет статус фосфорилирования p27Kip так, что ингибирующая активность при остановке клеточного цикла ослабляется, внося вклад в антиэстрогенную резистентность (Donovan и др., J. Biol. Chem. 276: 40838, 2001). Как сообщалось Donovan и др., ингибирование МАРК передачи сигнала путем обработки ингибитором МЕК изменяет статус фосфорилирования р 27 в гормонально невосприимчивых клеточных линиях рака молочной железы и при этом восстанавливает гормональную чувствительность. Соответственно, в одном аспекте соединения формул (I), (II), (III),(IV) и (V) можно использовать для лечения гормонально зависимых видов рака, таких как рак молочной железы и предстательной железы, для инвертирования гормональной устойчивости, обычно наблюдаемой при таких видах рака при лечении обычными противораковыми агентами. В гематологических видах рака, таких как хронический миелогенный лейкоз (CML), транслокация хромосом ответственна за основополагающие активированные тирозинкиназы BCR-AB1. Пораженные заболеванием пациенты проявляют ответную реакцию на глиевек (Gleevec), ингибитор тирозинкиназы,имеющий небольшую молекулу, в результате ингибирования активности киназы Ab1. Однако многие пациенты с заболеванием на развитой стадии первоначально проявляют ответную реакцию на глиевек,но затем позднее наблюдается рецидив вследствие резистентно вызванных мутаций в домене Ab1. Исследования in vitro продемонстрировали, что BCR-Avl использует путь Raf-киназы, чтобы добиться своего действия. В дополнение, ингибирование более чем одной киназы в данном пути обеспечивает дополнительную защиту против резистентно вызванных мутаций. Соответственно, в другом аспекте изобретения, соединения формул (I), (II), (III), (IV) и (V) используются в комбинации с по меньшей мере одни дополнительным агентом, таким как глиевек, для лечения гематологических видов рака, таких как хронический миелогенный лейкоз (CML), для инвертирования или предотвращения возникновения резистентности к по меньшей мере одному дополнительному агенту. Настоящее изобретение будет более понятно с ссылкой на следующие примеры, которые приведены для иллюстрации и не предназначены для ограничения настоящего изобретения. Иллюстративные боковые цепи для применения в соединениях следующих примеров обычно могут быть получены в соответствии со следующими способами. Пример 1. Синтез 4-[(2-[4-хлор-3-(трифторметилфенил)]амино-1 Н-бензимидазол-6-ил)окси]-Nметилпиридин-2-карбоксамида. Соединение 4-[(2-[4-хлор-3-(трифторметил)фенил]амино-1 Н-бензимидазол-6-ил)окси]-N-метилпиридин-2-карбоксамид синтезировали следующим образом. Стадия 1. Синтез 4-[(4-амино-3-нитрофенил)окси]-N-метилпиридин-2-карбоксамида. Смесь, содержащую 4-амино-3-нитрофенол (1 экв.) и бис(триметилсилил)амид калия (2 экв.) пере- 15011890 мешивали в диметилформамиде в течение 2 ч при комнатной температуре. К данной смеси добавляли (4 хлор(2-пиридил-N-метилкарбоксамид (1 экв.) и карбонат калия (1,2 экв.) и перемешивали при 90 С в течение 3 дней. Реакционную смесь затем концентрировали и распределяли между этилацетатом и водой. Органический слой отделяли и промывали насыщенным раствором соли, сушили, фильтровали и концентрировали в вакууме, получая коричневое твердое вещество. Очистка на силикагеле (2% триэтиламин/50% этилацетат в гексане) давала 4-[(4-амино-3-нитрофенил)окси]-N-метилпиридин-2 карбоксамид в виде оранжевого твердого вещества. Продукт имел удовлетворительный спектр ЯМР. ВЭЖХ, 3,39 мин; Масс-спектр: МН+=289. Стадия 2. Синтез 4-[(3,4-диаминофенил)окси]-N-метилпиридин-2-карбоксамида. Смесь, содержащую [4-(3-амино-4-нитрофенокси)(2-пиридил)]-N- в метаноле и каталитическое количество 10% Pd/C гидрировали до исчезновения желтой окраски, получая амин. ВЭЖХ, 2,5 мин; Массспектр: МН+=259. Стадия 3. Синтез 4-[(2-[4-хлор-3-(трифторметил)фенил]амино-1 Н-бензимидазол-6-ил)окси]-Nметилпиридин-2-карбоксамида. Смесь, содержащую 4-[(3,4-диаминофенил)окси]-N-метилпиридин-2-карбоксамид (1 экв.) и 4-хлор 3-(трифторметил)бензолизотиоцианат (1 экв.) в тетрагидрофуране перемешивали при комнатной температуре в течение 16 ч, получая соответсвующую тиомочевину. К полученной смеси добавляли гидрохлорид 1-этил-3-(3-диметиламинопропил)карбодиимида (2 экв.) и смесь перемешивали дополнительно в течение 10 ч. Смесь концентрировали и распределяли между этилацетатом и водой. Органический слой промывали насыщенным раствором соли и сушили. Очистка с помощью ВЭЖХ давала 4-[(2-[4-хлор-3(трифторметил)фенил]амино-1 Н-бензимидазол-6-ил)окси]-N-метилпиридин-2-карбоксамид. Массспектр: МН+=462. Примеры 2-108. Соединения, представленные в следующей табл. 1 (примеры 2-108), были получены с использованием способа, описанного в примере 1. Таблица 1 Пример 109. Синтез (4-2-[(4-бромфенил)амино]бензотиазол-5-илокси(2-пиридил-N-метилкарбоксамида. Стадия 1. Синтез 2-бром-5-метоксибензотиазола. Раствор брома (3,6 экв.) в хлороформе (0,75 М) добавляли по каплям в течение 1 ч к перемешиваемой суспензии 5-метокси-2-меркаптобензотиазола (1 экв.) в хлороформе при 0 С. Смесь перемешивали в течение 30 мин, после чего медленно добавляли ее в воду и перемешивали дополнительно в течение 20 мин. Смесь фильтровали, удаляя кремовое твердое вещество. Органическую фазу сушили и упаривали,получая в остатке коричневое твердое вещество. Коричневое твердое вещество растворяли в простом эфире и фильтровали. Остаток промывали эфиром, фильтрат и промывные жидкости объединяли, упари- 28011890 вали и хроматографировали (4:1 гексаны и этилацетат), получая указанное в заголовке соединение в виде бледно-желтого твердого вещества. Масс-спектр: МН+=244. Стадия 2. Синтез (4-бромфенил)(5-метоксибензотиазол-2-ил)амина. Смесь, содержащую 2-бром-5-метоксибензотиазол (1 экв.), 4-броманилин (2 экв.) и диизопропилэтиламин подвергали микроволновому облучению в NMP при 220 С. Полученную смесь концентрировали и распределяли между этилацетатом и водой. Органический слой промывали насыщенным раствором соли и сушили. Очистка на силикагеле давала целевой продукт. Масс-спектр: МН+=335. Стадия 3. Синтез 2-[(4-бромфенил)амино]бензотиазол-5-ола. Смесь (4-бромфенил)(5-метоксибензотиазол-2-ил)амина и бромисто-водородной кислоты (48%) подвергали микроволновому облучению при 150 С в течение 6 мин, получая целевой продукт. Массспектр: МН+=321. Стадия 4. Синтез (4-2-[(4-бромфенил)амино]бензотиазол-5-илокси(2-пиридил-N-метилкарбоксамида. Смесь, содержащую 2-[(4-бромфенил)амино]бензотиазол-5-ол (1 экв.), бис(триметилсилил)амид калия (4 экв.), перемешивали в диметилформамиде в течение 30 мин при комнатной температуре. К данной смеси добавляли 4-хлор(2-пиридил)-N-метилкарбоксамид (1 экв.) и карбонат калия (1,2 экв.) и подвергали микроволновому облучению в течение 6 мин при 150 С. Реакционную смесь затем концентрировали и распределяли между этилацетатом и водой. Органический слой отделяли и промывали насыщенным раствором соли, сушили, фильтровали и концентрировали. Очистка с использованием препаративной жидкостной хроматографии (ЖХ) давала целевой продукт. Масс-спектр: МН+=455. Каждый из примеров 110-119, представленных в следующей табл. 2, синтезировали в соответствии со способом, описанным в примере 109. Таблица 2 Стадия 1. Синтез 4-[3-амино-4-(метиламино)фенил]окси-N-метилпиридин-2-карбоксамида. Раствор 4-[(4-амино-3-нитрофенил)окси]-N-метилпиридин-2-карбоксамида (1 экв.) в хлористом метилене обрабатывали трифторуксусным ангидридом (1 экв.) и перемешивали в течение 10 мин при 0 С. Смесь гасили насыщенным раствором NaHCO3. Органический слой отделяли и промывали водой, насыщенным раствором соли, сушили и упаривали. Масс-спектр: МН+=385,2. К раствору трифторацетамида (1 экв.) в смеси толуола, ацетонитрила и раствора гидроксида натрия(50%) добавляли хлорид бензилтриметиламмония (1 экв.) и диметилсульфат (1,2 экв.). Двухфазную смесь перемешивали в течение ночи при комнатной температуре и упаривали. Смесь помещали в этилацетат, промывали водой, насыщенным раствором соли, сушили и упаривали. Неочищенный продукт очищали колоночной хроматографией, элюируя смесью гексаны и этилацетат в соотношении 1:1, затем 2% триэтиламином в смеси гексаны и этилацетат в соотношении 1:1, получая N-метил-4-[4(метиламино)-3-нитрофенил]оксипиридин-2-карбоксамид в виде красновато-оранжевого твердого вещества. Масс-спектр: МН+=303,1. Раствор нитрометиланилина в метаноле обрабатывали 5% палладием-на-угле и перемешивали в атмосфере водорода в течение 15 мин (до исчезновения желтой окраски) при комнатной температуре. Смесь фильтровали и фильтрат концентрировали, получая 0,36 г диамина 4-[3-амино-4(метиламино)фенил]окси-N-метилпиридин-2-карбоксамида. Масс-спектр: МН+=273,3. Стадия 2. Синтез 4-(2-[(4-бромфенил)амино]-1-метил-1 Н-бензимидазол-5-илокси)-N-метилпиридин-2-карбоксамида. Раствор диамина 4-[3-амино-4-(метиламино)фенил]окси-N-метилпиридин-2-карбоксамида (1 экв.) в метаноле обрабатывали 4-бромфенилизотиоцианатом (1 экв.) и перемешивали при 60-65 С в течение 2 ч. Реакционную смесь охлаждали до комнатной температуры и добавляли йодистый метил (1 экв.) и перемешивали в течение ночи при 60 С. Реакционную смесь охлаждали до комнатной температуры,упаривали, помещали в этилацетат и промывали водой и насыщенным раствором соли, сушили и упари- 30
МПК / Метки
МПК: C07D 407/14, C07D 471/08, C07D 413/12, C07D 401/14, C07D 405/14, A61K 31/41, C07D 409/14, C07D 413/14, C07D 417/14, C07D 401/12, C07D 417/12
Метки: качестве, raf-киназы, применение, ингибиторов, бензазолы, замещённые
Код ссылки
<a href="https://eas.patents.su/30-11890-zameshhyonnye-benzazoly-i-ih-primenenie-v-kachestve-ingibitorov-raf-kinazy.html" rel="bookmark" title="База патентов Евразийского Союза">Замещённые бензазолы и их применение в качестве ингибиторов raf-киназы</a>
Предыдущий патент: Применение композиции для защиты от коррозии профилированного изделия, оберточная лента, способ ее получения, профилированное изделие и способ его покрытия
Следующий патент: Способы получения соединений бензоксазолсульфонамида и их промежуточные соединения
Случайный патент: Устройство для игры в продвинутые шахматы и способ его использования