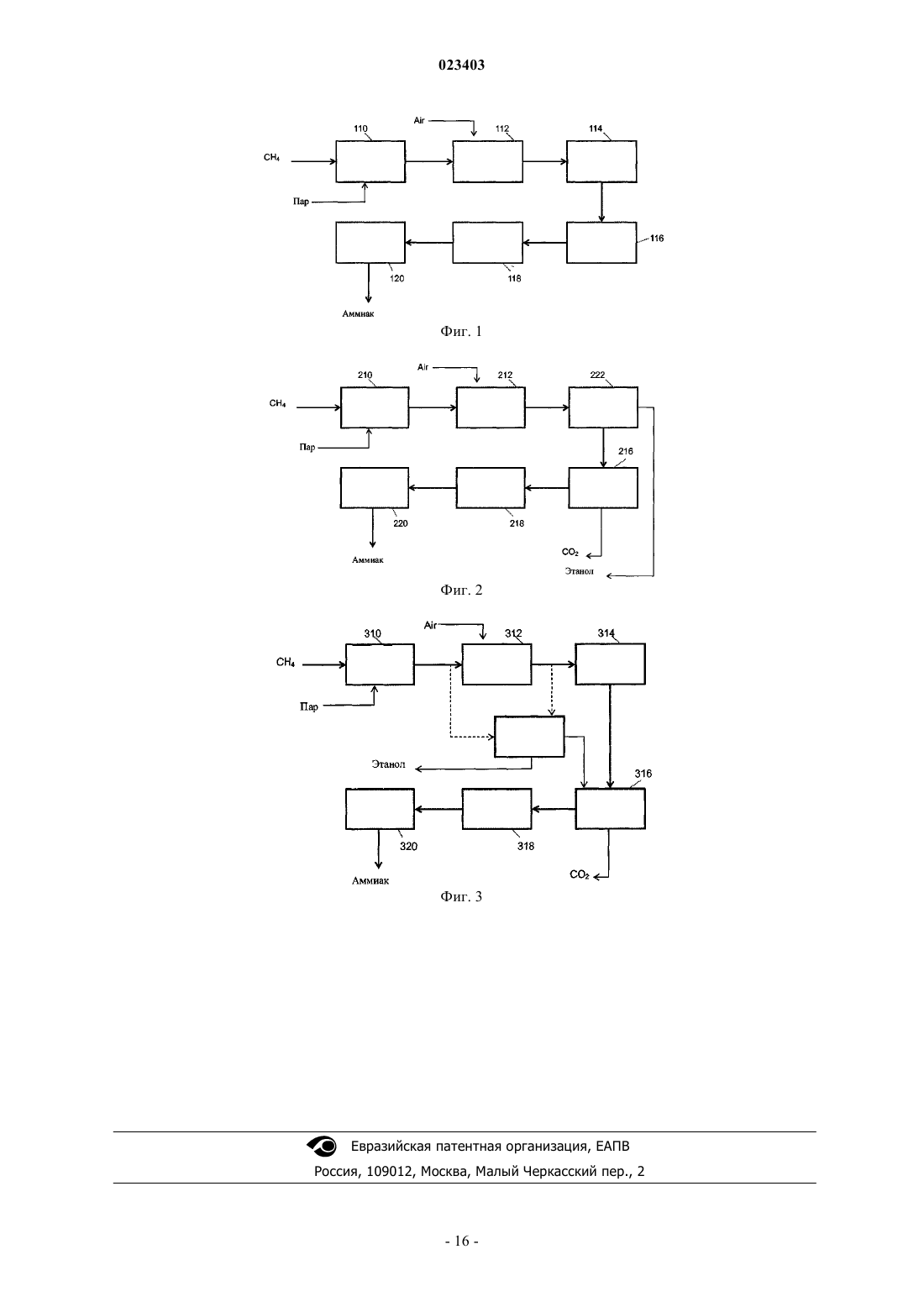
Способ ферментации
Формула / Реферат
1. Способ производства одного или более продуктов из потока газа, полученного в процессе производства аммиака, включающий следующие стадии:
a) преобразование по меньшей мере части потока газа, содержащего метан, в субстрат, содержащий СО, СО2 и Н2;
b) пропускание по меньшей мере части субстрата в биореактор, содержащий культуру одного или более карбоксидотрофных микроорганизмов, анаэробно ферментирующих по меньшей мере часть субстрата, содержащего СО и Н2, с получением одного или более продуктов, включающих спирты и/или кислоты, и потока отработанного газа, содержащего водород и диоксид углерода;
c) направление потока отработанного газа в зону отделения СО2, работающую в условиях, обеспечивающих удаление по меньшей мере части СО2, и получение очищенного потока отработанного газа; и
d) направление очищенного потока отработанного газа в зону синтеза аммиака, работающую при условиях, обеспечивающих получение аммиака.
2. Способ по п.1, при котором поток газа преобразуют в поток субстрата, содержащий СО, СО2 и Н2, способом парового риформинга.
3. Способ по п.2, при котором поток субстрата, выходящий из процесса парового риформинга, пропускают во вторичный реактор риформинга, где по меньшей мере часть метана в потоке субстрата преобразуют в СО, СО2 и Н2 перед пропусканием в биореактор.
4. Способ по любому из пп.1, или 2, или 3, в котором один или более продуктов стадии (b) выбраны из группы, состоящей из следующих веществ: этанола, 2,3-бутандиола и уксусной кислоты.
5. Способ по п.1, в котором карбоксидотрофный микроорганизм выбран из группы, включающей микроорганизмы следующих родов: Moorella, Clostridium, Ruminococcus, Acetobacterium, Eubacterium, Butyribacterium, Oxobacter, Methanosarcina и Desulfotomaculum.
6. Способ по п.1, в котором карбоксидотрофный микроорганизм представляет собой Clostridium autoethanogenum.
7. Способ по п.1, дополнительно включающий:
e) направление второй части субстрата в реактор конверсии водяного газа, работающий в условиях, обеспечивающих получение потока выходящего газа, содержащего СО2 и Н2; и
f) направление потока выходящего газа в зону отделения.
8. Способ по п.2, в котором СО2, отделенный от потока отработанного газа, подвергают рециркуляции в реакторе парового риформинга.
9. Способ по п.3, в котором СО2, отделенный от потока отработанного газа, подвергают рециркуляции во вторичном реакторе риформинга.
Текст
Изобретение относится к объединению способа производства аммиака со способом ферментации для производства продуктов, таких как спирты и/или кислоты, в дополнение к аммиаку. В конкретной форме осуществления поток природного газа, содержащий метан, пропускают в зону риформинга с получением субстрата, содержащего СО и Н 2. Затем этот субстрат пропускают в биореактор, содержащий культуру одного или более микроорганизмов, и ферментируют культуру с получением одного или более продуктов ферментации, включающих спирты и/или кислоты, и потока отработанного газа, содержащего СО 2 и Н 2. Затем этот поток отработанного газа можно пропускать в зону разделения для удаления по меньшей мере части СО 2 и получения очищенного потока отработанного газа, содержащего Н 2, который затем пропускают в зону производства аммиака и применяют для производства аммиака.(71)(73) Заявитель и патентовладелец: ЛАНЦАТЕК НЬЮ ЗИЛЭНД ЛИМИТЕД (NZ) Изобретение относится к объединению систем и способов производства жидких продуктов в существующих промышленных способах. Жидкие продукты, включающие спирт(ы) и/или кислоту (кислоты),получают путем микробиологической ферментации потоков газа, содержащих СО и необязательно Н 2. Предшествующий уровень техники Во всем мире этанол быстро становится основным богатым водородом жидким моторным топливом. Потребление этанола во всем мире в 2005 г. по оценкам составляло 12,2 млрд галлонов. По прогнозам мирового рынка производство этанольного топлива также продолжит расти в будущем благодаря повышенной заинтересованности в этаноле в Европе, Японии, США и в нескольких развивающихся странах. Например, в США этанол применяют для производства смесей Е 10, представляющих собой 10% смесь этанола в бензине. В смесях Е 10 этанольный компонент действует как обогащающий кислородом агент, улучшающий эффективность сгорания и уменьшающий выделение атмосферных загрязняющих веществ. В Бразилии этанол на 30% удовлетворяет потребности в моторном топливе, как в качестве обогащающего кислородом агента в смеси с бензином, так и в качестве чистого топлива сам по себе. В Европе экологические проблемы вокруг последствий выбросов газов, вызывающих парниковый эффект(GHG, Green House Gases), также стали стимулом для постановки Европейским Союзом (ЕС) для странчленов санкционированных целей потребления экологически рациональных видов моторного топлива,таких как этанол, полученный на основе биомассы. Подавляющее большинство топливного этанола получают посредством традиционных способов ферментации на основе дрожжей, которые в качестве единственного источника углерода используют углеводы, полученные из культурных растений, такие как сахароза, экстрагированная из сахарного тростника, или крахмал, экстрагированный из зерновых культур. Тем не менее на стоимость этого исходного углеводного сырья влияет его ценность в качестве продуктов питания для людей и кормов для животных, и выращивание культур, дающих крахмал или сахарозу, для производства этанола экономически нерационально во всех географических зонах. Поэтому представляет интерес развитие технологий преобразования более дешевых и/или более обильных источников углерода в топливный этанол. СО является основным, дешевым, богатым энергией побочным продуктом неполного сгорания органических материалов, таких как уголь или нефть и нефтепродукты. Например, сообщают, что сталеплавильное производство в Австралии производит и выделяет в атмосферу свыше 500000 т СО ежегодно. Дополнительно или альтернативно, потоки газа, богатые СО (синтетический газ), могут быть получены в результате газификации углеродистых материалов, таких как уголь, нефть и биомасса. Углеродистые материалы можно преобразовать в газообразные продукты, включающие СО, СО 2, Н 2 и в меньших количествах СН 4, посредством газификации, используя ряд способов, включающих пиролиз, крекинг дегтя и газификацию коксового остатка. Синтетический газ может быть также получен в процессе парового риформинга, такого как паровой риформинг метана или природного газа. Метан можно преобразовать в водород и монооксид углерода и/или диоксид углерода путем риформинга метана в присутствии металлического катализатора. Например, паровой риформинг метана происходит, как показано ниже Данный способ обеспечивает существенную долю водорода, производимого в настоящее время во всем мире. Для преобразования газов, состоящих, в основном, из СО и/или СО и водорода (Н 2), в разнообразные виды топлива и химические вещества можно применять каталитические процессы. Для преобразования этих газов в топливо и химические вещества можно также применять микроорганизмы. Эти биологические процессы, хотя они в целом медленнее, чем химические реакции, обладают несколькими преимуществами по сравнению с каталитическими процессами, включающими высокую специфичность,более высокие выходы, более низкие затраты энергии и более высокую устойчивость к отравлению. Способность микроорганизмов расти на СО в качестве единственного источника углерода была впервые открыта в 1903 г. Позже определили, что эта способность является свойством организмов, использующих для автотрофного роста биохимический путь ацетилкоэнзима А (ацетил СоА) (также известный как биохимический путь Вуда-Льюнгдаля и биохимический путь дегидрогеназы монооксида углерода/синтазы ацетил СоА (CODH/ACS. Показано, что большое число анаэробных микроорганизмов, включающих карбоксидотрофные, фотосинтезирующие, метаногенные и ацетогенные организмы,метаболизируют СО до различных конечных продуктов, а именно СО 2, Н 2, метана, н-бутанола, ацетата и этанола. Все такие организмы, используя СО в качестве единственного источника углерода, продуцируют по меньшей мере два из этих конечных продуктов. Показано, что анаэробные бактерии, такие как бактерии рода Clostridium, продуцируют этанол из СО, СО 2 и Н 2 посредством биохимического пути ацетил СоА. Например, различные штаммы Clostridiumljungdahlii, продуцирующие этанол из газов, описаны в следующих документах: WO 00/68407, ЕР 117309, патентах US 5173429, US 5593886 и US 6368819, WO 98/00558 и WO 02/08438. Также известно,что бактерия Clostridium autoethanogenum sp продуцирует этанол из газов (Abrini et al., Archives of Microbiology 161, pp 345-351 (1994. Тем не менее продуцирование этанола микроорганизмами путем ферментации газов в характерном случае сопровождается совместным продуцированием ацетата и/или уксусной кислоты. Поскольку некоторая часть доступного углерода в характерном случае вероятнее преобразуется в ацетат/уксусную кислоту, чем в этанол, эффективность производства этанола с применением таких способов ферментации может быть меньшей, чем нужно. Кроме того, хотя побочный продукт, представляющий собой ацетат/уксусную кислоту, можно применять для какой-либо другой цели, он может создавать проблему, связанную с утилизацией отходов. Ацетат/уксусная кислота преобразуется микроорганизмами в метан и,следовательно, потенциально может вносить вклад в выбросы газов, создающих парниковый эффект(GHG; англ. "Greenhouse gas"). В документах WO 2007/117157 и WO 2008/115080, описание которых включено в настоящее описание посредством ссылки, описаны способы, с помощью которых получают спирты, в частности, этанол,путем анаэробной ферментации газов, содержащих монооксид углерода. Ацетат, получаемый в качестве побочного продукта способа ферментации, описанного в документе WO 2007/117157, преобразуют в газ водород и газ диоксид углерода, любой из которых или оба можно применять в способе анаэробной ферментации. Ферментация газообразных субстратов, содержащих СО, с получением таких продуктов, как кислоты и спирты, в характерном случае идет в пользу получения кислоты. Продуктивность спирта можно повысить способами, известными в данной области техники, такими как способы, описанные в следующих документах: WO 2007/117157, WO 2008/115080, WO 2009/022925 и WO 2009/064200, которые полностью включены в настоящее описание посредством ссылки. В документах US 7078201 и WO 02/08438 также описаны способы ферментации для производства этанола путем изменения условий (например, рН и окислительно-восстановительного потенциала) жидкой питательной среды, в которой проводят ферментацию. Как описано в этих публикациях, подобные способы можно применять для производства других спиртов, таких как, например, бутанол. Микробиологическая ферментация СО в присутствии Н 2 может приводить к, по существу, полному переносу углерода в спирт. Тем не менее в отсутствие достаточного количества Н 2 некоторая часть СО преобразуется в спирт, тогда как значительная доля преобразуется в СО 2, как показано в приведенных ниже уравнениях Получение СО 2 приводит к неэффективности в общем улавливании углерода и в случае его выделения также потенциально вносит вклад в выбросы газов, создающих парниковый эффект. Кроме того, диоксид углерода и другие углеродсодержащие соединения, такие как метан, образующиеся в процессе газификации, могут также выделяться в атмосферу, если не потребляются в объединенной реакции ферментации. Задача настоящего изобретения состоит в разработке системы (систем) и/или способа (способов),преодолевающих недостатки, известные на уровне техники, и обеспечивающих общество новыми способами оптимального производства разнообразных полезных продуктов. Сущность изобретения В изобретении предложен способ и система, которые могут быть объединены с известными способами производства аммиака, обладающие повышенной эффективностью. Во-первых, результатом этого объединения является производство жидкого продукта, такого как этанол. Кроме того, объединение повышает эффективность общего улавливания углерода при способе производства аммиака за счет уменьшения образования СО 2. Кроме того, объединение способа и системы по настоящему изобретению повышает общую энергетическую эффективность способа производства аммиака. Согласно первому аспекту изобретения предложен способ производства одного или более продуктов путем микробиологической ферментации потока отработанного газа, использованного в процессе производства аммиака, включающий следующие стадии:a. пропускание потока газа, содержащего природный газ, в переходную зону, работающую в условиях, приводящих к преобразованию по меньшей мере части потока газа в субстрат, содержащий СО и Н 2;b. пропускание по меньшей мере части субстрата в биореактор, содержащий культуру одного или более микроорганизмов; иc. ферментацию культуры в биореакторе с получением одного или более продуктов ферментации,включающих спирты и/или кислоты. В конкретных формах осуществления желательна консервация Н 2 для производства аммиака, поскольку в данных конкретных формах осуществления анаэробная ферментация Н 2 с получением продукта ферментации минимальна. В качестве примера количество Н 2, потребленное для получения продукта ферментации, может составлять менее 20, менее 15, менее 10, менее 5, менее 2 или может составлять 0%. В некоторых формах осуществления изобретения природный газ преобразуется в поток газа, содержащий СО и Н 2, посредством парового риформинга в присутствии катализатора. Метан, остающийся в потоке газа после начального этапа парового риформинга, затем преобразуют в Н 2 во вторичном реак-2 023403 торе риформинга. В некоторых формах осуществления по меньшей мере часть потока газа, содержащего СО и Н 2, выходящего из реактора парового риформинга и/или из вторичного реактора риформинга, направляют в биореактор. По меньшей мере часть этого потока газа преобразуется посредством анаэробной ферментации в продукты ферментации, включающие спирт (спирты) и кислоту (кислоты). В предпочтительных формах осуществления продукт ферментации представляет собой этанол и/или 2,3-бутандиол. В альтернативной форме осуществления продукт ферментации представляет собой ацетат. В некоторых формах осуществления культура микроорганизмов, применяемая при анаэробной ферментации продукта ферментации, представляет собой культуру карбоксидотрофных бактерий. В различных формах осуществления карбоксидотрофная бактерия выбрана из следующих родов бактерий:Carboxydothermus. В различных формах осуществления бактерия выбрана из следующих бактерий: Clostridium autoethanogenum, Clostridium ljungdahlii, Clostridium acetobutylicm или Clostridium ragsdalei. В предпочтительных формах осуществления бактерия представляет собой Clostridium autoethanogenum. В конкретной форме осуществления бактерия имеет идентификационные характеристики, соответствующие номерам по каталогу DSM10061 или DSM23693 (депонирована в Немецкой коллекции микроорганизмов и клеточных культур). Согласно некоторым формам осуществления изобретения было бы предпочтительно, чтобы поток газа, направляемый в биореактор для реакции ферментации, был обогащен СО. В различных формах осуществления настоящего изобретения процентное содержание СО по объему в потоке газа может составлять по меньшей мере от 40 до 50% СО по объему, от 30 до 40% СО по объему, от 20 до 30% СО по объему и от 10 до 20% СО по объему. Специалисту в данной области техники понятно, что вышеописанные диапазоны содержания СО являются иллюстративными, и что настоящее изобретение не ограничено потоками газа, имеющими данные концентрации. В некоторых формах осуществления изобретения было бы целесообразно, чтобы концентрации СО в потоке газа были значительно более низкими, в частности,в потоках газа, в которых находятся значительные количества Н 2. В другом аспекте настоящего изобретения предложена система для производства жидких продуктов путем микробиологической ферментации, включающая следующие элементы: а. средства первичного риформинга, где природный газ преобразуется в поток субстрата, содержащий СО и Н 2;b. средства вторичного риформинга, где поток субстрата для стадии 1 претерпевает дальнейшее окисление в присутствии катализатора с получением большего количества СО и Н 2;c. средства для направления по меньшей мере части потока субстрата, выходящего из средств первичного и/или вторичного риформинга, в биореактор; где биореактор сконструирован таким образом, чтобы обеспечивать преобразование по меньшей мере части СО и/или Н 2, находящихся в потоке субстрата, в жидкие продукты посредством микробиологической ферментации. Известен ряд способов риформинга природного газа в поток субстрата, содержащий СО и Н 2. Примеры способов риформинга приведены в документе WO 2009/010347 и кратко изложены ниже. Основные способы риформинга, известные в данной области техники, включают паровой риформинг метанаreforming") и частичное окисление (РОХ; англ. "partial oxidation"). Паровой риформинг метана представляет собой способ, при котором сырье, содержащее метан, подвергают риформингу в реакторе риформинга с наружной топкой в присутствии молярного отношения пара к метану, составляющего более 2:1; автотермический риформинг представляет собой способ, при котором сырье, содержащее метан, подвергают риформингу в присутствии пара и кислорода; и частичное окисление представляет собой способ,при котором сырье, содержащее метан, подвергают риформингу в присутствии кислорода и относительно низких или нулевых концентраций пара. В некоторых формах осуществления настоящего изобретения система может дополнительно включать средства для направления потока отработанного газа, выходящего из биореактора, на известное промышленное применение. Например, в предпочтительных формах осуществления, где биореактор объединен с известным способом производства аммиака, по меньшей мере часть потока субстрата, выходящего из первичного и/или вторичного реактора риформинга, направляют в биореактор для реакции ферментации. Затем поток отработанного газа, выходящий из биореактора, направляют в зону отделения СО 2, где для удаления по меньшей мере части СО 2 из потока отработанного газа применяют средства разделения. Полученный в результате поток, богатый Н 2, можно применять для производства аммиака. Согласно одной конкретной форме осуществления изобретения биореактор объединен со способом производства аммиака. В одной форме осуществления реактор конверсии водяного газа, применяемый в характерном способе производства аммиака из природного газа, заменен биореактором. Поток субстрата,выходящий из первичных или вторичных реакторов риформинга, содержащий СО, СО 2 и Н 2, подвергается анаэробной ферментации в биореакторе с получением одного или более продуктов, и поток отработанного газа содержит Н 2 и СО 2. Затем этот поток отработанного газа направляют в зону отделения СО 2,-3 023403 и СО 2 удаляют с получением в результате потока, богатого Н 2, который можно применять для синтеза аммиака. В следующих формах осуществления изобретения газы из процесса производства аммиака (Н 2, N2 и СН 4), можно объединять с потоком, содержащим СО 2, для производства ацетата. В конкретной форме осуществления поток, содержащий СО 2, представляет собой остаточный газ из биореактора. В других формах осуществления поток, содержащий СО 2, представляет собой поток СО 2, удаляемый из потока отработанного газа в зоне отделения СО 2. В следующих формах осуществления изобретения по меньшей мере часть производимого аммиака можно применять для регуляции уровней рН в средах, применяемых в процессе ферментации. В некоторых формах осуществления настоящего изобретения система может включать средства для определения композиции потока субстрата, чтобы гарантировать, что поток субстрата имеет желаемую концентрацию СО и/или Н 2. Эти средства для определения композиции потока субстрата могут представлять собой любые известные средства, способные к выполнению этой функции. Описание графических материалов На фиг. 1 показан традиционный способ производства аммиака; на фиг. 2 - форма осуществления настоящего изобретения, в которой весь поток газа, выходящий из вторичного реактора риформинга, направляется в биореактор для ферментации СО и/или Н 2 до жидкого продукта (продуктов); на фиг. 3 - другая форма осуществления изобретения, в которой по меньшей мере часть потока газа,содержащего СО и Н 2, направляется в биореактор для ферментации СО и/или Н 2 до жидкого продукта(продуктов). Сведения, подтверждающие возможность осуществления изобретения Согласно определенным аспектам настоящего изобретения систему и способ ферментации потока субстрата, содержащего СО и/или Н 2, до жидкого продукта можно объединить с известными способами производства аммиака, и данное объединение дает возможность получать желаемые конечные продукты. При традиционном производстве аммиака газ преобразуют в Н 2, который затем объединяют с N2 с получением аммиака. Специалистам в данной области техники понятно, что этот газ может представлять собой, но не ограничен ими, природный газ, такой как, например, метан, или сжиженный нефтяной газ,такой как бутан или пропан. В качестве более подробного описания этого способа сначала природный газ поступает в реактор парового риформинга. Природный газ взаимодействует с паром в реакторе парового риформинга с образованием потока газа, содержащего Н 2 и СО. Затем этот поток газа поступает во вторичный реактор риформинга, в котором остаточный природный газ преобразуется в дополнительный Н 2 и СО, а также N2. Взаимодействие, которое происходит во вторичном реакторе риформинга, в характерном случае представляет собой стадию окислительного риформинга с использованием воздуха в качестве источника кислорода. N2, требующийся для производства аммиака, образуется в результате реакции, происходящей во вторичном реакторе риформинга. При некоторых известных способах перед поступлением газа в реактор риформинга природный газ может быть очищен, чтобы удалить из потока нежелательные соединения,такие как сера. Затем при характерном способе производства аммиака поток газа, содержащий Н 2 и СО, претерпевает стадию конверсии водяного газа, на которой по меньшей мере часть СО взаимодействует с Н 2 О с получением дополнительного Н 2, а также СО 2. Затем поток газа поступает в абсорбер СО 2, в котором СО 2 удаляют, оставляя поток газа, содержащий, в основном, Н 2 и N2. Затем поток газа поступает на стадию метанизации, на которой удаляют какой-либо остаточный СО. Таким образом, газ, богатый Н 2 и N2,готов к преобразованию в аммиак посредством цикла синтеза аммиака (процесса Габера-Боша). Согласно настоящему изобретению по меньшей мере часть потока газа, содержащего Н 2 и СО, направляют в биореактор вместо направления в реактор конверсии водяного газа. Объединение биореактора с процессом производства аммиака в сочетании с реактором конверсии водяного газа или в качестве замены этого реактора обеспечивает ряд преимуществ. Например, применение биореактора для обработки потока газа обеспечивает получение продукта ферментации, такого как, например, этанол, в дополнение к желаемому конечному продукту (аммиаку). За счет направления по меньшей мере части потока синтетического газа в биореактор СО, находящийся в перенаправленном потоке газа, может быть использован для производства этанола посредством способа ферментации. При традиционных способах производства аммиака этот СО был бы преобразован в СО 2 путем реакции конверсии водяного газа, а затем полученный в результате СО 2 был бы отделен от газа. В конкретных формах осуществления настоящего изобретения реакция ферментации, происходящая в биореакторе, заменяет реакцию конверсии водяного газа. Замена реакции конверсии водяного газа упрощает способ производства аммиака. Кроме того, замена реакции конверсии водяного газа реакцией ферментации уменьшает количество СО 2 в потоке субстрата по сравнению с характерным способом производства аммиака (риформингКВГ (конверсия водяного газа)удаление СО 2 метанизациясинтез аммиака), за счет чего упрощается стадия удаления СО 2 в процессе производства аммиака. Известно, что по меньшей мере часть потока газа, содержащего СО и Н 2, используемого на ранних стадиях процесса производства аммиака, можно преобразовать в этанол или другие жидкие продукты посредством микробиологической ферментации. В первом аспекте настоящего изобретения предложен способ, посредством которого по меньшей мере часть потока газа, содержащего Н 2 и СО, отводят в биореактор, содержащий один или более микроорганизмов, для производства этанола и/или других жидких продуктов. В предпочтительной форме осуществления изобретения по меньшей мере часть потока газа, содержащего Н 2 и СО, отводят в биореактор вместо пропускания в реактор конверсии водяного газа. В другой форме осуществления изобретения весь поток газа пропускают в биореактор, который заменяет реактор конверсии водяного газа. Определения Если не определено иное, описанные ниже термины, используемые на протяжении всего данного описания, определены, как описано ниже. Термины "улавливание углерода" и "общее улавливание углерода" относятся к эффективности преобразования источника углерода, такого как сырье, в продукты. Например, количество углерода в сырье,представляющем собой древесную биомассу, преобразуется в полезные продукты, такие как спирт. Термин "синтетический газ" относится к газовой смеси, содержащей по меньшей мере часть монооксида углерода и водорода, образующихся в результате газификации и/или риформинга углеродистого сырья. Термин "субстрат, содержащий монооксид углерода" и подобные термины следует понимать как включающие любой субстрат, в котором монооксид углерода доступен для роста и/или ферментации одного или более штаммов бактерий."Газообразные субстраты, содержащие монооксид углерода" включают любой газ, содержащий монооксид углерода. Газообразный субстрат в характерном случае содержит значительную долю СО, предпочтительно по меньшей мере приблизительно от 5 до приблизительно 95% СО по объему. Термин "биореактор" включает устройство ферментации, состоящее из одного или более сосудов и/или колонок или трубопроводных систем, причем, это устройство включает химический проточный реактор с мешалкой (CSTR, Continuous Stirred Tank Reactor), реактор с иммобилизованными клетками,газлифтный ферментер, барботирующий ферментер (BCR, bubble column reactor), мембранный реактор,такой как мембранный биореактор с системой полых волокон (HFMBR, Hollow Fibre Membrane Bioreactor) или реактор с орошаемым слоем (TBR, Trickle Bed Reactor), либо другой реактор или другое устройство, подходящее для газожидкостного контакта. Термин "кислота", используемый в настоящем описании, включает как карбоновые кислоты, так и ассоциированный карбоксилатный анион, например, смесь свободной уксусной кислоты и ацетата, находящихся в ферментативном бульоне, как описано в данной работе. Отношение молекулярной кислоты к карбоксилату в ферментативном бульоне зависит от рН системы. Кроме того, термин "ацетат" включает как исключительно соль ацетат, так и смесь молекулярной или свободной уксусной кислоты и соли ацетат, такую как смесь соли ацетат и свободной уксусной кислоты, находящуюся в ферментативном бульоне, как описано в данной работе. Термин "желаемая композиция" используют как относящийся к желаемому уровню и типам компонентов в веществе, например, в потоке газа. Более конкретно газ считают имеющим "желаемую композицию", если он содержит определенный компонент (например, СО и/или Н 2) и/или содержит определенный компонент на определенном уровне и/или не содержит определенный компонент (например, загрязняющее вещество, вредное для микроорганизмов) и/или не содержит определенный компонент на определенном уровне. Более чем один компонент можно учитывать при определении, имеет ли поток газа желаемую композицию. Термин "поток" используют по отношению к току материала в одну или более стадий процесса, через одну или более стадий процесса или из одной или более стадий процесса, например материала, который подают в биореактор и/или необязательный удалитель СО 2. Композиция потока может варьироваться по мере того, как он проходит через различные стадии. Например, когда поток проходит через биореактор, содержание СО потока может снижаться, тогда как содержание СО 2 может возрастать. Также, по мере прохождения потока через стадию удаления СО 2, содержание СО 2 снизится. Если контекст не требует иного, выражения "ферментация", "процесс ферментации" или "реакция ферментации" и тому подобное, как используют в данной работе, подразумевают как включающие как фазу роста, так и фазу биосинтеза продукта данного процесса. Термины "повышение эффективности", "повышенная эффективность" и тому подобное при использовании по отношению к процессу ферментации включают, но не ограничены ими, повышение одного или более следующих показателей: скорости роста микроорганизмов при ферментации, объема или массы желаемого продукта (такого как спирты), полученного на объем или массу потребленного субстрата(такого как монооксид углерода), скорости производства или уровню производства желаемого продукта и относительной доли произведенного желаемого продукта по сравнению с другими побочными продуктами ферментации и, кроме того, может отражать ценность (которая может быть положительной или отрицательной) любых побочных продуктов, образующихся в процессе. Традиционное производство аммиака в характерном случае включает стадию риформинга, на которой природный газ, содержащий метан (СН 4), преобразуется в СО и Н 2. Стадия риформинга осуществляется в зоне риформинга в присутствии металлического катализатора и при повышенных температурах. Распространенным способом риформинга является паровой риформинг, при котором метан взаимодействует с паром в присутствии металлического катализатора при повышенной температуре. Металлический катализатор, обычно применяемый для парового риформинга, представляет собой никелевый катализатор, и реакция обычно идет при температурах, составляющих от 700 до 1100 С. Стехиометрия этого преобразования показана ниже Поток синтетического газа, выходящий из реактора парового риформинга, в характерном случае содержит Н 2, СО, СО 2 и СН 4. Затем поток синтетического газа направляется во вторичный реактор риформинга. Во вторичный реактор риформинга вводят воздух в качестве источника кислорода, обеспечивающий подачу N2, требующегося для производства аммиака. Дополнительно на этой стадии избыток СН 4 в синтетическом газе преобразуется в СО и Н 2 при использовании такой же реакции, как описано выше. Поток синтетического газа, выходящий из вторичного реактора риформинга, в идеальном случае содержит Н 2, СО, СО 2, N2 и небольшие количества СН 4. Затем при традиционном производстве аммиака поток газа направляется в реактор конверсии водяного газа. Реакции, происходящие в первичном реакторе парового риформинга и во вторичном реакторе риформинга, являются эндотермическими по природе. На уровни СО, СО 2 и Н 2, производимых реакторами риформинга, можно воздействовать посредством ряда факторов, включающих уровни О 2, количество пара, подаваемого в реакторы риформинга, и количество подаваемого метана. Другие факторы, которые могут влиять на уровни производства СО, СО 2 и Н 2, включают уровни температуры и давления в реакторах риформинга во время проведения реакции. В других формах осуществления настоящего изобретения природный газ может быть окислен способами, альтернативными паровому риформингу. Другим способом окисления природного газа до СО и Н 2 является автотермический риформинг. При автотермическом риформинге природный газ, такой как метан, частично окисляется в присутствии кислорода при повышенной температуре и повышенном давлении, как показано ниже Другой альтернативой способу парового риформинга является сухой риформинг СО 2, преимущество которого состоит в том, что значительная доля СО 2, находящегося в биогазе или в других источниках природного газа, образует монооксид углерода и водород, как показано ниже В первой форме осуществления настоящего изобретения по меньшей мере часть синтетического газа, выходящего из первичного реактора парового риформинга, направляют в биореактор для преобразования в жидкие продукты посредством микробиологической ферментации. Во второй форме осуществления настоящего изобретения по меньшей мере часть синтетического газа, выходящего из вторичного реактора риформинга, направляют в биореактор для преобразования в жидкие продукты посредством микробиологической ферментации. В данных первой и второй формах осуществления настоящего изобретения поток отработанного газа, выходящий из биореактора, богат Н 2 и N2 и дополнительно содержит СО, СО 2, СН 4. Затем этот поток отработанного газа пропускают в зону отделения, включающую абсорбер СО 2. В данных первой и второй формах осуществления настоящего изобретения часть синтетического газа, не направляемую в биореактор, пропускают через реактор конверсии водяного газа. Синтетический газ в реакторе конверсии водяного газа претерпевает реакцию конверсии водяного газа, при которой СО и Н 2 О преобразуются в СО 2 и Н 2 согласно описанной ниже стехиометрии Согласно данным первой и второй формам осуществления изобретения отходящий газ, выходящий из биореактора, и остаточный газ, выходящий из реактора конверсии водяного газа, затем направляют в зону отделения, включающую абсорбер СО 2, применяемый в традиционном производстве аммиака. В третьей форме осуществления изобретения весь синтетический газ, выходящий из вторичного реактора риформинга, направляют в биореактор для преобразования в жидкие продукты посредством микробиологической ферментации. В данной третьей форме осуществления биореактор заменяет реактор конверсии водяного газа. В описанных выше формах осуществления остаточный газ, выходящий из биореактора и/или реактора конверсии водяного газа, проходит через традиционные стадии производства аммиака,-6 023403 включающие пропускание через зону отделения CO2, в которой удаляют СО 2. Затем остаточный газ из данного процесса пропускают через стадию метанизации, на которой из потока газа удаляют какой-либо остаточный СО. Остаточный газ очень богат Н 2 и N2 и может содержать следовые количества СН 4. Затем этот газ пропускают в зону синтеза аммиака, в которой производят аммиак. СО 2 можно удалять из остаточного газа известными способами. Для удаления СО 2 из потока газа можно применять ряд способов, включающих короткоцикловую абсорбцию (PSA; англ. "pressure swingadsorption"), абсорбцию с использованием растворителей и криогенное фракционирование. Другие способы отделения СО 2, которые можно применять, включают экстракцию оксидом металла, таким как СаО,и применение пористого углерода или селективную экстракцию растворителем, такую как, например,аминная экстракция. Такие амины, как водный моноэтаноламин (monoethanolamine, MEA), дигликольамин (diglycolamine, DGA), диэтаноламин (diethanolamine, DEA), диизопропаноламин (diisopropanolamine,DIPA) и метилдиэтаноламин (methyldiethanolamine, MDEA), широко применяют в промышленности для удаления СО 2 и сероводорода из потоков природного газа и потоков процессов нефтеочистки. В некоторых формах осуществления изобретения реакция ферментации, происходящая в биореакторе, может потреблять СО в потоке газа, при этом сохраняя Н 2. Сохранение Н 2 в потоке газа, результатом которого является поток газа, богатый Н 2, выходящий из биореактора, обладает преимуществом,поскольку дает возможность для оптимального совместного производства аммиака. Реакция ферментации более подробно описана ниже. Со ссылкой на фиг. 2 представлен конкретный пример осуществления настоящего изобретения. Природный газ (метан) направляют в реактор парового риформинга в присутствии пара. Метан взаимодействует с паром с образованием синтетического газа, содержащего СО, СО 2 и Н 2. Затем синтетический газ направляют во вторичный реактор риформинга. Во вторичный реактор риформинга также вводят воздух, и О 2 в воздухе взаимодействует с дополнительным количеством метана в потоке газа с получением большего количества Н 2. Введение воздуха на этой стадии вводит N2, требующийся для процесса производства аммиака. Поток газа, выходящий из вторичного реактора риформинга, содержащий Н 2, СО,СО 2 и N2, направляют в биореактор. Биореактор в данном примере осуществления настоящего изобретения заменяет реактор КВГ, применяемый в традиционных способах производства аммиака. Реакция ферментации в биореакторе преобразует СО и необязательно Н 2 в этанол посредством анаэробной ферментации. Желательно, чтобы преобразование Н 2 было минимальным, поскольку более высокие уровни Н 2 в потоке отработанного газа, выходящем из биореактора, приведут в результате к более высоким выходам аммиака. Затем поток газа направляют в зону отделения СО 2, в которой СО 2 отделяют от потока газа и получают очищенный поток отработанного газа. Затем очищенный поток отработанного газа, богатый Н 2 и N2, направляют в зону метанизации, в которой удаляют какой-либо остаточный СО в очищенном потоке газа с получением потока сырья для синтеза аммиака. Затем поток сырья для синтеза аммиака направляют в зону синтеза аммиака для производства аммиака. Отделенный СО 2 можно утилизировать в установке производства мочевины. Альтернативно существует возможность подвергать отделенный СО 2 рециркуляции в установках обработки аммиака, не связанных с установкой производства мочевины, обратно в реактор парового риформинга и вторичный реактор риформинга. Другим возможным применением отделенного СО 2 является производство ацетата(способом ферментации), в котором используют по меньшей мере часть потока газа H2/N2. На фиг. 3 показан другой пример осуществления настоящего изобретения, в котором по меньшей мере часть потока газа, выходящего из реактора парового риформинга и/или из вторичного реактора риформинга, направляют в биореактор для производства этанола. В отличие от фиг. 2, биореактор в данном примере осуществления не заменяет реактор КВГ. В конкретном аспекте вышеописанных форм осуществления жидкие продукты, производимые посредством микробиологической ферментации в биореакторе, включают кислоту (кислоты) и/или спирт(спирты). В конкретной форме осуществления продукт представляет собой этанол. Совместное производство аммиака и этанола было бы привлекательным для производства этиламинов посредством реакции, показанной ниже Этиламины полезны в химической промышленности в качестве промышленных растворителей. Как отмечено выше, этиламины можно применять для систем растворителей для удаления H2S и/или СО 2 из потоков промышленных газов. Этиламины можно также применять в производстве гербицидов. Специалистам в данной области техники понятно, что кислота (кислоты) и/или спирт (спирты),производимые посредством реакции анаэробной ферментации, не ограничены ацетатом и этанолом. Дополнительные примеры продуктов, образующихся в результате реакции ферментации, включают, но не ограничены ими, следующие вещества: ацетат, бутират, пропионат, капроат, этанол, пропанол, бутанол и водород. В качестве примера, эти продукты могут быть получены путем ферментации с использованием микроорганизмов следующих родов: Moorella, Clostridia, Ruminococcus, Acetobacterium, Eubacterium,Butyribacterium, Oxobacter, Methanosarcina и Desulfotomaculum.Co ссылкой на фиг. 1, обычный способ производства аммиака включает следующие стадии:a. очистку природного газа для удаления H2S,b. получение синтетического газа (СО и Н 2),c. очистку синтетического газа (удаление СО 2) иd. синтез аммиака. Первая стадия предназначена для удаления соединений серы из сырья, поскольку сера инактивирует катализаторы, впоследствии применяемые в процессе. Серу можно удалить с помощью каталитической гидрогенизации, в результате которой соединения серы, содержащиеся в сырье, преобразуются в газообразный сероводород, как показано ниже Затем газообразный сероводород абсорбируют и удаляют путем пропускания его через слои оксида цинка, где он преобразуется в твердый сульфид цинка Вторая стадия включает три реакции. Первая реакция представляет собой преобразование метана в СО, СО 2 и Н 2 (синтетический газ) при высоких температурах (770 С)в присутствии никелевого катализатора в реакторе парового риформинга 110. Стехиометрия этого преобразования показана ниже Затем синтетический газ слегка охлаждают и направляют во вторичный реактор 112 риформинга. Реакции показаны ниже Добавление воздуха во вторичный реактор риформинга вводит азот, который требуется для синтеза аммиака. Следующей реакцией является удаление СО. СО преобразуют в СО 2 в реакторе 114 конверсии водяного газа, как показано ниже Реакция конверсии водяного газа идет в две стадии. Сначала поток газа пропускают над катализатором, представляющим собой Cr/Fe3O4, при температуре, составляющей 360 С,а затем газ пропускают над катализатором, представляющим собой Cu/ZnO/Cr, при температуре, составляющей 210 С. Применение двухстадийной реакции максимально повышает конверсию СО до СО 2. Следующей стадией способа производства аммиака является удаление СО 2 в зоне 116 отделения СО 2. Как обсуждалось выше, существует ряд различных способов удаления СО 2 из потока газа, включающих короткоцикловую абсорбцию (pressure swing adsorption, PSA), абсорбцию с использованием растворителей и криогенное фракционирование с экстракцией растворителем. Стадию метанизации применяют, чтобы удалить остаточный СО из потока газа, как показано ниже Данная реакция представляет собой каталитическую реакцию, протекающую при температуре, составляющей 400-600 С. Полученный в результате поток газа содержит Н 2 и N2, и далее осуществляют синтез аммиака. Газ охлаждают, сжимают и подают в цикл синтеза аммиака. Взаимодействие между N2 и Н 2 с получением газообразного аммиака представляет собой экзотермическую равновесную реакцию, в результате которой выделяется 92,4 кДж/моль энергии при 298K. Путем применения давления, составляющего приблизительно 200 атм, и температуры, составляющей приблизительно 500 С, возможно получение выходов аммиака, составляющих приблизительно 1020%. Остаточную смесь газов подвергают рециркуляции через реактор, и теплоту, выделяемую в результате реакции, применяют для нагревания входящей газовой смеси. Реакция ферментации. Конкретные формы осуществления изобретения включают ферментацию потока субстрата, представляющего собой синтетический газ, с получением продуктов, включающих спирт (спирты) и необязательно кислоту (кислоты). Способы получения этанола и других спиртов из газообразных субстратов известны. Иллюстративные способы включают способы, описанные, например, в следующих документах: WO 2007/117157, WO 2008/115080, US 6340581, US 6136577, US 5593886, US 5807722 и US 5821111,каждый из которых включен в настоящее описание посредством ссылки. Известно, что большое число анаэробных бактерий способно осуществлять ферментацию СО до спиртов, включающих н-бутанол и этанол, и уксусной кислоты, и эти бактерии подходят для применения в способе по настоящему изобретению. Примеры таких бактерий, которые подходят для применения в изобретении, включают бактерии рода Clostridium, такие как штаммы Clostridium ljungdahlii, включающие штаммы, описанные в следующих документах: WO 00/68407, ЕР 117309, патенте US 5173429, патенте US 5593886 и патенте US 6368819, WO 98/00558 и WO 02/08438, Clostridium carboxydivorans (Liouet al., International Journal of Systematic and Evolutionary Microbiology 33: pp 2085-2091) и Clostridium autoethanogenum (Abrini et al., Archives of Microbiology 161: pp 345-351). Другие подходящие бактерии включают бактерии рода Moorella, включающего Moorella sp. HUC22-1 (Sakai et al., Biotechnology Letters 29: pp 1607-1612), и бактерии рода Carboxydothermus (Svetlichny V.A., Sokolova T.G. et al. (1991), Systematic and Applied Microbiology 14: 254-260). Дополнительные примеры включают Morelia thermoacetica,Moorella thermoautotrophica, Ruminococcus productus, Acetobacterium woodii, Eubactehum limosum, Butyhbactehum methylotrophicum, Oxobacter pfennigii, Methanosarcina barkeri, Methanosarcina acetivorans,Desulfotomaculum kuznetsovii (Simpa et al. Critical Reviews in Biotechnology, 2006 Vol. 26. pp. 41-65). Кроме того, понятно, что в настоящем изобретении могут быть применимы другие ацетогенные анаэробные бактерии, известные специалистам в данной области техники. Также понятно, что данное изобретение можно применять к смешанной культуре двух или более бактерий. Одним из иллюстративных микроорганизмов, подходящих для применения в настоящем изобретении, является бактерия Closthdium autoethanogenum. В одной форме осуществления Closthdium autoethanogenum представляет собой бактерию Closthdium autoethanogenum, обладающую идентификационными характеристиками штамма, депонированного в Немецкой коллекции микроорганизмов и клеточных культур (DSMZ) под идентификационным депозитным номером DSM 19630. В другой форме осуществления Closthdium autoethanogenum представляет собой бактерию Closthdium autoethanogenum, обладающую идентификационными характеристиками штамма, депонированного в DSMZ под депозитным номером DSMZ 10061. В другой форме осуществления Closthdium autoethanogenum представляет собой бактерию Closthdium autoethanogenum, обладающую идентификационными характеристиками штамма, депонированного в DSMZ под депозитным номером DSMZ 23693. Примеры ферментации субстрата, содержащего СО, с получением продуктов, включающих спирты, посредством Closthdium autoethanogenum приведены в следующих документах: WO 2007/117157, WO 2008/115080, WO 2009/022925, WO 2009/058028, WO 2009/064200, WO 2009/064201, WO 2009/113878 и WO 2009/151342; все эти документы включены в настоящее описание посредством ссылки. Культивирование бактерий, применяемое в способах по изобретению, можно выполнять, используя разнообразные способы, известные в данной области техники для культивирования и ферментации субстратов с использованием анаэробных бактерий. Иллюстративные методы приведены в разделе "Примеры" ниже. В качестве дополнительного примера можно использовать способы с применением газообразных субстратов, в общем описанные в следующих статьях: (i) K.Т. все эти статьи включены в настоящее описание посредством ссылки. Ферментацию можно выполнять в любом подходящем биореакторе, сконструированном для газожидкостного контакта, при котором субстрат может контактировать с одним или более микроорганизмов, таком как химический проточный реактор с мешалкой (CSTR, Continuous Stirred Tank Reactor), реактор с иммобилизованными клетками (ICR, Immobilized Cell Reactor), газлифтный ферментер, барботирующий ферментер (BCR, bubble column reactor), мембранный реактор, такой как мембранный биореактор с системой полых волокон (HFMBR, Hollow Fibre Membrane Bioreactor) или реактор с орошаемым слоем (TBR, trickle bed reactor), в монолитном биореакторе или в циркуляционных реакторах.). В некоторых формах осуществления изобретения биореактор может также включать первый реактор для выращивания, в котором культивируют микроорганизмы, и второй реактор ферментации, в который подают ферментативный бульон из реактора для выращивания, и в котором получают большую часть продукта ферментации (например, этанола и ацетата). Согласно различным формам осуществления изобретения источник углерода для реакции ферментации представляет собой синтетический газ, полученный в результате газификации. Субстрат, представляющий собой синтетический газ, в характерном случае содержит основную долю СО, составляющую, например, по меньшей мере от приблизительно 15 до приблизительно 75% СО по объему, от 20 до 70% СО по объему, от 20 до 65% СО по объему, от 20 до 60% СО по объему и от 20 до 55% СО по объему. В конкретных формах осуществления субстрат содержит приблизительно 25, либо приблизительно 30, либо приблизительно 35, либо приблизительно 40, либо приблизительно 45, либо приблизительно 50% СО, либо приблизительно 55% СО, либо приблизительно 60% СО по объему. Субстраты, имеющие более низкие концентрации СО, например 6%, могут быть также подходящими, в частности, когда также присутствуют Н 2 и СО 2. В конкретных формах осуществления присутствие водорода приводит в результате к повышению общей эффективности производства спирта. Газообразный субстрат может также содержать некоторое количество СО 2, например, составляющее от приблизительно 1 до приблизительно 80% СО 2 по объему или от 1 до приблизительно 30% СО 2 по объему. Согласно конкретнымформам осуществления изобретения содержание СО и/или содержание Н 2 риформированного потока субстрата можно обогатить перед пропусканием этого потока в биореактор. Например, водород можно обогащать, используя технологии, хорошо известные в данной области техники,такие как короткоцикловая абсорбция, криогенное разделение и мембранное разделение. Также можно обогатить СО, используя технологии, хорошо известные в данной области техники, такие как очистка газа в скруббере с использованием медно-аммиачного волокна, криогенное разделение, технология COSORB(абсорбция в дихлориде меди и алюминия в толуоле), вакуумная короткоцикловая адсорбция и мембранное разделение. Другие способы, применяемые для разделения и обогащения газов, подробно описаны в документе PCT/NZ2008/000275, полностью включенном в данную работу посредством ссылки. В характерном случае монооксид углерода добавляют в реакцию ферментации в газообразном состоянии. Тем не менее способы по изобретению не ограничены добавлением субстрата в данном состоянии. Например, монооксид углерода может быть получен в виде жидкости. Например, жидкость можно насыщать газом, содержащим монооксид углерода, и добавлять эту жидкость в биореактор. Данное действие может быть выполнено с использованием стандартной методологии. В качестве примера для этой цели можно применять генератор дисперсии микропузырьков (Hensirisak et al. Scale-up of microbubbledispersion generator for aerobic fermentation; Applied Biochemistry and BiotechnoloavVolume 101. Number 3/October. 2002). Понятно, что для выращивания бактерий для проведения ферментации от СО до спирта в дополнение к субстрату, представляющему собой СО-содержащий газ, в биореактор нужно подавать подходящую жидкую питательную среду. Питательная среда содержит достаточное количество витаминов и минералов, чтобы дать возможность для роста применяемого микроорганизма. Анаэробные среды, подходящие для ферментации этанола с использованием СО в качестве единственного источника углерода,известны в данной области техники. Например, подходящие среды описаны в патентах US 5173429 и 5593886, а также в следующих документах: WO 02/08438, WO 2007/117157, WO 2008/115080, WO 2009/022925, WO 2009/058028, WO 2009/064200, WO 2009/064201, WO 2009/113878 и WO 2009/151342,на которые ссылаются выше. В настоящем изобретении предложена новая среда, обладающая повышенной эффективностью при поддержании роста микроорганизмов и/или при производстве спирта в процессе ферментации. Данная среда более подробно описана ниже. Ферментацию желательно выполнять в соответствующих условиях для прохождения желаемой ферментации (например, от СО до этанола). Условия реакции, которые следует учитывать, включают следующие условия: давление, температуру, скорость потока газа, скорость потока жидкости, рН среды,окислительно-восстановительный потенциал среды, скорость перемешивания (при использовании химического проточного реактора с мешалкой), уровень инокулума, максимальные концентрации газообразного субстрата, чтобы гарантировать, что концентрация СО в жидкой фазе не станет ограничивающей, и максимальные концентрации продукта, чтобы избежать ингибирования продуктом. Подходящие условия описаны в следующих документах: WO 02/08438, WO 2007/117157, WO 2008/115080, WO 2009/022925,WO 2009/058028, WO 2009/064200, WO 2009/064201, WO 2009/113878 и WO 2009/151342; все эти документы включены в данную работу посредством ссылки. Оптимальные условия реакции отчасти зависят от конкретного применяемого микроорганизма. Тем не менее в целом предпочтительно проводить ферментацию при давлении, превышающем давление окружающей среды. Работа при повышенных давлениях дает возможность значительно повысить скорость переноса СО из газовой фазы в жидкую фазу, где он может поглощаться микроорганизмом в качестве источника углерода для продуцирования этанола. Это, в свою очередь, означает, что время пребывания(определяемое как объем жидкости в биореакторе, деленный на скорость входящего потока газа) можно уменьшить, если поддерживать биореакторы при повышенном давлении, а не при атмосферном давлении. Преимущества проведения ферментации газа до этанола при повышенных давлениях также описаны в других документах. Например, в документе WO 02/08438 описаны ферментации газа до этанола,проводимые при избыточных (манометрических) давлениях, составляющих 30 psig (фунтов на квадратный дюйм) и 75 psig (фунтов на квадратный дюйм), с получением производительности, составляющей 150 и 369 г/л/сутки этанола соответственно. Тем не менее было обнаружено, что иллюстративные ферментации, проведенные с использованием такой же среды и таких же композиций входящего газа при атмосферном давлении, производят в 10-20 раз меньше этанола на литр в сутки. Также желательно, чтобы скорость введения газообразного субстрата, содержащего СО и Н 2, имела такое значение, чтобы гарантировать, что концентрация СО в жидкой фазе не станет ограничивающей. Это связано с тем, что вследствие СО-ограничивающих условий продукт этанол потребляется культурой. Выделение продукта. Продукты реакции ферментации можно выделить, используя известные способы. Иллюстративные способы включают способы, описанные в следующих документах: WO 2007/117157, WO 2008/115080,WO 2009/022925, US 6340581, US 6136577, US 5593886, US 5807722 и US 5821111. Тем не менее в кратком изложении и в качестве примера, этанол можно выделить из ферментативного бульона такими способами, как фракционная перегонка или выпаривание, а также экстрактивная ферментация. В результате перегонки этанола из ферментационного бульона получают азеотропную смесь этанола и воды (т.е. 95% этанола и 5% воды). Затем можно получить безводный этанол посредством применения технологии дегидратации этанола с помощью молекулярных сит, что также хорошо известно в данной области техники. Методы экстрактивной ферментации включают применение для выделения этанола из разбавленного ферментативного бульона смешиваемого с водой растворителя, представляющего низкий риск токсичности для ферментирующего организма. Например, олеиловый спирт является растворителем, который можно применять в процессе экстракции данного типа. Олеиловый спирт непрерывно вводят в ферментер, где данный растворитель вызывает образование слоя в верхней части ферментера, который непрерывно экстрагируют и подают через центрифугу. Затем воду и клетки легко отделяют от олеилового спирта и возвращают в ферментер, при этом растворитель со слоем этанола подают в устройство мгновенного испарения. Большая часть этанола испаряется и конденсируется, тогда как олеиловый спирт является нелетучим, и его выделяют для повторного использования в ферментации. Ацетат, который может быть получен в качестве побочного продукта реакции ферментации, можно также выделить из ферментативного бульона, используя способы, известные в данной области техники. Например, можно использовать адсорбционную систему, включающую активированный угольный фильтр. В данном случае предпочтительно сначала удалить бактериальные клетки из ферментативного бульона, используя подходящее разделительное устройство. В данной области техники известны многочисленные способы получения бесклеточного ферментативного бульона для выделения продукта, основанные на фильтрации. Затем бесклеточный пермеат (фильтрат), содержащий этанол и ацетат, пропускают через колонну, содержащую активированный уголь, для адсорбции ацетата. Ацетат в форме кислоты (уксусная кислота) легче адсорбируется активированным углем, чем солевая форма (ацетат). Поэтому перед пропусканием ферментационного бульона через колонну с активированным углем предпочтительно снижать его рН до значения, составляющего менее чем приблизительно 3, чтобы преобразовать основную часть ацетата в форму уксусной кислоты. Уксусную кислоту, адсорбированную на активированном угле, можно выделить путем элюирования, используя способы, известные в данной области техники. Например, для элюирования связанного ацетата можно использовать этанол. В некоторых формах осуществления для элюирования ацетата можно использовать сам этанол, полученный посредством процесса ферментации. Поскольку точка кипения этанола составляет 78,8 С, а точка кипения уксусной кислоты составляет 107C, этанол и ацетат можно легко отделить друг от друга, используя способ, основанный на летучести, такой как перегонка. Другие способы выделения ацетата из ферментативного бульона также известны в данной области техники и могут быть использованы. Например, в патентах US 6368819 и US 6753170 описана система растворителя и сорастворителя, которую можно использовать для экстракции уксусной кислоты из ферментативных бульонов. Как и в случае примера системы на основе олеилового спирта, описанной для экстрактивной ферментации этанола, в системах, описанных в патентах US 6368819 и US 6753170, описан несмешиваемый с водой растворитель/сорастворитель, который можно смешивать с ферментативным бульоном либо в присутствии, либо в отсутствие ферментирующих микроорганизмов с целью экстракции продукта, представляющего собой уксусную кислоту. Затем растворитель/сорастворитель, содержащий продукт, представляющий собой уксусную кислоту, отделяют от бульона путем перегонки. Затем можно использовать вторую стадию перегонки, чтобы очистить уксусную кислоту от системы растворителя/сорастворителя. Продукты реакции ферментации (например, этанол и ацетат) можно выделять из ферментативного бульона путем непрерывного извлечения части бульона из биореактора ферментации, отделения бактериальных клеток от бульона (удобно с помощью фильтрования) и выделения одного или более продуктов из бульона одновременно или последовательно. В случае этанола его можно удобно выделять путем перегонки, а ацетат можно выделять путем адсорбции на активированном угле, используя описанные выше способы. Отделенные бактериальные клетки предпочтительно возвращают в биореактор ферментации. Бесклеточный пермеат, остающийся после выделения этанола и ацетата, также предпочтительно возвращают в биореактор ферментации. Чтобы пополнить питательную среду, перед возвращением в биореактор в клеточный пермеат можно добавлять дополнительные питательные вещества (такие как витамины В). Также, если рН бульона был доведен, как описано выше, для усиления адсорбции уксусной кислоты на активированном угле, перед возвращением в биореактор рН следует снова доводить до значения рН бульона в биореакторе ферментации. Общие сведения Формы осуществления изобретения описаны в качестве примера. Тем не менее понятно, что конкретные стадии или установки, обязательные в одной форме осуществления, могут не быть обязательны в другой. Напротив, стадии или установки, включенные в описание конкретной формы осуществления, можно необязательно предпочтительно применять в формах осуществления, где они специально не указаны. Хотя изобретение в широком смысле описано со ссылкой на какой-либо тип потока, который может перемещаться по системе или вокруг системы (систем) посредством любых известных средств перемещения, в некоторых формах осуществления биогаз и риформированные и/или смешанные потоки субстрата являются газообразными. Специалистам в данной области техники понятно, что конкретные установки могут быть связаны подходящими трубопроводными средствами или тому подобным, которые могут быть сконструированы для приема или пропускания потоков через систему. Можно обеспечить насос или компрессор, чтобы способствовать доставке потоков в конкретные установки. Кроме того,компрессор можно применять для повышения давления газа, подаваемого в одну или более установок,например, в биореактор. Как обсуждалось в данной работе выше, давление газов внутри биореактора может влиять на эффективность выполняемых в них реакций ферментации. Таким образом, давление можно регулировать для повышения эффективности ферментации. Подходящие давления для общепринятых реакций известны в данной области техники. Кроме того, системы или способы по изобретению могут необязательно включать средства регулирования и/или контроля других параметров, чтобы повысить общую эффективность способа. Например,конкретные формы осуществления могут включать средства определения, осуществляющие мониторинг композиции субстрата и/или отработанного потока (потоков). Дополнительно конкретные формы осуществления могут включать средства контроля доставки потока (потоков) субстрата в конкретные установки или элементы в пределах конкретной системы, если средства определения определяют, что композиция потока подходит для конкретной установки. Например, в случаях, где поток газообразного субстрата содержит низкие уровни СО или высокие уровни О 2, что может быть вредно для реакции ферментации,поток субстрата можно отводить от биореактора. В конкретных формах осуществления изобретения система включает средства для мониторинга и контроля целевого состояния потока субстрата и/или скорости тока, чтобы поток, имеющий желаемую или подходящую композицию, мог быть доставлен в конкретную установку. Кроме того, может быть необходимо нагревать или охлаждать конкретные компоненты системы или поток(и) субстрата перед поступлением или во время нахождения в одной или более установок в процессе. В таких случаях можно применять известные средства нагревания или охлаждения. Различные формы осуществления систем по изобретению описаны в сопроводительных графических материалах. Как показано на фиг. 2, в одном примере осуществления изобретения предложена система и способ производства одного или более продуктов из потока газа, используемого в процессе производства аммиака, где биореактор заменяет реактор конверсии водяного газа, находящийся в типичных системах производства аммиака. В соответствии с фиг. 2 поток природного газа подают в реактор 210 парового риформинга, где поток природного газа подвергают взаимодействию с получением риформированного потока, содержащего Н 2, СО и СО 2, а также не прореагировавший СН 4. Затем риформированный поток направляют во вторичный реактор 212 риформинга, где риформированный поток подвергают взаимодействию с получением потока субстрата, содержащего Н 2, СО, СО 2, N2 и следовые количества СН 4. Поток субстрата пропускают в биореактор 222. Поток субстрата подвергается ферментации в биореакторе культурой, содержащей один или более анаэробных микроорганизмов, с получением одного или более продуктов ферментации и потока отработанного газа, содержащего Н 2, СО 2, N2 и небольшие или следовые количества СН 4 и СО. Поток отработанного газа пропускают в зону 216 отделения СО 2, где СО 2 отделяют от потока отработанного газа с получением в результате потока газа, богатого водородом, и потока газа СО 2. Затем поток газа СО 2 можно направлять в установку производства мочевины. Поток газа,богатый водородом, направляют в реактор 218 метанизации, где удаляют какой-либо остаточный СО,находящийся в этом потоке. Затем полученный в результате поток газа, богатый водородом, пропускают в зону 220 синтеза аммиака для производства аммиака. На фиг. 3 изображены альтернативный способ и система по изобретению, обеспечивающие как биореактор, так и реактор конверсии водяного газа. На фиг. 3 поток природного газа подают в реактор 310 парового риформинга, где поток природного газа подвергают взаимодействию с получением риформированного потока, содержащего Н 2, СО и СО 2, а также СН 4. Затем по меньшей мере часть риформированного потока направляют во вторичный реактор 312 риформинга, где риформированный поток подвергают взаимодействию с получением потока субстрата, содержащего Н 2, СО, СО 2, N2 и следовые количества СН 4, который затем пропускают в реактор 314 конверсии водяного газа (КВГ), где СО, находящийся в этом потоке, подвергают взаимодействию с Н 2 О с получением СО 2. Как показано на фиг. 3, часть любого из потоков или обоих потоков, выходящих из реактора 310 парового риформинга и/или из вторичного реактора 312 риформинга, можно направлять в биореактор 322 вместо КВГ 314. Биореактор функционирует для удаления СО из потока и производит один или более продуктов ферментации. Поток отработанного газа, выходящий из биореактора 322, направляют в зону 316 отделения СО 2 параллельно с потоком газа, выходящего из КВГ 314. Абсорбер СО 2 отделяет СО 2 от потока газа с получением в результате потока газа, богатого водородом. Поток газа, богатый водородом, обрабатывают в реакторе 318 метанизации для удаления каких-либо следов СО в газе, после чего его пропускают в зону синтеза аммиака для производства аммиака. В настоящем описании изобретение описано со ссылкой на некоторые предпочтительные формы осуществления, чтобы дать возможность читателю осуществлять изобретение на практике без лишнего экспериментирования. Специалистам в данной области техники понятно, что изобретение может быть выполнено на практике в большом числе вариантов и модификаций, отличающихся от конкретно описанных. Понятно, что изобретение включает все такие варианты и модификации. Кроме того, заголовки, заглавие или тому подобное представлены, чтобы обеспечить читателю понимание данного документа, и их не следует считать ограничивающими объем данного изобретения. Полные описания всех заявок на патенты,патентов и публикаций, цитируемых в данной работе, включены в данную работу посредством ссылки. Более конкретно, как понятно специалистам в данной области техники, применения форм осуществления изобретения могут включать один или более дополнительных элементов. В конкретном примере или в описании могут быть показаны только элементы, необходимые для понимания изобретения в его различных аспектах. Тем не менее объем изобретения не ограничен описанными формами осуществления и включает системы и/или способы, включающие одну или более дополнительных стадий и/или одну или более заменяющих стадий, и/или системы и/или способы, исключающие одну или более стадий. В данном описании ссылка на какой-либо предшествующий уровень техники не является подтверждением или какой-либо формой предположения, что предшествующий уровень техники составляет часть общих знаний в области науки в любой стране мира, и не должна истолковываться таким образом. На протяжении всего данного описания и любого пункта нижеследующей формулы изобретения,если контекст не требует иного, слова "включает", "включающий" и тому подобное следует истолковывать в смысле включительно, противоположном смыслу исключения, то есть в смысле "включающий, но не ограниченный". Примеры Приготовление среды. 1,4 л раствора А среды асептически и анаэробно переносили в 2 л реактор CSTR и непрерывно продували N2. Сразу после перенесения в реактор ферментации окислительно-восстановительное состояние и рН перенесенной среды можно непосредственно измерять с помощью датчиков. Среду нагревали до 37 С и перемешивали при 400 об/мин; добавляли 1,5 мл резазурина (2 г/л). Добавляли 1,0 мл 85% Н 3 РО 4 до получения 10 мМ раствора. Доводили рН до 5,3, используя NH4OH. Добавляли ионы металлов согласно раствору В и добавляли 15 мл раствора С. Добавляли 3 ммоль цистеин-HCl и доводили рН до рН 5,5,используя NH4OH. Бактерии. Clostridium autoethanogenum был получен из Немецкой коллекции микроорганизмов и клеточных культур (DSMZ) под идентификационным депозитным номером DSM23693. Газообразный субстрат. Биогазовый источник газообразного субстрата для данного эксперимента был получен из метана. Метан преобразовывали в газообразный субстрат, содержащий СО, посредством процесса парового риформинга. Паровой риформинг выполняли в реакторе Inconel 800 при температуре, составляющей около 818 С, и при избыточном давлении, составляющем около 128 psig (фунтов на кв. дюйм). В реактор загружали алюмоникелевый катализатор и для риформинга биогаза использовали отношение пара к углероду (S/C), составляющее 3,6. Перед процессом риформинга метан смешивали с СО 2 с получением отношения СН 4/СО 2, составляющего приблизительно 1,5. В результате парового риформинга метана получили газообразный субстрат, имеющий следующий состав: Н 2 64,7%, N2 7,69%, СО 14,1%, СО 2 8,8%, H2S 0,0%. Ферментация в сывороточной бутылке. Инкубацию проводили в двух герметично закрытых сывороточных бутылках объемом 250 мл (SB1, SB2), содержащих 50 мл среды. Каждую бутылку инокулировали 1 мл растущей культуры Clostridium autoethanogenum (номер DSMZ 23693). Затем газ свободного пространства откачивали и заполняли до избыточного давления, составляющего 25 psig (фунтов на кв. дюйм), газообразным метаном, содержащим СО, из парового риформинга. Использовали встряхивательинкубатор и температуру реакции поддерживали при 37 С. Отбор образцов и аналитические методы. Образцы среды брали из сывороточных бутылок через интервалы, составляющие периоды вплоть до 44 ч. Каждый раз при отборе среды обращали внимание,чтобы гарантировать отсутствие поступления или выхода какого-либо газа внутрь или наружу сывороточной бутылки. Для количественного определения уровня ацетата и этанола в процессе ферментации использовали обычную ВЭЖХ (высокоэффективную жидкостную хроматографию). ВЭЖХ. Система ВЭЖХ Agilent серия 1100. Подвижная фаза: 0,0025 н. серная кислота. Скорость тока и давление: 0,800 мл/мин. Колонка: Alltech IOA;по каталогу 9648, 1506,5 мм, размер частиц 5 мкм. Температура колонки: 60 С. Детектор: показатель преломления. Температура детектора: 45 С. Способ приготовления образца. 400 мкл образца и 50 мкл 0,15 М ZnSO4 смешивают и загружают в пробирку Eppendorf. Пробирки центрифугируют в течение 3 мин при 12000 об/мин, 4 С. 200 мкл супернатанта переносят во флакон для ВЭЖХ и 5 мкл впрыскивают в прибор для ВЭЖХ. Измерения давления. Измерения давления свободного пространства в сывороточных бутылках проводили через интервалы, составляющие периоды вплоть до 3 суток. После завершения реакции конечную композицию свободного пространства анализировали с помощью газовой хроматографии. Газовая хроматография. Газовый хроматограф HP 5890 серия II, использующий пламенноионизационный детектор. Капиллярная колонка: ЕС 1000-Alltech EC1000 30 м 0,25 мм 0,25 мкм. Газовый хроматограф работал в режиме разделения при общей скорости потока водорода 50 мл/мин с продувочным потоком 5 мл (разделение 1:10), давление на входе в колонку 10 psi, приводящее в результате к линейной скорости 45 см/с. Температурную программу инициировали при 60 С, удерживали в течение 1 мин, затем быстро линейно увеличивали до 215 С на 30 С в мин, затем удерживали в течение 2 мин. Температура впрыска составляла 210 С, и температура детектора составляла 225 С. Результаты Таблица 1 В табл. 1 показана ВЭЖХ и давление свободного пространства для двух сывороточных бутылок на протяжении ферментации. Измерения метаболитов проводили сразу после инокуляции и через 1,0 и 1,8 суток инкубации. В табл. 2 показана исходная композиция газа в свободном пространстве на сутки 0,0 и конечная композиция газа в свободном пространстве на сутки 1,8. Результаты четко показывают утилизацию СО. В SB2 показано снижение концентрации СО в % с 14,1 до 0,0% и повышение концентрации СО 2 с 8,8 до 15,7%. Соответственно, в обеих сывороточных бутылках показано повышение уровней метаболитов между сутками 0,0 и сутками 2,9. Представленные выше результаты демонстрируют ферментацию СО микроорганизмом С. autoethanogenum с получением этанола и ацетата. Значения для водорода колеблются вследствие неэффективной калибровки ГХ при высоких уровнях Н 2, но не влияют на углеродный баланс. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Способ производства одного или более продуктов из потока газа, полученного в процессе производства аммиака, включающий следующие стадии:a) преобразование по меньшей мере части потока газа, содержащего метан, в субстрат, содержащий СО, СО 2 и Н 2;b) пропускание по меньшей мере части субстрата в биореактор, содержащий культуру одного или более карбоксидотрофных микроорганизмов, анаэробно ферментирующих по меньшей мере часть субстрата, содержащего СО и Н 2, с получением одного или более продуктов, включающих спирты и/или кислоты, и потока отработанного газа, содержащего водород и диоксид углерода;c) направление потока отработанного газа в зону отделения СО 2, работающую в условиях, обеспечивающих удаление по меньшей мере части СО 2, и получение очищенного потока отработанного газа; иd) направление очищенного потока отработанного газа в зону синтеза аммиака, работающую при условиях, обеспечивающих получение аммиака. 2. Способ по п.1, при котором поток газа преобразуют в поток субстрата, содержащий СО, СО 2 и Н 2, способом парового риформинга. 3. Способ по п.2, при котором поток субстрата, выходящий из процесса парового риформинга, пропускают во вторичный реактор риформинга, где по меньшей мере часть метана в потоке субстрата преобразуют в СО, СО 2 и Н 2 перед пропусканием в биореактор. 4. Способ по любому из пп.1, или 2, или 3, в котором один или более продуктов стадии (b) выбраны из группы, состоящей из следующих веществ: этанола, 2,3-бутандиола и уксусной кислоты. 5. Способ по п.1, в котором карбоксидотрофный микроорганизм выбран из группы, включающей микроорганизмы следующих родов: Moorella, Clostridium, Ruminococcus, Acetobacterium, Eubacterium,Butyribacterium, Oxobacter, Methanosarcina и Desulfotomaculum. 6. Способ по п.1, в котором карбоксидотрофный микроорганизм представляет собой Clostridium autoethanogenum. 7. Способ по п.1, дополнительно включающий:e) направление второй части субстрата в реактор конверсии водяного газа, работающий в условиях,обеспечивающих получение потока выходящего газа, содержащего СО 2 и Н 2; иf) направление потока выходящего газа в зону отделения. 8. Способ по п.2, в котором СО 2, отделенный от потока отработанного газа, подвергают рециркуляции в реакторе парового риформинга. 9. Способ по п.3, в котором СО 2, отделенный от потока отработанного газа, подвергают рециркуляции во вторичном реакторе риформинга.
МПК / Метки
МПК: C12P 5/02, C12M 1/107, C12P 7/54, C12R 1/145, C12P 7/06, C12P 7/16, C12N 1/20
Метки: ферментации, способ
Код ссылки
<a href="https://eas.patents.su/17-23403-sposob-fermentacii.html" rel="bookmark" title="База патентов Евразийского Союза">Способ ферментации</a>
Предыдущий патент: Амины жирного ряда, амидоамины жирных кислот и их производные из метатезиса натурального масла
Следующий патент: Способ лечения немелкоклеточного рака легких
Случайный патент: Гидраты 2-хлор-5-[3,6-дигидро-3-метил-2,6-диоксо-4-(трифторметил)-1-(2н)-пиримидинил]-4-фтор-n-[[метил-(1-метилэтил)амино]сульфонил]бензамида