Соединения для лечения расстройств, опосредованных рецепторами адгезии cd11/cd18
Номер патента: 7852
Опубликовано: 27.02.2007
Авторы: Рейнолдс Марк, Бурдик Даниел Дж., Макдауел Роберт С., Уиз Кеннет Дж., Стенли Марк Си., Марстерс Джеймс Си., Оаре Девид, Гадек Томас Р.
Формула / Реферат
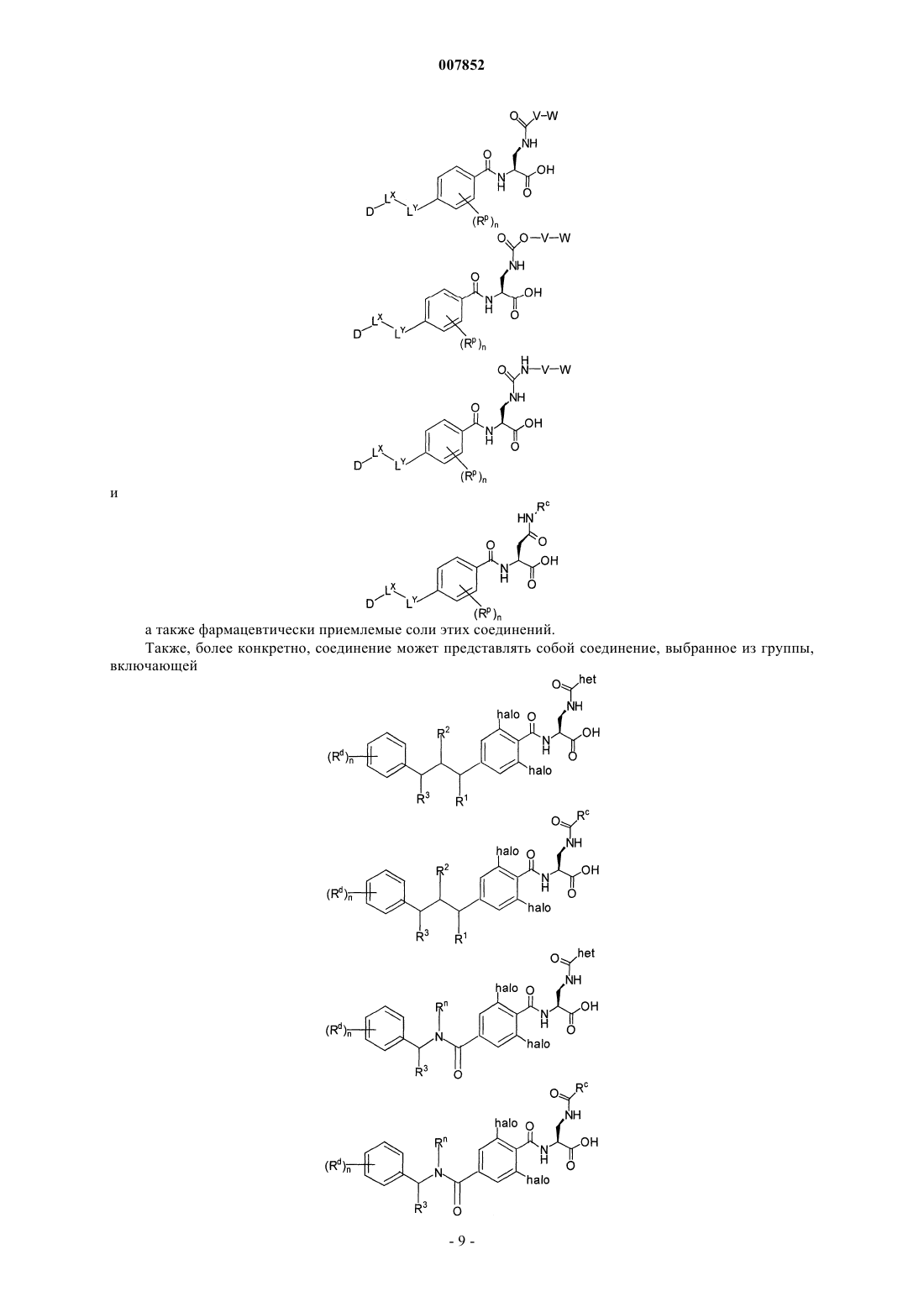
1. Соединение общей формулы
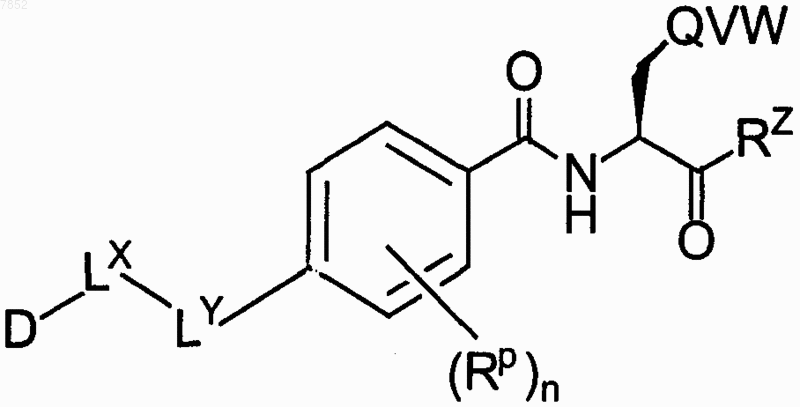
где D выбран из группы
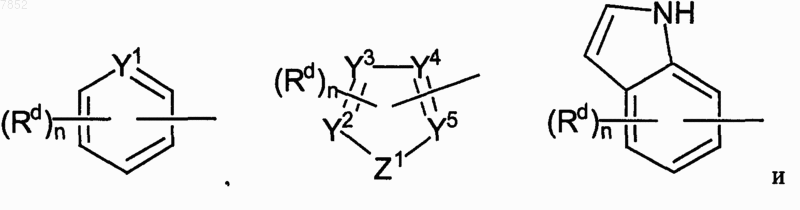
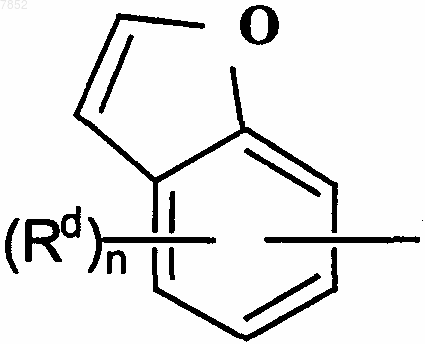
где Y1 выбран из группы, включающей СН и С-ОН;
Y2, Y3, Y4 и Y5 выбраны из группы, включающей СН;
Z1 выбран из группы, включающей NRn, О и S;
n=0-3;
LX выбран из группы, включающей замещенные или незамещенные
С2-С5-алкилен,
С3-С6-циклоалкилен,
С0-С3-алкилен-NRn-(С=O)-С0-С3-алкилен,
С0-С3-алкилен-(С=O)-NRn-С0-С3-алкилен,
С0-С3-алкилен-О-С0-С3-алкилен,
С0-С3-алкилен-NRn-С0-С3-алкилен,
С0-С3-алкилен-(С=O)-С0-С3-алкилен,
С0-С3-алкилен-СR1=СR2-С0-С3-алкилен,
С0-С3-алкилен-Су С-С0-С3-алкилен, и
С0-С3-алкилен-гет-С0-С3-алкилен,
при этом заместители выбираются из группы, включающей от 1 до 3 радикалов R1, R2 и R3;
LY выбран из группы, включающей замещенные или незамещенные
С0-С2-алкилен,
С0-С2-алкилен-NRn-(С=O)-С0-С2-алкилен, С0-С2-алкилен-(С=O)-NRn-С0-С2-алкилен,
С0-С2-алкилен-O-С0-С2-алкилен,
С0-С2-алкилен-NRn-С0-С2-алкилен,
С0-С2-алкилен-(С=O)-С0-С2-алкилен,
при этом заместители выбраны из группы, включающей от 1 до 3 радикалов R1, R2 и R3;
R1, R2 и R3 выбраны из группы, включающей
С1-С8-алкил,
водород,
гидроксигруппу,
феноксигруппу,
фенил и
RC выбран из группы, состоящей из водорода и замещенного или незамещенного гета, при этом заместители в гете представляют собой от 1 до 3 радикалов Rd;
гет является моно-, би- или трициклическим 5-, 6-, 7-, 9- или 10-звенным насыщенным, ненасыщенным или ароматическим кольцом, имеющим от 1 до 4 гетероатомов, выбранных из группы, включающей азот, кислород и серу;
Rp и Rd независимо выбраны из группы, включающей
ОН,
CN,
NO2,
галоген,
ORn,
SRn,
SORn,
CF3,
Rc,
NRnRn',
NRnC(=O)-O-Rn',
NRnC(=O)-Rn',
С0-С6-алкил-SО2-Rn,
C0-C6-алкил-SO2-NRnRn',
C(=O)-Rn,
O-C(=O)-Rn,
C(=O)-O-Rn,
C(=O)-NRnRn';
Rd представляет собой химическую связь, когда гет представляет собой двухвалентную соединительную группу;
Rn и Rn' независимо выбраны из группы, включающей
водород,
гидроксигруппу,
C1-С6-алкил,
галоген-C1-С6-алкил,
С1-С6-алкил-гет,
гет-С1-С6-алкил,
С6-С12-арил и
гет;
RZ представляет собой гидроксигруппу;
Q отсутствует или представляет собой С0-С3-алкил, замещенный группой, выбранной из
-N(Rn)-,
-N(Rn)-C(=O)-,
-N(Rn)-C(=O)-O-,
-N(Rn)-C(=O)-N(Rn)-,
-N(Rn)-SO2-,
-C(=O)-,
-O-C(=O)-N(Rn)-,
-C(=O)-N(Rn)-;
V отсутствует или представляет собой бивалентную группу, возможно, замещенную, выбранную из группы, включающей
С1-С11-алкилена,
С2-С6-алкенилена,
С0-С6-алкил-гета,
при этом заместители в любом алкиле представляют собой от 1 до 3 радикалов Ra, а заместители в любом ариле или гете представляют собой от 1 до 3 радикалов Rd;
W представляет собой С0-С3-алкил, замещенный группой, выбранной группы, включающей
Ra,
NH-C(=O)-RC,
C(=O)-RC,
C(=O)-NRnRn',
и RC,
обладающее способностью модулировать адгезию между внутриклеточными адгезионными молекулами и лейкоцитарным интегриновым семейством рецепторов, а также его фармацевтически приемлемые соли;
Ra представляет собой аминогруппу.
2. Соединение по п.1, выбранное из группы, включающей
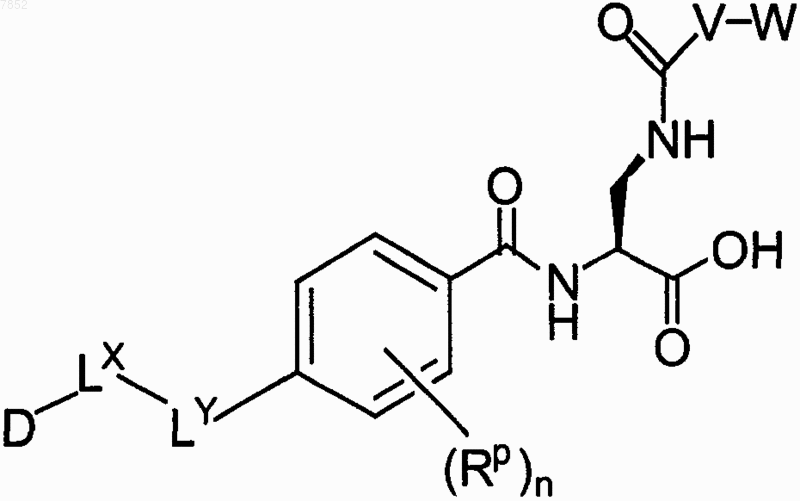
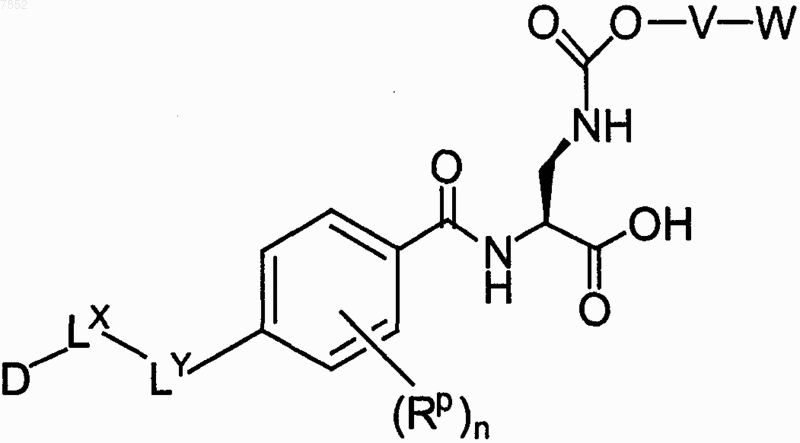
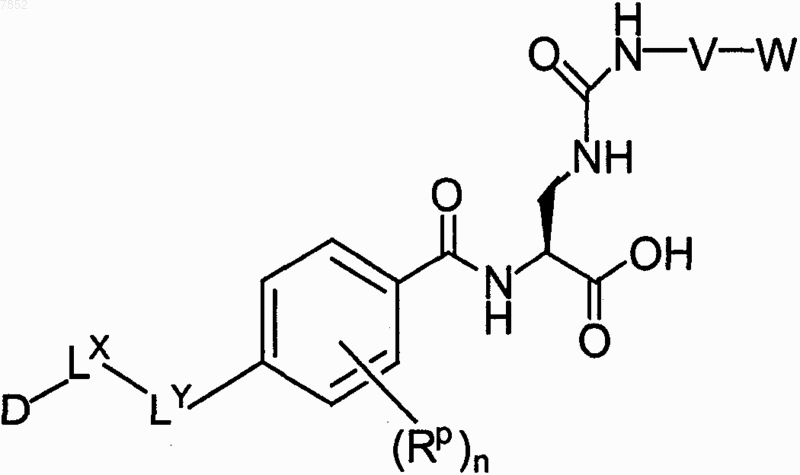
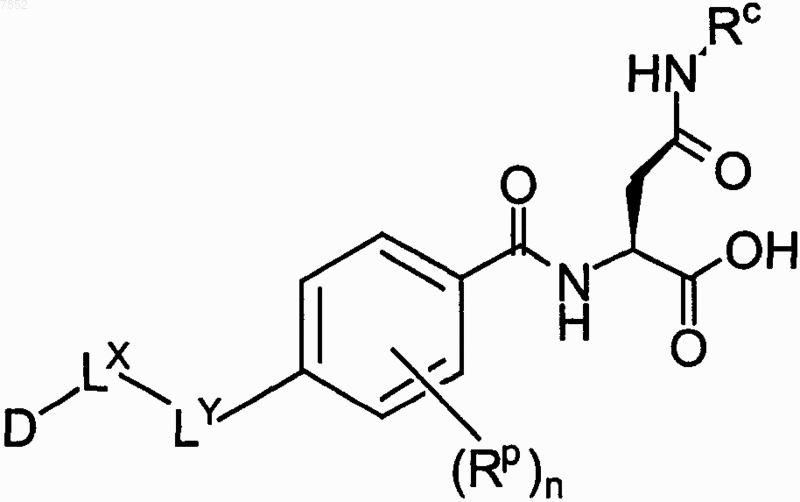
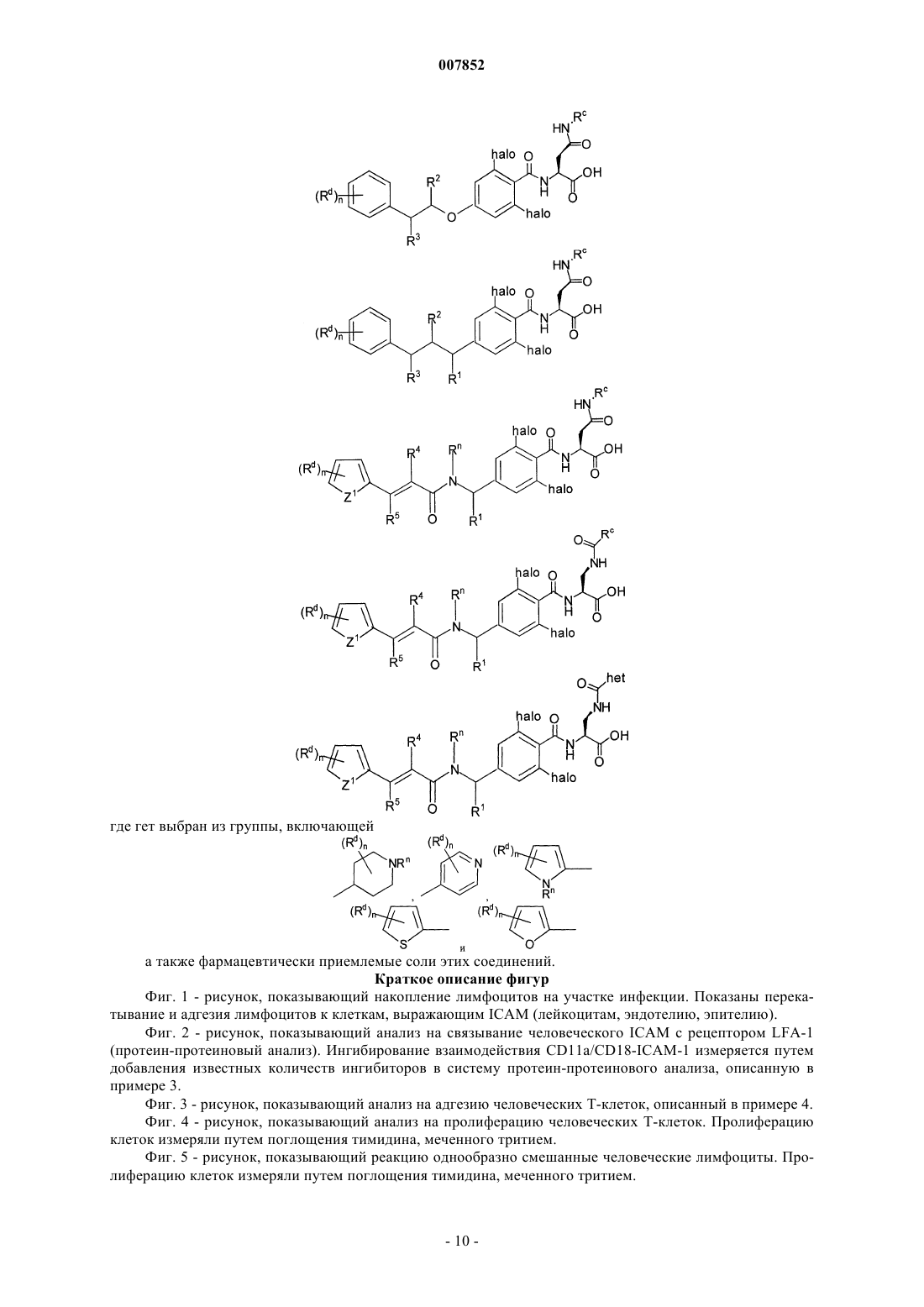
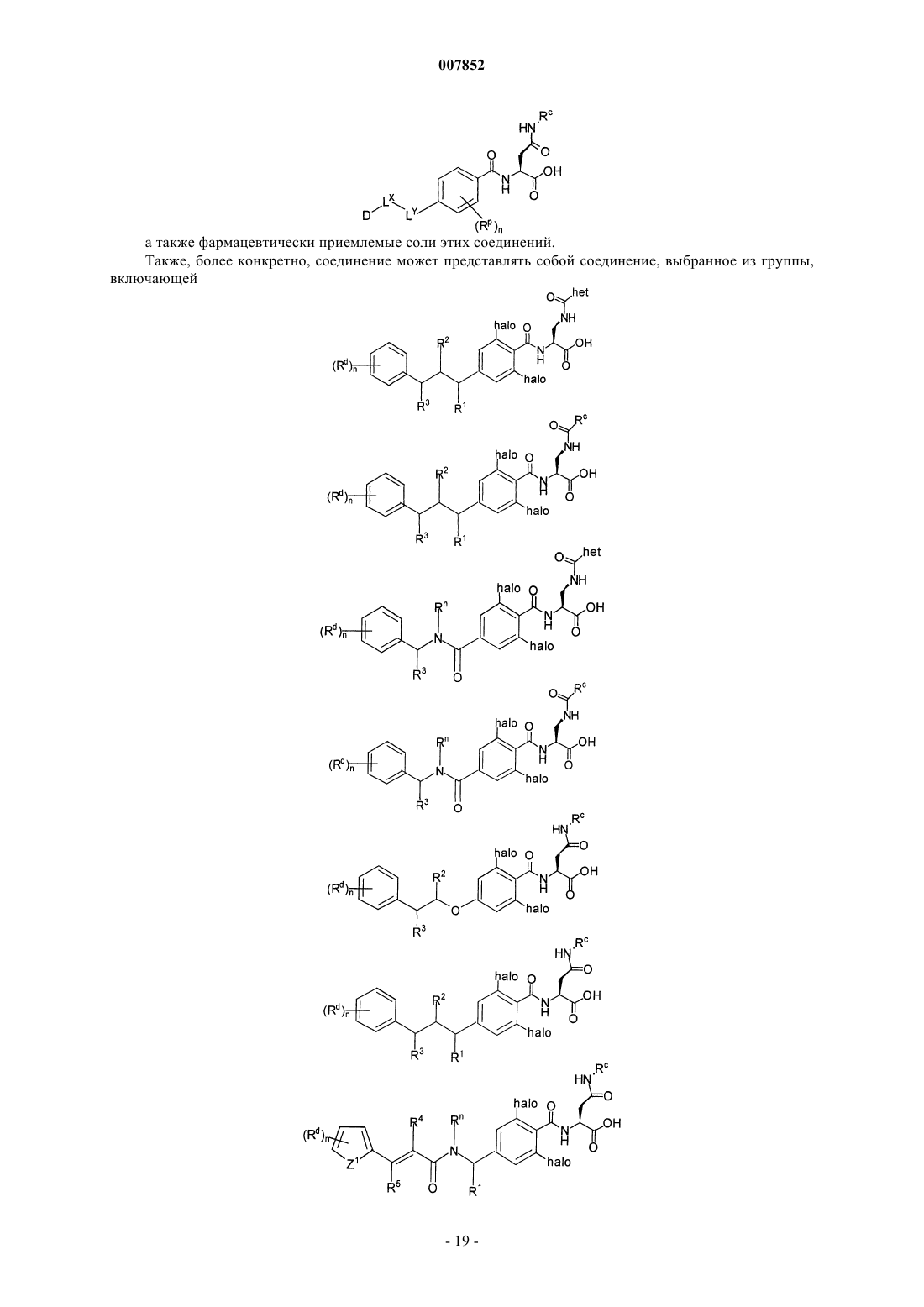
3. Соединение по п.1, выбранное из группы, включающей
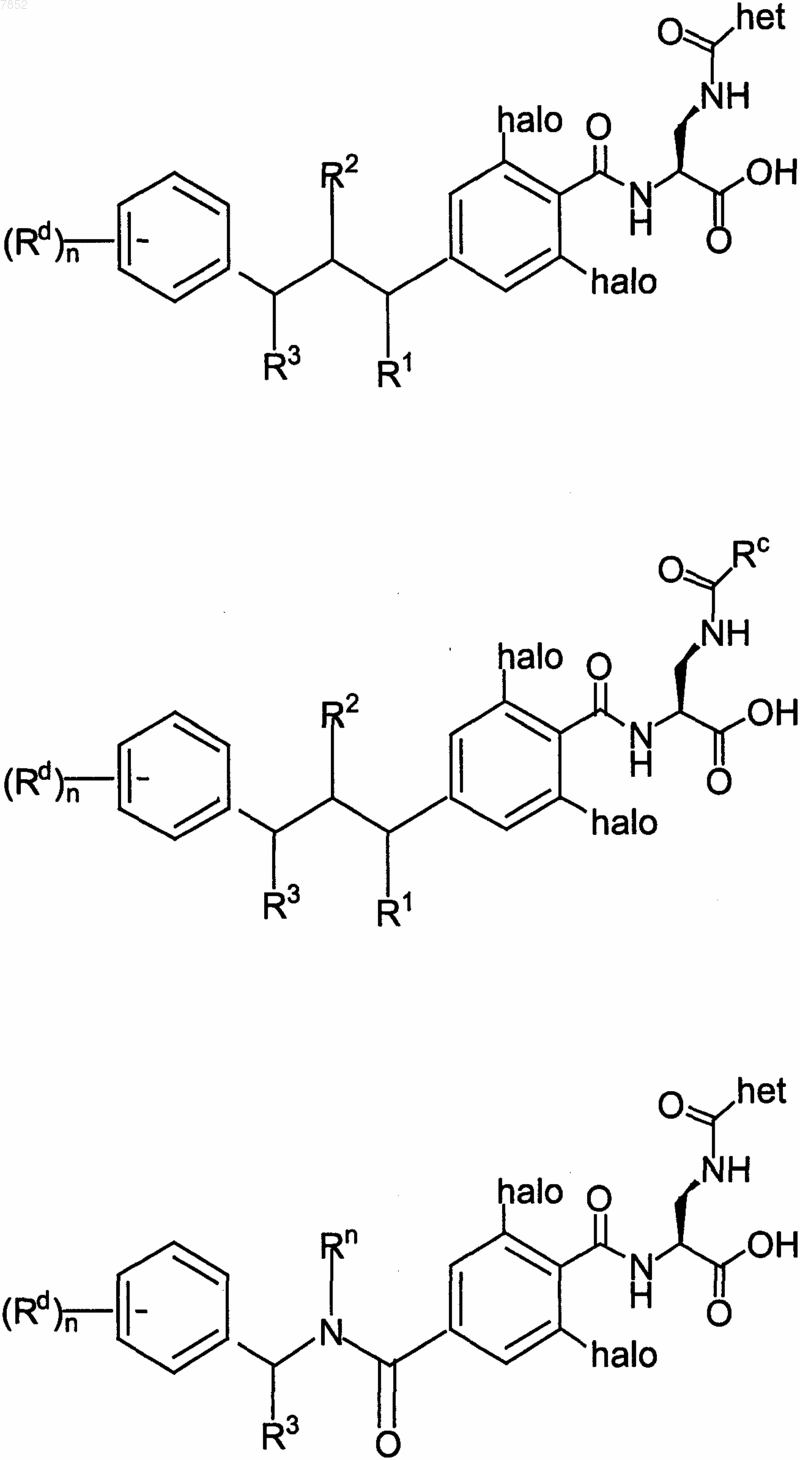
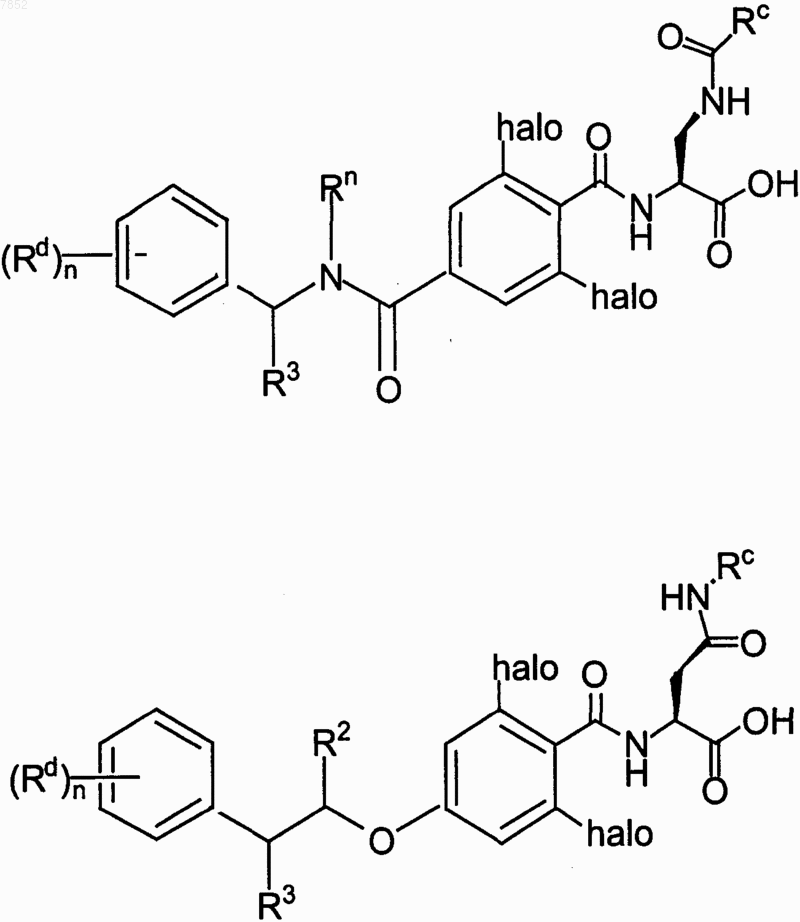
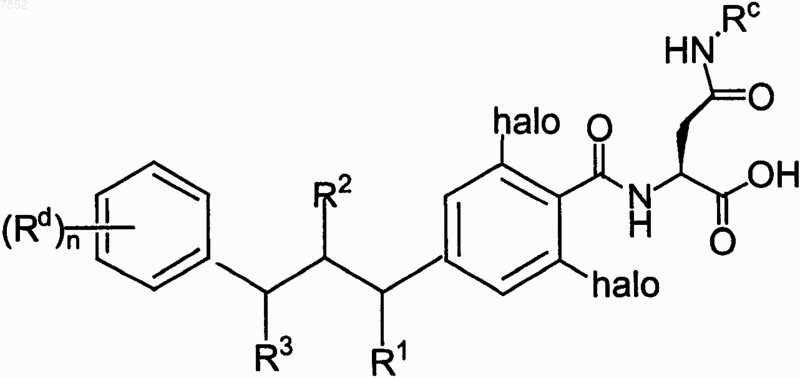
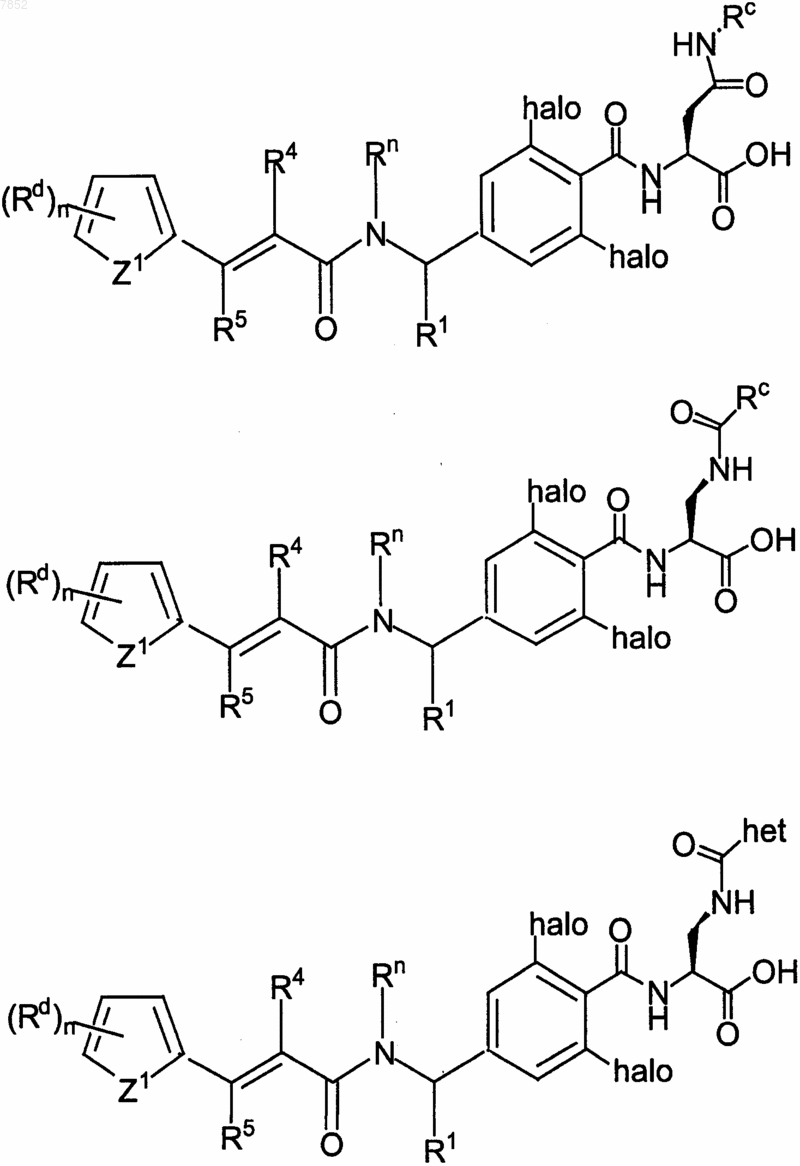
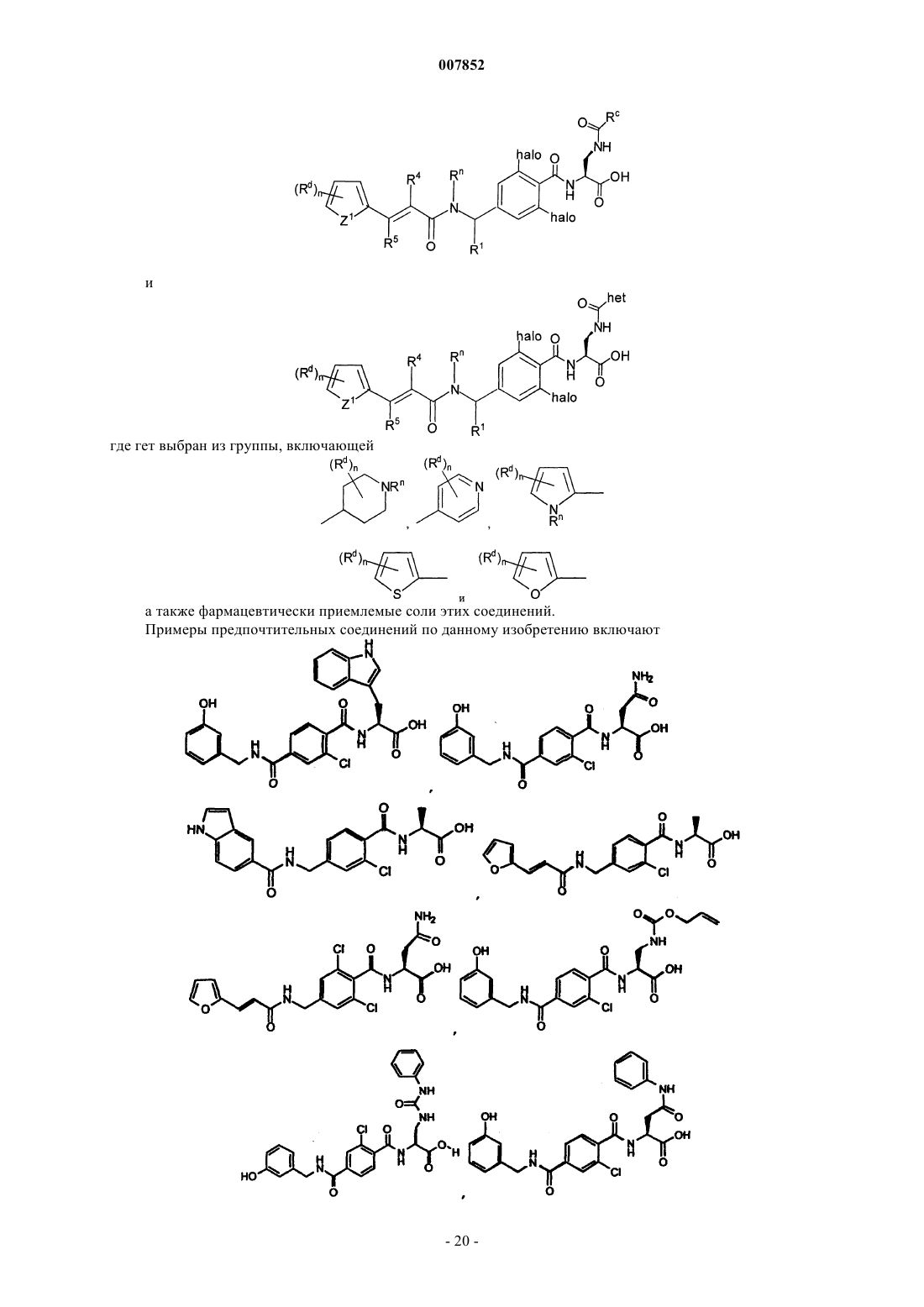
где гет выбран из группы, включающей
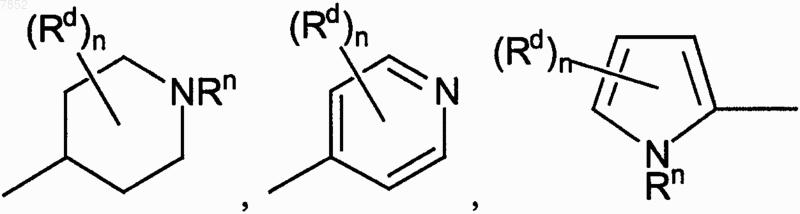
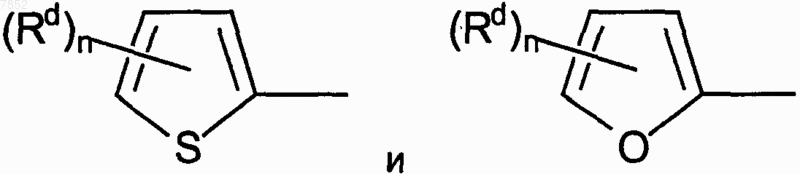
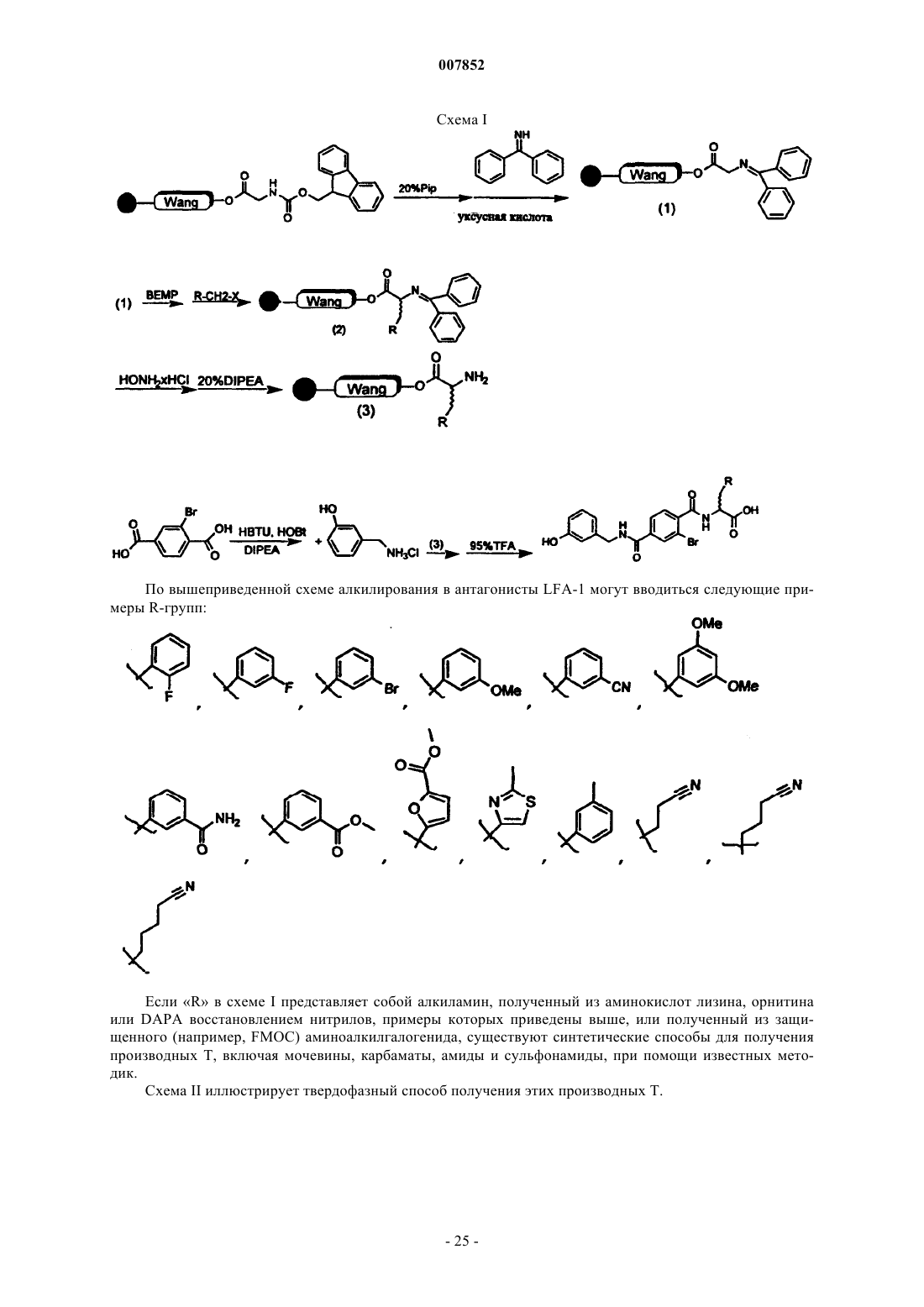
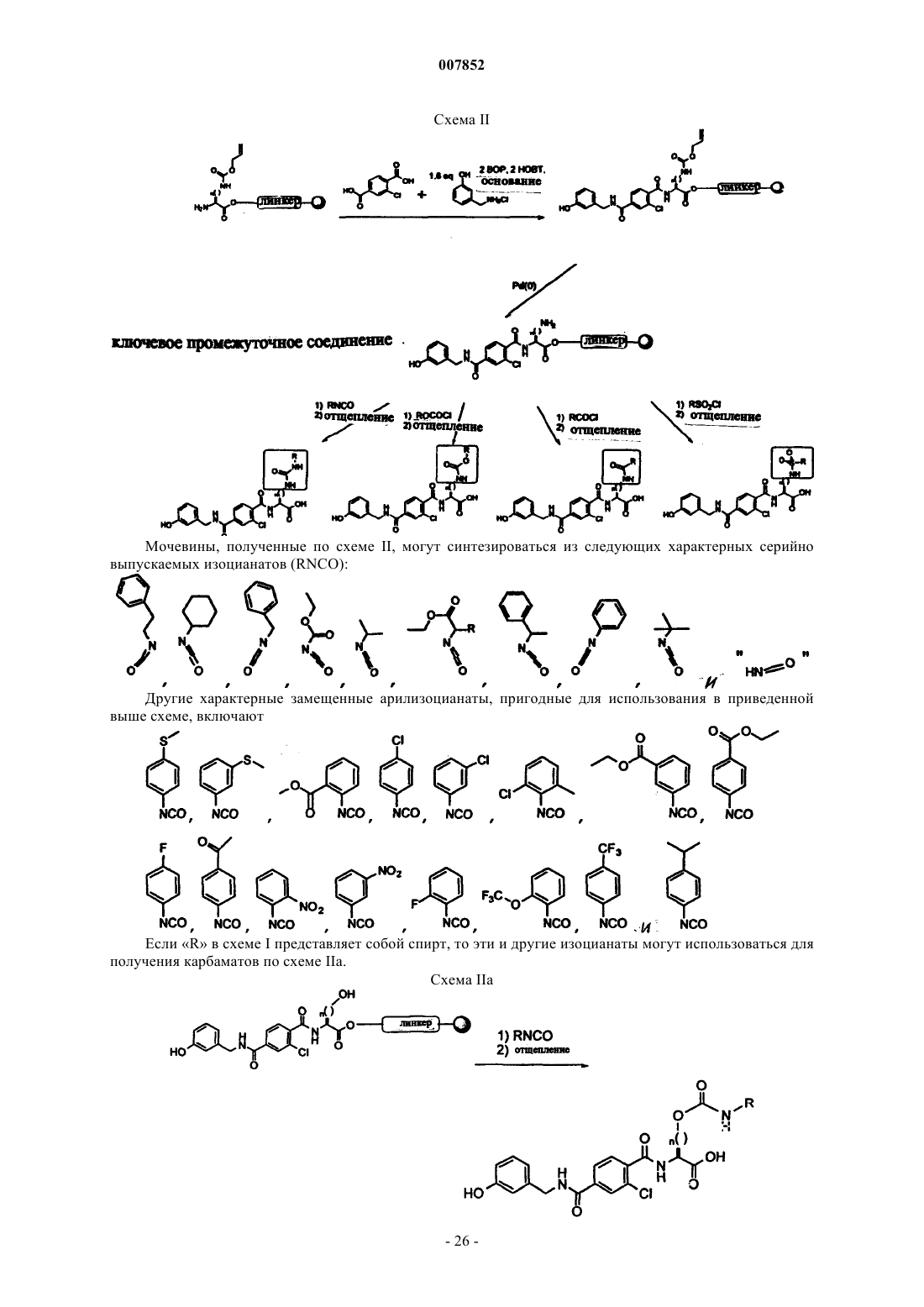
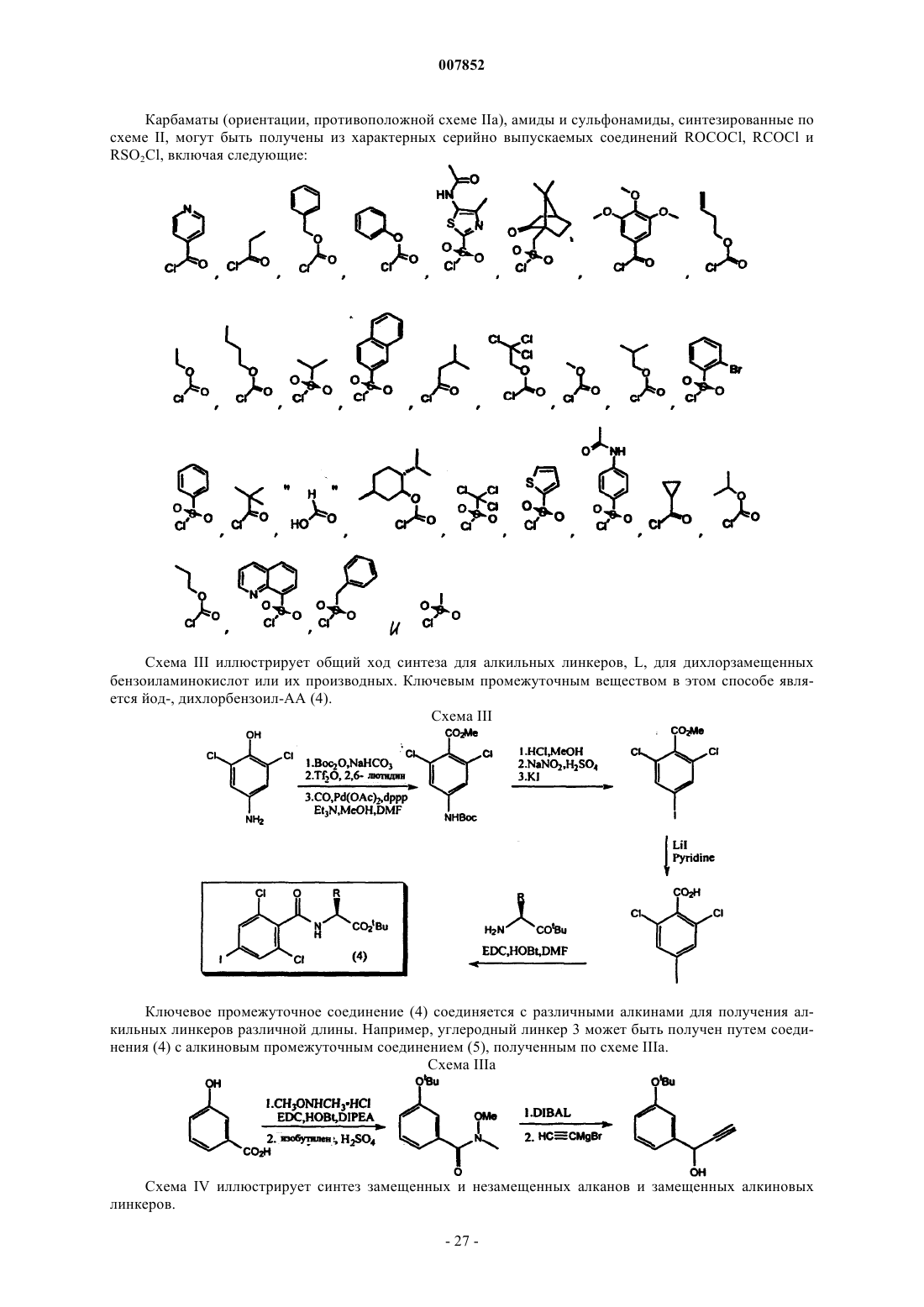
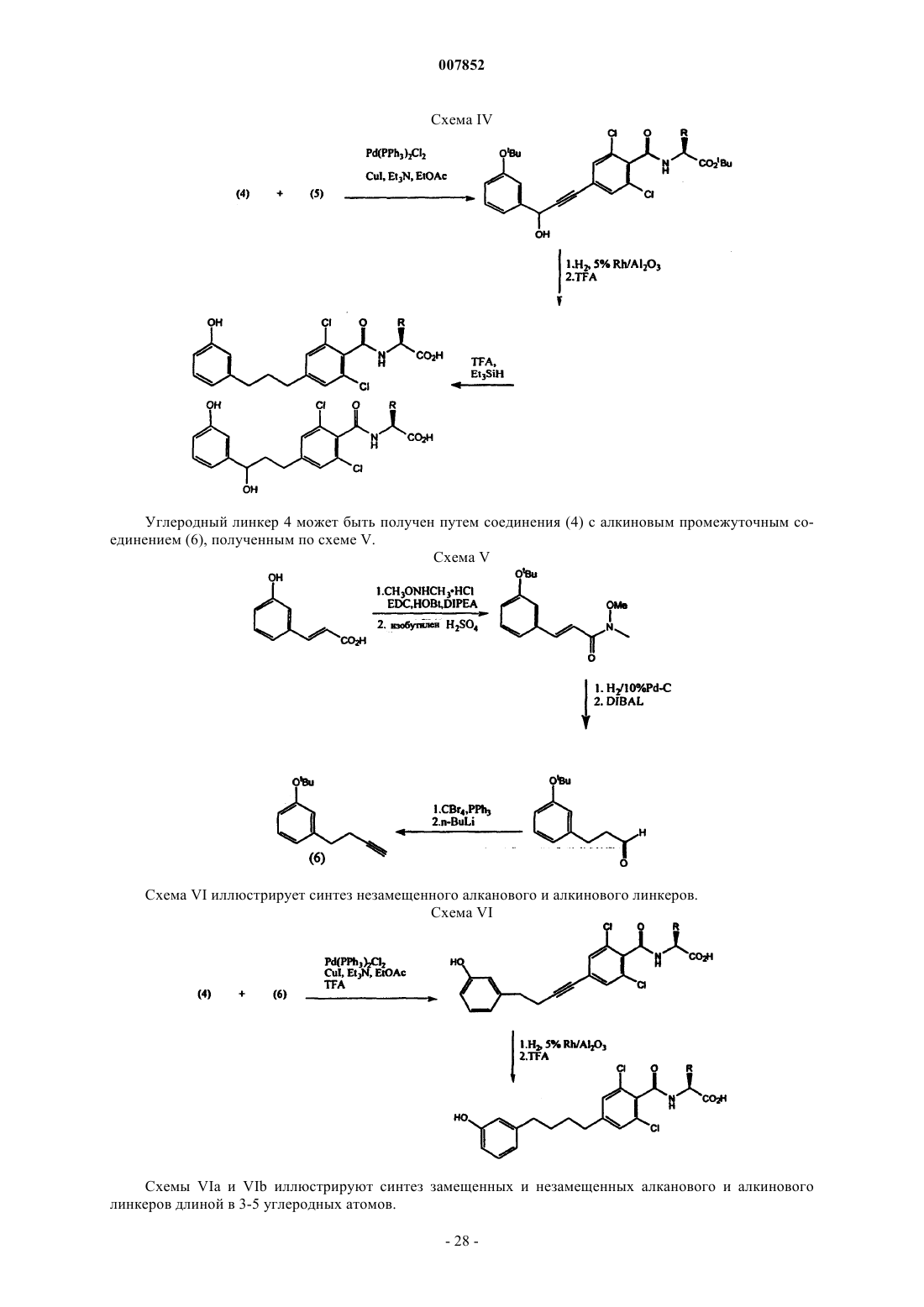
Текст
007852 Область изобретения Изобретение относится к способам и терапевтическим составам для лечения млекопитающих,предпочтительно людей, которые страдают или подвержены расстройствам, опосредованным рецепторами адгезии (CD11/CD18), особенно расстройствам, опосредованным лейкоцитарными LFA-1. В частности, оно относится к способам улучшения или модулирования иммунных реакций, например, вызываемых воспалительной, аутоиммунной реакцией и отторжением трансплантата, таких как псориаз, ревматоидный артрит, астма, множественный склероз, отторжение после пересадок и т.д. Предпосылки изобретения Воспаление. Периферическая кровь человека состоит, в основном, из красных кровяных телец (эритроцитов),тромбоцитов и белых кровяных телец или лейкоцитов. Семейство лейкоцитов дополнительно классифицируется на нейтрофилы, лимфоциты (основные подтипы - В- и Т-клетки), моноциты, эозинофилы и базофилы. Нейтрофилы, эозинофилы и базофилы иногда называют гранулоцитами или полиморфонуклеарными (ПМН) клетками из-за наблюдаемости гранул в их цитоплазме и множества ядер в них. Гранулоциты и моноциты часто классифицируются как фагоциты из-за их способности к фагоцитозу или расщеплению микроорганизмов и чужеродной материи, в целом называемых антигенами. Моноциты называются так благодаря их большим одиночным ядрам; эти клетки, в свою очередь, могут превращаться в макрофаги. Фагоциты важны для защиты организма от множества инфекций и вместе с лимфоцитами участвуют в воспалительных процессах. Нейтрофилы представляют собой лейкоциты, наиболее часто встречающиеся в нормальной периферической крови человека, за которыми следуют лимфоциты. В микролитре нормальной периферической крови человека содержится 6000 лейкоцитов, из которых около 4000 составляют нейтрофилы, 1500 - лимфоциты, 250 - моноциты, 150 - эозинофилы и 25 - базофилы. Во время воспалительного процесса лейкоциты периферической крови накапливаются на участке воспаления или повреждения путем серии специфических клеточных взаимодействий (см. фиг. 1). Инициирование и поддержание иммунных функций регулируются путем внутриклеточных адгезивных взаимодействий, а также трансдукции сигнала в результате взаимодействий между лейкоцитами и другими клетками. Адгезия лейкоцитов к васкулярному эндотелию и миграция из кровообращения к месту воспаления является критическим этапом в воспалительной реакции (фиг. 1). Иммунное узнавание Т-клеточных лимфоцитов требует взаимодействия Т-клеточных рецепторов с антигеном (в сочетании с главным комплексом тканевой совместимости, ГКТ), а также рецепторами адгезии, которые способствуют прикреплению Т-клеток к антигенпредставляющим клеткам и преобразуют сигналы для активации Т-клеток. Функциональная группа лимфоцитов, связывающая антиген-1, была идентифицирована как главный интегрин, который опосредует адгезию и активацию лимфоцитов, ведущую к нормальной иммунной реакции, а также несколько патологических состояний (Springer, T.A., Nature 346:425-434 (1990. Внутриклеточные адгезионные молекулы (IСАМ)-1, -2, -3, члены сверхсемейства иммуноглобулинов, являются лигандами для интегрина LFA-1, обнаруженного в эндотелиальных клетках, лейкоцитах и других типах клеток. Связывание LFA-1 с молекулами ICAM опосредует целый ряд функций лимфоцитов, включая продуцирование лимфокинов Т-клеток-помощников в ответ на присутствие антигенпредставляющих клеток, Т-лимфоцит-опосредованный лизис клеток-мишеней, природное уничтожение опухолевых клеток и продуцирование иммуноглобулина путем взаимодействий Т-клеток/В-клеток. Таким образом, многие грани функций лимфоцитов включают взаимодействие интегрина LFA-1 и его ICAM-лигандов. ЭтиLFA-1:ICAM-опосредованные взаимодействия непосредственно участвуют в многочисленных воспалительных состояниях, таких как отторжение трансплантата, дерматиты, псориаз, астма и ревматоидный артрит. В то время как LFA-1 (CD11a/CD18) в лимфоцитах играет ключевую роль в хронических воспалительных и иммунных реакциях, другие члены семейства лейкоцитарных интегринов (CD11b/CD18,CD11c/CD18 и CD11d/CD18) также играют важную роль в других лейкоцитах, таких как гранулоциты и моноциты, особенно во время первоначальной реакции на инфицирующие агенты и при острой воспалительной реакции. Основная функция полиморфонуклеарных лейкоцитов, производных от линий нейтрофилов, эозинофилов и базофилов, состоит в восприятии воспалительных стимулов и проникновении через эндотелиальный барьер для осуществления очистительной функции как первоочередной защиты организма. Интегрин Мас-1 (CD11b/CD18) быстро воздействует на эти клетки после активации и связывания с их многочисленными лигандами, что приводит к высвобождению кислород-производных свободных радикалов,протеаз и фосфолипаз. При некоторых хронических воспалительных состояниях это накопление регулируется неправильно, что приводит к значительным повреждениям клеток и тканей (Harlan, J.M., ActaLFA-1 (CD11a/CD18) и Mac-1 (CD11b/CD18). Семейство (CD11/CD18) молекул адгезионных рецепторов включает четыре близкородственных гликопротеина клеточной поверхности: LFA-1 (CD11a/CD18), Mac-1 (CD11b/CD18), LFA-1 p150.95 (CD11c/CD18) и (CD11d/CD18). LFA-1 присутствует на поверхности всех зрелых лейкоцитов, за исключением подмножества макрофагов, и считается главным лимфоидным интегрином. Экспрессия Мас-1, р 150.95 и CD11d/CD18,в первую очередь, ограничивается клетками миелоидного происхождения (которые включают нейтрофи-1 007852 лы, моноциты, макрофаги и мачтовые клетки). Функциональные исследования показали, что LFA-1 взаимодействует с несколькими лигандами, включая ICAM-1 (Rothlein et al., J. Immunol. 137:1270-1274(1990 и теленцефалин (Tian et al., J. Immunol. 158:928-936(1997. Семейство CD11/CD18 по структуре и генетике отнесено к более крупному интегриновому семейству рецепторов, которые модулируют клеточные адгезивные взаимодействия, включающие эмбриогенез, адгезию к внеклеточным субстратам и дифференциацию клеток (Hynes, R.O., Cell 48:549-554 (1987);Kishimoto et al., Adv. Immunol. 46:149-182 (1989); Kishimoto et al., Cell 48:681-690 (1987); Ruoslahti et al.,Science 238:491-497 (1987). Интегрины представляют собой класс мембраносвязующих гетеродимеров, включающий подгруппув нековалентной связи с подгруппой . Подгруппы , как правило, способны к связыванию с более чем одной подгруппой , и гетеродимеры, содержащие общую подгруппу , классифицируются как подсемейства внутри популяции интегрина (Larson and Springer, Structure and function of leukocyte integrins,Immunol. Rev. 114:181-217 (1990. Было обнаружено, что интегриновые молекулы семейства CD11/CD18 и их клеточные лиганды опосредуют множество междуклеточных взаимодействий, особенно при воспалении. Эти протеины имеют важнейшее значение для адгезивных функций в иммунной системе (Kishimoto et al., Adv. Immunol. 46:149-182 (1989. Показано, что моноклональные антитела к LFA-1 блокируют адгезию лейкоцитов к эндотелиальным клеткам (Dustin et al., J. Cell. Biol. 107:321-331 (1988); Smith et al., J. Clin. Invest. 83:20082017 (1989 и ингибируют активацию Т-клеток (Kuypers et al., Res. Immunol., 140:461 (1989, образование конъюгатов, необходимых для антигенспецифического уничтожения ЦТК (цитотоксических Т-клеток)ICAM-1 (CD54) представляет собой рецептор адгезии клеточной поверхности, являющийся членом сверхсемейства иммуноглобулиновых протеинов (Rothlein et al., J. Immunol. 137:1270-1274 (1986); Stauntoneet al., Cell 52:925-933 (1988. Для членов этого сверхсемейства характерно присутствие одного или более участков Ig-гомологичности, каждый из которых состоит из петли, связанной дисульфидным мостиком,которая содержит ряд противонаправленных -складчатых нитей, уложенных в виде двух листов. Идентифицировано три типа участков гомологичности, каждый из которых имеет типичную длину и согласованную последовательность аминокислотных остатков, расположенных между цистеинами дисульфидной связи (Williams, A.F. et al., Ann. Rev. Immunol. 6:381-405 (1988); Hunkapillar, T. et al., Adv. Immunol. 44:1-63 (1989. ICAM-1 выражены в разнообразных гематопоэтических и негематопоэтических клетках и подвергаются на участках воспаления воздействию различных воспалительных медиаторов (Dustin etal., J. Immunol., 137:256-254 (1986. ICAM-1 представляет собой гликопротеин с молекулярной массой(Мr) 90000-110000 с низкими уровнями РНК-посредников и умеренной поверхностной экспрессией в нестимулированных эндотелиальных клетках. LPS, IL-1 и TNF сильно воздействуют на мРНК ICAM-1 и поверхностную экспрессию с пиком экспрессии приблизительно через 18-24 ч (Dustin et al., J. Cell. Biol. 107:321-331 (1988); Staunton et al., Cell 52:925-933 (1988. ICAM-1 имеет пять внеклеточных иммуноглобулиноподобных доменов (обозначенных доменами 1, 2, 3, 4 и 5 или D1, D2, D3, D4 и D5) и внутриклеточный или цитоплазматический домен. Структуры и последовательности доменов описаны Staunton etICAM-1 первоначально был определен как противорецептор для LFA-1 (Springer et al., Ann. Rev.LFA-1/ICAM-1, по меньшей мере, частично ответственны за адгезию лимфоцитов (Dusting et al., J. Cell. Biol. 107:321-331 (1988); Mentzer et al., J. Cell. Physiol. 126:285-290 (1986, адгезию моноцитов (Amaout et al.,J. Cell. Phiysiol. 137:305 (1988); Mentzer et al., J. Cell. Phiysiol. 130:410-415 (1987); te Velde et al., Immunology 61:261-267 (1987, и адгезию нейтрофилов (Lo et al., J. Immunol. 143(10):3325-3329 (1989); Smith et al., J.Clin. Invest. 83:2008-2017 (1989 к эндотелиальным клеткам. Путем развития функции, блокирующей моноклональные антитела к ICAM-1, были идентифицированы дополнительные лиганды для LFA-1 ICAM-2 и ICAM-3 (Simmons, Cancer Surveys 24, Cell Adhesion and Cancer, 1995), которые опосредуют адгезию лимфоцитов к другим лейкоцитам, а также к негематопоэтическим клеткам. ВзаимодействияLFA-1 с ICAM-2 предположительно опосредуют природную губительную активность клеток (Helander etal., Nature 382:265-267 (1996, а связывание ICAM-3 предположительно играет роль в активации лимфоцитов и инициировании иммунной реакции (Simmons, там же). Точную роль этих лигандов в нормальной и аберрантной иммунной реакции еще предстоит выяснить. Расстройства, опосредованные Т-лимфоцитами. Функции, блокирующие моноклональные антитела, показали, что LFA-1 важен для Т-лимфоцитопосредованного уничтожения, реакций Т-вспомогательных лимфоцитов, природного уничтожения и ан-2 007852 тителозависимого уничтожения (Springer et al., Ann. Rev. Immunol., 5:223-252 (1987. Адгезия к клеткаммишеням, а также активация и сигнализация представляют собой этапы, блокируемые антителами кLFA-1. Многие расстройства и заболевания опосредованы через Т-лимфоциты, и существуют различные подходы к лечению этих заболеваний. Ревматоидный артрит (РА) - одно из таких расстройств. Современные методики лечения РА включают постельный режим, использование тепла и лекарств. Предпочитаемым в настоящее время лекарством является салицилат, в частности, поскольку альтернативные препараты, такие как иммуноподавляющие агенты и адренокортикостероиды, могут вызывать большую заболеваемость, чем само излечиваемое расстройство. Имеются многие нестероидные противовоспалительные средства, и многие из них проявляют анальгезирующую, жаропонижающую и противовоспалительную активность у пациентов, страдающих РА. Эти средства включают циклоспорин, индометацин,фенилбутазон, производные фенилуксусной кислоты, такие как ибупрофен и фенопрофен, нафталенуксусные кислоты (напроксен), пирролалкановая кислота (тометин), индолуксусные кислоты (сулиндак),галогенированная антраниловая кислота (меклофенамат натрия), пироксикам и дифлунизал. Другие средства для применения при РА включают противомалярийные препараты, такие как хлорохин, соли золота и пеницилламин. Эти альтернативные средства часто создают серьезные побочные эффекты,включая ретинальные повреждения и почечный и костно-мозговой токсический эффект. Иммунодепрессивные агенты, такие как метотрексат, используются только при лечении тяжелых и непрерывных РА изза их токсичности. Кортикостероиды также ответственны за нежелательные побочные эффекты (например, катаракты, остеопороз и синдром Кушинга) и плохо воспринимаются многими пациентами. Другое расстройство, опосредованное Т-лимфоцитами, - отторжение трансплантатов после пересадки. Попытки пролонгировать жизнеспособность пересаженных аллотрансплантатов и ксенотрансплантатов или предотвратить отторжение трансплантата организмом хозяина как в экспериментальных моделях, так и в медицинской практике сконцентрировались, в основном, на подавлении иммунного аппарата хозяина/реципиента. Это лечение направлено на превентивное иммуноподавление и/или лечение отторжения трансплантата. Примеры агентов, используемых для превентивного иммуноподавления,включают цитотоксические препараты, антиметаболиты, кортикостероиды и противолимфоцитную сыворотку. Неспецифические иммунодепрессивные средства, признанные особенно эффективными для превентивного иммуноподавления (азатиоприн, бромокриптин, метилпреднизолон, преднизон и, в недавнее время, циклоспорин А), существенно повышают клинический успех трансплантации. Нефротоксичность циклоспорина А после почечной трансплантации снижается путем сопутствующего применения стероидов, таких как преднизолон или преднизолон в сочетании с азатиоприном. Кроме того, почки успешно пересаживаются с использованием противолимфоцитного глобулина, а затем циклоспорина А. Другой исследуемый протокол лечения включает общее лимфоидное облучение реципиента перед трансплантацией с последующим минимальным иммуноподавлением после трансплантации. Лечение отторжения включает использование стероидов, 2-амино-6-арил-5-замещенных пиримидинов, гетерологичного противолимфоцитного глобулина и моноклональных антител к различным популяциям лейкоцитов, включая ОКТ-3. См., в целом, J. Pediatrics, 111: 1004-1007 (1987), и особенно патент США 4,665,077. Основное осложнение иммунодепрессивных лекарств состоит в инфекциях. Кроме того, системное иммуноподавление сопровождается нежелательными токсическими эффектами (например, нефротоксичностью при использовании циклоспорина А после почечной трансплантации) и снижением уровня гемопоэтических стволовых клеток. Иммунодепрессивные лекарства могут также привести к ожирению,плохому заживлению ран, стероидной гипергликемии, стероидному психозу, лейкопении, гастроинтестинальному кровотечению, лимфоме и гипертензии. Ввиду этих осложнений трансплантационные иммунологи изыскивают способы подавления иммунной реактивности антиген-специфическим образом (т.е., чтобы подавлялась лишь иммунная реакция на аллоантиген донора). Кроме того, терапевты, специализирующиеся на аутоиммунных заболеваниях,стремятся к использованию способов подавления аутоиммунной реактивности таким образом, чтобы подавлялась лишь реакция на самоантиген. Такое специфическое иммуноподавление, в целом, достигается путем модификации антигенности пересаживаемой ткани или специфических клеток, способных к опосредованию отторжения. В определенных случаях будет стимулироваться либо иммунитет, либо толерантность, в зависимости от способа, которым антиген будет представлен в иммунной системе. При исследовании в двух мышиных модельных системах было обнаружено, что предварительная обработка тканей аллотрансплантатов путем выращивания в тканевой культуре перед трансплантацией приводит к постоянному акцептированию через барьеры ГКТ. Lafferty et al., Transplantation, 22:138-149 (1976); Bowenet al., Lancet, 2:585-586 (1979). Было сделано предположение, что такая обработка приводит к угнетению лимфоидных клеток пассажира и, таким образом, к отсутствию популяции клеток-стимуляторов, необходимых для иммуногенности ткани. Lafferty et al., Annu. Rev. Immunol, 1:143 (1983). См. также Laffertyet al., Science, 188:259-261 (1975) (выдержка щитовидной железы в культуре органа), а также Gores et al.,J. Immunol., 137:1482-1485 (1986) и Faustman et al., Proc. Natl. Acad. Sci. U.S.A., 78: 5156-5159 (1981) (инсулоциты, обработанные мышиной антисывороткой к Ia и комплементированные перед трансплантаци-3 007852 ей). Кроме того, щитовидные железы, взятые у доноров-животных, и предварительно обработанные лимфоцитотоксическими препаратами и гамма-облучением, и культивированные в течение 10 дней in vitro,не были отторгнуты ни одним нормальным аллогенным реципиентом (Gose and Bach, J. Exp. Med. 149:1254-1259 (1979. Все эти методики используют угнетение или удаление лимфоцитных клеток донора. В некоторых моделях, таких как васкулярные и почечные трансплантаты, существует корреляция между соответствием класса II и пролонгированной жизнеспособностью аллотрансплантатов, кроме трансплантатов кожи (Pescovitz et al., J. Exp. Med., 160:1495-1508 (1984); Conti et al., Transplant. Proc., 19: 652-654 (1987. Поэтому используется соответствие ЛАЧ (лейкоцитарного антигена человека) донора и реципиента. Кроме того, была обнаружена эффективность переливаний крови перед трансплантацией(Opelz et al., Transplant. Proc., 4: 253 (1973); Persijn et al., Transplant. Proc., 23:396 (1979. Сочетание переливания крови перед трансплантацией, соответствия ЛАЧ донора и реципиента и иммунодепрессивной терапии (циклоспорин А) после трансплантации показало значительное улучшение степени жизнеспособности трансплантатов, а эффекты были признаны взаимодополняющими (Opelz et al., Transplant.Proc., 17:2179 (1985. Реакция на трансплантацию может быть также модифицирована антителами, действие которых направлено на иммунные рецепторы для антигенов ГКТ (Bluestone et al., Immunol. Rev. 90:5-27 (1986. Кроме того, жизнеспособность трансплантата может быть пролонгирована в присутствии антител к трансплантату, вызывающих реакцию организма хозяина, которая, в свою очередь, обеспечивает специфическое иммуноподавление (Lancaster et al., Nature, 315: 336-337 (1985. Иммунная реакция организмахозяина на антигены ГКТ может быть специфически модифицирована путем трансплантации костного мозга в качестве подготовительной операции перед пересадкой органа. Таким образом, моноклональные антитела к Т-клеткам используются для угнетения зрелых Т-клеток мозгового прививочного материала донора, чтобы обеспечить возможность трансплантации костного мозга, не навлекая опасности реакции трансплантат против хозяина (Mueller-Ruchholtz et al., Transplant. Proc., 8:537-541 (1976. В дополнение к этому, элементы лимфоидных клеток хозяина, остающиеся для трансплантации костного мозга,решают проблему иммунонекомпетентности, возникающую при использовании полностью аллогенных трансплантатов. Как показано на фиг. 1, сцепление лимфоцитов с эндотелием является ключевым событием в воспалительном процессе. Существует по меньшей мере три известных пути сцепления лимфоцитов с эндотелием, в зависимости от состояния активации Т-клеток и эндотелиальных клеток. Иммунное узнавание Тклеток требует участия рецептора Т-клеток, а также адгезионных рецепторов, которые способствуют прикреплению Т-клеток к антигенпредставляющим клеткам и передают регулятивные сигналы для активации Т-клеток. Антиген-1, связанный с лимфоцитной функцией (LFA-1, или CD11a/CD18, L2, гдеL=CD11 а, а 2=CD18), идентифицирован как главный интегриновый рецептор в лимфоцитах, участвующий в этих взаимодействиях клеточного сцепления, которые ведут к нескольким патологическим состояниям. ICAM-1, иммуноглобулиноподобная адгезионная молекула эндотелиальной клетки, является известным лигандом для LFA-1 и непосредственно причастна к отторжению трансплантатов, псориазу и артриту.LFA-1 необходим для ряда лейкоцитарных функций, включая выработку лимфокинов Т-клеткамипомощниками в ответ на присутствие антигенпредставляющих клеток, Т-лимфоцит-опосредованный лизис клеток-мишеней и продуцирование иммуноглобулина путем взаимодействий Т-клеток/В-клеток. Активация рецепторов антигена на поверхности Т-клеток и В-клеток позволяет LFA-1 связываться с его лигандом с более высоким сродством. Моноклональные антитела (Mab) к LFA-1 обеспечили первоначальную идентификацию и исследование функции LFA-1 (Davignon et al., J. Immunol., 127:590 (1981. LFA-1 присутствует только в лейкоцитах (Krenskey et al., J. Immunol., 131:611 (1983, a ICAM-1 распределен по поверхности активированных лейкоцитов, дермальных фибробластов и эндотелия (Dustin et al., J. Immunol., 137:245 (1986. В предыдущих работах было исследовано действие моноклональных антител к CD11a на многие иммунные функции, зависимые от Т-клеток, in vitro и ограниченное количество иммунных реакций inet al., выше, Fischer et al., J. Immunol., 136:3198 (1986, лизис клеток-мишеней цитотоксическими Т-лимфоцитами (Krensky et al., выше), образование иммунных конъюгатов (Sanders et al., J. Immunol., 137:2395(1986); Mentzer et al., J. Immunol., 135:9 (1985 и адгезию Т-клеток к васкулярному эндотелию (Lo et al.,J. Immunol., 143:3325 (1989. Кроме того, было обнаружено, что антитело 5 С 6 к CD11b/CD18 предотвращает внутриинсулоцитную инфильтрацию макрофагами и Т-клетками и ингибирует развитие инсулинзависимого сахарного диабета у мышей (Hutchings et al., Nature, 348: 639 (1990. Вывод, что взаимодействие LFA-1:ICAM-1 необходимо для оптимизации функции Т-клеток in vitro и что моноклональные антитела к CD11a индуцируют толерантность к антигенам протеинов Benjaminet al., Eur. J. Immunol., 18:1079 (1988 и пролонгируют жизнеспособность опухолевых трансплантатов у мышей (Heagy et al., Transplantation, 37: 520-523 (1984, был основой для испытаний моноклинальных-4 007852 антител к этим молекулам на предотвращение отторжения трансплантатов у людей. Опыты проводились также на приматах. Например, опыт на обезьянах позволил сделать вывод, чтоMab к ICAM-1 может предотвращать или даже поворачивать в обратную сторону отторжение пересаженной почки (Cosimi et al., Immunosuppression of Cynomolgus Recipients of Renal Allografts by R6.5, aMolecules New York: Springer, (1988), p. 274; Cosimi et al., J. Immunology, 144:4604-4612 (1990. Кроме того, введение in vivo MAb к CD11a обезьянам Cynomolgus пролонгировало жизнеспособность дермальных аллотрансплантатов (Berlin et al., Transplantation, 53: 840-849 (1992. Первое успешное использование антитела крысы к мышиному CD11 а (25-3; IgGI) у детей с наследственными заболеваниями для предотвращения отторжения гаплоидентичных трансплантатов несоответствующего костного мозга описано Fischer et al., Lancet, 2: 1058 (1986). Наблюдались минимальные побочные эффекты. См. также Fischer et al., Blood, 77: 249 (1991); van Dijken et al., Transplantation, 49:882(1990) и Perez et al., Bone Marrow Transplantation, 4:379 (1989). Кроме того, антитело 25-3 оказалось эффективным при регулировании стероид-устойчивой острой реакции трансплантат против хозяина у людей (Stoppa et al., Transplant. Int., 4:3-7 (1991. Однако эти результаты не показали воспроизводимости у взрослых лейкозных пациентов, привитых этим MAb (Maraninchi et al., Bone Marrow Transplant., 4:147-150 (1989 или Mab к CD18, действие которого направлено на инвариантную цепь LFA-1, в другом экспериментальном исследовании (Baume et al.,Transplantation, 47: 472 (1989. Кроме того, антитело крысы к мышиному CD11 а, 25-3, оказалось неспособным регулировать ход острого отторжения трансплантированной почки у людей (LeMauff et al.,Transplantation, 52: 291 (1991. Обзор использования моноклональных антител при трансплантациях у людей представлен Dantaland Soulillou, Current Opinion in Immunology, 3:740-747 (1991). В более ранней публикации указывалось, что кратковременное лечение моноклональными антителами к LFA-1 или к ICAM-1 минимально пролонгирует жизнеспособность первично васкуляризованных гетеротопных сердечных аллотрансплантатов у мышей (Isobe et al., Science, 255:1125 (1992. Однако для достижения длительной жизнеспособности трансплантатов в этой модели потребовалось комбинированное лечение обоими этими Mab. Независимо было продемонстрировано, что лечение только антителом к LFA-1 эффективно пролонгирует жизнеспособность гетеротопных (из наружных ушей) непервично васкуляризованных сердечных трансплантатов мыши с использованием максимальной дозы 4 мг/кг/день и применением раз в неделю после ежедневных дозировок (Nakakura et al., I. Heart Lung Transplant., 11:223 (1992. Непервично васкуляризованные сердечные аллотрансплантаты более иммуногенны и более устойчивы к пролонгированию жизнеспособности моноклональными антителами, чем первично васкуляризованные сердечные аллотрансплантаты (Warren et al., Transplant. Proc., 5:717 (1973); Trager et al., Transplantation, 47:587(1989. В последней ссылке описано лечение антителами L3T4 с использованием высокой начальной дозировки и более низкой последующей дозировки. Другое исследование в области лечения склерозоподобного заболевания у грызунов с использованием антител, подобных используемым Nakakura et al., выше, описано Yednock et al., Nature, 356:63-66(1992). Дополнительные описания использования антител к LFA-1, а также ICAM-1, ICAM-2 и ICAM-3 и их антител для лечения LFA-1-опосредованных расстройств включают WO 91/18011, опубл. 11/28/91,WO 91/16928, опубл. 11/14/91, WO 91/16927, опубл. 11/14/91, патентная заявка Канады 2,008,368, опубл. 6/13/91, WO 90/03400, WO 90/15076, опубл. 12/13/90, WO 90/10652, опубл. 9/20/90, ЕР 387,668, опубл. 9/19/90, WO 90/08187, опубл. 7/26/90, WO 90/13281, WO 90/13316, WO 90/13281, WO 93/06864, WO 93/21953, WO 93/13210, WO 94/11400, ЕР 379,904, опубл. 8/1/90, ЕР 346,078, опубл. 12/13/89, патент США 5,002,869, патент США 5,071,964, патент США 5,209,928, патент США 5,223,396, патент США 5,235,049, патент США 5,284,931, патент США 5,288,854, патент США 5,354,659,патентная заявка Австралии 15518/88, опубл. 11/10/88, ЕР 289,949, опубл. 11/9/88, и ЕР 303,692, опубл. 2/22/89, ЕР 365,837, ЕР 314,863, ЕР 319,815, ЕР 468,257, ЕР 362,526, ЕР 362,531, ЕР 438,310. Другие описания использования пептидных фрагментов и антагонистов LFA-1 и IСAM включают патент США 5,149,780, патент США 5,288,854, патент США 5,340,800, патент США 5,424,399,патент США 5,470,953, WO 90/03400, WO 90/13316, WO 90/10652, WO 91/19511, WO 92/03473,WO 94/11400, WO 95/28170, JP 4193895, EP 314,863, EP 362,526 и ЕР 362,531. Вышеописанные методики, успешно использующие антитела к LFA-1 или к IСAM, пептиды LFA-1 или IСAM, фрагменты или пептидные антагонисты, представляют собой шаг вперед по сравнению с традиционным лечением иммунодепрессивными препаратами. Эти исследования показывают, что LFA-1 иIСAM являются подходящими мишенями для антагонизма. Существует необходимость в улучшении лечения расстройств, опосредованных LFA-1, включая аутоиммунные заболевания, реакции трансплантат против хозяина или хозяин против трансплантата, а также воспалительные реакции Т-клеток, чтобы минимизировать побочные эффекты и выработать специфическую толерантность к собственным и чужеродным антигенам. Также существует необходимость в создании непептидных или пептидомиметиче-5 007852 ских антагонистов к взаимодействию LFA-1:ICAM-1. По меньшей мере один пептидомиметический антагонист взаимодействия LFA-1:ICAM-1 показал себя перспективным в различных опытах in vivo. 2-Бромбензоилтриптофан показывает значения IC50 около 2 и 10 мкМ, соответственно, в описанных здесь анализах на связывание человеческих рецепторов LFA-1:ICAM-1 и на адгезию человеческих Тклеток. Недавно в патенте США 5,472,973 были описаны флуореновые производные аминобензойной кислоты как полезные противовоспалительные агенты. Их представителем может служить соединение Задачи изобретения Таким образом, задачей данного изобретения является создание композиций и терапевтических методик для модулирования адгезии между внутриклеточными адгезионными молекулами (например,ICAM-1, -2 и -3) и лейкоцитарным интегриновым семейством рецепторов. Задачей является противодействие рецепторам CD11/CD18, связанным с лейкоцитами, особенно расстройствам, опосредованным Мас-1 и LFA-1, с минимальными побочными эффектами. Задачей является регулирование нежелательных воспалительных реакций и предотвращение повреждения здоровых тканей. Более конкретно, задачей является лечение LFA-1-опосредованных расстройств, включающих псориаз; реакции, связанные с воспалительными кишечными заболеваниями (такими как болезнь Крона и язвенный колит), дерматит, менингит, энцефалит, увеит, аллергические состояния, такие как экзема и астма, состояния, вызывающие инфильтрацию Т-клеток и хронические воспалительные реакции, реакции кожной гиперчувствительности (включая сумах укореняющийся); атеросклероз, аутоиммунные заболевания, такие как ревматоидный артрит, системная красная волчанка (СКВ), сахарный диабет, множественный склероз, синдром Рейнода, аутоиммунный тиреоидит, экспериментальный аутоиммунный энцефаломиелит, синдром Шегрена, юношеский диабет и иммунные реакции, связанные с замедленной гиперчувствительностью, опосредованной цитокинами и Т-лимфоцитами, обычно наблюдаемые при туберкулезе, саркоидозе, полимиозите, гранулематозе и васкулите; злокачественная анемия; заболевания,вызывающие лейкоцитарный диапедез; воспалительные расстройства ЦНС, синдром множественного поражения внутренних органов вследствие заражения крови или травмы; аутоиммунная гемолитическая анемия; тяжелая псевдопаралитическая миастения, заболевания, опосредованные комплексом антигенантитело; все типы трансплантаций, включая реакции трансплантат против хозяина или хозяин против трансплантата, ВИЧ и риновирусные инфекции, фиброз легких и т.д. Эти и другие задачи будут очевидны любому обычному специалисту в данной области. Резюме изобретения Данные задачи решаются путем создания способа и композиций антагонистов для модулирования адгезии между внутриклеточными адгезионными молекулами (например, ICAM-1, -2, и -3) и лейкоцитарным интегриновым семейством рецепторов. Способ и антагонисты особенно полезны для лечения расстройств, опосредованных CD11/CD18, особенно Мас-1 и LFA-1, у млекопитающих, особенно человека, и включают введение млекопитающему терапевтически эффективного количества антагониста. Подходящие антагонисты лейкоцитарных интегринов, особенно анагонисты Мас-1 и LFA-1, по данному изобретению представлены ниже структурной формулой I. Предпочтительно антагонист LFA-1 представляет собой специфический антагонист лейкоцитарного интегрина CD11a(L)/CD18(2). Такие антагонисты особенно полезны для лечения хронических расстройств, опосредованных LFA-1. Предпочтительно эти антагонисты LFA-1 используются для лечения псориаза, алопеции, трансплантации органов,воспалительного кишечного заболевания (ВКЗ), ревматоидного артрита (РА), системной красной волчанки (СКВ), диабетов 1-го типа, множественного склероза (МС), астмы, реакции трансплантат против хозяина (ТПX), склередемы, эндометриоза и витилиго. Иногда некоторые соединения, охватываемые формулой I, также способны к антагонизации связывания Мас-1 CD11b(M)/CD18(2) с ICAM и допол-6 007852 нительными лигандами, включая iC3b, фибриноген и фактор X. Таким образом, эти соединения полезны для ингибирования адгезии нейтрофилов и лейкоцитов, выражающих оба или один из интегринов LFA-1 и Мас-1 как при хронических, так и при острых расстройствах, опосредованных лейкоцитами/нейтрофилами. Более конкретно, эти расстройства включают поражение при ишемии/реперфузии, опосредованное нейтрофилами, такое как острый инфаркт миокарда, рестеноз после ЧТКА (чрескожной транслюминальной коронарной ангиопластики), инвазивных операций, таких как сердечно-легочная шунтирующая хирургия, церебральный отек, инсульт, травматическое поражение мозга, множественный склероз, системная красная волчанка, геморрагический шок, ожоги, ишемическая почечная болезнь, множественное поражение органов, заживление ран и образование шрамов, атеросклероз, а также посттрансплантационное повреждение органа. Указанный антагонист представлен соединением общей формулыLX выбран из группы, включающей замещенные или незамещенные С 2-С 5-алкилен,С 3-С 6-циклоалкилен,С 0-С 3-алкилен-NRn-(С=O)-С 0-С 3-алкилен,С 0-С 3-алкилен-(С=O)-NRn-С 0-С 3-алкилен,С 0-С 3-алкилен-О-С 0-С 3-алкилен,С 0-С 3-алкилен-NRn-С 0-С 3-алкилен,С 0-С 3-алкилен-(С=O)-С 0-С 3-алкилен,С 0-С 3-алкилен-СR1=СR2-С 0-С 3-алкилен,С 0-С 3-алкилен-СС-С 0-С 3-алкилен и С 0-С 3-алкилен-гет-С 0-С 3-алкилен,при этом заместители выбираются из группы, включающей от 1 до 3 радикалов R1, R2 и R3;LY выбран из группы, включающей замещенные или незамещенные С 0-С 2-алкилен,С 0-С 2-алкилен-NRn-(С=O)-С 0-С 2-алкилен,С 0-С 2-алкилен-(С=O)-NRn-С 0-С 2-алкилен,С 0-С 2-алкилен-О-С 0-С 2-алкилен,С 0-С 2-алкилен-NRn-С 0-С 2-алкилен,С 0-С 2-алкилен-(С=O)-С 0-С 2-алкилен,при этом заместители выбраны из группы, включающей от 1 до 3 радикалов R1, R2 и R3;RC выбран из группы, состоящей из водорода и замещенного или незамещенного гета, при этом заместители в гете представляют собой от 1 до 3 радикалов Rd; гет является моно-, би- или трициклическим 5-, 6-, 7-, 9- или 10-звенным насыщенным, ненасыщенным или ароматическим кольцом, имеющим от 1 до 4 гетероатомов, выбранных из группы, включающейRp и Rd независимо выбраны из группы, включающей ОН,CN,NO2,галоген,ORn,SRn,SORn,CF3,RC,NRnRn',NRnC(=O)-O-Rn',NRnC(=O)-Rn',C0-C6-aлкил-SO2-Rn,С 0-С 6-алкил-SО 2-NRnNRn',C(=O)-Rn,O-C(=O)-Rn,C(=O)-O-Rn,C(=O)-NRnRn';Rd представляет собой химическую связь, когда гет представляет собой двухвалентную соединительную группу;Rn и Rn' независимо выбраны из группы, включающей водород,гидроксигруппу,С 1-С 6-алкил,галоген-С 1-С 6-алкил,С 1-С 6-алкил-гет,гет-С 1-С 6-алкил,С 6-С 12-арил и гет;Q отсутствует или представляет собой С 0-С 3-алкил, замещенный группой, выбранной изV отсутствует или представляет собой бивалентную группу, возможно, замещенную, выбранную из группы, включающей С 1-С 11-алкилена,С 2-С 6-алкенилена,С 0-С 6-алкил-гета,при этом заместители в любом алкиле представляют собой от 1 до 3 радикалов Ra, a заместители в любом ариле или гете представляют собой от 1 до 3 радикалов Rd;Ra,NH-C(=O)-RC,C(=O)-RC,C(=O)-NRnRn',и RC,обладающим способностью модулировать адгезию между внутриклеточными адгезионными молекулами и лейкоцитарным интегриновым семейством рецепторов, а также его фармацевтически приемлемые соли;Ra представляет собой аминогруппу. Более конкретно, соединение может представлять собой соединение, выбранное из группы, включающей а также фармацевтически приемлемые соли этих соединений. Также, более конкретно, соединение может представлять собой соединение, выбранное из группы,включающей где гет выбран из группы, включающей а также фармацевтически приемлемые соли этих соединений. Краткое описание фигур Фиг. 1 - рисунок, показывающий накопление лимфоцитов на участке инфекции. Показаны перекатывание и адгезия лимфоцитов к клеткам, выражающим ICAM (лейкоцитам, эндотелию, эпителию). Фиг. 2 - рисунок, показывающий анализ на связывание человеческого ICAM с рецептором LFA-1(протеин-протеиновый анализ). Ингибирование взаимодействия CD11a/CD18-ICAM-1 измеряется путем добавления известных количеств ингибиторов в систему протеин-протеинового анализа, описанную в примере 3. Фиг. 3 - рисунок, показывающий анализ на адгезию человеческих Т-клеток, описанный в примере 4. Фиг. 4 - рисунок, показывающий анализ на пролиферацию человеческих Т-клеток. Пролиферацию клеток измеряли путем поглощения тимидина, меченного тритием. Фиг. 5 - рисунок, показывающий реакцию однообразно смешанные человеческие лимфоциты. Пролиферацию клеток измеряли путем поглощения тимидина, меченного тритием.- 10007852 Описание предпочтительных вариантов осуществления А. Определения. Выражение расстройства, опосредованные LFA-1 относится к патологическим состояниям, вызванным взаимодействиями клеточного сцепления, касающимися рецепторов LFA-1 и лимфоцитов. Примеры таких расстройств включают Т-клеточные воспалительные реакции, такие как воспалительные заболевания кожи, включая псориаз; реакции, связанные с воспалительным кишечным заболеванием (таким, как болезнь Крона и язвенный колит); респираторный дистресс-синдром взрослых; дерматит; менингит; энцефалит; увеит; аллергические состояния, такие как экзема и астма, и другие состояния, вызывающие инфильтрацию Т-клеток и хронические воспалительные реакции; реакции кожной гиперчувствительности (включая сумах укореняющийся), атеросклероз; лейкоцитарная адгезионная недостаточность; аутоиммунные заболевания, такие как ревматоидный артрит, системная красная волчанка (СКВ),сахарный диабет, множественный склероз, синдром Рейнода, аутоиммунный тиреоидит, экспериментальный аутоиммунный энцефаломиелит, синдром Шегрена, диабеты типа 1, юношеский диабет и иммунные реакции, связанные с замедленной гиперчувствительностью, опосредованной цитокинами и Тлимфоцитами, обычно наблюдаемые при туберкулезе, саркоидозе, полимиозите, гранулематозе и васкулите; злокачественная анемия; заболевания, вызывающие лейкоцитарный диапедез; воспалительные расстройства ЦНС, синдром множественного поражения внутренних органов вследствие заражения крови или травмы; аутоиммунная гемолитическая анемия; тяжелая псевдопаралитическая миастения, заболевания, опосредованные комплексом антиген-антитело; все типы трансплантаций, включая реакции трансплантат против хозяина или хозяин против трансплантата, и т.д. Лечение таких заболеваний включает терапию, профилактическое лечение, предотвращение отторжения трансплантатов и выработку толерантности трансплантатов на долговременной основе. Термин трансплантат здесь относится к биологическому материалу, взятому от донора для трансплантации реципиенту. Трансплантаты включают такой разнообразный материал, как, например,изолированные клетки, такие как инсулоциты, ткани, такие как амниотические оболочки новорожденных, костный мозг, гематопозтические клетки-предшественники, или органы, такие как кожа, сердце,печень, селезенка, поджелудочная железа, доля щитовидной железы, легкое, почка, трубчатые органы(например, кишки, кровеносные сосуды или пищевод) и т.д. Трубчатые органы могут использоваться для замены поврежденных частей пищевода, кровеносных сосудов или желчного протока. Трансплантаты кожи могут использоваться не только при ожогах, но также и в качестве оболочки для поврежденных кишок или для покрытия некоторых дефектов, таких как диафрагматическая грыжа. Трансплантаты получают из любого источника млекопитающего происхождения, включая человека, в том числе от трупов или от живых доноров. Предпочтительно трансплантат представляет собой костный мозг или орган, такой как сердце, а донор трансплантата и хозяин соответствуют друг другу по классу II ЛАЧ. Термин млекопитающие относится к любому животному, классифицированному как млекопитающее, включая людей, домашних и диких животных, таких как собаки, лошади, кошки, коровы и т.д. Предпочтительным млекопитающим здесь является человек. Выражение млекопитающий хозяин относится к любому совместимому реципиенту трансплантата. Совместимый относится к млекопитающему хозяину, для которого будет приемлемым донорский трансплантат. Предпочтительно хозяином является человек. Если донором трансплантата и хозяином являются люди, они предпочтительно соответствуют друг другу по классу II ЛАЧ, чтобы улучшить биосовместимость. Термин донор здесь относится к представителям млекопитающих, мертвым или живым, от которых берется трансплантат. Предпочтительно донором является человек. Человеческие доноры предпочтительно являются добровольными донорами-родственниками нормального физического статуса и той же основной группы крови АВО, поскольку преодоление барьеров основной группы крови может повредить жизнеспособности аллотрансплантата. Однако возможна, например, трансплантация почки донора группы О реципиенту группы А, В или АВ. Термин трансплантация и его вариации относятся к введению трансплантата в организм хозяина,где трансплантация может быть сингенной (когда донор и реципиент генетически идентичны), аллогенной (когда донор и реципиент имеют разное генетическое происхождение, но относятся к одному виду) или ксеногенной (когда донор и реципиент относятся к разным видам). Таким образом, в типичном сценарии хозяин является человеком, а трансплантат представляет собой изотрансплантат, полученный от человека того же или иного генетического происхождения. В другом сценарии трансплантат получают от вида, отличного от вида, в который его трансплантируют, например сердце бабуина, трансплантируемое человеку, включая животных из филогенетически разнообразных видов, например сердечный клапан свиньи, или -инсулоцитные клетки или нейроны животных, трансплантируемые хозяину-человеку. Выражение антагонист LFA-1 здесь относится, в целом, к бензоил-аминокислотным (АК) производным или их пептидомиметикам, которые действуют в качестве конкурентного ингибитора взаимодействия CD11 а и/или CD18 с ICAM-1, растворимыми формами ICAM-1 и связанными или растворимыми формами ICAM-2, ICAM-3 и теленцефалина. Выражение иммунодепрессивный агент, используемое здесь для вспомогательной терапии, отно- 11007852 сится к веществам, которые действуют для подавления или маскирования иммунной системы хозяина, в организм которого пересаживается трансплантат. Эти агенты могут включать вещества, подавляющие продуцирование цитокинов, снижающие или угнетающие экспрессию самоантигенов или маскирующие антигены ГКТ. Примеры таких агентов включают 2-амино-6-арил-5-замещенные пиримидины (см. патент США 4,665,077, выше, описание которого включено в данную заявку в виде ссылки), азатиоприн(или циклофосфамид, если имеется неблагоприятная реакция на азатиоприн); бромокриптин; глутаральдегид (который маскирует антигены ГКТ, как описано в патенте США 4,120,649, выше); антиидиотипические антитела для антигенов ГКТ и фрагментов ГКТ; циклоспорин А; стероиды, такие как глюкокортикостероиды, например преднизон, метилпреднизолон и дексаметазон; антагонисты цитокинов или цитокиновых рецепторов, включая антитела к интерферону- или -; антитела к факторуопухолевого некроза; антитела к факторуопухолевого некроза; антитела к интерлейкину-2 и антитела к рецептору интерлейкина-2; антитела к L3T4; гетерологичный противолимфоцитный глобулин; пан-Тантитела, предпочтительно антитела к CD-3 или к CD4/CD4a; растворимый пептид, содержащий LFA-3 связывающий домен (WO 90/08187, опубл. 7/26/90), стрептокиназу; РНК или ДНК от хозяина; FK506;RS-61443; дезоксиспергуалин; рапамицин; рецептор Т-клеток (Cohen et al., патент США 5,114,721); фрагменты рецепторов Т-клеток (Offner et al., Science, 251:430-432 (1991); заявка США, сер.07/853,362,от 18.03.1992, описание которой включено в данную заявку в виде ссылки; Howell, WO 90/11294; Ianeway,Nature, 341:482 (1989); и Vandenbark, WO 91/01133); и антитела к рецепторам Т-клеток (ЕР 340,109), такие как Т 10 В 9. Эти агенты принимаются в одно и то же время или в разное время с антагонистамиCD11a или CD18, применяемыми по данному изобретению, и используются при таких же или меньших дозировках, которые установлены в обычной практике. Предпочтительный вспомогательный иммунодепрессивный агент будет зависеть от многих факторов, включая тип излечиваемого расстройства, тип выполняемой трансплантации, а также историю пациента, но, в целом, предпочтение отдается агентам, выбранным из циклоспорина А, глюкокортикостероидов (наиболее предпочтительно преднизон или метилпреднизолон), моноклонального антитела ОКТ-3,азатиоприна, бромокриптина, гетерологичного противолимфоцитного глобулина или их смеси. Выражение повышение толерантности пересаженного трансплантата у хозяина относится к пролонгированию жизнеспособности трансплантата в организме хозяина, т.е. подавлению иммунной системы хозяина таким образом, чтобы он лучше принимал чужеродный трансплантат. Термин алкил означает разветвленный или неразветвленный насыщенный алифатический углеводородный радикал, содержащий указанное число углеродных атомов или, если число атомов не указано, содержащий до 12 углеродных атомов. Если не указано иное, термин также включает ненасыщенные алкилы, определяемые как циклоалкил, алкенил и алкинил, определение которых приведено ниже. Примеры предпочтительных алкильных радикалов включают метил, этил, n-пропил, изопропил, n-бутил,изобутил, втор-бутил, трет-бутил, n-пентил, 2-метилбутил, 2,2-диметилпропил, n-гексил, 2-метилпентил,2,2-диметилбутил, n-гептил, 2-метилгексил и т.п. Термин С 0-С 6-алкил и подобные термины, содержащие С 0, означают ковалентную связь, когда число углеродных атомов равно нулю (С 0) или C1-С 6 алкилу. Если необходимо предотвратить свободную валентность, термин С 0 может включать атом водорода. Предпочтительной группой C1-С 6-алкил является метил. Термин замещенный Cn-Сm-алкил, где n и m - целые числа, определяющие диапазон углеродных атомов, содержащихся в алкильной группе, обозначает вышеуказанные алкильные группы, замещенные перечисленными группами или, если группы не перечислены, одним, двумя или тремя галогенами, гидроксигруппой, защищенной гидроксигруппой, аминогруппой, защищенной аминогруппой, С 1-С 7-алкоксигруппой, нитрогруппой, карбоксигруппой, защищенной карбоксигруппой, карбамоилом, карбамоилоксигруппой, цианогруппой, метилсульфониламиногруппой или С 1-С 4-алкоксигруппами. Замещенные алкильные группы могут быть одним, двумя или тремя одинаковыми или разными заместителями. Примеры вышеупомянутых замещенных алкильных групп включают (но не ограничиваются ими) цианометил, нитрометил, гидроксиметил, триэтилоксиметил, пропионилоксиметил, аминометил, карбоксиметил, алкилоксикарбонилметил, алкилоксикарбониламинометил, карбамоилоксиметил, метоксиметил, этоксиметил, трет-бутоксиметил, ацетоксиметил, хлорметил, бромметил, иодметил, трифторметил,6-гидроксигексил, 2,4-дихлор(n-бутил), 2-амино(изопропил), 2-карбамоилоксиэтил и т.п. Предпочтительная группа примеров вышеупомянутых замещенных С 1-С 12-алкилов включает замещенную метильную группу, например метильную группу, замещенную теми же заместителями, что замещенный Сn-Сm-алкил. Примеры замещенной метильной группы включают такие группы, как гидроксиметил, защищенный гидроксиметил (например, тетрагидропиранилоксиметил), ацетоксиметил, карбамоилоксиметил,трифторметил, хлорметил, бромметил и иодметил. Термины С 1-С 12-алкилокси или С 1-С 12-алкокси здесь являются взаимозаменяемыми и обозначают такие группы, как метокси, этокси, n-пропокси, изопропокси, n-бутокси, трет-бутокси и т.п. Термины C1-C12-aцилокси или С 1-С 12-алканоилокси здесь являются взаимозаменяемыми и обозначают такие группы, как формилокси, ацетокси, пропионилокси, бутирилокси, пентаноилокси, гексаноилокси, гептаноилокси и т.п.- 12007852 Термины С 1-С 12-алкилкарбонил, С 1-С 12-алканоил или С 1-С 12-ацил здесь являются взаимозаменяемыми и обозначают такие группы, как формил, ацетил, пропионил, бутирил, пентаноил, гексаноил,гептаноил, бензоил и т.п. Термин циклоалкил здесь относится к моно-, би- или трициклическому насыщенному или ненасыщенному кольцу, где каждое кольцо содержит от 3 до 14 углеродных атомов, предпочтительно от 3 до 7 углеродных атомов. Как вариант, любое кольцо может быть оксидированным до образования карбонила. Термин алкенил означает разветвленный или неразветвленный углеводородный радикал, содержащий указанное число углеродных атомов и включающий одну или более углерод-углеродных двойных связей, где каждая двойная связь независимо образует цис-, транс- или негеометрический изомер. Термин алкинил означает разветвленный или неразветвленный углеводородный радикал, содержащий указанное число углеродных атомов и включающий одну или более углерод-углеродных двойных связей, где каждая двойная связь независимо образует цис-, транс- или негеометрический изомер. Термин алкинил означает разветвленный или неразветвленный углеводородный радикал, содержащий указанное число углеродных атомов и включающий одну или более углерод-углеродных тройных связей. Термины С 1-С 12-алкилтиогруппа и С 1-С 12-замещенная алкилтиогруппа обозначают C1-С 12-алкильную и С 1-С 12-замещенную алкильную группы, соответственно, прикрепленную к атому серы, которая, в свою очередь, является точкой прикрепления алкилтиогруппы или замещенной алкилтиогруппы к указанной группе или заместителю. Термин арил при использовании без дополнений обозначает гомоциклический ароматический радикал, слитый или неслитый и содержащий указанное число углеродных атомов. Предпочтительные арильные группы включают фенил, нафтил, бифенил, фенантренил, нафтаценил и т.п. (см., например,Lang's Handbook of Chemistry (Dean, J.A., ed.) 13th ed. табл. 7-2 (1985. Термин замещенный фенил или замещенный арил обозначает фенильную группу или арильную группу, замещенную одним, двумя или тремя заместителями, выбранными из перечисленных групп или выбранными из галогена (F, Сl, Вr, I), гидроксигруппы, замещенной гидроксигруппы, цианогруппы,нитрогруппы, С 1-С 6-алкила, С 1-С 6-алкоксигруппы, карбоксигруппы, защищенной карбоксигруппы, карбоксиметила, защищенного карбоксиметила, гидроксиметила, защищенного гидроксиметила, аминометила, защищенного аминометила, трифторметила, N-(метилсульфониламино)группы или других указанных групп. Примеры замещенного фенила включают (но не ограничиваются ими) моно- или ди(галогено)фенильную группу, такую как 4-хлорфенил, 2,6-дихлорфенил, 2,5-дихлорфенил, 3,4-дихлорфенил, 3-хлорфенил, 3-бромфенил, 3,4-дибромфенил, 3-хлор-4-фторфенил, 2-фторфенил и т.п.; моно- или ди(гидрокси) фенильную группу, такую как 4-гидроксифенил, 3-гидроксифенил, 2,4-дигидроксифенил, их производные с защищенной гидроксигруппой и т.п.; нитрофенильную группу, такую как 3- или 4-нитрофенил; цианофенильную группу, например 4-цианофенил; моно- или ди(низший алкил)фенильную группу, такую как 4-метилфенил, 2,4-диметилфенил, 2-метилфенил, 4-(изопропил)фенил, 4-этилфенил, 3-(n-пропил)фенил и т.п.; моно- или ди(алкокси)фенильную группу, такую как 2,6-диметоксифенил, 4-метоксифенил, 3-этоксифенил, 4-(изопропокси)фенил, 4-(трет-бутокси)фенил, 3-этокси-4-метоксифенил и т.п.; 3 или 4-трифторметилфенил; моно- или дикарбоксифенильную или (защищенную карбокси)фенильную группу, такую как 4-карбоксифенил; моно- или ди(гидроксиметил)фенил или (защищенный гидроксиметил)фенил, такой как 3-(защищенный гидроксиметил)фенил или 3,4-ди(гидроксиметил)фенил; моно- или ди(аминометил)фенил или (защищенный аминометил)фенил, такой как 2-(аминометил)фенил или 2,4(защищенный аминометил)фенил; или моно- или ди(N-(метилсульфониламинофенил, такой как 3-(Nметилсульфониламинофенил. Кроме того, термин замещенный фенил относится к дизамещенным фенильным группам, заместители в которых различны, например 3-метил-4-гидроксифенил, 3-хлор-4 гидроксифенил, 2-метокси-4-бромфенил, 4-этил-2-гидроксифенил, 3-гидрокси-4-нитрофенил, 2-гидрокси-4-хлорфенил и т.п. Предпочтительные замещенные фенильные группы включают 2- и 3-трифторметилфенил, 4-гидроксифенил, 2-аминометилфенил и 3-(N-(метилсульфониламинофенил. Термин арилалкил обозначает одну, две или три арильные группы, содержащие указанное число углеродных атомов, которые присоединены к алкильному радикалу, содержащему указанное число углеродных атомов, включая (но не ограничиваясь ими) бензил, нафтилметил, фенэтил, бензгидрил (дифенилметил), тритил и т.п. Предпочтительная арилалкильная группа представляет собой бензил. Термин замещенный С 6-С 10-арил-С 1-С 8-алкил обозначает С 1-С 8-алкильную группу, замещенную у одного углерода С 6-С 10-арильной группой, связанной с алкильной группой в любом арильном кольцевом положении и замещенной в C1-C8-алкильной части одной, двумя или тремя группами, выбранными из галогена (F, Cl, Вr, I), гидроксигруппы, защищенной гидроксигруппы, аминогруппы, защищенной аминогруппы, С 1-С 7-алкокси, нитрогруппы, карбоксигруппы, защищенной карбоксигруппы, карбамоила, карбамоилоксигруппы, цианогруппы, С 1-С 6-алкилтиогруппы, N-(метилсульфониламино)группы или С 1-С 4 алкоксигруппы. Как вариант, арильная группа может быть замещенной одной, двумя или тремя группами,выбранными из галогена, гидроксигруппы, замещенной гидроксигруппы, нитрогруппы, С 1-С 6-алкила, С 1 С 4-алкоксигруппы, карбоксигруппы, защищенной карбоксигруппы, карбоксиметила, защищенного карбоксиметила, гидроксиметила, защищенного гидроксиметила, аминометила, защищенного аминометила- 13007852 или N-(метилсульфониламино)группы. Как указано выше, если С 1-С 8-алкильная часть, или арильная часть, или обе эти части являются дизамещенными, заместители могут быть одинаковыми или разными. Примеры замещенного С 6-С 10-арил-С 1-С 8-алкила включают такие группы, как 2-фенил-1-хлорэтил, 2-(4-метоксифенилэтил), 2,6-дигидрокси-4-фенил(n-гексил), 5-циано-3-метокси-2-фенил(n-пентил),3-(2,6-диметилфенил)n-пропил, 4-хлор-3-аминобензил, 6-(4-метоксифенил)-3-карбокси(n-гексил), 5-(4 аминометилфенил)-3-(аминометил)(n-пентил) и т.п. Термин карбоксизащитная группа здесь относится к одному из сложноэфирных производных карбоксильной группы, обычно используемой для блокирования или защиты карбоксильной группы при проведении реакций на других функциональных группах соединения. Примеры таких карбоксизащитных групп включают 4-нитробензил, 4-метоксибензил, 3,4-диметоксибензил, 2,4-диметоксибензил, 2,4,6-триметоксибензил, 2,4,6-триметилбензил, пентаметилбензил, 3,4-метилендиоксибензил, бензгидрил, 4,4'-диметоксибензгидрил, 2,2',4,4'-тетраметоксибензгидрил, трет-бутил, трет-амил, тритил, 4-метокситритил,4,4'-диметокситритил, 4,4',4"-триметокситритил, 2-фенилпроп-2-ил, триметилсилил, трет-бутилдиметилсилил, фенацил, 2,2,2-трихлорэтил, b-(триметилсилил)этил, b-(ди(n-бутил)метилсилил)этил, р-толуолсульфонилэтил, 4-нитробензилсульфонилэтил, аллил, циннамил, 1-(триметилсилилметил)проп-1-ен-3-ил и другие подобные группировки. Выбранные представители карбоксизащитных групп не имеют решающей важности, при условии что дериватизованная карбоновая кислота устойчива к условиям последующей реакции (реакций) в других положениях бензодиазепиндионовой молекулы и может быть удалена в соответствующей точке без разрыва остальной части молекулы. В частности, важно не подвергать карбоксизащищенную бензодиазепиндионовую молекулу воздействиям сильных нуклеофильных оснований или восстановительным условиям, использующим высокоактивированные металлические катализаторы,такие как никелевый катализатор Ренея. (Следует также избегать таких жестких условий при удалении аминозащитных групп и гидроксизащитных групп, описанных ниже.) Предпочтительные карбоксизащитные группы включают аллильную и р-нитробензильную группы. Подобные карбоксизащитные группы, используемые в производстве цефалоспорина, пенициллина и пептидов, могут также использоваться для защиты заместителей карбоксигрупп в бензодиазепиндионе. Дополнительные примеры этих групп можно найти в Е. Haslam, Protective Groups in Organic Chemistry, J.G.W. McOmie, Ed., Plenum Press,New York, N.Y., 1973, Chapter 5, and T.W. Greene, Protective Groups in Organic Synthesis, John Wiley andSons, New York, NY, 1981, Chapter 5. Термин защищенная карбоксигруппа относится к карбоксигруппе, замещенной одной из вышеупомянутых карбоксизащитных групп. Термин амидзащитная группа относится к любой группе, обычно используемой в производстве пептидов для защиты азотных атомов в пептидах от нежелательных побочных реакций. Такие группы включают р-метоксифенил, 3,4-диметоксибензил, бензил, О-нитробензил, ди-(р-пиридилметил), m-2(пиколил)-N'-оксид, 5-дибензосуберил, триметилсилил, трет-бутилдиметилсилил и т.п. Дополнительные описания этих защитных групп можно найти в Protective Groups in Organic Chemistry, Theodora W.Greene, 1981, John Wiley and Sons, New York. Если не указано иное, термины гетероциклическая группа, гетероциклический, ГЕТ, гет или гетероциклил используются здесь взаимозаменяемо и относятся к любому моно-, би- или трициклическому насыщенному, ненасыщенному или ароматическому кольцу, содержащему указанное число атомов, где по меньшей мере одно кольцо представляет собой 5-, 6- или 7-звенное кольцо, содержащее от 1 до 4 гетероатомов, выбранных из группы, включающей азот, кислород и серу (Lang's Handbook ofChemistry, выше). Обычно 5-звенное кольцо содержит от 0 до 2 двойных связей, а 6- и 7-звенное кольцо содержит от 0 до 3 двойных связей, а атомы азота, углерода или серы в кольце могут быть, как вариант,оксидированными (например, NO2, С=O и SO2), и любой азотный гетероатом может быть кватернизирован. В область определения входят любые бициклические группы, в которых любое из вышеупомянутых гетероциклических колец слито с бензольным кольцом. Гетероциклилы, в которых гетероатомами являются кислород или сера, предпочтительны, когда гетероциклил образует всю или часть группы D в формуле I. Следующие кольцевые системы являются примерами гетероциклических (замещенных или незамещенных) радикалов, обозначенных термином гетероциклил или гет: тиенил, фурил, пирролил,имидазолил, пиразолил, тиазолил, изотиазолил, оксазолил, изоксазолил, триазолил, тиадиазолил, оксадиазолил, тетразолил, тиатриазолил, оксатриазолил, пиридил, пиримидил, пиразинил, пиридазинил, тиазинил, оксазинил, триазинил, тиадиазинил, оксадиазинил, дитиазинил, диоксазинил, оксатиазинил, тетразинил, тиатриазинил, оксатриазинил, дитиадиазинил, имидазолинил, дигидропиримидил, тетрагидропиримидил, тетразоло[1,5-b]пиридазинил и пуринил, а также бензослитые производные, например бензоксазолил, бензофурил, бензотиазолил, бензотиадиазолил, бензотриазолил, бензоимидазолил и индолил. Гетероциклические 5-звенные кольцевые системы, содержащие атом серы или кислорода и от 1 до 3 атомов азота, также пригодны для использования в данном изобретении. Примеры таких предпочтительных групп включают тиазолил, в частности тиазол-2-ил и тиазол-2-ила N-оксид, тиадиазолил, в частности 1,3,4-тиадиазол-5-ил и 1,2,4-тиадиазол-5-ил, оксазолил, предпочтительно оксазол-2-ил, и оксадиазолил, такой как 1,3,4-оксадиазол-5-ил и 1,2,4-оксадиазол-5-ил. Группа дополнительных предпочтительных примеров 5-звенных кольцевых систем с 2-4 атомами азота включает имидазолил, предпочтительно имидазол-2-ил; триазолил, предпочтительно 1,3,4-триазол-5-ил, 1,2,3-триазол-5-ил, 1,2,4-триазол- 14007852 5-ил, и тетразолил, предпочтительно 1 Н-тетразол-5-ил. Предпочтительная группа примеров бензослитых производных включает бензоксазол-2-ил, бензтиазол-2-ил и бензимидазол-2-ил. Дополнительные подходящие специфические примеры вышеупомянутых гетероциклических кольцевых систем включают 6-звенные кольцевые системы, содержащие от 1 до 3 атомов азота. Такие примеры включают пиридил, например пирид-2-ил, пирид-3-ил и пирид-4-ил; пиримидил, предпочтительно пиримид-2-ил и пиримид-4-ил; триазинил, предпочтительно 1,3,4-триазин-2-ил и 1,3,5-триазин-4-ил; пиридазинил, в частности пиридазин-3-ил, и пиразинил. Пиридина N-оксиды и пиридазина N-оксиды, а также пиридил, пиримид-2-ил, пиримд-4-ил, пиридазинил и 1,3,4-триазин-2-ил составляют предпочтительную группу радикалов. Заместители для замещенной (как вариант) гетероциклической кольцевой системы и дополнительные примеры 5- и 6-звенных кольцевых систем, описанных выше, можно найти в W. Druckheimer et al.,патент США 4,278,793. Другая предпочтительная группа гетероциклилов или гетов включает 1,3-тиазол-2-ил, 4-(карбоксиметил)-5-метил-1,3-тиазол-2-ил, 4-(карбоксиметил)-5-метил-1,3-тиазол-2-ила натриевую соль, 1,2,4 тиадиазол-5-ил, 3-метил-1,2,4-тиадиазол-5-ил, 1,3,4-триазол-5-ил, 2-метил-1,3,4-триазол-5-ил, 2-гидрокси-1,3,4-триазол-5-ил, 2-карбокси-4-метил-1,3,4-триазол-5-ила натриевую соль, 2-карбокси-4-метил 1,3,4-триазол-5-ил, 1,3-оксазол-2-ил, 1,3,4-оксадиазол-5-ил, 2-метил-1,3,4-оксадиазол-5-ил, 2-(гидроксиметил)-1,3,4-оксадиазол-5-ил, 1,2,4-оксадиазол-5-ил, 1,3,4-тиадиазол-5-ил, 2-тиол-1,3,4-тиадиазол-5-ил,2-(метилтио)-1,3,4-тиадиазол-5-ил, 2-амино-1,3,4-тиадиазол-5-ил, 1 Н-тетразол-5-ил, 1-метил-1 Н-тетразол-5 ил, 1-(1-(диметиламино)эт-2-ил)-1 Н-тетразол-5-ил, 1-(карбоксиметил)-1 Н-тетразол-5-ил, 1-(карбоксиметил)-1 Н-тетразол-5-ила натриевую соль, 1-(метилсульфоновой кислоты)-1 Н-тетразол-5-ил, 1-(метилсульфоновой кислоты)-1 Н-тетразол-5-ила натриевую соль, 2-метил-1 Н-тетразол-5-ил, 1,2,3-триазол-5-ил, 1 метил-1,2,3-триазол-5-ил, 2-метил-1,2,3-триазол-5-ил, 4-метил-1,2,3-триазол-5-ил, пирид-2-ила N-оксид,6-метокси-2-(n-оксид)пиридаз-3-ил, 6-гидроксипиридаз-3-ил, 1-метилперид-2-ил, 1-метилперид-4-ил, 2 гидроксипиримид-4-ил, 1,4,5,6-тетрагидро-5,6-диоксо-4-метил-аз-триазин-3-ил, 1,4,5,6-тетрагидро-4-(формилметил)-5,6-диоксо-аз-триазин-3-ил, 2,5-дигидро-5-оксо-6-гидрокси-аз-триазин-3-ил, 2,5-дигидро-5 оксо-6-гидрокси-аз-триазин-3-ила натриевую соль, 2,5-дигидро-5-оксо-6-гидрокси-2-метил-аз-триазин-3 ила натриевую соль, 2,5-дигидро-5-оксо-6-гидрокси-2-метил-аз-триазин-3-ил, 2,5-дигидро-5-оксо-6-метокси-2-метил-аз-триазин-3-ил, 2,5-дигидро-5-оксо-аз-триазин-3-ил, 2,5-дигидро-5-оксо-2-метил-аз-триазин-3-ил, 2,5-дагидро-5-оксо-2,6-диметил-аз-триазин-3-ил, тетразоло[1,5-b]пиридазин-6-ил и 8-аминотетразоло[1,5-b]пиридазин-6-ил. Альтернативная группа гетероциклилов включает 4-(карбоксиметил)-5-метил-1,3-тиазол-2-ил, 4(карбоксиметил)-5-метил-1,3-тиазол-2-ила натриевую соль, 1,3,4-триазол-5-ил, 2-метил-1,3,4-триазол-5 ил, 1 Н-тетразол-5-ил, 1-метил-1 Н-тетразол-5-ил, 1-(1-(диметиламино)эт-2-ил)-1 Н-тетразол-5-ил, 1-(карбоксиметил)-1 Н-тетразол-5-ил, 1-(карбоксиметил)-1 Н-тетразол-5-ила натриевую соль, 1-(метилсульфоновой кислоты)-1 Н-тетразол-5-ил, 1-(метилсульфоновой кислоты)-1 Н-тетразол-5-ила натриевую соль,1,2,3-триазол-5-ил, 1,4,5,6-тетрагидро-5,6-диоксо-4-метил-аз-триазин-3-ил, 1,4,5,6-тетрагидро-4-(2-формилметил)-5,6-диоксо-аз-триазин-3-ил, 2,5-дигидро-5-оксо-6-гидрокси-2-метил-аз-триазин-3-ила натриевую соль, 2,5-дигидро-5-оксо-6-гидрокси-2-метил-аз-триазин-3-ил, тетразоло[1,5-b]пиридазин-6-ил и 8-аминотетразоло[1,5-b]пиридазин-6-ил. Бивалентные радикалы L, разветвленные или неразветвленные, полученные из алканов, алкенов,алкадиенов, алкинов, алкадиинов и аренов, возможно, содержащие атомы О, N и/или S или гомо- и гетероциклы, ароматические или алифатические, обозначаются путем добавления свободной валентности на обоих концах соответствующего моновалентного радикала. Атомы, имеющие свободные валентности,могут включать любой из атомов С, О, N или S. Фармацевтически приемлемые соли включают соли, полученные в результате реакций как с кислотами, так и с основаниями. Выражение фармацевтически приемлемые соли с кислотами относится к тем солям, которые сохраняют биологическую эффективность и свойства свободных оснований и которые не являются нежелательными в биологическом или другом отношении, образованы с неорганическими кислотами, такими как соляная кислота, бромисто-водородная кислота, серная кислота, азотная кислота, угольная кислота, фосфорная кислота и т.п., и органическими кислотами, которые могут быть выбраны из алифатических, циклоалифатических, ароматических, аралифатических, гетероциклических,карбоновых и сульфоновых классов органических кислот, такими как муравьиная кислота, уксусная кислота, пропионовая кислота, гликолевая кислота, глюконовая кислота, молочная кислота, пировиноградная кислота, щавелевая кислота, яблочная кислота, малоновая кислота, малеиновая кислота, малоновая кислота, янтарная кислота, фумаровая кислота, винная кислота, лимонная кислота, аспарагиновая кислота, аскорбиновая кислота, глутаминовая кислота, антраниловая кислота, бензойная кислота, коричная кислота, миндальная кислота, эмбонатовая кислота, фенилуксусная кислота, метансульфокислота, этансульфокислота, р-толуолсульфокислота, салициловая кислота и т.п. Фармацевтически приемлемые соли с основаниями включают соли, полученные из неорганических оснований, такие как соли натрия, калия, лития, аммония, кальция, магния, железа, цинка, меди,марганца, алюминия и т.д. Особо предпочтительны аммониевые, калиевые, натриевые, кальциевые и- 15007852 магниевые соли. Соли, полученные из фармацевтически приемлемых органических нетоксических оснований, включают соли первичных, вторичных и третичных аминов, замещенных аминов, включая природные замещенные амины, циклические амины и основные ионообменные смолы, такие как изопропиламин, триметиламин, диэтиламин, триэтиламин, трипропиламин, этаноламин, 2-диэтиламиноэтанол,триметамин, дициклогексиламин, лизин, аргинин, гистидин, кофеин, прокаин, гидрабамин, холин, бетаин, этилендиамин, глюкозамин, метилглюкамин, теобромин, пурины, пиперизин, пиперидин, N-этилпиперидин, полиаминные смолы и т.п. Особо предпочтительны такие органические нетоксические основания, как изопропиламин, диэтиламин, этаноламин, триметамин, дициклогексиламин, холин и кофеин. Термин пролекарство здесь означает производное или предшественник молекулы основного лекарства, который улучшает фармацевтически желательные характеристики или свойства (например,транспорт, биоаккумулирование, фармакодинамику и т.д.) и который требует биотрансформации, спонтанной или ферментативной, внутри организма для высвобождения активного основного лекарства. Примеры карбоксильных пролекарств включают такие предшественники, как альдегиды, спирты или амины, или такие производные, как сложные эфиры. В. Применение. Антагонисты LFA-1 и/или Мас-1 по данному изобретению подходят для терапевтического применения при таких заболеваниях и состояниях, для которых показано ингибирование или модуляция взаимодействия LFA-1 и/или Мас-1 с IСAM, особенно ICAM-1. Такие заболевания и состояния включают Тклеточные воспалительные реакции, такие как воспалительные заболевания кожи, включая псориаз; реакции, связанные с воспалительным кишечным заболеванием (таким как болезнь Крона и язвенный колит); респираторный дистресс-синдром взрослых; дерматит; менингит; энцефалит; увеит; аллергические состояния, такие как экзема и астма, и другие состояния, вызывающие инфильтрацию Т-клеток и хронические воспалительные реакции; реакции кожной гиперчувствительности (включая сумах укореняющийся); аллергический контактный дерматит; атеросклероз; аутоиммунные заболевания, такие как ревматоидный артрит, системная красная волчанка (СКВ), сахарный диабет, множественный склероз, синдром Рейнода, аутоиммунный тиреоидит, экспериментальный аутоиммунный энцефаломиелит, синдром Шегрена, юношеский диабет и иммунные реакции, связанные с замедленной гиперчувствительностью, опосредованной цитокинами и Т-лимфоцитами, обычно наблюдаемые при туберкулезе, саркоидозе, полимиозите, гранулематозе и васкулите; злокачественную анемию; заболевания, вызывающие лейкоцитарный диапедез; воспалительные расстройства ЦНС, синдром множественного поражения внутренних органов вследствие заражения крови или травмы; аутоиммунную гемолитическую анемию; тяжелую псевдопаралитическую миастению, заболевания, опосредованные комплексом антиген-антитело; все типы трансплантаций, включая реакции трансплантат против хозяина или хозяин против трансплантата,ВИЧ-инфекцию и т.д. Другие лейкоцитарно-опосредованные заболевания, для которых могут быть использованы данные конкурентные ингибиторы, включают геморрагический шок, ишемическое/реперфузионное поражение,шунтирующую хирургию, ожоги, инсульт, последствия аортокоронарного шунтирования (АКШ), васкулит,церебральный отек (более широко - рестеноз, острый инфаркт миокарда и инфаркт миокарда без зубца Q). С. Предпочтительные варианты осуществления. 1. Конкурентные ингибиторы CD11a/CD18:ICAM-1. Один из вариантов осуществления изобретения включает соединение, которое способно ингибировать связывание лейкоцитарного рецептора LFA-1 с его нативным in vivo лигандом (лигандами), особенноICAM-1. Предпочтительные ингибиторы включают соединения, представленные структурной формулойLX выбран из группы, включающей замещенные или незамещенные С 2-С 5-алкилен,С 3-С 6-циклоалкилен,С 0-С 3-алкилен-NRn-(С=O)-С 0-С 3-алкилен,С 0-С 3-алкилен-(С=O)-NRn-С 0-С 3-алкилен,С 0-С 3-алкилен-О-С 0-С 3-алкилен,С 0-С 3-алкилен-NRn-С 0-С 3-алкилен,С 0-С 3-алкилен-(С=O)-С 0-С 3-алкилен,С 0-С 3-алкилен-СR1=СR2-С 0-С 3-алкилен,С 0-С 3-алкилен-СС-С 0-С 3-алкилен и С 0-С 3-алкилен-гет-С 0-С 3-алкилен,при этом заместители выбираются из группы, включающей от 1 до 3 радикалов R1, R2 и R3;LY выбран из группы, включающей замещенные или незамещенные С 0-С 2-алкилен,С 0-С 2-алкилен-NRn-(С=O)-С 0-С 2-алкилен,С 0-С 2-алкилен-(С=O)-NRn-С 0-С 2-алкилен,С 0-С 2-алкилен-O-С 0-С 2-алкилен,С 0-С 2-алкилен-NRn-С 0-С 2-алкилен,С 0-С 2-алкилен-(С=O)-С 0-С 2-алкилен,при этом заместители выбраны из группы, включающей от 1 до 3 радикалов R1, R2 и R3;RC выбран из группы, состоящей из водорода и замещенного или незамещенного гета, при этом заместители в гете представляют собой от 1 до 3 радикалов Rd; гет является моно-, би- или трициклическим 5-, 6-, 7-, 9- или 10-звенным насыщенным, ненасыщенным или ароматическим кольцом, имеющим от 1 до 4 гетероатомов, выбранных из группы, включающей азот, кислород и серу,Rp и Rd независимо выбраны из группы, включающей ОН,CN,NO2,галоген,ORn,SRn,SORn,CF3,RC,NRnRn',NRnC(=O)-O-Rn',NRnC(=O)-Rn',C0-C6-aлкил-SO2-Rn,C0-C6-алкил-SO2-NRnRn',C(=O)-Rn,O-C(=O)-Rn,C(=O)-O-Rn,C(=O)-NRnRn',Rd представляет собой химическую связь, когда гет представляет собой двухвалентную соединительную группу;Rn и Rn' независимо выбраны из группы, включающей водород,гидроксигруппу,С 1-С 6-алкил,галоген-С 1-С 6-алкил,С 1-С 6-алкил-гет,гет-С 1-С 6-алкил,- 17007852 С 6-С 12-арил и гет;Q отсутствует или представляет собой С 0-С 3-алкил, замещенный группой, выбранной изV отсутствует или представляет собой бивалентную группу, возможно, замещенную, выбранную из группы, включающей С 1-С 11-алкилена,С 2-С 6-алкенилена,С 0-С 6-алкил-гета,при этом заместители в любом алкиле представляют собой от 1 до 3 радикалов Ra, a заместители в любом ариле или гете представляют собой от 1 до 3 радикалов Rd;Ra,NH-C(=O)-RC,C(=O)-RC,C(=O)-NRnRn' и RC,обладающие способностью модулировать адгезию между внутриклеточными адгезионными молекулами и лейкоцитарным интегриновым семейством рецепторов, а также его фармацевтически приемлемые соли;Ra представляет собой аминогруппу. Более конкретно, соединение может представлять собой соединение, выбранное из группы, включающей а также фармацевтически приемлемые соли этих соединений. Также, более конкретно, соединение может представлять собой соединение, выбранное из группы,включающей где гет выбран из группы, включающей а также фармацевтически приемлемые соли этих соединений. Примеры предпочтительных соединений по данному изобретению включаютD. Способы производства. Один из способов получения антагонистов LFA-1 включает химический синтез пептида или пептидомиметика. Этот синтез может проводиться по методике, хорошо известной опытным специалистам в данной области (см. Stewart and Young, Solid Phase Peptide Synthesis Pierce Chemical Co. Rockford, IL(1984); см. также патенты США 4,105,603, 3,972,859, 3,842,067 и 3,862,925. Из обзора соединений, приведенных выше, становится ясно, что все они содержат одну или более амидных или пептидных связей и поэтому могут рассматриваться как пептидомиметики. Пептидомиметики по изобретению удобно также получать с использованием твердофазного пептидного синтеза (Merrifield,J. Am. Chem. Soc., 85:2149 (1964); Hougten, Proc. Natl. Acad. Sci. U.S.A., 82:5132-5159 (1985. Твердофазный синтез начинается с карбоксильного окончания предполагаемого пептида путем соединения защищенной аминокислоты с подходящей полимерной смолой (например, хлорметилированной полистирольной смолой), как показано на фиг. 1-1 и 1-2, на стр. 2 и 4 работы Stewart and Young, выше. После удаления -аминозащитной группы посредством, например, трифторуксусной кислоты (ТФУ) в метиленхлориде и нейтрализации, например, в TEA в синтез добавляются следующая -аминокислота и аминокислота с защищенной боковой цепью. Оставшиеся -аминокислоты и, если необходимо, аминокислоты с защищенной боковой цепью присоединяются последовательно в желаемом порядке путем конденсации для получения промежуточного соединения, соединенного с полимерной смолой. В альтернативе,некоторые амины и кислоты могут соединяться друг с другом, образуя пептид, до добавления пептида в растущую твердофазную пептидную цепь. Конденсация между двумя аминокислотами может проводиться обычными способами конденсации,такими как азидный способ, смешанный кислотно-ангидридный способ, способы ДЦК (N,N'-дициклогексилкарбодиимид) или ДИПК (N,N'-диизопропилкарбодиимид), способ активного эфира (способ р-нитрофенилового эфира, способ ВОР [бензотриазол-1-ил-окси-трис(диметиламино)фосфония гексафторфосфат], способ N-гидроксиянтарной кислоты имидоэфира и т.д., а также способ реагента К Вудворда. Общей для всех химических синтезов пептидов является защита любых реакционноспособных групп боковых цепей аминокислот подходящими защитными группами. В конечном счете, после последовательной сборки нужной полипептидной цепи эти защитные группы удаляются. Также общей является защита -аминогруппы в аминокислоте или фрагменте, пока этот элемент реагирует на участке карбоксильной группы, с последующим избирательным удалением -аминозащитной группы для обеспечения возможности реакции теперь на этом участке. Таким образом, для пептидного синтеза общим является то, что вырабатывается промежуточное соединение, в котором аминокислотные остатки располагаются в пептидной цепи в желаемой последовательности, а к боковым цепям этих остатков прикреплены защитные группы. Эти защитные группы затем удаляются вместе, по существу, одновременно, чтобы получить желаемый результирующий продукт после отделения от полимерной смолы.- 23007852 Подходящие защитные группы для защиты - и -аминогрупп боковых цепей включают бензилоксикарбонил (CBZ), изоникотинилоксикарбонил (iNOC), о-хлорбензилоксикарбонил (2-Сl- CBZ), р-нитробензилоксикарбонил [Z(NO2)], р-метоксибензилоксикарбонил [Z(OMe)], трет-бутоксикарбонил (ВОС),трет-амилоксикарбонил (АОС), изоборнилоксикарбонил, адаматилоксикарбонил, 2-(4-бифенил)-2-пропилоксикарбонил (ВРОС), 9-флуоренилметоксикарбонил (FMOC), метилсульфонаиэтоксикарбонил (Msc),трифторацетил, фталил, формил, 2-нитрофенилсульфенил (NPS), дифенилфосфинотиоил (Ppt), диметилфосфинотиоил (Mpt) и т.п. Защитные группы для карбоксильной функциональной группы представлены следующими примерами: бензиловый эфир (Obzl), циклогексиловый эфир (Chx), 4-нитробензиловый эфир (OtBu), 4-пиридилметиловый эфир (Opic) и т.п. Зачастую желательно, чтобы специфические аминокислоты, такие как аргинин, цистеин и серин, содержащие функциональную группу, отличную от амино- и карбоксильной групп, были защищены подходящей защитной группой. Например, гуанидиногруппа аргинина может быть защищена нитрогруппой, р-толуолсульфонилом, бензилоксикарбонилом, адамантилоксикарбонилом, р-метоксибензолсульфонилом, 4-метокси-2,6-диметилбензолсульфонилом (Mds), 1,3,5-триметилфенилсульфонилом (Mts) и т.п. Тиоловая группа цистеина может быть защищена р-метоксибензилом, трифенилметилом, ацетиламинометилэтилкарбамоилом, 4-метилбензилом, 2,4,6-триметилбензил (Tmb) и т.д., а гидроксильная группа серина может быть защищена бензилом, трет-бутилом, ацетилом, тетрагидропиранилом и т.п.Stewart and Young, выше, предоставляют детальную информацию относительно методик получения пептидов. Защита -аминогрупп описана на стр. 14-18, а блокирование боковых цепей описано на стр. 18-28. Таблица защитных групп для амино-, гидроксильной и сульфгидрильной функциональных групп приведена на стр. 149-151. После составления желаемой аминокислотной последовательности промежуточный пептид отделяется от полимерной подложки путем обработки соответствующим реагентом, таким как жидкий HF и один или более серосодержащих очистителей, которые не только отщепляют пептиды от смолы, но также отщепляют все оставшиеся защитные группы боковых цепей. После HF-отщепления пептидный остаток промывается эфиром и экстрагируется из смолы путем промывки водным ацетонитрилом и уксусной кислотой. Предпочтительно, для того чтобы избежать алкилирования остатков в полипептиде (например, алкилирования остатков метионина, цистеина и тирозина), используется тиокрезольная и крезольная очистительная смесь. Другие общие методики Пептидомиметические соединения по данному изобретению удобно также получать способами пептидного синтеза, описанными в таких монографиях, как Principles of Peptide Synthesis, M. Bodansky,Springer-Verlag, 2nd Ed., 1993; Synthetic Peptides: A Users Guide, G.A. Grant, Ed, W.H. Freeman and Co.,1992; и список ссылок к ним, или другими общеизвестными способами. Синтез соединений по данному изобретению, которые являются пептидомиметическими по природе (т.е., содержат отличные от стандартных амидные связи между двумя или более аминокислотами), могут быть получены путем усовершенствования методик, описанных в примере 6, и путем общих методов синтеза, описанных в ComprehensiveOrganic Transformations, R.C. Larock, VHC Publishers, 1989, а также другими общими способами, известными специалистам. Для соединений по п.1, в котором амидные связи (-C(=O)-NH-) заменены амидными изостерическими (Ai) связями, такими как (-C(=S)-NH-), (-S(=O)2-NH-), -CH2-NH-, -CH2-S-, -СН 2-О-, -СН 2-СН 2-,-СН=СН- (цис- и транс-), -C(=O)-CH2-, -CH(OH)-CH2-, -CH(CN)-NH-, -О-C(=O)-NH- и -СН 2-SO-, применяются известные методики замены амидных связей. Следующие ссылки описывают получение амидных изостерических связей, которые включают эти альтернативные соединительные группы: Spatola, A.F.,Vega Data 1(3): Peptide Backbone Modifications (General Review) (Mar 1983), Spatola, A.F., in ChemistryCalcagni et al., Int. J. Peptide Protein Res. 34:319-324 (1989) (-S(=O)2-NH-); TenBrink, J. Org. Chem. 52:418422 (1987) (-CH2-O-). Схема I иллюстрирует один из синтетических подходов, обеспечивающих получение неприродных аминокислотных боковых цепей, в частности, для заместителя Т в формуле I. Способ обеспечивает-алкилирование глициновой боковой цепи с использованием твердофазного синтеза в промышленно выпускаемом аппарате, таком как Argonaut Nautilus 2400. По вышеприведенной схеме алкилирования в антагонисты LFA-1 могут вводиться следующие примеры R-групп: Если R в схеме I представляет собой алкиламин, полученный из аминокислот лизина, орнитина или DAPА восстановлением нитрилов, примеры которых приведены выше, или полученный из защищенного (например, FMOC) аминоалкилгалогенида, существуют синтетические способы для получения производных Т, включая мочевины, карбаматы, амиды и сульфонамиды, при помощи известных методик. Схема II иллюстрирует твердофазный способ получения этих производных Т. Мочевины, полученные по схеме II, могут синтезироваться из следующих характерных серийно выпускаемых изоцианатов (RNCO): Другие характерные замещенные арилизоцианаты, пригодные для использования в приведенной выше схеме, включают Если R в схеме I представляет собой спирт, то эти и другие изоцианаты могут использоваться для получения карбаматов по схеме IIа. Схема IIаcхеме II, могут быть получены из характерных серийно выпускаемых соединений ROCOCl, RCOCl и Схема III иллюстрирует общий ход синтеза для алкильных линкеров, L, для дихлорзамещенных бензоиламинокислот или их производных. Ключевым промежуточным веществом в этом способе является йод-, дихлорбензоил-АА (4). Схема III Ключевое промежуточное соединение (4) соединяется с различными алкинами для получения алкильных линкеров различной длины. Например, углеродный линкер 3 может быть получен путем соединения (4) с алкиновым промежуточным соединением (5), полученным по схеме IIIа. Схема IIIа Схема IV иллюстрирует синтез замещенных и незамещенных алканов и замещенных алкиновых линкеров. Углеродный линкер 4 может быть получен путем соединения (4) с алкиновым промежуточным соединением (6), полученным по схеме V. Схема V Схема VI иллюстрирует синтез незамещенного алканового и алкинового линкеров. Схема VI Схемы VIa и VIb иллюстрируют синтез замещенных и незамещенных алканового и алкинового линкеров длиной в 3-5 углеродных атомов. Схема VII иллюстрирует синтез 3-углеродного алкильного линкера, где В представляет собой диметилзамещенный бензоильный антагонист LFA-1. Схема VII- 29007852 Схема VIII иллюстрирует синтез 3-5-атомного диэфирного линкера, где n=1-3. Промежуточный фенол (7) может быть также использован в синтезе моноэфиров, описанном ниже. Схема VIII Схема IX иллюстрирует синтез 3-5-атомных моноэфирных линкеров, где n=1-3. Вышеописанный промежуточный фенол (7) используется в этой методике. Схема IX Схема X иллюстрирует синтез 5-атомных алкильных линкеров, где дистальная группа D представляет собой 5-звенное ароматическое кольцо. Предпочтительные кольца включают тиофен, фуран,тиазол и оксазол, где Z1 представляет собой О или S, a Y2, Y3 или Y4 выбраны из N или СН.
МПК / Метки
МПК: A61P 37/00, C07C 255/30, A61K 31/452, A61K 31/17, A61K 31/166, A61K 31/4035
Метки: рецепторами, расстройств, лечения, адгезии, соединения, опосредованных
Код ссылки
<a href="https://eas.patents.su/30-7852-soedineniya-dlya-lecheniya-rasstrojjstv-oposredovannyh-receptorami-adgezii-cd11-cd18.html" rel="bookmark" title="База патентов Евразийского Союза">Соединения для лечения расстройств, опосредованных рецепторами адгезии cd11/cd18</a>
Предыдущий патент: Панель в качестве конструктивного элемента и стенка из этих панелей
Следующий патент: Жидкости для обработки скважин, содержащие хелатообразователи
Случайный патент: Способ изготовления армированного прокладочного материала