Гликозидные производные и их применение
Номер патента: 23781
Опубликовано: 29.07.2016
Авторы: Вявахаре Винод, Курхаде Суреш Экнат, Шаикх Надим С., Лян Джессика, Редди Думбала Сринивас, Бхосейл Сандип Бхаусахеб, Бок Марк Г., Салункхе Видеш, Бебернитц Грегори Раймонд, Фэн Лили, Палле П.Венката, Бхуния Дебнат, Хаджаре Атул Кашинат
Формула / Реферат
1. Соединение, выбранное из числа соединений (1)-(72), приведенных ниже, или его фармацевтически приемлемая соль
1) (2S,3R,4R,5S,6R)-2-[4-хлор-3-(4-метил-3,4-дигидро-2Н-бензо[1,4]-оксазин-7-илметил)фенил]-6-гидроксиметилтетрагидропиран-3,4,5-триол,
2) (2S,3R,4R,5S,6R)-2-[4-хлор-3-(4-этил-3,4-дигидро-2Н-бензо[1,4]-оксазин-7-илметил)фенил]-6-гидроксиметилтетрагидропиран-3,4,5-триол,
3) (2S,3R,4R,5S,6R)-2-[4-хлор-3-(4-циклопропил-3,4-дигидро-2Н-бензо[1,4]оксазин-7-илметил)фенил]-6-гидроксиметилтетрагидропиран-3,4,5-триол,
4) (2S,3R,4R,5S,6R)-2-[3-(4-бензил-3,4-дигидро-2Н-бензо[1,4]оксазин-6-илметил)-4-хлорфенил]-6-гидроксиметилтетрагидропиран-3,4,5-триол,
5) (2S,3R,4R,5S,6R)-2-{4-хлор-3-[4-(4-метоксибензил)-3,4-дигидро-2Н-бензо[1,4]оксазин-6-илметил]фенил}-6-гидроксиметилтетрагидропиран-3,4,5-триол,
6) (2S,3R,4R,5S,6R)-2-[3-(4-бензил-2,2-диметил-3,4-дигидро-2Н-бензо[1,4]оксазин-6-илметил)-4-хлорфенил]-6-гидроксиметилтетрагидропиран-3,4,5-триол,
7) (2S,3R,4R,5S,6R)-2-[3-(4-бензил-3,4-дигидро-2H-бензо[1,4]оксазин-6-илметил)-4-хлорфенил]-6-гидроксиметилтетрагидропиран-3,4,5-триол,
8) (2S,3R,4R,5S,6R)-2-[4-хлор-3-(3,4-дигидро-2Н-бензо[1,4]оксазин-6-илметил)фенил]-6-гидроксиметилтетрагидропиран-3,4,5-триол,
9) (2S,3R,4R,5S,6R)-2-[4-хлор-3-(4-этил-3,4-дигидро-2H-бензо[1,4]-оксазин-6-илметил)фенил]-6-гидроксиметилтетрагидропиран-3,4,5-триол,
10) (2S,3R,4R,5S,6R)-2-[4-хлор-3-(4-циклопропилметил-3,4-дигидро-2Н-бензо[1,4]оксазин-6-илметил)фенил]-6-гидроксиметилтетрагидропиран-3,4,5-триол,
11) (2S,3R,4R,5S,6R)-2-[4-хлор-3-(4-метил-3,4-дигидро-2H-бензо[1,4]-оксазин-6-илметил)фенил]-6-гидроксиметилтетрагидропиран-3,4,5-триол,
12) этиловый эфир 6-[2-хлор-5-((2S,3R,4R,5S,6R)-3,4,5-тригидрокси-6-гидроксиметилтетрагидропиран-2-ил)бензил]-2,3-дигидробензо[1,4]оксазин-4-карбоновой кислоты,
13) 1-{6-[2-хлор-5-((2S,3R,4R,5S,6R)-3,4,5-тригидрокси-6-гидроксиметилтетрагидропиран-2-ил)бензил]-2,3-дигидробензо[1,4]оксазин-4-ил}этанон,
14) (2S,3R,4R,5S,6R)-2-{4-хлор-3-[1-(4-метоксибензил)-1,2,3,4-тетрагидрохинолин-6-илметил]фенил}-6-гидроксиметилтетрагидропиран-3,4,5-триол,
15) (2S,3R,4R,5S,6R)-2-[4-хлор-3-(1,2,3,4-тетрагидрохинолин-6-илметил)фенил]-6-гидроксиметилтетрагидропиран-3,4,5-триол,
16) (2S,3R,4R,5S,6R)-2-[4-хлор-3-(1,2,3,4-тетрагидрохинолин-7-илметил)фенил]-6-гидроксиметилтетрагидропиран-3,4,5-триол,
17) (2S,3R,4R,5S,6R)-2-[4-хлор-3-(2,3-дигидро-1Н-индол-5-илметил)фенил]-6-гидроксиметилтетрагидропиран-3,4,5-триол,
18) (2S,3R,4R,5S,6R)-2-[3-(2-бензил-1,2,3,4-тетрагидроизохинолин-7-илметил)-4-хлорфенил]-6-гидроксиметилтетрагидропиран-3,4,5-триол,
19) (2S,3R,4R,5S,6R)-2-[4-хлор-3-(1,2,3,4-тетрагидроизохинолин-7-илметил)фенил]-6-гидроксиметилтетрагидропиран-3,4,5-триол,
20) (2S,3R,4R,5S,6R)-2-[4-хлор-3-(2,2-диметил-3,4-дигидро-2Н-бензо[1,4]-оксазин-6-илметил)фенил]-6-гидроксиметилтетрагидропиран-3,4,5-триол,
21) (2S,3R,4R,5S,6R)-2-(4-хлор-3-хроман-6-илметилфенил)-6-гидроксиметилтетрагидропиран-3,4,5-триол,
22) (2S,3R,4R,5S,6R)-2-[4-хлор-3-(2,3-дигидробензофуран-5-илметил)фенил]-6-гидроксиметилтетрагидропиран-3,4,5-триол,
23) (2R,3S,4R,5R,6S)-2-гидроксиметил-6-[4-метил-3-(1,2,3,4-тетрагидрохинолин-7-илметил)фенил]тетрагидропиран-3,4,5-триол,
24) (2S,3R,4R,5S,6R)-2-[3-(3,4-дигидро-2Н-бензо[1,4]оксазин-6-илметил)-4-фторфенил]-6-гидроксиметилтетрагидропиран-3,4,5-триол,
25) (2S,3R,4R,5S,6R)-2-[3-(2,3-дигидробензо[1,4]диоксин-6-илметил)-4-метоксифенил]-6-гидроксиметилтетрагидропиран-3,4,5-триол,
26) (2R,3S,4R,5R,6S)-2-гидроксиметил-6-[4-метокси-3-(1,2,3,4-тетрагидрохинолин-6-илметил)фенил]тетрагидропиран-3,4,5-триол,
27) (2R,3S,4R,5R,6S)-2-гидроксиметил-6-[4-метокси-3-(1,2,3,4-тетрагидрохинолин-7-илметил)фенил]тетрагидропиран-3,4,5-триол,
28) (2S,3R,4R,5S,6R)-2-[4-хлор-3-(3,4-дигидро-2H-бензо[1,4]оксазин-7-илметил)фенил]-6-гидроксиметилтетрагидропиран-3,4,5-триол,
29) (2S,3R,4R,5S,6R)-2-[4-хлор-3-(4,4-спироциклопропилхроман-6-илметил)фенил]-6-гидроксиметилтетрагидропиран-3,4,5-триол,
30) (2S,3R,4R,5S,6R)-2-[5-(2,3-дигидробензо[1,4]диоксин-6-илметил)-2-этоксифенил]-6-гидроксиметилтетрагидропиран-3,4,5-триол,
31) (2S,3R,4R,5S,6R)-2-[3-(3,4-дигидро-2Н-бензо[1,4]оксазин-6-илметил)-4-метоксифенил]-6-гидроксиметилтетрагидропиран-3,4,5-триол,
32) (2S,3R,4R,5S,6R)-2-(3-хроман-6-илметил-4-метоксифенил)-6-гидроксиметилтетрагидропиран-3,4,5-триол,
33) (2S,3R,4R,5S,6R)-2-(3-хроман-6-илметил-4-трифторметоксифенил)-6-гидроксиметилтетрагидропиран-3,4,5-триол,
34) 6-[2-хлор-5-((2S,3R,4R,5S,6R)-3,4,5-тригидрокси-6-гидроксиметилтетрагидропиран-2-ил)бензил]хромен-4-он,
35) 6-[2-хлор-5-((2S,3R,4R,5S,6R)-3,4,5-тригидрокси-6-гидроксиметилтетрагидропиран-2-ил)бензил]хроман-4-он,
36) (2S,3R,4R,5S,6R)-2-[4-хлор-3-(4-гидроксихроман-6-илметил)фенил]-6-гидроксиметилтетрагидропиран-3,4,5-триол,
37) (2S,3R,4R,5S,6R)-2-[4-хлор-3-(спиро[хроман-2,1'-циклопентан]-6-илметил)фенил]-6-(гидроксиметил)тетрагидропиран-3,4,5-триол,
38) (2S,3R,4R,5S,6R)-2-[4-хлор-3-(спиро[хроман-2,1'-циклопентан]-6-илметил)фенил]-6-(гидроксиметил)тетрагидропиран-3,4,5-триол,
39) 6-[2-хлор-5-[(2S,3R,4R,5S,6R)-3,4,5-тригидрокси-6-(гидроксиметил)тетрагидропиран-2-ил]фенилметил]спиро[хроман-2,4'-пиперидин]-4-он,
40) 6-(2-метокси-5-((2S,3S,4R,5R,6R)-3,4,5-трис(бензилокси)-6-(бензилоксиметил)тетрагидро-2Н-пиран-2-ил)бензил)спиро[хроман-2,1'-циклобутан],
41) (2S,3R,4R,5S,6R)-2-[4-метокси-3-(спиро[хроман-2,1'-циклобутан]-6-илметил)фенил]-6-(гидроксиметил)тетрагидропиран-3,4,5-триол,
42) 7-[2-хлор-5-((2S,3R,4R,5S,6R)-3,4,5-тригидрокси-6-гидроксиметилтетрагидропиран-2-ил)бензил]-4Н-бензо[1,4]оксазин-3-он,
43) 7-[2-метокси-5-((2S,3R,4R,5S,6R)-3,4,5-тригидрокси-6-гидроксиметилтетрагидропиран-2-ил)бензил]-4Н-бензо[1,4]оксазин-3-он,
44) (2S,3R,4R,5S,6R)-2-[4-хлор-3-(спиро[хроман-2,1'-циклобутан]-6-илметил)фенил]-6-(гидроксиметил)тетрагидропиран-3,4,5-триол,
45) [(2R,3R,4R,5S,6S)-3,4,5-триацетокси-6-[4-хлор-3-[(2,2-диметил-3-оксо-4Н-1,4-бензоксазин-6-ил)метил]фенил]тетрагидропиран-2-ил]метилацетат,
46) 6-[2-хлор-5-((2S,3R,4R,5S,6R)-3,4,5-тригидрокси-6-гидроксиметилтетрагидропиран-2-ил)бензил]-2,2-диметил-4Н-бензо[1,4]оксазин-3-он,
47) 6-(2-хлор-5-((2S,3R,4R,5S,6R)-3,4,5-тригидрокси-6-(гидроксиметил)тетрагидро-2Н-пиран-2-ил)бензил)-2Н-бензо[b][1,4]оксазин-3(4Н)-он,
48) (2S,3R,4R,5S,6R)-2-[3-[(4-бензилспиро[3H-1,4-бензоксазин-2,1'-циклопропан]-6-ил)метил]-4-хлорфенил]-6-(гидроксиметил)тетрагидропиран-3,4,5-триол,
49) (2S,3R,4R,5S,6R)-2-[4-хлор-3-(спиро[3,4-дигидро-1,4-бензоксазин-2,1'-циклопропан]-6-илметил)фенил]-6-(гидроксиметил)тетрагидропиран-3,4,5-триол,
50) (2R,3R,4R,5S,6S)-3,4,5-триацетокси-6-[4-хлор-3-(2-циано-3,4-дигидро-2Н-бензо[1,4]оксазин-6-илметил)фенил]тетрагидропиран-2-илметиловый эфир уксусной кислоты,
51) 6-[2-хлор-5-((2S,3R,4R,5S,6R)-3,4,5-тригидрокси-6-гидроксиметилтетрагидропиран-2-ил)бензил]-3,4-дигидро-2Н-бензо[1,4]оксазин-2-карбонитрил,
52) метиловый эфир 6-[2-хлор-5-((2S,3R,4R,5S,6R)-3,4,5-тригидрокси-6-гидроксиметилтетрагидропиран-2-ил)бензил]-3,4-дигидро-2Н-бензо[1,4]-оксазин-2-карбоновой кислоты,
53) 6-[2-хлор-5-((2S,3R,4R,5S,6R)-3,4,5-тригидрокси-6-гидроксиметилтетрагидропиран-2-ил)бензил]-3,4-дигидро-2Н-бензо[1,4]оксазин-2-карбоновую кислоту,
54) 6-[2-бром-5-((3S,4R,5R,6R)-3,4,5-трис-бензилокси-6-бензилоксиметилтетрагидропиран-2-ил)бензил]хроман,
55) 6-[2-циклопропил-5-((3S,4R,5R,6R)-3,4,5-трис-бензилокси-6-бензилоксиметилтетрагидропиран-2-ил)бензил]хроман,
56) (2S,3R,4R,5S,6R)-2-(3-хроман-6-илметил-4-циклопропилфенил)-6-гидроксиметилтетрагидропиран-3,4,5-триол,
57) [(2R,3R,4R,5S,6S)-3,4,5-триацетокси-6-[4-бром-3-(2,3-дигидро-1,4-бензодиоксин-6-илметил)фенил]тетрагидропиран-2-ил]метилацетат,
58) [(2R,3R,4R,5S,6S)-3,4,5-триацетокси-6-[4-бром-3-(2,3-дигидро-1,4-бензодиоксин-6-илметил)фенил]тетрагидропиран-2-ил]метилацетат,
59) (2R,3R,4R,5S)-3,4,5-триацетокси-6-[4-циклопропил-3-(2,3-дигидробензо[1,4]диоксин-6-илметил)фенил]тетрагидропиран-2-илметиловый эфир уксусной кислоты,
60) (2S,3R,4R,5S,6R)-2-[4-циклопропил-3-(2,3-дигидробензо[1,4]диоксин-6-илметил)фенил]-6-гидроксиметилтетрагидропиран-3,4,5-триол,
61) (2R,3R,4R,5S)-3,4,5-триацетокси-6-[3-(2,3-дигидробензо[1,4]диоксин-6-илметил)-4-этилфенил]тетрагидропиран-2-илметиловый эфир уксусной кислоты,
62) (2S,3R,4R,5S,6R)-2-[3-(2,3-дигидробензо[1,4]диоксин-6-илметил)-4-этилфенил]-6-гидроксиметилтетрагидропиран-3,4,5-триол,
63) 4-бензил-6-[2-бром-5-((2S,3S,4R,5R,6R)-3,4,5-трис-бензилокси-6-бензилоксиметилтетрагидропиран-2-ил)бензил]-3,4-дигидро-2Н-бензо[1,4]оксазин,
64) 4-бензил-6-[2-циклопропил-5-((2S,3S,4R,5R,6R)-3,4,5-трис-бензилокси-6-бензилоксиметилтетрагидропиран-2-ил)бензил]-3,4-дигидро-2Н-бензо[1,4]оксазин,
65) (2S,3R,4R,5S,6R)-2-[4-циклопропил-3-(3,4-дигидро-2H-бензо[1,4]оксазин-6-илметил)фенил]-6-гидроксиметилтетрагидропиран-3,4,5-триол,
66) (2S,3R,4R,5S,6R)-2-[3-(3,4-дигидро-2Н-бензо[1,4]оксазин-6-илметил)-4-этилфенил]-6-гидроксиметилтетрагидропиран-3,4,5-триол,
67) (2S,3R,4R,5S,6R)-2-[2-(3,4-дигидро-2Н-бензо[1,4]оксазин-6-илметил)-4'-метилбифенил-4-ил]-6-гидроксиметилтетрагидропиран-3,4,5-триол,
68) (2S,3R,4R,5S,6R)-2-[3-(4-бензил-3,4-дигидро-2Н-бензо[1,4]оксазин-6-илметил)-4-изопропилфенил]-6-гидроксиметилтетрагидропиран-3,4,5-триол,
69) (2S,3R,4R,5S,6R)-2-[3-(3,4-дигидро-2H-бензо[1,4]оксазин-6-илметил)-4-изопропилфенил]-6-гидроксиметилтетрагидропиран-3,4,5-триол,
70) (2S,3R,4R,5S,6R)-2-[3-(1-бензил-1,2,3,4-тетрагидрохинолин-7-илметил)-4-изопропилфенил]-6-гидроксиметилтетрагидропиран-3,4,5-триол,
71) (2R,3S,4R,5R,6S)-2-гидроксиметил-6-[4-изопропил-3-(1,2,3,4-тетрагидрохинолин-7-илметил)фенил]тетрагидропиран-3,4,5-триол,
72) (2R,3S,4R,5R,6S)-2-гидроксиметил-6-[4-изопропил-3-(1,2,3,4-тетрагидрохинолин-6-илметил)фенил]тетрагидропиран-3,4,5-триол.
2. Соединение, представляющее собой (2S,3R,4R,5S,6R)-2-[4-хлор-3-(3,4-дигидро-2Н-бензо[1,4]-оксазин-6-илметил)фенил]-6-гидроксиметилтетрагидропиран-3,4,5-триол, имеющее следующую структурную формулу:
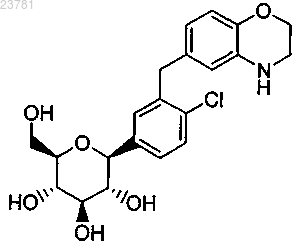
или его фармацевтически приемлемая соль.
3. Соединение, представляющее собой (2S,3R,4R,5S,6R)-2-[4-циклопропил-3-(2,3-дигидробензо[1,4]диоксин-6-илметил)фенил]-6-гидроксиметилтетрагидропиран-3,4,5-триол, имеющее следующую структурную формулу:
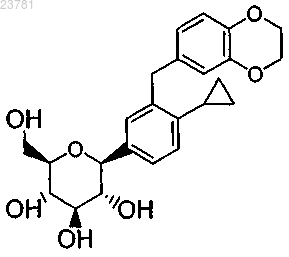
или его фармацевтически приемлемая соль.
4. Соединение, представляющее собой (2S,3R,4R,5S,6R)-2-[3-(2,3-дигидробензо[1,4]диоксин-6-илметил)-4-этилфенил]-6-гидроксиметилтетрагидропиран-3,4,5-триол, имеющее следующую структурную формулу:
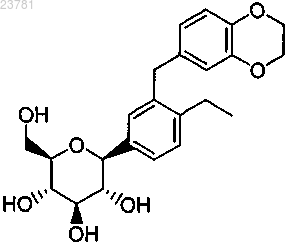
или его фармацевтически приемлемая соль.
5. Соединение по п.1, представляющее собой (2R,3S,4R,5R,6S)-2-гидроксиметил-6-[4-изопропил-3-(1,2,3,4-тетрагидрохинолин-7-илметил)фенил]тетрагидропиран-3,4,5-триол, имеющее следующую структурную формулу:
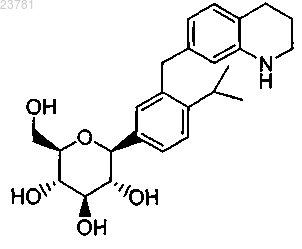
или его фармацевтически приемлемая соль.
6. Способ лечения диабета, включающий введение нуждающемуся в этом субъекту соединения по любому из пп.1-5 или его фармацевтически приемлемой соли.
7. Способ лечения заболевания или патологического состояния, опосредуемого натрийзависимым сопереносчиком D-глюкозы, у млекопитающего, включающий введение нуждающемуся в этом млекопитающему соединения по п.1 или его фармацевтически приемлемой соли в терапевтически эффективном количестве, где заболеванием или патологическим состоянием является диабет, синдром X, резистентность к инсулину, ухудшенная переносимость глюкозы, ожирение, дислипидемия, гипертензия, микроальбуминемия и осложнения при диабете.
Текст
Изобретение относится к соединениям, описываемым общей структурной формулой (I) ниже, в которой значения радикалов являются такими, что они соответствуют конкретным соединениям(1)-(72), как они определены в описании, которые применимы для лечения заболеваний и патологических состояний, опосредуемых натрийзависимым сопереносчиком D-глюкозы (SGLT),например диабета. Изобретение также относится к способам лечения таких заболеваний и патологических состояний. Описываются также композиции и т.п., предназначенные для лечения упомянутых заболеваний. Уровень техники Сахарный диабет является метаболическим нарушением, характеризующимся рецидивирующей или стойкой гипергликемией (повышенное содержание глюкозы в крови) и другими признаками, и это отличает его от отдельного заболевания или патологического состояния. Нарушения содержания глюкозы могут привести к тяжелым длительным осложнениям, которые включают сердечно-сосудистое заболевание, хроническую почечную недостаточность, поражение сетчатки, поражение нерва (нескольких типов), поражение капилляров и ожирение. Диабет типа 1, также известный как инсулинозависимый сахарный диабет (IDDM), характеризуется утратой продуцирующих инсулин -клеток островков Лангерганса поджелудочной железы, что приводит к недостатку инсулина. Диабет типа 2, ранее известный как диабет, возникающий у взрослых, диабет,возникающий в зрелом возрасте, или инсулиннезависимый сахарный диабет (NIDDM), возникает в результате комбинации повышенной выработки глюкозы печенью, дефектной секреции инсулина и резистентности к инсулину или пониженной чувствительности к инсулину (дефектная чувствительность тканей к инсулину). Хроническая гипергликемия также может привести к возникновению или прогрессированию токсичности глюкозы, характеризующейся снижением выработки инсулина -клетками, чувствительности к инсулину; в результате этого самопроизвольно обостряется сахарный диабет [Diabetes Care, 1990, 13, 610]. Хроническое повышенное содержание глюкозы в крови также приводит к поражению кровеносных сосудов. Проблемы, возникающие в результате диабета, подразделяют на группы "микрососудистое заболевание" (вследствие поражения небольших кровеносных сосудов) и "макрососудистое заболевание"(вследствие поражения артерий). Примеры микрососудистого заболевания включают диабетическую ретинопатию, невропатию и нефропатию, тогда как примеры макрососудистого заболевания включают заболевание коронарной артерии, удар, заболевание периферических сосудов и диабетический некроз мышц. Диабетическая ретинопатия, характеризующаяся увеличением количества ослабленных кровеносных сосудов в сетчатке, а также отеком желтого пятна (опухание желтого пятна), может привести к сильной потере зрения или слепоте. Поражение сетчатки (вследствие микроангиопатии) является самой распространенной причиной слепоты у непожилых людей в США. Диабетическая ретинопатия характеризуется нарушенной функцией нервов в нижних конечностях. В сочетании с пораженными кровеносными сосудами диабетическая ретинопатия может привести к диабетической стопе. Могут существовать другие формы диабетической ретинопатии, такие как мононеврит или автономная невропатия. Диабетическая ретинопатия характеризуется поражением почек, что может привести к хронической почечной недостаточности и в конечном счете к необходимости проведения диализа. Сахарный диабет является самой распространенной причиной почечной недостаточности взрослых во всем мире. Известно, что диета с высоким содержанием глюкозы (т.е. диета, которая состоит из пищи, приводящий к повышенному содержанию сахара в плазме после приема пищи) является одним из факторов, способствующих развитию ожирения. Диабет типа 2 характеризуется резистентностью к инсулину и/или нарушенной секрецией инсулина вследствие повышенного содержания глюкозы. Действие лекарственных средств, предназначенных для лечения диабета типа 2, направлено на повышение чувствительности к инсулину (такие как TZD - тиазолидиндионы), выработку глюкозы в печени (такие как бигуаниды), прямое изменение содержания инсулина (такие как инсулин, аналоги инсулина и средства, усиливающие секрецию инсулина), усиление действия гормона инкретина (такие как экзенатид и ситаглиптин) или подавление всасывания глюкозы из пищи (такие как ингибиторы альфа-глюкозидазы) [Nature 2001, 414, 821-827]. Глюкоза не способна диффундировать через клеточную мембрану и нуждается в транспортных белках. Перенос глюкозы в эпителиальные клетки опосредуется вторичной активной системой сопереноса, натрийзависимым сопереносчиком D-глюкозы (SGLT), который стимулируется градиентом натрия,вызванным Na+/K+-АТФазой (аденозинтрифосфатаза). Глюкоза, накопленная в эпителиальных клетках,переносится в кровь через мембрану с помощью диффузии, облегченной переносчиками GLUT [KidneySGLT относится к семейству натрийзависимых сопереносчиков глюкозы SLCA5. Установлено, что две различные изоформы SGLT, SGLT1 и SGLT2 опосредуют реабсорбцию глюкозы в почечных канальцах у людей [Curr. Opinon in Investigational Drugs (2007): 8(4), 285-292 и цитированная в ней литература]. Обе изоформы отличаются разным сродством к субстрату. Несмотря на то что обе изоформы обладают примерно 59% гомологией аминокислотных последовательностей, они являются функционально различными. SGLT1 переносит глюкозу, а также галактозу и экспрессируется в почках и кишечнике, в то время как SGLT2 обнаруживается только в сегментах S1 и S2 проксимального отдела почечных канальцев. Вследствие этого, глюкоза, профильтровавшаяся в почечных клубочках, реабсорбируется в эпителиальных клетках проксимального отдела почечных канальцев с помощью SGLT2, обладающей низким сродством/большой емкостью системой, находящейся на поверхности эпителиальных клеток, выстилающих сегменты S1 и S2 канальцев. Гораздо меньшее количество глюкозы восстанавливается с помощьюSGLT1, обладающей высоким сродством/малой емкостью системой, на более удаленном сегменте про-1 023781 ксимального отдела почечных канальцев. У здорового человека более 99% глюкозы в плазме, профильтровавшейся в почечных клубочках, реабсорбируется, в результате чего менее 1% общего количества профильтровавшейся глюкозы выделяется в мочу. Установлено, что абсорбция 90% от полного количества глюкозы, абсорбирующейся почками, опосредуется с помощью SGLT2; остальные 10%, вероятно,опосредуются с помощью SGLT1 [J. Parenter. Enteral Nutr. 2004, 28, 364-371].SGLT2 клонировали в качестве возможного натрийзависимого сопереносчика глюкозы и по имеющимся данным его распределение в тканях, субстратная специфичность и сродство очень сходны с соответствующими характеристиками обладающего низким сродством натрийзависимого сопереносчика глюкозы в проксимальном отделе почечных канальцев. Лекарственное средство, обладающее таким механизмом воздействия, как ингибирование SGLT2 станет новым средством в дополнение к существующим классам лекарственных средств, предназначенных для лечения диабета и связанных с ним заболеваний у пациентов, нуждающихся в регулировании содержания глюкозы в крови при сохранении секреции инсулина. Кроме того, ингибиторы SGLT2, которые способствуют снижению избытка глюкозы (и тем самым избытка калорий), могут предоставлять дополнительные возможности для лечения ожирения. В действительности, открыты небольшие молекулы-ингибиторы SGLT2, а возможные противодиабетические воздействия таких молекул описаны в литературе [Т-1095 (Diabetes, 1999, 48, 1794-1800),Dapagliflozin (Diabetes, 2008, 57, 1723-1729)]. Различные О-арил- и О-гетероарилгликозиды в качестве ингибиторов SGLT-2 описаны в патентных публикациях, таких как WO 01/74834, WO 03/020737, US 04/0018998, WO 01/68660, WO 01/16147, WO 04/099230, WO 05/011592, US 06/0293252 и WO 05/021566. Различные глюкопиранозилзамещенные ароматические и гетероароматические соединения в качестве ингибиторов SGLT-2 описаны в патентных публикациях, таких как WO 01/27128, WO 04/080990, US 06/0025349, WO 05/085265, WO 05/085237, WO 06/054629 и WO 06/011502.SGLT1 обнаруживается главным образом в кишечнике и играет важную роль в абсорбции Dглюкозы и D-галактозы. Поэтому ингибиторы SGLT1 перспективны для воздействия в почках, а также в кишечнике для уменьшения потребления калорий и гипергликемии. В WO 2004/018491 раскрыты производные пиразола, которые являются ингибиторами SGLT1. Описаны глюкопиранозилзамещенные ароматические и гетероароматические соединения, в которых в большинстве случаев фрагмент сахара модифицирован в положениях С 4, С 5 или С 6 пиранозы (US 06/0009400, US 06/0019948, US 06/0035841, US 06/0074031, US 08/0027014 и WO 08/016132). Описание чертежей На фиг. 1 приведена термограмма, полученная с помощью дифференциальной сканирующей калориметрии, совместного кристалла L-пролина и (2S,3R,4R,5S,6R)-2-[3-(2,3-дигидробензо[1,4]диоксин-6 илметил)-4-этилфенил]-6-гидроксиметилтетрагидропиран-3,4,5-триола состава 1:1, полученного по методике 1; на фиг. 2 приведена порошковая рентгенограмма совместного кристалла L-пролина и(2S,3R,4R,5S,6R)-2-[3-(2,3-дигидробензо[1,4]диоксин-6-илметил)-4-этилфенил]-6-гидроксиметилтетрагидропиран-3,4,5-триола состава 1:1, полученного по методике 1; на фиг. 3 приведена термограмма, полученная с помощью дифференциальной сканирующей калориметрии, совместного кристалла L-пролина и (2S,3R,4R,5S,6R)-2-[3-(2,3-дигидробензо[1,4]диоксин-6 илметил)-4-этилфенил]-6-гидроксиметилтетрагидропиран-3,4,5-триола состава 2:1, полученного по методике 3; На фиг. 4 приведена порошковая рентгенограмма совместного кристалла L-пролина и(2S,3R,4R,5S,6R)-2-[3-(2,3-дигидробензо[1,4]диоксин-6-илметил)-4-этилфенил]-6-гидроксиметилтетрагидропиран-3,4,5-триола состава 2:1, полученного по методике 3. Подробное описание изобретения Изобретение относится к соединениям, которые применимы для лечения заболеваний и патологических состояний, опосредуемых натрийзависимым сопереносчиком D-глюкозы (SGLT), например диабета. Изобретение также относится к способам лечения таких заболеваний и патологических состояний. Изобретение относится к новым гликозидным производным и их фармацевтически приемлемым солям. В настоящем описании раскрываются также способы получения соединений, предлагаемых в настоящем изобретении. Соединения, предлагаемые в настоящем изобретении, обладают ингибирующей активностью по отношению к натрийзависимому сопереносчику D-глюкозы (SGLT) и являются особенно полезными для профилактики, ведения, лечения, регулирования прогрессирования или вспомогательного лечения заболеваний и/или патологических состояний, при которых благоприятно ингибирование SGLT, таких как диабет (включая тип I и тип II), ожирение, дислипидемия, резистентность к инсулину и другие метаболические синдромы и/или осложнения, связанные с диабетом, включая ретинопатию, нефропатию, невропатию, ишемическую болезнь сердца, артериосклероз, нарушение функции -клеток, и в качестве терапевтических и/или профилактических средств, предназначенных для лечения ожирения. Согласно изобретению обнаружены соединения формулы (I), которые применимы для ингибирования SGLT. Соединения согласно настоящему изобретению относятся к общему классу соединений, описываемых общей структурной формулой (I) в которой кольцо А представляет собой С 6-С 10-арил, который необязательно содержит один или большее количество заместителей, независимо выбранных из группы, включающей галоген, гидроксигруппу, цианогруппу, нитрогруппу, C1-С 6-алкил, C2-С 6-алкенил, C2-С 6-алкинил, C1-С 6-алкоксигруппу,галоген-C1-С 6-алкоксигруппу, С 3-С 7-циклоалкил, С 3-С 7-циклоалкил-С 1-С 4-алкил, галоген-C1-С 6-алкил,С 6-С 10-арил, С 6-С 10-арил-С 1-С 4-алкил, -C(O)OR3, -C(O)R3, -C(O)NR4R5, -NR4R5, -CH2NR4R5, C1-С 6 алкоксигруппу, С 3-С 7-циклоалкоксигруппу, -S(O)pR3, -S(O)2NR4R5, -OS(O)2R3, -CH2C(O)OR3,-CH2C(O)NR4R5, -NR3C(O)NR4R5, -NR3C(O)OR3, С 6-С 10-арилоксигруппу, С 2-С 10-гетероциклил, С 2-С 10 гетероциклил-С 1-С 4-алкил,С 1-С 10-гетероарил-С 1-С 4-алкил,С 1-С 10-гетероарил,С 1-С 10-гетероарилоксигруппу и С 1-С 10-гетероциклооксигруппу; где алкильные, алкенильные, алкинильные, циклоалкильные, арильные, гетероциклильные и гетероарильные группы необязательно могут содержать один или большее количество заместителей, выбранных из группы, включающей галоген, гидроксигруппу, циано-S(O)pR3,-C(O)OR3,-C(O)R3,-C(O)NR4R5,-NR4R5,группу,нитрогруппу,C1-С 6-алкил,4 5-CH2NR R и C1-С 6-алкоксигруппу; кольцо А' представляет собой 5-, 6- или 7-членный гетероцикл при условии, что кольцо А' не представляет собой 1,3-диоксол;Ya обозначает связь или (C1-С 6)алкилен, который необязательно содержит один или большее количество заместителей, независимо выбранных из группы, включающей галоген, гидроксигруппу, C1-С 4 алкил, C1-С 4-алкоксигруппу, галоген C1-С 4-алкил;R1, R1a, R1b и R1c независимо выбраны из группы, включающей водород, С 1-С 6-алкил, С 6-С 10-арилС 1-С 4-алкил, -С(О)С 6-С 10-арил и -С(О)С 1-С 6-алкил;R2 в каждом случае независимо выбран из группы, включающей галоген, гидроксигруппу, цианогруппу, нитрогруппу, С 1-С 6-алкил, С 3-С 7-циклоалкил, С 3-С 7-циклоалкил-С 1-С 4-алкил, С 6-С 10-арил, С 6-С 10 арил-С 1-С 4-алкил, -C(O)OR3, -C(O)R3, -C(O)NR4R5, -NR4R5, -CH2NR4R5, С 1-С 6-алкоксигруппу, C3-C7 циклоалкоксигруппу, -S(O)pR3, -S(O)2NR4R5, -OS(O)2R3, -CH2C(O)OR3, -CH2C(O)NR4R5, -NR3C(O)NR4R5,-NR3C(O)OR3, С 6-С 10-арилоксигруппу, С 2-С 10-гетероциклил, C2-C10-гетероциклил-С 1-С 4-алкил, С 1-С 10 гетероарил-С 1-С 4-алкил, С 1-С 10-гетероарил, С 1-С 10-гетероарилоксигруппу и C1-С 10-гетероциклооксигруппу; где, если любой фрагмент R2 представляет собой алкил, циклоалкил, арил, гетероциклил или гетероарил, то в каждом случае он необязательно может содержать один или большее количество заместителей, которые независимо выбраны из группы, включающей галоген, гидроксигруппу, С 1-С 4-алкил и С 1-С 4-алкоксигруппу;R2a в каждом случае независимо выбран из группы, включающей оксогруппу, галоген, гидроксигруппу, цианогруппу, нитрогруппу, C1-С 6-алкил, С 3-С 7-циклоалкил, С 3-С 7-циклоалкил-С 1-С 4-алкил,С 6-С 10-арил, С 6-С 10-арил-С 1-С 4-алкил, -C(O)OR3, -C(O)R3, -C(O)NR4R5, -NR4R5, -CH2NR4R5, C1-С 6 алкоксигруппу, C3-C7-циклоалкоксигруппу, -S(O)pR3, -S(O)2NR4R5, -OS(O)2R3, -CH2C(O)OR3,-CH2C(O)NR4R5, -NR3C(O)NR4R5, -NR3C(O)OR3, С 6-С 10-арилоксигруппу, С 2-С 10-гетероциклил, С 2-С 10 гетероциклил-С 1-С 4-алкил, С 1-С 10-гетероарил-С 1-С 4-алкил, С 1-С 10-гетероарил, С 1-С 10-гетероарилоксигруппу и С 1-С 10-гетероциклооксигруппу; где, если любой фрагмент R2a представляет собой алкил, циклоалкил, арил, гетероциклил или гетероарил, то в каждом случае он необязательно может содержать один или большее количество заместителей, которые независимо выбраны из группы, включающей галоген,гидроксигруппу, цианогруппу, нитрогруппу, С 1-С 6-алкил, -S(O)pR3, -C(O)OR3, -C(O)R3, -C(O)NR4R5,-NR4R5, -CH2NR4R5 и С 1-С 6-алкоксигруппу; или два R2a, находящиеся у соседних атомов, вместе с атомами, с которыми они связаны, могут образовать конденсированный С 3-С 7-циклоалкил, С 6-арил, 3-7-членный гетероциклил или 5- или 6-членный гетероарил, где конденсированный циклоалкил, арил, гетероциклил и гетероарил необязательно может содержать один или большее количество заместителей, независимо выбранных из группы, включающей галоген, гидроксигруппу, С 1-С 4-алкил и С 1-С 4-алкоксигруппу; или два R2a, находящиеся у одного атома углерода, вместе с ним могут образовать спиросочлененный 37-членный гетероциклил или спиросочлененный С 3-С 7-циклоалкил, который необязательно может содержать один или большее количество заместителей, независимо выбранных из группы, включающей галоген, гидроксигруппу, С 1-С 4-алкил и С 1-С 4-алкоксигруппу; иR3 в каждом случае независимо выбран из группы, включающей водород, С 1-С 6-алкил, С 3-С 7-3 023781R6 и R7 в каждом случае независимо выбраны из водорода, С 1-С 6-алкила, OR1e и NR4R5; или, если t равно 1, то R6 и R7 вместе могут образовать оксогруппу,или, если R6 и R7 находятся у одного атома углерода, то вместе они могут образовать С 3-С 7 циклоалкил или 3-7-членный гетероцикл;R1e в каждом случае независимо выбран из группы, включающей водород, С 1-С 6-алкил, С 6-С 10-арилС 1-С 4-алкил, -С(О)С 6-С 10-арил и -С(О)С 1-С 6-алкил;R4 и R5 в каждом случае независимо выбраны из группы, включающей водород, C1-С 6-алкил, С 3-С 7 циклоалкил, С 3-С 7-циклоалкил-С 1-С 4-алкил, С 6-С 10-арил-С 1-С 4-алкил, С 6-С 10-арил, С 1-С 10-гетероарил,С 1-С 10-гетероарил-С 1-С 4-алкил, С 2-С 10-гетероциклил и С 2-С 10-гетероциклил-С 1-С 4-алкил; илиR4 и R5 вместе с атомом азота, с которыми они связаны, могут образовать моноциклический или бициклический гетероарил или гетероциклил, который необязательно может быть замещен одним или более галогеном или С 1-С 4-алкилом; или его фармацевтически приемлемая соль. При этом объектом настоящего изобретения являются конкретные соединения из числа соединений 1-72, приведенных ниже, или их фармацевтически приемлемые соли. 1. (2S,3R,4R,5S,6R)-2-[4-Хлор-3-(4-метил-3,4-дигидро-2H-бензо[1,4]-оксазин-7-илметил)фенил]-6 гидроксиметилтетрагидропиран-3,4,5-триол. 2. (2S,3R,4R,5S,6R)-2-[4-Хлор-3-(4-этил-3,4-дигидро-2 Н-бензо[1,4]оксазин-7-илметил)фенил]-6-гидроксиметилтетрагидропиран-3,4,5-триол. 3. (2S,3R,4R,5S,6R)-2-[4-Хлор-3-(4-циклопропил-3,4-дигидро-2 Н-бензо[1,4]оксазин-7-илметил)фенил]-6-гидроксиметилтетрагидропиран-3,4,5-триол. 4. (2S,3R,4R,5S,6R)-2-[3-(4-Бензил-3,4-дигидро-2 Н-бензо[1,4]оксазин-6-илметил)-4-хлорфенил]-6 гидроксиметилтетрагидропиран-3,4,5-триол. 5.(2R,3R,4R,5S)-3,4,5-Триацетокси-6-[4-циклопропил-3-(2,3-дигидробензо[1,4]диоксин-6-илметил)фенил]тетрагидропиран-2-илметиловый эфир уксусной кислоты. 60. (2S,3R,4R,5S,6R)-2-[4-Циклопропил-3-(2,3-дигидробензо[1,4]диоксин-6-илметил)фенил]-6-гидроксиметилтетрагидропиран-3,4,5-триол. 61. (2R,3R,4R,5S)-3,4,5-Триацетокси-6-[3-(2,3-дигидробензо[1,4]диоксин-6-илметил)-4-этилфенил] тетрагидропиран-2-илметиловый эфир уксусной кислоты. 62. (2S,3R,4R,5S,6R)-2-[3-(2,3-Дигидробензо[1,4]диоксин-6-илметил)-4-этилфенил]-6-гидроксиметилтетрагидропиран-3,4,5-триол. 63. 4-Бензил-6-[2-бром-5-2S,3S,4R,5R,6R)-3,4,5-трис-бензилокси-6-бензилоксиметилтетрагидропиран-2-ил)бензил]-3,4-дигидро-2 Н-бензо[1,4]оксазин. 64. 4-Бензил-6-[2-циклопропил-5-2S,3S,4R,5R,6R)-3,4,5-трис-бензилокси-6-бензилоксиметилтетрагидропиран-2-ил)бензил]-3,4-дигидро-2 Н-бензо[1,4]оксазин. 65. (2S,3R,4R,5S,6R)-2-[4-Циклопропил-3-(3,4-дигидро-2 Н-бензо[1,4]оксазин-6-илметил)фенил]-6 гидроксиметилтетрагидропиран-3,4,5-триол. 66. (2S,3R,4R,5S,6R)-2-[3-(3,4-Дигидро-2 Н-бензо[1,4]оксазин-6-илметил)-4-этилфенил]-6-гидроксиметилтетрагидропиран-3,4,5-триол. 67. (2S,3R,4R,5S,6R)-2-[2-(3,4-Дигидро-2 Н-бензо[1,4]оксазин-6-илметил)-4-метилбифенил-4-ил]-6 гидроксиметилтетрагидропиран-3,4,5-триол. 68. (2S,3R,4R,5S,6R)-2-[3-(4-Бензил-3,4-дигидро-2 Н-бензо[1,4]оксазин-6-илметил)-4-изопропилфенил]-6-гидроксиметилтетрагидропиран-3,4,5-триол. 69. (2S,3R,4R,5S,6R)-2-[3-(3,4-Дигидро-2 Н-бензо[1,4]оксазин-6-илметил)-4-изопропилфенил]-6-гидроксиметилтетрагидропиран-3,4,5-триол. 70. (2S,3R,4R,5S,6R)-2-[3-(1-Бензил-1,2,3,4-тетрагидрохинолин-7-илметил)-4-изопропилфенил]-6 гидроксиметилтетрагидропиран-3,4,5-триол. 71. (2R,3S,4R,5R,6S)-2-Гидроксиметил-6-[4-изопропил-3-(1,2,3,4-тетрагидрохинолин-7-илметил)фенил]тетрагидропиран-3,4,5-триол. 72. (2R,3S,4R,5R,6S)-2-Гидроксиметил-6-[4-изопропил-3-(1,2,3,4-тетрагидрохинолин-6-илметил)фенил]тетрагидропиран-3,4,5-триол. Более предпочтительно, если соединением является соединение примера 8 или его фармацевтически приемлемая соль. Более предпочтительно, если соединением является соединение примера 60 или его фармацевтически приемлемая соль. Более предпочтительно, если соединением является соединение примера 62 или его фармацевтически приемлемая соль. Более предпочтительно, если соединением является соединение примера 71 или его фармацевтически приемлемая соль. При использовании в настоящем изобретении термины "соединение, предлагаемое в настоящем изобретении" и "соединение формулы (I)" и т.п. включают их фармацевтически приемлемые производные и полиморфные формы, изомеры и их изотопно-меченые варианты. Фармацевтически приемлемые производные. Термин "фармацевтически приемлемое производное" включает любую фармацевтически приемлемую соль, сольват или гидрат соединения формулы (I). Фармацевтически приемлемые соли. Термин "фармацевтически приемлемая соль" включает соли, полученные из фармацевтически приемлемых нетоксичных кислот или оснований, включая неорганические и органические кислоты и основания. Соединения формулы (I), содержащие основные группы, например аминогруппу, могут образовывать фармацевтически приемлемые соли присоединения с кислотами. В одном варианте осуществления фармацевтически приемлемые соли присоединения с кислотами соединений формулы (I) включают, но не ограничиваются только ими, соли с неорганическими кислотами, такими как галогенводородные кислоты (например, хлористоводородная, бромистоводородная и йодистоводородная кислота), серная кислота, азотная кислота и фосфорная кислота. В одном варианте осуществления фармацевтически прием-6 023781 лемые соли присоединения с кислотами соединений формулы (I) включают, но не ограничиваются только ими, соли с органическими кислотами, такими как выбранные из классов алифатических ароматических, карбоновых и сульфоновых органических кислот, примеры которых включают алифатические монокарбоновые кислоты, такие как муравьиная кислота, уксусная кислота, пропионовая кислота или масляная кислота; алифатические гидроксикислоты, такие как молочная кислота, лимонная кислота, винная кислота или яблочная кислота; дикарбоновые кислоты, такие как малеиновая кислота или янтарная кислота; ароматические карбоновые кислота, такие как бензойная кислота, п-хлорбензойная кислота, фенилуксусная кислота, дифенилуксусная кислота или трифенилуксусная кислота; ароматические гидроксикислоты, такие как о-гидроксибензойная кислота, п-гидроксибензойная кислота, 1-гидроксинафталин-2 карбоновая кислота или 3-гидроксинафталин-2-карбоновая кислота; и сульфоновые кислоты, такие как метансульфоновая кислота, этансульфоновая кислота или бензолсульфоновая кислота. Другие фармацевтически приемлемые соли присоединения с кислотами соединений формулы (I) включают, но не ограничиваются только ими, соли с гликолевой кислотой, глюкуроновой кислотой, фуранкарбоновой кислотой,глутаминовой кислотой, антраниловой кислотой, салициловой кислотой, миндальной кислотой, эмбоновой (памовой) кислотой, пантотеновой кислотой, стеариновой кислотой, сульфаниловой кислотой, альгиновой кислотой и галактуроновой кислотой. Соединения формулы (I), содержащие кислотные группы, например карбоксигруппу, могут образовывать фармацевтически приемлемые соли присоединения с основаниями. В одном варианте осуществления приемлемые соли присоединения с основаниями соединений формулы (I) включают, но не ограничиваются только ими, соли металлов, такие как соли щелочных металлов или соли щелочно-земельных металлов (например, соли натрия, калия, магния или кальция) и соли цинка и алюминия. В одном варианте осуществления фармацевтически приемлемые соли присоединения с основаниями соединений формулы (I) включают, но не ограничиваются только ими, соли с аммиаком или фармацевтически приемлемыми органическими аминами или гетероциклическими основаниями, такими как этаноламины (например, диэтаноламин), бензиламины, N-метилглюкамин, аминокислоты (например, лизин) или пиридин. Также можно получить гемисоли кислот и оснований, например гемисульфат. Фармацевтически приемлемые соли соединений формулы (I) можно получить по методикам, хорошо известным в данной области техники. Обзор фармацевтически приемлемых солей приведен в публикации Stahl and Wermuth, Handbook ofPharmaceutical Salts: Properties, Selection and Use (Wiley-VCH, Weinheim, Germany, 2002). Сольваты и гидраты. Соединения, предлагаемые в настоящем изобретении, могут находиться в несольватированных и сольватированных формах. Термин "сольват" включает молекулярные комплексы, содержащие соединение, предлагаемое в настоящем изобретении, и одну или большее количество молекул фармацевтически приемлемого растворителя, такого как вода или С 1-С 6-спирты, например этанола. Термин "гидрат" означает "сольват", в котором растворителем является вода. Таким образом, соединения, предлагаемые в настоящем изобретении, могут находиться в форме гидрата, включая моногидрат, дигидрат, полугидрат,сесквигидрат, тригидрат, тетрагидрат и т.п., а также соответствующие сольватированные формы. Соединение, предлагаемое в настоящем изобретении, может быть истинным сольватом, а в других случаях соединение, предлагаемое в настоящем изобретении, может просто удерживать некоторое количество воды или являться смесью воды с каким-то дополнительным растворителем. Аморфные и кристаллические формы. Соединения, предлагаемые в настоящем изобретении, могут существовать в твердых состояниях в диапазоне от аморфных до кристаллических форм. Все такие твердые формы входят в объем настоящего изобретения. Формы совместных кристаллов. Соединения, предлагаемые в настоящем изобретении, могут существовать в виде совместных кристаллов. В одном варианте соединения, предлагаемые в настоящем изобретении, существуют в виде совместных кристаллов с L-пролином. Для исключения сомнений отметим, что термины "совместный кристалл L-пролина и соединения,предлагаемого в настоящем изобретении", такой как совместный кристалл L-пролина и(2S,3R,4R,5S,6R)-2-[4-хлор-3-(3,4-дигидро-2 Н-бензо[1,4]оксазин-6-илметил)фенил]-6-гидроксиметилтетрагидропиран-3,4,5-триола, совместный кристалл L-пролина и (2S,3R,4R,5S,6R)-2-[4-циклопропил-3(2,3-дигидробензо[1,4]диоксин-6-илметил)фенил]-6-гидроксиметилтетрагидропиран-3,4,5-триола, совместный кристалл L-пролина и (2S,3R,4R,5S,6R)-2-[3-(2,3-дигидробензо[1,4]диоксин-6-илметил)-4 этилфенил]-6-гидроксиметилтетрагидропиран-3,4,5-триола или совместный кристалл L-пролина и(2R,3S,4R,5R,6S)-2-гидроксиметил-6-[4-изопропил-3-(1,2,3,4-тетрагидрохинолин-7-илметил)фенил]тетрагидропиран-3,4,5-триола, означает все формы, образующиеся в результате взаимодействия между Lпролином и соединением, предлагаемым в настоящем изобретении. В частности, эти термины включают:(i) неионное взаимодействие между L-пролином и соединением, предлагаемым в настоящем изобретении(т.е. когда между L-пролином и соединением, предлагаемым в настоящем изобретении не происходит переноса протона); или (ii) ионное взаимодействие, когда между L-пролином и соединением, предлагаемым в настоящем изобретении происходит перенос протона с образованием соли соединения, предлагаемого в настоящем изобретении с L-пролином, или (iii) комбинации указанных выше взаимодействий (i) и (ii). В предпочтительном варианте совместный кристалл L-пролина образуется при неионном взаимодействии между соединением, предлагаемым в настоящем изобретении и L-пролином (т.е. когда междуL-пролином и соединением, предлагаемым в настоящем изобретении, не происходит переноса протона). В альтернативном варианте совместный кристалл L-пролина представляет собой соль соединения,предлагаемого в настоящем изобретении, с L-пролином. В одном из вариантов рассматривается кристаллическая форма совместного кристалла L-пролина и(2S,3R,4R,5S,6R)-2-[4-хлор-3-(3,4-дигидро-2 Н-бензо[1,4]оксазин-6-илметил)фенил]-6-гидроксиметилтетрагидропиран-3,4,5-триола. В одном из случаев данная кристаллическая форма является неионной. Данная кристаллическая форма по данным дифференциальной сканирующей калориметрии обладает эндотермой, расположенной примерно при 64 С, примерно при 104 С и/или примерно при 157 С. В данной кристаллической форме молярное отношение количества L-пролина к количеству (2S,3R,4R,5S,6R)2-[4-хлор-3-(3,4-дигидро-2 Н-бензо[1,4]оксазин-6-илметил)фенил]-6-гидроксиметилтетрагидропиран 3,4,5-триола может составлять 1:1. В другом случае кристаллическая форма на порошковой рентгенограмме обладает пиком (пиками), расположенным примерно при 19,3, примерно при 23,2, примерно при 17,0 и/или примерно при 5,7 градуса 2. Еще в одном случае кристаллическая форма на порошковой рентгенограмме обладает пиками, в основном такими же, как пики, перечисленные в табл. 1 А. В одном из вариантов рассматривается кристаллическая фора совместного кристалла L-пролина и(2S,3R,4R,5S,6R)-2-[4-циклопропил-3-(2,3-дигидробензо[1,4]диоксин-6-илметил)фенил]-6-гидроксиметилтетрагидропиран-3,4,5-триола. В одном из случаев кристаллическая форма является неионной. В другом случае кристаллическая форма по данным дифференциальной сканирующей калориметрии обладает эндотермой, расположенной примерно при 151 С. В данной кристаллической форме молярное отношение количества(2S,3R,4R,5S,6R)-2-[4-циклопропил-3-(2,3-дигидробензо[1,4]диоксин-6-илметил)фенил]-6-гидроксиметилтетрагидропиран-3,4,5-триола может составлять 1:1. В другом случае кристаллическая форма на порошковой рентгенограмме обладает пиком (пиками),расположенным примерно при 16,7, примерно при 19,9, примерно при 17,6 и/или примерно при 21,9 градуса 2. Еще в одном случае кристаллическая форма на порошковой рентгенограмме обладает пиками, в основном такими же, как пики, перечисленные в табл. 2 А. В одном из вариантов рассматривается кристаллическая форма совместного кристалла L-пролина и(2S,3R,4R,5S,6R)-2-[3-(2,3-дигидробензо[1,4]диоксин-6-илметил)-4-этилфенил]-6-гидроксиметилтетрагидропиран-3,4,5-триола. В одном из случаев кристаллическая форма является неионной. В другом случае кристаллическая форма по данным дифференциальной сканирующей калориметрии обладает эндотермой, расположенной примерно при 136 С. В данной кристаллической форме молярное отношение количества L-пролина к количеству (2S,3R,4R,5S,6R)-2-[3-(2,3-дигидробензо[1,4]диоксин-6-илметил)-4 этилфенил]-6-гидроксиметилтетрагидропиран-3,4,5-триола может составлять 1:1. В другом случае кристаллическая форма на порошковой рентгенограмме обладает пиком (пиками), расположенным примерно при 17,3, примерно при 20,4, примерно при 18,0, примерно при 18,9 и/или примерно при 23,8 градуса 2. В одном объекте кристаллическая форма на порошковой рентгенограмме обладает пиками, в основном такими же, как пики, перечисленные в табл. 3 А. Еще в одном случае кристаллическая форма обладает порошковой рентгенограммой, которая в основном такая же, как порошковая рентгенограмма, приведенная на фиг. 2. В другом случае в кристаллической форме молярное отношение количества L-пролина к количеству(2S,3R,4R,5S,6R)-2-[3-(2,3-дигидробензо[1,4]диоксин-6-илметил)-4-этилфенил]-6-гидроксиметилтетрагидропиран-3,4,5-триола может составлять 2:1. Еще в одном случае кристаллическая форма по данным дифференциальной сканирующей калориметрии обладает эндотермой, расположенной примерно при 176 С. В одном из вариантов рассматривается кристаллическая форма совместного кристалла L-пролина и(2R,3S,4R,5R,6S)-2-гидроксиметил-6-[4-изопропил-3-(1,2,3,4-тетрагидрохинолин-7-илметил)фенил]тетрагидропиран-3,4,5-триола. В одном случае данная кристаллическая форма является неионной. В другом случае кристаллическая форма по данным дифференциальной сканирующей калориметрии обладает эндотермой, расположенной примерно при 156 С и/или примерно при 158 С. В кристаллической форме молярное отношение количества L-пролина к количеству (2R,3S,4R,5R,6S)-2-гидроксиметил-6-[4 изопропил-3-(1,2,3,4-тетрагидрохинолин-7-илметил)фенил]тетрагидропиран-3,4,5-триола может составлять 1:1. Еще в одном случае кристаллическая форма на порошковой рентгенограмме обладает пиками, в основном такими же, как пики, перечисленные в табл. 4. В одном из вариантов рассматривается кристаллическая форма совместного кристалла L-пролина и(2S,3R,4R,5S,6R)-2-[3-(2,3-дигидробензо[1,4]диоксин-6-илметил)-4-этилфенил]-6-гидроксиметилтетрагидропиран-3,4,5-триола. В одном из случаев в кристаллической форме молярное отношение количестваL-пролина к количеству (2S,3R,4R,5S,6R)-2-[3-(2,3-дигидробензо[1,4]диоксин-6-илметил)-4-этилфенил]6-гидроксиметилтетрагидропиран-3,4,5-триола составляет 2:1. В другом случае кристаллическая форма является неионной. Еще в одном случае кристаллическая форма по данным дифференциальной скани-8 023781 рующей калориметрии обладает эндотермой, расположенной примерно при 176 С. В другом случае кристаллическая форма на порошковой рентгенограмме обладает пиком (пиками), расположенным примерно при 6,1, 9,1, 12,8, 15,2, 16,5, 17,8, 18,9, 20,9 и/или 28,4 градуса 2. Еще в одном случае кристаллическая форма обладает порошковой рентгенограммой, которая в основном такая же, как порошковая рентгенограмма, приведенная на фиг. 4. В предыдущих абзацах, в которых определено молярное отношение количества L-пролина к количеству соединения, предлагаемого в настоящем изобретении, в кристаллической форме, выражение "молярное отношение, составляющее примерно 1:1", означает, что в кристаллической форме содержится 0,91,1 моль соединения, предлагаемого в настоящем изобретении, в пересчете на 1 моль L-пролина. Аналогичным образом, "молярное отношение, составляющее примерно 1:2", означает, что в кристаллической форме содержится 0,9-1,1 моль соединения, предлагаемого в настоящем изобретении, в пересчете на 2 моль L-пролина. Когда в настоящем изобретении указано, что рассматривается кристаллическая форма совместного кристалла L-пролина и соединения, предлагаемого в настоящем изобретении, такого как(2S,3R,4R,5S,6R)-2-[4-хлор-3-(3,4-дигидро-2 Н-бензо[1,4]оксазин-6-илметил)фенил]-6-гидроксиметилтетрагидропиран-3,4,5-триол, (2S,3R,4R,5S,6R)-2-[4-циклопропил-3-(2,3-дигидробензо[1,4]диоксин-6-илметил)фенил]-6-гидроксиметилтетрагидропиран-3,4,5-триол, (2S,3R,4R,5S,6R)-2-[3-(2,3-дигидробензо[1,4] диоксин-6-илметил)-4-этилфенил]-6-гидроксиметилтетрагидропиран-3,4,5-триол или (2R,3S,4R,5R,6S)-2 гидроксиметил-6-[4-изопропил-3-(1,2,3,4-тетрагидрохинолин-7-илметил)фенил]тетрагидропиран-3,4,5 триол, то полученное с помощью порошковой рентгенографии подходящее значение степени кристалличности превышает примерно 60%, более подходящее значение превышает примерно 80%, предпочтительное значение превышает примерно 90%. В предыдущих абзацах, в которых определены пики, которыми обладает кристаллическая форма Lпролина и соединения, предлагаемого в настоящем изобретении, на порошковой рентгенограмме, термин"примерно при" означает, что точные значения положений пиков (т.е. перечисленные значения угла 2 тета) не следует считать абсолютными значениями, поскольку, как должны понимать специалисты в данной области техники, точные значения положения пиков могут немного меняться в зависимости от используемого прибора, образца или вследствие небольших изменений условий проведения измерения. В предыдущих абзацах также указано, что кристаллические формы совместного кристалла L-пролина иL-пролина и (2S,3R,4R,5S,6R)-2-[3-(2,3-дигидробензо[1,4]диоксин-6-илметил)-4-этилфенил]-6-гидроксиметилтетрагидропиран-3,4,5-триола состава 2:1 обладают порошковыми рентгенограммами, которые содержат в основном сходные наиболее интенсивные пики (значения угла 2-тета), характеристики которых приведены в таблицах 1 А, 2 А, 3 А, 4 и 5 соответственно; и что совместный кристалл L-пролина и(2S,3R,4R,5S,6R)-2-[3-(2,3-дигидробензо[1,4]диоксин-6-илметил)-4-этилфенил]-6-гидроксиметилтетрагидропиран-3,4,5-триола, обладающий молярным отношением 1:1, обладает порошковой рентгенограммой, которая в основном такая же, как порошковая рентгенограмма, приведенная на фиг. 2,и что совместный кристалл L-пролинаи (2S,3R,4R,5S,6R)-2-[3-(2,3-дигидробензо[1,4]диоксин-6-илметил)-4-этилфенил]-6-гидроксиметилтетрагидропиран-3,4,5-триола, обладающий молярным отношением 2:1, обладает порошковой рентгенограммой, которая в основном такая же, как порошковая рентгенограмма, приведенная на фиг. 4. Следует понимать, что использование в этом контексте термина "в основном" означает, что значения угла 2-тета на порошковой рентгенограмме может немного меняться в зависимости от используемого прибора, образца или вследствие небольших изменений условий проведения измерения, поэтому значения положений пиков, приведенные в таблице или представленные на спектре, также не следует считать абсолютными значениями. В данной области техники известно, что можно получить порошковую рентгенограмму, содержащую, в зависимости от условий проведения измерений (таких как оборудование, приготовление образца или используемый прибор), одну или большее количество погрешностей измерения. В частности, общеизвестно, что значения интенсивности пиков на порошковой рентгенограмме могут колебаться в зависимости от условий проведения измерений и приготовления образца. Например, специалистам в области порошковой рентгенографии следует понимать, что на относительную интенсивность пиков может оказывать влияние, например, размер зерна, составляющий более 30 мкм, и не равные единице отношения размеров, которые могут влиять на анализ образцов. Специалист в данной области техники также должен понимать, что на положение рефлексов может влиять точная высота, на которой образец установлен в дифрактометре, и различия в калибровке нулевого значения в дифрактометре. Также небольшое влияние может оказывать неплоскостность поверхности образца. Следовательно специалист в данной области техники должен понимать, что данные, полученные с помощью порошковой рентгенографии, представленные в настоящем изобретении, не следует считать абсолютными значениями (дополнительная информация приведена в публикации Jenkins R.Snyder R.L. Introduction to X-Ray Powder Diffractometry,John WileySons, 1996). Поэтому следует понимать, что кристаллическая форма совместного кристалла(2S,3R,4R,5S,6R)-2-[4-циклопропил-3-(2,3-дигидробензо[1,4]диоксин-6-илметил)фенил]-6-гидроксиметилтетрагидропиран-3,4,5-триола состава 1:1, совместного кристалла L-пролина и (2S,3R,4R,5S,6R)-2-[3(2,3-дигидробензо[1,4]диоксин-6-илметил)-4-этилфенил]-6-гидроксиметилтетрагидропиран-3,4,5-триола состава 1:1, совместного кристалла L-пролинаи (2R,3S,4R,5R,6S)-2-гидроксиметил-6-[4-изопропил-3(1,2,3,4-тетрагидрохинолин-7-илметил)фенил]тетрагидропиран-3,4,5-триола состава 1:1 и совместного кристалла L-пролина и (2S,3R,4R,5S,6R)-2-[3-(2,3-дигидробензо[1,4]диоксин-6-илметил)-4-этилфенил]-6 гидроксиметилтетрагидропиран-3,4,5-триола состава 2:1, описанные выше, не ограничиваются кристаллами, обладающими порошковыми рентгенограммами, которые содержат идентичные пики, значения которых приведены в таблицах 1 А, 2 А, 3 А, 4 и 5 соответственно, и любые кристаллы, обладающие порошковой рентгенограммой, которая в основном такая же, как порошковая рентгенограмма, приведенная в таблице 1 А, 2 А, 3 А, 4 и 5 соответственно, входят в объем настоящего изобретения. Аналогичным образом, следует понимать, что кристаллическая форма совместного кристалла L-пролина и(2S,3R,4R,5S,6R)-2-[3-(2,3-дигидробензо[1,4]диоксин-6-илметил)-4-этилфенил]-6-гидроксиметилтетрагидропиран-3,4,5-триола, описанные выше, не ограничиваются кристаллами, которые обладают порошковыми рентгенограммами, которые содержат идентичные пики, приведенные на фиг. 2 или 4 соответственно, и любые кристаллы, обладающие порошковой рентгенограммой, которая в основном такая же, как порошковая рентгенограмма, приведенная на фиг. 2 или 4, входят в объем настоящего изобретения. Специалист в области порошковой рентгенографии способен установить, являются ли порошковые рентгенограммы в основном идентичными. Обычно ошибка измерения угла дифракции в порошковой рентгенограмме составляет примерно 2= 0,5 градуса или менее (или, более предпочтительно, примерно 2 = 0,2 градуса или менее), и такое значение погрешности измерения следует принимать во внимание при интерпретации положений пиков,указанных в приведенном выше тексте и табл. 1, 1 А, 2, 2 А, 3, 3 А, 4 и 4 А и спектрах, приведенных на фиг. 2 и 4. Поэтому, если указано, например, что совместный кристалл на порошковой рентгенограмме обладает пиком, расположенным примерно при 2 = 17,3 градуса (или любых других значениях углов,указанных выше), то это можно интерпретировать, как 2 = 17,3 градуса, плюс или минус 0,5 градуса,или 2 = 17,3 градуса плюс или минус 0,2 градуса. Изомерные формы. Соединения, предлагаемые в настоящем изобретении, могут существовать в одной или большем количестве геометрических, оптических, энантиомерных, диастереоизомерных и таутомерных формах,включая, но не ограничиваясь только ими, цис- и трансформы, Е- и Z-формы, R-, S- и мезоформы, кето- и енольные формы. Все такие изомерные формы входят в объем настоящего изобретения. Изомерные формы могут являться чистыми изомерные формами или обогащенными формами, а также смесями изомеров (например, рацемические или диастереоизомерные смеси). Когда это целесообразно, соответствующие изомеры можно выделить из их смесей с помощью известных методик или их модификаций (например, хроматографические методики и методики перекристаллизации). Когда это целесообразно, соответствующие изомеры можно получить с помощью известных методик или их модификаций (например, с помощью асимметрического синтеза). Оптически активные (+) и (-), (R)- и (S)- или (D)- и (L)-изомеры можно получить с использованием хиральных синтонов или хиральных реагентов, или разделить по обычным методикам, таким как ВЭЖХ(высокоэффективная жидкостная хроматография) с использованием хиральной колонки. Если соединения, описанные в настоящем изобретении, содержат олефиновые двойные связи или другие центры геометрической асимметрии и если не указано иное, это означает, что соединения включают геометрические и Е-, и Z-изомеры. Аналогичным образом, в объем настоящего изобретения входят все таутомерные формы."Стереоизомер" означает соединение, состоящее из тех же атомов, связанных теми же связями, но обладающее иной невзаимозаменяемой трехмерной структурой. В объем настоящего изобретения входят различные стереоизомеры и их смеси и входят "энантиомеры", молекулы которых представляют собой не налагающиеся друг на друга зеркальные изображения. Изотопно-меченые соединения. В рамках настоящего изобретения рассматриваются фармацевтически приемлемые изотопномеченые соединения формулы (I), в которой один или большее количество атомов заменены атомами,обладающими таким же атомным номером, но атомной массой или массовым числом, отличающимся от атомной массы или массового числа, обычно встречающихся в природе. Примеры изотопов, подходящих для включения в соединения, предлагаемые в настоящем изобретении, включают изотопы водорода, такие как 2 Н и 3 Н, углерода, такие как 11 С, 13 С и 14 С, хлора, такие как 36Cl, фтора, такие как 18F, йода, такие как 123I и 125I, азота, такие как 13N и 15N, кислорода, такие как 15 О,17 О и 18 О, фосфора, такие как 32 Р, и серы, такие как 35S. Некоторые изотопно-меченые соединения формулы (I), например содержащие радиоактивный изотоп, применимы для исследования распределения лекарственного средства и/или субстрата в тканях. Радиоактивные изотопы 3H и 14 С являются особенно подходящими для этой цели вследствие легкости их включения и простых средств детектирования. Замещение изотопами, испускающими позитроны, такими как 11 С, 18F, 15O и 13N, может быть полезно для изучения занятости рецепторов субстрата с помощью позитронной эмиссионной томографии(ПЭТ). Изотопно-меченые соединения формулы (I) обычно можно получить по обычным методикам, известным специалистам в данной области техники, или по методикам, аналогичным описанным в настоящем изобретении, с использованием подходящего изотопно-меченого реагента вместо использовавшегося ранее немеченого реагента. Определения терапевтических терминов. При использовании в настоящем изобретении "лечение" включает излечивающее и профилактическое лечение. При использовании в настоящем изобретении "пациент" означает животное, предпочтительно млекопитающее, предпочтительно человека, нуждающегося в лечении. Количество соединения, предлагаемого в настоящем изобретении, которое вводят, должно быть терапевтически эффективным количеством в случае применения соединения или его производного для лечения заболевания или патологического состояния и профилактически эффективным количеством в случае применения соединения или его производного для предупреждения заболевания или патологического состояния. Термин "терапевтически эффективное количество" при использовании в настоящем изобретении означает количество соединения, необходимого для лечения или облегчения протекания соответствующего заболевания или патологического состояния. Термин "профилактически эффективное количество" при использовании в настоящем изобретении означает количество соединения, необходимого для предотвращения соответствующего заболевания или патологического состояния. Точная доза обычно зависит от состояния пациента во время введения. Факторы, которые следует принимать во внимание при определении дозы, включают тяжесть болезненного состояния пациента, общее состояние здоровья пациента, возраст, массу тела, пол, диету, время, периодичность и путь введения, комбинации лекарственных средств, чувствительность и переносимость пациентом или реакцию на лечение. Точное количество можно определить по стандартным методикам, но в конечном счете это может находится в компетенции лечащего врача. Обычно эффективная доза составляет от 0,01 мг/кг/сутки (отношение массы лекарственного средства к массе тела пациента) до 1000 мг/кг/сутки, например от 1 до 100 мг/кг/сутки или от 1 до 10 мг/кг/сутки. Композиции можно вводить пациенту по отдельности или их можно вводить в комбинации с другими средствами, лекарственными средствами или гормонами. При использовании в настоящем изобретении термины "заболевание" и "патологическое состояние" могут использоваться взаимозаменяемым образом или они могут различаться тем, что у конкретного расстройства или патологического состояния может не быть известного возбудителя (так что пока не выявлена этиология) и поэтому оно диагностируется не как заболевание, а только как нежелательное состояние или синдром, для которого клиницисты выявили более или менее специфичный набор симптомов. При использовании в настоящем изобретении термин "нарушение" является синонимом термина"патологическое состояние". Лечение заболеваний и патологических состояний. Обнаружено, что соединения формулы (I) являются ингибиторами SGLT. При использовании в настоящем изобретении ингибирование SGLT означает ингибирование только SGLT2, означает ингибирование только SGLT1 или означает ингибирование SGLT1 и SGLT2. Настоящее изобретение относится к соединению формулы (I), пригодному для применения для лечения. Соединение по настоящему изобретениюможет применяться в составе фармацевтической композиции, включающей соединение формулы (I) в комбинации с фармацевтически приемлемым инертным наполнителем. Настоящее изобретение также относится к способу лечения заболевания или патологического состояния, опосредуемого натрийзависимым сопереносчиком D-глюкозы, включающему стадию введения пациенту соединения формулы (I) в терапевтически эффективном количестве. Способность соединений,предлагаемых в настоящем изобретении, ингибировать SGLT можно продемонстрировать с помощью исследований SGLT2 и SGLT1, раскрытых ниже в настоящем изобретении. По данным исследования ингибирования SGLT2 предпочтительные соединения, предлагаемые в настоящем изобретении, характеризуются значением IC50 100 нМ, в одном варианте осуществления 30 нМ, в одном варианте осуществления 20 нМ, в одном варианте осуществления 10 нМ, в другом варианте осуществления 5 нМ, в другом варианте осуществления 1 нМ и в другом варианте осуществления 0,5 нМ. В другом варианте осуществления по данным исследования ингибирования SGLT1 предпочтительные соединения, предла- 11023781 гаемые в настоящем изобретении, характеризуются значением IC5010000 нМ, в одном варианте осуществления 1500 нМ, в одном варианте осуществления 1000 нМ, в одном варианте осуществления 700 нМ, в другом варианте осуществления 500 нМ и в другом варианте осуществления 200 нМ. Настоящее изобретение также относится к способу лечения диабета, включающему введение нуждающемуся в нем субъекту соединения формулы (I). Соединения, предлагаемые в настоящем изобретении, применимы для профилактического и терапевтического лечения заболеваний или патологических состояний, связанных с ингибированием SGLT-2 и SGLT-1. Заболевания или патологические состояния, опосредуемые натрийзависимым сопереносчиком Dглюкозы. Настоящее изобретение применимо для лечения заболевания или нарушения, опосредуемого натрийзависимым сопереносчиком D-глюкозы. Заболевания или патологические состояния, опосредуемые натрийзависимым сопереносчиком D-глюкозы, включают: метаболические нарушения, ретинопатию,нефропатию, диабетическую стопу, язвы, макроангиопатии, метаболический ацидоз или кетоз, реактивную гипогликемию, гиперинсулинемию, нарушение обмена глюкозы, резистентность к инсулину, метаболический синдром (такой как дислипидемия, ожирение, резистентность к инсулину, гипертензия, микроальбуминемия, гиперурикемия и гиперкоагуляция), дислипидимии различного генеза, атеросклероз и родственные заболевания, повышенное артериальное давление, хроническую сердечную недостаточность, отек и гиперурикемию, синдром X, диабет, резистентность к инсулину, ухудшенную переносимость глюкозы (также известную, как нарушенная переносимость глюкозы, IGT), инсулиннезависимый сахарный диабет, диабет типа II, диабет типа I, осложнения при диабете, нарушения, связанные с массой тела, потерю массы тела, заболевания, связанные с нарушением индекса массы тела или с лептином. В одном варианте осуществления заболевания и патологические состояния включают метаболический синдром (такой как дислипидемия, ожирение, резистентность к инсулину, гипертензия, микроальбуминемия), синдром X, диабет, резистентность к инсулину, ухудшенную переносимость глюкозы (также известную, как нарушенная переносимость глюкозы, IGT), инсулиннезависимый сахарный диабет, диабет типа II, диабет типа I, осложнения при диабете. В одном варианте осуществления заболеванием или нарушением является ухудшенная переносимость глюкозы, диабет типа II или ожирение. Другим объектом настоящего изобретения является способ лечения нарушения, выбранного из группы, включающей сахарный диабет типа I или типа II, осложнения при диабете, включающий введение соединения формулы (I) или его фармацевтически приемлемой соли в эффективном количестве. При использовании в настоящем изобретении пациент является страдающим от "ожирения", если у пациента проявляется по меньшей мере один из следующих признаков: индекс массы тела (BMI), т.е. отношение массы тела пациента (кг) к квадрату его роста (м), равен 30 или более; абсолютное значение обхвата талии составляет 102 см для мужчин или 88 см для женщин; отношение обхвата талии к обхвату бедер составляет 0,9 для мужчин или 0,85 для женщин; или количество телесного жира составляет 25% для мужчин или 30% для женщин. При использовании в настоящем изобретении пациент является страдающим от "диабета типа II",если он удовлетворяет критериям Всемирной организации здравоохранения для диагностики диабета(Definition and diagnosis of diabetes mellitus and intermediate hyperglycaemia, WHO, 2006), т.е. если пациент имеет по меньшей мере один из следующих признаков: концентрация глюкозы в плазме натощак составляет 7,0 ммоль/л (126 мг/дл); или концентрация глюкозы в плазме венозной крови составляет 11,1 ммоль/л (200 мг/дл) через 2 ч после перорального приема 75 г глюкозы. При использовании в настоящем изобретении пациент является страдающим от "IGT" если он удовлетворяет критериям Всемирной организации здравоохранения для диагностики IGT (Definition and diagnosis of diabetes mellitus and intermediate hyperglycaemia, WHO, 2006), т.е. если пациент имеет оба следующих признака: концентрация глюкозы в плазме натощак составляет 7,0 ммоль/л (126 мг/дл) и концентрация глюкозы в плазме венозной крови составляет 7,8 и 11,1 ммоль/л (200 мг/дл) через 2 ч после перорального приема 75 г глюкозы. Введение и композиции Общие положения. В фармацевтических целях соединения, предлагаемые в настоящем изобретении, можно вводить в качестве лекарственного средства энтеральным или парентеральным путем, включая внутривенное, внутримышечное, подкожное, чрескожное, введение в дыхательные пути (аэрозоль), пероральное, назальное, ректальное, вагинальное и местное (включая трансбуккальное и сублингвальное) введение. Следует оценить такие биофармацевтические характеристики соединений формулы (I), как растворимость и стабильность раствора (в диапазоне значений рН), проницаемость и т.п., для того чтобы выбрать наиболее подходящую дозированную форму и путь введения для лечения при соответствующих показаниях. Соединения, предлагаемые в настоящем изобретении, можно вводить в виде кристаллических или аморфных продуктов. Соединения, предлагаемые в настоящем изобретении, можно вводить по отдельности или в комбинации с одним или большим количеством других соединений, предлагаемых в настоящем изобретении, или в комбинации с одним или большим количеством других лекарственных средств (или в виде любой их комбинации). Обычно их вводят в виде композиции совместно с одним или большим количеством фармацевтически приемлемых инертных наполнителей. Термин "инертный наполнитель" включает любой ингредиент, не являющийся соединением (соединениями), предлагаемым в настоящем изобретении, который может придавать композиции функциональные (например, регулирование скорости высвобождения лекарственного средства) и/или нефункциональные (например, технологическая добавка или разбавитель) характеристики. Выбор инертного наполнителя во многом будет зависеть от таких факторов, как конкретный режим введения, влияние инертного наполнителя на стабильность и растворимость и тип дозированной формы. При реализации способа лечения по настоящему изобретению может использоваться фармацевтическая композиция, включающая соединение формулы (I) и фармацевтически приемлемый инертный наполнитель. Типичные фармацевтически приемлемые наполнители включают следующие: разбавители, например лактоза, декстроза, сахароза, маннит, сорбит, целлюлоза и/или глицин; смазывающие вещества, например диоксид кремния, тальк, стеариновая кислота, ее магниевая или кальциевая соль и/или полиэтиленгликоль; связующие, например алюмосиликат магния, крахмальная паста, желатин, трагакантовая камедь,метилцеллюлоза, натриевая соль карбоксиметилцеллюлозы и/или поливинилпирролидон; разрыхлители, например крахмалы, агар, альгиновая кислота или ее натриевая соль, или шипучие смеси; и/или абсорбенты, красители, ароматизаторы и/или подсластители. Подробное обсуждение фармацевтически приемлемых наполнителей приведено в публикации Gennaro, Remington: The Science and Practice of Pharmacy 2000, 20th edition (ISBN: 0683306472). Пероральное введение. Соединения, предлагаемые в настоящем изобретении, можно вводить перорально. Пероральное введение может включать проглатывание, при котором соединение попадает в желудочно-кишечный тракт, и/или трансбуккальное, лингвальное или сублингвальное введение, при котором соединение попадает в кровоток непосредственно из полости рта. Композиции, пригодные для перорального введения, включают твердые формы, твердые микрочастицы, полужидкие и жидкие (включая многофазные и дисперсные системы) формы, такие как таблетки; мягкие или твердые капсулы, содержащие множество частиц или наночастицы, жидкости (например,водные растворы), эмульсии или порошки; лепешки (включая заполненные жидкостью); жевательные резинки; гели; быстродиспергирующиеся дозированные формы; пленки; вагинальные суппозитории яйцевидной формы; спреи; и трансбуккальные/прилипающие к слизистой оболочке пластыри. Композиции, пригодные для перорального введения, могут быть созданы для доставки соединений формулы (I) путем немедленного высвобождения или путем замедленного высвобождения, где высвобождение может быть задержанным, импульсным, регулируемым, замедленным или задержанным и замедленным или изменено таким образом, чтобы оптимизировать терапевтическую эффективность указанных соединений. Средства для замедленной доставки соединений известны в данной области техники и включают полимеры для медленного высвобождения, которые можно приготовить вместе с указанными соединениями для регулирования их высвобождения. Примеры полимеров для замедленной доставки включают разлагающиеся и неразлагающиеся полимеры, которые можно использовать для высвобождения указанных соединений путем диффузии или комбинации диффузии и разложения полимера. Примеры полимеров для замедленной доставки включают гидроксипропилметилцеллюлозу, гидроксипропилцеллюлозу, метилцеллюлозу, этилцеллюлозу, натриевую соль карбоксиметилцеллюлозы, поливиниловый спирт, поливинилпирролидон, ксантановую камедь, полиметакрилаты, полиэтиленоксид и полиэтиленгликоль. Жидкие композиции (включая многофазные и дисперсные системы) включают эмульсии, суспензии, растворы, сиропы и эликсиры. Такие композиции могут присутствовать в качестве наполнителей в мягких или твердых капсулах (приготовленных, например, из желатина или гидроксипропилметилцеллюлозы) и обычно включают носитель, например воду, этанол, полиэтиленгликоль, пропиленгликоль,метилцеллюлозу или подходящее масло, и один или большее количество эмульгирующих агентов и/или суспендирующих агентов. Жидкие композиции также можно приготовить путем восстановления твердого вещества, например, из пакетика-саше. Соединения, предлагаемые в настоящем изобретении, также можно использовать в быстрорастворяющихся, быстроразлагающихся дозированных формах, таких как описанные в публикации Liang andChen, Expert Opinion in Therapeutic Patents 2001, 11(6): 981-986. Композиции таблеток описаны в публикации Н. Lieberman and L. Lachman, Pharmaceutical Dosage Парентеральное введение. Соединения, предлагаемые в настоящем изобретении, можно вводить парентерально. Соединения, предлагаемые в настоящем изобретении, можно вводить непосредственно в кровоток,в подкожные ткани, в мышцу или во внутренний орган. Подходящие пути введения включают внутривенное, внутриартериальное, внутриоболочечное, внутрижелудочковое, внутриуретральное, надчревное,внутричерепное, внутримышечное, внутрисуставное и подкожное. Подходящие устройства для введения включают устройства для введения с иглой (включая устройства для введения с микроиглой), шприцы без иглы и устройства для вливания. Парентеральные композиции обычно представляют собой водные или масляные растворы. Если раствор является водным, то он содержит инертные наполнители, такие как сахара (включая, но не ограничиваясь только ими, глюкозу, маннит, сорбит и т.п.), соли, углеводы и буферные агенты (предпочтительно, обеспечивающие значение рН, равное от 3 до 9), но для некоторых случаев применения может быть более предпочтительно, если композиции приготовлены в виде стерильных неводных растворов или в виде высушенных форм для применения в сочетании с подходящим разбавителем, таким как стерильная апирогенная вода (вода для инъекций). Парентеральные композиции могут включать имплантаты, полученные из разлагающихся полимеров, таких как сложные полиэфиры (т.е. полимолочная кислота, полилактид, сополимер лактида с гликолидом, поликапролактон, полигидроксибутират), полиортоэфиры и полиангидриды. Такие композиции можно вводить через хирургический надрез в подкожные ткани, в мышечные ткани или непосредственно в конкретные органы. Приготовление парентеральных композиций в стерильных условиях, например с путем лиофилизации, можно легко осуществить с помощью обычных фармацевтических методик, хорошо известных специалистам в данной области техники. Растворимость соединений формулы (I), использующихся для приготовления парентеральных растворов, можно увеличить путем использования соответствующих методик приготовления композиций,таких как введение сорастворителей и/или улучшающих растворимость агентов, таких как поверхностноактивные вещества, мицеллярные структуры и циклодекстрины. Ингаляционное и внутриназальное введение. Соединения, предлагаемые в настоящем изобретении, можно вводить внутриназально или путем ингаляции, обычно в форме сухого порошка (по отдельности или в виде смеси, например в виде сухой смеси с лактозой или в виде смеси с частицами компонентов, например в виде смеси с фосфолипидами,такими как фосфатидилхолин) с помощью сухого порошкового ингалятора, в виде распыляемого аэрозоля с помощью находящегося под давлением контейнера, насоса, разбрызгивателя, атомизатора (предпочтительно атомизатора с использованием электрогидродинамического устройства для получения мелкодисперсного тумана), или распылителя с добавлением или без добавления подходящего пропеллента,такого как 1,1,1,2-тетрафторэтан или 1,1,1,2,3,3,3-гептафторпропан, или в виде капель для носа. Для внутриназального применения порошок может содержать биоадгезивный агент, например хитозан или циклодекстрин. Находящийся под давлением контейнер, насос, разбрызгиватель, атомизатор или распылитель содержит раствор или суспензию соединения (соединений), предлагаемого в настоящем изобретении,включающую, например, этанол, водный раствор этанола или альтернативный агент, подходящий для диспергирования, растворения или улучшения высвобождения активного ингредиента, пропеллент (пропелленты) в качестве растворителя и необязательно поверхностно-активное вещество, такое как сорбитантриолеат, олеиновая кислота или олигомолочная кислота. В композиции сухого порошка или суспензии перед применением лекарственный продукт микронизируют с получением частиц с размером, подходящим для доставки путем ингаляции (обычно менее 5 мкм). Это можно осуществить с помощью соответствующей методики измельчения, такой как размол на спиральной струйной мельнице, размол струйной мельнице с псевдоожиженным слоем, обработку в надкритической жидкости с получением наночастиц, гомогенизация при высоком давлении или распылительная сушка. Капсулы (приготовленные, например, из желатина или гидроксипропилметилцеллюлозы), блистеры и картриджи для применения в ингаляторе или устройстве для вдувания порошков могут быть приготовлены с включением порошкообразной смеси соединения, предлагаемого в настоящем изобретении, подходящей порошкообразной основы, такой как лактоза или крахмал, и модификатора воздействия, такого как L-лейцин, маннит или стеарат магния. Лактоза может быть безводной или в форме моногидрата,предпочтительно последнее. Другие подходящие инертные наполнители включают декстран, глюкозу,мальтозу, сорбит, ксилит, фруктозу, сахарозу и трегалозу. Композиции для ингаляционного/внутриназально введения могут быть приготовлены в виде композиций немедленного и/или модифицированного высвобождения с использованием, например, сополимера гликолевой и молочной кислоты. Композиции модифицированного высвобождения включают композиции задержанного, замедленного, импульсного, регулируемого, адресного и программированного высвобождения. Чрескожное введение. Композиции, подходящие для чрескожного введения, включают терапевтически эффективное количество соединения, предлагаемого в настоящем изобретении, с носителем. Предпочтительные носители включают впитывающиеся фармакологически приемлемые растворители, предназначенные для содействия прохождению через кожу пациента. Обычно чрескожные устройства представляют собой повязку,включающую изнаночный слой, резервуар, содержащий соединение необязательно с носителями, необязательно регулирующий скорость барьерный элемент для доставки соединения в кожу пациента с регулируемой и заранее заданной скоростью в течение продолжительного периода времени и средства для закрепления устройства на коже. Комбинированная терапия. Соединение формулы (I), предлагаемое в настоящем изобретении, для применения в терапии можно эффективно объединять с другим фармакологически активным соединением или с двумя или большим количеством других фармакологически активных соединений. Например, соединение формулы (I) или его фармацевтически приемлемую соль, определенную выше, можно вводить одновременно, последовательно или по отдельности в комбинации с одним или большим количеством средств, предназначенных для лечения перечисленных выше нарушений. Терапевтические средства, которые являются подходящими для такой комбинации, включают, например, противодиабетические средства, такие как метформин, сульфонилмочевины (например, глибенкламид, толбутамид, глимепирид), натеглинид, репаглинид, тиазолидиндионы (например, розиглитазон, пиоглитазон), агонисты и антагонисты PPAR-гамма (например, Gl 262570), модуляторы PPARгамма/альфа (например, KRP 297), ингибиторы альфа-глюкозидазы (например, акарбоза, воглибоза), ингибиторы DPP-IV (например, LAF237, MK-431), альфа-2-антагонисты, инсулин и аналоги инсулина,GLP-1 и аналоги GLP-1 (например, эксендин-4) или амилин. Перечень также включает ингибиторы протенитирозинфосфатазы 1, вещества, влияющие на дерегуляцию продуцирования глюкозы в печени, такие как, например, ингибиторы глюкозо-6-фосфатазы или фруктозо-1,6-бисфосфатазы, гликогенфосфорилазы, антагонисты глюкагонового рецептора и ингибиторы фосфоенолпируваткарбоксикиназы, гликогенсинтазыкиназы или пируватдегидрогеназы, средства, снижающие содержание липидов в крови, такие как, например, ингибиторы HMG-CoA-редуктазы (например, симвастатин, аторвастатин), фибраты (например, безафибрат, фенофибрат), никотиновую кислоту и ее производные, агонисты PPAR-альфа, агонисты PPAR-дельта, ингибиторы АСАТ (например, авасимиб) или ингибиторы всасывания холестерина,такие как, например, эзетимиб, связывающие желчные кислоты вещества, такие как, например, холестирамин, ингибиторы подвздошного транспорта желчных кислот, соединения, повышающие содержание липопротеинов высокой плотности в крови, такие как ингибиторы СЕТР или регуляторы АВС 1, или активные вещества, предназначенные для лечения ожирения, такие как сибутрамин или тетрагидролипстатин, дексфенфлурамин, аксокин, антагонисты каннбиноидного рецептора 1, антагонисты рецептора МСН-1, агонисты рецептора МС 4, антагонисты NPY5 или NPY2 или 3-агонисты, такие как SB-418790 или AD-9677 и агонисты рецептора 5 НТ 2 с. Кроме того, являются подходящими комбинации с лекарственными средствами, влияющими на повышенное артериальное давление, хроническую сердечную недостаточность или атеросклероз, такими как, например, антагонисты А-II (ангиотензин II) или ингибиторы АСЕ, ингибиторы ЕСЕ, диуретики, блокаторы, антагонисты Са, обладающие центральным действием гипотензивные средства, антагонисты альфа-2-адренорецептора, ингибиторы нейтральной эндопептидазы, ингибиторы агрегации тромбоцитов и другие или их комбинации. Примерами антагонистов рецептора ангиотензина II являются кандесартан,цилексетил, калий-лосартан, эпросартанмезилат, валсартан, телмисартан, ирбесартан, ЕХР-3174,L-158809, ЕХР-3312, олмесартан, медоксомил, тазосартан, KT-3-671, GA-0113, RU-64276, EMD-90423,BR-9701 и т.п. Антагонисты рецептора ангиотензина II преимущественно используются для лечения или предупреждения повышенного артериального давления и осложнений при диабете, часто в сочетании с диуретиком, таким как гидрохлортиазид. Для лечения или предупреждения подагры применимы комбинации с ингибиторами синтеза мочевой кислоты или средствами, способствующими выведению из организма мочевой кислоты. Для лечения или предупреждения осложнений при диабете можно использовать комбинации с антагонистами GABA-рецептора, блокаторами Na-каналов, топираматом, ингибиторами протеинкиназы С,ингибиторами конечных продуктов гликозилирования или ингибиторами альдозоредуктазы. Такие комбинации могут обеспечивать значительные преимущества при лечении, включая синергетическую активность. Таким образом, могут использоваться фармацевтические композиции, включающие соединение формулы (I) в терапевтически эффективном количестве в комбинации с инсулином, производным или миметиком инсулина; средством, усиливающим секрецию инсулина; лигандом инсулинотропного рецептора сульфонилмочевины; лигандом PPAR; сенсибилизатором воздействия инсулина; бигуанидом; ингибиторами альфа-глюкозидазы; GLP-1, аналогом или миметиком GLP-1; ингибитором DPPIV; ингибитором HMG-CoA-редуктазы; ингибитором скваленсинтазы; лигандом FXR или LXR; холестирамином; фибратами; никотиновой кислотой или аспирином в терапевтически эффективном количестве. В другом варианте может использоваться продукт, включающий соединение формулы (I) и средство, выбранное из группы, включающей инсулин, производное или миметик инсулина; средство, усиливающее секрецию инсулина; лиганд инсулинотропного рецептора сульфонилмочевины; лиганд PPAR; сенсибилизатор воздействия инсулина; бигуанид; ингибиторы альфа-глюкозидазы; GLP-1, аналог или миметик GLP-1; ингибитор DPPIV; ингибитор HMG-CoA-редуктазы; ингибитор скваленсинтазы; лиганд FXR или LXR; холестирамин; фибраты; никотиновую кислоту и аспирин, предназначенный для одновременного, раздельного или последовательного применения в терапии. Химические определения. При использовании в настоящем изобретении термин "алкил" означает полностью насыщенный разветвленный или неразветвленный углеводородный фрагмент. Предпочтительно, если алкил включает от 1 до 20 атомов углерода, более предпочтительно от 1 до 16 атомов углерода, от 1 до 10 атомов углерода, от 1 до 6 атомов углерода или от 1 до 4 атомов углерода. Типичные примеры алкила включают, но не ограничиваются только ими, метил, этил, н-пропил, изопропил, н-бутил, втор-бутил, изобутил, третбутил, н-пентил, изопентил, неопентил, н-гексил, 3-метилгексил, 2,2- диметилпентил, 2,3 диметилпентил, н-гептил, н-октил, н-нонил или н-децил."Алкилен" означает линейную или разветвленную двухвалентную углеводородную цепь, состоящую только из атомов углерода и водорода, содержащую от 1 до 12 атомов углерода, предпочтительно от 1 до 6 атомов углерода, и присоединенную к остальной части молекулы или к радикальной группе. Примеры алкиленовых групп включают метилен, этилен, пропилен, н-бутилен и т.п. Алкилен присоединен к остальной части молекулы ординарной связью и к радикальной группе ординарной связью. Присоединение алкилена к остальной части молекулы и к радикальной группе может происходить через 1 атом углерода или через любые 2 атома углерода цепи."Галоген" может означать фтор, хлор, бром или йод. Термин "алкенил" означает одновалентный углеводород, содержащий по меньшей мере одну двойную углерод-углеродную связь. Термин "С 2-С 6-алкенил" означает одновалентный углеводород, содержащий от 2 до 6 атомов углерода и содержащий по меньшей мере одну двойную углерод-углеродную связь. Термин "алкинил" означает одновалентный углеводород, содержащий по меньшей мере одну тройную углерод-углеродную связь. Термин "С 2-С 6-алкинил" означает одновалентный углеводород, содержащий от 2 до 6 атомов углерода и содержащий по меньшей мере одну тройную углерод-углеродную связь. При использовании в настоящем изобретении термин "алкоксигруппа" означает алкил-О-, где алкил определен выше в настоящем изобретении. Типичные примеры алкоксигрупп включают, но не ограничиваются только ими, метоксигруппу, этоксигруппу, пропоксигруппу, 2-пропоксигруппу, бутоксигруппу, трет-бутоксигруппу, пентилоксигруппу, гексилоксигруппу, циклопропилоксигруппу, циклогексилоксигруппу и т.п. Предпочтительно, если алкоксигруппы содержат примерно 1-6, более предпочтительно примерно 1-4 атома углерода. Алкильные группы, алкенильные группы, алкинильные группы и алкоксигруппы, содержащие необходимое количество атомов углерода, могут быть неразветвленными или разветвленными. Необходимое количество атомов углерода может быть представлено, как C1-C6-, C1-C4- и т.п. Термин "арил" означает моноциклические или бициклические ароматические углеводородные группы, содержащие в кольцевом фрагменте 6-10 атомов углерода. Неограничивающие примеры включают фенил и нафтил. Термин "арил" также означает группу, в которой арильное кольцо сконденсировано с одним или большим количеством циклоалкильных или гетероциклических колец, где радикал или положение присоединения находится на арильном кольце. Неограничивающие примеры включают 2,3-дигидро-1 Нинден, 1,2,3,4-тетрагидронафтил и 3,4-дигидро-2 Н-бензо[b][1,4]оксазинил. Термин "арилалкил" означает арильную группу, которая связана с другим фрагментом с помощью алкильной группы, которая может быть разветвленной или неразветвленной. Примеры арилалкильных групп включают бензил, 2-фенилэтил, 2-(нафт-2-ил)-бутан-1-ил и т.п. Термин "арилоксигруппа" означает арильную группу, которая связана с другим фрагментом с помощью атома кислорода, такую как феноксигруппа. При использовании в настоящем изобретении термин "гетероциклил" означает необязательно замещенное насыщенное или ненасыщенное неароматическое кольцо или кольцевую систему, например,которая представляет собой 4-, 5-, 6-или 7-членную моноциклическую, 7-, 8-, 9-, 10-, 11- или 12-членную бициклическую или 10-, 11-, 12-, 13-, 14- или 15-членную трициклическую кольцевую систему и содержит по меньшей мере один гетероатом, выбранный из группы, включающей О, S и N, где N и S необязательно могут быть окислены до различных состояний окисления. Гетероциклическая группа может быть присоединена через гетероатом или атом углерода. Гетероциклил может включать конденсированные или мостиковые кольца, а также спироциклические кольца. Примеры гетероциклов включают дигидрофуранил, [1,3]диоксолан, 1,4-диоксан, 1,4-дитиан, пиперазинил, 1,3-диоксолан, имидазолидинил, имида- 16023781 золинил, пирролидин, дигидропиран, оксатиолан, дитиолан, 1,3-диоксан, 1,3-дитианил, оксатианил, тиоморфолинил, оксиранил, азиридинил, оксетанил, азетидинил, тетрагидрофуранил, пирролидинил, тетрагидропиранил, пиперидинил, морфолинил, пиперазинил, азепинил, оксапинил, оксазепинил и диазепинил. При использовании в настоящем изобретении термин "циклоалкил" означает насыщенные или частично ненасыщенные (но неароматические) моноциклические, бициклические или трициклические углеводородные группы, содержащие 3-12 атомов углерода, предпочтительно 3-9 или 3-7 атомов углерода. Типичные моноциклические углеводородные группы включают, но не ограничиваются только ими, циклопропил, циклобутил, циклопентил, циклопентенил, циклогексил или циклогексенил. Типичные бициклические углеводородные группы включают борнил, декагидронафтил, бицикло[2.1.1]гексил, бицикло[2.2.1]гептил,бицикло[2.2.1]гептенил,6,6-диметилбицикло[3.1.1]гептил,2,6,6-триметилбицикло[3.1.1]гептил или бицикло[2.2.2]октил. Типичные трициклические углеводородные группы включают адамантил. Термин "гетероциклооксигруппа" означает гетероциклил, который связана с другим фрагментом с помощью атома кислорода, например пиперазин-2-илоксигруппу. При использовании в настоящем изобретении термин "гетероарил" означает 5-14-членную моноциклическую или бициклическую, или полициклическую ароматическую кольцевую систему, содержащую от 1 до 8 гетероатомов, выбранных из группы, включающей N, О и S. Предпочтительно, если гетероарил представляет собой 5-10-членную или 5-7-членную кольцевую систему. Примеры моноциклических гетероарильных групп включают пиридил, тиенил, фуранил, пирролил, пиразолил, имидазолил,оксазолил, изоксазолил, тиазолил, изотиазолил, триазолил, оксадиазолил, тиадиазолил и тетразолил. Примеры бициклических гетероарильных групп включают индолил, бензофуранил, хинолил, изохинолил индазолил, индолинил, изоиндолил, индолизинил, бензамидазолил и хинолинил. Термин "гетероарил" также означает группу, в которой гетероароматическое кольцо сконденсировано с одним или большим количеством циклоалкильных или гетероциклических колец, где радикал или положение присоединения находится в гетероароматическом кольце. Неограничивающие примеры включают 5,6,7,8-тетрагидрохинолин и 6,7-дигидро-5 Н-пирроло[3,2-d]пиримидин. Гетероарильная группа может быть моно-, би-, три- или полициклической, предпочтительно моно-,би- или трициклической, более предпочтительно моно-или бициклической. Термин "гетероарилалкил" означает гетероарильную группу, которая связана с другим фрагментом с помощью алкильной группы, которая может быть разветвленной или неразветвленной. Примеры гетероарилалкильных групп включают 2-(пиридин-3-ил)-этил, 3-(хинолин-7-ил)-бутан-1-ил и т.п. Термин "гетероарилоксигруппа" означает гетероарильную группу, которая связана с другим фрагментом с помощью атома кислорода, такую как пиридин-3-илоксигруппа. Подразумевается, что "гетероарил" и "гетероциклил" также включают системы с окисленными атомами S или N, такие как сульфинил, сульфонил и N-оксид третичного кольцевого атома азота. Если явно не указано иное, в случаях, когда комбинацию групп в настоящем изобретении называют, как один фрагмент, например арилалкилом, то последняя упомянутая в названии группа содержит атом, с помощью которого фрагмент присоединен к остальной части молекулы."Аминогруппа" при использовании в настоящем изобретении означает -NH2. Термин "N(алкил)аминогруппа" означает аминогруппу, в которой один атом водорода заменен алкильной группой. Например, N-(С 1-С 6-алкил)аминогруппа означает аминогруппу, в которой один из атомов водорода заменен алкильной группой, содержащей от 1 до 6 атомов углерода. Термин "N,N-ди-(алкил)аминогруппа" означает аминогруппу, в которой оба атома водорода заменены алкильными группами, которые могут быть одинаковыми или разными. Например, N,N-ди-(С 1-С 6-алкил)аминогруппа означает аминогруппу, в которой оба атома водорода заменены алкильными группами, которые могут быть одинаковыми или разными и содержащими от 1 до 6 атомов углерода."Карбамоильная" группа при использовании в настоящем изобретении означает -C(O)NH2. Термин"N-(алкил)-карбамоил" означает карбамоильную группу, в которой один атом водорода заменен алкильной группой. Например, N-(С 1-С 6-алкил)-карбамоил означает карбамоильную группу, в которой один из атомов водорода заменен алкильной группой, содержащей от 1 до 6 атомов углерода. Термин "N,N-ди(алкил)-карбамоил" означает карбамоильную группу, в которой оба атома водорода заменены алкильными группами, которые могут быть одинаковыми или разными. Например, N,N-ди-(С 1-С 6-алкил)карбамоил означает карбамоильную группу, в которой оба атома водорода заменены алкильными группами, которые могут быть одинаковыми или разными и содержащими от 1 до 6 атомов углерода. Термин "алканоил" означает группу формулы -C(O)-R, в которой R обозначает алкильную группу. Например, С 1-С 6-алканоил означает алканоильную группу, которая содержит от 1 до 6 атомов углерода,такую как ацетил, изопропилкарбонил и т.п. Общие положения. В термин "включающий" входит "содержащий", а также "состоящий из", например композиция,"включающая" X, может состоять только из X или может включать еще что-то дополнительно, например,X + Y. Выражение "в основном" не исключает "полностью", например композиция, которая "в основном не содержит" Y может совсем не содержать Y. При необходимости выражение "в основном" можно исключить из определений, приведенных в настоящем изобретении. Термин "примерно" по отношению к численному значению х означает, например, х 10%. Когда это является подходящим, термины, использующиеся в единственном числе, включают множественное число и наоборот. Если явно не указано, что группа "является замещенной" или "необязательно может быть замещенной", то следует понимать, что группа является незамещенной."Необязательно" или "необязательный" означает, что описанное после этого событие или обстоятельства могут осуществиться или не осуществиться и что описание включает случаи, когда указанное событие или обстоятельства осуществляются, и случаи, когда событие или обстоятельства не осуществляются. Например, "необязательно замещенный арил" означает, что арильный радикал может быть и может не быть замещенным и что описание включает и замещенные арильные радикалы, и арильные радикалы, которые не замещены. Синтез. В объеме настоящего описания только легко удаляемая группа, которая не является компонентом конкретных конечных искомых соединений, предлагаемых в настоящем изобретении, называется "защитной группой", если в контексте не указано иное. Защита функциональных групп такими защитными группами, сами защитные группы и реакции их отщепления описаны, например, в стандартных справочниках, таких как, например, J.F.W. McOmie, "Protective Groups in Organic Chemistry", Plenum Press, London and New York 1973. Соли соединений, предлагаемых в настоящем изобретении, содержащие по меньшей мере одну солеобразующую группу, можно получить по известным методикам. Например, соли соединений, предлагаемых в настоящем изобретении, содержащих кислотные группы, можно получить, например, путем обработки этих соединений соединениями металлов, такими как соли щелочных металлов подходящих органических карбоновых кислот, например, натриевой солью 2-этилгексановой кислоты; органическими соединениями щелочных металлов или щелочно-земельных металлов, такими как соответствующие гидроксиды, карбонаты или гидрокарбонаты, такие как гидроксид, карбонат или гидрокарбонат натрия или калия, соответствующими соединениями кальция или аммиаком или подходящим органическим амином, предпочтительно использовать стехиометрические количества или небольшой избыток солеобразующего реагента. Соли присоединения с кислотами соединений, предлагаемых в настоящем изобретении, получают обычным образом, например, путем обработки соединений кислотой или подходящим ионообменным реагентом. Внутренние соли соединений, предлагаемых в настоящем изобретении, содержащих кислотную и основную солеобразующие группы, например свободную карбоксигруппу и свободную аминогруппу, можно получить, например, путем нейтрализации солей, таких как соли присоединения с кислотами, до изоэлектрической точки, например, слабыми основаниями или путем обработки ионообменниками. Соли можно обычным образом превратить в свободные соединения; соли металлов и аммония можно превратить, например, путем обработки подходящими кислотами и соли присоединения с кислотами, например, путем обработки подходящим основным реагентом. Смеси изомеров, получаемые в контексте настоящего изобретения, можно разделить по известной методике на отдельные изомеры; диастереоизомеры можно разделить, например, путем распределения в многофазной смеси растворителей, перекристаллизацией и/или с помощью хроматографического разделения, например, на силикагеле, или, например, с помощью жидкостной хроматографии среднего давления на колонке с обращенной фазой, и рацематы можно разделить, например, путем образования солей с оптически чистыми солеобразующими реагентами, и получаемую таким образом смесь диастереоизомеров разделить, например, с помощью фракционной кристаллизации или с помощью хроматографии на колонках с оптически активными веществами. Промежуточные и конечные продукты можно обработать и/или очистить по стандартным методикам,например, с помощью хроматографических методик, методик распределения, (пере)кристаллизации и т.п. Приведенное ниже в целом относится ко всем способам, указанным выше и ниже в настоящем изобретении. Все стадии способа, описанные выше, можно выполнить при известных условиях проведения реакций, включая специально указанные, при отсутствии или обычно в присутствии растворителей или разбавителей, включая, например, растворители или разбавители, которые инертны по отношению к используемым реагентам и растворяют их, при отсутствии или в присутствии катализаторов, конденсирующих реагентов или нейтрализующих реагентов, например, ионообменников, таких как катионообменники, например, в Н форме, в зависимости от природы реакции и/или реагентов при пониженной,нормальной или повышенной температуре, например при температуре в диапазоне от примерно -100 до примерно 190 С; включая, например, от примерно -80 до примерно 150 С, например от -80 до 60 С, при комнатной температуре, от -20 до 40 С или при температуре кипения используемого растворителя, при атмосферном давлении или в закрытом сосуде, когда это целесообразно, то под давлением и/или в инертной атмосфере, например в атмосфере аргона или азота. На всех стадиях реакций образующиеся смеси изомеров можно разделить на отдельные изомеры,например диастереоизомеры или энантиомеры, или на любую необходимую смесь изомеров, например рацематы или смеси диастереоизомеров, например, по методикам, аналогичным описанным в разделе"Дополнительные стадии способа". Растворители, из числа которых можно выбрать растворители, которые являются подходящими для любой конкретной реакции, включают указанные специально или, например, воду, сложные эфиры, такие как (низш.) алкил-(низш.) алканоаты, например этилацетат; простые эфиры, такие как алифатические простые эфиры, например диэтиловый эфир, или циклические простые эфиры, например тетрагидрофуран или диоксан, жидкие ароматические углеводороды, такие как бензол или толуол, спирты, такие как метанол, этанол или 1- или 2-пропанол, нитрилы, такие как ацетонитрил, галогенированные углеводороды, такие как метиленхлорид или хлороформ, амиды кислот, такие как диметилформамид или диметилацетамид, основания, такие как гетероциклические азотистые основания, например пиридин или Nметилпирролидин-2-он, ангидриды карбоновых кислот, такие как ангидриды (низш.) алкановых кислот,например уксусный ангидрид, циклические, линейные или разветвленные углеводороды, такие как циклогексан, гексан или изопентан, или смеси этих растворителей, например водные растворы, если в описании способов не указано иное. Такие смеси растворителей также можно использовать при обработке,например, с помощью хроматографии или распределения. Соединения, включая их соли, также можно получить в виде гидратов или их кристаллы могут, например, включать растворитель, применяющийся для кристаллизации. Могут содержаться разные кристаллические формы. Настоящее изобретение также относится к таким вариантам осуществления способа, в которых соединение, получаемое на любой стадии способа в качестве промежуточного продукта, применяется в качестве исходного вещества, а затем выполняются остальные стадии способа, или в которых исходное вещество образуется при условиях проведения реакции или применяется в виде производного, например,в защищенной форме или в форме соли, или соединение, получаемое способом, предлагаемым в настоящем изобретении, получают при условиях проведения реакции и затем обрабатывают in situ. Все исходные вещества, структурные фрагменты, реагенты, кислоты, основания, дегидратирующие реагенты, растворители и катализаторы, использующиеся для синтеза соединений, предлагаемых в настоящем изобретении, имеются в продаже или их можно получить по методикам органического синтеза,известным специалисту с общей подготовкой в данной области техники (Houben-Wey14th Ed. 1952,Methods of Organic Synthesis, Thieme, Volume 21). Обычно соединения формулы (I) можно получить в соответствии с приведенными ниже схемами. Методика получения. Другим объектом настоящего изобретения является способ получения соединения формулы (I). На приведенных ниже схемах представлены общие пути синтеза соединений формулы (I). В реакциях, приведенных на представленных ниже в настоящем изобретении схемах, любую содержащуюся реакционноспособную группу, такую как гидроксигруппа, аминогруппа, карбонильная группа или иминогруппа,на время проведения реакции можно защитить с помощью обычных защитных групп, таких как триметилсилильная, трет-бутилдиметилсилильная, бензильная, ацетальная, кетальная и т.п., которые отщепляют после проведения реакции. Схема 1 Соединения формулы (II), в которой Lg обозначает отщепляющуюся группу, такую как галоген, и все другие символы являются такими, как определено в настоящем изобретении, можно ввести в реакцию с алкиллитием или алкилмагнием и получить соединения формулы (III), в которой М выбран из группы, включающей галогенид Li или Mg, и все другие символы являются такими, как определено в настоящем изобретении. Соединения формулы (III) можно ввести в реакцию с соединениями формулы(IV), в которой все символы являются такими, как определено в настоящем изобретении. Полученный промежуточный продукт можно дегидроксилировать/деалкоксилировать с использованием такого реагента, как смесь триэтилсилан/эфират BF3, и получить соединения формулы (I), в которой все символы являются такими, как определено в настоящем изобретении. Соединения формулы (III), в которой М выбран из группы, включающей галогенид Li или Mg, и все другие символы являются такими, как определено в настоящем изобретении, можно ввести в реакцию с соединениями формулы (V), в которой Lg обозначает отщепляющуюся группу, такую как галоген, мезилат, тозилат или трифторметансульфонил, и все другие символы являются такими, как определено в настоящем изобретении, и получить соединения, в которых все символы являются такими, как определено в настоящем изобретении. Схема 3 Соединения формулы (VI), в которой Lg обозначает отщепляющуюся группу, такую как галоген, и все другие символы являются такими, как определено в настоящем изобретении, можно ввести в реакцию с алкиллитием или алкилмагнием и получить соединения формулы (VII), в которой М выбран из группы, включающей галогенид Li или Mg, и все другие символы являются такими, как определено в настоящем изобретении. Соединения формулы (VII) можно ввести в реакцию с соединениями формулы(VIII), в которой все символы являются такими, как определено в настоящем изобретении. Полученный промежуточный продукт можно дегидроксилировать с использованием такого реагента, как смесь триэтилсилан/эфират BF3 или Pd-C, в атмосфере водорода и получить соединения, в которых все символы являются такими, как определено в настоящем изобретении. Схема 4 Соединения формулы (IX), в которой все символы являются такими, как определено в настоящем изобретении, можно ввести в реакцию с кислотой формулы (X) или соответствующим хлорангидридом этой кислоты, в которой все символы являются такими, как определено в настоящем изобретении. Реакцию можно провести в присутствии кислоты Льюиса с последующей обработкой промежуточного кетона смесью триэтилсилан/эфират BF3 и получить соединения, в которых все символы являются такими, как определено в настоящем изобретении. Схема 5 Соединения формулы (XI), в которой R11 выбран из группы, включающей водород, алкил, ацил,трифторметансульфонил, и все символы являются такими, как определено в настоящем изобретении,можно циклизовать с использованием OR11 и получить соединения формулы (I), в которой кольцо А' со- 20023781 держит по меньшей мере один атом О и все другие символы являются такими, как определено в настоящем изобретении. Соединения формулы (I) можно получить из других соединений формулы (I) по методикам, хорошо известным специалисту в данной области техники. Схема 6 Соединения формулы (XII), в которой Lg обозначает отщепляющуюся группу, такую как галоген или трифлат, и все другие символы являются такими, как определено в настоящем изобретении, можно подвергнуть превращению при условиях реакции сочетания Судзуки или при условиях реакции сочетания Бухвальда и получить соединения формулы (I), в которой кольцо А содержит по меньшей мере один заместитель, и все другие символы являются такими, как определено в настоящем изобретении. Кольцо А' может образоваться до или после проведения реакции сочетания Судзуки из OR11 , как показано на схеме 5. Промежуточный продукт (II) Соединения формулы (IIa), в которой Lg обозначает отщепляющуюся группу, такую как галоген, и остальные переменные являются такими, как определено в настоящем изобретении, можно ввести в реакцию с соединениями формулы (IIb), в которой М выбран из группы, включающей галогенид лития или магния, и все другие символы являются такими, как определено в настоящем изобретении. Полученный промежуточный продукт можно дегидроксилировать/деалкоксилировать с использованием такого реагента, как смесь триэтилсилан/эфират BF3, или при условиях реакции гидрирования и получить соединения формулы (II), в которой все символы являются такими, как определено в настоящем изобретении. Соединения формулы (IIc), в которой Lg обозначает отщепляющуюся группу, такую как галоген, Z выбран из группы, включающей ОН, NH2 или SH, и остальные переменные являются такими, как определено в настоящем изобретении, можно ввести в реакцию с соединениями формулы (IId), в которой все символы являются такими, как определено в настоящем изобретении и получить промежуточный продукт (II), в которой все символы являются такими, как определено в настоящем изобретении. Реакцию можно провести в присутствии основания. Соединения формулы (IIe), в которой Lg обозначает отщепляющуюся группу, такую как галоген, и остальные символы являются такими, как определено в настоящем изобретении, можно ввести в реакцию с соединениями формулы (IIf) в которой Z выбран из группы, включающей ОН, NH2 или SH, и все другие символы являются такими, как определено в настоящем изобретении получить промежуточный продукт (II), в котором символы являются такими, как определено в настоящем изобретении. Реакцию можно провести в присутствии основания. Карбоновую кислоту формулы (IIg) или соответствующий галогенангидрид кислоты, в которой Lg обозначает отщепляющуюся группу, такую как галоген, и кольцо А является таким, как определено в настоящем изобретении, можно ввести в реакцию с соединениями формулы (IIh), в которой все символы являются такими, как определено в настоящем изобретении, и получить промежуточный продукт (II), в котором все символы являются такими, как определено в настоящем изобретении. Реакцию можно провести в присутствии кислоты Льюиса с последующей обработкой промежуточного кетона смесью три- 21023781 этилсилан/эфират BF3 или при условиях реакции гидрирования. Промежуточный продукт (VIII) и (X) Соединения формулы (VIIIa), в которой все символы являются такими, как определено в настоящем изобретении, можно ввести в реакцию с соединениями формулы (VIIIb), в которой М выбран из группы,включающей галогенид лития или магния, и получить промежуточный продукт формулы (VIIIc), который можно дегидроксилировать/деалкоксилировать с использованием такого реагента, как смесь триэтилсилан/эфират BF3 или Pd-C, в атмосфере водорода и получить соединения формулы (VIIId). Соединения формулы (VIIId) можно окислить и получить альдегид формулы (VIII), который можно дополнительно окислить, и получить кислоту формулы (X). Реакции окисления можно провести по методикам,известным из литературы. Соединения формулы (VIIIa), в которых все символы являются такими, как определено в настоящем изобретении, можно ввести в реакцию с кеталем формулы (VIIIe), в которой М выбран из группы,включающей галогенид лития или магния, и получить соединение формулы (VIIIf), которое можно дегидроксилировать/деалкоксилировать с использованием такого реагента, как смесь триэтилсилан/эфиратBF3 или Pd-C, в атмосфере водорода и получить соединения формулы (VIIIg). У соединения формулы(VIIIg) можно удалить защитную группу и получить альдегид формулы (VIII), который можно окислить,и получить кислоту формулы (X). Реакцию окисления можно провести по методикам, известным из литературы. Следует понимать, что способы, подробно описанные выше и ниже в настоящем изобретении,предназначены только для иллюстрации настоящего изобретения и их не следует рассматривать в качестве ограничивающих. Способы, в которых используются сходные или аналогичные реагенты и/или условия, известные специалисту в данной области техники, также можно использовать для получения соединения, предлагаемого в настоящем изобретении. Любые полученные смеси конечных продуктов или промежуточных продуктов на основе различий физико-химических характеристик компонентов можно по известным методикам разделить на чистые конечные продукты или промежуточные продукты, например, с помощью хроматографии, перегонки,фракционной кристаллизации или путем образования соли, если это при данных условиях представляется подходящим или возможным. Приведенные ниже примеры предназначены для иллюстрации настоящего изобретения и их не следует считать ограничивающими. Если не указано иное, все выпаривания проводят при пониженном давлении. Структуру конечных продуктов, промежуточных продуктов и исходных веществ подтверждают с помощью стандартных аналитических методов, например, с помощью микроанализа, измерения температуры плавления (tпл.) и спектроскопических методик, например МС (масс-спектроскопия), ИК (инфракрасная спектроскопия) и ЯМР (ядерный магнитный резонанс). Использованы аббревиатуры, обычно применяющиеся в данной области техники.(N,N-диметилформамид) (10 мл) при 0 С добавляли трет-бутоксид калия (2,81 г, 25,16 ммоль). После перемешивания в течение 5 мин добавляли метилйодид (3,54 г, 25,16 ммоль) и реакционную смесь перемешивали в течение еще 3 ч. Реакцию останавливали путем добавления воды и смесь экстрагировали этилацетатом (302 мл). Органический слой промывали водой (20 мл) и выпаривали и получали неочищенный продукт, 2,2 г. Стадия II. При перемешивании к раствору 4-метил-4 Н-бензо[1,4]оксазин-3-она (2,18 г, 13,37 ммоль) в ТГФ (тетрагидрофуран) (5 мл) при комнатной температуре добавляли комплекс борантетрагидрофуран (4,02 г, 46,8 ммоль). После перемешивания раствора в течение 2 ч реакционную смесь кипятили с обратным холодильником в течение 4 ч. После завершения превращения реакцию останавливали путем добавления МеОН (10 мл) и растворители выпаривали. Полученный остаток экстрагировали этилацетатом (302 мл) и органический слой промывали водой (20 мл), рассолом (20 мл) и растворитель выпаривали и получали 4-метил-3,4-дигидро-2 Н-бензо[1,4]оксазин, 2,0 г. МС (ЭР (электрораспыление m/z 150,2 (М+1). Промежуточный продукт 2 Стадия I. При перемешивании к суспензии LiAlH4 (7,6 г, 201 ммоль) в ТГФ при 0 С добавляли 4 Нбензо[1,4]оксазин-3-он (15 г, 100 ммоль) в 30 мл ТГФ и перемешивали при комнатной температуре в течение 4 ч. После охлаждения избыток LiAlH4 нейтрализовывали путем добавления EtOAc с последующим добавлением водного раствора NH4C1. Остаток фильтровали через слой целита и фильтрат концентрировали. Остаток разбавляли водой и экстрагировали этилацетатом (200 мл 2), объединенный органический слой промывали водой (100 мл) и рассолом (100 мл). Выпаривание растворителя давало 3,4 дигидро-2 Н-бензо[1,4]оксазин (12 г), который использовали на следующей стадии без обработки.MC (ЭР) m/z 136 (М+1). Стадия II. При перемешивании к раствору 3,4-дигидро-2 Н-бензо[1,4]оксазина (4,0 г, 29,6 ммоль) в ДМФ (20 мл) добавляли карбонат калия (10,22 г, 74,0 ммоль). После перемешивания в течение 5 мин добавляли йодэтан (3,5 мл, 44,4 ммоль) и нагревали при 60 С в течение ночи. Реакционную смесь охлаждали до комнатной температуры, реакцию останавливали путем добавления воды (20 мл), смесь экстрагировали этилацетатом (325 мл). Органический слой промывали водой (30 мл), рассолом (30 мл), сушили над сульфатом натрия, концентрировали и очищали с помощью колоночной хроматографии на силикагеле и получали 4-этил-3,4-дигидро-2 Н-бензо[1,4]оксазин (2,7 г). 1 Н ЯМР (400 МГц, CD3OD):1,10 (t, J = 6,8 Гц, 3 Н), 3,26-3,33 (m, 4H), 4,16 (t, J = 4,4 Гц, 2 Н), 4,40 Стадия I. При перемешивании к раствору 3,4-дигидро-2 Н-бензо[1,4]оксазина (5 г, 37,0 ммоль) в ДМФ (20 мл) при 0 С добавляли трет-бутоксид калия (6,22 г, 55,55 ммоль). После перемешивания в течение 5 мин добавляли бромциклопропан (4,44 мл, 55,55 ммоль) и реакционную смесь перемешивали при комнатной температуре в течение еще 4 ч. Реакцию останавливали путем добавления воды и смесь экстрагировали этилацетатом (502 мл). Органический слой промывали водой (20 мл), концентрировали и очищали с помощью колоночной хроматографии на силикагеле и получали 4-циклопропил-3,4 дигидро-2 Н-бензо[1,4]оксазин (4,42 г).(92 мл) при 0 С добавляли 2-бромизобутирилбромид (11,4 мл, 9,17 ммоль), затем триэтиламин (12,7 мл,9,2 ммоль) и реакционную смесь перемешивали при 0 С в течение 4 ч. Реакционную смесь разбавляли с помощью ДХМ (100 мл) и затем промывали водой (100 мл), сушили над сульфатом натрия, концентрировали в роторном испарителе и получали 2-бром-N-(2-гидроксифенил)-2-метилпропионамид (21,8 г),коричневое твердое вещество, которое использовали в следующей реакции без очистки. Стадия II. При перемешивании к раствору 2-бром-N-(2-гидроксифенил)-2-метилпропионамида (21,8 г, 84,4 ммоль) в ДМФ (85 мл) при 25 С добавляли карбонат калия (23,32 г, 168,99 ммоль) и реакционную смесь перемешивали при 80 С в течение 4 ч. После проведения ТСХ (тонкослойная хроматография) реакционную смесь фильтровали через целит и разбавляли этилацетатом (500 мл) и затем промывали водой(100 мл 3), рассолом (100 мл), сушили над безводным сульфатом натрия, концентрировали и получали 2,2-диметил-4 Н-бензо[1,4]оксазин-3-он (12,64 г) в виде коричневого твердого вещества, которое очищали с помощью колоночной хроматографии, и получали 8,5 г чистого соединения. МС (ЭУ (ионизация электронным ударом m/z 178,2 (М+1). Стадия III. При перемешивании к раствору АГЛ (алюмогидрид лития) (3,01 г, 79,10 ммоль) в ТГФ(80 мл) при 0 С порциями добавляли 2,2-диметил-4 Н-бензо[1,4]оксазин-3-он (7,00 г, 39,5 ммоль) и реакционную смесь перемешивали при 25 С в течение 1 ч и затем при 50 С в течение 3 ч. Реакцию останавливали путем добавления холодного насыщенного раствора сульфата натрия и смесь фильтровали через целит и экстрагировали с помощью ДХМ (100 мл 2), промывали рассолом (50 мл), сушили над сульфатом натрия, концентрировали и получали 2,2-диметил-3,4-дигидро-2 Н-бензо[1,4]оксазин (6,09 г), который использовали в следующей реакции использовали без очистки. МС (ЭУ) m/z 164,2 (М+1). Стадия IV. При перемешивании к раствору 2,2-диметил-3,4-дигидро-2 Н-бензо[1,4]оксазина (6 г,36,8 ммоль) в ДХМ (75 мл) при 0 С добавляли трифторуксусный ангидрид (6,2 мл, 44,2 ммоль), затем триэтиламин (6,2 мл, 44,2 ммоль) и реакционную смесь перемешивали при 0 С в течение 2 ч. Реакционную смесь разбавляли с помощью ДХМ (100 мл) и затем промывали водой (100 мл 2), рассолом (100 мл), сушили над безводным сульфатом натрия, концентрировали и получали 1-(2,2-диметил-2,3 дигидробензо[1,4]оксазин-4-ил)-2,2,2-трифторэтанон (9,46 г) в виде коричневого твердого вещества, которое очищали с помощью колоночной хроматографии, и получали 8,7 г чистого продукта. МС (ЭУ) m/z 260,2 (М+1). 1 Н ЯМР (400 МГц, CDCl3):1,38 (s, 6H), 3,65 (s, 2H), 6,86-6,96 (m, 2H), 7,12-7,16 (m, 1H), 7,97 (d, 1H). Промежуточный продукт 5 При перемешивании к раствору 6-бром-1,2,3,4-тетрагидрохинолина (3,00 г, 12,1 ммоль) в диметилформамиде (25 мл) добавляли карбонат калия (3,3 г, 24,1 ммоль), йодид натрия (0,905 г, 6,0 ммоль) и 4 метоксибензилхлорид (2,5 мл, 18,1 ммоль) и нагревали при 50 С. Через 18 ч реакционную смесь охлаждали до комнатной температуры и реакцию останавливали путем добавления воды и смесь экстрагировали этилацетатом (220 мл). Органический слой промывали водой (220 мл), рассолом (20 мл), сушили над сульфатом натрия, концентрировали и очищали с помощью колоночной хроматографии на силикагеле и получали 6-бром-1-(4-метоксибензил)-1,2,3,4-тетрагидрохинолин (2,5 г). 1 Н ЯМР (400 МГц, CDC13):1,96-2,02 (m, 2 Н), 2,78 (t, J = 6,0 Гц, 2 Н), 3,46 (t, J = 5,2 Гц, 2 Н), 3,80 (s,3 Н), 4,40 (s, 2 Н), 6,38 (d, J = 8,4 Гц, 1 Н), 6,86 (d, J = 8,4 Гц, 2H), 7,04 (d, J = 8,8 Гц, 1H), 7,07 (s, 1H), 7,15 дихлорметане (20 мл), затем добавляли AlCl3 (2,14 г, 16,1 ммоль). Через 2 ч температуру реакционной смеси доводили до комнатной и перемешивали в течение ночи. Реакцию останавливали, выливая смесь на дробленый лед, и смесь экстрагировали дихлорметаном (302 мл). Органический слой промывали водным раствором NaHCO3 (20 мл), с помощью Н 2 О (20 мл) и получали неочищенный продукт 3,0 г. Стадия II. К неочищенному продукту (0,9 г, 2,45 ммоль) в смеси 1,2-дихлорэтан/MeCN состава 1:2(12 мл) при 20 С одновременно добавляли Et3SiH (0,83 мл, 5,16 ммоль) и BF3 OEt2 (0,37 мл, 3,19 ммоль). После перемешивания в течение ночи реакционную смесь нагревали при 50 С в течение 2 ч. Реакцию останавливали путем добавления водного раствора NaHCO3 (5 мл). Летучие вещества выпаривали при пониженном давлении; полученную смесь экстрагировали дихлорметаном (220 мл), промывали рассолом (5 мл), сушили над сульфатом натрия, концентрировали и очищали с помощью колоночной хроматографии на силикагеле и получали 7-(5-бром-2-хлорбензил)-4-метил-3,4-дигидро-2 Н-бензо[1,4]оксазинMC (ЭР) m/z 351,8 (M+1). Стадия III. При перемешивании к раствору 7-(5-бром-2-хлорбензил)-4-метил-3,4-дигидро-2 Нбензо[1,4]оксазина (0,37 г, 1,06 ммоль) в смеси ТГФ:толуол (5 мл смеси состава 1:2) при -78 С добавляли 1,6 М раствор nBuLi в гексанах (0,68 мл, 1,06 ммоль). Реакционную смесь перемешивали в течение 1 ч и затем при перемешивании при -78 С переносили в раствор 2,3,4,6-тетракис-О-(триметилсилил)-Dглюкопиранона (0,49 г, 1,06 ммоль) в толуоле (5 мл). После перемешивания в течение 4 ч добавляли 0,6 н. раствор метансульфоновой кислоты в метаноле (5 мл) и реакционную смесь перемешивали при комнатной температуре в течение 12 ч. Реакцию останавливали путем добавления водного раствора NaHCO3(5 мл) и смесь экстрагировали дихлорметаном (310 мл), сушили над сульфатом натрия, концентрировали и очищали с помощью колоночной хроматографии на силикагеле и получали (2S,3R,4S,5S,6R)-2-[4 хлор-3-(4-метил-3,4-дигидро-2 Н-бензо[1,4]оксазин-7-илметил)фенил]-6-гидроксиметил-2 метокситетрагидропиран-3,4,5-триол (0,178 г). 1MC (ЭР) m/z 466,3 (M+1). Стадия IV. При перемешивании к раствору (2S,3R,4S,5S,6R)-2-[4-хлор-3-(4-метил-3,4-дигидро-2 Нбензо[1,4]оксазин-7-илметил)фенил]-6-гидроксиметил-2-метокситетрагидропиран-3,4,5-триола (0,17 г,0,37 ммоль) в смеси ацетонитрилдихлорметан (смесь состава 1:1,6 мл) при 10 С добавляли комплекс трифторид бора-диэтилэфират (0,09 мл, 0,75 ммоль) и триэтилсилан (0,24 мл, 1,50 ммоль). После перемешивания при такой же температуре в течение 4 ч реакцию останавливали водным раствором NaHCO3(4 мл). Летучие вещества выпаривали при пониженном давлении; полученную смесь экстрагировали дихлорметаном (220 мл), промывали рассолом (3 мл), сушили над сульфатом натрия, концентрировали и очищали с помощью препаративной ВЭЖХ и получали (2S,3R,4R,5S,6R)-2-[4-хлор-3-(4-метил-3,4 дигидро-2 Н-бензо[1,4]оксазин-7-илметил)фенил]-6-гидроксиметилтетрагидропиран-3,4,5-триол (40 мг). 1 Н ЯМР (400 МГц, CD3OD):2,80 (s, 3 Н), 3,15 (t, J = 4,4 Гц, 2 Н), 3,25-3,34 (m, 1 Н), 3,35-3,48 (m,3 Н), 3,68 (dd, J = 12,0, 5,6 Гц, 1H), 3,86 (d, J = 8,4 Гц, 1 Н), 3,92 (Abq, J = 15,2 Гц, 2 Н), 4,07 (d, J = 9,6 Гц,1 Н), 4,21 (t, J - 4,4 Гц, 2 Н), 6,50 (d, J = 0,8 Гц, 1 Н), 6,66 (d, J = 8,4 Гц, 1 Н), 6,64 (dd, J = 8,4, 1,2 Гц, 1 Н),7,24 (dd, J = 8,0, 1,6 Гц, 1H), 7,29 (s, 1H), 7,33 (d, J = 8,0, 1H).MC (ЭР) m/z 436,0 (M+1). Приведенные ниже соединения примеров получали по методикам, описанным в примере 1. Международный союз теоретической и прикладной химии. Пример 4. (2S,3R,4R,5S,6R)-2-[3-(4-Бензил-3,4-дигидро-2 Н-бензо[1.4]-оксазин-6-илметил)-4-хлорфенил]-6-гидроксиметилтетрагидропиран-3,4,5-триол Стадия I. При перемешивании к раствору 1-(2,3-дигидробензо[1,4]оксазин-4-ил)-2,2,2 трифторэтанона (6,5 г, 28,1 ммоль) в дихлорметане (45 мл) при 0 С добавляли 5-бром-2 хлорбензоилхлорид (8,54 г, 33,7 ммоль) в дихлорметане (35 мл) и AlCl3 (5,61 г, 42,2 ммоль). Через 2 ч температуру реакционной смеси доводили до комнатной и перемешивали в течение ночи. Реакцию останавливали, выливая смесь на дробленый лед, и смесь экстрагировали дихлорметаном (250 мл). Органический слой промывали водным раствором NaHCO3 (30 мл) с помощью H2O (20 мл), и растворитель выпаривали, и получали неочищенный продукт, который очищали с помощью колоночной хроматографии на силикагеле, и получали 1-[6-(5-бром-2-хлорбензоил)-2,3-дигидробензо[1,4]оксазин-4-ил]-2,2,2 трифторэтанон (10,0 г). 1 Н ЯМР (400 МГц, CDC13): 4,03 (t, J = 4,0 Гц, 2 Н), 4,48 (t, J = 4,2 Гц, 2 Н), 7,04 (d, J = 8,4 Гц, 1 Н),7,34 (d, J = 8,4 Гц, 1 Н), 7,50 (d, J = 2,0 Гц, 1 Н), 7,55 (dd, J = 8,4, 2,0 Гц, 1H), 7,68 (d, J = 8,4 Гц, 1H) 8,42II. При перемешивании к раствору 1-[6-(5-бром-2-хлорбензоил)-2,3 дигидробензо[1,4]оксазин-4-ил]-2,2,2-трифторэтанона (1,0 г, 2,23 ммоль) в смеси 1,2-дихлорэтан/MeCN состава 1:2 (12 мл) при 20 С одновременно добавляли Et3SiH (0,755 мл, 4,68 ммоль) и BF3OEt2 (0,34 мл,2,90 ммоль). Реакционную смесь нагревали при 50 С в течение 4 ч и реакцию останавливали путем добавления водного раствора NaHCO3 (10 мл). Летучие вещества выпаривали при пониженном давлении; полученную смесь экстрагировали дихлорметаном (220 мл), промывали рассолом (5 мл), сушили над сульфатом натрия, концентрировали и очищали с помощью колоночной хроматографии на силикагеле и получали 1-[6-(5-бром-2-хлорбензил)-2,3-дигидробензо[1,4]оксазин-4-ил]-2,2,2-трифторэтанон (0,60 г). 1 Н ЯМР (400 МГц, ДМСО (диметилсульфоксид:3,96 (t, J = 4,0 Гц, 2 Н), 3,99 (s, 2 Н), 4,37 (t, J = 4,4 Гц, 2 Н), 6,69 (d, J = 8,4 Гц, 1 Н), 7,03 (d, J = 7,6 Гц, 1H), 7,40 (d, J = 8,4 Гц, 1 Н), 7,46 (dd, J = 8,4, 2,0 Гц,1H), 7,53 (d, J = 2,4 Гц, 1 Н), 7,82 (широкий s, 1H). СтадияIII. При перемешивании к раствору 1-[6-(5-бром-2-хлорбензил)-2,3 дигидробензо[1,4]оксазин-4-ил]-2,2,2-трифторэтанона (8,6 г, 19,8 ммоль) в этаноле (40 мл) порциями добавляли NaBH4 и реакционную смесь перемешивали в течение ночи. Избыток NaBH4 нейтрализовывали путем добавления водного раствора HCl. Этанол выпаривали и остаток подвергали распределению между дихлорметаном и водой. Органический слой промывали рассолом, водой, сушили над сульфатом на- 26023781 трия; последующее выпаривание растворителя давало 6-(5-бром-2-хлорбензил)-3,4-дигидро-2 Нбензо[1,4]оксазин (6,1 г). Стадия IV. При перемешивании к раствору 6-(5-бром-2-хлорбензил)-3,4-дигидро-2 Нбензо[1,4]оксазина (8,0 г, 23,66 ммоль) в ДМФ (35 мл) добавляли карбонат калия (6,53 г, 36,0 ммоль),бензилбромид (4,33 мл, 35,50 ммоль) и нагревали при 50 С в течение 8 ч. Реакционную смесь охлаждали до комнатной температуры, реакцию останавливали путем добавления воды (50 мл), смесь экстрагировали этилацетатом (320 мл). Органический слой промывали водой (50 мл), рассолом (50 мл), сушили над сульфатом натрия, концентрировали и очищали с помощью колоночной хроматографии на силикагеле и получали 4-бензил-6-(5-бром-2-хлорбензил)-3,4-дигидро-2 Н-бензо[1,4]оксазин (7,0 г). 1 Н ЯМР (400 МГц, CD3OD):3,40 (t, J = 4,4 Гц, 2 Н), 3,85 (s, 2H), 4,24 (t, J = 4,4 Гц, 2 Н), 4,40 (s, 2 Н),6,40 (dd, J = 8,0, 2,0 Гц, 1 Н), 6,45 (d, J = 2,0 Гц, 1H), 6,66 (d, J = 8,0, Гц, 1H), 7,20-7,36 (m, 8H).MC (ЭР) m/z 429,9 (M+2). Стадия V. При перемешивании к раствору 4-бензил-6-(5-бром-2-хлорбензил)-3,4-дигидро-2 Нбензо[1,4]оксазина (7,0 г, 16,3 ммоль) в смеси ТГФ-толуол (40 мл смеси состава 1:2) при -78 С добавляли 1,6 М раствор n-BuLi в гексанах (10,46 мл, 16,35 ммоль). Реакционную смесь перемешивали в течение 1 ч и затем при перемешивании при -78 С переносили в раствор 2,3,4,6-тетракис-О-(триметилсилил)-Dглюкопиранона (7,62 г, 16,35 ммоль) в толуоле (25 мл). После перемешивания в течение 4 ч добавляли 0,6 н. раствор метансульфоновой кислоты в метаноле (50 мл) и перемешивали при комнатной температуре в течение 12 ч. Реакцию останавливали путем добавления насыщенного водного раствора бикарбоната натрия (25 мл) и смесь экстрагировали дихлорметаном (325 мл), сушили над сульфатом натрия, концентрировали и очищали с помощью колоночной хроматографии на силикагеле и получали(5,0 г, 9,24 ммоль) в смеси ацетонитрилдихлорметан (смесь состава 1:1, 40 мл) при -10 С добавляли комплекс трифторид бора-диэтилэфират (2,34 мл, 18,48 ммоль) и триэтилсилан (5,95 мл, 36,9 ммоль). После перемешивания при такой же температуре в течение 4 ч реакцию останавливали насыщенным водным раствором бикарбоната натрия (15 мл). Летучие вещества выпаривали при пониженном давлении; полученную смесь экстрагировали дихлорметаном (230 мл). Органический слой промывали рассолом (10 мл), сушили над сульфатом натрия, концентрировали и очищали с помощью препаративной ВЭЖХ и получали (2S,3R,4R,5S,6R)-2-[3-(4-бензил-3,4-дигидро-2H-бензо[1,4]оксазин-6-илметил)-4-хлорфенил]-6 гидроксиметилтетрагидропиран-3,4,5-триол (3,5 г). 1 Н ЯМР (400 МГц, CD3OD):3,20-3,50 (m, 6 Н), 3,68 (dd, J = 12,0, 4,4 Гц, 1 Н), 3,75-3,95 (m, 3 Н), 4,03MC (ЭР) m/z 511,8 (M+1). Приведенные ниже соединения примеров получали по методикам, описанным в примере 4. Стадия I. При перемешивании к суспензии LiAlH4 (7,6 г, 201 ммоль) в ТГФ (70 мл) при 0 С добавляли 4 Н-бензо[1,4]оксазин-3-он (15 г, 100 ммоль) в 30 мл ТГФ и смесь перемешивали при комнатной температуре в течение 4 ч. После охлаждения избыток LiAlH4 нейтрализовывали путем добавления этилацетата (30 мл) и последующего добавления водного раствора NH4Cl. Смесь фильтровали через слой целита и фильтрат концентрировали при пониженном давлении и экстрагировали этилацетатом (330 мл). Объединенные органические слои промывали рассолом (30 мл) и сушили над Na2SO4. Выпаривание растворителя давало бензоксазин (12 г), который использовали на следующей стадии без обработки.MC (ЭР) m/z 136 (М+1). Стадия II. К охлажденному льдом раствору бензоксазина (4,5 г, 33,3 ммоль) в дихлорметане (25 мл) добавляли трифторуксусный ангидрид (ТФУА) (6,95 мл, 49,9 ммоль) и реакционную смесь перемешивали в течение 2 ч, затем реакцию останавливали путем добавления водного раствора NaHCO3. Смесь подвергали распределению между дихлорметаном и водой. Органический слой отделяли и водный слой экстрагировали дихлорметаном. Объединенные органические слои промывали рассолом, сушили над Na2SO4 и концентрировали и получали 1-(2,3-дигидробензо[1,4]оксазин-4-ил)-2,2,2-трифторэтанон (6,5 г). МС (ЭР) m/z 232 (M+1). Стадия III. При перемешивании к раствору 2-бром-5-хлорбензойной кислоты (8 г, 34,0 ммоль) в дихлорметане (35 мл) при 0 С по каплям добавляли ДМФ (1 мл) и оксалилхлорид (3,54 мл, 37,4 ммоль). После завершения добавления реакционную смесь перемешивали при комнатной температуре в течение 3 ч. Летучие вещества выпаривали при пониженном давлении и получали 2-бром-5-хлорбензоилхлорид(8,5 г). Неочищенный продукт использовали без дополнительной очистки. К охлажденному льдом раствору 5-бром-2-хлорбензоилхлорида в дихлорметане (35 мл) добавляли 1-(2,3-дигидробензо[1,4]оксазин-4-ил)-2,2,2-трифторэтанон (6,5 г, 28,1 ммоль) в дихлорметане (45 мл),затем порциями добавляли AlCl3 (5,61 г, 42,2 ммоль). Через 2 ч температуру реакционной смеси доводили до комнатной и перемешивали в течение ночи. Реакцию останавливали, выливая смесь на дробленый лед. Полученную смесь экстрагировали дихлорметаном. Органический слой промывали водным раствором NaHCO3 (100 мл) и водой (100 мл) и растворитель выпаривали и получали неочищенный продукт,который перекристаллизовывали из горячего этилацетата, и получали 1-[6-(5-бром-2-хлорбензоил)-2,3 дигидробензо[1,4]оксазин-4-ил]-2,2,2-трифторэтанон (10,0 г). 1 Н ЯМР (400 МГц, CDC13): 4,03 (t, J = 4,0 Гц, 2 Н), 4,48 (t, J = 4,2 Гц, 2 Н), 7,04 (d, J = 8,4 Гц, 1 Н),7,34 (d, J = 8,4 Гц, 1H), 7,50 (d, J = 2,0 Гц, 1 Н), 7,55 (dd, J = 8,4, 2,0 Гц, 1H), 7,68 (d, J = 8,4 Гц, 1H) 8,42IV. При перемешивании к раствору 1-[6-(5-бром-2-хлорбензоил)-2,3 дигидробензо[1,4]оксазин-4-ил]-2,2,2-трифторэтанона (36 г, 80,35 ммоль) в смеси 1,2-дихлорэтан:MeCN состава 1:2 (180 мл) при 0 С добавляли BF3OEt2 (13,2 мл, 104 ммоль) и Et3SiH (26,9 мл, 168,7 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение ночи, затем реакцию останавливали путем добавления водного раствора NaHCO3 (200 мл). Полученную смесь экстрагировали этилацетатом (3200 мл) и объединенные органические слои промывали рассолом (200 мл) и сушили над сульфатом натрия. После выпаривания растворителя полученный неочищенный продукт очищали с помощью колоночной хроматографии на силикагеле и получали 1-[6-(5-бром-2-хлорбензил)-2,3 дигидробензо[1,4]оксазин-4-ил]-2,2,2-трифторэтанон (30 г). 1 Н ЯМР (400 МГц, ДМСО):3,96 (t, J = 4,0 Гц, 2 Н), 3,99 (s, 2H), 4,37 (t, J = 4,4 Гц, 2 Н), 6,69 (d, J =NaBH4 (1,5 г, 39,0 ммоль) и реакционную смесь перемешивали в течение ночи. Избыток NaBH4 нейтрализовывали путем добавления водного раствора NH4Cl и этанол выпаривали. Остаток подвергали распределению между этилацетатом и водой и органический слой отделяли, промывали рассолом (40 мл) и сушили над сульфатом натрия. После выпаривания растворителя полученный неочищенный продукт очищали с помощью колоночной хроматографии на силикагеле и получали 6-(5-бром-2-хлорбензил)-3,4 дигидро-2 Н-бензо[1,4]оксазин (6,1 г). МС (ЭР) m/z 340 (М+2). Стадия VI. При перемешивании к раствору 6-(5-бром-2-хлорбензил)-3,4-дигидро-2 Нбензо[1,4]оксазина (8,0 г, 23,66 ммоль) в ДМФ (35 мл) добавляли карбонат калия (6,53 г, 47,3 ммоль) и бензилбромид (4,33 мл, 35,50 ммоль). Реакционную смесь нагревали при 60 С в течение 8 ч, затем охлаждали до комнатной температуры и реакцию останавливали путем добавления охлажденной льдом воды(50 мл). Полученную смесь экстрагировали этилацетатом (330 мл) и объединенные органические слои промывали водой (50 мл) и рассолом (50 мл), затем сушили над сульфатом натрия. Сульфат натрия отфильтровывали и фильтрат концентрировали и получали неочищенный продукт, который очищали с помощью колоночной хроматографии на силикагеле, и получали 4-бензил-6-(5-бром-2-хлорбензил)-3,4 дигидро-2 Н-бензо[1,4]оксазин (7,0 г). 1 Н ЯМР (400 МГц, CD3OD):3,40 (t, J = 4,4 Гц, 2 Н), 3,85 (s, 2H), 4,24 (t, J = 4,4 Гц, 2 Н), 4,40 (s, 2 Н),6,40 (dd, J = 8,0, 2,0 Гц, 1 Н), 6,45 (d, J = 2,0 Гц, 1 Н), 6,66 (d, J = 8,0, Гц, 1H), 7,20-7,36 (m, 8H). МС (ЭР) m/z 430 (M+2). Стадия VII. При перемешивании к раствору 4-бензил-6-(5-бром-2-хлорбензил)-3,4-дигидро-2 Нбензо[1,4]оксазина (7,0 г, 16,3 ммоль) в смеси ТГФ-толуол состава 1:2 (40 мл) при -78 С добавляли 1,6 М раствор n-BuLi в гексанах (10,46 мл, 16,35 ммоль). Реакционную смесь перемешивали в течение 1 ч и затем при перемешивании при -78 С переносили в раствор 2,3,4,6-тетракис-О-(триметилсилил)-Dглюкопиранона (7,62 г, 16,35 ммоль) в толуоле (25 мл). После перемешивания в течение 1 ч добавляли 0,6 н. раствор метансульфоновой кислоты в метаноле (70 мл) и реакционную смесь перемешивали при комнатной температуре в течение 12 ч, затем реакцию останавливали путем добавления насыщенного водного раствора бикарбоната натрия (25 мл). Полученную смесь экстрагировали этилацетатом (3100 мл) и объединенные органические слои сушили над сульфатом натрия, концентрировали и очищали с помощью колоночной хроматографии на силикагеле и получали (2S,3R,4S,5S,6R)-2-[3-(4-бензил-3,4 дигидро-2 Н-бензо[1,4]оксазин-6-илметил)-4-хлорфенил]-6-гидроксиметил-2-метокситетрагидропиран 3,4,5-триол (5,0 г). Пример 7. (2S,3R,4R,5S,6R)-2-[3-(4-бензил-3,4-дигидро-2 Н-бензо[1,4]-оксазин-6-илметил)-4-хлорфенил]-6-гидроксиметилтетрагидропиран-3,4,5-триол. Стадия VIII. При перемешивании к раствору (2S,3R,4S,5S,6R)-2-[3-(4-бензил-3,4-дигидро-2 Нбензо[1,4]оксазин-6-илметил)-4-хлорфенил]-6-гидроксиметил-2-метокситетрагидропиран-3,4,5-триола(5,0 г, 9,24 ммоль) в смеси ацетонитрилдихлорметан состава 1:1 (40 мл) при -5 С добавляли комплекс трифторид бора-диэтилэфират (2,34 мл, 18,48 ммоль) и триэтилсилан (5,95 мл, 36,9 ммоль). После перемешивания при такой же температуре в течение 4 ч реакцию останавливали насыщенным водным раствором бикарбоната натрия (15 мл). Летучие вещества выпаривали при пониженном давлении и полученную смесь экстрагировали дихлорметаном (230 мл). Органические слои объединяли и промывали рассолом (10 мл), сушили над сульфатом натрия, концентрировали и очищали с помощью препаративной ВЭЖХ и получали (2S,3R,4R,5S,6R)-2-[3-(4-бензил-3,4-дигидро-2H-бензо[1,4]оксазин-6-илметил)-4 хлорфенил]-6-гидроксиметилтетрагидропиран-3,4,5-триол (3,5 г). 1 Н ЯМР (400 МГц, CD3OD):3,20-3,50 (m, 6 Н), 3,68 (dd, J = 12,0, 4,4 Гц, 1 Н), 3,75-3,95 (m, 3 Н), 4,03MC (ЭР) m/z 511,8 (M+1). Пример 8. (2S,3R,4R,5S,6R)-2-[4-Хлор-3-(3,4-дигидро-2 Н-бензо[1,4]-оксазин-6-илметил)фенил]-6 гидроксиметилтетрагидропиран-3,4,5-триол. Стадия IX. К раствору (2S,3R,4R,5S,6R)-2-[3-(4-бензил-3,4-дигидро-2 Н-бензо[1,4]оксазин-6 илметил)-4-хлорфенил]-6-гидроксиметилтетрагидропиран-3,4,5-триола (2,4 г, 4,68 ммоль) в метаноле (15 мл) добавляли 10% палладий на древесном угле (240 мг) и 0,05 мл концентрированной НС 1. Реакционную смесь перемешивали в атмосфере водорода в течение 2 ч, затем фильтровали через слой целита (который промывали метанолом). Полученный фильтрат концентрировали и получали остаток, который очищали с помощью препаративной ВЭЖХ, и получали (2S,3R,4R,5S,6R)-2-[4-хлор-3-(3,4-дигидро-2Hбензо[1,4]оксазин-6-илметил)фенил]-6-гидроксиметилтетрагидропиран-3,4,5-триол (1,6 г).
МПК / Метки
МПК: C07D 413/10, C07D 405/10, A61P 3/10, A61K 31/70, C07D 407/10
Метки: применение, гликозидные, производные
Код ссылки
<a href="https://eas.patents.su/30-23781-glikozidnye-proizvodnye-i-ih-primenenie.html" rel="bookmark" title="База патентов Евразийского Союза">Гликозидные производные и их применение</a>
Предыдущий патент: Лекарственное средство для экстренной контрацепции
Следующий патент: Механизм скребка ленточного транспортера сыпучих материалов
Случайный патент: Замещенные 2-[2-(фенил)этиламино]алканамидные производные и применение указанных соединений в качестве модуляторов натриевых и/или кальциевых каналов












