Производные бензоксазина в качестве модуляторов 5-нт-6, способ их получения, фармацевтические композиции, содержащие эти производные, и их применение
Формула / Реферат
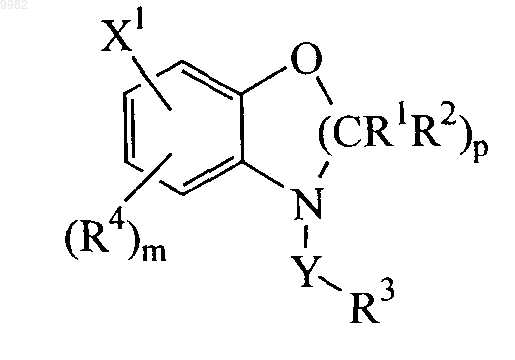
1. Соединение формулы
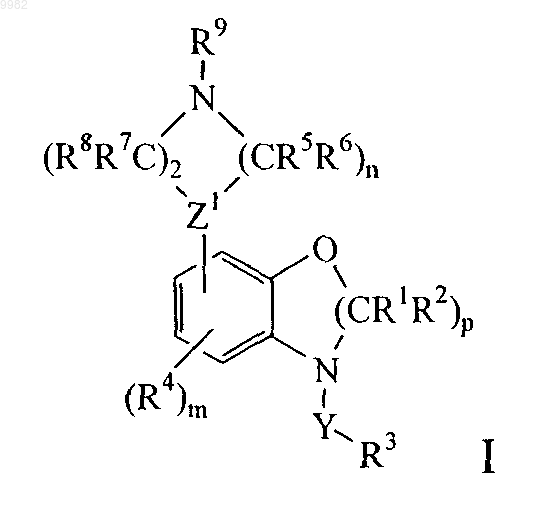
его фармацевтически приемлемая соль или пролекарство, где
m означает целое число от 0 до 3;
n означает 2 или 3;
р означает 2;
Y означает -S(O2)-;
Z1 означает N;
R1 и R2 означают водород;
R3 означает фенил или нафтил, которые необязательно замещены галогеном, алкилом, алкокси, гидрокси, циано, пиперазинилом, метилсульфониламино, метилсульфонилом, аминокарбонилом, или означает хинолинил, изохинолинил, тиофенил, бензотиадиазолил, бензоксадиазолил, имидазолил или 2,3-дигидробензо[1,4]диоксин, которые необязательно замещены галогеном или алкилом;
каждый R4 независимо означает галоген, алкил или алкокси;
каждый R5, R6, R7 и R8 независимо означает водород или алкил; а
R9 означает водород или алкил.
2. Соединение по п.1, где m означает целое число от 0 до 2.
3. Соединение по п.1, где m равно 0 или 1, а n, Y, Z1, R1-R9 имеют значения, указанные в п.1.
4. Соединение по любому из пп.1-3 формулы
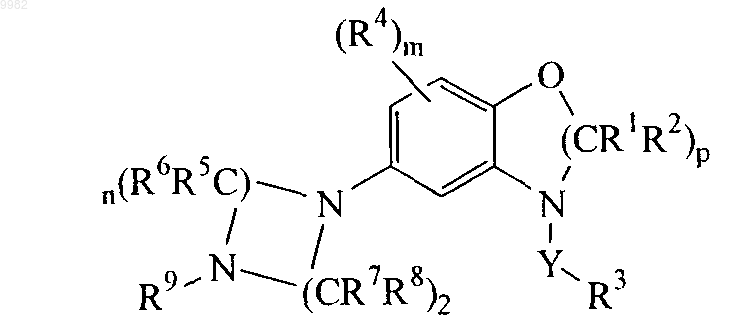
где R1, R2, R3, R4, R5, R6, R7, R8, R9, m, n, р и Y имеют значения, указанные в указанных пунктах.
5. Соединение по любому из пп.1-3 формулы
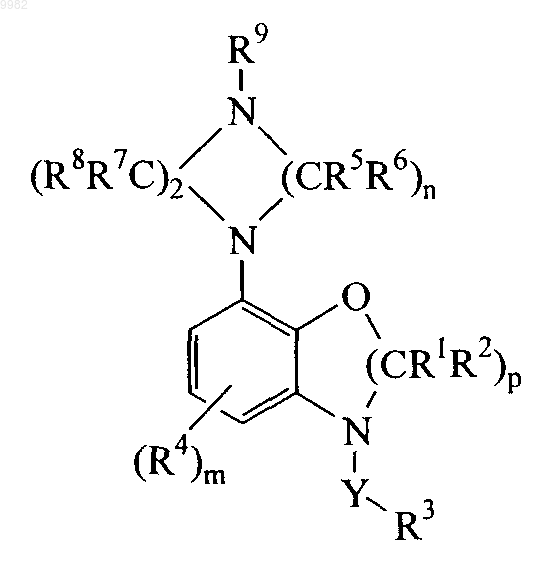
где R1, R2, R3, R4, R5, R6, R7, R8, R9, m, n, р и Y имеют значения, указанные в указанных пунктах.
6. Соединение по любому из пп.1-5, где n и р равны 2.
7. Соединение по любому из пп.1-6, где каждый R4 независимо означает хлор, фтор, метокси или метил.
8. Соединение по любому из пп.1-7, где m равно 1.
9. Соединение по любому из пп.1-8, где R3 означает фенил или нафтил, которые необязательно замещены, как указано в п.1.
10. Соединение по любому из пп.1-9, где R3 означает фенил или галогензамещенный фенил.
11. Соединение по любому из пп.1-9, где R3 означает фенил, 2-фторфенил, 2-хлорфенил, 3,4-дихлорфенил, 4-хлорфенил, 3-хлорфенил, 4-метоксифенил, 3,5-дихлорфенил, 2,6-дихлорфенил, 2,4-дихлорфенил, 3-метансульфониламинофенил, 2-метансульфонилфенил, 2-карбамоилфенил, 3-метансульфонилфенил, 4-метансульфонилфенил, 3-фторфенил, нафтил, 2,4-дифторфенил, 2-цианофенил, 2-хлор-4-фторфенил, 5-фтор-2-метилфенил, 5-хлорнафтил.
12. Соединение по любому из пп.1-9, где R3 означает 4-фтор-2-метилфенил, 2-гидроксифенил, 4-пиперазин-1-ил или 2,3-дигидробензо[1,4]диоксинил.
13. Соединение по любому из пп.1-10, где R3 означает фенил, 2-хлорфенил или 2-фторфенил.
14. Соединение по п.1, которое выбрано из группы, включающей
6-трет-бутил-4-(2-фторбензолсульфонил)-8-пиперазин-1-ил-3,4-дигидро-2Н-бензо[1,4]оксазин;
4-(2-фторбензолсульфонил)-8-метилпиперазин-1-ил-3,4-дигидро-2Н-бензо[1,4]оксазин;
6-фтор-4-(2-фторбензолсульфонил)-8-пиперазин-1-ил-3,4-дигидро-2Н-бензо[1,4]оксазин;
4-(2-фторбензолсульфонил)-6-метокси- 8-пиперазин-1-ил-3,4-дигидро-2Н-бензо[1,4]оксазин;
4-(2-фторбензолсульфонил)-6-метил-8-пиперазин-1-ил-3,4-дигидро-2Н-бензо[1,4]оксазин;
6-хлор-4-(2-фторбензолсульфонил)-8-пиперазин-1-ил-3,4-дигидро-2Н-бензо[1,4]оксазин;
4-(2-фторбензолсульфонил)-8-пиперазин-1-ил-3,4-дигидро-2Н-бензо[1,4]оксазин.
15. Соединение по любому из пп.1-6, где R3 означает хинолин-8-ил, 2-тиофенил, 5-хлортиофен-2-ил, изохинолин-5-ил, бензо[1,2,5]тиадиазол-4-ил, 1-метил-1Н-имидазол-4-ил или бензо[1,2,5]оксадиазол-4-ил.
16. Соединение по п.9, где R9 означает водород.
17. Соединение по любому из пп.1-3, где R5, R6, R7 и R8 означают водород.
18. Соединение по любому из пп.1-3, где m равно 0.
19. Способ получения соединения по п.1, включающий:
(а) взаимодействие галогенарила формулы
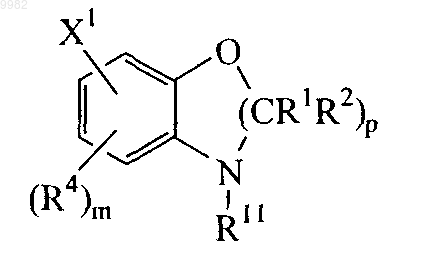
с гетероциклилом формулы
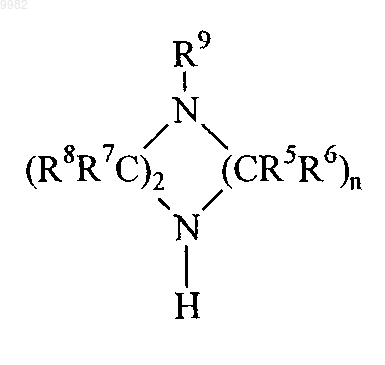
в присутствии катализатора конденсации с образованием гетероциклилзамещенного фенила формулы
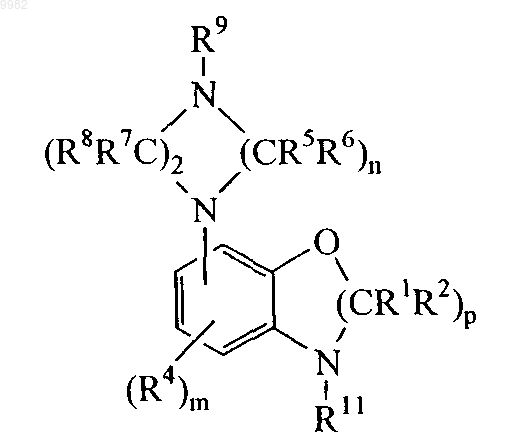
(б) удаление защитной группы в гетероциклилзамещенном фениле с образованием незащищенного гетероциклилзамещенного фенила формулы
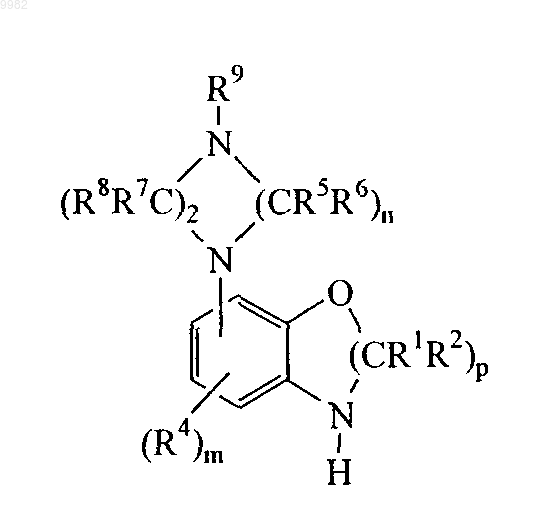
и
(в) взаимодействие незащищенного гетероциклилзамещенного фенила с соединением формулы R3-Y-W с образованием соединения по п.1, где R1, R2, R4, R5, R6, R7, R8, R9, m, n, р имеют значения, указанные в п.1, W означает активирующую группу, R11 означает аминозащитную группу, a X1 означает галоген.
20. Способ получения соединения по п.1, включающий:
(а) взаимодействие галогенарила формулы
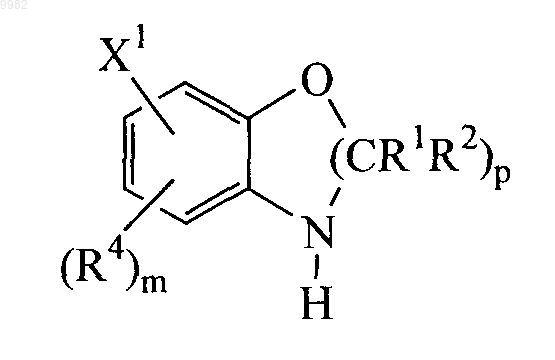
с соединением формулы
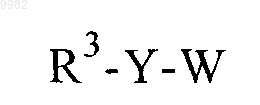
с образованием соединения, содержащего галогенфенил, формулы
и
(б) конденсацию соединения галогенированного фенила с гетероциклильным соединением формулы
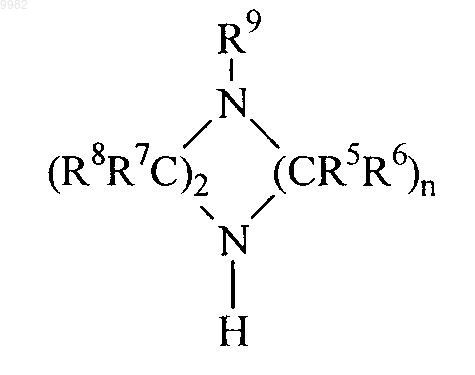
в присутствии катализатора конденсации с образованием соединения формулы I, где Y, R1, R2, R3, R4, R5, R6, R7, R8, R9, m, n и р имеют значения, указанные в п.1, W означает активирующую группу, а X1 означает галоген.
21. Фармацевтическая композиция, включающая терапевтически эффективное количество по меньшей мере одного соединения по пп.1-18 в смеси с одним или более фармацевтически приемлемым носителем, предназначенная для лечения заболеваний.
22. Применение одного или более соединений по любому из пп.1-18 для получения лекарственного средства, предназначенного для лечения или профилактики патологического состояния, которое облегчается агонистами рецептора 5-НТ6.
23. Применение по п.22, где патологическое состояние представляет собой нарушения ЦНС.
24. Применение по п.22, где заболевание включает психоз, шизофрению, маниакальные депрессии, неврологические нарушения, нарушения памяти, нарушение в форме потери внимания, болезнь Паркинсона, боковой амиотрофический склероз, болезнь Альцгеймера и болезнь Гентингтона.
25. Применение по п.22, где патологическое состояние представляет собой заболевание желудочно-кишечного тракта.
Текст
009982 Настоящее изобретение относится к производным бензоксазина, к соответствующим композициям,к способам применения в качестве терапевтических агентов и к способам их получения. Действие нейромедиатора 5-гидрокситриптамина (5-HT) в качестве главного модулирующего нейромедиатора в головном мозге опосредуется рядом рецепторных семейств, обозначаемых 5-НТ 1, 5-НТ 2,5- НТ 3, 5-НТ 4, 5-НТ 5, 5-НТ 6 и 5-НТ 7. Благодаря высокому уровню в мозговой ткани мРНК, кодирующей рецептор 5-НТ 6, предполагается, что рецептор 5-НТ 6 принимает участие в патологии и может использоваться при лечении нарушений центральной нервной системы. Например, лиганды, селективные в отношении рецептора 5-НТ 6, идентифицированы в качестве потенциально эффективных средств при лечении некоторых нарушений ЦНС, таких как болезнь Паркинсона, болезнь Гентингтона, тревога, депрессия, маниакальная депрессия, психоз, эпилепсия, навязчивые компульсивные нарушения, мигрень,болезнь Альцгеймера (для усиления познавательной способности), нарушения сна, нарушения питания,такие как анорексия и булимия, приступы паники, нарушение в форме гиперактивности при недостатке внимания (ADHD), недостаток внимания (ADD), синдром отмены при злоупотреблении лекарственными средствами, такими как кокаин, этанол, никотин и бензодиазепины, шизофрения, и также нарушений,ассоциированных с травмой спинного мозга и/или травмой головного мозга, такой как гидроцеяфалия. Предполагается также, что такие соединения можно использовать для лечения некоторых нарушений желудочно-кишечного тракта, таких как функциональное нарушение кишечника. См., например, В.L. Roth и др., J. Pharmacol. Exp. Ther., 268, 1403-14120 (1994), D.R. Sibley и др., Mol. Pharmacol., 43, 320-327(1993), A.J. Sleight и др., Neurotransmission, 11, 1-5 (1995), и A.J. Sleight и др., Serotonin ID Research Alert,2 (3), 115-118 (1997). В то время как в литературе описан ряд модуляторов 5-НТ 6, существует потребность в соединениях, которые могут использоваться в качестве модуляторов 5-НТ 6. Первым объектом изобретения являются его фармацевтически приемлемая соль или пролекарство, гдеm означает целое число от 0 до 3;R3 означает фенил или нафтил, которые необязательно замещены галогеном, алкилом, алкокси,гидрокси, циано, пиперазинилом, метилсульфониламино, метилсульфонилом, аминокарбонилом, или означает хинолинил, изохицолинил, тиофенил, бензотиадиазолил, бензокеадиазолил, имидазолил или 2,3-дигидробензо[1,4]диоксин, которые необязательно замещены галогеном или алкилом; каждый R4 независимо означает галоген, алкил или алкокси; каждый R5, R6, R7 и R8 независимо означает водород или алкил; аR9 означает водород или алкил. Кроме того, объектами настоящего изобретения являются:(II) соединение, где m означает целое число от 0 до 2;(III) соединение, где m равно 0 или 1, n, Y, Z1, R1-R9 имеют указанные выше значения;(IX) соединение, где R3 означает необязательно замещенный фенил или необязательно замещенный нафтил;(X) соединение, где R3 означает фенил или фенил, замещенный галогеном;(XIV) соединение, которое выбрано из группы, включающей 6-трет-бутил-4-(2-фторбензолсульфонил)-8-пиперазин-1-ил-3,4-дигидро-2 Н-бензо[1,4]оксазин; 4-(2-фторбензолсульфонил)-8-метилпиперазин-1-ил-3,4-дигидро-2 Н-бензо[1,4]оксазин; 6-фтор-4-(2-фторбензолсульфонил)-8-пиперазин-1-ил-3,4-дигидро-2 Н-бензо[1,4]оксазин; 4-(2-фторбензолсульфонил)-6-метокси-8-пиперазин-1-ил-3,4-дигидро-2 Н-бензо[1,4]оксазин; 4-(2-фторбензолсульфонил)-6-метил- 8-пиперазин-1-ил-3,4-дигидро-2 Н-бензо[1,4]оксазин; 6-хлор-4-(2-фторбензолсульфонил)-8-пиперазин-1-ил-3,4-дигидро-2 Н-бензо[1,4]оксазин; 4-(2-фторбензолсульфонил)-8-пиперазин-1-ил-3,4-дигидро-2 Н-бензо[1,4]оксазин;(XVIII) соединение, где m равно 0. Настоящее изобретение относится также к способам получения соединений формулы I, к композициям, содержащим указанные соединения, и к их применению. Если не указано иное, термины, используемые в тексте заявки, включая описание и пункты формулы изобретения, имеют значения, указанные ниже. Если не указано иное, формы единственного числа в описании и пунктах формулы изобретения включают также множественное число."Агонист" означает соединение, которое усиливает активность другого соединения или рецепторного участка, или, иными словами, имеет значение, известное специалисту в данной области, или значение, указанное, например в монографии Goodman и Gilman, The Pharmacological Basis of Therapeutics, 7th"Алкил" означает одновалентный прямой или разветвленный насыщенный углеводородный остаток, включающий только атомы углерода и водорода и содержащий от 1 до 12 атомов углерода."(Низш.)алкил" означает алкильную группу, содержащую от 1 до 6 атомов углерода. Примеры алкильных групп включают, без ограничения перечисленным, метил, этил, пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил, пентил, н-гексил, октил, додецил и т.п. или группы, указанные в описании заявки."Алкилен" означает прямой насыщенный двухвалентный углеводородный радикал, содержащий от 1 до 6 атомов углерода, или разветвленный насыщенный двухвалентный углеводородный радикал, содержащий от 3 до 6 атомов углерода, например метилен, этилен, 2,2-диметилэтилен, пропилен, 2-метилпропилен, бутилен, пентилен и т.п. или группы, указанные в описании заявки."Алкокси" означает группу формулы -O-Rz, где Rz означает алкильную группу, указанную выше. Примеры алкоксигруппы включают, без ограничения перечисленным, метокси, этокси, изопропокси и т.п. или группы, указанные в описании заявки."Антагонист" означает соединение, которое снижает или предотвращает действие другого соединения или рецепторного участка, или, иными словами, имеет значение, известное специалисту в данной области, или значение, указанное, например, в монографии Goodman и Gilman, The Pharmacological Basis"Арил" означает одновалентный циклический ароматический углеводородный радикал, включающий моно- или бициклический ароматический цикл. Арильная группа необязательно замещена одним,двумя или тремя, предпочтительно одним или двумя заместителями, причем каждый заместитель независимо выбран из группы, включающей, если не указано иное, гидрокси, циано, алкил, алкокси, тиол,тиоалкил, галоген, галогеналкил, нитро, амино, моноалкиламино, диалкиламино, пиперазинил или пиперидинил. Примеры арильной группы включают, без ограничения перечисленным, необязательно замещенный фенил и необязательно замещенный нафтил и т.п. или группы, указанные в описании заявки."Циклоалкил" означает одновалентный насыщенный карбоциклический радикал, включающий моно- или бициклический циклы. Циклоалкил необязательно замещен одним или более заместителями,причем каждый заместитель независимо означает, если не указано иное, гидрокси, алкил, алкокси, галоген, галогеналкил, амино, моноалкиламино или диалкиламино. Примеры циклоалкильной группы включают, без ограничения перечисленным, циклопропил, циклобутил, циклопентил, циклогексил, циклогептил и т.п. или группы, указанные в описании заявки."Циклоалкилалкил" означает радикал -R'R", где R' означает алкилен, a R" означает циклоалкил, указанный выше или приведенный в описании заявки."Патологическое состояние" означает заболевание, состояние, симптом или показание. Термин "галоген" означает заместитель фтор, хлор, бром или иод, предпочтительно фтор или хлор."Галогеналкил" означает алкил, указанный выше, в котором 1 или более атомов водорода замещены одним или разными галогенами. Примеры галогеналкилов включают -CH2Cl, -CH2CF3, -CH2CCl3, перфторалкил (например, -CF3) и т.п. или группы, указанные в описании заявки."Гетероарил" означает моноциклический или бициклический радикал, содержащий от 5 до 12,предпочтительно от 5 до 10 атомов в цикле, включающий по меньшей мере один ароматический цикл и,кроме того, содержащий в цикле 1, 2 или 3 гетероатома, выбранных из N, О или S (остальные атомы в цикле являются атомами углерода). Гетероарил необязательно замещен одним, двумя или тремя, предпочтительно одним или двумя, наиболее предпочтительно одним заместителем, причем каждый заместитель независимо выбран из группы, включающей гидрокси, циано, алкил, алкокси, тиоалкил, галоген,галогеналкил, гидроксиалкил, алкоксикарбонил, амино, алкиламино, диалкиламино, аминокарбонил, пиперазинил, пиперидинил или карбониламино, предпочтительно галоген или алкил, если не указано иное. Примеры гетероарильных радикалов включают, без ограничения перечисленным, имидазолил, оксазолил, тиазолил, пиразинил, тиофенил, фуранил, пиранил, пиридинил, хинолинил, изохинолинил, бензофурил, бензотиофенил, бензотиопиранил, бензимидазолил, бензооксазолил, бензооксадиазолил, бензотиазолил, бензотиадиазолил, бензопиранил, изоиндолил и т.п. или группы, указанные в описании заявки."Гетероциклоамино" означает насыщенный цикл, где по меньшей мере 1 атом в цикле означает N,NH или N-алкил, а остальные атомы образуют алкиленовую группу или группы, указанные в описании заявки."Гетероциклил" означает одновалентный насыщенный остаток, включающий от одного до трех циклов, содержащий 1, 2 или 3 гетероатома (выбранных из атомов азота, кислорода или серы). Гетероциклил необязательно замещен одним, двумя или тремя, предпочтительно одним или двумя заместителями, причем каждый заместитель независимо выбран из группы, включающей гидрокси, алкил, алкокси, тиоалкил, галоген, галогеналкил, гидроксиалкил, алкоксикарбонил, амино, алкиламино, диалкиламино, аминокарбонил или карбониламино, если не указано иное. Примеры гетероциклильных остатков включают, без ограничения перечисленным, морфолинил, пиперазинил, пиперидинил, пирролидинил,тетрагидропиранил и т.п. или группы, указанные в описании заявки."Уходящая группа" означает группу, название которой обычно ассоциируется с ее использованием в синтетической органической химии, т.е. означает атом или группу, которая замещается в условиях реакции замещения. Примеры уходящей группы включают, без ограничения перечисленным, галоген, алкан- или ариленсульфонилокси, такие как метансульфонилокси, этансульфонилокси, тиометил, бензолсульфонилокси, тозилокси и тиенилокси, дигалогенфосфиноилокси, необязательно замещенный бензилокси, изопропилокси, ацилокси и т.п. или группы, указанные в описании заявки."Модулятор" означает соединение, которое взаимодействует с мишенью. Взаимодействие включает, без ограничения перечисленным, действие типа агониста, действие типа антагониста и т.п., как указано в описании заявки."Необязательный" или "необязательно" означает, что последующее событие или обстоятельство может произойти, но не обязательно произойдет, и что описание включает случаи, когда это событие или обстоятельство происходит, и случаи, когда оно не происходит."Инертный органический растворитель" или "инертный растворитель" означает растворитель,инертный в условиях описываемой в тексте реакции, включающий, например, бензол, толуол, ацетонитрил, тетрагидрофуран, N,N-диметилформамид, хлороформ, хлористый метилен или дихлорметан, дихлорэтан, диэтиловый эфир, этилацетат, ацетон, метилэтилкетон, метанол, этанол, пропанол, изопропанол,трет-бутанол, диоксан, пиридин и т.п. Если не указано иное, растворители, использованные в реакциях по настоящему изобретению, являются инертными растворителями."Фармацевтически приемлемый" означает материал, который используют при получении фармацевтической композиции и который обычно является безопасным, нетоксичным, безопасным в биологическом или ином отношении и включает материал, приемлемый как в ветеринарии, так и в фармацевтике."Фармацевтически приемлемые соли" соединения означают соли, которые являются фармацевтически приемлемыми и которые обладают необходимой фармакологической активностью исходного соединения. Например, такие соли включают кислотно-аддитивные соли неорганических кислот, таких как хлористо-водородная кислота, бромисто-водородная кислота, серная кислота, азотная кислота, фосфорная кислота и т.п., или органических кислот, таких как уксусная кислота, бензолсульфоновая кислота,бензойная кислота, камфорсульфоновая кислота, лимонная кислота, этансульфоновая кислота, фумаровая кислота, глюкогептоновая кислота, глюконовая кислота, глутаминовая кислота, гликолевая кислота,гидроксинафтоевая кислота, 2-гидроксиэтансульфоновая кислота, молочная кислота, малеиновая кислота, яблочная кислота, малоновая кислота, миндальная кислота, метансульфоновая кислота, муконовая кислота, 2-нафталинсульфоновая кислота, пропионовая кислота, салициловая кислота, янтарная кислота,винная кислота, паратолуолсульфоновая кислота, триметилуксусная кислота и т.п., или соли, образующиеся при замене кислотного протона, присутствующего в исходном соединении, на ион металла, например ион щелочного металла, ион щелочно-земельного металла, ион алюминия, или при образовании протоном координационного соединения с органическим или неорганическим основанием. Приемлемые органические основания включают диэтаноламин, этаноламин, N-метилглюкамин, триэтаноламин, трометамин и т.п. Приемлемые неорганические основания включают гидроксид алюминия, гидроксид кальция, гидроксид калия, карбонат натрия и гидроксид натрия. Предпочтительными фармацевтически приемлемыми солями являются соли уксусной кислоты, соляной кислоты, серной кислоты, метансульфоновой кислоты, малеиновой кислоты, фосфорной кислоты,винной кислоты, лимонной кислоты, соли натрия, калия, кальция, цинка и магния. Предполагается, что все ссылки на фармацевтически приемлемые соли включают сольватированные формы (сольваты) или кристаллические формы (полиморфы) указанной кислотно-аддитивной соли."Пролекарство" означает фармакологически неактивную форму соединения, которое подвергается метаболической трансформации in vivo, например, под действием биологических жидкостей или ферментов после введения в организм субъекта с образованием фармакологически активной формы соединения, которая обеспечивает необходимое фармакологическое действие. Пролекарство может подвергаться метаболической трансформации до абсорбции, во время абсорбции, после абсорбции или в определенном органе. Хотя метаболическая трансформация многих веществ происходит, главным образом, в печени, в метаболизме могут принимать участие почти все остальные органы и ткани, прежде всего легкие. Пролекарственные формы соединений используются, например, с целью улучшения биодоступности, улучшения переносимости для субъекта, например маскирования или нейтрализации неприятных характеристик, таких как горький вкус, раздражение желудочно-кишечного тракта, изменение растворимости, например, при внутривенном введении, для обеспечения пролонгированного или замедленного высвобождения или доставки, для улучшения технологии переработки или обеспечения специфической доставки соединения. Ссылки в описании на любое соединение включают пролекарственные формы этого соединения."Защитная группа" означает группу, которая селективно блокирует одну реакционноспособную группу в полифункциональном соединении таким образом, что химическую реакцию можно провести избирательно по другой незащищенной реакционноспособной группе в соответствии с тем, как это принято в синтетической химии. Некоторые способы по настоящему изобретению рассчитаны на то, что защитные группы блокируют реакционноспособные атомы азота и/или кислорода, присутствующие в реагентах. Например, термин "аминозащитная группа" означает группы, предназначенные для защиты атома азота от нежелательных реакций при проведении синтезов. Примеры таких защитных групп включают, без ограничения перечисленным, трифторацетил, ацетамидо, бензил (Bn), бензилоксикарбонил(карбобензилокси, CBZ), параметоксибензилоксикарбонил, паранитробензилоксикарбонил, трет-бутоксикарбонил (BOC) и т.п. Выбор защитной группы, которая удаляется в мягких условиях и устойчива в условиях данной реакции, представляется очевидным для специалиста в данной области."Сольваты" означает сольватированные формы, содержащие стехиометрическое или нестехиометрическое количество растворителя. Некоторые соединения способны удерживать в кристаллической решетке фиксированное количество молекул растворителя, образуя сольват. Гидраты образуются в том случае, если в качестве растворителя используется вода, а алкоголяты образуются в том случае, если растворителем является спирт. Гидраты образуются благодаря комбинации 1 или более молекул воды с одной молекулой соединения, причем в указанной комбинации вода сохраняет молекулярную форму, та-4 009982 кую как H2O, и такие комбинации могут существовать в виде одного или более гидратов."Субъект" означает млекопитающих и не млекопитающих. Млекопитающие означают любого члена класса млекопитающих, включая, без ограничения перечисленным, человека, нечеловекообразных приматов, таких как шимпанзе и другие виды мартышек и обезьян, сельскохозяйственных животных,таких как крупный рогатый скот, лошади, овцы, козы и свиньи, домашних животных, таких как кролики,собаки и кошки, лабораторных животных, включая грызунов, таких как крысы, мыши и морские свинки и т.п. Примеры не млекопитающих включают, без ограничения перечисленным, птиц и т.п. Термин"субъект" не означает конкретный возраст или пол."Терапевтически эффективное количество" означает количество соединения, которое при введении субъекту для лечения патологического состояния является достаточным для излечения патологического состояния. Терапевтически эффективное количество варьирует в зависимости от типа соединения, патологического состояния, подлежащего лечению, тяжести болезни, возраста и относительного состояния здоровья субъекта, от способа и формы введения, от мнения лечащего врача или практикующего ветеринара и других факторов. Термины "указанный выше" или "указанный в описании заявки" при описании переменной включают (посредством ссылки) широкое определение переменной, а также предпочтительные, более предпочтительные и наиболее предпочтительные значения, если они упоминаются в тексте."Терапия" или "лечение" заболевания включает: (1) профилактику заболевания, т.е. предупреждение развития клинических симптомов заболевания у субъекта, который подвержен или предрасположен к заболеванию, но у которого не обнаруживаются или не проявляются симптомы заболевания; (2) подавление заболевания, т.е. остановку или подавление развития заболевания или его клинических симптомов,или (3) ослабление заболевания, например стимуляцию временной или долгосрочной регрессии заболевания или его клинических симптомов. Термины "обработка", "контактирование" и "взаимодействие" при описании реакции означают добавление или смешивание двух или более реагентов в соответствующих условиях с целью получения указанного и/или требуемого продукта. Предполагается, что реакция, по которой получают указанный и/или требуемый продукт, не обязательно происходит при непосредственной комбинации двух реагентов, добавляемых в начале процесса, т.е. в смеси может образоваться одно или более промежуточных соединений, из которых, в конечном счете, образуется указанный и/или требуемый продукт. В общем случае, номенклатура, использованная в описании заявки, основана на программном обеспечении AUTONOM, версия 4.0 компьютерной системы института Бельштейна для формирования систематической номенклатуры IUPAC. Приведенные в описании структуры получены с использованием программы ISIS, версия 2.2. Предполагется, что в приведенных структурах все свободные валентности у атома углерода, азота или кислорода заняты атомами водорода. Первым объектом изобретения (I) являются соединения формулы и их фармацевтически приемлемая соль или пролекарство, гдеm означает целое число от 0 до 3;R3 означает фенил или нафтил, которые необязательно замещены галогеном, алкилом, алкокси,гидрокси, циано, пиперазинилом, метилсульфониламино, метилсульфонилом, аминокарбонилом, или означает хинолинил, изохинолинил, тиофенил, бензотиадиазолил, бензоксадиазолил, имидазолил или 2,3-дигидробензо[1,4]диоксин, которые необязательно замещены галогеном или алкилом; каждый R4 независимо означает галоген, алкил или алкокси; каждый R5, R6, R7 и R8 независимо означает водород или алкил; аR9 означает водород или алкил.-5 009982 В объем настоящего изобретения включены соли соединений формулы I. В другом варианте изобретения соединения формулы I имеют формулу где R1, R2, R3, R4, R5, R6, R7, R8, R9, m, n, p и Y имеют значения, указанные выше. Еще в одном варианте изобретения соединения формулы I имеют формулу где R1, R2, R3, R4, R5, R6, R7, R8, R9, m, n, p и Y имеют значения, указанные выше. Более конкретно, если n равно 2, р равно 2, Y означает -S(O2)-, a R1, R2, R5, R6, R7 и R8 означают водород, то соединения формулы I имеют формулу где R3 и R9 имеют значения, указанные выше. Еще в одном варианте изобретения R3 означает необязательно замещенный фенил или необязательно замещенный нафтил. Более предпочтительно R3 означает фенил, 2-фторфенил, 2-хлорфенил, 3,4-дихлорфенил, 4-хлорфенил, 3-хлорфенил, 4-метоксифенил, 3,5-дихлорфенил, 2,6-дихлорфенил, 2,4-дихлорфенил, 3-метансульфониламинофенил, 2-метансульфонилфенил, 2-карбамоилфенил, 3-метансульфонилфенил, 4-метансульфонилфенил, 3-фторфенил, нафтил, 2,4-дифторфенил, 2-цианофенил, 2-хлор-4-фторфенил, 2-метил-5-фторфенил или 5-хлорнафтил. В другом варианте изобретения R3 предпочтительно означает фенил или галогензамещенный фенил. Более предпочтительно R3 означает фенил, 2-хлорзамещенный фенил или 2-фторзамещенный фенил. Кроме того, комбинации предпочтительных групп, указанных выше, образуют другие предпочтительные варианты осуществления изобретения. Благодаря этому настоящее изобретение включает множество предпочтительных соединений. Типичные соединения формулы I по настоящему изобретению приводятся в табл. 1. В таблице также приводятся номера примеров, в которых описано получение указанных соединений. Другим объектом настоящего изобретения является композиция, включающая терапевтически эффективное количество соединения формулы I и фармацевтически приемлемый носитель. Другим объектом изобретения является способ получения соединения формулы I. Соединения по настоящему изобретению получают различными методами, показанными на схемах и описанными ниже. Исходные материалы и реагенты, которые используются при получении указанных соединений, являются коммерческими препаратами, поставляемыми фирмами, такими как Aldrich Chemical Co., или их получают методами, известными специалисту в данной области, по методикам, описанным в литературе,такой как Fieser и Fieser's Reagents for Organic Synthesis, WileySons, New York, т.1-15 (1991), Rodd'sChemistry of Carbon Compounds, Elsevier Science Publishers, т.1-5 и Supplemental (1989) и Organic Reactions,WileySons: New York, т.1-40 (1991). Следующие схемы реакций лишь иллюстрируют некоторые методы синтеза соединений по настоящему изобретению, а различные модификации этих схем реакций могут быть разработаны и предложены специалистом в данной области со ссылкой на материалы настоящей заявки. Исходные материалы и промежуточные соединения в указанных схемах реакций можно получить и при необходимости очистить соответствующими способами, включая, без ограничения перечисленным,фильтрование, перегонку, кристаллизацию, хроматографию и т.п. Такие материалы можно охарактеризовать соответствующими методами, включая физические константы и спектральные данные. Если не указано иное, описанные реакции предпочтительно проводят в атмосфере инертного газа при атмосферном давлении и при температуре от приблизительно -78 до приблизительно 150C, более предпочтительно от приблизительно 0 до приблизительно 125C и наиболее предпочтительно и обычно при комнатной температуре, например при 20C. В одном варианте изобретения соединения формулы I получают при взаимодействии галогенарила формулы VI Реакции конденсации соединения формулы VI с соединением формулы R3-Y-W проводят в условиях, описанных выше для конденсации соединения формулы V с указанным активированным реагентом конденсации. Затем полученное соединение формулы VII, содержащее галогенированный фенил, конденсируют с гетероциклильным соединением формулы в присутствии катализатора конденсации с образованием соединения формулы I. Реакцию проводят в условиях, описанных выше для конденсации соединения формулы II с соединением формулы III. Более подробно условия получения соединений формулы I описаны в разделе "Примеры". Соединения по изобретению проявляют селективность в отношении рецептора 5-НТ 6 и могут применяться для лечения некоторых нарушений ЦНС, таких как болезнь Паркинсона, болезнь Гентингтона,тревога, депрессия, маниакальная депрессия, психоз, эпилепсия, навязчивые компульсивные нарушения,мигрень, болезнь Альцгеймера (для усиления познавательной способности), нарушения сна, нарушения питания, такие как анорексия и булимия, приступы паники, нарушение в форме гиперактивности при недостатке внимания (ADHD), недостаток внимания (ADD), синдром отмены при злоупотреблении лекарственными средствами, такими как кокаин, этанол, никотин и бензодиазепины, шизофрения, и также нарушений, ассоциированных с травмой спинного мозга и/или травмой головного мозга, такой как гидроцефалия. Кроме того, предполагается, что такие соединения могут применяться для лечения некоторых нарушений желудочно-кишечного тракта, таких как функциональное нарушение кишечника. Фармакологические свойства соединений по настоящему изобретению исследуют по известным методикам. Методика определения сродства анализируемых соединений с рецептором 5-НТ 6 по связыванию радиоактивно меченного лиганда in vitro и методика проведения функциональных испытаний описаны в примере 4. Настоящее изобретение включает фармацевтические композиции, содержащие по меньшей мере одно соединение по изобретению или фармацевтически приемлемую соль, в смеси по меньшей мере с одним фармацевтически приемлемым носителем и необязательно с другими терапевтическими и/или профилактическими ингредиентами. В общем случае, соединения по настоящему изобретению вводят в терапевтически эффективном количестве любыми приемлемыми способами введения, принятыми для агентов аналогичного назначения. Пригодные дозы обычно составляют 1-500 мг в сутки, предпочтительно 1-100 мг в сутки и наиболее предпочтительно 1-30 мг в сутки, в зависимости от множества факторов, таких как тяжесть излечиваемого заболевания, возраст и относительное состояние здоровья субъекта, активность используемого соединения, способ и форма введения, показания, на основании которых назначается введение лекарственного средства, опыт и квалификации лечащего врача. Специалист по указанным заболеваниям без особых экспериментов, на основании своего опыта и описания настоящего изобретения, сможет определить терапевтически эффективное количество соединений по настоящему изобретению, необходимое для данного заболевания.- 13009982 В общем случае, соединения по настоящему изобретению вводят в виде фармацевтических композиций, включающих композиции, пригодные для перорального (включая трансбуккальный и сублингвальный (подъязычный, ректального, назального, местного, легочного, вагинального или парентерального (включая внутримышечный, внутриартериальный, подоболочечный, подкожный и внутривенный) способов введения или в форме, пригодной для введения ингаляционным способом или вдуванием. Предпочтительным способом введения обычно является пероральный способ при соответствующей суточной схеме приема лекарственного средства, которая назначается в соответствии с тяжестью заболевания. Соединение или соединения по настоящему изобретению в смеси с одним или более соответствующих адъювантов, носителей или разбавителей можно изготовлять в форме фармацевтических композиций и стандартных доз. Фармацевтические композиции и стандартные дозы могут включать соответствующие ингредиенты в соответствующих пропорциях, могут содержать или не содержать дополнительные активные соединения или составные части, а стандартные дозы могут содержать любое приемлемое эффективное количество активного ингредиента в соответствии с назначенной суточной схемой применения лекарственного средства. Фармацевтические композиции могут использоваться в виде твердых форм, таких как таблетки или заполненные капсулы, в виде полутвердых, порошкообразных составов пролонгированного действия, или жидкостей, таких как растворы, суспензии, эмульсии, эликсиры, или заполненных капсул для перорального введения; или в форме суппозиториев для ректального или вагинального введения; или в форме стерильных инъекционных растворов для парентерального введения. Для типичных стандартных доз пригодны составы, содержащие в таблетке приблизительно 1 мг активного ингредиента или, в более общем виде, от приблизительно 0,01 до приблизительно 100 мг. Соединения по настоящему изобретению можно изготовить в виде множества форм для перорального введения. Фармацевтические композиции и дозировки могут включать в качестве активного компонента соединение или соединения по настоящему изобретению или их фармацевтически приемлемые соли. Фармацевтически приемлемые носители могут иметь твердую или жидкую консистенцию. Твердые формы препаратов включают порошки, таблетки, пилюли, капсулы, крахмальные облатки, суппозитории и диспергируемые гранулы. Твердый носитель может представлять собой одно или более веществ,которые могут действовать как разбавители, ароматизаторы, солюбилизаторы, замасливатели, суспендирующие агенты, связующие агенты, консерванты, дезинтегрирующие агенты или инкапсулирующий материал. При изготовлении в виде порошков носитель обычно представляет собой тонкоизмельченное твердое вещество, которое находится в смеси с тонкоизмельченным активным компонентом. При изготовлении таблеток активный компонент обычно смешивают с носителем, содержащим связующий компонент в соответствующей пропорции, и прессуют в таблетки необходимой формы и размера. Порошки и таблетки предпочтительно содержат от приблизительно 1 до приблизительно 70% активного соединения. Пригодные носители включают, без ограничения перечисленным, карбонат магния, стеарат магния,тальк, сахарозу, лактозу, пектин, декстрин, крахмал, желатин, трагакант, метилцеллюлозу, натриевую соль карбоксиметилцеллюлозы, низкоплавкий воск, масло какао и т.п. Предполагается, что термин "препарат" включает композицию активного соединения с инкапсулирующим материалом-носителем, при условии, что капсула содержит активный компонент в смеси с носителями или без них, причем активный компонент окружен носителем, который контактирует с активным компонентом. Аналогичное определение относится к облаткам и лепешкам. Таблетки, порошки, капсулы, пилюли, облатки и лепешки представляют собой твердые формы, пригодные для перорального введения. Другие формы, пригодные для перорального введения, включают жидкие формы препаратов,включающие эмульсии, сиропы, эликсиры, водные растворы, водные суспензии или твердые формы препаратов, которые непосредственно перед применением переводят в жидкую форму. Эмульсии можно получать в растворах, например в водных растворах пропиленгликоля, или они могут содержать эмульгирующие агенты, например такие, как лецитин, моноолеат сорбита или аравийская камедь. Водные растворы получают, растворяя активный компонент в воде и добавляя соответствующие красители, ароматизаторы,стабилизаторы и загустители. Водные суспензии готовят диспергированием тонкоизмельченного активного компонента в воде, содержащей вязкий материал, такой как природные или синтетические камеди, смолы, метилцеллюлоза, натриевая соль карбоксиметилцеллюлозы и прочие известные суспендирующие агенты. Жидкие формы препаратов включают растворы, суспензии и эмульсии и могут содержать, наряду с активным компонентом, красители, ароматизаторы, стабилизирующие агенты, буферные вещества, искусственные и природные подсластители, диспергирующие агенты, загустители,солюбилизирующие агенты и т.п. Соединения по настоящему изобретению можно получать в форме для парентерального введения(например, инъекцией, например инъекцией струйным вливанием или непрерывным вливанием) и можно поставлять в форме стандартной дозы в ампулах, одноразовых шприцах, небольших контейнерах для вливания или контейнерах с несколькими дозами, содержащих консервант. Композиции могут иметь форму суспензий, растворов или эмульсий в масляном или водном связующем, например растворов в водном полиэтиленгликоле. Примеры масляных или неводных носителей, разбавителей, растворов или связующих включают пропиленгликоль, полиэтиленгликоль, растительные масла (например, оливковое масло) и сложные эфиры органических кислот, пригодные для инъекций (например, этилолеат), и могут- 14009982 содержать дополнительные компоненты, такие как консервирующие, смачивающие, эмульгирующие или суспендирующие, стабилизирующие и/или диспергирующие агенты. В другом варианте активный ингредиент может находиться в порошкообразной форме, полученной выделением стерильного твердого вещества в асептических условиях или лиофилизацией раствора, для смешивания перед употреблением с соответствующим носителем, например стерильной, апирогенной водой. Соединения по настоящему изобретению можно получать для местного нанесения на эпидермис в виде мазей, кремов или лосьонов или в виде чрескожного пластыря. Например, мази и кремы получают на водной или масляной основе при добавлении пригодных загустителей и/или желирующих агентов. Лосьоны получают на водной или на масляной основе, кроме того, обычно содержащей один или более эмульгирующих агентов, стабилизирующих агентов, диспергирующих агентов, суспендирующих агентов, загущающих агентов или красителей. Составы, пригодные для местного введения в ротовую полость, представляют собой лепешки, включающие активные ингредиенты в смеси с ароматизированной основой, обычно с сахарозой и аравийской камедью или трагакантом; пастилки, включающие активный ингредиент на инертной основе, такой как желатин и глицерин или сахароза и аравийская камедь; и раствор для полоскания, включающий активный ингредиент в соответствующем жидком носителе. Соединения по настоящему изобретению можно получать в форме суппозиториев. Низкоплавкий воск, такой как смесь глицеридов жирных кислот или масло какао, сначала расплавляют, а затем в нем равномерно диспергируют активный компонент, например, перемешиванием. Расплавленную гомогенную смесь выливают в формы соответствующего размера и охлаждают для приобретения твердой консистенции. Соединения по настоящему изобретению можно получать для вагинального введения. Пригодными являются вагинальные суппозитории, тампоны, кремы, гели, пасты, пены и спреи, содержащие наряду с активным ингредиентом носители, известные в данной области техники. Соединения по настоящему изобретению можно получать для назального введения. Растворы или суспензии вводят непосредственно в носовую полость обычными способами, например капельницей,пипеткой или спреем. Составы могут поставляться в форме, содержащий одну или несколько доз. В случае капельницы или пипетки пациенту вводят определенный объем раствора или суспензии. Аэрозоли вводят дозирующим пульверизатором. Соединения по настоящему изобретению можно получать для аэрозольного введения, прежде всего,в дыхательные пути, включая интраназальное введение. Обычно частицы соединения имеют небольшие размеры, например приблизительно 5 или менее мкм. Такой размер частиц получают известными методами, например измельчением на микронной коллоидной мельнице (микронизацией). Активный ингредиент получают в герметичной упаковке с соответствующим газом-вытеснителем, таким как хлорфторуглерод (ХФУ), например дихлордифторметан, трихлорфторметан, или дихлортетрафторэтан, или диоксид углерода, или другой приемлемый газ. Аэрозоль может также содержать ПАВ, такое как лецитин. Доза лекарственного средства регулируется дозирующим клапаном. В другом варианте активные ингредиенты готовят в форме сухого порошка, например порошкообразной смеси соединения с соответствующей порошкообразной основой, такой как лактоза, крахмал, производные крахмала, такие как гидроксипропилметилцеллюлоза и поливинилпирролидон (ПВП). В полости носа порошкообразный носитель образует гель. Порошкообразную композицию можно изготовить в виде стандартной дозы, например в капсулах или картриджах, например, в желатиновой или блистерной упаковке, из которой порошок можно вводить ингалятором. При необходимости составы можно получать с энтеросолюбильным покрытием для введения с замедленным или регулируемым высвобождением активного ингредиента. Например, соединения по настоящему изобретению можно получать в виде систем для чрескожной и подкожной доставки. Эти системы обладают преимуществом в тех случаях, когда необходимо замедленное высвобождение соединения или если решающим фактором является согласие пациента с назначенным курсом лечения. В чрескожных системах доставки соединение часто фиксируют на твердой подложке, которую наклеивают на кожу. Указанное соединение может также находиться в комбинации с усилителем всасывания, например азоном (1-додецилазациклогептан-2-он). Системы замедленного высвобождения вводятся подкожно в субдермальный слой хирургом или с использованием инъекции. В подкожных имплантатах соединение включено в липидную растворимую мембрану, например в силиконовый каучук, или биодеградируемый полимер, например полимолочную кислоту. Фармацевтические препараты предпочтительно представляют собой стандартные лекарственные формы. В такой форме препарат разделен на стандартные дозы, содержащие соответствующие количества активного компонента. Стандартная форма может представлять собой упакованный препарат, причем упаковка содержит дискретные количества препарата, такие как упакованные таблетки, капсулы и порошки во флаконах или ампулах. Кроме того, стандартная форма может представлять собой капсулу,таблетку, облатку или лепешку или может представлять собой упаковку, содержащую определенное количество любой из указанных форм. Прочие фармацевтически приемлемые носители и их составы описаны в книге Remington, The Science- 15009982 Типичные фармацевтические составы, содержащие соединение по настоящему изобретению, описаны в примерах 6-12. Примеры Пример 1. В примере описан способ получения соединений формулы I по следующей схеме. Способ А. Синтез бензилового эфира 8-бром-6-хлор-2,3-дигидробензо[1,4]оксазин-4-карбоновой кислоты. К раствору 8-бром-6-хлор-3,4-дигидро-2 Н-бензо[1,4]оксазина (2,85 г, 0,01 моля) в смеси этилацетата (30 мл) и 10% раствора гидроксида натрия (30 мл) (1:1) добавляли по каплям бензилхлорформиат(1,877 г, 0,011 моля) и смесь перемешивали при комнатной температуре в течение 3 ч. Затем слои разделяли, органическую фазу промывали водой (250 мл), насыщенным раствором бикарбоната натрия (50 мл),сушили (K2CO3) и концентрировали в вакууме. Остаток очищали хроматографией на колонке с силикагелем (элюент: гексан/этилацетат, 7:3, об./об.), при этом получали бензиловый эфир 8-бром-6-хлор-2,3 дигидробензо[1,4]оксазин-4-карбоновой кислоты в виде масла (3,47 г, 98%). Продукт перекристаллизовывали из этанола/воды. tпл. 95,0-97,7 С. MC: 383 (MH+). По аналогичной методике получали бензиловый эфир 8-бром-2,3-дигидробензо[1,4]оксазин-4-карбоновой кислоты (81%),бензиловый эфир 8-бром-6-метокси-2,3-дигидробензо[1,4]оксазин-4-карбоновой кислоты,бензиловый эфир 8-бром-6-фтор-2,3-дигидробензо[1,4]оксазин-4-карбоновой кислоты и бензиловый эфир 8-бром-6-трет-бутил-2,3-дигидробензо[1,4]оксазин-4-карбоновой кислоты. Способ Б. Синтез бензилового эфира 8-бром-6-метил-2,3-дигидробензо[1,4]оксазин-4-карбоновой кислоты. К раствору 8-бром-6-метил-3,4-дигидро-2 Н-бензо[1,4]оксазина (1,78 г, 0,007 моля) и пиридина (1,06 г,0,013 моля) в дихлорметане (40 мл) при охлаждении на ледяной бане в атмосфере азота добавляли по каплям раствор бензилхлорформиата (1,32 г, 0,008 моля) в дихлорметане (20 мл) и смесь перемешивали- 16009982 при комнатной температуре в течение 1 ч. Затем к смеси добавляли 10% соляную кислоту, слои разделяли, органическую фазу промывали водой (250 мл), сушили (Na2SO4) и концентрировали, при этом получали бензиловый эфир 8-бром-6-метил-2,3-дигидробензо[1,4]оксазин-4-карбоновой кислоты в виде бесцветного масла (2,34 г, 96%), который использовали на стадии 2 без дополнительной очистки. Стадия 2. Синтез 8-(4-трет-бутоксикарбонилпиперазин-1-ил)-6-хлор-2,3-дигидробензо[1,4]оксазин 4-карбоновой кислоты. В трехгорлую колбу помещали трис-(дибензилиденацетон)дипалладий(0) (21,5 мг, 0,024 ммоля, 2 мол.%(159 мг, 1,65 ммоля) и через смесь пропускали ток азота. Затем добавляли раствор бензилового эфира 8 бром-6-хлор-2,3-дигидробензо[1,4]оксазин-4-карбоновой кислоты (450 мг, 1,18 ммоля) и трет-бутиловго эфира пиперазин-1-карбоновой кислоты (263 мг, 1,41 ммоля) в толуоле (2 мл). Смесь нагревали до 95C и перемешивали в течение 12 ч. Затем смесь охлаждали до комнатной температуры, переносили в этилацетат, фильтровали через целит и фильтрат концентрировали. Неочищенный продукт очищали экспресс-хроматографией на силикагеле (элюент: гексан/этилацетат, 7:3, об./об.), при этом получали бензиловый эфир 8-(4-трет-бутоксикарбонилпиперазин-1-ил)-6-хлор-2,3-дигидробензо[1,4]оксазин-4-карбоновой кислоты в виде бесцветного масла (275 мг, 48%). MC: 488 (MH+). По аналогичной методике при использовании соответственно замещенного метил-3,4-дигидро-2 Нбензо[1,4]оксазина получали следующие соединения: бензиловый эфир 8-(4-трет-бутоксикарбонилпиперазин-1-ил)-2,3-дигидробензо[1,4]оксазин-4-карбоновой кислоты (66%),бензиловый эфир 8-(4-трет-бутоксикарбонилпиперазин-1-ил)-6-метил-2,3-дигидробензо[1,4]оксазин 4-карбоновой кислоты (58%),бензиловый эфир 8-(4-трет-бутоксикарбонилпиперазин-1-ил)-6-метокси-2,3-дигидробензо[1,4]оксазин 4-карбоновой кислоты,бензиловый эфир 8-(4-трет-бутоксикарбонилпиперазин-1-ил)-6-фтор-2,3-дигидробензо[1,4]оксазин 4-карбоновой кислоты и бензиловый эфир 8-(4-трет-бутоксикарбонилпиперазин-1-ил)-6-трет-бутил-2,3-дигидробензо[1,4]оксазин-4-карбоновой кислоты. По аналогичной методике при замене 1 8-бром-6-метил-3,4-дигидро-2 Н-бензо[1,4]оксазина на стадии 1 на 6-бром-3,4-дигидро-2 Н-бензо[1,4]оксазин получали бензиловый эфир 6-(4-трет-бутоксикарбонилпиперазин-1-ил)-2,3-дигидробензо[1,4]оксазин-4-карбоновой кислоты. Стадия 3. Способ А. Синтез трет-бутилового эфира 4-(6-хлор-3,4-дигидро-2 Н-бензо[1,4]оксазин-8-ил)пиперазин-1-карбоновой кислоты (R1 означает Cl). Раствор бензилового эфира 8-(4-трет-бутоксикарбонилпиперазин-1-ил)-6-хлор-2,3-дигидробензо[1,4] оксазин-4-карбоновой кислоты (870 мг, 1,79 ммоля) в этаноле (10 мл) гидрировали при атмосферном давлении в присутствии 10% Pd/C (75 мг) в течение 0,5 ч. Катализатор удаляли фильтрованием и фильтрат концентрировали. Неочищенный продукт очищали экспресс-хроматографией на силикагеле (элюент: гексан/этилацетат, 1:1, об./об.), при этом получали трет-бутиловый эфир 4-(6-хлор-3,4-дигидро-2 Н-бензо[1,4] оксазин-8-ил)пиперазин-1-карбоновой кислоты в виде пены белого цвета (450 мг, 71%). MC: 354 (MH+). По аналогичной методике получали следующие соединения:(95%), MC: 320 (MH+),трет-бутиловый эфир 4-(6-метил-3,4-дигидро-2 Н-бензо[1,4]оксазин-8-ил)пиперазин-1-карбоновой кислоты (95%), MC: 334 (MH+) и трет-бутиловый эфир 4-(3,4-дигидро-2 Н-бензо[1,4]оксазин-6-ил)пиперазин-1-карбоновой кислоты. Способ Б. Синтез трет-бутилового эфира 4-(3,4-дигидро-2 Н-бензо[1,4]оксазин-8-ил)-пиперазин-1 карбоновой кислоты (R1 означает H). Раствор бензилового эфира 8-(4-трет-бутоксикарбонилпиперазин-1-ил)-6-хлор-2,3-дигидробензо[1,4] оксазин-4-карбоновой кислоты (640 мг, 1,32 ммоля) в этаноле (10 мл) гидрировали при 50 фунтов/кв.дюйм в присутствии палладия на угле в течение 12 ч. Катализатор удаляли фильтрованием и фильтрат концентрировали, при этом получали трет-бутиловый эфир 4-(3,4-дигидро-2 Н-бензо[1,4]оксазин-8-ил)пиперазин-1-карбоновой кислоты в виде твердого вещества светло-желтого цвета (350 мг, 84%). MC: 320 (MH+). По аналогичной методике получали следующие соединения: трет-бутиловый эфир 4-(6-метокси-3,4-дигидро-2 Н-бензо[1,4]оксазин-8-ил)пиперазин-1-карбоновой кислоты,трет-бутиловый эфир 4-(6-фтор-3,4-дигидро-2 Н-бензо[1,4]оксазин-8-ил)пиперазин-1-карбоновой кислоты и трет-бутиловый эфир 4-(6-трет-бутил-3,4-дигидро-2 Н-бензо[1,4]оксазин-8-ил)пиперазин-1-карбоновой кислоты. Стадия 4. Синтез 6-хлор-4-(3-метансульфонилбензолсульфонил)-8-пиперазин-1-ил-3,4-дигидро-2 Нбензо[1,4]оксазина. К раствору трет-бутилового эфира 4-(6-хлор-3,4-дигидро-2 Н-бензо[1,4]оксазин-8-ил)пиперазин-1 карбоновой кислоты (101 мг, 0,285 ммоля) и пиридина (50 мг, 0,628 ммоля) в дихлорметане (2 мл) на ледяной бане в атмосфере азота добавляли небольшими порциями 3-метансульфонилбензолсульфонилхлорид(80 мг, 0,314 ммолей) и полученную смесь перемешивали при комнатной температуре в течение 1,5 ч. Затем к смеси добавляли воду, слои разделяли, органическую фазу промывали насыщенным раствором бикарбоната натрия (20 мл), сушили (Na2SO4) и концентрировали, при этом получали трет-бутиловый эфир 4-[6-хлор-4-(3-метансульфонилбензолсульфонил)-3,4-дигидро-2 Н-бензо[1,4]оксазин-8-ил]пиперазин 1-карбоновой кислоты в виде масла (150 мг, 91%). Неочищенный продукт растворяли в этаноле (1 мл) и добавляли 10% раствор хлористого водорода в этаноле (1 мл). Смесь нагревали на паровой бане в течение 15 мин. При охлаждении до комнатной температуры в смеси выпадали кристаллы белого цвета, которые отделяли фильтрованием, промывали холодным этанолом и высушивали в вакууме, при этом получали гидрохлорид 6-хлор-4-(3-метансульфонилбензолсульфонил)-8-пиперазин-1-ил-3,4-дигидро-2 Н-бензо[1,4]оксазина в виде порошка белого цвета(130 мг, 95%). tпл. 147,2-153C. MC: 472 (MH+). По аналогичной методике при замене 3-метилсульфонилбезолсульфонилхлорида на соответствующие арилсульфонилхлориды и при последующем удалении защитных групп в трифторуксусной кислоте получали следующие соединения: трифторацетат 6-хлор-4-(3-фторбензолсульфонил)-8-пиперазин-1-ил-3,4-дигидро-2 Н-бензо[1,4]оксазина, MC: 412 (MH+),трифторацетат 6-хлор-4-(2,4-дифторбензолсульфонил)-8-пиперазин-1-ил-3,4-дигидро-2 Н-бензо[1,4] оксазина, MC: 430 (MH+),трифторацетат 6-хлор-4-(2,3-дихлорбензолсульфонил)-8-пиперазин-1-ил-3,4-дигидро-2 Н-бензо[1,4] оксазина, MC: 463 (MH+),трифторацетат 6-хлор-4-(2-хлор-4-фторбензолсульфонил)-8-пиперазин-1-ил-3,4-дигидро-2 Н-бензо[1,4]оксазина. По аналогичной методике при замене трет-бутилового эфира пиперазин-1-карбоновой кислоты на стадии 2 на N-метилпиперазин, при использовании соответствующих арил- или гетероарилхлоридов на стадии 4 и при последующем удалении защитных групп в HCl получали следующие соединения: гидрохлорид 6-хлор-8-(4-метилпиперазин-1-ил)-4-(нафталин-2-сульфонил)-3,4-дигидро-2 Н-бензо[1,4]оксазин получали по реакции 6-хлор-4-(2-фторбензолсульфонил)-8-пиперазин-1-ил-3,4-дигидро-2 Нбензо[1,4]оксазина с формальдегидом в водной среде в присутствии NaBH(OAc)3. Аналогичным образом 6-хлор-8-(4-метилпиперазин-1-ил)-4-(нафталин-2-сульфонил)-3,4-дигидро-2 Н-бензо[1,4]оксазин получали по реакции 6-хлор-4-(нафталин-1-сульфонил)-8-пиперазин-1-ил-3,4-дигидро-2 Н-бензо[1,4]оксазина с формальдегидом и NaBH(OAc)3 в водной среде. Аналогичным образом при замене трет-бутилового эфира 4-(6-хлор-3,4-дигидро-2 Н-бензо[1,4]оксазин-8-ил)пиперазин-1-карбоновой кислоты на трет-бутиловый эфир 4-(3,4-дигидро-2 Н-бензо[1,4]оксазин-8-ил)пиперазин-1-карбоновой кислоты, при замене 3-метилсульфонилбензолсульфонилхлорида на соответствующие арил- или гетероарилсульфонилхлориды и при последующем удалении защитных групп в трифторуксусной кислоте или при нагревании в растворе хлористого водорода в этаноле получали следующие соединения: трифторацетат 4-(4-хлорбензолсульфонил)-8-пиперазин-1-ил-3,4-дигидро-2 Н-бензо[1,4]оксазина, MC: 390 (MH+),трифторацетат 4-(3-хлорбензолсульфонил)-8-пиперазин-1-ил-3,4-дигидро-2 Н-бензо[1,4]оксазина, MC: 390 (MH+),трифторацетат 4-(3,4-дихлорбензолсульфонил)-8-пиперазин-1-ил-3,4-дигидро-2 Н-бензо[1,4]оксазина,MC: 429 (MH+),трифторацетат 4-(2,3-дихлорбензолсульфонил)-8-пиперазин-1-ил-3,4-дигидро-2 Н-бензо[1,4]оксазина,MC: 429 (MH+),трифторацетат 4-(2,6-дихлорбензолсульфонил)-8-пиперазин-1-ил-3,4-дигидро-2 Н-бензо[1,4]оксазина,MC: 429 (MH+),трифторацетат 4-(2,4-дихлорбензолсульфонил)-8-пиперазин-1-ил-3,4-дигидро-2 Н-бензо[1,4]оксазина,MC: 429 (MH+),трифторацетат 4-(3,5-дихлорбензолсульфонил)-8-пиперазин-1-ил-3,4-дигидро-2 Н-бензо[1,4]оксазина,MC: 429 (MH+),трифторацетат 4-(4-метоксибензолсульфонил)-8-пиперазин-1-ил-3,4-дигидро-2 Н-бензо[1,4]оксазина,MC: 429 (MH+),трифторацетат 8-пиперазин-1-ил-4-(хинолин-8-сульфонил)-3,4-дигидро-2 Н-бензо[1,4]оксазина, MC: 411 (MH+),гидрохлорид 4-бензолсульфонил-8-пиперазин-1-ил-3,4-дигидро-2 Н-бензо[1,4]оксазина в виде порошка белого цвета, tпл. 235,8-239,5C, MC: 360 (MH+),гидрохлорид 4-(2-хлорбензолсульфонил)-8-пиперазин-1-ил-3,4-дигидро-2 Н-бензо[1,4]оксазина в виде порошка белого цвета, tпл. 246,9-248,8C, MC: 390 (MH+),гидрохлорид 4-(3-фторбензолсульфонил)-8-пиперазин-1-ил-3,4-дигидро-2 Н-бензо[1,4]оксазина в виде порошка белого цвета, tпл. 186,6-187,9C, MC: 378 (MH+),гидрохлорид 4-(2-фторбензолсульфонил)-8-пиперазин-1-ил-3,4-дигидро-2 Н-бензо[1,4]оксазина в виде порошка белого цвета, tпл. 258,7-259,4C, MC: 378 (MH+),гидрохлорид 4-(3-метансульфонилбензолсульфонил)-8-пиперазин-1-ил-3,4-дигидро-2 Н-бензо[1,4]оксазина в виде порошка белого цвета, tпл. 193,9-203,8C, MC: 438 (MH+),гидрохлорид 4-(2-метансульфонилбензолсульфонил)-8-пиперазин-1-ил-3,4-дигидро-2 Н-бензо[1,4]ок- 19009982 сазина в виде порошка белого цвета, tпл. 168,7-171,9C, MC: 438 (MH+),гидрохлорид 4-(2,3-дихлорбензолсульфонил)-8-пиперазин-1-ил-3,4-дигидро-2 Н-бензо[1,4]оксазина в виде порошка белого цвета, tпл. 266,9-271,9C, MC: 429 (MH+),гидрохлорид 2-(8-пиперазин-1-ил-2,3-дигидробензо[1,4]оксазин-4-сульфонил)фенола, MC: 374 (MH+),гидрохлорид 4-(2-метоксибензолсульфонил)-8-пиперазин-1-ил-3,4-дигидро-2 Н-бензо[1,4]оксазина,MC: 388 (MH+),гидрохлорид 6-пиперазин-1-ил-4-(4-пиперазин-1-илбензолсульфонил)-3,4-дигидро-2 Н-бензо[1,4]оксазина, MC: 443 (MH+),2-(8-пиперазин-1-ил-2,3-дигидробензо[1,4]оксазин-4-сульфонил)бензамид. Аналогичным образом при замене бензилового эфира 8-бром-6-хлор-2,3-дигидробензо[1,4]оксазин 4-карбоновой кислоты и трет-бутилового эфира пиперазин-1-карбоновой кислоты на стадии 2, соответственно, на бензиловый эфир 8-бром-2,3-дигидробензо[1,4]оксазин-4-карбоновой кислоты и метилпиперазин, при последующем использовании на стадии 4 соответствующего арилсульфонилхлорида и при последующем удалении защитных групп получали следующие соединения: гидрохлорид 4-(3-метансульфонилбензолсульфонил)-8-(4-метилпиперазин-1-ил)-3,4-дигидро-2 Н-бензо[1,4]оксазина, MC: 451 (MH+),гидрохлорид 4-бензолсульфонил-8-(4-метилпиперазин-1-ил)-3,4-дигидро-2 Н-бензо[1,4]оксазина, MC: 372 (MH+),гидрохлорид 4-(2-фторбензолсульфонил)-8-(4-метилпиперазин-1-ил)-3,4-дигидро-2 Н-бензо[1,4]оксазина, MC: 390 (MH+). Аналогичным образом при замене трет-бутилового эфира 4-(6-хлор-3,4-дигидро-2 Н-бензо[1,4]оксазин-8-ил)пиперазин-1-карбоновой кислоты на трет-бутиловый эфир 4-(5-метил-3,4-дигидро-2 Н-бензо[1,4]оксазин-8-ил)пиперазин-1-карбоновой кислоты, при замене 3-метилсульфонилбензолсульфонилхлорида на соответствующие арил- или гетероарилсульфонилхлориды и при последующем удалении защитных групп в трифторуксусной кислоте или при нагревании в растворе хлористого водорода в этаноле получали следующие соединения: трифторацетат 4-(2-фторбензолсульфонил)-6-метил-8-пиперазин-1-ил-3,4-дигидро-2 Н-бензо[1,4]оксазина, MC: 390 (MH+),трифторацетат 2-(6-метил-8-пиперазин-1-ил-2,3-дигидробензо[1,4]оксазин-4-сульфонил)бензонитрила,MC: 397 (MH+),трифторацетат 6-метил-8-пиперазин-1-ил-4-(тиофен-2-сульфонил)-3,4-дигидро-2 Н-бензо[1,4]оксазина,MC: 379 (MH+),трифторацетат 6-метил-8-пиперазин-1-ил-4-(хинолин-8-сульфонил)-3,4-дигидро-2 Н-бензо[1,4]оксазина, MC: 424 (MH+),трифторацетат 4-(3-фторбензолсульфонил)-6-метил-8-пиперазин-1-ил-3,4-дигидро-2 Н-бензо[1,4]оксазина, MC: 390 (MH+),трифторацетат 4-(2,4-дифторбензолсульфонил)-6-метил-8-пиперазин-1-ил-3,4-дигидро-2 Н-бензо[1,4] оксазина, MC: 408 (MH+),трифторацетат 4-(2-хлор-4-фторбензолсульфонил)-6-метил-8-пиперазин-1-ил-3,4-дигидро-2 Н-бензо[1,4]оксазина, MC: 425 (MH+),трифторацетат 4-(5-фтор-2-метилбензолсульфонил)-6-метил-8-пиперазин-1-ил-3,4-дигидро-2 Н-бензо[1,4]оксазина, MC: 404 (MH+),трифторацетат 4-(изохинолин-5-сульфонил)-6-метил-8-пиперазин-1-ил-3,4-дигидро-2 Н-бензо[1,4]оксазина, MC: 424 (MH+),трифторацетат 6-метил-4-(1-метил-1 Н-имидазол-4-сульфонил)-8-пиперазин-1-ил-3,4-дигидро-2 Н-бензо[1,4]оксазина, MC: 376 (MH+),трифторацетат 4-бензолсульфонил-6-метил-8-пиперазин-1-ил-3,4-дигидро-2 Н-бензо[1,4]оксазина,трифторацетат 4-(2-хлорбензолсульфонил)-6-метил-8-пиперазин-1-ил-3,4-дигидро-2 Н-бензо[1,4]оксазина,трифторацетат 2-(6-метил-8-пиперазин-1-ил-2,3-дигидробензо[1,4]оксазин-4-сульфонил)фенола. Аналогичным образом при замене трет-бутилового эфира 4-(6-хлор-3,4-дигидро-2 Н-бензо[1,4]оксазин-8-ил)пиперазин-1-карбоновой кислоты на трет-бутиловый эфир 4-(6-метокси-3,4-дигидро-2 Н-бензо[1,4]оксазин-8-ил)пиперазин-1-карбоновой кислоты, при замене 3-метилсульфонилбензолсульфонилхлорида на соответствующие арил- или гетероарилсульфонилхлориды и при последующем удалении защитных групп в трифторуксусной кислоте или при нагревании в растворе хлористого водорода в этаноле получали следующие соединения: гидрохлорид 4-(2-фторбензолсульфонил)-6-метокси-8-пиперазин-1-ил-3,4-дигидро-2 Н-бензо[1,4]оксазина, MC: 406 (MH+),гидрохлорид 4-бензолсульфонил-6-метокси-8-пиперазин-1-ил-3,4-дигидро-2 Н-бензо[1,4]оксазина, MC: 388 (MH+),гидрохлорид 4-(2,3-дигидробензо[1,4]диоксин-6-сульфонил)-6-метокси-8-пиперазин-1-ил-3,4-дигидро 2 Н-бензо[1,4]оксазина, MC: 447 (MH+),трифторацетат 6-метокси-4-(нафталин-1-сульфонил)-8-пиперазин-1-ил-3,4-дигидро-2 Н-бензо[1,4]ок- 20009982 сазина, MC: 439 (MH+),трифторацетат 4-(2-хлорбензолсульфонил)-6-метокси-8-пиперазин-1-ил-3,4-дигидро-2 Н-бензо[1,4]оксазина, MC: 423 (MH+),трифторацетат 4-(3-хлорбензолсульфонил)-6-метокси-8-пиперазин-1-ил-3,4-дигидро-2 Н-бензо[1,4]оксазина, MC: 423 (MH+),трифторацетат 4-(5-фтор-2-метилбензолсульфонил)-6-метокси-8-пиперазин-1-ил-3,4-дигидро-2 Н-бензо[1,4]оксазина, MC: 420 (MH+),трифторацетат 6-метокси-8-пиперазин-1-ил-4-(толуол-2-сульфонил)-3,4-дигидро-2 Н-бензо[1,4]оксазина, MC: 402 (MH+). Аналогичным образом при замене трет-бутилового эфира 4-(6-хлор-3,4-дигидро-2 Н-бензо[1,4]оксазин-8-ил)пиперазин-1-карбоновой кислоты на трет-бутиловый эфир 4-(6-фтор-3,4-дигидро-2 Н-бензо[1,4] оксазин-8-ил)пиперазин-1-карбоновой кислоты, при замене 3-метилсульфонилбензолсульфонилхлорида на соответствующие арил- или гетероарилсульфонилхлориды и при последующем удалении защитных групп в трифторуксусной кислоте или при нагревании в растворе хлористого водорода в этаноле получали следующие соединения: гидрохлорид 6-фтор-4-(2-фторбензолсульфонил)-8-пиперазин-1-ил-3,4-дигидро-2 Н-бензо[1,4]оксазина, MC: 394 (MH+),гидрохлорид 4-бензолсульфонил-6-фтор-8-пиперазин-1-ил-3,4-дигидро-2 Н-бензо[1,4]оксазина, MC: 376 (MH+),гидрохлорид 4-(2,3-дигидробензо[1,4]диоксин-6-сульфонил)-6-фтор-8-пиперазин-1-ил-3,4-дигидро 2 Н-бензо[1,4]оксазина, MC: 434 (MH+). Аналогичным образом при замене трет-бутилового эфира 4-(6-хлор-3,4-дигидро-2 Н-бензо[1,4]оксазин-8-ил)пиперазин-1-карбоновой кислоты на трет-бутиловый эфир 4-(6-трет-бутил-3,4-дигидро-2 Н-бензо[1,4]оксазин-8-ил)пиперазин-1-карбоновой кислоты, при замене 3-метилсульфонилбензолсульфонилхлорида на соответствующие арил- или гетероарилсульфонилхлориды и при последующем удалении защитных групп в трифторуксусной кислоте или в нагретом растворе хлористого водорода в этаноле получали гидрохлорид 6-трет-бутил-4-(2-фторбензолсульфонил)-8-пиперазин-1-ил-3,4-дигидро-2 Н-бензо[1,4]оксазина, MC: 433 (MH+). Аналогичным образом при замене трет-бутилового эфира 4-(6-хлор-3,4-дигидро-2 Н-бензо[1,4]оксазин-8-ил)пиперазин-1-карбоновой кислоты на трет-бутиловый эфир 4-(3,4-дигидро-2 Н-бензо[1,4]оксазин-6-ил)пиперазин-1-карбоновой кислоты и при замене 3-метилсульфонилбензолсульфонилхлорида на соответствующие арилсульфонилхлориды получали следующие соединения: гидрохлорид 4-(3-хлорбензолсульфонил)-6-пиперазин-1-ил-3,4-дигидро-2 Н-бензо[1,4]оксазина, tпл. 192,3-201,0C, MC: 390 (MH+),гидрохлорид 4-(2-хлорбензолсульфонил)-6-пиперазин-1-ил-3,4-дигидро-2 Н-бензо[1,4]оксазина, tпл. 180,1-186,1C, MC: 390 (MH+),гидрохлорид 4-(4-хлорбензолсульфонил)-6-пиперазин-1-ил-3,4-дигидро-2 Н-бензо[1,4]оксазина, MC: 390 (MH+),гидрохлорид 6-пиперазин-1-ил-4-(4-пиперазин-1-илбензолсульфонил)-3,4-дигидро-2 Н-бензо[1,4]оксазина, MC: 440 (MH+). Пример 2. Синтез N-[3-(8-пиперазин-1-ил-2,3-дигидробензо[1,4]оксазин-4-сульфонил)фенил]метансульфонамида. К раствору трет-бутилового эфира 4-(3,4-дигидро-2 Н-бензо[1,4]оксазин-8-ил)пиперазин-1-карбоновой кислоты (161 мг, 0,504 ммоля) и пиридина (88 мг, 1,11 ммоля) в дихлорметане (2 мл) на ледяной бане в атмосфере азота добавляли небольшими порциями 3-нитробензолсульфонилхлорид (122,9 мг, 0,55 ммоля) и полученную смесь перемешивали при комнатной температуре в течение 0,5 ч. Затем к смеси добавляли воду, органический слой отделяли, промывали насыщенным раствором бикарбоната натрия (20 мл), сушили (Na2SO4) и концентрировали, при этом получали трет-бутиловый эфир 4-[4-(3-нитробензолсульфонил)-3,4-дигидро-2 Н-бензо[1,4]оксазин-8-ил]пиперазин-1-карбоновой кислоты в виде масла (260 мг). Раствор неочищенного продукта, полученного по методике а, в этаноле (5 мл) гидрировали при атмосферном давлении в присутствии 10% Pd/C (50 мг) в течение 0,5 ч. Катализатор удаляли фильтрованием, фильтрат концентрировали, при этом получали трет-бутиловый эфир 4-[4-(3-аминобензолсульфонил)-3,4-дигидро-2 Н-бензо[1,4]оксазин-8-ил]пиперазин-1-карбоновой кислоты в виде твердого вещества белого цвета (150 мг). MC: 475 (MH+). Стадия 3. К раствору неочищенного продукта, полученного по методике б (145 мг, 0,31 ммоля), и триэтиламина(65 мг, 0,65 ммоля) в дихлорметане (2 мл) на ледяной бане в атмосфере азота добавляли по каплям раствор метансульфонилхлорида (75 мг, 0,64 ммоля) в дихлорметане (0,5 мл) и полученную смесь перемешивали при комнатной температуре в течение 1 ч. Затем к смеси добавляли воду (2 мл), слои разделяли, органическую фазу промывали водой (2 мл), сушили (Na2SO4) и концентрировали, при этом получали трет-бутиловый эфир 4-[4-(3-диметансульфониламинобензолсульфонил)-3,4-дигидро-2 Н-бензо[1,4]оксазин-8-ил] пиперазин-1-карбоновой кислоты в виде масла (50 мг, 25%). К раствору полученного промежуточного соединения в тетрагидрофуране (1 мл) добавляли 2 н. раствор гидроксида натрия (1 мл). Через 12 ч к смеси добавляли этилацетат (10 мл), слои разделяли, органическую фазу сушили (Na2SO4) и концентрировали. Защитную группу удаляли, как описано выше на стадии 4, при этом получали N-[3-(8-пиперазин-1-ил-2,3-дигидробензо[1,4]оксазин-4-сульфонил)фенил]метансульфонамид (25 мг, 30%) в виде порошка грязно-белого цвета. tпл. 158,5-163,5C. MC: 453 (MH+). По аналогичной методике при замене 3-нитробензолсульфонилхлорида на 2-нитробензолсульфонилхлорид получали N-[2-(8-пиперазин-1-ил-2,3-дигидробензо[1,4]оксазин-4-сульфонил)фенил]метансульфонамид. Пример 3. В примере описан способ получения соединений формулы I по следующей схеме.(381 мг, 4,82 ммоля) в дихлорметане (20 мл) при охлаждении на ледяной бане в атмосфере азота добавляли небольшими порциями 4-хлорбензолсульфонилхлорид (560 мг, 2,65 ммоля) и полученную смесь перемешивали при комнатной температуре в течение 12 ч. Затем к смеси добавляли воду, слои разделяли,органическую фазу промывали насыщенным раствором бикарбоната натрия (20 мл), сушили (Na2SO4) и концентрировали, при этом получали указанное в заголовке соединение в виде твердого вещества (820 мг,84%), которое перекристаллизовывали из этанола. tпл. 143,0-145,1C. MC: 401 (MH+). Аналогичным образом при замене 8-бром-6-метил-3,4-дигидро-2 Н-бензо[1,4]оксазина на 8-бром-6 хлор-3,4-дигидро-2 Н-бензо[1,4]оксазин или на 8-бром-3,4-дигидро-2 Н-бензо[1,4]оксазин и при использовании соответствующих арилсульфонилхлоридов получали следующие соединения: 8-бром-4-(3,4-дихлорбензолсульфонил)-6-метил-3,4-дигидро-2 Н-бензо[1,4]оксазин в виде порошка белого цвета, tпл. 150-151C, MC: 435 (M+),4-бензолсульфонил-8-бром-6-хлор-3,4-дигидро-2 Н-бензо[1,4]оксазин, MC: 387 (M+),8-бром-6-хлор-4-(2-хлорбензолсульфонил)-3,4-дигидро-2 Н-бензо[1,4]оксазин в виде твердого вещества белого цвета, MC: 422 (M+),8-бром-6-хлор-4-(2-фторбензолсульфонил)-3,4-дигидро-2 Н-бензо[1,4]оксазин в виде твердого вещества белого цвета, MC: 405 (M+),8-бром-6-хлор-4-(нафталин-1-сульфонил)-3,4-дигидро-2 Н-бензо[1,4]оксазин в виде твердого вещества белого цвета, MC: 437 (M+),8-бром-4-(3-хлорбензолсульфонил)-3,4-дигидро-2 Н-бензо[1,4]оксазин в виде масла, которое затвердевало при хранении. Стадия 2. Способ А. Синтез 4-(4-хлорбензолсульфонил)-6-метил-8-пиперазин-1-ил-3,4-дигидро-2 Н-бензо[1,4] оксазина. В трехгорлую колбу помещали трис-(дибензилиденацетон)дипалладий(0) (9,1 мг, 0,001 ммоля, 2 мол.%(67 мг, 0,7 ммоля) и через смесь пропускали ток азота. Затем к смеси добавляли раствор 8-бром-4-(4 хлорбензолсульфонил)-6-метил-3,4-дигидро-2 Н-бензо[1,4]оксазина (201 мг, 0,5 ммоля) и пиперазина(129 мг, 1,5 ммоля) в толуоле (5 мл). Смесь нагревали до 95C и перемешивали в течение 18 ч. Затем смесь охлаждали до комнатной температуры, переносили в этилацетат и фильтровали. Органическую фазу промывали водой (220 мл) и экстрагировали 10% HCl (220 мл). Объединенные водные экстракты подщелачивали добавлением твердого карбоната натрия и экстрагировали этилацетатом (220 мл). Объединенные органические экстракты сушили (K2CO3), фильтровали и концентрировали, при этом получали указанное в заголовке соединение в виде масла (163 мг, 79,6%). Гидрохлорид соединения получали при обработке продукта этанолом/хлористым водородом. tпл. 147,9-152,9C. MC: 408 (MH+). Аналогичным образом при использовании соответствующих арил- или гетероарилсульфонилхлоридов получали следующие соединения:- 23009982 4-(3,4-дихлорбензолсульфонил)-6-метил-8-пиперазин-1-ил-3,4-дигидро-2 Н-бензо[1,4]оксазин в виде порошка белого цвета, tпл. 257-261 С, MC: 442 (MH+),4-(4-хлорбензолсульфонил)-8-(3,5-диметилпиперазин-1-ил)-6-метил-3,4-дигидро-2 Н-бензо[1,4]оксазин в виде твердого вещества грязно-белого цвета, tпл. 171,8-185,8C, MC: 436 (MH+). Способ Б. Синтез 4-бензолсульфонил-6-хлор-8-пиперазин-1-ил-3,4-дигидро-2 Н-бензо[1,4]оксазина. В трехгорлую колбу помещали трис-(дибензилиденацетон)дипалладий(0) (6,4 мг, 0,007 ммоля, 2 мол.%Pd), рацемат 2,2'-бис-(дифенилфосфино)-1,1'-динафтила (10,8 мг, 0,017 ммоля, 5 мол.%), трет-бутоксид натрия (47 мг, 0,48 ммоля) и смесь продували азотом. Затем к смеси добавляли раствор 4-бензолсульфонил-8-бром-6-хлор-3,4-дигидро-2 Н-бензо[1,4]оксазина (165 мг, 0,35 ммоля) и трет-бутилового эфира пиперазин-1-карбоновой кислоты (71,1 мг, 0,38 ммоля) в толуоле (2 мл). Смесь перемешивали при 95C в течение 12 ч, затем охлаждали до комнатной температуры, смесь переносили в этилацетат, фильтровали и концентрировали. Неочищенный продукт очищали экспресс-хроматографией на силикагеле (элюент: гексан/этилацетат, 7:3, об./об.), при этом получали трет-бутиловый эфир 4-(4-бензолсульфонил-6-хлор 3,4-дигидро-2 Н-бензо[1,4]оксазин-8-ил)пиперазин-1-карбоновой кислоты в виде масла (129 мг, 75%).MC: 494 (MH+). Неочищенный продукт растворяли в этаноле (1 мл), добавляли 10% раствор хлористого водорода в этаноле (1 мл) и смесь нагревали на паровой бане в течение 15 мин. При охлаждении до комнатной температуры в растворе выпадали кристаллы белого цвета, которые отделяли фильтрованием,промывали холодным этанолом и высушивали в вакууме, при этом получали гидрохлорид 4-бензолсульфонил-6-хлор-8-пиперазин-1-ил-3,4-дигидро-2 Н-бензо[1,4]оксазина в виде порошка белого цвета (90 мг,73%). tпл. 202-205C. MC: 394 (MH+). Аналогичным образом получали следующие соединения: гидрохлорид 6-хлор-4-(2-хлорбензолсульфонил)-8-пиперазин-1-ил-3,4-дигидро-2 Н-бензо[1,4]оксазина в виде порошка белого цвета, tпл.250C, MC: 428 (MH+),гидрохлорид 6-хлор-4-(3-хлорбензолсульфонил)-8-пиперазин-1-ил-3,4-дигидро-2 Н-бензо[1,4]оксазина в виде порошка белого цвета, tпл. 193,4-196,5C, MC: 428 (MH+),гидрохлорид 6-хлор-4-(2-фторбензолсульфонил)-8-пиперазин-1-ил-3,4-дигидро-2 Н-бензо[1,4]оксазина в виде порошка белого цвета, tпл. 194,8-204,5C, MC: 412 (MH+),гидрохлорид 6-хлор-4-(нафталин-1-сульфонил)-8-пиперазин-1-ил-3,4-дигидро-2 Н-бензо[1,4]оксазина в виде порошка белого цвета, tпл. 273,7-276,6C, MC: 444 (MH+). Аналогичным образом при замене трет-бутилового эфира пиперазин-1-карбоновой кислоты на третбутиловый эфир [1,4]диазепан-1-карбоновой кислоты, а 4-бензолсульфонил-8-бром-6-хлор-3,4-дигидро 2 Н-бензо[1,4]оксазина на 8-бром-4-(3-хлорбензолсульфонил)-3,4-дигидро-2 Н-бензо[1,4]оксазин получали следующее соединение: гидрохлорид 4-(3-хлорбензолсульфонил)-8-[1,4]диазепан-1-ил-3,4-дигидро-2 Н-бензо[1,4]оксазина в виде порошка белого цвета, tпл. 175,9-180,3C, MC: 408 (MH+). Пример 4. В примере описан способ получения 8-бром-2,3-дигидробензо[1,4]оксазина. Раствор 2-(2,6-дибромфенокси)ацетамида (9,3 г, 0,03 моля) в тетрагидрофуране (100 мл) нагревали до температуры кипения растворителя и в течение 15 мин добавляли по каплям борандиметилсульфид(4,5 мл, 0,045 мл). Через 3 ч к смеси добавляли 20 мл раствора хлористого водорода в этаноле (2M, 0,4 моля) и раствор кипятили с обратным холодильником в течение 30 мин. После охлаждения до комнатной температуры из раствора выпадало твердое вещество белого цвета, которое отделяли фильтрованием и промывали диэтиловым эфиром (20 мл), при этом получали гидрохлорид 2-(2,6-дибромфенокси)этиламина(7,25 г, 73,3%). tпл. 249,7-252,3C. MC: 294 (MH+). В трехгорлую колбу помещали трис-(дибензилиденацетон)дипалладий(0) (0,37 г, 0,0004 моля, 2 мол.%Pd), -рацемат-2,2'-бис-(дифенилфосфино)-1,1'-динафтила (0,64 г, 0,001 моля, 5 мол.%) и трет-бутоксид натрия (2,7 г, 0,028 моля) и смесь продували азотом. Затем к смеси добавляли раствор 2-(2,6-дибромфенокси)этиламина (6 г, 0,02 моля) в толуоле (50 мл) и смесь перемешивали при 95C в течение 12 ч.- 24009982 Затем смесь охлаждали до комнатной температуры, переносили в этилацетат, фильтровали и концентрировали. Неочищенный продукт очищали экспресс-хроматографией на силикагеле (элюент: гексан/этилацетат, 7:3, об./об.), при этом получали 8-бром-3,4-дигидро-2 Н-бензо[1,4]оксазин в виде масла (275 мг,48%). Гидрохлорид соединения получали при обработке продукта этанолом/хлористым водородом. tпл. 184,1-195,4C. MC: 214 (MH+). 6-Бром-3,4-дигидро-2 Н-бензо[1,4]оксазин получали по методике, описанной в статье Nugiel David A.,Jacobs Kim, Cornelius Lyndon, Chang Chong-Hwan, Jadhav Prabhakar K. и др., J. Med. Chem., 40,10, 14651474 (1997), включенной в текст заявки в качестве ссылки. 6-Бром-3,4-дигидро-2 Н-бензо[1,4]оксазин использовали в методиках, описанных в примерах 1 и 2, для получения соответствующих соединений формулы I. Пример 5. В примере описан анализ связывания соединений формулы I in vitro в присутствии радиоактивно меченного лиганда. Активность связывания соединений по изобретению in vitro определяли по следующей методике. Анализ сродства лиганда (в двух повторах) проводили методом конкурентного связывания [3H]LSD клеточными мембранами клеток HEK293, стабильно экспрессирующих рекомбинантный рецептор 5-НТ 6 человека (Boess и др., Neuropharmacology, 36,4/5, 713-720 (1997), Monsma и др., Molecular Pharmacology,43, 320-327 (1993. Анализ проводили в буферном растворе для анализа, содержащем 50 мМ трис-HCl, 10 мМ MgSO4,0,5 мМ EDTA, 1 мМ аскорбиновую кислоту, рН 7,4, при 37C, в объеме реакционной смеси 250 мкл. Пробирки для анализа, содержащие [3H]LSD (5 нМ), конкурирующий лиганд и мембранную фракцию,инкубировали при встряхивании на водяной бане в течение 60 мин при 37 С, раствор фильтровали на фильтрах Packard GF-B (предварительно пропитанных 0,3% PEI) с использованием 96-луночного сборщика клеток (фирмы Packard) и трижды промывали 50 мМ трис-HCl, охлажденного льдом. Связывание[3H]LSD определяли в виде количества импульсов в минуту на счетчике Packard TopCount. Вытеснение [3H]LSD из участков связывания рассчитывали при построении графика зависимости концентрация/связывание по логистическому уравнению с четырьмя параметрами где Hill означает коэффициент наклона по Хиллу, [лиганд] означает концентрацию конкурирующего радиоактивно меченного лиганда, a IC50 означает концентрацию радиоактивно меченного лиганда, при которой наблюдается специфическое связывание, равное половине от максимального значения. В числителе указано специфическое связывание, которое означает разность между Bmax и базисными данными (basal). При испытании соединений формулы I по методике, описанной в примере 5, было установлено, что соединения по изобретению являются селективными антагонистами рецептора 5-НТ 6. Результаты связывания радиоактивно меченного лиганда- 25009982 Пример 6. Свойство соединений по изобретению усиливать познавательные способности определяли на модели познавательных способностей у животных по узнаванию объекта. Для испытаний использовали самцов крыс Wistar возрастом 4 месяца (фирма Charles River, Нидерланды). Соединения получали ежедневно, растворяли в физиологическом растворе и анализировали при трех дозах. Введение проводили внутрибрюшинно (в объеме 1 мл/кг) за 60 мин до проведения испытаний. Через 30 мин после введения соединения животным вводили гидробромид скополамина. Испытания проводили в двух экспериментах на двух равных группах подопытных животных (по 24 особи). Дозы анализируемых соединений выбирали произвольно. Эксперименты проводили с использованием двойного слепого контроля. Каждую дозу вводили крысам однократно. Объект испытаний на узнавание выбирали, как описано в статье Ennaceur A.,Delacour J., A new one-trial test for neurobiological studies of memory in rats. 1: Behavioral data, Behav. Brain его фармацевтически приемлемая соль или пролекарство, гдеm означает целое число от 0 до 3;R3 означает фенил или нафтил, которые необязательно замещены галогеном, алкилом, алкокси,гидрокси, циано, пиперазинилом, метилсульфониламино, метилсульфонилом, аминокарбонилом, или означает хинолинил, изохинолинил, тиофенил, бензотиадиазолил, бензоксадиазолил, имидазолил или 2,3-дигидробензо[1,4]диоксин, которые необязательно замещены галогеном или алкилом; каждый R4 независимо означает галоген, алкил или алкокси; каждый R5, R6, R7 и R8 независимо означает водород или алкил; аR9 означает водород или алкил. 2. Соединение по п.1, где m означает целое число от 0 до 2. 3. Соединение по п.1, где m равно 0 или 1, а n, Y, Z1, R1-R9 имеют значения, указанные в п.1. 4. Соединение по любому из пп.1-3 формулы где R1, R2, R3, R4, R5, R6, R7, R8, R9, m, n, р и Y имеют значения, указанные в указанных пунктах. 5. Соединение по любому из пп.1-3 формулы- 26009982 где R1, R2, R3, R4, R5, R6, R7, R8, R9, m, n, р и Y имеют значения, указанные в указанных пунктах. 6. Соединение по любому из пп.1-5, где n и р равны 2. 7. Соединение по любому из пп.1-6, где каждый R4 независимо означает хлор, фтор, метокси или метил. 8. Соединение по любому из пп.1-7, где m равно 1. 9. Соединение по любому из пп.1-8, где R3 означает фенил или нафтил, которые необязательно замещены, как указано в п.1. 10. Соединение по любому из пп.1-9, где R3 означает фенил или галогензамещенный фенил. 11. Соединение по любому из пп.1-9, где R3 означает фенил, 2-фторфенил, 2-хлорфенил, 3,4-дихлорфенил, 4-хлорфенил, 3-хлорфенил, 4-метоксифенил, 3,5-дихлорфенил, 2,6-дихлорфенил, 2,4-дихлорфенил, 3-метансульфониламинофенил, 2-метансульфонилфенил, 2-карбамоилфенил, 3-метансульфонилфенил, 4-метансульфонилфенил, 3-фторфенил, нафтил, 2,4-дифторфенил, 2-цианофенил, 2-хлор-4-фторфенил, 5-фтор-2-метилфенил, 5-хлорнафтил. 12. Соединение по любому из пп.1-9, где R3 означает 4-фтор-2-метилфенил, 2-гидроксифенил, 4 пиперазин-1-ил или 2,3-дигидробензо[1,4]диоксинил. 13. Соединение по любому из пп.1-10, где R3 означает фенил, 2-хлорфенил или 2-фторфенил. 14. Соединение по п.1, которое выбрано из группы, включающей 6-трет-бутил-4-(2-фторбензолсульфонил)-8-пиперазин-1-ил-3,4-дигидро-2 Н-бензо[1,4]оксазин; 4-(2-фторбензолсульфонил)-8-метилпиперазин-1-ил-3,4-дигидро-2 Н-бензо[1,4]оксазин; 6-фтор-4-(2-фторбензолсульфонил)-8-пиперазин-1-ил-3,4-дигидро-2 Н-бензо[1,4]оксазин; 4-(2-фторбензолсульфонил)-6-метокси- 8-пиперазин-1-ил-3,4-дигидро-2 Н-бензо[1,4]оксазин; 4-(2-фторбензолсульфонил)-6-метил-8-пиперазин-1-ил-3,4-дигидро-2 Н-бензо[1,4]оксазин; 6-хлор-4-(2-фторбензолсульфонил)-8-пиперазин-1-ил-3,4-дигидро-2 Н-бензо[1,4]оксазин; 4-(2-фторбензолсульфонил)-8-пиперазин-1-ил-3,4-дигидро-2 Н-бензо[1,4]оксазин. 15. Соединение по любому из пп.1-6, где R3 означает хинолин-8-ил, 2-тиофенил, 5-хлортиофен-2 ил, изохинолин-5-ил, бензо[1,2,5]тиадиазол-4-ил, 1-метил-1 Н-имидазол-4-ил или бензо[1,2,5]оксадиазол 4-ил. 16. Соединение по п.9, где R9 означает водород. 17. Соединение по любому из пп.1-3, где R5, R6, R7 и R8 означают водород. 18. Соединение по любому из пп.1-3, где m равно 0. 19. Способ получения соединения по п.1, включающий: в присутствии катализатора конденсации с образованием гетероциклилзамещенного фенила формулы(б) удаление защитной группы в гетероциклилзамещенном фениле с образованием незащищенного гетероциклилзамещенного фенила формулы(в) взаимодействие незащищенного гетероциклилзамещенного фенила с соединением формулы R3Y-W с образованием соединения по п.1, где R1, R2, R4, R5, R6, R7, R8, R9, m, n, р имеют значения, указанные в п.1, W означает активирующую группу, R11 означает аминозащитную группу, a X1 означает галоген. 20. Способ получения соединения по п.1, включающий:(б) конденсацию соединения галогенированного фенила с гетероциклильным соединением формулы в присутствии катализатора конденсации с образованием соединения формулы I, где Y, R1, R2, R3, R4, R5,R6, R7, R8, R9, m, n и р имеют значения, указанные в п.1, W означает активирующую группу, а X1 означает галоген. 21. Фармацевтическая композиция, включающая терапевтически эффективное количество по меньшей мере одного соединения по пп.1-18 в смеси с одним или более фармацевтически приемлемым носителем, предназначенная для лечения заболеваний. 22. Применение одного или более соединений по любому из пп.1-18 для получения лекарственного средства, предназначенного для лечения или профилактики патологического состояния, которое облегчается агонистами рецептора 5-НТ 6. 23. Применение по п.22, где патологическое состояние представляет собой нарушения ЦНС. 24. Применение по п.22, где заболевание включает психоз, шизофрению, маниакальные депрессии,неврологические нарушения, нарушения памяти, нарушение в форме потери внимания, болезнь Паркинсона, боковой амиотрофический склероз, болезнь Альцгеймера и болезнь Гентингтона. 25. Применение по п.22, где патологическое состояние представляет собой заболевание желудочнокишечного тракта. Евразийская патентная организация, ЕАПВ Россия, 109012, Москва, Малый Черкасский пер., 2/6
МПК / Метки
МПК: C07D 413/04, C07D 265/36, A61P 25/18, A61K 31/536
Метки: 5-нт-6, модуляторов, получения, эти, композиции, бензоксазина, применение, качестве, способ, фармацевтические, содержащие, производные
Код ссылки
<a href="https://eas.patents.su/29-9982-proizvodnye-benzoksazina-v-kachestve-modulyatorov-5-nt-6-sposob-ih-polucheniya-farmacevticheskie-kompozicii-soderzhashhie-eti-proizvodnye-i-ih-primenenie.html" rel="bookmark" title="База патентов Евразийского Союза">Производные бензоксазина в качестве модуляторов 5-нт-6, способ их получения, фармацевтические композиции, содержащие эти производные, и их применение</a>
Предыдущий патент: Производные индол-2-карбоксамидина как антагонисты nmda рецептора
Следующий патент: Лекарственное средство для профилактики и лечения артериосклероза и гипертензии
Случайный патент: Способ определения пластового давления












