Производные бензоконденсированных гетероциклических оксимов, способ их получения, содержащие их фармацевтическая композиция и комбинация и их применение
Номер патента: 12437
Опубликовано: 30.10.2009
Авторы: Кторза Ален, Л'эльгуаль'ш Жан-Марсьяль, Юртеван Орели, Леклерк Вероник, Даке Катрин, Бертоло Паскаль, Кэньяр Даньель-Анри, Карато Паскаль, Лебеге Никола
Формула / Реферат
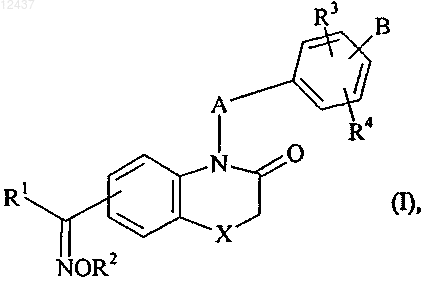
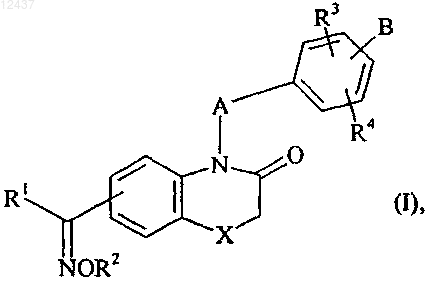
1. Соединения формулы (I)
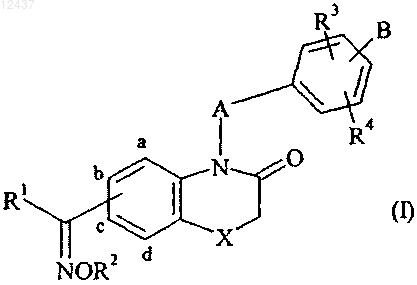
в которой
X представляет собой атом кислорода или атом серы,
А представляет собой (С1-С6)алкиленовую цепь, в которой СН2 группа необязательно может быть заменена атомом кислорода,
R1 представляет собой арильную группу, a
R2 представляет собой атом водорода либо линейную или разветвленную (С1-С6)алкильную группу,
R3 и R4 каждый представляет собой атом водорода,
В представляет собой линейную или разветвленную (С1-С6)алкильную группу, причем эта группа замещена группой формулы (II)
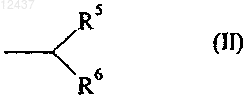
в которой R5 представляет собой 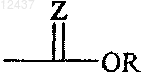 группу, где Z представляет собой атом кислорода и R представляет собой атом водорода, линейную или разветвленную (С1-С6)алкильную группу либо линейную или разветвленную (С1-С6)полигалоалкильную группу и
группу, где Z представляет собой атом кислорода и R представляет собой атом водорода, линейную или разветвленную (С1-С6)алкильную группу либо линейную или разветвленную (С1-С6)полигалоалкильную группу и
R6 представляет собой -OR, где R имеет такие же значения, как приведенные выше,
и подразумевается, что
оксим R'-C(=N-OR2)- может находиться в Z или Е конфигурации,
арил обозначает фенильную, нафтильную или бифенильную группу, которые необязательно могут быть частично гидрированы,
их энантиомеры и диастереоизомеры, а также их фармацевтически приемлемые соли присоединения с кислотой или основанием.
2. Соединения формулы (I) по п.1, в которых группа R1-C(=N-OR2)- находится в b или с положении, их энантиомеры и диастереоизомеры, а также их фармацевтически приемлемые соли присоединения с кислотой или основанием.
3. Соединения формулы (I) по п.1, в которых А представляет собой этиленоксигруппу, их энантиомеры и диастереоизомеры, а также их фармацевтически приемлемые соли присоединения с кислотой или основанием.
4. Соединения формулы (I) по п.1, в которых R2 представляет собой атом водорода, их энантиомеры и диастереоизомеры, а также их фармацевтически приемлемые соли присоединения с кислотой или основанием.
5. Соединения формулы (I) по п.1, в которых R2 представляет собой алкильную группу, их энантиомеры и диастереоизомеры, а также их фармацевтически приемлемые соли присоединения с кислотой или основанием.
6. Соединения формулы (I) по п.1, в которых R1 представляет собой незамещенную фенильную группу, их энантиомеры и диастереоизомеры, а также их фармацевтически приемлемые соли присоединения с кислотой или основанием.
7. Соединения формулы (I) по п.1, в которых В представляет собой алкильную группу, замещенную группой 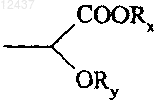 , в которой Rx и Ry, которые могут быть одинаковыми или разными, каждый представляет собой атом водорода или алкильную группу, их энантиомеры и диастереоизомеры, а также их фармацевтически приемлемые соли присоединения с кислотой или основанием.
, в которой Rx и Ry, которые могут быть одинаковыми или разными, каждый представляет собой атом водорода или алкильную группу, их энантиомеры и диастереоизомеры, а также их фармацевтически приемлемые соли присоединения с кислотой или основанием.
8. Соединения формулы (I) по п.1, в которых В представляет собой 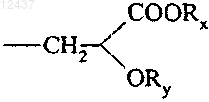 группу, в которой Rx и Ry, которые могут быть одинаковыми или разными, каждый представляет собой атом водорода или алкильную группу, их энантиомеры и диастереоизомеры, а также их фармацевтически приемлемые соли присоединения с кислотой или основанием.
группу, в которой Rx и Ry, которые могут быть одинаковыми или разными, каждый представляет собой атом водорода или алкильную группу, их энантиомеры и диастереоизомеры, а также их фармацевтически приемлемые соли присоединения с кислотой или основанием.
9. Соединения формулы (I) по п.1, которые представляют собой
этил 2-этокси-3-[4-(2-{7-[(метоксиимино)(фенил)метил]-3-оксо-2,3-дигидро-4H-1,4-бензотиазин-4-ил}этокси)фенил]пропаноат,
этил 3-[4-(2-{7-[(метоксиимино)(фенил)метил]-3-оксо-2,3-дигидро-4H-1,4-бензотиазин-4-ил}этокси)фенил]-2-(2,2,2-трифторэтокси)пропаноат,
этил 2-этокси-3-[4-(2-{6-[(метоксиимино)(фенил)метил]-3-оксо-2,3-дигидро-4H-1,4-бензоксазин-4-ил}этокси)фенил]пропаноат,
этил 2-этокси-3-[4-(2-{7-[(гидроксиимино)(фенил)метил]-3-оксо-2,3-дигидро-4H-1,4-бензотиазин-4-ил}этокси)фенил]пропаноат,
этил 3-[4-(2-{7-[(гидроксиимино)(фенил)метил]-3-оксо-2,3-дигидро-4H-1,4-бензотиазин-4-ил}этокси)фенил]-2-(2,2,2-трифторэтокси)пропаноат,
этил 2-этокси-3-[4-(2-{6-[(гидроксиимино)(фенил)метил]-3-оксо-2,3-дигидро-4H-1,4-бензоксазин-4-ил}этокси)фенил]пропаноат,
2-этокси-3-[4-(2-{7-[(гидроксиимино)(фенил)метил]-3-оксо-2,3-дигидро-4H-1,4-бензотиазин-4-ил}этокси)фенил]пропионовую кислоту,
2-этокси-3-[4-(2-{7-[(метоксиимино)(фенил)метил]-3-оксо-2,3-дигидро-4H-1,4-бензотиазин-4-ил}этокси)фенил]пропионовую кислоту,
3-[4-(2-{7-[(гидроксиимино)(фенил)метил]-3-оксо-2,3-дигидро-4H-1,4-бензотиазин-4-ил}этокси)фенил]-2-(2,2,2-трифторэтокси)пропионовую кислоту,
3-[4-(2-{7-[(метоксиимино)(фенил)метил]-3-оксо-2,3-дигидро-4H-1,4-бензотиазин-4-ил}этокси)фенил]-2-(2,2,2-трифторэтокси)пропионовую кислоту,
2-этокси-3-[4-(2-{6-[(гидроксиимино)(фенил)метил]-3-оксо-2,3-дигидро-4H-1,4-бензоксазин-4-ил}этокси)фенил]пропионовую кислоту,
2-этокси-3-[4-(2-{6-[(метоксиимино)(фенил)метил]-3-оксо-2,3-дигидро-4H-1,4-бензоксазин-4-ил}этокси)фенил]пропионовую кислоту,
их энантиомеры и диастереоизомеры, а также их фармацевтически приемлемые соли присоединения с кислотой или основанием.
10. Способ получения соединений формулы (I) по п.1, который характеризуется тем, что в качестве исходного вещества используют соединение (III)
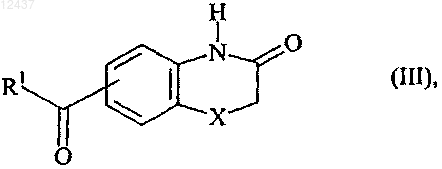
в которой R1 и X имеют значения, указанные для формулы (I), которое конденсируют в щелочной среде с соединением формулы (IV)
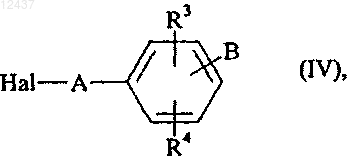
в которой А, В, R3 и R4 имеют значения, указанные для формулы (I), и Hal представляет собой атом галогена, получая соединение формулы (V)
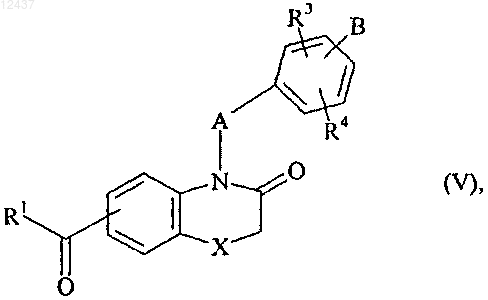
в которой R1, R3, R4, А, В и X имеют значения, указанные для формулы (I), которое подвергают воздействию соединения формулы R2O-NH2, в которой R2 имеет значения, указанные для формулы (I), получая соединение формулы (I)
которое может быть очищено в соответствии с обычной методикой разделения, превращено, если это является желательным, в соли присоединения с фармацевтически приемлемой кислотой или основанием, и необязательно разделено на изомеры в соответствии с обычной методикой разделения.
11. Способ получения соединений формулы (I) по п.1, который характеризуется тем, что в качестве исходного вещества используют соединение (III)
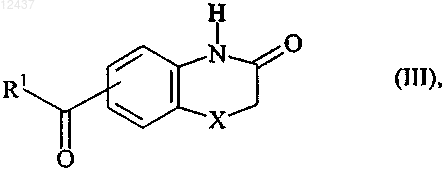
в которой R1 и X имеют значения, указанные для формулы (I), которое конденсируют с соединением формулы R2O-NH2, в которой R2 имеет значения, указанные для формулы (I), получая соединение формулы (VI)
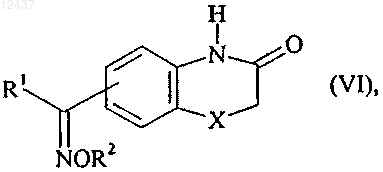
в которой R1, R2 и X имеют значения, указанные для формулы (I), которое конденсируют в щелочной среде с соединением формулы (IV)
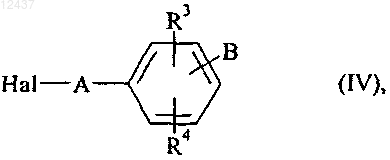
в которой А, В, R3 и R4 имеют значения, указанные для формулы (I), и Hal представляет собой атом галогена, получая соединение формулы (I)
которое может быть очищено в соответствии с обычной методикой разделения, превращено, если это является желательным, в соли присоединения с фармацевтически приемлемой кислотой или основанием, и необязательно разделено на изомеры в соответствии с обычной методикой разделения.
12. Фармацевтическая композиция, содержащая в качестве активного компонента по меньшей мере офэю соединение формулы (I) по любому из пп.1-9, или его фармацевтически приемлемую соль присоединения с кислотой или основанием, отдельно или в сочетании с одним или несколькими фармацевтически приемлемыми наполнителями.
13. Применение фармацевтической композиции по п.12 для приготовления лекарственного средства для лечения и/или профилактики гипергликемии, дислипидемии и более предпочтительно для лечения инсулиннезависимого диабета II типа, резистентности к инсулину, непереносимости глюкозы, заболеваний, связанных с сидромом X, заболевания коронарной артерии и других сердечно-сосудистых заболеваний, заболеваний почек, ретинопатии, заболеваний, связанных с активацией клеток эндотелия, псориаза, синдрома поликистоза яичника, слабоумия, остеопороза, воспалительных заболеваниях кишечника, дистрофической миотонии, панкреатита, артериосклерозы, ксантомы, а также для лечения или предотвращения диабета I типа, ожирения, регуляции аппетита, анорексии, булимии, нервно-психической анорексии, а также злокачественных патологий, и, в особенности, гормональнозависимых злокачественных новообразований, таких как рак молочной железы и рак ободочной кишки, и для применения в качестве ингибиторов ангиогенеза.
14. Комбинация, содержащая соединение формулы (I) по любому из пп.1-9 и антиоксидант.
15. Комбинация по п.14, в которой соединение формулы (I) представляет собой 3-{4-[2-(6-(гидроксииминофенил)метил-3-оксо-2,3-дигидро-4H-бензо[1,4]оксазин-4-ил)этокси]фенил}-2-этоксипропионовую кислоту, ее энантиомеры и диастереоизомеры, а также ее фармацевтически приемлемые соли присоединения с кислотой или основанием.
16. Комбинация по п.14 или 15, в которой антиоксидант представляет собой коэнзим Q10.
17. Комбинация по п.14 или 15, в которой антиоксидант представляет собой витамин Е.
18. Комбинация по п.14 или 15, которая представляет собой 3-{4-[2-(6-(гидроксииминофенил)метил-3-оксо-2,3-дигидро-4H-бензо[1,4]оксазин-4-ил)этокси]фенил}-2-этоксипропионовую кислоту и коэнзим Q10.
19. Применение фармацевтической композиции, содержащей в качестве активного компонента комбинацию по любому из пп.14-18, отдельно или в сочетании с одним или несколькими фармацевтически приемлемыми наполнителями.
20. Применение фармацевтической композиции по п.19 для приготовления лекарственного средства для лечения и/или предотвращения ожирения.
21. Применение фармацевтической композиции по п.19 для приготовления лекарственного средства для лечения и/или предотвращения избыточного веса, характеризующегося индексом массы тела, большим чем 25 и меньшим чем 30.
22. Применение комбинации по любому из пп.14-18 для получения фармацевтических композиций, предназначенных для лечения и/или предотвращения ожирения.
23. Применение комбинации по любому из пп.14-18 для получения фармацевтических композиций, предназначенных для лечения и/или предотвращения ожирения, вызванного терапевтическим лечением.
24. Применение комбинации по любому из пп.14-18 для получения фармацевтических композиций, предназначенных для лечения и/или предотвращения ожирения, вызванного лечением диабета I или II типа.
25. Применение комбинации по любому из пп.14-18 для получения фармацевтических композиций, предназначенных для лечения и/или предотвращения избыточного веса, характеризующегося индексом массы тела, большим чем 25 и меньшим чем 30.
26. Применение комбинации по любому из пп.14-18 для получения фармацевтических композиций, предназначенных для лечения и/или предотвращения избыточного веса, характеризующегося индексом массы тела, большим чем 25 и меньшим чем 30, вызванного терапевтическим лечением.
27. Применение комбинации по любому из пп.14-18 для получения фармацевтических композиций, предназначенных для лечения и/или предотвращения избыточного веса, характеризующегося индексом массы тела, большим чем 25 и меньшим чем 30, вызванного лечением диабета I или II типа.
Текст
012437 Настоящее изобретение относится к новым гетероциклическим соединениям оксима, способу их получения и фармацевтическим композициям, которые их содержат. Соединения, описанные в настоящем изобретении, являются новыми и обладают фармакологическими свойствами, представляющими чрезвычайный интерес: они являются очень хорошими гипогликемическими и гиполипемическими средствами. Лечение инсулиннезависимого диабета II типа остается неэффективным, несмотря на присутствие на рынке большого количества пероральных гипогликемических соединений, предназначенных для способствования секреции инсулина и стимулирования его действия на периферические целевые ткани. За последнее десятилетие для класса соединений, обладающих тиазолидиндионовой структурой(US 5089514, US 5306726), было показано значительное противодиабетическое действие путем стимулирования чувствительности к инсулину в целевых периферических тканях (скелетные мышцы, печень,жировая ткань) на животных моделях с инсулиннезависимым диабетом II типа. Эти соединения также снижают уровни инсулина и липидов на таких же животных моделях и индуцируют дифференциацию линий предшественников жировых клеток в линиях жировых клеток в условиях in vitro (A. Hiragun и др.,J. Cell. Physiol., 1988, 134, 124-130; R.F. Kleitzen u др, Mol. Pharmacol., 1992, 41, 393-398). Лечение линий предшественников жировых клеток с помощью тиазолидиндиона росиглитазона стимулирует экспрессию специфических генов метаболизма липидов, таких как аР 2 и адипсин, а также экспрессию переносчиков глюкозы GLUT1 и GLUT4, что указывает на то, что действие тиазолидиндионов, наблюдаемое в условиях in vivo, может осуществляться посредством жировой ткани. Это специфическое действие получается с помощью стимуляции ядерных факторов транскрипции: гамма рецептор,активируемый пролифератором пероксисом (PPAR 2). Такие соединения способны восстанавливать чувствительность к инсулину в периферических тканях, таких как жировая ткань или скелетные мышцы(троглитазон, росиглитазон), обладают нежелательными побочными действиями при применении у людей, в особенности, оказывают отрицательные влияния на печень ( документа 2470, 8 сентября 1999 г.,25). Большое количество гиполипемических средств обладают значительными побочными действиями(на печень, сердце, гематопоэз), которые ограничивают их длительное применение для лечения инсулиннезависимого диабета II типа. Для этой патологии существует острая необходимость развития новых терапевтических средств, которые были бы менее токсичными и более активными при длительном применении. Кроме того, у больных диабетом часто наблюдается гиперлипемия (Diabetes Care, 1995, 18 (дополнение 1), 86/8/93). Сочетание гипергликемии с гиперлипемией повышает риск сердечно-сосудистых заболеваний у больных диабетом. Гипергликемия, гиперлипемия и ожирение превратились в патологии современного общества, обусловленные излишним питанием и хроническим отсутствием физических нагрузок. Повышение частоты этих патологии обуславливает необходимость развития новых терапевтических средств, которые были бы активными при таких заболевания: поэтому соединения, обладающие очень хорошей гипогликемической и гиполипемической активность, но при этом без побочных действий,вызываемых тиазолидиндионами, являются очень благоприятными для лечения и/или предотвращения этих патологий, и в особенности для лечения инсулиннезависимого диабета II типа для уменьшения периферической резистентности к инсулину и для нормализации контроля за уровнем глюкозы. Соединения согласно настоящему изобретению являются новыми, кроме того, они соответствуют вышеописанным фармакологическим критериям и очень хорошими гипогликемическими и гиполипемическими средствами. Более конкретно, настоящее изобретение относится к соединениям формулы (I)X представляет собой атом кислорода или атом серы,А представляет собой (С 1-С 6)алкиленовую цепь, в которой СН 2 группа необязательно может быть заменена гетероатомом, выбранным из кислорода и серы, или NRa группой (в которой Ra представляет собой атом водорода или линейную или разветвленную (С 1-С 6)алкильную группу), или фениленовой или нафтиленовой группой,-1 012437R1 и R2, которые могут быть одинаковыми или разными, каждый представляет собой атом водорода, линейную или разветвленную (C1-С 6)алкильную группу, линейную или разветвленную (С 2 С 6)алкенильную группу, линейную или разветвленную (С 2-С 6)алкинильную группу, арильную группу,арил(С 1-С 6)алкильную группу, в которой алкильная часть может быть линейной или разветвленной,арил(С 2-С 6)алкенильную группу, в которой алкенильная часть может быть линейной или разветвленной,арил(С 2-С 6)алкинильную группу, в которой алкинильная часть может быть линейной или разветвленной,гетероарильную группу, гетероарил(С 1-С 6)алкильную группу, в которой алкильная часть может быть линейной или разветвленной, гетероарил(С 2-С 6)алкенильную группу, в которой алкенильная часть может быть линейной или разветвленной, гетероарил(С 2-С 6)алкинильную группу, в которой алкинильная часть может быть линейной или разветвленной, (С 3-С 8)циклоалкильную группу, (С 3-С 8)циклоалкил(С 1 С 6)алкильную группу, в которой алкильная часть может быть линейной или разветвленной, или линейную или разветвленную (С 1-С 6)полигалоалкильную группу,R3 и R4, которые могут быть одинаковыми или разными, каждый представляет собой атом водорода, атом галогена, или R, OR или NRR' группу, в которой R и R', которые могут быть одинаковыми или разными, каждый представляет собой атом водорода или линейную или разветвленную (С 1 С 6)алкильную группу, линейную или разветвленную (С 2-С 6)алкенильную группу, линейную или разветвленную (С 2-С 6)алкинильную группу, арильную группу, арил(С 1-С 6)алкильную группу, в которой алкильная часть может быть линейной или разветвленной, арил(С 2-С 6)алкенильную группу, в которой алкенильная часть может быть линейной или разветвленной, арил(С 2-С 6)алкинильную группу, в которой алкинильная часть может быть линейной или разветвленной, гетероарильную группу, гетероарил(С 1 С 6)алкильную группу, в которой алкильная часть может быть линейной или разветвленной, гетероарил(С 2-С 6)алкенильную группу, в которой алкенильная часть может быть линейной или разветвленной, гетероарил(С 2-С 6)алкинильную группу, в которой алкинильная часть может быть линейной или разветвленной, (С 3-С 8)циклоалкильную группу, (С 3-С 8)циклоалкил(С 1-С 6)алкильную группу, в которой алкильная часть может быть линейной или разветвленной, или линейную или разветвленную (С 1 С 6)полигалоалкильную группу, или R3 и R4, вместе в атомами углерода, к которым они присоединены, в том случае, когда они присоединены к двум смежным атомам углерода, образуют кольцо, которое имеет 5 или 6 кольцевых членов и которое необязательно может содержать гетероатом, выбранный из кислорода, серы и азота,В представляет собой линейную или разветвленную (С 1-С 6)алкильную группу или линейную или разветвленную (С 2-С 6)алкенильную группу, где эти группы замещены группой формулы (II) группу, где Z представляет собой атом кислорода или атом серы и R и R', которые могут быть одинаковыми или разными, имеют значения, указанные выше,и R6 представляет собой арильную группу, арилалкильную группу, в которой алкильная часть содержит от 1 до 6 атомов углерода и может быть линейной или разветвленной, гетероарильную группу,гетероарилалкильную группу, в которой алкильная часть содержит от 1 до 6 атомов углерода и может быть линейной или разветвленной, CN, тетразол, или-2 012437 где Z имеет значения, указанные выше, и R и R', которые могут быть одинаковыми или разными,могут иметь такие же значения, как и приведенные выше,или группой R7, R7 представляет собой CN, тетразол, или группу,где Z имеет значения, указанные выше, и R и R', которые могут быть одинаковыми или разными,могут иметь такие же значения, как и приведенные выше, n представляет собой 0, 1,2, 3, 4, 5 или 6, и R8 иR9, которые могут быть одинаковыми или разными, каждый представляет собой атом водорода или линейную или разветвленную (С 1-С 6)алкильную группу, в которой R8 и R9 не могут одновременно представлять собой атом водорода,или В представляет собой группу формулы (II) или группу R7, как определено выше,и подразумевается, что оксим R1-C(=N-OR2)- может находиться в Z или Е конфигурации,арил обозначает фенильную, нафтильную или бифенильную группу, которые необязательно могут быть частично гидрированы,гетероарил обозначает любую ароматическую моно- или бициклическую группу, содержащую от 5 до 10 кольцевых членов, которая может быть частично гидрирована в одном из колец в случае бициклических гетероарильных групп и которая содержит от 1 до 3 гетероатомов, выбранных из кислорода,азота и серы,где арильные и гетероарильные группы, определенные выше, необязательно могут быть замещены 1-3 одинаковыми или разными группами, выбранными из линейного или разветвленного (С 1-С 6)алкила,линейного или разветвленного (С 1-С 6)полигалоалкила, линейного или разветвленного (С 1-С 6)алкокси,гидрокси, карбокси, формила, линейного или разветвленного (С 1-С 6)ацила, ароила, NRbRc (где Rb и Rc,которые могут быть одинаковыми или разными, каждый представляет собой атом водорода, линейную или разветвленную (C1-С 6)алкильную группу, арильную группу или гетероарильную группу), сложного эфира, амидо, нитро, циано и атомов галогена, к их энантиомерам и диастереоизомерам, а также их фармацевтически приемлемым солям присоединения с кислотой или основанием. Среди фармацевтически приемлемых кислот можно отметить, но не ограничиваясь только ими, соляную кислоту, бромисто-водородную кислоту, серную кислоту, фосфоновую кислоту, уксусную кислоту, трифторуксусную кислоту, молочную кислоту, пировиноградную кислоту, малоновую кислоту, янтарную кислоту, глутаровую кислоту, фумаровую кислоту, винную кислоту, малеиновую кислоту, лимонную кислоту, аскорбиновую кислоту, метансульфоновую кислоту, камфорную кислоту, щавелевую кислоту и т.д. Среди фармацевтически приемлемых оснований можно отметить, но не ограничиваясь только ими,гидроксид натрия, гидроксид калия, триэтиламин, трет-бутиламин и т.д. Предпочтительно группа R1-C(=N-OR2)- находится в b- или с-положении. Предпочтительной группой для R3 и R4 является атом водорода. Предпочтительно А представляет собой алкиленовую цепь, в которой СН 2 группа необязательно может быть заменена гетероатомом и более предпочтительно атомом кислорода. Изобретение более предпочтительно относится к соединениям формулы (I), в которой А представляет собой этиленокси группу. Предпочтительными R2 группами являются атом водорода и алкильные группы, такие как, например, метильная группа.R1 благоприятно представляет собой фенильную группу, которая незамещена или замещена одним или несколькими заместителями, выбранными из таких групп, как алкил, алкокси, и атомов галогена, иR1 более предпочтительно представляет собой незамещенную фенильную группу. Предпочтительными группами В являются алкильные или алкенильные группы, и более предпочтительно алкильные группы замещены группой,-3 012437 где Rx, Ry и Rz, которые могут быть одинаковыми или разными каждый представляет собой: атом водорода или алкильную группу, такую как, например, метильная, этильная, гропильная, изопропильная, бутильная, изобутильная, трет-бутильная, пентильная, изопентильная, неопентильная или гексильная группа, полигалоалкильную группу, такую как, например, трифторметильная или трифторэтильная группа, или фенильную или бензильную группу. Изобретение более предпочтительно относится к соединениям формулы (I), в которой В представ ляет собой алкильную или алкенильную группу имеют значения, указанные выше. Также благоприятно, B представляет собой группу имеют значения, указанные выше. Еще более предпочтительно В представляет собой группу, в которой Rx и Ry имеют значения, указанные выше. Изобретение более предпочтительно относится к соединениям формулы (I), в которойX представляет собой атом кислорода или атом серы,А представляет собой цепь,R3 и R4 одновременно представляют собой атом водорода,R2 представляет собой атом водорода или алкильную группу,R1 представляет собой незамещенную фенильную группу и В представляет собой группу в которой Rv и Ry имеют значения, указанные выше. Еще более предпочтительно изобретение относится к следующим соединениям формулы (I): этил 2-этокси-3-[4-(2-7-[(метоксиимино)(фенил)метил]-3-оксо-2,3-дигидро-4H-1,4-бензотиазин-4 илэтокси)фенил]пропаноат,этил 3-[4-(2-7-[(метоксиимино)(фенил)метил]-3-оксо-2,3-дигидро-4H-1,4-бензотиазин-4-илэтокси)фенил]-2-(2,2,2-трифторэтокси)пропаноат,этил 2-этокси-3-[4-(2-6-[(метоксиимино)(фенил)метил]-3-оксо-2,3-дигидро-4H-1,4-бензоксазин-4 илэтокси)фенил]пропаноат,этил 2-этокси-3-[4-(2-7-[(гидроксиимино)(фенил)метил]-3-оксо-2,3-дигидро-4H-1,4-бензотиазин 4-илэтокси)фенил]пропаноат,этил 3-[4-(2-7-[(гидроксиимино)(фенил)метил]-3-оксо-2,3-дигидро-4H-1,4-бензотиазин-4-илэтокси)фенил]-2-(2,2,2-трифторэтокси)пропаноат этил 2-этокси-3-[4-(2-6-[(гидроксиимино)(фенил)метил]-3-оксо-2,3-дигидро-4H-1,4-бензоксазин 4-илэтокси)фенил]пропаноат,2-этокси-3-[4-(2-7-[(гидроксиимино)(фенил)метил]-3-оксо-2,3-дигидро-4H-1,4-бензотиазин-4 илэтокси)фенил]пропионовая кислота,2-этокси-3-[4-(2-7-[(метоксиимино)(фенил)метил]-3-оксо-2,3-дигидро-4H-1,4-бензотиазин-4 илэтокси)фенил]пропионовая кислота,3-[4-(2-7-[(гидроксиимино)(фенил)метил]-3-оксо-2,3-дигидро-4H-1,4-бензотиазин-4-илэтокси)фенил]-2-(2,2,2-трифторэтокси)пропионовая кислота,3-[4-(2-7-[(метоксиимино)(фенил)метил]-3-оксо-2,3-дигидро-4H-1,4-бензотиазин-4-илэтокси)фенил]-2-(2,2,2-трифторэтокси)пропионовая кислота,2-этокси-3-[4-(2-6-[(гидроксиимино)(фенил)метил]-3-оксо-2,3-дигидро-4H-1,4-бензоксазин-4 илэтокси)фенил]пропионовая кислота,2-этокси-3-[4-(2-6-[(метоксиимино)(фенил)метил]-3-оксо-2,3-дигидро-4H-1,4-бензоксазин-4 илэтокси)фенил]пропионовая кислота. Энантиомеры, диастереоизомеры, а также фармацевтически приемлемые соли присоединения с кислотой или основанием предпочтительных соединений по изобретению оставляют неотъемлемую часть изобретения. Настоящее изобретение также относится к способу получения соединений формулы (I), который характеризуется тем, что в качестве исходного вещества используют соединение формулы (III) в которой R1 и X имеют значения, указанные для формулы (I),которое конденсируют в щелочной среде с соединением формулы (IV) в которой А, В, R3 и R4 имеют значения, указанные для формулы (I), и Hal представляет собой атом галогена, получая соединение формулы (V) в которой R1, R3, R4, А, В и X имеют значения, указанные для формулы (I), которое подвергают воздействию соединения формулы R2O-NH2, в которой R2 имеет значения, указанные для формулы (I), получая соединение формулы (I) которое может быть очищено в соответствии с обычной методикой разделения, превращено, если это является желательным, в соли присоединения с фармацевтически приемлемой кислотой или основанием, и необязательно разделено на изомеры в соответствии с обычной методикой разделения. Благоприятный вариант осуществления относится к способу получения соединений формулы (I),который характеризуется тем, что в качестве исходного вещества используют соединение формулы (III) в которой R1 и X имеют значения, указанные для формулы (I), которое конденсируют с соединением формулы R2O-NH2, в которой R2 имеет значения, указанные для формулы (I), получая соединение формулы (VI) в которой R1, R2 и X имеют значения, указанные для формулы (I); которое конденсируют в щелочной среде с соединением формулы (IV) в которой А, В, R3 и R4 имеют значения, указанные для формулы (I), и Hal представляет собой атом галогена, получая соединение формулы (I) которое может быть очищено в соответствии с обычной методикой разделения, превращено, если это является желательным, в соли присоединения с фармацевтически приемлемой кислотой или основанием, и необязательно разделено на изомеры в соответствии с обычной методикой разделения. Соединения формулы (III) являются коммерческими продуктами, или легко могут быть получены специалистом в данной области техники с помощью обычных химических реакций, или описаны в литературе. Соединения согласно настоящему изобретению обладают очень ценными фармакологическими свойствами. В особенности соединения проявляют очень хорошую активность относительно снижения уровня глюкозы в крови. Эти свойства обуславливают их терапевтическое применение для лечения и/или профилактики гипергликемии, дислипидемии и, более предпочтительно, для лечения инсулиннезависимого,диабета II типа, непереносимости глюкозы, заболеваний, связанных с сидромом X (включая гипертонию,ожирение, резистентность к инсулину, атеросклероз, гиперлипемию), заболевания коронарной артерии и других сердечно-сосудистых заболеваний (включая артериальную гипертонию, сердечную недостаточность, венозную недостаточность), заболевания почек (включая гломерулонефрит, гломерулосклероз,нефротический синдром, гипертонический нефросклероз), ретинопатии, заболеваний, связанных с активацией клеток эндотелия, псориаза, синдрома поликистоза яичника, слабоумия, осложнений диабета и остеопороза. Они могут применяться в качестве ингибиторов альдоз-редуктазы для улучшения когнитивных функций при слабоумии и при осложнениях диабета, воспалительных заболеваниях кишечника, дистрофической миотонии, панкреатите, артериосклерозе, ксантоме. Действие этих соединений также рекомендуется для лечения и/или профилактики других заболеваний, включая диабет I типа, гипертриглицеридемию, синдром X, резистентность к инсулину, дислипидемию у диабетиков, гиперлипемию, гиперхолестеринемию, артериальную гипертонию, сердечную недостаточность и сердечно-сосудистое заболевание, в особенности атеросклероз. Кроме того, показаниями для применения соединений также является регуляция аппетита, в особенности регуляция потребления пищи у особей, страдающих от таких расстройств, как ожирение, анорексия, булимия и нервно-психическая анорексия. Следовательно, соединения могут применяться для предотвращения или лечения гиперхолестеринемии, ожирения с благоприятным воздействием на гиперлипемию, гипергликемию, остеопороз, непереносимость глюкозы, резистентность к инсулину или расстройств, при которых вторичным патофизиологическим механизмом является резистентность к инсулину. Применение этих соединений обеспечивает снижение общего холестерина, веса тела, резистентности к лептину, концентрации глюкозы в плазме крови, триглицеридов, ЛНП, ЛОНП и также концентрации в плазме крови свободных жирных кислот. Соединения также могут применяться в комбинации с ингибиторами HMG СоА редуктазы, фибратами, никотиновой кислотой, холестирамином, холестиполом,пробуколом, GLP1, метформином, бигуанидами или ингибиторами обратного всасывания глюкозы и могут вводиться совместно или отдельно для обеспечения синергетического влияния на пациента, подвергаемого лечению. Кроме того, они проявляют активность при злокачественных патологиях и, в особенности, при гормонально-зависимых злокачественных новообразованиях, таких как рак молочной железы и рак ободочной кишки, и также обладают ингибирующим влиянием на процессы ангиогенеза, задействованные в эти патологии. Среди фармацевтических композиций согласно изобретению особенно можно отметить те, которые являются пригодными для перорального, парентерального, назального, чрескожного, ректального, подъязычного, глазного введения или введения в дыхательные пути, в особенности таблетки или драже,подъязычные таблетки, саше, пакеты, желатиновые капсулы, таблетки для медленного растворения под языком, лепешки, суппозитории, кремы, мази, кожные гели, составы для питья или ампулы инъекций. Дозировка изменяется в зависимости от пола, возраста и веса пациента, пути введения, природы терапевтического показания или любых сопутствующих видов лечения, и находится в диапазоне от 0,1 мг до 1 г в сутки на одно или больше введений. Настоящее изобретение также относится к новой комбинации между гетероциклическим соединением формулы (I), как определено выше, и антиоксидантом для получения фармацевтических компози-6 012437 ций для применения для лечения и/или предотвращения ожирения и избыточного веса, характеризующегося индексом массы тела, большим, чем 25. Более предпочтительными антиоксидантами согласно изобретению являются вещества, направленные против свободных радикалов, или вещества, улавливающие свободные радикалы, антилипопероксиданты, хелатирующие вещества или вещества, способные восстанавливать эндогенные антиоксиданты, такие как глутатион, витамин С или витамин Е, а также их соли присоединения с фармацевтически приемлемой кислотой или основанием. Более предпочтительными антиоксидантами комбинации согласно изобретению являются хиноновые соединения, такие как убихинон или коэнзим Q10, который действует в качестве поглотителя свободных радикалов, а также способен восстанавливать витамин Е. Предпочтительной комбинацией согласно изобретению является 3-4-[2-(6(гидроксииминофенил)метил-3-оксо-2,3-дигидро-4 Н-бензо[1,4]оксазин-4-ил)этокси]фенил-2-этоксипропионовая кислота и коэнзим Q10. Кроме того, комбинация в соответствии с изобретением обладает совершенно неожиданными фармакологическими свойствами: заявитель обнаружил, что, в действительности, проявляется синергизм между этими двумя соединениям комбинации, который дает возможность получить весьма значительное снижение жира в организме, что делает ее пригодной для лечения и/или предотвращения ожирения и избыточного веса, характеризующегося индексом массы тела, большим, чем 25. В США ожирению подвержены 20% мужчин и 25% женщин. Пациенты, которые имеют индекс массы тела (BMI=вес(кг)/рост 2(м 2, больший или равный 30, считаются страдающими ожирением (Int. J.(25BMI30) могут иметь различное происхождение: они могут возникать вследствие нарушения регуляции потребления пищи, вследствие гормонального нарушения, или вследствие проведения лечения: лечение диабета II типа с помощью сульфонилмочевин вызывает у пациентов прибавку веса. Подобно этому, при диабете I типа (инсулинзависимом) инсулинотерапия также вызывает прибавку веса у пациентов (In Progress in Obesity Research, 8th International Congress on Obesity, 1999, 739-746; Annals of Internal Medicine, 1998, 128, 165-175). Ожирение и избыточный вес являются хорошо установленными факторами риска для сердечнососудистых заболеваний: они ассоциируются со значительным повышением риска возникновения церебро-васкулярных осложнений и инсулиннезависимого диабета, поскольку они обеспечивают предрасположенность к инсулин-резистентности, дислипидемии и возникновению макроваскулярных расстройств(нефропатии, ретинопатии, ангиопатии). Другими патологиями являются последствия ожирения или избыточного веса: среди них могут быть упомянуты, в частности, камни желчного пузыря, респираторная дисфункция,остеоартрит, некоторые формы рака, и в случае очень тяжелого ожирения преждевременная смерть (N.Engl. J. Med., 1995, 333, 677-385; JAMA, 1993, 270, 2207-2212). Комбинация в соответствии с изобретением позволяет получить потерю веса, которая даже если является умеренной, будет значительным образом снижать все факторы риска, ассоциированные с ожирением (Int. J. Obes., 1997, 21, 55-9; Int. J. Obes., 1992, 21, S5-9). Комбинация в соответствии с изобретением будет, таким образом, полезной для лечения и/или предотвращения ожирения и избыточного веса, характеризующегося индексом массы тела, большим, чем 25. Изобретение, таким образом, относится к применению комбинации соединения формулы (I) и антиоксиданта для получения фармацевтических композиций, предназначенных для лечения и/или предотвращения ожирения и избыточного веса, характеризующегося индексом массы тела, большим чем 25, и меньшим чем 30. В частности, комбинация в соответствии с изобретением используется для лечения и/или предотвращения ожирения и избыточного веса, характеризующегося индексом массы тела, большим, чем 25, и меньшим, чем 30, вызванного терапевтическим лечением, таким, как лечение диабета типа I или II. Изобретение, таким образом, относится к применению комбинации соединения формулы (I) и антиоксиданта для получения фармацевтических композиций, предназначенных для лечения и/или предотвращения ожирения и избыточного веса, характеризующегося индексом массы тела, большим, чем 25, и меньшим, чем 30, вызванного терапевтическим лечением, таким как лечение диабета типа I или II. Изобретение также относится к фармацевтическим композициям, содержащим комбинацию соединения формулы (I) и антиоксиданта, как определено выше, в сочетании с одним или несколькими фармацевтически приемлемыми наполнителями. Среди фармацевтических композиций согласно изобретению особенно можно отметить те, которые являются пригодными для перорального, парентерального или назального введения, таблетки или драже,подъязычные таблетки, желатиновые капсулы, лепешки, суппозитории, кремы, мази, кожные гели и т.д. В частности, изобретение относится к фармацевтическим композициям, содержащим соединение формулы (I), как определено выше, и антиоксидант, такой как коэнзим Q10 или витамин Е, в сочетании с одним или несколькими фармацевтически приемлемыми наполнителями.-7 012437 Применяемая дозировка изменяется в зависимости от пола, возраста и веса пациента, пути введения, природы терапевтического показания или любых ассоциированных лечений, и находится в пределах от 0,1 мг до 1 г для каждого компонента комбинации в сутки на одно или несколько введений. Последующие приготовления и примеры иллюстрируют изобретение, но никоим образом его не ограничивают. Приготовление 1: 7-[Метоксиимино]фенилметил-2H,4H-бензо[1,4]тиазин-3-он Этап А. 7-Бензоил-2 Н,4 Н-бензо[1,4]тиазин-3-он 7,4 г бензойной кислоты и затем 10 г 4H-бензо[1,4]тиазин-3-она добавляли к 100 г полифосфорной кислоты. Смесь нагревали при 160 С в течение 6 ч при механическом перемешивании. После этого раствор гидролизовали и осадок фильтровали в вакууме и промывали насыщенным раствором гидрокарбоната натрия и затем абсолютным спиртом. Полученное твердое вещество перекристаллизовывали из толуола, получая указанный в заглавии продукт в виде бежевого порошка. Точка плавления: 211-213 С Этап В. 7-[Метоксиимино]фенилметил-2 Н,4 Н-бензо[ 1,4]тиазин-3-он 5 г соединения, полученного на этапе А, растворяли в 40 мл метанола и затем 3 г гидрохлорида метоксиламина и 5,7 г пиридина. Смесь нагревали в колбе с обратным холодильником в течение 4 ч при перемешивании. После прекращения нагревания продукт оставляли осаждаться. Осадок отфильтровывали, и он соответствовал "Е" изомеру указанного в заглавии соединения. Фильтрат гидролизовали и подкисляли с помощью 3 н. HCl, и затем осадок, который соответствует "Z" изомеру указанного в заглавии соединения, отфильтровывали. Точка плавления: 214-216 С ("Е" изомер); 138-140 С (смесь "Е" и "Z" : 72/28%) Приготовление 2: 6-[Метоксиимино]фенилметил-2 Н,4 Н-бензо[1,4]оксазин-3-он Этап А. 6-Бензоил-2 Н,4 Н-бензо[1,4]оксазин-3-он 8,2 г бензойной кислоты и затем 10 г 2H-[1,4]-бензоксазин-3-она добавляли к 100 г полифосфорной кислоты. Смесь нагревали при 160 С в течение 6 ч при механическом перемешивании. После этого раствор гидролизовали и осадок фильтровали в вакууме и промывали насыщенным раствором гидрокарбоната натрия и затем абсолютным спиртом. Полученное твердое вещество перекристаллизовывали из толуола, получая указанный в заглавии продукт в виде белого порошка. Точка плавления: 154-156 С Этап В. 6-[Метоксиимино]фенилметил-2 Н,4 Н-бензо[1,4]оксазин-3-он 5 г соединения, полученного на этапе А, растворяли в 40 мл метанола и затем 3 г гидрохлорида метоксиламина и 5,7 г пиридина. Смесь нагревали в колбе с обратным холодильником в течение 4 ч при перемешивании. После прекращения нагревания фильтрат гидролизовали и подкисляли с помощью 3 н.HCl и затем осадок, который соответствует указанному в заглавии соединении, отфильтровывали. Точка плавления: 147-149 С Приготовление 3: Этил 3-4-[2-(7-бензоил-3-оксо-2,3-дигидро-4H-бензо[1,4]тиазин-4 ил)этокси]фенил-2-этоксипропаноат 1 г соединения, полученного на этапе А приготовления 1, растворяли в 30 мл диметилформамида и затем добавляли 1 г карбоната калия и перемешивали при 80 С в течение 1 ч. Этил 3-[4-(2 хлорэтокси)фенил]-2-этоксипропаноат (1,67 г) растворяли в небольшом количестве диметилформамида и перемешивали в течение ночи при 110 С. Затем диметилформамид упаривали и после этого раствор гидролизовали и подкисляли. Водную фазу экстрагировали дихлорметаном, высушивали над сульфатом магния и фильтровали и органическую фазу упаривали. Остаток очищали на силикагеле, используя толуол и этилацетат (8/2) в качестве элюента, при этом получали указанный в заглавии продукт в виде масла. Приготовление 4: Этил 3-4-[2-(7-бензоил-3-оксо-2,3-дигидро-4H-бензо[1,4]тиазин-4 ил)этокси]фенил-2-(2,2,2-трифторэтокси)пропаноат 1 г соединения, полученного на этапе А приготовления 1, растворяли в 30 мл диметилформамида и затем добавляли 1 г карбоната калия и перемешивали при 80 С в течение 1 ч. Этил 3-[4-(2 хлорэтокси)фенил]-2-(2,2,2-трифторэтокси)пропаноат (1,97 г) растворяли в небольшом количестве диметилформамида и перемешивали в течение ночи при 110 С. Затем диметилформамид упаривали, и после этого раствор гидролизовали и подкисляли. Водную фазу экстрагировали дихлорметаном, высушивали над сульфатом магния и фильтровали и органическую фазу упаривали. Остаток очищали на силикагеле,используя толуол и этилацетат (8/2) в качестве элюента, при этом получали указанный в заглавии продукт в виде масла. Приготовление 5: Этил 3-4-[2-(6-бензоил-3-оксо-2,3-дигидро-4H-бензо[1,4]оксазин-4 ил)этокси]фенил-2-этоксипропаноат 1 г соединения, полученного на этапе А приготовления 2, растворяли в 30 мл диметилформамида и затем добавляли 1,1 г карбоната калия и перемешивали при 80 С в течение 1 ч. Этил 3-[4-(2 хлорэтокси)фенил]-2-этоксипропаноат (1,78 г) растворяли в небольшом количестве диметилформамида и перемешивали в течение ночи при 110 С. Затем диметилформамид упаривали и после этого раствор гидролизовали и подкисляли. Водную-8 012437 фазу экстрагировали дихлорметаном, высушивали над сульфатом магния и фильтровали и органическую фазу упаривали. Остаток очищали на силикагеле, используя толуол и этилацетат (8/2) в качестве элюента, при этом получали указанный в заглавии продукт в виде масла. Приготовление 6: 6-[Метоксиимино]фенилметил-2H,4H-бензо[1,4]тиазин-3-он Этап А. 6-Бензоил-2 Н,4 Н-бензо[1,4]тиазин-3-он Этап В. 6-[Метоксиимино]фенилметил-2 Н,4 Н-бензо[1,4]тиазин-3-он Методику осуществляли, как описано в приготовлении 2, заменяя 2H-[1,4]-бензоксазин-3-он на 2H[1,4]-бензотиазин-3-он. Приготовление 7: 7-[Метоксиимино]фенилметил-2H,4H-бензо[1,4]оксазин-3-он Этап А. 7-Бензоил-2 Н,4 Н-бензо[1,4]оксазин-3-он Этап В. 7-[Метоксиимино]фенилметил-2 Н,-4 Н-бензо[1,4]оксазин-3-он Методику осуществляли, как описано в приготовлении 1, заменяя 4 Н-бензо[1,4]тиазин-3-он на 4H[1,4]-бензоксазин-3-он. Приготовление 8: Этил 3-4-[2-(6-бензоил-3-оксо-2,3-дигидро-4H-бензо[1,4]оксазин-4 ил)этокси]фенил-2-этоксипропаноат Методику осуществляли, как описано в приготовлении 5, заменяя продукт, полученный на этапе А приготовления 2, на продукт, полученный на этапе А приготовления 6. Приготовление 9: Этил 3-4-[2-(6-бензоил-3-оксо-2,3-дигидро-4H-бензо[1,4)тиазин-4 ил)этокси]фенил-2-(2,2,2-трифторэтокси)пропаноат Методику осуществляли, как описано в приготовлении 4, заменяя продукт, полученный на этапе А приготовления 1, на продукт, полученный на этапе А приготовления 6. Приготовление 10: Этил 3-4-[2-(7-бензоил-3-оксо-2,3-дигидро-4H-бензо[1,4]оксазин-4 ил)этокси]фенил-2-этоксипропаноат Методику осуществляли, как описано в приготовлении 3, заменяя продукт, полученный на этапе А приготовления 1, на продукт, полученный на этапе А приготовления 7. Приготовление 11: Этил 3-4-[2-(7-бензоил-3-оксо-2,3-дигидро-4H-бензо[1,4]оксазин-4 ил)этокси]фенил-2-(2,2,2-трифторэтокси)пропаноат Методику осуществляли, как описано в приготовлении 4, заменяя продукт, полученный на этапе А приготовления 1, на продукт, полученный на этапе А приготовления 7. Пример 1: 3-4-[2-(7-(Метоксииминофенил)метил-3-оксо-2,3-дигидро-4H-бензо[1,4]тиазин-4 ил)этокси]фенил-2-этоксипропаноат 1 г соединения, полученного в приготовлении 1, растворяли в 30 мл диметилформамида и затем добавляли 0,92 г карбоната калия и перемешивали при 80 С в течение 1 ч. Этил 3-[4-(2-хлорэтокси)фенил]2-этоксипропаноат (1,51 г) растворяли в небольшом количестве диметилформамида и перемешивали в течение ночи при 110 С. Затем диметилформамид упаривали, и после этого раствор гидролизовали и подкисляли. Водную фазу экстрагировали дихлорметаном, высушивали над сульфатом магния и фильтровали и органическую фазу упаривали. Остаток очищали на силикагеле, используя толуол и этилацетат (8/2) в качестве элюента, при этом получали указанный в заглавии продукт в виде масла. Элементный микроанализ: Пример 2: Этил 3-4-[2-(7-(метоксииминофенил)метил-3-оксо-2,3-дигидро-4H-бензо[1,4]тиазин-4 ил)этокси]фенил-2-(2,2,2-трифтор-этокси)пропаноат 1 г соединения, полученного в приготовлении 1, растворяли в 30 мл диметилформамида и затем добавляли 0,91 г карбоната калия и перемешивали при 80 С в течение 1 ч. Этил 3-[4-(2-хлорэтокси)фенил]2-(2,2,2-трифторэтокси)пропаноат (1,78 г) растворяли в небольшом количестве диметилформамида и перемешивали в течение ночи при 110 С. Затем диметилформамид упаривали, и после этого раствор гидролизовали и подкисляли. Водную фазу экстрагировали дихлорметаном, высушивали над сульфатом магния и фильтровали и органическую фазу упаривали. Остаток очищали на силикагеле, используя толуол и этилацетат (8/2) в качестве элюента, при этом получали указанный в заглавии продукт в виде зеленого масла. Пример 3. Этил 3-4-[2-(6-(метоксииминофенил)метил-3-оксо-2,3-дигидро-4H-бензо[1,4]оксазин-4 ил)этокси]фенил-2-этоксипропаноат 1 г соединения, полученного в приготовлении 2, растворяли в 30 мл диметилформамида и затем добавляли 1 г карбоната калия и перемешивали при 80 С в течение 1 ч. Этил 3-[4-(2-хлорэтокси)фенил]-2 этоксипропаноат (1,59 г) растворяли в небольшом количестве диметилформамида и перемешивали в течение ночи при 110 С. Затем диметилформамид упаривали и после этого раствор гидролизовали и подкисляли. Водную фазу экстрагировали дихлорметаном, высушивали над сульфатом магния и фильтровали и органическую фазу упаривали. Остаток очищали на силикагеле, используя толуол и этилацетат (8/2) в качестве элюента, при этом получали указанный в заглавии продукт. Пример 4. Этил 3-4-[2-(7-(гидроксииминофенил)метил-3-оксо-2,3-дигидро-4H-бензо[1,4]тиазин-4 ил)этокси]фенил-2-этоксипропаноат 1 г соединения, полученного в приготовлении 3, растворяли в 20 мл этанола и затем добавляли 0,4 г гидрохлорида гидроксиламина и 0,6 г пиридина. Смесь нагревали в колбе с обратным холодильником в течение 4 ч при перемешивании. Смесь гидролизовали и затем подкисляли с помощью 3 н. HCl и раствор экстрагировали этилацетатом, высушивали, фильтровали и упаривали. Остаток очищали на силикагеле, используя толуол и этилацетат (8/2) в качестве элюента, при этом получали указанный в заглавии продукт в виде масла. Элементный микроанализ: Пример 5. Этил 3-4-[2-(7-(гидроксииминофенил)метил-3-оксо-2,3-дигидро-4H-бензо[1,4]тиазин-4 ил)этокси]фенил-2-(2,2,2-трифторэтокси)пропаноат 1 г соединения, полученного в приготовлении 4, растворяли в 20 мл этанола и затем добавляли 0,36 г гидрохлорида гидроксиламина и 0,5 г пиридина. Смесь нагревали в колбе с обратным холодильником в течение 4 ч при перемешивании. Смесь гидролизовали и затем подкисляли с помощью 3 н. HCl и раствор экстрагировали этилацетатом, высушивали, фильтровали и упаривали. Остаток очищали на силикагеле, используя толуол и этилацетат (8/2) в качестве элюента, при этом получали указанный в заглавии продукт в виде зеленоватого порошка. Элементный микроанализ: Пример 6. Этил 3-4-[2-(6-(гидроксииминофенил)метил-3-оксо-2,3-дигидро-4H-бензо[1,4]оксазин 4-ил)этокси]фенил-2-этоксипропаноат 1 г соединения, полученного в приготовлении 5, растворяли в 20 мл этанола и затем добавляли 0,41 г гидрохлорида гидроксиламина и 0,6 г пиридина. Смесь нагревали в колбе с обратным холодильником в течение 4 ч при перемешивании. Смесь гидролизовали и затем подкисляли с помощью 3 н. HCl и раствор экстрагировали этилацетатом, высушивали, фильтровали и упаривали. Остаток очищали на силикагеле, используя толуол и этилацетат (8/2) в качестве элюента, при этом получали указанный в заглавии продукт в виде масла. Пример 7. 3-4-[2-(7-(Гидроксииминофенил)метил-3-оксо-2,3-дигидро-4H-бензо[1,4]тиазин-4 ил)этокси]фенил-2-этоксипропионовая кислота 1 г соединения, полученного в примере 4, растворяли в смеси тетрагидрофуран/вода (12/8 мл) и затем добавляли 0,13 г гидроксида лития, растворенного в небольшом количестве воды. Реакционную смесь перемешивали в течение ночи при 50 С. После этого тетрагидрофуран упаривали и затем раствор гидролизовали и потом подкисляли с помощью 3 н. HCl. После этого экстрагировали этилацетатом, высушивали, фильтровали и упаривали органическую фазу. Остаток очищали на силикагеле, используя дихлорметан и метанол (95/5) в качестве элюента, при этом получали указанный в заглавии продукт в виде бежевого порошка. Точка плавления: 74-76 С Пример 8. 3-4-[2-(7-(Метоксииминофенил)метил-3-оксо-2,3-дигидро-4H-бензо[1,4]тиазин-4 ил)этокси]фенил-2-этоксипропионовая кислота 1 г соединения, полученного в примере 1, растворяли в смеси тетрагидрофуран/вода (12/8 мл), и затем добавляли 0,13 г гидроксида лития, растворенного в небольшом количестве воды. Реакционную смесь перемешивали в течение ночи при 50 С. После этого тетрагидрофуран упаривали и затем раствор гидролизовали и потом подкисляли с помощью 3 н. HCl. После этого экстрагировали этилацетатом, высушивали, фильтровали и упаривали органическую фазу. Остаток очищали на силикагеле, используя дихлорметан и метанол (95/5) в качестве элюента, при этом получали указанный в заглавии продукт в виде желтоватого порошка. Точка плавления: 77-79 С. Элементный микроанализ: Пример 9. 3-4-[2-(7-(Гидроксииминофенил)метил-3-оксо-2,3-дигидро-4H-бензо[1,4]тиазин-4 ил)этокси]фенил-2-(2,2,2-трифторэтокси)пропионовая кислота 1 г соединения, полученного в примере 5, растворяли в смеси тетрагидрофуран/вода (12/8 мл), и затем добавляли 0,12 г гидроксида лития, растворенного в небольшом количестве воды. Реакционную смесь перемешивали в течение ночи при 50 С. После этого тетрагидрофуран упаривали и затем раствор гидролизовали и потом подкисляли с помощью 3 н. HCl. После этого экстрагировали этилацетатом, высушивали, фильтровали и упаривали органическую фазу. Остаток очищали на силикагеле, используя дихлорметан и метанол (95/5) в качестве элюента, при этом получали указанный в заглавии продукт в виде зеленого порошка. Точка плавления: 85-88 С . Элементный микроанализ: Пример 10. 3-4-[2-(7-(Метоксииминофенил)метил-3-оксо-2,3-дигидро-4H-бензо[1,4]тиазин-4 ил)этокси]фенил-2-(2,2,2-трифторэтокси)пропионовая кислота 1 г соединения, полученного в примере 2, растворяли в смеси тетрагидрофуран/вода (12/8 мл), и затем добавляли 0,11 г гидроксида лития, растворенного в небольшом количестве воды. Реакционную смесь перемешивали в течение ночи при 50 С. После этого тетрагидрофуран упаривали и затем раствор гидролизовали и потом подкисляли с помощью 3 н. HCl. После этого экстрагировали этилацетатом, высушивали, фильтровали и упаривали органическую фазу. Остаток очищали на силикагеле, используя дихлорметан и метанол (95/5) в качестве элюента, при этом получали указанный в заглавии продукт в виде зеленого порошка. Точка плавления: 64-66 С. Элементный микроанализ: Пример 11. 3-4-[2-(6-(гидроксииминофенил)метил-3-оксо-2,3-дигидро-4 Н-бензо[1,4]оксазин-4 ил)этокси]фенил-2-этоксипропионовая кислота 1 г соединения, полученного в примере 6, растворяли в смеси тетрагидрофуран/вода (12/8 мл), и затем добавляли 0,13 г гидроксида лития, растворенного в небольшом количестве воды. Реакционную смесь перемешивали в течение ночи при 50 С. После этого тетрагидрофуран упаривали и затем раствор гидролизовали и потом подкисляли с помощью 3 н. HCl. После этого экстрагировали этилацетатом, высушивали, фильтровали и упаривали органическую фазу. Остаток очищали на силикагеле, используя дихлорметан и метанол (95/5) в качестве элюента, при этом получали указанный в заглавии продукт в виде бежевого порошка. Точка плавления: 75-76 С. Пример 12. 3-4-[2-(6-(Метоксииминофенил)метил-3-оксо-2,3-дигидро-4H-бензо[1,4]оксазин-4 ил)этокси]фенил-2-этоксипропионовая кислота 1 г соединения, полученного в примере 3, растворяли в смеси тетрагидрофуран/вода (12/8 мл), и затем добавляли 0,13 г гидроксида лития, растворенного в небольшом количестве воды. Реакционную смесь перемешивали в течение ночи при 50 С. После этого тетрагидрофуран упаривали и затем раствор гидролизовали и потом подкисляли с помощью 3 н. HCl. После этого экстрагировали этилацетатом, высушивали, фильтровали и упаривали органическую фазу. Остаток очищали на силикагеле, используя дихлорметан и метанол (95/5) в качестве элюента, при этом получали указанный в заглавии продукт в виде желтоватого порошка. Точка плавления: 63-65 С. Элементный микроанализ: Пример 13. Этил 3-4-[2-(6-(метоксииминофенил)метил-3-оксо-2,3-дигидро-4H-бензо[1,4]тиазин-4 ил)этокси]фенил-2-этоксипропаноат Методику осуществляли, как описано в примере 1, заменяя соединение из приготовления 1 на соединение из приготовления 6. Указанный в заглавии продукт получали в виде масла. Элементный микроанализ: Пример 14. Этил 3-4-[2-(6-(метоксииминофенил)метил-3-оксо-2,3-дигидро-4H-бензо[1,4]тиазин-4 ил)этокси]фенил-2-(2,2,2-трифторэтокси)пропаноат Методику осуществляли, как описано в примере 2, заменяя соединение из приготовления 1 на соединение из приготовления 6. Указанный в заглавии продукт получали в виде желтого масла. Элементный микроанализ: Пример 15. Этил 3-4-[2-(7-(метоксииминофенил)метил-3-оксо-2,3-дигидро-4H-бензо[1,4]оксазин 4-ил)этокси]фенил-2-этоксипропаноат Методику осуществляли, как описано в примере 1, заменяя соединение из приготовления 1 на соединение из приготовления 7. Указанный в заглавии продукт получали в виде масла. Элементный микроанализ: Пример 16. Этил 3-4-[2-(7-(метоксииминофенил)метил-3-оксо-2,3-дигидро-4H-бензо[1,4]оксазин 4-ил)этокси]фенил-2-(2,2,2-трифторэтокси)пропаноат Методику осуществляли, как описано в примере 2, заменяя соединение из приготовления 1 на соединение из приготовления 7. Указанный в заглавии продукт получали в виде бесцветного масла. Элементный микроанализ: Пример 17: Этил 3-4-[2-(6-(гидроксииминофенил)метил-3-оксо-2,3-дигидро-4H-бензо[1,4]тиазин 4-ил)этокси]фенил-2-этоксипропаноат Методику осуществляли, как описано в примере 4, заменяя соединение из приготовления 3 на соединение из приготовления 8. Указанный в заглавии продукт получали в виде желтого порошка. Точка плавления: 65-66 С. Пример 18. Этил 3-4-[2-(6-(гидроксииминофенил)метил-3-оксо-2,3-дигидро-4H-бензо[1,4]тиазин 4-ил)этокси]фенил-2-(2,2,2-трифторэтокси)пропаноат Методику осуществляли, как описано в примере 5, заменяя соединение из приготовления 4 на соединение из приготовления 9. Указанный в заглавии продукт получали в виде белого порошка. Точка плавления: 171-173 С Элементный микроанализ: Пример 19. Этил 3-4-[2-(7-(гидроксииминофенил)метил-3-оксо-2,3-дигидро-4H-бензо[1,4]оксазин 4-ил)этокси]фенил-2-этоксипропаноат Методику осуществляли, как описано в примере 4, заменяя соединение из приготовления 3 на соединение из приготовления 10. Указанный в заглавии продукт получали в виде желтого порошка. Точка плавления: 84-86 С. Элементный микроанализ: Пример 20. Этил 3-4-[2-(7-(гидроксииминофенил)метил-3-оксо-2,3-дигидро-4H-бензо[1,4]оксазин 4-ил)этокси]фенил-2-(2,2,2-трифторэтокси)пропаноат Методику осуществляли, как описано в примере 5, заменяя соединение из приготовления 4 на соединение из приготовления 11. Указанный в заглавии продукт получали в виде белого порошка. Точка плавления: 84-86 С. Элементный микроанализ: Пример 21. 3-4-[2-(6-(Метоксииминофенил)метил-3-оксо-2,3-дигидро-4H-бензо[2,3]тиазин-4 ил)этокси]фенил-2-этоксипропионовая кислота Методику осуществляли, как описано в примере 8, заменяя соединение из примера 1 на соединение из примера 13. Указанный в заглавии продукт получали в виде желтого порошка. Точка плавления: 5861 С. Элементный микроанализ: Пример 22. 3-4-[2-(6-(Метоксииминофенил)метил-3-оксо-2,3-дигидро-4H-бензо[1,4]тиазин-4 ил)этокси]фенил-2-(2,2,2-трифторэтокси)пропионовая кислота Методику осуществляли, как описано в примере 10, заменяя соединение из примера 2 на соединение из примера 14. Указанный в заглавии продукт получали в виде белого порошка. Точка плавления: 6668 С. Элементный микроанализ: Пример 23. 3-4-[2-(6-(Гидроксииминофенил)метил-3-оксо-2,3-дигидро-4H-бензо[1,4]тиазин-4 ил)этокси]фенил-2-этоксипропионовая кислота Методику осуществляли, как описано в примере 7, заменяя соединение из примера 4 на соединение из примера 17. Указанный в заглавии продукт получали в виде бежевого порошка. Точка плавления: 127- 13012437 130 С. Пример 24. 3-4-[2-(6-(Гидроксииминофенил)метил-3-оксо-2,3-дигидро-4H-бензо[1,4]тиазин-4 ил)этокси]фенил-2-(2,2,2-трифторэтокси)пропионовая кислота Методику осуществляли, как описано в примере 9, заменяя соединение из примера 5 на соединение из примера 18. Указанный в заглавии продукт получали в виде белого порошка. Точка плавления: 9799 С. Элементный микроанализ: Пример 25. 3-4-[2-(7-(Метоксииминофенил)метил-3-оксо-2,3-дигидро-4H-бензо[1,4]оксазин-4 ил)этокси] фенил -2-этоксипропионовая кислота Методику осуществляли, как описано в примере 8, заменяя соединение из примера 1 на соединение из примера 15. Указанный в заглавии продукт получали в виде белого порошка. Точка плавления: 5457 С. Элементный микроанализ: Пример 26. 3-4-[2-(7-(Метоксииминофенил)метил-3-оксо-2,3-дигидро-4H-бензо[1,4]оксазин-4 ил)этокси]фенил-2-(2,2,2-трифторэтокси)пропионовая кислота Методику осуществляли, как описано в примере 10, заменяя соединение из примера 2 на соединение из примера 16. Указанный в заглавии продукт получали в виде желтого порошка. Точка плавления: 61-64 С. Элементный микроанализ: Пример 27. 3-4-[2-(7-(Гидроксииминофенил)метил-3-оксо-2,3-дигидро-4H-бензо[1,4]оксазин-3 ил)этокси]фенил-2-этоксипропионовая кислота Методику осуществляли, как описано в примере 7, заменяя соединение из примера 4 на соединение из примера 19. Указанный в заглавии продукт получали в виде белого порошка. Точка плавления: 9597 С. Элементный микроанализ: Пример 28. 3-4-[2-(7-(Гидроксииминофенил)метил-3-оксо-2,3-дигидро-4H-бензо[1,4]оксазин-4 ил)этокси]фенил-2-(2,2,2-трифторэтокси)пропионовая кислота Методику осуществляли, как описано в примере 9, заменяя соединение из примера 5 на соединение из примера 20. Указанный в заглавии продукт получали в виде белого порошка. Точка плавления: 8688 С. Элементный микроанализ: Фармакологическое исследование Пример А. Исследование острой токсичности Острую токсичность оценивали после перорального введения группам, которые включали 8 мышей каждая (262 г). За животными наблюдали через регулярные промежутки времени в течение первого дня,и затем ежедневно в течение двух недель на протяжении курса лечения. Была определена LD50 (доза, которая вызывает гибель 50% животных) и показана низкая токсичность соединений по изобретению. Пример В. Эффективность на генетических моделях Мутации у лабораторных животных, а также различные чувствительности к режиму питания пре- 14012437 доставляют возможность развития животных моделей, имеющих инсулиннезависимый диабет и гиперлипемию, связанную с ожирением и с резистентностью к инсулину. В различных лабораториях были разработаны генетические мышиные модели (ob/ob) (Diabetes,1982, 31 (1), 1-6) и крысы Zucker (fa/fa) для понимания патологической физиологии этих заболеваний и тестирования эффективности новых противодиабетических соединений (Diabetes, 1983, 32, 830-838). Противодиабетическое и гиполипемическое действие на мышах ob/ob Для тестов в условиях in vivo использовали самок мышей ob/ob (Harlan) в возрасте 10 недель. Животных выдерживали при 12-ти часовом цикле день-ночь при 25 С. У мыши наблюдалась исходная гипергликемия 2 г/л. Животных случайно отбирали, что касается их гликемии, в группы по 6 животных. Тестируемые соединения, для внутрибрюшинного применения, растворяли в смеси диметилсульфоксида(10%) и Солютола (15%) и вводили в дозе 10 мг/кг в объеме 2,5 мл/кг два раза в день в течение четырех дней. Тестируемые соединения, для перорального применения, вводили в дозе 30 мг/кг, которую вводили в объеме 2,5 мл/кг 1% НЕС два раза в день в течение четырех дней. Контрольные группы получали растворители в тех же условиях, что и группы, подвергнутые лечению. Активность продуктов оценивали путем измерения гликемии, триглицеридов и инсулинемии через 24 ч после последнего введения и измерения веса тела каждый день. Соединения по изобретению демонстрируют очень хорошую способность снижения гликемии,триглицеридов и инсулинемии: например, соединение из примера 11, которое вводили в дозе 3 мг/кг,обеспечило снижение на 25% гликемии, уменьшение на 45% триглицеридов и уменьшение на 22% инсулинемии, с незначительными изменениями веса тела, тогда как росиглитазон в аналогичных условиях проявлял значительное повышение в течение четырех дней. Дополнительно, при осуществлении тестов в условиях in vivo не было обнаружено побочных действий. Пример С. Фармацевтическая композиция 1000 таблеток, каждая содержит дозу 5 мг Пример D. Изменение веса тела Использовали самцов С 57 Black 6 ob/ob мышей в возрасте от 8 до 12 недель. После прохождения карантина в течение одной недели их взвешивали и затем рандомизировали в зависимости от их веса,при этом образовывалось 6 гомогенных групп (исходный вес существенно не отличался). После взвешивания мышей им вводили различные тестируемые комбинации интраперитонеально один раз в день в течение 7 дней. Молекулы вводили в растворе 5% ДМСО/15% Солютол / Н 2 О до необходимого количества, подогретом до температуры 65 С для обеспечения хорошей растворимости. Дополнительно раствор предварительно нагревали перед инъекцией. Мышей взвешивали каждый день и регистрировали вес,полученный через 7 дней лечения. Полученные результаты убедительно свидетельствуют о том, что комбинация в соответствии с изобретением между соединением формулы (I) и антиоксидантом позволяет значительно снизить вес мышей, страдающих ожирением, существует синергизм между двумя компонентами комбинации, потеря веса у мышей, страдающих ожирением, является намного больше в случае комбинации, чем в случае отдельного введения каждого компонента. Пример Е.: Фармацевтическая композиция 100 таблеток, каждая содержит дозу 30 мг 3-4-[2-(6-(гидроксииминофенил)метил-3-оксо-2,3 дигидро-4 Н-бензо[1,4]оксазин-4-ил)этокси]фенил-2-этоксипропионовой кислоты и 10 мг коэнзима Q10X представляет собой атом кислорода или атом серы,А представляет собой (С 1-С 6)алкиленовую цепь, в которой СН 2 группа необязательно может быть заменена атомом кислорода,R1 представляет собой арильную группу, aR2 представляет собой атом водорода либо линейную или разветвленную (С 1-С 6)алкильную группу,R3 и R4 каждый представляет собой атом водорода,В представляет собой линейную или разветвленную (С 1-С 6)алкильную группу, причем эта группа замещена группой формулы (II) в которой R5 представляет собой группу, где Z представляет собой атом кислорода и R представляет собой атом водорода, линейную или разветвленную (С 1-С 6)алкильную группу либо линейную или разветвленную (С 1-С 6)полигалоалкильную группу иR6 представляет собой -OR, где R имеет такие же значения, как приведенные выше,и подразумевается, что оксим R'-C(=N-OR2)- может находиться в Z или Е конфигурации,арил обозначает фенильную, нафтильную или бифенильную группу, которые необязательно могут быть частично гидрированы,их энантиомеры и диастереоизомеры, а также их фармацевтически приемлемые соли присоединения с кислотой или основанием. 2. Соединения формулы (I) по п.1, в которых группа R1-C(=N-OR2)- находится в b или с положении,их энантиомеры и диастереоизомеры, а также их фармацевтически приемлемые соли присоединения с кислотой или основанием. 3. Соединения формулы (I) по п.1, в которых А представляет собой этиленоксигруппу, их энантиомеры и диастереоизомеры, а также их фармацевтически приемлемые соли присоединения с кислотой или основанием. 4. Соединения формулы (I) по п.1, в которых R2 представляет собой атом водорода, их энантиомеры и диастереоизомеры, а также их фармацевтически приемлемые соли присоединения с кислотой или основанием. 5. Соединения формулы (I) по п.1, в которых R2 представляет собой алкильную группу, их энантиомеры и диастереоизомеры, а также их фармацевтически приемлемые соли присоединения с кислотой или основанием. 6. Соединения формулы (I) по п.1, в которых R1 представляет собой незамещенную фенильную- 16012437 группу, их энантиомеры и диастереоизомеры, а также их фармацевтически приемлемые соли присоединения с кислотой или основанием. 7. Соединения формулы (I) по п.1, в которых В представляет собой алкильную группу, замещенную группой, в которой Rx и Ry, которые могут быть одинаковыми или разными, каждый представляет собой атом водорода или алкильную группу, их энантиомеры и диастереоизомеры, а также их фармацевтически приемлемые соли присоединения с кислотой или основанием. 8. Соединения формулы (I) по п.1, в которых В представляет собой группу, в которойRx и Ry, которые могут быть одинаковыми или разными, каждый представляет собой атом водорода или алкильную группу, их энантиомеры и диастереоизомеры, а также их фармацевтически приемлемые соли присоединения с кислотой или основанием. 9. Соединения формулы (I) по п.1, которые представляют собой этил 2-этокси-3-[4-(2-7-[(метоксиимино)(фенил)метил]-3-оксо-2,3-дигидро-4H-1,4-бензотиазин-4 илэтокси)фенил]пропаноат,этил 3-[4-(2-7-[(метоксиимино)(фенил)метил]-3-оксо-2,3-дигидро-4H-1,4-бензотиазин-4 илэтокси)фенил]-2-(2,2,2-трифторэтокси)пропаноат,этил 2-этокси-3-[4-(2-6-[(метоксиимино)(фенил)метил]-3-оксо-2,3-дигидро-4H-1,4-бензоксазин-4 илэтокси)фенил]пропаноат,этил 2-этокси-3-[4-(2-7-[(гидроксиимино)(фенил)метил]-3-оксо-2,3-дигидро-4H-1,4-бензотиазин-4 илэтокси)фенил]пропаноат,этил 3-[4-(2-7-[(гидроксиимино)(фенил)метил]-3-оксо-2,3-дигидро-4H-1,4-бензотиазин-4 илэтокси)фенил]-2-(2,2,2-трифторэтокси)пропаноат,этил 2-этокси-3-[4-(2-6-[(гидроксиимино)(фенил)метил]-3-оксо-2,3-дигидро-4H-1,4-бензоксазин-4 илэтокси)фенил]пропаноат,2-этокси-3-[4-(2-7-[(гидроксиимино)(фенил)метил]-3-оксо-2,3-дигидро-4H-1,4-бензотиазин-4 илэтокси)фенил]пропионовую кислоту,2-этокси-3-[4-(2-7-[(метоксиимино)(фенил)метил]-3-оксо-2,3-дигидро-4H-1,4-бензотиазин-4 илэтокси)фенил]пропионовую кислоту,3-[4-(2-7-[(гидроксиимино)(фенил)метил]-3-оксо-2,3-дигидро-4H-1,4-бензотиазин-4 илэтокси)фенил]-2-(2,2,2-трифторэтокси)пропионовую кислоту,3-[4-(2-7-[(метоксиимино)(фенил)метил]-3-оксо-2,3-дигидро-4H-1,4-бензотиазин-4 илэтокси)фенил]-2-(2,2,2-трифторэтокси)пропионовую кислоту,2-этокси-3-[4-(2-6-[(гидроксиимино)(фенил)метил]-3-оксо-2,3-дигидро-4H-1,4-бензоксазин-4 илэтокси)фенил]пропионовую кислоту,2-этокси-3-[4-(2-6-[(метоксиимино)(фенил)метил]-3-оксо-2,3-дигидро-4H-1,4-бензоксазин-4 илэтокси)фенил]пропионовую кислоту,их энантиомеры и диастереоизомеры, а также их фармацевтически приемлемые соли присоединения с кислотой или основанием. 10. Способ получения соединений формулы (I) по п.1, который характеризуется тем, что в качестве исходного вещества используют соединение (III) в которой R1 и X имеют значения, указанные для формулы (I), которое конденсируют в щелочной среде с соединением формулы (IV) в которой А, В, R3 и R4 имеют значения, указанные для формулы (I), и Hal представляет собой атом галогена, получая соединение формулы (V) в которой R1, R3, R4, А, В и X имеют значения, указанные для формулы (I), которое подвергают воздействию соединения формулы R2O-NH2, в которой R2 имеет значения, указанные для формулы (I), получая соединение формулы (I) которое может быть очищено в соответствии с обычной методикой разделения, превращено, если это является желательным, в соли присоединения с фармацевтически приемлемой кислотой или основанием, и необязательно разделено на изомеры в соответствии с обычной методикой разделения. 11. Способ получения соединений формулы (I) по п.1, который характеризуется тем, что в качестве исходного вещества используют соединение (III) в которой R1 и X имеют значения, указанные для формулы (I), которое конденсируют с соединением формулы R2O-NH2, в которой R2 имеет значения, указанные для формулы (I), получая соединение формулы (VI) в которой R1, R2 и X имеют значения, указанные для формулы (I), которое конденсируют в щелочной среде с соединением формулы (IV) в которой А, В, R3 и R4 имеют значения, указанные для формулы (I), и Hal представляет собой атом галогена, получая соединение формулы (I) которое может быть очищено в соответствии с обычной методикой разделения, превращено, если это является желательным, в соли присоединения с фармацевтически приемлемой кислотой или основанием, и необязательно разделено на изомеры в соответствии с обычной методикой разделения. 12. Фармацевтическая композиция, содержащая в качестве активного компонента по меньшей мере одно соединение формулы (I) по любому из пп.1-9, или его фармацевтически приемлемую соль присоединения с кислотой или основанием, отдельно или в сочетании с одним или несколькими фармацевтически приемлемыми наполнителями. 13. Применение фармацевтической композиции по п.12 для приготовления лекарственного средства для лечения и/или профилактики гипергликемии, дислипидемии и более предпочтительно для лечения- 18012437 инсулиннезависимого диабета II типа, резистентности к инсулину, непереносимости глюкозы, заболеваний, связанных с сидромом X, заболевания коронарной артерии и других сердечно-сосудистых заболеваний, заболеваний почек, ретинопатии, заболеваний, связанных с активацией клеток эндотелия, псориаза,синдрома поликистоза яичника, слабоумия, остеопороза, воспалительных заболеваниях кишечника, дистрофической миотонии, панкреатита, артериосклерозы, ксантомы, а также для лечения или предотвращения диабета I типа, ожирения, регуляции аппетита, анорексии, булимии, нервно-психической анорексии, а также злокачественных патологий, и, в особенности, гормональнозависимых злокачественных новообразований, таких как рак молочной железы и рак ободочной кишки, и для применения в качестве ингибиторов ангиогенеза. 14. Комбинация, содержащая соединение формулы (I) по любому из пп.1-9 и антиоксидант. 15. Комбинация по п.14, в которой соединение формулы (I) представляет собой 3-4-[2-(6(гидроксииминофенил)метил-3-оксо-2,3-дигидро-4H-бензо[1,4]оксазин-4-ил)этокси]фенил-2 этоксипропионовую кислоту, ее энантиомеры и диастереоизомеры, а также ее фармацевтически приемлемые соли присоединения с кислотой или основанием. 16. Комбинация по п.14 или 15, в которой антиоксидант представляет собой коэнзим Q10. 17. Комбинация по п.14 или 15, в которой антиоксидант представляет собой витамин Е. 18. Комбинация по п.14 или 15, которая представляет собой 3-4-[2-(6-(гидроксииминофенил)метил-3-оксо-2,3-дигидро-4H-бензо[1,4]оксазин-4-ил)этокси]фенил-2-этоксипропионовую кислоту и коэнзим Q10. 19. Применение фармацевтической композиции, содержащей в качестве активного компонента комбинацию по любому из пп.14-18, отдельно или в сочетании с одним или несколькими фармацевтически приемлемыми наполнителями. 20. Применение фармацевтической композиции по п.19 для приготовления лекарственного средства для лечения и/или предотвращения ожирения. 21. Применение фармацевтической композиции по п.19 для приготовления лекарственного средства для лечения и/или предотвращения избыточного веса, характеризующегося индексом массы тела, большим чем 25 и меньшим чем 30. 22. Применение комбинации по любому из пп.14-18 для получения фармацевтических композиций,предназначенных для лечения и/или предотвращения ожирения. 23. Применение комбинации по любому из пп.14-18 для получения фармацевтических композиций,предназначенных для лечения и/или предотвращения ожирения, вызванного терапевтическим лечением. 24. Применение комбинации по любому из пп.14-18 для получения фармацевтических композиций,предназначенных для лечения и/или предотвращения ожирения, вызванного лечением диабета I или II типа. 25. Применение комбинации по любому из пп.14-18 для получения фармацевтических композиций,предназначенных для лечения и/или предотвращения избыточного веса, характеризующегося индексом массы тела, большим чем 25 и меньшим чем 30. 26. Применение комбинации по любому из пп.14-18 для получения фармацевтических композиций,предназначенных для лечения и/или предотвращения избыточного веса, характеризующегося индексом массы тела, большим чем 25 и меньшим чем 30, вызванного терапевтическим лечением. 27. Применение комбинации по любому из пп.14-18 для получения фармацевтических композиций,предназначенных для лечения и/или предотвращения избыточного веса, характеризующегося индексом массы тела, большим чем 25 и меньшим чем 30, вызванного лечением диабета I или II типа.
МПК / Метки
МПК: A61K 31/5415, A61P 3/06, A61K 31/538, C07D 265/36, A61P 3/10, C07D 279/16
Метки: производные, содержащие, бензоконденсированных, фармацевтическая, комбинация, способ, оксимов, композиция, применение, получения, гетероциклических
Код ссылки
<a href="https://eas.patents.su/20-12437-proizvodnye-benzokondensirovannyh-geterociklicheskih-oksimov-sposob-ih-polucheniya-soderzhashhie-ih-farmacevticheskaya-kompoziciya-i-kombinaciya-i-ih-primenenie.html" rel="bookmark" title="База патентов Евразийского Союза">Производные бензоконденсированных гетероциклических оксимов, способ их получения, содержащие их фармацевтическая композиция и комбинация и их применение</a>
Предыдущий патент: Композиции для иммунизации против микобактерий
Следующий патент: Способ и набор для определения тимидинкиназной активности и их применение
Случайный патент: Система и способ для поточной обработки озоном углеводородных жидкостей












