Производные [1,2,3]триазоло[4,5-d]пиримидина в качестве агонистов каннабиноидного рецептора 2
Номер патента: 23581
Опубликовано: 30.06.2016
Авторы: Гретер Уве, Адам Жан-Мишель, Неттекофен Маттиас, Кимбара Ацуси, Роджерс-Эванс Марк, Рёфер Штефан, Биссанц Катерина
Формула / Реферат
1. Соединение формулы (I)
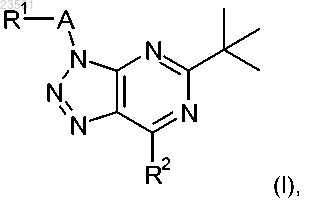
в котором А представляет собой алкил, гидроксиалкил, -СН2С(О)-, -С(О)-, -SO2- или отсутствует;
R1 представляет собой водород, алкил, галогеналкил, гидроксил, алкоксигруппу, галогеналкоксигруппу, фенил, галогенфенил, алкоксифенил, галогеналкилфенил, галогеналкоксифенил, (галоген)(галогеналкил)фенил, цианофенил, гидроксиалкоксифенил, алкилсульфонилфенил, алкилсульфониламинофенил, цианогруппу, циклоалкил, циклоалкилалкоксигруппу, аминогруппу, (алкилсульфонил)(алкил)[1,2,4]триазолил, (галоген)(диалкиламино)пиридинил, (алкил)(окси)пиридинил, нитробензо[1,2,5]оксадиазолиламинопиридинил, гетероциклил, алкилгетероциклил, гидроксигетероциклил, алкилгетероциклил, гетероарил, галогенгетероарил, алкилгетероарил, циклоалкилгетероарил или галогеналкилгетероарил, при этом указанный гетероциклил представляет собой карбоциклическое кольцо, включающее от трех до восьми членов, включая по меньшей мере один атом азота или кислорода, и при этом указанный гетероарил представляет собой пиридинил, пиразолил, оксадиазолил, фуразанил, тетразолил или триазолил;
R2 представляет собой галоген или -NR3R4 или -OR5;
один из R3 и R4 представляет собой водород или алкил, а другой представляет собой алкил или циклоалкил;
или R3 и R4 совместно с атомом азота, к которому они присоединены, образуют гетероциклил или замещенный гетероциклил, при этом указанный гетероциклил представляет собой морфолинил, пиперидинил, пиперазинил, пирролидинил, 2-окса-6-азаспиро[3,3]гептил, азетидинил, тиазолидинил, тиоморфолинил, диоксотиоморфолинил, оксазепанил, 2-окса-6-азаспиро[3,4]октил, 6-окса-1-азаспиро[3,3]гептил, 2-окса-5-азаспиро[3,4]октил, изоксазолидинил, азиридинил, диоксоизотиазолидинил или оксопиролидинил, и при этом указанный замещенный гетероциклил представляет собой гетероциклил, содержащий от одного до четырех заместителей, независимо выбранных из алкила, галогена, гидроксила, алкоксигруппы, гидроксиалкила, карбоксила, алкоксиалкила, цианогруппы, алкиламиногруппы, диалкиламиногруппы, алкилкарбониламиногруппы, алкилкарбонил(алкиламино)группы, фенила, алкоксикарбонила, аминоалкила, алкилпиразолила или алкилизоксазолила;
R5 представляет собой алкил, циклоалкил, циклоалкилалкил, галогеналкил или оксетанил;
или его фармацевтически приемлемая соль;
при условии, что 3-[(2-хлорфенил)метил]-5-(1,1-диметилэтил)-7-(4-морфолинил)-3Н-1,2,3-триазоло[4,5-d]пиримидина и N-циклопропил-5-(1,1-диметилэтил)-3-(фенилметил)-3Н-1,2,3-триазоло[4,5-d]пиримидин-7-амин исключены,
где "алкил", отдельно или в сочетании, обозначает алкильную группу с линейной или разветвленной цепью, включающую от 1 до 8 атомов углерода,
"циклоалкил", отдельно или в сочетании, обозначает циклоалкильное кольцо, включающее от 3 до 8 атомов углерода,
"алкокси", отдельно или в сочетании, обозначает группу формулы алкил-О-.
2. Соединение по п.1, в котором А представляет собой алкил или гидроксиалкил.
3. Соединение по п.1 или 2, в котором А представляет собой -СН2-, -СН2СН2-, -СН(СН3)- или -СН(ОН)СН2-.
4. Соединение по любому из пп.1-3, в котором R1 представляет собой водород, алкил, галогеналкил, гидроксил, алкоксигруппу, фенил, галогенфенил, алкоксифенил, галогеналкилфенил, галогеналкоксифенил, алкилсульфонилфенил, цианофенил, циклоалкил, алкилгетероциклил, гидроксигетероциклил, гетероарил, циклоалкилгетероарил, галогенгетероарил или алкилгетероарил, при этом указанный гетероциклил представляет собой карбоциклическое кольцо, содержащее по меньшей мере один атом азота, и при этом указанный гетероарил представляет собой пиридинил, пиразолил, оксадиазолил, тетразолил или фуразанил.
5. Соединение по любому из пп.1-4, в котором R1 представляет собой галогеналкил, фенил, галогенфенил, галогеналкилфенил, цианофенил, алкилсульфонилфенил, циклоалкил, гетероарил, циклоалкилгетероарил, галогенгетероарил или алкилгетероарил, при этом указанный гетероарил представляет собой пиридинил, пиразолил, оксадиазолил, тетразолил или фуразанил.
6. Соединение по любому из пп.1-5, в котором R1 представляет собой хлорфенил, циклогексил, дихлорфенил, пиридинил, хлорпиридинил, дихлорпиридинил, трифторметил, хлордифторфенил, трифторметилфенил, цианофенил, фенил, метилсульфонилфенил, метилтетразолил, метилфуразанил или циклопропилтетразолил.
7. Соединение по любому из пп.1-6, в котором один из R3 и R4 представляет собой водород или этил, а другой представляет собой этил или циклогексил.
8. Соединение по любому из пп.1-6, в котором R3 и R4 совместно с атомом азота, к которому они присоединены, образуют гетероциклил или замещенный гетероциклил, при этом указанный гетероциклил представляет собой пиперидинил, пирролидинил, азетидинил или 2-окса-6-азаспиро[3,3]гептил, и при этом указанный замещенный гетероциклил представляет собой гетероциклил, содержащий от одного до четырех заместителей, независимо выбранных из алкила, галогена, гидроксила, гидроксиалкила и алкоксиалкила.
9. Соединение по любому из пп.1-6, в котором R3 и R4 совместно с атомом азота, к которому они присоединены, образуют дифторпиперидинил, дифторпирролидинил, дифторазетидинил, (метил)(гидроксил)азетидинил, гидроксипирролидинил, гидроксиметилпирролидинил, тетрафторпирролидинил, метоксиметилпирролидинил, (гидроксил)(гидроксиметил)пирролидинил, (метил)(гидроксил)пирролидинил или 2-окса-6-азаспиро[3,3]гептил.
10. Соединение по любому из пп.1-9, в котором R5 представляет собой метил, этил, изопропил, пентил, циклобутил, циклопентил, циклопропилметил, циклопропилэтил, трифторпропил или оксетанил.
11. Соединение по любому из пп.1-10, выбранное из следующих:
5-трет-бутил-3-(2-хлорбензил)-7-морфолин-4-ил-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-(2-хлорбензил)-7-(пиперидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-(2-хлорбензил)-7-(4,4-дифторпиперидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-(2-хлорбензил)-7-(4-метилпиперазин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-(2-хлорбензил)-7-(пирролидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-(2-хлорбензил)-7-(3,3-дифторпирролидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-(2-хлорбензил)-N-этил-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-амин;
5-трет-бутил-3-(2-хлорбензил)-N-циклогексил-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-амин;
5-трет-бутил-3-(2-хлорбензил)-N,N-диэтил-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-амин;
6-(5-трет-бутил-3-(2-хлорбензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил)-2-окса-6-азаспиро[3,3]гептан;
7-(азетидин-1-ил)-5-трет-бутил-3-(2-хлорбензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-(2-хлорбензил)-7-(3,3-дифторазетидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
1-(5-трет-бутил-3-(2-хлорбензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил)азетидин-3-ол;
1-(5-трет-бутил-3-(2-хлорбензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил)-3-метилазетидин-3-ол;
5-трет-бутил-3-(2-хлорбензил)-7-(3-метоксиазетидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
(2S,6R)-4-(5-трет-бутил-3-(2-хлорбензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил)-2,6-диметилморфолин;
4-(5-трет-бутил-3-(2-хлорбензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил)-3-метилморфолин;
(4-(5-трет-бутил-3-(2-хлорбензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил)морфолин-2-ил)метанол;
3-(5-трет-бутил-3-(2-хлорбензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил)тиазолидин;
4-(5-трет-бутил-3-(2-хлорбензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил)тиоморфолин;
5-трет-бутил-3-(2-хлорбензил)-7-(1,1-диоксо-1l6-тиоморфолин-4-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
4-(5-трет-бутил-3-(2-хлорбензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил)-1,4-оксазепан;
4-(5-трет-бутил-3-(2-хлорбензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил)-2,2-диметилморфолин;
4-(5-трет-бутил-3-(2-хлорбензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил)-3,3-диметилморфолин;
5-трет-бутил-3-(2-хлорбензил)-7-((2R,5R)-2,5-диметилпирролидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
(S)-1-(5-трет-бутил-3-(2-хлорбензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил)пирролидин-3-ол;
(R)-1-(5-трет-бутил-3-(2-хлорбензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил)пирролидин-3-ол;
5-трет-бутил-3-(2-хлорбензил)-7-(3-метоксипирролидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-(2-хлорбензил)-7-(2,2-диметилпирролидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-(2-хлорбензил)-7-(2-метилпирролидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
6-(5-трет-бутил-3-(2-хлорбензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил)-2-окса-6-азаспиро[3,4]октан;
1-(5-трет-бутил-3-(2-хлорбензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил)пиперидин-4-ол;
(S)-1-(5-трет-бутил-3-(2-хлорбензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил)пиперидин-3-ол;
(R)-1-(5-трет-бутил-3-(2-хлорбензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил)пиперидин-3-ол;
1-(5-трет-бутил-3-(2-хлорбензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил)-6-окса-1-азаспиро[3,3]гептан;
(S)-5-трет-бутил-3-(2-хлорбензил)-7-(3-фторпирролидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
(R)-(1-(5-трет-бутил-3-(2-хлорбензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил)пирролидин-2-ил)метанол;
(S)-(1-(5-трет-бутил-3-(2-хлорбензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил)пирролидин-2-ил)метанол;
2-(5-трет-бутил-3-(2-хлорбензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил)морфолин;
2-(5-трет-бутил-3-(2-хлорбензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил)изоксазолидин;
7-(азиридин-1-ил)-5-трет-бутил-3-(2-хлорбензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
(R)-5-трет-бутил-3-(2-хлорбензил)-7-(3-фторпирролидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-(2-хлорбензил)-7-(3,3,4,4-тетрафторпирролидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
(R)-5-трет-бутил-3-(2-хлорбензил)-7-(2-(метоксиметил)пирролидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
(S)-5-трет-бутил-3-(2-хлорбензил)-7-(2-(метоксиметил)пирролидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
(2S,4S)-1-(5-трет-бутил-3-(2-хлорбензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил)-4-фторпирролидин-2-карбонитрил;
5-трет-бутил-3-(2-хлорбензил)-7-(1,1-диоксо-1l6-изотиазолидин-2-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
(4-(5-трет-бутил-3-(2-хлорбензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил)морфолин-3-ил)метанол;
(R)-1-(5-трет-бутил-3-(2-хлорбензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил)пирролидин-2-карбонитрил;
(S)-1-(5-трет-бутил-3-(2-хлорбензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил)пирролидин-2-карбонитрил;
(2S,3S)-1-(5-трет-бутил-3-(2-хлорбензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил)-2-(гидроксиметил)пирролидин-3-ол;
(2S,3R)-1-(5-трет-бутил-3-(2-хлорбензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил)-2-(гидроксиметил)пирролидин-3-ол;
5-трет-бутил-3-(2-хлорбензил)-7-(2-окса-5-азаспиро[3,4]окт-5-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
1-[5-трет-бутил-3-(2-хлорбензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил]-3-метилпирролидин-3-ол;
(3R,4R)-1-[5-трет-бутил-3-(2-хлорбензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил]пирролидин-3,4-диол;
(3S,4R)-1-[5-трет-бутил-3-(2-хлорбензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил]пирролидин-3,4-диол;
4-(5-трет-бутил-3-(4-метоксибензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил)морфолин;
4-(5-трет-бутил-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил)морфолин;
5-трет-бутил-3-(2-хлор-4-фторбензил)-7-морфолин-4-ил-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-7-(3,3-дифторпирролидин-1-ил)-3-(4-метоксибензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-7-(3,3-дифторпирролидин-1-ил)-3-этил-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-7-(3,3-дифторпирролидин-1-ил)-3-(2-метоксиэтил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
2-[5-трет-бутил-7-(3,3-дифторпирролидин-1-ил)-[1,2,3]триазоло[4,5-d]пиримидин-3-ил]этанол;
5-трет-бутил-3-циклогексилметил-7-(3,3-дифторпирролидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-(3-хлорбензил)-7-(3,3-дифторпирролидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-(4-хлорбензил)-7-(3,3-дифторпирролидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-(2,3-дихлорбензил)-7-(3,3-дифторпирролидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-(2,4-дихлорбензил)-7-(3,3-дифторпирролидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-(2,5-дихлорбензил)-7-(3,3-дифторпирролидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-(2,6-дихлорбензил)-7-(3,3-дифторпирролидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-(2-хлор-4-фторбензил)-7-(3,3-дифторпирролидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-(2-хлор-6-фторбензил)-7-(3,3-дифторпирролидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-7-(3,3-дифторпирролидин-1-ил)-3-пиридин-2-илметил-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-7-(3,3-дифторпирролидин-1-ил)-3-пиридин-3-илметил-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-7-(3,3-дифторпирролидин-1-ил)-3-пиридин-4-илметил-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-7-(3,3-дифторпирролидин-1-ил)-3-(2,2,2-трифторэтил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-(2-хлор-4,5-дифторбензил)-7-(3,3-дифторпирролидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-(2-хлор-3,6-дифторбензил)-7-(3,3-дифторпирролидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
3-(2-бромбензил)-5-трет-бутил-7-(3,3-дифторпирролидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-7-(3,3-дифторпирролидин-1-ил)-3-(2-трифторметилбензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-7-(3,3-дифторпирролидин-1-ил)-3-(2-метоксибензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-7-(3,3-дифторпирролидин-1-ил)-3-(2-трифторметоксибензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
2-[5-трет-бутил-7-(3,3-дифторпирролидин-1-ил)-[1,2,3]триазоло[4,5-d]пиримидин-3-илметил]бензонитрил;
5-трет-бутил-7-(3,3-дифторпирролидин-1-ил)-3-фенэтил-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
2-[5-трет-бутил-7-(3,3-дифторпирролидин-1-ил)-[1,2,3]триазоло[4,5-d]пиримидин-3-ил]-1-фенилэтанон;
5-трет-бутил-3-[(R)-1-(2-хлорфенил)этил]-7-(3,3-дифторпирролидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-[(S)-1-(2-хлорфенил)этил]-7-(3,3-дифторпирролидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
2-[5-трет-бутил-7-(3,3-дифторпирролидин-1-ил)-[1,2,3]триазоло[4,5-d]пиримидин-3-ил]-1-фенилэтанол;
5-трет-бутил-3-(2-хлор-3-фторбензил)-7-(3,3-дифторпирролидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-(2-хлор-5-фторбензил)-7-(3,3-дифторпирролидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-7-(3,3-дифторпирролидин-1-ил)-3-оксетан-3-ил-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
[5-трет-бутил-7-(3,3-дифторпирролидин-1-ил)-[1,2,3]триазоло[4,5-d]пиримидин-3-ил]-(2-хлорфенил)метанон;
(3S,5R)-1-[5-трет-бутил-3-(2-хлорбензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил]-5-гидроксиметилпирролидин-3-ол;
{(R)-1-[5-трет-бутил-3-(2-хлорбензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил]-4,4-дифторпирролидин-2-ил}метанол;
(R)-1-[5-трет-бутил-3-(2-хлорбензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил]-4,4-дифторпирролидин-3-ол;
5-трет-бутил-3-(2,6-дихлор-3-фторбензил)-7-(3,3-дифторпирролидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-(2-хлорпиридин-3-илметил)-7-(3,3-дифторпирролидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-(3-хлорпиридин-2-илметил)-7-(3,3-дифторпирролидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-(2,5-дихлорпиридин-3-илметил)-7-(3,3-дифторпирролидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-(3,6-дихлорпиридин-2-илметил)-7-(3,3-дифторпирролидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-7-(3,3-дифторпирролидин-1-ил)-3-(4-метилфуразан-3-илметил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-7-(3,3-дифторпирролидин-1-ил)-3-(3-метил-[1,2,4]оксадиазол-5-илметил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-[2-(2-хлорфенил)этил]-7-(3,3-дифторпирролидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-[2-(3-хлорфенил)этил]-7-(3,3-дифторпирролидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-[2-(4-хлорфенил)этил]-7-(3,3-дифторпирролидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
(S)-1-[5-трет-бутил-3-(4-метоксибензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил]пирролидин-3-ол;
5-трет-бутил-3-(2-хлорбензолсульфонил)-7-(3,3-дифторпирролидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-7-(3,3-дифторпирролидин-1-ил)-3-(R)-тетрагидрофуран-3-ил-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-7-(3,3-дифторпирролидин-1-ил)-3-(S)-тетрагидрофуран-3-ил-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
2-[5-трет-бутил-7-(3,3-дифторпирролидин-1-ил)-[1,2,3]триазоло[4,5-d]пиримидин-3-ил]-1-(2-хлорфенил)этанон;
5-трет-бутил-3-(2,3-дихлор-6-фторбензил)-7-(3,3-дифторпирролидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-7-(3,3-дифторпирролидин-1-ил)-3-(2-метансульфонилбензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-7-(3,3-дифторпирролидин-1-ил)-3-(2-пиридин-2-илэтил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-7-(3,3-дифторпирролидин-1-ил)-3-(3-метилоксетан-3-илметил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
2-[5-трет-бутил-7-(3,3-дифторпирролидин-1-ил)-[1,2,3]триазоло[4,5-d]пиримидин-3-ил]-1-(3-хлорфенил)этанон;
2-[5-трет-бутил-7-(3,3-дифторпирролидин-1-ил)-[1,2,3]триазоло[4,5-d]пиримидин-3-ил]-1-(4-хлорфенил)этанон;
2-[5-трет-бутил-7-(3,3-дифторпирролидин-1-ил)-[1,2,3]триазоло[4,5-d]пиримидин-3-ил]-1-пиридин-3-илэтанон;
2-[5-трет-бутил-7-(3,3-дифторпирролидин-1-ил)-[1,2,3]триазоло[4,5-d]пиримидин-3-ил]-1-пиридин-4-илэтанон;
5-трет-бутил-7-(3,3-дифторпирролидин-1-ил)-3-(2,3,6-трихлорбензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-(2-хлор-3-трифторметилбензил)-7-(3,3-дифторпирролидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-7-(3,3-дифторпирролидин-1-ил)-3-(2-пиридин-3-илэтил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-7-(3,3-дифторпирролидин-1-ил)-3-(2-пиридин-4-илэтил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-(2,3-дихлор-6-трифторметилбензил)-7-(3,3-дифторпирролидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-(3,4-дихлорпиридин-2-илметил)-7-(3,3-дифторпирролидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-7-(3,3-дифторпирролидин-1-ил)-3-(1,1-диоксо-1l6-тиетан-3-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-7-(3,3-дифторпирролидин-1-ил)-3-(1,1-диоксотетрагидро-1l6-тиофен-3-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
2-[5-трет-бутил-7-(3,3-дифторпирролидин-1-ил)-[1,2,3]триазоло[4,5-d]пиримидин-3-ил]-1-пиридин-2-илэтанон;
5-трет-бутил-7-(3,3-дифторпирролидин-1-ил)-3-(5-метил-[1,3,4]оксадиазол-2-илметил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-(3-хлорпиридин-4-илметил)-7-(3,3-дифторпирролидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-7-(3,3-дифторпирролидин-1-ил)-3-(5-метил-[1,2,4]оксадиазол-3-илметил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-7-(3,3-дифторпирролидин-1-ил)-3-(1-метил-1Н-тетразол-5-илметил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-7-(3,3-дифторпирролидин-1-ил)-3-(2-метил-2Н-[1,2,4]триазол-3-илметил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-7-(3,3-дифторпирролидин-1-ил)-3-(5-метансульфонил-4-метил-4Н-[1,2,4]триазол-3-илметил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
{3-[5-трет-бутил-7-(3,3-дифторпирролидин-1-ил)-[1,2,3]триазоло[4,5-d]пиримидин-3-илметил]-5-хлорпиридин-4-ил}диметиламин;
5-трет-бутил-7-(3,3-дифторпирролидин-1-ил)-3-(3-трифторметил-1Н-пиразол-4-илметил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
(S)-1-[5-трет-бутил-3-(4-метилфуразан-3-илметил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил]пирролидин-3-ол;
(S)-1-[5-трет-бутил-3-(3-метил-[1,2,4]оксадиазол-5-илметил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил]-пирролидин-3-ол;
(S)-1-[5-трет-бутил-3-(3-хлорпиридин-2-илметил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил]пирролидин-3-ол;
(S)-1-[5-трет-бутил-3-(3,6-дихлорпиридин-2-илметил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил]пирролидин-3-ол;
(S)-1-[5-трет-бутил-3-(2-хлорпиридин-3-илметил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил]пирролидин-3-ол;
(S)-1-[5-трет-бутил-3-(2,3-дихлорбензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил]пирролидин-3-ол;
(S)-1-[5-трет-бутил-3-(2-трифторметилбензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил]-пирролидин-3-ол;
(S)-1-[5-трет-бутил-3-(2-метансульфонилбензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил]пирролидин-3-ол;
5-трет-бутил-7-(3,3-дифторпирролидин-1-ил)-3-(2,5-диметил-2Н-пиразол-3-илметил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-7-(3,3-дифторпирролидин-1-ил)-3-(3-метил-3Н-[1,2,3]триазол-4-илметил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-7-(3,3-дифторпирролидин-1-ил)-3-(4,5-диметил-4Н-[1,2,4]триазол-3-илметил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-7-(3,3-дифторпирролидин-1-ил)-3-(2-метил-1-оксипиридин-3-илметил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
(S)-1-[5-трет-бутил-3-(3,4-дихлорпиридин-2-илметил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил]пирролидин-3-ол;
(S)-1-[5-трет-бутил-3-(5-метил-[1,2,4]оксадиазол-3-илметил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил]пирролидин-3-ол;
(S)-1-[5-трет-бутил-3-(5-метил-[1,3,4]оксадиазол-2-илметил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил]пирролидин-3-ол;
(S)-1-[5-трет-бутил-3-(1-метил-1Н-тетразол-5-илметил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил]пирролидин-3-ол;
(S)-1-[5-трет-бутил-3-(2-метил-2Н-[1,2,4]триазол-3-илметил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил]пирролидин-3-ол;
(S)-1-[5-трет-бутил-3-(4,5-диметил-4Н-[1,2,4]триазол-3-илметил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил]пирролидин-3-ол;
(S)-1-[5-трет-бутил-3-(3-метил-3Н-[1,2,3]триазол-4-илметил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил]пирролидин-3-ол;
(S)-1-[5-трет-бутил-3-(2,5-диметил-2Н-пиразол-3-илметил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил]пирролидин-3-ол;
5-трет-бутил-7-(3,3-дифторпирролидин-1-ил)-3-(3-трифторметил-[1,2,4]оксадиазол-5-илметил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-(1-циклопропил-1Н-тетразол-5-илметил)-7-(3,3-дифторпирролидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
(S)-1-{5-трет-бутил-3-[2-(7-нитробензо[1,2,5]оксадиазол-4-иламино)пиридин-3-илметил]-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил}пирролидин-3-ол;
(2S,3S)-1-[5-трет-бутил-3-(4-метоксибензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил]-2-гидроксиметилпирролидин-3-ол;
(S)-1-[5-трет-бутил-3-(1-циклопропил-1Н-тетразол-5-илметил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил]пирролидин-3-ол;
(S)-1-[5-трет-бутил-3-(2,5-диметил-2Н-[1,2,4]триазол-3-илметил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил]ирролидин-3-ол;
(S)-1-[5-трет-бутил-3-(2-метил-1-оксипиридин-3-илметил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил]пирролидин-3-ол;
5-трет-бутил-7-(3,3-дифторпирролидин-1-ил)-3-(2,5-диметил-2Н-[1,2,4]триазол-3-илметил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
(2S,3S)-1-[5-трет-бутил-3-(4-метилфуразан-3-илметил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил]-2-гидроксиметилпирролидин-3-ол;
(2S,3S)-1-[5-трет-бутил-3-(1-метил-1Н-тетразол-5-илметил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил]-2-гидроксиметилпирролидин-3-ол;
(2S,3S)-1-[5-трет-бутил-3-(1-циклопропил-1Н-тетразол-5-илметил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил]-2-гидроксиметилпирролидин-3-ол;
(2S,3S)-1-[5-трет-бутил-3-(3-хлорпиридин-2-илметил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил]-2-гидроксиметилпирролидин-3-ол;
(2S,3S)-1-[5-трет-бутил-3-(2-метансульфонилбензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил]-2-гидроксиметилпирролидин-3-ол;
(2S,3S)-1-[5-трет-бутил-3-(2-метил-2Н-[1,2,4]триазол-3-илметил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил]-2-гидроксиметилпирролидин-3-ол;
(2S,3S)-1-[5-трет-бутил-3-(4,5-диметил-4Н-[1,2,4]триазол-3-илметил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил]-2-гидроксиметилпирролидин-3-ол;
(2S,3S)-1-[5-трет-бутил-3-(3-метил-3Н-[1,2,3]триазол-4-илметил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил]-2-гидроксиметилпирролидин-3-ол;
(2S,3S)-1-[5-трет-бутил-3-(2-хлорпиридин-3-илметил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил]-2-гидроксиметилпирролидин-3-ол;
5-трет-бутил-3-(4-метилфуразан-3-илметил)-7-(3,3,4,4-тетрафторпирролидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-(3-метил-[1,2,4]оксадиазол-5-илметил)-7-(3,3,4,4-тетрафторпирролидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-(5-метил-[1,3,4]оксадиазол-2-илметил)-7-(3,3,4,4-тетрафторпирролидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-(1-метил-1Н-тетразол-5-илметил)-7-(3,3,4,4-тетрафторпирролидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-(4,5-диметил-4Н-[1,2,4]триазол-3-илметил)-7-(3,3,4,4-тетрафторпирролидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-(3-метил-3Н-[1,2,3]триазол-4-илметил)-7-(3,3,4,4-тетрафторпирролидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-(4-метилфуразан-3-илметил)-7-(2-окса-6-азаспиро[3,3]гепт-6-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-(3-метил-[1,2,4]оксадиазол-5-илметил)-7-(2-окса-6-азаспиро[3,3]гепт-6-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-(5-метил-[1,3,4]оксадиазол-2-илметил)-7-(2-окса-6-азаспиро[3,3]гепт-6-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-(1-метил-1Н-тетразол-5-илметил)-7-(2-окса-6-азаспиро[3,3]гепт-6-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-(1-циклопропил-1Н-тетразол-5-илметил)-7-(2-окса-6-азаспиро[3,3]гепт-6-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-(4,5-диметил-4Н-[1,2,4]триазол-3-илметил)-7-(2-окса-6-азаспиро[3,3]гепт-6-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-(3-метил-3Н-[1,2,3]триазол-4-илметил)-7-(2-окса-6-азаспиро[3,3]гепт-6-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-(2-метансульфонилбензил)-7-(2-окса-6-азаспиро[3,3]гепт-6-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-(3-хлорпиридин-2-илметил)-7-(2-окса-6-азаспиро[3,3]гепт-6-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
1-[5-трет-бутил-3-(2-хлорбензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил]пирролидин-3-он;
5-трет-бутил-3-(2-хлорбензил)-7-(3,3-диметилпирролидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
{1-[5-трет-бутил-3-(2-хлорбензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил]пирролидин-3-ил}метиламин;
{1-[5-трет-бутил-3-(2-хлорбензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил]пирролидин-3-ил}диметиламин;
N-{(S)-1-[5-трет-бутил-3-(2-хлорбензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил]пирролидин-3-ил}ацетамид;
N-{(R)-1-[5-трет-бутил-3-(2-хлорбензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил]пирролидин-3-ил}ацетамид;
N-{1-[5-трет-бутил-3-(2-хлорбензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил]пирролидин-3-ил}-N-метилацетамид;
5-трет-бутил-3-(2-хлорбензил)-7-(3-фенилпирролидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
N-{1-[5-трет-бутил-3-(2-хлорбензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил]пирролидин-3-ил}-N-этилацетамид;
метиловый эфир 1-[5-трет-бутил-3-(2-хлорбензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил]азетидин-3-карбоновой кислоты;
5-трет-бутил-3-(2-хлорбензил)-7-(3-метилпирролидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
С-{(S)-1-[5-трет-бутил-3-(2-хлорбензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил]пирролидин-2-ил}метиламин;
5-трет-бутил-3-(2-хлорбензил)-7-[2-(1-метил-1Н-пиразол-3-ил)пирролидин-1-ил]-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-(2-хлорбензил)-7-[2-(2-метил-2Н-пиразол-3-ил)пирролидин-1-ил]-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-(2-хлорбензил)-7-[2-(3-метилизоксазол-5-ил)пирролидин-1-ил]-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-(2-хлорбензил)-7-[2-(3-метил-[1,2,4]оксадиазол-5-ил)пирролидин-1-ил]-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
1-[5-трет-бутил-3-(2-хлорбензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил]пирролидин-3-ол;
5-трет-бутил-3-(2-хлорбензил)-7-циклобутокси-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-(2-хлорбензил)-7-(оксетан-3-илокси)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-(2-хлорбензил)-7-метокси-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-(2-хлорбензил)-7-этокси-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-(2-хлорбензил)-7-изопропокси-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-(2-хлорбензил)-7-циклопропилметокси-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-(2-хлорбензил)-7-(1-циклопропилэтокси)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-(2-хлорбензил)-7-циклопентилокси-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-(2-хлорбензил)-7-(2,2-диметилпропокси)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-(2-хлорбензил)-7-(2,2,2-трифтор-1-метилэтокси)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-(2-хлорбензил)-7-((S)-2,2,2-трифтор-1-метилэтокси)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-(2-хлорбензил)-7-((R)-2,2,2-трифтор-1-метилэтокси)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
(3S)-1-(3-бензил-5-трет-бутилтриазоло[4,5-d]пиримидин-7-ил)пирролидин-3-ол;
1-(5-трет-бутил-3-(2-хлорбензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил)пирролидин-3-ол;
(R)-1-(5-трет-бутил-3-((1-метил-1Н-тетразол-5-ил)метил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил)пирролидин-3-ол;
1-(5-трет-бутил-3-((1-метил-1Н-тетразол-5-ил)метил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил)пирролидин-3-ол;
(S)-1-(5-трет-бутил-3-(2-хлорбензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил)-3-метилпирролидин-3-ол;
(R)-1-(5-трет-бутил-3-(2-хлорбензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил)-3-метилпирролидин-3-ол;
(S)-1-(5-трет-бутил-3-(2-(трифторметил)бензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил)-3-метилпирролидин-3-ол;
(R)-1-(5-трет-бутил-3-(2-(трифторметил)бензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил)-3-метилпирролидин-3-ол;
(S)-1-(5-трет-бутил-3-(2-(метилсульфонил)бензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил)-3-метилпирролидин-3-ол;
(R)-1-(5-трет-бутил-3-(2-(метилсульфонил)бензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил)-3-метилпирролидин-3-ол;
(S)-1-(5-трет-бутил-3-((3-хлорпиридин-2-ил)метил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил)-3-метилпирролидин-3-ол;
(R)-1-(5-трет-бутил-3-((3-хлорпиридин-2-ил)метил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил)-3-метилпирролидин-3-ол;
(S)-1-(5-трет-бутил-3-((5-метил-1,3,4-оксадиазол-2-ил)метил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил)-3-метилпирролидин-3-ол;
(R)-1-(5-трет-бутил-3-((5-метил-1,3,4-оксадиазол-2-ил)метил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил)-3-метилпирролидин-3-ол;
(S)-1-(5-трет-бутил-3-((3-метил-1,2,4-оксадиазол-5-ил)метил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил)-3-метилпирролидин-3-ол;
(R)-1-(5-трет-бутил-3-((3-метил-1,2,4-оксадиазол-5-ил)метил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил)-3-метилпирролидин-3-ол;
(S)-1-(5-трет-бутил-3-((1-метил-1Н-тетразол-5-ил)метил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил)-3-метилпирролидин-3-ол;
(R)-1-(5-трет-бутил-3-((1-метил-1Н-тетразол-5-ил)метил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил)-3-метилпирролидин-3-ол;
(S)-1-(5-трет-бутил-3-((4-метил-1,2,5-оксадиазол-3-ил)метил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил)-3-метилпирролидин-3-ол;
(R)-1-(5-трет-бутил-3-((4-метил-1,2,5-оксадиазол-3-ил)метил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил)-3-метилпирролидин-3-ол;
(S)-1-(5-трет-бутил-3-(3,3,3-трифторпропил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил)-3-метилпирролидин-3-ол;
(R)-1-(5-трет-бутил-3-(3,3,3-трифторпропил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил)-3-метилпирролидин-3-ол;
(S)-1-(5-трет-бутил-3-((1-циклопропил-1Н-тетразол-5-ил)метил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил)-3-метилпирролидин-3-ол и
(R)-1-(5-трет-бутил-3-((1-циклопропил-1Н-тетразол-5-ил)метил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил)-3-метилпирролидин-3-ол.
12. Соединение по любому из пп.1-11, выбранное из следующих:
5-трет-бутил-3-(2-хлорбензил)-7-(4,4-дифторпиперидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-(2-хлорбензил)-7-(3,3-дифторпирролидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-(2-хлорбензил)-7-(3,3-дифторазетидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
1-(5-трет-бутил-3-(2-хлорбензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил)-3-метилазетидин-3-ол;
(S)-1-(5-трет-бутил-3-(2-хлорбензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил)пирролидин-3-ол;
(R)-(1-(5-трет-бутил-3-(2-хлорбензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил)пирролидин-2-ил)метанол;
5-трет-бутил-3-(2-хлорбензил)-7-(3,3,4,4-тетрафторпирролидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
(R)-5-трет-бутил-3-(2-хлорбензил)-7-(2-(метоксиметил)пирролидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
(2S,3S)-1-(5-трет-бутил-3-(2-хлорбензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил)-2-(гидроксиметил)пирролидин-3-ол;
1-[5-трет-бутил-3-(2-хлорбензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил]-3-метилпирролидин-3-ол;
5-трет-бутил-3-циклогексилметил-7-(3,3-дифторпирролидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-(2,6-дихлорбензил)-7-(3,3-дифторпирролидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-7-(3,3-дифторпирролидин-1-ил)-3-пиридин-2-илметил-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-7-(3,3-дифторпирролидин-1-ил)-3-пиридин-3-илметил-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-7-(3,3-дифторпирролидин-1-ил)-3-(2,2,2-трифторэтил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-(2-хлор-3,6-дифторбензил)-7-(3,3-дифторпирролидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-7-(3,3-дифторпирролидин-1-ил)-3-(2-трифторметилбензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
2-[5-трет-бутил-7-(3,3-дифторпирролидин-1-ил)-[1,2,3]триазоло[4,5-d]пиримидин-3-илметил]бензонитрил;
5-трет-бутил-7-(3,3-дифторпирролидин-1-ил)-3-фенэтил-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-[(R)-1-(2-хлорфенил)-этил]-7-(3,3-дифторпирролидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
2-[5-трет-бутил-7-(3,3-дифторпирролидин-1-ил)-[1,2,3]триазоло[4,5-d]пиримидин-3-ил]-1-фенилэтанол;
5-трет-бутил-3-(3-хлорпиридин-2-илметил)-7-(3,3-дифторпирролидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-(3,6-дихлорпиридин-2-илметил)-7-(3,3-дифторпирролидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-7-(3,3-дифторпирролидин-1-ил)-3-(1-метил-1Н-тетразол-5-илметил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-7-(3,3-дифторпирролидин-1-ил)-3-(2-метил-2Н-[1,2,4]триазол-3-илметил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
(S)-1-[5-трет-бутил-3-(4-метилфуразан-3-илметил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил]пирролидин-3-ол;
(S)-1-[5-трет-бутил-3-(3-хлорпиридин-2-илметил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил]пирролидин-3-ол;
(S)-1-[5-трет-бутил-3-(2-хлорпиридин-3-илметил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил]пирролидин-3-ол;
(S)-1-[5-трет-бутил-3-(2-метансульфонилбензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил]пирролидин-3-ол;
(S)-1-[5-трет-бутил-3-(1-метил-1Н-тетразол-5-илметил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил]пирролидин-3-ол;
(S)-1-[5-трет-бутил-3-(1-циклопропил-1Н-тетразол-5-илметил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил]пирролидин-3-ол;
5-трет-бутил-3-(4-метил-фуразан-3-илметил)-7-(3,3,4,4-тетрафторпирролидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-(3-хлорпиридин-2-илметил)-7-(2-окса-6-азаспиро[3,3]гепт-6-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
5-трет-бутил-3-(2-хлорбензил)-7-((R)-2,2,2-трифтор-1-метилэтокси)-3Н-[1,2,3]триазоло[4,5-d]пиримидин;
(S)-1-(5-трет-бутил-3-(2-хлорбензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил)-3-метилпирролидин-3-ол;
(R)-1-(5-трет-бутил-3-(2-хлорбензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил)-3-метилпирролидин-3-ол;
(S)-1-(5-трет-бутил-3-(2-(трифторметил)бензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил)-3-метилпирролидин-3-ол;
(R)-1-(5-трет-бутил-3-(2-(трифторметил)бензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил)-3-метилпирролидин-3-ол;
(S)-1-(5-трет-бутил-3-(2-(метилсульфонил)бензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил)-3-метилпирролидин-3-ол и
(R)-1-(5-трет-бутил-3-(2-(метилсульфонил)бензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил)-3-метилпирролидин-3-ол.
13. Соединение по п.1, представляющее собой (S)-1-[5-трет-бутил-3-(2-хлорбензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил]пирролидин-3-ол и имеющее формулу
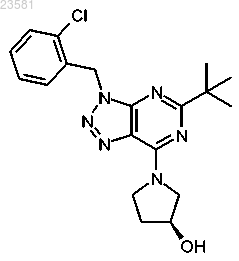
14. Соединение по п.1, представляющее собой 5-трет-бутил-3-(2-хлорбензил)-7-(3,3,4,4-тетрафторпирролидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин и имеющее формулу:
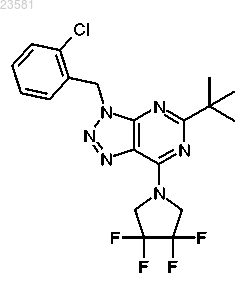
15. Соединение по п.1, представляющее собой 5-трет-бутил-3-(2-хлор-3,6-дифторбензил)-7-(3,3-дифторпирролидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин и имеющее формулу
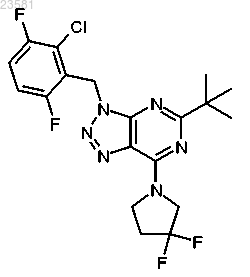
16. Соединение по п.1, представляющее собой 5-трет-бутил-3-(3-хлорпиридин-2-илметил)-7-(3,3-дифторпирролидин-1-ил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин и имеющее формулу
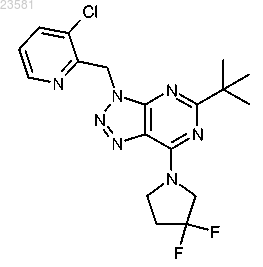
17. Соединение по п.1, представляющее собой (S)-1-[5-трет-бутил-3-(4-метилфуразан-3-илметил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил]пирролидин-3-ол и имеющее формулу
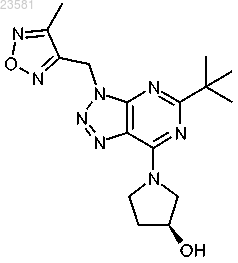
18. Соединение по п.1, представляющее собой (S)-1-[5-трет-бутил-3-(3-хлорпиридин-2-илметил)3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил]пирролидин-3-ол и имеющее формулу
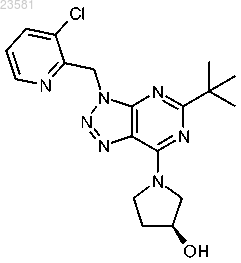
19. Соединение по п.1, представляющее собой (S)-1-[5-трет-бутил-3-(2-хлорпиридин-3-илметил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил]пирролидин-3-ол и имеющее формулу
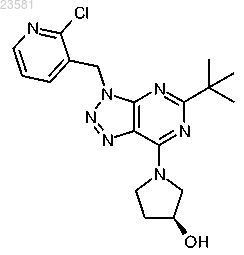
20. Соединение по п.1, представляющее собой (S)-1-[5-трет-бутил-3-(1-метил-1Н-тетразол-5-илметил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил]пирролидин-3-ол и имеющее формулу
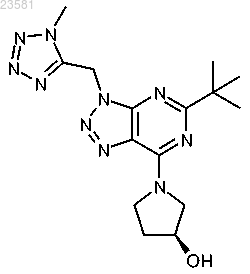
21. Соединение по п.1, представляющее собой (R)-1-(5-трет-бутил-3-((1-метил-1Н-тетразол-5-ил)метил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил)пирролидин-3-ол и имеющее формулу
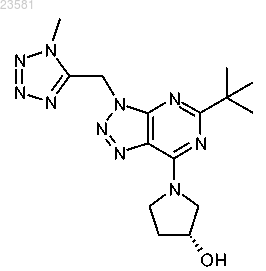
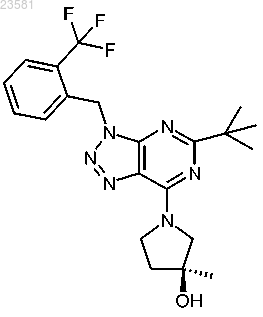
22. Соединение по п.1, представляющее собой (S)-1-(5-трет-бутил-3-(2-(трифторметил)бензил)-3Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил)-3-метилпирролидин-3-ол и имеющее формулу
23. Применение соединения по любому из пп.1-22 в качестве терапевтически активного вещества.
24. Фармацевтическая композиция, включающая соединение по любому из пп.1-12 и терапевтически инертный носитель.
25. Применение соединения по любому из пп.1-22 для лечения или профилактики боли, атеросклероза, возрастной макулярной дистрофии, диабетической ретинопатии, глаукомы, сахарного диабета, воспаления, воспалительного заболевания кишечника, ишемически-реперфузионного повреждения, острой печеночной недостаточности, фиброза печени, фиброза легких, фиброза почек, системного фиброза, острого отторжения аллотрансплантанта, хронической нефропатии аллотрансплантанта, диабетической нефропатии, гломерулонефропатии, кардиомиопатии, сердечной недостаточности, ишемии миокарда, инфаркта миокарда, системного склероза, термического повреждения, ожога, гипертрофических рубцов, келоидов, лихорадки при гингивите, цирроза печени или опухолей, регуляции костной массы, нейродегенерации, инсульта, преходящего нарушения мозгового кровообращения или увеита.
26. Применение соединения по любому из пп.1-22 для изготовления лекарственного средства для лечения или профилактики боли, атеросклероза, возрастной макулярной дистрофии, диабетической ретинопатии, глаукомы, сахарного диабета, воспаления, воспалительного заболевания кишечника, ишемически-реперфузионного повреждения, острой печеночной недостаточности, фиброза печени, фиброза легких, фиброза почек, системного фиброза, острого отторжения аллотрансплантанта, хронической нефропатии аллотрансплантанта, диабетической нефропатии, гломерулонефропатии, кардиомиопатии, сердечной недостаточности, ишемии миокарда, инфаркта миокарда, системного склероза, термического повреждения, ожога, гипертрофических рубцов, келоидов, лихорадки при гингивите, цирроза печени или опухолей, регуляции костной массы, нейродегенерации, инсульта, преходящего нарушения мозгового кровообращения или увеита.
27. Способ лечения или профилактики боли, атеросклероза, возрастной макулярной дистрофии, диабетической ретинопатии, глаукомы, сахарного диабета, воспаления, воспалительного заболевания кишечника, ишемически-реперфузионного повреждения, острой печеночной недостаточности, фиброза печени, фиброза легких, фиброза почек, системного фиброза, острого отторжения аллотрансплантанта, хронической нефропатии аллотрансплантанта, диабетической нефропатии, гломерулонефропатии, кардиомиопатии, сердечной недостаточности, ишемии миокарда, инфаркта миокарда, системного склероза, термического повреждения, ожога, гипертрофических рубцов, келоидов, лихорадки при гингивите, цирроза печени или опухолей, регуляции костной массы, нейродегенерации, инсульта, преходящего нарушения мозгового кровообращения или увеита, включающий введение эффективного количества соединения, раскрытого в любом из пп.1-22, пациенту, который в этом нуждается.
Текст
ПРОИЗВОДНЫЕ [1,2,3]ТРИАЗОЛО[4,5-d]ПИРИМИДИНА В КАЧЕСТВЕ АГОНИСТОВ КАННАБИНОИДНОГО РЕЦЕПТОРА 2 Настоящее изобретение относится к соединению формулы (I) в котором A, R1 и R2 раскрыты в описании и формуле изобретения. Соединение формулы (I) можно применять как лекарственное средство в качестве антагониста каннабиноидного рецептора 2. Настоящее изобретение касается органических соединений, полезных для лечения и/или профилактики у млекопитающих, и, в частности, к соединениям, которые представляют собой селективные агонисты каннабиноидного рецептора 2. Соединение формулы (I), в частности, полезно в лечении или профилактики, например, боли, атеросклероза, возрастной макулярной дистрофии, диабетической ретинопатии, глаукомы, сахарного диабета, воспаления, воспалительного заболевания кишечника, ишемическиреперфузионного повреждения, острой печеночной недостаточности, фиброза печени, фиброза легких,фиброза почек, системного фиброза, острого отторжения аллотрансплантанта, хронической нефропатии аллотрансплантанта, диабетической нефропатии, гломерулонефропатии, кардиомиопатии, сердечной недостаточности, ишемии миокарда, инфаркта миокарда, системного склероза, термического повреждения, ожога, гипертрофических рубцов, келоидов, лихорадки при гингивите, опухолей или цирроза печени, регуляции костной массы, нейродегенерации, инсульта, преходящего нарушения мозгового кровообращения или увеита. Настоящее изобретение относится, в частности, к соединению формулы (I)R1 представляет собой водород, алкил, галогеналкил, гидроксил, алкоксигруппу, галогеналкоксигруппу, фенил, галогенфенил, алкоксифенил, галогеналкилфенил, галогеналкоксифенил, (галоген)(галогеналкил)фенил, цианофенил, гидроксиалкоксифенил, алкилсульфонилфенил, алкилсульфониламинофенил, цианогруппу, циклоалкил, циклоалкилалкоксигруппу, аминогруппу, (алкилсульфонил)(алкил)[1,2,4]триазолил, (галоген)(диалкиламино)пиридинил, (алкил)(окси)пиридинил, нитробензо[1,2,5]оксадиазолиламинопиридинил, гетероциклил, алкилгетероциклил, гидроксигетероциклил, алкилгетероциклил, гетероарил, галогенгетероарил, алкилгетероарил, циклоалкилгетероарил или галогеналкилгетероарил, при этом указанный гетероциклил представляет собой карбоциклическое кольцо,включающее от трех- до восьми членов, включая по меньшей мере один атом азота или кислорода, и при этом гетероарил представляет собой пиридинил, пиразолил, оксадиазолил, фуразанил, тетразолил или триазолил;R2 представляет собой галоген или -NR3R4 или -OR5; один из R3 и R4 представляет собой водород или алкил, а другой представляет собой алкил или циклоалкил; или R3 и R4 совместно с атомом азота, к которому они присоединены, образуют гетероциклил или замещенный гетероциклил, при этом указанный гетероциклил представляет собой морфолинил, пиперидинил, пиперазинил, пирролидинил, 2-окса-6-азаспиро[3,3]гептил, азетидинил, тиазолидинил, тиоморфолинил, диоксотиоморфолинил, оксазепанил, 2-окса-6-азаспиро[3.4]октил, 6-окса-1-азаспиро[3,3]гептил,2-окса-5-азаспиро[3.4]октил, изоксазолидинил, азиридинил, диоксоизотиазолидинил или оксопиролидинил, и при этом замещенный гетероциклил представляет собой гетероциклил, содержащий от одного до четырех заместителей, независимо выбранных из алкила, галогена, гидроксила, алкоксигруппы, гидроксиалкила, карбоксила, алкоксиалкила, цианогруппы, алкиламиногруппы, диалкиламиногруппы, алкилкарбониламиногруппы, алкилкарбонил(алкиламино)группы, фенила, алкоксикарбонила, аминоалкила,алкилпиразолила или алкилизоксазолила;R5 представляет собой алкил, циклоалкил, циклоалкилалкил, галогеналкил или оксетанил; или к его фармацевтически приемлемой соли или эфиру; при условии,что 3-[(2-хлорфенил)метил]-5-(1,1-диметилэтил)-7-(4-морфолинил)-3 Н-1,2,3 триазоло[4,5-d]пиримидин и N-циклопропил-5-(1,1-диметилэтил)-3-(фенилметил)-3 Н-1,2,3-триазоло[4,5d]пиримидин-7-амин исключены. Каннабиноидные рецепторы представляют собой класс рецепторов клеточной мембраны, принадлежащих к суперсемейству рецепторов, сопряженных с G-белком. В настоящее время известны два подтипа, обозначаемые как каннабиноидный рецептор 1 (СВ 1) и каннабиноидный рецептор 2 (СВ 2). Рецептор СВ 1 в основном экспрессируется в центральной нервной системе (например, в мозжечковой миндалине, гиппокампе) и, в меньшей степени, на периферии. Рецептор СВ 2, кодируемый геном CNR2, главным образом экспрессируется на периферии, на клетках иммунной системы, таких как макрофаги и Тклетки (Ashton J. С. et al. Curr Neuropharmacol 2007, 5(2), 73-80; Miller A. M. et al. Br J Pharmacol 2008,153(2), 299-308; Centonze, D., et al. Curr Pharm Des 2008, 14(23), 2370-42), и в желудочно-кишечном тракте (Wright K. L. et al. Br J Pharmacol 2008, 153(2), 263-70). Рецептор СВ 2 также широко распространен в головном мозге, где он обнаруживается преимущественно на микроглии, а не на нейронах (Cabral G. A.et al. Br J Pharmacol 2008, 153(2): 240-51). Интерес к агонистам рецептора СВ 2 непрерывно возрастал в последние десять лет (на текущий мо-1 023581 мент поступает 30-40 патентных заявок в год), поскольку было показано, что несколько ранее открытых соединений оказывают положительные эффекты в преклинических моделях некоторых заболеваний человека, включая хронические боли (Beltramo, M. Mini Rev Med Chem 2009, 9(1), 11-25), атеросклероз(Mach, F. et al. J Neuroendocrinol 2008, 20 Suppl 1, 53-7), регуляцию костной массы (Bab, I. et al. Br JMunoz-Luque, J. et al. J Pharmacol Exp Ther2008, 324(2), 475-83). Ишемически-реперфузионное (I/R) повреждение является основной причиной повреждения ткани,которое происходит при таких состояниях, как инсульт, инфаркт миокарда, сердечно-легочное шунтирование и другие операции на сосудах, и пересадка органов, а также представляет собой основной механизм повреждений концевых органов, осложняющих течение циркуляторного шока различной этиологии. Все эти состояния характеризуются нарушением нормального кровоснабжения, что приводит к недостаточной оксигенации тканей. Повторная оксигенация, например реперфузия, является окончательной мерой для восстановления нормальной тканевой оксигенации. Однако отсутствие кислорода и питательных веществ из кровотока вызывает состояние, при котором восстановление кровотока приводит к дальнейшему повреждению ткани. Поражение, вызываемое реперфузионным повреждением, частично обусловлено воспалительным ответом поврежденных тканей. Белые кровяные клетки, доставленные вновь возвращающейся кровью,выделяют в ответ на повреждение ткани большое количество факторов воспаления, таких как интерлейкины, а также свободные радикалы. Восстановленный кровоток снова вызывает поступление кислорода внутрь клеток, что повреждает клеточные белки, ДНК и цитоплазматическую оболочку. Дистанционное ишемическое прекондиционирование (RIPC) представляет собой стратегию использования внутренних защитных способностей организма против повреждения, вызванного ишемией и реперфузией. Эта стратегия затрагивает необычное явление, при котором преходящая нелетальная ишемия и реперфузия одного органа или ткани придает устойчивость для последующего случая "летального" ишемически-реперфукзионного повреждения в отдаленном органе или ткани. Действующий механизм,по которому преходящая ишемия и реперфузия органа или ткани обеспечивает защиту, в настоящее время неизвестен, хотя было выдвинуто несколько гипотез. В соответствии с гуморальной гипотезой полагают, что некое эндогенное вещество (например аденозин, брадикинин, опиоиды, CGRP (кальцитонин-ген-связанный пептид), эндоканнабиноиды, Ангиотензин I или некоторые другие еще не известные гуморальные факторы), генерируемое в отдаленном органе или ткани, поступает в кровоток и активирует его соответствующий рецептор в ткани-мишени, и таким образом запускает различные внутриклеточные пути кардиопротекции, вовлеченные в ишемическое прекондиционирование. Недавно полученные данные указывают на то, что эндоканнабинноиды и их рецепторы, в частности, СВ 2, могут быть вовлечены в пре-кондиционирование и вносят свой вклад в предотвращение реперфузионного повреждения за счет понижающей регуляции воспалительного ответа (Pacher, P. et al. BrJ Pharmacol 2008, 153(2), 252-62). В частности, недавние исследования с применением в качестве инструмента агонистов СВ 2, продемонстрировали эффективность этой концепции для снижения ишемически-реперфузионного повреждения в сердце (Defer, N. et al. Faseb J 2009, 23(7), 2120-30), головном мозге(Zhang, M. et al. J Cereb Blood Flow Metab 2007, 27(7), 1387-96), печени (Batkai, S. et al. Faseb J 2007,21(8), 1788-800) и почках (Feizi, A. et al. Exp Toxicol Pathol 2008, 60(4-5), 405-10). Более того, за последние несколько лет возрастающий объем литературы свидетельствует о том,что СВ 2 может также представлять интерес в субхронической и хронической ситуации. Было показано,что специфическая активация СВ 1 и СВ 2 в животных моделях хронических заболеваний, обусловленных фиброзом (Garcia-Gonzalez, E. et al. Rheumatology (Oxford) 2009, 48(9), 1050-6; Yang, Y. Y. et al. Liver Int 2009, 29(5), 678-85) связана с соответствующей экспрессией СВ 2 в миофибробластах - клетках, ответственных за прогрессирование фиброза. Фактически было показано, что активация рецептора СВ 2 селективным агонистом СВ 2 оказывает антифибротический эффект в диффузном системном склерозе (Garcia-Gonzalez, E. et al. Rheumatology(Oxford) 2009, 48(9), 1050-6), и оказалось, что рецептор СВ 2 является ключевой мишенью в экспериментальном дермальном фиброзе (Akhmetshina, A. et al. Arthritis Rheum 2009, 60(4), 1129-36), а также в патофизологии печени, включая фиброгенез, связанный с хроническими заболеваниями печени (Lotersztajn,S. et al. Gastroenterol Clin Biol 2007, 31(3), 255-8; Mallat, A. et al. Expert Opin Ther Targets 2007, 11(3), 4039; Lotersztajn, S. etal. Br J Pharmacol 2008, 153(2), 286-9). Соединения по настоящему изобретению связываются с рецептором СВ 2 и модулируют его активность, и обладают более низкой активностью в отношении рецептора СВ 1. В настоящем описании термин "алкил", отдельно или в сочетании, обозначает алкильную группу с линейной или разветвленной цепью, включающую от 1 до 8 атомов углерода, в частности алкильную группу с линейной или разветвленной цепью, включающую от 1 до 6 атомов углерода, и в частном слу-2 023581 чае алкильную группу с линейной или разветвленной цепью, включающую от 1 до 4 атомов углерода. Примерами С 1-С 8 алкильных групп с линейной или разветвленной цепью являются метил, этил, пропил,изопропил, бутил, изобутил, трет-бутил, изомерные пентилы, изомерные гексилы, изомерные гептилы и изомерные октилы, в частности метил, этил, пропил, бутил и пентил, в частном случае метил, этил, пропил, изопропил, изобутил, трет-бутил и изопентил. Частными примерами алкила являются метил, этил и пентил, в частности, метил и этил. Термин "циклоалкил", отдельно или в сочетании, обозначает циклоалкильное кольцо, включающее от 3 до 8 атомов углерода, и в частности циклоалкильное кольцо, включающее от 3 до 6 атомов углерода. Примерами циклоалкила являются циклопропил, циклобутил, циклопентил и циклогексил, циклогептил и циклооктил. Частным случаем "циклоалкила" являются циклопропил, циклобутил, циклопентил и циклогексил. Частным примером циклоалкила является циклогексил. Термин "алкокси", отдельно или в сочетании, обозначает группу формулы алкил-О-, в которой термин "алкил" имеет указанное ранее значение, такую как метокси-, этокси-, н-пропокси-, изопропокси-, нбутокси-, изобутокси-, втор-бутокси- и трет-бутоксигруппу, в частности метоксигруппу. Термин "окси", отдельно или в сочетании, обозначает группу -О-. Термин "галоген", отдельно или в сочетании, обозначает фтор, хлор, бром или иод, в частности,фтор, хлор или бром, в частном случае фтор и хлор. Термин "галоген" в сочетании с другой группой обозначает замещение указанной группы по меньшей мере одним атомом галогена, в частности присутствие в качестве заместителей от одного до пяти атомов галогена, в частности от одного до четырех атомов галогена, т.е. одного, двух, трех или четырех атомов галогена. Галогены в частности представляют собой фтор, бром и хлор, в частном случае фтор и хлор. Термин "галогеналкил", отдельно или в сочетании, обозначает алкильную группу, содержащую в качестве заместителей по меньшей мере один атом галогена, в частности от одного до пяти атомов галогена, в частности от одного до трех атомов галогена. В частности "галогеналкил" представляет собой трифторметил и трифторпропил. В частности, "галогеналкил" представляет собой трифторметил. Термин "галогеналкокси", отдельно или в сочетании, обозначает алкоксигруппу, содержащую в качестве заместителей по меньшей мере один атом галогена, в частности от одного до пяти атомов галогена, в частности от одного до трех атомов галогена. В частности, "галогеналкокси"-группа представляет собой трифторметоксигруппу. Термин "галогенфенил", отдельно или в сочетании, обозначает фенильную группу, содержащую в качестве заместителей по меньшей мере один атом галогена, в частности от одного до трех атомов галогена. В частности, "галогенфенил" представляет собой хлорфенил, хлорфторфенил, дихлорфенил, бромфенил и хлордифторфенил. Термины "гидроксил" и "гидрокси", отдельно или в сочетании, обозначают группу -ОН. Термин "карбонил", отдельно или в сочетании, обозначает группу -С(О)-. Термин "амино", отдельно или в сочетании, обозначает первичную аминогруппу (-NH2), вторичную аминогруппу (-NH-), или третичную аминогруппу (-N-). Термин "сульфонил", отдельно или в сочетании, обозначает группу -SO2-. Термин "фармацевтически приемлемые соли" относится к таким солям, которые сохраняют биологическую эффективность и свойства свободных оснований или свободных кислот, которые не являются нежелательными с биологической или иной точки зрения. Такие соли образуются при участии неорганических кислот, таких как хлороводородная кислота, бромоводородная кислота, серная кислота, азотная кислота, фосфорная кислота, в частности хлороводородная кислота, и органических кислот, таких как уксусная кислота, пропионовая кислота, гликолевая кислота, пировиноградная кислота, щавелевая кислота, малеиновая кислота, малоновая кислота, янтарная кислота, фумаровая кислота, винная кислота,лимонная кислота, бензойная кислота, коричная кислота, миндальная кислота, метансульфоновая кислота, этансульфоновая кислота, п-толуолсульфоновая кислота, салициловая кислота, N-ацетилцистеин. Кроме того, такие соли можно получить путем добавления неорганического основания или органического основания к свободной кислоте. Соли, полученные из неорганического основания, включают, без ограничения, соли натрия, калия, лития, аммония, кальция, магния. Соли, полученные из органических оснований, включают, без ограничения, соли первичных, вторичных и третичных аминов, замещенных аминов, включая природные замещенные амины, циклические амины и основные ионообменные смолы,например изопропиламин, триметиламин, диэтиламин, триэтиламин, трипропиламин, этаноламин, лизин,аргинин, N-этилпиперидин, пиперидин, полиаминовые смолы. Соединение формулы (I) может быть также представлено в форме цвиттер-ионов. Особо предпочтительными фармацевтически приемлемыми солями соединений формулы (I) являются соли хлороводородной кислоты, бромоводородной кислоты,серной кислоты, фосфорной кислоты и метансульфоновой кислоты. Термин "фармацевтически приемлемые эфиры" означает, что соединения общей формулы (I) можно дериватизировать по функциональным группам с получением производных, которые способны превращаться обратно в исходные соединения in vivo. Примеры таких соединений включают физиологически приемлемые и метаболически лабильные эфирные производные, такие как метоксиметиловые эфиры, метилтиометиловые эфиры и пивалоилоксиметиловые эфиры. Кроме того, любые физиологически приемлемые эквиваленты соединений общей формулы (I), аналогичные метаболически лабильным эфирам, которые способны давать исходные соединения общей формулы (I) in vivo, включены в объем настоящего изобретения. Если одно из исходных веществ или соединений формулы (I) содержат одну или более функциональных групп, которые нестабильны или реакционноспособны в условиях реакций на одной или более стадий синтеза, можно вводить подходящие защитные группы (например, описанные в следующем источнике: "Protective Groups in Organic Chemistry", Т. W. Greene и Р. G. M. Wuts, 3rd Ed., 1999, Wiley, NewYork) до проведения рискованной стадии способами, хорошо известными в данной области техники. Такие защитные группы можно удалять на более поздних стадиях синтеза стандартными способами, описанными в литературе. Примерами защитных групп являются трет-бутоксикарбонил (Boc), 9 флюоренилметил карбамат (Fmoc), 2-триметилсилилэтил карбамат (Теос), карбобензилокси (Cbz) и пметоксибензилоксикарбонил (Moz). Соединение формулы (I) может содержать несколько асимметрических центров и может существовать в форме оптически чистых энантиомеров, смесей энантиомеров таких как, пример, рацематы, смеси диастереомеров, диастереомерные рацематы или смеси диастереомерных рацематов. Термин "асимметрический атом углерода" обозначает атом углерода с четырьмя различными заместителями. В соответствии с правилом Канна-Ингольда-Прелонга, асимметрический атом углерода может иметь конфигурацию "R" или "S". В определении радикала R1 примерами карбоциклических колец, включающих от трех до восьми членов, включая по меньшей мере один атом азота или кислорода, являются морфолинил, пиперидинил,пиперазинил, пирролидинил, 2-окса-6-азаспиро[3,3]гептил, азетидинил, 3,3-дифторазетидинил, 3 гидроксиазетидил, 3-метоксиазетидинил, тиазолидинил, тиоморфолинил, диоксотиоморфолинил, оксазепанил, 2-окса-6-азаспиро[3.4]октил, 6-окса-1-азаспиро[3,3]гептил, 2-окса-5-азаспиро[3.4]октил, азиридинил, диоксоизотиазолидинил, оксетанил, 3-алкилоксетанил, 3-фтороксетанил, тетрагидрофуранил, тетрагидропиранил, азетидин-2-онил, пирролидин-2-онил, пиперидин-2-онил, диоксотиазетидинил, диоксотиазетидинил, диоксотиазинанил, гидроксипирролидинил и дифторпирролидинил. В определении радикала R1, частными примерами карбоциклических колец, включающих от трех до восьми членов, включая по меньшей мере один атом азота или кислорода, являются морфолинил, пиперидинил, пиперазинил, пирролидинил, азетидинил, 3,3-дифторазетидинил, 3-гидроксиазетидил, 3 метоксиазетидинил, тиоморфолинил, диоксотиоморфолинил, диоксоизотиазолидинил, оксетанил, 3 алкилоксетанил, 3-фтороксетанил, тетрагидрофуранил и пирролидин-2-онил. В определении радикала R1 частными примерами карбоциклических колец, включающих от трех до восьми членов, включая по меньшей мере один атом азота или кислорода, являются морфолинил, пиперидинил, азетидинил, 3,3-дифторазетидинил, 3-метоксиазетидинил, тиоморфолинил, диоксотиоморфолинил, оксетанил, 3-алкилоксетанил и пирролидин-2-онил. В определении радикала R1 дополнительными частными примерами карбоциклических колец,включающих от трех до восьми членов, включая по меньшей мере один атом азота или кислорода, являются морфолинил и 2-окса-6-азаспиро[3,3]гептил. В определении радикала R1 гетероциклил представляет собой предпочтительно оксетанил, тетрагидрофуранил, 1,1-диоксотиетанил или 1,1-диоксотетрагидротиофенил. В определении радикала R5 алкил предпочтительно представляет собой метил, этил, изопропил или пентил; циклоалкил предпочтительно представляет собой циклопропил, циклобутил или циклопентил, в частности, циклобутил или циклопентил; циклоалкилалкил предпочтительно представляет собой циклопропилалкил или циклопропилэтил; галогеналкил предпочтительно представляет собой трифторпропил. Настоящее изобретение относится, в частности, к соединению формулы (I), в котором А представляет собой алкил, гидроксиалкил, -СН 2 С(О)-, -С(О)-, -SO2- или отсутствует; R1 представляет собой водород, алкил, галогеналкил, гидроксил, алкоксигруппу, галогенал циклоалкил, циклоалкилалкоксигруппу, аминогруппу, гетероциклил, алкилгетероциклил, гидроксигетероциклил, алкилгетероциклил, гетероарил или галогенгетероарил, при этом указанный гетероциклил представляет собой карбоциклическое кольцо, включающее от трех до восьми членов, включая по меньшей мере один атом азота или кислорода,и указанный гетероарил представляет собой пиридинил, пиразолил, оксадиазолил или фуразанил;R2 представляет собой галоген или -NR3R4; один из R3 и R4 представляет собой водород или алкил, а другой представляет собой алкил или циклоалкил; или R3 и R4 совместно с атомом азота, к которому они присоединены, образуют гетероциклил или замещенный гетероциклил, при этом указанный гетероциклил представляет собой морфолинил, пиперидинил, пиперазинил, пирролидинил, 2-окса-6-азаспиро[3,3]гептил, азетидинил, тиазолидинил, тиоморфолинил, диоксотиоморфолинил, оксазепанил, 2-окса-6-азаспиро[3.4]октил, 6-окса-1-азаспиро[3,3]гептил,2-окса-5-азаспиро[3.4]октил, изоксазолидинил, азиридинил или диоксоизотиазолидинил, и при этом замещенный гетероциклил представляет собой гетероциклил, содержащий от одного до четырех заместителей, независимо выбранных из алкила, галогена, гидроксила, алкоксигруппы, гидроксиалкила, карбок-4 023581 сила, алкоксиалкила и цианогруппы; или его фармацевтически приемлемая соль или эфир; при условии,что 3-[(2-хлорфенил)метил]-5-(1,1-диметилэтил)-7-(4-морфолинил)-3 Н-1,2,3 триазоло[4,5-d]пиримидин и N-циклопропил-5-(1,1-диметилэтил)-3-(фенилметил)-3 Н-1,2,3-триазоло[4,5d]пиримидин-7-амин исключены. Настоящее изобретение относится, в частности, к следующим соединениям: соединение формулы (I), в котором А представляет собой -СН 2-, -СН 2 СН 2-, -СН(СН 3)-,-СН(ОН)СН 2-, -СН 2 С(О)-, -С(О)-, -SO2- или отсутствует; соединение формулы (I), в котором А представляет собой алкил или гидроксиалкил; соединение формулы (I), в котором А представляет собой -СН 2-, -СН 2 СН 2-, -СН(СН 3)- или-СН(ОН)СН 2-; соединение формулы (I), в котором R1 представляет собой водород, алкил, галогеналкил, гидроксил, алкоксигруппу, фенил, галогенфенил, алкоксифенил, галогеналкилфенил, галогеналкоксифенил,алкилсульфонилфенил, цианофенил, циклоалкил, алкилгетероциклил, гидроксигетероциклил, гетероарил, циклоалкилгетероарил, галогенгетероарил или алкилгетероарил, при этом указанный гетероциклил представляет собой карбоциклическое кольцо, содержащее по меньшей мере один атом азота, и при этом гетероарил представляет собой пиридинил, пиразолил, оксадиазолил, тетразолил или фуразанил; соединение формулы (I), в котором R1 представляет собой водород, алкил, галогеналкил, гидроксил, алкоксигруппу, фенил, галогенфенил, алкоксифенил, галогеналкилфенил, галогеналкоксифенил,цианофенил, циклоалкил, алкилгетероциклил, гидроксигетероциклил, гетероарил или галогенгетероарил,при этом указанный гетероциклил представляет собой морфолинил или 2-окса-6-азаспиро[3,3]гептил, и при этом гетероарил представляет собой пиридинил, пиразолил или оксадиазолил; соединение формулы (I), в котором R1 представляет собой галогеналкил, фенил, галогенфенил, галогеналкилфенил, цианофенил, алкилсульфонилфенил, циклоалкил, гетероарил, циклоалкилгетероарил,галогенгетероарил или алкилгетероарил, при этом указанный гетероарил представляет собой пиридинил,пиразолил, оксадиазолил, тетразолил или фуразанил; соединение формулы (I), в котором R1 представляет собой галогеналкил, фенил, галогенфенил, галогеналкилфенил, цианофенил, циклоалкил или гетероарил, при этом указанный гетероарил представляет собой пиридинил, пиразолил или оксадиазолил; соединение формулы (I), в котором R1 представляет собой водород, метил, метоксигруппу, гидроксил, хлорфенил, бромфенил, метоксифенил, трифторметоксифенил, хлорфторфенил, циклогексил, дихлорфенил, трихлорфенил, гидроксиэтоксифенил, дихлорфторфенил, (хлор)(трифторметил)фенил, (дихлор)(трифторметил)фенил, метилсульфонилфенил, метилсульфониламинофенил, пиридинил, хлорпиридинил, дихлорпиридинил, метилпирролидинил, оксетанил, метилоксетанил, (метилсульфонил)(метил)[1,2,4]триазолил, (хлор)(диметиламино)пиридинил, (метил)(окси)пиридинил, нитробензо[1,2,5]оксадиазолиламинопиридинил, пиразолил, метилпиперидинил, морфолинил, 2-окса-6 азаспиро[3,3]гептил, гидроксипирролидинил, трифторметил, хлордифторфенил, трифторметилфенил,цианофенил, фенил, тетрагидрофуранил, метил-[1,2,4]оксадиазолил, фуразанил, метилфуразанил, метил[1,3,4]оксадиазолил, метил-[1,3,4]оксадиазолил, метилтетразолил, метил-[1,2,4]триазолил, диметил[1,2,4]триазолил, трифторметилпиразолил, диметилпиразолил, метил-[1,2,3]триазолил, трифторметил[1,2,4]оксадиазолил, циклопропилтетразолил или метилфуразанил; соединение формулы (I), в котором R1 представляет собой водород, метил, метоксигруппу, гидроксил, хлорфенил, бромфенил, метоксифенил, трифторметоксифенил, хлорфторфенил, циклогексил, дихлорфенил, гидроксиэтоксифенил, дихлорфторфенил, метилсульфонилфенил, метилсульфониламинофенил, пиридинил, хлорпиридинил, дихлорпиридинил, метилпирролидинил, оксетанил, метилоксетанил,пиразолил, метилпиперидинил, морфолинил, 2-окса-6-азаспиро[3,3]гептил, гидроксипирролидинил, трифторметил, хлордифторфенил, трифторметилфенил, цианофенил, фенил, тетрагидрофуранил, метил[1,2,4]оксадиазолил или фуразанил; соединение формулы (I), в котором R1 представляет собой водород, метил, метоксигруппу, гидроксил, хлорфенил, бромфенил, метоксифенил, трифторметоксифенил, хлорфторфенил, циклогексил, дихлорфенил, пиридинил, хлорпиридинил, пиразолил, фуразанил, метилпиперидинил, морфолинил, 2-окса 6-азаспиро[3,3]гептил, гидроксипирролидинил, трифторметил, хлордифторфенил, трифторметилфенил,цианофенил или фенил; соединение формулы (I), в котором R1 представляет собой галогеналкил, фенил, галогенфенил, галогеналкилфенил, цианофенил, алкилсульфонилфенил, циклоалкил, гетероарил, циклоалкилгетероарил,галогенгетероарил или алкилгетероарил, при этом гетероарил представляет собой пиридинил, пиразолил,оксадиазолил, тетразолил или фуразанил; соединение формулы (I), в котором R1 представляет собой хлорфенил, циклогексил, дихлорфенил,пиридинил, хлорпиридинил, дихлорпиридинил, трифторметил, хлордифторфенил, трифторметилфенил,цианофенил, фенил, метилсульфонилфенил, метилтетразолил, метилфуразанил или циклопропилтетразолил; соединение формулы (I), в котором R1 представляет собой хлорфенил, циклогексил, дихлорфенил,-5 023581 пиридинил, трифторметил, хлордифторфенил, трифторметилфенил, цианофенил или фенил; соединение формулы (I), в котором R1 представляет собой хлорфенил, метилфуразанил, хлорпиридинил, метилсульфонилфенил или метилтетразолил; соединение формулы (I), в котором R2 представляет собой -NR3R4; соединение формулы (I), в котором один из R3 и R4 представляет собой водород или этил, а другой представляет собой этил или циклогексил; соединение формулы (I), в котором R3 и R4 совместно с атомом азота, к которому они присоединены, образуют гетероциклил или замещенный гетероциклил, при этом указанный гетероциклил представляет собой пиперидинил, пиперазинил, пирролидинил, морфолинил, тиазолидинил, тиоморфолинил, диоксотиоморфолинил, оксазепанил, 2-азетидинил, 2-окса-6-азаспиро[3,3]гептил, оксопирролидинил, 2 окса-6-азаспиро[3.4]октил, 6-окса-1-азаспиро[3,3]гептил, изоксазолидинил, азиридинил, диоксоизотиазолидинил, 2-окса-5-азаспиро[3.4]октил, и при этом замещенный гетероциклил представляет собой гетероциклил, содержащий от одного до четырех заместителей, независимо выбранных из алкила, галогена,гидроксила, гидроксиалкила, алкоксигруппы, алкоксиалкила, цианогруппы, алкиламиногруппы, диалкиламиногруппы, алкилкарбониламиногруппы, алкилкарбонил(алкиламино)группы, фенила, аминоалкила,метилпиразолила и метилизоксазолила; соединение формулы (I), в котором R3 и R4 совместно с атомом азота, к которому они присоединены, образуют гетероциклил или замещенный гетероциклил, при этом указанный гетероциклил представляет собой пиперидинил, пирролидинил или азетидинил, и указанный замещенный гетероциклил представляет собой гетероциклил, содержащий от одного до четырех заместителей, независимо выбранных из алкила, галогена, гидроксила, гидроксиалкила и алкоксиалкила; соединение формулы (I), в котором R3 и R4 совместно с атомом азота, к которому они присоединены, образуют пиперидинил, пирролидинил, дифторпиперидинил, дифторпирролидинил, дифторазетидинил, (метил)(гидроксил)азетидинил, гидроксипирролидинил, гидроксиметилпирролидинил, (гидроксиметил)(дифтор)пирролидинил,(гидроксил)(дифтор)пирролидинил,(гидроксил)(гидроксиметил)пирролидинил, тетрафторпирролидинил, 2-окса-6-азаспиро[3,3]гептил, метоксиметилпирролидинил, метилпиперазинил, морфолинил, азетидинил, гидроксиазетидинил, метоксиазетидинил, диметилморфолинил,метилморфолинил, гидроксиметилморфолинил, тиазолидинил, тиоморфолинил, диоксотиоморфолинил,оксазепанил, диметилпирролидинил, метоксипирролидинил, метилпирролидинил, гидроксипиперидинил,(гидроксил)(гидроксиметил)пирролидинил,(метил)(гидроксил)пирролидинил,2-окса-6 азаспиро[3.4]октил, 6-окса-1-азаспиро[3,3]гептил, фторпирролидинил, изоксазолидинил, азиридинил,(циано)(фтор)пирролидинил, диоксоизотиазолидинил, цианопирролидинил, 2-окса-5-азаспиро[3.4]октил,дигидроксипирролидинил, оксопирролидинил, метиламинопирролидинил, диметиламинопирролидинил,метилкарбониламинопирролидинил, метилкарбонил(метиламинопирролидинил), фенилпирролидинил,метилкарбонил(этиламинопирролидинил), метоксикарбонилазетидинил, аминометилпирролидинил, метилпиразолилпирролидинил,метилизоксазолилпирролидинил или метил[1,2,4]оксадиазолилпирролидинил; соединение формулы (I), в котором R3 и R4 совместно с атомом азота, к которому они присоединены, образуют пиперидинил, пирролидинил, дифторпиперидинил, дифторпирролидинил, дифторазетидинил, (метил)(гидроксил)азетидинил, гидроксипирролидинил, гидроксиметилпирролидинил, (гидроксиметил)(дифтор)пирролидинил, (гидроксил)(дифтор)пирролидинил, (гидроксил)(гидроксиметил)пирролидинил, тетрафторпирролидинил, 2-окса-6-азаспиро[3,3]гептил, метоксиметилпирролидинил, метилпиперазинил, морфолинил, азетидинил, гидроксиазетидинил, метоксиазетидинил, диметилморфолинил,метилморфолинил, гидроксиметилморфолинил, тиазолидинил, тиоморфолинил, диоксотиоморфолинил,оксазепанил, диметилпирролидинил, метоксипирролидинил, метилпирролидинил, гидроксипиперидинил,(гидроксил)(гидроксиметил)пирролидинил,(метил)(гидроксил)пирролидинил,2-окса-6 азаспиро[3.4]октил, 6-окса-1-азаспиро[3,3]гептил, фторпирролидинил, изоксазолидинил, азиридинил,(циано)(фтор)пирролидинил, диоксо-изотиазолидинил, цианопирролидинил, 2-окса-5-азаспиро[3.4]октил или дигидроксипирролидинил; соединение формулы (I), в котором R3 и R4 совместно с атомом азота, к которому они присоединены, образуют пиперидинил, пирролидинил, дифторпиперидинил, дифторпирролидинил, дифторазетидинил, (метил)(гидроксил)азетидинил, гидроксипирролидинил, гидроксиметилпирролидинил, тетрафторпирролидинил, 2-окса-6-азаспиро[3,3]гептил, метоксиметилпирролидинил, метилпиперазинил, морфолинил, азетидинил, гидроксиазетидинил, метоксиазетидинил, диметилморфолинил, метилморфолинил,гидроксиметилморфолинил, тиазолидинил, тиоморфолинил, диоксотиоморфолинил, оксазепанил, диметилпирролидинил, метоксипирролидинил, метилпирролидинил, гидроксипиперидинил, (гидроксил)(гидроксиметил)пирролидинил, (метил)(гидроксил)пирролидинил, 2-окса-6-азаспиро[3.4]октил, 6 окса-1-азаспиро[3,3]гептил, фторпирролидинил, изоксазолидинил, азиридинил, (циано)(фтор)пирролидинил, диоксоизотиазолидинил, цианопирролидинил, (гидроксил)(гидроксиметил)пирролидинил, 2 окса-5-азаспиро[3.4]октил или дигидроксипирролидинил; соединение формулы (I), в котором R3 и R4 совместно с атомом азота, к которому они присоединены, образуют дифторпиперидинил, дифторпирролидинил, дифторазетидинил, (метил)(гидро-6 023581(метил)(гидроксил)пирролидинил; соединение формулы (I), в котором R3 и R4 совместно с атомом азота, к которому они присоединены, образуют гетероциклил или замещенный гетероциклил, при этом указанный гетероциклил представляет собой пиперидинил, пирролидинил, азетидинил или 2-окса-6-азаспиро[3,3]гептил, и при этом замещенный гетероциклил представляет собой гетероциклил, содержащий от одного до четырех заместителей, независимо выбранных из алкила, галогена, гидроксила, гидроксиалкила и алкоксиалкила; соединение формулы (I), в котором R3 и R4 совместно с атомом азота, к которому они присоединены,образуют дифторпиперидинил,дифторпирролидинил,дифторазетидинил,(метил)(гидроксил)азетидинил, гидроксипирролидинил, гидроксиметилпирролидинил, тетрафторпирролидинил, метоксиметилпирролидинил, (гидроксил)(гидроксиметил)пирролидинил, (метил)(гидроксил)пирролидинил или 2-окса-6-азаспиро[3,3]гептил; соединение формулы (I), в котором R2 представляет собой гидроксипирролидинил или метилгидроксипирролидинил, в частности, гидроксипирролидинил; и соединение формулы (I), в котором R5 представляет собой метил, этил, изопропил, пентил, циклобутил, циклопентил, циклопропилметил, циклопропилэтил, трифторпропил или оксетанил. В определении радикала R1 особенно предпочтительны галогенфенил, алкилфуразанил, галогенпиридинил, алкилсульфонилфенил и алкилтетразолил, и еще более предпочтительны галогенфенил и алкилтетразолил. В определении радикала R1 особенно предпочтительны хлорфенил, метилфуразанил, хлорпиридинил, метилсульфонилфенил и метилтетразолил, и более предпочтительны и хлорфенил и метилтетразолил. Особенно предпочтительно, если R2 представляет собой -NR3R4, a R3 и R4 совместно с атомом азота,к которому они присоединены, образуют гидроксипирролидинил. Особенно предпочтительно, если А представляет собой алкил, в частном случае -СН 2-. Таким образом, настоящее изобретение относится также к следующему предпочтительному воплощению: соединение формулы (I), в котором А представляет собой алкил;R1 представляет собой галогенфенил, алкилфуразанил, галогенпиридинил, алкилсульфонилфенил или алкилтетразолил иR3 и R4 совместно с атомом азота, к которому они присоединены, образуют гидроксипирролидинил. Настоящее изобретение относится также к следующему предпочтительному воплощению: соединение формулы (I), в котором А представляет собой -СН 2-;R1 представляет собой хлорфенил, метилфуразанил, хлорпиридинил, метилсульфонилфенил или метилтетразолил иR3 и R4 совместно с атомом азота, к которому они присоединены, образуют гидроксипирролидинил. Настоящее изобретение относится также к следующему предпочтительному воплощению: соединение формулы (I), в котором А представляет собой алкил;R1 представляет собой галогенфенил или алкилтетразолил иR3 и R4 совместно с атомом азота, к которому они присоединены, образуют гидроксипирролидинил. Настоящее изобретение относится также к следующему предпочтительному воплощению: соединение формулы (I), в котором А представляет собой -СН 2-; R1 представляет собой хлорфенил или метилтетразолил; иR3 и R4 совместно с атомом азота, к которому они присоединены, образуют гидроксипирролидинил. Настоящее изобретение относится также, в частности, к соединению формулы (I), выбранному из 5-трет-бутил-3-(2-хлорбензил)-7-морфолин-4-ил-3 Н-[1,2,3]триазоло[4,5-d]пиримидин; 5-трет-бутил-3-(2-хлорбензил)-7-(пиперидин-1-ил)-3 Н-[1,2,3]триазоло[4,5-d]пиримидин; 5-трет-бутил-3-(2-хлорбензил)-7-(4,4-дифторпиперидин-1-ил)-3 Н-[1,2,3]триазоло[4,5-d]пиримидин; 5-трет-бутил-3-(2-хлорбензил)-7-(4-метилпиперазин-1-ил)-3 Н-[1,2,3]триазоло[4,5-d]пиримидин; 5-трет-бутил-3-(2-хлорбензил)-7-(пирролидин-1-ил)-3 Н-[1,2,3]триазоло[4,5-d]пиримидин; 5-трет-бутил-3-(2-хлорбензил)-7-(3,3-дифторпирролидин-1-ил)-3 Н-[1,2,3]триазоло[4,5-d]пиримидин; 5-трет-бутил-3-(2-хлорбензил)-N-этил-3 Н-[1,2,3]триазоло[4,5-d]пиримидин-7-амин; 5-трет-бутил-3-(2-хлорбензил)-N-циклогексил-3 Н-[1,2,3]триазоло[4,5-d]пиримидин-7-амин; 5-трет-бутил-3-(2-хлорбензил)-N,N-диэтил-3 Н-[1,2,3]триазоло[4,5-d]пиримидин-7-амин;[5-трет-бутил-7-(3,3-дифторпирролидин-1-ил)-[1,2,3]триазоло[4,5-d]пиримидин-3-ил]-(2-хлорфенил)-метанон. Настоящее изобретение относится также, в частности, к соединению формулы (I), выбранному из следующих:(R)-1-(5-трет-бутил-3-(2-(метилсульфонил)бензил)-3 Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил)-3 метилпирролидин-3-ол. Особенно предпочтительны следующие соединения формулы (I):(S)-1-[5-трет-бутил-3-(1-метил-1 Н-тетразол-5-илметил)-3 Н-[1,2,3]триазоло[4,5-d]пиримидин-7 ил]пирролидин-3-ол. Особенно предпочтительным соединением является (S)-1-(5-трет-бутил-3-(2-хлорбензил)-3 Н[1,2,3]триазоло[4,5-d]пиримидин-7-ил)пирролидин-3-ол. Получение соединений формулы (I) по настоящему изобретению можно проводить параллельными или сходящимися путями синтеза. Синтез соединений по настоящему изобретению представлен на нижеследующих схемах. Навыки, которые требуются для проведения реакций и очистки получаемых продуктов, доступны специалистам в данной области техники. Заместители и индексы, используемые в ниже следующем описании способов, имеют значение, раскрытое ранее в данном тексте, если не указано противоположное. Более конкретно, соединения формулы (I) можно получать способами, раскрытыми ниже,способами, представленными в примерах, или аналогичными способами. Подходящие условия реакций для конкретных стадий синтеза известны специалисту в данной области техники. Кроме того, в литературе описаны условия проведения реакций, влияющие на приведенные реакции (см., например: Comprehensive Organic Transformations: A Guide to Functional Group Preparations, 2nd Edition, Richard С. Larock.John WileySons, New York, NY. 1999). Авторы изобретения считают удобным проводить данные реакции в присутствии или отсутствии растворителя. В отношении природы используемого растворителя не накладывается какого-либо особого ограничения, при условии, что растворитель не оказывает нежелательного воздействия на ход реакции или на используемые реагенты, и что он способен растворять реагенты, по меньшей мере, в некоторой степени. Описанные реакции могут протекать в широком диапазоне температур, и точная температура реакции не существенна в свете настоящего изобретения. Описанные реакции удобно проводить в интервале температур между -78 С и температурой флегмы. Время,необходимое для протекания реакции, также может меняться в широком диапазоне, в зависимости от многих факторов, в частности от температуры реакции и природы реагентов. При этом обычно достаточно инетрвала от 0,5 часов до нескольких суток для получения желаемых промежуточных продуктов и конечных соединений. Последовательность реакций не ограничена представленной на схемах, а наоборот, в зависимости от исходных веществ и их относительной реакционной способности, последовательность реакционных стадий можно легко изменять. Исходные вещества либо имеются в продаже, либо их можно получить способами, аналогичными способам, представленным ниже, способами, описанными в цитируемых источниках в описании или примерах, или способами, известными в данной области техники. Схема 1 а) Галиды II либо имеются в продаже, либо их можно синтезировать способами, известными в данной области техники. Галиды II удобно вводить в реакцию с азидом натрия в подходящем растворителе,таком как ацетонитрил, этанол или DMF, с получением азидных производных III. В других предпочтительных условиях используют растворители, такие как DMA, NMP или DMSO, и еще более предпочтительно - NMP и DMSO. В полярных апротонных растворителях, таких как NMP и DMSO, реакцию алкилирования обычно можно проводить при более низкой температуре, чем, например, в ацетонитриле, час- 16023581 то при температуре от комнатной до 40 С (как, например, в случае BnCI, 1-хлор-2-(хлорметил)бензола или PMB-CI (пара-метоксибензил хлорид); это зависит, разумеется, от реакционной способности галидовII), что обеспечивает улучшенное окно безопасности процесса (осторожно: известно, что органические азиды потенциально опасны, и всегда следует тщательно оценивать безопасность процесса). Внесение воды может давать преимущество, поскольку это повышает растворимость азида натрия и обеспечивает более устойчивый кинетический профиль, так как вода способствует растворению твердых комков NaN3. Это может также приводить к лучшей фильтруемости конечной азидной реакционной смеси. Фильтрация реакционной смеси может потребоваться, например, если последующее циклоприсоединение проводят в непрерывном режиме в реакторах с узкими каналами. Азид не выделяют, и его раствор проще вводить на следующей стадии. Это также позволяет обойтись без выделения, которое может также вызывать проблемы в технике безопасности.b) Производные триазола IV можно получить путем [3+2] циклоприсоединения азидных производных III с 2-цианоацетамидом в присутствии подходящего основания, такого как метоксид натрия или этоксид натрия, в подходящем растворителе, таком как метанол, этанол или DMF. Другие предпочтительные условия включают ведение в реакцию азида с 2-цианоацетамидом в растворителях, таких какNMP или DMSO, в присутствии гидроксида натрия. Периодический процесс обычно проводят при температуре от комнатной до 50 С, предпочтительно между комнатной температурой и 40 С (внимание: безопасность процесса всегда следует тщательно оценивать). Процесс циклоприсоединения также поддается переведению в непрерывный режим (по данному вопросу см. следующую литературу: Org. ProcessRes. Dev., 2009, 13 (6), pp 1401-1406), и в этом случае температуру реакции можно повышать до 50 С и выше, например (без ограничения) между 50 и 90 С, предпочтительно между 60 и 70 С.c) Производные триазола V можно получить ацилированием IV с помощью ацилгалида в присутствии основания, такого как DIEA, DMAP, пиридин и т.п. Наблюдалось двойное ацилирование и образование нитрильных побочных продуктов. Это имеет место в значительной мере при использовании, например, пиридина в качестве растворителя. Однако данное явление можно минимизировать при использовании DMA или NMP, предпочтительно DMA, в качестве растворителя вместо пиридина. Предпочтительные условия включают использование 1,0-2 экв. пиридина и пивалоилхлорида, предпочтительно от 1,0 до 1,5 экв., предпочтительно около 1,5 экв. при 50-100 С, предпочтительно между 75-85 С. Эти высококипящие полярные растворители позволяют также сокращать последующую стадию циклизации, что существенно упрощает процесс.d) Производные тиазолопиримидина VI можно получить путем внутримолекулярной циклизации производного триазола V в присутствии основания, такого как KHCO3, Na2CO3, и воды как в присутствии, так и в отсутствие растворителя, такого как метанол, этанол, диоксан и толуол. Другие предпочтительные условия включают применение DMA или NMP в качестве растворителей, предпочтительноDMA. Эту реакцию можно проводить в присутствии КНСО 3 при 130-170 С, предпочтительно между 140 и 160 С. Соединение VI может существовать в виде таутомера или смеси таутомеров, например:e) Хлориды VII можно получить реакцией соединения VI с хлорирующим реагентом, таким какPOCI3, SOCI2 или (СОС 1)2, в присутствии подходящего основания, такого как N,N-диэтиланилин, лутидин или пиридин. Другие предпочтительные условия включают применение реагента Вильсмейера в качестве хлорирующего агента. Его можно также получать in situ в ходе реакции оксалилхлорида с DMF. Хлорирование можно проводить, например, в ацетонитриле, DCM или AcOEt, предпочтительно в DCM. Эти условия позволяют применять мягкий температурный режим реакции и, например, избегать необходимости гасить избыток POCl3 после выделения продукта. Неочищенный продукт можно вводить в следующую стадию.f) Соединение VII удобно вводить в реакцию с различными нуклеофилами, в частности, с аминами,в присутствии подходящего основания, такого как триэтиламин, DIEA или DBU, в подходящем растворителе, таком как ацетонитрил, метанол, толуол или DMF, с получением производных триазолопиримидина I. Если таким нуклеофилом является спирт, реакцию можно проводить с использованием основания, такого как гидрид натрия, в растворителе, таком как DMF, предпочтительно при температуре между 0 и 50 С, или в других условиях, известных специалисту в данной области техники, с получением сложных эфиров I. Эти производные могут представлять собой конечные соединения, однако предпочтительно, в случае если R1-A = замещенная бензильная группа, например п-метоксибензил, чтобы эти группы можно отщеплять с помощью TFA, CAN (цериевый нитрат аммония), гидрогенирования и т.п., с получением производных I (R1-A =H). R1-A = бензил представляет собой подходящую альтернативную защитную группу. Таким путем можно избежать применения PMB-CI (для получения соответствующего азидного промежуточного продукта III), который, как известно, имеет некоторые ограничения по термической стабильности (см., например, Organic Process ResearchDevelopment 2005, 9, 1009-1012) и непостоянное качество, в зависимости от поставщика. Бензильную группу можно отщеплять в стандартных условиях гидролиза, также, например, в присутствии кислот. Если используют HCI, то производные I (R1-A =H) потенциально можно выделять в виде солей. Производные триазола I (R1-A =H) удобно вводить в реакцию с галидом (или сульфонатом) в присутствии подходящего основания, такого как DIEA, DBU, К 2 СО 3, или Cs2CO3, в растворителе, таком какDMF, диоксан или толуол, или, как вариант, со спиртом, в условиях реакции Мицунобу с использованием подходящего диазодикарбоксилата (DEAD, DIAD и т.п.) и фосфина, такого как PBu3 или PPh3, в подходящем растворителе, таком как THF, DCM и толуол, с получением конечных производных триазолопиримидина I. Настоящее изобретение относится также к способу получения соединения формулы (I), включающему одну из следующих реакций:(а) реакция соединения формулы (А), его таутомера или смеси его таутомеров, в частности в присутствии галогенирующего реагента и, возможно, в присутствии основания; или реакция соединения формулы (В) в присутствии NHR3R4 и, возможно, в присутствии основания, где A, R1, R3 и R4 описаны выше. На стадии (а) основание представляет собой, например, N,N-диэтиланилин, лутидин или пиридин. Галогенирующие реагенты хорошо известны специалистам в данной области техники. В частности,галогенирующие реагенты представляют собой хлорирующие реагенты. Примерами галогенирующих реагентов являются POCI3, SOCI2, (COCI)2 или реагент Вильсмейера. POCI3 и реагент Вильсмейера являются примерами галогенирующих реагентов, полезных для способа по настоящему изобретению. На стадии (b) основание представляет собой, например, триэтиламин, DIEA или DBU. На стадии (b) можно использовать растворитель, который можно выбирать, например, из ацетонитрила, метанола, толуола и DMF. Соединение формулы (I), если оно получено способом по настоящему изобретению, также является объектом настоящего изобретения. Настоящее изобретение относится также к соединению формулы (I) для применения в качестве терапевтически активного вещества. Настоящее изобретение относится также к фармацевтической композиции, включающей соединение формулы (I) и терапевтически инертный носитель. Еще одним объектом настоящего изобретения является применение соединения формулы (I) для лечения или профилактики боли, в частности, хронической боли, атеросклероза, регуляции костной массы, воспаления, ишемии, реперфузионного повреждения, системного фиброза, фиброза печени, фиброза легких, фиброза почек, хронической нефропатии аллотрансплантанта, застойной сердечной недостаточности, инфаркта миокарда, системного склероза, гломерулонефропатии, термического повреждения,ожога, гипертрофических рубцов, келоидов, лихорадки при гингивите, цирроза печени или опухолей. Еще одним объектом настоящего изобретения является применение соединения формулы (I) для изготовления лекарственного средства для лечения или профилактики хронической боли, в частности, хронической боли, атеросклероза, регуляции костной массы, воспаления, ишемии, реперфузионного повреждения, системного фиброза, фиброза печени, фиброза легких, фиброза почек, хронической нефропатии аллотрансплантанта, застойной сердечной недостаточности, инфаркта миокарда, системного склероза,гломерулонефропатии, термического повреждения, ожога, гипертрофических рубцов, келоидов, лихорадки при гингивите, цирроза печени или опухолей. Настоящее изобретение также относится к соединению формулы (I) для лечения или профилактики боли, в частности, хронической боли, атеросклероза, регуляции костной массы, воспаления, ишемии,реперфузионного повреждения, системного фиброза, фиброза печени, фиброза легких, фиброза почек,хронической нефропатии аллотрансплантанта, застойной сердечной недостаточности, инфаркта миокарда, системного склероза,гломерулонефропатии, термического повреждения, ожога, гипертрофических рубцов, келоидов, ли- 18023581 хорадки при гингивите, цирроза печени или опухолей. Еще одним объектом настоящего изобретения является применение 3-[(2-хлорфенил)метил]-5-(1,1 диметилэтил)-7-(4-морфолинил)-3 Н-1,2,3-триазоло[4,5-d]пиримидина илиN-циклопропил-5-(1,1 диметилэтил)-3-(фенилметил)-3 Н-1,2,3-триазоло[4,5-d]пиримидин-7-амина, в частности, 3-[(2-хлорфенил)метил]-5-(1,1-диметилэтил)-7-(4-морфолинил)-3 Н-1,2,3-триазоло[4,5-d]пиримидина, для изготовления лекарственного средства для лечения или профилактики хронической боли, в частности хронической боли, атеросклероза, регуляции костной массы, воспаления, ишемии, реперфузионного повреждения,системного фиброза, фиброза печени, фиброза легких, фиброза почек, хронической нефропатии аллотрансплантанта, застойной сердечной недостаточности, инфаркта миокарда, системного склероза, гломерулонефропатии, термического повреждения, ожога, гипертрофических рубцов, келоидов, лихорадки при гингивите, цирроза печени или опухолей. Настоящее изобретение также относится к 3-[(2-хлорфенил)метил]-5-(1,1-диметилэтил)-7-(4 морфолинил)-3 Н-1,2,3-триазоло[4,5-d]пиримидину или N-циклопропил-5-(1,1-диметилэтил)-3-(фенилметил)-3 Н-1,2,3-триазоло[4,5-d]пиримидин-7-амину,в частности,3-[(2-хлорфенил)метил]-5-(1,1 диметилэтил)-7-(4-морфолинил)-3 Н-1,2,3-триазоло[4,5-d]пиримидину для лечения или профилактики боли, в частности хронической боли, атеросклероза, регуляции костной массы, воспаления, ишемии, реперфузионного повреждения, системного фиброза, фиброза печени, фиброза легких, фиброза почек, хронической нефропатии аллотрансплантанта, застойной сердечной недостаточности, инфаркта миокарда,системного склероза, гломерулонефропатии, термического повреждения, ожога, гипертрофических рубцов, келоидов, лихорадки при гингивите, цирроза печени или опухолей. Настоящее изобретение относится, в частности, к следующему: применение соединения формулы(I) для лечения или профилактики боли, атеросклероза, возрастной макулярной дистрофии, диабетической ретинопатии, глаукомы, сахарного диабета, воспаления, воспалительного заболевания кишечника,ишемически-реперфузионного повреждения, острой печеночной недостаточности, фиброза печени, фиброза легких, фиброза почек, системного фиброза, острого отторжения аллотрансплантанта, хронической нефропатии аллотрансплантанта, диабетической нефропатии, гломерулонефропатии, кардиомиопатии,сердечной недостаточности, ишемии миокарда, инфаркта миокарда, системного склероза, термического повреждения, ожога, гипертрофических рубцов, келоидов, лихорадки при гингивите, цирроза печени или опухолей, регуляции костной массы, нейродегенерации, инсульта, преходящего нарушения мозгового кровообращения или увеита; применение соединения формулы (I) для изготовления лекарственного средства для лечения или профилактики боли, атеросклероза, возрастной макулярной дистрофии, диабетической ретинопатии, глаукомы, сахарного диабета, воспаления, воспалительного заболевания кишечника, ишемическиреперфузионного повреждения, острой печеночной недостаточности, фиброза печени, фиброза легких,фиброза почек, системного фиброза, острого отторжения аллотрансплантанта, хронической нефропатии аллотрансплантанта, диабетической нефропатии, гломерулонефропатии, кардиомиопатии, сердечной недостаточности, ишемии миокарда, инфаркта миокарда, системного склероза, термического повреждения, ожога, гипертрофических рубцов, келоидов, лихорадки при гингивите, цирроза печени или опухолей, регуляции костной массы, нейродегенерации, инсульта, преходящего нарушения мозгового кровообращения или увеита; соединение формулы (I) для лечения или профилактики боли, атеросклероза, возрастной макулярной дистрофии, диабетической ретинопатии, глаукомы, сахарного диабета, воспаления, воспалительного заболевания кишечника, ишемически-реперфузионного повреждения, острой печеночной недостаточности, фиброза печени, фиброза легких, фиброза почек, системного фиброза, острого отторжения аллотрансплантанта, хронической нефропатии аллотрансплантанта, диабетической нефропатии, гломерулонефропатии, кардиомиопатии, сердечной недостаточности, ишемии миокарда, инфаркта миокарда,системного склероза, термического повреждения, ожога, гипертрофических рубцов, келоидов, лихорадки при гингивите, цирроза печени или опухолей, регуляции костной массы, нейродегенерации, инсульта,преходящего нарушения мозгового кровообращения или увеита; и способ для лечения или профилактики боли, атеросклероза, возрастной макулярной дистрофии,диабетической ретинопатии, глаукомы, сахарного диабета, воспаления, воспалительного заболевания кишечника, ишемически-реперфузионного повреждения, острой печеночной недостаточности, фиброза печени, фиброза легких, фиброза почек, системного фиброза, острого отторжения аллотрансплантанта,хронической нефропатии аллотрансплантанта, диабетической нефропатии, гломерулонефропатии, кардиомиопатии, сердечной недостаточности, ишемии миокарда, инфаркта миокарда, системного склероза,термического повреждения, ожога, гипертрофических рубцов, келоидов, лихорадки при гингивите, цирроза печени или опухолей, регуляции костной массы, нейродегенерации, инсульта, преходящего нарушения мозгового кровообращения или увеита, включающий введение эффективного количества соединения формулы (I) пациенту, который в этом нуждается. Настоящее изобретение в частности относится к соединению формулы (I) для лечения или профилактики ишемии, реперфузионного повреждения, фиброза печени или фиброза почек, в частности, ишемии или реперфузионного повреждения. Настоящее изобретение также относится к соединению формулы (I), если оно получено способом по настоящему изобретению. Объектом настоящего изобретения является также способ лечения или профилактики боли, в частности хронической боли, атеросклероза, регуляции костной массы, воспаления, ишемии, реперфузионного повреждения, системного фиброза, фиброза печени, фиброза легких, фиброза почек, хронической нефропатии аллотрансплантанта, застойной сердечной недостаточности, инфаркта миокарда, системного склероза, гломерулонефропатии, термического повреждения, ожога, гипертрофических рубцов, келоидов, лихорадки при гингивите, цирроза печени или опухолей, включающий введение эффективного количества соединения формулы (I) пациенту, который в этом нуждается. В другом воплощении настоящего изобретению предложены фармацевтические композиции или лекарственные средства, содержащие соединения по настоящему изобретению и терапевтически инертный носитель, разбавитель или эксципиент, а также способы применения соединения по настоящему изобретению изготовления таких композиций и лекарственных средств. В одном примере соединения формулы (I) можно включать в лекарственную форму путем смешения при комнатной температуре, при подходящем значении рН и при желаемой степени чистоты с физиологически приемлемыми носителями,т.е., носителями, которые не токсичны для реципиентов при дозировках и концентрациях, применяемых в галеновой лекарственной форме. Значение рН композиции зависит в основном от конкретного применения и концентрации соединения, но в любом случае находится предпочтительно в интервале примерно от 3 до 8. В одном примере соединение формулы (I) включают в лекарственную форму в ацетатном буфере при рН 5. В другом воплощении соединения формулы (I) являются стерильными. Соединение можно хранить, например, в виде твердого вещества или аморфной композиции, в виде лиофилизованной композиции или в виде водного раствора. Изготовление лекарственных форм с композициями, их дозирование и введение осуществляют в соответствии с надлежащей медицинской практикой. Факторы, которые следует учитывать в данном контексте, включают конкретное расстройство, на которое направлено лечение, конкретное млекопитающее, которому проводят лечение, клиническое состояние конкретного пациента, причину расстройства, сайт доставки действующего вещества, способ введения, схему введения и другие факторы, известные практикующим врачам. Соединения по настоящему изобретению можно вводить любым удобным способом, включая оральное, местное (в т.ч. трансбуккальное и сублингвальное), ректальное, вагинальное, трансдермальное,парентеральное, подкожное, внутрибрюшинное, внутрилегочное, внутрикожное, интратекальное, эпидуральное и интраназальное, а также, в целях местного лечения, внутриочаговое введение. Парентеральные инфузии включают внутримышечное, внутривенное, внутриартериальное, внутрибрюшинное или подкожное введение. Соединения по настоящему изобретению можно вводить в любой удобной форме для введения, например, в виде таблеток, порошков, капсул, растворов, дисперсий, суспензий, сиропов, спрэев, суппозиториев, гелей, эмульсий, пластырей и т.п. Такие композиции могут содержать компоненты, которые обычно применяются в фармацевтических препаратах, например, разбавители, носители, модификаторы рН, подсластители, объемообразующие агенты и дополнительные действующие вещества. Типичную лекарственную форму изготавливают путем смешивания соединения по настоящему изобретению с носителем или эксципиентом. Подходящие носители и эксципиенты хорошо известны специалистам в данной области техники и подробно описаны, например, в следующих источниках:Excipients. Chicago, Pharmaceutical Press, 2005. Такие лекарственные формы могут также включать один или более буферных агентов, стабизизаторов, поверхностно-активных веществ, увлажняющих агентов,лубрикантов, эмульгаторов, суспендирующих агентов, консервантов, антиоксидантов, кроющих агентов,скользящих веществ, вспомогательных веществ для производственного процесса, красителей, подсластителей, отдушек, ароматизаторов, разбавителей и других известных добавок для обеспечения надлежащей формы выпуска лекарства (т.е., соединения по настоящему изобретению или его фармацевтической композиции) или вспомогательного средства при изготовлении фармацевтического продукта (т.е., лекарственного средства). Настоящее изобретение далее наглядно представлено в следующих примерах, которые не носят ограничивающий характер. Примеры Аббревиатура Хиральное разделение 1-(3-бензил-5-трет-бутил-3 Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил)-3 метилпирролидин-3-ола (пример 221, стадия а) давало соответствующие оптически чистые R- и Sпроизводные. Тем не менее, окончательное стехиометрическое соотношение на данный момент выясняется. Поэтому стереохимическое распределение для оптически чистых примеров 221-230 не было определено. Пример 1. 5-трет-Бутил-3-(2-хлорбензил)-7-морфолин-4-ил-3 Н-[1,2,3]триазоло[4,5-d]пиримидин Смесь 1-(бромметил)-2-хлорбензола (5 г, 24,3 ммоль) и азида натрия (2,37 г; 36,5 ммоль) в ацетонитриле (48,7 мл) нагревали с обратным холодильником в течение 3 ч в атмосфере азота. Затем эту смесь фильтровали и концентрировали в вакууме. Остаток разбавляли в DCM, промывали с помощью Н 2 О и солевого раствора, высушивали над Na2SO4 и концентрировали в вакууме с получением неочищенного 1(азидометил)-2-хлорбензола. Этот осадок использовали в следующей реакции без дополнительной очистки. Смесь описанного выше неочищенного осадка, 2-цианоацетамида (1,82 г; 21,7 ммоль) и этанолята натрия (1.47 г; 21,7 ммоль) в этаноле (43,3 мл) нагревали с обратным холодильником в течение 3 ч в атмосфере азота. Эту смесь концентрировали в вакууме, разбавляли водным 4 М раствором АсОН и фильтровали. Остаток промывали с помощью Н 2 О и высушивали в вакууме с получением 5-амино-1-(2 хлорбензил)-1 Н-1,2,3-триазол-4-карбоксамида в виде бледно-оранжевого твердого вещества (5,10 г; 94% в 2 стадии). MS(m/e): 252,1 (МН+). Смесь 5-амино-1-(2-хлорбензил)-1 Н-1,2,3-триазол-4-карбоксамида (2 г; 7,95 ммоль) и пивалоилхлорида (1.47 мл; 11,9 ммоль) в пиридине (3,98 мл) перемешивали при 80 С в течение 2 ч в атмосфере азота. Затем к реакционной смеси добавляли 8 М водный раствор гидроксида натрия (2,98 мл; 23,8 ммоль) и метанола (3,98 мл). Перемешивали при 80 С в течение 2 ч, после чего реакционную смесь вливали в 1 М водный раствор HCI, экстрагировали диэтиловым эфиром, промывали с помощью 2 М раствора HCI,воды и солевого раствора, высушивали над Na2SO4 и концентрировали в вакууме с получением смеси неочищенного 1-(2-хлорбензил)-5-пиваламидо-1 Н-1,2,3-триазол-4-карбоксамида и N-(1-(2-хлорбензил)4-циано-1 Н-1,2,3-триазол-5-ил)пиваламида. Этот осадок использовали в следующей реакции без дополнительной очистки. Смесь полученного выше неочищенного осадка и КНСО 3 (3,00 г; 30,0 ммоль) в Н 2 О (60,0 мл) нагревали с обратным холодильником в течение 18 ч. Реакционную смесь вливали в 1 М водный раствор HCI,экстрагировали с помощью EtOAc, промывали солевым раствором, высушивали над Na2SO4 и концентрировали в вакууме. Неочищенный остаток очищали флэш-хроматографией (силикагель, от 10 до 70%EtOAc в гептане) с получением 5-трет-бутил-3-(2-хлорбензил)-3 Н-[1,2,3]триазоло[4,5-d]пиримидин 7(4 Н)-она в виде белого твердого вещества (1,03 г; 41% в 2 стадии). MS(m/e): 318,2 (МН+). с) 5-трет-Бутил-3-(2-хлорбензил)-7-морфолин-4-ил-3 Н-[1,2,3]триазоло[4,5-d]пиримидин Смесь 5-трет-бутил-3-(2-хлорбензил)-3 Н-[1,2,3]триазоло[4,5-d]пиримидин-7(4 Н)-она (12,3 мг; 38,7 мкмоль) и N,N-диэтиланилина (12,3 мкл; 77,4 мкмоль) в POCI3 (250 мкл; 2,73 ммоль) нагревали с обратным холодильником в течение 3 ч в атмосфере азота. Реакционную смесь концентрировали в вакууме,разбавляли с помощью EtOAc, промывали холодной водой и солевым раствором, высушивали надNa2SO4 и концентрировали в вакууме с получением неочищенного 5-трет-бутил-7-хлор-3-(2 хлорбензил)-3 Н-[1,2,3]триазоло[4,5-d]пиримидина. Этот осадок использовали в следующей реакции без дополнительной очистки. Смесь полученного выше неочищенного осадка, морфолина (6,77 мкл; 77,4 мкмоль) и DIEA (13,5 мкл; 77,4 мкмоль) в ацетонитриле (200 мкл) перемешивали при комнатной температуре в течение ночи. Реакционную смесь непосредственно очищали с помощью препаративной ВЭЖХ (колонка: Gemini 5 мкм С 18 110 А 7530 мм; подвижная фаза: вода (0,05% Et3N): ацетонитрил от 50:50% до 5:95%; длина волны: 254 нм; поток: 30 мл/мин) с получением указанного в заголовке соединения в виде светло-желтого твердого вещества (5,8 мг; 39% в 2 стадии). MS(m/e): 387,3 (МН+). Пример 2. 5-трет-Бутил-3-(2-хлорбензил)-7-пиперидин-1-ил-3 Н-[1,2,3]триазоло[4,5-d]пиримидин По аналогии со способом, описанным для синтеза 5-трет-бутил-3-(2-хлорбензил)-7-морфолин-4-ил 3 Н-[1,2,3]триазоло[4,5-d]пиримидина (пример 1, стадия с), указанное в заголовке соединение получали из 5-трет-бутил-7-хлор-3-(2-хлорбензил)-3 Н-[1,2,3]триазоло[4,5-d]пиримидина и пиперидина и выделяли в виде светло-желтого твердого вещества (10,0 мг; 55%). MS(m/e): 385,4 (МН+). Пример 3. 5-трет-Бутил-3-(2-хлорбензил)-7-(4,4-дифторпиперидин-1-ил)-3 Н-[1,2,3]триазоло[4,5d]пиримидин По аналогии со способом, описанным для синтеза 5-трет-бутил-3-(2-хлорбензил)-7-морфолин-4-ил 3 Н-[1,2,3]триазоло[4,5-d]пиримидина (пример 1, стадия с), указанное в заголовке соединение получали из 5-трет-бутил-7-хлор-3-(2-хлорбензил)-3 Н-[1,2,3]триазоло[4,5-d]пиримидина и 4,4-дифторпиперидина гидрохлорида и выделяли в виде светло-желтой смолы (10,9 мг; 55%). MS(m/e): 421,4 (МН+). Пример 4. 5-трет-Бутил-3-(2-хлорбензил)-7-(4-метилпиперазин-1-ил)-3 Н-[1,2,3]триазоло[4,5-d]пиримидин По аналогии со способом, описанным для синтеза 5-трет-бутил-3-(2-хлорбензил)-7-морфолин-4-ил 3 Н-[1,2,3]триазоло[4,5-d]пиримидина (пример 1, стадия с), указанное в заголовке соединение получали из 5-трет-бутил-7-хлор-3-(2-хлорбензил)-3 Н-[1,2,3]триазоло[4,5-d]пиримидина и 1-метилпиперазина и выделяли в виде светло-желтого твердого вещества (13,4 мг; 71%). MS(m/e): 400,4 (МН+). Пример 5. 5-трет-Бутил-3-(2-хлорбензил)-7-пирролидин-1-ил-3 Н-[1,2,3]триазоло[4,5-d]пиримидин По аналогии со способом, описанным для синтеза 5-трет-бутил-3-(2-хлорбензил)-7-морфолин-4-ил 3 Н-[1,2,3]триазоло[4,5-d]пиримидина (пример 1, стадия с), указанное в заголовке соединение получали из 5-трет-бутил-7-хлор-3-(2-хлорбензил)-3 Н-[1,2,3]триазоло[4,5-d]пиримидина и пирролидина и выделяли в виде белого твердого вещества (12,4 мг; 71%). MS(m/e): 371,4 (МН+). Пример 6. 5-трет-Бутил-3-(2-хлорбензил)-7-(3,3-дифторпирролидин-1-ил)-3 Н-[1,2,3]триазоло[4,5d]пиримидин По аналогии со способом, описанным для синтеза 5-трет-бутил-3-(2-хлорбензил)-7-морфолин-4-ил 3 Н-[1,2,3]триазоло[4,5-d]пиримидина (пример 1, стадия с), указанное в заголовке соединение получали из 5-трет-бутил-7-хлор-3-(2-хлорбензил)-3 Н-[1,2,3]триазоло[4,5-d]пиримидина и 3,3-дифторпирролидина гидрохлорида и выделяли в виде бесцветной смолы (13,3 мг; 69%). MS(m/e): 407,4 (МН+). Пример 7. [5-трет-Бутил-3-(2-хлорбензил)-3 Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил]этиламин По аналогии со способом, описанным для синтеза 5-трет-бутил-3-(2-хлорбензил)-7-морфолин-4-ил 3 Н-[1,2,3]триазоло[4,5-d]пиримидина (пример 1, стадия с), указанное в заголовке соединение получали из 5-трет-бутил-7-хлор-3-(2-хлорбензил)-3 Н-[1,2,3]триазоло[4,5-d]пиримидина и этанамина гидрохлорида и выделяли в виде белого твердого вещества (1,1 мг; 7%). MS(m/e): 345,3 (МН+). Пример 8. [5-трет-Бутил-3-(2-хлорбензил)-3 Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил]циклогексиламин По аналогии со способом, описанным для синтеза 5-трет-бутил-3-(2-хлорбензил)-7-морфолин-4-ил 3 Н-[1,2,3]триазоло[4,5-d]пиримидина (пример 1, стадия с), указанное в заголовке соединение получали из 5-трет-бутил-7-хлор-3-(2-хлорбензил)-3 Н-[1,2,3]триазоло[4,5-d]пиримидина и циклогексанамина и выделяли в виде светло-желтого твердого вещества (3,8 мг; 20%). MS(m/e): 399,4 (МН+). Пример 9. [5-трет-Бутил-3-(2-хлорбензил)-3 Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил]диэтиламин По аналогии со способом, описанным для синтеза 5-трет-бутил-3-(2-хлорбензил)-7-морфолин-4-ил 3 Н-[1,2,3]триазоло[4,5-d]пиримидина (пример 1, стадия с), указанное в заголовке соединение получали из 5-трет-бутил-7-хлор-3-(2-хлорбензил)-3 Н-[1,2,3]триазоло[4,5-d]пиримидина и диэтиламина и выделяли в виде бесцветной смолы (11,5 мг; 65%). MS(m/e): 373,4 (МН+). Пример 10. 5-трет-Бутил-3-(2-хлорбензил)-7-(2-окса-6-азаспиро[3,3]гепт-6-ил)-3 Н-[1,2,3]триазоло По аналогии со способом, описанным для синтеза 5-трет-бутил-3-(2-хлорбензил)-7-морфолин-4-ил 3 Н-[1,2,3]триазоло[4,5-d]пиримидина (пример 1, стадия с), указанное в заголовке соединение получали из 5-трет-бутил-7-хлор-3-(2-хлорбензил)-3 Н-[1,2,3]триазоло[4,5-d]пиримидина и 2-окса-6-азаспиро[3,3]гептана оксалата и выделяли в виде белого твердого вещества (10,8 мг; 57%). MS(m/e): 399,4 По аналогии со способом, описанным для синтеза 5-трет-бутил-3-(2-хлорбензил)-7-морфолин-4-ил 3 Н-[1,2,3]триазоло[4,5-d]пиримидина (пример 1, стадия с), указанное в заголовке соединение получали из 5-трет-бутил-7-хлор-3-(2-хлорбензил)-3 Н-[1,2,3]триазоло[4,5-d]пиримидина и азетидина и выделяли в виде белого твердого вещества (9,8 мг; 52%). MS(m/e): 357,3 (МН+). Пример 12. 5-трет-Бутил-3-(2-хлорбензил)-7-(3,3-дифторазетидин-1-ил)-3 Н-[1,2,3]триазоло[4,5d]пиримидин По аналогии со способом, описанным для синтеза 5-трет-бутил-3-(2-хлорбензил)-7-морфолин-4-ил 3 Н-[1,2,3]триазоло[4,5-d]пиримидина (пример 1, стадия с), указанное в заголовке соединение получали из 5-трет-бутил-7-хлор-3-(2-хлорбензил)-3 Н-[1,2,3]триазоло[4,5-d]пиримидина и 3,3-дифторазетидина гидрохлорида и выделяли в виде светло-желтой смолы (11,9 мг; 64%). MS(m/e): 393,4 (МН+). Пример 13. 1-[5-трет-Бутил-3-(2-хлорбензил)-3 Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил]-3 метилазетидин-3-ол По аналогии со способом, описанным для синтеза 5-трет-бутил-3-(2-хлорбензил)-7-морфолин-4-ил 3 Н-[1,2,3]триазоло[4,5-d]пиримидина (пример 1, стадия с), указанное в заголовке соединение получали из 5-трет-бутил-7-хлор-3-(2-хлорбензил)-3 Н-[1,2,3]триазоло[4,5-d]пиримидина и азетидин-3-ола гидрохлорида и выделяли в виде светло-желтого твердого вещества (8,0 мг; 46%). MS(m/e): 373,4 (МН+). Пример 14. 1-[5-трет-Бутил-3-(2-хлорбензил)-3 Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил]-3-метилазетидин-3-ол По аналогии со способом, описанным для синтеза 5-трет-бутил-3-(2-хлорбензил)-7-морфолин-4-ил 3 Н-[1,2,3]триазоло[4,5-d]пиримидина (пример 1, стадия с), указанное в заголовке соединение получали из 5-трет-бутил-7-хлор-3-(2-хлорбензил)-3 Н-[1,2,3]триазоло[4,5-d]пиримидина и азетидин-3-ола гидрохлорида и выделяли в виде белого твердого вещества (10,3 мг; 56%). MS(m/e): 387,4 (МН+). Пример 15. 5-трет-Бутил-3-(2-хлорбензил)-7-(3-метоксиазетидин-1-ил)-3 Н-[1,2,3]триазоло[4,5d]пиримидин По аналогии со способом, описанным для синтеза 5-трет-бутил-3-(2-хлорбензил)-7-морфолин-4-ил 3 Н-[1,2,3]триазоло[4,5-d]пиримидина (пример 1, стадия с), указанное в заголовке соединение получали из 5-трет-бутил-7-хлор-3-(2-хлорбензил)-3 Н-[1,2,3]триазоло[4,5-d]пиримидина и 3-метоксиазетидина гидрохлорида и выделяли в виде белого твердого вещества (11,0 мг; 60%). MS(m/e): 387,4 (МН+). Пример 16. 5-трет-Бутил-3-(2-хлорбензил)-7-2R,6S)-2,6-диметил-морфолин-4-ил)-3 Н-[1,2,3]триазоло[4,5-d]пиримидин По аналогии со способом, описанным для синтеза 5-трет-бутил-3-(2-хлорбензил)-7-морфолин-4-ил 3 Н-[1,2,3]триазоло[4,5-d]пиримидина (пример 1, стадия с), указанное в заголовке соединение получали из 5-трет-бутил-7-хлор-3-(2-хлорбензил)-3 Н-[1,2,3]триазоло[4,5-d]пиримидина и (2S,6R)-2,6-диметилморфолина и выделяли в виде белого твердого вещества (13,1 мг; 67%). MS(m/e): 415,5 (МН+). Пример 17. 5-трет-Бутил-3-(2-хлорбензил)-7-(3-метилморфолин-4-ил)-3 Н-[1,2,3]триазоло[4,5d]пиримидин По аналогии со способом, описанным для синтеза 5-трет-бутил-3-(2-хлорбензил)-7-морфолин-4-ил 3 Н-[1,2,3]триазоло[4,5-d]пиримидина (пример 1, стадия с), указанное в заголовке соединение получали из 5-трет-бутил-7-хлор-3-(2-хлорбензил)-3 Н-[1,2,3]триазоло[4,5-d]пиримидина и 3-метилморфолина и выделяли в виде светло-желтой смолы (12,7 мг; 67%). MS(m/e): 401,5 (МН+). Пример 18. 4-[5-трет-Бутил-3-(2-хлорбензил)-3 Н-[1,2,3]триазоло[4,5-d]пиримидин-7-ил]морфолин 2-илметанол По аналогии со способом, описанным для синтеза 5-трет-бутил-3-(2-хлорбензил)-7-морфолин-4-ил 3 Н-[1,2,3]триазоло[4,5-d]пиримидина (пример 1, стадия с), указанное в заголовке соединение получали из 5-трет-бутил-7-хлор-3-(2-хлорбензил)-3 Н-[1,2,3]триазоло[4,5-d]пиримидина и морфолин-2-илметанола и выделяли в виде светло-желтой смолы (11,8 мг; 60%). MS(m/e): 417,5 (МН+). Пример 19. 5-трет-Бутил-3-(2-хлорбензил)-7-тиазолидин-3-ил-3 Н-[1,2,3]триазоло[4,5-d]пиримидин По аналогии со способом, описанным для синтеза 5-трет-бутил-3-(2-хлорбензил)-7-морфолин-4-ил 3 Н-[1,2,3]триазоло[4,5-d]пиримидина (пример 1, стадия с), указанное в заголовке соединение получали из 5-трет-бутил-7-хлор-3-(2-хлорбензил)-3 Н-[1,2,3]триазоло[4,5-d]пиримидина и тиазолидина и выделяли в виде светло-желтой смолы (10,6 мг; 58%). MS(m/e): 389,4 (МН+). Пример 20. 5-трет-Бутил-3-(2-хлорбензил)-7-тиоморфолин-4-ил-3 Н-[1,2,3]триазоло[4,5-d]пиримидин По аналогии со способом, описанным для синтеза 5-трет-бутил-3-(2-хлорбензил)-7-морфолин-4-ил 3 Н-[1,2,3]триазоло[4,5-d]пиримидина (пример 1, стадия с), указанное в заголовке соединение получали из 5-трет-бутил-7-хлор-3-(2-хлорбензил)-3 Н-[1,2,3]триазоло[4,5-d]пиримидина и тиоморфолина и выделяли в виде светло-желтой смолы (10,2 мг; 54%). MS(m/e): 403,4 (МН+). Пример 21. 5-трет-Бутил-3-(2-хлорбензил)-7-(1,1-диоксо-16-тиоморфолин-4-ил)-3 Н-[1,2,3]триазоло[4,5-d]пиримидин По аналогии со способом, описанным для синтеза 5-трет-бутил-3-(2-хлорбензил)-7-морфолин-4-ил 3 Н-[1,2,3]триазоло[4,5-d]пиримидина (пример 1, стадия с), указанное в заголовке соединение получали из 5-трет-бутил-7-хлор-3-(2-хлорбензил)-3 Н-[1,2,3]триазоло[4,5-d]пиримидина и тиоморфолина 1,1 диоксида и выделяли в виде белого твердого вещества (13,5 мг; 66%). MS(m/e): 435,4 (МН+). Пример 22. 5-трет-Бутил-3-(2-хлорбензил)-7-[1,4]оксазепан-4-ил-3 Н-[1,2,3]триазоло[4,5-d]пиримидин По аналогии со способом, описанным для синтеза 5-трет-бутил-3-(2-хлорбензил)-7-морфолин-4-ил 3 Н-[1,2,3]триазоло[4,5-d]пиримидина (пример 1, стадия с), указанное в заголовке соединение получали из 5-трет-бутил-7-хлор-3-(2-хлорбензил)-3 Н-[1,2,3]триазоло[4,5-d]пиримидина и 1,4-оксазепана гидрохлорида и выделяли в виде белой смолы (12,0 мг; 63%). MS(m/e): 401,5 (МН+). Пример 23. 5-трет-Бутил-3-(2-хлорбензил)-7-(2,2-диметил-морфолин-4-ил)-3 Н-[1,2,3]триазоло[4,5-d]пиримидин По аналогии со способом, описанным для синтеза 5-трет-бутил-3-(2-хлорбензил)-7-морфолин-4-ил 3 Н-[1,2,3]триазоло[4,5-d]пиримидина (пример 1, стадия с), указанное в заголовке соединение получали из 5-трет-бутил-7-хлор-3-(2-хлорбензил)-3 Н-[1,2,3]триазоло[4,5-d]пиримидина и 2,2-диметилморфолина и выделяли в виде бесцветной смолы (13,7 мг; 70%). MS(m/e): 415,4 (МН+). По аналогии со способом, описанным для синтеза 5-трет-бутил-3-(2-хлорбензил)-7-морфолин-4-ил 3 Н-[1,2,3]триазоло[4,5-d]пиримидина (пример 1, стадия с), указанное в заголовке соединение получали из 5-трет-бутил-7-хлор-3-(2-хлорбензил)-3 Н-[1,2,3]триазоло[4,5-d]пиримидина и 3,3-диметилморфолина и выделяли в виде бесцветной смолы (12,5 мг; 64%). MS(m/e): 415,4 (МН+). Пример 25. 5-трет-Бутил-3-(2-хлорбензил)-7-2R,5R)-2,5-диметилпирролидин-1-ил)-3 Н-[1,2,3]триазоло[4,5-d]пиримидин По аналогии со способом, описанным для синтеза 5-трет-бутил-3-(2-хлорбензил)-7-морфолин-4-ил 3 Н-[1,2,3]триазоло[4,5-d]пиримидина (пример 1, стадия с), указанное в заголовке соединение получали из 5-трет-бутил-7-хлор-3-(2-хлорбензил)-3 Н-[1,2,3]триазоло[4,5-d]пиримидина и(2R,5R)-2,5 диметилпирролидина и выделяли в виде бесцветной смолы (11,2 мг; 60%). MS(m/e): 399,4 (МН+). Пример 26. По аналогии со способом, описанным для синтеза 5-трет-бутил-3-(2-хлорбензил)-7-морфолин-4-ил 3 Н-[1,2,3]триазоло[4,5-d]пиримидина (пример 1, стадия с), указанное в заголовке соединение получали из 5-трет-бутил-7-хлор-3-(2-хлорбензил)-3 Н-[1,2,3]триазоло[4,5-d]пиримидина и (S)-пирролидин-3-ола и выделяли в виде бесцветной смолы (12,5 мг; 69%). MS(m/e): 387,3 (МН+). Другие условия: Стадия 1: 5-амино-1-[(2-хлорфенил)метил]триазол-4-карбоксамид В реактор загружали азид натрия (3,36 г; 51,1 ммоль; экв.: 1,05), а затем DMSO (35,2 г; 32,0 мл) и основание Хунига (642 мг; 868 мкл; 4,87 ммоль; экв.: 0,1). Эту суспензию перемешивали в течение 10 мин при 25 С. Затем добавляли по каплям 1-хлор-2-(хлорметил)бензол (8 г; 6,29 мл; 48,7 ммоль; экв.: 1,00) в течение 60 мин (ТК = 25 С) и перемешивали при 25 С до завершения реакции (2 ч). Полученную белую суспензию обрабатывали водой (1,6 г; 1,6 мл) и перемешивали в течение 45 мин при КТ. Эту суспензию фильтровали, и остаток на фильтре промывали с помощью DMSO (17,6 г; 16,0 мл) с получением бесцветного раствора 1-(азидометил)-2-хлорбензола. В раздельный реактор загружали DMSO (17,6 г; 16,0 мл), а затем 32% водный раствор NaOH (6,09 г; 4,51 мл; 48,7 ммоль; экв.: 1,0) и воду (5,00 г; 5,00 мл). Добавляли по каплям раствор, содержащий 2 цианоацетамид (6,2 г; 73,0 ммоль; экв.: 1,50) и DMSO (17,6 г; 16,0 мл), в течение 15 мин при 25 С. Добавляли по каплям полученный ранее раствор азида при 25 С в течение 4 ч. Проводили реакцию еще в течение 15 ч, после чего добавляли по каплям воду (120 г; 120 мл) в течение 10 мин (экзотермический процесс). Полученную суспензию охлаждали до 0 С. Через 1 ч 30 мин при 0 С суспензию фильтровали. Остаток на фильтре промывали водой (40,0 г; 40,0 мл) и высушивали при пониженном давлении 50 С/5 мбар до постоянного веса с получением 10,87 г указанного в заголовке соединения в виде белого порошка. MS(m/e): 251,9 (МН+). Стадия 2: 5-трет-Бутил-3-[(2-хлорфенил)метил]-4 Н-триазоло[4,5-d]пиримидин-7-он 5-Амино-1-(2-хлорбензил)-1 Н-1,2,3-триазол-4-карбоксамид (10,80 г; 42,9 ммоль; экв.: 1,00) суспендировали в N,N-диметилацетамиде (50,2 г; 54,0 мл). Добавляли пиридин (5,1 г; 5,19 мл; 64,4 ммоль; экв.: 1,5), а затем пивалоилхлорид (7,84 г; 8,00 мл; 64,4 ммоль; экв.: 1,5) и реакционную смесь нагревали примерно до 80 С. Проводили реакцию в течение 3 ч (и до полной конверсии исходного вещества в промежуточный продукт), добавляли КНСО 3 (21,6 г; 215 ммоль; экв.: 5,00), и эту суспензию нагревали до температуры перехода (Tj) = 155C в течение 24 ч для превращения промежуточного 1-[(2 хлорфенил)метил]-5-(2,2-диметилпропаноиламино)триазол-4-карбоксамида в продукт. Реакционную смесь охлаждали до КТ и добавляли по каплям воду (254 г; 254 мл) в течение 30 мин. Полученную коричневую суспензию охлаждали до 0 С, перемешивали в течение 1 ч 30 мин и фильтровали. Остаток на фильтре промывали водой (43,2 г; 43,2 мл) и высушивали при 50 С/5 мбар с получением 11 г указанного в заголовке соединения в виде грязно-белого порошка. MS(m/e): 318,0 (МН+). Стадия 3: 5-трет-Бутил-7-хлор-3-[(2-хлорфенил)метил]триазоло[4,5-d]пиримидин В реактор загружали DMF (10,1 г; 10,7 мл; 139 ммоль; экв.: 4,14) и дихлорметан (113 г; 85,6 мл) и этот раствор нагревали до 35 С. Добавляли оксалилхлорид (8,66 г; 5,86 мл; 66,9 ммоль; экв.: 2) в течение 1 ч при 35 С. Через 45 мин при 35 С добавляли светлый мутный раствор 5-трет-бутил-3-(2-хлорбензил)3 Н-[1,2,3]триазоло[4,5-d]пиримидин-7(4 Н)-она (10,7 г; 33,4 ммоль; экв.: 1,00) в дихлорметане (32 мл) иDMF (2 мл) в течение 15 мин при 35 С. Через 4 ч при 35 С реакционную смесь охлаждали до КТ и медленно вносили в холодный (0-5 С) полунасыщенный водный раствор NaHCO3 (160 мл). Органическую фазу отделяли и промывали водой(119 г; 119 мл) и полунасыщенным водным раствором NaCI (119 мл). Органическую фазу высушивали над MgSO4, выпаривали на роторном вакуумном испарителе и высушивали при 50 С/10 мбар с получением 10,89 г указанного в заголовке соединения в виде масла, которое отвердевало при стоянии, давая светло-желтое твердое вещество. MS(m/e): 335,9 (МН+). Стадия 4. (3S)-1-[5-трет-Бутил-3-[(2-хлорфенил)метил]триазоло[4,5-d]пиримидин-7-ил]пирролидин 3-ол 5-трет-Бутил-7-хлор-3-(2-хлорбензил)-3 Н-[1,2,3]триазоло[4,5-d]пиримидин (10 г; 29,7 ммоль; экв.: 1,00) растворяли в ацетонитриле (54,6 г; 70,0 мл). Добавляли по каплям N-этилдиизопропиламин (7,84 г; 10,3 мл; 59,5 ммоль; экв.: 2) в течение 5-10 мин. Через 10 мин при КТ добавляли по каплям раствор (S)пирролидин-3-ола (2,94 г; 2,8 мл; 32,7 ммоль; экв.: 1,1) в ацетонитриле (2,27 г; 2,91 мл) в течение 30 мин при 20 С. Проводили реакцию в течение 2 ч 30 мин, после чего добавляли толуол (86,5 г; 100 мл) и реакционную смесь концентрировали при пониженном давлении для удаления большей части ацетонитрила. Добавляли 10% водный раствор лимонной кислоты (100 мл). Водную фазу отделяли и экстрагировали толуолом (86,5 г; 100 мл). Органические фазы промывали последовательно полунасыщенным водным раствором NaHCO3 (50 мл) и полунасыщенным водным раствором NaCI (50 мл). Органические фазы объединяли, высушивали над MgSO4 и выпаривали на роторном вакуумном испарителе при 45 С/10 мбар. Неочищенный продукт разводили в этаноле (150 мл) и концентрировали при пониженном давлении. Эту процедуру повторяли дважды, чтобы удалить толуол, и получали 11,1 г неочищенного указанного в заголовке соединения в виде светло-желтого твердого вещества/пены. Этот продукт можно кристаллизовать, например, из смеси толуол/гептан или ацетон/вода. Кристаллизация из смеси толуол/н-гептан Неочищенный продукт (1,0 г) растворяли при комнатной температуре в 4 мл толуола. Затем добавляли одной порцией 8 мл н-гептана. В полученный прозрачный светло-желтый раствор вносили затравку(кристаллы для затравки получали путем кристаллизации в пробирке из смеси толуол/н-гептан). Процесс кристаллизации медленно начинался. Через 1 ч при КТ полученную белую суспензию отфильтровывали. Остаток на фильтре промывали н-гептаном и высушивали при пониженном давлении (5-10 мбар) при 50 С в течение ночи, затем при 80 С в течение 8 ч с получением 0,9 г указанного в заголовке соединения. Кристаллизация из смеси ацетон/вода Неочищенный продукт (5,5 г) растворяли при комнатной температуре в 30 мл ацетона. Затем добавляли одной порцией 13,6 мл воды. В полученный прозрачный светло-желтый раствор вносили затравку (кристаллы для затравки получали путем кристаллизации в пробирке из смеси ацетон/вода). Процесс кристаллизации медленно начинался. Перемешивали в течение ночи при КТ, после чего полученную белую суспензию охлаждали до 0 С, перемешивали в течение 2 ч при 0 С и фильтровали. Остаток на фильтре промывали холодной смесью ацетон/вода 1:1 и высушивали при 80 С при пониженном давлении с получением 4,9 г указанного в заголовке соединения. Пример 27. По аналогии со способом, описанным для синтеза 5-трет-бутил-3-(2-хлорбензил)-7-морфолин-4-ил 3 Н-[1,2,3]триазоло[4,5-d]пиримидина (пример 1, стадия с), указанное в заголовке соединение получали из 5-трет-бутил-7-хлор-3-(2-хлорбензил)-3 Н-[1,2,3]триазоло[4,5-d]пиримидина и (R)-пирролидин-3-ола и выделяли в виде бесцветной смолы (11,6 мг; 64%). MS(m/e): 387,3 (МН+). Пример 28. 5-трет-Бутил-3-(2-хлорбензил)-7-(3-метокси-пирролидин-1-ил)-3 Н-[1,2,3]триазоло[4,5d]пиримидин По аналогии со способом, описанным для синтеза 5-трет-бутил-3-(2-хлорбензил)-7-морфолин-4-ил 3 Н-[1,2,3]триазоло[4,5-d]пиримидина (пример 1, стадия с), указанное в заголовке соединение получали из 5-трет-бутил-7-хлор-3-(2-хлорбензил)-3 Н-[1,2,3]триазоло[4,5-d]пиримидина и 3-метоксипирролидина гидрохлорида и выделяли в виде бесцветной смолы (13,2 мг; 70%). MS(m/e): 401,4 (МН+). Пример 29. 5-трет-Бутил-3-(2-хлорбензил)-7-(2,2-диметилпирролидин-1-ил)-3 Н-[1,2,3]триазоло[4,5d]пиримидин По аналогии со способом, описанным для синтеза 5-трет-бутил-3-(2-хлорбензил)-7-морфолин-4-ил 3 Н-[1,2,3]триазоло[4,5-d]пиримидина (пример 1, стадия с), указанное в заголовке соединение получали из 5-трет-бутил-7-хлор-3-(2-хлорбензил)-3 Н-[1,2,3]триазоло[4,5-d]пиримидина и 2-метилпирролидина и выделяли в виде белого твердого вещества (13,2 мг; 70%). MS(m/e): 399,4 (МН+). Пример 30. 5-трет-Бутил-3-(2-хлорбензил)-7-(2-метилпирролидин-1-ил)-3 Н-[1,2,3]триазоло[4,5d]пиримидин
МПК / Метки
МПК: A61P 9/10, A61K 31/519, A61P 27/06, C07D 487/04, A61P 3/10
Метки: каннабиноидного, рецептора, качестве, агонистов, 1,2,3]триазоло[4,5-d]пиримидина, производные
Код ссылки
<a href="https://eas.patents.su/30-23581-proizvodnye-123triazolo45-dpirimidina-v-kachestve-agonistov-kannabinoidnogo-receptora-2.html" rel="bookmark" title="База патентов Евразийского Союза">Производные [1,2,3]триазоло[4,5-d]пиримидина в качестве агонистов каннабиноидного рецептора 2</a>
Предыдущий патент: Производные 2-амино-3-(имидазол-2-ил)пиридин-4-она и их применение в качестве ингибиторов киназы рецептора vegf
Следующий патент: Трубное соединение
Случайный патент: Способ и установка для отливки анодов












