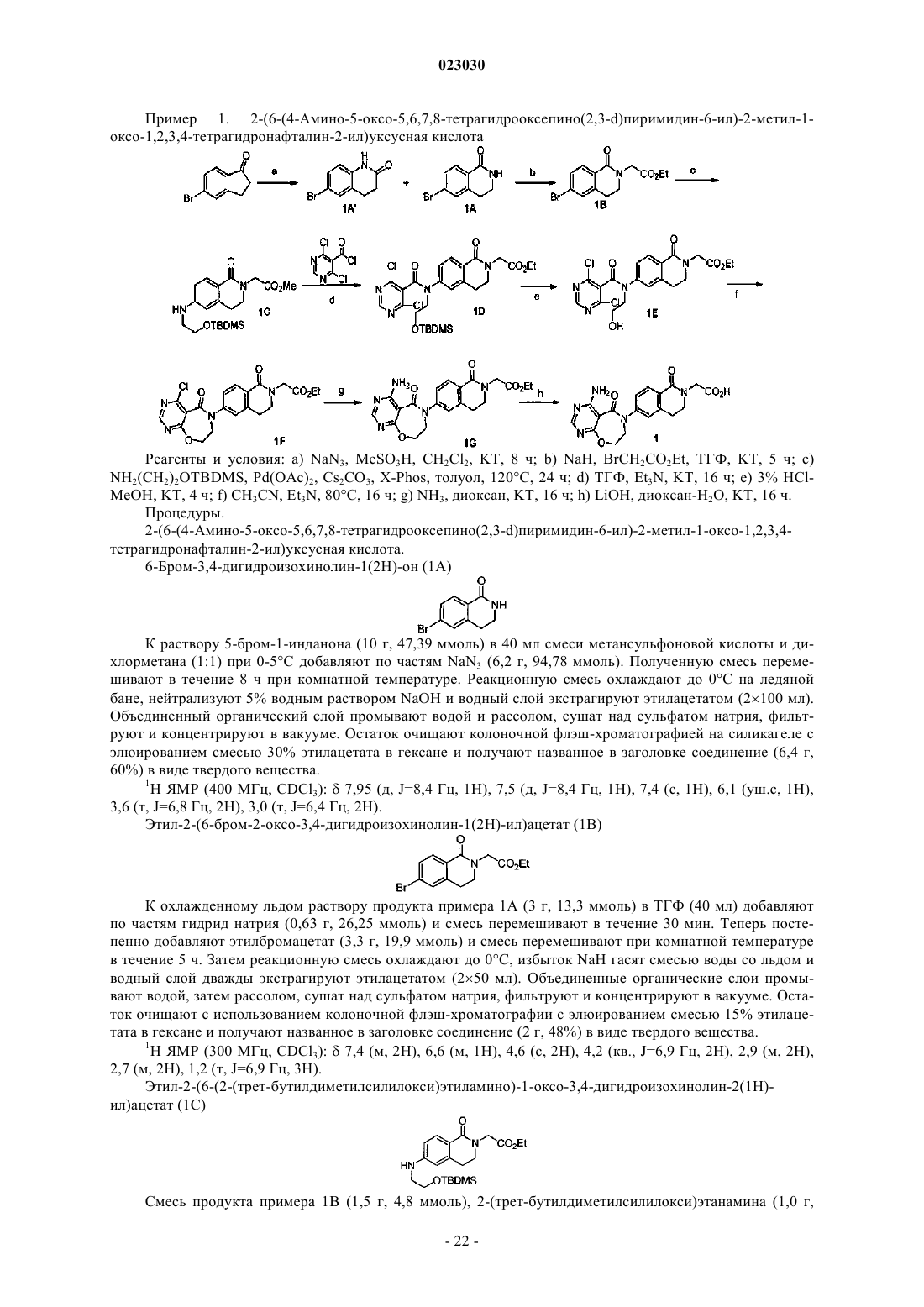
Новые соединения в качестве ингибиторов диацилглицеролацилтрансферазы
Номер патента: 23030
Опубликовано: 29.04.2016
Авторы: Бетхи Сридхар Редди, Чеунг Муи, Цинь Дунхой, Джоши Хемант, Тангирала Рагхурам
Формула / Реферат
1. Соединение формулы (I)
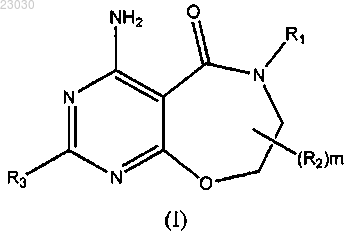
в которой R1 представляет собой 9-11-членную бициклическую систему, включающую 1-4 гетероатома, независимо выбранных из группы, состоящей из N, О и S, при этом указанная бициклическая система может быть замещена 1-3 группами, выбранными из группы, состоящей из (C1-C6)алкила, замещенного (C1-C6)алкила, (C3-C7)циклоалкила, галогена, гидроксила, оксо, -C(O)NRcRd, -COOH, C(O)Ra, -SO2Ra, фенилалкила, -((C1-C3)алкил)фенилокси, фенила, гетероарила и (C1-C4)алкокси,
при этом каждый Ra представляет собой независимо (C1-C6)алкил, замещенный (C1-C6)алкил или незамещенный (C3-C7)циклоалкил;
каждый R2 и R3 представляет собой независимо водород, (C1-C6)алкил, замещенный (C1-C6)алкил, галоген, гидроксил, -C(O)NRcRd, -СООН или (C1-C4)алкокси; и
m равен 0-2;
где любая (C3-C7)циклоалкильная группа выбрана из группы, состоящей из циклопропила, циклобутила, циклопентила, циклогексила и циклогептила;
любая гетероарильная группа выбрана из группы, состоящей из бензофурана, бензотиофена, фурана, имидазола, индола, изотиазола, оксазола, пиразина, пиразола, пиридазина, пиридина, пиримидина, пиррола, хинолина, хиназолина, хиноксалина, тиазола и тиофена;
любой замещенный (C1-C6)алкил замещен 1-3 группами, независимо выбранными из группы, состоящей из незамещенного (C3-C7)циклоалкила, метила, этила, пропила, изопропила, бутила, трет-бутила, дифторметила, трифторметила, галогена, NR'R'', циано, гидроксила, (C1-C4)алкокси, COOH, COO(метила), COO(этила) и C(O)NRcRd, где R' и R", каждый независимо, выбраны из группы, состоящей из водорода, незамещенного (C1-C6)алкила, C(O)Rb и незамещенного (C3-C7)циклоалкила, где Rb представляет собой незамещенный (C1-C6)алкил, (C3-C7)циклоалкил или гетероцикл;
каждый Rc и Rd независимо представляет собой водород или (C1-C6)алкил;
или его фармацевтически приемлемая соль.
2. Соединение по п.1, представленное формулой (I)(А)

при этом А представляет собой 5- или 6-членный гетероцикл, который может содержать 0-3 двойные связи и может быть замещен 1-3 группами, независимо выбранными из группы, состоящей из (C1-C6)алкила, замещенного (C1-C6)алкила, (C3-C7)циклоалкила, галогена, гидроксила, оксо, -C(O)NRcRd, -СООН, -C(O)Ra,
-SO2Ra, фенилалкила, -((C1-C3)алкил)фенилокси, фенила, гетероарила и (C1-C4)алкокси,
при этом каждый Ra представляет собой независимо (C1-C6)алкил, замещенный (C1-C6)алкил или незамещенный (C3-C7)циклоалкил;
каждый R2 и R3 представляет собой независимо водород, (C1-C6)алкил, замещенный (C1-C6)алкил, галоген, гидроксил, -C(O)NRcRd, -СООН или (C1-C4)алкокси;
R4 представляет собой галоген или алкокси;
X представляет собой N или СН;
m равен 0-2;
n равен 0-2;
где любой замещенный (C1-C6)алкил замещен 1-3 группами, независимо выбранными из группы, состоящей из незамещенного (C3-C7)циклоалкила, метила, этила, пропила, изопропила, бутила, трет-бутила, дифторметила, трифторметила, галогена, NR'R'', циано, гидроксила, (C1-C4)алкокси, СООН, COO(метила), COO(этила) и C(O)NRcRd, где R' и R", каждый независимо, выбраны из группы, состоящей из водорода, незамещенного (C1-C6)алкила, C(O)Rb и незамещенного (C3-C7)циклоалкила, где Rb представляет собой незамещенный (C1-C6)алкил, (C3-C7)циклоалкил или гетероцикл;
каждый Rc и Rd независимо представляет собой водород или (C1-C6)алкил;
или его фармацевтически приемлемая соль.
3. Соединение по п.2,
где А представляет собой 5-членный гетероцикл, который может содержать 1 или 2 двойные связи и может быть замещен 1-3 группами, независимо выбранными из группы, состоящей из (C1-C6)алкила, замещенного (C1-C6)алкила, (C3-C7)циклоалкила, галогена, гидроксила, оксо, -C(O)NRcRd, -СООН, -C(O)Ra, -SO2Ra, фенилалкила, -((C1-C3)алкил)фенилокси, фенила, гетероарила и (C1-C4)алкокси,
при этом каждый Ra представляет собой независимо (C1-C6)алкил, замещенный (C1-C6)алкил или незамещенный (C3-C7)циклоалкил;
где любой замещенный (C1-C6)алкил замещен 1-3 группами, независимо выбранными из группы, сосотоящей из незамещенного (C3-C7)циклоалкила, метила, этила, пропила, изопропила, бутила, трет-бутила, дифторметила, трифторметила, галогена, NR'R'', циано, гидроксила, (C1-C4)алкокси, СООН, COO(метила), COO(этила) и C(O)NRcRd, где R' и R", каждый независимо, выбраны из группы, состоящей из водорода, незамещенного (C1-C6)алкила, C(O)Rb и незамещенного (C3-C7)циклоалкила, где Rb представляет собой незамещенный (С1-С6)алкил, (С3-С7)циклоалкил или гетероцикл;
каждый Rc и Rd независимо представляет собой водород или (C1-C6)алкил;
или его фармацевтически приемлемая соль.
4. Соединение по п.2,
где А представляет собой 6-членный гетероцикл, который может содержать 1-3 двойные связи и может быть замещен 1-3 группами, независимо выбранными из группы, состоящей из (C1-C6)алкила, замещенного (C1-C6)алкила, (C3-C7)циклоалкила, галогена, гидроксила, оксо, -C(O)NRcRd, -COOH, C(O)Ra, -SO2Ra, фенилалкила, -((C1-C3)алкил)фенилокси, фенила, гетероарила и (C1-C4)алкокси,
при этом каждый Ra представляет собой независимо (C1-C6)алкил, замещенный (C1-C6)алкил или незамещенный (C3-C7)циклоалкил;
где любой замещенный (C1-C6)алкил замещен 1-3 группами, независимо выбранными из группы, сосотоящей из незамещенного (C3-C7)циклоалкила, метила, этила, пропила, изопропила, бутила, трет-бутила, дифторметила, трифторметила, галогена, NR'R'', циано, гидроксила, (C1-C4)алкокси, COOH, COO(метила), COO(этила) и C(O)NRcRd, где R' и R", каждый независимо, выбраны из группы, состоящей из водорода, незамещенного (C1-C6)алкила, C(O)Rb и незамещенного (C3-C7)циклоалкила, где Rb представляет собой незамещенный (C1-C6)алкил, (C3-C7)циклоалкил или гетероцикл;
каждый Rc и Rd независимо представляет собой водород или (C1-C6)алкил;
или его фармацевтически приемлемая соль.
5. Соединение по любому из пп.2-4,
где m равен 0;
n равен 0;
R3 представляет собой водород;
X представляет собой N;
или его фармацевтически приемлемая соль.
6. Соединение по любому из пп.2-4,
где m равен 0;
n равен 0;
R3 представляет собой водород;
X представляет собой CH;
или его фармацевтически приемлемая соль.
7. Соединение по п.1,
где m равен 0;
R3 представляет собой водород;
R1 представляет собой бициклическую систему, выбранную из группы, состоящей из тетрагидроизохинолинила, тетрагидрохинолинила, индолила, дигидроиндолила, индазолила, дигидроиндазолила, бензотиофенила, бензодиазолила, дигидробензодиазолила, бензимидазолила, индолинила, бензотриазолила, пирролопиридинила, бензотиазолила, бензофуранила, дигидрохиназолинила и пирролопиримидинила;
при этом указанная бициклическая система может быть замещена 1-3 группами, независимо выбранными из группы, состоящей из (C1-C6)алкила, замещенного (C1-C6)алкила, (C3-C7)циклоалкила, галогена, гидроксила, оксо, -C(O)NRcRd, -СООН, -C(O)Ra, -SO2Ra, фенилалкила, -((C1-C3)алкил)фенилокси, фенила, гетероарила и (C1-C4)алкокси,
при этом каждый Ra представляет собой независимо (C1-C6)алкил, замещенный (C1-C6)алкил или незамещенный (C3-C7)циклоалкил;
где любой замещенный (C1-C6)алкил замещен 1-3 группами, независимо выбранными из группы, сосотоящей из незамещенного (C3-C7)циклоалкила, метила, этила, пропила, изопропила, бутила, трет-бутила, дифторметила, трифторметила, галогена, NR'R'', циано, гидроксила, (C1-C4)алкокси, СООН, COO(метила), COO(этила) и C(O)NRcRd, где R' и R", каждый независимо, выбраны из группы, состоящей из водорода, незамещенного (C1-C6)алкила, C(O)Rb и незамещенного (C3-C7)циклоалкила, где Rb представляет собой незамещенный (C1-C6)алкил, (C3-C7)циклоалкил или гетероцикл;
каждый Rc и Rd независимо представляет собой водород или (C1-C6)алкил;
или его фармацевтически приемлемая соль.
8. Соединение по п.7,
где R1 представляет собой бициклическую систему, выбранную из группы, состоящей из тетрагидроизохинолинила, тетрагидрохинолинила, индолила, дигидроиндолила, индазолила, дигидроиндазолила и пирролопиридинила;
при этом указанная бициклическая система может быть замещена 1-3 группами, независимо выбранными из группы, состоящей из (C1-C6)алкила, замещенного (C1-C6)алкила, (C3-C7)циклоалкила, галогена, гидроксила, оксо, -C(O)NRcRd, -СООН, -C(O)Ra, -SO2Ra, фенилалкила, -((C1-C3)алкил)фенилокси, фенила, гетероарила и (C1-C4)алкокси,
при этом каждый Ra представляет собой независимо (C1-C6)алкил, замещенный (C1-C6)алкил или незамещенный (C3-C7)циклоалкил;
где любой замещенный (C1-C6)алкил замещен 1-3 группами, независимо выбранными из группы, состоящей из незамещенного (C3-C7)циклоалкила, метила, этила, пропила, изопропила, бутила, трет-бутила, дифторметила, трифторметила, галогена, NR'R'', циано, гидроксила, (C1-C4)алкокси, СООН, COO(метила), COO(этила) и C(O)NRcRd, где R' и R", каждый независимо, выбраны из группы, состоящей из водорода, незамещенного (C1-C6)алкила, C(O)Rb и незамещенного (C3-C7)циклоалкила, где Rb представляет собой незамещенный (C1-C6)алкил, (C3-C7)циклоалкил или гетероцикл;
каждый Rc и Rd независимо представляет собой водород или (C1-C6)алкил;
или его фармацевтически приемлемая соль.
9. Соединение по п.1, выбранное из группы, состоящей из
2-(6-{4-амино-5-оксо-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-6-ил}-1-оксо-1,2,3,4-тетрагидроизохинолин-2-ил)уксусной кислоты;
этил-2-(6-{4-амино-5-оксо-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-6-ил}-2-оксо-1,2,3,4-тетрагидрохинолин-1-ил)ацетата;
2-(6-{4-амино-5-оксо-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-6-ил}-2-оксо-1,2,3,4-тетрагидрохинолин-1-ил)уксусной кислоты;
этил-2-(6-{4-амино-5-оксо-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-6-ил}-1-оксо-1,2,3,4-тетрагидроизохинолин-2-ил)ацетата;
6-{4-амино-5-оксо-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-6-ил}-1-метил-1,2,3,4-тетрагидрохинолин-2-она;
6-{4-амино-5-оксо-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-6-ил}-2-метил-1,2,3,4-тетрагидроизохинолин-1-она;
6-{4-амино-5-оксо-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-6-ил}-2-бензил-1,2,3,4-тетрагидроизохинолин-1-она;
6-{4-амино-5-оксо-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-6-ил}-2-пропил-1,2,3,4-тетрагидроизохинолин-1-она;
6-{4-амино-5-оксо-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-6-ил}-1-пропил-1,2,3,4-тетрагидрохинолин-2-она;
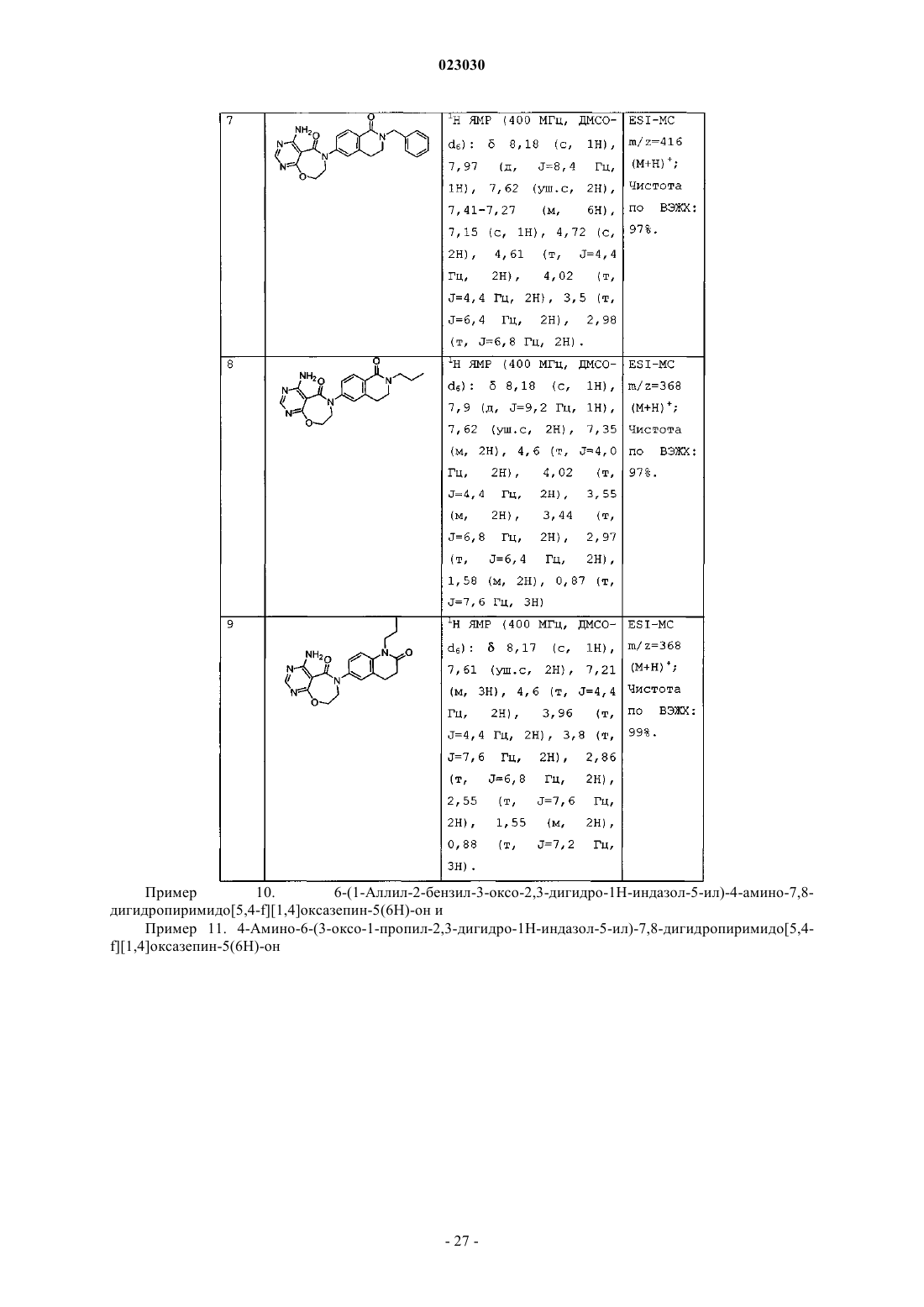
5-{4-амино-5-оксо-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-6-ил}-2-бензил-1-(проп-2-ен-1-ил)-2,3-дигидро-1Н-индазол-3-она;
5-{4-амино-5-оксо-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-6-ил}-1-пропил-2,3-дигидро-1Н-индазол-3-она;
4-амино-6-(1-пропил-1Н-индол-5-ил)-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
4-амино-6-(1-пропил-1Н-индазол-5-ил)-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
4-амино-6-(1-бензотиофен-5-ил)-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
5-{4-амино-5-оксо-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-6-ил}-1,3-дипропил-2,3-дигидро-1Н-1,3-бензодиазол-2-она;
4-амино-6-(2-пропил-2Н-индазол-5-ил)-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
4-амино-6-(1,3-бензотиазол-6-ил)-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
5-{4-амино-5-оксо-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-6-ил}-1-пропил-2,3-дигидро-1H-индол-2,3-диона;
4-амино-6-(1-бензофуран-5-ил)-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
4-амино-6-(1-циклопропил-1,2,3,4-тетрагидрохинолин-6-ил)-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
4-амино-6-(2-пропил-1,2,3,4-тетрагидроизохинолин-6-ил)-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
4-амино-6-[1-(2,2-дифторэтил)-1,2,3,4-тетрагидрохинолин-6-ил]-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
5-{4-амино-5-оксо-5Н,6Н,7Н,8Н-оксепино[2,3-d]пиримидин-6-ил}-1-(пропан-2-ил)-2,3-дигидро-1Н-индазол-3-она;
5-{4-амино-5-оксо-5Н,6Н,7Н,8Н-оксепино[2,3-d]пиримидин-6-ил}-1-(2-метоксиэтил)-2,3-дигидро-1Н-индазол-3-она;
5-{4-амино-5-оксо-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-6-ил}-1-(2,2-дифторэтил)-2,3-дигидро-1Н-индазол-3-она;
5-{4-амино-5-оксо-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-6-ил}-1-циклопропил-2,3-дигидро-1Н-индазол-3-она;
6-амино-4-(1-пропил-1Н-1,3-бензодиазол-5-ил)-2,3,4,5-тетрагидро-1,4-бензоксазепин-5-она;
4-амино-6-(1-пропил-1Н-1,3-бензодиазол-6-ил)-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
4-амино-6-(2-пропил-2Н-1,2,3-бензотриазол-5-ил)-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
4-амино-6-(1-пропил-1Н-1,2,3-бензотриазол-6-ил)-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
4-амино-6-(2-метил-1Н-1,3-бензотиазол-5-ил)-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
4-амино-6-[1-(2,2-дифторэтил)-1Н-пирроло[2,3-b]пиридин-5-ил]-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
4-амино-6-{1-циклопропил-1Н-пирроло[2,3-b]пиридин-5-ил}-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
4-амино-6-[1-(циклопропилметил)-1Н-индол-5-ил]-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
3-(5-{4-амино-5-оксо-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-6-ил}-1Н-индол-1-ил)пропановой кислоты;
4-амино-6-[1-(циклогексилметил)-1Н-индол-5-ил]-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
4-амино-6-[1-(пентан-3-ил)-1Н-индол-5-ил]-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
4-амино-6-{1-[(4-метоксифенил)метил]-1Н-индол-5-ил}-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
4-амино-6-{1-[(4-фторфенил)метил]-1Н-индол-5-ил}-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
4-амино-6-{1-[2-(бензилокси)этил]-1Н-индол-5-ил}-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
4-амино-6-(1-бензил-1Н-индол-5-ил)-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
4-амино-6-[1-(3-метоксипропил)-1Н-индол-5-ил]-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
4-амино-6-[1-(2,2-дифторэтил)-1Н-индол-5-ил]-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
4-амино-6-(1-метил-1Н-индол-5-ил)-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
4-амино-6-[1-(2-метоксиэтил)-1Н-индол-5-ил]-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
4-амино-6-[1-(пропан-2-ил)-1Н-индол-5-ил]-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
4-амино-6-(1H-индол-5-ил)-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
4-амино-6-(1-пропил-2,3-дигидро-1Н-индол-5-ил)-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
4-амино-6-(2,3-дигидро-1Н-индол-5-ил)-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
4-амино-6-[1-(2-метоксиэтил)-2,3-дигидро-1Н-индол-5-ил]-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
4-амино-6-(1,2-диметил-1Н-индол-5-ил)-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
4-амино-6-[1-(циклопропилметил)-1Н-пирроло[2,3-b]пиридин-5-ил]-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
4-амино-6-{1-пропил-1Н-пирроло[2,3-b]пиридин-5-ил}-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
4-амино-6-[1-(2-метоксиэтил)-1Н-пирроло[2,3-b]пиридин-5-ил]-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
4-амино-6-[1-(циклогексилметил)-1Н-пирроло[2,3-b]пиридин-5-ил]-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
4-амино-6-{1-циклогексил-1H-пирроло[2,3-b]пиридин-5-ил}-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
4-амино-6-[1-(пропан-2-ил)-1Н-пирроло[2,3-b]пиридин-5-ил]-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
4-амино-6-[1-(2-гидроксиэтил)-1Н-пирроло[2,3-b]пиридин-5-ил]-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
4-амино-6-(1-метансульфонил-1Н-индол-5-ил)-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
4-амино-6-(1-циклопропил-1Н-индол-5-ил)-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
5-{4-амино-5-оксо-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-6-ил}-1-пропил-1Н-индол-2-карбоновой кислоты;
4-амино-6-[1-пропил-3-(трифторацетил)-1Н-индол-5-ил]-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
4-амино-6-[1-пропил-3-(1,1,1-трифтор-2-метоксипропан-2-ил)-1H-индол-5-ил]-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
4-амино-6-(1-фенил-1Н-индол-5-ил)-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
4-амино-6-{[1-(4-трифторметил)фенил]-1H-пирроло[2,3-b]пиридин-5-ил}-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
4-амино-6-[1-(4-трифторфенил)-1Н-пирроло[2,3-b]пиридин-5-ил]-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
4-амино-6-[1-(3-хлорфенил)-1H-пирроло[2,3-b]пиридин-5-ил]-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
4-амино-6-[1-(3-хлорфенил)-1Н-индол-5-ил]-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
4-амино-6-[1-(2-метоксифенил)-1H-пирроло[2,3-b]пиридин-5-ил]-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
4-амино-6-[1-(2-метоксифенил)-1Н-индол-5-ил]-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
4-амино-6-{1-фенил-1Н-пирроло[2,3-b]пиридин-5-ил}-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
4-амино-6-[1-(2-фторфенил)-1Н-пирроло[2,3-b]пиридин-5-ил]-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
4-амино-6-[1-(3,4-дифторфенил)-1Н-индол-5-ил]-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
4-амино-6-[1-(3,4-дифторфенил)-1Н-пирроло[2,3-b]пиридин-5-ил]-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
4-амино-6-[1-(2-фторфенил)-1Н-индол-5-ил]-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
4-амино-6-{1-[4-(трифторметил)фенил]-1Н-индол-5-ил}-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
4-амино-6-[1-(4-хлорфенил)-1Н-пирроло[2,3-b]пиридин-5-ил]-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
4-амино-6-{1-[3-(трифторметил)фенил]-1H-индол-5-ил}-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
4-амино-6-{1-[3-(трифторметил)фенил]-1Н-пирроло[2,3-b]пиридин-5-ил}-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
4-амино-6-[1-(1,3-тиазол-2-ил)-1Н-индол-5-ил]-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
4-амино-6-{1-[6-(трифторметил)пиридин-3-ил]-1Н-индол-5-ил}-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
4-амино-6-[1-(пиридин-2-ил)-1Н-индол-5-ил]-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
4-амино-6-[1-(пиридин-2-ил)-1Н-пирроло[2,3-b]пиридин-5-ил]-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
4-амино-6-[1-(пиразин-2-ил)-1Н-пирроло[2,3-b]пиридин-5-ил]-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
4-амино-6-[1-(пиразин-2-ил)-1Н-индол-5-ил]-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
4-амино-6-{1-[5-(трифторметил)пиридин-2-ил]-1H-индол-5-ил}-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
4-амино-6-{1-[5-(трифторметил)пиридин-2-ил]-1Н-пирроло[2,3-b]пиридин-5-ил}-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
4-амино-6-[1-(1,3-тиазол-2-ил)-1Н-пирроло[2,3-b]пиридин-5-ил]-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
4-амино-6-{1-[6-(трифторметил)пиридин-3-ил]-1Н-пирроло[2,3-b]пиридин-5-ил}-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
4-амино-6-[1-фенил-3-(пропан-2-ил)-1Н-индол-5-ил]-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
4-амино-6-(2-фенил-1-пропил-1Н-индол-5-ил)-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
4-амино-6-(6-фтор-1-фенил-1Н-индол-5-ил)-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
6-{4-амино-5-оксо-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-6-ил}-3-бензил-3,4-дигидрохиназолин-4-она;
6-{4-амино-5-оксо-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-6-ил}-3,4-дигидрохиназолин-4-она;
4-амино-6-(1-бензил-6-фтор-1Н-индол-5-ил)-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
4-амино-6-{5-пропил-5Н-пирроло[3,2-d]пиримидин-2-ил}-5Н,6Н,7Н,8Н-пиримидо[5,4-f][1,4]оксазепин-5-она;
4-амино-6-(1-пропил-1Н-пирроло[3,2-b]пиридин-5-ил)-7,8-дигидропиримидо[5,4-f][1,4]оксазепин-5(6Н)-она;
4-амино-6-(1-(6-метилпиридин-3-ил)-1Н-индол-5-ил)-7,8-дигидропиримидо[5,4-f][1,4]оксазепин-5(6Н)-она;
4-амино-6-(1-(4-(дифторметил)фенил)-1Н-индол-5-ил)-7,8-дигидропиримидо[5,4-f][1,4]оксазепин-5(6Н)-она;
4-амино-6-(1-(4-(дифторметил)фенил)-1Н-пирроло[2,3-b]пиридин-5-ил)-7,8-дигидропиримидо[5,4-f][1,4]оксазепин-5(6Н)-она;
4-амино-6-(1-(4-(трифторметил)пиридин-2-ил)-1Н-пирроло[2,3-b]пиридин-5-ил)-7,8-дигидропиримидо[5,4-f][1,4]оксазепин-5(6Н)-она;
или его фармацевтически приемлемые соли.
10. Способ лечения ожирения, включающий введение человеку, нуждающемуся в этом, эффективного количества соединения или его соли по любому одному из предыдущих пунктов.
11. Фармацевтическая композиция, обладающая DGAT-1 ингибирующей активностью, включающая соединение или его соль по любому из пп.1-9 и фармацевтически приемлемый носитель.
Текст
Данное изобретение относится к новым соединениям, которые являются ингибиторами ацилкофермента А - диацилглицеролацилтрансферазы 1 (DGAT-1), к фармацевтическим композициям, содержащим их, к способам их получения и к их применению в терапии для предупреждения или лечения заболеваний, связанных с дисфункцией DGAT-1 или при которых модуляция активности DGAT-1 может иметь терапевтическое благоприятное действие, включая, но не ограничиваясь перечисленным, ожирение, расстройства, связанные с ожирением, гипертриглицеридемию, гиперлипопротеинемию, хиломикронемию, дислипидемию,неалкогольный стеатогепатит, диабет, инсулинорезистентность, метаболический синдром,заражение вирусом гепатита С и акне или другие расстройства. Цинь Дунхой, Чеунг Муи (US), Джоши Хемант, Тангирала Рагхурам, Бетхи Сридхар Редди (IN) Медведев В.Н. (RU)(71)(73) Заявитель и патентовладелец: ГЛЭКСОСМИТКЛАЙН ИНТЕЛЛЕКЧУАЛ ПРОПЕРТИ (NO.2) ЛИМИТЕД (GB) Область техники, к которой относится изобретение Данное изобретение относится к новым соединениям, которые являются ингибиторами ацилкофермента А-диацилглицеролацилтрансферазы 1 (DGAT-1), к фармацевтическим композициям, содержащим их, к способам их получения и к их применению в терапии для предупреждения или лечения заболеваний, связанных с дисфункцией DGAT-1, или при которых модуляция активности DGAT-1 может иметь терапевтическое благоприятное действие, включая, но не ограничиваясь перечисленным, ожирение, расстройства, связанные с ожирением, гипертриглицеридемию, гиперлипопротеинемию, хиломикронемию,дислипидемию, неалкогольный стеатогепатит, диабет, инсулинорезистентность, метаболический синдром, заражение вирусом гепатита С и акне или другие расстройства. Предпосылки создания изобретения Ожирение является болезненным состоянием, которое достигает эпидемических размеров среди людей во многих странах мира. Это состояние, которое также ассоциируется с или вызывает другие заболевания или состояния, которые нарушают жизнедеятельность и образ жизни. Ожирение признано серьезным фактором риска в случае других заболеваний и состояний, таких как диабет, гипертензия и артериосклероз. Также известно, что повышенная масса тела из-за ожирения может создать нагрузку на суставы, такие как коленные суставы, вызывая артрит, боль и тугоподвижность. Поскольку переедание и ожирение стали такой проблемой для населения в целом, многие люди теперь проявляют интерес к потере массы, снижению массы и поддержанию здоровой массы тела и желательного образа жизни. Одним из подходов к лечению ожирения должно быть уменьшение потребления пищи и/или гиперлипидемии. Предполагается, что молекулы, которые разрабатывают для предупреждения накопления триглицеридов, смогут не только уменьшить ожирение, но также будут оказывать дополнительное благоприятное действие по снижению инсулинорезистентности - первичного фактора,вносящего вклад в развитие диабета. Ацилкофермент А диацилглицеролацилтрансфераза 1 (DGAT-1) является одним из двух известных ферментов DGAT, которые катализируют конечную стадию в синтезе триглицеридов у млекопитающих.DGAT-1 представляет собой фермент, который вовлекается в развитие как диабета, так и инсулинорезистентности. Исследования на мышах с дефицитом DGAT-1 показывают, что недостаток DGAT-1 защищает от инсулинорезистентности и ожирения, см. Chen H.C. et al., J. Clin. Invest., 109(8), 1049-1055(2002). Следовательно, ингибиторы DGAT-1 должны быть применимыми для лечения метаболических расстройств, например ожирения, диабета типа 2 и синдрома инсулинорезистентности (или метаболического синдрома) и других ассоциированных или родственных расстройств и состояний. Сущность изобретения Данное изобретение относится к соединениям формулы (I) в которой R1 представляет собой 9-11-членную бициклическую систему, включающую 1-4 гетероатома, при этом указанная бициклическая система может быть замещена 1-3 группами, выбранными из группы, состоящей из (C1-C6)алкила, замещенного (C1-C6)алкила, (C3-C7)циклоалкила, галогена, гидроксила, оксо, амида, карбоксила, -C(O)Ra, -SO2Ra, арилалкила, -C1-C3)алкил)арилокси, арила, гетероарила и (C1-C4)алкокси,при этом каждый Ra представляет собой независимо (C1-C6)алкил, замещенный (C1-C6)алкил или незамещенный (C3-C7)циклоалкил; каждый R2 и R3 представляет собой независимо водород, (C1-C6)алкил, замещенный (C1-C6)алкил,галоген, гидроксил, амид, карбоксил или (C1-C4)алкокси;m равен 0-2; или их фармацевтически приемлемым солям. Данное изобретение также относится к фармацевтической композиции, включающей соединение формулы (I) и фармацевтически приемлемый носитель. Данное изобретение также относится к способу лечения ожирения, включающему введение человеку, нуждающемуся в этом, эффективного количества соединения формулы (I) или его фармацевтически приемлемой соли в фармацевтической композиции. Подробное описание изобретения Данное изобретение относится к соединениям формулы (I), определенным выше. Данное изобретение также относится к соединениям формулы (I)(А) при этом А представляет собой 5- или 6-членный гетероцикл, который может содержать 0-3 двойные связи и может быть замещен 1-3 группами, выбранными из группы, состоящей из (C1-C6)алкила, замещенного (C1-C6)алкила, (C3-C7)циклоалкила, галогена, гидроксила, оксо, амида, карбоксила, -C(O)Ra,-SO2Ra, арилалкила, -C1-C3)алкил)арилокси, арила, гетероарила и (C1-C4)алкокси,при этом каждый Ra представляет собой независимо (C1-C6)алкил, замещенный (C1-C6)алкил или незамещенный (C3-C7)циклоалкил; каждый R2 и R3 представляет собой независимо водород, (C1-C6)алкил, замещенный (C1-C6)алкил,галоген, гидроксил, амид, карбоксил или (C1-C4)алкокси;R4 представляет собой галоген или алкокси;n равен 0-2; или их фармацевтически приемлемым солям. Данное изобретение также относится к соединениям формулы (I)(А), в которых А представляет собой 5-членный гетероцикл, который может содержать 0-2 двойные связи и может быть замещен 1-3 группами, выбранными из группы, состоящей из (C1-C6)алкила, замещенного (C1-C6)алкила, (C3C7)циклоалкила, галогена, гидроксила, оксо, амида, карбоксила, -C(O)Ra, -SO2Ra, арилалкила, -C1C3)алкил)арилокси, арила, гетероарила и (C1-C4)алкокси,при этом каждый Ra представляет собой независимо (C1-C6)алкил, замещенный (C1-C6)алкил или незамещенный (C3-C7)циклоалкил; каждый R2 и R3 представляет собой независимо водород, (C1-C6)алкил, замещенный (C1-C6)алкил,галоген, гидроксил, амид, карбоксил или (C1-C4)алкокси;R4 представляет собой галоген или алкокси;n равен 0-2; или их фармацевтически приемлемым солям. Данное изобретение также относится к соединениям формулы (I)(А), в которых А представляет собой 6-членный гетероцикл, который может содержать 0-3 двойные связи и может быть замещен 1-3 группами, выбранными из группы, состоящей из (C1-C6)алкила, замещенного (C1-C6)алкила, (C3C7)циклоалкила, галогена, гидроксила, оксо, амида, карбоксила, -C(O)Ra, -SO2Ra, арилалкила, -C1C3)алкил)арилокси, арила, гетероарила и (C1-C4)алкокси,при этом каждый Ra представляет собой независимо (C1-C6)алкил, замещенный (C1-C6)алкил или незамещенный (C3-C7)циклоалкил; каждый R2 и R3 представляет собой независимо водород, (C1-C6)алкил, замещенный (C1-C6)алкил,галоген, гидроксил, амид, карбоксил или (C1-C4)алкокси;R4 представляет собой галоген или алкокси;n равен 0-2; или их фармацевтически приемлемым солям. Данное изобретение также относится к любому из вышеуказанных соединений,в котором m равен 0;X представляет собой N или СН; или его фармацевтически приемлемым солям. Данное изобретение также относится к соединениям формулы (I),в которых m равен 0;R1 представляет собой бициклическую систему, выбранную из группы, состоящей из тетрагидроизохинолинила, тетрагидрохинолинила, индолила, дигидроиндолила, индазолила, дигидроиндазолила,бензотиофенила, бензодиазолила, дигидробензодиазолила, бензимидазолила, индолинила, бензотриазолила, пирролопиридинила, бензотиазолила, бензофуранила, дигидрохиназолинила и пирролопиримидинила; при этом указанная бициклическая система может быть замещена 1-3 группами, выбранными из группы, состоящей из (C1-C6)алкила, замещенного (C1-C6)алкила, (C3-C7)циклоалкила, галогена, гидроксила, оксо, амида, карбоксила, -C(O)Ra, -SO2Ra, арилалкила, -C1-C3)алкил)арилокси, арила, гетероарила и (C1-C4)алкокси,при этом каждый Ra представляет собой независимо (C1-C6)алкил, замещенный (C1-C6)алкил или незамещенный (C3-C7)циклоалкил; или их фармацевтически приемлемым солям. Данное изобретение также относится к соединениям формулы (I),в которых m равен 0;R1 представляет собой бициклическую систему, выбранную из группы, состоящей из тетрагидроизохинолинила, тетрагидрохинолинила, индолила, дигидроиндолила, индазолила, дигидроиндазолила и пирролопиридинила; при этом указанная бициклическая система может быть замещена 1-3 группами,выбранными из группы, состоящей из (C1-C6)алкила, замещенного (C1-C6)алкила, (C3-C7)циклоалкила,галогена, гидроксила, оксо, амида, карбоксила, -C(O)Ra, -SO2Ra, арилалкила, -C1-C3)алкил)арилокси,арила, гетероарила и (C1-C4)алкокси,при этом каждый Ra представляет собой независимо (C1-C6)алкил, замещенный (C1-C6)алкил или незамещенный (C3-C7)циклоалкил; или их фармацевтически приемлемым солям. Данное изобретение также относится к соединениям формулы (I),в которых m равен 0;R1 представляет собой бициклическую систему, выбранную из группы, состоящей из тетрагидроизохинолинила, тетрагидрохинолинила, индолила, дигидроиндолила, индазолила, дигидроиндазолила,бензотиофенила, бензодиазолила, дигидробензодиазолила, бензимидазолила, индолинила, бензотриазолила, пирролопиридинила, бензотиазолила, бензофуранила, дигидрохиназолинила и пирролопиримидинила; при этом указанная бициклическая система может быть замещена 1-3 группами, выбранными из группы, состоящей из арила и гетероарила; или их фармацевтически приемлемым солям. Данное изобретение также относится к соединениям формулы (I)(В) где R1 представляет собой 9-11-членную бициклическую систему, включающую 1-4 гетероатома,при этом указанная бициклическая система может быть замещена 1-3 группами, выбранными из группы,состоящей из (C1-C6)алкила, замещенного (C1-C6)алкила, галогена, гидроксила, оксо, амида, карбоксила и алкокси; каждый R2 и R3 представляет собой независимо водород, (C1-C6)алкил, замещенный (C1-C6)алкил,галоген, гидроксил, амид, карбоксил или алкокси; иm равен 0-2; или их фармацевтически приемлемым солям. Данное изобретение также относится к соединениям формулы (I)(С) где А представляет собой 5- или 6-членный гетероцикл, который может содержать 0-3 двойные связи и может быть замещен 1-3 группами, выбранными из группы, состоящей из (C1-C6)алкила, замещенного (C1-C6)алкила, галогена, гидроксила, оксо, амида, карбоксила и алкокси; каждый R2 и R3 представляет собой независимо водород, (C1-C6)алкил, замещенный (C1-C6)алкил,галоген, гидроксил, амид, карбоксил или алкокси;m равен 0-2; или их фармацевтически приемлемым солям. Данное изобретение также относится к соединениям формулы (I)(С),в которых А представляет собой 5-членный гетероцикл, который может содержать 0-3 двойные связи и может быть замещен 1-3 группами, выбранными из группы, состоящей из (C1-C6)алкила, замещенного (C1-6)алкила, галогена, гидроксила, оксо, амида, карбоксила и алкокси; каждый R2 и R3 представляет собой независимо водород, (C1-C6)алкил, замещенный (C1-6)алкил, галоген, гидроксил, амид, карбоксил или алкокси;m равен 0-2; или их фармацевтически приемлемым солям. Данное изобретение также относится к соединениям формулы (I), (I)(А), (I)(В) или (I)(С), в которыхm равен 0, и R3 представляет собой водород, или их фармацевтически приемлемым солям. Данное изобретение также относится к соединениям, примеры которых приводятся в экспериментальном разделе. К конкретным соединениям по данному изобретению относятся 2-(6-4-амино-5-оксо-5 Н,6 Н,7 Н,8 Н-пиримидо[5,4-f][1,4]оксазепин-6-ил-1-оксо-1,2,3,4 тетрагидроизохинолин-2-ил)уксусная кислота; этил-2-(6-4-амино-5-оксо-5 Н,6 Н,7 Н,8 Н-пиримидо[5,4-f][1,4]оксазепин-6-ил-2-оксо-1,2,3,4 тетрагидрохинолин-1-ил)ацетат; 2-(6-4-амино-5-оксо-5 Н,6 Н,7 Н,8 Н-пиримидо[5,4-f][1,4]оксазепин-6-ил-2-оксо-1,2,3,4 тетрагидрохинолин-1-ил)уксусная кислота; этил-2-(6-4-амино-5-оксо-5 Н,6 Н,7 Н,8 Н-пиримидо[5,4-f][1,4]оксазепин-6-ил-1-оксо-1,2,3,4 тетрагидроизохинолин-2-ил)ацетат; 6-4-амино-5-оксо-5 Н,6 Н,7 Н,8 Н-пиримидо[5,4-f][1,4]оксазепин-6-ил-1-метил-1,2,3,4 тетрагидрохинолин-2-он; 6-4-амино-5-оксо-5 Н,6 Н,7 Н,8 Н-пиримидо[5,4-f][1,4]оксазепин-6-ил-2-метил-1,2,3,4 тетрагидроизохинолин-1-он; 6-4-амино-5-оксо-5 Н,6 Н,7 Н,8 Н-пиримидо[5,4-f][1,4]оксазепин-6-ил-2-бензил-1,2,3,4 тетрагидроизохинолин-1-он; 6-4-амино-5-оксо-5 Н,6 Н,7 Н,8 Н-пиримидо[5,4-f][1,4]оксазепин-6-ил-2-пропил-1,2,3,4 тетрагидроизохинолин-1-он; 6-4-амино-5-оксо-5 Н,6 Н,7 Н,8 Н-пиримидо[5,4-f][1,4]оксазепин-6-ил-1-пропил-1,2,3,4 тетрагидрохинолин-2-он; 5-4-амино-5-оксо-5 Н,6 Н,7 Н,8 Н-пиримидо[5,4-f][1,4]оксазепин-6-ил-2-бензил-1-(проп-2-ен-1-ил)2,3-дигидро-1 Н-индазол-3-он; 5-4-амино-5-оксо-5 Н,6 Н,7 Н,8 Н-пиримидо[5,4-f][1,4]оксазепин-6-ил-1-пропил-2,3-дигидро-1 Ниндазол-3-он; 4-амино-6-(1-пропил-1 Н-индол-5-ил)-5 Н,6 Н,7 Н,8 Н-пиримидо[5,4-f][1,4]оксазепин-5-он; 4-амино-6-(1-пропил-1 Н-индазол-5-ил)-5 Н,6 Н,7 Н,8 Н-пиримидо[5,4-f][1,4]оксазепин-5-он; 4-амино-6-(1-бензотиофен-5-ил)-5 Н,6 Н,7 Н,8 Н-пиримидо[5,4-f][1,4]оксазепин-5-он; 5-4-амино-5-оксо-5 Н,6 Н,7 Н,8 Н-пиримидо[5,4-f][1,4]оксазепин-6-ил-1,3-дипропил-2,3-дигидро 1 Н-1,3-бензодиазол-2-он; 4-амино-6-(2-пропил-2 Н-индазол-5-ил)-5 Н,6 Н,7 Н,8 Н-пиримидо[5,4-f][1,4]оксазепин-5-он; 4-амино-6-(1,3-бензотиазол-6-ил)-5 Н,6 Н,7 Н,8 Н-пиримидо[5,4-f][1,4]оксазепин-5-он; 5-4-амино-5-оксо-5 Н,6 Н,7 Н,8 Н-пиримидо[5,4-f][1,4]оксазепин-6-ил-1-пропил-2,3-дигидро-1 Ниндол-2,3-дион; 4-амино-6-(1-бензофуран-5-ил)-5 Н,6 Н,7 Н,8 Н-пиримидо[5,4-f][1,4]оксазепин-5-он; 4-амино-6-(1-бензил-6-фтор-1 Н-индол-5-ил)-5 Н,6 Н,7 Н,8 Н-пиримидо[5,4-f][1,4]оксазепин-5-он; 4-амино-6-5-пропил-5 Н-пирроло[3,2-d]пиримидин-2-ил-5 Н,6 Н,7 Н,8 Н-пиримидо[5,4f][1,4]оксазепин-5-он; 4-амино-6-(1-пропил-1 Н-пирроло[3,2-b]пиридин-5-ил)-7,8-дигидропиримидо[5,4-f][1,4]оксазепин 5(6 Н)-он; 4-амино-6-(1-(6-метилпиридин-3-ил)-1 Н-индол-5-ил)-7,8-дигидропиримидо[5,4-f][1,4]оксазепин 5(6 Н)-он; 4-амино-6-(1-(4-(дифторметил)фенил)-1 Н-индол-5-ил)-7,8-дигидропиримидо[5,4-f][1,4]оксазепин 5(6 Н)-он; 4-амино-6-(1-(4-(дифторметил)фенил)-1 Н-пирроло[2,3-b]пиридин-5-ил)-7,8-дигидропиримидо[5,4f][1,4]оксазепин-5(6 Н)-он; 4-амино-6-(1-(4-(трифторметил)пиридин-2-ил)-1 Н-пирроло[2,3-b]пиридин-5-ил)-7,8 дигидропиримидо[5,4-f][1,4]оксазепин-5(6 Н)-он или их фармацевтически приемлемые соли. Специалист в данной области техники признает, что соединения по настоящему изобретению могут иметь другие названия, когда используется другая программа наименования соединений. Далее приводятся примеры соединений, которые имеют другие химические названия, указанные ниже в таблице. Данное изобретение также относится к соединениям формулы (I), (I)(А), (I)(В), (I)(С) или любому из соединений, приведенных в качестве примеров, или их фармацевтически приемлемым солям для применения в качестве лекарственного средства. Данное изобретение также относится к соединениям формулы (I), (I)(А), (I)(В), (I)(С) или любому из соединений, приведенных в качестве примеров, или их фармацевтически приемлемым солям для применения при лечении ожирения. Данное изобретение также относится к соединениям формулы (I), (I)(А), (I)(В), (I)(С) или любому из соединений, приведенных в качестве примеров, или их фармацевтически приемлемым солям для применения при получении лекарственного средства для лечения ожирения. Специалисты в данной области техники оценят то, что соединение по настоящему изобретению также можно использовать в форме его фармацевтически приемлемой соли. Типично, но не обязательно, соли по настоящему изобретению являются фармацевтически приемлемыми солями. Соли, охватываемые термином "фармацевтически приемлемые соли", относятся к нетоксичным солям соединений по данному изобретению. Соли раскрытых соединений, содержащие основную аминную или другую основную функциональную группу, могут быть получены любым подходящим способом, известным в технике, включая обработку свободного основания неорганической кислотой, такой как хлористо-водородная кислота, бромисто-водородная кислота, серная кислота, азотная кислота, фосфорная кислота и т.п., или органической кислотой, такой как уксусная кислота, трифторуксусная кислота, малеиновая кислота, янтарная кислота, миндальная кислота, фумаровая кислота, малоновая кислота, пировиноградная кислота, щавелевая кислота, гликолевая кислота, салициловая кислота,пиранозидиловая кислота, такая как глюкуроновая кислота или галактуроновая кислота, альфагидроксикислота, такая как лимонная кислота или винная кислота, аминокислота, такая как аспарагиновая кислота или глутаминовая кислота, ароматическая кислота, такая как бензойная кислота или коричная кислота, сульфоновая кислота, такая как п-толуолсульфоновая кислота, метансульфоновая кислота,этансульфоновая кислота или подобная кислота. Примеры фармацевтически приемлемых солей включают сульфаты, пиросульфаты, бисульфаты, сульфиты, бисульфиты, фосфаты, хлориды, бромиды, иодиды,ацетаты, пропионаты, деканоаты, каприлаты, акрилаты, формиаты, изобутираты, капроаты, гептаноаты,пропиолаты, оксалаты, малонаты, сукцинаты, субераты, себацаты, фумараты, малеаты, бутин-1,4-диоаты,гексен-1,6-диоаты, бензоаты, хлорбензоаты, метилбензоаты, динитробензоаты, гидроксибензоаты, метоксибензоаты, фталаты, фенилацетаты, фенилпропионаты, фенилбутираты, цитраты, лактаты, гидроксибутираты, гликоляты, тартраты, манделаты и сульфонаты, такие как ксилолсульфонаты, метансульфонаты, пропансульфонаты, нафталин-1-сульфонаты и нафталин-2-сульфонаты. Соли раскрытых соединений, содержащих карбоксильную или другую кислотную функциональную группу, могут быть получены взаимодействием с подходящим основанием. Такая фармацевтически приемлемая соль может быть получена с основанием, которое дает фармацевтически приемлемый катион, и к такой соли относятся соли щелочных металлов (в частности, натрия и калия), соли щелочно-земельных металлов (в частности, кальция и магния), соли алюминия и аммониевые соли, а также соли, полученные с физиологически приемлемыми органическими основаниями, такими как триметиламин, триэтиламин,морфолин, пиридин, пиперидин, пиколин, дициклогексиламин, N,N'-дибензилэтилендиамин, 2- 10023030 гидроксиэтиламин, бис-(2-гидроксиэтил)амин, три(2-гидроксиэтил)амин, прокаин, дибензилпиперидин,дегидроабиетиламин, N,N'-бисдегидроабиетиламин, глюкамин, N-метилглюкамин, коллидин, холин, хинин, хинолин и основные аминокислоты, такие как лизин и аргинин. Другие соли, которые не являются фармацевтически приемлемыми солями, могут применяться при получении соединений по данному изобретению и должны рассматриваться как образующие еще один аспект изобретения. Такие соли, такие как оксалат или трифторацетат, которые сами по себе не являются фармацевтически приемлемыми, могут применяться при получении солей, применимых в качестве промежуточных соединений при получении соединений по изобретению и их фармацевтически приемлемых солей. Используемый в данном описании термин "соединение формулы (I)" относится к одному или нескольким соединениям, соответствующим формуле (I). Соединение формулы (I) может существовать в твердой или жидкой форме. В твердом состоянии оно может существовать в кристаллической или некристаллической форме или в виде их смеси. Для специалиста в данной области техники будет очевидно,что кристаллические или некристаллические соединения могут образовывать фармацевтически приемлемые сольваты. В кристаллических сольватах молекулы растворителя включаются в кристаллическую решетку во время кристаллизации. Сольваты могут включать неводные растворители, такие как, но без ограничения, этанол, изопропанол, ДМСО, уксусная кислота, этаноламин или этилацетат, или они могут включать воду в качестве растворителя, которая включена в кристаллическую решетку. Сольваты, в которых растворителем, включенным в кристаллическую решетку, является вода, обычно называют "гидратами". Гидраты включают стехиометрические гидраты, а также составы, содержащие различные количества воды. Изобретение включает все такие сольваты. Специалисты в данной области техники также признают, что некоторые соединения по изобретению, которые существуют в кристаллической форме, включая их различные сольваты, могут проявлять полиморфизм (т.е. способность существовать в различных кристаллических структурах). Такие различные кристаллические формы обычно известны как "полиморфы". Изобретение включает все такие полиморфы. Полиморфы имеют одинаковый химический состав, но различаются по упаковке, геометрическому расположению и другим свойствам, описывающим кристаллическое твердое состояние. Следовательно, полиморфы могут иметь различные физические свойства, такие как форма, плотность, твердость,деформируемость, устойчивость и растворимость. Полиморфы обычно показывают различные температуры плавления, ИК-спектры и дифрактограммы, что можно использовать для идентификации. Специалисты в данной области техники признают, что различные полиморфы можно получить, например, путем изменения или подгонки условий реакции или реагентов, используемых при получении соединений. Например, к полиморфам могут привести изменения температуры, давления или замена растворителя. Кроме того, в определенных условиях один полиморф может самопроизвольно превращаться в другой полиморф. Соединение формулы (I) или его соль могут существовать в стереоизомерных формах (например,когда содержат один или несколько асимметричных атомов углерода). Отдельные стереоизомеры (энантиомеры и диастереомеры) и их смеси включены в объем настоящего изобретения. Также понятно, что соединение формулы (I) или его соль могут существовать в таутомерных формах иных, чем показанные в формулах, и такие формы также входят в объем настоящего изобретения. Следует иметь в виду, что настоящее изобретение включает все комбинации и подгруппы определенных групп, определенных в данном описании выше. Объем настоящего изобретения включает смеси стереоизомеров, а также очищенные энантиомеры или энантиомерно/диастереомерно обогащенные смеси. Следует иметь в виду, что настоящее изобретение включает все комбинации и подгруппы определенных групп, определенных в данном описании выше. Объект изобретения также включает соединения, меченные изотопами, которые идентичны соединениям, описанным формулой (I) и другими, но в том случае, когда один или несколько атомов заменены атомами, имеющими атомную массу или массовый номер, отличающиеся от атомной массы или массового номера, обычно встречающихся в природе. Примеры изотопов, которые могут быть включены в соединения по изобретению и их фармацевтически приемлемые соли, включают изотопы водорода, углерода, азота, кислорода, фосфора, серы, фтора, йода и хлора, такие как 2 Н, 3 Н, 11 С, 13 С, 14 С, 15N, 17O,18O, 31 Р, 32 Р, 35S, 18F, 36Cl, 123I и 125I. Соединения по настоящему изобретению и фармацевтически приемлемые соли указанных соединений, которые содержат вышеупомянутые изотопы и/или другие изотопы других атомов, входят в объем настоящего изобретения. Меченные изотопами соединения по настоящему изобретению, например соединения, в которые введены радиоактивные изотопы, такие как 3 Н, 14 С, применимы в анализах лекарственных средств и/или распределения в тканях-субстратах. Изотопы тритированный водород, т.е. 3 Н, и углерод-14, т.е. 14 С, особенно предпочтительны за легкость их получения и детектируемость. Изотопы 11 С и 18F применимы, в частности, в PET (позитронная эмиссионная томография), и изотопы 125I применимы, в частности, в SPECT (эмиссионная компьютерная томография одиночных фотонов), применимых при получении изображения головного мозга. Далее, замена на более тяжелые изотопы, такие как дейтерий, т.е. 2 Н, может дать некоторые терапевтические преимущества, приводящие к большей метабо- 11023030 лической устойчивости, например, возрастанию периода полувыведения in vivo, или уменьшенным требованиям по дозировке, и поэтому могут быть предпочтительны в определенных обстоятельствах. Меченные изотопами соединения формулы I и других формул по изобретению, как правило, могут быть получены путем осуществления процедур, раскрытых ниже на схемах и/или в примерах, путем замены реагента, немеченного изотопами, на легко доступный меченный изотопами реагент. Определения. Термины используются в пределах их принятых значений. Для ясности, но не для ограничения,приводятся определения, следующие далее. Используемый в данном описании, если не указано иное, термин "алкил" (или "алкилен") относится к линейному или разветвленному алкилу, предпочтительно имеющему от одного до двенадцати атомов углерода, который может быть насыщенным или ненасыщенным, включенному в настоящее изобретение. Примеры "алкила", используемого в данном случае, включают метил, этил, пропил, изопропил, изобутил, н-бутил, трет-бутил, изопентил, н-пентил и т.п., а также их замещенные версии. Используемый в данном описании, если не указано иное, термин "замещенный алкил" (или "алкилен") относится к линейному или разветвленному алкилу, предпочтительно имеющему от одного до двенадцати атомов углерода, который может быть насыщенным или ненасыщенным, с несколькими степенями замещения, включенными в настоящее изобретение, предпочтительно, одной, двумя или тремя. Подходящие заместители выбирают из группы, состоящей из ненасыщенного (C3-C7)циклоалкила, метила, этила, пропила, изопропила, бутила, трет-бутила, дифторметила, трифторметила, галогена, амино,замещенного амино, мочевины, циано, гидроксила, алкокси, алкилтио, алкилсульфонила, сульфонамида,группы карбоновой кислоты (например, СООН), сложноэфирной группы (например, метилового эфира,этилового эфира) и карбоксамидной группы. Используемый в данном описании, если не указано иное, термин "замещенный амино" обозначает-NR'R, где каждый из R' и R" выбирают независимо из группы, включающей водород, незамещенный(C1-C6)алкил, ацил, незамещенный (C3-C7)циклоалкил, при этом по меньшей мере один из R' и R" не является водородом. Примеры замещенного амино включают, но не ограничиваются указанным, алкиламино, диалкиламино, ациламино и циклоалкиламино. Используемый в данном описании, если не указано иное, термин "арилокси" относится к группе -О(C1-C6)алкиларил. Примеры -О-(C1-C6)алкиларила включают, но не ограничиваются указанным, фенилметокси, нафтилметокси. Используемый в данном описании, если не указано иное, термин "арилалкил" относится к группе-(C1-C6)алкиларил. Примеры -(C1-C6)алкиларила включают, но не ограничиваются указанным, фенилметил, нафтилметил. Используемый в данном описании, если не указано иное, термин "циклоалкил" относится к незамещенному или замещенному моно- или полициклическому неароматическому насыщенному циклу,который необязательно включает алкиленовый линкер, через который может присоединяться циклоалкил. Подходящие заместители указаны в определении "замещенный". Примеры "циклоалкильных групп" включают, но не ограничиваются указанным, циклопропил, циклобутил, циклопентил, циклогексил,циклогептил и т.п., а также их незамещенные и замещенные версии. Используемый в данном описании, если не указано иное, термин "алкокси" относится к группе-ORa, где Ra представляет собой (C1-C4)алкил или циклоалкил, определенные выше. Используемый в данном описании, если не указано иное, термин "амид" относится к группеC(O)NRcRd, где Rc и Rd представляют собой, каждый независимо, Н или (C1-C6)алкил, или Rc представляет собой остальную часть природной или неприродной аминокислоты. Используемый в данном описании, если не указано иное, термин "гетероцикл" или "гетероциклил" или "гетероциклический" относится к незамещенной и замещенной моно- или полициклической неароматической системе, содержащей один или несколько гетероатомов. Предпочтительные гетероатомы включают N, О и S, в том числе N-оксиды, сульфоксиды и диоксиды. Предпочтительно цикл является 38-членным и является или полностью насыщенным или имеет одну или больше степеней ненасыщенности. В настоящее определение включены несколько степеней замещения. Примеры "гетероциклических" групп включают, но не ограничиваются указанным, тетрагидрофуранил, пиранил, 1,4-диоксанил, 1,3 диоксанил, пиперидинил, пирролидинил, морфолинил, азетидинил, пиперазинил, пирролидинонил, пиперазинонил, пиразолидинил и их различные таутомеры. Используемый в данном описании, если не указано иное, термин "арил", если не определяется иначе, обозначает ароматическую углеводородную циклическую систему. Циклическая система может быть моноциклической или конденсированной полициклической (например, бициклической, трициклической и т.д.), замещенной или незамещенной. Циклическая система С 6, т.е. фенильный цикл, представляет собой подходящую арильную группу. В различных воплощениях полициклический цикл представляет собой бициклическую арильную группу, где подходящие бициклические арильные группы представляют собой группы C8-C12 или C9-C10. Подходящую полициклическую арильную группу представляет собой нафтильный цикл, который имеет 10 атомов углерода. Подходящие заместители для арила описаны ниже в определении "необязательно замещенный". Используемый в данном описании, если не указано иное, термин "гетероарил", если не определяется иначе, обозначает ароматическую циклическую систему, содержащую атом(ы) углерода и по меньшей мере один гетероатом. Гетероарил может быть моноциклическим или полициклическим, замещенным или незамещенным. Моноциклическая гетероарильная группа может иметь 1-4 гетероатома в цикле, в то время как полициклическая гетероарильная группа может содержать 1-10 гетероатома. Полициклический гетероарильный цикл может содержать конденсированные, спиро или мостиковые соединения, например, бициклический гетероарил представляет собой полициклический гетероарил. Бициклические гетероарильные циклы могут содержать от 8 до 12 атомов-членов. Моноциклические гетероарильные циклы могут содержать от 5 до 8 атомов-членов (атомов углерода или гетероатомов). Примеры гетероарильных групп включают, но не ограничиваются указанным, бензофуран, бензотиофен, фуран, имидазол, индол,изотиазол, оксазол, пиразин, пиразол, пиридазин, пиридин, пиримидин, пиррол, хинолин, хиназолин,хиноксалин, тиазол и тиофен. Подходящие заместители для гетероарила описаны ниже в определении"необязательно замещенный". Используемый в данном описании, если не указано иное, термин "циано" относится к группе -CN. Используемый в данном описании, если не указано иное, термин "ацил" относится к группе-C(O)Rb, где Rb представляет собой алкил, циклоалкил или гетероциклил, каждый из которых имеет значения, указанные в данном описании. Используемый в данном описании, если не указано иное, термин "необязательно" означает, что по существу описанное(ые) событие(я) может(могут) или не может(могут) иметь место, и включает как событие(я), которое(ые) происходит(ят), так и событие(я), которое(ые) не происходит(ят). Используемое в данном описании, если не указано иное, выражение "замещенный" или его вариации отмечают необязательное замещение, включая несколько степеней замещения, одной или несколькими группами-заместителями, предпочтительно, одной, двумя или тремя. Выражение не следует интерпретировать как дубликат заместителей, описанных и отображенных в данном описании. Подходящие группы-заместители включают ацил, (C1-C6)алкил, замещенный (C1-C6)алкил, незамещенный (C3C7)циклоалкил, алкилсулльфонил, алкокси, алкоксикарбонил, циано, галоген, мочевину, амид, гидроксил, оксо и нитро. Фармацевтические композиции. Изобретение также относится к фармацевтической композиции (также называемой фармацевтическим препаратом), включающей соединение формулы I или его фармацевтически приемлемую соль и один или несколько эксципиентов (также называемых в области фармации носителями и/или разбавителями). Эксципиенты применимы в том смысле, что являются совместимыми с другими ингредиентами препарата и безвредны для их реципиентов (т.е. пациентов). Согласно другому аспекту изобретение относится к способу получения фармацевтической композиции, включающему смешивание (или подмешивание) соединения формулы I или его соли с по меньшей мере одним эксципиентом. Фармацевтические композиции могут находиться в стандартной лекарственной форме, содержащей предварительно установленное количество активного ингредиента на стандартную дозу. Такая единица может содержать терапевтически эффективную дозу соединения формулы I или его соли или часть терапевтически эффективной дозы, так что несколько стандартных лекарственных форм могут вводиться в данное время для достижения желательной терапевтически эффективной дозы. Предпочтительными стандартными лекарственными формами являются формы, содержащие суточную дозу активного ингредиента или субдозу, как описано выше, или ее соответствующую часть. Кроме того, такие фармацевтические композиции можно получить любым из способов, хорошо известных в технике фармации. Фармацевтические композиции можно адаптировать для введения любым соответствующим путем,например, пероральным (включая трансбуккальный или сублингвальный), ректальным, назальным, местным (включая трансбуккальный, сублингвальный или трансдермальный), вагинальным или парентеральным (включая подкожный, внутримышечный, внутривенный или интрадермальный) путем. Такие композиции можно получить любым из способов, хорошо известных в технике фармации, например,путем приведения в контакт активного ингредиента с эксципиентом(ами). Фармацевтические композиции, когда адаптированы для перорального введения, могут находиться в дискретных единицах, таких как таблетки или капсулы; порошки или гранулы; растворы или суспензии в водных или неводных жидкостях; съедобные пенки или кремы; жидкие эмульсии "масло в воде" или жидкие эмульсии "вода в масле". Соединение или его соль по изобретению или фармацевтическая композиция по изобретению также могут быть включены в состав леденцов, вафель и/или tongue tape для введения как "быстрорастворимого" лекарственного средства. Например, для перорального введения в форме таблетки или капсулы активный компонент лекарственного средства можно объединить с пероральным нетоксичным фармацевтически приемлемым инертным носителем, таким как этанол, глицерин, вода и т.п Порошки или гранулы получают, измельчая соединение до частиц подходящего малого размера и смешивая с соответствующим образом измельченным фармацевтическим носителем, таким как съедобный углевод, такой как, например, крахмал или маннит. Могут также присутствовать корригенты, консерванты, диспергирующие вещества и красители. Капсулы получают, получая порошкообразную смесь, как описано выше, и наполняя желатиновые или нежелатиновые оболочки. Перед операцией наполнения в порошкообразную смесь могут быть добавлены глиданты и смазывающие вещества, такие как коллоидный диоксид кремния, тальк, стеарат магния, стеарат кальция, твердый полиэтиленгликоль. Также может быть добавлено вещество, способствующее рассыпанию, или солюбилизатор для улучшения доступности лекарственного средства, когда капсулу проглатывают. Кроме того, когда желательно или необходимо, в смесь также могут быть включены подходящие связующие вещества, смазывающие вещества, вещества, способствующие рассыпанию, и красители. Подходящие связующие вещества включают крахмал, желатин, природные сахара, такие как глюкоза или бета-лактоза, подслащивающие добавки на основе кукурузы, природные и синтетические смолы,такие как аравийская камедь, трагакант, альгинат натрия, карбоксиметилцеллюлоза, полиэтиленгликоль,воски и подобные вещества. Смазывающие вещества, используемые в таких лекарственных формах,включают олеат натрия, стеарат натрия, стеарат магния, бензоат натрия, ацетат натрия, хлорид натрия и подобные вещества. Вещества, способствующие рассыпанию, включают, без ограничения, крахмал, метилцеллюлозу, агар, бентонит, ксантановую камедь и подобные вещества. Таблетки получают, например, получая порошкообразную смесь, гранулируя или камкуя ее, добавляя смазывающее вещество и вещество, способствующее рассыпанию, и прессуя в таблетки. Порошкообразную смесь получают, смешивая соединение, измельченное подходящим образом, с разбавителем или основой, описанными выше, и, необязательно, со связующим веществом, таким как карбоксиметилцеллюлоза и альгинат, желатин или поливинилпирролидон, замедлителем растворения, таким как парафин, ускорителем всасывания, таким как четвертичная соль, и/или абсорбентом, таким как бентонит,каолин или дикальцийфосфат. Порошкообразную смесь можно гранулировать, смачивая связующим веществом, таким как сироп, крахмальная паста, растительный клей acadia или растворы целлюлозы или полимерных материалов, и продавливая через сито. Как альтернатива грануляции, порошкообразную смесь можно пропустить через таблетирующую машину, и полученный продукт представляет собой несовершенные комки, разрушенные до гранул. Гранулы можно "смазать" для предотвращения прилипания к оформляющим таблетки головкам посредством добавления стеариновой кислоты, соли стеарата,талька или минерального масла. Затем смесь с добавлением смазывающего вещества прессуют в таблетки. Соединение или его соль по настоящему изобретению также можно объединить со свободно текущим инертным носителем и непосредственно спрессовать в таблетки без прохождения стадий гранулирования или комкования. Можно обеспечить прозрачное защитное покрытие, состоящее из тонкой пленки из шеллака, покрытие из сахара или полимерного материала, и отделочное покрытие из воска. В такие покрытия можно добавлять красители для того, чтобы различать различные дозировки. Пероральные жидкие препараты, такие как растворы, сиропы и эликсиры, можно получить в стандартной лекарственной форме так, что данное количество содержит предварительно установленное количество активного ингредиента. Сиропы можно получить, растворяя соединение или его соль по изобретению в соответственно корригированном водном растворе, в то время как эликсиры получают с использованием нетоксичного спиртового носителя. Суспензии можно получить, диспергируя соединение или его соль по изобретению в нетоксичном носителе. Также могут быть добавлены солюбилизаторы и эмульгаторы, такие как этоксилированные изостеариловые спирты и полиоксиэтиленсорбитовые эфиры,консерванты, отдушки, такие как мятное масло, природные подслащивающие вещества, сахарин или другие искусственные подслащивающие вещества, и подобные добавки. В соответствующем случае стандартные лекарственные формы могут быть микроинкапсулированными. Также можно получить препарат с пролонгированным или отсроченным высвобождением лекарственного средства, например, путем нанесения покрытия или заделывая частицы материала в полимеры,воск или подобный материал. В настоящем изобретении предпочтительными для доставки фармацевтической композиции являются таблетки и капсулы. Используемый в данном описании термин "лечение" включает профилактику и относится к облегчению специфического состояния, устранению или снижению одного или нескольких симптомов состояния, замедлению или прекращению развития состояния и предупреждению или отсрочке рецидива состояния у пациента или субъекта, ранее пораженного или с установленным диагнозом заболевания. Профилактику (или предупреждение или отсрочку начала заболевания) типично осуществляют, назначая лекарственное средство так же или подобно тому, как назначалось бы пациенту с развившимся заболеванием или состоянием. Настоящее изобретение относится к способу лечения млекопитающего, в частности, человека,страдающего от ожирения, диабета, гипертензии, депрессии, состояния тревоги, лекарственной зависимости, наркомании или их комбинации. Такое лечение включает стадию введения указанному млекопитающему, в частности, человеку, терапевтически эффективного количества соединения формулы I или его соли. Лечение также может включать стадию введения указанному млекопитающему, в частности человеку, терапевтически эффективного количество фармацевтической композиции, содержащей соединение формулы I или его соль. Используемый в данном описании термин "эффективное количество" обозначает количество лекарственного средства или фармацевтического средства, которое будет приводить к биологической или медицинской реакции ткани или системы животного или человека, которой добивается, например, исследователь или практикующий врач. Термин "терапевтически эффективное количество" обозначает любое количество, которое, при сравнении с соответствующим субъектом, который такое количество не получает, приводит к улучшенному лечению, заживлению, предупреждению или уменьшению интенсивности заболевания, расстройства или побочного действия, или снижению скорости прогрессирования заболевания или расстройства. Термин также включает в свой объем количества, эффективные для усиления нормальной физиологической функции. Для применения в терапии терапевтически эффективные количества соединения формулыI, а также его соли, могут вводиться в виде необработанного химического продукта. Кроме того, активный ингредиент может присутствовать в виде фармацевтической композиции. Хотя возможно, что для применения в терапии терапевтически эффективное количество соединения формулы I или его соли может вводиться в виде необработанного химического продукта, обычно оно присутствует как активный ингредиент фармацевтической композиции или препарата. Точное терапевтически эффективное количество соединения или его соли по изобретению будет зависеть от ряда факторов, включая, но не ограничиваясь указанным, возраст и массу субъекта (пациента),которого лечат, конкретного расстройства, требующего лечения, и его тяжести, природы фармацевтического препарата/композиции и способа введения, и в конечном итоге будет являться предписанием лечащего врача или ветеринара. Типично соединение формулы I или его соль будут назначаться для лечения в интервале примерно от 0,1 до 100 мг/кг массы тела реципиента (пациента, млекопитающего) в сутки, и чаще в интервале примерно от 0,1 до 10 мг/кг массы тела в сутки. Приемлемые суточные дозы могут составлять от примерно 1 до примерно 1000 мг/сутки, и предпочтительно, от примерно 1 до примерно 100 мг/сутки. Такое количество может даваться в одной дозе в сутки или в нескольких (например,двух, трех, четырех пяти или более) субдозах в сутки, так, чтобы общая доза была той же самой. Эффективное количество соли соединения можно определить как часть эффективного количества соединения формулы I самого по себе. Подобные дозировки должны соответствовать в случае лечения (в том числе,профилактики) других состояний, отнесенных в данном описании к подходящим для лечения. Как правило, определение соответствующей дозировки может быть легко выполнено специалистом в области медицины или фармации. Кроме того, настоящее изобретение включает соединение формулы I или его соль или фармацевтическую композицию с ними в сочетании по меньшей мере с одним другим лекарственным средством против ожирения и/или по меньшей мере одним лекарственным средством против диабета. Такие лекарственные средства против ожирения могут включать, например, метформин (или глюкофаг), антагонисты рецептора СВ 1, агонисты GLP-1, опиоидные антагонисты и ингибиторы повторного поглощения нейротрансмиттеров. Когда соединение по изобретению используют в комбинации с другим лекарственным средством против ожирения или лекарственным средством против диабета, специалистам в данной области техники следует признать, что каждое соединение или лекарственное средство в комбинации могут отличаться от случая, когда лекарственное средство или соединение используют одно. Соответствующие дозы будут легко оценены и определены специалистами в данной области техники. Соответствующие дозы соединения формулы I или его соли и другого(их) терапевтически активного(ых) средства(средств) и относительное время введения будут выбираться с целью достижения нужного комбинированного терапевтического действия и согласно компетенции и решению лечащего врача или практикующего врача. Получение соединений. Общие схемы синтеза. Соединения по данному изобретению можно получить различными способами, в том числе, хорошо известными стандартными синтетическими методами. Пояснительные общие схемы синтеза приводятся ниже, и далее в рабочих примерах получают конкретные соединения по изобретению. Специалисту в данной области техники будет понятно, что если заместитель, описанный в данном случае, несовместим с методами синтеза, описанными в данном описании, заместитель может быть защищен подходящей защитной группой, которая устойчива в условиях реакции. Защитную группу можно удалить в подходящий момент в последовательности реакций и получить нужное промежуточное соединение или целевое соединение. На всех схемах, описанных ниже, защитные группы для чувствительных или реакционноспособных групп используются при необходимости согласно общим принципам синтетической химии. С защитными группами работают согласно стандартным методам органического синтеза (T.W. Green andP.G.M. Wuts (1991), Protecting Groups in Organic Synthesis, John WileySons, работа включена как ссылка в связи с защитными группами). Такие группы удаляют на удобной стадии синтеза соединения с использованием способов, которые вполне очевидны для специалистов в данной области техники. Выбор способов, а также условий реакций и порядка их осуществления должен согласовываться с получением соединений по настоящему изобретению. Синтез соединений общей формулы (I) и их фармацевтически приемлемых производных и солей может осуществляться специалистом в данной области техники так, как описано ниже на схемах 1-10. В последующем описании группы имеют значения, указанные для соединений формулы (I) выше, если не указано иное. Исходные материалы являются коммерчески доступными или получаются из коммерчески доступных исходных материалов с использованием способов, известных специалистам в данной области техники.g) NH3, диоксан, KT; h) LiOH, диоксан-H2O, KT. Соединения формулы (I) можно получить так, как поясняется на схеме 1. Промежуточное соединение А можно получить перегруппировкой 5-бром-1-инданона с помощью NaN3 в MeSO3H в растворителях, таких как CH2Cl2. Алкилирование промежуточного соединения А соответствующим алкилгалогенидом, таким как этилбромацетат, в присутствии подходящего основания, такого как NaH, дает промежуточное соединение В. Промежуточное соединение А' также можно алкилировать подобным образом и обработать далее схоже с промежуточным соединением А. Затем промежуточное соединение В можно подвергнуть аминированию в условиях по Бухвальду с использованием соответствующего амина в присутствии таких реагентов, как ацетат палладия, лиганда, такого как X-Phos, и основания, такого как карбонат цезия, в толуоле при 120 С. Затем полученное таким образом промежуточное соединение С можно ввести в сочетание с соответствующим образом замещенным хлорангидридом и получить D. Десилилирование промежуточного соединения D в стандартных условиях в кислой среде ведет к Е, которое затем подвергают реакции замыкания цикла, нагревая реакционную смесь в ацетонитриле при 80 С в присутствии основания, такого как триэтиламин, и получают F. Замена остатка хлора в промежуточном соединении F на аминогруппу путем обработки аммиаком при комнатной температуре приводит к соединениям формулы (I) (1a). Гидролиз сложноэфирной группы в соединении 1 а с помощью основания LiOH дает другое соединение формулы (I) (1b). Схема 2. Реагенты и условия: a) NH2(CH2)2OTBDMS, Pd(OAc)2, Cs2CO3, X-Phos, толуол, 120C; b) ТГФ, Et3N, KT; c) 3% HCl-MeOH, KT; d) CH3CN, Et3N, 80C; e) NH3, диоксан, KT. Соединения формулы (I) также можно получить так, как поясняется на схеме 2. Промежуточное соединение Н можно получить аминированием соответствующего бромзамещенного гетероциклического соединения G подходящим амином с защитной группой в стандартных условиях по Бухвальду. Бромид G или является коммерчески доступным или синтезируется согласно стандартным методам органического синтеза, известным специалистам в данной области техники, с использованием или без соответствующих защитных групп. Затем промежуточный амин Н можно превратить в третичный амид I с помощью соот- 16023030 ветствующим образом замещенного хлорангидрида с использованием триэтиламина в качестве основания. Десилилирование промежуточного соединения I с последующим замыканием цикла полученного спирта J при нагревании в ацетонитриле дает промежуточное соединение K. Замена остатка хлора в промежуточном соединении K на аминогруппу путем обработки аммиаком при комнатной температуре приводит к соединениям формулы (I) (1 с). При необходимости соединение 1 с можно подвергнуть реакции удаления защитной группы из функциональной группы в стандартных условиях для удаления группы,которую вводили во время получения бромида G. Схема 3. Реагенты и условия: a) NH2NH2.H2O, EtOH, 80C; b) аллилбромид, KOH, NaOH, 100 С; с) бензилбромид, NaH, ДМФА, KT; d) Fe/NH4Cl, EtOH-H2O, 85C; e) Br (CH2)2OTBDMS, CH3CN, K2CO3,80 С; f) DCM, Et3N, KT; g) 3% HCl-MeOH, KT; h) CH3CN, Et3N, 80C; i) NH3, диоксан, KT; j) 10% Pd/C,H2, MeOH, KT. Соединения формулы (I) также можно получить так, как поясняется на схеме 3. Коммерчески доступную 2-хлор-5-нитробензойную кислоту L обрабатывают гидразингидратом в кипящем этаноле, и получают индазолон М. Затем промежуточное соединение М защищают двумя группами: сначала аллильной группой по азоту анилина, и получают N, и затем бензильной группой по азоту лактама, и получают О. Затем промежуточное соединение О восстанавливают до соответствующего амина Р в стандартных условиях. Затем анилин Р алкилируют подходящим алкилбромидом, и получают Q, которое затем превращают в третичный амид R с использованием соответствующим образом замещенного хлорангидрида. Десилилирование промежуточного соединения R с последующим замыканием цикла полученного спиртаS при нагревании в ацетонитриле дает промежуточное соединение Т. Замена остатка хлора в промежуточном соединении Т на аминогруппу путем обработки аммиаком при комнатной температуре приводит к соединениям формулы (I) (1d). Удаление бензильной группы от азота лактама соединения 1d с сопутствующим восстановлением олефина в аллильной части дает другое соединение формулы (I) (1 е).DCM, Et3N, KT; c) 3% HCl-MeOH, KT; d) CH3CN, Et3N, 80C; e) NH3, диоксан, KT. Соединения формулы (I) также можно получить так, как поясняется на схеме 4. Соответствующим образом замещенный индол или его производное U можно подвергнуть аминированию в условиях по Бухвальду с использованием соответствующего амина в присутствии таких реагентов, как ацетат палладия, лиганда, такого как X-Phos, и основания, такого как карбонат цезия, в толуоле при 120 С. Затем полученное таким образом промежуточное соединение V можно ввести в сочетание с соответствующим образом замещенным хлорангидридом и получить W. Десилилирование промежуточного соединения W в стандартных условиях в кислой среде ведет к X, которое затем подвергают реакции замыкания цикла,нагревая реакционную смесь в ацетонитриле при 80 С в присутствии основания, такого как триэтиламин,и получают Y. Замена остатка хлора в промежуточном соединении Y на аминогруппу путем обработки аммиаком при комнатной температуре приводит к соединениям формулы (I) (1f). Схема 5. Реагенты и условия: a) R4-Br/R4-I, Cs2CO3, ДМФА, 100 С; b) Cu(I)Br, Cu(OAc)2, K2CO3,NaOH, 140C; с) Cu(I)Br, Cu(OAc)2, K2CO3, NaOH, ДМФА, 110 С; d) R4-B(OH)2, 2,2'-бипиридин, Na2CO3,Cu(OAc)2, DCE, 110C; e) Cs2CO3, ДМФА, 100 С. Соединения формулы (I) также можно получить через промежуточные соединения U, АА и АВ, как поясняется на схеме 5. Соответствующим образом замещенный индол или его производное Z алкилируют с использованием соответствующего алкилбромида R4-Br (или иодида R4-I) или арил/гетероарилбороновой кислоты R4-B(ОН)2, соответственно, в стандартных условиях, и получают промежуточное соединение U с блокированным азотом. Такое соединение можно превратить в соединения формулы (I) 1g, используя такое промежуточное соединение U по схеме 4. Подобным образом Z также можно арилировать в условиях катализирования соединениями меди бромидом меди(I) и ацетатом меди с использованием соответствующим образом замещенного арилиодида с образованием промежуточного соединения АА. Такое промежуточное соединение можно снова трансформировать в соединения формулы (I) (1h) по схеме 4. Промежуточное соединение Z можно обработать 2-хлорзамещенными гетероциклическими соединениями при нагревании в присутствии слабого основания, такого как карбонат цезия. Полученное таким образом промежуточное соединение АВ можно трансформировать в соединения формулы (I) 1i по схеме 4. Схема 6. Реагенты и условия: а) AcOH, 120 С; b) Cu(I)Br, Cu(OAc)2, K2CO3, NaOH, 140C. Соединения формулы (I) также можно синтезировать через промежуточное соединение АЕ, синтез которого показан на схеме 6. Соответствующим образом замещенный фенилгидразин АС нагревают с соответствующим образом -замещенным альдегидом в уксусной кислоте при 120 С, и получают 3 замещенный индол AD. Затем промежуточное соединение AD вводят в сочетание с соответствующим образом замещенным арил- или гетероарилиодидом в условиях катализирования соединениями меди(подобно описанному для синтеза промежуточного соединения АА), и получают промежуточное соединение AE. Затем такое соединение можно подвергнуть синтетической последовательности, схожей с последовательностью на схеме 4, и получить соединения формулы (I) 1j. Схема 7. Реагенты и условия: a) R5-B(OH)2, AcOH, Pd(OAc)2, ацетат меди (II), 25 С; b) R4-Br/R4-I,Cs2CO3, ДМФА, 25 С; с) BBr3, DCM, 0C; d) трифторметансульфоновый ангидрид, Py, DCM, 0 С. Соединения формулы (I) также можно синтезировать через промежуточное соединение AJ, синтез которого описан на схеме 7. Коммерчески доступный 5-метоксииндол AF замещают соответственно группой R5 с использованием R5-замещенной бороновой кислоты в условиях катализирования палалдием, и получают 2-замещенное производное индола AG. Промежуточное соединение AG в свою очередь алкилируют (или арилируют) в стандартных условиях с использованием подходящего алкилирующего агента, такого как R4-бромид (или соответствующий иодид), и получают AH. Деметилирование метоксигруппы трибромидом бора и обработка трифторметансульфоновым ангидридом полученного промежуточного соединения AI дает соответствующим образом замещенное производное индола AJ. Затем полученное промежуточное соединение подвергают различным стадиям синтеза по схеме 4, и получают соединения формулы (I) 1k. Схема 8. Реагенты и условия: а) K-трет-OBu, ДМФА, -20 С; b) 10% Pd/C, этанол, 27 С; с) R4-Br/R4I, Cu(OAc)2, CuBr, K2CO3, NaOH, ДМФА, 80 С. Соединения формулы (I) также можно синтезировать через промежуточное соединение АО, синтез которого описан на схеме 8. Промежуточное соединение AM можно получить реакцией переноса цианометильной группы с использованием такого агента, как AL, при обработке субстрата AK в присутствии сильного основания, такого как трет-бутоксид калия. Затем нитроарен AM можно подвергнуть восстановлению с использованием палладия-на-угле, и полученный переходный анилин конденсируется внутримолекулярно и циклизуется с образованием индола AN, за счет чего теряется эквивалент аммиака. Затем AN можно соответствующим образом алкилировать (или арилировать) в стандартных условиях с образованием АО. Фториндол АО можно провести через стадии, подобные стадиям, описанным на схеме 7 для промежуточного соединения АН, с последующими стадиями по схеме 4, что в итоге ведет к синтезу соединений формулы (I) 11.HCl-MeOH, KT; d) CH3CN, Et3N, 80 С; е) NH3, диоксан, KT; f) ТФК, анизол, 90 С; g) K3PO4 двухосновный, CuI, (1S,2S)-циклогексан-1,2-диамин, 1,4-диоксан, 110 С; h) R4-Br, Cs2CO3, ДМФА, 25 С. На схеме 9 описана другая методология синтеза соединений формулы (I). п-Метоксибензиламин алкилируют TBS-защищенным бромэтанолом в ацетонитриле при нагревании с использованием слабого основания, такого как карбонат калия, и получают вторичный амин AQ. Промежуточное соединение AQ превращают в третичный амин AR после обработки соответствующим образом замещенным хлорангидридом в стандартных условиях. Десилилирование AR в кислой среде с последующей реакцией замыкания цикла в полученном спирте при нагревании в ацетонитриле дает PMB-замещенный оксазепинон AT. Конверсию хлор-группы в AT в амин осуществляют обработкой аммиаком в диоксане, и получают AU. Удаление РМВ-группы в среде с ТФК в присутствии акцептора анизола при 90 С дает ключевое промежуточное соединение AV. Затем оксазепинон AT вводят в сочетание с соответствующим образом замещенным 5-хлориндолом АХ в условиях катализирования соединениями меди, и получают соединения формулы (I) 1m. Само промежуточное соединение АХ можно получить алкилированием 5-хлориндола Схема 10. Реагенты и условия: а) хлорид ди(циклопента-2,4-диен-1-ил)циркония(IV), этоксиэтин,DCM, KT; b) K3PO4 двухосновный, Pd(OAc)2, дициклогексил(2',6'-диметокси[1,1'-бифенил]-2-ил)фосфин,ACN, 80 С; с) АсОН, 140 С. Соединения формулы (I) также можно синтезировать через промежуточные соединения, такие какAW, как описано на схеме 10. Различные замещенные индолы, представленные AW, можно синтезировать, исходя из этоксивинилбороната AZ, который сам получают обработкой борана пинаколата AY этоксиэтином в присутствии циркониевого катализатора при комнатной температуре. Затем промежуточное соединение AZ обрабатывают 2,4-дихлорзамещенным анилином в условиях с палладиевым катализатором с использованием подходящего лиганда и основания, такого как дикалийфосфат, и получают анилин ВА. Затем промежуточное соединение ВА нагревают в уксусной кислоте при 140 С, и получают индол AW. Затем промежуточное соединение AW проводят через соответствующие стадии синтеза, описанные на схеме 9, и наконец, получают соединения формулы (I) 1n. Экспериментальный раздел. Приведенные далее примеры поясняют изобретение. Указанные примеры не предназначены для ограничения объема настоящего изобретения, а являются руководством для специалистов в данной области техники по получению и применению соединений, композиций и способов по настоящему изобретению. Хотя описаны конкретные воплощения настоящего изобретения, специалистам будет понятно, что можно осуществить различные изменения и модификации без отхода от сущности и объема изобретения. Если не указано иное, реагенты являются коммерчески доступными, или их получают согласно процедурам, описанным в литературе. Символы и условные обозначения, используемые в описаниях способов,на схемах и в примерах, соответствуют используемым в современной научной литературе, например, вJournal of the American Chemical Society, или в Journal of Biological Chemistry. В примерах. Химические сдвиги выражены в частях на миллион (мд). Константы взаимодействия (J) приводятся в единицах Герц (Гц). Картины расщепления описывают кажущиеся мультиплетности и обозначаются как с (синглет), д (дублет), т (триплет), к (квартет), дд (двойной дублет), дт (тройной дублет), м (мультиплет), уш (уширенный). Колоночную флэш-хроматографию выполняют на силикагеле. Используемыми программами названий соединений являются ACDLABs 11.0 Namebatch, ACD IUPAC или Chem Draw. К раствору 5-бром-1-инданона (10 г, 47,39 ммоль) в 40 мл смеси метансульфоновой кислоты и дихлорметана (1:1) при 0-5 С добавляют по частям NaN3 (6,2 г, 94,78 ммоль). Полученную смесь перемешивают в течение 8 ч при комнатной температуре. Реакционную смесь охлаждают до 0 С на ледяной бане, нейтрализуют 5% водным раствором NaOH и водный слой экстрагируют этилацетатом (2100 мл). Объединенный органический слой промывают водой и рассолом, сушат над сульфатом натрия, фильтруют и концентрируют в вакууме. Остаток очищают колоночной флэш-хроматографией на силикагеле с элюированием смесью 30% этилацетата в гексане и получают названное в заголовке соединение (6,4 г,60%) в виде твердого вещества. 1 К охлажденному льдом раствору продукта примера 1 А (3 г, 13,3 ммоль) в ТГФ (40 мл) добавляют по частям гидрид натрия (0,63 г, 26,25 ммоль) и смесь перемешивают в течение 30 мин. Теперь постепенно добавляют этилбромацетат (3,3 г, 19,9 ммоль) и смесь перемешивают при комнатной температуре в течение 5 ч. Затем реакционную смесь охлаждают до 0 С, избыток NaH гасят смесью воды со льдом и водный слой дважды экстрагируют этилацетатом (250 мл). Объединенные органические слои промывают водой, затем рассолом, сушат над сульфатом натрия, фильтруют и концентрируют в вакууме. Остаток очищают с использованием колоночной флэш-хроматографии с элюированием смесью 15% этилацетата в гексане и получают названное в заголовке соединение (2 г, 48%) в виде твердого вещества. 1 Смесь продукта примера 1 В (1,5 г, 4,8 ммоль), 2-(трет-бутилдиметилсилилокси)этанамина (1,0 г,- 22023030 5,71 ммоль), карбоната цезия (1,87 г, 5,73 ммоль), ацетата палладия (0,11 г, 0,47 ммоль) и X-Phos (0,23 г,0,47 ммоль) в толуоле (15 мл) в атмосфере аргона кипятят с обратным холодильником при 120 С в течение 24 ч. Реакционную смесь охлаждают, смесь разбавляют этилацетатом и промывают водой (210 мл) и насыщенным водным рассолом. Органический слой сушат над сульфатом натрия, фильтруют и концентрируют, получают темное масло. Остаток очищают флэш-хроматографией с использованием смеси 10% этилацетата в гексане и получают названное в заголовке соединение (0,95 г, 48%) в виде твердого вещества. 1 К раствору продукта примера 1 С (0,95 г, 2,33 ммоль) и TEA (1,18 г, 11,67 ммоль) в ТГФ (15 мл) при перемешивании и охлажденнии (0 С) добавляют по каплям раствор 4,6-дихлорпиримидин-5 карбонилхлорида (0,74 г, 3,5 ммоль) в ТГФ (5 мл). Через 16 ч реакционную смесь концентрируют в вакууме, разбавляют этилацетатом и промывают водой (210 мл) и насыщенным водным рассолом. Органический слой сушат над сульфатом натрия, фильтруют, концентрируют в вакууме и получают масло. Остаток очищают флэш-хроматографией с использованием в качестве элюента смеси 12% этилацетата в гексане и получают названное в заголовке соединение (0,75 г, 55%) в виде твердого вещества. 1 Раствор продукта примера 1D (0,75 г, 1,29 ммоль) в метанольном растворе HCl (3 мл концентрированной соляной кислоты в 97 мл метанола) перемешивают при комнатной температуре в течение 4 ч. Метанол удаляют в вакууме. Остаток растворяют в этилацетате и промывают насыщенным водным раствором бикарбоната натрия и насыщением водным рассолом. Органический слой сушат над сульфатом натрия, фильтруют, концентрируют в вакууме и получают названное в заголовке соединение (0,45 г,75%) в виде твердого вещества, которое передают на следующую стадию без дополнительной очистки. 1 Взвесь продукта примера 1E (0,4 г, 0,85 ммоль) и TEA (0,43 г, 4,28 ммоль) в ацетонитриле (10 мл) перемешивают при 80 С в течение 16 ч. Реакционную смесь охлаждают, концентрируют в вакууме и разбавляют этилацетатом. Смесь промывают водой и насыщенным водным рассолом. Органический слой сушат над сульфатом натрия, фильтруют, концентрируют в вакууме и получают названное в заголовке соединение (0,35 г, 95%) в виде белого твердого вещества. 1 Раствор продукта примера 1F (0,3 г, 0,697 ммоль) в 0,5 М растворе аммиака в п-диоксане (10 мл) перемешивают при комнатной температуре в течение 16 ч. Реакционную смесь концентрируют в вакууме и разбавляют этилацетатом. Органический слой промывают водой и насыщенным водным рассолом, сушат над сульфатом натрия, фильтруют и концентрируют в вакууме, и получают названное в заголовке соединение (0,22 г, 70%) в виде белого твердого вещества. 1 Раствор продукта примера 1G (0,18 г, 0,43 ммоль) и гидроксида лития (0,055 г, 1,309 ммоль) в 5 мл смеси п-диоксан-вода (4:1) перемешивают при комнатной температуре в течение 16 ч. После удаления растворителя в вакууме остаток растворяют в воде и промывают этилацетатом. Водный слой подкисляют с использованием 2 н. соляной кислоты до тех пор, пока не достигнут рН 2. Полученный раствор охлаждают до 0 С, образовавшееся твердое вещество отфильтровывают и сушат в вакууме, получают названное в заголовке соединение (0,12 г, 72%) в виде белого твердого вещества. 1H ЯМР (300 МГц, ДМСО-d6):12,8 (уш.с, 1H), 8,45 (уш.с, 2H), 8,36 (с, 1H), 7,9 (д, J=9,0 Гц, 1 Н),7,4 (м, 2H), 4,7 (м, 2H), 4,21 (м, 2 Н), 4,13 (м, 2 Н), 3,64 (т, J=6,3 Гц, 2H), 3,03 (т, J=5,7 Гц, 2 Н); чистота по ВЭЖХ: 99%, m/z=384 (M+H)+. Соединения примеров 2-9 получают способом, описанным выше для примера 1, или его обычными вариациями, исходя из требуемого галогенхинолинона. К раствору 2-хлор-5-нитробензойной кислоты (5 г, 24,8 ммоль) в абсолютном этаноле (30 мл) добавляют гидразингидрат (4 мл, 124 ммоль) и полученную смесь кипятят с обратным холодильником в течение 16 ч. Реакционную смесь концентрируют при пониженном давлении. Остаток растирают в метаноле и получают 6,5 г сырого промежуточного соединения. К сырому продукту добавляют 2 н. соляную кислоту (40 мл) и смесь кипятят с обратным холодильником в течение 8 ч. Реакционную смесь охлаждают до 0 С, твердое вещество собирают фильтрацией, промывают холодной водой и сушат в вакууме. Остаток очищают флэш-хроматографией с использованием в качестве элюента смеси 1% метанола в хлороформе, и получают названное в заголовке соединение (2 г, 27%) в виде твердого вещества. 1 К смеси продукта примера 11 А (4 г, 22,34 ммоль) и 1 н. водного раствора KOH (25 мл) добавляют аллилбромид (2,7 г, 22,34 ммоль) и смесь кипятят с обратным холодильником в течение 2 ч. Добавляют 15% раствор NaOH (2 мл) и аллилбромид (0,54 г, 0,04 ммоль) и смесь снова кипятят с обратным холодильником в течение 1 ч. Реакционную смесь охлаждают до комнатной температуры и нейтрализуют с использованием 3 н. соляной кислоты. Полученное твердое вещество собирают фильтрацией, промывают холодной водой и сушат в вакууме, получают названный в заголовке продукт (4,5 г, 92%) в виде твердого вещества. 1 К охлажденному льдом раствору продукта примера 11 В (2,5 г, 11,4 ммоль) в ДМФА (20 мл) добавляют по частям гидрид натрия (0,55 г, 13,68 ммоль) и смесь перемешивают в течение 30 мин. Теперь постепенно добавляют бензилбромид (3,9 г, 22,8 ммоль) и смесь перемешивают при комнатной температуре в течение 16 ч. Затем реакционную смесь охлаждают до 0 С и реакцию гасят смесью воды со льдом. Водный слой дважды экстрагируют этилацетатом (250 мл). Объединенные органические слои промывают водой, затем рассолом, сушат над сульфатом натрия, фильтруют и концентрируют в вакууме. Остаток очищают колоночной флэш-хроматографией с использованием в качестве элюента смеси 5% этилацетата в гексане и получают названное в заголовке соединение (2,2 г, 62%) в виде твердого вещества. 1 К раствору продукта примера 11 С (2,2 г, 7,11 ммоль) в 80 мл смеси этанол-вода (4:1) добавляют порошок железа (0,77 г, 14,22 ммоль), а затем NH4Cl (0,19 г, 3,55 ммоль) и смесь кипятят с обратным холодильником в течение 4 ч. Растворитель удаляют при пониженном давлении и остаток обрабатывают этилацетатом и водой. Органический слой сушат над сульфатом натрия, фильтруют и концентрируют в вакууме. Остаток очищают флэш-хроматографией с использованием в качестве элюента смеси 20% этилацетата в гексане и получают названное в заголовке соединение в виде твердого вещества (1,6 г, 66%). 1 К смеси (2-бромэтокси)(трет-бутил)диметилсилана (0,92 г, 3,87 ммоль) и продукта примера 11D (0,9 г, 3,22 ммоль) в ацетонитриле (70 мл) добавляют карбонат калия (2,6 г, 19,32 ммоль) и смесь кипятят с обратным холодильником в течение 24 ч. Реакционную смесь охлаждают до комнатной температуры и обрабатывают этилацетатом и водой. Отделенный органический слой промывают рассолом, сушат над сульфатом натрия, фильтруют и концентрируют в вакууме. Остаток очищают флэш-хроматографией с использованием в качестве элюента смеси 15% этилацетата в гексане и получают названное в заголовке соединение (0,35 г, 25%) в виде твердого вещества. 1 К раствору продукта примера 11 Е (0,55 г, 1,23 ммоль) и TEA (0,5 г, 5,0 ммоль) в DCM (12 мл) при перемешивании и охлаждении (0 С) добавляют по каплям раствор 4,6-дихлорпиримидин-5 карбонилхлорида (0,26 г, 1,23 ммоль) в DCM (5 мл). Через 6 ч реакционную смесь концентрируют в вакууме, разбавляют этилацетатом и промывают водой (210 мл) и насыщенным водным рассолом. Органический слой сушат над сульфатом натрия, фильтруют, концентрируют в вакууме и получают масло. Остаток очищают флэш-хроматографией с использованием в качестве элюента смеси 12% этилацетата в гексане и получают названное в заголовке соединение (0,35 г, 46%) в виде масла. 1 Раствор продукта примера 11F (0,35 г, 0,57 ммоль) в метанольном растворе HCl (3 мл концентрированной соляной кислоты в 97 мл метанола) перемешивают при комнатной температуре в течение 1 ч.
МПК / Метки
МПК: C07D 498/04
Метки: новые, диацилглицеролацилтрансферазы, соединения, качестве, ингибиторов
Код ссылки
<a href="https://eas.patents.su/30-23030-novye-soedineniya-v-kachestve-ingibitorov-diacilglicerolaciltransferazy.html" rel="bookmark" title="База патентов Евразийского Союза">Новые соединения в качестве ингибиторов диацилглицеролацилтрансферазы</a>
Предыдущий патент: Способ получения 2-этокси-1-((2′-((гидроксиамино)иминометил)дифенил-4-ил)метил)-1h-бензо[d]имидазол-7-карбоновой кислоты и ее сложных эфиров
Следующий патент: Антиген-связывающая конструкция и ее применение
Случайный патент: 2-амино-3-сульфонилтетрагидропиразоло[1,5-a]пиридопиримидины - антагонисты серотониновых 5-нт6-рецепторов, способы их получения и применения