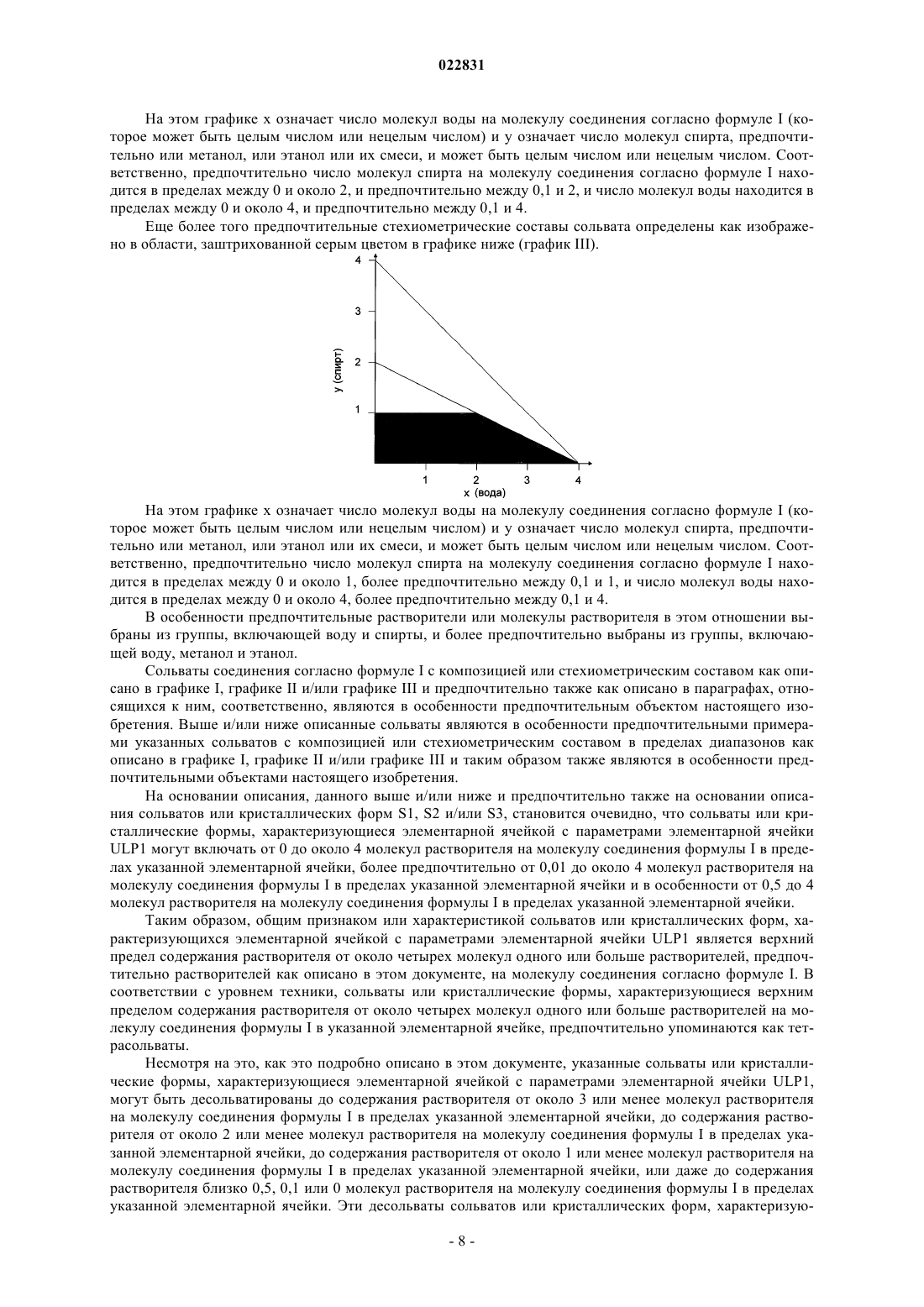
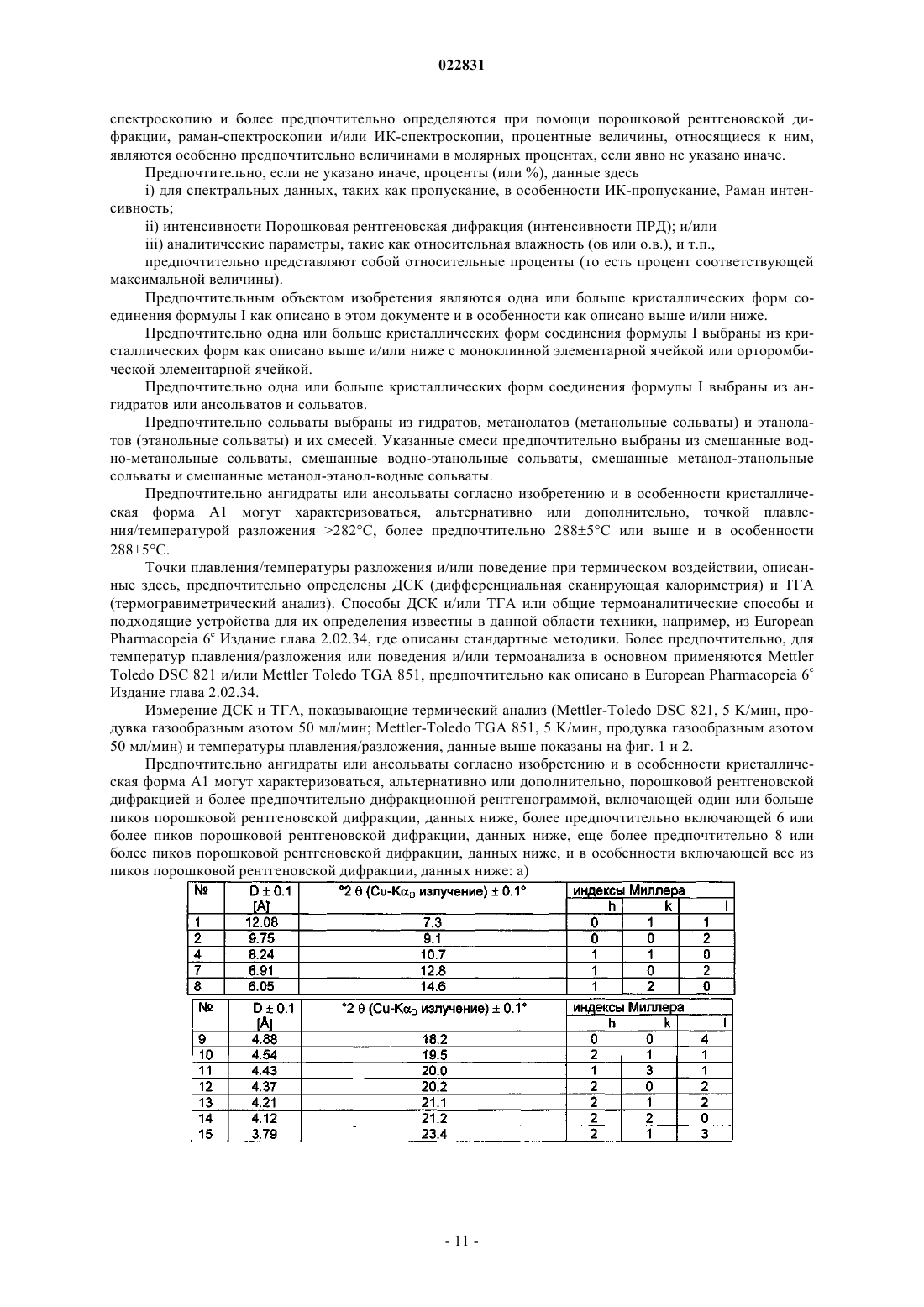
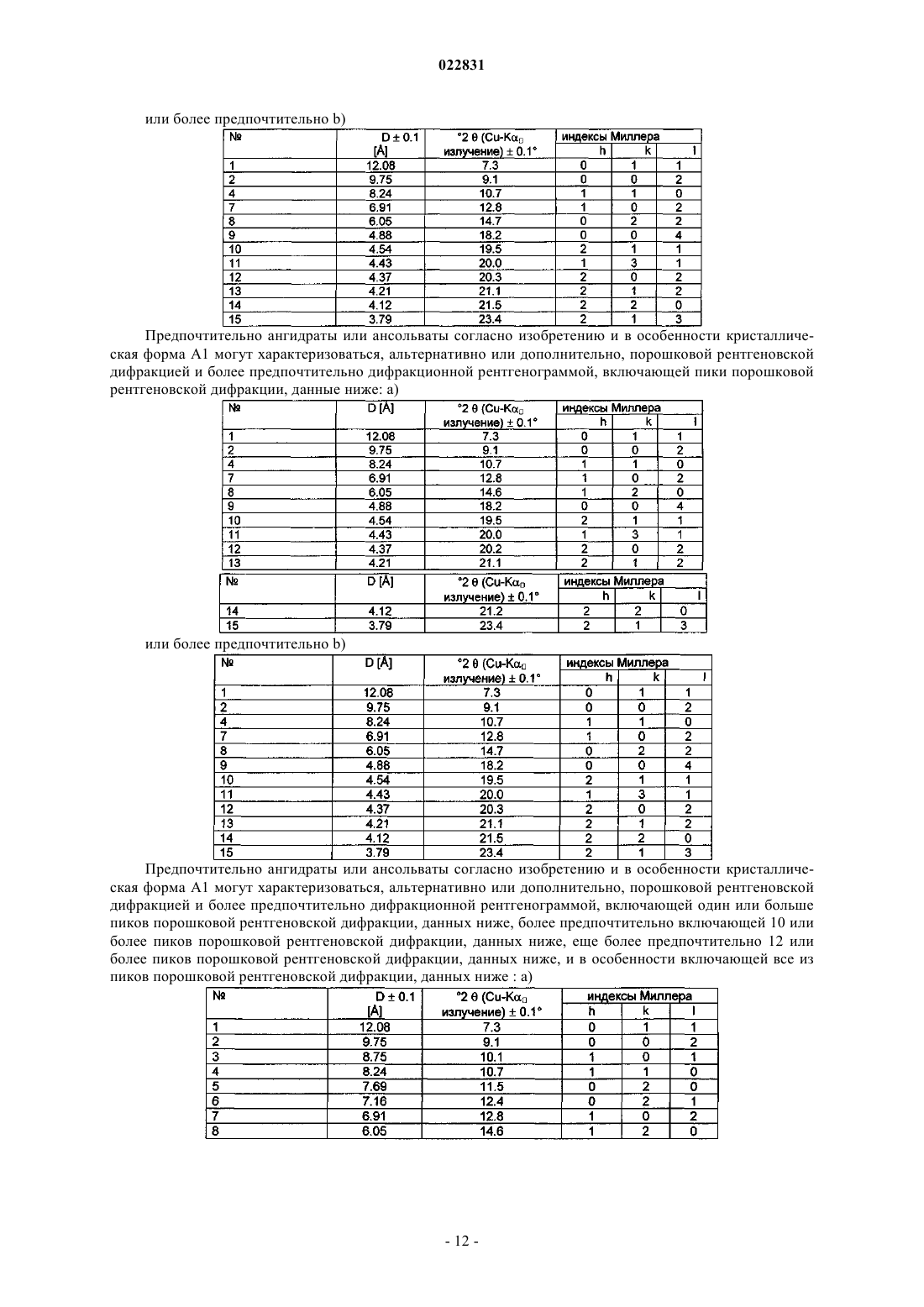
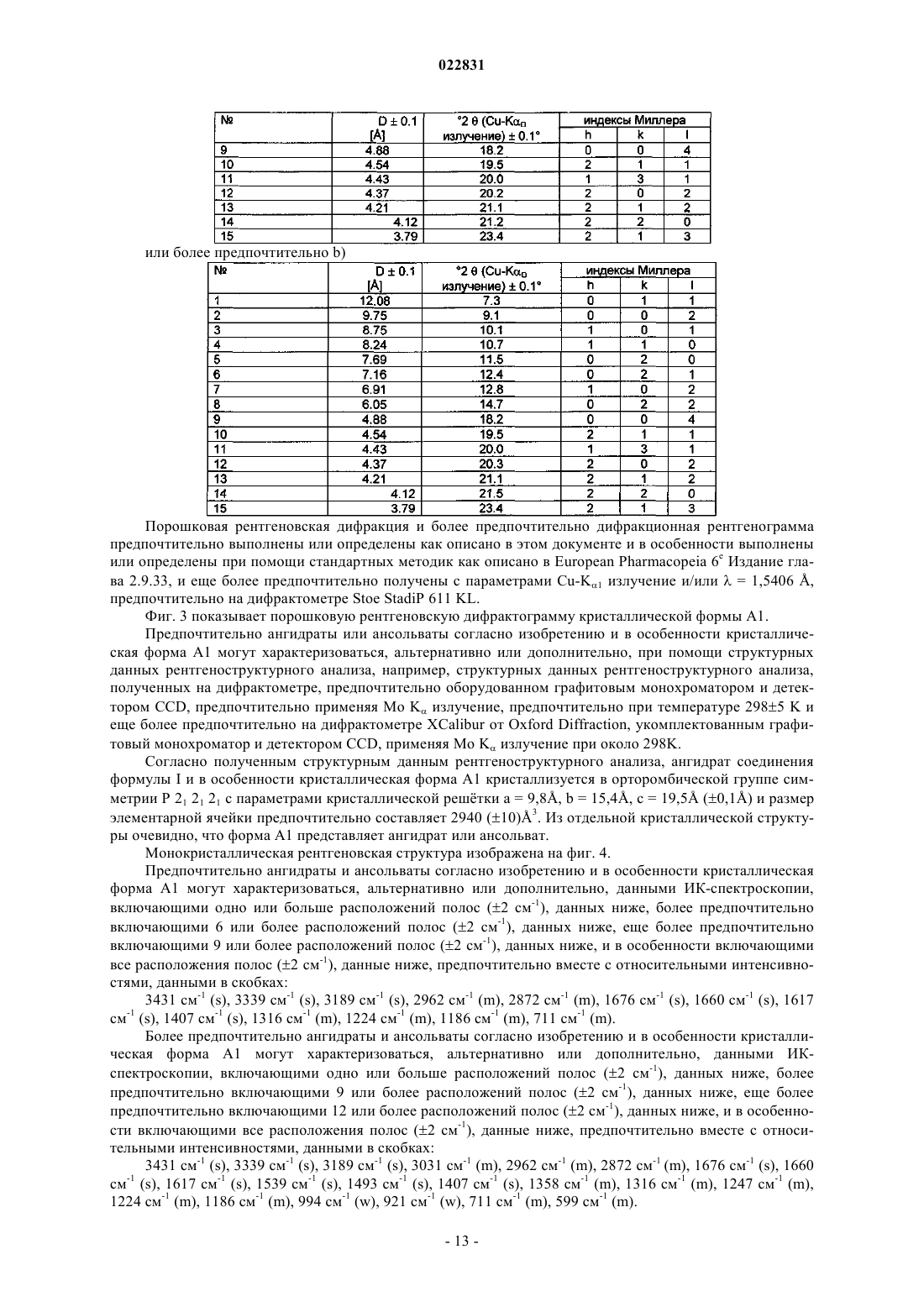
Твердые формы {[(2s,5r,8s,11s)-5-бензил-11-(3-гуанидинопропил)-8-изопропил-7-метил-3,6,9,12,15-пентаоксо-1,4,7,10,13-пентаазациклопентадец-2-ил]уксусной кислоты} и способы их получения
Номер патента: 22831
Опубликовано: 31.03.2016
Авторы: Шольц Геральд, Кюн Клеменс, Унтенеккер Харальд, Земанн Керстин, Ланге Михаэль, Заль Кристоф, Петерзен Зёнке, Йончик Альфред
Формула / Реферат
1. Кристаллическая форма А1 внутренней соли соединения формулы I
где кристаллическая форма А1 характеризуется элементарной ячейкой с параметрами кристаллической решетки а = 9,8±0,1 Å, b = 19,5±0,5 Å и с = 15,4±0,1 Å, c α= β = γ = 90±1°.
2. Кристаллическая форма S1 внутренней соли соединения формулы I
где кристаллическая форма S1 характеризуется элементарной ячейкой с параметрами кристаллической решетки а = 9,4±0,1 Å, b = 25,9±0,5 Å и с = 14,1±0,1 Å, с α = 90±1°, β = 91±1°, γ = 90±1°.
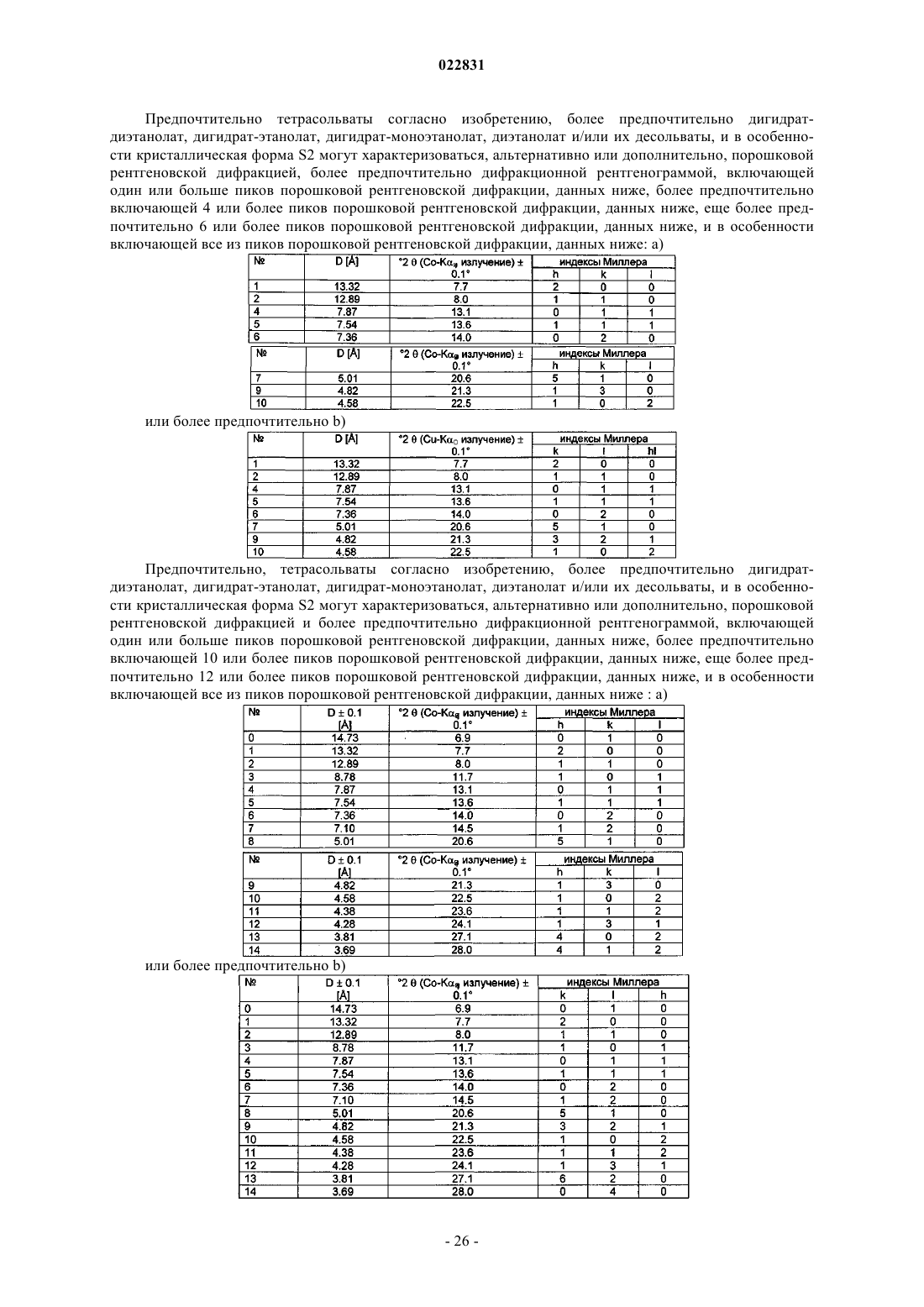
3. Кристаллическая форма S2 внутренней соли соединения формулы I
где кристаллическая форма S2 характеризуется элементарной ячейкой с параметрами кристаллической решетки а = 9,3±0,1 Å, b = 26,6±0,5 Å и с = 14,7±0,1 Å, с α = β = γ = 90±1°.
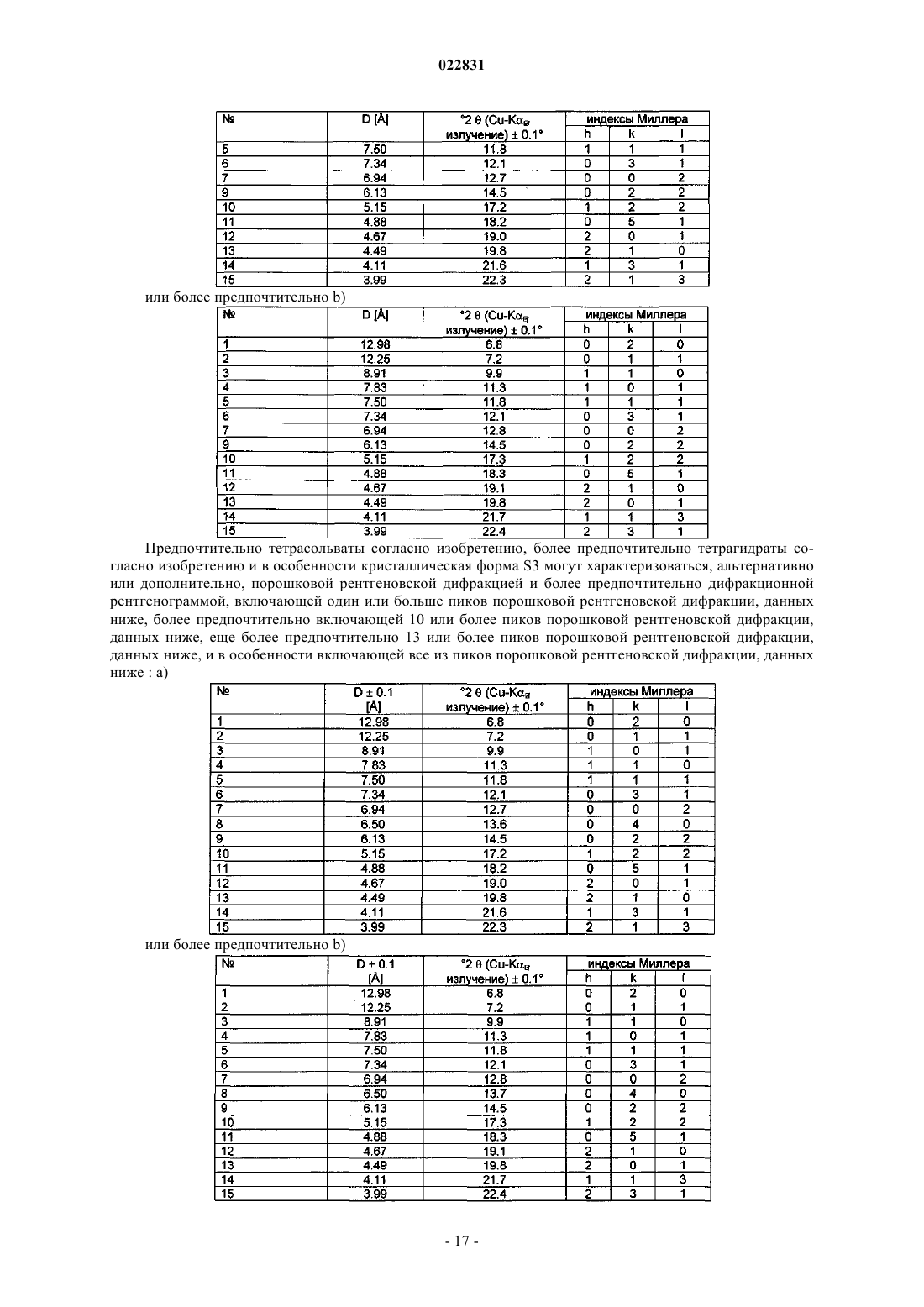
4. Кристаллическая форма S3 внутренней соли соединения формулы I
где кристаллическая форма S3 характеризуется элементарной ячейкой с параметрами кристаллической решетки а = 9,6±0,1 Å, b = 25,9±0,5 Å и с = 13,9±0,1 Å, с α = β = γ = 90±1°.
5. Твердая форма соединения формулы I
где указанная твердая форма содержит от 60 до 100 мас.% одной или нескольких кристаллических форм, выбранных из группы, включающей кристаллическую форму А1 по п.1, кристаллическую форму S1 по п.2, кристаллическую форму S2 по п.3 и кристаллическую форму S3 по п.4.
6. Твердая форма по п.5, содержащая от 95 до 100 мас.% одной или нескольких кристаллических форм, выбранных из группы, включающей кристаллическую форму А1 по п.1, кристаллическую форму S1 по п.2, кристаллическую форму S2 по п.3 и кристаллическую форму S3 по п.4.
7. Твердая форма по п.5, содержащая от 60 до 100 мас.% кристаллической формы А1.
8. Применение кристаллической формы по пп.1, 2, 3 и/или 4 в качестве лекарственного средства.
9. Применение по п.8, где указанное лекарственное средство является лекарственным средством для лечения раковых болезней.
10. Применение по п.9, где раковые болезни выбраны из группы, включающей рак мозга, рак легких, рак головы и шеи, рак молочной железы, рак предстательной железы и метастазы вследствие этих болезней.
11. Применение твердой формы по пп.5, 6 и/или 7 в качестве лекарственного средства.
12. Применение по п.11, где указанное лекарственное средство является лекарственным средством для лечения раковых болезней.
13. Применение по п.12, где раковые болезни выбраны из группы, включающей рак мозга, рак легких, рак головы и шеи, рак молочной железы, рак предстательной железы и метастазы вследствие этих болезней.
Текст
Изобретение относится к новым твердым формам [(2S,5R,8S,11S)-5-бензил-11-(3 гуанидинопропил)-8-изопропил-7-метил-3,6,9,12,15-пентаоксо-1,4,7,10,13-пентаазациклопентадец-2-ил]уксусной кислоты, способам их получения и применению упомянутых твердых форм в фармацевтических препаратах.(71)(73) Заявитель и патентовладелец: МЕРК ПАТЕНТ ГМБХ (DE) Изобретение относится к новым твердым формам [(2S,5R,8S,11S)-5-бензил-11-(3-гуанидинопропил)-8-изопропил-7-метил-3,6,9,12,15-пентаоксо-1,4,7,10,13-пентаазациклопентадец-2-ил]уксусной кислоты, способам их получения и применению упомянутых твердых форм в фармацевтических препаратах.[(2S,5R,8S,11S)-5-Бензил-11-(3-гуанидинопропил)-8-изопропил-7-метил-3,6,9,12,15-пентаоксо 1,4,7,10,13-пентаазациклопентадец-2-ил]уксусная кислота или цикло-(Arg-Gly-Asp-DPhe-NMe-Val) была впервые описана в патентах/патентных заявках US 6,001,961 и ЕР 0770622, которые были впервые опубликованы в 1997 году. В указанных патентах были описаны различные солевые формы упомянутого соединения, например гидрохлорид, ацетат и метансульфонат. Позднее в WO 00/53627 был описан улучшенный способ производства, который приводит к внутренней соли цикло-(Arg-Gly-Asp-DPhe-NMeVal). Несмотря на это твердые формы, полученные согласно описанным способам, были в аморфной форме. Фармацевтическая активность, конечно, является главной предпосылкой для реализации в качестве фармацевтически активного агента, фармацевтически действующего начала или активного фармацевтического ингредиента (АФИ), после подобное вещество одобряется как лекарственное средство на рынке. Однако есть различные дополнительные требования, которым должен соответствовать фармацевтически активный агент. Эти требования основаны на различных параметрах, которые непосредственно связаны с природой активного вещества. Не будучи ограниченными, примерами этих параметров являются стабильность активного агента или активного ингредиента при различных условиях внешней среды, его стабильность на протяжении производства фармацевтического препарата и стабильность активного агента или активного ингредиента в конечной лекарственной композиции. Фармацевтически активное вещество, применяемое для приготовления фармацевтических композиций, должно быть настолько чистым насколько возможно и его стабильность при длительном хранении должна быть гарантированна при различных условиях внешней среды. Абсолютно важно предотвратить применение фармацевтических композиций, которые содержат в дополнение к действующему активному веществу, например, продукты их разрушения или разложения. В таком случае содержание активного вещества в лекарственном средстве может быть меньше, чем определено, и/или лекарственное средство может исказить контроль количества. Технические факторы подобные размеру частиц или равномерному распределению действующего начала или активного ингредиента в препарате может быть критическом фактором, особенно когда лекарственное средство является комплексным препаратом и/или лекарственное средство может быть дано в малых дозах. Чтобы включить комплексные системы препарата и/или обеспечивать равномерное распределение, размер частиц активного вещества может быть скорректирован до подходящего уровня, например, размалыванием. Поскольку разрушение фармацевтически активного вещества, как побочный эффект производственных этапов, таких как очищение, растворение, плавление, размалывание, тонкое измельчение, смешивание и/или штамповка выдавливанием, должно быть минимизировано, несмотря на жесткие условия необходимые на протяжении указанных производственных этапов, абсолютно необходимо, чтобы активное вещество являлось высоко стабильным в продолжение производственных этапов. Только если активное вещество является эффективно стабильным на протяжении производственных этапов, является возможными производить гомогенный фармацевтический препарат, который всегда выполняет требования качества и содержит указанное количество активного вещества воспроизводимым образом. Другой проблемой, которая может возникать в процессе размалывания для приготовления заданного фармацевтического препарата является затрата энергии и/или давления, обусловленная этапами процесса, такими как воздействие на поверхность частицы АФИ, независимо от того является она аморфной или кристаллической. Это может в определенных обстоятельствах привести к полиморфным изменениям, к изменению в аморфной конфигурации или к изменениям в кристаллической решетке, в зависимости от твердого материала или формы используемой в производственных этапах. Поскольку фармацевтическое качество фармацевтического препарата требует, чтобы у активного вещества всегда была та же самая морфология, предпочтительно та же самая кристаллическая морфология, стабильность и свойства твердого АФИ являются предметом строгих требований также с этой точки зрения. Таким образом, стабильность, а также срок годности самого АФИ являются действительно важными. Много фармацевтических твердых веществ могут существовать в разных физических формах. Полиморфизм предпочтительно характеризуется как возможность соединения, такого как лекарственное вещество, существовать в двух или более кристаллических модификациях, которые имеют разные устройства и/или конформации молекул в кристаллической решетке (D. J. W. Grant. Theory and origin ofpolymorphism. In H. G. Brittain (ed.) Polymorphism in Pharmaceutical Solids. Marcel Dekker, Inc., New York,1999, pp. 1-34, раскрытие которого включено в это заявление ссылкой во всей полноте). Аморфные твердые вещества состоят из беспорядочных структур молекул и не обладают кристаллической решеткой и/или дальним порядком. Сольваты являются кристаллическими твердыми веществами, содержащими или стехиометрические или нестехиометрические количества растворителя, включенные во внутрь кристаллической структуры. Если включенным растворителем является вода, сольваты являются, как правило, также известными как гидраты. Полиморфизм относится к наличию разных кристаллических моди-1 022831 фикаций одного и того же соединения или лекарственного вещества. Полиморфизм в этом комментарии определяется как в International Conference on Harmonization (ICH) Guideline Q6A (International Conference on Harmonization Q6A Guideline: Specifications for New Drug Substances and Products: Chemical Substances, October 1999, раскрытие которого включено в это заявление ссылкой во всей полноте), включает сольваты и аморфные формы. Стехиометрические сольваты предпочтительно рассматриваются как молекулярные соединения. Термин предпочтительно предполагает фиксированное, хотя не обязательно целое, соотношение растворителя к соединению. Нестехиометрические сольваты предпочтительно являются типом инклюзионных соединений. Наиболее важной характерной чертой этого класса сольватов является то, что структура удерживается, пока содержание растворителя потенциально принимает значение между возможно нулевым и множественным молярным соотношением соединения. Количество растворителя в структуре зависит от парциального давления растворителя во внешней среде твердого вещества и температуры (смотреть: U.J. Griesser, "The Importance of Solvates" in R. Hilfiker (Editor) "Polymorphism in the Pharmaceutical Industry", Wiley VCH, 2006, раскрытие которого включено в это заявление ссылкой во всей его полноте). Полиморфы и/или сольваты фармацевтического твердого вещества могут иметь разные химические и физические свойства, такие как точка плавления, гигроскопичность, химическая активность, кажущаяся растворимость, соотношение растворения, оптические и электрические свойства, давление пара и/или плотность. Эти свойства могут иметь прямое влияние на эксплуатационные характеристики лекарственных веществ и качество/технические данные лекарственных продуктов, такие как стабильность, растворимость и/или биоактивность. Метастабильная фармацевтическая форма твердого состояния может менять кристаллическую структуру или сольват/десольват в ответ на изменение в условиях внешней среды,технологии, или по прошествии времени. Стабильность АФИ является также важной в фармацевтических композициях для определения срока хранения определенного лекарственного средства; сроком хранения является период времени, на протяжении которого лекарственный продукт, как ожидают, остается в пределах одобренных спецификацией, предусматривающих, что он хранится при определенных условиях. В пределах определенного срока хранения, лекарственное средство может быть введено без какого-либо риска для пациента. Высокая стабильность лекарственного средства вышеупомянутых фармацевтических композиций при различных условиях хранения является, следовательно, дополнительным преимуществом, как для пациента, так и для производителя. Отдельно от требований, указанных выше, должно быть, как правило, принято во внимание, что любое изменение формы твердого состояния фармацевтической композиции, которое способно к улучшению ее физической и химической стабильности, дает существенное преимущество перед менее устойчивыми формами того же самого лекарственного средства. Целью изобретения является также обеспечить новый, стабильный твердый материал соединения цикло-(Arg-Gly-Asp-DPhe-NMe-Val) которое удовлетворяет строгим требованиям, налагаемым на фармацевтически активные вещества как упомянуто выше. Таким образом, одной задачей настоящего изобретения является обеспечение новых твердых материалов или форм цикло-(Arg-Gly-Asp-DPhe-NMeVal) с улучшенными свойствами твердого состояния. Сейчас было найдено, что цикло-(Arg-Gly-Asp-DPhe-NMe-Val) и особенно его внутренняя соль может быть получена как кристаллический материал и также в особенности как кристаллические формы. Неожиданно был найден целый класс новых кристаллических форм подобных структурных типов (далее также называемые псевдополиморфными формами, ПП) цикло-(Arg-Gly-Asp-DPhe-NMe-Val), которые фактически показывают полезные свойства для твердого состояния и предпочтительно также обладают полезными комбинациями выгодных свойств для твердого состояния нового материала согласно изобретению. Дополнительно неожиданно было найдено, что разные способы для получения нового кристаллического материала предпочтительно приводят к разным кристаллическим формам или модификациям в пределах названого класса кристаллических форм. Эти кристаллические формы или модификации соединения цикло-(Arg-Gly-Asp-DPhe-NMe-Val) и особенно его внутренней соли и способы их получения являются предпочтительным объектом данной заявки. Упомянутая новая твердая форма и названные кристаллические формы или модификации демонстрируют ценные свойства и преимущества по сравнению с аморфными формами известными ранее,включая, но не ограничиваясь, более высокую термодинамическую стабильность, пониженную гигроскопичность, более высокую кристалличность, улучшенные транспортировочные свойства, выгодные свойства растворения и/или улучшенную стабильность при хранении. Соединение [(2S,5R,8S,11S)-5-бензил-11-(3-гуанидинопропил)-8-изопропил-7-метил-3,6,9,12,15 пентаоксо-1,4,7,10,13-пентаазациклопентадец-2-ил]уксусная кислота или цикло-(Arg-Gly-Asp-DPheNMe-Val), также известный под МНН (международное непатентированное название) Циленгитид, демонстрирует выгодную биологическую активность, включая, но не ограничиваясь, его ингибиторную активность интегрина, антиангиогенную активность и усиленную радиотерапевтическую активность, он широко используется в качестве действующего начала в фармацевтических применениях. Для применения в качестве действующего начала или сокращенно для применения в качестве АФИ,-2 022831 критическими являются факторы, такие как высокая чистота, отличные транспортировочные свойства,соответствующая стабильность и надежные производственные процессы. Дополнительно для таких пептидных соединений, имеющих как основные, так и кислотные центры или фрагменты, точная стехиометрия в солеобразовании является другим критическим фактором и также задачей для производства АФИ. Кислотные соли цикло-(Arg-Gly-Asp-DPhe-NMe-Val) как найдено, были легко получены, но как обнаружилось, являются менее устойчивыми из-за кислоты катализирующей распад. Основные соли в общем,как найдено, обладают нежелательной растворимостью и транспортировочными свойствами. Ранее известные и описанные амфотерные формы цикло-(Arg-Gly-Asp-DPhe-NMe-Val) как найдено, были невыгодно гигроскопичными, один главный недостаток в производстве дозированных форм, а также в разработке подходящих фармацевтических препаратов. Таким образом, твердая форма с улучшенной стабильностью, улучшенной транспортабельностью,более высокой чистотой и/или более высокой степенью очистки АФИ по сравнению с известной аморфной формой является в общем высоко успешной и действительно необходимой для надежного промышленного серийного производства АФИ. Особенно, если должна быть обеспечена твердая дозировка препарата или суспензионный препарат АФИ. Таким образом, объектами настоящего изобретения являются твердая форма соединения согласно формуле I цикло-(Arg-Gly-Asp-DPhe-NMeVal) (I),где указанная твердая форма содержит одну или больше кристаллических форм соединения формулы I, характеризующихся элементарной ячейкой с параметрами кристаллической рештки Указанная элементарная ячейка предпочтительно является кристаллографической элементарной ячейкой или кристаллографически определенной элементарной ячейкой. В указанной элементарной ячейке уголпредпочтительно составляет 902, уголпредпочтительно составляет 902 и/или уголпредпочтительно составляет 902. Предпочтительно твердая форма содержит по меньшей мере 10 мас.%, более предпочтительно по меньшей мере 30 мас.%, еще более предпочтительно 60 мас.% и в особенности по меньшей мере 90 мас.% или по меньшей мере 95 мас.%, одной или больше кристаллических форм соединения формулы I как определено выше и/или ниже. Например, твердая форма содержит около 25, около 50, около 75, около 95, около 99 или около 100 мас.% одной или больше кристаллических форм соединения формулы I как определено выше и/или ниже. Особенно предпочтительно твердая форма содержит по меньшей мере 10 мол.%, более предпочтительно по меньшей мере 30 мол.%, еще более предпочтительно 60 мол.% и в особенности по меньшей мере 90 мол.% или по меньшей мере 95 мол.%, одной или больше кристаллических форм соединения формулы I как определено выше и/или ниже. Например, твердая форма содержит около 25, около 50,около 75, около 95, около 99 или около 100 мол.% одной или больше кристаллических форм соединения формулы I как определено выше и/или ниже. Массовые проценты, данные для твердой формы согласно изобретению, предпочтительно относятся к соотношению между массой одной или больше кристаллических форм как определено выше/ниже,содержащихся в указанной твердой форме и общим количеством по массе соединения формулы I, содержащегося в указанной твердой форме. Другими словами данные массовые проценты предпочтительно являются массовыми процентами суммы одной или больше кристаллических форм как определено выше и/или ниже, в пересчете на общее количество по массе соединения формулы I. Таким образом,массовые проценты, данные для содержания одной или больше кристаллических форм в твердой форме согласно изобретению предпочтительно являются независимыми от количества или содержания соединений или примесей отличающихся от соединения согласно формуле I, содержащегося в указанной твердой форме. Таким образом, массовые проценты, данные для твердой формы, предпочтительно корректированы для содержащихся молекул растворителя, то есть массовые проценты, данные для твердой формы предпочтительно являются независимыми от или вычислены без молекул растворителя в указанной твердой форме. Мольные проценты (мол.%), данные для твердой формы согласно изобретению, предпочтительно относятся к молярному соотношению между одной или больше кристаллическими формами как определено выше/ниже, содержащимися в указанной твердой форме и общим молярным количеством соединения формулы I, содержащегося в указанной твердой форме. Другими словами, данные мольные проценты, предпочтительно являются мольными процентами суммы одной или больше кристаллических форм как определено выше и/или ниже в пересчете на общее молярное количество соединения формулы I. Таким образом, мольные проценты, данные для содержания одной или больше кристаллических форм в твердой форме согласно изобретению, предпочтительно являются независимыми от количества или содержания соединений или примесей, отличающихся от соединения согласно формуле I, содержащегося в указанной твердой форме. Таким образом, мольные проценты (мол.%), данные для твердой формы,предпочтительно корректированы для содержащихся молекул растворителя, то есть мольные проценты(мол.%), данные для твердой формы, предпочтительно являются независимыми от или вычислены без молекул растворителя в указанной твердой форме. Одна или больше кристаллических форм в отношении указанной твердой формы предпочтительно означает, что твердая форма содержит по меньшей мере одну или больше кристаллическую форму или модификацию соединения формулы I с элементарной ячейкой в пределах параметров кристаллической рештки как определено выше и/или ниже, или что твердая форма содержит смеси двух или больше, например двух или трех, кристаллических форм или модификаций соединения формулы I, каждая с элементарной ячейкой в пределах параметров кристаллической рештки как определено выше и/или ниже. Предпочтительно твердая форма содержит одну, две, три или четыре кристаллические формы соединения формулы I как определено выше и/или ниже. Более предпочтительно твердая форма содержит одну или больше, предпочтительно одну, две, три или четыре, еще более предпочтительно одну или две, кристаллические формы соединения формулы I,каждая с элементарной ячейкой с параметрами кристаллической рештки (ULP - unit cell with кристаллическая рештка параметры), выбранными из группы, состоящей из Более предпочтительно твердая форма содержит одну или больше, предпочтительно одну, две, три или четыре, еще более предпочтительно одну или две, кристаллические формы соединения формулы I,каждая с элементарной ячейкой с параметрами кристаллической рештки (ULP), выбранными из группы,состоящей из В элементарной ячейке с параметрами кристаллической рештки ULP1 и/или ULP2, уголпредпочтительно составляет 902, уголпредпочтительно составляет 902 и/или уголпредпочтительно составляет 902. Предпочтительно элементарная ячейка с параметрами кристаллической рештки ULP1 может характеризоваться, альтернативно или дополнительно, предпочтительно дополнительно, содержанием около 4 молекул соединения формулы I в пределах указанной элементарной ячейки. В элементарной ячейке с параметрами кристаллической рештки ULP2, уголпредпочтительно составляет 900,5, уголпредпочтительно составляет 900,5 и/или уголпредпочтительно составляет 900,5. В элементарной ячейке с параметрами кристаллической рештки ULP2, углы ,иболее предпочтительно составляют 900,1. Предпочтительно элементарная ячейка с параметрами кристаллической рештки ULP2 может характеризоваться, альтернативно или дополнительно, предпочтительно дополнительно, содержанием около 4 молекул соединения формулы I в пределах указанной элементарной ячейки. Более предпочтительно твердая форма содержит одну или больше, предпочтительно одну, две, три или четыре, еще более предпочтительно одну или две, кристаллические формы соединения формулы I,выбранные из таких: кристаллическая форма А 1, характеризующаяся элементарной ячейкой с параметрами кристаллической рештки,а = 9,80,1, b = 19,50,5 и с = 15,40,1,кристаллическая форма S1, характеризующаяся элементарной ячейкой с параметрами кристаллической рештки,а = 9,40,1, b = 25,90,5 и с = 14,10, ,кристаллическая форма S2, характеризующаяся элементарной ячейкой с параметрами кристаллической рештки,-4 022831 а = 9,30,1, b = 26,60,5 и с = 14,70,1 и кристаллическая форма S3, характеризующаяся элементарной ячейкой с параметрами кристаллической рештки,а = 9,60,1, b = 25,90,5 и с = 13,90,1. Более предпочтительно твердая форма содержит одну или больше, предпочтительно одну, две, три или четыре, еще более предпочтительно одну или две, кристаллические формы соединения формулы I,выбранные из таких: кристаллическая форма А 1, характеризующаяся элементарной ячейкой с параметрами кристаллической рештки,а = 9,80,1, b = 19,50,5 и с = 15,40,1, предпочтительно с=== 901 и в особенности с=== 90; кристаллическая форма S1, характеризующаяся элементарной ячейкой с параметрами кристаллической рештки,а = 9,40,1, b = 25,90,5 и с = 14,10,1, предпочтительно с=== 902, и в особенности с= 901,= 911,= 901 и в особенности с= 90,= 91,2,= 90; кристаллическая форма S2, характеризующаяся элементарной ячейкой с параметрами кристаллической рештки,а = 9,30,1, b = 26,60,5 и с = 14,70,1, предпочтительно с=== 901 и в особенности с=== 90; и кристаллическая форма S3, характеризующаяся элементарной ячейкой с параметрами кристаллической рештки,а = 9,60,1, b = 25,90,5 и с = 13,90,1, предпочтительно с=== 901 и в особенности с=== 90. Предпочтительно кристаллические формы S1, S2 и S3 могут характеризоваться, альтернативно или дополнительно, предпочтительно дополнительно, содержанием около 4 молекул соединения формулы I в пределах указанных элементарных ячеек. Кристаллические формы S1, S2 и S3 также предпочтительно характеризуются как сольваты. В контексте настоящего изобретения сольваты предпочтительно представляют собой кристаллические тврдые аддукты, содержащие или стехиометрические или нестехиометрические количества растворителя, включенного в кристаллическую структуру, то есть молекулы растворителя предпочтительно образуют часть кристаллической структуры. Если включенным растворителем является вода, сольваты также общеизвестны как гидраты. В результате растворитель в сольватах предпочтительно образует часть кристаллической структуры и таким образом в основном способен быть детектируемым рентгеновскими методами и предпочтительно детектируемый рентгеновскими методами как описано в этом документе. В основном для данной кристаллической структуры существует верхний предел для количества растворителя, включенного в указанную структуру (не вызывая переход в другую кристаллическую структуру). В некоторых случаях, несмотря на это, возможно удалить по меньшей мере часть включенного растворителя физической обработкой кристаллической структуры, например при помощи процедур сушки, например, путем хранения при повышенных температурах (но предпочтительно ниже точки плавления или другой точки фазового перехода), и/или пониженным давлением, предпочтительно включающим применение вакуума и пониженного парциального давления. В принципе в таких случаях растворитель может быть частично или полностью удален из кристаллической структуры, таким образом вводя пустоты в указанную кристаллическую структуру. Вероятность фазового перехода и/или полиморфного перехода, например, переход в различную полиморфную форму или в особенности переход в аморфную форму, сольват или гидрат, содержащий меньше молекул растворителя или воды, или негидратную форму, увеличивается с количеством включенного растворителя, приближающимся к нолю. В таких случаях, содержащийся растворитель и/или его количество и таким образом композиция соответствующих сольватов или структура сольватов предпочтительно может быть изменена надлежащей обработкой, включая, но не ограничиваясь ими, создание определнных условий и/или перекристаллизацию. Например, один растворитель может быть частично или полностью удален из такого сольвата,один растворитель может быть частично или полностью заменен другим растворителем в таком сольвате и/или количество растворителя в таком сольвате может быть увеличено или уменьшено. Таким образом,сольват содержащий определенный растворитель, может потенциально быть преобразован в сольват,содержащий смесь сольватов, и наоборот. Создание определнных условий в этом отношении предпочтительно относится к физическим обработкам, в которых главным образом сохранена исходная кристаллическая структура соответствующего сольвата. Подходящие способы и средства и/или параметры создания определнных условий сольватов в принципе известны квалифицированному специалисту. Примеры подходящих способов создания определнных условий раскрыты в данной заявке и предпочтительно включают, но не ограничиваются ими,подвергание испарению растворителя, действие тепловыми условиями (например, путем дифференци-5 022831 альной сканирующей калориметрии, термогравиметрии и/или хранения при определенных температурах или температурных градиентах), суспендирование (например, образование и/или обработка суспензии сольвата в жидкости, которая содержит один или более растворителей), действие переменным парциальным давлением на один или больше растворителей, действие определенным парциальным давлением и/или определенными градиентами парциального давления на один или больше растворителей, и комбинации этого. Например, суспендирование и/или действие переменным парциальным давлением на один или больше растворителей могут быть осуществлены при определенных температурах или температурных градиентах. Предпочтительной формой создания определнных условий является сольватирование или десольватирование. Суспензии и рабочие методики для суспензий или суспендирования известны в данной области техники, например из Martyn D. Ticehurst, Richard A. Storey, Claire Watt, InternationalJournal of Pharmaceutics 247 (2002) 1-10, раскрытие которого включено в эту заявку полностью. Дополнительно или альтернативно, содержащийся растворитель и/или его количество и таким образом композиция соответствующих сольватов или структура сольватов также предпочтительно может быть изменена перекристаллизацией, в особенности перекристаллизацией из другого растворителя или смеси растворителей, при этом воспроизводиться или главным образом воспроизводиться исходная кристаллическая структура сольвата. В этом отношении сольват предпочтительно означает, что элементарная ячейка или кристаллографическая элементарная ячейка содержит приблизительно стехиометрическое - целое или не целое количество молекул растворителя одного или больше растворителей на молекулу соединения формулы I,содержащуюся в указанной элементарной ячейке. Приблизительно стехиометрическое количество молекул растворителя в указанной элементарной ячейке на молекулу соединения формулы I, содержащуюся в указанной элементарной ячейке, предпочтительно находится в диапазоне от около 0,01 молекул растворителя до около 8 молекул растворителя, более предпочтительно в диапазоне от около 0,1 молекул растворителя до около 7 молекул растворителя и еще более предпочтительно в диапазоне от около 1,5 молекул растворителя вплоть до около 4,5 молекул растворителя, например около 0,1 молекул растворителя,около 0,5 молекул растворителя, около 1,5 молекул растворителя, около 3 молекул растворителя, около 4 молекул растворителя или около 7 молекул растворителя на молекулу соединения согласно формуле I. В особенности предпочтительными являются сольваты с около четырьмя молекулами растворителя на молекулу соединения согласно формуле I, содержащуюся в указанной элементарной ячейке. Если элементарная ячейка или кристаллографическая элементарная ячейка содержит около 4 молекул растворителя одного или больше растворителей на молекулу соединения формулы I, содержащуюся в указанной элементарной ячейке, это предпочтительно рассматривается как тетрасольват, и если содержится около 7 молекул растворителя одного или больше растворителей на молекулу соединения формулы I, содержащуюся в указанной элементарной ячейке, это предпочтительно рассматривается как гептасольват. В этом отношении сольват предпочтительно означает, что элементарная ячейка или кристаллографическая элементарная ячейка содержит приблизительно стехиометрическое, предпочтительно целое или не целое, более предпочтительно приблизительно целое, количество молекул растворителя одного или больше растворителей на молекулу соединения формулы I, содержащуюся в указанной элементарной ячейке. Приблизительно стехиометрическое количество молекул растворителя в указанной элементарной ячейке на молекулу соединения формулы I, содержащуюся в указанной элементарной ячейке предпочтительно находится в диапазоне от около 0,5 молекул растворителя до около 6 молекул растворителя, более предпочтительно в диапазоне от около 0,5 молекул растворителя до около 4,5 молекул растворителя и еще более предпочтительно в диапазоне от около 1,5 молекул растворителя вплоть до около 4 молекул растворителя на молекулу соединения согласно формуле I, содержащуюся в указанной элементарной ячейке, например около 0,5 молекул растворителя, около 1,5 молекул растворителя, около 4 молекул растворителя или около 6 молекул растворителя на молекулу соединения согласно формуле I,содержащуюся в указанной элементарной ячейке. В особенности предпочтительными являются сольваты с около четырьмя молекулами растворителя на молекулу соединения согласно формуле I, содержащуюся в указанной элементарной ячейке. Если элементарная ячейка или кристаллографическая элементарная ячейка содержит около 4 молекул растворителя одного или больше растворителей на молекулу соединения формулы I, содержащуюся в указанной элементарной ячейке, это предпочтительно рассматривается как тетрасольват. Предпочтительные растворители или молекулы растворителя в этом отношении выбраны из группы, включающей воду и спирты, и более предпочтительно выбраны из группы, включающей воду, метанол и этанол. Например, если элементарная ячейка кристаллической формы содержит одну молекулу соединения согласно формуле I и около четырех молекул растворителя, указанная форма предпочтительно будет рассматриваться как тетрасольват. Если элементарная ячейка кристаллической формы содержит две молекулы соединения формулы I и около восьми молекул растворителя, указанная форма предпочтительно также будет рассматриваться как тетрасольват. Если элементарная ячейка кристаллической формы содержит четыре молекулы соединения формулы I и около шестнадцати молекул растворителя, указанная форма предпочтительно также будет рассматриваться как тетрасольват. То же самое будет справедливо,-6 022831 если элементарная ячейка кристаллической формы содержит 2,5 молекулы соединения согласно формулеI и около 10 молекул растворителя. Таким образом, сольват более предпочтительно означает, что соответствующая кристаллическая форма содержит приблизительно стехиометрическое - целое или не целое количество молекул растворителя одного или больше растворителей на молекулу соединения формулы I. Приблизительно стехиометрическое количество (одной или больше) молекул растворителя в указанном сольвате предпочтительно находится в диапазоне от около 0,1 молекул растворителя до около 7 молекул растворителя на молекулу соединения согласно формуле I, более предпочтительно в диапазоне от около 0,5 молекул растворителя на молекулу соединения согласно формуле I вплоть до около 4,5 молекул растворителя на молекулу соединения согласно формуле I и еще более предпочтительно в диапазоне от около 1,5 молекул растворителя на молекулу соединения согласно формуле I вплоть до около 4 молекул растворителя на молекулу соединения согласно формуле I, например около 0,5 молекул растворителя, около 1,5 молекул растворителя, около 3 молекул растворителя, около 4 молекул растворителя или около 7 молекул растворителя на молекулу соединения согласно формуле I, содержащуюся в указанной элементарной ячейке. В особенности предпочтительными являются сольваты с около четырьмя молекулами растворителя на молекулу соединения согласно формуле I. Таким образом, сольват более предпочтительно означает, что соответствующая кристаллическая форма содержит приблизительно стехиометрическое количество молекул растворителя одного или больше растворителей на молекулу соединения формулы I. Приблизительно стехиометрическое количество (одной или больше) молекул растворителя в указанном сольвате предпочтительно находится в диапазоне от около 0,5 молекул растворителя до около 6 молекул растворителя на молекулу соединения согласно формуле I, более предпочтительно в диапазоне от около 0,5 молекул растворителя вплоть до около 4,5 молекул растворителя на молекулу соединения согласно формуле I и еще более предпочтительно в диапазоне от около 1,5 молекул растворителя на молекулу соединения согласно формуле I вплоть до около 4 молекул растворителя на молекулу соединения согласно формуле I, например около 0,5 молекул растворителя, около 1,5 молекул растворителя, около 4 молекул растворителя или около 6 молекул растворителя на молекулу соединения согласно формуле I. В особенности предпочтительными являются сольваты с около четырьмя молекулами растворителя на молекулу соединения согласно формуле I. Более предпочтительные стехиометрические составы сольвата определены как изображено в области, заштрихованной серым цветом в графике ниже (график I). График I На этом графике х означает число молекул воды на молекулу соединения согласно формуле I (которое может быть целым числом или нецелым числом) и у означает число молекул спирта, предпочтительно или метанол, или этанол или их смеси, и может быть целым числом или нецелым числом. Соответственно, предпочтительно число молекул спирта на молекулу соединения согласно формуле I находится в пределах между 0 и около 4, и предпочтительно между 0,1 и 4, и число молекул воды находится в пределах между 0 и около 4, и предпочтительно между 0,1 и 4. Еще более предпочтительные стехиометрические составы сольвата определены как изображено в области, заштрихованной серым цветом в графике ниже (график II). На этом графике х означает число молекул воды на молекулу соединения согласно формуле I (которое может быть целым числом или нецелым числом) и у означает число молекул спирта, предпочтительно или метанол, или этанол или их смеси, и может быть целым числом или нецелым числом. Соответственно, предпочтительно число молекул спирта на молекулу соединения согласно формуле I находится в пределах между 0 и около 2, и предпочтительно между 0,1 и 2, и число молекул воды находится в пределах между 0 и около 4, и предпочтительно между 0,1 и 4. Еще более того предпочтительные стехиометрические составы сольвата определены как изображено в области, заштрихованной серым цветом в графике ниже (график III). На этом графике х означает число молекул воды на молекулу соединения согласно формуле I (которое может быть целым числом или нецелым числом) и у означает число молекул спирта, предпочтительно или метанол, или этанол или их смеси, и может быть целым числом или нецелым числом. Соответственно, предпочтительно число молекул спирта на молекулу соединения согласно формуле I находится в пределах между 0 и около 1, более предпочтительно между 0,1 и 1, и число молекул воды находится в пределах между 0 и около 4, более предпочтительно между 0,1 и 4. В особенности предпочтительные растворители или молекулы растворителя в этом отношении выбраны из группы, включающей воду и спирты, и более предпочтительно выбраны из группы, включающей воду, метанол и этанол. Сольваты соединения согласно формуле I с композицией или стехиометрическим составом как описано в графике I, графике II и/или графике III и предпочтительно также как описано в параграфах, относящихся к ним, соответственно, являются в особенности предпочтительным объектом настоящего изобретения. Выше и/или ниже описанные сольваты являются в особенности предпочтительными примерами указанных сольватов с композицией или стехиометрическим составом в пределах диапазонов как описано в графике I, графике II и/или графике III и таким образом также являются в особенности предпочтительными объектами настоящего изобретения. На основании описания, данного выше и/или ниже и предпочтительно также на основании описания сольватов или кристаллических форм S1, S2 и/или S3, становится очевидно, что сольваты или кристаллические формы, характеризующиеся элементарной ячейкой с параметрами элементарной ячейкиULP1 могут включать от 0 до около 4 молекул растворителя на молекулу соединения формулы I в пределах указанной элементарной ячейки, более предпочтительно от 0,01 до около 4 молекул растворителя на молекулу соединения формулы I в пределах указанной элементарной ячейки и в особенности от 0,5 до 4 молекул растворителя на молекулу соединения формулы I в пределах указанной элементарной ячейки. Таким образом, общим признаком или характеристикой сольватов или кристаллических форм, характеризующихся элементарной ячейкой с параметрами элементарной ячейки ULP1 является верхний предел содержания растворителя от около четырех молекул одного или больше растворителей, предпочтительно растворителей как описано в этом документе, на молекулу соединения согласно формуле I. В соответствии с уровнем техники, сольваты или кристаллические формы, характеризующиеся верхним пределом содержания растворителя от около четырех молекул одного или больше растворителей на молекулу соединения формулы I в указанной элементарной ячейке, предпочтительно упоминаются как тетрасольваты. Несмотря на это, как это подробно описано в этом документе, указанные сольваты или кристаллические формы, характеризующиеся элементарной ячейкой с параметрами элементарной ячейки ULP1,могут быть десольватированы до содержания растворителя от около 3 или менее молекул растворителя на молекулу соединения формулы I в пределах указанной элементарной ячейки, до содержания растворителя от около 2 или менее молекул растворителя на молекулу соединения формулы I в пределах указанной элементарной ячейки, до содержания растворителя от около 1 или менее молекул растворителя на молекулу соединения формулы I в пределах указанной элементарной ячейки, или даже до содержания растворителя близко 0,5, 0,1 или 0 молекул растворителя на молекулу соединения формулы I в пределах указанной элементарной ячейки. Эти десольваты сольватов или кристаллических форм, характеризую-8 022831 щихся элементарной ячейкой с параметрами элементарной ячейки ULP1, также являются предпочтительным объектом настоящего изобретения. В результате термин "тетрасольват" и/или "тетрагидрат" как использовано здесь предпочтительно также включает частично или полностью десольватированные формы упомянутых тетрасольватов и/или тетрагидратов, предпочтительно до тех пор пока не изменена или главным образом не изменена соответствующая кристаллическая структура исходного тетрасольвата или тетрагидрата. В результате также термин "тетрасольват" как использовано здесь предпочтительно также включает спиртовые сольваты (или алкоголяты) или смешанные водно-спиртовые сольваты, предпочтительно включающие, но не ограниченные ими, дигидрат-диалкоголят, дигидрат-алкоголят и дигидратмоноалкоголят и/или их частично или полностью десольватированные формы, предпочтительно до тех пор пока не изменена или главным образом не изменена соответствующая кристаллическая структура исходного тетрасольвата и особенно предпочтительно исходная кристаллическая структура тетрагидратаS3. В результате также термин "тетрасольват" как использовано здесь предпочтительно также включает спиртовые сольваты (или алкоголяты) или смешанные водно-спиртовые сольваты, предпочтительно включающие, но не ограниченные ими, дигидрат-диалкоголят, дигидрат-алкоголят, дигидратмоноалкоголят и диалкоголят (предпочтительно данные формулой (Cil)1(Спирт)2(H2O)0), и/или их частично или полностью десольватированные формы, предпочтительно до тех пор пока соответствующая кристаллическая структура исходного тетрасольвата и особенно предпочтительно исходная кристаллическая структура тетрагидрата S3 не изменена или главным образом не изменена. Таким образом, все кристаллические формы в пределах параметров элементарной ячейки согласноULP1 как определено в этом документе предпочтительно рассматриваются как тетрасольваты согласно настоящего изобретения. Предпочтительно диалкоголяты согласно изобретению должны рассматриваться как их тетрасольваты и/или десольваты, которые предпочтительно содержат около двух молекул спирта на молекулу соединения формулы I, но при этом предпочтительно содержат менее, чем одну молекулу, более предпочтительно менее чем 0,5 молекулы и в особенности менее чем 0,1 молекулы воды на молекулу соединения формулы I. Таким образом, предпочтительные диалкоголяты согласно изобретению содержат около 4 молекул соединения формулы I и около 8 молекул спирта в элементарной ячейке, но предпочтительно менее, чем одну молекулу воды. Предпочтительно спирт в указанных диалкоголятах выбран из метанола и этанола и их смесей. Таким образом, диалкоголяты согласно изобретению предпочтительно также могут быть рассмотрены как десольваты или конкретнее как дегидраты дигидрат-диалкоголятов согласно изобретению. Кристаллическая форма А 1 предпочтительно также характеризуются как ангидрат или ансольват. В этом отношении ангидрат или ансольват предпочтительно означает, что элементарная ячейка не содержит или главным образом не содержит около стехиометрического количества молекул растворителя одного или больше растворителей. В этом отношении ангидрат или ансольват более предпочтительно означает, что элементарная ячейка главным образом не содержит воды и молекул растворителя. Главным образом не содержит молекул растворителя в этом отношении предпочтительно означает, что количество молекул растворителя в элементарной ячейке менее чем 0,5, более предпочтительно менее чем 0,1, еще более предпочтительно менее чем 0,01 и в особенности менее чем 0,001. Поскольку и ансольваты, и ангидраты характеризуются отсутствием соответствующих растворителей и таким образом характеризуются отсутствием любых растворителей, термины ангидрат и ансольват предпочтительно должны рассматриваться как синонимы в контексте настоящего изобретения. Количество молекул в элементарной ячейке предпочтительно определено кристаллографическими методами, более предпочтительно при помощи рентгеноструктурного анализа и/или порошковой рентгеновской дифракции. Альтернативно количество растворителя в указанных кристаллических формах, указанных сольватах и/или в соответствующей элементарной ячейке может быть определено или оценено путем элементного анализа, газовой хроматографии или титрованием Карла-Фишера. В этом контексте главным образом не содержащий молекулы растворителя предпочтительно означает содержание растворителя менее,чем 5%, еще более предпочтительно менее чем 2%, еще более предпочтительно менее чем 1% и в особенности менее чем 0,1%, например 5-0,1% или 2-0,01%. В этом отношении данные проценты (%) предпочтительно выбраны из мол.% и мас.% и особенно предпочтительно являются мас.%. Кристаллические формы А 1, S2 и/или S3 предпочтительно также характеризуются орторомбической элементарной ячейкой. Кристаллическая форма S1 предпочтительно также характеризуется моноклинной элементарной ячейкой. Элементарная ячейка и параметры кристаллической рештки, предпочтительно включающие, но не ограниченные ими, а, b, с, ,и/или , представляют собой кристаллографические параметры известные специалисту в данной области техники. Следовательно, они могут быть определены согласно способам известным в данной области техники. То же самое предпочтительно распространяется на орторомбиче-9 022831 скую и/или моноклинную форму элементарной ячейки. Данные выше элементарные ячейки и параметры кристаллической рештки, относящиеся к ним,предпочтительно определены при помощи рентгеновской дифракции, более предпочтительно рентгеноструктурным анализом и/или порошковой рентгеновской дифракцией, согласно стандартным способам,например способам или методикам как описано в European Pharmacopeia 6 е Издание глава 2.9.33, и/или как описано в Rolf Hilfiker, 'Polymorphism in the Pharmaceutical Industry', Wiley-VCH. Weinheim 2006Dekker Inc., New York 1999 (глава 6 и ссылки на нее). Альтернативно предпочтительно, данные выше элементарные ячейки и параметры кристаллической рештки, относящиеся к ним, могут быть получены при помощи рентгеноструктурного анализа, необязательно вместе с дополнительными структурными данными, предпочтительно проведнных на дифрактометре XCalibur от Oxford Diffraction, укомплектованным графитовым монохроматором и детекторомCCD, применяя Mo K излучение, предпочтительно при температуре 2985K; и/или на четырехкружном дифрактометре CAD4 от Nonius, укомплектованным графитовым монохроматором и сцинтилляционным счтчиком, применяя Mo K излучение, предпочтительно при температуре 2985K. Данные выше элементарные ячейки и параметры кристаллической рештки, относящиеся к ним предпочтительно определены при помощи рентгеновской дифракции, более предпочтительно порошковой рентгеновской дифракции, согласно стандартным способам, например способам или методикам как описано в European Pharmacopeia 6 е Издание глава 2.9.33, и/или как описано в Rolf Hilfiker, 'Polymorphismin the Pharmaceutical Industry', Wiley-VCH. Weinheim 2006 (Глава 6: X-Ray Diffraction), и/или H.G. Brittain, 'Polymorphism in Pharmaceutical Solids, TOM. 95, Marcel Dekker Inc., New York 1999 (глава 6 и ссылки на нее). В общем являются предпочтительными более высокие содержания одной или больше кристаллических форм как определено выше и/или ниже в твердой форме как описано выше и/или ниже. Твердая форма как описано выше и/или ниже, главным образом содержащая одну или больше кристаллических форм соединения формулы I, характеризуется элементарной ячейкой с параметрами кристаллической рештки и в особенности характеризуется как описано выше и/или ниже. Главным образом содержащая одну или больше кристаллических форм соединения формулы I предпочтительно означает, что соединение формулы I, содержащиеся в указанной твердой форме главным образом выбрано из указанной одной или больше кристаллических форм соединения формулы I,или другими словами, что одна или больше кристаллических форм в указанной твердой форме предназначены для для основного количества соединения формулы I в указанной твердой форме. Конкретнее,главным образом в этом отношении предпочтительно означает, что одна или больше кристаллических форм в указанной твердой форме предназначены для 90% или более, предпочтительно 95% или более,еще более предпочтительно 99% или более и в особенности 99,9% или более, количества соединения формулы I в указанной твердой форме. В этом отношении данные проценты (%) предпочтительно выбраны из мол.% и мас.% и особенно предпочтительно являются мол.%. Указанные количества могут быть обеспечены одной единичной кристаллической формой как описано в этом документе, или смесями двух или больше кристаллических форм как описано в этом документе. Предпочтительно указанные количества обеспечены одной единичной кристаллической формой как описано в этом документе. Более предпочтительно указанные количества обеспечены одной единичной кристаллической формой, выбранной из кристаллической формы А 1, кристаллической формы S1,кристаллической формы S2 и кристаллической формы S3 как описано в этом документе. Если твердая форма содержит две или более кристаллические формы как описано в этом документе, одна из этих кристаллических форм предпочтительно является основной кристаллической формой и одна или больше присутствующих дополнительных кристаллических форм присутствуют в незначительных количествах. Основная кристаллическая форма предпочтительно обеспечивает 60 мас.% или более,более предпочтительно 75% или более, еще более предпочтительно 90% или более и в особенности 95 или 99% или более, общего количества присутствующих кристаллических форм. В этом отношении данные проценты (%) предпочтительно выбраны из мол.% и мас.% и особенно предпочтительно являются мол.%. Если не указано иначе, проценты (или %), данные здесь для соединений и/или растворителей предпочтительно представляют собой либо проценты по массе, либо молярный процент, предпочтительно молярный процент. Поскольку содержание одной или больше кристаллических форм в твердой форме согласно изобретению и, если возможно, соотношение двух или больше кристаллических форм в твердой форме согласно изобретению, может преимущественно быть определено способами включая, но не ограничиваясь ими, порошковую рентгеновскую дифракцию, раман-спектроскопию и ИК- 10022831 спектроскопию и более предпочтительно определяются при помощи порошковой рентгеновской дифракции, раман-спектроскопии и/или ИК-спектроскопии, процентные величины, относящиеся к ним,являются особенно предпочтительно величинами в молярных процентах, если явно не указано иначе. Предпочтительно, если не указано иначе, проценты (или %), данные здесьii) интенсивности Порошковая рентгеновская дифракция (интенсивности ПРД); и/илиiii) аналитические параметры, такие как относительная влажность (ов или о.в.), и т.п.,предпочтительно представляют собой относительные проценты (то есть процент соответствующей максимальной величины). Предпочтительным объектом изобретения являются одна или больше кристаллических форм соединения формулы I как описано в этом документе и в особенности как описано выше и/или ниже. Предпочтительно одна или больше кристаллических форм соединения формулы I выбраны из кристаллических форм как описано выше и/или ниже с моноклинной элементарной ячейкой или орторомбической элементарной ячейкой. Предпочтительно одна или больше кристаллических форм соединения формулы I выбраны из ангидратов или ансольватов и сольватов. Предпочтительно сольваты выбраны из гидратов, метанолатов (метанольные сольваты) и этанолатов (этанольные сольваты) и их смесей. Указанные смеси предпочтительно выбраны из смешанные водно-метанольные сольваты, смешанные водно-этанольные сольваты, смешанные метанол-этанольные сольваты и смешанные метанол-этанол-водные сольваты. Предпочтительно ангидраты или ансольваты согласно изобретению и в особенности кристаллическая форма А 1 могут характеризоваться, альтернативно или дополнительно, точкой плавления/температурой разложения 282 С, более предпочтительно 2885 С или выше и в особенности 2885 С. Точки плавления/температуры разложения и/или поведение при термическом воздействии, описанные здесь, предпочтительно определены ДСК (дифференциальная сканирующая калориметрия) и ТГА(термогравиметрический анализ). Способы ДСК и/или ТГА или общие термоаналитические способы и подходящие устройства для их определения известны в данной области техники, например, из EuropeanPharmacopeia 6 е Издание глава 2.02.34, где описаны стандартные методики. Более предпочтительно, для температур плавления/разложения или поведения и/или термоанализа в основном применяются MettlerToledo DSC 821 и/или Mettler Toledo TGA 851, предпочтительно как описано в European Pharmacopeia 6 е Издание глава 2.02.34. Измерение ДСК и ТГА, показывающие термический анализ (Mettler-Toledo DSC 821, 5 K/мин, продувка газообразным азотом 50 мл/мин; Mettler-Toledo TGA 851, 5 K/мин, продувка газообразным азотом 50 мл/мин) и температуры плавления/разложения, данные выше показаны на фиг. 1 и 2. Предпочтительно ангидраты или ансольваты согласно изобретению и в особенности кристаллическая форма А 1 могут характеризоваться, альтернативно или дополнительно, порошковой рентгеновской дифракцией и более предпочтительно дифракционной рентгенограммой, включающей один или больше пиков порошковой рентгеновской дифракции, данных ниже, более предпочтительно включающей 6 или более пиков порошковой рентгеновской дифракции, данных ниже, еще более предпочтительно 8 или более пиков порошковой рентгеновской дифракции, данных ниже, и в особенности включающей все из пиков порошковой рентгеновской дифракции, данных ниже: а) или более предпочтительно b) Предпочтительно ангидраты или ансольваты согласно изобретению и в особенности кристаллическая форма А 1 могут характеризоваться, альтернативно или дополнительно, порошковой рентгеновской дифракцией и более предпочтительно дифракционной рентгенограммой, включающей пики порошковой рентгеновской дифракции, данные ниже: а) или более предпочтительно b) Предпочтительно ангидраты или ансольваты согласно изобретению и в особенности кристаллическая форма А 1 могут характеризоваться, альтернативно или дополнительно, порошковой рентгеновской дифракцией и более предпочтительно дифракционной рентгенограммой, включающей один или больше пиков порошковой рентгеновской дифракции, данных ниже, более предпочтительно включающей 10 или более пиков порошковой рентгеновской дифракции, данных ниже, еще более предпочтительно 12 или более пиков порошковой рентгеновской дифракции, данных ниже, и в особенности включающей все из пиков порошковой рентгеновской дифракции, данных ниже : а) или более предпочтительно b) Порошковая рентгеновская дифракция и более предпочтительно дифракционная рентгенограмма предпочтительно выполнены или определены как описано в этом документе и в особенности выполнены или определены при помощи стандартных методик как описано в European Pharmacopeia 6 е Издание глава 2.9.33, и еще более предпочтительно получены с параметрами Cu-K1 излучение и/или= 1,5406 ,предпочтительно на дифрактометре Stoe StadiP 611 KL. Фиг. 3 показывает порошковую рентгеновскую дифрактограмму кристаллической формы А 1. Предпочтительно ангидраты или ансольваты согласно изобретению и в особенности кристаллическая форма А 1 могут характеризоваться, альтернативно или дополнительно, при помощи структурных данных рентгеноструктурного анализа, например, структурных данных рентгеноструктурного анализа,полученных на дифрактометре, предпочтительно оборудованном графитовым монохроматором и детектором CCD, предпочтительно применяя Мо K излучение, предпочтительно при температуре 2985 K и еще более предпочтительно на дифрактометре XCalibur от Oxford Diffraction, укомплектованным графитовый монохроматор и детектором CCD, применяя Мо K излучение при около 298K. Согласно полученным структурным данным рентгеноструктурного анализа, ангидрат соединения формулы I и в особенности кристаллическая форма А 1 кристаллизуется в орторомбической группе симметрии Р 21 21 21 с параметрами кристаллической рештки а = 9,8, b = 15,4, с = 19,5 (0,1) и размер элементарной ячейки предпочтительно составляет 2940 (10)3. Из отдельной кристаллической структуры очевидно, что форма А 1 представляет ангидрат или ансольват. Монокристаллическая рентгеновская структура изображена на фиг. 4. Предпочтительно ангидраты и ансольваты согласно изобретению и в особенности кристаллическая форма А 1 могут характеризоваться, альтернативно или дополнительно, данными ИК-спектроскопии,включающими одно или больше расположений полос (2 см-1), данных ниже, более предпочтительно включающими 6 или более расположений полос (2 см-1), данных ниже, еще более предпочтительно включающими 9 или более расположений полос (2 см-1), данных ниже, и в особенности включающими все расположения полос (2 см-1), данные ниже, предпочтительно вместе с относительными интенсивностями, данными в скобках: 3431 см-1 (s), 3339 см-1 (s), 3189 см-1 (s), 2962 см-1 (m), 2872 см-1 (m), 1676 см-1 (s), 1660 см-1 (s), 1617-1 см (s), 1407 см-1 (s), 1316 см-1 (m), 1224 см-1 (m), 1186 см-1 (m), 711 см-1 (m). Более предпочтительно ангидраты и ансольваты согласно изобретению и в особенности кристаллическая форма А 1 могут характеризоваться, альтернативно или дополнительно, данными ИКспектроскопии, включающими одно или больше расположений полос (2 см-1), данных ниже, более предпочтительно включающими 9 или более расположений полос (2 см-1), данных ниже, еще более предпочтительно включающими 12 или более расположений полос (2 см-1), данных ниже, и в особенности включающими все расположения полос (2 см-1), данные ниже, предпочтительно вместе с относительными интенсивностями, данными в скобках: 3431 см-1 (s), 3339 см-1 (s), 3189 см-1 (s), 3031 см-1 (m), 2962 см-1 (m), 2872 см-1 (m), 1676 см-1 (s), 1660 Относительные интенсивности, данные в скобках, предпочтительно определяются в следующем виде:"s" = сильная (коэффициент пропускания предпочтительно 50%), "m" = средняя (предпочтительно 50%коэффициент пропускания 70%), "w" = слабая (коэффициент пропускания предпочтительно 70%). ИК или Инфракрасный спектр с Фурье-преобразованием предпочтительно получен при применении пеллеты KBr в качестве образца методики приготовления. Данные ИК-спектроскопии предпочтительно получены при помощи ИК-спектроскопии с Фурьепреобразованием, данные ИК-спектроскопии или данные ИК-спектроскопии с Фурье-преобразованием предпочтительно получены при помощи стандартных методик как описано в European Pharmacopeia 6 е Издание глава 2.02.24. Для измерения ИК-спектра с Фурье-преобразованием, предпочтительно применяется спектрометр Bruker Vector 22. ИК-спектры с Фурье-преобразованием предпочтительно откорректирован относительно базовой линии, предпочтительно, применяя программное обеспечение Bruker OPUS. ИК-спектр с Фурье-преобразованием ангидратов согласно изобретению и в частности кристаллической формы А 1 представлен на фиг. 5. Предпочтительно ангидраты или ансольваты согласно изобретению и в особенности кристаллическая форма А 1 могут характеризоваться, альтернативно или дополнительно, данными Раманспектроскопии включающими один или больше расположений полос (2 см-1), данных ниже, более предпочтительно включающими 9 или более расположений полос (2 см-1), данных ниже, еще более предпочтительно включающими 9 или более расположений полос (2 см-1), данных ниже, и в особенности включающими все расположения полос (2 см-1), данные ниже, предпочтительно вместе с относительными интенсивностями, данными в скобках: 3064 см-1 (w), 2976 см-1 (m), 2934 см-1 (m), 2912 см-1 (m),2881 см-1 (m), 1603 см-1 (w), 1209 см-1 (w), 1029 см-1 (w), 1003 см-1 (m), 852 см-1 (w). Более предпочтительно ангидраты или ансольваты согласно изобретению и в особенности кристаллическая форма A1 могут характеризоваться, альтернативно или дополнительно, данными Раманспектроскопии, включающими один или больше расположений полос (2 см-1), данных ниже, более предпочтительно включающими 12 или более расположений полос (2 см-1), данных ниже, еще более предпочтительно включающими 18 или более расположений полос (2 см-1), данных ниже, и в особенности включающими все расположения полос (2 см-1), данные ниже, предпочтительно вместе с относительными интенсивностями, данными в скобках: 3064 см-1 (w), 2976 см-1 (m), 2934 см-1 (m), 2912 см-1 (m), 2881 см-1 (m), 1677 см-1 (w), 1648 см-1 (w),1603 см-1 (w), 1584 см-1 (w), 1465 см-1 (w), 1407 см-1 (w), 1314 см-1 (w), 1242 см-1 (w), 1209 см-1 (w), 1129 см-1 (w), 1029 см-1 (w), 1003 см-1 (m), 943 см-1 (w), 901 см-1 (w), 852 см-1 (w), 623 см-1 (w), 589 см-1 (w). Относительные интенсивности, данные в скобках, предпочтительно определяются в следующем виде:"s" = сильная (относительная Раман-интенсивность предпочтительно 0,04), "m" = средняя (предпочтительно 0,04 относительная Раман-интенсивность 0,02), "w" = слабая (относительная Раманинтенсивность предпочтительно 0,02). Раман спектры или спектры Рамана с Фурье-преобразованием предпочтительно получены, применяя алюминиевые кюветы в качестве держателей образца для соответствующей твердой формы. Данные Раман-спектроскопии предпочтительно получены путем Раман-спектроскопии с Фурьепреобразованием, данные Раман-спектроскопии или данные Раман-спектроскопии с Фурьепреобразованием предпочтительно получены при помощи стандартных методик как описано в EuropeanPharmacopeia 6 е Издание глава 2.02.48. Для измерения Раман-спектров с Фурье-преобразованием, предпочтительно применяется спектрометр Bruker RFS 100. Раман-спектр с Фурье-преобразованием предпочтительно откорректирован относительно базовой линии, предпочтительно применяя программное обеспечение Bruker OPUS. Раман-спектр с Фурье-преобразованием ангидратов согласно изобретению и в частности кристаллической формы А 1 представлен на фиг. 6. Предпочтительно ангидраты или ансольваты согласно изобретению и в особенности кристаллическая форма А 1 могут характеризоваться, альтернативно или дополнительно, экспериментами динамической сорбции паров. Результаты могут быть получены при помощи стандартных методик как описано вVapour Sorption, и ссылки на нее). Поведение сорбции паров воды показывает невысокие уровни водопоглощения до 98% относительной влажности (ов или о.в.), и ангидраты или ансольваты согласно изобретению и в особенности кристаллическая форма А 1 могут быть классифицированы как негигроскопические согласно критериям Европейской Фармакопеи. Образование или преобразование в гидраты не наблюдается. Изотерма сорбции паров воды (25 С) кристаллической формы А 1 (SMS DVS Intrinsic) представлена на фиг. 7. Ангидраты или ансольваты согласно изобретению и в особенности кристаллическая форма А 1 показывают одну или больше характеристик, выбранных из выгодных характеристик, рассмотренных вы- 14022831 ше. Конкретнее, ангидраты или ансольваты согласно изобретению и в особенности кристаллическая форма А 1, как может быть показано, являются термодинамически стабильной ансольватированной формой и/или термодинамически стабильной формой и неожиданно термодинамически стабильной формой в присутствии растворителей на водной основе, предпочтительно включающие, но не ограниченные ими,суспензии и смачиваемый материал, и в частности в особенности водные системы, такие как водный раствор солей и т.п., такие как, но не ограниченные ими, суспензии и смачиваемый материал, и в особенности в таких водных системах при отсутствии метанола и/или этанола. Смачиваемый материал в этом отношении предпочтительно представляет собой смесь соответствующего ангидрата или ансольвата с по меньшей мере 5 мас.%, более предпочтительно по меньшей мере 10 мас.% и в особенности 20 мас.%,соответствующей водной системы. Конкретнее, ангидраты или ансольваты согласно изобретению и в особенности кристаллическая форма А 1 как может быть показано, являются термодинамически стабильный ансольватированной формой и/или термодинамически стабильной формой и неожиданно термодинамически стабильной формой даже при высокой относительной влажности. К тому же ангидраты согласно изобретению и в особенности кристаллическая форма А 1 показывают превосходные свойства с точки зрения поведения гигроскопичности, с физической стабильностью кристаллической формы по всему диапазону относительной влажности (0-98%) и/или кристалличность и поведение при тепловых нагрузках являются превосходными. Это приводит к превосходным свойствам подходящим для обработки (например, разделение фаз фильтрованием, сушкой, измельчением, микронизацией) и хранения, таким образом также делает их превосходными для состава суспензий. Ангидраты или ансольваты согласно изобретению и в особенности кристаллическая форма А 1 показывают превосходные свойства очистки соединения формулы I, поскольку может быть легко достигнуто уменьшение количества структурно родственных примесей, ионных соединений и остаточного растворителя. Таким образом, очистка может быть достигнута в одну стадию, при этом твердые формы, например, аморфные формы согласно обычным известным способам уровня техники, и/или другие неангидратные полиморфные кристаллические формы требуют значительно более высокого усилия для очистки в соответствии с стандартами GMP (Good Manufacturing Practice),например, три или более последующих стадий очистки. Соединение формулы I также образует класс псевдополиморфов, которые включают разные растворители в переменных количествах и/или соотношениях, предпочтительно соотношениях, и таким образом представляют собой сольваты. Эти сольваты структурно тесно связаны как показано, например,данными порошковой рентгеновской дифракции, включая индексацию этих форм, которая приводит к подобным элементарным ячейкам. Также выбранные примеры структур будут обсуждены на основании монокристаллической структуры и расчета структур на основании порошковых данных. Наконец будет дано обсуждение определенных выгодных свойств этого псевдополиморфного класса. Далее описаны три предпочтительных примера псевдополиморфных форм соединения согласно формуле I:S1 (предпочтительно также упоминаются как метанол-водный сольват и/или метанольный сольват),S2 (предпочтительно также упоминаются как этанол-водный сольват и/или этанольный сольват) иS3 (предпочтительно также упоминаются как гидрат и/или тетрагидрат). Эти предпочтительные примеры могут дополнительно быть охарактеризованы как тетрасольваты. Таким образом, твердые кристаллические формы с элементарной ячейкой с параметрами кристаллической рештки ULP1 как определено ранее предпочтительно дополнительно охарактеризованы в этом документе как сольваты и более предпочтительно как тетрасольваты. Сольваты и/или тетрасольваты предпочтительно включают одну или больше кристаллических форм, выбранных из S1, S2 и S3 как определено в этом документе, и предпочтительно также их смеси. Кристаллические формы S1, S2 и/или S3 предпочтительно дополнительно характеризуются как сольваты и в особенности как тетрасольваты, то есть они предпочтительно показывают приблизительно стехиометрическое количество молекул растворителя в соответствующей элементарной ячейке, которое составляет приблизительно до 4 молекул растворителя на элементарную ячейку и на молекулу соединения согласно формуле I. В этих сольватах и более предпочтительно в этих тетрасольватах молекулы растворителя предпочтительно выбраны из молекулы воды и спиртов и более предпочтительно выбраны из воды, метанола и этанола и их смесей. Соответственно, сольваты предпочтительно могут дополнительно характеризоваться как гидраты,спиртовые сольваты (или алкоголяты) или смешанные водно-спиртовые сольваты и более предпочтительно как гидраты, метанольные сольваты (или метанолаты), этанольные сольваты (или этанолаты),смешанные водно-метанольные сольваты, смешанные водно-этанольные сольваты или смешанные водаметанол-этанольные сольваты. Более определенно, если упомянутые сольваты получены из или были в контакте с смесями растворителей, например, смешанные сольваты могут быть получены перекристаллизацией из или кондиционированием с смесями растворителей. Особенно предпочтительно таким образом могут быть получены смешанные водно-спиртовые сольваты и в особенности смешанные водно- 15022831 метанольные сольваты, смешанные водно-этанольные сольваты и/или смешанные вода-метанолэтанольные сольваты. Дополнительно молекулы растворителя в пределах одного сольвата частично или полностью взаимозаменяемые для молекул растворителя другого растворителя. Таким образом ясно, что сольваты, более предпочтительно тетрасольваты, и в особенности кристаллические формы S1, S2 и S3 все принадлежат определенному классу твердых кристаллических форм. Предпочтительно тетрасольваты согласно изобретению, более предпочтительно тетрасольваты согласно изобретению, более предпочтительно тетрагидраты согласно изобретению и в особенности кристаллическая форма S3 могут характеризоваться альтернативно или дополнительно температурой плавления/разложения 210 С, более предпочтительно 2175 С точка плавления/разложения или выше, и в особенности 2175 С точка плавления/разложения. Предпочтительно точка плавления/температура разложения, полученная для тетрасольватов согласно изобретению, более предпочтительно тетрагидратов согласно изобретению и в особенности полученная для кристаллической формы S3250 С. Температуры плавления/разложения и/или поведение при термическом воздействии, описанные здесь, предпочтительно определены ДСК (дифференциальная сканирующая калориметрия) и ТГА (термогравиметрический анализ). Способы ДСК и/или ТГА или общие способы термоанализа и подходящие устройства для их определения известны в данной области техники, например из European Pharmacopeia 6 е Издание глава 2.02.34, где описаны стандартные методики. Более предпочтительно, для температур плавления/разложения или поведения и/или термоанализа в основном, применяются Mettler Toledo DSC 821 и/или Mettler Toledo TGA 851, предпочтительно как описано в European Pharmacopeia 6 е Издание глава 2.02.34. Измерение ДСК и ТГА, показывающие термический анализ (Mettler-Toledo DSC 821, 5 К/мин, продувка газообразным азотом 50 мл/мин; Mettler-Toledo TGA 851, 5 К/мин, продувка газообразным азотом 50 мл/мин) и температуры плавления/разложения, данные выше, показаны на фиг. 23 и 24. Предпочтительно тетрасольваты согласно изобретению, более предпочтительно тетрагидраты согласно изобретению и в особенности кристаллическая форма S3 могут характеризоваться, альтернативно или дополнительно, порошковой рентгеновской дифракцией и более предпочтительно дифракционной рентгенограммой, включающей один или больше пиков порошковой рентгеновской дифракции, данных ниже, более предпочтительно включающей 3 или более пиков порошковой рентгеновской дифракции,данных ниже, еще более предпочтительно 6 или более пиков порошковой рентгеновской дифракции,данных ниже, и в особенности включающей все из пиков порошковой рентгеновской дифракции, данных ниже: а) или более предпочтительно b) Предпочтительно тетрасольваты согласно изобретению, более предпочтительно тетрагидраты согласно изобретению и в особенности кристаллическая форма S3 могут характеризоваться, альтернативно или дополнительно, порошковой рентгеновской дифракцией, более предпочтительно дифракционной рентгенограммой, включающей один или больше пиков порошковой рентгеновской дифракции, данных ниже, более предпочтительно включающей 9 или более пиков порошковой рентгеновской дифракции,данных ниже, еще более предпочтительно 12 или более пиков порошковой рентгеновской дифракции,данных ниже, и в особенности включающей все из пиков порошковой рентгеновской дифракции, данных ниже : а) или более предпочтительно b) Предпочтительно тетрасольваты согласно изобретению, более предпочтительно тетрагидраты согласно изобретению и в особенности кристаллическая форма S3 могут характеризоваться, альтернативно или дополнительно, порошковой рентгеновской дифракцией и более предпочтительно дифракционной рентгенограммой, включающей один или больше пиков порошковой рентгеновской дифракции, данных ниже, более предпочтительно включающей 10 или более пиков порошковой рентгеновской дифракции,данных ниже, еще более предпочтительно 13 или более пиков порошковой рентгеновской дифракции,данных ниже, и в особенности включающей все из пиков порошковой рентгеновской дифракции, данных ниже : а) или более предпочтительно b) Фиг. 25 показывает порошковую рентгеновскую дифрактограмму кристаллической формы S3. Порошковая рентгеновская дифракция и более предпочтительно дифракционная рентгенограмма предпочтительно выполнены или определены как описано в этом документе и в особенности выполнены или определены при помощи стандартных методик как описано в European Pharmacopeia 6 е Издание глава 2.9.33, и еще более предпочтительно получены с параметрами Cu-K1 излучение и/или= 1.5406 ,предпочтительно на дифрактометре Stoe StadiP 611 KL. Предпочтительно тетрасольваты согласно изобретению, более предпочтительно тетрагидраты согласно изобретению и в особенности кристаллическая форма S3 могут характеризоваться, альтернативно или дополнительно, при помощи структурных данных рентгеноструктурного анализа, например, структурных данных рентгеноструктурного анализа, полученных на дифрактометре, предпочтительно оборудованном графитовым монохроматором и детектором CCD, предпочтительно, применяя Mo K излучение, предпочтительно при температуре 2985 К, и еще более предпочтительно на дифрактометре XCalibur от Oxford Diffraction, укомплектованном графитовым монохроматором и детектором CCD, применяя Мо K излучение при около 298 К. Согласно полученным структурным данным рентгеноструктурного анализа тетрагидраты соединения формулы I согласно изобретению и в особенности кристаллическая форма S3 кристаллизуется в орторомбической группе симметрии Р 21 21 21 с параметрами кристаллической рештки а = 9,6 , b = 25,9, с = 13,9(0,1 ) и размер элементарной ячейки предпочтительно составляет 3396 (10) 3. Из монокристаллической структуры очевидно, что форма S3 представляет тетрасольват и конкретнее тетрагидрат. Монокристаллическая рентгеновская структура изображена на фиг. 26. Дополнительная структурная информация на основании указанных структурных данных рентгеноструктурного анализа представлена на фиг. 26 а, 26b и 26 с. Предпочтительно тетрасольваты согласно изобретению, более предпочтительно тетрагидраты согласно изобретению и в особенности кристаллическая форма S3 могут характеризоваться, альтернативно или дополнительно, данными ИК-спектроскопии, включающими одно или больше расположений полос(2 см-1), данных ниже, более предпочтительно включающими 3 или более расположений полос (2 см-1),данных ниже, еще более предпочтительно включающими 6 или более расположений полос (2 см-1),данных ниже, и в особенности включающими все расположения полос (2 см-1), данные ниже, предпочтительно вместе с относительными интенсивностями, данными в скобках: 3319 см-1 (s), 3067 см-1 (s),2966 см-1 (s), 1668 см-1 (s), 1541 см-1 (s), 1395 см-1 (s), 704 см-1 (m) Более предпочтительно тетрасольваты согласно изобретению, более предпочтительно тетрагидраты согласно изобретению и в особенности кристаллическая форма S3 могут характеризоваться, альтернативно или дополнительно, данными ИК-спектроскопии, включающими одно или больше расположений полос (2 см-1), данных ниже, более предпочтительно включающими 6 или более расположений полос(2 см-1), данных ниже, еще более предпочтительно включающими 9 или более расположений полос (2 см-1), данных ниже, и в особенности включающими все расположения полос (2 см-1), данные ниже,предпочтительно вместе с относительными интенсивностями, данными в скобках: 3428 см-1 (s), 3319 см-1 (s), 3067 см-1 (s), 2966 см-1 (s), 2874 см-1 (m), 1668 см-1 (s), 1541 см-1 (s), 1455-1 см (s), 1395 см-1 (s), 1232 см-1 (m), 704 см-1 (m). Относительные интенсивности, данные в скобках, предпочтительно определяются в следующем виде:"s" = сильная (коэффициент пропускания предпочтительно 50%),"m" = средняя (предпочтительно 50%коэффициент пропускания 70%),"w" = слабая (коэффициент пропускания предпочтительно 70%). ИК или инфракрасный спектр с Фурье-преобразованием предпочтительно получен, применяя пеллеты KBr как образец способа приготовления. Данные ИК-спектроскопии предпочтительно получены ИК-спектроскопией с Фурьепреобразованием, данные ИК-спектроскопии или данные ИК-спектроскопии с Фурье-преобразованием предпочтительно получены при помощи стандартных методик как описано в European Pharmacopeia 6 е Издание глава 2.02.24. Для измерения ИК-спектра с Фурье-преобразованием предпочтительно применяется спектрометр Bruker Vector 22. ИК-спектр с Фурье-преобразованием предпочтительно откорректирован относительно базовой линии, предпочтительно применяя программное обеспечение Bruker OPUS. ИК-спектр с Фурье-преобразованием тетрасольватов согласно изобретению, более предпочтительно тетрагидратов согласно изобретению и в особенности кристаллической формы S3 представлен на фиг. 27. Предпочтительно тетрасольваты согласно изобретению, более предпочтительно тетрагидраты согласно изобретению и в особенности кристаллическая форма S3 могут характеризоваться, альтернативно или дополнительно, данными Раман-спектроскопии, включающими один или больше расположений полос (2 см-1), данных ниже, более предпочтительно включающими 4 или более расположений полос (2 см-1), данных ниже, еще более предпочтительно включающими 7 или более расположений полос(2 см-1), данных ниже, и в особенности включающими все расположения полос (2 см-1), данные ниже,предпочтительно вместе с относительными интенсивностями, данными в скобках: 3069 см-1 (m), 2931 см-1 (s), 1666 см-1 (m), 1607 см-1 (w), 1443 см-1 (w), 1339 см-1 (w), 1205 см-1 (w),1004 см-1 (s), 911 см-1 (m). Более предпочтительно тетрасольваты согласно изобретению, более предпочтительно тетрагидраты согласно изобретению и в особенности кристаллическая форма S3 могут характеризоваться, альтернативно или дополнительно, данными Раман-спектроскопии, включающими один или больше расположений (2 см-1), данных ниже, более предпочтительно включающими 9 или более расположений полос (2 см-1), данных ниже, еще более предпочтительно включающими 12 или более расположений полос (2 см 1), данных ниже, и в особенности включающими все расположения полос (2 см-1), данные ниже, предпочтительно вместе с относительными интенсивностями, данными в скобках: 3069 см-1 (m), 2931 см-1 (s), 1666 см-1 (m), 1607 см-1 (w), 1585 см-1 (w), 1443 см-1 (w), 1339 см-1 (w),1205 см-1 (w), 1122 см-1 (w), 1033 см-1 (w), 1004 см"1 (s), 936 см-1 (w), 911 см-1 (m), 825 см-1 (w), 624 см-1"s" = сильная (относительная Раман интенсивность предпочтительно 0,04), "m" = средняя (предпочтительно 0,04 относительная Раман интенсивность 0,02), "w" = слабая (относительная Раманинтенсивность предпочтительно 0,02) Раман-спекстры или спектры Рамана с Фурье-преобразованием предпочтительно получены, применяя алюминиевые кюветы в качестве держателей образца для соответствующей твердой формы. Данные Раман-спектроскопии предпочтительно получены путем Раман-спектроскопии с Фурьепреобразованием, данные Раман-спектроскопии или данные Раман-спектроскопии с Фурьепреобразованием предпочтительно получены при помощи стандартных методик как описано в EuropeanPharmacopeia 6 е Издание глава 2.02.24 и/или 2.02.48. Для измерения Раман-спектров с Фурьепреобразованием, предпочтительно применяется спектрометр Bruker RFS 100. Раман-спектр с Фурьепреобразованием предпочтительно откорректирован относительно базовой линии, предпочтительно применяя программное обеспечение Bruker OPUS. Раман-спектр с Фурье-преобразованием тетрасольватов согласно изобретению и в особенности кристаллической формы S3 представлен на фиг. 28. Предпочтительно тетрасольваты согласно изобретению, более предпочтительно тетрагидраты согласно изобретению и в особенности кристаллическая форма S3 могут характеризоваться, альтернативно или дополнительно, при помощи экспериментов динамической сорбции паров. Результаты могут быть получены при помощи стандартных методик как описано в Rolf Hilfiker, 'Polymorphism in the Pharmaceutical Industry', Wiley-VCH. Weinheim 2006 (Глава 9: Water Vapour Sorption, и ссылки на нее). Поведение сорбции паров воды показывает потерю молекул воды (пр. 9 мас. %) во время начального этапа высушивания (0% относительной влажности (ОВ. Во время цикла адсорбции воды при росте ОВ может быть показана ассоциация молекул воды в кристаллической решетке (пр. 10 мас.%). Во втором цикле десорбции может быть показана потеря этого количества воды. Изотерма сорбции паров воды(25 С) формы S3 показаны на фиг. 29. В целом данные термоанализа, представленные здесь, подтверждают структуру тетрагидрата с наблюдаемой полной дегидратацией при росте температура (для тетрагидрата вычисленное содержание воды составляет 10,9 мас.%) в ТГА. Данные сорбции паров воды показывают, что даже в сухих условиях 0% ОВ) при 25 С, выделяется только 9 мас.% воды, показывая, что предпочтительно не происходит полной дегидратации структуры. Изотерма сорбции паров воды (25 С) кристаллической формы S3 (SMS DVS Intrinsic) представлен на фиг. 29. Неожиданно было найдено, что молекулы воды внутри гидратов согласно изобретению и в особенности молекулы воды внутри тетрагидратов согласно изобретению могут быть замещены частично или полностью молекулами спирта, предпочтительно молекулами спирта, выбранного из группы, включающей моноолы, диолы или триолы, имеющие 1-6 атомов углерода, более предпочтительно моноолы, имеющие 1-4 атома углерода и в особенности моноолы, выбранные из группы, включающей метанол и этанол и их смеси. Экспериментальные способы, такие как эксперименты динамической сорбции паров/десорбции,эксперименты рентгеноструктурного анализа и/или эксперименты порошкового рентгеновского анализа показывают, что начиная например, с тетрагидрата охарактеризованного как кристаллической форме S3,молекулы воды упомянутого тетрагидрата могут быть частично и/или приблизительно полностью удалены из указанного тетрагидрата и/или заменены метанолом и/или этанолом. Например, эксперименты динамической сорбции паров/десорбции, предпочтительно применяющие испарения органических растворителей и/или воды, предпочтительно испарения органических растворителей, выбранных из одного или больше спиртов, предпочтительно спиртов как определено в этом доку- 19022831 менте, и/или воды и в особенности испарения метанола, этанола и/или воды, показывают, что молекулы воды из указанного тетрагидрата могут быть непрерывно заменены молекулами спирта и в особенности молекулами метанола и/или этанола, теоретически до тех пор пока образуется тетраспиртовой сольват или смешанный спиртово-водный сольват или тетрасольват. Как другой пример, создание определнных условий дляa) аморфного материала соединения согласно формуле I илиb) гидратных форм в смешанной водно-спиртовой атмосфере, предпочтительно водно-этанольной атмосфере, представляющей разные парциальные давления воды и спирта, приводит в обоих случаях к кристаллическим сольватам, показывающим разные стехиометрические составы, содержащие до 4 молекул воды или до 2 молекул этанола на молекулу соединения согласно формуле I, например тетрагидрат S3 (4 молекулы воды) или диэтанолат S2 (2 молекулы этанола, см., например, фиг. 31), в зависимости от соответствующих применяемых условий. Стехиометрические составы как определено титрованием Карла-Фишера для определения количества воды и HS-GC для определения количества этанола показаны на фиг. 30. В диаграмме также показано, что прослеживаются образованные определенные стехиометрические составы с более чем 4 молекулами воды на молекулу соединения согласно формуле I. Так как в кристаллической рештке тетрагидратов нет пространства более чем для 4 молекулы воды, избыточные количества более чем 4 молекул воды представляет адсорбированную влажность. Результаты (см. также пример 13) показывают, что с увеличением давления пара этанола происходит изменчивый переход из гидратной формы S3 в смешанную водно-этанольную или безводную этанольную сольватную форму S2. Все сольваты (включая гидраты) имеют сходные параметры кристаллической рештки, которые только незначительно увеличиваются с ассоциацией молекул этанола. Как еще другой пример, создание определнных условий для аморфной формы соединения согласно формуле I или гидратных форм в атмосфере метанола приводит к кристаллическим сольватам с 2 молекулами метанола на молекулу соединения согласно формуле I. Таким образом получают кристаллические формы, которые могут характеризоваться как тетрасольваты, которые имеют содержание растворителя между до примерно 100% воды (относится к 4 молекулам воды на молекулу соединения согласно формуле I, то есть относится к тетрагидрату) и содержанием растворителя до примерно 100% спирта (относится к 4 молекулам спирта на молекулу соединения согласно формуле I, то есть относится к тетраалкоголяту) и предпочтительно промежуточные соединения между ними. Результаты дополнительно рассмотренны выше и/или ниже и в особенности обсуждены в табл. 1 и 2, данных ниже. Например, метастабильные кристаллические сольваты, представляющие собой смешанные дигидрат-диалкоголяты (относящиеся к 2 молекулам воды и 2 молекулам спирта на молекулу соединения согласно формуле I), позднее детально охарактеризованы как дигидрат-диметанолат и кристаллическая форма S1 и как дигидрат-диэтанолат и кристаллическая форма S2, соответственно, могут быть получены и обсуждены детально выше и/или ниже. Эти стехиометрические составы происходят и/или выведены из описанных здесь экспериментов динамической сорбции паров. Новые рентгеновские эксперименты доказывают, что метастабильные кристаллические сольваты также могут присутствовать как смешанные дигидрат-алкоголяты или конкретнее дигидрат-моноалкоголяты (относящиеся к 2 молекулам воды и 1 молекуле спирта на молекулу соединения согласно формуле I) в качестве дополнительных проявлений этих нестехиометрических классов псевдополиморфов, позднее детально охарактеризованных как дигидрат-метанолат, дигидрат-монометанолат и/или другое проявление кристаллической формы S1,и как дигидрат-этанолат, дигидрат-моноэтанолат и/или другое проявление кристаллической формы S2,соответственно, могут быть получены и обсуждены детально выше и/или ниже. Специальная ссылка в этом отношении дана на табл. 1 и 2, данные ниже и параграфы, относящиеся к ним. Следующие таблицы показывают соответствующие расчетные гравиметрические содержания воды и/или метанола для тетрасольватов в диапазоне он тетрагидратов до тетраалкоголятов; в таком вычислении, применялись шаги целого числа в стехиометрическом составе сольвата на основании одной молекулы соединения согласно формуле I, и в общем четыре молекулы соответствующего растворителя или смеси растворителей в указанных тетрасольватах. Это может предпочтительно быть выражено следующими формулами:(для взаимного превращения между тетрагидратами и дигидрат-алкоголятами или конкретнее дигидрат-моноалкоголятами). ( = знак умножения). Таблица 1 (замена вода/метанол) В соответствующих экспериментах динамической сорбции паров, обсужденных здесь более детально, применяя пары метанола при 98% относительной насыщенности для Дигидрат-диметанолат/ кристаллической формы S1 при 25 С, начиная с тетрагидрата, было получено прибавление массы 9%. Это хорошо соответствует выше показанным результатам для тетраметанолата (вычислено 108,5 %, то есть 8,5% прибавления массы). В соответствующих экспериментах динамической сорбции паров, обсужденных здесь более детально, применяя испарение этанола при 98% относительной насыщенности для дигидратдиэтанолат/кристаллической формы S2 при 25 С, начиная с тетрагидрата, было получено прибавление массы 17%. Это хорошо соответствует выше показанным результатам для тетраэтанолата (вычислено 117,0%, то есть 17,0% прибавления массы). Как показано выше и/или ниже, тетрасольваты согласно изобретению предпочтительно являются превращаемыми, более предпочтительно превращаемыми, по существу, в чистые тетрагидраты и, по существу, чистые тетраалкоголяты и теоретически все промежуточные соединения между ними и предпочтительно их десольваты (показывая низкое содержание воды и/или спирта), предпочтительно представленные примерами: смешанные дигидрат-диалкоголяты, которые обсуждены детально выше и/или ниже,и дигидрат-алкоголяты или дигидрат-моноалкоголяты (которые описаны формулой [цикло-(Arg-Gly-AspDPhe-NMe-Val)][Спирт]х[Н 2 О](y) с 0 у 4 и х 2-0,5 у и х 1), и конкретнее S1 и/или S2. Поскольку такие тетрасольваты имеют очень подобные структурные особенности, например кристаллографические параметры, аналитические данные и/или физические свойства, а также являются превращаемыми, ясно, что такие тетрасольваты из класса или подкласса кристаллических форм согласно изобретению и/или твердых форм согласно изобретению. Соответственно, тетрасольваты являются предпочтительным объектом настоящего изобретения согласно изобретению, предпочтительно тетрасольваты как охарактеризовано в этом документе. Ввиду ясности, тетрасольваты, которые содержат три или более эквивалента воды (то есть имеют содержание воды 75 мол.%, в пересчете на общее количество растворителя, содержащегося в соответствующей кристаллической форме) и содержат менее, чем один эквивалент одного или больше растворителей отличимых от воды, предпочтительно менее, чем один эквивалент одного или больше спиртов,предпочтительно выбранных из метанола и этанола, предпочтительно упоминаются как гидраты, гидраты согласно изобретению или гидрат-тетрасольваты. Ввиду ясности, тетрасольваты, которые содержат близко к четырем эквивалентам воды (то есть имеют содержание воды 90 мол.% и предпочтительно 95 мол.%, в пересчете на общее количество растворителя, содержащегося в соответствующей кристаллической форме) предпочтительно упоминаются как тетрагидраты или тетрагидраты согласно изобретению. Ввиду ясности, тетрасолызаты, которые содержат один или больше эквивалентов спирта (то есть имеют содержание спирта 25 мол.% или выше, в пересчете на общее количество растворителя, содержащегося в соответствующей кристаллической форме) предпочтительно упоминаются как алкоголяты, алкоголяты согласно изобретению или алкоголят-тетрасольваты. Примерами таких алкоголятов или алкоголят-тетрасольватов являются метанолат и/или этанолат (или метанолат-тетрасольват и/или этанолаттетрасольват) согласно изобретению. Ввиду ясности, тетрасольваты, которые содержат близко к четырем эквивалентам одного или больше спиртов (то есть имеют общее содержание спирта 90 мол. % и предпочтительно 95 мол.%, в пересчете на общее количество растворителя, содержащегося в соответствующей кристаллической форме) предпочтительно упоминаются как тетраалкоголяты или тетраалкоголяты согласно изобретению. Примерами таких тетраалкоголяты являются тетраметанолат и/или тетраэтанолат или тетраметанолат и/или тетраэтанолат согласно изобретению. Еще два тетрасольвата, которые могут быть описаны как спиртовые сольваты, алкоголяттетрасольваты или их десольваты или более предпочтительно описаны как дигидрат-диалкоголяты, дигидрат-алкоголяты или дигидрат-моноалкоголяты, описаны ниже: Предпочтительно, тетрасольваты согласно изобретению, более предпочтительно дигидратдиметанолат, дигидрат-метанолат, дигидрат-моноэтанолат, диметанолат и/или их десольваты и в особенности кристаллическая форма S1 могут характеризоваться, альтернативно или дополнительно, температурой плавления/разложения 205 С, более предпочтительно 2105 С температурой плавления/разложения С или выше, и в особенности 2105 С температурой плавления/разложения. Предпочтительно указанная температура плавления/разложения, полученная для тетрасольватов согласно изобретению, более предпочтительно полученная для дигидрат-диметанолата, дигидрат-метанолата, дигидрат-моноэтанолата, диметанолата и/или их десольватов и в особенности полученная для кристаллической формы S1 составляет 250 С. Температура плавления/разложения и/или поведение при термическом воздействии, описанные здесь, предпочтительно определены ДСК (дифференциальная сканирующая калориметрия) и ТГА (термогравиметрический анализ). Способы ДСК и/или ТГА или общие термоаналитические способы и подходящие устройства для их определения известны в данной области техники, например из EuropeanPharmacopeia 6 е Издание глава 2.02.34, где описаны стандартные методики. Более предпочтительно, для температур плавления/разложения или поведения и/или термоанализа в основном, применяются MettlerToledo DSC 821 и/или Mettler Toledo TGA 851, предпочтительно как описано в European Pharmacopeia 6 е Издание глава 2.02.34. Измерения ДСК и ТГА, показывающие термический анализ (Mettler-Toledo DSC 821, 5 К/мин, продувка газообразным азотом 50 мл/мин; Mettler-Toledo TGA 851, 5 К/мин, продувка газообразным азотом 50 мл/мин) и температуры плавления/разложения, данные выше, показаны на фиг. 8 и 9. Предпочтительно тетрасольваты согласно изобретению, более предпочтительно дигидратдиметанолат, дигидрат-метанолат, дигидрат-моноэтанолат, диметанолат и/или их десольваты и в особенности кристаллическая форма S1 могут характеризоваться, альтернативно или дополнительно, порошковой рентгеновской дифракцией и более предпочтительно дифракционной рентгенограммой, включающей один или больше пиков порошковой рентгеновской дифракции, данных ниже, более предпочтительно включающей 6 или более пиков порошковой рентгеновской дифракции, данных ниже, еще более предпочтительно 9 или более пиков порошковой рентгеновской дифракции, данных ниже, и в особенности включающей все из пиков порошковой рентгеновской дифракции, данные ниже: Предпочтительно тетрасольваты согласно изобретению, более предпочтительно дигидратдиметанолат, дигидрат-метанолат, дигидрат-моноэтанолат, диметанолат и/или их десольваты, и в особенности кристаллическая форма S1 могут характеризоваться, альтернативно или дополнительно, порошковой рентгеновской дифракциейболее предпочтительно дифракционной рентгенограммой, включающей один или больше пиков порошковой рентгеновской дифракции, данных ниже, более предпочтительно включающей 8 или более пиков порошковой рентгеновской дифракции, данных ниже, еще более предпочтительно 12 или более пиков порошковой рентгеновской дифракции, данных ниже, и в особенности включающей все из пиков порошковой рентгеновской дифракции, данных ниже: Предпочтительно тетрасольваты согласно изобретению, более предпочтительно дигидратдиметанолат, дигидрат-метанолат, дигидрат-моноэтанолат, диметанолат и/или их десольваты и в особенности кристаллическая форма S1 могут характеризоваться, альтернативно или дополнительно, порошковой рентгеновской дифракцией и более предпочтительно дифракционной рентгенограммой, включающей один или больше пиков порошковой рентгеновской дифракции, данных ниже, более предпочтительно включающей 10 или более пиков порошковой рентгеновской дифракции, данных ниже, еще более предпочтительно 12 или более пиков порошковой рентгеновской дифракции, данных ниже, и в особенности включающей все из пиков порошковой рентгеновской дифракции, данные ниже : Порошковая рентгеновская дифрактограмма кристаллической формы S1 показана на фиг. 10. ПРД диаграмма может быть успешно проиндексирована соответственно следующей моноклинной элементарной ячейки (группа симметрии Р 21): а = 9,4 , b = 25,9 , с = 14,1(0,1 ),= 91,2 (0,1),V3430 ( 10) 3. Порошковая рентгеновская дифракция и более предпочтительно дифракционная рентгенбграмма предпочтительно выполнены или определены как описано в этом документе и в особенности выполнены или определены при помощи стандартных методик как описано в European Pharmacopeia 6 е Издание глава 2.9.33, и еще более предпочтительно получены с параметрами Cu-K1 излучение и/или= 1,5406 ,предпочтительно на дифрактометре Stoe StadiP 611 KL. Предпочтительно тетрасольваты согласно изобретению, более предпочтительно дигидратдиметанолат, дигидрат-метанолат, дигидрат-моноэтанолат, диметанолат и/или их десольваты, и в особенности кристаллическая форма S1 могут характеризоваться, альтернативно или дополнительно, при помощи структурных данных рентгеноструктурного анализа, например, структурных данных рентгеноструктурного анализа, полученных на дифрактометре, предпочтительно оборудованном графитовым монохроматором и детектором CCD, предпочтительно, применяя Mo K излучение, предпочтительно при температуре 2985 К, и еще более предпочтительно на дифрактометре XCalibur от Oxford Diffraction,укомплектованном графитовым монохроматором и детектором CCD, применяя Mo K излучение при около 298 К. Предпочтительно тетрасольваты согласно изобретению, более предпочтительно дигидратдиметанолат, дигидрат-метанолат, дигидрат-моноэтанолат, диметанолат и/или их десольваты, и в особенности кристаллическая форма S1 могут характеризоваться, альтернативно или дополнительно, данными ИК-спектроскопии, включающими одно или больше расположений полос (2 см-1), данных ниже,более предпочтительно включающими 3 или более расположений полос (2 см-1), данных ниже, еще более предпочтительно включающими 6 или более расположений полос (2 см-1),данных ниже, и в особенности включающими все расположения полос (2 см-1), данные ниже, предпочтительно вместе с относительными интенсивностями, данными в скобках: 3311 см-1 (s), 2965 см-1 (m), 2875 см-1 (w), 1668 см-1(s), 1542 см-1 (s), 1396 см-1 (m), 1028 см-1 (w), 707 см-1 (m). Более предпочтительно тетрасольваты согласно изобретению, более предпочтительно дигидратдиметанолат, дигидрат-метанолат, дигидрат-моноэтанолат, диметанолат и/или их десольваты, и в особенности кристаллическая форма S1 могут характеризоваться, альтернативно или дополнительно, данными ИК-спектроскопии, включающими одно или больше расположений полос (2 см-1), данных ниже,более предпочтительно включающими 6 или более расположений полос (2 см-1), данных ниже, еще более предпочтительно включающими 9 или более расположений полос (2 см-1), данных ниже, и в особенности включающими все расположения полос (2 см-1), данные ниже, предпочтительно вместе с относительными интенсивностями, данными в скобках:- 23022831 3311 см-1 (s), 3067 см-1 (m), 2965 см-1 (m), 2937 см-1 (m), 2875 см-1 (w), 1668 см-1 (s), 1542 см-1 (s),1456 см-1 (m), 1396 см-1 (m), 1028 см-1 (w), 707 см-1 (m). Относительные интенсивности, данные в скобках, предпочтительно определяются в следующем виде:"s" = сильная (коэффициент пропускания предпочтительно 50%), "m" = средняя (предпочтительно 50%коэффициент пропускания 70%), "w" = слабая (коэффициент пропускания предпочтительно 70%). ИК или инфракрасный спектр с Фурье-преобразованием предпочтительно получен, применяя пеллеты KBr как образец способа приготовления. Данные ИК-спектроскопии предпочтительно получены ИК-спектроскопией с Фурьепреобразованием, данные ИК-спектроскопии или данные ИК-спектроскопии с Фурье-преобразованием предпочтительно получены при помощи стандартных методик как описано в European Pharmacopeia 6 е Издание глава 2.02.24. Для измерения ИК-спектра с Фурье-преобразованием, предпочтительно применяется спектрометр Bruker Vector 22. ИК-спектр с Фурье-преобразованием предпочтительно откорректирован относительно базовой линии, предпочтительно применяя программное обеспечение Bruker OPUS. ИК-спектр с Фурье-преобразованием тетрасольватов согласно изобретению, более предпочтительно дигидрат-диметанолата, дигидрат-метанолата, дигидрат-моноэтанолата, диметанолата и/или их десольватов, и в особенности кристаллической формы S1 представлен на фиг. 11. Предпочтительно тетрасольваты согласно изобретению, более предпочтительно дигидратдиметанолат, дигидрат-метанолат, дигидрат-моноэтанолат, диметанолат и/или их десольваты, и в особенности кристаллическая форма S1 могут характеризоваться, альтернативно или дополнительно, данными Раман-спектроскопии, включающими одно или больше расположений полос (2 см-1), данных ниже, более предпочтительно включающими 5 или более расположений полос (2 см-1), данных ниже, еще более предпочтительно включающими 8 или более расположений полос (2 см-1), данных ниже, и в особенности включающими все расположения полос (2 см-1), данные ниже, предпочтительно вместе с относительными интенсивностями, данными в скобках: 3067 см-1 (w), 2936 см-1 (s), 1668 см-1 (m), 1606 см-1 (w), 1446 см-1 (w), 1338 см-1 (w), 1203 см-1 (w),1033 см-1 (w), 1004 см-1 (s), 904 см-1 (m), 624 см-1 (w). Более предпочтительно тетрасольваты согласно изобретению, более предпочтительно дигидратдиметанолат, дигидрат-метанолат, дигидрат-моноэтанолат, диметанолат и/или их десольваты, и в особенности кристаллическая форма S1 могут характеризоваться, альтернативно или дополнительно, данными Раман-спектроскопии, включающими один или больше расположений (2 см-1), данных ниже, более предпочтительно включающими 9 или более расположений полос (2 см-1), данных ниже, еще более предпочтительно включающими 12 или более расположений полос (2 см-1), данных ниже, и в особенности включающими все расположения полос (2 см-1), данные ниже, предпочтительно вместе с относительными интенсивностями, данными в скобках: 3067 см-1 (w), 2936 см-1 (s), 1668 см-1 (m), 1606 см-1 (w), 1585 см-1 (w), 1446 см-1 (w), 1338 см-1 (w),1203 см-1 (w), 1123 см-1 (w), 1033 см-1 (w), 1004 см-1 (s), 904 см-1 (m), 824 см-1 (w), 624 см-1 (w), 523 см-1"s" = сильная (относительная Раман интенсивность предпочтительно 0,04), "m" = средняя (предпочтительно 0,04 относительная Раман интенсивность 0,02), "w" = слабая (относительная Раман интенсивность предпочтительно 0,02). Раман-спекстры или спектры Рамана с Фурье-преобразованием предпочтительно получены, применяя алюминиевые кюветы в качестве держателей образца для соответствующей твердой формы. Данные Раман-спектроскопии предпочтительно получены путем Раман-спектроскопии с Фурьепреобразованием, данные Раман-спектроскопии или данные Раман-спектроскопии с Фурьепреобразованием предпочтительно получены при помощи стандартных методик как описано в EuropeanPharmacopeia 6 е Издание глава 2.02.48. Для измерения Раман-спектров с Фурье-преобразованием, предпочтительно применяется спектрометр Bruker RFS 100. Раман-спектр с Фурье-преобразованием предпочтительно откорректирован относительно базовой линии, предпочтительно применяя программное обеспечение Bruker OPUS. Раман-спектр с Фурье-преобразованием тетрасольватов согласно изобретению и в особенности кристаллической формы S1 представлен на фиг. 12. Предпочтительно тетрасольваты согласно изобретению, более предпочтительно дигидратдиметанолат, дигидрат-метанолат, дигидрат-моноэтанолат, диметанолат и/или их десольваты, и в особенности кристаллическая форма S1 могут характеризоваться, альтернативно или дополнительно, экспериментами динамического испарения, применяя пары воды и/или пары метанола. Результаты могут быть получены при помощи стандартных методик как описано в Rolf Hilfiker, 'Polymorphism in the Pharmaceutical Industry', Wiley-VCH. Weinheim 2006 (Глава 9: Water Vapour Sorption, и ссылки на нее). Поведение сорбции паров воды тетрасольватов согласно изобретению, более предпочтительно дигидрат-диметанолата, дигидрат-метанолата, дигидрат-моноэтанолата, диметанолата и/или их десольватов, и в особенности кристаллической формы S1 показывает потерю массы приблизительно 8 мас.% в первом цикле десорбции (которая немного ниже, чем наблюдаемое прибавление массы метанола в эксперименте сорбции паров метанола). В результате адсорбции паров воды, в кристаллической решетке наблюдается ассоциация молекул воды, с максимальным прибавлением массы приблизительно 8 мас.% при росте ов. Во втором цикле десорбции наблюдается общая потеря массы приблизительно 9,9 мас.%. Для дигидрат Ди-Метанолата соединения формулы I, вычисленное содержание метанола равно 9,3 мас.%. Форма S1 как может быть показано, являются термодинамически стабильной формой в атмосфере 100% паров метанола. Изотерма сорбции паров воды (25 С) кристаллической формы S1 (SMS DVS Intrinsic) представлен на фиг. 13. Изотерма сорбции паров метанола (25 С) гидратной формы для формы S1(SMS DVS Advantage) фиг. 14. Таким образом, кристаллическая форма S1 представляет собой кристаллическую метанольную сольватную форму или смешанную вода/метанол сольватную форму, предпочтительно выбранную из дигидрат-метанолат, дигидрат-моноэтанолат, диметанолат и/или их десольватов, которые могут быть получены например, сорбцией паров метанола, предпочтительно сорбцией паров метанола, начиная с гидратной структуры, такой как гидраты согласно изобретению и в особенности тетрагидрат согласно изобретению, то есть кристаллическая форма S3. С кривой сорбции паров метанола как показано на фиг. 13 и как рассмотрено выше, может быть заметно, что при росте парциального давления метанола, приблизительно 9 мас.% метанола поглощаются образцом. Предпочтительно тетрасольваты согласно изобретению, более предпочтительно дигидратдиэтанолат, дигидрат-этанолат, дигидрат-моноэтанолат, диэтанолат и/или их десольваты, и в особенности кристаллическая форма S2 могут характеризоваться, альтернативно или дополнительно, температурой плавления/разложения 205 С, более предпочтительно 2105 С температурой плавления/разложения С или выше, и в особенности 2105 С температурой плавления/разложения. Предпочтительно, указанная температура плавления/разложения, полученная для тетрасольватов согласно изобретению, более предпочтительно дигидрат-диэтанолата, дигидрат-этанолата, дигидрат-моноэтанолата, диэтанолата и/или их десольватов, и в особенности полученная для кристаллической формы S2 составляет 250 С. Температуры плавления/разложения и/или поведение при термическом воздействии, описанные здесь, предпочтительно определены ДСК (дифференциальная сканирующая калориметрия) и ТГА (термогравиметрический анализ). Способы ДСК и/или ТГА или общие способы термоанализа и подходящие устройства для их определения известны в данной области техники, например из European Pharmacopeia 6 е Издание глава 2.02.34, где описаны стандартные методики. Более предпочтительно, для температур плавления/разложения или поведения и/или термоанализа в основном, применяются Mettler Toledo DSC 821 и/или Mettler Toledo TGA 851, предпочтительно как описано в European Pharmacopeia 6 е Издание глава 2.02.34. Измерения ДСК и ТГА, показывающие термический анализ (Mettler-Toledo DSC 821, 5 К/мин, продувка газообразным азотом 50 мл/мин; Mettler-Toledo TGA 851, 5 К/мин, продувка газообразным азотом 50 мл/мин) и температуры плавления/разложения, данные выше, показаны на фиг. 15 и 16. Предпочтительно тетрасольваты согласно изобретению, более предпочтительно дигидратдиэтанолат, дигидрат-этанолат, дигидрат-моноэтанолат, диэтанолат и/или их десольваты, и в особенности кристаллическая форма S2 могут характеризоваться, альтернативно или дополнительно, порошковой рентгеновской дифракцией и более предпочтительно дифракционной рентгенограммой, включающей один или больше пиков порошковой рентгеновской дифракции, данных ниже, более предпочтительно включающей 3 или более пиков порошковой рентгеновской дифракции, данных ниже, еще более предпочтительно 5 или более пиков порошковой рентгеновской дифракции, данных ниже, и в особенности включающей все из пиков порошковой рентгеновской дифракции, данных ниже: а) или более предпочтительно b) Предпочтительно тетрасольваты согласно изобретению, более предпочтительно дигидратдиэтанолат, дигидрат-этанолат, дигидрат-моноэтанолат, диэтанолат и/или их десольваты, и в особенности кристаллическая форма S2 могут характеризоваться, альтернативно или дополнительно, порошковой рентгеновской дифракцией, более предпочтительно дифракционной рентгенограммой, включающей один или больше пиков порошковой рентгеновской дифракции, данных ниже, более предпочтительно включающей 4 или более пиков порошковой рентгеновской дифракции, данных ниже, еще более предпочтительно 6 или более пиков порошковой рентгеновской дифракции, данных ниже, и в особенности включающей все из пиков порошковой рентгеновской дифракции, данных ниже: а) или более предпочтительно b) Предпочтительно, тетрасольваты согласно изобретению, более предпочтительно дигидратдиэтанолат, дигидрат-этанолат, дигидрат-моноэтанолат, диэтанолат и/или их десольваты, и в особенности кристаллическая форма S2 могут характеризоваться, альтернативно или дополнительно, порошковой рентгеновской дифракцией и более предпочтительно дифракционной рентгенограммой, включающей один или больше пиков порошковой рентгеновской дифракции, данных ниже, более предпочтительно включающей 10 или более пиков порошковой рентгеновской дифракции, данных ниже, еще более предпочтительно 12 или более пиков порошковой рентгеновской дифракции, данных ниже, и в особенности включающей все из пиков порошковой рентгеновской дифракции, данных ниже : а) или более предпочтительно b) Порошковая рентгеновская дифрактограмма кристаллической формы S2 показана на фиг. 17. ПРД диаграмма может быть успешно проиндексирована следующей орторомбической элементарной ячейкой (группа симметрии P212121): а = 9,3 , b = 26,6 , с = 14,7( 0,1 ), V3600 ( 10) 3. Порошковая рентгеновская дифракция и более предпочтительно дифракционная рентгенограмма предпочтительно выполнены или определены как описано в этом документе и в особенности выполнены или определены при помощи стандартных методик как описано в European Pharmacopeia 6 е Издание глава 2.9.33, и еще более предпочтительно получены с параметрами Cu-K1 излучение и/или= 1,5406 ,предпочтительно на дифрактометре Stoe StadiP 611 KL. Предпочтительно тетрасольваты согласно изобретению, более предпочтительно дигидратдиэтанолат, дигидрат-этанолат, дигидрат-моноэтанолат, диэтанолат и/или их десольваты, и в особенности кристаллическая форма S2 могут характеризоваться, альтернативно или дополнительно, при помощи структурных данных рентгеноструктурного анализа, например, структурных данных рентгеноструктурного анализа, полученных на дифрактометре, предпочтительно оборудованном графитовым монохроматором и детектором CCD, предпочтительно, применяя Mo K излучение, предпочтительно при температуре 2985 К, и еще более предпочтительно на дифрактометре XCalibur от Oxford Diffraction, укомплектованном графитовым монохроматором и детектором CCD, применяя Mo K излучение при около 298 K. Согласно полученным структурным данным рентгеноструктурного анализа тетрасольваты согласно изобретению, более предпочтительно дигидрат-диэтанолат, дигидрат-этанолат, диэтанолат и/или их десольваты, и в особенности кристаллическая форма S2, кристаллизованы в орторомбической группе симметрии Р 212121 с параметрами кристаллической рештки а = 9,3 , b = 26,3 , с = 13,7( 0,1 ) и размер элементарной ячейки предпочтительно составляет 3351 (10) 3. Из монокристаллической структуры очевидно, что форма S2 представляет тетрасольват согласно изобретению и конкретнее смешанный этанол-водный сольват, а еще конкретнее дигидратмоноэтанолат. Монокристаллическая рентгеновская структура изображена на фиг. 32. Предпочтительно тетрасольваты согласно изобретению, более предпочтительно дигидратдиэтанолат, дигидрат-этанолат, дигидрат-моноэтанолат, диэтанолат и/или их десольваты, и в особенности кристаллическая форма S2 могут характеризоваться, альтернативно или дополнительно, данными ИК-спектроскопии, включающими одно или больше расположений полос (2 см-1), данных ниже, более предпочтительно включающими 3 или более расположений полос (2 см-1), данных ниже, еще более предпочтительно включающими 6 или более расположений полос (2 см-1), данных ниже, и в особенности включающими все расположения полос (2 см-1), данные ниже, предпочтительно вместе с относительными интенсивностями, данными в скобках: 3306 см-1 (s), 2968 см-1 (m), 1668 см-1 (s), 1546 см-1 (s), 1395 см-1 (m), 1223 см-1 (w), 1049 см-1 (w), 705-1 см (w). Более предпочтительно тетрасольваты согласно изобретению, более предпочтительно дигидратдиэтанолат, дигидрат-этанолат, дигидрат-моноэтанолат, диэтанолат и/или их десольваты, и в особенности кристаллическая форма S2 могут характеризоваться, альтернативно или дополнительно, данными ИК-спектроскопии, включающими одно или больше расположений полос (2 см-1), данных ниже, более предпочтительно включающими 6 или более расположений полос (2 см-1), данных ниже, еще более предпочтительно включающими 9 или более расположений полос (2 см-1), данных ниже, и в особенности включающими все расположения полос (2 см-1), данные ниже, предпочтительно вместе с относительными интенсивностями, данными в скобках: 3306 см-1 (s), 2968 см-1 (m), 2872 см-1 (m), 1668 см-1 (s), 1546 см-1 (s), 1452 см-1 (w), 1395 см-1 (m),1223 см-1 (w), 1086 см-1 (w), 1049 см-1 (w), 746 см-1 (w), 705 см-1 (w). Относительные интенсивности, данные в скобках, предпочтительно определяются в следующем виде:"s" = сильная (коэффициент пропускания предпочтительно 50%), "m" = средняя (предпочтительно 50%коэффициент пропускания 70%), "w" = слабая (коэффициент пропускания предпочтительно 70%). ИК или инфракрасный спектр с Фурье-преобразованием предпочтительно получен, применяя пеллеты KBr как образец способа приготовления. Данные ИК-спектроскопии предпочтительно получены ИК-спектроскопией с Фурьепреобразованием, данные ИК-спектроскопии или данные ИК-спектроскопии с Фурье-преобразованием предпочтительно получены при помощи стандартных методик как описано в European Pharmacopeia 6 е Издание глава 2.02.24. Для измерения ИК-спектра с Фурье-преобразованием, предпочтительно применяется спектрометр Bruker Vector 22. ИК-спектр с Фурье-преобразованием предпочтительно откорректирован относительно базовой линии, предпочтительно применяя программное обеспечение Bruker OPUS. ИК-спектр с Фурье-преобразованием тетрасольватов согласно изобретению и в особенности кристаллической формы S2 представлен на фиг. 18. Предпочтительно тетрасольваты согласно изобретению и более предпочтительно дигидрат- 27022831 диэтанолат, дигидрат-этанолат, дигидрат-моноэтанолат, диэтанолат и/или их десольваты, в особенности кристаллическая форма S2 могут характеризоваться, альтернативно или дополнительно, данными Раманспектроскопии, включающими одно или больше расположений полос (2 см-1), данных ниже, более предпочтительно включающими 5 или более расположений полос (2 см-1), данных ниже, еще более предпочтительно включающими 8 или более расположений полос (2 см-1), данных ниже, и в особенности включающими все расположения полос (2 см-1), данные ниже, предпочтительно вместе с относительными интенсивностями, данными в скобках: 3068 см-1 (w), 2934 см-1 (s), 1668 см-1 (w), 1606 см-1 (w), 1449 см-1 (w), 1337 см-1 (w), 1204 см-1 (w),1120 см-1 (w), 1004 см-1 (m), 904 см-1 (w), 825 см-1 (w), 624 см-1 (w), 521 см-1 (w). Более предпочтительно тетрасольваты согласно изобретению, более предпочтительно дигидратдиэтанолат, дигидрат-этанолат, дигидрат-моноэтанолат, диэтанолат и/или их десольваты, и в особенности кристаллическая форма S2 могут характеризоваться, альтернативно или дополнительно, данными Раман-спектроскопии, включающими один или больше расположений (2 см-1), данных ниже, более предпочтительно включающими 9 или более расположений полос (2 см-1), данных ниже, еще более предпочтительно включающими 12 или более расположений полос (2 см-1), данных ниже, и в особенности включающими все расположения полос (2 см-1), данные ниже, предпочтительно вместе с относительными интенсивностями, данными в скобках: 3068 см-1 (w), 2934 см-1 (s), 1668 см-1 (w), 1606 см-1 (w), 1586 см-1 (w), 1449 см-1 (w), 1337 см-1 (w),1204 см-1 (w), 1120 см-1 (w), 1033 см-1 (w), 1004 см-1 (m), 904 см-1 (w), 825 см-1 (w), 624 см-1 (w), 521 см-1s = сильная (относительная Раман интенсивность предпочтительно 0,04), "m" = средняя (предпочтительно 0,04 относительная Раман интенсивность 0,02), "w" = слабая (относительная Раман интенсивность предпочтительно 0,02). Раман-спекстры или спектры Рамана с Фурье-преобразованием предпочтительно получены, применяя алюминиевые кюветы в качестве держателей образца для соответствующей твердой формы. Данные Раман-спектроскопии предпочтительно получены путем Раман-спектроскопии с Фурьепреобразованием, данные Раман-спектроскопии или данные Раман-спектроскопии с Фурье-преобразованием предпочтительно получены при помощи стандартных методик как описано в European Pharmacopeia 6 е Издание глава 2.02.48. Для измерения Раман-спектров с Фурье-преобразованием, предпочтительно применяется спектрометр Bruker RFS 100. Раман-спектр с Фурье-преобразованием предпочтительно откорректирован относительно базовой линии, предпочтительно применяя программное обеспечение Bruker OPUS. Раман-спектр с Фурье-преобразованием тетрагидратов согласно изобретению, более предпочтительно дигидрат-диэтанолата, дигидрат-этанолата, дигидрат-моноэтанолата, диэтанолата и/или их десольватов, и в особенности кристаллической формы S2 представлен на фиг. 19. Предпочтительно тетрасольваты согласно изобретению, более предпочтительно дигидратдиэтанолат, дигидрат-этанолат, дигидрат-моноэтанолат,д и/или их десольваты, и в особенности кристаллическая форма S2 могут характеризоваться, альтернативно или дополнительно, экспериментами динамического испарения, применяя пары воды и/или пары метанола. Результаты могут быть получены при помощи стандартных методик как описано в Rolf Hilfiker, 'Polymorphism in the Pharmaceutical Industry',Wiley-VCH. Weinheim 2006 (Глава 9: Water Vapour Sorption, и ссылки на нее). Поведение сорбции паров воды тетрасольватов согласно изобретению, более предпочтительно дигидрат-диэтанолата, дигидрат-этанолата, дигидрат-моноэтанолата, диэтанолата и/или их десольватов, и в особенности кристаллической формы S2 показывает потерю массы приблизительно 6,5 мас.% в первом цикле десорбции (которое менее, чем наблюдаемое прибавление массы этанола в эксперименте сорбции паров этанола). В результате адсорбции паров воды, в кристаллической решетке наблюдается ассоциация молекул воды, с максимальным прибавлением массы приблизительно 6,4 мас.% при росте ОВ. Во втором цикле десорбции наблюдается общая потеря массы приблизительно 9,2 мас.%. Для дигидрат-диэтанолата соединения формулы I, вычисленное содержание этанола равно 12,5 мас.%. Форма S2 как может быть показано, являются термодинамически стабильной формой в атмосфере 100% паров этанола. Изотерма сорбции паров воды (25 С) кристаллической формы S2 (SMS DVS Intrinsic) представлена на фиг. 20. Изотерма сорбции паров этанола (25 С) гидратной формы для формы S2 (SMS DVS Advantage) представлен на фиг. 21. Таким образом, кристаллическая форма S2 представляет собой кристаллическую этанольную сольватную форму или смешанную вода/этанол сольватную форму, предпочтительно выбранную из дигидратэтанолата, дигидрат-моноэтанолата, диэтанолата и/или их десольватов, которые могут быть получены например, сорбцией паров этанола, предпочтительно сорбцией паров этанола, начиная с гидратной структуры, такой как гидраты согласно изобретению и в особенности тетрагидрат согласно изобретению,то есть кристаллическая форма S3. С кривой сорбции паров этанола как показано на фиг. 21 и как рас- 28022831 смотрено выше, может быть заметно, что при росте парциального давления этанола, приблизительно 17 мас.% этанола поглощаются образцом. Как может быть отмечено из данных, представленных и обсужденных здесь, сольваты и в особенности тетрасольваты соединения формулы I из класса новых кристаллических форм (дополнительно также называемые псевдополиморфные формы или аббревиатурой ПП) базирующиеся на том же самом структурном типе, имея очень подобные физические свойства и являющиеся легко превращаемыми,предпочтительно с потенциально получаемыми всеми переходными формами и особенно с потенциально получаемыми всеми переходными формами между псевдополиморфными формами, описанными здесь. Подобие структурного типа дополнительно показано наложением кривой ПРД диаграмм трех выбранных псевдополиморфов S1, S2 и S3, данных на фиг. 22. Может быть заметно, что все три выбранные псевдополиморфы показаны очень подобным ПРД диаграммами, и, кроме того, приводят в основном к тем же самым элементарным ячейкам, поскольку замена воды метанолом или этанолом приводит только к небольшому расширению элементарных ячеек и таким образом к небольшомуувеличению объема элементарной ячейки. Как ожидалось из молярных объмов растворителей, это является более явным для этанольного сольвата, чем для метанольного сольвата. В присутствии спиртов, предпочтительно метанола, и/или этанола, и/или воды, присутствующих в различных концентрациях или парциальных давлениях, легко происходит взаимное превращение в пределах псевдополиморфного класса, включающего сольваты и в особенности тетрасольваты согласно изобретению. Поскольку спирты, предпочтительно метанол и/или этанол, являются полезными растворителями в производственном процессе, использование псевдополиморфов предпочтительно является выгодной для получения соединения формулы I в кристаллической твердотельной модификации, показывающей полезно высокую растворимость, объединенную с хорошей кристалличностью. Сольваты и в особенности тетрасольваты в пределах псевдополиморфного класса или системы являются кристаллическими и предпочтительно показывают выгодных твердотельную стабильность без потери начальной структуры циленгитида по сравнению с ранее описанной аморфной твердой формой. Указанный класс псевдополиморфных форм, описанных здесь, показывает неожиданно высокую растворимость, в особенности в водной среде, что делает их особенно пригодными для приготовления жидких составов. Дополнительно указанный класс полиморфных форм показывает выгодно уменьшенную гигроскопичность по сравнению с ранее известной аморфной формой. Растворимость тетрагидрата Формы S3 в различных растворителях: Комбинация уменьшенной гигроскопичности, хорошей растворимости и хорошей кристалличности приводит к превосходным свойствам по сравнению с аморфной фазой. В сравнении очистка, обработка и применение в работе аморфной формы является очень трудной из-за, например, очень высокой гигроскопичности и низкой стабильности аморфной твердой формы. Кроме того, псевдополиморфные формы и/или ангидраты или ансольваты согласно изобретению показывают улучшенную физическую и/или химическую стабильность по сравнению с аморфной фазой,предпочтительно приводя к уменьшенному формированию продуктов разложения во время хранения,например гидролизом. Эта улучшенная гидролитическая стабильность твердой формы согласно изобретению и в особенности кристаллических форм согласно изобретению, как полагают, вызвана уменьшением следовых количеств ионных примесей, которые обычно присутствуют в аморфной форме уровня техники. В результате все такие факторы, обсужденные здесь, как полагают, составляют выгодно улучшенную стабильность твердого состояния твердой формы согласно изобретению, кристаллических форм согласно изобретению и в особенности сольватов и/или ангидратов или ансольватов согласно изобретению. Дополнительно все такие факторы, обсужденные здесь, как полагают, составляют выгодно улучшенную стабильность лекарственных средств согласно изобретению, которые содержат твердую форму согласно изобретению, предпочтительно кристаллические формы согласно изобретению и в особенности сольваты и/или ангидраты или ансольваты согласно изобретению, приводя например, к более длинному сроку годности, благодаря высокой термостабильности и/или стабильности при хранении. Предпочтительным объектом изобретения является твердая форма как описано выше и/или ниже для лечения болезней. Болезни, относящиеся к этому, предпочтительно выбраны из группы, включающей раковые болез- 29
МПК / Метки
МПК: C07K 7/64, A61P 35/00, A61K 38/12
Метки: кислоты, получения, твердые, формы, 2s,5r,8s,11s)-5-бензил-11-(3-гуанидинопропил)-8-изопропил-7-метил-3,6,9,12,15-пентаоксо-1,4,7,10,13-пентаазациклопентадец-2-ил]уксусной, способы
Код ссылки
<a href="https://eas.patents.su/30-22831-tverdye-formy-2s5r8s11s-5-benzil-11-3-guanidinopropil-8-izopropil-7-metil-3691215-pentaokso-1471013-pentaazaciklopentadec-2-iluksusnojj-kisloty-i-sposoby-ih-polucheniya.html" rel="bookmark" title="База патентов Евразийского Союза">Твердые формы {[(2s,5r,8s,11s)-5-бензил-11-(3-гуанидинопропил)-8-изопропил-7-метил-3,6,9,12,15-пентаоксо-1,4,7,10,13-пентаазациклопентадец-2-ил]уксусной кислоты} и способы их получения</a>
Предыдущий патент: Способ проведения спленосохранной гастрэктомии при раке желудка
Следующий патент: Выделенное антитело, способное взаимодействовать с tlr3
Случайный патент: Укупорочное средство для сосуда с жидкостью