Производные пиразинооксазепина
Номер патента: 21079
Опубликовано: 31.03.2015
Авторы: Номура Изуми, Маезаки Хиронобу, Кусумото Томоказу, Сасаки Сигеказу
Формула / Реферат
1. Соединение, представленное формулой (I0)
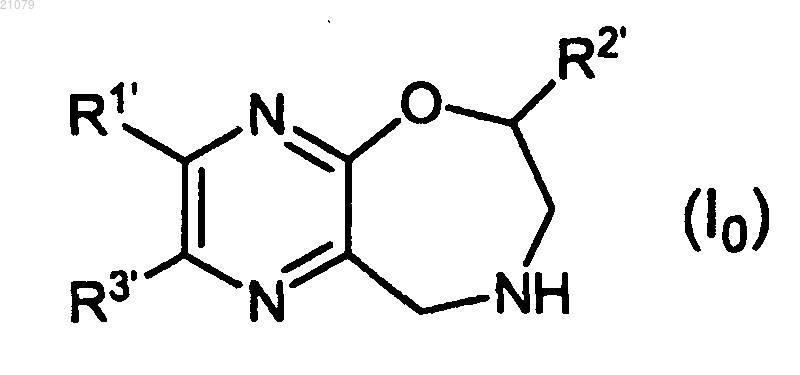
где R1' представляет собой
(1) морфолинильную группу, необязательно замещенную C1-6 алкильной группой(ами),
(2) пиперидинильную группу, необязательно замещенную C1-6 алкильной группой(ами),
(3) пирролидинильную группу, необязательно замещенную C1-6 алкильной группой(ами), необязательно замещенной С1-6 алкоксильной группой(ами),
(4) пирролильную группу, необязательно замещенную С1-6 алкильной группой(ами),
(5) имидазолильную группу, необязательно замещенную С1-6 алкильной группой(ами),
(6) аминогруппу, необязательно замещенную 1 или 2 заместителями, выбранными из
(a) C1-6 алкильной группы, необязательно замещенной заместителем(ями), выбранными из С3-6 циклоалкильной группы и фенильной группы, и
(b) C3-6 циклоалкильной группы,
(7) C1-6 алкилсульфанильную группу,
(8) С1-6алкоксильную группу, необязательно замещенную С3-6 циклоалкильной группой(ами),
(9) C3-6 циклоалкильную группу или
(10) С3-6 циклоалкенильную группу;
R2' представляет собой атом водорода или C1-6 алкильную группу, необязательно замещенную C1-6 алкоксильной группой(ами); и
R3' представляет собой атом водорода, атом галогена или C1-6 алкильную группу,
или его соль.
2. Соединение или его соль по п.1, где R1' представляет собой
(1) морфолинильную группу, необязательно замещенную C1-6 алкильной группой(ами),
(2) пиперидинильную группу, необязательно замещенную C1-6 алкильной группой(ами),
(3) пирролидинильную группу, необязательно замещенную C1-6 алкильной группой(ами), необязательно замещенной C1-6 алкоксильной группой(ами),
(4) пирролильную группу, необязательно замещенную C1-6 алкильной группой(ами),
(5) имидазолильную группу, необязательно замещенную С1-6 алкильной группой(ами),
(6) аминогруппу, необязательно замещенную 1 или 2 заместителями, выбранными из
(a) C1-6 алкильной группы, необязательно замещенной заместителем(ями), выбранными из С3-6 циклоалкильной группы и фенильной группы, и
(b) C3-6 циклоалкильной группы,
(7) C1-6 алкилсульфанильную группу,
(8) C1-6 алкоксильную группу, необязательно замещенную С3-6 циклоалкильной группой(ами),
(9) C3-6 циклоалкильную группу или
(10) С3-6 циклоалкенильную группу.
3. Соединение, представленное формулой (I)
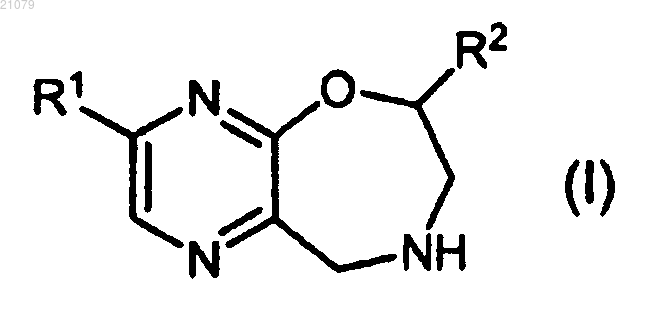
где R1 представляет собой морфолиногруппу, необязательно замещенную C1-6 алкильной группой(ами), ди(С1-6 алкил)аминогруппу, C1-6 алкоксильную группу, необязательно замещенную С3-6 циклоалкильной группой(ами), С3-6 циклоалкильную группу или С3-6 циклоалкенильную группу; и R2 представляет собой атом водорода или C1-6 алкильную группу,
или его соль.
4. Соединение или его соль по п.3, где R1 представляет собой морфолиногруппу, необязательно замещенную С1-6 алкильной группой(ами), ди(С3-6 алкил)аминогруппу, C1-6 алкоксильную группу или С3-6 циклоалкильную группу.
5. Соединение или его соль по п.3, где R1 представляет собой морфолиногруппу, необязательно замещенную заместителем(ями), выбранными из метильной группы и этильной группы, N-метил-N-(1-метилэтил)аминогруппу, изопропоксильную группу и циклопропильную группу; и
R2 представляет собой атом водорода или метильную группу.
6. 3-(1-Метилэтокси)-6,7,8,9-тетрагидропиразино[2,3-f][1,4]оксазепин или его соль.
7. 3-(3-Метилморфолин-4-ил)-6,7,8,9-тетрагидропиразино[2,3-f][1,4]оксазепин или его соль.
8. 6-Метил-3-(морфолин-4-ил)-6,7,8,9-тетрагидропиразино[2,3-f][1,4]оксазепин или его соль.
9. 6-Метил-3-(3-метилморфолин-4-ил)-6,7,8,9-тетрагидропиразино[2,3-f][1,4]оксазепин или его соль.
10. N-Метил-N-(1-метилэтил)-6,7,8,9-тетрагидропиразино[2,3-f][1,4]оксазепин-3-амин или его соль.
11. 3-(3-Этилморфолин-4-ил)-6,7,8,9-тетрагидропиразино[2,3-f][1,4]оксазепин или его соль.
12. 3-Циклопропил-6,7,8,9-тетрагидропиразино[2,3-f][1,4]оксазепин или его соль.
13. 3-(2-Метилпиперидин-1-ил)-6,7,8,9-тетрагидропиразино[2,3-f][1,4]оксазепин или его соль.
14. 3-(2-Метилпирролидин-1-ил)-6,7,8,9-тетрагидропиразино[2,3-f][1,4]оксазепин или его соль.
15. Лекарственное средство, обладающее активирующим действием в отношении серотонинового рецептора 5-НТ2С, содержащее соединение или его соль по любому из пп.1-14.
16. Лекарственное средство по п.15, представляющее собой лекарство для профилактики или лечения симптома нижних мочевыводящих путей, ожирения, выпадения тазовых органов, генитального пролапса, пролапса мочевого пузыря, пролапса прямой кишки, уретрального пролапса, гиперподвижности мочеточников, кишечной грыжи, грыжи прямой кишки, грыжи мочевого пузыря, разрыва сухожильного центра промежности и/или грыжи тазовой диафрагмы.
17. Способ профилактики или лечения симптома нижних мочевыводящих путей, ожирения, выпадения тазовых органов, генитального пролапса, пролапса мочевого пузыря, пролапса прямой кишки, уретрального пролапса, гиперподвижности мочеточников, кишечной грыжи, грыжи прямой кишки, грыжи мочевого пузыря, разрыва сухожильного центра промежности и/или грыжи тазовой диафрагмы у млекопитающего, включающий введение млекопитающему эффективного количества соединения или его соли по любому из пп.1-14.
18. Применение соединения или его соли по любому из пп.1-14 для получения лекарственного средства для профилактики или лечения симптома нижних мочевыводящих путей, ожирения, выпадения тазовых органов, генитального пролапса, пролапса мочевого пузыря, пролапса прямой кишки, уретрального пролапса, гиперподвижности мочеточников, кишечной грыжи, грыжи прямой кишки, грыжи мочевого пузыря, разрыва сухожильного центра промежности и/или грыжи тазовой диафрагмы.
Текст
Разработано соединение, обладающее активирующим действием в отношении серотонинового рецептора 5-НТ 2 С, которое можно использовать для лечения состояний нижних мочевыводящих путей, ожирения и рака. Соединение представлено формулой (I0), где каждый символ определен в описании, или представляет собой его соль.(71)(73) Заявитель и патентовладелец: ТАКЕДА ФАРМАСЬЮТИКАЛ КОМПАНИ ЛИМИТЕД (JP) Область техники, к которой относится изобретение Настоящее изобретение относится к производному пиразинооксазепина, обладающему превосходным активирующим действием в отношении серотонинового рецептора 5-HT2C и может использоваться в качестве агента для профилактики или лечения симптомов заболеваний нижних мочевыводящих путей,ожирения и/или выпадения органов и т.д. Предпосылки создания изобретения Серотониновый 5-HT2C рецептор представляет собой один из рецепторов биологического трансмиттера серотонина, который распределен, главным образом, в центральной нервной системе и контролирует множество физиологических функций in vivo. Иллюстративным примером является контроль аппетита. В исследовании с использованием грызунов было продемонстрировано, что стимулирование центрального серотонинового рецептора 5-HT2C понижает поведение при питании, приводя к уменьшению массы тела. Также сообщалось, что у людей введение активатора серотонинового рецептора 5-HT2C подавляет аппетит и снижает массу тела (см. непатентный документ 1). Кроме того, было продемонстрировано в тестах на крысах с использованием активатора серотонинового рецептора 5-HT2C, что стимулирование центрального серотонинового рецептора 5-HT2C подавляет поведение, связанное с депрессией (см. непатентный документ 2), и также сообщалось, что это является эффективным при многих заболеваниях центральной нервной системы, таких как тревожное состояние и т.д. (см. непатентный документ 3). Серотониновый рецептор 5-НТ 2 С экспрессируется в большом количестве в парасимпатических ядрах и двигательных нейронах в крестцовой части спинного мозга и рассматривается как контролирующий функции периферических нервов (см. непатентный документ 4). Как сообщалось, при введении активатора серотонинового рецептора 5-HT2C крысам индуцируется эрекция полового члена (см. непатентный документ 5) и повышается уретральная устойчивость (см. непатентный документ 1); все данные действия приписывают стимулированию серотонинового рецептора 5-HT2C в крестцовой части спинного мозга. Для активаторов серотонинового рецептора 5-HT2C возможны многочисленные клинические применения с особым ожидаемым результатом в случае лекарственных средств против ожирения, антидепрессантов,противотревожных препаратов, терапевтических лекарственных средств при эректильной дисфункции у мужчин и терапевтических лекарственных средств при стрессовом недержании мочи и т.п. Помимо этого активатор серотонинового рецептора 5-HT2C можно использовать в качестве лекарственного средства для профилактики или лечения заболеваний, вызванных выпадением органа из нормального положения вследствие ослабления мышц тазового дна, например выпадение органа (например,выпадение полового члена, генитальный пролапс, опущение матки, опущение мочевого пузыря, пролапс прямой кишки, пролапс мочеиспускательного канала, гиперподвижность мочеиспускательного канала,кишечная грыжа, грыжа мочевого пузыря, разрыв сухожильного центра промежности, грыжа тазового дна и т.д.) (см., например, патентный документ 2)."Выпадение тазовых органов" представляет собой заболевание, при котором передняя стенка влагалища, задняя стенка влагалища, матка, остаток влагалища после гистеректомии или мочевой пузырь опускаются и выступают за пределы отверстия влагалища, и, кроме того, пролапс прямой кишки характеризуется симптомами опущения и выхода за пределы анального отверстия прямой кишки. Помимо этого, кишечная грыжа и грыжа мочевого пузыря представляют собой заболевания, при которых мочевой пузырь и тонкий кишечник опускаются и выступают за пределы отверстия влагалища (см., например, непатентные документы 6 и 7). Такое опущение становится заметным, когда временно возрастает давление в брюшной полости в результате напряжения или тяжелой нагрузки и т.п. Такие заболевания широко распространены у женщин, при этом рождение ребенка, старение и ожирение известны как факторы риска, и одной из его предполагаемых причин является ослабление мышц тазового дна, соединительной оболочки и окружающей внутренние органы соединительной ткани, которая поддерживает тазовые органы, включая мочевой пузырь и т.п. Мышцы тазового дна представляют собой скелетные мышцы, которые объединены с подвздошной костью таза по типу гамака, служа постоянно для поддержания некоторого уплотнения и поддерживая тазовые органы от опущения. При пролапсе тазовых органов,пролапсе прямой кишки, кишечной грыже и грыже мочевого пузыря вес органов по имеющимся сведениям становится непереносимым вследствие ослабления данных мышц тазового дна, приводя к опущению тазовых органов и прямой кишки (см., например, непатентные документы 6 и 7); предполагается,что когда давление в брюшной полости особенно возрастает, повышенное давление становится непереносимым, и выпячивание становится более заметным. С другой стороны, сообщалось, что когда возрастает давление в брюшной полости, мочевой пузырь сдавливается, рефлекс через мочевой пузырь, спинной мозг - мышцы тазового дна и матку вызывает сокращение мышц тазового дна и уретрального сфинктера, вызывая уретральное внутреннее давление, тем самым предотвращая недержание мочи (см., например, непатентный документ 8). Аналогично, при возрастании давления в брюшной полости мышцы тазового дна рефлекторно сокращаются для предотвращения не только недержания мочи, но также и опущения тазовых органов, включая мочевой пузырь, тонкий кишечник (см., например, патентный документ 2). Когда имеется нарушение данного рефлекторного пути или мышц тазового дна, достаточное сокращение мышц тазового дна не может быть достигнуто, и поддержка тазовых органов, включая мочевой пузырь, тонкий кишечник, становится неадекватной. Выпадение органа представляет собой заболевание,-1 021079 при котором органы тазового дна (мочевой тракт, мочевой пузырь, матка, тонкий кишечник, прямая кишка и т.п.) и тому подобное выступают наружу из отверстия влагалища или отверстия прямой кишки вследствие недостаточной силы сокращения мышц тазового дна. Выпадение органов включает формы пролапса прямой кишки, опущения матки, уретрального пролапса, кишечной грыже и грыже мочевого пузыря и т.п. в зависимости от типа выступающего наружу органа. Известны конденсированные гетероциклические соединения, обладающие активирующим действием в отношении серотонинового рецептора 5-HT2C (см., например, патентные документы 3 и 4). Помимо этого, известно, что соединения, которые связываются с серотониновым рецептором 5-HT2C можно использовать для лечения стрессового недержания мочи и т.п. (например, см. патентные документы 5-9). Кроме того, также известны конденсированные гетероциклические соединения, такие как соединения бензодиазепина, соединения пиридооксазепина и т.п. (см., например, патентные документы 10 и 11). Предшествующий уровень развития данной области Патентные документы. Патентный документ 1: WO 04/096196. Патентный документ 2: WO 07/132841. Патентный документ 3: WO 02/040457. Патентный документ 4: WO 08/108445. Патентный документ 5: WO 02/083863. Патентный документ 6: WO 03/097636. Патентный документ 7: WO 04/000829. Патентный документ 8: WO 04/000830. Патентный документ 9: WO 02/008178. Патентный документ 10: WO 04/067008. Патентный документ 11: JP-A-2006-056881. Непатентные документы. Непатентный документ 1: Expert Opinion on Investigational Drugs, 2006, vol. 15, p. 257-266. Непатентный документ 2: J. Pharmacol. Exp. Ther., 1998, vol. 286, p. 913-924. Непатентный документ 3: Pharmacology Biochemistry Behavior, 2002, vol. 71, p. 533-554. Непатентный документ 4: Neuroscience, 1999, vol. 92, p. 1523-1537. Непатентный документ 5: Eur. J. Pharmacol., 2004, vol. 483, p.37-43. Непатентный документ 6: Lancet, 2007, vol. 369, p. 1027-38. Непатентный документ 7: European Urology, 2007, vol. 51, p. 884-886. Непатентный документ 8: American Journal of Physiology Renal Physiology, 2004, vol. 287, p. F434441. Описание изобретения Проблемы, решаемые с помощью изобретения Существует необходимость в разработке соединения, обладающего активирующим действием в отношении серотонинового 5-HT2C рецептора, которое можно использовать в качестве агента для профилактики или лечения симптомов заболеваний нижних мочевыводящих путей, ожирения и/или выпадения органа и т.п. и которое обладает превосходными свойствами с точки зрения селективности в отношении рецептора, эффективности, продолжительности действия, специфичности, пониженной токсичности и т.п. Авторы настоящего изобретения поставили задачу создания производного пиразинооксазепина, обладающего активирующим действием в отношении серотонинового 5-HT2C рецептора и т.п., которое имело бы структуру, отличающуюся от известных соединений (включая вышеуказанные соединения), и агента, содержащего производное пиразинооксазепина для профилактики или лечения таких заболеваний, как симптом нижних мочевыводящих путей, ожирение и/или выпадение органа и т.п. Способы решения проблем Авторы настоящего изобретения провели интенсивные исследования, пытаясь решить вышеуказанные проблемы, и установили, что соединение, представленное следующей формулой (I0), или его соль обладают превосходным активирующим действием в отношении серотонинового рецептора 5-HT2C, и провели дополнительные изыскания, которые привели к реализации настоящего изобретения. Соответственно, настоящее изобретение относится кR2 представляет собой атом водорода или C1-6 алкильную группу, необязательно замещенную C1-6 алкоксильной группой(ами); иR3' представляет собой атом водорода, атом галогена или C1-6 алкильную группу, или его соли [далее иногда упоминаемое как соединение (I0)],[2] соединению в соответствии с вышеуказанным п. [1],где R1' представляет собой где R1 представляет собой морфолиногруппу, необязательно замещенную C1-6 алкильной группой(ами),ди(C1-6 алкил)аминогруппу, C1-6 алкоксильную группу, необязательно замещенную C3-6 циклоалкильной группой(ами), C3-6 циклоалкильную группу или C3-6 циклоалкенильную группу; иR2 представляет собой атом водорода или C1-6 алкильную группу,или его соль [далее иногда упоминаемое как соединение (I)],[4] соединению в соответствии с вышеуказанным п. [3], где R1 представляет собой морфолиногруппу, необязательно замещенную C1-6 алкильной группой(ами), ди(С 1-6 алкил)аминогруппу, C1-6 алкоксильную группу или C3-6 циклоалкильную группу,или его соли;R1 представляет собой морфолиногруппу, необязательно замещенную заместителем(ями), выбранными из метильной группы и этильной группы, N-метил-N-(1-метилэтил)аминогруппу, изопропоксильную группу и циклопропильную группу; иR2 представляет собой атом водорода или метильную группу,или его соли;[15] пролекарству соединения в соответствии с любым из вышеуказанных пп. [1]-[14] или его соли;[16] лекарственному средству, содержащему соединение в соответствии с любым из вышеуказанных пп. [1]-[14] или его соль, или его пролекарство;[17] лекарственному средству в соответствии с вышеуказанным п. [16], которое представляет собой активатор серотонинового 5-НТ 2 С рецептора;[18] лекарственному средству в соответствии с вышеуказанным п. [16], которое представляет собой лекарство для профилактики или лечения симптомов заболеваний нижних мочевыводящих путей, ожирения и/или выпадения органа;[19] способу профилактики или лечения симптома нижних мочевыводящих путей, ожирения и/или выпадения органа у млекопитающего, включающий введение млекопитающему эффективного количества соединения по любому из вышеуказанных пп. [1]-[14], или его соли, или его пролекарства;[20] применению соединения по любому из вышеуказанных пп. [1]-[14] или его соли, или его пролекарства для получения лекарственного средства для профилактики или лечения симптома нижних мочевыводящих путей, ожирения и/или выпадения органа. Результат изобретения Поскольку соединение (I0) или его пролекарство обладает превосходным активирующим действием в отношении серотонинового 5-HT2C рецептора, его можно использовать в качестве безопасного лекарственного средства для профилактики или лечения любых связанных с серотонином 5-HT2C, например симптома нижних мочевыводящих путей, ожирения и/или выпадения органа и т.п. Способ осуществления изобретения Далее объясняется подробно определение каждого символа в формуле (I0). Выражение "C1-6 алкильная группа" в настоящем описании означает, если не указано другого, метильную группу, этильную группу, пропильную группу, изопропильную группу, бутильную группу, изобутильную группу, втор-бутильную группу, трет-бутильную группу, пентильную группу, изопентильную группу, неопентильную группу, 1-этилпропильную группу, гексильную группу, изогексильную группу,1,1-диметилбутильную группу, 2,2-диметилбутильную группу, 3,3-диметилбутильную группу, 2 этилбутильную группу и т.п. Выражение "C1-6 алкоксильная группа" в настоящем описании означает, если не указано другого,метоксильную группу, этоксильную группу, пропоксильную группу, изопропоксильную группу, бутоксильную группу, изобутоксильную группу, вторбутоксильную группу, трет-бутоксильную группу, пентилоксигруппу, изопентилоксигруппу, неопентилоксигруппу, 1-этилпропилоксигруппу, гексилоксигруппу,изогексилоксигруппу,1,1-диметилбутилоксигруппу,2,2-диметилбутилоксигруппу,3,3 диметилбутилоксигруппу, 2-этилбутилоксигруппу и т.п. Выражение "C3-6 циклоалкильная группа" в настоящем описании означает, если не указано другого,циклопропильную группу, циклобутильную группу, циклопентильную группу, циклогексильную группу и т.п."Морфолинильная группа" в выражении "морфолинильная группа, необязательно замещенная C1-6 алкильной группой(ами)" в случае R1 может быть замещена любым числом заместителей, выбранных из вышеуказанной "C1-6 алкильной группы". Число "C1-6 алкильных групп" не ограничено до тех пор, пока возможно замещение, и предпочтительно составляет от 1 до 3 (более предпочтительно 1 или 2, в особенности предпочтительно 1). Когда присутствует две или более "C1-6 алкильных групп", они могут быть одинаковыми или различными. В качестве "морфолинильной группы, необязательно замещенной C1-6 алкильной группой(ами)",морфолинильная группа, необязательно замещенная 1-3 (предпочтительно 1 или 2, более предпочтительно 1) C1-6 алкильными группами является предпочтительной, морфолинильная группа (предпочтительно морфолиногруппа), необязательно замещенная 1 или 2 (предпочтительно 1) C1-4 алкильными группами(предпочтительно метильной группой, этильной группой), является более предпочтительной, и морфолиногруппа, метилморфолиногруппа (предпочтительно 3-метилморфолиногруппа) и этилморфолиногруппа (предпочтительно 3-этилморфолиногруппа) являются более предпочтительными. В другом варианте осуществления в качестве "морфолинильной группы, необязательно замещенной"Пиперидильная группа" в выражении "пиперидильная группа, необязательно замещенная C1-6 алкильной группой(ами)" в случае R1' может быть замещена любым числом заместителей, выбранных из вышеуказанной "C1-6 алкильной группы". Число "C1-6 алкильных групп" не ограничено до тех пор, пока возможно замещение и предпочтительно составляет от 1 до 3 (более предпочтительно 1 или 2, в особенности предпочтительно 1). Когда присутствует две или более "C1-6 алкильных групп", они могут быть одинаковыми или различными. В качестве "пиперидильной группы, необязательно замещенной C1-6 алкильной группой(ами)", пиперидильная группа, необязательно замещенная 1-3 (предпочтительно 1 или 2, более предпочтительно 1) ридиногруппа), необязательно замещенная 1 или 2 (предпочтительно 1) C1-4 алкильными группами (метильными группами), является более предпочтительной, и метилпиперидино (предпочтительно, 2 метилпиперидино) является еще более предпочтительной. В другом варианте осуществления в качестве "пиперидильной группы, необязательно замещеннойC1-6 алкильной группой(ами), необязательно замещенной C1-6 алкоксильной группой(ами)" в случае R1' может быть замещена любым числом заместителей, выбранных из "C1-6 алкильной группы(пп), необязательно замещенной С 1-6 алкоксильной группой (ами)". В данном случае "C1-6 алкильная группа(ы), необязательно замещенная С 1-6 алкоксильной группой(ами)", представляет собой вышеуказанную "C1-6 алкильную группу", необязательно замещенную любым числом (предпочтительно 1-3, более предпочтительно 1 или 2, более предпочтительно 1) заместителей, выбранных из вышеуказанной "C1-6 алкоксильной группы". Когда присутствуют две или более "C1-6 алкоксильных группы", они могут быть одинаковыми или различными. Число "C1-6 алкильных групп, необязательно замещенных C1-6 алкоксильными группами", которое может содержаться в "пирролидинильной группе", не ограничено до тех пор, пока возможно замещение,и предпочтительно составляет 1-3 (более предпочтительно 1 или 2, в особенности предпочтительно 1). Когда присутствует две или более "C1-6 алкильных групп, необязательно замещенных C1-6 алкоксильными группами", они могут быть одинаковыми или различными. В качестве "пирролидинильной группы, необязательно замещенной С 1-6 алкильной группой(ами),необязательно замещенной C1-6 алкоксильной группой(ами)", пирролидинильная группа, необязательно замещенная 1-3 (предпочтительно 1 или 2, более предпочтительно 1) "C1-6 алкильными группами, необязательно замещенными 1-3 (предпочтительно 1 или 2, более предпочтительно 1) C1-6 алкоксильными группами",является предпочтительной,пирролидинильная группа(предпочтительно 1 пирролидинильная группа), необязательно замещенная 1 или 2 (предпочтительно 1) "C1-4 алкильными группами (предпочтительно метильными группами), необязательно замещенными 1 или 2 (предпочтительно 1) C1-4 алкоксильными группами (предпочтительно метоксильными группами)", является более предпочтительной, и метилпирролидинил (предпочтительно 2-метилпирролидин-1-ил) и (метоксиметил)пирролидинил (предпочтительно 2-(метоксиметил)пирролидин-1-ил) являются более предпочтительными. В другом варианте осуществления в качестве "пирролидинильной группы, необязательно замещенной C1-6 алкильной группой(ами), необязательно замещенной C1-6 алкоксильной группой(ами)", пирролидинильная группа, замещенная С 1-6 алкильной группой(ами), необязательно замещенной C1-6 алкоксильной группой(ами), является предпочтительной, пирролидинильная группа, замещенная 1-3 (предпочтительно 1 или 2, более предпочтительно 1) "C1-6 алкильными группами, необязательно замещенными 1-3"Пирролильная группа" в выражении "пирролильная группа, необязательно замещенная C1-6 алкильной группой(ами)" в случае R1' может быть замещена любым числом заместителей, выбранных из вышеуказанных "C1-6 алкильных групп". Число "C1-6 алкильных групп" не ограничено до тех пор, пока возможно замещение, и предпочтительно составляет от 1 до 3 (более предпочтительно 1 или 2). Когда присутствуют две или более "C1-6 алкильных групп", они могут быть одинаковыми или различными. В качестве "пирролильной группы, необязательно замещенной C1-6 алкильной группой(ами)", предпочтительной является пирролильная группа, необязательно замещенная 1-3 (предпочтительно 1 или 2)C1-6 алкильными группами, пирролильная группа (предпочтительно 1-пирролильная группа), необязательно замещенная 1 или 2 C1-4 алкильными группами (предпочтительно метильными группами), является более предпочтительной, и диметилпирролил (предпочтительно 2,5-диметилпиррол-1-ил) является более предпочтительным. В других вариантах осуществления в качестве "пирролильной группы, необязательно замещеннойC1-6 алкильной группой(ами)", пирролильная группа, замещенная C1-6 алкильной группой(ами), является предпочтительной, пирролильная группа, замещенная 1-3 (предпочтительно 1 или 2) C1-6 алкильными группами, является более предпочтительной и пирролильная группа (предпочтительно 1-пирролильная группа), замещенная 1 или 2 C1-4 алкильными группами (предпочтительно метильными группами), является еще более предпочтительной.-5 021079 алкильной группой(ами)," в случае R1' может быть замещена любым числом заместителей, выбранных из вышеуказанных "C1-6 алкильных групп". Число "C1-6 алкильных групп" не ограничено до тех пор, пока возможно замещение, и предпочтительно составляет от 1 до 3 (более предпочтительно 1 или 2, в особенности предпочтительно 1). Когда присутствуют две или более "C1-6 алкильных групп", они могут быть одинаковыми или различными. В качестве "имидазолильной группы, необязательно замещенной C1-6 алкильной группой(ами)",имидазолильная группа, необязательно замещенная 1-3 (предпочтительно 1 или 2, более предпочтительно 1) C1-6 алкильными группами, является предпочтительной, имидазолильная группа (предпочтительно 1-имидазолильная группа), необязательно замещенная 1 или 2 (предпочтительно 1) C1-4 алкильными группами (предпочтительно метильными группами), является более предпочтительной и метилимидазолил (предпочтительно 2-метилимидазол-1-ил) является еще более предпочтительным. В другом варианте осуществления в качестве "имидазолильной группы, необязательно замещеннойC1-6 алкильной группой(ами)", имидазолильная группа, замещенная C1-6 алкильной группой(ами), является предпочтительной, имидазолильная группа, замещенная 1-3 (предпочтительно 1 или 2, более предпочтительно 1) C1-6 алкильными группами, является более предпочтительной и имидазолильная группа(а) C1-6 алкильной группы, необязательно замещенной заместителем(ями), выбранными из C3-6 циклоалкильной группы и фенильной группы, и (b) C3-6 циклоалкильной группы" в случае R1' может быть замещена 1 или 2 заместителями, выбранными из (а) вышеуказанной "С 1-6 алкильной группы," необязательно замещенной любым числом (предпочтительно 1-3, более предпочтительно 1 или 2, более предпочтительно 1) заместителей, выбранных из вышеуказанной "С 3-6 циклоалкильной группы" и фенильной группы, и(b) вышеуказанной "C3-6 циклоалкильной группы". Когда присутствует два заместителя, они могут быть одинаковыми или различными. В качестве "аминогруппы, необязательно замещенной 1 или 2 заместителями, выбранными из (a)(b) C3-6 циклоалкильной группы (предпочтительно циклобутильной группы),является более предпочтительной, и аминогруппа, N-(1-метилэтил)аминогруппа, N-метил-Nпропиламиногруппа, N-метил-N-(1-метилэтил)аминогруппа, N-метил-N-(1-метилпропил)аминогруппа,N-этил-N-(1-метилэтил)аминогруппа, N-циклопропилметил-N-метиламиногруппа, N-(1-метилэтил)-N(фенилметил)аминогруппа и N-циклобутил-N-метиламиногруппа являются более предпочтительными. В другом варианте осуществления в качестве "аминогруппы, необязательно замещенной 1 или 2 заместителями, выбранными из (а) C1-6 алкильной группы, необязательно замещенной заместителем(ями),выбранными из C3-6 циклоалкильной группы и фенильной группы, и (b) C3-6 циклоалкильной группы","ди(С 1-6 алкил)аминогруппа" является предпочтительной. Примеры "C1-6 алкилсульфанильной группы" в случае R1' включают метилсульфанильную группу,этилсульфанильную группу, пропилсульфанильную группу, изопропилсульфанильную группу, бутилсульфанильную группу, изобутилсульфанильную группу, втор-бутилсульфанильную группу, третбутилсульфанильную группу, пентилсульфанильную группу, изопентилсульфанильную группу, неопентилсульфанильную группу, 1-этилпропилсульфанильную группу, гексилсульфанильную группу, изогексилсульфанильную группу, 1,1-диметилбутилсульфанильную группу, 2,2-диметилбутилсульфанильную группу, 3,3-диметилбутилсульфанильную группу, 2-этилбутилсульфанильную группу и т.п. В качестве "С 1-6 алкилсульфанильной группы" C1-4 алкилсульфанильная группа является предпочтительной, и изопропилсульфанильная группа является более предпочтительной."C1-6 алкоксильная группа" в "C1-6 алкоксильной группе, необязательно замещенной C3-6 циклоалкилгруппа(ами)" в случае R1' может быть замещена любым числом заместителей, выбранных из вышеуказанной "C3-6 циклоалкильной группы". Число "C3-6 циклоалкильных групп" не ограничено до тех пор,пока возможно замещение, и предпочтительно составляет от 1 до 3 (более предпочтительно 1 или 2, в особенности предпочтительно 1). Когда присутствует две или более "С 3-6 циклоалкильных групп", они могут быть одинаковыми или различными. В качестве "C1-6 алкоксильной группы, необязательно замещенной C3-6 циклоалкильной группой(ами)", C1-6 алкоксильная группа, необязательно замещенная 1-3 (более предпочтительно 1 или 2, в особенности предпочтительно 1) С 3-6 циклоалкильными группами, является предпочтительной, C1-4 алкоксильная группа (предпочтительно этоксильная группа, изопропоксильная группа), необязательно замещенная 1 или 2 (предпочтительно 1) C3-6 циклоалкильными группами (предпочтительно циклопропильными группами), является более предпочтительной, и циклопропилэтоксильная группа (предпочтительно 1-циклопропилэтоксильная группа) и изопропоксильная группа являются более предпочтительными. В качестве "C3-6 циклоалкильной группы" в случае R1' циклопропильная группа и циклопентильная группа являются предпочтительными. Примеры "C3-6 циклоалкенильной группы" в случае R1' включают циклопропенильную группу (например, 1-циклопропен-1-ильная группа, 2-циклопропен-1-ильная группа), циклобутенильную группу(например, 1-циклопентен-1-ильная группа, 2-циклопентен-1-ильная группа, 3-циклопентен-1-ильная группа), циклогексенильную группу (например, 1-циклогексен-1-ильная группа, 2-циклогексен-1-ильная группа, 3-циклогексен-1-ильная группа) и т.п. В качестве "C3-6 циклоалкенильной группы" циклопентенильная группа является предпочтительной,и 1-циклопентен-1-ильная группа является более предпочтительной.(1) морфолиногруппу, метилморфолиногруппу (предпочтительно 3-метилморфолиногруппу) или этилморфолиногруппу (предпочтительно 3-этилморфолиногруппу),(2) метилпиперидино (предпочтительно 2-метилпиперидино),(3) метилпирролидинил (предпочтительно 2-метилпирролидин-1-ил) или (метоксиметил)пирролидинил (предпочтительно 2-(метоксиметил)пирролидин-1-ил),(4) диметилпирролил (предпочтительно 2,5-диметилпиррол-1-ил),(5) метилимидазолил (предпочтительно 2-метилимидазол-1-ил),(6) аминогруппу, N-(1-метилэтил)аминогруппу, N-метил-N-пропиламиногруппу, N-метил-N-(1 метилэтил)аминогруппу, N-метил-N-(1-метилпропил)аминогруппу, N-этил-N-(1-метилэтил)аминогруппу,N-циклопропилметил-N-метиламиногруппу, N-(1-метилэтил)-N-(фенилметил)аминогруппу или Nциклобутил-N-метиламиногруппу,(7) изопропилсульфанильную группу,(8) циклопропилэтоксильную группу (предпочтительно 1-циклопропилэтоксильную группу) или изопропоксильную группу,(9) циклопропильную группу или циклопентильную группу или(10) циклопентенильную группу (предпочтительно 1-циклопентен-1-ильную группу). В другом варианте осуществления R1' предпочтительно представляет собой(10) C3-6 циклоалкенильную группу. Кроме того, в другом варианте осуществления R1' предпочтительно представляет собой морфолиногруппу, необязательно замещенную C1-6 алкильной группой(ами), ди(С 1-6 алкил)аминогруппу, C1-6 алкоксильную группу, замещенную C3-6 циклоалкильной группой(ами), С 3-6 циклоалкильную группу или С 3-6 циклоалкенильную группу."C1-6 алкильная группа" в "C1-6 алкильной группе, необязательно замещенной C1-6 алкоксильной группой(ами)" в случае R2 может быть замещена любым числом заместителей, выбранных из вышеуказанных "C1-6 алкоксильных групп". Число "C1-6 алкоксильных групп" не ограничено до тех пор, пока возможно замещение, и предпочтительно составляет от 1 до 3 (более предпочтительно 1 или 2, в особенности предпочтительно 1). Когда присутствуют две или более "C1-6 алкоксильных групп", они могут быть одинаковыми или различными. В качестве "C1-6 алкильной группы, необязательно замещенной C1-6 алкоксильной группой(ами)",C1-6 алкильная группа, необязательно замещенная 1-3 (предпочтительно 1 или 2, более предпочтительно 1) C1-6 алкоксильными группами, является предпочтительной, C1-4 алкильная группа (предпочтительно метильная группа), необязательно замещенная 1 или 2 (предпочтительно 1) C1-4 алкоксильными группами (предпочтительно метоксильными группами), является более предпочтительной, и метильная группа и метоксиметильная группа являются более предпочтительными.R2' предпочтительно представляет собой атом водорода или C1-6 алкильную группу, необязательно замещенную 1-3 (предпочтительно 1 или 2, более предпочтительно 1) C1-6 алкоксильными группами, более предпочтительно атом водорода или C1-4 алкильную группу (предпочтительно метильную группу),необязательно замещенную 1 или 2 (предпочтительно 1) C1-4 алкоксильными группами (предпочтительно метоксильными группами), и более предпочтительно представляет собой атом водорода, метильную группу или метоксиметильную группу. В другом варианте осуществления, R2' предпочтительно представляет собой атом водорода или C1-6 алкильную группу.R3' предпочтительно представляет собой атом водорода, атом галогена (предпочтительно атом хлора, атом брома) или C1-4 алкильную группу (предпочтительно метильную группу), более предпочтительно атом водорода. В качестве соединения (I0) соединение, в котором R1' представляет собой(1) морфолиногруппу, метилморфолиногруппу (предпочтительно 3-метилморфолиногруппу) или этилморфолиногруппу (предпочтительно 3-этилморфолиногруппу),(2) метилпиперидино (предпочтительно 2-метилпиперидино),(3) метилпирролидинил (предпочтительно 2-метилпирролидин-1-ил) или (метоксиметил)пирролидинил (предпочтительно 2-(метоксиметил)пирролидин-1-ил),(4) диметилпирролил (предпочтительно 2,5-диметилпиррол-1-ил),(5) метилимидазолил (предпочтительно 2-метилимидазол-1-ил),(6) аминогруппу, N-(1-метилэтил)аминогруппу, N-метил-N-пропиламиногруппу, N-метил-N-(1 метилэтил)аминогруппу, N-метил-N-(1-метилпропил)аминогруппу, N-этил-N-(1-метилэтил)аминогруппу,N-циклопропилметил-N-метиламиногруппу, N-(1-метилэтил)-N-(фенилметил)аминогруппу или Nциклобутил-N-метиламиногруппу,(7) изопропилсульфанильную группу,(8) циклопропилэтоксильную группу (предпочтительно 1-циклопропилэтоксильную группу) или изопропоксильную группу,(9) циклопропильную группу или циклопентильную группу или(10) циклопентенильную группу (предпочтительно 1-циклопентен-1-ильную группу),R2' представляет собой атом водорода или C1-6 алкильную группу, необязательно замещенную 1-3(предпочтительно 1 или 2, более предпочтительно 1) C1-6 алкоксильными группами, предпочтительно атом водорода или C1-4 алкильную группу (предпочтительно метильную группу), необязательно замещенную 1 или 2 (предпочтительно 1) С 1-4 алкоксильными группами (предпочтительно метоксильными группами), [более предпочтительно, атом водорода, метильную группу или метоксиметильную группу] иR3' представляет собой атом водорода, атом галогена или C1-6 алкильную группу [предпочтительно атом водорода, атом галогена (предпочтительно атом хлора, атом брома) или C1-4 алкильную группу(предпочтительно метильную группу)], или его соль является предпочтительным. В другом варианте осуществления в качестве соединения (I0), соединение, в котором R1' представляет собой(10) C3-6 циклоалкенильную группу],R2' представляет собой атом водорода или C1-6 алкильную группу, необязательно замещенную 1-3(предпочтительно 1 или 2, более предпочтительно 1) C1-6 алкоксильными группами предпочтительно атом водорода или C1-4 алкильную группу (предпочтительно метильную группу), необязательно замещенную 1 или 2 (предпочтительно 1) C1-4 алкоксильными группами (предпочтительно метоксильными группами) [более предпочтительно атом водорода, метильную группу или метоксиметильную группу], иR3' представляет собой атом водорода, атом галогена или C1-6 алкильную группу [предпочтительно атом водорода, атом галогена (предпочтительно атом хлора, атом брома) или C1-4 алкильную группу(предпочтительно метильную группу)], или его соль является предпочтительным. В качестве соединения (I0) соединения, описанные в следующих примерах 1-35, или их соли являются предпочтительными и в особенности 3-(1-метилэтокси)-6,7,8,9-тетрагидропиразино[2,3-f][1,4]оксазепин или его соль (пример 2),3-(3-метилморфолин-4-ил)-6,7,8,9-тетрагидропиразино[2,3-f][1,4]оксазепин (предпочтительно 3[(3R)-3-метилморфолин-4-ил]-6,7,8,9-тетрагидропиразино[2,3-f][1,4]оксазепин или его соль (пример 5),6-метил-3-(морфолин-4-ил)-6,7,8,9-тетрагидропиразино[2,3-f][1,4]оксазепин (предпочтительно (6S)6-метил-3-(морфолин-4-ил)-6,7,8,9-тетрагидропиразино[2,3-f][1,4]оксазепин) или его соль (пример 6),6-метил-3-(3-метилморфолин-4-ил)-6,7,8,9-тетрагидропиразино[2,3-f][1,4]оксазепин(пример 8),3-(3-этилморфолин-4-ил)-6,7,8,9-тетрагидропиразино[2,3-f][1,4]оксазепин (предпочтительно 3[(3R)-3-этилморфолин-4-ил]-6,7,8,9-тетрагидропиразино[2,3-f][1,4]оксазепин) или его соль (пример 9),3-циклопропил-6,7,8,9-тетрагидропиразино[2,3-f][1,4]оксазепин или его соль (пример 10),3-(2-метилпиперидин-1-ил)-6,7,8,9-тетрагидропиразино[2,3-f][1,4]оксазепин или его соль (пример 12) и 3-(2-метилпирролидин-1-ил)-6,7,8,9-тетрагидропиразино[2,3-f][1,4]оксазепин или его соль (пример 13) являются предпочтительными. В другом варианте осуществления, кроме того, в качестве соединения (I0) соединение (I) является предпочтительным. Определение каждого символа в формуле (I) подробно объясняется далее."Морфолиногруппа" в выражении "морфолиногруппа, необязательно замещенная C1-6 алкильной группой(ами)" в случае R1 может быть замещена любым числом заместителей, выбранных из вышеуказанной "C1-6 алкильной группы". Число "C1-6 алкильных групп" не ограничено до тех пор, пока возможно замещение, и предпочтительно составляет от 1 до 3 (более предпочтительно 1 или 2, в особенности предпочтительно 1). Когда присутствуют две или более "C1-6 алкильных групп", они могут быть одинаковыми или различными. В качестве "морфолиногруппы, необязательно замещенной C1-6 алкильной группой(ами)", морфолиногруппа, необязательно замещенная заместителем(ями), выбранными из метильной группы и этильной группы, является предпочтительной, и морфолиногруппа, метилморфолиногруппа (например, 3 метилморфолиногруппа) и этилморфолиногруппа (например, 3-этилморфолиногруппа) являются более предпочтительными. Примеры "ди(С 1-6 алкил)аминогруппы" в случае R1 включают аминогруппу, дизамещенную заместителями, выбранными из вышеуказанной "C1-6 алкильной группы". Две "С 1-6 алкильные группы" могут быть одинаковыми или различными. В качестве "ди(С 1-6 алкил)аминогруппы" аминогруппа, дизамещенная одинаковыми или различными C1-3 алкильными группами (например, метильной группой, этильной группой, пропильной группой,изопропильной группой), является предпочтительной, и N-метил-N-(1-метилэтил)аминогруппа является более предпочтительной. В качестве "C1-6 алкоксильной группы" в "C1-6 алкоксильной группе, необязательно замещенной C3-6 циклоалкильной группой(ами)" в случае R1, предпочтительной являются этоксильная группа, изопропоксильная группа и т.п. "C1-6 алкоксильная группа" может быть замещена любым числом заместителей,выбранных из вышеуказанной "C3-6 циклоалкильной группы". Число "C3-6 циклоалкильных групп" не ограничено до тех пор, пока возможно замещение, предпочтительно составляет от 1 до 3 (более предпочтительно 1 или 2, в особенности предпочтительно 1). Когда присутствует две или более "C3-6 циклоалкилгруппа", они могут быть одинаковыми или различными. В качестве "C1-6 алкоксильной группы, необязательно замещенной C3-6 циклоалкильной группой(ами)" в случае R1, этоксильная группа и изопропоксильная группа, которые могут быть соответственно замещены циклопропильной группой(ами),являются предпочтительными,и 1 циклопропилэтоксильная группа и изопропоксильная группа являются более предпочтительными. В качестве "С 3-6 циклоалкильной группы" в случае R1 циклопропильная группа и циклопентильная группа являются предпочтительными. Примеры "C3-6 циклоалкенильной группы" в случае R1 включают циклопропенильную группу (например, 1-циклопропен-1-ильную группу, 2-циклопропен-1-ильную группу), а циклобутенильную группу (например, 1-циклобутен-1-ильную группу, 2-циклобутен-1-ильную группу), циклопентенильную группу (например, 1-циклопентен-1-ильную группу, 2-циклопентен-1-ильную группу, 3-циклопентен-1 ильную группу), циклогексенильную группу (например, 1-циклогексен-1-ильную группу, 2-циклогексен 1-ильную группу, 3-циклогексен-1-ильную группу) и т.п. Циклопентенильная группа является предпочтительной, и 1-циклопентен-1-ильная группа является более предпочтительной.R1 предпочтительно представляет собой морфолиногруппу, необязательно замещенную заместителем(ями), выбранными из метильной группы и этильной группы; аминогруппу, дизамещенную заместителями, выбранными из C1-3 алкильной группы (например, метильная группа, этильная группа, пропильная группа, изопропильная группа); этоксильную группу или изопропоксильную группу, каждая из которых необязательно является замещенной циклопропильной группой(ами); циклопропильную группу; циклопентильную группу; или циклопентенильную группу.R1 более предпочтительно представляет собой морфолиногруппу, метилморфолиногруппу (предпочтительно 3-метилморфолиногруппу), этилморфолиногруппу (предпочтительно 3-этилморфолиногруппу), N-метил-N-(1-метилэтил)аминогруппу, 1-циклопропилэтоксильную группу, изопропоксильную группу, циклопропильную группу, циклопентильную группу или циклопентенильную группу (предпоч- 12021079 тительно 1-циклопентен-1-ильную группу). В другом варианте осуществления R1 предпочтительно представляет собой морфолиногруппу, необязательно замещенную C1-6 алкильной группой(ами), ди(С 1-6 алкил)аминогруппу, C1-6 алкоксильную группу или C3-6 циклоалкильную группу. R1 более предпочтительно представляет собой морфолиногруппу, необязательно замещенную заместителем(ями), выбранными из метильной группы и этильной группы, N-метил-N-(1-метилэтил)аминогруппу, изопропоксильную группу или циклопропильную группу. В качестве "C1-6 алкильной группы" в случае R2 метильная группа является предпочтительной.R предпочтительно представляет собой атом водорода или метильную группу. В качестве соединения (I) соединение, в котором R1 представляет собой морфолиногруппу, необязательно замещенную заместителем(ями), выбранными из метильной группы и этильной группы; аминогруппу, дизамещенную заместителями, выбранными из C1-3 алкильной группы (например, метильная группа, этильная группа, пропильная группа, изопропильная группа); этоксильную группу или изопропоксильную группу, каждая из которых необязательно является замещенной циклопропильной группой(ами); циклопропильную группу; циклопентильную группу; циклопентенильную группу [предпочтительно морфолиногруппу, метилморфолиногруппу (предпочтительно 3-метилморфолиногруппу), этилморфолиногруппу (предпочтительно 3-этилморфолиногруппу), N-метил-N-(1-метилэтил)аминогруппу, 1 циклопропилэтоксильную группу, изопропоксильную группу, циклопропильную группу, циклопентильную группу, циклопентенильную группу (предпочтительно 1-циклопентен-1-ил);R2 представляет собой атом водорода или метильную группу, или его соль является предпочтительным. В другом варианте осуществления в качестве соединения (I) соединение, в котором R1 представляет собой морфолиногруппу, необязательно замещенную C1-6 алкильной группой(ами), ди(С 1-6 алкил)аминогруппу, C1-6 алкоксильную группу или C3-6 циклоалкильную группу [предпочтительно морфолиногруппу, необязательно замещенную заместителем(ями), выбранными из метильной группы и этильной группы, N-метил-N-(1-метилэтил)аминогруппу, изопропоксильную группу или циклопропильную группу]; и R2 представляет собой атом водорода или метильную группу, или его соль является предпочтительным. В качестве соединения (I) соединения следующих примеров 1-11 или их соли являются предпочтительными, в частности 3-(1-метилэтокси)-6,7,8,9-тетрагидропиразино[2,3-f][1,4]оксазепин или его соль (пример 2),3-(3-метилморфолин-4-ил)-6,7,8,9-тетрагидропиразино[2,3-f][1,4]оксазепин (предпочтительно 3[(3R)-3-метилморфолин-4-ил]-6,7,8,9-тетрагидропиразино[2,3-f][1,4]оксазепин) или его соль (пример 5),6-метил-3-(морфолин-4-ил)-6,7,8,9-тетрагидропиразино[2,3-f][1,4]оксазепин (предпочтительно (6S)6-метил-3-(морфолин-4-ил)-6,7,8,9-тетрагидропиразино[2,3-f][1,4]оксазепин) или его соль (пример 6),6-метил-3-(3-метилморфолин-4-ил)-6,7,8,9-тетрагидропиразино[2,3-f][1,4]оксазепин(6S)-6-метил-3-[(3R)-3-метилморфолин-4-ил]-6,7,8,9-тетрагидропиразино[2,3-f][1,4]оксазепин) или его соль (пример 7),N-метил-N-(1-метилэтил)-6,7,8,9-тетрагидропиразино[2,3-f][1,4]оксазепин-3-амин или его соль(пример 8),3-(3-этилморфолин-4-ил)-6,7,8,9-тетрагидропиразино[2,3-f][1,4]оксазепин (предпочтительно 3[(3R)-3-этилморфолин-4-ил]-6,7,8,9-тетрагидропиразино[2,3-f][1,4]оксазепин) или его соль (пример 9) и 3-циклопропил-6,7,8,9-тетрагидропиразино[2,3-f][1,4]оксазепин или его соль (пример 10) являются предпочтительными. Когда соединение (I0) или (I) представляет собой соль, примеры солей включают соль с неорганическим основанием, аммониевую соль, соль с органическим основанием, соль с неорганической кислотой,соль с органической кислотой, соль с основной или кислотной аминокислотой и т.п. Предпочтительные примеры соли с неорганическим основанием включают соли щелочных металлов, такие как соль натрия, соль калия и т.п.; соли щелочно-земельных металлов, такие как соль кальция,соль магния, соль бария и т.п.; соль алюминия и т.п. Предпочтительные примеры соли с органическим основанием включают соли с триметиламином,триэтиламином, пиридином, пиколином, этаноламином, диэтаноламином, триэтаноламином, дициклогексиламином, N,N'-дибензилэтилендиамином и т.п. Предпочтительные примеры соли с неорганической кислотой включают соли хлористо-водородной кислоты, бромисто-водородной кислоты, азотной кислоты, серной кислоты, фосфорной кислоты и т.п. Предпочтительные примеры соли с органической кислотой включают соли с муравьиной кислотой,уксусной кислотой, трифторуксусной кислотой, фумаровой кислотой, щавелевой кислотой, винной кислотой, малеиновой кислотой, лимонной кислотой, янтарной кислотой, яблочной кислотой, метансульфоновой кислотой, бензолсульфоновой кислотой, п-толуолсульфоновой кислотой и т.п. Предпочтительные примеры соли с основной аминокислотой включают соли с аргинином, лизином,орнитином и т.п. Предпочтительные примеры соли с кислотной аминокислотой включают соли с аспарагиновой кислотой, глутаминовой кислотой и т.п. Среди данных солей фармацевтически приемлемые соли являются предпочтительными. Соединение (I0) или (I) могут представлять собой гидрат, не гидрат, сольват и не сольват. Соединения (I0) и (I) также охватывают меченные изотопом соединения (например, 2 Н, 3 Н, 14 С, 35S, 125I и т.д.) и т.п. Кроме того, соединения (I0) и (I) также охватывают соединения дейтерообмена, в которых 1 Н превращается в 2 Н. Далее объясняются способы получения соединений (I0) или (I) согласно настоящему изобретению. В каждом из следующих способов получения исходные соединения и промежуточные продукты можно использовать в виде солей. Примеры такой соли включают соли, подобные солям вышеуказанных соединений (I0) и (I) и т.п. Кроме того, промежуточные соединения, полученные в каждом из способов получения, также можно непосредственно использовать в виде реакционной смеси или в виде неочищенного продукта. Однако такой промежуточный продукт может быть выделен или очищен перед употреблением в соответствии с известными методами, такими как фазовый переход, концентрирование, экстракция растворителем, перегонка, преобразование жидкости, кристаллизация, перекристаллизация, хроматография и т.п. Более того, когда соединение каждой формулы является коммерчески доступным, такой продукт можно использовать как таковой. Соединение (I) по настоящему изобретению может быть получено в соответствии со следующими способом А, способом В, способом С, способом D или аналогичным им способом. В соединениях (I) соединение, представленное формулой (Ia), где R1 представляет собой C3-6 циклоалкильную группу или C3-6 циклоалкенильную группу, или его соль (далее иногда упоминаемое как соединение (Ia), и то же самое относится к другим формулам) может быть получено, например, в соответствии с приведенным ниже способом А или аналогичным этому способом. Способ А где Pg представляет собой защитную группу; R1a представляет собой C3-6 циклоалкильную группу или C3-6 циклоалкенильную группу; R1b представляет собой C3-6 циклоалкильную группу или C3-6 циклоалкенильную группу и R2 является таким, как определено выше."Защитная группа" в случае Pg представляет собой аминозащитную группу, обычно используемую для пептидного синтеза и т.п., которая не оказывает неблагоприятного влияния на ход реакции для каждой объясняемой далее стадии (например, бензильная группа, п-метоксибензильная группа) и т.п., и предпочтительно представляет собой бензильную группу. Стадия 1. На данной стадии соединение (IV) получают, подвергая соединение (II) и соединение (III) реакции восстановительного аминирования. Хотя данная реакция может быть проведена в соответствии с известным, по существу, способом[например, способ, описанный в 4 издании, Jikken Kagaku Koza, т. 14, стр. 370 и т.д.], обычно ее проводят в присутствии восстановителя в растворителе, где это необходимо, не оказывающего неблагоприятного влияния на реакцию. Соединение (II) может быть получено в соответствии с известным, по существу,способом [способ, описанный в Journal of Organometallic Chemistry, 1991, т. 412, ( 3), стр. 301] или аналогичным способом. Соединение (III) может быть получено в соответствии с известным, по существу,способом [способ, описанный в Synthetic Communications, 1994, т. 24, ( 10), стр. 1415] или аналогичным способом. Хотя используемое количество соединения (III) изменяется в зависимости от типа растворителя и других реакционных условий, оно обычно составляет примерно от 1 до примерно 10 моль, предпочтительно примерно от 1 до примерно 5 моль на 1 моль соединения (II). Примеры восстановителя включают алюминиевые реагенты (например, литийалюминийгидрид(NaBH(OAc)3) и т.д.) и т.п. Среди них боргидрид натрия, цианоборгидрид натрия и триацетоксиборгидрид натрия являются предпочтительными. Хотя используемое количество восстановителя изменяется в зависимости от типа растворителя и других реакционных условий, оно обычно составляет примерно от 1 до примерно 10 моль, предпочтительно примерно от 1 до примерно 5 моль на 1 моль соединения (II). Примеры растворителя, не оказывающего неблагоприятного влияния на реакцию, включают спирты(например, метанол, этанол, пропанол, 2-пропанол, бутанол, изобутанол, трет-бутанол и т.д.), углеводороды (например, бензол, толуол, ксилол, гексан, гептан и т.д.), галогенированные углеводороды (например, дихлорметан, хлороформ и т.д.), простые эфиры (например, диэтиловый эфир, диизопропиловый эфир, трет-бутилметиловый эфир, тетрагидрофуран, диоксан, диметоксиэтан и т.д.), нитрилы (например,ацетонитрил и т.д.), карбоновые кислоты (например, уксусная кислота, трифторуксусная кислота и т.д.) и т.п. Данные растворители можно использовать в смеси в подходящем соотношении. Температура реакции обычно составляет примерно от -80 до примерно 200 С, предпочтительно примерно от -80 до примерно 100 С. Время реакции обычно составляет примерно от 0,1 до примерно 100 ч, предпочтительно примерно 0,5 примерно 24 ч. Полученное таким образом соединение (IV) может быть выделено и очищено известными способами разделения и очистки, например, такими как концентрирование, концентрирование при пониженном давлении, экстракция растворителем, кристаллизация, перекристаллизация, фазовый переход, хроматография и т.п. Альтернативно, соединение (IV) можно использовать без выделения для следующей стадии реакции. Стадия 2. На данной стадии соединение (V) получают, подвергая соединение (IV) реакции внутримолекулярной циклизации. Хотя данная реакция может быть осуществлена известным, по существу, способом,обычно ее проводят в присутствии основания в растворителе, там, где это необходимо, не оказывающего неблагоприятного воздействия на реакцию. Примеры основания включают гидриды металлов (например, гидрид калия, гидрид натрия и т.д.),неорганические основания (например, гидроксиды щелочных металлов, такие как гидроксид лития, гидроксид натрия, гидроксид калия и т.п.; гидрокарбонаты щелочных металлов, такие как гидрокарбонат натрия, гидрокарбонат калия и т.п.; карбонаты щелочных металлов, такие как карбонат натрия, карбонат калия и т.п.; алкоксиды щелочных металлов, такие как метоксид натрия, этоксид натрия и т.д.), органические основания (например, триметиламин, триэтиламин, диизопропилэтиламин, N-метилморфолин,1,8-диазабицикло[5,4,0]ундец-7-ен, пиридин, N,N-диметиланилин, пиридазин, 4-диметиламинопиридин и т.д.), дисилазиды щелочных металлов (например, гексаметилдисилазид лития, гексаметилдисилазид натрия, гексаметилдисилазид калия и т.д.) и т.п. Среди них гидриды металлов, такие как гидрид калия, гидрид натрия и т.п.; алкоксиды щелочных металлов, такие как трет-бутоксид натрия, трет-бутоксид калия и т.д., являются предпочтительными. Хотя количество используемого основания изменяется в зависимости от типа растворителя и других условий реакции, обычно оно составляет примерно 0,1-10 моль, предпочтительно примерно 0,1-5 моль на 1 моль соединения (IV). Примеры растворителя, не оказывающего неблагоприятного влияния на реакцию, включают углеводороды (например, бензол, толуол, ксилол, гексан, гептан и т.д.), простые эфиры (например, диэтиловый эфир, диизопропиловый эфир, трет-бутилметиловый эфир, тетрагидрофуран, диоксан, диметоксиэтан и т.д.), нитрилы (например, ацетонитрил и т.д.), амиды (например, N,N-диметилформамид, N,Nдиметилацетамид и т.д.), сульфоксиды (например, диметилсульфоксид и т.д.) и т.п. Данные растворители можно использовать в смеси в подходящем соотношении. Температура реакции обычно составляет примерно от -50 до примерно 200 С, предпочтительно примерно от -20 до примерно 100 С. Время реакции изменяется в зависимости от типа соединения (IV), температуры реакции и т.п. и обычно составляет примерно от 0,1 до примерно 100 ч, предпочтительно примерно 0,5-24 ч. Полученное таким образом соединение (V) может быть выделено и очищено известными способами разделения и очистки, например, такими как концентрирование, концентрирование при пониженном давлении, экстракция растворителем, кристаллизация, перекристаллизация, фазовый переход, хроматография и т.п. Стадия 3. На данной стадии соединение (VI) получают, подвергая соединение (V) и соединение, представленное формулой R1a-В(ОН)2, где R1a является таким, как определено выше, или его соль (далее иногда сокращенно упоминаемое как R1a-B(OH)2) реакции сочетания. Данная реакция может быть проведена в соответствии с известным, по существу, способом [например, способ, описанный в Chemical Reviews, 1995, т. 95, стр. 2457 и т.д.] и может быть выполнена, например, в присутствии катализатора переходного металла и основания, в растворителе, не оказывающем неблагоприятного воздействия на реакцию. Используемое количество R1a-B(OH)2 обычно составляет примерно 1-10 моль, предпочтительно примерно 1-5 моль на 1 моль соединения (V). В качестве катализатора переходного металла можно использовать палладиевые катализаторы (на- 15021079 пример, ацетат палладия, хлорид палладия, тетракис(трифенилфосфин)палладий и т.д.), никелевые катализаторы (например, хлорид никеля и т.д.) и т.п. При необходимости можно добавить лиганд (например,трифенилфосфин, три-трет-бутилфосфин, трициклопропилфосфин и т.д.), а в качестве сокатализатора можно использовать оксид металла (например, оксид меди, оксид серебра и т.д.) и т.п. Хотя количество используемого катализатора переходного металла изменяется в зависимости от типа катализатора, оно обычно составляет примерно 0,0001-1 моль, предпочтительно примерно 0,01-0,5 моль на 1 моль соединения (V). Используемое количество лиганда обычно составляет примерно 0,0001- 4 моль, предпочтительно примерно 0,01-2 моль на 1 моль соединения (V). Используемое количество сокатализатора обычно составляет примерно 0,0001-4 моль, предпочтительно примерно 0,01-2 моль на 1 моль соединения (V). Примеры основания включают органические амины (например, триметиламин, триэтиламин, диизопропилэтиламин, N-метилморфолин, 1,8-диазабицикло[5,4,0]ундец-7-ен, пиридин, N,N-диметиланилин и т.д.), соли щелочных металлов (например, гидрокарбонат натрия, гидрокарбонат калия, карбонат натрия, карбонат калия, карбонат цезия, фосфат натрия, фосфат калия, гидроксид натрия, гидроксид калия и т.д.), гидриды щелочных металлов (например, гидрид калия, гидрид натрия и т.д.), алкоксиды щелочных металлов (например, метоксид натрия, этоксид натрия, трет-бутоксид натрия, трет-бутоксид калия и т.д.), дисилазиды щелочных металлов (например, гексаметилдисилазид лития, гексаметилдисилазид натрия, гексаметилдисилазид калия и т.д.) и т.п. Среди них соли щелочных металлов, такие как карбонат натрия, карбонат калия, карбонат цезия, фосфат натрия, фосфат калия и т.п.; алкоксиды щелочных металлов, такие как трет-бутоксид натрия, трет-бутоксид калия и т.п.; органические амины, такие как триэтиламин, диизопропилэтиламин и т.д.; и т.п. являются предпочтительными. Количество используемого основания обычно составляет примерно 0,1-10 моль, предпочтительно примерно 1-5 моль на 1 моль соединения (V). Примеры растворителя, который не отказывает неблагоприятного влияния на реакцию, включают углеводороды (например, бензол, толуол, ксилол и т.д.), галогенированные углеводороды (например,хлороформ, 1,2-дихлорэтан и т.д.), нитрилы (например, ацетонитрил и т.д.), простые эфиры (например,диметоксиэтан, тетрагидрофуран и т.д.), спирты (например, метанол, этанол и т.д.), апротонные полярные растворители (например, диметилформамид, диметилсульфоксид, гексаметилфосфортриамид и т.д.),воду и т.п. Данные растворители можно использовать в смеси в подходящем соотношении. Температура реакции обычно составляет от примерно 10 до примерно 200 С, предпочтительно от примерно 0 до примерно 150 С. Время реакции обычно составляет примерно 0,5-48 ч, предпочтительно примерно 0,5-16 ч. Полученное таким образом соединение (VI) может быть выделено и очищено известными способами разделения и очистки, например, такими как концентрирование, концентрирование при пониженном давлении, экстракция растворителем, кристаллизация, перекристаллизация, фазовый переход, хроматография и т.п. Альтернативно, соединение (VI) можно использовать, без выделения, для следующей реакции. Стадия 4. На данной стадии получают соединение (Ia), удаляя защитную группу в соединении (VI). Защитная группа может быть удалена с помощью реакции, известной, по существу, в качестве способа удаления защитной группы или аналогичным способом. Например, когда Pg представляет собой бензильную группу, защитная группа может быть удалена реакцией каталитического гидрирования. Реакцию каталитического гидрирования обычно можно проводить в атмосфере водорода в присутствии катализатора в растворителе, не оказывающем неблагоприятного воздействия на реакцию. Когда Rla представляет собой C3-6 циклоалкенильную группу, ее восстанавливают до C3-6 циклоалкильной группы с использованием реакции каталитического гидрирования. Примеры катализатора включают палладиевые катализаторы (например, палладий на угле, гидроксид палладия на угле, оксид палладия и т.д.), никелевые катализаторы (например, никелевый катализатор с развитой поверхностью и т.д.), платиновые катализаторы (например, оксид платины, платина на угле и т.д.), родиевые катализаторы (например, родий на угле и т.д.) и т.п. Количество используемого катализатора обычно составляет примерно от 0,001 до примерно 1 моль,предпочтительно примерно 0,01-0,5 моль на 1 моль соединения (VI). Примеры растворителя, который не отказывает неблагоприятного влияния на реакцию, включают спирты (например, метанол, этанол, пропанол, бутанол и т.д.), углеводороды (например, бензол, толуол,ксилол и т.д.), галогенированные углеводороды (например, дихлорметан, хлороформ и т.д.), простые эфиры (например, диэтиловый эфир, диоксан, тетрагидрофуран и т.д.), сложные эфиры (например, этилацетат и т.д.), амиды (например, N,N-диметилформамид и т.д.), карбоновые кислоты (например, уксусная кислота и т.д.), воду и т.п. Данные растворители можно использовать в смеси в подходящем соотношении. Давление водорода, при котором проводят реакцию, обычно составляет от примерно 1 до примерно 50 атм, предпочтительно примерно 1-10 атм. Температура реакции обычно составляет примерно от 0 до примерно 150 С, предпочтительно при- 16021079 мерно от 20 до примерно 100 С. Время реакции обычно составляет от примерно 5 мин до примерно 72 ч, предпочтительно примерно 0,5-40 ч. Полученное таким образом соединение (Ia) может быть выделено и очищено известными способами разделения и очистки, например, такими как концентрирование, концентрирование при пониженном давлении, экстракция растворителем, кристаллизация, перекристаллизация, фазовый переход, хроматография и т.п. В соединениях (I) соединение (Ib), где R1 представляет собой C1-6 алкоксильную группу, необязательно замещенную C3-6 циклоалкильной группой(ами), может быть получено, например, в соответствии со способом В, представленным ниже, или аналогичным способом. Способ В где R1c представляет собой C1-6 алкильную группу, необязательно замещенную C3-6 циклоалкильной группой(ами). Стадия 1. На данной стадии соединение (V) , полученное вышеуказанным способом А, стадии 1 и 2, преобразуют в соединение (VII) с помощью реакции замещения с использованием соединения, представленного формулой: R1cOH, где R1c является таким, как определено выше (далее иногда сокращенно упоминаемое как R1cOH). Данная стадия может быть осуществлена в соответствии с известным, по существу, способом [например, способ, описанный в J. Am. Soc. Chem., 1997, т. 119, стр. 3395 и т.д.] и может быть осуществлена в присутствии катализатора переходного металла и основания в растворителе, не оказывающем неблагоприятного влияния на реакцию. Количество используемого R1cOH обычно составляет примерно 1-10 моль, предпочтительно примерно 1-5 моль на 1 моль соединения (V). В качестве катализатора переходного металла можно использовать, например, палладиевые катализаторы (например, ацетат палладия(II), трис(дибензилиденацетон)дипалладий(0), хлорид палладия(II),тетракис(трифенилфосфин)палладий(0) и т.д.) и т.п. При необходимости может быть добавлен лиганд(например, 2,2'-бис(дифенилфосфино)-1,1'-бинафтил, 2,2'-бис(ди-п-толилфосфино)-1,1'-бинафтил, 2 дициклогексилфосфино-2',4',6'-триизопропил-1,1'-бифенил, трифенилфосфин, три-трет-бутилфосфин и т.п.). Хотя количество используемого катализатора переходного металла изменяется в зависимости от типа катализатора, оно обычно составляет примерно 0,0001-1 моль, предпочтительно примерно 0,01-0,5 моль на 1 моль соединения (V). Используемое количество лиганда обычно составляет примерно 0,0001-4 моль, предпочтительно примерно 0,01-0,2 моль на 1 моль соединения (V). Примеры основания включают органические амины (например, триметиламин, триэтиламин, диизопропилэтиламин, N-метилморфолин, 1,8-диазабицикло[5,4,0]ундец-7-ен, пиридин, N,N-диметиланилин и т.д.), соли щелочных металлов (например, гидрокарбонат натрия, гидрокарбонат калия, карбонат натрия, карбонат калия, карбонат цезия, фосфат натрия, фосфат калия, гидроксид натрия, гидроксид калия и т.д.), гидриды металлов (например, гидрид калия, гидрид натрия и т.д.), алкоксиды щелочных металлов(например, метоксид натрия, этоксид натрия, трет-бутоксид натрия, трет-бутоксид калия и т.д.), дисилазиды щелочных металлов (например, гексаметилдисилазид лития, гексаметилдисилазид натрия, гексаметилдисилазид калия и т.д.) и т.п. Среди них гидриды металлов, такие как гидрид калия, гидрид натрия и т.п.; алкоксиды щелочных металлов, такие как трет-бутоксид натрия, трет-бутоксид калия и т.п.; являются предпочтительными. Количество используемого основания обычно составляет примерно 0,1-10 моль, предпочтительно примерно 1-5 моль на 1 моль соединения (V). Примеры растворителя, не оказывающего неблагоприятного влияния на реакцию, включают углеводороды (например, бензол, толуол, ксилол и т.д.), галогенированные углеводороды (например, хлороформ, 1,2-дихлорэтан и т.д.), нитрилы (например, ацетонитрил и т.д.), простые эфиры (например, диметоксиэтан, тетрагидрофуран и т.д.), апротонные полярные растворители (например, N,Nдиметилформамид, диметилсульфоксид, гексаметилфосфортриамид и т.д.) и т.п. Данные растворители можно использовать в смеси в подходящем соотношении. Температура реакции обычно составляет примерно от -10 до примерно 200 С, предпочтительно примерно от 0 до примерно 150 С. Время реакции обычно составляет от примерно 0,5 до примерно 48 ч, предпочтительно примерно 0,5-16 ч. Полученное таким образом соединение (VII) может быть выделено и очищено известными способами разделения и очистки, например, такими как концентрирование, концентрирование при пониженном давлении, экстракция растворителем, кристаллизация, перекристаллизация, фазовый переход, хроматография и т.п. Альтернативно, соединение (VII) можно использовать, без выделения, для следующей реакции. Стадия 2. На данной стадии получают соединение (Ib) путем удаления защитной группы в соединении (VII). Данная стадия может быть осуществлена таким же образом, как в случае вышеописанного способа А,стадия 4. Полученное таким образом соединение (Ib) может быть выделено и очищено известными способами разделения и очистки, например, такими как концентрирование, концентрирование при пониженном давлении, экстракция растворителем, кристаллизация, перекристаллизация, фазовый переход, хроматография и т.п. В соединении (I) соединение (Ic), где R1 представляет собой морфолиногруппу, необязательно замещенную C1-6 алкильной группой(ами), или соединение (Ic), где R1 представляет собой ди(С 1-6 алкил)аминогруппу, может быть получено, например, в соответствии со способом С, представленным ниже, или аналогичным способом. Способ С где R1d и R1e являются одинаковыми или различными и каждый представляет собой C1-6 алкильную группу, или R1d и R1e могут образовывать вместе с атомом азота, с которым они связаны, морфолиногруппу, необязательно замещенную C1-6 алкильной группой(ами); а другие символы являются такими,как определено выше. Стадия 1. На данной стадии соединение (VIII) получают взаимодействием соединения (V), полученного вышеуказанным способом А, стадии 1 и 2, с соединением, представленным формулой: R1dR1eNH, где каждый символ является таким, как определено выше, или его солью (далее иногда сокращенно упоминаемым как R1dR1eNH). Данная реакция может быть осуществлена в соответствии с известным, по существу,способом [например, способ, описанный в J. Am. Chem. Soc, 2003, т. 125, стр. 6653 или J. Org. Chem.,2000, т. 65, стр. 1174 и т.д.] и может быть выполнена в присутствии катализатора переходного металла и основания в растворителе, которые не оказывают неблагоприятного влияния на реакцию. Количество используемого R1dR1eNH обычно составляет примерно 1-100 моль, предпочтительно примерно 1-3 моль на 1 моль соединения (V). Примеры катализатора переходного металла включают палладиевые катализаторы (например, ацетат палладия(II), трис(дибензилиденацетон)дипалладий(0), хлорид палладия(II), тетракис(трифенилфосфин)палладий(0) и т.д.), никелевые катализаторы (например, хлорид никеля и т.д.) и т.п. При необходимости может быть добавлен лиганд (например, 2-дициклогексилфосфино-2',4',6'-триизопропил-1,1'бифенил,трифенилфосфин,(R)-(-)-1-[(S)-2-(дициклогексилфосфино)ферроценил]этил(ди-третбутилфосфин, три-трет-бутилфосфин и т.д.). Хотя количество используемого катализатора переходного металла изменяется в зависимости от типа катализатора, оно обычно составляет примерно 0,0001-1 моль, предпочтительно примерно 0,01-0,5 моль на 1 моль соединения (V). Используемое количество лиганда обычно составляет примерно 0,0001-4 моль, предпочтительно примерно 0,01-2 моль на 1 моль соединения (V). Примеры основания включают органические амины (например, триметиламин, триэтиламин, диизопропилэтиламин, N-метилморфолин, 1,8-диазабицикло[5,4,0]ундец-7-ен, пиридин, N,N-диметиланилин и т.д.), соли щелочных металлов (например, гидрокарбонат натрия, гидрокарбонат калия, карбонат натрия, карбонат калия, карбонат цезия, фосфат натрия, фосфат калия, гидроксид натрия, гидроксид калия и т.д.), гидриды щелочных металлов (например, гидрид калия, гидрид натрия и т.д.), алкоксиды щелочных металлов (например, метоксид натрия, этоксид натрия, трет-бутоксид натрия, трет-бутоксид калия и т.д.), дисилазиды щелочных металлов (например, гексаметилдисилазид лития, гексаметилдисилазид натрия, гексаметилдисилазид калия и т.д.) и т.п. Среди них моли щелочных металлов, такие как карбонат калия, карбонат цезия, фосфат натрия, фосфат калия и т.п.; алкоксиды щелочных металлов, такие как трет-бутоксид натрия, трет-бутоксид калия и т.п.; органические амины, такие как триэтиламин, диизопропилэтиламин и т.д.; являются предпочтительными. Количество используемого основания обычно составляет примерно 0,1-10 моль, предпочтительно примерно 1-5 моль на 1 моль соединения (V). Примеры растворителя, который не отказывает неблагоприятного влияния на реакцию, включают углеводороды (например, бензол, толуол, ксилол и т.д.), галогенированные углеводороды (например,хлороформ, 1,2-дихлорэтан и т.д.), нитрилы (например, ацетонитрил и т.д.), простые эфиры (например,диметоксиэтан, тетрагидрофуран и т.д.), апротонные полярные растворители (например, N,Nдиметилформамид, диметилсульфоксид, гексаметилфосфорамид и т.д.) и т.п. Данные растворители можно использовать в смеси в подходящем соотношении. Температура реакции обычно составляет примерно от -10 до примерно 200 С, предпочтительно примерно от 0 до примерно 150 С. Время реакции обычно составляет от примерно 0,5 до примерно 48 ч, предпочтительно примерно 0,5-16 ч. Полученное таким образом соединение (VIII) может быть выделено и очищено известными способами разделения и очистки, например, такими как концентрирование, концентрирование при пониженном давлении, экстракция растворителем, кристаллизация, перекристаллизация, фазовый переход, хроматография и т.п. Альтернативно, соединение (VIII) можно использовать, без выделения, для следующей реакции. Стадия 2. На данной стадии получают соединение (Ic) путем удаления защитной группы в соединении (VIII). Данная стадия может быть осуществлена таким же образом, как в случае вышеописанного способа А,стадия 4. Полученное таким образом соединение (Ic) может быть выделено и очищено известными способами разделения и очистки, например, такими как концентрирование, концентрирование при пониженном давлении, экстракция растворителем, кристаллизация, перекристаллизация, фазовый переход, хроматография и т.п. Соединение (I) может быть получено, например, в соответствии со способом D, показанным ниже,или аналогичным способом. Способ D где каждый символ является таким, как определено выше. В данном способе соединение (I) получают, удаляя защитную группу в соединении (IX). Удаление защитной группы в данном способе может быть осуществлено в соответствии с реакцией, известной, по существу, как способ удаления защитной группы, или аналогичным способом. Когда Pg представляет собой бензильную группу, примеры способ удаления защитной группы включают способ обработки галогенангидридом кислоты и т.п. В качестве галогенангидрида кислоты можно использовать 1-хлорэтилхлороформиат, 2,2,2-трихлор-1,1-диметилэтилхлороформиат, триметилсилилэтилхлороформиат и т.п. Среди них предпочтительно используют 1-хлорэтилхлороформиат. Когда R1 представляет собой C3-6 циклоалкенильную группу, удаление защитной группы может быть осуществлено без восстановления циклоалкенила с использованием данного способа. При использовании 1-хлорэтилхлороформиата его применяемое количество обычно составляет примерно 1-10 моль, предпочтительно примерно 1-2 моль на 1 моль соединения (IX). Реакцию обычно проводят в растворителе, не оказывающем неблагоприятного влияния на реакцию. Примеры растворителя, который не отказывает неблагоприятного влияния на реакцию, включают углеводороды (например, бензол, толуол, ксилол и т.п.), галогенированные углеводороды (например,дихлорметан, хлороформ и т.п.), простые эфиры (например, диэтиловый эфир, диоксан, тетрагидрофуран и т.п.), сложные эфиры (например, этилацетат и т.п.), амиды (например, N,N-диметилформамид и т.п.),нитрилы (например, ацетонитрил и т.п.) и т.п. Данные растворители можно использовать в смеси в подходящем соотношении. Температура реакции обычно составляет примерно от -80 до примерно 150 С, предпочтительно примерно от 0 до примерно 100 С. Время реакции обычно составляет от примерно 5 мин до примерно 72 ч, предпочтительно примерно 0,5-20 ч. При использовании 1-хлорэтилхлороформиата соединение (IX) подвергают взаимодействию с 1 хлорэтилхлороформиатом и полученное соединение обрабатывают спиртом (например, метанол, этанол и т.п.), водным раствором (например, водный раствор гидроксида натрия и т.п.) или водой, при этом может быть получено соединение (I). Температура реакции обычно составляет примерно от 0 до примерно 150 С, предпочтительно при- 19021079 мерно от 5 до примерно 100 С. Время реакции обычно составляет от примерно 5 мин до примерно 24 ч, предпочтительно примерно 0,5-5 ч. Полученное таким образом соединение (I) может быть выделено и очищено известными способами разделения и очистки, например, такими как концентрирование, концентрирование при пониженном давлении, экстракция растворителем, кристаллизация, перекристаллизация, фазовый переход, хроматография и т.п. Соединение (VIII) в способе С также может быть получено в соответствии со следующим способом Е или аналогичным способом. Способ Е где каждый символ является таким, как определено выше. Стадия 1. На данной стадии соединение (XI) получают взаимодействием соединения (X) с R1dR1eNH. Данную реакцию обычно проводят в присутствии основания и, где это необходимо, в растворителе, не оказывающем неблагоприятного влияния на данную реакцию. Количество используемого R1dR1eNH обычно составляет примерно 1-100 моль, предпочтительно примерно 1-3 моль на 1 моль соединения (X). Примеры основания включают гидриды щелочных металлов (например, гидрид калия, гидрид натрия и т.д.), неорганические основания (например, гидроксиды щелочных металлов, такие как гидроксид лития, гидроксид натрия, гидроксид калия и т.п.; гидрокарбонаты щелочных металлов, такие как гидрокарбонат натрия, гидрокарбонат калия и т.п.; карбонаты щелочных металлов, такие как карбонат натрия,карбонат калия, карбонат цезия и т.п.; алкоксиды щелочных металлов, такие как метоксид натрия, этоксид натрия, и т.д. и т.п.), органические основания (например, триметиламин, триэтиламин, диизопропилэтиламин, N-метилморфолин, 1,8-диазабицикло[5,4,0]ундец-7-ен, пиридин, N,N-диметиланилин, пиридазин, 4-диметиламинопиридин и т.д.), и т.п. Среди них карбонаты щелочных металлов, такие как карбонат натрия, карбонат калия, карбонат цезия и т.п., являются предпочтительными. Хотя количество используемого основания изменяется в зависимости от типа растворителя и других условий реакции, обычно оно составляет примерно 0,1-10 моль, предпочтительно примерно 0,1-5 моль на 1 моль соединения (X). Примеры растворителя, не оказывающего неблагоприятного влияния на реакцию, включают углеводороды (например, бензол, толуол, ксилол, гексан, гептан и т.д.), простые эфиры (например, диэтиловый эфир, диизопропиловый эфир, трет-бутилметиловый эфир, тетрагидрофуран, диоксан, диметоксиэтан и т.д.), нитрилы (например, ацетонитрил и т.д.), амиды (например, N,N-диметилформамид, N,Nдиметилацетамид и т.д.), сульфоксиды (например, диметилсульфоксид и т.д.) и т.п. Данные растворители можно использовать в смеси в подходящем соотношении. Температура реакции обычно составляет примерно от -50 до примерно 300 С, предпочтительно примерно от 0 до примерно 200 С. Время реакции изменяется в зависимости от типа соединения (X), температуры реакции и т.п. и обычно составляет от примерно 0,1 до примерно 100 ч, предпочтительно примерно 0,5-36 ч. Полученное таким образом соединение (XI) может быть выделено и очищено известными способами разделения и очистки, например, такими как концентрирование, концентрирование при пониженном давлении, экстракция растворителем, кристаллизация, перекристаллизация, фазовый переход, хроматография и тому подобное. Альтернативно, соединение (XI) можно использовать, без выделения, для следующей реакции. Стадия 2. На данной стадии соединение (XII) получают, подвергая соединение (XI) реакции формилирования. Данная реакция может быть осуществлена в соответствии с известным, по существу, способом [например, способ, описанный в 4 издании, Jikken Kagaku Koza, т. 21, стр. 110 и т.д.], и обычно ее проводят с использованием комплекса Вильсмейера, который может быть получен из формамида (например, N,N- 20021079 диметилформамид, N-метилформанилид и т.д.) и галогенированного реагента (например, фосфорилхлорида, фосгена, оксалилхлорида, тионилхлорида, комплекса трифенилфосфина с бромом и т.д.) и т.п. и,где это необходимо, в растворителе, не оказывающем неблагоприятного влияния на реакцию. Хотя количество используемого формамида изменяется в зависимости от типа растворителя и других условий реакции, оно обычно составляет примерно 1-100 моль, предпочтительно примерно 1-10 моль на 1 моль соединения (XI) . Альтернативно, формамид можно использовать в качестве растворителя. Хотя количество используемого галогенированного реагента изменяется в зависимости от типа растворителя и других условий реакции, оно обычно составляет примерно 1-10 моль, предпочтительно примерно 1-5 моль на 1 моль соединения (XI). Примеры растворителя, который не отказывает неблагоприятного влияния на реакцию, включают углеводороды (например, бензол, толуол, ксилол, гексан, гептан и т.д.), простые эфиры (например, диэтиловый эфир, диизопропиловый эфир, трет-бутилметиловый эфир, тетрагидрофуран, диоксан, диметоксиэтан и т.д.), формамиды (например, N,N-диметилформамид, N-метилформанилид и т.д.) и т.п. Для получения комплекса Вильсмейера используемая температура реакции обычно составляет примерно от -50 до примерно 50 С, предпочтительно примерно от -20 до примерно 10 С. Время реакции обычно составляет примерно 0,1-10 ч, предпочтительно примерно 0,2-1 ч. В реакции комплекса Вильсмейера и соединения (XI) температура реакции обычно составляет примерно от -50 до примерно 300 С, предпочтительно примерно от 0 до примерно 200 С. Время реакции изменяется в зависимости от типа соединения (XI), температуры реакции и т.п. и обычно составляет примерно 0,1-100 ч, предпочтительно примерно 0,5-36 ч. Полученное таким образом соединение (XII) может быть выделено и очищено известными способами разделения и очистки, например, такими как концентрирование, концентрирование при пониженном давлении, экстракция растворителем, кристаллизация, перекристаллизация, фазовый переход, хроматография и т.п. Альтернативно, соединение (XII) можно использовать, без выделения, для следующей реакции. Стадия 3. На данной стадии соединение (XIII) получают из соединения (XII). Данная реакция может быть осуществлена в соответствии со способом А, стадия 1, или аналогичным способом. Полученное таким образом соединение (XIII) может быть выделено и очищено известными способами разделения и очистки, например, такими как концентрирование, концентрирование при пониженном давлении, экстракция растворителем, кристаллизация, перекристаллизация, фазовый переход, хроматография и тому подобное. Альтернативно, соединение (XIII) можно использовать, без выделения, для следующей реакции. Стадия 4. На данной стадии соединение (VIII) получают из соединения (XIII). Данная реакция может быть осуществлена в соответствии со способом А, стадия 2, или аналогичным способом. Полученное таким образом соединение (VIII) может быть выделено и очищено известными способами разделения и очистки, например, такими как концентрирование, концентрирование при пониженном давлении, экстракция растворителем, кристаллизация, перекристаллизация, фазовый переход, хроматография и т.п. Альтернативно, соединение (VIII) можно использовать, без выделения, для следующей реакции. Далее объясняются способы получения соединения (I0) согласно настоящему изобретению. Соединение (I0) по настоящему изобретению может быть получено в соответствии со следующими способом F,способом G, способом Н, способом I, способом J, способом K, способом L, способом М или способом N или аналогичным способом. Соединение (I0) охватывает соединения (I0a), (I0b), (I0c), (I0d), (I0e), (I0f), d0g),(I0h), (I0i), (I0j) и (I0k), полученные соответствующими способами получения. Способ F где R1f и R1g являются одинаковыми или различными и каждый представляет собой (а) C1-6 алкиль- 21021079 ную группу, необязательно замещенную заместителем(ями), выбранными из C3-6 циклоалкильной группы и фенильной группы, или (b) C3-6 циклоалкильную группу, или R1f и R1g образуют вместе с атомом азота, с которым они связаны, морфолинильную группу, необязательно замещенную C1-6 алкильной группой(ами), пиперидинильную группу, необязательно замещенную C1-6 алкильной группой(ами), или пирролидинильную группу, необязательно замещенную C1-6 алкильной группой(ами), необязательно замещенной C1-6 алкоксильной группой(ами); и другие символы являются такими, как определено выше. Стадия 1. На данной стадии соединение (XIV) получают взаимодействием соединения (X) с соединением,представленным формулой RlfR1gNH, или его солью (далее иногда сокращенно упоминаемым какR1fR1gNH). Данную реакцию обычно проводят в присутствии основания и, где это необходимо, в растворителе, не оказывающем неблагоприятного влияния на реакцию.R1fR1gNH может представлять собой коммерчески доступный продукт или может быть получен из соответствующих исходных соединений с использованием известных, по существу, способов. Количество используемого R1fR1gNH обычно составляет примерно 0,5-100 моль, предпочтительно примерно 1-10 моль на 1 моль соединения (X). Примеры основания включают гидриды щелочных металлов (например, гидрид калия, гидрид натрия и т.д.), неорганические основания (например, гидроксиды щелочных металлов, такие как гидроксид лития, гидроксид натрия, гидроксид калия и т.п.; гидрокарбонаты щелочных металлов, такие как гидрокарбонат натрия, гидрокарбонат калия и т.п.; карбонаты щелочных металлов, такие как карбонат натрия,карбонат калия, карбонат цезия и т.п.; алкоксиды щелочных металлов, такие как метоксид натрия, этоксид натрия и т.д. и т.п.), органические основания (например, триметиламин, триэтиламин, диизопропилэтиламин, N-метилморфолин, 1,8-диазабицикло[5,4,0]ундец-7-ен, пиридин, N,N-диметиланилин, пиридазин, 4-диметиламинопиридин и т.д.), и т.п. Среди них карбонаты щелочных металлов, такие как карбонат натрия, карбонат калия, карбонат цезия и т.п., являются предпочтительными. Хотя количество используемого основания изменяется в зависимости от типа растворителя и других условий реакции, обычно оно составляет примерно 0,1-10 моль, предпочтительно примерно 0,1-5 моль на 1 моль соединения (X). Примеры растворителя, не оказывающего неблагоприятного влияния на реакцию, включают углеводороды (например, бензол, толуол, ксилол, гексан, гептан и т.д.), простые эфиры (например, диэтиловый эфир, диизопропиловый эфир, трет-бутилметиловый эфир, тетрагидрофуран, диоксан, диметоксиэтан и т.д.), нитрилы (например, ацетонитрил и т.д.), амиды (например, N,N-диметилформамид, N,Nдиметилацетамид и т.д.), сульфоксиды (например, диметилсульфоксид и т.д.) и т.п. Данные растворители можно использовать в смеси в подходящем соотношении. Температура реакции обычно составляет примерно от -50 до примерно 300 С, предпочтительно примерно от 0 до примерно 200 С. Время реакции изменяется в зависимости от типа соединения RlfRlgNH, температуры реакции и т.п. и обычно составляет от примерно 0,1 до примерно 100 ч, предпочтительно примерно 0,5-36 ч. Полученное таким образом соединение (XIV) может быть выделено и очищено известными способами разделения и очистки, например, такими как концентрирование, концентрирование при пониженном давлении, экстракция растворителем, кристаллизация, перекристаллизация, фазовый переход, хроматография и т.п. Альтернативно, соединение (XIV) можно использовать, без выделения, для следующей реакции. Стадия 2. На данной стадии получают соединение (XV), подвергая соединение (XIV) реакции формилирования. Данная реакция может быть осуществлена в соответствии с известным, по существу, способом [например, способ, описанный в 4 изд., Jikken Kagaku Koza, т. 21, стр. 110 и т.д.], и обычно ее проводят с использованием комплекса Вильсмейера, который может быть получен из формамида (например, N,Nдиметилформамид, N-метилформанилид и т.д.) и галогенированного реагента (например, фосфорилхлорида, фосгена, оксалилхлорида, тионилхлорида, комплекса трифенилфосфина с бромом и т.д.) и т.п. и,где это необходимо, в растворителе, не оказывающем неблагоприятного влияния на реакцию. Хотя количество используемого формамида изменяется в зависимости от типа растворителя и других условий реакции, оно обычно составляет примерно 0,5-100 моль, предпочтительно примерно 1-10 моль на 1 моль соединения (XIV). Альтернативно, формамид можно использовать в качестве растворителя. Хотя количество используемого галогенированного реагента изменяется в зависимости от типа растворителя и других условий реакции, оно обычно составляет примерно 0,5-10 моль, предпочтительно примерно 1-5 моль на 1 моль соединения (XIV). Примеры растворителя, который не отказывает неблагоприятного влияния на реакцию, включают углеводороды (например, бензол, толуол, ксилол, гексан, гептан и т.д.), простые эфиры (например, диэтиловый эфир, диизопропиловый эфир, трет-бутилметиловый эфир, тетрагидрофуран, диоксан, диметоксиэтан и т.д.), формамиды (например, N,N-диметилформамид, N-метилформанилид и т.д.) и т.п. Для получения комплекса Вильсмейера используемая температура реакции обычно составляет примерно от -50 до примерно 50 С, предпочтительно примерно от -20 до примерно 10 С. Время реакции обычно составляет примерно 0,1-10 ч, предпочтительно примерно 0,2-1 ч. В реакции комплекса Вильсмейера и соединения (XIV) температура реакции обычно составляет примерно от -50 до примерно 300 С, предпочтительно примерно от 0 до примерно 200 С. Время реакции изменяется в зависимости от типа соединения (XIV), температуры реакции и т.п. и обычно составляет примерно 0,1-100 ч, предпочтительно примерно 0,5-36 ч. Полученное таким образом соединение (XV) может быть выделено и очищено известными способами разделения и очистки, например, такими как концентрирование, концентрирование при пониженном давлении, экстракция растворителем, кристаллизация, перекристаллизация, фазовый переход, хроматография и т.п. Альтернативно, соединение (XV) можно использовать, без выделения, для следующей реакции. Стадия 3. На данной стадии соединение (XVII) получают из соединения (XV) и соединения (XVI). Данная реакция может быть осуществлена в соответствии со способом А, стадия 1, или аналогичным способом. Полученное таким образом соединение (XVII) может быть выделено и очищено известными способами разделения и очистки, например, такими как концентрирование, концентрирование при пониженном давлении, экстракция растворителем, кристаллизация, перекристаллизация, фазовый переход, хроматография и т.п. Альтернативно, соединение (XVII) можно использовать, без выделения, для следующей реакции. Стадия 4. На данной стадии соединение (XVIII) получают из соединения (XVII). Данная реакция может быть осуществлена в соответствии со способом А, стадия 2, или аналогичным способом. Полученное таким образом соединение (XVIII) может быть выделено и очищено известными способами разделения и очистки, например, такими как концентрирование, концентрирование при пониженном давлении, экстракция растворителем, кристаллизация, перекристаллизация, фазовый переход, хроматография и т.п. Альтернативно, соединение (XVIII) можно использовать, без выделения, для следующей реакции. Стадия 5. На данной стадии соединение (I0a) получают, удаляя защитную группу в соединении (XVIII). Данная реакция может быть осуществлена в соответствии с вышеуказанным способом А, стадия 4. Полученное таким образом соединение (I0a) может быть выделено и очищено известными способами разделения и очистки, например, такими как концентрирование, концентрирование при пониженном давлении, экстракция растворителем, кристаллизация, перекристаллизация, фазовый переход, хроматография и т.п. Способ G где R1h представляет собой (a) C1-6 алкильную группу, необязательно замещенную заместителем(ями), выбранными из C3-6 циклоалкильной группы и фенильной группы, или (b) C3-6 циклоалкильную группу; R1i представляет собой C1-6 алкильную группу; X представляет собой атомы галогена, такие как атом хлора, атом брома, атом иода и т.п.; и другие символы являются такими, как определено выше. Стадия 1. На данной стадии соединение (XIX) получают взаимодействием соединения (X) с соединением,представленным формулой R1hNH2 или его солью. Данная стадия может быть осуществлена в соответствии с вышеописанным способом F, стадия 1, или аналогичным способом. Полученное таким образом соединение (XIX) может быть выделено и очищено известными способами разделения и очистки, например, такими как концентрирование, концентрирование при пониженном давлении, экстракция рас- 23021079 творителем, кристаллизация, перекристаллизация, фазовый переход, хроматография и т.п. Альтернативно, соединение (XIX) можно использовать, без выделения, для следующей реакции. Стадия 2. На данной стадии соединение (XX) получают, подвергая соединение (XIX) реакции алкилирования. Реакция алкилирования может быть осуществлена в соответствии с общепринятым способом в присутствии основания и алкилгалогенида, представленного формулой R1i-X (далее сокращенно упоминаемом какR1i-X), в растворителе, не оказывающем неблагоприятного влияния на реакцию. Примеры основания включают гидриды щелочных металлов (например, гидрид калия, гидрид натрия и т.д.), неорганические основания (например, гидроксиды щелочных металлов, такие как гидроксид лития, гидроксид натрия, гидроксид калия и т.п.; гидрокарбонаты щелочных металлов, такие как гидрокарбонат натрия, гидрокарбонат калия и т.п.; карбонаты щелочных металлов, такие как карбонат натрия,карбонат калия, карбонат цезия и т.п.; алкоксиды щелочных металлов, такие как метоксид натрия, этоксид натрия, трет-бутоксид натрия, трет-бутоксид калия и т.д. и т.п.), органические основания (например,триметиламин, триэтиламин, диизопропилэтиламин, N-метилморфолин, 1,8-диазабицикло[5,4,0]ундец-7 ен, пиридин, N,N-диметиланилин, пиридазин, 4-диметиламинопиридин и т.д.), литийорганические реагенты (например, н-бутиллитий, трет-бутиллитий, метиллитий и т.д.), дисилазиды щелочных металловR1i-X может представлять собой коммерчески доступный продукт или может быть получен из соответствующих исходных соединений с использованием известных, по существу, способов. Количество используемых как основания, так и R1i-X составляет примерно 0,5-20 моль, предпочтительно примерно 1-5 моль на 1 моль соединения (XIX). Примеры растворителя, который не отказывает неблагоприятного влияния на реакцию, включают простые эфиры, такие как тетрагидрофуран и т.п.; галогенированные углеводороды, такие как хлороформ и т.п.; ароматические углеводороды, такие как толуол и т.п.; амиды, такие как N,Nдиметилформамид и т.п.; сульфоксиды, такие как диметилсульфоксид и т.п., гексан и т.д.; и т.п. Данные растворители можно использовать в смеси в подходящем соотношении. Температура реакции обычно составляет примерно от -78 до примерно 250 С, предпочтительно(-78)-120 С. Время реакции обычно составляет примерно 0,5-24 ч. Полученное таким образом соединение (XX) может быть выделено и очищено известными способами разделения и очистки, например, такими как концентрирование, концентрирование при пониженном давлении, экстракция растворителем, кристаллизация, перекристаллизация, фазовый переход, хроматография и т.п. Альтернативно, соединение (XX) можно использовать, без выделения, для следующей реакции. Стадия 3. На данной стадии соединение (XXI) получают, подвергая соединение (XX) формилированию. Данная стадия может быть осуществлена в соответствии с вышеуказанным способом F, стадия 2, или аналогичным способом. Полученное таким образом соединение (XXI) может быть выделено и очищено известными способами разделения и очистки, например, такими как концентрирование, концентрирование при пониженном давлении, экстракция растворителем, кристаллизация, перекристаллизация, фазовый переход, хроматография и т.п. Альтернативно, соединение (XXI) можно использовать, без выделения,для следующей реакции. Стадия 4. На данной стадии соединение (XXII) получают, подвергая соединение (XXI) и соединение (XVI) реакции восстановительного аминирования. Данная стадия может быть осуществлена в соответствии с вышеуказанным способом А, стадия 1, или аналогичным способом. Полученное таким образом соединение (XXII) может быть выделено и очищено известными способами разделения и очистки, например,такими как концентрирование, концентрирование при пониженном давлении, экстракция растворителем,кристаллизация, перекристаллизация, фазовый переход, хроматография и т.п. Альтернативно, соединение (XXII) можно использовать, без выделения, для следующей реакции. Стадия 5. На данной стадии соединение (XXIII) получают из соединения (XXII). Данная стадия может быть осуществлена в соответствии с вышеуказанным способом А, стадия 2, или аналогичным способом. Полученное таким образом соединение (XXIII) может быть выделено и очищено известными способами разделения и очистки, например, такими как концентрирование, концентрирование при пониженном давлении, экстракция растворителем, кристаллизация, перекристаллизация, фазовый переход, хроматография и т.п. Альтернативно, соединение (XXIII) можно использовать, без выделения, для следующей реакции. Стадия 6. На данной стадии получают соединение (I0b), удаляя защитную группу в соединении (XXIII). Данная стадия может быть осуществлена в соответствии с вышеуказанным способом А, стадия 4. Полученное таким образом соединение (I0b) может быть выделено и очищено известными способа- 24021079 ми разделения и очистки, например, такими как концентрирование, концентрирование при пониженном давлении, экстракция растворителем, кристаллизация, перекристаллизация, фазовый переход, хроматография и т.п. Способ Н где R1j представляет собой C1-6 алкильную группу; Pg' представляет собой защитную группу; и другие символы являются такими, как определено выше. Примеры "защитной группы" Pg' включают аминозащитную группу, обычно используемую для пептидного синтеза, и т.п., которая не оказывает неблагоприятного влияния на процесс реакции на каждой из представленных ниже стадий (например, бензильная группа, п-метоксибензильная группа) и т.п.,при этом предпочтение отдается бензильной группе. Стадия 1. На данной стадии соединение (XXIV) получают взаимодействием соединения (X) с соединением,представленным формулой: R1jPgNH или его солью. Данная стадия может быть осуществлена таким же образом, как в вышеописанном способе F, стадия 1. Полученное таким образом соединение (XXIV) может быть выделено и очищено известными способами разделения и очистки, например, такими как концентрирование, концентрирование при пониженном давлении, экстракция растворителем, кристаллизация, перекристаллизация, фазовый переход,хроматография и т.п. Стадия 2. На данной стадии соединение (XXV) получают, подвергая соединение (XXIV) реакции формилирования. Данная стадия может быть осуществлена таким же образом, как в вышеописанном способе F, стадия 2. Полученное таким образом соединение (XXV) может быть выделено и очищено известными способами разделения и очистки, например, такими как концентрирование, концентрирование при пониженном давлении, экстракция растворителем, кристаллизация, перекристаллизация, фазовый переход, хроматография и т.п. Стадия 3. На данной стадии соединение (XXVI) получают из соединения (XXV) и соединения (XVI). Данная реакция может быть осуществлена в соответствии с вышеуказанным способом А, стадия 1, или аналогичным способом. Полученное таким образом соединение (XXVI) может быть выделено и очищено известными способами разделения и очистки, например, такими как концентрирование, концентрирование при пониженном давлении, экстракция растворителем, кристаллизация, перекристаллизация, фазовый переход, хроматография и т.п. Стадия 4. На данной стадии соединение (XXVII) получают из соединения (XXVI). Данная реакция может быть осуществлена в соответствии с вышеуказанным способом А, стадия 2, или аналогичным способом. Полученное таким образом соединение (XXVII) может быть выделено и очищено известными способами разделения и очистки, например, такими как концентрирование, концентрирование при пониженном давлении, экстракция растворителем, кристаллизация, перекристаллизация, фазовый переход,- 25021079 хроматография и т.п. Стадия 5. На данной стадии защитную группу (Pg) удаляют в соединении (XXVII) и вводят в него третбутоксикарбонильную группу, получая при этом соединение (XXVIII). На данной стадии защитную группу (Pg) удаляют таким же образом, как в вышеуказанном способе А, стадия 4, а третбутоксикарбонильная группа может быть введена в соответствии с известным способом. Реакцию трет-бутоксикарбонилирования проводят в соответствии с общепринятым способом с использованием ди-трет-бутилдикарбоната в присутствии основания, в растворителе, не оказывающем неблагоприятного влияния на реакцию. Примеры основания включают триэтиламин, трибутиламин, диизопропилэтиламин, карбонат калия,карбонат натрия, гидрид натрия, гидрид калия, гидроксид натрия, гидроксид калия и т.п. Количество используемого основания составляет примерно 0,5-20 моль, предпочтительно примерно 1-5 моль на 1 моль соединения (XXVII). Примеры растворителя, не оказывающего неблагоприятного влияния на реакцию, включают простые эфиры, такие как тетрагидрофуран и т.п.; галогенированные углеводороды, такие как хлороформ и т.п.; ароматические углеводороды, такие как толуол и т.п.; амиды, такие как диметилформамид и т.п.; сульфоксиды, такие как диметилсульфоксид и т.д.; и т.п. Данные растворители можно использовать в смеси в подходящем соотношении. Температура реакции обычно составляет примерно от -50 до примерно 250 С; предпочтительно 0120 С. Время реакции обычно составляет примерно 0,5- 24 ч. Полученное таким образом соединение (XXVIII) может быть выделено и очищено известными способами разделения и очистки, например, такими как концентрирование, концентрирование при пониженном давлении, экстракция растворителем, кристаллизация, перекристаллизация, фазовый переход,хроматография и т.п. Стадия 6. На данной стадии соединение (XXIX) получают, удаляя защитную группу (Pg') в соединении(XXVIII). Данная стадия может быть осуществлена таким же образом, как в вышеуказанном способе А,стадия 4. Полученное таким образом соединение (XXIX) может быть выделено и очищено известными способами разделения и очистки, например, такими как концентрирование, концентрирование при пониженном давлении, экстракция растворителем, кристаллизация, перекристаллизация, фазовый переход,хроматография и т.п. Стадия 7. На данной стадии соединение (XXIX) подвергают реакции алкилирования и преобразуют в соединение (XXX). Данная стадия может быть осуществлена таким же образом, как в вышеуказанном способеG, стадия 2. Полученное таким образом соединение (XXX) может быть выделено и очищено известными способами разделения и очистки, например, такими как концентрирование, концентрирование при пониженном давлении, экстракция растворителем, кристаллизация, перекристаллизация, фазовый переход, хроматография и т.п. Стадия 8. На данной стадии соединение (I0c) получают, удаляя трет-бутоксикарбонильную группу в соединении (XXX). Хотя данная реакция может быть осуществлена в соответствии с известным, по существу,способом, обычно ее приводят путем взаимодействия с кислотой в растворителе, не оказывающем неблагоприятного влияния на реакцию. Примеры кислоты включают соляную кислоту, бромисто-водородную кислоту, серную кислоту,трифторуксусную кислоту, трифторметансульфоновую кислоту, хлористый водород и т.п. Количество используемой кислоты составляет примерно 0,5-200 моль, предпочтительно примерно 1-100 моль на 1 моль соединения (XXX). Примеры растворителя, который не отказывает неблагоприятного влияния на реакцию, включают спирты (например, метанол и т.д.), простые эфиры (например, тетрагидрофуран и т.д.), галогенированные углеводороды (например, хлороформ и т.д.), ароматические углеводороды (например, толуол и т.д.),амиды (например, N,N-диметилформамид и т.д.), сульфоксиды (например, диметилсульфоксид и т.д.),сложные эфиры (например, этилацетат и т.д.) и т.п. Данные растворители можно использовать в смеси в подходящем соотношении. Температура реакции обычно составляет примерно от -50 до примерно 250 С; предпочтительно 0120 С. Время реакции обычно составляет примерно 0,5-24 ч. Полученное таким образом соединение (I0c) может быть выделено и очищено известными способами разделения и очистки, например, такими как концентрирование, концентрирование при пониженном давлении, экстракция растворителем, кристаллизация, перекристаллизация, фазовый переход, хроматография и т.п. где каждый символ является таким, как определено выше. Стадия 1. На данной стадии соединение (I0d) получают, удаляя трет-бутилоксикарбонильную группу в соединении (XXIX). Данная стадия может быть осуществлена таким же образом, как в вышеописанном способе Н, стадия 8. Полученное таким образом соединение (I0d) может быть выделено и очищено известными способами разделения и очистки, например, такими как концентрирование, концентрирование при пониженном давлении, экстракция растворителем, кристаллизация, перекристаллизация, фазовый переход, хроматография и т.п. Способ J где каждый из R4a и R4b независимо представляет собой C1-6 алкильную группу; и другие символы являются такими, как определено выше. Стадия 1. На данной стадии соединение (XXXI) получают из соединения (II) и соединения (XVI). Данная реакция может быть осуществлена в соответствии со способом А, стадия 1, или аналогичным способом. Полученное таким образом соединение (XXXI) может быть выделено и очищено известными способами разделения и очистки, например, такими как концентрирование, концентрирование при пониженном давлении, экстракция растворителем, кристаллизация, перекристаллизация, фазовый переход,хроматография и т.п. Стадия 2. На данной стадии соединение (XXXII) получают из соединения (XXXI). Данная реакция может быть осуществлена в соответствии со способом А, стадия 2, или аналогичным способом. Полученное таким образом соединение (XXXII) может быть выделено и очищено известными способами разделения и очистки, например, такими как концентрирование, концентрирование при пониженном давлении, экстракция растворителем, кристаллизация, перекристаллизация, фазовый переход,хроматография и т.п. Стадия 3. На данной стадии соединение (XXXIII) получают взаимодействием соединения (XXXII) с эквивалентом аммиака с последующей реакцией с кислотой или фторированным реагентом. Данная реакция может быть проведена в соответствии с известным, по существу, способом [например, способ, описанный в Organic Letters, 2001, т. 3, стр. 3417 и т.д.] и может быть проведена взаимодействием соединения (XXXII) с эквивалентом аммиака в присутствии катализатора переходного металла и основания, в растворителе, не оказывающем неблагоприятного влияния на реакцию, с последующей реакцией с кислотой или фторированным реагентом. Примеры эквивалента аммиака включают имин бензофенона, аминотрифенилсилан, дисилазиды щелочного металла (например, гексаметилдисилазид лития, гексаметилдисилазид натрия, гексаметилди- 27021079 силазид калия и т.д.) и т.п. Количество используемого эквивалента аммиака обычно составляет примерно 0,5-20 моль, предпочтительно примерно 1-5 моль на 1 моль соединения (XXXII). Примеры катализатора переходного металла включают палладиевые катализаторы (например, ацетат палладия(II), трис(дибензилиденацетон)дипалладий(0), хлорид палладия(II), тетракис(трифенилфосфин)палладий(0) и т.д.), никелевые катализаторы (например, хлорид никеля и т.д.) и т.п. При необходимости может быть добавлен лиганд (например, 2-дициклогексилфосфино-2',4',6'-триизопропил-1,1'бифенил, трифенилфосфин, 2-(дициклогексилфосфино)бифенил, три(трет-бутил)фосфин и т.д.). Хотя количество используемого катализатора переходного металла изменяется в зависимости от типа растворителя и других условий реакции, оно обычно составляет примерно 0,0001-1 моль, предпочтительно примерно 0,01-0,5 моль на 1 моль соединения (XXXII). Используемое количество лиганда обычно составляет примерно 0,0001-4 моль, предпочтительно примерно 0,01-0,2 моль на 1 моль соединения (XXXII). Примеры основания включают органические амины (например, триметиламин, триэтиламин, диизопропилэтиламин, N-метилморфолин, 1,8-диазабицикло[5,4,0]ундец-7-ен, пиридин, N,N-диметиланилин и т.д.), соли щелочных металлов (например, гидрокарбонат натрия, гидрокарбонат калия, карбонат натрия, карбонат калия, карбонат цезия, фосфат натрия, фосфат калия, гидроксид натрия, гидроксид калия и т.д.), гидриды щелочных металлов (например, гидрид калия, гидрид натрия и т.д.), алкоксиды щелочных металлов (например, метоксид натрия, этоксид натрия, трет-бутоксид натрия, трет-бутоксид калия и т.д.), дисилазиды щелочных металлов (например, гексаметилдисилазид лития, гексаметилдисилазид натрия, гексаметилдисилазид калия и т.д.) и т.п. Среди них соли щелочных металлов, такие как карбонат калия, карбонат цезия, фосфат натрия, фосфат калия и т.п.; алкоксиды щелочных металлов такие как трет-бутоксид натрия, трет-бутоксид калия и т.п.; органические амины, такие как триэтиламин, диизопропилэтиламин и т.д.; и т.п. являются предпочтительными. Количество используемого основания обычно составляет примерно 0,1-10 моль, предпочтительно примерно 1-5 моль на 1 моль соединения (XXXII). Примеры растворителя, который не отказывает неблагоприятного влияния на реакцию, включают углеводороды (например, бензол, толуол, ксилол и т.д.), галогенированные углеводороды (например,хлороформ, 1,2-дихлорэтан и т.д.), нитрилы (например, ацетонитрил и т.д.), простые эфиры (например,диметоксиэтан, тетрагидрофуран и т.д.), апротонные полярные растворители (например, N,Nдиметилформамид, диметилсульфоксид, гексаметилфосфорамид и т.д.) и т.п. Данные растворители можно использовать в смеси в подходящем соотношении. Температура реакции обычно составляет примерно от -10 до примерно 200 С, предпочтительно примерно от 0 до примерно 150 С. Время реакции обычно составляет примерно от 0,5 до примерно 48 ч, предпочтительно примерно 0,5-16 ч. После взаимодействия с эквивалентом аммония реакционную смесь подвергают взаимодействию с кислотой или фторированным реагентом, при этом может быть получено соединение (XXXIII). Примеры кислоты включают минеральные кислоты, такие как хлористо-водородная кислота, фосфорная кислота, серная кислота и т.п., органические кислоты, такие как толуолсульфоновая кислота, метансульфоновая кислота, уксусная кислота и т.п. Среди них хлористо-водородная кислота является предпочтительной. Количество используемой кислоты составляет примерно 0,1-100 моль, предпочтительно примерно 1-50 моль на 1 моль соединения (XXXII). Когда дисилазид щелочного металла (например, гексаметилдисилазид лития, гексаметилдисилазид натрия, гексаметилдисилазид калия и т.д.) используют в качестве эквивалента аммиака, можно использовать фторированный реагент. Среди них фторид тетрабутиламмония является предпочтительным. Количество используемого фторированного реагента составляет примерно 0,5-100 моль, предпочтительно примерно 1-10 моль на 1 моль соединения (XXXII). Температура реакции обычно составляет примерно от -10 до примерно 200 С, предпочтительно примерно от 0 до примерно 150 С. Время реакции обычно составляет примерно от 0,5 до примерно 48 ч, предпочтительно примерно 0,5-16 ч. Полученное таким образом соединение (XXXIII) может быть выделено и очищено известными способами разделения и очистки, например, такими как концентрирование, концентрирование при пониженном давлении, экстракция растворителем, кристаллизация, перекристаллизация, фазовый переход,хроматография и т.п. Альтернативно, соединение (XXXIII) можно использовать, без выделения, на следующей стадии реакции. Стадия 4. На данной стадии соединение (I0e) получают удалением защитной группы в соединении (XXXIII). Данная стадия может быть осуществлена таким же образом, как в вышеуказанном способе А, стадия 4. Полученное таким образом соединение (I0e) может быть выделено и очищено известными способа- 28021079 ми разделения и очистки, например, такими как концентрирование, концентрирование при пониженном давлении, экстракция растворителем, кристаллизация, перекристаллизация, фазовый переход, хроматография и т.п. Стадия 5. На данной стадии соединение (XXXIV) получают взаимодействием соединения (XXXIII) с дикетонной формой (XLI). При необходимости, может быть добавлена кислота (например, минеральные кислоты, такие как соляная кислота, фосфорная кислота, серная кислота и т.п., органические кислоты, такие как толуолсульфоновая кислота, метансульфоновая кислота, уксусная кислота и т.п.) в количестве от примерно 0,1-10 моль, предпочтительно примерно 0,5-10 моль на 1 моль соединения (XXXIII). Количество используемой дикетонной формы (XLI) составляет примерно 0,5-20 моль, предпочтительно примерно 1-10 моль на 1 моль соединения (XXXIII). Данную реакцию преимущественно проводят без растворителя или в растворителе, инертном по отношению к реакции. Хотя такие растворители не ограничены конкретным образом до тех пор, пока протекает реакция, например, спирты, такие как метанол, этанол, 1-пропанол, 2-пропанол, третбутиловый спирт и т.п.; галогенированные углеводороды, такие как дихлорметан, хлороформ, 1,2 дихлорэтан и т.п.; простые эфиры, такие как диэтиловый эфир, диизопропиловый эфир, дифениловый эфир, тетрагидрофуран, 1,4-диоксан, 1,2-диметоксиэтан и т.п.; ароматические углеводороды, такие как бензол, толуол и т.п.; насыщенные углеводороды, такие как циклогексан, гексан и т.п.; амиды, такие какN,N-диметилформамид, N,N-диметилацетамид, гексаметилфосфортриамид и т.п.; органические кислоты,такие как муравьиная кислота, уксусная кислота, пропановая кислота, трифторуксусная кислота, метансульфоновая кислота и т.д. и т.п.) или смешанный растворитель на их основе и т.п. являются предпочтительным. Хотя время реакции изменяется в зависимости от используемых реагентов и растворителя, обычно оно составляет примерно от 10 мин до примерно 100 ч, предпочтительно 30 мин - примерно 50 ч. Температура реакции обычно составляет примерно от -20 до примерно 150 С, предпочтительно примерно от 0 до примерно 100 С. Полученное таким образом соединение (XXXIV) может быть выделено и очищено известными способами разделения и очистки, например, такими как концентрирование, концентрирование при пониженном давлении, экстракция растворителем, кристаллизация, перекристаллизация, фазовый переход,хроматография и т.п. Стадия 6. На данной стадии соединение (I0f) получают удалением защитной группы в соединении (XXXIV). Данная стадия может быть осуществлена таким же образом, как в вышеуказанном способе А, стадия 4. Полученное таким образом соединение (I0f) может быть выделено и очищено известными способами разделения и очистки, например, такими как концентрирование, концентрирование при пониженном давлении, экстракция растворителем, кристаллизация, перекристаллизация, фазовый переход, хроматография и т.п. Способ K где R5 представляет собой C1-6 алкильную группу; и другие символы являются такими, как определено выше. Стадия 1. На данной стадии соединение (XXXVII) получают взаимодействием соединения (XXXV) с соединением (XXXVI). Данная реакция может быть проведена в присутствии основания, и, когда необходимо, в присутствии медной соли, в растворителе, не оказывающем неблагоприятного влияния на реакцию. Хотя используемое количество соединения (XXXVI) изменяется в зависимости от вида растворителя и других реакционных условий, оно обычно составляет примерно от 0,5 до примерно 50 моль, предпочтительно примерно от 1 до примерно 10 моль на 1 моль соединения (XXXV). Примеры основания включают гидриды металлов (например, гидрид калия, гидрид натрия и т.д.),неорганические основания (например, гидроксиды щелочных металлов, такие как гидроксид лития, гидроксид натрия, гидроксид калия и т.п.; гидрокарбонаты щелочных металлов, такие как гидрокарбонат натрия, гидрокарбонат калия и т.п.; карбонаты щелочных металлов, такие как карбонат натрия, карбонат калия, карбонат цезия и т.п.; алкоксиды щелочных металлов, такие как метоксид натрия, этоксид натрия,- 29
МПК / Метки
МПК: C07D 498/04, A61P 21/00, A61P 15/00, A61P 43/00, A61P 3/00, A61P 13/02
Метки: производные, пиразинооксазепина
Код ссылки
<a href="https://eas.patents.su/30-21079-proizvodnye-pirazinooksazepina.html" rel="bookmark" title="База патентов Евразийского Союза">Производные пиразинооксазепина</a>
Предыдущий патент: Электрический коммутационный аппарат
Следующий патент: Способ изготовления замороженного кондитерского изделия
Случайный патент: Способ кристаллизации лозартана












