Новые азагетероциклические соединения
Номер патента: 20302
Опубликовано: 30.10.2014
Авторы: Вандевер Харолд Джордж, Бруггер Надя, Лань Руокси, Потник Джастин, Хак Бейярд Р., Саттон Аманда Э., Ричардсон Томас Э.
Формула / Реферат
1. Соединение формулы (I)

и его фармацевтически приемлемые соли или сольваты,
где Т, Q означают S или СН при условии, что если Т означает S, то Q означает СН, и если Q означает S, то Т означает СН,
---- означает присутствие или отсутствие связи при условии, что одна из двух пунктирных линий всегда означает связь, тогда как другая всегда означает ее отсутствие,
R3 означает Н или А,
R4 означает А, Ar или А-Ar или
R3 и R4 вместе с атомом С, к которому они присоединены, могут образовывать Ar или циклический А, который может быть незамещенным или замещенным COO(LA) или CONH(LA),
Ar означает моно- или бициклический ароматический гомо- или гетероцикл, содержащий 1-4 атома N, О и/или S и 5-10 атомов скелета, который может быть незамещенным или независимо друг от друга моно-, ди- или тризамещенным Hal, А, ОН, SH, OA, NH2, NHA, NA2, NO2, CN, OCN, SCN, COOH, COOA, CONH2, CONHA, CONH(LAr), CONA2, NHCOA, NHCO(LAr), NHCONHA, NHCONH2, NHSO2A, CHO, COA, SO2NH2, SO2A и/или SO2Hal,
А означает неразветвленный или разветвленный линейный или циклический алкил, который содержит 1, 2, 3, 4, 5, 6, 7 или 8 атомов С, в котором одна или две СН2 группы могут быть заменены атомом О или S и/или NH, N(LA), SO2, CONH, NHCO или -СН=СН-группой, и в котором 1-3 атома Н могут быть заменены Hal, и в котором одна или две СН3 группы могут быть заменены ОН, SH, NH2, NH(LA), N(LA)2, NHCOOH, NHCONH2, N3, NO2 или CN,
LA означает неразветвленный или разветвленный линейный алкил, который содержит 1, 2, 3 или 4 атома С,
LAr означает моноциклический ароматический гомо- или гетероцикл, содержащий 1 или 2 атома N, О и/или S и 5-7 атомов скелета, который может быть незамещенным или моно-, ди- или тризамещенным Hal, LA, ОН, O(LA), NH2 или NH(LA),
Hal означает F, Cl, Br или I.
2. Соединения по п.1, которые соответствуют формулам (II), (III), (IV) или (V)
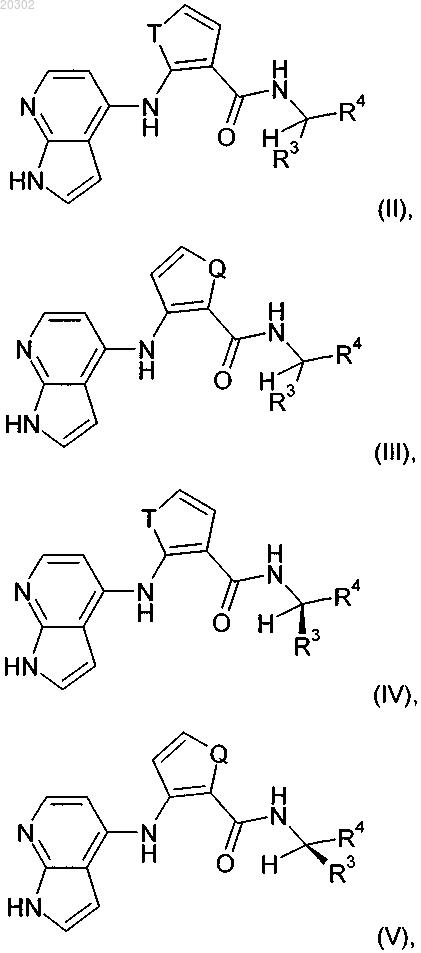
и их фармацевтически приемлемые соли или сольваты,
в которых Т и Q означают S, и остальные заместители имеют значения, указанные для формулы (I) в п.1.
3. Соединение по п.2, в котором остатки, не обозначенные более подробно, имеют значения, указанные для формулы (I) в п.1, но в которым
в подформуле А
Т, Q означают S,
R3 означает Н, гидроксиметил, аминометил, азидометил или цианометил,
или в подформуле В
Т, Q означают S,
R4 означает фенил или бензил, который может быть незамещенным или независимо друг от друга моно-, ди- или тризамещенным метилом, метокси, CF3, OCF3, амино, Cl или F; или
R4 означает бензиламинометил, где фенильное кольцо может быть незамещенным или независимо друг от друга моно-, ди- или тризамещенным метилом, метокси, CF3, OCF3, амино, Cl или F; или
R4 означает аминометил, (фторбензоиламино)бензил, (бензоиламино)бензил, (хлоразабензоиламино)бензил, пирролидинил, (тиофенилметил)аминоэтил, (индолилметил)аминометил, (1-фенилэтиламино)метил, бензилоксиметил, фениламинометил, изобутил, [(фуранилметил)амино]метил, [(пирролилметил)амино]метил, тиофенилметил, (сульфамоилфенил)метил, циклогексенилметил, бензоиламинометил, 1-гидрокси-1-фенилметил, (фуранилметилсульфанил)метил или бензолсульфониламинометил,
или в подформуле С
Т, Q означают S,
R3 означает Н, гидроксиметил, аминометил, азидометил или цианометил,
R4 означает фенил или бензил, который может быть незамещенным или независимо друг от друга моно-, ди- или тризамещенным метилом, метокси, CF3, OCF3, амино, Cl или F; или
R4 означает бензиламинометил, где фенильное кольцо может быть незамещенным или независимо друг от друга моно-, ди- или тризамещенным метилом, метокси, CF3, OCF3, амино, Cl или F; или
R4 означает аминометил, (фторбензоиламино)бензил, (бензоиламино)бензил, (хлоразабензоиламино)бензил, пирролидинил, (тиофенилметил)аминоэтил, (индолилметил)аминометил, (1-фенилэтиламино)метил, бензилоксиметил, фениламинометил, изобутил, [(фуранилметил)амино]метил, [(пирролилметил)амино]метил, тиофенилметил, (сульфамоилфенил)метил, циклогексенилметил, бензоиламинометил, 1-гидрокси-1-фенилметил, (фуранилметилсульфанил)метил или бензолсульфониламинометил,
или в подформуле D
Т, Q означают S,
R3 означает гидроксиметил, аминометил, азидометил или цианометил,
R4 означает фенил или бензил, который может быть незамещенным или независимо друг от друга моно-, ди- или тризамещенным метилом, метокси, CF3, OCF3, амино, Cl или F,
или в подформуле Е
Т, Q означают S,
R3 означает Н,
R4 означает бензиламинометил, где фенильное кольцо может быть незамещенным или независимо друг от друга моно-, ди- или тризамещенным метилом, метокси, CF3, OCF3, амино, Cl или F; или
R4 означает аминометил, (фторбензоиламино)бензил, (бензоиламино)бензил, (хлоразабензоиламино)бензил, пирролидинил, (тиофенилметил)аминоэтил, (индолилметил)аминометил, (1-фенилэтиламино)метил, бензилоксиметил, фениламинометил, изобутил, [(фуранилметил)амино]метил, [(пирролилметил)амино]метил, тиофенилметил, (сульфамоилфенил)метил, циклогексенилметил, бензоиламинометил, 1-гидрокси-1-фенилметил, (фуранилметилсульфанил)метил или бензолсульфониламинометил,
или в подформуле F
Т, Q означают S,
R3 и R4 вместе с атомом С, к которому они присоединены, образуют пиперидинил, фенил, пирролидинил, тетрагидрофуранил, каждый из которых может быть незамещенным или независимо друг от друга моно-, ди- или тризамещенным метилом, метокси, CF3, OCF3, амино, Cl или F,
или в подформуле G
Т, Q означают S,
R3 означает Н,
и остальные остатки имеют значения, указанные для формулы (I) выше,
и его фармацевтически приемлемые соли или сольваты.
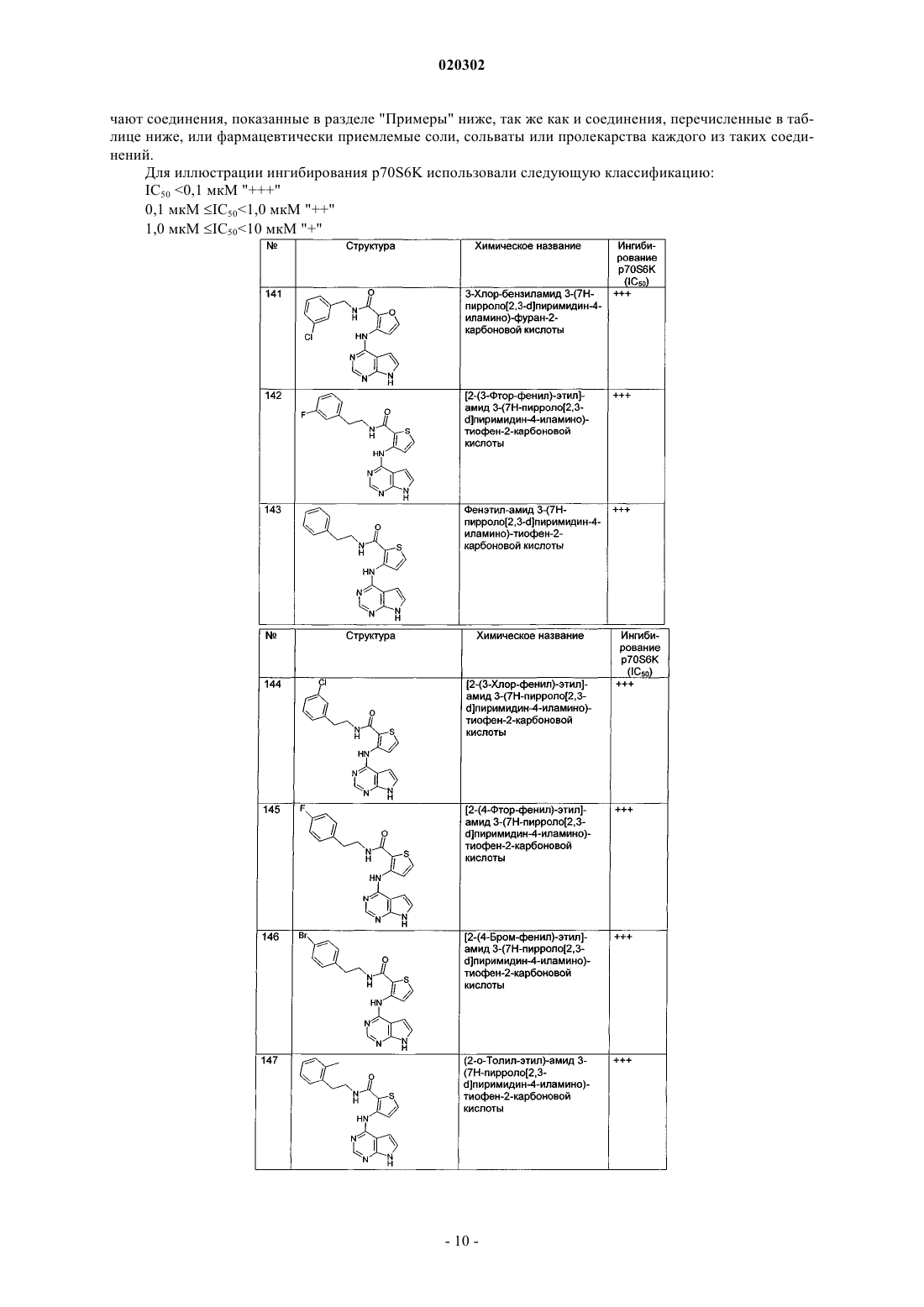
4. Соединение по п.1, где соединение выбрано из группы, состоящей из
[2-(3-фторфенил)этил]амида 3-(7Н-пирроло[2,3-d]пиримидин-4-иламино)тиофен-2-карбоновой кислоты,
фенэтиламида 3-(7Н-пирроло[2,3-d]пиримидин-4-иламино)тиофен-2-карбоновой кислоты,
[2-(3-хлорфенил)этил]амида 3-(7Н-пирроло[2,3-d]пиримидин-4-иламино)тиофен-2-карбоновой кислоты,
[2-(4-фторфенил)этил]амида 3-(7Н-пирроло[2,3-d]пиримидин-4-иламино)тиофен-2-карбоновой кислоты,
[2-(4-бромфенил)этил]амида 3-(7Н-пирроло[2,3-d]пиримидин-4-иламино)тиофен-2-карбоновой кислоты,
(2-о-толилэтил)амида 3-(7Н-пирроло[2,3-d]пиримидин-4-иламино)тиофен-2-карбоновой кислоты,
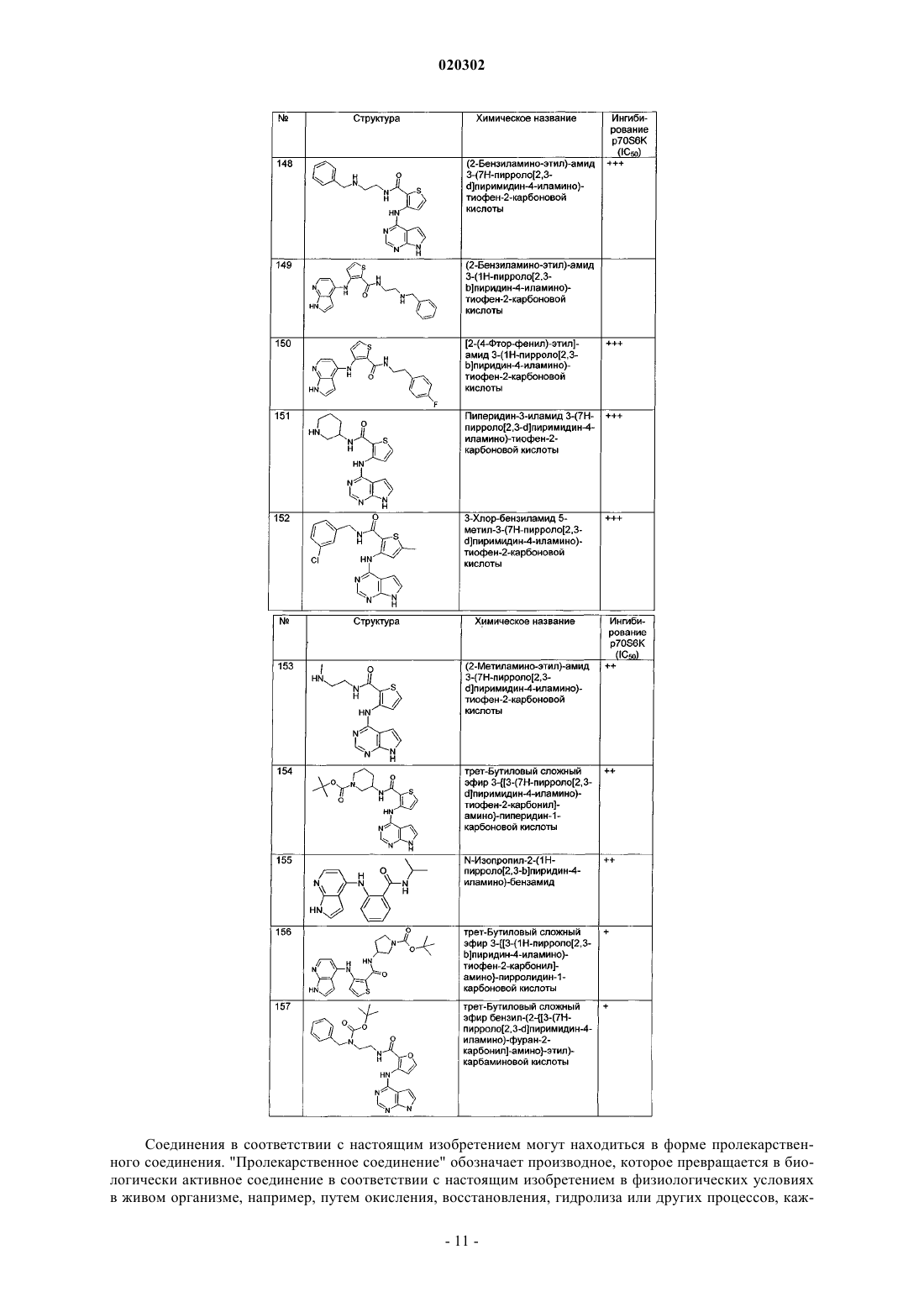
(2-бензиламиноэтил)амида 3-(7Н-пирроло[2,3-d]пиримидин-4-иламино)тиофен-2-карбоновой кислоты,
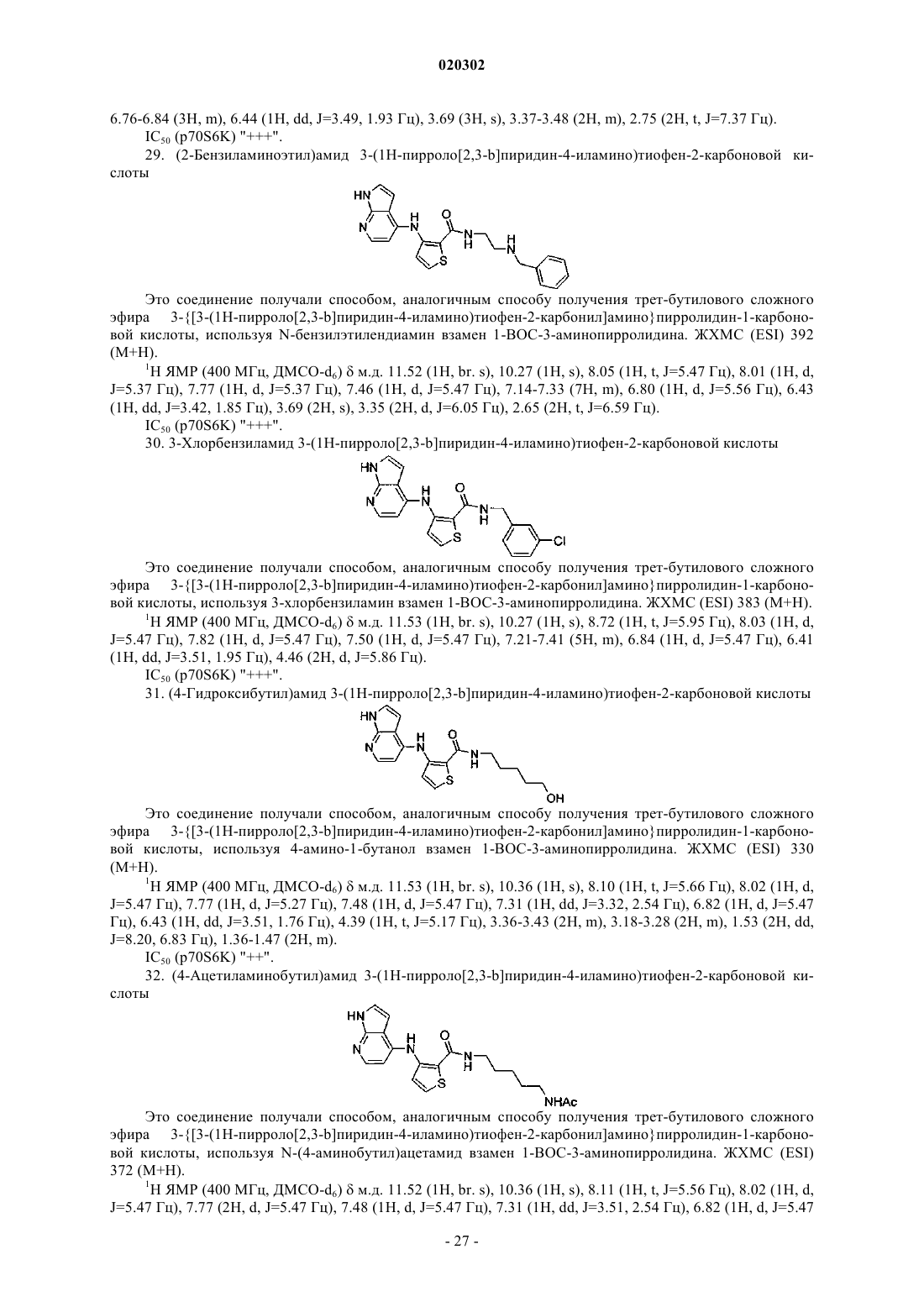
(2-бензиламиноэтил)амида 3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты,
[2-(4-фторфенил)этил]амида 3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты,
пиперидин-3-иламида 3-(7Н-пирроло[2,3-d]пиримидин-4-иламино)тиофен-2-карбоновой кислоты,
3-хлорбензиламида 5-метил-3-(7Н-пирроло[2,3-d]пиримидин-4-иламино)тиофен-2-карбоновой кислоты,
пирролидин-3-иламида 3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты,
[2-(4-сульфамоилфенил)этил]амида 3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты,
[2-(3-трифторметилфенил)этил]амида 3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты,
[2-(3-хлорфенил)этил]амида 3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты,
(2-тиофен-2-илэтил)амида 3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты,
[2-(3-фторфенил)этил]амида 3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты,
[2-(4-фторфенил)этил]амида 3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты,
[2-(фуран-2-илметилсульфанил)этил]амида 3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты,
(2-о-толилэтил)амида 3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты,
[2-(3-метоксифенил)этил]амида 3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты,
[2-(4-бромфенил)этил]амида 3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты,
[2-(4-метоксифенил)этил]амида 3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты,
(2-бензиламиноэтил)амида 3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты,
3-хлорбензиламида 3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты,
(2-фениламиноэтил)амида 3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты,
(4-хлорфенил)амида 3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты,
(4-метоксифенил)амида 3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты,
(4-фторфенил)амида 3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты,
[2-(4-метоксибензиламино)этил]амида 3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты,
{2-[(пиридин-2-илметил)амино]этил}амида 3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты,
(2-аминоэтил)амида 3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты,
(2-гидрокси-1-фенилэтил)амида S-[3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты],
{2-[(тиофен-3-илметил)амино]этил}амида 3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты,
[2-(2-трифторметоксибензиламино)этил]амида 3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты,
[2-(3-метоксибензиламино)этил]амида 3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты,
[2-(3-трифторметоксибензиламино)этил]амида 3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты,
[2-(4-трифторметоксибензиламино)этил]амида 3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты,
[2-(4-трифторметилбензиламино)этил]амида 3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты,
{2-[(фуран-3-илметил)амино]этил}амида 3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты,
{2-[(1Н-пиррол-2-илметил)амино]этил}амида 3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты,
[2-(3-метилбензиламино)этил]амида 3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты,
[2-(3-хлорбензиламино)этил]амида 3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты,
[2-(2-фторбензиламино)этил]амида 3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты,
{2-[(1Н-индол-5-илметил)амино]этил}амида 3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты,
[2-(2-метоксибензиламино)этил]амида 3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты,
[2-(4-фторбензиламино)этил]амида 3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты,
[2-(3-хлор-4-фторбензиламино)этил]амида 3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты,
(2-бензилоксиэтил)амида 3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты,
(2-бензоиламиноэтил)амида 3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты,
(2-бензиламиноэтил)амида 2-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-3-карбоновой кислоты,
((S)-2-гидрокси-1-фенилэтил)амида 2-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-3-карбоновой кислоты,
(2-азидо-1-фенилэтил)амида 3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты,
(2-амино-1-фенилэтил)амида 3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты,
(2-амино-2-фенилэтил)амида 3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты,
((S)-1-бензил-2-гидроксиэтил)амида 3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты,
3-аминобензиламида 3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты,
[2-(4-хлор-3-трифторметилбензиламино)этил]амида 3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты,
3-метоксибензиламида 3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты,
4-хлор-3-трифторметилбензиламида 3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты,
(2-гидрокси-2-фенилэтил)амида 3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты,
3-(4-фторбензоиламино)бензиламида 3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты,
пирролидин-3-иламида 2-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-3-карбоновой кислоты,
пиперидин-3-иламида 2-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-3-карбоновой кислоты,
[2-амино-1-(3-фторфенил)этил]амида 3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты,
[2-амино-1-(2-метоксифенил)этил]амида 3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты,
[2-амино-1-(3-фторфенил)этил]амида 2-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-3-карбоновой кислоты,
[2-амино-1-(2-метоксифенил)этил]амида 2-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-3-карбоновой кислоты,
[2-амино-1-(3,4-диметоксифенил)этил]амида 2-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-3-карбоновой кислоты,
3-аминобензиламида2-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-3-карбоновой кислоты,
бензиламида 2-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-3-карбоновой кислоты,
[2-амино-1-(3,4-диметоксифенил)этил]амида 3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты,
((S)-2-азидо-1-фенилэтил)амида 2-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-3-карбоновой кислоты,
((R)-2-циано-1-фенилэтил)амида 3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты,
(цианофенилметил)амида 2-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-3-карбоновой кислоты,
((S)-1-гидроксиметил-3-метилбутил)амида 2-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-3-карбоновой кислоты,
((S)-1-гидроксиметил-2-фенилэтил)амида 2-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-3-карбоновой кислоты,
((R)-2-карбамоил-1-фенилэтил)амида 3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты,
3-хлор-4-трифторметилбензиламида 2-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-3-карбоновой кислоты,
(2-амино-1-п-толилэтил)амида 3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты,
[2-амино-1-(3-метоксифенил)этил]амида 3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты,
[2-амино-1-(3-хлорфенил)этил]амида 3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты,
[2-амино-1-(3,4-дихлорфенил)этил]амида 3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты,
(2-амино-1-п-толилэтил)амида 2-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-3-карбоновой кислоты,
[2-амино-1-(3-метоксифенил)этил]амида 2-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-3-карбоновой кислоты,
[2-амино-1-(3,4-дихлорфенил)этил]амида 2-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-3-карбоновой кислоты,
2-хлор-N-[3-({[3-(1Н-пирроло[2,3-b]пиридин-4-иламино)-тиофен-2-карбонил]амино}метил)фенил]изоникотинамида,
[2-амино-1-(3-хлорфенил)этил]амида 2-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-3-карбоновой кислоты,
[2-(1-фенилэтиламино)этил]амида 3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты,
[2-амино-1-(4-трифторметилфенил)этил]амида 3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты,
[2-амино-1-(4-трифторметилфенил)этил]амида 2-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-3-карбоновой кислоты,
[2-(4-метилбензиламино)этил]амида 3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты,
[2-(3-хлор-4-метоксибензиламино)этил]амида 3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты,
((R)-2-циано-1-фенилэтил)амида 2-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-3-карбоновой кислоты,
((S)-2-амино-1-фенилэтил)амида 2-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-3-карбоновой кислоты,
[1-(3-фторфенил)-2-метиламиноэтил]амида 3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты,
[1-(3-хлорфенил)-2-метиламиноэтил]амида 3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты,
(2-метиламино-1-фенилэтил)амида 3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты,
((S)-2-амино-1-фенилэтил)амида 3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты,
[(S)-2-амино-1-(3-фторфенил)этил]амида 3-(1Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты,
бензиламида 3-(7Н-пирроло[2,3-d]пиримидин-4-иламино)тиофен-2-карбоновой кислоты,
[2-(3-фторфенил)этил]амида 3-(7Н-пирроло[2,3-d]пиримидин-4-иламино)тиофен-2-карбоновой кислоты,
[2-(3-хлорфенил)этил]амида 3-(7Н-пирроло[2,3-d]пиримидин-4-иламино)тиофен-2-карбоновой кислоты,
3-хлорбензиламида 3-(5-метил-7Н-пирроло[2,3-d]пиримидин-4-иламино)тиофен-2-карбоновой кислоты,
и его фармацевтически приемлемые соли или сольваты.
5. Фармацевтическая композиция, включающая в качестве активного компонента соединение по любому из пп.1-4 или его фармацевтически приемлемую соль или сольват совместно с фармацевтически приемлемым носителем.
6. Применение соединения по любому из пп.1-4 или его фармацевтически приемлемой соли или сольвата в качестве лекарственного средства.
7. Применение соединения по любому из пп.1-4 или его фармацевтически приемлемой соли или сольвата для лечения гиперпролиферативных заболеваний.
8. Применение по п.7, где заболевание выбирают из группы, состоящей из злокачественного новообразования, воспаления, панкреатита или заболевания почек, боли, доброкачественной гиперплазии кожи, рестеноза, простаты, заболеваний, связанных с васкулогенезом или ангиогенезом, опухолевого ангиогенеза, заболеваний кожи, выбранных из псориаза, экземы и склеродемы, диабета, диабетической ретинопатии, ретинопатии недоношенных, возрастной дегенерации желтого пятна, гемангиомы, глиомы, меланомы и саркомы Капоши.
Текст
Изобретение обеспечивает новые замещенные азагетероциклические соединения в соответствии с формулой (I), их получение и применение для лечения гиперпролиферативных заболеваний, таких как злокачественное новообразование.(71)(73) Заявитель и патентовладелец: МЕРК ПАТЕНТ ГМБХ (DE) Область техники, к которой относится изобретение Изобретение относится к ряду замещенных аминоазагетероциклических соединений, которые пригодны для лечения гиперпролиферативных заболеваний, таких как злокачественное новообразование, у млекопитающих. Также настоящим изобретением охватывается применение таких соединений для лечения гиперпролиферативных заболеваний у млекопитающих, в особенности у людей, и фармацевтические композиции, содержащие такие соединения. Краткое изложение известного уровня техники Протеинкиназы составляют большое семейство структурно сходных ферментов, которые отвечают за регулирование многих путей передачи сигналов в клетках (Hardie, G. и Hanks, S. (1995) The ProteinKinase Facts Book. I and II, Academic Press, Сан-Диего, Калифорния). Киназы могут подразделяться на семейства согласно субстратам, которые они фосфорилируют (например, протеин-тирозин, протеинсерин/треонин, липиды и т.д.). Были идентифицированы последовательности, которые в целом соответствуют каждому из этих семейств киназ (например, Hanks, S.K., Hunter, Т., FASEB J., 9:576-596 (1995);Knighton и др., Science, 253:407-414 (1991); Hiles и др., Cell, 70:419-429 (1992); Kunz и др., Cell, 73:585596 (1993); Garcia-Bustos и др., EMBO J., 13:2352-2361 (1994. Протеинкиназы могут быть охарактеризованы с помощью механизмов, регулирующих их активность. Эти механизмы включают, например, аутофосфорилирование, трансфосфорилирование с помощью других киназ, белок-белковые взаимодействия, белок-липидные взаимодействия и белокполинуклеотидные взаимодействия. Некоторые протеинкиназы могут регулироваться более чем одним механизмом. Киназы регулируют различные процессы в клетках, включая, но не ограничиваясь только ими, пролиферацию, апоптоз, подвижность, транскрипцию, трансляцию и другие сигнальные процессы,путем добавления фосфатных групп к белкам-мишеням. Такое фосфорилирование действует в качестве молекулярных "включающих"/"выключающих" "переключателей", которые могут модулировать или регулировать биологическую функцию белка-мишени. Фосфорилирование белков-мишеней происходит в ответ на действие различных внеклеточных сигналов (гормонов, нейромедиаторов, факторов роста и дифференциации и т.д.), событий клеточного цикла, факторов окружающей среды или пищевых стрессов и т.д. Характерной функцией протеинкиназ в путях передачи сигналов является активирование или инактивирование (непосредственно или косвенно), например, метаболического фермента, регуляторного белка, рецептора, белка цитоскелета, ионного канала или насоса, или фактора транскрипции. Неконтролируемая передача сигналов вследствие нарушения контроля фосфорилирования белков вовлечена в различные заболевания, включая, например, воспаление, злокачественное новообразование, аллергию/астму, заболевания и состояния иммунной системы, заболевания и состояния центральной нервной системы и ангиогенез. Хорошо известно, что путь передачи сигналов, в который вовлечены, в частности, ферменты фосфатидилинозитол 3-киназа (PI3K), PDK1 и PKB, опосредует во многих клетках повышенную устойчивость к апоптозу или ответные реакции выживания. Существует много данных, указывающих на то, что этот путь является важным механизмом выживания, используемым многими факторами роста для подавления апоптоза. Фермент PI3K активируется многими факторами роста и выживания, например EGF,PDGF, и путем образования полифосфатидилинозитолов инициирует активацию нижерасположенных событий передачи сигналов, включая активирование киназ PDK1 и протеинкиназы В (PKB), также известной как Akt. Это также происходит в тканях хозяина, например в клетках эндотелия сосудов, а также в новообразованиях. Протеинкиназа 70S6K, киназа 70 кДа рибосомного белка p70S6K (также известна как SK6, р 70/р 85 S6 киназа, р 70/р 85 рибосомная S6 киназа и pp70S6K), является представителем AGC субсемейства протеинкиназ. p70S6K является серин-треонин киназой, которая является компонентом фосфатидилинозитол 3 киназа (PI3K)/AKT пути. p70S6K расположена ниже PI3K, и активация происходит путем фосфорилирования в различных сайтах в ответ на действие различных митогенов, гормонов и факторов роста. Активность p70S6K также находится под контролем mTOR-содержащего комплекса(TORC1), поскольку рапамицин действует путем ингибирования p70S6K активности. p70S6K регулируется с помощью PI3K нижерасположенных мишеней AKT и PKC. AKT непосредственно фосфорилирует и инактивирует TSC2, таким образом активируя mTOR. Дополнительно, исследования с мутантными аллелями p70S6K, которая ингибируется вортманнином, но не рапамицином, свидетельствует от том, чтоPI3K путь может проявлять влияния на p70S6K независимо от регуляции активности mTOR. Ферментp70S6K модулирует синтез белка путем фосфорилирования S6 рибосомного белка. S6 фосфорилирование коррелирует с повышенной трансляцией мРНК, кодирующих компоненты трансляционного аппарата, включая рибосомные белки и факторы элонгации трансляции, повышенная экспрессия которых является важной для роста и пролиферации клеток. Эти мРНК содержат олигопиримидиновый участок на их 5' транскрипционном начале (обозначаемом 5'ТОР), который, как было показано, является важным для их регуляции на трансляционном уровне. Дополнительно к его вовлечению в трансляцию, активация p70S6K также задействована в контролирование клеточного цикла, дифференциацию нейронных клеток, регуляцию подвижности клеток и клеточную ответную реакцию, что является важным при метастазировании опухолей, иммунном ответе и восстановлении ткани. Антитела к p70S6K отменяют митогенный ответ, запускающий вхождение фиб-1 020302 робластов крыс в S фазу, указывая на то, что p70S6K функция является важной для прохождения из G1 вS фазу в клеточном цикле. Кроме того, ингибирование пролиферации клеточного цикла с G1 в S фазу клеточного цикла с помощью рапамицина было идентифицировано в виде следствия ингибирования продукции гиперфосфорилированной, активированной формы p70S6K. Роль p70S6K в пролиферации опухолевых клеток и защите клеток от апоптоза основывается на его участии в передаче сигналов рецепторов факторов роста, сверхэкспрессии и активации в опухолевых тканях. Например, при нозерн- и вестерн-анализах было установлено, что амплификация PS6K гена сопровождается соответствующими повышениями мРНК и экспрессией белка соответственно (Cancer Res.(1999) 59: 1408-11-Localization of PS6K to Chromosomal Region 17q23 and Determination of Its Amplification in Breast Cancer). Хромосома 17q23 амплифицирована вплоть до 20% первичных опухолей молочной железы, в 87% опухолей молочной железы, содержащей BRCA2 мутации и в 50% опухолей, содержащих BRCA1 мутаций, а также при других типах злокачественных новообразований, таких как поджелудочной железы,мочевого пузыря и нейробластомы (см. М. Barlund, О. Monni, J. Kononen, R. Cornelison, J. Torhorst, G.Sauter, O.-P. Kallioniemi и Kallioniemi A., Cancer Res., 2000, 60:5340-5346). Было показано, что 17q23 амфлификации при раке молочной железы вовлечены РАТ 1, RAD51C, PS6K и SIGMA1B гены (Cancer Res.(2000): 60, cc. 5371-5375). Ген p70S6K был идентифицирован в качестве мишени амплификации и сверхэкспрессии в этом участке, и наблюдается статистически достоверная связь между амплификацией и плохим прогнозом. Клиническое ингибирование p70S6K активации наблюдается у пациентов с раком почки, которых лечили с помощью CCI-779 (сложный эфир рапамицина), ингибитора вышерасположенной киназыmTOR. Описана достоверная линейная ассоциация между прогрессированием заболевания и ингибированием активности p70S6K. В ответ на энергетический стресс, опухолевый супрессор LKB1 активирует АМРК, который фосфорилирует TSC1/2 комплекс и предоставляет ему возможность инактивировать mTOR/p70S6K путь. Мутации в LKB1 вызывают синдром Пейтца-Егерса (PJS), где у пациентов PJS в 15 раз больше вероятность развития рака, чем у общей популяции. Дополнительно, 1/3 аденокарциномы легких заякоривают инактивирующие LKB1 мутации. p70S6K вовлечен в метаболические заболевания и нарушения. Было описано, что отсутствие p70S6K защищает от возрастного и индуцированного питанием ожирения, в то время как усиливает чувствительность к инсулину. Роль для p70S6K при метаболических заболеваниях и нарушениях, таких как ожирение, диабет, метаболический синдром, резистентность к инсулину, гипергликемия, гипераминоацидемия и гиперлипидемия подтверждается этими наблюдениями. Соединения, описанные в качестве пригодных для ингибирования p70S6K, раскрыты в WO 03/064397, WO 04/092154, WO 05/054237, WO 05/056014, WO 05/033086, WO 05/117909, WO 05/039506,WO 06/120573, WO 06/136821, WO 06/071819, WO 06/127587, WO 06/131835 и WO 08/140947. Описание изобретения Задачей настоящего изобретения является обеспечение новых p70S6K ингибиторов, пригодных для лечения гиперпролиферативных заболеваний, в особенности тех, которые связаны с гиперактивностьюp70S6K, так же как и заболеваний, модулируемых PI3K сигнальным путем, таких как злокачественное новообразование у млекопитающих, с улучшенными фармакологическими свойствами, как относительно их активностей, так и относительно их растворимости, метаболического клиренса и характеристик биодоступности. Таким образом, настоящее изобретение обеспечивает новые замещенные азагетероциклические соединения и их фармацевтически приемлемые соли, сольваты или пролекарства, которые являютсяp70S6K ингибиторами и пригодны для лечения вышеупомянутых заболеваний. Соединения определяются формулой (I) и включают свои фармацевтически приемлемые соли, сольваты или пролекарства, гдеX, Y, Z, каждый независимо друг от друга, означает N или CR2 при условии, что если Z означает N,Y означает CR2, и если Y означает N, Z означает CR2,Т, Q означают S, О или CR5 при условии, что если Т означает S или О, Q означает CR5, и если Q означает S или О, Т означает CR5, означает присутствие или отсутствие связи при условии, что одна из двух пунктирных линий всегда означает связь, тогда как другая всегда означает ее отсутствие,-2 020302R1, R2, R5, каждый независимо друг от друга, означает Н, A, Hal, ОН, SH, CN, NH2, NO2,R3 означает Н или А,R4 означает А, Ar или А-Ar, илиR3 и R4 вместе с атомом С, к которому они присоединены, могут образовывать Ar, или циклический А, который может быть незамещен или замещен с помощью COO(LA) или CONH(LA),Ar означает моно- или бициклический ароматический гомо- или гетероцикл, содержащий 1-4 атомов N, О и/или S и 5-10 атомов скелета, который может быть незамещен или независимо друг от друга моно-, ди- или тризамещен с помощью Hal, А, ОН, SH, ОА, NH2, NHA, NA2, NO2, CN, OCN, SCN, COOH,COOA, CONH2, CONHA, CONH(LAr), CONA2, NHCOA, NHCO(LAr), NHCONHA, NHCONH2, NHSO2A,CHO, COA, SO2NH2, SO2A и/или SO2Hal,А означает неразветвленный или разветвленный линейный или циклический алкил, который содержит 1, 2, 3, 4, 5, 6, 7 или 8 атомов С, в котором одна или две СН 2-группы могут быть заменены атомом О или S и/или NH, N(LA), SO2, CONH, NHCO или -CH=CH-группой, и в котором 1-3 Н атомов могут быть заменены Hal, и в котором одна или две СН 3-группы могут быть заменены ОН, SH, NH2, NH(LA),N(LA)2, NHCOOH, NHCONH2, N3, NO2 или CN группами,LA означает неразветвленный или разветвленный, линейный алкил, который содержит 1, 2, 3 или 4 атомов С,LAr означает моноциклический ароматический гомо- или гетероцикл, содержащий 1 или 2 атома N,О и/или S и 5-7 атомов скелета, который может быть незамещен или моно-, ди- или тризамещен с помощью Hal, LA, ОН, O(LA), NH2 или NH(LA),Hal означает F, Cl, Br или I. В целом, все остатки, которые встречаются более одного раза, могут быть одинаковыми или разными, то есть они являются независимыми друг от друга. Выше и ниже, остатки и параметры имеют значения, указанные для формулы (I), если специально не указано иначе. Таким образом, изобретение относится, в частности, к соединениям формулы (I), в которых по меньшей мене один из указанных остатков имеет одно из предпочтительных значений, указанных ниже.Hal означает фтор, хлор, бром или йод, в частности фтор или хлор. А означает, например, метил, кроме того, этил, пропил, изопропил, бутил, изобутил, втор-бутил или трет-бутил, кроме того, также пентил, 1-, 2- или 3-метилбутил, 1,1-, 1,2- или 2,2-диметилпропил, 1 этилпропил, гексил, 1-, 2-, 3- или 4-метилпентил, 1,1-, 1,2-, 1,3-, 2,2-, 2,3- или 3,3-диметилбутил, 1- или 2 этилбутил, 1-этил-1-метилпропил, 1-этил-2-метилпропил, 1,1,2- или 1,2,2-триметилпропил. А дополнительно означает алкил, как определено выше, в котором одна или две СН 2-группы могут быть заменены атомами О или S и/или NH, NA, CONH, NHCO или -СН=СН-группами и/или, кроме того,1-3 Н атома могут быть заменены F и/или Cl, такой как, например, трифторметил, пентафторэтил, 1,1 дифторметил, 1,1,1-трифторэтил, метокси, этокси, н-пропокси, изопропокси, н-бутокси, изобутокси,втор-бутокси или трет-бутокси. В других примерах А, таких как, например, N,N'-диметиламиноалкил, 2 аминоэтил, 3-аминопропил, 4-аминобутил, 5-аминопентил, 3-аминометилциклобутил или цианоалкил,одна или две СН 3-группы заменены ОН, SH, NH2, N(LA)H, N(LA)2, N3, NO2 или CN группами. А также может быть циклическим, где циклический фрагмент может быть замещен с помощью иной нециклической структуры, или введен в последнюю. Примеры для циклического А включают 2 или 3-фурил, 2,3-дигидро-2-, -3-, -4- или -5-фурил, тетрагидро-2- или -3-фурил, 1,3-диоксолан-4-ил, тетрагидро-2- или -3-тиенил, 2,3-дигидро-1-, -2-, -3-, -4- или -5-пирролил, 2,5-дигидро-1-, -2-, -3-, -4- или -5 пирролил, 1-, 2- или 3-пирролидинил, тетрагидро-1-, -2- или -4-имидазолил, 2,3-дигидро-1-, -2-, -3-, -4 или -5-пиразолил, тетрагидро-1-, -3- или -4-пиразолил, 1,4-дигидро-1-, -2-, -3- или -4-пиридил, 1,2,3,4 тетрагидро-1-, -2-, -3-, -4-, -5- или -6-пиридил, 2-, 3-, 5- или 6-пиперидин-1 или 4-ил, 2-, 3- или 4 морфолинил, тетрагидро-2-, -3- или -4-пиранил, 1,4-диоксанил, 1,3-диоксан-2-, -4- или -5-ил, гексагидро 1-, -3- или -4-пиридазинил, гексагидро-1-, -2-, -4- или -5-пиримидинил, 1-, 2- или 3-пиперазинил, 1,2,3,4 тетрагидро-1-, -2-, -3-, -4-, -5-, -6-, -7- или -8-хинолил, 1,2,3,4-тетрагидро-1-, -2-, -3-, -4-, -5-, -6-, -7- или-8-изохинолил, 2-, 3-, 5-, 6-, 7- или 8-3,4-дигидро-2 Н-бензо-1,4-оксазинил, более предпочтительно 2,3 метилендиоксифенил, 3,4-метилендиоксифенил, 2,3-этилендиоксифенил, 3,4-этилендиоксифенил, 3,4(дифторметилендиокси)фенил, 2,3-дигидробензофуран-5- или 6-ил, 2,3-(2-оксометилендиокси)фенил или также 3,4-дигидро-2 Н-1,5-бензодиоксепин-6- или -7-ил, кроме того, предпочтительно 2,3 дигидробензофуранил, индан-1-, 2-, 4- или 5-ил, 1,2,3,4-тетрагидронафталинил, тетрагидрофуран-2- или 3-ил или 2,3-дигидро-2-оксофуранил, каждый из которых незамещен или может быть моно-, ди- или тризамещен, например, карбонильным кислородом, F, Cl, Br, метилом, этилом, пропилом, -СН 2 циклогексилом, гидроксилом, метокси, этокси, амино, метиламино, диметиламино, нитро, циано, карбоксилом, метоксикарбонилом, аминокарбонилом, метиламинокарбонилом, диметиламинокарбонилом,ацетамино, уреидо, метилсульфониламино, формилом, ацетилом, аминосульфонилом и/или метилсульфонилом.LA означает неразветвленный или разветвленный, линейный алкил, который содержит 1, 2, 3 или 4 атома С, то есть метил, этил, пропил, изопропил, бутил, изобутил, втор-бутил или трет-бутил. например, фенил, нафтил или бифенил, каждый из которых моно-, ди- или тризамещен с помощью А,фтора, хлора, брома, йода, гидроксила, метокси, этокси, пропокси, бутокси, пентилокси, гексилокси,нитро, циано, формила, ацетила, пропионила, трифторметила, амино, метиламино, этиламино, диметиламино, диэтиламино, бензилокси, сульфонамидо, метилсульфонамидо, этилсульфонамидо, пропилсульфонамидо, бутилсульфонамидо, диметилсульфонамидо, фенилсульфонамидо, карбоксила, метоксикарбонила, этоксикарбонила, аминокарбонила.-5-ил или 2,1,3-бензоксадиазол-5-ил, фуран-2- или 3-ил, 2,3-дигидробензофуран-2-, 3-, 4- или 5-ил, каждый из которых незамещен или может быть моно-, ди- или тризамещен, например, с помощью F, Cl, Br,метила, этила, пропила, фенила, бензила, -СН 2-циклогексила, гидроксила, метокси, этокси, амино, метиламино, диметиламино, нитро, циано, карбоксила, метоксикарбонила, аминокарбонила, метиламинокарбонила, диметиламинокарбонила, ацетамино, уреидо, метилсульфониламино, формила, ацетила, аминосульфонила и/или метилсульфонила.LAr означает подсекцию Ar, где Ar ограничен моноциклическим ароматическим гомо- или гетероциклом, который может быть незамещен или моно-, ди- или тризамещен. Предпочтительные примерыLAr включают 4-фторфенил или 2-хлорпиридин-4-ил. Термин "замещенный" предпочтительно относится к замещению с помощью вышеуказанных заместителей, где возможно множество различных степеней замещения, если специально не указано иначе. Все физиологически приемлемые соли, производные, сольваты и стереоизомеры этих соединений,включая их смеси во всех соотношениях, также охватываются настоящим изобретением. Соединения формулы (I) могут иметь один или несколько центров хиральности. Следовательно,они могут встречаться в различных энантиомерных формах и могут быть в рацемической или оптически активной форме. Таким образом, изобретение также относится к оптически активным формам (стереоизомерам), энантиомерам, рацематам, диастереомерам и гидратам и сольватам этих соединений. Так как фармацевтическая активность рацематов или стереоизомеров соединений в соответствии с изобретением может отличаться, то может являться желательным использование энантиомеров. В этих случаях, конечный продукт или даже промежуточные продукты могут быть разделены на энантиомерные соединения химическими или физическими способами, известными специалисту в данной области техники, или даже использоваться как таковые в синтезе. В случае рацемических аминов диастереомеры выделяют из смеси реакцией с оптически активным разделяющим агентом. Примерами подходящих разделяющих агентов являются оптически активные кислоты, такие как R и S формы винной кислоты, диацетилвинной кислоты, дибензоилвинной кислоты,-4 020302(например, N-бензоилпролин или N-бензолсульфонилпролин), или различные оптически активные камфорсульфоновые кислоты. Также предпочтительным является хроматографическое разделение энантиомеров с помощью оптически активного разделяющего агента (например, динитробензоилфенилглицина,триацетата целлюлозы или других производных углеводородов или хирально модифицированных полимеров метакрилата, иммобилизированных на силикагеле). Подходящими для этой цели элюентами являются водные или спиртовые смеси растворителей, такие как, например, гексан/изопропанол/ацетонитрил, например, в отношении 82:15:3. Хорошим методом разделения рацематов, содержащих сложноэфирные группы (например, ацетиловых сложных эфиров) является применение ферментов,в частности эстераз. Предпочтительная группа соединений формулы (I) соответствует формулам (II), (III), (IV) или (V) в которых Т и Q означают S или О и остальные заместители имеют значения, указанные для формулы (I) выше. Еще более предпочтительными являются соединения подформул А, В, С, D, Е, F, G, H, J, K, L, M,N, О, Р, Q, R, S, T, U, V и W формул (I), (II), (III), (IV) и (V) и их фармацевтически приемлемые соли,сольваты или пролекарства, где в подформуле А Т, Q означают S,R5 означает Н или метил,и остальные остатки имеют значения, указанные для формулы (I) выше,в подформуле ВT, Q означают О,R5 означает Н или метил,и остальные остатки имеют значения, указанные для формулы (I) выше,в подформуле С и остальные остатки имеют значения, указанные для формулы (I) выше,в подформуле DX, Y, Z означают СН,Т, Q означают S,R5 означает Н или метил,и остальные остатки имеют значения, указанные для формулы (I) выше,в подформуле ЕY, Z означают СН,X означает N,Т, Q означают S,R5 означает Н или метил,и остальные остатки имеют значения, указанные для формулы (I) выше,в подформуле FX, Y, Z означают СН,Т, Q означают S,R5 означает Н или метил,R3 означает Н, гидроксиметил, аминометил, азидометил или цианометил,и остальные остатки имеют значения, указанные для формулы (I) выше,в подформуле GX, Y, Z означают СН,Т, Q означают S,R5 означает Н или метил,R4 означает фенил или бензил, который может быть незамещен или независимо друг от друга моно-,ди- или тризамещен метилом, метокси, CF3, OCF3, амино, Cl или F; илиR4 означает бензиламинометил, где фенильное кольцо может быть незамещено или независимо друг от друга моно-, ди- или тризамещено метилом, метокси, CF3, OCF3, амино, Cl или F; илиR4 означает аминометил,(фторбензоиламино)бензил,(бензоиламино)бензил,(хлоразабензоиламино)бензил, пирролидинил, (тиофенилметил)аминоэтил, (индолилметил)аминометил, (1 фенилэтиламино)метил, бензилоксиметил, фениламинометил, изобутил, (бис-фуран-3-илметиламино) метил, [фуранилметил)амино]метил, [пирролилметил)амино]метил, тиофенилметил, (сульфамоилфенил)метил, циклогексенилметил, бензоиламинометил, 1-гидрокси-1-фенилметил, (фуранилметилсульфанил)метил или бензолсульфониламинометил,и остальные остатки имеют значения, указанные для формулы (I) выше,в подформуле НY, Z означают СН,X означает N,R5 означает Н или метил,R4 означает фенил или бензил, который может быть незамещен или независимо друг от друга моно-,ди- или тризамещен метилом, метокси, CF3, OCF3, амино, Cl или F; илиR4 означает бензиламинометил, где фенильное кольцо может быть незамещено или независимо друг от друга моно-, ди- или тризамещено метилом, метокси, CF3, OCF3, амино, Cl или F; илиR4 означает аминометил, (фторбензоиламино)бензил, (бензоиламино)бензил, (хлоразабензоиламино)бензил, пирролидинил, (тиофенилметил)аминоэтил, (индолилметил)аминометил, (1-фенилэтиламино)метил, бензилоксиметил, фениламинометил, изобутил, (бис-фуран-3-илметиламино)метил,[фуранилметил)амино]метил, [пирролилметил)амино]метил, тиофенилметил, (сульфамоилфенил)метил,циклогексенилметил, бензоиламинометил, 1-гидрокси-1-фенилметил, (фуранилметилсульфанил)метил или бензолсульфониламинометил,и остальные остатки имеют значения, указанные для формулы (I) выше,в подформуле JY, Z означают СН,X означает N,Т, Q означают S,R5 означает Н или метил,R4 означает фенил или бензил, который может быть незамещен или независимо друг от друга моно-,ди- или тризамещен метилом, метокси, CF3, OCF3, амино, Cl или F; или R4 означает бензиламинометил,где фенильное кольцо может быть незамещено или независимо друг от друга моно-, ди- или тризамещено метилом, метокси, CF3, OCF3, амино, Cl или F; или или бензолсульфониламинометил,и остальные остатки имеют значения, указанные для формулы (I) выше,в подформуле KY, Z означают СН,X означает N,Т, Q означают О,R5 означает Н или метил,R4 означает фенил или бензил, который может быть незамещен или независимо друг от друга моно-,ди- или тризамещен метилом, метокси, CF3, OCF3, эмино, Cl или F; илиR4 означает бензиламинометил, где фенильное кольцо может быть незамещено или независимо друг от друга моно-, ди- или тризамещено метилом, метокси, CF3, OCF3, амино, Cl или F; илиR4 означает аминометил, (фторбензоиламино)бензил, (бензоиламино)бензил, (хлоразабензоиламино)бензил, пирролидинил, (тиофенилметил)аминоэтил, (индолилметил)аминометил, (1-фенилэтиламино)метил, бензилоксиметил, фениламинометил, изобутил, (бис-фуран-3-илметиламино)метил,[фуранилметил)амино]метил, [пирролилметил)амино]метил, тиофенилметил, (сульфамоилфенил)метил,циклогексенилметил, бензоиламинометил, 1-гидрокси-1-фенилметил, (фуранилметилсульфанил)метил или бензолсульфониламинометил,и остальные остатки имеют значения, указанные для формулы (I) выше,в подформуле LX, Y, Z означают СН,Т, Q означают S,R5 означает Н или метил,R4 означает фенил или бензил, который может быть незамещен или независимо друг от друга моно-,ди- или тризамещен метилом, метокси, CF3, OCF3, амино, Cl или F; илиR4 означает бензиламинометил, где фенильное кольцо может быть незамещено или независимо друг от друга моно-, ди- или тризамещено метилом, метокси, CF3, OCF3, амино, Cl или F; илиR4 означает аминометил, (фторбензоиламино)бензил, (бензоиламино)бензил, (хлоразабензоиламино)бензил, пирролидинил, (тиофенилметил)аминоэтил, (индолилметил)аминометил, (1-фенилэтиламино)метил, бензилоксиметил, фениламинометил, изобутил, (бис-фуран-3-илметиламино)метил,[фуранилметил)амино]метил, [пирролилметил)амино]метил, тиофенилметил, (сульфамоилфенил)метил,циклогексенилметил, бензоиламинометил, 1-гидрокси-1-фенилметил, (фуранилметилсульфанил)метил или бензолсульфониламинометил,и остальные остатки имеют значения, указанные для формулы (I) выше,в подформуле МX, Y, Z означают СН,Т, Q означают S,R5 означает Н,R4 означает фенил или бензил, который может быть незамещен или независимо друг от друга моно-,ди- или тризамещен метилом, метокси, CF3, OCF3, амино, Cl или F; илиR4 означает бензиламинометил, где фенильное кольцо может быть незамещено или независимо друг от друга моно-, ди- или тризамещено метилом, метокси, CF3, OCF3, амино, Cl или F; илиR4 означает аминометил, (фторбензоиламино)бензил, (бензоиламино)бензил, (хлоразабензоиламино)бензил, пирролидинил, (тиофенилметил)аминоэтил, (индолилметил)аминометил, (1-фенилэтиламино)метил, бензилоксиметил, фениламинометил, изобутил, (бис-фуран-3-илметиламино)метил,[фуранилметил)амино]метил, [пирролилметил)амино]метил, тиофенилметил, (сульфамоилфенил)метил,циклогексенилметил, бензоиламинометил, 1-гидрокси-1-фенилметил, (фуранилметилсульфанил)метил или бензолсульфониламинометил,и остальные остатки имеют значения, указанные для формулы (I) выше,в подформуле NX, Y, Z означают СН,Т, Q означают S,R5 означает Н или метил,R3 означает Н, гидроксиметил, аминометил, азидометил или цианометил,R4 означает фенил или бензил, который может быть незамещен или независимо друг от друга моно-,ди- или тризамещен метилом, метокси, CF3, OCF3, амино, Cl или F; илиR4 означает бензиламинометил, где фенильное кольцо может быть незамещено или независимо друг от друга моно-, ди- или тризамещено метилом, метокси, CF3, OCF3, амино, Cl или F; или или бензолсульфониламинометил,и остальные остатки имеют значения, указанные для формулы (I) выше,в подформуле ОY, Z означают СН,X означает N,R5 означает Н или метил,R3 означает Н, гидроксиметил, аминометил, азидометил или цианометил,R4 означает фенил или бензил, который может быть незамещен или независимо друг от друга моно-,ди- или тризамещен метилом, метокси, CF3, OCF3, амино, Cl или F; илиR4 означает бензиламинометил, где фенильное кольцо может быть незамещено или независимо друг от друга, моно-, ди- или тризамещено метилом, метокси, CF3, OCF3, амино, Cl или F; илиR4 означает аминометил, (фторбензоиламино)бензил, (бензоиламино)бензил, (хлоразабензоиламино)бензил, пирролидинил, (тиофенилметил)аминоэтил, (индолилметил)аминометил, (1-фенилэтиламино)метил, бензилоксиметил, фениламинометил, изобутил, (бис-фуран-3-илметиламино)метил,[фуранилметил)амино]метил, [пирролилметил)амино]метил, тиофенилметил, (сульфамоилфенил)метил,циклогексенилметил, бензоиламинометил, 1-гидрокси-1-фенилметил, (фуранилметилсульфанил)метил или бензолсульфониламинометил,и остальные остатки имеют значения, указанные для формулы (I) выше,в подформуле РY, Z означают СН,X означает N,Т, Q означают S,R5 означает Н или метил,R3 означает Н, гидроксиметил, аминометил, азидометил или цианометил,R4 означает фенил или бензил, который может быть незамещен или независимо друг от друга моно-,ди- или тризамещен метилом, метокси, CF3, OCF3, амино, Cl или F; илиR4 означает бензиламинометил, где фенильное кольцо может быть незамещено или независимо друг от друга моно-, ди- или тризамещено метилом, метокси, CF3, OCF3, амино, Cl или F; илиR4 означает аминометил, (фторбензоиламино)бензил, (бензоиламино)бензил, (хлоразабензоиламино)бензил, пирролидинил, (тиофенилметил)аминоэтил, (индолилметил)аминометил, (1-фенилэтиламино)метил, бензилоксиметил, фениламинометил, изобутил, (бис-фуран-3-илметиламино)метил,[фуранилметил)амино]метил, [пирролилметил)амино]метил, тиофенилметил, (сульфамоилфенил)метил,циклогексенилметил, бензоиламинометил, 1-гидрокси-1-фенилметил, (фуранилметилсульфанил)метил или бензолсульфониламинометил,и остальные остатки имеют значения, указанные для формулы (I) выше,в подформуле QY, Z означают СН,X означает N,Т, Q означают О,R5 означает Н или метил,R3 означает Н, гидроксиметил, аминометил, азидометил или цианометил,R4 означает фенил или бензил, который может быть незамещен или независимо друг от друга моно-,ди- или тризамещен метилом, метокси,CF3, OCF3, амино, Cl или F; или R4 означает бензиламинометил, где фенильное кольцо может быть незамещено или независимо друг от друга моно-, ди- или тризамещено метилом, метокси, CF3, OCF3,амино, Cl или F; илиR4 означает аминометил, (фторбензоиламино)бензил, (бензоиламино)бензил, (хлоразабензоиламино)бензил, пирролидинил, (тиофенилметил)аминоэтил, (индолилметил)аминометил, (1-фенилэтиламино)метил, бензилоксиметил, фениламинометил, изобутил, (бис-фуран-3-илметиламино)метил,[фуранилметил)амино]метил, [пирролилметил)амино]метил, тиофенилметил, (сульфамоилфенил)метил,циклогексенилметил, бензоиламинометил, 1-гидрокси-1-фенилметил, (фуранилметилсульфанил)метил или бензолсульфониламинометил,и остальные остатки имеют значения, указанные для формулы (I) выше,в подформуле RX, Y, Z означают СН,Т, Q означают S,R5 означает Н или метил,R3 означает Н, гидроксиметил, аминометил, азидометил или цианометил,R4 означает фенил или бензил, который может быть незамещен или независимо друг от друга моно-,ди- или тризамещен метилом, метокси, CF3, OCF3, амино, Cl или F; илиR4 означает бензиламинометил, где фенильное кольцо может быть незамещено или независимо друг от друга моно-, ди- или тризамещено метилом, метокси, CF3, OCF3, амино, Cl или F; илиR4 означает аминометил, (фторбензоиламино)бензил, (бензоиламино)бензил, (хлоразабензоиламино)бензил, пирролидинил, (тиофенилметил)аминоэтил, (индолилметил)аминометил, (1-фенилэтиламино)метил, бензилоксиметил, фениламинометил, изобутил, (бис-фуран-3-илметиламино)метил,[фуранилметил)амино]метил, [пирролилметил)амино]метил, тиофенилметил, (сульфамоилфенил)метил,циклогексенилметил, бензоиламинометил, 1-гидрокси-1-фенилметил, (фуранилметилсульфанил)метил или бензолсульфониламинометил,и остальные остатки имеют значения, указанные для формулы (I) выше,в подформуле SX, Y, Z означают СН,T, Q означают S,R5 означает Н,R3 означает Н, гидроксиметил, аминометил, азидометил или цианометил,R4 означает фенил или бензил, который может быть незамещен или независимо друг от друга моно-,ди- или тризамещен метилом, метокси, CF3, OCF3, амино, Cl или F; илиR4 означает бензиламинометил, где фенильное кольцо может быть незамещено или независимо друг от друга моно-, ди- или тризамещено метилом, метокси, CF3, OCF3, амино, Cl или F; илиR4 означает аминометил, (фторбензоиламино)бензил, (бензоиламино)бензил, (хлоразабензоиламино)бензил, пирролидинил, (тиофенилметил)аминоэтил, (индолилметил)аминометил, (1-фенилэтиламино)метил, бензилоксиметил, фениламинометил, изобутил, (бис-фуран-3-илметиламино)метил,[фуранилметил)амино]метил, [пирролилметил)амино]метил, тиофенилметил, (сульфамоилфенил)метил,циклогексенилметил, бензоиламинометил, 1-гидрокси-1-фенилметил, (фуранилметилсульфанил)метил или бензолсульфониламинометил,и остальные остатки имеют значения, указанные для формулы (I) выше,в подформуле ТX, Y, Z означают СН,Т, Q означают S,R5 означает Н,R3 означает гидроксиметил, аминометил, азидометил или цианометил,R4 означает фенил или бензил, который может быть незамещен или независимо друг от друга моно-,ди- или тризамещен метилом, метокси, CF3, OCF3, амино, Cl или F,и остальные остатки имеют значения, указанные для формулы (I) выше,в подформуле UX, Y, Z означают СН,Т, Q означают S,R5 означает Н,R3 означает Н,R4 означает бензиламинометил, где фенильное кольцо может быть незамещено или независимо друг от друга моно-, ди- или тризамещено метилом, метокси, CF3, OCF3, амино, Cl или F; илиR4 означает аминометил, (фторбензоиламино)бензил, (бензоиламино)бензил, (хлоразабензоиламино)бензил, пирролидинил, (тиофенилметил)аминоэтил, (индолилметил)аминометил, (1-фенилэтиламино)метил, бензилоксиметил, фениламинометил, изобутил, (бис-фуран-3-илметиламино)метил,[фуранилметил)амино]метил, [пирролилметил)амино]метил, тиофенилметил, (сульфамоилфенил)метил,циклогексенилметил, бензоиламинометил, 1-гидрокси-1-фенилметил, (фуранилметилсульфанил)метил или бензолсульфониламинометил,и остальные остатки имеют значения, указанные для формулы (I) выше,в подформуле VX, Y, Z означают СН,Т, Q означают S,R5 означает Н,R3 и R4 вместе с атомом С, к которому они присоединены, образуют пиперидинил, фенил, пирролидинил, тетрагидрофуранил, каждый из которых может быть незамещен или независимо друг от друга моно-, ди- или тризамещен метилом, метокси, CF3, OCF3, амино, Cl или F,и остальные остатки имеют значения, указанные для формулы (I) выше,в подформуле WX, Z означают СН,Y означает CR2,R2 означает метил,Т, Q означают S,R5 означает Н,R3 означает Н,и остальные остатки имеют значения, указанные для формулы (I) выше,Особенно предпочтительные соединения в соответствии с формулой (I) и/или формулой (II) вклю-9 020302 чают соединения, показанные в разделе "Примеры" ниже, так же как и соединения, перечисленные в таблице ниже, или фармацевтически приемлемые соли, сольваты или пролекарства каждого из таких соединений. Для иллюстрации ингибирования p70S6K использовали следующую классификацию: Соединения в соответствии с настоящим изобретением могут находиться в форме пролекарственного соединения. "Пролекарственное соединение" обозначает производное, которое превращается в биологически активное соединение в соответствии с настоящим изобретением в физиологических условиях в живом организме, например, путем окисления, восстановления, гидролиза или других процессов, каж- 11020302 дый из которых осуществляется ферментативно, или без задействования ферментативной среды. Примерами пролекарств являются соединения, где аминогруппа в соединении согласно настоящему изобретению ацилирована, алкилирована или фосфорилирована, например, эйкозаноиламино, аланиламино, пивалоилоксиметиламино, или где гидроксильная группа ацилирована, алкилирована, фосфорилирована или превращена в борат, например, ацетилокси, пальмитоилокси, пивалоилокси, сукцинилокси, фумарилокси, аланилокси, или где карбоксильная группа эстерифицирована или амидирована, или где сульфгидрильная группа образует дисульфидный мостик с молекулой носителя, например пептидом, которая доставляет лекарственное средство к мишени и/или в цитозоль клетки. Эти соединения могут быть получены из соединений согласно настоящему изобретению в соответствии с хорошо известными методами. Другими примерами пролекарств являются соединения, где карбоксилат в соединении согласно настоящему изобретению, например, превращен в алкил-, арил-, холин-, амино, ацилоксиметиловый сложный эфир, линоленоил-сложный эфир. Метаболиты соединений согласно настоящему изобретению также охватываются объемом настоящего изобретения. Если встречается таутомерия, например кето-енольная таутомерия, соединений согласно настоящему изобретению или их пролекарств, то индивидуальные формы, например кето- или енольная форма,заявляются отдельно и совместно в виде смесей в любом соотношении. Аналогичное применяется для стереоизомеров, например энантиомеров, цис/транс-изомеров, конформеров и т.п. Если это является желательным, то изомеры могут быть разделены с помощью методов, хорошо известных в данной области техники, например, путем жидкостной хроматографии. Аналогичное применяется для энантиомеров, например, путем применения хиральных неподвижных фаз. Дополнительно энантиомеры могут быть выделены путем их превращения в диастереомеры, то есть сочетания с энантиомерно чистым вспомогательным соединением, последующего разделения полученных диастереомеров и отщепления вспомогательного остатка. Альтернативно, любой энантиомер соединения согласно настоящему изобретению может быть получен при стереоселективном синтезе, используя оптически чистые исходные вещества. Соединения в соответствии с настоящим изобретением могут находиться в форме фармацевтически приемлемой соли или сольвата. Термин "фармацевтически приемлемые соли" относится к солям, полученным из фармацевтически приемлемых нетоксичных оснований или кислот, включая неорганические основания или кислоты и органические основания или кислоты. В тех случаях, когда соединения в соответствии с настоящим изобретением содержат одну или несколько кислотных или основных групп, то изобретение также охватывает их соответствующие фармацевтически или токсикологически приемлемые соли, в частности их фармацевтически используемые соли. Таким образом, соединения в соответствии с настоящим изобретением, которые содержат кислотные группы, могут быть представлены в солевой форме и могут использоваться в соответствии с изобретением, например, в виде солей щелочных металлов, солей щелочно-земельных металлов или в виде солей аммония. Более предпочтительные примеры таких солей включают соли натрия, соли калия, соли кальция, соли магния или соли с аммиаком или органическими аминами, такими как, например, этиламин, этаноламин, триэтаноламин или аминокислотами. Соединения согласно настоящему изобретению, которые содержат одну или несколько основных групп, то есть групп, которые могут быть протонированы, могут быть представлены в солевой форме и могут использоваться в соответствии с изобретением в форме их солей присоединения с неорганическими или органическими кислотами. Примерами подходящих кислот являются соляная кислота,бромисто-водородная кислота, фосфорная кислота, серная кислота, азотная кислота, метансульфоновая кислота, п-толуолсульфоновая кислота, нафталиндисульфоновые кислоты, щавелевая кислота, уксусная кислота, винная кислота, молочная кислота, салициловая кислота, бензойная кислота, муравьиная кислота, пропионовая кислота, пивалиновая кислота, диэтилуксусная кислота, малоновая кислота, янтарная кислота, пимелиновая кислота, фумаровая кислота, малеиновая кислота, яблочная кислота, сульфаминовая кислота, фенилпропионовая кислота, глюконовая кислота, аскорбиновая кислота, изоникотиновая кислота, лимонная кислота, адипиновая кислота и другие кислоты, известные специалисту в данной области техники. Если соединения в соответствии с настоящим изобретением одновременно содержат кислотные и основные группы в молекуле, то изобретение также включает дополнительно к указанным солевым формам внутренние соли или бетаины (цвиттер-ионы). Соответствующие соли соединений могут быть получены с помощью обычных методов, которые известны специалисту в данной области техники, например, путем введения их в контакт с органической или неорганической кислотой или основанием в растворителе или диспергаторе или путем обмена анионами или обмена катионами с другими солями. Настоящее изобретение также включает все соли соединений в соответствии с настоящим изобретением, которые вследствие их низкой физиологической совместимости не могут быть непосредственно пригодны для применения в лекарственных средствах, но которые могут применяться, например, в качестве промежуточных продуктов для химических реакций или для получения фармацевтически приемлемых солей. Кроме того, настоящее изобретение относится к фармацевтическим композициям, содержащим соединение согласно настоящему изобретению, или его пролекарственное соединение, или его фармацевтически приемлемую соль, или сольват в качестве активного компонента совместно с фармацевтически"Фармацевтическая композиция" обозначает один или несколько активных компонентов и один или несколько инертных компонентов, которые составляют носитель, а также любой другой продукт, которая образуется, непосредственно или опосредованно, при комбинации, комплексообразовании или агрегации любых двух или более компонентов, или при диссоциации одного или более компонентов, или при других типах реакций или взаимодействий одного или более компонентов. Следовательно, фармацевтические композиции согласно настоящему изобретению охватывают любую композицию, полученную при смешивании соединения согласно настоящему изобретению и фармацевтически приемлемого носителя. Фармацевтическая композиция согласно настоящему изобретению дополнительно может содержать одно или несколько других соединений в качестве активных компонентов, такие как одно или несколько дополнительных соединений согласно настоящему изобретению, или пролекарственное соединение, или другие p70S6K ингибиторы. Фармацевтические композиции включают композиции, пригодные для перорального, ректального,местного, парентерального (включая подкожное, внутримышечное и внутривенное), глазного (офтальмического), легочного (назальной или буккальной ингаляции), или назального введения, хотя наиболее подходящий путь для любого данного случая будет зависеть от природы и тяжести состояний, подвергаемых лечению, и природы активного компонента. Они подходяще могут быть представлены в единичной дозированной форме и могут быть приготовлены с помощью любого из способов, хорошо известных в области фармацевтики. В одном варианте осуществления указанные соединения и фармацевтическая композиция предназначены для лечения злокачественного новообразования, такого как рак головного мозга, легких, ободочной кишки, эпидермоидного, плоских клеток, мочевого пузыря, желудка, поджелудочной железы,молочной железы, головы, шеи, почки, печени, яичников, предстательной железы, ободочной и прямой кишки, матки, прямой кишки, пищевода, яичек, женских половых органов, щитовидной железы, меланомы, гемобластозов, таких как острый миелогенный лейкоз, множественная миелома, хронический миелогенный лейкоз, лейкоз миелоидных клеток, глиома, саркома Капоши, или любого другого типа солидных или жидких опухолей. Предпочтительно злокачественное новообразование, подвергаемое лечению, выбирают из рака молочной железы, ободочной и прямой кишки, легких, предстательной железы или поджелудочной железы или глиобластомы. Изобретение также относится к применению соединений в соответствии с изобретением для приготовления лекарственного средства для лечения гиперпролиферативных заболеваний, связанных с гиперактивностью p70S6K, a также заболеваний, модулируемых p70S6K путем у млекопитающих, или нарушений, опосредуемых аберрантной пролиферацией, таких как злокачественное новообразование и воспаление. Изобретение также относится к соединению или фармацевтической композиции для лечения заболевания, связанного с васкулогенеозом или ангиогенезом у млекопитающего, которая включает терапевтически эффективное количество соединения согласно настоящему изобретению, или его фармацевтически приемлемой соли, пролекарства или гидрата, и фармацевтически приемлемый носитель. В одном варианте осуществления указанное соединение или фармацевтическая композиция предназначена для лечения заболевания, выбранного из группы, включающей опухолевый ангиогенез, хроническое воспалительное заболевание, такое как ревматоидный артрит, воспалительное заболевание кишечника, атеросклероз, заболевания кожи, такие как псориаз, экзема и склеродема, диабет, диабетическую ретинопатию, ретинопатию недоношенных и возрастную дегенерацию желтого пятна. Настоящее изобретение также относится к соединению или фармацевтической композиции для ингибирования атипичного клеточного роста у млекопитающего, которая включает количество соединения согласно настоящему изобретению, или его фармацевтически приемлемой соли, или сольвата, или пролекарства в комбинации с количеством другого противоракового терапевтического средства, где количества соединения, соли, сольвата или пролекарства и химиотерапевтического средства совместно эффективны для ингибирования атипичного клеточного роста. В настоящее время в данной области известны многие противораковые терапевтические средства. В одном варианте осуществления противораковое терапевтическое средство представляет собой химиотерапевтическое средство, выбранное из группы,включающей ингибиторы митоза, алкилирующие средства, антиметаболиты, интеркалирующие антибиотики, ингибиторы факторов роста, ингибиторы клеточного цикла, фермента, ингибиторы типоизомеразы, модификаторы биологического отклика, антигормональные средства, ингибиторы ангиогенеза и антиандрогены. В другом варианте осуществления противораковое терапевтическое средство представляет собой антитело, выбранное из группы, включающей бевацизумаб, CD40-специфические антитела,chTNT-1/B, денозумаб, занолимумаб, IGF1R-специфические антитела, линтузумаб, эдреколомаб, WXG250, ритуксимаб, тицилимумаб, трастузумаб и цетуксимаб. В еще другом варианте осуществления противораковое терапевтическое средство представляет собой ингибитор другой протеинкиназы, такой как Настоящее изобретение также относится к способу ингибирования атипичного клеточного роста у млекопитающего или лечения гиперпролиферативного нарушения, который включает введение млекопитающему количества соединения согласно настоящему изобретению или его фармацевтически приемлемой соли, или сольвата, или пролекарства в комбинации с лучевой терапией, где количества соединения, соли, сольвата или пролекарства, представленные в комбинации с лучевой терапией, эффективны для ингибирования атипичного клеточного роста или лечения гиперпролиферативного нарушения у млекопитающего. Техники введения лучевой терапии известны из уровня техники, и эти техники можно использовать в комбинированной терапии, раскрытой в настоящей заявке. Введение соединения согласно изобретению в этой комбинированной терапии можно определить, как описано в настоящей заявке. Полагают, что соединения в соответствии с настоящим изобретением могут придавать атипичным клеткам большую чувствительность к лечению с применением лучевой терапии для уничтожения и/или ингибирования роста таких клеток. Следовательно, настоящее изобретение также относится к способу сенсибилизации атипичных клеток у млекопитающего к лечению с применением лучевой терапии, который включает введение млекопитающему количества соединения согласно настоящему изобретению или его фармацевтически приемлемой соли, или сольвата, или пролекарства, где количество является эффективным для сенсибилизации атипичных клеток к лечению с помощью лучевой терапии. Количество соединения, соли или сольвата в этом методе можно определить в соответствии с методами для установления эффективных количеств таких соединений, описанных в настоящей заявке. Изобретение также относится к способу ингибирования атипичного клеточного роста у млекопитающего, который включает применение количества соединения согласно настоящему изобретению или его фармацевтически приемлемой соли, или сольвата, его пролекарства или его производного, меченного радиоактивным изотопом, и количества одного или нескольких веществ, выбранных из антиангиогенных средств, ингибиторов передачи сигналов и антипролиферативных средств. При практическом использовании соединения в соответствии с настоящим изобретением можно комбинировать в качестве активного компонента в тесной смеси с фармацевтическим носителем в соответствии с общепринятыми техниками приготовления лекарственных средств. Носитель может иметь различные формы в зависимости от формы препарата, желательного для введения, например перорального или парентерального (включая внутривенное). Для приготовления композиций для пероральных дозированных форм можно использовать любые обычные фармацевтические среды, такие как, например,вода, гликоли, масла, спирты, ароматизаторы, консерванты, красители и другие. В случае пероральных жидких препаратов можно использовать любые обычные фармацевтические среды, такие как, например,суспензии, эликсиры и растворы; или носители, такие как крахмалы, сахара, микрокристаллическая целлюлоза, разбавители, гранулирующие средства, замасливатели, связующие, дезинтеграторы и другие. В случае твердых пероральных препаратов композиция может находиться в таких формах, как, например,порошки, твердые и мягкие капсулы и таблетки, при этом твердые пероральные препараты являются предпочтительными относительно жидких препаратов. В связи с простотой их введения таблетки и капсулы является наиболее благоприятными пероральными дозируемыми единичными формами, в этих случаях обязательно используются твердые фармацевтические носители. Если это является желательным, то таблетки могут быть покрыты оболочкой с помощью стандартных водных или неводных техник. Такие композиции и препараты должны содержать по меньшей мере 0,1% активного соединения. Процент активного соединения в этих композициях, очевидно, может изменяться и подходяще может составлять от приблизительно 2 до приблизительно 60% от массы единицы. Количество активного соединения в таких терапевтически пригодных композициях будет таким, чтобы получить эффективную дозу. Активные соединения также можно вводить интраназально, например, в виде жидких капель или спрея. Таблетки, пилюли, капсулы и другие формы также могут содержать связующее, такое как трагакантовую камедь, гуммиарабик, кукурузный крахмал или желатин; наполнители, такие как дикальций фосфат; дезинтегрирующее средство, такое как кукурузный крахмал, картофельный крахмал, альгиновую кислоту; замасливатель, такой как стеарат магния; и подсластитель, такой как сахароза, лактоза или сахарин. Если единичная дозированная форма представляет собой капсулу, то она может содержать дополнительно к веществам вышеописанного типа жидкий носитель, такой как жирное масло. Различные другие вещества могут присутствовать в виде покрытий или для модификации физической формы дозированной единицы. Например, таблетки могут быть покрыты с помощью шеллака, сахара или обоих веществ. Сироп или эликсир может содержать дополнительно к активному компоненту сахарозу в качестве подсластителя, метил и пропилпарабены в качестве консервантов, краситель и ароматизатор, такой как вишневый или апельсиновый ароматизатор. Соединения согласно настоящему изобретению также могут вводиться парентерально. Растворы или суспензии этих активных соединений могут быть приготовлены в воде, подходяще смешаны с поверхностно-активным веществом, таким как гидроксипропилцеллюлоза. Дисперсии также могут быть приготовлены в глицерине, жидких полиэтиленгликолях и их смесях в маслах. При обычных условиях хранения и применения, эти препараты содержат консервант для предотвращения роста микроорганизмов. Фармацевтические формы, подходящие для инъекций, включают стерильные водные растворы или дисперсии и стерильные порошки для экстемпоральных препаратов стерильных инъекционных растворов или дисперсий. Во всех случаях форма должна быть стерильной и должна быть жидкой до такой степени, чтобы ее легко можно было вводить с помощью шприца. Она должна быть стабильной в условиях изготовления и хранения и должна быть защищена от загрязняющего действия микроорганизмов, таких как бактерии и грибы. Носитель может представлять собой растворитель или дисперсионную среду, содержащую, например, воду, этанол, полиол (например, глицерин, пропиленгликоль и жидкий полиэтиленгликоль), их подходящие смеси и растительные масла. Любой подходящий путь введения может применяться для обеспечения млекопитающего, в особенности человека, эффективной дозой соединения согласно настоящему изобретению. Например, можно применять пероральный, ректальный, местный, парентеральный, глазной, легочный, назальный и другие пути. Дозированные формы включают таблетки, лепешки, дисперсии, суспензии, растворы, капсулы,кремы, мази, аэрозоли и другие. Предпочтительно соединения согласно настоящему изобретению вводят перорально. Эффективная дозировка применяемого активного компонента может изменяться в зависимости от конкретного применяемого соединения, способа введения, состояния, подвергаемого лечению, и тяжести состояния, подвергаемого лечению. Такие дозировки легко могут быть установлены специалистом в данной области техники. При лечении или предотвращении злокачественного новообразования, воспаления или других пролиферативных заболеваний, для которых показаны соединения согласно настоящему изобретению,обычно удовлетворительные результаты получают, если соединения в соответствии с настоящим изобретением вводят в суточной дозе от приблизительно 0,01 до приблизительно 100 мг на килограмм веса тела животного, предпочтительно представленных в виде единичной суточной дозы. Для наиболее крупных млекопитающих общая суточная доза составляет от приблизительно 0,1 до приблизительно 1000 мг,предпочтительно от приблизительно 0,2 до приблизительно 50 мг. Для взрослого человека весом 70 кг общая суточная доза обычно будет составлять от приблизительно 0,2 до приблизительно 200 мг. Эта схема дозирования может регулироваться для обеспечения оптимального терапевтического ответа. Изобретение также относится к комплекту (набору), состоящему из отдельных пакетов:a) эффективного количества соединения в соответствии с изобретением или его фармацевтически приемлемой соли, сольвата или пролекарства иb) эффективного количества дополнительного активного компонента лекарственного средства. Комплект включает подходящие контейнеры, такие как коробки, отдельные бутылки, пакеты или ампулы. Комплект может содержать, например, отдельные ампулы, каждая из которых содержит эффективное количество соединения в соответствии с изобретением и/или его фармацевтически пригодных производных, сольватов и стереоизомеров, включая их смеси во всех соотношениях, и эффективное количество дополнительного активного компонента лекарственного средства в растворенной или лиофилизированной форме. Экспериментальный раздел Некоторые сокращения, которые могут использоваться в настоящей заявке, имеют следующие значения: Сокращения Соединения в соответствии с настоящим изобретением могут быть получены в соответствии с методиками из следующих схем и примеров, используя подходящие вещества, и дополнительно иллюстрируются следующими специфическими примерами. Кроме того, при использовании методик, описанных в настоящей заявке, в сочетании с типичными знаниями для квалифицированного специалиста в данной области техники легко могут быть получены дополнительные соединения согласно настоящему изобретению, заявленные в настоящей заявке. Тем не менее, соединения, иллюстрируемые в примерах, не должны рассматриваться как составляющие только класс, охватываемый изобретением. Примеры дополнительно иллюстрируют детали получения соединений согласно настоящему изобретению. Для квалифицированных специалистов в данной области техники будет очевидным, что для получения этих соединений можно использовать известные модификации условий и процессов следующих препаративных методик. Растворимые соединения обычно выделяют в виде их фармацевтически приемлемых солей, таких как соли, описанные выше. Свободные основания - амины, соответствующие выделенным солям, могут быть получены путем нейтрализации подходящим основанием, таким как водный гидрокарбонат натрия,карбонат натрия, гидроксид натрия и гидроксид калия, и экстрагирования выделенного в свободном состоянии свободного основания - амина в органический растворитель с последующим упариванием. Свободное основание - амин, выделенный таким образом, в дальнейшем может быть превращено в другую фармацевтически приемлемую соль путем растворения в органическом растворителе с последующим добавлением подходящей кислоты и последующего упаривания, осаждения или кристаллизации. Изобретение иллюстрируется, но не ограничивается, путем ссылки на специфические варианты осуществления, описанные в последующих схемах и примерах. Если специально не указано иначе на схемах, то переменные имеют такие же значения, что и описано выше. Если специально не указано иначе, все исходные вещества получали от коммерческих поставщиков и использовали без дополнительной очистки. Если специально не указано иначе, все температуры выражали в С и все реакции осуществляли при комнатной температуре. Соединения очищали либо путем хроматографии на силикагеле, либо препаративной ЖХВД. Настоящее изобретение также относится к способам приготовления соединений формул (I), (II),(III) и подформул 1-39, а также соединений, описанных в таблице, в соответствии с нижеописанными схемами и примерами обработки. Настоящее изобретение также относится к способам получения соединений формул (I), (II), подформул А-U, так же как и соединений, описанных в таблице, в соответствии с нижеописанными схемами и демонстрационными примерами. Общие методы синтеза Все температуры приведены в градусах Цельсия. Реагенты приобретали в коммерческих источниках или получали, следуя методикам, приведенным в литературе. Общая схема синтеза тиофенкарбоновой кислоты - схема 1 После защиты азаиндольной NH группы с помощью "tips" промежуточный хлорид вводят в реакцию с тиофенаминокислотой с получением тиофенкарбоновой кислоты. Экспериментальная часть для схемы 1. 4-Хлор-1-триизопропилсилил-1 Н-пирроло[2,3-b]пиридин. К 1 л колбе добавляли 4-хлоразаиндол (23 г, 147 ммоль) и ТГФ (400 мл), охлаждали до 0 С и порциями в течение 10 мин добавляли NaH (60%, 18 г, 442 ммоль). Температуре в течение 30 мин позволяли повыситься до комнатной, и затем смесь повторно охлаждали до 0 С. После добавления триизопропилсилилхлорида (31 мл, 147 ммоль) реакционную смесь нагревали до 50 С в течение 18 ч. Реакционную смесь охлаждали до комнатной температуры и гасили путем медленного добавления воды. Водный слой экстрагировали этилацетатом (3), сушили над Na2SO4 и концентрировали в вакууме. Вещество очищали с помощью ISCO Companion (гептан - смесь 50% этилацетат/гептан) с обеспечением 30 г (66%) целевого вещества. ЖХМС (ESI) 309 (М+Н). 1 Н ЯМР (400 МГц, ДМСО-d6)м.д. 8.17 (1 Н, d, J=5.27 Гц), 7.56 (1 Н, d, J=3.51 Гц), 7.20 (1 Н, d,J=5.08 Гц), 6.65 (1 Н, d, J=3.51 Гц), 1.78-1.90 (3 Н, m), 1.00-1.08 (18 Н, m).(2,0 г, 143 ммоль), XPhos (3,1 г, 6,5 ммоль), метил 3-аминотиофен-2-карбоксилата (12,3 г, 78 ммоль) в трет-бутаноле (108 мл) дегазировали азотом в течение 30 мин. К реакционной смеси добавляли Pd2(dba)3(3,0 г, 3,3 ммоль) и получающийся раствор вакуумировали, снова наполняли азотом 3 и затем нагревали до 100 С в течение 2 дней. Реакционную смесь фильтровали через набивку целита, промывали этилацетатом, концентрировали в вакууме и переносили в виде сырого продукта на стадию гидролиза. Вышеупомянутое сырое вещество растворяли в смеси ТГФ/МеОН/Н 2 О (210/140/70 мл). К раствору добавляли гидроксид лития (14 г, 325 ммоль) и нагревали до 85 С в течение ночи. Реакционную смесь охлаждали до комнатной температуры и фильтровали через набивку целита. Набивку целита промывали водой и мета- 17020302 нолом. Фильтрат разбавляли водой (250 мл) и концентрировали до удаления органических растворителей. Раствор фильтровали через набивку целита и основной водный раствор подкисляли до рН 5 с обеспечением белого осадка, который собирали, промывали водой и гептанами и сушили в вакуумной печи в течение нескольких дней с обеспечением 3-(1 Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты (17.3 г, 99% для двух стадий). ЖХМС (ESI) 260 (М+Н). 1 Н ЯМР (400 МГц, ДМСО-d6)м.д. 11.59 (1 Н, br. s.), 9.65 (1 Н, br. s.), 8.05 (1 Н, d, J=5.47 Гц), 7.86 2-(1 Н-Пирроло[2,3-b]пиридин-4-иламино)тиофен-3-карбоновая кислота. Это соединение получали способом, аналогичным способу получения 3-(1 Н-пирроло[2,3b]пиридин-4-иламино)тиофен-2-карбоновой кислоты, используя метил 2-аминотиофен-3-карбоксилат взамен метил 3-аминотиофен-2-карбоксилата). ЖХМС (ESI) 260 (М+Н). 1 Н ЯМР (400 МГц, ДМСО-d6)м.д. 11.88 (1H, br. s.), 10.77 (1H, s), 8.16 (1H, d, J=5.66 Гц), 7.41 (1H,dd, J=3.22, 1.85 Гц), 7.23 (1H, d, J=5.86 Гц), 7.01 (1H, d, J=5.86 Гц), 6.94 (1H, d, J=5.66 Гц), 6.47 (1H, d,J=2.73 Гц). 5-Метил-3-(1 Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновая кислота. Это соединение получали способом, аналогичным способу получения 3-(1 Н-пирроло[2,3b]пиридин-4-иламино)тиофен-2-карбоновой кислоты, используя метил 3-амино-5-метилтиофен-2 карбоксилат взамен метил 3-аминотиофен-2-карбоксилата. ЖХМС (ESI) 274 (М+Н). 1 Н ЯМР (400 МГц, ДМСО-d6)м.д. 11.60 (1 Н, br. s), 9.66 (1 Н, s), 8.06 (1 Н, d, J=4.49 Гц), 7.30-7.38(1 Н, m), 6.95 (1 Н, d, J=5.47 Гц), 6.42 (1 Н, d, J=1.76 Гц), 2.50 (3 Н, s). Общая схема синтеза амида - схема 2 Для синтеза амида может быть использован один из следующих методов. 1. Синтез хлорангидрида кислоты с последующим добавлением амина. Хлорангидрид кислоты синтезируют в качестве промежуточного соединения, которое гасят амином с образованием целевого амида. 2. HATU - активирование карбоновой кислоты с последующим добавлением амина.HATU представляет собой агент сочетания для образования амидной связи, который позволяет прямой синтез амида из исходного веществакарбоновой кислоты, через промежуточное соединение HATU-активированную карбоновую кислоту. 3. AlMe3-активирование карбоновой кислоты с последующим добавлением амина.AlMe3 представляет собой реагент, используемый для прямого синтеза амида из карбоновой кислоты через промежуточное соединение Al-Me-карбоновая кислота. Так как AlMe3 является жестким реагентом, способы 1 и 2 являются предпочтительными. Общая схема восстановительного аминирования - схема 3 При необходимости другие замещенные алкильные группы могут быть введены в амин с помощью восстановительного аминирования посредством реакции амина с альдегидом (или кетоном) и затем восстановления получающегося имина до амина. Аналитические методики ЖХ/МС выполняли, используя следующих два метода. Метод А (быстрая ЖХ). Колонка Shimadzu Shim-pack XR-ODS, 3,030 мм, 2,2 мкм, использовали при температуре 50 С и при скорости потока 1,5 мл/мин, инжекция 2 мкл, подвижная фаза: (А) вода с 0,1% муравьиной кислоты и 1% ацетонитрила, подвижная фаза (В) метанол с 0,1% муравьиной кислоты; время удержания приведено в минутах. Подробности метода: (I) работали с использованием двойного насоса G1312B с УФ/видим. детектором на диодной матрице G1315C и масс-спектрометром Agilent 6130,электрораспылением в режиме положительных и отрицательных ионов с УФ-детектированием при 220 и 254 нм с градиентом 15-95% (В) за 2,2 мин линейный градиент, (II) удерживали в течение 0,8 мин при 95% (В), (III) уменьшали от 95 до 15% (В) за 0,1 мин линейный градиент, (IV) удерживали в течение 0,29 мин при 15% (В). Метод В (полярная "Stop-Gap"). Колонка Agilent Zorbax Bonus RP, 2,150 мм, 3,5 мкм, использовали при температуре 50 С и при скорости потока 0,8 мл/мин, инжекция 2 мкл, подвижная фаза: (А) вода с 0,1% муравьиной кислоты и 1% ацетонитрила, подвижная фаза (В) метанол с 0,1% муравьиной кислоты; время удержания приведено в минутах. Подробности метода: (I) работали с использованием двойного насоса G1312B с УФ/видим. детектором на диодной матрице G1315C и масс-спектрометром Agilent 6130,электрораспылением в режиме положительных и отрицательных ионов с УФ-детектированием при 220 и 254 нм с градиентом 5-95% (В) за 2,5 мин линейный градиент, (II) удерживали в течение 0,5 мин при 95%(В), (III) уменьшали от 95 до 5% (В) за 0,1 мин линейный градиент, (IV) удерживали в течение 0,29 мин при 5% (В). Препаративную ЖХВД выполняли с использованием системы, управляемой программным обеспечением Chromeleon и состоящей из двух насосов Varian PrepStar Model 218, УФ/видим. детектора VarianProStar Model 320, детектора SEDEX 55 ELSD и манипулятора жидкости Gilson 215. Типичные ЖХВД подвижные фазы состояли из воды и метанола. Стандартная колонка представляла собой VarianDynamax, диаметр 21,4 мм, Microsorb Guard-8 C18. Стандартные процедуры очистки выполняли, используя систему Teledyne Isco CombiFlash Companion, используя силикагелевые колонки RediSep Rf. Типичные подвижные фазы, состоящие из одного или двух растворителей, и использование изократического, линейного и/или ступенчатого градиентных режимов описаны в рамках экспериментального раздела. Пики обнаруживали с использованием детектора поглощения на фотодиодной матрице (200-360 нм). ЯМР-спектры снимали на спектрометре Varian UnityInova 400 МГц ЯМР, оборудованном автоматизированным трехдиапазонным широкополосным датчиком (Automation Triple Broadband, АТВ). АТВ датчик был одновременно настроен на 1 Н, 19F и 13 С. В случае типичных 1 Н ЯМР-спектров угол импульса составлял 45, суммировали 8 сканирований и спектральная ширина составляла 16 м.д. (от -2 м.д. до 14 м.д.). В сумме собирали 32768 комплексных точек в течение времени обнаружения 5,1 с, а задержку начала повторного цикла устанавливали равной 1 с. Спектры собирали при температуре 25 С. 1 Н ЯМРспектры типично обрабатывали с 0,2 Гц уширением линий и заполнением нулями до 131072 точек перед преобразованием Фурье. Примеры Примеры, представленные ниже, предназначены для иллюстрации отдельных вариантов осуществления изобретения и не предназначены для какого-либо ограничения объема описания или пунктов формулы изобретения. Химический синтез. 1. Амид 3-(1 Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты 4-Хлор-1 Н-пирроло(2,3-b)пиридин (150 мг, 0,90 ммоль) и 3-аминотиофен-2-карбоксамид (167 мг,1,2 ммоль) растворяли в растворе этанол:вода (4:2 мл) и заправляли 1 каплей HCl (конц.), затем смесь нагревали до 100 С в течение 48 ч. Реакционную смесь выливали в смесь NaHCO3/EtOAc, затем органический слой собирали, а водный слой экстрагировали с помощью EtOAc (2). Органические слои объединяли, сушили над сульфатом натрия, фильтровали и концентрировали в вакууме. Остаток очищали с помощью ISCO Companion (силикагель, (10% метанол, метиленхлорид, 0,5% гидроксид аммония) с обеспечением амида 3-(1 Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты (75 мг,32%) ЖХМС (ESI) 259 (М+Н). 1 Н ЯМР (400 МГц, ДМСО-d6)м.д 12.45 (1 Н, br. s), 10.71 (1 Н, s), 8.09 (1 Н, d, J=7.03 Гц), 7.88 (1 Н, d,J=5.27 Гц), 7.61 (1H, br. s), 7.43 (1H, dd, J=3.42, 2.44 Гц), 7.36 (1H, d, J=5.27 Гц), 6.77 (1H, d, J=6.83 Гц),6.66 (1H, d, J=1.56 Гц). 2. Сложный метиловый эфир 4-(1 Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-3-карбоновой кислоты 4-Хлор-1 Н-пирроло(2,3,b)пиридин (250 мг, 1,6 ммоль) и метил-4-аминотиофен-3-карбоксилат (632 мг, 3,3 ммоль) растворяли в растворе метанол:вода (4:2 мл) и заправляли 1 каплей HCl (конц.), затем смесь нагревали до 100 С в течение 16 ч. Реакционную смесь выливали в смесь NaHCO3/EtOAc, затем органический слой собирали, а водный слой экстрагировали с помощью EtOAc (2). Органические слои объединяли, сушили над сульфатом натрия, фильтровали и концентрировали в вакууме. Остаток очищали с помощью ISCO Companion (силикагель (10% метанол, метиленхлорид, 0,5% гидроксид аммония) с обеспечением сложного метилового эфира 4-(1 Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-3 карбоновой кислоты (32 мг, 7%). ЖХМС (ESI) 274 (М+Н). 1 Н ЯМР (400 МГц, ДМСО-d6)м.д. 11.52 (1 Н, br. s.), 9.20 (1 Н, s), 8.45 (1 Н, d, J=3.32 Гц), 8.04 (1 Н, d,J=5.47 Гц), 7.39 (1 Н, d, J=3.32 Гц), 7.30 (1 Н, dd, J=3.32, 2.34 Гц), 6.95 (1 Н, d, J=5.47 Гц), 6.45 (1 Н, dd,J=3.51, 1.76 Гц), 3.87 (3 Н, s). 3. (Тетрагидрофуран-2-илметил)амид 3-(1 Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты Это соединение получали способом, аналогичным способу получения трет-бутилового сложного эфира 3-[3-(1 Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбонил]аминопирролидин-1-карбоновой кислоты, используя 1-(тетрагидрофуран-2-ил)метанамин взамен 1-ВОС-3-аминопирролидина. ЖХМС (ESI) 343 (М+Н). 1 Н ЯМР (400 МГц, ацетонитрил-d3)м.д. 10.54 (1 Н, s), 8.01 (1 Н, d, J=7.03 Гц), 7.67 (1 Н, d, J=5.27 Гц), 7.42 (1 Н, d, J=5.27 Гц), 7.39 (1 Н, dd, J=3.42, 1.85 Гц), 6.97 (1 Н, d, J=6.83 Гц), 6.66 (1 Н, dd, J=3.42, 1.66 Гц), 3.95 (1 Н, qd, J=6.80, 4.59 Гц), 3.72 (1 Н, dt, J=8.15, 6.56 Гц), 3.57-3.66 (1 Н, m), 3.29-3.48 (2 Н, m), 1.871.97 (3 Н, m), 1.77-1.86 (2 Н, m), 1.48-1.60 (1 Н, m). Это соединение получали способом, аналогичным способу получения трет-бутилового сложного эфира 3-[3-(1 Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбонил]аминопирролидин-1-карбоновой кислоты, используя пирролидин взамен 1-ВОС-3-аминопирролидина. ЖХМС (ESI) 313 (М+Н). 1 Н ЯМР (400 МГц, ДМСО-d6)м.д. 12.40 (1 Н, br. s.), 10.62 (1 Н, s), 8.07 (1 Н, d, J=6.83 Гц), 7.88 (1 Н,d, J=5.27 Гц), 7.39 (1 Н, d, J=3.51 Гц), 7.29 (1 Н, d, J=5.47 Гц), 6.72 (1 Н, d, J=3.32 Гц), 6.70 (1 Н, d, J=6.64 Гц), 3.42 (1 Н, br. s.), 2.47 (4 Н, dt, J=3.66, 1.78 Гц), 1.75 (4H, br. s.). К раствору 3-(1 Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты (100 мг, 0,39 ммоль), диизопропилэтиламина (0,1 мл, 0,54 ммоль), 1-ВОС-3-аминопирролидина (143 мг, 0,77 ммоль) в диметилформамиде (2 мл) добавляли HATU (176 мг, 0,463 ммоль). Раствор перемешивали при комнатной температуре в течение 18 ч, затем разбавляли этилацетатом и промывали водным 1% хлоридом лития. Органический слой сушили, концентрировали в вакууме и очищали с помощью ISCO Companion с обеспечением трет-бутилового сложного эфира 3-[3-(1 Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2 карбонил]аминопирролидин-1-карбоновой кислоты (161 мг, 95%). ЖХМС (ESI) 428 (М+Н). 1 Н ЯМР (400 МГц, ДМСО-d6)м.д. 11.55 (1 Н, br. s), 10.24 (1 Н, s), 8.20 (1 Н, d, J=6.83 Гц), 8.02 (1 Н,d, J=5.47 Гц), 7.81 (1 Н, d, J=5.47 Гц), 7.47 (1 Н, d, J=5.47 Гц), 7.31 (1 Н, dd, J=3.32, 2.54 Гц), 6.80 (1 Н, d,- 20020302 К раствору трет-бутилового сложного эфира 3-[3-(1 Н-пирроло[2,3-b]пиридин-4-иламино)тиофен 2-карбонил]аминопирролидин-1-карбоновой кислоты (50 мг, 0,12 ммоль) в метиленхлориде (1,0 мл) добавляли трифторметилуксусную кислоту (1,0 мл). Спустя 1 ч раствор концентрировали в вакууме, растирали с диэтиловым эфиром с обеспечением пирролидин-3-иламида 3-(1 Н-пирроло[2,3-b]пиридин-4 иламино)тиофен-2-карбоновой кислоты (48 мг, 99%). ЖХМС (ESI) 328 (М+Н). 1 Н ЯМР (400 МГц, ДМСО-d6)м.д. 11.54 (1 Н, br. s.), 10.25 (1 Н, s), 8.08 (1 Н, d, J=6.83 Гц), 8.02 (1 Н,d, J=5.47 Гц), 7.81 (1 Н, d, J=5.27 Гц), 7.48 (1 Н, d, J=5.47 Гц), 7.32 (1 Н, d, J=3.51 Гц), 6.81 (1 Н, d, J=5.47 Гц), 6.44 (1 Н, d, J=3.51 Гц), 4.32-4.51 (1 Н, m), 3.14 (1 Н, dd, J=11.62, 6.74 Гц), 3.02-3.11 (1H, m), 2.89-2.98 Это соединение получали способом, аналогичным способу получения трет-бутилового сложного эфира 3-[3-(1 Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбонил]аминопирролидин-1-карбоновой кислоты, используя 2-(аминометил)пиридин взамен 1-ВОС-3-аминопирролидина. ЖХМС (ESI) 350 Это соединение получали способом, аналогичным способу получения трет-бутилового сложного эфира 3-[3-(1 Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбонил]аминопирролидин-1-карбоновой кислоты, используя 3-(аминометил)пиридин взамен 1-ВОС-3-аминопирролидина. 1 Н ЯМР (400 МГц, ДМСО-d6)м.д. 11.54 (1 Н, br. s), 10.28 (1 Н, s), 8.73 (1 Н, t, J=6.05 Гц), 8 55 (1 Н, d,J=1.76 Гц), 8.45 (1H, dd, J=4.78, 1.66 Гц), 8.02 (1H, d, J=5.47 Гц), 7.81 (1H, d, J=5.47 Гц), 7.67-7.74 (1H, m),7.50 (1 Н, d, J=5.47 Гц), 7.28-7.38 (2H, m), 6.84 (1 Н, d, J=5.47 Гц), 6.42 (1H, dd, J=3.42, 1.85 Гц), 4.48 (2H, d,J=6.05 Гц). Это соединение получали способом, аналогичным способу получения трет-бутилового сложного эфира 3-[3-(1 Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбонил]аминопирролидин-1-карбоновой кислоты, используя трет-бутил 3-аминопиперидин-1-карбоксилат взамен 1-ВОС-3-аминопирролидина. К раствору N-Boc (664 мг, 1,5 ммоль) в метиленхлориде (2,0 мл) добавляли трифторуксусную кислоту (2,0 мл). Реакционную смесь перемешивали при комнатной температуре в течение 4 ч, затем концентрировали досуха в вакууме. Остаток повторно растворяли в этилацетате, затем промывали 1 н.NaOH. Органический слой сушили сульфатом натрия, фильтровали, затем концентрировали. Остаток очищали с помощью колонки для флэш-хроматографии на силикагеле ISCO (9:1:1 метиленхлорид:метанол:гидроксид аммония) с обеспечением 500 мг (98%). ЖХМС (ESI) 342 (М+Н). 1 Н ЯМР (400 МГц, ДМСО-d6)м.д. 11.53 (1 Н, s), 10.21 (1 Н, s), 8.01 (1 Н, d, J=5.27 Гц), 7.88 (1 Н, d,J=7.81 Гц), 7.80 (1 Н, d, J=5.47 Гц), 7.46 (1 Н, d, J=5.27 Гц), 7.31 (1 Н, d, J=3.51 Гц), 6.78 (1 Н, d, J=5.27 Гц),6.43 (1 Н, d, J=3.51 Гц), 3.88-4.00 (1 Н, m, J=3.71 Гц), 2.99-3.07 (1 Н, m, J=3.90 Гц), 2.85-2.93 (1 Н, m, J=12.10 Гц), 2.46-2.57 (2 Н, m), 1.76-1.85 (1 Н, m), 1.60-1.69 (1 Н, m), 1.39-1.56 (2 Н, m). Это соединение получали способом, аналогичным способу получения трет-бутилового сложного эфира 3-[3-(1 Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбонил]аминопирролидин-1-карбоновой кислоты, используя 1-амино-2-пропанол взамен 1-ВОС-3-аминопирролидина. ЖХМС (ESI) 317 Это соединение получали способом, аналогичным способу получения трет-бутилового сложного эфира 3-[3-(1 Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбонил]аминопирролидин-1-карбоновой кислоты, используя 1-амино-2-пропанол взамен 1-ВОС-3-аминопирролидина. ЖХМС (ESI) 317 Это соединение получали способом, аналогичным способу получения трет-бутилового сложного эфира 3-[3-(1 Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбонил]аминопирролидин-1-карбоновой кислоты, используя 2-феноксиэтиламин взамен 1-ВОС-3-аминопирролидина. ЖХМС (ESI) 379 Это соединение получали способом, аналогичным способу получения трет-бутилового сложного эфира 3-[3-(1 Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбонил]аминопирролидин-1-карбоновой кислоты, используя 2-(1-циклогексенил)этиламин взамен 1-ВОС-3-аминопирролидина. ЖХМС (ESI) 367 (М+Н). 1 Н ЯМР (400 МГц, ДМСО-d6)м.д. 11.51 (1 Н, br. s), 10.20 (1 Н, s), 7.94-8.06 (2 Н, m), 7.76 (1 Н, d,J=5.37 Гц), 7.44 (1 Н, d, J=5.37 Гц), 7.30 (1 Н, dd, J=3.37, 2.49 Гц), 6.77 (1 Н, d, J=5.37 Гц), 6.43 (1 Н, dd,J=3.47, 1.90 Гц), 5.37 (1 Н, br. s), 3.25-3.37 (2 Н, m), 2.11 (2 Н, t, J=7.96 Гц), 1.91 (2 Н, t, J=5.81 Гц), 1.84 (2 Н,br. s), 1.49-1.60 (2 Н, m), 1.36-1.47 (2 Н, m). Это соединение получали способом, аналогичным способу получения трет-бутилового сложного эфира 3-[3-(1 Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбонил]аминопирролидин-1-карбоновой кислоты, используя 4-(2-аминоэтил)бензолсульфонамид взамен 1-ВОС-3-аминопирролидина. ЖХМС Это соединение получали способом, аналогичным способу получения трет-бутилового сложного эфира 3-[3-(1 Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбонил]аминопирролидин-1-карбоновой кислоты, используя гистамин взамен 1-ВОС-3-аминопирролидина. ЖХМС (ESI) 353 (М+Н). 1 Н ЯМР (400 МГц, ДМСО-d6)м.д. 11.69-11.97 (1 Н, m), 11.52 (1 Н, br. s), 10.35 (1 Н, s), 8.24 (1 Н, br. Это соединение получали способом, аналогичным способу получения трет-бутилового сложного эфира 3-[3-(1 Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбонил]аминопирролидин-1-карбоновой кислоты, используя 4-(2-аминоэтил)морфолин взамен 1-ВОС-3-аминопирролидина. ЖХМС (ESI) 372 Это соединение получали способом, аналогичным способу получения трет-бутилового сложного эфира 3-[3-(1 Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбонил]аминопирролидин-1-карбоновой кислоты, используя 4-(2-аминоэтил)пиридин взамен 1-ВОС-3-аминопирролидина.ЖХМС (ESI) 364 Это соединение получали способом, аналогичным способу получения трет-бутилового сложного эфира 3-[3-(1 Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбонил]аминопирролидин-1-карбоновой кислоты, используя 2-(3-трифторметилфенил)этиламин взамен 1-ВОС-3-аминопирролидина. ЖХМС Это соединение получали способом, аналогичным способу получения трет-бутилового сложного эфира 3-[3-(1 Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбонил]аминопирролидин-1-карбоновой кислоты, используя 2-(2-аминоэтил)пиридин взамен 1-ВОС-3-аминопирролидина. ЖХМС (ESI) 364 Это соединение получали способом, аналогичным способу получения трет-бутилового сложного эфира 3-[3-(1 Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбонил]аминопирролидин-1-карбоновой кислоты, используя 2-(3-хлорфенил)этиламин взамен 1-ВОС-3-аминопирролидина. ЖХМС (ESI) 396 Это соединение получали способом, аналогичным способу получения трет-бутилового сложного эфира 3-[3-(1 Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбонил]аминопирролидин-1-карбоновой кислоты, используя тиофен-2-этиламин взамен 1-ВОС-3-аминопирролидина. ЖХМС (ESI) 369 Это соединение получали способом, аналогичным способу получения трет-бутилового сложного эфира 3-[3-(1 Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбонил]аминопирролидин-1-карбоновой кислоты, используя 2-(3-фторфенил)этиламин взамен 1-ВОС-3-аминопирролидина. ЖХМС (ESI) 381 Это соединение получали способом, аналогичным способу получения трет-бутилового сложного эфира 3-[3-(1 Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбонил]аминопирролидин-1-карбоновой кислоты, используя 2-(4-фторфенил)этиламин взамен 1-ВОС-3-аминопирролидина. ЖХМС (ESI) 381 Это соединениеполучали способом, аналогичным способу получения трет-бутилового сложного эфира 3-[3-(1 Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбонил]аминопирролидин-1-карбоновой кислоты, используя 2-(фурфурилтио)этиламин взамен 1-ВОС-3-аминопирролидина. ЖХМС (ESI) 399 Это соединение получали способом, аналогичным способу получения трет-бутилового сложного эфира 3-[3-(1 Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбонил]аминопирролидин-1-карбоновой кислоты, используя 2-(2-метилфенил)этиламин взамен 1-ВОС-3-аминопирролидина. ЖХМС (ESI) 377 (М+Н). 1 Н ЯМР (400 МГц, ДМСО-d6)м.д. 11.97 (1 Н, br. s), 10.45 (1 Н, s), 8.28 (1 Н, t, J=5.66 Гц), 8.06 (1 Н, d,J=6.25 Гц), 7.84 (1 Н, d, J=5.47 Гц), 7.36-7.43 (2 Н, m), 7.01-7.15 (4 Н, m), 6.78 (1 Н, d, J=6.25 Гц), 6.59 (1 Н, d,J=3.51 Гц), 3.39 (2 Н, td, J=7.52, 6.05 Гц), 2.77 (2 Н, d, J=7.81 Гц), 2.29 (3H, s). Это соединение получали способом, аналогичным способу получения трет-бутилового сложного эфира 3-[3-(1 Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбонил]аминопирролидин-1-карбоновой кислоты, используя 2-(3-метоксифенил)этиламин взамен 1-ВОС-3-аминопирролидина. ЖХМС (ESI) 393 (М+Н). 1 Н ЯМР (400 МГц, ДМСО-d6)м.д. 11.68 (1 Н, br. s), 10.34 (1 Н, s), 8.19 (1 Н, t, J=5.61 Гц), 8.03 (1 Н, d,J=5.66 Гц), 7.79 (1 Н, d, J=5.37 Гц), 7.45 (1 Н, d, J=5.37 Гц), 7.34 (1 Н, d, J=3.32 Гц), 7.16 (1 Н, t, J=8.10 Гц),6.72-6.82 (4 Н, m), 6.48 (1 Н, d, J=3.32 Гц), 3.71 (3H, s), 3.46 (2 Н, dt, J=8.00, 6.25 Гц), 2.79 (2 Н, t, J=7.27 Гц). Это соединение получали способом, аналогичным способу получения трет-бутилового сложного эфира 3-[3-(1 Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбонил]аминопирролидин-1-карбоновой кислоты, используя 2-(4-бромфенил)этиламин взамен 1-ВОС-3-аминопирролидина. ЖХМС (ESI) 442 Это соединение получали способом, аналогичным способу получения трет-бутилового сложного эфира 3-[3-(1 Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбонил]аминопирролидин-1-карбоновой кислоты, используя 2-(4-метоксифенил)этиламин взамен 1-ВОС-3-аминопирролидина. ЖХМС (ESI) 393 (М+Н). 1 Н ЯМР (400 МГц, ДМСО-d6)м.д. 11.52 (1 Н, br. s), 10.24 (1 Н, s), 8.14 (0H, t), 8.02 (1 Н, d, J=5.42 Гц), 7.77 (1H, d, J=5.42 Гц), 7.46 (1H, d, J=5.37 Гц), 7.31 (1H, dd, J=3.34, 2.56 Гц), 7.13 (2H, d, J=8.69 Гц),- 26020302 Это соединение получали способом, аналогичным способу получения трет-бутилового сложного эфира 3-[3-(1 Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбонил]аминопирролидин-1-карбоновой кислоты, используя N-бензилэтилендиамин взамен 1-ВОС-3-аминопирролидина. ЖХМС (ESI) 392 Это соединение получали способом, аналогичным способу получения трет-бутилового сложного эфира 3-[3-(1 Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбонил]аминопирролидин-1-карбоновой кислоты, используя 3-хлорбензиламин взамен 1-ВОС-3-аминопирролидина. ЖХМС (ESI) 383 (М+Н). 1 Н ЯМР (400 МГц, ДМСО-d6)м.д. 11.53 (1 Н, br. s), 10.27 (1 Н, s), 8.72 (1 Н, t, J=5.95 Гц), 8.03 (1 Н, d,J=5.47 Гц), 7.82 (1 Н, d, J=5.47 Гц), 7.50 (1 Н, d, J=5.47 Гц), 7.21-7.41 (5 Н, m), 6.84 (1 Н, d, J=5.47 Гц), 6.41 Это соединение получали способом, аналогичным способу получения трет-бутилового сложного эфира 3-[3-(1 Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбонил]аминопирролидин-1-карбоновой кислоты, используя 4-амино-1-бутанол взамен 1-ВОС-3-аминопирролидина. ЖХМС (ESI) 330 Это соединение получали способом, аналогичным способу получения трет-бутилового сложного эфира 3-[3-(1 Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбонил]аминопирролидин-1-карбоновой кислоты, используя N-(4-аминобутил)ацетамид взамен 1-ВОС-3-аминопирролидина. ЖХМС (ESI) 372 (М+Н). 1 Н ЯМР (400 МГц, ДМСО-d6)м.д. 11.52 (1 Н, br. s), 10.36 (1 Н, s), 8.11 (1 Н, t, J=5.56 Гц), 8.02 (1 Н, d,J=5.47 Гц), 7.77 (2 Н, d, J=5.47 Гц), 7.48 (1 Н, d, J=5.47 Гц), 7.31 (1 Н, dd, J=3.51, 2.54 Гц), 6.82 (1 Н, d, J=5.47IC50 (p70S6K) . 33. Сложный этиловый эфир 3-[3-(1 Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбонил] аминопропионовой кислоты Это соединение получали способом, аналогичным способу получения трет-бутилового сложного эфира 3-[3-(1 Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбонил]аминопирролидин-1-карбоновой кислоты, используя сложный этиловый эфир 3-аминопропионовой кислоты взамен 1-ВОС-3 аминопирролидина. ЖХМС (ESI) 359 (М+Н). 1 Н ЯМР (400 МГц, ДМСО-d6)м.д. 11.54 (1 Н, br. s), 10.27 (1 Н, s), 8.17 (1 Н, t, J=5.37 Гц), 8.02 (1 Н, d,J=5.47 Гц), 7.78 (1 Н, d, J=5.47 Гц), 7.47 (1 Н, d, J=5.47 Гц), 7.32 (1 Н, d, J=3.32 Гц), 6.81 (1 Н, d, J=5.47 Гц),6.44 (1 Н, dd, J=3.42, 1.66 Гц), 4.03 (2 Н, q, J=7.03 Гц), 3.43-3.53 (2 Н, m), 2.55 (2 Н, t, J=7.03 Гц), 1.15 (3H, t,J=7.03 Гц). Это соединение получали способом, аналогичным способу получения трет-бутилового сложного эфира 3-[3-(1 Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбонил]аминопирролидин-1-карбоновой кислоты, используя N-фенилэтилендиамин взамен 1-ВОС-3-аминопирролидина. ЖХМС (ESI) 378 Это соединение получали способом, аналогичным способу получения трет-бутилового сложного эфира 3-[3-(1 Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбонил]аминопирролидин-1-карбоновой кислоты, используя 4-хлоранилин взамен 1-ВОС-3-аминопирролидина. ЖХМС (ESI) 369 (М+Н). 1 Н ЯМР (400 МГц, ДМСО-d6)м.д. 11.56 (1 Н, br. s), 10.12 (1 Н, s), 9.99 (1 Н, s), 8.04 (1 Н, d, J=5.47 Гц), 7.91 (1 Н, d, J=0.10 Гц), 7.71 (2 Н, d, J=8.93 Гц), 7.52 (1 Н, d, J=5.37 Гц), 7.37-7.43 (2 Н, m), 7.33 (1 Н, dd,J=3.25, 2.61 Гц), 6.85 (1 Н, d, J=5.42 Гц), 6.46 (1 Н, dd, J=3.49, 1.88 Гц). Это соединение получали способом, аналогичным способу получения трет-бутилового сложного эфира 3-[3-(1 Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбонил]аминопирролидин-1-карбоновой кислоты, используя 4-метоксианилин взамен 1-ВОС-3-аминопирролидина. ЖХМС (ESI) 365 (М+Н). 1 Н ЯМР (400 МГц, ДМСО-d6)м.д. 11.51 (1 Н, br. s), 10.14 (1 Н, s), 9.73 (1 Н, s), 8.00 (1 Н, d, J=5.42 Гц), 7.85 (1 Н, d, J=5.42 Гц), 7.44-7.55 (3H, m), 7.29 (1 Н, dd, J=3.20, 2.71 Гц), 6.89 (2 Н, d, J=8.98 Гц), 6.80 Это соединение получали способом, аналогичным способу получения трет-бутилового сложного эфира 3-[3-(1 Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбонил]аминопирролидин-1-карбоновой кислоты, используя 4-фторанилин взамен 1-ВОС-3-аминопирролидина. ЖХМС (ESI) 353 (М+Н). 1 Н ЯМР (400 МГц, ДМСО-d6)м.д. 11.53 (1 Н, br. s), 10.11 (1 Н, s), 9.90 (1 Н, s), 8.01 (1 Н, d, J=5.42 Гц), 7.88 (1 Н, d, J=5.42 Гц), 7.64 (2 Н, dd, J=9.13, 5.08 Гц), 7.49 (1 Н, d, J=5.42 Гц), 7.30 (1 Н, dd, J=3.25, 2.66 Гц), 7.16 (2 Н, t, J=8.93 Гц), 6.82 (1 Н, d, J=5.47 Гц), 6.43 (1 Н, dd, J=3.49, 1.93 Гц). Это соединение получали способом, аналогичным способу получения трет-бутилового сложного эфира 3-[3-(1 Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбонил]аминопирролидин-1-карбоновой кислоты, используя 3-метоксанилин взамен 1-ВОС-3-аминопирролидина. ЖХМС (ESI) 365 (М+Н). 1 Н ЯМР (400 МГц, ДМСО-d6)м.д. 11.55 (1 Н, br. s), 10.06 (1 Н, s), 9.83 (1 Н, s), 8.03 (1 Н, d, J=5.42 Гц), 7.90 (1 Н, d, J=5.42 Гц), 7.49 (1H, d, J=5.42 Гц), 7.32 (1 Н, dd, J=3.51, 2.44 Гц), 7.20-7.30 (3H, m), 6.81 К раствору (2-аминоэтил)амида 3-(1 Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты (45 мг, 0,13 ммоль), 4-метоксибензальдегида (16 мкл, 0,13 ммоль), и ледяной уксусной кислоты (8 мкл, 0,13 ммоль) в метаноле (1 мл) порциями добавляли триацетоксиборогидрид натрия (84 мг, 0,4 ммоль). Раствор перемешивали при 50 С в течение 18 ч. Раствор абсорбировали в целит и продукт очищали с помощью ISCO Companion (силикагель, 0-10% метанол, метиленхлорид, 1% гидроксид аммония) с обеспечением [2-(4-метоксибензиламино)этил]амида 3-(1 Н-пирроло[2,3-b]пиридин-4-иламино)тиофен 2-карбоновой кислоты (56 мг, 75%). ЖХМС (ESI) 422 (М+Н). 1 Н ЯМР (400 МГц, ДМСО-d6)м.д. 10.26 (1 Н, br. s), 7.98-8.07 (2 Н, m), 7.77 (1 Н, d, J=5.47 Гц), 7.46 Это соединение получали способом, аналогичным способу получения [2-(4-метоксибензиламино) этил]амида 3-(1 Н-пирроло[2,3-b]пиридин-4-иламино)тиофен-2-карбоновой кислоты, используя 2 пиридинкарбоксальдегид взамен 4-метоксибензальдегида. ЖХМС (ESI) 393 (М+Н). 1 Н ЯМР (400 МГц, ДМСО-d6)м.д. 11.51 (1 Н, br. s), 10.27 (1 Н, s), 8.46 (1 Н, ddd, J=4.81, 1.66, 0.76 Гц), 8.07 (1 Н, t, J=5.61 Гц), 8.01 (1 Н, d, J=5.37 Гц), 7.77 (1 Н, d, J=5.47 Гц), 7.68 (1 Н, td, J=7.68, 1.73 Гц),7.47 (1 Н, d, J=5.42 Гц), 7.39 (1 Н, d, J=7.71 Гц), 7.29 (1 Н, d, J=2.64 Гц), 7.20 (1 Н, ddd, J=7.47, 4.91, 0.90 Гц),6.80 (1 Н, d, J=5.47 Гц), 6.42 (1 Н, dd, J=3.49, 1.98 Гц), 3.78 (2 Н, s), 3.36 (2 Н, q, J=6.12 Гц), 2.68 (2 Н, t,J=6.83 Гц).
МПК / Метки
МПК: C07D 471/04, C07D 487/04, A61P 35/00, A61K 31/437, A61K 31/519
Метки: азагетероциклические, новые, соединения
Код ссылки
<a href="https://eas.patents.su/30-20302-novye-azageterociklicheskie-soedineniya.html" rel="bookmark" title="База патентов Евразийского Союза">Новые азагетероциклические соединения</a>
Предыдущий патент: Ингибиторы поли(адф-рибозо)полимеразы (parp)
Следующий патент: Применение 4-[этил(диметил)аммонио]бутаноата для лечения сердечно-сосудистых заболеваний
Случайный патент: Быстрый способ анализа связности коллектора с использованием быстрого метода прогонки