Соединения в качестве модуляторов пути hedgehog
Номер патента: 18302
Опубликовано: 30.07.2013
Авторы: У Сюй, Цзян Цзицин, Гао Вэнци, Пан Шифенг, Хань Дун, Ван Юнцинь, Чэн Дай
Формула / Реферат
1. Соединение формулы I
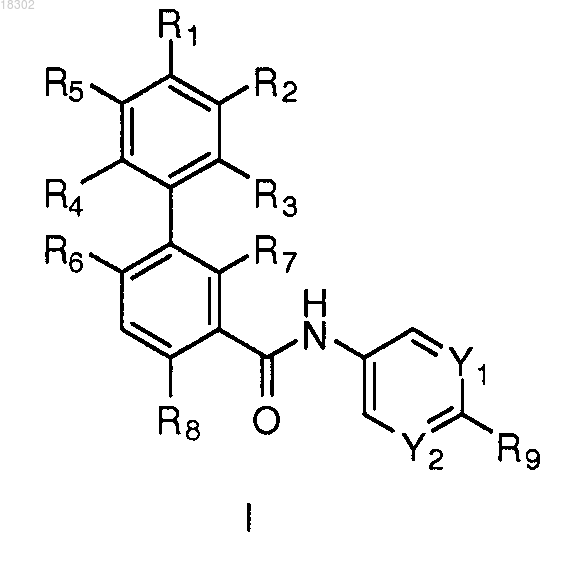
где Y1 и Y2 независимо выбраны из N и СН;
R1 выбран из циано, С1-6алкила, галогензамещенного С1-6алкила, С1-6алкокси, галогензамещенного С1-6алкокси, диметиламино, С1-6алкилсульфанила и пиперазинила, необязательно замещенного не более чем двумя C1-6алкильными радикалами;
R2 и R5 независимо выбраны из водорода, циано, галогена, С1-6алкила, галогензамещенного С1-6алкила и
С1-6алкокси;
R3 и R4 независимо выбраны из водорода, галогена, циано, C1-6алкила, С1-6алкокси и галогензамещенного
С1-6алкокси;
R6 и R7 независимо выбраны из водорода, хлора, фтора, брома, С1-6алкила, галогензамещенного С1-6алкила и С1-6алкокси при условии, что R6 и R7 одновременно не означают водород;
R8 означает водород;
R9 выбран из -S(O)2R11, -OR11, -C(O)R11, -NR12aR12b и -R11;
R11 выбран из сульфономорфолино, морфолино, циклогексила, фенила, азепан-1-ила, 2-оксопиперазин-1-ила, 1,4-оксазепан-4-ила, пиперидин-1-ила, тетрагидро-2Н-пиран-4-ила, пиперидин-3-ила, пиперазинила, пирролидинила и 1,4-диазепан-1-ила;
R12a и R12b независимо выбраны из изобутила, гидроксиэтила;
указанные сульфономорфолино, морфолино, циклогексил, фенил, азепан-1-ил, 2-оксопиперазин-1-ил, 1,4-оксазепан-4-ил, пиперидин-1-ил, тетрагидро-2Н-пиран-4-ил, пиперидин-3-ил, пиперазинил, пирролидинил или 1,4-диазепан-1-ил в R9 могут быть необязательно замещены 1-3 радикалами, независимо выбранными из метила, этила, метокси, бензила, тиенилметила и пиридинилметила;
указанный бензильный заместитель R9 необязательно замещен 1-3 радикалами, независимо выбранными из метокси, этокси, метилпиперазинила, метила, трифторметокси, хлора, фтора и трифторметила;
или его фармацевтически приемлемые соли и стереоизомеры.
2. Соединение по п.1, в котором R6 и R7 независимо выбраны из водорода, метила, хлора, фтора, брома, трифторметила и метокси при условии, что R6 и R7 одновременно не означают водород.
3. Соединение по п.1 или 2, в котором
R1 выбран из циано, метила, этила, трет-бутила, пропила, изобутила, изопропила, изопропилокси, бутокси, метокси, диметиламино, этокси, метилсульфанила, трифторметила, трифторметокси и пиперазинила, необязательно замещенного не более чем двумя метильными радикалами;
R2 и R5 независимо выбраны из водорода, хлора, фтора, циано, метила, трифторметила, изопропилокси, метокси, этокси;
R3 и R4 независимо выбраны из водорода, хлора, метила, метокси и циано.
4. Соединение по п.3, выбранное из
N-(6-((2R,6S)-2,6-диметилморфолино)пиридин-3-ил)-2-метил-4'-(трифторметокси)бифенил-3-карбоксамида;
[4-(морфолин-4-сульфонил)фенил]амида 4'-циано-6-метилбифенил-3-карбоновой кислоты;
[6-(2,6-диметилморфолин-4-ил)пиридин-3-ил]амида 4'-циано-6-метилбифенил-3-карбоновой кислоты;
(6-азепан-1-илпиридин-3-ил)амида 4'-циано-2-метилбифенил-3-карбоновой кислоты;
(6-азепан-1-илпиридин-3-ил)амида 4'-метокси-2-метилбифенил-3-карбоновой кислоты;
(4-циклогексилфенил)амида 4'-метокси-2-метилбифенил-3-карбоновой кислоты;
[6-(2-метилморфолин-4-ил)пиридин-3-ил]амида 4'-метокси-2-метилбифенил-3-карбоновой кислоты;
(4-циклогексилфенил)амида 4'-диметиламино-2-метилбифенил-3-карбоновой кислоты;
(4-морфолин-4-илфенил)амида 4'-диметиламино-2-метилбифенил-3-карбоновой кислоты;
(6-[1,4]оксазепан-4-илпиридин-3-ил)амида 6-хлор-4'-диметиламинобифенил-3-карбоновой кислоты;
(6-морфолин-4-илпиридин-3-ил)амида 6-хлор-4'-диметиламинобифенил-3-карбоновой кислоты;
(6-азепан-1-илпиридин-3-ил)амида 6-хлор-4'-диметиламинобифенил-3-карбоновой кислоты;
[6-(2-метилморфолин-4-ил)пиридин-3-ил]амида 6-хлор-4'-метоксибифенил-3-карбоновой кислоты;
(6-[1,4]оксазепан-4-илпиридин-3-ил)амида 6-хлор-4'-метоксибифенил-3-карбоновой кислоты;
(6-азепан-1-илпиридин-3-ил)амида 6-хлор-4'-метоксибифенил-3-карбоновой кислоты;
(6-морфолин-4-илпиридин-3-ил)амида 6-хлор-4'-метоксибифенил-3-карбоновой кислоты;
(6-морфолин-4-илпиридин-3-ил)амида 4'-метокси-6-метилбифенил-3-карбоновой кислоты;
(6-[1,4]оксазепан-4-илпиридин-3-ил)амида 4'-метокси-6-метилбифенил-3-карбоновой кислоты;
[6-(2-метилморфолин-4-ил)пиридин-3-ил]амида 4'-метокси-6-метилбифенил-3-карбоновой кислоты;
[6-(2-метилморфолин-4-ил)пиридин-3-ил]амида 4'-диметиламино-6-метилбифенил-3-карбоновой кислоты;
(6-[1,4]оксазепан-4-илпиридин-3-ил)амида 4'-диметиламино-6-метилбифенил-3-карбоновой кислоты;
(6-морфолин-4-илпиридин-3-ил)амида 4'-диметиламино-6-метилбифенил-3-карбоновой кислоты;
(6-азепан-1-илпиридин-3-ил)амида 4'-метокси-6-метилбифенил-3-карбоновой кислоты;
(6-азепан-1-илпиридин-3-ил)амида 4'-этокси-6-метилбифенил-3-карбоновой кислоты;
(6-азепан-1-илпиридин-3-ил)амида 6-метил-4'-метилсульфанилбифенил-3-карбоновой кислоты;
(6-азепан-1-илпиридин-3-ил)амида 4'-диметиламино-6-метилбифенил-3-карбоновой кислоты;
(6-азепан-1-илпиридин-3-ил)амида 3'-хлор-6-метил-4'-трифторметилбифенил-3-карбоновой кислоты;
(6-азепан-1-илпиридин-3-ил)амида 6,4'-диметилбифенил-3-карбоновой кислоты;
(6-азепан-1-илпиридин-3-ил)амида 4'-этил-6-метилбифенил-3-карбоновой кислоты;
(6-азепан-1-илпиридин-3-ил)амида 4'-трет-бутил-6-метилбифенил-3-карбоновой кислоты;
(6-азепан-1-илпиридин-3-ил)амида 6-метил-4'-пропилбифенил-3-карбоновой кислоты;
(6-азепан-1-илпиридин-3-ил)амида 4'-изобутил-6-метилбифенил-3-карбоновой кислоты;
(6-азепан-1-илпиридин-3-ил)амида 4'-изопропил-6-метилбифенил-3-карбоновой кислоты;
(6-азепан-1-илпиридин-3-ил)амида 6-метил-4'-трифторметилбифенил-3-карбоновой кислоты;
(6-азепан-1-илпиридин-3-ил)амида 6-метил-4'-трифторметоксибифенил-3-карбоновой кислоты;
(4-морфолин-4-илфенил)амида 4'-метокси-6-метилбифенил-3-карбоновой кислоты;
(4-морфолин-4-илфенил)амида 6-метил-4'-(4-метилпиперазин-1-ил)бифенил-3-карбоновой кислоты;
(6-[1,4]оксазепан-4-илпиридин-3-ил)амида 4'-циано-6-метилбифенил-3-карбоновой кислоты;
(6-азепан-1-илпиридин-3-ил)амида 4'-циано-6-метилбифенил-3-карбоновой кислоты;
[6-(2-метилморфолин-4-ил)пиридин-3-ил]амида 4'-циано-6-метилбифенил-3-карбоновой кислоты;
(3,4,5,6-тетрагидро-2Н-[1,2']бипиридинил-5'-ил)амида 4'-циано-6-метилбифенил-3-карбоновой кислоты;
(6-морфолин-4-илпиридин-3-ил)амида 4'-циано-6-метилбифенил-3-карбоновой кислоты;
[6-(4-метилпиперазин-1-ил)пиридин-3-ил]амида 4'-циано-6-метилбифенил-3-карбоновой кислоты;
(4-морфолин-4-илфенил)амида 4'-циано-6-метилбифенил-3-карбоновой кислоты;
(4-циклогексилфенил)амида 4'-циано-6-метилбифенил-3-карбоновой кислоты;
бифенил-4-иламида 4'-циано-6-метилбифенил-3-карбоновой кислоты;
(4'-метоксибифенил-4-ил)амида 4'-циано-6-метилбифенил-3-карбоновой кислоты;
[4-(4-бензилпиперазин-1-ил)фенил]амида 4'-циано-6-метилбифенил-3-карбоновой кислоты;
[4-(пиперидин-1-сульфонил)фенил]амида 4'-циано-6-метилбифенил-3-карбоновой кислоты;
[4-(пирролидин-1-сульфонил)фенил]амида 4'-циано-6-метилбифенил-3-карбоновой кислоты;
(6-азепан-1-илпиридин-3-ил)амида 4'-циано-6-метоксибифенил-3-карбоновой кислоты;
(6-азепан-1-илпиридин-3-ил)амида 4'-циано-2-метоксибифенил-3-карбоновой кислоты;
(6-азепан-1-илпиридин-3-ил)амида 4'-циано-2-метилбифенил-3-карбоновой кислоты;
(6-азепан-1-илпиридин-3-ил)амида 3'-фтор-4'-метокси-6-метилбифенил-3-карбоновой кислоты;
(6-азепан-1-илпиридин-3-ил)амида 4'-изопропокси-6-метилбифенил-3-карбоновой кислоты;
(6-азепан-1-илпиридин-3-ил)амида 4'-бутокси-6-метилбифенил-3-карбоновой кислоты;
(6-азепан-1-илпиридин-3-ил)амида 3'-хлор-4'-метокси-6-метилбифенил-3-карбоновой кислоты;
(6-азепан-1-илпиридин-3-ил)амида 4'-метокси-6,3'-диметилбифенил-3-карбоновой кислоты;
[4-(пиперидин-1-сульфонил)фенил]амида 4'-циано-2-метилбифенил-3-карбоновой кислоты;
[4-(пиперидин-1-сульфонил)фенил]амида 4'-циано-6-фторбифенил-3-карбоновой кислоты;
[4-(пиперидин-1-сульфонил)фенил]амида 6-бром-4'-цианобифенил-3-карбоновой кислоты;
[6-(4-бензил[1,4]диазепан-1-ил)пиридин-3-ил]амида 4'-циано-6-метилбифенил-3-карбоновой кислоты;
[6-(4-тиофен-3-илметил[1,4]диазепан-1-ил)пиридин-3-ил]амида 4'-циано-6-метилбифенил-3-карбоновой кислоты;
[6-(2,6-диметилморфолин-4-ил)пиридин-3-ил]амида 4'-циано-2-метилбифенил-3-карбоновой кислоты;
[6-(2,6-диметилморфолин-4-ил)пиридин-3-ил]амида 4'-метокси-2-метилбифенил-3-карбоновой кислоты;
[6-(2,6-диметилморфолин-4-ил)пиридин-3-ил]амида 2-метил-4'-трифторметилбифенил-3-карбоновой кислоты;
[6-(2,6-диметилморфолин-4-ил)пиридин-3-ил]амида 2-метил-4'-трифторметоксибифенил-3-карбоновой кислоты;
[6-(2-метилморфолин-4-ил)пиридин-3-ил]амида 4'-циано-2-метилбифенил-3-карбоновой кислоты;
[4-(пиперидин-1-сульфонил)фенил]амида 4'-циано-2-фторбифенил-3-карбоновой кислоты;
[4-(пиперидин-1-сульфонил)фенил]амида 4'-циано-6-трифторметилбифенил-3-карбоновой кислоты;
[6-(4-пиридин-4-илметил[1,4]диазепан-1-ил)пиридин-3-ил]амида 4'-циано-6-метилбифенил-3-карбоновой кислоты;
[6-(4-пиридин-3-илметил[1,4]диазепан-1-ил)пиридин-3-ил]амида 4'-циано-6-метилбифенил-3-карбоновой кислоты;
{6-[4-(2,6-диметоксибензил)-[1,4]диазепан-1-ил]пиридин-3-ил}амида 4'-циано-6-метилбифенил-3-карбоновой кислоты;
{6-[4-(2-этоксибензил)-[1,4]диазепан-1-ил]пиридин-3-ил}амида 4'-циано-6-метилбифенил-3-карбоновой кислоты;
(6-{4-[2-(4-метилпиперазин-1-ил)бензил]-[1,4]диазепан-1-ил}пиридин-3-ил)амида 4'-циано-6-метилбифенил-3-карбоновой кислоты;
{6-[4-(4-метокси-2,3-диметилбензил)-[1,4]диазепан-1-ил]пиридин-3-ил}амида 4'-циано-6-метилбифенил-3-карбоновой кислоты;
[6-(4-пиридин-2-илметил[1,4]диазепан-1-ил)пиридин-3-ил]амида 4'-циано-6-метилбифенил-3-карбоновой кислоты;
{6-[4-(2-трифторметоксибензил)-[1,4]диазепан-1-ил]пиридин-3-ил}амида 4'-циано-6-метилбифенил-3-карбоновой кислоты;
{6-[4-(2-хлор-5-трифторметилбензил)-[1,4]диазепан-1-ил]пиридин-3-ил}амида 4'-циано-6-метилбифенил-3-карбоновой кислоты;
{6-[4-(2,3-дифторбензил)-[1,4]диазепан-1-ил]пиридин-3-ил}амида 4'-циано-6-метилбифенил-3-карбоновой кислоты;
{6-[4-(2-хлор-4-фторбензил)-[1,4]диазепан-1-ил]пиридин-3-ил}амида 4'-циано-6-метилбифенил-3-карбоновой кислоты;
{6-[4-(2,6-дифторбензил)-[1,4]диазепан-1-ил]пиридин-3-ил}амида 4'-циано-6-метилбифенил-3-карбоновой кислоты;
[4-(пиперидин-1-сульфонил)фенил]амида 2-хлор-4'-цианобифенил-3-карбоновой кислоты;
[6-(2,6-диметилморфолин-4-ил)пиридин-3-ил]амида 4'-циано-6-трифторметилбифенил-3-карбоновой кислоты;
[6-(2,6-диметилморфолин-4-ил)пиридин-3-ил]амида 2-хлор-4'-цианобифенил-3-карбоновой кислоты;
[6-(2,6-диметилморфолин-4-ил)пиридин-3-ил]амида 4'-циано-6-этилбифенил-3-карбоновой кислоты;
{6-[4-(3-фторбензил)пиперазин-1-ил]пиридин-3-ил}амида 4'-циано-6-метилбифенил-3-карбоновой кислоты;
{6-[4-(2-трифторметоксибензил)пиперазин-1-ил]пиридин-3-ил}амида 4'-циано-6-метилбифенил-3-карбоновой кислоты;
{6-[4-(3-хлорбензил)пиперазин-1-ил]пиридин-3-ил}амида 4'-циано-6-метилбифенил-3-карбоновой кислоты;
[6-(4-бензилпиперазин-1-ил)пиридин-3-ил]амида 4'-циано-6-метилбифенил-3-карбоновой кислоты;
[6-(4-пиридин-3-илметилпиперазин-1-ил)пиридин-3-ил]амида 4'-циано-6-метилбифенил-3-карбоновой кислоты;
[6-(4-пиридин-4-илметилпиперазин-1-ил)пиридин-3-ил]амида 4'-циано-6-метилбифенил-3-карбоновой кислоты;
[6-(4-пиридин-2-илметилпиперазин-1-ил)пиридин-3-ил]амида 4'-циано-6-метилбифенил-3-карбоновой кислоты;
(R)-2-метил-N-(6-(2-метилморфолино)пиридин-3-ил)-4'-(трифторметокси)бифенил-3-карбоксамида;
4'-циано-2-метил-N-(6-сульфонилморфолинопиридин-3-ил)бифенил-3-карбоксамида;
(S)-4'-циано-2-метил-N-(6-(2-метилморфолино)пиридин-3-ил)бифенил-3-карбоксамида;
(R)-6-хлор-N-(6-(2-метилморфолино)пиридин-3-ил)-4'-(трифторметокси)бифенил-3-карбоксамида;
4'-циано-N-(6-(диизобутиламино)пиридин-3-ил)-2-метилбифенил-3-карбоксамида;
4'-циано-N-(2-((2S,6R)-2,6-диметилморфолино)пиримидин-5-ил)-2-метилбифенил-3-карбоксамида;
N-(2-((2S,6R)-2,6-диметилморфолино)пиримидин-5-ил)-2-метил-4'-(трифторметил)бифенил-3-карбоксамида;
N-(2-((2S,6R)-2,6-диметилморфолино)пиримидин-5-ил)-2-метил-4'-(трифторметокси)бифенил-3-карбоксамида;
N-(2-(бис-(2-гидроксиэтил)амино)пиримидин-5-ил)-2-метил-4'-(трифторметокси)бифенил-3-карбоксамида;
2-метил-N-(6-(тетрагидро-2Н-пиран-4-илокси)пиридин-3-ил)-4'-(трифторметокси)бифенил-3-карбоксамида;
N-(6-(4-этилпиперазин-1-карбонил)пиридин-3-ил)-2-метил-4'-(трифторметокси)бифенил-3-карбоксамида;
2-метил-N-(6-(2-оксопиперазин-1-ил)пиридин-3-ил)-4'-(трифторметокси)бифенил-3-карбоксамида;
2-метил-N-(6-(2-оксо-4-(пиридин-4-илметил)пиперазин-1-ил)пиридин-3-ил)-4'-(трифторметокси)бифенил-3-карбоксамида;
2-метил-N-(6-(1-(пиридин-4-илметил)пиперидин-3-ил)пиридин-3-ил)-4'-(трифторметокси)бифенил-3-карбоксамида и
N-(6-(1-этилпиперидин-3-ил)пиридин-3-ил)-2-метил-4'-(трифторметокси)бифенил-3-карбоксамида.
5. Соединение, представляющее собой N-(6-((2R,6S)-2,6-диметилморфолино)пиридин-3-ил)-2-метил-4'-(трифторметокси)-[1,1'-бифенил]-3-карбоксамид следующей формулы:
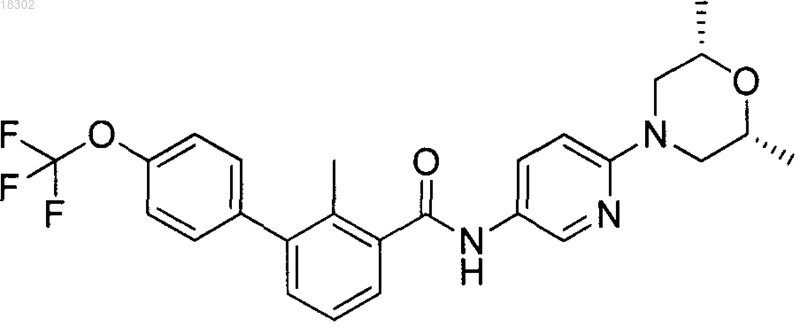
или его фармацевтически приемлемая соль или стереоизомеры.
6. Способ ингибирования пути Hedgehog в клетке, включающий контактирование клетки с соединением по любому из пп.1-5.
7. Способ по п.6, где клетка имеет фенотип утраты функции Ptc, усиления функции Hedgehog, усиления функции рецептора Smoothened или усиления функции Gli.
8. Способ по п.7, где клетка контактирует с антагонистом Hedgehog in vivo или in vitro.
9. Способ по п.8, где соединение вводят животному в качестве части терапевтического применения.
10. Способ по п.9, где терапевтическое применение выбрано из рака поджелудочной железы, рака простаты, медуллобластомы, базальноклеточной карциномы и мелкоклеточного рака легкого.
11. Способ ингибирования нежелательной пролиферации клетки, включающий контактирование клетки с соединением по любому из пп.1-5.
12. Способ по п.11, где клетка выбрана из клеток рака поджелудочной железы, рака простаты, медуллобластомы, базальноклеточной карциномы и мелкоклеточного рака легкого.
Текст
СОЕДИНЕНИЯ В КАЧЕСТВЕ МОДУЛЯТОРОВ ПУТИ HEDGEHOG В изобретении предлагаются соединения формулы I и способ модуляции активности сигнального пути Hedgehog. В частности, в изобретении предлагается способ ингибирования состояний аномального роста, возникающих вследствие таких фенотипов, как утрата функции Ptc, усиление функции Hedgehog, усиление функции рецептора Smoothened или усиление функции Gli,включающий контактирование клетки с достаточным количеством соединения формулы I Перекрестная ссылка на родственные заявки Заявка на настоящий патент представляет собой национальную заявку 371 US, составленную на основании международной заявкиPCT/US2007/068292, поданной 4 мая 2007 г. По настоящей заявке испрашивается приоритет на основании предварительной заявки на патент США 60/797949, зарегистрированной 5 мая 2006 г. Полное раскрытие этой заявки включено в данное описание в качестве ссылки в полном объеме для всех целей. Известный уровень техники Область техники, к которой относится изобретение В изобретении предлагается способ модуляции активности сигнального пути Hedgehog. В частности, в изобретении предлагается способ ингибирования аберрантных состояний роста, возникающих при таких фенотипах, как потеря функции Ptc, усиление функции Hedgehog, усиление функции рецептораSmoothened или усиление функции Gli, включающий контактирование клетки с достаточным количеством соединения формулы I. Характеристика известного уровня техники В течение эмбрионального развития сигнальный путь Hedgehog существенен для множества процессов, таких как контроль клеточной пролиферации, дифференцировки и построение тканей. Аберрантная активность сигнального пути Hedgehog, например, в результате повышенной активации, однако, может иметь патологические последствия. В этом смысле активация пути Hedgehog в тканях взрослого организма может приводить к конкретным типам рака, которые включают, но не ограничиваются этим, рак мозга, мышц и кожи, простаты, медуллобластому, аденокарциномы поджелудочной железы и мелкоклеточные карциномы легких. Повышенная активация сигнального пути Hedgehog вносит вклад в патологию и/или симптоматику ряда заболеваний. Соответственно, молекулы, которые модулируют активность сигнального пути Hedgehog, применимы в качестве терапевтических средств при лечении таких заболеваний. Краткое изложение сущности изобретения В одном аспекте настоящее изобретение относится к соединениям формулы I где Y1 и Y2 независимо выбраны из N и СН;R1 выбран из циано, C1-6 алкила, галогензамещенного C1-6 алкила, С 1-6 алкокси, галогензамещенного С 1-6 алкокси, диметиламино, С 1-6 алкилсульфанила и пиперазинила, необязательно замещенного не более чем двумя С 1-6 алкильными радикалами;R2 и R5 независимо выбраны из водорода, циано, галогена, С 1-6 алкила, галогензамещенного С 1-6 алкила и С 1-6 алкокси;R3 и R4 независимо выбраны из водорода, галогена, циано, C1-6 алкила, С 1-6 алкокси и галогензамещенного C1-6 алкокси;R6 и R7 независимо выбраны из водорода, хлора, фтора, брома, C1-6 алкила, галогензамещенногоC1-6 алкила и С 1-6 алкокси при условии, что R6 и R7 одновременно не означают водород;R12a и R12b независимо выбраны из изобутила, гидроксиэтила; указанные сульфономорфолино, морфолино, циклогексил, фенил, азепан-1-ил, 2-оксопиперазин-1 ил, 1,4-оксазепан-4-ил, пиперидин-1-ил, тетрагидро-2 Н-пиран-4-ил, пиперидин-3-ил, пиперазинил, пирролидинил или 1,4-диазепан-1-ил в R9 могут быть необязательно замещены 1-3 радикалами, независимо выбранными из метила, этила, метокси, бензила, тиенилметила и пиридинилметила; указанный бензильный заместитель R9 необязательно замещен 1-3 радикалами, независимо выбранными из метокси, этокси, метилпиперазинила, метила, трифторметокси, хлора, фтора и трифторметила; или их фармацевтически приемлемым солям и стереоизомерам. В еще одном аспекте настоящее изобретение относится к соединению, представляющему собой N(6-2R,6S)-2,6-диметилморфолино)пиридин-3-ил)-2-метил-4'-(трифторметокси)-[1,1'-бифенил]-3-1 018302 или его фармацевтически приемлемой соли или стереоизомерам. В другом аспекте в настоящем изобретении предлагается способ ингибирования пути Hedgehog в клетке, включающий контактирование клетки с любым из вышеуказанных соединений. В предпочтительном варианте осуществления клетка имеет фенотип утраты функции Ptc, усиления функции Hedgehog, усиления функции рецептора Smoothened или усиления функции Gli. Предпочтительно клетка контактирует с антагонистом Hedgehog in vivo или in vitro. Предпочтительно соединение вводят животному в качестве части терапевтического применения. В конкретных вариантах воплощения терапевтическое применение выбрано из рака поджелудочной железы, рака простаты, медуллобластомы, базальноклеточной карциномы и мелкоклеточного рака легкого. В еще одном варианте воплощения настоящее изобретение относится к способу ингибирования нежелательной пролиферации клетки, включающему контактирование клетки с одним из вышеуказанных соединений. В частном варианте воплощения клетка выбрана из клеток рака поджелудочной железы, рака простаты, медуллобластомы, базальноклеточной карциномы и мелкоклеточного рака легкого. Определения"Алкил" как группа и как структурный элемент других групп, например галогензамещенный алкил и алкокси, может иметь линейную цепь или быть разветвленным. C1-4 алкокси включает метокси, этокси и т.п. Галогензамещенный алкил включает трифторметил, пентафторэтил и т.п."Арил" обозначает моноциклическую или конденсированную бициклическую ароматическую кольцевую структуру, содержащую от шести до десяти углеродных атомов кольца. Например, арил может представлять собой фенил или нафтил, предпочтительно фенил. "Арилен" обозначает двухвалентный радикал, происходящий из арильной группы."Гетероарил" представляет собой определяемое для арила выше, где один или более членов кольца являются гетероатомами. Например, С 5-10 гетероарил имеет минимум 5-членное кольцо, как указано для углеродных атомов, но эти углеродные атомы могут быть заменены гетероатомом. Следовательно,С 5-10 гетероарил включает пиридил, индолил, индазолил, хиноксалинил, хинолинил, бензофуранил, бензопиранил, бензотиопиранил, бензо[1,3]диоксол, имидазолил, бензоимидазолил, пиримидинил, фуранил,оксазолил, изоксазолил, триазолил, тетразолил, пиразолил, тиенил и т.п."Циклоалкил" обозначает насыщенную или частично ненасыщенную, моноциклическую, конденсированную бициклическую или мостиковую полициклическую кольцевую структуру, содержащую указанное количество атомов кольца. Например, С 3-10 циклоалкил включает циклопропил, циклобутил, циклопентил, циклогексил и т.п."Гетероциклоалкил" обозначает циклоалкил, как определено в данном изобретении, предлагаемый так, что один или более указанных углеродов кольца заменены частью, выбранной из -O-, -N=, -NR-,-С(O)-, -S-, -S(O)- или -S(O)2-, где R представляет собой водород, С 1-4 алкил или азотную защитную группу. Например, С 3-8 гетероциклоалкил, как применяется в данном патенте для описания соединений изобретения, включает морфолино, пирролидинил, пирролидинил-2-он, пиперазинил, пиперидинил, пиперидинилон, 1,4-диокса-8-азаспиро[4.5]дец-8-ил, тиоморфолино, сульфаноморфолино, сульфономорфолино и т.п."Галоген" предпочтительно представляет собой хлор или фтор, но может также представлять собой бром или йод."Усиление функции пути Hedgehog" относится к аберрантной модификации или мутации гена Ptc,гена Hedgehog или гена рецептора Smoothened или к снижению (или потере) уровня экспрессии такого гена, что ведет к фенотипу, который напоминает контактирование клетки с белком Hedgehog, например к аберрантной активации пути Hedgehog. Усиление функции может включать потерю способности продукта гена Ptc регулировать уровень экспрессии генов Gli, например Gli1, Gli2 и Gli3. Термин "усиление функции Hedgehog" применяется здесь также для обозначения любого сходного клеточного фенотипа(например, проявляющего избыточную пролиферативную активность), который возникает благодаря изменению на любом этапе пути передачи сигнала Hedgehog, включая, но не ограничиваясь этим, модификацию или мутацию самого Hedgehog. Например, опухолевая клетка с аномально высокой скоростью пролиферации из-за активации сигнального пути Hedgehog должна иметь фенотип "усиления функцииHedgehog", даже если Hedgehog в этой клетке не мутирован."Потеря функции белка Patched" относится к аберрантной модификации или мутации гена Ptc или пониженному уровню экспрессии гена, что ведет к фенотипу, который напоминает контактирование клетки с белком Hedgehog, например к аберрантной активации пути Hedgehog. Потеря функции может включать потерю способности продукта гена Ptc регулировать уровень экспрессии генов Gli, например"Усиление функции Gli" относится к аберрантной модификации или мутации гена Gli или повышенному уровню экспрессии гена, что ведет к фенотипу, который напоминает контактирование клетки с белком Hedgehog, например к аберрантной активации пути Hedgehog."Усиление функции рецептора Smoothened" относится к аберрантной модификации или мутации гена Smo или повышенному уровню экспрессии гена, что ведет к фенотипу, который напоминает контактирование клетки с белком Hedgehog, например к аберрантной активации пути Hedgehog."Лечить", "лечение" и "терапия" относятся к методу облегчения или прекращения заболевания и/или сопровождающих его симптомов. Настоящее изобретение относится к открытию того, что пути передачи сигнала, регулируемыеHedgehog, белком Patched (Ptc), Gli и/или рецептором Smoothened, могут модулироваться соединениями формулы I. Описание предпочтительных осуществлений В одном из предпочтительных осуществлений в отношении соединений формулы IR6 и R7 независимо выбраны из водорода, метила, хлора, фтора, брома, трифторметила и метокси при условии, что R6 и R7 одновременно не означают водород. В другом предпочтительном осуществлении в отношении соединений формулы IR1 выбран из циано, метила, этила, трет-бутила, пропила, изобутила, изопропила, изопропилокси,бутокси, метокси, диметиламино, этокси, метилсульфанила, трифторметила, трифторметокси и пиперазинила, необязательно замещенного не более чем двумя метильными радикалами;R2 и R5 независимо выбраны из водорода, хлора, фтора, циано, метила, трифторметила, изопропилокси, метокси, этокси;R3 и R4 независимо выбраны из водорода, хлора, метила, метокси и циано. В еще одном предпочтительном варианте осуществления предлагается соединение, выбранное изN-(6-(1-этилпиперидин-3-ил)пиридин-3-ил)-2-метил-4'-(трифторметокси)бифенил-3-карбоксамида. Следовательно, специально предполагается, что соединения формулы I, которые влияют на активность передачи сигнала Hedgehog, Ptc или рецептора Smoothened, должны также ингибировать пролиферацию (или другие биологические последствия) в нормальных клетках и/или клетках, обладающих фенотипом потери функции белка Patched, фенотипом усиления функции Hedgehog, фенотипом усиления функции рецептора Smoothened или фенотипом усиления функции Gli. Таким образом, предполагается,что в определенных осуществлениях эти соединения могут быть пригодны для ингибирования активности Hedgehog в нормальных клетках, например, таких, которые не имеют генетической мутации, которая активирует путь Hedgehog. В предпочтительных осуществлениях соединения способны ингибировать, по меньшей мере, некоторые биологические активности белков Hedgehog, предпочтительно конкретно в клетках-мишенях. Таким образом, в настоящем документе описано применение соединений формулы I, которые являются агонистами ингибирования с помощью Ptc сигнального пути Hedgehog, например путем ингиби-5 018302 рования активации рецептора Smoothened или нижележащих компонентов сигнального пути, для регуляции репарации и/или функциональной активности широкого спектра клеток, тканей и органов, включая нормальные клетки, ткани и органы, а также те, которые обладают фенотипом потери функции Ptc, усиления функции Hedgehog, усиления функции рецептора Smoothened или усиления функции Gli. Например, обсуждаемый способ имеет терапевтическое и косметическое применение в диапазоне регуляции нервных тканей, образования и репарации костной и хрящевой ткани, регуляции сперматогенеза, регуляции гладких мышц, регуляции легких, печени и других органов, происходящих из первичной кишки,регуляции гематопоэтической функции, регуляции кожи и роста волос и т.д. Более того, обсуждаемые способы могут осуществляться на клетках, которые предлагаются в культуре (in vitro) или на клетках целого животного (in vivo). В другом осуществлении обсуждаемый способ может быть использован для обработки эпителиальных клеток, имеющих фенотип утраты функции Ptc, усиления функции Hedgehog, усиления функции рецептора Smoothened или усиления функции Gli. Например, рассматриваемый способ может быть применен для лечения или профилактики базальноклеточной карциномы или других связанных с путемHedgehog нарушений. В некоторых осуществлениях соединение формулы I может ингибировать активацию пути Hedgehog путем связывания с Smoothened рецептором или его нижележащими белками. В некоторых осуществлениях рассматриваемый антагонист может ингибировать активацию пути Hedgehog за счет связывания с белком Patched. В другом предпочтительном осуществлении рассматриваемый способ может быть использован в качестве части режима лечения злокачественных медуллобластом и других первичных злокачественных нейроэктодермальных опухолей ЦНС. В другом аспекте в настоящем документе описаны фармацевтические препараты, включающие в качестве активного ингредиента модулятор сигнального пути Hedgehog, такой как соединение формулыI, агонист Ptc, антагонист рецептора Smoothened или антагонист нижележащего белка пути Hedgehog,такой как описанный здесь, составленных в количестве, достаточном для ингибирования in vivo пролиферации или других биологических последствий утраты функции Ptc, усиления функции Hedgehog, усиления функции рецептора Smoothened или усиления функции Gli. Рассматриваемое лечение с применением соединения формулы I, агонистов белка Patched, антагонистов рецептора Smoothened или антагонистов нижележащего белка пути Hedgehog может быть эффективным и для человека, и для животных субъектов. Животные субъекты, к которым применимо изобретение, включают и домашних животных, и домашний скот, содержащихся либо в качестве компаньонов,либо для коммерческих целей. Примерами служат собаки, кошки, рогатый скот, лошади, овцы, свиньи и козы. Фармакология и применение В настоящем документе описаны способы и соединения для ингибирования активации сигнального пути Hedgehog, например, для ингибирования состояний аномального роста, возникающих из фенотипов,таких как утрата функции Ptc, усиление функции Hedgehog, усиление функции рецептора Smoothened или усиление функции Gli, включающие контактирование клетки с соединением формулы I, в количестве, достаточном для противодействия нормальной активности Ptc, противодействия нормальной активности Hedgehog, противодействия активности рецептора Smoothened или противодействия активностиGli, например, для обращения или контроля аномального состояния роста. Члены семейства Hedgehog сигнальных молекул опосредуют многие важные близко- и дальнодействующие процессы формирования плана структуры в течение развития позвоночных. Формирование плана структуры представляет собой активность, с помощью которой эмбриональные клетки образуют упорядоченные пространственные структуры дифференцирующихся тканей. Физическая сложность высших организмов возникает во время эмбриогенеза благодаря взаимодействию присущей клетке линии дифференцировки и внешней по отношению к клетке сигнализации. Индуцирующие взаимодействия существенны в развитии позвоночных для эмбрионального формирования плана структуры с самого раннего установления плана организма до формирования плана систем органов и до образования различных типов клеток во время дифференцировки тканей. Влияния клеточных взаимодействий при развитии варьируются: отвечающие клетки отклоняются от одного пути клеточной дифференцировки в сторону другого пути под влиянием индуцирующих клеток, которые отличны как от неиндуцированного, так и от индуцированного состояний отвечающих клеток (индукции). Иногда клетки индуцируют дифференцировку соседних клеток по подобному себе пути (гомеогенетическая индукция); в других случаях клетка ингибирует дифференцировку своих соседей по подобному себе пути. Клеточные взаимодействия в раннем развитии могут быть последовательными, так что исходная индукция между двумя типами клеток ведет к прогрессирующему усилению различий. Более того, индуцирующие взаимодействия имеют место не только в эмбрионах, но также и в клетках взрослого организма и могут действовать для установления и поддержания морфогенетического плана структуры, а также для индукции дифференцировки. Семейство генов Hedgehog у позвоночных включает три члена, имеющихся у млекопитающих и известных как Desert (Dhh), Sonic (Shh) и Indian (Ihh) Hedgehog, каждый из которых кодирует секретируе-6 018302 мый белок. Эти разные белки Hedgehog состоят из сигнального пептида, высококонсервативной Nконцевой области и более вариабельного С-концевого домена. В биохимических исследованиях было показано, что аутопротеолитическое расщепление предшественника белка Hh происходит через внутренний тиоэфирный промежуточный продукт, который затем расщепляется при нуклеофильном замещении. Вероятно, нуклеофил представляет собой небольшую липофильную молекулу, которая ковалентно связывается с С-концом N-пептида, связывая его с клеточной поверхностью. Биологические последствия являются глубокими. В результате присоединения на поверхности клеток, продуцирующих Hedgehog,возникает высокая местная концентрация N-концевого пептида Hedgehog. Именно этот N-концевой пептид необходим и достаточен для осуществления коротко- и дальнодействующей сигнальной активностиHedgehog. Неактивный путь Hedgehog сигнализации имеет место тогда, когда трансмембранный рецепторный белок Patched (Ptc) ингибирует активность рецептора Smoothened (Smo), белка с семью трансмембранными доменами. При этом предотвращается вхождение транскрипционного фактора Gli, нижележащего компонента сигнализации Hh, в ядро за счет взаимодействий с цитоплазматическими белками, включая слитый белок и супрессор слитого белка (Sufu). Вследствие этого транскрипционная активация геновмишеней Hedgehog репрессирована. Активация пути инициируется посредством связывания любого из трех лигандов млекопитающих (Dhh, Shh или Ihh) с Ptc. Связывание лиганда приводит к снятию репрессии Smo, тем самым приводя к активации каскада, который ведет к транслокации активной формы транскрипционного фактора Gli в ядро. Ядерный Gli активирует экспрессию генов-мишеней, включая сами Ptc и Gli. Повышенный уровень сигнализации Hedgehog достаточен для инициации развития рака и необходим для выживания опухоли. Такие типы рака включают, но не ограничиваются этим, рак простатыM.W., Datta S., Ruiz i Altaba A., Proc Natl Acad Sci USA, 2004 Aug 24; 101(34):12561-6), рак молочной железы ("Hedgehog signaling pathway is a new therapeutic target for patients with breast cancer", Kubo M., Nakamura M., Tasaki A., Yamanaka N., Nakashima H., Nomura M., Kuroki S., Katano M., Cancer Res. 2004 Sep 1; 64(17):6071-4), медуллобластому ("Medulloblastoma growth inhibition by hedgehog pathway blockade",Berman D.M., Karhadkar S.S., Hallahan A.R., Pritchard J.I., Eberhart C.G., Watkins D.N., Chen J.K., CooperF.J., Nature, 1998 Jan 1; 391(6662):90-2), рак поджелудочной железы ("Hedgehog is an early and late mediator of pancreatic cancer tumorigenesis", Thayer S.P., di Magliano M.P., Heiser P.W., Nielsen C.M., Robertsstimulation in growth of digestive tract tumours", Berman D.M., Karhadkar S.S., Maitra A., Montes De Oca R.,Gerstenblith M.R., Briggs K., Parker A.R., Shimada Y., Eshleman J.R., Watkins D.N., Beachy P.A., Nature,2003 Oct 23; 425(6960):846-51) и мелкоклеточный рак легкого ("Hedgehog signalling within airway epithelial progenitors and in small-cell lung cancer", Watkins D.N., Berman D.M., Burkholder S.G., Wang B., BeachyP.A., Baylin S.B., Nature, 2003 Mar 20; 422(6929):313-7). В соответствии с вышеизложенным в настоящем изобретении дополнительно раскрыт способ предупреждения или лечения любого из заболеваний или нарушений, описанных выше, у субъекта, нуждающегося в таком лечении, причем способ включает введение указанному субъекту терапевтически эффективного количества (см. далее раздел "Введение и фармацевтические композиции") соединения формулы I или его фармацевтически приемлемой соли. Для любого из указанных выше применений необходимая доза должна варьироваться в зависимости от способа введения, конкретного состояния, подлежащего лечению, и желаемого эффекта. Введение и фармацевтические композиции. В целом соединения изобретения должны вводиться в терапевтически эффективных количествах посредством любого из обычных и приемлемых способов, известных в данной области техники, либо изолированно, либо в сочетании с одним или более терапевтическими агентами. Терапевтически эффективное количество может широко варьироваться в зависимости от тяжести заболевания, возраста и относительного здоровья субъекта, эффективности применяемого соединения и других факторов. В целом удовлетворительные результаты, как указывается, получают при систематических ежедневных дозах от приблизительно 0,03 до 2,5 мг/кг массы тела. Указанная дневная доза у более крупного млекопитающего,например человека, находится в диапазоне от приблизительно 0,5 до приблизительно 100 мг при тради-7 018302 ционном введении, например, в раздельных дозах до 4 раз в день или в замедленной форме. Подходящие единицы лекарственной формы для перорального введения включают от приблизительно 1 до 50 мг активного ингредиента. Соединения изобретения можно вводить в виде фармацевтических композиций любым традиционным путем, в частности энтерально, например перорально, например в форме таблеток или капсул, или парентерально, например в форме растворов для инъекций или суспензий, местно, например в форме лосьонов, гелей, мазей или кремов или в назальной или суппозиторной форме. Фармацевтические композиции, включающие соединение настоящего изобретения в свободной форме или в форме фармацевтически приемлемой соли в сочетании по меньшей мере с одним фармацевтически приемлемым носителем или разбавителем, может быть получено традиционным способом путем способов смешивания, гранулирования или покрытия. Например, пероральные композиции могут представлять собой таблетки или желатиновые капсулы, включающие активный ингредиент вместе с а) разбавителями, например лактозой,декстрозой, сахарозой, маннитом, сорбитом, целлюлозой и/или глицином; b) увлажняющими агентами,например диоксидом кремния, тальком, стеариновой кислотой, ее магниевой или кальциевой солью и/или полиэтиленгликолем; для таблеток также с) связующими агентами, например магнийалюмосиликатом,крахмальным клейстером,желатином,трагакантом,метилцеллюлозой,натрийкарбоксиметилцеллюлозой и/или поливинилпирролидоном; если желательно d) разрыхлителями, например крахмалами, агаром, альгиновой кислотой или ее натриевой солью, или шипучими смесями; и/или е) абсорбентами, красителями, отдушками и подсластителями. Композиции для инъекций могут быть водными изотоническими растворами или суспензиями, а суппозитории могут быть получены из жировых эмульсий или суспензий. Композиции могут быть стерилизованы и/или содержать адъюванты, такие как консервирующие, стабилизирующие, увлажняющие или эмульгирующие агенты, стимулирующие растворение агенты, соли для регуляции осмотического давления и/или буферы. Кроме того, они могут также содержать другие терапевтически ценные вещества. Подходящие составы для чрескожного нанесения включают эффективное количество соединения настоящего изобретения с носителем. Носитель может включать всасываемые фармацевтически приемлемые растворители для обеспечения прохождения через кожу хозяина. Например, чрескожные устройства находятся в форме повязки, включающей оболочку,резервуар, содержащий соединение, необязательно с носителями, необязательно барьер, контролирующий скорость доставки соединения в кожу хозяина при контролируемой и заранее предопределенной скорости на протяжении продолжительного периода времени, и средства для прикрепления устройства к коже. Могут быть также использованы матриксные чрескожные составы. Подходящие составы для местного нанесения, например на кожу или глаза, представляют собой предпочтительно водные растворы,мази, кремы или гели, хорошо известные в данной области техники. Они могут содержать солюбилизаторы, стабилизаторы, повышающие тоничность агенты, буферы и консерванты. Соединения изобретения можно вводить в терапевтически эффективных количествах в сочетании с одним или более терапевтическими средствами (фармацевтические комбинации). Например, синергетические эффекты могут иметь место с иммуномодулирующими или противовоспалительными веществами или другими противоопухолевыми терапевтическими средствами. Когда соединения изобретения вводят в сочетании с другими типами терапии, дозы совместно вводимых соединений должны, разумеется, зависеть от типа совместно применяемого лекарственного средства, конкретно применяемого лекарственного средства, состояния, подлежащего лечению, и т.п. В настоящем документе также описаны фармацевтические комбинации, например набор, включающий а) первый агент, который представляет собой соединение изобретения, как здесь раскрыто, в свободной форме или в фармацевтически приемлемой солевой форме, и b) по меньшей мере один совместно действующий агент. Набор может включать инструкции по его введению. Термины "совместное введение" или "сочетанное введение" либо т.п. в применении здесь предназначены для охвата введения выбранных терапевтических средств отдельному больному и предназначены для включения режимов лечения, при которых средства необязательно вводят одним и тем же путем введения или в одно и то же время. Применяемый здесь термин "фармацевтическая комбинация" означает продукт, который образуется при смешивании или объединении более одного активного ингредиента и включает как фиксированные,так и нефиксированные комбинации активных ингредиентов. Термин "фиксированное сочетание" означает, что активные ингредиенты, например соединение формулы I, и совместно действующее средство вводят больному одновременно в форме единого объекта или дозы. Термин "нефиксированное сочетание" означает, что активные ингредиенты, например соединение формулы I, и совместно действующее средство вместе вводят больному в виде отдельных единиц либо одновременно, параллельно, либо последовательно без конкретных ограничений по времени, причем такое введение обеспечивает терапевтически эффективные уровни 2 соединений в организме больного. Последнее также применимо к лекарственным коктейлям, например введению 3 или более активных ингредиентов. Способы получения соединений изобретения В настоящем документе также описаны способы получения соединений изобретения. В описываемых реакциях может иметься необходимость защиты реакционных функциональных групп, например гидрокси, амино, имино, тио или карбоксигрупп, когда они желательны в конечном продукте, во избежание их нежелательного участия во взаимодействиях. Могут быть использованы традиционные защитные группы в соответствии со стандартной практикой, например, см. T.W. Greene and P.G.M. Wuts в "Protective Groups in Organic Chemistry", John Wiley and Sons, 1991. Соединения формулы I могут быть получены в соответствии со следующей схемой реакций I. Схема реакций I где Y1, Y2, R1, R2, R3, R4, R5, R6, R7, R8 и R9 определены для формулы I в разделе "Краткое изложение сущности изобретения". Соединение формулы I может быть получено путем взаимодействия соединения формулы 2 (или 2') с соединением формулы 3 в присутствии подходящего растворителя (например, дихлорметана, N,Nдиметилформамида или т.п.) в температурном диапазоне от приблизительно -20 до приблизительно 100 С. Реакция может происходить в течение до приблизительно 20 ч до завершения. Подробные примеры синтеза соединений формулы I можно найти в нижеприведенных примерах. Дополнительные способы получения соединений изобретения Соединение изобретения может быть получено в виде фармацевтически приемлемой кислотноаддитивной соли путем взаимодействия соединения в форме свободного основания с фармацевтически приемлемой неорганической или органической кислотой. Альтернативно, фармацевтически приемлемая аддитивная соль с основанием соединения изобретения может быть получена путем взаимодействия соединения в форме свободной кислоты с фармацевтически приемлемым неорганическим или органическим основанием. Альтернативно, солевые формы соединений изобретения могут быть получены при применении солей исходных веществ или промежуточных продуктов. Соединения изобретения в форме свободной кислоты или свободного основания могут быть получены из соответствующей формы аддитивной соли с основанием или кислотно-аддитивной соли соответственно. Например, соединение изобретения в форме кислотно-аддитивной соли может быть превращено в соответствующее свободное основание обработкой подходящим основанием (например, раствором гидроксида аммония, гидроксидом натрия и т.п.). Соединение изобретения в форме аддитивной соли с основанием может быть превращено в соответствующую свободную кислоту путем обработки подходящей кислотой (например, хлористо-водородной кислотой и т.д.). Соединения изобретения в неокисленной форме могут быть получены из N-оксидов соединений изобретения обработкой восстанавливающим агентом (например, серой, диоксидом серы, трифенилфосфином, боргидридом лития, боргидридом натрия, трихлоридом фосфора, трибромидом и т.п.) в подходящем инертном органическом растворителе (например, ацетонитриле, этаноле, водном диоксане и т.п.) при температуре от 0 до 80 С. Пролекарственные производные соединений изобретения могут быть получены способами, известными специалистам в данной области техники (дополнительные подробности см., например, в Saulnier etal. (1994), Bioorganic and Medicinal Chemistry Letters, vol. 4, p. 1985). Например, подходящие пролекарства могут быть получены путем взаимодействия недериватизированного соединения изобретения с подходящим карбамилирующим агентом (например, 1,1-ацилоксиалкилкарбанохлоридатом, паранитрофенолкарбонатом и т.п.). Защищенные производные соединений изобретения могут быть получены с помощью способов, известных специалистам в данной области техники. Подробное описание способов, применимых для создания защитных групп и их удаления, можно найти в Т.W. Greene "Protecting Groups in Organic Chemistry", 3rd edition, John Wiley and Sons, Inc., 1999. Соединения настоящего изобретения могут быть получены традиционно или образованы в процессе осуществления способа по изобретению в виде сольватов (например, гидратов). Гидраты соединений настоящего изобретения могут быть получены традиционно путем перекристаллизации из смеси водного/органического растворителей при применении таких органических растворителей, как диоксин, тетрагидрофуран или метанол. Соединения изобретения могут быть получены в виде их индивидуальных стереоизомеров с помощью взаимодействия рацемической смеси соединения с оптически активным разделяющим агентом с образованием пары диастереоизомерных соединений, разделения диастереомеров и выделения оптически чистых энантиомеров. Хотя разделение энантиомеров может быть произведено при использовании ковалентных диастереомерных производных соединений изобретения, предпочтительны диссоциирующие комплексы (например, кристаллические диастереомерные соли). Диастереомеры обладают разными физическими свойствами (например, точками плавления, точками кипения, растворимостью, реакционной способностью и т.д.) и могут быть легко разделены путем использования преимуществ этих различий. Диастереомеры могут быть разделены с помощью хроматографии или предпочтительно с помощью способов разделения/разложения, основанных на различиях в растворимости. Затем выделяют оптически чистый энантиомер вместе с разделяющим агентом с помощью любых использующихся средств, которые не приводят к рацемизации. Более подробное описание способов, применимых для разделения стереоизомеров соединений из их рацемической смеси, можно найти в Jean Jacques, Andre Collet, Samuel H.(a) реакцию, представленную на схеме I; и(b) необязательное превращение соединения изобретения в фармацевтически приемлемую соль;(c) необязательное превращение солевой формы соединения изобретения в несолевую форму;(d) необязательное превращение неокисленной формы соединения изобретения в фармацевтически приемлемый N-оксид;(e) необязательное превращение N-оксидной формы соединения изобретения в ее неокисленную форму;(f) необязательное выделение индивидуального изомера соединения изобретения из смеси изомеров;(g) необязательное превращение недериватизированного соединения изобретения в фармацевтически приемлемое пролекарственное производное и(h) необязательное превращение пролекарственного производного соединения изобретения в его недериватизированную форму. Если получение исходных веществ не описано конкретно, могут быть использованы известные соединения или соединения, полученные аналогично способам, известным в данной области техники, или как раскрыто в представленных ниже примерах. Специалисту в данной области техники должно быть ясно, что указанные выше превращения являются лишь иллюстрациями способов получения соединений настоящего изобретения и что сходным образом могут быть использованы другие хорошо известные способы. Примеры Настоящее изобретение дополнительно иллюстрируется, но не ограничивается, следующим примером, который демонстрирует получение соединений формулы I по изобретению. Пример 1. [4-(Морфолин-4-сульфонил)фенил]амид 4'-циано-6-метилбифенил-3-карбоновой кислоты Стадия 1. К раствору 3-йод-4-метилбензойной кислоты (10,0 г, 38,2 ммоль) в метаноле (70 мл) добавляют концентрированную серную кислоту (0,5 мл). Реакционную смесь нагревают при 70 С в течение 48 ч, охлаждают до температуры окружающей среды и затем концентрируют. После этого к остатку добавляют этилацетат (100 мл) и водный раствор NaHCO3 (насыщенный, 100 мл). Органический слой отделяют и вновь промывают водным раствором NaHCO3 (насыщенный, 100 мл). Органический слой отде- 10018302 ляют, сушат над безводным Na2SO4 и концентрируют с получением сложного метилового эфира 3-йод-4 метилбензойной кислоты 1. Его используют на следующей стадии без дополнительной очистки. 1 Н ЯМР (400 МГц, ДМСО-d6):8,31 (с, 1 Н), 7,87 (д, 1 Н, J=8,4 Гц), 7,48 (д, 1 Н, J=8,4 Гц), 3,85 (с,3 Н), 3,35 (с, 3 Н). ЖХ-МС m/z: 277, 0 (М+1). Стадия 2. В круглодонный сосуд, содержащий сложный метиловый эфир 3-йод-4-метилбензойной кислоты (1,38 г, 5,00 ммоль), 4-цианофенилбороновую кислоту (1,10 г, 7,48 ммоль), ацетат палладия(168 мг, 5,00 ммоль), 2-(дициклогексилфосфино)бифенил (0,526 г, 1,50 ммоль) и фторид калия (0,870 г,15 ммоль), добавляют безводный 1,4-диоксан (15 мл). Сосуд продувают аргоном и закрывают. Смесь перемешивают при 130 С в течение 18 ч, охлаждают до температуры окружающей среды и затем добавляют воду (20 мл) и этилацетат (20 мл). Твердое вещество удаляют фильтрованием в вакууме. Фильтрат экстрагируют EtOAc (220 мл). Органические слои объединяют, промывают водной HCl (5%, 20 мл) и насыщенным NaHCO3 (20 мл). Их сушат над MgSO4 и концентрируют. Остаток очищают колоночной хроматографией на силикагеле (EtOAc/гексан, градиент) с получением сложного метилового эфира 4'циано-6-метилбифенил-3-карбоновой кислоты 2. ЖХ-МС m/z: 252,1 (М+1). Стадия 3. К раствору сложного метилового эфира 4'-циано-6-метилбифенил-3-карбоновой кислоты 2 (2,56 г, 10,3 ммоль) в смеси 1,4-диоксан-Н 2 О (смесь 1:1, 20 мл) добавляют NaOH (1,22 г, 30,2 ммоль). Реакционную смесь перемешивают при температуре окружающей среды в течение 24 ч. К этой смеси добавляют водную HCl (1 н., 36 мл) и затем ее экстрагируют этилацетатом (340 мл). Органические слои объединяют, сушат над безводным Na2SO4. Растворитель удаляют. Полученное твердое вещество промывают небольшим количеством ацетонитрила и сушат на воздухе с получением 4'-циано-6 метилбифенил-3-карбоновой кислоты 3. 1 Н ЯМР (ДМСО-d6):7,94 (д, 2 Н, J=8,0 Гц), 7,84 (дд, 1 Н, J1=8,4 Гц, J2=1,2 Гц), 7,75 (д, 1 Н, J=1,2 Гц), 7,61 (д, 2 Н, J=8,0 Гц), 7,48 (д, 1 Н, J=8,4 Гц), 2,29 (с, 3 Н). ЖХ-МС m/z: 238,1 (М+1). Стадия 4. К суспензии 4'-циано-6-метилбифенил-3-карбоновой кислоты 3 (40 мг, 0,17 ммоль) в безводном метиленхлориде (5 мл) добавляют 2 капли ДМФ. Затем добавляют оксалилхлорид (32 мг, 22 мкл,0,25 ммоль). Смесь перемешивают при температуре окружающей среды до ее просветления. После этого ее концентрируют, повторно растворяют в безводном метиленхлориде (3 мл) и добавляют к раствору 4(морфолин-4-сульфонил)фениламина (61 мг, 0,25 ммоль) и триэтиламина (34 мг, 47 мкл, 0,33 ммоль) в метиленхлориде (2 мл). Смесь перемешивают в течение 2 ч, концентрируют и остаток очищают с помощью препаративной управляемой по массе ВЭЖХ (колонка С 18, элюируемая CH3CN-H2O с 0,05% ТФУ) с получением 4'-циано-6-метилбифенил-3-карбоновой кислоты [4-(морфолин-4-сульфонил)фенил]амида. 1 Н ЯМР (ДМСО-d6):10,64 (с, 1 Н), 8,07 (д, 2 Н, J=8,8 Гц), 7,97 (д, 2 Н, J=8,4 Гц), 7,95 (д, 1 Н, J=8,8 Гц), 7,89 (с, 1 Н), 7,43 (д, 2 Н, J=8,4 Гц), 7,67 (д, 2 Н, J=8,8 Гц), 7,53 (д, 2 Н, J=8,8 Гц), 3,63 (м, 4 Н), 2,84 (м,4 Н), 2,32 (с, 3 Н). ЖХ-МС m/z: 462,1 (М+1). Пример 2.(1,73 г, 15 ммоль) добавляют K2CO3 (4,14 г, 30 ммоль). Смесь нагревают при 50 С в течение ночи. После концентрирования остаток подвергают распределению между EtOAc и водой. Слой EtOAc сушат над безводным Na2SO4 и концентрируют с получением сырого продукта 6 в виде желтого твердого вещества. Сырой продукт используют непосредственно на следующей стадии без дополнительной очистки. ЖХ-МС m/z: 238,1 (М+1). Стадия 2. Указанное выше сырое вещество 6 гидрогенизируют в присутствии Pd-C (0,2 г) в МеОН(100 мл) в атмосфере водорода на протяжении 10 ч. Суспензию фильтруют через целит и фильтрат концентрируют с получением сырого продукта 7 в виде темно-коричневого масла, которое используют непосредственно на следующей стадии без дополнительной очистки. ЖХ-МС m/z: 208,1 (М+1). Стадия 3. К раствору 3-бром-4-метилбензойной кислоты (108 мг, 0,5 ммоль), 6-(2,6 диметилморфолин-4-ил)пиридин-3-иламина 7 (104 мг, 0,5 ммоль) и HATU (190 мг, 0,5 ммоль) в сухом ДМФ (5 мл) добавляют триэтиламин (139 мкл, 1,0 ммоль) по каплям. Полученную смесь перемешивают при комнатной температуре в течение 2 ч. После концентрирования остаток подвергают распределению между EtOAc и водой. Органический слой сушат и концентрируют с получением сырого продукта. Конечное соединение очищают моментальной колоночной хроматографией с применением 50% EtOAc в гексане в качестве элюента с получением 8 в виде белого твердого вещества. ЖХ-МС m/z: 404,1 (М+1). Стадия 4. Смесь 4-цианофенилбороновой кислоты (18 мг, 0,12 ммоль), 3-бром-N-[6-(2,6 диметилморфолин-4-ил)пиридин-3-ил]-4-метилбензамида 8 (40 мг, 0,1 ммоль), Pd(PPh3)4 (11 мг, 0,01 ммоль) и Na2CO3 (42 мг, 0,4 ммоль) в смеси растворителей из толуола (0,2 мл), воды (0,2 мл) и этанола(0,05 мл) нагревают при 140 С при микроволновом облучении в течение 30 мин. Реакционную смесь разбавляют EtOAc и водой. Водный слой экстрагируют EtOAc. Объединенный органический слой промывают насыщенным раствором соли и концентрируют с получением сырого продукта, который очищают препаративной управляемой по массе ВЭЖХ (колонка C18, элюция смесью CH3CN-H2O, содержащей 0,05% ТФУ) с получением 4'-циано-6-метилбифенил-3-карбоновой кислоты [6-(2,6 диметилморфолин-4-ил)пиридин-3-ил]амида. ЖХ-МС m/z: 427,2 (М+1). С помощью воспроизведения процедур, описанных в приведенных выше примерах, при применении соответствующих исходных веществ получают следующие указанные в таблице соединения формулы I.
МПК / Метки
МПК: C07D 213/75, A61P 35/00, C07D 401/04, C07C 233/65, C07D 413/04, C07D 295/135, C07D 295/26, C07D 239/49, A61K 31/4433, C07C 233/75, C07D 405/12, C07D 401/14, C07D 409/12
Метки: hedgehog, пути, качестве, соединения, модуляторов
Код ссылки
<a href="https://eas.patents.su/30-18302-soedineniya-v-kachestve-modulyatorov-puti-hedgehog.html" rel="bookmark" title="База патентов Евразийского Союза">Соединения в качестве модуляторов пути hedgehog</a>
Предыдущий патент: Фармацевтические композиции, содержащие антагонистическое моноклональное антитело к cd40, и их применение
Следующий патент: Способ управления передачей, передатчик, устройство обработки сигнала и базовая станция для системы связи
Случайный патент: Защитные вещества на основе производных ароматически-алифатических карбоновых кислот












