Пирроло[2,3-d]пиридины и их применение в качестве ингибиторов тирозинкиназы
Номер патента: 17952
Опубликовано: 30.04.2013
Авторы: Писсо-Зольдерманн Кароль, Гауль Кристоф, Гершпахер Марк, Хольцер Филипп
Формула / Реферат
1. Соединение формулы (I)
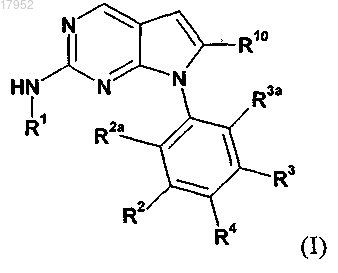
в которой
R1 обозначает фенил или пиридил, в каждом случае необязательно содержащий один или два заместителя, заместители выбранны из группы, включающей С1-С4-алкил, С1-С4-алкилоксигруппу, галоген, 4-метилпиперазин-1-илметил, 4-метилпиперазин-1-илкарбонил или 3,5-диметилпиперазин-1-ил;
R2 обозначает водород, фтор, хлор, метил;
R3 обозначает водород, фтор, хлор, метил;
R2a обозначает водород, фтор, хлор, метил;
R3a обозначает водород, фтор, хлор, метил;
R4 обозначает группу

в которой А1 обозначает одну из следующих групп:
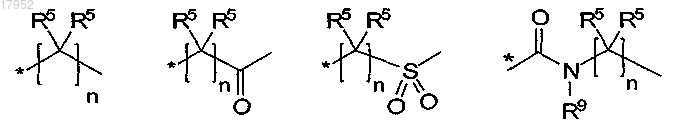
в которых атом, отмеченный значком *, обозначает связь с фенильным кольцом;
R5 независимо друг от друга обозначают водород, С1-С4-алкил, C1-С2-галогеналкил или циклопропил;
R6 и R7 вместе с атомом азота, к которому они присоединены, образуют необязательно замещенную морфолинильную группу, где указанные заместители выбраны из группы, включающей оксогруппу, гидроксигруппу, галоген, С1-С7-алкил, С1-С7-алкилоксигруппу, С1-С7-галогеналкил, С1-С7-галогеналкилоксигруппу, С3-С6-циклоалкил, С3-С6-циклоалкилоксигруппу, С3-С6-галогенциклоалкил, С3-С6-галогенциклоалкилоксигруппу, гидрокси-С1-С7-алкил, С1-С7-алкиламиногруппу, ди-С1-С7-алкиламиногруппу;
R9 обозначает Н или С1-С7-алкил;
R10 обозначает водород, C1-C4-алкил, С1-С2-галогеналкил или циклопропил;
n равно 0, 1 или 2;
или его соли.
2. Соединение формулы I по п.1, в которой
R2 обозначает водород, фтор, хлор, метил;
R2a обозначает водород;
R3 обозначает водород, фтор, хлор, метил;
R3a обозначает водород;
R10 обозначает водород или метил;
или его соль.
3. Соединение по п.1, выбранное из группы, включающей
{4-[7-(3,5-дифтор-4-морфолин-4-илметилфенил)-7Н-пирроло[2,3-d]пиримидин-2-иламино]фенил}-(4-метилпиперазин-1-ил)метанон;
{2-фтор-4-[2-(4-фторфениламино)пирроло[2,3-d]пиримидин-7-ил]фенил}морфолин-4-илметанон;
{4-[2-(4-фторфениламино)пирроло[2,3-d]пиримидин-7-ил]фенил}морфолин-4-илметанон;
4-[2-(4-фторфениламино)пирроло[2,3-d]пиримидин-7-ил]-N-(2-морфолин-4-илэтил)бензамид;
{2,6-дифтор-4-[2-(4-изопропоксифениламино)пирроло[2,3-d]пиримидин-7-ил]фенил}морфолин-4-илметанон;
2-{4-[2-(4-изопропоксифениламино)пирроло[2,3-d]пиримидин-7-ил]фенил}-2-метил-1-морфолин-4-илпропан-1-он;
(1-{4-[2-(4-изопропоксифениламино)пирроло[2,3-d]пиримидин-7-ил]фенил}циклопропил)морфолин-4-илметанон;
{2,6-дифтор-4-[2-(4-фтор-3-метилфениламино)пирроло[2,3-d]пиримидин-7-ил]фенил}морфолин-4-илметанон;
{2-хлор-4-[2-(4-фтор-3-метилфениламино)пирроло[2,3-d]пиримидин-7-ил]фенил}морфолин-4-илметанон;
{4-[2-(4-фтор-3-метилфениламино)пирроло[2,3-d]пиримидин-7-ил]-2-метилфенил}морфолин-4-илметанон;
{2-фтор-4-[2-(4-фтор-3-метилфениламино)пирроло[2,3-d]пиримидин-7-ил]фенил}морфолин-4-илметанон;
[7-(3-фтор-4-морфолин-4-илметилфенил)-7Н-пирроло[2,3-d]пиримидин-2-ил]-(4-изопропоксифенил)амин;
{2-фтор-4-[2-(4-изопропоксифениламино)пирроло[2,3-d]пиримидин-7-ил]фенил}морфолин-4-илметанон;
{2-хлор-4-[2-(4-изопропоксифениламино)пирроло[2,3-d]пиримидин-7-ил]фенил}морфолин-4-илметанон;
{4-[2-(4-изопропоксифениламино)пирроло[2,3-d]пиримидин-7-ил]-2-метилфенил}морфолин-4-илметанон;
2-{4-[2-(4-изопропоксифениламино)пирроло[2,3-d]пиримидин-7-ил]фенил}-1-морфолин-4-илэтанон;
(4-изопропоксифенил)-[7-(4-морфолин-4-илметилфенил)-7Н-пирроло[2,3-d]пиримидин-2-ил]амин;
[7-(3-хлор-4-морфолин-4-илметилфенил)-7Н-пирроло[2,3-d]пиримидин-2-ил]-(4-изопропоксифенил)амин;
(4-изопропоксифенил)-[7-(3-метил-4-морфолин-4-илметилфенил)-7Н-пирроло[2,3-d]пиримидин-2-ил]амин;
(4-изопропоксифенил)-{7-[4-(2-морфолин-4-илэтил)фенил]-7Н-пирроло[2,3-d]пиримидин-2-ил}амин;
{4-[2-(3-хлор-4-метилфениламино)пирроло[2,3-d]пиримидин-7-ил]-2,6-дифторфенил}морфолин-4-илметанон;
(3-хлор-4-метилфенил)-[7-(3-фтор-4-морфолин-4-илметилфенил)-7Н-пирроло[2,3-d]пиримидин-2-ил]амин;
(3-хлор-4-метилфенил)-[7-(4-морфолин-4-илметилфенил)-7Н-пирроло[2,3-d]пиримидин-2-ил]амин;
(4-фтор-3-метилфенил)-[7-(4-морфолин-4-илметилфенил)-7Н-пирроло[2,3-d]пиримидин-2-ил]амин;
[7-(3,5-дифтор-4-морфолин-4-илметилфенил)-7Н-пирроло[2,3-d]пиримидин-2-ил]-(4-изопропоксифенил)амин;
(4-фтор-3-метилфенил)-[7-(3-фтор-4-морфолин-4-илметилфенил)-7Н-пирроло[2,3-d]пиримидин-2-ил]амин;
(3-хлор-4-метилфенил)-[7-(3,5-дифтор-4-морфолин-4-илметилфенил)-7Н-пирроло[2,3-d]пиримидин-2-ил]амин;
[7-(3,5-дифтор-4-морфолин-4-илметилфенил)-7Н-пирроло[2,3-d]пиримидин-2-ил]-(4-фтор-3-метилфенил)амин;
[7-(3,5-дифтор-4-морфолин-4-илметилфенил)-7Н-пирроло[2,3-d]пиримидин-2-ил]-(4-метоксиметилфенил)амин;
1-морфолин-4-ил-2-[4-(2-п-толиламинопирроло[2,3-d]пиримидин-7-ил)фенил]этанон;
2-{4-[2-(4-фтор-3-метоксифениламино)пирроло[2,3-d]пиримидин-7-ил]фенил}-1-морфолин-4-илэтанон;
1-морфолин-4-ил-2-[4-(2-фениламинопирроло[2,3-d]пиримидин-7-ил)фенил]этанон;
[7-(4-морфолин-4-илметилфенил)-7Н-пирроло[2,3-d]пиримидин-2-ил]-п-толиламин;
(3,4-диэтоксифенил)-[7-(4-морфолин-4-илметилфенил)-7Н-пирроло[2,3-d]пиримидин-2-ил]амин;
{2-фтор-4-[2-(4-фтор-3-метоксифениламино)пирроло[2,3-d]пиримидин-7-ил]фенил}морфолин-4-илметанон;
{4-[2-(3,4-диметилфениламино)пирроло[2,3-d]пиримидин-7-ил]-2-фторфенил}морфолин-4-илметанон;
{2-фтор-4-[7-(3-фтор-4-морфолин-4-илметилфенил)-7Н-пирроло[2,3-d]пиримидин-2-иламино]фенил}-(4-метилпиперазин-1-ил)метанон;
(3,4-диметилфенил)-[7-(4-морфолин-4-илметилфенил)-7Н-пирроло[2,3-d]пиримидин-2-ил]амин;
(3,4-диметилфенил)-[7-(3-фтор-4-морфолин-4-илметилфенил)-6-метил-7Н-пирроло[2,3-d]пиримидин-2-ил]амин;
(4-фтор-3-метоксифенил)-[7-(3-фтор-4-морфолин-4-илметилфенил)-6-метил-7Н-пирроло[2,3-d]пиримидин-2-ил]амин;
2-{4-[2-(3,4-диметилфениламино)пирроло[2,3-d]пиримидин-7-ил]фенил}-1-морфолин-4-илэтанон;
(3,4-диэтоксифенил)-[7-(3-фтор-4-морфолин-4-илметилфенил)-6-метил-7Н-пирроло[2,3-d]пиримидин-2-ил]амин;
{4-[2-(3,4-диметилфениламино)пирроло[2,3-d]пиримидин-7-ил]фенил}морфолин-4-илметанон;
[7-(3,5-дифтор-4-морфолин-4-илметилфенил)-7Н-пирроло[2,3-d]пиримидин-2-ил]-[4-(4-метилпиперазин-1-илметил)фенил]амин;
[7-(3-хлор-4-морфолин-4-илметилфенил)-7Н-пирроло[2,3-d]пиримидин-2-ил]-(4-метоксиметилфенил)амин;
[7-(3-хлор-4-морфолин-4-илметилфенил)-7Н-пирроло[2,3-d]пиримидин-2-ил]-(3,4-диэтоксифенил)амин;
(4-изопропоксифенил)-{7-[4-(1-морфолин-4-илэтил)фенил]-7Н-пирроло[2,3-d]пиримидин-2-ил}амин (рацемический);
[7-(3,5-дифтор-4-морфолин-4-илметилфенил)-7Н-пирроло[2,3-d]пиримидин-2-ил]-[3-(4-метилпиперазин-1-илметил)фенил]амин;
(2,6-дифтор-4-{2-[4-(4-метилпиперазин-1-илметил)фениламино]пирроло[2,3-d]пиримидин-7-ил} фенил)морфолин-4-илметанон;
[7-(3,5-дифтор-4-морфолин-4-илметилфенил)-7Н-пирроло[2,3-d]пиримидин-2-ил]фениламин;
[7-(3,5-дифтор-4-морфолин-4-илметилфенил)-7Н-пирроло[2,3-d]пиримидин-2-ил]пиридин-2-иламин;
[7-(3,5-дифтор-4-морфолин-4-илметилфенил)-7Н-пирроло[2,3-d]пиримидин-2-ил]пиридин-3-иламин;
[7-(3,5-дифтор-4-морфолин-4-илметилфенил)-7Н-пирроло[2,3-d]пиримидин-2-ил]пиридин-4-иламин;
[2,6-дифтор-4-(2-фениламинопирроло[2,3-d]пиримидин-7-ил)фенил]морфолин-4-илметанон;
{2,6-дифтор-4-[2-(пиридин-2-иламино)пирроло[2,3-d]пиримидин-7-ил]фенил}морфолин-4-илметанон;
{2,6-дифтор-4-[2-(пиридин-3-иламино)пирроло[2,3-d]пиримидин-7-ил]фенил}морфолин-4-илметанон;
{2,6-дифтор-4-[2-(пиридин-4-иламино)пирроло[2,3-d]пиримидин-7-ил]фенил}морфолин-4-илметанон;
{2,6-дифтор-4-[2-(6-метилпиридин-3-иламино)пирроло[2,3-d]пиримидин-7-ил]фенил}морфолин-4-илметанон;
{2,6-дифтор-4-[2-(4-фтор-3-метилфениламино)пирроло[2,3-d]пиримидин-7-ил]фенил}морфолин-4-илметанон;
{2,6-дифтор-4-[2-(4-фтор-3-метилфениламино)пирроло[2,3-d]пиримидин-7-ил]фенил}морфолин-4-илметанон;
{4-[2-(5,6-диметилпиридин-2-иламино)пирроло[2,3-d]пиримидин-7-ил]-2-фторфенил}морфолин-4-илметанон;
{2,6-дифтор-4-[2-(4-фтор-3-метилфениламино)пирроло[2,3-d]пиримидин-7-ил]фенил}морфолин-4-илметанон;
{2-фтор-4-[2-(пиридин-3-иламино)пирроло[2,3-d]пиримидин-7-ил]фенил}морфолин-4-илметанон;
{2-фтор-4-[2-(6-метоксипиридин-3-иламино)пирроло[2,3-d]пиримидин-7-ил]фенил}морфолин-4-илметанон;
{2-фтор-4-[2-(6-изопропоксипиридин-3-иламино)пирроло[2,3-d]пиримидин-7-ил]фенил}морфолин-4-илметанон;
{4-[2-(4-изопропоксифениламино)пирроло[2,3-d]пиримидин-7-ил]фенил}морфолин-4-илметанон;
{4-[2-(6-изопропоксипиридин-3-иламино)пирроло[2,3-d]пиримидин-7-ил]фенил}морфолин-4-илметанон;
{4-[2-(3-фтор-4-метилфениламино)пирроло[2,3-d]пиримидин-7-ил]фенил}морфолин-4-илметанон;
{4-[2-(6-метоксипиридин-3-иламино)пирроло[2,3-d]пиримидин-7-ил]фенил}морфолин-4-илметанон;
{4-[2-(6-метилпиридин-3-иламино)пирроло[2,3-d]пиримидин-7-ил]фенил}морфолин-4-илметанон;
{4-[2-(4-метоксиметилфениламино)пирроло[2,3-d]пиримидин-7-ил]фенил}морфолин-4-илметанон;
{4-[2-(3-метокси-4-метилфениламино)пирроло[2,3-d]пиримидин-7-ил]фенил}морфолин-4-илметанон;
{2,6-дифтор-4-[2-(5-метилпиридин-3-иламино)пирроло[2,3-d]пиримидин-7-ил]фенил}морфолин-4-илметанон;
(2,6-дифтор-4-{2-[3-(4-метилпиперазин-1-илметил)фениламино]пирроло[2,3-d]пиримидин-7-ил}фенил)морфолин-4-илметанон;
(4-{2-[6-(цис-3,5-диметилпиперазин-1-ил)пиридин-3-иламино]пирроло[2,3-d]пиримидин-7-ил}-2,6-дифторфенил)морфолин-4-илметанон;
[7-(3,5-дифтор-4-морфолин-4-илметилфенил)-7Н-пирроло[2,3-d]пиримидин-2-ил]-[6-(цис-3,5-диметилпиперазин-1-ил)пиридин-3-ил]амин;
(4-{2-[6-((2R,5S)-2,5-диметилпиперазин-1-ил)пиридин-3-иламино]пирроло[2,3-d]пиримидин-7-ил}-2,6-дифторфенил)морфолин-4-илметанон (рацемический);
[7-(3,5-дифтор-4-морфолин-4-илметилфенил)-7Н-пирроло[2,3-d]пиримидин-2-ил]-[6-((2R,5S)-2,5-диметилпиперазин-1-ил)пиридин-3-ил]амин (рацемический);
{4-[2-(3,4-диэтоксифениламино)-6-метилпирроло[2,3-d]пиримидин-7-ил]-2-фторфенил}морфолин-4-илметанон;
{2-фтор-4-[2-(4-морфолин-4-илметилфениламино)пирроло[2,3-d]пиримидин-7-ил]фенил}морфолин-4-илметанон;
[7-(3,5-дифтор-4-морфолин-4-илметилфенил)-7Н-пирроло[2,3-d]пиримидин-2-ил]-(3,4-диметилфенил)амин;
{4-[2-(3,4-диметилфениламино)пирроло[2,3-d]пиримидин-7-ил]-2-метилфенил}морфолин-4-илметанон;
{4-[2-(4-хлор-3-метоксифениламино)пирроло[2,3-d]пиримидин-7-ил]-2-фторфенил}морфолин-4-илметанон;
{4-[2-(4-фтор-3-метоксифениламино)пирроло[2,3-d]пиримидин-7-ил]-2-метилфенил}морфолин-4-илметанон;
4-[2-(3,4-диметилфениламино)пирроло[2,3-d]пиримидин-7-ил]-2-фтор-N-(2-морфолин-4-илэтил)бензамид;
{2-фтор-4-[2-(3-метокси-4-метилфениламино)пирроло[2,3-d]пиримидин-7-ил]фенил}морфолин-4-илметанон;
[7-(3,5-дифтор-4-морфолин-4-илметилфенил)-7Н-пирроло[2,3-d]пиримидин-2-ил]-(3-метокси-4-метилфенил)амин;
{7-[4-(3,3-диметилморфолин-4-илметил)-3,5-дифторфенил]-7Н-пирроло[2,3-d]пиримидин-2-ил}-(3,4-диметилфенил)амин;
[2-фтор-4-(2-п-толиламинопирроло[2,3-d]пиримидин-7-ил)фенил]морфолин-4-илметанон;
[7-(3,5-дифтор-4-морфолин-4-илметилфенил)-7Н-пирроло[2,3-d]пиримидин-2-ил]-п-толиламин;
(2-фтор-4-{2-[4-метил-3-(4-метилпиперазин-1-илметил)фениламино]пирроло[2,3-d]пиримидин-7-ил}фенил)морфолин-4-илметанон;
[7-(3,5-дифтор-4-морфолин-4-илметилфенил)-7Н-пирроло[2,3-d]пиримидин-2-ил]-[4-метил-3-(4-метилпиперазин-1-илметил)фенил]амин;
[7-(3,5-дифтор-4-морфолин-4-илметилфенил)-7Н-пирроло[2,3-d]пиримидин-2-ил]-[3-(цис-3,5-диметилпиперазин-1-илметил)-4-метилфенил]амин;
{4-[7-(3,5-дифтор-4-морфолин-4-илметилфенил)-7Н-пирроло[2,3-d]пиримидин-2-иламино]пиридин-2-ил}-(4-метилпиперазин-1-ил)метанон;
[7-(3,5-дифтор-4-морфолин-4-илметилфенил)-7Н-пирроло[2,3-d]пиримидин-2-ил]-[2-(4-метилпиперазин-1-илметил)пиридин-4-ил]-амин;
(4-{2-[4-метил-3-(4-метилпиперазин-1-илметил)фениламино]пирроло[2,3-d]пиримидин-7-ил}фенил)морфолин-4-илметанон;
{5-[7-(3,5-дифтор-4-морфолин-4-илметилфенил)-7Н-пирроло[2,3-d]пиримидин-2-иламино]-2-метилфенил}-(4-метилпиперазин-1-ил)метанон;
{5-[7-(3,5-дифтор-4-морфолин-4-илметилфенил)-7Н-пирроло[2,3-d]пиримидин-2-иламино]пиридин-2-ил}-(4-метилпиперазин-1-ил)метанон;
[7-(3,5-дифтор-4-морфолин-4-илметилфенил)-7Н-пирроло[2,3-d]пиримидин-2-ил]-[6-(4-метилпиперазин-1-илметил)пиридин-3-ил]амин;
4-(4-{2-[6-(цис-3,5-диметилпиперазин-1-ил)-5-метилпиридин-3-иламино]пирроло[2,3-d]пиримидин-7-ил}-2,6-дифторбензил)морфолин-3-он;
[5-хлор-6-(цис-3,5-диметилпиперазин-1-ил)пиридин-3-ил]-[7-(3,5-дифтор-4-морфолин-4-илметилфенил)-7Н-пирроло[2,3-d]пиримидин-2-ил]амин;
[4-хлор-3-(4-метилпиперазин-1-илметил)фенил]-[7-(3,5-дифтор-4-морфолин-4-илметилфенил)-7Н-пирроло[2,3-d]пиримидин-2-ил]амин;
[7-(3,5-дифтор-4-морфолин-4-илметилфенил)-7Н-пирроло[2,3-d]пиримидин-2-ил]-[6-(цис-3,5-диметилпиперазин-1-ил)-5-метоксипиридин-3-ил]амин;
(4-{2-[6-(цис-3,5-диметилпиперазин-1-ил)пиридин-3-иламино]пирроло[2,3-d]пиримидин-7-ил}-2-фторфенил)морфолин-4-илметанон;
[7-(3,5-дифтор-4-морфолин-4-илметилфенил)-7Н-пирроло[2,3-d]пиримидин-2-ил]-[6-(цис-3,5-диметилпиперазин-1-ил)-5-метилпиридин-3-ил]амин и
{3-фтор-4-[2-(4-изопропоксифениламино)пирроло[2,3-d]пиримидин-7-ил]фенил}морфолин-4-илметанон.
4. Соединение по п.1, которое представляет собой [7-(3,5-дифтор-4-морфолин-4-илметилфенил)-7Н-пирроло[2,3-d]пиримидин-2-ил]-[6-(цис-3,5-диметилпиперазин-1-ил)пиридин-3-ил]амин и имеет следующую структуру:
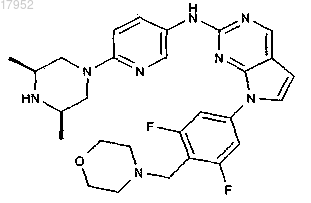
или его фармацевтически приемлемая соль.
5. Соединение по п.1, которое представляет собой {2-фтор-4-[2-(4-фтор-3-метоксифениламино) пирроло[2,3-d]пиримидин-7-ил]фенил}морфолин-4-илметанон, и имеет следующую структуру:
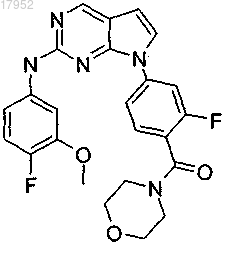
или его фармацевтически приемлемая соль.
6. Применение соединения формулы (I) по любому из пп.1-5 в свободной форме или в форме фармацевтически приемлемой соли для лечения одного или более заболевания, опосредуемого протеинтирозинкиназой.
7. Применение соединения формулы (I) по любому из пп.1-5 в свободной форме или в форме фармацевтически приемлемой соли для приготовления лекарственного средства, предназначенного для лечения одного или более заболевания, опосредуемого протеинтирозинкиназой.
8. Применение по п.6 или 7, где заболевания, опосредуемые протеинтирозинкиназой, выбраны из группы, включающей опухолевые заболевания, лейкозы, истинную полицитемию, эссенциальную тромбоцитемию, миелофиброз с миелоидной метаплазией, отторжение трансплантата органа, обыкновенную волчанку, рассеянный склероз, ревматоидный артрит, псориаз, дерматит, болезнь Крона, диабет типа 1 и осложнения при диабете типа 1.
9. Способ лечения заболевания, опосредуемого протеинтирозинкиназой, включающий стадию введения нуждающемуся в этом субъекту соединения формулы (I) по любому из пп.1-5 в свободной форме или в форме фармацевтически приемлемой соли в терапевтически эффективном количестве.
10. Способ лечения по п.8, где заболевания, опосредуемые протеинтирозинкиназой, выбраны из группы, включающей опухолевые заболевания, лейкозы, истинную полицитемию, эссенциальную тромбоцитемию, миелофиброз с миелоидной метаплазией, отторжение трансплантата органа, обыкновенную волчанку, рассеянный склероз, ревматоидный артрит, псориаз, дерматит, болезнь Крона, диабет типа 1 и осложнения при диабете типа 1.
11. Фармацевтическая композиция, включающая соединение формулы (I) по любому из пп.1-5 в свободной форме или в форме фармацевтически приемлемой соли в терапевтически эффективном количестве в качестве активного ингредиента; один или более фармацевтически приемлемых носителей и/или разбавителей.
12. Комбинированная фармацевтическая композиция, адаптированная для одновременного или последовательного введения, включающая соединение формулы (I )по любому из пп.1-5 в свободной форме или в форме фармацевтически приемлемой соли в терапевтически эффективном количестве; один или более компонентов комбинации в терапевтически эффективном (эффективных) количестве (количествах); один или более фармацевтически приемлемых носителей и/или разбавителей.
13. Способ получения соединения формулы (I) по любому из пп.1-5, включающий или
способ А) на первой стадии взаимодействие соединения формулы (II)
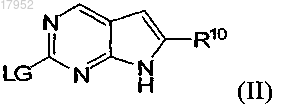
в которой заместители являются такими, как определено для соединения формулы (I), и LG обозначает отщепляющуюся группу, с соединением формулы (IV))
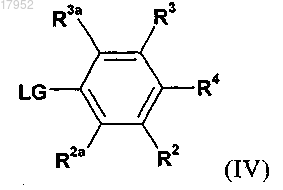
в которой заместители являются такими, как определено для соединения формулы (I), и LG обозначает отщепляющуюся группу, в катализируемой Cu реакции Бухвальда с получением соединения формулы (VI)
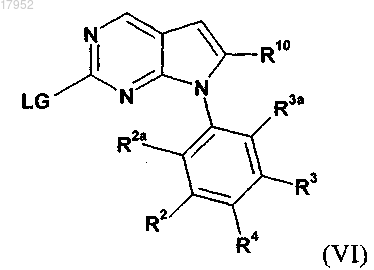
в которой заместители являются такими, как определено выше, и на второй стадии взаимодействие полученного соединения формулы (VI) с соединением формулы (III)
в которой R1 является таким, как определено для формулы (I), с получением соединения формулы (I); или
способ В) на первой стадии взаимодействие соединения формулы (II)
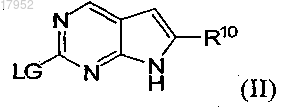
в которой заместители являются такими, как определено для соединения формулы (I), и LG обозначает отщепляющуюся группу, с соединением формулы (III)
в которой R1 является таким, как определено для соединения формулы (I), или в катализируемой Pd реакции Бухвальда, или в кислой среде, с получением соединения формулы (V)
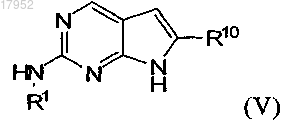
в которой заместители являются такими, как определено выше, и на второй стадии взаимодействие полученного соединения формулы (V) с соединением формулы (IV)
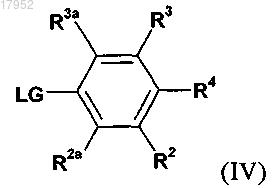
в которой заместители являются такими, как определено для соединения формулы (I) и LG обозначает отщепляющуюся группу, с получением соединения формулы (I);
и необязательно превращение соединения формулы (I), полученного способом А) или способом В), в другое соединение формулы (I), и/или превращение полученной соли соединения формулы (I) в другую его соль, и/или превращение полученного свободного соединения формулы (I) в его соль, и/или отделение полученного изомера соединения формулы (I) от одного или более других полученных изомеров формулы (I).
Текст
В патенте описаны соединения формулы (I) и их соли в которой заместители являются такими, как определено в описании, способы их получения,лекарственные препараты, содержащие такие соединения, в частности, предназначенные для применения при одном или более заболевании, опосредуемом протеинтирозинкиназой. 017952 Изобретение относится к 7-фенил-7 Н-пирроло[2,3d]пиримидин-2-иламинопроизводным формулы I,приведенной ниже, а также к их солям, к способам их получения, фармацевтической композиции, содержащей соединение формулы (I), необязательно в присутствии компонента комбинации, к применению соединения формулы (I) в способе лечения организма человека или животного (предпочтительно пролиферативного заболевания), к применению соединения формулы (I) для приготовления лекарственного средства, предназначенного для лечения таких заболеваний. Киназы Janus (JAK) образуют семейство внутриклеточных протеинтирозинкиназ, содержащее четыре представителя, JAK1, JAK2, JAK3 и TYK2. Эти киназы важны для опосредования путей сигналов цитокинового рецептора, которые индуцируют различные биологические ответы, включая пролиферацию, дифференциацию и апоптоз клеток. Эксперименты на мышах, у которых отсутствуют JAK, показали, что JAK, в частности, важны для гемопоэза. Кроме того, показано, что JAK2 участвует в миелопролиферативных заболеваниях и разных типах рака. Активация JAK2 при перегруппировке хромосом и/или потере негативных регуляторов пути JAK/STAT (STAT = фактор(ы) передачи и активации сигнала) обнаружены в гематологических злокачественных новообразованиях, а также в некоторых солидных опухолях. В WO 2005/080393, в частности, раскрыты 7 Н-пирроло[2,3d]пиримидин-2-иламинопроизводные,которые применимы для лечения заболеваний, связанных с аномальной или характеризующейся нарушенной регуляцией активностью киназы. В публикации BioorganicMedical Chemistry Letters 16 (2006), 2689 описана разработка и синтез некоторых 7 Н-пирроло[2,3d]пиримидинов в качестве ингибиторов киназы фокальной адгезии. Согласно изобретению было установлено, что 7-фенил-7 Н-пирроло[2,3d]пиримидин-2-иламинопроизводные формулы I, приведенной ниже, обладают благоприятными фармакологическими характеристиками и ингибируют, например, тирозинкиназную активность киназ Janus, таких как киназа JAK2 и/или киназа JAK3 (а также киназы JAK-1). Поэтому соединения формулы I являются подходящими, например,для применения для лечения заболеваний, зависящих от тирозинкиназной активности киназы JAK2(и/или JAK3), предпочтительно пролиферативных заболеваний, таких как опухолевые заболевания, лейкозы, истинная полицитемия, эссенциальная тромбоцитемия и миелофиброз с миелоидной метаплазией. Вследствие ингибирование киназы JAK-3 соединения, предлагаемые в настоящем изобретении, также применяются в качестве иммуносупрессивных средств, например, для лечения таких заболеваний, как отторжение трансплантата органа, обыкновенная волчанка, рассеянный склероз, ревматоидный артрит,псориаз, дерматит, болезнь Крона, диабет типа 1 и осложнения при диабете типа 1. Первым объектом настоящего изобретения являются соединения формулы IR1 обозначает фенил или пиридил, в каждом случае необязательно содержащий один или два заместителя, заместители выбранны из группы, включающей С 1-С 4-алкил, С 1-С 4-алкилоксигруппу, галоген, 4 метилпиперазин-1-илметил, 4-метилпиперазин-1-илкарбонил или 3,5-диметилпиперазин-1-ил; в которой А обозначает одну из следующих групп:R5 независимо друг от друга обозначают водород, С 1-С 4-алкил, С 1-С 2-галогеналкил или циклопроR6 и R7 вместе с атомом азота, к которому они присоединены, образуют необязательно замещенную морфолинильную группу, где указанные заместители выбраны из группы, включающей оксогруппу, гидроксигруппу, галоген, С 1-С 7 алкил, C1-C7-алкилоксигруппу, С 1-С 7-галогеналкил, С 1-С 7-галогеналкилоксигруппу, С 3-С 6-циклоалкил, С 3-С 6-циклоалкилоксигруппу, С 3-С 6-галогенциклоалкил, С 3-С 6-галогенциклоалкилоксигруппу, гидрокси-С 1-С 7-алкил, С 1-С 7 алкиламиногруппу, ди-С 1-С 7-алкиламиногруппу;n равно 0, 1 или 2; или их солям. Настоящее изобретение можно полнее понять с помощью приведенного ниже описания, включая приведенный ниже словарь терминов и последующие примеры. Для краткости укажем, что раскрытия публикаций, цитированных в настоящем описании, включены в настоящее изобретение в качестве ссылки. При использовании в настоящем изобретении термины "включая", "содержащий и "включающий" применяются в широком, не ограничительном смысле. Любая формула, приведенная в настоящем изобретении, предназначена для описания соединений,обладающих структурой, представленной структурной формулой, а также некоторых их вариантов и форм. В частности, соединения любой формулы, приведенной в настоящем изобретении, могут содержать асимметрические центры и поэтому существовать в разных энантиомерных формах. Если в соединении формулы I содержится по меньшей мере один асимметрический атом углерода, то такое соединение может существовать в оптически активной форме или в виде смеси оптических изомеров, например,в виде рацемической смеси. Все оптические изомеры и их смеси, включая рацемические смеси, входят в объем настоящего изобретения. Таким образом, любая конкретная формула, приведенная в настоящем изобретении, означает рацемат, одну или более энантиомерных форм, одну или более диастереоизомерных форм, одну или более атропоизомерных форм и их смеси. Кроме того, некоторые структуры могут существовать в виде геометрических изомеров (т.е. цис- и транс-изомеров), в виде таутомеров или в виде атропоизомеров. Кроме того, любая формула, приведенная в настоящем изобретении, характеризует гидраты, сольваты и полиморфные формы таких соединений и их смеси. Любая формула, приведенная в настоящем изобретении, также характеризует немеченые формы, а также изотопно-меченые формы соединений. Изотопно-меченые соединения обладают структурами,описывающимися формулами, приведенными в настоящем изобретении, за исключением того, что один или более атомов заменены на атомы, обладающими указанными атомными массами или массовыми числами. Примеры изотопов, которые можно вводить в соединения, предлагаемые в настоящем изобретении, включают изотопы водорода, углерода, азота, кислорода, фосфора, серы, фтора и хлора, такие как 2 Н, 3 Н, 11 С, 13 С, 14 С, 15N, 18F 31P, 32P, 35S, 36Cl, 125I соответственно. В объем настоящего изобретения входят различные изотопно-меченые соединения, предлагаемые в настоящем изобретении, например, в которые включены радиоактивные изотопы, такие как 3 Н, 13 С и 14 С. Такие изотопно-меченые соединения применимы для изучения метаболизма (предпочтительно содержащие 14 С), кинетики реакций (содержащие,например, 2 Н или 3 Н), в методологиях детектирования и визуализации [таких как позитронная эмиссионная томография (ПЭТ) или однофотонная эмиссионная компьютерная томография (ОФЭКТ), включая исследование распределения лекарственного средства или субстрата в тканях или лучевую терапию пациентов. В частности, содержащее 18F или меченое им соединение может быть особенно предпочтительным для исследований с помощью ПЭТ или ОФЭКТ. Кроме того, замещение более тяжелыми изотопами,такими как дейтерий (т.е. 2 Н), может обеспечить некоторые терапевтические преимущества, обусловленные их более высокой метаболической стабильностью, например увеличенной длительностью полувыведения in vivo или возможностью использования меньших доз. Изотопно-меченые соединения, предлагаемые в настоящем изобретении, и их пролекарства обычно можно получить по методикам, раскрытым на схемах или в примерах и синтезах, описанных ниже, путем замены не содержащего изотопа реагента на легко доступный изотопно-меченый реагент. Выбор значения конкретного фрагмента из перечня возможных значений при описании любой формулы, приведенной в настоящем изобретении, не означает задание значения этого фрагмента для остальной части настоящего описания. Другими словами, если переменная содержится более одного раза, то выбор ее значений из перечня значений не зависит от выбора значений этой переменной в формуле находящейся в другой части настоящего описания (где в вариантах осуществления одно или более и вплоть до всех более общих значений, охарактеризованных выше или ниже, как предпочтительные,можно заменить на более предпочтительное определение и таким образом образовать соответствующий более предпочтительный вариант осуществления настоящего изобретения). Если используется множественное число (например, соединения, соли), то она включает и единственное число (например, одно соединение, одну соль). Использование термина "соединение" не исключает того, что (например, в фармацевтическом препарате) содержится больше, чем одно соединение формулы I (или его соль). Соли присоединения с кислотами соединений формулы I предпочтительно представляют собой фармацевтически приемлемые соли. Такие соли известны в данной области техники. Если не указано иное, то в настоящем описании применимы указанные ниже общие определения. Галоген означает фтор, бром, хлор или йод, предпочтительно фтор, хлор. Галогензамещенные группы и фрагменты, такие как алкил, замещенный галогеном (галогеналкил), могут быть моно-, полиили пергалогенированными. Гетероатомы представляют собой атомы, не являющиеся атомами углерода и водорода, предпочти-2 017952 тельно азот (N), кислород (О) или серу (S). Углеродсодержащие группы, фрагменты или молекулы содержат от 1 до 8, предпочтительно от 1 до 6, более предпочтительно от 1 до 4, наиболее предпочтительно 1 или 2 атома углерода. Любая нециклическая углеродсодержащая группа или фрагмент, содержащий более 1 атома углерода, обладает линейной или разветвленной цепью. Приставка "низш." или "С 1-С 7" означает радикал, содержащий максимально до 7 включительно,предпочтительно максимально до 4 включительно атомов углерода, использующиеся радикалы являются линейными или разветвленными и содержат одно или несколько разветвлений."Алкил" означает обладающую линейной или разветвленной цепью алкильную группу, предпочтительно представляет собой обладающий линейной или разветвленной цепью С 1-С 12-алкил, особенно предпочтительно представляет собой обладающий линейной или разветвленной цепью C1-C7-алкил; например, метил, этил, н- или изопропил, н-, изо-, втор- или трет-бутил, н-пентил, н-гексил, н-гептил, ноктил, н-нонил, н-децил, н-ундецил, н-додецил, особенно предпочтительными являются метил, этил, нпропил, изопропил и н-бутил и изобутил. Алкил может быть незамещенным или замещенным. Типичные заместители включают, но не ограничиваются только ими, гидроксигруппу, алкоксигруппу, оксогруппу(т. е. =O), галоген и аминогруппу. Примером замещенного алкил является трифторметил. Циклоалкил также может быть заместителем алкила. Примером такого случая является фрагмент (алкил)циклопропил или алкандиилциклопропил, например, -СН 2-циклопропил. С 1-С 7-алкил предпочтительно представляет собой алкил, содержащий от 1 включительно до 7 включительно, предпочтительно от 1 включительно до 4 включительно атомов углерода, и является линейным или разветвленным; низш. алкил предпочтительно представляет собой бутил, такой как н-бутил, втор-бутил, изобутил, трет-бутил,пропил, такой как н-пропил или изопропил, этил или, предпочтительно, метил. Каждый алкильный фрагмент других групп, таких как "алкоксигруппа", "алкоксиалкил", "алкоксикарбонил", "алкоксикарбонилалкил", "алкилсульфонил", "алкилсульфинил", "алкиламиногруппа", "галогеналкил" обладает таким же значением, как указано в приведенном выше определении "алкила"."Алкандиил" означает обладающую линейной или разветвленной цепью алкандиильную группу, с помощью двух разных атомов углерода связанную с фрагментом, он предпочтительно представляет собой обладающий линейной или разветвленной цепью С 1-С 12-алкандиил, особенно предпочтительно представляет собой обладающий линейной или разветвленной цепью C1-С 6-алкандиил; например метандиил (-СН 2-), 1,2-этандиил (-СН 2-СН 2-), 1,1-этандиил (-СН(СН 3)-), 1,1-, 1,2-, 1,3-пропандиил и 1,1-, 1,2-,1,3-, 1,4-бутандиил, особенно предпочтительно метандиил, 1,1-этандиил, 1,2-этандиил, 1,3-пропандиил,1,4-бутандиил."Алкендиил" означает обладающую линейной или разветвленной цепью алкендиильную группу, с помощью двух разных атомов углерода связанную с молекулой, он предпочтительно представляет собой обладающий линейной или разветвленной цепью С 2-С 6-алкендиил; например, -СН=СН-, -СН=С(СН 3)-,-СН=СН-СН 2-,-С(СН 3)=СН-СН 2-,-СН=С(СН 3)-СН 2-,-СН=СН-С(СН 3)Н-,-СН=СН-СН=СН-,-С(СН 3)=СН-СН=СН-, -СН=С(СН 3)-СН=СН-, особенно предпочтительными являются -СН=СН-СН 2-,-СН=СН-СН=СН-. Алкендиил может быть замещенным или незамещенным."Циклоалкил" означает насыщенный или частично насыщенный моноциклический, конденсированный полициклический или спиросочлененный полициклический карбоцикл, содержащий от 3 до 12 кольцевых атомов в одном карбоцикле. Иллюстративные примеры циклоалкильных групп включают следующие фрагменты: циклопропил, циклобутил, циклопентил и циклогексил. Циклоалкил может быть незамещенным или замещенным; типичные заместители указаны в определении алкила."Арил" означает ароматическую гомоциклическую кольцевую систему, содержащую 6 или более атомов углерода; арил предпочтительно представляет собой ароматический фрагмент, содержащий от 6 до 14 кольцевых атомов углерода, более предпочтительно от 6 до 10 кольцевых атомов углерода, такую как фенил или нафтил, предпочтительно фенил. Арил может быть незамещенным или содержать один или более, предпочтительно до трех, более предпочтительно до двух заместителей, независимо выбранных из группы, включающей незамещенный или замещенный гетероциклил, описанный выше, предпочтительно пирролидинил, такой как пирролидиновую группу, оксопирролидинил, такой как оксопирролидиновую группу, С 1-С 7-алкилпирролидинил, 2,5-ди-(С 1-С 7-алкил)пирролидинил, такой как 2,5-ди-(С 1-С 7 алкил)-пирролидиновую группу, тетрагидрофуранил, тиофенил, С 1-С 7-алкилпиразолидинил, пиридинил,С 1-С 7-алкилпиперидинил, пиперидиновую группу, пиперидиновую группу, содержащую в качестве заместителей аминогруппу или N-моно- ИЛИ N,N-ди-[низш. алкил, фенил, С 1-С 7-алканоил и/или фенилнизш. алкил)аминогруппу, незамещенный или N-низш. алкилзамещенный пиперидинил, присоединенный через кольцевой атом углерода, пиперазиновую группу, низш. алкилпиперазиновую группу, морфолиновую группу, тиоморфолиновую группу, S-оксотиоморфолиновую группу или S,S-диоксотиоморфо линовую группу; С 1-С 7-алкил, амино-С 1-С 7-алкил, N-С 1-С 7-алканоиламино-С 1-С 7-алкил, N-С 1-С 7-алкан сульфониламино-С 1-С 7-алкил, карбамоил-С 1-С 7-алкил, [N-моно- или N,N-ди-(С 1-С 7-алкил)карбамоил]-С 1 С 7-алкил, С 1-С 7-алкансульфинил-С 1-С 7-алкил, С 1-С 7-алкансульфонил-С 1-С 7-алкил, фенил, нафтил, моно-три-[С 1-С 7-алкил, галоген и/или циано]фенил или моно- - три-[С 1-С 7-алкил, галоген и/или циано]нафтил; С 3-С 8-циклоалкил, моно- - три-[С 1-С 7-алкил и/или гидрокси]-С 3-С 8-циклоалкил; галоген, гидро-3 017952 ксигруппу, низш. алкоксигруппу, низш.-алкокси-низш. алкоксигруппу, (низш.-алкокси)-низш. алкоксинизш. алкоксигруппу, галоген-С 1-С 7-алкоксигруппу, феноксигруппу, нафтилоксигруппу, фенил- или нафтил-низш. алкоксигруппу; амино-С 1-С 7-алкоксигруппу, низш.-алканоилоксигруппу, бензоилоксигруппу, нафтоилоксигруппу, формил (СНО), аминогруппу, N-моно- или N,N-ди-(С 1-С 7-алкил)аминогруппу, С 1-С 7-алканоиламиногруппу, С 1-С 7-алкансульфониламиногруппу, карбоксигруппу, низш. алкоксикарбонил, например фенил- или нафтил-низш. алкоксикарбонил, такой как бензилоксикарбонил; С 1-С 7-алканоил, такой как ацетил, бензоил, нафтоил, карбамоил, N-моно- или N,N-дизамещенный карбамоил, такой как N-моно- или N,N-дизамещенный карбамоил, где заместители выбраны из группы, включающей низш. алкил, (низш.-алкокси)-низш. алкил и гидрокси-низш. алкил; амидиновую группу, гуанидиновую группу, уреидную группу, меркаптогруппу, низш. алкилтиогруппу, фенил- или нафтилтиогруппу, фенил- или нафтил-низш. алкилтиогруппу, низш. алкилфенилтиогруппу, низш. алкилнафтилтиогруппу, галоген-низш. алкилмеркаптогруппу, сульфогруппу (-SO3H), низш. алкансульфонил, фенил- или нафтилсульфонил, фенил- или нафтил-низш. алкилсульфонил, алкилфенилсульфонил, галоген-низш. алкилсульфонил, такой как трифторметансульфонил; сульфонамидную группу, бензосульфонамидную группу,азидную группу, азидо-С 1-С 7-алкил, предпочтительно азидометил, C1-С 7-алкансульфонил, сульфамоил,N-моно- или N,N-ди-(С 1-С 7-алкил)сульфамоил, морфолиносульфонил, тиоморфолиносульфонил, цианогруппу и нитрогруппу; где каждый фенил или нафтил (также в феноксигруппе или нафтоксигруппе), указанный выше в качестве заместителя или части заместителя замещенного алкила (или также замещенного арила, гетероциклила и т.п., указанного в настоящем изобретении), сам является незамещенным или содержит один или более, например до трех, предпочтительно 1 или 2 заместителя, независимо выбранных из группы, включающей галоген, галоген-низш. алкил, такой как трифторметил, гидроксигруппу,низш. алкоксигруппу, азидную группу, аминогруппу, N-моно- или N,N-ди-(низш. алкил и/или С 1-С 7 алканоил)аминогруппу, нитрогруппу, карбоксигруппу, низш.-алкоксикарбонил, карбамоил, цианогруппу и/или сульфамоил."Гетероциклил" означает гетероциклический радикал, который является ненасыщенным (= содержащим в кольце (кольцах) наибольшее возможное количество сопряженных двойных связей, т. е. гетероарил), насыщенным или частично насыщенным и предпочтительно представляет собой моноциклическое или, в более широком объекте настоящего изобретения, бициклическое, трициклическое или спиросочлененное полициклическое кольцо; и содержит от 3 до 24, более предпочтительно от 4 до 16, наиболее предпочтительно от 5 до 10 и наиболее предпочтительно 5 или 6 кольцевых атомов; где один или более, предпочтительно от 1 до 4, предпочтительно 1 или 2 кольцевых атома углерода заменены на гетероатом, присоединенное кольцо предпочтительно содержит от 4 до 12, предпочтительно от 5 до 7 кольцевых атомов. Гетероциклический радикал (гетероциклил) может быть незамещенным или содержать один или более, предпочтительно от 1 до 3 заместителей, независимо выбранных из группы, включающей заместители, определенных выше для замещенного алкила, и/или один или более следующих заместителей: оксогруппу (=О), тиокарбонил (=S), иминогруппу (=NH), имино-низш. алкил. Кроме того, гетероциклил предпочтительно представляет собой гетероциклильный радикал, выбранный из группы,включающей оксиранил, азиринил, азиридинил, 1,2-оксатиоланил, тиенил (= тиофенил), фуранил, тетрагидрофурил, пиранил, тиопиранил, тиантренил, изобензофуранил, бензофуранил, хроменил, 2 Нпирролил, пирролил, пирролинил, пирролидинил, имидазолил, имидазолидинил, бензимидазолил, пиразолил, пиразинил, пиразолидинил, тиазолил, изотиазолил, дитиазолил, оксазолил, изоксазолил, пиридил,пиразинил, пиримидинил, пиперидинил, пиперазинил, пиридазинил, морфолинил, тиоморфолинил, (Sоксогруппу или S,S-диоксо)тиоморфолинил, индолизинил, азепанил, диазепанил, предпочтительно 1,4 диазепанил, изоиндолил, 3 Н-индолил, индолил, бензимидазолил, кумарил, индазолил, триазолил, тетразолил, пуринил, 4 Н-хинолизинил, изохинолил, хинолил, тетрагидрохинолил, тетрагидризохинолил, декагидрохинолил, октагидризохинолил, бензофуранил, дибензофуранил, бензотиофенил, дибензотиофенил,фталазинил, нафтиридинил, хиноксалил, хиназолинил, хиназолинил, циннолинил, птеридинил, карбазолил, бета-карболинил, фенантридинил, акридинил, пиримидинил, фенантролинил, фуразанил, феназинил, фенотиазинил, феноксазинил, хроменил, изохроманил, хроманил, бензо[1,3]диоксол-5-ил и 2,3 дигидробензо[1,4]диоксин-6-ил, каждый из этих радикалов является незамещенным или содержит один или более, предпочтительно до трех, заместителей, выбранных из числа указанных выше для замещенного арила, и/или один или более следующих заместителей: оксогруппу (=O), тиокарбонил (=S), иминогруппу (=NH), имино-низш. алкил."Арилалкил" означает арильную группу, присоединенную к молекуле через алкильную группу, такую как метильную или этильную группу, предпочтительно фенетильную или бензильную, более предпочтительно бензильную. Аналогичным образом, циклоалкилалкил и гетероциклил означает циклоалкильную группу, присоединенную к молекуле через алкильную группу, или гетероциклильную группу,присоединенную к молекуле через алкильную группу. В каждом случае арил, гетероциклил, циклоалкил и алкил может быть замещенным, как определено выше."Лечение" включает профилактическое (предупредительное) и терапевтическое лечение, а также задержку прогрессирования заболевания или нарушения.JAK2 и/или JAK3 заболевания) предпочтительно представляют собой нарушения, которые реагируют благоприятным образом (например, происходит ослабление одного или более симптомов, задержка начала заболевания, вплоть до временного или полного излечивания заболевания) на ингибирование протеинтирозинкиназы, предпочтительно на ингибирование киназы JAK (предпочтительно JAK2 и/илиJAK3) или TYK2, более предпочтительно на ингибирование JAK2 (где из числа подвергающихся лечению заболеваний в особенности можно отметить пролиферативные заболевания, такие как опухолевые заболевания, лейкозы, истинная полицитемия, эссенциальная тромбоцитемия и миелофиброз с миелоидной метаплазией) и/или киназы JAK3 (в этом случае в качестве предпочтительно подвергающихся лечению (например, путем иммуносупрессии) можно отметить такие заболевания, как отторжение трансплантата органа, обыкновенная волчанка, рассеянный склероз, ревматоидный артрит, псориаз, дерматит,болезнь Крона, диабет типа 1 и осложнения при диабете типа 1. Соли (то, что означает выражение "или его соли" или "или его соль") могут содержаться по отдельности или в смеси со свободным соединением формулы (I) и предпочтительно представляют собой фармацевтически приемлемые соли. Такие соли, например, образуются в виде солей присоединения с кислотами, предпочтительно с органическими или неорганическими кислотами, из соединений формулы I,содержащих основной атом азота, предпочтительно фармацевтически приемлемые соли. Подходящими неорганическими кислотами являются, например, галогенводородные кислоты, такие как хлористоводородная кислота, серная кислота или фосфорная кислота. Подходящими органическими кислотами являются, например, карбоновые кислоты или сульфоновые кислоты, такие как фумаровая кислота или метансульфоновая кислота. Для выделения и очистки также можно использовать фармацевтически неприемлемые соли, например пикраты или перхлораты. Для терапевтического применения используют только фармацевтически приемлемые соли или свободные соединения (если они применимы в виде фармацевтических препаратов), и поэтому они являются предпочтительными. Вследствие близкого родства новых соединений в свободной форме и в форме их солей, включая соли, которые можно использовать в качестве промежуточных продуктов, например, при очистке или идентификации новых соединений, любое указание на свободное соединение выше и ниже в настоящем изобретении следует понимать также и как указание на соответствующие соли, если это является подходящим или целесообразным."Комбинация" означает фиксированную комбинацию в одной разовой дозированной форме или набор компонентов для комбинированного введения, при котором соединение формулы I и компонент комбинации (например, другое лекарственное средство, как указано ниже, также называющееся, как "терапевтическое средство" или "совместно вводимое средство") можно независимо вводить одновременно или по отдельности через определенные промежутки времени, предпочтительно так, чтобы эти промежутки времени позволяли компонентам комбинации оказывать совместное, например, синергетическое воздействие. Термины "совместное введение" или "комбинированное введение" и т.п. при использовании в настоящем изобретении означают введение выбранного компонента комбинации одному нуждающемуся в нем субъекту (например, пациенту) и включают режимы лечения, при которых средства необязательно вводят одним и тем же путем или в одно и то же время. Термин "фармацевтическая комбинация" при использовании в настоящем изобретении означает препарат, полученный смешиванием или комбинированием более одного активного ингредиента, и включает фиксированные и нефиксированные комбинации активных ингредиентов. Термин "фиксированная комбинация" означает, что активные ингредиенты, например, соединение формулы I и компонент комбинации, оба вводят пациенту одновременно в виде одного объекта или дозы. Термин "нефиксированная комбинация" означает, что активные ингредиенты, например, соединение формулы I и компонент комбинации, оба вводят пациенту в виде отдельных объектов совместно, одновременно или последовательно без установленных временных ограничений и такое введение обеспечивает терапевтически эффективные содержания этих двух соединений в организме пациента. Последнее также относится к смешанному лечению, например введению трех или более активных ингредиентов. В предпочтительных вариантах осуществления, которые являются предпочтительными независимо,совместно или в любой комбинации или субкомбинации, настоящее изобретение относится к соединению формулы I в форме свободного основания или в форме соли присоединения с кислотой, в котором заместители являются такими, как определено в настоящем изобретении. В одном варианте осуществления настоящее изобретение относится к соединению формулы IA в которой заместители являются такими, как определено для соединения формулы I. В другом варианте осуществления настоящее изобретение относится к соединению формулы IB в которой заместители являются такими, как определено для соединения формулы I. В другом варианте осуществления настоящее изобретение относится к соединению формулы IC в которой заместители являются такими, как определено для соединения формулы I. В другом варианте осуществления настоящее изобретение относится к соединению формулы ID в которой заместители являются такими, как определено для соединения формулы I. В другом варианте осуществления настоящее изобретение относится к соединению формулы IE в которой заместители являются такими, как определено для соединения формулы I. В другом варианте осуществления настоящее изобретение относится к соединениям формулы (I), в которой R2a и R3a оба обозначают Н, т.е. этот вариант осуществления относится к соединениям формулы в которой R1 обозначает фенил или пиридил, в каждом случае необязательно содержащий один или два заместителя, заместители выбранны из группы, включающей С 1-С 4-алкил, С 1-С 4-алкилоксигруппу,галоген, 4-метилпиперазин-1-илметил, 4-метилпиперазин-1-илкарбонил или 3,5-диметилпиперазин-1-ил; в которой А 1 обозначает одну из следующих групп:R5 независимо друг от друга обозначают водород, С 1-С 4-алкил, C1-С 2-галогеналкил или циклопроR6 и R7 вместе с атомом азота, к которому они присоединены, образуют необязательно замещенную морфолинильную группу, где указанные заместители выбраны из группы, включающей оксогруппу, гидроксигруппу, галоген, С 1-С 7-алкил, С 1-С 7-алкилоксигруппу, С 1-С 7-галогеналкил, С 1-С 7-галогеналкилоксигруппу, С 3-С 6-пиклоалкил, С 3-С 6-никлоалкилоксигруппу, С 3-С 6-галогенциклоалкил, С 3-С 6-галогенциклоалкилоксигруппу, гидрокси-С 1-С 7-алкил, С 1-С 7-алкиламиногруппу, ди-С 1-С 7-алкиламиногруппу;-6 017952 или их солям. В другом варианте осуществления настоящее изобретение относится к соединению формулы I'А в которой заместители являются такими, как определено для соединения формулы I. В другом варианте осуществления настоящее изобретение относится к соединению формулы I'В в которой заместители являются такими, как определено для соединения формулы I. В другом варианте осуществления настоящее изобретение относится к соединению формулы I'С в которой заместители являются такими, как определено для соединения формулы I. В другом варианте осуществления настоящее изобретение относится к соединению формулы I'D в которой заместители являются такими, как определено для соединения формулы I. В другом варианте осуществления настоящее изобретение относится к соединению формулы I'Е в которой заместители являются такими, как определено для соединения формулы I. А 1 предпочтительно обозначает непосредственную связь, карбонил (-С(=О)-) или метандиил (-СН 2-). Настоящее изобретение также относится к фармацевтически приемлемым пролекарствам соединения формулы (I). Настоящее изобретение также относится к фармацевтически приемлемым метаболитам соединения формулы (I). Настоящее изобретение предпочтительно относится к соединениям формулы I, приведенным в примерах, а также к способам получения, описанным в настоящем изобретении. Соединения формулы I обладают ценными фармакологическими характеристиками, описанными выше и ниже в настоящем изобретении. Они ингибируют различные протеинтирозинкиназы и предпочтительно тирозинкиназу рецептора JAK2 и/или JAK3. Предпочтительно, если соединения формулы I более селективно ингибируют JAK2 и JAK3, чем киназы JAK1 и TYK2. Наиболее предпочтительно, если соединения формулы I более селективно ингибируют JAK2, чем другие киназы семейства JAK, т.е. предпочтительно, если селективность по отношению к JAK2 проявляется в большей степени, чем по отношению к киназам JAK1, JAK3 и TYK2. Предпочтительно, если соединения формулы I более селективно ингибируют JAK2, чем другие киназы, например, cMet, cKit, ALK и/или PDGFRa. Соединения формулы I обычно характеризуются значениями IC50 для ингибирования JAK2, находящимися в диапазоне от 0,003 до 2 мкмоль/л, предпочтительно от 0,003 до 1 мкмоль/л, более предпочтительно от 0,003 до 0,100 мкмоль/л, еще более предпочтительно от 0,003 до 0,050 мкмоль/л. Эффективность соединений, предлагаемых в настоящем изобретении, в качестве ингибиторов активности киназы JAK/TYK, можно продемонстрировать следующим образом (результаты приведены в конце описания). Все четыре киназы семейства киназ JAK/TYK используют в качестве очищенных рекомбинантных белков слияния GST, содержащих активные киназные домены. GST-JAK1(866-1154), GST-JAK3(8111124) и GST-TYK2(888-1187) экспрессируют и очищают с помощью аффинной хроматографии в биологическом отделении EPK. GST-JAK2(808-1132) получают от фирмы Invitrogen (Carlsbad, USA, 4288).-7 017952 Исследования киназ основаны на схеме анализе по сдвигу пятна фирмы Caliper с использованием систем LabChip 3000. Эта технология аналогична капиллярному электрофорезу и в ней используется обусловленное зарядом разделение субстрата и продукта в микрофлюидном чипе. Все реакции киназ проводят в 384-луночных микропланшетах для титрования при полном объеме реакционной смеси, равном 18 мкл. Планшеты для анализа готовят путем добавления исследуемого соединения по 0,1 мкл/лунка при подходящей для исследования концентрации, как это описано в разделе"приготовление разведений соединения". Реакции инициируют путем объединения 9 мкл субстратной смеси (содержащей пептид и АТФ (аденозинтрифосфат с 9 мкл разведения киназы. Реакционные смеси инкубируют в течение 60 мин при 30 С и реакции останавливают путем добавления 70 мкл останавливающего буфера (100 мМ Hepes (4-(2-гидроксиэтил)-1-пиперазинэтансульфоновая кислота), 5% ДМСО,0,1% реагента, образующего покрытие, 10 мМ ЭДТК (этилендиаминтетрауксусная кислота), 0,015% Brij 35). Во всех реакциях в качестве субстратов используют синтетические пептиды с флуоресцентной меткой. Пептид, полученный из последовательности IRS-1 (пептид IRS-1, FITC-Ahx-KKSRGDYMTMQIGNH2 (SEQ ID NO: 1); см. публикацию J. Biol. Chem. 268(33), 25146-51 (1993, используют для JAK1 иTYK2 и пептид под названием JAK3tide (FITC-GGEEEEYFELVKKKK-NH2 (SEQ ID NO: 2); Upstate (Millipore), Temecula, California, USA для JAK2 и JAK3. Конкретные условия проведения исследований описаны в табл. 1. Таблица 1. Условия проведения исследований отдельных киназ БСА - бычий сывороточный альбумин Смеси, в которых остановлены реакции, переносят в считывающее устройство Caliper LabChip 3000(Caliper Life Siciences, Mountain View, California, USA) и протекание каждой реакции исследуют путем определения отношения субстрат/продукт. Приготовление разведений соединения Исследуемые соединения растворяют в ДМСО (10 мМ) и переносят в плоскодонные или Vобразные пробирки Matrix объемом 1,4 мл, содержащие специальный двумерный матричный чип, с помощью отдельных устройств для каждого соединения. Номера этих чипов соответствуют идентификационным номерам отдельных соединений. Если исходные растворы не используются сразу, то их хранят при -20 С. Для проведения исследования флаконы размораживают и идентифицируют сканером и таким образом формируют рабочий лист, который используют при проведении последующих стадий обработки. Разведения соединений проводят в 96-луночных планшетах. Такая методика позволяет изучить максимально 40 отдельных исследуемых соединений при 8 концентрациях (одиночные значения), включая 4 соединения для сравнения. Схема разведения включает приготовление планшетов с предварительными разведениями, эталонных планшетов и планшетов для анализа. Планшеты с предварительными разведениями: в качестве планшетов с предварительными разведениями используют 96-луночные полипропиленовые планшеты. Готовят всего 4 планшета с предварительными разведениями, содержащих 10 исследуемых соединений, каждое в положениях планшета А 1 А 10, одно стандартное соединение в положении А 11 и один контроль - ДМСО в положении А 12. Все стадии разведения проводят с помощью робота HamiltonSTAR. Эталонные планшеты: 100 мкл разведений отдельных соединений, включая стандартное соедине-8 017952 ние и контроли 4 "планшетов с предварительными разведениями" переносят в 384-луночный "эталонный планшет", включая следующие концентрации: 1820, 564, 182, 54,6, 18,2, 5,46, 1,82 и 0,546 мкМ соответственно в 90 % ДМСО. Планшеты для анализа. Затем идентичные планшеты для анализа готовят путем перенесения пипетками по 100 нл каждого разведения соединений из "эталонных планшетов" в 384-луночные "планшеты для анализа". Затем соединения смешивают с 9 мкл исследуемых компонентов с добавлением 9 мкл фермента, соответствующего ступеням разведения 1:181, и получают конечные концентрации, равные 10, 3,0, 1,0, 0,3, 0,1, 0,03,0,01 и 0,003 мкМ соответственно. Приготовление эталонных планшетов проводят с помощью робота Matrix PlateMate Plus Matrix PlateMate Plus и репликацию планшетов для анализа проводят с помощью робота HummingBird. По данным этих исследований соединение, предлагаемое в настоящем изобретении, обладает терапевтической эффективностью, предпочтительно по отношению к нарушениям, зависящим от протеинкиназы, предпочтительно по отношению к пролиферативным заболеваниям, опосредуемым активностью киназы JAK/TYK. Исследования ядерной транслокации STAT. Альтернативно, активность соединений, предлагаемых в настоящем изобретении, в качестве ингибиторов пути JAK/STAT, можно продемонстрировать следующим образом (результаты приведены в конце описания). Обладающее средней производительностью (с использованием 96-луночных планшетов) автоматизированное исследование клеток с помощью флуоресцентной микроскопии Cellomics можно стандартным образом использовать для оценки функциональной активации киназ Janus (JAK) на основе ядерной транслокации их субстрата, переносчика сигнала и активатора транскрипции (STAT). За ядерной транслокацией можно следить в клетках НТ 1080 фибросаркомы, стабильно трансфицированных с помощьюSTAT1, слитого с зеленым флуоресцентным белком (GFP), или в клетках остеосаркомы U-2 OS, стабильно трансфицированных с помощью STAT5, слитого с зеленым флуоресцентным белком (GFP). Стимулирование клеток НТ 1080 интерфероном- (IFN-) приводит к зависимой от JAK1/JAK2 ядерной транслокации STAT1-GFP, тогда как стимулирование клеток U-2 OS рекомбинантным эритропоэтином человека(rhEpo) приводит к зависимой от JAK2 ядерной транслокации STAT5-GFP, которые обе можно количественно исследовать с помощью программного обеспечения Cellomics Cyto/NucTrans. Это исследование можно использовать для оценки ядерно-цитоплазматической разности (NCD) для STAT-GFP с использованием красителя Hoechst для определения границ ядра. Генерация клеток НТ 1080 фибросаркомы, стабильно экспрессирующих GFP-STAT1. Клетки НТ 1080 фибросаркомы можно получить у фирмы АТСС и вырастить в модифицированной среде Игла альфа с добавлением 10% ФТС (фетальная телячья сыворотка). Клетки можно трансфицировать посредством pEGFP-N2 STAT1 с использованием трансфицирующего реагента Fugene 6 в соответствии с инструкцией изготовителя. Через 24 ч после трансфекции среду можно заменить и провести отбор в 1 мг/мл растворе генетицина. Генерация клеток U2OS остеосаркомы, стабильно экспрессирующих STAT5a-GFP и EpoR. Клетки U-2 OS остеосаркомы можно получить у фирмы АТСС и вырастить в стандартной средеRPMI с добавлением 10% ФТС и 2 мМ L-глутамина. Клетки можно стабильно трансфицировать посредством STAT5a-GFP с использованием липофектомина в соответствии с инструкцией изготовителя. Через 24 ч после трансфекции среду можно заменить и провести отбор в 400 мкг/мл растворе генетицина. Затем клетки можно стабильно трансфицировать посредством EpoR с использованием липофектомина в соответствии с инструкцией изготовителя. Через 24 ч после трансфекции среду можно заменить и провести отбор в 100 мкг/мл растворе гигромицина В. Приготовление исходных растворов соединений. Соединения можно растворить в ДМСО с получением конечных исходных растворов при концентрации 10 мМ и хранить в виде аликвот при 4 С. Соединения можно предварительно развести в 100% ДМСО при концентрациях 10 мМ, 3 мМ 1 мМ, 0,3 мМ, 0,1 мМ, 0,03 мМ, 0,01 мМ и 0,003 мМ. Затем соединения можно развести в среде и по 50 мкл добавить к клеткам. Конечные концентрации исследуемого соединения могут быть равны 10 мкМ, 3 мкМ 1 мкМ, 0,3 мкМ, 0,1 мкМ, 0,03 мкМ, 0,01 мкМ и 0,003 мкМ и конечная концентрация ДМСО может равняться 0,1%. Исследование ядерной транслокации STAT-GFP с помощью Cellomics. Клетки НТ 1080 STAT1-GFP можно посеять при плотности 10000 клеток/лунка в черные с прозрачным дном 96-луночные планшеты Packard View-Plates. Через 16-24 ч клетки можно обработать в течение 2 ч с помощью 100 нг/мл IFN-, дважды промыть в предварительно нагретом ЗФФ (забуференный фосфатом физиологический раствор) и зафиксировать в 200 мкл предварительно нагретого фиксирующего раствора (ЗФФ, 3,7% формальдегид) в течение 10 мин. Планшеты можно дважды промыть с помощью 200 мкл ЗФФ и инкубировать, защитив от света, в 100 мкл окрашивающего ДНК раствора (ЗФФ, 0,5 мкг/мл Hoechst-33342) в течение 1 мин. Затем планшеты можно один раз промыть с помощью ЗФФ и в-9 017952 заключение в каждую лунку добавить 200 мкл ЗФФ. Затем планшеты, закрытые черной пленкой, можно или сразу считать, или хранить при 4 С для последующей визуализации. Если это является подходящим,то соединения можно добавить за 30 мин до стимуляции посредством IFN-. Клетки U-2 OS можно посеять при плотности 12000 клеток/лунка в черные с прозрачным дном 96 луночные планшеты Packard View-Plates. На следующий день среду можно удалить и заменить средой,содержащей разбавитель или исследуемые соединения при увеличивающихся концентрациях, и выдержать в течение 30 мин при 37 С. Затем клетки можно стимулировать в течение 1 ч путем добавления 10 мкл/лунка 50 Ед/мл rhEpo и получить 5 Ед/мл rhEpo в качестве конечной концентрации. После такой обработки клетки можно зафиксировать и обработать так, как описано выше. Исследование ядерной транслокации STAT1-GFP с помощью визуализации и анализа, проводимого посредством автоматической флуоресцентной микроскопии Cellomics. Планшеты можно считать с помощью автоматического флуоресцентного микроскопа для считывания планшетов Cellomics ArrayscanII, снабженного ртутно-ксеноновым источником белого света и инвертационным микроскопом Zeiss Axiovert, с использованием дихроично/эмиссионного фильтрующего куба XF100 и согласующих фильтров возбуждения, увеличения 10 и объектива с числовой апертурой,равной 0,3. Получение и анализ изображений можно провести по специальной методике, основанной на'Nuclear Translocation" Bioapplication. Для каждой клетки можно накапливать множество изображений(полей), пока не будут обработаны не менее 1000 клеток, с использованием 2 каналов: канал 1 (красительHoechst) = фокус + маска ядра, канал 2 (GFP) = количественное измерение сигналов в областях масок,описанное ниже. Ядра можно сначала идентифицировать на основе окрашивания красителем Hoechst и маски, сгенерированной для каждого ядра, которые затем служат в качестве образа для создания цикла(разрушенного внутренним 1 пикселем) и 3-широкопиксельного кольца подобного ожерелью (смещенного наружу 1 пикселем), в котором ядерная и цитоплазматическая интенсивность GFP, соответственно,количественно измеряется в соответствующем канале. Высокое качество полученных результатов анализа многочисленных измерений в клетке и разность интенсивностей GPF между ядерными и цитоплазматическими масками можно выбрать в качестве меры внутриклеточного перемещения GFP-STAT1. Полученные значения можно усреднить по всем клеткам лунки и получить одно значение и стандартное отклонение. Для получения значений IC50 ядерно-цитоплазматическую разность STAT-GFP для необработанных клеток можно использовать в качестве исходного значения и для определения выраженного в процентах увеличения ядерной транслокации использовать следующее уравнение: Значение в % = 100(NCD для предварительно обработанного и стимулированного соединения - NCD для необработанного)/(NCD ДМСО - предварительно обработанного и стимулированного - NCD для необработанного). По данным этих исследований соединения формулы (I) обычно ингибируют киназы JAK2 при концентрациях, находящихся в диапазоне 1-10000 нМ. Активность соединений формулы I также можно исследовать in vivo. Исследование JAK-2 in vivo. Исследование можно провести так, как описано в публикации G. Wernig, Т. Mercher, R. Okabe, R.L.Levine, В. Н. Lee, D.G. Gilliland, Blood First Edition paper, published online February 14, 2006; DOI 10,1182/blood-2005-12-4824. По данным этих исследований соединение формулы I, предлагаемое в настоящем изобретении, обладает терапевтической эффективностью, предпочтительно по отношению к нарушениям, зависимым от протеинкиназы, предпочтительно пролиферативным заболеваниям, опосредуемым активностью киназыJAK2. Кроме того, соединения, предлагаемые в настоящем изобретении, способны к ингибированию других протеинкиназ, таких как Tyk2, c-src, Flt-3, KDR и другие, системы исследований каждой из которых известны в данной области техники. Соединение формулы I можно вводить по отдельности или в комбинации с одним или большим количеством других терапевтических средств, возможная комбинированная терапия представляет собой прием фиксированной комбинации или введение соединения, предлагаемого в настоящем изобретении, и одного или более других терапевтических средств поочередно или независимо друг от друга, или комбинированное введение фиксированных комбинаций и одного или более других терапевтических средств. Соединение формулы I можно вводить независимо или дополнительно, предпочтительно для лечения опухоли, в комбинации с химиотерапией, лучевой терапией, иммунотерапией, хирургическим вмешательством, или использовать их комбинации. Также возможно применение длительной терапии в качестве вспомогательной терапии в контексте других стратегий лечения, описанных выше. Другими возможными методиками лечения являются терапия для поддержания состояния пациента после регрессии опухоли или даже профилактическая химиотерапия, например, для пациентов, находящихся в группе риска. Таким образом, соединение формулы I с успехом можно применять в комбинации с другими антипролиферативными соединениями. Такие антипролиферативные соединения включают, но не ограничиваются только ими, ингибиторы ароматазы; антиэстрогены; ингибиторы топоизомеразы I; ингибиторы- 10017952 топоизомеразы II; средства, активные по отношению к микротрубочкам; алкилирующие средства; ингибиторы гистондезацетилазы; соединения, которые индуцируют процессы дифференциации клеток; ингибиторы циклооксигеназы; ингибиторы ММР; ингибиторы mTOR; противоопухолевые антиметаболиты; соединения платины; соединения, предназначенные для избирательного воздействия/уменьшения активности протеин- или липидкиназы и другие антиангиогенные соединения; соединения, которые предназначены для избирательного воздействия/уменьшения или ингибирования активности протеин- или липидфосфатазы; агонисты гонадорелина; антиандрогены; ингибиторы метионинаминопептидазы; бисфосфонаты; модификаторы биологического ответа; антипролиферативные антитела; ингибиторы гепараназы; ингибиторы онкогенных изоформ Ras; ингибиторы теломеразы; ингибиторы протеосомы; соединения, применяющиеся при лечении злокачественных заболеваний крови; соединения, которые предназначены для уменьшения или ингибирования активности Flt-3; ингибиторы Hsp90, такие как 17-AAG (17 аллиламиногелданамицин, NSC330507), 17-DMAG (17-диметиламиноэтиламино-17-деметоксигелданамицин, NSC707545), IPI-504, CNF1010, CNF2024, CNF1010, выпускающиеся фирмой Conforma Therapeutics; темозоломид (ТЕМОДАЛ); ингибиторы кинезинового белка веретена, такие как SB715992 илиSB743921, выпускающиеся фирмой GlaxoSmithKline, или пентамидин/хлорпромазин, выпускающиеся фирмой CombinatoRx; ингибиторы МЕК, такие как ARRY142886, выпускающийся фирмой Array PioPharma, AZD6244, выпускающийся фирмой AstraZeneca, PD181461, выпускающийся фирмой Pfizer, лейковорин, средства, связывающие EDG, противолейкозные соединения, ингибиторы рибонуклеотидредуктазы, ингибиторы S-аденозилметиониндекарбоксилазы, антипролиферативные антитела и другие химиотерапевтические соединения. Кроме того, альтернативно или в дополнение их можно применять в комбинации с другими методиками борьбы с опухолями, включая хирургию, применение ионизирующего излучения, фотодинамическую терапию, имплантаты, например, совместно с кортикостероидами, гормонами, или их можно применять в качестве радиосенсибилизаторов. Кроме того, в противовоспалительное и/или антипролиферативное лечение включают комбинации с противовоспалительными лекарственными веществами. Также возможны комбинации с антигистаминными лекарственными веществами, бронхорасширяющими лекарственными веществами, нестероидными противовоспалительными средствами или антагонистами хемокиновых рецепторов. Термин "ингибитор ароматазы" при использовании в настоящем изобретении означает соединение,которое ингибирует продуцирование эстрогена, т. е. превращение субстратов андростендиона и тестостерона в эстрон и эстрадиол соответственно. Термин предпочтительно включает, но не ограничивается только ими, атаместан, экземестан и форместан и, предпочтительно, нестероидные соединения, предпочтительно аминоглютетимид, роглетимид, пироглютетимид, трилостан, тестолактон, кетоконазол, ворозол, фадрозол, анастрозол и летрозол. Экземестан можно вводить, например, в той форме, в которой он продается, например, под торговым названием АРОМАЗИН. Форместан можно вводить, например, в той форме, в которой он продается, например, под торговым названием ЛЕНТАРОН. Фадрозол можно вводить, например, в той форме, в которой он продается, например, под торговым названием АФЕМА. Анастрозол можно вводить, например, в той форме, в которой он продается, например, под торговым названием АРИМИДЕКС. Летрозол можно вводить, например, в той форме, в которой он продается, например, под торговым названием ФЕМАРА или ФЕМАР. Аминоглютетимид можно вводить, например, в той форме, в которой он продается, например, под торговым названием ОРИМЕТЕН. Комбинация, предлагаемая в настоящем изобретении, включающая химиотерапевтическое средство, которое представляет собой ингибитор ароматазы, является особенно подходящей для лечения гормонально-рецептороположительных опухолей, например опухолей молочной железы. Термин "антиэстроген" при использовании в настоящем изобретении относится к соединению, которое противодействует воздействию эстрогена на уровне эстрогенного рецептора. Термин включает, но не ограничивается только ими, тамоксифен, фулвестрант, ралоксифен и ралоксифенгидрохлорид. Тамоксифен можно вводить, например, в той форме, в которой он продается, например, под торговым названием НОЛВАДЕКС. Ралкосифенгидрохлорид можно вводить, например, в той форме, в которой он продается, например, под торговым названием ЭВИСТА. Фулвестрант можно приготовить так, как это раскрыто в US 4659516, или его можно вводить, например, в той форме, в которой он продается, например,под торговым названием ФАСЛОДЕКС. Комбинация, предлагаемая в настоящем изобретении, включающая хемотерапевтическое средство, которое представляет собой антиэстроген, является особенно полезной для лечения эстрогенных рецептороположительных опухолей, например, опухолей молочной железы. Термин "антиандроген" при использовании в настоящем изобретении относится к любому соединению, которое может ингибировать биологические воздействие андрогенных гормонов, и включает, но не ограничивается только ими, бикалутамид (КАСОДЕКС), который можно приготовить, например, так, как это раскрыто в US 4636505. Термин "агонист гонадорелина" при использовании в настоящем изобретении включает, но не ограничивается только ими, абареликс, госерелин и госерелинацетат. Госерелин раскрыт в US 4100274 и его можно вводить, например, в той форме, в которой он продается, например, под торговым названием ЗОЛАДЕКС. Абареликс можно приготовить, например, так, как это раскрыто в US 5843901.- 11017952 Термин "ингибитор топоизомеразы I" при использовании в настоящем изобретении включает, но не ограничивается только ими, топотекан, гиматекан, иринотекан, камптотецин и его аналоги, 9 нитрокамптотецин и макромолекулярный конъюгат камптотецина PNU-166148 (соединение А 1 в WO 99/17804). Иринотекан можно вводить, например, в той форме, в которой он продается, например, под торговым названием КАПМТОСАР. Топотекан можно вводить, например, в той форме, в которой он продается, например, под торговым названием ГИКАМТИН. Термин "ингибитор топоизомеразы II" при использовании в настоящем изобретении включает, но не ограничивается только ими, антрациклины, такие как доксорубицин (включая липосомную композицию, например, КАЕЛИКС), даунорубицин, эпирубицин, идарубицин, неморубицин, антрахиноны митоксантрон и лозоксантрон и подофиллотоксины этопозид и тенипозид. Этопозид можно вводить, например, в той форме, в которой он продается, например, под торговым названием ЭТОПОФОС. Тенипозид можно вводить, например, в той форме, в которой он продается, например, под торговым названиемVM 26-БРИСТОЛ. Доксорубицин можно вводить, например, в той форме, в которой он продается, например, под торговым названием АДРИБЛАСТИН или АДРИАМИЦИН. Эпирубицин можно вводить,например, в той форме, в которой он продается, например, под торговым названием ФАРМОРУБИЦИН. Идарубицин можно вводить, например, в той форме, в которой он продается, например, под торговым названием ЗАВЕДОС. Митоксантрон можно вводить, например, в той форме, в которой он продается,например, под торговым названием НОВАНТРОН. Термин "соединение, активное по отношению к микротрубочкам" относится к стабилизирующим микротрубочки, дестабилизирующим микротрубочки соединениям и ингибиторам полимеризации микротубулина и включая, но не ограничиваясь только ими, таксаны, например паклитаксел и доцетаксел; алкалоиды барвинка, например винбластин, предпочтительно винбластинсульфат, винкристин, предпочтительно винкристинсульфат и винорелбин, дискодермолиды, колхицин и эпотилоны и их производные,например эпотилон В или D или его производные. Паклитаксел можно вводить, например, в той форме, в которой он продается, например ТАКСОЛ. Доцетаксел можно вводить, например, в той форме, в которой он продается, например, под торговым названием ТАКСОТЕР. Винбластинсульфат можно вводить, например, в той форме, в которой он продается, например, под торговым названием ВИНБЛАСТИН R.P. Винкристинсульфат можно вводить, например, в той форме, в которой он продается, например, под торговым названием ФАРМИСТИН. Дискодермолид можно получить, например, так, как это раскрыто в US 5010099. Также включены производные эпотилона, которые раскрыты в WO 98/10121, US 6194181, WO 98/25929, WO 98/08849, WO 99/43653, WO 98/22461 и WO 00/31247. Особенно предпочтительными являются эпотилон А и/или В. Термин "алкилирующиее соединение" при использовании в настоящем изобретении включает, но не ограничивается только ими, циклофосфамид, ифосфамид, мелфалан и нитрозомочевину (BCNU или глиадел). Циклофосфамид можно вводить, например, в той форме, в которой он продается, например,под торговым названием ЦИКЛОСТИН. Ифосфамид можно вводить, например, в той форме, в которой он продается, например, под торговым названием ГОЛОКСАН. Термин "ингибиторы гистондезацетилазы" или "ингибиторы HDAC" относится к соединениям, которые ингибируют гистондезацетилазу и которые обладают антипролиферативной активностью. Они включают соединения, раскрытые в WO 02/22577, предпочтительно N-гидрокси-3-[4-(2-гидроксиэтил)[2-(1H-индол-3-ил)этил]амино]метил]фенил]-2E-2-пропенамид, N-гидрокси-3-[4-2-(2-метил-1H-индол 3-ил)этил]амино]метил]фенил]-2E-2-пропенамид и их фармацевтически приемлемые соли. Они также предпочтительно включают субероиланилид гидроксамовой кислоты (САГА). Термин "противоопухолевый антиметаболит" включает, но не ограничивается только ими, 5 фторурацил, или 5-FU, капецитабин, гемцитабин, деметилирующие ДНК соединения, такие как 5 азацитидин и децитабин, метотрексат и эдатрексат, и антагонисты фолиевой кислоты, такие как пеметрексед. Капецитабин можно вводить, например, в той форме, в которой он продается, например, под торговым названием КСЕЛОДА. Гемцитабин можно вводить, например, в той форме, в которой он продается, например, под торговым названием ГЕМЗАР. Термин "соединение платины" при использовании в настоящем изобретении включает, но не ограничивается только ими, карбоплатин, цисплатин, цисплатинум и оксалиплатин. Карбоплатин можно вводить, например, в той форме, в которой он продается, например, под торговым названием КАРБОПЛАТ. Оксалиплатин можно вводить, например, в той форме, в которой он продается, например, под торговым названием ЭЛОКСАТИН. Термин "соединения, избирательно действующие/уменьшающие активность протеин- или липидкиназы"; или "активности протеин- или липидфосфатазы"; или "другие антиангиогенные соединения" при использовании в настоящем изобретении включает, но не ограничивается только ими, ингибиторы протеинтирозинкиназы и/или серин- и/или треонинкиназы или липидкиназы, например:a) соединения, избирательно действующие, уменьшающие или ингибирующие активность рецепторов тромбоцитарного фактор роста (PDGFR), такие как соединения, которые избирательно действуют,уменьшают или ингибируют активность PDGFR, предпочтительно соединения, которые ингибируют рецептор PDGF, например производное N-фенил-2-пиримидинамина, например иматиниб, SU101,- 12017952b) соединения, избирательно действующие, уменьшающие или ингибирующие активность рецепторов фактора роста фибробластов (FGFR);c) соединения, избирательно действующие, уменьшающие или ингибирующие активность рецептора инсулиноподобного фактора роста I (IGF-IR), такие как соединения, которые избирательно действуют,уменьшают или ингибируют активность IGF-IR, предпочтительно соединения, которые ингибируют активность киназы рецептора IGF-I, такие как соединения, раскрытые в WO 02/092599, или антитела, которые избирательно действуют на внеклеточный домен рецептора IGF-I или его факторы роста;d) соединения, избирательно действующие, уменьшающие или ингибирующие активность семейства тирозинкиназ рецептора Trk, или ингибиторы эфрина В 4;e) соединения, избирательно действующие, уменьшающие или ингибирующие активность семейства тирозинкиназ рецептора Axl;f) соединения, избирательно действующие, уменьшающие или ингибирующие активность тирозинкиназы рецептора Ret;g) соединения, избирательно действующие, уменьшающие или ингибирующие активность тирозинкиназы рецептора Kit/SCFR, например иматиниб;h) соединения, избирательно действующие, уменьшающие или ингибирующие активность тирозинкиназ рецептора C-kit - (часть семейства PDGFR), такие как соединения, которые избирательно действуют, уменьшают или ингибируют активность семейства тирозинкиназ рецептора c-Kit, предпочтительно соединения, которые ингибируют рецептор c-Kit, например иматиниб;i) соединения, избирательно действующие, уменьшающие или ингибирующие активность представителей семейства с-Abl, продуктов их слияния с генами (например, BCR-Abl киназы) и мутантов, такие как соединения, которые избирательно действуют, уменьшают или ингибируют активность представителей семейства с-Abl и продуктов их слияния с генами, например производное N-фенил-2-пиримидинамина, например, иматиниб или нилотиниб (AMN107); PD180970; AG957; NSC 680410; PD173955, выпускающийся фирмой ParkeDavis; или дасатиниб (BMS-354825).j) соединения, избирательно действующие, уменьшающие или ингибирующие активность представителей семейства протеинкиназ С (PKC) и семейства Raf серин/треонинкиназ MEK, SRC, JAK, FAK,PDK1, PKB/Akt, и представителей семейства Ras/MAPK, и/или представителей семейства циклинзависимых киназ (CDK) и в особенности производные стауроспорина, раскрытые в US 5093330, например, мидостаурин; примеры других соединений включают, например, UCN-01, сафингол, BAY 43-9006, бриостатин 1; перифосин; илмофосин; RO 318220 и RO 320432; GO 6976; Isis 3521; LY333531/LY379196; изохинолиновые соединения, такие как раскрытые в WO 00/09495; FTIs; PD184352 или QAN697 (ингибитор Р 13K) или АТ 7519 (ингибитор CDK);k) соединения, избирательно действующие, уменьшающие или ингибирующие активность ингибиторов протеинтирозинкиназы, включая иматинибмезилат (ГЛЕЕВЕК) и тирфостин. Тирофостин предпочтительно представляет собой соединение с низкой молекулярной массой (Mr1500) или его фармацевтически приемлемую соль, предпочтительно соединение, выбранное из группы, включающей класс бензилиденмалонитрилов или класс S-арилбензолмалонитрилов или класс бисубстратных хинолинов,более предпочтительно любое соединение, выбранное из группы, включающей тирфостин A23/RG50810; AG 99; тирфостин AG 213; тирфостин AG 1748; тирфостин AG 490; тирфостин В 44; тирфостин В 44 (+)-энантиомер; тирфостин AG 555; AG 494; тирфостин AG 556, AG957 и адафостин (адамантиловый эфир 4-[(2,5-дигидроксифенил)метил]аминобензойной кислоты; NSC 680410, адафостин);l) соединения, избирательно действующие, уменьшающие или ингибирующие активность семейства тирозинкиназ рецептора эпидермального фактора роста (EGFR, ErbB2, ErbB3, ErbB4 в виде гомо- или гетеродимеров) и их мутантов, такие как соединения, которые избирательно действуют, уменьшают или ингибируют активность семейства рецепторов эпидермального фактора роста, предпочтительно соединения, белки или антитела, которые ингибируют представителей семейства тирозинкиназ рецептораEGF, например, рецептора EGF, ErbB2, ErbB3 и ErbB4, или связываются с относящимися к EGF или EGF лигандами и предпочтительно являются такими соединениями, белками или моноклональными антителами, которые в общем и конкретно раскрыты в WO 97/02266, например, соединение примера 39, или в ЕР 0564409, WO 99/03854, ЕР 0520722, ЕР 0566226, ЕР 0787722, ЕР 0837063, US 5747498, WO 98/10767,WO 97/30034, WO 97/49688, WO 97/38983 и, в особенности, в WO 96/30347 (например, соединение, известное, как СР 358774), WO 96/33980 (например, соединение ZD 1839) и WO 95/03283 (например, соединение ZM105180); например, трастузумаб (герцептин), цетуксимаб (эрбутукс), иресса, тарцева,OSI-774, CI-1033, EKB-569, GW-2016, Е 1.1, Е 2.4, Е 2.5, Е 6.2, Е 6.4, E2.11, Е 6.3 или Е 7.6.3, и производные 7H-пирроло-[2,3-d]пиримидина, которые раскрыты в WO 03/013541; иm) соединения, избирательно действующие, уменьшающие или ингибирующие активность рецептора c-Met, такие как соединения, которые избирательно действуют, уменьшают или ингибируют активность рецептора с-Met, предпочтительно соединения, которые ингибируют киназную активность рецептора c-Met, или антитела, которые избирательно действуют на внеклеточный домен c-Met или связываются с HGF.- 13017952 Другие антиангиогенные соединения включают соединения, характеризующиеся другим механизмом своей активности, например, не относящейся к ингибированию протеин- или липидкиназы, например, талидомид (ТАЛОМИД) и TNP-470. Термин "соединения, которые избирательно действуют, уменьшают или ингибируют активность протеин- или липидфосфатазы", включает, но не ограничивается только ими, ингибиторы фосфатазы 1,фосфатазы 2 А или CDC25, например окадаевая кислота или ее производные. Термин "соединения, которые индуцируют процессы дифференциации клеток", включает, но не ограничивается только ими, ретиноевую кислоту, -, -или -токоферол или -, - или -токотриенол. Термин "ингибитор циклооксигеназы" при использовании в настоящем изобретении включает, но не ограничивается только ими, например ингибиторы Сох-2,5-алкилзамещенную 2-ариламинофенилуксусную кислоту и производные, такие как целекоксиб (ЦЕЛЕБРЕКС), рофекоксиб (ВИОКС), эторикоксиб, валдекоксиб и 5-алкил-2-ариламинофенилуксусная кислота, например 5-метил-2-(2'-хлор-6'фторанилино)фенилуксусная кислота и лумиракоксиб. Термин "бисфосфонаты" при использовании в настоящем изобретении включает, но не ограничивается только ими, этридоновую, клодроновую, тилудроновую, памидроновую, алендроновую, ибандроновую, риседроновую и золендроновую кислоту. "Этридроновую кислоту" можно вводить, например, в той форме, в которой она продается, например, под торговым названием ДИДРОНЕЛ. "Клодроновую кислоту" можно вводить, например, в той форме, в которой она продается, например, под торговым названием БОНЭФОС. "Тилудроновую кислоту" можно вводить, например, в той форме, в которой она продается,например, под торговым названием СКЕЛИД. "Памидроновую кислоту" можно вводить, например, в той форме, в которой она продается, например, под торговым названием АРЕДИА. "Алендроновую кислоту" можно вводить, например, в той форме, в которой она продается, например, под торговым названием ФОСАМАКС. "Ибандроновую кислоту" можно вводить, например, в той форме, в которой она продается, например, под торговым названием БОНДРАНАТ. "Риседроновую кислоту" можно вводить, например, в той форме, в которой она продается, например, под торговым названием АКТОНЕЛ. "Золендроновую кислоту" можно вводить, например, в той форме, в которой она продается, например, под торговым названием ЗОМЕТА. Термин "ингибиторы mTOR" относится к соединениям, которые ингибируют мишень воздействия рапамицина у млекопитающих (mTOR) и которые обладают антипролиферативной активностью, такие как сиролимус (рапамун), эверолимус (цертикан), CCI-779 и АВТ 578. Термин "ингибитор гепариназы" при использовании в настоящем изобретении означает соединения, которые избирательно действуют, уменьшают или ингибируют разложение гепаринсульфата. Термин включает, но не ограничивается только им, PI-88. Термин "модификатор биологического ответа" при использовании в настоящем изобретении означает лимфокин или интерфероны, например, интерферон . Термин "ингибитор онкогенных изоформ Ras", например, H-Ras, K-Ras, или N-Ras, при использовании в настоящем изобретении означает соединения, которые избирательно действуют, уменьшают или ингибируют онкогенную активность Ras, например, "ингибитор фарнезилтрансферазы", например L744832, DK8G557 или R115777 (зарнестра). Термин "ингибитор теломеразы" при использовании в настоящем изобретении означает соединения, которые избирательно действуют, уменьшают или ингибируют активность теломеразы. Соединения,которые избирательно действуют, уменьшают или ингибируют активность теломеразы, предпочтительно представляют собой соединения, которые ингибируют рецептор теломеразы, например теломестатин. Термин "ингибитор метионинаминопептидазы" при использовании в настоящем изобретении означает соединения, которые избирательно действуют, уменьшают или ингибируют активность метионинаминопептидазы. Соединения, которые избирательно действуют, уменьшают или ингибируют активность метионинаминопептидазы, представляют собой, например, бенгамид или его производное. Термин "ингибитор протеосомы" при использовании в настоящем изобретении означает соединения, которые избирательно действуют, уменьшают или ингибируют активность протеосомы. Соединения, которые избирательно действуют, уменьшают или ингибируют активность протеосомы, включают,например, бортезомид (велкаде) и MLN 341. Термин "ингибитор матричной металлопротеиназы" или "ингибитор ММР" при использовании в настоящем изобретении включает, но не ограничивается только ими, пептидомиметические и непептидомиметические ингибиторы коллагена, производные тетрациклина, например, пептидомиметический ингибитор гидроксамата - батимастат и его обладающий пероральной биологической доступностью аналог маримастат (ВВ-2516), приномастат (AG3340), метастат (NSC 683551) BMS-279251, BAY 12-9566,ТАА 211, MMI270B или AAJ996. Термин "соединения, применяющиеся при лечении злокачественных заболеваний крови" при использовании в настоящем изобретении включает, но не ограничивается только ими, FMS-подобные ингибиторы тирозинкиназы, например соединения, избирательно действующие, уменьшающие или ингибирующие активность рецепторов FMS-подобной тирозинкиназы (Flt-3R); интерферон, 1-b-D- 14017952 арабинофурансилцитозин (ara-с) и бисульфан; и ингибиторы ALK, например соединения, которые избирательно действуют, уменьшают или ингибируют киназы анапластической лимфомы. Соединения, которые избирательно действуют, уменьшают или ингибируют активность рецепторовFMS-подобной тирозинкиназы (Flt-3R), предпочтительно представляют собой соединения, белки или антитела, которые ингибируют представителей семейства тирозинкиназ рецептора Flt-3R, например,РКС 412, мидостаурин, производное стауроспорина, SU11248 и MLN518. Термин "ингибиторы HSP90" при использовании в настоящем изобретении включает, но не ограничивается только ими, соединения, которые избирательно действуют, уменьшают или ингибируют специфическую АТФазную активность HSP90; разрушают избирательно действуют, уменьшают или ингибируют клиентные белки HSP90 по убиквитиновому пути протеосомы. Соединения, избирательно действующие, уменьшающие или ингибирующие специфическую АТФазную активность HSP90, предпочтительно представляют собой соединения, белки или антитела, которые ингибируют специфическую АТФазную активность HSP90, например, 17-аллиламино,17-деметоксигелданамицин (17AAG), производное гелданамицина, другие родственные гелданамицину соединения, радицикол и ингибиторы HDAC. Термин "антипролиферативные антитела" при использовании в настоящем изобретении включает,но не ограничивается только ими, трастузумаб (герцептин), трастузумаб-DM1, эрбутукс, бевацизумаб(авастин), ритуксимаб (ритуксан ), PRO64553 (анти-CD40) и 2 С 4 антитела. Под антителами понимаются, например, интактные моноклональные антитела, поликлональные антитела, поливалентные антитела, сформированные по меньшей мере из двух интактных антител, и фрагменты антител, если они обладают необходимой биологической активностью. Для лечения острого миелолейкоза (ОМЛ) соединения формулы (I) можно использовать в комбинации со стандартными противолейкозными препаратами, предпочтительно в комбинации с препаратами,применяющимися для лечения ОМЛ. Предпочтительно соединения формулы (I) можно вводить в комбинации, например, с ингибиторами фарнезилтрансферазы и/или другими лекарственными препаратами,применяющимися для лечения ОМЛ, такими как даунорубицин, адриамицин, Ara-C, VP-16, тенипозид,митоксантрон, идарубицин, карбоплатин и PKC412. Термин "противолейкозные соединения" включает, например, Ara-С, аналог пиримидина, который представляет собой 2'-альфа-гидроксирибозное (арабинозид) производное дезоксицитидина. Также включен пуриновый аналог гипоксантина, 6-меркаптопурин (6-МР) и флударабинфосфат. Соединения, которые избирательно действуют, уменьшают или ингибируют активность ингибиторов гистондезацетилазы (HDAC), такие как бутират натрия и субероиланилид гидроксамовой кислоты(SAHA), которые ингибируют активность ферментов, известных, как гистондезацетилазы. Специфические ингибиторы HDAC включают MS275, SAHA, FK228 (ранее FR901228), трихостатин А и соединения, раскрытые в US 6552065, в частности N-гидрокси-3-[4-2-(2-метил-1H-индол-3-ил)этил]амино] метил]фенил]-2E-2-пропенамид или его фармацевтически приемлемую соль и N-гидрокси-3-[4-[(2 гидроксиэтил)[2-(1H-индол-3-ил)этил]амино]метил]фенил-2E-2-пропенамид или его фармацевтически приемлемую соль, предпочтительно лактат."Антагонисты соматостатинового рецептора" при использовании в настоящем изобретении означают соединения, которые избирательно действуют, уменьшают или ингибируют соматостатиновый рецептор, такие как октреотид и SOM230."Методики повреждения опухолевых клеток" представляют собой такие, как использующие ионизирующее излучение. Термин "ионизирующее излучение", использованный выше и ниже в настоящем изобретении, означает ионизирующее излучение, представляющее собой электромагнитное излучение(такое как рентгеновское излучение и гамма-излучение) или частицы (такие как альфа- и бета-частицы). Ионизирующее излучение применяется в лучевой терапии, но не ограничивается только ею, и известно в данной области техники. См публикацию Hellman, Principles of Radiation Therapy, Cancer, in Principles andPractice of Oncology, Devita et al., Eds., 4th Edition, Vol. 1, pp. 248-275 (1993). Термин "средства, связывающие EDG" при использовании в настоящем изобретении означает класс иммуносупрессивных средств, которые модулируют рециркуляцию лимфоцитов, такие как FTY720. Термин "ингибиторы рибонуклеотидредуктазы" означает аналоги пиримидиновых или пуриновых нуклеозидов, включая, но не ограничиваясь только ими, флударабин и/или цитозинарабинозид (ara-С), 6 тиогуанин, 5-фторурацил, кладрибин, 6-меркаптопурин (предпочтительно в комбинации с ara-С противALL) и/или пентостатин. Ингибиторы рибонуклеотидредуктазы предпочтительно являются гидроксимочевина или производные 2-гидрокси-1H-изоиндол-1,3-диона, такие как PL-1, PL-2, PL-3, PL-4, PL-5, PL6, PL-7 или PL-8, указанные в публикации Nandy et al., Acta Oncologica, Vol. 33, No. 8, pp. 953-961 (1994). Термин "ингибиторы S-аденозинметиониндекрабоксилазы" при использовании в настоящем изобретении включает, но не ограничивается только ими, соединения, раскрытые в US 5461076. Также включены, в частности, соединения, белки или моноклональные антитела к VEGF, раскрытые в WO 98/35958, например, 1-(4-хлоранилино)-4-(4-пиридилметил)фталазин или его фармацевтически приемлемая соль, например сукцинат, или в WO 00/09495, WO 00/27820, WO 00/59509, WO 98/11223,WO 00/27819 и ЕР 0769947; описанные в публикации Prewett et al, Cancer Res, Vol. 59, pp. 5209-5218WO 94/10202; АНГИОСТАТИН, описанный в публикации O'Reilly et al., Cell, Vol. 79, pp. 315-328 (1994); ЭНДОСТАТИН, описанный в публикации O'Reilly et al., Cell, Vol. 88, pp. 277-285 (1997); амиды антраниловой кислоты; ZD4190; ZD6474; SU5416; SU6668; бевацизумаб; или анти-VEGF антитела или антитела к рецептору анти-VEGF, например rhuMAb и RHUFab, аптамер VEGF, например, макугон; ингибиторы ингибиторы FLT-4, FLT-3, антитела к VEGFR-2 IgG1, ангиозим (RPI 4610) и бевацизумаб (Авастин)."Фотодинамическая терапия" при использовании в настоящем изобретении означает терапию, в которой используются некоторых вещества, известные, как фотосенсибилизирующие соединения, применяющиеся для лечения или предупреждения рака. Примеры фотодинамической терапии включают лечение такими соединениями, как, например, ВИЗУДИН и порфимер натрия."Ангиостатические стероиды" при использовании в настоящем изобретении означают соединения,которые блокируют или ингибируют ангиогенез, такие как, например, анекортав, триамцинолон, гидрокортизон, 11 эпигидрокортизол, кортексолон, 17-гидроксипрогестерон, кортикостерон, дезоксикортикостерон, тестостерон, эстрон и дексаметазон."Имплантаты, содержащие кортикостероиды" при использовании в настоящем изобретении включают, но не ограничиваются только ими, такие соединения, как, например, флуоцинолон, дексаметазон."Другие химиотерапевтические соединения" включают, но не ограничиваются только ими, растительные алкалоиды, гормональные соединения и антагонисты; модификаторы биологического ответа,предпочтительно лимфокины или интерфероны; антисмысловые олигонуклеотиды или производные олигонуклеотидов; shPHK или siPHK; или разные соединения, или соединения, обладающие другим или неизвестным механизмом действия. Соединения, предлагаемые в настоящем изобретении, также применимы в качестве совместно применяющихся терапевтических соединений, предназначенных для использования в комбинации с другими лекарственными веществами, такими как противовоспалительные, бронхорасширяющие или антигистаминные лекарственные вещества, предпочтительно для лечения воспалительных заболеваний, таких как указанные выше в настоящем изобретении, например, в качестве средств, усиливающих терапевтическую активность таких лекарственных средств, или в качестве средств, обеспечивающих снижение необходимой дозы или ослабление возможных побочных эффектов таких лекарственных средств. Соединение, предлагаемое в настоящем изобретении, можно смешивать с другим лекарственным веществом в фиксированной фармацевтической композиции или можно вводить отдельно, до, одновременно или после другого лекарственного вещества. В соответствии с этим настоящее изобретение относится к комбинации соединения, предлагаемого в настоящем изобретении, описанного выше в настоящем изобретении, с противовоспалительным или антигистаминным лекарственным веществом, указанное соединение,предлагаемое в настоящем изобретении, и указанное лекарственное вещество находятся в одной или в разных фармацевтических композициях. Подходящие противовоспалительные лекарственные средства включают стероиды, в частности,глюкокортикостероиды, такие как будезонид, бекламетазондипропионат, флутиказонпропионат, циклезонид или мометазонфуроат, или стероиды, описанные в WO 02/88167, WO 02/12266, WO 02/100879, WO 02/00679 (в особенности указанные в примерах 3, 11, 14, 17, 19, 26, 34, 37, 39, 51, 60, 67, 72, 73, 90, 99 и 101), WO 03/035668, WO 03/048181, WO 03/062259, WO 03/064445, WO 03/072592, нестероидные агонисты глюкокортикоидного рецептора, такие как описанные в WO 00/00531, WO 02/10143, WO 03/082280,WO 03/082787, WO 03/104195, WO 04/005229; антагонисты LTB4, такие как LY293111, CGS025019C,СР-195543, SC-53228, BIIL 284, ONO 4057, SB 209247 и описанные в US 5451700; антагонисты LTD4,такие как монтелукаст и зафирлукаст; ингибиторы PDE4, такие как циломиласт (арифло GlaxoSmithKline), рофлумиласт (Byk Gulden),V-11294A (Napp), BAY19-8004 (Bayer), SCH-351591 (Schering-Plough),арофиллин (Almirall Prodesfarma), PD189659 / PD168787 (Parke-Davis), AWD-12-281 (Asta Medica), CDC801 (Celgene), SelCID(TM) CC-10004 (Celgene), VM554/UM565 (Vernalis), T-440 (Tanabe), KW-4490(Kyowa Hakko Kogyo), и также описанные в WO 92/19594, WO 93/19749, WO 93/19750, WO 93/19751,WO 98/18796, WO 99/16766, WO 01/13953, WO 03/104204, WO 03/104205, WO 03/39544, WO 04/000814,WO 04/000839, WO 04/005258, WO 04/018450, WO 04/018451, WO 04/018457, WO 04/018465, WO 04/ 018431, WO 04/018449, WO 04/018450, WO 04/018451, WO 04/018457, WO 04/018465, WO 04/019944, WO 04/019945, WO 04/045607 и WO 04/037805; агонисты А 2 а, такие как раскрытые в ЕР 409595 А 2, ЕР 1052264, ЕР 1241176, WO 94/17090, WO 96/02543, WO 96/02553, WO 98/28319, WO 99/24449, WO 99/24450, WO 99/24451, WO 99/38877, WO 99/41267, WO 99/67263, WO 99/67264, WO 99/67265, WO 99/67266, WO 00/23457, WO 00/77018, WO 00/78774, WO 01/23399, WO 01/27130, WO 01/27131, WO 01/60835, WO 01/94368, WO 02/00676, WO 02/22630, WO 02/96462, WO 03/086408, WO 04/ 039762, WO 04/039766, WO 04/045618 и WO 04/046083; антагонисты А 2b, такие как описанные в WO 02/42298; и агонисты бета-2-адренорецептора, такие как албутерол (салбутамол), метапротеренол, тербуталин, салметерол, фенотерол, прокатерол и, предпочтительно, формотерол, кармотерол и их фармацевтически- 16017952 приемлемые соли, и соединения (в свободной форме или в форме соли, или сольвата) формулы I, указанные в WO 0075114, и этот документ включен в настоящее изобретение в качестве ссылки, предпочтительно соединения, указанные в приведенных в этой публикации примерах, предпочтительно соединение формулы и их фармацевтически приемлемые соли, а также соединения (в свободной форме или в форме соли,или сольвата) формулы I, указанные в WO 04/16601, и также соединения, указанные в WO 04/033412. Подходящие бронхорасширяющие лекарственные средства включают антихолинергические или антимускариновые средства, в частности ипратропийбромид, окситропийбромид, тиотропиевые соли иCHF 4226 (Chiesi), и гликопирролат, а также описанные в WO 01/04118, WO 02/51841, WO 02/53564, WO 03/00840, WO 03/87094, WO 04/05285, WO 02/00652, WO 03/53966, ЕР 424021, US 5171744, US 3714357,WO 03/33495 и WO 04/018422. Подходящие антигистаминные лекарственные средства включают цетиризингидрохлорид, ацетаминофен, клемастинфумарат, прометазин, лоратидин, деслоратидин, дифенилгидрамин и фексофенадингидрохлорид, активастин, астемизол, азеластин, эбастин, эпинастин, мизоластин и тефенадин, а также раскрытые в WO 03/099807, WO 04/026841 и JP 2004107299. Другими полезными комбинациями соединений, предлагаемых в настоящем изобретении, с противовоспалительными лекарственными средствами являются комбинации с антагонистами хемокиновых рецепторов, например CCR-1, CCR-2, CCR-3, CCR-4, CCR-5, CCR-6, CCR-7, CCR-8, CCR-9 и CCR10,CXCR1, CXCR2, CXCR3, CXCR4, CXCR5, в особенности с антагонистами CCR-5, такими как выпускающиеся фирмой Schering-Plough антагонисты SC-351125, SCH-55700 и SCH-D, выпускающиеся фирмой Takeda антагонисты, такие как N-4-6,7-дигидро-2-(4-метилфенил)-5H-бензоциклогептен-8 ил]карбонил]амино]фенил]метил]тетрагидро-N,N-диметил-2H-пиран-4-аминийхлорид (TAK-770), и антагонисты CCR-5, описанные в US 6166037 (в особенности в пп.18 и 19 формулы изобретения), WO 00/66558 (в особенности в пункте 8 формулы изобретения), WO 00/66559 (в особенности в п.9 формулы изобретения), WO 04/018425 и WO 04/026873. Терапевтические средства, предназначенные для возможных комбинаций предпочтительно представляют собой одно или более антипролиферативных, цитостатических или цитотоксических соединений, например одно или несколько средств, выбранных из группы, которая включает, но не ограничивается только ими, ингибитор биосинтеза полиамина, ингибитор протеинкиназы, предпочтительно серин/треонинпротеинкиназы, такой как протеинкиназа С, или тирозинпротеинкиназы, такой как тирозинкиназа рецептора EGF, например, иресса, тирозинкиназы рецептора VEGF, например, РТК 787 или авастин, или тирозинкиназы рецептора PDGF, например, STI571 (гливек), цитокин, негативный регулятор роста, такой как TGF- или IFN-, ингибитор ароматазы, например, летрозол (фемара) или анастрозол, ингибитор взаимодействия домена SH2 с фосфорилированным белком, антиэстрогены, ингибиторы топоизомеразы I, такие как иринотекан, ингибиторы топоизомеразы II, агенты, активные по отношению к микротрубочкам, например паклитаксел или эпотилон, алкилирующие агенты, антипролиферативные антиметаболиты, такие как гемцитабин или капецитабин, соединения платины, такие как карбоплатин или цисплатин, бисфосфонаты, например АРЕДИА или ЗОМЕТА, и моноклональные антитела,например, к HER2, такие как трастузумаб. Структура активных агентов, у которых имеются кодовые номера, родовые или торговые названия,приведена в последнем издании справочника "The Merck Index" и в базах данных, например, Patents International (например, IMS World Publications). Соответствующее их содержание включено в настоящее изобретение в качестве ссылки. Указанные выше соединения, которые можно использовать в комбинации с соединением формулыI, можно получить и вводить так, как описано в данной области техники, например, в цитированных выше документах. Таким образом, другим объектом настоящего изобретения является комбинация, включающая соединение формулы I в свободной форме или в форме фармацевтически приемлемой соли в терапевтически эффективном количестве и второе лекарственное вещество, предназначенная для одновременного или последовательного введения. Другим объектом настоящего изобретения также является фармацевтический препарат (композиция), включающий соединение формулы I, определенное в настоящем изобретении, или фармацевтически приемлемую соль такого соединения, или его гидрат или сольват и по меньшей мере один фармацевтически приемлемый носитель и/или разбавители и необязательно одно или более других лекарственных веществ. Соединения, предлагаемые в настоящем изобретении, можно вводить любым подходящим путем, в- 17017952 частности парентерально, например, в виде растворов или суспензий для инъекций, энтерально, например, перорально, например в виде таблеток или капсул, местно, например в виде лосьонов, гелей, мазей или кремов, или в назальной форме или в форме суппозитория. Местное нанесение проводят, например,на кожу. Другим путем местного введения является введение в глаза. Фармацевтические композиции,включающие соединение, предлагаемое в настоящем изобретении, совместно по меньшей мере с одним фармацевтически приемлемым носителем или разбавителем, можно приготовить по обычным методикам путем смешивания с фармацевтически приемлемым носителем или разбавителем. Настоящее изобретение также относится к фармацевтическим композициям, включающим эффективное количество, предпочтительно количество, эффективное для лечения одного из указанных выше заболеваний (= нарушений), соединения формулы I или его фармацевтически приемлемой соли вместе с одним или большим количеством фармацевтически приемлемых носителей, которые пригодны для местного, энтерального, например, перорального или ректального, или парентерального введения и которые могут быть неорганическими, органическими, твердыми или жидкими. Для перорального введения предпочтительно можно использовать таблетки или желатиновые капсулы, которые содержат активный ингредиент вместе с разбавителями, например лактозой, декстрозой, маннитом и/или глицерином, и/или смазывающими веществами, и/или полиэтиленгликолем. Таблетки также могут включать связующие,например, алюмосиликат магния, крахмалы, такие как кукурузный, пшеничный или рисовый крахмал,желатин, метилцеллюлозу, натриевую соль карбоксиметилецеллюлозы и/или поливинилпирролидон, и при необходимости разрыхлители, например крахмалы, агар-агар, альгиновую кислоту или ее соль, такую как альгинат натрия, и/или шипучие смеси, или адсорбенты, красители, вкусовые добавки и подсластители. Фармакологически активные соединения, предлагаемые в настоящем изобретении, также можно применять в виде композиций, вводимых парентерально, или в виде растворов для вливания. Фармацевтические композиции могут быть стерилизованы и/или могут содержать инертные наполнители, например консерванты, стабилизаторы, смачивающие соединения и/или эмульгаторы, солюбилизаторы, соли для регулирования осмотического давления и/или буферы. Фармацевтические композиции, предлагаемые в настоящем изобретении, которые при необходимости могут включать другие фармакологически активные вещества, готовят по известным методикам, например, с помощью обычных технологий смешивания, гранулирования, приготовления лекарственных препаратов, растворения или лиофилизации, и они содержат примерно от 1 до 99%, предпочтительно от примерно 1 до примерно 20% активного ингредиента (ингредиентов). Доза активного ингредиента, которую вводят теплокровному животному, зависит от множества факторов, включая тип, вид, возраст, массу тела и состояние здоровья пациента, тяжесть подвергающегося лечению патологического состояния, путь введения, функция почек и печени пациента и то, какое конкретное соединение используется. Врач, клиницист или ветеринар с общей подготовкой в данной области техники может без труда определить и назначить эффективное количество лекарственного средства, необходимое для предупреждения прогрессирования патологического состояния, противодействия ему или задержки его развития. Для оптимальной точности в подборе концентрации лекарственного средства в диапазоне, который обеспечивает эффективность без проявления токсичности, необходим режим, основанный на кинетике доступности лекарственного средства для центров воздействия. Для этого необходимо учитывать распределение, равновесие и выведение лекарственного средства. Доза соединения формулы I или его фармацевтически приемлемой соли, вводимая теплокровным животным, например, людям, обладающим массой тела около 70 кг, предпочтительно равна от примерно 3 мг до примерно 5 г, более предпочтительно от примерно 10 мг до примерно 1,5 г/сутки для одного пациента, предпочтительно разделенная на 1-3 разовые дозы, которые, например, могут быть одинаковыми. Детям обычно вводят половину от дозы для взрослого. Другим объектом настоящего изобретения является соединение формулы I или его фармацевтически приемлемая соль в качестве лекарственного средства/предназначенное для применения в качестве лекарственного средства, предпочтительно для лечения одного или более заболеваний, опосредуемых протеинтирозинкиназой. Другим объектом настоящего изобретения является применение соединения формулы I или его фармацевтически приемлемой соли, в качестве активного ингредиента в лекарственном средстве, предпочтительно предназначенного для лечения одного или более заболеваний, опосредуемых протеинтирозинкиназой. Другим объектом настоящего изобретения является применение соединения формулы I или его фармацевтически приемлемой соли в качестве лекарственного средства, предпочтительно предназначенного для лечения одного или более заболеваний, опосредуемых протеинтирозинкиназой. Другим объектом настоящего изобретения является применение соединения формулы I или его фармацевтически приемлемой соли для приготовления лекарственного средства, предназначенного для лечения одного или более заболеваний, опосредуемых протеинтирозинкиназой. Другим объектом настоящего изобретения является соединение формулы I или фармацевтически приемлемая соль такого соединения, предназначенное для применения в способе лечения нуждающегося в нем субъекта, предпочтительно лечения заболевания, опосредуемого протеинтирозинкиназой, наиболее- 18017952 предпочтительно у пациента, нуждающегося в таком лечении. Другим объектом настоящего изобретения является способ лечения заболевания, которое реагирует на ингибирование киназы JAK-2 и/или Jak-3, который включает введение соединения формулы I или его фармацевтически приемлемой соли, в которой радикалы и обозначения обладают указанными выше значениями, предпочтительно в количестве, эффективном для лечения такого заболевания, теплокровному животному, которому необходимо такое лечение. Другим объектом настоящего изобретения является фармацевтическая композиция, включающая соединение формулы I в качестве активного ингредиента вместе по меньшей мере с одним фармацевтическим носителем или разбавителем. Такие композиции можно приготовить по обычным методикам. Другим объектом настоящего изобретения является способ лечения одного или более заболеваний,опосредуемых протеинтирозинкиназой, у субъекта, нуждающегося в таком лечении, который включает введение такому субъекту соединения формулы I в терапевтически эффективном количестве. Другим объектом настоящего изобретения являются фармацевтические композиции, включающие:(а) соединение формулы I и его фармацевтически приемлемые соли, фармацевтически приемлемые пролекарства и фармацевтически активные метаболиты в эффективном количестве, и (b) один или более фармацевтически приемлемых носителей и/или разбавителей. Другим объектом настоящего изобретения является фармацевтическая композиция, предназначенная для лечения заболевания, например, солидных или несолидных (так называемых "жидких") опухолей у теплокровных животных, включая людей, включающая эффективную для лечения указанного заболевания дозу соединения формулы I, описанного выше, или фармацевтически приемлемой соли такого соединения вместе с фармацевтически приемлемым носителем (= материалом носителя). Соединение формулы I или I' можно получить способами, которые хотя не применялись ранее для получения новых соединений, предлагаемых в настоящем изобретении, когда они представляли бы собой новые способы, все же являются общеизвестными: приведенная ниже схема иллюстрирует способы такого получения. Предпочтительный способ получения соединения формулы I включает или способ а) на первой стадии взаимодействие соединения формулы II, в которой заместители являются такими, как определено для соединения формулы I, и LG обозначает отщепляющуюся группу (такую как тозилат, мезилат или галоген, предпочтительно хлор) с соединением формулы IV или IV в которой заместители являются такими, как определено для соединения формулы I, и LG обозначает отщепляющуюся группу (такую как тозилат, мезилат или галоген, предпочтительно бром) в катализируемой Cu реакции Бухвальда, с получением соединения формулы (VI) или (VI') в которой заместители являются такими, как определено выше, с соединением формулы I и на второй стадии взаимодействие полученного соединения формулы VI с соединением формулы (III) в которой R1 является таким, как определено для формулы I, с получением соединения формулы I; или способ В) на первой стадии взаимодействие соединения формулы II в которой заместители являются такими, как определено для соединения формулы I, и LG обозначает отщепляющуюся группу (такую как тозилат, мезилат или галоген, предпочтительно хлор), с соединением формулы III в которой R1 является таким, как определено для соединения формулы I, или в катализируемой Pd реакции Бухвальда, или в кислой среде, с получением соединения формулы (V) в которой заместители являются такими, как определено выше для соединения формулы I, и на второй стадии взаимодействие полученного соединения формулы V с соединением формулы IV в которой заместители являются такими, как определено для соединения формулы I, и LG обозначает отщепляющуюся группу (такую как тозилат, мезилат или галоген, предпочтительно бром), с получением соединения формулы I; и при необходимости превращение соединения формулы I, полученного способом А) или способом В), в другое соединение формулы I, и/или превращение полученной соли соединения формулы I в другую его соль, и/или превращение полученного свободного соединения формулы I в его соль, и/или отделение полученного изомера соединения формулы I от одного или более других полученных изомеров формулы I. Условия проведения реакций Когда выше или ниже в настоящем изобретении указаны значения температуры, к ним следует добавить слово "примерно", как указание на небольшие отклонения от приведенных числовых значений,например, допустимыми являются отклонения, составляющие 10%. Все реакции могут протекать в присутствии одного или более разбавителей и/или растворителей. Исходные вещества можно использовать в эквимольрных количествах; альтернативно, соединение можно использовать в избытке, например, в качестве растворителя или для смещения равновесия или для общего повышения скоростей реакций. Средства, способствующие протеканию реакций, такие как кислоты, основания или катализаторы, можно добавить в подходящих количествах, как это известно в данной области техники, необходимых для протекания реакции и в соответствии с общеизвестными методиками. Реакция Бухвальда Эта реакция, также известная, как аминирование по Бухвальду или реакция Бухвальда-Гартвига, в целом известна в данной области техники. Реакция катализируется переходными металлами, предпочтительно комплексами или солями Cu или Pd; протекает в присутствии одного или более основных соединений (таких как амин или алкоксид щелочного металла) и одного или более разбавителей (таких как полярные апротонные разбавители). Дополнительные подробности приведены в примерах. Защитные группы Если в исходном веществе, описанном в настоящем изобретении, или в любом другом предшественнике одну или более других функциональных групп, например карбоксигруппу, гидроксигруппу,аминогруппу сульфгидрил и т.п., необходимо снабдить защитной группой, поскольку они не должны принимать участие в реакции или влиять на реакцию, то ими являются защитные группы, которые обычно используются при синтезе пептидных соединений, а также цефалоспоринов и пенициллинов, а также производных нуклеиновых кислот и сахаров. Защитные группы являются такими группами, которые по- 20017952 сле удаления не должны содержаться в конечных соединениях, а группы, которые остаются в качестве заместителей, в использованном в настоящем описании смысле не являются защитными группами, которые вводят в исходное вещество или на промежуточной стадии и удаляют для получения конечного соединения. Также и в случае превращений соединения формулы I в другое соединение формулы I защитные группы можно вводить и удалять, если это целесообразно или необходимо. Защитные группы могут уже содержаться в предшественниках и должны защищать соответствующие функциональные группы от вступления в нежелательные вторичные реакции, такие как ацилирование, образование простого эфира, образование сложного эфира, окисление, сольволиз и аналогичные реакции. Особенностью защитных групп является то, что их можно легко, т.е. без нежелательных вторичных реакций, удалять, обычно с помощью ацетолиза, протолиза, сольволиза, восстановления, фотолиза, а также при воздействии ферментов, например, при условиях, аналогичных физиологическим условиям, и они не содержатся в конечных продуктах. Специалисту в данной области техники известно или он без труда может установить, какие защитные группы являются подходящими для проведения реакций, указанных выше и ниже. Защита таких функциональных групп с помощью таких защитных групп, сами защитные группы и реакции их удаления описаны, например, в стандартных справочниках, таких как J. F. W. McOmie, "Protective Groups in Organic Chemistry", Plenum Press, London and New York 1973, в Т. W. Greene, "ProtectiveChemie, Weinheim, Deerfield Beach, and Basel 1982 и в Jochen Lehmann, "Chemie der Kohlenhydrate: Monosaccharide und Derivate" (Chemistry of carbohydrates: monosaccharides and derivatives), Georg Thieme Verlag, Stuttgart 1974. Необязательные реакции и превращения Соединение формулы I можно превратить в другое соединение формулы I. Например, в соединении формулы I, в которой R1 или предпочтительно R4 содержит аминогруппу или амино-С 1-С 7-алкил в качестве заместителя, аминогруппу можно превратить в ациламиногруппу, например, C1-С 7-алканоиламиногруппу или С 1-С 7-алкансульфониламиногруппу, по реакции с соответствующим C1-C7-алканоилгалогенидом или С 1-С 7-алкансульфонилгалогенидом, например соответствующим хлоридом, в присутствии третичного азотистого основания, такого как триэтиламин или пиридин,при отсутствии или в присутствии подходящего растворителя, такого как метиленхлорид, например, при температурах в диапазоне от -20 до 50 С, например, примерно при комнатной температуре. В соединении формулы I, в которой R1 или предпочтительно R4 содержит цианогруппу в качестве заместителя, цианогруппу можно превратить в аминометильную группу, например, путем гидрирования в присутствии подходящего катализатора на основе метала, такого как никель Ренея или кобальт Ренея, в подходящем растворителе, например низш. алканоле, таком как метанол и/или этанол, например, при температурах в диапазоне от -20 до 50 С, например, примерно при комнатной температуре. В соединении формулы I, в которой R1 или предпочтительно R4 содержит карбоксигруппу (СООН) в качестве заместителя, последнюю можно превратить в амидную группу, например, N-С 1-С 7 алкилкарбамоильную группу по реакции с соответствующим амином, например, в присутствии реагента сочетания, который in situ образует предпочтительное реакционноспособное производное карбоксигруппы, например, с дициклогексилкарбодиимид/1-гидроксибензотриазолом (DCC/HOBT), хлорангидридом бис(2-оксо-3-оксазолидинил)фосфиновой кислоты (ВОРСl), O-(1,2-дигидро-2-оксо-1-пиридил)-N,N,N',N'тетраметилуронийтетрафторборатом(РуВОР), О-(1 Н-6-хлорбензотриазол-1-ил)-1,1,3,3-тетраметилуронийгексафторфосфатом, 1-(3-диметиламинопропил)-3-этилкарбодиимидгидрохлорид/гидроксибензотриазолом или 1-гидрокси-7-азабензотриазолом (EDC/HOBT или EDC/HOAt) или только с HOAt, или с (1-хлор-2-метилпропенил)диметиламином. Обзор по некоторым другим возможным реагентам сочетания приведен, например, в публикацииKlauser; Bodansky, Synthesis (1972), 453-463. Реакционную смесь предпочтительно перемешивают при температуре, равной примерно от -20 до 50 С, предпочтительно от 0 до 30 С, например, при комнатной температуре. В соединении формулы I, в которой R1 или предпочтительно R4 содержит две вицинальные аминогруппы, два атома азота этих двух аминогрупп могут быть связаны мостиковой группой -CH= (и тем самым вместе с двумя атомами углерода, которые связывают исходные аминогруппы, и связью между ними образовать 1H-имидазольное кольцо, аннелированное с R1 или R4); например, по этой методике вицинальный диаминофенил можно превратить в бензимидазолил. Реакция предпочтительно протекает путем проводимой сначала реакции соединения формулы I, содержащего две вицинальные аминогруппы, с муравьиной кислотой, например, в присутствии реагента сочетания, указанного в предыдущем абзаце, такого как этилкарбодиимидгидрохлорид, основания, такого как N,N-диметиламинопиридин (ДМАП), и предпочтительно в подходящем растворителе, таком как метиленхлорид, например, при температурах в- 21017952 диапазоне от -20 до 50 С, например, примерно при комнатной температуре, тем самым с превращением одной (предпочтительно расположенной в пара-положении) из вицинальных аминогрупп в формиламиногруппу. На второй стадии аминогруппу и формиламиногруппу вводят в реакцию с образованием-N=C-N- путем нагревания в присутствии кислоты, предпочтительно уксусной кислоты, например, при температурах в диапазоне от 50 до 110 С, например, примерно при 100 С. Соли соединения формулы I с солеобразующей группой можно получить по известным методикам. Так, соли присоединения соединений формулы I с кислотами можно получить обработкой кислотой или подходящим анионообменным реагентом. Соль с двумя молекулами кислоты (например, дигалогенид соединения формулы I) также можно превратить в соль с одной молекулой кислоты на молекулу соединения (например, моногалогенид); это можно выполнить путем нагревания до плавления или например,путем нагревания в виде твердого вещества в высоком вакууме при повышенной температуре, например,равной от 130 до 170 С, в результате чего из одной молекулы соединения формулы I удаляется одна молекула кислоты. Соли обычно можно превратить в свободные соединения, например, путем обработки подходящими основными соединениями, например, карбонатами щелочных металлов, гидрокарбонатами щелочных металлов или гидроксидами щелочных металлов, обычно карбонатом калия или гидроксидом натрия. Смеси стереоизомеров, например смеси диастереоизомеров, можно разделить на соответствующие изомеры по известным процедурам, с помощью подходящих методик разделения. Например, смеси диастереоизомеров можно разделить на индивидуальные диастереоизомеры с помощью фракционированной кристаллизации, хроматографии, распределения в растворителях и аналогичных методик. Это разделение можно проводить или для исходного соединения или для самого соединения формулы I. Энантиомеры можно разделить путем образования диастереоизомерных солей, например, путем образования соли с энантиомерно чистой хиральной кислотой или с помощью хроматографии, например, ВЭЖХ (высокоэффективная жидкостная хроматография), с использованием хроматографических субстратов, содержащих хиральные лиганды. Следует подчеркнуть, что реакции, аналогичные реакциям превращения, указанным в этом разделе,также можно проводить с подходящими промежуточными продуктами (и таким образом, они применимы для получения соответствующих исходных веществ). Исходные вещества. Исходные вещества формул II, III и IV, а также другие исходные вещества, указанные в настоящем изобретении, например, ниже, можно получить по методикам, которые известны в данной области техники, или по аналогичным методикам, или они имеются в продаже. Новые исходные вещества, а также способы их получения также являются вариантами осуществления настоящего изобретения. В предпочтительных вариантах осуществления используют такие исходные вещества и реакцию выбирают так,чтобы можно было получить предпочтительные соединения. В исходных веществах (включая промежуточные продукты), которые также можно использовать и/или получить в виде солей, если это является подходящим или целесообразным, заместители предпочтительно являются такими, как определено для соединения формулы I. Приведенные ниже примеры иллюстрируют настоящее изобретение без ограничения его объема. Температуры приведены в градусах Цельсия. Если не указано иное, то реакции проводят при комнатной температуре. Значения Rf в ТСХ являются отношениями расстояния, на которое переместилось каждое вещество,к расстоянию, на которое переместился фронт элюента. Значения Rf в ТСХ определяют на пластинах 510 см для ТСХ, силикагель F254, Merck, Darmstadt, Germany; системы растворителей в примерах отмечены следующим образом:10% метанол/90% метиленхлорид (CH2Cl2);5% метанол/95% метиленхлорид;2% метанол/98% метиленхлорид;50% гексан/50% этилацетат;66% гексан/33% этилацетат; Если не указано иное, то условия проведения аналитической ВЭЖХ являются следующими. Методика А. Колонка SunFire C18 204,6 мм, 3,5 мкм. Температура колонки 40 С. Элюенты А: Н 2 О, В: ацетонитрил, оба содержат 0,1% ТФК. Скорость потока 3,0 мл/мин. Градиентный режим 5-100% В за 4,0 мин. Методика В. Колонка Column Engineering, Inc., Matrix, 3 мкм С 18 1504,6 мм (Lot205). Детектирование по поглощению в УФ-области при длине волны, равной 215 и 254 нм.- 22017952 Температура колонки 35 С. Элюенты А: Н 2 О, В: ацетонитрил, оба содержат 0,1% ТФК. Скорость потока 1 мл/мин. Градиентный режим вода (0,1% ТФК)/ацетонитрил (0,1% ТФК) = 98/2 в течение 1 мин, затем до 100% ацетонитрила (0,1% ТФК) за 10 мин. Выдерживание при 100% в течение 2 мин (полная продолжительность цикла: 13 мин). Методика С. Колонка Macherey-Nagel СС 125/4 Nucleosil 100-3 С 18 HD. Температура колонки 30 С. Элюенты А: Н 2 О, В: ацетонитрил, оба содержат 0,1% ТФК. Скорость потока 1,0 мл/мин. Градиентный режим 2-100% В за 7,0 мин. Методика D. Колонка Macherey-Nagel СС 125/4 Nucleosil 100-3 С 18 HD. Температура колонки 30 С. Элюенты А: Н 2 О, В: ацетонитрил, оба содержат 0,1% ТФК. Скорость потока 1,0 мл/мин. Градиентный режим 20-100% В за 7,0 мин. Методика Е. Система Agilent 1100 Series с Waters Micromass ZQ. Колонка XBridge С 18, 330 мм, 2,5 мкм. Элюенты А: Н 2 О, содержащая 5% ацетонитрила и 0,8% НСООН. В: ацетонитрил, содержащий 0,6% НСООН. Скорость потока 1,4-2,4 мл/мин. Градиентный режим 10-95% В за 2,4 мин (Е 1) или 1-95% В за 2,9 мин (Е 2). Методика F. Колонка Macherey-Nagel СС 125/4 Nucleosil 100-3 С 18 HD. Температура колонки 30 С. Элюенты А: Н 2 О, В: ацетонитрил, оба содержат 0,1% ТФК. Скорость потока 1,0 мл/мин. Градиентный режим 2-100% В за 7,0 мин затем за 2 мин до 100% В. Методика G. Колонка Acquity UPLC ВЕН С 18/2,150 мм/1,7 мкм. Температура колонки 40 С. Элюенты А: Н 2 О, В: ацетонитрил, оба содержат 0,1% ТФК. Скорость потока 1,0 мл/мин. Градиентный режим в течение 0,1 мин 2% В; от 2 до 100% В за 1,5 мин; в течение 0,4 мин 100% В. Аббревиатуры АИБН - ,'-азо-изобутиронитрил;tR - время удерживания; УФ - ультрафиолетовое излучение. Исходные вещества. Различные арилбромиды и анилины, использующиеся в соответствии со схемами 1-3, закупали, если это было возможно. В противном случае арилбромиды и анилины/аминогетероциклы получали по приведенным в качестве примеров общим процедурам. Общая процедура I синтеза арилбромидных структурных элементов (в приведенной ниже формуле в качестве примера использован 2-(4-бромфенил)-1-морфолин-4-илэтанон): Соединение, приведенное выше слева, 2-(4-бромфенил)-1-морфолин-4-илэтанон, получают по реакции соответствующего хлорангидрида кислоты (А), (4-бромфенил)ацетилхлорида, с морфолином иEt3N в ДХМ при КТ. Получают продукт с высоким выходом. Промежуточный хлорангидрид кислоты (А) получают по реакции (4-бромфенил)уксусной кислоты (В) и оксалилхлорида (С) в ДХМ при КТ и с использованием ДМФ в качестве инициатора реакции. Промежуточный продукт (А) получают с хорошим выходом. Альтернативно, образования амидной связи можно провести путем сочетания подходящей карбоновой кислоты (В) и подходящего амина в присутствии HATU и N-метилморфолина в ДМФ при КТ. Следующие арилбромиды, использующиеся в приведенных ниже примерах, синтезируют аналогично с использованием подходящих исходных веществ: 2-(4-бромфенил)-1-(4-метилпиперазин-1-ил)этанон;(4-бром-3-фторфенил)морфолин-4-илметанон. Общая процедура II синтеза арилбромидных структурных элементов (в приведенной ниже формуле в качестве примера использован 4-(4-бром-2-метилбензил)морфолин): Соединение, приведенное выше слева, 4-(4-бром-2-метилбензил)морфолин, получают по реакции соответствующего бензилбромида (А), 4-бром-1-бромметил-2-метилбензола, с морфолином в ДМФ при КТ. Получают продукт с высоким выходом. Промежуточный бензилбромид (А) получают по реакции (4 бром-2-метилфенил)метанола (В) с PPh3 и CBr4 в ДХМ при КТ. Промежуточный продукт (А) получают с высоким выходом. Промежуточный бензиловый спирт В получают восстановлением соответствующей карбоновой кислоты (С), 4-бром-2-метилбензойной кислоты, посредством АГЛ в ТГФ. Промежуточный продукт (В) получают с хорошим выходом. Следующие арилбромиды, использующиеся в приведенных ниже примерах, синтезируют аналогично с использованием соответствующих подходящих исходных веществ: 4-(4-бром-2-фторбензил)морфолин; 4-(4-бром-2-хлорбензил)морфолин; 4-(4-бром-2-метилбензил)морфолин; 4-(4-бром-2,6-дифторбензил)морфолин; 4-[1-(4-бромфенил)этил]морфолин; 4-(6-бромпиридин-3-илметил)морфолин; 4-(5-бромпиридин-2-илметил)морфолин; 4-[2-(4-бромфенил)этил]морфолин; 1-(4-бром-2-фторбензил)-4-этилпиперазин; 1-(4-бром-2,6-дифторбензил)-4-этилпиперазин; 4-(4-бром-2,6-дифторбензил)-1-этилпиперазин-2-он; 1-[4-(4-бром-2,6-дифторбензил)пиперазин-1-ил]этанон; 4-(4-бром-2,6-дифторбензил)тиоморфолин 1,1-диоксид; 4-(4-бром-2-фторбензил)тиоморфолин 1,1-диоксид; 4-(4-бром-2-хлорбензил)тиоморфолин 1,1-диоксид; 1-(4-бром-2,6-дифторбензил)-4-метилпиперазин; 1-(4-бром-2,6-дифторбензил)-4-изопропилпиперазин; 1-(4-бром-2,6-дифторбензил)-4-циклопропилпиперазин; 4-(4-бром-2,6-дифторбензил)-3,3-диметилморфолин; 4-(4-бром-2,6-дифторбензил)-1-метилпиперазин-2-он; 4-(4-бром-2,6-дифторбензил)пиперазин-2-он; 8-(4-бром-2,6-дифторбензил)-2,5-диокса-8-азаспиро[3,5]нонан; 4-(4-бром-2,6-дифторбензил)цис-2,6-диметилморфолин; 1-(4-бром-2,6-дифторбензил)пирролидин-2-он; 1-(4-бром-2,6-дифторбензил)-3-метоксиазетидин; 4-(4-бром-2,6-дифторбензил)морфолин-3-он. Общая процедура III синтеза анилиновых структурных элементов (в приведенной ниже формуле в качестве примера использован (4-аминофенил)морфолин-4-илметанон). Соединение, приведенное выше слева, (4-аминофенил)морфолин-4-илметанон, получают гидрированием соответствующего нитросоединения (А), морфолин-4-ил-(4-нитрофенил)метанона, с помощьюPd/C или никеля Ренея и H2 или NH4CO2H в МеОН при КТ. Альтернативно, восстановление нитрогруппы можно провести с помощью SnCl2 в EtOH при 90 С. Промежуточное нитросоединение (А) получают по реакции 4-нитробензоилхлорида (В) и морфолина и Et3N в ДХМ при КТ. Промежуточный продукт (А) получают с хорошим выходом. При необходимости аналоги (В) получают из производных соответствующей карбоновой кислоты путем кипячения обратным холодильником в течение 2 ч с тионилхлоридом или оксалилхлоридом в ДХМ или дихлорэтане.- 25017952 Альтернативно, образования амидной связи можно провести путем сочетания подходящего производного карбоновой кислоты (В) и подходящего амина в присутствии TBTU и Et3N в ТГФ при температуре от 0 С до КТ. Следующие анилины, использующиеся в приведенных ниже примерах, синтезируют аналогично с использованием соответствующих подходящих исходных веществ: 4-амино-N-(1-метилпиперидин-4-ил)бензамид;(5-амино-2-метилфенил)-(цис-3,5-диметилпиперазин-1-ил)метанон. Общая процедура IV синтеза анилиновых структурных элементов (в приведенной ниже формуле в качестве примера использован (4-аминофенил)-(4-метилпиперазин-1-ил)метанон) Соединение, приведенное выше слева, (4-аминофенил)-(4-метилпиперазин-1-ил)метанон, получают путем обработки промежуточного продукта (А), трет-бутилового эфира [4-(4-метилпиперазин-1 карбонил)фенил]карбаминовой кислоты, посредством ТФК в ДХМ при КТ. Промежуточное соединение(А) получают путем сочетания 4-трет-бутоксикарбониламинобензойной кислоты (В) и N-метилпиперазина (С) в присутствии HATU и N-метилморфолина в ДХМ при КТ. Промежуточный продукт (А) получают с хорошим выходом. Использование защитной группы Вос не является необходимым для получения некоторых анилиновых структурных элементов. Следующие анилины, использующиеся в приведенных ниже примерах, синтезируют аналогично с использованием соответствующих подходящих исходных веществ: 4-амино-N-(2-диметиламиноэтил)-N-метилбензамид; 4-амино-N-(2-диметиламиноэтил)-бензамид; 4-амино-N-(2-гидроксиэтил)-бензамид;(5-аминопиридин-2-ил)-(4-метилпиперазин-1-ил)метанон; Общая процедура V синтеза анилиновых структурных элементов (в приведенной ниже формуле в качестве примера использован 3-(2-диметиламиноэтокси)-4-метоксифениламин): Соединение, приведенное выше слева, 3-(2-диметиламиноэтокси)-4-метоксифениламин, получают путем обработки промежуточного продукта (А), [2-(2-метокси-5-нитрофенокси)этил]диметиламина, посредством Pd/C и NH4CO2H в МеОН/ТГФ при КТ. Промежуточное соединение (А) получают алкилированием 2-метокси-5-нитрофенола (В) (2-хлорэтил)диметиламином (С) в присутствии NaH в ДМФ при 150 С. Следующие анилины, использующиеся в приведенных ниже примерах, синтезируют аналогично с использованием соответствующих подходящих исходных веществ: 3-(3-диметиламинопропокси)-4-метоксифениламин; 4-метокси-3-(2-пирролидин-1-илэтокси)фениламин; 4-метокси-3-(2-морфолин-4-илэтокси)фениламин; 3-(2-морфолин-4-илэтокси)-фениламин; 3-[2-(4-метилпиперазин-1-ил)этокси]фениламин; 3-(2-диэтиламиноэтокси)фениламин; 4-(2-диэтиламиноэтокси)фениламин; 4-(2-морфолин-4-илэтокси)фениламин; 4-(2-пирролидин-1-илэтокси)фениламин; 3,5-диметил-4-(2-морфолин-4-илэтокси)фениламин. Общая процедура VI синтеза анилиновых структурных элементов (в приведенной ниже формуле в качестве примера использован 4-(цис-3,5-диметилпиперазин-1-илметил)фениламин): Соединение, приведенное выше слева, 4-(цис-3,5-диметилпиперазин-1-илметил)фениламин, получают путем обработки промежуточного продукта (А), цис-3,5-диметил-1-(4-нитробензил)пиперазина,гидратом SnCl2 в МеОН при КТ. Альтернативно, восстановление нитрогруппы можно провести с помощью Pd/C или никеля Ренея и H2 или NH4CO2H в МеОН при КТ. Промежуточное соединение (А) получают по реакции цис-2,6-диметилпиперазина (В) с 1-бромметил-4-нитробензолом (С) в присутствии Et3N или ДИПЭА в ДМФ при КТ. При необходимости (замещенный) бензилбромид (С) синтезируют из соответствующей карбоновой кислоты (D) путем восстановления в спирт и превращения в галогенсодержащее соединение. Следующие анилины, использующиеся в приведенных ниже примерах, синтезируют аналогично с использованием соответствующих подходящих исходных веществ: 4-2R,5S)-2,5-диметилпиперазин-1-илметил)фениламин (рацемический); 4-(4-аминобензил)пиперазин-2-он; 4-(4,7-диазаспиро[2,5]окт-7-илметил)фениламин; трет-бутиловый эфир 4-(4-аминобензил)пиперазин-1-карбоновой кислоты; 1-[4-(4-аминобензил)пиперазин-1-ил]этанон; 4-(4-циклопропилпиперазин-1-илметил)фениламин; 4-метил-3-(4-метилпиперазин-1-илметил)фениламин; 4-метил-3-морфолин-4-илметилфениламин; 5-(4-этилпиперазин-1-илметил)пиридин-2-иламин; 4-метил-3-(4-метилпиперазин-1-илметил)фениламин; трет-бутиловый эфир 4-(5-амино-2-метилбензил)пиперазин-1-карбоновой кислоты; 4-(5-амино-2-метилбензил)-пиперазин-2-он; 4-(4-аминобензил)-1-метилпиперазин-2-он; 4-(4-метилпиперазин-1-илметил)фениламин; 3-(цис-3,5-диметилпиперазин-1-илметил)-4-метилфениламин; 3-(2,5-диокса-8-азаспиро[3,5]нон-8-илметил)-4-метилфениламин; 3-(4-циклопропилпиперазин-1-илметил)-4-метилфениламин;[1-(5-амино-2-метилбензил)пирролидин-3-ил]диметиламин; 3-(7-азабицикло[2.2.1]гепт-7-илметил)-4-метилфениламин; трет-бутиловый эфир 4-(4-амино-2-метилбензил)пиперазин-1-карбоновой кислоты; 4-(цис-3,5-диметилпиперазин-1-илметил)-3-метилфениламин; 4-(3,3-дифторпирролидин-1-илметил)фениламин; 6-(4-метилпиперазин-1-илметил)пиридин-3-иламин; 4-(3,3-диметилпиперазин-1-илметил)фениламин; 4-(3-трифторметилпиперазин-1-илметил)фениламин (рацемический); 4-(цис-3,5-диметилпиперазин-1-илметил)-2-фторфениламин; 1-(4-аминобензил)азетидин-3-ол; 6-морфолин-4-илметилпиридин-3-иламин; 6-пиперазин-1-илметилпиридин-3-иламин; 4-хлор-3-(4-метилпиперазин-1-илметил)фениламин; трет-бутиловый эфир 4-(4-аминобензил)-3-оксопиперазин-1-карбоновой кислоты; 4-(5-аминопиридин-2-илметил)-1-метилпиперазин-2-он; 4-(3-метоксипирролидин-1-илметил)фениламин; 1-(5-аминопиридин-2-илметил)пирролидин-3-ол (рацемический); 4-метил-3-(7-метил-2,7-диазаспиро[4,4]нон-2-илметил)фениламин; 4-метил-3-(4-метилпиразол-1-илметил)фениламин; 2-[1-(5-амино-2-метилбензил)-1 Н-пиразол-4-ил]этанол; Альтернативно, (А) получают по реакции 2-бромметил-1-метил-4-нитробензола (С) с азидом натрия в смеси этанол/вода 1:2 при КТ, проводимой в течение ночи, с последующим образованием триазола по реакции с диметилпроп-2-иниламином в смеси трет-бутанол/вода 1:1 в присутствии сульфата меди(I)[1-(5-амино-2-метилбензил)-1 Н-[1,2,3]триазол-4-ил]метанол. Альтернативно, (В) получают по реакции трет-бутилового эфира 3-оксопиперазин-1-карбоновой кислоты, активированного гидридом натрия, с (2-бромэтил)-диметиламином в ДМФ. Из полученного вещества с помощью HCl в диоксане удаляют защитную группу Boc и получают (В) в виде соли с HCl. 4-(5-Амино-2-метилбензил)-1-(2-диметиламиноэтил)-пиперазин-2-он. Общая процедура VII синтеза анилиновых структурных элементов (в приведенной ниже формуле в качестве примера использован 6-(цис-3,5-диметилпиперазин-1-ил)пиридин-3-иламин): Соединение, приведенное выше слева, 6-(цис-3,5-диметилпиперазин-1-ил)пиридин-3-иламин, получают путем обработки промежуточного продукта (А), цис-3,5-диметил-1-(5-нитропиридин-2-ил)пиперазина, с помощью H2 (или формиата аммония) и Pd/C (или никеля Ренея) в МеОН (и ТГФ) при КТ. Про- 28017952 межуточное соединение (А) получают по реакции цис-2,6-диметилпиперазина (В) с 2-хлор-5 нитропиридином (С) в присутствии Et3N в ТГФ при температуре от КТ до 70 С. Альтернативно, в случае, если (В) является спиртом, то для получения некоторых мета-замещенных производных в качестве (С) используют 2-бром-5-нитропиридин или 2-хлор-4-нитропиридин-1-оксид и реакцию проводят в присутствии KOtBu или Cs2CO3 или NaH в ДМА или ТГФ при температуре от КТ до 80 С. Следующие анилины, использующиеся в приведенных ниже примерах, синтезируют аналогично с использованием соответствующих подходящих исходных веществ: 6-2R,5S)-2,5-диметилпиперазин-1-ил)пиридин-3-иламин (рацемический); 6-(4,7-диазаспиро[2,5]окт-7-ил)пиридин-3-иламин; 2-[4-(5-аминопиридин-2-ил)пиперазин-1-ил]этанол; 2-(4,7-диазаспиро[2,5]окт-7-ил)пиридин-4-иламин; 2-(4-метилпиперазин-1-ил)пиримидин-5-иламин; 6-изопропоксипиридин-3-иламин; трет-бутиловый эфир 4-(4-аминопиридин-2-илоксиметил)пиперидин-1-карбоновой кислоты; 6-(цис-3,5-диметилпиперазин-1-ил)-5-метилпиридин-3-иламин; 5-хлор-6-(цис-3,5-диметилпиперазин-1-ил)пиридин-3-иламин; 2-(4-циклопропилпиперазин-1-ил)пиридин-4-иламин; 6-(4-циклопропилпиперазин-1-ил)пиридин-3-иламин; 6-[4-(2-диметиламиноэтил)пиперазин-1-ил]пиридин-3-иламин; 6-(3-трифторметилпиперазин-1-ил)пиридин-3-иламин (рацемический); трет-бутиловый эфир 4-(5-аминопиридин-2-ил)-3-оксопиперазин-1-карбоновой кислоты; трет-бутиловый эфир 4-(5-амино-3-метилпиридин-2-ил)пиперазин-1-карбоновой кислоты; 6-(3,3-диметилпиперазин-1-ил)-5-метилпиридин-3-иламин; 5-хлор-6-(цис-3,5-диметилпиперазин-1-ил)пиридин-3-иламин; 5-амино-2-(цис-3,5-диметилпиперазин-1-ил)никотинонитрил; 4-(5-амино-3-хлорпиридин-2-ил)пиперазин-2-он; 1-(5-аминопиридин-2-ил)-3,3-диметилпиперазин-2-он; 1-(5-амино-3-метилпиридин-2-ил)-3,3-диметилпиперазин-2-он; трет-бутиловый эфир 4-(5-амино-3-метилпиридин-2-ил)-3-оксопиперазин-1-карбоновой кислоты; 6-(цис-3,5-диметилпиперазин-1-ил)-5-трифторметилпиридин-3-иламин; 6-(цис-3,5-диметилпиперазин-1-ил)-5-метоксипиридин-3-иламин; 4-(4-аминопиридин-2-ил)пиперазин-2-он; трет-бутиловый эфир 4-(5-амино-3-хлорпиридин-2-ил)пиперазин-1-карбоновой кислоты; 1-(4-аминопиридин-2-ил)-3,3-диметилпиперазин-2-он; 4-(4-аминопиридин-2-ил)-1-метилпиперазин-2-он; 6-(6,6-дифтор-[1,4]диазепан-1-ил)-5-метилпиридин-3-иламин(В получен в соответствии с WO 2003042172 р.51); 6-(2-морфолин-4-илэтокси)пиридин-3-иламин; трет-бутиловый эфир 3-(5-аминопиридин-2-илокси)азетидин-1-карбоновой кислоты; 6-(тетрагидропиран-4-илокси)пиридин-3-иламин; 6-(2-метоксиэтокси)пиридин-3-иламин; 6-(тетрагидропиран-4-илметокси)пиридин-3-иламин; 6-[2-(трет-бутилдифенилсиланилокси)этокси]пиридин-3-иламин; трет-бутиловый эфир 3-(5-аминопиридин-2-илокси)пирролидин-1-карбоновой кислоты; 6-[3-(трет-бутилдифенилсиланилокси)пирролидин-1-ил]пиридин-3-иламин; 2-(тетрагидропиран-4-илокси)пиридин-4-иламин; 2-(2-морфолин-4-илэтокси)пиридин-4-иламин; 2-(3-трифторметилпиперазин-1-ил)пиридин-4-иламин (рацемический); 5-(4-метилпиперазин-1-ил)пиридин-2-иламин. Общая процедура VIII синтеза анилиновых структурных элементов (в приведенной ниже формуле в качестве примера использован 4-(4-этилпиперазин-1-ил)-3-метилфениламин): Соединение, приведенное выше слева, 4-(4-этилпиперазин-1-ил)-3-метилфениламин, получают путем обработки промежуточного продукта (А), 1-этил-4-(2-метил-4-нитрофенил)-пиперазина, с помощью
МПК / Метки
МПК: C07D 487/04, A61K 31/519
Метки: качестве, ингибиторов, применение, пирроло[2,3-d]пиридины, тирозинкиназы
Код ссылки
<a href="https://eas.patents.su/30-17952-pirrolo23-dpiridiny-i-ih-primenenie-v-kachestve-ingibitorov-tirozinkinazy.html" rel="bookmark" title="База патентов Евразийского Союза">Пирроло[2,3-d]пиридины и их применение в качестве ингибиторов тирозинкиназы</a>
Предыдущий патент: Бумажный рулон с центральным отверстием и упрочненным элементом и способ изготовления такого рулона
Следующий патент: Способ управления антиблокировочной системой торможения транспортного средства
Случайный патент: Шарнирные соединения