Пирролопиримидины и их применение
Номер патента: 16301
Опубликовано: 30.04.2012
Авторы: Сун Му Че, Брейн Кристофер Томас, Тома Гебхард
Формула / Реферат
1. Соединение формулы I
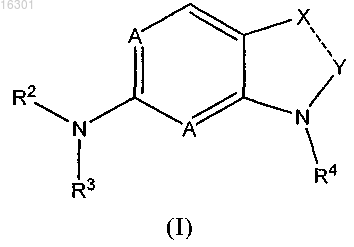
или его фармацевтически приемлемая соль, в которой
штриховая линия обозначает двойную связь;
А обозначает N;
R2 обозначает водород;
R3 выбран из группы, включающей фенил; замещенный фенил; пиридинил; замещенный пиридинил; пиримидинил и замещенный пиримидинил; где указанные замещенный фенил, замещенный пиридинил и замещенный пиримидинил каждый замещен одним заместителем, выбранным из группы, включающей метил; метокси; нитрогруппу; хлор; цианогруппу; имидазолил; N(CH3)2; N(CH2CH3)2; N(Н)С(О)-пиридинил; С(О)N(Н)C1-C4-алкил; C(O)N(C1-С4-алкил)2; С(О)N(Н)С3-С6-циклоалкил; морфолинил-СО-; пиперидинил, необязательно замещенный одним COCH3, СОСН2СН3, метилом, COCH2CN или SO2CH3; пиперазинил, необязательно замещенный одним COCH3 или СОСН2СН3; морфолинил; пиперидинил-СН2; пиперазинил-СН2 и морфолинил-СН2;
R4 выбран из группы, включающей водород; C1-C8-алкил; C1-C8-алкил, замещенный одним фенилом, COOH, COOCH3, COOCH2CH3 или CONH2; С3-С8-циклоалкил; C3-C8-циклоалкил, замещенный одним OH, COOH, СН2ОН, NH2, CH2N(CH3)2 или оксогруппой; метилпиридинил; тиазолил и имидазолил;
X обозначает CR11 и Y обозначает CR12;
R11 обозначает галоген, водород, C1-C3-алкил и
R12 обозначает -BC(O)NR13R14, где В обозначает связь, C1-C3-алкил или разветвленный C1-C3-алкил; где R13 и R14, каждый независимо, выбран из группы, включающей водород, C1-C3-алкил, С3-C8-циклоалкил, фенил, 4-метоксифенил, 4-метилфенил, 4-трет-бутилфенил, 3-трет-бутилфенил, фуранилметил, 3-трифторметилфенил, пиридинил, 4-фторфенил, 3-фторфенил и 1-бензил-4-метилпиперазинил.
2. Соединение по п.1, где R4 выбран из группы, включающей водород, разветвленный C1-C5-алкил, разветвленный C1-C5-алкил, замещенный фенилом, и C3-C6-циклоалкил.
3. Соединение по п.1, где R4 обозначает C(H)(CH2CH3)2, C(H)(CH2CH3)Ph, CH2CH3, циклопропил, циклопентил или циклогексил.
4. Соединение по п.1, где R11 обозначает водород.
5. Соединение по п.1, где R3 обозначает замещенный фенил.
6. Соединение по п.5, где фенильная группа замещена N(H)C(O)-пиридинилом, C(O)N(H)C1-C4-алкилом, C(O)N(C1-С4-алкил)2 или C(O)N(H)C3-C6-циклоалкилом.
7. Фармацевтическая композиция, включающая соединение по любому из пп.1-6 и фармацевтически приемлемый носитель.
Текст
Брейн Кристофер Томас (US), Тома Гебхард (DE), Сун Му Че (US) В патенте описаны органические соединения формулы (I), которые применимы для лечения,предупреждения и/или облегчения протекания заболеваний,предпочтительно описаны пирролопиримидины и их производные, которые ингибируют протеинкиназы. Эти органические соединения применимы для лечения пролиферативного заболевания. 016301 Уровень техники В последние годы поиску новых терапевтических средств значительно способствовало лучшее изучение структуры ферментов и других биомолекул, связанных с заболеваниями. Одним важным классом ферментов, оказавшимся объектом многочисленных исследований, являются протеинкиназы. Протеинкиназы представляют собой большую группу структурно родственных ферментов, которые обеспечивают регулирование различных процессов передачи сигналов в клетке (Hardie, G. and Hanks, S.The Protein Kinase Facts Book, I and II, Academic Press, San Diego, Calif.: 1995). Ввиду сохранения своей структуры и каталитического действия, предполагается, что протеинкиназы образовались из общего анцестрального гена. Почти все киназы включают сходный, содержащий 250-300 аминокислот каталитической домен. Киназы можно разделить на группы в соответствии с субстратами, которых они фосфорилируют (например, протенитирозин, протеинсерин/треонин, липиды и т.п.). Идентифицированы группы последовательностей, которые обычно соответствуют каждой из этих групп киназ (см., например, Hanks,S. K., Hunter, Т., FASEB J. 1995, 9, 576-596; Knighton et al., Science 1991, 253, 407-414; Hiles et al., Cell 1992, 70, 419-429; Kunz et al., Cell 1993, 73, 585-596; Garcia-Bustos et al., EMBO J. 1994, 13, 2352-2361). Обычно протеинкиназы опосредуют внутриклеточные сигналы путем воздействия на перенос фосфорильных групп от нуклеозидтрифосфата к акцепторному белку, который участвует в пути передачи сигнала. Эти акты фосфорилирования выступают в качестве молекулярных переключателей, которые могут модулировать или регулировать биологические функции целевого белка. Эти акты фосфорилирования в конечном счете инициируются в ответ на различные внутриклеточные и другие воздействия. Примеры таких воздействий включают сигналы, вызванные окружающей средой и химическими стрессами (например, осмотического шока, теплового шока, ультрафиолетового излучения, бактериального эндотоксина и Н 2 О 2), цитокинов (например, интерлейкина-1 (IL-1) и факторанекроза опухоли (TNF и факторов роста (например, колониеобразующего гранулоцитарно-моноцитарно-макрофагального фактора (GM-CSF) и фактора роста фибробластов (FGF. Внеклеточные воздействия могут влиять на один или большее количество клеточных ответов, связанных с ростом, миграцией, дифференциацией клеток, секрецией гормонов, активацией факторов транскрипции, сокращением мышц, метаболизмом глюкозы, регулирования синтеза белка и регулирования клеточного цикла. Многие заболевания связаны с аномальными ответами клеток, вызванными опосредуемыми протеинкиназой проявлениями, описанными выше. Эти заболевания включают, но не ограничиваются только ими, аутоиммунные заболевания, воспалительные заболевания, заболевания кости, метаболические заболевания, неврологические и нейродегенеративные заболевания, рак, сердечно-сосудистые заболевания,аллергии и астму, болезнь Альцгеймера и связанные с гормонами заболевания. В связи с этим в медицинской химии предпринимались значительные усилия по поиску ингибиторов протеинкиназы, которые эффективны в качестве лекарственных средств. Киназы Janus (JAK) представляют собой группу тирозинкиназ, включающую JAK1, JAK2, JAK3 иTYK2. Киназы JAK играют критически важную роль в передаче сигналов цитокинов. Расположенные в прямом направлении субстраты киназ группы JAK включают белки, передающие сигналы, и белки, активирующие транскрипцию (STAT). Передача сигналов JAK/STAT участвует в опосредовании многих аномальных иммунных ответов, таких как аллергии, астма, аутоиммунные заболевания, такие как отторжение трансплантата, ревматоидный артрит, боковой амиотрофический склероз и рассеянный склероз, а также в солидных злокачественных заболеваниях и злокачественных заболеваниях крови, таких как лейкозы и лимфомы. Фармацевтическое воздействие на путь JAK/STAT освещено в обзоре [Frank Mol. Med. 5: 432-456 (1999)Seidel, et al., Oncogene 19: 2645-2656 (2000)].JAK1, JAK2 и TYK2 экспрессируются повсеместно, тогда как JAK3 экспрессируется преимущественно в гематопоэтических клетках. JAK3 связываются только с гамма-цепью общего цитокинового рецептора (с) и активируются с помощью IL-2, IL-4, IL-7, IL-9 и IL-15. В действительности, показано, что пролиферация и жизнеспособность мастоцитов мышей, индуцированная с помощью IL-4 и IL-9, зависят от передачи сигналов JAK3- и 65c [Suzuki et al., Blood 96: 2172-2180 (2000)]. Сшивка высокоафинных рецепторов иммуноглобулина (Ig) E сенсибилизированных мастоцитов приводит к высвобождению противовоспалительных медиаторов, включая целый ряд вазоактивных цитокинов, что приводит к острым аллергическим реакциям или немедленным (типа I) реакциям гиперчувствительности [Gordon et al, Nature 346: 274-276 (1990)Galli, N. Engl. J. Med., 328: 257-265 (1993)]. С помощью исследований in vitro и in vivo установлена критически важная роль JAK3 для ответов опосредуемых рецептором IgE мастоцитов [Malaviya, et al., Biochem. Biophys. Res. Commun. 257: 807-813(1999)]. Кроме того, обнаружено предупреждение реакций гиперчувствительности типа I, включая анафилаксию, опосредуемое активацией мастоцитов путем ингибирования JAK3 [Malaviya et al., J. Biol.Chem. 274:27028-27038 (1999)]. Также показано, что группа тирозинкиназ JAK участвует в подавлении иммунного ответа и приживлении аллотрансплантата [Kirken, Transpl. Proc. 33: 3268-3270 (2001)], ревматоидном артрите [MullerLadner, et al., J. Immunol. 164: 3894-3901 (2000)], наследственном боковом амиотрофическом склерозеRes. 5: 1569-1582 (1999)]. Инициирование, прогрессирование и завершение клеточного цикла у млекопитающих регулируется различными комплексами циклин-зависимой киназы (CDK), которые являются критически важными для роста клеток. Эти комплексы включают, по меньшей мере, каталитическую (сама CDK) и регуляторную(циклин) субъединицы. Некоторые из комплексов, наиболее важных для регуляции клеточного цикла,включают циклин A (CDK1, также обозначаемый как cdc2 и CDK2), циклин В 1-В 3 (CDK1) и циклин D1D3 (CDK2, CDK4, CDK5, CDK6), циклин Е (CDK2). Каждый из этих комплексов участвует в конкретной фазе клеточного цикла. Однако не все представители группы CDK участвуют только в регулировании клеточного цикла. Так CDK 7, 8 и 9 участвуют в регуляции транскрипции и CDK5 участвует в нейронной и секреторной функции клетки. Активность CDK регулируется после трансляции с помощью временных ассоциаций с другими белками и с помощью изменения их положения в клетке. Развитие опухоли тесно связано с генетическим изменением и нарушением регуляции CDK и их регуляторов и это показывает, что ингибиторы CDK могут быть полезными противораковыми лекарственными средствами. И действительно, полученные ранее результаты показывают, что изменившиеся и нормальные клетки различаются по их потребности, например, в циклине A/CDK2, и что можно разработать новые противоопухолевые средства, не проявляющие обычной токсичности по отношению к реципиенту, наблюдающейся у обычных цитотоксичных и цитостатических лекарственных средств. Хотя ингибирование связанных с клеточным циклом CDK прямо относится, например, к применению в онкологии, к ней может не относится ингибирование CDK, регулирующих РНК-полимеразу. С другой стороны, ингибирование функции CDK9/циклин Т недавно было связано с предупреждением репликации ВИЧ (вирус иммунодефицита человека) и исследование новых биологических характеристик CDK продолжает способствовать появлению новых терапевтических показаний для ингибиторов CDK (Sausville, E. A. Trends Molec. Med. 2002, 8, S32-S37). Функцией CDK является фосфорилирование и тем самым активация или дезактивация некоторых белков, включая, например, белки ретинобластомы, ламины, гистон H1 и компоненты митотического веретена. Каталитическая стадия, опосредуемая с помощью CDK, включает реакции переноса фосфорсодержащих групп от АТФ (аденозинтрифосфат) к макромолекулярному ферменту субстрата. Обнаружено,что некоторые группы соединений (обзор приведен, например, в публикации Fischer, P. M. Curr. Opin.Drug Discovery Dev. 2001, 4, 623-634) обладают антипролиферативной способностью вследствие CDKспецифического антагонизма к АТФ. Таким образом, постоянно необходимо проводить поиск новых лекарственных средств для лечения заболеваний людей. В соответствии с этим необходимы новые ингибиторы протеинкиназ, таких как Jak1,Jak2 и Jak3, a также CDK1, CDK2, CDK4, CDK5, CDK6, CDK7, CDK8 и CDK9. Краткое изложение сущности изобретения Необходимы новые средства и методики лечения нарушений, связанных с протеинкиназой. Также необходимы новые соединения, применимые для устранения, предупреждения или облегчения одного или большего количества симптомов рака, отторжения трансплантатов и аутоиммунных заболеваний. Кроме того, необходимы способы модулирования активности протеинкиназ, таких как Jakl, Jak2 и Jak3, а также CDK1, CDK2, CDK4, CDK5, CDK6, CDK7, CDK8 и CDK9, с использованием соединений, предлагаемых в настоящем изобретении. Одним объектом настоящего изобретения является соединение формулы I В рамках настоящего изобретения протеинкиназа представляет собой протеинтирозинкиназу. В одном варианте осуществления протеинкиназа выбрана из группы, включающей abl, ATK, ber-abl, Blk, Brk,Btk, c-fms, е-kit, c-met, c-src, CDK, cRafl, CSFIR, CSK, EGFR, ErbB2, ErbB3, ErbB4, ERK, Fak, fes, FGFRI,25 FGFR2, FGFR3, FGFR4, FGFR5, Fgr, FLK-4, flt-1, Fps, Frk, Fyn, GSK, Gst-Flkl, Hck, Her-2, Her-4, IGF1R, INS-R, Jak, JNK, KDR, Lck, Lyn, MEK, p38, PANHER, PDGFR, PLK, PKC, PYK2, Raf, Rho, ros, SRC,t'eII t'e2, TRK, TYK2, UL97, VEGFR, Yes и Zap70. В другом варианте осуществления протеинкиназа выбрана из группы, включающей CDK1, CDK2, CDK4, CDK5, CDK6, CDK7, CDK8 и CDK9. В еще одном варианте осуществления протеинкиназа выбрана из группы, включающей Jak1, Jak2 и Jak3. В еще одном варианте осуществления протеинкиназа выбрана из группы, включающей Jak3 и CDK4. Предпочтительно протеинкиназа находится в культуре клеток. В еще одном объекте протеинкиназа находится в млекопитающем. Соединение формулы I может быть использовано для лечения нарушения, связанного с протеинкиназой, которое включает введение нуждающемуся в нем субъекту фармацевтически приемлемого количества соединения формулы I, так что подвергается лечению нарушение, связанное с протеинкиназой. Предпочтительно, протеинкиназа выбрана из группы, включающей CDK1, CDK2, CDK4, CDK5, CDK6,CDK7, CDK8, CDK9, Jakl, Jak2 и Jak3. Более предпочтительно протеинкиназа выбрана из группы, вклю-2 016301 чающей Jak3 и CDK4. Предпочтительно нарушение, связанное с протеинкиназой, выбрано из группы, включающей пролиферативные нарушения кровеносных сосудов, фиброзные нарушения, пролиферативные нарушения мезангиальных клеток, нарушения метаболизма, аллергии, астму, тромбоз, заболевания нервной системы и рак. Более предпочтительно нарушение, связанное с протеинкиназой, представляет собой рак. Предпочтительно рак выбран из группы, включающей рак молочной железы, желудка, яичников, толстой кишки,легких, головного мозга, гортани, лимфатической системы, мочеполового тракта (включая мочевого пузыря и предстательной железы), яичников, желудка, кости и поджелудочной железы. Предпочтительно нарушение, связанное с протеинкиназой, выбрано из группы, включающей отторжение трансплантата органа, ксенотрансплантацию, волчанку, рассеянный склероз, ревматоидный артрит, псориаз, диабет типа 1 и осложнения при диабете, рак, астму, атопический дерматит, аутоиммунные нарушения щитовидной железы, язвенный колит, болезнь Крона, болезнь Альцгеймера и лейкоз. Предпочтительно заболевание выбрано из группы, включающей иммунный ответ, аутоиммунное заболевание, нейродегенеративное заболевание и солидное гематологическое злокачественное новообразование. Более предпочтительно заболевание выбрано из группы, включающей аллергическую реакцию и реакцию гиперчувствительности типа I, астму, реакцию "трансплантант против хозяина", ревматоидный артрит, боковой амиотрофический склероз, рассеянный склероз, наследственный боковой амиотрофический склероз, лейкоз и лимфому. Соединение формулы I может быть использовано для лечения аутоиммунного заболевания, в котором лечение включает введение нуждающемуся в нем субъекту фармацевтически приемлемого количества соединения формулы I, так что подвергается лечению аутоиммунное заболевание. Предпочтительно аутоиммунное заболевание выбрано из группы, включающей аутоиммунную гемолитическую анемию,аутоиммунную тромбоцитопению новорожденных, идиопатическую тромбоцитопеническую пурпуру,аутоиммунную цитопению, гемолитическую анемию, антифосфолипидный синдром, дерматит, аллергический энцефаломиелит, миокардит, рецидивирующую полихондрию, ревматический порок сердца, гломерулонефрит, рассеянный склероз, неврит, увеит, офтальмит, полиэндокринные синдромы, пурпуру,болезнь Рейтера, синдром негнущегося человека, аутоиммунное воспаление легких, аутизм, синдром Гийена-Барре, сахарный инсулинозависимый диабет, аутоиммунное воспаление глаза, аутоиммунный тиреоидит, гипотиреоз, системную красную волчанку, синдром Гудпасчера, пемфигоид, аутоиммунные реакции рецептора, аутоиммунную гемолитическую анемию, аутоиммунную тромбоцитопеническую пурпуру, ревматоидный артрит, смешанное заболевание соединительной ткани, полимиозит/дерматомиозит, пернициозную анемию, идиопатическую Аддисонову болезнь, бесплодие, гломерулонефрит, буллезный пемфигоид, синдром Шегрена, сахарный диабет, адренергическую резистентность к лекарственному средству, хронический активный гепатит, первичный биллиарный цирроз, витилиго,васкулит, состояние после инфаркта миокарда, посткардиотомный синдром, уртикарию, атопический дерматит, астму, воспалительные миопатии, хронический активный гепатит, первичный биллиарный цирроз и опосредуемые Т-клетками аллергические заболевания. Соединение формулы I может быть использовано для лечения отторжения трансплантата, в котором лечение включает введение нуждающемуся в нем субъекту фармацевтически приемлемого количества соединения формулы I, так что подвергается лечению отторжение трансплантата. Предпочтительно отторжение трансплантата выбрано из группы, включающей реакцию "трансплантант против хозяина",отторжение, связанное с ксенотрансплантацией, отторжение, связанное с трансплантацией органа, отторжение, связанное с неотложной трансплантацией, отторжение гетеротрансплантата или гомотрансплантата и ишемическое или реперфузионное поражение, возникшее при трансплантации органа. Соединение формулы I может быть использовано для лечения рака, который включает введение нуждающемуся в нем субъекту фармацевтически приемлемого количества соединения формулы I, так что подвергается лечению раковое заболевание или нарушение. Предпочтительно рак выбран из группы,включающей мочевого пузыря, головы и шеи, молочной железы, желудка, яичников, толстой кишки,легких, головного мозга, гортани, лимфатической системы, мочеполового тракта, желудочно-кишечного тракта, яичников, предстательной железы, желудка, кости, мелкоклеточный рак легких, глиому, колоректальный рак и рак поджелудочной железы. Предпочтительно соединение формулы I или его соль вводят одновременно или последовательно с противовоспалительным, антипролиферативным, химиотерапевтическим средством, иммунодепрессантом, противораковым, цитотоксическим средством или ингибитором, которые не являются соединением формулы I или его солью. Предпочтительно соединение формулы I или его соль вводят одновременно или последовательно с одним или большим количеством следующих средств: ингибитор РТК, циклоспорин А, CTLA4-Ig, антитела, выбранные из группы, включающей анти-ICAM-3, анти-IL-2 рецептора, анти-CD45RB, анти-CD2, анти-CD3, анти-CD4, анти-CD80, анти-CD86 и моноклональные антитела OKT3,средства, блокирующие взаимодействия между CD40 и gp39, белки слияния, образованные из CD40 иgp39, ингибиторы NF-каппа В функции, нестероидные противовоспалительные лекарственные средства,стероиды, соединения золота, антипролиферативные средства, FK506, микофенолят мотефил, цитоток-3 016301 сические лекарственные средства, ингибиторы TNF-, анти-TNF антитела или растворимый рецепторTNF, рапамицин, лефлунимид, ингибиторы циклооксигеназы-2, паклитаксел, цисплатин, карбоплатин,доксорубицин, карминомицин, даунорубицин, аминоптерин, метотрексат, метоптерин, митомицин С,эктеинасцидин 743, порфиромицин, 5-фторурацил, 6-меркаптопурин, гемцитабин, цитозинарабинозид,подофиллотоксин, этопозид, этопозидфосфат, тенипозид, мелфалан, винбластин, винкристин, лейрозидин, эпотилон, виндезин, лейрозин или их производные. Соединение формулы I может быть использовано в виде упакованного средства для лечения нарушения, связанного с протеинкиназой, которое включает модулирующее протеинкиназу соединение формулы I, упакованное вместе с инструкциями по применению эффективного количества модулирующего протеинкиназу соединения, предназначенного для лечения нарушения, связанного с протеинкиназой. Подробное описание изобретения Настоящее изобретение относится к соединениям, например пирролопиримидинам, а также к фармацевтическим композициям, содержащим соединения, предназначенным для применения для лечения нарушений, связанных с протеинкиназой. Настоящее изобретение также относится к соединениям, предлагаемым в настоящем изобретении, или к их композициям как модуляторам Jak1, Jak2 и Jak3, а такжеCDK1, CDK2, CDK4, CDK5, CDK6, CDK7, CDK8 и CDK9. Такие соединения могут быть использованы в составе комбинированной терапии для ингибирования активности протеинкиназы в клетках или для устранения, предупреждения или облегчения одного или большего количества симптомов рака, отторжения трансплантатов и аутоиммунных заболеваний у пациентов с применением соединений, предлагаемых в настоящем изобретении, или фармацевтических композиций, содержащих их. Одним объектом настоящего изобретения являются соединения формулы I: или их фармацевтически приемлемая соль, в которой: штриховая линия обозначает двойную связь; А обозначает N;R3 выбран из группы, включающей фенил; замещенный фенил; пиридинил; замещенный пиридинил; пиримидинил и замещенный пиримидинил; где указанные замещенный фенил, замещенный пиридинил и замещенный пиримидинил каждый замещен одним заместителем, выбранным из группы, включающей метил; метокси; нитрогруппу; хлор; цианогруппу; имидазолил; N(CH3)2; N(CH2CH3)2; N(H)C(O)пиридинил; С(О)N(Н)С 1-С 4-алкил; C(O)N(C1-C4-алкил)2; С(О)N(Н)С 3-С 6-циклоалкил; морфолинил-СО-; пиперидинил, необязательно замещенный одним СОСН 3, COCH2CH3, метилом, COCH2CN или SO2CH3; пиперазинил, необязательно замещенный одним COCH3 или СОСН 2 СН 3; морфолинил; пиперидинилСН 2; пиперазинил-СН 2 и морфолинил-СН 2;R11 обозначает галоген, водород, C1-C3-алкил; и R12 обозначает -BC(O)NR13R14; где В обозначает связь, C1-C3-алкил или разветвленный C1-C3 алкил; где R13 и R14 каждый независимо выбран из группы, включающей водород, C1-C3-алкил, C3-C8 циклоалкил, фенил, 4-метоксифенил, 4-метилфенил, 4-трет-бутилфенил, 3-трет-бутилфенил, фуранилметил, 3-трифторметилфенил, пиридинил, 4-фторфенил, 3-фторфенил и 1-бензил-4-метилпиперазинил. В одном варианте осуществления R4 выбран из группы, включающей водород, разветвленный C1C5-алкил, разветвленный C1-C5-алкил, замещенный фенилом, и C3-C6-циклоалкил. В другом варианте осуществления R4 обозначает C(H)(CH2CH3)2, C(H)(CH2CH3)Ph, CH2CH3, циклопропил, циклопентил или циклогексил. В еще одном варианте осуществления R11 обозначает водород. В еще одном варианте осуществления R3 обозначает обозначает замещенный фенил, который дополнительно независимо один или большее количество раз замещен N(H)C(O)-пиридинилом,C(O)N(Н)С 1-С 4-алкилом, С(О)N(C1-С 4-алкил)2 или С(О)N(Н)C3-C6-циклоалкилом. Предпочтительные варианты осуществления соединения формулы I (включая его фармацевтически приемлемые соли) приведены ниже в табл. А, табл. В, табл. С и табл. D и также рассматриваются как"соединения, предлагаемые в настоящем изобретении". Соединения, предлагаемые в настоящем изобретении, в настоящем изобретении также называются "ингибиторами протеинкиназы".
МПК / Метки
МПК: A61P 17/06, A61K 31/52, A61P 35/02, A61P 15/00, A61P 25/28, A61K 31/522, C07D 487/04, A61P 35/00, A61P 1/00, A61P 11/06, A61P 37/06, A61P 17/00, A61P 3/10, A61P 19/02, A61P 9/00, A61K 31/519
Метки: пирролопиримидины, применение
Код ссылки
<a href="https://eas.patents.su/30-16301-pirrolopirimidiny-i-ih-primenenie.html" rel="bookmark" title="База патентов Евразийского Союза">Пирролопиримидины и их применение</a>











