Макроциклические ингибиторы вируса гепатита с
Номер патента: 13475
Опубликовано: 30.04.2010
Авторы: Валльберг Ханс Кристиан, Йенссон Карл Эрик Даниель, Симмен Кеннет Алан, Нильссон Карл Магнус, Росенквист Оса Анника Кристина, Де Кок Херман Аугустинус, Классон Бьерн Олоф, Самуэльссон Бенгт Бертил, Айеса Алварес Сусана
Формула / Реферат
1. Соединение формулы
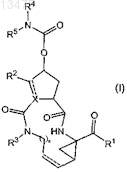
его N-оксид, соль или стереоизомер,
где каждая пунктирная линия (представленная как ![]() представляет собой необязательную двойную связь;
представляет собой необязательную двойную связь;
X представляет собой N, СН и, когда X содержит двойную связь, он представляет собой С;
R1 представляет собой -OR6, -NH-SO2R7;
R2 представляет собой водород и, когда X представляет собой С или СН, R2 также может представлять собой C1-6-алкил;
R3 представляет собой водород, C1-6-алкил, С1-6-алкокси-С1-6-алкил или С3-7-циклоалкил;
n равно 3, 4, 5 или 6;
R4 и R5, взятые вместе с атомом азота, к которому они присоединены, образуют бициклическую кольцевую систему, выбранную из
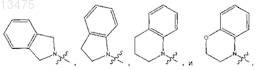
где указанная кольцевая система необязательно может быть замещена одним, двумя или тремя заместителями, независимо выбранными из галогена, гидрокси, оксо, нитро, циано, карбоксила, С1-6-алкила, C1-6-алкокси, С1-6-алкокси-С1-6-алкила, C1-6-алкилкарбонила, C1-6-алкоксикарбонила, амино, азидо, меркапто, полигалоген-С1-6-алкила;
R6 представляет собой водород; арил; Het; С3-7-циклоалкил, необязательно замещенный C1-6-алкилом; или C1-6-алкил, необязательно замещенный С3-7-циклоалкилом, арилом или Het;
R7 представляет собой арил; Het; С3-7-циклоалкил, необязательно замещенный C1-6-алкилом; или C1-6-алкил, необязательно замещенный С3-7-циклоалкилом, арилом или Het;
арил в виде группы или части группы представляет собой фенил или нафтил, каждый из которых необязательно может быть замещен одним, двумя или тремя заместителями, выбранными из галогена, гидрокси, нитро, циано, карбоксила, C1-6-алкила, C1-6-алкокси, С1-6-алкокси-С1-6-алкила, C1-6-алкилкарбонила, амино, моно- или ди-С1-6-алкиламино, азидо, меркапто, полигалоген-С1-6-алкила, полигалоген-С1-6-алкокси, С3-7-циклоалкила, пирролидинила, пиперидинила, пиперазинила, 4-C1-6-алкилпиперазинила, 4-С1-6-алкилкарбонилпиперазинила и морфолинила; где морфолинильные и пиперидинильные группы необязательно могут быть замещены одним или двумя C1-6-алкильными радикалами; и
каждый Het в виде группы или части группы представляет собой 5- или 6-членное насыщенное, частично ненасыщенное или полностью ненасыщенное гетероциклическое кольцо, содержащее от 1 до 4 гетероатомов, каждый из которых независимо выбран из атомов азота, кислорода и серы, и необязательно замещенное одним, двумя или тремя заместителями, каждый из которых независимо выбран из группы, состоящей из галогена, гидрокси, нитро, циано, карбоксила, C1-6-алкила, C1-6-алкокси, C1-6-алкокси-C1-6-алкила, C1-6-алкилкарбонила, амино, моно- или ди-С1-6-алкиламино, азидо, меркапто, полигалоген-С1-6-алкила, полигалоген-С1-6-алкокси, С3-7-циклоалкила, пирролидинила, пиперидинила, пиперазинила, 4-С1-6-алкилпиперазинила, 4-C1-6-алкилкарбонилпиперазинила и морфолинила; где морфолинильные и пиперидинильные группы необязательно могут быть замещены одним или двумя C1-6-алкильными радикалами.
2. Соединение по п.1, в котором соединение имеет формулу (I-c), (I-d) или (I-е)
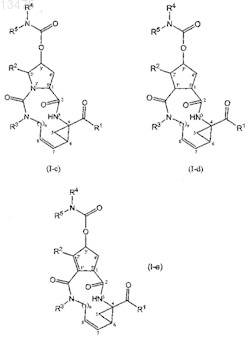
3. Соединение по любому из пп.1 и 2, в котором R4 и R5, взятые вместе с атомом азота, к которому они присоединены, образуют бициклическую кольцевую систему, выбранную из
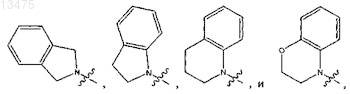
в которых фенил упомянутой бициклической кольцевой системы необязательно замещен одним или двумя заместителями, независимо выбранными из галогена, гидрокси, циано, карбоксила, C1-6-алкила, C1-6-алкокси, C1-6-алкоксикарбонила, амино и полигалоген-C1-6-алкила.
4. Соединение по любому из пп.1 и 2, в котором R4 и R5, взятые вместе с атомом азота, к которому они присоединены, образуют бициклическую кольцевую систему, выбранную из
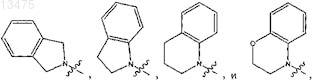
в которых пирролидиновые, пиперидиновые или морфолиновые кольца упомянутой бициклической кольцевой системы необязательно замещены одним или двумя заместителями, независимо выбранными из C1-6-алкила, C1-6-алкокси и С1-6-алкокси-С1-6-алкила.
5. Соединение по любому из пп.1-4, в котором:
(a) R1представляет собой -OR6, где R6 представляет собой C1-6-алкил или водород; или
(b) R1представляет собой -NHS(=O)2R7, где R7представляет собой метил, циклопропил или фенил.
6. Соединение по любому из пп.1-5, отличающееся от N-оксида или соли.
7. Комбинация, содержащая:
(a) соединение по любому из пп.1-6 или его фармацевтически приемлемую соль и
(b) ритонавир или его фармацевтически приемлемую соль.
8. Фармацевтическая композиция, содержащая носитель и в качестве активного ингредиента эффективное против вируса количество соединения по любому из пп.1-6.
9. Применение соединения по любому из пп.1-6 в качестве лекарственного средства.
10. Применение соединения по любому из пп.1-6 для производства лекарственного средства для ингибирования репликации HCV.
11. Способ ингибирования репликации HCV у теплокровного животного, включающий в себя введение эффективного количества соединения по любому из пп.1-6.
12. Способ получения соединения по любому из пп.1-6, который включает в себя:
(а) получение соединения формулы (I), в котором связь между атомами углерода С7 и С8 является двойной связью, такое соединение представлено формулой (I-i), путем образования двойной связи между атомами углерода С7 и С8 с помощью реакции метатезиса олефинов с сопутствующей циклизацией до макроцикла, как показано на следующей реакционной схеме:
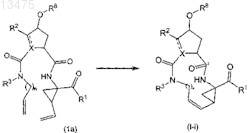
где R8на указанной выше и следующих схемах представляет собой радикал
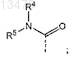
(b) преобразование соединения формулы (I-i) в соединение формулы (I), в котором связь между атомами углерода С7 и С8 в макроцикле является одинарной связью, являющееся соединением формулы (I-j)
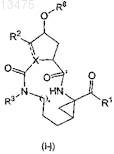
путем восстановления двойной связи между атомами углерода С7 и С8 в соединениях формулы (I-j);
(с) получение соединения формулы (I), в котором R1 представляет собой -NHSO2R7, упомянутые соединения представлены формулой (I-k-1) путем образования амидной связи между промежуточным продуктом (2а) и сульфониламином (2b); или получение соединения формулы (I), в котором R1 представляет собой -OR6, являющееся соединением (I-k-2), путем образования сложноэфирной связи между промежуточным продуктом (2а) и спиртом (2с), как показано на следующей схеме, на которой G представляет собой группу:
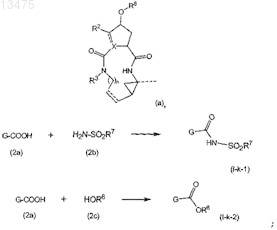
(d) получение соединения формулы (I), в котором R3 представляет собой водород, упомянутое соединение представлено формулой (I-1) из соответствующего азотзащищенного промежуточного продукта (3а), в котором PG представляет собой азотзащитную группу
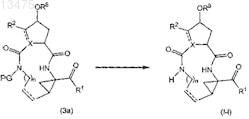
(е) взаимодействие промежуточного продукта (4а) с амином (4b) в присутствии карбамат-образующего реагента по следующей реакционной схеме:
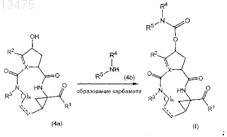
(f) преобразование соединений формулы (I) друг в друга с помощью реакции трансформации функциональных групп или
(g) получение соединения в форме соли путем взаимодействия свободной формы соединения формулы (I) с кислотой или основанием.
Текст
013475 Настоящее изобретение относится к макроциклическим соединениям, обладающим ингибиторной активностью в отношении репликации вируса гепатита С (HCV). Кроме того, изобретение относится к композициям, содержащим такие соединения в качестве активных ингредиентов, а также к способам получения таких соединений и композиций. Во всем мире вирус гепатита С служит основной причиной хронического заболевания печени и стал центром внимания значительного количества медицинских исследований. HCV является представителем семейства вирусов Flaviviridae из рода hepacivirus и является близкородственным роду flavivirus,который включает в себя ряд вирусов, участвующих в заболеваниях человека, таких как вирус денге и вирус желтой лихорадки, и семейству pestivirus вирусов животных, которое включает в себя вирус диареи быков (BVDV). HCV представляет собой позитивно-смысловой, однонитевой РНК-содержащий вирус с геномом приблизительно из 9600 оснований. Геном содержит как 5'-, так и 3'-нетранслируемые области, которые воспроизводят вторичные структуры РНК, и центральную открытую рамку считывания,которая кодирует единый полипротеин длиной приблизительно из 3010-3030 аминокислот. Полипротеин содержит продукты, которые кодируются десятью генами и генерируются из полипротеинапредшественника в результате целой серии ко- и пострансляционных эндопротеолитических расщеплений, опосредованных как хозяйскими, так и вирусными протеазами. Вирусные структурные протеины включают в себя ядерный нуклеокапсидный протеин и два оболочечных гликопротеина Е 1 и Е 2. Неструктурные (NS) протеины обуславливают некоторые жизненно важные вирусные ферментативные функции (геликаза, полимераза, протеаза), а также протеины с неизвестной функцией. Репликация вирусного генома опосредована РНК-зависимой РНК-полимеразой, представленной неструктурным протеином 5b (NS5B). Было доказано, что кроме полимеразы важными для репликации РНК HCV являются функции вирусной геликазы и протеазы, обе из которых представлены бифункциональнымNS3-протеином. Кроме сериновой протеазы NS3, HCV кодирует также и металлопротеиназу в NS2 области. После первоначальной острой инфекции у большинства инфицированных развивается хронической гепатит, поскольку HCV реплицируется предпочтительно в гепатоцитах, хотя не является непосредственно цитопатическим. В частности, отсутствие достаточно интенсивного ответа Т-лимфоцитов и высокая предрасположенность вируса к мутации, по-видимому, способствуют высокой скорости распространения хронической инфекции. Хронический гепатит может прогрессировать до фиброза печени, приводя на конечной стадии заболевания к циррозу печени и НСС (гепатоклеточной карциноме), что является главной причиной трансплантации печени. Существует 6 основных генотипов HCV и более 50 подтипов, которые географически распространены неодинаково. Тип 1 HCV представляет собой генотип, преобладающий в Европе и США. Обширная генетическая гетерогенность HCV имеет важные диагностические и клинические последствия, возможно объясняющие трудности в разработке вакцин и недостаточный ответ на терапию. Передача вируса HCV может происходить через контакт с зараженной кровью или кровепродуктами, например после переливания крови или внутривенного введения лекарственного средства. Внедрение диагностических тестов, применяемых при скрининге крови, ведет к снижению частоты случаевHCV после переливания. Однако с учетом медленного прогресса в отношении болезни печени в конечной стадии, существующие инфекции будут сохраняться в течение десятилетий, обеспечивая серьезное медицинское и экономическое бремя. Современные терапии HCV основаны на (пегилированном) интерфероне-альфа (IFN-) в сочетании с рибавирином. Такая комбинированная терапия дает в результате долговременный ответ на вирус более чем у 40% пациентов, инфицированных вирусами генотипа 1, и приблизительно у 80% пациентов, инфицированных вирусами генотипов 2 и 3. Наряду с ограниченной эффективностью в отношении HCV типа 1 такая комбинированная терапия имеет значительные побочные эффекты и плохо переносится многими пациентами. Основные побочные эффекты включают в себя гриппоподобные симптомы, гематологические нарушения и психоневрологические симптомы. Следовательно, существует необходимость в более эффективных, удобных и лучше переносимых способах лечения. Недавно в качестве клинических кандидатов внимание привлекли два пептидомиметикаингибитора HCV-протеазы, а именно BILN-2061, описанный в заявке WO 00/59929, и VX-950, описанный в заявке WO 03/87092. Ряд подобных ингибиторов HCV-протеазы также описан в научной и патентной литературе. В настоящее время уже очевидно, что продолжительное введение BILN-2061 илиVX-950 способствует селекции мутантов HCV, которые резистентны к соответствующему лекарственному средству так называемых мутантов, ускользающих от лекарственного средства. Такие мутанты,ускользающие от лекарственного средства, имеют характерные мутации в геноме HCV-протеазы, а именно D168V, D168A и/или A156S. Соответственно, чтобы обеспечить потерпевших неудачу пациентов вариантами лечения, требуются дополнительные лекарственные средства с другими характеристиками резистентности, а комбинированная терапия с помощью нескольких лекарственных средств, вероятно,станет нормой в будущем, даже для терапии первого порядка. Кроме того, опыт работы с ВИЧ-лекарственными средствами и, в частности, с ингибиторами ВИЧпротеазы, делает акцент на том факте, что недостаточно оптимальная фармакокинетика и сложные схе-1 013475 мы приема лекарственного средства быстро приводят к нечаянным ошибкам в соблюдении требований приема. Это, в свою очередь, означает, что 24-часовая минимальная концентрация (минимальная концентрация в плазме) соответствующих лекарственных средств при схеме приема против ВИЧ часто опускается ниже пороговых значений IC90 или ED90 в течение значительных отрезков дня. Считается, что 24-часовой минимальный пороговый уровень, составляющий по меньшей мере IC50 и более реалистичноIC90 или ED90, имеет существенное значение для сдерживания роста мутантов, ускользающих от лекарственного средства. Достижение нужной фармакокинетики и метаболизма лекарственного средства для обеспечения таких минимальных пороговых уровней предъявляет строгие требования к созданию (к дизайну) лекарственных средств. Сильная природа пептидомиметиков-ингибиторов HCV-протеазы известного уровня техники с многократными пептидными связями создает фармакокинетические затруднения для эффективных схем приема лекарственного средства. Необходимы ингибиторы HCV, которые могут преодолеть недостатки современной HCV-терапии,такие как побочные эффекты, ограниченная эффективность, появление резистентности и ошибки в соблюдении требований приема. Заявка WO 05/037214 относится к макроциклическим карбоновым кислотам и ацилсульфонамидам как ингибиторам репликации HCV, a также к фармацевтическим композициям, способам лечения вируса гепатита С и способам лечения фиброза печени. Настоящее изобретение относится к ингибиторам HCV, которые имеют преимущества по одному или нескольким нижеперечисленным фармакологическим взаимосвязанным свойствам, то есть активности, пониженной цитотоксичности, улучшенной фармакокинетике, улучшенному профилю резистентности, приемлемой дозировке и уменьшению количества приемов. Кроме того, соединения по настоящему изобретению обладают относительно низкой молекулярной массой и легко синтезируются, исходя из исходных материалов, которые имеются в продаже или легко доступны благодаря процедурам синтеза, известным в данной области. Настоящее изобретение относится к ингибиторам репликации HCV, которые можно представить формулой (I) и к их N-оксидам, солям и стереоизомерам, в которой каждая пунктирная линия (представленная представляет собой необязательную двойную связь; какX представляет собой N, СН и, когда X содержит двойную связь, он представляет собой С;R2 представляет собой водород и, когда X представляет собой С или СН, R2 также может представлять собой C1-6-алкил;R4 и R5, взятые вместе с атомом азота, к которому они присоединены, образуют бициклическую кольцевую систему, выбранную из где указанная кольцевая система необязательно может быть замещена одним, двумя или тремя заместителями, независимо выбранными из галогена, гидрокси, оксо, нитро, циано, карбоксила, С 1-6-алкила,C1-6-алкокси, С 1-6-алкокси-С 1-6-алкила, C1-6-алкилкарбонила, C1-6-алкоксикарбонила, амино, азидо, меркапто, полигалоген-С 1-6-алкила;C1-6-алкил, необязательно замещенный С 3-7-циклоалкилом, арилом или Het; арил в виде группы или части группы представляет собой фенил или нафтил, каждый из которых необязательно может быть замещен одним, двумя или тремя заместителями, выбранными из галогена,-2 013475 гидрокси, нитро, циано, карбоксила, C1-6-алкила, C1-6-алкокси, С 1-6-алкокси-С 1-6-алкила, С 1-6 алкилкарбонила,амино, моно- или ди-С 1-6-алкиламино, азидо, меркапто, полигалоген-С 1-6-алкила, полигалоген-С 1-6-алкокси, С 3-7 циклоалкила, пирролидинила, пиперидинила, пиперазинила, 4-С 1-6-алкилпиперазинила, 4-С 1-6-алкилкарбонилпиперазинила и морфолинила, где морфолинильные и пиперидинильные группы необязательно могут быть замещены одним или двумя С 1-6-алкильными радикалами; и каждый Het в виде группы или части группы представляет собой 5 или 6-членное насыщенное, частично ненасыщенное или полностью ненасыщенное гетероциклическое кольцо, содержащее от 1 до 4 гетероатомов, каждый из которых независимо выбран из атомов азота, кислорода и серы, и необязательно замещенное одним, двумя или тремя заместителями, каждый из которых независимо выбран из группы, состоящей из галогена, гидрокси, нитро, циано, карбоксила, C1-6-алкила, C1-6-алкокси, С 1-6-алкокси-C1-6-алкила, C1-6-алкилкарбонила, амино, моно- или ди-С 1-6-алкиламино, азидо, меркапто, полигалоген-С 1-6-алкила, полигалоген-С 1-6-алкокси, С 3-7-циклоалкила, пирролидинила, пиперидинила, пиперазинила, 4-С 1-6-алкилпиперазинила, 4-C1-6-алкилкарбонилпиперазинила и морфолинила, где морфолинильные и пиперидинильные группы необязательно могут быть замещены одним или двумя C1-6-алкильными радикалами. Изобретение дополнительно относится к способам получения соединений формулы (I), N-оксидов,аддитивных солей, четвертичных аминов, комплексов с металлами и их стереохимически изомерных форм, их промежуточных продуктов, и применению промежуточных продуктов для получения соединений формулы (I). Изобретение относится к соединениям формулы (I) как таковым, их N-оксидам, аддитивным солям,четвертичным аминам, комплексам с металлами и их стереохимически изомерным формам для применения в качестве лекарственного средства. Изобретение дополнительно относится к фармацевтическим композициям, содержащим вышеупомянутые соединения, предназначенные для введения субъекту, страдающему от HCV-инфекции. Фармацевтические композиции могут содержать комбинации вышеупомянутых соединений с другими средствами против HCV. Изобретение также относится к применению соединения формулы (I) или его N-оксида, аддитивной соли, четвертичного амина, комплекса с металлом или их стереохимически изомерных форм для производства лекарственного средства, предназначенного для ингибирования репликации HCV. Или изобретение относится к способу ингибирования репликации HCV у теплокровного животного упомянутым способом, включающим в себя введение эффективного количества соединения формулы (I) или егоN-оксида, аддитивной соли, четвертичного амина, комплекса с металлом или их стереохимически изомерных форм. Если не указано иначе, в качестве применяемых выше и в дальнейшем используются следующие определения. Термин галоген относится к фтору, хлору, брому и йоду. Термин полигалоген-С 1-6-алкил в виде группы или части группы, например в полигалоген-С 1-6 алкокси, определяется как моно- или полигалогензамещенный C1-6-алкил, в частности C1-6-алкил, замещенный одним, двумя, тремя, четырьмя, пятью, шестью или более атомами галогенов, такой как метил или этил с одним или несколькими атомами фтора, например дифторметил, трифторметил, трифторэтил. Предпочтительным является трифторметил. Также включены перфтор-С 1-6-алкильные группы, которые представляют собой C1-6-алкильные группы, в которых все атомы водорода замещены атомами фтора,например пентафторэтил. В том случае, когда к алкильной группе присоединяется более одного атома галогена, в пределах определения полигалоген-С 1-6-алкила атомы галогенов могут быть одинаковыми или разными. Применяемый здесь термин C1-4-алкил в виде группы или части группы определяет насыщенные углеводородные радикалы с прямой или разветвленной цепью, содержащие от 1 до 4 атомов углерода,такие как, например, метил, этил, 1-пропил, 2-пропил, 1-бутил, 2-бутил, 2-метил-1-пропил; C1-6-алкил охватывает С 1-4-алкильные радикалы и их высшие гомологи, содержащие 5 или 6 атомов углерода, такие как, например, 1-пентил, 2-пентил, 3-пентил, 1-гексил, 2-гексил, 2-метил-1-бутил, 2-метил-1-пентил,2-этил-1-бутил, 3-метил-2-пентил и т.п. Среди C1-6-алкильных групп интерес представляет C1-4-алкил. Термин С 2-6-алкенил в виде группы или части группы определяет углеводородные радикалы с прямой и разветвленной цепью, содержащие насыщенные углерод-углеродные связи и по меньшей мере одну двойную связь и содержащие от 2 до 6 атомов углерода, такие как, например, этенил (или винил),1-пропенил, 2-пропенил (или аллил), 1-бутенил, 2-бутенил, 3-бутенил, 2-метил-2-пропенил, 2-пентенил,3-пентенил, 2-гексенил, 3-гексенил, 4-гексенил, 2-метил-2-бутенил, 2-метил-2-пентенил и т.п. Среди С 2-6-алкенильных групп интерес представляет С 2-4-алкенил. Термин С 2-6-алкинил в виде группы или части группы определяет углеводородные радикалы с прямой и разветвленной цепью, содержащие насыщенные углерод-углеродные связи и по меньшей мере одну тройную связь и содержащие от 2 до 6 атомов углерода, такие как, например, этинил, 1-пропинил,2-пропинил, 1-бутинил, 2-бутинил, 3-бутинил, 2-пентинил, 3-пентинил, 2-гексинил, 3-гексинил и т.п. Среди С 2-6-алкинильных групп интерес представляет С 2-4-алкинил. С 3-7-Циклоалкил относится к циклопропилу, циклобутилу, циклопентилу, циклогексилу и цикло-3 013475 гептилу.C1-б-Алкандиил определяет двухвалентные насыщенные углеводородные радикалы с прямой и разветвленной цепью, содержащие от 1 до 6 атомов углерода, такие как, например, метилен, этилен,1,3-пропандиил, 1,4-бутандиил, 1,2-пропандиил, 2,3-бутандиил, 1,5-пентандиил, 1,6-гександиил и т.п. Среди C1-6-алкандиильных групп интерес представляет C1-4-алкандиил.C1-6-Алкокси означает C1-6-алкилокси, в которой C1-6-алкил имеет указанное выше значение. Уже применяемый здесь термин (=O) или оксо образует карбонильный фрагмент, когда присоединяется к атому углерода, сульфоксидный фрагмент, когда присоединяется к атому серы, и сульфонильный фрагмент, когда два упомянутых оксо присоединяются к атому серы. Всякий раз, когда кольцо или кольцевая система замещена оксогруппой, атом углерода, с которым соединяется оксогруппа, представляет собой насыщенный атом углерода. Радикал Het представляет собой гетероцикл, который подробно описан в данном описании и формуле изобретения. Примеры Het включают в себя, например, пирролидинил, пиперидинил, морфолинил,тиоморфолинил, пиперазинил, пирролил, имидазолил, оксазолил, изоксазолил, тиазинолил, изотиазинолил, тиазолил, изотиазолил, оксадиазолил, тиадиазолил, триазолил (включая 1,2,3-триазолил, 1,2,4 триазолил), тетразолил, фуранил, тиенил, пиридил, пиримидил, пиридазинил, пиразолил, триазинил и т.п. Среди радикалов Het представляют интерес те радикалы Het, которые являются ненасыщенными, в частности радикалы, имеющие ароматический характер. Дополнительный интерес представляют те радикалы Het, которые содержат один или два атома азота. Каждый из радикалов Het, упомянутых в данном и следующих параграфах, необязательно может быть замещен некоторым числом и типом заместителей, упомянутых в определениях соединений формулы (I) или любых подгрупп соединений формулы (I). Некоторые из радикалов Het, упомянутых в данном и следующих параграфах, могут быть замещены одним, двумя или тремя гидроксизаместителями. Такие гидроксизамещенные кольца могут встречаться в виде своих таутомерных форм, содержащих кетогруппы. Например, 3-гидроксипиридазиновый фрагмент может встречаться в своей таутомерной форме 2 Н-пиридазин-3-она. Когда Het представляет собой пиперазинил, он предпочтительно замещен в своем положении 4 заместителем, присоединенным к 4-азоту с помощью атома углерода, например 4-С 1-6-алкилом,4-полигалоген-C1-6-алкилом, С 1-6-алкокси-С 1-6-алкилом, C1-6-алкилкарбонилом, С 3-7-циклоалкилом. Представляющие интерес радикалы Het включают в себя, например, пирролидинил, пиперидинил, морфолинил, тиоморфолинил, пиперазинил, пирролил, пиразолил, имидазолил, оксазолил, изоксазолил, тиазолил, изотиазолил, оксадиазолил, тиадиазолил, триазолил (включая 1,2,3-триазолил, 1,2,4-триазолил), тетразолил, фуранил, тиенил, пиридил, пиримидил, пиридазинил, пиразолил, триазинил или любые из таких гетероциклов, конденсированных с бензольным кольцом, такие как индолил, индазолил (в частности, 1 Н-индазолил), индолинил,хинолинил, тетрагидрохинолинил (в частности, 1,2,3,4-тетрагидрохинолинил), изохинолинил, тетрагидроизохинолинил (в частности, 1,2,3,4-тетрагидроизохинолинил), хиназолинил, фталазинил, бензимидазолил, бензоксазолил, бензизоксазолил, бензотиазолил, бензоксадиазолил, бензотиадиазолил, бензофуранил, бензотиенил. Радикалы Het пирролидинил, пиперидинил, морфолинил, тиоморфолинил, пиперазинил, 4-замещенный пиперазинил предпочтительно присоединяются с помощью своего атома азота (то есть 1-пирролидинил, 1 пиперидинил, 4-тиоморфолинил, 4-морфолинил, 1-пиперазинил, 4-замещенный 1-пиперазинил). Следует отметить, что положения радикалов на любом молекулярном фрагменте, указанные в определениях, могут находиться на таком фрагменте где угодно, при условии, что он химически стабилен. Если не указано иначе, радикалы, применяемые в определениях переменных, включают в себя все возможные изомеры. Например, пиридил включает в себя 2-пиридил, 3-пиридил и 4-пиридил; пентил включает в себя 1-пентил, 2-пентил и 3-пентил. Когда любая переменная в любом составляющем элементе встречается более одного раза, каждое определение является независимым. Всякий раз, когда в дальнейшем применяется термин соединения формулы (I) или настоящие соединения или подобные термины, это означает, что они включают в себя соединения формулы (I),каждую и любую из их подгрупп, их пролекарства, N-оксиды, аддитивные соли, четвертичные амины,комплексы с металлами и стереохимически изомерные формы. Один из вариантов осуществления изобретения включает в себя соединения формулы (I) или любую указанную здесь подгруппу соединений формулы (I), а также N-оксиды, соли в виде их возможных стереоизомерных форм. Другой вариант осуществления включает в себя соединения формулы (I) или любую указанную здесь подгруппу соединений формулы (I), а также соли в виде их возможных стереоизомерных форм. Соединения формулы (I) имеют несколько центров хиральности и существуют в виде стереохимически изомерных форм. Применяемый здесь термин стереохимически изомерные формы определяет все возможные соединения, состоящие из одинаковых атомов, связанных одинаковой последовательностью связей, но имеющие разные трехмерные структуры, которые не являются взаимно заменяемыми и которыми соединения формулы (I) могут обладать. При ссылке на примеры, в которых для обозначения абсолютной конфигурации хирального атома в заместителе применяются (R) или (S), соединение рассматривается в целом и без отрыва заместителя. Если не упомянуто или не указано иначе, химическое название соединения охватывает смесь всех-4 013475 возможных стереохимически изомерных форм, которыми упомянутое соединение может обладать. Упомянутая смесь может содержать все диастереомеры и/или энантиомеры основной молекулярной структуры упомянутого соединения. Разумеется, все стереохимически изомерные формы соединений по настоящему изобретению как в чистой форме, так и смешанные друг с другом подлежат включению в объем настоящего изобретения. Чистые стереоизомерные формы соединений и промежуточных продуктов, которые здесь упоминаются, определяются как изомеры, по существу, не содержащие других энантиомерных или диастереомерных форм той же самой основной молекулярной структуры упомянутых соединений или промежуточных продуктов. В частности, термин стереоизомерно чистый относится к соединениям или промежуточным продуктам, содержащим избыток стереоизомера по меньшей мере от 80% (то есть минимум 90% одного изомера и максимум 10% других возможных изомеров) вплоть до избытка стереоизомера 100% (то есть 100% одного изомера и отсутствие другого изомера), более конкретно, к соединениям или промежуточным продуктам, содержащим избыток стереоизомера от 90 вплоть до 100%, еще более конкретно, содержащим избыток стереоизомера от 94 вплоть до 100%, и наиболее конкретно, содержащим избыток стереоизомера от 97 вплоть до 100%. Термины энантиомерно чистый и диастереомерно чистый в обсуждаемом вопросе следует понимать подобным образом, однако в таком случае они относятся, соответственно, к избытку энантиомера и избытку диастереомера в смеси. Чистые стереоизомерные формы соединений и промежуточных продуктов по данному изобретению можно получать путем применения известных в данной области процедур. Например, энантиомеры можно отделять друг от друга с помощью избирательной кристаллизации их диастереомерных солей с оптически активными кислотами или основаниями. Их примерами являются винная кислота, дибензоилвинная кислота, дитолуоилвинная кислота и камфорсульфокислота. Альтернативно, энантиомеры можно разделять с помощью хроматографических способов, применяя хиральные неподвижные фазы. Упомянутые чистые стереохимически изомерные формы также можно получать из соответствующих стереохимически чистых изомерных форм подходящих исходных материалов, при условии, что происходит стереоспецифическая реакция. Если требуется определенный стереоизомер, предпочтительно упомянутое соединение синтезировать с помощью стереоспецифических способов получения. В таких способах преимущественно будут использоваться энантиомерно чистые исходные материалы. Диастереомерные рацематы соединений формулы (I) можно получать по отдельности с помощью традиционных способов. Подходящими физическими способами разделения, которые преимущественно можно использовать, например, являются избирательная кристаллизация и хроматография, например колоночная хроматография. Для некоторых из соединений формулы (I), их пролекарств, N-оксидов, солей, сольватов, четвертичных аминов или комплексов с металлами и промежуточных продуктов, применяемых для их получения, абсолютные стереохимические конфигурации экспериментально не определялись. Специалист в данной области способен определить абсолютную конфигурацию таких соединений, применяя известные в данной области способы, такие как, например, рентгенодифракционный метод. Также, разумеется, что настоящее изобретение включает в себя все изотопы атомов, встречающихся в настоящих соединениях. Изотопы включают в себя те атомы, которые имеют одинаковый атомный номер, но разные массовые числа. В качестве обычного примера и без ограничения изотопы водорода включают в себя тритий и дейтерий. Изотопы углерода включают в себя С-13 и С-14. Также, разумеется, что настоящее изобретение включает в себя пролекарства соединений формулы(I). Применяемый на всем протяжении данного текста термин пролекарство означает фармакологически приемлемые производные, такие как сложные эфиры, амиды и фосфаты, такие, что полученный в результате продукт биотрансформации производного в организме (in vivo) представляет собой активное лекарственное средство, которое определено в соединениях формулы (I). Здесь включена ссылка на публикацию авторов Goodman и Gilman (The Pharmacological Basis of Therapeutics, 8-е изд., McGraw-Hill, Int.Ed. 1992, Biotransformation of Drugs, с.13-15), описывающая пролекарства в целом. Пролекарства предпочтительно обладают прекрасной растворимостью в воде, повышенной биодоступностью и в процессе обмена веществ в организме (in vivo) легко превращаются в активные ингибиторы. Пролекарства соединения по настоящему изобретению можно получать путем модификации присутствующих в соединении функциональных групп таким образом, чтобы модификации расщеплялись до исходного соединения либо с помощью обычной манипуляции, либо в организме (in vivo). Предпочтительными являются фармацевтически приемлемые, сложноэфирные пролекарства, которые гидролизуются в организме (in vivo) и являются производными от тех соединений формулы (I), которые содержат гидрокси- или карбоксильную группу. Гидролизуемый в организме (in vivo) сложный эфир представляет собой сложный эфир, который гидролизуется в организме человека или животного с образованием исходной кислоты или спирта. Подходящие фармацевтически приемлемые сложные эфиры для карбоксигруппы включают в себя сложные C1-6-алкоксиметиловые эфиры, например метоксиметиловый, сложные C1-6-алканоилоксиметиловые эфиры, например сложные пивалоилоксиметиловые,фталидиловые эфиры, сложные С 3-8-циклоалкоксикарбонилокси-С 1-6-алкиловые эфиры, например 1-циклогексилкарбонилоксиэтиловый; сложные 1,3-диоксолен-2-онилметиловые эфиры, например-5 013475 5-метил-1,3-диоксолен-2-онилметиловый, и сложные C1-6-алкоксикарбонилоксиэтиловые эфиры, например 1-метоксикарбонилоксиэтиловый, которые можно образовывать в соединениях по данному изобретению на любой карбоксигруппе. Гидролизуемый в организме (in vivo) сложный эфир соединения формулы (I), содержащего гидрокси-группу, включает в себя неорганические сложные эфиры, такие как сложные эфиры фосфорной кислоты, простые -ацилоксиалкиловые эфиры и родственные соединения, которые в результате гидролиза сложного эфира в организме (in vivo) разлагаются, давая при этом исходную гидроксигруппу. Примеры простых -ацилоксиалкиловых эфиров включают в себя ацетоксиметокси и 2,2-диметилпропионилоксиметокси. Выбор гидролизуемого в организме (in vivo) сложного эфира, образующего группы для гидрокси, включает в себя алканоил, бензоил, фенилацетил и замещенные бензоил и фенилацетил, алкоксикарбонил (для получения сложных алкилкарбонатных эфиров), диалкилкарбамоил и N-(диалкиламиноэтил)-N-алкилкарбамоил (для получения карбаматов), диалкиламиноацетил и карбоксиацетил. Примеры заместителей на бензоиле включают в себя морфолино- и пиперазиногруппы, соединенные с кольцевым атомом азота через посредство метиленовой группы в 3- или 4-положении бензоильного кольца. Соли соединения формулы (I) для терапевтического применения представляют собой те соли, в которых противоион является фармацевтически приемлемым. Однако также могут найти применение соли кислот и оснований, которые не являются фармацевтически приемлемыми, например, для получения или очистки фармацевтически приемлемого соединения. Все соли, являются они фармацевтически приемлемыми или нет, включены в объем настоящего изобретения. Разумеется, что упомянутые выше фармацевтически приемлемые аддитивные соли кислот и оснований содержат терапевтически активные, нетоксичные формы аддитивных солей кислот и оснований,которые способны образовывать соединения формулы (I). Фармацевтически приемлемые аддитивные соли кислот можно удобно получать путем обработки основной формы такой подходящей кислотой. Подходящие кислоты включают в себя, например, неорганические кислоты, такие как галогенводородные кислоты, например хлористо-водородную или бромисто-водородную кислоты, серную, азотную,фосфорную и тому подобные кислоты, или органические кислоты, такие как, например, уксусная, пропановая, гидроксиуксусная (гликолевая), молочная, пировиноградная, щавелевая (то есть этандикислота),малоновая, янтарная (то есть бутандикислота), малеиновая, фумаровая, яблочная (то есть гидроксибутандикислота), винная, лимонная, метансульфоновая, этансульфоновая, бензолсульфоновая, п-толуолсульфоновая, цикламовая, салициловая, п-аминосалициловая, памовая и тому подобные кислоты. С другой стороны, упомянутые формы солей путем обработки подходящим основанием можно преобразовывать в форму свободного основания. Соединения формулы (I), содержащие кислотный протон, путем обработки подходящими органическими и неорганическими основаниями также можно преобразовывать в формы их аддитивных солей с нетоксичными металлами или аминами. Формы подходящих основных солей включают в себя, например, соли аммония, соли щелочных и щелочно-земельных металлов, например соли лития, натрия, калия,магния, кальция и т.п., соли с органическими основаниями, например соли бензатина, N-метил-Dглюкамина, гидрабамина, и соли с аминокислотами, такими как, например, аргинин, лизин и т.п. Применяемый выше термин аддитивная соль также включает в себя сольваты, которые способны образовывать соединения формулы (I), а также их соли. Такие сольваты представляют собой, например,гидраты, алкоголяты и т.п. Применяемый выше термин четвертичный амин определяет соли четвертичного аммония, которые способны образовывать соединения формулы (I) при взаимодействии атома основного азота соединения формулы (I) и подходящего кватернизирующего агента, такого как, например, необязательно замещенный алкилгалогенид, арилгалогенид или арилалкилгалогенид, например метилйодид или бензилйодид. Также можно применять другие реагенты с подходящими удаляемыми группами, такие как алкилтрифторметансульфонаты, алкилметансульфонаты и алкил-п-толуолсульфонаты. Четвертичный амин содержит положительно заряженный атом азота. Фармацевтически приемлемые противоионы включают в себя хлор, бром, йод, трифторацетат и ацетат. Выбранный противоион можно вводить, применяя ионообменные смолы. Подразумевается, что N-оксидная форма настоящих соединений включает в себя соединения формулы (I), в которых один или несколько атомов азота окислены до так называемого N-оксида. Следует учитывать, что соединения формулы (I) могут образовывать связи с металлами, иметь хелатообразующие и комплексообразующие свойства и, следовательно, могут существовать в виде комплексов с металлами или хелатов металлов. Разумеется, что такие металлированные производные соединений формулы (I) подлежат включению в объем настоящего изобретения. Некоторые из соединений формулы (I) также могут существовать в своей таутомерной форме. Разумеется, такие формы, хотя и в неявной форме указанные в вышеупомянутой формуле, подлежат включению в объем настоящего изобретения. Как упомянуто выше, соединения формулы (I) содержат несколько центров асимметрии. Для того-6 013475 чтобы более эффективно ссылаться на каждый из таких центров асимметрии, будет применяться система нумерации, указанная в следующей структурной формуле. Центры асимметрии находятся в положениях 1, 4 и 6 макроцикла, а также на атоме углерода 3' в 5-членном кольце, атоме углерода 2', когда заместитель R2 представляет собой C1-6-алкил, и на атоме углерода 1', когда X представляет собой СН. Каждый из таких центров асимметрии может встречаться в своей R-или S-конфигурации. Стереохимия в положении 1 предпочтительно соответствует стереохимии конфигурацииL-аминокислоты, то есть стереохимии L-пролина. Когда X представляет собой СН, 2 карбонильные группы, замещающие циклопентановое кольцо в положениях 1' и 5', предпочтительно находятся в транс-конфигурации. Карбонильный заместитель в положении 5' предпочтительно находится в той конфигурации, которая соответствует конфигурации Соединения формулы (I) включают в себя циклопропильную группу, которая представлена ниже в структурном фрагменте в котором С 7 представляет собой атом углерода в положении 7, и атомы углерода в положении 4 и 6 являются асимметрическими атомами углерода циклопропанового кольца. Невзирая на другие возможные центры асимметрии, находящиеся в других сегментах соединений формулы (I), присутствие двух таких центров асимметрии означает, что соединения могут существовать в виде смесей диастереомеров, таких как диастереомеры соединений формулы (I), в которых атом углерода в положении 7 имеет конфигурацию либо син- по отношению к карбонилу, либо син- по отношению к амиду, как показано ниже. Один из вариантов осуществления изобретения относится к соединениям формулы (I), в которых-7 013475 атом углерода в положении 7 имеет син-конфигурацию по отношению к карбонилу. Другой вариант осуществления изобретения относится к соединениям формулы (I), в которых конфигурация на атоме углерода в положении 4 представляет собой R-конфигурацию. Специфическую подгруппу соединений формулы (I) представляют соединения, в которых атом углерода в положении 7 имеет син-конфигурацию по отношению к карбонилу и в которых конфигурация на атоме углерода в положении 4 представляет собой R-конфигурацию. Соединения формулы (I) могут включать в себя пролиновый остаток (когда X представляет собойN) или циклопентильный или циклопентенильный остаток (когда X представляет собой СН или С). Предпочтительными являются соединения формулы (I), в которых заместитель в положении 1 (или 5') и карбаматный заместитель в положении 3' находятся в транс-конфигурации. Особый интерес представляют соединения формулы (I), которые в положении 1 имеют конфигурацию, соответствующую Lпролину, и карбаматный заместитель в положении 3' находится в транс-конфигурации по отношению к положению 1. Предпочтительно соединения формулы (I) имеют такую стереохимию, которая указана ниже в структурных формулах (I-а) и (I-b) Один из вариантов осуществления настоящего изобретения относится к соединениям формулы (I) или формулы (I-а), или к любой подгруппе соединений формулы (I), в которых осуществляется одно или несколько из следующих условий:(c) между атомами углерода 7 и 8 присутствует двойная связь. Один из вариантов осуществления настоящего изобретения относится к соединениям формулы (I) или формул (I-a), (I-b), или к любой подгруппе соединений формулы (I), в которых осуществляется одно или несколько из следующих условий:(c) между атомами углерода 7 и 8 присутствует двойная связь. Особыми подгруппами соединений формулы (I) являются подгруппы, представленные следующими структурными формулами: Среди соединений формулы (I-c) и (I-d) особый интерес представляют собой соединения, имеющие стереохимические конфигурации соединений формул (I-а) и (I-b) соответственно. Двойная связь между атомами углерода 7 и 8 в соединениях формулы (I) или в любой подгруппе соединений формулы (I) может иметь цис- или транс-конфигурацию. Предпочтительно двойная связь между атомами углерода 7 и 8 имеет цис-конфигурацию, которая изображена в формулах (I-c) и (I-d).-8 013475 В соединениях формулы (I) или в любой подгруппе соединений формулы (I) между атомами углерода 1' и 2' может присутствовать двойная связь, которая изображена ниже в формуле (I-е). Еще одну особую подгруппу соединений формулы (I) представляют соединения, представленные следующими структурными формулами: Среди соединений формул (I-f), (I-g) или (I-h) особый интерес представляют соединения, имеющие стереохимическую конфигурацию соединений формул (I-а) и (I-b). В формулах (I-a), (I-b), (I-с), (I-d), (I-е), (I-f), (I-g) и (I-h), где это применимо, X, n, R1, R2, R3, R4 и R5 имеют значения, указанные в определениях соединений формулы (I) или в любой из указанных здесь подгрупп соединений формулы (I). Разумеется, следует понимать, что определенные выше подгруппы соединений формул (I-а), (I-b),(I-с), (I-d), (I-е), (I-f), (I-g) или (I-h), а также любых других указанных здесь подгрупп также включают в себя любые пролекарства, N-оксиды, аддитивные соли, четвертичные амины, комплексы с металлами и стереохимически изомерные формы таких соединений. Когда n равно 2, заключенный в скобки фрагмент (-СН 2-)n в соединениях формулы (I) или в любой подгруппе соединений формулы (I) соответствует этандиилу. Когда n равно 3, заключенный в скобки фрагмент (-СН 2-)n в соединениях формулы (I) или в любой подгруппе соединений формулы (I) соответствует пропандиилу. Когда n равно 4, заключенный в скобки фрагмент (-СН 2-)n в соединениях формулы(I) или в любой подгруппе соединений формулы (I) соответствует бутандиилу. Когда n равно 5, заключенный в скобки фрагмент (-СН 2-)n в соединениях формулы (I) или в любой подгруппе соединений формулы (I) соответствует пентандиилу. Когда n равно 6, заключенный в скобки фрагмент (-СН 2-)n в соединениях формулы (I) или в любой подгруппе соединений формулы (I) соответствует гександиилу.-9 013475 Соединения, в которых n равно 4 или 5, представляют собой особые подгруппы соединений формулы (I). Варианты осуществления изобретения относятся к соединениям формулы (I) или любой из подгрупп соединений формулы (I), в которой:(a) R1 представляет собой группу -OR6, в частности группу, в которой R6 представляет собой(b) R1 представляет собой группу -NHS(=O)2R7, в частности группу, в которой R7 представляет собой C1-6-алкил, С 3-С 7-циклоалкил или арил, например в которых R7 представляет собой метил, циклопропил или фенил; или(с) R1 представляет собой группу -NHS(=O)2R7, в частности группу, в которой R7 представляет собой С 3-7-циклоалкил, замещенный C1-6-алкилом, предпочтительно в которых R7 представляет собой циклопропил, циклобутил, циклопентил или циклогексил, любой из которых замещен C1-4-алкилом, то есть метилом, этилом, пропилом, изопропилом, бутилом, трет-бутилом или изобутилом. Дополнительные варианты осуществления изобретения относятся к соединениям формулы (I) или любой из подгрупп соединений формулы (I), в которой R1 представляет собой NHS(=O)2R7, в частности в которой R7 представляет собой циклопропил, замещенный C1-4-алкилом, то есть метилом, этилом, пропилом или изопропилом. Дополнительные варианты осуществления изобретения относятся к соединениям формулы (I) или любой из подгрупп соединений формулы (I), в которой R1 представляет собой NHS(=O)2R7, в частности,в которой R7 представляет собой 1-метилциклопропил. Дополнительные варианты осуществления изобретения относятся к соединениям формулы (I) или любой из подгрупп соединений формулы (I), в которой:(b) R2 представляет собой C1-6-алкил, предпочтительно метил. Варианты осуществления изобретения относятся к соединениям формулы (I) или любой из подгрупп соединений формулы (I), в которой:C1-6-алкил, предпочтительно метил. Дополнительные варианты осуществления изобретения относятся к соединениям формулы (I) или любой из подгрупп соединений формулы (I), в которой:(d) R3 представляет собой С 1-6-алкокси-С 1-6-алкил или С 3-7-циклоалкил. Предпочтительные варианты осуществления изобретения относятся к соединениям формулы (I) или любой из подгрупп соединений формулы (I), в которых R3 представляет собой водород или C1-6-алкил,более предпочтительно водород или метил. Варианты осуществления изобретения относятся к соединениям формулы (I) или любой из подгрупп соединений формулы (I), в которой R4 и R5, взятые вместе с атомом азота, к которому они присоединены, образуют бициклическую кольцевую систему, выбранную из где указанная кольцевая система необязательно может быть замещена одним или двумя заместителями, независимо выбранными из галогена, гидрокси, оксо, циано, карбоксила C1-6-алкила, C1-6-алкокси,С 1-6-алкокси-С 1-6-алкила, С 1-6-алкоксикарбонила, амино и полигалоген-С 1-6-алкила. Другая подгруппа соединений формулы (I) представляет собой соединения формулы (I) или любую указанную здесь подгруппу соединений формулы (I), в которых R4 и R5, взятые вместе с атомом азота, к которому они присоединены, образуют бициклическую кольцевую систему, выбранную из где указанная кольцевая система необязательно может быть замещена одним или двумя заместителями, независимо выбранными из фтора, хлора, гидрокси, оксо, циано, карбоксила, метила, этила, изопропила, т-бутила, метокси, этокси, изопропокси, трет-бутокси, метоксиэтила, этоксиметила, метокси- 10013475 карбонила, этоксикарбонила, амино и трифторметила. Варианты осуществления изобретения относятся к соединениям формулы (I) или любой из подгрупп соединений формулы (I), в которых R4 и R5, взятые вместе с атомом азота, к которому они присоединены, образуют бициклическую кольцевую систему, выбранную из в которых фенил упомянутой бициклической кольцевой системы необязательно замещен одним или двумя заместителями, независимо выбранными из галогена, гидрокси, циано, карбоксила, C1-6-алкила,С 1-6-алкокси, C1-6-алкоксикарбонила, амино и полигалоген-C1-6-алкила. Варианты осуществления изобретения относятся к соединениям формулы (I) или любой из подгрупп соединений формулы (I), в которых R4 и R5, взятые вместе с атомом азота, к которому они присоединены, образуют бициклическую кольцевую систему, выбранную из в которых упомянутая бициклическая кольцевая система необязательно замещена на фенильной части, предпочтительно в положениях, указанных выше с помощью пунктирных линий, одним или двумя заместителями, независимо выбранными из галогена, гидрокси, циано, карбоксила, C1-6-алкила,C1-6-алкокси, C1-6-алкоксикарбонила, амино и полигалоген-С 1-6-алкила. Варианты осуществления изобретения относятся к соединениям формулы (I) или любой из подгрупп соединений формулы (I), в которых R4 и R5, взятые вместе с атомом азота, к которому они присоединены, образуют бициклическую кольцевую систему, выбранную из в которых пирролидиновые, пиперидиновые или морфолиновые кольца упомянутой бициклической кольцевой системы необязательно замещены одним или двумя заместителями, независимо выбранными из C1-6-алкила, C1-6-алкокси и С 1-6-алкокси-С 1-6-алкила. Варианты осуществления изобретения относятся к соединениям формулы (I) или любой из подгрупп соединений формулы (I), в которых R4 и R5, взятые вместе с атомом азота, к которому они присоединены, образуют бициклическую кольцевую систему, выбранную из в которых фенил упомянутой бициклической кольцевой системы необязательно замещен одним заместителем, независимо выбранным из галогена, гидрокси, циано, карбоксила, C1-6-алкила, C1-6-алкокси,C1-6-алкоксикарбонила, амино и полигалоген-С 1-6-алкила; и в которых пирролидиновые, пиперидиновые или морфолиновые кольца упомянутой бициклической кольцевой системы необязательно замещены одним заместителем, независимо выбранным из C1-6-алкила, C1-6-алкокси и С 1-6-алкокси-С 1-6-алкила.- 11013475 Варианты осуществления изобретения относятся к соединениям формулы (I) или любой из подгрупп соединений формулы (I), в которых R4 и R5, взятые вместе с атомом азота, к которому они присоединены, образуют бициклическую кольцевую систему, выбранную из в которых упомянутая бициклическая кольцевая система необязательно замещена в указанных выше положениях одним или двумя заместителями, независимо выбранными из C1-6-алкила, C1-6-алкокси и С 1-6-алкокси-С 1-6-алкила. Предпочтительные варианты осуществления изобретения относятся к соединениям формулы (I) или любой из подгрупп соединений формулы (I), в которых R4 и R5, взятые вместе с атомом азота, к которому они присоединены, образуют бициклическую кольцевую систему, выбранную из Соединения формулы (I) состоят из трех структурных элементов Р 1, Р 2, Р 3. Структурный элемент Р 1 дополнительно содержит концевую часть Р 1'. Карбонильная группа, ниже в соединении (I-c) отмеченная звездочкой, может быть частью либо структурного элемента Р 2, либо структурного элемента Р 3. По химическим соображениям структурный элемент Р 2 соединений формулы (I), в котором X представляет собой С, включает в себя карбонильную группу, присоединенную в положении 1'. Соединение структурных элементов Р 1 с Р 2, Р 2 с Р 3 и Р 1 с Р 1' (когда R1 представляет собой-NH-SO2R7) предусматривает образование амидной связи. Соединение элементов Р 1 и Р 3 предусматривает образование двойной связи. Соединение структурных элементов P1, P2 и Р 3 для получения соединений (I-i) или (I-j) может выполняться в любой заданной последовательности. Одна из стадий предусматривает циклизацию, с помощью которой образуется макроцикл. Ниже представлены соединения (I-i), которые относятся к соединениям формулы (I), в которой атомы углерода С 7 и С 8 соединены двойной связью, и соединения (I-j), которые относятся к соединениям формулы (I), в которой атомы углерода С 7 и С 8 соединены одинарной связью. Соединения формулы(I-j) можно получать из соответствующих соединений формулы (I-i) путем восстановления двойной связи в макроцикле. Разумеется, что описанные в дальнейшем процедуры синтеза должны быть применимы в равной степени к рацематам, стереохимически чистым промежуточным продуктам или конечным продуктам или любым смесям стереоизомеров. Рацематы или смеси стереоизомеров можно разделять на стереоизомерные формы на любой стадии процедур синтеза. В одном из вариантов осуществления изобретения промежуточные продукты и конечные продукты имеют стереохимию, указанную выше в соединениях фор- 12013475 мулы (I-а) и (I-b). В описанных далее процедурах синтеза R8 представляет собой радикал в котором пунктирная линия представляет собой связь, с помощью которой радикал присоединяется к остальной молекуле. В предпочтительном варианте осуществления изобретения соединения (I), в которых связь между атомами углерода С 7 и С 8 является двойной связью и которые представляют собой указанные выше соединения формулы (I-i), можно получать, как кратко изложено на следующей реакционной схеме: Образование макроцикла можно осуществлять с помощью реакции метатезиса олефинов в присутствии подходящего металлического катализатора, такого как, например, катализатор на основе Ru, о котором сообщается в публикациях Miller S.J., Blackwell H.E., Grubbs R.H. J. Am. Chem. Soc. 118, (1996),9606-9614; Kingsbury J.S., Harrity J.P.A., Bonitatebus P.J., Hoveyda A.H. J. Am. Chem. Soc. 121, (1999),791-799 и Huang и др. J. Am. Chem. Soc. 121, (1999), 2674-2678; например катализатор Ховейды-Граббса(Hoveyda-Grubbs). Можно применять устойчивые на воздухе рутениевые катализаторы, такие как хлорид бис-(трициклогексилфосфин)-3-фенил-1 Н-инден-1-илиденрутения (Neolyst M1) или дихлорид бис-(трициклогексилфосфин)-[(фенилтио)метилен]рутения(IV). Другие катализаторы, которые можно применять,представляют собой катализаторы Граббса первого и второго поколений, то есть бензилиден-бис(трициклогексилфосфин)дихлоррутений и(1,3-бис-(2,4,6-триметилфенил)-2-имидазолидинилиден)дихлор(фенилметилен)-(трициклогексилфосфин)рутений соответственно. Особый интерес представляют катализаторы Ховейды-Граббса первого и второго поколений, которые представляют собой дихлор(оизопропоксифенилметилен)(трициклогексилфосфин)рутений(II) и 1,3-бис-(2,4,6-триметилфенил)-2 имидазолидинилиден)дихлор(о-изопропоксифенилметилен)рутений соответственно. Также для такой реакции можно применять другие катализаторы, содержащие другие переходные металлы, такие как Мо. Реакции метатезиса можно проводить в подходящем растворителе, например, таком как простые эфиры, например ТГФ, диоксан; галогенированные углеводороды, например дихлорметан, CHCl3,1,2-дихлорэтан и т.п., углеводороды, например толуол. В предпочтительном варианте осуществления реакцию метатезиса проводят в толуоле. Такие реакции проводят при повышенных температурах в атмосфере азота. Соединения формулы (I), в которых связь между атомами углерода С 7 и С 8 в макроцикле представляет собой одинарную связь, то есть соединения формулы (I-j), можно получать из соединений формулы(I-i) путем восстановления двойной связи С 7-С 8 в соединениях формулы (I-i). Такое восстановление можно проводить с помощью каталитического гидрирования водородом в присутствии катализатора на основе благородных металлов, например, таких как Pt, Pd, Rh, Ru или никель Ренея. Интерес представляет Rh на оксиде алюминия. Реакцию гидрирования предпочтительно проводят в растворителе, например,таком как спирт, такой как метанол, этанол или простой эфир, такой как ТГФ, или их смеси. К таким растворителям или смесям растворителей также можно добавлять воду. Группу R1 можно присоединять к структурному элементу Р 1 на любой стадии синтеза, то есть до или после циклизации, или до или после циклизации и восстановления, которые описаны выше. Соединения формулы (I), в которой R1 представляет собой NHSO2R7, упомянутые соединения представлены формулой (I-k-1), можно получать путем присоединения группы R1 к Р 1 с помощью образования между обоими фрагментами амидной связи. Подобным образом соединения формулы (I), в которых R1 представляет собой -OR6, то есть соединения (I-k-2), можно получать путем присоединения группы R1 к Р 1 с помощью образования сложноэфирной связи. В одном из вариантов осуществления изобретения группы-OR6 вводятся на последней стадии синтеза соединений (I), как кратко изложено в следующих схемах реакций, на которых G представляет собой группу: Промежуточный продукт (2 а) можно связывать с амином (2b) с помощью реакции образования амида, такой как любая из описанных в дальнейшем процедур образования амидной связи. В частности,(2 а) можно обрабатывать конденсирующим агентом, например N,N'-карбонилдиимидазолом (CDI),EEDQ, IIDQ, EDCI или гексафторфосфатом бензотриазол-1-илокси-трис-пирролидинофосфония (имеется в продаже под торговой маркой РуВОР) в растворителе, таком как простой эфир, например ТГФ или галогенированном углевороде, например дихлорметане, хлороформе, дихлорэтане, и проводить реакцию с требуемым сульфонамидом (2b) предпочтительно после взаимодействия (2 а) с конденсирующим агентом. Реакции промежуточного продукта (2 а) с промежуточным продуктом (2b) предпочтительно осуществляют в присутствии основания, например триалкиламина, такого как триэтиламин или диизопропилэтиламин, или в присутствии 1,8-диазабицикло[5.4.0]ундец-7-ена (DBU). Промежуточный продукт (2 а) также можно переводить в активированную форму, например в активированную форму общей формулыG-CO-Z, в которой Z представляет собой галоген или остаток активного сложного эфира, например Z представляет собой арилоксигруппу, такую как фенокси, п-нитрофенокси, пентафторфенокси, трихлорфенокси, пентахлорфенокси и т.п.; или Z может представлять собой остаток смешанного ангидрида. В одном из вариантов осуществления изобретения G-CO-Z представляет собой хлорангидрид (G-CO-Cl) или смешанный ангидрид (G-CO-O-CO-R или G-CO-O-CO-OR, в последнем случае R представляет собой, например, C1-4-алкил, такой как метил, этил, пропил, изопропил, бутил, т-бутил, изобутил или бензил). Активированную форму G-CO-Z подвергают взаимодействию с сульфонамидом (2b). Активация карбоновой кислоты в (2 а), как описано для упомянутых выше реакций, может приводить к реакции внутренней циклизации промежуточного азалактона формулы в которой значения X, R2, R3, R4, R5, n такие, как указано выше, и в которой стереогенные центры могут иметь указанные выше стереохимические конфигурации, например, как в соединениях (I-а) или(I-b). Промежуточные продукты (2 а-1) можно выделять из реакционной смеси, применяя традиционную методику, и выделенный промежуточный продукт (2 а-1) затем подвергать взаимодействию с (2b), или реакционную смесь, содержащую (2 а-1), можно дополнительно подвергать взаимодействию с (2b) без выделения (2 а-1). В одном из вариантов осуществления изобретения, когда реакцию с конденсирующим агентом осуществляют в несмешивающемся с водой растворителе, реакционную смесь, содержащую(2 а-1), можно промывать водой или слегка щелочной водой для того, чтобы удалить все водорастворимые побочные продукты. Полученный таким образом промытый раствор затем можно подвергать взаимодействию с (2b) без дополнительных стадий очистки. С другой стороны, выделение промежуточных продуктов (2 а-1) может обеспечить некоторые преимущества в том смысле, что выделенный продукт- 14013475 после необязательной дополнительной очистки можно подвергать взаимодействию с (2b), получая при этом меньшее количество побочных продуктов и добиваясь более простого осуществления реакции. Промежуточный продукт (2 а) можно связывать со спиртом (2 с) с помощью реакции образования сложного эфира. Например, (2 а) и (2 с) подвергают совместному взаимодействию с удалением воды либо физически, например путем азеотропного удаления воды, либо химически, применяя дегидратирующий агент. Промежуточный продукт (2 а) также можно переводить в активированную форму G-CO-Z, такую как упомянутые выше активированные формы, и затем подвергать взаимодействию со спиртом (2 с). Реакции образования сложных эфиров предпочтительно проводят в присутствии основания, такого как карбонат или гидрокарбонат щелочного металла, например гидрокарбонат натрия или калия, или третичного амина, такого как амины, упомянутые здесь в связи с реакциями образования амидов, в частности в присутствии триалкиламина, например триэтиламина. Растворители, которые можно применять в реакциях образования сложных эфиров, включают в себя простые эфиры, такие как ТГФ; галогенированные углеводороды, такие как дихлорметан, CH2Cl2; углеводороды, такие как толуол; полярные апротонные растворители, такие как ДМФА, DMSO, DMA; и тому подобные растворители. Соединения формулы (I), в которых R3 представляет собой водород, упомянутые соединения представлены формулой (I-1), также можно получать путем удаления защитной группы PG из соответствующего азотзащищенного промежуточного продукта (3 а), как показано на следующей реакционной схеме. Защитная группа PG, в частности, представляет собой любую из азотзащитных групп, упомянутых в дальнейшем, и может быть удалена с помощью процедур, также упомянутых в дальнейшем Исходные материалы (3 а) для указанной выше реакции можно получать, следуя процедурам получения соединений формулы (I), но применяя промежуточные продукты, в которых группа R3 представляет собой PG. Соединения формулы (I) также можно получать путем взаимодействия промежуточного продукта(4 а) с амином (4b) в присутствии реагента для образования карбамата, как кратко изложено на следующей реакционной схеме, на которой различные радикалы имеют указанные выше значения Реакцию промежуточных продуктов (4 а) с реагентом для образования карбамата проводят в присутствии таких же растворителей и оснований, которые применяются для образования амидной связи,как описано в дальнейшем. Реакции образования карбамата можно осуществлять с помощью ряда способов, в частности, путем взаимодействия аминов с алкилхлорформиатами; путем взаимодействия спиртов с карбамоилхлоридами или изоцианатами; с помощью реакций, включающих в себя комплексы металлов или агентов передачи ацильной группы. См., например, публикацию Greene T.W. и Wuts P.G.M. Protective Groups in OrganicSynthesis; 1999; Wiley and Sons, с.309-348. Для синтеза карбаматов из некоторых исходных соединений,включая амины, можно применять моноксид углерода и некоторые металлические катализаторы. В качестве катализаторов можно применять металлы, такие как палладий, иридий, уран и платину. Также можно применять способы, в которых для синтеза карбаматов применяется диоксид углерода, о которых также сообщалось ранее (см., например, публикации Yoshida Y. и др. Bull. Chem. Soc. Japan, 1989, 62,1534 и Aresta M. и др. Tetrahedron, 1991, 47, 9489).- 15013475 Один из подходов для получения карбаматов предусматривает применение промежуточных продуктов формулы в которой Q представляет собой удаляемую группу, такую как галоген, в частности хлор и бром,или группу, применяемую в активных сложных эфирах для образования амидной связи, такую как упомянутая выше группа, например фенокси или замещенная феноксигруппа, такая как п-хлор- и п-нитрофенокси, трихлорфенокси, пентахлорфенокси, N-гидроксисукцинимидил и т.п. Промежуточные продукты (4b) можно получать из спиртов (4 а) и фосгена, образуя при этом хлорформиат, или во втором случае путем переноса хлора в промежуточные продукты (5 а), которые представляют собой промежуточные продукты формулы (5), в которой Q представляет собой Q1. В данной и последующих процедурах осуществления реакции Q1 представляет собой любой из активных сложноэфирных фрагментов, таких как упомянутые выше фрагменты. Промежуточные продукты (4b) подвергают взаимодействию с соединением (4 а), получая при этом соединения (I). Промежуточные продукты (4b-1), которые представляют собой промежуточные продукты (4b), в которых Q представляет собой Q1, также можно получать путем взаимодействия спирта (4 а) с карбонатами Q1-CO-Q1, такими как, например, карбонат бисфенола, карбонат бис-(замещенного фенола) или карбонат бис-N-гидроксисукцинимидила Реагенты (5 а) также можно получать из хлорформиатов Cl-CO-Q1 следующим образом: Упомянутые выше реакции для получения реагентов (4b-1) можно проводить в присутствии оснований и растворителей, упомянутых в дальнейшем для синтеза амидных связей, в частности, в присутствии триэтиламина и дихлорметана. Альтернативно, для получения соединений формулы (I) сначала образуют амидную связь между структурными элементами Р 2 и Р 1, с последующим сочетанием структурного элемента Р 3 с фрагментом Р 1 в Р-Р 2 и последующим образованием карбаматной или сложноэфирной связи между Р 3 и фрагментом Р 2 в Р 2-Р 1-Р 3 с сопутствующим замыканием цикла. Еще один альтернативный способ синтеза заключается в образовании амидной связи между структурными элементами Р 2 и Р 3, с последующим сочетанием структурного элемента Р 1 с фрагментом Р 3 в Р 3-Р 2 и с образованием в конце амидной связи между Р 1 и Р 2 в Р 1-Р 3-Р 2 с сопутствующим замыканием цикла. Структурные элементы Р 1 и Р 3 можно присоединять к последовательности Р 1-Р 3. Если необходимо, можно восстанавливать двойную связь, соединяющую Р 1 и Р 3. Образованную таким образом последовательность Р 1-Р 3, либо восстановленную, либо нет, можно связывать со структурным элементом Р 2 и образованную таким образом последовательность Р 1-Р 3-Р 2 затем циклизировать путем образования амидной связи. Структурные элементы Р 1 и Р 3 в любом из предыдущих способов можно соединять путем образования двойной связи, например с помощью реакции метатезиса олефинов, описанной в дальнейшем, или с помощью реакции типа реакции Виттига. Если необходимо, образованную таким образом двойную связь можно восстанавливать, подобно тому, как описано выше для превращения (I-i) в (I-j). Двойную связь также можно восстанавливать на более поздней стадии, например после добавления третьего структурного элемента или после образования макроцикла. Структурные элементы Р 2 и Р 1 соединяются с помощью образования амидной связи, и Р 3 и Р 2 соединяются с помощью образования карбамата или- 16013475 сложного эфира. Концевую часть Р 1' можно присоединять к структурному элементу Р 1 на любой стадии синтеза соединений формулы (I), например до или после сочетания структурных элементов Р 2 и Р 1, до или после сочетания структурного элемента Р 3 с Р 1 или до или после замыкания цикла. Сначала можно получать отдельные структурные элементы и затем связывать их вместе или, альтернативно, можно связывать вместе предшественников структурных элементов и изменять их на более поздней стадии до требуемого молекулярного состава. Образование амидных связей можно осуществлять с помощью стандартных процедур, таких как процедуры, применяемые для сочетания аминокислот при синтезе пептидов. Последний предусматривает дегидратирующее сочетание карбоксильной группы одного реагента с аминогруппой другого реагента с образованием соединяющей амидной связи. Образование амидной связи можно осуществлять путем взаимодействия исходных материалов в присутствии конденсирующего агента или путем преобразования карбоксильной функциональной группы в активную форму, такую как активный сложный эфир,смешанный ангидрид или хлорангидрид, или бромангидрид карбоновых кислот. Общие описания таких реакций сочетания и применяемых в них реагентов можно найти в общих руководствах по химии пептидов, например в книге Bodanszky М. Peptide Chemistry, 2nd rev. ed., Springer-Verlag, Berlin, Germany,(1993). Примеры реакций сочетания с образованием амидной связи включают в себя азидный способ синтеза, способ смешанных ангидридов угольной-карбоновых кислот (с применением изобутилхлорформиата), карбодиимидный способ (с применением дициклогексилкарбодиимида, диизопропилкарбодиимида или водорастворимого карбодиимида, такого как N-этил-N'-[(3-диметиламино)пропил]карбодиимид),способ активированных сложных эфиров (например, сложных п-нитрофениловых, п-хлорфениловых,трихлорфениловых, пентахлорфениловых, пентафторфениловых эфиров, N-гидроксисукцинимидоэфира и тому подобных сложных эфиров), способ с применением K-реагента Вудворда, 1,1-карбонилдиимидазольный (CDI или N,N'-карбонилдиимидазольный) способ, способ с применением фосфорных реагентов или окислительно-восстановительных способов. Некоторые из таких способов можно усовершенствовать путем добавления подходящих катализаторов, например при карбодиимидном способе путем добавления 1-гидроксибензотриазола, DBU (1,8-диазабицикло[5.4.0]ундец-7-ена) или 4-DMAP. Дополнительными конденсирующими агентами являются гексафторфосфат (бензотриазол-1-илокси)трис(диметиламино)фосфония, либо сам по себе, либо в присутствии 1-гидроксибензотриазола или 4-DMAP; или тетрафторборат 2-(1H-бензотриазол-1-ил)-N,N,N'N'-тетраметилурония или гексафторфосфат О-(7-азабензотриазол-1-ил)-N,N,N',N'-тетраметилурония. Такие реакции сочетания можно осуществлять либо в растворе (в жидкой фазе), либо в твердой фазе. Предпочтительно образование амидной связи осуществляют, применяя N-этилоксикарбонил-2 этилокси-1,2-дигидрохинолин (EEDQ) или N-изобутилоксикарбонил-2-изобутилокси-1,2-дигидрохинолин (IIDQ). В отличие от классического ангидридного способа EEDQ и IIDQ не требуют ни основания, ни низких температур реакции. Обычно процедура предусматривает взаимодействие эквимолярных количеств карбоксильного и аминного компонентов в органическом растворителе (можно применять большое разнообразие растворителей). Затем в избытке добавляют EEDQ или IIDQ и дают возможность смеси перемешиваться при комнатной температуре. Реакции сочетания предпочтительно проводят в инертном растворителе, таком как галогенированные углеводороды, например дихлорметан, хлороформ, в диполярных апротонных растворителях, таких как ацетонитрил, диметилформамид, диметилацетамид, DMSO, НМРТ, в простых эфирах, таких как тетрагидрофуран (ТГФ). Во многих случаях реакции сочетания проводятся в присутствии подходящего основания, такого как третичный амин, например триэтиламин, диизопропилэтиламин (DIPEA), N-метилморфолин,N-метилпирролидин, 4-DMAP или 1,8-диазабицикло[5.4.0]ундец-7-ен (DBU). Температура реакции может находиться в диапазоне от 0 и 50 С, и время взаимодействия может находиться в диапазоне от 15 мин до 24 ч. Функциональные группы в структурных элементах, которые соединяются вместе, можно защищать,чтобы предотвратить образование нежелательных связей. Подходящие защитные группы, которые можно применять, перечислены, например, в публикациях: Greene, Protective Groups in Organic Chemistry,John WileySons, New York (1999) и The Peptides: Analysis, Synthesis, Biology, Vol. 3, Academic Press,New York (1987). Карбоксильные группы можно защищать в виде сложного эфира, который можно удалять, получая при этом карбоновую кислоту. Защитные группы, которые можно применять, включают в себя 1) сложные алкиловые эфиры, такие как метиловый, триметилсилиловый и трет-бутиловый; 2) сложные арилалкиловые эфиры, такие как бензиловый и замещенный бензиловый; или 3) сложные эфиры, которые можно удалять с помощью слабого основания или слабого восстановителя, такие как сложные трихлорэтиловые и фенациловые эфиры. Аминогруппы можно защищать с помощью различных N-защитных групп, таких как: 1) ацильные группы, такие как формил, трифторацетил, фталил и п-толуолсульфонил;- 17013475 2) ароматические карбаматные группы, такие как бензилоксикарбонил (Cbz или Z) и замещенные бензилоксикарбонилы, и 9-флуоренилметилоксикарбонил (Fmoc); 3) алифатические карбаматные группы, такие как трет-бутилоксикарбонил (Boc), этоксикарбонил,диизопропилметоксикарбонил и аллилоксикарбонил; 4) циклические алкилкарбаматные группы, такие как циклопентилоксикарбонил и адамантилоксикарбонил; 5) алкильные группы, такие как трифенилметил, бензил или замещенный бензил, такой как 4-метоксибензил; 6) триалкилсилил, такой как триметилсилил или т-Bu-диметилсилил; и 7) тиолсодержащие группы, такие как фенилтиокарбонил и дитиасукциноил. Аминозащитными группами, представляющими интерес, являются Boc- и Fmoc-группы. Предпочтительно аминозащитную группу удаляют перед следующей стадией сочетания. УдалениеN-защитных групп можно осуществлять, следуя известным в данной области процедурам. Когда применяется Вос-группа, выбор способов заключается в выборе трифторуксусной кислоты, чистой или в дихлорметане, или HCl диоксане или в этилацетате. Полученную в результате соль аммония затем нейтрализуют либо перед сочетанием, либо в процессе его проведения с помощью основных растворов, таких как водные буферы или третичные амины в дихлорметане, или ацетонитриле, или диметилформамиде. Когда применяется Fmoc-группа, выбор реагентов включает пиперидин или замещенный пиперидин в диметилформамиде, хотя можно применять любой вторичный амин. Снятие защиты осуществляют при температуре от 0 С до комнатной температуры, обычно около 15-25 С или 20-22 С. Другие функциональные группы, которые могут вмешиваться в реакции сочетания структурных элементов, также можно защищать. Например, гидроксильные группы можно защищать в виде простых бензиловых или замещенных бензиловых эфиров, например простого 4-метоксибензилового эфира,сложных бензоиловых или замещенных бензоиловых эфиров, например сложного 4-нитробензоилового эфира, или с помощью триалкилсилильных групп (например, триметилсилила или трет-бутилдиметилсилила). Дополнительные аминогруппы можно защищать с помощью защитных групп, которые можно удалять избирательно. Например, когда в качестве -аминозащитной группы применяется Вос-группа, подходящими защитными группами для следующей боковой цепи являются: п-толуолсульфонильные (тозильные) фрагменты, которые можно применять для защиты дополнительных аминогрупп; простые бензиловые (Bn) эфиры, которые можно применять для защиты гидроксигрупп; и сложные бензиловые эфиры, которые можно применять для защиты дополнительных карбоксильных групп. Или когда в качестве-аминозащитной группы выбирается Fmoc-группа, обычно приемлемыми являются защитные группы на основе трет-бутила. Например, Вос-группу можно применять для дополнительных аминогрупп; простые трет-бутиловые эфиры - для гидроксильных групп и сложные трет-бутиловые эфиры - для дополнительных карбоксильных групп. Любую из защитных групп можно удалять на любой стадии процедуры синтеза, однако предпочтительно защитные группы любой из функциональных групп, не участвующих в реакции, удалять после завершения построения макроцикла. Удаление защитных групп можно осуществлять тем или иным способом, который диктуется выбором защитных группп, и такие способы хорошо известны специалисту в данной области. Промежуточные продукты формулы (1 а), в которых X представляет собой N, упомянутые промежуточные продукты представлены формулой (1 а-1), можно получать с помощью реакции образования мочевины, исходя из промежуточных продуктов (5 а), которые подвергают взаимодействию с алкенамином (5b) в присутствии агента, вводящего карбонильную группу, как кратко изложено на следующей реакционной схеме. Агенты, вводящие карбонил (СО), включают в себя фосген или производные фосгена, такие как карбонилдиимидазол (CDI) и т.п. В одном из вариантов осуществления изобретения соединение (5 а) подвергают взаимодействию с агентом, вводящим СО, в присутствии подходящего основания и растворителя, которые могут представлять собой основания и растворители, применяемые в реакциях образо- 18013475 вания амидов, как описано выше. Затем добавляют амин (5b), получая при этом промежуточные продукты (1 а-1), как показано на приведенной выше схеме. В конкретном варианте осуществления изобретения основание представляет собой гидрокарбонат, например NaHCO3, или третичный амин, такой как триэтиламин и т.п., и растворитель представляет собой простой эфир или галогенированный углеводород,например ТГФ, CH2Cl2, CHCl3 и т.п. Альтернативный путь синтеза с применением подобных условий реакции предусматривает сначала взаимодействие агента, вводящего СО, с амином (5b) и затем взаимодействие образовавшегося при этом промежуточного продукта с (5 а). Промежуточные продукты (1 а-1), альтернативно, можно получать следующим образом:PG1 представляет собой О-защитную группу, которая может представлять собой любую из упомянутых здесь групп и, в частности, представляет собой бензоильную или замещенную бензоильную группу, такую как 4-нитробензоил. В последнем случае такую группу можно удалять с помощью реакции с гидроксидом щелочного металла (LiOH, NaOH, KOH), в частности когда PG1 представляет собой 4-нитробензоил, с помощью LiOH в водной среде, содержащей воду и водорастворимый органический растворитель, такой как алканол (метанол, этанол) и ТГФ. Промежуточные продукты (6 а) подвергают взаимодействию с (5b) в присутствии агента, вводящего карбонил, подобно описанному выше, и в результате такой реакции получают промежуточные продукты(6 с). С них снимают защиту, в частности, применяя упомянутые выше условия реакции. Полученный в результате спирт (6d) подвергают взаимодействию с промежуточными продуктами (4b) для осуществления реакции образования карбамата, которая описана выше для взаимодействия (4 а) с (4b), и такая реакция приводит к промежуточным продуктам (1 а-1). Промежуточные продукты формулы (1 а), в которых X представляет собой С, упомянутые промежуточные продукты представлены формулой (1 а-2), можно получать с помощью реакции образования амидов, исходя из промежуточных продуктов (7 а), которые подвергают взаимодействию с алкенамином (5b),как показано на следующей реакционной схеме, применяя такие же условия реакции для получения амидов, как описанные выше.- 19013475 Промежуточные продукты (1 а-1) альтернативно можно получать следующим образом:PG1 представляет собой описанную выше О-защитную группу. Можно применять такие же условия проведения реакции, как описанные выше: образование амида, как описано выше, удаление PG1, как в описании защитных групп, и введение R8, как в реакциях соединения (4 а) с аминами (4b). Промежуточные продукты формулы (2 а) можно получать сначала циклизацией открытого амида(9 а) до сложного макроциклического эфира (9b), который в свою очередь преобразуется в промежуточный продукт (2 а) следующим образом:PG2 представляет собой карбоксилзащитную группу, например одну из упомянутых выше карбоксилзащитных групп, в частности сложный C1-4-алкиловый или бензиловый эфир, например сложный метиловый, этиловый или т-бутиловый эфир. Реакция (9 а) с образованием (9b) является реакцией метатезиса и осуществляется, как описано выше. Удаление группы PG2, как описано выше, приводит к промежуточным продуктам (2 а). Когда PG1 представляет собой сложный C1-4-алкиловый эфир, ее удаляют щелочным гидролизом, например, с NaOH или предпочтительно с LiOH в водосодержащем растворителе,например в смеси С 1-4-алканол/вода, такой как метанол/вода или этанол/вода. Бензильную группу можно удалять с помощью каталитического гидрирования. При альтернативном синтезе промежуточные продукты (2 а) можно получать следующим образом: Группу PG1 выбирают так, чтобы она была способна удаляться селективно по отношению к PG2.PG2 может представлять собой, например, сложные метиловые или этиловые эфиры, которые можно удалять при обработке гидроксидом щелочного металла в водной среде, в тех случаях, когда PG1, например, представляет собой т-бутил или бензил. Или, альтернативно, PG2 может представлять собой сложные т-бутиловые эфиры, удаляемые в слабокислых условиях, или PG1 может представлять собой сложные бензиловые эфиры, удаляемые с помощью сильной кислоты или путем каталитического гидрирования; в последних двух случаях PG1, например, представляет собой сложный эфир бензойной кислоты,такой как сложный эфир 4-нитробензойной кислоты. Сначала промежуточные продукты (10 а) подвергают циклизации до сложных макроциклических эфиров (10b), затем с последних снимают защиту путем удаления группы PG1 с получением промежуточных соединений (10 с), которые подвергают взаимодействию с аминами (4b), с последующим удалением карбоксилзащитной группы PG2. Циклизацию, снятие защиты PG1 и PG2 и сочетание с (4b) проводят, как описано выше. Группы R1 можно вводить на любой стадии синтеза, либо в виде последней стадии, как описано выше, либо раньше, до образования макроцикла, как проиллюстрировано на следующей схеме: На приведенной выше схеме значения R2, R6, R7, R8, X и PG2 такие, как указано выше, и L1 представляет собой группу Р 3 в которой n и R3 определены выше, и когда X представляет собой N, L1 также может представлять собой азотзащитную группу (PG, которая определена выше), и когда X представляет собой С, L1 также может представлять собой группу -COOPG2a, в которой группа PG2a представляет собой карбоксилзащитную группу, подобную PG2, но в которой PG2a удаляется селективно по отношению к PG2. В одном из вариантов осуществления изобретения PG2a представляет собой т-бутил, a PG2 представляет собой метил или этил. Промежуточные продукты (11 с) и (11d), в которых L1 представляет собой группу (b), соответствующую промежуточным продуктам (1 а), можно обрабатывать дополнительно, как указано выше. Сочетание структурных элементов Р 1 и Р 2 Структурные элементы Р 1 и Р 2 соединяют с применением реакции образования амида, следуя описанным выше процедурам. Структурный элемент Р 1 может содержать карбоксилзащитную группу PG2(как в (12b или может быть уже соединен с группой P1' (как в (12 с. L2 представляет собойN-защитную группу (PG) или группу (b), как указано выше. L3 представляет собой гидрокси, -OPG1 или группу -O-R8, которая указана выше. Когда на любой из следующих реакционных схем L3 представляет собой гидрокси, перед каждой реакционной стадией ее можно защищать в виде группы -OPG1 и, если необходимо, затем снова снимать защиту с образованием свободной гидроксифункции. Подобно тому,как описано выше, гидроксифункцию можно преобразовывать в группу -O-R8. В процедуре, описанной выше на схеме, циклопропиламинокислоту (12b) или (12 с) связывают с кислотной функцией (группой) структурного элемента Р 2 (12 а) с образованием амидной связи, следуя описанным выше процедурам. Получают промежуточные продукты (12d) или (12 е). Когда в последнем продукте L2 представляет собой группу (b), полученные в результате продукты представляют собой последовательности Р 3-Р 2-Р 1, охватывающие некоторые из промежуточных продуктов (11 с) или (11d) на предыдущей реакционной схеме. Удаление из соединения (12d) кислотозащитной группы в подходящих для применяемой защитной группы условиях с последующим сочетанием с амином H2N-SO2R7 (2b) или сHOR6 (2 с), как описано выше, вновь дает промежуточные продукты (12 е), в которых -COR1 представляют собой амидные или сложноэфирные группы. Когда L2 представляет собой N-защитную группу, ее можно удалять, получая при этом промежуточные продукты (5 а) или (6 а). В одном из вариантов осуществления изобретения PG в данной реакции представляет собой ВОС-группу, a PG2 представляет собой метил или этил. Кроме того, когда L3 представляет собой гидрокси, исходный материал (12 а) представляет собой Boc-L-гидроксипролин. В конкретном варианте осуществления изобретения PG представляет собой ВОС, PG2 представляет собой метил или этил, и L3 представляет собой -O-R8. В одном из вариантов осуществления изобретения L2 представляет собой группу (b), и указанные реакции включают в себя сочетание Р 1 с Р 2-Р 3, которое приводит к промежуточным продуктам (1 а-1) или (1 а), упомянутым выше. В другом варианте осуществления изобретения L2 представляет N-защитную группу PG, которая указана выше, и реакция сочетания приводит к промежуточным продуктам (12d-l) или (12 е-1), из которых группу PG можно удалять, применяя упомянутые выше условия реакции и получая при этом промежуточные продукты (12-f) или, соответственно, (12g), которые охватывают промежуточные продукты (5 а) и (6 а), которые указаны выше В одном из вариантов осуществления изобретения группа L3 на указанных выше схемах представляет собой группу -OPG1, которую можно вводить в исходный материал (12 а), в котором L3 представляет собой гидрокси. В таком случае группу PG1 выбирают таким образом, чтобы ее можно было удалять селективно по отношению к группе L2, представляющей собой PG. Подобным образом структурные элементы Р 2, в которых X представляет собой С, который представляет собой циклопентановые или циклопентеновые производные, можно соединять со структурными элементами Р 1, как кратко изложено на следующей схеме, на которой R1, R2, L3, PG2 и PG2a представляют собой карбоксилзащитные группы. Группу PG2a обычно выбирают так, чтобы ее можно было удалять селективно по отношению к группе PG2. Удаление группы PG2a из (13 с) приводит к промежуточным продуктам (7 а) или (8 а), которые можно подвергать взаимодействию с (5b), как описано выше. В одном из конкретных вариантов осуществления изобретения, где X представляет собой С, R2 представляет собой Н и где X и атом углерода, несущий R2, соединены одинарной связью (Р 2 представляет собой циклопентановый фрагмент), взятые вместе PG2a и L3 образуют связь, а структурный элемент Р 2 представлен формулой: Бициклическая кислота (14 а) подвергается взаимодействию с (12b) или (12 с), подобно тому, как описано выше, с получением (14b) и (14 с), соответственно, в которых лактон раскрывается, давая промежуточные продукты (14 с) и (14 е). Раскрытие лактона можно осуществлять с помощью процедур гидролиза сложных эфиров, например, применяя условия реакции, описанные выше для щелочного удаления группы PG1 из (9b), и, в частности, применяя основные условия, такие как гидроксид щелочного металла, например NaOH, KOH и, в частности, LiOH. Промежуточные продукты (14 с) и (14 е) можно обрабатывать дополнительно, как описано в дальнейшем. Синтез структурных элементов Р 2 Структурные элементы Р 2 содержат либо пирролидиновый, циклопентановый либо циклопентеновый фрагмент, замещенный группой -O-R8. Структурные элементы Р 2, содержащие пирролидиновый фрагмент, можно получать из имеющегося в продаже гидроксипролина. Получение структурных элементов Р 2, которые содержат циклопентановое кольцо, можно осуществлять, как показано на схеме ниже.- 23013475 процедуры предусматривает восстановление кетогруппы с помощью восстановителя типа борогидрида натрия в растворителе, таком как метанол, с последующим гидролизом сложных эфиров и заключительным замыканием цикла до бициклического лактона (17b) с помощью процедур образования лактона, в частности с применением уксусного ангидрида в присутствии слабого основания, такого как пиридин. Затем можно защитить функциональные группы карбоновой кислоты в (17b), вводя подходящую карбоксилзащитную группу, такую как группа PG2, которая представляет собой указанную выше группу, тем самым обеспечивая получение сложного бициклического эфира (17 с). Группа PG2, в частности, под воздействием кислоты является лабильной группой, такой как т-бутильная группа, и вводится, например,путем обработки изобутеном в присутствии кислоты Льюиса или ди-трет-бутилдикарбонатом в присутствии основания, такого как третичный амин типа диметиламинопиридина или триэтиламина, в растворителе типа дихлорметана. Раскрытие кольца лактона (17 с) с помощью описанных выше условий реакции, в частности с помощью гидроксида лития, приводит к кислоте (17d), которую можно дополнительно применять в реакциях сочетания со структурными элементами Р 1. Свободную кислоту (17d) также можно защищать предпочтительно с помощью кислотозащитной группы PG2a, которую можно удалять селективно по отношению к группе PG2, а гидроксифункцию можно преобразовывать до группы -OPG1 или до группы -O-R8. Продукты, получаемые при удалении группы PG2, представляют собой промежуточные продукты (17g) и (17i), которые соответствуют промежуточным продуктам (13 а) или (16 а), указанным выше. Промежуточные продукты с определенной стереохимией можно получать путем разделения промежуточных продуктов в приведенной выше последовательности реакций. Например, (17b) можно разделять, следуя известным в данной области процедурам, например с помощью образования активной формы соли с оптически активным основанием или с помощью хиральной хроматографии, и полученные в результате стереоизомеры можно дополнительно обрабатывать, как описано выше. Группы ОН и СООН в (17d) находятся в цис-положении. Трансаналоги можно получать путем изменения стереохимии у атома углерода, несущего ОН-группу (функцию), с помощью специфических реагентов в реакциях введения OPG1 или -OR8, которые меняют стереохимию, например в таких реакциях, как реакция Мицунобу. В одном из вариантов осуществления изобретения промежуточные продукты (17d) связывают с элементами P1 (12b) или (12 с) с помощью реакций сочетания, которые соответствуют сочетанию (13 а) или (16 а) с аналогичными элементами Р 1, применяя аналогичные условия. Последующее введение заместителя -OR8, как описано выше, с последующим удалением кислотозащитной группы PG2 приводит к промежуточным продуктам (8a-1), которые представляют собой подкласс промежуточных продуктов(7 а) или часть промежуточных продуктов (16 а). Продукты реакции после удаления PG2 можно дополнительно связывать со структурным элементом Р 3. В одном из вариантов осуществления изобретения PG2 в(17d) представляет собой т-бутил, который можно удалять в кислотных условиях, например, с помощью трифторуксусной кислоты. Ненасыщенный структурный элемент Р 2, то есть циклопентеновое кольцо, можно получать, как проиллюстрировано ниже на схеме.(17 а), которая описана в публикации Dolby и др. J. Orq. Chem. 36, 1971, 1277-1285, с последующим восстановлением функциональной кетогруппы с помощью восстановителя типа борогидрида натрия получают циклопентенол (19 а). С помощью избирательного гидролиза сложного эфира, например с помощью гидроксида лития в растворителе типа смеси диоксана и воды, получают сложный моноэфир гидроксизамещенного циклопентенола (19b).- 24013475 Ненасыщенный структурный элемент Р 2, в котором R2 может также отличаться от водорода, можно получать, как показано ниже на схеме. Окисление имеющегося в продаже 3-метил-3-бутен-1-ола (20 а), в частности, с помощью окислителя типа хлорохромата пиридиния приводит к (20b), который преобразуют до соответствующего сложного метилового эфира, например, путем обработки ацетилхлоридом в метаноле с последующей реакцией бромирования бромом, получая при этом сложный -бромэфир (20 с). Последний можно затем конденсировать со сложным алкениловым эфиром (20 е), полученным из (20d) с помощью реакции образования сложного эфира. Сложный эфир (20 е) предпочтительно представляет собой сложный т-бутиловый эфир,который можно получать из соответствующей кислоты (20d), имеющейся в продаже, например, путем обработки ди-трет-бутилдикарбонатом в присутствии основания типа диметиламинопиридина. Промежуточный продукт (20 е) обрабатывают основанием, таким как литийдиизопропиламид, в растворителе типа тетрагидрофурана и подвергают взаимодействию с (20 с), получая при этом сложный алкениловый диэфир (20f). Циклизацией (20f) с помощью реакции метатезиса олефинов, осуществляемой, как описано выше, получают циклопентеновое производное (20g). Для получения эпоксида (20h) можно осуществлять стереоизбирательное эпоксидирование (20g), применяя способ асимметрического эпоксидирования по Якобсену. И наконец, реакция раскрытия эпоксида в основных условиях, например при добавлении основания, в частности DBN (1,5-диазабицикло[4.3.0]нон-5-ена), приводит к спирту (20i). Необязательно двойную связь в промежуточном продукте (20i) можно восстанавливать, например, с помощью каталитического гидрирования, применяя катализатор типа палладия на углероде и получая при этом соответствующее циклопентановое соединение. Сложный т-бутиловый эфир можно удалять с получением соответствующей кислоты, которую затем связывают со структурным элементом Р 1. Группу -O-R8 можно вводить в пирролидиновые, циклопентановые или циклопентеновые циклы на любой удобной стадии синтеза соединений по настоящему изобретению. Один из подходов заключается в том, что сначала в упомянутые циклы вводят группу -O-R8 и затем добавляют другие требуемые структурные элементы, то есть Р 1 (необязательно с концевой частью Р 1') и Р 3, с последующим образованием макроцикла. Другой подход заключается в сочетании структурных элементов Р 2, не содержащих заместитель -O-R8, с каждым из Р 1 и Р 3 и добавлении группы -O-R8 либо до, либо после образования макроцикла. В последней процедуре фрагменты Р 2 содержат гидроксигруппу, которую можно защищать с помощью гидроксизащитной группы PG1. Группы -R8 можно вводить в структурные элементы Р 2 путем взаимодействия гидроксизамещенных промежуточных продуктов (21 а) или (21b) с промежуточными продуктами (4b) подобно тому, как описано выше для синтеза (I), исходящего из (4 а). Такие реакции представлены ниже на схемах, на которых значение L2 указано выше и L5 и L5a независимо друг от друга представляют собой гидрокси или карбоксилзащитную группу -OPG2 или -OPG2a, или L5 может также представлять собой группу Р 1, такую как указанные выше группы (d) или (е), или L5a может также представлять собой группу Р 3, такую как указанная выше группа (b). Группы PG2 или PG2a указаны выше. Когда группы L5 и L5a представляют собой PG2 или PG2a, их выбирают так, чтобы каждую группу можно было удалять селективно по отношению к другой. Например, одна из групп L5 и L5a может представлять собой метильную или этильную группу, а другая - бензильную или т-бутильную группу. В одном из вариантов осуществления изобретения в соединении (21 а) L2 представляет собой PG и 5 В другом варианте осуществления изобретения группа L2 представляет собой ВОС, L5 представляет собой гидрокси и исходный материал (21 а) представляет собой имеющийся в продаже ВОС-гидроксипролин или любую другую его стереоизомерную форму, например BOC-L-гидроксипролин, в частности транс-изомер последнего. Когда L5 в соединении (21b) представляет собой карбоксилзащитную группу,ее можно удалять, следуя описанным выше процедурам, с получением (21 с). В еще одном варианте осуществления изобретения PG в соединении (21b-1) представляет собой Вос и PG2 представляет собой низший сложный алкиловый эфир, в частности сложный метиловый или этиловый эфир. Гидролиз последнего сложного эфира до кислоты можно осуществлять с помощью стандартных процедур, например проводя кислотный гидролиз с помощью хлористо-водородной кислоты в метаноле или проводя гидролиз с помощью гидроксида щелочного металла, такого как NaOH, в частности спомощью LiOH. В другом варианте осуществления изобретения гидроксизамещенные циклопентановые или циклопентеновые аналоги (21d) преобразуют до (21 е), которые, когда L5 и L5a представляют собой -OPG2 или -OPG2a, можно преобразовывать до соответствующих кислот (21f) путем удаления группы PG2. Удаление PG2a из(21 е-1) приводит к аналогичным промежуточным продуктам. Промежуточные продукты (4b), которые представляют собой аминопроизводные, являются известными соединениями или могут быть получены с помощью известных в данной области процедур. Синтез структурных элементов Р 1 Циклопропанаминокислота, применяемая для получения фрагмента Р 1, имеется в продаже или ее можно получать с помощью известных в данной области процедур. В частности, сложный аминовинилциклопропилэтиловый эфир (12b) можно получать по процедуре,описанной в заявке WO 00/09543, или процедуре, проиллюстрированной на следующей схеме, на которой PG2 представляет собой указанную выше карбоксилзащитную группу:- 26013475 Обработкой имеющегося в продаже или легко получаемого имина (31 а) 1,4-дигалогенбутеном в присутствии основания получают соединение (31b), которое после гидролиза приводит к циклопропиламинокислоте (12b), содержащей аллильный заместитель в син-положении по отношению к карбоксильной группе. Разделение смеси энантиомеров (12b) приводит к (12b-1). Разделение осуществляют с помощью известных в данной области процедур, таких как ферментативное разделение; кристаллизация с хиральной кислотой; или получение химических производных; или с помощью хиральной колоночной хроматографии. Промежуточные продукты (12b) или (12b-1) можно связывать с подходящими производными Р 2, как описано выше. Структурные элементы Р 1 для получения соединений общей формулы (I), в которой R1 представляет собой -OR6 или -NH-SO2R7, можно получать путем взаимодействия аминокислот (32 а) с подходящим спиртом или амином, соответственно, в стандартных условиях, предназначенных для образования сложного эфира или амида. Циклопропиламинокислоты (32 а) получают путем введения N-защитной группыPG, удаления PG2 и преобразования аминокислот (32 а) до амидов (12 с-1) или сложных эфиров (12 с-2),которые являются подгруппами промежуточных продуктов (12 с), как кратко изложено на следующей реакционной схеме, на которой PG представляет собой указанную выше группу. Реакция соединения (32 а) с амином (2b) является процедурой образования амида. Подобная реакция с (2 с) является реакцией образования сложного эфира. Обе реакции можно осуществлять, следуя описанным выше процедурам. Данная реакция приводит к промежуточным продуктам (32b) или (32 с), из которых аминозащитная группа удаляется стандартными способами, такими как описанные выше способы. Такое удаление в свою очередь приводит к требуемому промежуточному продукту (12 с-1). Исходные материалы (32 а) можно получать из вышеупомянутых промежуточных продуктов (12b) с помощью первоначального введения N-защитной группы PG и последующего удаления группы PG2. В одном из вариантов осуществления изобретения реакцию соединения (32 а) с (2b) осуществляют путем обработки аминокислоты конденсирующим агентом, например N,N'-карбонилдиимидазолом (CDI) или т.п., в растворителе типа ТГФ с последующим взаимодействием с (2b) в присутствии основания, такого как 1,8-диазабицикло[5.4.0]ундец-7-ен (DBU). Альтернативно, аминокислоту можно обрабатывать с помощью (2b) в присутствии основания типа диизопропилэтиламина с последующей обработкой конденсирующим агентом, таким как гексафторфосфат бензотриазол-1-илокси-трис-пирролидинофосфония (имеется в продаже под маркой РуВОР), для введения сульфонамидной группы. Промежуточные продукты (12 с-1) или (12 с-2) в свою очередь можно связывать с подходящими пролиновыми, циклопентановыми или циклопентеновыми производными, как описано выше. Синтез структурных элементов Р 3 Структурные элементы Р 3 имеются в продаже или их можно получать согласно методикам, известным специалисту в данной области. Одна из таких методик показана ниже на схеме, и в ней применяются моноацилированные амины, такие как трифторацетамид или Вос-защищенный амин. На приведенной выше схеме R вместе с группой СО образует N-защитную группу, в частности R представляет собой т-бутокси, трифторметил; значения R3 и n определены выше, и LG представляет собой удаляемую группу, в частности галоген, например хлор или бром. Моноацилированные амины (33 а) обрабатывают сильным основанием, таким как гидрид натрия, и затем подвергают взаимодействию с LG-С 5-8-алкенильным реагентом (33b), в частности с галоген-С 5-8-алкенилом, для образования соответствующих защищенных аминов (33 с). Снятие защиты с(33 с) обеспечивает получение (5b), который является структурным элементом Р 3. Снятие защиты будет зависить от функциональной группы R таким образом, что если R представляет собой т-бутокси, снятие защиты с соответствующих Вос-защищенных аминов можно осуществлять путем обработки кислотой,например трифторуксусной кислотой. Альтернативно, когда R представляет собой, например, трифтор- 27013475 метил, удаление группы R осуществляют с помощью основания, например гидроксида натрия. На следующей схеме иллюстрируется еще один способ получения структурного элемента Р 3, а именно синтез первичных С 5-8-алкениламинов по Габриэлю, который можно осуществлять с помощью обработки фталимида (34 а) основанием, таким как NaOH или KOH, и с помощью (33b), который указан выше, с последующим гидролизом промежуточного продукта N-алкенилимида до образования первичного C5-8-алкениламина (5b-1). На приведенной выше схеме n имеет значение, указанное выше. Соединения формулы (I) можно преобразовывать друг в друга, следуя известным в данной области реакциям трансформации функциональных групп. Например, аминогруппы можно N-алкилировать, нитрогруппы восстанавливать до аминогрупп, атом галогена можно заменять на атом другого галогена. Соединения формулы (I) можно преобразовывать до соответствующих N-оксидных форм, следуя известным в данной области процедурам преобразования трехвалентного азота в его N-оксидную форму. Упомянутую реакцию N-окисления обычно можно осуществлять путем взаимодействия исходного материала формулы (I) с подходящим органическим или неорганическим пероксидом. Подходящие неорганические пероксиды включают в себя, например, пероксид водорода, пероксиды щелочных или щелочно-земельных металлов, например пероксид натрия, пероксид калия; подходящие органические пероксиды могут включать в себя пероксикислоты (надкислоты), такие как, например, бензолкарбопероксикислота или галогензамещенная бензолкарбопероксикислота, например 3-хлорбензолкарбопероксикислота,пероксоалкановые кислоты, например пероксоуксусная (надуксусная) кислота, алкилгидропероксиды,например трет-бутилгидропероксид. Подходящими растворителями являются, например, вода, низшие спирты, например этанол и т.п.,углеводороды, например толуол, кетоны, например 2-бутанон, галогенированные углеводороды, например дихлорметан, и смеси таких растворителей. Стереохимически чистые изомерные формы соединений формулы (I) можно получать, применяя известные в данной области процедуры. Диастереомеры можно разделять физическими способами, такими как избирательная кристаллизация, и хроматографическими способами, например противоточным распределением, жидкостной хроматографией и т.п. Соединения формулы (I) можно получать в виде рацемических смесей энантиомеров, которые можно отделять друг от друга, следуя известным в данной области процедурам разделения. Рацемические соединения формулы (I), которые являются достаточно основными или кислотными, можно преобразовывать в соответствующие диастереомерные формы солей путем взаимодействия с подходящей хиральной кислотой или хиральным основанием соответственно. Упомянутые диастереомерные формы солей затем разделяют, например, с помощью избирательной или дробной кристаллизации и выделяют из них энантиомеры с помощью щелочи или кислоты. Альтернативный способ разделения энантиомерных форм соединений формулы (I) предусматривает жидкостную хроматографию, в частности жидкостную хроматографию с применением хиральной неподвижной фазы. Упомянутые стереохимически чистые изомерные формы также можно получать из соответствующих стереохимически чистых изомерных форм подходящих исходных материалов, при условии, что осуществляется стереоспецифическая реакция. Если требуется определенный стереоизомер, предпочтительно упомянутое соединение можно синтезировать с помощью стереоспецифических способов получения. В таких способах можно преимущественно использовать энантиомерно чистые исходные материалы. В дополнительном аспекте настоящее изобретение относится к фармацевтической композиции, содержащей терапевтически эффективное количество соединения формулы (I), которое здесь определено,или соединения любой из подгрупп соединений формулы (I), которые здесь указаны, и фармацевтически приемлемый носитель. Терапевтически эффективное количество в данном контексте означает количество, достаточное для профилактического воздействия на вирусную инфекцию, для стабилизации или уменьшения вирусной инфекции и, в частности, вирусной HCV-инфекции у инфицированных субъектов или субъектов, подвергающихся риску быть инфицированными. В еще одном дополнительном аспекте изобретение относится к способу получения фармацевтической композиции, которая здесь определена,который включает в себя непосредственное смешивание фармацевтически приемлемого носителя с терапевтически эффективным количеством соединения формулы (I), которое здесь указано, или соединения любой из подгрупп соединений формулы (I), которые здесь указаны. Следовательно, с целью введения соединения по настоящему изобретению или любую их подгруппу можно получать в различных фармацевтических формах. В качестве подходящих композиций здесь можно сослаться на все композиции, обычно используемые для систематического введения лекарственных средств. Для получения фармацевтических композиций по данному изобретению эффективное ко- 28013475 личество конкретного соединения, необязательно в форме аддитивной соли или комплекса с металлом в качестве активного ингредиента, объединяют для получения непосредственной смеси с фармацевтически приемлемым носителем, где носитель может принимать большое разнообразие форм в зависимости от формы препарата, требуемой для введения. Такие фармацевтические композиции требуются в виде стандартной лекарственной формы, подходящей, в частности, для введения перорально, ректально, подкожно или путем парентеральной инъекции. Например, при получении композиций в лекарственной форме для перорального применения можно использовать любую из обычных фармацевтических сред, такую как,например, вода, гликоли, масла, спирты и т.п., в случае жидких препаратов для перорального применения, таких как суспензии, сиропы, эликсиры, эмульсии и растворы; или твердые носители, такие как крахмалы, сахара, каолин, смазки, связующие вещества, дезинтегрирующие агенты и т.п., в случае порошков, пилюль, капсул и таблеток. Благодаря удобству их введения таблетки и капсулы представляют наиболее предпочтительную стандартную лекарственную форму для перорального применения, в случае которой безусловно используются твердые фармацевтические носители. В композициях для парентерального применения носитель обычно будет содержать стерильную воду, по меньшей мере, в значительной степени, несмотря на то, что могут быть включены другие ингредиенты, например, для облегчения растворимости. Например, можно получать растворы для инъекций, в которых носитель содержит физиологический раствор, раствор глюкозы или смесь физиологического раствора и раствора глюкозы. Также можно получать суспензии для инъекций, в случае которых можно использовать подходящие жидкие носители, суспендирующие агенты и т.п. Также включены препараты в твердой форме, которые предназначены для превращения в препараты в форме жидкости незадолго до применения. В композициях, подходящих для подкожного введения, носитель необязательно содержит вещество, способствующее проникновению внутрь, и/или подходящий смачивающий реагент, необязательно объединенный с подходящими добавками любой природы в незначительных пропорциях, которые не оказывают значительного отрицательного воздействия на кожу. Соединения по настоящему изобретению также можно вводить с помощью пероральной ингаляции или инсуффляции с помощью способов и препаратов, используемых в данной области для введения таким путем. Таким образом, в общем случае соединения по настоящему изобретению можно вводить в легкие в форме раствора, суспензии или сухого порошка, раствор является предпочтительным. Для введения настоящих соединений подходит любая система, разработанная для доставки растворов, суспензий или сухих порошков с помощью пероральной ингаляции или инсуффляции. Таким образом, настоящее изобретение также относится к фармацевтической композиции, адаптированной для введения путем ингаляции или инсуффляции через рот и содержащей соединение формулы(I) и фармацевтически приемлемый носитель. Соединения по настоящему изобретению предпочтительно вводятся с помощью ингаляции раствора в виде распыленных или аэролизованных доз. Особенно предпочтительно получать вышеупомянутые фармацевтические композиции в стандартной лекарственной форме для облегчения введения и равномерности дозировки. Применяемый здесь термин стандартная лекарственная форма относится к физически дискретным элементам, подходящим в качестве однократных дозировок; каждый элемент содержит заданное количество активного ингредиента, рассчитанное для получения требуемого терапевтического эффекта, совместно с требуемым фармацевтическим носителем. Примерами таких стандартных лекарственных форм являются таблетки(включая таблетки с насечкой или таблетки с покрытием), капсулы, пилюли, суппозитории, пакетики с порошком, облатки, растворы или суспензии для инъекции и т.п., и их сегрегированные множества. Соединения формулы (I) проявляют антивирусные свойства. Вирусные инфекции и ассоциированные с ними заболевания, излечиваемые с помощью соединений и способов по настоящему изобретению,включают в себя инфекции, провоцируемые HCV и другими патогенными флавивирусами, такими как вирус желтой лихорадки, вирус лихорадки Денге (типы 1-4), вирус энцефалита Сент-Луис, вирус японского энцефалита, вирус энцефалита долины Муррея, вирус лихорадки Западного Нила и вирус Кунджин. Заболевания, ассоциированные с HCV, включают в себя прогрессирующий фиброз печени, воспаление и некроз, приводящие к циррозу печени, заболеванию печени в конечной стадии и НСС; и заболевания, ассоциированные с другими патогенными флавивирусами, включают в себя желтую лихорадку,лихорадку денге, геморрагическую лихорадку и энцефалит. Кроме того, ряд соединений по настоящему изобретению проявляют активность в отношении мутировавших штаммов HCV. Кроме того, многие из соединений по настоящему изобретению обладают благоприятным фармакокинетическим профилем и свойствами, привлекательными с точки зрения биодоступности, включая приемлемый период полувыведения, AUC (площадь под кривой), пиковые значения и отсутствие неблагоприятных эффектов, таких как недостаточно быстрая реакция и ретенция в тканях. Антивирусную активность соединений формулы (I) в отношении HCV in vitro испытывали на клеточной системе репликации HCV, основанной на публикации Lohmann и др., (1999) Science, 285:110-113,с дополнительными модификациями, описанными в публикации Krieger и др., (2001), Journal of Virology,75:4614-4624, которая дополнительно представлена в разделе примеры. Данная модель, хотя и не является полной моделью HCV-инфекции, широко распространена в качестве наиболее надежной и эффек- 29013475 тивной модели автономной репликации РНК HCV среди существующих. Соединения, проявляющие антивирусную активность в отношении HCV в этой клеточной модели, рассматриваются в качестве соединений-кандидатов при дальнейшем развитии средств для лечения HCV-инфекций у млекопитающих. Следует принимать во внимание, что важно проводить различие между соединениями, которые специфически препятствуют проявлению функций HCV, и соединениями, которые вызывают цитотоксические или цитостатические эффекты в модели подавления репликации РНК репликона HCV и, как следствие,вызывают уменьшение концентрации РНК HCV или концентрации сцепленного репортерного фермента. Известны исследования в области оценки клеточной цитотоксичности, например, на основе активности митохондриальных ферментов с помощью флуорогенных редокс-красителей, таких как резазурин. Кроме того, существуют защитные клеточные экраны для оценки неселективного ингибирования активности сцепленного репортерного гена, такого как люцифераза светляка. Подходящие типы клеток могут быть наделены стабильной трансфекцией с помощью репортерного люциферазного гена, экспрессия которого зависит от конститутивно активного генного промотора, и такие клетки могут быть использованы в качестве защитных экранов для элиминации неселективных ингибиторов. Благодаря своим антивирусным свойствам, в частности антивирусным свойствам в отношении HCV соединения формулы (I) или любая их подгруппа, их пролекарства, N-оксиды, аддитивные соли, четвертичные амины, комплексы с металлами и стереохимически изомерные формы применимы для лечения индивидуумов, подвергшихся действию вирусной инфекции, в частности HCV-инфекции, и для профилактики таких инфекций. В общем случае соединения по настоящему изобретению можно применять для лечения теплокровных животных, инфицированных вирусами, в частности флавивирусами, такими какHCV. Следовательно, соединения по настоящему изобретению или любую их подгруппу можно применять в качестве лекарственных средств. Упомянутое применение в качестве лекарственного средства или способ лечения включает в себя системное введение субъектам, инфицированным вирусом, или субъектам, подверженным вирусным инфекциям, количество, эффективное для борьбы с состояниями, ассоциированными с вирусной инфекцией, в частности с HCV-инфекцией. Настоящее изобретение также относится к применению настоящих соединений или любой их подгруппы для производства лекарственного средства для лечения или профилактики вирусных инфекций,особенно HCV-инфекции. Кроме того, настоящее изобретение относится к способу лечения теплокровного животного, инфицированного вирусом или подвергающегося риску инфицирования вирусом, в частности вирусом HCV; упомянутый способ включает в себя введение эффективного количества антивирусного соединения формулы (I), которое здесь указано, или соединения любой из подгрупп соединений формулы (I), которые здесь указаны. При комбинированной терапии в качестве лекарственного средства также можно применять комбинацию ранее известного антивирусного в отношении HCV соединения, такого как, например, интерферон- (IFN-), пегилированный интерферон- и/или рибавирин, и соединения формулы (I). Термин комбинированная терапия относится к продукту, содержащему в обязательном порядке (а) соединение формулы (I) и (b) необязательно другое антивирусное в отношении HCV соединение в виде комбинированного препарата для одновременного, отдельного или последовательного применения при леченииHCV-инфекций, в частности при лечении инфекций, вызванных HCV. Антивирусные в отношении HCV соединения охватывают средства, выбранные из ингибитора полимеразы HCV, ингибитора протеазы HCV, ингибитора другого объекта в жизненном цикле HCV, и иммуномодулирующее средство, антивирусное средство и их комбинации. Ингибиторы полимеразы HCV включают в себя, но не ограничиваются перечисленным, NM283(валопицитабин), R803, JTK-109, JTK-003, HCV-371, HCV-086, HCV-796 и R-1479. Ингибиторы протеаз HCV (NS2-NS3-ингибиторы и NS3-NS4A-ингибиторы) включают в себя, но не ограничиваются перечисленным, соединения по заявке WO 02/18369 (см., например, строки 9-22 на с.273 и от строки 4 на с.274 до строки 11 на с.276,); BILN-2061, VX-950, GS-9132 (АСН-806), SCH-503034 иSCH-6. Дополнительные средства, которые можно применять, представляют собой средства, описанные в заявках WO 98/17679, 00/056331 (Vertex); 98/22496 (Roche); 99/07734 (Boehringer Ingelheim),2005/073216, 2005073195 (Medivir) и структурно подобные средства. Ингибиторы других объектов в жизненном цикле HCV включают в себя NS3-геликазу; ингибиторы металлопротеазы; ингибиторы антисмысловых олигонуклеотидов, такие как ISIS-14803, AVI-4065 и т.п.; малые интерферирующие РНК (миРНК), такие как SIRPLEX-140-N и т.п.; кодируемую вектором короткую шпильку РНК (РНК-шпилька); ДНК-ферменты; HCV-специфические рибозимы, такие как гептазим,RPI.13919 и т.п.; ингибиторы входа, такие как НереХ-С, HuMax-НерС и т.п.; ингибиторы -глюкозидазы,такие как целгосивир, UT-231B и т.п.; КРЕ-02003002 и BIVN 401. Иммуномодулирующие средства включают в себя, но не ограничиваются перечисленным, соединения природных и рекомбинантных изоформ интерферона, включая -интерферон, -интерферон,-интерферон, -интерферон и т.п., такие как Intron, Roferon, Canferon-А 300, Advaferon, Infer- 30
МПК / Метки
МПК: C07D 401/12, A61P 31/14, A61K 31/538, C07D 403/12, C07D 413/12
Метки: гепатита, ингибиторы, вируса, макроциклические
Код ссылки
<a href="https://eas.patents.su/30-13475-makrociklicheskie-ingibitory-virusa-gepatita-s.html" rel="bookmark" title="База патентов Евразийского Союза">Макроциклические ингибиторы вируса гепатита с</a>
Предыдущий патент: Композиция в виде гранул с модифицированным и немедленным высвобождением мемантина
Следующий патент: Фунгицидные смеси на основе триазолов
Случайный патент: Телескопический удлинитель для электробытовой техники












