Тетразольные производные и способы лечения расстройств, связанных с метаболизмом
Номер патента: 11484
Опубликовано: 28.04.2009
Авторы: Тата Джеймс Р., Шмидт Дарби, Скиннер Филип Дж., Сэмпл Грэем, Шрадер Томас, Гхарбауи Тавфик, Дзунг Дзае-Киу, Колетти Стивен Л., Лян Жуй, Имбрильио Джейсон Э., Рагхаван Субхарекха
Формула / Реферат
1. Соединение, имеющее формулу (Ih)
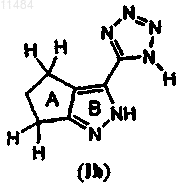
где кольцо А необязательно замещено 1 или 2 заместителями, выбранными из группы, состоящей из галогена, С1-4алкила, C1-4алкокси и C3-5циклоалкила;
или его фармацевтически приемлемая соль, сольват или гидрат.
2. Соединение по п.1, где кольцо А является незамещенным или замещено этилом; или его фармацевтически приемлемая соль, сольват или гидрат.
3. Соединение по п.1, где кольцо А замещено 1 или 2 заместителями, выбранными из группы, состоящей из галогена, н-пропила, н-бутила, С1-4алкокси и C3-5циклоалкила; или его фармацевтически приемлемая соль, сольват или гидрат.
4. Соединение по п.1, которое представляет собой 3-(1Н-тетразол-5-ил)-2,4,5,6-тетрагидроциклопентапиразол, или его фармацевтически приемлемая соль, сольват или гидрат.
5. Соединение по п.1, которое представляет собой 5-этил-3-(1Н-тетразол-5-ил)-2,4,5,6-тетрагидроциклопентапиразол, или его фармацевтически приемлемая соль, сольват или гидрат.
6. Соединение по п.1, которое представляет собой 5-бутил-3-(1Н-тетразол-5-ил)-2,4,5,6-тетрагидроциклопентапиразол, или его фармацевтически приемлемая соль, сольват или гидрат.
7. Соединение по п.1, которое представляет собой 5-пропил-3-(1Н-тетразол-5-ил)-2,4,5,6-тетрагидроциклопентапиразол, или его фармацевтически приемлемая соль, сольват или гидрат.
8. Соединение по п.1, которое представляет собой 5-пропокси-3-(1Н-тетразол-5-ил)-2,4,5,6-тетрагидроциклопентапиразол, или его фармацевтически приемлемая соль, сольват или гидрат.
9. Соединение по п.1, которое представляет собой 5-циклопентил-3-(1Н-тетразол-5-ил)-2,4,5,6-тетрагидроциклопентапиразол, или его фармацевтически приемлемая соль, сольват или гидрат.
10. Соединение по п.1, которое представляет собой 5-фтор-3-(1Н-тетразол-5-ил)-2,4,5,6-тетрагидроциклопентапиразол, или его фармацевтически приемлемая соль, сольват или гидрат.
11. Соединение по п.1, которое представляет собой 5-изобутокси-3-(1Н-тетразол-5-ил)-2,4,5,6-тетрагидроциклопентапиразол, или его фармацевтически приемлемая соль, сольват или гидрат.
12. Соединение по п.1, которое представляет собой 5-бутокси-3-(1Н-тетразол-5-ил)-2,4,5,6-тетрагидроциклопентапиразол, или его фармацевтически приемлемая соль, сольват или гидрат.
13. Соединение по п.1, которое представляет собой 5-метокси-3-(1Н-тетразол-5-ил)-2,4,5,6-тетрагидроциклопентапиразол, или его фармацевтически приемлемая соль, сольват или гидрат.
14. Соединение по п.1, которое представляет собой 5,5-дифтор-3-(1Н-тетразол-5-ил)-2,4,5,6-тетрагидроциклопентапиразол, или его фармацевтически приемлемая соль, сольват или гидрат.
15. Соединение по п.1, которое представляет собой 5-этокси-3-(1Н-тетразол-5-ил)-2,4,5,6-тетрагидроциклопентапиразол, или его фармацевтически приемлемая соль, сольват или гидрат.
16. Фармацевтическая композиция, содержащая соединение по любому из пп.1-15 в комбинации с фармацевтически приемлемым носителем.
17. Способ лечения связанных с метаболизмом расстройств, включающий введение индивидууму, нуждающемуся в таком лечении, терапевтически эффективного количества соединения по любому из пп.1-15.
18. Способ по п.17, в котором указанное, связанное с метаболизмом расстройство выбирают из группы, состоящей из дислипидемии, атеросклероза, коронарного заболевания сердца, резистентности к инсулину и диабета типа 2.
19. Способ по п.17, в котором указанное связанное с метаболизмом расстройство представляет собой атеросклероз.
20. Способ повышения уровней HDL у индивидуума, включающий введение указанному индивидууму терапевтически эффективного количества соединения по любому из пп.1-15.
21. Применение соединения по любому из пп.1-15 для лечения связанного с метаболизмом расстройства организма человека или животного.
22. Применение соединения по любому из пп.1-15 для лечения связанного с метаболизмом расстройства организма человека или животного, в котором указанное связанное с метаболизмом расстройство выбирают из группы, состоящей из дислипидемии, атеросклероза, коронарного заболевания сердца, резистентности к инсулину и диабета типа 2.
23. Применение соединения по любому из пп.1-15 для лечения атеросклероза в организме человека или животного.
24. Применение соединения по любому из пп.1-15 для повышения уровней HDL в организме человека или животного.
25. Применение соединения по любому из пп.1-15 для изготовления лекарственного средства для лечения связанного с метаболизмом расстройства.
26. Применение соединения по любому из пп.1-15 для изготовления лекарственного средства для лечения связанного с метаболизмом расстройства, выбранного из группы, состоящей из дислипидемии, атеросклероза, коронарного заболевания сердца, резистентности к инсулину и диабета типа 2.
27. Применение соединения по любому из пп.1-15 для изготовления лекарственного средства для лечения атеросклероза.
28. Применение соединения по любому из пп.1-15 для изготовления лекарственного средства для повышения уровней HDL у индивидуума.
29. Способ получения фармацевтических композиций, включающий смешивание соединения по любому из пп.1-15 и фармацевтически приемлемого носителя.
Текст
011484 Область техники, к которой относится изобретение Настоящее изобретение относится к определенным тетразольным производным и их фармацевтически приемлемым солям, которые демонстрируют полезные фармакологические свойства, например, в качестве агонистов рецептора никотиновой кислоты, RUP25. Настоящим изобретением также предусматриваются фармацевтические композиции, содержащие одно или несколько соединений настоящего изобретения, и способы применения соединений и композиций настоящего изобретения при лечении расстройств, связанных с метаболизмом, включая дислипидемию, атеросклероз, коронарное заболевание сердца, резистентность к инсулину, диабет типа 2, синдром-Х и т.п. В дополнение, настоящее изобретение также предусматривает применение соединений настоящего изобретения в комбинации с другими активными агентами, которые принадлежат к классу ингибиторов -глюкозидазы, ингибиторов альдозаредуктазы, бигуанидов, ингибиторов HMG-CoA редуктазы, ингибиторов синтеза скваленов, фибратов,усилителей катаболизма LDL, ингибиторов ангиотензин-превращающего фермента (АСЕ), усилителей секреции инсулина, тиазолидиндиона и т.п. Предшествующий уровень техники Соединения настоящего изобретения в качестве антилиполитических агентов. Атеросклероз и удар представляют собой первую и третью по значению главные причины смерти как мужчин, так и женщин в Соединенных Штатах. Диабет типа 2 представляет собой проблему общественного здоровья, которая является серьезной, широко распространенной и увеличивающейся. Повышенные уровни холестерина с липопротеинами низкой плотности (LDL) или низкие уровни холестерина с липопротеинами высокой плотности (HDL) представляют собой, независимо, факторы риска для атеросклероза и связанных с ним сердечно-сосудистых патологий. В дополнение, высокие уровни свободных жирных кислот в плазме крови связаны с резистентностью к инсулину и диабетом типа 2. Одна из стратегий понижения уровня LDL-холестерина, повышения HDL-холестерина и уменьшения уровня свободных жирных кислот в плазме заключается в ингибировании липолиза в жировой ткани. Этот подход включает регуляцию гормон-чувствительной липазы, которая представляет собой фермент, лимитирующий скорость при липолизе. Липолитические агенты повышают клеточные уровни цАМФ, что приводит к активированию гормон-чувствительной липазы в адипоцитах. Агенты, которые понижают внутриклеточные уровни цАМФ,наоборот, должны быть антилиполитическими. В прошлом также замечено, что повышение клеточных уровней цАМФ отрицательно регулирует секрецию адипонектина из адипоцитов [Delporte, M.L. et al. Biochem. J. (2002) July]. Пониженные уровни адипонектина в плазме ассоциируются с расстройствами, связанными с метаболизмом, включая атеросклероз, коронарное заболевание сердца, резистентность к инсулину и диабет типа 2 [Matsuda, M. et al. JBiol. Chem. (2002) July, и приведенные там ссылки]. Никотиновая кислота (ниацин, пиридин-3-карбоновая кислота) представляет собой водорастворимый витамин, необходимый организму человека для здоровья, роста и размножения; часть комплекса витамина В. Никотиновая кислота также представляет собой одно из самых старых лекарственных средств, используемых для лечения дислипидемии. Она представляет собой лекарственное средство,ценное тем, что оно благоприятно воздействует практически на все параметры липидов, перечисленные выше [Goodman and Gilman's Pharmacological of Therapeutics, editors Harmon J.G. and Limbird I.E., Chapter 36, Mahley R.W. and Bersot T.P. (2001) pages 971-1002]. Преимущества никотиновой кислоты при лечении или профилактике атеросклеротического сердечно-сосудистого заболевания документированы в шести главных клинических испытаниях [Guyton J.R. (1998) Am. J. Cardiol. 82:18U-23U]. Никотиновая кислота и связанные с ней производные, такие как аципимокс, были обсуждены недавно [Lorenzen A. et al.(2001)Molecular Pharmacology 59:349-357]. Структура и синтез дополнительных аналогов или производных никотиновой кислоты обсуждаются в Merck Index, An Encyclopedia of Chemicals, Drugs, and Biologicals, Tenth Edition (1983), которые включаются в данное описание посредством ссылок во всей их полноте. Никотиновая кислота ингибирует продуцирование и высвобождение свободных жирных кислот из жировой ткани, вероятно, посредством ингибирования аденилилциклазы, уменьшения внутриклеточных уровней цАМФ и одновременного уменьшения активности гормон-чувствительной липазы. Агонисты,которые отрицательно регулируют активность гормон-чувствительной липазы, приводя к снижению уровней свободных жирных кислот в плазме крови, вероятно, должны иметь терапевтическое значение. Последствия понижения уровней свободных жирных кислот в плазме крови являются двоякими. Вопервых, это, в конечном счете, снижает уровни LDL-холестерина и повышает уровни HDL-холестерина,независимых факторов риска, тем самым, снижая риск смертности из-за сердечно-сосудистого приступа после образования атеромы. Во-вторых, оно будет обеспечивать повышение чувствительности к инсулину у индивидуумов с резистентностью к инсулину или диабетом типа 2. К сожалению, применение никотиновой кислоты в качестве терапевтического средства частично ограничивается рядом связанных с ним отрицательных побочных эффектов. Они включают гиперемию, повторное связывание свободных жирных кислот и токсичность для печени. Рациональная разработка новых агонистов рецепторов никотиновой кислоты, которые имеют-1 011484 меньше побочных эффектов, была бы очень полезной, но в настоящее время она замедляется неспособностью к молекулярной идентификации рецептора никотиновой кислоты. Кроме того, другие рецепторы того же класса могут существовать на поверхности адипоцитов и подобным образом уменьшать активность гормон-чувствительной липазы посредством снижения уровня внутриклеточного цАМФ, но, не вызывая отрицательных воздействий, таких как гиперемия, тем самым представляя собой перспективные новые терапевтические мишени. В недавней работе говорится о том, что никотиновая кислота, вероятно,действует посредством специфического GPCR (рецептора, связанного с G-белком) [Lorenzen A. et al.(2001) Molecular Pharmacology 59:349-357 и приведенные там ссылки]. В еще одной работе говорится,что воздействия никотиновой кислоты на макрофаги, селезенку и, вероятно, на адипоциты, медиируются посредством этого специфического GPCR [Lorenzen A. et al. (2002) Biochemical Pharmacology 64:645-648 и приведенные там ссылки]. Сущность изобретения Один из аспектов настоящего изобретения охватывает тетразольные производные, как показано в формуле (Ih) где кольцо А необязательно замещено 1 или 2 заместителями, выбранными из группы, состоящей из галогена, C1-4 алкила, C1-4 алкокси и C3-5 циклоалкила; или их фармацевтически приемлемую соль, сольват или гидрат. Один из аспектов настоящего изобретения охватывает фармацевтические композиции, содержащие по меньшей мере одно соединение в соответствии с формулой (Ih), как описано выше. Один из аспектов настоящего изобретения относится к способам лечения расстройств, связанных с метаболизмом, включающим введение индивидууму, нуждающемуся в таком лечении, терапевтически эффективного количества соединения в соответствии с формулой (Ih), как описано выше. Один из аспектов настоящего изобретения относится к способам повышения уровней HDL у индивидуума, включающим введение индивидууму терапевтически эффективного количества соединения в соответствии с формулой (Ih), как описано выше. Один из аспектов настоящего изобретения относится к применению соединения формулы (Ih), как описано выше, для лечения расстройств, связанных с метаболизмом, организма человека или животного. Один из аспектов настоящего изобретения относится к применению соединений формулы (Ih), как описано выше, для изготовления лекарственного средства, применяемого при лечении расстройства, связанного с метаболизмом. В некоторых вариантах осуществления настоящего изобретения расстройство, связанное с метаболизмом, выбирают из группы, состоящей из дислипидемии, атеросклероза, коронарного заболевания сердца, резистентности к инсулину и диабета типа 2. В некоторых вариантах осуществления расстройство, связанное с метаболизмом, представляет собой дислипидемию. В некоторых вариантах осуществления расстройство, связанное с метаболизмом, представляет собой атеросклероз. В некоторых вариантах осуществления расстройство, связанное с метаболизмом, представляет собой коронарное заболевание сердца. В некоторых вариантах осуществления расстройство, связанное с метаболизмом, представляет собой резистентность к инсулину. В некоторых вариантах осуществления расстройство, связанное с метаболизмом, представляет собой диабет типа 2. Один из аспектов настоящего изобретения охватывает способ получения фармацевтической композиции, включающий смешивание по меньшей мере одного соединения в соответствии с формулой (Ih),как описано выше, и фармацевтически приемлемого носителя. Эти и другие аспекты настоящего изобретения, раскрываемого в данном описании, будут приведены более подробно по ходу описания патента. Подробное описание изобретения Соединения формулы (Ih) настоящего изобретения являются подгруппой новых тетразольных производных формулы (I)R2 выбирают из группы, состоящей из Н, галогена, гидрокси, тиокси, циано, нитро, C1-4 галогеналкила, амино, C1-4 алкиламино, С 2-8 диалкиламино, C1-4 алкила, С 1-4 алкокси, С 2-4 алкенила, С 2-4 алкинила,C3-5 циклоалкила, C1-4 галогеналкокси, C1-4 алкилтио, С 1-4 алкилсульфинила, C1-4 алкилсульфонила, C1-4 галогеналкилтио, С 1-4 галогеналкилсульфинила и C1-4 галогеналкилсульфонила; или R2 отсутствует; представляет собой одинарную связь, когда R2 присутствует, или представляет собой двойную связь, когда R2 отсутствует; кольцо А представляет собой 5-, 6- или 7-членное карбоциклическое кольцо или 5-, 6- или 7-членное гетероциклическое кольцо, необязательно замещенное 1-4 заместителями, выбранными из группы,состоящей из галогена, гидрокси, тиокси, циано, нитро, C1-4 галогеналкила, амино, C1-4 алкиламино,C2-8 диалкиламино, С 1-4 алкила, С 1-4 алкокси, C2-4 алкенила, С 2-4 алкинила, С 3-5 циклоалкила, С 1-4 галогеналкокси, С 1-4 алкилтио, С 1-4 алкилсульфинила, С 1-4 алкилсульфонила, С 1-4 галогеналкилтио, С 1-4 галогеналкилсульфинила и С 1-4 галогеналкилсульфонила; или их фармацевтически приемлемой соли, сольвата или гидрата. В научной литературе принят ряд терминов, и для краткости и ясности, следующие определения будут использоваться в настоящем патентном документе. Термин агонисты означает остатки, которые взаимодействуют с рецептором и активируют его,например рецептор RUP25, и инициируют физиологическую или фармакологическую реакцию, характерную для этого рецептора. Например, когда остатки активируют внутриклеточную реакцию при связывании с рецептором или усиливают связывание GTP с мембранами. Сокращенные наименования аминокислот, используемые в данном описании, приведены в табл. 1. Таблица 1 Термин антагонисты предназначен для обозначения остатков, которые конкурентно связываются с рецептором на том же участке, что и агонисты (например, эндогенный лиганд), но которые не активируют внутриклеточную реакцию, инициируемую активной формой рецептора, и могут, по этой причине,ингибировать внутриклеточные реакции агонистами или частичными агонистами. Антагонисты не уменьшают базовую внутриклеточную реакцию в отсутствие агониста или частичного агониста. Термин атеросклероз предназначен в данном описании для охвата расстройств артерий большего и среднего размера, которые приводят к непрерывной аккумуляции внутри них клеток гладких мышц и липидов. Химическая группа, остаток и радикал. Термин "С 1-4 ацил" означает С 1-4 алкильный радикал, соединенный с карбонилом, где алкил имеет такие же значения, как описано выше; некоторые примеры включают, но, не ограничиваясь ими, ацетил,пропионил, н-бутаноил, изобутаноил, втор-бутаноил, трет-бутаноил (т.е. пивалоил), пентаноил и т.п. Термин "C1-4 ацилокси" означает ацильный радикал, соединенный с атомом кислорода, где ацил имеет такие же значения, как описано выше; некоторые примеры включают, но, не ограничиваясь ими,ацетилокси, пропионилокси, бутаноилокси, изобутаноилокси, втор-бутаноилокси, трет-бутаноилокси и т.п.-3 011484 Термин "С 2-4 алкенил" означает радикал, содержащий 2-4 атома углерода, где присутствует по меньшей мере одна двойная связь углерод-углерод, некоторые варианты осуществления содержат 2-3 атома углерода, и некоторые варианты осуществления имеют 2 атома углерода. Термин "алкенил" охватывает как Е, так и Z изомеры. Кроме того, термин "алкенил" включает диены. Соответственно, если присутствует более одной двойной связи, тогда связи могут представлять собой все, Е или Z или смеси Е и Z. Примеры алкенила включают винил, пропенил, аллил, изопропенил, 2-метилпропенилметилпропенил,бут-1-енил, бут-2-енил, бут-3-енил, бута-1,3-диенил и т.п. Термин "С 1-4 алкокси" означает алкильный радикал, как определено выше, соединенный непосредственно с атомом кислорода. Примеры включают метокси, этокси, н-пропокси, изопропокси, н-бутокси,трет-бутокси, изобутокси, втор-бутокси и т.п. Термин "С 1-4 алкил" означает углеродный радикал с прямой или разветвленной цепью, содержащий указанное количество атомов углерода, например, в некоторых вариантах осуществления алкил представляет собой "С 1-4 алкил" и группа содержит 1-4 атома углерода. В некоторых вариантах осуществления алкил содержит 1-3 атомов углерода, некоторые варианты осуществления содержат 1-2 атома углерода,некоторые варианты осуществления содержат 1 атом углерода. Примеры алкила включают, но, не ограничиваясь ими, метил, этил, н-пропил, изопропил, н-бутил, изобутил, трет-бутил, втор-бутил и т.п. Термин "С 1-4 алкилсульфинил" означает С 1-4 алкильный радикал, соединенный с сульфоксидным радикалом формулы -S(O)-, где алкильный радикал имеет такие же значения, как описано выше. Примеры включают, но, не ограничиваясь ими, метилсульфинил, этилсульфинил, н-пропилсульфинил, изопропилсульфинил, н-бутилсульфинил, втор-бутилсульфинил, изобутилсульфинил, трет-бутил и т.п. Термин "С 1-4 алкилсульфонил" означает С 1-4 алкильный радикал, соединенный с сульфоновым радикалом формулы -S(O)2-, где алкильный радикал имеет такие же значения, как описано выше. Примеры включают, но, не ограничиваясь ими, метилсульфонил, этилсульфонил, н-пропилсульфонил, изопропилсульфонил, н-бутилсульфонил, втор-бутилсульфонил, изобутилсульфонил, трет-бутилсульфонил и т.п. Термин "С 1-4 алкилтио" означает С 1-4 алкильный радикал, соединенный с сульфидной группой формулы -S-, где алкильный радикал имеет такие же значения, как описано выше. Примеры включают, но,не ограничиваясь ими, метилсульфанил (т.е. CH3S-), этилсульфанил, н-пропилсульфанил, изопропилсульфанил, н-бутилсульфанил, втор-бутилсульфанил, изобутилсульфанил, трет-бутил и т.п. Термин "С 1-4 алкинил" означает радикал, содержащий 2-4 атома углерода и по меньшей мере одну тройную связь углерод-углерод, некоторые варианты осуществления имеют 2-3 атома углерода, и некоторые варианты осуществления имеют 2 атома углерода. Примеры алкинила включают, но, не ограничиваясь ими, этинил, проп-1-инил, 3-проп-2-инил, бут-1-инил, 1-метилпроп-2-инил, бута-1,3-диинил и т.п. Термин "алкинил" включает диины. Термин "амино" означает группу -NH2. Термин "С 1-4 алкиламино" означает один алкильный радикал, соединенный с аминорадикалом, где алкильный радикал имеет такие же значения, как указано выше. Некоторые примеры включают, но, не ограничиваясь ими, метиламино, этиламино, н-пропиламино, изопропиламино, н-бутиламино, вторбутиламино, изобутиламино, трет-бутиламино и т.п. Некоторые варианты осуществления представляют собой "С 1-2 алкиламино". Термин "арил" означает ароматический циклический радикал, содержащий 6-10 атомов углерода в кольце. Примеры включают фенил и нафтил. Термин "карбо-C1-4 алкокси" означает С 1-4 алкиловый эфир карбоновой кислоты, где алкильная группа является такой, как определено выше. Примеры включают, но, не ограничиваясь ими, карбометокси,карбоэтокси, карбопропокси, карбоизопропокси, карбобутокси, карбо-втор-бутокси, карбоизобутокси,карбо-трет-бутокси и т.п. Термин "карбоксамид" относится к группе -CONH2. Термин "карбокси" или "карбоксил" означает группу -CO2H; также указанную как группа карбоновой кислоты. Термин "циано" означает группу -CN. Термин "C3-5 циклоалкил" означает насыщенный циклический радикал, содержащий 3-6 атомов углерода; некоторые варианты осуществления содержат 3-5 атомов углерода; некоторые варианты осуществления содержат 3-4 атома углерода. Примеры включают циклопропил, циклобутил, циклопентил,циклогексил. Термин "С 2-8 диалкиламино" означает амино, замещенную двумя одинаковыми или различными алкильными радикалами, где алкильный радикал имеет такие же значения, как описано выше.C2-8 циалкиламино может быть представлено следующими группами:-4 011484 Термин "С 1-4 галогеналкокси" означает галогеналкил, как определено выше, который непосредственно соединен с атомом кислорода. Примеры включают, но, не ограничиваясь ими, дифторметокси,трифторметокси, 2,2,2-трифторэтокси, пентафторэтокси и т.п. Термин "С 1-4 галогеналкил" означает алкильную группу, где алкил замещен галогеном в пределах от одного атома до полного замещения, где полностью замещенный галогеналкил может быть представлен формулой ChL2h+1, где L представляет собой галоген и "h" представляет количество атомов углерода; когда присутствует более одного атома галогена, тогда галогены могут быть одинаковыми или различными и выбираться из группы, состоящей из F, Cl, Br и I; считается, что термины "алкил" и "галоген" имеют такие же значения, как определено выше. В некоторых вариантах осуществления галогеналкил представляет собой "С 1-4 галогеналкил", и группа содержит 1-4 атома углерода, некоторые варианты осуществления содержат 1-3 атома углерода, некоторые варианты осуществления содержат 1-2 атома углерода, некоторые варианты осуществления содержат 1 атом углерода. Когда галогеналкил является полностью замещенным атомами галогена, эта группа указана как пергалогеналкил, один из примеров представляет собой алкил, полностью замещенный атомами фтора, и указана как "перфторалкил." В некоторых вариантах осуществления примеры галогеналкила включают, но, не ограничиваясь ими, дифторметил, фторметил, 2,2,2-трифторэтил, 2,2-дифторэтил, 2-фторэтил, 1,2,2-трифторэтил, 1,2-дифторэтил, 1,1 дифторэтил, 1,1,2-трифторэтил, 3,3,3-трифторпропил, 2,2-дифторпропил, 3,3-дифторпропил, 3 фторпропил, 2,3,3-трифторпропил, 2,3-дифторпропил, 2,2,3,3,3-пентафторпропил, 2,2,3,3-тетрафторпропил, 2,2,3-трифторпропил, 1,2,3,3-тетрафторпропил, 1,2,3-трифторпропил, 3,3-дифторпропил, 1,2,2,3 тетрафторпропил, 4,4-дифторбутил, 3,3-дифторбутил, 4,4,4-трифторбутил, 3,3-дифторбутил и т.п. В некоторых вариантах осуществления примеры перфторалкила включают, но, не ограничиваясь ими, трифторметил, пентафторэтил, гептафторпропил, 1,2,2,2-тетрафтор-1-трифторметилэтил и т.п. Термин "С 1-4 галогеналкилсульфинил" означает галогеналкильный радикал, соединенный с сульфоксидной группой формулы: -S(O)-, где галогеналкильный радикал имеет такие же значения, как описано выше. Термин "С 1-4 галогеналкилсульфонил" означает галогеналкильный радикал, соединенный с сульфоновой группой формулы: -S(O)2-, где галогеналкил имеет такие же значения, как описано выше. Термин "С 1-4 галогеналкилтио" означает галогеналкильный радикал, непосредственно соединенный с атомом серы, где галогеналкил имеет такие же значения, как указано выше. Термин "галоген" или "гало" означает группу фтора, хлора, брома или йода. Термин "гидроксил" означает группу -ОН. Термин "нитро" означает группу -NO2. Термин "тиокси" означает группу -SH. Сокращение ДМФА означает диметилформамид. Сокращение ДМСО означает диметилсульфоксид. Сокращение ТГФ означает тетрагидрофуран. Сокращение DCM означает дихлометан. Сокращение Hex означает гексан. Сокращение TBDMS означает трет-бутилдиметилсилил. Сокращение PTSA означает паратолуолсульфоновую кислоту. Сокращение LDA означает диизопропиламид лития. Сокращение LHMDS означает гексаметилдисилазанлития. Сокращение TFA означает трифторуксусную кислоту. Сокращение EDC означает гидрохлорид 1-этил-3-(3-диметиламино пропил)карбодиимида. Сокращение dppf означает 1,1'-бис-(дифенилфосфино)ферроцен. Термин CODON означает группу из трех нуклеотидов (или эквивалентов нуклеотидов), которая,как правило, содержит нуклеозид (аденозин (А), гуанозин (G), цитидин (С), уридин (U) и тимидин (Т,соединенный с фосфатной группой и который, когда транслируется, кодирует аминокислоту. Термин композиция означает состав, содержащий по меньшей мере два соединения или два компонента; например, но без ограничения, фармацевтическая композиция представляет собой композицию,содержащую соединение настоящего изобретения и фармацевтически приемлемый носитель. Термин эффективность соединения означает измерение способности соединения к ингибированию или стимулированию функционирования рецептора, в противоположность аффинности связывания рецептора. Термин конститутивно активируемый рецептор означает рецептор, подвергающийся конститутивному активированию рецептора. Термин конститутивное активирование рецептора означает стабилизацию рецептора в активном состоянии с помощью средств, иных, чем связывание рецептора с его эндогенным лигандом или его химическим эквивалентом. Термины контакт или контактирование означают сведение указанных остатков вместе либо в системе in vitro, либо в системе in vivo. Таким образом, "контактирование" рецептора RUP25 с соединением настоящего изобретения включает введение соединения настоящего изобретения индивидууму,-5 011484 например человеку, имеющему рецептор RUP25, а также, например, введение соединения настоящего изобретения в образец, содержащий клеточный или более очищенный препарат, содержащий рецепторRUP25. Термин коронарное заболевание сердца предназначен для охвата расстройств, включающих сужение малых кровеносных сосудов, которые снабжают кровью и кислородом сердце. Коронарное заболевание сердца обычно является следствием отложения жирового материала и образования бляшек. Когда коронарные артерии сужаются, поток крови к сердцу может замедляться или останавливаться. Коронарное заболевание сердца может вызывать боль в груди (стабильную стенокардию), одышку, сердечный приступ или другие симптомы. Уменьшение используется в данном описании для указания уменьшения на измеримую величину и используется взаимозаменяемо с терминами "сокращают", "ослабляют", "снижают" и "облегчают". Термин диабет используется в данном описании для охвата обычного диагноза диабет, полученного с помощью любого способа, включая, но, не ограничиваясь ими, следующий список: симптомы диабета (например, полиурия, полидипсия, полифагия) плюс нерегулярные уровни глюкозы в плазме крови, равные или большие чем 200 мг/дл, где нерегулярный уровень глюкозы в плазме определяется в любое время дня, независимо от временного графика потребления пищи или напитков; уровни глюкозы в плазме крови при 8-часовом голодании, равные или меньшие чем 126 мг/дл; и уровни глюкозы в плазме крови, равные или большие чем 200 мг/дл, через 2 ч после перорального введения 75 г безводной глюкозы, растворенной в воде. Фраза расстройства метаболизма липидов предназначена в данном описании для включения, но без ограничения, дислипидемии. Термин дислипидемия предназначен в данном описании для охвата расстройств, включающих один из признаков: повышенный уровень свободных жирных кислот в плазме, повышенный уровень холестерина в плазме, повышенный уровень LDL-холестерина, повышенный уровень HDL-холестерина и повышенный уровень триглицеридов в плазме крови. Фраза нуждающийся в лечении, как используется в данном описании, относится к суждению, делаемому наблюдающим специалистом (например, врачом, медицинской сестрой, медицинским работником и т.п., в случае людей; ветеринаром, в случае животных, включая млекопитающих, отличных от людей), что индивидуум или животное требует лечения или получит облегчение от лечения. Это суждение делается на основе множества факторов, которые оцениваются наблюдающим специалистом, исходя из его опыта, который включает знание того, что индивидуум болен или заболеет в результате заболевания,состояния или расстройства, которое может лечиться посредством соединений настоящего изобретения. Кроме того, фраза "нуждающийся в лечении" относится также к "профилактике" индивидуума, о котором наблюдающий специалист делает суждение, что индивидуум заболеет. В этом контексте, соединения настоящего изобретения используются для защиты или профилактики. Соответственно, "нуждающийся в лечении" относится к суждению наблюдающего специалиста о том, что индивидуум уже болен или заболеет, и соединения настоящего изобретения могут применяться для ослабления, ингибирования, облегчения или предотвращения заболевания, состояния или расстройства. Термин индивидуум, как используется в данном описании, относится к любому животному,включая млекопитающих, например, мышей, крыс, других грызунов, кроликов, собак, кошек, свиней,крупный рогатый скот, овец, лошадей или приматов, и в одном из вариантов осуществления людей. Термины ингибировать или ингибирование, в связи с термином "реакция" означают, что реакция уменьшается или предотвращается в присутствии соединения, в противоположность отсутствию соединения. Термин резистентность к инсулину, как используется в данном описании, предназначен для охвата обычного диагноза резистентности к инсулину, сделанного посредством ряда способов, включая, но,не ограничиваясь этим, внутривенное исследование на толерантность к глюкозе или измерение уровня инсулина натощак. Хорошо известно, что имеется превосходная корреляция между ростом уровня инсулина натощак и степенью резистентности к инсулину. По этой причине, можно использовать повышенные уровни инсулина натощак в качестве суррогатного маркера для резистентности к инсулину, для целей идентификации того, какие индивидуумы с нормальной толерантностью к глюкозе (NGT) имеют резистентность к инсулину. Диагноз резистентности к инсулину также может быть поставлен с использованием теста с фиксацией эугликемической глюкозы. Термин обратные агонисты означает остатки, которые связывают эндогенную форму рецептора или конститутивно активируемую форму рецептора, и которые ингибируют базовую внутриклеточную реакцию, инициируемую активной формой рецептора, ниже нормального базового уровня активности,который наблюдается в отсутствие агонистов или частичных агонистов, или уменьшают связывание GTP с мембранами. В некоторых вариантах осуществления базовая внутриклеточная реакция ингибируется в присутствии обратного агониста по меньшей мере на 30%, в других вариантах осуществления по меньшей мере на 50% и в других вариантах осуществления по меньшей мере на 75%, по сравнению с базовой реакцией в отсутствие обратного агониста. Термин лиганд означает эндогенную, природную молекулу, специфичную к эндогенному при-6 011484 родному рецептору. Фраза расстройства, связанные с метаболизмом предназначена для включения, но, не ограничиваясь ими, дислипидемии, атеросклероза, коронарного заболевания сердца, резистентности к инсулину,тучности, нарушенной толерантности к глюкозе, атероматозного заболевания, гипертензии, удара, синдрома X, заболевания сердца и диабета типа 2. Как используется в данном описании, термины модулировать или модулирование означают указание увеличения или уменьшения количества, качества, реакции или воздействия конкретной активности, функции или молекулы. Термин фармацевтическая композиция означает композицию для профилактики, лечения или контроля болезненного статуса или состояния, содержащую по меньшей мере одно активное соединение,например, соединение настоящего изобретения, включая его фармацевтически приемлемые соли, фармацевтически приемлемые сольваты и/или гидраты, и по меньшей мере один фармацевтически приемлемый носитель. Термин фармацевтически приемлемый носитель или эксципиент означает любое, по существу,инертное вещество, используемое в качестве разбавителя или растворителя для соединения настоящего изобретения. Фраза терапевтически эффективное количество, как используется в данном описании, относится к количеству активного соединения или фармацевтического агента, которое вызывает биологическую или медицинскую реакцию в ткани, системе, у животного, индивидуума или человека, которая рассматривается исследователем, ветеринаром, врачом или другим клиницистом, которая включает одну или более из следующих:(1) профилактика заболевания; например профилактика заболевания, состояния или расстройства у индивидуума, который может быть предрасположен к заболеванию, состоянию или расстройству, но еще не испытывает или не демонстрирует патологии или симптоматологии заболевания;(2) ингибирование заболевания, например ингибирование заболевания, состояния или расстройства у индивидуума, который испытывает или проявляет патологию или симптоматологию заболевания, состояния или расстройства (т.е. приостановка дальнейшего развития патологии и/или симптоматологии); и(3) облегчение заболевания, например облегчение заболевания, состояния или расстройства у индивидуума, который испытывает или проявляет патологию или симптоматологию заболевания, состояния или расстройства (т.е. обращение патологии и/или симптоматологии). Соединения настоящего изобретения. Один из аспектов настоящего изобретения охватывает тетразольные производные формулы (Ih) где кольцо А необязательно замещено 1 или 2 заместителями, выбранными из группы, состоящей из галогена, C1-4 алкила, C1-4 алкокси и C3-5 циклоалкила; или их фармацевтически приемлемую соль, сольват или гидрат. Соединения настоящего изобретения могут существовать в различных таутомерных формах. Например, специалисту в данной области будет понятно, что тетразолы могут существовать по меньшей мере в двух таутомерных формах, и хотя формула (Ih) представляет одну форму, подразумевается, что настоящим изобретением охватываются все таутомерные формы. Кроме того, понятно, что могут существовать таутомеры как для кольца В, так и для тетразольного кольца, в сочетании. Понятно, что все таутомеры, которые могут существовать для соединений, описанных в данном описании, входят в объем настоящего изобретения. Настоящее изобретение также охватывает диастереомеры, а также оптические изомеры, например,смеси энантиомеров, включая рацемические смеси, а также индивидуальные энантиомеры и диастереомеры, которые возникают как следствие структурной асимметрии в определенных соединениях настоящего изобретения. В некоторых вариантах осуществления соединения настоящего изобретения представляют собой R изомеры. В некоторых вариантах осуществления соединения настоящего изобретения представляют собой S изомеры. В некоторых вариантах осуществления соединения настоящего изобретения представляют собой рацемические смеси. Понятно, что определенные признаки настоящего изобретения, которые, для ясности, описаны в контексте отдельных вариантов осуществления, могут также предусматриваться в сочетании в едином варианте осуществления. Наоборот, различные признаки настоящего изобретения, которые, для ясности,описаны в контексте единого варианта осуществления, могут также предусматриваться по отдельности или в любом пригодном для использования подсочетании.-7 011484 Как используется в данном описании, "замещенный" указывает на то, что по меньшей мере один атом водорода химической группы заменен неводородными заместителями или группой. Когда химическая группа является "замещенной", она может быть замещена вплоть до полного замещения; например,метильная группа может быть замещена 1, 2 или 3 заместителями, метиленовая группа может быть замещена 1 или 2 заместителями, фенильная группа может быть замещена 1, 2, 3, 4 или 5 заместителями и т.п. Один из вариантов осуществления настоящего изобретения относится к соединениям, имеющим формулу (Ih) где кольцо А замещено 1 или 2 заместителями, выбранными из группы, состоящей из галогена,н-пропила, н-бутила, С 1-4 алкокси и C3-5 циклоалкила; или их фармацевтически приемлемой соли, сольвату или гидрату. Один из вариантов осуществления настоящего изобретения относится к соединениям, имеющим формулу (Ih) где кольцо А является незамещенным или замещено этилом; или их фармацевтически приемлемой соли, сольвату или гидрату. Один из вариантов осуществления настоящего изобретения относится к соединениям формулы (Ih),представляющим собой 3-(1 Н-тетразол-5-ил)-2,4,5,6-тетрагидроциклопентапиразол или его фармацевтически приемлемую соль, сольват или гидрат; 5-этил-3-(1 Н-тетразол-5-ил)-2,4,5,6-тетрагидроциклопентапиразол или его фармацевтически приемлемую соль, сольват или гидрат; 5-бутил-3-(1 Н-тетразол-5-ил)-2,4,5,6-тетрагидроциклопентапиразол или его фармацевтически приемлемую соль, сольват или гидрат; 5-пропил-3-(1 Н-тетразол-5-ил)-2,4,5,6-тетрагидроциклопентапиразол или его фармацевтически приемлемую соль, сольват или гидрат; 5-пропокси-3-(1 Н-тетразол-5-ил)-2,4,5,6-тетрагидроциклопентапиразол или его фармацевтически приемлемую соль, сольват или гидрат; 5-циклопентил-3-(1 Н-тетразол-5-ил)-2,4,5,6-тетрагидроциклопентапиразол или его фармацевтически приемлемую соль, сольват или гидрат; 5-фтор-3-(1 Н-тетразол-5-ил)-2,4,5,6-тетрагидроциклопентапиразол или его фармацевтически приемлемую соль, сольват или гидрат; 5-изобутокси-3-(1 Н-тетразол-5-ил)-2,4,5,6-тетрагидроциклопентапиразол или его фармацевтически приемлемую соль, сольват или гидрат; 5-бутокси-3-(1 Н-тетразол-5-ил)-2,4,5,6-тетрагидроциклопентапиразол или его фармацевтически приемлемую соль, сольват или гидрат; 5-метокси-3-(1 Н-тетразол-5-ил)-2,4,5,6-тетрагидроциклопентапиразол или его фармацевтически приемлемую соль, сольват или гидрат; 5,5-дифтор-3-(1 Н-тетразол-5-ил)-2,4,5,6-тетрагидроциклопентапиразол или его фармацевтически приемлемую соль, сольват или гидрат; 5-этокси-3-(1 Н-тетразол-5-ил)-2,4,5,6-тетрагидроциклопентапиразол или его фармацевтически приемлемую соль, сольват или гидрат. Химия настоящего изобретения Синтез соединений Соединения настоящего изобретения могут быть легко получены в соответствии с новым способом получения новых тетразолов формулы (I), использующим различные исходные вещества, которые являются коммерчески доступными или легко получаются с помощью условий синтеза, которые должны быть известны специалистам в данной области. В иллюстрируемых схемах синтеза, приведенных ниже,если не указано иное, помеченные заместители имеют такие же значения, как приведено в определениях соединения, описанных выше для формулы (I).-8 011484 Один из способов, который может использоваться для получения соединений формулы (I), где X представляет собой NH (т.е. кольцо В представляет собой пиразол), использует промежуточные соединения, полученные из циклического кетона формулы (А), как проиллюстрировано на схеме реакции I ниже. Схема I Соединения формулы (Ia) могут быть получены взаимодействием циклического кетона формулы(А) с диалкилоксалатом формулы (C(O)OR10)2, где R10 представляет собой C1-8 алкил, в присутствии основания и полярного растворителя, такого как, но, не ограничиваясь ими, C1-8 алканол, метанол, этанол, бутанол, пентанол, гексанол, 2-метоксиэтанол, изопропанол, ТГФ, ДМФА и т.п., с получением кетоэфира формулы (В). Соответствующие основания включают алкоксиды щелочных металлов, например, метоксид натрия, этоксид натрия, этоксид калия, трет-бутоксид калия и т.п.; амиды щелочных металлов (т.е. щелочной металл-NR11, где R11 представляет собой С 1-8 алкил или силил-C1-8 алкил), например, литийдиизопропиламид, литийгексаметилдисилазан, натрийгексаметилдисилазан, калийгексаметилдисилазан и т.п. Кетоэфир (В) подвергают взаимодействию с гидразином, при этом может использоваться либо защищенный, либо незащищенный гидразин, в соответствующих условиях, с получением сложного эфира пиразола формулы (С). Необязательно, пиразол может быть защищен, например, с помощью бензильной группы и т.п. Сложный эфир преобразуют в амид формулы (D) с использованием способов, известных специалисту в данной области, например, обработкой аммиаком в полярном растворителе при температуре от комнатной до температуры кипения растворителя. Амид (D) подвергают взаимодействию с дегидратирующим реагентом, таким как оксихлорид фосфора, пентоксид фосфора, тионилхлорид и т.п.,либо как таковым, либо в присутствии апротонного растворителя, такого как ацетонитрил, ДМФА и т.п.,с получением нитрила (Е). Нитрил (Е) подвергают взаимодействию с азидом (т.е. N3) или эквивалентом азида, таким как азид натрия, азид калия, триметилсилилазид (т.е. (CH3)SiN3) и т.п., с получением тетразола формулы (Ia). В некоторых случаях, может быть полезным включить присутствие кислоты Льюиса,например AlCl3, ZnBr2 и т.п., в соответствующем растворителе, таком как ДМФА и т.п. Один из способов, который может использоваться для получения соединений формулы (I), где X представляет собой атом кислорода в кольце (т.е. кольцо В представляет собой изоксазол), использует промежуточные соединения, полученные из алкинилового спирта формулы (J), как проиллюстрировано на схеме реакции II ниже. Схема II Соединения формулы (Ic) могут быть получены посредством защиты алкинилового спирта формулы (J) с помощью соответствующей защитной группы, например ТГФ, TBDMS и т.п., с получением алкинила (K). Алкинил (K) преобразуют в сложный алкиниловый эфир формулы (L, где R15 представляет собой C1-8 алкил) обработкой сильным основанием, с последующим взаимодействием с C1-8 алкилхлорформиатом. Соответствующее сильное основание представляет собой алкиллитий, например, но, не ограничиваясь ими, н-бутиллитий, трет-бутиллитий и т.п. Промежуточное соединение (L) впоследствии подвергают снятию защиты с использованием способов, известных специалистам в данной области, на-9 011484 пример, группа ТГФ, как правило, может быть удалена обработкой кислотой (например, PTSA), а группаTBDMS, как правило, может быть удалена обработкой тетраалкиламмонийфторидом. Полученный спирт окисляется до альдегида (М) с использованием различных способов, например, периодинана ДессаМартина (т.е. 1,1,1-триацетокси-1,1-дигидро-1,2-бензиодоксол-3(1 Н)-она), окисления по Сверну, окисления Кори с помощью NCS или любого другого соответствующего способа, как описано у Hudlicky, M., вOxidations in Organic Chemistry, ACS Monograph 186 (1990). Альдегид (М) обрабатывают гидроксиламином в присутствии основания, затем NCS и основанием, с получением сложного алкилового эфира изоксазола (N). Изоксазол (N) может быть преобразован в соединения формулы (Ic) способом, по существу,аналогичным описанному для схемы реакции I, (т.е. -CO2-C1-8 алкилCONH2-CN-тетразол). Один из способов, который может использоваться для получения определенных соединений формулы (I), использует промежуточное соединение (AJ), как проиллюстрировано на схемах реакций III и IV ниже. Схема III Соединения структуры (AJ) (где R представляет собой С 1-4 алкил, C2-4 алкенил и С 2-4 алкинил) могут быть получены обработкой ненасыщенного пиразола (АА) бензилбромидом в соответствующем растворителе, типа ТГФ, в присутствии NaOH в качестве основания, с получением N-бензилпиразола (АВ). Пиразол (АВ) может быть омылен с использованием способов, известных специалистам в данной области,например, обработкой водным раствором гидроксида натрия в смеси растворителей, такой как ТТФ/МеОН. Кислоту (АС) связывают с N-гидроксисукцинимидом с использованием реагента связывания, такого как EDC. Сложный эфир (AD) преобразуют в амид (АЕ) обработкой концентрированным раствором NH4OH в растворителе, таком как 1,4-диоксан. Амид (АЕ) может быть подвергнут взаимодействию с дегидратирующим реагентом, таким как цианурхлорид, трифторуксусный ангидрид, тионилхлорид и т.п., в присутствии апротонного растворителя, такого как ДМФА, с получением нитрила (AF). Нитрил (AF) обрабатывают избытком раствора борана-ТГФ в растворителе, подобном ТГФ, при низкой температуре, с последующим окислением перекисью водорода в присутствии гидроксида натрия, с получением смеси спиртов 1:1, показанных как (AG') и (AG"). Используя либо спирт (AG'), либо спирт (AG"), можно получить различные простые эфиры. Репрезентативный синтез показан на схеме реакции IV, с использованием спирта (АС). Понятно, что подобная же схема синтеза может использоваться, исходя из спирта (AG"). Схема IV Соединения структуры (АН) могут быть получены обработкой спиртового промежуточного соеди- 10011484 нения (АG') избытком алкилгалогенида в присутствии основания, такого как гидрид натрия, в апротонном растворителе, таком как ДМФА. Нитрил (АН) подвергают взаимодействию с азидом, таким как азид натрия, в присутствии кислоты Льюиса, такой как бромид цинка, с получением тетразола структуры (AI). Конечные соединения могут быть получены посредством удаления бензильной защитной группы в условиях окисления в растворителе, подобном ДМСО, с использованием основания, такого как трет-бутоксид калия, и газообразного кислорода. Один из способов, который может использоваться для получения определенных соединений формулы (I), использует промежуточное соединение (AS), как проиллюстрировано на схеме реакции V ниже. Схема V Соединения структуры (AV) могут быть получены из 3-этоксициклопентенона обработкой диалкилоксалатом, таким как ди-трет-бутилоксалат или диэтилоксалат, в присутствии ненуклеофильного основания, такого как LDA или LHMDS, в растворителе, таком как ТГФ, с получением кетоэфира (AM). Кетоэфир (AM) подвергают взаимодействию с бензилгидразином при кипении с обратным холодильником,в полярном растворителе, таком как этанол или метанол, содержащем ледяную уксусную кислоту, с получением пиразола (AN). Альтернативно, кетоэфир (AM) может быть подвергнут взаимодействию с гидразином, с последующим алкилированием пиразола с помощью бензилбромида, с использованием карбоната цезия в качестве основания, в апротонном растворителе, таком как ДМФА. Сложный эфир пиразола (AN) может быть преобразован в нитрил (AR), с использованием последовательности стадий, подобно описанной для (АС). Кетон (AR) преобразовывают в винилтрифлат (AS) с использованием реагента Комминса в присутствии LDA в растворителе, таком как ТГФ. Используя соединения (AS), различные заместители (где R' представляет собой С 1-4 алкил, C2-4 алкенил и C2-4 алкинил) могут вводиться по положению С-5, как показано на схеме реакции VI. Схема VI Трифлат (AS) может быть подвергнут взаимодействию с соответствующим станнановым реагентом в присутствии основания, такого как хлорид лития, и катализатора, такого как тетракистрифенилфосфинпалладий(0), в соответствующем растворителе, таком как ТГФ или толуол. Альтернативно, трифлат(AS) может быть подвергнут взаимодействию с соответствующей алкенилбороновой кислотой в присутствии основания, такого как фосфат калия, и катализатора, такого как тетракистрифенилфосфинпалладий(0), в соответствующем растворителе, таком как 1,4-диоксан. Нитрил (AT) подвергают взаимодействию с азидом, таким как азид натрия, в присутствии кислоты Льюиса, такой как бромид цинка, с получением тетразола структуры (AU). Конечные соединения получают посредством удаления бензильной защитной группы, которое может осуществляться в условиях восстановления с использованием палладиевой черни в полярном растворителе, таком как метанол или этанол, и кислоты, такой как муравьиная кислота или концентрированная хлористоводородная кислота. Альтернативно, спирт (AG') может быть фторирован с использованием способов, известных специалистам в данной области, например, с использованием DAST [трифторид(диэтиламино)серы], с получением соединения фтора, которое может быть обработано до получения его тетразольного производного и подвергнуто снятию защиты с использованием способов, описанных выше. Один из способов, который может быть использован для получения определенных соединений формулы (I), проиллюстрирован на схеме реакции VII ниже. Схема VII Соединение структуры (BF) может быть получено из кетоэфира (AM) взаимодействием с гидразингидратом в полярном растворителе, таком как этанол, содержащем ледяную уксусную кислоту, с получением пиразола (AW). Пиразол (AW) может быть подвергнут взаимодействию с сульфонилхлоридом,таким как п-толуолсульфонилхлорид, в растворителе, таком как CH2Cl2, в присутствии основания, такого как пиридин, с получением N-сульфонированного производного (АХ). Сложный эфир пиразола (АХ) может быть подвергнут снятию защиты в кислотных условиях, используя кислоту, такую как TFA, вCH2Cl2, с образованием (AY). Пиразоловая кислота (AY) может быть преобразована в нитрил (ВВ) с использованием последовательности стадий, подобно описанной для (AG'). Кетон (ВВ) может быть преобразован в винилтрифлат(ВС) с использованием реагента Комминза, в присутствии основания, такого как LDA, в растворителе,таком как ТГФ. Трифлат (ВС) может быть связан с тетраметилоловом в присутствии основания, такого как хлорид лития, и катализатора, такого как тетракистрифенилфосфинпалладий(0), в соответствующем растворителе, таком как ТГФ или толуол. Сульфонильная группа п-толуола может быть удалена взаимодействием с раствором тетрабутиламмонийфторида в растворителе, таком как ТГФ, с получением пиразола (BE). Ко- 12011484 нечное соединение получают взаимодействием нитрила (BE) с азидом, таким как азид натрия, в присутствии кислоты Льюиса, такой как бромид цинка, с получением тетразола (BF). Различные преобразования используемых органических групп и защитных групп могут быть осуществлены посредством ряда методов, иных, чем описанные выше. Ссылки на другие методы синтеза,которые могут использоваться для получения промежуточных соединений или соединений, описанных выше, можно найти, например, у Smith, M.B.; and March, J., в Advanced Organic Chemistry, 5th Edition,Wiley-Ihterscience (2001); Larock, R.C., Comprehensive Organic Transformations, A Guide to FunctionalGroups in Organic Synthesis, 3rd Edition, John Wiley and Sons, (1999), которые включены в данное описание посредством ссылок во всей их полноте. Соединения формулы (I) могут иметь один или несколько хиральных центров, и по этой причине они существуют как энантиомеры или диастереомеры. Настоящее изобретение, как считается, распространяется на все такие энантиомеры, диастереомеры и их смеси, включая рацематы. Формула (I) и формулы, описанные выше, предназначены для представления всех индивидуальных изомеров и их смесей,если не утверждается или не указано иное. Рацемические смеси могут быть разделены на оптически чистые энантиомеры с помощью известных методов, например, путем разделения их диастереомерных солей с помощью оптически активной кислоты и высвобождения оптически активного аминного соединения обработкой основанием. Другой метод разделения рацематов на оптически чистые энантиомеры основывается на хроматографии на оптически активной матрице или на хиральной подложке. Определенные рацемические соединения настоящего изобретения могут, таким образом, быть разделены на их оптические антиподы, например, посредством фракционированной кристаллизации, например, d- или l-(тартратных, манделатных или камфорсульфонатных) солей. Соединения настоящего изобретения также могут быть разделены посредством образования диастереомерных амидов или сложного эфира путем взаимодействия соединений настоящего изобретения с оптически активной активированной карбоновой кислотой, например, полученной из (+) или (-) фенилаланина, (+) или (-) фенилглицина, (+) или (-) камфановой кислоты или путем образования диастереомерных карбаматов путем взаимодействия соединений настоящего изобретения с оптически активным хлорформиатом или подобным, с последующим гидролизом. Дополнительные методы разделения оптических изомеров, известные специалистам в данной области, могут использоваться и будут очевидны специалисту в данной области. Такие способы включают способы, обсуждаемые J. Jaques, A. Collet, and S. Wilen в "Enantiomers, Racemates, and Resolutions", JohnWiley and Sons, New York (1981). Понятно, что химические механизмы, описанные выше, являются репрезентативными и не предназначаются для ограничения каким-либо образом. Репрезентативные примеры соединений формулы (I) представлены ниже в табл. А. Методы и применения Соединения настоящего изобретения являются полезными при ингибировании продуцирования свободных жирных кислот. Кроме того, соединения настоящего изобретения являются полезными при ингибировании продуцирования свободных жирных кислот, в то же время, приводя к значительно более низким побочным воздействиям гиперемии или, в некоторых случаях, к отсутствию таких измеряемых воздействий, эти воздействия обычно связываются с введением ниацина. Соединения настоящего изобретения, как правило, не вызывают расширения сосудов при дозах, достигающих примерно 300 мг/кг массы тела, измеряемых с использованием методов, известных в данной области, таких как способ, показанный в примере 7. В некоторых вариантах осуществления соединения настоящего изобретения, по существу, не вызывают измеряемой гиперемии у индивидуума, по сравнению с дозой ниацина, по существу, с такой же эффективностью. В других вариантах осуществления соединения настоящего изобретения вызывают менее примерно чем 80, 75, 70, 65, 60, 55, 50, 45, 40, 35, 30, 25, 20, 15, 10, 5 или 1% от гиперемии, измеряемой у индивидуума, по сравнению с дозой ниацина, по существу, с такой же эффективностью. Соединения настоящего изобретения могут модулировать активность рецептора RUP25. Имеется в виду, что термин "модулировать" относится к способности увеличивать или уменьшать активность рецептора. В некоторых вариантах осуществления соединения настоящего изобретения могут использоваться в способах модулирования рецептора RUP25 посредством контактирования рецептора с одним или несколькими соединениями, как описано выше. В других вариантах осуществления соединения настоящего изобретения могут использоваться в методах модулирования рецептора RUP25 для лечения расстройства, связанного с метаболизмом, у индивидуума, нуждающегося в таком модулировании,включающего контактирование рецептора с терапевтически эффективным количеством соединения формулы (Ih). В некоторых вариантах осуществления соединения настоящего изобретения увеличивают активность рецептора RUP25. В других вариантах осуществления соединения настоящего изобретения представляют собой агонисты рецептора RUP25. Термин "агонист", как используется в данном описании,относится к агентам, которые могут стимулировать активность рецептора (т.е. активировать), подобного рецептору RUP25. В некоторых вариантах осуществления соединения настоящего изобретения являются частичными агонистами рецептора RUP25. Другой аспект настоящего изобретения относится к способам лечения расстройства, связанного с метаболизмом, включающим введение индивидууму, нуждающемуся в таком лечении, терапевтически эффективного количества соединения формулы (Ih). Другой аспект настоящего изобретения относится к способам повышения уровней HDL у индивидуума, включающим введение указанному индивидууму терапевтически эффективного количества соединения формулы (Ih). Другой аспект настоящего изобретения относится к применению соединения формулы (Ih), как описано выше, для лечения расстройства, связанного с метаболизмом, организма человека или животного. Другой аспект настоящего изобретения относится к применению соединений формулы (Ih), как описано выше, для лечения расстройства, связанного с метаболизмом, организма человека или животно- 16011484 го, где указанное расстройство, связанное с метаболизмом, выбирают из группы, состоящей из дислипидемии, атеросклероза, коронарного заболевания сердца, резистентности к инсулину и диабета типа 2. Другой аспект настоящего изобретения относится к применению соединения формулы (Ih), как описано выше, для лечения атеросклероза организма человека или животного. Другой аспект настоящего изобретения относится к применению соединения формулы (Ih) для повышения уровней HDL организма человека или животного. Другой аспект настоящего изобретения относится к применению соединений формулы (Ih), как описано выше, для изготовления лекарственного средства, применяемого при лечении расстройства, связанного с метаболизмом. Другой аспект настоящего изобретения относится к применению соединений формулы (Ih), как описано выше, для изготовления лекарственного средства для лечения расстройства, связанного с метаболизмом, выбранного из группы, состоящей из дислипидемии, атеросклероза, коронарного заболевания сердца, резистентности к инсулину и диабета типа 2. Другой аспект настоящего изобретения относится к применению соединений формулы (Ih), как описано выше, для изготовления лекарственного средства для лечения атеросклероза. Другой аспект настоящего изобретения относится к применению соединений формулы (Ih), как описано выше, для изготовления лекарственного средства для повышения уровня HDL у индивидуума. Некоторые варианты осуществления настоящего изобретения относятся к способам лечения расстройства, связанного с метаболизмом. В некоторых вариантах осуществления расстройство, связанное с метаболизмом, выбирают из группы, состоящей из дислипидемии, атеросклероза, коронарного заболевания сердца, резистентности к инсулину и диабета типа 2. В некоторых вариантах осуществления расстройство, связанное с метаболизмом, представляет собой дислипидемию. В некоторых вариантах осуществления расстройство, связанное с метаболизмом, представляет собой атеросклероз. В некоторых вариантах осуществления расстройство, связанное с метаболизмом, представляет собой коронарное заболевание сердца. В некоторых вариантах осуществления расстройство, связанное с метаболизмом,представляет собой резистентность к инсулину. В некоторых вариантах осуществления расстройство,связанное с метаболизмом, представляет собой диабет типа 2. В некоторых вариантах осуществления,связанных со способами настоящего изобретения, индивидуум представляет собой млекопитающее. В других вариантах осуществления млекопитающим является человек. Другой аспект настоящего изобретения относится к способам получения фармацевтической композиции, включающим смешивание или объединение соединения формулы (Ih), как описано выше, и фармацевтически приемлемого носителя. Композиции настоящего изобретения Некоторые варианты осуществления настоящего изобретения включают фармацевтические композиции, содержащие соединение в соответствии с формулой (Ih) в комбинации с фармацевтически приемлемым носителем. Некоторые варианты осуществления настоящего изобретения включают способ получения фармацевтической композиции, включающий смешивание по меньшей мере одного соединения в соответствии с любым из вариантов осуществления соединения, описанного выше, и фармацевтически приемлемого носителя. Композиции могут быть получены с помощью любого пригодного для использования способа, как правило, посредством однородного смешивания активного соединения (соединений) с жидкостями или тонкоизмельченными твердыми носителями, или с обоими, в требуемых пропорциях, и затем, если это необходимо, формования полученной смеси в желаемую форму. В таблетках и капсулах для перорального введения могут использоваться обычные эксципиенты,такие как связывающие агенты, наполнители, приемлемые смачивающие агенты, лубриканты для таблетирования и дезинтегранты. Жидкие композиции для перорального введения могут находиться в форме растворов, эмульсий, водных или масляных суспензий и сиропов. Альтернативно, композиции для перорального введения могут находиться в форме сухого порошка, который может восстанавливаться водой или другим пригодным жидким носителем перед использованием. В жидкие композиции могут добавляться дополнительные добавки, такие как суспендирующие или эмульгирующие агенты, неводные носители (включая пищевые масла), консерванты и ароматизирующие вещества, и красящие вещества. Дозированные формы для парентерального введения могут приготавливаться посредством растворения соединения настоящего изобретения в соответствующем жидком носителе и стерилизации на фильтре раствора перед заполнением и герметизацией соответствующего флакона или ампулы. Это всего несколько примеров из множества соответствующих способов для получения дозированных форм, хорошо известных в данной области. Соединение настоящего изобретения может составляться в фармацевтические композиции с использованием технологий, хорошо известных специалистам в данной области. Соответствующие фармацевтически приемлемые носители, кроме тех, которые рассмотрены в данном описании, известны в данной области; например, см. Remington, The Science and Practice of Pharmacy, 20th Edition, 2000, Lippincott- 17011484 Хотя является возможным, чтобы соединение для применения при лечении настоящего изобретения могло, при альтернативном использовании, вводиться в виде неочищенного или чистого вещества, предпочтительно, однако, представить соединение или "активный ингредиент" в качестве фармацевтического состава или композиции, дополнительно содержащей фармацевтически приемлемый носитель. По этой причине один из аспектов настоящего изобретения охватывает фармацевтические композиции, содержащие фармацевтически приемлемый носитель в комбинации по меньшей мере с одним соединением в соответствии с формулой (Ih). Настоящее изобретение предусматривает фармацевтические композиции, содержащие соединение настоящего изобретения или его фармацевтически приемлемую соль, гидрат или сольват, вместе с одним или несколькими фармацевтически приемлемыми носителями. Носитель (носители) должны быть "приемлемыми" в смысле совместимости с другими ингредиентами композиции и не слишком вредными для реципиента. Фармацевтические композиции включают такие, которые пригодны для перорального, ректального,назального, местного (включая буккальное и сублингвальное), вагинального или парентерального(включая внутримышечное, подкожное и внутривенное) введения или в форме, пригодной для введения посредством ингаляции, инсуффляции или посредством трансдермального пластыря. Трансдермальные пластыри распределяют лекарственное средство при контролируемой скорости, предоставляя лекарственное средство для поглощения эффективным образом при минимальной деградации лекарственного средства. Как правило, трансдермальные пластыри содержат непроницаемый слой подкладки, один чувствительный к давлению адгезив и удаляемый защитный слой со снимаемой прокладкой. Специалисту в данной области будет понятны и очевидны технологии, пригодные для получения желаемого эффективного трансдермального пластыря на основе потребностей специалиста. Соединения настоящего изобретения, вместе с обычным вспомогательным веществом, носителем или разбавителем, могут быть, таким образом, представлены в форме фармацевтических композиций и их единичных дозированных форм, и в такой форме могут использоваться как твердые продукты, такие как таблетки или заполненные капсулы, или как жидкости, такие как растворы, суспензии, эмульсии,эликсиры, гели или капсулы, заполненные ими, все для перорального применения, в форме суппозиториев для ректального введения; или в форме стерильных растворов для инъекций, для парентерального(включая подкожное) применения. Такие фармацевтические композиции и их единичные дозированные формы могут содержать обычные ингредиенты в обычных пропорциях с дополнительными активными соединениями или веществами или без них, и такие единичные дозированные формы могут содержать любое пригодное эффективное количество активного ингредиента, совместимое с предполагаемым диапазоном ежедневной дозировки, которая должна применяться. Для перорального введения фармацевтическая композиция может быть в форме, например, таблетки, капсулы, суспензии или жидкости. Фармацевтическую композицию предпочтительно изготавливать в виде дозированной единицы, содержащей конкретное количество активного ингредиента. Примеры таких дозированных единиц представляют собой капсулы, таблетки, порошки, гранулы или суспензию, с обычными добавками, такими как лактоза, маннит, кукурузный крахмал или картофельный крахмал; со связующими веществами, такими как кристаллическая целлюлоза, производные целлюлозы, смола акации, кукурузный крахмал или желатины; с дезинтегрантами, такими как кукурузный крахмал, картофельный крахмал или натрийкарбоксиметилцеллюлоза; и с лубрикантами, такими как тальк или стеарат магния. Активный ингредиент может также вводиться посредством инъекции в виде композиции, в которой, например, солевой раствор, декстроза или вода может использоваться в качестве соответствующего фармацевтически приемлемого носителя. Соединения настоящего изобретения или их сольват или физиологически функциональное производное могут использоваться в качестве активных ингредиентов в фармацевтических композициях, в частности, как агонисты рецептора RUP25. Термин "активный ингредиент" определяется в контексте"фармацевтической композиции" и означает компонент фармацевтической композиции, который обеспечивает первичное фармакологическое воздействие, в противоположность "неактивному ингредиенту",который должен, как правило, рассматриваться как не дающий фармацевтической пользы. Доза при использовании соединений настоящего изобретения может изменяться в широких пределах и, обычно и, как известно врачу, должна подбираться для индивидуальных условий в каждом индивидуальном случае. Она зависит, например, от природы и тяжести заболевания, которое должно лечиться, от состояния пациента, от применяемого соединения или от того, осуществляется ли лечение острого или хронического болезненного состояния или вводятся ли другие активные соединения, в дополнение к соединениям настоящего изобретения. Репрезентативные дозы настоящего изобретения включают, но, не ограничиваясь ими, примерно от 0,001 до 5000 мг, примерно от 0,001 до 2500 мг, примерно от 0,001 до 1000 мг, примерно от 0,001 до 500 мг, примерно от 0,001 до 250 мг, примерно от 0,001 до 100 мг, примерно от 0,001 до 50 мг и примерно от 0,001 до 25 мг. В течение дня может вводиться несколько доз, в особенности, если считается, что потребуются относительно большие количества, например 2, 3 или 4 дозы. В зависимости от индивидуума и как считается необходимым врачом или наблюдающим пациента специалистом, может оказаться- 18011484 необходимым отклонение вверх или вниз от доз, описанных выше. Количество активного ингредиента или его активной соли, или производного, необходимое для использования при лечении, будет изменяться не только вместе с конкретной выбранной солью, но также вместе со способом введения, природой и состоянием, которое лечится, и возрастом и состоянием пациента, и, в конечном счете, будет возлагаться ответственность на лечащего врача или клинициста. Как правило, специалисту в данной области будет понятно, как экстраполировать данные in vivo, полученные на модельной системе, на другую систему, например, с животной модели на человека. Как правило, животные модели включают, но, не ограничиваясь ими, модели диабета у грызунов, как описано в примере 1 ниже, модель атеросклероза у мышей, как описано в примере 2 ниже; или модель атеросклероза у животных in vivo, как описано в примере 5 ниже. При некоторых обстоятельствах, эти экстраполяции могут основываться только лишь на массе животной модели, по сравнению с другой, такой как млекопитающее, предпочтительно, человек, однако, чаще, эти экстраполяции не просто основываются на разнице в массе, но скорее включают множество факторов. Репрезентативные факторы включают тип, возраст,массу, пол, диету и медицинское состояние пациента, тяжесть заболевания, способ введения, фармакологические соображения, такие как активность, эффективность, фармакокинетические и токсикологические профили конкретного применяемого соединения, используется ли система доставки лекарственных средств, осуществляется ли лечение острого или хронического болезненного состояния или вводятся ли другие активные соединения, в дополнение к соединениям формулы (I) и в качестве части комбинации лекарственных средств. Режим дозировки для лечения болезненного состояния с помощью соединений и/или композиций настоящего изобретения выбирается в соответствии с множеством таких факторов,которые цитируются выше. Таким образом, реальный используемый режим дозировки может изменяться в широких пределах и по этой причине может отклоняться от предпочтительного режима дозировки, и специалист в данной области заметит, что дозировка и режим дозировки вне этих типичных пределов может исследоваться, и там, где это соответствует, может использоваться в способах настоящего изобретения. Желаемую дозу удобно представлять в одной дозе или в разделенных дозах, вводимых через соответствующие интервалы, например, как две, три, четыре или более субдоз в день. Сама субдоза может быть дополнительно разделена, например, на ряд отдельных свободно осуществляемых введений. Дневная доза может быть разделена на несколько введений, особенно, если считается, что необходимо вводить относительно большие количества, например, на 2, 3 или 4 отдельных введения. Если это необходимо, в зависимости от поведения индивидуума, может быть необходимым отклонение вверх или вниз от указанной дневной дозы. Соединения настоящего изобретения могут вводиться в виде разнообразных пероральных и парентеральных дозированных форм. Специалисту в данной области будет очевидно, что следующие дозированные формы могут содержать в качестве активного компонента либо соединение настоящего изобретения, либо фармацевтически приемлемую соль соединения настоящего изобретения. Для получения фармацевтических композиций из соединений настоящего изобретения, фармацевтически приемлемые носители могут быть либо твердыми, либо жидкими. Композиции в твердой форме включают порошки, таблетки, пилюли, капсулы, облатки, суппозитории и диспергируемые гранулы. Твердый носитель может представлять собой одно или несколько веществ, которые могут также действовать как разбавители, ароматизирующие агенты, солюбилизаторы, лубриканты, суспендирующие агенты, связующие вещества, консерванты, дезинтегранты для таблеток или инкапсулирующее средство. В порошках носитель представляет собой тонкоизмельченное твердое вещество, которое находится в смеси с тонкоизмельченным активным компонентом. В таблетках активный компонент смешивается с носителем, имеющим необходимую способность к связыванию, в соответствующих пропорциях и спрессовывается в желаемой форме и размерах. Порошки и таблетки могут содержать различные процентные количества активного соединения. Репрезентативное количество в порошке или таблетке может содержать примерно от 0,5 до 90% активного соединения; однако, специалист должен знать, когда необходимы количества вне этих пределов. Носители, пригодные для порошков и таблеток, представляют собой карбонат магния, стеарат магния,тальк, сахар, лактозу, пектин, декстрин, крахмал, желатин, смолу трагаканта, метилцеллюлозу, натрийкарбоксиметилцеллюлозу, воск с низкой температурой плавления, масло какао и т.п. Предполагается,что термин "получение" включает получение активного соединения с инкапсулирующим средством в качестве носителя, обеспечивающего капсулу, в которой активный компонент с носителями или без окружен носителем, который, таким образом, связан с ним. Подобным же образом, термин включает облатки и лепешки. Таблетки, порошки, капсулы, пилюли, облатки и лепешки могут использоваться в виде твердых форм, пригодных для перорального введения. Для получения суппозиториев, воск с низкой температурой плавления, например с примесью глицеридов жирных кислот или масла какао, сначала расплавляют и активный компонент гомогенно диспергируют в нем, например, посредством перемешивания. Затем расплавленную гомогенную смесь выливают в формы удобного размера, дают остыть и, тем самым, затвердеть. Композиции, пригодные для вагинального введения, могут быть представлены как пессарии, там- 19011484 поны, кремы, гели, пасты, пены или спреи, содержащие, в дополнение к активному ингредиенту, носители, известные как пригодные в данной области. Композиции в жидкой форме включают растворы, суспензии и эмульсии, например, растворы в воде или смеси вода-пропиленгликоль. Например, жидкие композиции для парентеральных инъекций могут быть получены как растворы в водном растворе полиэтиленгликоля. Композиции для инъекций, например, стерильные водные или масляные суспензии для инъекций могут быть получены, как известно в данной области, с использованием соответствующих диспергирующих или смачивающих агентов и суспендирующих агентов. Стерильный препарат для инъекций может также представлять собой стерильный раствор или суспензию для инъекций в нетоксичном парентерально приемлемом разбавителе или растворителе, например, в виде раствора в 1,3-бутандиоле. Среди пригодных носителей и растворителей,которые могут использоваться, находятся вода, раствор Рингера и изотонический раствор хлорида натрия. В дополнение, в качестве растворителя обычно используются стерильные, фиксированные масла или суспендирующие среды. Для этой цели может использоваться любое мягкое фиксированное масло,включая синтетические моно- или диглицериды. В дополнение, при получении композиций для инъекций находят применение жирные кислоты, такие как олеиновая кислота. Соединения в соответствии с настоящим изобретением могут, таким образом, составляться в композиции для парентерального введения (например, посредством инъекции, такой как инъекции болюса или непрерывного вливания) и могут быть представлены в единичной дозированной форме в ампулах,предварительно заполненных шприцах, контейнерах малого объема для вливаний или в контейнерах для множественных доз с добавлением консерванта. Композиции могут принимать такие формы, как суспензии, растворы или эмульсии в масляных или водных носителях, и могут содержать агенты, необходимые для получения, такие как суспендирующие, стабилизирующие и/или диспергирующие агенты. Альтернативно, активный ингредиент может находиться в форме порошка, полученного посредством асептического выделения стерильного твердого продукта или посредством лиофилизации из раствора, для восстановления перед применением соответствующим носителем, например, стерильной, не содержащей пирогенов воде. Водные растворы, пригодные для перорального применения, могут быть получены посредством растворения активного компонента в воде и добавления соответствующих красящих веществ, ароматизаторов, стабилизирующих и загущающих агентов, по желанию. Водные суспензии, пригодные для перорального применения, могут быть получены посредством диспергирования тонкоизмельченного активного компонента в воде с вязким веществом, таким как натуральные или синтетические декстрины, смолы, метилцеллюлоза, натрийкарбоксиметилцеллюлоза или другие хорошо известные суспендирующие агенты. Включаются сюда также композиции в твердой форме, которые предназначены для превращения,незадолго перед применением, в композиции в жидкой форме для перорального введения. Такие жидкие формы включают растворы, суспензии и эмульсии. Эти композиции могут содержать, в дополнение к активному компоненту, красящие вещества, ароматизаторы, стабилизаторы, буферы, искусственные и натуральные подсластители, диспергирующие агенты, загущающие агенты, солюбилизирующие агенты и т.п. Для местного введения в эпидермис, соединения в соответствии с настоящим изобретением могут быть получены в виде мази, крема или лосьона либо в виде трансдермального пластыря. Мази и кремы могут быть составлены, например, вместе с водной или масляной основой, с добавлением соответствующих загущающих и/или гелеобразующих агентов. Лосьоны могут быть составлены вместе с водной или масляной основой и будут, как правило, содержать также один или несколько эмульгирующих агентов, стабилизирующих агентов, диспергирующих агентов, суспендирующих агентов, загущающих агентов или красящих агентов. Композиции, пригодные для местного введения в ротовую полость, включают лепешки, содержащие активный агент в ароматизированной основе, обычно, в сахарозе и смоле акации или трагаканта; пастилки, содержащие активный ингредиент в инертной основе, такой как желатин и глицерин или сахароза и смола акации; и полоскания для рта, содержащие активный ингредиент в соответствующем жидком носителе. Растворы или суспензии наносятся непосредственно в носовую полость с помощью обычных средств, например с помощью капельницы, пипетки или спрея. Композиции могут предусматриваться в единичной дозированной форме или в форме нескольких доз. В последнем случае, из капельницы или пипетки это может достигаться посредством введения пациенту соответствующего заданного объема раствора или суспензии. В случае спрея, это может достигаться, например, посредством отмеряющего насоса распылительного устройства. Введение в дыхательный тракт может также достигаться посредством композиции аэрозоля, в котором активный ингредиент предусматривается в упаковке под давлением вместе с соответствующим пропеллентом. Если соединения формулы (I) или фармацевтические композиции, содержащие их, вводятся как аэрозоли, например, как назальные аэрозоли, или посредством ингаляции, это может быть осуществлено, например, с использованием спрея, распылителя, распылителя с насосом, устройства для ингаля- 20011484 ции, отмеривающего ингалятора или ингалятора с сухим порошком. Фармацевтические формы для введения соединения формулы (I) в виде аэрозоля могут быть получены с помощью способов, хорошо известных специалистам в данной области. Для их изготовления могут использоваться, например, растворы или дисперсии соединений формулы (I) в воде, смесях вода/спирт или в соответствующих солевых растворах с использованием обычных добавок, например, бензилового спирта или других соответствующих консервантов, усилителей абсорбции для увеличения биодоступности, солюбилизаторов, диспергирующих агентов и других, и. если требуется, соответствующих пропеллентов, например, включая двуокись углерода, CFC (хлофторуглероды), такие как дихлордифторметан, трихлорфторметан или дихлортетрафторэтан; и тому подобное. Удобно, чтобы аэрозоль также содержал поверхностно-активное вещество, такое как лецитин. Доза лекарственного средства может контролироваться посредством обеспечения отмеряющего клапана. В композициях, предназначенных для введения в дыхательный тракт, включая интраназальные композиции, соединение, как правило, будет иметь малый размер частиц, например, порядка 10 микрон(мкм) или меньше. Такой размер частиц может быть получен с помощью средств, известных в данной области, например, посредством микронизации. Когда это желательно, могут использоваться композиции, адаптированные для получения длительного высвобождения активного ингредиента. Альтернативно, активные ингредиенты могут предусматриваться в форме сухого порошка, например, порошкообразной смеси соединения в соответствующей порошковой основе, такой как лактоза,крахмал, производные крахмала, такие как гидроксипропилметилцеллюлоза и поливинилпирролидон(PVP). Удобно, чтобы порошкообразный носитель образовывал гель в носовой полости. Порошковая композиция может быть предоставлена в единичной дозированной форме, например, в капсулах или картриджах, например, из желатина, или блистерных упаковках, из которых порошок может вводиться посредством ингалятора. Фармацевтические композиции предпочтительно находятся в форме единичных дозированных форм. В такой форме препарат разделяется на единичные дозы, содержащие соответствующие количества активного компонента. Вид единичной дозированной формы может представлять собой упакованный препарат, упаковка содержит отдельные количества препарата, такие как упакованные таблетки, капсулы и порошки во флаконах или ампулах. Также единичная дозированная форма может представлять собой капсулу, таблетку, облатки или лепешку, сама по себе, или может представлять собой соответствующее количество любых из них в упакованной форме. Таблетки или капсулы для перорального введения и жидкости для внутривенного введения представляют собой предпочтительные композиции. Соединения настоящего изобретения могут быть превращены в "пролекарства". Термин "пролекарство" относится к соединениям, которые модифицируются конкретными химическими группами, известными в данной области и, когда их вводят индивидууму, эти группы подвергаются биотрансформации с получением исходного соединения. Таким образом, пролекарства могут рассматриваться как соединения настоящего изобретения, содержащие одну или несколько специализированных нетоксичных защитных групп, временно используемых для изменения или устранения свойства соединения. Как правило, подход "пролекарств" используется для облегчения пероральной абсорбции. Подробное обсуждение приведено у Т. Higuchi and V. Stella, в "Pro-drugs as Novel Delivery Systems," Volume. 14 of A.C.S. Symposiumand Pergamon Press, 1987, обе тем самым включаются посредством ссылок во всей их полноте. Комбинированная терапия. Хотя соединения настоящего изобретения могут вводиться как единственный активный фармацевтический агент (т.е. как монотерапия), они также могут использоваться в комбинации с другими фармацевтическими агентами (т.е. как комбинированная терапия), например, для лечения заболеваний/состояний/расстройств, описанных в данном изобретении. По этой причине, другой аспект настоящего изобретения включает способы лечения заболеваний, связанных с метаболизмом, включающие введение индивидууму, нуждающемуся в таком лечении, терапевтически эффективного количества соединения настоящего изобретения в комбинации с одним или несколькими дополнительными фармацевтическими агентами, как описано выше. Соответствующие фармацевтические агенты, которые могут использоваться в комбинации с соединениями настоящего изобретения, включают агенты против тучности, такие как ингибиторы белка секреции аполипопротеина-В/микросомального переноса триглицеридов (аро-В/МТР), агонисты MCR-4,агонисты холецистокинина-А (CCK-A), ингибиторы повторного поглощения серотонина и норэпинефрина (например, сибутрамин), симпатомиметические агенты, агонисты адренергических рецепторов 3,агонисты допамина (например, бромокриптин), аналоги рецептора гормона, стимулирующего меланоциты, антагонисты рецепторов 1 канабиноидов [например, SR141716: N-(пиперидин-1-ил)-5-(4-хлорфенил)1-(2,4-дихлорфенил)-4-метил-1 Н-пиразол-3-карбоксамид], антагонисты гормона, концентрирующего меланин, лептоны (белок ОВ), аналоги лептина, агонисты рецептора лептина, антагонисты галанина, ингибиторы липазы (такие как тетрагидролипстатин, т.е. орлистат), аноректические агенты (такие как агонист бомбезина), антагонисты нейропептида-Y, тиромиметические агенты, дегидроэпиандростерон или- 21011484 его аналог, агонисты или антагонисты рецептора глюкокортикоидов, антагонисты рецептора орексина,антагонисты белка, связывающего урокортин, агонисты рецептора 1 глюкагон-подобного пептида, цилиарные нейтротропные факторы (такие как Axokine, доступный от Regeneron Pharmaceuticals, Ihc.,Tarrytown, NY, и ProcterGamble Company, Cincinnati, OH), белки, родственные агути человека (AGRP),антагонисты рецептора грелина, антагонисты или обратные агонисты рецептора 3 гистамина, агонисты рецептора U нейромедина, норадренергические аноректические агенты (например, фентермин, мазиндол и т.п.) и подавители аппетита (например, бупропион). Другие агенты против тучности, включая агенты, приведенные ниже, хорошо известны специалисту в данной области или будут очевидны в свете настоящего описания. В некоторых вариантах осуществления агенты против тучности выбираются из группы, состоящей из орлистата, сибутрамина, бромокриптина, эфедрина, лептина и псевдоэфедрина. В другом варианте осуществления соединения настоящего изобретения и комбинированные терапии вводятся наряду с упражнениями и/или разумной диетой. Понятно, что рамки комбинированной терапии соединениями настоящего изобретения вместе с другими агентами против тучности, аноректическими агентами, подавителем аппетита и родственными агентами не ограничиваются тем, что перечислено выше, но включают, в принципе, любую комбинацию с любым фармацевтическим агентом или фармацевтической композицией, пригодными для лечения индивидуумов, имеющих лишний вес, и тучных индивидуумов. Другие соответствующие фармацевтические агенты, в дополнение к агентам против тучности, которые могут использоваться в комбинации с соединениями настоящего изобретения, включают агенты,пригодные для лечения сопутствующих расстройств. Лечение таких расстройств включает применение одного или нескольких фармацевтических агентов, известных в данной области, которые принадлежат к классам лекарственных средств, относящихся, но, не ограничиваясь ими, к следующим: сульфонилмочевинам, меглитинидам, бигуанидам, ингибиторам -глюкозидазы, агонистам активируемого пролифераторами пероксисом рецептора- (т.е. PPAR-), инсулину, аналогам инсулина, ингибиторам HMG-CoA редуктазы, лекарственным средствам, понижающим уровень холестерина (например, фибратамы, которые включают: фенофибрат, безафибрат, гемфиброзил, клофибрат и т.п.; секвестрантам желчных кислот,которые включают: холестирамин, колестипол и т.п.; и ниацин), агентам против образования бляшек(например, аспирин и антагонистам рецептора аденозиндифосфата, которые включают: клопидогрель,тиклопидин и т.п.), ингибиторам ангиотензин-превращающего фермента, антагонистам рецептора II ангиотензина и адипонектину. В соответствии с одним из аспектов настоящего изобретения соединение настоящего изобретения может использоваться в комбинации с фармацевтическим агентом или агентами, принадлежащими к одному или нескольким классам лекарственных средств, перечисленных выше. Понятно, что рамки комбинированной терапии соединениями настоящего изобретения вместе с другими фармацевтическими агентами не ограничиваются тем, что перечислено выше или ниже, но включают, в принципе, любую комбинацию с любым фармацевтическим агентом или фармацевтической композицией, пригодной для лечения заболеваний, состояний или расстройств, которые связаны с расстройствами, связанными с метаболизмом. Некоторые варианты осуществления настоящего изобретения включают способы лечения заболевания, расстройства или состояния, как описано выше, включающие введение индивидууму, нуждающемуся в таком лечении, терапевтически эффективного количества или дозы соединений настоящего изобретения в комбинации по меньшей мере с одним фармацевтическим агентом, выбранным из группы, состоящей из сульфонилмочевин, меглитинидов, бигуанидов, ингибиторов -глюкозидазы, агонистов активируемого пролифераторами пероксисом рецептора- (т.е. PPAR-), инсулина, аналогов инсулина, ингибиторов HMG-CoA редуктазы, лекарственных средств, понижающих уровень холестерина (например,фибратов, которые включают: фенофибрат, безафибрат, гемфиброзил, клофибрат и т.п.; секвестрантов желчных кислот, которые включают: холестирамин, колестипол и т.п.; и ниацин), агентов против образования бляшек (например, аспирин и антагонисты рецептора аденозиндифосфата, которые включают: клопидогрель, тиклопидин и т.п.), ингибиторов ангиотензин-превращающего фермента, антагонистов рецептора II ангиотензина и адипонектина. В некоторых вариантах осуществления фармацевтическая композиция дополнительно содержит один или несколько агентов, выбранных из группы, состоящей из ингибитора -глюкозидазы, ингибитора альдозаредуктазы, бигуанида, ингибитора HMG-CoA редуктазы,ингибитора синтеза скваленов, фибрата, усилителя катаболизма LDL, ингибитора ангиотензинпревращающего фермента, усилителя секреции инсулина и тиазолидиндиона. Один из аспектов настоящего изобретения охватывает фармацевтические композиции, содержащие по меньшей мере, одно соединение в соответствии с формулой (I), как описано выше. В некоторых вариантах осуществления фармацевтическая композиция дополнительно содержит один или несколько агентов, выбранных из группы, состоящей, например, из ингибитора -глюкозидазы, ингибиторы альдозаредуктазы, бигуанида, ингибитора HMG-CoA редуктазы, ингибитора синтеза скваленов, фибрата, усилителя катаболизма LDL, ингибитора ангиотензин-превращающего фермента, усилителя секреции инсулина и тиазолидиндиона.- 22011484 Соответствующие фармацевтические агенты, которые могут использоваться в комбинации с соединениями настоящего изобретения, включают ингибиторы -глюкозидазы. Ингибиторы -глюкозидазы принадлежат к классу лекарственных средств, которые конкурентно ингибируют дигестивные ферменты,такие как -амилаза, мальтаза, -декстриназа, сукраза и т.п., в поджелудочной железе и/или тонком кишечнике. Обратное ингибирование посредством ингибиторов -глюкозидазы замедляет, уменьшает или иным образом снижает уровни глюкозы в крови посредством замедления переваривания крахмала и сахаров. Некоторые репрезентативные примеры ингибиторов -глюкозидазы включают акарбозу, N-(1,3 дигидрокси-2-пропил)валиоламин (общее наименование воглибоза), миглитол и ингибиторы глюкозидазы, известные в данной области. Соответствующие фармацевтические агенты, которые могут использоваться в комбинации с соединениями настоящего изобретения, включают сульфонилмочевины. Сульфонилмочевины (SU) представляют собой лекарственные средства, которые облегчают секрецию инсулинаклетками поджелудочной железы посредством передачи сигналов секреции инсулина через рецепторы SU в клеточных мембранах. Примеры сульфонилмочевин включают глибурид, глипизид, глимепирид и другие сульфонилмочевины,известные в данной области. Соответствующие фармацевтические агенты, которые могут использоваться в комбинации с соединениями настоящего изобретения, включают меглитиниды. Меглитиниды представляют собой производные бензойной кислоты, представляющие собой новый класс агентов, облегчающих секрецию инсулина. Эти агенты нацелены на послеобеденную гипергликемию и показывают эффективность, сравнимую с сульфонилмочевинами, при восстановлении HbA1c. Примеры меглитинидов включают репаглинид, натеглинид и другие меглитиниды, известные в данной области. Соответствующие фармацевтические агенты, которые могут использоваться в комбинации с соединениями настоящего изобретения, включают бигуаниды. Бигуаниды представляют собой класс лекарственных средств, которые стимулируют анаэробный гликолиз, увеличивают чувствительность к инсулину в периферийных тканях, ингибируют поглощение глюкозы в кишечнике, подавляют глюконеогенез в печени и ингибируют окисление жирных кислот. Примеры бигуанидов включают фенформин, метформин, буформин и бигуаниды, известные в данной области. Соответствующие фармацевтические агенты, которые могут использоваться в комбинации с соединениями настоящего изобретения, включают ингибиторы -глюкозидазы. Ингибиторы -глюкозидазы конкурентно ингибируют дигестивные ферменты, такие как -амилаза, мальтаза, -декстриназа, сукраза и т.п., в поджелудочной железе и/или в тонком кишечнике. Обратимое ингибирование посредством ингибиторов -глюкозидазы замедляет, уменьшает или иным образом снижает уровни глюкозы в крови посредством замедления переваривания крахмала и сахаров. Примеры ингибиторов -глюкозидазы включают акарбозу, N-(1,3-дигидрокси-2-пропил)валиоламин (общее наименование воглибоза), миглитол и ингибиторы -глюкозидазы, известные в данной области. Соответствующие фармацевтические агенты, которые могут использоваться в комбинации с соединениями настоящего изобретения, включают агонисты активируемого пролифераторами пероксисом рецептора- (т.е. PPAR-). Агонисты активируемого пролифераторами пероксисом рецептора- представляют собой класс соединений, которые активируют ядерный рецептор PPAR- и таким образом регулируют транскрипцию инсулин-чувствительных генов, вовлеченных в контроль продуцирования, переноса и утилизации глюкозы. Агенты этого класса также облегчают регуляцию метаболизма жирных кислот. Примеры агонистов PPAR- включают розиглитазон, пиоглитазон, тезаглитазар, нетоглитазон, GW409544, GW-501516 и агонисты PPAR-, известные в данной области. Соответствующие фармацевтические агенты, которые могут использоваться в комбинации с соединениями настоящего изобретения, включают ингибиторы HMG-CoA редуктазы. Ингибиторы HMG-CoA редуктазы представляют собой агенты, указанные также как соединения статина, которые принадлежат к классу лекарственных средств, которые снижают уровни холестерина в крови посредством ингибирования гидроксиметилглуталил-СоА (HMG-СоА) редуктазы. HMG-CoA редуктаза представляет собой фермент, лимитирующий скорость превращения при биосинтезе холестерина. Статины понижают концентрации LDL в сыворотке крови посредством положительного регулирования активности рецепторов LDL и являются ответственными за удаление LDL из крови. Некоторые репрезентативные примеры соединений статина включают розувастатин, правастатин и его натриевую соль, симвастатин, ловастатин, аторвастатин, флувастатин, церивастатин, питавастатин, "суперстатин" BMS и ингибиторы HMG-CoA редуктазы, известные в данной области. Соответствующие фармацевтические агенты, которые могут использоваться в комбинации с соединениями настоящего изобретения, включают ингибиторы ангиотензин-превращающего фермента (АСЕ). Ингибиторы ангиотензин-превращающего фермента принадлежат к классу лекарственных средств, которые частично снижают уровни глюкозы в крови, а также снижают кровяное давление посредством ингибирования ангиотензин-превращающих ферментов. Примеры ингибиторов ангиотензин-превращающих ферментов включают каптоприл, эналаприл, алацеприл, делаприл; рамиприл, лизиноприл, имидаприл,беназеприл, церонаприл, цилазаприл, эналаприлат, фозиноприл, мувелтоприл, периндоприл, кинаприл,- 23011484 спираприл, темокаприл, трандолаприл и ингибиторы ангиотензин-превращающего фермента, известные в данной области. Соответствующие фармацевтические агенты, которые могут использоваться в комбинации с соединениями настоящего изобретения, включают антагонисты рецептора II ангиотензина. Антагонисты рецептора II ангиотензина нацелены на субтип 1 рецептора II ангиотензина (т.е. ATI) и демонстрируют положительное воздействие на гипертензию. Примеры антагонистов рецептора II ангиотензина включают лозартан (и форму калиевой соли) и антагонисты рецептора II ангиотензина, известные в данной области. Другие виды лечения для одного или нескольких из заболеваний, цитируемых в данном описании,включают применение одного или нескольких фармацевтических агентов, известных в данной области,которые принадлежат к классам лекарственных средств, относящихся, но, не ограничиваясь ими, к следующим: агонистам амилина (например, прамлинтиду), агентам, стимулирующим секрецию инсулина(например, агонистам GLP-1; эксендину-4; инсулинотропину (NN2211); ингибиторам дипептилпептидазы (например, NVP-DPP-728), ингибиторам ацил СоА-холестеринацетилтрансферазы (например, эзетимибу, эфлуцимибу и подобным соединениям), ингибиторам поглощения холестерина (например, эзетимибу, памаквезиду и подобным соединениям), ингибиторам белков переноса эфира холестерина (например, СР-529414, JTTPET-705, CETi-1, торцетрапибу и подобным соединениям), ингибиторам белков переноса микросомальных триглицеридов (например, имплитапиду и подобным соединениям), модуляторам холестерина (например, НЕ-1886 и подобным соединениям), модуляторам желчных кислот (например, GT103-279, и подобным соединениям) и ингибиторам скваленсинтазы. Ингибиторы синтеза скваленов принадлежат к классу лекарственных средств, которые понижают уровни холестерина в крови посредством ингибирования синтеза скваленов. Примеры ингибиторов синтеза скваленов включают монокалиевую соль (S)[бис-[(2,2-диметил-1-оксопропокси)метокси]фосфинил]-3-феноксибензолбутансульфоновой кислоты (BMS-188494) и ингибиторы синтеза скваленов,известные в данной области. В соответствии с настоящим изобретением комбинация может использоваться посредством смешивания соответствующих активных компонентов, либо всех вместе, либо независимо, с фармацевтически приемлемым носителем, эксципиентом, связующим веществом, разбавителем и т.п., как описано в данном описании выше, и введения смеси или смесей либо перорально, либо неперорально, в виде фармацевтической композиции. Когда соединение или смесь соединений формулы (I) вводится в виде комбинированной терапии с другим активным соединением, терапевтические агенты могут быть получены как отдельные фармацевтические композиции, которые вводят пациенту в одно и то же время или в различные моменты времени, или терапевтические агенты могут вводиться в виде одной композиции. В соответствии с настоящим изобретением комбинация соединений настоящего изобретения и фармацевтического агента может быть получена посредством смешивания соответствующих активных компонентов, либо всех вместе, либо независимо, с фармацевтически приемлемым носителем, эксципиентом, связующим веществом, разбавителем и т.п., как описано выше, и введения смеси или смесей либо перорально, либо неперорально в виде фармацевтической композиции. Когда соединение или смесь соединений формулы (I) вводится в виде комбинированной терапии с другим активным соединением, терапевтические агенты могут быть получены как отдельные фармацевтические композиции, которые вводят пациенту в одно и то же время или в различные моменты времени, или терапевтические агенты могут вводиться в виде одной композиции. Меченые соединения и способы анализа. Другой объект настоящего изобретения относится к радиоактивно-меченым соединениям формулы(I), которые являются полезными не только при получении радиоактивных изображений, но также при анализах как in vitro, так и in vivo, для определения локализации и количественного определения RUP25 в образцах тканей, включая человека, и для идентификации лигандов RUP25 посредством ингибирования связывания радиоактивно-меченого соединения. Другим объектом настоящего изобретения является включение новых анализов RUP25, которые включают такие радиоактивно-меченые соединения. Настоящее изобретение охватывает изотопно-меченые соединения формулы (I) и любые подгруппы, указанные выше, такие как, но, не ограничиваясь ими, соединения формул (Ia)-(Iz) и (IIa)-(IId). "Изотопно- или радиоактивно-меченые" соединения представляют собой такие соединения, которые идентичны соединениям, описанным выше, но с тем отличием, что один или несколько атомов заменены или замещены атомом, имеющим атомную массу или массовый номер, отличный от атомной массы или массового номера, обычно обнаруживаемого в природе (т.е. встречающегося в природе). Соответствующие радионуклиды, которые могут вводиться в соединения настоящего изобретения, включают, но, не ограничиваясь ими, 2 Н (также записываемый как D для дейтерия), 3 Н (также записываемый как Т для трития),11 С, 13 С, 14 С, 13N, 15N, 15O, 17O, 18O, 18F, 35S, 36Cl, 82Br, 75Br, 76Br, 77Br, 123I, 124I, 125I и 131I. Радионуклид, который вводится в настоящие радиоактивно-меченые соединения, будет зависеть от конкретного применения этого радиоактивно-меченого соединения. Например, для анализов с мечением и конкуренциейRUP25 in vitro, как правило, будут наиболее полезными соединения, которые включают 3 Н, 14 С, 82Br, 125I,131 35I, S. Для применения с получением радиоактивных изображений, как правило, будут наиболее полез- 24011484 ными 11C, 18F, 125I, 123I, 124I, 131I, 75Br, 76Br или 77Br. Понятно, что "радиоактивно-меченое" или "меченое соединение" представляет собой соединение формулы (I), которое содержит по меньшей мере один радионуклид; в некоторых вариантах осуществления радионуклид выбирают из группы, состоящей из 3 Н, 14 С, I25I, 35S и 82Br. Определенные изотопно-меченые соединения настоящего изобретения являются полезными при анализах распределения соединения и/или субстрата в тканях. В некоторых вариантах осуществления при этих исследованиях являются полезными радионуклидные изотопы 3 Н и/или 14 С. Кроме того, замещение более тяжелыми изотопами, такими как дейтерий (т.е. 2 Н), может дать определенные терапевтические преимущества, возникающие в результате большей метаболической стабильности (например, увеличение времени полураспада in vivo или пониженные требования к дозировке), и по этой причине, могут быть предпочтительными в некоторых обстоятельствах. Изотопно-меченые соединения настоящего изобретения могут, как правило, быть получены с помощью следующих методик, аналогично приведенным на схемах выше, и в примерах ниже, посредством замещения изотопно-меченым реагентом изотопно-немеченого реагента. Другие способы синтеза, которые являются полезными, обсуждаются ниже. Кроме того, необходимо понять, что все атомы, представленные в соединениях настоящего изобретения,могут представлять собой либо наиболее часто встречающиеся изотопы таких атомов, либо более редкий радиоактивный изотоп или нерадиоактивный изотоп. Способы синтеза для введения радиоактивных изотопов в органические соединения применимы к соединениям настоящего изобретения и хорошо известны в данной области. Эти синтетические способы,например введение уровней активности трития в целевые молекулы, являются следующими.A. Каталитическое восстановление газообразным тритием - эта методика обычно дает продукты с высокой удельной активностью и требует галогенированных или ненасыщенных предшественников.B. Восстановление боргидридом натрия [3 Н] - эта методика является скорее недорогой и требует предшественников, содержащих восстанавливаемые функциональные группы, такие как альдегиды, кетоны, лактоны, сложные эфиры и т.п.C. Восстановление литийалюминийгидридом [3 Н] - эта методика дает продукты с почти теоретическими удельными активностями. Она также требует предшественников, содержащих восстанавливаемые функциональные группы, такие как альдегиды, кетоны, лактоны, сложные эфиры и т.п.D. Мечение посредством воздействия газообразным тритием - эта методика включает воздействие газообразным тритием в присутствии соответствующего катализатора на предшественники, содержащие обмениваемые протоны.E. N-Метилирование с использованием метилйодида [3 Н] - эта методика обычно используется для получения продуктов О-метила или N-метила (3 Н) обработкой соответствующих предшественников метилйодидом (3 Н) высокой удельной активности. Эта методика, как правило, дает более высокую удельную активность, такую, например, как примерно 70-90 Кюри/ммоль. Способы синтеза для введения уровней активности 125I в целевые молекулы включают следующее. А. Реакцию Сандмейера и подобные ей - эта методика преобразует арил или гетероариламин в диазониевую соль, такую как тетрафторборатная соль, и затем в соединение, меченое 125I, с использованиемNa125I. О представленной методике сообщено Zhu, D.-G. and co-workers in J. Org. Chem. 2002, 67, 943-948.B. Орто-125 йодирование фенолов - эта методика делает возможным введение 125I в орто-положении фенола, как сообщалось Collier, T.L. and co-workers в J. Labeled Compd. Radiopharm. 1999, 42, S264-S266.C. Обмен арил- и гетероарилбромида с 125I - эта методика, как правило, представляет собой двухстадийный процесс. Первая стадия представляет собой преобразование арил- или гетероарилбромида в соответствующее промежуточное соединение триалкилолова с использованием, например, реакции, катализируемой Pd [т.е. Pd(Ph3P)4] или через арил или гетероариллитий, в присутствии триалкилгалогенида олова или гексаалкилдиолова [например, (CH3)3SnSn(CH3)3]. О представленной методике сообщено Bas,M.-D. and co-workers, J. Labeled Compd Radiopharm. 2001, 44, S280-S282. Радиоактивно-меченое соединение RUP25 формулы (I) может использоваться при скрининговом анализе для идентификации/оценки соединений. В общих терминах вновь синтезируемое или идентифицируемое соединение (т.е. исследуемое соединение) может оцениваться на его способность к уменьшению связывания "радиоактивно-меченого соединения формулы (I)" с рецептором RUP25. Соответственно, способность исследуемого соединения к конкуренции с "радиоактивно-меченым соединением формулы (I)" за связывание с рецептором RUP25 прямо коррелирует с его способностью к связыванию. Меченые соединения настоящего изобретения связываются с рецептором RUP25. В одном из вариантов осуществления меченое соединение имеет IC50, меньшую примерно чем 500 мкМ, в другом варианте осуществления меченое соединение имеет IC50, меньшую примерно чем 100 мкМ, еще в одном варианте осуществления меченое соединение имеет IC50, меньшую примерно чем 10 мкМ, еще в одном варианте осуществления меченое соединение имеет IC50, меньшую примерно чем 1 мкМ, и еще в одном варианте осуществления меченый ингибитор имеет IC50, меньшую примерно чем 0,1 мкМ. Другие применения описанных рецепторов и способов будут ясны специалисту в данной области на основе, среди прочего, ознакомления с настоящим описанием. Как будет ясно, стадии способов настоящего изобретения не должны осуществляться какое-либо- 25011484 конкретное количество раз или в какой-либо конкретной последовательности. Дополнительные цели,преимущества и новые признаки настоящего изобретения станут ясны специалисту в данной области при рассмотрении следующих примеров, которые рассматриваются как иллюстративные примеры и не предназначены для ограничения. Примеры Следующие примеры предусматриваются для иллюстративных целей, а не в качестве средств ограничения. Специалист в данной области сможет провести эквивалентные анализы и способы на основе настоящего описания, все из которых составляют часть настоящего изобретения. Пример 1. Модели диабета у грызунов. Разработаны модели диабета у грызунов типа 2, связанного с тучностью и резистентностью к инсулину. Генетические модели, такие как db/db и ob/ob мышей [см. Diabetes (1982) 31:1-6] и fa/fa крыс Цукера, разработаны для понимания патофизиологии заболевания и для исследования терапевтических соединений-кандидатов [Diabetes (1983) 32:830-838; Annu. Rep. Sankyo Res. Lab (1994) 46:1-57]. Гомозиготные животные, мыши С 57 BL/KsJ-db/db, полученные в Jackson Laboratory, являются тучными, гипергликемическими, гиперинсулинемическими и резистентными к инсулину [J. Clin. Ihvest. (1990) 85:962-967], в то время как гетерозиготные являются тощими и нормогликемическими. На модели db/db мышей постепенно с возрастом развивается инсулинопения, особенность, обычно наблюдаемая на поздних стадиях диабета типа 2 у людей, когда уровни сахара контролируются недостаточно. Поскольку эта модель напоминает модель диабета типа 2 человека, соединения настоящего изобретения исследуют на активности, включая, но, не ограничиваясь ими, снижение уровней глюкозы и триглицеридов в плазме крови. Крысы Цукера (fa/fa) имеют острое ожирение, гиперинсулинемию и резистентность к инсулинуPublishing Co, New York, ed. 4, (1990), pp. 299-340], и мутация fa/fa может представлять собой крысиный эквивалент мышиной мутации db [Friedman et al., Cell (1992) 69:217-220; Truett et al., Proc. Natl. Acad. Sci.USA (1991) 88:7806]. Коротконогие (tub/tub) мыши характеризуются тучностью, умеренной резистентностью к инсулину и гиперинсулинемией без значительной гипергликемии [Coleman et al., Heredity (1990) 81:424]. Настоящее изобретение охватывает применение соединений настоящего изобретения для снижения резистентности к инсулину и гипергликемии на всех из указанных выше моделях диабета у грызунов, у людей с диабетом типа 2 или другими преимущественными расстройствами, связанными с метаболизмом, или расстройствами метаболизма липидов, описанными ранее, или на моделях на основе других млекопитающих. Уровни глюкозы и инсулина в плазме крови будут исследоваться, также как и другие факторы, включая, но, не ограничиваясь ими, свободные жирные кислоты и триглицериды в плазме. Исследование in vivo на антигипергликемическую активность соединений настоящего изобретения. Генетически измененных тучных диабетических мышей (db/db) (самцы, возраст 7-9 недель) содержат (7-9 мышей/клетка) в стандартных лабораторных условиях, при 22 С и 50% относительной влажности, и выдерживают на диете из корма для грызунов Purina и воды по потребности. Перед обработкой собирают кровь из хвостовой вены каждого животного и определяют концентрацию глюкозы в крови с использованием One Touch Basic Glucose Monitor System (Lifescan). Используют мышей, которые имеют уровни глюкозы в плазме крови в пределах 250-500 мг/дл. Каждая обработанная группа состоит из семи мышей, которые распределены таким образом, что средние уровни глюкозы в каждой группе в начале исследования являются эквивалентными. Мышей db/db дозируют с помощью микроосмотических насосов, вставленных с использованием изофлурановой анестезии для подкожной (s.c.) доставки мышам соединений настоящего изобретения, солевого раствора или нерелеверантного соединения. Кровь отбирают из хвостовой вены через некоторые интервалы после этого и анализируют на концентрацию глюкозы в крови. Значимые различия между группами (сравнивая животных, обработанных соединениями настоящего изобретения с обработанными солевым раствором) оценивают с использованием проверки по критерию Стьюдента. Пример 2. Модель атеросклероза мышей. Мыши с дефицитом адипонектина, созданные посредством нокаута гена адипонектина, как было показано, предрасположены к атеросклерозу и резистентности к инсулину. Мыши также представляют собой пригодную для использования модель ишемической болезни сердца [Matsuda, M et al. J Biol. Chem.(2002) July и цитируемые там ссылки, описания которых включаются в данное описание посредством ссылок во всей их полноте]. Мышей, нокаутированных по адипонектину, содержат (7-9 мышей/клетка) в стандартных лабораторных условиях, при 22 С и 50% относительной влажности. Мышей дозируют посредством микроосмотического насоса, вставленного с использованием изофлурановой анестезии для подкожной (s.c) доставки мышам соединений настоящего изобретения, солевого раствора или нерелевантного соединения. Неоинтимальное утолщение и ишемическую болезнь сердца определяют для различных групп мышей,умерщвляемых через различные интервалы времени. Значимые различия между группами (сравнивая- 26011484 мышей, обработанных соединениями настоящего изобретения, и обработанных солевым раствором) оценивают с использованием проверки по критерию Стьюдента. Пример 3. Биологическая активность in vitro. Модифицированный набор Flash Plate Adenylyl Cyclase (New England Nucleart; Cat. No. SMP004A) используют для непосредственной идентификации соединений-кандидатов в агонисты по отношению кhRUP25 в соответствии со следующим протоколом. Термин hRUP25 включает последовательности, находящиеся в GenBank Accession He. HM177551 для нуклеотида человека, и GenBank Accession No. NP 808219 для полипептида человека, и встречающиеся в природе аллельные варианты, ортологи млекопитающих и их рекомбинантные мутанты. Клетки СНО, стабильно трансфицированные вектором экспрессии, кодирующим hROP25 и культивируемые в условиях, дающих возможность для экспрессии на поверхности клеток кодируемого рецептора hRUP25, собирают из флаконов с помощью неферментативных средств. Клетки промывают в PBS и ресуспендируют в буфере для анализа от производителя. Живые клетки считают с использованием гематоцитометра и эксклюзии на Trypan blue, и концентрацию клеток устанавливают при 2106 клеток/мл. Стандарты цАМФ и буфер для детектирования (содержащий 2 мкКюри трассера [125I]-цАМФ (100 мкл) на 11 мл буфера для детектирования) приготавливают и поддерживают в соответствии с инструкциями производителя. Соединения-кандидаты, идентифицированные, как указано выше (если замороженные,оттаивают при комнатной температуре), добавляют в соответствующие лунки (предпочтительно, лунки 96-луночного планшета), при увеличении концентраций (3 мкл/лунка; 12 мкМ - конечная концентрация при анализе). К этим лункам добавляют 100000 клеток в 50 мкл буфера для анализа и затем смесь инкубируют в течение 30 мин при комнатной температуре при осторожном встряхивании. После инкубирования в каждую лунку добавляют 100 мкл буфера для детектирования, с последующим инкубированием в течение 2-24 ч. Планшеты считают на планшет-ридере Wallac MicroBeta, используя "Prot. 31" (согласно инструкциям производителя). Определенные соединения настоящего изобретения в способе цАМФ Whole Cell имеют ЕС 50, равную примерно 25 мкМ или менее. Пример 4. Биологическая активность in vitro. Анализ связывания 35S-GTPS. Мембраны, полученные из клеток (СНО)-K1 яичников китайского хомячка, стабильно экспрессирующие рецептор ниацина, или контрольный вектор (7 мкг/анализ) разводят в буфере для анализа(100 мМ HEPES, 100 мМ NaCl и 10 мМ MgCl2, pH 7,4) в планшетах Wallac Scintistrip и предварительно инкубируют вместе с исследуемыми соединениями, разведенными в буфере для анализа, содержащем 40 мкМ GDP (конечная [GDP] равна 10 мкМ), в течение 10 мин перед добавлением 35S-GTPS до 0,3 нМ. Для устранения возможного осаждения соединений все соединения сначала приготавливают в 100% ДМСО и затем разводят буфером для анализа, получая при анализе конечную концентрацию 3% ДМСО. Дают возможность происходить связыванию в течение 1 ч, затем планшеты центрифугируют при 4000 об/мин в течение 15 мин при комнатной температуре и с последующим подсчетом в сцинцилляционном счетчике TopCount. Нелинейный регрессионный анализ кривых связывания осуществляют в Методика. Аспирация среды для культивирования клеток из 15 см 2 планшетов, промывка 5 мл холодного PBS и аспирация. Добавление 5 мл буфера для отделения мембран и отделение мембран от клеток. Перенос клеток и- 27011484 отделенных мембран в 50 мл пробирку для центрифугирования. Добавление 50 мкл коктейля ингибиторов протеаз. Вращение при 20000 об/мин в течение 17 мин при 4 С. Аспирация супернатанта и ресуспендирование осадка после центрифугирования в 30 мл буфера для отмывки мембран. Добавление 50 мкл коктейля ингибиторов протеаз. Вращение при 20000 об/мин в течение 17 мин при 4 С. Аспирация супернатанта из осадка после центрифугирования мембран. Осадок можно заморозить при -80 С для использования в дальнейшем, или он может использоваться непосредственно. Анализ. Материалы. Натриевая соль гуанозин-5'-дифосфата (GDP, Sigma-Aldrich Catalog 87127). Триэтиламмониевая соль гуанозин-5'-[35S] тиотрифосфата ([35S]GTPS, Amersham Biosciences Catalog SJ 1320, 1000 Кюри/ммоль). 96-луночные планшеты Scintiplates (Perkin-Elmer 1450-501). Буфер для связывания: 20 мМ HEPES, pH 7,4, 100 мМ NaCl, 10 мМ MgCl2. Буфер с GDP: буфер для связывания плюс GDP, в пределах от 0,4 до 40 мкМ, берут свежим перед анализом. Методика.(Общий объем анализа=100 мкл/лунка). 25 мкл буфера GDP с соединениями или без них (конечный объем GDP 10 мкМ - так что используется 40 мкМ исходный раствор). 50 мкл мембран в буфере для связывания (0,4 мг белка/мл). 25 мкл [35S]GTPS в буфере для связывания. Получают добавлением 5 мкл исходного раствора[35S]GTPS к 10 мл буфера для связывания (этот буфер не содержит GDP). Оттаивание планшетов с соединениями, которые должны исследоваться (дочерние планшеты с 5 мкл соединения и 2 мМ в 100% ДМСО). Разбавление 2 мМ соединений 1:50 с помощью 245 мкл буфера GDP до 40 мкМ в 2% ДМСО. Оттаивание замороженного осадка мембран на льду. Гомогенизация мембран сразу после этого в суспензии с использованием POLYTRON PT3100 (датчик PTPET-DA 3007/2 при настройке 7000 об/мин). Определение концентрации белка в мембранах посредством анализа Брэдфорда. Разбавление мембран до концентраций белка 0,40 мг/мл в буфере для связывания. (Примечание: конечная концентрация для анализа равна 20 мкг/лунка). Добавление 25 мкл соединений в буфере GDP на лунку в Scintiplate. Добавление 50 мкл мембран на лунку в Scintiplate. Предварительное инкубирование в течение 5-10 мин при комнатной температуре. Добавление 25 мкл разведенного [35S]GTPS. Инкубирование на шейкере (Lab-Line model 1314,встряхивание при настройке 4) в течение 60 мин при комнатной температуре. Прекращение анализа посредством центрифугирования планшетов герметизированных с помощью крышек для планшетов при 2500 об/мин в течение 20 мин, при 22 С. Подсчет на сцинцилляционном счетчике TopCount NXT протокол 35S. Определенные соединения настоящего изобретения имеют ЕС 50 при функциональном анализе связывания GTPS in vitro в диапазоне примерно 10-100 мкМ. Более предпочтительные соединения настоящего изобретения имеют значение ЕС 50 при этом анализе в диапазоне примерно 1-10 мкМ. Еще более предпочтительные соединения имеют значение ЕС 50 в этом анализе, меньшее примерно чем 1 мкМ. Пример 5. Животная модель in vivo. Одно из применений соединения настоящего изобретения в качестве лекарственного средства для профилактики и лечения высокого общего отношения холестерин/HDL-холестерин и состояний, связанных с этим, демонстрируется посредством активности соединения при снижении отношения общего уровня холестерина к HDL-холестерину, при повышении уровня HDL-холестерина или при защите от атеросклероза на модели свиней in vivo. Свиней используют в качестве животной модели, поскольку они отражают физиологию человека, в особенности метаболизм липидов, более чем большинство других животных моделей. Здесь представлена иллюстративная модель свиней in vivo, не предполагающаяся в качестве ограничения. Йоркширских белых свиней (масса тела 25,54 кг) откармливают кормом, обогащенным насыщенными жирными кислотами и насыщенным холестерином (SFA-CHO) в течение 50 дней (1 кг корма на 35 кг-1 массы свиньи), состоящим из стандартного корма, дополненного 2% холестерина и 20% говяжьего сала [Royo T. et al., European Journal of Clinical Ihvestigation (2000) 30:843-52; описание которой тем самым включается в данное описание посредством ссылки во всей ее полноте]. Отношение насыщенных жирных кислот к ненасыщенным изменяется от 0,6 в нормальном корме для свиней до 1,12 в корме SFA- 28011484CHO. Животных разделяют на две группы, одну группу (n=8) откармливают кормом SFA-CHO и обрабатывают плацебо, другую группу (n=8) откармливают кормом SFA-CHO и обрабатывают соединением(3,0 мгкг-1). Контрольных животных откармливают стандартным кормом в течение 50 дней. Образцы крови собирают на базовом уровне (через 2 дня после приема животных) и через 50 дней после начала кормления. Анализируют липиды в крови. Животных умерщвляют и делают некропсию. Альтернативно, приведенный выше анализ включает несколько групп, каждую из которых обрабатывают различными дозами соединения. Предпочтительные указанные дозы выбирают из группы, состоящей из 0,1 мгкг-1, 0,3 мгкг-1, 1,0 мгкг-1, 3,0 мгкг-1, 10 мгкг-1, 30 мгкг-1 и 100 мгкг-1. Альтернативно,приведенный выше анализ осуществляют в нескольких временных точках. Предпочтительные временные точки выбирают из группы, состоящей из 10 недель, 20 недель, 30 недель, 40 недель и 50 недель.HPL-Холестерин. Кровь собирают в тринатрийцитрате (3,8%, 1:10). Плазму получают после центрифугирования(1200 g, 15 мин) и сразу обрабатывают. Общий уровень холестерина, HDL-холестерина и LDLхолестерина измеряют с использованием автоматического анализатора Kodak Ektachem DT System(Eastman Kodak Company, Rochester, NY, USA). Образцы со значениями параметров выше диапазона разводят раствором, поставляемым производителем, и затем анализируют повторно. Определяют отношение общий холестерин/HDL-холестерин. Сравнивают уровни HDL-холестерина между группами. Сравнивают отношение общий холестерин/HDL-холестерин между группами. Повышение уровня HDL-холестерина или снижение отношения общий холестерин/HDLхолестерин при введении соединения берут в качестве показателя соединения, имеющего указанное выше применение. Атеросклероз. Торакальную и абдоминальную аорты удаляют интактными, открывают продольно вдоль вентральной поверхности и фиксируют в нейтральном формалине с буфером после иссечения образцов со стандартных участков в торакальной и абдоминальной аорте для гистологического исследования и изучения композиции и синтеза липидов. После фиксации аорты целиком окрашивают с помощью Sudan IV, накалывают в плоском состоянии и получают цифровые изображения с помощью ТВ камеры, соединенной с компьютеризированной системой анализа изображений (Image Pro Plus; Media Cybernetics, Silver Spring,MD) для определения процента поверхности аорты, вовлеченной в атеросклеротические поврежденияBiology (1985) 5:415-26; описания которых тем самым включены в данное описание посредством ссылок во всей их полноте]. Сравнивают между группами процент поверхности аорты, вовлеченной в атеросклеротические повреждения. Уменьшение процента поверхности аорты, вовлеченной в атеросклеротические повреждения, при введении соединения, берется как показатель соединения, имеющего указанное выше применение. Пример 6. Анализ связывания рецептора. В дополнение к способам, описанным в данном описании, другие средства для оценки исследуемого соединения представляет собой определение аффинности связывания с рецептором RUP25. Это тип анализа, как правило, требует радиоактивно-меченого лиганда рецептора RUP25. В отсутствии использования известных лигандов рецептора RUP25 и его радиоактивных меток, соединения формулы (I) могут метиться радиоактивным изотопом и использоваться при анализе для оценки аффинности исследуемого соединения к рецептору RUP25. Радиоактивно-меченое RUP25 соединение формулы (I) может использоваться при скрининговом анализе для идентификации/оценки соединений. В общих терминах, вновь синтезируемое или идентифицируемое соединение (т.е. исследуемое соединение) может оцениваться на его способность уменьшать связывание "радиоактивно-меченого соединения формулы (I)" с рецептором RUP25. Соответственно,способность конкурировать с "радиоактивно-меченым соединением формулы (I)" или - лигандом сRUP25 за связывание с рецептором RUP25 непосредственно коррелирует с его аффинностью связывания исследуемого соединения с рецептором RUP25. Протокол анализа для определения связывания рецептора RUP25. А. Приготовление рецептора RUP25. Клетки 293 (почки человека, АТСС), временно трансфицированные 10 мкг рецептора RUP25 человека и 60 мкл липофектамина (на 15-см чашку), выращивают в чашке в течение 24 ч (конфлюентность 75%) со сменой сред и удаляют с помощью 10 мл/чашка буфера Hepes-EDTA (20 мМ Hepes+10 мМEDTA, pH 7,4). Клетки центрифугируют в центрифуге Beckman Coulter в течение 20 мин, при 17000 об/мин (ротор JA-25.50). Затем осадок после центрифугирования ресуспендируют в 20 мМHepes+1 мМ EDTA, pH 7,4, гомогенизируют с помощью 50-мл гомогенизатора Dounce и снова центрифугируют. После удаления супернатанта осадки после центрифугирования хранят при -80 С до использования при анализе связывания. Когда они используются при анализе, мембраны оттаивают на льду в течение 20 мин и затем добавляют 10 мл буфера для инкубирования (20 мМ Hepes, 1 мМ MgCl2, 100 мМNaCl, pH 7,4). Мембраны встряхивают для ресуспендирования исходного осадка после центрифугирования мембран и гомогенизируют с помощью гомогенизатора Brinkmann PTPET-3100 Polytron в течение 15 с при настройке 6. Концентрацию мембранных белков определяют с использованием анализа белкаB. Анализ связывания. Для общего связывания, общий объем 50 мкл соответствующим образом разведенных мембран(разводят в буфере для анализа, содержащем 50 мМ Трис HCl (pH 7,4), 10 мМ MgCl2 и 1 MM EDTA; 5-50 мкг белка) добавляют в 96-луночные полипропиленовые планшеты для микротитрования, с последующим добавлением 100 мкл буфера для анализа и 50 мкл радиоактивно-меченого лиганда RUP25. Для неспецифического связывания добавляют 50 мкл буфера для анализа вместо 100 мкл и перед добавлением 50 мкл радиоактивно-меченого лиганда RUP25 добавляют дополнительные 50 мкл 10 мкМ холодногоRUP25. Затем планшеты инкубируют при комнатной температуре в течение 60-120 мин. Реакцию связывания завершают фильтрованием планшетов для анализа через фильтрационную пластину MicroplateDevices GF/C Unifilter с 96-луночным планшетным харвестером Brandell, с последующей промывкой холодным 50 мМ Трис HCl, pH 7,4, содержащим 0,9% NaCl. Затем нижнюю сторону фильтрационной пластины герметизируют, добавляют 50 мкл Optiphase SupermiX в каждую лунку, герметизируют верхнюю сторону пластин и считают пластины в сцинцилляционном счетчике Trilux MicroBeta. Для конкурентных исследований соединений, вместо добавления 100 мкл буфера для анализа, в соответствующие лунки добавляют 100 мкл соответственным образом разведенного исследуемого соединения, с последующим добавлением 50 мкл радиоактивно-меченого лиганда RUP25.C. Вычисление. Сначала исследуемые соединения анализируют при концентрации 1 и 0,1 мкМ и затем диапазон концентраций выбирают таким образом, чтобы средняя доза вызывала примерно 50% ингибирование связывания радиоактивного лиганда с RUP25 (т.е. IC50). Специфическое связывание в отсутствие исследуемого соединения (Bo) представляет собой разность общее связывание (BT) минус неспецифическое связывание (NSB), и, подобным образом, специфическое связывание (в присутствии исследуемого соединения) (B) представляет собой разность замещающее связывание (BD) минус неспецифическое связывание (NSB). IC50 определяют по кривой реакции ингибирования, двойного логарифмического графика %B/Bo как функция концентрации исследуемого соединения.Ki вычисляют посредством преобразования Cheng and Prustoff: где [L] представляет собой концентрацию используемого радиоактивно-меченого лиганда RUP25, используемого при анализе,KD представляет собой константу диссоциации радиоактивно-меченого лиганда RUP25, определяемую независимо при таких же условиях связывания.D. Альтернативная методика анализа связывания. Анализ конкурентного связывания 3 Н-никотиновой кислоты. Клетки CHO-KI, стабильно экспрессирующие рецептор ниацина, используют для получения мембран для анализа связывания. Клетки выращивают до 80% конфлюентности в среде роста (F-12 модифицированная среда Kaighn (ATCC, 30-2004), содержащая 10% FBS (GIBCO, 10438-026), 1 мг/мл G418(GIBCO, 10131-027) и 1X Pen-Strep (Sigma P-0871, собирают посредством соскребания и центрифугируют при 12000g, 4 С, 10 мин. Осадки клеток ресуспендируют в буфере для сбора (20 мМ HEPES,10 мМ EDTA, pH 7,4) и гомогенизируют с помощью 410 секундных сеансов работы 12 мм гомогенизатора Polytron, настройка 5. Лизат центрифугируют при 2000g, 4 С, 10 мин, для удаления нелизированных клеток и ядер, и полученный супернатант центрифугируют при 39000g, 4 С, 45 мин для осаждения мембран. Полученный осадок ресуспендируют в промывочном буфере (20 мМ HEPES, 0,1 мМ EDTA,pH 7,4), гомогенизируют с помощью 310 секундных сеансов работы 12 мм Polytron, настройка 4, и повторно центрифугируют при 39000g, 4 С, 45 мин. Полученный осадок ресуспендируют в промывочном буфере и хранят в жидком азоте до использования. Концентрацию мембранных белков в этом препарате определяют с использованием анализа белков Pierce ВСА, с BSA в качестве стандарта. Равновесное связывание 3 Н-никотиновой кислоты осуществляют в 96-луночных полипропиленовых планшетах. Реакционные смеси содержат 140 мкл мембран, разведенных в буфере для анализа (20 мМHEPES, pH 7,4, 1 мМ MgCl2, и 0,01% CHAPS; 15-30 мкг мембранных белков/анализ), 20 мкл исследуемых соединений разводят в буфере для анализа (исходные растворы с соединением находятся в 100% ДМСО; конечная концентрация ДМСО при анализе равна 0,25%), и 40 мкл 250 нМ тритированного ниацина ([5,6-3 Н]-никотиновой кислоты: American Radiolabeled Chemicals, Ihc., 20 мкМ в этаноле; конечная концентрация этанола при каждом анализе равна 1,5%). Неспецифическое связывание определяют в присутствии 250 мкМ немеченой никотиновой кислоты. После перемешивания в течение 3-4 ч при комнатной температуре реакционные смеси фильтруют через пластины Packard Unifilter GF/C, с использованием Packard Harvester, и промывают 8200 мкл буфера для связывания, находящегося на льду. Пластины сушат в течение ночи и их обратные стороны герметизируют с использованием ленты PerkinElmer, раз- 30
МПК / Метки
МПК: C07D 495/04, A61K 31/41, C07D 491/04, C07D 403/04
Метки: метаболизмом, связанных, способы, расстройств, производные, тетразольные, лечения
Код ссылки
<a href="https://eas.patents.su/30-11484-tetrazolnye-proizvodnye-i-sposoby-lecheniya-rasstrojjstv-svyazannyh-s-metabolizmom.html" rel="bookmark" title="База патентов Евразийского Союза">Тетразольные производные и способы лечения расстройств, связанных с метаболизмом</a>
Предыдущий патент: Способ приготовления ферментированных или частично ферментированных мясопродуктов и продукты, полученные данными способами
Следующий патент: Средство для устранения нарушений нейрогенной и эндокринной регуляции системы капиллярного кровотока кожи
Случайный патент: Способ каталитической полимеризации олефинов и реакторная система












