Производные имидазохинолина в качестве лигандов аденозиновых а3 рецепторов
Номер патента: 7595
Опубликовано: 29.12.2006
Авторы: Вальц Эржебет, Гербер Каталин, Урбан-Сабо Каталин, Капуи Зольтан, Т.Надь Лайош, Балаж Ласло, Варгане Середи Юдит, Батори Шандор, Микуш Эндре, Боэр Кинга, Балог Мария, Араньи Петер, Тимари Геза
Формула / Реферат
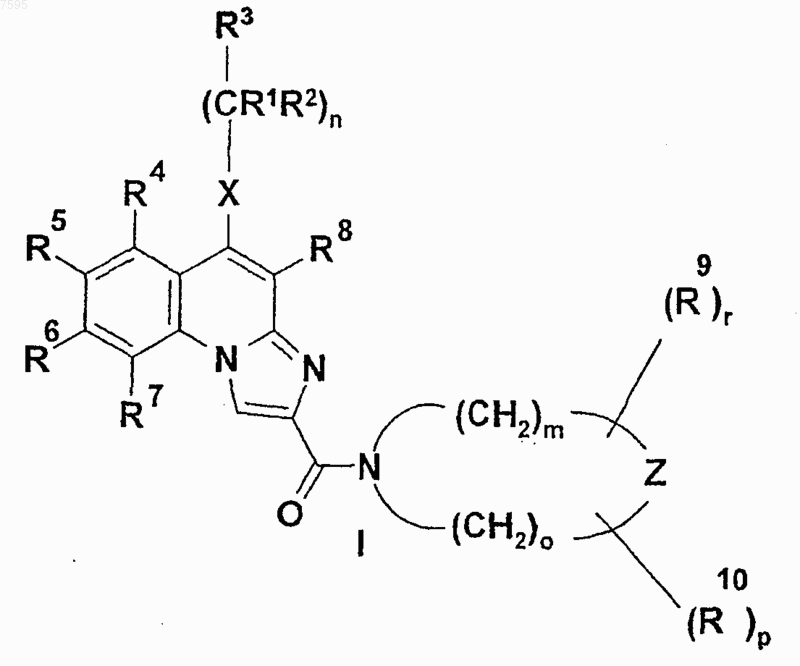
1. Соединения общей формулы (I)
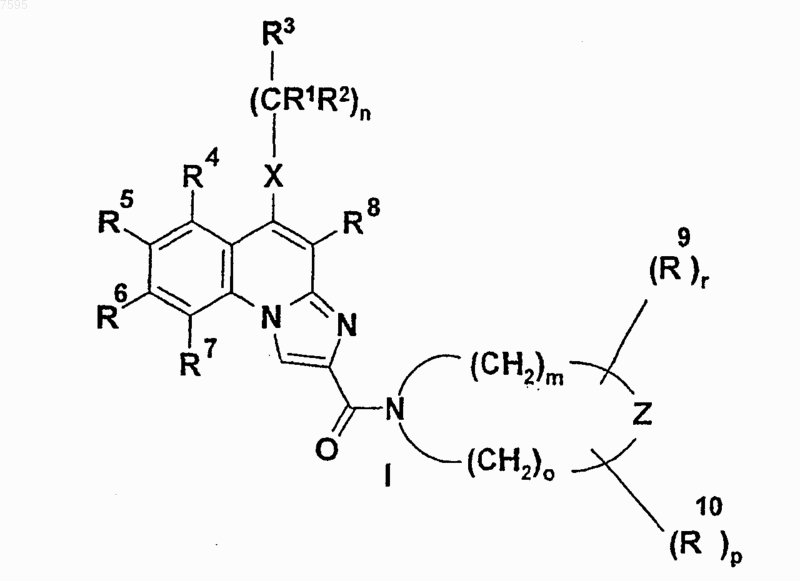
где R1 обозначает атом водорода или неразветвленную или разветвленную C1-4 алкильную группу;
R2 - атом водорода или неразветвленную или разветвленную C1-4 алкильную группу;
R3 - атом водорода или неразветвленную или разветвленную C1-4 алкильную группу, С3-6 циклоалкильную группу, фенильную, тиенильную или фурильную группу, необязательно замещенную одной или несколькими неразветвленными или разветвленными C1-4 алкильными группами, неразветвленными или разветвленными C1-4 алкоксигруппами или атомом галогена; или обозначает шести- или пятичленный гетероароматический цикл, содержащий один, два или три атома азота, или пятичленный гетероароматический цикл, содержащий один атом азота и один атом кислорода, или один атом азота и один атом серы, необязательно замещенный одной или несколькими неразветвленными или разветвленными C1-4 алкильными группами, неразветвленными или разветвленными C1-4 алкоксигруппами, или атомом галогена;
R4, R5, R6 и R7 независимо обозначают атом водорода, неразветвленную или разветвленную C1-4 алкильную группу, неразветвленную или разветвленную C1-4 алкоксигруппу, гидроксильную группу или атом галогена, или R4 и R7 обозначают атом водорода и R5 и R6 вместе образуют метилендиоксигруппу;
R8 обозначает атом водорода или цианогруппу, аминокарбонильную группу, C1-4 алкоксикарбонильную группу, карбоксильную группу;
R9 и R10 независимо друг от друга обозначают атом водорода, неразветвленную или разветвленную C1-4 алкильную группу, С3-6 циклоалкильную группу;
X обозначает -СН2-группу, -NH-группу, -NR11-группу или атом серы, атом кислорода, сульфогруппу или сульфоксигруппу, где R11 обозначает неразветвленную или разветвленную C1-4 алкильную группу или С3-6 циклоалкильную группу;
Z обозначает атом кислорода, атом серы, -NH-группу или -NR12-группу, где R12 обозначает неразветвленную или разветвленную C1-4 алкильную группу или С3-6 циклоалкильную группу;
n равно нулю, 1 или 2;
m равно нулю, 1, 2 или 3;
о равно нулю, 1, 2 или 3;
р равно нулю или 1;
r равно нулю или 1, при условии, что по меньшей мере один из m и о отличен от нуля,
и их соли, сольваты и изомеры, а также соли и сольваты изомеров.
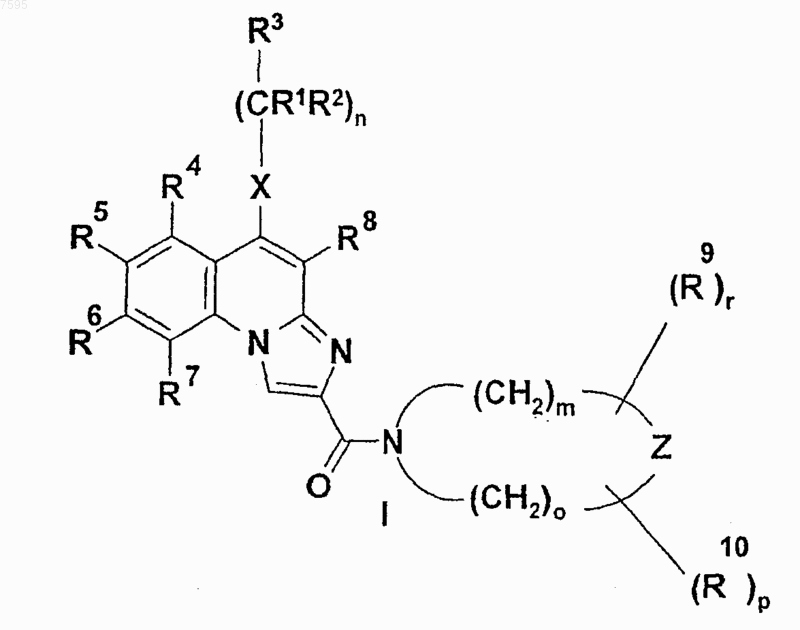
2. Соединения общей формулы (I) по п.1

где R1 обозначает атом водорода или неразветвленную или разветвленную C1-4 алкильную группу;
R2 - атом водорода или неразветвленную или разветвленную C1-4 алкильную группу;
R3 - атом водорода или неразветвленную или разветвленную C1-4 алкильную группу, С3-6 циклоалкильную группу, фенильную, тиенильную или фурильную группу, необязательно замещенную одной или несколькими неразветвленными или разветвленными С1-4 алкильными группами, неразветвленными или разветвленными C1-4 алкоксигруппами или атомом галогена;
R4, R5, R6 и R7 независимо друг от друга обозначают атом водорода, неразветвленную или разветвленную C1-4 алкильную группу, неразветвленную или разветвленную C1-4 алкоксигруппу, гидроксильную группу или атом галогена, или R4 и R7 обозначают атом водорода и R5 и R6 вместе образуют метилендиоксигруппу;
R8 обозначает атом водорода или цианогруппу, аминокарбонильную группу, C1-4 алкоксикарбонильную группу, карбоксильную группу;
R9 и R10 независимо друг от друга обозначают атом водорода, неразветвленную или разветвленную C1-4 алкильную группу, С3-6 циклоалкильную группу;
X обозначает -СН2-группу, -NH-группу, -NR11-группу или атом серы, атом кислорода, сульфогруппу или сульфоксигруппу, где R11 обозначает неразветвленную или разветвленную C1-4 алкильную группу или С3-6 циклоалкильную группу;
Z обозначает атом кислорода, атом серы, -NH-группу или -NR12-группу, где R12 обозначает неразветвленную или разветвленную C1-4 алкильную группу или С3-6 циклоалкильную группу;
n равно нулю, 1 или 2;
m равно нулю, 1, 2 или 3;
о равно нулю, 1, 2 или 3;
р равно нулю или 1;
r равно нулю или 1, при условии, что по меньшей мере один из m и о отличен от нуля,
и их соли, сольваты и изомеры, а также соли и сольваты изомеров.
3. Соединения общей формулы (I) по пп.1 и 2
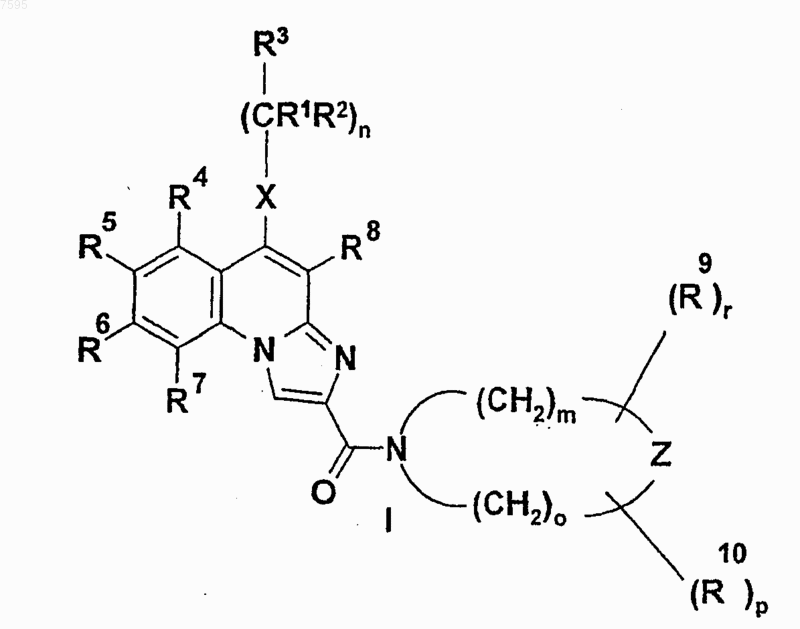
где R1 обозначает атом водорода или метильную группу;
R2 - атом водорода или метильную группу;
R3 - фенильную, тиенильную или фурильную группу;
R4, R5, R6 и R7 независимо друг от друга обозначают атом водорода, неразветвленную или разветвленную C1-4 алкильную группу, неразветвленную или разветвленную C1-4 алкоксигруппу, гидроксильную группу или атом галогена; или
R4 и R7 обозначают атом водорода и R5 и R6 вместе образуют метилендиоксигруппу;
R8 - атом водорода или цианогруппу;
R9 и R10 обозначают атом водорода, метильную, этильную или циклопропильную группу;
X обозначает -NH-группу или атом кислорода;
Z обозначает атом кислорода, атом серы, -NH-группу или -NR12-группу, где R12 обозначает неразветвленную или разветвленную C1-4 алкильную группу или С3-6 циклоалкильную группу; и
n равно 1;
m равно 2;
о равно 2;
р равно нулю;
r равно нулю,
и их соли, сольваты и изомеры, а также соли и сольваты изомеров.
4. Соединения по пп.1-3, указанные ниже
1-(9-бензиламино-10-цианоимидазо[1,2-а]хинолин-2-карбонил)-4-метилпиперазин,
1-(9-бензиламино-10-цианоимидазо[1,2-а]хинолин-2-карбонил)морфолин,
1-(9-фурфуриламино-10-цианоимидазо[1,2-а]хинолин-2-карбонил)-4-метилпиперазин,
1-(9-фурфуриламино-10-цианоимидазо[1,2-а]хинолин-2-карбонил)пиперазин,
1-(9-фурфуриламино-10-цианоимидазо[1,2-а]хинолин-2-карбонил)морфолин,
1-(9-тиениламино-10-цианоимидазо[1,2-а]хинолин-2-карбонил)морфолин,
1-(9-тиениламино-10-цианоимидазо[1,2-а]хинолин-2-карбонил)пиперазин,
и их соли, сольваты и изомеры, а также соли и сольваты изомеров.
5. Способ получения соединений общей формулы (I)
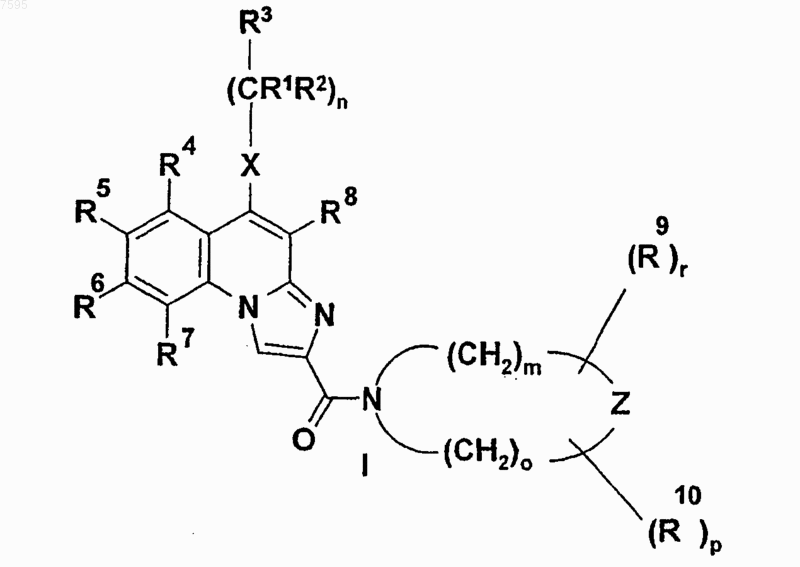
и их солей, сольватов и изомеров,
где R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, X, Z, n, m, о, р и r такие, как указано в п.1, отличающийся тем, что соединение общей формулы (VIII)
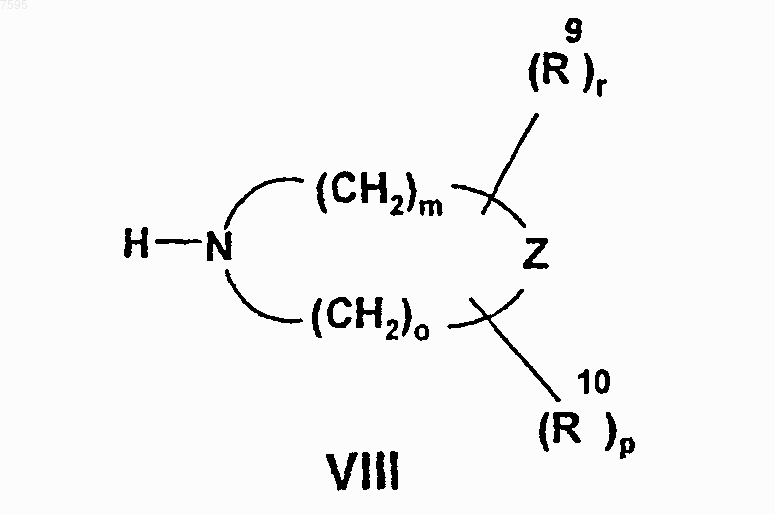
где R9, R10, Z, m, о, р и r такие, как указано в п.1, ацилируют кислотой или реакционноспособным производным кислоты общей формулы (II)
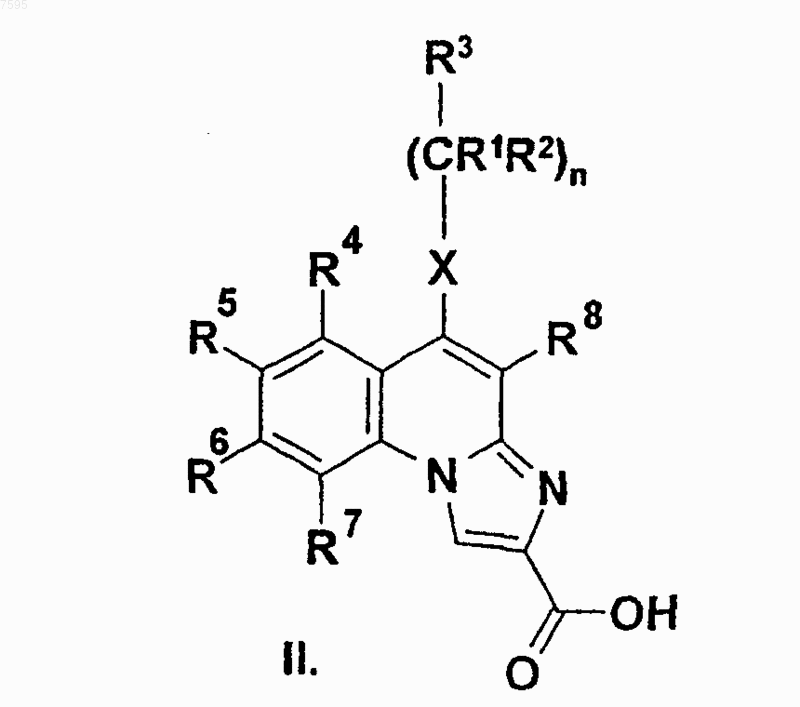
где R1, R2, R3, R4, R5, R6, R7, R8, X и n такие, как указано в п.1, и, если требуется, заместители полученного соединения общей формулы (I) известными способами преобразуют друг в друга, и/или соединение общей формулы (I) переводят в хую соль или сольват, или выделяют из его соли или сольвата, и/или разделяют его на оптически активные изомеры, или оптически активный изомер преобразуют в рацемическое соединение.
6. Способ по п.5, отличающийся тем, что ацилирование проводят в присутствии основания в органическом растворителе.
7. Способ по пп.5 и 6, отличающийся тем, что реакционноспособное производное кислоты общей формулы (I) представляет собой соответствующий галогенангидрид кислоты или смешанный ангидрид.
8. Способ по пп.5-7, отличающийся тем, что органический растворитель представляет собой галогенированный углеводород, предпочтительно хлороформ.
9. Способ по пп.5-8, отличающийся тем, что основание представляет собой органическое основание, предпочтительно триэтиламин.
10. Фармацевтическая композиция, отличающаяся тем, что содержит одно или несколько соединений общей формулы (I)
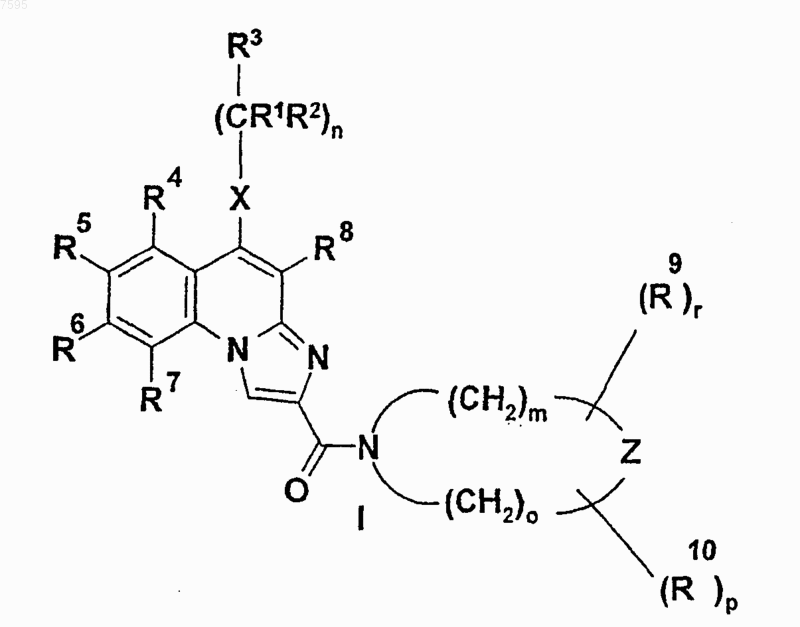
где R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, X, Z, n, m, о, р и r такие, как указано в п.1; и/или их соли, сольваты, изомеры, соли и сольваты изомеров и одно или несколько вспомогательных веществ, обычно используемых в фармацевтической промышленности.
11. Фармацевтическая композиция по п.10, отличающаяся тем, что в качестве активного вещества она содержит одно или несколько соединений, указанных в п.3.
12. Применение соединений общей формулы (I)
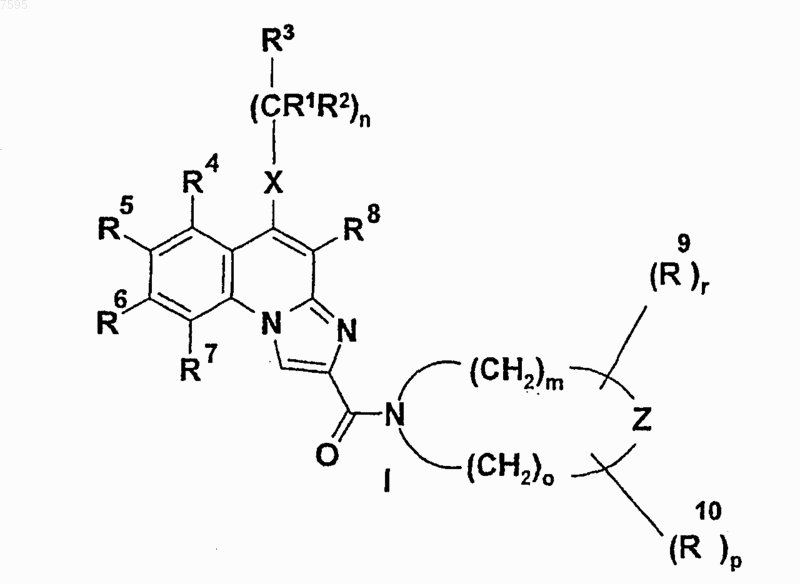
где R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, X, Z, n, m, о, р и r такие, как указано в п.1; для лечения патологий, где A3 рецептор участвует в развитии заболевания.
13. Применение соединений общей формулы (I)
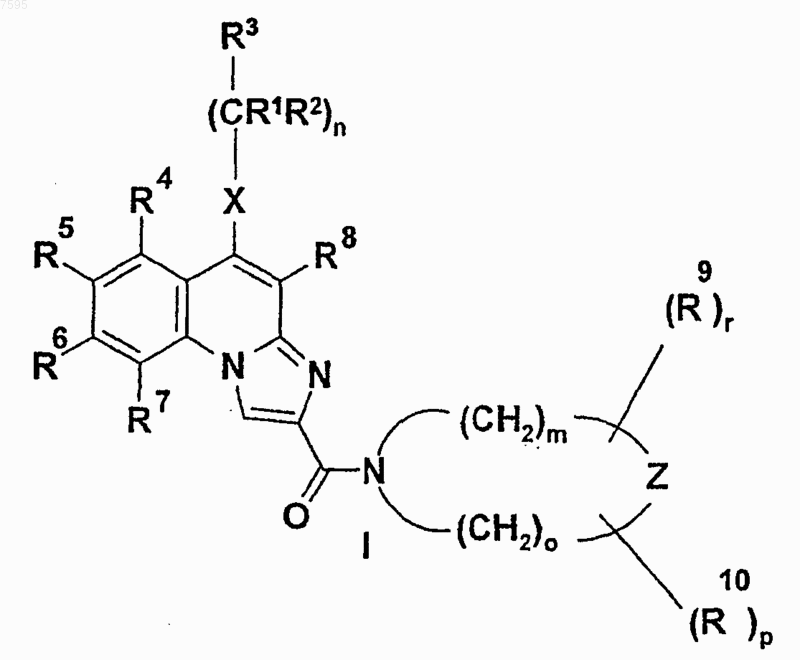
где R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, X, Z, n, m, о, р и r имеют такие значения, как указано в п.1; в качестве лигандов А3 рецепторов в случае нарушений деятельности сердца, почек, дыхательной системы и центральной нервной системы, для ингибирования защитного действия аденозина на растущие опухолевые клетки, предотвращения дегрануляции тучных клеток, для ингибирования образования цитокинов, понижения внутриглазного давления, для ингибирования выделения TNFa, для затруднения миграции эозинофильных и нейтрофильных гранулоцитов и других клеток зоны воспаления, для ингибирования сужения трахеи и для затруднения инфильтрации плазмы крови через кровеносный сосуд.
14. Применение соединений общей формулы (I)
где R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, X, Z, n, m, о, р и r имеют такие значения, как указано в п.1; в качестве антагонистов А3 рецепторов, в качестве активных ингредиентов противовоспалительных, противоастматических, противоишемических, антидепрессивных, антиаритмических, защищающих функции почек, предупреждающих возникновение опухолей, активных против болезни Паркинсона или усиливающих когнитивные способности фармацевтических композиций, и в качестве активных компонентов композиций, которые можно применять для лечения или профилактики следующих заболеваний: реперфузионного повреждения сердечной мышцы, хронических обструктивных заболеваний легких (COPD), респираторного дисстресс-синдрома у взрослых (ARDS), включая хронический бронхит, эмфизему легких или одышку, аллергических реакций (например, ринита, реакций, вызванных растением сумах, уртикарной сыпи, склеродермы, артрита), других аутоиммунных болезней, воспалительных заболеваний кишечника, болезни Аддисона, болезни Крона, псориаза, заболевания суставов, гипертонии, аномальных неврологических функций, глаукомы и диабета.
15. Применение соединений общей формулы (I)
где R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, X, Z, n, m, о, р и r имеют такие значения, как указано в п.1; в качестве активных компонентов для лечения патологий, таких как астма, COPD и ARDS, глаукома, опухоли, аллергические и воспалительные заболевания, ишемия, гипоксия, сердечная аритмия и заболевания почек.
Текст
007595 Данное изобретение относится к лигандам аденозиновых A3 рецепторов общей формулы (I) которые предпочтительно являются антагонистами, а также к их солям, сольватам и изомерам, к содержащим их фармацевтическим композициям и к применению соединений общей формулы (I), а также их солей, сольватов и изомеров, к получению соединений общей формулы (I) и их солей, сольватов и изомеров. Аденозин представляет собой хорошо известный компонент нескольких эндогенных молекул(АТФ, НАД+, нуклеиновых кислот). Кроме того, он играет важную регуляторную роль во многих физиологических процессах. Воздействие аденозина на функцию сердца было открыто в 1929 г. (Drury andSzentgyrgyi, J. Physiol. 68:213, 1929). Определение возрастающего числа физиологических функций,опосредованных аденозином, и открытие новых подтипов аденозиновых рецепторов открывают возможности для терапевтического применения конкретных лигандов (Poulse, S.A. and Quinn, R.J. Bioorganic andMedicinal Chemistry 6:619, 1998). В настоящее время аденозиновые рецепторы делят на три основных класса: A1, A2 и A3. Подтип A1 является частично ответственным за ингибирование аденилатциклазы путем связывания с Gi белком мембраны, частично влияет на другие системы вторичных мессенджеров. Подтип А 2 рецепторов можно подразделить на два дополнительных подтипа - А 2 а и А 2b, которые являются рецепторами, стимулирующими активность аденилатциклазы. Последовательность аденозиновых A3 рецепторов недавно была установлена на основании изучения библиотеки сДНК яичек крыс. Позже было доказано, что она соответствует новому функциональному аденозиновому рецептору. Активация А 3 рецепторов связана также с несколькими системами вторичных мессенджеров: например, ингибирование аденилатциклазы и стимуляция фосфолипазы С и D. Аденозиновые рецепторы обнаружены в нескольких органах и регулируют функции этих органов. Как A1, так и А 2 а рецепторы играют важную роль в центральной нервной и сердечно-сосудистой системах. В ЦНС аденозин ингибирует высвобождение синаптических медиаторов, действие которых опосредовано A1 рецепторами. A1 рецепторы также опосредуют отрицательные инотропный, хронотропный и дромотропный эффекты аденозина в сердце. Аденозиновые А 2 а рецепторы, расположенные в стриатуме в относительно большом количестве, демонстрируют функциональное взаимодействие с допаминовыми рецепторами в регулировании синаптической трансмиссии. Аденозиновые А 2 а рецепторы на эндотелиальных и гладкомышечных клетках ответственны за вазодилатацию, вызванную аденозином. На основе идентификации mРНК полагают, что аденозиновые А 2b рецепторы широко распределены в различных тканях. Они идентифицированы почти в каждом типе клеток, но самой высокой является их экспрессия в кишечнике и мочевом пузыре. Указанный подтип, вероятно, также имеет важную регуляторную функцию в регуляции сосудистого тонуса и участвует в функционировании тучных клеток. В отличие от рецепторов A1 и А 2 а, распределение которых в тканях определяют на белковом уровне, наличие A2b и А 3 рецепторов определяют, исходя из уровня mРНА. Уровни экспрессии для аденозиновых A3 рецепторов довольно низки по сравнению с другими подтипами и сильно зависят от вида. Аденозиновые A3 рецепторы экспрессированы прежде всего в центральной нервной системе, яичке, иммунной системе и, по-видимому, вовлечены в модуляцию высвобождения медиаторов из тучных клеток в немедленной реакции гиперчувствительности. Антагонисты А 3, сведения о которых опубликованы в литературе, принадлежат к группам флавоноидов, производным 1,4-дигидропиридина, триазолохиназолинам, тиазолонафтиридинам и тиазолопиримидинам. Данное изобретение относится к новому типу эффективных антагонистов A3 рецепторов,которые имеют аминохинолиновую структуру. Для терапевтического применения важно обеспечить, чтобы связывание молекулы с аденозиновыми рецепторами A1, А 2 а и А 2b подтипов не происходило или происходило только в случае очень высокой концентрации. Данное изобретение относится к соединениям общей формулы (I), а также к их солям,сольватам и изомерам, которые обладают высокой селективностью в отношении аденозиновых рецепторов А 3 подтипа. Цель авторов данного изобретения состояла прежде всего в том, чтобы получить лиганды A3 рецеп-1 007595 торов, предпочтительно являющиеся антагонистами, прежде всего хинолиновой структуры, которые обладают сильным антагонистическим действием и высокой селективностью в отношении рецепторов А 3,т.е. они ингибируют рецепторы A3 в намного более низкой концентрации, чем они ингибируют рецепторы A1, A2a и А 2b. Другой целью авторов были новые соединения с такими стабильностью, биодоступностью, терапевтическим индексом и данными по токсичности, которые позволяют разработать на их основе лекарственные средства, и, благодаря их подходящему энтеральному всасыванию, данные соединения можно вводить перорально. Авторы данной заявки пришли к выводу, что соединения общей формулы (I) где R1 обозначает атом водорода или неразветвленную или разветвленную C1-4 алкильную группу;R2 обозначает атом водорода или неразветвленную или разветвленную C1-4 алкильную группу;R3 обозначает атом водорода или неразветвленную или разветвленную C1-4 алкильную группу, С 3-6 циклоалкильную группу, фенильную, тиенильную или фурильную группу, необязательно замещенную одной или несколькими неразветвленными или разветвленными C1-4 алкильными группами, неразветвленными или разветвленными C1-4 алкоксигруппами, или атомом галогена; или обозначает шести- или пятичленный гетероароматический цикл, содержащий один, два или три атома азота; или пятичленный гетероароматический цикл, содержащий один атом азота и один атом кислорода, или один атом азота и один атом серы, необязательно замещнный одной или несколькими неразветвленными или разветвленными C1-4 алкильными группами, неразветвленными или разветвленными C1-4 алкоксигруппами, или атомом галогена;R4, R5, R6 и R7 независимо обозначают атом водорода, неразветвленную или разветвленную C1-4 алкильную группу, неразветвленную или разветвленную C1-4 алкоксигруппу, гидроксильную группу или атом галогена, или R4 и R7 обозначают атом водорода и R5 и R6 вместе образуют метилендиоксигруппу;R8 обозначает атом водорода или цианогруппу, аминокарбонильную группу, C1-4 алкоксикарбонильную группу или карбоксильную группу;R9 и R10 независимо друг от друга обозначают атом водорода, неразветвленную или разветвленнуюX обозначает -СН 2-группу, -NH-группу, -NR11-группy или атом серы, атом кислорода, сульфогруппу или сульфоксигруппу, где R11 обозначает неразветвленную или разветвленную C1-4 алкильную группу или С 3-6 циклоалкильную группу;Z обозначает атом кислорода, атом серы, -NH-группу или -NR12-группу, где R12 обозначает неразветвленную или разветвленную C1-4 алкильную группу или С 3-6 циклоалкильную группу;p равно нулю или 1;r равно нулю или 1, при условии, что по меньшей мере один из m и o отличен от нуля,и их соли, сольваты и изомеры, а также соли и сольваты изомеров, которые отвечают вышеуказанным критериям. Значения перечисленных выше заместителей подробно представлены ниже. Под термином неразветвленная или разветвленная C1-4 алкильная группа авторы изобретения имеют в виду метильную, этильную, пропильную, изопропильную, бутильную, изобутильную, вторбутильную, трет-бутильную группу, предпочтительно, этильную или метильную группу. Используя термин неразветвленная или разветвленная C1-4 алкоксигруппа, авторы имеют в виду метокси-, этокси-, пропокси-, изопропокси-, бутокси-, изобутокси-, втор-бутокси-, трет-бутокси-, предпочтительно, этокси- или метоксигруппу. Под термином С 3-6 циклоалкильная группа авторы имеют в виду циклопропильную, циклобутильную, циклопентильную или циклогексильную группу.-2 007595 Гетероароматический цикл, содержащий один или два или три атома азота, обозначает пиррольный,имидазольный, пиразольный, 1,2,3-триазольный, 1,2,4-триазольный, пиридиновый, пиримидиновый, пиридазиновый, пиразиновый и 1,3,4-триазиновый цикл. Цикл необязательно замещен С 1-4 алкильной группой или алкоксигруппами, или атомом галогена. Гетероароматический цикл, содержащий один атом азота и один атом кислорода или серы, обозначает оксазольный, изоксазольный, тиазольный и изотиазольный цикл. Цикл необязательно замещен C1-4 алкильной группой или алкоксигруппами, или атомом галогена. Группа - (CH2)m-Z-(СН 2)о - образует вместе с атомом азота оксазиридино-, диазиридино-, 1,2 диазетидино-, 1,3-диазетидино-, изоксазолидино-, оксазолидино-, имидазолидино-, пиразолидино-, тиазолидино-, морфолино-, пиперазино- или 4-метилпиперазиногруппу, необязательно замещенную С 1-4 алкильной группой или С 3-6 циклоалкильной группой. Соли соединений общей формулы (I) обозначают соли, образованные с неорганическими и органическими кислотами и основаниями. Предпочтительными солями являются соли, образованные с фармацевтически приемлемыми кислотами, такими, например, как соляная кислота, серная кислота, этансульфоновая кислота, винная кислота, янтарная кислота, яблочная кислота, лимонная кислота, и с фармацевтически приемлемыми основаниями, такими, например, как гидроксид натрия, гидроксид калия, этаноламин. Сольваты означают сольваты, образованные с различными растворителями, например, с водой или этанолом. Соединения общей формулы (I) обладают геометрической и оптической изомерией, следовательно,данное изобретение также относится к смесям геометрических изомеров, к рацематам или оптически активным геометрическим изомерам, а также к их солям и сольватам. Предпочтительной группой соединений общей формулы (I) являются соединения где R1 обозначает атом водорода или неразветвленную или разветвленную C1-4 алкильную группу;R2 обозначает атом водорода или неразветвленную или разветвленную C1-4 алкильную группу;R3 обозначает атом водорода или неразветвленную или разветвленную C1-4 алкильную группу, С 3-6 циклоалкильную группу, фенильную, тиенильную или фурильную группу, необязательно замещенную одной или несколькими неразветвленными или разветвленными C1-4 алкильными группами, неразветвленными или разветвленными C1-4 алкоксигруппами или атомом галогена;R4, R5, R6 и R7 независимо друг от друга обозначают атом водорода, неразветвленную или разветвленную C1-4 алкильную группу, неразветвленную или разветвленную C1-4 алкоксигруппу, гидроксильную группу или атом галогена, или R4 и R7 обозначают атом водорода и R5 и R6 вместе образуют метилендиоксигруппу;R8 обозначает атом водорода или цианогруппу, аминокарбонильную группу, C1-4 алкоксикарбонильную группу или карбоксильную группу;R9 и R10 независимо друг от друга обозначают атом водорода, неразветвленную или разветвленнуюC1-4 алкильную группу или С 3-6 циклоалкильную группу;X обозначает -СН 2-группу, -NH-группу, -NR11-группу или атом серы, атом кислорода, сульфогруппу или сульфоксигруппу, где R11 обозначает неразветвленную или разветвленную C1-4 алкильную группу или С 3-6 циклоалкильную группу;Z обозначает атом кислорода, атом серы, -NH-группу или -NR12- группу, где R12 обозначает неразветвленную или разветвленную C1-4 алкильную группу или С 3-6 циклоалкильную группу;p равно нулю или 1;r равно нулю или 1, при условии, что по меньшей мере один из m и о отличен от нуля,и их соли, сольваты и оптически активные изомеры, а также соли и сольваты изомеров.-3 007595 Более предпочтительной группой соединений общей формулы (I) являются соединения где R1 обозначает атом водорода или метильную группу;R2 обозначает атом водорода или метильную группу;R3 обозначает фенильную, тиенильную или фурильную группу;R4, R5, R6 и R7 независимо друг от друга обозначают атом водорода, неразветвленную или разветвленную C1-4 алкильную группу, неразветвленную или разветвленную C1-4 алкоксигруппу, гидроксильную группу или атом галогена, илиR4 и R7 обозначают атом водорода и R5 и R6 вместе образуют метилендиоксигруппу;R8 обозначает атом водорода или цианогруппу;R9 и R10 обозначают атом водорода, метильную, этильную или циклопропильную группу;Z обозначает атом кислорода, атом серы, -NH-группу или -NR12-группу, где R12 обозначает неразветвленную или разветвленную C1-4 алкильную группу или С 3-6 циклоалкильную группу, иr равно нулю,и их соли, сольваты и изомеры, а также соли и сольваты изомеров. Особенно предпочтительными являются следующие соединения, которые отвечают вышеуказанным критериям: 1-(9-бензиламино-10-цианоимидазо[1,2-а]хинолин-2-карбонил)-4-метилпиперазин; 1-(9-бензиламино-10-цианоимидазо[1,2-а]хинолин-2-карбонил)морфолин; 1-(9-фурфуриламино-10-цианоимидазо[1,2-а]хинолин-2-карбонил)-4-метилпиперазин; 1-(9-фурфуриламино-10-цианоимидазо[1,2-а]хинолин-2-карбонил)пиперазин; 1-(9-фурфуриламино-10-цианоимидазо[1,2-а]хинолин-2-карбонил)морфолин; 1-(9-тениламино-10-цианоимидазо[1,2-а]хинолин-2-карбонил)морфолин; 1-(9-тениламино-10-цианоимидазо[1,2-а]хинолин-2-карбонил)пиперази. и их соли, сольваты и изомеры, а также соли и сольваты изомеров. Данное изобретение также относится к фармацевтическим композициям, содержащим в качестве действующего начала соединения общей формулы (I) или их изомеры, соли и сольваты, которые предпочтительно являются композициями для перорального введения, но соответствующие композиции для ингаляции, парентерального и трансдермального введения также являются объектами данного изобретения. Вышеуказанные фармацевтические композиции могут быть твердыми или жидкими, например, в виде таблеток, пилюль, капсул, пастилок, растворов, суспензий или эмульсий. Твердые композиции,прежде всего таблетки и капсулы, являются предпочтительными фармацевтическими формами. Вышеуказанные фармацевтические композиции получают, применяя обычные фармацевтические вспомогательные вещества и стандартные способы. Соединения общей формулы (I) могут быть использованы для лечения патологий, в развитии которых участвует рецептор A3. Соединения по данному изобретению, обладающие селективной активностью в отношении A3 рецептора, могут быть использованы в лечении и/или профилактике нарушений деятельности сердца, почек, дыхательной системы и центральной нервной системы. Они блокируют защитное действие аденозина на растущие опухолевые клетки, предотвращают дегрануляцию тучных клеток, препятствуют образованию цитокинов, уменьшают внутриглазное давление, предотвращают выделение TNF, затрудняют миграцию эозинофильных и нейтрофильных гранулоцитов и других клеток зоны воспаления, предотвращают сужение трахеи и препятствуют прохождению плазмы крови через стенку кровеносного сосуда. На основании указанных выше эффектов антагонисты аденозиновых рецепторов A3 по данному-4 007595 изобретению могут быть применимы в терапии в качестве противовоспалительных, противоастматических, противоишемических, антидепрессивных антиаритмических средств, лекарств для защиты функции почек, средств, предупреждающих возникновение опухолей, лекарств против болезни Паркинсона и средств, усиливающих когнитивные способности. Они также применимы для лечения и профилактики следующих заболеваний: реперфузионного повреждения сердечной мышцы, хронических обструктивных заболеваний легких (COPD), респираторного дисстресс-синдрома у взрослых (ARDS) - включая хронический бронхит, эмфизему легких или одышку -, аллергические реакции (например ринит, реакции, вызванные растением сумах, уртикарная сыпь, склеродерма, артрит), другие аутоиммунные заболевания,воспалительные заболевания кишечника, болезнь Аддисона, болезнь Крона, псориаз, заболевания суставов, гипертония, аномальные неврологические функции, глаукома и диабет (K.N. Klotz, NaunynSchmiedberg's Arch. Pharmacol. 362:382, 2000; P.G. Baraldi s P.A. Borea, TiPS 21:456, 2000). Соединения по данному изобретению могут быть предпочтительными для применения в лечении таких заболеваний, как, например, астма, COPD и ARDS, глаукома, опухоли, аллергические и воспалительные заболевания, ишемия, гипоксия, аритмия и болезни почек. Данное изобретение, кроме того, относится к применению соединений общей формулы (I) для лечения вышеуказанных видов патологий. Предлагаемая дневная доза составляет от 0,1 до 1000 мг активного ингредиента и зависит от природы и тяжести заболевания, пола, массы тела и т.п. больного. Дополнительным объектом данного изобретения является получение соединений общей формулы (I). Заместители в формулах промежуточных соединений общих формул (II), (III), (IV), (V), (VI), (VII) и(VIII) имеют такие значения, как указано выше. В способе по данному изобретению соединения общей формулы (VIII) ацилируют кислотами или их реакционноспособными производными общей формулы (II) применяя известный в органической химии способ ацилирования. В качестве ацилирующего агента предпочтительно применяют галогениды и смешанные ангидриды кислот. Полученное соединение общей формулы (I) переводят, если требуется, в одну из его солей или в один из его сольватов или выделяют из его соли или сольвата и разделяют на геометрические или оптические изомеры.-5 007595 Заместители в соединениях общей формулы (I) могут быть преобразованы друг в друга известными способами. Смешанный ангидрид, используемый для реакции ацилирования, можно получить с пивалоилхлоридом, лучше с помощью органических оснований, растворенных в хлороформе, предпочтительно с помощью триэтиламина, но можно также применять и другие способы, известные в органической химии. Ацилирование можно проводить в широком интервале температур, предпочтительно от 0 до 100 С. Промежуточные соединения общей формулы (II) где значения R1, R2, R3, R4, R5, R6, R7, R8, X и n такие, как указано выше, могут быть получены несколькими известными способами, например способом, показанным на схеме 1. из исходных соединений формулы (III) используя способ гидролиза, известный в органической химии. В качестве гидролизующего агента можно использовать щелочные гидроксиды, но можно применять и другие соединения, способствующие гидролизу сложных эфиров. Соединения общей формулы (III) где значения R1, R2, R3, R4, R5, R6, R7, R8, X и n такие, как указано выше,и R14 обозначает C1-4 алкильную группу,могут быть получены из соединений формулы (IV) способами, которые сами по себе известны (I.R. Ager and R. Westwood, J. Med. Chem. 31, 1098, 1988). Соединения общей формулы (IV) где значения R1, R2, R3, R4, R5, R6, R7, R8, X и n такие, как указано выше, могут быть получены из соединений формулы (V) способами, которые сами по себе известны (Nan Zhang, Bioorg. и Med. Chem. Lett., 10, 2825, 2000). Соединения общей формулы (V), где значения R4, R5, R6, R7 и R8 такие, как указано выше, можно получать из соединений формулы (VI) с помощью способов, которые сами по себе известны (D.L. Leysen, J. Heterocyclic Chem., 24, 1611, 1987). Соединения общей формулы (VI) где значения R4, R5, R6, R7 и R8 такие, как указано выше, можно получать с помощью способов, которые сами по себе известны (Pfizer (Inc) USP 4,175,193). Соединения по данному изобретению общих формул (I), (II) , (III), (IV) и (V), их получение и биологическая активность наглядно показаны в приведенных ниже примерах, причем объем притязаний изобретения не ограничивается данными примерами. Примеры Пример 1. 1-(9-Бензиламино-10-цианоимидазо[1,2-а]хинолин-2- карбонил)-4-метилпиперазин В общей формуле (I) R1 и R2 обозначают атом водорода, R3 обозначает фенильную группу, R4, R5,6a. 2-Амино-3-циано-4-хлорхинолин Смесь 10 г 2-амино-3-циано-4-гидроксихинолина и 15 мл фосфорилхлорида нагревают при перемешивании при 110 С. Реакционную смесь охлаждают, выливают в ледяную воду (100 мл) и нейтрализуют 60 мл 10% раствора гидроксида натрия. Образовавшийся желтый осадок отфильтровывают и промывают 50 мл воды. После сушки получают 7,5 г указанного в заголовке соединения, т.пл. 210 С. ЯМР, H (400 МГц, ДМСО-d6): 7,21 м.д. (с, 2 Н, NH2), 7,35-7,40 м.д. (дд, 1 Н, 6-Н), 7,53-7,57 м.д. (д,1 Н, 5-Н), 7,70-7,75 м.д. (дд, 1 Н, 7-Н), 7,93-7,98 м.д. (д, 1 Н, 8-Н).b. 2-Амино-3-циано-4-бензиламинохинолин 2-Амино-3-циано-4-хлорхинолин (5 г) и бензиламин (11 мл) нагревают при 130 С при перемешивании. Реакционную смесь выливают в 50 мл воды, образовавшийся осадок отфильтровывают, промывают 50 мл воды. Светло-желтый осадок перекристаллизовывают из 25 мл диметилформамида, получая 5,2 г указанного в заголовке соединения, т.пл. 206 С. ЯМР, Н (400 МГц, ДМСО-d6): 5,02-5,03 м.д. (д, 2 Н, N-CH2), 6,22 м.д. (с, 2 Н, NH2), 7,14-7,16 м.д.-8 007595 Соответствующие соединения общей формулы (IV) могут быть получены при использовании 2 аминометилпиридина или 3-аминометилпиридина или 4-аминометилпиридина вместо бензиламина. с. Моногидрат этил-9-бензиламино-10-цианоимидазо[1,2-а]хинолин-2-карбоксилата К раствору 2,74 г 2-амино-3-циано-4-бензиламинохинолина в 100 мл абс. этанола прибавляют 2,14 г этилбромпирувата при 70 С и при перемешивании. Реакционную смесь нагревают и кипятят с обратным холодильником в течение 2 ч, образовавшийся осадок отфильтровывают. Белые кристаллы перекристаллизовывают из 120 мл ацетонитрила. Получают 1,1 г указанного в заголовке соединения, т.пл. 112-114 С. ЯМР, H (400 МГц, ДМСО-d6): 1,32 м.д. (т, 3 Н, СООСН 2 СН 3), 4,30 м.д. (кв, 2 Н, СООСН 2 СН 3), 5,09 м.д. (д, 2 Н, PhCH2), 7,25-7,38 м.д. (м, 5 Н), 7,64-7,67 м.д. (м, 1 Н), 7,85-7,88 м.д. (м, 1 Н), 8,43-8,53 м.д. (м,3 Н), 9,04 м.д. (с, 1 Н, 3-Н).d. 9-Бензиламино-10-цианоимидазо[1,2-а]хинолин-2-карбоновая кислота Смесь 2,71 г моногидрата этил-9-бензиламино-10-цианоимидазо[1,2-а]хинолин-2-карбоксилата, 42 мл этанола и 40 мл 10% гидроксида натрия перемешивают при 25 С в течение 6 ч. К густой суспензии прибавляют 100 мл воды и 96% уксусной кислотой доводят рН смеси до 3. Светло-желтые кристаллы отфильтровывают, 3 раза промывают водой (по 25 мл) и сушат. Получают 2,3 г указанного в заголовке соединения, т.пл. 178-182 С. ЯМР, Н (200 МГц, ДМСО-d6): 5,09 м.д. (д, 2 Н, PhCH2), 7,22-7,40 м.д. (м, 5 Н), 7,59-7,67 м.д. (м, 1 Н),7,81-7,89 м.д. (м, 1 Н), 8,37-8,54 м.д. (м, 3 Н), 8,90 м.д. (с, 1 Н, 3-Н).e. 1-(9-Бензиламино-10-цианоимидазо[1,2-а]хинолин-2-карбонил)-4-метилпиперазин К раствору 1,71 г 9-бензиламино-10-цианоимидазо[1,2-а]хинолин-2-карбоновой кислоты и 0,8 мл триэтиламина в 15 мл хлороформа прибавляют по каплям при перемешивании раствор 0,6 г пивалоилхлорида в 10 мл хлороформа при 5 С в течение 15 мин. Реакционную смесь перемешивают при 5 С в течение 1 ч, затем прибавляют смесь 0,5 г N-метилпиперазина, 10 мл хлороформа и 0,8 мл триэтиламина. Смесь перемешивают при 25 С в течение 7 ч, разбавляют 100 мл хлороформа, экстрагируют последовательно 50 мл воды, 50 мл 5% раствора гидрокарбоната натрия и 50 мл воды, сушат над сульфатом натрия и концентрируют в вакууме. Светло-желтое кристаллическое вещество перекристаллизовывают из 6 мл(м, 2 Н), 8,50-8,52 м.д. (м, 1 Н), 8,80 м.д. (с, 1 Н, 3-Н). Пример 2. 1-(9-Бензиламино-10-цианоимидазо[1, 2-а]хинолин-2-карбонил)морфолин В общей формуле (I) R1 и R2 обозначают атом водорода, R3 обозначает фенильную группу, R4, R5,R6 и R7 обозначают атом водорода, R8 обозначает цианогруппу, X обозначает -NH-группу, Z обозначает атом кислорода, n равно 1, m и о равны 2, r и р равны 0. К смеси 1,71 г 9-бензиламино-10-цианоимидазо[1,2-а]хинолин-2-карбоновой кислоты и 0,8 мл триэтиламина в 15 мл хлороформа прибавляют при перемешивании раствор 0,6 г пивалоилхлорида в 10 мл хлороформа при 5 С в течение 15 мин. Реакционную смесь перемешивают при 5 С в течение 1 ч, затем прибавляют смесь 0,45 г морфолина, 10 мл хлороформа и 1,6 мл триэтиламина. Смесь перемешивают при 25 С в течение 3 ч, затем обрабатывают, как описано в предыдущем примере. Полученные светложелтые кристаллы перекристаллизовывают из 10 мл N,N-диметилформамида и получают 0,55 г указанного в заголовке соединения, т.пл. 279 С. ЯМР, Н (400 МГц, ДМСО-d6): 3,6 м.д. (м, 6 Н), 4,2 м.д. (м, 2 Н), 5,08 м.д. (д, 2 Н, PhCH2), 7,23-7,38 м.д. (м, 5 Н), 7,62-7,65 м.д. (м, 1 Н), 7,84-7,87 м.д. (м, 1 Н), 8,37-8,39 м.д. (м, 2 Н), 8,50-8,53 м.д. (м, 1 Н), 8,75 м.д. (с, 1 Н, 3-Н). Пример 3. 1-(9-Фурфуриламино-10-цианоимидазо[1,2-а]хинолин-2-карбонил)-4-метилпиперазин В общей формуле (I) R1 и R2 обозначают атом водорода, R3 обозначает 2-фурильную группу, R4, R5,R6 и R7 обозначают атом водорода, R8 обозначает цианогруппу, R12 обозначает метильную группу, X обозначает -NH-группу, Z обозначает атом азота, n равно 1, m и o равны 2, r и р равны 0.a. 2-Амино-3-циано-4-фурфуриламинохинолин 2-Амино-3-циано-4-хлорхинолин (10 г) нагревают с 19 г фурфуриламина при 120 С в течение 3 ч. Реакционную смесь охлаждают до 25 С и 6 раз смешивают с 50 мл воды. Кристаллы отфильтровывают и сушат. Полученный продукт перекристаллизовывают из 60 мл N,N-диметилформамида и получают 5,8 г соединения, указанного в заголовке, т.пл. 206 С. ЯМР, H (200 МГц, ДМСО-d6): 4,98 м.д. (д, 2 Н, фурил-СН 2), 6,29 м.д. (с, 2 Н), 6,35-6,42 м.д. (м, 2 Н),7,10-7,18 м.д. (м, 1 Н), 7,31-7,35 м.д. (м, 1 Н), 7,47-7,60 м.д. (м, 2 Н), 8,13-8,20 м.д. (м, 2 Н).b. Моногидрат этил-9-фурфуриламино-10-цианоимидазо[1,2-а]хинолин-2-карбоксилат К раствору 2,64 г 2-амино-3-циано-4-фурфуриламинохинолина в 100 мл абс. этанола прибавляют при перемешивании 2,14 г этилбромпирувата при 70 С. Реакционную смесь нагревают и кипятят с обратным холодильником в течение 2 ч, отфильтровывают выпавшие в осадок кристаллы и получают 1,15 г указанного в заголовке соединения, т.пл. 242-245 С. ЯМР, Н (200 МГц, ДМСО-d6): 1,33 м.д. (т, 3 Н, СООСН 2 СН 3), 4,31 м.д. (кв, 2 Н, СООСН 2 СН 3), 5,05c. 9-Фурфуриламино-10-цианоимидазо[1,2-а]хинолин-2-карбоновая кислота Смесь 2,52 г моногидрата этил-9-фурфуриламино-10-цианоимидазо[1,2-а]хинолин-2-карбоксилата,40 мл этанола и 33 мл 10% гидроксида натрия перемешивают при 25 С в течение 3 ч. К густой суспензии прибавляют 80 мл воды и смесь подкисляют 96% уксусной кислотой до рН=3. Светло-желтые кристаллы отфильтровывают, три раза промывают водой (по 25 мл) и сушат. Получают 2,32 г указанного в заголовке соединения, т.пл. 180-185 С. ЯМР, H (200 МГц, ДМСО-d6): 5,05 м.д. (д, 2 Н, фурил-СН 2), 6,39-6,42 м.д. (м, 2 Н), 7,56-7,64 м.д. (м,2 Н), 7,79-7,87 м.д. (м, 1 Н), 8,27 м.д. (т, 1 Н), 8,36-8,46 м.д. (м, 2 Н), 8,93 м.д. (с, 1 Н, 3-Н).d. 1- (9-Фурфуриламино-10-цианоимидазо [1, 2-a] хинолин-2-карбонил)-4-метилпиперазин К смеси 1,79 г 9-фурфуриламино-10-цианоимидазо[1,2-а]хинолин-2-карбоновой кислоты и 0,8 мл триэтиламина в 15 мл хлороформа прибавляют по каплям раствор 0,6 г пивалоилхлорида в 10 мл хлороформа при перемешивании и температуре 5 С в течение 15 мин. Реакционную смесь перемешивают при 5 С в течение 1 ч, затем прибавляют смесь 0,46 г N-метилпиперазина, 10 мл хлороформа и 0,8 мл триэтиламина. Смесь перемешивают при 25 С в течение 3 ч, разбавляют 100 мл хлороформа, экстрагируют последовательно 50 мл воды, 50 мл 5% раствора гидрокарбоната натрия и 50 мл воды, сушат над сульфатом натрия и концентрируют в вакууме. Светло-желтое кристаллическое вещество перекристаллизовывают из 50 мл этанола. Получают 0,18 г указанного в заголовке соединения, т.пл. 237 С. ЯМР, Н (200 МГц, ДМСО-d6): 2,17 м.д. (с, 3 Н), 2,24 м.д. (м, 4 Н), 3,57 м.д. (м, 2 Н), 4,11 м.д. (м, 2 Н),5,05 м.д. (д, 2 Н, фурил-СН 2), 6,40-6,44 м.д. (м, 2 Н), 7,57-7,65 м.д. (м, 2 Н), 7,80-7,88 м.д. (м, 1 Н), 8,23 м.д.R7 обозначают атом водорода, R8 обозначает цианогруппу, X обозначает -NH-группу, Z обозначает -NHгруппу, n равно 1, m и о равны 2, r и р равны 0. К смеси 1,79 г 9-фурфуриламино-10-цианоимидазо[1,2-а]хинолин-2-карбоновой кислоты, полученной по методике, описанной в примере 3, и 0,8 мл триэтиламина в 15 мл хлороформа прибавляют по каплям при перемешивании раствор 0,6 г пивалоилхлорида в 10 мл хлороформа при 5 С в течение 15 мин. Реакционную смесь перемешивают при 5 С в течение 1 ч, затем прибавляют смесь 0,46 г пиперазина, 10 мл хлороформа и 0,8 мл триэтиламина. Смесь перемешивают при 25 С в течение 3 ч, разбавляют 100 мл хлороформа, экстрагируют последовательно 50 мл воды, 50 мл 5% раствора гидрокарбоната натрия и 50 мл воды, сушат над сульфатом натрия и концентрируют в вакууме. Светло-желтое кристаллическое вещество перекристаллизовывают из 50 мл этанола. Получают 0,14 г указанного в заголовке соединения,т.пл. 239 С. ЯМР, Н (200 МГц, ДМСО-d6): 2,7 м.д. (м, 4 Н), 3,5 м.д. (м, 2 Н), 4,05 м.д. (м, 2 Н), 5,05 м.д. (д, 2 Н,фурил-СН 2), 6,40-6,44 м.д. (м, 2 Н), 7,57-7,65 м.д. (м, 2 Н), 7,80-7,88 м.д. (м, 1 Н), 8,23 м.д. (т, 1 Н), 8,39-8,46 м.д. (м, 2 Н), 8,81 м.д. (с, 1 Н, 3-Н) . Пример 5. 1-(9-Фурфуриламино-10-цианоимидазо[1,2-а]хинолин-2-карбонил)морфолин В общей формуле (I) R1 и R2 обозначают атом водорода, R3 обозначает 2-фурильную группу, R4, R5,R6 и R7 обозначают атом водорода, R8 обозначает цианогруппу, X обозначает -NH-группу, Z обозначает атом кислорода, n равно 1, m и о равны 2, r и р равны 0. К смеси 1,79 г 9-фурфуриламино-10-цианоимидазо[1,2-а]хинолин-2-карбоновой кислоты, полученной по методике, описанной в примере 3, и 0,8 мл триэтиламина в 15 мл хлороформа прибавляют по каплям при перемешивании раствор 0,6 г пивалоилхлорида в 10 мл хлороформа при 5 С в течение 15 мин. Реакционную смесь перемешивают при 5 С в течение 1 ч, затем к ней прибавляют смесь 0,66 г морфолина, 10 мл хлороформа и 0,8 мл триэтиламина. Смесь перемешивают при 25 С в течение 3 ч, разбавляют 100 мл хлороформа, экстрагируют последовательно 50 мл воды, 50 мл 5% раствора гидрокарбоната натрия и 50 мл воды, сушат над сульфатом натрия и концентрируют в вакууме. Светло-желтое кристаллическое вещество перекристаллизовывают из 50 мл этанола. Получают 0,18 г указанного в заголовке соединения, т.пл. 267 С. ЯМР, Н (200 МГц, ДМСО-d6): 3,6 м.д. (м, 6 Н), 4,2 м.д. (м, 2 Н), 5,05 м.д. (д, 2 Н, фурил-СН 2), 6,406,44 м.д. (м, 2 Н), 7,57-7,65 м.д. (м, 2 Н), 7,80-7,88 м.д. (м, 1 Н), 8,23 м.д. (т, 1 Н), 8,39-8,46 м.д. (м, 2 Н), 8,81 м.д. (с, 1 Н, 3-Н). Пример 6. 1-(9-Тиениламино-10-цианоимидазо[1,2-а]хинолин-2-карбонил)морфолин В общей формуле (I) R1 и R2 обозначают атом водорода, R3 обозначает 2-тиенильную группу, R4, R5,R6 и R7 обозначают атом водорода, R8 обозначает цианогруппу, X обозначает -NH-группу, Z обозначает атом кислорода, n равно 1, m и о равны 2, r и р равны 0.a. 2-Амино-3-циано-4-тиениламинохинолин 2-Амино-3-циано-4-хлорхинолин (10 г) нагревают с 19 г тиенилметиламина при 115 С в течение 4 ч. Реакционную смесь охлаждают до 25 С и смешивают 6 раз с 50 мл воды. Кристаллы отфильтровыва- 10007595 ют, 2 раза промывают 50 мл воды и сушат. Полученный продукт перекристаллизовывают из 60 мл N,Nдиметилформамида, получают 6,8 г светло-желтого соединения, указанного в заголовке, т.пл. 208-209 С. ЯМР, H (200 МГц, ДМСО-d6): 5,18 м.д. (д, 2 Н, тиенил-СН 2), 6,28 м.д. (с, 2 Н), 6,96-7,00 м.д. (м, 1 Н),7,07-7,19 м.д. (м, 2 Н), 7,31-7,42 м.д. (м, 2 Н), 7,48-7,56 м.д. (м, 1 Н), 8,09-8,13 м.д. (м, 1 Н), 8,30 м.д. (т, 1 Н).b. Этил-9-тиениламино-10-цианоимидазо[1,2-а]хинолин-2-карбоксилат К раствору 5,61 г 2-амино-3-циано-4-тиениламинохинолина в 200 мл абс. этанола прибавляют при перемешивании 4,29 г этилбромпирувата при 70 С. Реакционную смесь нагревают и кипятят с обратным холодильником в течение 2 ч, выпавшие в осадок кристаллы отфильтровывают и получают 2,54 г указанного в заголовке соединения, т.пл. 255-256 С. ЯМР, Н (200 МГц, ДМСО-d6): 1,33 м.д. (т, 3 Н, СООСН 2 СН 3), 4,31 м.д. (кв, 2 Н, СООСН 2 СН 3), 5,24 м.д. (д, 2 Н, тиенил-СН 2), 6,96-7,00 м.д. (м, 1 Н), 7,14 м.д. (м, 1 Н), 7,40-7,43 м.д. (м, 1 Н), 7,61-7,68 м.д. (м,1 Н), 7,82-7,90 м.д. (м, 1 Н), 8,42-8,46 м.д. (м, 3 Н), 9,05 м.д. (с, 1 Н, 3-Н).c. 9-Тиениламино-10-цианоимидазо[1,2-a] хинолин-2-карбоновая кислота Смесь 2,54 г этил-9-тиениламино-10-цианоимидазо[1,2-а]хинолин-2-карбоксилата, 40 мл этанола и 33 мл 10% гидроксида натрия перемешивают при 25 С в течение 6 ч. К густой суспензии прибавляют 80 мл воды и смесь подкисляют 96% уксусной кислотой до рН=3. Светло-желтые кристаллы отфильтровывают, 5 раз промывают водой (по 10 мл) и сушат. Получают 2,18 г указанного в заголовке соединения,т.пл. 209-217 С (при разложении). ЯМР, Н (400 МГц, ДМСО-d6): 5,24 м.д. (д, 2 Н, тиенил-СН 2), 8,88 м.д. (с, 1 Н, 3-Н).d. 1-(9-Тиениламино-10-цианоимидазо[1,2-а]хинолин-2-карбонил)морфолин К смеси 1,80 г 9-тениламино-10-цианоимидазо[1,2-а]хинолин-2-карбоновой кислоты и 1,1 мл триэтиламина в 10 мл хлороформа прибавляют по каплям раствор 0,87 г пивалоилхлорида в 10 мл хлороформа при перемешивании и температуре 5 С в течение 15 мин. Реакционную смесь перемешивают при 5 С в течение 1 ч, затем прибавляют смесь 0,61 г морфолина, 10 мл хлороформа и 1,1 мл триэтиламина. Полученную смесь перемешивают при 25 С в течение 3 ч, разбавляют 100 мл хлороформа, экстрагируют последовательно 50 мл воды, 50 мл 5% раствора гидрокарбоната натрия и 50 мл воды, сушат над сульфатом натрия и концентрируют в вакууме. Светло-желтое кристаллическое вещество перекристаллизовывают из 200 мл этанола. Получают 0,19 г указанного в заголовке соединения, т.пл. 315 С. ЯМР, H (400 МГц, ДМСО-d6): 3,6 м.д. (м, 6 Н), 4,2 м.д. (м, 2 Н), 5,24 м.д. (д, 2 Н, тиенил-СН 2), 6,977,00 м.д. (м, 1 Н), 7,14 м.д. (м, 1 Н), 7,41 м.д. (м, 1 Н), 7,61-7,65 м.д. (м, 1 Н), 7,83-7,87 м.д. (м, 1 Н), 8,37-8,45 м.д. (м, 3 Н), 8,82 м.д. (с, 1 Н, 3-Н). Пример 7. 1-(9-Тиениламино-10-цианоимидазо[1,2-а]хинолин-2-карбонил)пиперазин В общей формуле (I) R1 и R2 обозначают атом водорода, R3 обозначает 2-тиенильную группу, R4, R5, R6 иR7 обозначают атом водорода, R8 обозначает цианогруппу, X обозначает -NH-группу, Z обозначает -NH-группу,n равно 1, m и о равны 2, r и р равны 0. К смеси 1,80 г 9-тениламино-10-цианоимидазо[1,2-а]хинолин-2-карбоновой кислоты, полученной по методике, описанной в примере 6, и 1,1 мл триэтиламина в 10 мл хлороформа, прибавляют по каплям при перемешивании раствор 0,87 г пивалоилхлорида в 10 мл хлороформа при 5 С в течение 15 мин. Реакционную смесь перемешивают при 5 С в течение 1 ч, затем прибавляют смесь 0,61 г пиперазина, 10 мл хлороформа и 1,1 мл триэтиламина. Смесь перемешивают при 25 С в течение 3 ч, разбавляют 100 мл хлороформа, экстрагируют последовательно 50 мл воды, 50 мл 5% раствора гидрокарбоната натрия и 50 мл воды, сушат над сульфатом натрия и концентрируют в вакууме. Светло-желтое кристаллическое вещество перекристаллизовывают из 50 мл этанола. Получают 0,19 г указанного в заголовке соединения,т.пл. 269 С. ЯМР, H (400 МГц, ДМСО-d6): 2,7 м.д. (м, 4 Н), 3,5 м.д. (м, 2 Н), 4,05 м.д. (м, 2 Н), 5,24 м.д. (д, 2 Н,тиенил-СН 2), 6,97-7,00 м.д. (м, 1 Н), 7,14 м.д. (м, 1 Н), 7,41 м.д. (м, 1 Н), 7,61-7,65 м.д. (м, 1 Н), 7,83-7,87 м.д. (м, 1 Н), 8,37-8,45 м.д. (м, 3 Н), 8,82 м.д. (с, 1 Н, 3-Н). Структура и физические характеристики соединений формулы (III), полученных в соответствии с примером 1, представлены в табл. I. Структура и физические характеристики соединений формулы (IV), полученных в соответствии с примером 1, представлены в табл. II. Структура и физические характеристики соединений формулы (V), полученных в соответствии с примером 1, представлены в табл. III. Пример 51. Таблетку из композиции следующего состава получают известными способами: Активный ингредиент 25 мг Лактоза 50 мг Авицел 21 мг Кросповидон 3 мг Стеарат магния 1 мг Биология Методики Связывание аденозиновых A3 рецепторов человека Получение суспензии мембран: клетки яичника клонированного золотистого хомячка, экспрессирующие А 3 рецепторы человека (именуемые далее СНО-hА 3), соответствующим образом культивируют и разводят. После получения слоя сливающихся клеток культуральную жидкость удаляют из клеток промыванием PBS (37 С), затем клетки суспендируют в ледяном PBS, центрифугируют (1000g 10 perc)(Sigma 3K30) и гомогенизируют, используя тефлоновый гомогенизатор (В. Braun Potter S) при скорости вращения 1500 об/мин в течение 15 с в указанном ниже буфере: 50 мМ трис, 10 мМ MgCl2, 1 мМ ЭДТУ(EDTA), рН 8,0. Гомогенат центрифугируют (43000g, 10 мин). Осадок суспендируют в вышеуказанном буфере, концентрация белка 0,1 мг/мл (Bradford method). Аликвоты препарата мембран хранят при -80 С. Процедура связывания: инкубируют препарат мембран (содержание белка 2 мкг) в инкубационном буфере (50 мМ трис, 10 мМ MgCl2, 1 мМ ЭДТУ, 3 ед./мл аденозиндезаминазы, рН 8,0), в присутствии 0,5 нМ[125I]АВ-МЕСА (п-амино-3-иодбензил-5'-N-метилкарбоксамидоаденозин) (100000 имп./мин) и 100 мкМ R-PIA (N6-[L-2-фенилизопропил]аденозин) для определения неспецифического связывания тестируемого соединения в общем объеме 50 мкл в течение 1 ч при комнатной температуре. Фильтруют через фильтры из стекловолокна от Whatman GF/B (предварительно погруженные в 0,5% полиэтиленимин на 3 ч), промывают 4 х 1 мл ледяного раствора 50 мМ трис, 10 мМ MgCl2, 1 мМ ЭДТУ (рН 8,0) на 96 луночном коллекторе клеток (Brandel Cell Harvester). Определение активности в счетчике гаммаизлучения (1470 Wizard, Wallac). Ингибирование [%]=100-активность в присутствии тестируемого соединения неспецифическая активность)/(общая активность - неспецифическая активность 100. Связывание аденозиновых A1 рецепторов человека Получение суспензии мембран: клетки яичника клонированного золотистого хомячка, экспрессирующие A1 рецепторы человека (именуемые далее CHO-hA1), соответствующим образом культивируют и разводят. После получения слоя сливающихся клеток культуральную жидкость удаляют из клеток промыванием PBS (37 С), затем клетки суспендируют в ледяном PBS, промывают 3 раза ледяным PBS, центрифугируют (1000g 10 perc) (Sigma 3K30) и гомогенизируют, используя тефлоновый гомогенизатор (В.Braun Potter S) при скорости вращения 1500 об/мин в течение 15 с в указанном ниже буфере: 50 мМ трис,10 мМ НСl, рН 7,4. Гомогенат центрифугируют (43000g, 10 мин). Осадок суспендируют в вышеуказанном буфере, концентрация белка 0,5 мг/мл (способ Бредфорда). Аликвоты препарата мембран хранят при-80 С. Процедура связывания: инкубируют препарат мембран CHO-hA1 (содержание белка 50 мкг) в инкубационном буфере (50 мМ трис, 3 ед./мл аденозиндезаминазы, рН 7,4), 10 нМ [3 Н]ССРА (2-хлор-N6- 15007595 циклопентиладенозин) (80000 распадов/мин) и 10 мкМ R-PIA (N6-[L-2-фенилизопропил]аденозин) для определения неспецифического связывания тестируемого соединения, в общем объеме 100 мкл в течение 3 ч при комнатной температуре. Фильтруют через фильтры из стекловолокна от Whatman GF/B (предварительно погруженные в 0,5% полиэтиленимин на 3 ч), промывают 4x1 мл ледяного раствора 50 мМ трис(рН 7,4) на 96-луночном коллекторе клеток (Brandel Cell Harvester). Определение активности: в присутствии 200 мкл смеси HiSafe-3 в счетчике -излучения (1450 Microbeta, Wallac). Ингибирование [%]=100 активность в присутствии тестируемого соединения -неспецифическая активность)/(общая активность неспецифическая активность 100. Связывание аденозиновых A2a рецепторов человека Процедура связывания: инкубируют 7 мкг мембран (человеческие аденозиновые рецепторы A2 а,трансфецированные в клетки НЕK-293, источник: Receptor Biology, Inc.), буфер (50 мМ трис-HCl, 10 мМNECA (5'-N-этилкарбоксамидоаденозина) для определения неспецифического связывания тестируемого соединения, в общем объеме 100 мкл в течение 90 мин при комнатной температуре. Фильтруют в вакууме через фильтры из стекловолокна от Whatman GF/B (предварительно погруженные в 0,5% полиэтиленимин на 3 ч), промывают 4 х 1 мл ледяного раствора (50 мМ трис, 10 мМ MgCl2, 1 мМ ЭДТУ, 0,9% NaCl,рН 7,4) на 96-луночном коллекторе клеток (Brandel Cell Harvester). Определение активности: в счетчике-излучения (1450 Microbeta, Wallac) в присутствии смеси 200 мкл HiSafe-3. Ингибирование [%]=100 активность в присутствии тестируемого соединения - неспецифическая активность)/(общая активность-неспецифическая активность 100. Связывание аденозиновых А 2b рецепторов человека Процедура связывания: инкубируют 20,8 мкг мембран (человеческие аденозиновые рецепторы А 2b,трансфецированные в клетки НЕK-293, источник: Receptor Biology, Inc.), буфер (50 мМ трис-HCl, 10 мМ(5'-Nэтилкарбоксамидоаденозина) для определения неспецифического связывания тестируемого соединения,в общем объеме 100 мкл в течение 30 мин при комнатной температуре. Фильтруют в вакууме 25 мм рт. ст. через фильтры из стекловолокна от Whatman GF/C (предварительно погруженные в 0,5% полиэтиленимин на 3 ч), промывают (4x1 мл) ледяным 50 мМ трис-HCl (рН 6,5) на 96-луночном коллекторе клеток(Brandel Cell Harvester). Определение активности: в присутствии 200 мкл смеси HiSafe-3 в счетчике излучения (1450 Microbeta, Wallac). Ингибирование [%]=100-активность в присутствии тестируемого соединения -неспецифическая активность)/(общая активность - неспецифическая активность 100. Результаты Авторы считают соединения биологически активными, если они ингибируют связывание радиолиганда на аденозиновых A3 рецепторах человека с активностью свыше 80% при 1 мкМ в условиях проводимых ими экспериментов. Константу диссоциации (Kd) [125I] AB-MECA на препарате мембран CHO-hA3 определяют изучением изотопной насыщенности с помощью анализа Скатчарда (G. Scatchard, Ann. N. Y. Acad. Sci. 51:660,1949). ИК 50 (IC50) переводят в константу аффинности (Ki), применяя уравнение Ченга-Прусоффа (Y.J.Cheng and W.H. Prusoff, Biochem. Pharmacol. 22:3099, 1973). Несколько соединений общей формулы (I), (II), (III), (IV) и (V) проявляют поразительные биологические эффекты. Соединения общей формулы (I), определенные в пп.1-3 формулы изобретения, обладают самой высокой активностью. Особенно предпочтительными являются соединения, приведенные в примерах, их значения Ki составляют от 0,8 до 700 нМ. Значения Ki наиболее полезных соединений составляют 0,8 и 15 нМ. Соединения обладают необходимой биодоступностью и селективностью по меньшей мере третьего порядка в отношении аденозиновых Ai, A2a и А 2b подтипов рецепторов человека. Кроме того, продолжительность действия при внутривенном и пероральном введении достаточно велика, значения ED50 низкие, токсикологический профиль и данные о побочном действии дают преимущества указанным соединениям. Приведенные выше данные способствуют применению соединений общей формулы (I) для терапевтических целей. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Соединения общей формулы (I) где R1 обозначает атом водорода или неразветвленную или разветвленную C1-4 алкильную группу;R2 - атом водорода или неразветвленную или разветвленную C1-4 алкильную группу;R3 - атом водорода или неразветвленную или разветвленную C1-4 алкильную группу, С 3-6 циклоалкильную группу, фенильную, тиенильную или фурильную группу, необязательно замещенную одной или несколькими неразветвленными или разветвленными C1-4 алкильными группами, неразветвленными или разветвленными C1-4 алкоксигруппами или атомом галогена; или обозначает шести- или пятичленный гетероароматический цикл, содержащий один, два или три атома азота, или пятичленный гетероароматический цикл, содержащий один атом азота и один атом кислорода, или один атом азота и один атом серы,необязательно замещенный одной или несколькими неразветвленными или разветвленными C1-4 алкильными группами, неразветвленными или разветвленными C1-4 алкоксигруппами, или атомом галогена;R4, R5, R6 и R7 независимо обозначают атом водорода, неразветвленную или разветвленную C1-4 алкильную группу, неразветвленную или разветвленную C1-4 алкоксигруппу, гидроксильную группу или атом галогена, или R4 и R7 обозначают атом водорода и R5 и R6 вместе образуют метилендиоксигруппу;R8 обозначает атом водорода или цианогруппу, аминокарбонильную группу, C1-4 алкоксикарбонильную группу, карбоксильную группу;R9 и R10 независимо друг от друга обозначают атом водорода, неразветвленную или разветвленнуюX обозначает -СН 2-группу, -NH-группу, -NR11-группу или атом серы, атом кислорода, сульфогруппу или сульфоксигруппу, где R11 обозначает неразветвленную или разветвленную C1-4 алкильную группу или С 3-6 циклоалкильную группу;Z обозначает атом кислорода, атом серы, -NH-группу или -NR12-группу, где R12 обозначает неразветвленную или разветвленную C1-4 алкильную группу или С 3-6 циклоалкильную группу;m равно нулю, 1, 2 или 3; о равно нулю, 1, 2 или 3; р равно нулю или 1;r равно нулю или 1, при условии, что по меньшей мере один из m и о отличен от нуля,и их соли, сольваты и изомеры, а также соли и сольваты изомеров. 2. Соединения общей формулы (I) по п.1 где R1 обозначает атом водорода или неразветвленную или разветвленную C1-4 алкильную группу;R2 - атом водорода или неразветвленную или разветвленную C1-4 алкильную группу;R3 - атом водорода или неразветвленную или разветвленную C1-4 алкильную группу, С 3-6 циклоалкильную группу, фенильную, тиенильную или фурильную группу, необязательно замещенную одной или несколькими неразветвленными или разветвленными С 1-4 алкильными группами, неразветвленными или- 17007595 разветвленными C1-4 алкоксигруппами или атомом галогена;R4, R5, R6 и R7 независимо друг от друга обозначают атом водорода, неразветвленную или разветвленную C1-4 алкильную группу, неразветвленную или разветвленную C1-4 алкоксигруппу, гидроксильную группу или атом галогена, или R4 и R7 обозначают атом водорода и R5 и R6 вместе образуют метилендиоксигруппу;R8 обозначает атом водорода или цианогруппу, аминокарбонильную группу, C1-4 алкоксикарбонильную группу, карбоксильную группу;R9 и R10 независимо друг от друга обозначают атом водорода, неразветвленную или разветвленнуюX обозначает -СН 2-группу, -NH-группу, -NR11-группу или атом серы, атом кислорода, сульфогруппу или сульфоксигруппу, где R11 обозначает неразветвленную или разветвленную C1-4 алкильную группу или С 3-6 циклоалкильную группу;Z обозначает атом кислорода, атом серы, -NH-группу или -NR12-группу, где R12 обозначает неразветвленную или разветвленную C1-4 алкильную группу или С 3-6 циклоалкильную группу;m равно нулю, 1, 2 или 3; о равно нулю, 1, 2 или 3; р равно нулю или 1;r равно нулю или 1, при условии, что по меньшей мере один из m и о отличен от нуля,и их соли, сольваты и изомеры, а также соли и сольваты изомеров. 3. Соединения общей формулы (I) по пп.1 и 2 где R1 обозначает атом водорода или метильную группу;R2 - атом водорода или метильную группу;R3 - фенильную, тиенильную или фурильную группу;R4, R5, R6 и R7 независимо друг от друга обозначают атом водорода, неразветвленную или разветвленную C1-4 алкильную группу, неразветвленную или разветвленную C1-4 алкоксигруппу, гидроксильную группу или атом галогена; илиR4 и R7 обозначают атом водорода и R5 и R6 вместе образуют метилендиоксигруппу;R8 - атом водорода или цианогруппу;R9 и R10 обозначают атом водорода, метильную, этильную или циклопропильную группу;Z обозначает атом кислорода, атом серы, -NH-группу или -NR12-группу, где R12 обозначает неразветвленную или разветвленную C1-4 алкильную группу или С 3-6 циклоалкильную группу; и- 18007595 5. Способ получения соединений общей формулы (I) и их солей, сольватов и изомеров,где R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, X, Z, n, m, о, р и r такие, как указано в п.1, отличающийся тем, что соединение общей формулы (VIII) где R9, R10, Z, m, о, р и r такие, как указано в п.1, ацилируют кислотой или реакционноспособным производным кислоты общей формулы (II) где R1, R2, R3, R4, R5, R6, R7, R8, X и n такие, как указано в п.1, и, если требуется, заместители полученного соединения общей формулы (I) известными способами преобразуют друг в друга, и/или соединение общей формулы (I) переводят в его соль или сольват, или выделяют из его соли или сольвата,и/или разделяют его на оптически активные изомеры, или оптически активный изомер преобразуют в рацемическое соединение. 6. Способ по п.5, отличающийся тем, что ацилирование проводят в присутствии основания в органическом растворителе. 7. Способ по пп.5 и 6, отличающийся тем, что реакционноспособное производное кислоты общей формулы (I) представляет собой соответствующий галогенангидрид кислоты или смешанный ангидрид. 8. Способ по пп.5-7, отличающийся тем, что органический растворитель представляет собой галогенированный углеводород, предпочтительно хлороформ. 9. Способ по пп.5-8, отличающийся тем, что основание представляет собой органическое основание, предпочтительно триэтиламин. 10. Фармацевтическая композиция, отличающаяся тем, что содержит одно или несколько соединений общей формулы (I) где R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, X, Z, n, m, о, р и r такие, как указано в п.1; и/или их соли,сольваты, изомеры, соли и сольваты изомеров и одно или несколько вспомогательных веществ, обычно используемых в фармацевтической промышленности. 11. Фармацевтическая композиция по п.10, отличающаяся тем, что в качестве активного вещества она содержит одно или несколько соединений, указанных в п.3. 12. Применение соединений общей формулы (I) где R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, X, Z, n, m, о, р и r такие, как указано в п.1; для лечения патологий, где A3 рецептор участвует в развитии заболевания. 13. Применение соединений общей формулы (I) где R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, X, Z, n, m, о, р и r имеют такие значения, как указано в п.1; в качестве лигандов А 3 рецепторов в случае нарушений деятельности сердца, почек, дыхательной системы и центральной нервной системы, для ингибирования защитного действия аденозина на растущие опухолевые клетки, предотвращения дегрануляции тучных клеток, для ингибирования образования цитокинов,понижения внутриглазного давления, для ингибирования выделения TNF, для затруднения миграции эозинофильных и нейтрофильных гранулоцитов и других клеток зоны воспаления, для ингибирования сужения трахеи и для затруднения инфильтрации плазмы крови через кровеносный сосуд. 14. Применение соединений общей формулы (I) где R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, X, Z, n, m, о, р и r имеют такие значения, как указано в п.1; в качестве антагонистов А 3 рецепторов, в качестве активных ингредиентов противовоспалительных, противоастматических, противоишемических, антидепрессивных, антиаритмических, защищающих функции почек, предупреждающих возникновение опухолей, активных против болезни Паркинсона или усиливающих когнитивные способности фармацевтических композиций, и в качестве активных компонентов композиций, которые можно применять для лечения или профилактики следующих заболеваний: реперфузионного повреждения сердечной мышцы, хронических обструктивных заболеваний легких(COPD), респираторного дисстресс-синдрома у взрослых (ARDS), включая хронический бронхит, эмфизему легких или одышку, аллергических реакций (например, ринита, реакций, вызванных растением сумах, уртикарной сыпи, склеродермы, артрита), других аутоиммунных болезней, воспалительных заболеваний кишечника, болезни Аддисона, болезни Крона, псориаза, заболевания суставов, гипертонии, аномальных неврологических функций, глаукомы и диабета. 15. Применение соединений общей формулы (I) где R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, X, Z, n, m, о, р и r имеют такие значения, как указано в п.1; в качестве активных компонентов для лечения патологий, таких как астма, COPD и ARDS, глаукома, опухоли, аллергические и воспалительные заболевания, ишемия, гипоксия, сердечная аритмия и заболевания почек.
МПК / Метки
МПК: A61P 29/00, C07D 471/04, A61P 17/00, C07D 235/00, A61P 13/12, A61P 3/00, A61K 31/415, A61P 11/00, A61P 35/00, A61P 9/00, A61P 25/00
Метки: аденозиновых, лигандов, качестве, имидазохинолина, производные, рецепторов
Код ссылки
<a href="https://eas.patents.su/22-7595-proizvodnye-imidazohinolina-v-kachestve-ligandov-adenozinovyh-a3-receptorov.html" rel="bookmark" title="База патентов Евразийского Союза">Производные имидазохинолина в качестве лигандов аденозиновых а3 рецепторов</a>
Предыдущий патент: Конструкция катетера и области ее применения
Следующий патент: Кристаллическая натриевая соль телмисартана и её применение в качестве антагониста ангиотензина
Случайный патент: Способ ингибирования резорбции костей












