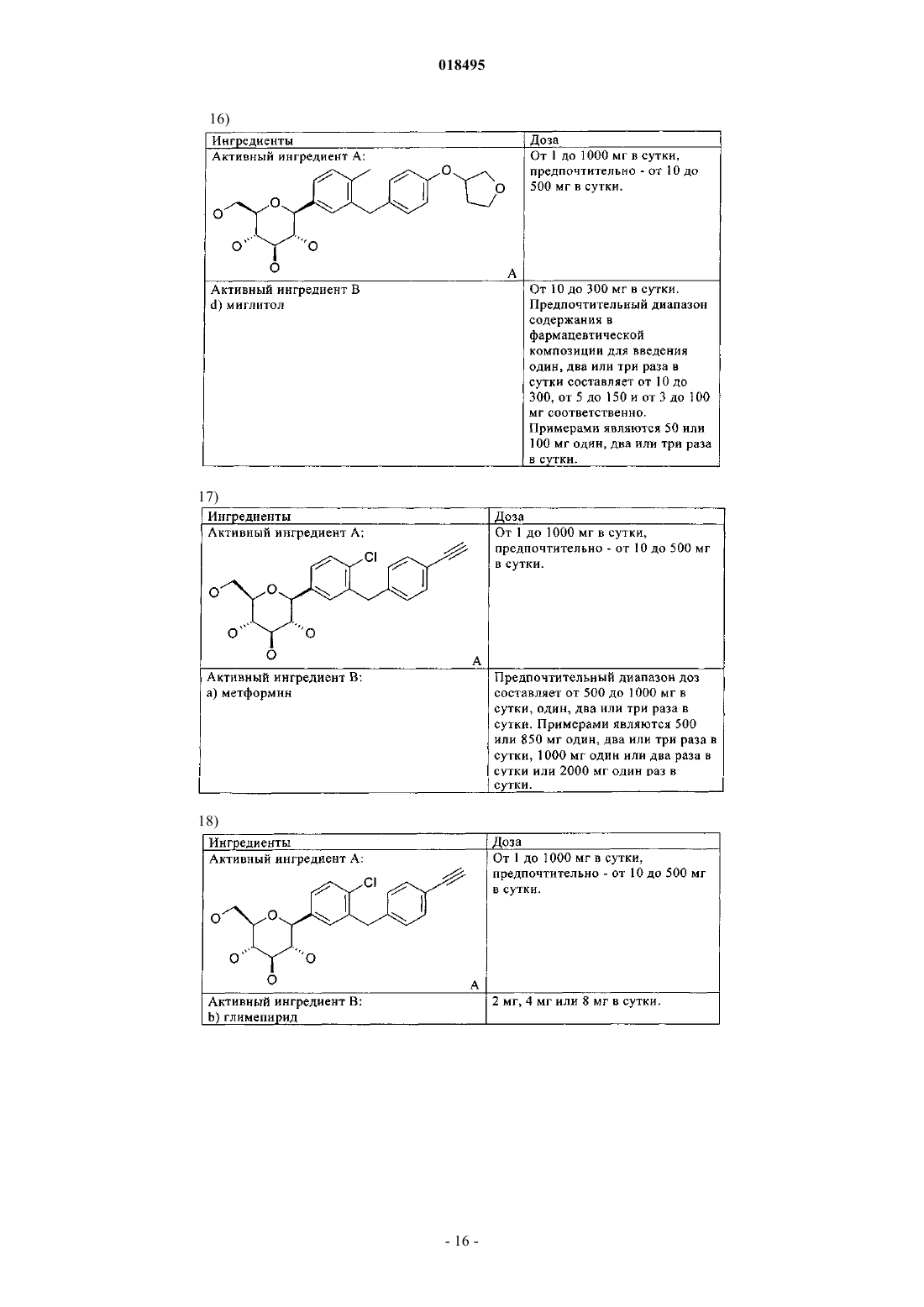
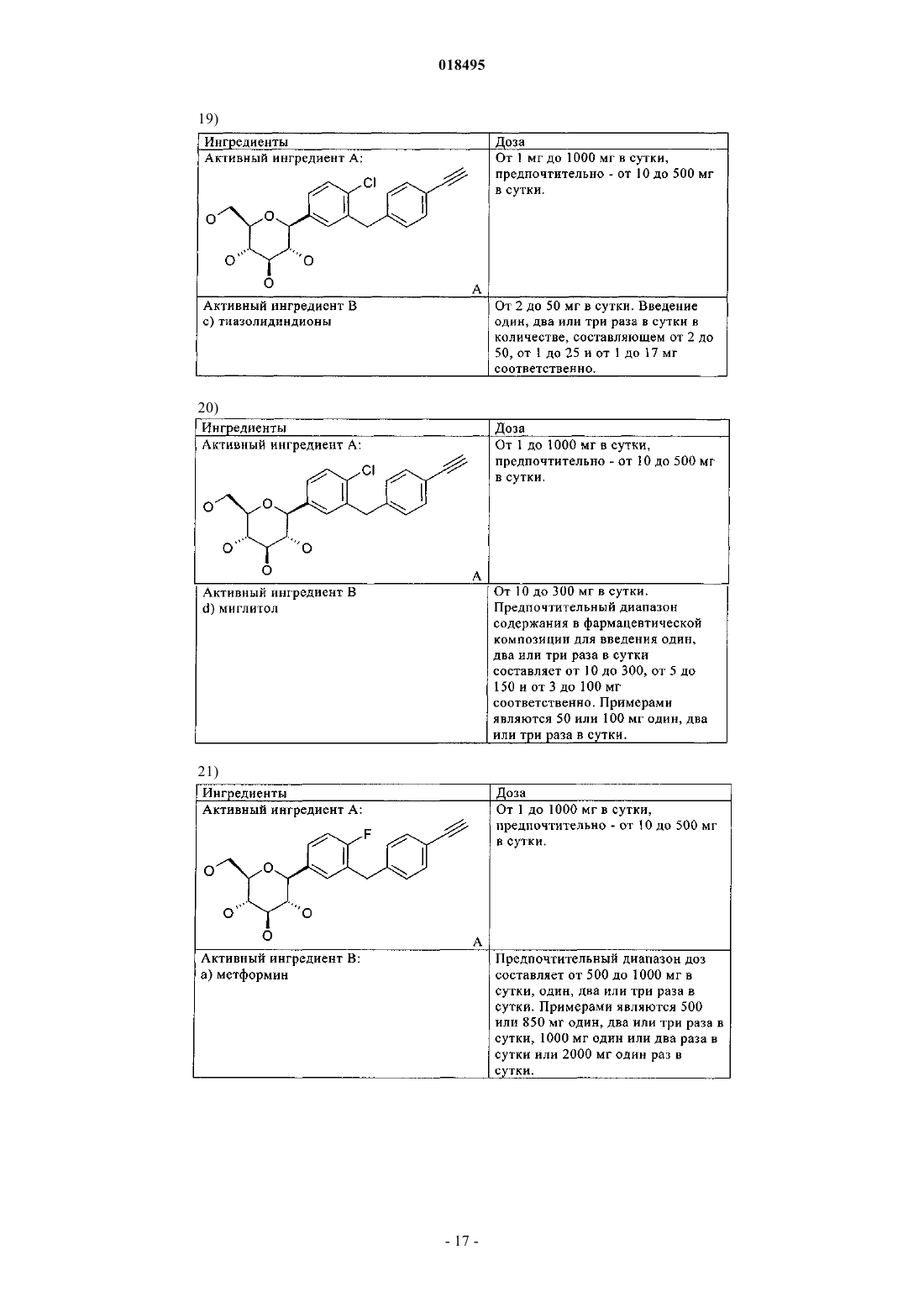
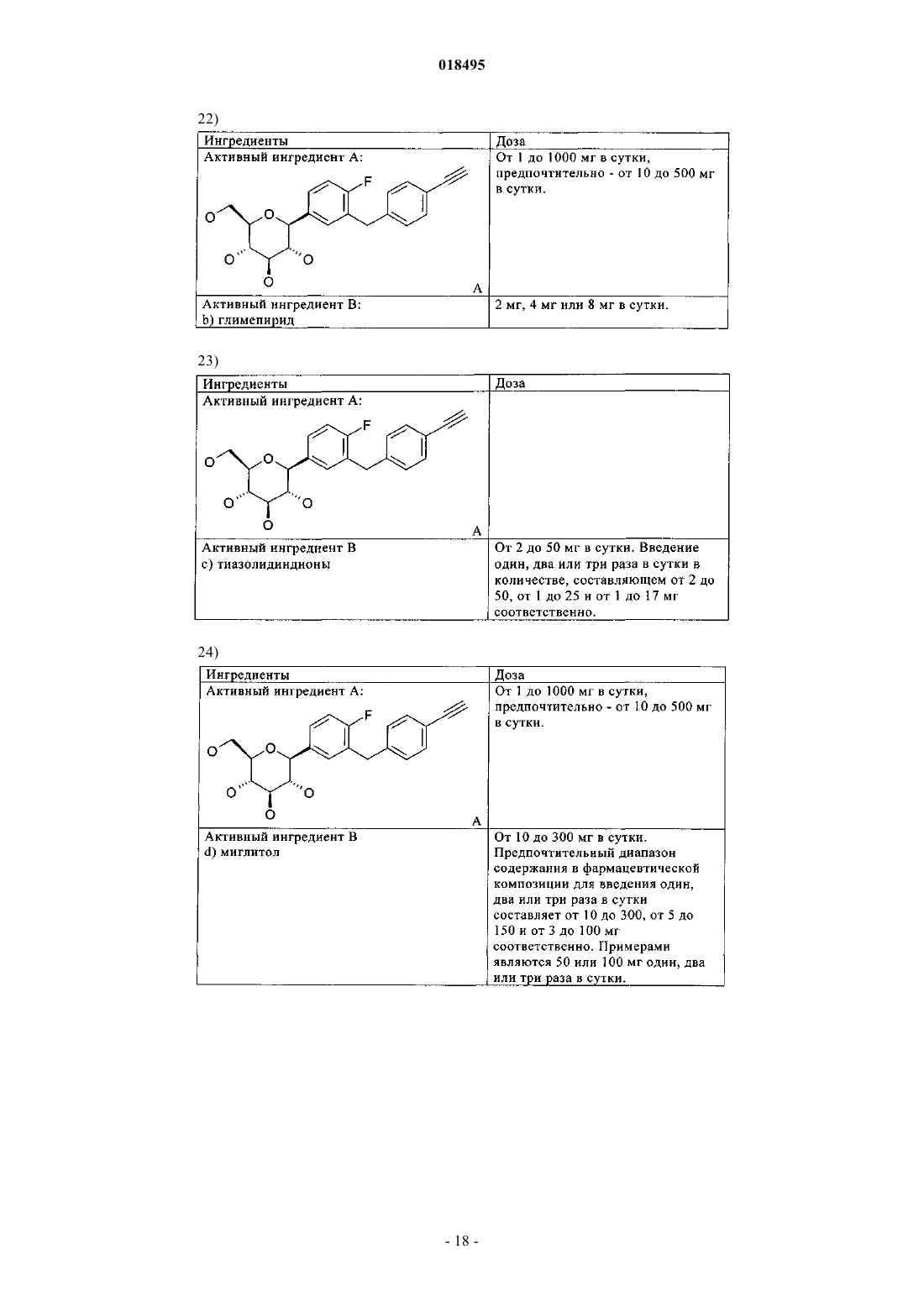
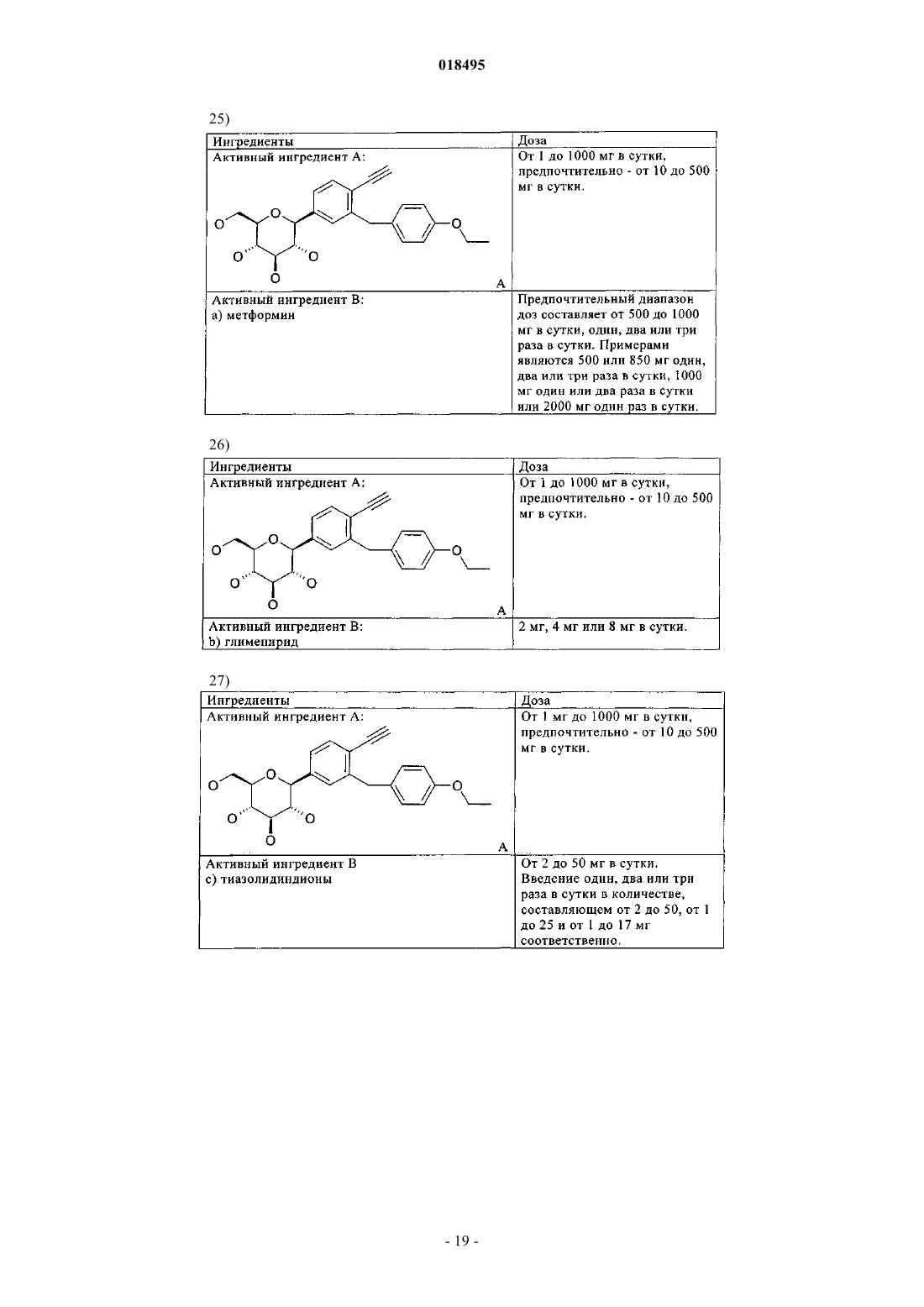
Комбинированное лечение ингибиторами sglt-2 (натрийзависимый сопереносчик глюкозы 2) и содержащими их фармацевтическими композициями
Номер патента: 18495
Опубликовано: 30.08.2013
Авторы: Томас Лео, Айккельманн Петер, Манучехри Алиреза, Дуги Клаус
Формула / Реферат
1. Фармацевтическая композиция, включающая ингибитор НЗСГ-2 (натрийзависимый сопереносчик глюкозы 2) в комбинации со вторым терапевтическим средством, которое применимо для лечения одного или большего количества метаболических нарушений, в которой:
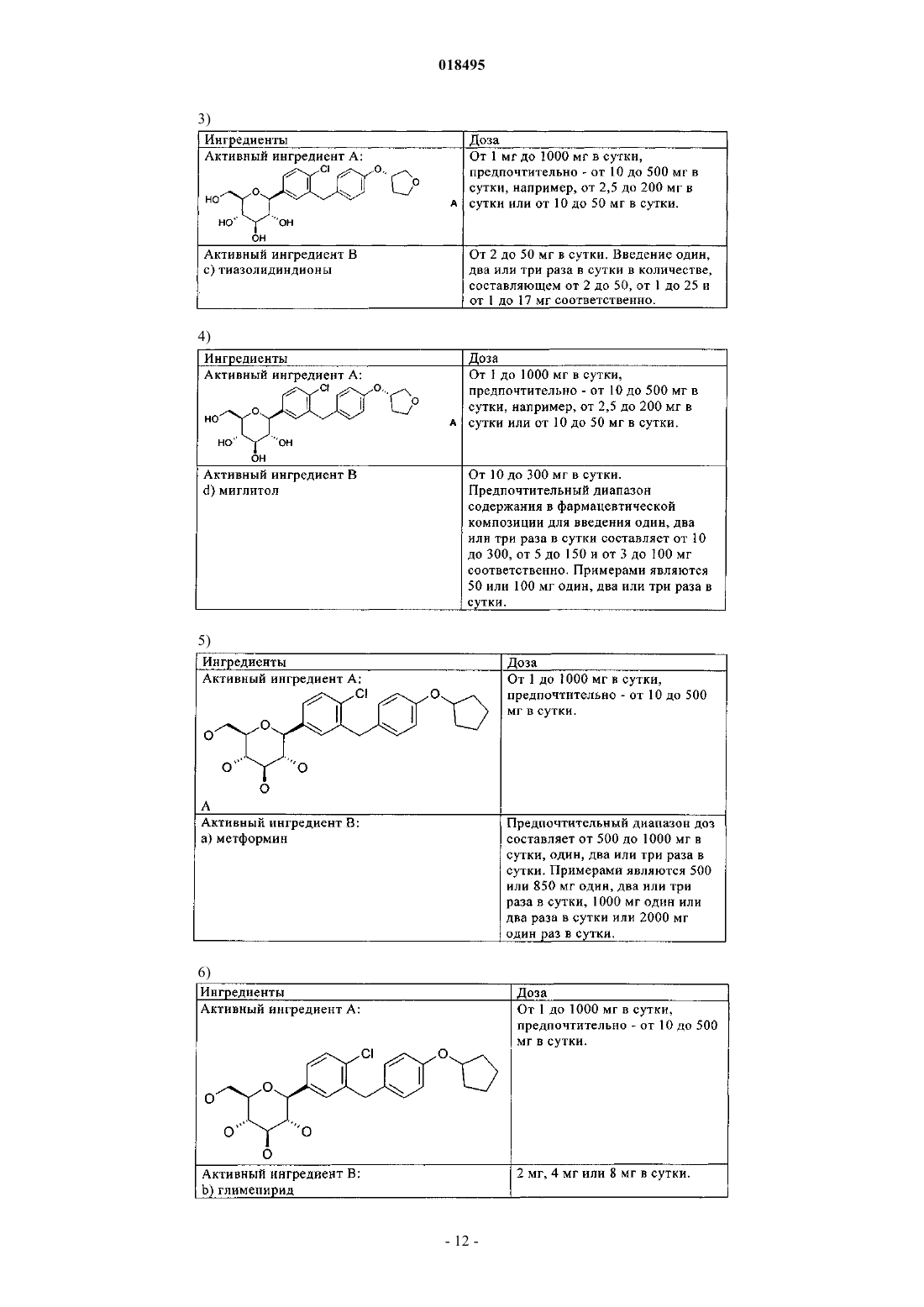
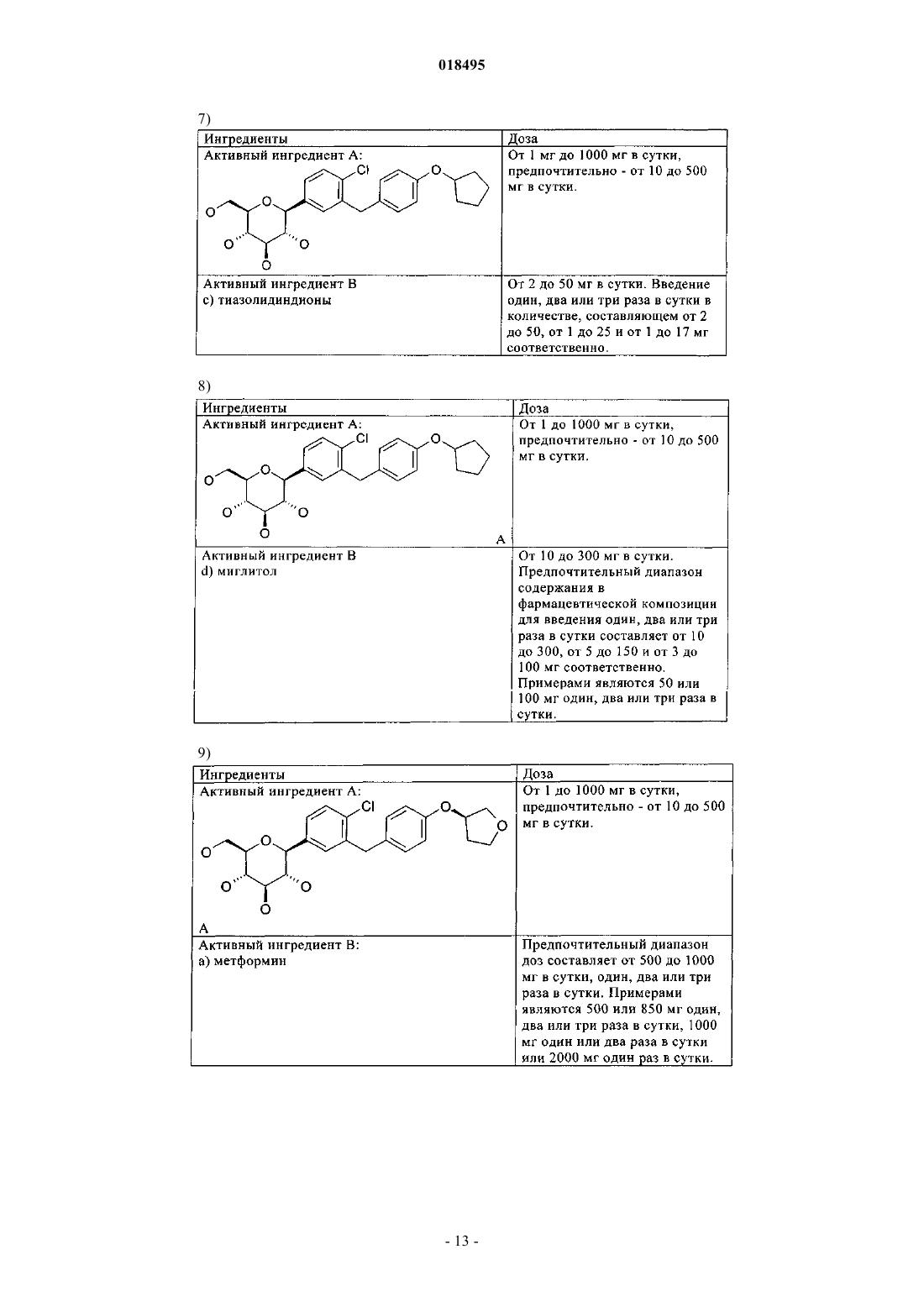
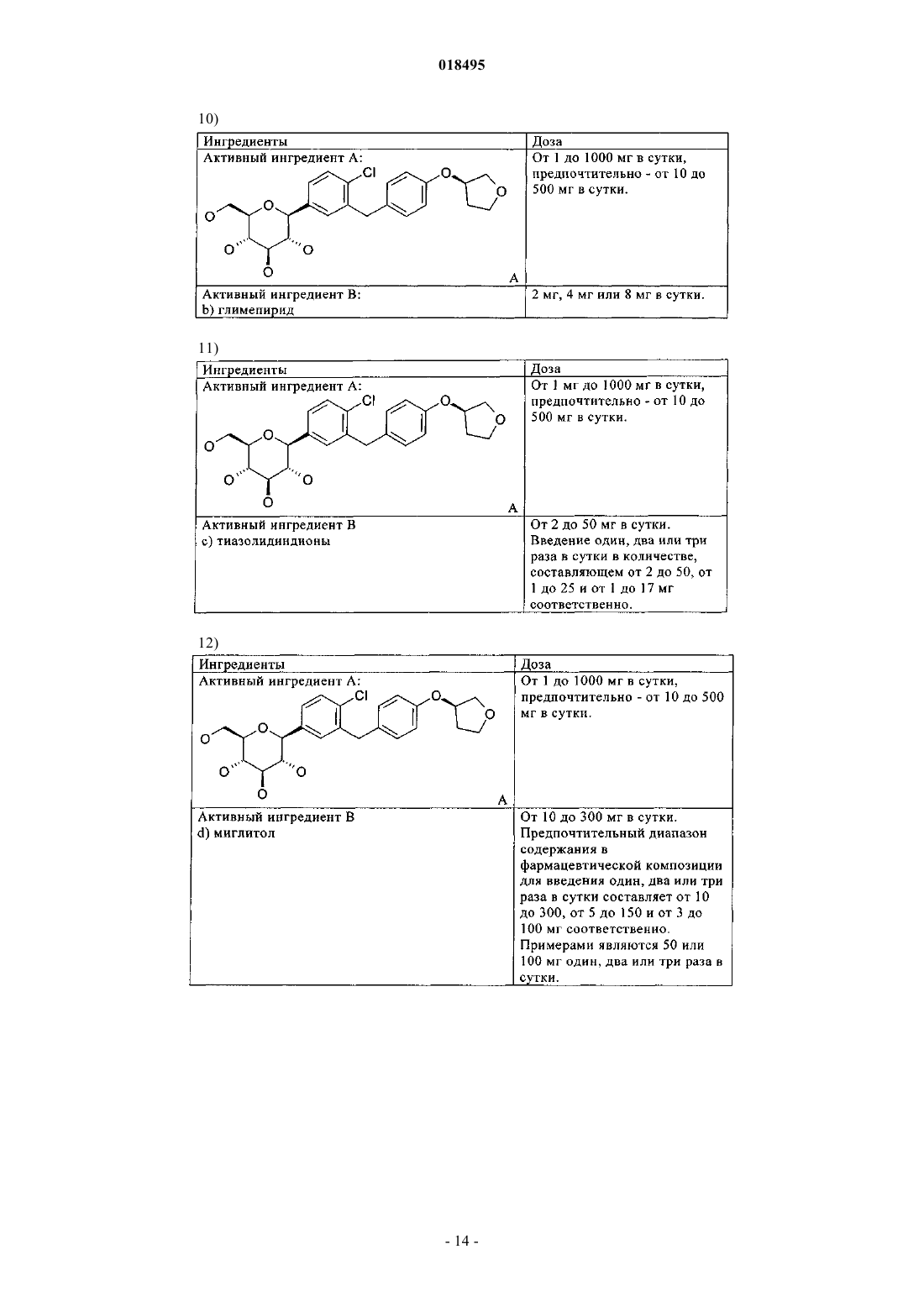
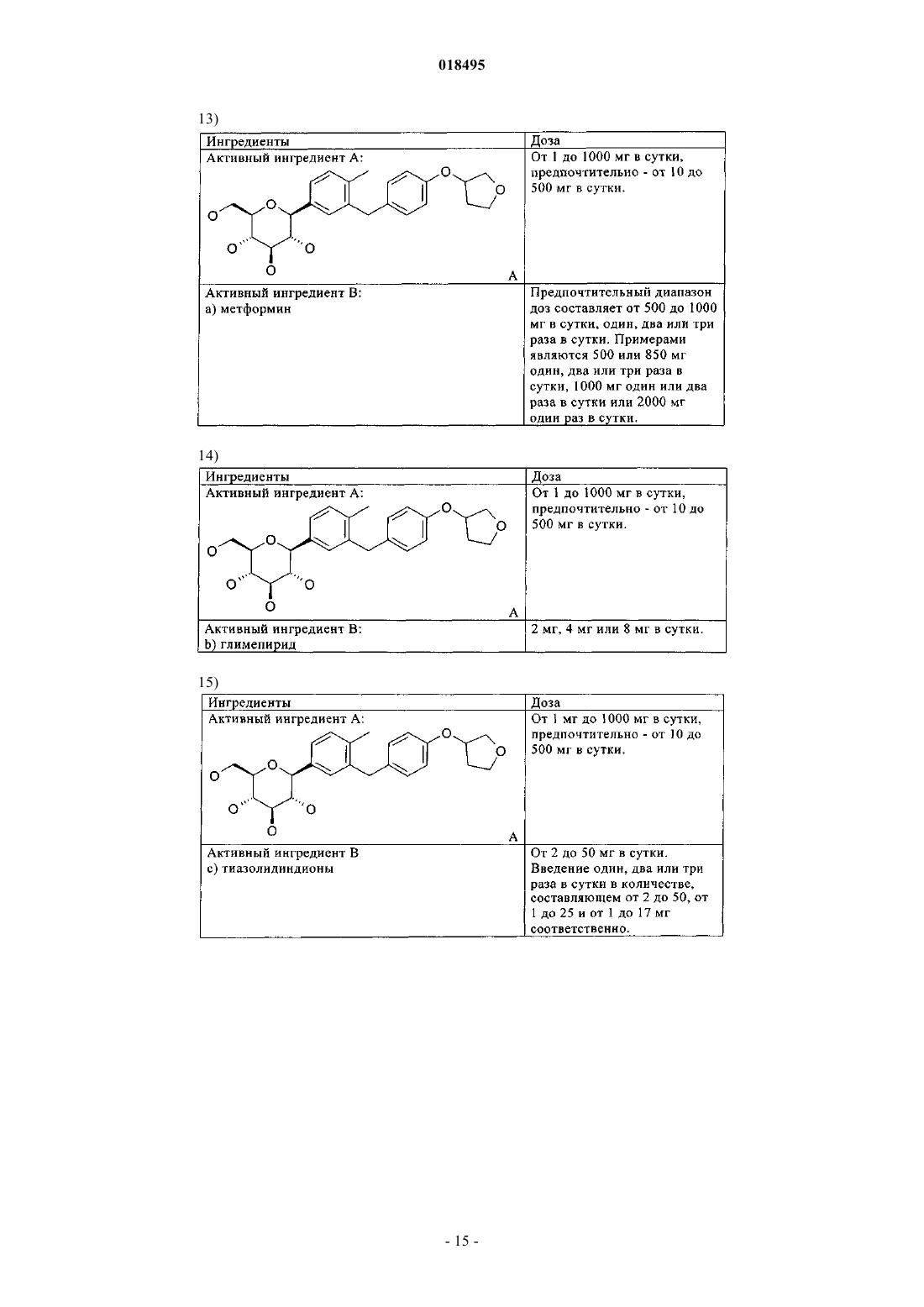
i) указанный ингибитор НЗСГ-2 представляет собой глюкопиранозилзамещенное производное бензола - 1-хлор-4-(β-D-глюкопираноз-1-ил)-2-[4-((S)-тетрагидрофуран-3-илокси)бензил]бензол;
ii) указанное второе терапевтическое средство, которое применимо для лечения одного или большего количества метаболических нарушений, представляет собой метформин.
2. Способ лечения или предупреждения метаболического нарушения, включающий введение нуждающемуся в нем пациенту фармацевтической композиции по п.1.
3. Способ по п.2, в котором соединение-ингибитор НЗСГ-2 1-хлор-4-(β-D-глюкопираноз-1-ил)-2-[4-((S)-тетрагидрофуран-3-илокси)бензил]бензол и второе терапевтическое средство метформин содержатся в одной дозированной форме.
4. Способ по п.2, в котором соединение-ингибитор НЗСГ-2 1-хлор-4-(β-D-глюкопираноз-1-ил)-2-[4-((S)-тетрагидрофуран-3-илокси)бензил]бензол и второе терапевтическое средство метформин содержатся каждое в отдельной дозированной форме.
5. Способ по любому из пп.2-4, характеризующийся дозировкой от 500 до 1000 мг метформина.
6. Способ по любому из пп.2-5, характеризующийся дозировкой от 1 до 100 мг указанного соединения-ингибитора НЗСГ-2.
7. Применение фармацевтической композиции, включающей соединение-ингибитор НЗСГ-2 в комбинации со вторым терапевтическим средством по п.1, для приготовления лекарственного средства, предназначенного для лечения или предупреждения метаболического нарушения посредством введения нуждающемуся в нем пациенту указанной фармацевтической композиции.
8. Применение по п.7, в котором указанное метаболическое нарушение выбрано из группы, включающей сахарный диабет типа 1, сахарный диабет типа 2, нарушенную переносимость глюкозы, гипергликемию, гипергликемию после приема пищи, избыточную массу тела, ожирение, включая ожирение класса I, ожирение класса II, ожирение класса III, висцеральное ожирение и абдоминальное ожирение, и метаболический синдром.
9. Применение по п.8, в котором указанное метаболическое нарушение представляет собой сахарный диабет типа 2.
10. Применение по пп.7, 8 или 9, в котором указанное соединение-ингибитор НЗСГ-2 и указанное терапевтическое средство вводят в одной фармацевтической композиции.
11. Применение 1-хлор-4-(β-D-глюкопираноз-1-ил)-2-[4-((S)-тетрагидрофуран-3-илокси)бензил]бензола для приготовления фармацевтической композиции по п.1 для использования в способе лечения метаболического нарушения, которое выбрано из группы, включающей сахарный диабет типа 1, сахарный диабет типа 2, нарушенную переносимость глюкозы, гипергликемию, гипергликемию после приема пищи, избыточную массу тела, ожирение, включая ожирение класса I, ожирение класса II, ожирение класса III, висцеральное ожирение и абдоминальное ожирение, и метаболический синдром.
12. Применение по п.11, в котором указанное метаболическое нарушение представляет собой сахарный диабет типа 2.
13. Применение второго терапевтического средства, определенного в п.1, для приготовления фармацевтической композиции по п.1 для использования в способе лечения метаболического нарушения, которое выбрано из группы, включающей сахарный диабет типа 1, сахарный диабет типа 2, нарушенную переносимость глюкозы, гипергликемию, гипергликемию после приема пищи, избыточную массу тела, ожирение, включая ожирение класса I, ожирение класса II, ожирение класса III, висцеральное ожирение и абдоминальное ожирение, и метаболический синдром.
14. Применение по п.13, в котором указанное метаболическое нарушение представляет собой сахарный диабет типа 2.
Текст
КОМБИНИРОВАННОЕ ЛЕЧЕНИЕ ИНГИБИТОРАМИ SGLT-2 (НАТРИЙЗАВИСИМЫЙ СОПЕРЕНОСЧИК ГЛЮКОЗЫ 2) И СОДЕРЖАЩИМИ ИХ ФАРМАЦЕВТИЧЕСКИМИ КОМПОЗИЦИЯМИ В изобретении описана фармацевтическая композиция, включающая ингибитор НЗСГ-2(натрийзависимый сопереносчик глюкозы 2) в комбинации со вторым терапевтическим средством,которое применимо для лечения одного или большего количества метаболических нарушений,выбранных из группы, включающей сахарный диабет типа 1, сахарный диабет типа 2, нарушенную переносимость глюкозы, гипергликемию, гипергликемию после приема пищи, избыточную массу тела, ожирение, включая ожирение класса I, ожирение класса II, ожирение класса III, висцеральное ожирение и абдоминальное ожирение, и метаболический синдром.(71)(73) Заявитель и патентовладелец: БРИНГЕР ИНГЕЛЬХАЙМ ИНТЕРНАЦИОНАЛЬ ГМБХ (DE) Область техники, к которой относится изобретение Настоящее изобретение относится к ингибиторам натрийзависимого сопереносчика глюкозы 2(НЗСГ-2) в комбинации с другими активными ингредиентами, к их фармацевтическим композициям, к способам их получения и к их применению для лечения метаболических заболеваний, таких как сахарный диабет типа 1, сахарный диабет типа 2, нарушенная переносимость глюкозы, гипергликемия и родственные заболевания. Уровень техники Метаболические заболевания и связанные с ними нарушения распространяются во все большей степени. В частности, сахарный диабет типа 2 (СДТ 2) - метаболическое заболевание, распространяющееся во все большей степени, что обусловлено высокой частотой осложнений, приводящих к значительному уменьшению средней продолжительности жизни. Вследствие связанных с диабетом осложнений,влияющих на капилляры, в настоящее время в промышленно-развитых странах диабет типа 2 является самой частой причиной ухудшения зрения у взрослых, почечной недостаточности и ампутации. Кроме того, наличие диабета типа 2 связывают с 2-5-кратным увеличением опасности сердечно-сосудистых заболеваний. Большинство имеющихся пероральных антидиабетических средств, которые имеются время в продаже или проходят последнюю стадию клинических исследований, преимущественно предназначены для одного из следующих типов воздействия: снижение эндогенной выработки глюкозы в печени: бигуаниды (например, метформин); стимулирование выработки инсулина -клетками, которые еще продолжают функционировать: сульфонилмочевины, меглитиниды; уменьшение периферической резистентности к инсулину: тиазолидиндионы (ТАД); задержка всасывания глюкозы в кишечнике: ингибиторы -глюкозидазы; стимулирование зависимой от глюкозы выработки инсулина, подавление повышенных уровней глюкагона и задержка опорожнения желудка: миметики инкретина (например, экзенатид), аналоги амилина (например, прамлинтид), ингибиторы дипептидилпептидазы IV (например, ситаглиптин). Несмотря на различные типы воздействия, первые три класса веществ в значительной степени сходны по эффективности гликемического контроля (равное 1,0-1,5% абсолютное уменьшение содержанияHbA1c, если среднее базовое значение составляет 8,0%). Однако поскольку типы их воздействия различны, они пригодны для комбинированного лечения. Эффективность специфических ингибиторов всасывания глюкозы (ингибиторы кишечной глюкозидазы, прототип - акарбоза) для гликемического контроля меньше, чем при воздействии средств других типов. Почечная фильтрация и повторное поглощение глюкозы наряду с другими механизмами способствуют поддержанию стационарной концентрации глюкозы в плазме и поэтому могут являться объектами антидиабетического воздействия. Повторное поглощение фильтрованной глюкозы через клетки эпителия почек протекает с помощью натрийзависимых сопереносчиков глюкозы (НЗСГ), расположенных на кисточковой кайме мембран в проксимальных канальцах вдоль градиента натрия (1). Существуют по меньшей мере 3 изоформы НЗСГ, которые различаются по своим характеристикам экспрессии, а также по физико-химическим характеристикам (2). НЗСГ 2 экспрессируется только в почках (3), тогда как НЗСГ 1 дополнительно экспрессируется в других тканях, таких как кишечник, ободочная кишка, скелетные и сердечные мышцы (4, 5). Обнаружено, что НЗСГ 3 является сенсором глюкозы в интерстициальных клетках кишечника и не участвуют в переносе (6). Повторному поглощению глюкозы в почках могут способствовать другие родственные, но пока не охарактеризованные гены (7, 8, 9). При нормогликемии глюкоза полностью повторно поглощается в почках с помощью НЗСГ и способность почек повторно поглощать насыщается при концентрациях глюкозы, превышающих 10 мМ, что приводит к глюкозурии ("сахарный диабет"). Эту пороговую концентрацию можно повысить путем ингибирования НЗСГ 2. В экспериментах с ингибитором НЗСГ флоризином показано, что ингибирование НЗСГ частично подавляет обратное поглощение глюкозы из гломерулярного фильтрата в кровь, что приводит к снижению концентрации глюкозы в крови и к глюкозурии (10, 11).(11) Gouvea, W.L. (1989), Kidney Int. 35(4): 1041-1048. Диабет типа 2 является все чаще встречающимся заболеванием, которое вследствие очень частых осложнений приводит к значительному уменьшению средней продолжительности жизни. Вследствие связанных с диабетом осложнений, влияющих на капилляры, в настоящее время в промышленно развитых странах диабет типа 2 является самой частой причиной ухудшения зрения у взрослых, почечной недостаточности и ампутации. Кроме того, наличие диабета типа 2 связывают с 2-5-кратным увеличением опасности сердечно-сосудистых заболеваний. При длительном протекании заболевания для большинства пациентов, страдающих диабетом типа 2, пероральное лечение становится недостаточным и они становятся зависимыми от инсулина и им необходимо ежедневно делать инъекции и несколько раз в сутки определять концентрацию глюкозы для подбора дозы инсулина. Проведенное в Великобритании проспективное исследование диабета показало, что интенсивное лечение метформином, сульфонилмочевинами или инсулином приводит лишь к ограниченному улучшению гликемического контроля (различия содержания HbA1c 0,9%). Кроме того, даже у пациентов, подвергающихся интенсивному лечению, гликемический контроль значительно ухудшается во времени, и это было приписано нарушению функций -клеток. Существенно, что интенсивное лечение не приводит к значительному уменьшению количества осложнений, влияющих на крупные сосуды, т.е. сердечнососудистых нарушений. В US 20050209166 ( 11/080150) описаны новые глюкопиранозилзамещенные фенилпроизводные. Глюкопиранозилзамещенные производные применимы для лечения метаболических заболеваний. Глюкопиранозилоксизамещенные ароматические группы и их получение, и их возможная активность в качестве ингибиторов НЗСГ-2 известны из опубликованных международные заявок WO 98/31697,WO 01/27128, WO 02/083066, WO 03/099836, WO 2004/063209, WO 2004/080990, WO 2004/013118,WO 2004/052902, WO 2004/052903 и заявки US 2003/0114390, содержание которые включено в настоящее изобретение в качестве ссылки. Поэтому наблюдается нехватка способов, лекарственных средств и фармацевтических композиций,эффективных для гликемического контроля, улучшающих протекание заболевания и снижающих заболеваемость и смертность от сердечно-сосудистых заболеваний. Краткое изложение сущности изобретения Настоящее изобретение относится к фармацевтической композиции, включающей один или большее количество ингибиторов НЗСГ-2 в комбинации с одним или большим количеством терапевтических средств, которые применимы для лечения метаболических нарушений. В более предпочтительном варианте осуществления настоящее изобретение относится к фармацевтической композиции, в которой ингибитором является активный ингредиент А, описанный в настоящем изобретении, в комбинации с активным ингредиентом В, описанным в настоящем изобретении, предназначенной для лечения метаболических нарушений. В другом варианте осуществления настоящего изобретения метаболическое нарушение выбрано из группы, включающей сахарный диабет типа 1, сахарный диабет типа 2, нарушенную переносимость глюкозы, гипергликемию, гипергликемию после приема пищи, избыточную массу тела, ожирение, включая ожирение класса I, ожирение класса II, ожирение класса III, висцеральное ожирение, абдоминальное ожирение и метаболический синдром. Активные ингредиенты можно вводить в одной фармацевтической композиции или вводить по отдельности. В одном варианте осуществления фармацевтическая композиция, предлагаемая в настоящем изобретении, применима для комбинированного, или одновременного, или последовательного применения одного или большего количества ингибиторов НЗСГ-2 и одного или большего количества дополнительных терапевтических средств. В одном варианте осуществления один или большее количество ингибиторов НЗСГ-2 и одно или большее количество дополнительных терапевтических средств содержатся в одной дозированной форме. В другом варианте осуществления один или большее количество ингибиторов НЗСГ-2 и одно или большее количество дополнительных терапевтических средств содержатся каждое в отдельной дозированной форме. Настоящее изобретение также относится к композиции, включающей глюкопиранозилзамещенное фенилпроизводное,включающее 1-хлор-4-(-D-глюкопираноз-1-ил)-2-[4-S)-тетрагидрофуран-3 илокси)бензил]бензол или его пролекарство, в котором одна или большее количество гидроксигрупп D-глюкопиранозильной группы ацилированы группами, выбранными из группы, включающей (C1-C3 алкил)карбонил, (C1-C6-алкил)оксикарбонил, фенилкарбонил, фенил(C1-C3-алкил)карбонил, фенилоксикарбонил и фенил(C1-C3-алкил)оксикарбонил, или его фармацевтически приемлемую соль; в комбинации по меньшей мере с одним дополнительным терапевтическим средством, которое применимо для лечения или предупреждения одного или большего количества нарушений, выбранных из группы, включающей сахарный диабет типа 1, сахарный диабет типа 2, нарушенную переносимость глюкозы и гипергликемию. Настоящее изобретение также относится к способам лечения и предупреждения метаболических нарушений с применением фармацевтических композиций, предлагаемых в настоящем изобретении. Настоящее изобретение также относится к способу лечения метаболического заболевания, выбранного из группы, включающей сахарный диабет типа 1, сахарный диабет типа 2, нарушенную переносимость глюкозы, гипергликемию, гипергликемию после приема пищи, избыточную массу тела, ожирение,включая ожирение класса I, ожирение класса II, ожирение класса III, висцеральное ожирение и абдоминальное ожирение, и метаболический синдром, указанный способ включает введение нуждающемуся в нем пациенту комбинации активного ингредиента А с активным ингредиентом В в терапевтическом количестве, которое необходимо пациенту. Настоящее изобретение также относится к применению фармацевтической композиции, предлагаемой в настоящем изобретении, для приготовления лекарственного средства, предназначенного для терапевтического или предупредительного способа, раскрытого в настоящем изобретении. В одном варианте осуществления настоящее изобретение также относится к применению глюкопиранозилзамещенного производного бензола, раскрытого в настоящем изобретении, для приготовления лекарственного средства, предназначенного для применения в способе, раскрытом в настоящем изобретении. В другом варианте осуществления настоящее изобретение также относится к применению дополнительного терапевтического средства, раскрытого в настоящем изобретении, для приготовления лекарственного средства,предназначенного для применения в способе, раскрытом в настоящем изобретении. Подробное описание предпочтительных вариантов осуществления Вследствие низкого сродства НЗСГ-2 к глюкозе ингибирование этого переносчика при гипогликемических состояниях будет эффективным, и это ограничивает опасность гипогликемии у подвергающихся лечению пациентов, поскольку она предупреждена активностью оставшегося НЗСГ-1 (обладающего высоким сродством). Об этом свидетельствует тот факт, что у пациентов, у которых имеется гомозиготный дефект в гене НЗСГ-2, обнаруживается почечная глюкозурия, но содержания глюкозы в плазме являются нормальными и в остальном они являются здоровыми. Поэтому предполагается, что ингибиторы НЗСГ-2 вследствие своего специфического воздействия будут уменьшать содержание глюкозы и HbA1c в крови, и в связи с этим будет низкой опасность гипогликемии. Кроме того, с учетом того, что выведение глюкозы с мочой вследствие ингибирования НЗСГ-2 может привести к слабому диурезу (что наблюдается у лиц с врожденным дефицитом НЗСГ-2), может представить особый интерес применение глюкопиранозилзамещенных фенилпроизводных в комбинации с инсулином и ТАД, т.е. лекарственными средствами, для которых известно, что они приводят к удерживанию жидкости. Эта потенциальная особенность может быть особенно важной при лечении страдающих диабетом в острой фазе инфаркта миокарда. Такие пациенты подвержены острой сердечной недостаточности после удерживания жидкости вследствие инсулиновой терапии, которую в настоящее время рекомендуют для этих пациентов в руководствах по лечению. Превосходный терапевтический эффект, в особенности аддитивный или превышающий аддитивный эффект или общее ослабление побочных эффектов лечения, желателен для лечения метаболических заболеваний и в особенности сахарного диабета у пациентов, у которых гликемический контроль является плохим или меньшим оптимального при использовании одного антидиабетического средства, у пациентов, у которых наблюдается метаболический синдром, преддиабет/нарушенная переносимость глюкозы, ожирение и метаболические патологические состояния, связанные с ожирением и резистентностью к инсулину, такие как синдром поликистозных яичников (СПКЯ). Введение одного или большего количества активных ингредиентов А и активных ингредиентов В может привести к аддитивному или превышающему аддитивный эффекту соответствующей фармацевтической комбинаций и обеспечить снижение дозы, ослабление побочного эффекта и/или увеличение интервала между введениями по сравнению с отдельным активным ингредиентом А и активным ингредиентом В, применяющимся в монотерапии обычным образом. Указанные эффекты наблюдаются, когда эти два активных вещества вводят одновременно в одной композиции активных веществ, и когда их вводят последовательно в отдельных композициях. В случае, когда активный ингредиент В предназначен для инъекции, в особенности если он является биологическим средством, могут наблюдаться другие преимущества прибавления активного ингредиента А. Например, уменьшение стоимости вследствие увеличения интервала между введениями и/или снижения дозы. Определения. Термин "ожирение" определяется как состояние, в котором индивидуум обладает ИМТ больше чем 30 кг/м 2. В соответствии с нормами ВОЗ (Всемирная организация здравоохранения) определение термина ожирение можно подразделить следующим образом: термин "ожирение I степени" определяется как состояние, в котором ИМТ больше или равен 30 кг/м 2, но меньше 35 кг/м 2; термин "ожирение II степени" определяется как состояние, в котором ИМТ больше или равен 35 кг/м 2, но меньше 40 кг/м 2; термин"ожирение III степени" определяется как состояние, в котором ИМТ больше или равен 40 кг/м 2. Термин "гипергликемия" определяется как патологическое состояние, в котором у субъекта концентрация глюкозы в крови натощак превышает соответствующую нормальному диапазону и составляет более 110 мг/дл (6,11 ммоль/л). Термин "натощак" обладает обычным значением, принятым в медицине. Термин "резистентность к инсулину" определяется, как состояние, в котором для поддержания эуг-3 018495 ликемического статуса необходимы концентрации инсулина в кровотоке, превышающие нормальные,образующиеся в ответ на введение глюкозы (Ford E.S., et al. JAMA. (2002) 287:356-9). Методикой установления резистентности к инсулину является методика фиксации состояния эугликемиигиперинсулинемии. Отношение количества инсулина к количеству глюкозы определяют по методике комбинированного вливания инсулина-глюкозы. Резистентность к инсулину считается установленной,если поглощение глюкозы ниже 25-го процентиля от нормального значения для исследованной популяции (определение, установленное ВОЗ). Существенно менее трудоемкими, чем методики фиксации состояния, являются так называемые минимальные модели, в которых при исследовании переносимости глюкозы посредством внутривенного введения концентрации инсулина и глюкозы в крови измеряют через установленные промежутки времени и по ним рассчитывают резистентность к инсулину. В этой методике невозможно установить различие между гепатической и периферической резистентностью к инсулину. Термин "диабет типа 2" определяется как состояние, в котором субъект обладает концентрацией глюкозы в крови или концентрацией глюкозы в сыворотке натощак, равной более 125 мг/дл(6,94 ммоль/л). Определение концентрации глюкозы в крови является стандартной методикой обычного медицинского исследования. При исследовании переносимости глюкозы концентрация сахара в крови диабетиков превышает 200 мг глюкозы в 1 дл плазмы через 2 ч после приема 75 г глюкозы на пустой желудок. При исследовании переносимости глюкозы 75 г глюкозы вводят пациенту перорально после голодания в течение 10-12 ч и концентрацию сахара в крови определяют непосредственно перед приемом глюкозы и через 1 и 2 ч после ее приема. У здоровых субъектов концентрация сахара в крови перед приемом глюкозы должна составлять от 60 до 110 мг в 1 дл плазмы, менее 200 мг в 1 дл через 1 ч после приема глюкозы и менее 140 мг в 1 дл через 2 ч. Если через 2 ч это значение составляет от 140 до 200 мг,то это считается свидетельством нарушенной переносимости глюкозы. Термин "поздняя стадия сахарного диабета типа 2" относится к пациентам, которым недостаточно принимать вторичное лекарственное средство, для которых существуют показания к инсулиновой терапии и у которых наблюдается прогрессирование осложнений, связанных с капиллярами и крупными сосудами, например, диабетическая нефропатия, ишемическая болезнь сердца (ИБС). Термин "HbA1c" означает продукт неферментативного гликозилирования цепи гемоглобина бета. Определение его концентрации хорошо известно специалисту в данной области техники. При мониторинге лечения сахарного диабета значение концентрации HbA1c является весьма важным. Поскольку его продуцирование в основном зависит от концентрации сахара в крови и времени жизни эритроцитов, концентрация HbA1c в смысле "памяти концентрации сахара в крови" характеризует средние концентрации сахара в крови за предшествующие 4-6 недель. Диабетики, у которых концентрации HbA1c постоянно регулируется путем интенсивного лечения диабета (т.е. составляет 6,5%, предпочтительно 6,0% от полной концентрации гемоглобина в пробе), значительно лучше защищены от диабетической микроангиопатии. Например, сам по себе метформин обеспечивает среднее снижение концентрации HbA1c у диабетиков на величину порядка 1,0-1,5%. Это снижение концентрации HbA1c не является достаточным для того, чтобы у всех диабетиков концентрация HbA1c достигла необходимого значения в диапазоне 6,5% и предпочтительно 6%."Метаболический синдром", также называющийся "синдромом X" (при использовании в контексте метаболического нарушения), также называющийся "дисметаболическим синдромом" представляет собой сложный синдром, основной особенностью которого является резистентность к инсулину (Laaksonenof the American Medical Association (2001) 285:2486-2497), диагноз метаболического синдрома ставят,когда существуют три или большее количество из следующих факторов риска. 1. Абдоминальное ожирение, определяемое, как объем талии, составляющий 40 дюймов или 102 см у мужчин и 35 дюймов или 94 см у женщин; или для японцев, определяемое, как объем талии,составляющий 85 см у мужчин и 90 см у женщин. 2. Концентрация триглицеридов: 150 мг/дл. 3. Концентрация ЛВП-холестерина (ЛВП - липопротеины высокой плотности) 40 мг/дл у мужчин. 4. Артериальное давление 130/85 мм рт.ст. (САД 130 или ДАД 85). 5. Концентрация глюкозы в крови натощак 110 мг/дл. Определение NCEP прошло валидацию (Laaksonen D.E., et al. Am J. Epidemiol. (2002), 156:1070-7). Концентрации триглицеридов и ЛВП-холестерина в крови также можно определить по стандартным методикам медицинского анализа, и они описаны, например, в публикации Thomas L. (Editor): "Labor undDiagnose", TH-Books Verlagsgesellschaft mbH, Frankfurt/Main, 2000. А) Активные ингредиенты А, которые можно применять в контексте настоящего изобретения. Активные ингредиенты А обычно представляют собой ингибитор НЗСГ-2. Подходящие активные ингредиенты А включают соединения, выбранные из числа раскрытых в заявке US 20050209166, содер-4 018495 жание которой во всей его полноте включено в настоящее изобретение в качестве ссылки. Фармацевтические композиции, предлагаемые в настоящем изобретении, могут содержать ингибиторы НЗСГ-2 формулы I в которой R1 выбран из числа определений группы А и если R3 выбран из числа определений группы В, то R1 также дополнительно может быть выбран из группы значений, включающей водород, фтор, хлор, бром, йод, C1-C4-алкил, C2-C4-алкенил-C1-C4-алкил,C2-C4-алкинил-C1-C4-алкил, C2-C4-алкенил-C1-C4-алкоксигруппу, C2-C4-алкинил-C1-C4-алкоксигруппу,C3-С 7-циклоалкил-C1-C4-алкил, C5-C7-циклоалкенил-C1-C4-алкил, метильную группу, замещенную 1-3 атомами фтора, этильную группу, замещенную 1-5 атомами фтора, C1-C4-алкоксигруппу, метоксигруппу,замещенную 1-3 атомами фтора, этоксигруппу, замещенную 1-5 атомами фтора, C1-C4-алкильную группу, замещенную гидроксигруппой, или C1-C3-алкилоксигруппой, C2-C4-алкоксигруппу, замещенную гидроксигруппой или C1-C3-алкоксигруппой, C3-C6-циклоалкил-C1-C3-алкоксигруппу, гидроксигруппу,где в указанных выше циклоалкильных и циклоалкенильных кольцах одна или две метиленовые группы независимо друг от друга могут быть заменены на O или CO;R2 обозначает водород, фтор, хлор, бром, гидроксигруппу, C1-C4-алкил, C1-C4-алкоксигруппу, цианогруппу или нитрогруппу, где алкильная или алкоксигруппа могут быть моно- или полизамещенными фтором;R3 выбран из числа определений группы В и если R1 выбран из числа определений группы А, то R3 также дополнительно может быть выбран из группы значений, включающей водород, фтор, хлор, бром, йод, C1-C6-алкил, C2-C4-алкенил-C1-C4-алкил,C2-C4-алкинил-C1-C4-алкил, C2-C4-алкенил-C1-C4-алкоксигруппу, C2-C4-алкинил-C1-C4-алкоксигруппу,C3-C7-циклоалкил, C5-C7-циклоалкенил, C3-C7-циклоалкил-C1-C4-алкил, C5-C7-циклоалкенил-C1-C4-алкил,C3-C6-циклоалкилиденметил,гидроксигруппу,C1-C6-алкоксигруппу,C3-C6-циклоалкил-C1-C3 алкоксигруппу, арил, арил-C1-C3-алкил, гетероарил, гетероарил-C1-C3-алкил, арилоксигруппу, арил-C1C3-алкилоксигруппу, метильную или метоксигруппу, замещенную 1-3 атомами фтора, C2-C4-алкильную или C2-C4-алкоксигруппу, замещенную 1-5 атомами фтора, C1-C4-алкильную группу, замещенную цианогруппой, C1-C4-алкильную группу, замещенную гидроксигруппой или C1-C3-алкилоксигруппой, цианогруппу, карбоксигруппу, C1-C3-алкоксикарбонил, аминокарбонил, (C1-C3-алкиламино)карбонил, ди(C1C3-алкил)аминокарбонил, пирролидин-1-илкарбонил, пиперидин-1-илкарбонил, морфолин-4-илкарбонил,пиперазин-1-ил-карбонил, 4-(C1-C3-алкил)пиперазин-1-илкарбонил, (C1-C4-алкил)карбониламиногруппу,C1-C4-алкилсульфониламиногруппу,C1-C4-алкилсульфанил,C1-C4-алкилсульфинил,C1-C4 алкилсульфонил, арилсульфониламиногруппу, арил-C1-C3-алкилсульфониламиногруппу или арилсульфонил;R4, R5 независимо друг от друга обозначают водород, фтор, хлор, бром, йод, цианогруппу, нитрогруппу, C1-C3-алкил, C1-C3-алкоксигруппу, метильную или метоксигруппу, замещенную 1-3 атомами фтора; А обозначает C2-C6-алкин-1-ил, C2-C6-алкен-1-ил, C3-C7-циклоалкил, C5-C7-циклоалкенил, арил, гетероарил, C1-C4-алкилкарбонил, арилкарбонил, гетероарилкарбонил, аминокарбонил, C1-C4 алкиламинокарбонил,ди(C1-C3-алкил)аминокарбонил,пирролидин-1-илкарбонил,пиперидин-1 илкарбонил, морфолин-4-илкарбонил, пиперазин-1-илкарбонил, 4-(C1-C4-алкил)пиперазин-1-илкарбонил,ариламинокарбонил, гетероариламинокарбонил, C1-C4-алкоксикарбонил, арил-C1-C3-алкоксикарбонил,аминогруппу,C1-C4-алкиламиногруппу,ди(C1-C3 гетероарил-C1-C3-алкоксикарбонил,алкил)аминогруппу, пирролидин-1-ил, пирролидин-2-он-1-ил, пиперидин-1-ил, пиперидин-2-он-1-ил,морфолин-4-ил,морфолин-3-он-4-ил,пиперазин-1-ил,4-(С 1-C3-алкил)пиперазин-1-ил,C1-C4 алкилкарбониламиногруппу, арилкарбониламиногруппу, гетероарилкарбониламиногруппу, C3-C7 циклоалкилоксигруппу, C5-C7-циклоалкенилоксигруппу, арилоксигруппу, гетероарилоксигруппу, C1-C4 алкилсульфинил, C1-C4-алкилсульфонил, C3-C7-циклоалкилсульфанил, C3-C7-циклоалкилсульфинил, C3C7-циклоалкилсульфонил,C5-C7-циклоалкенилсульфанил,C5-C7-циклоалкенилсульфинил,C5-C7 циклоалкенилсульфонил, арилсульфанил, арилсульфинил, арилсульфонил, гетероарилсульфанил, гетероарилсульфинил, гетероарилсульфонил, цианогруппу или нитрогруппу,где указанные выше алкинильная и алкенильная группы могут быть моно- или полизамещенными фтором или хлором, указанные выше алкинильная и алкенильная группы могут быть моно- или дизамещенными одинаковыми или разными группами L1, и указанные выше циклоалкильные и циклоалкенильные кольца независимо друг от друга могут быть моно- или дизамещенными заместителями, выбранными из группы, включающей фтор и C1-C3-алкил, и в указанных выше циклоалкильных и циклоал-5 018495 кенильных кольцах одна или две метиленовые группы независимо друг от друга могут быть заменены на О, S, СО, SO, SO2 или NRN; В обозначает три(C1-C4-алкил)силил-C1-C6-алкил, C2-C6-алкин-1-ил, C2-C6-алкен-1-ил, аминогруппу,C1-C3-алкиламиногруппу, ди(C1-C3-алкил)аминогруппу, пирролидин-1-ил, пирролидин-2-он-1-ил, пиперидин-1-ил, пиперидин-2-он-1-ил, морфолин-4-ил, морфолин-3-он-4-ил, пиперазин-1-ил, 4-(C1-C3 алкил)пиперазин-1-ил, арилкарбониламиногруппу, гетероарилкарбониламиногруппу, нитрогруппу, C3C10-циклоалкилоксигруппу, C5-C10-циклоалкенилоксигруппу, C3-C10-циклоалкилсульфанил, C3-C10 циклоалкилсульфинил,C3-C10-циклоалкилсульфонил,C5-C10-циклоалкенилсульфанил,C5-C10 циклоалкенилсульфинил, C5-C10-циклоалкенилсульфонил, арилсульфанил, арилсульфинил, гетероарилсульфанил или гетероарилсульфинил, где указанные выше алкинильная и алкенильная группы могут быть моно- или полизамещенными фтором или хлором, и указанные выше алкинильная и алкенильная группы могут быть моно- или дизамещенными одинаковыми или разными группами L1; где указанные выше циклоалкильные и циклоалкенильные кольца независимо друг от друга могут быть моно- или дизамещенными заместителями, выбранными из группы, включающей фтор и C1-C3-алкил, и в указанных выше циклоалкильных и циклоалкенильных кольцах одна или две метиленовые группы независимо друг от друга могут быть заменены на О, S, СО, SO, SO2 или NRN;L1 независимо друг от друга выбраны из группы, включающей гидроксигруппу, цианогруппу, нитрогруппу, C3-C7-циклоалкил, арил, гетероарил, C1-C4-алкилкарбонил, арилкарбонил, гетероарилкарбонил, аминокарбонил, C1-C4-алкиламинокарбонил, ди(C1-C3-алкил)аминокарбонил, пирролидин-1 илкарбонил, пиперидин-1-илкарбонил, морфолин-4-илкарбонил, ариламинокарбонил, гетероариламинокарбонил, C1-C4-алкоксикарбонил, арил-C1-C3-алкоксикарбонил, гетероарил-C1-C3-алкоксикарбонил, C1C4-алкилоксигруппу, арилоксигруппу, гетероарилоксигруппу, C1-C4-алкилсульфанил, арилсульфанил,гетероарилсульфанил,C1-C4-алкилсульфинил,арилсульфинил,гетероарилсульфинил,C1-C4 алкилсульфонил, арилсульфонил и гетероарилсульфонил;L2 независимо друг от друга выбраны из группы, включающей фтор, хлор, бром, йод, C1-C3-алкил,дифторметил, трифторметил, C1-C3-алкоксигруппу, дифторметоксигруппу, трифторметоксигруппу и цианогруппу;R6, R7a, R7b, R7c независимо друг от друга обладают значением, выбранным из группы, включающей водород, (C1-C18-алкил)карбонил, (C1-C18-алкил)оксикарбонил, арилкарбонил и арил(C1-C3 алкил)карбонил; где арильные группы, указанные в определении приведенных выше групп, означают фенильные или нафтильные группы, которые независимо друг от друга могут быть моно- или дизамещенными одинаковыми или разными группами L2; гетероарильные группы, указанные в определении приведенных выше групп, означают пирролильную, фуранильную, тиенильную, пиридильную, индолильную, бензофуранильную, бензотиофенильную,хинолинильную, изохинолинильную или тетразолильную группу или означают пирролильную, фуранильную, тиенильную или пиридильную группу, в которой одна или две метановые группы заменены на атомы азота, или означают индолильную, бензофуранильную, бензотиофенильную, хинолинильную или изохинолинильную группу, в которой от одной до трех метановых групп заменены на атомы азота,где указанные выше гетероарильные группы независимо друг от друга могут быть моно- или дизамещенными одинаковыми или разными группами L2; где, если не указано иное, указанные выше алкильные группы могут обладать линейной или разветвленной цепью,их таутомеры, их стереоизомеры, их смеси и их соли. В другом варианте осуществления активный ингредиент А представляет собой глюкопиранозилзамещенный фенил общей формулы I.2 в которой группы R1-R6 и R7a, R7b и R7c являются такими, как определено непосредственно перед этим. Более предпочтительно, если активный ингредиент А представляет собой 1-хлор-4-(-Dглюкопираноз-1-ил)-2-[4-S)-тетрагидрофуран-3-илокси)бензил]бензол. В другом варианте осуществления активный ингредиент А представляет собой 1-хлор-4-(-Dглюкопираноз-1-ил)-2-[4-S)-тетрагидрофуран-3-илокси)бензил]бензол (далее называется "соединение 1.а") и описан в международной заявке WO 2005/092877 и обладает химической структурой формулы 1.а В) Ингибиторы - активные ингредиенты В, которые можно применять в контексте настоящего изобретения. Активные ингредиенты В, которые пригодны для таких комбинаций, включают, например, такие,которые усиливают терапевтический ингибиторов НЗСГ-2, таких как активные ингредиенты А. Терапевтические средства, которые пригодны для таких комбинаций, включают, например, антидиабетические средства, такие как метформин, сульфонилмочевины (например, глибенкламид, толбутамид, глимепирид), меглитиниды (например, натеглинид, репаглинид), агонисты (например, розиглитазон, пиоглитазон) и антагонисты АПРП-гамма (активированный пролифератором рецептор пероксисом) (например,SR-202), модуляторы АПРП-гамма/альфа (например, KRP 297), ингибиторы альфа-глюкозидазы (например, акарбоза, воглибоза). Предпочтительно, если активный ингредиент В выбран из бигуанидов, которыми являются метформин, фенформин и буформин. Ингибиторы НЗСГ-2 в комбинации с метформином могут улучшать гликемический контроль и могут действовать синергетически с метформином для снижения массы, что оказывает общее благоприятное воздействие при метаболическом синдроме, который обычно связывают с СДТ 2. Другие характеристики комбинаций. Настоящее изобретение также относится к фармацевтическим препаратам, содержащим один или большее количество активных ингредиентов А и активных ингредиентов В или их фармацевтически приемлемых производных, необязательно в комбинации с обычными инертными наполнителями и/или носителями. Любое указание на указанный выше НЗСГ-2 и/или активный ингредиент А и В включает указание на любые их "фармацевтически приемлемые производные", что означает указание на любую фармацевтически приемлемую соль или сложный эфир соединения, предлагаемого в настоящем изобретении, или любое другое соединение, которое после введения пациенту способно образовать (прямо или косвенно) его фармакологически активный метаболит или фармакологически активный остаток. Фармакологически активный метаболит означает любой активный ингредиент А или В, предлагаемый в настоящем изобретении, способный ферментативным или химическим путем подвергаться метаболизму. Фармацевтически приемлемые соли соединений, предлагаемых в настоящем изобретении, включают соли, полученные из фармацевтически приемлемых неорганических и органических кислот и оснований. Примеры подходящих кислот включают хлористо-водородную, бромисто-водородную, серную,азотную, хлорную, фумаровую, малеиновую, фосфорную, гликолевую, молочную, салициловую, янтарную, толуол-п-сульфоновую, винную, уксусную, лимонную, метансульфоновую, муравьиную, бензойную, малоновую, нафталин-2-сульфоновую и бензолсульфоновую кислоты. Другие кислоты, такие как щавелевую кислоту, которые сами по себе не являются фармацевтически приемлемыми, можно использовать при получении солей, использующихся в качестве промежуточных продуктов при получении соединений, предлагаемых в настоящем изобретении, и их фармацевтически приемлемых солей присоединения с кислотами. Соли, полученные из подходящих оснований, включают соли щелочного металла(например, натрия), щелочно-земельного металла (например, магния), аммония и N-(C1-C4-алкила)4+. Кроме того, соединения, предлагаемые в настоящем изобретении, включают пролекарства НЗСГ-2 и активные ингредиенты А и В. Пролекарства включают такие соединения, которые после простого химического превращения изменяются с образованием соединений, предлагаемых в настоящем изобретении. Простые химические превращения включают гидролиз, окисление и восстановление. Точнее, если пролекарство вводится пациенту, то пролекарство может превратиться в соединение В, предлагаемое в настоящем изобретении, и тем самым обеспечить необходимое фармакологическое воздействие. При терапевтическом применении фармацевтические комбинации одного или большего количества активных ингредиентов А и активных ингредиентов В в контексте настоящего изобретения можно вводить в любой обычной дозированной форме любым общепринятым образом. Пути введения включают,но не ограничиваются только ими, внутривенный, внутримышечный, подкожный, внутрисуставной, путем вливания, сублингвальный, чрескожный, пероральный, местный и ингаляционный. Предпочтительными путями введения являются пероральный, местный или внутривенный. Фармацевтические комбинации активного ингредиента А и активного ингредиента В в контексте настоящего изобретения можно вводить по отдельности или в комбинированном препарате вместе со вспомогательными веществами, которые повышают стабильность ингибиторов, облегчают введение содержащих их фармацевтических композиций в некоторых вариантах осуществления, обеспечивают улучшенное растворение или диспергирование, повышают ингибирующую активность, обеспечивают вспомогательное лечение и т. п., включая другие активные ингредиенты. При таких комбинированных методиках лечения используют меньшие дозы обычных терапевтических средств, что устраняет возможную токсичность и неблагоприятные побочные эффекты, наблюдающиеся при использовании этих средств в виде монотерапии. Поэтому фармацевтические комбинации активного ингредиента А и активного ингредиента В можно механически объединять с обычными терапевтическими средствами или другими вспомогательными веществами в одной фармацевтической композиции. Оптимальное содержание (мас./мас.) соединения,предлагаемого в настоящем изобретении, может меняться и его выбирают специалисты в данной области техники. Как отмечено выше, дозированные формы соединений, описанных в настоящем изобретении,включают фармацевтически приемлемые носители и вспомогательные вещества, известные специалистам с общей подготовкой в данной области техники. Эти носители и вспомогательные вещества включают, например, ионообменники, оксид алюминия, стеарат алюминия, лецитин, сывороточные белки,буферные вещества, воду, соли электролитов и вещества на основе целлюлозы. Предпочтительные дозированные формы включают таблетки, капсулы, таблетки в форме капсул, жидкости, растворы, суспензии, эмульсии, ромбовидные таблетки, сиропы, восстанавливающиеся порошки, гранулы, суппозитории и чрескожные пластыри. Методики изготовления таких дозированных форм являются известными (см.,например, публиациию С. Ansel and N.G. Popovish, Pharmaceutical Dosage Forms and Drug Delivery Systems, 5th ed., Lea and Febiger (1990. Дозировки и требования хорошо известны в данной области техники и для конкретного пациента могут быть выбраны специалистом с общей подготовкой в данной области техники из числа имеющихся методик и подходов. Для активного ингредиента А в некоторых вариантах осуществления дозы находятся в диапазоне примерно от 1 до 1000 мг/доза или предпочтительно от 10 до 500 мг для пациента массой 70 кг. Хотя может быть достаточной одна доза в сутки, можно вводить до 5 доз в сутки. При пероральном введении может потребоваться доза, составляющая до 2000 мг/сутки. В связи с этим можно дать ссылку наUS 20050209166. Доза активного ингредиента А, необходимая для обеспечения соответствующей активности для лечения или предупреждения, обычно зависит от соединения, которое необходимо ввести, пациента, характера и тяжести заболевания или патологического состояния и пути и частоты введения и ее назначает лечащий врач пациента. Подходящая доза может составлять от 1 до 100 мг, предпочтительно от 1 до 30 мг при внутривенном введении и от 1 до 1000 мг, предпочтительно от 1 до 100 мг при пероральном введении, в каждом случае вводимая от 1 до 4 раз в сутки. Для этого соединения формулы I,полученные в контексте настоящего изобретения, можно приготовить в виде препарата, необязательно вместе с другими активными веществами, вместе с одним или большим количеством обычных инертных носителей и/или разбавителей, например с кукурузным крахмалом, лактозой, глюкозой, микрокристаллической целлюлозой, стеаратом магния, поливинилпирролидоном, лимонной кислотой, винной кислотой, водой, смесями вода/этанол, вода/глицерин, вода/сорбит, вода/полиэтиленгликоль, пропиленгликолем, цетилстеариловым спиртом, карбоксиметилцеллюлозой или жировыми веществами, такими как твердый жир, или их смесями и получить обычные галеновы препараты, такие как обычные или содержащие покрытие таблетки, капсулы, порошки, суспензии или суппозитории. Как должен понимать специалист в данной области техники, в зависимости от конкретных факторов могут потребоваться меньшие или более значительные дозы. Например, конкретные режимы дозировки и лечения зависят от таких факторов, как общее состояние здоровья пациента, тяжести и течения нарушения у пациента или его предрасположенности и решения лечащего врача. В другом варианте осуществления настоящее изобретение относится к фармацевтической композиции, пригодной для ингаляции, которая содержит одну или большее количество солей и одно или большее количество соединений, необязательно в форме их сольватов или гидратов. Активные вещества можно объединять в одном препарате или включать в два отдельных препарата. Фармацевтические композиции, которые содержат активные вещества А и В в одном препарате являются предпочтительными в контексте настоящего изобретения. Настоящее изобретение также относится к применению активного ингредиента А и активного ингредиента В для приготовления фармацевтических комбинаций, содержащих терапевтически эффективные количества активного ингредиента А и активного ингредиента В, предназначенных для лечения диабета путем одновременного или последовательного введения, при условии, что лечение ингибиторами не противопоказано с терапевтической точки зрения. В содержащих активное вещество комбинациях активного ингредиента А и активного ингредиента В, предлагаемых в настоящем изобретении, ингредиенты А и В могут содержаться в форме их энантиомеров, смесей энантиомеров или в форме рацематов. Соотношения, в которых эти два активных ингредиента А и В можно использовать в комбинациях активных веществ, предлагаемых в настоящем изобретении, меняются в определенных пределах. Активные ингредиенты А и В могут содержаться в форме их сольватов или гидратов. В зависимости от выбора активных ингредиентов А и В массовые соотношения, которые можно использовать в объеме настоящего изобретения, меняются в зависимости от молекулярных масс разных соединений и различий их активности. Выбор массовых соотношений зависит от конкретных активных ингредиентов А и В, их выбирают специалисты в данной области техники. Активное вещество комбинации активных ингредиентов А и В, предлагаемой в настоящем изобретении, можно вводить путем ингаляции или путем введения в нос. Для этого активные ингредиенты А и В необходимо приготовить в пригодных для ингаляции формах. Препараты для ингаляции включают порошки для ингаляции, содержащие пропеллент дозирующие аэрозольные упаковки или не содержащие пропеллент растворы для ингаляции. Порошки для ингаляции, предлагаемые в настоящем изобретении,содержащие комбинацию активных веществ А и В, могут включать чистые активные вещества или смеси активных веществ с физиологически приемлемыми инертными наполнителями. В объеме настоящего изобретения термин "не содержащий пропеллент раствор для ингаляции" также включает концентраты и стерильные растворы для ингаляции, готовые к применению. Препараты, предлагаемые в настоящем изобретении, могут содержать комбинацию активных ингредиентов А и В вместе в одном препарате или в двух отдельных препаратах. Эти препараты,которые можно применять в объеме настоящего изобретения, более подробно описаны в следующем разделе изобретения. Приведенные ниже примеры предназначены для более подробной иллюстрации настоящего изобретения без ограничения объема настоящего изобретения вариантами осуществления, приведенными в качестве примеров. Исходные вещества. Активный ингредиент А, ингибитор НЗСГ-2. Указанный выше ингибитор НЗСГ-2, активный ингредиент А, использующийся в приведенных ниже примерах, можно получить так, как описано в US 11/406971 и US 13/416683. В одном варианте осуществления настоящего изобретения активный ингредиент В выбран из группы, включающей метформин, глибенкламид, толбутамид, глимепирид, глипизид, глихидон, глиборнурид, гликлазид, натеглинид, репаглинид, пиоглитазон, розиглитазон, миглитол, инсулин, метаглидазен и прамлинтид. В другом варианте осуществления настоящего изобретения по меньшей мере один активный ингредиент В представляет собой метформин. Обычно количество активного ингредиента В, применяющееся в композиции, предлагаемой в настоящем изобретении, предпочтительно составляет от 1/5 от обычно рекомендуемой минимальной дозы до 1/1 от обычно рекомендуемой дозы. Предпочтительный диапазон доз метформина составляет от 100 до 3000 мг, предпочтительно от 250 до 3000 мг или 200 до 2000 мг, предпочтительно от 500 до 2000 мг, наиболее предпочтительно от 500 до 1000 в сутки. Предпочтительный диапазон содержания в фармацевтической композиции для введения один, два или три раза в сутки составляет от 100 до 3000, 50 до 1500 и 35 до 1000 мг соответственно. Примерами являются 500 или 850 мг один, два или три раза в сутки, 1000 мг один или два раза в сутки или 2000 мг один раз в сутки. Применение активных ингредиентов, предлагаемых в настоящем изобретении, или их физиологически приемлемой солей в комбинации с другим активным веществом можно проводить одновременно или поочередно через определенные промежутки времени, но предпочтительно - через небольшие промежутки времени. Если их вводят одновременно, то эти два активных вещества вводят пациенту совместно; если их вводят поочередно через определенные промежутки времени, то эти два активных вещества вводят пациенту через промежутки времени, меньшие или равные 12 ч, но предпочтительно - меньшие или равные 6 ч. Комбинация активных ингредиентов, предлагаемых в настоящем изобретении, и их физиологически приемлемых солей, может содержаться в одном препарате, например таблетке или капсуле, или ингредиенты по отдельности могут входить в два одинаковых или разных препарата, например, в виде так называемого набора компонентов. Приведенные ниже примеры предназначены для более подробной иллюстрации настоящего изобретения без его ограничения:I. Примеры фармацевтических препаратов, содержащих активный ингредиент А. Пример А. Таблетки, содержащие 100 мг активного вещества Состав. 1 таблетка содержит: Методика приготовления. Активное вещество, лактозу и крахмал смешивают и равномерно увлажняют водным раствором поливинилпирролидона. После пропускания влажной композиции через сито (отверстия размером 2,0 мм) и сушки в стеллажной сушилке при 50C ее повторно пропускают через сито (отверстия размером 1,5 мм) и прибавляют смазывающее вещество. Готовую смесь прессуют и получают таблетки. Масса таблетки: 220 мг. Диаметр: 10 мм, бипланарная, с фасками с обеих сторон и насечкой с одной стороны. Пример В. Таблетки, содержащие 150 мг активного вещества. Состав. 1 таблетка содержит: Приготовление. Активное вещество смешивают с лактозой, кукурузным крахмалом и диоксидом кремния, увлажняют 20% водным раствором поливинилпирролидона и пропускают через сито с отверстиями размером 1,5 мм. Гранулы, высушенные при 45C, повторно пропускают через то же сито и смешивают указанным количеством стеарата магния. Таблетки прессуют из смеси. Масса таблетки: 300 мг. Пуансон: 10 мм, плоский. Пример С. Капсулы из твердого желатина, содержащие 150 мг активного вещества. Состав. 1 капсула содержит: Приготовление. Активное вещество смешивают с инертными наполнителями, пропускают через сито с отверстиями размером 0,75 мм и перемешивают до однородного состояния в подходящем аппарате. Готовую смесь расфасовывают в капсулы из твердого желатина размера 1. Содержимое капсулы: примерно 320 мг. Оболочка капсулы: капсула из твердого желатина размера 1. Приготовление. После плавления массы суппозитория в ней равномерно распределяют активное вещество и расплав выливают в охлажденные формы. Пример Е. Ампулы, содержащие 10 мг активного вещества. Состав: Приготовление. Активное вещество растворяют в необходимом количестве 0,01 н. HCl, раствор делают изотоническим путем прибавления хлорида натрия, стерильно фильтруют и помещают в ампулы объемом 2 мл. Пример F. Ампулы, содержащие 50 мг активного вещества. Состав. Приготовление. Активное вещество растворяют в необходимом количестве 0,01 н. HCl, раствор делают изотоническим путем прибавления хлорида натрия, стерильно фильтруют и помещают в ампулы объемом 10 мл.II. Конкретные примеры фармацевтических комбинаций А и В. 1) Другие препараты, содержащие конкретные активные ингредиенты А и В, без проведения чрезмерного количества экспериментов можно приготовить на основании данных и примеров, приведенных в настоящем изобретении, и из материалов и по методикам, известным в данной области техники. Эти варианты входят в объем настоящего изобретения. Экспериментальные модели на животных. Любую из указанных выше комбинаций, входящих в объем настоящего изобретения, можно исследовать с помощью экспериментальных моделей на животных, известных в данной области техники. Ниже описаны эксперименты in vivo, которые пригодны для оценки соответствующих фармакологических характеристик фармацевтических композиций и способов, предлагаемых в настоящем изобретении. Фармацевтические композиции и способы, предлагаемые в настоящем изобретении, можно исследовать с помощью обладающих генетической гиперинсулинемией или диабетом животных, таких как мыши db/db, мыши ob/ob, страдающие ожирением крысы Zucker (fa/fa) или страдающие ожирением и диабетом крысы Zucker (ZDF). Кроме того, их можно исследовать с помощью животных, у которых экспериментально вызван диабет, таких как крысы Han Wistar или Sprague Dawley, на которых воздействовали стрептозотоцином. Влияние на гликемический контроль комбинаций, предлагаемых в настоящем изобретении, можно исследовать после введения одной дозы ингибитора (ингибиторов) НЗСГ-2 и дополнительного терапевтического средства (средств), которое применимо для лечения метаболических нарушений, по отдельности или в комбинации с помощью перорального исследования переносимости глюкозы на экспериментальных моделях на животных, описанных выше в настоящем изобретении. После перорального введения глюкозы животным, голодавшим в течение ночи, исследуют зависимость содержания глюкозы в крови от времени. По данным о снижении пиковых концентраций глюкозы или снижении площади под кривой для глюкозы комбинации, предлагаемые в настоящем изобретении, значительно улучшают выведение глюкозы по сравнению с любой монотерапией. Кроме того, после введения нескольких доз ингибитора (ингибиторов) НЗСГ-2 и дополнительного терапевтического средства (средств), которое применимо для лечения метаболических нарушений, по отдельности или в комбинации в экспериментальных моделях на животных, описанных выше в настоящем изобретении, путем измерения содержания HbA1c в крови можно исследовать влияние на гликемический контроль. Возможное снижение дозы ингибитора (ингибиторов) НЗСГ-2 и дополнительного терапевтического средства (средств), которое применимо для лечения метаболических нарушений или обоих активных ингредиентов, можно исследовать путем изучения влияния на гликемический контроль меньших доз комбинаций и монотерапии экспериментальных моделях на животных, описанных выше в настоящем изобретении. Уменьшение зависимости от лечения инсулином, предлагаемое в настоящем изобретении, можно продемонстрировать после перорального введения одной дозы с помощью перорального исследования переносимости глюкозы на экспериментальных моделях на животных, описанных выше в настоящем изобретении. После введения глюкозы животным, голодавшим в течение ночи, исследуют зависимость содержания инсулина в плазме от времени. Увеличение содержаний активного GLP-1 с помощью лечения, предлагаемого в настоящем изобретении, после введения одной или нескольких доз можно исследовать путем измерения доз в плазме в экспериментальных моделях на животных, описанных выше в настоящем изобретении, натощак или после приема пищи. Аналогичным образом, при таких же условиях можно установить снижение содержания глюкагона в плазме. Влияние комбинации ингибитора (ингибиторов) НЗСГ-2 и дополнительного терапевтического средства (средств), которое применимо для лечения метаболических нарушений, на восстановление бетаклеток и неогенез можно исследовать после введения нескольких доз в экспериментальных моделях на животных, описанных выше в настоящем изобретении путем определения увеличения содержания инсулина, поступающего из поджелудочной железы, или путем определения увеличенной массы -клеток с помощью морфометрического анализа после иммуногистохимического окрашивания срезов поджелудочной железы или путем определения увеличенной выработки инсулина, стимулированной глюкозой, в отдельных панкреатических островках. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Фармацевтическая композиция, включающая ингибитор НЗСГ-2 (натрийзависимый сопереносчик глюкозы 2) в комбинации со вторым терапевтическим средством, которое применимо для лечения одного или большего количества метаболических нарушений, в которой:i) указанный ингибитор НЗСГ-2 представляет собой глюкопиранозилзамещенное производное бензола - 1-хлор-4-(-D-глюкопираноз-1-ил)-2-[4-S)-тетрагидрофуран-3-илокси)бензил]бензол;ii) указанное второе терапевтическое средство, которое применимо для лечения одного или большего количества метаболических нарушений, представляет собой метформин. 2. Способ лечения или предупреждения метаболического нарушения, включающий введение нуждающемуся в нем пациенту фармацевтической композиции по п.1. 3. Способ по п.2, в котором соединение-ингибитор НЗСГ-2 1-хлор-4-(-D-глюкопираноз-1-ил)-2-[4S)-тетрагидрофуран-3-илокси)бензил]бензол и второе терапевтическое средство метформин содержатся в одной дозированной форме. 4. Способ по п.2, в котором соединение-ингибитор НЗСГ-2 1-хлор-4-(-D-глюкопираноз-1-ил)-2-[4S)-тетрагидрофуран-3-илокси)бензил]бензол и второе терапевтическое средство метформин содержатся каждое в отдельной дозированной форме. 5. Способ по любому из пп.2-4, характеризующийся дозировкой от 500 до 1000 мг метформина. 6. Способ по любому из пп.2-5, характеризующийся дозировкой от 1 до 100 мг указанного соединения-ингибитора НЗСГ-2. 7. Применение фармацевтической композиции, включающей соединение-ингибитор НЗСГ-2 в комбинации со вторым терапевтическим средством по п.1, для приготовления лекарственного средства,предназначенного для лечения или предупреждения метаболического нарушения посредством введения нуждающемуся в нем пациенту указанной фармацевтической композиции. 8. Применение по п.7, в котором указанное метаболическое нарушение выбрано из группы, включающей сахарный диабет типа 1, сахарный диабет типа 2, нарушенную переносимость глюкозы, гипергликемию, гипергликемию после приема пищи, избыточную массу тела, ожирение, включая ожирение класса I, ожирение класса II, ожирение класса III, висцеральное ожирение и абдоминальное ожирение, и метаболический синдром. 9. Применение по п.8, в котором указанное метаболическое нарушение представляет собой сахарный диабет типа 2. 10. Применение по пп.7, 8 или 9, в котором указанное соединение-ингибитор НЗСГ-2 и указанное терапевтическое средство вводят в одной фармацевтической композиции. 11. Применение 1-хлор-4-(-D-глюкопираноз-1-ил)-2-[4-S)-тетрагидрофуран-3 илокси)бензил]бензола для приготовления фармацевтической композиции по п.1 для использования в способе лечения метаболического нарушения, которое выбрано из группы, включающей сахарный диабет типа 1, сахарный диабет типа 2, нарушенную переносимость глюкозы, гипергликемию, гипергликемию после приема пищи, избыточную массу тела, ожирение, включая ожирение класса I, ожирение класса II, ожирение класса III, висцеральное ожирение и абдоминальное ожирение, и метаболический синдром. 12. Применение по п.11, в котором указанное метаболическое нарушение представляет собой сахарный диабет типа 2. 13. Применение второго терапевтического средства, определенного в п.1, для приготовления фармацевтической композиции по п.1 для использования в способе лечения метаболического нарушения,которое выбрано из группы, включающей сахарный диабет типа 1, сахарный диабет типа 2, нарушенную переносимость глюкозы, гипергликемию, гипергликемию после приема пищи, избыточную массу тела,ожирение, включая ожирение класса I, ожирение класса II, ожирение класса III, висцеральное ожирение и абдоминальное ожирение, и метаболический синдром. 14. Применение по п.13, в котором указанное метаболическое нарушение представляет собой сахарный диабет типа 2. Евразийская патентная организация, ЕАПВ Россия, 109012, Москва, Малый Черкасский пер., 2
МПК / Метки
МПК: A61P 3/10, A61K 31/70, A61K 31/341, A61P 3/00
Метки: глюкозы, фармацевтическими, комбинированное, sglt-2, композициями, ингибиторами, натрийзависимый, сопереносчик, содержащими, лечение
Код ссылки
<a href="https://eas.patents.su/22-18495-kombinirovannoe-lechenie-ingibitorami-sglt-2-natrijjzavisimyjj-soperenoschik-glyukozy-2-i-soderzhashhimi-ih-farmacevticheskimi-kompoziciyami.html" rel="bookmark" title="База патентов Евразийского Союза">Комбинированное лечение ингибиторами sglt-2 (натрийзависимый сопереносчик глюкозы 2) и содержащими их фармацевтическими композициями</a>
Предыдущий патент: Способ получения комплексной консистентной смазки
Случайный патент: Способ изготовления роторных и статорных пластин