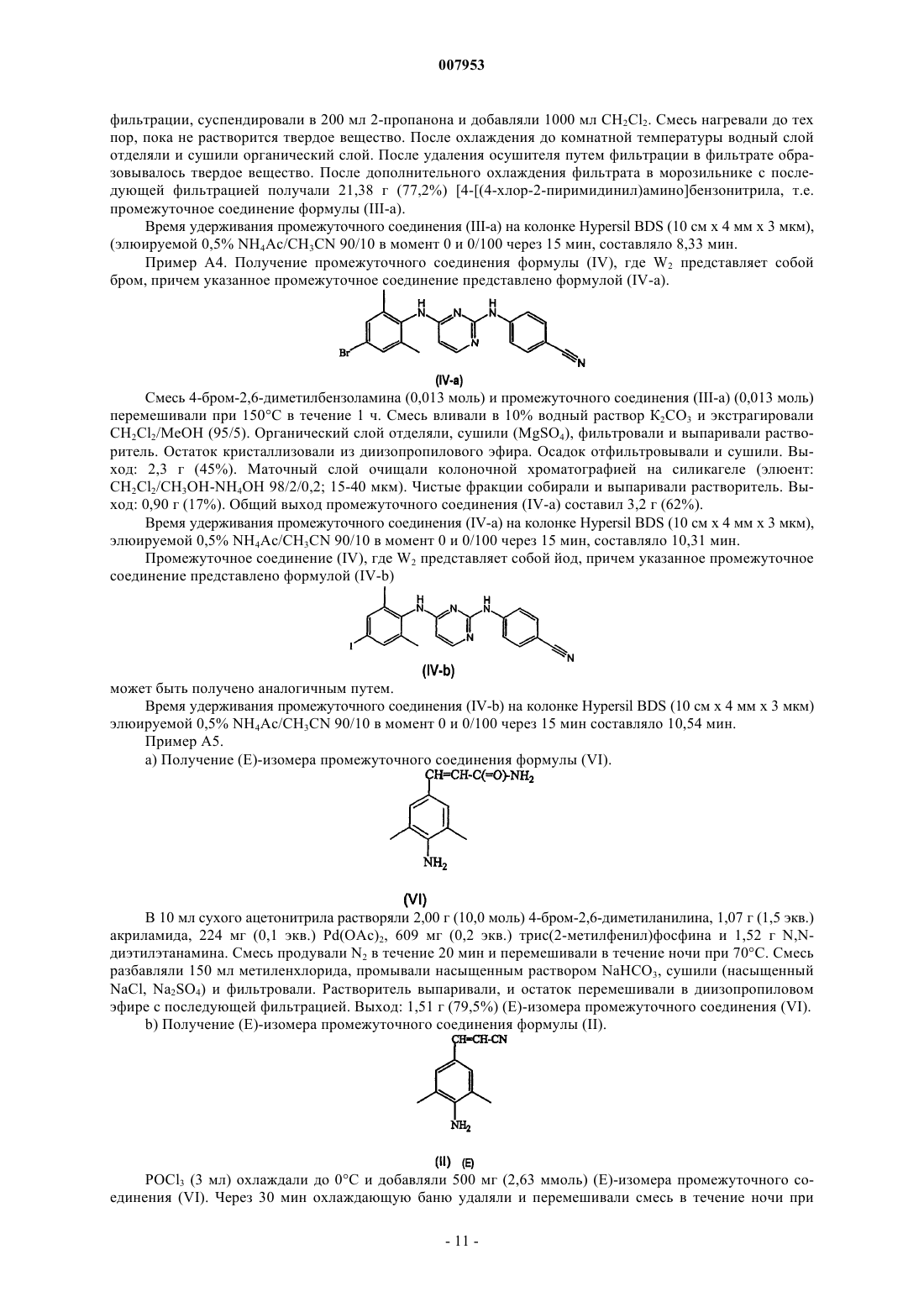
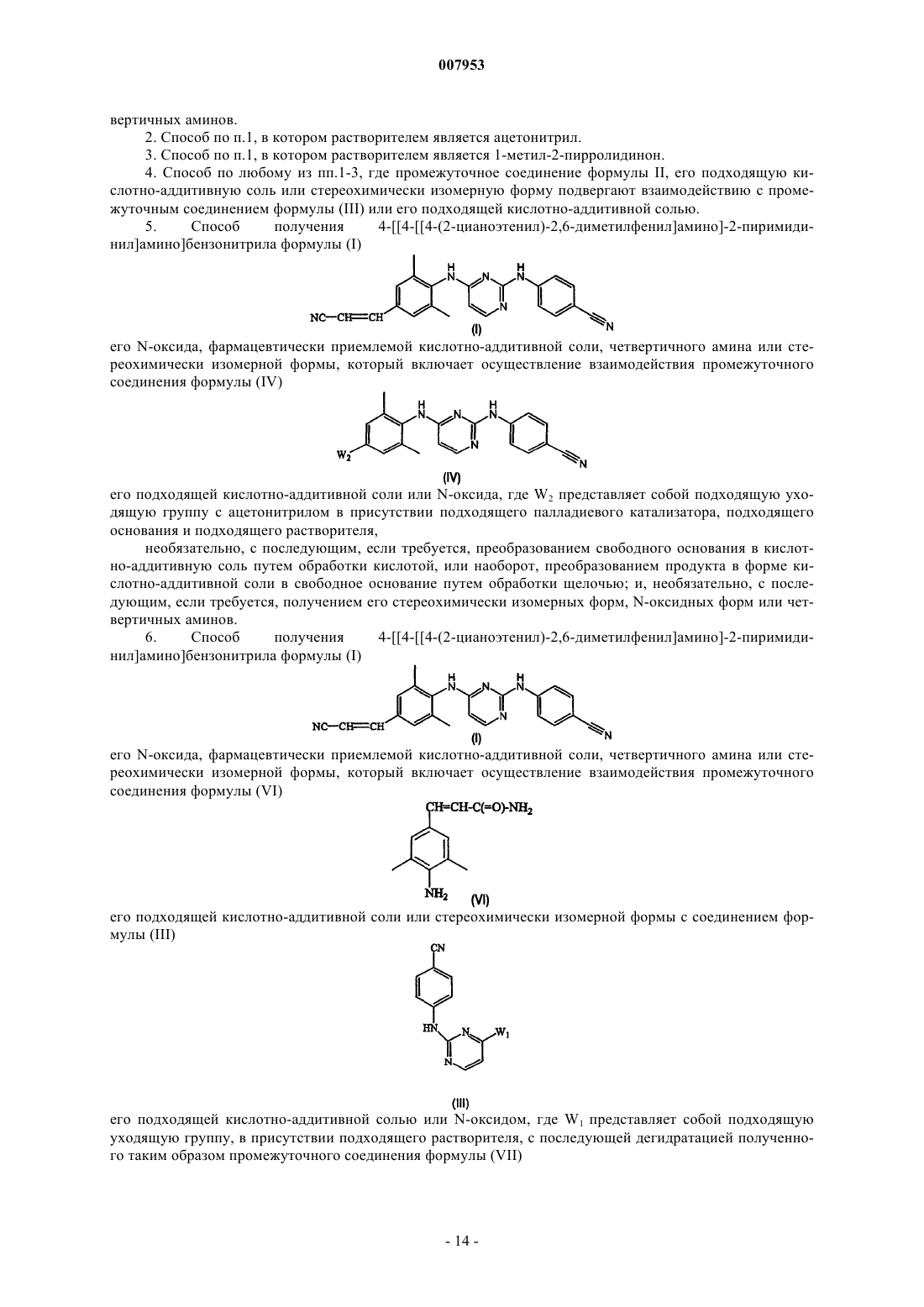
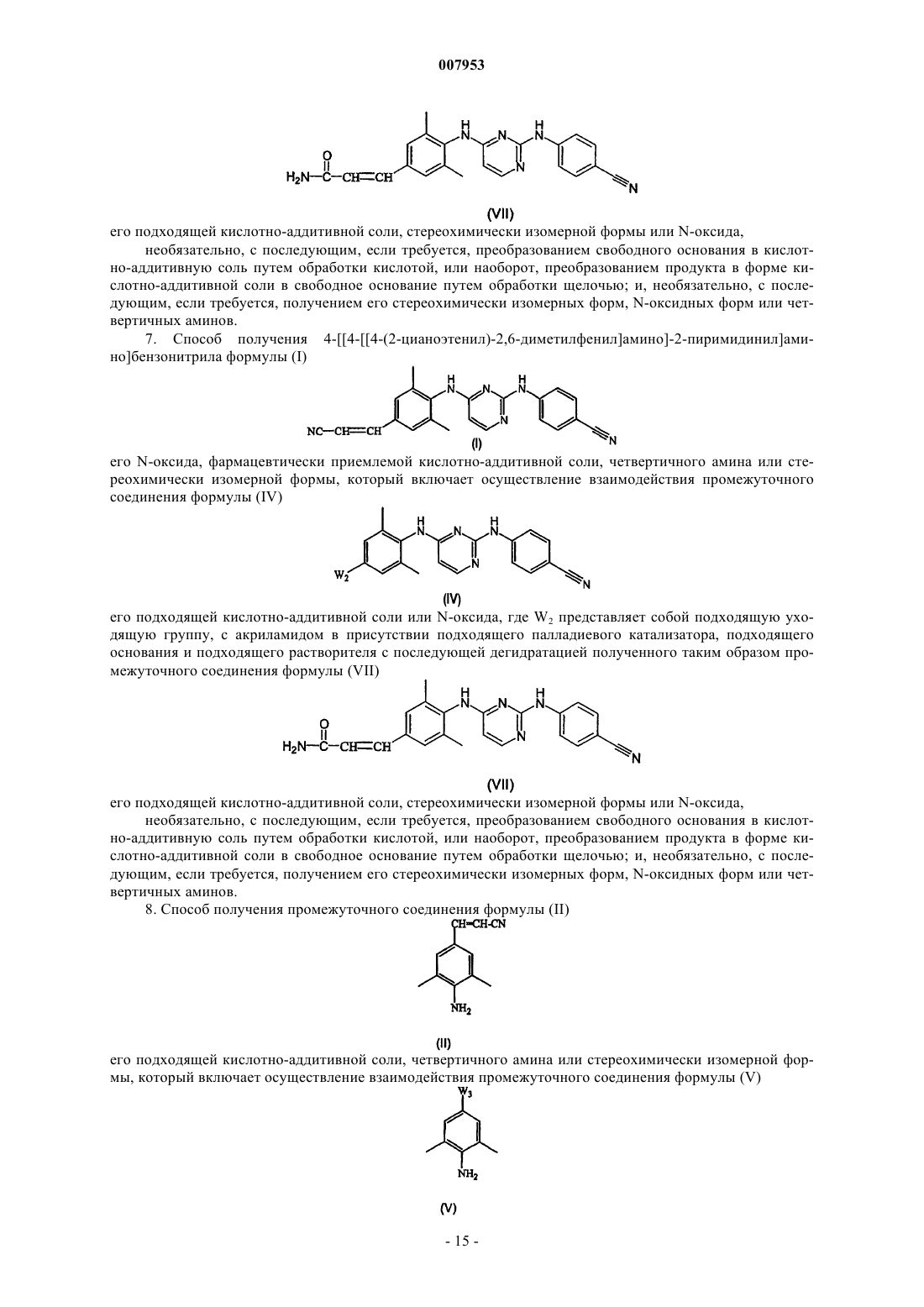
Способы получения 4-[[4-[[4-(2-цианоэтенил)-2,6-диметилфенил]амино]-2-пиримидинил]амино]бензонитрила
Номер патента: 7953
Опубликовано: 27.02.2007
Авторы: Гийемон Жером Эмиль Жорж, Виллемс Йоаннес Йозефус Мария, Паскье Элизабет Тереза Жанна, Медар Барт Петрус Анна Мария Йозеф, Лендерс Рубен Герардус Жорж, Схилс Дидье Филипп Робер, Хэрес Ян, Жанссен Поль Адриан Ян
Формула / Реферат
1. Способ получения 4-[[4-[[4-(2-цианоэтенил)-2,6-диметилфенил]амино]-2-пиримидинил]амино]бензонитрила формулы (I)
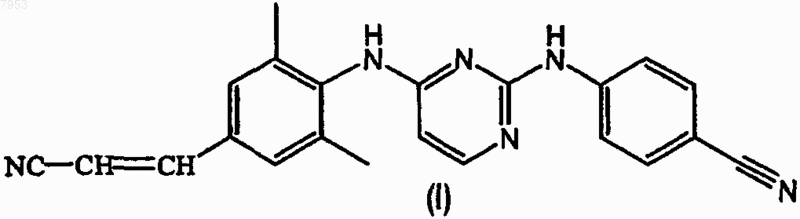
его N-оксида, фармацевтически приемлемой кислотно-аддитивной соли, четвертичного амина или стереохимически изомерной формы, который включает осуществление взаимодействия промежуточного соединения формулы (II)
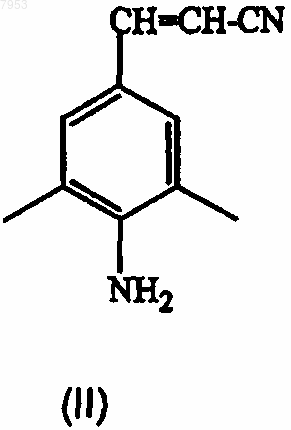
его подходящей кислотно-аддитивной соли или стереохимически изомерной формы с промежуточным соединением формулы (III)

его подходящей кислотно-аддитивной солью или N-оксидом, где W1 представляет собой подходящую уходящую группу, в присутствии подходящего растворителя,
необязательно, с последующим, если требуется, преобразованием свободного основания в кислотно-аддитивную соль путем обработки кислотой, или наоборот, преобразованием продукта в форме кислотно-аддитивной соли в свободное основание путем обработки щелочью; и, необязательно, с последующим, если требуется, получением его стереохимически изомерных форм, N-оксидных форм или четвертичных аминов.
2. Способ по п.1, в котором растворителем является ацетонитрил.
3. Способ по п.1, в котором растворителем является 1-метил-2-пирролидинон.
4. Способ по любому из пп.1-3, где промежуточное соединение формулы II, его подходящую кислотно-аддитивную соль или стереохимически изомерную форму подвергают взаимодействию с промежуточным соединением формулы (III) или его подходящей кислотно-аддитивной солью.
5. Способ получения 4-[[4-[[4-(2-цианоэтенил)-2,6-диметилфенил]амино]-2-пиримидинил]амино]бензонитрила формулы (I)
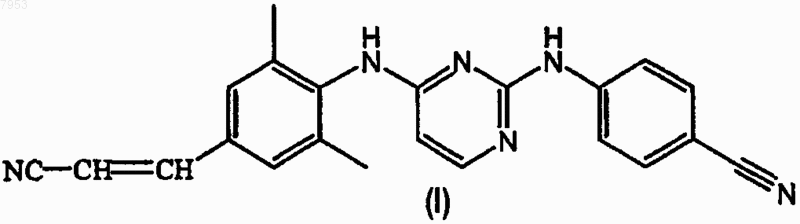
его N-оксида, фармацевтически приемлемой кислотно-аддитивной соли, четвертичного амина или стереохимически изомерной формы, который включает осуществление взаимодействия промежуточного соединения формулы (IV)
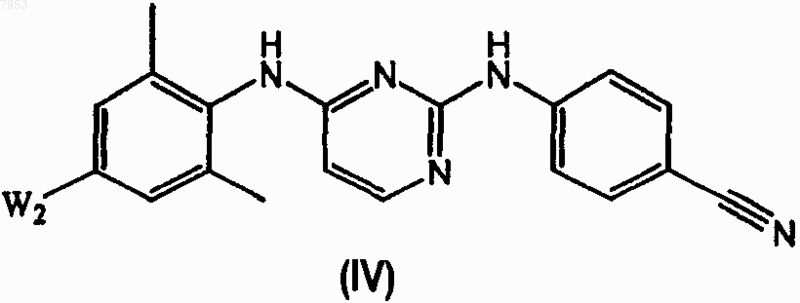
его подходящей кислотно-аддитивной соли или N-оксида, где W2 представляет собой подходящую уходящую группу с ацетонитрилом в присутствии подходящего палладиевого катализатора, подходящего основания и подходящего растворителя,
необязательно, с последующим, если требуется, преобразованием свободного основания в кислотно-аддитивную соль путем обработки кислотой, или наоборот, преобразованием продукта в форме кислотно-аддитивной соли в свободное основание путем обработки щелочью; и, необязательно, с последующим, если требуется, получением его стереохимически изомерных форм, N-оксидных форм или четвертичных аминов.
6. Способ получения 4-[[4-[[4-(2-цианоэтенил)-2,6-диметилфенил]амино]-2-пиримидинил]амино]бензонитрила формулы (I)
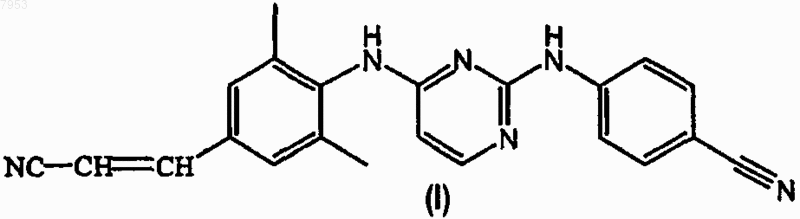
его N-оксида, фармацевтически приемлемой кислотно-аддитивной соли, четвертичного амина или стереохимически изомерной формы, который включает осуществление взаимодействия промежуточного соединения формулы (VI)
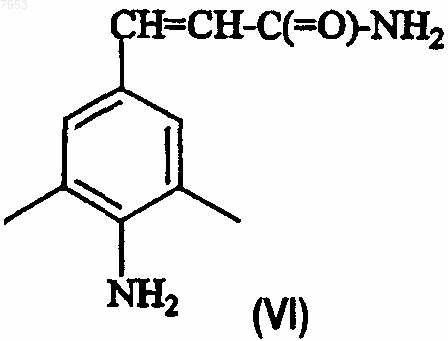
его подходящей кислотно-аддитивной соли или стереохимически изомерной формы с соединением формулы (III)

его подходящей кислотно-аддитивной солью или N-оксидом, где W1 представляет собой подходящую уходящую группу, в присутствии подходящего растворителя, с последующей дегидратацией полученного таким образом промежуточного соединения формулы (VII)
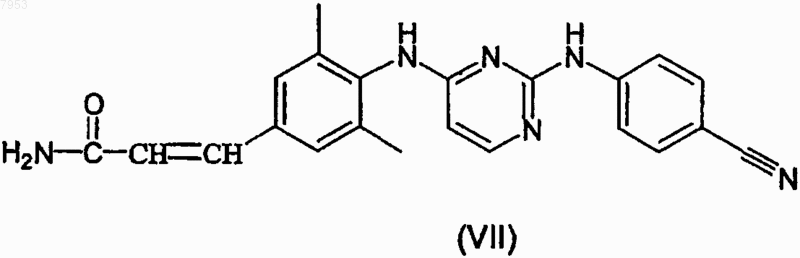
его подходящей кислотно-аддитивной соли, стереохимически изомерной формы или N-оксида,
необязательно, с последующим, если требуется, преобразованием свободного основания в кислотно-аддитивную соль путем обработки кислотой, или наоборот, преобразованием продукта в форме кислотно-аддитивной соли в свободное основание путем обработки щелочью; и, необязательно, с последующим, если требуется, получением его стереохимически изомерных форм, N-оксидных форм или четвертичных аминов.
7. Способ получения 4-[[4-[[4-(2-цианоэтенил)-2,6-диметилфенил]амино]-2-пиримидинил]амино]бензонитрила формулы (I)
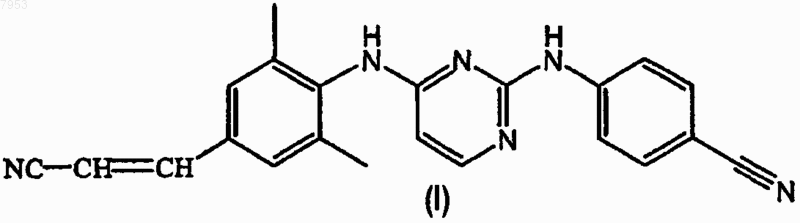
его N-оксида, фармацевтически приемлемой кислотно-аддитивной соли, четвертичного амина или стереохимически изомерной формы, который включает осуществление взаимодействия промежуточного соединения формулы (IV)
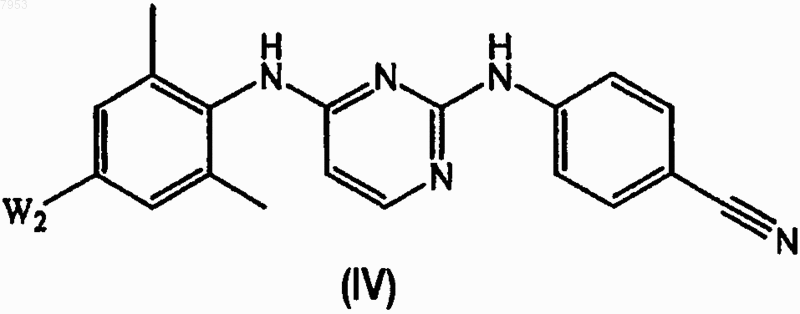
его подходящей кислотно-аддитивной соли или N-оксида, где W2 представляет собой подходящую уходящую группу, с акриламидом в присутствии подходящего палладиевого катализатора, подходящего основания и подходящего растворителя с последующей дегидратацией полученного таким образом промежуточного соединения формулы (VII)
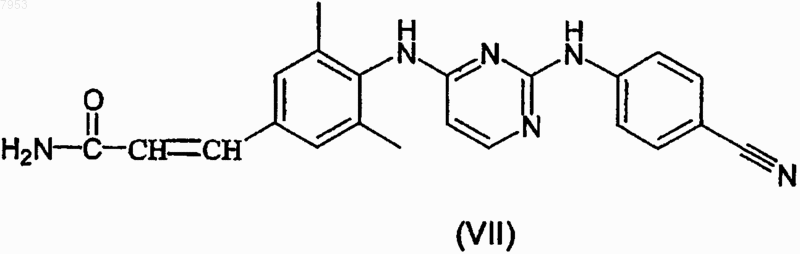
его подходящей кислотно-аддитивной соли, стереохимически изомерной формы или N-оксида,
необязательно, с последующим, если требуется, преобразованием свободного основания в кислотно-аддитивную соль путем обработки кислотой, или наоборот, преобразованием продукта в форме кислотно-аддитивной соли в свободное основание путем обработки щелочью; и, необязательно, с последующим, если требуется, получением его стереохимически изомерных форм, N-оксидных форм или четвертичных аминов.
8. Способ получения промежуточного соединения формулы (II)
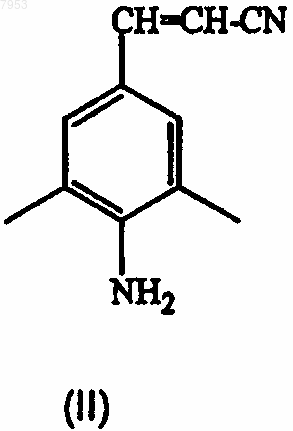
его подходящей кислотно-аддитивной соли, четвертичного амина или стереохимически изомерной формы, который включает осуществление взаимодействия промежуточного соединения формулы (V)
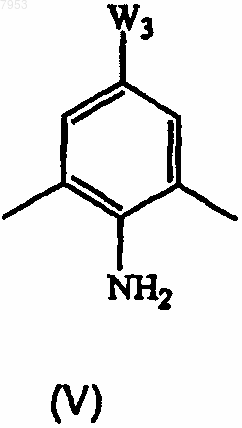
его подходящей кислотно-аддитивной соли или четвертичного амина, где W3 представляет собой подходящую уходящую группу, с ацетонитрилом в присутствии подходящего палладиевого катализатора, подходящего основания и подходящего растворителя,
необязательно, с последующим, если требуется, преобразованием свободного основания в кислотно-аддитивную соль путем обработки кислотой, или наоборот, преобразованием соединения в форме кислотно-аддитивной соли в свободное основание путем обработки щелочью; и, необязательно, с последующим, если требуется, получением его стереохимически изомерных форм, N-оксидных форм или четвертичных аминов.
9. Способ по п.5 или 8, в котором палладиевый катализатор представляет собой гетерогенный палладиевый катализатор.
10. Способ по п.9, в котором гетерогенным палладиевым катализатором является палладий на угле.
11. Способ получения промежуточного соединения формулы (II)
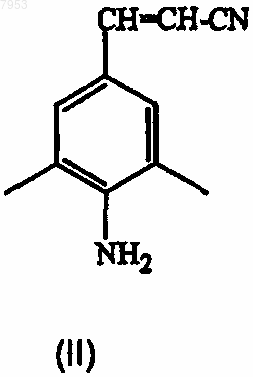
его подходящей кислотно-аддитивной соли, четвертичного амина или стереохимически изомерной формы, который включает осуществление взаимодействия промежуточного соединения формулы (V)
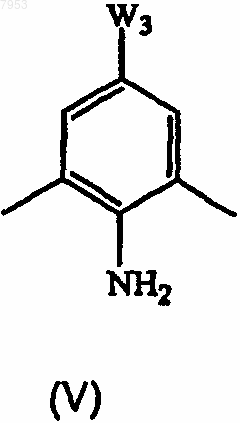
его подходящей кислотно-аддитивной соли или четвертичного амина, где W3 представляет собой подходящую уходящую группу, с акриламидом в присутствии подходящего палладиевого катализатора, подходящего основания и подходящего растворителя с последующей дегидратацией полученного таким образом промежуточного соединения формулы (VI)
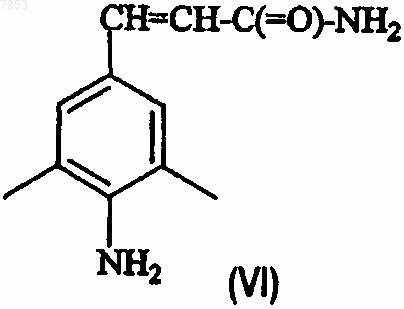
его подходящей кислотно-аддитивной соли, четвертичного амина или стереохимически изомерной формы,
необязательно, с последующим, если требуется, преобразованием свободного основания в кислотно-аддитивную соль путем обработки кислотой, или наоборот, преобразованием продукта в форме кислотно-аддитивной соли в свободное основание путем обработъш щелочью; и, необязательно, с последующим, если требуется, получением его стереохимически изомерных форм, N-оксидных форм или четвертичных аминов.
12. Способ по любому из пп.1-7, в котором 4-[[4-[[4-(2-цианоэтенил)-2,6-диметилфенил]амино]-2-пиримидинил]амино]бензонитрил формулы (I), его N-оксид, фармацевтически приемлемая кислотно-аддитивная соль, четвертичный амин или стереохимически изомерная форма представляет собой (Е)-4-[[4-[[4-(2-цианоэтенил)-2,6-диметилфенил]амино]-2-пиримидинил]амино]бензонитрил.
Текст
007953 Настоящее изобретение относится к 4-4-4-(2-цианоэтенил)-2,6-диметилфенил]амино]-2-пиримидинил]амино]бензонитрилу, его N-оксиду, фармацевтически приемлемой аддитивной соли, четвертичному амину или стереохимически изомерной форме, к способу их получения, а также к получению ключевого промежуточного соединения в указанном способе получения. В WO 99/50250 раскрыты замещенные диаминопиримидиновые соединения, обладающие способностью ингибировать ВИЧ (вирус иммунодефицита человека), и их получение. В WO 03/16306 раскрыт способ получения 4-4-4-(2-цианоэтенил)-2,6-диметилфенил]амино]-2-пиримидинил]амино]бензонитрила из расплава [4-[(4-хлор-2-пиримидинил)амино]бензонитрила и 3-(4-амино-3,5-диметилфенил)-2-пропеннитрила. 4-4-4-(2-Цианоэтенил)-2,6-диметилфенил]амино]-2-пиримидинил]амино]бензонитрил, его Nоксиды, фармацевтически приемлемые аддитивные соли, четвертичные амины и стереохимически изомерные формы являются новыми, очень эффективными соединениями, ингибирующими репликацию ВИЧ, в особенности ВИЧ-1. Они обладают высокой способностью ингибировать репликацию дикого типа вируса иммунодефицита человека, а также его резистентных мутантных штаммов. Поэтому 4-4-4-(2-цианоэтенил)-2,6-диметилфенил]амино]-2-пиримидинил]амино]бензонитрил,его N-оксиды, фармацевтически приемлемые аддитивные соли, четвертичные амины и стереохимически изомерные формы могут применяться в качестве лекарственного средства. Они могут быть пригодны для профилактики или лечения ВИЧ-инфекции, включая профилактику или лечение ВИЧ-инфекции, вызванной мутантными штаммами, т.е. штаммами, которые становятся устойчивыми к действию известного из уровня техники лекарства (лекарств) (штаммы ВИЧ, резистентные к лекарственному средству или лекарственным средствам); они могут быть пригодны для лечения теплокровных животных, включая людей,инфицированных ВИЧ или другими вирусами, чье существование опосредуется ферментом обратной транскриптазой или зависит от него, или для профилактики этих инфекций у теплокровных животных. Поэтому настоящее изобретение также относится к применению 4-4-4-(2-цианоэтенил)-2,6-диметилфенил]амино]-2-пиримидинил]амино]бензонитрила, его N-оксида, фармацевтически приемлемой аддитивной соли, четвертичного амина и стереохимически изомерной формы для производства лекарственного препарата для профилактики или лечения ВИЧ-инфекции. Настоящее изобретение также относится к способу лечения теплокровных животных, включая людей, страдающих вирусными инфекциями, в особенности ВИЧ-инфекциями, или к способу профилактики теплокровных животных, включая людей, подверженных риску заболевания вирусными инфекциями, в особенности ВИЧ-инфекциями. Указанный способ включает введение, предпочтительно пероральное введение, эффективного количества соединения формулы (I) , его N-оксидной формы, фармацевтически приемлемой аддитивной соли, четвертичного амина или возможной стереоизомерной формы, теплокровным животным, включая людей. Настоящее изобретение также относится к композициям для лечения вирусных инфекций, содержащим терапевтически эффективное количество 4-4-4-(2-цианоэтенил)-2,6-диметилфенил]амино]-2-пиримидинил] амино]бензонитрила, его N-оксида, фармацевтически приемлемой аддитивной соли, четвертичного амина или возможной стереохимической изомерной формы, и фармацевтически приемлемый носитель или разбавитель. Для целей введения соединения по настоящему изобретению или любая их подгруппа могут быть включены в состав различных фармацевтических форм. Подходящими композициями могут считаться все композиции, обычно применяемые для системного введения лекарств. Для получения фармацевтических композиций по настоящему изобретению эффективное количество определенного соединения, необязательно в форме аддитивной соли, в качестве активного ингредиента, объединяют в однородную смесь с фармацевтически приемлемым носителем, причем носитель может принимать широкое разнообразие форм в зависимости от желаемой для введения формы препарата. Желательно, чтобы данные фармацевтические композиции находились в единичной дозированной форме, пригодной, в частности, для перорального, ректального, чрезкожного введения или введения путем парентеральной инъекции. Например, при получении композиций в пероральной дозированной форме, в случае жидких лекарственных препаратов для перорального приема, таких как суспензии, сиропы, эликсиры, эмульсии и растворы, могут применяться любые обычные фармацевтические среды, такие как, например, вода, гликоли, масла,спирты и тому подобное; в случае порошков, пилюль, капсул и таблеток могут применяться твердые носители, такие как крахмалы, сахара, каолин, разбавители, лубриканты, связующие вещества, дезинтегранты и тому подобное. В силу простоты введения наиболее предпочтительными единичными дозированными формами для перорального введения являются таблетки и капсулы и в этом случае, безусловно,применяются твердые фармацевтические носители. В случае композиций для парентерального введения носитель обычно должен содержать, по крайней мере, в большей своей части, стерильную воду, хотя может содержать и другие ингредиенты, например, улучшающие растворимость. Например, могут быть приготовлены инъецируемые растворы, в которых носитель содержит солевой раствор, раствор глюкозы или смесь солевого раствора и раствора глюкозы. Также могут быть приготовлены инъецируемые суспензии, в которых могут применяться подходящие жидкие носители, суспендирующие агенты и тому подобное. В число форм также включены препараты в виде твердых форм, которые предназначены для преобразования в жидкие формы препарата непосредственно перед применением. В композициях, пригодных для чрезкожного введения, носитель необязательно содержит усиливающий проникновение агент и/или подходящее смачивающее вещество, необязательно объединенное с подходящими добавками раз-1 007953 личной природы в меньших пропорциях, причем добавки не вызывают значительного отрицательного воздействия на кожу. Указанные добавки могут способствовать введению в кожу и/или могут быть вспомогательными средствами при получении желаемых композиций. Эти композиции могут вводиться различными путями, например, в виде чрезкожного пластыря, в виде наклейки, в виде мази. Соединения по настоящему изобретению могут также вводиться путем ингаляции или инсуффляции при помощи способов и составов, применяемых в данной области техники для введения таким путем. Поэтому соединения по настоящему изобретению, как правило, могут вводиться в легкие в форме раствора, суспензии или сухого порошка. Любая система, разработанная для доставки растворов, суспензий или сухих порошков путем пероральной или назальной ингаляции или инсуффляции, пригодна для введения соединений по настоящему изобретению. Способность 4-4-4-(2-цианоэтенил)-2,6-диметилфенил]амино]-2-пиримидинил]амино]бензонитрила,его N-оксида, фармацевтически приемлемой аддитивной соли, четвертичного амина или стереохимически изомерной формы ингибировать репликацию ВИЧ может быть испытана с применением следующего теста. Определение анти-ВИЧ активности Для оценки эффективности анти-ВИЧ агентов in vitro применяли быструю, чувствительную и автоматизированную методику анализа. В качестве линии клеток-мишеней служила трансформированная ВИЧ-1 Т 4-клеточная линия МТ-4, которая известна (Koyanagi et al., Int. J. Cancer, 36, 445-451, 1985) своей высокой чувствительностью к ВИЧ-инфекции и рекомендуется для ее исследований. В качестве конечной точки служило ингибирование индуцированного ВИЧ цитопатического эффекта. Жизнеспособность ВИЧ-инфицированных и ложно инфицированных клеток оценивали спектрофотометрически по восстановлению in situ бромида 3-(4,5-диметилтиазол-2-ил)-2,5-дифенилтетразолия (МТТ). Вызывающую 50% цитотоксический эффект концентрацию (СС 50 в М) определяли как концентрацию соединения,вызывающую в контрольном образце ложно инфицированных клеток снижение оптической плотности на 50%. Достигаемый путем применения тестируемого соединения процент защиты в ВИЧ-инфицированных клетках рассчитывали по выраженной в процентах формуле в которой (ODT)HIV представляет собой оптическую плотность, измеренную в ВИЧ-инфицированных клетках с тестируемым соединением в известной концентрации; (ODC)HIV представляет собой оптическую плотность, измеренную в контрольных необработанных тестируемым соединением ВИЧинфицированных клетках; (ODC)MOCK представляет собой оптическую плотность, измеренную в контрольных необработанных тестируемым соединением ложно инфицированных клетках; все значения оптической плотности измеряли при 540 нм. Дозу, при которой достигалась 50% защита в соответствии с приведенной выше формулой, определяли как вызывающую 50% ингибирование концентрацию (IС 50 в М). Отношение СС 50 к IС 50 определяли как индекс избирательности (SI). Результаты, полученные для соединения X, т.е.SI составляло 10-5 М/10-9,4 М=25119. Соединение X было также протестировано на его способность ингибировать репликацию в резистентных мутантных штаммах ВИЧ-1 (одиночных и двойных мутантах). Полученные результаты выявили высокую эффективность соединения X против резистентных штаммов. При производстве соединений по настоящему изобретению требуется эффективный способ синтеза,который может выполняться для широкомасштабного коммерческого производства с целью обеспечения экономической эффективности соединений по настоящему изобретению для целей развития и маркетинга. Настоящее изобретение относится к способам получения 4-4-4-(2-цианоэтенил)-2,6-диметилфенил]амино]-2-пиримидинил]амино]бензонитрила, его N-оксида, фармацевтически приемлемой аддитивной соли, четвертичного амина или стереохимически изомерной формы с высоким выходом и в условиях, при которых обеспечиваются экономические преимущества для широкомасштабного коммерческого производства. Поэтому настоящее изобретение относится к способу получения 4-4-4-(2-цианоэтенил)-2,6-диметилфенил]амино]-2-пиримидинил]амино]бензонитрила формулы (I)-2 007953 его N-оксида, фармацевтически приемлемой кислотно-аддитивной соли, четвертичного амина или стереохимически изомерной формы, который включает осуществление взаимодействия промежуточного соединения формулы (II) его подходящей кислотно-аддитивной соли или стереохимически изомерной формы с промежуточным соединением формулы (III) его подходящей кислотно-аддитивной солью или N-оксидом, где W1 представляет собой подходящую уходящую группу, в присутствии подходящего растворителя. Представленные W1 подходящие уходящие группы представляют собой, например, галоген, трифлат, тозилат, метилсульфонил и тому подобное. Предпочтительно, W1 представляет собой галоген, более конкретно хлор. Подходящими растворителями для приведенной выше реакции являются, например, ацетонитрил; спирт, такой как, например, этанол, 2-пропанол, 2-пропанол-НСl; N,N-диметилформамид; N,Nдиметилацетамид; 1-метил-2-пирролидинон; 1,4-диоксан; монометиловый эфир пропиленгликоля. Предпочтительно, растворителем является ацетонитрил; спирт, такой как, например, этанол, 2-пропанол, 2 пропанол-НСl; N,N-диметилформамид; N,N-диметилацетамид; монометиловый эфир пропиленгликоля. Более предпочтительно, растворителем является 2-пропанол, 6 н. НСl в 2-пропаноле или ацетонитрил,особенно ацетонитрил. Предпочтительно промежуточное соединение формулы (II) применяется в форме кислотноаддитивной соли, особенно в форме аддитивной соли хлористо-водородной кислоты, и промежуточное соединение формулы (III) предпочтительно применяется в форме свободного основания. Полученный в описанной выше реакции продукт может быть удобным образом выделен в форме основания или в форме кислотно-аддитивной соли, и затем он может быть преобразован в кислотноаддитивную соль путем обработки кислотой, или наоборот, продукт в форме кислотно-аддитивной соли может быть преобразован в свободное основание путем обработки щелочью, и, если требуется, могут быть получены стереохимически изомерные формы, N-оксиды или четвертичные амины соединения. Выделение соединения реакции из реакционной среды и, при необходимости, его дальнейшая очистка могут быть выполнены в соответствии с общеизвестными в данной области техники методиками, такими как, например, экстракция, кристаллизация, перегонка, растирание в порошок сухим способом и хроматография. В соответствии с другим аспектом настоящее изобретение относится к способу получения 4-4-4(2-цианоэтенил)-2,6-диметилфенил]амино]-2-пиримидинил]амино]бензонитрила формулы (I) его N-оксида, фармацевтически приемлемой кислотно-аддитивной соли, четвертичного амина или стереохимически изомерной формы, который включает осуществление взаимодействия промежуточного соединения формулы (IV) его подходящей кислотно-аддитивной соли или N-оксида, где W2 представляет собой подходящую уходящую группу, с ацетонитрилом в присутствии подходящего палладиевого катализатора, подходящего-3 007953 основания и подходящего растворителя. Представленные W2 подходящие уходящие группы представляют собой, например, галоген, трифлат, тозилат, мезилат и тому подобное. Предпочтительно W2 представляет собой галоген, более конкретно йод или бром. Палладиевый (Pd) катализатор может представлять собой гомогенный Pd катализатор, такой как,например, Pd(OAc)2, PdCl2, Pd(PPh3)4, Pd(PPh3)2Cl2, Pd2(dba)3(трис(дибензилиденацетон)дипалладий),металлацикл палладийтиометилфенилглутарамида и тому подобное, или гетерогенный Pd катализатор,такой как, например, палладий на угле, палладий на оксидах металлов, палладий на цеолитах. Предпочтительно, палладиевый катализатор представляет собой гетерогенный Pd катализатор, более предпочтительно палладий на угле (Pd/C). Pd/C представляет собой регенерируемый катализатор и является стабильным и сравнительно недорогим. Он может быть легко отделен (фильтрацией) от реакционной смеси, снижая тем самым риск содержания следов Pd в конечном продукте. С применением Pd/C также избегается необходимость применения лигандов, таких как, например, фосфиновые лиганды, которые являются дорогими, токсичными и загрязняющими синтезируемые продукты. Подходящими основаниями являются, например, ацетат натрия, ацетат калия, N,N-диэтилэтанамин,гидрокарбонат натрия, гидроксид натрия и тому подобное. Подходящими растворителями являются, например, ацетонитрил, N,N-диметилацетамид, ионогенная жидкость, например [bmim]PF6, N,N-диметилформамид, вода, тетрагидрофуран, диметилсульфоксид,1-метил-2-пирролидинон и тому подобное. Полученное в описанной выше реакции соединение может быть, если требуется, преобразовано в кислотно-аддитивную соль путем обработки кислотой, и, если требуется, могут быть получены стереохимически изомерные формы, N-оксиды или четвертичные амины соединения. Выделение продукта реакции из реакционной среды и, при необходимости, его дальнейшая очистка могут быть выполнены в соответствии с общеизвестными в данной области техники методиками, такими как, например, экстракция, кристаллизация, перегонка, растирание в порошок сухим способом и хроматография. Альтернативно, соединение формулы (I) может быть также получено путем дегидратирования соответствующего амидного производного. Поэтому настоящее изобретение также относится к способу получения 4-4-4-(2-цианоэтенил)2,6-диметилфенил]амино]-2-пиримидинил]амино]бензонитрила формулы (I) его N-оксида, фармацевтически приемлемой кислотно-аддитивной соли, четвертичного амина или стереохимически изомерной формы, который включает осуществление взаимодействия промежуточного соединения формулы (VI) его подходящей кислотно-аддитивной соли или стереохимически изомерной формы с промежуточным соединением формулы (III) его подходящей кислотно-аддитивной солью или N-оксидом, где W1 представляет собой подходящую уходящую группу, в присутствии подходящего растворителя с последующей дегидратацией полученного таким образом промежуточного соединения формулы (VII) его подходящей кислотно-аддитивной соли, стереохимически изомерной формы или N-оксида. Представленные W1 подходящие уходящие группы представляют собой, например, галоген, трифлат, тозилат, метилсульфонил и тому подобное. Предпочтительно W1 представляет собой галоген, более конкретно хлор. Подходящими растворителями для приведенной выше реакции являются, например, ацетонитрил; спирт, такой как, например, этанол, 2-пропанол, 2-пропанол-НСl; N,N-диметилформамид; N,Nдиметилацетамид; 1-метил-2-пирролидинон; 1,4-диоксан; монометиловый эфир пропиленгликоля. Предпочтительно, растворителем является ацетонитрил; спирт, такой как, например, этанол, 2-пропанол, 2 пропанол-НС 1; N,N-диметилформамид; N,N-диметилацетамид; монометиловый эфир пропиленгликоля. Более предпочтительно растворителем является 2-пропанол, 6 н. НСl в 2-пропаноле или ацетонитрил. Преобразование промежуточного соединения формулы (VII) в соединение формулы (I), т.е. стадия дегидратации, может быть выполнено в соответствии с методиками, хорошо известными специалисту в данной области, такими как изложенные в работе "Comprehensive Organic Transformations. A guide tofunctional group preparations" by Richard C. Larock, John WileySons, Inc., 1999, p 1983-1985, которая включена в этот документ в качестве ссылки. В указанной работе перечислены различные подходящие реагенты, такие как, например, SOCl2, HOSO2NH2, ClSO2NCO, MeO2CNSO2NEt3, PhSO2Cl, TsCl, P2O5,(Ph3PO3SCF3)O3SCF3, полифосфатный сложный эфир, (EtO)2POP(OEt)2, (EtO)3PI2, 2-хлор-1,3,2-диоксафосфолан, 2,2,2-трихлор-2,2-дигидро-1,3,2-диоксафосфолан, РOСl3, PPh3, P(NCl2)3, P(NEt2)3, COCl2,NaClAlCl3, ClCOCOCl, ClCO2Me, Cl3CCOCl, (CF3CO)2O, Cl3CN=CCl2, 2,4,6-трихлор-1,3,5-триазин,HN(SiMe2)3, N(SiMe2)4, метансульфонилхлорид и тому подобное. Все перечисленные в указанной публикации реагенты включены в этот документ посредством ссылки. Полученное в описанной выше реакции соединение может быть удобным образом выделено в форме основания или в форме кислотно-аддитивной соли, и затем оно может быть преобразовано в кислотно-аддитивную соль путем обработки кислотой, или наоборот, соединение в форме кислотно-аддитивной соли может быть преобразовано в свободное основание путем обработки щелочью, и, если требуется,могут быть получены стереохимически изомерные формы, N-оксиды или четвертичные амины соединения. Выделение продукта реакции из реакционной среды и, при необходимости, его дальнейшая очистка могут быть выполнены в соответствии с общеизвестными в данной области техники методиками, такими как, например, экстракция, кристаллизация, перегонка, растирание в порошок сухим способом и хроматография. Дополнительно настоящее изобретение относится к способу получения 4-4-4-(2-цианоэтенил)2,6-диметилфенил]амино]-2-пиримидинил]амино]бензонитрила формулы (I) его N-оксида, фармацевтически приемлемой кислотно-аддитивной соли, четвертичного амина или стереохимически изомерной формы, который включает осуществление взаимодействия промежуточного соединения формулы (IV) его подходящей кислотно-аддитивной соли или N-оксида, где W2 представляет собой подходящую уходящую группу, с акриламидом в присутствии подходящего палладиевого катализатора, подходящего основания и подходящего растворителя с последующей дегидратацией полученного таким образом промежуточного соединения формулы (VII)-5 007953 его подходящей кислотно-аддитивной соли, стереохимически изомерной формы или N-оксида. Представленные W2 подходящие уходящие группы представляют собой, например, галоген, трифлат, тозилат, мезилат и тому подобное. Предпочтительно W2 представляет собой галоген, более конкретно йод или бром. Палладиевый (Pd) катализатор может представлять собой гомогенный Pd катализатор, такой как,например, Pd(OAc)2, PdCl2, Pd(PPh3)4, Pd(PPh3)2Cl2, Pd2(dba)3(трис(дибензилиденацетон)дипалладий),металлацикл палладийтиометилфенилглутарамида и тому подобное, или гетерогенный Pd катализатор,такой как, например, палладий на угле, палладий на оксидах металлов, палладий на цеолитах. Предпочтительно палладиевый катализатор представляет собой гетерогенный Pd катализатор, более предпочтительно палладий на угле (Pd/C). Pd/C представляет собой регенерируемый катализатор и является стабильным и сравнительно недорогим. Он может быть легко отделен (фильтрацией) от реакционной смеси, снижая тем самым риск содержания следов Pd в конечном соединении. С применением Pd/C также избегается необходимость применения лигандов, таких как, например, фосфиновые лиганды, которые являются дорогими, токсичными и загрязняющими синтезируемые продукты. Подходящими основаниями являются, например, ацетат натрия, ацетат калия, N,N-диэтилэтанамин,гидрокарбонат натрия, гидроксид натрия и тому подобное. Подходящими растворителями являются, например, ацетонитрил, N,N-диметилацетамид, ионогенная жидкость, например, [bmim]PF6, N,N-диметилформамид, вода, тетрагидрофуран, диметилсульфоксид, 1-метил-2-пирролидинон и тому подобное. Преобразование промежуточного соединения формулы (VII) в соединение формулы (I), т.е. стадия дегидратации, может быть выполнено в соответствии с методиками, хорошо известными специалисту в данной области, такими как изложенные в работе "Comprehensive Organic Transformations. A guide tofunctional group preparations" by Richard C. Larock, John WileySons, Inc., 1999, pp.1983-1985, которая включена в этот документ в качестве ссылки. В указанной работе перечислены различные подходящие реагенты, такие как, например, SOCl2, HOSO2NH2, ClSO2NCO, MeO2CNSO2NEt3, PhSO2Cl, TsCl, P2O5,(Ph3PO3SCF3)O3SCF3, полифосфатный сложный эфир, (EtO)2POP(OEt)2, (EtO)3PI2, 2-хлор-1,3,2-диоксафосфолан, 2,2,2-трихлор-2,2-дигидро-1,3,2-диоксафосфолан, РOСl3, PPh3, P(NCl2)3, P(NEt2)3, COCl2,NaClAlCl3, ClCOCOCl, ClCO2Me, Cl3CCOCl, (CF3CO)2O, Cl3CN=CCl2, 2,4,6-трихлор-1,3,5-триазин,HN(SiMe2)3, N(SiMe2)4, метансульфонилхлорид и тому подобное. Все перечисленные в указанной публикации реагенты включены в этот документ посредством ссылки. Полученное в описанной выше реакции соединение может быть, если требуется, преобразовано в кислотно-аддитивную соль путем обработки кислотой, и, если требуется, могут быть получены стереохимически изомерные формы, N-оксиды или четвертичные амины соединения. Выделение продукта реакции из реакционной среды и, при необходимости, его дальнейшая очистка могут быть выполнены в соответствии с общеизвестными в данной области техники методиками, такими как, например, экстракция, кристаллизация, перегонка, растирание в порошок сухим способом и хроматография. Для достижения эффективного процесса синтеза является недостаточным оптимизировать только конечную стадию реакции, т.е. стадию реакции, на которой образуется желаемый продукт реакции, а оптимизации также требуют стадии синтеза промежуточных соединений. Поэтому дополнительный аспект настоящего изобретения относится к способу получения ключевого промежуточного соединения, т.е. промежуточного соединения формулы (II), при синтезе соединения формулы (I) или его N-оксида, фармацевтически приемлемой аддитивной соли, четвертичного амина или стереохимически изомерной формы. Таким образом, настоящее изобретение также относится к способу получения промежуточного соединения формулы (II) его подходящей кислотно-аддитивной соли, четвертичного амина или стереохимически изомерной формы, который включает осуществление взаимодействия промежуточного соединения формулы (V) его подходящей кислотно-аддитивной соли или четвертичного амина, где W3 представляет собой подхо-6 007953 дящую уходящую группу, с ацетонитрилом в присутствии подходящего палладиевого катализатора, подходящего основания и подходящего растворителя. Представленные W3 подходящие уходящие группы представляют собой, например, галоген, трифлат, тозилат, мезилат и тому подобное. Предпочтительно W3 представляет собой галоген, более конкретно йод или бром. Наиболее предпочтительным является йод. Палладиевый (Pd) катализатор может представлять собой гомогенный Pd катализатор, такой как,например, Pd(OAc)2, PdCl2, Pd(PPh3)4, Pd(PPh3)2Cl2, Pd2(dba)3(трис(дибензилиденацетон)дипалладий),металлацикл палладийтиометилфенилглутарамида и тому подобное, или гетерогенный Pd катализатор,такой как, например, палладий на угле, палладий на оксидах металлов, палладий на цеолитах. Предпочтительно палладиевый катализатор представляет собой гетерогенный Pd катализатор, более предпочтительно палладий на угле (Pd/C). Pd/C представляет собой регенерируемый катализатор и является стабильным и сравнительно недорогим. Он может быть легко отделен (фильтрацией) от реакционной смеси, снижая тем самым риск содержания следов Pd в конечном соединении. С применением Pd/C также избегается необходимость применения лигандов, таких как, например, фосфиновые лиганды, которые являются дорогими, токсичными и загрязняющими синтезируемые продукты. Подходящими основаниями являются, например, ацетат натрия, ацетат калия, N,N-диэтилэтанамин,гидрокарбонат натрия, гидроксид натрия и тому подобное. Подходящими растворителями являются, например, ацетонитрил, N,N-диметилацетамид, ионогенная жидкость, например [bmim]PF6, N,N-диметилформамид, вода, тетрагидрофуран, диметилсульфоксид,1-метил-2-пирролидинон и тому подобное. Полученное в описанной выше реакции соединение может быть, если требуется, преобразовано в кислотно-аддитивную соль путем обработки кислотой, и, если требуется, могут быть получены стереохимически изомерные формы, N-оксиды или четвертичные амины соединения. Выделение продукта реакции из реакционной среды и, при необходимости, его дальнейшая очистка могут быть выполнены в соответствии с общеизвестными в данной области техники методиками, такими как, например, экстракция, кристаллизация, перегонка, растирание в порошок сухим способом и хроматография. Альтернативно, промежуточное соединение формулы (II) может быть также получено путем дегидратирования соответствующего амидного производного. Такимобразом, настоящее изобретение также относится к способу получения промежуточного соединения формулы (II) его подходящей кислотно-аддитивной соли, четвертичного амина или стереохимически изомерной формы, который включает осуществление взаимодействия промежуточного соединения формулы (V) его подходящей кислотно-аддитивной соли или четвертичного амина, где W3 представляет собой подходящую уходящую группу, с акриламидом в присутствии подходящего палладиевого катализатора, подходящего основания и подходящего растворителя с последующей дегидратацией полученного таким образом промежуточного соединения формулы (VI) его подходящей кислотно-аддитивной соли, четвертичного амина или стереохимически изомерной формы. Представленные W3 подходящие уходящие группы представляют собой, например, галоген, трифлат, тозилат, мезилат и тому подобное. Предпочтительно W3 представляет собой галоген, более конкрет-7 007953 но йод или бром. Палладиевый (Pd) катализатор может представлять собой гомогенный Pd катализатор, такой как,например, Pd(OAc)2, PdCl2, Pd(PPh3)4, Pd(PPh3)2Cl2, Pd2(dba)3(трис(дибензилиденацетон)дипалладий),металлацикл палладийтиометилфенилглутарамида и тому подобное, или гетерогенный Pd катализатор,такой как, например, палладий на угле, палладий на оксидах металлов, палладий на цеолитах. Предпочтительно палладиевый катализатор представляет собой гетерогенный Pd катализатор, более предпочтительно палладий на угле (Pd/C). Pd/C представляет собой регенерируемый катализатор и является стабильным и сравнительно недорогим. Он может быть легко отделен (фильтрацией) от реакционной смеси, снижая тем самым риск содержания следов Pd в конечном соединении. С применением Pd/C также избегается необходимость применения лигандов, таких как, например, фосфиновые лиганды, которые являются дорогими, токсичными и загрязняющими синтезируемые продукты. Подходящими основаниями являются, например, ацетат натрия, ацетат калия, N,N-диэтилэтанамин,гидрокарбонат натрия, гидроксид натрия и тому подобное. Подходящими растворителями являются, например, ацетонитрил, N,N-диметилацетамид, ионогенная жидкость, например, [bmim]PF6, N,N-диметилформамид, вода, тетрагидрофуран, диметилсульфоксид, 1-метил-2-пирролидинон и тому подобное. Преобразование промежуточного соединения формулы (VI) в соединение формулы (II), т.е. стадия дегидратации, может быть выполнено в соответствии с методиками, хорошо известными специалисту в данной области техники, такими как изложенные в работе "Comprehensive Organic Transformations. Aguide to functional group preparations" by Richard C. Larock, John WileySons, Inc., 1999, pp.1983-1985,которая включена в этот документ в качестве ссылки. В указанной работе перечислены различные подходящие реагенты, такие как, например, SOCl2, HOSO2NH2, ClSO2NCO, MeO2CNSO2 NEt3, PhSO2Cl,TsCl, P2O5, (Ph3PO3SCF3)O3SCF3, полифосфатный сложный эфир, (EtO)2POP(OEt)2, (EtO)3PI2, 2-хлор 1,3,2-диоксафосфолан, 2,2,2-трихлор-2,2-дигидро-1,3,2-диоксафосфолан, РOСl3, PPh3, P(NCl2)3, P(NEt2)3,COCl2, NaClAlCl3; ClCOCOCl, ClCO2Me, Cl3CCOCl, (CF3CO)2O, Cl3CN=CCl2, 2,4,6-трихлор-1,3,5 триазин, HN(SiMe2)3, N(SiMe2)4, метансульфонилхлорид и тому подобное. Все перечисленные в указанной публикации реагенты включены в этот документ посредством ссылки. Полученное в описанной выше реакции соединение может быть, если требуется, преобразовано в кислотно-аддитивную соль путем обработки кислотой, и, если требуется, могут быть получены стереохимически изомерные формы, N-оксиды или четвертичные амины соединения. Выделение продукта реакции из реакционной среды и, при необходимости, его дальнейшая очистка могут быть выполнены в соответствии с общеизвестными в данной области техники методиками, такими как, например, экстракция, кристаллизация, перегонка, растирание в порошок сухим способом и хроматография. Используемый выше в этом документе и далее в этом документе термин галоген является обобщенным для фтора, хлора, брома и йода. Пригодными для терапевтического применения солями соединения формулы (I) являются соли, в которых противоион является фармацевтически приемлемым. Однако соли кислот и оснований, которые не являются фармацевтически приемлемыми, могут также находить применение, например, при получении или очистке фармацевтически приемлемого соединения. Все соли, являющиеся фармацевтически приемлемыми или не являющиеся ими, подпадают под объем настоящего изобретения. Под упоминаемыми выше в этом документе и далее в этом документе фармацевтически приемлемыми аддитивными солями понимают терапевтически активные формы нетоксичных кислотноаддитивных солей, которые способно образовывать соединение формулы (I). Последние могут быть подходящим образом получены путем обработки соединения в основной форме подходящими кислотами,такими как неорганические кислоты, например, галогенводородные кислоты, например, хлористоводородная, бромисто-водородная и тому подобное; серная кислота; азотная кислота; фосфорная кислота и тому подобное; или органические кислоты, например, уксусная, пропионовая, гидроксиуксусная, 2 гидроксипропионовая, 2-оксопропионовая, щавелевая, малоновая, янтарная, малеиновая, фумаровая, яблочная, винная, 2-гидрокси-1,2,3-пропантрикарбоновая, метансульфоновая, этансульфоновая, бензолсульфоновая, 4-метилбензолсульфоновая, циклогексансульфамовая, 2-гидроксибензойная, 4-амино-2 гидроксибензойная и тому подобные кислоты. Обратно кислотная форма может быть преобразована в форму свободного основания путем обработки основанием. Термин аддитивная соль также включает в себе гидраты и аддитивные формы растворителя, которые способно образовывать соединение формулы (I). Примерами таких форм являются, например,гидраты, алкоголяты и тому подобное. Используемый выше в этом документе и далее в этом документе термин четвертичные амины обозначает четвертичные соли аммония, которые соединение формулы (I) способно образовывать при взаимодействии основного азота соединения формулы (I) и подходящего кватернизирующего агента,такого как, например, необязательно замещенный алкилгалогенид, арилгалогенид или арилалкилгалогенид, например, метилйодид или бензилйодид. Также могут применяться другие реагенты с хорошо уходящими группами, такие как алкилтрифторметансульфонаты, алкилметансульфонаты и алкил-пара-8 007953 толуолсульфонаты. Четвертичный амин содержит положительно заряженный атом азота. Фармацевтически приемлемые противоионы включают хлор, бром, йод, трифторацетат и ацетат. Противоион по выбору может быть введен с применением ионообменных смол. Подразумевается, что N-оксидные формы соединений по настоящему изобретению включают соединения формулы (I), в которых один или несколько третичных атомов азота окислены до так называемого N-оксида. Соединение формулы (I) может быть преобразовано в соответствующие N-оксидные формы, следуя известным в данной области техники методикам преобразования трехвалентного азота в его N-оксидную форму. Указанная реакция N-оксидирования, как правило, может быть выполнена путем осуществления взаимодействия исходного соединения формулы (I) с подходящим органическим или неорганическим пероксидом. Подходящие неорганические пероксиды включают, например, пероксид водорода, пероксиды щелочных и щелочно-земельных металлов, например пероксид натрия, пероксид калия; подходящие органические пероксиды могут включать надкислоты, такие как, например, бензолпероксокарбоновая кислота или галогензамещенная бензолпероксокарбоновая кислота, например 3-хлорбензолпероксокарбоновая кислота, пероксоалкановые кислоты, например пероксоуксусная, алкилгидропероксиды, например трет-бутилгидропероксид. Подходящими растворителями являются, например, вода, низшие спирты, например этанол и тому подобное, углеводороды, например толуол, кетоны, например 2 бутанон, галогенированные углеводороды, например дихлорметан, и смеси таких растворителей. Следует принимать во внимание, что соединение формулы (I) и его N-оксиды, аддитивные соли,четвертичные амины и стереохимически изомерные формы могут содержать один или несколько центров хиральности и существовать в стереохимически изомерных формах. Используемый выше в этом документе и далее в этом документе термин стереохимически изомерные формы обозначает все возможные стереоизомерные формы, которые могут принимать соединение формулы (I) и его N-оксиды, аддитивные соли, четвертичные амины или физиологически активные производные. Если не упомянуто или не указано иначе, химическое изображение соединений обозначает смесь всех возможных стереохимически изомерных форм, причем указанные смеси содержат все диастереомеры и энантиомеры основной структуры молекулы, а также каждую из индивидуальных изомерных форм формулы (I) и его N-оксидов, солей, сольватов и четвертичных аминов, по существу, свободными,т.е. связанными менее чем с 10%, предпочтительно менее чем с 5%, конкретно менее чем с 2% и наиболее предпочтительно менее чем с 1% других изомеров. Конкретно, способные к пространственной изомерии центры могут иметь R- или S-конфигурацию или цис- или транс-конфигурацию; например, заместители в двухвалентных циклических (необязательно) замещенных радикалах могут иметь цис- или транс-конфигурацию. Соединение формулы (I) может обладать Е(entgegen)- или Z(zusammen)стереохимией по двойной связи. Если соединение формулы (I) обозначено как (Е), то это означает, что соединение по существу свободно от (Z)-изомера. Термин цис, транс, R, S, Е и Z хорошо известны специалистам в данной области. Следует понимать, что стереохимически изомерные формы соединения формулы (I), несомненно, подпадают под объем настоящего изобретения. Подразумевается, что используемый выше в этом документе и далее в этом документе термин соединение формулы (I) всякий раз также включает его N-оксидные формы, аддитивные соли, четвертичные амины и стереохимически изомерные формы. Особый интерес представляют собой стереохимически чистые соединения формулы (I). Предпочтительным соединением является соединение X.Z-изомер 4-4-4-(2-цианоэтенил)-2,6-диметилфенил]амино]-2-пиримидинил]амино]бензонитрила может быть также получен в соответствии с реакциями по настоящему изобретению и может быть выделен в соответствии с известными в данной области техники методиками. Следовательно, (Z)-изомер 44-4-(2-цианоэтенил)-2,6-диметилфенил]амино]-2-пиримидинил]амино]бензонитрила также подпадает под объем настоящего изобретения. Следующие примеры иллюстрируют настоящее изобретение. Экспериментальная часть А. Получение промежуточных соединений. Пример А 1. Получение промежуточного соединения (II). а) К раствору 159 г 4-йод-2,6-диметилбензоламина в 650 мл N,N-диметилацетамида добавляли 63,8 г ацетата натрия. Реакционную смесь выдерживали в атмосфере азота. Добавляли 7 г увлажненного палладия на угле (Pd/C 10%) и 64,4 мл ацетонитрила. Реакционную смесь нагревали до 130 С и перемешивали-9 007953 в течение ночи. После охлаждения до комнатной температуры добавляли 0,5 л толуола и 0,5 л N,Nдиметилацетамида. Реакционную смесь фильтровали через Dicalite и промывали остаток 0,5 л толуола. К перемешиваемой в течение 30 мин смеси добавляли воду (6 л). Разделяли слои. К водному слою добавляли 1 л толуола и перемешивали смесь в течение 30 мин. Снова разделяли слои. Отделенные органические слои собирали и выпаривали растворитель. Выход: 123 г промежуточного соединения формулы (II). Время удерживания промежуточного соединения формулы (II) на продуваемой гелием колонкеCPSIL8CB (25 м х 0,32 мм х 0,5 мкм) (начальная температура 40 С с повышением на 10 С/мин до момента достижения температуры 300 С) составляло 17,5 мин для (Z)-изомера и 18,77 мин для (Е)-изомера. Пример А 2. Получение аддитивной соли хлористо-водородной кислоты (1:1) промежуточного соединения формулы (II).a) К смеси 123 г промежуточного соединения формулы (II) в 630 мл этанола добавляли 1,25 л диизопропилового эфира. Реакционную смесь выдерживали в атмосфере азота. Смесь нагревали до 60 С и перемешивали в течение 30 мин. Добавляли 120 мл 6 н. раствора хлористо-водородной кислоты в 2 пропаноле и перемешивали смесь в течение 30 мин. После охлаждения до комнатной температуры реакционную смесь фильтровали и промывали остаток 100 мл 2-пропанола. Полученный остаток сушили при пониженном давлении при 50 С. Выход: 103 г (77%) аддитивной соли хлористо-водородной кислоты(1:1) промежуточного соединения формулы (II).b) В реактор загружали 1,012 кг увлажненного палладия на угле (Pd/C 10%), 9,361 кг ацетата натрия и 34,41 кг N,N-диметилацетамида и помещали в атмосферу азота. Смесь перемешивали и нагревали при 140 С. Во второй реактор загружали 23,497 кг 4-йод-2,6-диметилбензоламина, 7,569 кг акрилонитрила и 54,98 кг N,N-диметилацетамида и помещали в атмосферу азота. Смесь перемешивали при комнатной температуре в течение 30 мин. Раствор из второго реактора переносили в течение 1 ч в первый реактор и в первом реакторе поддерживали температуру 140 С. Реакционную смесь перемешивали при 140 С в течение ночи, а затем оставляли охлаждаться до комнатной температуры. Затем реакционную смесь фильтровали (1) и промывали фильтр 95,1 л толуола (2). К полученной таким образом органической фазе, т.е. (1)+(2), добавляли 380,4 л воды и энергично перемешивали смесь. Затем перемешивание останавливали и разделяли фазы (3). Водный слой однократно промывали 95,1 л толуола и снова разделяли фазы(4). Объединенные органические фазы, т.е. (3)+(4), переносили во второй реактор и перегоняли при пониженном давлении. Добавляли 190,2 л EtOH и перемешивали смесь при комнатной температуре. При комнатной температуре добавляли раствор НСl (6 н.) в 2-пропаноле (18,13 л), реакционную смесь оставляли перемешиваться при комнатной температуре в течение ночи, а затем фильтровали . Полученное твердое вещество промывали 14,74 л 2-пропанолаи сушили при пониженном давлении при 50 С. Выход: 50-60% соли хлористо-водородной кислоты (1:1) промежуточного соединения формулы (II). Дополнительное количество соединения (10-15%) рекуперировали путем перегонки фильтратаи промывной жидкостис последующей фильтрацией при комнатной температуре. Пример A3. Получение промежуточного соединения формулы (III), где W1 представляет собой хлор, причем указанное промежуточное соединение представлено формулой (III-а). Промежуточное соединение формулы (III-а) получали на основании методики, описанной в WO 99/50250. Конкретно, смесь 4-[(1,4-дигидро-4-оксо-2-пиримидинил)амино]бензонитрила (0,12 моль) в РОСl3(90 мл) перемешивали и нагревали при кипении с обратным холодильником в атмосфере аргона в течение 20 мин. Реакционную смесь медленно вливали в 750 мл смеси воды со льдом, и отделяли твердое вещество путем фильтрации. Твердое вещество суспендировали в 500 мл воды и доводили рН суспензии до нейтральных значений добавлением 20% раствора NaOH. Твердое вещество снова отделяли путем- 10007953 фильтрации, суспендировали в 200 мл 2-пропанона и добавляли 1000 мл СН 2 Сl2. Смесь нагревали до тех пор, пока не растворится твердое вещество. После охлаждения до комнатной температуры водный слой отделяли и сушили органический слой. После удаления осушителя путем фильтрации в фильтрате образовывалось твердое вещество. После дополнительного охлаждения фильтрата в морозильнике с последующей фильтрацией получали 21,38 г (77,2%) [4-[(4-хлор-2-пиримидинил)амино]бензонитрила, т.е. промежуточное соединение формулы (III-а). Время удерживания промежуточного соединения (III-а) на колонке Hypersil BDS (10 см х 4 мм х 3 мкм),(элюируемой 0,5% NH4Ac/CH3CN 90/10 в момент 0 и 0/100 через 15 мин, составляло 8,33 мин. Пример А 4. Получение промежуточного соединения формулы (IV), где W2 представляет собой бром, причем указанное промежуточное соединение представлено формулой (IV-а). Смесь 4-бром-2,6-диметилбензоламина (0,013 моль) и промежуточного соединения (III-а) (0,013 моль) перемешивали при 150 С в течение 1 ч. Смесь вливали в 10% водный раствор К 2 СO3 и экстрагировали СН 2 Сl2/МеОН (95/5). Органический слой отделяли, сушили (MgSO4), фильтровали и выпаривали растворитель. Остаток кристаллизовали из диизопропилового эфира. Осадок отфильтровывали и сушили. Выход: 2,3 г (45%). Маточный слой очищали колоночной хроматографией на силикагеле (элюент:CH2Cl2/CH3OH-NH4OH 98/2/0,2; 15-40 мкм). Чистые фракции собирали и выпаривали растворитель. Выход: 0,90 г (17%). Общий выход промежуточного соединения (IV-a) составил 3,2 г (62%). Время удерживания промежуточного соединения (IV-a) на колонке Hypersil BDS (10 см х 4 мм х 3 мкм),элюируемой 0,5% NH4Ac/CH3CN 90/10 в момент 0 и 0/100 через 15 мин, составляло 10,31 мин. Промежуточное соединение (IV), где W2 представляет собой йод, причем указанное промежуточное соединение представлено формулой (IV-b) может быть получено аналогичным путем. Время удерживания промежуточного соединения (IV-b) на колонке Hypersil BDS (10 см х 4 мм х 3 мкм) элюируемой 0,5% NH4Ac/CH3CN 90/10 в момент 0 и 0/100 через 15 мин составляло 10,54 мин. Пример А 5. а) Получение (Е)-изомера промежуточного соединения формулы (VI). В 10 мл сухого ацетонитрила растворяли 2,00 г (10,0 моль) 4-бром-2,6-диметиланилина, 1,07 г (1,5 экв.) акриламида, 224 мг (0,1 экв.) Pd(OAc)2, 609 мг (0,2 экв.) трис(2-метилфенил)фосфина и 1,52 г N,Nдиэтилэтанамина. Смесь продували N2 в течение 20 мин и перемешивали в течение ночи при 70 С. Смесь разбавляли 150 мл метиленхлорида, промывали насыщенным раствором NaHCO3, сушили (насыщенныйb) Получение (Е)-изомера промежуточного соединения формулы (II). РОСl3 (3 мл) охлаждали до 0 С и добавляли 500 мг (2,63 ммоль) (Е)-изомера промежуточного соединения (VI). Через 30 мин охлаждающую баню удаляли и перемешивали смесь в течение ночи при- 11007953 20 С. Смесь по каплям добавляли к 150 мл диизопропилового эфира при энергичном перемешивании. Остаток фильтровали и промывали диизопропиловым эфиром. Остаток добавляли к 100 мл этилацетата/100 мл насыщенного раствора NaHCO3 и перемешивали. Этилацетатный слой отделяли, сушили (насыщенный NaCl, Na2SO4) и фильтровали. Растворитель выпаривали. Выход: 380 мг (84%) (Е)-изомера промежуточного соединения (II). с) Получение (Е)-изомера промежуточного соединения формулы (VII). В сосуд емкостью 100 мл в атмосфере N2 помещали 0,8 г (4,33 ммоль; 1 экв.) (Е)-изомера промежуточного соединения формулы (VI), 1 г (4,33 ммоль; 1 экв.) промежуточного соединения (III-а) и 16 мл 2 пропанола. К этой смеси добавляли 0,72 мл 6 н. НСl в 2-пропаноле. Смеси перемешивали при температуре кипения с обратным холодильником в течение 72 ч, а затем охлаждали с получением соли НСl (Е)изомера промежуточного соединения (VII). Соль НСl (Е)-изомера промежуточного соединения (VII) может быть преобразована в свободное основание в соответствии с известными в данной области методиками (см. также пример В 1). (Е)-изомер промежуточного соединения (VII) может быть преобразован в соединение X в соответствии со способом,описанным выше в примере А 5b. Пример А 6. Получение (Е)-изомера промежуточного соединения формулы (VII). В сосуд емкостью 100 мл в атмосфере азота помещали 2,53 мл ацетонитрила, 0,056 г (0,253 ммоль)Pd(OAc)2 и 0,154 г (0,506 ммоль) трис(2-метилфенил)фосфина и перемешивали смесь в течение 10 мин. К смеси добавляли 1 г (2,53 ммоль) промежуточного соединения (IV-а), 0,51 мл (3,8 ммоль) N,Nдиэтилэтанамина и 0,36 г (5,06 ммоль) акриламида. Смесь нагревали при кипении с обратным холодильником (80 С) в течение 5 суток с получением 28% (Е)-изомера промежуточного соединения (VII). Время удерживания (Е)-изомера промежуточного соединения (VII) на колонке Hypersil BDS (10 см х 4 мм х 3 мкм), элюируемой 0,5% NH4Ac/CH3CN 90/10 в момент 0 и 0/100 через 15 мин, составляло 6,59 мин.(Е)-изомер промежуточного соединения (VII) может быть преобразован в соединение X в соответствии со способом, описанным выше в примере А 5b. В. Получение (Е)-изомера 4-4-4-(2-цианоэтенил)-2,6-диметилфенил]амино]-2-пиримидинил]амино]бензонитрила (соединение X) (точка плавления 245 С).a) В атмосфере азота получали смесь 93,9 г (0,45 моль) соли хлористо-водородной кислоты промежуточного соединения (II), полученной в соответствии с примером А 2, и 109 г (0,4725 моль) промежуточного соединения (III-а) в 1,8 л ацетонитрила. Смесь перемешивали и нагревали при кипении с обратным холодильником в течение 69 ч, а затем оставляли охлаждаться до 55 С. Смесь фильтровали, промывали остаток 200 мл ацетонитрила, затем сушили при пониженном давлении при 50 С в течение ночи. В 1 л 10% водного раствора К 2 СO3 помещали 144,6 г (0,3666 моль) полученного твердого вещества. Смесь перемешивали при комнатной температуре, а затем фильтровали. Полученный остаток дважды промывали водой, а затем сушили при 50 С при пониженном давлении. Остаток помещали в 6,55 л изопропанола,нагревали смесь при кипении с обратным холодильником, затем перемешивали в течение ночи и фильтровали при комнатной температуре. Остаток сушили при 50 С при пониженном давлении. Выход: 113,2 гb) В атмосфере азота получали смесь 93,9 г (0,45 моль) соли хлористо-водородной кислоты промежуточного соединения (II), полученной в соответствии с примером А 2, и 103,8 г (0,45 моль) промежуточного соединения (III-а) в 0,9 л ацетонитрила. Смесь перемешивали и нагревали при кипении с обратным холодильником в течение 24 ч, а затем оставляли охлаждаться до 50 С. В течение 15-20 мин при 4050 С добавляли раствор К 2 СO3 (124,4 г, 0,9 моль) в Н 2O (0,45 л), а затем перемешивали в течение 1 ч при- 12007953 50 С. Осадок отделяли, дважды промывали 0,045 л ацетонитрила, а затем сушили при 50 С при пониженном давлении. Смешивали 73,3 г полученного твердого вещества и 400 мл EtOH, нагревали при кипении с обратным холодильником в течение 2 ч, а затем оставляли охлаждаться до комнатной температуры. Осадок фильтровали и промывали остаток 50 мл EtOH. Полученный остаток сушили в течение ночи при 50 С при пониженном давлении. Выход: 65,7 г (89,6%) (Е)-изомера 4-4-4-(2-цианоэтенил)2,6-диметилфенил]амино]-2-пиримидинил]амино]бензонитрила (соединение X). Пример В 2. Смесь промежуточного соединения (IV-a) (0,00021 моль), полученного в соответствии с примером А 4, акрилонитрила (CH2=CH-CN) (0,00213 моль), Pd(OAc)2 (0,000043 моль), N,N-диэтилэтанамина(0,000043 моль) и трис(2-метилфенил)фосфина (0,00021 моль) в CH3CN (7 мл) перемешивали в загерметизированном сосуде при 150 С в течение ночи. Добавляли Н 2O. Смесь экстрагировали СН 2 Сl2. Органический слой отделяли, сушили (MgSO4), фильтровали и выпаривали растворитель. Остаток (0,15 г) очищали колоночной хроматографией на силикагеле (элюент: СН 2 Сl2/этилацетат 80/20; 15-40 мкм). Фракцию 1 собирали и выпаривали растворитель с получением 0,045 г 4-4-4-(2-цианоэтенил)-2,6-диметилфенил]амино]-2-пиримидинил]амино]бензонитрила (E/Z=80/20). Твердое вещество кристаллизовали из диэтилового эфира. Выход: 0,035 г (Е)-изомера 4-4-4-(2-цианоэтенил)-2,6-диметилфенил]амино]-2 пиримидинил]амино]бензонитрила (соединение X) (55%). Пример В 3. В сосуд емкостью 100 мл в атмосфере азота помещали 4,41 г (10 ммоль) промежуточного соединения(IV-b) и 15 мл N,N-диметилацетамида. К этой смеси добавляли 0,98 г ацетата натрия (12 ммоль), 107 мг 10% влажного Pd/C (0,1 ммоль Pd) и 1 мл (15 ммоль) акрилонитрила. Смесь нагревали при 140 С и после развития реакции подвергали жидкостной хроматографии. В результате реакции получали 4-4-4-(2 цианоэтенил)-2,6-диметилфенил]амино]-2-пиримидинил]амино]бензонитрил (E/Z=80/20), который может быть посвящен в (Е)-изомер 4-4-4-(2-цианоэтенил)-2,6-диметилфенил]амино]-2-пиримидинил] амино]бензонитрила, как описано в примере В 2 выше. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Способ получения нил]амино]бензонитрила формулы (I) 4-4-4-(2-цианоэтенил)-2,6-диметилфенил]амино]-2-пиримиди его N-оксида, фармацевтически приемлемой кислотно-аддитивной соли, четвертичного амина или стереохимически изомерной формы, который включает осуществление взаимодействия промежуточного соединения формулы (II) его подходящей кислотно-аддитивной соли или стереохимически изомерной формы с промежуточным соединением формулы (III) его подходящей кислотно-аддитивной солью или N-оксидом, где W1 представляет собой подходящую уходящую группу, в присутствии подходящего растворителя,необязательно, с последующим, если требуется, преобразованием свободного основания в кислотно-аддитивную соль путем обработки кислотой, или наоборот, преобразованием продукта в форме кислотно-аддитивной соли в свободное основание путем обработки щелочью; и, необязательно, с последующим, если требуется, получением его стереохимически изомерных форм, N-оксидных форм или чет- 13007953 вертичных аминов. 2. Способ по п.1, в котором растворителем является ацетонитрил. 3. Способ по п.1, в котором растворителем является 1-метил-2-пирролидинон. 4. Способ по любому из пп.1-3, где промежуточное соединение формулы II, его подходящую кислотно-аддитивную соль или стереохимически изомерную форму подвергают взаимодействию с промежуточным соединением формулы (III) или его подходящей кислотно-аддитивной солью. 5. Способ получения 4-4-4-(2-цианоэтенил)-2,6-диметилфенил]амино]-2-пиримидинил]амино]бензонитрила формулы (I) его N-оксида, фармацевтически приемлемой кислотно-аддитивной соли, четвертичного амина или стереохимически изомерной формы, который включает осуществление взаимодействия промежуточного соединения формулы (IV) его подходящей кислотно-аддитивной соли или N-оксида, где W2 представляет собой подходящую уходящую группу с ацетонитрилом в присутствии подходящего палладиевого катализатора, подходящего основания и подходящего растворителя,необязательно, с последующим, если требуется, преобразованием свободного основания в кислотно-аддитивную соль путем обработки кислотой, или наоборот, преобразованием продукта в форме кислотно-аддитивной соли в свободное основание путем обработки щелочью; и, необязательно, с последующим, если требуется, получением его стереохимически изомерных форм, N-оксидных форм или четвертичных аминов. 6. Способ получения 4-4-4-(2-цианоэтенил)-2,6-диметилфенил]амино]-2-пиримидинил]амино]бензонитрила формулы (I) его N-оксида, фармацевтически приемлемой кислотно-аддитивной соли, четвертичного амина или стереохимически изомерной формы, который включает осуществление взаимодействия промежуточного соединения формулы (VI) его подходящей кислотно-аддитивной соли или стереохимически изомерной формы с соединением формулы (III) его подходящей кислотно-аддитивной солью или N-оксидом, где W1 представляет собой подходящую уходящую группу, в присутствии подходящего растворителя, с последующей дегидратацией полученного таким образом промежуточного соединения формулы (VII) его подходящей кислотно-аддитивной соли, стереохимически изомерной формы или N-оксида,необязательно, с последующим, если требуется, преобразованием свободного основания в кислотно-аддитивную соль путем обработки кислотой, или наоборот, преобразованием продукта в форме кислотно-аддитивной соли в свободное основание путем обработки щелочью; и, необязательно, с последующим, если требуется, получением его стереохимически изомерных форм, N-оксидных форм или четвертичных аминов. 7. Способ получения 4-4-4-(2-цианоэтенил)-2,6-диметилфенил]амино]-2-пиримидинил]амино]бензонитрила формулы (I) его N-оксида, фармацевтически приемлемой кислотно-аддитивной соли, четвертичного амина или стереохимически изомерной формы, который включает осуществление взаимодействия промежуточного соединения формулы (IV) его подходящей кислотно-аддитивной соли или N-оксида, где W2 представляет собой подходящую уходящую группу, с акриламидом в присутствии подходящего палладиевого катализатора, подходящего основания и подходящего растворителя с последующей дегидратацией полученного таким образом промежуточного соединения формулы (VII) его подходящей кислотно-аддитивной соли, стереохимически изомерной формы или N-оксида,необязательно, с последующим, если требуется, преобразованием свободного основания в кислотно-аддитивную соль путем обработки кислотой, или наоборот, преобразованием продукта в форме кислотно-аддитивной соли в свободное основание путем обработки щелочью; и, необязательно, с последующим, если требуется, получением его стереохимически изомерных форм, N-оксидных форм или четвертичных аминов. 8. Способ получения промежуточного соединения формулы (II) его подходящей кислотно-аддитивной соли, четвертичного амина или стереохимически изомерной формы, который включает осуществление взаимодействия промежуточного соединения формулы (V)- 15007953 его подходящей кислотно-аддитивной соли или четвертичного амина, где W3 представляет собой подходящую уходящую группу, с ацетонитрилом в присутствии подходящего палладиевого катализатора, подходящего основания и подходящего растворителя,необязательно, с последующим, если требуется, преобразованием свободного основания в кислотно-аддитивную соль путем обработки кислотой, или наоборот, преобразованием соединения в форме кислотно-аддитивной соли в свободное основание путем обработки щелочью; и, необязательно, с последующим, если требуется, получением его стереохимически изомерных форм, N-оксидных форм или четвертичных аминов. 9. Способ по п.5 или 8, в котором палладиевый катализатор представляет собой гетерогенный палладиевый катализатор. 10. Способ по п.9, в котором гетерогенным палладиевым катализатором является палладий на угле. 11. Способ получения промежуточного соединения формулы (II) его подходящей кислотно-аддитивной соли, четвертичного амина или стереохимически изомерной формы, который включает осуществление взаимодействия промежуточного соединения формулы (V) его подходящей кислотно-аддитивной соли или четвертичного амина, где W3 представляет собой подходящую уходящую группу, с акриламидом в присутствии подходящего палладиевого катализатора, подходящего основания и подходящего растворителя с последующей дегидратацией полученного таким образом промежуточного соединения формулы (VI) его подходящей кислотно-аддитивной соли, четвертичного амина или стереохимически изомерной формы,необязательно, с последующим, если требуется, преобразованием свободного основания в кислотно-аддитивную соль путем обработки кислотой, или наоборот, преобразованием продукта в форме кислотно-аддитивной соли в свободное основание путем обработки щелочью; и, необязательно, с последующим, если требуется, получением его стереохимически изомерных форм, N-оксидных форм или четвертичных аминов. 12. Способ по любому из пп.1-7, в котором 4-4-4-(2-цианоэтенил)-2,6-диметилфенил]амино]-2 пиримидинил]амино]бензонитрил формулы (I), его N-оксид, фармацевтически приемлемая кислотноаддитивная соль, четвертичный амин или стереохимически изомерная форма представляет собой (Е)-44-4-(2-цианоэтенил)-2,6-диметилфенил]амино]-2-пиримидинил]амино]бензонитрил.
МПК / Метки
МПК: C07C 255/42, A61K 31/505, C07C 253/20, C07D 239/48, C07C 253/30
Метки: получения, способы, 4-[[4-[[4-(2-цианоэтенил)-2,6-диметилфенил]амино]-2-пиримидинил]амино]бензонитрила
Код ссылки
<a href="https://eas.patents.su/17-7953-sposoby-polucheniya-4-4-4-2-cianoetenil-26-dimetilfenilamino-2-pirimidinilaminobenzonitrila.html" rel="bookmark" title="База патентов Евразийского Союза">Способы получения 4-[[4-[[4-(2-цианоэтенил)-2,6-диметилфенил]амино]-2-пиримидинил]амино]бензонитрила</a>
Предыдущий патент: Применение ирбесартана для изготовления лекарств, которые пригодны для предупреждения или лечения лёгочной артериальной гипертензии
Следующий патент: Фармацевтическая препаративная форма, включающая мелатонин
Случайный патент: Движущийся тротуар, движущаяся наклонная плоскость или эскалатор