Производные замещенного 2-пиримидинил-6, 7, 8, 9-тетрагидропиримидо [1,2-а]пиримидин-4-она и 7-пиримидинил-2,3-дигидроимидазо[1, 2-а]пиримидин-5( 1н )она для нейродегенеративных нарушений
Номер патента: 7165
Опубликовано: 25.08.2006
Авторы: Маргери Северен, Галле Тьерри, Саади Мурад, Словински Франк, Локхид Алистер, Ларденуа Патрик, Неделек Ален, Йеш Филипп
Формула / Реферат
1. Производное пиримидона, представленное формулой (I), или его соль, или его сольват, или его гидрат
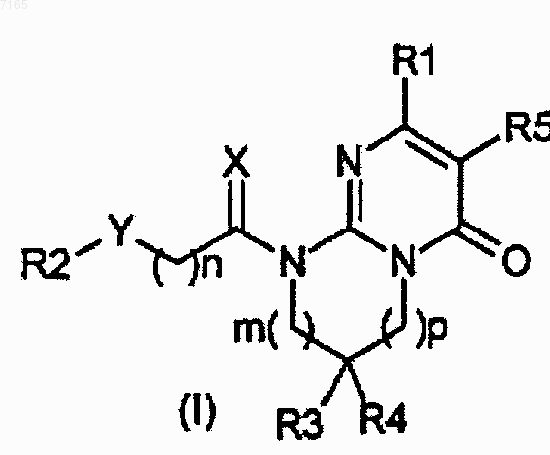
где X представляет собой два атома водорода, атом серы, атом кислорода или C1-2алкильную группу и атом водорода;
Y представляет собой связь, этениленовую группу, этиниленовую группу, атом кислорода, атом серы, сульфонильную группу, сульфоксидную группу, карбонильную группу, атом азота, возможно замещенный C1-6алкильной группой, фенильной или бензильной группой; или метиленовую группу, возможно замещенную одной или двумя группами, выбранными из C1-6алкильной группы, бензильной группы, гидроксигруппы, C1-4алкоксигруппы, С3-6циклоалкилметилокси, C1-2пергалогенированной алкильной группы, аминогруппы, ацетиламиногруппы или фенильной группы;
R1 представляет собой пиримидиновое кольцо, возможно замещенное C3-6циклоалкильной группой, C1-4алкильной группой, C1-4алкоксигруппой, бензильной группой или атомом галогена;
когда Y представляет собой связь, возможно замещенную метиленовую группу или карбонильную группу, тогда R2 представляет собой C1-6алкильную группу, возможно замещенную С6,10арилокси или С6,10ариламиногруппой; C3-6циклоалкильную группу, C1-4алкилтиогруппу, C1-4алкоксигруппу, C1-2пергалогенированную алкильную группу, C1-3галогенированную алкильную группу, фенилтиогруппу, бензильную группу, бензольное кольцо, индановое кольцо, 5,6,7,8-тетрагидронафталиновое кольцо, нафталиновое кольцо, пиридиновое кольцо, пиррольное кольцо, тиофеновое кольцо, фурановое кольцо или имидазольное кольцо; бензильную группу или кольца, возможно замещенные 1-4 заместителями, выбранными из C1-6алкильной группы, метилендиоксигруппы, атома галогена, C1-2пергалогенированной алкильной группы, C1-3галогенированной алкильной группы, гидроксигруппы, C1-4алкоксигруппы, нитро, циано, амино, C1-5моноалкиламиногруппы, C2-10диалкиламиногруппы, C1-6алкилкарбониламиногруппы, С6,10арилкарбониламиногруппы, C1-4алкилсульфонильной группы, C1-4алкилсульфонилоксигруппы или фенильной группы;
когда Y представляет собой этениленовую группу, этиниленовую группу, атом кислорода, атом серы, сульфонильную группу, сульфоксидную группу или возможно замещенный атом азота, тогда R2 представляет собой C1-6алкильную группу (возможно замещенную С6,10арилокси или С6,10ариламиногруппой), С3-6циклоалкильную группу, C1-2пергалогенированную алкильную группу, C1-3галогенированную алкильную группу, бензильную группу, бензольное кольцо, индановое кольцо, 5,6,7,8-тетрагидронафталиновое кольцо, нафталиновое кольцо, пиридиновое кольцо, пиррольное кольцо, тиофеновое кольцо, фурановое кольцо или имидазольное кольцо; бензильную группу или кольца, возможно замещенные 1-4 заместителями, выбранными из C1-6алкильной группы, метилендиоксигруппы, атома галогена, C1-2пергалогенированной алкильной группы, C1-3галогенированной алкильной группы, гидроксильной группы, C1-4алкоксигруппы, нитро, циано, амино, C1-5моноалкиламиногруппы, C2-10диалкиламиногруппы, C1-6алкилкарбониламиногруппы, С6,10арилкарбониламиногруппы, С1-4алкилсульфонильной группы, С1-4алкилсульфонилоксигруппы или фенильной группы;
R3 и R4 представляют собой, каждый независимо, атом водорода, C1-6алкильную группу, гидроксигруппу, C1-4алкоксигруппу или атом галогена;
R5 представляет собой атом водорода, C1-6алкильную группу или атом галогена;
когда m равно 0, р равно 1, 2 или 3,
когда m равно 1, р равно 0, 1 или 2,
когда m равно 2, р равно 0 или 1 и
n представляет собой 0-3.
2. Производное пиримидона, или его соль, или его сольват, или его гидрат по п.1, где R1 представляет собой незамещенное 4-пиримидиновое кольцо.
3. Производное пиримидона, которое выбрано из группы, состоящей из
9-(3-фенилпропил)-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(2-хлор-4-фторфенил)этил]-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-(2-фенилсульфанилэтил)-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-(2-оксо-2-фенилэтил)-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-(3-гидрокси-3-фенилпропил)-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-(2-гидрокси-2-фенилэтил)-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-(3-оксо-3-фенилпропил)-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-(2(R)-гидрокси-2-фенилэтил)-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-(2(S)-гидрокси-2-фенилэтил)-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(3-хлорфенил)-2-оксоэтил]-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(3-фторфенил)-2-оксоэтил]-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она.
9-[2-(3-фторфенил)-2-гидроксиэтил]-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(3-хлорфенил)-2-гидроксиэтил]-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-(1-метил-2-оксо-2-фенилэтил)-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-(2-гидрокси-1-метил-2-фенилэтил)-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(3-хлорфенил)-2(R)-гидроксиэтил]-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
7,7-дифтор-9-(2-оксо-2-фенилэтил)-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
7,7-диметил-9-(2-оксо-2-фенилэтил)-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-(2(S)-гидрокси-2-фенилэтил)-7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(3-хлорфенил)-2-оксоэтил]-7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(3-хлорфенил)-2-гидроксиэтил]-7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(3-фторфенил)-2-оксоэтил]-7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
3-метил-9-(2-оксо-2-фенилэтил)-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
3-хлор-9-(2(S)-гидрокси-2-фенилэтил)-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(2(S)-гидрокси-2-фенилэтил)]-3-метил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(3-фторфенил)-2-гидроксиэтил]-7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-оксо-2-(5,5,8,8-тетраметил-5,6,7,8-тетрагидронафталин-2-илэтил]-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(4-хлорфенил)-2-оксоэтил]-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(4-фторфенил)-2-оксоэтил]-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-(2-нафталин-2-ил-2-оксоэтил)-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-(2-оксо-2-паратолилэтил)-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-(2-бифенил-4-ил-2-оксоэтил)-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(3-метоксифенил)-2-оксоэтил]-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(7-метоксибензо[1,3]диоксол-5-ил)-1-метил-2-оксоэтил]-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она.
9-[2-(7-метоксибензо[1,3]диоксол-5-ил)-1-метил-2-оксоэтил]-7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(4-хлорфенил)-2-оксоэтил]-7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
7,7-диметил-9-[2-оксо-2-(5,5,8,8-тетраметил-5,6,7,8-тетрагидронафталин-2-ил)этил]-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(4-фторфенил)-2-оксоэтил]-7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-бифенил-4-ил-2-оксоэтил]-7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
7,7-диметил-9-(2-оксо-2-паратолилэтил)-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(3-метоксифенил)-2-оксоэтил]-7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
7,7-диметил-9-(2-нафталин-2-ил-2-оксоэтил)-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-гидрокси-2-(7-метоксибензо[1,3]диоксол-5-ил)-1-метилэтил]-7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-гидрокси-2-(7-метоксибензо-[1,3]диоксол-5-ил)-1-метилэтил]-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-(2-гидрокси-2-фенилпропил)-7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(2-метоксифенил)-2-оксоэтил]-7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(2-метоксифенил)этил]-7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-гидрокси-2-(2-метоксифенил)этил]-7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(2,5-диметоксифенил)-2-оксоэтил]-7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(2,5-диметоксифенил)-2-гидроксиэтил]-7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-(2(S)-циклопропилметокси-2-фенилэтил)-7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(2,5-диметоксифенил)-2-этоксиэтил]-7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(3-фенил)-2-гидроксипропил]-7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-(2(S)-этокси-2-фенилэтил)-7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-этокси-2-(2-метоксифенил)этил]-7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она.
9-[2-гидрокси-2-(2-метоксифенил)пропил]-7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидро-пиримидо[1,2-а]пиримидин-4-она,
9-[2-(2-хлор-4-фторфенил)этил]-7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(бензо-[1,3]диоксол-5-ил)-2-гидроксипропил]-7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-гидрокси-2-(3-метоксифенил)пропил]-7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидро-пиримидо[1,2-а]пиримидин-4-она,
9-[2-(4-фторфенил)-2-гидроксипропил]-7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(4-фторфенил)этил]-7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(3-фторфенил)этил]-7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(2-фторфенил)этил]-7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
4-[2-(3,3-диметил-6-оксо-8-пиримидин-4-ил-3,4,дигидро-2H,6H-пиримидо[1,2-а]пиримидин-1-ил)этил]бензонитрила,
9-[2-(4-метоксифенил)этил]-7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(3,4-диметоксифенил)этил]-7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
7,7-диметил-2-(пиримидин-4-ил)-9-(2-ортотолилэтил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
7,7-диметил-2-(пиримидин-4-ил)-9-(2-паратолилэтил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(4-фтор-2-метоксифенил)-2-гидроксиэтил]-7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидро-пиримидо[1,2-а]пиримидин-4-она,
9-[2-(4-фтор-2-метоксифенил)-2-оксоэтил]-7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидро-пиримидо[1,2-а]пиримидин-4-она,
9-[2-(4-хлорфенил)этил]-7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(2-хлорфенил)этил]-7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(2,4-дихлорфенил)этил]-7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(4-бромфенил)этил]-7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(4-этоксифенил)этил]-7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-циклогексилэтил]-7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(4-нитрофенил)этил]-7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(2-трифторметилфенил)этил]-7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(3-хлорфенил)этил]-7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(2,5-диметоксифенил)этил]-7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
7,7-диметил-2-(пиримидин-4-ил)-9-[2-(3,4,5-триметоксифенил)этил]-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(3-метоксифенил)этил]-7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-метокси-2-(2-метоксифенил)этил]-7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-(2(R)-метокси-2-фенилэтил)-7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(2,5-диметоксифенил)-2-метоксиэтил]-7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидро-пиримидо[1,2-а]пиримидин-4-она,
9-[2-(4-фтор-2-метоксифенил)-2-метоксиэтил]-7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидро-пиримидо[1,2-а]пиримидин-4-она,
7,7-диметил-9-(2-фенилэтил)-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(3-хлорфенил)-2-метоксиэтил]-7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(3-фторфенил)-2-метоксиэтил]-7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(4-фтор-2-метоксифенил)этил]-7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(4-фтор-2-метоксифенил)этил]-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(2,6-дихлорфенил)этил]-7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
7,7-диметил-9-(2-нафталин-1-илэтил)-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(2,6-диметоксифенил)этил]-7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
7,7-диметил-2-(пиримидин-4-ил)-9-[2-(2-трифторметоксифенил)этил]-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(2,4-дихлор-5-фторфенил)этил]-7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
7,7-диметил-2-(пиримидин-4-ил)-9-[2-(2,4,5-трифторфенил)этил]-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(2,4-дифторфенил)этил]-7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-индан-2-илметил-7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
3-хлор-9-индан-2-илметил-7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(2-этокси-4-фторфенил)этил]-7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(4-фтор-2-изопропоксифенил)этил]-7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(4-фтор-2-гидроксифенил)этил]-7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(5-хлор-2,3-дигидробензофуран-7-ил)этил]-7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
или его соль, либо его гидрат или его сольват.
4. Производное пиримидона, которое выбрано из группы, состоящей из
1-(3-фенилпропил)-7-пиримидин-4-ил-2,3-дигидро-1H-имидазо[1,2-а]пиримидин-5-она,
1-[3-(2-фторфенил)пропил]-2,2-диметил-7-пиримидин-4-ил-2,3-дигидро-1Н-имидазо[1,2-а]пиримидин-5-она,
1-(2-оксо-2-фенилэтил)-7-пиримидин-4-ил-2,3-дигидро-1H-имидазо[1,2-а]пиримидин-5-она,
1-(2-гидрокси-2-фенилэтил)-7-пиримидин-4-ил-2,3-дигидро-1H-имидазо[1,2-а]пиримидин-5-она,
1-[2-(3-метоксифенил)-2-оксоэтил]-2,2-диметил-7-пиримидин-4-ил-2,3-дигидро-1H-имидазо[1,2-а]пиримидин-5-она,
1-[2-(7-метоксибензо[1,3]диоксол-5-ил)-1-метил-2-оксоэтил]-2,2-диметил-7-пиримидин-4-ил-2,3-дигидро-1Н-имидазо[1,2-а]пиримидин-5-она,
1-(2-бифенил-4-ил-2-оксоэтил)-2,2-диметил-7-пиримидин-4-ил-2,3-дигидро-1Н-имидазо[1,2-а]пиримидин-5-она,
1-[2-(4-фторфенил)-2-оксоэтил]-2,2-диметил-7-пиримидин-4-ил-2,3-дигидро-1H-имидазо[1,2-а]пиримидин-5-она,
2,2-диметил-1-(2-оксо-2-паратолилэтил)-7-пиримидин-4-ил-2,3-дигидро-1Н-имидазо[1,2-а]пиримидин-5-она,
2,2-диметил-1-(2-нафталин-2-ил-2-оксоэтил)-7-пиримидин-4-ил-2,3-дигидро-1Н-имидазо[1,2-а]пиримидин-5-она,
1-[2-(4-хлорфенил)-2-оксоэтил]-2,2-диметил-7-пиримидин-4-ил-2,3-дигидро-1Н-имидазо[1,2-а]пиримидин-5-она,
2,2-диметил-1-[2-оксо-2-(5,5,8,8-тетраметил-5,6,7,8-тетрагидронафталин-2-ил)этил]-7-пиримидин-4-ил-2,3-дигидро-1H-имидазо[1,2-а]пиримидин-5-она,
или его соль, либо его гидрат, или его сольват.
5. Производное пиримидона, которое выбрано из группы, состоящей из
9-[2-(4-фтор-2-метоксифенил)этил]-8-метил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(4-фтор-2-метоксифенил)этил]-8,8-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(4-фторфенил)этил]-8-метил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
8-метил-9-(2-оксо-2-фенилэтил)-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(2,5-диметоксифенил)этил]-8-метил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(2-метоксифенил)этил]-8-метил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2(S)-гидрокси-2-фенилэтил]-8-метил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2(R)-метокси-2-фенилэтил]-8-метил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(2,5-диметоксифенил)этил]-8,8-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
8-метил-9-[нафталин-1-илметил]-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2(S)-гидрокси-2-фенилэтил]-8,8-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
8-метил-9-[нафталин-2-илметил]-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2(R)-гидрокси-2-фенилэтил]-8,8-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(4-фторфенил)этил]-8,8-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
8,8-диметил-9-[2-оксо-2-фенилэтил]-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(3-метоксифенил)-2-оксоэтил]-8-метил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(3-хлорфенил)-2-оксоэтил]-8-метил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
8,8-диметил-9-[нафталин-1-илметил]-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
8-этил-9-[2-оксо-2-фенилэтил]-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(4-фторфенил)-2(S)-гидроксиэтил]-8,8-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
8-этил-9-[2(S)-гидрокси-2-фенилэтил]-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2(S)-гидрокси-2-(4-метоксифенил)этил]-8,8-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидро-пиримидо[1,2-а]пиримидин-4-она,
9-[2-(3-фторфенил)-2-гидроксиэтил]-8-метил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(2,4-диметоксифенил)-2(S)-гидроксиэтил]-8,8-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидро-пиримидо[1,2-а]пиримидин-4-она,
9-[2-(3-бромфенил)-2(S)-гидроксиэтил]-8,8-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-бензо[1,3]диоксол-5-ил-2-оксоэтил]-8-метил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(2,3-дигидробензо[1,4]диоксин-6-ил)-2-оксоэтил]-8-метил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(3,5-дихлорфенил)-2-гидроксиэтил]-8-метил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(3-фторфенил)-2(S)-гидроксиэтил]-8,8-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2(S)-гидрокси-2-нафталин-2-илэтил]-8,8-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидро-пиримидо[1,2-а]пиримидин-4-она,
9-(2-бифенил-4-ил-2(S)-гидроксиэтил)-8,8-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(2,5-диметоксифенил)-2(S)-гидроксиэтил]-8,8-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидро-пиримидо[1,2-а]пиримидин-4-она,
9-[2(S)-гидрокси-2-паратолилэтил]-8,8-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2(S)-гидрокси-2-(3-метоксифенил)этил]-8,8-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидро-пиримидо[1,2-а]пиримидин-4-она,
9-[2-(4-хлорфенил)-2(S)-гидроксиэтил]-8,8-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(2,4-дихлорфенил)-2(S)-гидроксиэтил]-8,8-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидро-пиримидо[1,2-а]пиримидин-4-она,
3-бром-8-метил-9-(2-оксо-2-фенилэтил)-2-пиримидин-4-ил-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
8,8-диметил-9-(2-оксо-2-паратолилэтил)-2-пиримидин-4-ил-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(3,4-дихлорфенил)-2(S)-гидроксиэтил]-8,8-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидро-пиримидо[1,2-а]пиримидин-4-она,
9-[2-(3-метоксифенил)-2-оксоэтил]-8,8-диметил-2-пиримидин-4-ил-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
4-[2-(2,2-диметил-6-оксо-8-пиримидин-4-ил-3,4-дигидро-2Н,6Н-пиримидо[1,2-а]пиримидин-1-ил)-1(S)-гидроксиэтил]бензонитрила,
9-[2-(4-фторфенил)-2-оксоэтил]-8,8-диметил-2-пиримидин-4-ил-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(4-хлорфенил)-2-оксоэтил]-8,8-диметил-2-пиримидин-4-ил-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(4-метоксифенил)-2-оксоэтил]-8,8-диметил-2-пиримидин-4-ил-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
8,8-диметил-9-(2-нафталин-2-ил-2-оксоэтил)-2-пиримидин-4-ил-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(3,4-дихлорфенил)-2-оксоэтил]-8,8-диметил-2-пиримидин-4-ил-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(2,5-диметоксифенил)-2-оксоэтил]-8,8-диметил-2-пиримидин-4-ил-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-(2-бифенил-4-ил-2-оксоэтил)-8,8-диметил-2-пиримидин-4-ил-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(3-бромфенил)-2-оксоэтил]-8,8-диметил-2-пиримидин-4-ил-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(3-фторфенил)-2-оксоэтил]-8,8-диметил-2-пиримидин-4-ил-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
8-этил-9-(2-гидрокси-2-паратолилэтил)-2-пиримидин-4-ил-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(4-хлopфенил)-2-оксоэтил]-8,8-диметил-2-пиримидин-4-ил-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
9-[2-(4-хлорфенил)-2-гидроксиэтил]-8-этил-2-пиримидин-4-ил-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,
или его соль, либо его гидрат, или его сольват.
6. Лекарсттю, содержащее в качестве активного ингредиента вещество, выбранное из группы, состоящей из производного пиримидона, представленного формулой (I), или его солей, или его сольвата, или его гидрата по пп.1-5.
7. Ингибитор GSK3b или GSK3b и cdk5/p25, выбранный из группы производных пиримидона, представленных формулой (I), или их солей, или их сольвата, или их гидрата по пп.1-5.
8. Применение производного пиримидона по пп.1-5 для изготовления лекарства для профилактического и/или терапевтического лечения заболевания, вызванного ненормальной активностью GSK3b или GSK3b и cdk5/p25.
9. Применение производного пиримидона по пп.1-5 для изготовления лекарства для профилактического и/или терапевтического лечения нейродегенеративного заболевания.
10. Применение по п.9, где нейродегенеративное заболевание выбрано из группы, состоящей из болезни Альцгеймера, болезни Паркинсона, бокового амиотрофического склероза, таупатий, сосудистых деменций; острого инсульта, травматических повреждений; цереброваскулярных травм, травмы головного мозга, травмы спинного мозга; периферических невропатий; ретинопатий или глаукомы.
11. Применение производного пиримидона по пп.1-5 для изготовления лекарства для профилактического и/или терапевтического лечения инсулиннезависимого диабета; ожирения; маниакально-депрессивного расстройства; шизофрении; алопеции; прекращения курения; эпилепсии или видов рака.
12. Применение по п.11, где рак представляет собой рак молочной железы, немелкоклеточный рак легких, рак щитовидной железы, T- или В-клеточную лейкемию или опухоль, индуцированную вирусом.
Текст
007165 Область изобретения Настоящее изобретение относится к соединениям, которые пригодны в качестве активного ингредиента лекарства для профилактического и/или терапевтического лечения нейродегенеративных заболеваний, вызываемых ненормальными активностями GSK3 самой по себе или объединенными действиями GSK3 и cdk5/p25. Предшествующий уровень техникиGSK3 (киназа-3 гликогенсинтазы) представляет собой пролин-направленную серин-треонин киназу, которая играет важную роль в регуляции метаболизма, дифференцировки и выживания. Первоначально она была определена как фермент, способный фосфорилировать и, следовательно, ингибировать гликогенсинтазу. Позже открыли, что GSK3 идентична тау-протеинкиназе 1 (ТРК 1), ферменту, который фосфорилирует тау-протеин в эпитопах, которые, как обнаружено, также являются гиперфосфорилированными при болезни Альцгеймера и при некоторых таупатиях. Интересно, что фосфорилирование GSK3 при помощи протеинкиназы В (АКТ) приводит к потере ее киназной активности, и было высказано предположение, что это ингибирование может являться промежуточным звеном некоторых действий нейротропных факторов. Кроме того, фосфорилирование при помощи GSK3 -катенина, белка, вовлеченного в выживание клеток, ведет к его расщеплению зависимым от убиквитинилирования протеасомным путем. Таким образом, оказывается, что ингибирование GSK3 активности может привести к нейротропному действию. Действительно, существует доказательство того, что литий, неконкурентный ингибиторGSK3, усиливает нейритогенез в некоторых моделях и также увеличивает выживание нейронов через индукцию факторов выживания, таких как Всl-2, и ингибирование экспрессии проапоптозных факторов,таких как Р 53 и Вах. В недавних исследованиях было показано, что -амилоид увеличивает активность GSK3 и фосфорилирование тау-протеина. Кроме того, это гиперфосфорилирование, а также нейротоксические действия-амилоида блокируются хлоридом лития и антисмысловой mRNA (матричной рибонуклеиновой кислотой) GSK3. Эти наблюдения позволяют уверенно предположить, что GSK3 может являться связью между двумя основными патологическими процессами болезни Альцгеймера: ненормальным процессингом APP (предшественника амилоидного белка) и гиперфосфорилированием тау-протеина. Хотя тау-гиперфосфорилирование приводит к дестабилизации цитоскелета нейронов, патологические следствия ненормальной GSK3 активности имеют место, вероятнее всего, не только благодаря патологическому фосфорилированию тау-протеина, так как, как указано выше, излишняя активность этой киназы может влиять на выживание через модуляцию экспрессии апоптозных и антиапоптозных факторов. Кроме того, было показано, что -амилоид-индуцированное увеличение GSK3 активности ведет к фосфорилированию и, следовательно, ингибированию пируватдегидрогеназы, основного фермента в производстве энергии и синтезе ацетилхолина. Сdk5(циклинзависимая киназа)/р 25, также известная как тау-протеинкиназа 2 (ТРК 2) представляет собой пролиннаправленную Ser/Thr киназу, необходимую для развития центральной нервной системы и,в частности, для нейрональной миграции и роста нейритов. Cdk5 представляет собой гомолог циклинзависимых киназ и экспрессируется повсеместно. Ее активатор р 35 (305 аа белок) или усеченная форма р 25 (208 аа с отсутствием N-концевого богатого пролином домена, не требующегося для активности) селективно экспрессируются в нейронах, ограничивая cdk5 киназную активность, по существу, CNScdk5/p25 используют в описании для активного фермента, так как есть доказательство, которое позволяет предположить, что р 25 и в меньшей степени р 35 могут быть вовлечены в патологические процессы. Физиологические субстраты cdk5/p25 включают в себя DARPP-32 (дофамин- и цАМФрегулируемый фосфопротеин 32), Munc-18, PAK1 (р 21-активируемую киназу), синапсин 1 и возможно некоторые другие. Кроме того, теперь установлено, что cdk5/p25 фосфорилирует тау-протеиновые эпитопы, которые гиперфосфорилированы при болезни Альцгеймера. Совсем недавно в мозге пациентов с болезнью Альцгеймера была обнаружена увеличенная активность cdk5/p25, неправильная локализацияcdk5 и увеличение р 25 активатора. Интересно, что предварительное фосфорилирование тау-протеина при помощи cdk5/p25 значительно усиливает тау-фосфорилирование при помощи GSK3 на других эпитопах, где также обнаружено гиперфосфорилирование при болезни Альцгеймера. Кроме того, нейрофибриллярные клубки, признак болезни Альцгеймера, помечены антисывороткой к GSK3 и cdk5, а не кGSK3 и MAP (митогенактивируемая протеинкиназа) киназе, также GSK3 и cdk5 связаны с микротрубочками и обе, больше чем PKA (протеинкиназа А) и CK (креатинкиназа), вносят вклад в АD(болезнь Альцгеймера)-подобное фосфорилирование тау-протеина. Эти результаты, взятые вместе, позволяют предположить, что смешанные ингибиторы GSK3 и cdk5 должны быть эффективными для защиты таупротеина от гиперфосфорилирования. Следовательно, они должны быть полезными при лечении любого патологического нарушения, связанного с ненормальным фосфорилированием тау-протеина, в частности болезни Альцгеймера, а также других таупатий (например, лобно-височно-теменной деменции, кортикобазальной дегенерации, болезни Пика, прогрессирующего супрануклеарного паралича).Cdk5/p25 связана с апоптозом и нейродегенерацией в более широком понимании. Ее сверхэкспрессия вызывает апоптоз в культивируемых нейронах, в ткани мозга апоптические клетки проявляют сильную иммунореактивность к cdk5. Нейротоксические агенты, включая А(1-42), повреждение нейронов,ишемия или удаление факторов роста ведут к активации и неправильной локализации cdk5/p25, ненормальному фосфорилированию cdk5 субстратов, разрушению цитоскелета и клеточной смерти. Кроме того, фосфорилирование при помощи cdk5/p25 превращает DARPP-32 в ингибитор протеинкиназы А,уменьшая передачу сигнала в стриатум с очевидными осложнениями болезни Паркинсона. Также предполагается, что роль cdk5 в ALS (боковой амиотрофический склероз) основана на ее способности фосфорилировать нейрофиламенты. Совсем недавно в мышиной модели бокового амиотрофического склероза было обнаружено прекращение регулирования cdk5. Все вместе, эти экспериментальные наблюдения указывают на то, что GSK3 ингибиторы могут найти применение при лечении нейропатологических последствий и дефицита внимания и познавательных способностей, связанных с болезнью Альцгеймера, а также других острых и хронических нейродегенеративных заболеваний. Они включают в себя, без ограничения, болезнь Паркинсона, таупатии (например, лобно-височно-теменную деменцию, кортикобазальную дегенерацию, болезнь Пика, прогрессирующий супрануклеарный паралич) и другие виды деменции, включая мультиинфарктную деменцию; острый инсульт и другие травматические повреждения; цереброваскулярные повреждения (например возрастную дистрофию желтого пятна); травмы головного и спинного мозга; периферические невропатии; ретинопатии и глаукому. Кроме того, ингибирование GSK3 может найти применение при лечении других заболеваний, таких как инсулиннезависимый диабет (например диабет II типа) и ожирение; маниакально-депрессивное расстройство; шизофрения; алопеция; виды рака, такие как рак молочной железы, немелкоклеточный рак легких, рак щитовидной железы, T- или В-клеточная лейкемия и некоторые вызванные вирусом опухоли. Так как представляется, что обе GSK3 и cdk5/p25 играют главную роль в индукции апоптоза в нейрональных клетках, совместное ингибирование этих двух ферментов может найти применение при лечении не только болезни Альцгеймера и других указанных выше таупатий, но также ряда других нейродегенеративных заболеваний, в частности болезни Паркинсона и бокового амиотрофического склероза; других деменций, включая мультиинфарктную деменцию, острый инсульт и другие травматические повреждения; цереброваскулярные повреждения (например, возрастную дистрофию желтого пятна); травмы головного и спинного мозга; периферические невропатии; ретинопатии и глаукому. Кроме того,смешанные ТРК 1/TРК 2 ингибиторы могут найти применение при лечении других заболеваний, таких как: прекращение курения и другие синдромы отмены, эпилепсия. Описание сущности изобретения Цель данного изобретения заключается в том, чтобы предложить соединения, пригодные в качестве активного ингредиента лекарства для профилактического и/или терапевтического лечения заболевания,вызванного ненормальной активностью GSK3 или GSK3 и cdk5/p25, более конкретно нейродегенеративных заболеваний. Более конкретно, целью является предложить новые соединения, пригодные в качестве активного ингредиента лекарства, которое дает возможность профилактики и/или лечения нейродегенеративного заболевания, такого как болезнь Альцгеймера. Таким образом, авторы данного изобретения обнаружили соединения, обладающие ингибирующей активностью в отношении GSK3 или GSK3 и cdk5/p25. B результате они обнаружили, что соединения,представленные следующей формулой (I), обладают требуемой активностью и пригодны в качестве активного ингредиента лекарства для профилактического и/или терапевтического лечения указанных выше заболеваний. Таким образом, в настоящем изобретении предложены производные пиримидона, представленные формулой (I), или его соли, сольваты или гидраты где X представляет собой два атома водорода, атом серы, атом кислорода или С 1-2 алкильную группу и атом водорода;Y представляет собой связь, этениленовую группу, этиниленовую группу, атом кислорода, атом серы, сульфонильную группу, сульфоксидную группу, карбонильную группу, атом азота, возможно замещенный С 1-6 алкильной группой, фенильной или бензильной группой; или метиленовую группу, возможно замещенную одной или двумя группами, выбранными из C1-6 алкильной группы, бензильной группы,гидроксильной группы, C1-4 алкоксигруппы, С 3-6 циклоалкилметилокси, С 1-2 пергалогенированной алкильной группы, аминогруппы, ацетиламиногруппы или фенильной группы;R1 представляет собой пиримидиновое кольцо, возможно замещенное C3-6 циклоалкильной группой,-2 007165C1-4 алкильной группой, С 1-4 алкоксигруппой, бензильной группой или атомом галогена; когда Y представляет собой связь, возможно замещенную метиленовую группу или карбонильную группу, тогда R2 представляет собой C1-6 алкильную группу, возможно замещенную С 6,10 арилокси или С 6,10 ариламиногруппой; С 3-6-циклоалкильную группу, C1-4 алкилтиогруппу, C1-4 алкоксигруппу, С 1-2 пергалогенированную алкильную группу, C1-3 галогенированную алкильную группу, фенилтиогруппу,бензильную группу, бензольное кольцо, индановое кольцо, 5,6,7,8-тетерагидронафталиновое кольцо,нафталиновое кольцо, пиридиновое кольцо, пиррольное кольцо, тиофеновое кольцо, фурановое кольцо или имидазольное кольцо; бензильную группу или кольца, возможно замещенные 1-4 заместителями,выбранными изC1-6 алкильной группы,метилендиоксигруппы,атома галогена,C1-2 пергалогенированной алкильной группы, С 1-3 галогенированной алкильной группы, гидроксильной группы, C1-4 алкоксигруппы, нитро, циано, амино, C1-5 моноалкиламиногруппы, C2-10 диалкиламиногруппы, С 1-6 алкилкарбониламиногруппы, С 6,10 арилкарбониламиногруппы, C1-4 алкилсульфонильной группы, C1-4 алкилсульфонилоксигруппы или фенильной группы; когда Y представляет собой этениленовую группу, этиниленовую группу, атом кислорода, атом серы, сульфонильную группу, сульфоксидную группу или возможно замещенный атом азота, тогда R2 представляет собой(возможно замещенную С 6,10 арилокси или С 6,10 ариламиногруппой), C3-6 циклоалкильную группу, С 1-2 пергалогенированную алкильную группу, C1-3 галогенированную алкильную группу, бензильную группу, бензольное кольцо, индановое кольцо,5,6,7,8-тетрагидронафталиновое кольцо, нафталиновое кольцо, пиридиновое кольцо, пиррольное кольцо,тиофеновое кольцо, фурановое кольцо или имидазольное кольцо; бензильную группу или кольца, возможно замещенные 1-4 заместителями, выбранными из C1-6 алкильной группы, метилендиоксигруппы,атома галогена, C1-2 пергалогенированной алкильной группы, C1-3 галогенированной алкильной группы,гидроксильной группы, C1-4 алкоксигруппы, нитро, циано, амино, C1-5 моноалкиламиногруппы, С 2-10 диалкиламиногруппы, C1-6 алкилкарбониламиногруппы, С 6,10 арилкарбониламиногруппы, C1-4 алкилсульфонильной группы, C1-4 алкилсульфонилоксигруппы или фенильной группы;R3 и R4, каждый независимо, представляют собой атом водорода, C1-6 алкильную группу, гидроксигруппу, C1-4 алкоксигруппу или атом галогена;R5 представляет собой атом водорода, C1-6 алкильную группу или атом галогена; когда m равно 0, р равно 1, 2 или 3,когда m равно 1, р равно 0, 1 или 2,когда m равно 2, р равно 0 и 1 иn представляет собой 0-3. В соответствии с еще одним аспектом настоящего изобретения предложено лекарство, содержащее в качестве активного ингредиента вещество, выбранное из группы, состоящей из производных пиримидона, представленных формулой (I), и их физиологически приемлемых солей, и их сольватов и гидратов. В качестве предпочтительных воплощений лекарства предложено указанное выше лекарство, которое применяют для профилактического и/или терапевтического лечения заболеваний, вызванных ненормальной активностью GSK3 или GSK3 и cdk5/p25, и указанное выше лекарство, которое применяют для профилактического и/или терапевтического лечения нейродегенеративных заболеваний и, кроме того, других заболеваний, таких как инсулиннезависимый диабет (например диабет II типа) и ожирение; маниакально-депрессивное расстройство; шизофрения; алопеция; прекращение курения и другие синдромы отмены, эпилепсия; виды рака, такие как рак молочной железы, немелкоклеточный рак легких,рак щитовидной железы, T- или В-клеточная лейкемия и некоторые вызванные вирусом опухоли. В качестве других предпочтительных воплощений настоящего изобретения предложено указанное выше лекарство, где заболевания представляют собой нейродегенеративные заболевания и выбраны из группы, состоящей из болезни Альцгеймера, болезни Паркинсона, бокового амиотрофического склероза,таупатий (например, лобно-височно-теменной деменции, кортикобазальной дегенерации, болезни Пика,прогрессирующего супрануклеарного паралича) и других виды деменции, включая мультиинфарктную деменцию; острый инсульт и другие травматические повреждения; цереброваскулярных повреждений(например, возрастной дистрофия желтого пятна); травмы головного и спинного мозга; периферических невропатий; ретинопатий и глаукомы; и указанное выше лекарство в форме фармацевтической композиции, содержащей указанное выше вещество в качестве активного ингредиента вместе с одной или более чем одной фармацевтической добавкой. В настоящем изобретении, кроме того, предложен ингибитор GSK3 или GSK3 и cdk5/p25 активности, содержащий в качестве активного ингредиента вещество, выбранное из группы, состоящей из производных пиримидона формулы (I) и их солей, и их сольватов и их гидратов. В соотвествии с другими аспектами данного изобретения предложен способ для профилактического и/или терапевтического лечения нейродегенеративных заболеваний, вызванных ненормальной активностью GSK3 или GSK3 и cdk5/p25, который включает в себя стадию, на которой пациенту вводят профилактически и/или терапевтически эффективное количество вещества, выбранного из группы, состоящей из производных пиримидона формулы (I) и его физиологически приемлемых солей и их сольватов и-3 007165 гидратов; и применение вещества, выбранного из группы, состоящей из производных пиримидона формулы (I) и их физиологически приемлемых солей и их сольватов и гидратов для изготовления указанного выше лекарства. При использовании здесь, C1-6 алкильная группа представляет собой прямую или разветвленную алкильную группу, имеющую от 1 до 6 атомов углерода, например, метильную группу, этильную группу,н-пропильную группу, изопропильную группу, н-бутильную группу, изобутильную группу, вторбутильную группу, трет-бутильную группу, н-пентильную группу, изопентильную группу, неопентильную группу, 1,1-диметилпропильную группу, н-гексильную группу, изогексильную группу и подобные; этениленовая группа представляет собой двухвалентную группу формулы этиниленовая группа представляет собой двухвалентную группу формулыC1-4 алкоксигруппа представляет собой алкилоксигруппу, имеющую от 1 до 4 атомов углерода, например, метоксигруппу, этоксигруппу, пропоксигруппу, изопропоксигруппу, бутоксигруппу, изобутоксигруппу, втор-бутоксигруппу, трет-бутоксигруппу и подобные; атом галогена представляет собой атом фтора, хлора, брома или йода; С 1-2 пергалогенированная алкильная группа представляет собой алкильную группу, где все водороды замещены галогеном, например, CF3 или C2F5;C1-3 галогенированная алкильная группа представляет собой алкильную группу, где по меньшей мере один водород не был замещен атомом галогена;C1-5 моноалкиламиногруппа представляет собой аминогруппу, замещенную одной C1-5 алкильной группой, например, метиламиногруппу, этиламиногруппу, пропиламиногруппу, изопропиламиногруппу,бутиламиногруппу, изобутиламиногруппу, трет-бутиламиногруппу, пентиламиногруппу и изопентиламиногруппу; С 2-10 диалкиламиногруппа представляет собой аминогруппу, замещенную двумя С 1-5 алкильными группами, например, диметиламиногруппу, этилметиламиногруппу, диэтиламиногруппу, метилпропиламиногруппу и дииизопропиламиногруппу; С 6-10 ариламино представляет собой фениламиногруппу или нафтиламиногруппу; С 6-10 арилокси представляет собой фенилоксигруппу или нафтилоксигруппу. Уходящая группа представляет собой группу, которую можно легко отщепить и заместить, такой группой может быть, например, тозилокси, мезилокси, бромид и подобные. Соединения, представленные указанной выше формулой (I), могут образовывать соль. Примеры этих солей включают в себя, когда имеется кислотная группа, соли щелочных металлов и щелочноземельных металлов, таких как литий, натрий, калий, магний и кальций; соли аммония и амины, такие как метиламин, диметиламин, триметиламин, дициклогексиламин, трис(гидроксиметил)аминометан,N,N-бис(гидроксиэтил)пиперазин, 2-амино-2-метил-1-пропанол, этаноламин, N-метилглюкамин и Lглюкамин; или соли с основными аминокислотами, такими как лизин, -гидроксилизин и аргинин. Соли присоединения оснований кислых соединений получают стандартными способами, хорошо известными в данной области техники. Когда присутствует основная группа, примеры включают в себя соли с минеральными кислотами,такими как соляная кислота, бромисто-водородная кислота, серная кислота, азотная кислота, фосфорная кислота; соли с органическими кислотами, такими как метансульфоновая кислота, бензолсульфоновая кислота, паратолуолсульфоновая кислота, уксусная кислота, пропионовая кислота, винная кислота, фумаровая кислота, малеиновая кислота, яблочная кислота, щавелевая кислота, янтарная кислота, лимонная кислота, бензойная кислота, миндальная кислота, коричная кислота, молочная кислота, гликолевая кислота, глюкуроновая кислота, аскорбиновая кислота, никотиновая кислота и салициловая кислота; или соли с кислыми аминокислотами, такими как аспарагиновая кислота и глутаминовая кислота. Соли присоединения кислоты основных соединений получают стандартными способами, хорошо известными в данной области техники, которые включают в себя, но не ограничены ими, растворение свободного основания в водном растворе спирта, содержащем подходящую кислоту, и выделение соли путем упаривания раствора, или путем взаимодействия свободного основания и кислоты в органическом растворителе, в этом случае соль отделяют непосредственно или осаждают вторым органическим растворителем, или ее можно получить путем концентрирования раствора. Кислоты, которые можно использовать для получения солей присоединения кислоты, предпочтительно включают в себя такие кислоты, которые образуют, при объединении со свободным основанием, фармацевтически приемлемые соли, то есть соли, анионы которых относительно безопасны для организма животного в фармацевтических дозах этих солей, таким образом, что полезные свойства, имеющиеся в свободном основании, не-4 007165 подвержены побочным действиям, относимым за счет анионов. Хотя предпочтительными являются медицински приемлемые соли основных соединений, все соли присоединения кислот входят в объем настоящего изобретения. Кроме производных пиримидона, представленных указанной выше формулой (I), и их солей, их сольваты и гидраты также входят в объем настоящего изобретения. Производные пиримидона, представленные указанной выше формулой (I), могут иметь один или более чем один асимметрический атом углерода. Что касается стереохимии таких асимметрических атомов углерода, они могут независимо находиться как в (R), так и в (S) конфигурации, и производное пиримидона может существовать в виде стереоизомеров, таких как оптические изомеры или диастереоизомеры. Любые стереоизомеры в чистой форме, любые смеси стереоизомеров, рацематы и тому подобное входят в область настоящего изобретения. Примеры предпочтительных соединений по настоящему изобретению представлены в табл. 1 ниже. Однако объем настоящего изобретения не ограничен этими соединениями. Предпочтительные соединения по настоящему изобретению, представленные формулой (I), включают в себя также(1) соединения, где R1 представляет собой 4- или 5-пиримидиновое кольцо и более предпочтительно 4-пиримидиновое кольцо, которое может быть замещено C1-2 алкильной группой, C1-2 алкоксигруппой или атомом галогена; и/или(2) X представляет собой атомы водорода или C1-2 алкильную группу и атом водорода;(3) Y представляет собой карбонильную группу или метиленовую группу, возможно замещенную одной или двумя группами, выбранными из C1-6 алкильной группы, бензильной группы, гидроксильной группы, C1-4 алкоксигруппы, С 3-6 циклоалкилметилокси; и/или(5) R2 представляет собой бензольное кольцо, индановое кольцо, 5,6,7,8-тетрагидронафталиновое кольцо, нафталиновое кольцо или циклогексильное кольцо. Более предпочтительные соединения по настоящему изобретению, представленные формулой (I),включают в себя также(1) соединения, где R1 представляет собой незамещенное 4-пиримидиновое кольцо, и соединения,где R1 представляет собой незамещенное 4-пиримидиновое кольцо, и X, Y и R2 такие, как определено для предпочтительных соединений. Особенно предпочтительные соединения по настоящему изобретению, представленные формулой[1,2-а]пиримидин-4-он. В качестве дополнительного объекта настоящее изобретение также касается способов получения соединений, представленных указанной выше формулой (I). Эти соединения можно получить, например, способами, объясненными ниже. Способ получения Пиримидоновые соединения, представленные указанной выше формулой (I), можно получить в со- 10007165 отвествии со схемой 1. Схема 1(В указанной выше схеме определения R1, R2, R3, R4, R5, X, р, m и n такие, как описано ранее для соединения формулы (I. Проводят взаимодействие пиримидин-5(1 Н)-онового производного, представленного указанной выше формулой (III), где R1 такой, как он определен для соединения формулы (I), с основанием, таким как гидрид натрия, карбонат натрия или карбонат калия, в растворителе, таком как N,Nдиметилформамид, N-метилпирролидин, N,N-диметилацетамид или хлороформ, при подходящей температуре в интервале от 0 до 130C в атмосфере обычного воздуха, затем добавляют соединение формулы(II), где R2, X, Y и n такие, как определено для соединения формулы (I), и L представляет собой уходящую группу, предпочтительно бромид или мезилоксигруппу, с получением соединения указанной выше формулы (I). Соединения формулы (II) имеются в продаже или их можно синтезировать способами, хорошо известными специалистам в данной области техники. Соединения формулы (III) можно получить способом, описанным в схеме 2. Схема 2(В указанной выше схеме определения R1, R3, R4, R5, р и m такие, как описано ранее). В соотвествии с этим способом, проводят взаимодействие 3-кетоэфира формулы (IV) с соединением формулы (V). Эту реакцию можно осуществлять в присутствии карбоната калия, в спиртовом растворителе, таком как метанол, этанол и подобные, или без него, при подходящей температуре в интервале от 25-140C в атмосфере обычного воздуха. Альтернативно, соединения формулы (III), где R5 представляет собой атом водорода, можно галогенировать для того, чтобы получить соединения формулы (III), где R5 представляет собой атом галогена, такой как атом брома или атом хлора. Эту реакцию можно осуществить в кислой среде, такой как уксусная кислота или пропионовая кислота, в присутствии бромсукцинимида или хлорсукцинимида, или брома. Кроме того, соединения формулы (III), где R5 представляет собой атом фтора, можно получить по аналогии со способом, описанным в Tetrahedron Letters, Vol. 30,45, pp. 613-616, 1989. Соединения формулы (V) или (IV) имеются в продаже или их можно синтезировать способами, хорошо известными специалистам в данной области техники. Например, соединения формулы (IV), где R1 представляет собой пиримидиновое кольцо, возможно замещенное C1-4 алкильной группой, C1-4 алкоксигруппой или атомом галогена, можно получить путем взаимодействия пиримидин-4-карбоновой кислоты, возможно замещенной C1-4 алкильной группой,C1-4 алкоксигруппой или галогеном, с моноэфиром малоновой кислоты. Это взаимодействие можно осуществлять способами, хорошо известными специалистам в данной области техники, например, в присутствии связывающего агента, такого как 1,1'-карбонилбис-1H-имидазол, в растворителе, таком как тетрагидрофуран, при температуре в интервале от 20 до 70oC. Соединения формулы (I) также можно получать, начиная с другого соединения формулы (I), используя способы, хорошо известные специалистам в данной области техники. В указанных выше реакциях иногда может быть необходима защита и удаление защиты функциональной группы. Подходящую защитную группу Pg можно выбрать в зависимости от типа функциональной группы, и можно использовать способ, описанный в литературе. Примеры защитных групп, способов защиты и удаления защиты, приведены, например, в Protective groups in Organic Synthesis, Greene et al.,2nd Ed. (John WileySons, Inc., New York). Соединения по настоящему изобретению обладают ингибирующей активностью в отношенииGSK3 или GSK3 и cdk5/p25. Соответственно соединения по настоящему изобретению полезны в каче- 11007165 стве активного ингредиента для получения лекарства, которое делает возможным профилактическое и/или терапевтическое лечение заболевания, вызываемого ненормальной активностью GSK3 илиGSK3 и cdk5/p25, и в более частном случае нейродегенеративных заболеваний, таких как болезнь Альцгеймера. Кроме того, соединения по настоящему изобретению также пригодны в качестве активного ингредиента для получения лекарства для профилактического и/или терапевтического лечения нейродегенеративных заболеваний, таких как болезнь Паркинсона, боковой амиотрофический склероз, таупатий(например лобно-височно-теменной деменции, кортикобазальной дегенерации, болезни Пика, прогрессирующего супрануклеарного паралича) и других деменций, включая мультиинфарктную деменцию; острого инсульта и других травматических повреждений; цереброваскулярных повреждений (например,возрастной дистрофии желтого пятна); травмы головного и спинного мозга; периферических невропатий; ретинопатий и глаукомы, и других заболеваний, таких как инсулиннезависимый диабет (например,диабет II типа) и ожирение; маниакально-депрессивных расстройств; шизофрении; алопеции; отказа от курения и других синдромов отмены, эпилепсии; видов рака, таких как рак молочной железы, немелкоклеточный рак легких, рак щитовидной железы, T- или В-клеточная лейкемия и некоторые вызванные вирусом опухоли. Настоящее изобретение, кроме того, относится к способу лечения нейродегенеративных заболеваний, вызываемых ненормальной активностью GSK3 или GSK3 и cdk5/p25, и указанных выше заболеваний, при котором в организм млекопитающего, нуждающегося в таком лечении, вводят эффективное количество соединения формулы (I). В качестве активного ингредиента лекарства по настоящему изобретению можно использовать вещество, которое выбрано из группы, состоящей из соединения, представленного приведенной выше формулой (I), и его фармакологически приемлемых солей, и его сольватов, и его гидратов. Это вещество,само по себе, можно вводить в качестве лекарства по настоящему изобретению, однако, желательно вводить это лекарство в форме фармацевтической композиции, которая содержит указанное выше вещество в качестве активного ингредиента и одно или более чем одно вспомогательное вещество. В качестве активного ингредиента лекарства по настоящему изобретению можно использовать в комбинации два или более чем два указанные выше соединения. Указанная выше фармацевтическая композиция может быть дополнена активным ингредиентом другого лекарства для лечения указанных выше заболеваний. Тип фармацевтической композиции не является строго ограниченным, и эта композиция может быть представлена в виде любого препарата для перорального или парентерального введения. Например, фармацевтическую композицию можно приготовить, например, в форме фармацевтических композиций для перорального введения, таких как гранулы, мелкие гранулы, порошки, твердые капсулы, мягкие капсулы, сиропы, эмульсии, суспензии, растворы и тому подобное, или в форме фармацевтических композиций для парентеральных введений, таких как инъекции для внутривенного, внутримышечного или подкожного введения, капельные вливания, чрескожные препараты, средства для введения через слизистую,капли в нос, средства для ингаляции, суппозитории и подобные. Инъекции или капельные вливания можно приготовить в виде порошковых препаратов, например, в форме лиофильно высушенных препаратов, и их можно использовать путем растворения непосредственно перед применением в подходящей водной среде, такой как физиологический солевой раствор. Препараты с замедленным высвобождением,например, покрытые оболочкой полимера, можно вводить непосредственно в мозг. Типы фармацевтических вспомогательных веществ, используемых для изготовления фармацевтической композиции, соотношения содержания фармацевтических вспомогательных веществ относительно активного ингредиента, и способы получения фармацевтической композиции может правильно выбрать специалист в данной области техники. Неорганические или органические вещества или твердые или жидкие вещества можно использовать в качестве фармацевтических вспомогательных веществ. В общем случае, фармацевтические вспомогательные вещества можно вводить в соотношение от 1 до 90 мас.%, исходя из массы активного ингредиента. Примеры эксципиентов, используемых для получения твердых фармацевтических композиций,включают в себя, например, лактозу, сахарозу, крахмал, тальк, целлюлозу, декстрин, каолин, карбонат кальция и подобное. Для получения жидких композиций для перорального введения можно использовать подходящий инертный разбавитель, такой как вода или растительное масло. Жидкая композиция может содержать, кроме инертного разбавителя, вспомогательные вещества, такие как увлажняющие агенты,суспендирующие средства, подсластители, ароматизирующие вещества, красители и консерванты. Жидкую композицию можно поместить в капсулы, изготовленные из рассасывающегося вещества, такого как желатин. Примеры растворителей или суспензионных сред, используемых для получения композиций для парентерального введения, например инъекций, суппозиториев, включают в себя воду, пропиленгликоль, полиэтиленгликоль, бензиловый спирт, этилолеат, лецитин и подобные. Примеры веществ для основы, используемых для суппозиториев, включают в себя, например, какао-масло, эмульгированное какао-масло, лауриновый липид, витепсол. Доза и частота введения лекарства по настоящему изобретению не являются конкретно ограниченными, и их можно соответственно выбирать в зависимости от состояния, например от задачи профилак- 12007165 тического и/или терапевтического лечения, типа заболевания, массы тела или возраста пациента, тяжести заболевания и подобного. В общем случае, суточная доза для перорального введения взрослому может составлять от 0,01 до 1000 мг (масса активного ингредиента), и эту дозу можно вводить один раз в сутки или несколько раз в сутки в виде разделенных доз или один раз в несколько дней. Когда это лекарство применяют в виде инъекции, введения можно предпочтительно осуществлять постоянно или с перерывами в суточной дозе от 0,001 до 100 мг (масса активного ингредиента) для взрослого. Химические примеры Настоящее изобретение далее объяснено более конкретно со ссылкой на следующие основные примеры, однако, объем настоящего изобретения не ограничивается этими примерами. Пример 1. (Соединение 24 табл. 1). 3-Хлор-9-(2(S)-гидрокси-2-фенилэтил)-2-(пиримидин-4-ил)6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-он. 1.1. 2-(Пиримидин-4-ил)-6,7,8,9-тетрагидро-4H-пиримидо[1,2-а]пиримидин-4-он. Смесь 1,75 г (9,0 ммоль) этил-3-(4-пиримидинил)-3-оксопропионата (полученного по аналогии со способом, описанным в патенте DE 2705582), 5,0 г (30,55 ммоль), 1,4,5,6-тетрагидро-2-пиримидинамина дигидрохлорида (полученного аналогично патенту США 4262122) и 2,49 г (18,0 ммоль) карбоната калия в 30 мл метанола нагревали при температуре дефлегмации в течение 18 ч. Реакционную смесь охлаждали и растворитель удаляли путем выпаривания. Полученный остаток обрабатывали водой и осадок выделяли фильтрацией с получением 1,15 г (56%) продукта. Точка плавления: 268-272C. 1.2. 3-Хлор-2-(пиримидин-4-ил)-6,7,8,9-тетрагидро-4H-пиримидо[1,2-а]пиримидин-4-он. Суспензию 3,0 г (13,09 ммоль) 2-(пиримидин-4-ил)-6,7,8,9-тетрагидро-4 Н-пиримидо[1,2-а] пиримидин-4-она в 60 мл уксусной кислоты обрабатывали 1,75 г (15,7 ммоль) N-хлорсукцинимида. Реакционную смесь нагревали при 90C в течение 18 ч. Охлажденный раствор выпаривали для удаления растворителя и добавляли воду. Продукт выделяли, промывали диэтиловым эфиром и сушили с получением 2,95 г (86%) твердого вещества. Точка плавления 208-210C. 1.3. 3-Хлор-9-(2(S)-гидрокси-2-фенилэтил)-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а] пиримидин-4-он. К раствору 0,6 г (2,27 ммоль) 3-хлор-2-(пиримидин-4-ил)-6,7,8,9-тетрагидро-4H-пиримидо[1,2-а] пиримидин-4-она в 6,7 мл безводного диметилформамида добавляли 0,20 г (5,10 ммоль) гидрида натрия(60%-ная суспензия в минеральном масле) и смесь оставляли перемешиваться при 50C в течение 20 мин. Добавляли 0,361 мл (2,73 ммоль) (S)-хлор-1-фенилэтанола и перемешивание продолжали в течение 18 ч. Добавляли воду и смесь экстрагировали дихлорметаном. Экстракты промывали насыщенным водным раствором хлорида натрия, сушили и упаривали с получением неочищенного продукта. После очистки путем хроматографии на силикагеле, элюируя смесью дихлорметан/метанол в соотношениях от 100/0 до 96/4, получали 0,598 г (69%) чистого продукта. Точка плавления 158-160C. Пример 2. (Соединение 23 табл. 1). 3-Метил-9-(2-оксо-2-фенилэтил)-2-(пиримидин-4-ил)-6,7,8,9 тетрагидропиримидо[1,2-а]пиримидин-4-он. 2.1. 3-Метил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидро-4 Н-пиримидо[1,2-а]пиримидин-4-он. Смесь 10,72 г (51,48 ммоль) этил-3-(4-пиримидинил)-2-метил-3-оксипропионата (полученного по аналогии со способом, описанным в патенте DE 2705641 и US 4110450), 6,98 г (51,48 ммоль), 1,4,5,6 тетрагидро-2-пиримидинамина дигидрохлорида (полученного аналогично патенту США 4262122) и 7,11 г (51,48 ммоль) карбоната калия в 250 мл этанола нагревали при температуре дефлегмации в течение 5 ч. Реакционную смесь охлаждали и растворитель удаляли путем выпаривания. Полученный остаток обрабатывали водой и осадок выделяли фильтрацией. Фильтрат растворяли в хлороформе и раствор фильтровали и упаривали с получением 8,6 г (69%) продукта . Точка плавления: 206-207C. 2.2. 3-Метил-9-(2-оксо-2-фенилэтил)-2-(пиримидин-4-ил)-6,7,8,9-тетрагидро-4H-пиримидо[1,2-а] пиримидин-4-он. Раствор, содержащий 0,608 г 3-метил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидро-4 Н-пиримидо[1,2-а] пиримидин-4-она в безводном диметилформамиде, обрабатывали 0,11 г (2,5 ммоль) гидрида натрия(60%-ная суспензия в минеральном масле) и смесь нагревали до 40C в течение 1 ч. По каплям добавляли 0,497 г (2,5 ммоль) фенацилбромида, растворенного в 5 мл диметилформамида, и полученный в результате раствор перемешивали при комнатной температуре в течение 3 ч. Реакционную смесь обрабатывали насыщенным водным раствором хлорида натрия и затем экстрагировали этилацетатом. Органические экстракты сушили и упаривали с получением неочищенного продукта, который очищали хроматографией на силикагеле, элюируя смесью дихлорметан/метанол/аммиак в соотношениях от 100/0/0 до 98/2/0,2. Получали чистый продукт, который растирали в диэтиловом эфире с получением 0,309 г (34%) желтого твердого вещества. Точка плавления 184-185C. Пример 3. (Соединение 17 в табл. 1). 7,7-Дифтор-9-(2-оксо-2-фенилэтил)-2-(пиримидин-4-ил)- 13007165 6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-он. 3.1. 5,5-Дифтор-1,4,5,6-тетрагидро-2-пиримидинамин. Смесь 2,95 г (16,12 ммоль) 2,2-дифтор-1,3-пропандиамина дигидрохлорида (Tetrahedron (1994) 50(29), 8617-8632), 1,54 г (16,12 ммоль) гуанидина гидрохлорида и 2,19 г (32,23 ммоль) метилата натрия нагревали при 150C в течение 18 ч. Охлажденную смесь использовали как таковую на следующей стадии. 3.2. 7,7-Дифтор-2-(пиримидин-4-ил)-6,7,8,9-тетрагидро-4 Н-пиримидо[1,2-а]пиримидин-4-он. Суспензию 2,17 г (16,12 ммоль) 5,5-дифтор-1,4,5,6-тетрагидро-2-пиримидинамина и 1,81 г (16,12 г) карбоната калия в 30 мл этанола обрабатывали 2,55 г (13,13 ммоль) этил-3-(4-пиримидинил)-3 оксопропионата. Реакционную смесь нагревали при температуре дефлегмации в течение 32 ч. Охлажденную реакционную смесь выпаривали и полученный в результате остаток обрабатывали водой и экстрагировали дихлорметаном. Экстракты сушили и выпаривали и остаток очищали хроматографией на силикагеле, элюируя смесью дихлорметан/метанол/аммиак в соотношениях 97,5/2,5/0,25. Таким образом получали 0,22 г (6,3%) продукта. 3.3. 7,7-Дифтор-9-(2-оксо-2-фенилэтил)-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а] пиримидин-4-он. Раствор 0,22 г (0,829 ммоль) 7,7-дифтор-2-(пиримидин-4-ил)-6,7,8,9-тетрагидро-4H-пиримидо[1,2 а]пиримидин-4-она в 4 мл безводного диметилформамида обрабатывали 36,2 мг (0,829 ммоль) гидрида натрия (60%-ная суспензия в минеральном масле) и смесь оставляли нагреваться до 40C в течение 30 мин. Охлажденный раствор (-10C) обрабатывали 0,165 г (0,829 ммоль) фенацилбромида и полученную в результате смесь перемешивали при комнатной температуре в течение 1 ч. Добавляли воду и реакционную смесь экстрагировали этилацетатом. Экстракты сушили и упаривали с получением остатка, который очищали хроматографией на силикагеле, элюируя смесью дихлорметан/метанол/аммиак в соотношении 98/2/0,2 с получением 56 мг (17%) продукта. Точка плавления 233-234C. Пример 4. (Соединение 19 в табл. 1). 9-(2(S)-Гидрокси-2-фенилэтил)-7,7-диметил-(пиримидин-4 ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-он. 4.1. 7,7-Диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидро-4H-пиримидо[1,2-а]пиримидин-4-он. Смесь, содержащую 5,15 г (26,52 ммоль) этил-3-(4-пиримидинил)-3-оксопропионата (полученного по аналогии со способом, описанным в патенте DE 2705582), 4,34 г (26,52 ммоль) 5,5-диметил-1,4,5,6 тетрагидро-2-пиримидинамина моногидрохлорида (полученного по аналогии с патентом США US 4262122) и 3,66 г (26,5 ммоль) карбоната калия в 60 мл метанола, нагревали при температуре дефлегмации в течение 18 ч. Охлажденную реакционную смесь выпаривали и добавляли воду. Полученный в результате осадок выделяли фильтрацией и сушили с получением 4,86 г (71%) продукта. Точка плавления: 194-196C. 4.2. 9-(2(S)-Гидрокси-2-фенилэтил)-7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она в 10 мл безводного диметилформамида добавляли 0,132 г (3,42 ммоль) гидрида натрия (60%-ная суспензия в минеральном масле) и полученную в результате смесь перемешивали в течение 15 мин при комнатной температуре. Добавляли 0,535 г (3,42 ммоль) (S)-2-хлор-1-фенилэтанола и реакционную смесь нагревали при 50C в течение 7 ч. Охлажденную реакционную смесь обрабатывали водой и экстрагировали этилацетатом. Экстракты сушили и упаривали и полученный остаток очищали хроматографией на силикагеле, элюируя смесью дихлорметан/метанол в соотношениях от 100/0 до 95/5 с получением 0,084 г (14%) продукта, который превращали в солянокислую соль обычным способом. Точка плавления 113-115C. [a]D + 54,7C (с = 0,6,CH3OH). Пример 5. (Соединение 54 в табл. 1). 9-(2(S)-Этокси-2-фенилэтил)-7,7-диметил-2-(пиримидин-4 ил)-6,7,8,9-тетрагидро-4H-пиримидо[1,2-а]пиримидин-4-он. К раствору 0,092 г (0,244 ммоль) 7,7-диметил-9-[2-(2(S)-гидроксифенилэтил)]-2-(пиримидин-4-ил)6,7,8,9-тетрагидро-4H-пиримидо[1,2-а]пиримидин-4-она в 3 мл безводного диметилформамида добавляли 0,010 г (0,244 ммоль) гидрида натрия (60%-ная суспензия в минеральном масле) и смесь перемешивали при комнатной температуре в течение 1 ч. К этому раствору, охлажденному до 0C, добавляли 0,019 мл (0,244 ммоль) йодэтана и смесь нагревали при 60C в течение 2 ч. Добавляли воду и смесь экстрагировали дихлорметаном. Экстракты промывали насыщенным водным раствором хлорида натрия, сушили и выпаривали. Остаток очищали хроматографией на силикагеле,элюируя смесью дихлорметан/метанол/аммиак в соотношениях от 95/5/0,5 с получением 57 мг (56%) продукта. Точка плавления 113-115C. [а]D +19,4 (с = 0,82, CH3OH). Пример 6. (Соединение 58 в табл. 1). 9-(2-Бензо[1,3]диоксол-5-ил-2-гидроксипропил)-7,7 диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-он. 6.1. 7,7-Диметил-9-(2-оксопропил)-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-он.- 14007165 К раствору 3,815 г (14,83 ммоль) 7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2 а]пиримидин-4-она в 50 мл безводного диметилформамида добавляли 0,771 г (19,28 ммоль) гидрида натрия (60%-ная суспензия в минеральном масле). Суспензию перемешивали при комнатной температуре в течение 30 мин. Добавляли 1,54 мл (19,28 ммоль) 1-хлорпропанона и раствор нагревали при 60C в течение 4 ч. К охлажденному раствору добавляли воду и смесь экстрагировали дихлорметаном. Экстракты промывали насыщенным водным раствором хлорида натрия, сушили и выпаривали. Остаток очищали хроматографией на силикагеле, элюируя смесью дихлорметан/метанол в соотношениях от 100/0 до 90/10 с получением 2,58 г (85%) продукта. 6.2. 9-(2-Бензо[1,3]диоксол-5-ил-2-гидроксипропил)-7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-он. К раствору 0,3 г (0,957 ммоль) 7,7-диметил-9-(2-оксопропил)-2-(пиримидин-4-ил)-6,7,8,9 тетрагидро-4H-пиримидо[1,2-а]пиримидин-4-она в 2 мл безводного тетрагидрофурана при -2C добавляли 2,1 мл (9,57 ммоль) раствора 3,4-(метилендиокси)фенилмагнийбромида (1 M раствор в смеси тетрагидрофуран/толуол 50/50) в течение 20 мин. После перемешивания в течение 15 мин при комнатной температуре реакционную смесь гасили добавлением насыщенного водного раствора хлорида аммония. Реакционную смесь экстрагировали дихлорметаном и экстракты промывали насыщенным водным раствором хлорида натрия, сушили и упаривали. Остаток очищали хроматографией на силикагеле, элюируя смесью этилацетат/циклогексан в соотношениях от 50/50 до 100/0 с получением 0,210 г (50%) продукта. Точка плавления: 194-196C. Пример 7. (Соединение 2 в табл. 2). 1-[3-(2-Фторфенил)пропил]-2,2-диметил-7-пиримидин-4-ил 2,3-дигидро-1 Н-имидазо[1,2-а]пиримидин-5-она гидрохлорид (1:1). 7.1. 5,5-Диметил-4,5-дигидро-1 Н-имидазол-2-иламина гидробромид (1:1). К раствору 15 г (0,17 ммоль) 1,2-диамино-2-метилпропана в 150 мл воды при 0C частями добавляли 18 г (0,17 моль) бромциана и температуре позволяли нагреваться до комнатной в течение 4 ч. Воду удаляли выпариванием и этанол добавляли и выпаривали. После растирания в смеси диэтилового эфира и этанола получали 29,5 г (89%) продукта в виде аморфного гигроскопического твердого вещества. 7.2. 2,2-Диметил-7-пиримидин-4-ил-2,3-дигидро-1 Н-имидазо[1,2-а]пиримидин-5-он. Смесь, содержащую 2,0 г (10,3 ммоль) этил-3-(4-пиримидинил)-3-оксопропионата, 2,0 г (10,3 ммоль) 5,5-диметил-4,5-дигидро-1 Н-имидазол-2-иламина гидробромида и 2,85 г (20,6 ммоль) карбоната калия в 15 мл метанола нагревали при температуре дефлегмации в течение 18 ч. Растворитель удаляли выпариванием и остаток обрабатывали водой и экстрагировали дихлорметаном. Экстракты сушили и выпаривали с получением 0,960 (39%) продукта. Точка плавления: 238-240C. 7.3. 1-[3-(2-Фторфенил)пропил]-2,2-диметил-7-пиримидин-4-ил-2,3-дигидро-1H-имидазо[1,2-а] пиримидин-5-она гидрохлорид (1:1). К раствору 0,2 г (0,822 ммоль) 2,2-диметил-7-пиримидин-4-ил-2,3-дигидро-1 Н-имидазо[1,2 а]пиримидин-5-она в 6 мл безводного диметилформамида обрабатывали 39 мг (0,986 ммоль) гидрида натрия (60%-ная суспензия в минеральном масле) и смесь нагревали при 60C в течение 10 мин. К охлажденной реакционной смеси добавляли 0,210 г (0,904 ммоль) 1-[3-(метилсульфонилокси)пропил]-2 фторбензола и нагревание поддерживали при 130C в течение 1 ч. Добавляли воду и реакционную смесь экстрагировали этилацетатом. Объединенные экстракты промывали насыщенным водным раствором хлорида натрия, сушили и выпаривали. Полученный остаток очищали хроматографией на силикагеле, элюируя смесью дихлорметан/метанол в соотношениях от 99/1 до 90/10 с получением 0,25 г (80%) продукта, который обрабатывали одним эквивалентом хлористого водорода в изопропаноле с получением моногидрохлорида. Точка плавления: 170-172C. Пример 8. (Соединение 1 в табл. 3). 9-[2-(4-Фтор-2-метоксифенил)этил]-8-метил-2-(пиримидин 4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-он. 8.1. 8-Метил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-он. Смесь 7,76 г (40,0 ммоль) этил-3-(4-пиримидинил)-3-оксопропионата (полученного по аналогии со способом, описанным в патенте DE 2705582), 6,0 г (40,0 ммоль) 6-метил-1,4,5,6-тетрагидропиримидин-2 иламина гидрохлорида (полученного в соотвествии с J. Org. Chem., 20, 1955, 829-838) и 8,29 г (60,0 ммоль) карбоната калия в 50 мл этанола нагревали при температуре дефлегмации в течение 18 ч. Реакционную смесь охлаждали и растворитель удаляли выпариванием. Полученный остаток обрабатывали водой и осадок выделяли фильтрацией с получением 3,81 г (39%) продукта. Точка плавления: 199-201C. 8.2. (4-Фтор-2-метоксифенил)уксусной кислоты метиловый эфир. К суспензии 14,34 г (32,47 ммоль) ацетата свинца(IV) в 100 мл безводного толуола добавляли смесь 5,2 г (30,92 ммоль) 1-(4-фтор-2-метоксифенил)этанона и 15,02 мл (123,13 ммоль) эфирата трифторида бора в 9 мл этанола. Реакционную смесь дополнительно перемешивали при комнатной температуре в течение 16 ч. К охлажденной смеси добавляли воду и полученный в результате раствор экстрагировали- 15007165 толуолом. Экстракты промывали насыщенным раствором гидрокарбоната натрия, насыщенным раствором хлорида натрия и сушили сульфатом натрия. Растворитель выпаривали до сухости с получением 6 г в виде масла, которое использовали на следующей стадии без дополнительной очистки. 8.3. 2-(4-Фтор-2-метоксифенил)этанол. К суспензии 1,72 г (45,41 ммоль) литийалюминийгидрида в 120 мл тетрагидрофурана при 0C по каплям добавляли 6 г (30,27 ммоль) растворенного в 120 мл (4-фтор-2-метоксифенил)уксусной кислоты метилового эфира и полученную в результате смесь перемешивали при комнатной температуре в течение 1 ч. Реакционную смесь разбавляли 100 мл диэтилового эфира при 0C и обрабатывали избытком насыщенного водного раствора сульфата натрия. Добавляли дополнительно твердый сульфат натрия и органическую фазу фильтровали для удаления солей. Растворитель выпаривали до сухости с получением 5,1 г (99%) продукта в виде масла. 8.4. Метансульфоновой кислоты 2-(4-фтор-2-метоксифенил)этиловый эфир. К раствору 5,1 г (29,97 ммоль) 2-(4-фтор-2-метоксифенил)этанола в 30 мл безводного дихлорметана добавляли при 0C 6,26 мл (44,95 ммоль) триэтиламина и 3,5 мл (44,95 ммоль) метансульфонилхлорида. Полученную в результате смесь перемешивали при 0C в течение 1 ч. Эту смесь затем разбавляли водой и дихлорметаном и экстрагировали дихлорметаном. Органический слой сушили и выпаривали с получением 7 г (100%) метансульфоновой кислоты 2-(4-фтор-2-метоксифенил)этилового эфира. 8.5. 9-[2-(4-Фтор-2-метоксифенил)этил]-8-метил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-он. К раствору 0,18 г (0,74 ммоль) 8-метил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а] пиримидин-4-она в 4 мл безводного диметилформамида добавляли 0,033 г (0,81 ммоль) гидрида натрия(60%-ная суспензия в минеральном масле) и смесь оставляли перемешиваться при 50C в течение 20 мин. Добавляли 0,202 г (0,81 ммоль) метансульфоновой кислоты 2-(4-фтор-2-метоксифенил)этилового эфира и перемешивание продолжали в течение 18 ч. Добавляли воду и смесь экстрагировали дихлорметаном. Экстракты промывали насыщенным водным раствором хлорида натрия, сушили и выпаривали с получением неочищенного продукта. После очистки хроматографией на силикагеле, элюируя смесью дихлорметан/метанол в соотношениях от 100/0 до 96/4 получали 0,154 г (53%) чистого продукта. Точка плавления: 148-150C. Пример 9. (Соединение 2 в табл. 3). 9-[2-(4-Фтор-2-метоксифенил)этил]-8,8-диметил-2(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-он. 9.1. 8,8-Диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-он. Смесь 2,39 г (12,31 ммоль) этил-3-(4-пиримидинил)-3-оксопропионата (полученного по аналогии со способом, описанным в патенте DE 2705582), 2,33 г (11,19 ммоль) 6,6-диметил-1,4,5,6-тетрагидропиримидин-2-иламина гидробромида (полученного в соотвествии с Bull. Soc. Chim. Belg., 1950, 59, 573587) и 3,25 г (23,5 ммоль) карбоната калия в 25 мл этанола нагревали при температуре дефлегмации в течение 18 ч. Реакционную смесь охлаждали и растворитель удаляли выпариванием. Полученный остаток обрабатывали водой и осадок выделяли фильтрацией с получением 1 г (35%) продукта. Точка плавления: 265267C. 9.2. 9-[2-(4-Фтор-2-метоксифенил)этил]-8,8-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-он. К раствору 0,2 г (0,78 ммоль) 8,8-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2 а]пиримидин-4-она в 5 мл безводного диметилформамида добавляли 0,035 г (0,86 ммоль) гидрида натрия(60%-ная суспензия в минеральном масле) и смесь оставляли перемешиваться при 50C в течение 20 мин. Добавляли 0,212 г (0,86 ммоль) метансульфоновой кислоты 2-(4-фтор-2-метоксифенил)этилового эфира и перемешивание продолжали в течение 18 ч. Добавляли воду и смесь экстрагировали дихлорметаном. Экстракты промывали насыщенным водным раствором хлорида натрия, сушили и выпаривали с получением неочищенного продукта. После очистки хроматографией на силикагеле, элюируя смесью дихлорметан/метанол в соотношениях от 100/0 до 96/4 получали 0,136 г (43%) чистого продукта. Точка плавления: 196-198C. Пример 10. (Соединение 11 в табл. 3). 9-(2(S)-Гидрокси-2-фенилэтил)-8,8-диметил-2-пиримидин 4-ил-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-он. К раствору 0,2 г (0,78 ммоль) 8,8-диметил-2-пиримидин-4-ил-6,7,8,9-тетрагидро-4H-пиримидо[1,2 а]пиримидин-4-она в 3 мл безводного диметилформамида добавляли 0,07 г (1,71 ммоль) гидрида натрия(60%-ная суспензия в минеральном масле), и смесь оставляли перемешиваться при 500C в течение 1 ч. Добавляли 0,158 г (1,01 ммоль) 1(S)-2-хлор-1-фенилэтанола и смесь оставляли перемешиваться при 120C в течение 12 ч. Добавляли воду и смесь экстрагировали этилацетатом. Экстракты промывали насыщенным водным раствором хлорида натрия, сушили и выпаривали с получением неочищенного продукта. После очистки хроматографией на силикагеле, элюируя смесью дихлорметан/метанол в соотношениях от 100/0 до 96/24- 16007165 получали 0,21 г (72%) чистого продукта. Точка плавления 178-179C, []D +45,7 (с = 0,784, CHCl3). Пример 11. (Соединение 15 в табл. 3). 8,8-Диметил-9-(2-оксо-2-фенилэтил)-2-пиримидин-4-ил 6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-он. К раствору 0,24 мл (3,3 ммоль) диметилсульфоксида в 3 мл безводного дихлорметана при -78C добавляли 0,42 мл (2,93 ммоль) трифторуксусного ангидрида в 2 мл безводного дихлорметана и смесь оставляли перемешиваться при -78C в течение 20 мин. Добавляли 0,201 г (0,53 ммоль) 9-(2(S)-гидрокси-2 фенилэтил)-8,8-диметил-2-пиримидин-4-ил-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она в 2 мл безводного дихлорметана при -78C и перемешивание продолжали в течение 30 мин. Добавляли 0,62 мл (4,47 ммоль) триэтиламина и смесь оставляли перемешиваться при комнатной температуре в течение 12 ч. Добавляли воду и смесь экстрагировали этилацетатом, экстракты промывали насыщенным водным, раствором хлорида аммония, насыщенным водным раствором хлорида натрия,сушили и выпаривали с получением неочищенного продукта. После очистки хроматографией на силикагеле, элюируя этилацетатом, получали 0,045 г (23%) чистого продукта. Точка плавления 203-205C. Пример 12. (Соединение 19 в табл. 3). 8-Этил-9-(2-оксо-2-фенилэтил)-2-пиримидин-4-ил-6,7,8,9 тетрагидропиримидо[1,2-а]пиримидин-4-он. 12.1. 8-Этил-2-пиримидин-4-ил-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-он. Смесь 5 г (25,75 ммоль) этил-3-(4-пиримидинил)-3-оксопропионата, 3,83 г (23,41 ммоль) 6-этил 1,4,5,6-тетрагидропиримидин-2-иламина гидрохлорида (полученного в соотвествии с J. Org. Chem., 20,1955, 829-838) и 6,794 г (49,16 ммоль) карбоната калия в 50 мл этанола нагревали при температуре дефлегмации в течение 18 ч. Реакционную смесь охлаждали и растворитель удаляли выпариванием. Полученный остаток обрабатывали водой и осадок выделяли фильтрацией с получением 3,62 г (60%) продукта. Точка плавления: 226-228C. 12.2. 8-Этил-9-(2-оксо-2-фенилэтил)-2-пиримидин-4-ил-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-он. К раствору 0,35 г (1,36 ммоль) 8-этил-2-пиримидин-4-ил-6,7,8,9-тетрагидро-4H-пиримидо[1,2 а]пиримидин-4-она в 7 мл безводного диметилформамида добавляли 0,071 г (1,77 ммоль) гидрида натрия(60%-ная суспензия в минеральном масле) и смесь оставляли перемешиваться при 25C в течение 15 мин. При 0C добавляли 0,352 мл (1,77 ммоль) фенацилбромида. Смесь оставляли перемешиваться при 0C в течение 3 ч и температуре позволяли нагреваться до комнатной температуры в течение 12 ч. Добавляли воду и смесь экстрагировали этилацетатом. Экстракты промывали насыщенным водным раствором хлорида натрия, сушили и упаривали с получением неочищенного продукта. После очистки хроматографией на силикагеле, элюируя смесью дихлорметан/метанол в соотношениях от 100/0 до 98/2,получали 0,163 г (32%) чистого продукта. Точка плавления: 187-189C. Пример 13. (Соединение 20 в табл. 3). 9-[2-(4-Фторфенил)-2(S)-гидроксиэтил]-8,8-диметил-2 пиримидин-4-ил-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-он. 13.1. (1S)-2-бром-1-фенилэтанол. К раствору 2,30 мл (2,30 ммоль) комплекса боран-тетрагидрофуран (1 M раствор в тетрагидрофуране) добавляли при -30C 0,46 мл (0,46 ммоль) (S)-2-метил-CBS (Corey, Bakshi, Shibata)-оксазаборолидина(1 M раствор в толуоле). К раствору за 1 ч добавляли 0,5 г (2,30 ммоль) 4'-фторфенацилбромида в 1,85 мл безводного дихлорметана, в это время температуру внутри поддерживали при -30C. Смесь перемешивали при -20C в течение 1 ч. К реакционной смеси добавляли 1,85 мл метанола. Раствор нагревали до комнатной температуры, добавляли 5,55 мл водной соляной кислоты (1 н.). Смесь экстрагировали этилацетатом, экстракты сушили над сульфатом натрия и концентрировали в вакууме с получением 0,498 г 2 бром-1-фенилэтанола, который использовали без очистки в следующей реакции. 13.2. 9-[2-(4-Фторфенил)-2(S)-гидроксиэтил]-8,8-диметил-2-пиримидин-4-ил-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-он. К раствору 0,3 г (1,17 ммоль) 8,8-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2 а]пиримидин-4-она в 5 мл безводного диметилформамида добавляли 0,105 г (2,57 ммоль) гидрида натрия(60%-ная суспензия в минеральном масле) и смесь оставляли перемешиваться при 50C в течение 1 ч. Добавляли 0,332 г (1,01 ммоль) (1S)-2-бром-1-фенилэтанола и смесь оставляли перемешиваться при 120C в течение 12 ч. Добавляли воду и смесь экстрагировали дихлорметаном. Экстракты промывали насыщенным водным раствором хлорида натрия, сушили и выпаривали с получением неочищенного продукта. После очистки хроматографией на силикагеле, элюируя этилацетатом, получали 0,24 г (52%) чистого продукта. Точка плавления: 176-178C. []D = +51,6 (с = 0,844, CHCl3). Перечень химических структур и физических данных для соединений указанной выше формулы (I),иллюстрирующих настоящее изобретение, приведен в табл. 1, 2 и 3. Соединения готовили способами из примера. В этих таблицах R1 представляет собой незамещенную пиримидин-4-ильную группу, Ph представляет собой фенильную группу, Et представляет собой этильную группу, Me представляет собой метиль- 17007165 ную группу, (S), (R) или (рац.) указывает в колонке Y стереохимию атома углерода, (рац.) означает рацемическую смесь, (R) означает абсолютную R-конфигурацию, (S) означает абсолютную S-конфигурацию. В табл. 1 для соединений формулы (I) m и р равны 1; в табл. 2 для соединений формулы (I) m равно 0 и р равно 1 и в табл. 3 для соединений формулы (I) m равно 0 и р равно 2.- 27007165 Пример испытания 1. Ингибирующая активность лекарства по настоящему изобретению в отношении GSK3: Можно использовать два разных протокола. По первому протоколу 7,5 мкМ предварительно фосфорилированного GS1 (гликогенсинтазы 1) пептида и 10 мкМ ATP (аденозинтрифосфата) (содержащего 300000 импульсов в минуту 33P-ATP) инкубировали в 25 мМ Tris-HCl (трис(гидроксиметил)аминометан), рН 7,5, 0,6 мМ DTT (дитиотреитола), 6 мМ MgCl2, 0,6 мМ EGTA (этиленбис(оксиэтиленнитрило)тетрауксусной кислоты), 0,05 мг/мл BSA (бычий сывороточный альбумин) буфера в течение 1 ч при комнатной температуре в присутствии GSK3(общий объем реакционной смеси: 100 мкл). По второму протоколу 4,1 мкМ предварительно фосфорилированного GS1 пептида и 42 мкМ ATP(содержащего 260000 импульсов в минуту 33P-ATP) инкубировали в 80 мМ Mes (2-(N-морфолино) этансульфоновая кислота)-NаОН, рН 6,5, 1 мМ ацетата Mg, 0,5 мМ EGTA, 5 мМ 2-меркаптоэтанола,0,02% Твин-20, 10% глицеринового буфера в течение 2 ч при комнатной температуре в присутствииP2O5), 126 мл 85%-ной H3PO4, H2O до 500 мл и затем перед применением разбавленного до 1:100. Аликвоту реакционной смеси затем переносили на Whatman P81 катионообменные фильтры и промывали раствором, описанным выше. Внедренную 33 Р радиоактивность определяли при помощи жидкостной сцинтилляционной спектрометрии. Фосфорилированный GS-1 пептид имел следующую последовательность:GSK3 ингибирующую активность соединений по настоящему изобретению выражают в IC50 (концентрации, вызывающей 50%-ное ингибирование) и в качестве иллюстрации интервал IC50 значений соединений табл. 1 находится между концентрациями 2 нмоль и 2 мкмоль, соединений табл. 2 находится между концентрациями 30 нмоль и 2 мкмоль и соединений табл. 3 находится между концентрациями 1 нмоль и 2 мкмоль. Пример испытания 2. Ингибирующая активность лекарства по настоящему изобретению в отношении cdk5/p25: Можно использовать следующий протокол: 0,4 мг/мл гистона Н 1 и 10 мкМ ATP (содержащего 300000 импульсов в минуту 33P-ATP) инкубировали в 50 мМ HEPES, рН 7,2, 1 мМ DTT, 1 мМ MgCl2, 1 мМ EGTA, 0,02% Твин-20 буфера в течение 1 ч при комнатной температуре в присутствии cdk5/p25 (общий объем реакционной смеси: 100 мкл). Ингибиторы растворяли в DMSO (конечная концентрация в реакционной среде 1%). Реакцию останавливали 100 мкл раствора из 25 г полифосфорной кислоты (85% Р 2 О 5), 126 мл 85%ной Н 3 РО 4, H2O до 500 мл (разбавленного до 1:100 перед применением). Аликвоту реакционной смеси затем переносили на Whatman P81 катионообменные фильтры и промывали раствором, описанным выше. Внедренную 33P радиоактивность определяли при помощи жидкостной сцинтилляционной спектрометрии.Cdk5/p25 ингибирующую активность соединений по настоящему изобретению выражали в виде значений IC50. Обычно использовали 3-кратные серийные разведения ингибитора для по меньшей мере 1000-кратного интервала концентраций. В качестве иллюстрации интервал IC50 значений соединений табл. 1 находится между концентрациями 200 нмоль и 5 мкмоль, соединений табл. 2 находится между концентрациями 100 нмоль и 5 мкмоль и соединений табл. 3 находится между концентрациями 100 нмоль и 5 мкмоль. В качестве иллюстрации, конкретные значения IC50 некоторых соединений указанной выше формулы (I), иллюстрирующие настоящее изобретение, приведены в табл. 4. Таблица 4(1) Таблетки. Указанные ниже ингредиенты смешивали обычным способом и прессовали, используя традиционные приспособления. Соединение примера 1 30 мг Кристаллическая целлюлоза 60 мг Кукурузный крахмал 100 мг Лактоза 200 мг Стеарат магния 4 мг(2) Мягкие капсулы. Указанные ниже ингредиенты смешивали обычным способом и заполняли мягкие капсулы. Соединение примера 1 30 мг Оливковое масло 300 мг Лецитин 20 мг(3) Парентеральные препараты. Указанные ниже ингредиенты смешивали обычным способом для приготовления инъекций, содержащихся в 1 мл ампуле. Соединение примера 1 3 мг Хлорид натрия 4 мг Дистиллированная вода для инъекций 1 мл Промышленная применимость Соединения по настоящему изобретению обладают GSK3 или GSK3 и cdk5/p25 ингибирующей активностью и их применяют в качестве активного ингредиента лекарства для профилактического и/или терапевтического лечения заболеваний, обусловленных ненормальной активностью GSK3 или GSK3 и где X представляет собой два атома водорода, атом серы, атом кислорода или C1-2 алкильную группу и атом водорода;Y представляет собой связь, этениленовую группу, этиниленовую группу, атом кислорода, атом серы, сульфонильную группу, сульфоксидную группу, карбонильную группу, атом азота, возможно замещенный C1-6 алкильной группой, фенильной или бензильной группой; или метиленовую группу, возможно замещенную одной или двумя группами, выбранными из C1-6 алкильной группы, бензильной группы,гидроксигруппы, C1-4 алкоксигруппы, С 3-6 циклоалкилметилокси, C1-2 пергалогенированной алкильной группы, аминогруппы, ацетиламиногруппы или фенильной группы;R1 представляет собой пиримидиновое кольцо, возможно замещенное C3-6 циклоалкильной группой,C1-4 алкильной группой, C1-4 алкоксигруппой, бензильной группой или атомом галогена; когда Y представляет собой связь, возможно замещенную метиленовую группу или карбонильную группу, тогда R2 представляет собой C1-6 алкильную группу, возможно замещенную С 6,10 арилокси или С 6,10 ариламиногруппой; C3-6 циклоалкильную группу, C1-4 алкилтиогруппу, C1-4 алкоксигруппу, C1-2 пергалогенированную алкильную группу, C1-3 галогенированную алкильную группу, фенилтиогруппу, бензильную группу, бензольное кольцо, индановое кольцо, 5,6,7,8-тетрагидронафталиновое кольцо, нафталиновое кольцо, пиридиновое кольцо, пиррольное кольцо, тиофеновое кольцо, фурановое кольцо или имидазольное кольцо; бензильную группу или кольца, возможно замещенные 1-4 заместителями, выбранными из C1-6 алкильной группы, метилендиоксигруппы, атома галогена, C1-2 пергалогенированной алкильной группы, C1-3 галогенированной алкильной группы, гидроксигруппы, C1-4 алкоксигруппы, нитро,циано, амино, C1-5 моноалкиламиногруппы, C2-10 диалкиламиногруппы, C1-6 алкилкарбониламиногруппы,С 6,10 арилкарбониламиногруппы, C1-4 алкилсульфонильной группы, C1-4 алкилсульфонилоксигруппы или фенильной группы; когда Y представляет собой этениленовую группу, этиниленовую группу, атом кислорода, атом серы, сульфонильную группу, сульфоксидную группу или возможно замещенный атом азота, тогда R2(возможно замещенную С 6,10 арилокси или представляет собойC1-6 алкильную С 6,10 ариламиногруппой), С 3-6 циклоалкильную группу, C1-2 пергалогенированную алкильную группу,C1-3 галогенированную алкильную группу, бензильную группу, бензольное кольцо, индановое кольцо,5,6,7,8-тетрагидронафталиновое кольцо, нафталиновое кольцо, пиридиновое кольцо, пиррольное кольцо,тиофеновое кольцо, фурановое кольцо или имидазольное кольцо; бензильную группу или кольца, возможно замещенные 1-4 заместителями, выбранными из C1-6 алкильной группы, метилендиоксигруппы,атома галогена, C1-2 пергалогенированной алкильной группы, C1-3 галогенированной алкильной группы,гидроксильной группы, C1-4 алкоксигруппы, нитро, циано, амино, C1-5 моноалкиламиногруппы, C2-10 диалкиламиногруппы, C1-6 алкилкарбониламиногруппы, С 6,10 арилкарбониламиногруппы, С 1-4 алкилсульфонильной группы, С 1-4 алкилсульфонилоксигруппы или фенильной группы;R3 и R4 представляют собой, каждый независимо, атом водорода, C1-6 алкильную группу, гидроксигруппу, C1-4 алкоксигруппу или атом галогена;R5 представляет собой атом водорода, C1-6 алкильную группу или атом галогена; когда m равно 0, р равно 1, 2 или 3,когда m равно 1, р равно 0, 1 или 2,когда m равно 2, р равно 0 или 1 иn представляет собой 0-3. 2. Производное пиримидона, или его соль, или его сольват, или его гидрат по п.1, где R1 представляет собой незамещенное 4-пиримидиновое кольцо. 3. Производное пиримидона, которое выбрано из группы, состоящей из 9-(3-фенилпропил)-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,9-[2-(2-хлор-4-фторфенил)этил]-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин 4-она,9-(2-фенилсульфанилэтил)-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4 она,9-(2-оксо-2-фенилэтил)-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,9-(3-гидрокси-3-фенилпропил)-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин 4-она,9-(2-гидрокси-2-фенилэтил)-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4 она,9-(3-оксо-3-фенилпропил)-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,9-(2(R)-гидрокси-2-фенилэтил)-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин 4-она,9-(2(S)-гидрокси-2-фенилэтил)-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин 4-она,9-[2-(3-хлорфенил)-2-оксоэтил]-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин 4-она,9-[2-(3-фторфенил)-2-оксоэтил]-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин 4-она. 9-[2-(3-фторфенил)-2-гидроксиэтил]-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,9-[2-(3-хлорфенил)-2-гидроксиэтил]-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,9-(1-метил-2-оксо-2-фенилэтил)-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин 4-она,9-(2-гидрокси-1-метил-2-фенилэтил)-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,9-[2-(3-хлорфенил)-2(R)-гидроксиэтил]-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,7,7-дифтор-9-(2-оксо-2-фенилэтил)-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,7,7-диметил-9-(2-оксо-2-фенилэтил)-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,9-(2(S)-гидрокси-2-фенилэтил)-7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2 а]пиримидин-4-она,9-[2-(3-хлорфенил)-2-оксоэтил]-7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2 а]пиримидин-4-она,9-[2-(3-хлорфенил)-2-гидроксиэтил]-7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин-4-она,9-[2-(3-фторфенил)-2-оксоэтил]-7,7-диметил-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2 а]пиримидин-4-она,3-метил-9-(2-оксо-2-фенилэтил)-2-(пиримидин-4-ил)-6,7,8,9-тетрагидропиримидо[1,2-а]пиримидин- 30
МПК / Метки
МПК: C07D 487/04, A61K 31/519, A61P 25/28
Метки: нейродегенеративных, она, производные, нарушений, 9-тетрагидропиримидо, 2-пиримидинил-6, 7-пиримидинил-2,3-дигидроимидазо[1, 1,2-а]пиримидин-4-она, 2-а]пиримидин-5, замещенного
Код ссылки
<a href="https://eas.patents.su/30-7165-proizvodnye-zameshhennogo-2-pirimidinil-6-7-8-9-tetragidropirimido-12-apirimidin-4-ona-i-7-pirimidinil-23-digidroimidazo1-2-apirimidin-5-1n-ona-dlya-nejjrodegenerativnyh-narushenij.html" rel="bookmark" title="База патентов Евразийского Союза">Производные замещенного 2-пиримидинил-6, 7, 8, 9-тетрагидропиримидо [1,2-а]пиримидин-4-она и 7-пиримидинил-2,3-дигидроимидазо[1, 2-а]пиримидин-5( 1н )она для нейродегенеративных нарушений</a>
Предыдущий патент: Фунгицидные триазолопиримидины, способ их получения и их применение для борьбы с фитопатогенными грибами, а также содержащие их средства
Следующий патент: Способ создания скважины в земном пласте
Случайный патент: Способ получения гидразингидрата












