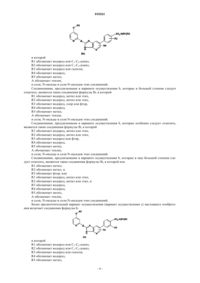
Производные имидазопиридина как ингибиторы индуцируемой no – синтазы
Номер патента: 10261
Опубликовано: 30.06.2008
Авторы: Фуксс Томас, Штруб Андреас, Мартин Томас, Бёр Райнер, Ульрих Вольф-Рюдигер, Ленер Мартин, Эльтце Манфрид
Формула / Реферат
1. Соединения формулы I

в которой
R1 обозначает водород или С1-С4-алкил,
R2 обозначает водород или С1-С4-алкил,
R3 обозначает водород или галоген,
R4 обозначает водород, галоген, С1-С4-алкил или С1-С4-алкоксигруппу,
R5 обозначает С1-С4-алкил,
А обозначает С1-С4-алкилен,
и соли, N-оксиды и соли N-оксидов этих соединений.
2. Соединения по п.1, где указанные соединения обладают формулами Ia, Ib или Ic:


и соли, N-оксиды и соли N-оксидов этих соединений.
3. Соединения по п.1, где указанные соединения обладают формулами I, Ia, Ib или Ic, в которых
R1 обозначает водород или С1-С4-алкил,
R2 обозначает водород или С1-С4-алкил,
R3 обозначает водород или галоген,
R4 обозначает водород,
R5 обозначает метил,
А обозначает этилен,
и соли, N-оксиды и соли N-оксидов этих соединений.
4. Соединения по п.1, где указанные соединения обладают формулами I, Ia, Ib или Ic, в которых
R1 обозначает водород, метил или этил,
R2 обозначает водород, метил или этил,
R3 обозначает водород или фтор,
R4 обозначает водород,
R5 обозначает метил,
А обозначает этилен,
и соли, N-оксиды и соли N-оксидов этих соединений.
5. Соединения по п.1, где указанные соединения обладают формулами I, Ia, Ib или Ic, в которых
или
R1 обозначает метил,
R2 обозначает метил и
R3 обозначает фтор, или
R1 обозначает водород, метил или этил,
R2 обозначает водород, метил или этил и
R3 обозначает водород,
R4 обозначает водород,
R5 обозначает метил,
А обозначает этилен,
и соли, N-оксиды и соли N-оксидов этих соединений.
6. Соединения по п.1, где указанные соединения обладают формулами Ib или Ic, в которых
R1 обозначает водород, метил или этил,
R2 обозначает водород, метил или этил,
R3 обозначает водород или фтор,
R4 обозначает водород,
R5 обозначает метил,
А обозначает этилен,
и соли, N-оксиды и соли N-оксидов этих соединений.
7. Соединения по п.1, где указанные соединения обладают формулой Ic, в которой
или
R1 обозначает метил,
R2 обозначает метил и
R3 обозначает фтор, или
R1 обозначает водород, метил или этил,
R2 обозначает водород, метил или этил и
R3 обозначает водород,
R4 обозначает водород,
R5 обозначает метил,
А обозначает этилен,
и соли, N-оксиды и соли N-оксидов этих соединений.
8. Соединения по п.1, где указанные соединения обладают формулой [d]
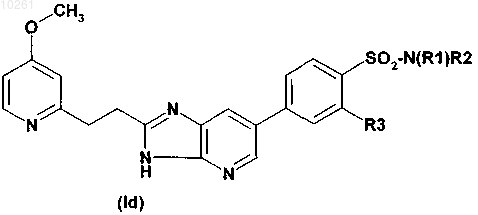
в которой Rl, R2 и R3 имеют любое из указанных ниже значений от 1 до 12:
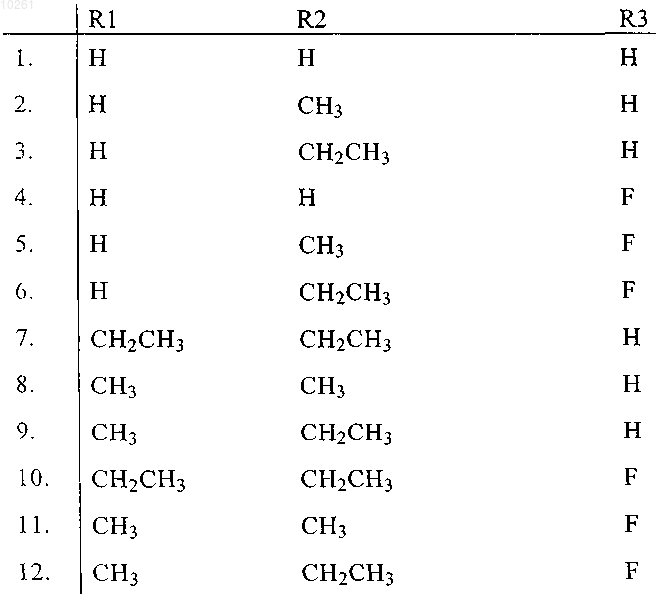
и соли, N-оксиды и соли N-оксидов этих соединений.
9. Соединения формулы I по п.1, обладающие активностью ингибитора NO-синтазы.
10. Фармацевтическая композиция, содержащая одно или несколько соединений формулы I по п.1 совместно с обычными фармацевтическими вспомогательными веществами и/или инертными наполнителями.
11. Применение соединений формулы I по п.1 для изготовления фармацевтических композиций, предназначенных для лечения острых воспалительных заболеваний.
12. Применение соединений формулы I по п.1 для изготовления фармацевтических композиций, предназначенных для лечения хронических воспалительных заболеваний периферических органов и ЦНС (центральной нервной системы).
13. Способ лечения острых воспалительных заболеваний у пациента, включающий введение указанному пациенту терапевтически эффективного количества соединения формулы I по п.1.
14. Способ лечения хронических воспалительных заболеваний периферических органов и ЦНС у пациента, включающий введение указанному пациенту терапевтически эффективного количества соединения формулы I по п.1.
Текст
010261 Область техники, к которой относится изобретение Настоящее изобретение относится к новым производным имидазопиридина, которые применяются в фармацевтической промышленности для приготовления фармацевтических композиций. Уровень техники В заявке на патент Германии DE 2504252 и в заявке на европейский патент ЕР 0125756 описаны производные 3 Н-имидазо[4,5-b]пиридина, обладающие противоязвенной активностью. В заявке на международный патент WO 0049015 описаны пиридиновые соединения, оказывающие ингибирующее воздействие на выработку оксида азота. В заявке на международный патент WO 0380607 описаны производные алкоксипиридина, оказывающие ингибирующее воздействие на iNOS. Описание изобретения Согласно изобретению обнаружено, что некоторые новые, специально выбранные аминосульфонилфенилзамещенные производные имидазопиридина, которые более подробно описаны ниже, значительно отличаются от выбранных ранее соединений и обладают неожиданными и особенно полезными и необходимыми свойствами. Таким образом, настоящее изобретение относится к соединениям формулы IR1 обозначает водород или С 1-С 4-алкил,R2 обозначает водород или С 1-С 4-алкил,R3 обозначает водород или галоген,R4 обозначает водород, галоген, С 1-С 4-алкил или С 1-С 4-алкоксигруппу,R5 обозначает С 1-С 4-алкил,А обозначает С 1-С 4-алкилен,и к солям, N-оксидам и солям N-оксидов этих соединений. С 1-С 4-алкил обозначает линейный или разветвленный алкильный радикал, содержащий 1-4 атома углерода. Примерами являются бутильный, изобутильный, втор-бутильный, трет-бутильный, пропильный, изопропильный и предпочтительно этильный и метильный радикалы. С 1-С 4-алкоксигруппа обозначает радикал, который в дополнение к атому кислорода содержит линейный или разветвленный алкильный радикал, содержащий 1-4 атома углерода. Алкоксильными радикалами, содержащими 1-4 атома углерода, которые можно отметить в контексте настоящего изобретения,являются, например, бутоксильный, изобутоксильный, втор-бутоксильный, трет-бутоксильный, пропоксильный, изопропоксильный и, предпочтительно, этоксильный и метоксильный радикалы. С 1-С 4-алкилен обозначает алкиленовый радикал с линейной цепью, содержащий 1-4 атома углерода. Примерами, которые можно отметить в контексте настоящего изобретения, являются метиленовый (-СН 2-),этиленовый (-СН 2-СН 2-), триметиленовый (-СН 2-СН 2-СН 2-) и тетраметиленовый (-СН 2-СН 2-СН 2-СН 2-) радикалы. Галоген обозначает хлор или фтор.N-Оксид обозначает N-оксид пиридина, который замещен с помощью радикала -O-R5. Подходящими солями соединений, предлагаемых в настоящем изобретении - в зависимости от замещения - являются все молекулярные соли с кислотами или все соли с основаниями. Можно особо отметить фармакологически переносимые неорганические и органические кислоты и основания, обычно применяющиеся в фармацевтике. Подходящими являются, с одной стороны, нерастворимые в воде и в особенности растворимые в воде молекулярные соли с кислотами, такими как, например, хлористоводородная кислота, бромистоводородная кислота, фосфорная кислота, азотная кислота, серная кислота, уксусная кислота, лимонная кислота, D-глюконовая кислота, бензойная кислота, 2-(4 гидроксибензоил)бензойная кислота, масляная кислота, сульфосалициловая кислота, малеиновая кислота, лауриновая кислота, яблочная кислота, фумаровая кислота, янтарная кислота, щавелевая кислота,виннокаменная кислота, эмбоновая кислота, стеариновая кислота, толуолсульфоновая кислота, метансульфоновая кислота и 3-гидрокси-2-нафтойная кислота, кислоты, применяющиеся при получении солей- в зависимости от того, является ли кислота моно- или многоосновной, и в зависимости от того, какая соль необходима - в количественном эквимолярном или отличающемся от него соотношении. С другой стороны, подходящими также являются - в зависимости от замещения - соли с основаниями. В качестве примеров солей с основаниями отмечаются литиевые, натриевые, калиевые, кальциевые,алюминиевые, магниевые, титановые, аммониевые, меглуминовые и гуанидиниевые соли, и в этом слу-1 010261 чае при получении солей основания применяются в количественном эквимолярном или отличающемся от него соотношении. Фармакологически переносимые соли, которые можно получить, например, в виде продуктов при получении соединений, предлагаемых в настоящем изобретении, в промышленном масштабе, превращают в фармакологически переносимые соли по методикам, известными специалисту в данной области техники. В соответствии с заключением экспертов соединения, предлагаемые в настоящем изобретении, а также их соли, например, при выделении в кристаллической форме могут содержать различные количества растворителей. Поэтому в объем настоящего изобретения включены все сольваты и, в частности, все гидраты соединений, предлагаемых в настоящем изобретении, а также все сольваты и, в частности, все гидраты солей соединений, предлагаемых в настоящем изобретении. Специалист в данной области техники на основании своей профессиональной подготовки знает, что по отношению к конденсированному имидазольному кольцу имидазопиридиновой системы соединения,предлагаемые в настоящем изобретении, могут находиться в разных таутомерных формах, таких как,например, 1-Н-форма или предпочтительно 3-Н-форма, которая показана в формуле I. Настоящее изобретение включает все возможные таутомеры в чистом виде, а также в любом соотношении смешивания. В частности, настоящее изобретение включает чистые 1-Н- и предпочтительно 3-Н-таутомеры, а также любые их смеси. Вариант осуществления соединений, предлагаемых в настоящем изобретении, включает такие соединения формулы I, в которой R5 обозначает метил. Другой вариант осуществления соединений, предлагаемых в настоящем изобретении, включает такие соединения формулы I, в которой А обозначает этилен. Другой вариант осуществления соединений, предлагаемых в настоящем изобретении, включает такие соединения формулы I, в которой R4 обозначает водород. Другой вариант осуществления соединений, предлагаемых в настоящем изобретении, включает такие соединения формулы I, в которой R5 обозначает метил и А обозначает этилен. Другой вариант осуществления соединений, предлагаемых в настоящем изобретении, включает такие соединения формулы I, в которой R4 обозначает водород, R5 обозначает метил и А обозначает этилен. Другой вариант осуществления соединений, предлагаемых в настоящем изобретении, включает такие соединения формулы I, в которой замещенный аминосульфонилом фенильный фрагмент присоединен в положении 6 имидазопиридинового кольца. Заместитель R3 и аминосульфонильный радикал соединений, предлагаемых в настоящем изобретении, можно присоединить в орто-, мета- или пара-положении по отношению к положению связывания, в котором фенильное кольцо присоединено к имидазопиридиновой кольцевой системе, и в варианте осуществления настоящего изобретения аминосульфонильный радикал присоединен в пара-положении. В этом контексте другой вариант осуществления соединений, предлагаемых в настоящем изобретении, включает такие соединения формулы I, в которой R3 присоединен в мета-положении и аминосульфонильный радикал присоединен в пара-положении по отношению к положению связывания, в котором фенильное кольцо присоединено к имидазопиридиновой кольцевой системе. Другой специальный вариант осуществления соединений, предлагаемых в настоящем изобретении,включает такие соединения, которые обладают одной из приведенных ниже формул Ia, Ib или Ic. Соединениями, предлагаемыми в настоящем изобретении, которые следует отметить, являются такие соединения формулы I, в которой R1 обозначает водород или С 1-С 4-алкил, R2 обозначает водород или С 1-С 4-алкил, R3 обозначает водород или галоген, R4 обозначает водород, R5 обозначает метил, А обозначает этилен, и соли, N-оксиды и соли N-оксидов этих соединений. Соединениями, предлагаемыми в настоящем изобретении, которые в еще большей степени следует отметить, являются такие соединения формулы I, в которой R1 обозначает водород, метил или этил, R2 обозначает водород, метил или этил, R3 обозначает водород, хлор или фтор, R4 обозначает водород, R5 обозначает метил, А обозначает этилен, и соли, N-оксиды и соли N-оксидов этих соединений. Соединениями, предлагаемыми в настоящем изобретении, которые особенно следует отметить, являются такие соединения формулы I, в которой R1 обозначает водород, метил или этил, R2 обозначает водород, метил или этил, R3 обозначает водород или фтор, R4 обозначает водород, R5 обозначает метил,А обозначает этилен, и соли, N-оксиды и соли N-оксидов этих соединений. Соединениями, предлагаемыми в настоящем изобретении, которые в еще большей степени следует отметить, являются такие соединения формулы I, в которой илиR4 обозначает водород,R5 обозначает метил,А обозначает этилен,и соли, N-оксиды и соли N-оксидов этих соединений. Вариант осуществления настоящего изобретения (вариант осуществления а), который следует отметить, включает соединения формулы IaR1 обозначает водород или С 1-С 4-алкил,R2 обозначает водород или С 1-С 4-алкил,R3 обозначает водород или галоген,R4 обозначает водород,R5 обозначает С 1-С 4-алкил,А обозначает С 1-С 4-алкилен,и соли, N-оксиды и соли N-оксидов этих соединений. Соединениями, предлагаемыми в варианте осуществления а, которые следует отметить, являются такие соединения формулы Ia, в которой R1 обозначает водород или С 1-С 4-алкил, R2 обозначает водород или С 1-С 4-алкил, R3 обозначает водород или галоген, R4 обозначает водород, R5 обозначает метил, А обозначает этилен, и соли, N-оксиды и соли N-оксидов этих соединений. Соединениями, предлагаемыми в варианте осуществления а, которые в большей степени следует отметить, являются такие соединения формулы Ia, в которойR1 обозначает водород, метил или этил,R2 обозначает водород, метил или этил,R3 обозначает водород, хлор или фтор,R4 обозначает водород,R5 обозначает метил,А обозначает этилен,и соли, N-оксиды и соли N-оксидов этих соединений. Соединениями, предлагаемыми в варианте осуществления а, которые особенно следует отметить,являются такие соединения формулы Ia, в которойR1 обозначает водород, метил или этил,R2 обозначает водород, метил или этил, R3 обозначает водород или фтор,R4 обозначает водород,R5 обозначает метил,А обозначает этилен,и соли, N-оксиды и соли N-оксидов этих соединений. Соединениями, предлагаемыми в варианте осуществления а, которые в еще большей степени следует отметить, являются такие соединения формулы Ia, в которой илиR3 обозначает водород,R4 обозначает водород,R5 обозначает метил,А обозначает этилен,и соли, N-оксиды и соли N-оксидов этих соединений. Предпочтительный вариант осуществления (вариант осуществления b) настоящего изобретения включает соединения формулы IbR1 обозначает водород или С 1-С 4-алкил,R2 обозначает водород или С 1-С 4-алкил,R3 обозначает водород или галоген,R4 обозначает водород,R5 обозначает метил,А обозначает этилен,и соли, N-оксиды и соли N-оксидов этих соединений. Соединениями, предлагаемыми в варианте осуществления b, которые в большей степени следует отметить, являются такие соединения формулы Ib, в которойR1 обозначает водород, метил или этил,R2 обозначает водород, метил или этил,R3 обозначает водород, хлор или фтор,R4 обозначает водород,R5 обозначает метил,А обозначает этилен,и соли, N-оксиды и соли N-оксидов этих соединений. Соединениями, предлагаемыми в варианте осуществления b, которые особенно следует отметить,являются такие соединения формулы Ib, в которойR1 обозначает водород, метил или этил,R2 обозначает водород, метил или этил,R3 обозначает водород или фтор,R4 обозначает водород,R5 обозначает метил,А обозначает этилен,и соли, N-оксиды и соли N-оксидов этих соединений. Соединениями, предлагаемыми в варианте осуществления b, которые в еще большей степени следует отметить, являются такие соединения формулы Ib, в которой илиR3 обозначает водород,R4 обозначает водород,R5 обозначает метил,А обозначает этилен,и соли, N-оксиды и соли N-оксидов этих соединений. Более предпочтительный вариант осуществления (вариант осуществления с) настоящего изобретения включает соединения формулы IcR1 обозначает водород или С 1-С 4-алкил,R2 обозначает водород или С 1-С 4-алкил,R3 обозначает водород или галоген,R4 обозначает водород,R5 обозначает метил,-4 010261 А обозначает этилен,и соли, N-оксиды и соли N-оксидов этих соединений. Соединениями, предлагаемыми в варианте осуществления с, которые в большей степени следует отметить, являются такие соединения формулы Ic, в которойR1 обозначает водород, метил или этил,R2 обозначает водород, метил или этил,R3 обозначает водород, хлор или фтор,R4 обозначает водород,R5 обозначает метил,А обозначает этилен,и соли, N-оксиды и соли N-оксидов этих соединений. Соединениями, предлагаемыми в варианте осуществления с, которые особенно следует отметить,являются такие соединения формулы Ic, в которой илиR1 обозначает водород, метил или этил,R2 обозначает водород, метил или этил,R3 обозначает водород или фтор,R4 обозначает водород,R5 обозначает метил, А обозначает этилен,и соли, N-оксиды и соли N-оксидов этих соединений. Соединениями, предлагаемыми в варианте осуществления с, которые еще более следует отметить,являются такие соединения формулы Ic, в которой илиR1 обозначает водород, метил или этил,R2 обозначает водород, метил или этил иR3 обозначает водород,R4 обозначает водород,R5 обозначает метил,А обозначает этилен,и соли, N-оксиды и соли N-оксидов этих соединений. В качестве типичных соединений, предлагаемых в настоящем изобретении, следует отметить указанные ниже соединения формулы Id со значениями заместителей R1, R2 и R3, приведенными в представленной ниже табл. 1. Таблица 1 и соли, N-оксиды и соли N-оксидов этих соединений. Соединения, предлагаемые в настоящем изобретении, можно получить так, как описано ниже и представлено на приведенных ниже схемах реакций, или по методикам, описанным в качестве примеров в приведенных ниже примерах, или аналогично или сходным образом с ними. Так, как показано ниже на схеме реакций 1, соединение формулы II, в которой R4, R5 и А обладают-5 010261 указанными выше значениями и X обозначает подходящую отщепляющуюся группу, предпочтительно бром или, более предпочтительно, йод, вводят в реакцию с бороновыми кислотами или, предпочтительно, эфирами бороновых кислот (например, пинаколиновыми эфирами) формулы IIa, в которой Rl, R2 иR3 обладают указанными выше значениями и Y обозначает остаток бороновой кислоты или, предпочтительно, остаток эфира бороновой кислоты, предпочтительно остаток циклического эфира бороновой кислоты такой как, например, остаток пинаколинового эфира бороновой кислоты, при условиях, подходящих для проведения реакции Судзуки, и получают соединения формулы I, в которой R1, R2, R3, R4, R5 и А обладают указанными выше значениями. Схема реакций 1 Реакцию Судзуки предпочтительно проводить так, как это известно специалисту с общей подготовкой в данной области техники и/или по методикам, представленным ниже и описанным в качестве примеров в приведенных ниже примерах, или аналогично или сходным образом с ними. Точнее, указанную реакцию Судзуки можно провести только в органических растворителях, например в толуоле, бензоле, диметилформамиде или в эфирных (например, метоксиэтане или, предпочтительно диоксане) или в спиртовых растворителях или в их смеси, или, предпочтительно в смеси, включающей органический растворитель (предпочтительно диоксан) и воду, с органическим (например, триэтиламином) или, предпочтительно с неорганическим основанием (например, гидроксидом калия, гидроксидом таллия, бикарбонатом натрия, карбонатом цезия, фторидом цезия или, предпочтительно - карбонатом калия) в присутствии катализатора на основе переходного металла, например, никелевого или,предпочтительно - палладиевого катализатора (например, Pd(OAC)2, PdCl2(PPh3)2 или, предпочтительно Pd(PPh3)4) и, необязательно, хлорида лития. Реакцию проводят при температуре в диапазоне от 20 до 160 С, обычно от 60 до 130 С в течение периода времени, составляющего от 10 мин до 5 дней, обычно от 30 мин до 24 ч. Предпочтительно дегазировать применяющиеся растворители и проводить реакцию в атмосфере защитного газа. Реакция Судзуки описана, например, в публикации Tetrahedron Lett., 1998, т. 39, с. 4467, J. Org.Chem., 1999, т. 64, с. 1372 или Heterocycles, 1992, т. 34, с. 1395. Общий обзор кросс-сочетания по Судзуки бороновых кислот с арилгалогенидами приведен в публикации Miyaura, N; Suzuki, A. Chem. Rev., 1995, т. 95, с. 2457. Бороновые кислоты и эфиры бороновых кислот (например, пинаколиновые эфиры) формулы IIa, в которой R1, R2, R3 и Y обладают указанными выше значениями, известны или их можно получить по известной в данной области техники методике или аналогично или сходным образом с известными соединениями. Эфиры бороновых кислот (например, пинаколиновые эфиры) формулы IIа можно получить,например, как это описано в приведенных ниже примерах, используя в качестве исходных веществ фенилтрифлаты или, предпочтительно фенилгалогениды, предпочтительно бромиды или йодиды с использованием, например, бис-(пинаколято)дибора в присутствии катализатора на основе переходного металла, предпочтительно палладия. Полученные эфиры бороновых кислот необязательно можно выделить или, предпочтительно, их получают in situ и без выделения используют в последующей реакции Судзуки. Соединения формулы II, в которой R4, R5, X и А обладают указанными выше значениями получают так, как в качестве примеров описано в приведенных ниже примерах, или представлено на приведенной ниже схеме реакций 2 или аналогичным или сходным образом. На приведенной ниже схеме реакций 2 в качестве примера описан синтез соединений формулы II, в которой R4, R5 и X обладают указанными выше значениями и А обозначает этилен. Углеродную цепь в положении 2 соединений формулы VII удлиняют, например, с помощью конденсации (с производным малоновой кислоты) и последующей реакции гидрирования. Альтернативно,углеродную цепь можно удлинить по реакции Виттига с последующей реакцией гидрирования. Метил-3-(4-(С 1-С 4)алкоксипиридин-2-ил)пропионат (соединение формулы V) или соответствующую кислоту (соединение формулы IV), которую можно получить по известной в данной области техники методике, подвергают превращению с помощью производного 2,3-диаминопиридина (соединение формулы III) и получают искомые соединения формулы II. Синтез 4-метоксипиридин-2-карбальдегида (соединение формулы VII) описан, например, в публикации Ashimori и др., Chem. Pharm. Bull., т. 38, cc. 2446-2458(1990). Соединения формулы VII также можно получить, используя в качестве исходного вещества имеющийся в продаже 4-нитро-2-пиколин-N-оксид путем обмена нитрогруппы на С 1-С 4-алкоксигруппу. Полученный 4-(С 1-С 4)алкокси-2-пиколин-N-оксид затем с помощью перегруппировки и окисления превращают в 4-(С 1-С 4)алкоксипиридин-2-карбальдегид (соединение формулы VII). Синтез 3-(4-метоксипиридин-2-ил)пропионовой кислоты (соединение формулы IV) описан в разделе, посвященном исходным веществам. Соединения формулы III, в которой R4 и X обладают указанными выше значениями, известны или их можно получить по известным методикам или аналогично или сходным образом с известными в данной области техники соединениями. Соединения, предлагаемые в настоящем изобретении, необязательно можно превратить в их соли или, необязательно, соли соединений, предлагаемых в настоящем изобретении, можно превратить в свободные соединения. Соответствующие методики известны специалисту в данной области техники. Соединения, предлагаемые в настоящем изобретении, необязательно можно превратить в их Nоксиды, например с помощью пероксида водорода в метаноле или с помощью м-хлорпербензойной кислоты в дихлорметане. Специалист в данной области техники на основании своей подготовки знаком с условиями проведения реакций, которые необходимы для выполнения N-окисления. Специалисту в данной области техники известно, что, если в исходном или промежуточном соединении имеется несколько реакционных центров, то может оказаться необходимым временное блокирование одного или большего количества реакционных центров с помощью защитных групп, чтобы обеспечить протекание реакции именно по необходимому реакционному центру. Подробное описание использования большого количества проверенных защитных групп приведено, например, в публикацииKocienski, Protecting Groups, Thieme MediCal Publishers, 2000. Соединения, предлагаемые в настоящем изобретении, выделяют и очищают по методике, которая сама по себе известна, например, путем отгонки растворителя в вакууме и перекристаллизации полученного остатка из подходящего растворителя или его обработки с помощью обычных методик очистки,таких как хроматография на колонке на подходящем носителе. Соли получают путем растворения соединения в подходящем растворителе (например, кетоне, таком как ацетон, метилэтилкетон или метилизобутилкетон, простом эфире, таком как диэтиловый эфир,тетрагидрофуран или диоксан, хлорированном углеводороде, таком как метиленхлорид или хлороформ,или обладающем низкой молекулярной массой алифатическом спирте, таком как этанол, изопропанол),который содержит необходимую кислоту или к которому затем прибавляют необходимую кислоту. Соли получают фильтрованием, переосаждением, осаждением из вещества, не являющегося растворителем для молекулярной соли, или путем выпаривания растворителя. Полученные соли путем подщелачивания-7 010261 можно превратить в свободные соединения, которые, в свою очередь, можно превратить в соли. Таким образом фармакологически непереносимые соли можно превратить в фармакологически переносимые соли. Методики превращений, указанные в настоящем изобретении, предпочтительно можно провести аналогичным или сходным образом с методиками, которые сами по себе известны специалисту в данной области техники, например, по методикам, описанным в качестве примеров в приведенных ниже примерах. Специалист в данной области техники на основании своей профессиональной подготовки и на основании этих путей синтеза, которые описаны и представлены в описании настоящего изобретения, знает, как найти другие возможные пути синтеза соединений, предлагаемых в настоящем изобретении. Все эти другие возможные пути синтеза также являются частью настоящего изобретения. Настоящее изобретение описано подробно и объем настоящего изобретения не ограничивается только описанными характеристиками и вариантами осуществления. Как должно быть понятно специалистам в данной области техники на основании имеющейся в данной области техники информации и/или, в особенности на основании раскрытия (например, явного, неявного и специфического раскрытия) настоящего изобретения без отклонения об сущности и объема настоящего изобретения, определяемых объемом прилагаемой формулы изобретения, в него можно внести модификации, аналогии, изменения,вариации, гомологизации и адаптации. Приведенные ниже примеры более подробно иллюстрируют настоящее изобретение, не налагая ограничений. Кроме того, другие соединения, предлагаемые в настоящем изобретении, получение которых явно не описано, можно получить аналогичным образом или образом, известным специалисту в данной области техники с использованием обычных методик получения и способов. Соединения, указанные в примерах, а также их соли являются предпочтительными соединениями,предлагаемыми в настоящем изобретении. В примерах т.пл. обозначает температуру плавления, ТСХ обозначает тонкослойную хроматографию, Rf обозначает коэффициент удерживания, МС - масс-спектр, М - молекулярный ион, другие аббревиатуры обладают значениями, которые сами по себе известны специалисту в данной области техники. Примеры Конечные продукты 4-2-[2-(4-Метоксипиридин-2-ил)этил]-3 Н-имидазо[4,5-b]пиридин-6-ил-N,N-диметилбензолсульфонамид Смесь 1,984 г N,N-диметил-4-бромбензолсульфонамида, 2,1 г бис-(пинаколято)дибора, 0,125 г 1,1'бис-(дифенилфосфино)ферроцена, 0,165 г [1,1'-бис(дифенилфосфино)ферроцен]палладийдихлорида(комплекс с CH2Cl2), 2,21 г ацетата натрия в 50 мл дегазированного диоксана кипятят с обратным холодильником в атмосфере N2 в течение 16 ч. К полученной смеси в атмосфере N2 прибавляют 40 мл дегазированного диоксана, 2,14 г 2-[2-(4-метоксипиридин-2-ил)этил]-6-йод-3 Н-имидазо[4,5-b]пиридина (исходное вещество А 1), 0,65 г тетракис(трифенилфосфин)палладия(0) и раствор 1,56 г карбоната калия и 0,48 г хлорида лития в 40 мл дегазированной воды. Смесь кипятят с обратным холодильником в атмосфере N2 в течение 7 ч и после охлаждения, прибавления воды и доведения значения рН до 7 его трижды экстрагируют дихлорметаном. Объединенные органические фазы сушат над сульфатом натрия, концентрируют и остаток хроматографируют на колонке с силикагелем (дихлорметан/метанол 30-15:1). Концентрирование хроматографически чистых фракций, кристаллизация из метанола и перекристаллизация из этилацетата дает 2,01 г искомого соединения в виде твердого вещества, обладающего т.пл., равной 217-218 С. В масс-спектре обнаруживается молекулярный пик МН+ при 438,3 Да. 2.(комплекс с CH2Cl2), 0,442 г ацетата натрия в 6 мл дегазированного диоксана нагревают при 90 С в запаянной трубке в атмосфере N2 в течение 7 ч. К полученной смеси в атмосфере N2 прибавляют 10 мл дегазированного диоксана, 0,371 г 2-[2-(4-метоксипиридин-2-ил)этил]-6-йод-3 Н-имидазо[4,5-b]пиридина (исходное вещество А 1), 0,113 г тетракис(трифенилфосфин)палладия(0) и раствор 0,27 г карбоната калия и 0,083 г хлорида лития в 10 мл дегазированной воды. Смесь кипятят с обратным холодильником в атмосфере N2 в течение 16 ч и после охлаждения, прибавления воды и доведения значения рН до 7 его трижды экстрагируют дихлорметаном. Объединенные органические фазы сушат над сульфатом натрия, концентрируют и остаток хроматографируют на колонке с силикагелем (дихлорметан/метанол 30-25:1). Концентрирование хроматографически чистых фракций и кристаллизация из этилацетата дает 0,155 г искомого соединения в виде твердого вещества, обладающего т.пл., равной 127-129 С. В масс-спектре обнаруживается молекулярный пик МН+ при 466,3 Да. 3. 4-(2-[2-(4-Метоксипиридин-2-ил)этил]-3 Н-имидазо[4,5-b]пиридин-6-ил-N-метилбензолсульфонамид Смесь 0,375 г N-метил-4-бромбензолсульфонамида, 0,42 г бис-(пинаколято)дибора, 0,025 г 1,1'-бис-8 010261(дифенилфосфино)ферроцена, 0,033 г [1,1'-бис(дифенилфосфино)ферроцен]палладийдихлорида (комплекс с CH2Cl2), 0,442 г ацетата натрия в 6 мл дегазированного диоксана нагревают при 90 С в запаянной трубке в атмосфере N2 в течение 16 ч. К полученной смеси в атмосфере N2 прибавляют 5 мл дегазированного диоксана, 0,371 г 2-[2-(4-метоксипиридин-2-ил)этил]-6-йод-3 Н-имидазо[4,5-b]пиридина (исходное вещество Аl), 0,113 г тетракис(трифенилфосфин)палладия(0) и раствор 0,27 г карбоната калия и 0,083 г хлорида лития в 5 мл дегазированной воды. Трубку повторно запаивают, смесь нагревают при 90 в атмосфере N2 в течение 8 ч и после охлаждения, прибавления воды и доведения значения рН до 7 его трижды экстрагируют дихлорметаном. Объединенные органические фазы сушат над сульфатом натрия,концентрируют и остаток хроматографируют на колонке с силикагелем (дихлорметан/метанол 20-15:1). Концентрирование хроматографически чистых фракций и кристаллизация из этилацетата дает 0,219 г искомого соединения в виде твердого вещества, обладающего т.пл., равной 225-227 С. В масс-спектре обнаруживается молекулярный пик МН+ при 424,3 Да. 4. 4-2-[2-(4-Метоксипиридин-2-ил)этил]-3 Н-имидазо[4,5-b]пиридин-6-илбензолсульфонамид Смесь 0,354 г 4-бромбензолсульфонамида, 0,42 г бис-(пинаколято)дибора, 0,025 г 1,1'-бис(дифенилфосфино)ферроцена, 0,033 г [1,1'-бис(дифенилфосфино)ферроцен]палладийдихлорид (комплекс с CH2Cl2), 0,442 г ацетата натрия в 6 мл дегазированного диоксана нагревают при 125 С в запаянной трубке в атмосфере N2 в течение 16 ч. К полученной смеси в атмосфере N2 прибавляют 5 мл дегазированного диоксана, 0,371 г 2-[2-(4-метоксипиридин-2-ил)этил]-6-йод-3 Н-имидазо[4,5-b]пиридина (исходное вещество А 1), 0,113 г тетракис(трифенилфосфин)палладия(0) и раствор 0,27 г карбоната калия и 0,083 г хлорида лития в 5 мл дегазированной воды. Трубку повторно запаивают, смесь нагревают при 115C в атмосфере N2 в течение 7 ч и после охлаждения, прибавления воды и доведения значения рН до 7 его трижды экстрагируют дихлорметаном. Объединенные органические фазы сушат над сульфатом натрия, концентрируют и остаток хроматографируют на колонке с силикагелем (дихлорметан/метанол 12:1 + 1%NH4OH). Концентрирование хроматографически чистых фракций дает 0,08 г искомого соединения в виде коричневатого твердого вещества, обладающего т.пл., равной 216-218 С. В масс-спектре обнаруживается молекулярный пик МН+ при 410,2 Да. 5.N-Этил-4-2-[2-(4-метоксипиридин-2-ил)этил]-3 Н-имидазо-[4,5-b]пиридин-6-илбензолсульфонамид Смесь 0,348 г N-этил-4-бромбензолсульфонамида, 0,42 г бис-(пинаколято)дибора, 0,025 г 1,1'-бис(дифенилфосфино)ферроцена, 0,033 г [1,1'-бис(дифенилфосфино)ферроцен]палладийдихлорида (комплекс с CH2Cl2), 0,442 г ацетата натрия в 6 мл дегазированного диоксана нагревают при 90 С в запаянной трубке в атмосфере N2 в течение 17 ч. К полученной смеси в атмосфере N2 прибавляют 5 мл дегазированного диоксана, 0,371 г 2-[2-(4-метоксипиридин-2-ил)этил]-6-йод-3 Н-имидазо[4,5-b]пиридина (исходное вещество А 1), 0,113 г тетракис(трифенилфосфин)-палладия(0) и раствор 0,27 г карбоната калия и 0,083 г хлорида лития в 5 мл дегазированной воды. Трубку повторно запаивают, смесь нагревают при 115 в атмосфере N2 в течение 7 ч и после охлаждения, прибавления воды и доведения значения рН до 7 его трижды экстрагируют дихлорметаном. Объединенные органические фазы сушат над сульфатом натрия, концентрируют и остаток хроматографируют на колонке с силикагелем (дихлорметан/метанол 2515:1). Концентрирование хроматографически чистых фракций и кристаллизация из этилацетата дает 0,248 г искомого соединения в виде твердого вещества, обладающего т.пл., равной 214-216 С. В массспектре обнаруживается молекулярный пик МН+ при 438,4 Да. 6. 2-Фтор-4-2-[2-(4-метоксипиридин-2-ил)этил]-3 Н-имидазо[4,5-b]пиридин-6-ил)-N,N-диметилбензолсульфонамид Смесь 0,423 г N,N-диметил-4-бром-2-фторбензолсульфонамида, 0,42 г бис-(пинаколято)дибора,0,025 г 1,1'-бис-(дифенилфосфино)ферроцена,0,033 г[1,1'-бис(дифенилфосфино)ферроцен]палладийдихлорида (комплекс с CH2Cl2), 0,442 г ацетата натрия в 6 мл дегазированного диоксана нагревают при 90 С в запаянной трубке в атмосфере N2 в течение 17 ч. К полученной смеси в атмосфереN2 прибавляют 5 мл дегазированного диоксана, 0,371 г 2-[2-(4-метоксипиридин-2-ил)этил]-6-йод-3 Нимидазо[4,5-b]пиридина (исходное вещество А 1), 0,113 г тетракис(трифенилфосфин)палладия(0) и раствор 0,27 г карбоната калия и 0,083 г хлорида лития в 5 мл дегазированной воды. Трубку повторно запаивают, смесь нагревают при 115 С в атмосфере N2 в течение 7 ч и после охлаждения, прибавления воды и доведения значения рН до 7 его трижды экстрагируют дихлорметаном. Объединенные органические фазы сушат над сульфатом натрия, концентрируют и остаток хроматографируют на колонке с силикагелем (дихлорметан/метанол 25-22:1). Концентрирование хроматографически чистых фракций и кристаллизация из этилацетата дает 0,27 г искомого соединения в виде твердого вещества, обладающего т.пл., равной 211-212 С. В масс-спектре обнаруживается молекулярный пик МН+ при 456,3 Да. Исходные вещества: А 1. 2-[2-(4-Метоксипиридин-2-ил)этил]-6-йод-3 Н-имидазо[4,5-b]пиридин При перемешивании смесь 8,06 г 3-(4-метоксипиридин-2-ил)пропионовой кислоты (исходное вещество В 1), 9,5 г 2,3-диамино-5-йодпиридина (Cugola и др., Bioorg.Med. Chem.Lett. 22, 2749-2754 (1996 и 150 г полифосфорной кислоты (ПФК) нагревают при 140 С в течение 22 ч. После охлаждения смесь выливают примерно в 1000 мл смеси воды со льдом и затем нейтрализуют (рН 7-8) с помощью 6 н. водного-9 010261 раствора гидроксида натрия. Смесь 4 раза экстрагируют этилацетатом и объединенные органические фазы выпаривают досуха. Остаток кристаллизуют сначала из этилацетата и затем из метанола и получают 9,4 г искомого соединения в виде светло-бежевого порошкообразного вещества, обладающего т.пл.,равной 207-208 С; в масс-спектре обнаруживается молекулярный пик МН+ при 381,2 Да. В 1. 3 -(4-Метоксипиридин-2-ил)пропионовая кислота 41,95 г Метил-3-(4-метоксипиридин-2-ил)пропионата (исходное вещество С 1) растворяют в 700 мл тетрагидрофурана и прибавляют 217 мл 1 н. раствора гидроксида натрия. Смесь перемешивают при комнатной температуре, пока не перестанет обнаруживаться исходное вещество (ТСХ). Смесь нейтрализуют с помощью 217 мл 1 н. раствора хлористо-водородной кислоты, выпаривают досуха и сушат в высоком вакууме. Бесцветный остаток размалывают и 4 раза экстрагируют смесью дихлорметан/метанол (9:1). Объединенные экстракты выпаривают досуха. Это дает 33,2 г искомого соединения в виде бесцветного порошкообразного вещества, обладающего т.пл., равной 131-132 С. В масс-спектре обнаруживается молекулярный пик МН при 182 Да. С 1. Метил-3-(4-метоксипиридин-2-ил)пропионат 43,1 г Метил-3-(4-метоксипиридин-2-ил)акрилата (исходное вещество D1) в 600 мл метанола гидрируют над 3,0 г Pd/C (10%), пока не исчезнет исходное вещество (ТСХ). Катализатор отфильтровывают и затем смесь концентрируют и сушат в высоком вакууме. Это дает 41,95 г искомого соединения в виде светло-желтого масла. В масс-спектре обнаруживается молекулярный пик МН+ при 196 Да.(1990, 75,80 г пиридингидрохлорида, 102,45 г калиевой соли монометилмалоната и 4,1 мл пиперидина в 700 мл пиридина при перемешивании медленно нагревают до 120 С. После начала выделения газа нагревательное устройство временно удаляют для того, чтобы реакция протекала не слишком бурно. После замедления реакции смесь перемешивают при 120 С в течение еще 5 ч и затем пиридин отгоняют при пониженном давлении. Остаток подвергают распределению в системе этилацетат/вода и органическую фазу промывают водой и сушат. Полученный после концентрирования остаток хроматографируют на колонке с силикагелем с использованием смеси этилацетат/петролейный эфир 2:1. Это сначала дает 43,2 г искомого соединения в виде желтого масла, которое при выдерживании кристаллизуется и затем обладает т.пл., равной 80-82 С. В масс-спектре обнаруживается молекулярный пик МН+ при 194 Да. Коммерческое применение Соединения, предлагаемые в настоящем изобретении, обладают ценными фармакологическими характеристиками, которые делают их пригодными для коммерческого применения. Они являются селективными ингибиторами фермента индуцируемой синтазы оксида азота. Синтазы оксида азота (NOсинтазы, NOS) являются ферментами, которые продуцируют NO и цитруллин из аминокислоты аргинина. Для некоторых патофизиологических ситуаций, таких как уменьшение содержания аргинина или уменьшение содержания тетрагидробиоптерина, описано продуцирование O2- из NO-синтаз вместо или совместно с NO. NO давно известна, как сигнальная молекула для большинства живых организмов,включая млекопитающих и человека. Наиболее примечательным воздействием является способность NO воздействовать на релаксацию гладких мышц, что на молекулярном уровне обусловлено активацией растворимой гуанилатциклазы. В последние годы показано, что с помощью NO или продуктов реакций NO регулируется множество других ферментов. Существуют 3 изоформы NO-синтаз, которые подразделяются на 2 класса и различаются по своим физиологическим функциям и молекулярным характеристикам. Первый класс, известный под названием конститутивных NO-синтаз, включает эндотелиальные NO-синтазы и нейронные NO-синтазы. Оба изофермента конститутивно экспрессируются в различных типах клеток, но в наибольшей степени - в эндотелиальных клетках кровеносных сосудов (поэтому они называются эндотелиальными NO-синтазами,eNOS или NOS-III) и в нейронных клетках (поэтому они называются нейронными NO-синтазами, nNOS или NOS-I). Активация этих двух ферментов зависит от отношения Са 2+/кальмодулин, который продуцируется путем временного увеличения внутриклеточной концентрации свободного Са 2+. Активация конститутивных изоформ приводит к временному скачку концентрации оксида азота, что приводит к наномолярным концентрациям NO в клетках или ткани. Эндотериальная изоформа участвует в физиологической регуляции артериального давления. NO, продуцируемый нейронной изоформой, видимо, обладает нейротрансмиттерной функцией и нейронная изоформа наряду с другими процессами регуляции участвует в работе функции памяти (длительное усиление). В отличие от конститутивных изоформ активация индуцируемой NO-синтазы (iNOS, NOS-II), единственного представителя второго класса, осуществляется путем транскрипциональной активации iNOSпромотора. Провоспалительные стимулы приводят к транскрипции гена для индуцируемой NO-синтазы,которая каталитически активна без увеличения внутриклеточной концентрации Са 2+. Вследствие длительного полупериода существования индуцируемой NO-синтазы и нерегулированной активности фермента высокая микромолярная концентрация NO создается на длительные периоды времени. Эти высокие концентрации NO сами по себе или в сочетании с другими реакционноспособными радикалами, такими как O2-, являются цитотоксичными. Поэтому в случаях микробной инфекции iNOS участвует в- 10010261 уничтожении клеток макрофагами и другими иммунными клетками при ранних неспецифических иммунных реакциях. Имеется целый ряд патофизиологических ситуаций, которые наряду с другими факторами характеризуются значительной экспрессией индуцируемой NO-синтазы и сопутствующими высокими концентрациями NO или О 2-. Показано, что эти высокие концентрации NO сами по себе или в сочетании с другими радикальными частицами приводят к поражению тканей и органов и одновременно участвуют в этих патологиях. Поскольку воспаление характеризуется экспрессией провоспалительных ферментов,включая индуцируемую NO-синтазу, острые и хронические воспалительные процессы являются заболеваниями, для которых перспективно терапевтическое применение селективных ингибиторов индуцируемой NO-синтазы. Другие патофизиологические проявления, сопровождающиеся значительным продуцированием NO с помощью индуцируемой NO-синтазы, представляют собой различные формы шока (септический, геморрагический и вызванный цитокинами). Ясно, что неселективные ингибиторы NO-синтазы приведут к сердечно-сосудистым и нейронным побочным эффектам вследствие сопутствующего ингибирования конститутивных изоформ NO-синтазы. На моделях септического шока in vivo у подопытных животных показано, что снижение уровнейNO в циркулирующей плазме с помощью поглотителя NO или ингибирования индуцируемой NOсинтазы восстанавливает системное артериальное давление, уменьшает поражения органов и увеличивает выживаемость (deAngelo Exp. Opin. Pharmacother., 19-29, 1999; Redl и др Shock 8, Suppl. 51, 1997;NO при септическом шоке способствует успокоению сердца и нарушению функции миокарда (Sun и др.,J. Mol. Cell. Cardiol., т. 30, cc. 989-997, 1998). Кроме того, имеются сообщения, свидетельствующие об уменьшении очага инфаркта после окклюзии левой передней коронарной артерии в присутствии ингибиторов NO-синтазы (Wang и др., Am. J. Hyperttens., т. 12, cc. 174-182, 1999). Значительная активность индуцируемой NO-синтазы обнаружена при кардиомиопатии и миокардите у людей, что свидетельствует в пользу гипотезы о том, что NO по меньшей мере частично обеспечивает расширение и нарушение сократительной способности при этих патофизиологических явлениях (de Belder и др., Br. Heart. J., т. 4, cc. 426-430, 1995). При исследовании моделей острого и хронического воспаления на подопытных животных обнаружено, что блокирование индуцируемой NO-синтазы селективными или неселективными по отношению к изоформе ингибиторами или блокирование вследствие генетического нарушения улучшает результат лечения. Сообщают, что экспериментальный артрит (Connor и др. Eur. J. Pharmacol., т. 273, cc. 15-24,1995) и остеоартрит (Pelletier и др., ArthritisRheum., т. 41, cc. 1275-1286, 1998), экспериментальные воспаления желудочно-кишечного тракта (Zingarelli и др., Gut, т. 45, cc. 199-209, 1999), экспериментальный гломерулонефрит (Narita и др., Lab. Invest., т. 72, cc. 17-24, 1995), экспериментальный диабет (Corbett и др., PNAS, т. 90, cc. 8992-8995, 1993), вызванное липополисахаридами экспериментальное поражение легких ослабляются путем ингибирования индуцируемой NO-синтазы или при нарушении функцииiNOS у мышей (Kristof и др., Am. J. Crit. Care. Med., т. 158, cc. 1883-1889, 1998). Патофизиологическия роль NO и О 2-, образовавшихся с помощью индуцируемой NO-синтазы, также обсуждена для хронических воспалительных заболеваниях, таких как астма, бронхит и ХОЗЛ (хроническое обструктивное заболевание легких). Кроме того, для моделей нейродегенеративных заболеваний ЦНС (центральной нервной системы),таких как вызванный 1-метил-4-фенил-1,2,3,6-тетрагидропиридином паркинсонизм, вызванная амилоидным пептидом болезнь Альцгеймера (Ishii и др., FASEB J., т. 14, cc. 1485-1489, 2000), вызванная малонатом болезни Гентингтона (Соnnор и др., Neuropharmacol., т. 35, cc. 459-465, 1996), экспериментальный менингит (KorytkoBoje Neuropharmacol., т. 35, cc. 231-237, 1996) и экспериментальный энцефалит(Parkinson и др J. Mol. Med., т. 75, cc. 174-186, 1997) подтверждено участие NO и индуцируемой NOсинтазы. В головном мозге страдающих СПИД обнаружена усиленная экспрессия iNOS и разумно предположить участие iNOS в связанном со СПИД слабоумии (Bagasra и др., J. Neurovirol., т. 3, cc. 153-167,1997). В других исследованиях показано участие оксида азота, как потенциального медиатора зависящего от микроглии первичного разрушения миелинового слоя, отличительного признака рассеянного склероза(Parkinson и др., J. Mol. Med., т. 75, cc. 174-186, 1997). Воспалительная реакция при сопутствующей экспрессии индуцируемой NO-синтазы также проявляется во время ишемии головного мозга и реперфузии (Iadecola и др., Stroke, т. 27, cc. 1373-1380, 1996). Образовавшийся NO совместно с О 2- из инфильтрующихся нейтрофилов предположительно вызывают поражения клеток и органов. Кроме того, на моделях травматического повреждения головного мозга (Mesenge и др., J. Neurotrauma, т. 13, cc. 209-214, 1996; Wada и др., Neurosurgery, т. 43, cc. 1427-1436, 1998) показано, что ингибиторы NO-синтазы обладают защитными свойствами. Регулятивная роль индуцируемой NO-синтазы описана для различных линий опухолевых клеток (TozerEverett, Clin Oncol., т. 9. cc. 357-264, 1997). Вследствие своей способности ингибировать индуцируемую NO-синтазу соединения предлагаемые- 11010261 в настоящем изобретении, можно применять в медицине и ветеринарии и терапевтике в случаях, когда проявляется избыток NO или О 2- вследствие усиления активности индуцируемой NO-синтазы. Их можно без ограничений применять для лечения и профилактики следующих заболеваний: Острые воспалительные заболевания: септический шок, сепсис, ССВР (синдром системной воспалительной реакции), геморрагический шок, шоковые состояния, вызванные цитокиновой терапией (IL-2,TNF), трансплантация органов и отторжение трансплантата, травма головы, острое поражение легких,ОРДС (острый респираторный дистресс синдром), воспалительные патологические состояния кожи, такие как солнечный ожог, воспалительные патологические состояния глаз, такие как увеит, глаукома и конъюнктивит. Хронические воспалительные заболевания периферических органов и ЦНС: воспалительные заболевания желудочно-кишечного тракта, такие как болезнь Крона, воспалительное заболевание кишечника,язвенный колит, воспалительные заболевания легких, такие как астма и ХОЗЛ, артриты, такие как ревматоидный артрит, остеоартрит и подагрический артрит, заболевания сердца, такие как кардиомиопатия и миокардит, атеросклероз, нейрогенное воспаление, заболевания кожи, такие как псориаз, дерматит и экзема, диабет, гломерулонефрит, типы слабоумия, такие как слабоумие типа Альцгеймера, мультиинфарктное слабоумие, слабоумие вследствие генерализованного патологического состояния, такое как вызванная СПИД болезнь Паркинсона, типы слабоумия, вызванные болезнью Гентингтона, БАС (боковой амиотрофический склероз), рассеянный склероз; некротизирующие васкулиты, такие как нодозный полиартрит, сывороточная болезнь, синдром Кавасаки; головные боли, такие как мигрень, головные боли,вызванные хроническим напряжением, гистаминовая и сосудистая головная боль, посттравматическое стрессовое расстройство; болезненные нарушения, такие как невропатическая боль; ишемия миокарда и головного мозга/реперфузионное поражение. Эти соединения также можно применять при лечении типов рака, которые экспрессируют синтазу оксида азота. Настоящее изобретение также относится к способу лечения млекопитающих, включая людей, которые страдают от одного из указанных выше заболеваний. Способ характеризуется тем, что терапевтически активное и фармакологически эффективное и переносимое количество одного или большего количества соединений, предлагаемых в настоящем изобретении, вводят больному млекопитающему. Настоящее изобретение также относится к соединениям, предлагаемым в настоящем изобретении,предназначенным для применения при лечении и/или профилактике заболеваний, предпочтительно указанных заболеваний. Настоящее изобретение также относится к применению соединений, предлагаемых в настоящем изобретении, для приготовления фармацевтических композиций, которые применяются для лечения и/или профилактики указанных заболеваний. Настоящее изобретение также относится к применению соединений, предлагаемых в настоящем изобретении, для приготовления фармацевтических композиций, обладающих способностью ингибировать iNOS. Настоящее изобретение кроме того относится к фармацевтическим композициям, предназначенным для лечения и/или профилактики указанных заболеваний, которые содержат одно или несколько соединений, предлагаемых в настоящем изобретении. Настоящее изобретение также относится к фармацевтическим композициям, предлагаемым в настоящем изобретении, обладающим способностью ингибировать iNOS. Фармацевтические композиции готовят способами, которые известны сами по себе и известны специалисту в данной области техники. В качестве фармацевтических композиций соединения, предлагаемые в настоящем изобретении, (= активные соединения) применяются сами по себе или, предпочтительно, в комбинации с подходящими фармацевтическими вспомогательными веществами и/или инертными наполнителями, например, в виде таблеток, таблеток с покрытием, капсул, таблеток в форме капсул,суппозиториев, пластырей (например, в виде ЧТС (чрескожная терапевтическая система, эмульсий,суспензий, гелей или растворов, содержание активного соединения предпочтительно составляет от 0,1 до 95% и при соответствующем выборе вспомогательных веществ и/или инертных наполнителей можно получить фармацевтическую вводимую форму (например, форму замедленного выделения или энтеросолюбильную форму), в точности подходящую для активного соединения и/или обеспечивающую необходимое начало воздействия. Специалист в данной области техники знаком с вспомогательными веществами и инертными наполнителями, которые на основании имеющихся у него профессиональных знаний пригодны для необходимых фармацевтических композиций. В дополнение к растворителям, гелеобразующим веществам,основам мазей и другим инертным наполнителям активного соединения, можно использовать, например,антиоксиданты, диспергирующие вещества, эмульгаторы, консерванты, солюбилизаторы, красители,комплексообразующие агенты или вещества, способствующие проникновению. Введение фармацевтических композиций, предлагаемых в настоящем изобретении, можно проводить по любому общепринятому пути, применяющемуся в данной области техники. Иллюстративные примеры подходящих путей введения включают внутривенное, пероральное, назальное, парентеральное,- 12010261 местное, чрескожное и ректальное введение. Предпочтительными являются пероральное и внутривенное введение. Для лечения нарушений дыхательных путей соединения, предлагаемые в настоящем изобретении,также предпочтительно вводить путем ингаляции в форме аэрозоля; твердые, жидкие и обладающие смешанным составом аэрозольные частицы предпочтительно обладают диаметром от 0,5 до 10 мкм, более предпочтительно от 2 до 6 мкм. Генерацию аэрозоля можно провести, например, с помощью струйных устройств с распылением под давлением или ультразвуковых распылительных устройств, но предпочтительно - с помощью дозирующих распылительных устройств с использованием пропеллентов или введения тонкоизмельченных активных веществ из ингаляционных капсул без пропеллентов. В зависимости от типа применяющегося ингалятора вводимые формы в дополнение к активным соединениям дополнительно содержат необходимые инертные наполнители, такие как, например, пропелленты (например, Frigen в случае дозируемых аэрозолей), поверхностно-активные вещества, эмульгаторы, стабилизаторы, консерванты, ароматизаторы, наполнители (например, лактозу в случае порошковых ингаляторов) или, при необходимости, дополнительные активные соединения. Для проведения ингаляции имеется большое количество приборов, в которых можно создать аэрозоли с оптимальным размером частиц и ввести их с использованием процедуры ингаляции, которая наилучшим возможным образом подходит для пациента. В дополнение к использованию переходников (разделителей, расширителей) и грушеобразных контейнеров (например, Nebulator, VolumatiC) и автоматических устройств, выполняющих более объемное распыление (Autohaler ), для дозирования аэрозолей, в особенности в случае порошковых ингаляторов, имеется ряд технических новинок (например,Diskhaler, Rotadisk, Turbohaler и ингалятор, описанный в Заявке на Европейский патент ЕР 0505321), при использовании которых можно обеспечить оптимальное введение активного соединения. Для лечения дерматозов соединения, предлагаемые в настоящем изобретении, предпочтительно вводить в виде таких фармацевтических композиций, которые пригодны для местного применения. Для приготовления фармацевтических композиций соединения, предлагаемые в настоящем изобретении (= активные соединения) предпочтительно смешивать с подходящими фармацевтическими вспомогательными веществами и обработать и получить подходящие фармацевтические композиции. Подходящими фармацевтическими композициями являются, например, порошки, эмульсии, суспензии, аэрозоли, масла,мази, жировые мази, кремы, пасты, гели и растворы. Фармацевтические композиции, предлагаемые в настоящем изобретении, получают способами, которые сами по себе известны. Дозировка активных соединений по порядку величины совпадает с обычно применяющейся для ингибиторов iNOS. Поэтому формы, предназначенные для местного применения(такие как мази) при лечении дерматозов, содержат активные соединения в концентрациях, составляющих, например, 0,1-99%. Доза для введения путем ингаляции обычно составляет от 0,1 до 10 мг в сутки. Обычная доза при системной терапии (пероральная) составляет от 0,3 до 30 мг/кг в сутки, а внутривенная - от 0,3 до 30 мг/кг/ч. Биологические исследования Измерение активности индуцируемой NO-синтазы Этот анализ проводят в 96-луночных F-планшетах для микротитрования (Greiner, Frickenhausen,FRG) при полном объеме, равном 100 мкл, в присутствии 100 нМ калмодулина, 226 мкМ CaCl2, 477 мкМMgCl2, 5 мкМ флавин-аденинового динуклеотида (ФАН), 5 мкМ флавинового мононуклеотида (ФМН),0,1 мМ NADPH, 7 мМ глутатиона, 10 мкМ ВН 4 и 100 мМ HEPES рН 7,2. В экспериментах по ингибированию фермента концентрация аргинина равна 0,1 мкМ. К смеси для анализа прибавляют [3 Н]аргинин в дозе 150000 распадов/мин. Ферментную реакцию запускают путем прибавления 4 мкг неочищенной цитозольной фракции, содержащей индуцируемую NO-синтазу человека, и реакционную смесь инкубируют в течение 45-60 мин при 37 С. Ферментную реакцию останавливают путем прибавления 10 мкл 2 МMES-буфера рН 5,0. 50 мкл инкубационной смеси переносят в фильтрационный планшет для микротитрования MADP N65 (Millipore, Eschborn, FRG), содержащий 50 мкл катионообменной смолы AG-50WX8 (Biorad, Mtinchen, FRG). Смолу в Na-форме предварительно приводят в равновесие с водой и с помощью 8-канальной пипетки при энергичном перемешивании в фильтрационные планшеты прибавляют 70 мкл (что соответствует 50 мкл сухих гранул). После прибавления в фильтрационные планшеты 50 мкл ферментной реакционной смеси планшеты помещают в фильтрационный коллектор (Porvair, Shepperton,UK) и проходящий поток собирают в сцинтилляционные планшеты Pico (Packard, Meriden, CT). Смолу в фильтрационных планшетах промывают с помощью 75 мкл воды (150 мкл и 1 25 мкл), которую также собирают в тех же планшетах, что и образцы. Суммарный поток, равный 125 мкл, смешивают с 175 мкл сцинтилляционной смеси Microscint-40 (Packard) и сцинтилляционные планшеты герметизируют сверху с помощью фольги TopSeal P-foil (Packard). Измерение активности сцинтилляционных планшетов проводят с помощью сцинтилляционного счетчика. Для измерения активности соединений при ингибировании индуцируемой NO-синтазы в инкубационную смесь включали ингибиторы в возрастающих концентрациях. Значения IC50 рассчитывали по вы- 13010261 раженной в процентах степени ингибирования при данной концентрации с помощью аппроксимации нелинейным методом наименьших квадратов. Показатели ингибирования, полученные для соединений, предлагаемых в настоящем изобретении,представлены в приведенной ниже таблице А, в которой номера соединений совпадают с номерами примеров. Таблица А. Ингибирование активности iNOS [измеряется в виде -logIc50 (моль/л)]R1 обозначает водород или С 1-С 4-алкил,R2 обозначает водород или С 1-С 4-алкил,R3 обозначает водород или галоген,R4 обозначает водород, галоген, С 1-С 4-алкил или С 1-С 4-алкоксигруппу,R5 обозначает С 1-С 4-алкил,А обозначает С 1-С 4-алкилен,и соли, N-оксиды и соли N-оксидов этих соединений. 2. Соединения по п.1, где указанные соединения обладают формулами Ia, Ib или Ic:- 14010261 и соли, N-оксиды и соли N-оксидов этих соединений. 3. Соединения по п.1, где указанные соединения обладают формулами I, Ia, Ib или Ic, в которыхR1 обозначает водород или С 1-С 4-алкил,R2 обозначает водород или С 1-С 4-алкил,R3 обозначает водород или галоген,R4 обозначает водород,R5 обозначает метил,А обозначает этилен,и соли, N-оксиды и соли N-оксидов этих соединений. 4. Соединения по п.1, где указанные соединения обладают формулами I, Ia, Ib или Ic, в которыхR1 обозначает водород, метил или этил,R2 обозначает водород, метил или этил,R3 обозначает водород или фтор,R4 обозначает водород,R5 обозначает метил,А обозначает этилен,и соли, N-оксиды и соли N-оксидов этих соединений. 5. Соединения по п.1, где указанные соединения обладают формулами I, Ia, Ib или Ic, в которых илиR1 обозначает водород, метил или этил,R2 обозначает водород, метил или этил иR3 обозначает водород,R4 обозначает водород,R5 обозначает метил,А обозначает этилен,и соли, N-оксиды и соли N-оксидов этих соединений. 6. Соединения по п.1, где указанные соединения обладают формулами Ib или Ic, в которыхR1 обозначает водород, метил или этил,R2 обозначает водород, метил или этил,R3 обозначает водород или фтор,R4 обозначает водород,R5 обозначает метил,А обозначает этилен,и соли, N-оксиды и соли N-оксидов этих соединений. 7. Соединения по п.1, где указанные соединения обладают формулой Ic, в которой илиR1 обозначает водород, метил или этил,R2 обозначает водород, метил или этил иR3 обозначает водород,R4 обозначает водород,R5 обозначает метил,А обозначает этилен,и соли, N-оксиды и соли N-оксидов этих соединений. 8. Соединения по п.1, где указанные соединения обладают формулой [d] в которой Rl, R2 и R3 имеют любое из указанных ниже значений от 1 до 12: и соли, N-оксиды и соли N-оксидов этих соединений. 9. Соединения формулы I по п.1, обладающие активностью ингибитора NO-синтазы. 10. Фармацевтическая композиция, содержащая одно или несколько соединений формулы I по п.1 совместно с обычными фармацевтическими вспомогательными веществами и/или инертными наполнителями. 11. Применение соединений формулы I по п.1 для изготовления фармацевтических композиций,предназначенных для лечения острых воспалительных заболеваний. 12. Применение соединений формулы I по п.1 для изготовления фармацевтических композиций,предназначенных для лечения хронических воспалительных заболеваний периферических органов и ЦНС (центральной нервной системы). 13. Способ лечения острых воспалительных заболеваний у пациента, включающий введение указанному пациенту терапевтически эффективного количества соединения формулы I по п.1. 14. Способ лечения хронических воспалительных заболеваний периферических органов и ЦНС у пациента, включающий введение указанному пациенту терапевтически эффективного количества соединения формулы I по п.1.
МПК / Метки
МПК: A61K 31/444, A61P 29/00, A61P 25/00, C07D 471/04, A61P 31/00, A61K 31/437
Метки: ингибиторы, производные, индуцируемой, имидазопиридина, синтазы
Код ссылки
<a href="https://eas.patents.su/17-10261-proizvodnye-imidazopiridina-kak-ingibitory-induciruemojj-no-sintazy.html" rel="bookmark" title="База патентов Евразийского Союза">Производные имидазопиридина как ингибиторы индуцируемой no – синтазы</a>