N-замещённые производные пирролидина в качестве ингибиторов дипептидилпептидазы
Номер патента: 7968
Опубликовано: 27.02.2007
Авторы: Вессель Ханс Петер, Кюне Хольгер, Бёрингер Маркус, Сарабу Рамакант, Лёффлер Бернд Михаэль, Хунцикер Даниель
Формула / Реферат
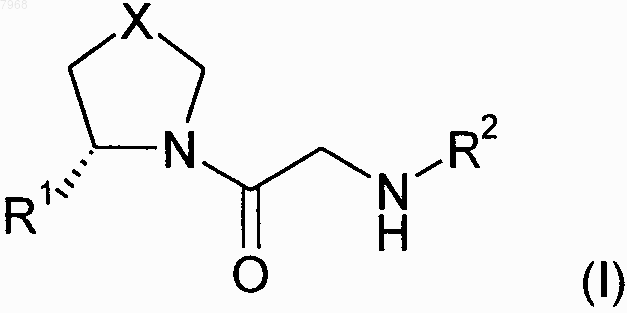
1. Соединения формулы (I)
в которой
R1 обозначает Н или CN,
R2 обозначает -C(R3,R4)-(CH2)n-R5, -C(R3,R4)-CH2-NH-R6, -C(R3,R4)-CH2-O-R7, тетралинил, тетрагидрохинолинил или тетрагидроизохинолинил, причем эта тетралинильная, тетрагидрохинолинильная или тетрагидроизохинолинильная группа может быть необязательно замещенной 1-3 заместителями, независимо выбранными из ряда, включающего (низш.)алкил, (низш.)алкокси, атом галогена, CN и CF3,
R3 обозначает водородный атом, (низш.)алкил, бензил, гидроксибензил или индолилметилен,
R4 обозначает водородный атом или (низш.)алкил или
R3 и R4 связаны между собой с образованием совместно с углеродным атомом, с которым они соединены, кольца, а сочетание -R3-R4- обозначает -(СН2)2-5-,
R5 обозначает 5-членный гетероарил, би- или трициклический гетероциклил или аминофенил, необязательно замещенный 1-3 заместителями, независимо выбранными из ряда, включающего (низш.)алкил, (низш.)алкокси, атом галогена, CN, CF3, трифторацетил, тиофенил, фенил, гетероарил и моноциклический гетероциклил, причем этот фенил, гетероарил или моноциклический гетероциклил может быть необязательно замещенным 1-3 заместителями, независимо выбранными из ряда, включающего (низш.)алкил, (низш.)алкокси, бензилокси, атом галогена, CF3, CF3-O, CN и NН-СО-(низш.)алкил,
R6 обозначает
а) пиридинил или пиримидинил, который замещен 1-3 заместителями, независимо выбранными из ряда, включающего арил и гетероарил, причем эта арильная или гетероарильная группа может быть необязательно замещенной 1-3 заместителями, независимо выбранными из ряда, включающего (низш.)алкил, (низш.)алкокси, атом галогена, CN и CF3, или
б) 5-членный гетероарил или би- или трициклический гетероциклил, причем этот 5-членный гетероарил или би- или трициклический гетероциклил может быть необязательно замещенным 1-3 заместителями, независимо выбранными из ряда, включающего (низш.)алкил, карбонил, арил и гетероарил, причем эта арильная или гетероарильная группа может быть необязательно замещенной 1-3 заместителями, независимо выбранными из ряда, включающего (низш.)алкил, (низш.)алкокси, атом галогена, CN и CF3, а карбонильная группа может быть необязательно замещенной (низш.)алкилом, (низш.)алкокси, атомом галогена, CN, CF3, арилом или гетероарилом, причем эта арильная или гетероарильная группа может быть необязательно замещенной 1-3 заместителями, независимо выбранными из ряда, включающего (низш.)алкил, (низш.)алкокси, атом галогена, CN и CF3,
R7 обозначает аминофенил, нафтил или хинолинил, необязательно замещенный 1-3 заместителями, независимо выбранными из ряда, включающего (низш.)алкил, (низш.)алкокси, атом галогена, CN и CF3,
X обозначает C(R8,R9) или S,
R8 и R9 независимо друг от друга обозначают Н или (низш.)алкил,
n обозначает 0, 1 или 2,
используемое выше понятие "арил" относится к фенильной или нафтильной группе, предпочтительно к фенильной группе, которая может быть необязательно моно- или полизамещенной (низш.)алкилом, (низш.)алкокси, атомом галогена, CN, CF3, гидроксилом, NO2, NH2, N(H, (низш.)алкилом), N((низш.)алкилом)2, карбокси, аминокарбонилом, фенилом, бензилом, фенокси и/или бензилокси;
используемое выше понятие "гетероарил" относится к ароматическому 5- или 6-членному кольцу, которое может включать 1, 2 или 3 атома, выбранных из атомов азота, кислорода и серы, причем гетероарильная группа может иметь такие же заместители, как и представленная выше арильная группа;
используемое выше понятие "5-членный гетероарил" относится к ароматическому 5-членному кольцу, которое может включать от 1 до 4 атомов, выбранных из атомов азота, кислорода и серы, причем 5-членная гетероарильная группа может быть замещена (низш.)алкилом, (низш.)алкокси, атомом галогена, CN, CF3, трифторацетилом, арилом, гетероарилом, карбонилом, причем эта карбонильная группа может быть необязательно замещенной (низш.)алкилом, (низш.)алкокси, атомом галогена, CN, CF3, арилом или гетероарилом;
используемое выше понятие "моноциклический гетероциклил" относится к неароматическим моноциклическим гетероциклам с 5 или 6 кольцевыми членами, которые включают 1, 2 или 3 гетероатома, выбранные из атомов азота, кислорода и серы, и необязательно замещены (низш.)алкилом;
используемое выше понятие "би- или трициклический гетероциклил" относится к бициклическим или трициклическим ароматическим группам, включающим два или три 5- или 6-членных кольца, среди которых одно или несколько колец могут включать 1, 2 или 3 атома, выбранных из атомов азота, кислорода и серы, и которые могут быть частично гидрированными, причем би- или трициклическая гетероциклильная группа может быть необязательно замещена такими же заместителями, как и представленная выше 5-членная гетероарильная группа;
и их фармацевтически приемлемые соли,
при условии, что перечисленные ниже соединения исключены
дигидрохлорид (S)-1-[2-(2-хиноксалиниламино)этиламино]ацетил-2-пирролидинкарбонитрила,
диметансульфонат (S)-1-{2-[2-(4-пиридил)-4-хиназолиниламино)этиламино]ацетил-2-пирролидин-карбонитрила,
дигидрохлорид (S)-1-[2-(2-хинолиламино)этиламино]ацетил-2-пирролидинкарбонитрила,
дигидрохлорид (S)-1-[2-(4-метил-2-хинолиламино)этиламино]ацетил-2-пирролидинкарбонитрила,
дигидрохлорид (S)-1-[2-(4-хинолиламино)этиламино]ацетил-2-пирролидинкарбонитрила,
дигидрохлорид (S)-1-[2-(1-изохинолиламино)этиламино]ацетил-2-пирролидинкарбонитрила,
дигидрохлорид (S)-1-[2-(2-бензотиазолиламино)этиламино]ацетил-2-пирролидинкарбонитрила,
дигидрохлорид (S)-1-[2-метил-1-(2-хиноксалиниламино)-2-пропиламино]ацетил-2-пирролидин-карбонитрила,
фумарат (S)-1-[2-метил-1-(2-хинолиламино)-2-пропиламино]ацетил-2-пирролидинкарбонитрила,
дигидрохлорид (S)-1-[1-(1-изохинолиламино)-2-метил-2-пропиламино]ацетил-2-пирролидинкарбонитрила,
фумарат (S)-1-[2-метил-1-(4-хинолиламино)-2-пропиламино]ацетил-2-пирролидинкарбонитрила,
фумарат (S)-1-[2-метил-1-(2-тиазолиламино)-2-пропиламино]ацетил-2-пирролидинкарбонитрила,
фумарат (S)-1-[2-метил-1-(1,3,4-тиадиазол-2-иламино)-2-пропиламино]ацетил-2-пирролидинкарбонитрила,
фумарат (S)-1-[2-метил-1-(4-фенил-2-тиазолиламино)-2-пропиламино]ацетил-2-пирролидинкарбонитрила,
фумарат (S)-1-[2-метил-1-(5-метил-2-тиазолиламино)-2-пропиламино]ацетил-2-пирролидинкарбонитрила,
фумарат (S)-1-[2-метил-1-(1-фталазиниламино)-2-пропиламино]ацетил-2-пирролидинкарбонитрила.
2. Соединения по п.1, у которых
R1 обозначает Н или CN,
R2 обозначает -C(R3,R4)-(CH2)n-R5, -C(R3,R4)-CH2-NH-R6, -C(R3,R4)-CH2-O-R7 или тетралинил, необязательно замещенный 1-3 заместителями, независимо выбранными из ряда, включающего (низш.)алкил, (низш.)алкокси, атом галогена, CN и CF3,
R3 обозначает водородный атом, (низш.)алкил, бензил, гидроксибензил или индолилметилен,
R4 обозначает водородный атом или (низш.)алкил или
R3 и R4 связаны между собой с образованием совместно с углеродным атомом, с которым они соединены, кольца, а сочетание -R3-R4- обозначает -(СН2)2-5-,
R5 обозначает 5-членный гетероарил, би- или трициклический гетероциклил или аминофенил, необязательно замещенный 1-3 заместителями, независимо выбранными из ряда, включающего (низш.)алкил, (ншчш.)алкокси, атом галогена, CN, CF3, трифторацетил, тиофенил и фенил, который может быть необязательно замещенным 1-3 заместителями, независимо выбранными из ряда, включающего (низш.)алкил, (низш.)алкокси, бензилокси, атом галогена, CF3 и CN,
R6 обозначает
а) пиридинил или пиримидинил, который замещен 1-3 заместителями, независимо выбранными из ряда, включающего арил и гетероарил, причем эта арильная или гетероарильная группа может быть необязательно замещенной 1-3 заместителями, независимо выбранными из ряда, включающего (низш.)алкил, (низш.)алкокси, атом галогена, CN и CF3, или
б) 5-членный гетероарил, который может быть необязательно замещенным 1-3 заместителями, независимо выбранными из ряда, включающего (низш.)алкил, карбонил, арил и гетероарил, причем эта арильная или гетероарильная группа может быть необязательно замещенной 1-3 заместителями, независимо выбранными из ряда, включающего (низш.)алкил, (низш.)алкокси, атом галогена, CN и CF3, а карбонильная группа может быть необязательно замещенной (низш.)алкилом, (низш.)алкокси, атомом галогена, CN, CF3, арилом или гетероарилом, причем эта арильная или гетероарильная группа может быть необязательно замещенной 1-3 заместителями, независимо выбранными из ряда, включающего (низш.)алкил, (низш.)алкокси, атом галогена, CN и CF3,
R7 обозначает аминофенил, нафтил или хинолинил, необязательно замещенный 1-3 заместителями, независимо выбранными из ряда, включающего (низш.)алкил, (низш.)алкокси, атом галогена, CN и CF3,
X обозначает C(R8,R9) или S,
R8 и R9 независимо друг от друга обозначают Н или (низш.)алкил,
и их фармацевтически приемлемые соли.
3. Соединения по одному из пп.1 или 2, у которых R1 обозначает CN.
4. Соединения по одному из пп.1-3, у которых X обозначает -СН2-.
5. Соединения по одному из пп.1-4, у которых R2 обозначает -C(R3,R4)-(CH2)n-R5, R5 обозначает 5-членный гетероарил, би- или трициклический гетероциклил или аминофенил, необязательно замещенный 1-3 заместителями, независимо выбранными из ряда, включающего (низш.)алкил, (низш.)алкокси, атом галогена, CN, CF3, трифторацетил, тиофенил, фенил, гетероарил и моноциклический гетероциклил, причем этот фенил, гетероарил или моноциклический гетероциклил может быть необязательно замещенным 1-3 заместителями, независимо выбранными из ряда, включающего (низш.)алкил, (низш.)алкокси, бензилокси, атом галогена, CF3, CF3-O, CN и NH-CO-(низш.)алкил, a R3, R4 и n имеют значения, указанные в п.1.
6. Соединения по п.5, у которых R5 обозначает оксазолил, тиазолил, пиразолил, триазолил, имидазолил, бензимидазолил, индолил, азаиндолил, индолинил, аминофенил или карбазолил, необязательно замещенный 1-3 заместителями, независимо выбранными из ряда, включающего (низш.)алкил, (низш.)алкокси, атом галогена, CN, CF3, трифторацетил, тиофенил, пиразинил, пиридинил, морфолинил, пиперидинил и фенил, причем этот пиридинил может быть необязательно замещенным 1-3 заместителями, независимо выбранными из ряда, включающего (низш.)алкил, (низш.)алкокси, атом галогена и CF3, а фенил может быть необязательно замещенным 1-3 заместителями, независимо выбранными из ряда, включающего (низш.)алкил, (низш.)алкокси, бензилокси, атом галогена, CF3, CF3-O, CN и NН-СО-(низш.)алкил, a R3 и R4 независимо друг от друга обозначают водородный атом или (низш.)алкил или R3 и R4 связаны между собой с образованием совместно с углеродным атомом, с которым они соединены, кольца и сочетание -R3-R4-обозначает -(CH2)2-5-.
7. Соединения по п.6, у которых R5 имеет значения, выбранные из ряда, включающего 5-метокси-2-метилиндол-1-ил, 5-цианоиндол-1-ил, 2-метилиндол-1-ил, 2,3-диметилиндол-1-ил, 3-метилиндол-1-ил, 5-броминдол-1-ил, 5-бром-2,3-дигидроиндол-1-ил, 7-азаиндол-1-ил, 2-азаиндол-1-ил, 5-фенил-2,3-дигидроиндол-1-ил, 5-циано-2-метилиндол-1-ил, 2-фенилиндол-1-ил, карбазол-9-ил, 6-броминдол-1-ил, 7-метилиндол-1-ил, 7-броминдол-1-ил, 4-хлориндол-1-ил, 5,6-диметоксииндол-1-ил, 5,6-диметокси-3-трифторацетилиндол-1-ил, 6-(4-метоксифенил)-2,3-дигидроиндол-1-ил, 4-N,N-диметиламинофенил, 3-N,N-диметиламинофенил, 5-метил-2-фенилоксазол-4-ил, 2-(4-фторфенил)-5-метилоксазол-4-ил, 2-(4-бензилоксифенил)-5-метилоксазол-4-ил, 2-(2-этокси-4-фторфенил)-5-метилоксазол-4-ил, 2-(4-хлор-фенил)-5-метилоксазол-4-ил, 5-метил-2-фенилтиазол-4-ил, 2-(3-метилфенил)-5-метилоксазол-4-ил, 2-(3,5-диметоксифенил)-5-метилоксазол-4-ил, 2-(4-фтор-3-метилфенил)-5-метилоксазол-4-ил, 2-(3-метил-фенил)-5-метилтиазол-4-ил, 2-(2-этилпиридин-4-ил)-5-метилтиазол-4-ил, 5-метил-2-(5-трифторметил-пиридин-2-ил)тиазол-4-ил, 5-метил-2-(6-метилпиридин-3-ил)тиазол-4-ил, 2-(3-хлорфенил)-5-метилоксазол-4-ил, 2-(2-хлорфенил)-5-метилоксазол-4-ил, 2-фенилоксазол-4-ил, 2-фенилтиазол-4-ил, 2-морфолин-4-илтиазол-4-ил, 2-пиперидин-1-илтиазол-4-ил, 5-метил-3-фенилпиразол-1-ил, 5-метил-3-(3-трифторметилфенил)пиразол-1-ил, 5-метил-3-(3-трифторметоксифенил)пиразол-1-ил, 5-этил-3-фенилпиразол-1-ил, 5-метил-3-пиридин-3-илпиразол-1-ил, 3-метил-5-пиридин-3-илпиразол-1-ил, 3-(3-хлорфенил)-5-метилпиразол-1-ил, 3-(3,4-дихлорфенил)-5-метилпиразол-1-ил, 3-фенил-5-трифторметилпиразол-1-ил, 5-изопропил-3-фенилпиразол-1-ил, 5-метил-3-тиофен-2-илпиразол-1-ил, 5-метил-3-пиридин-4-илпиразол-1-ил, 5-метил-3-(6-метилпиридин-3-ил)пиразол-1-ил, 5-циклопропил-3-фенилпиразол-1-ил, 5-метил-3-пиразин-2-илпиразол-1-ил, 3-(5-хлорпиридин-3-ил)-5-метилпиразол-1-ил, 5-метил-3-пиридин-2-илпиразол-1-ил, 3-пиридин-3-ил-5-трифторметилпиразол-1-ил, 3-пиридин-3-илпиразол-1-ил, 5-метил-3-пиридин-3-ил[1,2,4]триазол-1-ил, 3-пиридин-3-ил-5-трифторметил[1,2,4]триазол-1-ил, 5-метил-3-пиразин-2-ил[1,2,4]триазол-1-ил, 2-метилбензимидазол-1-ил, 2-метил-4-пиридин-3-илимидазол-1-ил, 4-фенилимидазол-1-ил, 4-пиридин-2-илимидазол-1-ил, 4-пиридин-3-илимидазол-1-ил, 3-фенилпиразол-1-ил, 3-(4-метоксифенил)пиразол-1-ил, 3-(4-метоксифенил)-[1,2,4]триазол-1-ил, 5-метил-3-фенил[1,2,4]триазол-1-ил, 2-фенил-1Н-имидазол-4-ил, 5-метил-2-фенил-1Н-имидазол-4-ил, 5-метил-2-пиридин-4-ил-1Н-имидазол-4-ил, 5-метил-2-пиридин-3-ил-1Н-имидазол-4-ил, 5-метил-2-пиридин-2-ил-1Н-имидазол-4-ил, 2-(3-фтор-4-метилфенил)-5-метил-1H-имидазол-4-ил, 5-метил-2-(4-трифторметилфенил)-1Н-имидазол-4-ил, 5-метил-2-метатолил-1Н-имидазол-4-ил, 5-метил-2-(3-хлорфенил)-1Н-имидазол-4-ил, 2-(3,5-бистрифторметилфенил)-5-метил-1Н-имидазол-4-ил, 2-(3,5-дихлорфенил)-5-метил-1Н-имидазол-4-ил, 1-метил-2-фенил-1Н-имидазол-4-ил, 1,5-диметил-2-фенил-1Н-имидазол-4-ил, 2-(3-фторфенил)-5-метил-1Н-имидазол-4-ил, 2-(3-метоксифенил)-5-метил-1Н-имидазол-4-ил, 2-(3-этоксифенил)-5-метил-1Н-имидазол-4-ил, 2-(3,5-дифторфенил)-5-метил-1Н-имидазол-4-ил, 2-(3,5-диметоксифенил)-5-метил-1Н-имидазол-4-ил, 5-метил-2-(3-трифторметилфенил)-1H-имидазол-4-ил, 5-метил-2-(3-трифторметоксифенил)-1Н-имидазол-4-ил, 2-(4-хлорфенил)-5-метил-1Н-имидазол-4-ил, 5-метил-2-паратолил-1Н-имидазол-4-ил, 2-(3-хлор-4-метилфенил)-5-метил-1Н-имидазол-4-ил и 2-(3-ацетамидофенил)-5-метил-1Н-имидазол-4-ил, a
R3 и R4 независимо друг от друга обозначают водородный атом или метил или R3 и R4 связаны между собой с образованием совместно с углеродным атомом, с которым они соединены, кольца и сочетание -R3-R4- обозначает -(СН2)2-5-.
8. Соединения по п.7, у которых R5 имеет значения, выбранные из ряда, включающего 5-метокси-2-метилиндол-1-ил, 2-метилиндол-1-ил, 2,3-диметилиндол-1-ил, 5-циано-2-метилиндол-1-ил, 2-(4-фторфенил)-5-метилоксазол-4-ил, 2-(4-бензилоксифенил)-5-метилоксазол-4-ил, 5-метил-2-фенилоксазол-4-ил, 5-метил-3-пиридин-3-илпиразол-1-ил, 5-метил-3-пиразин-2-илпиразол-1-ил, 3-пиридин-3-илпиразол-1-ил, 5-метил-3-пиридин-3-ил[1,2,4]триазол-1-шы, 2-метил-4-пиридин-3-илимидазол-1-ил, 4-пиридин-3-илимидазол-1-ил и 5-цианоиндол-1-ил,
а каждый из R3 и R4 независимо друг от друга обозначает водородный атом или метил.
9. Соединения по одному из пп.1-4, у которых R2 обозначает -C(R3,R4)-CH2-NH-R6, a R6 обозначает
а) пиридинил или пиримидинил, который замещен 1-3 заместителями, независимо выбранными из ряда, включающего арил и гетероарил, причем эта арильная или гетероарильная группа может быть необязательно замещенной 1-3 заместителями, независимо выбранными из ряда, включающего (низш.)алкил, (низш.)алкокси, атом галогена, CN и CF3, или
б) 5-членный гетероарил или би- или трициклический гетероциклил, причем этот 5-членный гетероарил или би- или трициклический гетероциклил может быть необязательно замещенным 1-3 заместителями, независимо выбранными из ряда, включающего (низш.)алкил, карбонил, арил и гетероарил, причем эта арильная или гетероарильная группа может быть необязательно замещенной 1-3 заместителями, независимо выбранными из ряда, включающего (низш.)алкил, (низш.)алкокси, атом галогена, CN и CF3, а карбонильная группа может быть необязательно замещенной (низш.)алкилом, (низш.)алкокси, атомом галогена, CN, CF3, арилом или гетероарилом, причем эта арильная или гетероарильная группа может быть необязательно замещенной 1-3 заместителями, независимо выбранными из ряда, включающего (низш.)алкил, (низш.)алкокси, атом галогена, CN и CF3, a
R3 и R4 имеют значения, указанные в п.1.
10. Соединения по п.9, у которых R6 обозначает
а) пиридинил или пиримидинил, который замещен 1-3 заместителями, независимо выбранными из ряда, включающего пиридинил, оксадиазолил и фенил, причем этот оксадиазолил может быть необязательно замещенным (низш.)алкилом, а фенил может быть необязательно замещенным 1-3 заместителями, независимо выбранными из ряда, включающего (низш.)алкил, (низш.)алкокси, CN и CF3, или
б) тиазолил или оксадиазолил, который может быть необязательно замещенным 1-3 заместителями, независимо выбранными из ряда, включающего (низш.)алкил, фенил, бензоил, фенилизоксазолил и пиридил, причем этот пиридил может быть необязательно замещенным (низш.)алкилом или атомом галогена, а фенил может быть необязательно замещенным 1-3 заместителями, независимо выбранными из ряда, включающего (низш.)алкокси, атом галогена, CN и CF3,
в) 8Н-индено[1,2-d]тиазолил, 4,5,6,7-тетрагидробензотиазолил, 4,5,6,7-тетрагидротиазоло[5,4-с]пиридинил, бензотиазолил, бензоксазолил или 1Н-бензимидазолил, причем этот 1Н-бензимидазолил может быть необязательно замещенным (низш.)алкилом, 4,5,6,7-тетрагидротиазоло[5,4-с]пиридинил может быть необязательно замещенным (низш.)алкилкарбонилом или (низш.)алкоксикарбонилом,
а каждый из R3 и R4 независимо друг от друга обозначает водородный атом или (низш.)алкил.
11. Соединения по п.10, у которых R6 имеет значения, выбранные из ряда, включающего 5-(4-метоксифенил)пиридин-2-ил, 5-(3-метоксифенил)пиридин-2-ил, 5-(2-метоксифенил)пиридин-2-ил, 5-(4-цианофенил)пиридин-2-ил, 5-фенилпиридин-2-ил, 6-фенилпиридин-2-ил, 5-(5-метил[1,3,4]оксадиазол-2-ил)пиридин-2-ил, 3-(5-метил[1,3,4]оксадиазол-2-ил)пиридин-2-ил, 4,5-диметилтиазол-2-ил, 4-(4-циано-фенил)тиазол-2-ил, 4-(4-метоксифенил)тиазол-2-ил, 4-(3-фенилизоксазол-5-ил)тиазол-2-ил, 5-фенил-пиридин-2-ил, 5-(3-цианофенил)пиридин-2-ил, 5-(3-трифторметилфенил)пиридин-2-ил, 5-(4-трифтор-метилфенил)пиридин-2-ил, 5-(2-трифторметилфенил)пиридин-2-ил, 5-(3,5-бистрифторметилфенил)пиридин-2-ил, [3,3']бипиридинил-6-ил, 5-(2,4-диметоксифенил)пиридин-2-ил, 6-(4-метоксифенил)пиридин-2-ил, 6-(4-цианофенил)пиридин-2-ил, 6-(3-метоксифенил)пиридин-2-ил, 6-(3-цианофенил)пиридин-2-ил, 6-(2-метоксифенил)пиридин-2-ил, 6-(3,5-бистрифторметилфенил)пиридин-2-ил, 6-(4-трифторметилфенил)пиридин-2-ил, 6-(2-трифторметилфенил)пиридин-2-ил, 6-(3-трифторметилфенил)пиридин-2-ил, [2,3']бипиридинил-6-ил, 6-(2,4-диметоксифенил)пиридин-2-ил, 6-метатолилпиридин-2-ил, 5-фенилпиримидин-2-ил, 5-(3-метоксифенил)пиримидин-2-ил, 5-(3-цианофенил)пиримидин-2-ил, 5-(4-цианофенил)пиримидин-2-ил, 4-(2,4-диметоксифенил)тиазол-2-ил, 4-(2-метоксифенил)тиазол-2-ил, 4-фенилтиазол-2-ил, 4-(3-метоксифенил)тиазол-2-ил, 8Н-индено[1,2-d]тиазол-2-ил, 5-метил-4-фенил-тиазол-2-ил, 4,5-дифенилтиазол-2-ил, 4-бензоилтиазол-2-ил, 4-(4-фторфенил)тиазол-2-ил, 4-(4-трифтор-метилфенил)тиазол-2-ил, 4-пиридин-2-илтиазол-2-ил, 4-пиридин-4-илтиазол-2-ил, 5-метил-4-(4-трифтор-метилфенил)тиазол-2-ил, 4-(4-цианофенил)-5-метилтиазол-2-ил, 4-пиридин-3-илтиазол-2-ил, 4,5,6,7-тетрагидробензотиазол-2-ил, 6-этоксикарбонил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-ил, 6-ацетил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-ил, бензотиазол-2-ил, бензоксазол-2-ил, 1-метил-1Н-бензимидазол-2-ил, 5-фенил[1,3,4]оксадиазол-2-ил, 3-пиридин-3-ил[1,2,4]оксадиазол-5-ил, 3-фенил[1,2,4]оксадиазол-5-ил, 3-пиридин-2-ил[1,2,4]оксадиазол-5-ил, 3-пиридин-4-ил[1,2,4]оксадиазол-5-ил, 3-(6-метилпиридин-3-ил)-[1,2,4]оксадиазол-5-ил, 3-(2-хлорпиридин-4-ил)-[1,2,4]оксадиазол-5-ил и 3-(3,5-дихлорфенил)-[1,2,4]оксадиазол-5-ил, а каждый из R3 и R4 независимо друг от друга обозначает водородный атом или метил.
12. Соединения по п.11, у которых R6 имеет значения, выбранные из ряда, включающего 5-(4-метоксифенил)пиридин-2-ил, 5-(3-метоксифенил)пиридин-2-ил, 5-(2-метоксифенил)пиридин-2-ил, 5-(4-цианофенил)пиридин-2-ил, 5-фенилпиридин-2-ил, 5-(5-метил[1,3,4]оксадиазол-2-ил)пиридин-2-ил, 4-(4-цианофенил)тиазол-2-ил, 4-(3-фенилизоксазол-5-ил)тиазол-2-ил, 6-ацетил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-ил, бензотиазол-2-ил, 5-фенил[1,3,4]оксадиазол-2-ил, 3-пиридин-3-ил[1,2,4]оксадиазол-5-ил, 3-пиридин-2-ил[1,2,4]оксадиазол-5-ил, 3-пиридин-4-ил[1,2,4]оксадиазол-5-ил и 3-(6-метилпиридин-3-ил)-[1,2,4]оксадиазол-5-ил, а каждый из R3 и R4 независимо друг от друга обозначает водородный атом или метил.
13. Соединения по одному из пп.1-4, у которых R2 обозначает -C(R3,R4)-CH2-O-R7, R7 обозначает аминофенил, нафтил или хинолинил, необязательно замещенный 1-3 заместителями, независимо выбранными из ряда, включающего (низш.)алкил, (низш.)алкокси, атом галогена, CN и CF3, a R3 и R4 имеют значения, указанные в п.1.
14. Соединения по п.13, у которых R7 обозначает аминофенил, нафтил или хинолинил, необязательно замещенный 1-3 метильными заместителями, а R3 и R4 независимо друг от друга обозначают водородный атом или метил.
15. Соединения по одному из пп.1-4, у которых R2 обозначает тетралинил или тетрагидрохинолинил, необязательно замещенный 1-3 заместителями, независимо выбранными из ряда, включающего (низш.)алкил, (низш.)алкокси, атом галогена, CN и CF3.
16. Соединения по п.15, у которых R2 обозначает тетралинил или тетрагидрохинолинил, необязательно замещенный метоксигруппой.
17. Соединения по п.16, у которых R2 обозначает 6-метокситетралин-2-ил.
18. Соединение по одному из пп.1-17, выбранное из ряда, включающего
(2S)-1-({2-[5-(5-метил[1,3,4]оксадиазол-2-ил)пиридин-2-иламино]этиламино}ацетил)пирролидин-2-карбонитрил,
(2S)-1-{[(1S)-2-(5-циано-2-метилиндол-1-ил)-1-метилэтиламино]ацетил}пирролидин-2-карбонитрил,
(2S)-1-{[2-(5-метил-2-фенилоксазол-4-ил)этиламино]ацетил}пирролидин-2-карбонитрил,
(2S)-1-[((2R/S)-6-мeтокси-1,2,3,4-тетрагидронафталин-2-иламино)ацетил]пирролидин-2-карбонитрил,
(2S)-1-({2-[2-(4-фторфенил)-5-метилоксазол-4-ил]этиламино}ацетил)пирролидин-2-карбонитрил,
(2S)-1-({2-[5-(4-метоксифенил)пиридин-2-иламино]-1,1-диметилэтиламино}ацетил)пирролидин-2-карбонитрил,
(2S)-1-({2-[4-(4-цианофенил)тиазол-2-иламино]этиламино}ацетил)пирролидин-2-карбонитрил
и их фармацевтически приемлемые соли.
19. Соединение по одному из пп.1-17, выбранное шч ряда, включающего
(2S)-1-({2-[5-(3-метоксифенил)пиридин-2-иламино]этиламино}ацетил)пирролидин-2-карбонитрил,
(2S)-1-{[(1S)-2-(5-метокси-2-метилиндол-1-ил)-1-метилэтиламино]ацетил}пирролидин-2-карбонитрил,
(2S)-1-({2-[5-(4-цианофенил)пиридин-2-иламино]этиламино}ацетил)пирролидин-2-карбонитрил,
(2S)-1-({2-[5-фенилпиридин-2-иламино]этиламино}ацетил)пирролидин-2-карбонитрил,
(2S)-1-({2-[4-(3-фенилизоксазол-5-ил)тиазол-2-иламино]этиламино}ацетил)пирролидин-2-карбонитрил,
(2S)-1-{[(1S)-1-метил-2-(2-метилиндол-1-ил)этиламино]ацетил}пирролидин-2-карбонитрил,
(2S)-1-({2-[5-(4-метоксифенил)пиридин-2-иламино]этиламино}ацетил)пирролидин-2-карбонитрил,
(2S)-1-({2-[2-(4-бензилоксифенил)-5-метилоксазол-4-ил]этиламино}ацетил)пирролидин-2-карбонитрил,
(2S)-1-{[(1S)-2-(2,3-диметилиндол-1-ил)-1-метилэтиламино]ацетил}пирролидин-2-карбонитрил,
(2S)-1-({2-[5-(2-метоксифенил)пиридин-2-иламино]этиламино}ацетил)пирролидин-2-карбонитрил,
(2S)-1-{[(1S)-2-(5-цианиндол-1-ил)-1-метилэтиламино]ацетил}пирролидин-2-карбонитрил
и их фармацевтически приемлемые соли.
20. Соединение по одному из пп.1-17, выбранное из ряда, включающего
(2S)-1-{[1,1-диметил-2-(5-метил-2-фенилоксазол-4-ил)этиламино]ацетил}пирролидин-2-карбонитрил,
(2S)-1-{[1,1-диметил-3-(5-метил-3-пиридин-3-илпиразол-1-ил)пропиламино]ацетил}пирролидин-2-карбонитрил,
(2S)-1-{[1,1-диметил-3-(5-метил-3-пиразин-2-илпиразол-1-ил)пропиламино]ацетил}пирролидин-2-карбонитрил,
(2S)-1-{[1,1-диметил-3-(3-пиридин-3-илпиразол-1-ил)пропиламино]ацетил}пирролидин-2-карбонитрил,
(2S)-1-{[1,1-диметил-3-(5-метил-3-пиридин-3-ил[1,2,4]триазол-1-ил)пропиламино]ацетил}пирролидин-2-карбонитрил,
(2S)-1-{[1,1-диметил-3-(2-метил-4-пиридин-3-илимидазол-1-ил)пропиламино]ацетил}пирролидин-2-карбонитрил,
(2S)-1-{[1,1-диметил-3-(4-пиридин-3-илимидазол-1-ил)пропиламино]ацетил}пирролидин-2-карбонитрил,
(2S)-1-{[1,1-диметил-2-(6-ацетил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-иламино)этиламино]ацетил}пирролидин-2-карбонитрил,
(2S)-1-{[2-(бензотиазол-2-иламино)-1,1-диметилэтиламино]ацетил}пирролидин-2-карбонитрил,
(2S)-1-{[1,1-диметил-2-(5-фенил[1,3,4]оксадиазол-2-иламино)этиламино]ацетил}пирролидин-2-карбонитрил,
(2S)-1-{[1,1-диметил-2-(3-пиридин-3-ил[1,2,4]оксадиазол-5-иламино)этиламино]ацетил}пирролидин-2-карбонитрил,
(2S)-1-{[1,1-диметил-2-(3-пиридин-2-ил[1,2,4]оксадиазол-5-иламино)этиламино]ацетил}пирролидин-2-карбонитрил,
(2S)-1-{[1,1-диметил-2-(3-пиридин-4-ил[1,2,4]оксадиазол-5-иламино)этиламино]ацетил}пирролидин-2-карбонитрил,
(2S)-1-({1,1-диметил-2-[3-(6-метилпиридин-3-ил)-[1,2,4]оксадиазол-5-иламино]этиламино}ацетил)пирролидин-2-карбонитрил
и их фармацевтически приемлемые соли.
21. Соединение по одному из пп.1-20, представляющее собой (2S)-1-{[2-(5-метил-2-фенилоксазол-4-ил)этиламино]ацетил}пирролидин-2-карбонитрил или одну из его фармацевтически приемлемых солей.
22. Соединение по одному из пп.1-20, представляющее собой (2S)-1-{[1,1-диметил-3-(4-пиридин-3-илимидазол-1-ил)пропиламино]ацетил}пирролидин-2-карбонитрил или одну из его фармацевтически приемлемых солей.
23. Способ получения соединений формулы (I) по одному из пп.1-22, включающий взаимодействие соединения формулы (II)
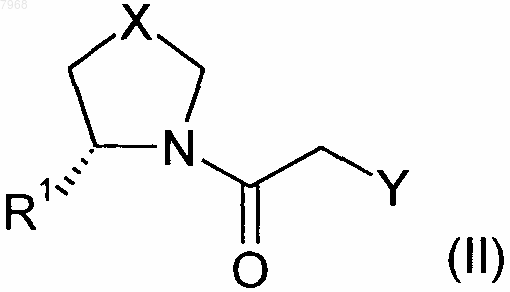
с соединением R2-NH2, где R1, R2 и X имеют значения, указанные в п.1, a Y обозначает уходящую группу, с получением указанного соединения формулы (I) и необязательное превращение соединения формулы (I) в фармацевтически приемлемую соль.
24. Соединения по одному из пп.1-22, полученные согласно способу по п.23.
25. Фармацевтическая композиция, включающая соединение по одному из пп.1-22 и фармацевтически приемлемые носитель и/или адъювант.
26. Применение соединений по одному из пп.1-22 в качестве терапевтически активных веществ.
27. Применение соединений по одному из пп.1-22 в качестве терапевтически активных веществ при лечении и/или профилактике заболеваний, которые связаны с DPP IV.
28. Способ лечения и/или профилактики заболеваний, которые связаны с DPP IV, таких как диабет, инсулиннезависимый сахарный диабет, пониженная толерантность к глюкозе, заболевания пищеварительного тракта, неспецифический язвенный колит, болезнь Крона, ожирение и/или метаболический синдром, включающий введение человеку или животному соединения по одному из пп.1-22.
29. Применение соединений по одному из пп.1-22 для лечения и/или профилактики заболеваний, которые связаны с DPP IV.
30. Применение соединений по одному из пп.1-22 для лечения и/или профилактики диабета, инсулиннезависимого сахарного диабета, пониженной толерантности к глюкозе, заболеваний пищеварительного тракта, неспецифического язвенного колита, болезни Крона, ожирения и/или метаболического синдрома.
31. Применение соединений по одному из пп.1-22 при приготовлении лекарственных средств для лечения и/или профилактики заболеваний, которые связаны с DPP IV.
32. Применение соединений по одному из пп.1-22 при приготовлении лекарственных средств для лечения и/или профилактики диабета, инсулиннезависимого сахарного диабета, пониженной толерантности к глюкозе, заболеваний пищеварительного тракта, неспецифического язвенного колита, болезни Крона, ожирения и/или метаболического синдрома.
Текст
007968 Настоящее изобретение относится к новым пирролидиновым производным, их получению и их применению в качестве лекарственных средств. Так, в частности, объектом изобретения являются соединения формулы (I)R1 обозначает Н или CN,R2 обозначает -C(R3,R4)-(CH2)n-R5, -C(R3,R4)-CH2-NH-R6, -C(R3,R4)-CH2-O-R7, тетралинил, тетрагидрохинолинил или тетрагидроизохинолинил, причем эта тетралинильная, тетрагидрохинолинильная или тетрагидроизохинолинильная группа может быть необязательно замещенной 1-3 заместителями, независимо выбранными из ряда, включающего низший алкил, соответственно (низш.)алкил, (низш.)алкокси,атом галогена, CN и CF3,R3 обозначает водородный атом, (низш.)алкил, бензил, гидроксибензил или индолилметилен,R4 обозначает водородный атом или (низш.)алкил илиR3 и R4 связаны между собой с образованием совместно с углеродным атомом, с которым они соединены, кольца, а сочетание -R3-R4- обозначает -(СН 2)2-5-,R5 обозначает 5-членный гетероарил, би- или трициклический гетероциклил или аминофенил, необязательно замещенный 1-3 заместителями, независимо выбранными из ряда, включающего(низш.)алкил, (низш.)алкокси, атом галогена, CN, CF3, трифторацетил, тиофенил, фенил, гетероарил и моноциклический гетероциклил, причем этот фенил, гетероарил или моноциклический гетероциклил может быть необязательно замещенным 1-3 заместителями, независимо выбранными из ряда, включающего (низш.)алкил, (низш.)алкокси, бензилокси, атом галогена, CF3, CF3-O, CN и NН-СО-(низш.)алкил;R6 обозначает а) пиридинил или пиримидинил, который замещен 1-3 заместителями, независимо выбранными из ряда, включающего арил и гетероарил, причем эта арильная или гетероарильная группа может быть необязательно замещенной 1-3 заместителями, независимо выбранными из ряда, включающего(низш.)алкил, (низш.)алкокси, атом галогена, CN и CF3, или б) 5-членный гетероарил или би- или трициклический гетероциклил, причем этот 5-членный гетероарил или би- или трициклический гетероциклил может быть необязательно замещенным 1-3 заместителями, независимо выбранными из ряда, включающего (низш.)алкил, карбонил, арил и гетероарил, причем эта арильная или гетероарильная группа может быть необязательно замещенной 1-3 заместителями,независимо выбранными из ряда, включающего (низш.)алкил, (низш.)алкокси, атом галогена, CN и CF3, а карбонильная группа может быть необязательно замещенной (низш.)алкилом, (низш.)алкокси, атомом галогена, CN, CF3, арилом или гетероарилом, причем эта арильная или гетероарильная группа может быть необязательно замещенной 1-3 заместителями, независимо выбранными из ряда, включающего(низш.)алкил, (низш.)алкокси, атом галогена, CN и CF3,R7 обозначает аминофенил, нафтил или хинолинил, необязательно замещенный 1-3 заместителями,независимо выбранными из ряда, включающего (низш.)алкил, (низш.)алкокси, атом галогена, CN и CF3,X обозначает C(R8,R9) или S,R8 и R9 независимо друг от друга обозначают Н или (низш.)алкил,n обозначает 0, 1 или 2,и их фармацевтически приемлемые соли. Фермент дипептидилпептидаза IV (ЕС.3.4.14.5, обозначенный в настоящей заявке в сокращенном виде как DPP-IV) участвует в регулировании активности нескольких гормонов. DPP-IV, в частности, эффективно и быстро разрушает глюкагонподобный пептид 1 (GLP-1), являющийся одним из наиболее сильных стимуляторов синтеза и выделения инсулина. Ингибирование DPP-IV должно усиливать действие эндогенного GLP-1 и приводить к более высокой концентрации инсулина в плазме. У пациентов,страдающих пониженной толерантностью к глюкозе и сахарным диабетом типа 2, повышенная концентрация инсулина в плазме должна смягчать опасную гипергликемию и, соответственно, снижать риск повреждения ткани. Поэтому были высказаны предположения (например, Vilhauer, WO 98/19998), что ингибиторы DPP-IV могут служить кандидатами лекарств для лечения пониженной толерантности к глюкозе и сахарного диабета типа 2. Другие соответствующие сведения можно найти в WO 99/38501, DE 19616486, DE 19834591, WO 01/40180, WO 01/55105, US 6110949, WO 00/43241 и US 6011155. При создании настоящего изобретения было установлено, что новые ингибиторы DPP-IV очень эффективно снижают уровень глюкозы в плазме. В связи с этим соединения по настоящему изобретению могут быть использованы для лечения и/или профилактики диабета, в частности инсулиннезависимого сахарного диабета, и/или пониженной толерантности к глюкозе, а также других состояний, при которых усиление действия пептида, в норме инактивированного DPP-IV, оказывает терапевтическое действие. Было установлено, что соединения по настоящему изобретению могут быть также использованы для лечения и/или профилактики заболевания пищеварительного тракта, неспецифического язвенного колита,-1 007968 болезни Крона, ожирения и/или метаболического синдрома. Кроме того, было установлено, что соединения по настоящему изобретению проявляют улучшенные терапевтические и фармакологические свойства по сравнению с другими ингибиторами DPP-IV, известными в данной области техники, такие как, например, фармокинетика и биологическая доступность. Во всех случаях, если не указано иное, для иллюстрации и определения значения и объема различных терминов, используемых в описании настоящего изобретения, приведены следующие понятия. В настоящем описании префикс "низш." использован как обозначающий группу, содержащую от 1 до 7, предпочтительно от 1 до 4, углеродных атомов. Понятие "атом галогена" относится к атомам фтора, хлора, брома и иода, предпочтительно к атомам фтора и хлора. Понятие "алкил", взятое в отдельности или в сочетании с другими группами, относится к разветвленному или прямоцепочечному одновалентному насыщенному алифатическому углеводородному радикалу, содержащему от 1 до 20 углеродных атомов, предпочтительно от 1 до 16 углеродных атомов, более предпочтительно от 1 до 10 углеродных атомов. Алкильные группы могут быть необязательно замещенными, например, атомом галогена, гидроксилом, (низш.)алкокси, (низш.)алкоксикарбонилом, NH2,N(H, (низш.)алкилом) и/или Nнизш.)алкилом)2. Предпочтительны незамещенные алкильные группы. Понятие "(низш.)алкил", взятое в отдельности или в сочетании с другими группами, относится к разветвленному или прямоцепочечному одновалентному алкильному радикалу, содержащему от 1 до 7 углеродных атомов, предпочтительно от 1 до 4 углеродных атомов. Это понятие дополнительно иллюстрируется такими радикалами, как метил, этил, н-пропил, изопропил, н-бутил, втор-бутил, трет-бутил и т.п. (Низш.)алкильная группа может, что необязательно, обладать такой картиной замещения, как представленная выше в связи с понятием "алкил". Предпочтительны незамещенные (низш.)алкильные группы. Понятие "алкокси" относится к группе R'-O-, в которой R' обозначает алкил. Понятие(низш.)алкоксигрупп являются, в частности, метокси, этокси, пропокси, изопропокси, бутокси, изобутокси и гексилокси. Алкокси- и (низш.)алкоксигруппы могут, что необязательно, обладать такой картиной замещения, как представленная выше в связи с понятием "алкил". Предпочтительны незамещенные алкокси- и (низш.)алкоксигруппы. Понятие "арил" относится к фенильной или нафтильной группе, предпочтительно к фенильной группе, которая может быть необязательно моно- или полизамещенной (низш.)алкилом, (низш.)алкокси,атомом галогена, CN, CF3, гидроксилом, NO2, NH2, N(H, (низш.)алкилом), Nнизш.)алкилом)2, карбокси,аминокарбонилом, фенилом, бензилом, фенокси и/или бензилокси. Предпочтительными заместителями являются (низш.)алкил, (низш.)алкокси, атом галогена, CN и/или CF3. Понятие "гетероарил" относится к ароматическому 5- или 6-членному кольцу, которое может включать 1, 2 или 3 атома, выбранных из атомов азота, кислорода и серы, к такому как фурил, пирролил,пиридил, 1,2-, 1,3- и 1,4-диазинилы, тиенил, оксазолил, оксадиазолил, изоксазолил, тиазолил, изотиазолил и имидазолил. Гетероарильная группа может, что необязательно, обладать такой картиной замещения, как представленная выше в связи с понятием "арил". Понятие "5-членный гетероарил" относится к ароматическому 5-членному кольцу, которое может включать от 1 до 4 атомов, выбранных из атомов азота, кислорода и серы, к такому как фурил, тиенил,пирролил, имидазолил, пиразолил, оксазолил, изоксазолил, тиазолил, изотиазолил, оксадиазолил, такой как 1,3,4- и 1,2,4-оксадиазолилы, триазолил и тетразолил. Предпочтительными 5-членными гетероарильными группами являются оксазолил, имидазолил, пиразолил, триазолил, 1,3,4- и 1,2,4-оксадиазолилы и тиазолил. 5-членная гетероарильная группа может быть необязательно замещенной (низш.)алкилом,(низш.)алкокси, атомом галогена, CN, CF3, трифторацетилом, арилом, гетероарилом, карбонилом, причем эта карбонильная группа может быть необязательно замещенной (низш.)алкилом, (низш.)алкокси,атомом галогена, CN, CF3, арилом или гетероарилом. Понятие "моноциклический гетероциклил" относится к неароматическим моноциклическим гетероциклам с 5 или 6 кольцевыми членами, которые включают 1, 2 или 3 гетероатома, выбранные из атомов азота, кислорода и серы. Примерами приемлемых моноциклических гетероциклильных групп являются пиперидинил и морфолинил. Моноциклический гетероциклил может быть замещен(низш.)алкилом. Понятие "би- или трициклический гетероциклил" относится к бициклическим или трициклическим ароматическим группам, включающим два или три 5- или 6-членных кольца, среди которых одно или несколько колец могут включать 1, 2 или 3 атома, выбранных из атомов азота, кислорода и серы, и которые могут быть частично гидрированными. Примерами би- или трициклических гетероциклильных групп являются, в частности, индолил, азаиндолил, такой как 2-, 3-, 4-, 5-, 6- или 7-азаиндолил, индолинилкарбазолил, бензотиофенил, бензотиазолил, бензоксазолил, бензимидазолил, 4,5,6,7-тетрагидротиазоло[5,4-с] пиридинил, 4,5,6,7-тетрагидробензтиазолил, 8 Н-индено[1,2-d]тиазолил и хинолинил. Предпочтительными би- или трициклическими гетероциклильными группами являются бензотиазолил и 4,5,6,7-тетрагидротиазоло[5,4-с]пиридинил. Би- или трициклическая гетероциклильная группа может, что необязательно, обладать такой картиной замещения, как представленная выше в связи с понятием "5-членный-2 007968 гетероарил". Понятие "фармацевтически приемлемые соли" охватывает соли соединений формулы (I) с неорганическими или органическими кислотами, такими как соляная кислота, бромисто-водородная кислота,азотная кислота, серная кислота, фосфорная кислота, лимонная кислота, муравьиная кислота, малеиновая кислота, уксусная кислота, фумаровая кислота, янтарная кислота, винная кислота, метансульфоновая кислота, п-толуолсульфоновая кислота и т.п., которые для живых организмов нетоксичны. Предпочтительными солями с кислотами являются формиаты, малеаты, цитраты, гидрохлориды, гидробромиды и соли метансульфоновой кислоты. Понятие "уходящая группа" относится к группе, которую во время реакции удаляют или замещают. Примерами уходящих групп являются атомы галогена, мезилат и тозилат. Более конкретно объектом настоящего изобретения являются соединения формулы (I)R1 обозначает Н или CN,R2 обозначает -C(R3,R4)-(CH2)n-R5, -C(R3,R4)-CH2-NH-R6, -C(R3,R4)-CH2-O-R7, тетралинил, тетрагидрохинолинил или тетрагидроизохинолинил, причем эта тетралинильная, тетрагидрохинолинильная или тетрагидроизохинолинильная группа может быть необязательно замещенной 1-3 заместителями, независимо выбранными из ряда, включающего (низш.)алкил, (низш.)алкокси, атом галогена, CN и CF3,R3 обозначает водородный атом, (низш.)алкил, бензил, гидроксибензил или индолилметилен,R4 обозначает водородный атом или (низш.)алкил илиR3 и R4 связаны между собой с образованием совместно с углеродным атомом, с которым они соединены, кольца, а сочетание -R3-R4- обозначает -(СН 2)2-5-,R5 обозначает 5-членный гетероарил, би- или трициклический гетероциклил или аминофенил, необязательно замещенный 1-3 заместителями, независимо выбранными из ряда, включающего(низш.)алкил, (низш.)алкокси, атом галогена, CN, CF3, трифторацетил, тиофенил, фенил, гетероарил и моноциклический гетероциклил, причем этот фенил, гетероарил или моноциклический гетероциклил может быть необязательно замещенным 1-3 заместителями, независимо выбранными из ряда, включающего (низш.)алкил, (низш.)алкокси, бензилокси, атом галогена, CF3, CF3-O, CN и NH-СО-(низш.)алкил,R6 обозначает а) пиридинил или пиримидинил, который замещен 1-3 заместителями, независимо выбранными из ряда, включающего арил и гетероарил, причем эта арильная или гетероарильная группа может быть необязательно замещенной 1-3 заместителями, независимо выбранными из ряда, включающего(низш.)алкил, (низш.)алкокси, атом галогена, CN и CF3, или б) 5-членный гетероарил или би- или трициклический гетероциклил, причем этот 5-членный гетероарил или би- или трициклический гетероциклил может быть необязательно замещенным 1-3 заместителями, независимо выбранными из ряда, включающего (низш.)алкил, карбонил, арил и гетероарил, причем эта арильная или гетероарильная группа может быть необязательно замещенной 1-3 заместителями,независимо выбранными из ряда, включающего (низш.)алкил, (низш.)алкокси, атом галогена, CN и CF3, а карбонильная группа может быть необязательно замещенной (низш.)алкилом, (низш.)алкокси, атомом галогена, CN, CF3, арилом или гетероарилом, причем эта арильная или гетероарильная группа может быть необязательно замещенной 1-3 заместителями, независимо выбранными из ряда, включающего(низш.)алкил, (низш.)алкокси, атом галогена, CN и CF3,R7 обозначает аминофенил, нафтил или хинолинил, необязательно замещенный 1-3 заместителями,независимо выбранными из ряда, включающего (низш.)алкил, (низш.)алкокси, атом галогена, CN и CF3,X обозначает C(R8,R9) или S,R8 и R9 независимо друг от друга обозначают Н или (низш.)алкил,n обозначает 0, 1 или 2,и их фармацевтически приемлемые соли. В предпочтительном варианте объектом настоящего изобретения являются соединения формулыR1 обозначает Н или CN,R2 обозначает -C(R3,R4)-CH2-R5, -C(R3,R4)-CH2-NH-R6, -C(R3,R4)-CH2-O-R7 или тетралинил, необязательно замещенный 1-3 заместителями, независимо выбранными из ряда, включающего (низш.)алкил,(низш.)алкокси, атом галогена, CN и CF3,R3 обозначает водородный атом, (низш.)алкил, бензил, гидроксибензил или индолилметилен,R4 обозначает водородный атом или (низш.)алкил илиR3 и R4 связаны между собой с образованием совместно с углеродным атомом, с которым они соединены, кольца, а сочетание -R3-R4- обозначает -(СН 2)2-5-,-3 007968R5 обозначает 5-членный гетероарил, би- или трициклический гетероциклил или аминофенил, необязательно замещенный 1-3 заместителями, независимо выбранными из ряда, включающего(низш.)алкил, (низш.)алкокси, атом галогена, CN, CF3, трифторацетил, тиофенил и фенил, который может быть необязательно замещенным 1-3 заместителями, независимо выбранными из ряда, включающего(низш.)алкил, (низш.)алкокси, бензилокси, атом галогена, CF3 и CN,R6 обозначает а) пиридинил или пиримидинил, который замещен 1-3 заместителями, независимо выбранными из ряда, включающего арил и гетероарил, причем эта арильная или гетероарильная группа может быть необязательно замещенной 1-3 заместителями, независимо выбранными из ряда, включающего(низш.)алкил, (низш.)алкокси, атом галогена, CN и CF3, или б) 5-членный гетероарил, который может быть необязательно замещенным 1-3 заместителями, независимо выбранными из ряда, включающего (низш.)алкил, карбонил, арил и гетероарил, причем эта арильная или гетероарильная группа может быть необязательно замещенной 1-3 заместителями, независимо выбранными из ряда, включающего (низш.)алкил, (низш.)алкокси, атом галогена, CN и CF3, а карбонильная группа может быть необязательно замещенной (низш.)алкилом, (низш.)алкокси, атомом галогена, CN, CF3, арилом или гетероарилом, причем эта арильная или гетероарильная группа может быть необязательно замещенной 1-3 заместителями, независимо выбранными из ряда, включающего(низш.)алкил, (низш.)алкокси, атом галогена, CN и CF3,R7 обозначает аминофенил, нафтил или хинолил, необязательно замещенный 1-3 заместителями,независимо выбранными из ряда, включающего (низш.)алкил, (низш.)алкокси, атом галогена, CN и CF3,X обозначает C(R8,R9) или S,R8 и R9 независимо друг от друга обозначают Н или (низш.)алкил,и их фармацевтически приемлемые соли. В другом предпочтительном варианте объектом настоящего изобретения являются соединения формулы (I), как она представлена выше, в которой R1 обозначает CN. Другими предпочтительными соединениями являются те, у которых X обозначает -СН 2-. Кроме того, к предпочтительному варианту выполнения настоящего изобретения относятся соединения формулы (I), как она представлена выше, в которой R2 обозначает -C(R3,R4)-CH2-R5, R5 обозначает оксазолил, тиазолил, индолил, азаиндолил, индолинил, аминофенил или карбазолил, необязательно замещенный 1-3 заместителями, независимо выбранными из ряда, включающего (низш.)алкил,(низш.)алкокси, атом галогена, CN, CF3, трифторацетил, тиофенил и фенил, который может быть необязательно замещенным 1-3 заместителями, независимо выбранными из ряда, включающего (низш.)алкил,(низш.)алкокси, бензилокси, атом галогена, CF3 и CN, a R3 и R4 имеют указанные выше значения. Из этих соединений более предпочтительны те, у которых R5 обозначает а) индолил, замещенный 1-3 заместителями, независимо выбранными из ряда, включающего метил, метокси, цианогруппу, атомы хлора и брома, трифторацетил и фенил; или б) аминофенил, необязательно замещенный 1-2 метильными группами; или в) индолинил, замещенный метоксифенилом; или г) оксазолил, замещенный 1-3 заместителями, независимо выбранными из ряда, включающего метил и фенил, который необязательно замещен 1-3 заместителями, независимо выбранными из ряда, включающего атомы фтора и хлора, этокси и бензилокси; или д) 2-азаиндолил, 7-азаиндолил или карбазолил; а каждый из R3 и R4 независимо друг от друга обозначает водородный атом или метил. Соединения каждого из вышеупомянутых определений а), б), в), г) и д) индивидуально относятся к предпочтительному варианту. Особенно предпочтительны соединения,как они представлены выше, у которых R5 обозначает 5-циано-2-метилиндолил, 5-метил-2 фенилоксазолил или 2-(4-фторфенил)-5-метилоксазолил и у которых R3 обозначает метил, a R4 обозначает водородный атом. Соединения формулы (I), в которой R2 обозначает -C(R3,R4)-CH2-NH-R6, R6 обозначает а) пиридинил,который замещен 1-3 заместителями, независимо выбранными из ряда, включающего арил и гетероарил,причем эта арильная или гетероарильная группа может быть необязательно замещенной 1-3 заместителями,независимо выбранными из ряда, включающего (низш.)алкил, (низш.)алкокси, атом галогена, CN и CF3,или б) тиазолил, который может быть необязательно замещенным 1-3 заместителями, независимо выбранными из ряда, включающего (низш.)алкил, карбонил, арил и гетероарил, причем эта арильная или гетероарильная группа может быть необязательно замещенной 1-3 заместителями, независимо выбранными из ряда, включающего (низш.)алкил, (низш.)алкокси, атом галогена, CN и CF3, а карбонильная группа может быть необязательно замещенной (низш.)алкилом, (низш.)алкокси, атомом галогена, CN, CF3,арилом или гетероарилом, причем эта арильная или гетероарильная группа может быть необязательно замещенной 1-3 заместителями, независимо выбранными из ряда, включающего (низш.)алкил,(низш.)алкокси, атом галогена, CN и CF3, a R3 и R4 имеют указанные выше значения, представляют другой предпочтительный вариант выполнения настоящего изобретения. Соединения каждого из вышеупомянутых определений а) и б) индивидуально относятся к предпочтительному варианту выполнения изобретения. Эти соединения, у которых R6 обозначает а) пиридинил, замещенный фенилом, метоксифенилом, цианофенилом или метилоксадиазолилом, или б) тиазолил, замещенный 1-2 заместителями, независимо выбранными из ряда, включающего метил, цианофенил, метоксифенил и фенилизоксазолил, а каж-4 007968 дый из R3 и R4 независимо друг от друга обозначает водородный атом или метил, являются более предпочтительными. Соединения каждого из вышеупомянутых определений а) и б) индивидуально относятся к предпочтительному варианту. Особенно предпочтительны соединения формулы (I), как она представлена выше, в которой R6 обозначает 5-(4-метоксифенил)пиридин-2-ил, 5-(5-метилоксадиазол-2-ил) пиридин-2-ил или 4-(4-цианофенил)тиазол-2-ил, a R3 и R4 обозначают водородный атом или R3 и R4 обозначают метил. По другому предпочтительному варианту выполнения настоящего изобретения его объектом являются соединения формулы (I), как она представлена выше, в которой R2 обозначает -C(R3,R4)-CH2-O-R7,R7 обозначает аминофенил, нафтил или хинолинил, необязательно замещенный 1-3 заместителями, независимо выбранными из ряда, включающего (низш.)алкил, (низш.)алкокси, атом галогена, CN и CF3, R3 иR4 имеют указанные выше значения, причем особенно предпочтительны соединения, у которых R7 обозначает аминофенил, нафтил или хинолинил, необязательно замещенный 1-3 метильными заместителями, и каждый из R3 и R4 независимо друг от друга обозначает водородный атом или метил. Другими предпочтительными соединениями формулы (I) являются те, у которых R2 обозначает тетралинил, необязательно замещенный 1-3 заместителями, независимо выбранными из ряда, включающего(низш.)алкил, (низш.)алкокси, атом галогена, CN и CF3, причем более предпочтительны соединения, у которых R2 обозначает тетралинил, необязательно замещенный метоксигруппой, а наиболее предпочтительны соединения, у которых R2 обозначает 6-метокситетралин-2-ил. В предпочтительном варианте выполнения настоящего изобретения R2 обозначает -C(R3,R4)-(CH2)n-R5,5R обозначает 5-членный гетероарил, би- или трициклический гетероциклил или аминофенил, необязательно замещенный 1-3 заместителями, независимо выбранными из ряда, включающего (низш.)алкил,(низш.)алкокси, атом галогена, CN, CF3, трифторацетил, тиофенил, фенил, гетероарил и моноциклический гетероциклил, причем этот фенил, гетероарил или моноциклический гетероциклил может быть необязательно замещенным 1-3 заместителями, независимо выбранными из ряда, включающего(низш.)алкил, (низш.)алкокси, бензилокси, атом галогена, CF3, CF3-O, CN и NH-CO-(низш.)алкил, a R3,R4 и n имеют указанные выше значения. В более предпочтительном варианте R5 обозначает оксазолил, тиазолил, пиразолил, триазолил,имидазолил, бензимидазолил, индолил, азаиндолил, индолинил, аминофенил или карбазолил, необязательно замещенный 1-3 заместителями, независимо выбранными из ряда, включающего (низш.)алкил,(низш.)алкокси, атом галогена, CN, CF3, трифторацетил, тиофенил, пиразинил, пиридинил, морфолинил,пиперидинил и фенил, причем пиридинил может быть необязательно замещенным 1-3 заместителями,независимо выбранными из ряда, включающего (низш.)алкил, (низш.)алкокси, атом галогена и CF3, а фенил может быть необязательно замещенным 1-3 заместителями, независимо выбранными из ряда,включающего (низш.)алкил, (низш.)алкокси, бензилокси, атом галогена, CF3, CF3-O, CN и НН-СО(низш.)алкил, каждый из R3 и R4 независимо друг от друга обозначает водородный атом или(низш.)алкил или R3 и R4 связаны между собой с образованием совместно с углеродным атомом, с которым они соединены, кольца, а сочетание -R3-R4- обозначает -(СН 2)2-5-. В еще более предпочтительном варианте R5 выбирают из ряда, включающего 5-метокси-2 метилиндол-1-ил, 5-цианоиндол-1-ил, 2-метилиндол-1-ил, 2,3-диметилиндол-1-ил, 3-метилиндол-1-ил, 5 броминдол-1-ил, 5-бром-2,3-дигидроиндол-1-ил, 7-азаиндол-1-ил, 2-азаиндол-1-ил, 5-фенил-2,3-дигидроиндол-1-ил, 5-циано-2-метилиндол-1-ил, 2-фенилиндол-1-ил, карбазол-9-ил, 6-броминдол-1-ил, 7-метилиндол-1-ил, 7-броминдол-1-ил, 4-хлориндол-1-ил, 5,6-диметоксииндол-1-ил, 5,6-диметокси-3-трифторацетилиндол-1-ил, 6-(4-метоксифенил)-2,3-дигидроиндол-1-ил, 4-N,N-диметиламинофенил, 3-N,N-диметиламинофенил, 5-метил-2-фенилоксазол-4-ил, 2-(4-фторфенил)-5-метилоксазол-4-ил, 2-(4-бензилоксифенил)-5-метилоксазол-4-ил, 2-(2-этокси-4-фторфенил)-5-метилоксазол-4-ил, 2-(4-хлорфенил)-5-метилоксазол-4-ил, 5-метил-2-фенилтиазол-4-ил, 2-(3-метилфенил)-5-метилоксазол-4-ил, 2-(3,5-диметоксифенил)-5-метилоксазол-4-ил, 2-(4-фтор-3-метилфенил)-5-метилоксазол-4-ил, 2-(3-метилфенил)-5-метилтиазол-4-ил, 2-(2-этилпиридин-4-ил)-5-метилтиазол-4-ил, 5-метил-2-(5-трифторметилпиридин-2-ил)тиазол 4-ил, 5-метил-2-(6-метилпиридин-3-ил)тиазол-4-ил, 2-(3-хлорфенил)-5-метилоксазол-4-ил, 2-(2-хлорфенил)-5-метилоксазол-4-ил, 2-фенилоксазол-4-ил, 2-фенилтиазол-4-ил, 2-морфолин-4-илтиазол-4-ил, 2 пиперидин-1-илтиазол-4-ил, 5-метил-3-фенилпиразол-1-ил, 5-метил-3-(3-трифторметилфенил)пиразол-1 ил, 5-метил-3-(3-трифторметоксифенил)пиразол-1-ил, 5-этил-3-фенилпиразол-1-ил, 5-метил-3-пиридин 3-илпиразол-1-ил, 3-метил-5-пиридин-3-илпиразол-1-ил, 3-(3-хлорфенил)-5-метилпиразол-1-ил, 3-(3,4 дихлорфенил)-5-метилпиразол-1-ил, 3-фенил-5-трифторметилпиразол-1-ил, 5-изопропил-3-фенилпиразол-1-ил, 5-метил-3-тиофен-2-илпиразол-1-ил, 5-метил-3-пиридин-4-илпиразол-1-ил, 5-метил-3-(6-метилпиридин-3-ил)пиразол-1-ил, 5-циклопропил-3-фенилпиразол-1-ил, 5-метил-3-пиразин-2-илпиразол-1-ил,3-(5-хлорпиридин-3-ил)-5-метилпиразол-1-ил, 5-метил-3-пиридин-2-илпиразол-1-ил, 3-пиридин-3-ил-5 трифторметилпиразол-1-ил, 3-пиридин-3-илпиразол-1-ил, 5-метил-3-пиридин-3-ил[1,2,4]триазол-1-ил, 3 пиридин-3-ил-5-трифторметил[1,2,4]триазол-1-ил, 5-метил-3-пиразин-2-ил[1,2,4]триазол-1-ил, 2-метилбензимидазол-1-ил, 2-метил-4-пиридин-3-илимидазол-1-ил, 4-фенилимидазол-1-ил, 4-пиридин-2-илимидазол-1-ил, 4-пиридин-3-илимидазол-1-ил, 3-фенилпиразол-1-ил, 3-(4-метоксифенил)пиразол-1-ил, 3-(4 метоксифенил)-[1,2,4]триазол-1-ил, 5-метил-3-фенил[1,2,4]триазол-1-ил, 2-фенил-1 Н-имидазол-4-ил, 5-5 007968 метил-2-фенил-1 Н-имидазол-4-ил, 5-метил-2-пиридин-4-ил-1 Н-имидазол-4-ил, 5-метил-2-пиридин-3-ил 1 Н-имидазол-4-ил, 5-метил-2-пиридин-2-ил-1 Н-имидазол-4-ил, 2-(3-фтор-4-метилфенил)-5-метил-1 Н-имидазол-4-ил, 5-метил-2-(4-трифторметилфенил)-1 Н-имидазол-4-ил, 5-метил-2-м-толил-1 Н-имидазол-4-ил, 5 метил-2-(3-хлорфенил)-1H-имидазол-4-ил, 2-(3,5-бистрифторметилфенил)-5-метил-1 Н-имидазол-4-ил, 2(3,5-дихлорфенил)-5-метил-1 Н-имидазол-4-ил, 1-метил-2-фенил-1 Н-имидазол-4-ил, 1,5-диметил-2-фенил 1 Н-имидазол-4-ил, 2-(3-фторфенил)-5-метил-1 Н-имидазол-4-ил, 2-(3-метоксифенил)-5-метил-1 Н-имидазол 4-ил, 2-(3-этоксифенил)-5-метил-1 Н-имидазол-4-ил, 2-(3,5-дифторфенил)-5-метил-1 Н-имидазол-4-ил, 2(3,5-диметоксифенил)-5-метил-1 Н-имидазол-4-ил, 5-метил-2-(3-трифторметилфенил)-1 Н-имидазол-4-ил,5-метил-2-(3-трифторметоксифенил)-1 Н-имидазол-4-ил, 2-(4-хлорфенил)-5-метил-1 Н-имидазол-4-ил, 5 метил-2-п-толил-1 Н-имидазол-4-ил, 2-(3-хлор-4-метилфенил)-5-метил-1 Н-имидазол-4-ил и 2-(3-ацетамидофенил)-5-метил-1 Н-имидазол-4-ил, каждый из R3 и R4 независимо друг от друга обозначает водородный атом или метил или R3 и R4 связаны между собой с образованием совместно с углеродным атомом, с которым они соединены, кольца, а сочетание -R3-R4- обозначает -(СН 2)2-5-. В наиболее предпочтительном варианте R5 обозначает 5-метокси-2-метилиндол-1-ил, 2-метилиндол 1-ил, 2,3-диметилиндол-1-ил, 5-циано-2-метилиндол-1-ил, 2-(4-фторфенил)-5-метилоксазол-4-ил, 2-(4 бензилоксифенил)-5-метилоксазол-4-ил, 5-метил-2-фенилоксазол-4-ил, 5-метил-3-пиридин-3-илпиразол 1-ил, 5-метил-3-пиразин-2-илпиразол-1-ил, 3-пиридин-3-илпиразол-1-ил, 5-метил-3-пиридин-3-ил[1,2,4] триазол-1-ил, 2-метил-4-пиридин-3-илимидазол-1-ил, 4-пиридин-3-илимидазол-1-ил или 5-цианоиндол 1-ил, а каждый из R3 и R4 независимо друг от друга обозначает водородный атом или метил. Другими предпочтительными соединениями формулы (I), как она представлена выше, являются те,у которых R2 обозначает -C(R3,R4)-CH2-NH-R6, a R6 обозначает а) пиридинил или пиримидинил, который замещен 1-3 заместителями, независимо выбранными из ряда, включающего арил и гетероарил, причем эта арильная или гетероарильная группа может быть необязательно замещенной 1-3 заместителями, независимо выбранными из ряда, включающего(низш.)алкил, (низш.)алкокси, атом галогена, CN и CF3, или б) 5-членный гетероарил или би- или трициклический гетероциклил, причем этот 5-членный гетероарил или би- или трициклический гетероциклил может быть необязательно замещенным 1-3 заместителями, независимо выбранными из ряда, включающего (низш.)алкил, карбонил, арил и гетероарил, причем эта арильная или гетероарильная группа может быть необязательно замещенной 1-3 заместителями,независимо выбранными из ряда, включающего (низш.)алкил, (низш.)алкокси, атом галогена, CN и CF3, а карбонильная группа может быть необязательно замещенной (низш.)алкилом, (низш.)алкокси, атомом галогена, CN, CF3, арилом или гетероарилом, причем эта арильная или гетероарильная группа может быть необязательно замещенной 1-3 заместителями, независимо выбранными из ряда, включающего(низш.)алкил, (низш.)алкокси, атом галогена, CN и CF3, a R3 и R4 имеют указанные выше значения. Более предпочтительными соединениями являются те, у которых R6 обозначает а) пиридинил или пиримидинил, который замещен 1-3 заместителями, независимо выбранными из ряда, включающего пиридинил, оксадиазолил и фенил, причем этот оксадиазолил может быть необязательно замещенным (низш.)алкилом, а фенил может быть необязательно замещенным 1-3 заместителями,независимо выбранными из ряда, включающего (низш.)алкил, (низш.)алкокси, CN и CF3,б) тиазолил или оксадиазолил, который может быть необязательно замещенным 1-3 заместителями,независимо выбранными из ряда, включающего (низш.)алкил, фенил, бензоил, фенилизоксазолил и пиридил, причем этот пиридил может быть необязательно замещенным (низш.)алкилом или атомом галогена, а фенил может быть необязательно замещенным 1-3 заместителями, независимо выбранными из ряда,включающего (низш.)алкокси, атом галогена, CN и CF3, или в) 8 Н-индено[1,2-d]тиазолил, 4,5,6,7-тетрагидробензотиазолил, 4,5,6,7-тетрагидротиазоло[5,4-с]пиридинил, бензотиазолил, бензоксазолил или 1 Н-бензимидазолил, причем этот 1 Н-бензимидазолил может быть необязательно замещенным (низш.)алкилом, 4,5,6,7-тетрагидротиазоло[5,4-с]пиридинил может быть необязательно замещенным (низш.)алкилкарбонилом или (низш.)алкоксикарбонилом, а каждый изR3 и R4 независимо друг от друга обозначает водородный атом или (низш.)алкил. Еще более предпочтительны те, у которых R6 имеет значения, выбранные из ряда, включающего 5(4-метоксифенил)пиридин-2-ил, 5-(3-метоксифенил)пиридин-2-ил, 5-(2-метоксифенил)пиридин-2-ил, 5(4-цианофенил)пиридин-2-ил, 5-фенилпиридин-2-ил, 6-фенилпиридин-2-ил, 5-(5-метил[1,3,4]оксадиазол 2-ил)пиридин-2-ил, 3-(5-метил[1,3,4]оксадиазол-2-ил)пиридин-2-ил, 4,5-диметилтиазол-2-ил, 4-(4-цианофенил)тиазол-2-ил, 4-(4-метоксифенил)тиазол-2-ил, 4-(3-фенилизоксазол-5-ил)тиазол-2-ил, 5-фенилпиридин-2-ил, 5-(3-цианофенил)пиридин-2-ил, 5-(3-трифторметилфенил)пиридин-2-ил, 5-(4-трифторметилфенил)пиридин-2-ил, 5-(2-трифторметилфенил)пиридин-2-ил, 5-(3,5-бистрифторметилфенил)пиридин-2-ил,[3,3']бипиридинил-6-ил, 5-(2,4-диметоксифенил)пиридин-2-ил, 6-(4-метоксифенил)пиридин-2-ил, 6-(4-цианофенил)пиридин-2-ил, 6-(3-метоксифенил)пиридин-2-ил, 6-(3-цианофенил)пиридин-2-ил, 6-(2-метоксифенил)пиридин-2-ил, 6-(3,5-бистрифторметилфенил)пиридин-2-ил, 6-(4-трифторметилфенил)пиридин-2-ил,6-(2-трифторметилфенил)пиридин-2-ил, 6-(3-трифторметилфенил)пиридин-2-ил, [2,3']бипиридинил-6-ил,6-(2,4-диметоксифенил)пиридин-2-ил, 6-м-толилпиридин-2-ил, 5-фенилпиримидин-2-ил, 5-(3-метоксифенил) пиримидин-2-ил, 5-(3-цианофенил)пиримидин-2-ил, 5-(4-цианофенил)пиримидин-2-ил, 4-(2,4-диметокси-6 007968 фенил)тиазол-2-ил, 4-(2-метоксифенил)тиазол-2-ил, 4-фенилтиазол-2-ил, 4-(3-метоксифенил)тиазол-2-ил,8 Н-индено[1,2-d]тиазол-2-ил, 5-метил-4-фенилтиазол-2-ил, 4,5-дифенилтиазол-2-ил, 4-бензоилтиазол-2 ил, 4-(4-фторфенил)тиазол-2-ил, 4-(4-трифторметилфенил)тиазол-2-ил, 4-пиридин-2-илтиазол-2-ил, 4-пиридин-4-илтиазол-2-ил, 5-метил-4-(4-трифторметилфенил)тиазол-2-ил, 4-(4-цианофенил)-5-метилтиазол 2-ил, 4-пиридин-3-илтиазол-2-ил, 4,5,6,7-тетрагидробензотиазол-2-ил, 6-этоксикарбонил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-ил, 6-ацетил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-ил, бензотиазол 2-ил, бензоксазол-2-ил, 1-метил-1 Н-бензимидазол-2-ил, 5-фенил[1,3,4]оксадиазол-2-ил, 3-пиридин-3-ил[1,2,4]оксадиазол-5-ил, 3-фенил[1,2,4]оксадиазол-5-ил, 3-пиридин-2-ил[1,2,4]оксадиазол-5-ил, 3-пиридин-4 ил[1,2,4]оксадиазол-5-ил, 3-(6-метилпиридин-3-ил)-[1,2,4]оксадиазол-5-ил, 3-(2-хлорпиридин-4-ил)-[1,2,4] оксадиазол-5-ил и 3-(3,5-дихлорфенил)-[1,2,4]оксадиазол-5-ил, а каждый из R3 и R4 независимо друг от друга обозначает водородный атом или метил. Наиболее предпочтительны те, у которых R6 выбирают из ряда, включающего 5-(4-метоксифенил) пиридин-2-ил, 5-(3-метоксифенил)пиридин-2-ил, 5-(2-метоксифенил)пиридин-2-ил, 5-(4-цианофенил)пиридин-2-ил, 5-фенилпиридин-2-ил, 5-(5-метил[1,3,4]оксадиазол-2-ил)пиридин-2-ил, 4-(4-цианофенил)тиазол-2-ил, 4-(3-фенилизоксазол-5-ил)тиазол-2-ил, 6-ацетил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2 ил, бензотиазол-2-ил, 5-фенил[1,3,4]оксадиазол-2-ил, 3-пиридин-3-ил[1,2,4]оксадиазол-5-ил, 3-пиридин 2-ил[1,2,4]оксадиазол-5-ил, 3-пиридин-4-ил[1,2,4]оксадиазол-5-ил и 3-(6-метилпиридин-3-ил)-[1,2,4]оксадиазол-5-ил, а каждый из R3 и R4 независимо друг от друга обозначает водородный атом или метил. Другими предпочтительными соединениями являются те, у которых R2 обозначает тетралинил или тетрагидрохинолинил, необязательно замещенный 1-3 заместителями, независимо выбранными из ряда,включающего (низш.)алкил, (низш.)алкокси, атом галогена, CN и CF3. В более предпочтительном варианте R2 обозначает тетралинил или тетрагидрохинолинил, необязательно замещенный метоксигруппой. Соединения формулы (I) представляют предпочтительный вариант выполнения настоящего изобретения и фармацевтически приемлемые соли соединений формулы (I) индивидуально также представляют предпочтительный вариант выполнения настоящего изобретения. Предпочтительные соединения общей формулы (I) представляют собой те, которые выбраны из ряда, включающего(2S)-1-(2-[2-(2-этокси-4-фторфенил)-5-метилоксазол-4-ил]этиламиноацетил)пирролидин-2-карбонитрил,(2S)-1-(2-[2-(4-хлорфенил)-5-метилоксазол-4-ил]этиламиноацетил)пирролидин-2-карбонитрил,(2S)-1-(2-[5-(4-метоксифенил)пиридин-2-иламино]-1,1-диметилэтиламиноацетил)пирролидин-2 карбонитрил,(2S)-1-(2-[5-(4-метоксифенил)пиридин-2-иламино]этиламиноацетил)пирролидин-2-карбонитрил,1-(2-[5-(4-метоксифенил)пиридин-2-иламино]этиламиноацетил)пирролидин,(2S)-1-(2-[5-(3-метоксифенил)пиридин-2-иламино]этиламиноацетил)пирролидин-2-карбонитрил,(2S)-1-(2-[5-(2-метоксифенил)пиридин-2-иламино]этиламиноацетил)пирролидин-2-карбонитрил,(2S)-1-(2-[5-(4-цианофенил)пиридин-2-иламино] этиламиноацетил)пирролидин-2-карбонитрил,(2S)-1-(2-[5-фенилпиридин-2-иламино]этиламиноацетил)пирролидин-2-карбонитрил,1-(2-[5-фенилпиридин-2-иламино]этиламиноацетил)пирролидин,(2S)-1-(2-[6-фенилпиридин-2-иламино]этиламиноацетил)пирролидин-2-карбонитрил,(2S)-1-(2-[5-(5-метил[1,3,4]оксадиазол-2-ил)пиридин-2-иламино]этиламиноацетил)пирролидин-2 карбонитрил,(2S)-1-(2-[3-(5-метил[1,3,4]оксадиазол-2-ил)пиридин-2-иламино]этиламиноацетил)пирролидин-2 карбонитрил,(2S)-1-[2-(4,5-диметилтиазол-2-иламино)этиламино]ацетилпирролидин-2-карбонитрил,(2S)-1-(2-[4-(4-цианофенил)тиазол-2-иламино]этиламиноацетил)пирролидин-2-карбонитрил,1-(2-[4-(4-цианофенил)тиазол-2-иламино]этиламиноацетил)пирролидин,(2S)-1-(2-[4-(4-метоксифенил)тиазол-2-иламино]этиламиноацетил)пирролидин-2-карбонитрил,(2S)-1-(2-[4-(3-фенилизоксазол-5-ил)тиазол-2-иламино]этиламиноацетил)пирролидин-2-карбонитрил и их фармацевтически приемлемые соли. Другие предпочтительные соединения общей формулы (I) представляют собой те, которые выбраны из ряда, включающего(2S)-1-[2-(5-метил-2-фенилтиазол-4-ил)этиламино]ацетилпирролидин-2-карбонитрил,(2S)-1-(2-[2-(3-метилфенил)-5-метилоксазол-4-ил]этиламиноацетил)пирролидин-2-карбонитрил,(2S)-1-(2-[2-(3,5-диметоксифенил)-5-метилоксазол-4-ил]этиламиноацетил)пирролидин-2-карбонитрил,(2S)-1-(2-[2-(4-фтор-3-метилфенил)-5-метилоксазол-4-ил]этиламиноацетил)пирролидин-2-карбонитрил,(2S)-1-(2-[2-(3-метилфенил)-5-метилтиазол-4-ил]этиламиноацетил)пирролидин-2-карбонитрил,(2S)-1-(2-[2-(2-этилпиридин-4-ил)-5-метилтиазол-4-ил]этиламиноацетил)пирролидин-2-карбонитрил,(2S)-1-(2-[5-метил-2-(5-трифторметилпиридин-2-ил)тиазол-4-ил]этиламиноацетил)пирролидин-2 карбонитрил,(2S)-1-(2-[5-метил-2-(6-метилпиридин-3-ил)тиазол-4-ил]этиламиноацетил)пирролидин-2-карбонитрил,(2S)-1-[1,1-диметил-2-(5-метил-2-фенилоксазол-4-ил)этиламино]ацетилпирролидин-2-карбонитрил,(2S)-1-(1,1-диметил-2-[2-(3-метилфенил)-5-метилоксазол-4-ил]этиламиноацетил)пирролидин-2 карбонитрил,(2S)-1-[1-(5-метил-2-фенилоксазол-4-илметил)циклопентиламино]ацетилпирролидин-2-карбонитрил,(2S)-1-[1-(5-метил-2-фенилоксазол-4-илметил)циклобутиламино]ацетилпирролидин-2-карбонитрил,(2S)-1-[1-(5-метил-2-фенилоксазол-4-илметил)циклопропиламино]ацетилпирролидин-2-карбонитрил,(2S)-1-[1,1-диметил-2-(5-метил-2-фенилтиазол-4-ил)этиламино]ацетилпирролидин-2-карбонитрил,(2S)-1-[1-(5-метил-2-фенилтиазол-4-илметил)циклопентиламино]ацетилпирролидин-2-карбонитрил,(2S)-1-[1-(5-метил-2-фенилтиазол-4-илметил)циклобутиламино]ацетилпирролидин-2-карбонитрил,(2S)-1-(2-[2-(4-фтор-3-метилфенил)-5-метилоксазол-4-ил]-1,1-диметилэтиламиноацетил)пирролидин 2-карбонитрил,(2S)-1-(2-[2-(3-хлорфенил)-5-метилоксазол-4-ил]-1,1-диметилэтиламиноацетил)пирролидин-2 карбонитрил,(2S)-1-(2-[2-(2-хлорфенил)-5-метилоксазол-4-ил]-1,1-диметилэтиламиноацетил)пирролидин-2 карбонитрил,(2S)-1-(1-[2-(4-фтор-3-метилфенил)-5-метилоксазол-4-илметил]циклопропиламиноацетил)пирролидин-2-карбонитрил,(2S)-1-(1-[2-(3-хлорфенил)-5-метилоксазол-4-илметил]циклопропиламиноацетил)пирролидин-2 карбонитрил,(2S)-1-(1-[2-(2-хлорфенил)-5-метилоксазол-4-илметил]циклопропиламиноацетил)пирролидин-2 карбонитрил,(2S)-1-[1,1-диметил-2-(2-фенилоксазол-4-ил)этиламино]ацетилпирролидин-2-карбонитрил,(2S)-1-[1,1-диметил-2-(2-фенилтиазол-4-ил)этиламино]ацетилпирролидин-2-карбонитрил,(2S)-1-[1,1-диметил-2-(2-морфолин-4-илтиазол-4-ил)этиламино]ацетилпирролидин-2-карбонитрил,(2S)-1-[1,1-диметил-2-(2-пиперидин-1-илтиазол-4-ил)этиламино]ацетилпирролидин-2-карбонитрил,соль метансульфоновой кислоты (2S)-1-[1,1-диметил-3-(5-метил-3-фенилпиразол-1-ил)пропиламино]ацетилпирролидин-2-карбонитрила,соль метансульфоновой кислоты (2S)-1-[3-(5-метил-3-фенилпиразол-1-ил)пропиламино]ацетил пирролидин-2-карбонитрила,-8 007968 соль метансульфоновой кислоты (2S)-1-(1,1-диметил-3-[5-метил-3-(3-трифторметилфенил)пиразол-1-ил]пропиламиноацетил)пирролидин-2-карбонитрила,соль метансульфоновой кислоты (2S)-1-(1,1-диметил-3-[5-метил-3-(3-трифторметоксифенил)пиразол-1-ил]пропиламиноацетил)пирролидин-2-карбонитрила,соль метансульфоновой кислоты (2S)-1-[3-(5-этил-3-фенилпиразол-1-ил)-1,1-диметилпропиламино]ацетилпирролидин-2-карбонитрила,соль метансульфоновой кислоты (2S)-1-[1,1-диметил-3-(5-метил-3-пиридин-3-илпиразол-1-ил)пропиламино]ацетилпирролидин-2-карбонитрила,соль метансульфоновой кислоты (2S)-1-[1,1-диметил-3-(3-метил-5-пиридин-3-илпиразол-1-ил)пропиламино]ацетилпирролидин-2-карбонитрила,соль метансульфоновой кислоты (2S)-1-(3-[3-(3-хлорфенил)-5-метилпиразол-1-ил]-1,1-диметилпропиламиноацетил)пирролидин-2-карбонитрила,соль метансульфоновой кислоты (2S)-1-(3-[3-(3,4-дихлорфенил)-5-метилпиразол-1-ил]-1,1-диметилпропиламиноацетил)пирролидин-2-карбонитрила,соль метансульфоновой кислоты (2S)-1-[1,1-диметил-3-(3-фенил-5-трифторметилпиразол-1-ил) пропиламино]ацетилпирролидин-2-карбонитрила,соль метансульфоновой кислоты (2S)-1-[3-(5-изопропил-3-фенилпиразол-1-ил)-1,1-диметилпропиламино]ацетилпирролидин-2-карбонитрила,соль метансульфоновой кислоты (2S)-1-[1,1-диметил-3-(5-метил-3-тиофен-2-илпиразол-1-ил)пропиламино]ацетилпирролидин-2-карбонитрила,соль метансульфоновой кислоты (2S)-1-[1,1-диметил-3-(5-метил-3-пиридин-4-илпиразол-1-ил)пропиламино]ацетилпирролидин-2-карбонитрил а,соль метансульфоновой кислоты (2S)-1-(1,1-диметил-3-[5-метил-3-(6-метилпиридин-3-ил)пиразол 1-ил]пропиламиноацетил)пирролидин-2-карбонитрила,соль метансульфоновой кислоты (2S)-1-[3-(5-циклопропил-3-фенилпиразол-1-ил)-1,1-диметилпропиламино]ацетилпирролидин-2-карбонитрила,соль метансульфоновой кислоты (2S)-1-[1,1-диметил-3-(5-метил-3-пиразин-2-илпиразол-1-ил)пропиламино]ацетилпирролидин-2-карбонитрила,соль метансульфоновой кислоты (2S)-1-(3-[3-(5-хлорпиридин-3-ил)-5-метилпиразол-1-ил]-1,1-диметилпропиламиноацетил)пирролидин-2-карбонитрила,соль метансульфоновой кислоты (2S)-1-[1,1-диметил-3-(5-метил-3-пиридин-2-илпиразол-1-ил)пропиламино]ацетилпирролидин-2-карбонитрила,соль метансульфоновой кислоты (2S)-1-[1,1-диметил-3-(3-пиридин-3-ил-5-трифторметилпиразол 1-ил)пропиламино]ацетилпирролидин-2-карбонитрила,соль метансульфоновой кислоты (2S)-1-[1,1-диметил-3-(3-пиридин-3-илпиразол-1-ил)пропиламино]ацетилпирролидин-2-карбонитрила,соль метансульфоновой кислоты (2S)-1-[1,1-диметил-3-(5-метил-3-пиридин-3-ил[1,2,4]триазол-1 ил)пропиламино]ацетилпирролидин-2-карбонитрила,соль метансульфоновой кислоты (2S)-1-[1,1-диметил-3-(3-пиридин-3-ил-5-трифторметил[1,2,4] триазол-1-ил)пропиламино]ацетилпирролидин-2-карбонитрила,(2S)-1-[1,1-диметил-3-(5-метил-3-пиразин-2-ил[1,2,4]триазол-1-ил)пропиламино]ацетилпирролидин 2-карбонитрил,(2S)-1-[1,1-диметил-3-(2-метилбензимидазол-1-ил)пропиламино]ацетилпирролидин-2-карбонитрил,(2S)-1-[1,1-диметил-3-(2-метил-4-пиридин-3-илимидазол-1-ил)пропиламино]ацетилпирролидин 2-карбонитрил,соль метансульфоновой кислоты (2S)-1-[1,1-диметил-3-(4-фенилимидазол-1-ил)пропиламино]ацетилпирролидин-2-карбонитрила,соль метансульфоновой кислоты (2S)-1-[1,1-диметил-3-(4-пиридин-2-илимидазол-1-ил)пропиламино]ацетилпирролидин-2-карбонитрила,соль метансульфоновой кислоты (2S)-1-[1,1-диметил-3-(4-пиридин-3-илимидазол-1-ил)пропиламино]ацетилпирролидин-2-карбонитрила,соль метансульфоновой кислоты (2S)-l-[(6R/S)-(2-мeтокси-5,6,7,8-тетрагидрохинолин-6-иламино) ацетил]пирролидин-2-карбонитрила,(2S)-1-[1,1-диметил-3-(5-циано-2-метилиндол-1-ил)пропиламино]ацетилпирролидин-2-карбонитрил,(2S)-1-[(1S)-1-метил-2-(3-фенилпиразол-1-ил)этиламино]ацетилпирролидин-2-карбонитрил,(2S)-1-1S)-2-[3-(4-метоксифенил)пиразол-1-ил]-1-метилэтиламиноацетил)пирролидин-2-карбонитрил,(2S)-1-1S)-2-[3-(4-метоксифенил)-[1,2,4]триазол-1-ил]-1-метилэтиламиноацетил)пирролидин-2 карбонитрил,(2S)-1-[(1S)-1-метил-2-(5-метил-3-фенил[1,2,4]триазол-1-ил)этиламино]ацетилпирролидин-2-карбонитрил,(2S)-1-[(1S)-1-метил-2-(5-метил-3-фенилпиразол-1-ил)этиламино]ацетилпирролидин-2-карбонитрил,гидрохлоридная соль (2S)-1-[1,1-диметил-2-(5-фенилпиридин-2-иламино)этиламино]ацетилпир-9 007968 ролидин-2-карбонитрила,гидрохлоридная соль (2S)-1-(2-[5-(3-метоксифенил)пиридин-2-иламино]-1,1-диметилэтиламино ацетил)пирролидин-2-карбонитрила,гидрохлоридная соль (2S)-1-(2-[5-(4-цианофенил)пиридин-2-иламино]-1,1-диметилэтиламиноацетил)пирролидин-2-карбонитрила,гидрохлоридная соль (2S)-1-(2-[5-(2-метоксифенил)пиридин-2-иламино]-1,1-диметилэтиламино ацетил)пирролидин-2-карбонитрила,гидрохлоридная соль (2S)-1-(2-[5-(3-цианофенил)пиридин-2-иламино]-1,1-диметилэтиламиноацетил)пирролидин-2-карбонитрила,гидрохлоридная соль (2S)-1-(2-[5-(3-цианофенил)пиридин-2-иламино]этиламиноацетил)пирролидин-2-карбонитрила,соль метансульфоновой кислоты (2S)-1-(1,1-диметил-2-[5-(3-трифторметилфенил)пиридин-2-иламино]этиламиноацетил)пирролидин-2-карбонитрила,соль метансульфоновой кислоты (2S)-1-(1,1-диметил-2-[5-(4-трифторметилфенил)пиридин-2-иламино]этиламиноацетил)пирролидин-2-карбонитрила,соль метансульфоновой кислоты (2S)-1-(1,1-диметил-2-[5-(2-трифторметилфенил)пиридин-2-иламино]этиламиноацетил)пирролидин-2-карбонитрила,соль метансульфоновой кислоты (2S)-l-(2-[5-(3,5-бистрифторметилфенил)пиридин-2-иламино]-1,1 диметилэтиламиноацетил)пирролидин-2-карбонитрила,соль метансульфоновой кислоты (2S)-1-[2-([3,3']бипиридинил-6-иламино)-1,1-диметилэтиламино] ацетилпирролидин-2-карбонитрила,соль метансульфоновой кислоты (2S)-1-(2-[5-(2,4-диметоксифенил)пиридин-2-иламино]-1,1-диметилэтиламиноацетил)пирролидин-2-карбонитрила,гидрохлоридная соль (2S)-1-(2-[6-(4-метоксифенил)пиридин-2-иламино]этиламиноацетил)пирролидин-2-карбонитрила,гидрохлорид соль (2S)-1-(2-[6-(4-цианофенил)пиридин-2-иламино]этиламиноацетил)пирролидин 2-карбонитрила,гидрохлоридная соль (2S)-1-(2-[6-(3-метоксифенил)пиридин-2-иламино]этиламиноацетил)пирролидин-2-карбонитрила,гидрохлоридная соль (2S)-1-(2-[6-(4-цианофенил)пиридин-2-иламино]-1,1-диметилэтиламиноацетил)пирролидин-2-карбонитрила,гидрохлоридная соль (2S)-1-[1,1-диметил-2-(6-фенилпиридин-2-иламино)этиламино]ацетилпирролидин-2-карбонитрила,гидрохлоридная соль (2S)-1-(2-[6-(3-цианофенил)пиридин-2-иламино]этиламиноацетил)пирролидин-2-карбонитрила,соль метансульфоновой кислоты (2S)-1-(2-[6-(3-метоксифенил)пиридин-2-иламино]-1,1-диметилэтиламиноацетил)пирролидин-2-карбонитрила,соль метансульфоновой кислоты (2S)-1-(2-[6-(4-метоксифенил)пиридин-2-иламино]-1,1-диметилэтиламиноацетил)пирролидин-2-карбонитрила,соль метансульфоновой кислоты (2S)-1-(2-[6-(2-метоксифенил)пиридин-2-иламино]-1,1-диметилэтиламиноацетил)пирролидин-2-карбонитрила,соль метансульфоновой кислоты (2S)-1-(2-[6-(2-метоксифенил)пиридин-2-иламино]этиламино ацетил)пирролидин-2-карбонитрила,соль метансульфоновой кислоты (2S)-1-(2-[6-(3-цианофенил)пиридин-2-иламино]-1,1-диметилэтиламиноацетил)пирролидин-2-карбонитрила,соль метансульфоновой кислоты (2S)-1-(2-[6-(3,5-бистрифторметилфенил)пиридин-2-иламино]1,1-диметилэтиламиноацетил)пирролидин-2-карбонитрила,соль метансульфоновой кислоты (2S)-1-(1,1-диметил-2-[6-(4-трифторметилфенил)пиридин-2-иламино]этиламиноацетил)пирролидин-2-карбонитрила,соль метансульфоновой кислоты (2S)-1-(1,1-диметил-2-[6-(2-трифторметилфенил)пиридин-2-иламино]этиламиноацетил)пирролидин-2-карбонитрила,соль метансульфоновой кислоты (2S)-1-(1,1-диметил-2-[6-(3-трифторметилфенил)пиридин-2-иламино]этиламиноацетил)пирролидин-2-карбонитрила,соль метансульфоновой кислоты (2S)-1-[2-([2,3']бипиридинил-6-иламино)-1,1-диметилэтиламино] ацетилпирролидин-2-карбонитрила,соль метансульфоновой кислоты (2S)-1-(2-[6-(2,4-диметоксифенил)пиридин-2-иламино]-1,1-диметилэтиламиноацетил)пирролидин-2-карбонитрила,соль метансульфоновой кислоты (2S)-1-[1,1-диметил-2-(6-м-толилпиридин-2-иламино)этиламино] ацетилпирролидин-2-карбонитрила,(2S)-1-[1,1-диметил-2-(5-фенилпиримидин-2-иламино)этиламино]ацетилпирролидин-2-карбонитрил,(2S)-1-(2-[5-(3-метоксифенил)пиримидин-2-иламино]-1,1-диметилэтиламиноацетил)пирролидин 2-карбонитрил,- 10007968- 11007968 пирролидин-2-карбонитрил,(2S)-1-[1,1-диметил-2-(5-метил-2-м-толил-1 Н-имидазол-4-ил)этиламино]ацетилпирролидин-2 карбонитрил,(2S)-1-(1,1-диметил-2-[5-метил-2-(3-хлорфенил)-1 Н-имидазол-4-ил]этиламиноацетил)пирролидин 2-карбонитрил,(2S)-1-(2-[2-(3,5-бистрифторметилфенил)-5-метил-1 Н-имидазол-4-ил]-1,1-диметилэтиламиноацетил)пирролидин-2-карбонитрил,(2S)-1-(2-[2-(3,5-дихлорфенил)-5-метил-1 Н-имидазол-4-ил]-1,1-диметилэтиламиноацетил)пирролидин-2-карбонитрил,(2S)-1-[1,1-диметил-2-(2-фенил-1 Н-имидазол-4-ил)этиламино]ацетилпирролидин-2-карбонитрил,(2S)-1-[1,1-диметил-2-(1-метил-2-фенил-1 Н-имидазол-4-ил)этиламино]ацетилпирролидин-2-карбонитрил,(2S)-1-[2-(1,5-диметил-2-фенил-1 Н-имидазол-4-ил)-1,1-диметилэтиламино]ацетилпирролидин-2 карбонитрил,(2S)-1-(2-[2-(3-фторфенил)-5-метил-1 Н-имидазол-4-ил]-1,1-диметилэтиламиноацетил)пирролидин 2-карбонитрил,(2S)-1-(2-[2-(3-метоксифенил)-5-метил-1 Н-имидазол-4-ил]-1,1-диметилэтиламиноацетил)пирролидин-2-карбонитрил,(2S)-1-(2-[2-(3-этоксифенил)-5-метил-1 Н-имидазол-4-ил]-1,1-диметилэтиламиноацетил)пирролидин 2-карбонитрил,(2S)-1-(2-[2-(3,5-дифторфенил)-5-метил-1 Н-имидазол-4-ил]-1,1-диметилэтиламиноацетил)пирролидин-2-карбонитрил,(2S)-1-(2-[2-(3,5-диметоксифенил)-5-метил-1 Н-имидазол-4-ил]-1,1-диметилэтиламиноацетил)пирролидин-2-карбонитрил,(2S)-1-(1,1-диметил-2-[5-метил-2-(3-трифторметилфенил)-1 Н-имидазол-4-ил]этиламиноацетил) пирролидин-2-карбонитрил,(2S)-1-[1,1-диметил-2-(5-метил-2-пиридин-2-ил-1 Н-имидазол-4-ил)этиламино]ацетилпирролидин 2-карбонитрил,(2S)-1-[1,1-диметил-2-(5-метил-2-пиридин-3-ил-1 Н-имидазол-4-ил)этиламино]ацетилпирролидин 2-карбонитрил,(2S)-1-[1,1-диметил-2-(5-метил-2-пиридин-4-ил-1 Н-имидазол-4-ил)этиламино]ацетилпирролидин 2-карбонитрил,(2S)-1-(1,1-диметил-2-[5-метил-2-(3-трифторметоксифенил)-1 Н-имидазол-4-ил]этиламиноацетил) пирролидин-2-карбонитрил,(2S)-1-[1,1-диметил-2-(5-метил-2-фенил-1 Н-имидазол-4-ил)этиламино]ацетилпирролидин-2-карбонитрил,(2S)-1-(2-[2-(4-хлорфенил)-5-метил-1 Н-имидазол-4-ил]-1,1-диметилэтиламиноацетил)пирролидин 2-карбонитрил,(2S)-1-[1,1-диметил-2-(5-метил-2-п-толил-1 Н-имидазол-4-ил)этиламино]ацетилпирролидин-2-карбонитрил,(2S)-1-(2-[2-(3-хлор-4-метилфенил)-5-метил-1 Н-имидазол-4-ил]-1,1-диметилэтиламиноацетил) пирролидин-2-карбонитрил,(2S)-1-(1,1-диметил-2-[2-(3-ацетамидофенил)-5-метил-1 Н-имидазол-4-ил]этиламиноацетил)пирролидин-2-карбонитрил и их фармацевтически приемлемые соли. Особенно предпочтительные соединения общей формулы (I) представляют собой те, которые выбраны из ряда, включающего(2S)-1-(2-[5-(5-метил[1,3,4]оксадиазол-2-ил)пиридин-2-иламино]этиламиноацетил)пирролидин-2 карбонитрил,(2S)-1-[(1S)-2-(5-циано-2-метилиндол-1-ил)-1-метилэтиламино]ацетилпирролидин-2-карбонитрил,(2S)-1-[2-(5-метил-2-фенилоксазол-4-ил)этиламино]ацетилпирролидин-2-карбонитрил,(2S)-1-[2R/S)-6-метокси-1,2,3,4-тетрагидронафталин-2-иламино)ацетил]пирролидин-2-карбонитрил,(2S)-1-(2-[2-(4-фторфенил)-5-метилоксазол-4-ил]этиламиноацетил)пирролидин-2-карбонитрил,(2S)-1-(2-[5-(4-метоксифенил)пиридин-2-иламино]-1,1-диметилэтиламиноацетил)пирролидин-2 карбонитрил,(2S)-1-(2-[4-(4-цианофенил)тиазол-2-иламино]этиламиноацетил)пирролидин-2-карбонитрил и их фармацевтически приемлемые соли. Другие особенно предпочтительные соединения общей формулы (I) представляют собой те, которые выбраны из ряда, включающего(2S)-1-(2-[5-фенилпиридин-2-иламино]этиламиноацетил)пирролидин-2-карбонитрил,(2S)-1-(2-[4-(3-фенилизоксазол-5-ил)тиазол-2-иламино]этиламиноацетил)пирролидин-2-карбонитрил,(2S)-1-[(1S)-1-метил-2-(2-метилиндол-1-ил)этиламино]ацетилпирролидин-2-карбонитрил,(2S)-1-(2-[5-(4-метоксифенил)пиридин-2-иламино]этиламиноацетил)пирролидин-2-карбонитрил,(2S)-1-(2-[2-(4-бензилоксифенил)-5-метилоксазол-4-ил]этиламиноацетил)пирролидин-2-карбонитрил,(2S)-1-[(1S)-2-(2,3-диметилиндол-1-ил)-1-метилэтиламино]ацетилпирролидин-2-карбонитрил,(2S)-1-(2-[5-(2-метоксифенил)пиридин-2-иламино]этиламиноацетил)пирролидин-2-карбонитрил,(2S)-1-[(1S)-2-(5-цианоиндол-1-ил)-1-метилэтиламино]ацетилпирролидин-2-карбонитрил и их фармацевтически приемлемые соли. Другие особенно предпочтительные соединения общей формулы (I) представляют собой те, которые выбраны из ряда, включающего(2S)-1-[1,1-диметил-2-(5-метил-2-фенилоксазол-4-ил)этиламино]ацетилпирролидин-2-карбонитрил,(2S)-1-[1,1-диметил-3-(5-метил-3-пиридин-3-илпиразол-1-ил)пропиламино]ацетилпирролидин-2 карбонитрил,(2S)-1-[1,1-диметил-3-(5-метил-3-пиразин-2-илпиразол-1-ил)пропиламино]ацетилпирролидин-2 карбонитрил,(2S)-1-[1,1-диметил-3-(3-пиридин-3-илпиразол-1-ил)пропиламино]ацетилпирролидин-2-карбонитрил,(2S)-1-[1,1-диметил-3-(5-метил-3-пиридин-3-ил[1,2,4]триазол-1-ил)пропиламино]ацетилпирролидин 2-карбонитрил,(2S)-1-[1,1-диметил-3-(2-метил-4-пиридин-3-илимидазол-1-ил)пропиламино]ацетилпирролидин 2-карбонитрил,(2S)-1-[1,1-диметил-3-(4-пиридин-3-илимидазол-1-ил)пропиламино]ацетилпирролидин-2-карбонитрил,(2S)-1-[1,1-диметил-2-(6-ацетил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-иламино)этиламино] ацетилпирролидин-2-карбонитрил,(2S)-1-[2-(бензотиазол-2-иламино)-1,1-диметилэтиламино]ацетилпирролидин-2-карбонитрил,(2S)-1-[1,1-диметил-2-(5-фенил[1,3,4]оксадиазол-2-иламино)этиламино]ацетилпирролидин-2-карбонитрил,(2S)-1-[1,1-диметил-2-(3-пиридин-3-ил[1,2,4]оксадиазол-5-иламино)этиламино]ацетилпирролидин 2-карбонитрил,(2S)-1-[1,1-диметил-2-(3-пиридин-2-ил[1,2,4]оксадиазол-5-иламино)этиламино]ацетилпирролидин 2-карбонитрил,(2S)-1-[1,1-диметил-2-(3-пиридин-4-ил[1,2,4]оксадиазол-5-иламино)этиламино]ацетилпирролидин 2-карбонитрил,(2S)-1-(1,1-диметил-2-[3-(6-метилпиридин-3-ил)-[1,2,4]оксадиазол-5-иламино]этиламиноацетил) пирролидин-2-карбонитрил и их фармацевтически приемлемые соли. Соединения формулы (I) могут обладать одним или несколькими асимметрическими углеродными атомами и могут существовать в форме оптически чистых энантиомеров или в форме рацематов. Изобретение охватывает все эти формы. Необходимо принять во внимание, что соединения общей формулы (I) при выполнении настоящего изобретения могут быть подвергнуты дериватизации по функциональным группам с получением производных, которые in vivo способны к обратному превращению в исходное соединение. Объектом настоящего изобретения является также способ получения соединений формулы (I), как она представлена выше, причем этот способ включает реакцию соединения формулы (II) с соединением R2-NH2, у которого R1, R2 и X имеют указанные выше значения, а Y обозначает уходящую группу, с получением указанного соединения формулы (I) и необязательное превращение соединения формулы (I) в фармацевтически приемлемую соль. Предпочтителен способ, который описан выше, где Y обозначает атом галогена, мезилат или тозилат, более предпочтительно атом хлора или брома. Обычно соединение формулы (II) обрабатывают 1-5 экв. соединения R2-NH2 при необязательном присутствии дополнительного основания, такого как третичный амин, карбонат и гидроксид, при температуре в интервале от -78 до 70, в инертном растворителе, таком как ТГФ или ДМФ, в течение от 0,1 до 7 дней, и полученное соединение формулы (I) выделяют по стандартным методам выделения. Полученное соединение формулы (I) можно, но необязательно, превращать в соль (кислотно-аддитивную соль) с применением методов, специалисту в данной области техники известных. Объектом изобретения являются, кроме того, соединения формулы (I), как она представлена выше,когда они получены в соответствии со способом, который описан выше. Как сказано выше, соединения по настоящему изобретению формулы (I) могут быть использованы в качестве лекарственных средств для лечения и/или профилактики заболеваний, связанных с DPP IV, таких- 13007968 как диабет, в частности инсулиннезависимый сахарный диабет, пониженная толерантность к глюкозе,заболевания пищеварительного тракта, неспецифический язвенный колит, болезнь Крона, ожирение и/или метаболический синдром, преимущественно инсулиннезависимый сахарный диабет и/или пониженная толерантность к глюкозе. Кроме того, было установлено, что соединения по настоящему изобретению могут быть использованы в качестве мочегонного средства или для лечения и/или профилактики гипертонии. Таким образом, объектом изобретения являются фармацевтические композиции, включающие представленные выше соединения и фармацевтически приемлемые носители и/или адъюванты. Более того, объектом изобретения являются вышеописанные соединения, предназначенные для их использования в качестве терапевтически активных веществ, преимущественно терапевтически активных веществ для лечения и/или профилактики заболеваний, связанных с DPP IV, таких как диабет, в частности инсулиннезависимый сахарный диабет, пониженная толерантность к глюкозе, заболевания пищеварительного тракта, неспецифический язвенный колит, болезнь Крона, ожирение и/или метаболический синдром, преимущественно для использования в качестве терапевтически активных веществ при лечении и/или профилактике инсулиннезависимого сахарного диабета и/или пониженной толерантности к глюкозе. Кроме того, объектом изобретения являются описанные выше соединения, предназначенные для их использования в качестве мочегонных средств или для использования в качестве терапевтически активных веществ при лечении и/или профилактике гипертонии. По другому варианту объектом изобретения является способ лечения и/или профилактики заболеваний, связанных с DPP IV, таких как диабет, в частности инсулиннезависимый сахарный диабет, пониженная толерантность к глюкозе, заболевания пищеварительного тракта, неспецифический язвенный колит, болезнь Крона, ожирение и/или метаболический синдром, преимущественно для лечения и/или профилактики инсулиннезависимого сахарного диабета и/или пониженной толерантности к глюкозе,причем этот способ включает введение вышеописанного соединения человеку или животному. Кроме того, объектом изобретения является способ, который описан выше, лечения и/или профилактики, при осуществлении которого заболеванием является гипертония или при осуществлении которого мочегонное средство оказывает положительное действие. Далее, объектом изобретения является применение вышеописанных соединений для лечения и/или профилактики заболеваний, связанных с DPP IV, таких как диабет, в частности инсулиннезависимый сахарный диабет, пониженная толерантность к глюкозе, заболевания пищеварительного тракта, неспецифический язвенный колит, болезнь Крона, ожирение и/или метаболический синдром, преимущественно для лечения и/или профилактики инсулиннезависимого сахарного диабета и/или пониженной толерантности к глюкозе. Кроме того, объектом изобретения является применение, как оно описано выше,при котором заболеванием является гипертония, или применение в качестве мочегонного средства. Кроме того, объектом изобретения является применение описанных выше соединений при приготовлении лекарственных препаратов для лечения и/или профилактики заболеваний, связанных с DPP IV, таких как диабет, в частности инсулиннезависимый сахарный диабет, пониженная толерантность к глюкозе,заболевания пищеварительного тракта, неспецифический язвенный колит, болезнь Крона, ожирение и/или метаболический синдром, преимущественно для лечения и/или профилактики инсулиннезависимого сахарного диабета и/или пониженной толерантности к глюкозе. Такие лекарственные препараты включают вышеописанные соединения. Кроме того, объектом изобретения является применение, как оно описано выше,при котором заболеванием является гипертония, или применение при приготовлении мочегонных средств. В контексте представленных выше способов и применения к предпочтительным относятся следующие заболевания: диабет, в частности инсулиннезависимый сахарный диабет, пониженная толерантность к глюкозе, ожирение и/или метаболический синдром, преимущественно инсулиннезависимый сахарный диабет и/или пониженная толерантность к глюкозе. Соединения формулы (I) могут быть получены по методам, приведенным ниже, по методам, приведенным в примерах, или по аналогичным методам. Соответствующие реакционные условия для отдельных реакционных стадий специалисту в данной области техники известны. Исходные материалы либо технически доступны, либо могут быть получены по методам, аналогичным методам, приведенным ниже или в примерах, или по методам, в данной области техники известным. Для определения активности соединений формулы I были выполнены следующие испытания. Активность ингибиторов DPP IV тестировали с использованием природной DPP IV человека, выделенной из пула плазмы человека, или рекомбинантной DPP IV человека. Цитратную плазму человека от различных доноров объединяли, фильтровали в стерильных условиях через 0,2-микронную мембрану и 1-миллилитровые аликвоты замораживали и хранили при -120 С до их применения. При суммарном объеме 100 мкл в качестве источника ферментов использовали: при колориметрическом анализе DPP-IV - от 5 до 10 мкл плазмы человека, при флуориметрическом анализе - 1 мкл плазмы человека. кДНК аминокислотной последовательности DPP IV человека с 31 по 766 с удаленными N-концом и трансмембранным доменом клонировали в pichia pastoris. DPP IV человека экспрессировали и очищали от культуральной среды,используя стандартную колоночную хроматографию, включая гель-хроматографию, анионную и катионную хроматографии. Чистота полученного конечного препарата фермента, окрашенного красителем синим Кумасси, составляла, по данным SDS-электрофореза в ПАА-геле, 95%. В качестве источника фер- 14007968 мента при суммарном объеме 100 мкл для колориметрического определения DPP-IV использовали 20 нг рекомбинантной DPP-IV, а при флуориметрическом - 2 нг рекомбинантной DPP-IV человека. При флуориметрическом определении в качестве субстрата использовали Аlа-Рrо-7-амидо-4 трифторметилкумарин (Calbiochem125510). 20 мМ исходный раствор в 10%-ном водном диметилформамиде хранили до начала эксперимента при -20 С. Для определения ИК 50 субстрат применяли в конечной концентрации, равной 50 мкМ. В опытах по определению кинетических параметров, таких какKm, Vmax и Kj, концентрацию субстрата варьировали от 10 до 500 мкМ. При колориметрическом определении в качестве субстрата использовали Н-Ala-Pro-pNA.HCl(Bachem L-1115). 10 мМ исходный раствор в 10% МеОН/Н 2O до начала эксперимента хранили при -20 С. Для определения ИК 50 субстрат использовали в конечной концентрации, равной 200 мкМ. В опытах по определению кинетических параметров, таких как Km, Vmax и Kj, концентрацию субстрата варьировали от 100 до 2000 мкМ. Флуоресценцию определяли при длине волны возбуждения 400 нм и длине волны эмиссии 505 нм постоянно через каждые 15 с в течение от 10 до 30 мин на люминесцентном спектрометре Perkin Elmer LS 50 В. Начальную константу скорости реакции рассчитывали по методу линейной регрессии. Абсорбцию pNA, выделяемой цветным субстратом, постоянно определяли при 405 нМ каждые 2 мин в течение от 30 до 120 мин на приборе Packard Spectra Count. Начальную константу скорости реакции рассчитывали по методу линейной регрессии. Определение активности DPP-IV проводили при 37 С в суммарном объеме 100 мкл в 96-луночном планшете. Использованный буфер включал 50 мМ Tris/HCl, содержавший 0,1 мг/мл BSA и 100 мМ NaCl,с рН 7,8. Тестируемые соединения растворяли в 100% ДМСО и разбавляли до желаемой концентрации 10% ДМСО/Н 2 О. Конечная концентрация ДМСО в определяемом растворе составляла 1 об.%. При такой концентрации инактивация фермента ДМСО составляла 5%. Соединения использовали как с предварительным инкубированием (10 мин при 37 С), так и без инкубирования с ферментом. Ферментативные реакции инициировали непосредственно после введения субстрата при перемешивании. Значения ИК 50 тестируемых соединений рассчитывали по методу нелинейной регрессии по данным ингибирования при 5 различных концентрациях субстрата и 5 различных концентрациях тестируенмых соединений. Предпочтительные соединения по настоящему изобретению показывают значения ИК 50 от 1 нМ до 10 мкМ, наиболее предпочтительно от 1 до 100 нМ, как представлено в следующей таблице. Пример ИК 50 (мкМ). Соединения формулы I и/или их фармацевтически приемлемые соли можно использовать в качестве лекарственных средств, например в форме фармацевтических препаратов для энтерального, парентерального или местного введения в организм. Они могут быть введены, например, перорально, в частности в форме таблеток, таблеток с покрытием, драже, твердых и мягких желатиновых капсул, растворов,эмульсий или суспензий; ректально, например в форме суппозиториев, или парентерально, например в форме растворов для инъекций или растворов для вливания, или местной обработкой, например в форме мазей, кремов или масел. Пероральный путь введения предпочтителен. Процесс приготовления фармацевтических препаратов можно проводить таким путем, который знаком любому специалисту в данной области техники, приданием описанным соединениям формулы I и/или их фармацевтически приемлемым солям, необязательно в сочетании с другими терапевтически ценными веществами, формы галеновых препаратов для введения в организм совместно с приемлемыми,нетоксичными, инертными терапевтически совместимыми твердыми или жидкими материаламиносителями и, если необходимо, обычными фармацевтическими адъювантами. Приемлемыми материалами-носителями являются не только неорганические материалы-носители,но также органические материалы-носители. Так, например, в качестве материалов-носителей для таблеток,таблеток с покрытием, драже и твердых желатиновых капсул можно использовать лактозу, кукурузный крахмал или его производные, тальк, стеариновую кислоту или ее соли. Приемлемыми материаламиносителями для мягких желатиновых капсул являются, например, растительные масла, воски, твердые жиры,а также полутвердые и жидкие полиолы (однако в зависимости от природы активного компонента в случае мягких желатиновых капсул никакие носители могут не потребоваться). Приемлемыми для приготовления растворов и сиропов материалами-носителями являются, например, вода, полиолы, сахароза, инвертный сахар и т.п. Приемлемыми при приготовлении растворов для инъекция материалами-носителями являются, например, вода, спирты, полиолы, глицерин и растительные масла. Приемлемыми для суппозиториев материаламиносителями являются, например, натуральные или отвержденные масла, воски, жиры и полужидкие или жид- 15007968 кие полиолы. При приготовлении препаратов для местной обработки приемлемыми материалами-носителями являются глицериды, полусинтетические и синтетические глицериды, отвержденные масла, жидкие воски,жидкие парафины, жидкие жирные спирты, стерины, полиэтиленгликоли и производные целлюлозы. В качестве фармацевтических адъювантов подходящими считают обычные стабилизаторы, консерванты, смачивающие агенты и эмульгаторы, улучшающие консистенцию вещества, корригенты, соли для варьирования осмотического давления, буферные вещества, солюбилизаторы, красящие и маскирующие вещества и антиоксиданты. Дозу соединений формулы I можно варьировать в широких интервалах в зависимости от заболевания, при котором проводят лечение, возраста, индивидуального состояния пациента и пути введения,причем в каждом конкретном случае она, разумеется, должна соответствовать индивидуальным потребностям. Для взрослых пациентов целесообразная ежедневная доза составляет от примерно 1 до 1000 мг,преимущественно от примерно 1 до 100 мг. В зависимости от серьезности заболевания и точного фармакокинетического профиля предлагаемое соединение можно было бы вводить в виде одной или нескольких ежедневных доз, например от 1 до 3 доз. В целесообразном варианте фармацевтические препараты содержат примерно от 1 до 500 мг, предпочтительно от 1 до 100 мг, соединения формулы I. Следующие примеры служат для более подробной иллюстрации настоящего изобретения. Однако они не предназначены для ограничения каким-либо образом его объема. Общие методыX=СН 2, R1=H, Y=Вr: IIС Соединения формулы (I) могут быть получены по методам, приведенным ниже, по методам, представленным в общих чертах в примерах, или по аналогичным методам. -Галоамиды (II) получали из (S)пролиламида аналогично методам, описанным в WO 98/19998. Исходные амины общей формулы (III) технически доступны или могут быть получены по методам, приведенным в литературе, или в соответствии с методами, приведенными ниже и в разделе примеров (в частности, IIIА-IIIТ). Обычно -галоамидII обрабатывают 1-5 экв. амина III при необязательном присутствии дополнительного основания, такого как третичный амин, карбонат и гидроксид, при температуре в интервале от -78 до 70 в инертном растворителе, таком как ТГФ или ДМФ, в течение от 0,1 до 7 дней, и полученный продукт I выделяют по стандартным методам выделения. Кислотно-аддитивная соль может быть, что необязательно, получена с применением методов, которые специалисту в данной области техники известны. Соединения, у которыхX обозначает S, могут быть получены либо по аналогичным методам, либо по методам, которые специалисту в данной области техники известны. Соединения формулы (I), в которой X обозначает C(R8,R9), a R8 и R9 независимо друг от друга обозначают (низш.)алкил, могут быть получены из подходящим образом защищенных аналогов глутаминовой кислоты алкилированием и последующей циклизацией до пролиновых производных. В дальнейшем их можно обрабатывать до получения -галоамидов II аналогично тому, как это описано для случая с (S)-пролиламидом. В случае соединений формулы (I), в которой R2 обозначает -C(R3,R4)-CH2-NH-R6, может потребоваться синтез соответствующих аминовых предшественников IIIЕ, IIIF, IIIN, IIIO и IIIР. Получение этих аминовых производных представлено ниже в описании общих схем. Схема 1 Аминовые производные IIIЕ могут быть получены реакцией дибромпиридинового или пиримидинового производного XIII с соответствующим 1,2-диаминоэтаном с получением продукта XIV. В дальнейшем продукт IIIЕ может быть получен реакцией типа реакции Сузуки соединения XIV с соответствующим фенильным или гетероарильным производным. Аминовые производные IIIF могут быть получены реакцией необязательно защищенной (2 аминоэтил)тиомочевины XV с -галокарбонильным соединением с получением соответствующего N1 тиазол-2-илэтан-1,2-диамина XVI. Наконец, удаление защитной группы приводит к образованию продукта IIIF. Исходная тиомочевина XV известна [R3 и R4 обозначают Н: CAS 331779-96-5] или может быть дериватизирована аналогичным образом из соответствующих диамина и бензоилизотиоцианата. Схема 3 Аминовые производные IIIO могут быть получены, если соответствующими 1,2-диаминоэтанами обработать 2-хлор[1,3,4]оксадиазолы XXXII. Исходные [1,3,4]оксадиазолы известны или могли бы быть получены аналогично описанным в литературе методам (например, Singh, H. и др. Ind. J. Chem., 1983, 22,1177-1178 и Golfier, M.J. Heterocycl. Chem., 1973, 10, 989). Схема 5 Аминовые производные IIIР могут быть получены из нитрильных производных XXXIII превращением в соответствующие гидроксиамидины XXXIV и последующей циклизацией в присутствии трихлоруксусного ангидрида и трихлоруксусной кислоты до [1,2,4]оксадиазолов XXXV, которые обрабатывают соответствующим 1,2-диаминоэтаном. В случае соединений формулы (I), в которой R2 обозначает -C(R3,R4)-(CH2)n-R5, может потребоваться синтез соответствующих аминовых предшественников IIIА, IIIС, IIID, IIIG, IIIН, IIIK, IIIL, IIIМ, IIIQ,IIIR, IIIS и IIIТ. Получение этих аминовых производных представлено ниже в описании общих схемы. Схема 6 Аминовые производные IIIА могут быть получены реакцией индольных производных V с сульфимидатом IV с образованием промежуточных продуктов VI, у которых в дальнейшем защитные группы могут быть удалены. Перед стадией удаления защитных групп промежуточные продукты VI можно подвергать необязательному восстановлению. Сульфимидаты, представленные общей формулой IV, могут быть получены из соответствующим образом замещенной -аминокислоты. Этот исходный материал восстанавливают по методам, известным из литературы, с получением соответствующего 2-аминоспирта. Затем полученный таким образом промежуточный продукт превращают в N-БОК-защищенное производное по стандартным методам. В результате дальнейшей обработки SОСl2/имидазолом и последующе- 17007968 го окисления NaIO4/RuO2 получают целевой сульфимидат IV. Схема 7 Аминовые производные IIIС могут быть получены из замещенных ароматических бромидов или иодидов IX, которые литиируют и в дальнейшем обрабатывают сульфимидатом IV с получением БОКзащищенных промежуточных продуктов X. После этого с применением методов, известных из литературы, у них удаляют защитные группы (Greene, T.W. и др. Protective Groups in Organic Synthesis; John WileySons, Inc.: New York, Chichester, Brisban, Toronto, Singapore, 1991). Схема 8 Аминовые производные IIID могут быть получены превращением этанольных производных XI в азидные производные XII и последующим восстановлением. Исходные этанольные производные известны или могут быть получены из амидов или тиоамидов аналогично методам, описанным в литературе Аминовые производные IIIG могут быть получены, исходя из соответствующих замещенных галометилоксазольных или тиазольных производных XVII. В результате алкилирования сложного эфира и последующего омыления образуются кислотные промежуточные продукты XVIII. Их подвергают перегруппировке Курциуса. На конечной стадии удаления защитных групп образуются амины IIIG. Исходные материалы XVII известны или их получают аналогично методам, описанным в литературе (WO 01/19805 A1, US 545531, Chem.Pharm.Bull. 1971, 19, 2050-2057, и J.Med.Chem. 1972, 15, 419-420). Аминовые производные IIIН-А и IIIН-В могут быть получены реакцией производных пиразолаXXII с сульфимидатными реагентами XIX и последующим удалением защитной группы у промежуточных продуктов XXV-A и XXV-B. Для синтеза неизвестных до настоящего времени 6-членных сульфимидатных реагентов XIX БОК-защищенный 3-аминопропан-1-ол XX (полученный, например, восстановлением из азетидинона XXI) циклизуют с использованием SOCl2 в присутствии имидазола. Эти промежуточные продукты обычно не выделяют, но в дальнейшем окисляют до БОК-защищенных производных сульфоновой кислотыXIX. Как 5-членные сульфимидаты IV, эти соединения являются универсальными алкилирующими агентами, которые легко взаимодействуют со множеством нуклеофилов на азотной и углеродной основе. Используемые пиразольные производные XXII технически доступны или могут быть получены осуществлением известных по литературе путей А или Б, включающих применение 1,3-дикетонов XXIII и XXIV в качестве синтетических промежуточных продуктов (например, Аli и др., Pak. J. Sci. Ind. Res. 1993, 36 (12), 502). Схема 11 Амиловые производные IIIK-А (и IIIК-В) могут быть получены реакцией [1,2,4]триазольных производных XXVI с сульфимидатными реагентами XIX и последующим удалением защитных групп у промежуточных продуктов XXVII-A (и XXVII-B). Используемые [1,2,4]триазолы XXVI технически доступны, известны из литературы или могут быть получены аналогично описанным в литературе методам (например, Francis и др., Tetrahedron Lett. 1987, 28 (43), 5133). Схема 12- 19007968 Аминовые производные IIIL-A (и IIIL-B) могут быть получены реакцией имидазольных производныхXXVII с сульфимидатными реагентами XIX и последующим удалением защитных групп у промежуточных продуктов XXIX-A (и XXIX-B). Используемые имидазолы XXVI технически доступны, известны из литературы или могут быть получены аналогично описанным в литературе методам (например, Heterocycles 1994, 39 (1), 139). Схема 13 Аминовые производные IIIМ-А (и IIIМ-В) могут быть получены реакцией пиразольных производных XXII, [1,2,4]триазольных производных XXVI и имидазольных производных XXVII с сульфимидатными реагентами IV и последующим удалением защитных групп у промежуточных продуктов ХХХ-А (и ХХХ-В). Исходные пиразолы XXII, [1,2,4]триазолы XXVI и имидазолы XXVIII технически доступны,известны или получают так, как изложено в предыдущих примерах. Схема 14 Аминовые производные IIIQ могут быть получены циклизацией амидиновых производных XXXVI с использованием N-защищенных 4-оксопентиламиновых производных XXXVII, активированных в положении 5 при первичном атоме. Амидины XXXVI известны из литературы или могут быть легко получены из соответствующих нитрильных производных с применением стандартных методов, например таких, как реакция Пиннера. N-защищенные 4-оксопентиламины XXXVII известны из литературы Аминовые производные IIIR могут быть получены из имидазолов XXXVIII посредством образования азида и восстановления. Имидазолы XXXVIII технически доступны или могут быть получены аналогично методам, описанным в литературе (WO 96/10018). Схема 16 Аминовые производные IIIS могут быть получены циклизацией амидиновых производных XXXVI с использованием N-защищенных 4-оксопентиламиновых производных XXXIX, активированных в положении 3. Амидины XXXVI известны из литературы или могут быть легко получены из соответствующих нитрильных производных с применением стандартных методов, например таких, как реакция Пиннера. N-защищенные 4-оксопентиламины XXXIX известны из литературы (Schunack, W. и др., Z. Naturforschung 1987, 42 В, 238-24). Аминовые производные IIIТ могут быть получены из имидазолов XL хлорированием, реакцией с алифатическими нитросоединениями в основных условиях (как изложено, например, в Eur. J. Med. Chem. 1995, 30, 219-225) и последующим восстановлением промежуточных нитропродуктов XLI. Перед заключительным восстановлением до аминовых производных IIIТ осуществляют необязательную стадию N-алкилирования. Имидазолы XL известны или могли бы быть получены из амидинов XXXVI реакцией с 2,3 бутадионом или 1,3-дигидроксиацетоном так, как изложено в литературе (WO 96/10018 или в DE 2528640). В случае соединений формулы (I), в которой R2 обозначает -C(R3,R4)-CH2-O-R7, может потребоваться синтез соответствующих аминовых предшественников IIIВ. Получение этих аминовых производных представлено ниже на общей схеме. Схема 18 Аминовые производные IIIВ могут быть получены реакцией фенольных производных VII с сульфимидатом IV с образованием промежуточных продуктов VIII, у которых в дальнейшем могут быть удалены защитные группы. Примеры Аббревиатуры.BuLi означает бутиллитий, БОК означает трет-бутилоксикарбонил, ТГФ означает тетрагидрофуран,ДИПЭА означает диизопропилэтиламин (основание Хюнига), АГЛ означает алюмогидрид лития, ТФК означает трифторуксусную кислоту, КТ означает комнатную температуру, МС означает массспектрометрию, ЯМР означает ядерно-магнитную резонансную спектроскопию, ISP означает ионизацию пучком положительных ионов, что соответствует ESI (электрораспылению ионизацией в виде положительно заряженного иона), ТСХ означает тонкослойную хроматографию, МсХл означает метансульфонилхлорид, Восст. означает восстановление, ТМС означает тетраметилсилан, EI означает ионизацию электронами. Общие примечания. 1 Н-ЯМР-спектр определяли при 250 или 300 МГц в растворителе, указанном в разделе примеров. Хим.сдвиги приведены в частях на миллион относительно ТМС. Замечание "(+ оптически активный изомер)" указывает на присутствие в спектре второго, менее интенсивного сигнала, который может быть обусловлен оптически активным изомером. Масс-спектр получали по методу ионизации, указанному в разделе примеров. Пример 1. (2S)-1-[1R/S)-1,2,3,4-Тетрагидронафталин-1-иламино)ацетил]пирролидин-2-карбонитрил. Рацемический 1-амино-1,2,3,4-тетрагидронафталин (330 мг) в аргоновой атмосфере растворяли в сухом ТГФ (6 мл). В течение 5-часового периода при КТ по каплям добавляли раствор соединения ПА(130 мг) в 6 мл ТГФ и смесь перемешивали в течение дополнительных 20 ч. Образовавшуюся суспензию разбавляли этилацетатом и промывали насыщенным раствором NаНСО 3 и рассолом. Органический слой отделяли, сушили над Na2SO4, фильтровали и выпаривали. Остаток очищали экспресс-хроматографией(CH2Cl2/MeOH/NH4OH 95:5:0,5) и соответствующие фракции объединяли и выпаривали с получением в виде масла целевого продукта в форме смеси двух диастереоизомеров (166 мг). МС (ISP): 284,2 (МН+). 1 Н-ЯМР (CDCl3): 1,53 (широкий s, 1 Н), 1,73 (m, 1 Н), 1,83 (m, 2 Н), 1,95-2,35 (m, 4 Н), 2,71 (m, 1 Н),- 21007968 2,82 (m, 1 Н), 3,42 (m, 1 Н), 3,46 (s, 3 Н), 3,59 (m, 1 Н), 3,81 (m, 1 Н), 4,79 (m, 1 Н), 7,10 (m, 1 Н), 7,16 (m, 2 Н),7,44 (m, 1 Н). Пример 2. Гидрохлоридная соль (2S)-1-[2R/S)-6-метокси-1,2,3,4-тетрагидронафталин-2-иламино) ацетил]пирролидин-2-карбонитрила. Стадия А. 2-Aмино-6-метокси-1,2,3,4-тетрагидронафталин. 6-Метокси-3,4-дигидро-2(1H)нафталиноноксим (1,0 г), полученный из 6-метокси-2-тетралона в соответствии с работой Qizhuang, Y. и др. в J. Med. Chem. 1989, 32, 478-486, суспендировали в этаноле/воде 1:1 и порциями добавляли никелеалюминиевого сплава (1,58 г). В течение 5-минутного периода с интенсивным перемешиванием по каплям добавляли раствор гидроксида натрия (32%-ный, 5,8 мл) - отмечали слабое нагревание смеси. Суспензию интенсивно перемешивали и анализировали ТСХ - после 60 мин расходовали весь исходный материал. Суспензию фильтровали через продукт dicalite и фильтрат экстрагировали CH2Cl2. Органический слой промывали рассолом, сушили и выпаривали. Сырой продукт очищали экспресс-хроматографией (3 15-сантиметровые колонки с силикагелем) с использованием в качестве элюентов CH2Cl2/MeOH/NH4OH 95:5:0,5 и CH2Cl2/MeOH/NH4OH 90:5:10,5. Продукт получали в виде темно-зеленого масла (660 мг). МС (ISP): 178,1 (МН+), 161,3 ([MH-NH3]+). 1 Н-ЯМР (CDCl3): 1,48 (широкий s, 2H), 1,58 (m, 1H), 1,99 (m, 1H), 2,54 (dd, 1H), 2,80 (m, 2 Н), 2,96(dd, 1 Н), 3,17 (m, 1 Н), 3,77 (s, 3H), 6,61 (d, 1H), 6,69 (dd, 1H), 7,00 (d, 1H). Стадия Б. Гидрохлоридная соль (2S)-1-[2R/S)-6-мeтокси-1,2,3,4-тетрагидронафталин-2-иламино) ацетил]пирролидин-2-карбонитрила. Указанное в заглавии соединение получали аналогично примеру 1 из рацемического 2-амино-6 метокси-1,2,3,4-тетрагидронафталина (357 мг) и продукта IIА (116 мг). Выход: 156 мг. Это соединение растворяли в ТГФ/диэтиловом эфире 1:3 (10 мл) и обрабатывали 2,2 М НСl в этилацетате (1 мл). Полученный твердый продукт выделяли фильтрованием и сушили под вакуумом. Выход: 138 мг, смесь 2 диастереоизомеров.MC (ISP): 314,4 (МН+). 1 Н-ЯМР (ДМСО-d6): 1,73 (m, 1 Н), 2,05 (m, 2 Н), 2,20 (m, 3 Н), 2,70 (m, 1 Н), 2,88 (m, 2 Н), 3,19 (m, 1 Н),3,40 (m, 1 Н), 3,50 (q, 1 Н), 3,69 (m, 1H), 3,71 (s, 3 Н), 4,17 (m 2 Н), 4,87 (m, 1 Н), 6,66 (s, 1H), 6,73 (d, 1H),7,02 (d, 1H), 9,18 (широкий s, 2 Н). Пример 3. (2S)-1-[2R/S)-1,2,3,4-тетрагидронафталин-1-иламино)ацетил]пирролидин-2-карбонитрил. Стадия А. 2-Амино-1,2,3,4-тетрагидронафталин. Рацемический 2-амино-1,2,3,4-тетрагидронафталин получали аналогично примеру 2, стадия А, из тетралоноксима (CAS 3349-65-3). 1 Н-ЯМР (CDCl3): 1,48 (широкий s, 2 Н), 1,60 (m, 1 Н), 2,01 (m, 1 Н), 2,56 (dd, 1 Н), 2,87 (m, 2 Н), 3,00(dd, 1 Н), 3,19 (m, 1 Н), 7,10 (m, 4 Н). Стадия Б. (2S)-1-[2R/S)-1,2,3,4-Тетрагидронафталин-2-иламино)ацетил]пирролидин-2-карбонитрил. Это соединение получали аналогично примеру 1 из рацемического 2-амино-1,2,3,4-тетрагидронафталина (153 мг) и соединения IIВ (75 мг). Выход: 83 мг, смесь 2 диастереоизомеров. МС (ISP): 284,2 (МН+). 1 Н-ЯМР (CDCl3): 1,66 (m, 1 Н), 1,87 (широкий s, 1H), 2,00-2,40 (m, 5H), 2,67 (m, 1H), 2,75-3,05 (m,5H), 3,46 (m, 1H), 3,52 (s, 2H), 3,62 (m, 1H), 4,78 (m, 1H), 7,10 (m, 4H). Пример 4. Гидрохлоридная соль (2S)-1-([(1S)-2-(5-метокси-2-метилиндол-1-ил)-1-метилэтиламино] ацетилпирролидин-2-карбонитрила. Для синтеза этого соединения в соответствии с приведенной выше общей схемой требуется получение соответствующего аминового предшественника IIIА. На начальной стадии индоловое или индолиновое производное V обрабатывают подходящим основанием, таким как NaH или трет-бутилат калия, в инертном растворителе, таком как ТГФ или ДМФ, или т.п., а затем сульфимидатом IV с получением промежуточного продукта VI. Сульфимидаты, представленные общей формулой IV, могут быть получены из соответствующим образом замещенной -аминокислоты. Этот исходный материал восстанавливают по методам, известным из литературы, с получением соответствующего 2-аминоспирта. Далее полученный таким образом промежуточный продукт превращают в N-БОК-защищенное производное по стандартным методам. В результате дальнейшей обработки SОCl2/имидазолом и последующего окисления NaIO4/RuO2 получают целевой сульфимидат IV. На этой стадии восстановление индолового ядра до соответствующего индолина можно проводить не- 22007968 обязательно восстановлением NaCNBH3 или т.п. Затем у БОК-защищенного промежуточного продукта VI удаляют защитную группу с применением методов, известных из литературы (Greene, T.W. и др. ProtectiveGroups in Organic Synthesis; John WileySons, Inc.: New York, Chichester, Brisbane, Toronto, Singapore, 1991),таких как с использованием ТФК/СН 2 Сl2 или НСl, и амин IIIА выделяют из его соли обработкой основанием. Стадия А. трет-Бутиловый эфир (S)-[2-(5-метокси-2-метилиндол-1-ил)-1-метилэтил]карбаминовой кислоты. 5-Метокси-2-метилиндол (806 мг) растворяли в ДМФ (25 мл) и с помощью ледяной бани охлаждали до 0 С. В течение 15 мин добавляли трет-бутилата калия (1M в ТГФ, 6 мл) и образовавшуюся смесь перемешивали в течение дополнительных 30 мин. Одной порцией добавляли трет-бутилового эфира (S)-4 метил-2,2-диоксо[1,2,3]оксатиазолидин-3-карбоновой кислоты IV (1,42 г) и перемешивание продолжали при КТ до тех пор, пока данные ТСХ анализа не указывали на полное потребление исходного материала. Реакционную смесь разделяли между диэтиловым эфиром и насыщенным раствором NH4Cl и органический слой отделяли, промывали насыщ. NH4Cl и рассолом, сушили над Na2SO4, фильтровали и выпаривали под вакуумом. Остаток очищали экспресс-хроматографией (CH2Cl2). Соответствующие фракции объединяли и выпаривали с получением продукта в виде не совсем белого твердого вещества (1,42 г). МС (ISP): 341,3 (MNa+), 319,4 (МН+). 1 Н-ЯМP (CDCl3): 1,08 (d, 3 Н), 1,41 (s, 9 Н), 2,43 (s, 3 Н), 3,83 (s, 3 Н), 3,88 (m, 1 Н), 4,06 (m, 1H), 2,22(широкий m, 1H), 4,44 (широкий s, 1H), 6,17 (s, 1H), 6,79 (dd, 1H), 6,98 (d, 1H), 7,26 (m, 1H) (+ оптически активный изомер). Стадия Б. (S)-2-(5-Метокси-2-метилиндол-1-ил)-1-метилэтиламин. Продукт, полученный в примере 4, стадия А, (796 мг), обрабатывали ТФК/СН 2 Сl2 1:3 (25 мл) при 0C в течение 4 ч и затем при КТ в течение 1 ч с перемешиванием магнитной мешалкой. Смесь концентрировали под вакуумом и остаток растворяли в этилацетате. Органический слой дважды промывали насыщенным NaHCO3 и затем рассолом, сушили (Na2SO4) и концентрировали. Остаток очищали экспресс-хроматографией с использованием CH2Cl2/MeOH/NH4OH 95:5:0,5 в качестве элюента. Фракции,содержавшие чистый продукт, объединяли и выпаривали с получением целевого соединения в виде желтого масла (427 мг). МС (ISP): 219,3 (МН+), 202,2 ([MH-NH3]+). 1 Н-ЯМР (CDCl3): 1,13 (d, 3 Н), 1,15 (широкий s, 2H), 2,43 (s, 3 Н), 3,35 (m, 1 Н), 3,84 (s, 3 Н), 3,87 (dd,1H), 3,95 (dd, 1H), 6,18 (s, 1H), 6,78 (dd, 1H), 7,00 (d, 1 Н), 7,18 (d, 1H). Стадия В. Гидрохлоридная соль (2S)-1-[(1S)-2-(5-метокси-2-метилиндол-1-ил)-1-метилэтиламино] ацетилпирролидин-2-карбонитрила.(151 мг) в соответствии с примером 1. Полученный таким образом свободный амин (66 мг) превращали в гидрохлоридную соль так, как изложено в примере 2. МС (ISP): 377,3 (MNa+), 355,3 (МН+). 1 Н-ЯМР (ДМСО-d6): 1,06 (d, 3 Н), 2,05 (m, 2 Н), 2,20 (m, 2 Н), 2,40 (s, 3 Н), 3,45 (q, 1 Н), 3,55 (m, 1 Н),3,67 (m, 1 Н), 3,74 (s, 3 Н), 4,11 (m, 2 Н), 4,26 (m, 1 Н), 4,49 (m, 1 Н), 4,85 (m, 1 Н), 6,19 (s, 1H), 6,75 (d, 1H),6,97 (s, 1H), 7,36 (d, 1H), 9,35 (широкий s, 2H) (+ оптически активный изомер). Пример 5. Гидрохлоридная соль (2S)-[(1S)-2-(5-цианоиндол-1-ил)-1-метилэтиламино]ацетилпирролидин-2-карбонитрила. Стадия А. трет-Бутиловый эфир (S)-[2-(5-цианоиндол-1-ил)-1-метилэтил]карбаминовой кислоты. Это соединение получали в соответствии с примером 4, стадия А, из 5-цианоиндола (500 мг) и третбутилового эфира (S)-4-метил-2,2-диоксо[1,2,3]оксатиазолидин-3-карбоновой кислоты IV (1,0 г). Выход: 1,09 г, желтый твердый продукт.H-ЯМР (CDCl3): 1,12 (d, 3 Н), 1,41 (s, 9H), 3,95-4,20 (m, 2H), 4,20-4,40 (m, 2 Н), 6,59 (d, 1H), 7,18 (d,1H), 7,40-7,60 (m, 2H), 7,96 (s, 1H). Стадия Б. (S)-2-(5-Цианоиндол-1-ил)-1-метилэтиламин. Продукт, полученный на стадии А (500 мг), при КТ в течение 60 мин обрабатывали 2,2 М НСl в этилацетате (15 мл). После полного потребления исходного материала реакционную смесь разбавляли этилацетатом, промывали насыщенным раствором NaHCO3 и рассолом, сушили, фильтровали и выпаривали. Сырой продукт очищали экспресс-хроматографией с использованием CH2Cl2/MeOH/NH4OH 95:5:0,5 в качестве элюента. Фракции, содержавшие чистый продукт, объединяли и выпаривали с получением указанного в заглавии соединения в виде бесцветного масла (251 мг). МС (ISP): 200,2 (МН+), 183,1 ([MH-NH3]+). 1 Н-ЯМР (CDCl3): 1,10 (широкий s, 2H), 1,15 (d, 3 Н), 3,44 (m, 1H), 3,95 (dd, 1 Н), 4,11 (dd, 1H), 6,60 (d,1H), 7,26 (d, 1H), 7,43 (m, 2H), 7,96 (d, 1H). Стадия В. Гидрохлоридная соль (2S)-1-[(1S)-2-(5-циaноиндол-1-ил)-1-метилэтиламино]ацетил пирролидин-2-карбонитрила. В соответствии с примером 1 проводили реакцию сочетания амина, образовавшегося на предыдущей стадии (215 мг), и соединения IIВ (80 мг). Полученный продукт превращали в гидрохлоридную соль- 23007968 так, как изложено в примере 2, стадия Б, с получением 125 мг указанного в заглавии соединения. МС (ISP): 358,3 (MNa+), 336,2 (МН+). 1 Н-ЯМР (ДМСО-d6): 1,16 (d, 3 Н), 2,05 (m, 2 Н), 2,19 (m, 2 Н), 3,43 (m, 2 Н), 3,60 (m, 1H), 3,70 (m, 1 Н),4,43 (dd, 1 Н), 4,74 (dd, 1 Н), 4,86 (m, 1 Н), 6,68 (d, 1H), 7,57 (d, 1H), 7,65 (d, 1H), 7,83 (d, 1H), 8,15 (s, 1H),9,47 (широкий s, 1H), 9,55 (широкий s, 1H) (+ оптически активный изомер). Пример 6. (2S)-1-[(1S)-1-Метил-2-(2-метилиндол-1-ил)этиламино]ацетилпирролидин-2-карбонитрил. Указанное в заглавии соединение получали в соответствии с примером 4, стадии с А по В, в виде коричневатого масла из 2-метилиндола, трет-бутилового эфира (S)-4-метил-2,2-диоксо[1,2,3]оксатиазолидин-3-карбоновой кислоты и соединения IIВ. МС (ISP): 347,4 (MNa+), 325,4 (МН+). 1(d, 1 Н), 2,96 (d, 1 Н), 3,08 (m, 1 Н), 3,19 (m, 1 Н), 4,02 (m, 2 Н), 4,57 (m, 1 Н), 6,25 (s, 1 Н), 7,00-7-17 (m, 2 Н),7,28 (m, 1 Н), 7,48 (d, 1H) (+ оптически активный изомер). Пример 7. (2S)-1-[(1S)-2-(2,3-Диметилиндол-1-ил)-1-метилэтиламино]ацетилпирролидин-2-карбонитрил. Это соединение получали из 2,3-диметилиндола, трет-бутилового эфира (S)-4-метил-2,2-диоксо[1,2,3]оксатиазолидин-3-карбоновой кислоты и соединения IIВ в соответствии с примером 5, стадии с А по В. МС (ISP): 361,3 (MNa+), 339,3 (МН+). 1 Н-ЯМР (ДМСО-d6): 0,95 (d, 3 Н), 1,85-2,10 (m, 5H), 2,18 (s, 3 Н), 2,35 (s, 3 Н), 3,02 (m, 1 Н), 3,15 (m,1 Н), 3,24 (широкий s, 2 Н), 3,39 (m, 1 Н), 3,93 (dd, 1H), 4,07 (dd, 1H), 4,65 (m, 1H), 6,95 (t, 1H), 7,02 (t, 1H),7,36 (m, 2H) (+ оптически активный изомер). Пример 8. Гидрохлоридная соль (2S)-1-[(1S)-1-метил-2-(3-метилиндол-1-ил)этиламино]ацетил пирролидин-2-карбонитрила. Это соединение получали из 3-метилиндола, трет-бутилового эфира (S)-4-метил-2,2-диоксо[1,2,3] оксатиазолидин-3-карбоновой кислоты и соединения IIА в соответствии с примером 5, стадии с А по В. Гидрохлоридную соль указанного в заглавии соединения получали в соответствии с примером 2. МС (ISP): 347,4 (MNa+), 325,4 (МН+). 1 Н-ЯМР (ДМСО-d6): 1,15 (d, 3 Н), 2,04 (m, 2 Н); 2,17 (m, 2 Н), 2,26 (s, 3 Н), 3,40 (m, 2 Н), 3,54 (m, 1 Н),3,66 (m, 2 Н), 4,05 (широкий s, 2H), 4,24 (dd, 1H), 4,58 (dd, 1 Н), 4,84 (dd, 1 Н), 7,06 (m, 1 Н), 7,18 (m, 2 Н),7,52 (m, 2 Н), 9,23 (широкий s, 1 Н), 9,30 (широкий s, 1H) (+ оптически активный изомер). Пример 9. (2S)-1-[(1S)-2-(5-Броминдол-1-ил)-1-метилэтиламино]ацетилпирролидин-2-карбонитрил. Это соединение получали из 5-броминдола, трет-бутилового эфира (S)-4-метил-2,2-диоксо[1,2,3]оксатиазолидин-3-карбоновой кислоты и соединения IIА в соответствии с примером 5, стадии с А по В. МС (ISP): 411,5 (MNa+), 389,2 (МН+). 1H-ЯМР (ДМСО-d6): 0,92 (d, 3 Н), 1,95 (m, 2 Н), 2,07 (m, 2 Н), 3,02 (m, 1H), 3,22 (m, 1 Н), 3,28 (широкий s, 2 Н), 3,42 (m, 1 Н), 4,04 (dd, 1H), 4,16 (dd, 1H), 4,68 (t, 1H), 6,42 (d, 1H), 7,21 (dd, 1H), 7,42 (d, 1H),7,49 (d, 1H), 7,72 (d, 1H) (+ оптически активный изомер). Пример 10. Гидрохлоридная соль (2S)-1-[2-(5-бром-2,3-дигидроиндол-1-ил)этиламино]ацетил пирролидин-2-карбонитрила. Это соединение получали из 5-бром-2,3-дигидроиндола и трет-бутилового эфира 2,2-диоксо[1,2,3] оксатиазолидин-3-карбоновой кислоты в соответствии с примером 5, стадии с А по В. Гидрохлоридную соль указанного в заглавии соединения получали в соответствии с примером 2. МС (ISP): 399,3 (MNa+), 377,3 (МН+). 1 Н-ЯМР (ДМСО-d6): 2,05 (m, 2 Н), 2,17 (m, 2H), 2,94 (t, 2H), 3,16 (m, 2H), 3,38 (m, 5 Н), 3,60 (m, 1 Н),4,00-4,30 (m, 5H), 4,85 (t, 1H), 6,55 (d, 1H), 7,20 (d, 2H), 7,21 (s, 1H), 9,10 (широкий s, 2H) (+ оптически активный изомер). Пример 11. (2S)-1-[(1S)-2-(7-Азаиндол-1-ил)-1-метилэтиламино]ацетилпирролидин-2-карбонитрил. Это соединение получали из 7-азаиндола, трет-бутилового эфира (S)-4-метил-2,2-диоксо[1,2,3]оксатиазолидин-3-карбоновой кислоты и соединения IIВ в соответствии с примером 5, стадии с А по В. МС (ISP): 334,3 (MNa+), 312,2 (МН+). 1 Н-ЯМР (ДМСО-d6): 0,93 (d, 3H), 1,97 (m, 2H), 2,0 (очень широкий s, 1H), 2,08 (m, 2 Н), 3,12 (m,1H), 3,20-3,40 (m, 3 Н), 3,49 (m, 1 Н), 4,14 (dd, 1H), 4,27 (dd, 1 Н), 4,69 (t, 1H), 6,46 (d, 1H), 7,07 (dd, 1H),7,55 (d, 1H), 7,95 (d, 1H), 8,23 (d, 1H) (+ оптически активный изомер). Пример 12. (2S)-1-[(1S)-2-(2-Азаиндол-1-ил)-1-метилэтиламино]ацетилпирролидин-2-карбонитрил. Это соединение получали из 2-азаиндола (индазол), трет-бутилового эфира (S)-4-метил-2,2-диоксо(d, 1H), 7,75 (d, 1H), 8,07 (s, 1H) (+ оптически активный изомер). Пример 13. (2S)-1-[(1S)-1-Метил-2-(5-фенил-2,3-дигидроиндол-1-ил)этиламино]ацетилпирролидин 2-карбонитрил. Это соединение получали из 5-фенил-2,3-дигидроиндола (синтезированного из 5-броминдола в со- 24007968 ответствии с WO 95/01976), трет-бутилового эфира (S)-4-метил-2,2-диоксо[1,2,3]оксатиазолидин-3-карбоновой кислоты и соединения IIА в соответствии с примером 4, стадии с А по В. МС (ISP): 389,3 (МН+). 1 Н-ЯМР (CDCl3): 1,13 (d, 3 Н), 1,70 (широкий s, 1 Н), 2,10-2,35 (m, 4H), 2,89 (m, 1H), 3,06 (m, 3H),3,17 (dd, 1H), 3,27 (q, 1H), 3,35-3,70 (m, 5H), 4,76 (m, 1H), 6,56 (d, 1H), 7,20-7,40 (m, 5H), 7,51 (d, 1H) (+ оптически активный изомер). Пример 14. (2S)-1-[(1S)-2-(5-Циано-2-метилиндол-1-ил)-1-метилэтиламино]ацетилпирролидин-2 карбонитрил. Это соединение получали из 5-циано-2-метилиндола (синтезированного аналогично изложенномуAggarwal, А. и др. в Synth.Commun. 1993, 23, 1101-1110, из 5-бром-2-метилиндола), трет-бутилового эфира (S)-4-метил-2,2-диоксо[1,2,3]оксатиазолидин-3-карбоновой кислоты и соединения IIА в соответствии с примером 5, стадии с А по В, за исключением того, что с целью добиться приемлемого выхода на стадии В реакцию нужно было продолжать в течение 72 ч. МС (ISP): 350,4 (МН+). 1 Н-ЯМР (CDCl3): 1,15 (d, 3H), 1,60 (широкий s, 1H), 1,95-2,30 (m, 4H), 2,51 (s, 3 Н), 2,82 (d, 1 Н), 2,86(m, 1H), 3,01 (d, 1 Н), 3,05-3,25 (m, 2 Н), 4,02 (m, 2 Н), 4,63 (m, 1 Н), 6,35 (s, 1 Н), 7,36 (m, 2 Н), 7,84 (s, 1H) (+ оптически активный изомер). Пример 15. (2S)-1-[(1S)-1-Метил-2-(2-фенилиндол-1-ил)этиламино]ацетил)пирролидин-2-карбонитрил. Это соединение получали из 2-фенилиндола, трет-бутилового эфира (S)-4-метил-2,2-диоксо[1,2,3] оксатиазолидин-3-карбоновой кислоты и соединения IIА в соответствии с примером 5, стадии с А по В. МС (ISP): 387,3 (МН+). 1 Н-ЯМР (ДМСО-d6): 0,69 (d, 3 Н), 1,93 (m, 2 Н), 2,07 (m, 2 Н), 2,80 (m, 1 Н), 2,91 (d, 1 Н), 3,02 (m, 1 Н),3,05 (d, 1 Н), 3,31 (m, 1 Н), 4,06 (dd, 1H), 4,28 (dd, 1H), 4,61 (dd, 1 Н), 6,52 (s, 1 Н), 7,05 (t, 1 Н), 7,16 (t, 1 Н),7,40-7,62 (т, 7 Н) (+ оптически активный изомер). Пример 16. (2S)-1-[1S)-2-Карбазол-9-ил-1-метилэтиламино)ацетил]пирролидин-2-карбонитрил. Это соединение получали из карбазола, трет-бутилового эфира (S)-4-метил-2,2-диоксо[1,2,3]оксатиазолидин-3-карбоновой кислоты и соединения IIА в соответствии с примером 5, стадии с А по В, в виде свободного основания.MC(ISP): 361,3 (МН+). 1 Н-ЯМР (ДМСО-d6): 0,98 (d, 3 Н), 1,90 (m, 2 Н), 2,06 (m, 2 Н), 3,21 (m, 2 Н), 3,30-3,5 (m, 4 Н), 4,23 (dd, 1H),4,39 (dd, 1H), 4,63 (dd, 1H), 7,19 (t, 2H), 7,44 (t, 2 Н), 7,63 (d, 2H), 8,14 (d, 2H) (+ оптически активный изомер). Пример 17. (2S)-1-[(1S)-2-(6-Броминдол-1-ил)-1-метилэтиламино]ацетилпирролидин-2-карбонитрил. Указанное в заглавии соединение получали из 6-броминдола, трет-бутилового эфира (S)-4-метил 2,2-диоксо[1,2,3]оксатиазолидин-3-карбоновой кислоты и соединения IIА в соответствии с примером 5,стадии с А по В, в виде свободного основания. МС (ISP): 411,3 (MNa+), 389,1 (МН+). 1(dd, 1H), 4,15 (dd, 1H), 4,67 (t, 1H), 6,45 (d, 1H), 7,12 (dd, 1H), 7,39 (d, 1H), 7,49 (d, 1H), 7,77 (s, 1H) (+ оптически активный изомер). Пример 18. (2S)-1-[(1S)-1-Метил-2-(7-метилиндол-1-ил)этиламино]ацетилпирролидин-2-карбонитрил. Это соединение получали из 7-метилиндола, трет-бутилового эфира (S)-4-метил-2,2-диоксо[1,2,3] оксатиазолидин-3-карбоновой кислоты и соединения IIА в соответствии с примером 5, стадии с А по В, в виде свободного основания. МС (ISP): 347,4 (MNa+), 325,4 (МН+). 1 Н-ЯМР (ДМСО-d6): 0,94 (d, 3 Н), 1,85-2,10 (m, 5H), 2,67 (s, 3 Н), 2,96 (m, 1 Н), 3,10-3,23 (m, 3 Н), 3,38(m, 1 Н), 4,15 (dd, 1 Н), 4,32 (dd, 1 Н), 4,66 (m, 1H), 6,39 (d, 1 Н), 6,86 (m, 2 Н), 7,26 (d, 1H), 7,36 (d, 1H) (+ оптически активный изомер). Пример 19. (2S)-1-[(1S)-2-(7-Броминдол-1-ил)-1-метилэтиламино]ацетилпирролидин-2-карбонитрил. Это соединение получали из 7-броминдола, трет-бутилового эфира (S)-4-метил-2,2-диоксо[1,2,3]оксатиазолидин-3-карбоновой кислоты и соединения IIА в соответствии с примером 5, стадии с А по В, в виде свободного основания. МС (ISP): 411,3 (MNa+), 389,1 (МН+). 1 Н-ЯМР (ДМСО-d6): 0,94 (d, 3H), 1,85-2,10 (m, 5H), 3,00-3,30 (m, 4 Н), 3,41 (m, 1 Н), 4,41 (m, 2 Н), 4,66(m, 1 Н), 6,50 (d, 1H), 6,92 (t, 1H), 7,31 (d, 1H), 7,41 (d, 1H), 7,57 (d, 1H) (+ оптически активный изомер). Пример 20. (2S)-1-[2-(4-Хлориндол-1-ил)этиламино]ацетилпирролидин-2-карбонитрил. Это соединение получали из 4-хлориндола, трет-бутилового эфира 2,2-диоксо[1,2,3]оксатиазолидин-3-карбоновой кислоты и соединения IIА в соответствии с примером 5, стадии с А по В, в виде свободного основания.- 25007968 Это соединение получали из 5-метокси-2-метилиндола, трет-бутилового эфира 2,2-диоксо[1,2,3] оксатиазолидин-3-карбоновой кислоты и соединения IIА в соответствии с примером 5, стадии с А по В, в виде свободного основания. МС (ISP): 363,3 (MNa+), 341,4 (МН+). 1 Н-ЯМР (CDCl3): 1,60 (широкий s, 1H), 2,00-2,30 (m, 4H), 2,44 (s, 3H), 2,99 (t, 2 Н), 3,07-3,40 (m, 3 Н),3,83 (s, 3 Н), 4,18 (t, 2 Н), 4,68 (m, 1 Н), 6,16 (s, 1H), 6,78 (dd, 1H), 6,89 (d, 1H), 7,18 (d, 1H). Пример 22. (2S)-1-[(1S)-2-(5,6-Диметоксииндол-1-ил)-1-метилэтиламино]ацетилпирролидин-2 карбонитрил. Это соединение получали из 5,6-диметоксииндола, трет-бутилового эфира (S)-4-метил-2,2-диоксо[1,2,3]оксатиазолидин-3-карбоновой кислоты и соединения IIВ в соответствии с примером 4, стадии с А по В, за следующим исключением на стадии В: целевой промежуточный 1-метил-2-[5,6-диметоксииндол 1-ил] получали с всего лишь 25%-ным выходом. Основной продукт представлял собой (S)-1-[1-(2 аминопропил)-5,6-диметокси-1 Н-индол-3-ил]-2,2,2-трифторэтанон (50%-ный выход).(m, 2 Н), 3,91 (s, 3 Н), 3,94 (8s, 3 Н), 3,95 (m, 2 Н), 4,62 (m, 1 Н), 6,39 (d, 1 Н), 6,85 (s, 1 Н), 7,02 (d, 1 Н), 7,06 (s, 1H). Пример 23. Гидрохлоридная соль (2S)-1-[(1S)-2-(5,6-диметокси-3-трифторацетилиндол-1-ил)-1-метилэтиламино]ацетилпирролидин-2-карбонитрила. Реакцию сочетания (S)-1-[1-(2-аминопропил)-5,6-диметокси-1 Н-индол-3-ил]-2,2,2-трифторэтанона,полученного в примере 22, стадия Б, с соединением IIВ проводили в соответствии с примером 1. МС (ISP): 467,2 (МН+). 1 Н-ЯМР (ДМСО-d6): 1,21 (d, 3 Н), 2,05 (m, 2 Н), 2,19 (m, 2 Н), 3,37 (m, 2 Н), 3,46 (m, 1 Н), 3,59 (m, 1H),3,77 (m, 1 Н), 3,83 (s, 3 Н), 3,90 (s, 3 Н), 4,10 (m, 2 Н), 4,55 (m, 1 Н), 4,78 (m, 1 Н), 4,86 (m, 1 Н), 7,49 (s, 1H),7,68 (s, 1H), 8,45 (s, 1H), 9,37 (широкий s, 1H), 9,55 (широкий s, 1H). Пример 24. (2S)-1-1S)-2-[6-(4-Метоксифенил)-2,3-дигидроиндол-1-ил]-1-метилэтиламиноацетил) пирролидин-2-карбонитрил. Стадия А. трет-Бутиловый эфир (S)-2-[6-(4-метоксифенил)индол-1-ил]-1-метилэтилкарбаминовой кислоты. Это соединение синтезировали из 6-(4-метоксифенил)индола (синтезированного из 6-броминдола в соответствии с изложенным Carrera, G.M. и др. в Synlett 1994, 1, 93-94) и трет-бутилового эфира (S)-4 метил-2,2-диоксо[1,2,3]оксатиазолидин-3-карбоновой кислоты так, как изложено в примере 4, стадия А.(1,80 г) растворяли в уксусной кислоте (25 мл) и CH2Cl2 (10 мл) и охлаждали до 0 С. Порциями добавляли NaCNBH3 (1,41 г) и образовавшуюся смесь перемешивали в течение 4 ч. Реакционную смесь разбавляли этилацетатом и экстрагировали концентрированным раствором NaOH. Органический слой промывали рассолом, сушили (Na2SO4) и выпаривали. Остаток очищали экспресс-хроматографией (градиент этилацетата в гексанах) с получением указанного в заглавии соединения в виде коричневого масла (1,7 г). МС (ISP): 405,6 (MNa+), 383,4 (МН+). 1 Н-ЯМР (CDCl3): 1,25 (d, 3 Н), 1,41 (s, 9H), 3,01 (t, 2H), 3,12 (d, 2H), 3,46 (m, 2 Н), 3,84 (s, 3 Н), 3,94(m, 1 Н), 4,57 (широкий s, 1 Н), 6,62 (s, 1H), 6,82 (d, 1H), 6,94 (m, 2H), 7,10 (d, 1H), 7,49 (m, 2H). Стадия В. (S)-2-[6-(4-Метоксифенил)-2,3-дигидроиндол-1-ил]-1-метилэтиламин. Указанное в заглавии соединение получали из трет-бутилового эфира (S)-2-[6-(4-метоксифенил) индол-1-ил]-1-метилэтилкарбаминовой кислоты в соответствии с примером 4, стадия Б, в виде смолы. МС (ISP): 283,4 (МН+). 1 Н-ЯМР (CDCl3): 1,20 (d, 3 Н), 2,88 (dd, 1H), 2,96 (m, 2H), 3,14-3,29 (m, 4H), 3,51 (m, 1H), 3,83 (s, 3H),6,70 (s, 1H), 6,85 (d, 1H), 6,94 (m, 2H), 7,06 (d, 1H), 7,49 (m, 2H). Стадия Г. (2S)-1-1S)-2-[6-(4-Метоксифенил)-2,3-дигидроиндол-1-ил]-1-метилэтиламиноацетил) пирролидин-2-карбонитрил. Указанное в заглавии соединение получали из (S)-2-[6-(4-метоксифенил)-2,3-дигидроиндол-1-ил]1-метилэтиламина и соединения IIА аналогично примеру 1 в виде пены. Для синтеза этого соединения в соответствии с приведенной выше общей схемой требуется получение соответствующего аминового предшественника IIIВ. На начальной стадии аминофенольное или нафтольное производное VII обрабатывают подходящим основанием, таким как NaH и трет-бутилат калия, в инертном растворителе, таком как ТГФ, ДМФ и т.п., а затем сульфимидатом IV. Сульфимидаты, представленные общей формулой IV, могут быть получены из соответствующим образом замещенной осаминокислоты. Этот материал восстанавливают по методам, известным из литературы, с получением соответствующего 2-аминоспирта. Далее полученный таким образом промежуточный продукт по стандартным методам превращают в N-БОК-защищенное производное. В результате дальнейшей обработкиSОСl2/имидазолом и последующего окисления NaIO4/RuO2 получают целевой сульфимидат IV. Затем у полученного БОК-защищенного промежуточного продукта VIII с применением методов,известных из литературы (Greene, Т.W. и др., Protective Groups in Organic Synthesis; John WileySons,Inc.: New York, Chichester, Brisbane, Toronto, Singapore, 1991), таких как с использованием ТФК/СН 2 Сl2 или НСl, удаляют защитную группу и амин IIIBis выделяют из его соли обработкой основанием. Стадия А. трет-Бутиловый эфир (S)-[1-метил-2-(нафталин-2-илокси)этил]карбаминовой кислоты.-Нафтол (721 мг) растворяли в ДМФ (25 мл) и охлаждали до 0 С. По каплям в течение 15-минутного периода добавляли трет-бутилата калия (1M в ТГФ, 6,0 мл) и смесь перемешивали в течение 30 мин. Одной порцией добавляли трет-бутилового эфира (S)-4-метил-2,2-диоксо[1,2,3]оксатиазолидин-3 карбоновой кислоты (IV, 1,42 г) и перемешивание продолжали в течение 3 ч. Реакционную смесь выливали в 1 М NH4Cl и экстрагировали диэтиловым эфиром. Органическую фазу промывали 1 М NH4Cl и рассолом, сушили над Na2SO4 и выпаривали с получением желтого твердого продукта. Сырой продукт очищали экспресс-хроматографией (этилацетат/гексаны 1:9) с получением целевого продукта в виде бесцветного твердого веществ (1,5 г). МС (ISP): 324,3 (MNa+), 302,3 (МН+). 1 Н-ЯМР (CDCl3): 1,38 (d, 3 Н), 1,46 (s, 9H), 4,00-4,20 (m, 3H), 4,82 (широкий s, 1 Н), 7,14 (m, 2 Н), 7,34(m, 1 Н), 7,44 (m, 1 Н), 7,74 (m, 3 Н). Стадия Б. (S)-1-Метил-2-(нафталин-2-илокси)этиламин. Удаление защитной группы БОК у материала, полученного на предыдущей стадии (610 мг), осуществляли с применением метода с ТФК/СН 2 Сl2 так, как изложено в примере 4, стадия Б. Бесцветное твердое вещество, 268 мг. МС (ISP): 202,2 (МН+). 1 Н-ЯМР (CDCl3): 1,21 (d, 3 Н), 1,53 (широкий s, 2H), 3,41 (m, 1H), 3,80 (dd, 1 Н), 3,99 (dd, 1 Н), 7,107,20 (m, 2 Н), 7,33 (t, 1H), 7,43 (t, 1H), 7,70-7,80 (m, 3 Н). Стадия В. (2S)-1-[(S)-1-Метил-2-(нафталин-2-илокси)этиламино]ацетилпирролидин-2-карбонитрил. Указанное в заглавии соединение получали из (S)-1-метил-2-(нафталин-2-илокси)этиламина (139 мг) и соединения IIВ (50 мг) в соответствии с методом, в общих чертах представленным в примере 1. В результате экспресс-хроматографии выделяли вещество в виде бесцветного стекла (75 мг). МС (ISP): 360,2 (MNa+), 338,2 (МН+). 1 Н-ЯМР (CDCl3): 1,24 (d, 3 Н), 1,85 (широкий s, 1H), 2,00-2,40 (m, 4H), 3,21 (m, 1 Н), 3,40-3,80 (m,4 Н), 4,00 (m, 2 Н), 4,77 (m, 1 Н), 7,10-7,20 (m, 2 Н), 7,33 (t, 1 Н), 7,43 (t, 1H), 7,70-7,80 (m, 3 Н) (+ оптически активный изомер). Пример 26. (2S)-1-([2-(Хинолин-6-илокси)этиламино]ацетилпирролидин-2-карбонитрил. Это соединение получали аналогично примеру 25, стадии с А по В, из 6-гидроксихинолина, третбутилового эфира 2,2-диоксо[1,2,3]оксатиазолидин-3-карбоновой кислоты и соединения IIВ со следующим изменением на стадии Б: аминовый промежуточный продукт, полученный на этой стадии, был очень водорастворимым, и не мог быть выделен экстракцией. Поэтому водную фазу нейтрализовали твердым NаНСО 3 и под высоким вакуумом удаляли растворитель. Полученный твердый материал суспендировали в этаноле, перемешивали в течение 1 ч, а затем фильтровали. Фильтрат концентрировали под вакуумом и остаток очищали экспресс-хроматографией с получением свободного амина III, который использовали на конечной стадии сочетания. МС (ISP): 347,4 (MNa+), 325,4 (МН+). 1 Н-ЯМР (CDCl3): 1,75 (широкий s, 1H), 2,10-2,30 (m, 4H), 3,15 (m, 2H), 3,45 (m, 1 Н), 3,54 (s, 2 Н),3,63 (m, 1 Н), 4,21 (m, 2 Н), 4,76 (m, 1 Н), 7,08 (d, 1H), 7,33-7,41 (m, 2 Н), 7,99 (d, 1 Н), 8,04 (d, 1 Н), 8,77 (m,1 Н) (+ оптически активный изомер). Пример 27. (2S)-1-[2-(3-N,N-Диметиламинофенокси)этиламино]ацетилпирролидин-2-карбонитрил. Это соединение получали аналогично примеру 25, стадии с А по В, из 3-N,N-диметиламинофенола,трет-бутилового эфира 2,2-диоксо[1,2,3]оксатиазолидин-3-карбоновой кислоты и соединения IIВ. Для синтеза этого соединения в соответствии с приведенной выше общей схемой требуется получение соответствующего аминового предшественника IIIС. Замещенный ароматический бромид или иодидIX при низкой температуре (от -100 до 0 С) обрабатывают BuLi в инертном растворителе, таком как ТГФ. Затем получаемые таким образом литиированные материалы дополнительно обрабатывают сульфимидатом IV и получают БОК-защищенный промежуточный продукт X. Далее с применением методов,известных из литературы (Greene, T.W. и др. Protective Groups in Organic Synthesis; John WileySons,Inc.: New York, Chichester, Brisbane, Toronto, Singapore, 1991), таких как с использованием ТФК/СН 2 Сl2 или НСl, у соединения X удаляют защитную группу и амин общей формулы IIIС выделяют из его соли обработкой основанием. Стадия А. трет-Бутиловый эфир (S)-[2-(4-N,N-диметиламинофенил)-1-метилэтил]карбаминовой кислоты. 4-Бром-N,N-диметиланилин (1,0 г) растворяли в сухом ТГФ (17 мл) и на бане из сухого льда/ацетона охлаждали до -78. С помощью шприца по каплям добавляли BuLi (1,6 М в гексанах, 3,75 мл) и после добавления отмечали наличие бесцветного осадка. Смесь перемешивали в течение 20 мин и затем одной порцией добавляли трет-бутилового эфира (S)-4-метил-2,2-диоксо[1,2,3]оксатиазолидин-3-карбоновой кислоты (1,54 г). Суспензию перемешивали при -78C в течение 30 мин, а затем удаляли избыток твердого, сухого льда и в течение 60-минутного периода смеси давали нагреться до -30 С. Суспензия постепенно осветлялась с образованием слегка мутного желтого раствора. Реакцию гасили добавлением насыщенного раствора NH4Cl и смесь экстрагировали CH2Cl2 (густая эмульсия). Органический слой промывали рассолом (эмульсия) и сушили над Na2SO4. Постепенно органический слой становился темноголубым. Под вакуумом удаляли растворитель и остаток очищали экспресс-хроматографией (CH2Cl2 и затем СН 2 Сl2/МеОН 95:5) с получением указанного в заглавии соединения в виде светло-коричневого твердого вещества (563 мг). МС (ISP): 301,3 (MNa+), 279,2 (МН+). 1 Н-ЯМР (CDCl3): 1,06 (d, 3 Н), 1,43 (s, 9H), 2,56 (dd, 1H), 2,74 (dd, 1H), 2,92 (s, 6H), 4,84 (широкий s,1H), 4,37 (широкий s, 1H), 6,69 (d, 2H), 7,04 (d, 2H). Стадия Б. (S)-2-(4-N,N-Диметиламинофенил)-1-метилэтиламин. Удаление защитной группы БОК у соединения, полученного на предыдущей стадии (150 мг), осуществляли в соответствии с примером 4, стадия Б, с использованием ТФК/СН 2Cl2 (10 мл). Бесцветное твердое вещество: 75 мг.MC (ISP): 179,1 (МН+). 1 Н-ЯМР (CDCl3): 1,05 (d, 3H), 1,32 (широкий s, 2H), 2,40 (dd, 1H), 2,63 (dd, 1 Н), 2,91 (s, 6H), 3,09 (m,1H), 6,70 (d, 2H), 7,06 (d, 2H). Стадия В. (2S)-1-[(1S)-2-(4-N,N-Диметиламинофенил)-1-метилэтиламино]ацетилпирролидин-2 карбонитрил. Указанное в заглавии соединение получали из (S)-2-(4-N,N-диметиламинофенил)-1-метилэтиламина (124 мг) и соединения IIВ (50 мг) в соответствии с методом, в общих чертах представленным в примере 1. В результате экспресс-хроматографии выделяли бесцветный твердый продукт (67 мг). МС (ISP): 337,2 (MNa+), 315,3 (МН+). 1 Н-ЯМР (CDCl3): 1,06 (d, 3 Н), 2,08-2,30 (m, 5H), 2,50-2,68 (m, 2H), 2,86 (m, 1 Н), 2,91 (s, 6 Н), 3,283,60 (m, 4 Н), 4,74 (m, 1 Н), 6,69 (d, 2H), 7,06 (d, 2H). Пример 29. (2S)-1-[(1R)-2-(4-N,N-Диметиламинофенил)-1-метилэтиламино]ацетилпирролидин-2 карбонитрил. Это соединение в виде бесцветного твердого продукта получали аналогично примеру 28, стадии с А по В, из 4-бром-N,N-диметиланилина, трет-бутилового эфира (R)-4-метил-2,2-диоксо[1,2,3]оксатиазолидин-3-карбоновой кислоты и соединения IIВ. МС (ISP): 337,3 (MNa+), 315,4 (МН+). 1 Н-ЯМР (CDCl3): 1,06 (d, 3H), 1,15 (очень широкий s, 1H), 2,08-2,30 (m, 4H), 2,53 (dd, 1H), 2,60 (dd,1H), 2,87 (m, 1H), 2,91 (s, 6H), 3,30-3,50 (m, 4H), 4,74 (m, 1H), 6,69 (d, 2H), 7,06 (d, 2H) (+ оптически активный изомер).- 28007968 Пример 30. (2S)-1-[(1S)-2-(3-N,N-Диметиламинофенил)-1-метилэтиламино]ацетилпирролидин-2 карбонитрил. Это соединение получали аналогично примеру 28, стадии с А по В, из 3-бром-N,N-диметиланилина,трет-бутилового эфира (S)-4-метил-2,2-диоксо[1,2,3]оксатиазолидин-3-карбоновой кислоты и соединения Для синтеза этого соединения требуется получение соответствующего аминового предшественникаIIID в три стадии, начиная, в соответствии с представленной выше общей схемой, с этанольного производного XI. В результате реакции соединения XI с I) метансульфонилхлоридом, II) азидом натрия и последующего восстановления азидного производного XII с использованием либо трифенилфосфина/воды,либо водорода в присутствии палладия/угля амин IIID образуется в виде свободного основания или его соли. Исходные этанольные производные известны или могут быть получены из амидов или тиоамидов аналогично методам, описанным в WO 00/08002 или Collins, J.L. и др. в J.Med.Chem. 1998, 41, 5037-5054. Стадия А. 4-(2-Азидоэтил)-5-метил-2-фенилоксазол. 2-(5-Метил-2-фенилоксазол-4-ил)этанол [CAS 103788-65-4, технически доступен] (2,1 г) и ДИПЭА(2,6 мл) растворяли в CH2Cl2 и смесь охлаждали до 0 С. Затем добавляли метансульфонилхлорида (0,85 мл) и перемешивание продолжали при 0 С в течение 4 ч. После разбавления CH2Cl2 реакционную смесь промывали водой и рассолом и органический слой сушили MgSO4. Фильтрованием и выпариванием растворителя получали остаток (2,81 г), который повторно растворяли в ДМФ (20 мл). Добавляли азида натрия (0,78 г) и реакционную смесь нагревали до 60 С в течение 4 ч. Затем добавляли воды и образовавшуюся смесь три раза экстрагировали этилацетатом. Объединенные экстракты промывали водой и рассолом и сушили MgSO4. После фильтрования и выпаривания растворителя остаток очищали хроматографией (гексан/этилацетат 1:1) с получением целевого продукта в виде светло-желтого масла (2,2 г).MS (EI): 228,1 (М+). 1 Н-ЯМР (ДМСО-d6): 2,37 (s, 3H), 2,77 (t, 2H), 3,59 (t, 2H), 7,51 (m, 3H), 7,92 (m, 2 Н). Стадия Б. 4-(2-Аминоэтил)-5-метил-2-фенилоксазол. Азидное производное, полученное в соответствии со стадией А (5,25 г), растворяли в смеси МеОН(200 мл) и конц.НCl (20 мл). Затем добавляли каталитически эффективное количество 10%-ного палладия/угля и реакционный сосуд заполняли водородом. После полного потребления исходного материала(как показывали данные ТСХ) катализатор отфильтровывали и из фильтрата удаляли большую часть МеОН. Оставшуюся смесь разбавляли водой, промывали этилацетатом, а затем добавлением твердого карбоната натрия рН водной фазы доводили до 10. Водную фазу 3 раза экстрагировали этилацетатом и объединенные органические слои промывали рассолом и сушили над MgSO4. Фильтрованием и выпариванием растворителя указанное в заглавии соединение получали (4,6 г) в виде коричневого твердого вещества. 1 Н-ЯМР (CDCl3): 1,39 (широкий s, 2H+H2O), 2,35 (s, 3H), 2,63 (t, 2H), 3,03 (t, 2 Н), 7,42 (m, 3 Н), 7,99(m, 2 Н). Стадия В. (2S)-1-[2-(5-Метил-2-фенилоксазол-4-ил)этиламино]ацетилпирролидин-2-карбонитрил. Указанное в заглавии соединение получали из аминового производного, полученного в соответствии со стадией Б, (2,6 г) и соединения IIА (0,74 г) в соответствии с методом, в общих чертах представленным в примере 1. Заключительной хроматографией (этилацетат/МеОН 2:1) продукт получали в виде светло-желтого масла (1,1 г). МС (ISP): 339,3 (МН+). 1 Н-ЯМР (ДМСО-d6): 2,00 (m, 2H), 2,10 (m, 3 Н), 2,34 (s, 3H), 2,60 (t, 2H), 2,80 (t, 2 Н), 3,39 (m, 3 Н),3,53 (m, 1 Н), 4,74 (m, 1 Н), 7,49 (m, 3 Н), 7,90 (d, 2H) (+ оптически активный изомер). Пример 32. (2S)-1-(2-[2-(4-Фторфенил)-5-метилоксазол-4-ил]этиламиноацетил)пирролидин-2-карбонитрил. Это соединение получали аналогично примеру 31, стадии с А по В, начиная с 2-[2-(4-фторфенил)-5 метилоксазол-4-ил]этанола [CAS 196810-30-7]. Его выделяли в виде светло-коричневого масла. МС (ISP): 357,4 (МН+). Н-ЯМР (ДМСО-d6): 2,00 (m, 2H), 2,13 (m, 3 Н), 2,33 (s, 3 Н), 2,59 (t, 2H), 2,79 (t, 2 Н), 3,38 (m, 3 Н),3,55 (m, 1H), 4,73 (dd, 1H), 7,34 (t, 2H), 7,94 (dd, 2H) (+ оптически активный изомер). Пример 33. (2S)-1-2-[2-(4-Бензилоксифенил)-5-метилоксазол-4-ил]этиламиноацетил)пирролидин 2-карбонитрил. Это соединение получали аналогично примеру 31, начиная с 2-[2-(4-бензилоксифенил)-5-метилоксазол-4-ил]этанола. Исходный материал получали из 4-бензилоксибензамида [CAS 56442-43-4, технически доступен] и 4-бром-3-оксопентаноата так, как изложено для случая 4-фторбензамида в работе Collins,J.L. и др. в J. Med. Chem. 1998, 41, 5037-5054. Стадии А и В осуществляли так, как в общих чертах представлено в примере 31, но превращение азида в амин на стадии Б проводили по другому варианту. В раствор 4-(2-азидоэтил)-2-(4-бензилоксифенил)-5-метилоксазола (660 мг) в ТГФ (10 мл) добавляли воды (0,3 мл) и трифенилфосфина (570 мг). Реакционную смесь перемешивали в течение ночи при КТ. Затем растворитель удаляли и остаток очищали хроматографией (СН 2 С 2/МеОН 4:1) с получением 2-[2(4-бензилоксифенил)-5-метилоксазол-4-ил]этиламина (380 мг) в виде белого твердого вещества. МС (ISP): 309,0 (МН+). Н-ЯМР (ДМСО-d6): 1,49 (широкий s, 2 Н), 2,31 (s, 3 Н), 2,47 (m, 2H), 2,77 (t, 2 Н), 5,16 (s, 2H), 7,12 (d,2H), 7,36-7,49 (m, 5H), 7,83 (d, 2H). После стадии В указанное в заглавии соединение получали в виде светло-коричневого масла. МС (ISP): 446,2 (МН+). 1 Н-ЯМР (ДМСО-d6): 1,99 (m, 2H), 2,12 (m, 3 Н), 2,31 (s, 3 Н), 2,57 (t, 2H), 2,78 (t, 2 Н), 3,38 (m, 3 Н),3,55 (m, 1 Н), 4,73 (dd, 1H), 5,17 (s, 2H), 7,12 (d, 2H), 7,36-7,49 (m, 5 Н), 7,83 (d, 2H) (+ оптически активный изомер). Пример 34. (2S)-1-(2-[2-(2-Этокси-4-фторфенил)-5-метилоксазол-4-ил]этиламиноацетил)пирролидин-2-карбонитрил. Это соединение получали аналогично примеру 31, начиная с 2-[2-(2-этокси-4-фторфенил)-5-метилоксазол-4-ил]этанола. Исходный материал получали из 4-фтор-2-гидроксибензамида [СAS 1643-77-2] реакцией с этилбромидом в присутствии основания аналогично методу, описанному в работе Freedman, J. и др. в J. Heterocycl. Chem. 1990, 27, 343-6, и затем реакцией с 4-бром-3-оксопентаноатом так, как изложено для случая 4-фторбензамида в работе Collins, J.L. и др. в J. Med. Chem. 1998, 41, 5037-5054. Осуществлением стадий с А по В указанное в заглавии соединение выделяли в виде светло-коричневого масла. МС (ISP): 402,1 (МН+). 1 Н-ЯМР (ДМСО-d6): 1,35 (t, 3 Н), 2,00 (m, 2 Н), 2,12 (m, 2 Н), 2,29 (s, 3 Н), 2,58 (t, 2 Н), 2,76 (t, 2 Н), 3,37(m, 3 Н), 3,57 (m, 1 Н), 4,13 (q, 2H), 4,73 (dd, 1H), 6,86 (dt, 1H), 7,06 (dd, 1H), 7,78 (dd, 1H) (+ оптически активный изомер). Пример 35. (2S)-1-(2-[2-(4-Хлорфенил)-5-метилоксазол-4-ил]этиламиноацетил)пирролидин-2-карбонитрил. Это соединение получали аналогично примеру 31, начиная с 2-[2-(4-хлорфенил)-5-метилоксазол-4 ил]этанола. Исходный материал получали из 4-хлорбензамида и 4-бром-3-оксопентаноата так, как изложено для случая 4-фторбензамида в работе Collins, J.L. и др. в J. Med. Chem. 1998, 41, 5037-5054. Стадии А и В осуществляли так, как в общих чертах представлено в примере 31, стадию Б осуществляли в соответствии с примером 33. Указанное в заглавии соединение выделяли в виде светлокоричневого масла. Для синтеза этого соединения требуется получение соответствующего аминового предшественникаIIIЕ. Возможный путь получения соединения IIIЕ представлен на общей схеме выше. В соответствии с этой схемой дибромпиридиновое или пиримидиновое производное XIII обрабатывают соответствующим 1,2-диаминоэтаном. В дальнейшем продукт IIIЕ может быть получен превращением соединения XIV с использованием соответствующего фенильного производного в реакции типа реакции Сузуки. Стадия А. N1-(5-Бромпиридин-2-ил)-2-метилпропан-1,2-диамин. Раствор 2,5-дибромпиридина (1,7 г) и пиридина (0,75 мл) в 1,2-диамино-2-метилпропане (8,5 мл)
МПК / Метки
МПК: A61K 31/437, A61K 31/428, C07D 403/12, A61K 31/4025, A61K 31/401, A61K 31/4155, C07D 207/16, A61K 31/4178, A61K 31/427, A61K 31/454, A61K 31/416
Метки: ингибиторов, производные, качестве, n-замещённые, дипептидилпептидазы, пирролидина
Код ссылки
<a href="https://eas.patents.su/30-7968-n-zameshhyonnye-proizvodnye-pirrolidina-v-kachestve-ingibitorov-dipeptidilpeptidazy.html" rel="bookmark" title="База патентов Евразийского Союза">N-замещённые производные пирролидина в качестве ингибиторов дипептидилпептидазы</a>
Предыдущий патент: Защита, восстановление и усиление эритропоэтинреактивных клеток, тканей и органов
Следующий патент: 3-замещённые пиразолы с инсектицидными и акарицидными свойствами
Случайный патент: Способ утилизации попутного нефтяного газа