Пирролбензодиазепиновые соединения, их конъюгаты, фармацевтические композиции, содержащие указанные конъюгаты, и применение указанных конъюгатов
Номер патента: 24730
Опубликовано: 31.10.2016
Авторы: Мастерсон Люк, Ховард Филип Уилсон, Полсон Эндрю, Спенсер Сьюзен Д., Полакис Пол, Тибергьен Арно, Рааб Хельга E., Ганзнер Дженет Л., Флайгэр Джон А.
Формула / Реферат
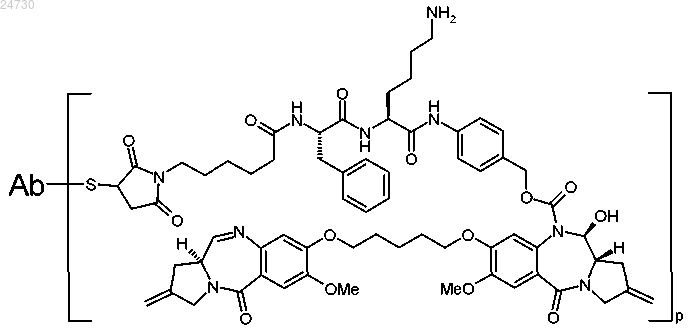
1. Конъюгат формулы (АВ) или (АС)
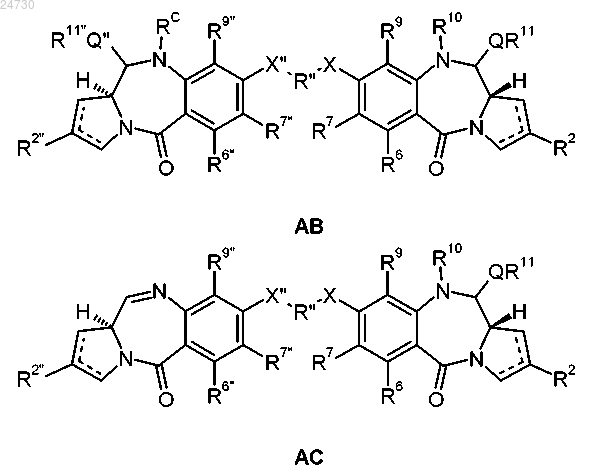
и его соли и сольваты, где
пунктирные линии обозначают необязательное наличие двойной связи между С1 и С2 или С2 и С3;
R2 независимо выбран из Н, ОН, =O, =СН2, CN, R, OR, =CH-RD, =C(RD)2, O-SO2-R, CO2R, COR, галогена и дигалогена;
где RD независимо выбран из R, CO2R, COR, CHO, CO2H и галогена;
R6 и R9 независимо выбраны из Н, R, ОН, OR, SH, SR, NH2, NHR, NRR', NO2, Ma3Sn и галогена;
R7 независимо выбран из Н, R, ОН, OR, SH, SR, NH2, NHR, NRR', NO2, Me3Sn и галогена;
R10 представляет собой линкер, соединенный со связывающимся с клетками агентом, выбранным из антитела, фрагмента антитела, который содержит по меньшей мере один сайт связывания, и циклического полипептида;
Q независимо выбран из О, S и NH;
R11 представляет собой Н или R или, если Q представляет собой О, SO3M, где М представляет собой катион металла и обозначает Na+;
каждый R и R' независимо выбран из необязательно замещенных C1-12 алкильной группы, С3-20 гетероциклильной группы, представляющей собой моновалентный фрагмент, полученный путем удаления атома водорода от атома кольца гетероциклического соединения, содержащего от 3 до 20 атомов в кольце, от 1 до 10 из которых представляют собой гетероатомы кольца, выбранные из О, S и N, и С5-20 арильной группы, и необязательно в отношении группы NRR'R и R' вместе с атомом азота, к которому они присоединены, образуют необязательно замещенное 4-, 5-, 6- или 7-членное гетероциклическое кольцо, в котором гетероатомы выбраны из О, S и N;
R" представляет собой С3-12 алкиленовую группу, углеводородная цепь которой может прерываться одним или более гетероатомами О, S, N(H) или NMe и/или ароматическими кольцами, выбранными из бензольного или пиридинового кольца;
каждый X представляет собой О, S или N(H); и
где R2", R6", R7", R9", X", Q" и R11" являются такими, как определено для R2, R6, R7, R9, X, Q и R11, соответственно, и RC представляет собой кэпирующую группу.
2. Конъюгат по п.1, где R10 представляет собой группу
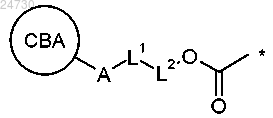
где звездочка обозначает место присоединения к положению N10, СВА представляет собой связывающийся с клетками агент, L1 представляет собой способный к расщеплению линкер, А представляет собой связывающую группу, соединяющую L1 со связывающимся с клетками агентом, L2 представляет собой ковалентную связь или вместе с -ОС(=О)- образует саморасщепляющийся линкер.
3. Конъюгат по п.2, где L1 способен к расщеплению под действием ферментов.
4. Конъюгат по п.3, где L1 содержит дипептид, а группа -Х1-Х2- в дипептиде -NH-X1-X2-CO- выбрана из
-Phe-Lys-,
-Val-Ala-,
-Val-Lys-,
-Ala-Lys-,
-Val-Cit-,
-Phe-Cit-,
-Leu-Cit-,
-Ile-Cit-,
-Phe-Arg-,
-Trp-Cit-.
5. Конъюгат по п.3, где группа -X1-Х2- в дипептиде -NH-X1-X2-CO- представляет собой -Phe-Lys-, -Val-Ala- или -Val-Cit-.
6. Конъюгат по любому из пп.3 или 4, где группа Х2-СО- связана с L2 и где группа NH-X1- связана с А.
7. Конъюгат по любому из пп.4-6, где L2 вместе с ОС(=О) образует саморасщепляющийся линкер.
8. Конъюгат по п.7, где С(=О)О и L2 вместе образуют группу
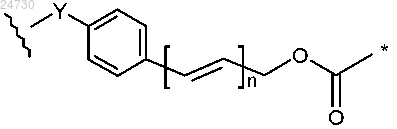
где звездочка обозначает место присоединения к положению N10, волнистая линия обозначает место присоединения к линкеру L1, Y представляет собой NH, О, C(=O)NH или С(=О)О и n равен от 0 до 3.
9. Конъюгат по п.8, где Y представляет собой NH, и n равен 0.
10. Конъюгат по п.2, где L1 и L2 вместе с -ОС(=О)- образуют группу, выбранную из
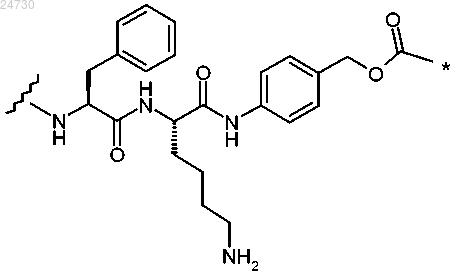
или
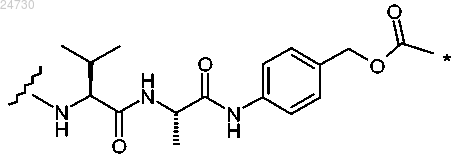
где звездочка обозначает место присоединения к положению N10 и волнистая линия обозначает место присоединения к А.
11. Конъюгат по любому из пп.2-10, где А представляет собой
(i)
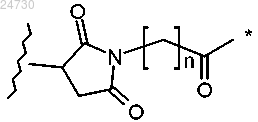
где звездочка обозначает место присоединения к L1, волнистая линия обозначает место присоединения к связывающемуся с клетками агенту и n равен от 0 до 6; или
(ii)
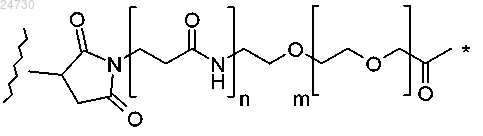
где звездочка обозначает место присоединения к L1, волнистая линия обозначает место присоединения к связывающемуся с клетками агенту, n равен 0 или 1 и m равен от 0 до 30.
12. Конъюгат по любому из пп.2-11, где связывающийся с клетками агент соединен с А через тиоэфирную связь, образованную между тиоловым остатком цистеина в связывающемся с клетками агенте и малеимидной группой в А.
13. Конъюгат по любому из пп.1-12, где связывающийся с клетками агент в составе R10 представляет собой антитело или его активный фрагмент.
14. Конъюгат по п.13, где антитело или фрагмент антитела представляет собой антитело или фрагмент антитела к опухолеассоциированному антигену.
15. Конъюгат по любому из пп.1-14, где R9 независимо представляет собой Н и R6 независимо представляет собой Н.
16. Конъюгат по любому из пп.1-15, где R7 независимо представляет собой ОМе.
17. Конъюгат по любому из пп.1-16, где X представляет собой О.
18. Конъюгат по любому из пп.1-17, где R11 представляет собой Н.
19. Конъюгат по любому из пп.1-18, где пунктирные линии обозначают необязательное наличие двойной связи между С2 и С3.
20. Конъюгат по любому из пп.1-19, где R2 независимо выбран из Н, =O, =CH2, R, =CH-RD и =C(RD)2.
21. Конъюгат по п.20, где R2 независимо представляет собой =CH2.
22. Конъюгат по п.20, где R2 независимо представляет собой необязательно замещенный С5-20 арил.
23. Конъюгат по любому из пп.1-22, где R" представляет собой С3 алкиленовую группу или C5 алкиленовую группу.
24. Конъюгат по любому из пп.1-23, где RC способен удаляться из положения N10 с образованием N10-C11 иминной связи.
25. Конъюгат по п.24, где RC представляет собой карбаматную защитную группу, выбранную из
аллилоксикарбонила (Alloc);
9N-флуорен-9-илметоксикарбонила (Fmoc);
ди-трет-бутилдикарбоната (Boc);
2,2,2-трихлорэтоксикарбонилхлорида (Troc);
2-(триметилсилил)этоксикарбонила (Теос);
2-(фенилсульфонил)этоксикарбонила (Psec);
бензилоксикарбонила (Cbz);
n-нитробензилкарбамата (PNZ).
26. Конъюгат по п.24, где RC представляет собой группу
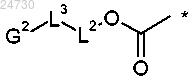
где звездочка обозначает место присоединения к положению N10, G2 представляет собой концевую группу, L3 представляет собой ковалентную связь или способный к расщеплению линкер L1, L2 представляет собой ковалентную связь или вместе с ОС(=О) образует саморасщепляющийся линкер.
27. Конъюгат по п.26, где L3 представляет собой способный к расщеплению линкер L1 по любому из пп.3-6.
28. Конъюгат по п.26 или 27, где L2 вместе с ОС(=О) образует саморасщепляющийся линкер, и указанный саморасщепляющийся линкер является таким, как определено в любом из пп.8 или 9.
29. Конъюгат по любому из пп.26-28, где G2 представляет собой Ас или Moc или представляет собой карбаматную защитную группу, выбранную из
аллилоксикарбонила (Alloc);
9N-флуорен-9-илметоксикарбонила (Fmoc);
ди-трет-бутилдикарбоната (Boc);
2,2,2-трихлорэтоксикарбонилхлорида (Troc);
2-(триметилсилил)этоксикарбонила (Теос);
2-(фенилсульфонил)этоксикарбонила (Psec);
бензилоксикарбонила (Cbz);
n-нитробензилкарбамата (PNZ).
30. Конъюгат по любому из пп.1-29 для применения для лечения пролиферативного заболевания у субъекта, где указанное заболевание представляет собой рак.
31. Конъюгат, имеющий формулу
Ab-(L-D)p,
где Ab представляет собой антитело, присоединенное с помощью линкерного фрагмента (L) к пирролбензодиазепиновому (PBD) фрагменту лекарственного средства (D) формулы (АВ) или (АС), и р равен целому числу от 1 до примерно 8, где линкерный фрагмент (L) и PBD фрагмент лекарственного средства (D) формулы (АВ) или (АС) определены в любом из пп.1-29.
32. Конъюгат по п.31, где Ab представляет собой антитело, которое связывается с одним или более опухолеассоциированными антигенами или рецепторами клеточной поверхности, выбранными из (1)-(36):
(1) BMPR1B (рецептор костного морфогенетического белка типа IB);
(2) E16 (LAT1, SLC7A5);
(3) STEAP1 (антиген эпителиальных клеток предстательной железы с шестью трансмембранными сегментами);
(4) 0772Р (СА125, MUC16);
(5) MPF (MPF, MSLN, SMR, мегакариоцит-потенциирующий фактор, мезотелин);
(6) Napi3b (NAPI-3B, NPTIIb, SLC34A2, семейство носителей растворенных веществ 34 (фосфат натрия), член 2, тип II, натрий-зависимый фосфатный транспортер 3b);
(7) Sema 5b (FLJ10372, KIAA1445, Mm.42015, SEMA5B, SEMAG, семафорин 5b Hlog, sema-домен, содержащий семь тромбоспондиновых повторов (1 типа и подобный 1 типу), трансмембранный домен (ТМ) и короткий цитоплазматический домен, (семафорин) 5В);
(8) PSCA hlg (2700050C12Rik, C530008O16Rik, RIKEN кДНК 2700050С12, RIKEN кДНК 2700050С12 ген);
(9) ETBR (рецептор эндотелина типа В);
(10) MSG783 (RNF124, гипотетический белок FLJ20315);
(11) STEAP2 (HGNC-8639, IPCA-1, PCANAP1, STAMP1, STEAP2, STMP, ассоциированный с раком предстательной железы ген 1, ассоциированный с раком предстательной железы белок 1, антиген эпителиальных клеток предстательной железы с шестью трансмембранными сегментами 2, белок предстательной железы с шестью трансмембранными сегментами);
(12) TrpM4 (BR22450, FLJ20041, TRPM4, TRPM4B, катионный канал транзиторного рецепторного потенциала, подсемейство М, член 4);
(13) CRIPTO (CR, CR1, CRGF, CRIPTO, TDGF1, фактор роста тератокарциномного происхождения);
(14) CD21 (CR2 (рецептор комплемента 2) или C3DR (C3d/рецептор вируса Эпштейна-Барра) или Hs 73792);
(15) CD79b (CD79B, CD79β, IGb (иммуноглобулин-ассоциированный бета), В29);
(16) FcRH2 (IFGP4, IRTA4, SPAP1A (содержащий SH2-домен фосфатазный якорный белок 1a), SPAP1B, SPAP1C);
(17) HER2;
(18) NCA;
(19) MDP;
(20) IL20Rα;
(21) Бревикан;
(22) EphB2R;
(23) ASLG659;
(24) PSCA;
(25) GEDA;
(26) BAFF-R (рецептор фактора активации В-клеток, рецептор BLyS 3, BR3);
(27) CD22 (В-клеточный рецептор CD22-B изоформы);
(28) CD79а (CD79A, CD79α, иммуноглобулин-ассоциированный альфа);
(29) CXCR5 (Рецептор лимфомы Беркитта1);
(30) HLA-DOB (бета-субъединица молекулы МНС II класса (Ia антиген));
(31) Р2Х5 (пуринергический рецептор Р2Х, лиганд-зависимый ионный канал 5);
(32) CD72 (антиген В-клеточной дифференцировки CD72, Lyb-2);
(33) LY64 (антиген лимфоцитов 64 (RP105), мембранный белок семейства лейцин-богатых повторов (LRR) типа I);
(34) FcRH1 (подобный Fc-рецептору белок 1);
(35) IRTA2 (рецептор иммуноглобулинового суперсемейства, ассоциированный с транслокацией 2); и
(36) TENB2 (предполагаемый трансмембранный протеогликан).
33. Конъюгат по п.31, где Ab представляет собой сконструированное на основе цистеина антитело.
34. Конъюгат по п.31 или 32, где Ab представляет собой антитело, которое связывается с рецептором ErbB.
35. Конъюгат по п.34, где Ab представляет собой трастузумаб.
36. Конъюгат по п.31 или 32, где Ab представляет собой антитело к HER2, к Steap1 или к CD22.
37. Конъюгат по любому из пп.31-36, где р равен 1, 2, 3 или 4.
38. Конъюгат по любому из пп.31-37, имеющий формулу, выбранную из
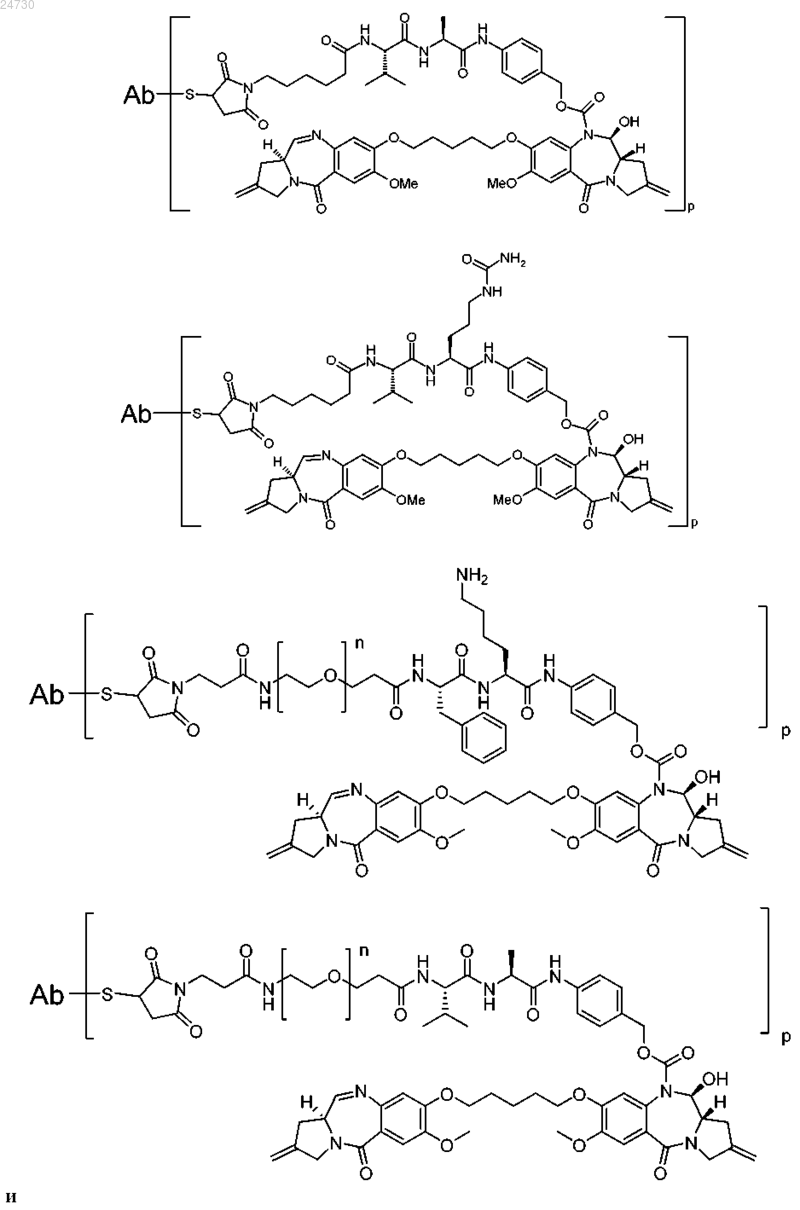
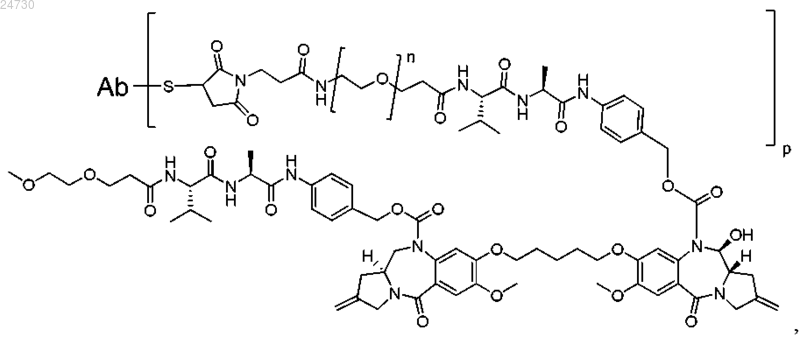
где n равен целому числу от 1 до 24.
39. Конъюгат по п.38, где n равен целому числу от 1 до 12.
40. Конъюгат по п.39, где n равен 4 или 8.
41. Композиция для лечения пролиферативных заболеваний, содержащая смесь соединений, представляющих собой конъюгаты антитело-лекарственное средство по любому из пп.31-39, где средняя нагрузка лекарственного средства на антитело в смеси соединений (среднее р), представляющих собой конъюгаты антитело-лекарственное средство, составляет от примерно 2 до примерно 5.
42. Фармацевтическая композиция для лечения пролиферативных заболеваний, содержащая конъюгат по любому из пп.1-40, фармацевтически приемлемый разбавитель, носитель или наполнитель.
43. Фармацевтическая композиция по п.42, дополнительно содержащая терапевтически эффективное количество химиотерапевтического агента.
44. Применение конъюгата по любому из пп.1-40 для получения лекарственного средства для лечения пролиферативного заболевания у субъекта.
45. Соединение формулы (ЕВ) или (ЕС)
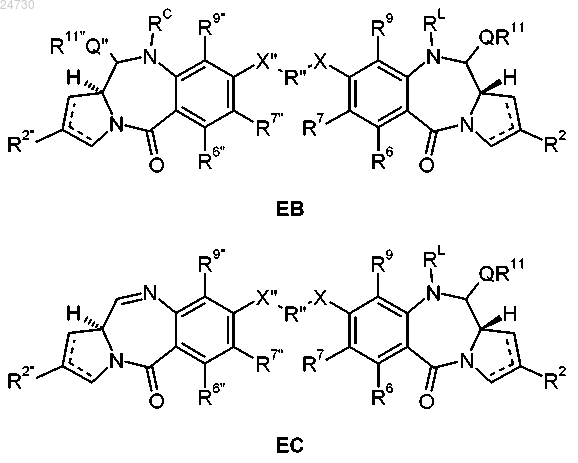
и его соли и сольваты, где
пунктирные линии обозначают необязательное наличие двойной связи между С1 и С2 или С2 и С3;
R2 независимо выбран из Н, ОН, =O, =СН2, CN, R, OR, =CH-RD, =C(RD)2, O-SO2-R, CO2R, COR, галогена и дигалогена;
где RD независимо выбран из R, CO2R, COR, CHO, CO2H и галогена;
R6 и R9 независимо выбраны из Н, R, ОН, OR, SH, SR, NH2, NHR, NRR', NO2, Ma3Sn и галогена;
R7 независимо выбран из Н, R, ОН, OR, SH, SR, NH2, NHR, NRR', NO2, Me3Sn и галогена;
RL представляет собой линкер для соединения со связывающимся с клетками агентом, выбранным из антитела, фрагмента антитела, который содержит по меньшей мере один сайт связывания, и циклического полипептида;
Q независимо выбран из О, S и NH;
R11 представляет собой Н или R или, если Q представляет собой О, R11 представляет собой SO3M, где М представляет собой катион металла и обозначает Na+;
каждый R и R' независимо выбран из необязательно замещенных C1-12 алкильной группы, С3-20 гетероциклильной группы, представляющей собой моновалентный фрагмент, полученный путем удаления атома водорода от атома гетероциклического соединения, содержащей от 3 до 20 атомов в кольце, из которых от 1 до 10 атомов кольца представляют собой гетероатомы, выбранные из О, S и N, и С5-20 арильной группы, и необязательно в отношении группы NRR' R и R' вместе с атомом азота, к которому они присоединены, образуют необязательно замещенное 4-, 5-, 6- или 7-членное гетероциклическое кольцо, в котором гетероатомы выбраны из О, и S и N;
R" представляет собой С3-12 алкиленовую группу, углеводородная цепь которой может прерываться одним или более гетероатомами О, S, N(H) или NMe и/или ароматическими кольцами, выбранными из бензольного или пиридинового кольца;
каждый X представляет собой О, S или N(H); и
где R2", R6", R7", R9", R11", Q" и X" являются такими, как определено для R2, R6, R7, R9, R11, Q и X, соответственно, и RC представляет собой кэпирующую группу.
46. Соединение по п.45, имеющее структуру
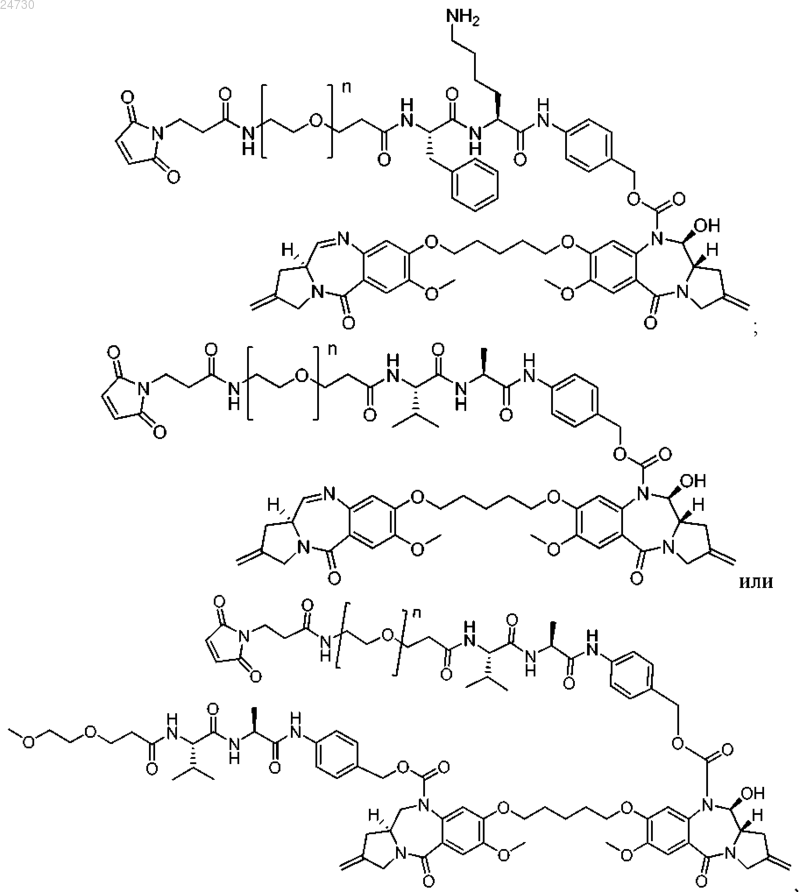
где n равен целому числу от 1 до 24.
47. Соединение по п.46, где n равен целому числу от 1 до 12.
48. Соединение по п.47, где n равен 4 или 8.
49. Соединение по п.45, выбранное из
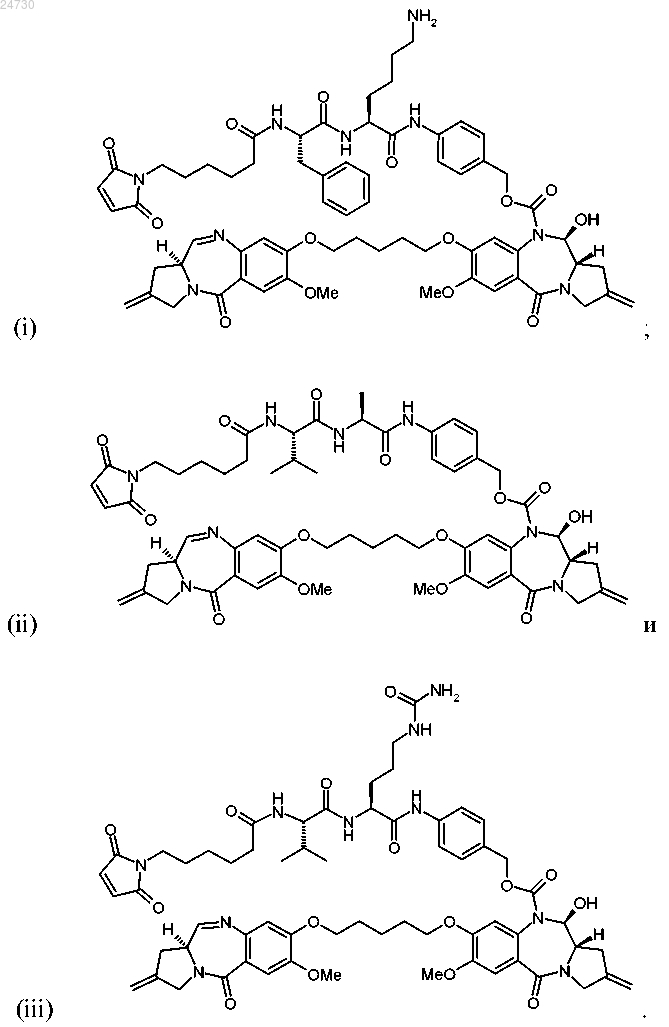
Текст
Описаны конъюгаты и соединения для создания конъюгатов, которые представляют собой PBD молекулы, связанные через положение N10, а также применение указанных конъюгатов для лечения пролиферативных заболеваний, включая рак. 024730 Настоящее изобретение относится к пирролбензодиазепинам (PBD), в частности пирролбензодиазепинам, содержащим лабильную защитную группу в положении N10, представляющую собой линкер к связывающемуся с клетками агенту. Уровень техники Пирролбензодиазепины Некоторые пирролбензодиазепины (PBD) способны распознавать конкретные последовательности ДНК и связываться с ними, при этом предпочтительная последовательность представляет собой PuGPu. Первый пирролбензодиазепиновый (PBD) противоопухолевый антибиотик, антрамицин, был открыт в 1965 г. (Leimgruber, et al., J. Am. Chem. Soc., 87, 5793-5795 (1965); Leimgruber, et al., J. Am. Chem. Soc.,87, 5791-5793 (1965. С тех пор был описан ряд природных PBD, и было разработано более 10 способов синтеза различных их аналогов (Thurston, et al., Chem. Rev. 1994, 433-465 (1994. Представители указанного семейства включают эббимицин (abbeymycin) (Hochlowski, et al., J. Antibiotics, 40, 145-148 (1987,чикамицин (chicamycin) (Konishi, et al., J. Antibiotics, 37, 200-206 (1984, DC-81 (патент Японии 58-180 487; Thurston, et al., Chem. Brit., 26, 767-772 (1990); Bose, et al., Tempahedron, 48, 751-758 (1992, мазетрамицин (mazethramycin) (Kuminoto, et al., J. Antibiotics, 33, 665-667 (1980, неотрамицины(tomamycin) (Arima, et al., J. Antibiotics, 25, 437-444 (1972. PBD имеют следующую общую структуру: Они различаются по числу, типу и положению заместителей, как в своих ароматических А-кольцах,так и в пиррольных С-кольцах, и по степени насыщения С-кольца. В положении N10-C11 В-кольца, которое представляет собой электрофильный центр, ответственный за алкилирование ДНК, находится либо имин (N=C), либо карбиноламин (NH-CH(OH, либо метиловый эфир карбиноламина (NH-CH(OMe. Все известные природные продукты имеют (S)-конфигурацию хирального центра С 11 а, что обеспечивает правозакрученную "твист"-форму если смотреть со стороны С-кольца в направлении А-кольца. Это придает им подходящую трехмерную форму для изоспиральности с малой бороздкой В-формы ДНК, что приводит к точному соответствию в сайте связывания (Kohn, In Antibiotics III. Springer-Verlag, New York,pp. 3-11 (1975); Hurley and Needham-VanDevanter, Acc. Chem. Res., 19, 230-237 (1986. Их способность образовывать аддукт в малой бороздке ДНК позволяет им препятствовать процессингу ДНК, обеспечивая возможность их применения в качестве противоопухолевых агентов. Авторы настоящего изобретения ранее в WO 2005/085251 описали димерные PBD соединения, содержащие арильные заместители в положении С 2, такие как Было показано, что указанные соединения являются высокоэффективными цитотоксическими агентами. Особыми преимуществами обладает пирролбензодиазепиновое соединение, описанное в источникеChem. 2001, 44, 1161-1174, как соединение 4 а. Указанное соединение, также известное как SJG-136, показано ниже Авторами настоящего изобретения ранее было показано, что PBD соединения можно использовать в качестве пролекарств с помощью введения в положение N10 защитной группы для азота, при этом защитная группа способна удаляться in vivo (WO 00/12507). Многие из указанных защитных групп представляют собой карбаматы и имеют, например, следующую структуру: где звездочкаобозначает место присоединения к атому N10 в PBD. Авторы настоящего изобретения также описали получение PBD соединений, содержащих защитную карбаматную группу при атоме азоте в положении N10 (WO 2005/023814). Защитные группы способны удаляться из положения N10 фрагмента PBD с образованием N10-C11 иминной связи. Описан ряд защитных групп, включая группы, которые могут отщепляться под действием ферментов. В WO 2007/085930 описано получение димерных PBD соединений, содержащих линкерные группы для присоединения к связывающемуся с клетками агенту, такому как антитело. Линкер присутствует в мостике, связывающем мономерные звенья PBD димера. Конъюгаты антитело-лекарственное средство Терапия с использованием антител применяется для направленного лечения пациентов, страдающих раком, иммунологическими и ангиогенными нарушениями (Carter, P. (2006) Nature Reviews Immunology 6:343-357). Применение конъюгатов антитело-лекарственное средство (ADC), т.е. иммуноконъюгатов, для местной доставки цитотоксических или цитостатических агентов, т.е. лекарственных средств для уничтожения или подавления опухолевых клеток при лечении рака, обеспечивает направленную доставку фрагмента лекарственного средства к опухоли и внутриклеточное накопление в ней, тогда как системное введение указанных неконъюгированных лекарственных агентов может проводить к неприемлемым уровням токсичности по отношению к здоровым клеткам наряду с опухолевыми клетками, которые предполагается уничтожить (Xie et al. (2006) Expert. Opin. Biol. Ther. 6(3):281-291; Kovtun et al. (2006)Immunother. 52:328-337; Syrigos and Epenetos (1999) Anticancer research 19:605-614). Таким образом, исследования направлены на получение препаратов с максимальной эффективностью при их минимальной токсичности. Попытки разработки и очистки ADC были сосредоточены на селективности моноклональных антител (mAb), а также на механизме действия лекарственного средства,свойствах связывания с лекарственным средством, отношении лекарственное средство/антитело (нагрузка) и высвобождения лекарственного средства (Junutula, et al., 2008b Nature Biotech., 26(8):925-932; Dornan et al. (2009) Blood 114(13):2721-2729; US 7521541; US 7723485; WO 2009/052249; McDonagh (2006)Chem. 48:1344-1358; Hamblett et al. (2004) Clin. Cancer res. 10:7063-7070). Фрагменты лекарственных средств могут оказывать свое цитотоксическое и цитостатическое действие по механизмам, включающим связывание тубулина, связывание ДНК или ингибирование топоизомеразы. Некоторые цитотоксические лекарственные средства склонны инактивироваться или становиться менее активными при конъюгировании с большими антителами или белковыми рецепторными лигандами. Авторы настоящего изобретения разработали новый подход к получению конъюгатов PBD со связывающимися с клетками агентами и, в частности, конъюгатов PBD с антителами. Краткое описание изобретения Согласно общему аспекту настоящего изобретения предложен конъюгат, содержащий PBD соединение, присоединенное через положение N10 к связывающемуся с клетками агенту с помощью линкера. Линкер представляет собой лабильный линкер и может представлять собой ферментативно-лабильный линкер. Связывающийся с клетками агент предпочтительно представляет собой антитело. Согласно одному варианту реализации изобретения конъюгат содержит связывающийся с клетками агент, соединенный со спейсером, при этом спейсер соединен с триггером, триггер соединен с саморасщепляющимся линкером, а саморасщепляющийся линкер связан с положением N10 PBD соединения. Согласно первому аспекту настоящего изобретения предложены новые соединения, представляющие собой конъюгаты, формулы (А) и их соли и сольваты, где пунктирные линии обозначают необязательное наличие двойной связи между С 1 и С 2 или С 2 и С 3;R2 независимо выбран из Н, ОН, =O, =СН 2, CN, R, OR, =CH-RD, =C(RD)2, O-SO2-R, CO2R и COR и необязательно дополнительно выбран из галогена или дигалогена;-2 024730 где RD независимо выбран из R, CO2R, COR, CHO, СО 2 Н и галогена;R6 и R9 независимо выбраны из Н, R, ОН, OR, SH, SR, NH2, NHR, NRR', NO2, Me3Sn и галогена;R7 независимо выбран из Н, R, ОН, OR, SH, SR, NH2, NHR, NRR', NO2, Me3Sn и галогена;R8 независимо выбран из Н, R, ОН, OR, SH, SR, NH2, NHR, NRR', NO2, Me3Sn и галогена;R10 представляет собой линкер, соединенный со связывающимся с клетками агентом;Q независимо выбран из О, S и NH;R11 представляет собой Н или R или, если Q представляет собой О, SO3M, где М представляет собой катион металла; каждый R и R' независимо выбран из необязательно замещенных C1-12 алкильной группы, C3-20 гетероциклильной группы, представляющей собой моновалентый фрагмент, полученный путем удаления атома водорода от атома кольца гетероциклического соединения, содержащего от 3 до 20 атомов в кольце, от 1 до 10 из которых представляют собой гетероатомы кольца, выбранные из О, S и N, и C5-20 арильной группы, и необязательно в отношении группы NRR' R и R' вместе с атомом азота, к которому они присоединены, образуют необязательно замещенное 4-, 5-, 6-или 7-членное гетероциклическое кольцо, в котором гетероатомы выбраны из О, S и N; или любая пара смежных групп из R6-R9 вместе образуют группу -О-(СН 2)p-О-, где р равен 1 или 2,или указанное соединение представляет собой димер, каждый мономер которого имеет формулу(А), или один мономер которого имеет формулу (А), а другой мономер имеет формулу (В) где R2, R6, R9, R7 и R8 являются такими, как определено для соединения формулы (А), и группы R7 или группы R8 каждого мономера вместе образуют димерный мостик, имеющий формулу -X-R"-X-, связывающий мономеры; где R" представляет собой С 3-12 алкиленовую группу, углеводородная цепь которой может прерываться одним или более гетероатомами и/или ароматическими кольцами, выбранными из бензольного или пиридинового кольца; и каждый X представляет собой О, S или N(H); или где указанное соединение представляет собой димер, каждый мономер которого имеет формулу(А), причем группа R10 в одном из мономеров представляет собой кэпирующую группу RC или представляет собой линкер, соединенный со связывающимся с клетками агентом. Во избежание неопределенности связывающийся с клетками агент представляет собой часть группы R10. Настоящее изобретение также относится к применению конъюгата для получения соединения формулы (С) в области-мишени и его соли и сольвата, где пунктирные линии обозначают необязательное наличие двойной связи между С 1 и С 2 или С 2 и С 3;R2 независимо выбран из Н, ОН, =O, =СН 2, CN, R, OR, =CH-RD, =C(RD)2, O-SO2-R, CO2R и COR и необязательно дополнительно выбран из галогена или дигалогена; где RD независимо выбран из R, CO2R, COR, CHO, СО 2 Н и галогена;R6 и R9 независимо выбраны из Н, R, ОН, OR, SH, SR, NH2, NHR, NRR', NO2, Ma3Sn и галогена;R7 независимо выбран из Н, R, ОН, OR, SH, SR, NH2, NHR, NRR', NO2, Me3Sn и галогена;R8 независимо выбран из Н, R, ОН, OR, SH, SR, NH2, NHR, NRR', NO2, Me3Sn и галогена;R и R' независимо выбраны из необязательно замещенных C1-12 алкильной группы, С 3-20 гетероциклильной группы, представляющей собой моновалентый фрагмент, полученный путем удаления атома водорода от атома кольца гетероциклического соединения, содержащего от 3 до 20 атомов в кольце, от 1 до 10 из которых представляют собой гетероатомы кольца, выбранные из О, S и N, и С 5-20 арильной групп, и необязательно в отношении группы NRR' R и R' вместе с атомом азота, к которому они присоединены, образуют необязательно замещенное 4-, 5-, 6-или 7-членное гетероциклическое кольцо, в котором гетероатомы выбраны из О, S и N; или любая пара смежных групп из R6-R9 вместе образуют группу -О-(СН 2)p-О-, где р равен 1 или 2,или указанное соединение представляет собой димер, каждый мономер которого имеет формулу(С), а группы R7 или группы R8 каждого мономера вместе образуют димерный мостик, имеющий форму-3 024730 лу -X-R"-X-, связывающий мономеры; где R" представляет собой C3-12 алкиленовую группу, углеводородная цепь которой может прерываться одним или более гетероатомами и/или ароматическими кольцами, выбранными из бензольного или пиридинового кольца; и каждый X представляет собой О, S или N(H). Настоящее изобретение также относится к применению конъюгата для получения соединения формулы (D) в области-мишени и его соли и сольвата, где пунктирные линии обозначают необязательное наличие двойной связи между С 1 и С 2 или С 2 и С 3;R2 независимо выбран из Н, ОН, =O, =СН 2, CN, R, OR, =CH-RD, =C(RD)2, O-SO2-R, CO2R и COR и необязательно дополнительно выбран из галогена или дигалогена; где RD независимо выбран из R, CO2R, COR, CHO, СО 2 Н и галогена;R6 и R9 независимо выбраны из Н, R, ОН, OR, SH, SR, NH2, NHR, NRR', NO2, Ma3Sn и галогена;R7 независимо выбран из Н, R, ОН, OR, SH, SR, NH2, NHR, NRR', NO2, Me3Sn и галогена;R8 независимо выбран из Н, R, ОН, OR, SH, SR, NH2, NHR, NRR', NO2, Me3Sn и галогена;Q независимо выбран из О, S и NH;R11 представляет собой Н или R или, если Q представляет собой О, SO3M, где М представляет собой катион металла; каждый R и R' независимо выбран из необязательно замещенных C1-12 алкильной группы, C3-20 гетероциклильной группы, представляющей собой моновалентый фрагмент, полученный путем удаления атома водорода от атома кольца гетероциклического соединения, содержащего от 3 до 20 атомов в кольце, от 1 до 10 из которых представляют собой гетероатомы кольца, выбранные из О, S и N, и C3-20 арильной групп, и необязательно в отношении группы NRR' R и R' вместе с атомом азота, к которому они присоединены, образуют необязательно замещенное 4-, 5-, 6-или 7-членное гетероциклическое кольцо, в котором гетероатомы выбраны из О, S и N; или любая пара смежных групп из R6-R9 вместе образуют группу -О-(СН 2)р-О-, где р равен 1 или 2; или указанное соединение представляет собой димер, каждый мономер которого имеет формулу(D), или один мономер которого имеет формулу (D), а другой мономер имеет формулу (С); и группы R7 или группы R8 каждого мономера вместе образуют димерный мостик, имеющий формулу -X-R"-X-, связывающий мономеры; где R" представляет собой C3-12 алкиленовую группу, углеводородная цепь которой может прерываться одним или более гетероатомами и/или ароматическими кольцами, выбранными из бензольного или пиридинового кольца; и каждый X представляет собой О, S или N(H); где мономерная единица формулы (С) является такой, как определено выше. Согласно настоящему изобретению также предложены соединения формулы (Е) для применения для получения соединений, представляющих собой конъюгаты согласно настоящему изобретению и их солей и сольватов, где пунктирные линии обозначают необязательное наличие двойной связи между С 1 и С 2 или С 2 и С 3;R2 независимо выбран из Н, ОН, =O, =СН 2, CN, R, OR, =CH-RD, =C(RD)2, O-SO2-R, CO2R и COR и необязательно дополнительно выбран из галогена или дигалогена; где RD независимо выбран из R, CO2R, COR, CHO, СО 2 Н и галогена;R6 и R9 независимо выбраны из Н, R, ОН, OR, SH, SR, NH2, NHR, NRR', NO2, Ma3Sn и галогена;R7 независимо выбран из Н, R, ОН, OR, SH, SR, NH2, NHR, NRR', NO2, Me3Sn и галогена;R8 независимо выбран из Н, R, ОН, OR, SH, SR, NH2, NHR, NRR', NO2, Me3Sn и галогена;RL представляет собой линкер для соединения со связывающимся с клетками агентом;Q независимо выбран из О, S и NH;-4 024730 катион металла; каждый R и R' независимо выбран из необязательно замещенной C1-12 алкильной группы, C3-20 гетероциклильной группы, представляющей собой моновалентый фрагмент, полученный путем удаления атома водорода от атома кольца гетероциклического соединения, содержащего от 3 до 20 атомов в кольце, от 1 до 10 из которых представляют собой гетероатомы кольца, выбранные из О, S и N, C3-20 гетероциклильной и C3-20 арильной группы, и необязательно, в отношении группы NRR', R и R' вместе с атомом азота, к которому они присоединены, образуют необязательно замещенное 4-, 5-, 6- или 7-членное гетероциклическое кольцо, в котором гетероатомы выбраны из О, S и N; или любая пара смежных групп из R6-R9 вместе образуют группу -О-(СН 2)p-О-, где р равен 1 или 2; или указанное соединение представляет собой димер, каждый мономер которого имеет формулу(Е), или один мономер которого имеет формулу (Е), а другой мономер имеет формулу (В) где R2, R6, R9, R7 и R8 являются такими, как определено для соединения формулы (А), и группы R7 или группы R8 каждого мономера вместе образуют димерный мостик, имеющий формулу -X-R"-X-, связывающий мономеры; где R" представляет собой C3-12 алкиленовую группу, углеводородная цепь которой может прерываться одним или более гетероатомами и/или ароматическими кольцами, выбранными из бензольного или пиридинового кольца; и каждый X представляет собой О, S или N(H); и где указанное соединение представляет собой димер, каждый мономер которого имеет формулу(Е), при этом группа RL в одном из мономеров представляет собой кэпирующую группу, RC, или представляет собой линкер для соединения со связывающимся с клетками агентом. Альтернативно, согласно одному варианту реализации изобретения R" представляет собой C3-12 алкиленовую группу, углеводородная цепь которой может прерываться одним или более гетероатомами и/или ароматическими кольцами, выбранными из бензольного или пиридинового кольца. Альтернативно, новые соединения, представляющие собой конъюгаты, могут быть выбраны из соединений формулы (А), как описано выше, и (A-I), где (A-I) выбрано из (А-А) и (А-В)R6, R9, R10, Q, R11, R и R' являются такими, как определено для соединения формулы (А);R7 независимо выбран из Н, R, ОН, OR, SH, SR, NH2, NHR, NRR', NO2, Me3Sn и галогена;R8 независимо выбран из Н, R, ОН, OR, SH, SR, NH2, NHR, NRR', NO2, Me3Sn и галогена; или любая пара смежных групп из R6-R9 вместе образуют группу -О-(СН 2)р-О-, где р равен 1 или 2,R2 с любым из R1 или R3 вместе с атомами углерода С-кольца, к которым они присоединены, образует необязательно замещенное бензольное кольцо; каждый V и W выбран из (СН 2)n, О, S, NR, CHR и CRR', где n равен 1, 2 или 3, за исключением того,что V представляет собой С, когда R1 и R2 вместе с атомами углерода С-кольца, к которому они присоединены, образуют необязательно замещенное бензольное кольцо, и W представляет собой С, когда R3 иR2 вместе с атомами углерода С-кольца, к которому они присоединены, образуют необязательно замещенное бензольное кольцо; Т выбран из СН 2, NR, CO, BH, SO и SO2;U выбран из СН 2, NR, О и S;Y представляет собой (СН 2)n, где n равен 1, 2, 3 или 4; за исключением того, что не все из Т, U и Y представляют собой СН 2; или указанное соединение представляет собой димер, каждый мономер которого имеет формулу(А), каждый мономер которого имеет формулу (A-I), один мономер которого имеет формулу (А), а другой мономер имеет формулу (В), как описано выше, или (B-I), или один мономер которого имеет формулу (A-I), а другой мономер имеет формулу (В) или (B-I),и (B-I) выбран из (В-А) и (В-В) где R1, R2, R3, R6, R9, R7 и R8 являются такими, как определено для соединения формулы (A-I), и группы R7 или группы R8 каждого мономера вместе образуют димерный мостик, имеющий формулу-X-R"-X-, связывающий мономеры; где R" представляет собой С 3-12 алкиленовую группу, углеводородная цепь которой может прерываться одним или более гетероатомами и/или ароматическими кольцами, выбранными из бензольного или пиридинового кольца; и каждый X представляет собой О, S или N(H); и где указанное соединение представляет собой димер, каждый мономер которого имеет формулу(A-I) и/или формулы (А), при этом группа R10 в одном из мономеров представляет собой кэпирующую группу RC или представляет собой линкер, соединенный со связывающимся с клетками агентом. Для удобства все ссылки на соединение А могут применяться к A-I (и А-А, и А-В) и все ссылки на соединение В могут применяться к B-I (и В-А, и В-В). Аналогично, ссылки на соединения С, D и Е также относится к (C-I), (D-I) и (E-I) соответственно. Альтернативно, указанный конъюгат можно применять для получения соединения в областимишени, где соединение представляет собой соединение формулы (С), как описано выше, или (C-I),где (C-I) выбрано из (С-А) и (С-В)R6, R9, R и R' являются такими, как определено для соединения формулы (С);R7 независимо выбран из Н, R, ОН, OR, SH, SR, NH2, NHR, NRR', NO2, Me3Sn и галогена;R8 независимо выбран из Н, R, ОН, OR, SH, SR, NH2, NHR, NRR', NO2, Me3Sn и галогена; или любая пара смежных групп из R6-R9 вместе образует группу -О-(СН 2)p-О-, где р равен 1 или 2,R2 с любым из R1 или R3 вместе с атомами углерода С-кольца, к которым они присоединены, образует необязательно замещенное бензольное кольцо; каждый V и W выбран из (СН 2)n, О, S, NR, CHR, и CRR', где n равен 1, 2 или 3, за исключением того, что V представляет собой С, когда R1 и R2 вместе с атомами углерода С-кольца, к которому они присоединены, образуют необязательно замещенное бензольное кольцо, и W представляет собой С, когда R3 и R2 вместе с атомами углерода С-кольца, к которым они присоединены, образуют необязательно замещенное бензольное кольцо; Т выбран из СН 2, NR, CO, BH, SO и SO2;U выбран из СН 2, NR, О и S;Y представляет собой (СН 2)n, где n равен 1, 2, 3 или 4; за исключением того, что не все из Т, U и Y представляют собой СН 2; или указанное соединение представляет собой димер, каждый мономер которого имеет формулу(С), каждый мономер которого имеет формулу (C-I), или один мономер которого имеет формулу (С), а другой мономер имеет формулу (C-I), a группы R7 или группы R8 каждого мономера вместе образуют димерный мостик, имеющий формулу -X-R"-X-, связывающий мономеры; где R" представляет собой C3-12 алкиленовую группу, углеводородная цепь которой может прерываться одним или более гетероатомами и/или ароматическими кольцами, выбранными из бензольного или пиридинового кольца; и каждый X представляет собой О, S или N(H). Настоящее изобретение также относится к применению конъюгата для получения соединения в области-мишени, где указанное соединение представляет собой соединение формулы (D), как описано выше, или формулы (D-I); где (D-I) выбрано из (D-A) и (D-B)R6, R9, R и R' являются такими, как определено для соединения формулы (D);R7 независимо выбран из Н, R, ОН, OR, SH, SR, NH2, NHR, NRR', NO2, Me3Sn и галогена;R8 независимо выбран из Н, R, ОН, OR, SH, SR, NH2, NHR, NRR', NO2, Me3Sn и галогена; или любая пара смежных групп из R6-R9 вместе образует группу -О-(СН 2)р-О-, где р равен 1 или 2,Q независимо выбран из О, S и NH;R11 представляет собой Н или R или, если Q представляет собой О, SO3M, где М представляет собой катион металла;R2 с любым из R1 или R3 вместе с атомами углерода С-кольца, к которым они присоединены, образует необязательно замещенное бензольное кольцо; каждый V и W выбран из (СН 2)n, О, S, NR, CHR и CRR', где n равен 1, 2 или 3, за исключением того,что V представляет собой С, когда R1 и R2 вместе с атомами углерода С-кольца, к которым они присоединены, образуют необязательно замещенное бензольное кольцо, и W представляет собой С, когда R3 иR2 вместе с атомами углерода С-кольца, к которым они присоединены, образуют необязательно замещенное бензольное кольцо; Т выбран из СН 2, NR, CO, BH, SO и SO2;U выбран из СН 2, NR, О и S;Y представляет собой (СН 2)n, где n равен 1, 2, 3 или 4; за исключением того, что на все из Т, U и Y представляют собой СН 2; или указанное соединение представляет собой димер, каждый мономер которого имеет формулу(D), каждый мономер которого имеет формулу (D-I), или один мономер которого имеет формулу (D), а другой мономер имеет формулу (D-I), и группы R7 или группы R8 каждого мономера вместе образуют димерный мостик, имеющий формулу -X-R"-X-, связывающий мономеры; где R" представляет собой С 3-12 алкиленовую группу, углеводородная цепь которой может прерываться одним или более гетероатомами и/или ароматическими кольцами, выбранными из бензольного или пиридинового кольца; и каждый X представляет собой О, S или N(H). Альтернативно, согласно настоящему изобретению также предложены соединения формулы (Е),как описано выше, и (E-I) для применения для получения соединений, представляющие собой конъюгаты согласно настоящему изобретению; где (E-I) выбрано из (Е-А) и (Е-В)R6, R9, R и R' являются такими, как определено для соединения формулы (D);R7 независимо выбран из Н, R, ОН, OR, SH, SR, NH2, NHR, NRR', NO2, Me3Sn и галогена;R8 независимо выбран из Н, R, ОН, OR, SH, SR, NH2, NHR, NRR', NO2, Me3Sn и галогена; или любая пара смежных групп из R6-R9 вместе образует группу -О-(СН 2)p-О-, где р равен 1 или 2,RL представляет собой линкер для соединения со связывающимся с клетками агентом;Q независимо выбран из О, S и NH;R11 представляет собой Н или R или, если Q представляет собой О, SO3M, где М представляет собой катион металла;R2 с любым из R1 или R3 вместе с атомами углерода С-кольца, к которым они присоединены, образует необязательно замещенное бензольное кольцо; каждый V и W выбран из (СН 2)n, О, S, NR, CHR и CRR', где n равен 1, 2 или 3, за исключением того,что V представляет собой С, когда R1 и R2 вместе с атомами углерода С-кольца, к которым они присоединены, образуют необязательно замещенное бензольное кольцо, и W представляет собой С, когда R3 иR2 вместе с атомами углерода С-кольца, к которым они присоединены, образуют необязательно замещенное бензольное кольцо; Т выбран из СН 2, NR, CO, BH, SO и SO2;U выбран из СН 2, NR, О и S;Y представляет собой (СН 2)n, где n равен 1, 2, 3 или 4; за исключением того, что не все из Т, U и Y представляют собой СН 2; или указанное соединение представляет собой димер, каждый мономер которого имеет формулу(Е), каждый мономер которого имеет формулу (E-I), или один мономер которого имеет формулу (Е) или(Е-1), а другой мономер имеет формулу (Е), (E-I), (В) или (В-1); и группы R7 или группы R8 каждого мономера вместе образуют димерный мостик, имеющий формулу -X-R"-X-, связывающий мономеры; где R" представляет собой С 3-12 алкиленовую группу, углеводородная цепь которой может прерываться одним или более гетероатомами и/или ароматическими кольцами, выбранными из бензольного или пиридинового кольца; и каждый X представляет собой О, S или N(H). Краткое описание фигур На фиг. 1 показаны конкретные варианты реализации настоящего изобретения. На фиг. 2-6 показаны результаты биологических анализов для конкретных вариантов реализации настоящего изобретения. Подробное описание изобретения Согласно настоящему изобретению предложен конъюгат, содержащий PBD соединение, присоединенное через положение N10 к связывающемуся с клетками агенту с помощью линкера. Согласно одному варианту реализации изобретения конъюгат содержит связывающийся с клетками агент, соединенный со спейсерной связывающей группой, при этом спейсер соединен с триггером, а триггер соединен с саморасщепляющимся линкером, и саморасщепляющийся линкер соединен с положением N10 PBD соединения. Описанный конъюгат показан ниже где СВА представляет собой связывающийся с клетками агент, a PBD представляет собой пирролбензодиазепиновое соединение согласно настоящему изобретению. На иллюстрации показаны фрагменты, которые соответствуют R10, A, L1 и L2 в конкретных вариантах реализации изобретения. Настоящее изобретение подходит для применения для получения PBD соединения в предпочтительной области в теле субъекта. Согласно предпочтительным вариантам реализации настоящего изобретения конъюгат обеспечивает высвобождение активного PBD соединения, не содержащего каких-либо фрагментов линкера. При этом не наблюдается каких-либо остатков, которые могли бы влиять на реакционную способность PBD соединения. Согласно определенным вариантам реализации изобретения предложены конъюгаты, содержащиеPBD димерную группу, содержащую линкер, соединенный со связывающимся с клетками агентом. Авторы настоящего изобретения описывают в настоящем тексте способы синтеза, которые позволяют получить такие димерные конъюгаты путем применения новых методов десимметризации PBD. Предпочтительные варианты Следующие предпочтительные варианты могут быть применимы ко всем аспектам изобретения,описанным выше, или могут относиться к одному аспекту. Предпочтительные варианты можно объединять в любой комбинации. Двойная связь Согласно одному варианту реализации двойная связь между С 1 и С 2 и С 2 и С 3 отсутствует. Согласно одному варианту реализации пунктирные линии обозначают необязательное наличие двойной связи между С 2 и С 3, как показано ниже Согласно одному варианту реализации двойная связь присутствует между С 2 и С 3, когда R2 представляет собой С 5-20 арил или C1-12 алкил. Согласно одному варианту реализации пунктирные линии обозначают необязательное наличие двойной связи между С 1 и С 2, как показано ниже Согласно одному варианту реализации двойная связь между С 1 и С 2 присутствует, когда R2 представляет собой С 5-20 арил или C1-12 алкил.R2 Согласно одному варианту реализации R2 независимо выбран из Н, ОН, =O, =СН 2, CN, R, OR, =CHDR , =C(RD)2, O-SO2-R, CO2R и COR и необязательно дополнительно выбран из галогена или дигалоген. Согласно одному варианту реализации R2 независимо выбран из Н, ОН, =O, =СН 2, CN, R, OR, =CHDR , =C(RD)2, O-SO2-R, CO2R и COR. Согласно одному варианту реализации R независимо выбран из Н, =O, =СН 2, R, =СН-RD и =C(RD)2. Согласно одному варианту реализации R2 независимо представляет собой Н. Согласно одному варианту реализации R2 независимо представляет собой =O. Согласно одному варианту реализации R2 независимо представляет собой =СН 2. Согласно одному варианту реализации R2 независимо представляет собой =CH-RD. В PBD соединении группа =CH-RD может иметь любую конфигурацию, показанную ниже Согласно одному варианту реализации указанная конфигурация представляет собой конфигурацию Согласно одному варианту реализации R2 независимо представляет собой =C(RD)2. Согласно одному варианту реализации R2 независимо представляет собой =CF2. Согласно одному варианту реализации R2 независимо представляет собой R. Согласно одному варианту реализации R2 независимо представляет собой необязательно замещенный C5-20 арил. Согласно одному варианту реализации R2 независимо представляет собой необязательно замещенный C1-12 алкил. Согласно одному варианту реализации R2 независимо представляет собой необязательно замещенный С 5-20 арил. Согласно одному варианту реализации R2 независимо представляет собой необязательно замещенный С 5-7 арил. Согласно одному варианту реализации R2 независимо представляет собой необязательно замещенный C8-10 арил. Согласно одному варианту реализации R2 независимо представляет собой необязательно замещенный фенил. Согласно одному варианту реализации R2 независимо представляет собой необязательно замещенный нафтил. Согласно одному варианту реализации R2 независимо представляет собой необязательно замещенный пиридил. Согласно одному варианту реализации R2 независимо представляет собой необязательно замещенный хинолинил или изохинолинил. Согласно одному варианту реализации R2 содержит от одной до трех групп в качестве заместителей, более предпочтительно 1 и 2 группы и наиболее предпочтительно содержит в качестве заместителя одну группу. Заместители могут находиться в любом положении. Когда R2 представляет собой С 5-7 арильную группу, единственный заместитель предпочтительно находится у атома кольца, который не является смежным со связью с остальной частью соединения, т.е. предпочтительно находится вили у положении по отношению к связи с остальной частью соединения. Следовательно, когда С 5-7 арильная группа представляет собой фенил, заместитель предпочтительно находится в мета- или пара-положении и более предпочтительно в пара-положении. Согласно одному варианту реализации R2 выбран из где звездочка обозначает место присоединения. Когда R2 представляет собой С 8-10 арильную группу, например хинолинил или изохинолинил, он может содержать любое количество заместителей в любом положении в хинолиновом или изохинолиновом кольце. Согласно некоторым вариантам реализации он содержит один, два или три заместителя, и-9 024730 указанные заместители могут находиться как в проксимальном, так и в дистальном кольце, или в обоих кольцах (если содержится более одного заместителя). Согласно одному варианту реализации, если R2 является необязательно замещенным, заместители выбраны из таких заместителей, которые представлены ниже в разделе с описанием заместителей. Когда R является необязательно замещенным, заместители предпочтительно выбраны из галогена,гидроксила, простой эфирной группы, формила, ацила, карбокси, сложноэфирной группы, ацилокси,амино, амидо, ациламидо, аминокарбонилокси, уреидо, нитро, циано и тиоэфирной группы. Согласно одному варианту реализации, когда R или R2 являются необязательно замещенными, заместители выбраны из группы, состоящей из R, OR, SR, NRR', NO2, галогена, CO2R, COR, CONH2,CONHR и CONRR'. Когда R2 представляет собой C1-12 алкил, необязательный заместитель может дополнительно включать С 3-20 гетероциклильные и С 5-20 арильные группы. Когда R2 представляет собой С 3-20 гетероциклил, необязательный заместитель может дополнительно включать С 1-12 алкильные и С 5-20 арильные группы. Когда R2 представляет собой С 5-20 арильные группы, необязательный заместитель может дополнительно включать С 3-20 гетероциклильные и C1-12 алкильные группы. Очевидно, что термин "алкил" включает подклассы алкенил и алкинил, а также циклоалкил. Таким образом, если R2 представляет собой необязательно замещенный C1-12 алкил, это означает, что алкильная группа необязательно содержит одну или более углерод-углеродную двойную или тройную связь, которые могут образовывать фрагмент конъюгированной системы. Согласно одному варианту реализации необязательно замещенная C1-12 алкильная группа содержит по меньшей мере одну углерод-углеродную двойную или тройную связь, и указанная связь является конъюгированной с двойной связью, присутствующей между С 1 и С 2 или С 2 и С 3. Согласно одному варианту реализации C1-12 алкильная группа представляет собой группу, выбранную из насыщенного C1-12 алкила, С 2-12 алкенила, С 2-12 алкинила и С 3-12 циклоалкила. Если заместитель в R2 представляет собой галоген, то он предпочтительно представляет собой F или Cl, более предпочтительно Cl. Если заместитель в R2 представляет собой простую эфирную группу, то согласно некоторым вариантам реализации изобретения он может представлять собой алкоксигруппу, например, С 1-7 алкоксигруппу (например метокси, этокси) или согласно некоторым вариантам реализации он может представлять собой С 5-7 арилоксигруппу (например, фенокси, пиридилокси, фуранилокси). Если заместитель в R2 представляет собой С 1-7 алкил, то он предпочтительно может представлять собой C1-4 алкильную группу (например метил, этил, пропил, бутил). Если заместитель в R2 представляет собой C3-7 гетероциклил, то согласно некоторым вариантам реализации он может представлять собой C6 азотсодержащую гетероциклильную группу, например, морфолино, тиоморфолино, пиперидинил, пиперазинил. Указанные группы могут быть связаны с остальной частью PBD фрагмента через атомом азота. Указанные группы также могут содержать заместитель, например, C1-4 алкильную группу. Если заместитель в R2 представляет собой бис-окси-C1-3 алкилен, то он предпочтительно представляет собой бис-оксиметилен или бис-оксиэтилен. Особо предпочтительные заместители для R2 включают метокси, этокси, фтор, хлор, циано, бисоксиметилен, метилпиперазинил, морфолино и метилтиенил. Особо предпочтительные замещенные R2 группы включают, но не ограничиваются ими, 4-метоксифенил, 3-метоксифенил, 4-этоксифенил, 3-этоксифенил, 4-фторфенил, 4-хлорфенил, 3,4-бисоксиметиленфенил, 4-метилтиенил, 4-цианофенил, 4-феноксифенил, хинолин-3-ил и хинолин-6-ил, изохинолин 3-ил и изохинолин-6-ил, 2-тиенил, 2-фуранил, метоксинафтил и нафтил. Согласно одному варианту реализации R2 представляет собой галоген или дигалоген. Согласно одному варианту реализации R2 представляет собой -F или -F2, указанные заместители показаны ниже какRD Согласно одному варианту реализации RD независимо выбран из R, CO2R, COR, CHO, СО 2 Н и галоСогласно одному варианту реализации RD независимо представляет собой R. Согласно одному варианту реализации RD независимо представляет собой галоген.- 10024730 Согласно одному варианту реализации R6 независимо выбран из Н, R, ОН, OR, SH, SR, NH2, NHR,NRR', NO2, Me3Sn- и галогена. Согласно одному варианту реализации R6 независимо выбран из Н, ОН, OR, SH, NH2, NO2 и галогена. Согласно одному варианту реализации R6 независимо выбран из Н и галогена. Согласно одному варианту реализации R6 независимо представляет собой Н. Согласно одному варианту реализации R6 и R7 вместе образуют группу -О-(СН 2)p-О-, где р равен 1 или 2.R7 независимо выбран из Н, R, ОН, OR, SH, SR, NH2, NHR, NRR', NO2, Me3Sn и галогена. Согласно одному варианту реализации R7 независимо представляет собой OR. Согласно одному варианту реализации R7 независимо представляет собой OR7, где R7A независимо представляет собой необязательно замещенный C1-6 алкил. Согласно одному варианту реализации R7 независимо представляет собой необязательно замещенный насыщенный C1-6 алкил. Согласно одному варианту реализации R7A независимо представляет собой необязательно замещенный C2-4 алкенил. Согласно одному варианту реализации R7A независимо представляет собой Me. Согласно одному варианту реализации R7A независимо представляет собой CH2Ph. Согласно одному варианту реализации R7 независимо представляет собой аллил. Согласно одному варианту реализации указанное соединение представляет собой димер, где группы R7 каждого мономера вместе образуют димерный мостик, связывающий мономеры, имеющий формулу X-R"-X.R8 Согласно одному варианту реализации указанное соединение представляет собой димер, где группы R8 каждого мономера вместе образуют димерный мостик, связывающий мономеры, имеющий формулу X-R"-X. Согласно одному варианту реализации R8 независимо представляет собой OR8A, где R8A независимо представляет собой необязательно замещенный C1-4 алкил. Согласно одному варианту реализации R8A независимо представляет собой необязательно замещенный насыщенный C1-6 алкил или необязательно замещенный C2-4 алкенил. Согласно одному варианту реализации R8A независимо представляет собой Me. Согласно одному варианту реализации R8A независимо представляет собой CH2Ph. Согласно одному варианту реализацииR8A независимо представляет собой аллил. Согласно одному варианту реализации R8 и R7 вместе образуют группу -О-(СН 2)p-О-, где р равен 1 или 2. Согласно одному варианту реализации R8 и R9 вместе образуют группу -О-(СН 2)p-О-, где р равен 1 или 2.R9 Согласно одному варианту реализации R9 независимо выбран из Н, R, ОН, OR, SH, SR, NH2, NHR,NRR', NO2, Me3Sn- и галогена. Согласно одному варианту реализации R9 независимо представляет собой Н. Согласно одному варианту реализации R9 независимо представляет собой R или OR.R10 Во избежание неправильного толкования, если R10 представляет собой линкер, соединенный со связывающимся с клетками агентом, указанный связывающийся с клетками агент представляет собой фрагмент группы R10. Согласно определенным вариантам реализации настоящего изобретения, если конъюгат представляет собой димер, содержащий два мономера А, то один мономер содержит группу R10, которая представляет собой линкер, соединенный со связывающимся с клетками агентом, а другой мономер содержит группу R10, которая представляет собой линкер, соединенный со связывающимся с клетками агентом,или кэпирующую группу RC. Предпочтительно другой мономер содержит группу R10, которая представляет собой кэпирующую группу RC. Таким образом, согласно указанному предпочтительному варианту реализации изобретения существует только одна связь со связывающимся с клетками агентом. Согласно одному варианту реализации группа R10 способна удаляться из положения N10 PBD фрагмента с образованием N10-C11 иминной связи, карбиноламина, замещенного карбиноламина, гдеQR11 представляет собой OSO3M, бисульфитный аддукт, тиокарбиноламин, замещенный тиокарбиноламин или замещенный карбиналамин, как показано ниже где R и М являются такими, как определено для конъюгатов согласно настоящему изобретению. Согласно одному варианту реализации группа R10 способна удаляться из положения N10 PBD фрагмента с образованием N10-C11 иминной связи. Согласно некоторым вариантам реализации конъюгат согласно настоящему изобретению представляет собой димерное соединение, содержащее мономер формулы (А) и мономер формулы (В). Согласно указанному варианту реализации группа R10 не должна быть способной удаляться из положения N10, так как мономер (В) содержит подходящую функциональную группу в положениях N10 и С 11, обеспечивающую биологическую активность. Однако предпочтительно группа R10 способна удаляться с получением димера, содержащего подходящую функциональную группу в положениях N10 и С 11 в обоих мономерных звеньях. Такая функциональная группа считается необходимой для обеспечения перекрестного сшивания PBD димера. Настоящая заявка, в частности, относится к таким R10 группам, которые соединены с положениемN10 карбаматной связью. Линкер соединяет связывающийся с клетками агент (СВА), например антитело, с фрагментом D лекарственного средства PBD посредством ковалентной связи (связей). Линкер представляет собой бифункциональный или мультифункциональный фрагмент, который можно использовать для связывания одного или более фрагментов лекарственного средства (D) и единицы антитела (Ab) с образованием конъюгата антитело-лекарственное средство (ADC). Линкер (L) может являться стабильным за пределами клетки, т.е. внеклеточно, или же он может поддаваться расщеплению под действием ферментативной активности, гидролиза или в условиях других процессов метаболизма. Конъюгат антитело-лекарственное средство (ADC) удобно получать с использованием линкера, содержащего реакционноспособную функциональную группу для связывания с фрагментом лекарственного средства и с антителом. Тиоловая группа цистеина или аминная группа, например, N-концевая или боковая цепь аминокислоты, такой как лизин, в антителе (Ab) может образовывать связь с функциональной группой линкерного или спейсерного реагента, фрагментом PBD лекарственного средства (D) или комплексом лекарственное средстволинкерный реагент (D-L). Многие функциональные группы в линкере, присоединенном к положению N10 PBD фрагмента,могут быть задействованы для связывания со связывающимся с клетками агентом. Например, сложнэфирные, сложнотиоэфирные, амидные, тиоамидные, карбаматные, тиокарбаматные, мочевинные, тиомочевинные, простые эфирные, простые тиоэфирные или дисульфидные связи могут образовываться в результате взаимодействия интермедиата линкер-PBD лекарственное средство со связывающимся с клетками агентом. Линкеры ADC предпочтительно предотвращают агрегацию молекул ADC и обеспечивают нахождение ADC в свободно растворимой в водной среде форме и в мономерном состоянии. Линкеры ADC предпочтительно являются стабильными вне клеток. До транспортировки или доставки в клетку конъюгат антитело-лекарственное средство (ADC) предпочтительно является стабильным и остается интактным, т.е. антитело остается связанным с фрагментом лекарственного средства. Линкеры являются стабильными вне клеток-мишеней и могут расщепляться с некоторой эффективной скоростью внутри клеток. Эффективный линкер: (i) поддерживает свойства специфического связывания антитела;(ii) обеспечивает внутриклеточную доставку конъюгата или фрагмента лекарственного средства; (iii) остается стабильным и интактным, т.е. не расщепляется до момента доставки или транспортировки указанного конъюгата к области-мишени; и (iv) поддерживает цитотоксическое, приводящее к уничтожению клеток, действие или цитостатическое действие фрагмента PBD лекарственного средства. СтабильностьADC можно определить с помощью стандартных аналитических методов, таких как масс-спектрометрия,ВЭЖХ и метод разделения/анализа ЖХ/МС. Для ковалентного связывания антитела и фрагмента лекарственного средства необходимо, чтобы линкер имел две реакционноспособные функциональные группы, т.е. являлся бивалентным с точки зрения реакционноспособности. Бивалентные линкерные реагенты, которые могут использоваться для связывания двух или более функциональных или биологически активных фрагментов, таких как пептиды,нуклеиновые кислоты, лекарственные средства, токсины, антитела, гаптены и репортерные группы, яв- 12024730 ляются известными, и описаны способы получения конъюгатов с использованием указанных линкеров(Hermanson, G.T. (1996) Bioconjugate Techniques; Academic Press: New York, p. 234-242). Согласно другому варианту реализации линкер может содержать в качестве заместителей группы,модулирующие агрегацию, растворимость или реакционноспособность. Например, сульфонатный заместитель может повышать растворимость реагента в воде и облегчать реакцию сочетания линкерного реагента с антителом или фрагментом лекарственного средства, или облегчать реакцию сочетания Ab-L с D или D-L с Ab, в зависимости от схемы синтеза, используемого для получения ADC. Согласно одному варианту реализации R10 представляет собой следующую группу: где звездочка обозначает место присоединения к положению N10, СВА представляет собой связывающийся с клетками агент, L представляет собой линкер, А представляет собой связывающую группу,соединяющую L со связывающимся с клетками агентом, L представляет собой ковалентную связь или вместе с -ОС(=О)- образует саморасщепляющийся линкер, a L или L представляет собой способный к расщеплению линкер.L предпочтительно представляет собой способный к расщеплению линкер и может называться триггером для активации расщепления линкера. Природа L1 и L2, при его наличии, может сильно варьироваться. Указанные группы выбираются в соответствии с их способностью к расщеплению, которая может зависеть от условий в области-мишени,в которую доставляется конъюгат. Линкеры, которые расщепляются под действием ферментов, являются предпочтительными, несмотря на то, что также могут использоваться линкеры, способные к расщеплению при изменении рН (например, кислотолабильные или щелочнолабильные), температуры или при облучении (например, фотолабильные). Линкеры, способные к расщеплению в присутствии восстановителя или окислителя, также могут использоваться согласно настоящему изобретению.L1 может содержать непрерывную последовательность аминокислот. Аминокислотная последовательность может представлять собой субстратную мишень для ферментативного расщепления, обеспечивая за счет этого высвобождение R10 из положения N10. Согласно одному варианту реализации L расщепляется под действием фермента. Согласно одному варианту реализации фермент представляет собой эстеразу или пептидазу. Согласно одному варианту реализации L присутствует и вместе с -С(=О)О- образует саморасщепляющийся линкер. Согласно одному варианту реализации L представляет собой субстрат для ферментативной активности, таким образом, обеспечивая высвобождение R10 из положения N10. Согласно одному варианту реализации, когда L1 расщепляется под действием фермента, и присутствует L2, фермент расщепляет связь между L1 и L2.L1 и L2, при наличии, могут быть связаны посредством связи, выбранной из-NHC(=O)NH-. Аминогруппа L1, которая связывается с L2, может представлять собой N-конец аминокислоты или может происходить из аминогруппы боковой цепи аминокислоты, например, боковой цепи аминокислоты лизина. Карбоксильная группа L1, которая связывается с L2, может представлять собой С-конец аминокислоты или может происходить из карбоксильной группы боковой цепи аминокислоты, например, боковой цепи глутаминовой кислоты. Гидроксильная группа L1, которая связывается с L2, может происходить из гидроксильной группы боковой цепи аминокислоты, например, боковой цепи аминокислоты серина. Термин "боковая цепь аминокислоты" включает группы, которые встречаются в: (i) природных аминокислотах, таких как аланин, аргинин, аспарагин, аспарагиновая кислота, цистеин, глутамин, глутаминовая кислота, глицин, гистидин, изолейцин, лейцин, лизин, метионин, фенилаланин, пролин, серин,треонин, триптофан, тирозин и валин; (ii) минорных аминокислотах, таких как орнитин и цитруллин; (iii) не природных аминокислотах, бета-аминокислотах, синтетических аналогах и производных природных аминокислот; и (iv) всех энантиомерах, диастереомерах, изомерно обогащенных формах, меченых изотопом формах (например, 2 Н, 3 Н, 14 С, 15N), защищенных формах и их рацемических смесях. Согласно одному варианту реализации -С(=О)О- и L2 вместе образуют группу где звездочка обозначает место присоединения к положению N10, волнистая линия обозначает место присоединения к линкеру L1, Y представляет собой -N(H)-, -О-, -C(=O)N(H)- или -С(=О)О-, а n равен 0-3. Фениленовое кольцо необязательно содержит в качестве заместителя один, два или три заместителя,описанных в настоящем тексте. Согласно одному варианту реализации фениленовая группа необязательно содержит в качестве заместителя галоген, NO2, R или OR. Согласно одному варианту реализации Y представляет собой NH. Согласно одному варианту реализации n равен 0 или 1. Предпочтительно n равен 0. Когда Y представляет собой NH, и n равен 0, саморасщепляющийся линкер может называться паминобензилкарбонильным линкером (РАВС). Саморасщепляющийся линкер обеспечивает высвобождение защищенного соединения при активации удаленного сайта, действуя таким образом, как показано ниже (для n=0) где L представляет собой активированную форму оставшегося фрагмента части линкера. Указанные группы имеют преимущество, которое заключается в том, что сайт активации отделен от соединения, подвергаемого защите. Как описано выше, фениленовая группа может быть необязательно замещенный. Согласно одному варианту реализации, описанному в настоящем тексте, группа L представляет собой линкер L1 согласно настоящему описанию, который может содержать дипептидную группу. Согласно другому варианту реализации -С(=О)О- и L2 вместе образуют группу, выбранную из следующих: где звездочка, волнистая линия, Y и n являются такими, как определено выше. Каждое фениленовое кольцо необязательно содержит один, два или три заместителя, описанных в настоящем тексте. Согласно одному варианту реализации фениленовое кольцо, содержащее заместительY, является необязательно замещенным, и фениленовое кольцо, не содержащее заместитель Y, является незамещенным. Согласно одному варианту реализации фениленовое кольцо, содержащее заместитель Y,является незамещенным, и фениленовое кольцо, не содержащее заместитель Y, является необязательно замещенным. Согласно другому варианту реализации -С(=О)О- и L2 вместе образуют группу, выбранную из где звездочка, волнистая линия, Y и n являются такими, как определено выше, Е представляет собой О, S или NR, D представляет собой N, СН или CR, и F представляет собой N, СН или CR. Согласно одному варианту реализации D представляет собой N. Согласно одному варианту реализации D представляет собой СН. Согласно одному варианту реализации Е представляет собой О или S. Согласно одному варианту реализации F представляет собой СН. Согласно предпочтительному варианту реализации линкер представляет собой катепсиновый лабильный линкер. Согласно одному варианту реализации L1 содержит дипептид. Указанный дипептид может пред- 14024730 ставлять собой -NH-X1-X2-CO-, где -NH- и -СО- представляют собой N- и С-концы аминокислотных групп X1 и Х 2 соответственно. Аминокислоты в дипептиде могут представлять собой любую комбинацию природных аминокислот. Когда линкер представляет собой катепсиновый лабильный линкер, дипептид может представлять собой место действия для катепсин-опосредованного расщепления. Кроме того, для указанных аминокислотных групп, содержащих карбоксильную или аминную функциональную группу боковой цепи, например, Glu и Lys соответственно, СО и NH могут представлять собой указанные функциональные группы боковой цепи. Согласно одному варианту реализации группа -X1-Х 2- в дипептиде -NH-X1-X2-CO- выбрана из-Phe-Lys-,-Val-Ala-,-Val-Lys-,-Ala-Lys-,-Val-Cit-. Наиболее предпочтительно группа -X1-Х 2- в дипептиде -NH-X1-Х 2-СО- представляет собой -PheLys- или -Val-Ala-. Могут использоваться другие комбинации дипептидов, включая комбинации, описанные в источнике Dubowchik et al., Bioconjugate Chemistry, 2002, 13, 855-869, включенном в настоящую заявку посредством ссылки. Согласно одному варианту реализации боковая цепь аминокислоты является дериватизированной,если это приемлемо. Например, аминогруппа или карбоксильная группа боковой цепи аминокислоты может быть дериватизированной. Согласно одному варианту реализации аминогруппа NH2 боковой цепи аминокислоты, такой как лизин, находится в дериватизированной форме, выбранной из группы, состоящей из NHR и NRR'. Согласно одному варианту реализации карбоксигруппа СООН боковой цепи аминокислоты, такой как аспарагиновая кислота, находится в дериватизированной форме, выбранной из группы, состоящей изCOOR, CONH2, CONHR и CONRR'. Согласно одному варианту реализации боковая цепь аминокислоты является химически защищенной, если это приемлемо. Защитная группа боковой цепи может представлять собой группу, описанную ниже в отношении группы RL. Авторы настоящего изобретения обнаружили, что защищенные аминокислотные последовательности поддаются ферментативному расщеплению. Например, было обнаружено,что дипептидная последовательность, содержащая боковую цепь остатка Lys, защищенную Вос-группой,поддается расщеплению катепсином. Защитные группы боковых цепей аминокислот хорошо известны в данной области техники и описаны в каталоге Novabiochem. Дополнительные стратегии использования защитных групп представлены в источнике Protective Groups in Organic Synthesis, Greene and Wuts. Возможные защитные группы боковых цепей аминокислот, содержащих реакционноспособную функциональную группу в боковой цепи, показаны нижеTyr: Bzl, Z, Z-Br. Согласно одному варианту реализации защитная группа боковой цепи выбрана таким образом, что- 15024730 она расположена ортогонально по отношению к группе, представляющей собой кэпирующую группу или ее часть (при наличии указанной кэпирующей группы). Таким образом, удаление защитной группы боковой цепи не приводит к удалению кэпирующей группы или какой-либо защитной группы функциональной группы, которая является частью кэпирующей группы. Согласно другим вариантам реализации настоящего изобретения, выбранные аминокислоты представляют собой аминокислоты, не содержащие реакционноспособную функциональную группу в боковой цепи. Например, аминокислоты могут быть выбраны из: Ala, Gly, Ile, Leu, Met, Phe, Pro и Val. Согласно одному варианту реализации дипептид используется в комбинации с саморасщепляющимся линкером. Саморасщепляющийся линкер может быть связан с -Х 2-. Если саморасщепляющийся линкер присутствует, то -Х 2- непосредственно связан с указанным саморасщепляющимся линкером. Предпочтительно группа -Х 2-СО- связана с Y, где Y представляет собой-NH-X1- непосредственно связан с группой А. Указанная группа А может содержать функциональную группу -СО- с образованием, таким образом, амидной связи с -X1-. Согласно одному варианту реализации L1 и L2 вместе с -ОС(=О)- составляют группу NH-X1-Х 2-COPABC-. РАВС-группа непосредственно связана с положением N10. Предпочтительно саморасщепляющийся линкер и дипептид вместе образуют группу -NH-Phe-Lys-CO-NH-PABC-, которая показана ниже где звездочка обозначает место присоединения к положению N10, и волнистая линия обозначает место присоединения к остальной части линкера L1 или место присоединения к А. Предпочтительно волнистая линия обозначает место присоединения к А. Боковая цепь аминокислоты Lys может содержать защитную группу, например, Boc, Fmoc или Alloc, как описано выше. Альтернативно, саморасщепляющийся линкер и дипептид вместе образуют группу -NH-Val-AlaCO-NH-PABC-, которая показана ниже где звездочка и волнистая линия являются такими, как определено выше. Альтернативно, саморасщепляющийся линкер и дипептид вместе образуют группу -NH-Val-Cit-CONH-PABC-, которая показана ниже где звездочка и волнистая линия являются такими, как определено выше. Согласно некоторым вариантам реализации настоящего изобретения, предпочтительным может являться то, что если PBD/фрагмент лекарственного средства содержит незащищенную иминную связь,например, при присутствии фрагмента В, то линкер не содержит свободную аминогруппу (H2N-). Таким образом, если линкер имеет структуру -A-L1-L2-, то он предпочтительно не содержит свободную аминогруппу. Указанный предпочтительный вариант особенно применим, если линкер содержит дипептид,например, как L1; согласно указанному варианту реализации предпочтительно одна из двух аминокислот не выбрана из лизина. Не ограничиваясь какой-либо теорией, авторы настоящего изобретения обнаружили, что комбинация незащищенной иминной связи во фрагменте лекарственного средства и свободной аминогруппы в линкере может вызывать димеризацию соединения лекарственное средство-линкерный фрагмент, которая может препятствовать конъюгации указанного соединения лекарственное средство-линкерный фраг- 16024730 мент с антителом. Перекрестное сшивание указанных группы может усиливаться при наличии свободной аминогруппы, такой как ион аммония (H3N+-), например, при использовании сильной кислоты (например, TFA) для снятия защиты со свободной аминогруппы. Согласно одному варианту реализации А представляет собой ковалентную связь. Таким образом, L1 и связывающийся с клетками агент связаны напрямую. Например, если L1 содержит непрерывную аминокислотную последовательность, то N-конец указанной последовательности может непосредственно связываться со связывающимся с клетками агентом. Таким образом, если А представляет собой ковалентную связь, то связь между связывающимся с клетками агентом и L1 может быть выбрана из=N-NH-. Аминогруппа L1, которая связывается со связывающимся с клетками агентом, может представлять собой N-конец аминокислоты или может происходить из аминогруппы боковой цепи аминокислоты, например, боковой цепи аминокислоты лизина. Карбоксильная группа L1, которая связывается со связывающимся с клетками агентом, может представлять собой С-конец аминокислоты или может происходить из карбоксильной группы боковой цепи аминокислоты, например боковой цепи глутаминовой кислоты. Гидроксильная группа L1, которая связывается со связывающимся с клетками агентом, может происходить из гидроксильной группы боковой цепи аминокислоты, например, боковой группы аминокислоты серина. Тиоловая группа L1, которая связывается со связывающимся с клетками агентом, может происходить из тиоловой группы боковой цепи аминокислоты, например, боковой цепи аминокислоты серина. Комментарии, приведенные выше в отношении аминогрупп, карбоксильных, гидроксильных и тиоловых групп L1, также применимы к связывающемуся с клетками агенту. Согласно одному варианту реализации L2 вместе с -ОС(=О)- представляет собой где звездочка обозначает место присоединения к положению N10, волнистая линия обозначает место присоединения к L1, n равен 0-3, Y представляет собой ковалентную связь или функциональную группу, и Е представляет собой активируемую группу, например, в результате действия ферментов или света, с получением, таким образом, саморасщепляющейся единицы. Фениленовое кольцо необязательно дополнительно содержит один, два или три заместителя, описанных в настоящем тексте. Согласно одному варианту реализации фениленовая группа необязательно дополнительно содержит в качестве заместителя галоген, NO2, R или OR. Предпочтительно n равен 0 или 1, наиболее предпочтительно 0. Е выбран таким образом, что указанная группа является чувствительной к активации, например,светом или под действием фермента. Е может представлять собой -NO2 или глюкуроновую кислоту, при этом первая из указанных групп может быть чувствительной к действию нитроредуктазы, а последняя - к действию -глюкуронидазы. Согласно указанному варианту реализации саморасщепляющийся линкер обеспечивает высвобождение защищенного соединения, когда Е активирован, действуя таким образом, как показано ниже (для- 17024730 где звездочка обозначает место присоединения к положению N10, Е представляет собой активированную форму Е, и Y является таким, как описано выше. Указанные группы имеют преимущество, заключающееся в том, что сайт активации отделен от защищаемого соединения. Как описано выше, фениленовая группа может быть необязательно дополнительно замещена. Группа Y может представлять собой ковалентную связь с L1. Группа Y может представлять собой функциональную группу, выбранную из-S-,где L1 представляет собой дипептид, Y предпочтительно представляет собой -NH- или -С(=О)- с образованием, таким образом, амидной связи между L1 и Y. Согласно указанному варианту реализации дипептидная последовательность не обязательно является субстратом для ферментативной активности. Согласно другому варианту реализации А представляет собой спейсерную группу. Таким образом,L1 и связывающийся с клетками агент являются связанными не напрямую.L1 и А могут быть связаны с помощью связи, выбранной из-NHC(=O)NH-. Предпочтительно линкер содержит электрофильную функциональную группу для взаимодействия с нуклеофильной функциональной группой связывающегося с клетками агента. Нуклеофильные группы антител включают, но не ограничиваются ими: (i) N-концевые аминогруппы, (ii) аминогруппы боковых цепей, например, лизина, (iii) тиоловые группы боковых цепей, например, цистеина, и (iv) гидроксильные группы сахара или аминогруппы, где антитело является гликозилированным. Аминогруппы, тиоловые и гидроксильные группы являются нуклеофильными и способны реагировать с образованием ковалентных связей с электрофильными группами линкерных фрагментов и линкерных реагентов, включая:(i) малеимидные группы (ii) активированные дисульфиды, (iii) активные сложные эфиры, такие как сложные эфиры NHS (N-гидроксисукцинимида), сложные эфиры HOBt (N-гидроксибензотриазола), галогенформиаты и галогенангидриды; (iv) алкил- и бензилгалогениды, такие как галогенацетамиды; и (v) альдегиды, кетоны, карбоксильные группы, примеры некоторых из них Некоторые антитела содержат способные к восстанавлению межцепьевые дисульфиды, т.е. цистеиновые мостики. Антитела можно активировать для конъюгирования с линкерными реагентами путем обработки восстановителем, таким как ДТТ (дитиотреитол). В результате каждый цистеиновый мостик теоретически сможет образовать два реакционноспособных тиоловых нуклеофила. В антитела можно вводить дополнительные нуклеофильные группы посредством реакции лизинов с 2-иминотиоланом (реагентом Траута), что приводит к превращению амина в тиол. Реакцонноспособные тиоловые группы могут вводиться в антитело (или его фрагмент) путем введения одного, двух, трех, четырех или более цис- 18024730 теиновых остатков (например, при получении мутантных антител, содержащих один или более чужеродных цистеиновых аминокислотных остатков). В US 7521541 описано получение антитела путем введения реакционноспособных цистеиновых аминокислот. Согласно некоторым вариантам реализации линкер содержит реакционноспособную нуклеофильную группу, которая является реакционноспособной по отношению к электрофильной группе, присутствующей в антителе. Пригодные для использования электрофильные группы антитела включают, но не ограничиваются ими, карбонильные группы альдегидов и кетонов. Гетероатом нуклеофильной группы линкера может взаимодействовать с электрофильной группой антитела и образовывать ковалентную связь с единицей антитела. Пригодные для использования нуклеофильные группы линкера включают, но не ограничиваются ими, гидразид, оксим, амино, гидроксил, гидразин, тиосемикарбазон, гидразинкарбоксилат и арилгидразид. Электрофильная группа антитела обеспечивает удобный сайт для присоединения линкера. Согласно одному варианту реализации группа А представляет собой где звездочка обозначает место присоединения к L1, волнистая линия обозначает место присоединения к связывающемуся с клетками агенту, и n равен 0-6. Согласно одному варианту реализации n равен 5. Согласно одному варианту реализации группа А представляет собой где звездочка обозначает место присоединения к L1, волнистая линия обозначает место присоединения к связывающемуся с клетками агенту, и n равен 0-6. Согласно одному варианту реализации n равен 5. Согласно одному варианту реализации группа А представляет собой где звездочка обозначает место присоединения к L1, волнистая линия обозначает место присоединения к связывающемуся с клетками агенту, n равен 0 или 1, и m равен 0-30. Согласно предпочтительному варианту реализации n равен 1, и m равен 0-10, 1-8, предпочтительно 4-8 и наиболее предпочтительно 4 или 8. Согласно другому варианту реализации m равен 10-30 и предпочтительно 20-30. Альтернативно,m равен 0-50. Согласно указанному варианту реализации m предпочтительно равен 10-40, и n равен 1. Согласно одному варианту реализации группа А представляет собой где звездочка обозначает место присоединения к L1, волнистая линия обозначает место присоединения к связывающемуся с клетками агенту, n равен 0 или 1, и m равен 0-30. Согласно предпочтительному варианту реализации n равен 1 и m равен 0-10, 1-8, предпочтительно 4-8 и наиболее предпочтительно 4 или 8. Согласно другому варианту реализации m равен 10-30 и предпочтительно 20-30. Альтернативно,m равен 0-50. Согласно указанному варианту реализации m предпочтительно равен 10-40, и n равен 1. Согласно одному варианту реализации связь между связывающимся с клетками агентом и группой А осуществляется через тиоловый остаток связывающегося с клетками агента и малеимидную группу А. Согласно одному варианту реализации связь между связывающимся с клетками агентом и А представляет собой где звездочка обозначает место присоединения к остальной части А, и волнистая линия обозначает место присоединения к остальной части связывающегося с клетками агента. Согласно указанному варианту реализации атом S, как правило, принадлежит остатку связывающегося с клетками агента. Согласно каждому из вариантов реализации изобретения, указанных выше, вместо группы, полученной из малеимида, можно использовать альтернативную функциональную группу, показанную ниже: где волнистая линия обозначает место присоединения к связывающемуся с клетками агенту, как показано ранее, а звездочка обозначает связь с остальной частью группы А. Согласно одному варианту реализации группа, полученная из малеимида, заменена на следующую группу где волнистая линия обозначает место присоединения к связывающемуся с клетками агенту, а звездочка обозначает связь с остальной частью группы А. Согласно одному варианту реализации группа, полученная из малеимида, заменена на группу, которая необязательно вместе со связывающимся с клетками агентом выбрана из-NH-N=. Согласно одному варианту реализации группа, полученная из малеимида, заменена на группу, которая необязательно вместе со связывающимся с клетками агентом выбрана из где волнистая линия обозначает место присоединения к связывающемуся с клетками агенту или связь с остальной частью группы А, и звездочка обозначает другую место присоединения к связывающемуся с клетками агенту или связь с остальной частью группы А. Другие группы, подходящие для связывания L1 со связывающимся с клетками агентом, описаны вWO 2005/082023. Группа R10 происходит из группы RL. Группа RL может быть превращена в группу R10 путем связывания связывающегося с клетками агента с функциональной группой RL. Для превращения RL в R10 можно использовать другие способы. Другие способы могут включать удаление защитных групп при их наличии или введение соответствующей функциональной группы.Q Согласно одному варианту реализации Q выбрана из О, S или N(H). Предпочтительно Q представляет собой О.R11 Согласно одному варианту реализации R11 представляет собой Н или R или, если Q представляет собой О, SO3M, где М представляет собой катион металла. Согласно одному варианту реализации R11 представляет собой Н. Согласно одному варианту реализации R11 представляет собой R. Согласно одному варианту реализации, если Q представляет собой О, то R11 представляет собойSO3M, где М представляет собой катион металла. Катион может представлять собой Na+.RL Согласно одному варианту реализации RL представляет собой линкер для связывания со связывающимся с клетками агентом.- 20024730 Согласно одному варианту реализации линкер содержит функциональную группу для образования связи со связывающимся с клетками агентом. Настоящая заявка, в частности, относится к таким группамRL, которые содержат карбаматную связь с положением N10. В настоящем тексте описание связывающей группы в вышеуказанной группе R10 также относится к ее ближайшим предшественникам.RL отличается от группы RC, которая не подходит для реакции со связывающимся с клетками агентом. Однако, согласно некоторым вариантам реализации RC может быть превращена в группу RL, например, с помощью соответствующих манипуляций с защитными группами и другими функциональными группами, которые представляют собой RC (или образуют его часть). Согласно одному варианту реализации RL представляет собой следующую группу: где звездочка обозначает место присоединения к положению N10, G1 представляет собой функциональную группу, образующую связь со связывающимся с клетками агентом, L1 представляет собой линкер, L2 представляет собой ковалентную связь или вместе с -ОС(=О)- образует саморасщепляющийся линкер, a L1 или L2 представляют собой способные к расщеплению линкеры.L1 и L2 являются такими, как определено выше в отношении R10. Указание на связь с группой А могут рассматриваться в настоящем тексте как указание на связь с группой G1. Согласно одному варианту реализации, когда L1 содержит аминокислоту, боковая цепь указанной аминокислоты может являться защищенной. Могут использоваться любые подходящие защитные группы. Согласно одному варианту реализации защитные группы боковой цепи удаляются вместе с другими защитными группами в соединении (при их наличии). Согласно другим вариантам реализации защитные группы могут быть расположены ортогонально по отношению к другим защитным группам в молекуле(при их наличии). Подходящие защитные группы для боковой цепи аминокислот включают группы, описанные в каталоге Novabiochem 2006/2007. Защитные группы для использования в катепсин-лабильном линкере также описаны в источнике Dubowchik et al. Согласно определенным вариантам реализации группа L1 включает остаток аминокислоты Lys. Боковая цепь указанной аминокислоты может содержать защитную группу Boc или Alloc. Защитная группаBoc является наиболее предпочтительной. Функциональная группа G1 образует связывающую группу А при ее взаимодействии со связывающимся с клетками агентом. Согласно одному варианту реализации функциональная группа G1 представляет собой или содержит аминогруппу, карбоксильную группу, гидроксильную, тиоловую или малеимидную группу, взаимодействующую с соответствующей группой связывающегося с клетками агента. Согласно предпочтительному варианту реализации G1 содержит малеимидную группу. Согласно одному варианту реализации группа G1 представляет собой алкилмалеимидную группу. Указанная группа является подходящей для реагирования с тиоловыми группами, в частности, тиоловыми группами цистеина, присутствующими в связывающемся с клетками агенте, например, присутствующими в антителе. Согласно одному варианту реализации группа G1 представляет собой где звездочка обозначает место присоединения к L1, и n равен 0-6. Согласно одному варианту реализации n равен 5. Согласно одному варианту реализации группа G1 представляет собой где звездочка обозначает место присоединения к L1, и n равен 0-6. Согласно одному варианту реализации n равен 5. Согласно одному варианту реализации группа G1 представляет собой где звездочка обозначает место присоединения к L1, n равен 0 или 1, и m равен 0-30. Согласно предпочтительному варианту реализации n равен 1, и m равен 0-10, 1-2, предпочтительно 4-8 и наиболее- 21024730 предпочтительно 4 или 8. Альтернативно, m равен 0-50. Согласно указанному варианту реализации m предпочтительно равен 10-40, и n равен 1. Согласно одному варианту реализации группа G1 представляет собой где звездочка обозначает место присоединения к L1, n равен 0 или 1, и m равен 0-30. Согласно предпочтительному варианту реализации n равен 1, и m равен 0-10, 1-8, предпочтительно 4-8 и наиболее предпочтительно 4 или 8. Альтернативно, m равен 0-50. Согласно указанному варианту реализации m предпочтительно равен 10-40, и n равен 1. Согласно каждому из вариантов реализации, указанных выше, вместо малеимидной группы можно использовать альтернативную функциональную группу, показанную ниже где звездочка обозначает связь с остальной частью группы G. Согласно одному варианту реализации изобретения произошедшая из малеимида группа заменена на следующую группу: где звездочка обозначает связь с остальной частью группы G. Согласно одному варианту реализации малеимидная группа заменена на группу, выбранную из-N3 (азид). Согласно одному варианту реализации, если присутствует L1, то G1 представляет собой -NH2,-NHMe, -COOH, -ОН или -SH. Согласно одному варианту реализации, если присутствует L1, то G1 представляет собой -NH2 или-NHMe. Любая из указанных группа может представлять собой N-конец аминокислотной последовательности L1. Согласно одному варианту реализации, если присутствует L1, то G1 представляет собой -NH2, и L1 представляет собой аминокислотную последовательность -Х 1-Х 2-, как определено выше в отношенииR10. Согласно одному варианту реализации, если присутствует L1, то G1 представляет собой СООН. Указанная группа может представлять собой С-конец аминокислотной последовательности L1. Согласно одному варианту реализации, если присутствует L1, то G1 представляет собой ОН. Согласно одному варианту реализации, если присутствует L1, то G1 представляет собой SH. Группа G1 может быть превращена из одной функциональной группы в другую. Согласно одному варианту реализации, если присутствует L1, то G1 представляет собой -NH2. Указанная группа поддается превращению в другую группу G1, содержащую малеимидную группу. Например, группа -NH2 может взаимодействовать с кислотами или активированной кислотой (например, N-сукцинимидной формой) указанных групп G1, содержащих малеимид, показанных выше. Группа G1, таким образом, может превращаться в функциональную группу, которая является более подходящей для взаимодействия со связывающимся с клетками агентом. Согласно другим вариантам реализации RL представляет собой группу, которая представляет собой предшественник линкера, представленного с функциональной группой. Как отмечено выше, согласно одному варианту реализации, если присутствует L1, то G1 представляет собой -NH2, -NHMe, -СООН, -ОН или -SH. Согласно другому варианту реализации указанные группы используются в химически защищенной форме. Химически защищенная форма, таким образом, является предшественником линкера, содержащего функциональную группу. Согласно одному варианту реализации G1 представляет собой -NH2 в химически защищенной фор- 22024730 ме. Указанная группа может содержать карбаматную защитную группу. Карбаматная защитная группа может быть выбрана из группы, состоящей из Alloc, Fmoc, Boc, Troc, Teoc, Cbz и PNZ. Предпочтительно, если G1 представляет собой -NH2, то он содержит защитную группу Alloc илиFmoc. Согласно одному варианту реализации, если G1 представляет собой -NH2, то он содержит защитную группу Fmoc. Согласно одному варианту реализации указанная защитная группа представляет собой такую же карбаматную защитную группу, как карбаматная защитная группа для кэпирующей группы. Согласно одному варианту реализации, указанная защитная группа не представляет собой такую же карбаматную защитную группу, как карбаматная защитная группа для кэпирующей группы. Согласно указанному варианту реализации предпочтительно, что указанная защитная группа удаляется в условиях,в которых карбаматная защитная группа кэпирующей группы не удаляется. Химическую защитную группу можно удалять с получением функциональной группы, образующей связь со связывающимся с клетками агентом. Указанная функциональная группа затем необязательно может быть превращена в другую функциональную группу, как описано выше. Согласно одному варианту реализации, активная группа представляет собой амин. Указанный амин предпочтительно представляет собой N-концевой амин пептида и может представлять собой N-концевой амин предпочтительных дипептидов согласно настоящему изобретению. Активная группа может подвергаться реакции, приводящей к получению функциональной группы,склонной образовывать связь со связывающимся с клетками агентом. Согласно другим вариантам реализации, линкер представляет собой предшественник линкера, содержащего активную группу. Согласно указанному варианту реализации, линкер содержит активную группу, защищенную с помощью защитной группы. Защитная группа может быть удалена с получением линкера, содержащего активную группу. Когда активная группа представляет собой амин, защитная группа может представлять собой защитную группу для аминогруппы, такую как группы, описанные в источнике Green and Wuts. Защитная группа предпочтительно расположена ортогонально по отношению к другим защитным группам, при их наличии, в группе RL. Согласно одному варианту реализации защитная группа расположена ортогонально по отношению к кэпирующей группе. Таким образом, защитная группа активной группы способна удаляться при сохранении кэпирующей группы. Согласно другим вариантам реализации защитная группа и кэпирующая группа удаляются в тех же условиях, которые используются для удаления кэпирующей группы. Согласно одному варианту реализации RL представляет собой где звездочка обозначает место присоединения к положению N10, и волнистая линия обозначает место присоединения к остальной части линкера L1 или место присоединения к G1. Предпочтительно волнистая линия обозначает место присоединения к G1. Согласно одному варианту реализации RL представляет собой где звездочка и волнистая линия являются такими, как определено выше. Согласно одному варианту реализации RL представляет собой где звездочка и волнистая линия являются такими, как определено выше.- 23024730 Другие функциональные группы, подходящие для использования для формирования связи междуL1 и связывающимся с клетками агентом, описаны в WO 2005/082023. Линкеры могут содержать способные к расщеплению под действием протеазы пептидные фрагменты, содержащие одно или более аминокислотных звеньев. Пептидные линкерные реагенты могут быть получены с помощью способов твердофазного или жидкофазного синтеза (Е. Schroder and K. Lbke, ThePeptides, volume 1, pp 76-136 (1965) Academic Press), которые хорошо известны в области пептидной химии, включая химию t-BOC (Geiser et al. "Automation of solid-phase peptide synthesis" in MacromolecularProtein Res. 35:161-214), на автоматическом синтезаторе, таком как синтезатор пептидов Rainin Symphony (Protein Technologies, Inc., Туксон, Аризона), или Model 433 (Applied Biosystems, Фостер-Сити,Калифорния). Примеры аминокислотных линкеров включают дипептид, трипептид, тетрапептид или пентапептид. Примеры дипептидов включают: валин-цитруллин (vc или val-cit), аланин-фенилаланин (af или ala-phe). Примеры трипептидов включают: глицин-валин-цитруллин (gly-val-cit) и глицин-глицин-глицин (gly-glygly). Аминокислотные остатки, которые содержат аминокислотный линкерный компонент, включают остатки природных аминокислот, а также минорных аминокислот и не природных аналогов аминокислот, таких как цитруллин. Аминокислотные линкерные компоненты могут быть получены и по селективности для ферментативного расщепления определенными ферментами, например, опухолеассоциированной протеазой, катепсином В, С и D или протеазой плазмином. Боковые цепи аминокислот включают боковые цепи природных аминокислот, а также минорных аминокислот и неприродных аналогов аминокислот, таких как цитруллин. Боковые цепи аминокислот включают водород, метил, изопропил, изобутил, втор-бутил, бензил, и-гидроксибензил, -СН 2 ОН,-СН(ОН)СН 3,-CH2CH2SCH3,-CH2CONH2,-СН 2 СООН,-CH2CH2CONH2,-CH2CH2COOH,-(CH2)3NHC(=NH)NH2,-(CH2)3NH2, -(CH2)3NHCOCH3, -(CH2)3NHCHO, -(CH2)4NHC(=NH)NH2,-(CH2)4NH2,(CH2)4NHCOCH3,-(CH2)4NHCHO,-(CH2)3NHCONH2,-(CH2)4NHCONH2,CH2CH2CH(OH)CH2NH2, 2-пиридилметил-, 3-пиридилметил-, 4-пиридилметил-, фенил, циклогексил, а также следующие структуры: Когда боковая цепь аминокислоты содержит более одного атома водорода (глицин), атом углерода,к которому присоединена указанная боковая цепь аминокислоты, является хиральным. Каждый атом углерода, к которому присоединена боковая цепь аминокислоты, независимо находится в (S) или (R) конфигурации, или образует рацемическую смесь. Соединение лекарственное средство-линкерный реагент,таким образом, может находиться в виде энантиомерно чистой, рацемической или диастереомерной смеси. Согласно примерам вариантов реализации боковые цепи аминокислот выбраны из боковых цепей природных и неприродных аминокислот, включая аланин, 2-амино-2-циклогексилуксусную кислоту, 2 амино-2-фенилуксусную кислоту, аргинин, аспарагин, аспарагиновую кислоту, цистеин, глутамин, глутаминовую кислоту, глицин, гистидин, изолейцин, лейцин, лизин, метионин, норлейцин, фенилаланин,пролин, серин, треонин, триптофан, тирозин, валин, -аминомасляную кислоту, ,-диметиламиномасляную кислоту, ,-диметиламиномасляную кислоту, орнитин и цитруллин (Cit). Пример дипептидного линкерного реагента валин-цитруллин (val-cit или vc), пригодного для создания интермедиата линкер-фрагмент PBD лекарственного средства для конъюгирования со связывающимся с клетками агентом, например, антителом, содержащим парааминобензилкарбамоильный (РАВ) саморасщепляющийся спейсер, имеет следующую структуру: где Q представляет собой С 1-С 8 алкил, -O-(С 1-С 8 алкил), -галоген, -NO2 или -CN; и m равен целому числу в диапазоне от 0 до 4. Пример дипептидного линкерного реагента phe-lys(Mtr), содержащего п-аминобензильную группу,может быть получен в соответствии с источником Dubowchik, et al. (1997) Tetrahedron Letters, 38:5257-60 и имеет следующую структуру: где Mtr представляет собой моно-4-метокситритил, Q представляет собой С 1-С 8 алкил, -O-(С 1-С 8 алкил), -галоген, -NO2 или -CN; и m равен целому числу в диапазоне от 0 до 4. Саморасщепляющийся линкер РАВ (парааминобензилоксикарбонил) присоединяет фрагмент лекарственного средства к антителу в конъюгате антитело-лекарственное средство (Carl et al. (1981) J. Med.Chem. 24:479-480; Chakravarty et al. (1983) J. Med. Chem. 26:638-644; US 6214345; US 20030130189; US 20030096743; US 6759509; US 20040052793; US 6218519; US 6835807; US 6268488; US 20040018194; WO 98/13059; US 20040052793; US 6677435; US 5621002; US 20040121940; WO 2004/032828). Другие примеры саморасщепляющихся спейсеров, кроме РАВ, включают, но не ограничиваются ими: (i) ароматические соединения, которые по электронному строению подобны РАВ-группе, такие как производные 2 аминоимидазол-5-метанола (Hay et al. (1999) Bioorg. Med. Chem. Lett. 9:2237), тиазолы (US 7375078),множество последовательно соединенных РАВ звеньев (de Groot et al. (2001) J. Org. Chem. 66:8815-8830); и орто- или парааминобензилацетали; и (ii) гомологичные стирольные аналоги РАВ (US 7223837). Могут использоваться спейсеры, которые подвергаются циклизации при гидролизе амидной связи, такие как замещенные и незамещенные амиды 4-аминомасляной кислоты (Rodrigues et al. (1995) Chemistry Biology 2:223), замещенные подходящим образом бицикло[2.2.1] и бицикло[2.2.2] кольцевые системы (Storm et(1990) J. Org. Chem. 55:5867). Способные к элиминированию аминсодержащие лекарственные средства с замещенным глицином (Kingsbury et al. (1984) J. Med. Chem. 27:1447) также являются примерами саморасщепляющихся спейсеров, применимых в ADC. Согласно одному варианту реализации реагент, представляющий собой дипептидный РАВ аналог валин-цитруллин, содержит 2,6-диметилфенильную группу и имеет следующую структуру: Линкерные реагенты, пригодные для получения конъюгатов антитело-лекарственное средство, согласно настоящему изобретению включают, но не ограничиваются ими: ВМРЕО, BMPS, EMCS, GMBS,HBVS, LC-SMCC, MBS, MPBH, SBAP, SIA, SIAB, SMCC, SMPB, SMPH, сульфо-EMCS, сульфо-GMBS,сульфо-KMUS, сульфо-MBS, сульфо-SIAB, сульфо-SMCC и сульфо-SMPB и SVSB (сукцинимидил-(4 винилсульфон)бензоат), и бис-малеимидные реагенты: DTME, BMB, BMDB, ВМН, ВМОЕ, 1,8-бис-малеимидодиэтиленгликоль (ВМ(РЕО)2) и 1,11-бис-малеимидотриэтиленгликоль (ВМ(РЕО)з), которые являются коммерчески доступными от компании Pierce Biotechnology, Inc., ThermoScientific, Rockford, Иллинойс, США, и других поставщиков реагентов. Бис-малеимидные реагенты обеспечивают присоединение свободной тиоловой группы цистеинового остатка антитела к тиолсодержащему фрагменту лекарственного средства, метки или линкерного интермедиата, последовательное или параллельное. Другие функциональные группы помимо малеимида, которые являются реакционноспособными по отношению к тиоловой группе антитела, PBD фрагменту лекарственного средства или линкерному интермедиату,включают йодацетамид, бромацетамид, винилпиридин, дисульфид, пиридилдисульфид, изоцианат и изотиоцианат. Другие варианты линкерных реагентов представляют собой: N-сукцинимидил-4-(2-пиридилтио)пентаноат (SPP), N-сукцинимидил-3-(2-пиридилдитио)пропионат (SPDP, Carlsson et al. (1978) Biochem. J. 173:723-737), сукцинимидил-4-(N-малеимидометил)циклогексан-1-карбоксилат (SMCC), иминотиолан (IT), бифункциональные производные сложных имидоэфиров (такие как диметиладипимидатHCl), активные сложные эфиры (такие как дисукцинимидилсуберат), альдегиды (такие как глутаральдегид), бис-азидосоединения (такие как бис-(n-азидобензоил)гександиамин), производные бис-диазония(такие как бис-(n-диазонийбензоил)этилендиамин), диизоцианаты (такие как толуол-2,6-диизоцианат) и бис-активные фторсодержащие соединения (такие как 1,5-дифтор-2,4-динитробензол). Пригодные для применения линкерные реагенты также могут быть получены из других коммерческих источников, таких как Molecular Biosciences Inc. (Боулдер, Колорадо, США), или получены в соответствии со способами,описанными в источнике Toki et al. (2002) J. Org. Chem. 67:1866-1872; US 6214345; WO 02/088172; US 2003130189; US 2003096743; WO 03/026577; WO 03/043583 и WO 04/032828. Линкер может представлять собой линкер разветвленного типа для ковалентного связывания более чем одного фрагмента лекарственного средства через разветвленный мультифункциональный линкерный фрагмент с антителом (US 2006/116422; US 2005/271615; de Groot et al. (2003) Angew. Chem. Int. Ed. 42:4490-4494; Amir et al. (2003) Angew. Chem. Int. Ed. 42:4494-4499; Shamis et al. (2004) J. Am. Chem. Soc. 126:1726-1731; Sun et al. (2002) BioorganicMedicinal Chemistry Letters 12:2213-2215; Sun et al. (2003)BioorganicMedicinal Chemistry 11:1761-1768; King et al. (2002) Tetrahedron Letters 43:1987-1990). Разветвленные линкеры могут повышать молярное соотношение лекарственного средства к антителу, т.е. нагрузку, которая связана с активностью ADC. Таким образом, когда антитело имеет только одну реакционноспособную тиоловую группу цистеина, множество фрагментов лекарственного средства может быть присоединено через разветвленный, или дендритный, линкер. В одном из примеров вариантов реализации линкер разветвленного типа имеет следующую структуру: где звездочка обозначает место присоединения к положению N10 PBD фрагмента. Связывающийся с клетками агент Связывающийся с клетками агент может быть любого типа и включает пептиды и непептиды. Непептиды могут включать антитела или фрагмент антитела, который содержит по меньшей мере один сайт связывания, лимфокины, гормоны, факторы роста, молекулы переноса биогенных веществ или любые другие связывающиеся с клетками молекулы или вещества. Термин "антитело" в настоящей заявке используется в широком смысле и в частности включает моноклональные антитела, поликлональные антитела, димеры, мультимеры, мультиспецифичные антитела(например, биспецифичные антитела) и фрагменты антител, при условии, что они проявляют желаемую биологическую активность (Miller et al. (2003) Jour. of Immunology 170:4854-4861). Антитела могут быть мышиными, человеческими, гуманизированными, гибридными или произошедшими из других видов. Антитело представляет собой белок, продуцируемый клетками иммунной системы, способный распознавать и связываться со специфическим антигеном. (Janeway, С., Travers, P., Walport, M., Shlomchik (2001)Immuno Biology, 5th Ed., Garland Publishing, New York). Антиген-мишень в целом имеет многочисленные сайты связывания, также называемые эпитопами, которые распознают участки CDR множества антител. Каждое антитело, которое специфически связывается с отдельным эпитопом, имеет отличную структуру. Таким образом, один антиген может иметь более одного соответствующего ему антитела. Антитело включает полноразмерную молекулу иммуноглобулина или иммунологически активную часть полноразмерной молекулы иммуноглобулина, т.е. молекулу, которая содержит антиген-связывающий сайт,- 26024730 иммуноспецифически связывающийся с антигеном интересующей мишени или его частью, при этом указанные мишени включают, но не ограничиваются ими, раковые клетки или клетки, которые продуцируют аутоиммунные антитела, ассоциированные с аутоиммунным заболеванием. Иммуноглобулин может относиться к любому типу (например, IgG, IgE, IgM, IgD и IgA), классу (например, IgG1, IgG2, IgG3,IgG4, IgA1 и IgA2) или подклассу молекул иммуноглобулинов. Иммуноглобулины могут иметь различное происхождение, включая иммуноглобулины человека, мыши или кролика."Фрагменты антител" включают часть полноразмерного антитела, в целом, его антигенсвязывающую или вариабельную область. Примеры фрагментов антител включают Fab, Fab', F(ab')2 и Fvфрагменты; диатела; линейные антитела; фрагменты, полученные из Fab-экспрессионной библиотеки,антиидиотипические (анти-Id) антитела, CDR (определяющую комплементарность область) и связывающиеся с эпитопом фрагменты любого из указанных выше фрагментов, которые иммуноспецифично связываются с антигенами раковых клеток, вирусными антигенами или микробными антигенами, молекулы одноцепочечных антител и мультиспецифические антитела, образованные из фрагментов антител. В настоящем описании термин "моноклональное антитело" относится к антителу, полученному из популяции по существу гомогенных антител, т.е. отдельные антитела, содержащие указанную популяцию, являются идентичными за исключением возможных природных мутаций, которые могут присутствовать в минимальном количестве. Моноклональные антитела являются высоко специфичными, при этом они направлены против одного антигенного сайта. Более того, в отличие от составов поликлональных антител, которые содержат различные антитела, направленные против различных детерминант (эпитопов), каждое моноклональное антитело направлено против одной детерминанты на антигене. Помимо их специфичности преимуществом моноклональных антител является также в возможности их синтеза без загрязнения другими антителами. Определение "моноклональное" указывает характеристику антитела, полученного из по существу гомогенной популяции антител, при этом указанное определение не подразумевает продукцию антител каким-либо определенным способом. Например, моноклональные антитела для применения в соответствии с настоящим изобретением могут быть получены с помощью гибридомных способов, впервые описанных в источнике Kohler et al. (1975) Nature 256:495, или могут быть получены с помощью способов рекомбинации ДНК (см. US 4816567). Моноклональные антитела также могут быть выделены из фаговых библиотек антител с использованием методов, описанных в источнике Clackson et al. (1991) Nature, 352:624-628; Marks et al. (1991) J. Mol. Biol., 222:581-597. В настоящем описании моноклональные антитела, в частности, включают "гибридные" антитела, в которых часть тяжелой и/или легкой цепи идентична или гомологична соответствующим последовательностям в антителах, полученных из определенных видов или принадлежащих определенному классу или подклассу антител, тогда как остальная часть цепи (цепей) является идентичной или гомологичной соответствующим последовательностям антител, произошедших из другого вида или принадлежащих другому классу или подклассу антител, а также фрагментам таких антител, при условии, что они проявляют желаемую биологическую активность (US 4816567; и Morrison et al. (1984) Proc. Natl. Acad. Sci. USA,81:6851-6855). Гибридные антитела включают "приматизированные" антитела, содержащие вариабельные доменные антиген-связывающие последовательности, произошедшие из последовательностей константной области примата, не представляющего собой человека (например, мартышковых или человекообразных обезьян), и человека. В настоящем описании "интактное антитело" представляет собой антитело, содержащее домены VL и VH, а также константный домен легкой цепи (CL) и константные домены тяжелой цепи CH1, CH2 и СН 3. Константные домены могут представлять собой константные домены нативных последовательностей (например, константные домены нативной последовательности человека) или вариантных аминокислотных последовательностей. Интактное антитело может иметь одну или более "эффекторных функций", которые относятся к биологическим активностям, свойственным Fc-области (нативной последовательности Fc-области или вариантной аминокислотной последовательностью Fc области) антитела. Примеры эффекторных функций антител включают C1q-связывание; зависимую от комплемента цитотоксичность; Fc-рецепторное связывание; антитело-зависимая опосредованная клетками цитотоксичность(ADCC); фагоцитоз и отрицательная регуляция рецепторов клеточной поверхности, таких как Вклеточный рецептор и BCR. В зависимости от аминокислотной последовательности константного домена их тяжелых цепей интактные антитела могут быть отнесены к различным "классам". Существует пять основных классов интактных антител: IgA, IgD, IgE, IgG и IgM, и некоторые из указанных классов могут быть дополнительно разделены на "подклассы" (изотипы), например, IgG1, IgG2, IgG3, IgG4, IgA и IgA2. Константные домены тяжелой цепи, которые соответствуют различным классам антител, называются , , ,исоответственно. Субъединичная структура и трехмерные конфигурации различных классов иммуноглобулинов хорошо известны. Примеры связывающихся с клетками агентов включают агенты, описанные для применения в WO 2007/085930, которая включена в настоящую заявку. Связывающийся с клетками агент может представлять собой или включать полипептид. Указанный полипептид может представлять собой циклический полипептид. Связывающийся с клетками агент мо- 27024730 жет представлять собой антитело. Таким образом, согласно одному варианту реализации настоящего изобретения предложен конъюгат антитело-лекарственное средство (ADC). Нагрузка лекарственного средства Нагрузка лекарственного средства представляет собой среднее количество PBD лекарственного средства на антитело. Нагрузка лекарственного средства может варьироваться от 1 до 8 фрагментов лекарственного средства (D) на антитело (Ab), т.е. при этом 1, 2, 3, 4, 5, 6, 7 и 8 фрагментов лекарственного средства ковалентно связаны с антителом. Композиции ADC включают совокупность антител, конъюгированных с фрагментами лекарственных средств в количестве от 1 до 8. Среднее число лекарственных средств на антитело в композициях ADC, полученных в результате реакций конъюгации, может быть определено стандартными способами, таким как масс-спектрометрия, твердофазный ИФА-анализ (ELISA), электрофорез и ВЭЖХ. Также можно определить количественное распределение ADC в единицах р. Среднее значение р в конкретной композиции ADC можно определить с помощью ELISA (Hamblett et al.(2004) Clin. Cancer Res. 10:7063-7070; Sanderson et al. (2005) Clin. Cancer Res. 11:843-852). Однако распределение значений р (нагрузка лекарственного средства) невозможно определить вследствие связывания антитело-антиген и предела обнаружения ELISA. Также с помощью ELISA при использовании метода для выявления конъюгата антитело-лекарственное средство нельзя определить, в каких сайтах фрагменты лекарственного средства присоединены к антителу, например, к фрагментам тяжелых цепей или легких цепей или определенным аминокислотным остаткам. В некоторых примерах разделение, очистка и характеристика однородных ADC, где р принимает определенное значение, может достигаться такими способами, как обращенно-фазовая ВЭЖХ или электрофорез. Для некоторых конъюгатов антитело-лекарственное средство р может ограничиваться числом сайтов присоединения на антителе. Например, антитело может содержать одну или несколько тиоловых групп цистеина или может содержать только одну или несколько достаточно реакционноспособных тиоловых групп, через которые может присоединяться линкер. Более высокая нагрузка лекарственного средства, например, р 5, может вызывать агрегацию, нерастворимость, токсичность или потерю проницаемости в клетки определенных конъюгатов антитело-лекарственное средство. Как правило, во время реакции конъюгации с антителом связывается число фрагментов лекарственного средства, меньше теоретического максимума. Антитело может содержать, например, много остатков лизина, которые не взаимодействуют с интермедиатом лекарственное средство-линкер (D-L) или линкерным реагентом. Только наиболее реакционноспособные группы лизина могут реагировать с реакционноспособным по отношению к аминам линкерным реагентом. Подобным образом, только наиболее реакционноспособные тиоловые группы цистеина могут реагировать с реакционноспособным по отношению к тиоловым группам линкерным реагентом. В целом, антитела содержат немного, если вообще содержат, свободных и реакционноспособных тиоловых групп цистеина, которые могут связываться с фрагментом лекарственного средства. Большинство тиоловых групп остатков цистеина в антителах в указанных соединениях существуют в виде дисульфидных мостиков и должны восстанавливаться с помощью восстановителей, таких как дитиотреитол (ДТТ) или ТСЕР, в частично или полностью восстановительных условиях. Нагрузка (отношение лекарственное средство/антитело) в ADC может контролироваться несколькими различными способами, включая: (i) ограничение молярного избытка интермедиата лекарственное средство-линкер (D-L) или линкерного реагента по отношению к антителу, (ii) ограничение времени или температуры реакции конъюгации, и (iii) частичные или ограничивающие восстановительные условия для модификации тиоловых групп цистеина. В реакционноспособных сайтах антитела могут быть сконструированы цистеиновые аминокислоты,которые не образуют межцепьевые или межмолекулярные дисульфидные связи (Junutula, et al., 2008bNature Biotech., 26(8):925-932; Doman et al. (2009) Blood 114(13):2721-2729; US 7521541; US 7723485; WO 2009/052249). Полученные тиоловые группы цистеинов могут взаимодействовать с линкерными реагентами или соединениями лекарственное средство-линкерный реагент согласно настоящему изобретению,содержащими реакционноспособные по отношению к тиольным группам электрофильные группы, такие как малеимидная или альфа-галогенамиды, с образованием ADC со сконструированными на основе цистеина антителами и фрагментами PBD лекарственного средства. Положение фрагмента лекарственного средства, таким образом, может планироваться, контролироваться и быть известным. Нагрузку лекарственного средства можно контролировать, так как сконструированные тиоловые группы цистеина, как правило, взаимодействуют с реакционноспособными по отношению к тиоловым группам линкерными реагентами или соединениями лекарственное средство-линкерный реагент с высокой эффективностью. Конструирование антитела IgG с введением аминокислоты цистеина путем замещения одного сайта в тяжелой или легкой цепи приводит к появлению двух новых цистеинов в симметричном антителе. Можно достичь нагрузку лекарственного средства со значением около 2 и относительную однородность продукта конъюгации ADC. Когда более одной нуклеофильной или электрофильной группы антитела реагирует с интермедиатом лекарственное средство-линкер или линкерным реагентом с последующим взаимодействием с фрагментом лекарственного средства, полученный продукт представляет собой смесь ADC соединений с рас- 28024730 пределением фрагментов лекарственного средства, присоединенных к антителу, например 1, 2, 3 и т.д. С помощью методов жидкостной хроматографии, таких как полимерная обращенно-фазовая хроматография (PLRP) и хроматография гидрофобного взаимодействия (HIC), можно разделять соединения в смеси в соответствии с нагрузкой лекарственного средства. Могут быть выделены композиции ADC с одним значением нагрузки лекарственного средства (р), однако указанные композиции ADC с одним значением нагрузки могут все еще представлять собой гетерогенные смеси, так как фрагменты лекарственного средства могут присоединяться с помощью линкера к различным сайтам антитела. Таким образом, композиции конъюгата антитело-лекарственное средство согласно настоящему изобретению включают смеси соединений антитело-лекарственное средство, представляющие собой конъюгаты, где антитело содержит один или более фрагментов PBD лекарственного средства и где фрагменты лекарственного средства могут быть присоединены к антителу через связывание с различными аминокислотными остатками. Согласно одному варианту реализации среднее количество мономерных или димерных пирролбензодиазепиновых групп в связывающемся с клетками агенте находится в диапазоне от 1 до 20. Согласно некоторым вариантам реализации диапазон выбран из от 1 до 8, от 2 до 8, от 2 до 6, от 2 до 4 и от 4 до 8. Согласно некоторым вариантам реализации на один связывающийся с клетками агент приходится одна мономерная или димерная пирролбензодиазепиновая группа. Пептиды Согласно одному варианту реализации связывающийся с клетками агент представляет собой линейный или циклический пептид, содержащий 4-20, предпочтительно 6-20 непрерывно расположенных аминокислотных остатков. Согласно указанному варианту реализации один связывающийся с клетками агент предпочтительно связан с одним мономерным или димерным пирролбензодиазепиновым соединением. Согласно одному варианту реализации связывающийся с клетками агент содержит пептид, который связывается с интегрином v6. Указанный пептид может являться селективным в отношении v6 по сравнению с XYS. Согласно одному варианту реализации связывающийся с клетками агент содержит полипептидA20FMDV-Cys. Указанный полипепетид A20FMDV-Cys имеет последовательность: NAVPNLRGDLQVLAQKVARTC. Альтернативно, могут использоваться другие последовательностиA20FMDV-Cys, в которых один, два, три, четыре, пять, шесть, семь, восемь, девять или десять аминокислотных остатков замещены другими аминокислотными остатками. Согласно одному варианту реализации антитело представляет собой моноклональное антитело; гибридное антитело; гуманизированное антитело; полностью гуманизированное антитело или одноцепочечное антитело. Согласно одному варианту реализации антитело представляет собой фрагмент одного из указанных антител, обладающий биологической активность. Примеры указанных фрагментов включают Fab-, Fab'-, F(ab')2- и Fv-фрагменты. Согласно указанным вариантам реализации каждое антитело может быть связано с одним или несколькими мономерными или димерными пирролбензодиазепиновыми группами. Предпочтительные соотношения пирролбензодиазепина к связывающемуся с клетками агенту приведены выше. Антитело может представлять собой доменное антитело (DAB). Согласно одному варианту реализации антитело представляет собой моноклональное антитело. Антитела для применения согласно настоящему изобретению включают антитела, описанные в WO 2005/082023, которая включена в настоящую заявку. В частности, предпочтительными являются антитела к опузолеассоциированным антигенам. Примеры указанных антигенов, известных в данной области техники, включают, без ограничения, указанные опухолеассоциированные антигены, приведенные в WO 2005/082023. См., например, с. 41-55. Конъюгаты согласно настоящему изобретению разработаны для направленного воздействия на опухолевые клетки через антигены их клеточной поверхности. Антигены обычно представляют собой антигены поверхности здоровых клеток, в случае нарушений наблюдается их экспрессия или гиперэкспрессия. В идеальном случае антиген-мишень экспрессируется только на пролиферативных клетках(предпочтительно опухолевых клетках), что, однако, редко наблюдается в действительности. В результате антигены-мишени обычно выбирают по разнице в уровне экспрессии между пролиферативными и здоровыми тканями. Были созданы антитела, специфично направленные против связанных с опухолями антигенов,включающих: крипто, CD30, CD19, CD33, гликопротеин NMB, CanAg, Her2 (ErbB2/Neu), CD56 (NCAM), CD22(Siglec2), CD33 (Siglec3), CD79, CD138, PSCA, PSMA (специфический мембранный антиген клеток предстательной железы), ВСМА, CD20, CD70, Е-селектин, EphB2, меланотрансферин, Muc16 и TMEFF2. Опухолеассоциированные антигены (tumor-associated antigens, TAA) известны в данной области техники и могут быть получены для применения для создания антител с использованием способов и сведений, хорошо известных в данной области техники. В попытках поиска эффективных клеточных мишеней для диагностики и терапии рака исследователи пытались идентифицировать трансмембранные или
МПК / Метки
МПК: A61K 47/48, A61P 35/00, C07D 487/04
Метки: конъюгаты, указанных, композиции, применение, конюгатов, фармацевтические, содержащие, соединения, пирролбензодиазепиновые, указанные
Код ссылки
<a href="https://eas.patents.su/30-24730-pirrolbenzodiazepinovye-soedineniya-ih-konyugaty-farmacevticheskie-kompozicii-soderzhashhie-ukazannye-konyugaty-i-primenenie-ukazannyh-konyugatov.html" rel="bookmark" title="База патентов Евразийского Союза">Пирролбензодиазепиновые соединения, их конъюгаты, фармацевтические композиции, содержащие указанные конъюгаты, и применение указанных конъюгатов</a>
Предыдущий патент: Киназные ингибиторы
Следующий патент: Способ безопочной формовки и машина для безопочной формовки
Случайный патент: Гидрат тартрата 1-{(2s)-2-амино-4-[2,4-бис-(трифторметил)-5,8-дигидропиридо[3,4-d]пиримидин-7(6h)-ил]-4-оксобутил}-5,5-дифторпиперидин-2-она












